Область техники
Приоритет
Настоящая заявка утверждает преимущество предварительной заявки США № 61/089972, поданной 19 августа 2008 года, содержание которой полностью включено в настоящий документ в качестве ссылки.
Область техники
Настоящее изобретение относится к области биологической науки, более конкретно к области терапии рака. В частности, настоящее изобретение относится к новым пептидам, которые являются крайне эффективными в качестве противоопухолевых вакцин и лекарственных средств для лечения и предотвращения опухолей.
Предшествующий уровень техники
Было продемонстрировано, что CD8-позитивные ЦТЛ распознают эпитопные пептиды, полученные из опухоль-ассоциированных антигенов (ОАА) и находящиеся на молекуле главного комплекса гистосовместимости (MHC) класса I, а затем убивают опухолевые клетки. С момента открытия семейства антигенов меланомы (MAGE) как первого примера ОАА, было обнаружено много других ОАА, главным образом, с помощью иммунологических подходов (NPL 1: Boon T, Int J Cancer 1993 May 8, 54(2): 177-80; NPL 2: Boon T & van der Bruggen P, J Exp Med 1996 Mar 1, 183(3): 725-9). Некоторые из этих ОАА в настоящее время проходят клинические исследования в качестве мишеней для иммунотерапии.
Выявление новых ОАА, способных индуцировать мощный и специфический противоопухолевый иммунный ответ, требует дальнейшего развития и применения в клинике стратегий пептидной вакцинации для различных типов рака (NPL 3: Harris CC, J Natl Cancer Inst 1996 Oct 16, 88(20): 1442-55; Butterfield LH et al., Cancer Res 1999 Jul 1,59(13): 3134-42; NPL 5: Vissers JL et al., Cancer Res 1999 Nov 1,59(21): 5554-9; NPL 6: van der Burg SH et al., J Immunol 1996 May 1, 156(9): 3308-14; NPL 7: Tanaka F et al., Cancer Res 1997 Oct 15 57(20): 4465-8; NPL 8: Fujie T et al., Int J Cancer 1999 Jan 18, 80(2): 169-72; NPL 9: Kikuchi M et al., Int J Cancer 1999 May 5, 81(3): 459-66; NPL 10: Oiso M et al., Int J Cancer 1999 May 5, 81(3): 387-94). До настоящего времени было несколько сообщений о клинических испытаниях c применением таких пептидов, полученных из опухоль-ассоциированных антигенов. К сожалению, до сих пор в этих исследованиях противоопухолевых вакцин наблюдали только низкую частоту объективных ответов (NPL 11: Belli F et al., J Clin Oncol 2002 Oct 15, 20(20): 4169-80; NPL 12: Coulie PG et al., Immunol Rev 2002 Oct, 188: 33-42; NPL 13: Rosenberg SA et al., Nat Med 2004 Sep, 10(9): 909-15).
Существует несколько типов HLA-A в мире. Из известных генотипов HLA - генотипы HLA-A0201, HLA-A0206, HLA-A1101, HLA-A2402, HLA-A2601, HLA-A3101 и HLA-A3303 известны, как имеющие более высокую частоту экспрессии, чем остальные типы (NPL 14: Lee K W, et al., Tissue Antigens 2005: 65: 437-447). Однако каждый генотип имеет различную аминокислотную последовательность и различное сродство к эпитопному пептиду (NPL 15: Journal of Immunological Methods, (1995), Vol.185, pp.181-190). Например, аминокислотный остаток альфа 1-домена генотипа HLA-A0206 отличается от такового у генотипа HLA-A0201 (т.е. тирозиновый остаток 33-ей аминокислоты SEQ ID NO:8 заменен на фенилаланин). С учетом этих различий, маловероятно, что ограниченный по HLA-A0201 эпитопный пептид будет пригоден для пациента с генотипом HLA-A0206. Таким образом, целью в данной области остается пептид, пригодный для различных типов пациентов.
С помощью анализа на микрочипах подтверждено, что HIG2 (hypoxia-inducible gene 2) и URLC10 (также именуемый LY6K; lymphocyte antigen 6 complex, locus K) активированы в некоторых опухолевых тканях, таких как рак почки и рак легких (PTL 1: WO2005/019475, PTL 2: WO2004/031413). Таким образом, HIG2 и URLC10 представляют собой интересные мишени для иммунотерапии рака, и специалисты в данной области ведут поиск эпитопных пептидов, полученных из них и индуцирующих ЦТЛ.
Список литературы
Непатентная литература
Патентная литература
[PTL 1]: WO2005/019475
[PTL 2]: WO2004/031413
Сущность изобретения
Настоящее изобретение частично основано на открытии нового применения двух пептидов с аминокислотной последовательностью, указанной в SEQ ID NO:1 или SEQ ID NO:2. В контексте настоящего изобретения мононуклеарные клетки периферической крови (PBMC), полученные от здорового донора, стимулировали кандидатными пептидами, полученными из HIG2 или URLC10. Были созданы ЦТЛ, которые специфически распознают HLA-A0206-позитивные клетки-мишени, активированные соответствующими кандидатными пептидами, и определены эпитопные пептиды, ограниченные по HLA-A0206, которые могут индуцировать мощный и специфический иммунный ответ против HIG2 или URLC10, презентированных на поверхности клеток-мишеней.
Таким образом, настоящее изобретение относится к пептидам, способным индуцировать ЦТЛ, а также к аминокислотным последовательностям SEQ ID NO:1 или 2. В дополнение к этому настоящее изобретение относится к применению модифицированных пептидов, где одна, две или более аминокислот замещены, удалены, вставлены и/или добавлены, при условии, что полученные модифицированные пептиды сохраняют способность исходного пептида индуцировать ЦТЛ.
При введении пациенту, чей антиген HLA является HLA-A0206, предлагаемые пептиды презентируются на поверхности антигенпрезентирующих клеток и затем индуцируют ЦТЛ, нацеленные на соответствующие пептиды. Таким образом, настоящее изобретение относится к антигенпрезентирующим клеткам и экзосомам, которые презентируют любой из предлагаемых пептидов с антигеном HLA-A0206, а также к способам индукции антигенпрезентирующих клеток.
Противоопухолевый иммунный ответ индуцируется введением указанных полипептидов HIG2 или URLC10 или полинуклеотида, кодирующего полипептиды, а также экзосом и антигенпрезентирующих клеток, которые презентируют полипептиды HIG2 или URLC10. Таким образом, еще одной целью настоящего изобретения является создание фармацевтических средств, содержащих в качестве активных ингредиентов полипептиды или полинуклеотиды, кодирующие их, а также экзосомы и антигенпрезентирующие клетки, и которые предназначены для введения пациенту, у которого HLA антиген является HLA-A0206. Фармацевтические средства по настоящему изобретению находят применение в качестве вакцин.
Кроме того, еще одной целью настоящего изобретения является создание способов лечения и/или профилактики (т.е. предупреждения) раков (опухолей), и/или предупреждения их послеоперационных рецидивов, а также способы индукции ЦТЛ, способы индукции иммунного противоракового (противоопухолевого) ответа и также противоопухолевого иммунитета, где пациент имеет HLA-A0206 антиген; такие способы включают этап введения пептидов с последовательностью SEQ ID NO:1 или SEQ ID NO:2, экзосом или антигенпрезентирующих клеток, презентирующих последовательность SEQ ID NO:1 или SEQ ID NO:2, или фармацевтических средств по изобретению. В дополнение к этому ЦТЛ по настоящему изобретению также находят применение в качестве противоопухолевых вакцин. Примеры раков-мишеней включают в качестве неограничивающих примеров рак почки, рак мочевого пузыря, рак шейки матки, холангиоцеллюлярную карциному, рак пищевода, рак желудка, немелкоклеточный рак легкого, остеосаркому, рак поджелудочной железы и опухоль мягких тканей.
Следует понимать, что как вышеизложенная сущность изобретения, так и последующее подробное описание представляют собой примеры вариантов осуществления и не ограничиваются изобретением или другими альтернативными вариантами осуществления изобретения.
Краткое описание фигур
Различные аспекты и применение настоящего изобретения станут очевидны специалистам в данной области после рассмотрения краткого описания фигур и подробного описания настоящего изобретения и предпочтительных вариантов его осуществления, которые следуют далее:
[фиг.1] фигура 1 включает серию фотографий, показывающих результаты ELISPOT анализа на IFN-гамма на ЦТЛ, которые были индуцированы пептидом, полученным из HIG2. ЦТЛ в лунках #1, #2, #5, #7, #8, #10, #13 и #14, стимулированные HIG2-A0206-9-4 (SEQ ID NO:1), демонстрируют мощную выработку IFN-гамма по сравнению с контролем. На фигурах "+" указывает, что клетки-мишени были активированы соответствующим пептидом, и "-" указывает, что клетки-мишени не были активированы никакими пептидами.
[фиг.2] фигура 2 показывает серию линейных графиков с данными твердофазного иммуноферментного анализа на IFN-гамма, отображающих результаты создания линий ЦТЛ, стимулированных HIG2-A0206-9-4 (SEQ ID NO:1). Они демонстрируют, что линии ЦТЛ, созданные посредством стимуляции HIG2-A0206-9-4 (SEQ ID NO:1), показали мощную выработку IFN-гамма по сравнению с контролем. На фигурах "+" указывает, что клетки-мишени были активированы соответствующим пептидом, и "-" указывает, что клетки-мишени не были активированы никакими пептидами.
[фиг.3] фигура 3 показывает линейный график с данными твердофазного иммуноферментного анализа на IFN-гамма, демонстрирующий результаты создания клона ЦТЛ, стимулированного HIG2-A0206-9-4 (SEQ ID NO:1). Результаты показывают, что клон ЦТЛ, созданный посредством стимуляции HIG2-A0206-9-4 (SEQ ID NO:1), показал мощную выработку IFN-гамма по сравнению с контролем. На фигурах "+" указывает, что клетки-мишени были активированы соответствующим пептидом, и "-" указывает, что клетки-мишени не были активированы никакими пептидами.
[фиг.4] фигура 4 показывает линейный график, демонстрирующий специфическую активность ЦТЛ против клеток-мишеней, которые экспрессируют HIG2 и HLA-A*0206. В качестве контроля были приготовлены клетки COS7, трансфецированные только HLA-A*0206 и активированные несоответствующим пептидом, полученным из HIG2, или трансфецированные только HIG2. Клон ЦТЛ, созданный при помощи HIG2-A0206-9-4 (SEQ ID NO:1), показал высокоспецифичную активность ЦТЛ против клеток COS7, трансфецированных как HIG2, так и HLA-A0206 (черная ромбовидная метка). С другой стороны, не выявлено никакой значительной специфической активности ЦТЛ против клеток-мишеней, экспрессирующих или HLA-A0206 (пустая треугольная метка) или HIG2 (пустой круг).
[фиг.5] фигура 5 включает серию фотографий, показывающих результаты ELISPOT анализа на IFN-гамма на ЦТЛ, которые были индуцированы пептидом, полученным из URLC10. ЦТЛ в лунке #7, стимулированные URLC10-A0206-10-211 (SEQ ID NO:2), показали мощную выработку IFN-гамма по сравнению с контролем. На фигурах "+" указывает, что клетки-мишени были активированы соответствующим пептидом, и "-" указывает, что клетки-мишени не были активированы никакими пептидами.
[фиг.6] фигура 6 показывает линейный график с данными твердофазного иммуноферментного анализа на IFN-гамма, демонстрирующий результаты создания линий ЦТЛ, стимулированных URLC10-A0206-10-211 (SEQ ID NO:2). Результаты демонстрируют, что линия ЦТЛ, созданная посредством стимуляции URLC10-A0206-10-211 (SEQ ID NO: 2), показала мощную выработку IFN-гамма по сравнению с контролем. На фигурах "+" указывает, что клетки-мишени были активированы соответствующим пептидом, и "-" указывает, что клетки-мишени не были активированы никакими пептидами.
[фиг.7] фигура 7 показывает линейный график с данными твердофазного иммуноферментного анализа на IFN-гамма, демонстрирующий результаты создания клона ЦТЛ, стимулированного URLC10-A0206-10-211 (SEQ ID NO:2). Результаты демонстрируют, что клон ЦТЛ, созданный посредством стимуляции URLC10-A0206-10-211 (SEQ ID NO:2), показал мощную выработку IFN-гамма по сравнению с контролем. На фигурах "+" указывает, что клетки-мишени были активированы соответствующим пептидом, и "-" указывает, что клетки-мишени не были активированы никакими пептидами.
[фиг.8] фигура 8 показывает линейный график, демонстрирующий специфическую активность ЦТЛ против клеток-мишеней, которые экспрессируют URLC10 и HLA-A*0206. В качестве контроля были приготовлены клетки COS7, трансфецированные только полноразмерным геном URLC10 или только геном HLA-A*0206. Клон ЦТЛ, созданный при помощи URLC10-A0206-10-211 (SEQ ID NO:2), показал высокоспецифичную активность ЦТЛ против клеток COS7, трансфецированных как HIG2, так и HLA-A0206 (черная ромбовидная метка). С другой стороны, не выявлено никакой значительной специфической активности ЦТЛ против клеток-мишеней, экспрессирующих или HLA-A0206 (пустая треугольная метка), или URLC10 (пустой круг). На фигурах "R" означает Респондер и "S" означает Стимулятор.
Описание вариантов осуществления
Хотя можно использовать в практическом осуществлении или тестировании вариантов осуществления настоящего изобретения любые способы и материалы, сходные или эквивалентные тем, которые описаны в настоящем документе, предпочтительные способы, приборы и материалы описаны здесь. Однако перед тем как настоящие материалы и способы будут описаны, следует иметь в виду, что настоящее изобретение не ограничено конкретными величинами, формами, размерами, материалами, методиками, протоколами и т.д., описываемыми в настоящем документе, поскольку они могут варьировать в соответствии с рутинными экспериментами и оптимизацией. Следует также понимать, что терминология, которая использована при описании, применяется только с целью описания конкретных версий или вариантов осуществления и не имеет целью ограничить объем настоящего изобретения, который ограничен только прилагаемой формулой изобретения.
Раскрытие каждой публикации, патента или патентной заявки, упомянутой в данном описании конкретным образом, в полном объеме включено в настоящий документ в качестве ссылки. Однако ничто в настоящем документе не должно истолковываться как признание того, что изобретение не имеет права датировать более ранним числом такое раскрытие в силу предшествующего изобретения.
В случае конфликта настоящее описание, включая определения, будет иметь преимущество. Кроме того, материалы, способы и примеры являются только иллюстрирующими и неограничивающими.
I.Определения
Слова "a", "an", и "the", как применяют в настоящем документе, означают "по меньшей мере, один", если не указано иное.
Термины "полипептид", "пептид" и "белок" используют в данном документе взаимозаменяемо по отношению к полимеру из аминокислотных остатков. Термины употребляют по отношению к аминокислотным полимерам, в которых один или несколько аминокислотных остатков представляют собой модифицированный остаток или неприродный остаток, такой как искусственный химический миметик соответствующей природной аминокислоты, а также по отношению к природным аминокислотным полимерам.
Как применяют в настоящем документе, термин "аминокислота" относится к природным и синтетическим аминокислотам, а также к аминокислотным аналогам и миметикам аминокислот, которые функционируют сходно с природными аминокислотами. Природными аминокислотами являются те, которые кодированы генетическим кодом, а также те, которые модифицированы в клетках после трансляции (например, гидроксипролин, гамма-карбоксиглутамат и O-фосфосерин). Фраза "аминокислотный аналог" относится к соединениям, которые имеют такую же основную химическую структуру (альфа-углерод, связанный с водородом, карбоксигруппу, аминогруппу и R-группу), что и природная аминокислота, но с модифицированной R-группой или модифицированным остовом (например, гомосерин, норлейцин, метионин, сульфоксид, метионин метилсульфония). Фраза "аминокислотный миметик" относится к химическим соединениям, которые имеют различные структуры, но сходные функции с основными аминокислотами.
Аминокислоты могут быть обозначены в данном документе общеизвестными трехбуквенными символами или однобуквенными символами, рекомендованными Комиссией по Химической Номенклатуре IUPAC-IUB.
Термины "ген", "полинуклеотиды", "нуклеотиды" и "нуклеиновые кислоты" используются в данном документе взаимозаменяемо, если конкретно не указано иное, и подобно аминокислотам обозначенаются своими общепринятыми однобуквенными кодами.
Если не определено иное, термин "рак" относится к ракам со сверхэкспрессией гена HIG2 или URLC10. Примеры раков со сверхэкспрессией гена HIG2 включают в качестве неограничивающих примеров рак почки и карциному мягких тканей; примеры раков со сверхэкспрессией гена URLC10 включают в качестве неограничивающих примеров рак мочевого пузыря, рак шейки матки, рак пищевода, рак желудка, немелкоклеточный рак легкого (NSCLC), остеосаркому, рак поджелудочной железы и опухоль мягких тканей.
Если не определено иное, термины "цитотоксический T-лимфоцит", "цитотоксическая T-клетка" и "ЦТЛ" используют в данном документе взаимозаменяемо и, если конкретно не указано иное, по отношению к подгруппе T-лимфоцитов, которые способны распознавать чужеродные клетки (например, опухолевые клетки, вирус-инфицированные клетки) и индуцировать гибель этих клеток.
Если не определено иное, все технические и научные термины, использованные в данном документе, имеют то же самое значение, в котором их обычно понимает специалист в области, к которой относится изобретение.
II.Пептиды
Чтобы продемонстрировать, что пептиды HIG2-A0206-9-4 (SEQ ID NO:1) и URLC10-A0206-10-211 (SEQ ID NO:2) функционируют как антигены, распознающиеся цитотоксическими T-лимфоцитами (ЦТЛ), данные пептиды исследовали, для того чтобы установить, являются ли они антигенными эпитопами, ограниченными по HLA-A0206. После стимуляции Т-клеток in vitro дендритными клетками (DC), нагруженными данными пептидами, были успешно созданы ЦТЛ с использованием каждого из пептидов HIG2-A0206-9-4 (SEQ ID NO: 1) и URLC10-A0206-10-211 (SEQ ID NO: 2).
Эти полученные ЦТЛ показывают мощную специфическую цитотоксическую активность против клеток-мишеней, экспрессирующих антиген HLA-A0206, при обработке соответствующими пептидами. Результаты в настоящем документе демонстрируют, что эти пептиды могут быть эпитопными пептидами HIG2 и URLC10, ограниченными по HLA-A0206. Поскольку эти пептиды могут также быть эпитопными пептидами HIG2 или URLC10, ограниченными по HLA-A0201 (WO2008/102557, PCT/JP2008/000290, включенные в качестве ссылки в настоящий документ), фармацевтическое средство или композиция, которая содержит эти пептиды, могут быть применимы как для HLA-A0201-позитивных пациентов, так и для HLA-A0206-позитивных пациентов.
Поскольку гены HIG2 или URLC10 сверхэкспрессируются в большинстве опухолевых тканей, таких как рак мочевого пузыря, рак шейки матки, холангиоцеллюлярная карцинома, рак пищевода, рак желудка, немелкоклеточный рак легкого, остеосаркома, рак поджелудочной железы и опухоль мягких тканей, они являются хорошей мишенью для иммунотерапии. В частности, примеры раков со сверхэкспрессией HIG2 включают рак почки и опухоль мягких тканей. Также, примеры раков со сверхэкспрессией URLC10 включают рак мочевого пузыря, рак шейки матки, холангиоцеллюлярную карциному, рак пищевода, рак желудка, немелкоклеточный рак легкого, остеосаркому, рак поджелудочной железы и опухоль мягких тканей. Таким образом, настоящее изобретение относится к нонапептидам (пептидам, состоящим из девяти аминокислотных остатков) и декапептидам (пептидам, состоящим из десяти аминокислотных остатков), которые соответствуют эпитопным пептидам HIG2 или URLC10, ограниченным по HLA-A0206. Конкретно, предпочтительные примеры нонапептидов и декапептидов по настоящему изобретению включают пептиды с аминокислотной последовательностью, выбранной из SEQ ID NO:1 и 2. Более конкретно, примеры эпитопных пептидов HIG2, ограниченных по HLA-A0206, включают пептид, который содержит аминокислотную последовательность SEQ ID NO:1, и примеры эпитопных пептидов URLC10, ограниченных по HLA-A0206, включают пептид, который содержит аминокислотную последовательность SEQ ID NO:2.
В основном, модификация одной, двух или более аминокислот в белке не будет влиять на функцию белка или в некоторых случаях даже усилит желаемую функцию исходного белка. Действительно, известны модифицированные пептиды (т.е. пептиды, включающие аминокислотную последовательность, в которой один, два или несколько аминокислотных остатков модифицированы (т.е. замещены, удалены, добавлены и/или вставлены) по сравнению с исходной референсной последовательностью), которые сохраняют биологическую активность исходного пептида (Mark et al., Proc Natl Acad Sci USA 1984, 81: 5662-6; Zoller и Smith, Nucleic Acids Res 1982, 10: 6487-500; Dalbadie-McFarland et al., Proc Natl Acad Sci USA 1982, 79: 6409-13). Таким образом, в одном из вариантов осуществления пептиды по настоящему изобретению способны индуцировать ЦТЛ и имеют аминокислотную последовательность SEQ ID NO:1 или 2, где одна, две или даже более аминокислот добавлены, вставлены, удалены и/или замещены.
Специалисты в данной области признают, что единичные добавления или замены в аминокислотной последовательности, которые изменяют одну аминокислоту или небольшой процент аминокислот, как правило, приводят к сохранению свойств исходной аминокислотной боковой цепи. В связи с этим они обычно обозначаются как "консервативные замены" или "консервативные модификации", при которых результатом изменения белка является модифицированный белок со свойствами и функциями, аналогичными исходному белку. Таблицы консервативных замен, обеспечивающих получение функционально сходных аминокислот, хорошо известны в данной области. Примеры характеристик аминокислотных боковых цепей, которые желательно сохранить, включают, например, гидрофобные аминокислоты (A, I, L, M, F, P, W, Y, V), гидрофильные аминокислоты (R, D, N, C, E, Q, G, H, K, S, T) и боковые цепи, имеющие следующие функциональные группы или характеристики, в общем: алифатическая боковая цепь (G, A, V, L, I, P); боковая цепь, содержащая гидроксильную группу (S, T, Y); боковая цепь, содержащая атом серы (C, M); боковая цепь, содержащая карбоновую кислоту и амид (D, N, E, Q); боковая цепь, содержащая основание (R, K, H) и ароматическая боковая цепь (H, F, Y, W). Кроме того, следующие восемь групп, каждая из которых содержит аминокислоты, приемлемые в данной области в качестве консервативных замен друг для друга:
1) Аланин (A), Глицин (G);
2) Аспарагиновая кислота (D), Глутаминовая кислота (E);
3) Аспарагин (N), Глутамин (Q);
4) Аргинин (R), Лизин (K);
5) Изолейцин (I), Лейцин (L), Метионин (M), Валин (V);
6) Фенилаланин (F), Тирозин (Y), Триптофан (W);
7) Серин (S), Треонин (T); и
8) Цистеин (C), Метионин (M) (смотри, например, Creighton, Proteins 1984).
Такие консервативно модифицированные пептиды также рассматриваются в качестве пептидов по настоящему изобретению. Однако пептиды по настоящему изобретению этим не ограничиваются и могут включать неконсервативные модификации при условии, что пептид сохраняет способность исходного пептида индуцировать ЦТЛ. Кроме того, модифицированные пептиды не должны исключать ЦТЛ-индуцирующих пептидов полиморфных вариантов, межвидовых гомологов и аллелей HIG2 или URLC10.
При использовании в контексте иммунотерапии, пептиды по настоящему изобретению должны быть презентированы на поверхности клетки или экзосомы, предпочтительно в виде комплекса с антигеном HLA-A0206. Таким образом, предпочтительно выбирать пептиды, которые не только индуцируют ЦТЛ, но также обладают высокой аффинностью связывания с антигеном HLA-A0206. С этой целью пептиды могут быть модифицированы посредством замены, вставки, делеции и/или добавления аминокислотных остатков для получения модифицированного пептида с улучшенной аффинностью связывания. Поскольку закономерность последовательностей пептидов, которые отображаются посредством связывания с антигенами HLA, уже известна (J Immunol 1994, 152: 3913; Immunogenetics 1995, 41: 178; J Immunol 1994, 155: 4307), то в дополнение к пептидам, которые отображаются естественным образом, в иммуногенные пептиды по изобретению можно вводить модификации на основании такой закономерности. Замены можно вводить не только в терминальные аминокислоты, но также по позициям потенциального TCR-распознавания пептидов. Несколько исследований продемонстрировали, что замены аминокислот в пептиде могут быть эквивалентны исходным или лучше, например CAP1, p53 (264-272), Her-2/neu (369-377) или gp100 (209-217) (Zaremba et al., Cancer Res. 57, 4570-4577, 1997, T.K. Hoffmann et.al., J Immunol. (2002) Feb 1; 168(3): 1338-47., S.O. Dionne et.al. Cancer Immunol immunother. (2003) 52: 199-206 and S.O. Dionne et al. Cancer Immunology Immunotherapy (2004) 53, 307-314).
Настоящее изобретение также предусматривает добавление одной или двух аминокислот, которые можно добавлять к N- и/или C-концу пептидов по изобретению. Такие модифицированные пептиды с высокой аффинностью связывания антигена HLA и сохраненной способностью индуцировать ЦТЛ также включены в настоящее изобретение.
Однако, когда последовательность пептида идентична части аминокислотной последовательности эндогенного или экзогенного белка с другой функцией, можно индуцировать побочные эффекты, такие как аутоиммунные нарушения и/или аллергические симптомы по отношению к специфическим веществам. Таким образом, предпочтительно сначала провести поиски гомологии с использованием доступных баз данных, для того чтобы избежать ситуаций, в которых последовательность пептида совпадает с аминокислотной последовательностью другого белка. Когда из поиска гомологии станет ясно, что не существует пептида с различием даже по одной или двум аминокислотам по сравнению с пептидом по изобретению, пептид по изобретению может быть модифицирован для повышения аффинности связывания с антигенами HLA и/или для усиления его способности индуцировать ЦТЛ без какой-либо опасности таких побочных эффектов.
Хотя ожидается, что пептиды, модифицированные, как описано выше, будут высокоэффективными, кандидатные пептиды проверяют на наличие способности индуцировать ЦТЛ для выбора более высокоэффективных пептидов. В настоящем документе фраза "способность индуцировать ЦТЛ" указывает на способность пептида индуцировать цитотоксические лимфоциты (ЦТЛ), когда он презентирован на антигенпрезентирующих клетках. Далее, "способность индуцировать ЦТЛ" включает в себя способность пептида индуцировать активацию ЦТЛ, пролиферацию ЦТЛ, способствовать ЦТЛ-опосредованному лизису клеток-мишеней и повышать выработку IFN-гамма цитотоксическими лимфоцитами.
Подтверждение способности индуцировать ЦТЛ осуществляют путем индукции антигенпрезентирующих клеток, несущих антигены MHC человека (например, B-лимфоцитов, макрофагов и дендритных клеток (DC)), или, более конкретно, DC, полученных из мононуклеарных лейкоцитов периферической крови человека; после стимуляции пептидами их смешивают с CD8-позитивными клетками и затем измеряют IFN-гамма, который произведен и высвобожден цитотоксическими лимфоцитами против клеток-мишеней. В качестве реакционной системы можно использовать трансгенных животных, которые созданы для экспрессии антигена человека HLA-A0206 (BenMohamed L, Krishnan R, Longmate J, Auge C, Low L, Primus J, Diamond DJ, Hum Immunol 2000 Aug, 61(8): 764-79). Например, клетки-мишени можно пометить радиоактивной меткой 51Cr и т.п., и цитотоксическую активность можно рассчитать по радиоактивности, высвобожденной из клеток-мишеней, у которых антиген HLA является HLA-A0206. Альтернативно, способность индуцировать ЦТЛ можно оценить путем измерения IFN-гамма, который произведен и высвобожден цитотоксическими лимфоцитами в присутствии антигенпрезентирующих клеток (APC), несущих иммобилизованные пептиды, и путем визуализации зоны ингибирования в среде для клеток с использованием моноклональных антител к IFN-гамма.
В дополнение к вышеописанным модификациям пептиды по настоящему изобретению могут также быть связаны с другими веществами, при условии, что полученный связанный пептид сохраняет необходимую способность исходного пептида индуцировать ЦТЛ. Примеры подходящих веществ включают в качестве неограничивающих примеров: пептиды, липиды, сахар и цепи сахаров, ацетильные группы, природные и синтетические полимеры и т.д. Пептиды могут содержать модификации, такие как гликозилирование, окисление боковой цепи или фосфорилирование, и т.д., при условии, что модификации не нарушают биологическую активность исходного пептида. Такие типы модификаций можно осуществлять для придания дополнительных функций (например, функции нацеливания и функции доставки) или для стабилизации полипептида.
Например, для увеличения стабильности полипептида in vivo, существует известное в данной области введение D-аминокислот, миметиков аминокислот неприродных аминокислот; этот подход можно также применять по отношению к полипептидам по изобретению. Стабильность полипептида можно анализировать различными способами. Например, для проверки стабильности можно использовать пептидазы и различные биологические среды, такие как плазма и сыворотка человека (смотри, например, Verhoef et al., Eur J Drug Metab Pharmacokin 1986, 11: 291-302).
Далее, пептиды по настоящему изобретению можно присоединять к другим пептидам посредством спейсеров или линкеров. Примеры других пептидов включают в качестве неограничивающих примеров пептиды, полученные из других ОАА и способные индуцировать ЦТЛ. Альтернативно, два или более пептида по настоящему изобретению могут быть связаны посредством спейсеров или линкеров. Пептиды, связанные посредством спейсеров или линкеров, могут быть одинаковыми или отличаться друг от друга. Спейсеры или линкеры конкретно не ограничены, но предпочтительно являются пептидами, более предпочтительно пептидами с одним или несколькими сайтами расщепления, которые можно расщепить ферментами, такими как пептидазы, протеазы и протеасомы. Примеры линкеров или спейсеров включают в качестве неограничивающих примеров: AAY (P. M. Daftarian et al., J Trans Med 2007, 5:26), AAA, NKRK (R. P. M. Sutmuller et al., J Immunol. 2000, 165: 7308-7315) или от одного до нескольких остатков лизина (S. Ota et al., Can Res. 62, 1471-1476, K. S. Kawamura et al., J Immunol. 2002, 168: 5709-5715). Пептиды по настоящему изобретению охватывают такие пептиды, связанные с другими пептидами посредством спейсеров или линкеров.
Пептиды по настоящему изобретению могут существовать на поверхности клетки, несущей антигены MHC человека (например, антигенпрезентирующая клетка), или экзосомы в виде комплексов в сочетании с молекулами MHC и таким образом индуцировать ЦТЛ. Клетки и экзосомы можно получать способами, широко известными в данной области, например клетки можно получать посредством контакта с пептидами по настоящему изобретению и экзосомы можно получать посредством сбора фракции, содержащей экзосомы, из клеток, контактировавших с пептидами по настоящему изобретению (смотри, например, Japanese Patent Application Kohyo Publications No. Hei 11-510507 и WO99/03499). Пептиды по настоящему изобретению охватывают пептиды, существующие на поверхности клетки или экзосомы в виде комплексов в сочетании с молекулами MHC.
В настоящем документе пептиды по настоящему изобретению могут быть также описаны как "пептид(ы) HIG2 или URLC10" или "полипептид(ы) HIG2 или URLC10".
III. Препараты пептидов
Пептиды по настоящему изобретению можно приготовить с использованием хорошо известных техник. Например, пептиды можно приготовить синтетически с использованием технологии рекомбинантных ДНК или химического синтеза. Пептиды по настоящему изобретению могут быть синтезированы по отдельности или в виде более длинных полипептидов, состоящих из двух или более пептидов. Пептиды затем можно изолировать, т.е. очищать или выделять таким образом, чтобы они стали по существу свободными от других природных белков клетки-хозяина и их фрагментов или любых других химических веществ.
Пептид по настоящему изобретению можно получать посредством химического синтеза, основываясь на выбранной аминокислотной последовательности. Примеры подходящих способов пептидного синтеза, которые можно применять для синтеза, включают в качестве неограничивающих примеров:

Альтернативно, пептиды по изобретению можно получать, применяя любые известные способы генетической инженерии для получения пептидов (например, Morrison J, J Bacteriology 1977, 132: 349-51; Clark-Curtiss & Curtiss, Methods in Enzymology (eds. Wu et al.) 1983, 101: 347-62). Например, сначала готовят подходящий вектор, который содержит полинуклеотид, кодирующий пептид по изобретению в экспрессирующейся форме (например, после регуляторной последовательности, которая соответствует промоторной последовательности), и трансформируют подходящую клетку-хозяина. Клетку-хозяина затем культивируют для получения интересующего пептида. Пептид также можно получать in vitro, применяя систему трансляции in vitro.
IV. Полинуклеотиды
Настоящее изобретение также относится к полинуклеотиду, который кодирует указанные выше пептиды по настоящему изобретению. Таковые включают в себя полинуклеотиды, полученные из природных генов HIG2 или URLC10 (SEQ ID NO:3 или 5, GenBank Accession NO NM_013332 или NM_017527), а также те, которые содержат их консервативно модифицированную нуклеотидную последовательность. В настоящем документе фраза "консервативно модифицированная нуклеотидная последовательность" относится к последовательности, которая кодирует идентичные или по существу идентичные аминокислотные последовательности. В связи с вырожденностью генетического кода большое число функционально идентичных нуклеиновых кислот кодирует любой заданный белок. Например, кодоны GCA, GCC, GCG и GCU - все кодируют аминокислоту аланин. Таким образом, в каждой позиции, где кодоном предусмотрен аланин, кодон можно изменить на любой соответствующий описанный кодон без изменения закодированного полипептида. Такие вариации нуклеиновых кислот являются "молчащими мутациями", которые представляют собой один из видов консервативно модифицированных вариаций. Каждая последовательность нуклеиновой кислоты в настоящем документе, которая кодирует пептид, описывает также каждую возможную молчащую мутацию нуклеиновой кислоты. Специалисту в данной области будет понятно, что каждый кодон в нуклеиновой кислоте (за исключением AUG, который является, как правило, единственным кодоном для метионина, и TGG, который является, как правило, единственным кодоном для триптофана) может быть модифицирован для получения функционально идентичной молекулы. Таким образом, каждая молчащая мутация нуклеиновой кислоты, кодирующей пептид, косвенно описана в каждой раскрытой последовательности.
Полинуклеотид по настоящему изобретению может быть составлен из ДНК, РНК и их производных. ДНК обычно состоит из оснований, таких как A, T, C, и G; в РНК T заменена на U.
Полинуклеотид по настоящему изобретению может кодировать множество пептидов по настоящему изобретению, со вставками или без вставок аминокислотных последовательностей между ними. Например, вставленная аминокислотная последовательность может содержать сайт щепления (например, сайт распознавания фермента) полинуклеотида или транслируемых пептидов. Кроме того, полинуклеотид может включать в себя любые последовательности дополнительно к кодирующей последовательности, которая кодирует пептид по настоящему изобретению. Например, полинуклеотид может быть рекомбинантным полинуклеотидом, который включает в себя регуляторные последовательности, необходимые для экспрессии пептида, или может быть экспрессирующим вектором (плазмидой) с маркерными генами и т.п. В основном, такие рекомбинантные полинуклеотиды могут быть приготовлены путем воздействия на полинуклеотиды подходящими рекомбинантными способами, например с использованием полимераз и эндонуклеаз.
Для получения полинуклеотидов по настоящему изобретению можно использовать технологии как рекомбинантного, так и химического синтеза. Например, полинуклеотид может быть получен посредством вставки в подходящий вектор, который экспрессируется в компетентных клетках после трансфекции. Альтернативно, полинуклеотид можно амплифицировать с использованием методов ПЦР или экспрессии в подходящих носителях (смотри, например, Sambrook et al., Molecular Cloning: A Laboratory Manual, Cold Spring Harbor Laboratory, New York, 1989). Альтернативно, полинуклеотид может быть синтезирован с использованием методов твердой фазы, как описано в Beaucage SL & Iyer RP, Tetrahedron 1992, 48: 2223-311; Matthes et al., EMBO J 1984, 3: 801-5.
Векторы, содержащие полинуклеотид по настоящему изобретению, и клетки-хозяева, которые содержат такие векторы, также включены в настоящее изобретение.
V. Экзосомы
Настоящее изобретение дополнительно относится к внутриклеточным пузырькам, которые называются экзосомами и презентируют на своей поверхности комплексы, образованные пептидами и антигенами HLA. Экзосомы могут быть получены, например, с использованием способов, подробно описанных в Japanese Patent Application Kohyo Publications Nos. Hei 11-510507 и WO99/03499, и могут быть приготовлены с использованием APC, полученных от пациентов, которых лечат и/или которым проводят профилактику. Экзосомы по данному изобретению можно прививать как вакцины, некоторым образом сходно с пептидами по данному изобретению.
В контексте настоящего изобретения тип антигенов HLA, включенных в комплексы, должен быть HLA-A0206, и пациент, которому прививают экзосомы, должен иметь антиген HLA-A0206. Обычно, в клинике, тип антигена HLA у пациента, которому необходимо лечение, определяют заранее, что делает возможным соответствующий отбор пациентов, у которых ожидается благоприятный эффект от лечения экзосомами по настоящему изобретению.
VI. Антигенпрезентирующие клетки (APC)
Настоящее изобретение также относится к изолированным APC, которые презентируют на своей поверхности комплексы, сформированные между антигенами HLA-A0206 и пептидами по данному изобретению. APC, которые получены путем контакта с пептидами по данному изобретению или посредством введения нуклеотидов, кодирующих пептиды по данному изобретению в экспрессирующейся форме, можно выделять у пациентов, у которых проводят профилактику или которых лечат, и можно вводить в виде вакцин сами по себе или в сочетании с другими лекарственными средствами, включая пептиды по данному изобретению, экзосомы или цитотоксические T-клетки.
APC не ограничены определенным типом клеток и включают дендритные клетки(DC), клетки Лангерганса, макрофаги, B-клетки и активированные T-клетки, которые известны тем, что презентируют белковые антигены на своей клеточной поверхности, таким образом, что лимфоциты могут их распознать. Поскольку DC являются представителем APC с наиболее сильным индуцирующим действием в отношении ЦТЛ среди APC, они являются предпочтительными APC по настоящему изобретению.
Например, APC можно получать путем индуцирования DC из моноцитов периферической крови и последующего контакта (стимуляции) их с пептидами по данному изобретению in vitro, ex vivo или in vivo. Когда пептиды по данному изобретению вводят пациенту с антигеном HLA-A - HLA-A0206, APC, которые презентируют пептиды по данному изобретению, индуцируются в организме пациента. Фраза "индукция APC" включает в себя контакт (стимулирование) клетки с пептидами по данному изобретению или нуклеотидами, кодирующими пептиды по данному изобретению, для презентирования комплексов, образованных антигенами HLA-A0206 и пептидами по данному изобретению на поверхности клетки. Альтернативно, после добавления пептидов по данному изобретению к APC, для того чтобы APC могли презентировать пептиды, APC можно вводить пациенту в виде вакцины. Например, введение ex vivo может включать этапы:
a: сбор APC от первого субъекта с антигеном HLA-A - HLA-A0206,
b: контакт APC с этапа a с пептидом и
c: введение APC, нагруженных пептидом, второму субъекту с антигеном HLA-A - HLA-A0206.
Первый субъект и второй субъект могут быть одним и тем же индивидуумом или разными. Альтернативно, по настоящему изобретению предлагается применение пептидов по изобретению для производства фармацевтической композиции, индуцирующей антигенпрезентирующие клетки. Кроме того, настоящее изобретение относится к способу или процессу для производства фармацевтической композиции, индуцирующей антигенпрезентирующие клетки, где способ включает этап смешивания или соединения пептида по настоящему изобретению с фармацевтически приемлемым носителем. Далее, настоящее изобретение также относится к пептидам по настоящему изобретению для индукции антигенпрезентирующих клеток. APC, полученные на этапе b, можно вводить пациенту в виде вакцины.
По одному из аспектов настоящего изобретения APC имеет высокий уровень способности индуцировать ЦТЛ. Термин "высокий уровень способности индуцировать ЦТЛ" означает высокий уровень по отношению к уровню тех APC, которые не контактировали с пептидом или контактировали с пептидами, которые не индуцируют ЦТЛ. Такие APC с высоким уровнем способности индуцировать ЦТЛ можно приготовить способом, который включает этап переноса генов, содержащих полинуклеотиды, которые кодируют пептиды по данному изобретению, в APC in vitro. Введенные гены могут быть в форме ДНК или РНК. Примеры способов введения, которые можно использовать, включают, без ограничений, различные способы, которые обычно применяют в данной области, такие как липофекция, электропорация и фосфатно-кальциевый способ. Более конкретно, это может быть выполнено, как описано в Cancer Res 1996, 56: 5672-7; J Immunol 1998, 161: 5607-13; J Exp Med 1996, 184: 465-72; Published Japanese Translation of International Publication No. 2000-509281. В результате переноса гена в APC, ген подвергается транскрипции, трансляции и т.п. в клетке, и затем полученный белок процессируется при помощи MHC класса I или класса II и проходит дальше путь презентации для презентирования пептидов.
VII. Цитотоксические T-клетки (ЦТЛ)
Цитотоксическая T-клетка, индуцированная против любого из пептидов по настоящему изобретению, усиливает иммунный ответ, направленный на опухоль-ассоциированный эндотелий in vivo, и таким образом может быть использована в качестве вакцин, некоторым образом сходно с пептидами как таковыми. Таким образом, настоящее изобретение также относится к изолированным цитотоксическим T-клеткам, которые специфически индуцированы или активированы любым пептидом по изобретению.
Такие цитотоксические T-клетки можно получать путем (1) введения пациенту пептидов по настоящему изобретению и последующего забора цитотоксических T-клеток у пациента или (2) при контакте (стимуляции) антигенпрезентирующих клеток пациента, и CD8-положительных клеток, или мононуклеарных лейкоцитов периферической крови in vitro с пептидами по настоящему изобретению.
Цитотоксические T-клетки, которые были индуцированы стимуляцией при помощи APC, презентирующих пептиды по данному изобретению, можно получать от пациентов, обладающих антигеном HLA-A0206 и проходящих лечение и/или профилактику, и можно вводить сами по себе или в сочетании с другими лекарственными средствами, включая пептиды по данному изобретению или экзосомы, для регулирования эффектов. Полученные цитотоксические T-клетки действуют специфически против клеток-мишеней, презентирующих пептиды по данному изобретению, или, например, те пептиды, которые использовали для индуцирования. Другими словами, эти цитотоксические T-клетки могут распознавать (т.е. связывать) при помощи Т-клеточного рецептора комплекс, сформировавшийся между HLA-A0206 и пептидом по настоящему изобретению на поверхности клетки-мишени, и затем атаковать клетку-мишень для индуцирования гибели клетки-мишени. Клетки-мишени могут быть клетками, которые эндогенно экспрессируют HIG2 или URLC10, или клетками, которые трансфецированы генами HIG2 или URLC10; и клетки, которые презентируют пептид по данному изобретению на своей поверхности вследствие стимуляции пептидом, могут также служить мишенями для атаки активированными ЦТЛ.
VIII. T-клеточный рецептор (TCR)
Настоящее изобретение также относится к полинуклеотиду, содержащему последовательность нуклеиновой кислоты, которая кодирует полипептиды, способные формировать субъединицу T-клеточного рецептора (TCR), и способам его применения. Субъединицы TCR обладают способностью образовывать TCR, которые придают специфичность T-клеткам против опухолевых клеток, презентирующих пептиды HIG2 или пептиды URLC10 с антигеном HLA-A0602. Последовательность нуклеиновых кислот альфа- и бета-цепей TCR, экспрессирующихся в ЦТЛ, которые индуцированы пептидом по данному изобретению, можно определить с использованием известных способов в данной области (WO2007/032255 и Morgan et al., J Immunol, 171, 3288 (2003)). Полученные TCR могут связывать с высокой авидностью пептиды HIG2 или URLC10, расположенные на клетках-мишенях, и необязательно опосредовать эффективный цитолиз клеток-мишеней, презентирующих пептид HIG2 или URLC10 с антигеном HLA-A0602, in vivo и in vitro.
Последовательность нуклеиновых кислот, кодирующих субъединицы TCR, можно вставлять в подходящие векторы, например в ретровирусные векторы. Такие векторы хорошо известны в данной области. Нуклеиновые кислоты или векторы, содержащие их, могут быть эффективно перенесены в T-клетку, например в T-клетку от пациента, у которого антиген HLA-A представляет собой HLA-A0206. Предпочтительно, настоящее изобретение относится к готовой композиции, позволяющей быстро модифицировать собственные T-клетки пациента (или клетки другого млекопитающего) для быстрого и легкого получения модифицированных T-клеток с превосходными цитолитическими свойствами по отношению к злокачественной клетке.
Также настоящее изобретение относится к ЦТЛ, которые получены путем трансдукции полинуклеотида с последовательностью нуклеиновой кислоты, кодирующей полипептиды субъединиц TCR, которые связывают комплекс, образованный пептидом HIG2 или URLC10 и антигеном HLA-A0206. Трансдуцированные ЦТЛ обладают свойством хоуминга в отношении злокачественных клеток in vivo и могут быть наращены хорошо известными способами культивирования in vitro (например, Kawakami et al., J Immunol., 142, 3452-3461 (1989)). T-клетки по настоящему изобретению можно использовать для создания иммуногенной композиции, которую можно применять для лечения или предупреждения рака у пациента, который нуждается в терапии или защите (WO2006/031221).
IX. Фармацевтические средства или композиции
Термины "предупреждение" и "профилактика" применяют в данном документе взаимозаменяемо по отношению к любой деятельности, которая уменьшает бремя смертности и заболеваемость. Предупреждение и профилактика могут происходить "на первичном, вторичном и третичном уровнях". В то время как первичное предупреждение и профилактика предотвращают развитие заболевания, вторичный и третичный уровни предупреждения и профилактики охватывают деятельность, нацеленную на предупреждение и профилактику прогрессирования заболевания и появления симптомов, а также на снижение негативного воздействия уже развившегося заболевания за счет восстановления функций и уменьшения осложнений, связанных с заболеванием. Альтернативно, предупреждение и профилактика могут включать широкий спектр профилактической терапии, нацеленной на облегчение тяжести конкретного расстройства, например снижение пролиферации и метастазирования опухолей.
Лечение и/или профилактика рака и/или предупреждение его послеоперационного рецидива включает в себя любой из следующих шагов, таких как хирургическое удаление злокачественных клеток, ингибирование роста злокачественных клеток, инволюцию или регрессию опухоли, индукцию ремиссии и подавление развития рака, регрессию опухоли и уменьшение или ингибирование метастазирования. Эффективное лечение и/или профилактика рака снижает смертность и улучшает прогноз пациентов с раком, снижает уровни опухолевых маркеров в крови и облегчает выявляемые симптомы, сопровождающие рак. Например, уменьшение или улучшение симптомов, составляющих эффективное лечение и/или профилактику, включают 10%, 20%, 30% или более уменьшение или стабилизацию заболевания.
Поскольку экспрессия HIG2 или URLC10 повышена при некоторых видах рака по сравнению с нормальными тканями, пептиды по данному изобретению или полинуклеотиды, кодирующие такие пептиды, можно использовать для лечения и/или для профилактики рака, и/или предупреждения его послеоперационного рецидива. Таким образом, настоящее изобретение относится к фармацевтическому средству или композиции для лечения и/или предупреждения рака, и/или предупреждения его послеоперационного рецидива, которое включает в качестве активного ингредиента один или несколько пептидов по данному изобретению или полинуклеотиды, кодирующие эти пептиды. Альтернативно, пептиды по изобретению могут экспрессироваться на поверхности любой из вышеупомянутых экзосом или клеток, таких как APC, для применения в качестве фармацевтических средств или композиций. Кроме того, указанные выше цитотоксические T-клетки, которые нацелены на любой из пептидов по настоящему изобретению, также можно использовать в качестве активного ингредиента фармацевтических средств или композиций по изобретению. В контексте настоящего изобретения, фраза "нацеленные на пептид” относится к распознаванию (т.е. связыванию) комплекса, сформированного антигеном HLA-A0206 и пептидом на поверхности клетки-мишени, с Т-клеточным рецептором, и последующей атаке клетки-мишени для индуцирования гибели клетки-мишени.
В другом варианте осуществления настоящее изобретение также относится к применению активного ингредиента, выбранного из:
a) пептида по настоящему изобретению,
(b) нуклеиновой кислоты, кодирующей такой пептид, как описано в настоящем документе в экспрессирующейся форме,
(c) APC по настоящему изобретению и
(d) цитотоксической T-клетки по настоящему изобретению для производства фармацевтической композиции или вещества для лечения рака.
Альтернативно, настоящее изобретение дополнительно относится к активному ингредиенту, выбранному из:
(a) пептида по настоящему изобретению,
(b) нуклеиновой кислоты, кодирующей такой пептид, как описано в настоящем документе в экспрессирующейся форме,
(c) APC по настоящему изобретению, и
(d) цитотоксической T-клетки по настоящему изобретению для применения в лечении рака.
Альтернативно, настоящее изобретение дополнительно относится к способу или процессу для производства фармацевтической композиции или вещества для лечения рака, где способ или процесс включают этап соединения фармацевтически или физиологически приемлемого носителя с активным ингредиентом, выбранным из:
(a) пептида по настоящему изобретению,
(b) нуклеиновой кислоты, кодирующей такой пептид, как описано в настоящем документе, в экспрессирующейся форме,
(c) APC по настоящему изобретению, и
(d) цитотоксических T-клеток по настоящему изобретению
в качестве активных ингредиентов.
В другом варианте осуществления настоящее изобретение также относится к способу или процессу для производства фармацевтической композиции или вещества для лечения рака, где способ или процесс включают этап смешивания активного ингредиента с фармацевтически или физиологически приемлемым носителем, где активный ингредиент выбран из:
(a) пептида по настоящему изобретению,
(b) нуклеиновой кислоты, кодирующей такой пептид, как описано в настоящем документе, в экспрессирующейся форме,
(c) APC по настоящему изобретению и
(d) цитотоксических T-клеток по настоящему изобретению.
Альтернативно, фармацевтическую композицию или вещество по настоящему изобретению можно использовать как для профилактики рака, так и для предупреждения его послеоперационного рецидива.
Данные фармацевтические средства или композиции находят применение в виде вакцины. В контексте настоящего изобретения фраза "вакцина" (также обозначаемая как "иммуногенная композиция") относится к веществу, которое обладает функцией индукции противоопухолевого иммунитета после прививки животным.
Фармацевтические средства или композиции по настоящему изобретению можно использовать для лечения и/или предупреждения раков, и/или предупреждения их послеоперационных рецидивов у субъектов или пациентов, включая человека и любое другое млекопитающее, включая в качестве неограничивающих примеров мышь, крысу, морскую свинку, кролика, кошку, собаку, овцу, козу, свинью, крупный рогатый скот, лошадь, мартышку, бабуина и шимпанзе, в особенности коммерчески важное животное или одомашненное животное.
Согласно настоящему изобретению обнаружено, что полипептиды с аминокислотной последовательностью, выбранной из SEQ ID NO:1 и 2, являются ограниченными по HLA-A0206 эпитопными пептидами, которые могут индуцировать мощный и специфический иммунный ответ против клеток-мишеней, экспрессирующих HIG2 или URLC10 и HLA-A0206. Таким образом, эти фармацевтические средства или композиции, которые содержат любой из полипептидов с аминокислотной последовательностью, выбранной из SEQ ID NO:1 и 2, особенно подходят для введения пациентам, у которых антиген HLA представляет собой HLA-A0206. То же самое касается фармацевтических средств или композиций, которые содержат полинуклеотиды, кодирующие любые из указанных полипептидов.
Опухоли, которые можно лечить с помощью фармацевтических средств или композиций по настоящему изобретению, не ограничены и включают все типы раков, где задействованы HIG2 или URLC10, включая, например, рак мочевого пузыря, рак шейки матки, холангиоцеллюлярную карциному, рак пищевода, рак желудка, немелкоклеточный рак легкого, остеосаркому, рак поджелудочной железы, карциному почек и опухоль мягких тканей. В частности, фармацевтические средства или композиции, нацеленные на HIG2, предпочтительно применять при карциноме почек и опухоли мягких тканей, и фармацевтические средства или композиции, нацеленные на URLC10, предпочтительно применять при раке мочевого пузыря, раке шейки матки, холангиоцеллюлярной карциноме, раке пищевода, раке желудка, немелкоклеточном раке легкого, остеосаркоме, раке поджелудочной железы и опухоли мягких тканей.
Указанные фармацевтические средства или композиции могут содержать, в дополнение к указанным выше активным ингредиентам, дополнительные пептиды, которые обладают свойством индуцировать ЦТЛ против злокачественных клеток, другие полинуклеотиды, кодирующие дополнительные пептиды, другие клетки, презентирующие дополнительные пептиды, или т.п. В настоящем документе дополнительные пептиды, которые обладают свойством индуцировать ЦТЛ против злокачественных клеток, представлены в качестве примера, но не ограничены опухолеспецифическими антигенами (например, установленными ОАА).
Если необходимо, фармацевтические средства или композиции по настоящему изобретению могут, но не обязательно, содержать в качестве активного ингредиента дополнительные терапевтические вещества, при условии, что вещество не ингибирует противоопухолевое действие активного ингредиента, например любого из указанных пептидов. Например, составы могут содержать противовоспалительные средства или композиции, обезболивающие, химиотерапевтические средства и т.п. В дополнение к включению других терапевтических веществ в лекарственное средство как таковых, лекарственные средства по настоящему изобретению можно также вводить последовательно или одновременно с одним или несколькими дополнительными фармакологическими препаратами или композициями. Количества лекарства и фармакологического препарата или композиции зависят, например, от того, какой тип фармакологического препарата(-ов) или композиции(-ий) применяют, от заболевания, которое лечат, и от схемы применения и путей введения.
Следует понимать, что в дополнение к ингредиентам, частично указанным в настоящем документе, фармацевтические средства или композиции по данному изобретению могут содержать другие вещества или композиции, общепринятые в данной области, имеющие отношение к типу обсуждаемого состава.
В одном из вариантов осуществления настоящего изобретения указанные фармацевтические средства или композиции можно включать в промышленные изделия и наборы, которые содержат материалы для лечения патологических состояний заболевания, которое лечат, например рака. Промышленное изделие может содержать контейнер с любым из данных фармацевтических средств или композиций с этикеткой. Подходящие контейнеры включают бутылки, флаконы и пробирки. Контейнеры могут быть произведены из различных материалов, таких как стекло или пластик. Этикетка на контейнере должна указывать вещество или композиции, которые применяются для лечения или предупреждения одного или нескольких состояний заболевания. Этикетка может также содержать указания по введению и т.д.
В дополнение к вышеописанному контейнеру набор, содержащий фармацевтическое средство или композиции по настоящему изобретению, может необязательно дополнительно включать в себя второй контейнер с фармацевтически приемлемым растворителем. Он может дополнительно включать другие материалы, желательные с коммерческой и потребительской точки зрения, включая другие буферы, растворители, фильтры, иглы, шприцы и вкладыш в упаковки с инструкциями по применению.
Фармацевтические композиции могут, при желании, быть представлены в упаковке или распылителе, которые могут содержать одну или несколько стандартных лекарственных форм с активным ингредиентом. Упаковка, например, может содержать металлическую или пластиковую пленку, как, например, блистерная упаковка. Упаковка или распылитель могут сопровождаться инструкциями по введению.
(1) Фармацевтические средства или композиции, которые содержат в качестве активного ингредиента пептиды
Пептиды по данному изобретению можно вводить непосредственно в виде фармацевтического средства или композиции, или, при необходимости, они могут быть соединены удобными способами для составления фармацевтических средств. В последнем случае, в дополнение к пептидам по данному изобретению, при необходимости, без конкретных ограничений, можно включать носители, эксципиенты, и т.п., которые, как правило, применяются для лекарственных средств. Примерами таких носителей являются стерилизованная вода, физиологический раствор, фосфатный буфер, культуральная жидкость и т.п. Кроме того, фармацевтические средства или композиции могут содержать по мере необходимости, стабилизаторы, суспензии, консерванты, поверхностно-активные вещества и т.п. Фармацевтические средства или композиции по данному изобретению можно использовать с противоопухолевыми целями.
Пептиды по данному изобретению можно приготовлять в виде комбинации, состоящей из двух или более пептидов по изобретению для индукции ЦТЛ in vivo. Пептидная комбинация может быть в форме коктейля или пептиды могут быть конъюгированы друг с другом с использованием стандартных техник. Например, пептиды могут быть связаны химически или экспрессироваться в виде единой слитой полипептидной последовательности. Пептиды в комбинации могут быть одинаковыми или разными. При введении пептидов по данному изобретению пептиды презентируются посредством антигена HLA-A0206 с высокой плотностью на APC, затем происходит индукция ЦТЛ, которые специфически реагируют на комплекс, образованный представленным пептидом и антигеном HLA-A0206. Альтернативно, APC, которые презентируют любой из пептидов по данному изобретению на своей поверхности и которые можно получить посредством стимуляции пептидами по изобретению APC (например, DC) от пациента с антигеном HLA-A - HLA-A0206, можно вводить пациенту, и в результате ЦТЛ пациента индуцируются, и может быть увеличена агрессивность в отношении злокачественных клеток, таких как рак мочевого пузыря, рак шейки матки, холангиоцеллюлярная карцинома, рак пищевода, рак желудка, немелкоклеточный рак легкого, остеосаркома, рак поджелудочной железы и опухоль мягких тканей.
Фармацевтические средства или композиции для лечения и/или предупреждения рака, которые содержат в качестве активного ингредиента пептид по данному изобретению, могут также содержать адъювант, известный эффективным установлением клеточного иммунитета. Альтернативно, их можно вводить с другими активными ингредиентами и их можно вводить в составе гранул. «Адъювант» относится к соединению, которое усиливает иммунный ответ против белка, когда вводится совместно (или последовательно) с иммунологически активным белком. Адъюванты, предусмотренные в настоящем документе, включают описанные в литературе (Clin Microbiol Rev 1994, 7: 277-89). Примеры подходящих адъювантов включают в качестве неограничивающих примеров, фосфат алюминия, гидроксид алюминия, алюмокалиевые квасцы, холерный токсин, токсин сальмонеллы и т.п.
Кроме того, удобно использовать липосомные составы, гранулярные составы, в которых пептид связан с бусинами диаметром в несколько микрометров, и составы, в которых пептид связан с липидом.
В некоторых вариантах осуществления фармацевтические средства или композиции по настоящему изобретению могут дополнительно включать компонент, праймирующий ЦТЛ. Липиды были идентифицированы как вещества или композиции, способные праймировать ЦТЛ in vivo против вирусных антигенов. Например, остатки пальмитиновой кислоты могут быть присоединены к эпсилон- и альфа-аминогруппам лизиновых остатков и затем связаны с пептидом по изобретению. Липидированный пептид можно затем вводить или непосредственно в мицелле или частице, инкорпорированной в липосому, или эмульгированным в адъюванте. В качестве другого примера липидного праймирования ответа ЦТЛ можно использовать для праймирования ЦТЛ липопротеины E. coli, такие как трипальмитоил-S-глицерилцистеинлисерил-серин (P3CSS), когда он ковалентно присоединен к подходящему пептиду (смотри, например, Deres et al., Nature 1989, 342: 561-4).
Способ введения может быть оральным, внутрикожным, подкожным, внутривенным или т.п., а также системным введением или местным введением рядом с областью-мишенью. Введение может быть однократным или усилено за счет многократных введений. Дозировка пептидов по данному изобретению может быть скорректирована соответствующим образом согласно заболеванию, которое лечат, возрасту пациента, весу, способу введения и т.п., и представляет собой, как правило, 0,001 мг на 1000 мг, например 0,001 мг на 1000 мг, например 0,1 мг на 10 мг, и может вводиться однократно в период от нескольких дней до нескольких месяцев. Специалист в данной области может выбрать подходящую дозу соответствующим образом.
(2) Фармацевтические средства или композиции, которые содержат в качестве активного ингредиента полинуклеотиды
Фармацевтические средства или композиции по настоящему изобретению могут также содержать нуклеиновые кислоты, кодирующие пептиды, описываемые в настоящем документе, в экспрессирующейся форме. В настоящем документе фраза "в экспрессирующейся форме" означает, что полинуклеотид при введении в клетку будет экспрессироваться in vivo как полипептид, который индуцирует противоопухолевый иммунитет. В примерном варианте осуществления последовательность нуклеиновой кислоты интересующего полинуклеотида включает в себя регуляторные элементы, необходимые для экспрессии полинуклеотида. Полинуклеотид(ы) может быть оснащен подобным образом для получения стабильной вставки в геноме клетки-мишени (смотри, например, Thomas KR & Capecchi MR, Cell 1987, 51: 503-12 для описания кассетных векторов для гомологической рекомбинации). Смотри, например, Wolff et al., Science 1990, 247: 1465-8; патенты США №№ 5580859; 5589466; 5804566; 5739118; 5736524; 5679647; и WO 98/04720. Примеры технологий доставки, основанных на ДНК, включают «оголенную ДНК», облегченную доставку (бупивакаин, полимеры, пептид-опосредованная), катионные липидные комплексы и опосредованную частицами ("генная пушка") или доставку, опосредованную давлением (смотри, например, патент США № 5922687).
Пептиды по настоящему изобретению могут также быть экспрессированы с помощью вирусных или бактериальных векторов. Примеры экспрессирующих векторов включают ослабленные вирусные носители, такие как вирус осповакцины или вирус оспы птиц. Этот подход включает использование вируса осповакцины, например, в качестве вектора для экспрессии нуклеотидных последовательностей, кодирующих пептид. После введения в носитель рекомбинантный вирус осповакцины экспрессирует иммуногенный пептид и, таким образом, вызывает иммунный ответ. Векторы на основе осповакцины и способы, которые используют в протоколах иммунизации, описаны, например, в патенте США № 4722848. Примеры других векторов включают BCG (Bacille Calmette Guerin). Векторы на основе BCG описаны в Stover et al., Nature 1991, 351: 456-60. Очевиден широкий спектр других векторов, применимых для терапевтического введения или иммунизации, например аденовирусные и ассоциированные с аденовирусами векторы, ретровирусные векторы, векторы на основе Salmonella typhi, векторы на основе обезвреженного токсина сибирской язвы и т.п. Смотри, например, Shata et al., Mol Med Today 2000, 6: 66-71; Shedlock et al., J Leukoc Biol 2000, 68: 793-806; Hipp et al., In Vivo 2000, 14: 571-85.
Доставка полинуклеотида пациенту может быть либо прямой, в этом случае пациент напрямую подвергается воздействию вектора, несущего полинуклеотид, либо непрямой, в этом случае клетки сначала трансформируют при помощи интересующего полинуклеотида in vitro, затем клетки трансплантируют пациенту. Эти два подхода известны как генная терапия in vivo и ex vivo соответственно.
Для общих обзоров способов генной терапии смотри Goldspiel et al., Clinical Pharmacy 1993, 12: 488-505; Wu и Wu, Biotherapy 1991, 3: 87-95; Tolstoshev, Ann Rev Pharmacol Toxicol 1993, 33: 573-96; Mulligan, Science 1993, 260: 926-32; Morgan & Anderson, Ann Rev Biochem 1993, 62: 191-217; Trends in Biotechnology 1993, 11(5): 155-215. Общеизвестные способы в области технологии рекомбинантных ДНК, которые также можно использовать для настоящего изобретения, описаны в eds. Ausubel et al., Current Protocols in Molecular Biology, John Wiley & Sons, NY, 1993; и Krieger, Gene Transfer и Expression, A Laboratory Manual, Stockton Press, NY, 1990.
Способ введения может быть оральным, внутрикожным, подкожным, внутривенным или т.п., и системным введением или местным введением рядом с областью-мишенью. Введение может быть однократным или усилено за счет многократных введений. Дозировка полинуклеотида в подходящем носителе или клетках, трансформированных полинуклеотидом, который кодирует пептиды по данному изобретению, может быть скорректирована соответствующим образом согласно заболеванию, которое лечат, возрасту пациента, весу, способу введения и т.п., и представляет собой, обычно, 0,001 мг на 1000 мг, например 0,001 мг на 1000 мг, например 0,1 мг на 10 мг, и может вводиться однократно каждые несколько дней или однократно каждые насколько месяцев. Специалист в данной области может соответствующим образом выбрать подходящую дозу.
X. Способы применения пептидов, экзосом, APC и ЦТЛ
Пептиды по настоящему изобретению и полинуклеотиды, кодирующие такие пептиды, можно использовать для индукции APC и ЦТЛ. Экзосомы и APC по настоящему изобретению также можно использовать для индукции ЦТЛ. Пептиды, полинуклеотиды, экзосомы и APC можно использовать в сочетании с любыми другими соединениями при условии, что соединения не ингибируют их способность индуцировать ЦТЛ. Таким образом, любые из указанных выше фармацевтических средств или композиций по настоящему изобретению можно использовать для индукции ЦТЛ и, кроме того, те, что включают пептиды и полинуклеотиды, также можно использовать для индукции APC, как обсуждается далее.
(1) Способ индукции антигенпрезентирующих клеток (APC)
Настоящее изобретение относится к способам индукции APC с использованием пептидов по данному изобретению или полинуклеотидов, кодирующих эти пептиды. Индукцию APC можно проводить как описано выше в разделе "VI. Антигенпрезентирующие клетки". Изобретение также предлагает способ индукции APC с высоким уровнем способности индуцировать ЦТЛ, индукция которых также упоминалась выше в разделе "VI. Антигенпрезентирующие клетки". Предпочтительно, способы для индукции APC включают, по меньшей мере, один шаг, выбранный из:
a: контакт APC, чей антиген HLA-A представляет собой HLA-A0206, с пептидами по настоящему изобретению, и
b: введение полипептидов по настоящему изобретению в экспрессирующейся форме в APC, чей антиген HLA-A представляет собой HLA-A0206.
Такие способы индукции APC предпочтительно использовать in vitro или ex vivo. Когда способы используют in vitro или ex vivo, APC для индукции можно получить от пациента, которого будут лечить, или от других субъектов, чей антиген HLA-A представляет собой HLA-A0206.
(2) Способ индукции ЦТЛ
Кроме того, настоящее изобретение относится к способам индукции ЦТЛ с использованием пептидов по данному изобретению, полинуклеотидов, кодирующих эти пептиды, или экзосом, или APC, презентирующих эти пептиды.
Настоящее изобретение также относится к способам индукции ЦТЛ с использованием полинуклеотида, кодирующего полипептид, который способен формировать субъединицу Т-клеточного рецептора (TCR), распознающую (т.е. связывающую) комплекс из пептидов по настоящему изобретению и антигена HLA-A0206 на поверхности клетки. Предпочтительно, способы для индукции ЦТЛ включают, по меньшей мере, один шаг, выбранный из:
a: контакт CD8-позитивной T-клетки с антигенпрезентирующей клеткой и/или экзосомой, которые презентируют на своей поверхности комплекс из антигена HLA-A0206 и пептида по настоящему изобретению, и
b: введение в CD8-позитивную T-клетку полинуклеотида, кодирующего полипептид, который способен формировать субъединицу Т-клеточного рецептора (TCR), распознающую комплекс из пептида по настоящему изобретению и антигена HLA-A0206.
Когда пептиды по данному изобретению вводят пациенту, ЦТЛ индуцируются в организме пациента, и сила иммунного ответа, направленного против злокачественных клеток, возрастает. Альтернативно, пептиды и полинуклеотиды, кодирующие эти пептиды, можно использовать для способа терапии ex vivo, при котором APC, полученные у пациента, и CD8-позитивные клетки или мононуклеарные лейкоциты периферической крови приводят в контакт (стимулируют) с пептидами по данному изобретению in vitro, и после индукции ЦТЛ активированные ЦТЛ возвращают пациенту. Например, способ может включать шаги:
a: выделение APC у пациента, чей антиген HLA-A представляет собой HLA-A0206,
b: контакт APC из шага a с пептидом по настоящему изобретению,
c: смешивание APC из шага b с CD8+ T-клетками, чей антиген HLA-A представляет собой HLA-A0206, и совместное культивирование для индукции ЦТЛ и
d: выделение CD8+ T-клеток из совместной культуры из шага c. Альтернативно, настоящее изобретение предлагает использование пептидов по данному изобретению для производства фармацевтической композиции для индукции ЦТЛ. Кроме того, настоящее изобретение относится к способу или процессу для производства фармацевтического средства или композиции для индукции ЦТЛ, где способ включает шаг смешивания или соединения пептида по настоящему изобретению с фармацевтически приемлемым носителем. Далее, настоящее изобретение также относится к пептиду по настоящему изобретению для индукции ЦТЛ.
CD8+ T-клетки с цитотоксической активностью, полученные на этапе d можно вводить пациенту в виде вакцины. APC, которые смешивают с CD8+ T-клетками, на вышеуказанном этапе также можно получать путем переноса в APC генов, кодирующих данные пептиды, как подробно описано выше в разделе "VI". Антигенпрезентирующие клетки, но без ограничений любая APC или экзосома, которая эффективно презентирует данные пептиды Т-клеткам, могут быть использованы для данного способа.
Следующие примеры представлены для того, чтобы проиллюстрировать настоящее изобретение и помочь специалистам в его создании и применении. Примеры никоим образом не ограничивают объем изобретения.
Примеры
Материалы и способы
Клеточные линии
PSCCA0922 (HLA-A0206) была приобретена у Pharma SNP Consortium; PSC. B-лимфобластная клеточная линия человека и COS7 были приобретены у ATCC.
Кандидатные пептиды, полученные из HIG2 и URLC10
9-мерные и 10-мерные пептиды, полученные из HIG2 или URLC10, были синтезированы Sigma (Sapporo, Japan) или Biosynthesis Inc. (Lewisville, TX) стандартным способом твердофазного синтеза и очищены с помощью обратнофазной высокоэффективной жидкостной хроматографии (ВЭЖХ). Чистота (>90%) и тождественность пептидов были установлены посредством аналитической ВЭЖХ и масс-спектрометрического анализа соответственно. Пептиды были растворены в диметилсульфоксиде (DMSO) из расчета 20 мг/мл и хранились при -80°C.
Индукция ЦТЛ in vitro
Моноцитарные дендритные клетки (DC) были использованы в качестве антигенпрезентирующих клеток (APC) для индукции ответа цитотоксических T-лимфоцитов (ЦТЛ) против пептидов, презентированных на лейкоцитарном антигене человека (HLA). DC получали in vitro, как описано в другом месте (Nakahara S et al., Cancer Res 2003 Jul 15, 63(14): 4112-8). В частности, мононуклеарные клетки периферической крови (PBMC), выделенные у здорового добровольца (HLA-A0206-позитивного) при помощи раствора Ficoll-Plaque (Pharmacia), разделяли путем адгезии на пластиковой чашке Петри (Becton Dickinson), так чтобы обогатить их фракцией моноцитов. Обогащенную моноцитами популяцию культивировали в присутствии 1000 U/мл гранулоцит-макрофаг колониестимулирующего фактора (GM-CSF) (R&D System) и 1000 U/мл интерлейкина (IL)-4 (R&D System) в среде AIM-V (Invitrogen), содержащей 2% аутологичную сыворотку, инактивированную нагреванием (AS). После семи дней культивирования, индуцированные цитокином DC активировали 20 мкг/мл каждого из синтезированных пептидов в присутствии 3 мкг/мл β2-микроглобулина в течение 3 часов при 37°C в среде AIM-V. Показано, что полученные клетки экспрессируют на своей поверхности DC-ассоциированные молекулы, такие как CD80, CD83, CD86 и HLA класса II (данные не показаны). Такие активированные пептидом DC были затем инактивированы Митомицином C (MMC) (30 мкг/мл в течение 30 мин) и смешаны в соотношении 1:20 с аутологичными CD8+ T-клетками, полученными позитивной селекцией при помощи CD8 Positive Isolation Kit (Dynal). Эти культуры высеяли в 48-луночные планшеты (Corning); каждая лунка содержала 1,5×104 активированных пептидом DC, 3×105 CD8+ T-клеток и 10 нг/мл IL-7 (R&D System) в 0,5 мл среды AIM-V/2% AS. Через три дня к культурам добавляли IL-2 (CHIRON) до конечной концентрации 20 IU/мл. На 7 и 14 дни, T-клетки были дополнительно стимулированы аутологичными DC, активированными пептидом. DC готовили каждый раз способом, описанным выше. ЦТЛ тестировали против клеток PSCCA0922, активированных пептидом, после 3-го раунда стимуляции пептидом на 21 день (Tanaka H et al., Br J Cancer 2001 Jan 5, 84(1): 94-9; Umano Y et al., Br J Cancer 2001 Apr 20, 84(8): 1052-7; Uchida N et al., Clin Cancer Res 2004 Dec 15, 10(24): 8577-86; Suda T et al., Cancer Sci 2006 May, 97(5): 411-9; Watanabe T et al., Cancer Sci 2005 Aug, 96(8): 498-506).
Процедура наращивания ЦТЛ
ЦТЛ наращивали в культуре с использованием способа, сходного с описанным Riddell et al. (Walter EA et al., N Engl J Med 1995 Oct 19, 333(16): 1038-44; Riddell SR et al., Nat Med 1996 Feb, 2(2): 216-23). ЦТЛ в количестве 5×104 клеток суспендировали в 25 мл среды AIM-V/5%AS с 2 типами В-лимфобластных клеточных линий человека, инактивированных MMC, в присутствии 40 нг/мл моноклональных антител против CD3 (Pharmingen). Через день после начала культивирования, к культурам добавляли 120 IU/мл IL-2. На 5, 8 и 11 дни культуры подкармливали свежей средой AIM-V/5%AS, содержащей 30 IU/мл IL-2 (Tanaka H et al., Br J Cancer 2001 Jan 5, 84(1): 94-9; Umano Y et al., Br J Cancer 2001 Apr 20, 84(8): 1052-7; Uchida N et al., Clin Cancer Res 2004 Dec 15, 10(24): 8577-86; Suda T et al., Cancer Sci 2006 May, 97(5): 411-9; Watanabe T et al., Cancer Sci 2005 Aug, 96(8): 498-506).
Создание клонов ЦТЛ
Делали разведения для получения 0,3, 1 и 3 ЦТЛ/лунку в 96-луночном круглодонном титрационном микропланшете (Nalge Nunc International). ЦТЛ культивировали с 2 типами В-лимфобластных клеточных линий человека (7×104 клеток/лунку), 30 нг/мл антител против CD3 и 125 U/мл IL-2 в общем количестве 150 мкл/лунку среды AIM-V, содержащей 5%AS. Через 10 дней добавляли в среду 50 мкл/лунку IL-2, так что конечная концентрация IL-2 составляла 125 U/мл. Цитотоксическую активность ЦТЛ проверяли на 14 день и наращивали клоны ЦТЛ способом, описанным выше.
Специфическая активность ЦТЛ
Для изучения специфической активности ЦТЛ делали иммуноферментный спот-анализ (ELISPOT) на интерферон (IFN)-гамма и твердофазный иммуноферментный анализ (ELISA) на IFN-гамма. В частности, в качестве стимуляторных клеток готовили PSCCA0922 (1×104/лунку), активированные пептидом. Культивированные клетки в 48 лунках использовали в качестве клеток-респондеров. ELISPOT анализ на IFN-гамма и ELISA на IFN-гамма проводили согласно протоколам поизводителя.
Создание клеток, принудительно экспрессирующих любой из двух или оба гена-мишени и ген HLA-A0206
кДНК, кодирующую открытую рамку считывания генов-мишеней, (HIG2; SEQ ID NO:3 и URLC10; SEQ ID NO:5) или HLA-A0206 (SEQ ID NO:7) амплифицировали при помощи ПЦР. Амплифицированный продукт клонировали в вектор pcDNA3,1 myc-His (Invitrogen). Плазмиды, содержащие любой из двух или оба гена-мишени и HLA-A0206, были трансфецированы в клетки COS7 с использованием липофектамина (Invitrogen) согласно методикам, рекомендованным производителем. В кратком изложении, 2,5×106 клеток COS7 трансфецировали при помощи 10 мкг плазмиды при 140V и 1000 микроF. Через 2 дня после трансфекции, трансфецированные клетки обрабатывали раствором для диссоциации клеток и использовали в качестве клеток-мишеней для анализа активности ЦТЛ.
Результаты
Повышенная экспрессия HIG2 и URLC10 при опухолях
Данные общего профиля экспрессии генов, полученные из различных опухолей с использованием кДНК-микрочипов, выявили, что экспрессия HIG2 (инвентарный номер GenBank NM_013332; SEQ ID No:3) и URLC10 (инвентарный номер GenBank NM_017527; SEQ ID No:5) была повышена. Экспрессия HIG2 была достоверно увеличена в 19 из 20 злокачественных опухолей почки и в 7 из 9 опухолей мягких тканей по сравнению с соответствующими здоровыми тканями. Экспрессия URLC10 была достоверно увеличена в 29 из 29 раков мочевого пузыря, в 15 из 16 раков шейки матки, в 7 из 7 холангиоцеллюлярных карцином, в 7 из 19 раков пищевода, в 3 из 3 раков желудка, в 24 из 27 NSCLC, в 15 из 19 остеосарком, в 4 из 5 раков поджелудочной железы и в 33 из 43 опухолей мягких тканей по сравнению с соответствующими здоровыми тканями.
Индукция ЦТЛ при помощи пептида из HIG2, ограниченного по HLA-A0206, и создание линий ЦТЛ, стимулированных пептидами, полученными из HIG2
ЦТЛ для пептида, полученного из HIG2, получали согласно протоколам, как описано в "Материалах и Способах". Пептидспецифическую активность ЦТЛ определяли посредством ELISPOT анализа на IFN-гамма (фиг.1). Результаты здесь показывают, что HIG2-A0206-9-4 (SEQ ID NO:1) демонстрирует мощную выработку IFN-гамма по сравнению с контрольными лунками. Кроме того, клетки в позитивных лунках под номерами 1, 2, 5, 7, 8, 10, 13 и 14, стимулированные посредством SEQ ID NO:1, наращивали для получения линий ЦТЛ. Цитотоксическую активность этих линий ЦТЛ определяли посредством ELISA анализа на IFN-гамма (фиг.2). Результаты здесь показывают, что все линии ЦТЛ демонстрируют мощную выработку IFN-гамма против клеток-мишеней, активированных соответствующим пептидом, по сравнению с клетками-мишенями, не активированными пептидом. Таким образом, HIG2-A0206-9-4 могут индуцировать активные линии ЦТЛ против клеток-мишеней, экспрессирующих HLA-A0206.
Создание клонов ЦТЛ, стимулированных пептидами, полученными из HIG2
Серийные разведения таких линий ЦТЛ производили согласно протоколам, указанным выше в разделе "Материалы и Способы". Получение клона ЦТЛ из линии ЦТЛ HIG2-A0206-9-4 (SEQ ID NO:1) показано на фиг.3. Эти клоны ЦТЛ обладали мощной и специфической цитотоксической активностью против мишени, активированной пептидом по сравнению с активностью против мишени, не активированной пептидом.
Специфическая активность ЦТЛ против клеток-мишеней, экспрессирующих HIG2 и HLA-A0206
Созданные клоны ЦТЛ, индуцированные против HIG2-A0206-9-4 (SEQ ID NO:1), проверяли на их способность распознавать клетки-мишени, экспрессирующие HIG2 и HLA-A0206. Специфическую активность ЦТЛ против клеток COS7, трансфецированных полноразмерным геном HIG2 и молекулой HLA-A0206 и которые служат специфической моделью клеток-мишеней, эндогенно экспрессирующих HIG2 и HLA-A0206, проверяли с использованием в качестве эффекторных клеток клона ЦТЛ, индуцированного HIG2-A0206-9-4 (SEQ ID NO:1). В качестве контроля использовали клетки COS7, трансфецированные HLA-A0206, но не полноразмерным HIG2, и активированные другим пептидом (HIG2-9-8:YLLGVVLTL), и COS7, трансфецированные полноразмерным HIG2, но не HLA-A0206. Клоны ЦТЛ продемонстрировали наиболее высокую специфическую цитотоксическую активность против COS7, трансфецированных как HIG2, так и HLA-A0206 (фиг.4).
Результаты здесь ясно демонстрируют, что HIG2-A0206-9-4 (SEQ ID NO:1) естественным образом процессируется и презентируется на поверхности клетки-мишени с молекулой HLA-A0206, и распознается ЦТЛ. Таким образом, HIG2-A0206-9-4 может служить в качестве противоопухолевой вакцины, нацеленной на злокачественные клетки, экспрессирующие HIG2, у пациента с антигеном HLA - HLA-A0206.
Индукция ЦТЛ пептидом из URLC10, ограниченным по HLA-A0206, и создание линий ЦТЛ, стимулированных пептидами, полученными из URLC10
ЦТЛ для пептидов, полученных из URLC10, были получены согласно протоколам, как описано в "Материалах и Способах". Пептидспецифическую активность ЦТЛ определяли посредством ELISPOT анализа на IFN-гамма (фиг.5). Результаты здесь показывают, что URLC10-A0206-10-211 (SEQ ID NO:2) демонстрирует мощную продукцию IFN-гамма по сравнению с контрольными лунками. Кроме того, наращивали клетки в положительной лунке номер 7, стимулированные при помощи SEQ ID NO:2, и создавали линию ЦТЛ. Цитотоксическую активность линии ЦТЛ определяли посредством ELISA анализа на IFN-гамма (фиг.6). Результаты здесь показывают, что линия ЦТЛ демонстрирует мощную продукцию IFN-гамма против клеток-мишеней, активированных соответствующим пептидом, по сравнению с клетками-мишенями, не активированными пептидом. Таким образом, URLC10-A0206-10-211 может индуцировать активную линию ЦТЛ.
Создание клона ЦТЛ, стимулированного пептидом, полученным из URLC10
Готовили серийные разведения из таких линий ЦТЛ согласно протоколам, изложенным выше в разделе "Материалы и Способы". Создание клона ЦТЛ из линии ЦТЛ URLC10-A0206-10-211 (SEQ ID NO: 2) показано на фиг.7. Этот клон ЦТЛ обладает мощной и специфической ЦТЛ активностью против мишени, активированной пептидом, по сравнению с активностью против мишени, не активированной пептидом.
Специфическая активность ЦТЛ против клеток-мишеней, экспрессирующих URLC10 и HLA-A0206
Была изучена способность созданных клонов ЦТЛ, индуцированных против URLC10-A0206-10-211 (SEQ ID NO:2), распознавать клетки-мишени, экспрессирующие URLC10 и HLA-A0206. Специфическую активность ЦТЛ против клеток COS7, трансфецированных полноразмерным геном URLC10 и молекулой HLA-A0206 и которые служат специфической моделью клеток-мишеней, эндогенно экспрессирующих URLC10 и HLA-A0206, проверяли с использованием в качестве эффекторных клеток клона ЦТЛ, индуцированного URLC10-A0206-10-211 (SEQ ID NO:2). В качестве контроля использовали клетки COS7, трансфецированные полноразмерным URLC10 без HLA-A0206 и COS7, трансфецированные HLA-A0206 без полноразмерного URLC10. Клон ЦТЛ продемонстрировал наиболее высокую специфическую цитотоксическую активность против COS7, трансфецированных как URLC10, так и HLA-A0206 (фиг.8).
Результаты здесь ясно демонстрируют, что URLC10-A0206-10-211 (SEQ ID NO: 2) естественным образом процессируется и презентируется на поверхности клетки-мишени с молекулой HLA-A0206 и распознается ЦТЛ. Кроме того, URLC10-A0206-10-211 может служить в качестве противоопухолевой вакцины, нацеленной на злокачественные клетки, экспрессирующие URLC10, у пациента с антигеном HLA - HLA-A0206.
В заключение были идентифицированы новые HLA-A0206-эпитопные пептиды HIG2-A0206-9-4 (SEQ ID NO:1) и URLC10-A0206-10-211 (SEQ ID NO:2) и продемонстрирована их применимость для иммунотерапии рака у пациента, антиген HLA-A которого представляет собой HLA-A0206.
Промышленная применимость
Настоящее изобретение описывает новые ОАА, в частности производные HIG2 или URLC10, которые индуцируют мощные и специфические противоопухолевые иммунные ответы и применимы для широкого спектра типов рака. Такие ОАА требуют дальнейшей разработки в качестве пептидных вакцин против заболеваний, ассоциированных с HIG2 или URLC10, например раков, таких как рак мочевого пузыря, рак шейки матки, холангиоцеллюлярная карцинома, рак пищевода, рак желудка, немелкоклеточный рак легких (NSCLC), остеосаркома, рак поджелудочной железы, карцинома почек и опухоль мягких тканей.
Хотя изобретение описано здесь подробно и со ссылкой на конкретные варианты его осуществления, следует понимать, что вышеизложенное описание является по своей природе иллюстративным и пояснительным и предназначено для иллюстрации изобретения и его предпочтительных вариантов осуществления. Посредством рутинных экспериментов специалист в данной области легко узнает, что различные изменения и модификации могут быть сделаны в нем в пределах сущности и объема изобретения, которые определяются прилагаемой формулой изобретения.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПЕПТИДНЫЕ ВАКЦИНЫ ДЛЯ РАКОВ, ЭКСПРЕССИРУЮЩИХ ОПУХОЛЕСПЕЦИФИЧЕСКИЕ АНТИГЕНЫ | 2008 |
|
RU2464275C2 |
| ПЕПТИД, ПОЛУЧЕННЫЙ ИЗ URLC10, И СОДЕРЖАЩАЯ ЕГО ВАКЦИНА | 2015 |
|
RU2700881C2 |
| ЭПИТОПНЫЕ ПЕПТИДЫ RAB6KIFL/KIF20A И СОДЕРЖАЩИЕ ИХ ВАКЦИНЫ | 2009 |
|
RU2532105C2 |
| CDCA1 ЭПИТОП-ПЕПТИДЫ И СОДЕРЖАЩИЕ ИХ ВАКЦИНЫ | 2009 |
|
RU2502740C2 |
| ПЕПТИДЫ UBE2T И СОДЕРЖАЩИЕ ИХ ВАКЦИНЫ | 2013 |
|
RU2663350C2 |
| ПЕПТИДЫ ТОРК И СОДЕРЖАЩИЕ ИХ ВАКЦИНЫ | 2012 |
|
RU2633503C2 |
| ПЕПТИД, ПОЛУЧЕННЫЙ ИЗ KOC1, И СОДЕРЖАЩАЯ ЕГО ВАКЦИНА | 2015 |
|
RU2699542C2 |
| ПЕПТИД, ПОЛУЧЕННЫЙ ИЗ CDCA1, И СОДЕРЖАЩАЯ ЕГО ВАКЦИНА | 2015 |
|
RU2699543C2 |
| HLA-A*3303-РЕСТРИКТИРОВАННЫЙ ПЕПТИД WT1 И СОДЕРЖАЩАЯ ЕГО ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 2007 |
|
RU2435782C2 |
| ОЛИГОПЕПТИДЫ IMP-3 И СОДЕРЖАЩИЕ ИХ ВАКЦИНЫ | 2010 |
|
RU2550695C2 |







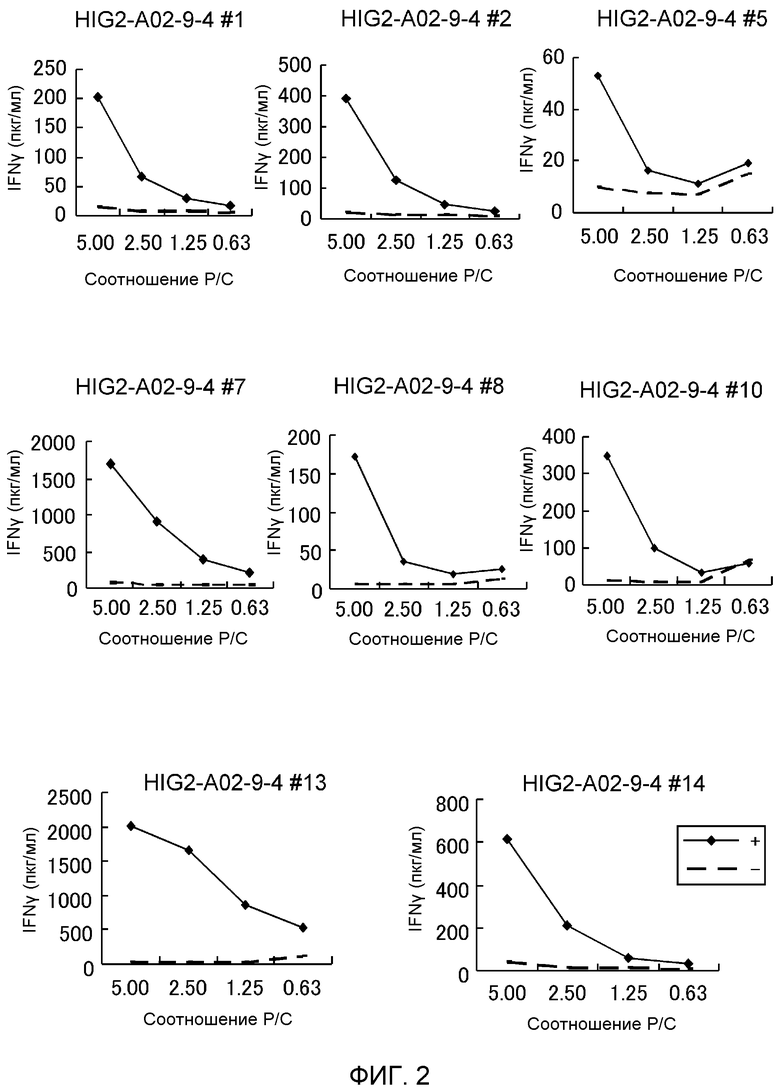
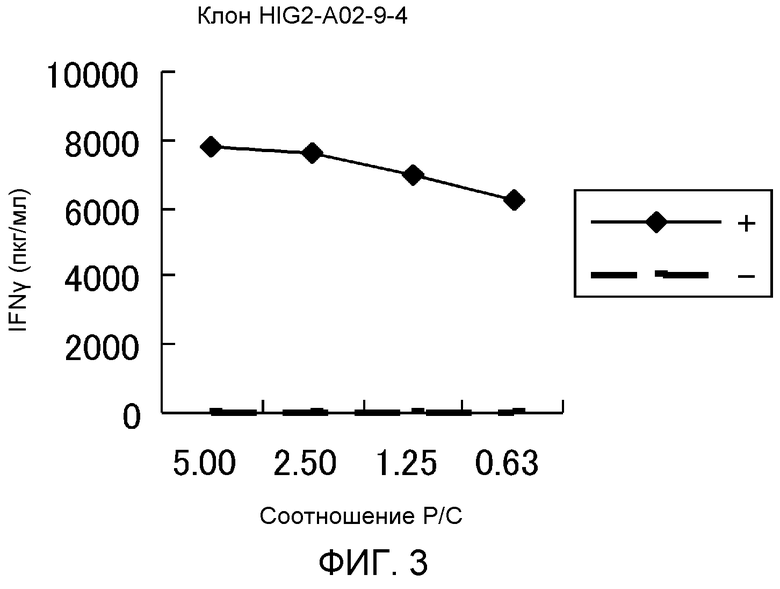
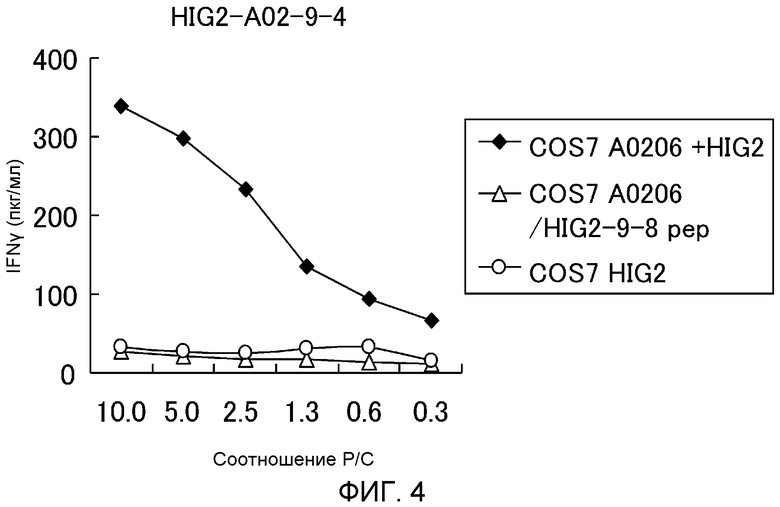

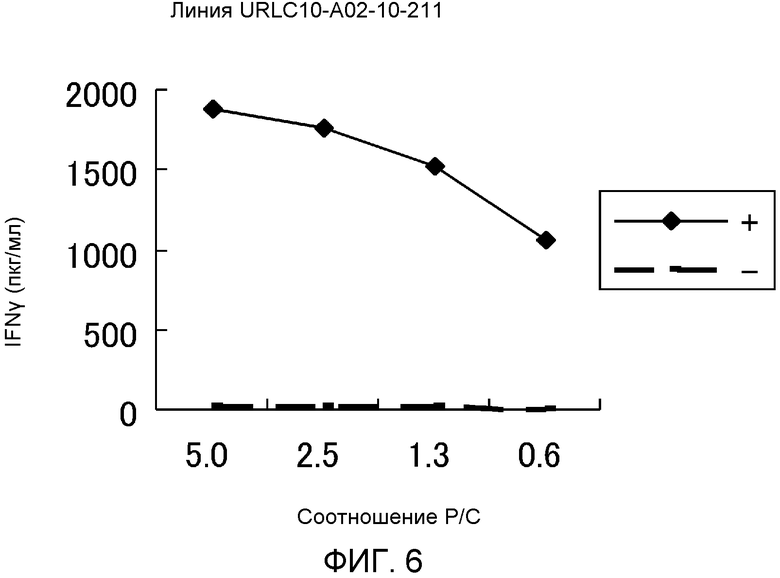

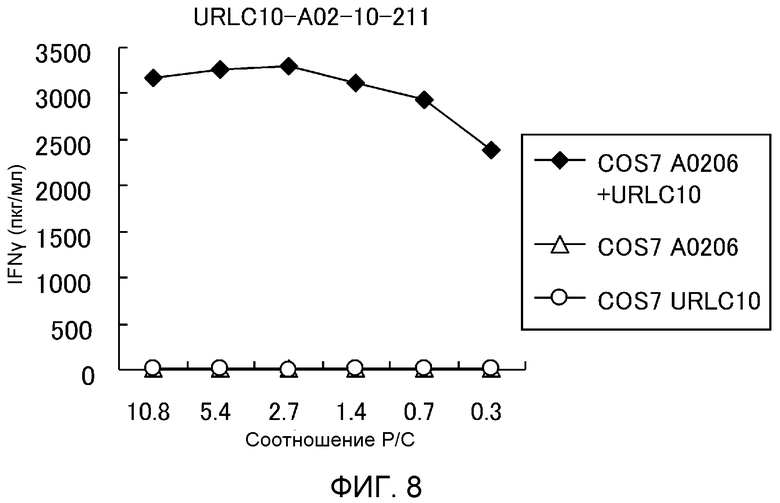
Представленные решения относятся к области иммунологии. Предложены фармацевтическое средство, содержащее пептид, полученный из HIG2 или URLC10, способный индуцировать цитотоксические Т-лимфоциты (ЦТЛ) посредством образования антигенпрезентирующего комплекса с антигеном HLA-A0206. Описаны изолированные антигенпрезентирующая клетка и ЦТЛ и способы и средства для их индукции. Антигенпрезентирующую клетку индуцируют путем контакта клетки, экспрессирующей антиген HLA-A0206, с пептидом, полученным из HIG2 или URLC10. Цитотоксический лимфоцит индуцируют путем контакта CD8-положительной Т-клетки с антигенпрезентирующей клеткой, презентирующей на своей поверхности комплекс из антигена HLA-A0206 и пептида, полученного из HIG2 или URLC10. Охарактеризованы способ и средство индукции иммунного противоопухолевого ответа путем введения пациенту средства, содержащего пептид, который имеет способность индуцировать ЦТЛ. Представленные изобретения могут быть использованы в лечении раковых заболеваний, характеризующихся повышенной экспрессией HIG2 или URLC10. 9 н. и 3 з.п. ф-лы, 8 ил.
1. Фармацевтическое средство для лечения рака, экспрессирующего HIG2 и/или URLC10 у пациента, у которого антиген HLA-A является HLA-A0206, содержащее:
- один или несколько пептидов, обладающих способностью индуцировать цитотоксический T-лимфоцит (ЦТЛ) и состоящих из аминокислотной последовательности, выбранной из группы, состоящей из SEQ ID NO:1 и 2; или
- один или несколько полинуклеотидов, кодирующих такой пептид, в сочетании с фармакологически приемлемым носителем.
2. Фармацевтическое средство по п.1, где указанный рак выбран из группы, состоящей из рака мочевого пузыря, рака шейки матки, холангиоцеллюлярной карциномы, рака пищевода, рака желудка, немелкоклеточного рака легких (NSCLC), остеосаркомы, рака поджелудочной железы, карциномы почек и опухоли мягких тканей.
3. Фармацевтическое средство по п.1, которое применяется в виде вакцины.
4. Способ индукции антигенпрезентирующей клетки, имеющей высокую способность индуцировать ЦТЛ, где способ включает шаг, который выбран из группы, состоящей из следующего:
(a) контакт антигенпрезентирующей клетки с пептидом, состоящим из аминокислотной последовательности, выбранной из группы, состоящей из SEQ ID NO:1 и 2; и
(b) введение полинуклеотида, кодирующего пептид, состоящий из аминокислотной последовательности, выбранной из группы, состоящей из SEQ ID NO:1 и 2, в антигенпрезентирующую клетку,
где антигенпрезентирующая клетка экспрессирует антиген HLA-A0206.
5. Способ индукции ЦТЛ, включающий шаг, выбранный из группы, состоящей из следующего:
a) контакт CD8-положительной Т-клетки с антигенпрезентирующей клеткой, которая презентирует на своей поверхности комплекс из антигена HLA-A0206 и пептида, состоящего из аминокислотной последовательности, выбранной из группы, состоящей из SEQ ID NO:1 и 2; и
(b) введение в CD8-положительную Т-клетку полинуклеотида, кодирующего полипептид, который способен формировать субъединицу Т-клеточного рецептора (TCR), распознающую комплекс из пептида и антигена HLA-A0206, где пептид состоит из аминокислотной последовательности, выбранной из группы, состоящей из SEQ ID NO:1 и 2,
где ЦТЛ распознает комплекс антигена HLA-A0206 и указанного пептида.
6. Изолированная антигенпрезентирующая клетка, которая презентирует на своей поверхности комплекс из антигена HLA-A0206 и пептида, состоящего из аминокислотной последовательности, выбранной из группы, состоящей из SEQ ID NO:1 и 2, индуцированная посредством способа по п.4.
7. Изолированный ЦТЛ, который распознает комплекс из антигена HLA-A0206 и пептида, состоящего из аминокислотной последовательности, выбранной из группы, состоящей из SEQ ID NO:1 и 2, индуцированный посредством способа по п.5.
8. Средство для индукции антигенпрезентирующей клетки, экспрессирующей антиген HLA-A0206, с высокой способностью индуцировать ЦТЛ, где средство содержит:
(a) пептид, имеющий способность индуцировать ЦТЛ, где указанный пептид состоит из аминокислотной последовательности, выбранной из группы, состоящей из SEQ ID NO:1 и 2;
(b) один или несколько полинуклеотидов, кодирующих такой пептид.
9. Средство для индукции ЦТЛ, содержащее:
(a) пептид, имеющий способность индуцировать ЦТЛ, где указанный пептид состоит из аминокислотной последовательности, выбранной из группы, состоящей из SEQ ID NO:1 и 2;
(b) один или несколько полинуклеотидов, кодирующих такой пептид;
(с) одну или несколько антигенпрезентирующих клеток (АРС), которые презентируют на своей поверхности комплекс из антигена HLA-A0206 и пептида, состоящего из аминокислотной последовательности, выбранной из группы, состоящей из SEQ ID NO:1 и 2.
10. Способ индукции иммунного противоопухолевого ответа у пациента, у которого антиген HLA-A является HLA-A0206, где указанный способ включает этап введения указанному пациенту средства, содержащего пептид, который имеет способность индуцировать ЦТЛ и состоит из аминокислотной последовательности, выбранной из группы, состоящей из SEQ ID NO:1 и 2, полинуклеотид, кодирующий такой пептид, отдельную антигенпрезентирующую клетку по п.6 или полученную при помощи средства по п.8 или отдельный ЦТЛ по п.7 или полученный при помощи средства по п.9.
11. Способ по п.10, где указанная опухоль выбрана из группы, состоящей из рака мочевого пузыря, рака шейки матки, холангиоцеллюлярной карциномы, рака пищевода, рака желудка, немелкоклеточного рака легкого, остеосаркомы, рака поджелудочной железы, карциномы почек и опухоли мягких тканей.
12. Средство для индукции иммунного противоопухолевого ответа у пациента, у которого антиген HLA-A является HLA-A0206, где указанное средство содержит:
(a) пептид, способный индуцировать ЦТЛ, где указанный пептид состоит из аминокислотной последовательности, выбранной из группы, состоящей из SEQ ID NO:1 и 2;
(b) один или несколько полинуклеотидов, кодирующих такой пептид;
(c) одну или несколько изолированных антигенпрезентирующих клеток по п.6 или полученных при помощи средства по п.8;
(d) один или несколько изолированных ЦТЛ по п.7 или полученных при помощи средства по п.9; или
(e) их комбинацию
в сочетании с фармакологически приемлемым носителем.
| WO 2006090810 A2, 31.08.2006 | |||
| WO 2007029778 A1, 15.03.2007 | |||
| WO 2005019475 A2, 03.03.2005 | |||
| SPARC-ПРОИЗВОДНЫЕ АНТИГЕННЫЕ ПЕПТИДЫ ОТТОРЖЕНИЯ ОПУХОЛИ И ЛЕКАРСТВЕННЫЕ СРЕДСТВА, СОДЕРЖАЩИЕ ИХ | 2007 |
|
RU2451521C2 |
Авторы
Даты
2014-09-27—Публикация
2009-08-14—Подача