Область техники
Настоящее изобретение относится к агенту для придания кокуми и комплексному агенту для придания кокуми, содержащему пептид, проявляющий активность агониста CaSR. Кроме того, настоящее изобретение также относится к приправе, содержащей пептид, проявляющий активность агониста CaSR, в концентрации не менее заданного уровня.
Уровень техники
Требования потребителей к вкусу и привлекательности пищевых продуктов в последнее время повысились, например, из-за разнообразия пищевых привычек людей. В этой связи вкус и привлекательность пищи общепринятым образом выражают посредством пяти основных вкусов - сладкого, соленого, кислого, горького и умами («мясного» вкуса), но соответственно увеличивается потребность в создании нового агента, способного придавать пище прекрасный кокуми. Кокуми обозначает вкус, который нельзя выразить упомянутыми пятью основными вкусами, поскольку он предоставляет дополнительные ощущения к основным вкусам, такие как густота, полнота (наполненность), непрерывность и гармоничность (прим. «Kokumi» приблизительно соответствует термину «mouthfeel» - «ощущение во рту»).
С другой стороны, кальций-чувствительный рецептор (CaSR) также называют кальциевым рецептором, и сигналы от этого рецептора могут контролировать множество биологических функций в живых организмах, поэтому вещества, проявляющие активность агониста CaSR, можно использовать в качестве агентов для придания кокуми (см. Патентные документы 1 и 2 и Непатентный документ 4, как указано ниже).
Возможны различные профили развития вкуса в упомянутом «кокуми». В этой связи существует потребность в создании агента, способного придавать пище кокуми среднего вкуса и послевкусия, и имеющего высокий титр. Кроме того, поскольку агент для придания кокуми используют обычно в пищевых продуктах, то соответственно, он должен обладать отличной стабильностью. Дополнительно, вещество для придания кокуми должно иметь низкую стоимость производства.
Соответственно, потребовался поиск среди множества вариантов соединений, проявляющих желательную активность агониста CaSR, чтобы таким образом обнаружить вещество, способное придавать кокуми другому материалу (т.е. пищевым продуктам или напиткам), обладающее более выдающимся эффектом придания кокуми, в частности, кокуми начального вкуса, которое обладает отличной стабильностью, и которое можно легко получать с низкой стоимостью, и чтобы таким образом предоставить агент для придания кокуми, состоящий из такого вещества, а также комплексный агент для придания кокуми, содержащий вещество и другие вещества, проявляющие активность агониста CaSR, в комбинации.
С другой стороны, что касается некоторых γ-глутамил-пептидов, каждый из которых несет остаток γ-глутамина на N-конце, известны пептиды, синтезированные в качестве субстратов, например, для исследований ферментативной активности (см. Патентный документ 3 и Непатентные документы 1-3, указанные позже), но еще не известно каких-либо случаев, когда γ-Glu-Nva-Gly действительно использовали в пищевых продуктах, или каких-либо случаев его выделения из природных материалов для добавления в пищу. В этом отношении, полное содержание Патентных документов 1 и 2 включено сюда путем ссылки, как если бы их содержание было непосредственно включено в настоящее описании.
Документы уровня техники
Патентные документы
Патентный документ 1: WO 2007/055393, реферат;
Патентный документ 2: WO 2008/139945, реферат;
Патентный документ 3: WO 2007/066430, реферат.
Непатентные документы
Непатентный документ 1: Molecular Pharmacology (1982), 21(3), 629-36;
Непатентный документ 2: Agricultural and Biological Chemistry (1981), 45(12), 2893-45;
Непатентный документ 3: The Journal of Biological Chemistry, (1979), 254 (12), 5184-90;
Непатентный документ 4: The Journal of Biological Chemistry, (2010), 285 (2), 1016-22.
Сущность изобретения
Задача настоящего изобретения состоит в обнаружении большинства соединений, проявляющих желательную активность агониста CaSR, чтобы таким образом обнаружить вещество, способное придавать кокуми улучшенного вкуса, в частности, кокуми среднего вкуса/послевкусия, и при этом обладающее отличной стабильностью, и имеющее высокий титр, чтобы таким образом обеспечить агент для придания кокуми, состоящий из такого вещества, а также комплексный агент для придания кокуми, содержащий комбинацию такого вещества с другими веществами, проявляющими активность агониста CaSR. Еще одной задачей изобретения является обеспечение приправы, содержащей вышеуказанное вещество в концентрации не менее заданного уровня.
В результате поиска множества соединений авторы этого изобретения неожиданно обнаружили, что γ-Glu-Nva-Gly (L-γ-глутамил-L-норвалил-глицин) проявляет высокую активность агониста CaSR и придает прекрасный кокуми, а также что он, в частности, придает пище кокуми с рисунком развития вкуса, соответствующего кокуми среднего вкуса/послевкусия. Кроме того, авторы изобретения обнаружили, что обнаруженный γ-Glu-Nva-Gly имеет очень высокий титр, не менее чем в 10 раз превышающего титр, наблюдаемый для γ-Glu-Val-Gly в качестве одного из трипептидов, сходных с γ-Glu-Nva-Gly, обладает отличной стабильностью и обладает таким благоприятным характером развития вкуса, что демонстрирует высокую способность придания кокуми среднего вкуса/послевкусия. Кроме того, авторы изобретения далее обнаружили, что γ-Glu-Nva-Gly может служить самостоятельным агентом для придания кокуми. Кроме того, авторы изобретения подобным образом обнаружили, что предпочтительную приправу с улучшенным кокуми можно получать включением γ-Glu-Nva-Gly в пищевую композицию. Кроме того, комплексный агент для придания кокуми можно получать комбинированием указанного вещества с другими веществами, каждое из которых проявляет активность агониста CaSR. Авторы таким образом пришли к настоящему изобретению.
Более конкретно, настоящее изобретение в настоящем документе относится к агенту для придания вкуса кокуми, состоящему из γ-Glu-Nva.
Кроме того, настоящее изобретение также относится к пищевой композиции, содержащей γ-Glu-Nva (в настоящем документе эта композиция обозначена также как «пищевая композиция по изобретению»). Настоящее изобретение также предоставляет комплексный агент для придания кокуми, содержащий, в комбинации, (a) γ-Glu-Nva и (b) одну или по меньшей мере две аминокислоты или пептида, выбранных из группы, состоящей из γ-Glu-X-Gly, где X представляет собой аминокислоту или производное аминокислоты, γ-Glu-Val-y, где Y представляет собой аминокислоту или производное аминокислоты, γ-Glu-Abu, γ-Glu-Ala, γ-Glu-Gly, γ-Glu-Cys, γ-Glu-Met, γ-Glu-Thr, γ-Glu-Val, γ-Glu-Orn, Asp-Gly, Cys-Gly, Cys-Met, Glu-Cys, Gly-Cys, Leu-Asp, D-Cys, γ-Glu-Met(O), γ-Glu-γ-Glu-Val, γ-Glu-Val-NH2, γ-Glu-Val-ола, γ-Glu-Ser, γ-Glu-Tau, γ-Glu-Cys (S-Me) (O), γ-Glu-Leu, γ-Glu-Ile, γ-Glu-t-Leu и γ-Glu-Cys (S-Me).
Настоящее изобретение предоставляет агент для придания кокуми с прекрасным действием и, в частности, придающий отличный и уникальный кокуми среднего вкуса/послевкусия, с характером развития вкуса, который имеет профиль, показанный, например, на Фиг.1, а также обладающий отличной стабильностью, и который можно легко получать с низкой стоимостью, так же как комплексный агент для придания кокуми, содержащий его. Кроме того, настоящее изобретение предоставляет отличную приправу, обладающую отличным эффектом придания кокуми в концентрации не менее заданного уровня.
Агент для придания кокуми по изобретению демонстрирует профиль развития вкусоаромата, подобный таковому у поваренной соли, и таким образом, при использовании данного агента для придания кокуми, он может придавать пище с низким содержанием соли или подобным продуктам солености и начального соленого вкуса. Соответственно, полученный пищевой продукт, содержащий агент по изобретению, может сохранять ощущение соленого вкуса продукта до снижения в нем содержания соли, даже когда содержание соли в этом продукте снижено, и таким образом, агент по изобретению позволяет получать пищевые продукты, полезные для здоровья. Примеры таких пищевых продуктов включают множество супов и различные виды соусов. В частности, при потреблении пищевого продукта, содержащего агент для придания кокуми по изобретению, потребитель может получить явное ощущение соленого вкуса и эффект (или придание) начального вкуса непосредственно после его потребления.
Краткое описание чертежей
На фиг. 1 показан профиль развития вкуса, наблюдаемый для агента для придания кокуми начального вкуса.
Способ осуществления изобретения
Вещество, γ-Glu-Nva, используемое по изобретению, содержит L-γ-глутамил-L-норвалин, в котором две аминокислоты связаны друг с другом через пептидную связь, и/или его соли, в частности, его пригодные к потреблению в пищу соли.
Вещество, γ-Glu-Nva, обладает отличным эффектом придания кокуми и таким образом, его можно использовать в качестве агента для придания кокуми. γ-Glu-Nva можно использовать таким образом, что пищевая композиция, которой придают кокуми, содержит дипептид в количестве (все части и проценты весовые) в диапазоне от 0,1 млр.д. (миллиардных долей) до 99,9 вес.%, предпочтительно, от 1 млр.д. до 10 вес.% и более предпочтительно, от 0,01 м.д. (миллионных долей) до 1 вес.% от общего веса пищевой композиции. Иными словами, другой вариант осуществления настоящего изобретения относится к пищевой композиции, содержащей γ-Glu-Nva, и предпочтительно, пищевой композиции, содержащей γ-Glu-Nva в количестве, лежащем в диапазоне от 0,1 млр.д. до 99,9 вес.%, предпочтительно, от 1 млр.д. до 10 вес.% и более предпочтительно, от 0,01 м.д. до 1 вес.%. Более конкретно, настоящее изобретение относится, например, к пищевой композиции, содержащей γ-Glu-Nva в количестве не менее 0,1 млр.д., не менее 0,005 м.д., не менее 0,02 м.д. или от не менее 0,01 вес.% до не более 99,9 вес.%, не более 90,0 вес.%, не более 50 вес.%, не более 600000 м.д., не более 100000 м.д., не более 80 м.д., не более 30 м.д. или не более 10 м.д. по весу.
Более того, агент для придания кокуми по изобретению или γ-Glu-Nva можно использовать также в комбинации по меньшей мере с одним дополнительным ингредиентом для приправ, выбранным из группы, состоящей из аминокислот, таких как глутамат натрия (MSG), нуклеиновых кислот, таких как инозинмонофосфат (IMP), неорганических солей, таких как хлорид натрия, органических кислот, таких как лимонная кислота, и различных видов дрожжевых экстрактов, чтобы таким образом получить обеспечивающую преимущества приправу с улучшенным кокуми, по сравнению с кокуми, полученным при использовании таких дополнительных ингредиентов для приправ по отдельности. При использовании γ-Glu-Nva в комбинации с вышеуказанными дополнительными ингредиентами для приправ концентрацию первого упомянутого может легко или подходящим образом определить или установить специалист в данной области после проведения исследований, например, посредством сенсорной оценки.
По настоящему изобретению, термин «кокуми» обозначает вкус, который нельзя выразить посредством пяти основных вкусов или сладкого вкуса, соленого вкуса, кислого вкуса, горького вкуса и умами, и более конкретно, обозначает вкус, при котором дополнительные вкусы основных вкусов, такие как густота, распространение (наполнение рта), продолжительность и гармоничность, усилены в дополнение к основным вкусам. Кроме того, термин «придание кокуми» в настоящем документе означает, что пять основных вкусов, выраженные сладким вкусом, соленым вкусом, кислым вкусом, горьким вкусом и умами, усилены, в то время как у субъекта одновременно создается ощущение вкусов, дополнительных к основными вкусами, таких как густота, распространение (наполнение рта), продолжительность и гармоничность, ассоциированные с первым упомянутым. Более того, это можно обозначать также как эффект усиления вкуса. Таким образом, γ-Glu-Nva, служащий в качестве агента для придания кокуми по изобретению, можно подобным образом обозначать как «усилитель вкуса». Агент для придания кокуми по изобретению, или γ-Glu-Nva, можно использовать также как усилитель сладкого вкуса, усилитель соленого вкуса, усилитель кислого вкуса, усилитель горького вкуса или усилитель умами.
Кроме того, изменение вкуса пищи с течением времени при потреблении и после него обычно обозначают как начальный вкус, средний вкус и послевкусие, по порядку, начиная от момента потребления пищи. Хотя в действительности они представляют собой относительное понятие, но начальный вкус, средний вкус и послевкусие у субъекта, в целом, определяют как вкус, наблюдаемый в пределах времени, продолжающегося от 0 до 2 секунд, от 2 до 5 секунд и не менее 5 секунд после потребления пищи, соответственно. Вкус, наблюдаемый в течение времени, продолжающегося от 0 до 5 секунд, обозначают в настоящем документе как «начальный/средний вкус», и вкус, наблюдаемый в течение времени, продолжающегося от 2 до приблизительно 30 секунд, обозначают как «средний вкус/послевкусие» (см. данные, нанесенные на график на Фиг. 1). Что касается оценки вкуса, в случае, когда вкус разделяют на три подразделения, для дегустаторов (лиц, употребляющих пищу, подлежащую оценке) сложно концентрировать внимание на оценке, и привычно используемый тест содержит оценку вкуса с разделением на два подразделения.
Более того, объединенный начальный вкус и средний вкус обозначают как «начальный/средний вкус», и объединенный средний вкус и послевкусие обозначают как «средний вкус/послевкусие».
Эффекты вещества, проявляющего активность агониста CaSR, на кокуми и характер развития вкуса можно подтверждать, например, таким способом, как человеческая сенсорная проба для оценки вкуса. Пример такой человеческой сенсорной пробы для оценки вкуса проиллюстрирован в примерах этой патентной заявки, но сенсорная проба для оценки вкуса, пригодная по изобретению, не ограничена этой конкретной пробой.
Термин «CaSR», используемый в этом описании, обозначает кальций-чувствительный рецептор, который принадлежит к классу С 7-тяжевого трансмембранного рецептора, и который, таким образом, также обозначают как «кальциевый рецептор». Термин «агонист CaSR», используемый в этом описании, обозначает вещество, связывающееся с вышеупомянутым CaSR, чтобы таким образом активировать рецептор CaSR. Кроме того, термин «активировать CaSR», применяемый в настоящем документе, обозначает, что лиганд связывается с CaSR, чтобы таким образом активировать белок, связанный с гуаниновым нуклеотидом, и чтобы передавать сигналы, получаемые от него. Более того, способность вещества образовывать связь с CaSR, чтобы таким образом активировать его, обозначают как «активность агониста CaSR».
В настоящее время способ скрининга соединения, проявляющего активность агониста CaSR, конкретно представлен в настоящем документе, но стадии скрининга соединений нисколько не ограничены стадиями, указанными ниже.
1) Стадия добавления тестируемого вещества в систему для измерения активности CaSR, используемую для определения активности CaSR, и стадия определения активности CaSR;
2) Стадия сравнения активности CaSR, наблюдаемой при добавлении тестируемого вещества в систему для измерения активности, с активностью, наблюдаемой до добавления вещества; и
3) Стадия отбора вещества, проявляющего активность агониста CaSR при добавлении в систему для измерения активности CaSR.
Определение активности CaSR подобным образом можно проводить с использованием, например, системы измерения с использованием клеток, обладающих способностью экспрессировать CaSR. Вышеуказанные клетки могут представлять собой клетки с эндогенной экспрессией CaSR или генетически рекомбинантные клетки с экзогенно введенным геном для экспрессии CaSR. Вышеуказанная система для измерения активности CaSR не является ограниченной никакой конкретной системой, пока она позволяет детекцию связи (или реакции) между активирующим CaSR веществом и CaSR, или пока она может испускать или выдавать поддающий детекции сигнал в ответ на образование связи (или реакцию) между активирующим CaSR веществом и CaSR внутри клеток при добавлении внеклеточного лиганда (активирующего вещества), специфического для CaSR, к вышеуказанным клеткам, обладающим способностью экспрессировать CaSR. Если активность CaSR детектируют в ходе реакции с тестируемым веществом, можно заключить, что тестируемое вещество обладает желательной активностью стимуляции CaSR.
Примером вышеуказанного CaSR, предпочтительно используемого в настоящем документе, является CaSR человека, кодируемый геном CaSR человека, зарегистрированным в GenBank под номером доступа NM_000388. В этом отношении, однако, CaSR не является ограниченным белком, кодируемым геном, обладающим вышеуказанной последовательностью зарегистрированного CaSR, и может представлять собой любой белок, который способен быть кодированным геном, обладающим не менее 60%, предпочтительно не менее 80%, и более предпочтительно, не менее 90% гомологии последовательности с последовательностью вышеуказанного гена, при условии, что белок, кодируемый таким геном, обладает желательной функцией CaSR. В этой связи, функцию CaSR можно проверять посредством получения клеток, экспрессирующих эти гены, и определения затем любого изменения силы тока и/или любого изменения концентрации иона кальция внутри клеток, наблюдаемого при добавлении кальция в систему, содержащую клетки.
В отношении вышеуказанного CaSR, его источник не является ограниченным каким-либо конкретным источником и он может представлять собой CaSR, полученный из совокупности видов животных, включая мышей, крыс и собак, в дополнение к вышеуказанному CaSR человека.
Как обсуждали выше, активность CaSR можно подтверждать посредством использования живых клеток, способных экспрессировать CaSR или его фрагмент, мембран клеток, способных экспрессировать CaSR или его фрагмент, или системы in vitro, содержащей CaSR или белок в виде его фрагмента.
Пример, в котором используют такие живые клетки, приведен ниже, но настоящее изобретение совершенно никаким образом не ограничено этим примером.
CaSR экспрессируют в культивируемых клетках, таких как ооциты ксенопуса, клетки яичника, полученные от хомяков, и фетальные клетки почки человека. Эту экспрессию CaSR можно осуществлять посредством введения, в плазмиде, обладающей экзогенным геном, гена CaSR, который подвергали обработке клонированием в форме плазмиды или кРНК, полученных с использованием гена в качестве матрицы. Пригодными для детекции такой реакции могут являться электрофизиологические способы или флуоресцентный индикатор для детекции какого-либо увеличения концентрации кальция внутри клеток.
Экспрессию CaSR исходно подтверждали по присутствию любого ответа, наблюдаемого при добавлении кальция или активатора, обладающего специфичностью к нему. Более конкретно, пригодными по изобретению в качестве желательных клеток являются клетки, в которых внутриклеточный электрический ток детектируют при добавлении кальция в концентрации приблизительно 5 мМ, или клетки, в которых испускание флуоресцентных лучей наблюдают при добавлении флуоресцентного индикатора. В этой связи концентрацию кальция, добавляемого к клеткам, различным образом изменяют для определения зависимости интенсивности внутриклеточной силы тока от концентрации кальция. Затем тестируемое вещество разводят до концентрации в диапазоне от приблизительно 1 мкМ до 1 мМ, полученную суспензию добавляют к ооцитам или культивируемым клеткам, и затем активность CaSR в присутствии вышеуказанного тестируемого вещества измеряют, чтобы таким образом определить активность агониста CaSR для тестируемого вещества.
Более конкретно, в качестве такого теста для определения активности агониста CaSR по изобретению пригоден, например, тест, проиллюстрированный в тестовых примерах, описанных в этом описании, но тест для определения активности совсем не является ограниченным таким конкретным тестом.
Аминокислоты или пептиды, используемые в агенте для придания кокуми по изобретению в комбинации с γ-Glu-Nva, включают в себя, например, одну или по меньшей мере две аминокислоты или пептида, выбранных из группы, состоящей из γ-Glu-X-Gly (где X представляет собой аминокислоту или производное аминокислоты), γ-Glu-Val-Y (где Y представляет собой аминокислоту или производное аминокислоты), γ-Glu-Abu, γ-Glu-Ala, γ-Glu-Gly, γ-Glu-Cys, γ-Glu-Met, γ-Glu-Thr, γ-Glu-Val; γ-Glu-Orn, Asp-Gly, Cys-Gly, Cys-Met, Glu-Cys, Gly-Cys, Leu-Asp, D-Cys, γ-Glu-Met (О), γ-Glu-γ-Glu-Val, γ-Glu-Val-NH2, γ-Glu-Val-ола, γ-Glu-Ser, γ-Glu-Tau, γ-Glu-Cys (S-Me) (О), γ-Glu-Leu, γ-Glu-Ile, γ-Glu-t-Leu и γ-Glu-Cys (S-Me). В этом отношении, аминокислоты могут подобным образом включать в себя, например, нейтральные аминокислоты, такие как Gly, Ala, Val, Leu, Ile, Ser, Thr, Cys, Met, Asn, Gln, Pro, Hyp, t-Leu; кислые аминокислоты, такие как Asp, Glu; основные аминокислоты, такие как Lys, Arg, His; ароматические аминокислоты, такие как Phe, Tyr, Trp; также, как гомосерин, цитруллин, орнитин, α-аминомасляную кислоту, норвалин, норлейцин и таурин. Более того, аминокислоты, используемые по изобретению, могут представлять собой также искусственные аминокислоты (имеющие небелковую конструкцию), такие как трет-лейцин, циклолейцин, α-аминоизомасляная кислота, L-пеницилламин, аллотреонин и аллоизолейцин. В этой связи, в пептиде: γ-Glu-X-Gly X может представлять собой вышеуказанную аминокислоту или ее производное, но предпочтительно используемыми по изобретению являются аминокислоты или их производные, отличные от Cys. Из них предпочтительно используемые по изобретению в комбинации с γ-Glu-Nva включают в себя, например, γ-Glu-Val-Gly, γ-Glu-Abu-Gly, γ-Glu-tLeu-Gly, γ-Glu-Nva-Gly и γ-Glu-Abu.
В частности, агент для придания кокуми по изобретению состоит из γ-Glu-Nva, и этот агент обладает уникальным и отличным эффектом придания кокуми начального вкуса и профилем развития вкуса (вкуса), как показано на фиг. 1. Соответственно, является предпочтительным, чтобы γ-Glu-Nva использовали в комбинации с пептидом, таким как γ-Glu-Val-Gly, обладающим профилем развития вкуса, отличным от первого упомянутого.
В описании этой патентной заявки каждую аминокислоту (остаток) выражают в обозначении следующей сокращенной формы:
(1) Gly: глицин;
(2) Ala: аланин;
(3) Val: валин;
(4) Leu: лейцин;
(5) Ile: изолейцин;
(6) Met: метионин;
(7) Phe: фенилаланин;
(8) Tyr: тирозин;
(9) Trp: триптофан;
(10) His: гистидин;
(11) Lys: лизин;
(12) Arg: аргинин;
(13) Ser: серин;
(14) Thr: треонин;
(15) Asp: аспарагиновая кислота;
(16) Glu: глутаминовая кислота;
(17) Asn: аспарагин;
(18) Gln: глутамин;
(19) Cys: цистеин;
(20) Pro: пролин;
(21) Orn: орнитин;
(22) Sar: саркозин;
(23) Cit: цитруллин;
(24) N-Val: (или Nva): норвалин (2-аминовалериановая кислота);
(25) N-Leu (или Nle): норлейцин;
(26) Abu: α-аминомасляная кислота;
(27) Tau: таурин;
(28) Hyp: гидроксипролин;
(29) t-Leu: трет-лейцин;
(30) Cle: циклолейцин;
(3l) Aib: α-амино-изомасляная кислота (2-метилаланин);
(32) Pen: L-пеницилламин;
(33) алло-Thr: аллотреонин;
(34) алло-Ile: аллоизолейцин.
Более того, термин «производное аминокислоты», применяемый в настоящем документе, обозначает множество производных вышеуказанных аминокислот, и их конкретные примеры включают особые аминокислоты и искусственные аминокислоты, аминоспирты или аминокислоты, аминокислотные боковые цепи которых, такие как карбоксильные группы, аминогруппы и/или тиоловая группа цистеина, являются замещенными множеством заместителей. Примеры таких заместителей включают алкильную группу, ацильную группу, гидроксильную группу, аминогруппу, алкиламиногруппу, нитрогруппу, сульфонильную группу или различные защитные группы. Таким образом, примеры таких производных аминокислот включают Arg (NO2): N-γ-нитроальгинин, Cys (SNO): S-нитроцистеин, Cys (S-Me): S-метилцистеин, Cys (S-аллил): S-аллилцистеин, Val-NH2: валинамид, и Val-ол: валинол (2-амино-3-метил-1-бутанол). В то же время, пептид: γ-Glu-Cys(SNO)-Gly, используемый по изобретению, представляет собой пептид, представленный следующей структурной формулой, и символ: «(О)», представленный в вышеуказанных формулах: γ-Glu-Met (O) и γ-Glu-Cys (S-Me) (O), означает, что каждый из этих пептидов обладает сульфоксидной структурой. Символ «(γ)» из γ-Glu означает, что другая аминокислота связана с глутаминовой кислотой через карбоксильную группу, расположенную в γ-положении последнего.
[Химическая формула 1]
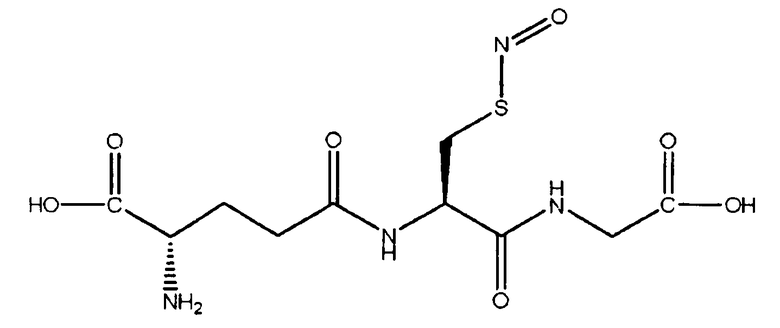
S-нитрозоглутатион (GNSO)
γ-Glu-Nva и аминокислоты и пептиды, используемые в комбинации по изобретению, могут представлять собой коммерчески доступные аминокислоты и пептиды, если их можно закупать на рынке, или их можно получать любым известным способом, таким как (l) способы химического синтеза или (2) способ с использованием ферментативной реакции, но более удобным является использование способа химического синтеза. γ-Glu-Nva, используемый по изобретению, является очень коротким по длине, поскольку он содержит только два аминокислотных остатка, и таким образом, является более удобным принять способ химического синтеза. Более конкретно, его можно получать просто и с низкой стоимостью по сравнению с любым трипептидом, содержащим три аминокислотных остатка, и соответственно, использование этого дипептида является достаточно предпочтительным с промышленной точки зрения. Кроме того, при химическом синтезе γ-Glu-Nva, используемого по изобретению, и аминокислот и пептидов, используемых в комбинации с ним, их получение можно проводить посредством синтеза или полусинтеза этих олигопептидов с использованием устройства для синтеза пептидов. В качестве такого способа химического синтеза этих пептидов по изобретению может являться пригодным, например, способ твердофазного пептидного синтеза. Полученный таким образом пептид можно затем очищать обычными способами, такими как способ ионообменной хроматографии, способ обращеннофазовой высокоэффективной жидкостной хроматографии или способ аффинной хроматографии. Такой способ твердофазного пептидного синтеза и используемый затем способ очистки пептидов хорошо известны в данной области.
Альтернативно, при получении γ-Glu-Nva, используемого по изобретению, и аминокислот и пептидов, используемых в комбинации с ним, при использовании ферментативной реакции, их получение можно осуществлять с использованием способа, описанного в документации Международного патента, находящегося в открытом доступе, WO 2004/011653. Более конкретно, их можно получать посредством реакции аминокислоты или пептида, в которых концевая карбоксильная группа эстерифицирована или аминирована, с другой аминокислотой, аминогруппа которой находится в свободном состоянии (например, аминокислотой, карбоксильная группа которой защищена) в присутствии пептидообразующего фермента и затем посредством очистки полученного дипептида или трипептида. Примерами таких пептидообразующих ферментов являются культуры микроорганизмов, обладающих способностью продуцировать пептид; клеточные тела микроорганизмов, выделенные из культуры; или продукт, полученный переработкой клеточных тел микроорганизмов; или пептидообразующий фермент, полученный из микроорганизмов. В то же время в настоящем документе подразумевают, что описание WO 2004/011653 включено в описание этой заявки.
В дополнение к вышеуказанным способам ферментативного получения и способам химического синтеза, пептиды, используемые по изобретению, часто включены в природные продукты, например, растения, такие как овощи и фрукты, микроорганизмы, такие как дрожжи, и другие природные ресурсы. Когда они присутствуют в природных веществах, их можно выделять из этих веществ, и полученные выделенные продукты можно подобным образом использовать по изобретению.
Агент для придания кокуми или комплексный агент для придания кокуми по изобретению можно использовать в качестве приправы без какой-либо специальной последующей обработки или можно смешивать с носителями, пригодными для пищевых продуктов и напитков, или с ингредиентами для других приправ, чтобы таким образом получать различные приправы. Примеры таких других ингредиентов для приправ включают специи, сахариды, подсластители, пищевые волокна, витамины, аминокислоты, такие как глутамат натрия (MSG), нуклеиновые кислоты, такие как инозинмонофосфат (IMP), неорганические соли, такие как хлорид натрия, и органические кислоты, такие как лимонная кислота, также, как различные виды дрожжевых экстрактов.
В частности, пищевые продукты с низким содержанием соли, предпочтительные в качестве пищевых композиций, каждая из которых содержит агент для придания кокуми или комплексный агент для придания кокуми по изобретению, представляют собой по существу соленые пищевые продукты, и, в частности, пищевые продукты, содержание поваренной соли в которых снижено.
Примеры таких пищевых продуктов с пониженным содержанием соли включают молочные продукты, такие как масло и сыр; животные жиры и жиросодержащие масла и/или растительные масла, и жиросодержащие пищевые продукты, такие как маргарин, соусы и заправка для соусов; эмульгированные пищевые продукты, такие как заправки для салатов и майонез; различные виды карри и рагу; и множество супов, содержащих мясные экстракты или мясные эссенции и/или сливки. Более того, такие пищевые продукты с пониженным содержанием соли подобным образом включают в себя, например, ферментированные или сброженные продукты, такие как «мисо» и соевый соус; переработанные растительные пищевые продукты, такие как соленые овощи и пикули; продукты переработки мяса, такие как ветчина и колбаса; переработанные морепродукты, такие как паштет из отварной рыбы, сушеные морепродукты и пищевые продукты, вываренные в сое; приготовленные тефтели, рубленый бифштекс; жареные пищевые продукты и цыпленка-гриль. Из них предпочтительными пищевыми продуктами с пониженным содержанием соли являются пищевые продукты, имеющие концентрацию поваренной соли, при их потреблении, в диапазоне от 0,01 до 0,5 вес.%.
Если агент для придания кокуми по изобретению включают в вышеуказанные пищевые продукты с пониженным содержанием соли, пищевые продукты становятся способными создавать у потребителя сильное ощущение вкуса, подобного соленому, и ощущение (или придание) начального вкуса на начальной стадии, при потреблении этих пищевых продуктов с пониженным содержанием соли.
Кроме того, при рассмотрении настоящего изобретения с другой точки зрения, травы и специи, полученные из растений, принадлежащих к Labiatae (семейству мяты), или пищевые продукты, к которым добавляют эти травы и специи, полученные из растений, принадлежащих к Labiatae, подобным образом являются предпочтительными в качестве пищевых композиций, содержащих агент для придания кокуми или комплексный агент для придания кокуми по изобретению. Примеры трав, полученных из растений, принадлежащих к Labiatae, включают анис, ореган, шалфей, тимьян, мяту японскую, мяту перечную, бергамот, майоран, мяту, лаванду и розмарин в дополнение к печеночнице и базилику, однако, настоящее изобретение совсем не является ограниченным этими конкретными травами. В случае пищевых продуктов, каждый из которых содержит такие травы и/или специи, полученные из растений, принадлежащих к Labiatae, и агент для придания кокуми или комплексный агент для придания кокуми по изобретению, вышеуказанные пищевые продукты предпочтительно представляют собой пищевые продукты, содержащие травы и/или специи в количестве в диапазоне от 0,01 до 10 вес.%, как выражено в отношении содержания в них сухого вещества, наблюдаемого при их потреблении.
Примерами таких пищевых продуктов, каждый из которых содержит γ-Glu-Nva и травы и/или специи, полученные из растений, принадлежащих к Labiatae, являются соусы, заправки для салатов, супы, закусочные пищевые продукты или продукты переработки мяса (такие как ветчина и колбаса).
Более того, если рассматривать настоящее изобретение с другой точки зрения, пищевые продукты, содержащие «мисо», также являются предпочтительными по изобретению в качестве пищевой композиции, содержащей агент для придания кокуми или комплексный агент для придания кокуми по изобретению. Примеры такого «мисо» включают «мисо», полученное с использованием осоложенного риса, солода (осоложенного ячменя) и осоложенных соевых бобов, также как смешанное «мисо», полученное смешиванием по меньшей мере двух из них, однако настоящее изобретение не является ограниченным этими конкретными «мисо». Такие пищевые продукты, содержащие «мисо», не являются ограниченными конкретными пищевыми продуктами, поскольку они содержат «мисо», но можно перечислить, например, супы «мисо», различные виды переработанных пищевых продуктов, содержащих «мисо» в качестве приправы, приправленное «мисо», содержащие «мисо» супы для китайской лапши и содержащие «мисо» соусы. В случае пищевых продуктов, содержащих «мисо» и агент для придания кокуми или комплексный агент для придания кокуми по изобретению, предпочтительными являются вышеуказанные содержащие «мисо» пищевые продукты, в которых «мисо» или т.п. присутствует в количестве в диапазоне от 0,01 до 99,9 вес.%, как выражено в отношении содержания в них сухого вещества, при их потреблении.
Кроме того, если рассматривать настоящее изобретение с другой точки зрения, также предпочтительными в качестве пищевых композиций, содержащих агент для придания кокуми или комплексный агент для придания кокуми по изобретению, являются содержащие томаты пищевые продукты. Такие содержащие томаты пищевые продукты не являются ограниченными конкретными пищевыми продуктами, поскольку они содержат томаты, но их конкретные примеры включают томатные соусы, томатный кетчуп, томатные пасты и множество содержащих томат супов. В случае пищевых продуктов, содержащих томат и агент для придания кокуми или комплексный агент для придания кокуми по изобретению, вышеуказанные содержащие томат пищевые продукты предпочтительно содержат томат или т.п. в количестве в диапазоне от 0,01 до 99,9 вес.%, как выражено в отношении содержания в них сухого вещества, наблюдаемого при их потреблении.
γ-Glu-Nva, используемый по изобретению, и аминокислоты или пептиды, используемые в комбинации с ним, могут подобным образом включать аминокислоты или пептиды в форме их солей. Если γ-Glu-Nva, используемый по изобретению, и аминокислоты или пептиды, используемые в комбинации с ним, присутствуют в форме их солей, соли не являются ограниченными конкретными солями, пока они представляют собой фармакологически пригодные и растворимые соли, и их конкретные примеры включают соли аммония, соли щелочных металлов, таких как натрий и калий, соли щелочноземельных металлов, таких как кальций и магний, соли алюминия, соли цинка, соли органических аминов, таких как триэтиламин, этаноламин, морфолин, пирролидин, пиперидин, пиперазин и дициклогексиламин, и соли основных аминокислот, таких как альгинин и лизин, и кислых групп, таких как карбоксильные группы. Более того, примеры вышеуказанных соединений подобным образом включают соли неорганических кислот, таких как соляная кислота, серная кислота, фосфорная кислота, азотная кислота и бромистоводородная кислота; соли органических кислот, таких как уксусная кислота, лимонная кислота, бензойная кислота, малеиновая кислота, фумаровая кислота, виннокаменная кислота, янтарная кислота, дубильная кислота, масляная кислота, hibenzoic acid, памовая кислота, энантовая кислота, декановая кислота, теоклиновая кислота, салициловая кислота, молочная кислота, щавелевая кислота, миндальная кислота и яблочная кислота; и соли органических сульфоновых кислот, таких как метансульфоновая кислота, бензолсульфоновая кислота и п-толуолсульфоновая кислота, с основными группами соединений.
Агент для придания кокуми, пищевую композицию или комплексный агент для придания кокуми по изобретению можно использовать в любой форме, такой как сухие порошки, пасты и растворы, без какого-либо ограничения их физических свойств.
Агент для придания кокуми, пищевую композицию или комплексный агент для придания кокуми по изобретению можно использовать, для включения, например, во множество пищевых продуктов и напитков, таких как пищевые продукты, напитки и приправы.
Если агент для придания кокуми, пищевую композицию или комплексный агент для придания кокуми по изобретению используют для включения, например, во множество пищевых продуктов и напитков, таких как пищевые продукты, напитки и приправы, окончательное количество γ-Glu-Nva и окончательное количество аминокислоты или пептида, используемого в комбинации с ним, не является ограниченным каким-либо конкретным количеством, пока оно может обеспечивать достижение желательных эффектов по изобретению, однако, каждое из количества γ-Glu-Nva и/или количества аминокислоты или пептида попадает в диапазон от приблизительно 0,1 млр.д. до 99,9 вес.%, и предпочтительно, от приблизительно 1 млр.д. до 10 вес.% и более предпочтительно, от приблизительно 0,01 м.д. до 1 вес.% от общего веса каждого соответствующего пищевого продукта, напитка, приправы или т.п.
Множество пищевых продуктов, таких как пищевые продукты, напитки или приправы, каждый из которых содержит включенный агент для придания кокуми, пищевую композицию или комплексный агент для придания кокуми по изобретению, может дополнительно содержать, например, любой твердый или жидкий носитель и/или пригодные ингредиенты приправы, пригодные для пищевых продуктов и напитков.
В качестве вышеуказанных носителей можно перечислить, например, глюкозу, лактозу, сахарозу, крахмал, маннит, декстрин, глицериды жирных кислот, полиэтиленгликоль, гидроксиэтилкрахмал, этиленгликоль, сложные эфиры жирных кислот и полиоксиэтиленсорбитана, желатин, альбумин, аминокислоты, воду и физиологический солевой раствор.
Вышеуказанные ингредиенты для приправы не являются ограниченными каким-либо одним конкретным ингредиентом и могут представлять собой любые ингредиенты, в настоящее время используемые в данной области, однако их конкретными примерами являются примеры, уже описанные выше.
Содержание вышеуказанных носителей, других ингредиентов приправы или т.п. не является ограниченным конкретным содержанием.
Среди вышеуказанных ингредиентов приправ, дрожжевой экстракт не является конкретно ограниченным какими-либо из клеточных тел микроорганизмов, из которых происходит экстракт, условиями культивирования микроорганизмов и способами его экстракции, и соответственно, любой дрожжевой экстракт можно использовать в продуктах по изобретению Более того, эти дрожжевые экстракты могут представлять собой экстракты, которые подвергали, например, тепловой обработке, обработке ферментом, обработке концентрированием и/или обработке для превращения экстракта в порошок.
Агент для придания кокуми, пищевую композицию или комплексный агент для придания кокуми по изобретению можно использовать в любой форме, такой как сухие порошки, пасты и растворы, без какого-либо ограничения их физических свойств.
Агент для придания кокуми, пищевую композицию или комплексный агент для придания кокуми по изобретению можно использовать для включения, например, во множество пищевых продуктов и напитков, таких как пищевые продукты, напитки и приправы.
Настоящее изобретение относится также к способу получения множества пищевых продуктов и напитков, включающему стадию добавления ко множеству полуфабрикатов, используемых для получения различных видов пищевых продуктов и напитков, γ-Glu-Nva таким образом, что полученные пищевые продукты и напитки содержат γ-Glu-Nva в количестве в диапазоне от 1 млр.д. до 99,9 вес.%. В этом отношении, различные виды пищевых продуктов и напитков предпочтительно представляют собой пищевые продукты с пониженным содержанием соли.
Настоящее изобретение также относится к способу получения множества пищевых продуктов или напитков, включающему стадию включения пищевой композиции по изобретению в полуфабрикаты, используемые для получения различных видов пищевых продуктов или напитков. В этой связи, различные виды пищевых продуктов и напитков предпочтительно представляют собой пищевые продукты с пониженным содержанием соли.
Что касается способа получения полуфабриката, используемого для получения других пищевых продуктов или напитков по изобретению, является предпочтительным, чтобы способ включал стадии добавления усилителя вкуса, состоящего из γ-Glu-Nva, к ингредиенту пищевого продукта (такому как придающий умами ингредиент, гидролизаты белков или травы, и/или специи) во время их смешивания и, в зависимости от необходимости, дополнительной кулинарной обработки полученной смеси пищевых ингредиентов, чтобы таким образом получать пищевые продукты или напитки, или полуфабрикаты для их получения.
В этом отношении, стадия добавления усилителя вкуса, состоящего из γ-Glu-Nva, к ингредиенту пищевого продукта, предпочтительно включает стадию контроля концентрации γ-Glu-Nva в полуфабрикате, используемом для получения пищевого продукта или напитка, на уровне в диапазоне от 0,005 до 600000 м.д. и предпочтительно, от 0,1 до 100000 м.д.
Кроме того, является также предпочтительным, чтобы способ дополнительно включал стадию добавления полуфабриката для получения пищевых продуктов или напитков к другим пищевым ингредиентам (таким как сельскохозяйственные продукты, морепродукты, продукты животноводства, молочные продукты или продукты их переработки) при контроле концентрации γ-Glu-Nva в полученных пищевых продуктах или напитках на уровне от 0,005 до 30 м.д. и предпочтительно, от 0,05 до 10 м.д.
Более того, стадия добавления усилителя вкуса, состоящего из γ-Glu-Nva, к ингредиенту пищевого продукта во время их смешивания, предпочтительно включает стадию контроля концентрации γ-Glu-Nva в полученных пищевых продуктах или напитках на уровне от 0,005 до 30 м.д. и предпочтительно, от 0,05 до 10 м.д.
В вышеуказанном способе получения, является предпочтительным, чтобы пищевые продукты или напитки представляли собой пищевые продукты или напитки, содержащие травы и/или специи, полученные из растений, принадлежащих к Labiatae (такие как соусы, заправки для салатов, супы, закусочные пищевые продукты или продукты переработки мяса). В этом случае, каждый пищевой продукт или напиток предпочтительно содержит от 0,005 до 30 м.д. γ-Glu-Nva; от 0,01 до 10 вес.% трав и/или специй, полученных из растений, принадлежащих к Labiatae, и другие пищевые ингредиенты.
Более того, в вышеуказанном способе получения, является предпочтительным, чтобы пищевой продукт или напиток представлял собой пищевой продукт или напиток, содержащий «мисо». В этом случае, каждый продукт или напиток предпочтительно содержит от 0,02 до 80 м.д. γ-Glu-Nva; от 0,01 to 99,9 вес.% (или более предпочтительно, от 0,1 до 90,0 вес.%) «мисо»; и другие пищевые ингредиенты.
Более того, в вышеуказанном способе получения, является предпочтительным, чтобы пищевой продукт или напиток представлял собой пищевой продукт или напиток, содержащий томат. В этом случае, каждый продукт или напиток предпочтительно содержит от 0,02 до 80 м.д. γ-Glu-Nva; от 0,01 до 99,9 вес.% (или более предпочтительно, от 0,1 до 90,0 вес.%) томата; и другие пищевые ингредиенты.
Более того, настоящее изобретение также относится к способу усиления вкуса пищевых продуктов или напитков, включающему стадию добавления композиции, содержащей γ-Glu-Nva, к пищевым продуктам или напиткам в количестве в диапазоне от 0,01 до 50 вес.%. В этой связи, является предпочтительным, чтобы усиление вкуса представляло собой стадию придания кокуми.
Настоящее изобретение описано в настоящем документе более подробно со ссылкой на следующие примеры, однако, настоящее изобретение совсем не является ограниченным этими конкретными примерами.
Пример
(Пример синтеза 1): Синтез γ-Glu-Nva (γ-L-глутамил-L-норвалина)
В метиленхлориде (CH2Cl2, 60 мл) растворяли Boc-Nva·DCHA (т-бутоксикарбонил-L-норвалин·соль дициклогексил-аммония, 3,39 г, 25 8,49 мМ) и бензиловый спирт (1,01 г, 9,34 мМ). Затем к полученному раствору добавляли DMAP (4-диметиламинопиридин, 0,21 г, 0,2 экв., 1,70 мМ) и WSC·HCl (гидрохлорид 1-этил-3-(3-диметиламинопропил)-карбодиимида, 1,81 г, 1,1 экв., 9,34 мМ), при поддержании реакционного раствора при 0°C. Температуру реакционного раствора постепенно повышали и перемешивали при комнатной температуре в течение ночи (16 часов). Затем реакционный раствор концентрировали под пониженным давлением, к полученному осадку добавляли этилацетат (500 мл), температуру органической фазы повышали до 60°C, затем ее промывали водой (100 мл), дважды 5% водным раствором лимонной кислоты (100 мл), насыщенным раствором поваренной соли (100 мл), дважды 5% водным раствором гидрокарбоната натрия (100 мл) и насыщенным раствором поваренной соли (100 мл), и затем органическую фазу сушили над безводным сульфатом магния. Сульфат магния удаляли фильтрацией, и фильтрат концентрировали под пониженным давлением. Кристаллы преципитировали в ходе концентрации под пониженным давлением и таким образом, кристаллы собирали фильтрацией с последующим их высушиванием под пониженным давлением для получения кристаллов Boc-Nva-OBzl (2,41 г, 7,83 мМ).
К Boc-Nva-OBzl, объединенному с отдельно синтезированным Boc-Nva-OBzl (2,68 г, 8,72 мМ), добавляли раствор 4 Н HCl/диоксана (43,6 мл), и смесь перемешивали при комнатной температуре в течение одного часа. Реакционную систему концентрировали под пониженным давлением для удаления диоксана, к полученному осадку добавляли н-гексан (30 мл) и затем полученную смесь концентрировали под пониженным давлением. В этом отношении, последние две стадии повторяли три раза, чтобы таким образом получить H-Nva-OBzl·HC1 с количественным выходом.
Полученный H-Nva-OBzl·HC1 растворяли в метиленхлориде (60 мл), и полученный реакционный раствор поддерживали при 0°C. К реакционному раствору добавляли Z-Glu-OBzl (бензиловый сложный эфир N-α-карбобензокси-L-глутаминовой кислоты, 3,24 г, 8,72 мМ), триэтиламин (1,34 мл, 1,1 экв., 9,59 мМ), HOBt·H2O (1-гидроксибензотриазолгидрат (1,47 г, 1,1 экв., 9,59 мМ) и WSC·HCl (1,84 г, 1,1 экв., 9,59 мМ). Температуру реакционного раствора постепенно повышали и перемешивали при комнатной температуре в течение ночи (16 часов). Затем реакционный раствор концентрировали под пониженным давлением, к полученному осадку добавляли этилацетат (200 мл), и затем органическую фазу промывали водой (80 мл), дважды 5% водным раствором лимонной кислоты (80 мл), насыщенным раствором поваренной соли (80 мл), дважды 5% водным раствором гидрокарбоната натрия (80 мл) и насыщенным раствором поваренной соли (80 мл), и затем органическую фазу сушили над безводным сульфатом магния. Сульфат магния удаляли фильтрацией, и фильтрат концентрировали под пониженным давлением. Полученный осадок перекристаллизовывали из этилацетата и н-гексана, полученные таким образом кристаллы собирали фильтрацией и высушивали под пониженным давлением для получения кристаллов Z-Glu(Nva-OBzl)-OBzl (4,06 г).
К смешанному раствору этанола (150 мл) и воды (30 мл) добавляли Z-Glu(Nva-OBzl)-OBzl (4,06 г) и 5% палладий на углероде (5% палладий/углерод, 0,70 г), и реакцию каталитического восстановления проводили при 50°C в течение ночи (14 часов) в атмосфере газообразного водорода. В реакционную систему добавляли воду (50 мл) малыми порциями во время реакции. Палладий/углерод удаляли из реакционной системы фильтрацией, и полученный фильтрат концентрировали под пониженным давлением. Осадок перекристаллизовывали из небольшого количества воды и этанола, чтобы таким образом получить γ-Glu-Nva (1,50 г) в виде белых кристаллов. Затем кристаллы растворяли в воде (100 мл) с последующей лиофилизацией раствора для получения γ-Glu-Nva (1,27 г, 5,16 мМ) в виде белого порошка. Характерные значения для него приведены ниже:
ESI-MS: (M+H)+=247,1; (M-H)-=245,2.
1H-ЯМР (400 МГц, D2O): δ (ppm): 0,77 (3H, т, J=7,3 Гц), 1,18-1,33 (2H, м), 1,50-1,73 (2H, м), 1,97-2,08 (2H, м), 2,36 (2H, дд, J=,6 и 8,4 Гц), 3,68 (1H, т, J=8,4Hz), 4,15 (1H, дд, J=5,2 и 8,8 Гц).
(Пример синтеза 2): Синтез γ-Glu-Nle (γ-L-глутамил-L-норлейцин) (Сравнительный пример)
В метиленхлориде (CH2Cl2, 30 мл), растворяли Boc-Nle·0,2 AcOEt (т-бутоксикарбонил-L-норлейцин·0,2 М этилацетат, 0,51 г, 2,00 мМ) и бензиловый спирт (0,24 г, мМ). Затем к полученному раствору добавляли DMAP (4-диметиламинопиридин, 0,05 г, 0,2 экв., 0,40 мМ) и WSC·HCl (гидрохлорид 1-этил-3-(3-диметиламинопропил)-карбодиимида, 0,43 г, 1,1 экв., 2,20 мМ), при поддержании реакционного раствора при 0°C. Температуру реакционного раствора постепенно повышали и перемешивали при комнатной температуре в течение ночи (16 часов). Затем реакционный раствор концентрировали под пониженным давлением, к полученному осадку добавляли этилацетат (100 мл), затем органическую жидкую фазу промывали водой (30 мл), дважды 5% водным раствором лимонной кислоты (30 мл), насыщенным раствором поваренной соли (30 мл), дважды 5% водным раствором гидрокарбоната натрия (30 мл) и затем насыщенным раствором поваренной соли (30 мл), и затем органическую фазу сушили над безводным сульфатом магния. Сульфат магния удаляли фильтрацией, и фильтрат концентрировали под пониженным давлением, чтобы таким образом получить Boc-Nle-OBzl (0,61 г, 1,90 мМ) в виде масляного продукта.
К Boc-Nle-OBzl (0,81 г, 1,90 мМ) добавляли раствор 4 Н HCl/диоксана (9,40 мл) и смесь перемешивали при комнатной температуре в течение одного часа. Реакционную систему концентрировали под пониженным давлением для удаления диоксана. К полученному осадку добавляли н-гексан (6,0 мл), и затем полученную смесь концентрировали под пониженным давлением. В этой связи, последние две стадии повторяли три раза, чтобы таким образом получить H-Nle-OBzl·HCl с количественным выходом.
Полученный H-Nle-OBzl·HC1 растворяли в метиленхлориде (30 мл), и полученный реакционный раствор поддерживали при 0°C. К реакционному раствору добавляли Z-Glu-OBzl (бензиловый сложный эфир N-α-карбобензокси-L-глутаминовой кислоты, 0,70 г, 1,90 мМ), триэтиламин (0,29 мл, 1,1 экв., 2,10 мМ), HOBt·H2O (1-гидроксибензотриазолгидрат (0,32 г, 1,1 экв., 2,10 мМ) и WSC·HC1 (0,41 г, 1,1 экв., 2,10 мМ). Температуру реакционного раствора постепенно повышали и перемешивали при комнатной температуре в течение ночи (16 часов). Затем реакционную смесь концентрировали под пониженным давлением, к полученному осадку добавляли этилацетат (100 мл), и затем органическую фазу промывали водой (30 мл), дважды 5% водным раствором лимонной кислоты (30 мл), насыщенным раствором поваренной соли (30 мл), дважды 5% водным раствором гидрокарбоната натрия (30 мл) и насыщенным раствором поваренной соли (30 мл), и затем органическую фазу сушили над безводным сульфатом магния. Сульфат магния удаляли фильтрацией, и фильтрат концентрировали под пониженным давлением. Полученный осадок перекристаллизовывали из этилацетата и н-гексана, полученные таким образом кристаллы собирали фильтрацией и высушивали под пониженным давлением для получения Z-Glu(Nle-OBzl)-OBzl (0,91 г).
К смешанному раствору этанола (60 мл) и воды (10 мл) добавляли Z-Glu(Nle-OBzl)-OBzl (4,05 г) и 5% палладий на углероде (5% палладий/углерод, 0,40 г), и реакцию каталитического восстановления проводили при 50°C в течение ночи (14 часов) в атмосфере газообразного водорода. В реакционную систему добавляли воду (10 мл) малыми порциями во время реакции. Палладий/углерод удаляли из реакционной системы фильтрацией, и полученный фильтрат концентрировали под пониженным давлением. Осадок перекристаллизовывали из небольшого количества воды и этанола, чтобы таким образом получить γ-Glu-Nle (0,29 г) в виде гигроскопичных кристаллов. Затем кристаллы растворяли в воде (30 мл) с последующей лиофилизацией раствора для получения γ-Glu-Nle (0,13 г, 0,50 мМ) в виде белого порошка. Характерные значения для него приведены ниже:
ESI-MS: (M+H)+=261,1; (M-H)-=259,0.
1H-ЯМР (400 МГц, D2O): δ (ppm): 0,79 (3H, т, J=7,1 Гц), 1,18-1,30 (4H, м), 1,60-1,70 (1H, м), 1,70-1,80 (1H, м), 2,04-2,10 (2H, м), 2,38-2,44 (2H, м), 3,73 (1H, т, J=6,3 Гц), 4,19 (1H, дд, J=5,0 и 8,8 Гц),
Тестовый пример 1): Получение CaSR-экспрессирующей плазмиды
CaSR-экспрессирующую плазмиду получали согласно следующим способам.
Синтезировали синтетическую олиго-ДНК, используемую для способов ПЦР (т.е. прямой праймер (Последовательность No. 3: ACTAATACGACTCACTATAGGGACCATGGCATTTTATAGCTGCTGCTGG) и обратный праймер (Последовательность No. 4: TTATGAATTCACTACGTTTTCTGTAACAG) на основе последовательности ДНК, зарегистрированной в NCBI (CaSR (кальциевый рецептор): NM_000388, Последовательности No. 1 и 2).
Способы ПЦР осуществляли в условиях, указанных ниже, с использованием кДНК (доступной из компании Clontech), полученной из почки человека в качестве материала, с использованием вышеуказанных праймеров и ДНК-полимеразы Pfu Ultra (доступной из компании Stratagene): реакционную систему обрабатывали при 94°C в течение 3 минут, и затем при 94°C в течение 30 секунд, при 55°C в течение 30 секунд и при 72°C в течение 2 минут, где эти стадии повторяли 35 раз, и в системе проводили конечную реакцию при 72°C в течение 7 минут. Затем реакционную систему подвергали обработке электрофорезом в агарозе в качестве поддержки, агарозу окрашивали средством для окрашивания ДНК, и затем ее облучали лучами ультрафиолетового цвета для детекции, действительно ли кДНК является амплифицированной способами ПЦР или нет. В то же самое время, картину электрофореза сравнивали с маркером ДНК, электрофоретический размер которого известен, чтобы таким образом подтвердить длину цепей продуктов ПЦР.
Плазмидный вектор pBR322 расщепляли рестрикционным ферментом EcoRV (доступным из Tikara Co., Ltd) и фрагмент гена, амплифицированный способами ПЦР, лигировали в плазмидный вектор по участку расщепления, с использованием набора для лигирования (доступного из компании Promega). Клетки Escherichia coli штамма DH5 трансформировали реакционным раствором, с последующим отбором трансформантов, содержащих плазмиду, в которой был клонирован амплифицированный продукт ПЦР, и затем амплифицированный продукт ПЦР подтверждали анализом последовательности ДНК-оснований.
Эту рекомбинантную плазмиду использовали для получения плазмиды, экспрессирующей CaSR человека, hCaSR/pcDNA3.1.
(Тестовый пример 2): Оценка активности агониста CaSR
Клетки 293E (EBNA1-экспрессирующие клетки HEK293, ATCC No. CRL-10852) культивировали в DMEN/Ham's-F12 (содержащей 3,15/мл глюкозы, модифицированной по способу Дульбекко среде Игла, доступной из компании Nakaraitesk), дополненной 10% эмбриональной телячьей сывороткой, в присутствии 200 мкг/мл G418 (доступного из Genetisin). Культивированные клетки инокулировали во флакон F25 при плотности 3x106 клеток/10 мл, флакону позволяли стоять в течение 24 часов в CO2-инкубаторе (5% CO2, 37°C), и затем трансформировали или трансфицировали плазмидой, экспрессирующей CaSR человека hCaSR/pcDNA3.1, с помощью реагента для трансфекции Fugene6 (доступного из компании Roche). Трансфицированную плазмиду поддерживали в CO2-инкубаторе в течение 6-7 часов, затем клетки восстанавливали с использованием содержащей 10% эмбриональную телячью сыворотку DMEM/Ham's-F12, и клетки инокулировали в каждую лунку покрытого поли-D-лизином 96-луночного планшета (BDBiocoat) при плотности 70000 клеток/лунку.
96-луночному планшету позволяли стоять в течение 24 часов в CO2-инкубаторе, затем культуральную среду удаляли из каждой лунки 96-луночного планшета, в который инокулировали клетки, с последующим добавлением в каждую лунку, флуоресцентного индикатора Ca2+ из набора Calcium 4 Assay (доступного из компании Molecular Devices), растворенного в буфере для анализа (содержащем 146 мМ NaCl, 5 мМ KCl, 1 мМ MgSO4, 1 мг/мл глюкозы, 20 мМ HKPES (pH 7,2) и от 0,75 до 1,25 мМ CaCl2), в количестве 200 мкл/лунку, и затем позволяли 96-луночному планшету стоять при 37°C в течение одного часа, и затем при комнатной температуре в течение 10 минут, так что индикатор включался в клетки.
В каждую лунку 96-луночного планшета добавляли каждое тестируемое соединение, растворенное в буфере для анализа, содержащем 0,1% BSA, в количестве 50 мкл/лунку, и затем любые изменения интенсивности мониторировали в течение 3 минут с использованием установки FLEX (доступной из компании Molecular Devices).
(Способ определения EC 50 )
Различие (RFU (Макс-Мин)) между максимальной и минимальной интенсивностями флуоресценции, наблюдаемыми для каждой лунки до и после добавления каждого конкретного тестируемого соединения, определяли посредством автоматического вычисления с использованием установки FLEX. Рассчитывали степень активности, в то время как значение RFU (Макс-Мин), наблюдаемое при добавлении соединения в максимальной концентрации, определяли как 100%, и значение RFU (Макс-Мин), наблюдаемое при использовании буфера для анализа, содержащего 0,1% BSA, свободного от какого-либо тестируемого соединения, определяли как 0%, с последующим подверганием полученных данных процедурам подбора кривых с использованием программного обеспечения для обработки электронных таблиц Xfit или Graph-Pad-Prism, чтобы таким образом определять EC50, которая представляла собой концентрацию соединения при степени активности 50%. Полученные таким образом результаты обобщены в следующей таблице 1.
Кроме того, повторяли такие же способы определения EC50, использованные выше, за исключением использования других дипептидов, как в сравнительных примерах. Полученные таким образом результаты обобщены в следующей таблице 2.
При сравнении с другими дипептидами обнаружили, что γ-Glu-Nva обладает сильной активностью агониста CaSR по сравнению с активностью, наблюдаемой для γ-Glu-Cys. Известно, что пептид с низкой молекулярной массой, обладающей активностью агониста CaSR, является пригодным в качестве агента для придания кокуми (см. Патентный документ 1, указанный выше) и соответственно, предположили, что γ-Glu-Nva способен служить в качестве особенно превосходного агента для придания кокуми.
Пример 1: Оценка активности придания кокуми
В этом примере проверяли γ-Glu-Nva по силе его активности придания кокуми согласно тесту количественной сенсорной оценки.
Этот тест количественной сенсорной оценки проводили следующими способами. Силу активности придания кокуми, наблюдаемой для каждого тестируемого соединения, определяли как значение, наблюдаемое при смешивании от 0,00001 до 0,5 г/дл соответствующего тестируемого соединения с дистиллированной водой, содержащей глутамат натрия (0,05 г/дл), монофосфат инозиновой кислоты (0,05 г/дл) и хлорид натрия (0,5 г/дл). В этой связи, когда для образца показывали кислый характер после растворения тестируемого соединения по сравнению с контролем без тестируемого соединения, значение pH образца доводили, с использованием NaOH, до уровня значения pH (наблюдаемого для контроля) ±0,2 перед практическим использованием образца в оценке. Критерии оценки принимали следующие: контроль: 0 балов: сильный: 3 балла; очень сильный: 5 баллов. Более того, чтобы сделать критерии более ясными, начальный вкус и средний вкус/послевкусие γ-Glu-Val-Gly принимали за 3,0 балла, соответственно. Выставление баллов или классификацию проводили с использованием способа линейной шкалы, и более конкретно, их проводили посредством указания каждого соответствующего балла на прямой линии, на которой были обозначены точки, соответствующие -5~0~5. Дегустаторов для участия в этом тесте определяли как лиц, которые занимались разработкой приправ для пищевых продуктов в течение не менее одного года суммарного периода времени и которые могли судить, что различия в титре между γ-Glu-Cys-Gly и γ-Glu-Val-Gly, добавленными в раствор, обладающий вкусом умами/ соленым вкусом, составляет приблизительно 10 раз (при регулярном подтверждении способности этих лиц). Оценку проводили при n (число участвовавших дегустаторов) = 4. В этой связи, термин «начальный вкус» обозначает развитие вкуса, детектированное на протяжении времени, продолжающегося от 0 до 2 секунд после того, как дегустатор удерживал образец во рту, в то время как термин «средний вкус/послевкусие» обозначает развитие вкуса, детектированное после этого. Для тестируемого соединения показали активность придания кокуми широко по всему вышеуказанному диапазону его добавленных концентраций. Однако результаты, наблюдаемые для его типичных концентраций, обобщены в следующей таблице 3.
Кроме того, γ-Glu-Val-Gly, γ-Glu-Cys, γ-Glu-Val, γ-Glu-Ala и γ-Glu-Ser подобным образом проверяли по их эффекту придания кокуми, такими же способами, как использованные выше. Полученные результаты также перечислены в таблице 3.
Таким образом, обнаружено, что γ-Glu-Nva обладает отличной активностью придания кокуми, и что он также отлично повышает начальный вкус по отношению к развитию вкуса или характеру приправы. Это отличное повышение начального вкуса, наблюдаемое для γ-Glu-Nva, является одним из его необычайно предпочтительных особенностей по сравнению с тем, что наблюдали для γ-Glu-Cys. Более того, γ-Glu-Nva обладает также отличной стабильностью, и это также является предпочтительной особенностью по сравнению с γ-Glu-Cys. Относительно активности придания кокуми, γ-Glu-Nva обладает высоким титром, превосходящим титры общеизвестных дипептидов. Кроме того, γ-Glu-Nva обладает короткой длиной цепи, поскольку он содержит только два аминокислотных остатка. Соответственно, его можно относительно просто получать при низкой стоимости по сравнению с получением любого трипептида, содержащего 3 аминокислотных остатка, и соответственно, агент по изобретению подобным образом обладает достаточными преимуществами с промышленной точки зрения.
Пример 2: Эффект γ-Glu-Nva на базилик
γ-Glu-Nva представляет собой дипептид начального вкуса. Однако обнаружили, что при потреблении дипептида в пищу, он проявляет эффект придания кокуми и действие немного позже по сравнению с общеизвестным дипептидом начального вкуса, обладающим высокими титрами, таким как γ-Glu-Abu и γ-Glu-Val. С другой стороны, обнаружено также, что при сравнении этого дипептида с общепринятыми трипептидами среднего вкуса/послевкусия, такими как γ-Glu-Cys-Gly (глутатион) и γ-Glu-Val-Gly, дипептид может довольно быстро проявлять эффект придания кокуми. Авторы этого изобретения обратили внимание на этот вопрос и провели поиск трав и/или специй, которые можно синхронизировать со временем, в течение которого γ-Glu-Nva может проявлять эффект придания кокуми и активность, чтобы таким образом усиливать вкус первых упомянутых, и авторы изобретения исследовали их подробно. В этой связи, такие характеристики не обнаружены у других γ-Glu пептидов, обладающих сильными эффектом придания кокуми и активностью.
Более конкретно, тест количественной сенсорной оценки проводили следующими способами. Коммерчески доступные типичные травы/специи в порошкообразной форме диспергировали в воде в концентрации 0,5 вес.%, чтобы таким образом получить раствор трав/специй. Этот раствор смешивали с γ-Glu-Nva, γ-Glu-Cys-Gly, или γ-Glu-Abu в качестве тестируемого соединения. Согласно критерию парного сравнения, у дегустаторов требовали сравнительной оценки следующих трех образцов и решения, «какой из них являлся предпочтительным, поскольку мог усиливать вкусоаромат раствора трав/специй без изменения равновесия между ними»: (1) 0,02 вес.% γ-Glu-Cys-Gly, активность придания кокуми которого являлась идентичной 0,00015 вес.% γ-Glu-Nva; (2) 0,00015 вес.% γ-Glu-Abu, количество которого являлось идентичным 0,00015 вес.% γ-Glu-Nva; (3) 0,003 вес.% γ-Glu-Abu, активность придания кокуми которого являлась идентичной активности, наблюдаемой для 0,00015 вес.% γ-Glu-Nva. Дегустаторов для участия в этом тесте определяли как лиц, которые занимались разработкой приправ для пищевых продуктов в течение не менее одного года суммарного периода времени и которые могли судить, что различия в титре между γ-Glu-Cys-Gly и γ-Glu-Val-Gly, добавленными в раствор, обладающий вкусом умами/ соленым вкусом, составляет приблизительно 10 раз (при регулярном подтверждении способности этих лиц). Оценку проводили при N (количество участвовавших дегустаторов)=9.
В следующей таблице 4 показано количество дегустаторов, решивших, что 0,00015 вес.% γ-Glu-Nva являлось «более предпочтительным, поскольку оно могло усиливать вкусоаромат раствора трав/специй без изменения равновесия между ними». Для трав и/или специй, полученных из растений, принадлежащих к Labiatae, определенно показаны желательные эффекты, однако результаты, наблюдаемые для базилика, показаны в качестве их типичного примера.
Из полученных таким образом результатов можно заключить следующее: для γ-Glu-Nva показали заметный эффект того, что он может значимо и сильно усиливать вкусоаромат трав и/или специй, полученных из растений, принадлежащих к Labiatae, даже в случаях, когда титры кокуми идентичны между собой, как в случаях (1) и (3).
N=9
**: Результат показывает, что γ-Glu-Nva является более предпочтительным, поскольку он может усиливать вкусоаромат раствора базилика, принадлежащего к Labiatae, без изменения равновесия между ними, на уровне значимости 1%.
***: Результат показывает, что γ-Glu-Nva является более предпочтительным, поскольку он может усиливать вкусоаромат раствора базилика, принадлежащего к Labiatae, без изменения равновесия между ними, на уровне значимости 5%.
Вышеуказанные результаты ясно указывают на то, что для γ-Glu-Nva показан следующий достаточно заметный эффект: он может «усиливать и делать более благоприятным вкусоаромат трав и/или специй, полученных из растений, принадлежащих к Labiatae, без изменения равновесия между ними», при сравнении с эффектом, наблюдаемым для γ-Glu пептидов, обладающих высокой активностью придания кокуми, таких как γ-Glu-Cys-Gly и γ-Glu-Abu, в концентрациях, способных проявлять такую же активность придания кокуми. Примеры трав и/или специй, полученных из растений, принадлежащих к Labiatae, включают множество растений, в дополнение к печеночнице и базилику, анис, ореган, шалфей, тимьян, мяту японскую, мяту перечную, бергамот, майоран, мяту, лаванду и розмарин, и их широко используют во всем мире, например, в приправах, супах, соусах, переработанных мясных продуктах, готовых и переработанных продуктах и кондитерских изделиях, включая итальянские блюда. Как обсуждали выше, γ-Glu-Nva может позволять улучшение вкуса и вкуса пищевых продуктов, в которых используют травы и/или специи, полученные из растений, принадлежащих к Labiatae, при низкой стоимости, с использованием его в то же время только в следовом количестве, и таким образом, его использование является достаточно предпочтительным с промышленной точки зрения.
Пример 3: Эффект γ-Glu-Nva на «мисо»
γ-Glu-Nva представляет собой дипептид начального вкуса. Однако обнаружили, что при потреблении дипептида в пищу, он проявляет эффект придания кокуми и действие немного позже по сравнению с другим известным дипептидом начального вкуса, обладающим высокими титрами, таким как γ-Glu-Abu и γ-Glu-Val. С другой стороны, обнаружено также, что при сравнении этого дипептида с общепринятыми трипептидами среднего вкуса/послевкусия, такими как γ-Glu-Cys-Gly (глутатион) и γ-Glu-Val-Gly, дипептид может довольно быстро проявлять эффект придания кокуми. Авторы этого изобретения обратили внимание на этот вопрос и провели поиск приправ или подобного, которые можно синхронизировать со временем, в течение которого γ-Glu-Nva может проявлять эффект придания кокуми и активность, чтобы таким образом усиливать вкус первых упомянутых, и авторы изобретения исследовали их подробно. В этой связи, такие характеристики не обнаружены у других γ-Glu пептидов, обладающих сильными эффектом придания кокуми и активностью.
Более конкретно, тест количественной сенсорной оценки проводили следующими способами. Коммерчески доступный «мисо» (ингредиенты: соевые бобы и ячмень) для общепринятого использования диспергировали в горячей воде в концентрации 10,0 вес.%, чтобы таким образом получить раствор «мисо». Этот раствор смешивали с γ-Glu-Nva, γ-Glu-Cys-Gly или γ-Glu-Abu в качестве тестируемого соединения. Согласно способу критерия парного сравнения (парного теста), у дегустаторов требовали сравнительной оценки следующих трех образцов и решения, «какой из них являлся предпочтительным или благоприятным, поскольку мог усиливать вкусоаромат раствора «мисо» без изменения равновесия между ними»: (1) 0,02 вес.% γ-Glu-Cys-Gly, активность придания кокуми которого являлась идентичной 0,0001 вес.% γ-Glu-Nva; (2) 0,0004 вес.% γ-Glu-Abu, количество которого являлось идентичным 0,0004 вес.% γ-Glu-Nva; (3) 0,003 вес.% γ-Glu-Abu, активность придания кокуми которого являлась идентичной активности, наблюдаемой для 0,0004 вес.% γ-Glu-Nva. Дегустаторов для участия в этом тесте определяли как лиц, которые занимались разработкой приправ для пищевых продуктов в течение не менее одного года суммарного периода времени и которые могли судить, что различия в титре между γ-Glu-Cys-Gly и γ-Glu-Val-Gly, добавленными в раствор, обладающий вкусом умами/соленым вкусом, составляет приблизительно 10 раз (при регулярном подтверждении способности этих лиц). Оценку проводили при N (количество участвовавших дегустаторов)=9.
В следующей таблице 5 показано количество дегустаторов, решивших, что 0,0004 вес.% γ-Glu-Nva являлось «более предпочтительным, поскольку оно могло усиливать вкусоаромат раствора «мисо» без изменения равновесия между ними».
Из полученных таким образом результатов можно заключить следующее: для γ-Glu-Nva показали заметный эффект того, что он может значимо и сильно усиливать вкусоаромат «мисо», даже в случаях, когда титры кокуми были идентичны между собой, как в случаях (1) и (3).
N=9
**: Результат показывает, что γ-Glu-Nva является более предпочтительным, поскольку он может усиливать вкусоаромат раствора «мисо», без изменения равновесия между ними, на уровне значимости 5%.
***: Результат показывает, что γ-Glu-Nva является более предпочтительным, поскольку он может усиливать вкусоаромат раствора «мисо», без изменения равновесия между ними, на уровне значимости 1%.
Вышеуказанные результаты ясно указывают на то, что для γ-Glu-Nva показан следующий достаточно заметный эффект: он может «усиливать и делать более благоприятным вкусоаромат «мисо» без изменения равновесия между ними», при сравнении с эффектом, наблюдаемым для γ-Glu пептидов, обладающих высокой активностью придания кокуми, таких как γ-Glu-Cys-Gly и γ-Glu-Abu, в концентрациях, способных проявлять такую же активность придания кокуми, «мисо» широко используют, например, в приправах, супе или бульоне, соусах и готовых и переработанных продуктах. Как обсуждали выше, γ-Glu-Nva может позволять улучшение вкуса и вкуса пищевых продуктов, в которых используют «мисо», при низкой стоимости, с использованием его в то же время только в следовом количестве и таким образом, его использование является достаточно предпочтительным с промышленной точки зрения.
Пример 4: Эффект γ-Glu-Nva на томатный кетчуп
γ-Glu-Nva представляет собой дипептид начального вкуса. Однако обнаружили, что при потреблении дипептида в пищу, он проявляет эффект придания кокуми и действие немного позже по сравнению с другим известным дипептидом начального вкуса, обладающим высокими титрами, таким как γ-Glu-Abu и γ-Glu-Val. С другой стороны, обнаружено также, что при сравнении этого дипептида с общепринятыми трипептидами среднего вкуса/послевкусия, такими как γ-Glu-Cys-Gly (глутатион) и γ-Glu-Val-Gly, дипептид может довольно быстро проявлять эффект придания кокуми. Авторы этого изобретения обратили внимание на этот вопрос и провели поиск приправ или подобного, которые можно синхронизировать со временем, в течение которого γ-Glu-Nva может проявлять эффект придания кокуми и активность, чтобы таким образом усиливать вкус первых упомянутых, и авторы изобретения исследовали их подробно. В этой связи, такие характеристики не обнаружены у других γ-Glu пептидов, обладающих сильными эффектом придания кокуми и активностью.
Более конкретно, тест количественной сенсорной оценки проводили следующими способами. Коммерчески доступный томатный кетчуп для общепринятого использования диспергировали в горячей воде в концентрации 33,3 вес.%, чтобы таким образом получить раствор томатного кетчупа. Этот раствор смешивали с γ-Glu-Nva, γ-Glu-Cys-Gly или γ-Glu-Abu в качестве тестируемого соединения. Согласно способу критерия парного сравнения (парного теста), у дегустаторов требовали сравнительной оценки следующих трех образцов и решения, «какой из них являлся предпочтительным или благоприятным, поскольку мог усиливать вкусоаромат раствора томатного кетчупа без изменения равновесия между ними»: (l) 0,02 вес.% γ-Glu-Cys-Gly, активность придания кокуми которого являлась идентичной 0,0004 вес.% γ-Glu-Nva; (2) 0,0004 вес.% γ-Glu-Abu, количество которого являлось идентичным 0,0004 вес.% γ-Glu-Nva; (3) 0,003 вес.% γ-Glu-Abu, активность придания кокуми которого являлась идентичной активности, наблюдаемой для 0,0004 вес.% γ-Glu-Nva. Дегустаторов для участия в этом тесте определяли как лиц, которые занимались разработкой приправ для пищевых продуктов в течение не менее одного года суммарного периода времени и которые могли судить, что различия в титре между γ-Glu-Cys-Gly и γ-Glu-Val-Gly, добавленными в раствор, обладающий вкусом умами/ соленым вкусом, составляет приблизительно 10 раз (при регулярном подтверждении способности этих лиц). Оценку проводили при N (количество участвовавших дегустаторов)=9.
В следующей таблице 6 показано количество дегустаторов, решивших, что 0,0004 вес.% γ-Glu-Nva являлось «более предпочтительным, поскольку оно могло усиливать вкусоаромат раствора томатного кетчупа без изменения равновесия между ними». Для других соусов или подобного, содержащих томат в качестве ингредиента, определенно показаны желательные эффекты. Однако результаты, наблюдаемые для томатного кетчупа, показаны в таблице 6 в качестве их типичного примера.
Из полученных таким образом результатов можно заключить следующее: для γ-Glu-Nva показали заметный эффект того, что он может значимо и сильно усиливать вкусоаромат томата, даже в случаях, когда титры кокуми были идентичны между собой, как в случаях (1) и (3).
N=9
**: Результат показывает, что γ-Glu-Nva является более предпочтительным, поскольку он может усиливать вкусоаромат раствора томатного кетчупа, без изменения равновесия между ними, на уровне значимости 1%.
Вышеуказанные результаты ясно указывают на то, что для γ-Glu-Nva показан следующий достаточно заметный эффект: он может «усиливать и делать более благоприятным томатный вкусоаромат, например, приправ и соусов, содержащих томат, без изменения равновесия между ними», при сравнении с эффектом, наблюдаемым для γ-Glu пептидов, обладающих высокой активностью придания кокуми, таких как γ-Glu-Cys-Gly и γ-Glu-Abu, в концентрациях, способных проявлять такую же активность придания кокуми. Томат широко используют, например, в приправах, супе или бульоне, соусах и готовых и переработанных продуктах. Как обсуждали выше, γ-Glu-Nva может позволять улучшение вкуса и вкуса пищевых продуктов, в которых используют томат, при низкой стоимости, с использованием его в то же время только в следовом количестве и таким образом, его использование является предпочтительным с точки зрения производства.
| название | год | авторы | номер документа |
|---|---|---|---|
| АГЕНТ ДЛЯ ПРИДАНИЯ КОКУМИ | 2010 |
|
RU2532106C2 |
| ПРИМЕНЕНИЕ ПЕПТИДОВ ДЛЯ ПРИДАНИЯ КОКУМИ | 2010 |
|
RU2536934C2 |
| ПРОИЗВОДНЫЕ ЛАНТИОНИНА | 2010 |
|
RU2518890C2 |
| СОЕДИНЕНИЯ, МОДУЛИРУЮЩИЕ АКТИВНОСТЬ КАЛЬЦИЙЧУВСТВИТЕЛЬНЫХ РЕЦЕПТОРОВ, ДЛЯ МОДУЛЯЦИИ ВКУСА КОКУМИ И КОРМОВЫЕ ПРОДУКТЫ ДЛЯ ДОМАШНИХ ЖИВОТНЫХ, СОДЕРЖАЩИЕ ИХ | 2017 |
|
RU2759563C2 |
| ДРОЖЖЕВОЙ ЭКСТРАКТ, СОДЕРЖАЩИЙ ГАММА-Glu-X ИЛИ ГАММА-Glu-X-Gly, И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2010 |
|
RU2496864C2 |
| АРОМАТИЗИРУЮЩАЯ КОМПОЗИЦИЯ И ПИЩЕВЫЕ КОМПОЗИЦИИ, СОДЕРЖАЩИЕ ЕЕ | 2014 |
|
RU2662770C2 |
| СОЕДИНЕНИЯ, МОДУЛИРУЮЩИЕ АКТИВНОСТЬ РЕЦЕПТОРОВ GPR92, И КОРМОВЫЕ ПРОДУКТЫ ДЛЯ ДОМАШНИХ ЖИВОТНЫХ, СОДЕРЖАЩИЕ ИХ | 2019 |
|
RU2807217C2 |
| ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ НА ОСНОВЕ α-ЦИКЛОДЕКСТРИНА ДЛЯ ПЕРОРАЛЬНОГО ВВЕДЕНИЯ АНАЛОГОВ РИЛИЗИНГ-ГОРМОНА ЛЮТЕИНИЗИРУЮЩЕГО ГОРМОНА (LH-RH) | 1999 |
|
RU2214270C2 |
| ФОСФОРИЛИРОВАННЫЕ ПОЛИМЕРЫ И ИХ КОНЪЮГАТЫ | 1999 |
|
RU2202563C2 |
| ПЕПТИДНЫЕ ВЕКТОРЫ | 2004 |
|
RU2361876C2 |










Изобретение относится к области биотехнологии, конкретно к агенту для придания кокуми, и может быть использовано в пищевой промышленности. Изобретение относится также к пищевой композиции, содержащей травы и/или специи, полученные из растений, принадлежащих к Labiatae, «мисо» или томат, способу получения пищевого продукта, включающему стадию добавления агента для придания кокуми к пищевым ингредиентам, пищевому продукту, полученному вышеуказанным способом, и способу усиления вкуса и/или запаха пищевого продукта с использованием агента для придания кокуми. Изобретение позволяет получить агент для придания кокуми γ-Glu-Nva, который проявляет повышенную активность CASR по сравнению с известными аналогами и обладает улучшенным эффектом придания кокуми. 7 н. и 13 з.п. ф-лы, 1 ил., 6 табл., 4 пр.
1. Агент для придания кокуми, состоящий из γ-Glu-Nva.
2. Пищевая композиция, содержащая от 0,0000005 до 0,003 вес.% γ-Glu-Nva; от 0,01 до 10 вес.% трав и/или специй, полученных из растений, принадлежащих к Labiatae; и любые другие пищевые ингредиенты.
3. Пищевая композиция, содержащая от 0,000002 до 0,008 вес.% γ-Glu-Nva; от 0,01 до 99,9 вес.% «мисо»; и любые другие пищевые ингредиенты, из расчета на 100 весовых частей пищевой композиции.
4. Пищевая композиция, содержащая от 0,000002 до 0,008 вес.% γ-Glu-Nva; от 0,01 до 99,9 вес.% томата; и любые другие пищевые ингредиенты, из расчета на 100 весовых частей пищевой композиции.
5. Способ получения пищевого продукта, включающий стадии:
добавления агента для придания кокуми, состоящего из γ-Glu-Nva, к другим пищевым ингредиентам, при смешивании их вместе; и
если требуется, кулинарной обработки полученной смеси пищевых ингредиентов.
6. Способ по п.5, в котором пищевой продукт содержит траву и/или специю, полученную из растения, принадлежащего к Labiatae.
7. Способ по п.5, в котором указанные пищевые ингредиенты включают «мисо».
8. Способ по п.5, в котором указанные пищевые ингредиенты включают томат.
9. Способ по п.5, в котором указанный продукт находится в форме напитка.
10. Способ по п.5, в котором указанный продукт представляет собой полуфабрикат для получения пищевого продукта.
11. Способ по п.5, в котором указанный продукт представляет собой полуфабрикат для получения пищевого продукта в форме напитка.
12. Способ по любому из пп.5-11, в котором стадия добавления агента для придания кокуми, состоящего из γ-Glu-Nva, к пищевым ингредиентам при смешивании их вместе включает стадию контроля концентрации γ-Glu-Nva в полуфабрикате пищевого продукта на уровне от 0,0000005 до 60 вес.%.
13. Способ по п.12, дополнительно включающий стадию добавления полученного полуфабриката к другим пищевым ингредиентам при контроле концентрации γ-Glu-Nva в полученном пищевом продукте на уровне от 0,0000005 до 0,003 вес.%.
14. Способ по любому из пп.5-11, в котором стадия добавления агента для придания кокуми, состоящего из γ-Glu-Nva, к пищевым ингредиентам при смешивании их вместе включает стадию контроля концентрации γ-Glu-Nva в полученном пищевом продукте, включая пищевой продукт в форме напитка, на уровне от 0,0000005 до 0,003 вес.%.
15. Пищевой продукт, полученный способом по любому из пп.5-14.
16. Пищевой продукт по п.15, который находится в форме напитка.
17. Пищевой продукт по п.15, который представляет собой полуфабрикат для получения пищевого продукта.
18. Пищевой продукт по п.15, который представляет собой полуфабрикат для получения пищевого продукта в форме напитка.
19. Способ усиления вкуса и/или запаха пищевого продукта, включающий стадию добавления агента для придания кокуми по п.1 или пищевой композиции по любому из пп.2-4, содержащей γ-Glu-Nva, в пищевой продукт.
20. Способ по п.19, в котором указанный продукт находится в форме напитка.
| US 2009239310 A1, 24.09.2009 | |||
| БЕСПРОВОДНАЯ ДАТЧИКОВАЯ СИСТЕМА И СПОСОБ ЕЕ ИСПОЛЬЗОВАНИЯ | 2014 |
|
RU2686805C2 |
| УСТРОЙСТВО ДЛЯ УДЕРЖАНИЯ И СОХРАНЕНИЯ СТЕКЛЯННЫХ ИЗДЕЛИЙ | 2015 |
|
RU2686795C2 |
| RU 2006138600 A, 27.05.2008 | |||
| RU 2008124153 A, 20.12.2009 | |||
Авторы
Даты
2014-11-10—Публикация
2010-12-28—Подача