Настоящее изобретение относится к области фармации. Более конкретно изобретение относится к применению α-циклодекстрина или его производных для получения фармацевтических композиций для перорального введения пептидных аналогов LH-RH (рилизинг-гормона лютеинизирущего гормона). Изобретение относится также к пероральным фармацевтическим композициям, содержащим пептидные аналоги LH-RH в комбинации с α-циклодекстрином.
Природные и модифицированные циклодекстрины (CDs) являются хорошо известными ингредиентами, применяемыми в самых разнообразных фармацевтических составах, обладающих преимуществом в одном или нескольких своих свойств, относящихся к растворению препарата и его стабилизации (Loftsson and Brewster, 1996, J. Pharm. Sci. , 85 (10):1017-1025) или к общему улучшению доставки препарата in vivо (Rajewski and Stella, 1996, J. Pharm. Sci., 85 (11): 1142-1169). Циклодекстрины представляют собой циклические олигосахариды, содержащие, по меньшей мере, шесть остатков α-D-(+)-глюкопиранозы, соединенные α(1-4)-гликозидной связью (Nash, Handbook of Pharmaceutical Excipiеnts, ed. by Wade and Weller, 1994, American Pharmaceutical Association, Washington, and The Pharmaceutical Press, London, pp.145-148); тремя наиболее известными циклодекстринами являются α-, β- и γ-CD, которые состоят из 6, 7 и 8 углеводных остатков соответственно. Многочисленные производные каждого типа циклодекстринов могут быть получены путем случайной или направленной модификации одной, нескольких или всех свободных гидроксильных групп углеводных остатков.
Рилизинг-гормон лютеинизирущего гормона является нейрогормоном, продуцируемым нейронами гипоталамуса и секретируемым в гипофизарную портальную сосудистую систему для стимуляции высвобождения лютеинизирующего гормона (LН) и фолликулостимулирующего гормона (FSН) с помощью гипофиза. В свою очередь, LH и FSH регулируют эндокринную и герминативную функции яичника у женщин и семенника у мужчин. Рилизинг-гормон лютеинизирующего гормона является пептидом следующей структуры: pGlu-His-Trp-Ser-Tyr-Gly-Leu-Arg-Pro-Gly-NН2. В течение ряда лет были синтезированы многочисленные нормальные и укороченные, линейные или циклические пептидные аналоги LH-RH, включающие природные, необычные или химически модифицированные аминокислоты и обладающие мощными агонистическими или антагонистическими свойствами (Kartеn and Rivier, 1986, Endocr. Rev., 7 (1):44-46; Dutta, 1988, Drugs of the Future, 13 (8): 761-787; Kutscher et al., 1997, Angew. Chem. Int. Ed., Engl., 36:2148-2161. Однако из-за их полной или частично пептидной структуры все эти аналоги обладают низкой биодоступностью и биологической активностью.
К настоящему времени сообщено только о непероральном введении пептидных аналогов LH-RH. Например, Matsubara et al. (1996, J. Pharm. Sci., 84 (11): 1295-1300) описывают назальную лекарственную форму бусерелина на основе диметил-β-CD с улучшенной биодоступностью.
Для того чтобы создать удобства для пациентов, необходимо обеспечить лекарственные формы, которые облегчают пероральное применение пептидных аналогов LH-RH.
Неожиданно было обнаружено, что α-CD или их производные усиливают биологическую активность пептидных аналогов LH-RH при пероральном применении.
Так, в соответствие с одним из этих признаков изобретение относится к применению α-циклодекстрина или его производных с целью получения фармацевтических композиций для перорального введения пептидных аналогов LH-RH.
Примеры пептидных аналогов LH-RH, которые могут использоваться в объеме изобретения, включают аналоги, описанные в заявках на международные патенты WO 98/21229 и WO 98/55505, содержание которых включается в виде ссылки, а также стандартные агонисты и антагонисты LH-RH, такие, как, например, бусорелин, нафарелин, лейпрорелин, госерелин, гистрелин, трипторелин, деслорелин, лутрелин, аворелин, цетрореликс, антид, ганиреликс, азалин В, антареликс, детиреликс, рамореликс, тевереликс или абареликс.
Предпочтительно эти пептидные аналоги имеют формулу (SEQ ID :1, последовательность с идентификационным номером 1):
A1-A2-A3-A4-A5-A6-A7-A8-Pro-Z (A),
где A1 означает pGlu; D-pGlu; Sar; AcSar; Pro или их производные, такие, как AcPro, ForPro, OH-Pro, Ac-OH-Pro, дегидро-Рrо или Ас-дегидро-Pro; Ser; D-Ser; Ac-D-Ser; Thr; D-Thr; Ac-D-Thr; или ароматическую аминокислоту, которая может быть ацилированной, такой, как D-Phe; D-HPhe, D-Tyr, D-HTyr, D-Trp, D-2MeTrp, D-Nal, D-1Nal, D-дифенил-Аlа, D-Bal, D-Pal, D-4Раl или D-Qal, где D-Phe, D-Hphe, D-Tyr, D-HTyr и D-Trp могут быть замещены одним или несколькими атомами галоида, (C1-C4)-алкильной, (C1-C4)-алкоксильной, нитро- или трифторметильной группами;
А2 означает непосредственную связь; His или ароматическую D-аминокислоту, такую, как D-Phe, D-HPhe, D-Tyr, D-HTyr, D-Trp, D-2MeTrp, D-Nal, D-1Nal, D-дифeнил-Ala, D-Bal, D-Pal, D-4Pal или D-Qal, где D-Phe, D-Hphe, D-Tyr, D-HTyr и D-Trp могут быть замещены одним или несколькими атомами галоида, (C1-C4)-алкильной, (C1-C4)-алкоксильной, нитро- или трифторметильной группами;
A3 означает ароматические L- или D-аминокислоты, такие, как Phe, HPhe, Тyr, НТyr, Тrp, 2MeTrp, Nal, 1Nal, дифенил-Ala, Bal, Pal, 4Pal или Qal, где Phe, HPhe, Тyr, НТyr и Тrp могут быть замещены одним или несколькими атомами галоида, (C1-C4)-алкильной, (C1-C4)-алкоксильной, нитро- или трифторметильной группами;
A4 означает Ala, Ser, D-Ser, MeSer, Ser(OBut), Ser(OBzl) или Thr;
А5 означает ароматическую L-аминокислоту, такую, как Phe, HPhe, Тyr, HTyr, Trp, 2MeTrp, Nal, 1Nal, дифенил-Ala, Bal, Pal, 4Pal или Qal, где Phe, HPhe, Tyr, HTyr и Trp могут быть замещены одним или несколькими атомами галоида, (C1-C4)-алкильной, (C1-C4)-алкоксильной, нитро- или трифторметильной группами, и/или N-α-замещены (C1-С4)-алкильной группой, необязательно замещенной одним или несколькими атомами фтора; или основные L- или D-аминокислоты, такие, как Arg, HArg, Orn, Lys, HLys, Cit, HCit, APhe или ACha, где Аrg и НАrg могут быть N-замещены (C1-C6)-алкильной или (C3-C6)-циклоалкильной группой по одному или обоим атомам азота, и где Orn, Lys, HLys, APhe и ACha могут быть N-замещены одной или двумя (C1-С6)-алкильной или (С3-С6)-циклоалкильной группами, или аминотриазолильной или никотиноильной, изоникотикоильной, 6-метилникотиноильной, глицилникотиноильной, никотинилазаглицильной, фурильной, глицилфурильной, фурилазаглицильной, пиразинильной, пиразинилкарбонильной, пиколиноильной, 6-метилпиколиноильной, шикимильной, шикимилглицильной, Fmoc- или Вос-группой;
А6 означает Gly; (S)-спиролактам-Рro; D-Pro; D-Ser; D-Thr; D-Cys; D-Met; D-Asn; D-Pen; D-(S-Me)Pen; D-(S-Et)Pen; D-Ser (OBut); D-Asp(OBut); D-Glu (O-But); D-Thr (OBut); D-Cys(ОВut); D-Ser (OR1), где R1 означает остаток углевода; азааминокислоту, такую, как azaGly или azaAla; D-His, который может быть замещен по имидазольнoму кольцу (C1-С6)-алкильной, (С2-С7)-ацильной или бензильной группой; алифатическую D-аминокислоту с (C1-C8)-алкильной или (C3-C6)-циклоалкильной боковой цепью, такую, как D-Ala, D-Abu, D-Aib, D-3Aib, D-Val, D-Nva, D-Leu, D-Ile, D-Tle, D-Nle, D-Hol, D-Npg, D-CPa, D-Cpa, D-Cba или D-Cha; ароматическую D-аминокислоту, такую, как D-Phe, D-HPhe, D-Tyr, D-HTyr, D-Trp, D-2MeTrp, D-Nal, D-1Nal, D-дифенил-Аlа, D-антрил-Ala, D-фенантрил-Аlа, D-бензгидрил-Ala, D-флуоренил-Аlа, D-Bal, D-Pal, D-4Pal или D-Qal, где D-Phe, D-HPhe, D-Tyr, D-HTyr или D-Trp могут быть замещены одним или несколькими атомами галоида, (C1-C4)-алкильной, (C1-C4)-алкоксильной, нитро- или трифторметильной группами; D-циклогексадиенил-Gly; D-пергидронафтил-Ala, D-пергидродифенил-Ala; или основные L- или D-аминокислоты, как Arg, HArg, Orn, Lys, HLys, Cit, HCit, APhe или ACha, где Arg и HArg могут быть N-замещены (С1-С6)-алкильной или (С3-С6)-циклоалкильной группой по одному или обоим атомам азота, где Orn, Lys, HLys, APhe и ACha могут быть N-замещены одной или двумя (C1-С6)-алкильными или (С3-С6)-циклоалкильными группами, или аминотриазолильной или никотиноильной, изоникотиноильной, 6-метилникотиноильной, глицилникотиноильной, никотинилазаглицильной, фурильной, глицилфурильной, фурилазаглицильной, пиразинильной, пиразинилкарбонильной, пиколиноильной, 6-метилпиколиноильной, шикимильной, шикимилглицильной, Fmoc- или Вос-группой;
А7 означает линейную, разветвленную или циклическую алифатическую L-аминокислоту из от 3 до 20 атомов углерода, такую, как Ala, Abu, Aib, 3Aib, Val, Nva, Leu, Ile, Tle, Nle, Hol, Npg, СPa, Cpa, Cba, Cha или Ada, которые могут быть N-α-замещены (C1-C4)-алкильной группой, необязательно замещенной одним или несколькими атомами фтора;
А8 означает основные L- или D-аминокислоты, как Arg, HArg, Orn, Lys, HLys, Сit, НСit, APhe или ACha, где Arg и HArg могут быть N-замещены (C1-С6)-алкильной или (С3-С6)-циклоалкильной группой по одному или обоим атомам азота и где Orn, Lys, HLys, APhe или ACha могут быть N-замещены одной или двумя (С1-С6)-алкильными или (С3-С6)-циклоалкильными группами либо аминотриазолильной или никотиноильной, изоникотиноильной, 6-метилникотиноильной, глицилникотиноильной, никотинилазаглицильной, фурильной, глицилфурильной, фурилазаглицильной, пиразинильной, пиразинилкарбонильной, пиколиноильной, 6-метил-пиколиноильной, шикимильной, шикимилглицильной, Fmос-или Воc-группой;
Z означает GlyNH2; D-AlaNH2; azaGlyNH2 или группу -NHR2, где R2 означает (C1-C4)-алкил, который может быть замещен гидроксильной группой или одним или несколькими атомами фтора; (С3-С6)-циклоалкил или гетероциклический радикал, выбранный из морфолинильного, пирролидинильного и пиперидильного,
а также их фармацевтически приемлемые соли.
В данном описании термин "(C1-C4)-алкил" означает метильную, этильную, н-пропильную, изопропильную, н-бутильную, изобутильную, втор-бутильную и трет-бутильную группы.
Термин "(C1-С6)-алкил" означает метильную, этильную, н-пропильную, изопропильную, н-бутильную, изобутильную, втор-бутильную, трет-бутильную, н-пентильную, изопентильную, втор-пентильную, трет-пентильную и гексильную группы.
Термин "(C1-C8)-алкил" означает метильную, этильную, н-пропильную, изо-пропильную, н-бутильную, изо-бутильную, втор-бутильную, трет-бутильную, н-пентильную, изо-пентильную, втор-пентильную, трет-пентильную, гексильную, гептильную и октильную группы.
Термин "(C1-C4)-алкокси" означает группу -OR, где R означает (C1-C4)-алкил.
Термин "(С2-С7)-ацил" означает группу -COR, где R означает (C1-C6)-алкил.
Термин "(C3-C6)-циклоалкил" означает циклопропильную, циклобутильную, циклопентильную и циклогексильную группы.
Термин "углеводная часть" означает D- или L-пентозы либо гексозы и их аминопроизводные.
Термин "аналоги LH-RH" означает пептиды, у которых в последовательности рилизинг-гормона лютеинизирующего гормона модифицирована, по меньшей мере, одна аминокислота.
Термин "(S)спиролактам-Рro" означает остаток формулы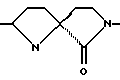
Термин "пероральное введение" означает доставку пептидных аналогов в желудочно-кишечный тракт посредством пероральной лекарственной формы или композиции.
Пептидомиметические аналоги LH-RH, характеризуемые отсутствием, по меньшей мере, одной пептидной амидной связи, как приведенные в качестве примеров в самом последнем обзоре Kutscher et al. (1997, Angew. Chem. Int. Ed., Engl., 36: 2148-2161), не входят в область настоящего изобретения.
В данном описании и в формуле изобретения использованы следующие аббревиатуры:
Abu: 2-аминомасляная кислота - Ас: ацетил
ACha: аминоциклогексилаланин - Aib: 2-аминоизомасляная кислота
3Aib: 3-аминоизомасляная кислота - Аlа: аланин
AlaNH2: аланинамид - APhe: п-аминофенилаланин
Arg: аргинин - Asp: аспарагиновая кислота
AzaAla: азааланин - AzaGly: азаглицин
AzaGlyNН2: азаглицинамид - Bal: бензотиенилаланин
Вос: трет-бутоксикарбонил - Сbа: циклобутилаланин
Cha: циклогексилаланин - Cit: цитруллин
СРа: циклопропилаланин - Сра: циклопентилаланин
Fmoc: флуоренилметоксикарбонил - For: формил
Glu: глутаминовая кислота - Gly: глицин
GlyNH2: глицинамид - HArg: гомоаргинин
HCit: гомоцитруллин - His: гистидин
HLys: гомолизин - Ноl: гомолейцин
Ilе: изолейцин - IprLys: Nε-изопропиллизин
Leu: лейцин - Lys: лизин
MeSer: N-метилсерин - Met: метионин
Nal: 3-(2-нафтил)аланин - 1Nal: 3-(1-нафтил)аланин
NEt: N-этиламид - NicLys: Nε-никотиноиллизин
Nle: норлейцин - Npg: неопентилглицин
Nva: норвалин - ОВut: трет-бутокси
OBzl: бензиловый эфир - Оrn: орнитин
Pal: 3-(3-пиридил)аланин - pClPhe: 3-(4-хлорфенил)аланин
Pen: пеницилламин - pGlu: пироглутаминовая кислота
Phe: фенилаланин - Pro: пролин
Qal: 3-(3-хинолил) аланин - Sar: саркозин
Ser: серин - (S-Me)Pen: S-метилпеницилламин
(S-Et)Pen: S-этилпеницилламин - Thr: треонин
Tle: трет-лейцин - Тrp: триптофан
Тyr: тирозин - Val: валин
Ada: адамантилаланин - HPhe: гомофенилаланин
MeNpg: N-метилнеопентилглицин - 4Раl: 3-(4-пиридил)аланин
HTyr: гомотирозин - 2МеТrp: 2-метилтриптофан
Bzl: бензил - SPL: (S)-спиролактам пролина
Asn: аспарагин - MeLeu: N-метиллейцин
МеТyr: N-метилтирозин - МеНТyr: N-метилгомотирозин
Предпочтительная группа пептидных аналогов (А) включает пептиды формулы (SEQ ID :2):
A1-His-A3-A4-A5-A6-A7-A8-Pro-Z (I),
где А1 означает pGlu, Sar или AcSаr;
A3 означает ароматическую L-аминокислоту, такую, как Phe, HPhe, Тyr, HTyr, Trp, 2MeTrp, Nal, 1Nal, дифенил-Ala, Bal, Pal, 4Pal или Qal, где Phe, HPhe, Тyr, НТyr и Тrp могут быть замещены одним или несколькими атомами галоида, (C1-C4)-алкильной, (C1-C4)-алкоксильной, нитро- или трифторметильной группами;
А4 означает Ala, Ser, D-Ser, MeSer, Ser(OBut), Ser(OBzl) или Thr;
A5 означает ароматическую L-аминокислоту, такую, как Phe, HPhe, Тyr, НТyr, Тrр, 2МеТrр, Nal, 1Nal, дифенил-Ala, Bal, Pal, 4Pal или Qal, где Phe, HPhe, Тyr, НТyr и Тrp могут быть замещены одним или несколькими атомами галоида, (C1-C4)-алкильной, (C1-C4)-алкоксильной, нитро- или трифторметильной группами;
А6 означает Gly; D-Pro; (S)-спиролактам-Рro; D-Ser; D-Thr; D-Cys; D-Met; D-Pen; D-(S-Me)Pen; D-(S-Et)Pen; D-Ser(OBut); D-Asp(OBut); D-Clu (O-But); D-Thr(OBut); D-Сys(ОВut); D-Ser(OR1), где R1 означает остаток углевода; азааминокислоту, такую, как azaGly или azaAla; D-His, который может быть замещен по имидазольному кольцу (C1-С6)-алкильной или бензильной группой; алифатическую D-аминокислоту с (C1-C8)-алкильной или (С3-С6)-циклоалкильной боковой цепью, такую, как D-Ala, D-Abu, D-Aib, D-3Aib, D-Val, D-Nva, D-Leu, D-Ile, D-Tle, D-Nle, D-Hol, D-Npg, D-CPa, D-Cpa, D-Cba или D-Cha; ароматическую D-аминокислоту, такую, как D-Phe, D-HPhe, D-Tyr, D-HTyr, D-Trp, D-2MeTrp, D-Nal, D-1Nal, D-дифенил-Аlа, D-антрил-Ala, D-фенантрил-Аlа, D-бензгидрил-Аlа, D-флуоренил-Аlа, D-Bal, D-Pal, D-4Pal или D-Qal, где D-Phe, D-HPhe, D-Tyr, D-HTyr или D-Trp могут быть замещены одним или несколькими атомами галоида, (C1-C4)-алкильной, (C1-C4)-алкоксильной, нитро- или трифторметильной группами; D-циклогексадиенил-Gly; D-пергидронафтил-Аlа, D-пергидродифенил-Ala; или основные D-аминокислоты, как D-Arg, D-HArg, D-Orn, D-Lys, D-HLys, D-Cit, D-HCit, D-APhe, необязательно замещенные аминотриазолильной группой, или D-ACha, где D-Arg и D-HArg могут быть N-замещены (C1-C6)-алкильной или (С3-C6)-циклоалкильной группами или Fmос- или Вос-группой;
А7 означает линейную, разветвленную или циклическую алифатическую L-амииокислоту из от 3 до 20 атомов углерода, такую, как Ala, Abu, Aib, 3Aib, Val, Nva, Leu, Ile, Tle, Nle, Hol, Npg, CPa, Cpa, Cba, Cha или Ada, которые могут быть N-α-замещены (C1-C4)-алкильной группой, необязательно замещенной одним или несколькими атомами фтора;
А8 означает основные L-аминокислоты, как Arg, HArg, Orn, Lys, HLys, Cit, HCit, APhe, необязательно замещенные аминотриазолильной группой, или ACha;
Z означает GlyNH2; azaGlyNH2 или группу -NHR2, где R2 означает (C1-C4)-алкил, который может быть замещен гидроксильной группой или одним или несколькими атомами фтора; (С3-C6)-циклоалкил или гетероциклический радикал, выбранный из морфолинильного, пирролидинильного и пиперидильного,
а также их фармацевтически приемлемые соли.
В числе пептидных аналогов формулы (I) предпочтительными являются те, которые имеют формулу (SEQ ID :3):
pGlu-His-A3-Ser-A5-A6-A7-Arg-Pro-Z (II),
где A3 и А5 означают ароматические L-аминокислоты, как определено для формулы (I);
А6 имеет значение, определенное для формулы (I);
А7 означает Leu, Tle, Nle, Hol, Npg, Cha или Ada, которые могут быть N-α-замещены метильной или этильной группой, необязательно замещенной одним или несколькими атомами фтора;
Z имеет значение, определенное для формулы (I),
а также их фармацевтически приемлемые соли.
Особо предпочтительными являются пептидные аналоги формулы (SЕQ ID :4):
pGlu-His-A3-Ser-A5-A6-A7-Arg-Pro-Z (III),
где A3 и А5 означают каждый независимо друг от друга Phe, Тyr, Trp, 2MeTrp, HPhe, HTyr, Nal, 1Nal, Bal, Pal, 4Pal или pClPhe;
А6 означает (S)-спиролактам-Рro; Gly; D-Pro; D-Sеr(ОВut); D-Asp(OBut); D-Glu(OBut); D-Thr (OBtt); D-Cys (OBut); D-His или D-His(Bzl); D-Ala, D-Leu, D-Tle, D-Nle, D-Hol, D-Npg или D-Cha; D-Phe, D-HPhe, D-Tyr, D-HTyr, D-Trp, D-2MeTrp, D-Nal, D-1Nal, D-Bal, D-Pal, D-4Pal или D-pClPhe; D-циклогексадиенил-Сly; D-пергидронафтил-Аlа; D-пергидродифенил-Ala или D-APhe, необязательно замещенный аминотриазолильной группой;
А7 означает Leu, Npg или Cha, которые могут быть N-α-замещены метильной группой;
Z означает GlyNH2; azaGlyNH2 или -NC2H5.
Особо предпочтительными также являются пептидные аналоги формулы (SEQ ID :5):
pGlu-His-Trp-Ser-Tyr-A6-A7-Arg-Pro-Z (IV),
где А6 означает (S)-спиролактам-Рro, D-Leu, D-Ala, D-Nal, D-Phe, D-Ser(OBut) или D-Trp;
A7 означает Leu, MeLeu, Npq или MeNpq;
Z означает GlyNH2; azaGlyNH2 или -NC2H5.
Пептидные аналоги формул (I)-(IV), в которых A7 означает Npg, являются особенно предпочтительными.
Типичные пептидные аналоги формул (I)-(IV) включают лейпрорелин, [Npg7] -лейпрорелин, трипторелин, [Npg7]-трипторелин, госерелин, [Npg7]-госерелин, бусерелин и [Npg7]-бусерелин.
Другая предпочтительная группа пептидных аналогов (А) включает пептиды формулы (SEQ ID :6):
A1-A2-A3-A4-A5-A6-A7-A8-Pro-Z (I'),
где А1 означает pGlu; D-pGlu; Sar; AcSar; Pro или их производные, такие, как АсРrо, ForPro, OH-Pro, Ас-ОН-Рrо, дегидро-Рrо или Ас-дегидро-Рrо; Ser; D-Ser; Ac-D-Ser; Thr; D-Thr; Ac-D-Thr, или ароматическую D-аминокислоту, которая может быть ацилированной, предпочтительно ацетилированной, такой, как D-Phe; D-HPhe, D-Tyr, D-Trp, D-Nal, D-1Nal, D-дифенил-Alа, D-Bal, D-Pal, D-4Pal или D-Qal, где D-Phe и D-Trp могут быть замещены одним или несколькими атомами галоида, (C1-C4)-алкильной, (C1-C4)-алкоксильной, нитро- или трифторметильной группами;
А2 означает непосредственную связь или ароматическую D-аминокислоту, такую, как D-Pho, D-HPhe, D-Tyr, D-Trp, D-Nal, D-1Nal, D-дифенил-Ala, D-Bal, D-Pal, D-4Pal или D-Qal, где D-Phe и D-Trp могут быть замещены одним или несколькими атомами галоида, (C1-C4)-алкильной, (C1-C4)-алкоксильной, нитро- или трифторметильной группами;
A3 означает ароматическую L- или D-аминокислоту, такую, как Phe, HPhe, Тyr, Trp, Nal, 1Nal, дифенил-Ala, Bal, Pal, 4Pal или Qal, где Phe и Тrp могут быть замещены одним или несколькими атомами галоида, (C1-C4)-алкильной, (C1-C4)-алкоксильной, нитро- или трифторметильной группами;
А4 означает Ala, Ser, D-Ser, MeSer, Ser(ОВut), Ser(OBzl) или Thr;
А5 означает ароматическую L-аминокислоту, такую, как Phe, HPhe, Тyr, НТyr, Тrp, Nal, 1Nal, дифенил-Ala, Bal, Pal, 4Pal или Qal, где Phe, Тyr, HТyr и Тrp могут быть замещены одним или несколькими атомами галоида, (C1-C4)-алкильной, (C1-C4)-алкоксильной, нитро- или трифторметильной группами и/или N-α-замещены (C1-C4)-алкильной группой, необязательно замещенной одним или несколькими атомами фтора; или основные L- или D-аминокислоты, такие, как Аrg, НАrg, Orn, Lys, HLys, Сit, HCit, APhe или ACha, где Аrg и НАrg могут быть N-замещены (C1-C6)-алкильной или (С3-С6)-циклоалкильной группой по одному или обоим атомам азота и где Orn, Lys, HLys, HPhe и ACha могут быть N-замещены одной или двумя (C1-С6)-алкильными или (С3-С6)-циклоалкильными группами, или никотиноильной, изоникотиноильной, 6-метилникотиноильной, глицилникотиноильной, никотинилазаглицильной, фурильной, глицилфурильной, фурилазаглицильной, пиразинильной, пиразинилкарбонильной, пиколиноильной, 6-метилпиколиноильной, шикимильной, шикимилглицильной, Fmoc-или Вос-группой;
А6 означает Gly; (S)-спиролактам-Рro; D-Pro; D-Ser; D-Thr; D-Cys; D-Met; D-Asn; D-Pen; D-(S-Me)Pen; D-(S-Et)Pen; D-Ser(OBut); D-Asp(OBut); D-Glu(OBut); D-Thr (OBut); D-Сys(ОВut); D-Ser (OR1), где R1 означает остаток углевода; алифатическую D-аминокислоту с (C1-C8)-алкильной или (С3-С6)-циклоалкильной боковой цепью, такую, как D-Ala, D-Abu, D-Aib, D-3Aib, D-Val, D-Nva, D-Leu, D-Ile, D-Tle, D-Nle, D-Hol, D-Npg, D-CPa, D-Cpa, D-Cba или D-Cha; ароматическую D-аминокислоту, такую, как D-Phe, D-HPhe, D-Tyr, D-Trp, D-Nal, D-1Nal, D-дифенил-Аlа, D-антрил-Ala, D-фенантрил-Аlа, D-бензгидрил-Аlа, D-флуоренил-Ala, D-Bal, D-Pal, D-4Pal или D-Qal, где D-Phe и D-Trp могут быть замещены одним или несколькими атомами галоида, (C1-C4)-алкильной, (C1-C4-алкокоильной, нитро- или трифторметильной группами; D-циклогексадиенил-Gly; D-пергидронафтил-Аlа; D-пергидродифенил-Аlа; или основные L- или D-аминокислоты, как Аrg, НАrg, Orn, Lys, HLys, Cit, HCit, APhe или ACha, где Аrg и HArg могут быть N-замещены (C1-C6)-алкильной или (С3-С6)-циклоалкильной группой по одному или обоим атомам азота и где Orn, Lys, HLys, APhe и ACha могут быть N-замещены одной или двумя (C1-C6)-алкильными или (С3-С6)-циклоалкильными группами, или никотиноильной, изоникотиноильной, 6-метилникотиноильной, глицилникотиноильной, никотинилазаглицильной, фурильной, глицилфурильной, фурилазаглицильной, пиразинильной, пиразинилкарбонильной, пиколиноильной, 6-метилпиколиноильной, шикимильной, шикимилглицильной, Fmoc- или Boc-группой;
А7 означает линейную, разветвленную или циклическую алифатическую L-аминокислоту из от 3 до 20 атомов углерода, такую, как Ala, Abu, Aib, 3Aib, Val, Nva, Leu, Ile, Tle, Nle, Hol, Npg, CPa, Cpa, Cba, Cha или Ada, которые могут быть N-α-замещены (C1-C4)-алкильной группой, необязательно замещенной одним или несколькими атомами фтора;
А8 означает основные L- или D-аминокислоты, как Аrg, HArg, Orn, Lys, HLys, Сit, HCit, APhe или ACha, где Arg и HArg могут быть N-замещены (C1-С6)-алкильной или (С3-С6)-циклоалкильной группой по одному или обоим атомам азота и где Orn, Lys, HLys, APhe или ACha могут быть N-замещены одной или двумя (C1-C6)-алкильными или (С3-С6)-циклоалкильными группами либо никотиноильной, изоникотиноильной, 6-метилникотиноильной, глицилникотиноильной, никотинилазаглицильной, фурильной, глицилфурильной, фурилазаглицильной, пиразинильной, пиразинилкарбонильной, пиколиноильной, 6-метилпиколиноильной, шикимильной, шикимилглицильной, Fmoc- или Вос-группой;
Z означает GlyNH2 или D-AlaNH2,
а также их фармацевтически приемлемые соли.
В число пептидов формулы (I') входят являющиеся предпочтительными аналоги формулы (SEQ ID :7):
Ac-D-Nal-D-pClPhe-D-Pal-Ser-A5-A6-A7-A8-Pro-D-AlaNH2 (II'),
где А5 означает Тyr, HTyr, MeTyr, MeHTyr, NicLys или IprLys;
А6 означает (S)-спиролактам-Рro, D-Arg, D-NicLys, D-IprLys, D-Cit, D-HCit или D-Asn;
A7 означает Leu, MeLeu, Npg или MeNpg;
A8 означает Arg, NicLys или IprLys,
и их фармацевтически приемлемые соли.
Пептидные аналоги формулы (I') и (II'), в которых A7 означает Npg, являются особенно предпочтительными.
Типичные представители пептидных аналогов формулы (I') и (II') включают антид, [Npq7]-антид, цетрореликс, [Npg7]-цетрореликс, абареликс и [Npg7]-абареликс.
Другие предпочтительные пептидпые аналоги включают таковые формулы (А), в которой А6 имеет приведенные значения, за исключением D-Asn.
Примерами солей с фармацевтически приемлемыми кислотами являются соли с минеральными кислотами, такие, как, например, гидрохлорид, гидробромид, сульфат, фосфат, борат, гидросульфат, дигидрофосфат или нитрат, и соли с органическими кислотами, такие, как, например, ацетат, оксалат, тартрат, сукцинат, малеат, фумарат, глюконат, цитрат, памоат, малат, аскорбат, бензоат, п-толуолсульфонат или нафталинсульфонат.
Примерами солей с фармацевтически приемлемыми основаниями являются соли со щелочными или щелочноземельными металлами, такими, как натрий, калий, кальций или магний, и с органическими основаниями, такими, как амины, трометамол (2-амино-2-гидроксиметил-1,3-пропандиол), N-метилглутамин и тому подобное.
Пептиды, применяемые по настоящему изобретению, могут быть получены хорошо известными методами пептидной химии, такими, как, например, синтез пептидов в растворе или твердофазным пептидным синтезом. В общем, эти методы включают ступенчатое добавление одной или нескольких аминокислот, которые могут быть соответствующим образом защищены с образованием пептидной цепи. Можно, например, сослаться на справочник "Синтетические пептиды: руководство пользователя" (ed. by G.A. Grant, 1992, UWBC Biotechnical Resource Series, Washington University Press, Saint-Louis, USA).
Каждая молекула α-циклодекстрина имеет 6 первичных гидроксильных групп и 12 вторичных гидроксильных групп, соответственно относящихся к первичной 6-ОН-группе и ко вторичным 2-ОН-группе и 3-ОН-группе в каждом из шести остатков глюкопиранозы. В другом общем аспекте настоящее изобретение относится к α-циклодекстрину и его производным, которые являются результатом химических или биохимических модификаций, включающих точное или среднее число гидроксильных групп от 1 до 18 молекулы α-CD, с помощью произвольного или региоселективного метода и реакций одного или нескольких различных типов, таких, как окисление, восстановление, алкилирование, гидроксиалкилирование, этерификация с органической или минеральной кислотами, внутримолекулярная дегидратация, тозилирование, сопровождаемое восстановительным аминированием либо замещением атомом галоида, разветвление углевода или дальнейшая полимеризация, и их различные возможные комбинации и сочетания. Примеры производных α-CD включают α-циклодекстрин, модифицированный с помощью одной или нескольких групп, выбранных из метила, карбоксиметила, этила, бутила, октила, гидроксиэтила, гидроксипропила, гидроксибутила, ацетила, пропионила, бутирила, сукцинила, бензоила, пальмитила, сульфонила, толуолсульфонила, амино, аминопропила, глюкозила, мальтозила, димальтозила, карбоксиметилового эфира, сульфобутилового эфира и эфира фосфорной кислоты.
Предпочтительные производные α-циклодекстрина по изобретению включают метилированный α-CD; гексакис(2,3,6-три-О-метил)-α-СD, известный также как "перметилированный" α-CD; карбоксиметилированный α-CD и фосфорилированный α-CD. При применении для приготовления фармацевтических композиций по изобретению особенно полезными являются α-CD и гексакис(2,3,6-три-О-метил)-α-CD.
Как упомянуто выше, α-CD или его производные усиливают биологическую активность пептидных аналогов рилизинг-гормона лютеинизирующего гормона в фармацевтических композициях для перорального применения.
Таким образом, в соответствии с другим отличительным признаком изобретение относится к пероральным фармацевтическим композициям, которые включают в качестве активного ингредиента пептидный аналог LH-RH, описанный выше, в виде комбинации с α-CD или его производным, причем упомянутые композиции предполагается доставлять в желудочно-кишечный тракт.
Пептиды, соответствующие общей формуле (I), проявляют агонистическую активность in vivo в отношении рецепторов LH-RH, приводящую к стимуляции гипофизом секреции лютеинизирующего гормона, который у мужчин стимулирует секрецию тестостерона семенниками.
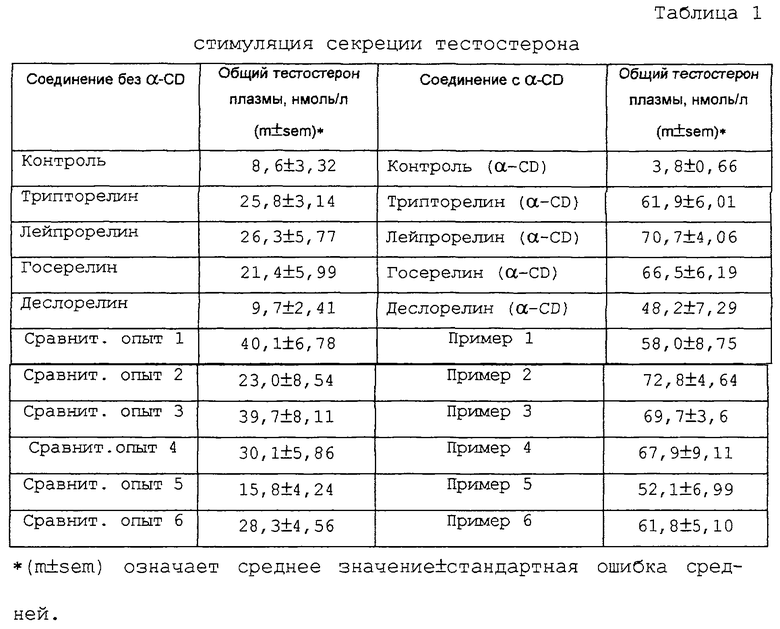
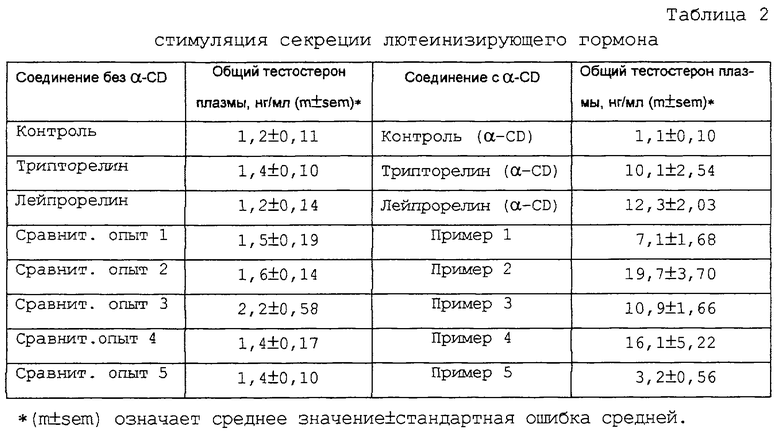
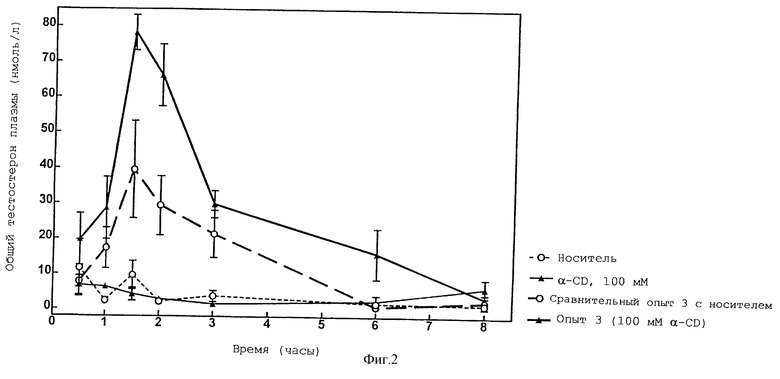
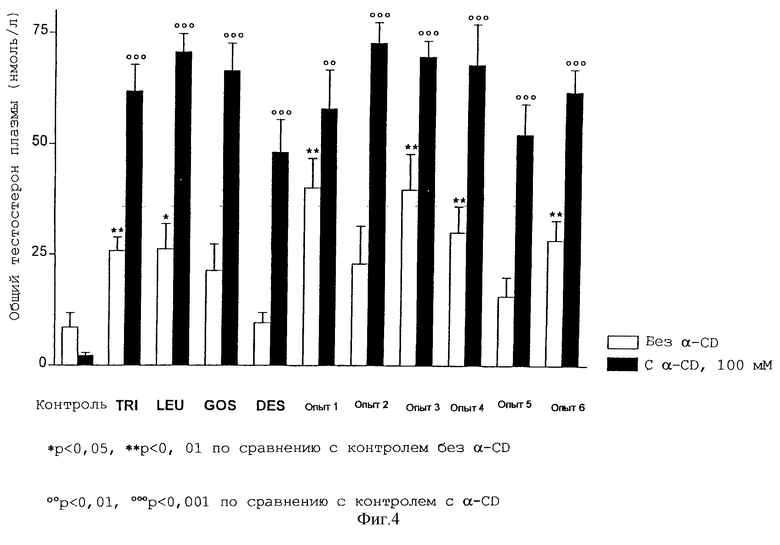
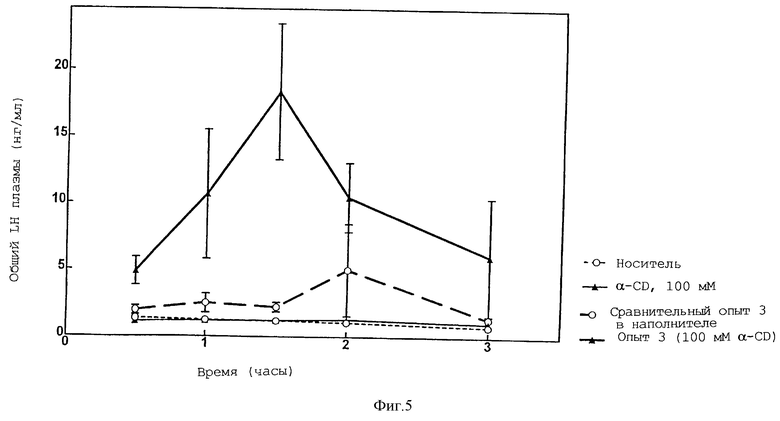
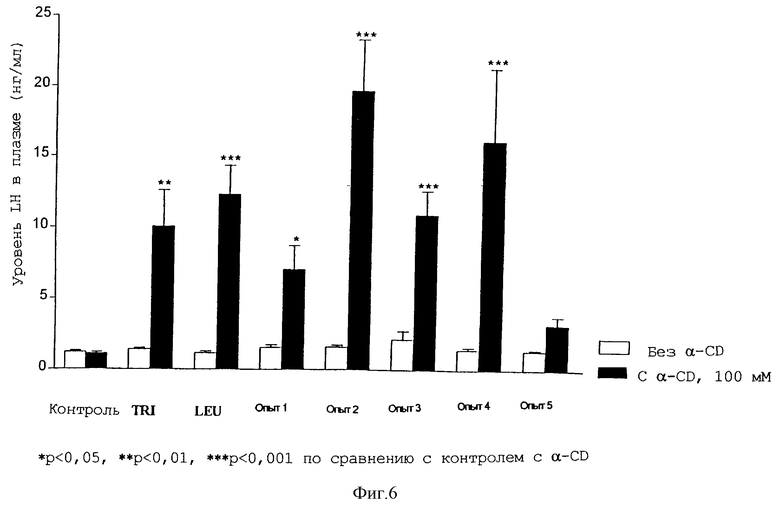
Взрослым крысам-самцам линил Sprague-Dawley с помощью зонда вводили перорально соответствующую лекарственную форму, включающую лейпрорелин (LEU, фирмы Bachem), трипторелин (TRI, фирмы Bachem), деслорелин (DES, фирмы Saxon Biochemicals), госерелин (GOS, фирмы Saxon Biochemicals) или другие аналоги из следующих примеров: пример 1: [(S)-спиролактам-(Pro6, Npg7), дезGly10-РroNЕt9] LH-RH; пример 2: (D-Ala6, Npg7, дезGly10-Рro-NEt9)LH-RH; пример 3: Nрg7-лейпроролин; пример 4: (D-Phe6, Npg7, дезGly10-РroNЕt9) LH-RH; пример 5: Nрg7-трипторелин и пример 6: (D-Ala6, дезGly10-РroNЕt9)LH-RH (фирмы Bachem), в комбинации с α-CD (фирмы Sigma или Wacker Chemie). Для сравнения те же самые агонисты вводили перорально с помощью зонда в стандартном водном носителе без включения α-CD (сравнительные примеры). Для скрининговых целей образцы крови брали через 2 часа после перорального введения пептидного агониста LH-RH в общей дозе 2 нмоль/крысу в водном растворе, содержащем 10 или 100 мМ α-CD (таблицы 1 и 2; фиг.1, 4 и 6). Для кинетических целей влияние доз 2 нмоль/крысу (по примеру 3) с добавлением или без 100 мМ α-CD на уровни лютеинизирующего гормона и тестостерона в плазме исследовали между 0,5 и 8 часами (фиг.2 и 5). Влияние увеличивающихся концентраций α-CD (5, 10 или 14%) исследовали в примере 2 при дозе 5 мкг/кг через 2 часа после перорального введения (фиг.3). Определение общего тестостерона в плазме (Diagnostic System Laboratories) и лютеинизирующего гормона LH (Amersham Pharmacia Biotech) проводили с помощью радиоиммуноанализа. При проведении двухчасовых скриннинговых экспериментов каждая группа включала 6-8 крыс; в каждый момент кинетического исследования включали данные от четырех животных.
Как можно видеть из приведенных выше результатов, а также из данных, приведенных на фиг.1-4, пероральные лекарственные формы с α-CD значительно усиливают стимуляцию секреции тестостерона, индуцируемую аналогами LH-RH. Особенно деслорелин, который один в предельной дозе 2 нмоль/крысу был неактивен, но проявил выраженную активность при введении в лекарственную форму с α-CD. Решающая роль α-CD демонстрируется зависимостью его эффектов от концентрации: в комбинации с 10 мМ α-циклодекстрина (0,972%) активность при пероральном введении в примере 3 значительно не улучшилась (фиг.1); при 5% (51,4 мМ) α-циклодекстрин заметно усилил симуляцию секреции тестостерона, индуцированную в примере 2 путем перорального введения, хотя и не до максимального уровня, достигнутого при 10% (103 мМ), а также при 14% (144 мМ) (фиг.3).
Заслуживает также внимания тот факт, что (см. фиг.1 и 3) β-циклодекстрин (β-CD), гидроксипропил-βCD (HP-β-CD) и γ-циклодекстрин (γ-СD) не оказывают потенцирующего эффекта на индуцируемую аналогами LH-RH стимуляцию секреции тестостерона.
Как можно видеть из приведенных выше результатов, а также из данных, приведенных на фиг. 5 и 6, потенцирующий эффект α-CD в лекарственной форме для перорального применения, содержащей аналоги LH-RН, на высвобождение лютеинизирующего гормона является даже более выраженным, чем на секрецию тестостерона: все тестируемые аналоги LH-RН были неактивны при введении по отдельности в той же самой дозе 2 нмоль/крысу, тогда как в зависимости от структуры аналога они индуцировали 3-16-кратное усиление по сравнению с контролем, если вводились в комбинации с α-CD.
Подобные или даже еще лучшие результаты были получены с производными α-CD, такими, как метилированный α-CD, гексакис(2,3,6-три-О-метил)-α-CD, карбоксиметилированный α-CD или фосфорилированный α-CD. Все производные α-CD приобретены у фирмы Cyclolab (Budapest, Hungary). В примере 3 влияние производных α-CD на потенцирование агонистической активности LH-RH сопоставляли с воздействием самого α-CD при пероральном введении крысам с помощью желудочного зонда в низкой дозе 5 мкг/кг: уровни общего тестостерона в плазме измеряли через 2 часа после введения (таблица 3).
Производные α-CD, испытанные выше, по меньшей мере, удваивали эффект, полученный в примере 3 при пероральном применении. Нативный α-CD и его перметилированные аналоги, по-видимому, являются особенно подходящими, приводя соответственно к 2,9- и 3,8-кратному усилению агонистического действия из примера 3 на тестостерон при данном дозовом уровне, составляющем 5 мкг/кг перорально.
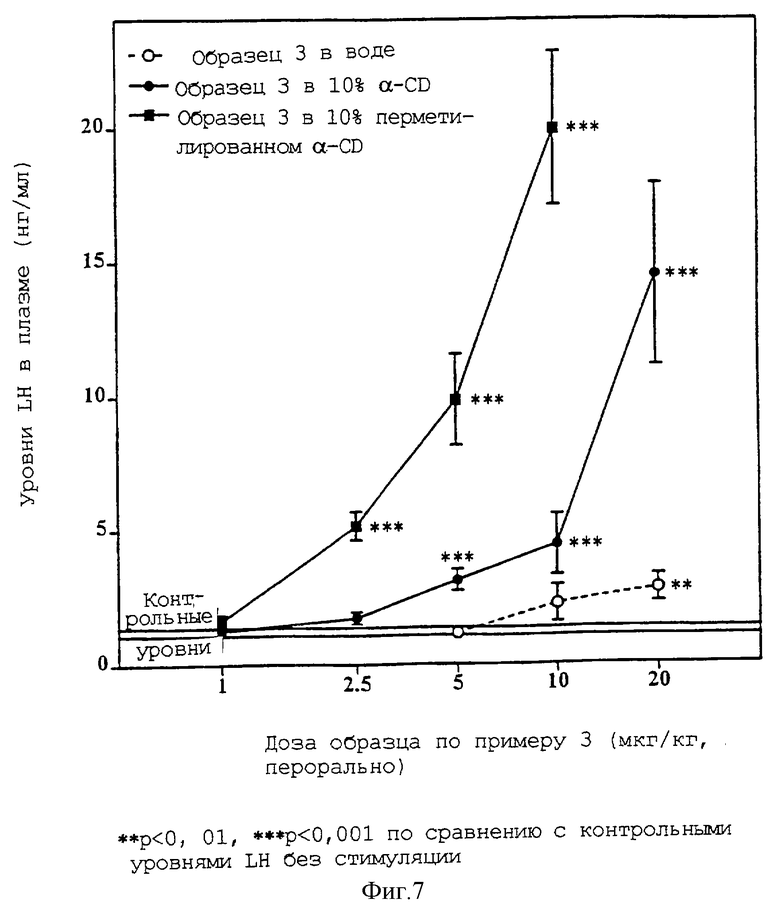
В дальнейшем эксперименте образец по примеру 3 исследовали с α-CD или перметилированным α-CD в равных концентрациях, составляющих 10%. Через 2 часа после введения измеряли уровни лютеинизирующего гормона в плазме у восьми крыс на каждую дозу (фиг.7). Доза аналога из примера 3, равная 5 мкг/кг и введенная перорально, не влияла на уровни LH в этот момент времени, а дозы 10 и 20 мкг/кг, введенные перорально, были несомненно пороговыми дозами в этих условиях эксперимента.
Комбинация аналога из примера 3 с 10% α-CD приводила к легкой, но заметной стимуляции при дозах 5 и 10 мкг/кг перорально и к намного большему эффекту при дозе 20 мкг/кг перорально по сравнению только с аналогом примера 3 (более чем пятикратное усиление активности, вызывающей секрецию лютеинизирующего гормона). Более того, комбинация аналога из примера 3 с 10% перметилированного α-CD привела даже к более высокому потенцированию: дозы 2,5, 5 и 10 мкг/кг перорально, которые были неактивными при введении только аналога из примера 3, вызывали быструю дозозависимую стимулирующую реакцию (фиг.7).
Пептиды, соответствующие общей формуле (I'), проявляют антагонистическую активность in vivo в отношении рецепторов LH-RH, приводя, в частности, к подавлению овуляции.
Исследовали влияние α-, β- и γ-CD на активность антида (пример пептидного антагониста LH-RH) при пероральном введении с помощью зонда взрослым с нормальным циклом самкам крыс линии Wistar в период между 1 час 30 мин и 3 час пополудни в день проэструса после, по меньшей мере, двух полных регулярных эстральных циклов, контролируемых с помощью ежедневных вагинальных мазков. Антиовуляционную эффективность контролировали на следующее утро, в день ожидаемого эструса путем наблюдения за зародышевыми клетками в маточных трубах обработанных самок. Наличие, по меньшей мере, одной зародышевой клетки свидетельствовало о том, что в некоторой степени происходила спонтанная овуляция, и только полное отсутствие зародышевых клеток рассматривалось как эффективное подавление овуляции, вызываемое антагонистом LH-RH. Антид растворяли в носителе, состоящем из 20% (объем/объем) пропиленгликоля в воде, уже содержавшей 1% бычьего альбумина, куда затем прибавляли 10% (вес/объем) или α-, β- и γ-CD. Результаты экспериментов суммированы в следующей таблице 4.
Носитель с α-CD или без него не дает никакого эффекта. Пороговая эффективная доза антида при пероральном введении составила 400 мкг/кг, при этом только у 3 животных из 22 обнаружилось подавление овуляции. При этом дозовом уровне β-CD и γ-CD не влияли на минимальную активность антида.
Однако α-СD значительно усиливал эффективность антида в дозе 400 мкг/кг, увеличивая подавление овуляции от 14 до 73%. В комбинации с 10% α-CD даже вдвое меньшая доза, равная 200 мкг/кг, проявляла незначительную эффективность (подавление 25%). Следовательно, α-CD, но не β-CD или γ-CD, был способен потенцировать активность пептидного антагониста LH-RH при пероральном введении.
Пероральные лекарственные формы по изобретению могут быть получены методами, хорошо известными специалистам в этой области, обычно следующим. Известное количество препарата прибавляют к водному раствору циклодекстрина достаточной концентрации; взаимодействие препарата с циклодекстрином может происходить в растворе или в суспензии в течение минут или после перемешивания в течение периода до 1 недели при определенной температуре и при облучении ультразвуком или без него, в зависимости от природы препарата и циклодекстрина и от их соответственных концентраций. Затем образующаяся комбинация или комплекс препарата с циклодекстрином может быть далее получена в сухом виде путем фильтрации, центрифугирования, упаривания или сублимации.
В качестве иллюстрации в примерах комбинаций аналогов LH-RH с α-CD далее описывается один основной метод получения лекарственных форм по изобретению в растворе, независимо от того, будут ли они в дальнейшем переработаны в любую соответствующую сухую форму, преимуществом которой будут те же самые потенцирующие свойства.
Такие лекарственные формы могут в дальнейшем включать один или несколько других фармацевтически приемлемых наполнителей для перорального введения, таких, как лактоза, фруктоза, глюкоза, сахароза, спрессованный сахар, сахарин, повидон, кросс-повидон, стеарат магния, каолин, бентонит, коллоидный кремний, маннит, сорбит, крахмал и его производные, микрокристаллическая или порошкообразная целлюлоза, метилцеллюлоза, карбоксиметилцеллюлоза, этилцеллюлоза или другие химически модифицированные целлюлозы, другие циклодекстрины, мальтодекстрин, декстраты, декстрин, декстроза, альгинаты, пектины, пектаты, эфиры сорбита, полисорбат 80, хитозан, гуаровая или ксантановая смолы, моно-, ди- или триэтаноламин, олеиновая кислота или этилолеат, стеариновая кислота, вода, жидкая глюкоза, пропиленгликоль, молочная кислота, яблочная кислота, этанол, изопропилмиристат или пальмитат, глицерин, глицерилмоноолеат, глицерилмоностеарат, глицерилпальмитостеарат, лецитин, триглицериды со средней или короткой цепью, разнообразные масла из зерновых, хлопка, оливов, арахиса, кунжута или сои и тому подобное. Эти лекарственные формы вводят через рот (или носожелудочную трубку) в различных водных или неводных растворах или суспензиях, таких, как истинные растворы, сиропы, эликсиры, слизи, желе, гели, молочко, густые водные суспензии, макро-, микро- или наноэмульсии, или в различных твердых формах, таких, как прессованные, покрытые оболочкой, защечные, подъязычные, шипучие и формованные таблетки, жесткие или мягкие капсулы, пилюли, пастилки или крахмальные капсулы. Предпочтительными средствами доставки активного начала являются обычные твердые лекарственные формы с энтеросолюбильным покрытием или мягкие капсулы, содержащие жидкие смеси, а также формы или приспособления для непрерывного, замедленного или программированного высвобождения активного начала в желудке, тонком и толстом кишечнике.
Основной мишенью пептидных агонистов LH-RH, соответствующих формуле (I), служит гипофиз, однако было сообщено о прямом действии на сами половые железы (семенники и яичники), на тимус и некоторые лимфоидные линии клеток и на опухоли грудной железы, простаты, поджелудочной железы или нервной системы. На любой чувствительной к LH-RH мишени они проявляют или стимулирующую активность при краткосрочном интенсивном или дробном введении, или ингибирующий эффект при повторном или непрерывном введениях, индуцируя десенсибилизацию и понижая регуляцию рецепторов LH-RH. В случае гипоталамо-гипофизарно-гонадной системы продолжительное введение приводит к так называемой "химической" кастрации.
Основной мишенью пептидных антагонистов, соответствующих формуле (I'), также является гипофиз, где они связываются с рецепторами LH-RH и препятствуют активности эндогенного LH-RH. По этому механизму гипофизарно-гонадная система может быть ингибирована. Программируемое применение антагонистов LH-RH может также иметь преимущество для получения спонтанной стимуляции гипофизарно-гонадной системы в любое заданное время путем прекращения их введения в соответствующий более ранний момент времени.
Следовательно, агонисты или антагонисты LH-RH, соответствующие формуле (А), применимы во всех случаях, когда активности LH-RH должны быть или подавлены, или предотвращены, или стимулированы. Пептидные аналоги по изобретению особенно полезны при лечении заболеваний, чувствительных к LH-RH, a именно заболеваний, при которых требуется агонист или антагонист LH-RH.
Соответственно пероральные фармацевтические композиции по изобретению могут находить надлежащее терапевтическое применение у человека, а также у животных в зависимости от доз и схем лечения, в репродуктивной эндокринологии и в лечении или предупреждении зависимых от половых гормонов доброкачественных и злокачественных опухолей; упомянутое лечение или предупреждение может включать параллельные и/или последовательные дополнительные лечебные или превентивные схемы, основанные на других гормональных или противоопухолевых агентах. Чувствительные к LH-RH независимые от половых гормонов доброкачественные или злокачественные опухоли могут также регрессировать при лечении только пероральными фармацевтическими композициями по изобретению или в сочетании с другой параллельной и/или последовательной противоопухолевой терапией. Иммунные механизмы также могут быть модифицированы с помощью только пероральных фармацевтических композиций по изобретению или в сочетании с другими параллельными и/или последовательными курсами лечения, основанными на иммуномодулирующих или -супрессивных агентах, таких, как глюкокортикоиды, циклоспорин, рапамицин, такролимус, их производные и тому подобное. Вследствие этого пероральные фармацевтические композиции по изобретению очень ценны при лечении и предупреждении аутоиммунных заболеваний, отторжении трансплантата или атопических заболеваниях и при лечении доброкачественных или злокачественных лимфопролиферативных расстройств.
Пероральные фармацевтические композиции по изобретению особенно полезны при подавлении, планировании и запуске овуляции в программах оплодотворения in vitro и в лечении мужского и женского бесплодия или гипогонадных состояний. В противоположность этому они также могут применяться в мужской и женской контрацепции или в лечении гипергонадных состояний. В обоих случаях упомянутое лечение может включать другие параллельные и/или последовательные курсы со стероидными половыми гормонами и/или гонадотропиками. Это применимо к мужчинам и женщинам, но также к диким или домашним животным в таких случаях, как улучшение или контроль детородной функции, или в качестве средства для оптимизации стратегии размножения.
Пероральные фармацевтические композиции по изобретению также особенно полезны в лечении прогрессирующего рака простаты у мужчин, но могут также применяться в качестве терапии первой линии при этом показании и при доброкачественной гипертрофии простаты; в обоих случаях упомянутое лечение может также включать дополнительные параллельные и/или последовательные курсы, основанные на ингибировании действия андрогенов, т.е. на антиандрогенах, таких, как ацетат ципротерона, ацетат осатерона, ацетат хлормадинона, флутамид, нилутамид или бикалутамид и тому подобное, и/или на ингибиторах 5α-редуктазы, таких, как финастерид, эпристерид или туростерид и тому подобное, и/или на ингибиторах C17-C20-лиазы, таких, как абиратерон и тему подобное.
Пероральные фармацевтические композиции по изобретению также особенно полезны в лечении или предупреждении рака грудной железы у женщин и мужчин, особенно положительных по эстрогеновым рецепторам опухолей; упомянутое лечение или предупреждение может включать параллельные или последовательные лечебные или превентивные схемы, основанные на антиэстрогенах, таких, как тамоксифен, ралоксифен или дролоксифен и тому подобное, и/или на ингибиторах ароматазы, таких, как атаместан, форместан, летрозол, анастрозол и тому подобное, и/или на ингибиторах С17-С20-лиазы, таких, как абиратерон и тому подобное. Пероральные фармацевтические композиции по изобретению также очень полезны в лечении или предупреждении некоторых отрицательных по эстрогеновым рецепторам опухолей, которые отвечают на прямые эффекты аналогов LH-RH или косвенно на их гонадосупрессивную активность.
Другие гинекологические проявления, такие, как гиперплазия эндометрия, лейомиома, аденомиома, эндометриоз, синдром поликистоза яичников, гирсутизм и доброкачественные заболевания грудной железы (боль, кисты или фиброз), могут также быть предотвращены или облегчены с помощью лечения пероральными фармацевтическими композициями по изобретению; упомянутое лечение или предотвращение могут включать дополнительные параллельные и/или последовательные лечебные или превентивные курсы, основанные на антиэстрогенах (перечислены выше), прогестинах, таких, как ацетат ципротерона, ацетат осатерона, ацетат хлормадинона, ацетат номегестрола, промегестон, демегестон, тримегестон и тому подобное, и/или их контрацептивных или постклимактерических заместительных комбинированных составов с эстрогенами, такими, как эстрадиол или этинилэстрадиол. Пероральные композиции по изобретению могут также вмешиваться в ход беременности, вызывая аборт или возбуждая родовую деятельность; в этом случае они могут также применяться параллельно или последовательно с курсами лечения, основанными на эстрогенах (перечислены выше), антипрогестинах, таких, как мифепристон и/или аналогах простагландина, таких, как сулпростон.
Подобные показания могут встречаться в ветеринарии для самцов или самок домашних или диких животных, что может потребовать применения фармацевтических композиций по изобретению.
Дополнительный аспект изобретения относится к способу лечения и/или предупреждения указанных выше заболеваний, который включает пероральное введение нуждающимся в этом пациентам или животным фармацевтической композиции по изобретению, упомянутой композиции, включающей эффективное количество пептидного аналога LH-RH, как описано ранее, в комбинации с α-циклодекстрином или его производным. Упомянутый способ может включать дополнительное введение, по меньшей мере, одного из активных элементов, упомянутых выше, таких, как, например, гормональный агент, противоопухолевый агент, иммуномодулирующий или иммуносупрессивный агент, стероидный половой гормон, гонадотропин, ингибитор андрогенного действия, ингибитор 5α-редуктазы, ингибитор C17-C20-лиазы, антиэстроген, ингибитор ароматазы, прогестин, эстроген, антипрогестин или аналог простагландина, причем упомянутое дополнительное введение является параллельным, последовательным или проводится в течение какого-либо периода времени.
Единичная доза для перорального введения аналогов пептидов LH-RH, соответствующих формуле (А), может изменяться от 0,1 до 100 мг на пациента-человека, вводиться от одного до 16 раз в день (в случае дробного введения) в комбинации, по меньшей мере, с эквимолярным количеством α-CD или его производных и вплоть до всей остающейся части перорального состава.
Все вышеупомянутые пероральные фармацевтические композиции могут дополнительно содержать один или несколько ингибиторов протеаз и/или один или несколько других усилителей абсорбции.
Примеры приготовления лейпрорелина, трипторелина, госерелина, деслорелина и составов примеров 1-6 в сочетании со 100 мМ α-CD в растворе
В каждый экспериментальный день растворы α-CD готовили заново путем растворения 9,72 г в 100 мл чистой воды или 4,86 г в 50 мл в течение 1 часа при комнатной температуре с осторожным перемешиванием на магнитной мешалке; между тем соответствующий объем каждого аналога LH-RH брали из оттаявших флаконов с индивидуальным исходным сырьем, содержащих 50 мкг чистого пептида в 50 мкл забуференного фосфатом физиологического раствора, содержащего 0,1% бычьего сывороточного альбумина, чтобы довести до 20 нмоль (24,2 мкл для LEU, 26,2 мкл для TRI, 23,4 мкл для GOS, 25,4 мкл для DES, 24,7 мкл для примера 1, 23,6 мкл для примера 2, 24,5 мкл для примера 3, 25,1 мкл для примера 4, 26,5 мкл для примера 5 и 23,4 мкл для примера 6), и помещали в мерную колбу на 10 мл. Затем прибавляли раствор α-CD, чтобы заполнить колбу до метки 10 мл и получить раствор с концентрацией 2 нмоль/мл, из которого 1 мл вводили перорально каждой крысе с помощью зонда.
Примеры приготовления составов примера 2 в комбинации с 5, 10 или 14% растворами α-CD
В каждый экспериментальный день 45 мкл из одного оттаявшего индивидуального флакона, содержащего 50 мкл чистого пептида из примера 2 в 50 мкл забуференного фосфатом физиологического раствора, содержащего 0,1% бычьего сывороточного альбумина, разводили в 36 мл дистиллированной воды, чтобы получить раствор с концентрацией 1,25 мкг/мл, из которого брали три фракции по 3,8 мл; затем в каждую фракцию прибавляли 190, 380 или 532 мг α-СD, чтобы получить концентрацию 5, 10 или 14%, соответственно. После перемешивания на магнитной мешалке в течение ночи при комнатной температуре каждый раствор давали крысам с помощью перорального зонда в объеме 4 мл/кг, чтобы ввести ту же дозу 5 мкг/кг из примера 2 с увеличивающимися концентрациями α-CD или без них.
Примеры приготовления составов примера 3 для перорального введения в комбинации с производными α-CD
В каждый экспериментальный день замороженные флаконы, содержащие 50 мкг чистого пептида из примерз 3 в 50 мкл забуференного фосфатом физиологического раствора, содержащего 0,1% бычьего сывороточного альбумина, оттаивали и разбавляли пополам равным объемом такого же раствора свежего бычьего сывороточного альбумина. Затем прибавляли 12,5 мкл этого раствора с концентрацией 0,5 мкг/мкл к 5 мл водного носителя для перорального введения (с производным α-CD или без него), чтобы получить после осторожного перемешивания на магнитной мешалке в течение ночи конечный состав, содержащий 1,25 мкг/мл пептида из примера 3, для введения с помощью зонда при объеме 4 мл/кг.
Растворы производных α-CD получали путем взвешивания соответствующего количества, чтобы поместить в мерные колбы на 10 мл, заполненные до метки водой: 5 г карбоксиметилированого α-CD (50%), 3 г метиллированного α-CD (30%), 3 г фосфорилированного α-CD (30%) или 1 г, или 1,5 г перметилированного α-CD (10 или 15%).
Соответствующие объемы подходящих разведении 50 мкг/50 мкл исходных находящихся во флаконах растворов чистого состава примера 3 прибавляли к 10%-ным растворам α-CD или перметилированного α-CD в воде, чтобы получить интервал доз, показанный на фиг.7.
Примеры приготовления составов для перорального введения антида в комбинации с α-, β- и γ-CD
Каждые 5 мг порошка антида из флакона (от фирмы Bachem, Bubendorf, Switzerland), содержащего 4,2434 мг чистого пептида, растворяли в смеси 2,122 мл пропиленгликоля с 8,487 мл воды, содержащей 0,1% бычьего альбумина. К каждым 10,609 мл раствора антида (400 мкг/мл) немедленно прибавляли 1,061 г или α-, β- или γ-CD, чтобы получить концентрацию 10%. Каждая крыса-самка получала одинаковый объем 1 мл тестируемого состава с помощью зонда.
Такой же объем использовали для введения доз 200 и 600 мкг/крысу. Подходящие концентрации вводимого антида (200 и 600 мкг/мл) получали соответственно путем разбавления наполовину раствора с концентрацией 400 мкг/мл с той же самой смесью (20 об.% пропиленгликоля/80 об.% раствора альбумина в воде/10 вес.% α-CD) и путем растворения других 5 мг порошка из флакона в смеси 1,415 мл пропиленгликоля с 5,658 мл воды, заранее содержащей 0,1% бычьего альбумина, к которой в заключение прибавляли 0,707 мг α-CD.
| название | год | авторы | номер документа |
|---|---|---|---|
| АНАЛОГИ ПЕПТИДА ЛГ-РФ, ИХ ПРИМЕНЕНИЕ И СОДЕРЖАЩИЕ ИХ ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ | 1998 |
|
RU2212247C2 |
| ПРОИЗВОДНЫЕ МЕТАСТИНА И ИХ ПРИМЕНЕНИЕ | 2007 |
|
RU2454425C2 |
| ПРОИЗВОДНЫЕ МЕТАСТИНА И ИХ ПРИМЕНЕНИЕ | 2006 |
|
RU2430107C2 |
| АГОНИСТЫ РЕЦЕПТОРОВ НЕЙРОМЕДИНА В И СОМАТОСТАТИНА | 2000 |
|
RU2263680C2 |
| ПЕПТИДНЫЕ КОМПОЗИЦИИ | 2014 |
|
RU2725150C2 |
| НОВЫЕ АНАЛОГИ ГЛЮКАГОН-ПОДОБНОГО ПЕПТИДА, КОМПОЗИЦИЯ И СПОСОБ ПРИМЕНЕНИЯ | 2010 |
|
RU2557301C2 |
| ПИРИМИДИНОВОЕ СОЕДИНЕНИЕ ИЛИ ЕГО СОЛЬ | 2020 |
|
RU2787992C1 |
| ПРОИЗВОДНЫЕ 5-АРИЛ-1Н-1,2,4-ТРИАЗОЛА И СОДЕРЖАЩАЯ ИХ ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 2000 |
|
RU2249588C2 |
| АНТАГОНИСТИЧЕСКИЕ АНАЛОГИ РИЛИЗИНГ-ГОРМОНА ГОРМОНА РОСТА (GH-RH), ИНГИБИРУЮЩИЕ ИНСУЛИНОПОДОБНЫЕ ФАКТОРЫ РОСТА (IGF-I И-II) | 1999 |
|
RU2235099C2 |
| Лечение гипопаратиреоидизма | 2021 |
|
RU2827712C1 |



Изобретение относится к области медицинской эндокринологии. Сущность изобретения составляет применение по новому назначению α-циклодекстрина, а именно для обеспечения перорального введения пептидных аналогов рилизинг-гормона лютеинизирующего гормона (LH-RH). Изобретение содержит также сведения о фармацевтических композициях, включающих α-циклодекстрин или его производные и упомянутые пептидные аналоги LH-RH. Технический результат изобретения - расширение арсенала неинвазивных средств для устранения эндокринологических нарушений у женщин. 2 c. и 32 з.п. ф-лы, 7 ил., 4 табл.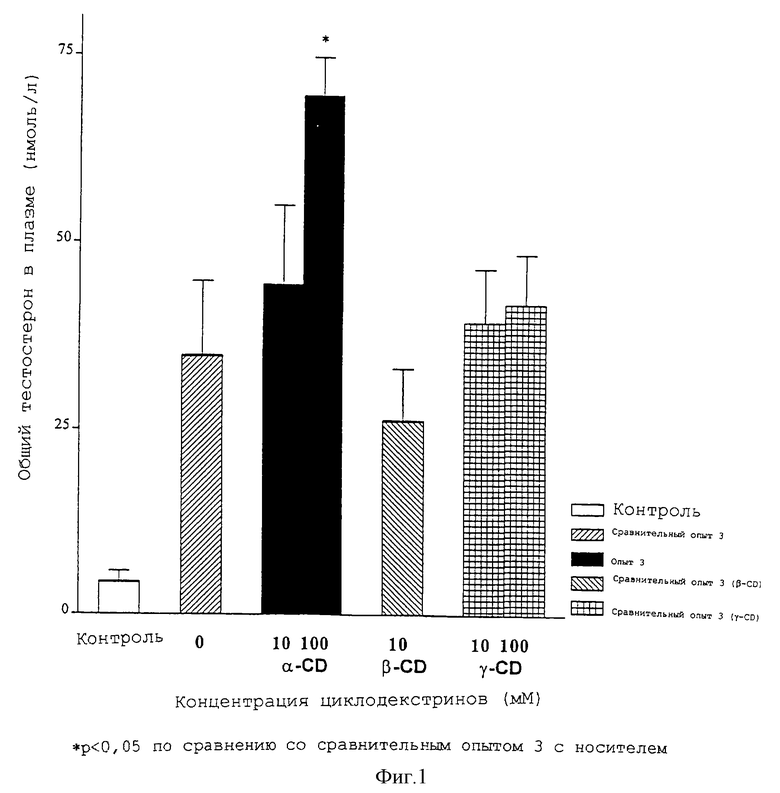
A1-A2-A3-A4-A5-A6-A7-A8-Pro-Z, (A)
где А1 означает pGlu; D-pGlu; Sar; AcSar; Pro или их производные; Ser; D-Ser; Ac-D-Ser; Thr; D-Thr; Ac-D-Thr; или необязательно замещенную и/или ацилированную ароматическую D-аминокислоту;
А2 означает непосредственную связь; His; или необязательно замещенную ароматическую D-аминокислоту;
A3 означает необязательно замещенную ароматическую L- или D-аминокислоту;
А4 означает Ala, Ser, D-Ser, MeSer, Sеr(ОВut), Ser(OBzl) или Thr;
А5 означает необязательно замещенную ароматическую L-аминокислоту или необязательно замещенную основную L- или D-аминокислоту;
А6 означает Gly; (S)-спиролактам-Рrо; D-Pro; D-Ser; D-Thr; D-Cys; D-Met; D-Asn; D-Pen; D-(S-Me)Pen; D-(S-Et)Pen; D-Ser(OBut); D-Аsр(OBut); D-Glu(OBut); D-Thr(OBut); D-Cys(OBut); D-Ser(OR1), где R1 означает остаток углевода; азааминокислоту; D-His, который может быть замещен по имидазольному кольцу (С1-С6)-алкильной, (С2-С7)-ацильной или бензильной группой; алифатическую D-аминокислоту с (С1-С8)-алкильной или (С3-С6)-циклоалкильной боковой цепью; необязательно замещенную ароматическую D-аминокислоту; D-циклогексадиенил-Glу; D-пергидронафтил-Аlа, D-пергидродифенил-Аlа; или необязательно замещенную основную L- или D-аминокислоту;
А7 означает линейную, разветвленную или циклическую алифатическую L-аминокислоту из 3-20 атомов углерода, которая может быть N-α-замещена (С1-С4)-алкильной группой, необязательно замещенной одним или несколькими атомами фтора;
А8 означает необязательно замещенную основную L- или D-аминокислоту;
Z означает GlyNH2; D-AlaNH2; azaGlyNH2; или группу -NHR2, где R2 означает (C1-C4)-алкил, который может быть замещен гидроксильной группой или одним или несколькими атомами фтора; (С3-С6)-циклоалкил; или гетероциклический радикал, выбранный из морфолинильного, пирролидинильного и пиперидильного.
A1-His-A3-A4-A5-A6-A7-A8-Pro-Z, (I)
где А1 означает pGlu, Sar или AcSar;
A3 означает необязательно замещенную ароматическую L-аминокислоту;
А4 означает Ala, Ser, D-Ser, MeSer, Ser(OBut), Ser(OBzl) или Thr;
A5 означает необязательно замещенную ароматическую L-аминокислоту;
А6 означает Gly; D-Pro; (S)-спиролактам-Pro; D-Ser; D-Thr; D-Cys; D-Met; D-Pen; D-(S-Me)Pen; D-(S-Et)Pen; D-Ser(OBut); D-Asp(OBut); D-Glu(OBut); D-Thr(OBut); D-Cys(OBut); D-Ser(OR1), где R1 означает остаток углевода; азааминокислоту; D-His, который может быть замещен по имидазольному кольцу (C1-C6)-алкильной или бензильной группой; алифатическую D-аминокислоту с (C1-C8)-алкильной или (С3-С6)-циклоалкильной боковой цепью; необязательно замещенную ароматическую D-аминокислоту; D-циклогексадиенил-Gly; D-пepгидpoнaфтил-Ala, D-пергидродифенил-Аlа; или необязательно замещенную основную D-аминокислоту;
А7 означает линейную, разветвленную или циклическую алифатическую L-аминокислоту из 3-20 атомов углерода, которая может быть N-α-замещена (C1-C4)-алкильной группой, необязательно замещенной одним или несколькими атомами фтора;
А8 означает необязательно замещенную основную L-аминокислоту;
Z означает GlyNH2; azaGlyNH2; или группу -NHR2, где R2 означает (C1-C4)-алкил, который может быть замещен гидроксильной группой или одним или несколькими атомами фтора; (С3-С6)-циклоалкил; или гетероциклический радикал, выбранный из морфолинила, пирролидинила и пиперидила.
pGlu-His-A3-Ser-A5-A6-A7-Arg-Pro-Z, (II)
где А7 означает Leu, Tle, Nle, Hol, Npg, Cha или Ada, которые могут быть N-α-замещены метильной или этильной группой, необязательно замещенной одним или несколькими атомами фтора.
pGlu-His-A3-Ser-A5-A6-A7-Arg-Pro-Z, (III)
где A3 и А5 означают каждый независимо Phe, Туr, Тrр, 2MeTrp, HPhe, HTyr, Nal, 1Nal, Bal, Pal, 4Pal или pClPhe;
А6 означает (S)-спиролактам-Рrо; Gly; D-Pro; D-Ser(OBut); В-Аsр(OBut); D-Glu(OBut); D-Thr(OBut); D-Cys(OBut); D-His или D-His(Bzl); D-Ala, D-Leu, D-Tle, D-Nle, D-Hol, D-Npg или D-Cha; D-Phe, D-HPhe, D-Tyr, D-HTyr, D-Trp, D-2MeTrp, D-Nal, D-1Nal, D-Bal, D-Pal, D-4 Pal или D-pClPhe; D-циклогексадиенил-Glу; D-пергидронафтил-Ala; D-пергидродифенил-Аlа; или D-Phe, необязательно замещенный аминотриазолильной группой;
А7 означает Leu, Npg или Cha, которые могут быть N-α-замещены метильной группой;
Z означает GlyNH2; azaGlyNH2 или -NC2H5.
pGlu-His-Trp-Ser-Tyr-A6-A7-Arg-Pro-Z, (IV)
где А6 означает (S)-спиролактам-Рrо, D-Leu, D-Ala, D-Nal, D-Phe, D-Ser(OBut) или D-Trp;
A7 означает Leu, MeLeu, Npg или MeNpg;
Z означает GlyNH2; azaGlyNH2 или -NC2H5.
A1-A2-A3-A4-A5-A6-A7-A8-Pro-Z, (I')
где A1 означает pGlu; D-pGlu; Sar; AcSar; Pro или их производные; Ser; D-Ser; Ac-D-Ser; Thr; D-Thr; Ac-D-Thr или необязательно замещенную и/или ацилированную ароматическую D-аминокислоту;
А2 означает непосредственную связь или необязательно замещенную ароматическую D-аминокислоту;
A3 означает необязательно замещенную ароматическую L- или D-аминокислоту;
А4 означает Ala, Ser, D-Ser, MeSer, Ser(OBut), Ser(OBzl) или Thr;
А5 означает необязательно замещенную ароматическую L-аминокислоту или необязательно замещенную основную L- или D-аминокислоту;
А6 означает Gly; (S)-спиролактам-Pro; D-Pro; D-Ser; D-Thr; D-Cys; D-Met; D-Asn; D-Pen; D-(S-Me)Pen; D-(S-Et)Pen; D-Ser(OBut); D-Asp(OBut); D-Glu(OBut); D-Thr(OBut); D-Cys(OBut); D-Ser(OR1), где R1 означает остаток углевода; алифатическую D-аминокислоту с (C1-С8)-алкильной или (С3-С6)-циклоалкильной боковой цепью; необязательно замещенную ароматическую D-аминокислоту; D-циклoгeкcaдиeнил-Gly; D-пepгидpoнaфтил-Ala; D-пергидродифенил-Ala; или необязательно замещенную основную L- или D-аминокислоту;
А7 означает линейную, разветвленную или циклическую алифатическую L-аминокислоту из 3-20 атомов углерода, которая может быть N-α-замещена (C1-C4)-алкильной группой, необязательно замещенной одним или несколькими атомами фтора;
А8 означает необязательно замещенную основную L- или D-аминокислоту;
Z означает GlyNH2; D-AlaNH2.
Ac-D-Nal-D-pClPhe-D-Pal-Ser-A5-A6-A7-A8-Pro-D-AlaNH2, (II')
где А5 означает Туг, HTyr, MeTyr, MeHTyr, NicLys или IprLys;
А6 означает (S)-спиролактам-Рrо, D-Arg, D-NicLys, D-IprLys, D-Cit, D-HCit или D-Asn;
A7 означает Leu, MeLeu, Npg или MeNpg;
A8 означает Arg, NicLys или IprLys.
A1-A2-A3-A4-A5-A6-A7-A8-Pro-Z, (A)
где А1 означает pGlu; D-pGlu; Sar; AcSar; Pro или их производные; Ser; D-Ser; Ac-D-Ser; Thr; D-Thr; Ac-D-Thr; или необязательно замещенную и/или ацилированную ароматическую D-аминокислоту;
А2 означает непосредственную связь; His; или необязательно замещенную ароматическую D-аминокислоту;
A3 означает необязательно замещенную ароматическую L- или D-аминокислоту;
А4 означает Ala, Ser, D-Ser, MeSer, Ser(OBut), Ser(OBzl) или Thr;
A5 означает необязательно замещенную ароматическую L-аминокислоту или необязательно замещенную основную L- или D-аминокислоту;
А6 означает Gly; (S)-спиролактам-Рrо; D-Pro; D-Ser; D-Thr; D-Cys; D-Met; D-Asn; D-Pen; D-(S-Me)Pen; D-(S-Et)Pen; D-Ser(OBut); D-Asp(OBut); D-Glu(O-But); D-Thr(OBut); D-Cys(OBut); D-Ser(OR1), где R1 означает остаток углевода; азааминокислоту; D-His, который может быть замещен по имидазольному кольцу (C1-C6)-алкильной, (C2-C7)-ацильной или бензильной группой; алифатическую D-аминокислоту с (C1-C8)-алкильной или (С3-С6)-циклоалкильной боковой цепью; необязательно замещенную ароматическую D-аминокислоту; D-циклoгeкcaдиeнил-Gly; D-пергидронафтил-Ala; D-пергидродифенил-Аlа; или необязательно замещенную основную L- или D-аминокислоту;
А7 означает линейную, разветвленную или циклическую алифатическую L-аминокислоту из 3-20 атомов углерода, которая может быть N-α-замещена (C1-C4)-алкильной группой, необязательно замещенной одним или несколькими атомами фтора;
А8 означает необязательно замещенную основную L- или D-аминокислоту;
Z означает GlyNH2; D-AlaNH2; azaGlyNH2; или группу -NHR2, где R2 означает (C1-C4)-алкил, который может быть замещен гидроксильной группой или одним или несколькими атомами фтора; (С3-С6)-циклоалкил; или гетероциклический радикал, выбранный из морфолинила, пирролидинила и пиперидила.
A1-His-A3-A4-A5-A6-A7-A8-Pro-Z, (I)
где А1 означает pGlu, Sar или AcSar;
A3 означает необязательно замещенную ароматическую L-аминокислоту;
А4 означает Ala, Ser, D-Ser, MeSer, Ser(OBut), Ser(OBzl) или Thr;
A5 означает необязательно замещенную ароматическую L-аминокислоту;
А6 означает Gly; D-Pro; (S)-спиролактам-Рrо; D-Ser; D-Thr; D-Cys; D-Met; D-Pen; D-(S-Me)Pen; D-(S-Et)Pen; D-Ser (OBut); D-Asp(OBut); D-Glu(OBut); D-Thr(OBut); D-Cys(OBut); D-Ser(OR1), где R1 означает остаток углевода; азааминокислоту; D-His, который может быть замещен по имидазольному кольцу (C1-С6)-алкильной или бензильной группой; алифатическую D-аминокислоту с (C1-C8)-алкильной или (С3-С6)-циклоалкильной боковой цепью; необязательно замещенную ароматическую D-аминокислоту; D-циклогексадиенил-Gly; D-пергидронафтил-Аlа; D-пергидродифенил-Аlа; или, возможно, замещенную основную D-аминокислоту;
А7 означает линейную, разветвленную или циклическую алифатическую L-аминокислоту из 3-20 атомов углерода, которая может быть N-α-замещена (C1-C4)-алкильной группой, необязательно замещенной одним или несколькими атомами фтора;
А8 означает необязательно замещенную основную L-аминокислоту;
Z означает GlyNH2; azaGlyNH2; или группу -NHR2, где R2 означает (C1-C4)-алкил, который может быть замещен гидроксильной группой или одним или несколькими атомами фтора; (С3-С6)-циклоалкил; или гетероциклический радикал, выбранный из морфолинила, пирролидинила и пиперидила.
pGlu-His-A3-Ser-A5-A6-A7-Arg-Pro-Z, (II)
где А7 означает Leu, Tle, Nle, Hol, Npg, Cha или Ada, которые могут быть N-α-замещены метильной или этильной группой, необязательно замещенной одним или несколькими атомами фтора.
pGlu-His-A3-Ser-A5-A6-A7-Arg-Pro-Z, (III)
где A3 и А5 означают каждый независимо Phe, Туr, Тrр, 2MeTrp, HPhe, HTyr, Nal, 1Nal, Bal, Pal, 4Pal или pClPhe;
А6 означает (S)-спиролактам-Рrо; Gly; D-Pro; D-Ser(OBut);
D-Asp (OBut); D-Glu(OBut); D-Thr(OBut); D-Cys(OBut); D-His или D-His(Bzl); D-Ala, D-Leu, D-Tle, D-Nle, D-Hol, D-Npg или D-Cha; D-Phe, D-HPhe, D-Tyr, D-HTyr, D-Trp, D-2MeTrp, D-Nal, D-1Nal, D-Bal, D-Pal, D-4Pal или D-pClPhe; D-циклогексадиенил-Сlу; D-пергидронафтил-Аlа; D-пергидродифенил-Ala; или D-APhe, необязательно замещенный аминотриазолильной группой;
А7 означает Leu, Npg или Cha, которые могут быть N-α-замещены метильной группой;
Z означает GlyNH2; azaGlyNH2 или -NC2H5.
pGlu-His-Trp-Ser-Tyr-A6-A7-Arg-Pro-Z, (IV)
где А6 означает (S)-спиролактам-Рrо, D-Leu, D-Ala, D-Nal, D-Phe, D-Ser(OBut) или D-Trp;
A7 означает Leu, MeLeu, Npg или MeNpg;
Z означает GlyNH2; azaGlyNH2 или -NC2H5.
A1-A2-A3-A4-A5-A6-A7-A8-Pro-Z, (I')
где А1 означает pGlu; D-pGlu; Sar; AcSar; Pro или их производные; Ser; D-Ser; Ac-D-Ser; Thr; D-Thr; Ac-D-Thr или необязательно замещенную и/или ацилированную ароматическую D-аминокислоту;
А2 означает непосредственную связь или необязательно замещенную ароматическую D-аминокислоту;
A3 означает необязательно замещенную ароматическую L- или D-аминокислоту;
А4 означает Ala, Ser, D-Ser, MeSer, Ser(OBut), Ser(OBzl) или Thr;
А5 означает необязательно замещенную ароматическую L-аминокислоту или необязательно замещенную основную L- или D-аминокислоту;
А6 означает Gly; (S)-спиролактам-Рrо; D-Pro; D-Ser; D-Thr; D-Cys; D-Met; D-Asn; D-Pen; D-(S-Me)Pen; D-(S-Et)Pen; D-Ser(OBut); D-Asp(OBut); D-Glu(OBut); D-Thr(OBut); D-Cys(OBut); D-Ser(OR1), где R1 означает остаток углевода; алифатическую D-аминокислоту с (C1-C8)-алкильной или (С3-С6)-циклоалкильной боковой цепью; необязательно замещенную ароматическую D-аминокислоту; D-циклогексадиенил-Gly; D-пepгидpoнaфтил-Ala; D-пергидродифенил-Ala; или необязательно замещенную основную L- или D-аминокислоту;
А7 означает линейную, разветвленную или циклическую алифатическую L-аминокислоту из 3-20 атомов углерода, которая может быть N-α-замещена (C1-C4)-алкильной группой, необязательно замещенной одним или несколькими атомами фтора;
А8 означает необязательно замещенную основную L- или D-аминокислоту;
Z означает GlyNH2 или D-AlaNH2.
Ac-D-Nal-D-pClPhe-D-Pal-Ser-A5-A6-A7-A8-Pro-D-AlaNH2, (II')
где А5 означает Туг, HTyr, MeTyr, MeHTyr, NicLys или IprLys;
А6 означает (S)-спиролактам-Рrо, D-Arg, D-NicLys, D-IprLys, D-Cit, D-HCit или D-Asn;
A7 означает Leu, MeLeu, Npg или MeNpg;
A8 означает Arg, NicLys или IprLys.
| АЛМАЗНАЯ КОРОНКА | 0 |
|
SU308181A1 |
| US 4659696 А, 21.04.1887 | |||
| Mitsubara et al | |||
| J | |||
| Pharm | |||
| Sci., 1996, 84(11), p.1295-1300. | |||
Авторы
Даты
2003-10-20—Публикация
1999-09-23—Подача