Изобретение относится к химико-фармацевтической промышленности, медицине, фармакологии и касается получения сульфатированных биополимеров на основе арабиногалактана, обладающих широким спектром фармакологической активности, в частности антикоагулянтной, гиполипидемической и т.д.
Описывается способ получения сульфатированных производных арабиногалактана, выделенного из лиственницы сибирской, путем его взаимодействия с калием надсернокислым (калием персульфатом, K2S2O8) в присутствии свежеперегнанного диметилсульфоксида (ДМСО) в течение не более 12 часов при температуре не более +50°С, с дальнейшей его нейтрализацией или без нее, ультрафильтрацией и сублимацией или распылительной сушкой.
Описаны сульфатированные производные арабиногалактана формулой AG-SO3R,
где AG - арабиногалактан,
SO3R - сульфатная группировка,
R=H - кислотная форма сульфатированного производного AG,
R=Me - солевая форма, где Me - металлы I и II групп.
Степень замещения макромолекулы биополимера в пересчете на количественное содержание серы составляет 9,3-14.2%.
В литературе известно несколько способов получения сульфатированного производного AG как в кислотной, так и в солевой формах, а именно:
1. Chemical Abstracts 1968, vol.69, №11, 44182q.
2. Kamitakahara H., Mikawa Y., Hori M., Tsujihata S., Minato K., Nakatsubo F. Syntheses, characterization, and biological activities of sulfated polysaccharides // 10th Int. Symp. on Wood Pulp Chem. Yokohama, Japan. 1999. Vol.2. P.238-241.
3. CN 01054420 (2007 г.).
4. RU 2466143 (2012 г.).
Во всех этих литературных источниках в качестве сульфатирующей смеси используется комплекс SO3 (серный ангидрид) - пиридин в чистом виде (1, 4) или в присутствии диметилформамида (ДМФА) (2, 3). Сульфатирование AG проводят в различном температурном диапазоне (t=20; 50-55; 65; 70; 85; 95°C), варьируя время реакции от 0,5-3 часов до нескольких дней.
Кроме того, в литературном источнике 1 описан способ получения сульфатированных производных AG еще и комплексом SO3 - триэтиламин. При этом сульфатирование происходит в течение 3 часов при 50-55°C, затем 2 часа при t=20°C.
Все вышеперечисленные сульфатирующие смеси имеют ряд недостатков:
1. Получение комплекса SO3 - пиридин производят путем добавления хлорсульфоновой кислоты к избытку пиридина. При этом кроме сульфатирующего комплекса образуется побочный продукт пиридинийхлорид, присутствие которого трудно устранимо. А его наличие в реакционной смеси ведет к получению сульфатированных производных полисахарида пониженной физиологической активности.
2. При использовании этих сульфатирующих смесей встает проблема устранения стойкого неприятного запаха конечных продуктов, к тому же комплекс SO3 - триэтиламин является очень токсичным.
3. Если в качестве растворителя как сульфатирующей смеси, так и самого AG используется ДМФА (способ 2, 3), то это ведет к снижению эффективности реакции, т.к. AG в ДМФА не растворяется, следовательно образуется гетерогенная система синтеза.
4. Температура и время реакции существенным образом влияют на строение и выход конечного продукта. И не важно, проводят сульфатирование AG в течение 0,5-3 ч, но при высокой t=50-95°C или в течение нескольких дней при t=20°C, в любом случае это приводит к деградации молекулы полисахарида.
Существенно отличающимся от вышеперечисленных способов (1-4) получения сульфатированных производных AG является следующий способ 5, описанный в RU 2319707 (2008). Где в качестве сульфатирующей смеси используется комплекс SO3 - ДМФА с концентрацией SO3 не менее 18%.
Этот способ имеет ряд технологических недостатков:
1. Комплекс SO3 - ДМФА получают путем перегонки газообразного SO3 из олеума в свежеперегнанный ДМФА. Это весьма опасный процесс, т.к. олеум и серный ангидрид обладают сильным разъедающим действием. К тому же это чисто лабораторный способ, который очень трудно воспроизвести в промышленном масштабе в виду технологических сложностей.
2. Данный способ, а также способы 2 и 3 предполагают проведение таких трудоемких и малопроизводительных технологических операций, как очистка от низкомолекулярных примесей методом диализа в течение 5-7 дней. В результате процесс получения сульфатированных производных AG является длительным, что приводит к снижению выхода конечного продукта, изменению его внешнего вида и элементного состава вследствие возможной деструкции и деградации макромолекулы биополимера. При этом диализ характеризуется большим расходом электроэнергии и дистиллированной воды, так как для полной очистки образца от примесей требуется многократная замена диализной среды.
3. В способах 1 и 4 очистка от низкомолекулярных примесей вообще никак не проводится, а как указывают авторы изобретения (4), для повышения эффективности и сокращения продолжительности процесса используется только очистка конечного продукта осаждением в этанол с последующим его промыванием этанолом. Данная процедура никоим образом не способствует очистке сульфатированных производных AG от низкомолекулярных примесей, образующихся в процессе нейтрализации реакционной среды, к тому же AG и его сульфатированные производные способны к адсорбированию неорганических ионов, в частности сульфат-анионов, что в результате приводит к получению завышенных показателей количественного содержания серы (%) и получению конечных продуктов с очень низкой фармакологической активностью (Дрозд Н.Н., Кузнецова С.А., Лапикова B.C., Давыдова А.И., Макаров В.А., Кузнецов Б.Н., Бутылкина А.И., Васильева Н.Ю., Скворцова Г.П. Антикоагулянтная активность in vitro сульфатированного арабиногалактана и экстракта коры кедра // экспериментальная и клиническая фармакология. - 2008. - Т.71. №4. - С.30-34.)
Наиболее близкими к заявляемому способу сульфатирования AG являются SU 1244151 (6) и Капутский Ф.Н., Торгашов В.И., Юркштович Т.Л., Голуб Н.В., Островская И.Л., Алиновская В.А. Исследование процесса сульфатирования полисахаридов пиросульфатом натрия в среде диметилсульфоксида // Журнал прикладной химии. - 2007. - Т.80. №10. - С.1716-1720 (7), где в качестве сульфатирующих агентов для полисахаридов (амилопектин, крахмал, целлюлоза и декстран) использованы неорганические соли, такие как KHSO3 - гидросульфит калия, Na2SO3 - сульфит натрия, Na2SaO5 - пиросульфит натрия, Na2SO4 - сульфат натрия, Na2S3O10 - натриевая соль трисерной кислоты (6) и Na2S2O7 - пиросульфат натрия (7).
Эти способы имеют ряд недостатков:
1. В качестве реакционной среды в способе 6 применяются высокотоксичные растворители 2 класса опасности (диметилацетамид и ДМФА).
2. Использование в качестве сульфатирующих агентов вышеперечисленных солей подразумевает их длительное (до 48 часов) воздействие на полисахарид, что может привести к деградации макромолекул биополимеров.
3. Получаемые сульфатированные производные характеризуются небольшим количественным содержанием серы от 0-12,1%, которое существенно зависит от температуры и продолжительности реакции. Так как максимальные значения количественного содержания серы в 9,4-10,5% у производных полисахаридов, полученных по способу 7, достигаются при использовании высокой температуры +60°C, а максимальные значения количественного содержания серы в 9,38-12,1% у производных полисахаридов, полученных по способу 6, достигаются не менее чем за 24 часа.
Техническим результатом предлагаемого изобретения является разработка высокотехнологичного способа сульфатирования полисахаридов, в частности AG.
Технический результат данного изобретения достигается тем, что для получения сульфатированных производных AG используются нетоксичные реагенты 3 класса опасности (диметилсульфоксид (ДМСО) и калий надсернокислый [персульфат калия] (K2S2O8)); сам процесс сульфатирования проводится в мягких условиях (t≤+50°C, время реакции не более 12 часов), для очистки и выделения конечных продуктов используются совокупности высокотехнологичных процессов ультрафильтрации и сублимационной или распылительной сушки, что позволяет повысить эффективность и рентабельность процесса сульфатирования, а в дальнейшем будет способствовать масштабированию процесса получения сульфатированных производных AG.
Сущность заявляемого изобретения состоит в следующем.
Сульфатированные производные AG получают путем взаимодействия раствора AG в ДМСО с K2S2O8 при массовом соотношении (1:3-10:5-10) при непрерывном перемешивании, t≤+50°C, не более 12 часов. После этого реакционную смесь нейтрализуют 10% водным раствором гидроксидов металлов (КОН, NaOH, Са(ОН)2, Ва(ОН)2, Zn(ОН)2, Cu(ОН)2 и т.д.) или сухими порошками оксидов металлов (CaO, ZnO и т.д.), фильтруют через нутч-фильтр с фильтрующим диском размером пор не более 100 микрон. Полученный фильтрат замораживают и подвергают сублимации при t≤-85°C, затем проводят очистку от низкомолекулярных примесей методом ультрафильтрации через полиэфирсульфоновый мембранный модуль с размером пор 1-5 кДальтон. Полученный ретант замораживают и подвергают сублимации при t≤-55°C или высушивают в распылительной сушилке при температуре на входе не более +120°C, а на выходе +50°C.
Заявленный способ позволяет получить сульфатированные производные AG как в кислотной, так и в солевой формах. Кислотную форму сульфатированных производных AG получают без нейтрализации реакционной смеси. Для этого ее сразу же фильтруют через нутч-фильтр с фильтрующим диском размером пор не более 100 микрон. Далее поступают, как описано выше.
Предлагаемый способ характеризуется следующими преимуществами:
1. В качестве сульфатирующего агента используется K2S2O8 - широкодоступный, нетоксичный и дешевый реактив.
2. Для очистки сульфатированных производных AG от низкомолекулярных веществ в отличие от всех вышеназванных способов (1-7) применен метод ультрафильтрации, позволяющий сократить время очистки с 5-7 дней (диализ) до 2-3 часов. При этом достигаются высокие выходы конечных продуктов до 95-99% вследствие исключения возможной деструкции и деградации макромолекулы биополимера.
3. Для оптимизации процесса выделения сульфатированных производных AG как на промежуточной, так и на конечной стадиях технологического процесса используются такие способы сушки, как распылительная или сублимационная. Их применение позволяет исключить использование больших количеств органических растворителей (этанола) и в несколько раз увеличить производительность данной стадии.
Полученные сульфатированные производные AG сохраняют структурную организацию, водорастворимость и мембранотропность исходного природного полисахарида, обладают широким спектром фармакологической активности, в частности антикоагулянтной, гиполипидемической и т.д.
Ранее было показано (патент 2319707 и Костыро Я.А. Разработка технологии получения, исследование свойств сульфатированного арабиногалактана и создание таблетированной лекарственной формы препарата антикоагулянтного и гиполипидемического действия: автореф. дис.: канд. фарм. наук: 15.00.01; 15.00.02 - М., 2008. - 23 с.), что получаемые согласно способу 5 сульфатированные производные AG являются веществами малотоксичными (LD50=>5 г/кг) и обладают высокой фармакологической активностью (например, "терапевтическая" гипокоагуляционная доза в опытах in vitro равна 0,025 мг/мл плазмы). Сульфатированные производные AG, получаемые согласно заявляемому способу, обладают аналогичной активностью в концентрациях, не превосходящих исходную, что свидетельствует о полной идентичности сравниваемых соединений. Полученные результаты подтверждаются и данными, полученными физико-химическими методами (структурная организация, содержание сульфатных группировок, растворимость и т.д.).
Содержание сульфатных группировок в полученных препаратах определяли в пересчете на количественное содержание серы титриметрическим методом (барийметрией) с использованием специфических реагентов. Количественный анализ полученных заявляемым способом сульфатированных производных AG показал, что независимо от способа получения (заявляемый или способ 5) степень замещения макромолекулы биополимера в пересчете на количественное содержание серы в соединениях составляет 9.3-14.2% и 8.1-12.6% соответственно.
Следующие примеры иллюстрируют изобретение:
Пример 1.
1 г AG растворяли при перемешивании в 8 мл ДМСО, затем добавляли 9 г K2S2O8. Сульфатирование проводили при интенсивном перемешивании при t=+50°C не более 6 часов. После этого реакционную смесь нейтрализовали 18 мл 10% водного раствора КОН и фильтровали через нутч-фильтр с фильтрующим диском размером пор не более 100 микрон. Полученный фильтрат замораживали при t=-40°C и сублимировали при t≤-85°C не более 6 часов, затем полученную сухую массу растворяли в 150 мл дистиллированной воды и проводили очистку от низкомолекулярных примесей методом ультрафильтрации через полиэфирсульфоновый мембранный модуль с размером пор 1-5 кДальтон в течение 1 часа. Полученный ретант распыляли через пневматическую форсунку (размер капель до 150 мкм) в течение 15 минут при давлении в системе -65 мБар и температуре на входе распылительной сушилки +120°C, а на выходе +50°C.
Выход полученного продукта составил 98%, степень замещения макромолекулы биополимера в пересчете на количественное содержание серы составила 14.2%.
Пример 2.
1 г AG растворяли при перемешивании в 5,5 мл ДМСО, затем добавили 8 г K2S2O8. Сульфатирование проводили при интенсивном перемешивании при t=+40°C не более 9 часов. После этого реакционную смесь добавляли к 15 мл дистиллированной воды и нейтрализовали 2 г ZnO, фильтровали через нутч-фильтр с фильтрующим диском размером пор не более 100 микрон. Полученный фильтрат замораживали при t=-40°C и сублимировали при t≤-85°C не более 6 часов, затем полученную сухую массу растворяли в 150 мл дистиллированной воды и проводили очистку от низкомолекулярных примесей методом ультрафильтрации через полиэфирсульфоновый мембранный модуль с размером пор 1-5 кДальтон в течение 1 часа.
Полученный ретант замораживали при t=-40°C и подвергали сублимации при t≤-55°C не более 3 часов.
Выход полученного продукта составил 96%, степень замещения макромолекулы биополимера в пересчете на количественное содержание серы составила 13.0%.
Пример 3.
1 г AG растворяли при перемешивании в 3 мл ДМСО, затем добавляли 5 г K2S2O8. Сульфатирование проводили при интенсивном перемешивании при t=+30°C не более 3 часов. После этого реакционную смесь фильтровали через нутч-фильтр с фильтрующим диском размером пор не более 100 микрон. Полученный фильтрат замораживали при t=-40°C и сублимировали при t≤-85°C не более 6 часов, затем полученную сухую массу растворяли в 150 мл дистиллированной воды и проводили очистку от низкомолекулярных примесей методом ультрафильтрации через полиэфирсульфоновый мембранный модуль с размером пор 1-5 кДальтон в течение 1 часа. Полученный ретант замораживали при t=-40°C и подвергали сублимации при t≤-55°C не более 3 часов.
Выход полученного продукта составил 95%, степень замещения макромолекулы биополимера в пересчете на количественное содержание серы составила 9.3%.
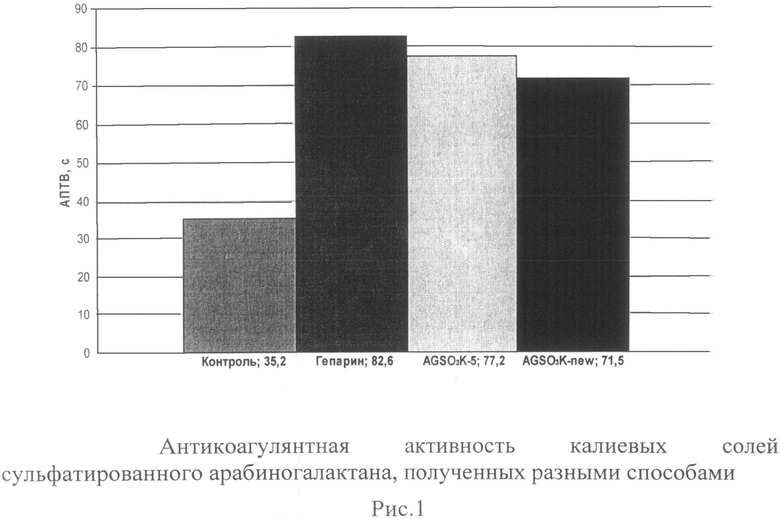
Сравнение антикоагулянтной активности сульфатированных производных AG, полученных заявляемым и №5 способами.
Исследование проводили в опытах in vitro на референтной нормальной пулированной плазме (РНП-плазма) (ООО "Технология - Стандарт, г. Барнаул), представляющей собой лиофильно высушенную контрольную плазму крови человека с нормальным диапазоном значений. Дозы препарата сравнения - гепарина (5000 ЕД/мл, Московский эндокринный завод) 0,18 ЕД/мл плазмы и исследуемых образцов на примере калиевых солей сульфатированного арабиногалактана, полученных разными способами (AGSO3K-5 и AGSO3K-new), 0,025 мг/мл и 0,01 мг/мл плазмы соответственно были подобраны экспериментальным путем по влиянию на коагуляционный тест АПТВ (активированное парциальное тромбопластиновое время) (рис.1). Тест АПТВ - стандартизированная проба, чувствительная к дефициту всех плазменных факторов свертывания крови. Увеличение времени АПТВ в 1,5-2 раза по сравнению с исходными значениями является пределом допустимой лечебной дозы используемого нефракционированного гепарина, то есть это доза, вызывающая "терапевтическую" гипокоагуляцию плазмы крови.
Как видно из данных, представленных на рис.1, использование подобранных доз гепарина и калиевых солей сульфатированного арабиногалактана, полученных разными способами, вызывает сопоставимый антикоагулянтный эффект - увеличение времени АПТВ в 2,3 раза для гепарина и в 2,2 и в 2,0 раза для калиевых солей сульфатированного арабиногалактана, полученных разными способами, соответственно. При этом сульфатированное производное AG, полученное согласно заявляемому способу, оказалось более активным (его "терапевтическая" гипокоагуляционная доза в 2,5 раза меньше).
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ СУЛЬФАТИРОВАННЫХ ПРОИЗВОДНЫХ АРАБИНОГАЛАКТАНА, ОБЛАДАЮЩИХ АНТИКОАГУЛЯНТНОЙ И ГИПОЛИПИДЕМИЧЕСКОЙ АКТИВНОСТЬЮ | 2007 |
|
RU2319707C1 |
| СПОСОБ ПОЛУЧЕНИЯ СУЛЬФАТИРОВАННЫХ ПРОИЗВОДНЫХ АРАБИНОГАЛАКТАНА | 2013 |
|
RU2521649C1 |
| СПОСОБ ПОЛУЧЕНИЯ СУЛЬФАТИРОВАННЫХ ПРОИЗВОДНЫХ АРАБИНОГАЛАКТАНА | 2011 |
|
RU2466143C1 |
| СПОСОБ ПОЛУЧЕНИЯ СУЛЬФАТИРОВАННЫХ ПРОИЗВОДНЫХ АРАБИНОГАЛАКТАНА | 2014 |
|
RU2546965C1 |
| СПОСОБ СУЛЬФАТИРОВАНИЯ АРАБИНОГАЛАКТАНА ДРЕВЕСИНЫ ЛИСТВЕННИЦЫ СУЛЬФАМИНОВОЙ КИСЛОТОЙ | 2021 |
|
RU2760432C1 |
| ПОЛУЧЕНИЕ ПОЛИФУНКЦИОНАЛЬНЫХ СУЛЬФАТИРОВАННЫХ ПРОИЗВОДНЫХ НА ОСНОВЕ ПОРОШКОВОЙ ЦЕЛЛЮЛОЗЫ, ОБЛАДАЮЩИХ АНТИКОАГУЛЯНТНОЙ АКТИВНОСТЬЮ | 2009 |
|
RU2430729C2 |
| Способ получения флуоресцентных производных арабиногалактана | 2021 |
|
RU2768707C1 |
| ПРОИЗВОДНЫЕ ПОЛИСАХАРИДОВ С ВЫСОКОЙ АНТИТРОМБОТИЧЕСКОЙ АКТИВНОСТЬЮ В ПЛАЗМЕ | 2004 |
|
RU2361881C2 |
| ГЛИКОЗАМИНОГЛИКАНЫ, ПРОИЗВОДНЫЕ К5-ПОЛИСАХАРИДА, ОБЛАДАЮЩИЕ ВЫСОКОЙ АНТИКОАГУЛЯНТНОЙ И АНТИТРОМБОТИЧЕСКОЙ АКТИВНОСТЬЮ, И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2001 |
|
RU2283319C2 |
| ЭПИМЕРИЗОВАННЫЕ ПРОИЗВОДНЫЕ ПОЛИСАХАРИДА К5 С ВЫСОКОЙ СТЕПЕНЬЮ СУЛЬФАТИРОВАНИЯ | 2003 |
|
RU2333222C2 |
Изобретение относится к способу получения сульфатированного арабиногалактана и может быть использовано в химико-фармацевтической промышленности, медицине, фармакологии. В предложенном способе сульфатированные производные арабиногалактана, выделенного из древесины лиственницы сибирской, получают путем взаимодействия арабиногалактана в растворителе с сульфатирующим агентом при непрерывном перемешивании и постоянной температуре не более +50°С в течение не более 12 часов с дальнейшим выделением, очисткой и сушкой продукта, в качестве сульфатирующей смеси используют сухой калий надсернокислый (калий персульфат, K2S2O8) в растворе диметилсульфоксида. Предложен новый эффективный способ, позволяющий получить сульфатированные производные AG как в кислотной, так и в солевой формах. Степень замещения макромолекулы биополимера в пересчете на количественное содержание серы составляет 9.3-14.2%. Полученные сульфатированные производные AG сохраняют структурную организацию, водорастворимость и мембранотропность природного полисахарида, а также проявляют высокую фармакологическую активность. 3 з.п. ф-лы, 1 ил., 3 пр.
1. Способ получения сульфатированных производных арабиногалактана, выделенного из древесины лиственницы сибирской, путем взаимодействия арабиногалактана в растворителе с сульфатирующим агентом при непрерывном перемешивании и постоянной температуре не более +50°С в течение не более 12 часов с дальнейшим выделением, очисткой и сушкой продукта, отличающийся тем, что в качестве сульфатирующей смеси используют сухой калий надсернокислый (калий персульфат, K2S2O8) в растворе диметилсульфоксида.
2. Способ по п.1, отличающийся тем, что выделение продукта производят нейтрализацией как водными растворами гидроксидов металлов I и II групп, так и их сухими оксидами, с последующей фильтрацией через нутч-фильтр с фильтрующим диском размером пор не более 100 микрон и сублимационной сушкой при t≤-85°C.
3. Способ по п.1, отличающийся тем, что очистку промежуточного продукта от низкомолекулярных примесей проводят методом ультрафильтрации через полиэфирсульфоновый мембранный модуль с размером пор 1-5 кДальтон.
4. Способ по п.1, отличающийся тем, что конечный продукт получают из ретанта при помощи сублимации при t≤-55°C или в распылительной сушилке при температуре на входе не более +120°С, а на выходе +50°С.
Авторы
Даты
2014-11-20—Публикация
2013-08-06—Подача