Область техники, к которой относится изобретение
Настоящее изобретение относится к азотсодержащему гетероциклическому соединению и способу его получения. Более конкретно, настоящее изобретение относится к: (1) замещенному производному аминопиридин-N-оксида, которое применимо в качестве синтетического промежуточного соединения при получении сельскохозяйственных химических препаратов или т.п.; (2) способу получения замещенного производного амино-6-метилпиридин-N-оксида; и (3) способу получения галогеналкильного азотсодержащего гетероциклического производного.
Заявка имеет приоритет японской патентной заявки № 2010-087915, поданной 6 апреля 2010 г., японской патентной заявки № 2010-087916, поданной 6 апреля 2010 г., и японской патентной заявки № 2010-107195, поданной 7 мая 2010 г., содержание которых включено в настоящий документ путем ссылки.
Уровень техники
2-Замещенное производное амино-6-метилпиридин-N-оксида применимо в качестве промежуточного соединения для синтеза химических веществ для фармацевтических и агрохимических препаратов, таких как производное тетразолилоксима, описанное в патентном документе 1, поскольку галогенирование или т.п. метильной группы в 6-положении проходит легко.
В общем случае производные пиридин-N-оксида можно получать путем окисления производных пиридина. Например, в патентном документе 2 описан способ получения 2-хлорпиридин-N-оксида путем окисления 2-хлорпиридина с применением перекиси водорода в присутствии катализатора, представленного формулой Y[PW2O13(OH)] (в которой Y представляет собой атом водорода, алкил или ион аммония).
Кроме того, учитывая реакцию производных пиридин-N-оксида, в качестве способа введения галогена в метильную группу производных 2-пиколина в непатентном документе 1, например, описано, что 6-хлор-2-хлорметилпиридин можно получать путем перегруппировки 6-хлор-2-метилпиридин-N-оксида с участием уксусного ангидрида для введения кислорода в метильную группу с последующим воздействием на полученный продукт тионилхлоридом.
В непатентном документе 2 описан способ галогенирования путем взаимодействия трифосгена или дифосгена с 2-пиколин-N-оксидом в присутствии диизопропиламина или триэтиламина.
Кроме того, в патентном документе 3 описан способ синтеза 2-хлор-5-метилпиридина из 3-метилпиридин-1-оксида. В патентном документе 3 описано, что требуемый продукт можно получать с помощью способа, основанного на реакции перегруппировки с применением триметиламина и фосгена, вводя во второе положение пиридинового цикла триметиламмоний с последующим его хлорированием.
Список литературы
Патентные документы
Патентный документ 1: WO 2008/006873.
Патентный документ 2: KR-A-10-2005-0025453.
Патентный документ 3: нерассмотренная японская патентная заявка, первая публикация № Hei 7-252226.
Патентный документ 4: нерассмотренная японская патентная заявка, первая публикация № Sho 62-142136.
Непатентные документы
Непатентный документ 1: Barnes J.H. и др., Tetrahedron 38 (22), 3277-3280, 1982.
Непатентный документ 2: Narendar P. и др., Synthetic Communications 34 (6), 1097-1103, 2004.
Сущность изобретения
Техническая проблема
Задачей авторов настоящего изобретения является разработка способа получения замещенного производного аминопиридин-N-оксида, представленного формулой (1), в частности замещенного производного амино-6-алкилпиридин-N-оксида, которое является высокоселективным, легко отделяется от катализатора и также применимо в качестве промежуточного соединения для синтеза сельскохозяйственных химических препаратов и т.п. Кроме того, еще одной задачей настоящего изобретения является разработка высокоселективного и также высокопродуктивного способа получения галогеналкильного, азотсодержащего гетероциклического производного, представленного формулой (5), которое также применимо в качестве промежуточного соединения для синтеза фармацевтических и агрохимических препаратов.
Решение проблемы
Чтобы достичь указанных выше целей, в результате интенсивных и обширных исследований авторы настоящего изобретения обнаружили, что если из числа солей вольфрамофосфорной кислоты, представленных формулой Q3[PW4O24], которые известны как катализаторы реакции эпоксидирования в патентном документе 4 или т.п., в качестве катализатора применять соли, в которых Q представляет собой катион четвертичного азота, можно с высокой селективностью получать замещенное производное амино-6-метилпиридин-N-оксида посредством реакции окисления замещенного производного амино-6-метилпиридина с пероксидом, и что после завершения реакции катализатор можно легко выделять.
Кроме того, авторы настоящего изобретения обнаружили, что соединение, представленное формулой (5), можно получать с высоким выходом и также с высокой селективностью путем взаимодействия соединения, представленного формулой (4), с галогенирующим агентом, таким как тионилхлорид, тионилбромид или сульфурилхлорид. Кроме того, авторы настоящего изобретения также обнаружили, что соединение, представленное формулой (5), можно получать с высоким выходом и также с высокой селективностью путем взаимодействия соединения, представленного формулой (4), с галогенирующим агентом, таким как фосген, дифосген, трифосген или оксихлорид фосфора, в присутствии источника галоген-ионов, который растворим в органическом растворителе.
Настоящее изобретение было завершено благодаря дополнительным исследованиям, основанным на таких установленных фактах.
То есть настоящее изобретение включает следующие аспекты.
[1] Замещенный аминопиридин-N-оксид, представленный формулой (1):
[Химическая формула 1]
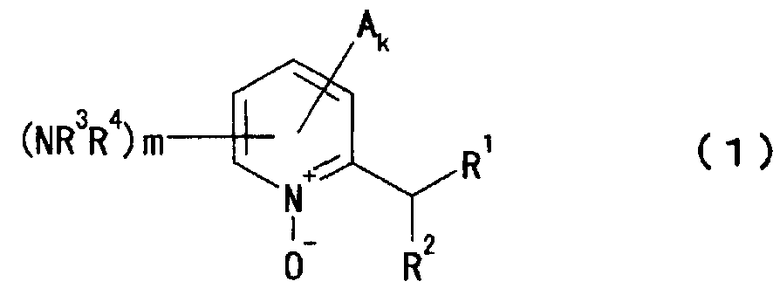
(в формуле (1) каждый из R1 и R2 независимо представляет собой атом водорода или незамещенную или замещенную алкильную группу; и R1 и R2 вместе могут образовывать цикл;
R3 представляет собой атом водорода, незамещенную или замещенную алкилкарбонильную группу, незамещенную или замещенную арилкарбонильную группу или незамещенную или замещенную алкоксикарбонильную группу;
R4 представляет собой незамещенную или замещенную алкилкарбонильную группу, незамещенную или замещенную арилкарбонильную группу, незамещенную или замещенную гетероарилкарбонильную группу, незамещенную или замещенную алкоксикарбонильную группу, незамещенную или замещенную алкилсульфонильную группу или незамещенную или замещенную арилсульфонильную группу;
А представляет собой гидроксильную группу, тиольную группу, аминогруппу, нитрогруппу, атом галогена или органическую группу,
m представляет собой любое из целых чисел от 1 до 4, и
k представляет собой любое из целых чисел от 0 до 3,
в котором k+m≤4),
при условии, что исключен 2-этоксикарбониламино-6-метилпиридин-N-оксид.
[2] Способ получения замещенного производного амино-6-метилпиридин-N-оксида, представленного формулой (1-a), включающий окисление замещенного производного амино-6-метилпиридина, представленного формулой (2), с применением пероксида в присутствии соли вольфрамофосфорной кислоты, представленной формулой (3):
[Химическая формула 2]
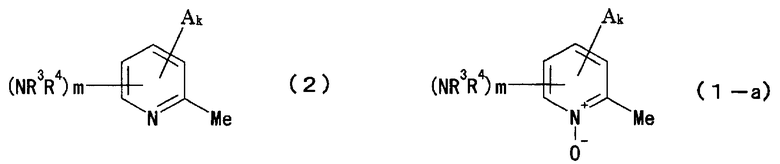
Q3[PW4O24] (3)
(в формулах
A представляет собой гидроксильную группу, тиольную группу, аминогруппу, нитрогруппу, атом галогена или органическую группу,
k представляет собой любое из целых чисел от 0 до 3,
R3 представляет собой атом водорода, незамещенную или замещенную алкилкарбонильную группу, незамещенную или замещенную арилкарбонильную группу или незамещенную или замещенную алкоксикарбонильную группу,
R4 представляет собой незамещенную или замещенную алкилкарбонильную группу, незамещенную или замещенную арилкарбонильную группу, незамещенную или замещенную гетероарилкарбонильную группу, незамещенную или замещенную алкоксикарбонильную группу, незамещенную или замещенную алкилсульфонильную группу или незамещенную или замещенную арилсульфонильную группу,
m представляет собой любое из целых чисел от 1 до 4,
в которых k+m≤4 и Q представляет собой катион четвертичного азота).
[3] Способ получения замещенного производного амино-6-метилпиридин-N-оксида согласно вышеупомянутому аспекту [2], в котором R3 в формуле (2) и в формуле (1-a) представляет собой атом водорода.
[4] Способ получения замещенного производного амино-6-метилпиридин-N-оксида согласно вышеупомянутому аспекту [2], в котором катион четвертичного азота, представленный Q в формуле (3), представляет собой катион четвертичного аммония.
[5] Способ получения замещенного производного амино-6-метилпиридин-N-оксида согласно вышеупомянутому аспекту 2, в котором соль вольфрамофосфорной кислоты, представленную формулой (3), получают без процедуры выделения после ее получения.
[6] Способ получения соединения, представленного формулой (5), включающий взаимодействие соединения, представленного формулой (4), с галогенирующим агентом:
[Химическая формула 3]

(в данных формулах каждый из a1-a4 независимо представляет собой атом углерода, атом азота, атом кислорода или атом серы;
каждый из R1 и R2 независимо представляет собой атом водорода или незамещенную или замещенную алкильную группу; и R1 и R2 вместе могут образовывать цикл;
A представляет собой гидроксильную группу, тиольную группу, аминогруппу, нитрогруппу, атом галогена или органическую группу;
n представляет собой любое из целых чисел от 0 до 4; и несколько групп A могут связываться с образованием цикла, когда n равно 2 или более, и
X представляет собой атом галогена).
[7] Способ получения азотсодержащего гетероциклического соединения согласно вышеупомянутому аспекту [6], в котором все a1-a4 в формуле (4) и формуле (5) представляют собой атомы углерода.
[8] Способ получения азотсодержащего гетероциклического соединения согласно вышеупомянутому аспекту [6], в котором по меньшей мере одна группа A в формуле (4) и формуле (5) представляет собой группу, представленную формулой (6):
[Химическая формула 4]
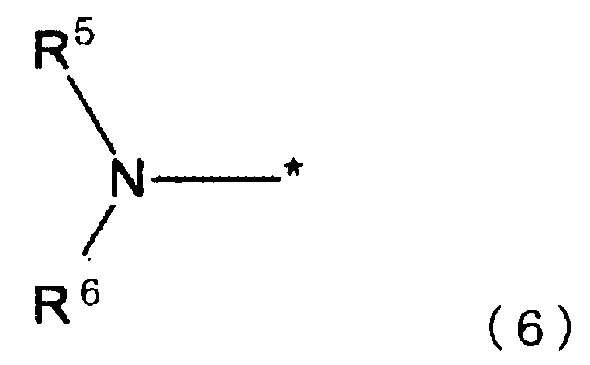
(в данной формуле (6) * указывает место связывания,
R5 представляет собой атом водорода, незамещенную или замещенную алкилкарбонильную группу, незамещенную или замещенную арилкарбонильную группу, незамещенную или замещенную гетероарилкарбонильную группу, незамещенную или замещенную алкоксикарбонильную группу, незамещенную или замещенную алкилсульфонильную группу или незамещенную или замещенную арилсульфонильную группу,
R6 представляет собой незамещенную или замещенную алкилкарбонильную группу, незамещенную или замещенную арилкарбонильную группу, незамещенную или замещенную гетероарилкарбонильную группу, незамещенную или замещенную алкоксикарбонильную группу, незамещенную или замещенную алкилсульфонильную группу или незамещенную или замещенную арилсульфонильную группу, и R5 и R6 могут связываться с образованием цикла).
[9] Способ получения азотсодержащего гетероциклического соединения согласно вышеупомянутому аспекту [6], в котором соединение, представленное формулой (4), представляет собой соединение, представленное формулой (7), и соединение, представленное формулой (5), представляет собой соединение, представленное формулой (8):
[Химическая формула 5]
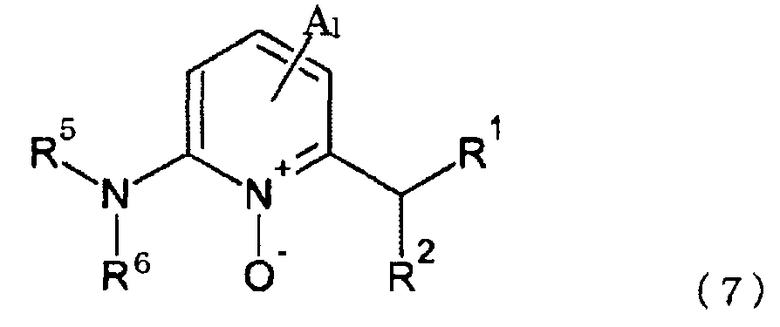
(в формуле (7) A, R1 и R2 имеют те же значения, которые указаны выше;
l представляет собой любое из целых чисел от 0 до 3;
R5 представляет собой атом водорода, незамещенную или замещенную алкилкарбонильную группу, незамещенную или замещенную арилкарбонильную группу, незамещенную или замещенную гетероарилкарбонильную группу, незамещенную или замещенную алкоксикарбонильную группу, незамещенную или замещенную алкилсульфонильную группу или незамещенную или замещенную арилсульфонильную группу;
R6 представляет собой незамещенную или замещенную алкилкарбонильную группу, незамещенную или замещенную арилкарбонильную группу, незамещенную или замещенную гетероарилкарбонильную группу, незамещенную или замещенную алкоксикарбонильную группу, незамещенную или замещенную алкилсульфонильную группу или незамещенную или замещенную арилсульфонильную группу; и R5 и R6 могут связываться с образованием цикла).
[Химическая формула 6]
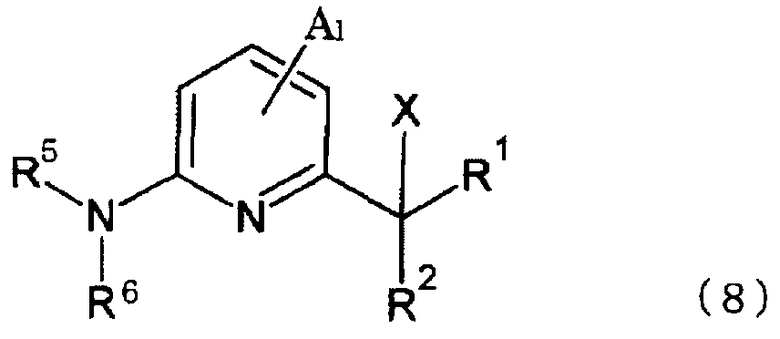
(в формуле (8) A, l, R1, R2, X, R5 и R6 имеют те же значения, которые указаны выше).
[10] Способ получения азотсодержащего гетероциклического соединения согласно вышеупомянутому аспекту [8], в котором R5 представляет собой незамещенную или замещенную алкилкарбонильную группу, незамещенную или замещенную арилкарбонильную группу или незамещенную или замещенную алкоксикарбонильную группу.
[11] Способ получения азотсодержащего гетероциклического соединения согласно вышеупомянутому аспекту [6], в котором галогенирующий агент, представляет собой по меньшей мере один агент, выбранный из группы, состоящей из тионилхлорида, тионилбромида и сульфурилхлорида.
[12] Способ получения азотсодержащего гетероциклического соединения согласно вышеупомянутому аспекту [6], в котором реакцию осуществляют в присутствии источника галоген-ионов, который растворим в органическом растворителе.
[13] Способ получения азотсодержащего гетероциклического соединения согласно вышеупомянутому аспекту [6], в котором галогенирующий агент представляет собой по меньшей мере один агент, выбранный из группы, состоящей из фосгена, дифосгена, трифосгена и оксихлорида фосфора.
[14] Способ получения соединения, представленного формулой (11), включающий стадию превращения соединения, представленного формулой (9), в соединение, представленное формулой (10), и стадию взаимодействия соединения, представленного формулой (10), с галогенирующим агентом с превращением его в соединение, представленное формулой (11):
[Химическая формула 7]

(в данных формулах каждый из R1 и R2 независимо представляет собой атом водорода или незамещенную или замещенную алкильную группу; и R1 и R2 вместе могут образовывать цикл;
R6 представляет собой незамещенную или замещенную алкилкарбонильную группу, незамещенную или замещенную арилкарбонильную группу, незамещенную или замещенную гетероарилкарбонильную группу, незамещенную или замещенную алкоксикарбонильную группу, незамещенную или замещенную алкилсульфонильную группу или незамещенную или замещенную арилсульфонильную группу;
R7 представляет собой незамещенную или замещенную алкилкарбонильную группу, незамещенную или замещенную арилкарбонильную группу, незамещенную или замещенную гетероарилкарбонильную группу, незамещенную или замещенную алкоксикарбонильную группу, незамещенную или замещенную алкилсульфонильную группу или незамещенную или замещенную арилсульфонильную группу;
A представляет собой гидроксильную группу, тиольную группу, аминогруппу, нитрогруппу, атом галогена или органическую группу;
X представляет собой атом галогена;
m представляет собой любое из целых чисел от 1 до 4; и
k представляет собой любое из целых чисел от 0 до 3;
в которых k+m≤4).
[15] Способ получения азотсодержащего гетероциклического соединения согласно вышеупомянутому аспекту [14], в котором стадию синтеза соединения, представленного формулой (11), осуществляют в присутствии источника галоген-ионов, который растворим в органическом растворителе.
[16] Способ получения соединения, представленного формулой (13), включающий взаимодействие соединения, представленного формулой (9), с галогенирующим агентом в присутствии соединения, представленного формулой (12):
[Химическая формула 8]
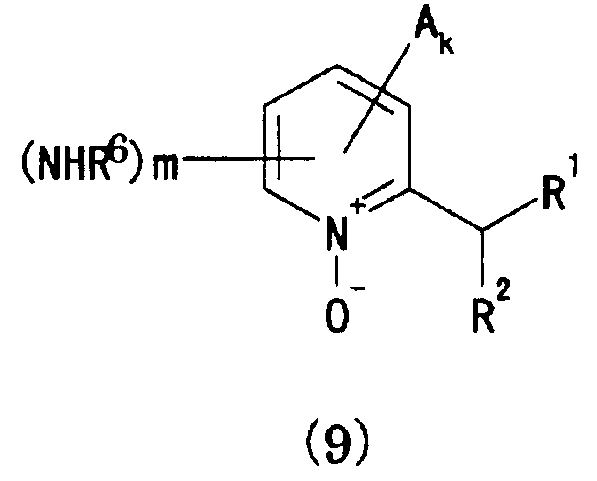
[Химическая формула 9]
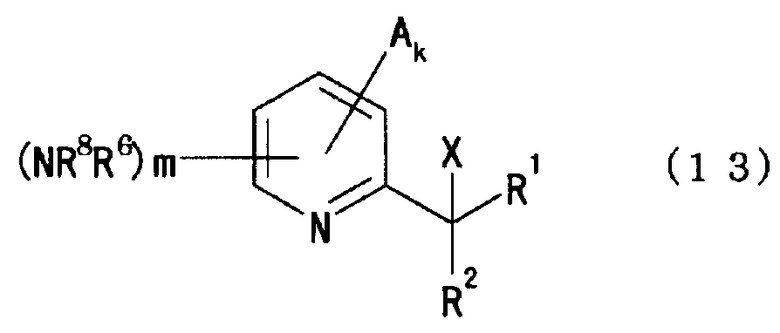
R8X1 (12)
(в данных формулах каждый из R1 и R2 независимо представляет собой атом водорода или незамещенную или замещенную алкильную группу, и R1 и R2 вместе могут образовывать цикл;
R6 представляет собой незамещенную или замещенную алкилкарбонильную группу, незамещенную или замещенную арилкарбонильную группу, незамещенную или замещенную гетероарилкарбонильную группу, незамещенную или замещенную алкоксикарбонильную группу, незамещенную или замещенную алкилсульфонильную группу или незамещенную или замещенную арилсульфонильную группу;
R8 представляет собой незамещенную или замещенную алкилкарбонильную группу, незамещенную или замещенную арилкарбонильную группу или незамещенную или замещенную алкоксикарбонильную группу;
A представляет собой гидроксильную группу, тиольную группу, аминогруппу, нитрогруппу, атом галогена или органическую группу;
m представляет собой любое из целых чисел от 1 до 4;
k представляет собой любое из целых чисел от 0 до 3;
в которых k+m≤4,
Х представляет собой атом галогена; и
Х1 представляет собой атом хлора или атом брома).
[17] Способ получения азотсодержащего гетероциклического соединения согласно вышеупомянутому аспекту [16], в котором реакцию осуществляют в присутствии источника галоген-ионов, который растворим в органическом растворителе.
[18] Способ получения согласно вышеупомянутым аспектам [12], [15] или [17], в котором источник галоген-ионов, который растворим в органическом растворителе, представляет собой галогенированную соль аммония или галогенированную соль фосфония.
[19] Способ получения согласно вышеупомянутым аспектам [12], [15] или [17], в котором источник галоген-ионов, который растворим в органическом растворителе, представляет собой галогенидную соль третичного или четвертичного алкиламмония, содержащую C2-алкильную группу или алкильную группу с большим числом атомов углерода, или галогенидную соль алкилфосфония, содержащую C2-алкильную группу или алкильную группу с большим числом атомов углерода.
[20] Способ получения по любому из вышеупомянутых аспектов 14-19, в котором галогенирующий агент представляет собой по меньшей мере один агент, выбранный из группы, состоящей из тионилхлорида, тионилбромида, оксихлорида фосфора, сульфурилхлорида, фосгена, дифосгена и трифосгена.
Полезные эффекты изобретения
В соответствии со способом получения согласно настоящему изобретению замещенное производное аминопиридин-N-оксида, замещенное производное амино-6-метилпиридин-N-оксида и галогеналкильное, азотсодержащее гетероциклическое производное можно получать с высокой селективностью и также с высоким выходом. Азотсодержащее гетероциклическое соединение, полученное по способу получения согласно настоящему изобретению, применимо в качестве промежуточного соединения для промышленного производства сельскохозяйственных химических препаратов или т.п.
Описание вариантов осуществления изобретения
[1] Замещенное производное аминопиридин-N-оксида, которое применимо в качестве синтетического промежуточного соединения при синтезе сельскохозяйственных химических препаратов или т.п.
Замещенное производное аминопиридин-N-оксида, которое применимо в качестве синтетического промежуточного соединения при синтезе сельскохозяйственных химических препаратов или т.п. согласно настоящему изобретению, представляет собой соединение, представленное формулой (1).
В формуле (1) каждый из R1 и R2 независимо представляет собой атом водорода или незамещенную или замещенную алкильную группу. R1 и R2 могут связываться с образованием цикла.
Следует отметить, что в настоящем изобретении термин "незамещенная" означает, что соответствующая группа состоит только из центральной группы.
С другой стороны, в настоящем изобретении термин "замещенная" означает, что любой из атомов водорода, составляющий центральную группу, может быть замещен группой, содержащей структуру, отличающуюся от структуры центральной группы. Соответственно термин "заместитель" относится к любой другой группе, которая замещает атомы центральной группы. Число заместителей может равняться одному или двум или более. Если присутствует два или более заместителей, заместители могут быть одинаковыми или могут отличаться друг от друга.
Примеры группы, которая может служить в качестве "заместителя", включают нитрогруппу; атом галогена, такой как атом хлора, атом фтора и атом брома; гидроксигруппу; алкоксигруппу, такую как метоксигруппа, этоксигруппа, изопропоксигруппа, н-пропоксигруппа, н-бутоксигруппа, изобутоксигруппа, втор-бутоксигруппа и трет-бутоксигруппа; арилоксигруппу, такую как феноксигруппа и 1-нафтилоксигруппа; галогеналкоксигруппу, такую как фторметоксигруппа, дифторметоксигруппа, трифторметоксигруппа, 2-хлорэтоксигруппа, 2,2,2-трихлорэтоксигруппа, 1,1,1,3,3,3-гексафтор-2-пропоксигруппа; алкилтиогруппу, такую как метилтиогруппа и этилтиогруппа; арилтиогруппу, такую как фенилтиогруппа и 1-нафтилтиогруппа; алкильную группу, такую как метильная группа и этильная группа; арильную группу, такую как фенильная группа и нафтильная группа; гетероарильную группу, такую как пирролильная группа, тиазолильная группа и пиримидинильная группа; алкилкарбонильную группу; арилкарбонильную группу; гетероарилкарбонильную группу; алкоксикарбонильную группу; алкилсульфонильную группу и арилсульфонильную группу.
Конкретные примеры незамещенной алкильной группы R1 и R2 включают метильную группу, этильную группу, н-пропильную группу, изопропильную группу, н-бутильную группу, изобутильную группу, втор-бутильную группу, трет-бутильную группу и н-пентильную группу; и C1-6-алкильные группы являются предпочтительными.
Примеры замещенной алкильной группы R1 и R2 включают цианоалкильную группу, такую как цианометильная группа, 1-цианоэтильная группа и 2-цианоэтильная группа (циано-C1-6-алкильные группы являются предпочтительными); нитроалкильную группу, такую как нитрометильная группа (нитро-C1-6-алкильные группы являются предпочтительными); галогеналкильную группу, такую как хлорметильная группа, фторметильная группа, дифторметильная группа, трифторметильная группа, 2-фторэтильная группа и 2,2,2-трифторэтильная группа (галоген-C1-6-алкильные группы являются предпочтительными); алкоксиалкильную группу, такую как метоксиметильная группа, этоксиметильная группа, 1-метоксиэтильная группа и 2-метоксиэтильная группа (C1-6-алкокси-C1-6-алкильные группы являются предпочтительными); арилалкильную группу, такую как фенилметильная группа и 1-нафтилэтильная группа (C6-10-арил-C1-6-алкильные группы являются предпочтительными); и гетероарилалкильную группу, такую как 2-пиридилметильная группа (5-6-членный гетероарил-C1-6-алкильные группы являются предпочтительными).
Примеры цикла, образующегося при связывании R1 и R2, включают циклоалкильную группу, такую как циклопропильная группа и циклобутильная группа (C3-8-циклоалкильные группы являются предпочтительными); циклоалкенильную группу, такую как циклогексенильная группа (C3-8-циклоалкенильные группы являются предпочтительными); и насыщенную гетероциклическую группу, такую как морфолиногруппа (3-8-членные насыщенные гетероциклические группы являются предпочтительными).
В формуле (1) R3 представляет собой атом водорода, незамещенную или замещенную алкилкарбонильную группу, незамещенную или замещенную арилкарбонильную группу или незамещенную или замещенную алкоксикарбонильную группу.
Примеры незамещенной алкилкарбонильной группы R3 включают ацильную группу и этилкарбонильную группу; и C1-6-алкилкарбонильные группы являются предпочтительными.
Примеры замещенной алкилкарбонильной группы R3 включают цианоалкилкарбонильную группу, такую как цианометилкарбонильная группа (циано-C1-6-алкилкарбонильные группы являются предпочтительными); нитроалкилкарбонильную группу, такую как 1-нитроэтилкарбонильная группа (нитро-C1-6-алкилкарбонильные группы являются предпочтительными); галогеналкилкарбонильную группу, такую как хлорметилкарбонильная группа, дифторметилкарбонильная группа и 2,2,2-трифторэтилкарбонильная группа (галоген-C1-6-алкилкарбонильные группы являются предпочтительными); алкоксиалкилкарбонильную группу, такую как метоксиацильная группа и 2-метоксиэтилкарбонильная группа (C1-6-алкокси-C1-6-алкилкарбонильные группы являются предпочтительными); арилалкилкарбонильную группу, такую как фенилметилкарбонильная группа и 1-нафтилэтилкарбонильная группа (C6-10-арил-C1-6-алкилкарбонильные группы являются предпочтительными); и гетероарилалкилкарбонильную группу, такую как 2-пиридилметилкарбонильная группа (5-6-членный гетероарил-C1-6-алкилкарбонильные группы являются предпочтительными).
Примеры незамещенной арилкарбонильной группы R3 включают бензоильную группу и 2-нафтилкарбонильную группу; и C6-10-арилкарбонильные группы являются предпочтительными.
Примеры замещенной арилкарбонильной группы R3 включают арилкарбонильную группу, замещенную нитрогруппой, такую как 4-нитрофенилкарбонильная группа (C6-10-арилкарбонильные группы, замещенные нитрогруппой, являются предпочтительными); арилкарбонильную группу, замещенную цианогруппой, такую как 2-цианофенилкарбонильная группа (C6-10-арилкарбонильные группы, замещенные цианогруппой, являются предпочтительными); арилкарбонильную группу, замещенную алкильной группой, такую как 2-метилфенилкарбонильная группа и 3,5-диметилфенилкарбонильная группа (C6-10-арилкарбонильные группы, замещенные C1-6-алкильной группой, являются предпочтительными); и арилкарбонильную группу, замещенную атомом галогена, такую как 4-хлорфенилкарбонильная группа и 3,5-дифторфенилкарбонильная группа (C6-10-арилкарбонильные группы, замещенные атомом галогена, являются предпочтительными).
Примеры незамещенной алкоксикарбонильной группы R3 включают метоксикарбонильную группу и этоксикарбонильную группу; и C1-6-алкоксикарбонильные группы являются предпочтительными.
Примеры замещенной алкоксикарбонильной группы R3 включают цианоалкоксикарбонильную группу, такую как цианометоксикарбонильная группа (циано-C1-6-алкоксикарбонильные группы являются предпочтительными); нитроалкоксикарбонильную группу, такую как 1-нитроэтоксикарбонильная группа (нитро-C1-6-алкоксикарбонильные группы являются предпочтительными); галогеналкоксикарбонильную группу, такую как хлорметоксикарбонильная группа, дифторметоксикарбонильная группа и 2,2,2-трифторэтоксикарбонильная группа (галоген-C1-6-алкоксикарбонильные группы являются предпочтительными); алкоксиалкоксикарбонильную группу, такую как метоксиметоксикарбонильная группа и 2-метоксиэтоксикарбонильная группа (C1-6-алкокси-C1-6-алкоксикарбонильные группы являются предпочтительными); арилалкоксикарбонильную группу, такую как фенилметоксикарбонильная группа и 1-нафтилэтоксикарбонильная группа (C6-10-арил-C1-6-алкоксикарбонильные группы являются предпочтительными); и гетероарилалкоксигруппу, такую как 2-пиридилметоксикарбонильная группа (5-6-членный гетероарил-C1-6-алкоксикарбонильные группы являются предпочтительными).
В формуле (1) R4 представляет собой незамещенную или замещенную алкилкарбонильную группу, незамещенную или замещенную арилкарбонильную группу, незамещенную или замещенную гетероарилкарбонильную группу, незамещенную или замещенную алкоксикарбонильную группу, незамещенную или замещенную алкилсульфонильную группу или незамещенную или замещенную арилсульфонильную группу.
Конкретные примеры незамещенной или замещенной алкилкарбонильной группы, незамещенной или замещенной арилкарбонильной группы и незамещенной или замещенной алкоксикарбонильной группы R4 включают те же примеры, которые описаны выше в качестве конкретных примеров группы R3.
Гетероарилкарбонильная группа R4 представляет собой группу, в которой моноциклический гетероарильный цикл или конденсированный гетероарильный цикл, содержащий по меньшей мере один гетероатом, выбранный из группы, состоящей из атома кислорода, атома азота и атома серы, связан с карбонильной группой; и 5-6-членная гетероарилкарбонильная группа является предпочтительной.
Примеры незамещенной гетероарилкарбонильной группы R4 включают пирролилкарбонильную группу, фурилкарбонильную группу, тиенилкарбонильную группу, имидазолилкарбонильную группу, пиразолилкарбонильную группу, тиазолилкарбонильную группу, изотиазолилкарбонильную группу, оксазолилкарбонильную группу, изооксазолилкарбонильную группу, триазолилкарбонильную группу, тетразолилкарбонильную группу, оксадиазолилкарбонильную группу, 1,2,3-тиадиазолилкарбонильную группу, 1,2,4-тиадиазолилкарбонильную группу, 1,3,4-тиадиазолилкарбонильную группу, пиридилкарбонильную группу, пиразинилкарбоксильную группу, пиримидинилкарбонильную группу, пиридазинилкарбоксильную группу, 1,2,4-триазинилкарбонильную группу, 1,3,5-триазинилкарбонильную группу, индолилкарбонильную группу, бензофуранилкарбонильную группу, бензотиенилкарбонильную группу, бензимидазолилкарбонильную группу, бензопиразолилкарбонильную группу, бензооксазолилкарбонильную группу, бензоизооксазолилкарбонильную группу, бензотиазолилкарбонильную группу, бензоизотиазолилкарбонильную группу, индазолилкарбонильную группу, пуринилкарбонильную группу, хинолилкарбонильную группу, изохинолилкарбонильную группу, фталазинилкарбонильную группу, нафтиридинилкарбонильную группу, хиноксалинилкарбонильную группу, хиназолинилкарбонильную группу, циннолинилкарбонильную группу, птеридинилкарбонильную группу и пиридо[3,2-b]пиридилкарбонильную группу.
Примеры замещенной гетероарилкарбонильной группы R4 включают гетероарилкарбонильную группу, замещенную цианогруппой, такую как 3-циано-2-пиридилкарбонильная группа; гетероарилкарбонильную группу, замещенную нитрогруппой, такую как 4-нитро-2-пиридилкарбонильная группа; гетероарилкарбонильную группу, замещенную атомом галогена, такую как 5-фтор-2-пиридилкарбонильная группа; гетероарилкарбонильную группу, замещенную алкильной группой, такую как 6-метил-2-пиридилкарбонильная группа (C1-6-алкил-(5-6-членный гетероарил)карбонильные группы являются предпочтительными); гетероарилкарбонильную группу, замещенную алкоксигруппой, такую как 2-метокси-3-пиридилкарбонильная группа (C1-6-алкокси-(5-6-членный гетероарил)карбонильные группы являются предпочтительными); гетероарилкарбонильную группу, замещенную арильной группой, такую как 4-фенил-3-пиридилкарбонильная группа (C6-10-арил-(5-6-членный гетероарил)карбонильные группы являются предпочтительными); и гетероарилкарбонильную группу, замещенную гетероарильной группой, такую как 5-(2-пиридил)-3-пиридилкарбонильная группа ((5-6-членный гетероарил)-(5-6-членный гетероарил)карбонильные группы являются предпочтительными).
Примеры незамещенной алкилсульфонильной группы R4 включают метилсульфонильную группу и этилсульфонильную группу; и C1-6-алкилсульфонильные группы являются предпочтительными.
Примеры замещенной алкилсульфонильной группы R4 включают цианоалкилсульфонильную группу, такую как цианометилсульфонильная группа (циано-C1-6-алкилсульфонильные группы являются предпочтительными); нитроалкилсульфонильную группу, такую как 1-нитроэтилсульфонильная группа (нитро-C1-6-алкилсульфонильные группы являются предпочтительными); галогеналкилсульфонильную группу, такую как хлорметилсульфонильная группа, дифторметилсульфонильная группа и 2,2,2-трифторэтилсульфонильная группа (галоген-C1-6-алкилсульфонильные группы являются предпочтительными); алкоксиалкилсульфонильную группу, такую как метоксиметилсульфонильная группа и 2-метоксиэтилсульфонильная группа (C1-6-алкокси-C1-6-алкилсульфонильные группы являются предпочтительными); арилалкилсульфонильную группу, такую как фенилметилсульфонильная группа и 1-нафтилэтилсульфонильная группа (C6-10-арил-C1-6-алкилсульфонильные группы являются предпочтительными); и гетероарилалкилсульфонильную группу, такую как 2-пиридилметилсульфонильная группа (5-6-членный гетероарил-C1-6-алкилсульфонильные группы являются предпочтительными).
Примеры незамещенной арилсульфонильной группы R4 включают фенилсульфонильную группу и 2-нафтилсульфонильную группу; и C6-10-арилсульфонильные группы являются предпочтительными.
Примеры замещенной арилсульфонильной группы R4 включают арилсульфонильную группу, замещенную цианогруппой, такую как 2-цианофенилсульфонильная группа (C6-10-арилсульфонильные группы, замещенные цианогруппой, являются предпочтительными); арилсульфонильную группу, замещенную нитрогруппой, такую как 4-нитрофенилсульфонильная группа (C6-10-арилсульфонильные группы, замещенные нитрогруппой, являются предпочтительными); арилсульфонильную группу, замещенную атомом галогена, такую как 4-хлорфенилсульфонильная группа и 3,5-дифторфенилсульфонильная группа (C6-10-арилсульфонильные группы, замещенные атомом галогена, являются предпочтительными); арилсульфонильную группу, замещенную алкильной группой, такую как 2-метилфенилсульфонильная группа и 3,5-диметилфенилсульфонильная группа (C6-10-арилсульфонильные группы, замещенные C1-6-алкильной группой, являются предпочтительными); и арилсульфонильную группу, замещенную алкоксигруппой, такую как 4-метоксифенилсульфонильная группа (C6-10-арилсульфонильные группы, замещенные C1-6-алкоксигруппой, являются предпочтительными).
В формуле (1) A представляет собой гидроксильную группу, тиольную группу, аминогруппу, нитрогруппу, атом галогена или органическую группу.
Примеры атома галогена в качестве группы A включают атом фтора, атом хлора, атом брома и атом йода.
Органическая группа A является общим описанием, которое представляет собой все группы, содержащие атом углерода внутри заместителя, и ее примеры включают цианогруппу, аминогруппу, содержащую заместитель (аминогруппы, замещенные C1-6-алкильной группой или C6-10-арильной группой, являются предпочтительными); незамещенную или замещенную алкильную группу (C1-6-алкильные группы, замещенные нитрогруппой, атомом галогена, C1-6-алкоксигруппой или C6-10-арильной группой, являются предпочтительными), незамещенную или замещенную алкенильную группу (C2-6-алкенильные группы, замещенные нитрогруппой, атомом галогена, C1-6-алкоксигруппой или C6-10-арильной группой, являются предпочтительными), незамещенную или замещенную алкинильную группу (C2-6-алкинильные группы, замещенные нитрогруппой, атомом галогена, C1-6-алкоксигруппой или C6-10-арильной группой, являются предпочтительными), незамещенную или замещенную арильную группу (C6-10-арильные группы, замещенные нитрогруппой, атомом галогена, C1-6-алкильной группой или галоген-C1-6-алкильной группой, являются предпочтительными), незамещенную или замещенную гетероарильную группу (5-6-членные гетероарильные группы, замещенные нитрогруппой, атомом галогена, C1-6-алкильной группой или галоген-C1-6-алкильной группой, являются предпочтительными), незамещенную или замещенную алкоксигруппу (C1-6-алкоксигруппы, замещенные нитрогруппой, атомом галогена, C1-6-алкоксигруппой или C6-10-арильной группой, являются предпочтительными), незамещенную или замещенную алкенилоксигруппу (C2-6-алкенилоксигруппы, замещенные нитрогруппой, атомом галогена, C1-6-алкоксигруппой или C6-10-арильной группой, являются предпочтительными), незамещенную или замещенную алкинилоксигруппу (C2-6-алкинилоксигруппы, замещенные нитрогруппой, атомом галогена, C1-6-алкоксигруппой или C6-10-арильной группой, являются предпочтительными), незамещенную или замещенную арилоксигруппу (C6-10-арилоксигруппы, замещенные нитрогруппой, атомом галогена, C1-6-алкильной группой или галоген-C1-6-алкильной группой, являются предпочтительными), незамещенную или замещенную гетероарилоксигруппу (5-6-членные гетероарилоксигруппы, замещенные нитрогруппой, атомом галогена, C1-6-алкильной группой или галоген-C1-6-алкильной группой, являются предпочтительными), формильную группу, незамещенную или замещенную алкилкарбонильную группу (C1-6-алкилкарбонильные группы, замещенные нитрогруппой, атомом галогена, C1-6-алкоксигруппой или C6-10-арильной группой, являются предпочтительными), незамещенную или замещенную алкенилкарбонильную группу (C2-6-алкенилкарбонильные группы, замещенные нитрогруппой, атомом галогена, C1-6-алкоксигруппой или C6-10-арильной группой, являются предпочтительными), незамещенную или замещенную алкинилкарбонильную группу (C2-6-алкинилкарбонильные группы, замещенные нитрогруппой, атомом галогена, C1-6-алкоксигруппой или C6-10-арильной группой, являются предпочтительными), незамещенную или замещенную арилкарбонильную группу (C6-10-арилкарбонильные группы, замещенные нитрогруппой, атомом галогена, C1-6-алкильной группой или галоген-C1-6-алкильной группой, являются предпочтительными), незамещенную или замещенную гетероарилкарбонильную группу (5-6-членные гетероарилкарбонильные группы, замещенные нитрогруппой, атомом галогена, C1-6-алкильной группой или галоген-C1-6-алкильной группой, являются предпочтительными), незамещенную или замещенную алкилтиогруппу (C1-6-алкилтиогруппы, замещенные нитрогруппой, атомом галогена, C1-6-алкоксигруппой или C6-10-арильной группой, являются предпочтительными), незамещенную или замещенную алкенилтиогруппу (C2-6-алкенилтиогруппы, замещенные нитрогруппой, атомом галогена, C1-6-алкоксигруппой или C6-10-арильной группой, являются предпочтительными), незамещенную или замещенную алкинилтиогруппу (C2-6-алкинилтиогруппы, замещенные нитрогруппой, атомом галогена, C1-6-алкоксигруппой или C6-10-арильной группой, являются предпочтительными), незамещенную или замещенную арилтиогруппу (C6-10-арилтиогруппы, замещенные нитрогруппой, атомом галогена, C1-6-алкильной группой или галоген-C1-6-алкильной группой, являются предпочтительными), незамещенную или замещенную гетероарилтиогруппу (5-6-членные гетероарилтиогруппы, замещенные нитрогруппой, атомом галогена, C1-6-алкильной группой или галоген-C1-6-алкильной группой, являются предпочтительными), незамещенную или замещенную алкилсульфинильную группу (C1-6-алкилсульфинильные группы, замещенные нитрогруппой, атомом галогена, C1-6-алкоксигруппой или C6-10-арильной группой, являются предпочтительными), незамещенную или замещенную алкенилсульфинильную группу (C2-6-алкенилсульфинильные группы, замещенные нитрогруппой, атомом галогена, C1-6-алкоксигруппой или C6-10-арильной группой, являются предпочтительными), незамещенную или замещенную алкинилсульфинильную группу (C2-6-алкинилсульфинильные группы, замещенные нитрогруппой, атомом галогена, C1-6-алкоксигруппой или C6-10-арильной группой, являются предпочтительными), незамещенную или замещенную арилсульфинильную группу (C6-10-арилсульфинильные группы, замещенные нитрогруппой, атомом галогена, C1-6-алкильной группой или галоген-C1-6-алкильной группой, являются предпочтительными), незамещенную или замещенную гетероарилсульфинильную группу (5-6-членные гетероарилсульфинильные группы, замещенные нитрогруппой, атомом галогена, C1-6-алкильной группой или галоген-C1-6-алкильной группой, являются предпочтительными), незамещенную или замещенную алкилсульфонильную группу (C1-6-алкилсульфонильные группы, замещенные нитрогруппой, атомом галогена, C1-6-алкоксигруппой или C6-10-арильной группой, являются предпочтительными), незамещенную или замещенную алкенилсульфонильную группу (C2-6-алкенилсульфонильные группы, замещенные нитрогруппой, атомом галогена, C1-6-алкоксигруппой или C6-10-арильной группой, являются предпочтительными), незамещенную или замещенную алкинилсульфонильную группу (C2-6-алкинилсульфонильные группы, замещенные нитрогруппой, атомом галогена, C1-6-алкоксигруппой или C6-10-арильной группой, являются предпочтительными), незамещенную или замещенную арилсульфонильную группу (C6-10-арилсульфонильные группы, замещенные нитрогруппой, атомом галогена, C1-6-алкильной группой или галоген-C1-6-алкильной группой, являются предпочтительными) и незамещенную или замещенную гетероарилсульфонильную группу (5-6-членные гетероарилсульфонильные группы, замещенные нитрогруппой, атомом галогена, C1-6-алкильной группой или галоген-C1-6-алкильной группой, являются предпочтительными).
В формуле (1) m представляет собой любое из целых чисел от 1 до 4 и предпочтительно равно 1.
В формуле (1) k представляет собой любое из целых чисел от 0 до 3.
Кроме того, k+m≤4, при условии, что из формулы (1) исключен 2-этоксикарбониламино-6-метилпиридин-N-оксид.
[2] Способ получения замещенного производного амино-6-метилпиридин-N-оксида
Способ получения согласно настоящему изобретению включает окисление замещенного производного амино-6-метилпиридина, представленного формулой (2), с помощью пероксида в присутствии соли вольфрамофосфорной кислоты, представленной формулой (3). С помощью способа получения согласно настоящему изобретению можно получать замещенное производное амино-6-метилпиридин-N-оксида, представленное формулой (1-a).
Замещенное производное амино-6-метилпиридина, применяемое в способе получения согласно настоящему изобретению, представляет собой соединение, представленное формулой (2).
Конкретные примеры A, R3 и R4 в формуле (2) или формуле (1-а) включают те же примеры, которые описаны выше в качестве конкретных примеров вышеупомянутой формулы (1). m и k в формуле (2) или формуле (1-a) имеют те же значения, которые указаны выше для m и k в вышеупомянутой формуле (1).
Помимо указанных значений, R3 предпочтительно представляет собой незамещенную или замещенную алкоксикарбонильную группу, более предпочтительно незамещенную или замещенную C1-6-алкоксикарбонильную группу и еще более предпочтительно - трет-бутоксигруппу.
Помимо указанных значений, R4 предпочтительно представляет собой атом водорода или незамещенную или замещенную арилкарбонильную группу, более предпочтительно атом водорода или бензоильную группу и еще более предпочтительно атом водорода.
В качестве положения для размещения заместителя NR3R4 предпочтительным является 2-положение пиридина.
Замещенное производное амино-6-метилпиридина, представленное формулой (2), можно получать, например, путем взаимодействия хлорангидрида или ангидрида кислоты с имеющимся в продаже 2-амино-6-метилпиридином в присутствии основания, такого как пиридин или триэтиламин. Более конкретно, можно получать 2-(трет-бутоксикарбонил)амино-6-метилпиридин с применением в реакции ди-трет-бутилдикарбоната в качестве ангидрида кислоты.
Соль вольфрамофосфорной кислоты, применяемая в способе получения согласно настоящему изобретению, представляет собой соединение, представленное формулой (3).
[PW4O24] в формуле (3) представляет собой пероксовольфраматный гетерополианион. Анион также можно представить формулой {PO4[W(О)(О2)2]4}.
Q в формуле (3) представляет собой катион четвертичного азота.
В качестве катиона четвертичного азота предлагаются катионы четвертичного аммония, иминия, диазония, катионы со скелетами, в которых азот не является циклическим, катионы с циклическими азотсодержащими скелетами и т.п.
Примеры катиона четвертичного аммония включают катионы тетраметиламмония, тетраэтиламмония, тетра-(н-бутил)аммония, тетрафениламмония, тетрабензиламмония, N,N,N-триметилбензиламмония, N,N,N-три(н-бутил)бензиламмония, гексадецилтриметиламмония, дигексадецилдиметиламмония, триоктадецилметиламмония, диоктадецилдиметиламмония, триоктилметиламмония, N,N,N-триметиланилиния и N,N,N,N',N',N'-гексаметилэтан-1,2-диаминия.
Примеры иминия включают бензилиден-трет-бутилметиламмоний и дибензгидрилиденаммоний.
Примеры диазония включают бензолдиазоний, нафталин-2-диазоний и бензол-1,4-бис(диазоний).
Примеры катионов со скелетами, в которых азот не является циклическим, включают 1,1-диметил-1-фенилдиазан-1-ий, гексаметилдиазан-1,2-дий, 2,2-диметилтриазан-2-ий, 1,2-диметилтриазан-1-ий, 1,1,1,3-тетраметилтриаза-2-ен-1-ий и 1H-4λ5-пиридо[1,2,3-de]хиноксалин-4-илий.
Примеры катионов с циклическими азотсодержащими скелетами включают 2,2-диэтил-2,5-диазабицикло[4.2.2]декан-2-ий, 1,3-диметилпиридин-1-ий, 3,7-дибром-5-метилфеназин-5-ий, 1,3-диметил-1H-бензимидазол-3-ий, 1,1,4,4-тетраметилпиперазин-1,4-дий и цетилпиридиний.
В их число, с точки зрения селективности и реакционной способности, входят те, в которых Q предпочтительно представляет собой четвертичный аммоний, более предпочтительно тетра-(н-бутил)аммоний или бензилтри-(н-бутил)аммоний и особенно предпочтительно тетра-(н-бутил)аммоний.
Соль вольфрамофосфорной кислоты, представленную формулой (3), можно получать с помощью способа, описанного в патентном документе 4 или т.п.
Например, путем растворения вольфрамата (VI) натрия в дистиллированной воде с добавлением к полученному раствору водного раствора фосфорной кислоты и последующим добавлением концентрированной серной кислоты, чтобы довести pH раствора до кислотного диапазона, с последующим добавлением перекиси водорода, перемешиванием при комнатной температуре и затем добавлением галогенированного четвертичного аммония, такого как хлорид тетра-(н-бутил)аммония, можно получать соль вольфрамофосфорной кислоты, представленную формулой (3), такую как соль три[тетра-(н-бутил)аммоний]тетра(дипероксовольфрамо)фосфорной кислоты.
Соль вольфрамофосфорной кислоты, представленную формулой (3), которая применяется в способе получения согласно настоящему изобретению, можно выделять и очищать после получения, чтобы подвергнуть ее реакции окисления, хотя ее также можно подвергать реакции окисления в непрерывном режиме без осуществления процедуры выделения. С точки зрения удобства процедуры, полученную соль вольфрамофосфорной кислоты, которая представлена формулой (3), предпочтительно подвергать реакции окисления в непрерывном режиме без осуществления процедуры выделения. Следует отметить, что процедура выделения включает фильтрование, промывание и т.п.
Применяемое количество соли вольфрамофосфорной кислоты, представленной формулой (3), специально не ограничивается, хотя предпочтительно составляет от 0,001 мол.% до 1000 мол.%, более предпочтительно от 0,01 мол.% до 100 мол.% и особенно предпочтительно от 0,1 мол.% до 10 мол.% относительно замещенного производного амино-6-метилпиридина, представленного формулой (2).
Пероксид, применяемый в реакции окисления, в способе получения согласно настоящему изобретению специально не ограничивается. Примеры пероксида включают органические пероксиды, такие как дикумилпероксид, 1,1-ди-трет-бутилперокси-3,3,5-триметилциклогексан, 1,1-ди-трет-бутилпероксициклогексан, 2,2-ди-трет-бутилпероксибутан, н-бутил-4,4-трет-бутилпероксивалерат, 2,2-бис-(4,4-ди-трет-бутилпероксициклогексан)пропан, 2,2,4-триметилпентилпероксинеодеканоат, α-кумилпероксинеодеканоат, трет-бутилпероксинеогексаноат, трет-бутилпероксиацетат, трет-бутилпероксилаурат, трет-бутилпероксибензоат, трет-бутилпероксиизофталат, надуксусная кислота и надмуравьиная кислота; и неорганические пероксиды, такие как перекись водорода и пероксид натрия.
Из упомянутого выше перекись водорода является предпочтительной с точки зрения безопасности, экономики и селективности.
Применяемое количество пероксида специально не ограничивается, хотя предпочтительно составляет от 100 мол.% до 2000 мол.%, более предпочтительно от 100 мол.% до 1000 мол.% и особенно предпочтительно от 100 мол.% до 200 мол.% относительно замещенного производного амино-6-метилпиридина, представленного формулой (2).
Кроме того, в качестве пероксида можно применять водный раствор перекиси водорода. Концентрация водного раствора перекиси водорода специально не ограничивается, хотя предпочтительно она составляет от 0,1 до 70 масс.%, более предпочтительно от 5 до 40 масс.% и особенно предпочтительно от 30 до 35 масс.%.
В способе получения согласно настоящему изобретению реакцию можно осуществлять в присутствии органического растворителя. Органический растворитель специально не ограничивается при условии, что он представляет собой органический растворитель, способный растворять замещенное производное амино-6-метилпиридина, представленного формулой (2), без окисления. Примеры растворителя включают ацетонитрил, бензол, ацетон, метиленхлорид, хлороформ и диоксан. Например, когда в качестве пероксида применяется перекись водорода, в качестве растворителя предпочтительным является метиленхлорид или хлороформ, и особенно предпочтительным является хлороформ.
Температура с момента начала реакции окисления до конца реакции окисления специально не ограничивается, хотя температура предпочтительно находится в диапазоне от -78°C до 200°C, более предпочтительно от -20°C до 120°C и особенно предпочтительно от 10°C до 100°C. Когда температура слишком высокая, имеют обыкновение протекать побочные реакции. Когда температура слишком низкая, реакции имеют обыкновение протекать слабо. Время реакции окисления можно соответствующим образом выбирать в зависимости от масштаба реакции. За течением реакции можно наблюдать, например, с помощью обычного анализа, такого как газовая хроматография, высокоэффективная жидкостная хроматография, тонкослойная хроматография, ЯМР или ИК-спектроскопия.
С помощью реакции окисления, которая описана выше, можно получать замещенное производное амино-6-метилпиридин-N-оксида, представленное формулой (1-a). После завершения реакции окисления замещенное производное амино-6-метилпиридин-N-оксида, представленное формулой (1-a), которое образовалось, можно выделять. Способ выделения можно соответствующим образом выбирать в соответствии с типом пероксида, применяемого в реакции окисления, или природы требуемого продукта. Например, когда в качестве пероксида применяется перекись водорода, после завершения реакции окисления или после разложения оставшейся перекиси водорода под действием восстановителя, такого как сульфит натрия, к реакционному раствору, в случае необходимости, добавляют воду и органический растворитель с последующим проведением экстракции и процедуры разделения жидких фаз, и затем осуществляют концентрацию полученного органического слоя, чтобы выделить требуемый продукт.
Кроме того, водный слой, полученный при процедуре разделения жидких фаз, содержит соль вольфрамофосфорной кислоты, представленную формулой (3), и, следовательно, водный слой можно повторно использовать в том виде, как он есть, или после проведения обработки с целью концентрации или т.п. по мере необходимости для реакции окисления в способе получения согласно настоящему изобретению.
Способ получения согласно настоящему изобретению является экономически выгодным, поскольку удаление соли вольфрамофосфорной кислоты, представленной формулой (3), после реакции происходит легко, и также возможно ее повторное использование.
Кроме того, замещенное производное амино-6-метилпиридин-N-оксида, представленное формулой (1-a), которое получают с помощью способа получения согласно настоящему изобретению, применимо в качестве промежуточного соединения при производстве сельскохозяйственных химических препаратов или т.п.
[3] Способ получения галогеналкильного азотсодержащего гетероциклического производного
[3-1] Первый вариант осуществления изобретения
Способ получения галогеналкильного азотсодержащего гетероциклического соединения согласно настоящему изобретению включает стадию взаимодействия соединения, представленного формулой (4), с галогенирующим агентом для синтеза соединения, представленного формулой (5).
Исходный материал, применяемый в способе получения согласно настоящему изобретению, представляет собой соединение, представленное формулой (4).
В формуле (4) каждый из a1, a2, a3 и a4 независимо представляет собой атом углерода, атом азота, атом кислорода или атом серы. Из существующих возможностей предпочтительно, чтобы все из a1, a2, a3 и a4 представляли собой атом углерода.
Конкретные примеры R1, R2 и A в формуле (4) включают те же значения, которые описаны выше в качестве конкретных примеров для вышеупомянутой формулы (1).
n указывает число заместителей A и равно любому числу из целых чисел от 0 до 4. Когда n равно 2 или более, каждый из A может быть одинаковым или они могут отличаться друг от друга.
Кроме того, в случае присутствия более одного A такие заместители могут связываться друг с другом с образованием цикла, такого как хинолиновый цикл, изохинолиновый цикл, 2,6-нафтиридиновый цикл, 1,8-нафтиридиновый цикл, фталазиновый цикл, хиноксалиновый цикл, хиназолиновый цикл, птеридиновый цикл или пуриновый цикл.
В настоящем изобретении по меньшей мере один из A предпочтительно представляет собой группу, представленную формулой (6).
В формуле (6) * указывает место связывания.
В формуле (6) R5 представляет собой атом водорода, незамещенную или замещенную алкилкарбонильную группу, незамещенную или замещенную арилкарбонильную группу, незамещенную или замещенную гетероарилкарбонильную группу, незамещенную или замещенную алкоксикарбонильную группу, незамещенную или замещенную алкилсульфонильную группу или незамещенную или замещенную арилсульфонильную группу, и конкретные примеры R5 включают те же примеры, которые описаны выше в качестве конкретных примеров R4 в вышеупомянутой формуле (1). Из них предпочтительными являются незамещенная или замещенная алкилкарбонильная группа (более предпочтительно незамещенная или замещенная C1-6-алкилкарбонильная группа), незамещенная или замещенная арилкарбонильная группа (более предпочтительно незамещенная или замещенная C6-10-арилкарбонильная группа) или незамещенная или замещенная алкоксикарбонильная группа (более предпочтительно незамещенная или замещенная C1-6-алкоксикарбонильная группа).
В формуле (6) R6 представляет собой незамещенную или замещенную алкилкарбонильную группу, незамещенную или замещенную арилкарбонильную группу, незамещенную или замещенную гетероарилкарбонильную группу, незамещенную или замещенную алкоксикарбонильную группу, незамещенную или замещенную алкилсульфонильную группу или незамещенную или замещенную арилсульфонильную группу и конкретные примеры R6 включают те же примеры, которые описаны выше в качестве конкретных примеров R4 для вышеупомянутой формулы (1).
R5 и R6 могут связываться с образованием цикла.
В способе получения согласно настоящему изобретению среди соединений, представленных формулой (4), которые являются исходными материалами, предпочтительно применяется соединение, представленное формулой (7).
В формуле (7) A, R1, R2, R5 и R6 имеют те же значения, которые указаны выше для A, R1, R2, R5 и R6 в формуле (4) и формуле (6).
В формуле (7) l указывает число заместителей A и равно любому числу из целых чисел от 0 до 3. Когда l равно 2 или более, каждый из A может одинаковым или они могут отличаться друг от друга и могут связываться друг с другом с образованием цикла.
Соединения, представленные формулой (4) или формулой (7), можно получать окислением соответствующего производного 2-пиколина с применением известного способа, например способа окисления с применением мета-хлорнадбензойной кислоты, способа окисления с применением пероксида водорода в присутствии вольфрамовой кислоты (см. патент США № 3047579) или т.п.
Галогенирующий агент
Галогенирующий агент, применяемый в настоящем изобретении, специально не ограничивается при условии, что он представляет собой агент, применяемый для галогенирования в известной реакции синтеза.
Примеры галогенирующего агента включают тионилхлорид, тионилбромид, сульфурилхлорид, фосген, дифосген, трифосген и оксихлорид фосфора.
Среди упомянутых агентов тионилхлорид, тионилбромид или сульфурилхлорид способны подавлять образование побочных продуктов и повышать селективность и выход соединения, представленного формулой (4), в реакции синтеза даже без присутствия источника галоген-ионов, описанного далее.
Кроме того, фосген, дифосген, трифосген или оксихлорид фосфора позволяют реакции протекать в мягких условиях и также повышают селективность и выход соединения, представленного формулой (4) в реакции синтеза. Фосген, дифосген, трифосген или оксихлорид фосфора можно соответственно применять, когда R5 в формуле (6) представляет собой атом водорода.
Количество применяемого галогенирующего агента специально не ограничивается, хотя предпочтительно оно составляет от 0,8 до 10 эквивалентов и более предпочтительно от 1,5 до 2,5 эквивалентов относительно соединения, представленного формулой (4). Однако при применении дифосгена и трифосгена предпочтительно пересчитывать каждое из эквивалентных значений, описанных выше для фосгена.
Источник галоген-ионов
Источник галоген-ионов, растворимый в органических растворителях, который применяется в настоящем изобретении, представляет собой соль, содержащую анион галогена, которая растворима в органических растворителях.
Примеры источника галоген-ионов включают галогенидную соль аммония, предпочтительно галогенидную соль третичного или четвертичного алкиламмония и более предпочтительно гидрогалогенидную соль триэтиламина или гидрогалогенидную соль диизопропилэтиламина.
Кроме того, примеры других источников галоген-ионов, которые растворимы в органических растворителях, включают галогенидную соль фосфония, предпочтительно галогенидную соль алкилфосфония, содержащую C2-алкильную группу или алкильную группу с большим числом атомов углерода.
Путем создания источника галоген-ионов, который растворим в органическом растворителе, присутствующем в реакционной системе, можно подавлять образование побочных продуктов и повышать селективность и выход соединения, представленного формулой (4), в реакции синтеза. Источник галоген-ионов обладает более значительными эффектами, когда в качестве галогенирующего агента применяется фосген, дифосген, трифосген или оксихлорид фосфора.
Применяемое количество источника галоген-ионов, который растворим в органических растворителях, специально не ограничивается, хотя по отношению к соединению, представленному формулой (4), предпочтительно равно молярному количеству атома галогена, умноженному на 0,8 или более, более предпочтительно молярному количеству атома галогена, умноженному на 1-6.
Органический растворитель
В способе получения согласно настоящему изобретению можно применять органический растворитель. Приемлемые органические растворители специально не ограничиваются, хотя галогеналканы являются предпочтительными, и более предпочтительными являются метиленхлорид или хлороформ.
Другие реакционные материалы
В способе получения согласно настоящему изобретению предпочтительно, чтобы в дополнение к источнику галоген-ионов присутствовал восстановитель (акцептор галогенида водорода). В качестве восстановителя желательным является амин, растворимый в органических растворителях, и более предпочтительными являются третичные алкиламины, содержащие C2-алкильную группу или алкильную группу с большим числом атомов углерода, и особенно предпочтительным является триэтиламин или диизопропилэтиламин.
Количество применяемого восстановителя (акцептора галогенида водорода) предпочтительно равно по меньшей мере количеству, которое может почти полностью поглотить галогенид водорода, образующийся в результате реакции, и более конкретно, равно по меньшей мере однократному молярному количеству образующегося галогенида водорода. Верхний предел применяемого количества предпочтительно равен шестикратному молярному количеству образующегося галогенида водорода. В настоящем изобретении предпочтительными являются совместимые источник галоген-ионов и восстановитель.
Реакция между соединением, представленным формулой (4), и галогенирующим агентом
С точки зрения применяемой методики осуществления, реакция между соединением, представленным формулой (4), и галогенирующим агентом специально не ограничивается. Например, реакцию можно осуществлять путем растворения источника галоген-ионов и восстановителя, которые применяются по мере необходимости в органическом растворителе, добавляя соединение, представленное формулой (4), в раствор с последующим добавлением к реакционной смеси галогенирующего агента. В настоящем изобретении, чтобы достичь особенно высокого выхода, предпочтительно растворять источник галоген-ионов и восстановитель, которые применяются по мере необходимости в органическом растворителе с последующим почти одновременным добавлением в раствор соединения, представленного формулой (4), и галогенирующего агента. Добавление галогенирующего агента можно осуществлять путем добавления по каплям раствора галогенирующего агента в органическом растворителе или вдувания газообразного галогенирующего агента. Кроме того, добавление соединения, представленного формулой (4), можно осуществлять путем добавления жидкости по каплям.
Температура от начала реакции до окончания реакции специально не ограничивается, хотя с точки зрения повышения селективности, температура предпочтительно составляет не более 40°C и более предпочтительно находится в диапазоне от -40°C до 20°C.
С помощью способа получения согласно настоящему изобретению можно получать соединение, представленное формулой (5). A, a1, a2, a3, a4, R1, R2 и n в формуле (5) имеют те же значения, которые указаны выше для A, a1, a2, a3, a4, R1, R2 и n в формуле (4). X представляет собой атом галогена, такой как атом фтора, атом хлора, атом брома или атом йода. Следует отметить, что в тех случаях, когда соединение, представленное формулой (4), служащее в качестве исходного материала, представляет собой соединение, представленное формулой (7), можно получать соединение, представленное формулой (8). В формуле (8) A, l, R1, R2, R5 и R6 имеют те же значения, которые указаны выше для A, l, R1, R2, R5 и R6 в формуле (7), и X представляет собой атом галогена.
[3-2] Второй вариант осуществления изобретения
Способ получения азотсодержащего гетероциклического соединения согласно настоящему изобретению включает стадию превращения соединения, представленного формулой (9), в соединение, представленное формулой (10), и стадию взаимодействия соединения, представленного формулой (10), с галогенирующим агентом для синтеза соединения, представленного формулой (11).
Исходный материал, применяемый в способе получения согласно настоящему изобретению, представляет собой соединение, представленное формулой (9). Соединение соответствует соединению, представленному формулой (4), в которой все a1, a2, a3 и a4 представляют собой атомы углерода, и также по меньшей мере один из заместителей A представляет собой группу, представленную формулой (6a). Следует отметить, что * указывает место связывания в формуле (6a).
[Химическая формула 10]

Конкретные примеры A, R1 и R2 в формуле (9) включают те же значения, которые указаны выше в качестве конкретных примеров для вышеупомянутых формул (4) и (5). Кроме того, k и m в формуле (9), формуле (10) и формуле (11) имеют те же значения, которые указаны выше для k и m в формуле (1).
В формуле (9) или формуле (6a) R6 представляет собой незамещенную или замещенную алкилкарбонильную группу, незамещенную или замещенную арилкарбонильную группу, незамещенную или замещенную гетероарилкарбонильную группу, незамещенную или замещенную алкоксикарбонильную группу, незамещенную или замещенную алкилсульфонильную группу или незамещенную или замещенную арилсульфонильную группу, и конкретные примеры R6 включают те же значения, которые указаны выше в качестве конкретных примеров для R3 и R4. Из них предпочтительными являются незамещенная или замещенная алкилкарбонильная группа, незамещенная или замещенная арилкарбонильная группа, незамещенная или замещенная гетероарилкарбонильная группа или незамещенная или замещенная алкоксикарбонильная группа; более предпочтительной является незамещенная или замещенная алкоксикарбонильная группа; и особенно предпочтительной является незамещенная или замещенная C3-8-алкоксикарбонильная группа.
Соединения, представленные формулой (9) (за исключением 2-этоксикарбониламино-6-метилпиридин-N-оксида), являются новыми веществами. Соединение можно получать с помощью способа, в котором соответствующее производное 2-пиколина окисляется с помощью мета-хлорнадбензойной кислоты; с помощью способа, в котором соответствующее производное 2-пиколин окисляется с помощью перекиси водорода в присутствии вольфрамовой кислоты (см. патент США № 3047579) или т.п.
Стадия превращения соединения, представленного формулой (9), в соединение, представленное формулой (10)
Примеры способа превращения соединения, представленного формулой (9), в соединение, представленное формулой (10), включают способ, в котором соединение, представленное формулой R7X1, подвергается взаимодействию с соединением, представленным формулой (9). Здесь R7 имеет то же самое значение, которое указано для R7 в формуле (10), описанной далее; и X1 представляет собой атом хлора или атом брома.
Выполняя стадию превращения, можно получать соединение, представленное формулой (10).
А, k, R1, R2, R6 и m в формуле (10) имеют те же значения, которые указаны для A, k, R1, R2, R6 и m в формуле (9).
В формуле (10) R7 представляет собой незамещенную или замещенную алкилкарбонильную группу, незамещенную или замещенную арилкарбонильную группу, незамещенную или замещенную гетероарилкарбонильную группу, незамещенную или замещенную алкоксикарбонильную группу, незамещенную или замещенную алкилсульфонильную группу или незамещенную или замещенную арилсульфонильную группу; и конкретные примеры R7 включают те же значения, которые указаны выше в качестве конкретных примеров для R3 и R4. Когда m равно 2 или более, каждый из R7 может быть одинаковым или они могут отличаться друг от друга.
Реакция между соединением, представленным формулой (10), и галогенирующим агентом
Для осуществления реакции между соединением, представленным формулой (10), и галогенирующим агентом можно использовать те же методики, которые применяются для осуществления реакции между соединением, представленным формулой (4), и галогенирующим агентом в первом варианте осуществления изобретения. Кроме того, примеры галогенирующих агентов, источники галоген-ионов, органические растворители и другие вспомогательные реакционные материалы, которые можно применять во втором варианте осуществления изобретения, включают те же материалы, которые можно применять в первом варианте осуществления изобретения.
С помощью способа получения согласно второму варианту осуществления настоящего изобретения можно получать соединение, представленное формулой (11).
В формуле (11) A, k, R1, R2, R6, R7 и m имеют те же значения, которые указаны выше для A, k, R1, R2, R6, R7 и m в вышеупомянутой формуле (9) и формуле (10).
В формуле (11) X представляет собой атом галогена, такой как атом фтора, атом хлора, атом брома или атом йода.
[3-3] Третий вариант осуществления изобретения
Способ получения азотсодержащего гетероциклического соединения согласно настоящему изобретению включает стадию взаимодействия соединения, представленного формулой (9), с галогенирующим агентом в присутствии соединения, представленного формулой (12), для синтеза соединения, представленного формулой (13).
Для осуществления способа взаимодействия соединения, представленного формулой (9), с галогенирующим агентом в присутствии соединения, представленного формулой (12), можно использовать те же методики, которые применяются в способе взаимодействия соединения, представленного формулой (4), с галогенирующим агентом в первом варианте осуществления изобретения, за исключением того, что соединение, представленное формулой (12), присутствует в реакционной системе. Кроме того, примеры галогенирующих агентов, источники галоген-ионов, органические растворители и другие вспомогательные реакционные материалы, которые можно применять в третьем варианте осуществления изобретения, включают те же материалы, которые можно применять в первом варианте осуществления изобретения.
С помощью способа получения согласно третьему варианту осуществления настоящего изобретения можно получать соединение, представленное формулой (13).
В формуле (12) R8 представляет собой незамещенную или замещенную алкилкарбонильную группу, незамещенную или замещенную арилкарбонильную группу или незамещенную или замещенную алкоксикарбонильную группу; и конкретные примеры R8 включают те же значения, которые указаны выше в качестве конкретных примеров для R3. Кроме того, X1 в формуле (12) представляет собой атом хлора или атом брома.
В формуле (13) конкретные примеры A, R1, R2, R6 и R8 включают те же значения, которые указаны выше в качестве конкретных примеров для A, R1, R2, R6 и R8 в вышеупомянутых формуле (9) и формуле (12). В формуле (13) k и m имеют те же значения, которые указаны выше для k и m в вышеупомянутых формуле (9) и формуле (12). Кроме того, X в формуле (13) представляет собой атом галогена, такой как атом фтора, атом хлора, атом брома или атом йода.
Соединения, представленные формулами (5), (8), (11) или (13), которые получают с помощью способа получения согласно настоящему изобретению, применимы в качестве промежуточных соединений при синтезе сельскохозяйственный химических препаратов, фармацевтических продуктов или т.п.
Примеры
Далее настоящее изобретение будет описано более подробно с применением ряда примеров и сравнительных примеров. Однако технический объем настоящего изобретения никоим образом не ограничивается данными примерами.
Пример A1
1,65 г (5 ммоль) дигидрата вольфрамата (VI) натрия (Na2WO4·2H2O) растворяли в 20 мл дистиллированной воды. К полученному раствору добавляли 6 мл 10%-й фосфорной кислоты (H3PO4) и затем добавляли к раствору концентрированную серную кислоту, чтобы довести pH до 2,0.
К раствору добавляли 8 мл 25%-го водного раствора перекиси водорода и полученную смесь перемешивали при комнатной температуре в течение 20 минут. К реакционной смеси медленно по каплям добавляли водный раствор хлорида тетра-(н-бутил)аммония (4 моль) при энергичном перемешивании. После завершения добавления по каплям полученную смесь перемешивали при комнатной температуре в течение 50 минут.
Полученный реакционный раствор фильтровали, и остаток промывали водой. Полученный остаток растворяли в хлороформе, затем обезвоживали и сушили с помощью безводного сульфата натрия и фильтровали полученный раствор. Затем путем отгонки растворитель удаляли из фильтрата, получая при этом бесцветные кристаллы ([(н-C4H9)4N]3[PW4O24]).
В реакционный сосуд загружали 0,567 г 30%-го водного раствора перекиси водорода. К этому добавляли 0,093 г полученной выше соли вольфрамофосфорной кислоты.
Затем к полученной смеси добавляли 1,25 мл раствора 2-(трет-бутоксикарбонил)амино-6-метилпиридина в метиленхлориде, имеющего концентрацию 2 моль/л, и полученную смесь перемешивали при комнатной температуре в течение 20 минут. Затем смесь перемешивали в течение 1 часа при кипячении с обратным холодильником.
К реакционному раствору добавляли 2 мл воды и 3 мл метиленхлорида с последующей экстракцией и разделением жидких фаз. Полученный водный слой дважды экстрагировали 3 мл метиленхлорида, и все полученные органические слои объединяли вместе. Полученный органический слой анализировали с помощью ВЭЖХ. В результате, как было показано, получали 2-(трет-бутоксикарбонил)амино-6-метилпиридин-N-оксид с выходом 97,6%.
Результаты измерений 1H-ЯМР-спектра полученного 2-(трет-бутоксикарбонил)амино-6-метилпиридин-N-оксида приведены ниже.
1Н-ЯМР (CDCl3, δ м.д.): 1,53 (9Н, с), 2,55 (3Н, с), 6,87 (1Н, д, J=7,6 Гц), 7,19 (1Н, т, J=8,2 Гц), 8,01 (1Н, д, J=8,8 Гц), 9,43 (1Н, ушир.с).
Пример A2
В реакционный сосуд, в который было загружено 0,041 г дигидрата вольфрамата (VI) натрия (Na2WO4·2H2O), добавляли 0,2 г 10%-го водного раствора фосфорной кислоты (Н3РО4) и затем к полученной смеси добавляли 0,567 г 30%-го водного раствора перекиси водорода.
Затем в сосуд добавляли 0,031 г хлорида бензилтри(н-бутил)аммония и перемешивали полученную смесь при комнатной температуре в течение 10 минут. Из реакционного раствора выпадали в осадок белые кристаллы.
Затем в сосуд добавляли 1,25 мл раствора 2-(трет-бутоксикарбонил)амино-6-метилпиридина в метиленхлориде, имеющего концентрацию 2 моль/л, и перемешивали полученную смесь при комнатной температуре в течение 5 минут. Затем смесь перемешивали в течение 2 часов при кипячении с обратным холодильником.
К полученному реакционному раствору добавляли 5 мл воды для проведения экстракции и разделения жидких фаз, и полученный водный слой дважды экстрагировали 3 мл метиленхлорида. Все полученные органические слои объединяли вместе. Полученный органический слой анализировали с помощью ВЭЖХ. В результате было показано, что 2-(трет-бутоксикарбонил)амино-6-метилпиридин-N-оксид был получен с выходом 97,1%.
Пример A3
В реакционный сосуд, в который было загружено 0,274 г дигидрата вольфрамата (VI) натрия (Na2WO4·2H2O), добавляли 1,63 г 10%-го водного раствора фосфорной кислоты (H3PO4) и затем к полученной смеси добавляли 2,45 г 30%-го водного раствора перекиси водорода.
Затем в сосуд добавляли 0,207 г хлорида бензилтри(н-бутил)аммония и полученную смесь перемешивали при комнатной температуре в течение 10 минут. Из реакционного раствора выпадали в осадок белые кристаллы.
Затем в сосуд добавляли 8,3 мл раствора 2-(трет-бутоксикарбонил)амино-6-метилпиридина в хлороформе, имеющего концентрацию 2 моль/л, и полученную смесь перемешивали при комнатной температуре в течение 5 минут. Затем смесь перемешивали в течение 2 часов при кипячении с обратным холодильником.
К полученному реакционному раствору добавляли 10 мл воды для проведения экстракции и разделения жидких фаз, и полученный водный слой дважды экстрагировали 5 мл хлороформа. Все полученные органические слои объединяли вместе. Полученный органический слой анализировали с помощью ВЭЖХ. В результате было показано, что 2-(трет-5-бутоксикарбонил)амино-6-метилпиридин-N-оксид был получен с выходом почти 100%.
Из приведенных выше результатов ясно, что замещенное производное амино-6-метилпиридин-N-оксида можно получать с высокой селективностью путем окисления замещенного производного амино-6-метилпиридина с применением пероксида, такого как перекись водорода, в присутствии соли вольфрамофосфорной кислоты, такой как [(н-C4H9)4N]3[PW4O24] или [(C6H5CH2)(н-C4H9)3N]3[PW4O24]. Кроме того, из сравнения примера A1 и примера A2 очевидно, что селективность реакции окисления замещенного производного амино-6-метилпиридина не ухудшается, даже когда соль вольфрамофосфорной кислоты применяется в реакции окисления, как она есть, без выделения после ее получения. Из сравнения примера A1 и примера A3 очевидно, что требуемый продукт можно получать с высоким выходом с меньшим количеством катализатора и окислителя, когда в качестве растворителя в реакции применяется хлороформ.
Пример В1
7 мл раствора, содержащего 0,54 г (2,4 ммоль) 2-трет-бутоксикарбониламино-6-метилпиридин-N-оксида в метиленхлориде, охлаждали до -17°C. К раствору добавляли 0,63 г (5,3 ммоль) тионилхлорида и затем добавляли по каплям 3 мл раствора, содержащего 1,02 г (8,6 ммоль) триэтиламина в метиленхлориде. Давали реакции протекать в течение 3 часов при -15°C. Затем к реакционной смеси добавляли 20 мл воды при -10°C. Затем с помощью каустической соды доводили pH раствора до 11. 2-трет-бутоксикарбониламино-6-хлорметилпиридин, который представлял собой требуемый продукт, получался с выходом 60% в органическом слое, полученном при разделении жидких фаз.
Пример B2
Раствор A получали путем растворения 1,35 г (6,0 ммоль) 2-трет-бутоксикарбониламино-6-метилпиридин-N-оксида в 18 мл метиленхлорида и охлаждали до -15°C.
Раствор В получали путем растворения 1,57 г (13,2 ммоль) тионилхлорида в 18 мл метиленхлорида.
Раствор С получали путем растворения 2,43 г (24,0 ммоль) триэтиламина в 18 мл метиленхлорида.
Раствор В добавляли по каплям к раствору A. Когда от начала добавления капель проходило 5 минут, начинали добавление по каплям раствора С. Раствор В добавляли по каплям в течение 70 минут, и раствор С добавляли по каплям в течение 105 минут, так что каждый из растворов добавлялся полностью. Когда после завершения добавления капель проходил один час, к смеси добавляли 100 мл воды. Затем pH раствора доводили до 3,7 путем добавления насыщенного водного раствора бикарбоната натрия. 2-трет-бутоксикарбониламино-6-хлорметилпиридин, который представлял собой требуемый продукт, получался с выходом 62% в органическом слое, полученном при разделении жидких фаз.
Пример B3
0,3 г (3,0 ммоль) триэтиламина и 2,48 г (18,0 ммоль) гидрохлорида триэтиламина растворяли в 18 мл метиленхлорида. Раствор охлаждали до -14°C и добавляли по каплям 18 мл раствора, содержащего 1,34 г (6,0 ммоль) 2-трет-бутоксикарбониламино-6-метилпиридин-N-оксида и 2,13 г (21,1 ммоль) триэтиламина в метиленхлориде, и одновременно 18 мл раствора, содержащего 1,57 г (13,2 ммоль) тионилхлорида в метиленхлориде. Давали реакции протекать в течение 2 часов при -15°C. Затем к реакционной смеси добавляли 15 мл воды. Затем доводили pH раствора до 13 с помощью каустической соды. После разделения жидких фаз органический слой промывали разбавленной хлористоводородной кислотой. 2-трет-бутоксикарбониламино-6-хлорметилпиридин, который представлял собой требуемый продукт, получался с выходом 55% в полученном органическом слое.
Пример B4
0,31 г (3,1 ммоль) триэтиламина и 2,57 г (18,7 ммоль) гидрохлорида триэтиламина растворяли в 18 мл хлороформа. Раствор охлаждали до -14°C и добавляли по каплям 18 мл раствор, содержащий 1,34 г (6,0 ммоль) 2-трет-бутоксикарбониламино-6-метилпиридин-N-оксида и 2,20 г (21,8 ммоль) триэтиламина в хлороформе, и одновременно в течение 105 минут 18 мл раствора, содержащего 1,63 г (13,7 ммоль) тионилхлорида в метиленхлориде. Давали реакции протекать в течение 2 часов при -15°C. Затем к реакционной смеси добавляли 30 мл воды. Затем pH раствора доводили до 5 с помощью насыщенного водного раствора бикарбоната натрия. 2-трет-бутоксикарбониламино-6-хлорметилпиридин, который представлял собой требуемый продукт, получался с выходом 77% в органическом слое, полученном при разделении жидких фаз.
Пример В5
0,224 г (1,0 ммоль) 2-трет-бутоксикарбониламино-6-хлорметилпиридин-N-оксида растворяли в 2 мл хлороформа. Во время охлаждения льдом полученного в результате раствора при перемешивании последовательно добавляли 0,139 мл (1,0 ммоль) триэтиламина, 0,174 мл (1,5 ммоль) бензоилхлорида, 0,088 мл (1,2 ммоль) тионилхлорида и 0,14 г (1,0 ммоль) гидрохлорида триэтиламина. После завершения добавления в течение 15 минут по каплям добавляли 0,418 мл (3,0 ммоль) триэтиламина, который был растворен в 2 мл хлороформа. После завершения добавления по каплям полученную смесь перемешивали при охлаждении льдом в течение 5 минут и затем в течение 30 минут при комнатной температуре. Затем полученный в результате продукт анализировали с помощью ВЭЖХ для количественного определения. 2-бензоил-трет-бутоксикарбониламино-6-хлорметилпиридин, который представлял собой требуемый продукт, получался с выходом 72%.
Пример B6
1 мл раствора, содержащего 0,22 г (1,0 ммоль) 2-трет-бутоксикарбониламино-6-метилпиридин-N-оксида в хлороформе, в течение 10 минут при комнатной температуре добавляли по каплям к 5 мл раствора, содержащего 2,0 ммоль пара-нитробензоилхлорида в хлороформе. Спустя 20 минут после добавления реакционную смесь охлаждали до -15°C и в течение 5 минут добавляли к ней по каплям 0,30 г (3,0 ммоль) триэтиламина. Спустя 5 минут после этого в течение 5 минут добавляли по каплям 1 мл раствора, содержащего 0,20 г (0,67 ммоль) трифосгена в хлороформе. Спустя еще 20 минут после этого к раствору в течение 5 минут добавляли по каплям 0,20 г (2,0 ммоль) триэтиламина и затем перемешивали полученную смесь в течение 30 минут. Полученный реакционный раствор выливали в насыщенный водный раствор бикарбоната натрия и экстрагировали этилацетатом. Органический слой сушили с помощью сульфата магния, фильтровали и концентрировали. Полученный сырой продукт очищали колоночной хроматографией (гексан/этилацетат), получая при этом 2-трет-бутоксикарбонил-2-пара-нитробензоиламино-6-хлорметилпиридин, который представлял собой требуемый продукт, с выходом 64% (по результатам ВЭЖХ).
Пример В7
Раствор С получали путем растворения 0,27 г (2,5 ммоль) триэтиламина и 2,07 г (15 ммоль) гидрохлорида триэтиламина в 15 мл хлороформа.
Раствор A получали путем добавления хлороформа к 1,14 г (5,07 ммоль) 2-трет-бутоксикарбониламино-6-хлорметилпиридин-N-оксида и 1,77 г (17,5 ммоль) триэтиламина до общего объема 10 мл.
Для получения раствора В 1,16 г (11,77 ммоль) фосгена растворяли в хлороформе и доводили объем раствора до общего объема 10 мл.
Раствор С охлаждали приблизительно до -15°C. К нему одновременно в течение 40 минут добавляли по каплям раствор A и раствор В. После завершения добавления капель реакционную смесь перемешивали в течение 30 минут при -15°C. К вышеупомянутой реакционной смеси, сохраняемой при температуре 0°C или ниже, добавляли 10 мл воды. Доводили pH раствора до 11 или выше путем добавления водного раствора каустической соды с концентрацией 28%. После разделения жидких фаз полученный водный слой экстрагировали хлороформом. Когда органический слой анализировали с помощью ВЭЖХ для количественного определения, было показано, что 2-трет-бутоксикарбониламино-6-хлорметилпиридин, который представлял собой требуемый продукт, получался с выходом 69%. В этот процент включен 1% побочных продуктов (в терминах относительных процентов площади при ВЭЖХ).
Пример В8
Реакцию осуществляли по примеру B7 за исключением того, что триэтиламин заменяли диизопропилэтиламином, и гидрохлорид триэтиламина заменяли гидрохлоридом диизопропилэтиламина, соответственно. Органический слой, полученный при экстракции хлороформом, анализировали с помощью ВЭЖХ. В результате содержание побочных продуктов составляло 1% (относительные проценты площади при ВЭЖХ). Органический слой концентрировали и полученный сырой продукт очищали колоночной хроматографией на силикагеле (гексан/этилацетат), получая при этом 0,67 г 2-трет-бутоксикарбониламино-6-хлорметилпиридина (выход: 55%), который представлял собой требуемый продукт.
Пример B9
20,37 г (92,2 ммоль) 2-трет-бутоксикарбониламино-6-метилпиридина растворяли в 100 мл хлороформа и полученный раствор охлаждали водой со льдом. К раствору добавляли 25 г (101,4 ммоль) мета-хлорнадбензойной кислоты (с содержанием продукта 70% масс.). После подтверждения того факта, что не происходит большого выделения тепла, температуру повышали до комнатной температуры. Спустя 2 часа к реакционной смеси добавляли 20 мл воды. Затем pH раствора доводили до 14 путем добавления водного раствора каустической соды с концентрацией 28%. После разделения жидких фаз полученный водный слой экстрагировали хлороформом. Хлороформный слой промывали 28%-м водным раствором каустической соды, затем водой и сушили с помощью сульфата магния. Хлороформ удаляли отгонкой при пониженном давлении, чтобы получить 21,30 г 2-трет-бутоксикарбониламино-6-метилпиридин-N-оксида (выход: 99,6%) в форме маслянистого продукта светло-оранжевого цвета.
Измеряли ЯМР-спектр и МС-спектр полученного 2-трет-бутоксикарбониламино-6-метилпиридин-N-оксида и получали следующие результаты.
1Н ЯМР: 1,53 (9Н, с), 2,55 (3Н, с), 6,87 (1Н, д, J=7,6 Гц), 7,19 (1Н, т, J=8,2 Гц), 8,01 (1Н, д, J=8,8 Гц), 9,43 (1Н, ушир.с).
13С ЯМР: 18,09, 28,01, 81,76, 110,23, 117,65, 126,68, 144,31, 146,85, 151,37.
MC m/z: 224 (M+), 168, 151, 124, 107.
Пример В10
Получали 4 мл раствора, содержащего 0,45 г (2 ммоль) 2-трет-бутоксикарбониламино-6-метилпиридин-N-оксида и 0,26 г (2 ммоль) диизопропилэтиламина в хлороформе, и доводили его температуру до 10°C. К полученному раствору в течение более 10 минут при 10°С добавляли по каплям 0,29 г (2 ммоль) бензоилхлорида. После перемешивания в течение дополнительных 40 минут при 10°C добавляли 5 мл воды с последующим разделением жидких фаз. Хлороформный слой, полученный при разделении жидких фаз, дважды промывали 5 мл воды и затем сушили с помощью сульфата магния с последующим фильтрованием. Полученный раствор концентрировали при пониженном давлении и сушили, получая при этом 0,64 г 2-трет-бутоксикарбонил-2-бензоиламино-6-метилпиридин-N-оксида (выход: 97%) в форме желто-коричневого аморфного вещества, которое представляло собой требуемый продукт.
Измеряли ЯМР-спектр полученного 2-трет-бутоксикарбонил-2-бензоиламино-6-метилпиридин-N-оксида и получали следующие результаты.
1Н ЯМР: 1,23 (9H, c), 2,54 (3H, c), 7,20 (д, J=7,6 Гц, 1Н), 7,23 (д, J=5,4 Гц, 1Н), 7,35 (дд, J=7,6, 2,4 Гц, 1Н), 7,44 (т, J=7,4 Гц, 2Н), 7,53 (тт, J=7,4, 1,2 Гц, 1Н), 7,92 (дд, J=6,8, 1,2 Гц, 2Н).
13С-ЯМР: 18,2, 27,5, 84,3, 123,4, 124,5, 124,8, 128,0, 128,7, 131,9, 135,6, 144,7, 149,2, 151,0, 170,9.
Пример В11
Получали 2 мл раствора, содержащего 0,24 г (1 ммоль) 2-трет-бутоксикарбониламино-6-метилпиридина и 0,26 г (2 ммоль) диизопропилэтиламина в хлороформе и охлаждали его водой со льдом. Раствор вышеупомянутой смеси добавляли по каплям при температуре 0°C к 0,3 мл раствора, содержащего 0,11 г (1,2 ммоль) метилхлорформиата в хлороформе. После перемешивания в течение дополнительных 20 минут температуру повышали до комнатной температуры. После перемешивания в течение дополнительных 5 часов при комнатной температуре к смеси добавляли 5 мл воды и 1 мл 3н раствора хлористоводородной кислоты с последующим разделением жидких фаз. Органический слой, полученный при разделении жидких фаз, сушили с помощью сульфата магния с последующим фильтрованием и концентрировали полученный раствор при пониженном давлении, чтобы получить 0,27 г 2-трет-бутоксикарбонилметоксикарбониламино-6-метилпиридин-N-оксид (выход: 96%) в виде светло-желтой маслянистой жидкости, которая представляла собой требуемый продукт.
Измеряли ЯМР-спектр полученного 2-трет-бутоксикарбонилметоксикарбониламино-6-метилпиридин-N-оксида и получали следующие результаты.
1Н ЯМР: 1,44 (9Н, с), 2,54 (3Н, с), 3,79 (3Н, с), 7,13-7,26 (м, 3Н).
Сравнительный пример B1
10 мл раствора, содержащего 1,99 г (6,7 ммоль) трифосгена в метиленхлориде, охлаждали до 0°C. К нему по каплям одновременно добавляли каждый из следующих растворов: 5 мл раствора, содержащего 1,12 г (5 ммоль) 2-трет-бутоксикарбониламино-6-метилпиридин-N-оксида в метиленхлориде, и 5 мл раствора, содержащего 1,01 г (10 ммоль) диизопропиламина в метиленхлориде. После завершения добавления капель температуру жидкости доводили до комнатной температуры и затем перемешивали полученную смесь в течение 1 часа. Реакционный раствор выливали в насыщенный водный раствор бикарбоната натрия и затем экстрагировали метиленхлоридом. Органический слой сушили с помощью сульфата магния, фильтровали и концентрировали. Полученный сырой продукт очищали колоночной хроматографией (гексан/этилацетат). Получали всего 73 мг 2-трет-бутоксикарбониламино-6-хлорметилпиридина, который представлял собой требуемый продукт (выход: 3%). С другой стороны, получали 503 мг (67%) побочных продуктов в форме белого твердого вещества.
Сравнительный пример B2
1,03 г (8 ммоль) диизопропилэтиламина и 0,67 г (3 ммоль) 2-трет-бутоксикарбониламино-6-метилпиридин-N-оксида растворяли в 10 мл метиленхлорида и затем охлаждали полученный раствор до -15°C. К полученному раствору по каплям в течение 2 часов добавляли 20 мл раствора, содержащего 0,60 г (2 ммоль) трифосгена в метиленхлориде, поддерживая при этом внутреннюю температуру раствора при -15°C. После завершения добавления капель полученную жидкость перемешивали в течение 1 час при -15°C. К вышеупомянутой реакционной смеси, поддерживаемой при температуре 0°C или ниже, добавляли 20 мл воды. Доводили pH раствора до 11 или выше путем добавления водного раствора каустической соды с концентрацией 28%. После разделения жидких фаз полученный водный слой экстрагировали этилацетатом. Органический слой промывали водой, сушили с помощью безводного сульфата магния и затем концентрировали при пониженном давлении. Полученный сырой продукт очищали колоночной хроматографией на силикагеле (гексан/этилацетат). Получали 0,18 г 2-трет-бутоксикарбониламино-6-хлорметилпиридина, который представлял собой требуемый продукт (выход: 25%). При этом получалось 4% побочных продуктов (в терминах относительных процентов площади при ВЭЖХ).
Сравнительный пример B3
Реакцию осуществляли по примеру В8 за исключением того, что не добавляли гидрохлорид диизопропилэтиламина. Выход 2-трет-бутоксикарбониламино-6-хлорметилпиридина после очистки колоночной хроматографией на силикагеле составлял 32%. При этом получалось 13% побочных продуктов (в терминах относительных процентов площади при ВЭЖХ).
Промышленная применимость
В способе получения согласно настоящему изобретению азотсодержащие гетероциклические соединения, такие как замещенное производное амино-6-метилпиридин-N-оксида и галогеналкильное азотсодержащее гетероциклическое производное можно получать с высокой селективностью и также с высоким выходом. Азотсодержащее гетероциклическое соединение, полученное по способу получения согласно настоящему изобретению, применимо в качестве промежуточного соединения для промышленного производства сельскохозяйственных химических препаратов или т.п.
Изобретение относится к замещенному аминопиридин-N-оксиду формулы (1), где R4 представляет собой С1-6алкоксикарбонильную группу. Также изобретение относится к способу получения аминопиридин-N-оксида формулы (1), включающему окисление производного амино-6-метилпиридина формулы (2) пероксидом в присутствии соли вольфрамофосфорной кислоты формулы Q3[PW4O24], где Q представляет собой четвертичный аммоний, и к способу получения соединения формулы (8) (где R6 представляет собой С1-6алкоксикарбонильную группу и Х представляет собой атом галогена) путем взаимодействия соединения формулы (1) с тионилхлоридом в присутствии триэтиламингалогенида. Технический результат - соединение формулы (1) в качестве промежуточного для получения фармацевтических и агрохимических веществ. 3 н. и 1 з.п. ф-лы, 17 пр.
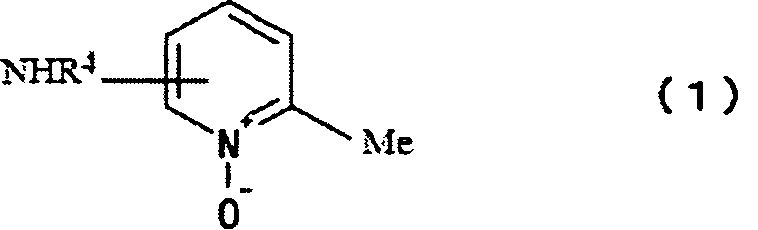
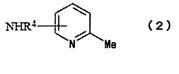
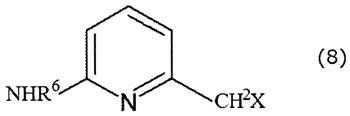
1. Замещенный аминопиридин-N-оксид, представленный формулой (1):

в формуле (1)
R4 представляет собой незамещенную C1-6алкоксикарбонильную группу;
при условии, что 2-этоксикарбониламино-6-метилпиридин-N-оксид исключен.
2. Способ получения замещенного производного амино-6-метилпиридин-N-оксида, представленного формулой (1-а), включающий окисление замещенного производного амино-6-метилпиридина, представленного формулой (2), с применением пероксида в присутствии соли вольфрамофосфорной кислоты, представленной формулой (3):
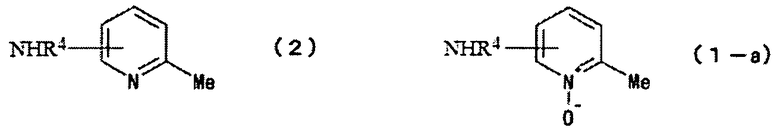
Q3[PW4O24] (3),
в которых
R4 представляет собой незамещенную C1-6алкоксикарбонильную группу; и
Q представляет собой четвертичный аммоний.
3. Способ получения замещенного производного амино-6-метилпиридин-N-оксида по п.2, в котором соль вольфрамофосфорной кислоты, представленную формулой (3), получают без процедуры выделения после ее получения.
4. Способ получения соединения, представленного формулой (8), включающий взаимодействие соединения, представленного формулой (7), с тионилхлоридом в присутствии триэтиламингалогенида:
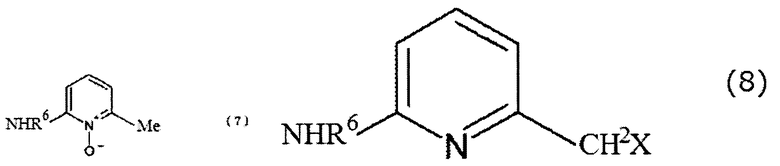
каждый
R6 представляет собой незамещенную C1-6алкоксикарбонильную группу; и
Х представляет собой атом галогена.
| Бесколесный шариковый ход для железнодорожных вагонов | 1917 |
|
SU97A1 |
| Станок для изготовления деревянных ниточных катушек из цилиндрических, снабженных осевым отверстием, заготовок | 1923 |
|
SU2008A1 |
| ПРОИЗВОДНЫЕ ИМИДАЗОЛА | 1997 |
|
RU2225405C2 |
| US 5712294 A1, 27.01.1998 | |||
| US 5300478 A1, 05.04.1994 | |||
| Пломбировальные щипцы | 1923 |
|
SU2006A1 |
| GOSWAMI S | |||
| et al.: "Directed H-bonding inhibition in molecular recognition: an NMR case study of the H-bonding of a dicarboxylic acid with a new mixed diamide receptor having one | |||
Авторы
Даты
2014-11-20—Публикация
2011-03-28—Подача