РОДСТВЕННЫЕ ЗАЯВКИ
Данная заявка испрашивает приоритет по предварительной заявке США №62/220192, поданной 17 сентября 2015 г., полное содержание которой включено в данный документ посредством ссылки.
ЗАЯВЛЕНИЕ ОТНОСИТЕЛЬНО ФИНАНСИРУЕМЫХ ГОСУДАРСТВОМ ИССЛЕДОВАНИЙ
Данное изобретение было выполнено при государственной поддержке в соответствии с грантом R01AI054193, предоставленным Национальными институтами здравоохранения (НИЗ). Правительство обладает определенными правами на данное изобретение.
УРОВЕНЬ ТЕХНИКИ
Существует острая необходимость в новых способах лечения микобактериальных инфекций в мировом и национальном масштабах. Микобактериальные инфекции вызваны такими патогенами, как Mycobacterium tuberculosis (Mtb, МБТ), возбудитель туберкулеза (ТБ), и близкородственными видами, такими как Mycobacterium avium (MAC). Каждые двадцать секунд один человек умирает от ТБ, а показатель эффективности лечения инфекции MAC может составлять всего лишь 30%. Более одной трети людей в мире инфицированы МБТ, представляя значительную угрозу глобальному здоровью. Наибольшее беспокойство вызывает быстрое возрастание числа трудно уничтожаемых, резистентных к лекарственным средствам штаммов МБТ. Ими на данный момент инфицировано 450000 людей во всем мире, и они с повышенной частотой появляются в США. ТБ представляет собой переносимый по воздуху патоген, он легко передается от человека к человеку при кашле, что делает даже один случай потенциально очень опасным. Имеющиеся способы лечения для этих штаммов являются ограниченно эффективными, но чрезвычайно дорогими.
В данном документе описаны агенты, которые могут представлять собой способ лечения инфекции, вызванной МБТ, или инфекции, вызванной MAC, или и той и другой. Существует нереализованная потребность в области медицины в соединениях, эффективных против патогена МБТ, или патогена MAC, или и того и другого, и соединения по настоящему изобретению считаются эффективными против резистентных к лекарственным средствам штаммом в виде отдельных агентов или в составе комбинированной терапии.
ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
На Фиг. 1 графически представлена in vivo переносимость, наблюдаемая у мышей, для двух иллюстративных соединений ND-11598 и ND-11622, вводимых перорально в дозе 100 мг/кг в течение двух недель и перорально в дозе 250 мг/кг в течение одной недели. Мыши не продемонстрировали признаков недомогания, потери веса, и все выжили после курса лечения.
На Фиг. 2 графически представлена in vivo эффективность ND-10885 у мышей, инфицированных Mycobacterium avium 101, при введении перорально в дозах 25 мг/кг и 100 мг/кг. Вставка А представляет собой log 10 уменьшения колониеобразующих единиц (КОЕ) бактерий в легких при лечении ND-10885 (при 25 и 100 мг/кг), рифампицином (RMP, 20 мг/кг) и комбинацией ND-10885 (100 мг/кг) и рифампицина (20 мг/кг). Вставка В представляет собой log 10 уменьшения колониеобразующих единиц (КОЕ) бактерий в селезенке при лечении ND-10885 (при 25 и 100 мг/кг), рифампицином (RMP, 20 мг/кг) и комбинацией ND-10885 (100 мг/кг) и рифампицина (20 мг/кг). Вставка С представляет собой log 10 уменьшения колониеобразующих единиц (КОЕ) бактерий в печени при лечении ND-10885 (при 25 и 100 мг/кг), рифампицином (RMP, 20 мг/кг) и комбинацией ND-10885 (100 мг/кг) и рифампицина (20 мг/кг). Статистически подтверждено улучшение эффективности комбинации лекарственных средств в легких и селезенке.
На Фиг. 3 в форме таблицы представлена in vitro активность нескольких соединений против различных серотипов Mycobacterium avium и штамма М. avium, устойчивого к гентамицину. Рифампин включен в качестве положительного контроля, а ДМСО - в качестве отрицательного контроля. Значения МИК представлены в мкг/мл и определены с использованием красителя резазурина.
На Фиг. 4 в форме таблицы представлена in vitro активность нескольких соединений против Mycobacterium intracellulare (АТСС 13950). Рифампин, кларитромицин, этамбутол и азитромицин включены в качестве положительных контролей, а ДМСО - в качестве отрицательного контроля. Значения МИК представлены в мкг/мл и определены с использованием красителя резазурина.
На Фиг. 5 в форме таблицы представлена in vitro активность нескольких соединений против клинических штаммов Mycobacterium avium, а кларитромицин использовали в качестве положительного контроля. Значения МИК представлены в мкг/мл и определены с использованием красителя 3-(4,5-диметилтиазол-2-ил)-2,5-дифенилтетразолия бромида (МТТ).
На Фиг. 6 в форме таблицы представлена in vitro активность нескольких соединений против клинических штаммов Mycobacterium kansasii; кларитромицин использовали в качестве положительного контроля. Значения МИК представлены в мкг/мл и определены с использованием красителя 3-(4,5-диметилтиазол-2-ил)-2,5-дифенилтетразолия бромида (МТТ).
На Фиг. 7 графически представлены значения МИК ND-11176 и клофазимина, как отдельно, так и в комбинации против Mycobacterium abscessus при оценке методом «шахматного анализа». Кларитромицин использовали в качестве положительного контроля. Значения МИК представлены в мкг/мл и определены с использованием красителя резазурина. На фигуре темные клетки представляют мертвых, более светлые клетки представляют живых.
На Фиг. 8 в форме таблицы представлены соединения и результаты скрининга против Mycobacterium tuberculosis (МБТ) H37Rv в различных средах (GAS, 7Н12), в условиях с низким содержанием кислорода (LORA), токсичность к клеткам Vero, а также активность против Mycobacterium avium (101 и 2151) и Mycobacterium intracellulare. Краситель резазурин использовали для определения значений МИК по отношению к М. avium и М. intracellulare, а МАВА использовали для определения МИК по отношению к МБТ.
ОПИСАНИЕ НЕКОТОРЫХ ВАРИАНТОВ ОСУЩЕСТВЛЕНИЯ ИЗОБРЕТЕНИЯ
В одном варианте осуществления изобретения предложено соединение, имеющее одну из следующих формул:
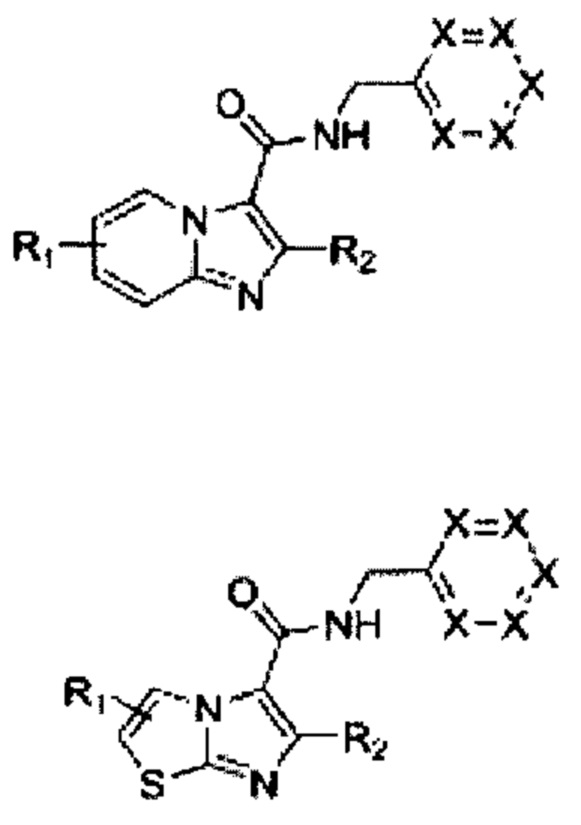
где каждый X независимо представляет собой N, C-R3 или C-R4; при условии, что не более чем два X представляют собой N, и одна или большее количество групп C-R3 или C-R4 могут присоединяться к другим C-R3 или C-R4 с образованием конденсированного кольца;
где R1 и R2, каждый независимо, представляют собой водород, ацильную группу, алкенильную группу, алкоксигруппу, алкоксикарбонильную группу, алкоксикарбонилоксигруппу, алкоксисульфонилоксигруппу, алкильную группу, алкиламиногруппу, алкиламинокарбонильную группу, алкилкарбонильную группу, алкилкарбонилоксигруппу, алкилсульфонильную группу, алкилсульфонилоксигруппу, алкилтиогруппу, алкинильную группу, амидную группу, амидиновую группу, аминогруппу, арилалкоксигруппу, арилалкильную группу, арильную группу, арилкарбонильную группу, арилкарбонилоксигруппу, арилоксигруппу, арилоксикарбонильную группу, арилоксикарбонилоксигруппу, арилоксисульфонилоксигруппу, арилсульфонильную группу, арилсульфонилоксигруппу, азидогруппу, карбамидогруппу, карбамоильную группу, карбазоильную группу, карбонильную группу, карбоксилатную группу, карбоксильную группу, цианатогруппу, цианогруппу, циклоалкенильную группу, циклоалкильную группу, диалкиламинокарбонильную группу, диалкиламиногруппу, гуанидиногруппу, гуанильную группу, галогенную группу, гетероарилалкоксигруппу, гетероарилалкильную группу, гетероарильную группу, гетероарилкарбонильную группу, гетероарилоксигруппу, гетероциклическую группу, гидроксиаминогруппу, гидроксигруппу, иминогруппу, изоцианатогруппу, изоцианогруппу, меркаптогруппу, нитрогруппу, оксогруппу, пергалогеналкенильную группу, пергалогеналкоксигруппу, пергалогеналкильную группу, пергалогеналкинильную группу, пергалогенарилалкильную группу, пергалогенарильную группу, пергалогенциклоалкильную группу, фосфатную группу, фосфиновую группу, фосфогруппу, сульфатную группу, сульфогруппу, сульфонильную группу, их окисленную форму, их замещенную форму, их форму, содержащую гетероатомы, или их комбинацию;
где каждый R3 независимо представляет собой водород, «С-группу», ацильную группу, алкенильную группу, алкоксигруппу, алкоксикарбонильную группу, алкоксикарбонилоксигруппу, алкоксисульфонилоксигруппу, алкильную группу, алкиламиногруппу, алкиламинокарбонильную группу, алкилкарбонильную группу, алкилкарбонилоксигруппу, алкилсульфонильную группу, алкилсульфонилоксигруппу, алкилтиогруппу, алкинильную группу, амидную группу, амидиновую группу, аминогруппу, арилалкоксигруппу, арилалкильную группу, арильную группу, арилкарбонильную группу, арилкарбонилоксигруппу, арилоксигруппу, арилоксикарбонильную группу, арилоксикарбонилоксигруппу, арилоксисульфонилоксигруппу, арилсульфонильную группу, арилсульфонилоксигруппу, азидогруппу, карбамидогруппу, карбамоильную группу, карбазоильную группу, карбонильную группу, карбоксилатную группу, карбоксильную группу, цианатогруппу, цианогруппу, циклоалкенильную группу, циклоалкильную группу, диалкиламинокарбонильную группу, диалкиламиногруппу, гуанидиногруппу, гуанильную группу, галогенную группу, гетероарилалкоксигруппу, гетероарилалкильную группу, гетероарильную группу, гетероарилкарбонильную группу, гетероарилоксигруппу, гетероциклическую группу, гидроксиаминогруппу, гидроксигруппу, иминогруппу, изоцианатогруппу, изоцианогруппу, меркаптогруппу, нитрогруппу, оксогруппу, пергалогеналкенильную группу, пергалогеналкоксигруппу, пергалогеналкильную группу, пергалогеналкинильную группу, пергалогенарилалкильную группу, пергалогенарильную группу, пергалогенциклоалкильную группу, фосфатную группу, фосфиновую группу, фосфогруппу, сульфатную группу, сульфогруппу, сульфонильную группу, их окисленную форму, их замещенную форму, их форму, содержащую гетероатомы, или их комбинацию; и
где каждый R4 независимо представляет собой водород, «D-группу», ацильную группу, алкенильную группу, алкоксигруппу, алкоксикарбонильную группу, алкоксикарбонилоксигруппу, алкоксисульфонилоксигруппу, алкильную группу, алкиламиногруппу, алкиламинокарбонильную группу, алкилкарбонильную группу, алкилкарбонилоксигруппу, алкилсульфонильную группу, алкилсульфонилоксигруппу, алкилтиогруппу, алкинильную группу, амидную группу, амидиновую группу, аминогруппу, арилалкоксигруппу, арилалкильную группу, арильную группу, арилкарбонильную группу, арилкарбонилоксигруппу, арилоксигруппу, арилоксикарбонильную группу, арилоксикарбонилоксигруппу, арилоксисульфонилоксигруппу, арилсульфонильную группу, арилсульфонилоксигруппу, азидогруппу, карбамидогруппу, карбамоильную группу, карбазоильную группу, карбонильную группу, карбоксилатную группу, карбоксильную группу, цианатогруппу, цианогруппу, циклоалкенильную группу, циклоалкильную группу, диалкиламинокарбонильную группу, диалкиламиногруппу, гуанидиногруппу, гуанильную группу, галогенную группу, гетероарилалкоксигруппу, гетероарилалкильную группу, гетероарильную группу, гетероарилкарбонильную группу, гетероарилоксигруппу, гетероциклическую группу, гидроксиаминогруппу, гидроксигруппу, иминогруппу, изоцианатогруппу, изоцианогруппу, меркаптогруппу, нитрогруппу, оксогруппу, пергалогеналкенильную группу, пергалогеналкоксигруппу, пергалогеналкильную группу, пергалогеналкинильную группу, пергалогенарилалкильную группу, пергалогенарильную группу, пергалогенциклоалкильную группу, фосфатную группу, фосфиновую группу, фосфогруппу, сульфатную группу, сульфогруппу, сульфонильную группу, их окисленную форму, их замещенную форму, их форму, содержащую гетероатомы, или их комбинацию;
или его резонансная форма, или его соль, или соль его резонансной формы.
В другом варианте осуществления изобретения предложена композиция, которая содержит соединение и физиологически приемлемый носитель.
В другом варианте осуществления изобретения предложен способ, который включает в себя введение соединения или композиции субъекту, нуждающемуся в этом, для лечения указанного субъекта.
В некоторых вариантах осуществления изобретения форма соединения особым образом не ограничена. Например, она может представлять собой резонансную форму, солевую форму или соль резонансной формы. Возможны смеси различных форм и композиции, которые содержат смеси форм.
В некоторых вариантах осуществления изобретения соединение находится в форме соли. В некоторых вариантах осуществления изобретения соединение находится в резонансной форме. В некоторых вариантах осуществления изобретения резонансная форма представляет собой ионную резонансную форму.
В некоторых вариантах осуществления изобретения каждая группа R1-R4 может независимо и необязательно быть выбрана из одной или большего количества замещающих групп, описанных в данном документе. В некоторых вариантах осуществления изобретения каждая группа R1-R4 может независимо и необязательно быть дополнительно замещена одной или большим количеством замещающих групп, описанных в данном документе. В некоторых вариантах осуществления изобретения каждая группа R1-R4 может независимо и необязательно быть присоединена непосредственно к соответствующей исходной структуре с помощью одной или большего количества химических связей, или может независимо и необязательно быть непрямо присоединена к соответствующей исходной структуре посредством одной или большего количества двухвалентных промежуточных замещающих групп, описанных в данном документе. Возможны комбинации 1, 2, 3 или 4 двухвалентных промежуточных замещающих групп.
В некоторых вариантах осуществления изобретения R1 и R2, каждый независимо, представляет собой водород, ацильную группу, алкенильную группу, алкоксигруппу, алкоксикарбонильную группу, алкоксикарбонилоксигруппу, алкоксисульфонилоксигруппу, алкильную группу, алкиламиногруппу, алкиламинокарбонильную группу, алкилкарбонильную группу, алкилкарбонилоксигруппу, алкилсульфонильную группу, алкилсульфонилоксигруппу, алкилтиогруппу, алкинильную группу, амидную группу, амидиновую группу, аминогруппу, арилалкоксигруппу, арилалкильную группу, арильную группу, арилкарбонильную группу, арилкарбонилоксигруппу, арилоксигруппу, арилоксикарбонильную группу, арилоксикарбонилоксигруппу, арилоксисульфонилоксигруппу, арилсульфонильную группу, арилсульфонилоксигруппу, азидогруппу, карбамидогруппу, карбамоильную группу, карбазоильную группу, карбонильную группу, карбоксилатную группу, карбоксильную группу, цианатогруппу, цианогруппу, циклоалкенильную группу, циклоалкильную группу, диалкиламинокарбонильную группу, диалкиламиногруппу, гуанидиногруппу, гуанильную группу, галогенную группу, гетероарилалкоксигруппу, гетероарилалкильную группу, гетероарильную группу, гетероарилкарбонильную группу, гетероарилоксигруппу, гетероциклическую группу, гидроксиаминогруппу, гидроксигруппу, иминогруппу, изоцианатогруппу, изоцианогруппу, меркаптогруппу, нитрогруппу, оксогруппу, пергалогеналкенильную группу, пергалогеналкоксигруппу, пергалогеналкильную группу, пергалогеналкинильную группу, пергалогенарилалкильную группу, пергалогенарильную группу, пергалогенциклоалкильную группу, фосфатную группу, фосфиновую группу, фосфогруппу, сульфатную группу, сульфогруппу, сульфонильную группу, их окисленную форму, их замещенную форму, их форму, содержащую гетероатомы, или их комбинацию.
В некоторых вариантах осуществления изобретения каждый R3 независимо представляет собой водород, «С-группу», ацильную группу, алкенильную группу, алкоксигруппу, алкоксикарбонильную группу, алкоксикарбонилоксигруппу, алкоксисульфонилоксигруппу, алкильную группу, алкиламиногруппу, алкиламинокарбонильную группу, алкилкарбонильную группу, алкилкарбонилоксигруппу, алкилсульфонильную группу, алкилсульфонилоксигруппу, алкилтиогруппу, алкинильную группу, амидную группу, амидиновую группу, аминогруппу, арилалкоксигруппу, арилалкильную группу, арильную группу, арилкарбонильную группу, арилкарбонилоксигруппу, арилоксигруппу, арилоксикарбонильную группу, арилоксикарбонилоксигруппу, арилоксисульфонилоксигруппу, арилсульфонильную группу, арилсульфонилоксигруппу, азидогруппу, карбамидогруппу, карбамоильную группу, карбазоильную группу, карбонильную группу, карбоксилатную группу, карбоксильную группу, цианатогруппу, цианогруппу, циклоалкенильную группу, циклоалкильную группу, диалкиламинокарбонильную группу, диалкиламиногруппу, гуанидиногруппу, гуанильную группу, галогенную группу, гетероарилалкоксигруппу, гетероарилалкильную группу, гетероарильную группу, гетероарилкарбонильную группу, гетероарилоксигруппу, гетероциклическую группу, гидроксиаминогруппу, гидроксигруппу, иминогруппу, изоцианатогруппу, изоцианогруппу, меркаптогруппу, нитрогруппу, оксогруппу, пергалогеналкенильную группу, пергалогеналкоксигруппу, пергалогеналкильную группу, пергалогеналкинильную группу, пергалогенарилалкильную группу, пергалогенарильную группу, пергалогенциклоалкильную группу, фосфатную группу, фосфиновую группу, фосфогруппу, сульфатную группу, сульфогруппу, сульфонильную группу, их окисленную форму, их замещенную форму, их форму, содержащую гетероатомы, или их комбинацию. Каждая группа R3 может независимо и необязательно быть дополнительно замещена одной или большим количеством замещающих групп, описанных в данном документе. В некоторых вариантах осуществления изобретения каждая группа R3 может независимо и необязательно быть присоединена непосредственно к боковой группе с помощью одной или большего количества химических связей, или может независимо и необязательно быть непрямо присоединена к боковой группе посредством одной или большего количества двухвалентных промежуточных замещающих групп, описанных в данном документе. Возможны комбинации 1, 2, 3 или 4 двухвалентных промежуточных замещающих групп.
В некоторых вариантах осуществления изобретения, в которых группа R3 дополнительно замещена замещающей группой, описанной в данном документе, замещающая группа может независимо и необязательно быть присоединена непосредственно к группе R3 с помощью одной или большего количества химических связей или может независимо и необязательно быть непрямо присоединена к группе R3 посредством одной или большего количества независимых двухвалентных промежуточных замещающих групп, описанных в данном документе. Возможны комбинации 1, 2, 3 или 4 независимых двухвалентных промежуточных замещающих групп между группой R3 и замещающей группой.
В некоторых вариантах осуществления изобретения каждый R4 независимо представляет собой водород, «D-группу», ацильную группу, алкенильную группу, алкоксигруппу, алкоксикарбонильную группу, алкоксикарбонилоксигруппу, алкоксисульфонилоксигруппу, алкильную группу, алкиламиногруппу, алкиламинокарбонильную группу, алкилкарбонильную группу, алкилкарбонилоксигруппу, алкилсульфонильную группу, алкилсульфонилоксигруппу, алкилтиогруппу, алкинильную группу, амидную группу, амидиновую группу, аминогруппу, арилалкоксигруппу, арилалкильную группу, арильную группу, арилкарбонильную группу, арилкарбонилоксигруппу, арилоксигруппу, арилоксикарбонильную группу, арилоксикарбонилоксигруппу, арилоксисульфонилоксигруппу, арилсульфонильную группу, арилсульфонилоксигруппу, азидогруппу, карбамидогруппу, карбамоильную группу, карбазоильную группу, карбонильную группу, карбоксилатную группу, карбоксильную группу, цианатогруппу, цианогруппу, циклоалкенильную группу, циклоалкильную группу, диалкиламинокарбонильную группу, диалкиламиногруппу, гуанидиногруппу, гуанильную группу, галогенную группу, гетероарилалкоксигруппу, гетероарилалкильную группу, гетероарильную группу, гетероарилкарбонильную группу, гетероарилоксигруппу, гетероциклическую группу, гидроксиаминогруппу, гидроксигруппу, иминогруппу, изоцианатогруппу, изоцианогруппу, меркаптогруппу, нитрогруппу, оксогруппу, пергалогеналкенильную группу, пергалогеналкоксигруппу, пергалогеналкильную группу, пергалогеналкинильную группу, пергалогенарилалкильную группу, пергалогенарильную группу, пергалогенциклоалкильную группу, фосфатную группу, фосфиновую группу, фосфогруппу, сульфатную группу, сульфогруппу, сульфонильную группу, их окисленную форму, их замещенную форму, их форму, содержащую гетероатомы, или их комбинацию. Каждая группа R4 может независимо и необязательно быть дополнительно замещена одной или большим количеством замещающих групп, описанных в данном документе. В некоторых вариантах осуществления изобретения каждая группа R4 может независимо и необязательно быть присоединена непосредственно к боковой группе с помощью одной или большего количества химических связей, или может независимо и необязательно быть непрямо присоединена к боковой группе посредством одной или большего количества двухвалентных промежуточных замещающих групп, описанных в данном документе. Возможны комбинации 1, 2, 3 или 4 двухвалентных промежуточных замещающих групп.
В некоторых вариантах осуществления изобретения, в которых группа R4 дополнительно замещена замещающей группой, описанной в данном документе, замещающая группа может независимо и необязательно быть присоединена непосредственно к группе R4 с помощью одной или большего количества химических связей или может независимо и необязательно быть непрямо присоединена к группе R4 посредством одной или большего количества независимых двухвалентных промежуточных замещающих групп, описанных в данном документе. Возможны комбинации 1, 2, 3 или 4 независимых двухвалентных промежуточных замещающих групп между группой R4 и замещающей группой.
В некоторых вариантах осуществления изобретения R1-R4 каждая независимо представляет собой водород, алкильную группу, циклоалкильную группу, циклоалкенильную группу, галогенную группу, алкенильную группу, алкинильную группу, арильную группу, гидроксигруппу, ацильную группу, оксогруппу, меркаптогруппу, алкилтиогруппу, алкоксигруппу, гетероциклическую группу, гетероарильную группу, гетероарилкарбонильную группу, арилоксигруппу, гетероарилоксигруппу, арилалкильную группу, гетероарилалкильную группу, арилалкоксигруппу, гетероарилалкоксигруппу, аминогруппу, алкиламиногруппу, диалкиламиногруппу, амидиновую группу, амидную группу, карбамоильную группу, алкилкарбонильную группу, алкоксикарбонильную группу, алкиламинокарбонильную группу, диалкиламинокарбонильную группу, арилкарбонильную группу, арилоксикарбонильную группу, алкилсульфонильную группу, арилсульфонильную группу, пергалогеналкильную группу, пергалогеналкоксигруппу, пергалогенциклоалкильную группу, пергалогеналкенильную группу, пергалогеналкинильную группу, пергалогенарильную группу, пергалогенарилалкильную группу, их окисленную форму, их замещенную форму, их форму, содержащую гетероатомы, или их комбинацию.
В некоторых вариантах осуществления изобретения каждая группа R1-R4 может независимо и необязательно быть выбрана из одной или большего количества из следующих групп: водород, алкильная группа, циклоалкильная группа, циклоалкенильная группа, галогенная группа, алкенильная группа, алкинильная группа, арильная группа, гидроксигруппа, ацильная группа, оксогруппа, меркаптогруппа, алкилтиогруппа, алкоксигруппа, гетероциклическая группа, гетероарильная группа, гетероарилкарбонильная группа, арилоксигруппа, гетероарилоксигруппа, арилалкильная группа, гетероарилалкильная группа, арилалкоксигруппа, гетероарилалкоксигруппа, аминогруппа, алкиламиногруппа, диалкиламиногруппа, амидиновая группа, амидная группа, карбамоильная группа, алкилкарбонильная группа, алкоксикарбонильная группа, алкиламинокарбонильная группа, диалкиламинокарбонильная группа, арилкарбонильная группа, арилоксикарбонильная группа, алкилсульфонильная группа, арилсульфонильная группа, их окисленной формы, их замещенной формы, их формы, содержащей гетероатомы, или их комбинации.
В некоторых вариантах осуществления изобретения каждая группа R1-R4 может независимо и необязательно быть выбрана из одной или большего количества из следующих групп: водород, алкильная группа, циклоалкильная группа, циклоалкенильная группа, галогенная группа, алкенильная группа, алкинильная группа, арильная группа, гидроксигруппа, ацильная группа, алкоксигруппа, гетероциклическая группа, гетероарильная группа, гетероарилкарбонильная группа, арилоксигруппа, гетероарилоксигруппа, арилалкильная группа, гетероарилалкильная группа, арилалкоксигруппа, гетероарилалкоксигруппа, аминогруппа, алкиламиногруппа, диалкиламиногруппа, амидиновая группа, амидная группа, карбамоильная группа, алкилкарбонильная группа, алкоксикарбонильная группа, алкиламинокарбонильная группа, диалкиламинокарбонильная группа, арилкарбонильная группа, арилоксикарбонильная группа, их окисленной формы, их замещенной формы, их формы, содержащей гетероатомы, или их комбинации.
В некоторых вариантах осуществления изобретения каждая группа R1-R4 может независимо и необязательно быть выбрана из одной или большего количества из следующих групп: водород, алкильная группа, циклоалкильная группа, циклоалкенильная группа, алкенильная группа, алкинильная группа, арильная группа, ацильная группа, алкоксигруппа, гетероциклическая группа, гетероарильная группа, гетероарилкарбонильная группа, арилоксигруппа, гетероарилоксигруппа, арилалкильная группа, гетероарилалкильная группа, арилалкоксигруппа, гетероарилалкоксигруппа, карбамоильная группа, алкилкарбонильная группа, алкоксикарбонильная группа, алкиламинокарбонильная группа, диалкиламинокарбонильная группа, арилкарбонильная группа, арилоксикарбонильная группа, их окисленной формы, их замещенной формы, их формы, содержащей гетероатомы, или их комбинации.
В некоторых вариантах осуществления изобретения каждая группа R1-R4 может независимо и необязательно быть выбрана из одной или большего количества из следующих групп: водород, алкильная группа, циклоалкильная группа, циклоалкенильная группа, алкенильная группа, алкинильная группа, арильная группа, гетероциклическая группа, гетероарильная группа, арилалкильная группа, гетероарилалкильная группа, их окисленной формы, их замещенной формы, их формы, содержащей гетероатомы, или их комбинации.
В некоторых вариантах осуществления изобретения каждый R1-R4 независимо представляют собой водород, алкил, замещенный алкил, линейный алкил, разветвленный алкил аллил, замещенный аллил, гетероалкил, циклоалкил, арил, замещенный арил, гетероарил, ацил, ароил, гетероароил, их замещенную форму, их форму, содержащую гетероатомы, или их комбинацию.
В некоторых вариантах осуществления изобретения R1-R4, каждый независимо, представляют собой водород, алкил, замещенный алкил аллил, замещенный аллил, отличающееся тем, что циклоалкил, арил, замещенный гетероатомом арил, гетероарил, ацил, ароил, гетероароил, их замещенную форму, их форму, содержащую гетероатомы, или их комбинацию.
В некоторых вариантах осуществления изобретения R1-R4, каждый независимо, представляют собой водород, алкил, аллил, циклоалкил, арил, ацил, ароил, их замещенную форму, их форму, содержащую гетероатомы, или их комбинацию.
В некоторых вариантах осуществления изобретения каждая группа R1-R4 может независимо и необязательно быть замещенной, незамещенной, насыщенной, ненасыщенной или включать в себя комбинацию этих характеристик. В случае замещенных групп замещающая группа или группы могут быть выбраны из любых, определенных в данном документе.
В некоторых вариантах осуществления изобретения один или более чем один атом в одном или большем количестве R1-R4 независимо заменены одним или большим количеством независимых гетероатомов, их окисленной формой или их комбинацией.
В некоторых вариантах осуществления изобретения каждая группа R1-R4 может независимо и необязательно содержать один или большее количество атомов, которые заменены одним или большим количеством гетероатомов, например N, О, Р, S, их окисленной формой или их комбинацией.
В некоторых вариантах осуществления изобретения один или более чем один атом углерода в одном или большем количестве R1-R4 независимо заменены одним или большим количеством независимых гетероатомов, выбранных из группы, состоящей из N, О, S, или их комбинацией.
В некоторых вариантах осуществления изобретения одна или более чем одна группа R1-R4 могут быть независимо и необязательно дополнительно замещены, одна или более чем одна группа R1-R4 могут быть независимо и необязательно присоединены непосредственно к соответствующей исходной структуре с помощью одной или большего количества химических связей или могут независимо и необязательно быть непрямо присоединены к соответствующей исходной структуре посредством одной или большего количества двухвалентных промежуточных замещающих групп. Возможны комбинации 1, 2, 3, 4 и 5 независимых двухвалентных промежуточных замещающих групп, и они могут представлять собой любые из определенных в данном документе.
В некоторых вариантах осуществления изобретения одна или более чем одна группа R1 могут независимо и необязательно быть дополнительно замещены одной или большим количеством независимых замещающих групп, описанных в данном документе. В некоторых вариантах осуществления изобретения одна или более чем одна группа R1 могут независимо и необязательно быть присоединены непосредственно к пиридиновой или тиазольной части с помощью одной или большего количества химических связей или могут независимо и необязательно быть непрямо присоединены к пиридиновой или тиазольной части посредством одной или большего количества двухвалентных промежуточных замещающих групп, описанных в данном документе. Возможны 1, 2, 3, 4 или 5 независимых двухвалентных промежуточных замещающих групп, и они могут представлять собой любые из определенных в данном документе.
В некоторых вариантах осуществления изобретения одна или более чем одна группа R2 могут независимо и необязательно быть дополнительно замещены одной или большим количеством независимых замещающих групп, описанных в данном документе. В некоторых вариантах осуществления изобретения одна или более чем одна группа R2 могут независимо и необязательно быть присоединены непосредственно к имидазольной части с помощью одной или большего количества химических связей или могут независимо и необязательно быть непрямо присоединены к имидазольной части посредством одной или большего количества двухвалентных промежуточных замещающих групп, описанных в данном документе. Возможны 1, 2, 3, 4 или 5 независимых двухвалентных промежуточных замещающих групп, и они могут представлять собой любые из определенных в данном документе.
В некоторых вариантах осуществления изобретения одна или более чем одна группа R3 могут независимо и необязательно быть дополнительно замещены одной или большим количеством независимых замещающих групп, описанных в данном документе. В некоторых вариантах осуществления изобретения одна или более чем одна группа R3 могут независимо и необязательно быть присоединены непосредственно к боковой группе с помощью одной или большего количества химических связей или могут независимо и необязательно быть непрямо присоединены к боковой группе посредством одной или большего количества двухвалентных промежуточных замещающих групп, описанных в данном документе. Возможны 1, 2, 3, 4 или 5 независимых двухвалентных промежуточных замещающих групп, и они могут представлять собой любые из определенных в данном документе.
В некоторых вариантах осуществления изобретения одна или более чем одна группа R4 могут независимо и необязательно быть дополнительно замещены одной или большим количеством независимых замещающих групп, описанных в данном документе. В некоторых вариантах осуществления изобретения одна или более чем одна группа R4 могут независимо и необязательно быть присоединены непосредственно к боковой группе с помощью одной или большего количества химических связей или могут независимо и необязательно быть непрямо присоединены к боковой группе посредством одной или большего количества двухвалентных промежуточных замещающих групп, описанных в данном документе. Возможны 1, 2, 3, 4 или 5 независимых двухвалентных промежуточных замещающих групп, и они могут представлять собой любые из определенных в данном документе.
В некоторых вариантах осуществления изобретения R1 представляет собой галоген, Cl, F, Br, алкил, алкенил, алкинил, алкокси, гидроксил, нитрил, нитро.
В некоторых вариантах осуществления изобретения R1 представляет собой Cl, F, Br, С1-С4 алкил, С2-С4 алкенил, С2-С4 алкинил, С1-С4 алкокси, гидроксил, нитрил, нитро.
В некоторых вариантах осуществления изобретения R1 представляет собой Cl, F или С1-С4 алкил.
В некоторых вариантах осуществления изобретения R2 представляет собой галоген, Cl, F, Br, CF3, алкил, алкенил, алкокси.
В некоторых вариантах осуществления изобретения R2 представляет собой Cl, F, CF3, C1-С4 алкил, С2-С4 алкенил, C1-C4 алкокси.
В некоторых вариантах осуществления изобретения R2 представляет собой Cl, F, CF3, C1-С4 алкил.
В некоторых вариантах осуществления изобретения R3 представляет собой «С-группу». В некоторых вариантах осуществления изобретения R3 может содержать один или большее количество независимых заместителей «D-группы». В некоторых вариантах осуществления изобретения R3 может включать в себя одну или большее количество независимых групп R4, замещающих его. В некоторых вариантах осуществления изобретения R3 может представлять собой «С-группу» и также содержать один или большее количество независимых заместителей R4. В некоторых вариантах осуществления изобретения R3 может представлять собой «С-группу» и также содержать один или большее количество независимых заместителей «D-группы». В некоторых вариантах осуществления изобретения по меньшей мере один R3 представляет собой галоген.
В некоторых вариантах осуществления изобретения R4 представляет собой «D-группу». В некоторых вариантах осуществления изобретения по меньшей мере один R4 представляет собой галоген.
В некоторых вариантах осуществления изобретения R1 не является водородом. В некоторых вариантах осуществления изобретения R2 не является водородом. В некоторых вариантах осуществления изобретения R3 представляет собой водород. В некоторых вариантах осуществления изобретения R4 представляет собой водород.
В следующих формулах:
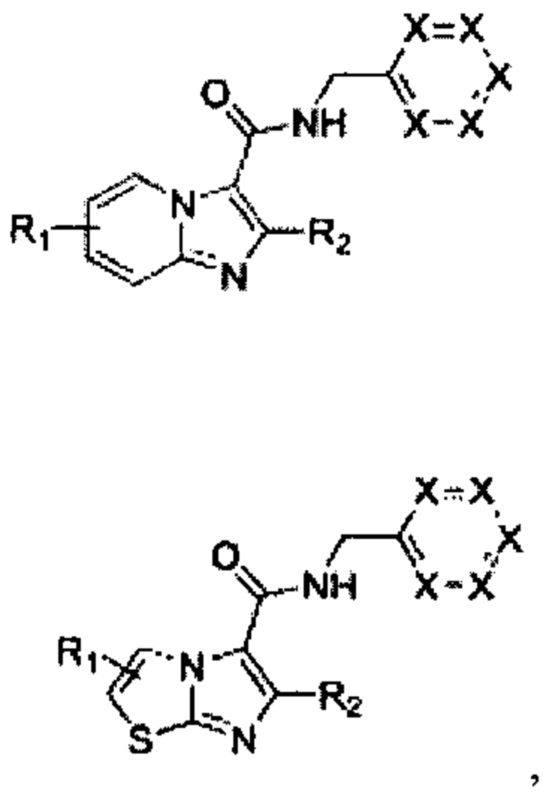
следующая часть:
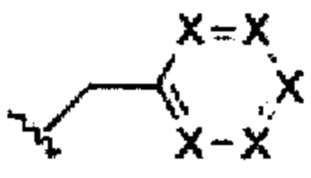
обозначена в данном документе как «боковая группа».
В некоторых вариантах осуществления изобретения в боковой группе:
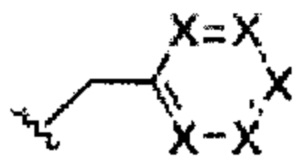
ни один из X не является азотом. В таком варианте осуществления изобретения каждый X в боковой группе независимо представляет собой C-R3 или C-R4, и при наличии более чем одного C-R3, они могут быть одинаковыми или различными, и при наличии более чем одного C-R4, они могут быть одинаковыми или различными. В некоторых вариантах осуществления изобретения ни один из X не представляет собой C-R3. В некоторых вариантах осуществления изобретения ни один из X не представляет собой C-R4. В некоторых вариантах осуществления изобретения присутствует как C-R4, так и C-R3. В некоторых вариантах осуществления изобретения одна или большее количество групп C-R3 или C-R4 могут образовывать кольцо с одной или большим количеством других групп C-R3, одной или большим количеством других групп C-R4 или комбинацией групп C-R3 и C-R4 с получением кольца, конденсированного с кольцом боковой группы.
В других вариантах осуществления изобретения в боковой группе:
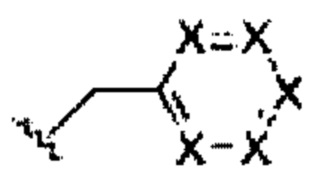
один или два X представляют собой азот, и боковая группа имеет одну из следующих структур:
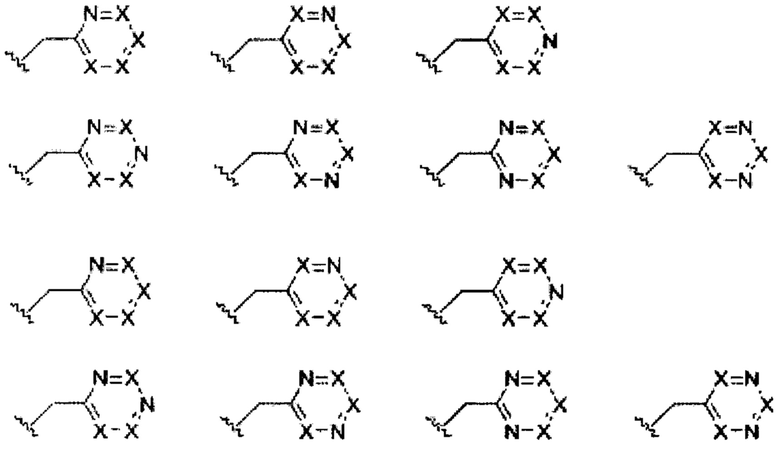
где каждый X независимо представляет собой C-R3 или C-R4, и при наличии более чем одного C-R3, они могут быть одинаковыми или различными, и при наличии более чем одного С-R4, они могут быть одинаковыми или различными. В некоторых вариантах осуществления изобретения ни один из X не представляет собой C-R3. В некоторых вариантах осуществления изобретения ни один из X не представляет собой C-R4. В некоторых вариантах осуществления изобретения присутствует как C-R3, так и C-R4. В некоторых вариантах осуществления изобретения одна или большее количество групп C-R3 или C-R4 могут образовывать конденсированное кольцо с одной или большим количеством других групп C-R3, одной или большим количеством других групп C-R4 или комбинацией групп C-R3 и C-R4.
В некоторых вариантах осуществления изобретения одна или большее количество групп C-R3 или C-R4 могут соединяться и образовывать конденсированное кольцо с одной или большим количеством других групп C-R3, одной или большим количеством других групп C-R4 или комбинацией групп C-R3 и C-R4.
В некоторых вариантах осуществления изобретения, в которых одна или большее количество групп C-R3 или C-R4 могут соединяться и образовывать конденсированное кольцо с одной или большим количеством других групп C-R3, одной или большим количеством других групп C-R4 или комбинацией групп C-R3 и C-R4, боковая группа:
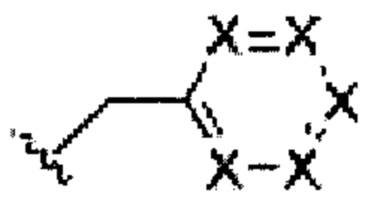
имеет одну из следующих конденсированных кольцевых структур:
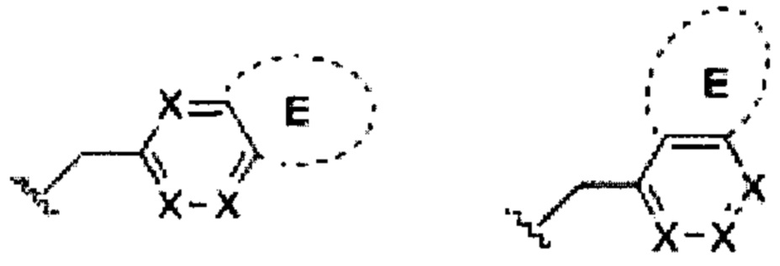
где каждый X независимо представляет собой N, C-R3 или C-R4; и «Е» представляет кольцо, показанное пунктирной линией, которое образуется из одной или большего количества групп R3 или R4, соединенных с одной или большим количеством других R3, R4 или комбинацией групп R3 и R4. Кольцо Е может быть карбоциклическим или гетероциклическим, насыщенным или ненасыщенным, замещенным или незамещенным. Под карбоциклическим предполагают, что кольцо Е представляет собой циклоалкан, циклоалкен, арил или тому подобное. В случае гетероциклической структуры кольцо Е может иметь 1, 2 или 3 атома углерода в кольце, независимо замененных одним или большим количеством независимых атомов кислорода, азота, серы или их комбинацией. Учитывая атомы углерода C-R3 и C-R4, общие для двух циклов, кольцо Е может содержать 4-12 членов, этот интервал включает 4, 5, 6, 7, 8, 9, 10, 11, 12 членов. В некоторых вариантах осуществления изобретения группы C-R3 или C-R4, которые образуют кольцо Е, являются соседними, хотя они могут быть разделены промежуточными N, C-R3 или С-R4.
В некоторых вариантах осуществления изобретения кольцо Е образуется путем соединения двух соседних независимых групп C-R3. В некоторых вариантах осуществления изобретения кольцо Е образуется путем соединения двух соседних независимых групп C-R4. В некоторых вариантах осуществления изобретения кольцо Е образуется путем соединения группы C-R3 с соседней группой C-R4.
В некоторых вариантах осуществления изобретения кольцо Е представляет собой карбоциклическое или гетероциклическое, насыщенное или ненасыщенное, замещенное или незамещенное 5-, 6-, 7- или 8-членное кольцо. В некоторых вариантах осуществления изобретения кольцо Е представляет собой карбоциклическое или гетероциклическое 5-6-членное кольцо, которое может быть насыщенным или ненасыщенным, замещенным или незамещенным. В некоторых вариантах осуществления изобретения пунктирной линией на приведенной выше фигуре представлена часть кольца Е, которая является насыщенной или ненасыщенной, замещенной или незамещенной или содержит или не содержит гетероатомы в кольце; и атомы углерода кольца Е не являются общими для конденсированного кольца и кольца боковой группы.
В некоторых вариантах осуществления изобретения, в которых имеется кольцо Е, боковая группа имеет одну из следующих формул:
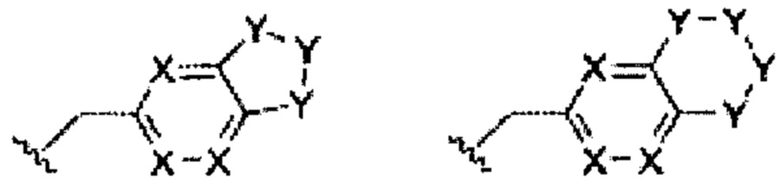
где каждый Y независимо представляет собой C-R5, C(R5)(R5), С=O, N, N-R5, О, S, S=O или S(=O)2; при условии, что не более чем два Y представляют собой С=O, N, N-R5, О, S, S=O или S(=O)2;
где, когда каждый из двух соседних Y независимо представляет собой C-R5 или N и C-R5, связь между указанными соседними Y может представлять собой двойную связь;
и где каждый R5 независимо представляет собой водород, «С-группу», «D-группу», ацильную группу, алкенильную группу, алкоксигруппу, алкоксикарбонильную группу, алкоксикарбонилоксигруппу, алкоксисульфонилоксигруппу, алкильную группу, алкиламиногруппу, алкиламинокарбонильную группу, алкилкарбонильную группу, алкилкарбонилоксигруппу, алкилсульфонильную группу, алкилсульфонилоксигруппу, алкилтиогруппу, алкинильную группу, амидную группу, амидиновую группу, аминогруппу, арилалкоксигруппу, арилалкильную группу, арильную группу, арилкарбонильную группу, арилкарбонилоксигруппу, арилоксигруппу, арилоксикарбонильную группу, арилоксикарбонилоксигруппу, арилоксисульфонилоксигруппу, арилсульфонильную группу, арилсульфонилоксигруппу, азидогруппу, карбамидогруппу, карбамоильную группу, карбазоильную группу, карбонильную группу, карбоксилатную группу, карбоксильную группу, цианатогруппу, цианогруппу, циклоалкенильную группу, циклоалкильную группу, диалкиламинокарбонильную группу, диалкиламиногруппу, гуанидиногруппу, гуанильную группу, галогенную группу, гетероарилалкоксигруппу, гетероарилалкильную группу, гетероарильную группу, гетероарилкарбонильную группу, гетероарилоксигруппу, гетероциклическую группу, гидроксиаминогруппу, гидроксигруппу, иминогруппу, изоцианатогруппу, изоцианогруппу, меркаптогруппу, нитрогруппу, оксогруппу, пергалогеналкенильную группу, пергалогеналкоксигруппу, пергалогеналкильную группу, пергалогеналкинильную группу, пергалогенарилалкильную группу, пергалогенарильную группу, пергалогенциклоалкильную группу, фосфатную группу, фосфиновую группу, фосфогруппу, сульфатную группу, сульфогруппу, сульфонильную группу, их окисленную форму, их замещенную форму, их форму, содержащую гетероатомы, или их комбинацию.
Каждая группа R5 может независимо и необязательно быть дополнительно замещена одной или большим количеством замещающих групп, описанных в данном документе. В некоторых вариантах осуществления изобретения каждая группа R5 может независимо и необязательно быть присоединена непосредственно к кольцу Е с помощью одной или большего количества химических связей или может независимо и необязательно быть непрямо присоединена к кольцу Е посредством одной или большего количества двухвалентных промежуточных замещающих групп, описанных в данном документе. Возможны комбинации 1, 2, 3 или 4 двухвалентных промежуточных замещающих групп.
В некоторых вариантах осуществления изобретения, в которых группа R5 дополнительно замещена замещающей группой, описанной в данном документе, замещающая группа может независимо и необязательно быть присоединена непосредственно к группе R5 с помощью одной или большего количества химических связей или может независимо и необязательно быть непрямо присоединена к группе R5 посредством одной или большего количества независимых двухвалентных промежуточных замещающих групп, описанных в данном документе. Возможны комбинации 1, 2, 3 или 4 независимых двухвалентных промежуточных замещающих групп между группой R5 и замещающей группой.
В некоторых вариантах осуществления изобретения, в которых имеется кольцо Е, боковая группа имеет одну из следующих формул:
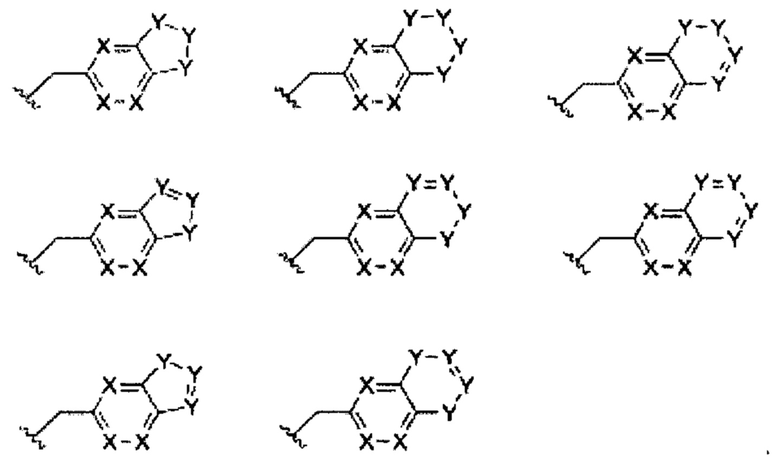
Например, боковая группа может иметь одну из следующих формул боковых групп:
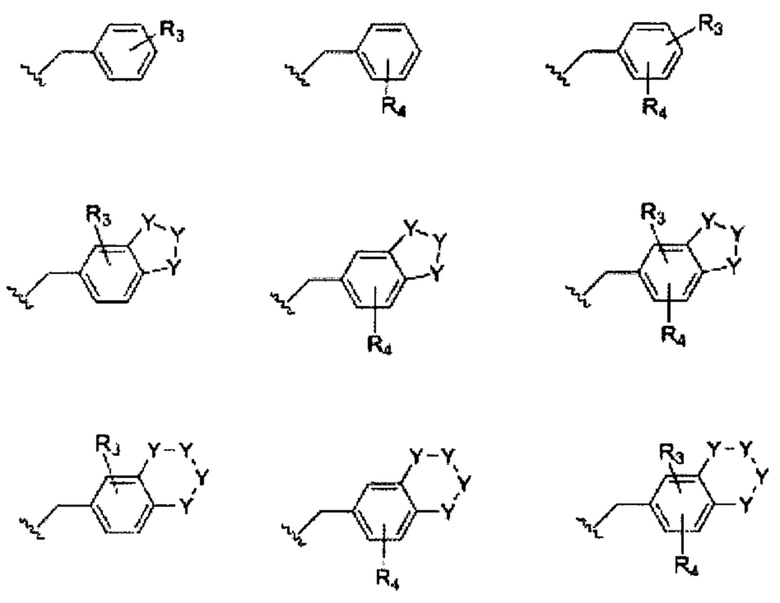
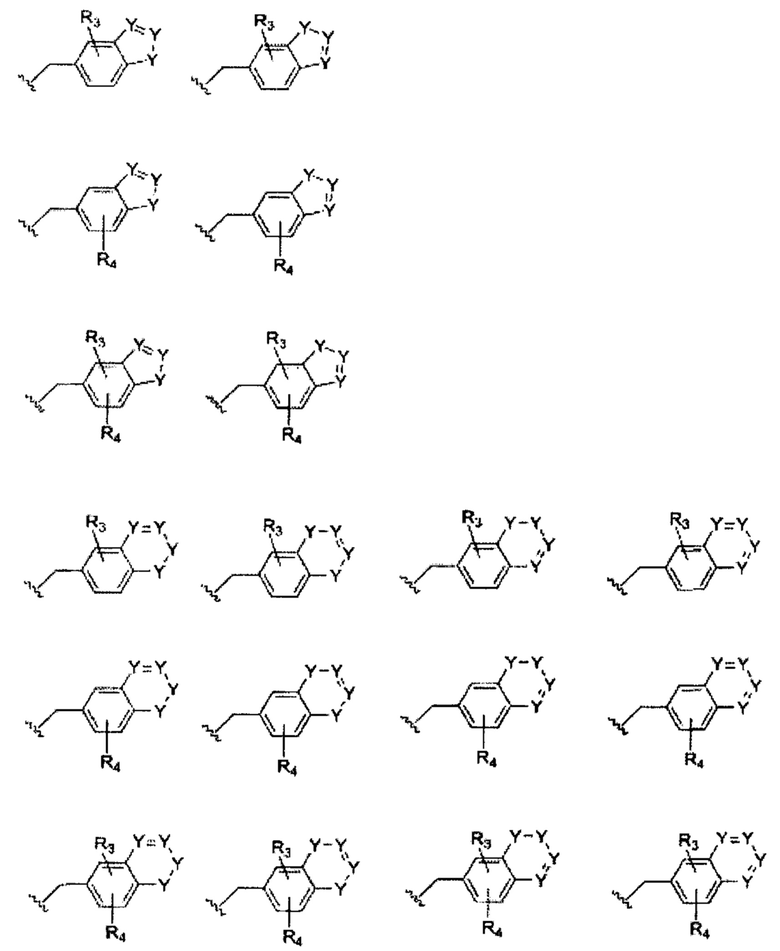
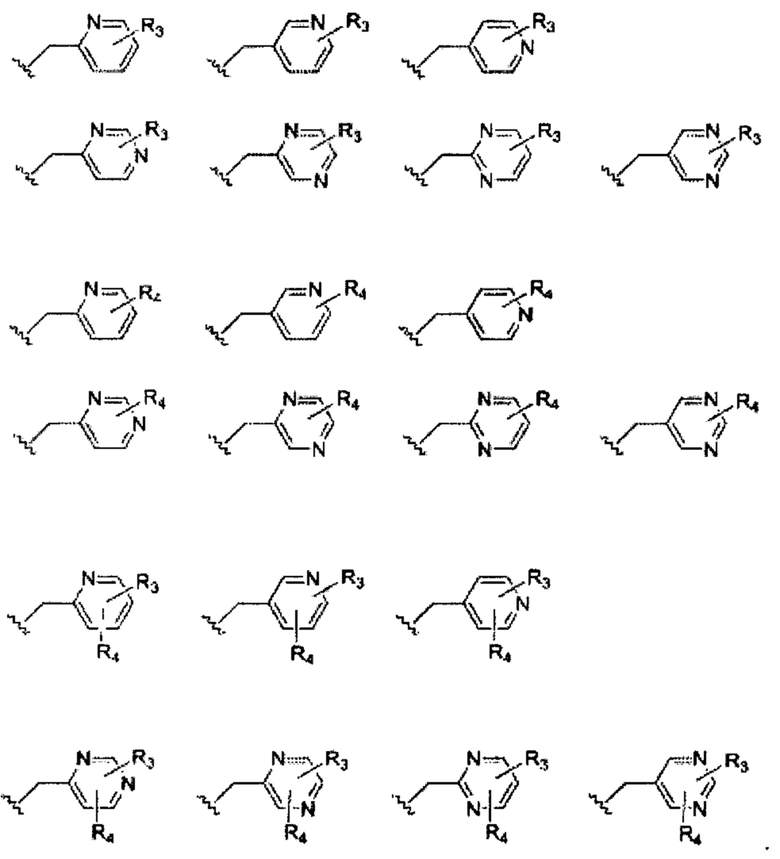
Предполагается, что в вышеприведенных формулах боковых групп положения различных групп R3 и R4 относительно друг друга на кольце боковой группы, положения азота и/или положение конденсированного кольца не ограничены. Рассматривая одну структуру в качестве примера, и если не указано иное, структура, изображенная следующим образом:
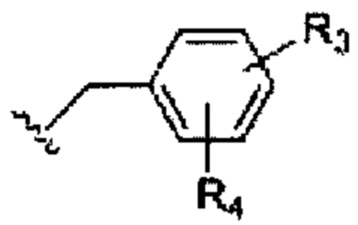
может быть изображена следующим образом:
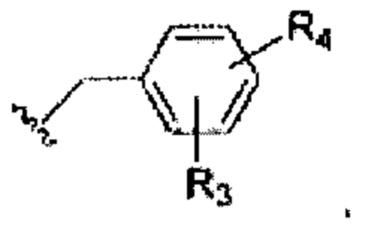
Дополнительно, в ранее указанных формулах боковых групп, когда показан один -R3, один или более чем один -R3, каждый независимо, могут быть присоединены к кольцу боковой группы. Подобным образом, когда показан один -R4, один или более чем один -R4, каждый независимо, могут быть присоединены к кольцу боковой группы.
В некоторых вариантах осуществления изобретения, в которых имеется кольцо Е, боковая группа имеет одну из следующих формул, где один или большее количество Y, обозначенных ниже как G, каждый независимо, выбраны из N, N-R5, О, S, S=O или S(=O)2:
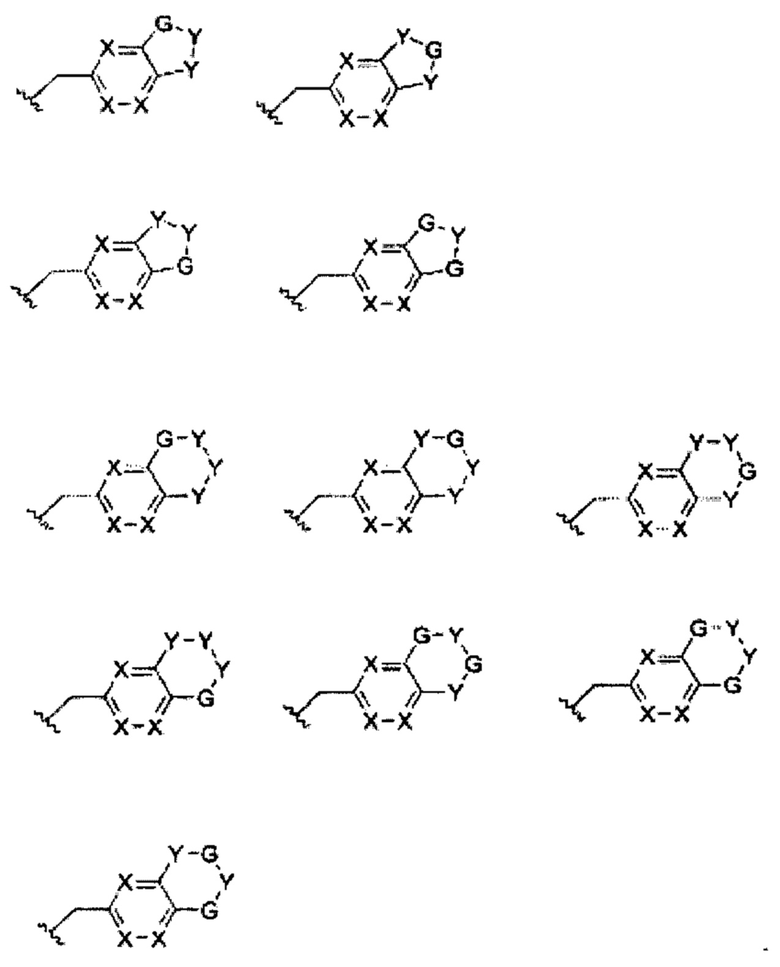
в которых каждый из оставшихся показанных Y независимо представляет собой C-R5, C(R5)(R5) или С=O;
и где, когда каждый из двух соседних Y независимо представляет собой C-R5 или N и С-R5, связь между указанными соседними Y может представлять собой двойную связь.
В некоторых вариантах осуществления изобретения R3 представляет собой группу, имеющую следующую формулу:
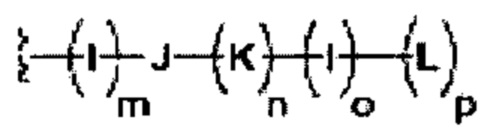
где I в каждом случае независимо представляет собой двухвалентный заместитель, описанный в данном документе; и m равен 0, 1 или 2, а o равен 0, 1 или 2;
где J представляет собой необязательно замещенный вторичный амин, третичный амин, циклический амин, гетероцикл, гетероцикл, содержащий спирогруппу, N-содержащий гетероцикл, О-содержащий гетероцикл, N- и О-содержащий гетероцикл, гетероарил, N-содержащий гетероарил, арил, их окисленную форму, их форму, содержащую гетероатомы, их замещенную форму или их комбинацию;
где K в каждом случае независимо представляет собой R4, арил, гетероарил, гетероцикл, циклоалкил, циклоалкенил, их окисленную форму, их форму, содержащую гетероатомы, их замещенную форму или их комбинацию; и n равен 0, 1 или 2;
и где L в каждом случае независимо представляет собой необязательно замещенный R4, его окисленную форму, его форму, содержащую гетероатомы, его замещенную форму или их комбинацию; и p равен 0, 1, 2, 3, 4, 5 или 6.
В некоторых вариантах осуществления изобретения I в каждом случае может независимо представлять собой алкилен, алкенилен, алкиленокси, алкениленокси или алкинилен, их окисленную форму, их форму, содержащую гетероатомы, или их замещенную форму; и m равен 0 или 1, а о равен 0 или 1.
В некоторых вариантах осуществления изобретения J представляет собой необязательно замещенную «С-группу», третичный амин, циклический амин, гетероцикл, N-содержащий гетероцикл, О-содержащий гетероцикл, N- и О-содержащий гетероцикл, гетероарил, N-содержащий гетероарил, арил, их окисленную форму, их форму, содержащую гетероатомы, их замещенную форму или их комбинацию.
В некоторых вариантах осуществления изобретения K в каждом случае независимо представляет собой необязательно замещенный R4, арил, гетероарил, гетероцикл, циклоалкил, циклоалкенил, их окисленную форму, их форму, содержащую гетероатомы, их замещенную форму или их комбинацию; и n равен 0 или 1.
В некоторых вариантах осуществления изобретения L в каждом случае независимо представляет собой необязательно замещенный R4 или «D-группу», их окисленную форму, их форму, содержащую гетероатомы, их замещенную форму; и p равен 0, 1, 2, 3, 4, 5 или 6.
В некоторых вариантах осуществления изобретения, если n, о и р равны 0, то J представляет собой одновалентный остаток необязательно замещенной «С-группы», третичного амина, циклического амина, гетероцикла, N-содержащего гетероцикла, О-содержащего гетероцикла, N- и О-содержащего гетероцикла, гетероарила, N-содержащего гетероарила, арила или их комбинацию, но если любой из n, о или р не равен 0, то J представляет собой двухвалентный остаток необязательно замещенной «С-группы», третичного амина, циклического амина, гетероцикла, N-содержащего гетероцикла, О-содержащего гетероцикла, N- и О-содержащего гетероцикла, гетероарила, N-содержащего гетероарила, арила или их комбинацию.
В некоторых вариантах осуществления изобретения, если о и р равны 0, то K представляет собой одновалентный остаток необязательно замещенного R4, арила, гетероарила, гетероцикла, циклоалкила, циклической группы или их комбинацию, но если любой из о или р не равен 0, то K представляет собой двухвалентный остаток необязательно замещенного R4, арила, гетероарила, гетероцикла, циклоалкила, циклической группы или их комбинацию.
В некоторых вариантах осуществления изобретения R3 представляет собой или замещен так, что содержит 3-, 4-, 5-, 6-членное кольцо или большее кольцо, которое содержит один или большее количество атомов углерода, замещенных атомов углерода и/или гетероатомов (N, О, S) в дополнение к их окисленным вариантам, включая алкены и циклоалкены, гетероциклы и смешанные карбоциклические и гетероциклические фрагменты.
В некоторых вариантах осуществления изобретения R3 включает в себя циклический амин, при этом атом азота и атомы углерода образуют С3-С10 циклический амин.
В некоторых вариантах осуществления изобретения R3 включает в себя циклический амин, при этом атом азота и атомы углерода образуют С3-С6 циклическую группу.
В некоторых вариантах осуществления изобретения циклический амин имеет следующую структуру:
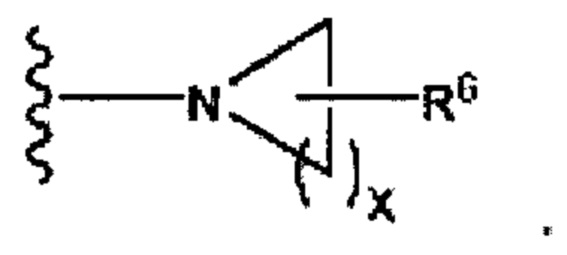
Индекс х в циклическом амине особым образом не ограничен и может принимать любое значение. В некоторых вариантах осуществления изобретения х равен 1-10. Этот интервал включает в себя все значения и подынтервалы между ними, в том числе 1, 2, 3, 4, 5, 6, 7, 8, 9 и 10.
В некоторых вариантах осуществления изобретения один или более чем один атом углерода в вышеуказанной структуре циклического амина могут независимо и необязательно быть замещены одной или большим количеством независимых замещающих групп, описанных в данном документе. В некоторых вариантах осуществления изобретения один или более чем один атом углерода в структуре циклического амина окислен. В некоторых вариантах осуществления изобретения одна или большее количество замещающих групп могут независимо и необязательно быть присоединены непосредственно к структуре циклического амина с помощью одной или большего количества химических связей или могут независимо и необязательно быть непрямо присоединены к структуре циклического амина посредством одной или большего количества двухвалентных промежуточных замещающих групп, описанных в данном документе. Возможны 1, 2, 3, 4 или 5 независимых двухвалентных промежуточных замещающих групп, и они могут представлять собой любые из определенных в данном документе. В некоторых вариантах осуществления изобретения один или более чем один атом углерода в вышеуказанной структуре циклического амина заменены на гетероатом, такой как S, О или N. В некоторых вариантах осуществления изобретения циклический амин выбран из «С-группы».
При наличии азота, оставшаяся часть кольца циклического амина особым образом не ограничена. Оставшуюся часть кольца можно пригодным образом получать из двухвалентной циклоалкиленовой группы, двухвалентной гетероциклоалкиленовой группы, двухвалентной ариленовой группы, двухвалентной гетероариленовой группы, одной или большего количества двухвалентных промежуточных замещающих групп, их окисленной формы или их комбинации. Циклический амин может содержать одно или более чем одно кольцо. Возможны комбинации различных колец.
В циклическом амине один или большем чем один из атомов в кольце могут необязательно и независимо заменены одним или большим количеством гетероатомов, например N, О, Р, S, их окисленной формой или их комбинацией.
В циклическом амине один или больше чем один из атомов в кольце могут быть необязательно и независимо замещены одним или большим количеством замещающих групп R6. При наличии более одной замещающей группы они могут быть одинаковыми или различными.
В циклическом амине одна или более чем одна из замещающих групп R6 могут быть дополнительно замещены одной или большим количеством дополнительных замещающих групп. При наличии более одной дополнительной замещающей группы они могут быть одинаковыми или различными.
В некоторых вариантах осуществления изобретения каждая замещающая группа и/или дополнительные замещающие группы могут независимо и необязательно быть выбраны из одной или большего количества замещающих групп, описанных в данном документе.
В некоторых вариантах осуществления изобретения каждая группа R6 может независимо и необязательно быть выбрана из одной или большего количества из следующих групп: «D-группа», водород, алкильная группа, циклоалкильная группа, циклоалкенильная группа, галогенная группа, алкенильная группа, алкинильная группа, арильная группа, гидроксигруппа, ацильная группа, оксогруппа, меркаптогруппа, алкилтиогруппа, алкоксигруппа, гетероциклическая группа, гетероарильная группа, гетероарилкарбонильная группа, арилоксигруппа, гетероарилоксигруппа, арилалкильная группа, гетероарилалкильная группа, арилалкоксигруппа, гетероарилалкоксигруппа, аминогруппа, алкиламиногруппа, диалкиламиногруппа, амидиновая группа, амидная группа, карбамоильная группа, алкилкарбонильная группа, алкоксикарбонильная группа, алкиламинокарбонильная группа, диалкиламинокарбонильная группа, арилкарбонильная группа, арилоксикарбонильная группа, алкилсульфонильная группа, арилсульфонильная группа, их окисленной формы, их формы, содержащей гетероатомы, их замещенной формы или их комбинации.
В некоторых вариантах осуществления изобретения каждая группа R6 может независимо и необязательно быть выбрана из одной или большего количества из следующих групп: «D-группа», водород, алкильная группа, циклоалкильная группа, циклоалкенильная группа, галогенная группа, алкенильная группа, алкинильная группа, арильная группа, гидроксигруппа, ацильная группа, алкоксигруппа, гетероциклическая группа, гетероарильная группа, гетероарилкарбонильная группа, арилоксигруппа, гетероарилоксигруппа, арилалкильная группа, гетероарилалкильная группа, арилалкоксигруппа, гетероарилалкоксигруппа, аминогруппа, алкиламиногруппа, диалкиламиногруппа, амидиновая группа, амидная группа, карбамоильная группа, алкилкарбонильная группа, алкоксикарбонильная группа, алкиламинокарбонильная группа, диалкиламинокарбонильная группа, арилкарбонильная группа, арилоксикарбонильная группа, их окисленной формы, их формы, содержащей гетероатомы, их замещенной формы или их комбинации.
В некоторых вариантах осуществления изобретения каждая группа R6 может независимо и необязательно быть выбрана из одной или большего количества из следующих групп: водород, алкильная группа, циклоалкильная группа, циклоалкенильная группа, алкенильная группа, алкинильная группа, арильная группа, ацильная группа, алкоксигруппа, гетероциклическая группа, гетероарильная группа, гетероарилкарбонильная группа, арилоксигруппа, гетероарилоксигруппа, арилалкильная группа, гетероарилалкильная группа, арилалкоксигруппа, гетероарилалкоксигруппа, карбамоильная группа, алкилкарбонильная группа, алкоксикарбонильная группа, алкиламинокарбонильная группа, диалкиламинокарбонильная группа, арилкарбонильная группа, арилоксикарбонильная группа, их окисленной формы, их формы, содержащей гетероатомы, их замещенной формы или их комбинации.
В некоторых вариантах осуществления изобретения каждая группа R6 может независимо и необязательно быть выбрана из одной или большего количества из следующих групп: водород, алкильная группа, циклоалкильная группа, циклоалкенильная группа, алкенильная группа, алкинильная группа, арильная группа, гетероциклическая группа, гетероарильная группа, арилалкильная группа, гетероарилалкильная группа, их окисленной формы, их формы, содержащей гетероатомы, их замещенной формы или их комбинации.
Каждая группа R6 может быть независимо и необязательно дополнительно замещена, и каждая группа R6 может независимо и необязательно быть присоединена непосредственно к соответствующей исходной структуре с помощью одной или большего количества химических связей или может независимо и необязательно быть непрямо присоединена к соответствующей исходной структуре посредством одной или большего количества двухвалентных промежуточных замещающих групп.
В некоторых вариантах осуществления изобретения соединение имеет одну из следующих формул:
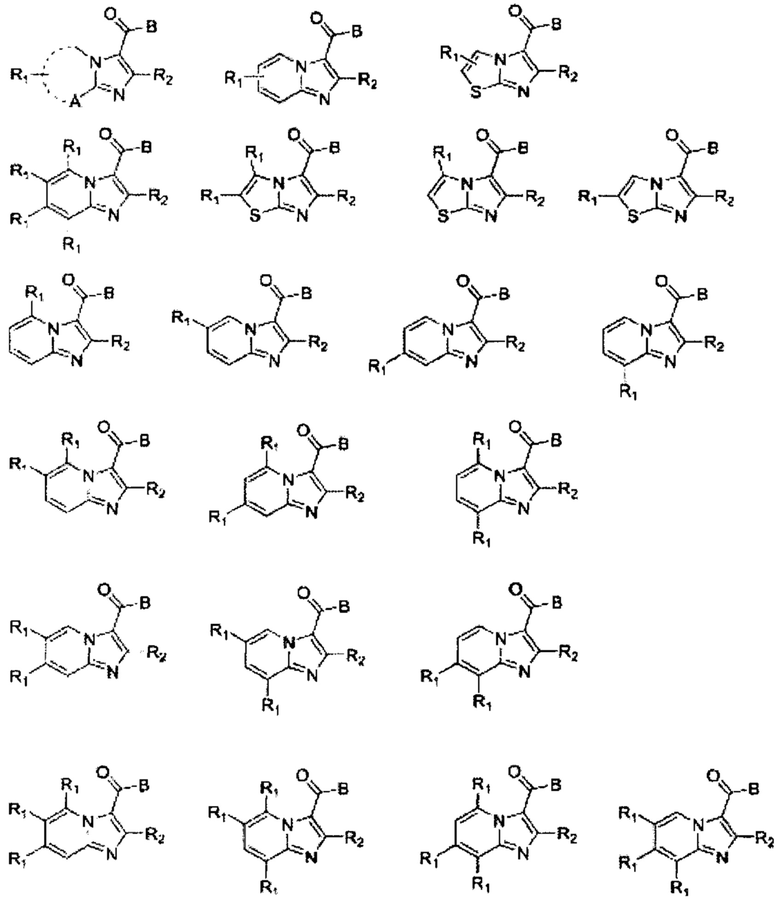
где А представляет собой =С- или -S-, и кольцо, определенное с помощью «А-C-N» и пунктирной линии, представляет собой 5-6-членное кольцо;
где R1 и R2 определены ранее;
где при наличии более одного R1 они могут быть одинаковыми или различными;
и где В имеет одну из следующих формул:
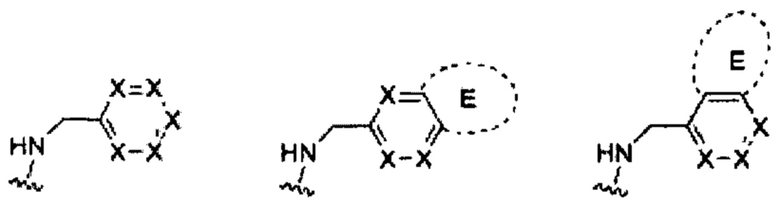
где X и Е определены ранее.
В некоторых вариантах осуществления изобретения В может представлять собой бензиламин, замещенный различными циклогетероалкилами, такими как морфолин, пиперидин, пиперазин, конденсированными или замещенными по различным положениям, которые можно легко получить из циклического амина или замещенного циклического амина. Неограничивающие примеры циклических аминов включают в себя, например, морфолин, тиоморфолин, пиперидин, пиперазин и тому подобное.
В некоторых вариантах осуществления изобретения В имеет одну из следующих формул:
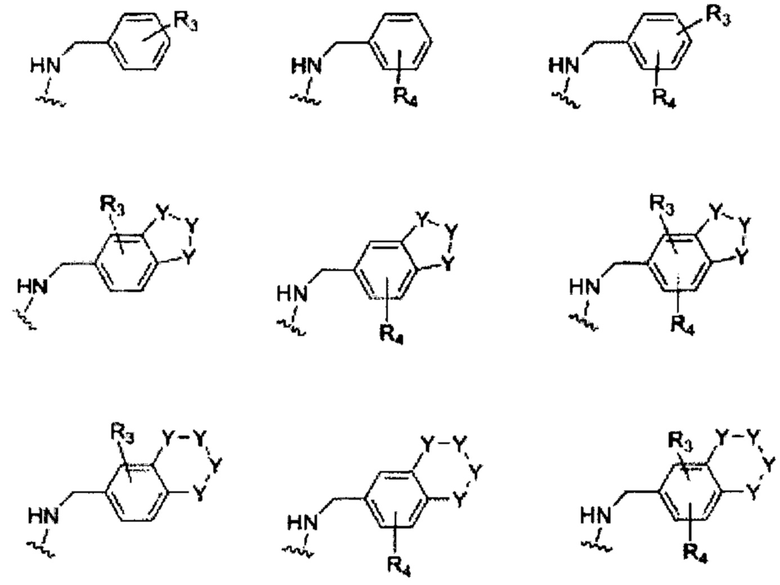
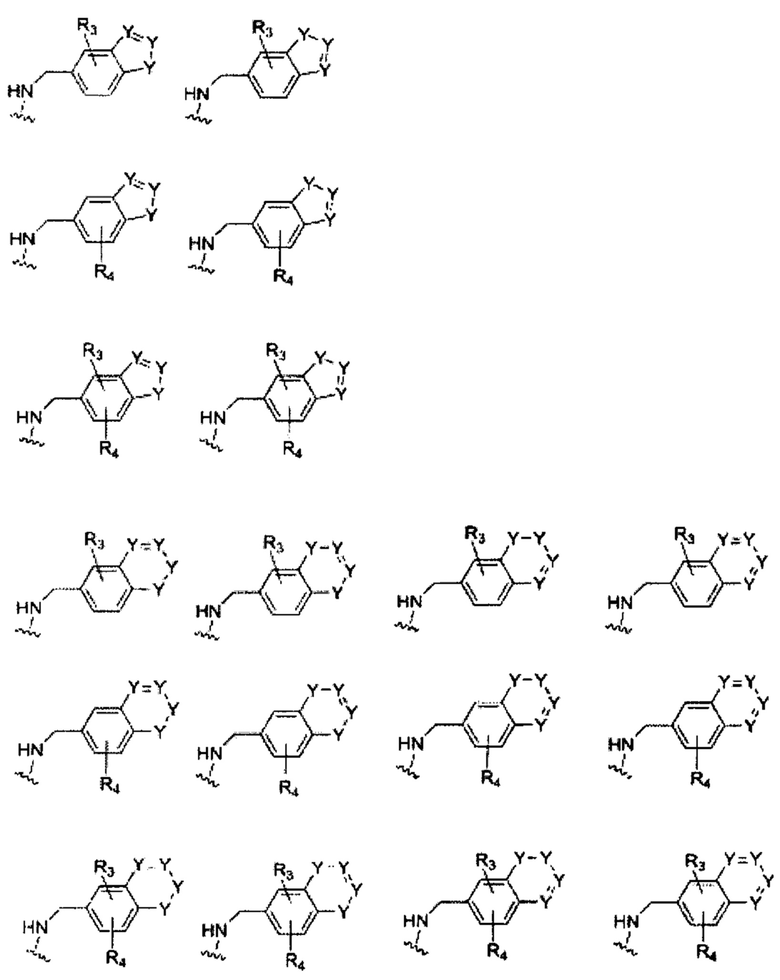
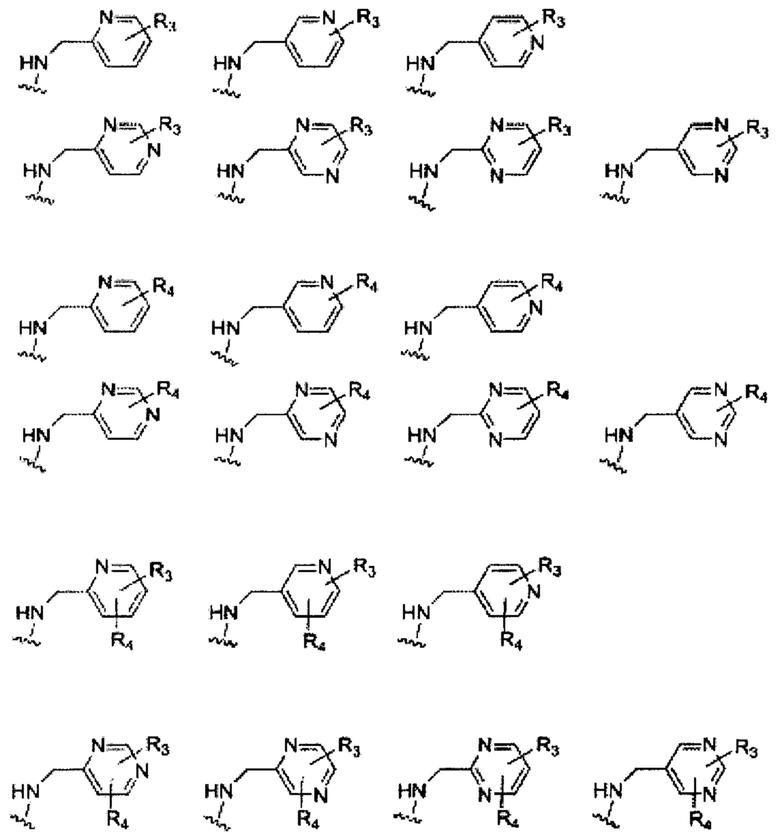
где R3, R4 и Y определены ранее.
Некоторые неограничивающие примеры В показаны ниже:
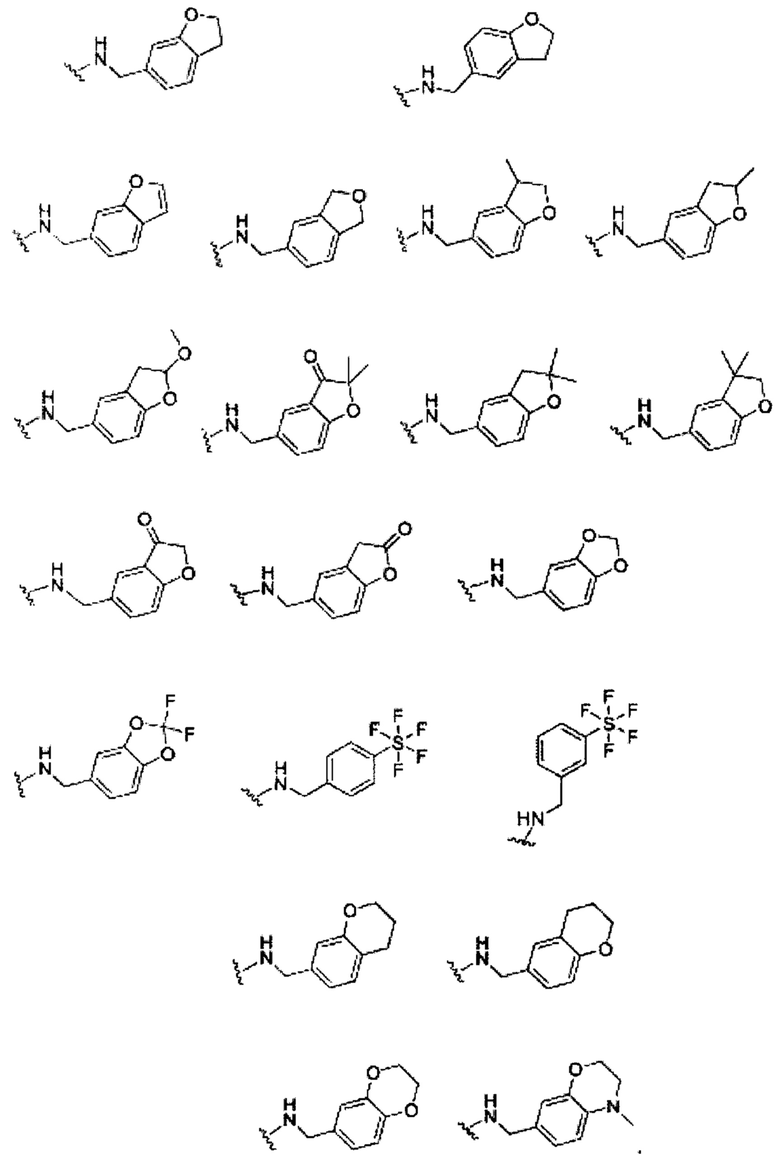
Некоторые неограничивающие примеры R3 или «С-группы» показаны ниже:
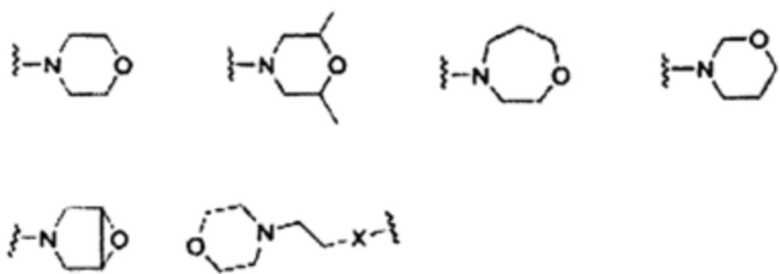
(X представляет собой О, NH)
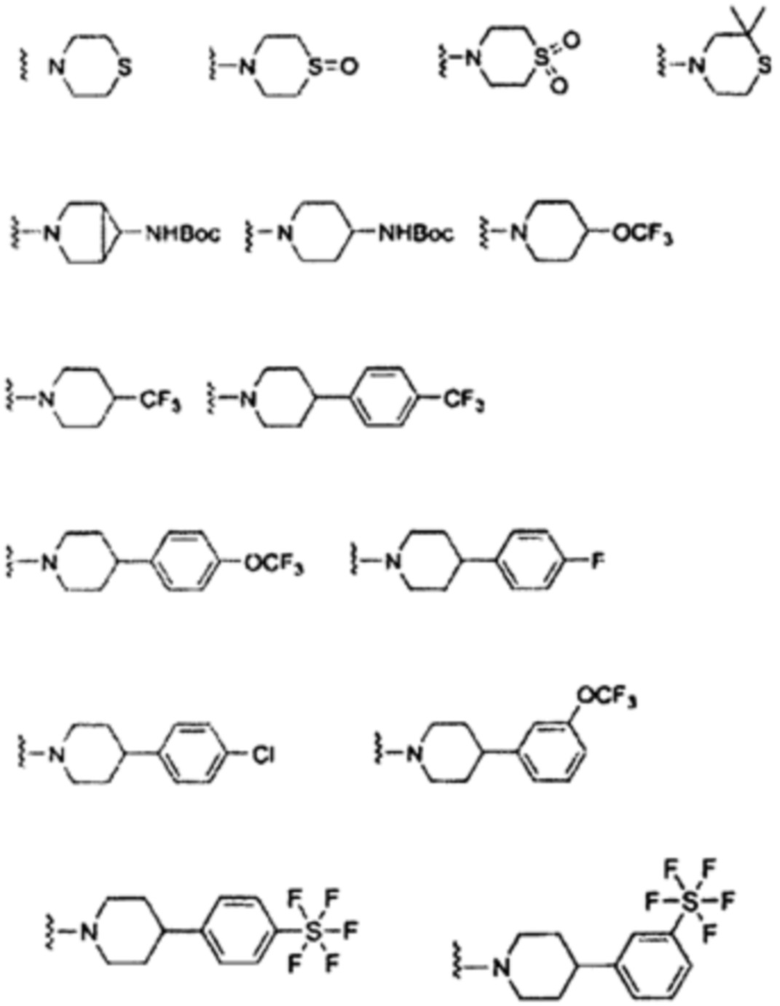
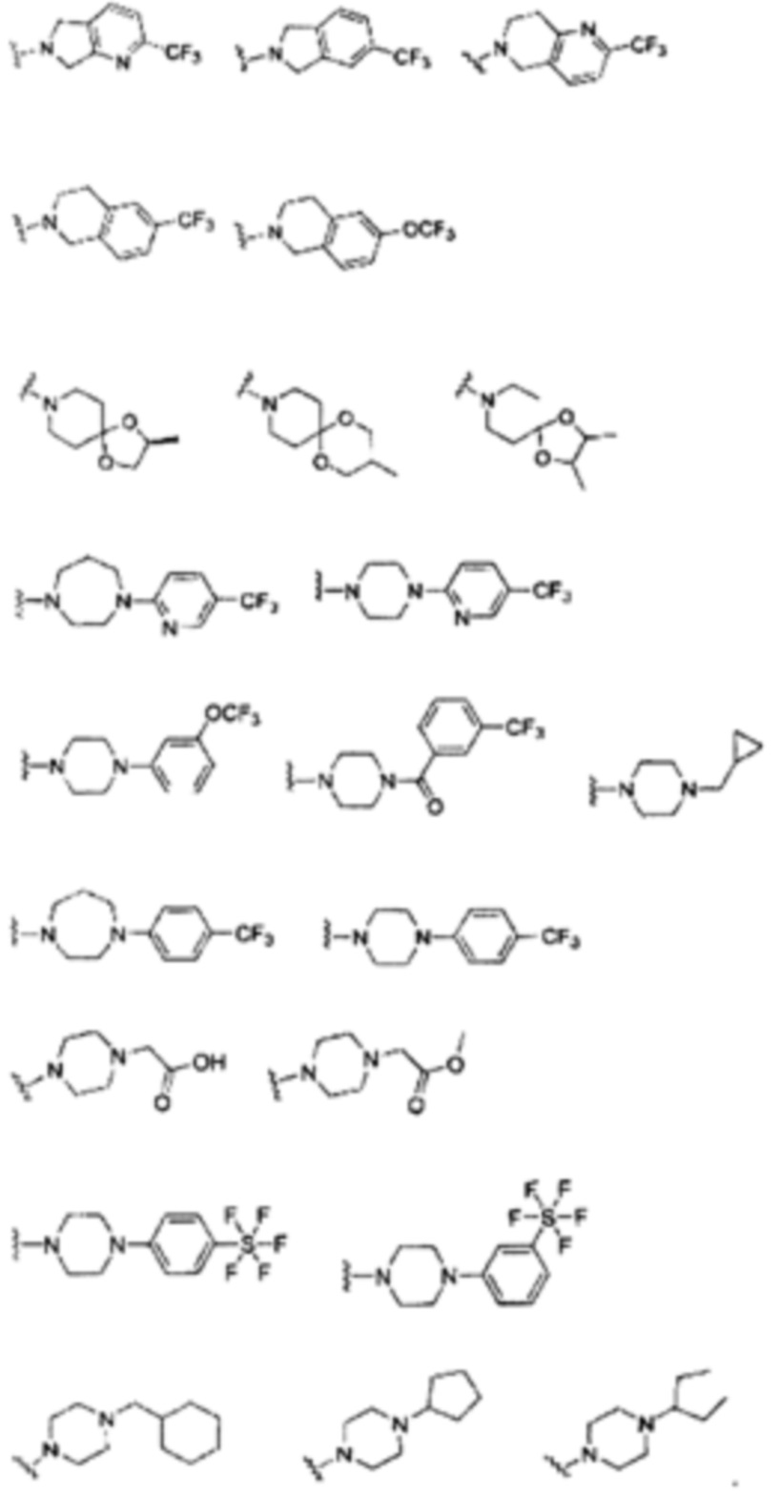
В некоторых вариантах осуществления изобретения «D-группа» представляет собой водород, галоген, Cl, F, СН3, СН2СН3, ОСН3, ОСН2СН3, CF3, OCF3, SF5.
В некоторых вариантах осуществления изобретения «D-группа» представляет собой Cl, F, СН3, CN, CF3, OCF3 SF5.
В некоторых вариантах осуществления изобретения «D-группа» представляет собой F, СН3, CN, CF3, OCF3, SF5.
В некоторых вариантах осуществления изобретения алкильная группа представляет собой одновалентный ациклический неразветвленный или разветвленный, замещенный или незамещенный, насыщенный или ненасыщенный углеводородный радикал. В некоторых вариантах осуществления изобретения алкильная группа имеет общую формулу (без учета необязательной ненасыщенности, замещения или тому подобного) -CnH2n+1. В некоторых вариантах осуществления изобретения n равен 1-20 ((С1-С20) алкил), что может соответственно включать в себя C1, С2, С3, С4, С5, С6, С7, С8, С9, С10, С11, C12, C13, С14, С15, C16, С17, C18, С19 и С20 алкильные группы. В некоторых вариантах осуществления изобретения алкильная группа может быть неразветвленной или разветвленной, замещенной или незамещенной, насыщенной или ненасыщенной или включать в себя любую комбинацию этих характеристик. В некоторых вариантах осуществления изобретения один или большее количество атомов водорода могут быть необязательно и независимо заменены одной или большим количеством замещающих групп. В некоторых вариантах осуществления изобретения один или большее количество атомов углерода могут быть необязательно и независимо заменены одним или большим количеством гетероатомов, таких как О, S, N, В, или их любой комбинацией. В некоторых вариантах осуществления изобретения алкильная группа может содержать одну или большее количество двойных связей, одну или большее количество тройных связей или любую их комбинацию. В некоторых вариантах осуществления изобретения алкильная группа присоединена к исходной структуре посредством одной или большего количества независимых двухвалентных промежуточных замещающих групп. Некоторые примеры алкильных групп, которые, как предполагается, не являются ограничивающими, включают в себя метил, этил, н-пропил, изопропил, н-бутил, изобутил, втор-бутил, трет-бутил и тому подобное.
В некоторых вариантах осуществления изобретения циклоалкильная группа представляет собой одновалентный, моно- или полициклический, замещенный или незамещенный, насыщенный или ненасыщенный углеводородный радикал. В некоторых вариантах осуществления изобретения циклоалкильная группа имеет общую формулу (без учета необязательной ненасыщенности, замещения или тому подобного) -CnH2n-1. В некоторых вариантах осуществления изобретения n равен 3-20 ((С3-С20) циклоалкил), что может соответственно включать в себя С3, С4, С5, С6, С7, C8, С9, С10, Cn, С12, С13, С14, C15, C16, С17, C18, С19 и С20 циклоалкильные группы. В некоторых вариантах осуществления изобретения циклоалкильная группа может быть замещенной или незамещенной, насыщенной или ненасыщенной, моно-, би-, три- или полициклической или включать в себя любую комбинацию этих характеристик. В некоторых вариантах осуществления изобретения один или большее количество атомов водорода могут быть необязательно и независимо заменены одной или большим количеством замещающих групп. В некоторых вариантах осуществления изобретения циклоалкильная группа может содержать один или большее количество участков ненасыщенности, например, она может содержать одну или большее количество двойных связей, одну или большее количество тройных связей или любую их комбинацию с образованием циклоалкенильной или циклоалкинильной группы или их комбинации. В некоторых вариантах осуществления изобретения один или большее количество атомов углерода могут быть необязательно и независимо заменены одним или большим количеством гетероатомов, таких как О, S, N, В, или их любой комбинацией. В некоторых вариантах осуществления изобретения циклоалкильная группа присоединена к исходной структуре посредством одной или большего количества независимых двухвалентных промежуточных замещающих групп. Некоторые примеры циклоалкильных групп, которые, как предполагается, не являются ограничивающими, включают в себя циклопропил, циклобутил, циклопентил, циклогексил, циклогептил, циклооктил, циклононил, циклопентенил, циклогексенил, бицикло[2.2.1]гептанил, бицикло[3.2.1]октанил и бицикло[5.2.0]нонанил и тому подобное. В случае полициклических групп одно или большее количество колец могут быть связаны вместе посредством связи или другой двухвалентной промежуточной замещающей группы, сконденсированы (например, когда одно или большее количество колец имеют два или большее количество общих атомов углерода или гетероатомов), соединены с помощью одного атома (например, спиросоединение) или соединены мостиковой связью.
В некоторых вариантах осуществления изобретения алкенильная группа представляет собой одновалентный неразветвленный или разветвленный, замещенный или незамещенный, ненасыщенный углеводородный радикал. В некоторых вариантах осуществления изобретения алкенильная группа имеет общую формулу (без учета необязательного замещения, ненасыщенности более высокой степени или тому подобного) -CnH2n-2. В некоторых вариантах осуществления изобретения n равен 2-20 ((С2-С20)алкенил), что может соответственно включать в себя С2, С3, С4, С5, С6, С7, С8, С9, С10, С11, С12, C13, С14, С15, C16, С17, С18, C19 и С20 алкенильные группы. В некоторых вариантах осуществления изобретения алкенильная группа может быть неразветвленной или разветвленной, замещенной или незамещенной, иметь разную степень ненасыщенности или включать в себя любую комбинацию этих характеристик. В некоторых вариантах осуществления изобретения один или большее количество атомов углерода могут быть необязательно и независимо заменены одним или большим количеством гетероатомов, таких как О, S, N, В, или их любой комбинацией. В некоторых вариантах осуществления изобретения алкенильная группа присоединена к исходной структуре посредством одной или большего количества независимых двухвалентных промежуточных замещающих групп. Некоторые примеры алкенильных групп, которые, как предполагается, не являются ограничивающими, включают в себя этенил, 1-пропенил, 2-пропенил (аллил), изопропенил, 2-метил-1-пропенил, 1-бутенил, 2-бутенил, алкадиены, алкатриены и тому подобное.
В некоторых вариантах осуществления изобретения алкинильная группа представляет собой одновалентный, неразветвленный или разветвленный, замещенный или незамещенный углеводородный радикал, который содержит одну или большее количество тройных связей углерод-углерод. В некоторых вариантах осуществления изобретения алкенильная группа имеет общую формулу (без учета необязательного замещения, ненасыщенности более высокой степени или тому подобного) -C2H2n-3. В некоторых вариантах осуществления изобретения n равен 2-20 ((С2-С20) алкинил), что может соответственно включать в себя С2, С3, С4, С5, С6, С7, C8, С9, С10, С11, С12, С13, С14, С15, C16, С17, С18, C19 и C20 алкинильные группы. В некоторых вариантах осуществления изобретения алкинильная группа может быть неразветвленной или разветвленной, замещенной или незамещенной, иметь разную степень ненасыщенности или включать в себя любую комбинацию этих характеристик. В некоторых вариантах осуществления изобретения один или большее количество атомов углерода могут быть необязательно и независимо заменены одним или большим количеством гетероатомов, таких как О, S, N, В, или их любой комбинацией. В некоторых вариантах осуществления изобретения алкинильная группа присоединена к исходной структуре посредством одной или большего количества независимых двухвалентных промежуточных замещающих групп. Некоторые примеры алкинильных групп, которые, как предполагается, не являются ограничивающими, включают в себя алкадиины, алкатриины, этинил, пропинил, бутинил и тому подобное.
В некоторых вариантах осуществления изобретения арильная группа представляет собой одновалентный, замещенный или незамещенный, моноциклический или полициклический, ароматический углеводородный радикал. В некоторых вариантах осуществления изобретения арильная группа представляет собой радикал, который в соответствии с теорией Хюккеля включает в себя циклическую делокализованную (4n+2) пи-электронную систему. В некоторых вариантах осуществления изобретения арильная группа представляет собой С5-С20 арильную группу. С5-С20 арильная группа может соответственно включать в себя С5, С6, С7, C8, С9, С10, С11, С12, С13, С14, С15, C16, С17, C18, С19 и C20 арильные группы. В некоторых вариантах осуществления изобретения арильная группа может быть замещенной или незамещенной, замещенной двумя или большим количеством групп, которые взятые вместе образуют циклическую группу, или включать в себя любую комбинацию этих характеристик. В некоторых вариантах осуществления изобретения арильная группа присоединена к исходной структуре посредством одной или большего количества независимых двухвалентных промежуточных замещающих групп. Некоторые примеры арильных групп, которые, как предполагается, не являются ограничивающими, включают в себя фенил, нафтил, тетрагидронафтил, фенантрил, пиренил, антрил, инданил, крезил и тому подобное.
В некоторых вариантах осуществления изобретения гетероциклическая группа представляет собой одновалентный, замещенный или незамещенный, насыщенный или ненасыщенный, моно- или полициклический углеводородный радикал, который содержит один или большее количество гетероатомов в одном или большем количестве колец. В некоторых вариантах осуществления изобретения гетероциклическая группа представляет собой С3-С20 циклическую группу, в которой один или большее количество атомов углерода в кольце независимо заменены одним или большим количеством гетероатомов. С3-С20 гетероциклическая группа может соответственно включать в себя С3, С4, С5, С6, С7, С8, С9, С10, С11, C12, С13, С14, С15, C16, С17, C18, С19 и С20 циклические группы, в которых один или большее количество атомов углерода независимо заменены одним или большим количеством гетероатомов. В некоторых вариантах осуществления изобретения гетероатомы выбраны из одного или большего количества из N, О или S или любой их комбинации. В некоторых вариантах осуществления изобретения N или S или оба могут быть независимо замещены одним или большим количеством заместителей. В некоторых вариантах осуществления изобретения гетероциклическая группа может быть замещенной или незамещенной, насыщенной или ненасыщенной, моно-, би-, три- или полициклической или включать в себя любую комбинацию этих характеристик. В некоторых вариантах осуществления изобретения один или большее количество атомов водорода могут быть необязательно и независимо заменены одной или большим количеством замещающих групп. В некоторых вариантах осуществления изобретения гетероциклическая группа может содержать одну или большее количество двойных связей углерод-углерод, тройных связей углерод-углерод, двойных связей углерод-азот или любую их комбинацию. В некоторых вариантах осуществления изобретения гетероциклическая группа присоединена к исходной структуре посредством одной или большего количества независимых двухвалентных промежуточных замещающих групп. Некоторые примеры гетероциклических групп, которые, как предполагается, не являются ограничивающими, включают в себя циклический амин, азетидинил, тетрагидрофуранил, имидазолидинил, пирролидинил, пиперидинил, пиперазинил, оксазолидинил, тиазолидинил, пиразолидинил, тиоморфолинил, тетрагидротиазинил, тетрагидротиадиазинил, морфолинил, оксетанил, тетрагидродиазинил, оксазинил, оксатиазинил, индолинил, изоиндолинил, хинуклидинил, хроманил, изохроманил, бензоксазинил, тетрагидрофуран-2-ил, тетрагидрофуран-3-ил, имидазолидин-1-ил, имидазолидин-2-ил, имидазолидин-4-ил, пирролидин-1-ил, пирролидин-2-ил, пирролидин-3-ил, пиперидин-1-ил, пиперидин-2-ил, пиперидин-3-ил, пиперазин-1-ил, пиперазин-2-ил, пиперазин-3-ил, 1,3-оксазол идин-3-ил, изотиазолидин, 1,3-тиазолидин-3-ил, 1,2-пиразолидин-2-ил, 1,3-пиразолидин-1-ил, тиоморфолинил, 1,2-тетрагидротиазин-2-ил, 1,3-тетрагидротиазин-3-ил, тетрагидротиадиазинил, морфолинил, 1,2-тетрагидродиазин-2-ил, 1,3-тетрагидродиазин-1-ил, 1,4-оксазин-2-ил, 1,2,5-оксатиазин-4-ил и тому подобное.
В некоторых вариантах осуществления изобретения гетероарильная группа представляет собой одновалентный, замещенный или незамещенный, моноциклический или полициклический, ароматический углеводородный радикал, в котором один или большее количество атомов углерода в кольце независимо заменены одним или большим количеством гетероатомов, выбранных из О, S и N. В некоторых вариантах осуществления изобретения в дополнение к указанному гетероатому гетероарильная группа может необязательно содержать до 1, 2, 3 или 4 атомов N в кольце. В некоторых вариантах осуществления изобретения гетероарильная группа представляет собой арильную группу, в которой один или большее количество атомов углерода в кольце независимо заменены одним или большим количеством гетероатомов. В некоторых вариантах осуществления изобретения гетероарильная группа представляет собой ароматический радикал, который содержит один или большее количество гетероатомов, и который в соответствии с теорией Хюккеля включает в себя циклическую делокализованную (4n+2) пи-электронную систему. В некоторых вариантах осуществления изобретения гетероарильная группа представляет собой С5-С20 гетероарильную группу. С5-С20 гетероарильная группа может соответственно включать в себя С5, С6, С7, С8, С9, С10, С11, С12, С13, С14, С15, С16, С17, C18, С19 и С20 арильные группы, в которых один или более чем один атом углерода в кольце независимо заменены одним или большим количеством гетероатомов. В некоторых вариантах осуществления изобретения гетероарильная группа может быть замещенной или незамещенной, замещенной двумя или большим количеством групп, которые взятые вместе образуют циклическую группу, или включать в себя любую комбинацию этих характеристик. В некоторых вариантах осуществления изобретения гетероарильная группа присоединена к исходной структуре посредством одной или большего количества независимых двухвалентных промежуточных замещающих групп. Некоторые примеры алкинильных групп, которые, как предполагается, не являются ограничивающими, включают в себя пиридил, пиразинил, пиримидинил, пиридазинил, тиенил, фурил, имидазолил, пирролил, оксазолил (например, 1,3-оксазолил, 1,2-оксазолил), тиазолил (например, 1,2-тиазолил, 1,3-тиазолил), пиразолил, тетразолил, триазолил (например, 1,2,3-триазолил, 1,2,4-триазолил), оксадиазолил (например, 1,2,3-оксадиазолил), тиадиазолил (например, 1,3,4-тиадиазолил), хинолил, изохинолил, бензотиенил, бензофурил, индолил и тому подобное.
В некоторых вариантах осуществления изобретения алкиленовая, циклоалкиленовая, алкениленовая, алкиниленовая, ариленовая, гетероариленовая группы представляют собой двухвалентные радикалы, полученные при отщеплении водорода от соответствующей алкильной, циклоалкильной, алкенильной, алкинильной, ариленовой и гетероариленовой групп и тому подобного.
В некоторых вариантах осуществления изобретения арилалкильная группа представляет собой одновалентный радикал, полученный из одной или большего количества арильных групп, присоединенных к одной или большему количеству из алкиленовой группы, циклоалкиленовой группы, алкениленовой группы, алкиниленовой группы или их комбинации. Алкиленовая, циклоалкиленовая, алкениленовая и алкиниленовая группы представляют собой двухвалентные радикалы, полученные при отщеплении водорода от соответствующих алкильной, циклоалкильной, алкенильной или алкинильной групп. В этом контексте подразумевается любая комбинация арильной группы и алкильной, циклоалкильной, алкенильной или алкинильной группы. В некоторых вариантах осуществления изобретения арильная группа присоединена к исходной структуре посредством одной или большего количества из алкиленовой группы, циклоалкиленовой группы, алкениленовой группы, алкиниленовой группы или их комбинации в зависимости от конкретного случая. В некоторых вариантах осуществления изобретения арилалкильная группа может быть присоединена к исходной структуре посредством одной или большего количества независимых двухвалентных промежуточных замещающих групп.
В некоторых вариантах осуществления изобретения гетероарилалкильная группа представляет собой одновалентный радикал, полученный из одной или большего количества гетероарильных групп, присоединенных к одной или большему количеству из алкиленовой группы, циклоалкиленовой группы, алкениленовой группы, алкиниленовой группы или их комбинации. Алкиленовая, циклоалкиленовая, алкениленовая и алкиниленовая группы представляют собой двухвалентные радикалы, полученные при отщеплении водорода от соответствующих алкильной, циклоалкильной, алкенильной или алкинильной групп. В этом контексте подразумевается любая комбинация гетероарильной группы и алкильной, циклоалкильной, алкенильной или алкинильной группы. В некоторых вариантах осуществления изобретения гетероарильная группа присоединена к исходной структуре посредством одной или большего количества из алкиленовой группы, циклоалкиленовой группы, алкениленовой группы, алкиниленовой группы или их комбинации в зависимости от конкретного случая. В некоторых вариантах осуществления изобретения гетероарилалкильная группа может быть присоединена к исходной структуре посредством одной или большего количества независимых двухвалентных промежуточных замещающих групп.
В некоторых вариантах осуществления изобретения галогенная группа представляет собой одновалентный галогенный радикал или галогенсодержащую замещающую группу, например, которая представляет собой или содержит один или большее количество F, Br, Cl, I или их комбинацию. При использовании в данном документе, термин «галоген» или «галогено» включает в себя фтор, хлор, бром или йод или фторид, хлорид, бромид или йодид. В некоторых вариантах осуществления изобретения галогенсодержащая замещающая группа может соответственно включать в себя замещающую группу, в которой один или большее количество атомов водорода независимо заменены одним или большим количеством галогенов. В некоторых вариантах осуществления изобретения галогенная группа может быть присоединена к исходной структуре посредством одной или большего количества независимых двухвалентных промежуточных замещающих групп.
В некоторых вариантах осуществления изобретения гидроксигруппа представляет собой одновалентный гидроксильный радикал (-ОН) или гидрокси-содержащую замещающую группу, например, которая представляет собой или содержит один или большее количество -ОН. При использовании в данном документе, термин «гидрокси» включает в себя группу -ОН. В некоторых вариантах осуществления изобретения гидрокси-содержащая замещающая группа может соответственно включать в себя замещающую группу, в которой один или большее количество атомов водорода независимо заменены одной или большим количество групп -ОН. В некоторых вариантах осуществления изобретения гидроксильная группа может быть присоединена к исходной структуре посредством одной или большего количества независимых двухвалентных промежуточных замещающих групп.
В некоторых вариантах осуществления изобретения оксогруппа представляет собой одновалентный радикал, который содержит атом кислорода =O, присоединенный двойной связью к углероду или другому элементу. В некоторых вариантах осуществления изобретения оксогруппа представляет собой двухвалентный радикал, который содержит атом кислорода -О-, присоединенный к двум атомам углерода или двум другим элементам. В некоторых вариантах осуществления изобретения оксогруппа соответственно включает в себя альдегиды, карбоновые кислоты, кетоны, сульфоновые кислоты, амиды, сложные эфиры и их комбинации. В некоторых вариантах осуществления изобретения оксогруппа может быть присоединена к исходной структуре посредством одной или большего количества независимых двухвалентных промежуточных замещающих групп.
В некоторых вариантах осуществления изобретения меркапто- или тиоловая группа представляет собой одновалентный радикал -SR или группу, содержащую -SR. Группа R подходящим образом выбрана из любой из замещающих групп. В некоторых вариантах осуществления изобретения меркаптогруппа может быть присоединена к исходной структуре посредством одной или большего количества независимых двухвалентных промежуточных замещающих групп.
В некоторых вариантах осуществления изобретения аминогруппа представляет собой одновалентный радикал -NH2 или замещающую группу, содержащую -NH2. В некоторых вариантах осуществления изобретения аминогруппа может быть присоединена к исходной структуре посредством одной или большего количества независимых двухвалентных промежуточных замещающих групп.
В некоторых вариантах осуществления изобретения алкиламиногруппа представляет собой одновалентный радикал -NRH или замещающую группу, содержащую -NRH. Группа R подходящим образом выбрана из любой из замещающих групп. В некоторых вариантах осуществления изобретения алкиламиногруппа может быть присоединена к исходной структуре посредством одной или большего количества независимых двухвалентных промежуточных замещающих групп.
В некоторых вариантах осуществления изобретения диалкиламиногруппа представляет собой одновалентный радикал -NRR или замещающую группу, содержащую -NRR. Группы R могут быть одинаковыми или различными и подходящим образом и независимо выбраны из любой из замещающих групп. В некоторых вариантах осуществления изобретения диалкиламиногруппа может быть присоединена к исходной структуре посредством одной или большего количества независимых двухвалентных промежуточных замещающих групп.
В некоторых вариантах осуществления изобретения ацильная или карбонильная группа представляет собой одновалентный радикал, который содержит группу -С(=O)R. В некоторых вариантах осуществления изобретения ацильная группа соответственно включает в себя альдегиды, кетоны и их комбинации. Группа R подходящим образом выбрана из любой из замещающих групп. В некоторых вариантах осуществления изобретения карбонильная группа может быть присоединена к исходной структуре посредством одной или большего количества независимых двухвалентных промежуточных замещающих групп.
В некоторых вариантах осуществления изобретения карбоксильная группа представляет собой одновалентный радикал -С(=O)ОН или замещающую группу, содержащую -С(=O)ОН. В некоторых вариантах осуществления изобретения карбоксильная группа может быть присоединена к исходной структуре посредством одной или большего количества независимых двухвалентных промежуточных замещающих групп.
В некоторых вариантах осуществления изобретения карбоксилатная группа представляет собой одновалентный анион -С(=O)O-, -C(=O)OR или -С(=O)ОМ, где М представляет собой катион металла, или замещающую группу, содержащую анион -С(=O)O-, -C(=O)OR или -С(=O)ОМ. Группа R подходящим образом выбрана из любой из замещающих групп. Катион металла может быть подходящим образом выбран из Li, Na, K и тому подобного. В некоторых вариантах осуществления изобретения карбоксилатная группа может быть присоединена к исходной структуре посредством одной или большего количества независимых двухвалентных промежуточных замещающих групп.
В некоторых вариантах осуществления изобретения амидиновая группа представляет собой одновалентный радикал -C(=NR)NRR или замещающую группу, содержащую -C(=NR)NRR. Группы R могут быть одинаковыми или различными и подходящим образом и независимо выбраны из любой из замещающих групп. В некоторых вариантах осуществления изобретения амидиновая группа может быть присоединена к исходной структуре посредством одной или большего количества независимых двухвалентных промежуточных замещающих групп.
В некоторых вариантах осуществления изобретения амидная группа представляет собой одновалентный радикал -E(=O)NRR или замещающую группу, содержащую -E(=O)NRR, в которой Е может представлять собой атом, отличный от углерода, например халькоген (например, S, Se, Те) или Р. В некоторых вариантах осуществления изобретения амидная группа соответственно включает в себя одновалентные лактамы, пептиды, фосфорамиды или сульфамиды, -S(=O)2NRR, -P(=O)(OH)NRR и тому подобное. Группы R могут быть одинаковыми или различными и подходящим образом и независимо выбраны из любой из замещающих групп. В некоторых вариантах осуществления изобретения амидная группа может быть присоединена к исходной структуре посредством одной или большего количества независимых двухвалентных промежуточных замещающих групп.
В некоторых вариантах осуществления изобретения карбамоильная группа представляет собой одновалентный радикал -C(=O)NRR или замещающую группу, содержащую -C(=O)NRR. Группы R могут быть одинаковыми или различными и подходящим образом и независимо выбраны из любой из замещающих групп. В некоторых вариантах осуществления изобретения карбамоильная группа может быть присоединена к исходной структуре посредством одной или большего количества независимых двухвалентных промежуточных замещающих групп.
В некоторых вариантах осуществления изобретения сульфонильная группа представляет собой одновалентный радикал -S(=O)2R или замещающую группу, содержащую -S(=O)2R. Группа R подходящим образом выбрана из любой из замещающих групп. В некоторых вариантах осуществления изобретения сульфонильная группа может быть присоединена к исходной структуре посредством одной или большего количества независимых двухвалентных промежуточных замещающих групп.
В некоторых вариантах осуществления изобретения алкилтио- или сульфидная группа представляет собой одновалентный радикал -SR или замещающую группу, содержащую -SR. Группа R подходящим образом выбрана из любой из замещающих групп. В некоторых вариантах осуществления изобретения алкилтиогруппа может быть присоединена к исходной структуре посредством одной или большего количества независимых двухвалентных промежуточных замещающих групп.
В некоторых вариантах осуществления изобретения алкоксигруппа представляет собой одновалентный радикал, полученный из -О-алкильной группы. В некоторых вариантах осуществления изобретения алкилтиогруппа может быть присоединена к исходной структуре посредством одной или большего количества независимых двухвалентных промежуточных замещающих групп.
В некоторых вариантах осуществления изобретения арилоксигруппа представляет собой одновалентный радикал, полученный из -О-арильной группы. В некоторых вариантах осуществления изобретения арилоксигруппа может быть присоединена к исходной структуре посредством одной или большего количества независимых двухвалентных промежуточных замещающих групп.
В некоторых вариантах осуществления изобретения гетероарилоксигруппа представляет собой одновалентный радикал, полученный из -О-гетероарильной группы. В некоторых вариантах осуществления изобретения гетероарилоксигруппа может быть присоединена к исходной структуре посредством одной или большего количества независимых двухвалентных промежуточных замещающих групп.
В некоторых вариантах осуществления изобретения арилалкоксигруппа представляет собой одновалентный радикал, полученный из -О-арилалкильной группы. В некоторых вариантах осуществления изобретения арилалкоксигруппа может быть присоединена к исходной структуре посредством одной или большего количества независимых двухвалентных промежуточных замещающих групп.
В некоторых вариантах осуществления изобретения гетероарилалкоксигруппа представляет собой одновалентный радикал, полученный из -О-гетероарильной группы. В некоторых вариантах осуществления изобретения гетероарилалкоксигруппа может быть присоединена к исходной структуре посредством одной или большего количества независимых двухвалентных промежуточных замещающих групп.
В некоторых вариантах осуществления изобретения алкилкарбонильная группа представляет собой одновалентный радикал, полученный из -карбонилалкильной группы. В некоторых вариантах осуществления изобретения алкилкарбонильная группа может быть присоединена к исходной структуре посредством одной или большего количества независимых двухвалентных промежуточных замещающих групп.
В некоторых вариантах осуществления изобретения алкоксикарбонильная группа представляет собой одновалентный радикал, полученный из -карбонил-О-алкильной группы. В некоторых вариантах осуществления изобретения алкоксикарбонильная группа может быть присоединена к исходной структуре посредством одной или большего количества независимых двухвалентных промежуточных замещающих групп.
В некоторых вариантах осуществления изобретения алкиламинокарбонильная группа представляет собой одновалентный радикал, полученный из -карбонилалкиламиногруппы. В некоторых вариантах осуществления изобретения гетероарилалкоксигруппа может быть присоединена к исходной структуре посредством одной или большего количества независимых двухвалентных промежуточных замещающих групп.
В некоторых вариантах осуществления изобретения диалкиламинокарбонильная группа представляет собой одновалентный радикал, полученный из -карбонилдиалкиламиногруппы. В некоторых вариантах осуществления изобретения диалкиламинокарбонильная группа может быть присоединена к исходной структуре посредством одной или большего количества независимых двухвалентных промежуточных замещающих групп.
В некоторых вариантах осуществления изобретения арилкарбонильная группа представляет собой одновалентный радикал, полученный из -карбониларильной группы. В некоторых вариантах осуществления изобретения арилкарбонильная группа может быть присоединена к исходной структуре посредством одной или большего количества независимых двухвалентных промежуточных замещающих групп.
В некоторых вариантах осуществления изобретения гетероарилкарбонильная группа представляет собой одновалентный радикал, полученный из -карбонилгетероарильной группы. В некоторых вариантах осуществления изобретения гетероарилкарбонильная группа может быть присоединена к исходной структуре посредством одной или большего количества независимых двухвалентных промежуточных замещающих групп.
В некоторых вариантах осуществления изобретения арилоксикарбонильная группа представляет собой одновалентный радикал, полученный из -карбонил-О-арильной группы. В некоторых вариантах осуществления изобретения арилоксикарбонильная группа может быть присоединена к исходной структуре посредством одной или большего количества независимых двухвалентных промежуточных замещающих групп.
В некоторых вариантах осуществления изобретения алкилсульфонильная группа представляет собой одновалентный радикал, полученный из -сульфонилалкильной группы. В некоторых вариантах осуществления изобретения алкилсульфонильная группа может быть присоединена к исходной структуре посредством одной или большего количества независимых двухвалентных промежуточных замещающих групп.
В некоторых вариантах осуществления изобретения арилсульфонильная группа представляет собой одновалентный радикал, полученный из -сульфониларильной группы. В некоторых вариантах осуществления изобретения арилсульфонильная группа может быть присоединена к исходной структуре посредством одной или большего количества независимых двухвалентных промежуточных замещающих групп.
В некоторых вариантах осуществления изобретения пергалогеналкильная группа представляет собой одновалентный радикал, полученный из полностью или практически полностью галогенированной алкильной группы. В некоторых вариантах осуществления изобретения пергалогеналкильная группа может быть присоединена к исходной структуре посредством одной или большего количества независимых двухвалентных промежуточных замещающих групп.
В некоторых вариантах осуществления изобретения пергалогеналкоксигруппа представляет собой одновалентный радикал, полученный из полностью или практически полностью галогенированной алкоксигруппы. В некоторых вариантах осуществления изобретения арилсульфонильная группа может быть присоединена к исходной структуре посредством одной или большего количества независимых двухвалентных промежуточных замещающих групп.
В некоторых вариантах осуществления изобретения пергалогенциклоалкильная группа представляет собой одновалентный радикал, полученный из полностью или практически полностью галогенированной циклоалкильной группы. В некоторых вариантах осуществления изобретения пергалогенциклоалкильная группа может быть присоединена к исходной структуре посредством одной или большего количества независимых двухвалентных промежуточных замещающих групп.
В некоторых вариантах осуществления изобретения пергалогеналкенильная группа представляет собой одновалентный радикал, полученный из полностью или практически полностью галогенированной алкенильной группы. В некоторых вариантах осуществления изобретения пергалогеналкенильная группа может быть присоединена к исходной структуре посредством одной или большего количества независимых двухвалентных промежуточных замещающих групп.
В некоторых вариантах осуществления изобретения пергалогеналкинильная группа представляет собой одновалентный радикал, полученный из полностью или практически полностью галогенированной алкинильной группы. В некоторых вариантах осуществления изобретения пергалогеналкинильная группа может быть присоединена к исходной структуре посредством одной или большего количества независимых двухвалентных промежуточных замещающих групп.
В некоторых вариантах осуществления изобретения пергалогенарильная группа представляет собой одновалентный радикал, полученный из полностью или практически полностью галогенированной арильной группы. В некоторых вариантах осуществления изобретения пергалогенарильная группа может быть присоединена к исходной структуре посредством одной или большего количества независимых двухвалентных промежуточных замещающих групп.
В некоторых вариантах осуществления изобретения пергалогенарилалкильная группа представляет собой одновалентный радикал, полученный из полностью или практически полностью галогенированной арилалкильной группы. В некоторых вариантах осуществления изобретения пергалогенарилалкильная группа может быть присоединена к исходной структуре посредством одной или большего количества независимых двухвалентных промежуточных замещающих групп.
В некоторых вариантах осуществления изобретения в отношении замещения одного или более чем одного атома в каждой группе одним или большим количеством гетероатомов, гетероатомы могут быть подходящим образом выбраны из N, О, Р, S, В или любой их комбинации.
Замещающие группы особым образом не ограничены. В некоторых вариантах осуществления изобретения замещающая группа может подходящим образом и независимо быть выбрана из одной или большего количества ацильной группы, алкенильной группы, алкоксигруппы, алкоксикарбонильной группы, алкоксикарбонилоксигруппы, алкоксисульфонилоксигруппы, алкильной группы, алкиламиногруппы, алкиламинокарбонильной группы, алкилкарбонильной группы, алкилкарбонилоксигруппы, алкилсульфонильной группы, алкилсульфонилоксигруппы, алкилтиогруппы, алкинильной группы, амидной группы, амидиновой группы, аминогруппы, арилалкоксигруппы, арилалкильной группы, арильной группы, арилкарбонильной группы, арилкарбонилоксигруппы, арилоксигруппы, арилоксикарбонильной группы, арилоксикарбонилоксигруппы, арилоксисульфонилоксигруппы, арилсульфонильной группы, арилсульфонилоксигруппы, азидогруппы, карбамидогруппы, карбамоильной группы, карбазоильной группы, карбонильной группы, карбоксилатной группы, карбоксильной группы, цианатогруппы, цианогруппы, циклоалкенильной группы, циклоалкильной группы, диалкиламинокарбонильной группы, диалкиламиногруппы, гуанидиногруппы, гуанильной группы, галогенной группы, гетероарилалкоксигруппы, гетероарилалкильной группы, гетероарильной группы, гетероарилкарбонильной группы, гетероарилоксигруппы, гетероциклической группы, гидроксиаминогруппы, гидроксигруппы, иминогруппы, изоцианатогруппы, изоцианогруппы, меркаптогруппы, нитрогруппы, оксогруппы, пергалогеналкенильной группы, пергалогеналкоксигруппы, пергалогеналкильной группы, пергалогеналкинильной группы, пергалогенарилалкильной группы, пергалогенарильной группы, пергалогенциклоалкильной группы, фосфатной группы, фосфиновой группы, фосфогруппы, сульфатной группы, сульфогруппы, сульфонильной группы, их окисленной формы или их комбинации. Возможны окисленные формы групп. В некоторых вариантах осуществления изобретения замещающая группа может быть необязательно и независимо непосредственно присоединена к соответствующей исходной структуре с помощью одной или большего количества химических связей. В некоторых вариантах осуществления изобретения замещающая группа может быть необязательно и независимо непрямо присоединена к соответствующей исходной структуре посредством одной или большего количества двухвалентных промежуточных замещающих групп. В некоторых вариантах осуществления изобретения замещающая группа может быть необязательно и независимо дополнительно замещена одной или большим количеством замещающих групп.
Двухвалентные промежуточные замещающие группы особым образом не ограничены. В некоторых вариантах осуществления изобретения двухвалентная промежуточная замещающая группа может подходящим образом и независимо быть выбрана из одной или большего количества из азогруппы, азиногруппы, азоксигруппы, карбонильной группы, диольной группы, диазоаминогруппы, дисульфинильной группы, дитиогруппы, оксигруппы, гидразогруппы, оксалильной группы, сульфонильной группы, тиокарбонильной группы, тионильной группы, фосфоновой сложноэфирной группы, карбоксилатной группы, тиогруппы; двухвалентного остатка одной или большего количества из следующих групп: ацильной группы, алкенильной группы, алкоксигруппы, алкоксикарбонильной группы, алкоксикарбонилоксигруппы, алкоксисульфонилоксигруппы, алкильной группы, алкиламиногруппы, алкиламинокарбонильной группы, алкилкарбонильной группы, алкилкарбонилоксигруппы, алкилсульфонильной группы, алкилсульфонилоксигруппы, алкилтиогруппы, алкинильной группы, амидной группы, амидиновой группы, аминогруппы, арилалкоксигруппы, арилалкильной группы, арильной группы, арилкарбонильной группы, арилкарбонилоксигруппы, арилоксигруппы, арилоксикарбонильной группы, арилоксикарбонилоксигруппы, арилоксисульфонилоксигруппы, арилсульфонильной группы, арилсульфонилоксигруппы, азидогруппы, карбамидогруппы, карбамоильной группы, карбазоильной группы, карбонильной группы, карбоксилатной группы, карбоксильной группы, цианатогруппы, цианогруппы, циклоалкенильной группы, циклоалкильной группы, диалкиламинокарбонильной группы, диалкиламиногруппы, гуанидиногруппы, гуанильной группы, гетероарилалкоксигруппы, гетероарилалкильной группы, гетероарильной группы, гетероарилкарбонильной группы, гетероарилоксигруппы, гетероциклической группы, гидроксиаминогруппы, гидроксигруппы, иминогруппы, изоцианатогруппы, изоцианогруппы, меркаптогруппы, нитрогруппы, оксогруппы, пергалогеналкенильной группы, пергалогеналкоксигруппы, пергалогеналкильной группы, пергалогеналкинильной группы, пергалогенарилалкильной группы, пергалогенарильной группы, пергалогенциклоалкильной группы, фосфатной группы, фосфиновой группы, фосфогруппы, сульфатной группы, сульфогруппы, сульфонильной группы, их окисленной формы или их комбинации; их окисленной формы или их комбинации. Возможны окисленные формы групп.
Необходимо понимать, что термины одновалентный и двухвалентный в большинстве случаев относятся к частицам радикалов, полученным при отщеплении одного или большего количества протонов или других атомов от исходной группы или молекулы. Например, метальная группа (-СН3) представляет собой одновалентную форму, радикал или остаток метана. Подобным образом, метиленовая группа(-СН2-) представляет собой двухвалентную форму, радикал или остаток метана. Эти термины используются для удобства при описании различных структур и формул в данном документе, и их не следует рассматривать как ограничивающие конкретный синтетический путь.
В некоторых вариантах осуществления изобретения соединение может входить в смесь диастереомеров. Если необходимо, диастереомеры можно разделять, воспользовавшись их различными физическими свойствами, как, например, с использованием или перекристаллизации, или хроматографии, или их комбинации. Перекристаллизацию можно выполнять в таких органических растворителях, как, но не ограничиваясь ими, пентан, гексан, циклогексан, толуол, бензол, хлорбутан, дихлорметан, диэтиловый эфир, тетрагидрофуран, диметоксиэтан, ацетонитрил, метанол, этанол или бутанол, или в комбинации органических растворителей с водой или без нее. Хроматографию можно выполнять с использованием твердой фазы на основе силикагеля или оксида алюминия, элюируя смесью органических растворителей с кислотными или основными модификаторами, такими как триэтиламин, водный раствор аммиака, уксусная кислота или водная соляная кислота, или без них.
В некоторых вариантах осуществления изобретения соединения пригодны для лечения и/или профилактики заболеваний или расстройств, характеризующихся микобактериальной активностью или инфекцией. Микобактерии могут быть патогенными или непатогенными. Микобактерии могут быть грамположительными или грамотрицательными.
В некоторых вариантах осуществления изобретения предложена композиция, которая содержит одно или большее количество соединений и необязательно физиологически приемлемый носитель.
В некоторых вариантах осуществления изобретения предложен способ, который включает в себя введение соединения или композиции субъекту, нуждающемуся в этом, для лечения субъекта.
В некоторых вариантах осуществления изобретения соединения, композиции и способы пригодны для лечения людей (или иммунокомпетентных, или и со сниженным иммунитетом, или и тех и других) и животных от туберкулезных, лепроматозных и нетуберкулезных микобактерии. Неограничивающие примеры этих бактерий включают в себя, но не ограничиваясь ими, следующие виды и штаммы: туберкулезные микобактерии, например М tuberculosis, М. bovis, М. africanum, М. microti, М. canetti; лепроматозные микобактерии, например М. leprae, М. lepromatosis; нетуберкулезные микобактерии, например М. abscessus, комплекс М. abcessus, М. avium, М. intracellularae, комплекс М. avium, М. kansasii, М. malmoense, М. xenopi, М. malmoense, М. flavences, М scrofulaceum, М. chelonae, М. peregrinum, М. haemophilum, М. fortuitum, М. marinum, М. ulcerans, М. gordonae, М, haemophilum, М. mucogenicum, М. nonchromogenicum, М. terrae, комплекс М. terrae, М. asiaticum, М. celatum, М. shimoidei, М. simiae, М. smegmatis, М. szulgai, М. celatum, М. conspicuum, М. genavense, М. immunogenum, М. xenopi.
В некоторых вариантах осуществления изобретения соединения, композиции и способы пригодны для лечения людей (как иммунокомпетентных, так и со сниженным иммунитетом) и животных от инфекционных заболеваний, не вызванных микобактериями.
В некоторых вариантах осуществления изобретения известно или предполагается, что субъекту необходимо лечение одного или большего количества заболеваний, связанных с непатогенным микобактериальным штаммом М. smegmatis, М. vaccae, М. aurum или их комбинацией.
В некоторых вариантах осуществления изобретения известно или предполагается, что субъекту необходимо лечение одного или большего количества заболеваний, связанных с грамположительными бактериями S. aureus, М. luteus или их комбинацией.
В некоторых вариантах осуществления изобретения известно или предполагается, что субъекту необходимо лечение одного или большего количества заболеваний, связанных с грамотрицательными бактериями P. aeruginosa, A. baumanii или их комбинацией.
В некоторых вариантах осуществления изобретения известно или предполагается, что субъекту необходимо лечение одного или большего количества заболеваний, связанных с патогенным микобактериальным штаммом М. tuberculosis, М. bovis, М. marinum, М. kansasaii, H37Rv, М. africanum, М. canetti, М. caprae, М. microti, М. mungi, М. pinnipedii, М. leprae, М. avium, микобактериальным туберкулезным комплексом, туберкулеза или их комбинации.
В некоторых вариантах осуществления изобретения известно или предполагается, что субъекту необходимо лечение одного или большего количества заболеваний, связанных с непатогенным микобактериальным штаммом М. smegmatis, М. vaccae, М. aurum, грамположительными бактериями S. aureus, М. luteus, грамотрицательными бактериями Р. aeruginosa, A. baumanii, патогенными микобактериальным штаммом М. tuberculosis, М. bovis, М. marinum, М. kansasaii, H37Rv, М. africanum, М. canetti, М. caprae, М. microti, М. mungi, М. pinnipedii, М. avium, микобактериальным туберкулезным комплексом, туберкулеза или их комбинации.
В некоторых вариантах осуществления изобретения предложен способ, который включает в себя уничтожение или ингибирование роста популяции одного или большего количества из непатогенного микобактериального штамма М. smegmatis, М. vaccae, М. aurum, грамположительных бактерий S. aureus, М. luteus, грамотрицательных бактерий P. aeruginosa, А. baumanii, патогенного микобактериального штамма М. tuberculosis, М. bovis, М. marinum, М. kansasaii, H37Rv, М africanum, М. canetti, М. caprae, М. microti, М. mungi, М. pinnipedii, М. avium, микобактериального туберкулезного комплекса, бактерий, способных вызывать туберкулез, или их комбинации путем приведения в контакт одного или большего количества членов указанной популяции с соединением или композицией.
В некоторых вариантах осуществления изобретения соединения, композиции и способы пригодны для применения или лечения отдельно или в комбинации с одним или большим количеством дополнительных способов лечения, например или одновременно, или с отсроченным введением.
В некоторых вариантах осуществления изобретения соединения, композиции и способы пригодны для применения в комбинации с одним или большим количеством дополнительных способов лечения с использованием противомикробных агентов, например, включая изониазид, этамбутол, рифампин, рифабутин, аминогликозиды (например, стрептомицин, амикацин, тобрамицин), макролиды (например, азитромицин, кларитромицин), хинолоны (напимер, офлоксацин, ципрофлоксацин, моксифлоксацин), тетрациклины (например, доксициклин, миноциклин), сульфонамиды и их комбинации (например, сульфонамиды, триметоприм/ сульфаметоксазол), противомикробные агенты, содержащие бета-лактам (в том числе пенициллины и цефалоспорины), бензофураны (например, нитрофурантоин), оксазолидиноны (например, линезолид), гликопептиды (например, ванкомицин), липопептиды (например, даптомицин), стрептограмины (например, квинпристин/дальфопристин), плевромутилины (например, ретапамулин), полимиксины (например, колистин), липогликопептиды (например, телаванцин), глицилциклины (например, тигециклин), полиеновые противогрибковые агенты (например, амфотерицин В), противогрибковые агенты на основе имидазола (например, кетоконазол), противогрибковые агенты на основе аллиламинов (например, аморолфин), противогрибковые агенты на основе триазола (например, вориконазол), противогрибковые агенты на основе тиазола (например, абафунгин), противогрибковые агенты на основе эхинокандинов (например, анидулафунгин), клофазимин и тому подобное или другие противомикробные агенты (например, противомалярийные, противогельминтные, противопротозойные агенты), ингибиторы цитохрома Р450 (CYP), 1-аминобензотриазол (АВТ), циметидин, амиодарон, эритромицин, флуконазол, миконазол, дильтиазем, верапамил, делавирдин, ампренавир, фосампренавир, кониваптан, ритонавир. Возможны комбинации.
В некоторых вариантах осуществления изобретения, например в случае ТБ, соединение можно вводить субъекту, которому это необходимо, вместе с или в дополнение к одному или более из изониазида, рифампина, рифадина, римактана, этамбутола, миамбутола, пиразинамида, антибиотика, фторхинолона, амикацина, канамицина, капреомицина, бедаквилина, деламанида, РА-824, линезолида, сутезолида или любой их комбинации.
В некоторых вариантах осуществления изобретения соединения, композиции и способы пригодны для применения в качестве единственного агента или в комбинации с другими агентами для лечения воспалительных заболеваний. Противовоспалительные лекарственные средства также можно вводить совместно в процессе лечения. Воспалительные заболевания хорошо известны и, как правило, относятся к, характеризуются, вызывают, обусловлены или находятся под влиянием воспаления. Неограничивающие примеры воспалительных заболеваний или расстройств включают в себя, без ограничения, астму, воспаление легких, ХОБЛ, послеинфекционное воспаление, атеросклероз, боль, дерматит, хронические гранулематозные заболевания, такие как туберкулез, лепру, саркоидоз и силикоз, нефрит, амилоидоз, ревматоидный артрит, анкилозирующий спондилоартрит, хронический бронхит, склеродермию, волчанку, полимиозит, аппендицит, воспалительное заболевание кишечника, язвы, синдром Шегрена, синдром Рейтера, псориаз, воспалительное заболевание тазовых органов, воспалительное заболевание глазницы, тромботическое заболевание и неприемлемые аллергические реакции на стимулы окружающей среды, такие как сумах укореняющийся, цветочная пыльца, укусы насекомых и некоторые пищевые продукты, включая атопический дерматит и контактный дерматит.
В некоторых вариантах осуществления изобретения субъект представляет собой млекопитающее, человека, домашний скот, корову, свинью, лошадь или тому подобное.
В некоторых вариантах осуществления изобретения популяция присутствует на поверхности, и соединение или композицию приводят в контакт с указанной поверхностью.
В некоторых вариантах осуществления изобретения соединение можно вводить пациенту-человеку как таковое или в фармацевтических композициях, где оно может быть смешано с пригодными носителями или вспомогательными веществами в дозах для лечения или ослабления различных патологических состояний, которые характеризуются микобактериальной активностью или инфекцией. Терапевтически эффективная доза может относиться к количеству соединения, достаточному для ингибирования микобактериальной активности или инфекции, понятно, что такое ингибирование может осуществляться при различных концентрациях, так что специалист в данной области техники может определить требуемую дозировку соединения, необходимую для ингибирования целевой микобактериальной активности или инфекции. Терапевтически эффективные дозы можно вводить отдельно или в виде смежной терапии в комбинации с другими способами лечения. Некоторые примеры методик изготовления составов и введения соединений можно найти в  Pharmaceutical Sciences, 18th Edition, A.R. Gennaro, Ed., Mack Publishing Co., Easton, PA (1990).
Pharmaceutical Sciences, 18th Edition, A.R. Gennaro, Ed., Mack Publishing Co., Easton, PA (1990).
Пригодные пути введения, которые, как предполагается, не являются ограничивающими, могут включать в себя, например, пероральный, внутривенный, ингаляционный, внутрибрюшинный, ректальный, трансмукозальный, трансбуккальный, внутривлагалищный, через кишечник, местный, внутрикожный, парентеральную доставку, внутримышечную, подкожную, интрамедуллярную инъекцию, интратекальный, прямой интравентрикулярный, внутривенный, внутрибрюшинный, интраназальный, интраокулярный, перитонеальный, плевральный и необязательно в виде депо-препаратов или составов с замедленным высвобождением. Кроме того, можно вводить соединение в системе направленной доставки лекарственного средства, например в липосоме.
Соединения можно вводить системно (например, пероральное, внутривенное, ингаляционное, внутрибрюшинное, ректальное) или локально (например, местное, внутрикожное, интратекальное, перитонеальное, плевральное, внутриглазное, внутрипузырное, внутривлагалищное введение или доставка непосредственно к участку инфекции).
Фармацевтические композиции и соединения могут быть произведены способом, который сам по себе известен, например, с помощью способов традиционного смешивания, растворения, дражирования, растирания в порошок, эмульгации, инкапсулирования, захватывания или лиофилизации. Таким образом, фармацевтические композиции могут быть составлены традиционным способом с использованием одного или большего количества физиологически приемлемых носителей, включающих в себя вспомогательные вещества и добавки, облегчающие переработку активных соединений в препараты, которые могут быть использованы фармацевтически. Подходящий состав может зависеть от выбранного способа введения.
В композиции может содержаться любая комбинация одного или большего количества соединений по настоящему изобретению, их солей, их резонансных форм, пролекарств, метаболитов, изотопно меченых соединений, таутомеров, изомеров и/или атропоизомеров.
Для введения путем инъекции соединения могут быть включены в состав водных растворов, предпочтительно в физиологически совместимых буферных растворах, таких как раствор Хэнкса, раствор Рингера или физиологический солевой буферный раствор. Для трансмукозального введения в составе применяются проникающие вещества, подходящие для барьера, сквозь который будет осуществляться проникновение. Такие проникающие вещества известны в данной области техники.
Для перорального введения соединения можно легко вводить в состав путем объединения активных соединений с фармацевтически приемлемыми носителями, хорошо известными в данной области техники. Такие носители обеспечивают возможность введения соединений в состав таблеток, пилюль, драже, капсул, жидкостей, гелей, сиропов, взвесей, суспензий и тому подобного для перорального приема пациентом, которого подвергают лечению. Фармацевтические препараты для перорального применения могут быть получены путем объединения соединения с твердым вспомогательным веществом, необязательно с помолом полученной смеси и изготовлением смеси гранул, после добавления подходящих добавок, если это желательно, для получения таблеток или ядер драже. Подходящие вспомогательные вещества включают в себя, но не ограничиваясь ими, наполнители, такие как сахара, включая лактозу, сахарозу, маннит или сорбит; целлюлозные препараты, такие как, например, кукурузный крахмал, пшеничный крахмал, рисовый крахмал, картофельный крахмал, желатин, трагакантовая камедь, метилцеллюлоза, гидроксипропилметилцеллюлоза, карбоксиметилцеллюлоза натрия, и/или поливинилпирролидон (ПВП). Если необходимо, могут быть добавлены разрыхляющие агенты, такие как поперечно сшитый поливинилпирролидон, агар или альгиновая кислота или ее соль, такая как альгинат натрия.
Ядра драже покрывают соответствующими покрытиями. Для этой цели можно использовать концентрированные растворы сахаров, которые могут необязательно содержать гуммиарабик, тальк, поливинилпирролидон, гель карбопола, полиэтиленгликоль и/или диоксид титана, растворы глазурей и пригодные органические растворители или смеси растворителей. В покрытия таблеток или драже можно добавлять красящие вещества или пигменты для идентификации или определения различных комбинаций доз активного соединения.
Фармацевтические препараты, которые могут быть использованы перорально, включают в себя твердые капсулы из желатина, а также мягкие закрытые капсулы из желатина и пластификатора, такого как глицерин или сорбит. Твердые капсулы могут содержать активные ингредиенты в смеси с наполнителем, таким как лактоза, связывающими веществами, такими как крахмалы, и/или смазывающими веществами, такими как тальк или стеарат магния, и необязательно со стабилизаторами. В мягких капсулах активные соединения могут быть растворены или суспендированы в подходящих жидкостях, таких как жирные масла, жидкий парафин или жидкие полиэтиленгликоли. Дополнительно, могут быть добавлены стабилизаторы. Все составы для перорального введения должны быть приготовлены в виде дозировок, пригодных для такого введения.
Для трансбуккального введения композиции могут иметь форму таблеток или пастилок, приготовленных традиционным способом.
Для введения с помощью ингаляции соединения можно традиционно доставлять в виде аэрозольного спрея из упаковок под давлением или распылителя с использованием подходящего распыляющего вещества, например дихлордифторметана, трихлорфторметана, дихлортетрафторэтана, диоксида углерода или другого подходящего газа. В случае аэрозоля под давлением, единица дозирования может быть определена путем обеспечения клапана для доставки дозированного количества. Для использования в ингаляторе или инсуффляторе могут быть разработаны капсулы и картриджи из, например, желатина, содержащие порошкообразную смесь соединения и подходящую порошковую основу, такую как лактоза или крахмал.
Соединения могут быть введены в состав для парентерального введения посредством инъекции, такой как болюсная инъекция или непрерывная инфузия. Составы для инъекции могут быть представлены в единичной лекарственной форме, например, в ампулах или в многодозовых контейнерах, с добавленным консервантом. Композиции могут быть в таких формах, как суспензии, растворы или эмульсии в масляных или водных носителях, и могут содержать вспомогательные агенты, такие как суспендирующие, стабилизирующие и/или диспергирующие агенты.
Фармацевтические составы для парентерального введения включают в себя водные растворы активных соединений в водорастворимой форме. Дополнительно, суспензии активных соединений могут быть получены в виде подходящих масляных суспензий для инъекций. Подходящие липофильные растворители или среды включают в себя жирные масла, такие как кунжутное масло, или синтетические сложные эфиры жирных кислот, такие как этилолеат, или триглицериды, или липосомы. Водные суспензии для инъекций могут содержать вещества, которые увеличивают вязкость суспензии, такие как полиионный блок-(со)полимер, карбоксиметилцеллюлоза натрия, сорбит или декстран. Суспензия также может необязательно содержать подходящие стабилизаторы или агенты, которые увеличивают растворимость соединений.
В альтернативном варианте активный ингредиент может быть в форме порошка для разбавления подходящей средой, например стерильной апирогенной водой, перед использованием.
Соединения также могут быть введены в состав ректальных композиций, таких как суппозитории или удерживающие клизмы, например, содержащих традиционные основы для суппозиториев, такие как масло какао или другие глицериды.
Соединения также могут быть введены в состав депо-препарата. Такие длительно действующие составы можно вводить путем имплантации (например, подкожно или внутримышечно) или путем внутримышечной инъекции. Таким образом, например, соединения могут быть введены в состав с подходящими полимерными или гидрофобными материалами (например, в виде эмульсии в приемлемом масле) или ионообменными смолами или разработаны в виде умеренно растворимых производных, например, в виде умеренно растворимой соли.
Фармацевтические композиции могут также содержать пригодные твердо- или гель-фазные носители или вспомогательные вещества. Примеры таких носителей или вспомогательных веществ включают в себя, но не ограничиваясь ими, карбонат кальция, фосфат кальция, различные сахара, крахмалы, производные целлюлозы, желатин или полимеры, такие как полиэтиленгликоли.
В некоторых вариантах осуществления изобретения соединения могут быть представлены в виде солей с фармацевтически совместимыми противоионами. Фармацевтически совместимые соли могут быть получены с многими кислотами, включая, но не ограничиваясь ими, соляную, серную, уксусную, молочную, винную, яблочную, янтарную и т.д.; или основаниями. Неограничивающие примеры фармацевтически приемлемых солей включают в себя соли натрия, калия, лития, кальция, магния, железа, цинка, гидрохлоридные, гидробромидные, гидроиодидные, ацетатные, цитратные, тартратные и малеатные соли и тому подобное.
Как правило, фармацевтические композиции содержат активное соединение в количестве, эффективном для достижения предполагаемой задачи. В одном варианте осуществления изобретения терапевтически эффективное количество означает количество, которое является эффективным для профилактики или ингибирования развития или прогрессирования заболевания, которое характеризуется микобактериальной инфекцией или активностью, у субъекта, которого подвергают лечению. Определение эффективных количеств находится в пределах возможностей специалистов в данной области техники, с учетом описания, представленного в данном документе.
Любая группа, описанная в данном документе, или явно обозначенная как «группа», или не обозначенная таким образом (например, с использованием таких терминов, как «алкил», «арил», «ароил» и тому подобное, отдельно) может быть необязательно и независимо неразветвленной или разветвленной; может быть необязательно и независимо замещенной одним или большим количеством независимых замещающих групп; может быть необязательно и независимо присоединена непосредственно к соответствующей исходной структуре; может быть необязательно и независимо непрямо присоединена к соответствующей исходной структуре посредством одной или большего количества промежуточных замещающих групп; и/или может иметь один или более чем один атом, которые необязательно и независимо заменены одним или большим количеством гетероатомов.
Использование единственного числа в сочетании с термином «содержащий» в формуле изобретения и/или описании может означать «один», но оно также соответствует значению «один или большее количество», «по меньшей мере один» и «один или более чем один».
Термин «около» используется для указания того, что значение включает в себя стандартное отклонение ошибки.
Термин «или» означает «и/или», если явно не указано, что он обозначает только альтернативные варианты или альтернативные варианты являются взаимоисключающими, хотя описание поддерживает определение, которое относится только к альтернативным вариантам и «и/или».
Слова «содержащий» (и любая форма слова содержащий, такая как «содержать» и «содержит»), «имеющий» (и любая форма слова имеющий, такая как «иметь» или «имеет»), «включающий в себя» (и любая форма фразы включающий в себя, такая как «включает в себя» и «включать в себя») или «вмещающий» (и любая форма слова вмещающий, такая как «вмещает» и «вмещать») являются охватывающими или неисчерпывающими и не исключают дополнительных неперечисленных элементов или стадий способов.
Другие варианты осуществления изобретения рассматриваются повсеместно в этой заявке. Любой вариант осуществления изобретения, который рассматривается по отношению к одному аспекту изобретения, применим к другим вариантам осуществления изобретения, равно как и наоборот. Понятно, что каждый вариант осуществления изобретения, описанный в данном документе, и любая очевидная его разновидность применимы ко всем вариантам осуществления изобретения. Учитывая описание, представленное в данном документе, в сочетании со знаниями специалиста в области техники, к которой данное изобретение принадлежит, любой вариант осуществления изобретения, описанный в данном документе, можно легко осуществить и/или дополнительно реализовать в отношении любого применения, способа, соединения, композиции, набора, их очевидного варианта или их любой комбинации.
ПРИМЕРЫ
Примеры в данном документе представлены для иллюстрации и не предназначены для ограничения, если не указано иное.
Соединения по настоящему изобретению имеют высокую эффективность, хорошие фармакокинетические свойства и сниженную токсичность. Например, было установлено, что ND-10823 обладает дозолимитирующей токсичностью, составляющей для мышей 100 мг/кг, что ограничивает его возможную эффективность, поскольку мыши погибнут при дозах выше 100 мг/кг. Однако добавление фтора в положение 3 увеличивает активность и значительно уменьшает in vivo токсичность до 250 мг/кг для ND-10890.
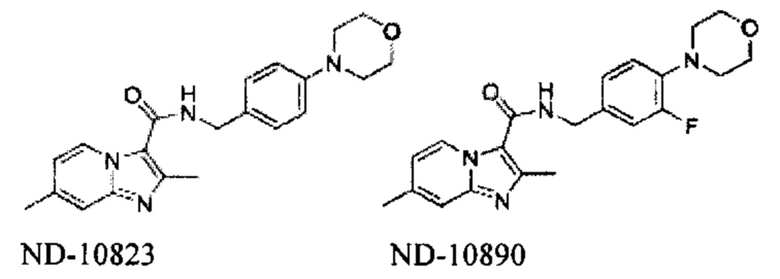
МИК МБТ=0,3 - 1,3 мкМ МИК МБТ=0,08 - 0,4 мкМ
МПД=100 мг/кг (мыши) МПД=250 мг/кг (мыши)
Другие соединения, содержащие 3-фтор-фрагмент, продемонстрировали высокую in vitro активность (наномолярный диапазон) и высокую in vivo безопасность (например, все ND-11543, ND-11544, ND-11598, ND-11622 характеризовались МПД≥250 мг/кг).
На Фиг. 1 изображена in vivo переносимость двух иллюстративных соединений ND-11598 и ND-11622, вводимых перорально в дозе 100 мг/кг в течение двух недель и перорально в дозе 250 мг/кг в течение одной недели. Мыши не продемонстрировали признаков недомогания, потери веса, и все выжили после курса лечения. Это свидетельствует о том, что максимальная переносимая доза для этих соединений составляет >250 мг/кг.
Результаты, представленные на Фиг. 2, подтверждают in vivo эффективность ND-10885 у мышей, инфицированных Mycobacterium avium 101 при введении перорально в дозах 25 мг/кг и 100 мг/кг. Вставка А представляет собой log 10 уменьшения колониеобразующих единиц (КОЕ) бактерий в легких при лечении ND-10885 (при 25 и 100 мг/кг), рифампицином (RMP, 20 мг/кг) и комбинацией ND-10885 (100 мг/кг) и рифампицина (20 мг/кг). Вставка В представляет собой log 10 уменьшения колониеобразующих единиц (КОЕ) бактерий в селезенке при лечении ND-10885 (при 25 и 100 мг/кг), рифампицином (RMP, 20 мг/кг) и комбинацией ND-10885 (100 мг/кг) и рифампицина (20 мг/кг). Вставка С представляет собой log 10 уменьшения колониеобразующих единиц (КОЕ) бактерий в печени при лечении ND-10885 (при 25 и 100 мг/кг), рифампицином (RMP, 20 мг/кг) и комбинацией ND-10885 (100 мг/кг) и рифампицина (20 мг/кг). Статистически подтверждено улучшение эффективности комбинации лекарственных средств в легких и селезенке.
Результаты, представленные на Фиг. 3, демонстрируют in vitro активность соединений против различных серотипов Mycobacterium avium и штамма М. avium, устойчивого к гентамицину. Рифампин включен в качестве положительного контроля, а ДМСО - в качестве отрицательного контроля. Значения МИК представлены в мкг/мл и определены с использованием красителя резазурина.
Результаты, представленные на Фиг. 4, демонстрируют in vitro активность соединений против Mycobacterium intracellular (АТСС 13950). Рифампин, кларитромицин, этамбутол и азитромицин включены в качестве положительных контролей, а ДМСО - в качестве отрицательного контроля. Значения МИК представлены в мкг/мл и определены с использованием красителя резазурина.
Результаты, представленные на Фиг. 5, демонстрируют in vitro активность соединений против клинических штаммов Mycobacterium avium, а кларитромицин использовали в качестве положительного контроля. Значения МИК представлены в мкг/мл и определены с использованием красителя 3-(4,5-диметилтиазол-2-ил)-2,5-дифенилтетразолия бромида (МТТ).
Результаты, представленные на Фиг. 6, демонстрируют in vitro активность соединений против клинических штаммов Mycobacterium kansasii; кларитромицин использовали в качестве положительного контроля. Значения МИК представлены в мкг/мл и определены с использованием красителя 3-(4,5-диметилтиазол-2-ил)-2,5-дифенилтетразолия бромида (МТТ).
Результаты, представленные на Фиг. 7, демонстрируют взаимоусиливающее действие ND-11176 и клофазимина против Mycobacterium abscessus при оценке методом «шахматного анализа». Кларитромицин использовали в качестве положительного контроля. Значения МИК представлены в мкг/мл и определены с использованием красителя резазурина. На фигуре темные клетки представляют мертвых, более светлые клетки представляют живых.
На Фиг. 8 изображена таблица соединений и результаты скрининга соединений против Mycobacterium tuberculosis (МБТ) H37Rv в различных средах (GAS, 7Н12), в условиях с низким содержанием кислорода (LORA), токсичность к клеткам Vero, а также активность против Mycobacterium avium (101 и 2151) и Mycobacterium intracellulare. Краситель резазурин использовали для определения значений МИК по отношению к М. avium и М. intracellular, а МАВА использовали для определения МИК по отношению к МБТ.
Анализы
In vitro активность по отношению к МБТ - H37Rv оценивали как в среде GAS (глицерин-соль аланина), так и в среде 7Н12, при этом метаболическую активность измеряли с использованием анализа в микропланшете с красителем аламаровым синим (Alamar Blue) (МАВА) по протоколам, описанным Cho, S.; Lee, Н.S.; Franzblau, S.G. в статье "Microplate Alamar Blue Assay (MABA) and Low Oxygen Recovery Assay (LORA) for Mycobacterium tuberculosis." Mycobacteria Protocols 2015, 281-292. Активность против нереплицирующихся (латентных) МБТ оценивали, регистрируя люминесценцию, с использованием анализа выживаемости в условиях с низким содержанием кислорода (LORA).
Описание анализа в микропланшете с красителем аламаровым синим (МАВА) для ТБ (GAS, 7Н12) для определения значений МИК90 по отношению к реплицирующимся ТБ.
Значения МИК исследуемых соединений по отношению к МБТ H37Rv (АТСС №27294) оценивали с использованием МАВА (Cho, S.; Lee, Н.S.; Franzblau, S.G. "Microplate Alamar Blue Assay (MABA) and Low Oxygen Recovery Assay (LORA) for Mycobacterium tuberculosis." Mycobacteria Protocols 2015, 281-292) с использованием рифампина и РА-824 в качестве положительных контролей. Исходные растворы соединений получали в ДМСО с концентрацией 128 мкМ, а конечные исследуемые концентрации были в интервале от 128 мкМ до 0,5 мкМ. Двукратные разбавления соединений выполняли в среде, содержащей глицерин / соль аланина, в объеме 100 мкл в 96-луночных микропланшетах (BD Optilux™, 96-луночные микропланшеты, черное/прозрачное плоское дно) для анализа GAS (Collins, L., and Franzblau, S.G. (1997) Microplate alamar blue assay versus BACTEC 460 system for high-throughput screening of compounds against Mycobacterium tuberculosis and Mycobacterium avium. Antimicrob. Agents Chemother. 41, 1004-1009), в железодефицитной среде, содержащей глицерин / соль аланина с 20% добавленного Твина 80 в анализе GAST и в среде Middlebrook 7Н12 (бульон 7Н9, содержащий 0,1% масса/объем казитона, 5,6 мкг/мл пальмитиновой кислоты, 5 мг/мл бычьего сывороточного альбумина, 4 мг/мл каталазы; De Voss, J.J., Rutter, K., Schroeder, В.G., Su, H., Zhu, Y., and Barry, С.E. (2000) The salicylate-derived mycobactin siderophores of Mycobacterium tuberculosis are essential for growth in macrophages. Proc. Nat. Acad. Sci. U.S.A. 97, 1252-1257). В объеме 100 мкл в 96-луночных микропланшетах (BD Optilux™, 96-луночные микропланшеты, черное/прозрачное плоское дно) для анализа 7Н12. Культуры ТБ (100 мкл инокулята 2×105 КОЕ/мл) добавляли к средам, что давало конечный объем анализа 200 мкл. Планшеты инкубировали при 37°С. На седьмой день инкубации в лунки исследуемых планшетов добавляли 12,5 мкл 20%-ного Твина 80 и 20 мкл красителя аламаровый синий (Invitrogen BioSource™). После инкубации при 37°С в течение 16-24 ч измеряли флуоресценцию в лунках при 530 нм (возбуждение) и 590 нм (эмиссия). Величины МИК определяли как наименьшую концентрацию, вызывающую уменьшение флуоресценции на ≥90% по отношению к среднему значению для контрольных образцов, содержащих только реплицирующиеся бактерии.
Описание анализа MDR- и XDR-МБТ
МИК определяли, как описано в Wong et al. (Wong, S.Y., Lee J.S., Kwak, H.K., Via, L.E., Boshoff, H.I., and Barry, С.E. 3rd. (2011) Antimicrob Agents Chemother. 55, 2515-22).
Вкратце, штаммы M. tuberculosis выращивали в бульоне Middlebrook 7Н9 (Becton Dickinson, Нью-Джерси), дополненном 10% альбумина/декстрозы/каталазы, 0,05% Твина 80 и 0,2% глицерина так, чтобы оптическая плотность при 650 нм составляла 0,25. Клетки разбавляли в 1000 раз в указанной выше среде. Соединения добавляли в первый вертикальный ряд круглодонного 96-луночного планшета в трех повторениях, а затем последовательно разбавляли в 2 раза в оставшихся рядах, используя дополненную среду Middlebrook 7Н9 в качестве разбавителя. Одинаковый объем разбавленной суспензии клеток добавляли в каждую лунку, чтобы конечный объем составлял 100 мкл на лунку. Планшеты инкубировали при 37°С в течение 14 дней, после чего визуально изучали рост клеток. Величину МИК определяли как наиболее низкую концентрацию лекарственного средства, которая полностью ингибирует визуально определяемый рост.
Описание (Falzari, K., Zhou, Z, Pan, D., Liu, H., Hongmanee, P., and Franzblau, S.G. (2005) In Vitro and In Vivo Activities of Macrolide Derivatives against Mycobacterium tuberculosis. Antimicrob Agents Chemother. 49, 1447-1454) анализа на цитотоксичность в клеточной линии VERO для определения величин IC50.
Образцы растворяли в концентрации 12,8 мМ в ДМСО. Разбавления в геометрической прогрессии (трехкратные) выполняли в среде для роста MEM (Gibco, Гранд-Айленд, Нью-Йорк), содержащей 10% фетальной бычьей сыворотки S5 (HyClone, Логан, Юта), 25 мМ N-{2-гидроксиэтил)-пиперазин-N'-2-этансульфоновой кислоты (HEPES, Gibco), 0,2% NaHCO3 (Gibco), и 2 мМ глутамина (Irvine Scientific, Санта-Ана, Калифорния). Конечные концентрации ДМСО не превышали 1% объем/объем. Разбавленные растворы лекарственного вещества наносили в двух повторениях на 96-луночные планшеты для тканевых культур (Becton Dickinson Labware, Линкольн Парк, Нью-Джерси) в объеме 50 мкл на лунку. Равный объем, содержащий 5×105 клеток VERO в лог-фазе (клетки почки африканской зеленой мартышки, CCL-81; Американская коллекция типовых культур, Роквилл, Мэриленд), добавляли в каждую лунку и культуры инкубировали при 37°С в атмосфере, содержащей 5% CO2. Через 72 ч определяли жизнеспособность клеток с использованием водного нерадиоактивного анализа пролиферации клеток CellTiter 96 (Promega Corp., Мэдисон, Висконсин) в соответствии с инструкциями производителя. Затем регистрировали поглощение при 490 нм с использованием многорежимного анализатора для планшетов Victor (PerkinElmer). Значения IC50 (концентрация ингибирования на 50%) определяли с использованием программы аппроксимации кривой по точкам.
In vitro активность по отношению к MAC. Одиннадцать штаммов М. avium подвергали воздействию соединений в течение 3 дней и измеряли метаболическую активность и бактериостатическую/бактерицидную активность с помощью резазурина. Это осуществляли в соответствии с методиками, описанными в J. Antimicrob. Chemother. (2007) 60(1): 152-155.
Эффективность соединений типа ND-10890 против инфекций MAC продемонстрирована на мышиной модели инфекции, см. в ANTIMICROBIAL AGENTS AND CHEMOTHERAPY, 1995, 39(8), 1647-1654 рассмотрение модели инфекций MAC и в Antimicrob Agents Chemother. 1992, 36(11): 2413-7 типовой эксперимент (выполненный с кларитромицином). В двухнедельном эксперименте с инфицированным мышами Balb/c, которым вводили дозы 25 мг и 100 мг ND-10890, наблюдалось уменьшение на >2 log10 КОЕ количества М. avium в легких мышей, получавших лечение. В этом случае наблюдалось большее уменьшение количества бактерий, чем для контрольного рифампицина (1,8 log10 КОЕ). Комбинированная терапия с использованием ND-10890 (100 мг) и рифампицина (20 мг) была еще более эффективной с практически полным устранением бактерий М. avium (уменьшение на ~3 log10 КОЕ). Эти данные свидетельствуют о том, что эти соединения будут эффективными при лечении микобактериальных инфекций.
Для серии ключевых соединений изучали эффективность против ряда различных организмов, которые включают в себя пять грамположительных штаммов (Bacillus subtilis, Staphylococcus aureus, Staphylococcus aureus, устойчивый к метициллину (MRSA), Enterococcus Faecalis, устойчивый к ванкомицину (VRE), Mycobacterium vaccae), два грамотрицательных штамма (E. coli, Pseudomonas aeruginosa), дрожжи (Sporobolomyces salmonicolor) и грибы (Candida albicans и Penicillium notatum). Примечательно, что этот класс был слабо эффективен против всех изученных контрольных организмов за исключением хорошей активности против М. vaccae, а также других микобактерий. Было установлено, что в отношении ряда штаммов нетуберкулезных микобактерий (HTM, NTM) этот класс представляет собой возможные ингибиторы М. avium, М. bovis BCG, M. kansasii (<0,08 мМ) и наиболее слабо М. abscessus, М. chelonae, М. marinum и М. smegmatis (>10 мМ). Эти соединения характеризуются наномолярной активностью по отношению к монорезистентным к одному лекарственному средству, мультирезистентным (MDR) и с расширенной резистентностью (XDR). МБТ, Исследования механизма действия (МОА) посредством образования мутантов МБТ показали высокую частоту спонтанных мутаций (>10-8) и то, что эти соединения воздействуют на комплекс bc1 дыхательной цепи (комплекс III). Скрининг ключевых соединений проводили по отношению к шести клеточным линиям млекопитающих (РС-3, MCF-7, Huvec, K-562, HeLa и VERO), и они не продемонстрировали токсического действия, IC50>50 мкМ.
Синтез:
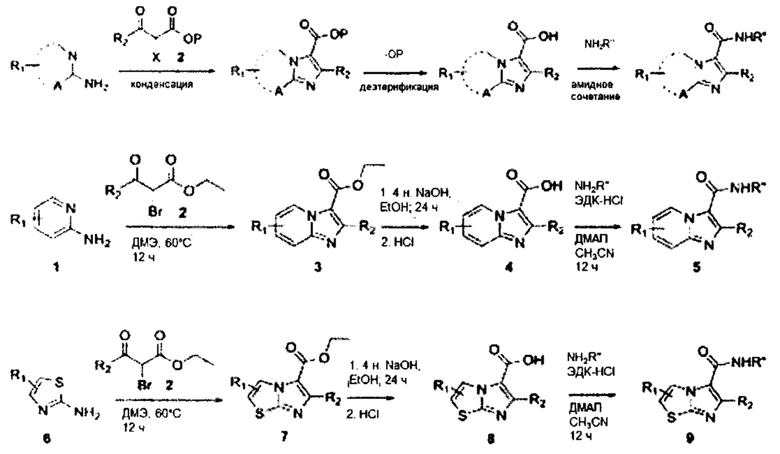
Общая схема синтеза включает в себя, во-первых, образование гетероциклического остова в виде метилового или этилового сложного эфира путем нагревания 2-аминопиридина 1 или 2-аминотиазола 6 с α-галогенкетоном 2 (т.е. 2-бромацетоацетатом или 2-хлорацетоацетатом) в пригодном растворителе, таком как диметоксиэтан или этанол. Деэтерификация с помощью основания (LiOH, NaOH, KOH и т.д.) в пригодном спиртовом растворителе (МеОН, EtOH) с последующим подкислением HCl дает центральный фрагмент гетероциклическую карбоновую кислоту (4 и 8). Гетероциклические карбоновые кислоты (4 или 8) потом сочетают с различными аминами (NH2R") с помощью любого способа образования амидов, как описано в Bodansky, М., "Principles of Peptide Synthesis", Springer-Verlag, 1988, что дает требуемые амиды 5 и 9.
Различные реагенты со структурой 2 коммерчески доступны, например этил-2-хлорацетоацетат [CAS: 609-15-4, Sigma-Aldrich] и этил-2-бром-3-оксобутаноат [CAS: 609-13-2, Ark Pharm], тогда как другие можно получить или с помощью способа, описанного в Synthetic Communications, 37(23), 4149-4156; 2007 с использованием N-хлорсукцинимида (NCS, ХСИ) или N-бромсукцинимида (NBS, БСИ) в ДМСО;

или с помощью способов, описанных в Journal of Medicinal Chemistry, 57(12), 5293-5305; 2014 (с использованием БСИ или ХСИ с ацетатом аммония в диэтиловом эфире).
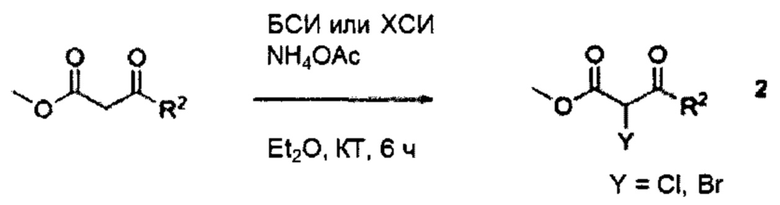
Конкретнее, этил-2-бром-3-оксобутаноат можно получить по следующей методике:
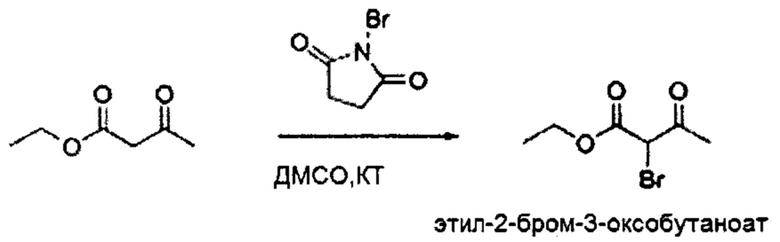
К N-бромсукцинимиду (9,2 г, 49 ммоль) добавляли этилацетоацетат (5,2 мл, 37,7 ммоль), а затем 40 мл сухого ДМСО. Реакционную смесь перемешивали в течение 2 часов при КТ или до того завершения реакции, что определяли с помощью ТСХ (50% гексан : CH2Cl2). Реакционную смесь разбавляли смесью изомеров гексана и органический слой промывали насыщенным раствором NH4Cl (2×), водой, затем органический слой сушили над сульфатом натрия. Осушающий агент удаляли фильтрованием, и после концентрирования в вакууме неочищенный материал очищали на колонке из силикагеля с использованием смеси 50% смесь изомеров гексана : CH2Cl2, что давало этил-2-бром-3-оксобутаноат в виде светло-желтого масла. ИК (для очищенного): 1718, 1462, 1227 см-1; 1H ЯМР (400 МГц, CDCl3): δ м.д. 4,67 (1Н, с), 4,28 (2Н, к, J=7,0 Гц), 2,43 (3Н, с), 1,32 (3Н, т, J=7,0 Гц); 13С ЯМР (50 МГц, CDCl3): δ 197,6, 167,3, 6,8, 54,6, 27,1, 14,2.
Конкретнее, метил-2-бром-3-оксопентаноат можно получить по следующей методике:
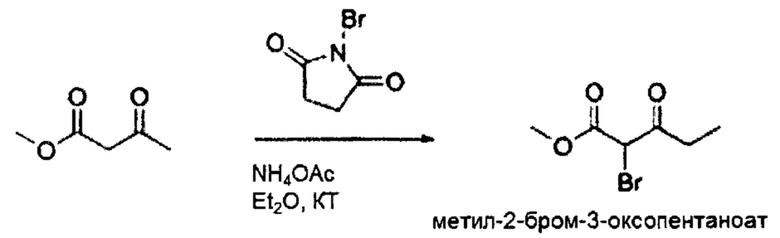
В круглодонной колбе, охлажденной на ледяной бане, смешивали вместе метилпропионилацетат (8,7 мл, 69,2 ммоль), БСИ (13,5 г, 76,1 ммоль) и ацетат аммония (53 мг, 0,7 ммоль) и перемешивали в виде густой взвеси в течение 3 часов. Затем добавляли 25 мл диэтилового эфира и реакционной смеси давали нагреться до комнатной температуры, при этом ее перемешивали в течение 3 часов, пока реакционная смесь становилась белой. После этого реакционную смесь поглощали 100 мл диэтилового эфира, и промывали (3×) водой, насыщенным водным раствором хлорида натрия, и сушили над сульфатом натрия. Осушающий агент отфильтровывали, и органические фазы концентрировали, что давало метил-2-бром-3-оксопентаноат в виде прозрачного масла, 13,45 грамм. 1Н ЯМР (200 МГц, CDCl3): δ м.д. 1,12 (т, J=7,2 Гц, 3Н, СН3СН2), 2,79 (к, J=7,2 Гц, 2Н, СН3СН2), 3,82 (с, 3Н, ОСН3), 4,81 (с, 1H, CHBr).
Общая схема синтеза центральных фрагментов имидазо[1,2-α]пиридин-3-карбоновых кислот (4а, 4b, 4с, 4d) путем сочетания с различными аминами (NH2R") дает в целом:
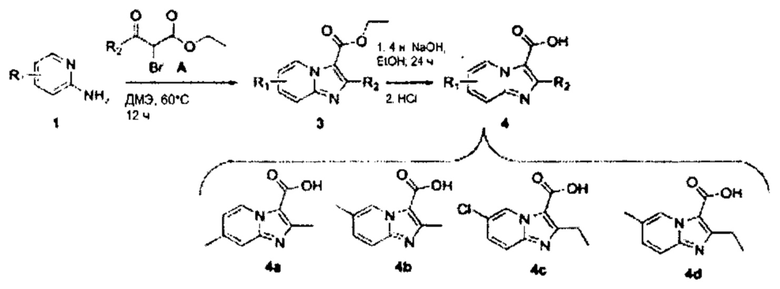
Конкретнее, центральные фрагменты имидазо[1,2-α]пиридин-3-карбоновые кислоты 4а и 4b можно получить с использованием методик, представленных в ACS Med. Chem. Lett., 2013, 4 (7), pp 675-679 и ACS Med. Chem. Lett., 2011, 2 (6), pp. 466-470.
В качестве конкретного примера, 2,7-диметилимидазо[1,2-α]пиридин-3-карбоновую кислоту можно получить следующим образом. 2-Амино-4-пиколин (10,0 г, 91,5 ммоль) и этил-2-хлорацетоацетат (7,93 г, 45,8 ммоль) растворяли в 92 мл 1,2-диметоксиэтана (ДМЭ) и нагревали с обратным холодильником в течение 36 ч. Реакционную смесь фильтровали и твердое вещество (гидрохлоридную соль 2-амино-4-пиколина) собирали и промывали смесью изомеров гексана. Фильтрат концентрировали в вакууме и остаток растворяли в CH2Cl2 и промывали 5%-ным раствором уксусной кислоты (2×) и насыщенным водным раствором хлорида натрия. Органическую фазу собирали, сушили над сульфатом натрия (Na2SO4), фильтровали, а затем концентрировали в вакууме. Полученное неочищенное вещество очищали с помощью хроматографии на колонке из силикагеля с использованием системы растворителей 20% этилацетата: CH2Cl2, что давало 7,8 г (78%) этил-2,7-диметилимидазо[1,2-α]пиридин-3-карбоксилата в виде желтовато-коричневого твердого вещества. Т. пл. 59-61°С; 1Н ЯМР (300 МГц, CDCl3) δ 9,14 (д, J=7,1 Гц, 1Н), 7,34 (с, 1H), 6,78 (дд, J=7,1,1,7 Гц, 1Н), 4,40 (к, J=7,1, 7,1, 7,1 Гц, 2Н), 2,66 (с, 3Н), 2,42 (с, 3Н), 1,42 (т, J=7,1, 7,1 Гц, 3Н). МСВР (ЭИ), М+1 рассчитанное для C12H15N2O2, 219,1155; найденное 219,1128.
Этил-2,7-диметилимидазо[1,2-α]пиридин-3-карбоксилат (6,64 г, 30,4 г) растворяли в 75 мл этанола (95:5) и добавляли 61 мл 1 н. раствора LiOH (61 ммоль). Реакционную смесь перемешивали при нагревании с обратным холодильником в течение 36 ч. После завершения реакционную смесь концентрировали в вакууме практически досуха, и рН доводили до 3 путем медленного добавления 4 н. HCl, при этом охлаждая на ледяной бане. Полученные твердые вещества собирали путем фильтрования и сушили под вакуумом в течение ночи, что давало 3,86 г (67%) 2,7-диметилимидазо[1,2-α]пиридин-3-карбоновой кислоты в виде желтоватого твердого вещества. Т. пл. 180-183°С; 1Н ЯМР (300 МГц, CD3OD) δ 9,52 (д, J=7,1 Гц, 1Н), 7,73 (тд, J=1,8, 0,9, 0,9 Гц, 1Н), 7,48 (дд, J=7,1, 1,3 Гц, 1Н), 2,81 (с, 3Н), 2,63 (с, 3Н). МСВР (ЭИ), М+1 рассчитанное для C10H11N2O2, 191,0815; найденное 191,0837.
Центральный фрагмент 2-этил-6-хлоримидазо[1,2-α]пиридин-3-карбоновую кислоту 4с можно получить по методике, описанной в Journal of Medicinal Chemistry, 57(12), 5293-5305; 2014. Центральный фрагмент 2-этил-6-метилимидазо[1,2-α]пиридин-3-карбоновую кислоту 4d (CAS: 1216036-36-0) можно получить путем модификации вышеуказанной методики, что включает в себя нагревание 2-амино-4-пиколина (CAS: 695-34-1) и метил-2-бром-3-оксопентаноата (CAS: 117481-97-7) в пригодном растворителе (ДМЭ, EtOH) с последующим гидролизом полученного метилового сложного эфира с получением целевой карбоновой кислоты.
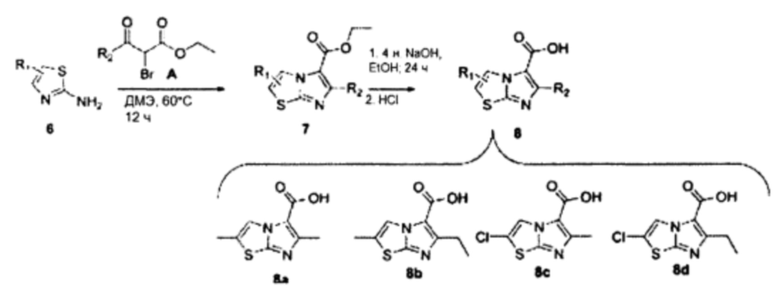
С использованием тех же методик, которые описаны выше для синтеза имидазо[1,2-α]пиридин-3-карбоновых кислот (4а-4d), можно получить имидазо[2,1-b]тиазол-5-карбоновые кислоты (8а-8d).
Например, 2,6-диметилимидазо[2,1-b]тиазол-5-карбоновую кислоту (4а) можно получить путем смешивания 5-метил-2-аминотиазола (10 г, 86,7 ммоль) и этил-2-хлорацетоацетата (13,3 мл, 86,7 ммоль) и нагревания реакционной смеси до 60°С в минимальном количестве 1,2-дихлорэтана (15 мл), добавленном для облегчения перемешивания в атмосфере аргона в течение ночи. После этого добавляли гидрокарбонат натрия (1 экв.) и реакционную смесь барботировали в течение 5 мин. Реакционную смесь концентрировали практически досуха на воздухе. Остаток растворяли в EtOAc и промывали водой (2×), а затем 1 н. HCl (3×), насыщенным водным раствором хлорида натрия, а затем сушили над сульфатом натрия. Удаляли осушающий агент и концентрировали в вакууме. Остаток растворяли в CH2Cl2 и очищали на колонке из силикагеля, элюируя CH2Cl2, для удаления зоны, выходящей первой, а затем 20%-ной смесью EtOAc: CH2Cl2, чтобы собрать продукт после концентрирования в виде желто-оранжевого твердого вещества. 4,78 г (25%) этил-2,6-диметилимидазо[2,1-b]тиазол-5-карбоксилата. 1Н ЯМР (300 МГц, CDCl3) δ м.д. 7,78 (с, 1Н), 4,38 (дц, J=14,0, 7,0 Гц, 2Н), 2,59 (с, 3Н), 2,44 (с, 3Н), 1,40 (т, J=7,0, 7,0 Гц, 3Н).
Этил-2,6-диметилимидазо[2,1-b]тиазол-5-карбоксилат (4,78 г, 21,3 ммоль) растворяли в 90 мл EtOH, а затем добавляли 4 н. водный раствор NaOH (10,6 мл, 42,6 ммоль) и реакционную смесь перемешивали в течение ночи при 50°С, и пока ТСХ не показала превращение в более полярное пятно. Реакционную смесь концентрировали до 1/4 объема путем продувания воздуха через реакционную смесь. Остаток охлаждали на ледяной бане, а затем доводили рН до 2-3 путем осторожного добавления конц. HCl (~2 мл), а потом 4 н. раствора HCl. Продукт осаждался из раствора, и его собирали путем фильтрования и сушили под вакуумом в течение ночи. Было собрано 1,9 грамма 2,6-диметилимидазо[2,1-b]тиазол-5-карбоновой кислоты (4а) в виде светло-желтого твердого вещества. 1Н ЯМР (300 МГц, CH3OD) δ м.д. 7,67 (с, 1Н), 2,51 (с, 1Н), 2,44 (с, 1Н).
В некоторых вариантах осуществления изобретения В в общих структурах:
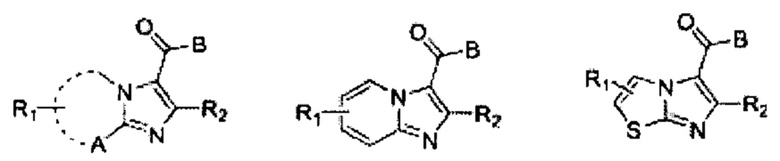
может быть получен из одного из следующих аминов представленных ниже.
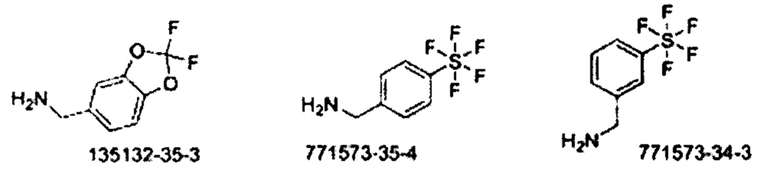
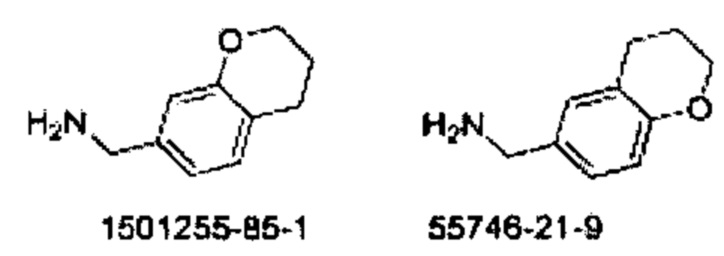
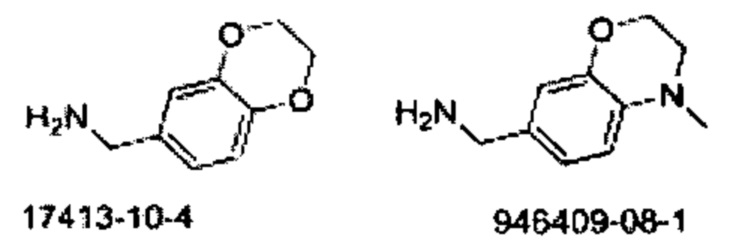
В некоторых вариантах осуществления изобретения группа R3, например «С-группа», в боковой группе ниже:
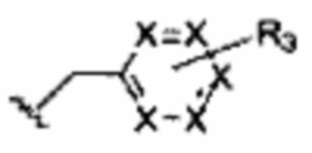
может быть получена из одного из следующих циклических аминов и замещенных циклических аминов, показанных ниже:
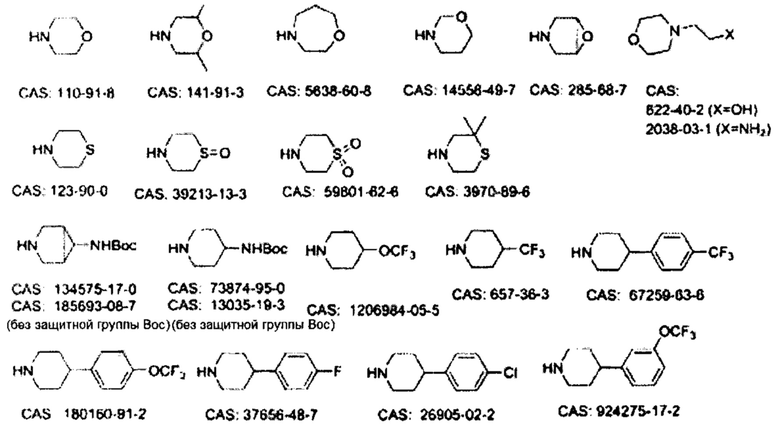
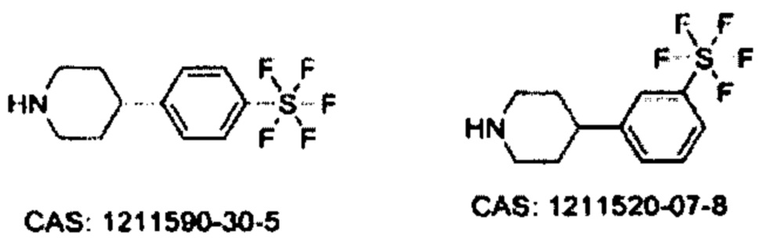
Производные пиперидинарила могут быть получены, например, в соответствии с публикацией заявки на патент США 20070032469, 8 февраля 2007 года; международной заявкой РСТ 2004058727, 15 июля 2004 г., и международной заявкой РСТ 2011028947, 10 марта 2011 г.
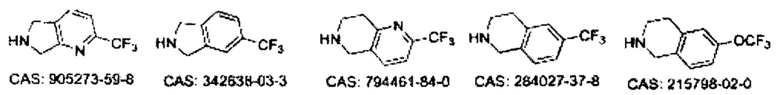
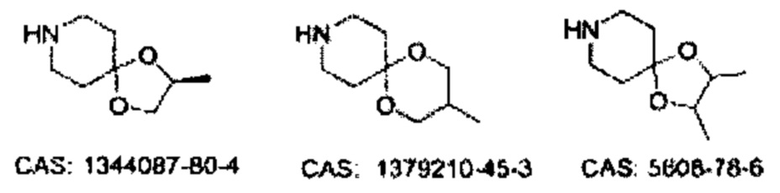
Производные спиропиперидина можно получать, например, в соответствии с ACS Medicinal Chemistry Letters, 5(5), 587-591; 2014; Bioorganic & Medicinal Chemistry Letters, 24(10), 2288-2294; 2014; Beilstein Journal of Organic Chemistry, 8, 1700-1704, No. 193; 2012.
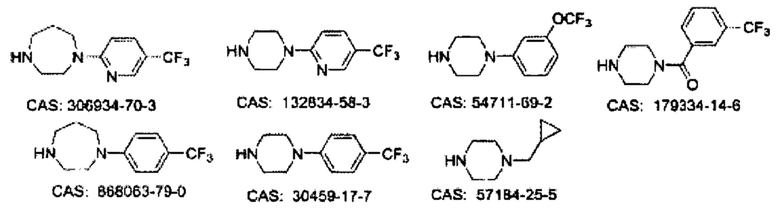
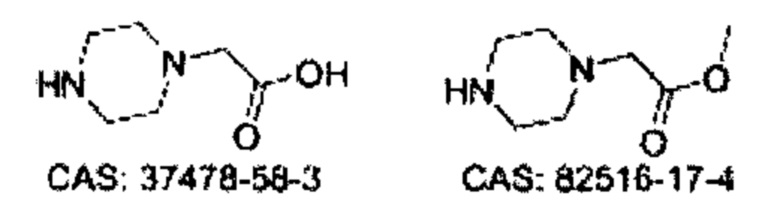
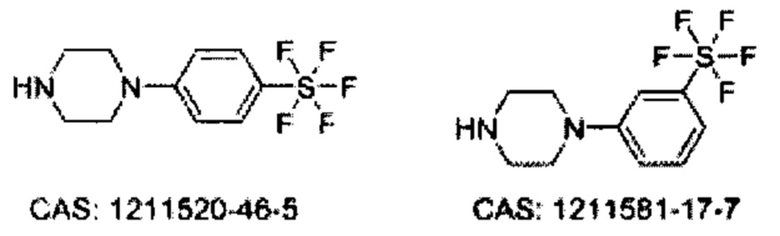
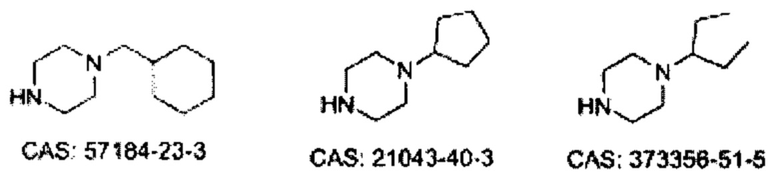
Производные пиперазинарила можно получать в соответствии с Medicinal Chemistry, 56(24), 10158-10170; 2013; международной заявкой РСТ 9900386, 7 января 1999 г.; Tetrahedron Letters, 47(15), 2549-2552; 2006; международной заявкой РСТ 2009095773, 6 августа 2009 г.; публикацией заявки на патент США 20140142114, 22 мая 2014 г.; Journal of Medicinal Chemistry, 57(3), 1063-1078; 2014; и международной заявкой РСТ 2010094126, 26 августа 2010 г.
Возможны другие циклические амины и замещенные циклические амины.
Общая схема ниже демонстрирует методику сочетания С-групп R3 («С» в реакционной схеме) с арилфторидом (11) по реакции SNAr (см. международную заявку РСТ 2010097410, 2 сентября 2010 г.). Реакция SNAR протекает при повышенных температурах (как правило, 100°С или выше) с ненуклеофильными основаниями (такими как K2CO3) в полярных растворителях (таких как ДМФА или ДМСО). Полученное промежуточное соединение (11) будет приводить к образованию амина для группы В 12 при восстановлении нитрила 11 с помощью любого из ряда способов (палладий и водород, PtO2 и водород, никель Ренея, Red-Al, алюмогидрид лития, бораны).
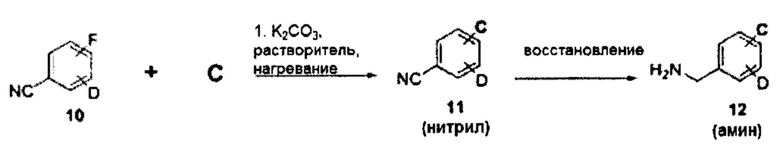
где в предыдущей схеме в некоторых вариантах осуществления изобретения С представляет собой циклические амины и замещенные циклические амины; и D представляет собой водород, галоген, Cl, F, СН3, CF3, OCF3, SF5.
Конкретные примеры применения реакции замещения SNAR к нитрилу 11 с последующим восстановлением до амина 12, включают в себя:
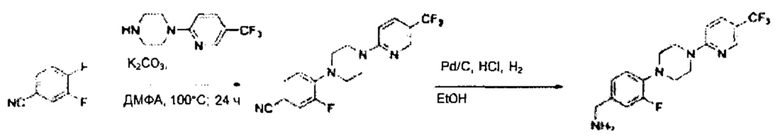
который может быть получен смешиванием [5-(трифторметил)-2-пиридил]пиперазина [CAS: 132834-58-3] (9 г, 38,9 ммоль), карбоната калия (10,8 г, 77,8 ммоль) и 3,4-дифторбензонитрила (5,4 г, 38,9 ммоль) в 50 мл ДМФА. Реакционную смесь нагревали до 100°С в течение ночи.
Реакционную смесь продували воздухом до сухого остатка и остаток поглощали EtOAc и промывали водой (2×), насыщенным водным раствором хлорида натрия, а затем сушили над сульфатом натрия. Осушающий агент удаляли фильтрованием, а органический слой концентрировали до желтовато-коричневого твердого вещества. Неочищенное твердое вещество можно очищать на колонке из силикагеля или с помощью перекристаллизации из горячего изопропанола, что давало 11,95 г 3-фтор-4-(4-(5-(трифторметил)пиридин-2-ил)пиперазин-1-ил)бензонитрил в виде светло-желтого твердого вещества.
3-Фтор-4-(4-(5-(трифторметил)пиридин-2-ил)пиперазин-1-ил)бензонитрил (4,0 г, 11,4 ммоль) растворяли в 120 мл EtOH. Затем в атмосфере аргона добавляли 9,5 мл HCl (114,2 ммоль, 10 экв.) и Pd/c (5%, 2,43 г, 1,1 ммоль). Через раствор продували газообразный водород из трех шаров и реакционную смесь перемешивали под 1 атм Н2 в течение 3 ч. Реакцию контролировали с помощью ТСХ (пятно, окрашенное нингидрином, элюент EtOH) и останавливали после завершения. После этого реакционную смесь фильтровали через стекловолокно (или целит), чтобы удалить палладий, и промывали CH2Cl2, затем фильтрат концентрировали в вакууме. Остаток перемешивали в 4 н. NaOH (100 мл) в течение 10 мин (пока он не становился основным) и экстрагировали CH2Cl2 (5×). Органический слой промывали насыщенным водным раствором хлорида натрия, а затем сушили над сульфатом натрия. Осушающий агент удаляли путем фильтрования, и органические фазы концентрировали, что давало 3,85 г (3-фтор-4-(4-(5-(трифторметил)пиридин-2-ил)пиперазин-1-ил)фенил)метанамина в виде желтоватого твердого вещества.
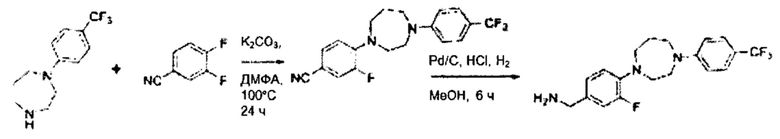
1-(4-(трифторметил)фенил)-1,4-диазепан [CAS: 868063-79-0] (2 г, 8,2 ммоль) и карбонат калия (1,7 г, 12,3 ммоль) растворяли в 25 мл ДМФА и добавляли 3,4-дифторбензонитрил (1,14 г, 8,2 ммоль). Реакционную смесь нагревали до 100°С в течение ночи. Реакционную смесь продували до сухого остатка и остаток поглощали EtOAc и промывали водой (2×), насыщенным водным раствором хлорида натрия, а затем сушили над Na2SO4. Осушающий агент удаляли фильтрованием, а органические фазы концентрировали. Остаток можно очищать с использованием силикагеля или с помощью перекристаллизации из горячего изопропанола, что давало 2 грамма 3-фтор-4-(4-(4-(трифторметил)фенил)-1,4-диазепан-1-ил)бензонитрила в виде светлого желтовато-коричневого твердого вещества.
3-Фтор-4-(4-(4-(трифторметил)фенил)-1,4-диазепан-1-ил)бензонитрил (2 г, 5,5 ммоль) растворяли в 50 мл МеОН. Затем в атмосфере аргона добавляли 4,6 мл HCl и Pd/c (5%, 1,2 г, 0,55 ммоль). Через раствор продували газообразный водород из двух шаров и реакционную смесь перемешивали под 1 атм Н2 в течение 3 часов. Реакцию контролировали с помощью ТСХ (пятно, окрашенное нингидрином, элюент EtOH) и останавливали после завершения. После этого реакционную смесь фильтровали через стекловолокно (или целит), чтобы удалить палладий, и промывали CH2Cl2, затем фильтрат концентрировали в вакууме. Остаток перемешивали в 4 н. NaOH (100 мл) в течение 10 мин (пока он не становился основным) и экстрагировали CH2Cl2 (5×). Органический слой промывали насыщенным водным раствором хлорида натрия, а затем сушили над сульфатом натрия. Осушающий агент удаляли путем фильтрования, и органические фазы концентрировали, что давало 1,8 г (3-фтор-4-(4-(4- (трифторметил)фенил)-1,4-диазепан-1-ил)фенил)метанамина.
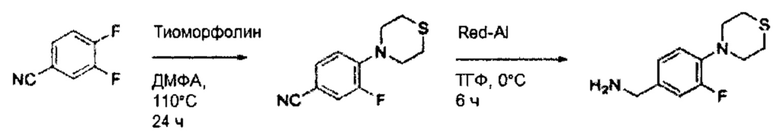
Тиоморфолин (4,9 мл, 48,5 ммоль) и карбонат калия (13,4 г, 96,9 ммоль) растворяли в 50 мл ДМФА и добавляли 3,4-дифторбензонитрил (6,7 г, 48,5 ммоль). Реакционную смесь нагревали до 100°С в течение ночи. Реакционную смесь продували до сухого остатка и остаток поглощали EtOAc и промывали водой (2×), насыщенным водным раствором хлорида натрия, а затем сушили над сульфатом натрия. Осушающий агент удаляли путем фильтрования, а затем органические фазы концентрировали и остаток перекристаллизовывали из горячего изопропанола, что давало 8,74 г 3-фтор-4-тиоморфолинобензонитрила в виде светло-желтого твердого вещества. Остаток можно также очищать с использованием силикагеля.
3-Фтор-4-тиоморфолинобензонитрил (3 г, 13,5 ммоль) растворяли в 25 мл сухого ТГФ и охлаждали до 0°С (температура ледяной бани) в атмосфере аргона. В охлажденный раствор по каплям добавляли Red-Al (11,3 мл, 7,9 ммоль). После завершения реакции реакционную смесь перемешивали при комнатной температуре в течение 3 часов. Реакцию гасили 1 мл воды, при этом охлаждая реакционную смесь до 0°С (температура ледяной бани). Затем добавляли 20 мл 1 н. раствора NaOH и реакционную смесь перемешивали в течение 30 мин. Раствор фильтровали через слой целита и этот слой промывали ТГФ. Фильтрат концентрировали в вакууме, и остаток делали основным, используя 50 мл 4 н. NaOH, и экстрагировали CH2Cl2 (5×). Объединенные органические фазы промывали насыщенным водным раствором хлорида натрия, а затем сушили над сульфатом натрия. Осушающий агент удаляли фильтрованием, а органические фазы концентрировали до получения желтого полутвердого вещества. Неочищенное вещество очищали на колонке из силикагеля, элюируя 10% EtOH : EtOAc, полярность увеличивали до 100% EtOH, чтобы собрать 2,2 г (3-фтор-4-тиоморфолинофенил)метанамина в виде светлого твердого вещества.
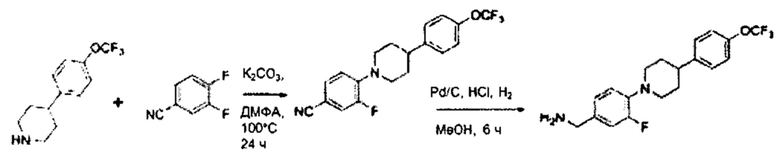
4-(4-(Трифторметокси)фенил)пиперидин [CAS: 180160-91-2] (2 г, 8,2 ммоль) и карбонат калия (2,3 г, 16,3 ммоль) растворяли в 25 мл ДМФА и добавляли 3,4-дифторбензонитрил (1,14 г, 8,2 ммоль). Реакционную смесь нагревали до 100°С в течение ночи. Реакционную смесь продували до сухого остатка и остаток поглощали EtOAc и промывали водой (2×), насыщенным водным раствором хлорида натрия, а затем сушили над Na2SO4. Осушающий агент удаляли фильтрованием, а органические фазы концентрировали. Остаток можно очищать с использованием силикагеля или с помощью перекристаллизации из горячего изопропанола, что давало 1,75 грамма 3-фтор-4-(4-(5-(трифторметил)пиридин-2-ил)пиперазин-1-ил)бензонитрила в виде светлого желтовато-коричневого твердого вещества.
3-Фтор-4-(4-(5-(трифторметил)пиридин-2-ил)пиперазин-1-ил)бензонитрил (1,75 г, 4,8 ммоль) растворяли в 50 мл МеОН. Затем в атмосфере аргона добавляли 4 мл HCl и Pd/c (5%, 1,0 г, 0,48 ммоль). Через раствор продували газообразный водород из двух шаров и реакционную смесь перемешивали под 1 атм Н2 в течение 3 часов. Реакцию контролировали с помощью ТСХ (пятно, окрашенное нингидрином, элюент EtOH) и останавливали после завершения. После этого реакционную смесь фильтровали через стекловолокно (или целит), чтобы удалить палладий, и промывали CH2Cl2, затем фильтрат концентрировали в вакууме. Остаток перемешивали в 4 н. NaOH (100 мл) в течение 10 мин (пока он не становился основным) и экстрагировали CH2Cl2 (5×). Органический слой промывали насыщенным водным раствором хлорида натрия, а затем сушили над сульфатом натрия. Осушающий агент удаляли путем фильтрования и органические фазы концентрировали, что давало 1,1 г (3-фтор-4-(4-(5-(трифторметил)пиридин-2-ил)пиперазин-1-ил)фенил)метанамина.
Как альтернативный вариант, получение нитрила 11 можно осуществлять по реакции кросс-сочетания Бухвальда с использованием палладия, как описано в международной заявке РСТ 2012113850, 30 августа 2012 г. для получения пиперидинилкарбонил(гомо)пиперазинов, в международной заявке РСТ 2008076243, 26 июня 2008 г., и в международной заявке РСТ 2013122897, 22 августа 2013 г.
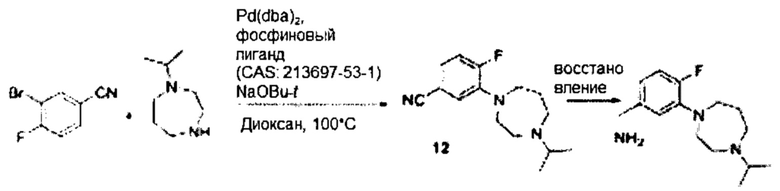
Дополнительно, получение нитрила 12 можно осуществлять по другим методикам. Например, можно использовать опосредованное титаном аминирование реактивов Гриньяра, как описано в Angewandte Chemie, International Edition, 2022, 50(36), 8325-8328. Эта методика была использована для получения 4-фтор-3-морфолинобензонитрила, который потом можно восстановить до требуемого амина.
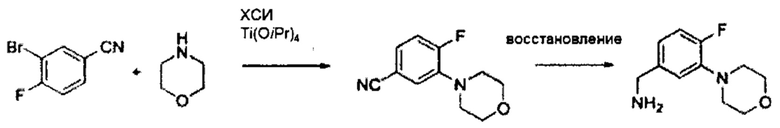
Нитрилы 11 также можно восстанавливать в амины 12 с помощью борана, как описано в J. Med. Chem. 2007, 50, 3651-3660 для получения (4-(2,6-диметилморфолино)-3-фторфенил)метанамина гидрохлорида.
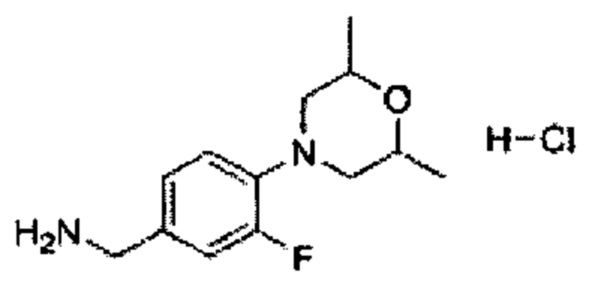
(4-(2,6-Диметилморфолино)-3-фторфенил)метанамина гидрохлорид
Конкретнее, 4-(2,6-диметилморфолино)-3-фторбензонитрил (1,23 г, 3,99 ммоль) поглощали 10 мл ТГФ, а затем добавляли 1 М ВН3 ТГФ (12,0 мл, 12,0 ммоль) и смесь нагревали с обратным холодильником. Через 2 ч раствор охлаждали до температуры окружающей среды, и реакцию гасили путем осторожного добавления 3 н. раствора NaOH, и перемешивали в течение 30 мин. Смесь распределяли между EtOAc и H2O, и отделенную органическую фазу промывали насыщенным водным раствором хлорида натрия, сушили (Na2SO4) и концентрировали в вакууме. Флеш-хроматография (5-10% CH3OH/CH2Cl2) дала целевое соединение в виде бесцветного масла. (2,5-Дифтор-4-(8-азаспиро[бицикло[3.2.1]октан-3,2-[1,3]диоксолан]-8-ил)фенил)метанамин, выход 73%. 1Н ЯМР (ДМСО-d6): δ 7,18 (дд, J=14,6, 7,1 Гц, 1Н), 6,77 (дд, J=12,6, 7,5 Гц, 1Н), 4,28 (м, 2Н), 3,94 (т, J=6,4 Гц, 2Н), 3,70 (т, J=6,4 Гц, 2Н), 3,61 (с, 2Н), 2,03 (м, 2Н), 1,64-1,94 (м, 8Н).
Нитрилы 11 также можно восстанавливать в амины 12 с помощью LiAlH4, как описано в публикации заявки на патент США 20050113576, 26 мая 2005 г., для получения гидрохлорида.
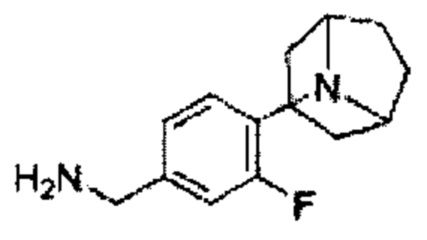
(4-(8-Азабицикло[3.2.1]октан-8-ил)-3-фторфенил)метанамин
4-(8-Азабицикло[3.2.1]окт-8-ил)-3-фторбензиламин. Алюмогидрид лития (1,6 г; 43,2 ммоль) в ТГФ по каплям обрабатывали 4-(8-азабицикло[3.2.1]окт-8-ил)-3-фторбензонитрилом (2,48 г; 10,8 ммоль). После завершения добавления взвесь нагревали с обратным холодильником в течение 2 часов, давали остыть до температуры окружающей среды и гасили декагидратом сульфата натрия. Смесь фильтровали и остаток на фильтре промывали ТГФ (2×50 мл). Органические фазы объединяли и концентрировали при пониженном давлении. Остаток хроматографировали (SiO2; 5% метанола в метиленхлориде). 4-(8-Азабицикло[3.2.1]окт-8-ил)-3-фторбензиламин. 1Н ЯМР (ДМСО-d6) δ 7,03 (дд, 1Н), 7,92 (дд, 1Н), 7,85 (т, 1Н), 4,21 (с, 2Н), 3,60 (с, 2Н), 1,93 (м, 2Н), 1,77 (м, 5Н), 1,42 (м, 1Н), 1,32 (м, 2Н).
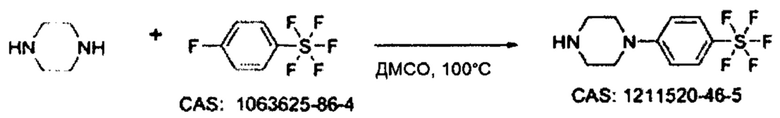
4-Фторбензопентафторсульфид (CAS: 1063625-86-3, 1,0 г, 13,3 ммоль) растворяли в 6 мл ДМСО, и добавляли пиперазин (2 г, 19,9 ммоль), и реакционную смесь нагревали до 110°С в течение ночи (12 ч). Реакционную смесь концентрировали досуха и остаток очищали на колонке из силикагеля (110 г), элюируя EtOAc (для удаления зоны, выходящей первой, продукт дисочетания), затем полярность растворителя постепенно увеличивали до 100% EtOH, чтобы собрать 1,1 грамма 1-(4-(пентафтор-λ6-сульфанил)фенил)пиперазина (наиболее полярная зона). 1Н ЯМР (300 МГц, CDCl3) δ м.д. 7,64 (д, J=9,1 Гц, 2Н), 6,87 (д, J=8,9 Гц, 2Н), 3,52-3,44 (м, 4Н), 3,30-3,23 (м, 4Н).
1-(3-(Пентафтор-λ6-сульфанил)фенил)пиперазин (CAS: 1211581-17-7) можно получить по методикам, описанным выше, но используя 3-фторбензопентафторсульфид (CAS: 1422-41-9).
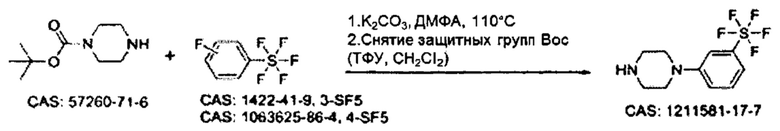
Как альтернативный вариант, Вос-защищенный пиперазин (CAS: 57260-71-6) можно нагревать с 4-фторбензопентафторсульфидом или 3-фторбензопентафторсульфидом для осуществления реакции SNAr. Затем с продукта сочетания снимают защиту с использованием трифторуксусного ангидрида (ТФУА) или газообразного HCl, чтобы получить 1-(4-(пентафтор-λ6-сульфанил)фенил)пиперазин или 1-(3-(пентафтор-λ6-сульфанил)фенил)пиперазин в случае ТФУА или HCl, соответственно. Эти соли можно нейтрализовать с помощью основания (NaOH в метаноле), чтобы получить свободные амины.

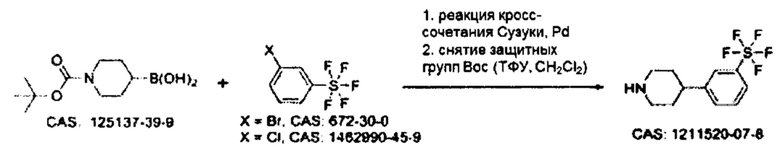
4-(4-(Пентафтор-λ6-сульфанил)фенил)пиперидин (CAS: 1211590-30-5) и 4-(3-(пентафтор-λ6-сульфанил)фенил)пиперидин (CAS: 1211520-07-8) можно получить по методикам, приведенным в J. Med. Chem., 2014, 57 (12), 5293-5305, но с использованием или 4-бромбензопентафторсульфида (CAS: 774-93-6), 4-хлорбензопентафторсульфида (CAS: 5310-68-9), или 3-бромбензопентафторсульфида (CAS: 672-30-0), 3-хлорбензопентафторсульфида (CAS: 1462990-45-9) в качестве галогенидов в реакции сочетания Сузуки. С полученного продукта сочетания Сузуки снимали защиту с помощью или трифторуксусной кислоты (ТФУ), или газообразного азота, а затем эти соли можно нейтрализовать основанием, чтобы получить свободные амины.
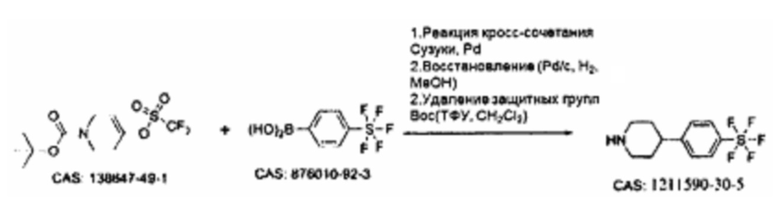
Как альтернативный вариант, 4-(4-(пентафтор-λ6-сульфанил)фенил)пиперидин (CAS: 1211590-30-5) можно получить по методикам, приведенным в ACS Med. Chem. Lett., 2015, 6 (7), 814-818, но используя (4-(пентафтор-λ6-сульфанил)фенил)бороновую кислоту (CAS: 876010-92-3) в качестве бороновой кислоты в реакции сочетания Сузуки. Продукт реакции Сузуки затем восстанавливают с использованием палладия на угле и водорода с последующим удалением защитных групп Вос и нейтрализацией, чтобы получить свободный амин.
Сочетание аминов 12 с гетероциклическими фрагментами (4а-4d; 8а-8d) осуществляют по стандартным реакциям образования амидной связи (как описано в "The Practice of Peptide Synthesis," by M. Bodansky and A. Bodansky, Springer-Verlag, New York. 1994, 2nd ed.) или, как альтернативный вариант, карбоновые кислоты можно превратить хлорангидриды (с помощью оксалилхлорида или тионилхлорида), а затем перемешивать с 12 и основанием (триметиламином, диизопропилэтиламином, пиридином) в апротонном растворителе (CH3CN, CH2Cl2, ДМФА).
Примеры амидного сочетания для получения требуемых соединений включают в себя:
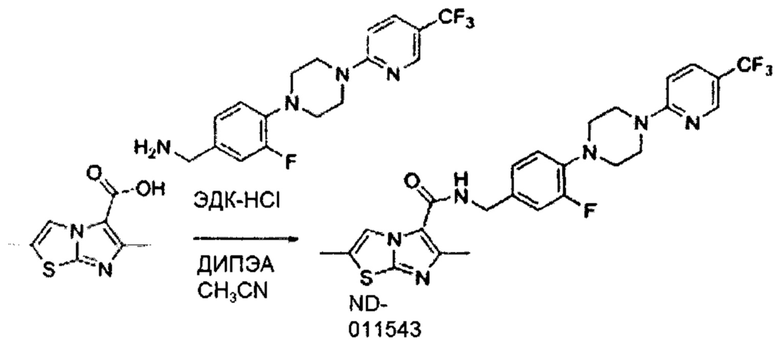
2,6-Диметилимидазо[2,1-b]тиазол-5-карбоновую кислоту (1,17 г, 5,9 ммоль) растворяли в сухом CH3CN, а затем добавляли ЭДК-HCl (1,38 г, 7,2 ммоль) и реакционную смесь перемешивали в течение 10 мин. Затем в круглодонную колбу добавляли (3-фтор-4-(4-(5-(трифторметил)пиридин-2-ил)пиперазин-1-ил)фенил)метанамин (2,29 г, 7,2 ммоль) и диизопропилэтиламин (1,3 мл, 7,2 ммоль). Реакционную смесь перемешивали в атмосфере аргона в течение 12 часов. Реакционную смесь концентрировали в вакууме. Остаток поглощали CH2Cl2 и промывали насыщенным водным раствором NaHCO3 (2×), 5%-ным водным раствором уксусной кислоты (2×), насыщенным водным раствором хлорида натрия, а затем сушили над сульфатом натрия. Осушающий агент удаляли фильтрованием, а органические фазы концентрировали в вакууме. Полученный остаток очищали на колонке из силикагеля или с помощью перекристаллизации из горячего CH3CN, что давало N-(3-фтор-4-(4-(5-(трифторметил)пиридин-2-ил)пиперазин-1-ил)бензил)-2,6-диметилимидазо[2,1-b]тиазол-5-карбоксамид в виде желтоватого твердого вещества, 945 мг. 1Н ЯМР (500 МГц, CDCl3) 8,42 (с, 1Н), 7,99 (с, 1Н), 7,67 (дд, J=8,9, 1,9 Гц, 1Н), 7,38 (д, J=8,3 Гц, 1Н), 7,31 (д, J=12,5 Гц, 1Н), 6,95 (т, J=8,5, 8,5 Гц, 1Н), 6,69 (д, J=9,0 Гц, 1H), 4,57 (д, J=5,4 Гц, 2Н), 3,85-3,79 (м, 4Н), 3,35-3,30 (м, 4Н).
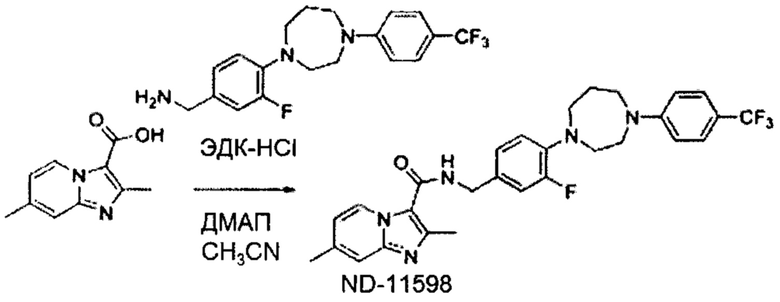
2,7-Диметилимидазо[1,2-a]пиридин-3-карбоновую кислоту (420 мг, 2,2 ммоль) растворяли в сухом CH3CN, а затем добавляли ЭДК-HCl (510 мг, 2,6 ммоль) и реакционную смесь перемешивали в течение 10 мин. Затем в круглодонную колбу под атмосферой аргона добавляли (3-фтор-4-(4-(4-(трифторметил)фенил)-1,4-диазепан-1-ил)фенил)метанамин (878 мг, 2,3 ммоль) и ДМАП (323 мг, 2,7 ммоль). Реакционную смесь перемешивали в атмосфере аргона в течение 12 часов. Реакционную смесь концентрировали в вакууме. Остаток поглощали CH2Cl2 и промывали насыщенным водным раствором NaHCO3 (2×), 5%-ным водным раствором уксусной кислоты (2×), насыщенным водным раствором хлорида натрия, а затем сушили над сульфатом натрия. Осушающий агент удаляли фильтрованием, а органические фазы концентрировали в вакууме. Полученный остаток очищали на колонке из силикагеля или с помощью перекристаллизации из горячего CH3CN, что давало N-(3-фтор-4-(4-(4-(трифторметил)фенил)-1,4-диазепан-1-ил)бензил)-2,7-диметилимидазо[1,2-а]пиридин-3-карбоксамид в виде желтоватого твердого вещества, 847 мг.
1Н ЯМР (500 МГц, CDCl3) δ м. д. 9,30 (д, J=7,1 Гц, 1Н), 7,43 (д, J=8,8 Гц, 2Н), 7,32 (с, 1Н), 6,86 (т, J=8,7, 8,7 Гц, 2Н), 6,76 (д, J=7,2, 1Н), 6,73 (д, J=8,8, 2Н), 5,98 (ш. с., 1Н, NH), 4,57 (д, J=5,7 Гц, 2Н), 3,75-3,71 (м, 2Н), 3,63 (т, J=6,2, 6,2 Гц, 2Н), 3,54-3,50 (м, 2Н), 3,30 (т, J=5,7, 5,7 Гц, 2Н), 2,66 (с, 3Н), 2,42 (с, 3Н), 2,13-2,04 (м, 2Н).
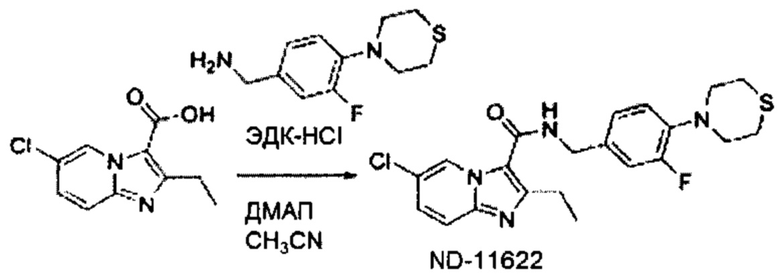
6-Хлор-2-этилимидазо[1,2-а]пиридин-3-карбоновую кислоту (900 мг, 4 ммоль) растворяли в сухом CH3CN, а затем добавляли ЭДК-HCl (921 мг, 4,8 ммоль) и реакционную смесь перемешивали в течение 10 мин. Затем в круглодонную колбу добавляли (3-фтор-4-тиоморфолинофенил)метанамин (998 мг, 4,4 ммоль) и ДМАП (587 мг, 4,8 ммоль). Реакционную смесь перемешивали в атмосфере аргона в течение 12 часов. Реакционную смесь концентрировали в вакууме. Остаток поглощали CH2Cl2 и промывали насыщенным водным раствором NaHCO3 (2×), 5%-ным водным раствором уксусной кислоты (2×), насыщенным водным раствором хлорида натрия, а затем сушили над сульфатом натрия. Осушающий агент удаляли фильтрованием, а органические фазы концентрировали в вакууме. Полученный остаток очищали на колонке из силикагеля или с помощью перекристаллизации из горячего CH3CN, что давало 6-хлор-2-этил-N-(3-фтор-4-тиоморфолинобензил)имидазо[1,2-а]пиридин-3-карбоксамид, 777 мг. 1Н ЯМР (500 МГц, CDCl3) δ м. д. 9,50 (с, 1Н), 7,56 (д, J=9,3 Гц, 1Н), 7,32 (д, J=9,2 Гц, 1Н), 7,06 (т, J=8,9, 8,9 Гц, 1Н), 6,94 (т, J=8,4, 8,4 Гц, 1Н), 6,25 (ш. с., 1Н, NH), 4,61 (д, J=5,5 Гц, 1Н), 3,35-3,26 (м, 4Н), 2,99 (к, J=7,4 Гц, 2Н), 2,84-2,77 (м, 4Н), 1,41 (т, J=7,4, 7,4 Гц, 3Н).
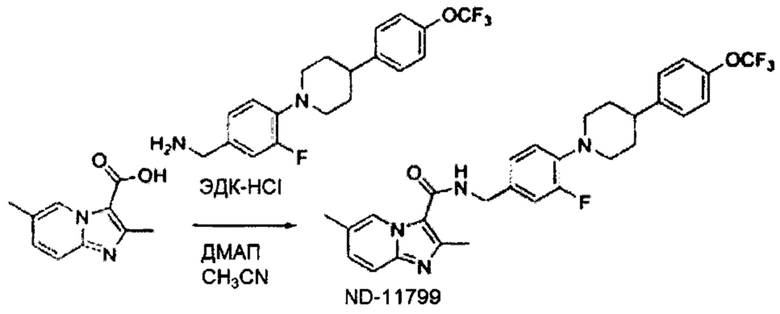
2,6-Диметилимидазо[1,2-a]пиридин-3-карбоновую кислоту (814 мг, 3,6 ммоль) растворяли в сухом CH3CN, а затем добавляли ЭДК-HCl (757 мг, 3,9 ммоль) и реакционную смесь перемешивали в течение 10 мин. Затем добавляли (3-фтор-4-(4-(4-(трифторметокси)фенил)пиперидин-1-ил)фенил)метанамин (1,19 г, 3,3 ммоль) и ДМАП (523 мг, 4,3 ммоль) и реакционную смесь перемешивали под атмосферой аргона в течение ночи. Реакционную смесь концентрировали в вакууме. Остаток поглощали CH2Cl2 и промывали насыщенным водным раствором NaHCO3 (2×), 5%-ным водным раствором уксусной кислоты (2×), насыщенным водным раствором хлорида натрия, а затем сушили над сульфатом натрия. Осушающий агент удаляли фильтрованием, а органические фазы концентрировали в вакууме. Полученный остаток очищали на колонке из силикагеля или с помощью перекристаллизации из горячего CH3CN, что давало N-(3-фтор-4-(4-(4-(трифторметокси)фенил)пиперидин-1-ил)бензил)-2,6-диметилимидазо[1,2-а]пиридин-3-карбоксамид, 1,1 г.
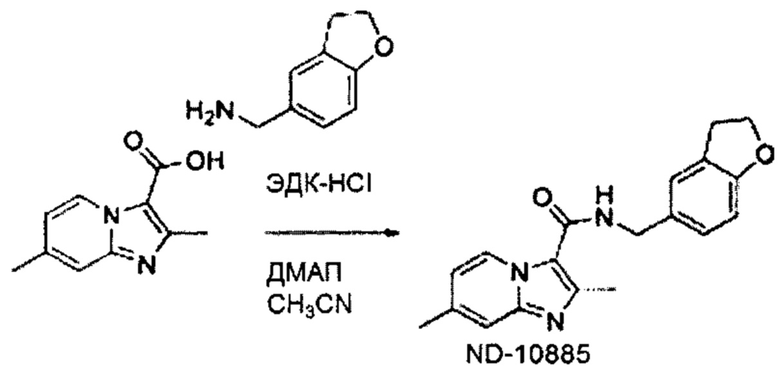
2,7-Диметилимидазо[1,2-а]пиридин-3-карбоновую кислоту (4 г, 21 ммоль) и ЭДК-HCl (4,8 г, 25,2 ммоль) объединяли вместе и реакционную смесь перемешивали в течение 10 мин. в сухом CH3CN. Затем добавляли 5-(аминометил)-2,3-дигидробензо[b]фуран (CAS: 55745-74-9, 3,5 г, 23,1 ммоль) и ДМАП (3,1 г, 25,2 ммоль) и реакционную смесь перемешивали в течение 16 часов под атмосферой аргона. Реакционную смесь концентрировали в вакууме. Остаток поглощали CH2Cl2 и промывали насыщенным водным раствором NaHCO3 (2×), 5%-ным водным раствором уксусной кислоты (2×), насыщенным водным раствором хлорида натрия, а затем сушили над сульфатом натрия. Осушающий агент удаляли фильтрованием, а органические фазы концентрировали в вакууме. Полученный остаток очищали на колонке из силикагеля или с помощью перекристаллизации из горячего CH3CN, что давало N-((2,3-дигидробензофуран-5-ил)метил)-2,7-диметилимидазо[1,2-а]пиридин-3-карбоксамид в виде белого твердого вещества, 4,2 г. 1Н ЯМР (300 МГц, CDCl3) δ м. д. 9,28 (д, J=7,1 Гц, 1Н), 7,37 (с, 1Н), 7,21 (с, 1H), 7,10 (д, J=7,8 Гц, 1Н), 6,75 (д, J=7,8 Гц, 1Н), 6,04 (ш. с., 1Н, NH), 4,58 (д, J=7,4 Гц, 1Н), 4,55 (кажущийся т, 2Н, скрытый), 3,19 (т, J=8,6, 8,6 Гц, 1Н), 2,63 (с, 3Н), 2,41 (с, 3Н). 13С (126 МГц, CDCl3) δ м. д. 161,4, 159,7, 146,3, 138,4, 130,3, 127,7, 127,3, 127,2, 124,7, 115,7, 115,0, 114,9, 109,4, 71,4, 43,2, 29,7, 21,3, 16,7. Точка плавления = 140-141,5°С. МСВР (ЭИ), М+1 рассчитанное для C19H20N3O2, 322,1550; найденное 322,1568. ВЭЖХ tR=1,2-1,4 мин (чистота 99%).
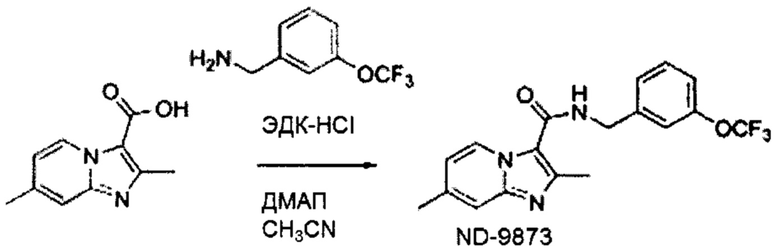
2,7-Диметилимидазо[1,2-а]пиридин-3-карбоновую кислоту (200 мг, 1 ммоль) и ЭДК-HCl (287 мг, 1,5 ммоль) растворяли в 15 мл сухого CH3CN (сушили с использованием молекулярных сит). Затем добавляли 3-трифторметоксибензиламин (0,15 мл, 1,06 ммоль) и ДМАП (305 мг, 2,5 ммоль). Реакционную смесь перемешивали под атмосферой аргона при комнатной температуре в течение 12 часов. Реакционную смесь концентрировали в вакууме. Остаток поглощали CH2Cl2 и промывали насыщенным водным раствором NaHCO3 (2×), 5%-ным водным раствором уксусной кислоты (2×), насыщенным водным раствором хлорида натрия, а затем сушили над сульфатом натрия. Осушающий агент удаляли фильтрованием, а органические фазы концентрировали в вакууме. Полученный остаток очищали на колонке из силикагеля (используя 10% EtOAc : CH2Cl2 для удаления выходящего первым амина и полярность увеличивали до 50% EtOAc : CH2Cl2, чтобы собрать продукт) или с помощью перекристаллизации из горячего CH3CN, что давало 2,7-диметил-N-(3-(трифторметокси)бензил)имидазо[1,2-а]пиридин-3-карбоксамид в виде белого твердого вещества, 265 мг. 1H ЯМР (500 МГц, CDCl3) δ м. д. 9,24 (д, J=7,1 Гц, 1Н), 7,36 (т, J=7,9, 7,9 Гц, 1Н), 7,31-7,20 (м, 3Н), 7,13 (д, J=8,0 Гц, 1Н), 6,73 (д, J=7,1 Гц, 1Н), 6,26 (ш. с., 1Н, NH), 4,69 (д, J=5,9 Гц, 2Н), 2,65 (с, 3Н), 2,40 (с, 3Н). 13С (126 МГц, CDCl3) δ м. д. 161,2, 149,5, 146,5, 145,5, 140,9, 138,5, 130,1, 127,2, 125,7, 120,7 (к, J=257,4 Гц), 120,0, 119,9, 115,8, 115,0, 114,7, 42,7, 21,3, 16,7. Точка плавления = 110-111°С. МСВР (ЭИ), М+1 рассчитанное для C18H17F3N3O2, 364,1267; найденное 364,1271. ВЭЖХ tR = 2,8 мин (чистота 99%).
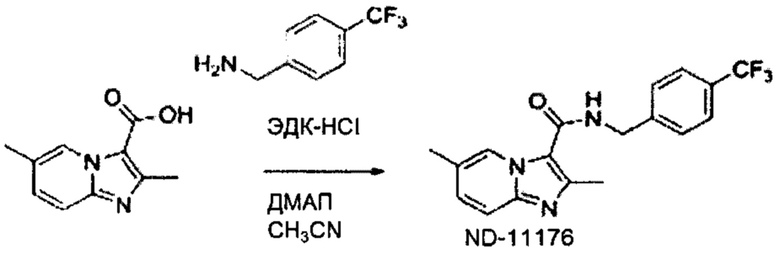
2,6-Диметилимидазо[1,2-а]пиридин-3-карбоновую кислоту (3,5 г, 18,4 ммоль) растворяли в сухом CH3CN, а затем добавляли ЭДК-HCl (4,2 г, 22,1 ммоль) и реакционную смесь перемешивали в течение 10 мин. под атмосферой аргона. Затем добавляли 4-(трифторметокси)бензиламин (3,5 г, 20,2 ммоль) и ДМАП (2,7 г, 22,1 ммоль) и реакционную смесь перемешивали в течение 16 часов под атмосферой аргона. Реакционную смесь концентрировали в вакууме. Остаток поглощали CH2Cl2 и промывали насыщенным водным раствором NaHCO3 (2×), 5%-ным водным раствором уксусной кислоты (2×), насыщенным водным раствором хлорида натрия, а затем сушили над сульфатом натрия. Осушающий агент удаляли фильтрованием, а органические фазы концентрировали в вакууме. Полученный остаток очищали на колонке из силикагеля или с помощью перекристаллизации из горячего CH3CN, что давало 2,6-диметил-N-(4-(трифторметил)бензил)имидазо[1,2-а]пиридин-3-карбоксамид в виде белого твердого вещества, 5,1 грамма. 1Н ЯМР (500 МГц, CDCl3) δ м. д. 9,25 (с, 1Н), 7,66 (д, J=7,8 Гц, 1Н), 7,55 (д, J=7,9 Гц, 1Н), 7,29 (м, 4Н), 6,38 (ш. с., 1Н, NH), 4,79 (д, J=5,7 Гц, 2Н), 2,75 (с, 3Н), 2,40 (с, 3Н). Точка плавления = 110,5-111,1°С. МСВР (ЭИ), М+1 рассчитанное для C18H17F3N3O, 348,1318; найденное 348,1332. ВЭЖХ tR = 2,7-2,9 мин (чистота 99%).
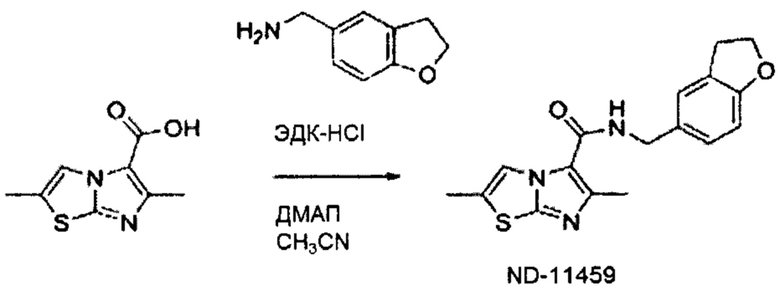
2,6-Диметилимидазо[2,1-b]тиазол-5-карбоновую кислоту (250 мг, 1,3 ммоль) и ЭДК-HCl (268 мг, 1,4 ммоль) добавляли вместе в 12 мл сухого CH3CN и реакционную смесь перемешивали в течение 10 мин. Затем добавляли гидрохлоридную соль 5-(аминометил)-2,3-дигидробензо[b]фурана (CAS: 635309-62-5, 236 мг, 1,4 ммоль) и ДМАП (342 г, 2,8 ммоль) и реакционную смесь перемешивали в течение 16 часов под атмосферой аргона. Реакционную смесь концентрировали в вакууме. Остаток поглощали CH2Cl2 и промывали насыщенным водным раствором NaHCO3 (2×), 5%-ным водным раствором уксусной кислоты (2×), насыщенным водным раствором хлорида натрия, а затем сушили над сульфатом натрия. Осушающий агент удаляли фильтрованием, а органические фазы концентрировали в вакууме. Полученный остаток очищали на колонке из силикагеля (градиент растворителей ДХМ : EtOAc) или с помощью перекристаллизации из горячего CH3CN, что давало N-((2,3-дигидробензофуран-5-ил)метил)-2,6-диметилимидазо[2,1-b]тиазол-5-карбоксамид в виде белого твердого вещества (ND-11459), 173 мг. 1Н ЯМР (300 МГц, CDCl3) δ м. д. 8,02 (с, Гц, 1Н), 7,21 (с, 1Н), 7,10 (д, J=8,0 Гц, 1Н), 6,75 (д, J=8,13 Гц, 1Н), 6,02 (ш. с., 1H, NH), 4,66-4,49 (м, 4Н, перекрывание) 3,19 (т, J=8,7, 8,7 Гц, 1Н), 2,59 (с, 3Н), 2,45 (с, 3Н).
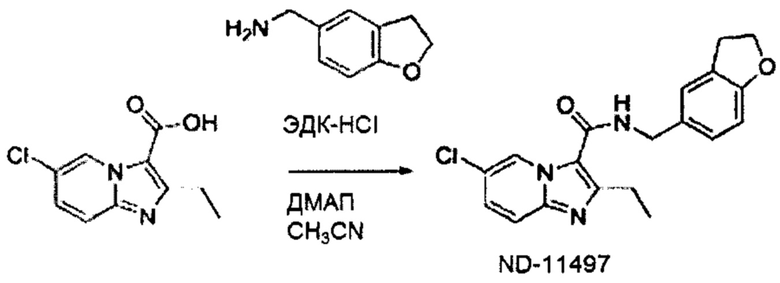
6-Хлор-2-этилимидазо[1,2-а]пиридин-3-карбоновую кислоту (107 мг, 0,48 ммоль) и ЭДК-HCl (110 мг, 0,57 ммоль) добавляли вместе в 5 мл сухого CH3CN и реакционную смесь перемешивали в течение 10 мин. Затем добавляли гидрохлоридную соль 5-(аминометил)-2,3-дигидробензо[b]фурана (CAS: 635309-62-5, 100 мг, 0,52 ммоль) и ДМАП (128 г, 1,0 ммоль) и реакционную смесь перемешивали в течение 16 часов под атмосферой аргона. Реакционную смесь концентрировали в вакууме. Остаток поглощали CH2Cl2 и промывали насыщенным водным раствором NaHCO3 (×), 5%-ным водным раствором уксусной кислоты (2×), насыщенным водным раствором хлорида натрия, а затем сушили над сульфатом натрия. Осушающий агент удаляли фильтрованием, а органические фазы концентрировали в вакууме. Полученный остаток очищали на колонке из силикагеля (градиент растворителей ДХМ : EtOAc) или с помощью перекристаллизации из горячего CH3CN, что давало 6-хлор-N-((2,3-дигидробензофуран-5-ил)метил)-2-этилимидазо[1,2-а]пиридин-3-карбоксамид (ND-11497) в виде белого твердого вещества, 81 мг. 1Н ЯМР (300 МГц, CDCl3) δ м. д. 9,53 (с, 1Н), 7,54 (д, J=9,5 Гц, 1H), 7,24 (м, 2Н), 7,11 (д, J=7,0 Гц, 1H), 6,77 (д, J=8,0 Гц, 1Н), 6,08 (ш. с., 1Н, NH2), 4,58 (м, 4Н, перекрывание), 3,22 (д, J=8,5 Гц, 2Н), 2,96 (д, J=7,41 Гц, 2Н), 1,39 (т, J=7,2, 7,2 Гц, 3Н).
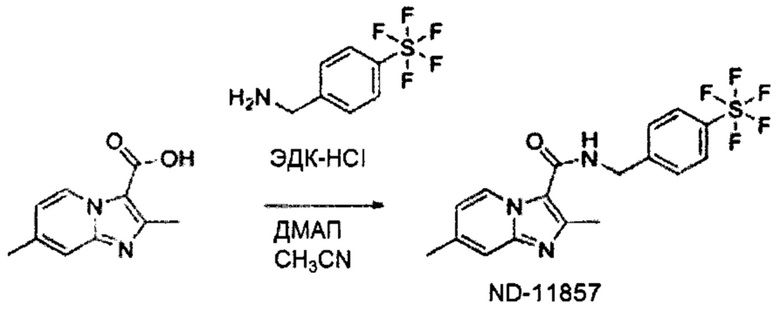
2,7-Диметилимидазо[1,2-а]пиридин-3-карбоновую кислоту (150 мг, 0,79 ммоль) растворяли в 7 мл сухого CH3CN, а затем добавляли ЭДК-HCl (181 мг, 0,95 ммоль) и реакционную смесь перемешивали в течение 10 мин. В круглодонную колбу под атмосферой аргона добавляли 4-(пентафторсера)бензиламин (CAS: 771573-35-4, 202 мг, 0,87 ммоль) и ДМАП (116 мг, 0,95 ммоль). Реакционную смесь перемешивали в атмосфере аргона в течение 12 часов. Реакционную смесь концентрировали в вакууме. Остаток поглощали CH2Cl2 и промывали насыщенным водным раствором NaHCO3 (2×), 5%-ным водным раствором уксусной кислоты (2×), насыщенным водным раствором хлорида натрия, а затем сушили над сульфатом натрия. Осушающий агент удаляли фильтрованием, а органические фазы концентрировали в вакууме. Полученный остаток очищали на колонке из силикагеля (градиент растворителей ДХМ : EtOAc) или с помощью перекристаллизации из горячего CH3CN, что давало 180 мг 2,7-диметил-N-(4-(пентафтор-λ6-сульфанил)бензил)имидазо[1,2-a]пиридин-3-карбоксамида (ND-11857) в виде белого твердого вещества. Точка плавления = 186-187°С, стандарт бензойная кислота измерен при 113-114°С; 1Н ЯМР (300 МГц, CDCl3) δ м. д. 9,20 (д, J=7,1 Гц, 1Н), 7,73 (д, J=8,6 Гц, 2Н), 7,47 (д, J=8,3 Гц, 2Н), 7,40 (с, 1Н), 6,77 (д, J=7,1 Гц, 1Н), 6,51 (ш. с., 1Н, NH2), 4,72 (д, J=5,9 Гц, 2Н), 2,69 (с, 3Н), 2,41 (с, 3Н). 19F ЯМР (282 МГц, CDCl3) δ м. д. 84,4 (пентет, J=150,0 Гц, 1F), 63,0 (д, J=150,07 Гц, 4F).
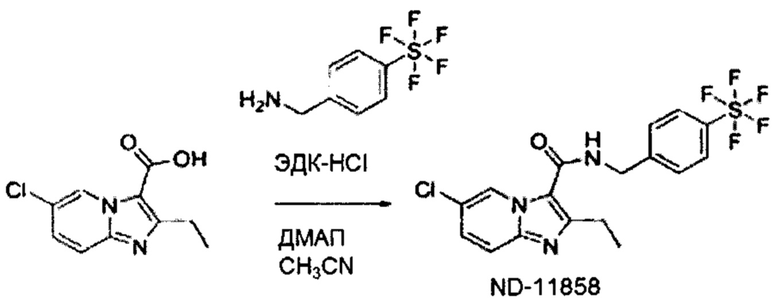
6-Хлор-2-этилимидазо[1,2-а]пиридин-3-карбоновую кислоту (150 мг, 0,66 ммоль) растворяли в 7 мл сухого CH3CN, а затем добавляли ЭДК-HCl (153 мг, 0,80 ммоль) и реакционную смесь перемешивали в течение 10 мин. В круглодонную колбу под атмосферой аргона добавляли 4-(пентафторсера)бензиламин (CAS: 771573-35-4, 171 мг, 0,73 ммоль) и ДМАП (98 мг, 0,80 ммоль). Реакционную смесь перемешивали в атмосфере аргона в течение 12 часов. Реакционную смесь концентрировали в вакууме. Остаток поглощали CH2Cl2 и промывали насыщенным водным раствором NaHCO3 (2×), 5%-ным водным раствором уксусной кислоты (2×), насыщенным водным раствором хлорида натрия, а затем сушили над сульфатом натрия. Осушающий агент удаляли фильтрованием, а органические фазы концентрировали в вакууме. Полученный остаток очищали на колонке из силикагеля (градиент растворителей ДХМ : EtOAc) или с помощью перекристаллизации из горячего CH3CN, что давало 115 мг 6-хлор-2-этил-N-(4-(пентафтор-λ6-сульфанил)бензил)имидазо[1,2-а]пиридин-3-карбоксамида (ND-11858) в виде белого твердого вещества. Точка плавления = 191-192°С, для стандарта бензойной кислоты измерена при 113-114°С; 1Н ЯМР (300 МГц, CDCl3) δ м. д. 9,50 (с, 1Н), 7,75 (д, J=8,6 Гц, 2Н), 7,55 (д, J=9,5 Гц, 1Н), 7,46 (д, J=8,3 Гц, 2Н), 7,32 (д, J=9,5 Гц, 1H), 6,30 (ш. с., 1Н, NH2) 4,74 (д, J=5,9 Гц, 2Н), 3,01 (к, J=7,5, 7,5, 7,5 Гц, 2Н), 1,43 (т, J=7,5, 7,5 Гц, 3Н). 19F ЯМР (282 МГц, CDCl3) δ м. д. 84,4 (пентет, J=150,1 Гц, 1F), 63,0 (д, J=150,1 Гц, 4F).
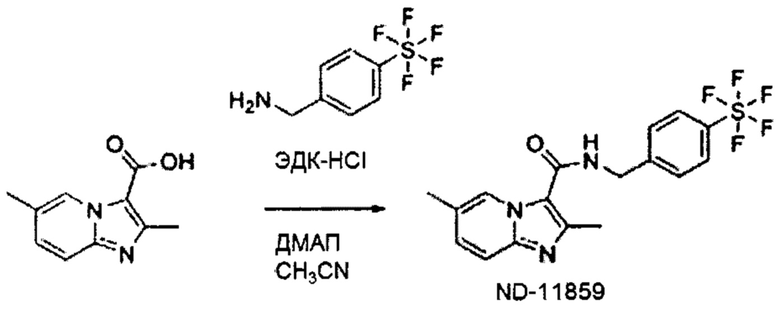
2,6-Диметилимидазо[1,2-a]пиридин-3-карбоновую кислоту (150 мг, 0,79 ммоль) растворяли в 7 мл сухого CH3CN, а затем добавляли ЭДК-HCl (181 мг, 0,95 ммоль) и реакционную смесь перемешивали в течение 10 мин. В круглодонную колбу под атмосферой аргона добавляли 4-(пентафторсера)бензиламин (CAS: 771573-35-4, 202 мг, 0,87 ммоль) и ДМАП (116 мг, 0,95 ммоль). Реакционную смесь перемешивали в атмосфере аргона в течение 12 часов. Реакционную смесь концентрировали в вакууме. Остаток поглощали CH2Cl2 и промывали насыщенным водным раствором NaHCO3 (2×), 5%-ным водным раствором уксусной кислоты (2×), насыщенным водным раствором хлорида натрия, а затем сушили над сульфатом натрия. Осушающий агент удаляли фильтрованием, а органические фазы концентрировали в вакууме. Полученный остаток очищали на колонке из силикагеля (градиент растворителей ДХМ : EtOAc) или с помощью перекристаллизации из горячего CH3CN, что давало 180 мг 2,6-диметил-N-(4-(пентафтор-λ6-сульфанил)бензил)имидазо[1,2-а]пиридин-3-карбоксамида (ND-11859) в виде белого твердого вещества. Точка плавления = 176-177°С, для стандарта бензойной кислоты измерена при 113-114°С; 1Н ЯМР (300 МГц, CDCl3) δ м. д. 9,21 (с, 1Н), 7,73 (д, J=8,6 Гц, 2Н), 7,46 (д, J=8,8 Гц, 2Н), 7,19 (д, J=8,2 Гц, 1Н), 6,33 (ш. с., 1Н, NH2), 4,73 (д, J=5,9 Гц, 2Н), 2,69 (с, 3Н), 2,34 (с, 3Н). 19F ЯМР (282 МГц, CDCl3) δ м. д. 84,5 (пентет, J=150,0 Гц, 1F), 63,0 (д, J=150,05 Гц, 4F).
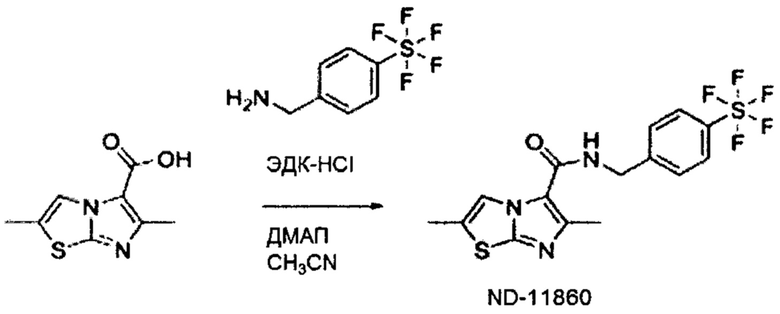
2,6-Диметилимидазо[2,1-b]тиазол-5-карбоновую кислоту (150 мг, 0,76 ммоль) растворяли в 7 мл сухого CH3CN, а затем добавляли ЭДК-HCl (196 мг, 0,92 ммоль) и реакционную смесь перемешивали в течение 10 мин. В круглодонную колбу под атмосферой аргона добавляли 4-(пентафторсера)бензиламин (CAS: 771573-35-4, 196 мг, 0,84 ммоль) и ДМАП (112 мг, 0,92 ммоль). Реакционную смесь перемешивали в атмосфере аргона в течение 12 часов. Реакционную смесь концентрировали в вакууме. Остаток поглощали CH2Cl2 и промывали насыщенным водным раствором NaHCO3 (2×), 5%-ным водным раствором уксусной кислоты (2×), насыщенным водным раствором хлорида натрия, а затем сушили над сульфатом натрия. Осушающий агент удаляли фильтрованием, а органические фазы концентрировали в вакууме. Полученный остаток очищали на колонке из силикагеля (градиент растворителей ДХМ : EtOAc) или с помощью перекристаллизации из горячего CH3CN, что давало 131 мг 2,6-диметил-N-(4-(пентафтор-λ6-сульфанил)бензил)имидазо[2,1-b]тиазол-5-карбоксамида (ND-11860) в виде белого твердого вещества. Точка плавления = 147-148°С, для стандарта бензойной кислоты измерена при 113-114°С. 1Н ЯМР (300 МГц, CDCl3) δ м. д. 7,96 (с, 1Н), 7,73 (д, J=8,7 Гц, 2Н), 7,44 (д, J=8,3 Гц, 2Н), 6,17 (ш. с., 1Н, NH2), 4,69 (д, J=6,0 Гц, 2Н), 2,59 (с, 3Н), 2,42 (с, 3Н). 19F ЯМР (282 МГц, CDCl3) δ м. д. 84,5 (пентет, J=150,1 Гц, 1F), 63,0 (д, J=150,04 Гц, 4F).
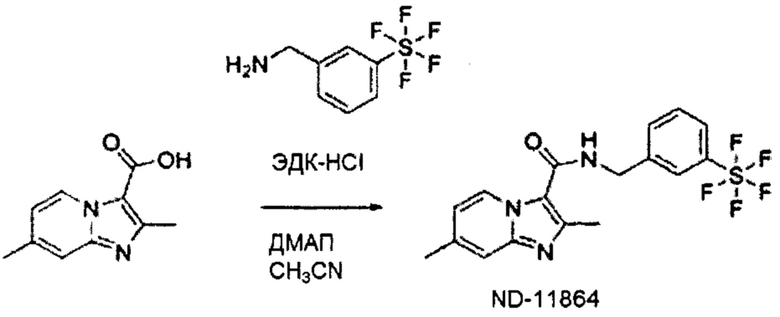
2,7-Диметилимидазо[1,2-а]пиридин-3-карбоновую кислоту (100 мг, 0,52 ммоль) растворяли в 5 мл сухого CH3CN, а затем добавляли ЭДК-HCl (82 мг, 0,57 ммоль) и реакционную смесь перемешивали в течение 10 мин. В круглодонную колбу под атмосферой аргона добавляли 3-(пентафторсера)бензиламин (CAS: 771573-34-3, 134 мг, 0,57 ммоль) и ДМАП (77 мг, 0,63 ммоль). Реакционную смесь перемешивали в атмосфере аргона в течение 12 часов. Реакционную смесь концентрировали в вакууме. Остаток поглощали CH2Cl2 и промывали насыщенным водным раствором NaHCO3 (2×), 5%-ным водным раствором уксусной кислоты (2×), насыщенным водным раствором хлорида натрия, а затем сушили над сульфатом натрия. Осушающий агент удаляли фильтрованием, а органические фазы концентрировали в вакууме. Полученный остаток очищали на колонке из силикагеля (градиент растворителей ДХМ : EtOAc) или с помощью перекристаллизации из горячего CH3CN, что давало 111 мг 2,7-диметил-N-(3-(пентафтор-λ6-сульфанил)бензил)имидазо[1,2-а]пиридин-3-карбоксамида (ND-11864) в виде белого твердого вещества. 1Н ЯМР (300 МГц, CDCl3) δ м. д. 9,25 (д, J=7,1 Гц, 1Н), 7,77 (с, 1Н), 7,68 (д, J=8,1 Гц, 1Н), 7,33 (с, 1Н), 7,59-7,41 (м, 2Н), 6,78 (д, J=7,1, 1Н), 6,32 (ш. с., 1Н, NH2), 4,75 (д, J=6,0 Гц, 2Н), 2,68 (с, 3Н), 2,42 (с, 3Н). 19F ЯМР (282 МГц, CDCl3) δ м. д. 84,4 (пентет, J=149,5 Гц, 1F), 62,9 (д, J=150,00 Гц, 4F).
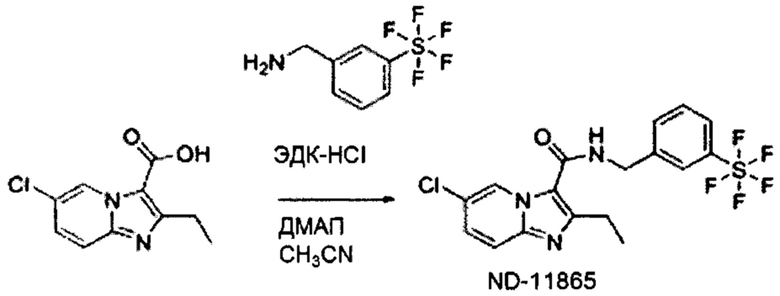
6-Хлор-2-этилимидазо[1,2-а]пиридин-3-карбоновую кислоту (100 мг, 0,45 ммоль) растворяли в 5 мл сухого CH3CN, а затем добавляли ЭДК-HCl (69 мг, 0,45 ммоль) и реакционную смесь перемешивали в течение 10 мин. В круглодонную колбу под атмосферой аргона добавляли 3-(пентафторсера)бензиламин (CAS: 771573-34-3, 114 мг, 0,49 ммоль) и ДМАП (65 мг, 0,53 ммоль). Реакционную смесь перемешивали в атмосфере аргона в течение 12 часов. Реакционную смесь концентрировали в вакууме. Остаток поглощали CH2Cl2 и промывали насыщенным водным раствором NaHCO3 (2×), 5%-ным водным раствором уксусной кислоты (2×), насыщенным водным раствором хлорида натрия, а затем сушили над сульфатом натрия. Осушающий агент удаляли фильтрованием, а органические фазы концентрировали в вакууме. Полученный остаток очищали на колонке из силикагеля (градиент растворителей ДХМ : EtOAc) или с помощью перекристаллизации из горячего CH3CN, что давало 71 мг 6-хлор-2-этил-N-(3-(пентафтор-λ6-сульфанил)бензил)имидазо[1,2-а]пиридин-3-карбоксамида (ND-11865) в виде белого твердого вещества. 1Н ЯМР (300 МГц, CDCl3) δ м. д. 9,49 (с, 1Н), 7,77 (с, 1Н), 7,70 (д, J=8,0 Гц, 1H), 7,63-7,43 (м, 4Н), 7,33 (д, J=9,4 Гц, 1Н), 6,36 (ш. с., 1Н, NH2), 4,76 (д, J=5,9 Гц, 2Н), 3,02 (к, J=7,5, 7,5, 7,5 Гц, 2Н), 1,42 (т, J=7,5, 7,5 Гц, 3Н). 19F ЯМР (282 МГц, CDCl3) δ м. д. 84,6 (пентет, J=149,8 Гц, 1F), 62,8 (д, J=150,00 Гц, 4F).
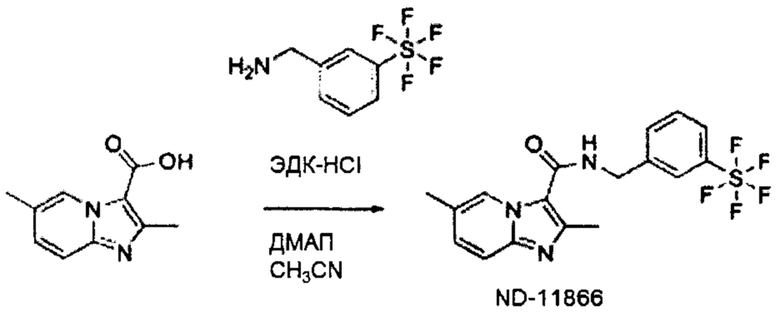
2,6-Диметилимидазо[1,2-а]пиридин-3-карбоновую кислоту (100 мг, 0,52 ммоль) растворяли в 5 мл сухого CH3CN, а затем добавляли ЭДК-HCl (82 мг, 0,57 ммоль) и реакционную смесь перемешивали в течение 10 мин. В круглодонную колбу под атмосферой аргона добавляли 3-(пентафторсера)бензиламин (CAS: 771573-34-3, 134 мг, 0,57 ммоль) и ДМАП (77 мг, 0,63 ммоль). Реакционную смесь перемешивали в атмосфере аргона в течение 12 часов. Реакционную смесь концентрировали в вакууме. Остаток поглощали CH2Cl2 и промывали насыщенным водным раствором NaHCO3 (2×), 5%-ным водным раствором уксусной кислоты (2×), насыщенным водным раствором хлорида натрия, а затем сушили над сульфатом натрия. Осушающий агент удаляли фильтрованием, а органические фазы концентрировали в вакууме. Полученный остаток очищали на колонке из силикагеля (градиент растворителей ДХМ : EtOAc) или с помощью перекристаллизации из горячего CH3CN, что давало 75 мг 2,6-диметил-N-(3-(пентафтор-λ6-сульфанил)бензил)имидазо[1,2-a]пиридин-3-карбоксамида (ND-11866) в виде белого твердого вещества. 1Н ЯМР (300 МГц, CDCl3) δ м. д. 9,19 (с, 1Н), 7,77 (с, 1Н), 7,69 (д, J=8,2 Гц, 1Н), 7,60-7,45 (м, 3Н), 7,21 (д, J=9,1 Гц, 1Н), 6,34 (ш. с., 1Н, NH2), 4,76 (д, J=6,0 Гц, 2Н), 2,70 (с, 3Н), 2,36 (с, 3Н). 19F ЯМР (282 МГц, CDCl3) δ м. д. 84,4 (пентет, J=149,5 Гц, 1F), 62,3 (д, J=150,00 Гц, 4F).
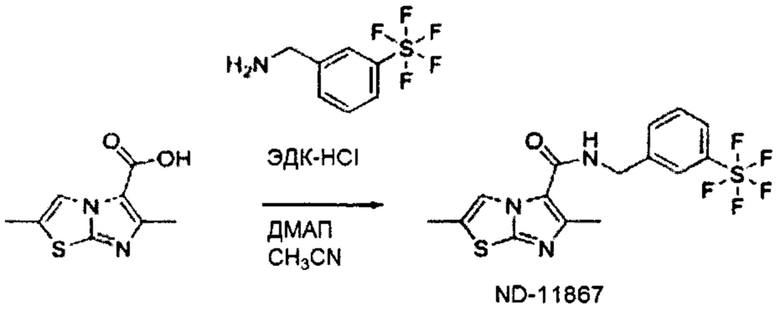
2,6-Диметилимидазо[2,1-b]тиазол-5-карбоновую кислоту (100 мг, 0,51 ммоль) растворяли в 5 мл сухого CH3CN, а затем добавляли ЭДК-HCl (72 мг, 0,46 ммоль) и реакционную смесь перемешивали в течение 10 мин. В круглодонную колбу под атмосферой аргона добавляли 3-(пентафторсера)бензиламин (CAS: 771573-34-3, 118 мг, 0,51 ммоль) и ДМАП (68 мг, 0,55 ммоль). Реакционную смесь перемешивали в атмосфере аргона в течение 12 часов. Реакционную смесь концентрировали в вакууме. Остаток поглощали CH2Cl2 и промывали насыщенным водным раствором NaHCO3 (2×), 5%-ным водным раствором уксусной кислоты (2×), насыщенным водным раствором хлорида натрия, а затем сушили над сульфатом натрия. Осушающий агент удаляли фильтрованием, а органические фазы концентрировали в вакууме. Полученный остаток очищали на колонке из силикагеля (градиент растворителей ДХМ : EtOAc) или с помощью перекристаллизации из горячего CH3CN, что давало 109 мг 2,6-диметил-N-(3-(пентафтор-λ6-сульфанил)бензил)имидазо[2,1-b]тиазол-5-карбоксамида (ND-11867) в виде белого твердого вещества. 1Н ЯМР (300 МГц, CDCl3) δ м. д. 7,97 (с, 1Н), 7,74 (с, 1Н), 7,69 (д, J=8,2 Гц, 1Н), 7,55-7,43 (м, 2Н), 6,07 (ш. с., 1H, NH2), 4,72 (д, J=6,0 Гц, 2Н), 2,59 (с, 3Н), 2,44 (с, 3Н).
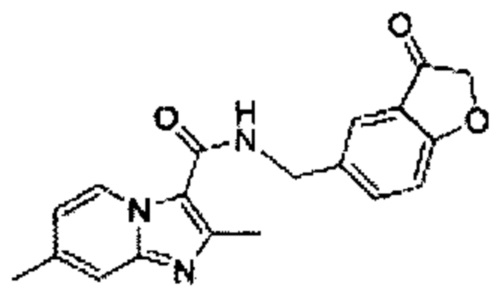
2,7-диметил-N-((3-оксо-2,3-дигидробензофуран-5-ил)метил)имидазо[1,2-а]пиридин-3-карбоксамид
2,7-Диметилимидазо[1,2-а]пиридин-3-карбоновую кислоту (1 ммоль) и ЭДК-HCl (1,2 ммоль) добавляли вместе и реакционную смесь перемешивали в течение 10 мин в сухом CH3CN. Затем добавляли 5-(аминометил)бензофуран-3(2H)-он (CAS: 1630261-74-3) (1,1 ммоль) и ДМАП (1,2 ммоль) и реакционную смесь перемешивали в течение 16 часов под атмосферой аргона. Реакционную смесь концентрировали в вакууме.
Остаток поглощали CH2Cl2 и промывали насыщенным водным раствором NaHCO3 (2×), 5%-ным водным раствором уксусной кислоты (2×), насыщенным водным раствором хлорида натрия, а затем сушили над сульфатом натрия. Осушающий агент удаляли фильтрованием, а органические фазы концентрировали в вакууме. Полученный остаток очищали на колонке из силикагеля (градиент CH2Cl2 : EtOAc или EtOAc : EtOH) или с помощью перекристаллизации из горячего CH3CN, что давало требуемый продукт 2,7-диметил-N-((3-оксо-2,3-дигидробензофуран-5-ил)метил)имидазо[1,2-а]пиридин-3-карбоксамид.
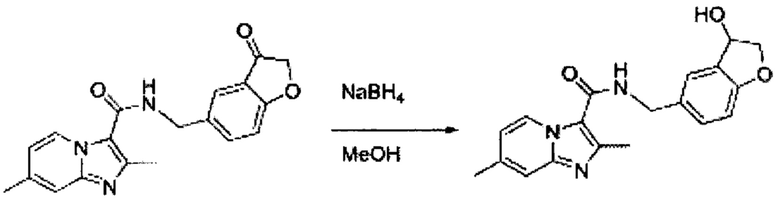
2,7-Диметил-N-((3-оксо-2,3-дигидробензофуран-5-ил)метил)имидазо[1,2-а]пиридин-3-карбоксамид можно восстанавливать с помощью NaBH4, как описано в Tetrahedron, 45(5), 1441-6; 1989 или Beilstein Journal of Organic Chemistry, 6, 1061-1069, No. 121; 2010.
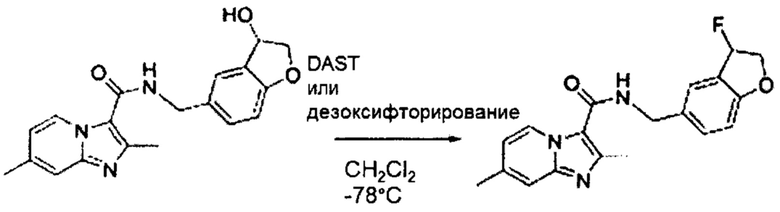
Спирт можно превратить во фторид с использованием DAST (диэтиламиносератрифторида), как описано в Journal of Heterocyclic Chemistry, 45(3), 887-896; 2008.
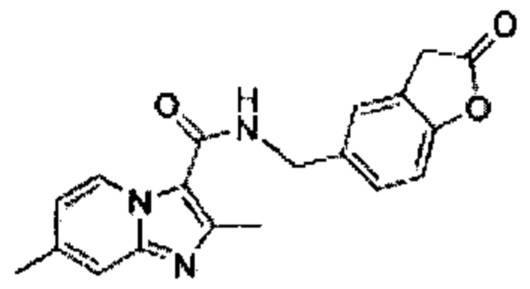
2,7-диметил-N-((2-оксо-2,3-дигидробензофуран-5-ил)метил)имидазо[1,2-а]пиридин-3-карбоксамид
2,7-Диметилимидазо[1,2-а]пиридин-3-карбоновую кислоту (1 ммоль) и ЭДК-HCl (1,2 ммоль) объединяли вместе и реакционную смесь перемешивали в течение 10 мин в сухом CH3CN. Затем добавляли 5-(аминометил)бензофуран-2(3H)-он (CAS: 16933726-57-9) (1,1 ммоль) и ДМАП (1,2 ммоль) и реакционную смесь перемешивали в течение 16 часов под атмосферой аргона. Реакционную смесь концентрировали в вакууме.
Остаток поглощали CH2Cl2 и промывали насыщенным водным раствором NaHCO3 (2×), 5%-ным водным раствором уксусной кислоты (2×), насыщенным водным раствором хлорида натрия, а затем сушили над сульфатом натрия. Осушающий агент удаляли фильтрованием, а органические фазы концентрировали в вакууме. Полученный остаток очищали на колонке из силикагеля (градиент CH2Cl2 : EtOAc или EtOAc : EtOH) или с помощью перекристаллизации из горячего CH3CN, что давало требуемый продукт 2,7-диметил-N-((2-оксо-2,3-дигидробензофуран-5-ил)метил)имидазо[1,2-а]пиридин-3-карбоксамид.
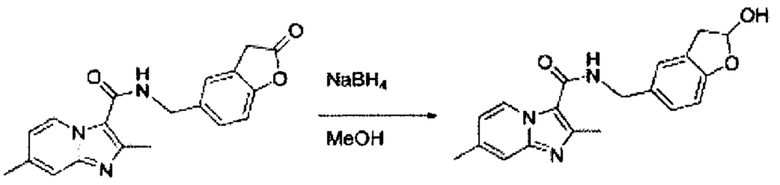
2,7-Диметил-N-((3-оксо-2,3-дигидробензофуран-5-ил)метил)имидазо[1,2-a]пиридин-3-карбоксамид можно восстанавливать с помощью NaBH4, как описано в Tetrahedron, 45(5), 1441-6; 1989 или Beilstein Journal of Organic Chemistry, 6, 1061-1069, No. 121; 2010.
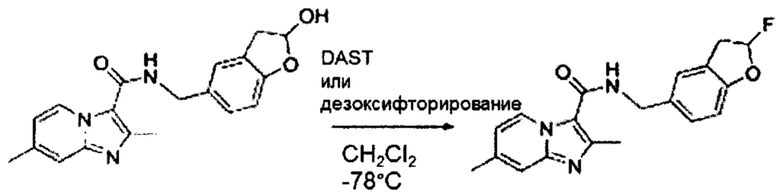
Спирт можно превращать во фторид с использованием DAST, как описано в Journal of Heterocyclic Chemistry, 45(3), 887-896; 2008.
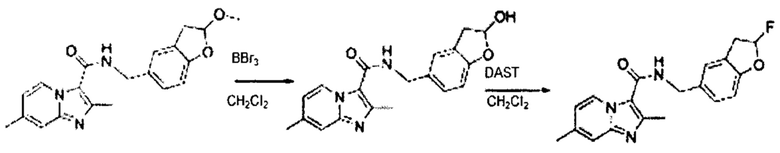
Как альтернативный вариант, гидрокси-соединение можно получать при синтезе N-((2-метокси-2,3-дигидробензофуран-5-ил)метил)-2,7-диметилимидазо[1,2-а]пиридин-3-карбоксамида с последующим деметилированием с использованием трибромида бора (BBr3) с помощью способа, описанного в Bioorganic & Medicinal Chemistry Letters, 19(16), 4882-4884; 2009.
N-((2-Метокси-2,3-дигидробензофуран-5-ил)метил)-2,7-диметилимидазо[1,2-а]пиридин-3-карбоксамид получают с помощью опосредованного ЭДК сочетания 2,7-диметилимидазо[1,2-а]пиридин-3-карбоновой кислоты и (2-метокси-2,3-дигидробензофуран-5-ил)метанамина (CAS: 1431851-43-2) по общей методике, описанной ранее.
Каждое из соединений, изображенных на фигурах, включено в данный документ и составляет часть этого описания.
Полное содержание каждого упоминания, патентного документа, статьи и тому подобного, описанных в данном документе, независимо включено в данный документ посредством ссылки.
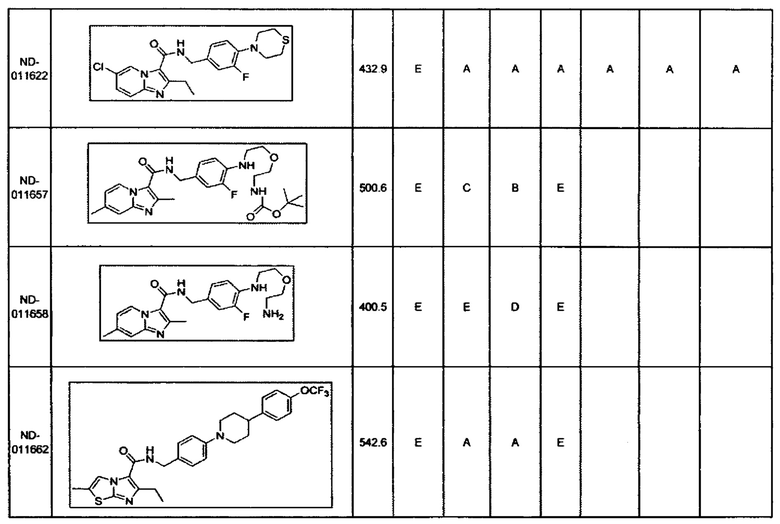
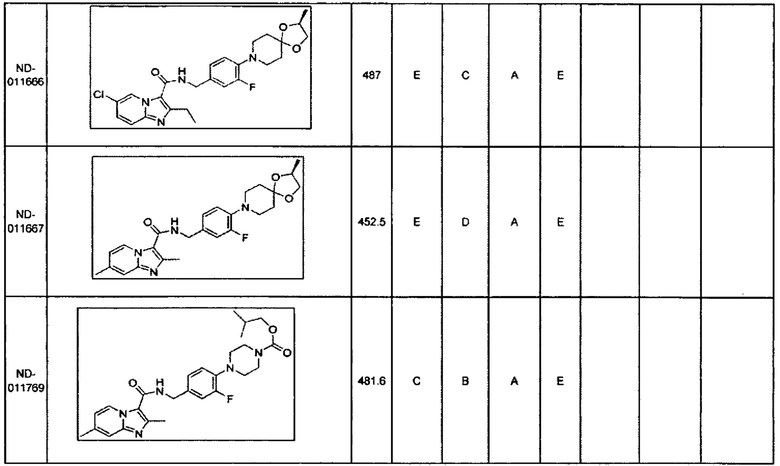
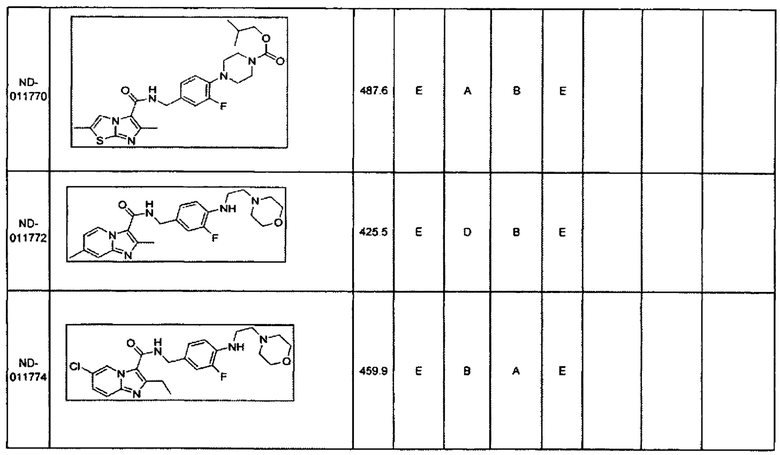
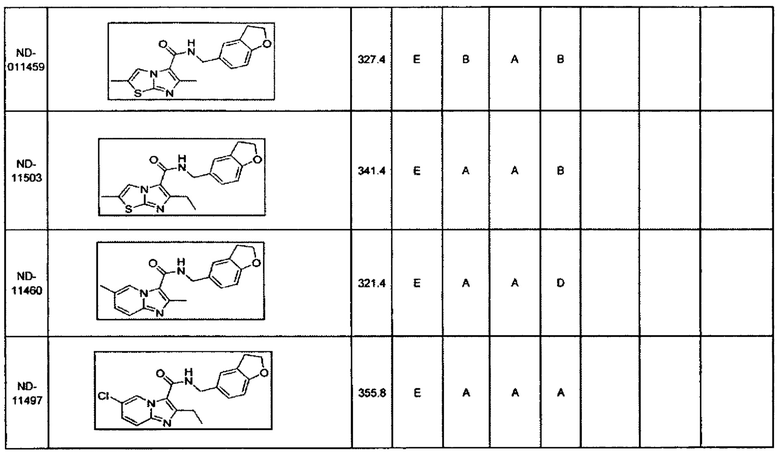
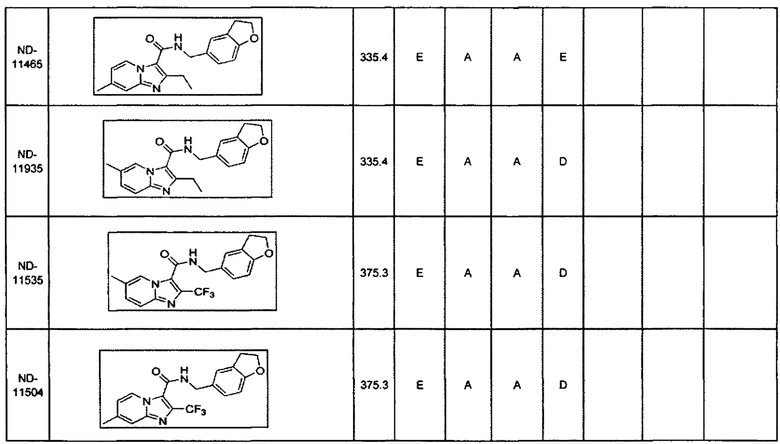
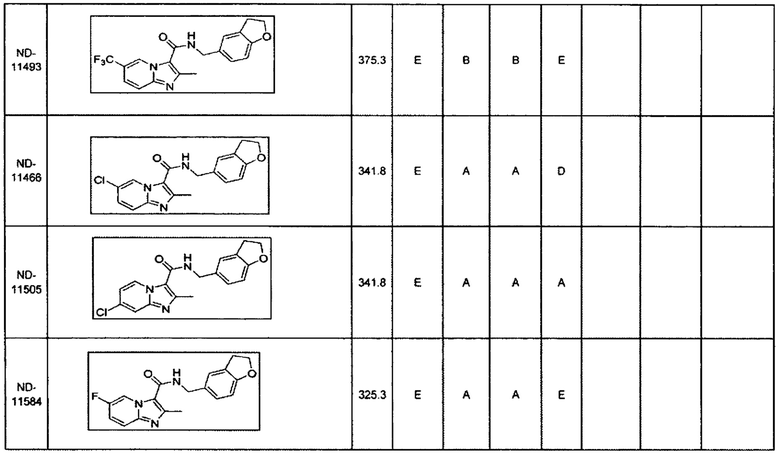
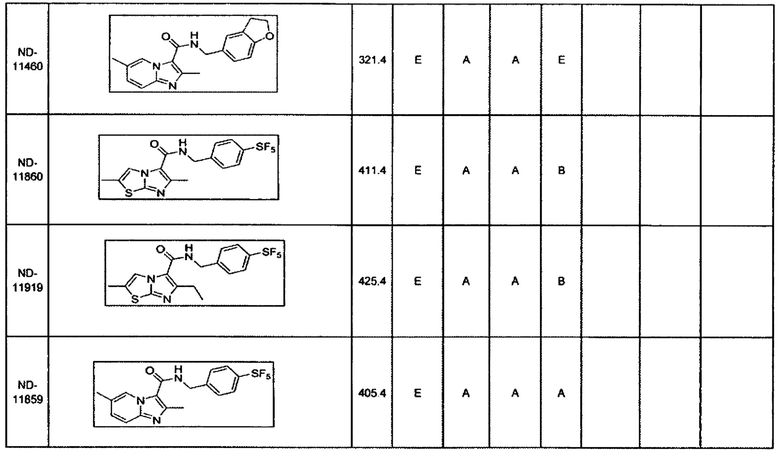
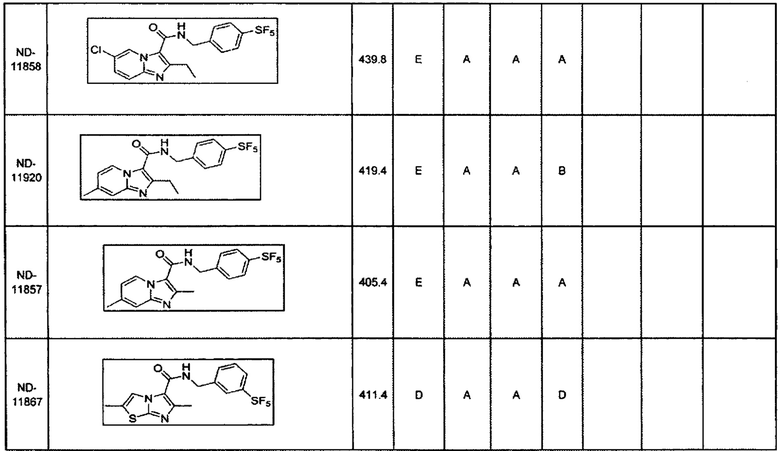
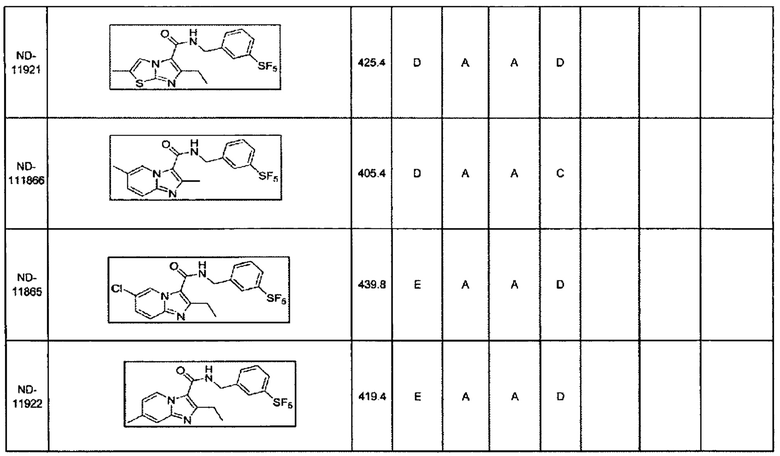
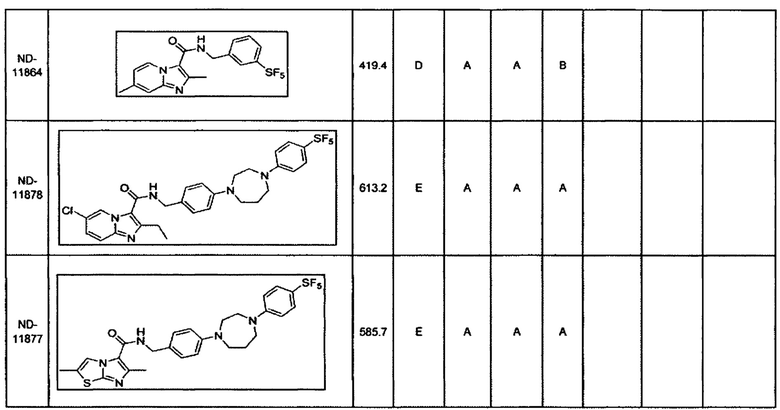
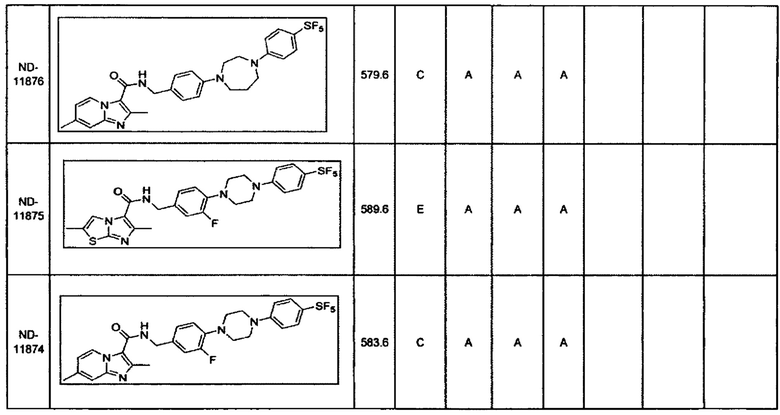
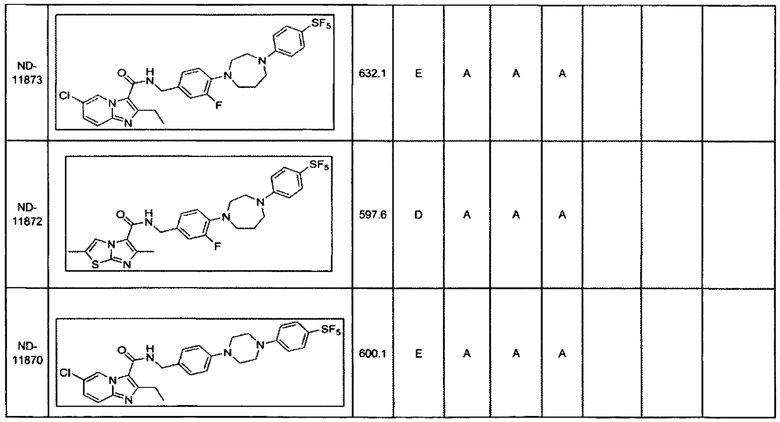
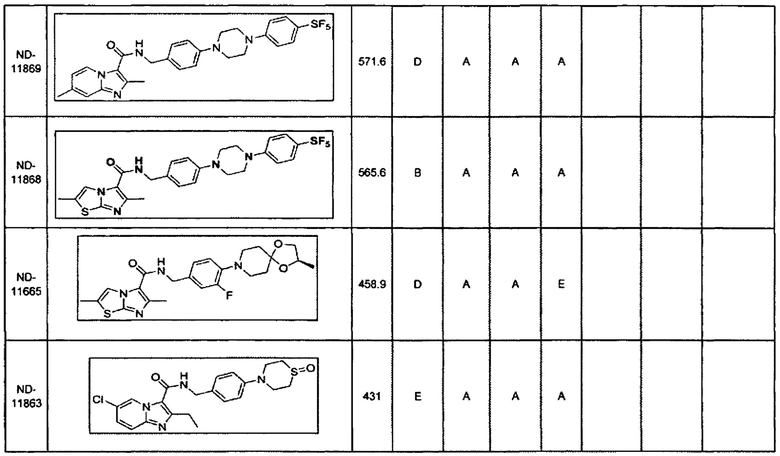
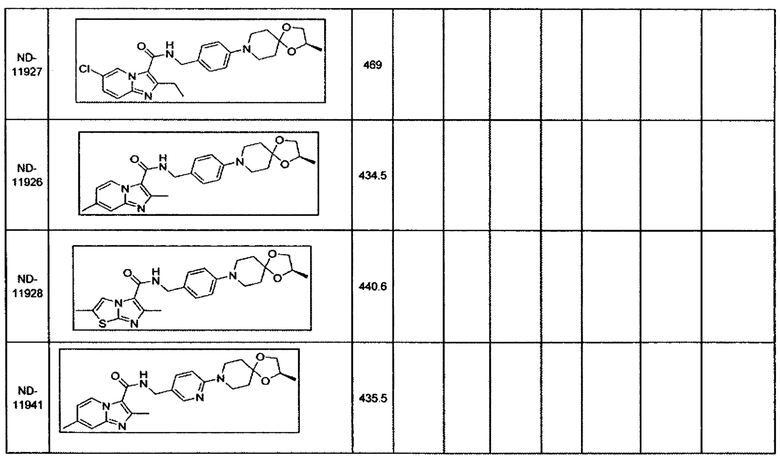
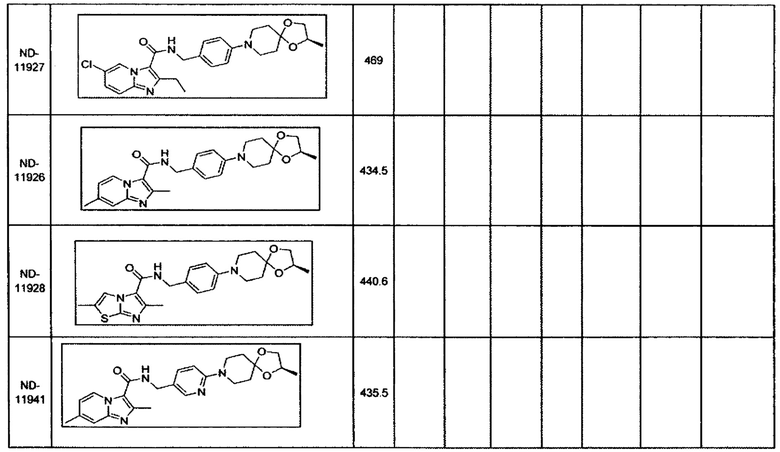
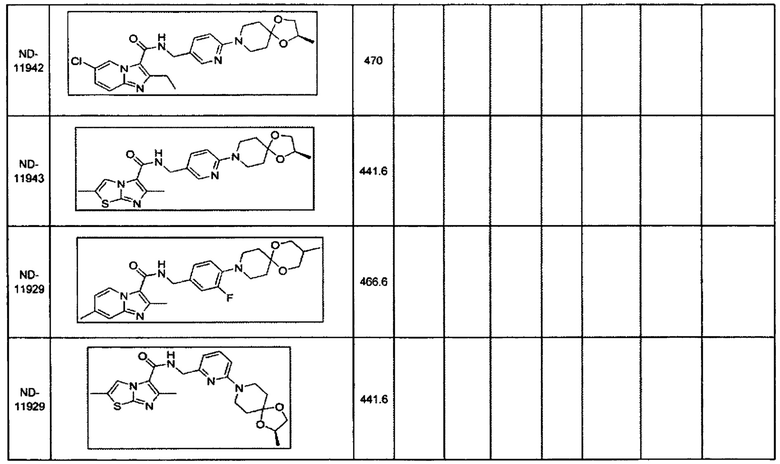
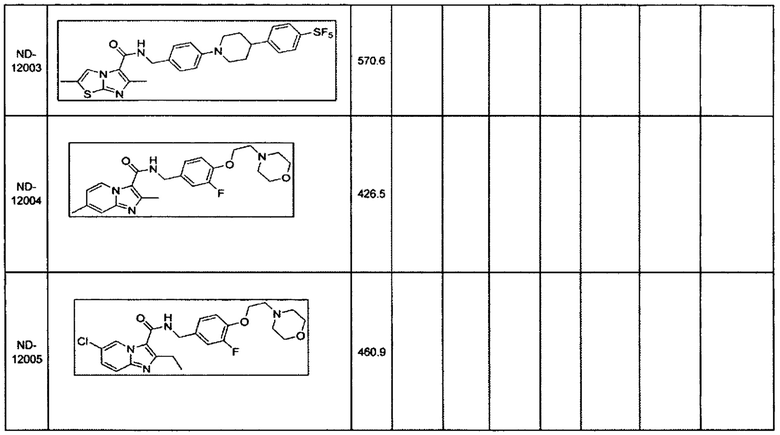
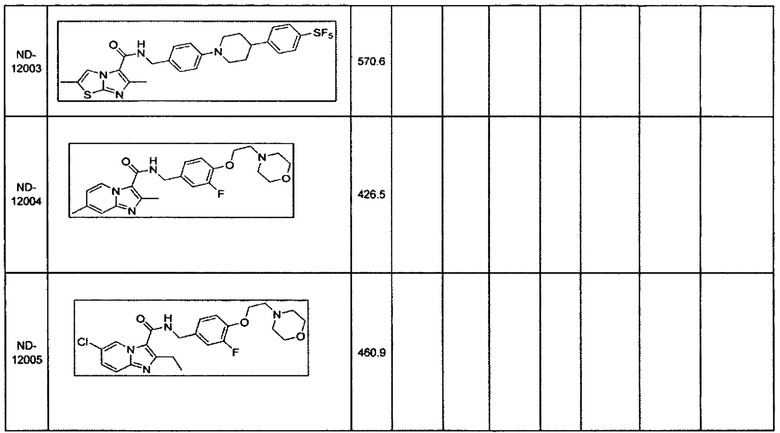
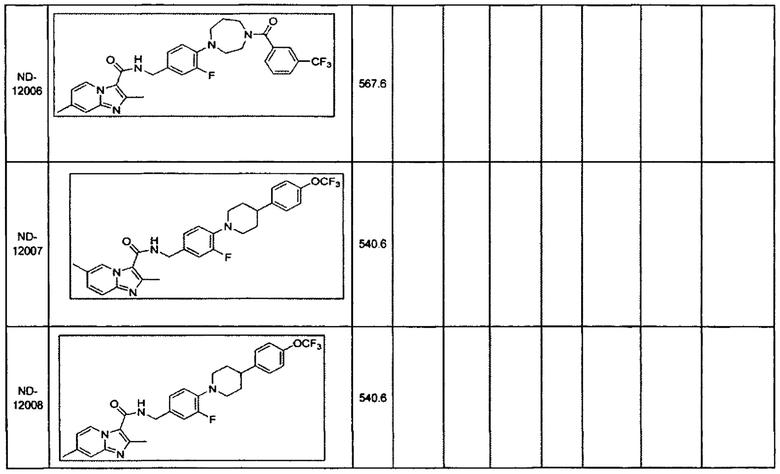
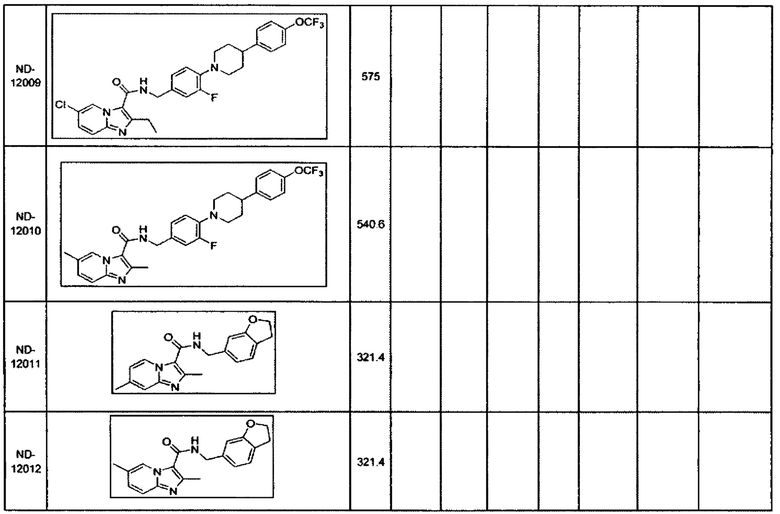
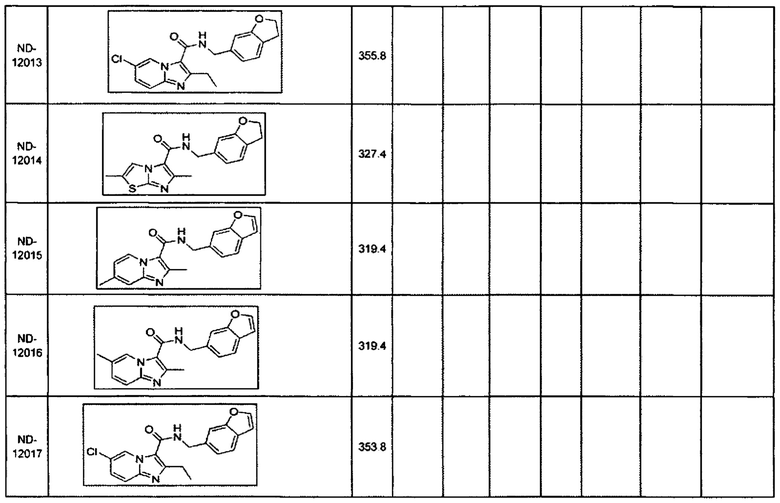
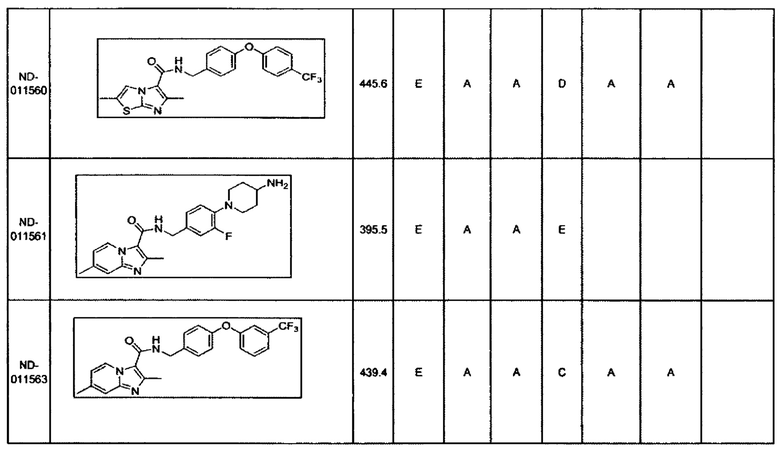
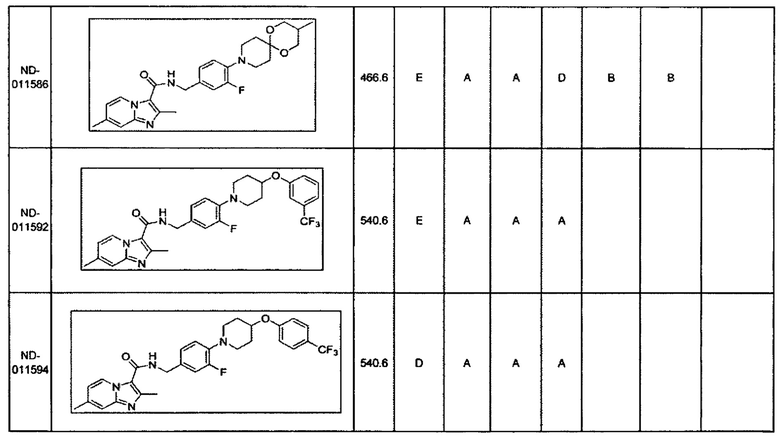
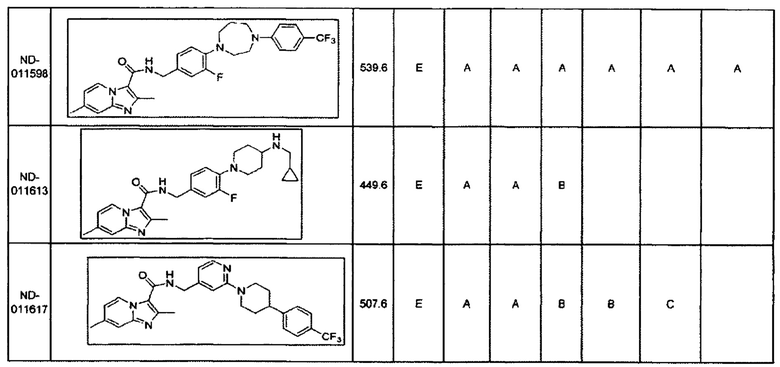
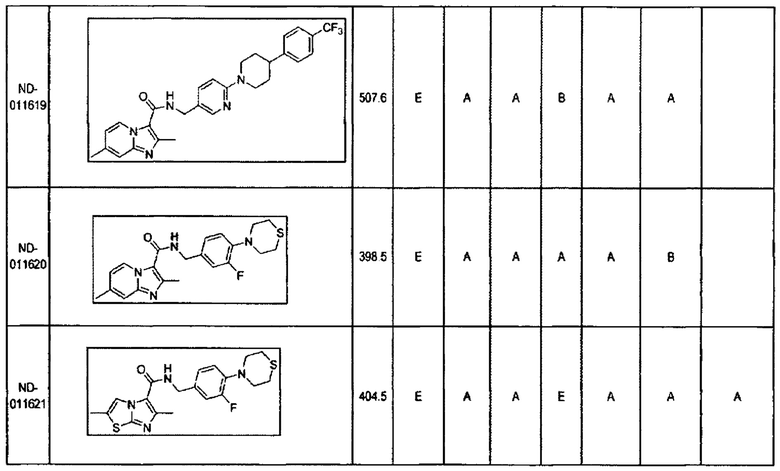
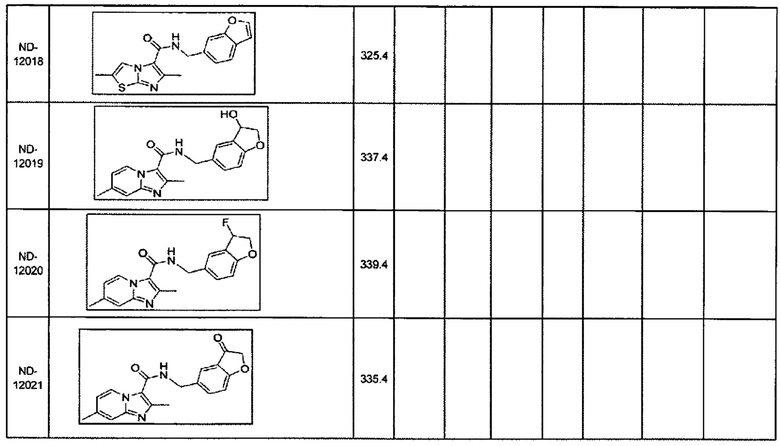
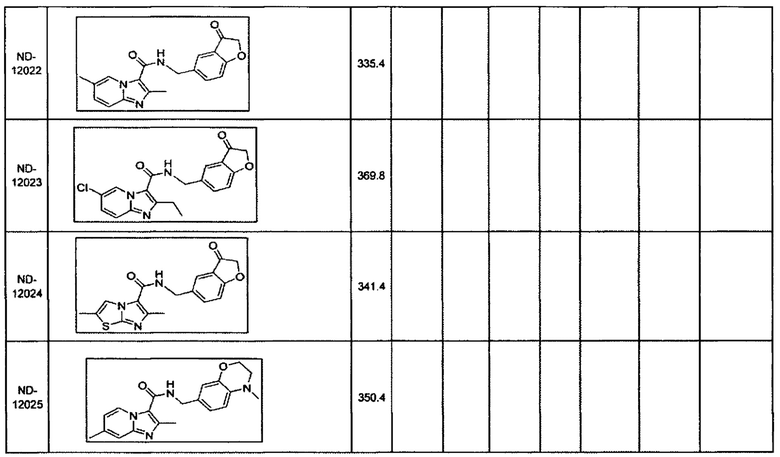
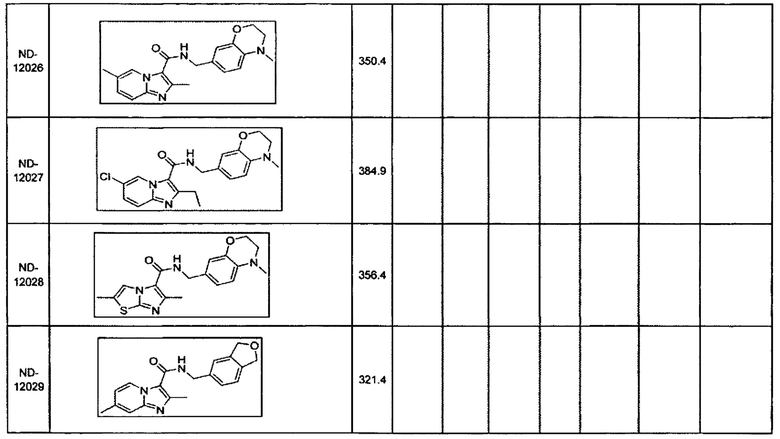
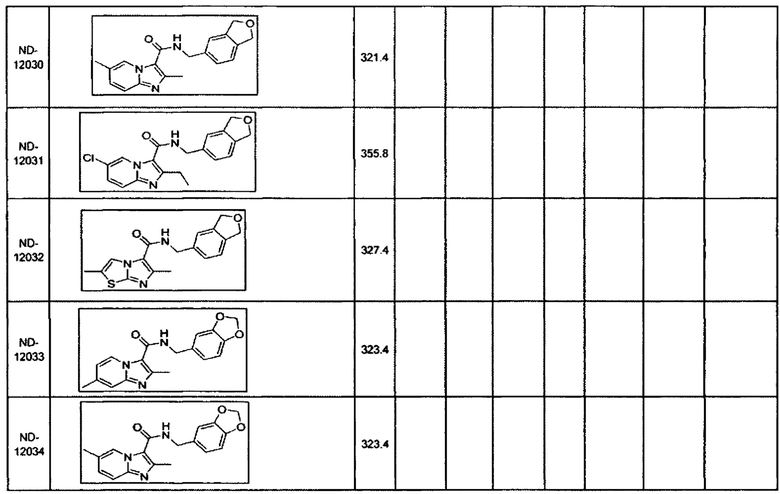
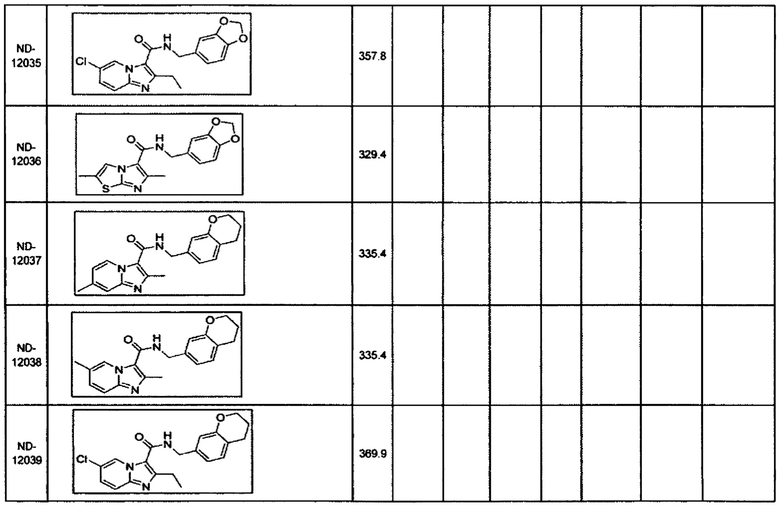
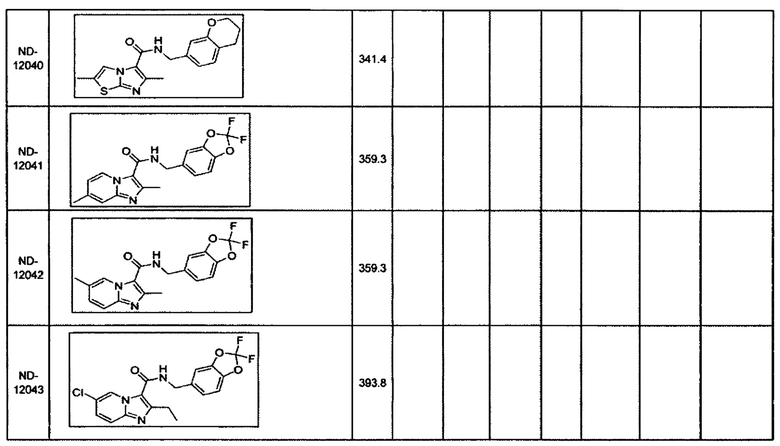
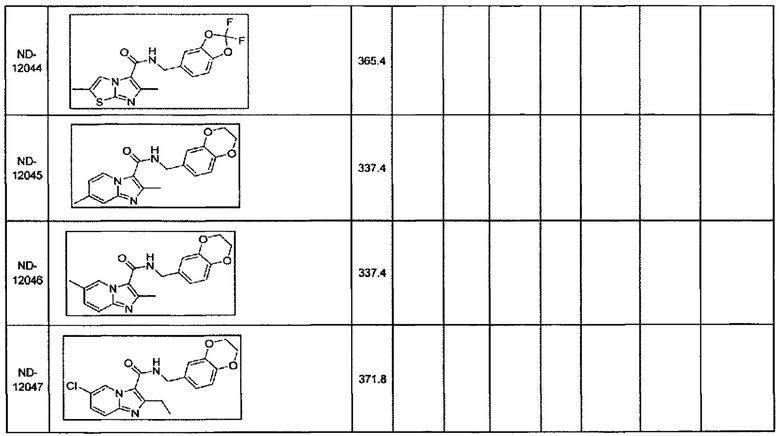
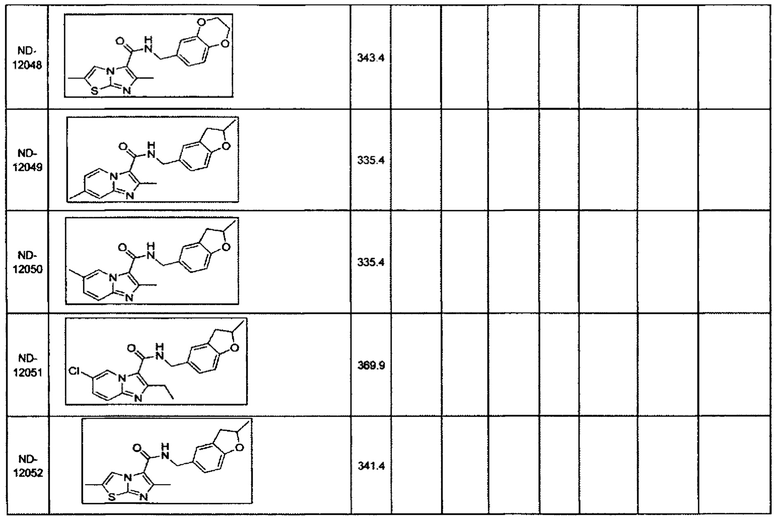
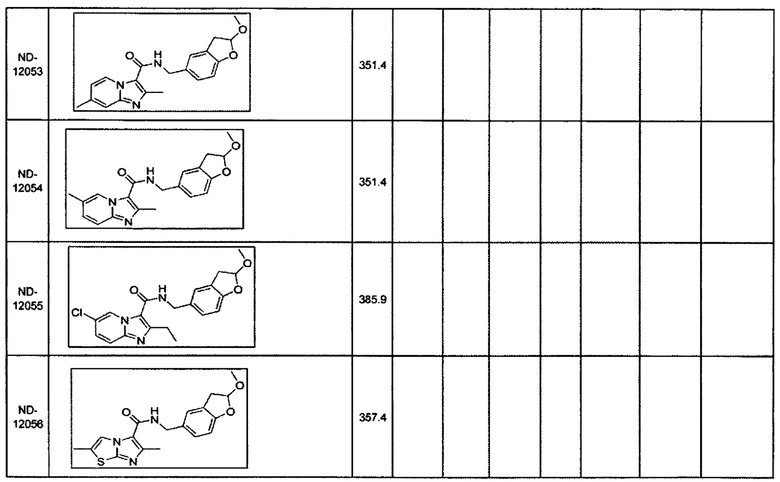
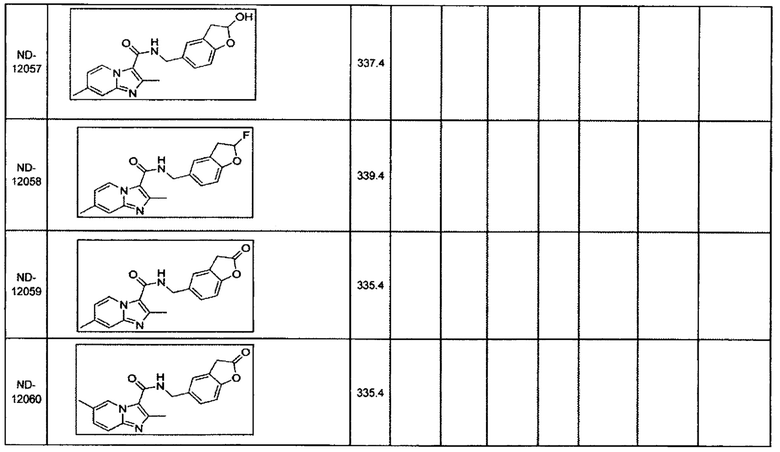
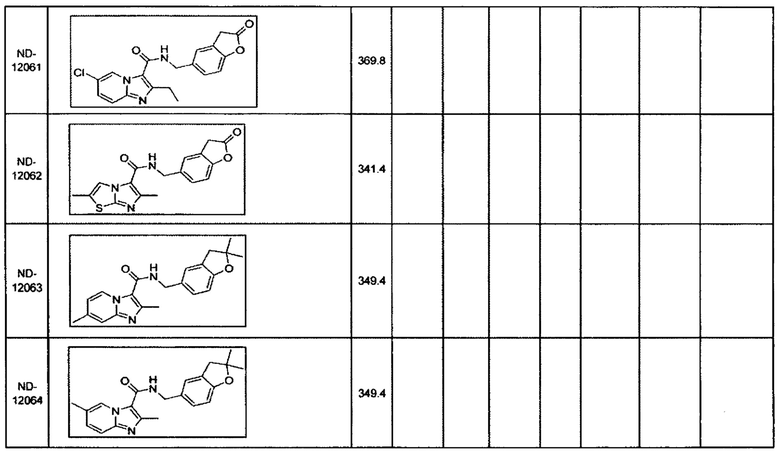
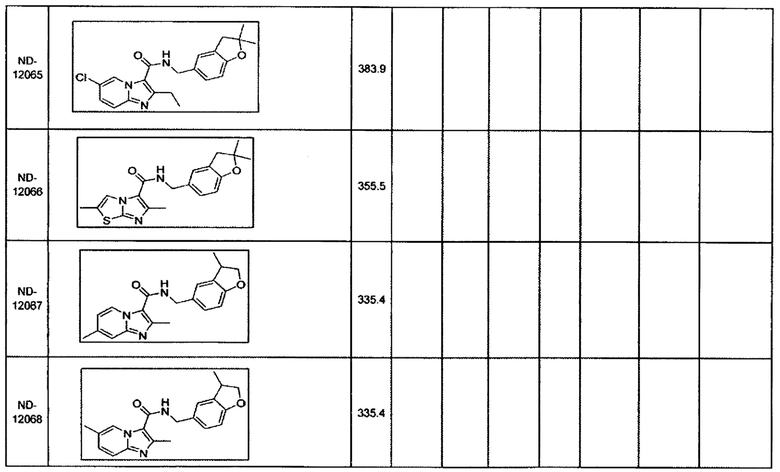
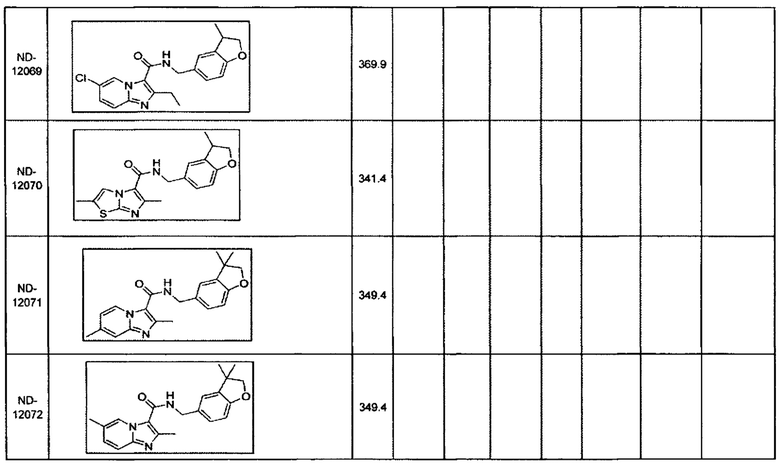
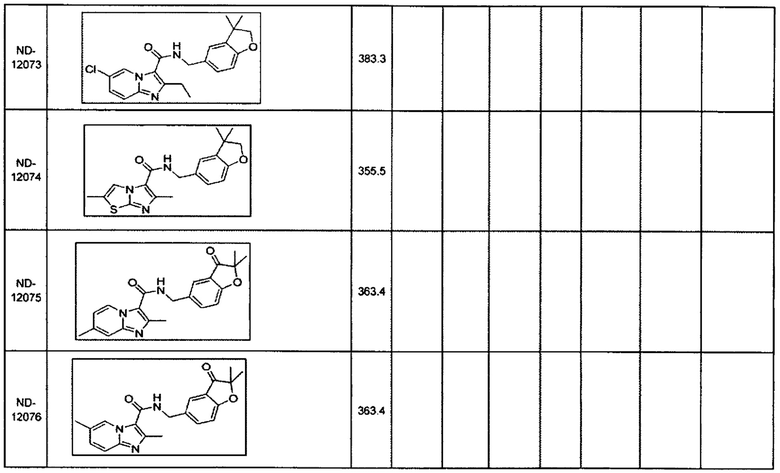
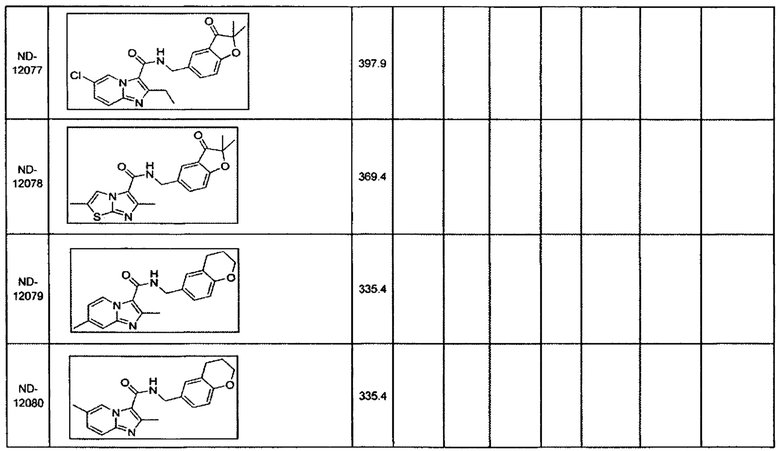
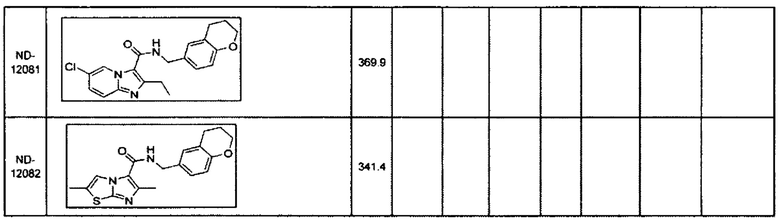
| название | год | авторы | номер документа |
|---|---|---|---|
| 5,5-ГЕТЕРОАРОМАТИЧЕСКИЕ ПРОТИВОИНФЕКЦИОННЫЕ СОЕДИНЕНИЯ | 2013 |
|
RU2696278C2 |
| β-ЛАКТАМИЛЗАМЕЩЕННЫЕ АНАЛОГИ ФЕНИЛАЛАНИНА, ЦИСТЕИНА И СЕРИНА В КАЧЕСТВЕ АНТАГОНИСТОВ ВАЗОПРЕССИНА | 2006 |
|
RU2466991C2 |
| ЦИТОТОКСИЧЕСКИЕ ПРОИЗВОДНЫЕ БЕНЗОДИАЗЕПИНА | 2012 |
|
RU2631498C2 |
| ТИЕНО[2,3-d]ПИРИМИДИНЫ В КАЧЕСТВЕ АНТИМИКРОБНЫХ АГЕНТОВ | 2018 |
|
RU2803136C2 |
| СОЕДИНЕНИЯ ИМИДАЗО[1,2-а] ПИРИДИНА, ИХ СИНТЕЗ И СПОСОБЫ ПРИМЕНЕНИЯ | 2010 |
|
RU2608611C2 |
| 2, 5-ДИЗАМЕЩЕННЫЕ АРИЛСУЛЬФОНАМИДНЫЕ АНТАГОНИСТЫ ССR3 | 2010 |
|
RU2527165C2 |
| ТЕРАПЕВТИЧЕСКИЕ СОЕДИНЕНИЯ И КОМПОЗИЦИИ | 2015 |
|
RU2733405C2 |
| ЗАМЕЩЕННЫЕ ИМИДАЗО[1,2-b]ПИРИДАЗИНЫ, ЗАМЕЩЕННЫЕ ИМИДАЗО[1,5-b]ПИРИДАЗИНЫ, РОДСТВЕННЫЕ СОЕДИНЕНИЯ И ИХ ПРИМЕНЕНИЕ ДЛЯ ЛЕЧЕНИЯ ПАТОЛОГИЧЕСКИХ СОСТОЯНИЙ | 2017 |
|
RU2773333C2 |
| СОЕДИНЕНИЯ, МОДУЛИРУЮЩИЕ ЭСТРОГЕНОВЫЕ РЕЦЕПТОРЫ | 2019 |
|
RU2826635C2 |
| ГЕТЕРОЦИКЛИЧЕСКИЕ МОДУЛЯТОРЫ ТРАНСПОРТЕРОВ АТФ-СВЯЗЫВАЮЩЕЙ КАССЕТЫ | 2016 |
|
RU2765714C2 |

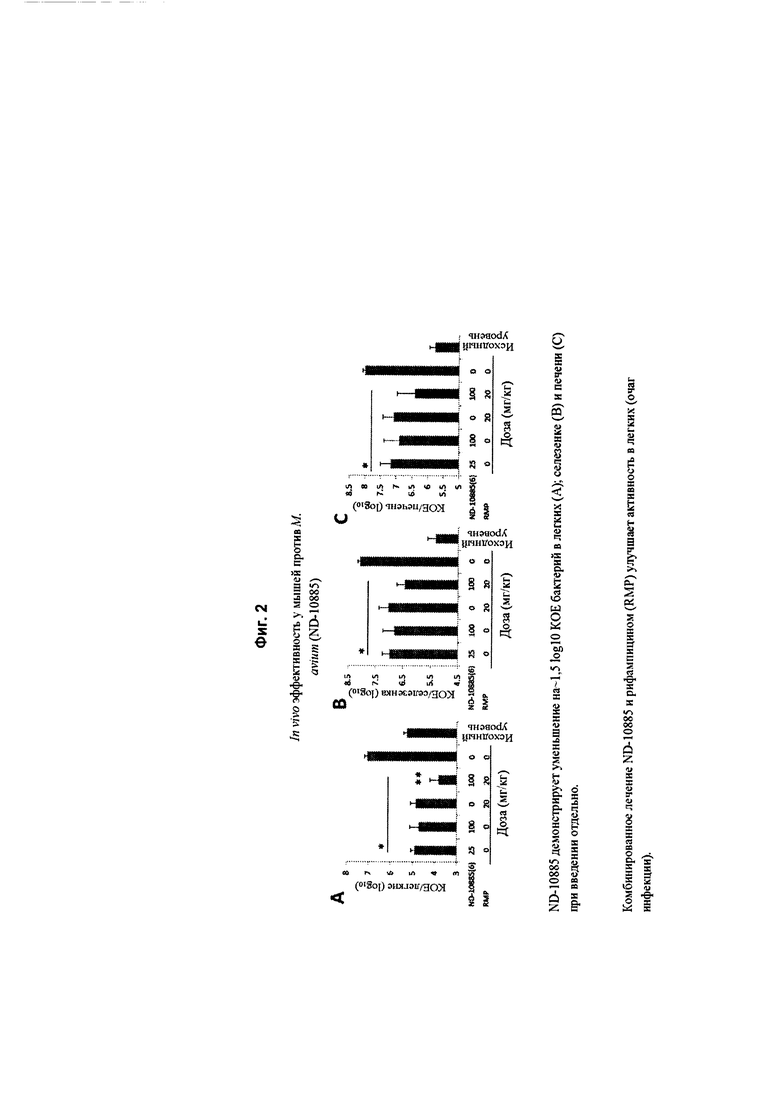
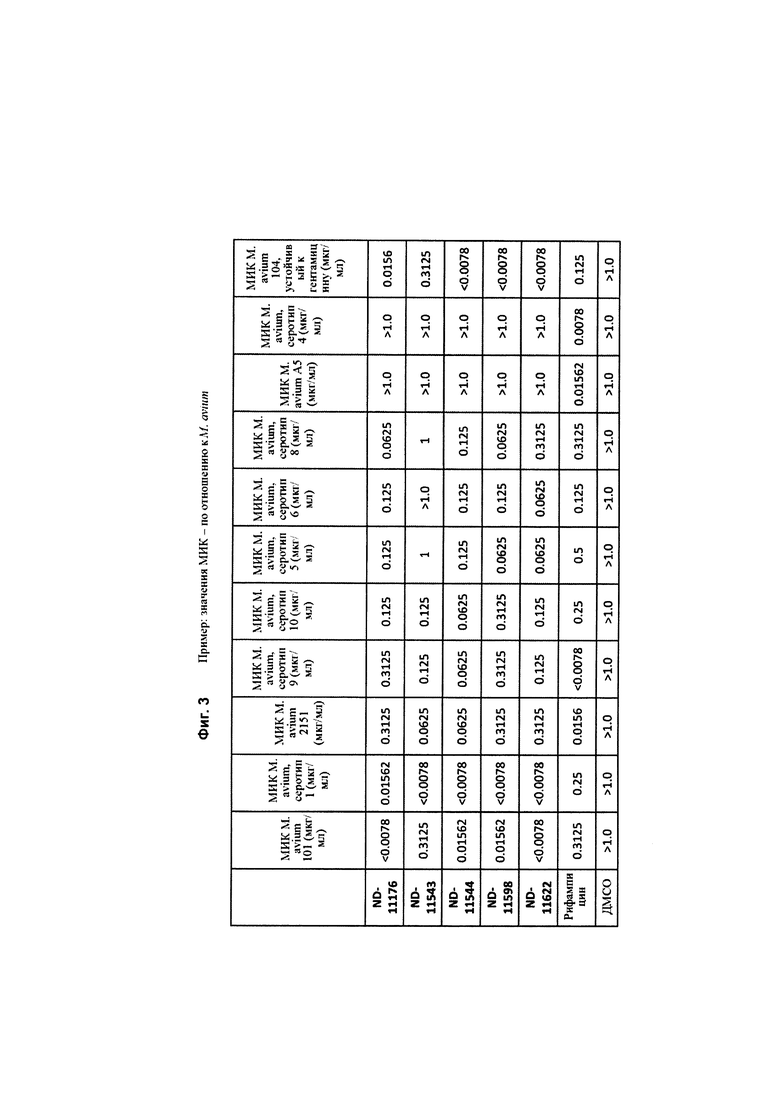
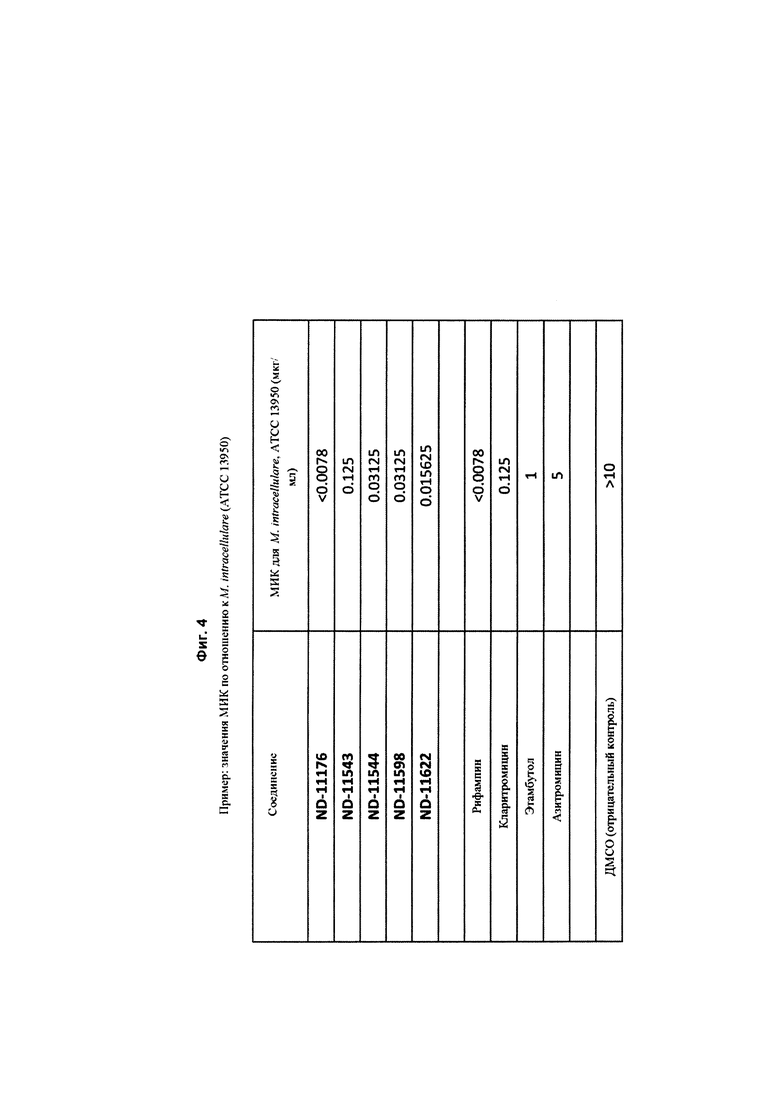
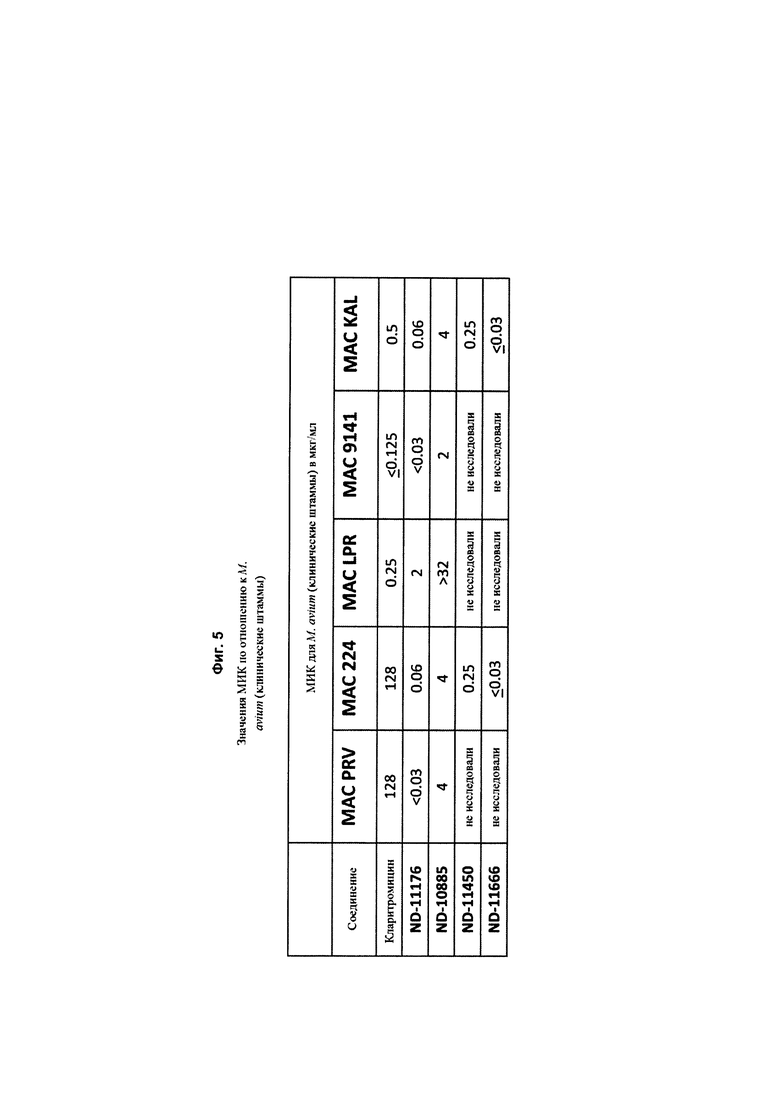
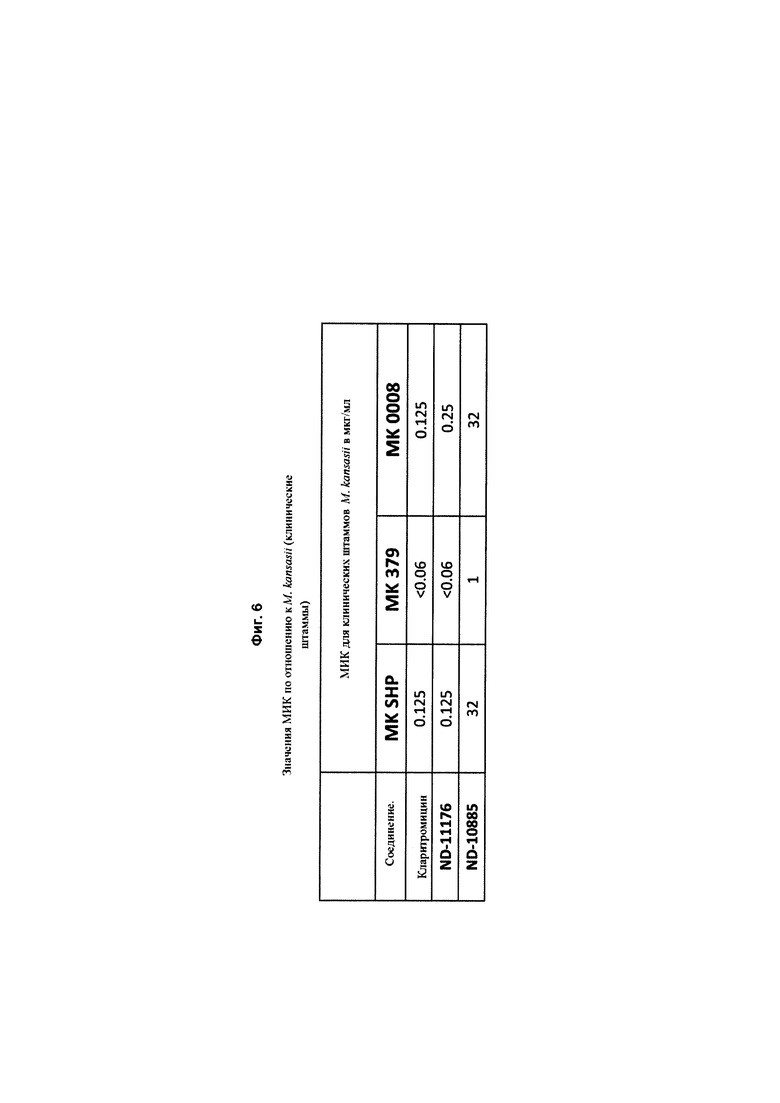
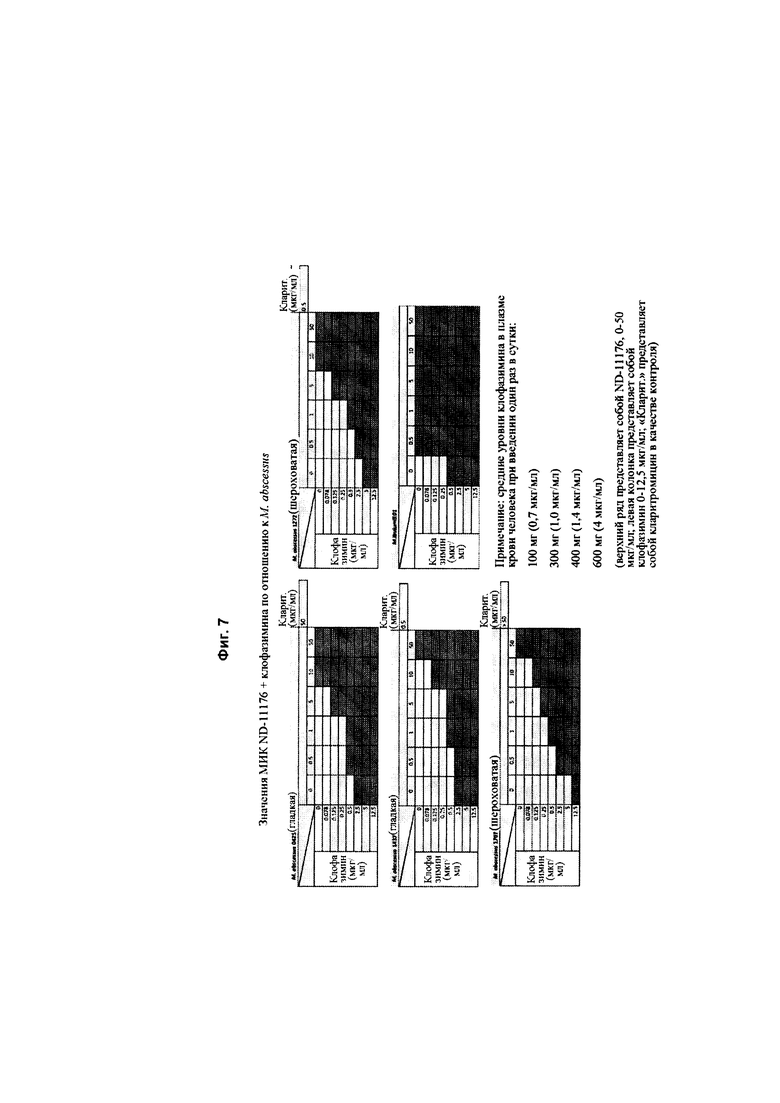
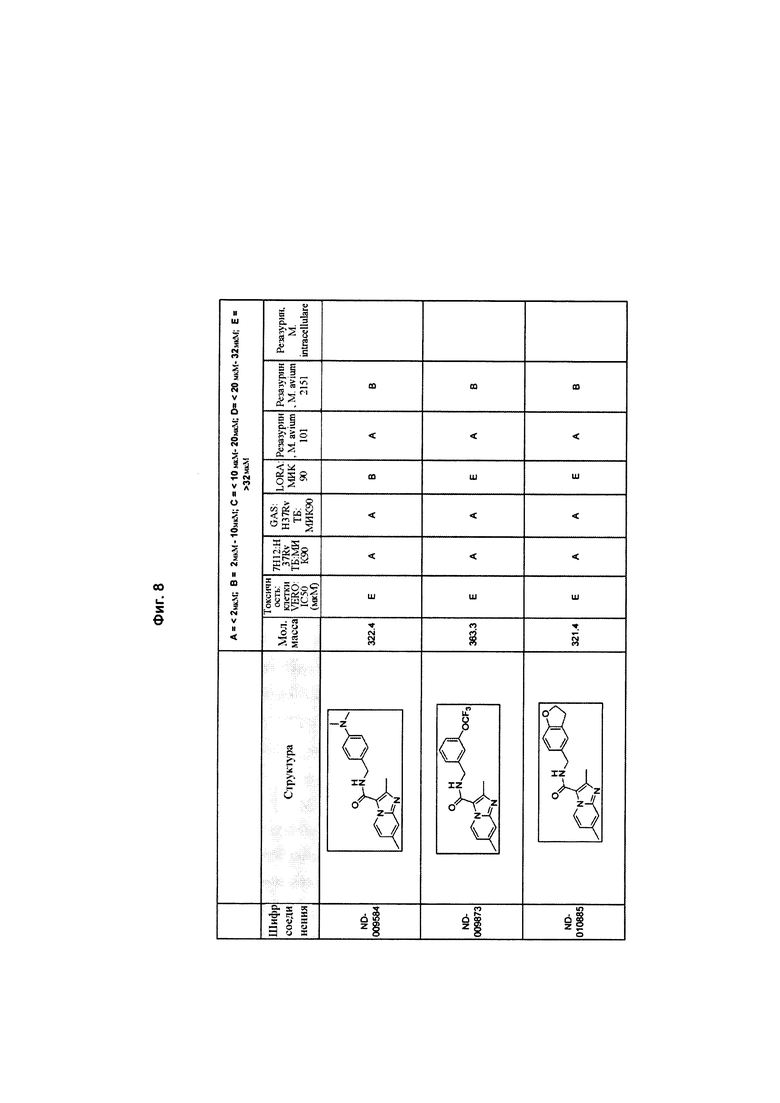
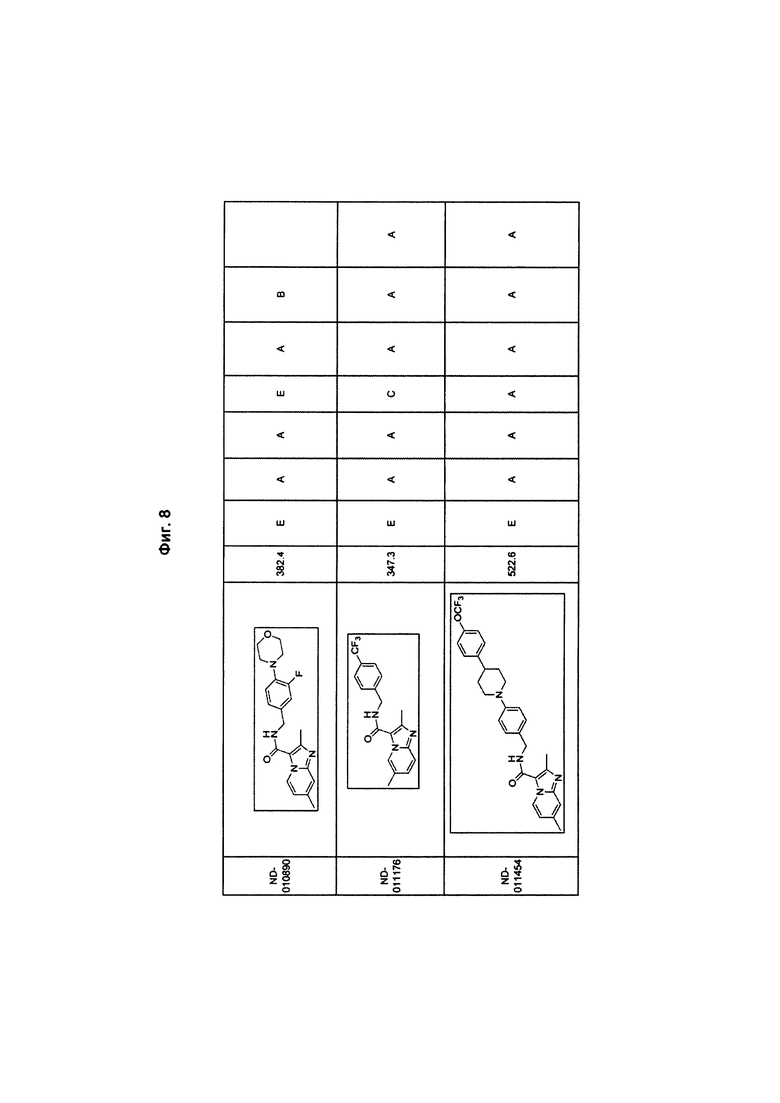
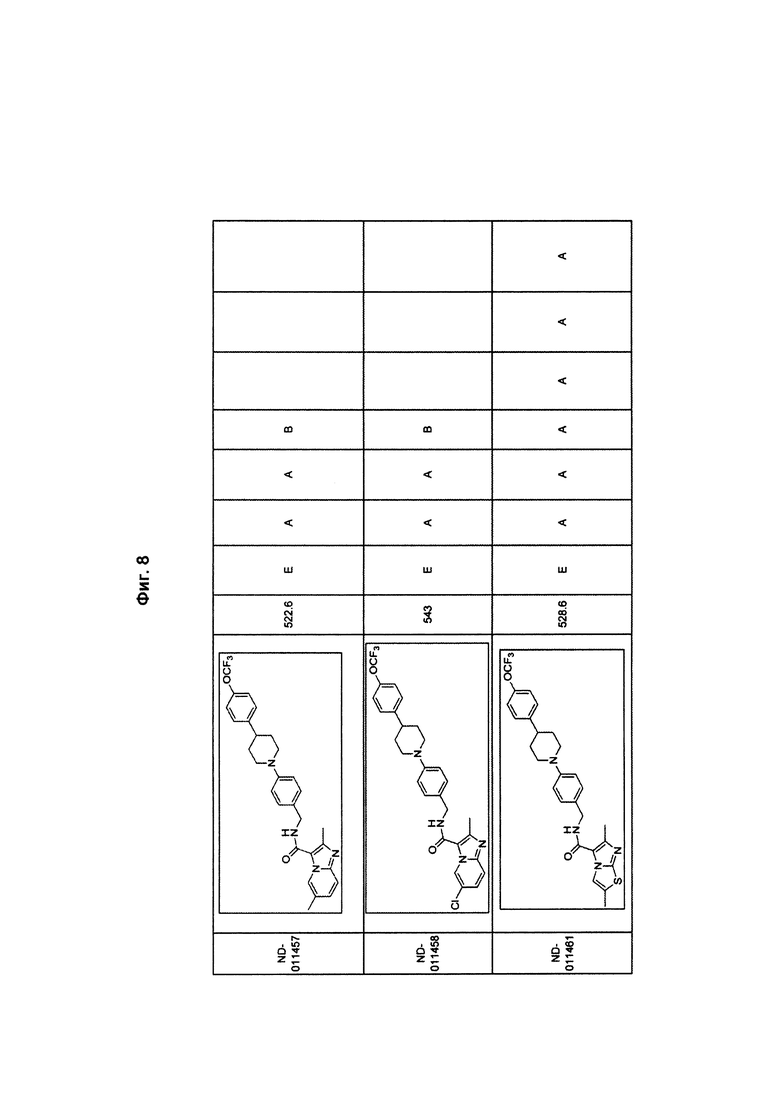
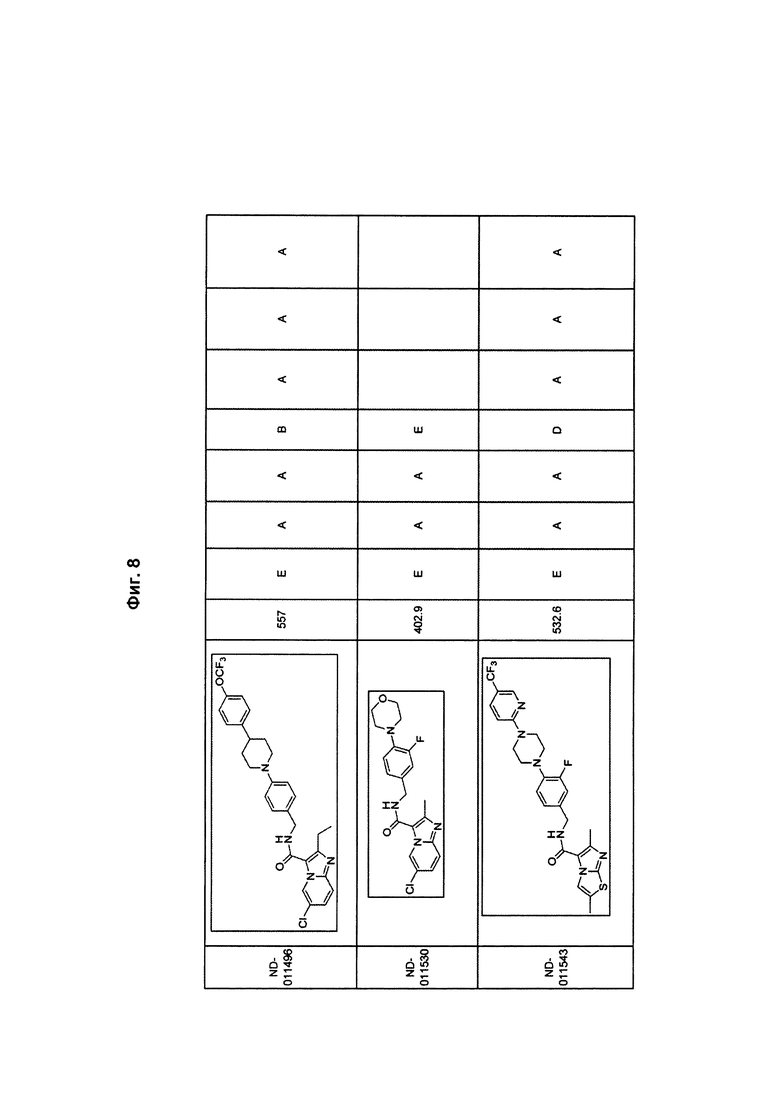
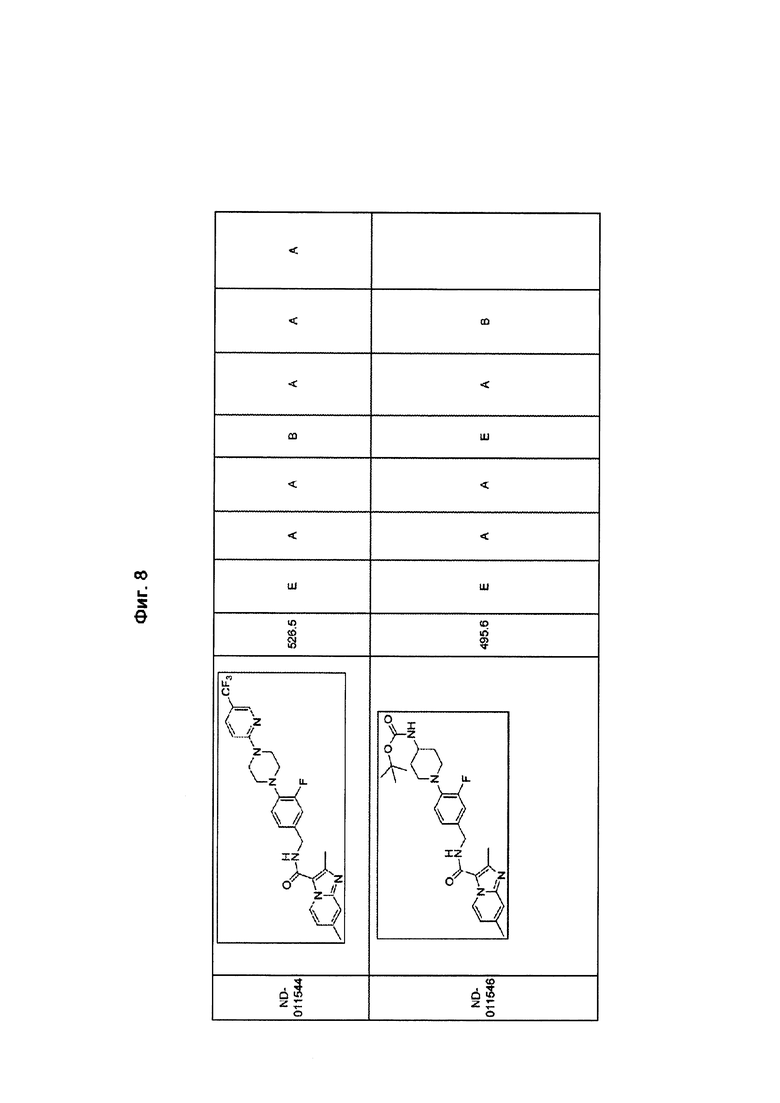
Изобретение относится к соединению, имеющему одну из следующих формул ND-011544, ND-011598, ND-011622, ND-10885. Также изобретение относится к фармацевтической композиции для лечения патологических состояний, характеризующихся микобактериальной активностью или инфекцией, содержащей эффективное количество соединения по изобретению и физиологически приемлемый носитель. Технический результат – соединения, обладающие микобактериальной активностью. 2 н. и 4 з.п. ф-лы, 8 ил., 1 пр.
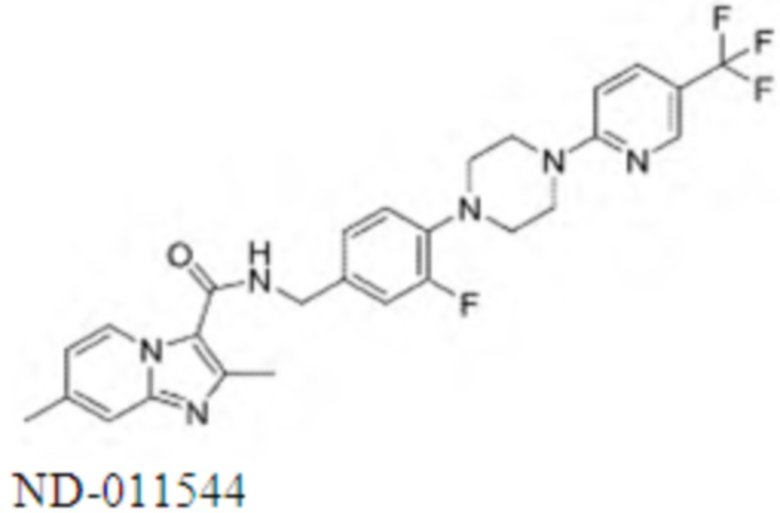
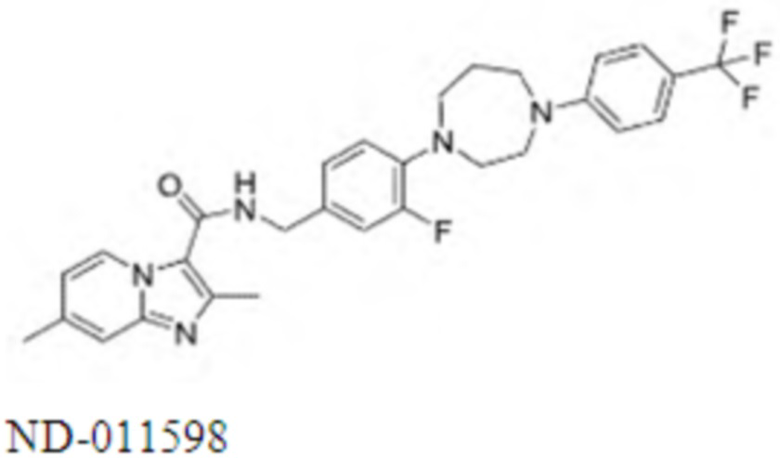
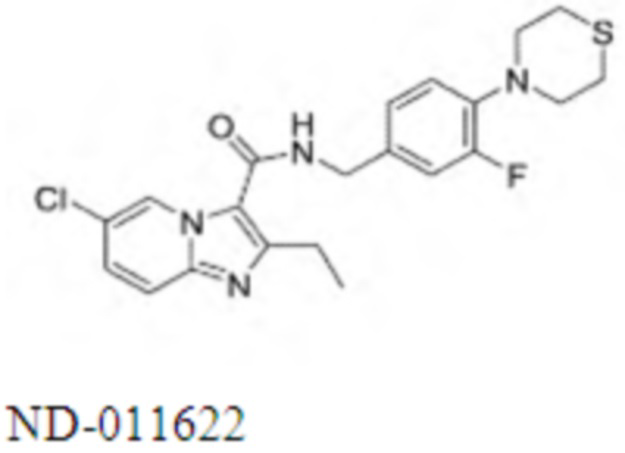
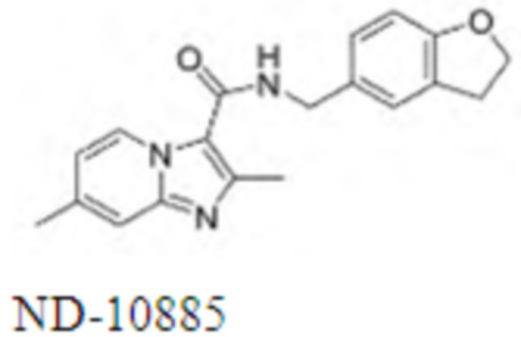
1. Соединение, имеющее одну из следующих формул:
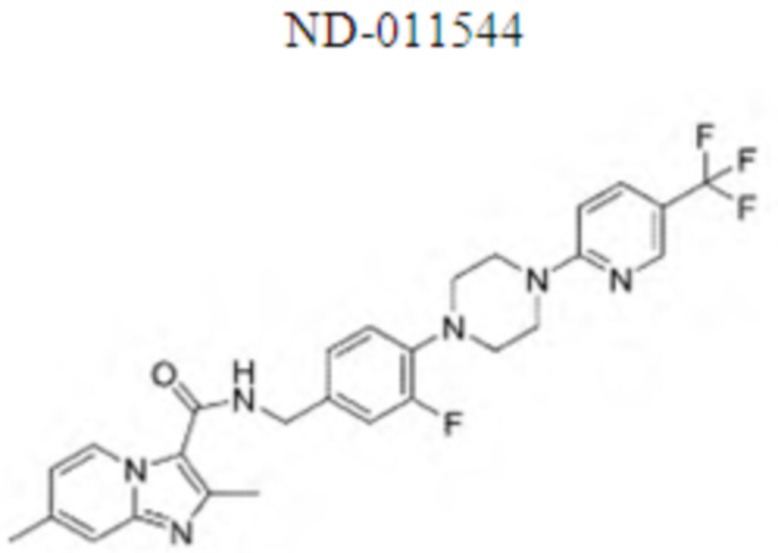 ,
,
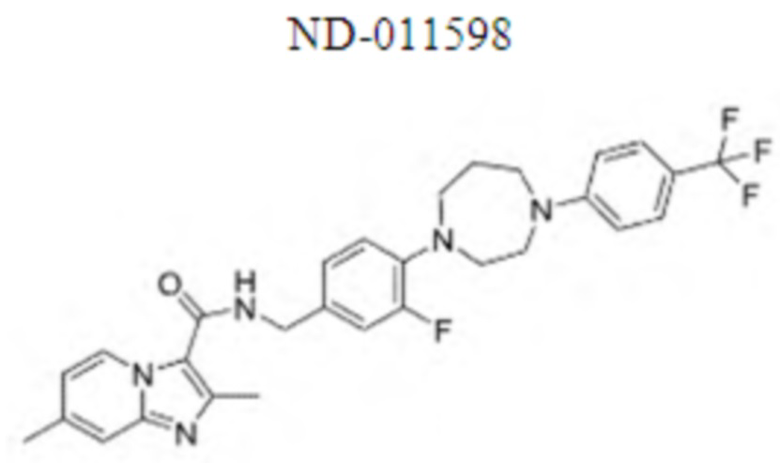 ,
,
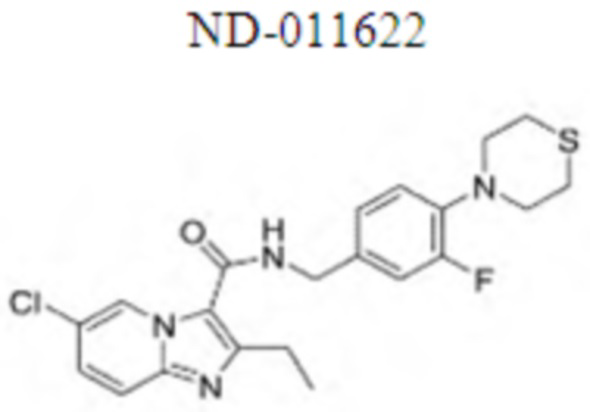 ,
,
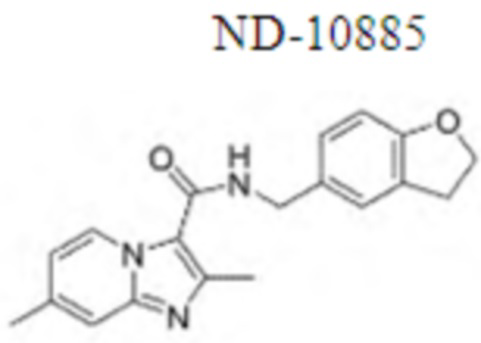 .
.
2. Соединение по п. 1, имеющее формулу ND-011544
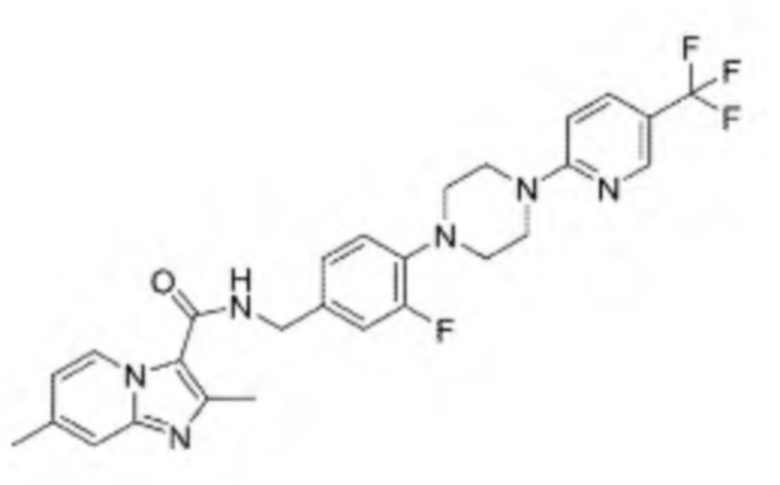 .
.
3. Соединение по п. 1, имеющее формулу ND-011598
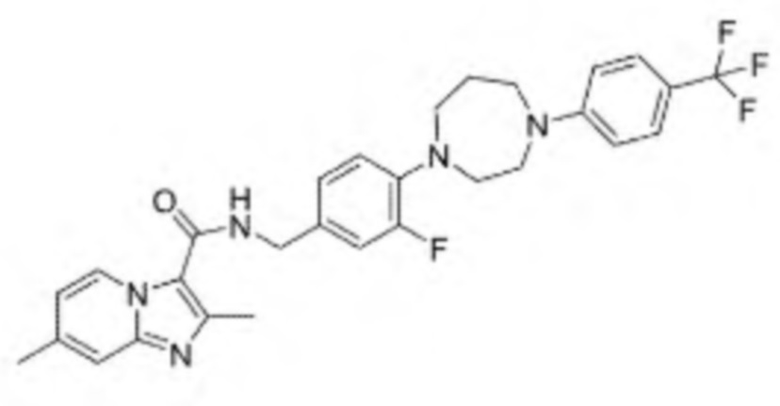 .
.
4. Соединение по п. 1, имеющее формулу ND-011622
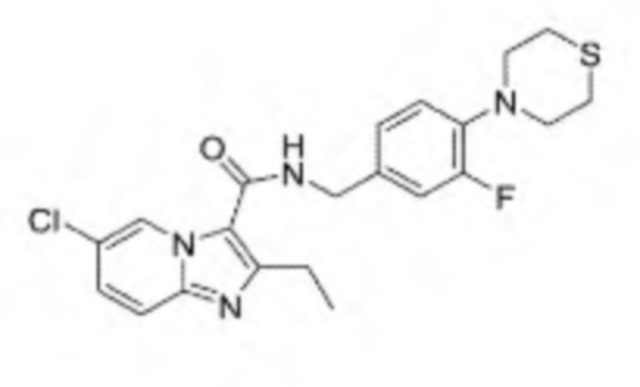 .
.
5. Соединение по п. 1, имеющее формулу ND-10885
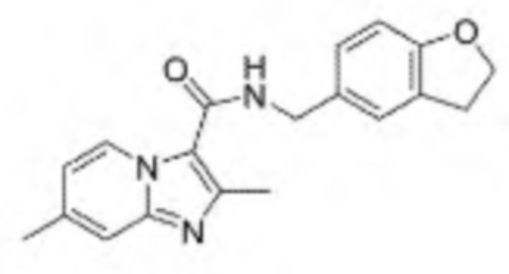 .
.
6. Фармацевтическая композиция для лечения патологических состояний, характеризующихся микобактериальной активностью или инфекцией, содержащая эффективное количество соединения по любому из пп. 1-5 и физиологически приемлемый носитель.
| Способ защиты переносных электрических установок от опасностей, связанных с заземлением одной из фаз | 1924 |
|
SU2014A1 |
| Устройство для закрепления лыж на раме мотоциклов и велосипедов взамен переднего колеса | 1924 |
|
SU2015A1 |
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| GARRETT C.MORASKI et al.: " Advancement of | |||
Авторы
Даты
2023-04-10—Публикация
2016-09-19—Подача