Изобретение относится к медицине, в частности к нейрохирургии, и может быть использовано для уточняющей диагностики пациентов с опухолью мозга с выделением их из когорты здоровых лиц на основании определения параметров иммунограммы у индивида и соотнесения результатов с выведенной нами дискриминантной формулой между группами нормы и нейроонкологическими пациентами.
Развитие новообразования головного мозга в полости черепа оказывает многогранное влияние на организм больного, сопровождаясь не только структурными изменениями вещества мозга, но и нарушениями центральной регуляции многих систем, в частности иммунной системы, гемостаза, эндокринной системы и обменных процессов [1]. Это означает, что в распознавании опухоли мозга возможно использовать не только прямые признаки новообразования, но и вызываемые опухолью разнообразные дисфункции организма.
В настоящее время ведущим способом идентификации опухоли головного мозга [2] является методика нейровизуализации - компьютерная (КТ) или магнитно-резонасная томография (МРТ), основанная на построении структурного (виртуального) изображения головного мозга, изменяющегося в зоне роста мозговой опухоли.
Однако на ранних стадиях новообразования или при некоторых других обстоятельствах патологическую «тень» в мозге не всегда возможно однозначно трактовать как «опухоль» [3]. Это может быть «след» бывшего ранее повреждения или порок развития и другие явления. В этих случаях используют повторные исследования КТ или МРТ через интервал времени или применяют другие уточняющие методы.
Одной из характеристик опухолевого процесса головного мозга является нарушение «иммунного надзора», сформулированное Ф. Бернетом в середине XX века [4]. С тех пор исследование совокупности иммунных показателей у больных первичными опухолями головного мозга нашло широкое распространение в уточнении изменений состояния иммунного гомеостаза нейроонкологического больного.
При этом проводимые иммунологические исследования, по данным литературы [5-6], использовались в 3-х аспектах: 1) для характеристики иммунного статуса у больных опухолью мозга; 2) как индикатор операционного риска - инфекционных осложнений; 3) как критерий обоснования дополнительного лечебного фактора - иммунотерапии опухолей или иммунокоррекции - при ослаблении иммунной защиты.
У нейроонкологических пациентов были установлены облигатные отклонения параметров в спектре иммунограммы от нормальных значений, иллюстрирующие недостаточность иммунной защиты различной степени выраженности.
Однако ранее в литературе не сообщалось о попытке использовать иммунологические отличия у больных как индикатор опухолевой патологии мозга в отличие от здоровых лиц и в подкреплении других диагностических процедур.
Предлагаемый нами «Способ диагностики опухоли мозга у пациента» основан на статистически достоверных количественных отличиях иммунного статуса пациентов первичной опухолью мозга в сравнении с нормой. Это позволило с помощью дискриминатного анализа [7] выделить из спектра показателей иммунограммы различительные критерии развития нейроонкологического процесса у больных.
Первоначально исследовано 26 показателей иммунограммы, используемых в клинической практике, характеризующих состояние различных звеньев иммунитета - клеточное и гуморальное звено, неспецифическая резистентность, факторы регуляции и цитокины. В полученных матрицах переменных проведен пошаговый дискриминантный анализ по Wilks в группах больных с опухолью мозга и здоровых лиц (табл.1) с целью выявления наиболее значимых факторов.
Как видно из табл.1, уже на втором шаге дискриминантного анализа групп здоровых лиц и больных опухолью мозга частный F-критерий для второй переменной (CD16) становится в десятки раз меньше по сравнению с уже включенной переменной CD25. Из этого следует, что функция, включающая лишь одну переменную - CD25, забирает большую часть информации иммунологической матрицы и дает безошибочное распознавание здоровых и больных как на обучающей, так и на экзаменующей матрице (табл.2).
Таким образом, в результате пошагового дискриминантного анализа выделена только одна переменная иммунограммы - CD25, которая обладает наибольшей разделяющей силой нормы и патологии мозга.
Полученные дискриминантные функции, обозначаемые далее как D1 и D2, содержат только одну переменную CD25 и имеют следующий вид:
(1) D1=2,0177×CD25 - 26,7;
D2=0,0933×CD25 - 0,40,
где CD25 - фактор регуляции лимфоцитов,
D1 и D2 - дискриминантные функции.
Решающее правило имеет два возможных варианта: если D1>D2, то обследуемый распределяется в группу здоровых лиц (норма); если же D1<D2, то принимается диагноз «опухоль мозга».
В дальнейшем проведено упрощение решающего правила дискриминации здоровых и больных опухолью испытуемых. Поскольку распознаваемых классов всего два, то возможно перейти к одной дискриминантной функции:
(2) D=D1-D2=1,9244×CD25 - 26,4,
То есть при D>0 состояние обследуемого расценивается как «норма»; если же D<0, то принимается диагноз «опухоль».
Для облегчения практического использования найденной формулы предложено ее преобразование. Как следует из формулы (3), разделяющая граница между состояниями нормы и больных с опухолью мозга проходит через точку D=0. Решение уравнения приводит к очень простому правилу принятия диагностического решения (4).
(3) 1,9244×CD25 - 26,4=0 и следовательно →
(4) 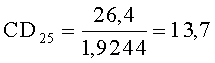
В окончательном виде (4) решающее правило сводится к сравнению значения параметра CD25 у индивидуального испытуемого с выведенным в формуле числом 13,7 - границей между нормой и опухолью мозга. При этом если значение параметра CD25 у испытуемого больше 13,7, то решение принимается в пользу «отсутствия опухоли». Если же величина параметра CD25 меньше 13,7, то принимается решение в пользу «наличия опухоли».
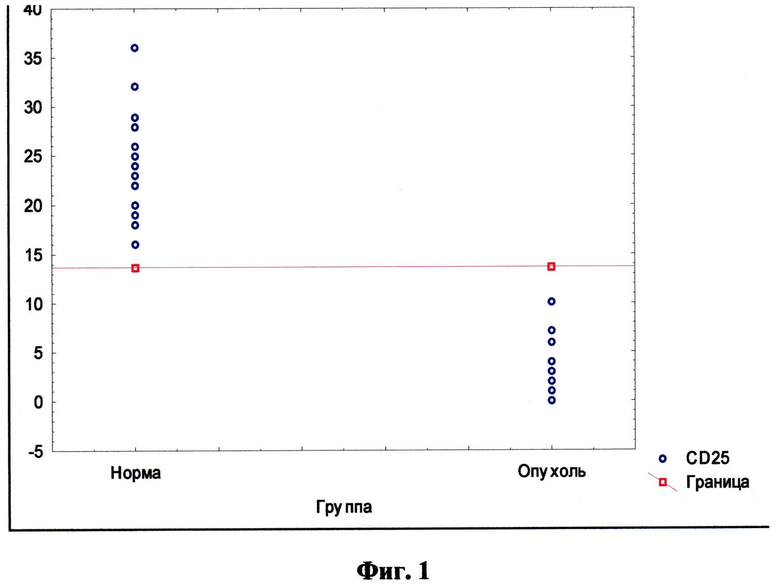
Для наглядности избирательное (100%) распределение параметров CD25 в исследуемых когортах показано на графике (фиг.1), где разделительная линия, выделенная красным цветом, соответствует значению 13,7 по оси ординат. В норме величина CD25 выше «разделительной» линии, равной 13,7; у больных с опухолью мозга все значения данного маркера расположены ниже контрольной величины 13,7.
Доказательством высокой вероятности диагностики состояния здоровья у испытуемых - из 50 здоровых лиц и 117 больных с первичной опухолью головного мозга (позднее верифицированной посредством операции и биопсии) - явилось нулевое значение ошибок по обучающей и экзаменующей выборкам (см. табл.2).
Из табл.2 следует, что машинный анализ иммунограмм обеспечивает корректное распределение испытуемых по искомым группам в 100% случаев - как при обучении, так и экзаменации дискриминантной формулы.
То же следует из графика распределения параметров показателя CD25 относительно разделительной линии, равной 13,7 (фиг.1). Видно, что для групп испытуемых - «норма» и «опухоль» - расположение значений CD25 происходит по различным сторонам разделительной линии. Это иллюстрирует нулевое значение ошибок при проверке решающего правила и, следовательно, его высокое диагностическое значение.
Таким образом, предлагаемый «способ диагностики опухоли мозга у пациента» имеет ряд принципиальных отличий от аналогов. Предлагаемый способ диагностики основан на исследовании состояния иммунной защиты - на показателях иммунограммы у обследуемых лиц, в частности на уровне компонента CD25, что принципиально отличается от используемых до настоящего времени методов распознавания опухоли мозга - нейровизуализации головного мозга (т.е. выявления структурных изменений головного мозга на МРТ или КТ), хирургической биопсии измененного участка мозга, требующей мини-операции с забором кусочка измененной мозговой ткани для анализа.
Предлагаемый способ диагностики хотя и основан на известном методе оценки иммунной защиты по комплексу показателей иммунограммы, но использован в ином направлении - для диагностики состояния нормы и нейроонкологической патологии.
При этом посредством дискриминантного анализа из всего спектра показателей иммунного статуса вычленен главный фактор, отражающий внутренние различия иммунограммы у здоровых лиц и у больных опухолью мозга. Этот фактор - CD25 - вбирает до 96% всей информации и потому служит диагностическим маркером состояния здоровья в группах здоровых лиц и больных нейроонкологическим заболеванием.
Нулевой уровень ошибок свидетельствует о высокой вероятности (до 100%) правильного распределения испытуемых по группам здоровых и больных с опухолью головного мозга, что позволяет реально использовать данный метод в дополнительной диагностике церебральной патологии по патологической перестройке иммунной защиты у больных (в комплексе с методиками нейровизуализации и другими).
Предлагаемый метод реален в связи с тем, что иммунограмма входит в стандарт обследования больных с предполагаемой опухолью мозга (как показатель состояния иммунной защиты для определения риска операции и показания к иммунотерапии). Эти полезные стороны иммунного анализа расширены в нашем предложении использовать значение параметра CD25 для дифференциации групп больных опухолью мозга от здоровых лиц согласно рассчитанной формуле дискриминантной функции и диагностического правила.
Преобразованная дискриминантная формула различения состояния нормы и опухоли мозга по значению показателя CD25 предельно проста для практического применения.
Источники информации
1. Бейн Б.Н., Мухачева М.В., Кочмашев В.Ф. и др. Нарушение адаптации больных церебральной опухолью // Вестник неврол., психиат., нейрохир., 2011, 6.
2. Холин А.В. Магнитно-резонасная томография при заболеваниях центральной нервной системы. - Изд-во Гиппократ: СПб, 1999. - 191 с.
3. Методы исследования в неврологии и нейрохирургии / руководство для врачей (ред. акад. Е.И. Гусев). - Изд-во Нолидж: М., 2000. - 336 с.
4. Бернет. Целостность организма и иммунитет. - М.: Изд-во Мир, 1964. - 184 с.
5. Старченко А.А. Клиническая иммунопатология хирургических заболеваний головного мозга (в 2 частях). - СПб.: 2001. - 651 с
6. Противоопухолевый иммунитет и его нарушения при церебральных опухолях / учебное пособие для врачей (сост. - Б.Н. Бейн, М.В. Селюкова и другие). - Кировская ГМА: Киров, 2004. - 49 с. с илл.
7. Иванов Ю.И., Погорелюк О.Н. Статистическая обработка результатов медико-биологических исследований. - М.: Медицина, 1990. - с.117-141.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ДИАГНОСТИКИ РИСКА ФОРМИРОВАНИЯ ДЕФИЦИТА ПРОТИВООПУХОЛЕВОЙ ИММУННОЙ ЗАЩИТЫ | 2015 |
|
RU2605310C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ПРОДОЛЖИТЕЛЬНОСТИ ЖИЗНИ БОЛЬНЫХ С МЕСТНО-РАСПРОСТРАНЕННЫМ И ДИССЕМИНИРОВАННЫМ ПОЧЕЧНО-КЛЕТОЧНЫМ РАКОМ | 2009 |
|
RU2405150C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РАЗВИТИЯ ОПУХОЛЕЙ ГОЛОВНОГО МОЗГА У ДЕТЕЙ | 2008 |
|
RU2360611C1 |
| СПОСОБ ОЦЕНКИ ПСИХИЧЕСКОГО СОСТОЯНИЯ | 1996 |
|
RU2099009C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ СТЕПЕНИ ТЯЖЕСТИ ДЕТСКОГО ЦЕРЕБРАЛЬНОГО ПАРАЛИЧА У ДЕТЕЙ РАННЕГО ВОЗРАСТА | 2013 |
|
RU2554752C2 |
| СПОСОБ ДИАГНОСТИКИ ШИЗОФРЕНИЧЕСКОГО РАССТРОЙСТВА | 2017 |
|
RU2676657C1 |
| Способ прогнозирования индивидуального риска развития расстройств поведения аддиктивного характера | 2016 |
|
RU2621171C1 |
| СПОСОБ КОМПЛЕКСНОЙ ОЦЕНКИ ВАЗОМОТОРНОЙ ФУНКЦИИ СОСУДИСТОГО ЭНДОТЕЛИЯ | 2001 |
|
RU2209587C2 |
| СПОСОБ ДИАГНОСТИКИ И ПРОГНОЗИРОВАНИЯ РАЗВИТИЯ ЭПИЛЕПСИИ У ПАЦИЕНТОВ С ДОКЛИНИЧЕСКОЙ СТАДИЕЙ БОЛЕЗНИ | 2001 |
|
RU2188575C1 |
| СПОСОБ ЛЕЧЕНИЯ ОСТРОГО ЦЕРЕБРАЛЬНОГО ИНСУЛЬТА | 2005 |
|
RU2268064C1 |
Изобретение относится к области медицины, в частности к нейрохирургии, и касается способа диагностики опухоли мозга у пациентов. Сущность способа: в забранной крови определяют процентное количество CD25-лимфоцитов. При его значении 13,7 устанавливают отсутствие опухоли мозга, а при его значении меньше 13,7 диагностируют наличие опухоли мозга у пациента. Изобретение обеспечивает нулевой уровень ошибок, что свидетельствует о высокой вероятности правильного распределения испытуемых по группам здоровых и больных с опухолью головного мозга, что позволяет реально использовать данный метод в дополнительной диагностике церебральной патологии. Способ прост для практического применения. 2 табл., 1 ил.
Способ диагностики опухоли мозга у пациента, характеризующийся тем, что в забранной крови определяют процентное количество CD25-лимфоцитов, и при его значении 13,7 устанавливают отсутствие опухоли мозга, а при его значении меньше 13,7 диагностируют наличие опухоли мозга у пациента.
Авторы
Даты
2014-12-10—Публикация
2011-08-03—Подача