Изобретение относится к биотехнологии, в частности к генетической инженерии, и позволяет получать микробиологическим синтезом по оптимизированной технологии новый гибридный бифункциональный полипептид CmAP/MBL-T со свойствами высокоактивной щелочной фосфатазы морской бактерии и высокоспецифичного к цервикальным онкомаркерам маннан-связывающего лектина С-типа дальневосточного трепанга, который может быть использован для ранней дифференциальной диагностики рака шейки матки, а также для исследования механизмов канцерогенеза в практической онкологии.
Данные об углеводной специфичности пектинов и их способности выявлять углеводные детерминанты в составе гликоконъюгатов опухолевых клеток, особенно метастазирующих, нашли широкое применение в онкологии. Лектины используются как инструмент исследования перерождения нормальных клеток в злокачественные [1-3]. Полученная информация, в свою очередь, является составной частью изучения механизма канцерогенеза. Наиболее интересными с этой точки зрения являются пектины с высоконаправленной углеводной специфичностью. Нами было показано, что к числу таких пектинов относится маннан-связывающий лектин С-типа дальневосточного трепанга Apostichopus japonicus (MBL-T) [4]. Лектин MBL-T не взаимодействует с компонентами сыворотки крови здорового человека, что является крайне важным при использовании в различных диагностических исследованиях, в частности, с применением методов иммуноцитохимии, что позволяет избежать ложно-положительных результатов и получать достоверную информацию о структурных изменениях углеводных цепей гликоконъюгатов, сопровождающих патологические изменения. Результаты исследований углеводного профиля гликоконъюгатов пектинами находят практическое применение при разработке методов диагностики рака [5-7].
Использование пектинов для диагностики рака реализуется по двум основным направлениям. Первое направление осуществляется при выявлении пектинами углеводных детерминант исследуемых маркеров в сыворотке крови на твердой фазе или в геле (лектин-ферментные, лектин-иммуноферментные, лектин-иммунные методы), и второе направление заключается во взаимодействии лектинов с соответствующими лигандами, экспрессированными на поверхности клеток, получаемых путем смывов, выделением из крови, а также на срезах биопсийного материала.
Классическим примером перспективности использования лектинов в диагностике служит коммерческий набор японской фирмы WAKO, позволяющий проводить раннюю и дифференциальную диагностику рака печени, цирроза печени и беременности. В основе метода заложена способность лектинов LCA-A (Lens culinaris agglutinin A - лектин, выделенный из бобов чечевицы) и РНА-Е4 (phaseolus vulgaris isolectin E-4 - лектин, выделенный из бобов фасоли обыкновенной) выявлять углеводные изоформы альфа-фетопротеинов (АФП) в сыворотке крови. Метод обладает высокой чувствительностью и информативен даже при концентрации АФП 5 нг/мл. Объем исследуемого образца - 3 мкл, срок проведения анализа - 3 часа, количество одновременно анализируемых проб - 10. Метод позволяет за 2-3 месяца до появления первых клинических симптомов выявлять рецидивы роста опухоли вследствие его высокой чувствительности.
Уникальность углеводной специфичности лектина дальневосточного трепанга MBL-T и перспективность его использования как диагностического маркера подтверждается результатами экспериментов по взаимодействию с раковоэмбриональными антигенами. Лектин трепанга показал способность взаимодействовать с такими маркерами опухолевого роста, как альфа-фетопротеин, раковоэмбриональный антиген, эмбриональный альфа-1-кислый гликопротеин, эмбриональный альфа-2-глобулин.
На основе наличия у лектина MBL-T уникального углевод-распознающего домена, определяющего его способность распознавать микрогетерогенность гликоконъюгатов раковых и нормальных клеток, заявителем разработан новый метод диагностики рака шейки матки [8].
Определение концентрации пектин-связанных структур в эпителиальном секрете является принципиально новым подходом при выявлении злокачественных новообразований. Однако и такой анализ требует повышения эффективности наряду с простотой выполнения метода. Это возможно при использовании методов генной инженерии. Методами молекулярного клонирования установлена структура лектина дальневосточного трепанга MBL-T [GenBank, код доступа ААТ42221] и щелочной фосфатазы морской бактерии CmAP [GenBank, код доступа ABD92772]. Известен 3 способ получения высокоактивной рекомбинантной щелочной фосфатазы морской бактерии CmAP [9].
Задача изобретения - конструирование рекомбинантного штамма-продуцента Escherichia coli, несущего такую экспрессирующую конструкцию (плазмиду), которая позволит нарабатывать целевой высокоочищенный недеградированный гибридный бифункциональный полипептид CmAP/MBL-T в препаративных количествах, при сохранении как иммуногенных свойств высокоспецифичного лектина дальневосточного трепанга MBL-T, так и ферментативных свойств высокоактивной щелочной фосфатазы морской бактерии CmAP, используемой для цветной визуализации лектин-связанных комплексов в лектин-иммуноферментном методе ранней диагностики рака шейки матки.
Поставленная задача решена путем конструирования рекомбинантной плазмидной ДНК pET40CmAP/MBL-T, кодирующей химерный полипептид CmAP/MBL-Т, и рекомбинантного штамма E.coli Rosetta(DE3)/pET40CmAP/MBL-T, обеспечивающие индуцируемый синтез с высоким и стабильным выходом активного растворимого бифункционального белка CmAP/MBL-T, обладающего свойствами высокоактивной щелочной фосфатазы морской бактерии CmAP и высокочувствительного маннан-связывающего лектина С-типа дальневосточного трепанга MBL-T.
Технический результат заявленного изобретения - получение активного гибридного бифункционального полипептида CmAP/MBL-T со свойствами высокоактивной щелочной фосфатазы CmAP и высокочувствительного маннан-связывающего лектина С-типа дальневосточного трепанга MBL-T с высоким выходом и уровнем очистки.
Плазмида pET40CmAP/MBL-T имеет 8194 пар оснований (п.о.) и характеризуется наличием NcoI/SalI-фрагмента плазмиды pET-40b(+) (Novagen) и последовательности фрагмента ДНК размером 2034 п.о., содержащего химерный ген, начинающий трансляцию со щелочной фосфатазы CmAP (N-конец) и заканчивающийся маннан-связывающим лектином С-типа MBL-T с С-концевой части молекулы рекомбинантного белка, соединенным со щелочной фосфатазой гибким линкером (G)4S(G)4S(G)4SEL.
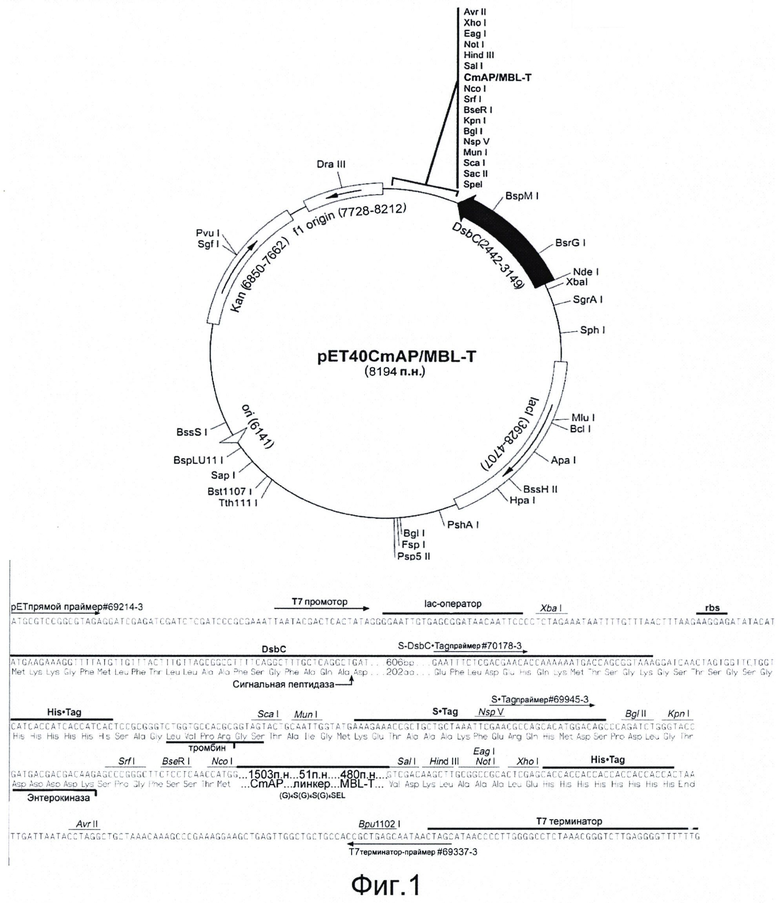
На фигуре 1 представлена физическая карта плазмиды pET40CmAP/MBL-T и область плазмиды, ответственная за экспрессию гибридного белка CmAP/MBL-T. Нуклеотидная последовательность фрагмента плазмиды pET40CmAP/MBL-T, фланкированная сайтами NcoI и SalI, содержит последовательность структурного гена CwAP, соответствующую открытой рамке считывания для белка СтАР, последовательность соединяющего линкера (G)4S(G)4S(G)4SEL и последовательность структурного гена MBL-Т, соответствующую открытой рамке считывания для белка MBL-T (SEQ ID N1).
Рекомбинантный штамм E.coli Rosetta(DE3)/pET40CmAP/MBL-T получен трансформацией клеток E.coli Rosetta(DE3) (Novagen) плазмидой pET40CwAP/MBL-T с использованием традиционной генно-инженерной технологии [10].
Рекомбинантный штамм E.coli Rosetta(DE3)/pET40CmAP/MBL-T характеризуется следующими признаками.
Культурально-морфологические признаки.
Клетки штамма образуют крупные круглые с ровными краями, выпуклые колонии до 5 мм в диаметре, поверхность колоний гладкая, консистенция слизистая. Пигмент не накапливается. Грамотрицательны, спор не образуют, капсулы не имеют. Колонии хорошо растут на простых питательных средах (LB). При росте в жидких средах образуют интенсивную ровную муть.
Физико-биологические признаки.
Рекомбинантный штамм E.coli Rosetta(DE3)/pET40CmAP/MBL-T видотипичен по своим биохимическим свойствам. Штамм не обладает желатиназной активностью, не ферментирует лизин; расщепляет глюкозу, лактозу, маннит, сахарозу до кислоты и газа. Имеет мутацию в гене lac, обеспечивающую контроль уровня экспрессии, а также трансляцию редких кодонов. Оптимальной для роста является температура 37°С, а для продукции белка CmAP/MBL-T -16°С.
Устойчивость к антибиотикам.
Клетки штамма характеризуются устойчивостью к хлорамфениколу (34 мкг/мл) и канамицину (25 мкг/мл).
Патогенность и токсичность.
Рекомбинантный штамм E.coli Rosetta(DE3)/pET400CmAP/MBL-T не патогенен и не токсичен для теплокровных животных.
Штамм хранится обычным способом в суспензии с глицерином (30%) при -20°С.
Заявляемый способ получения гибридного бифункционального белка CmAP/MBL-T заключается в культивировании клеток штамма E.coli Rosetta(DE3)/pET40CmAP/MBL-T в жидкой питательной среде LB в течение 12 ч при 16°С, затем бактериальные клетки осаждают центрифугированием, суспензию клеток дезинтегрируют в буфере, далее экстракт центрифугируют, затем надосадочную жидкость помещают на колонку с ионообменной смолой, далее элюируют белок, затем белковый элюат помещают на колонку с металлоаффинной смолой, далее активные фракции концентрируют на ионообменной смоле и выделяют целевой продукт гель-фильтрацией.
Выход рекомбинантного гибридного бифункционального белка CmAP/MBL-T в результате применения описанного способа составляет не менее 10 мг рекомбинантного белка с 1 л культуры с удельной активностью щелочной фосфатазы не менее 10000 ед/мг белка и иммуногенными свойствами маннан-связывающего лектина С-типа, характерными для природного аналога MBL-T [4, 8].
Рекомбинантный гибридный бифункциональный белок CmAP/MBL-T имеет молекулярную массу 105,5 кДа, включая плазмидный шаперон DsbC с молекулярной массой 32,5 кДа, широкий диапазон значений температуры (25-37°С) и рН (7,5-9,5) для проявления фосфатазной активности и аффинных свойств лектина в присутствии 2 мМ ионов Са2+. Плазмидный шаперон Dsb не дает существенного вклада в функциональную способность обоих частей химеры CmAP/MBL-T, поэтому этап его удаления из рекомбинантного белка с помощью энтерокиназы по предусмотренному генетической конструкцией сайту рестрикции не обязателен.
Рекомбинантный гибридный бифункциональный полипептид CmAP/MBL-T успешно использован в доклинических испытаниях способности связывания лектинового компонента химеры с муцином, раковоэмбриональным антигеном (РЭА), а также другими онкомаркерами методом лектин-иммуноферментного анализа. Использование маннан-связывающего лектина в составе гибридного бифункционального полипептида CmAP/MBL-T с активностью щелочной фосфатазы позволяет сократить стадии и время иммуноферментного анализа, которые раньше требовались для получения конъюгатов лектина и фермента.
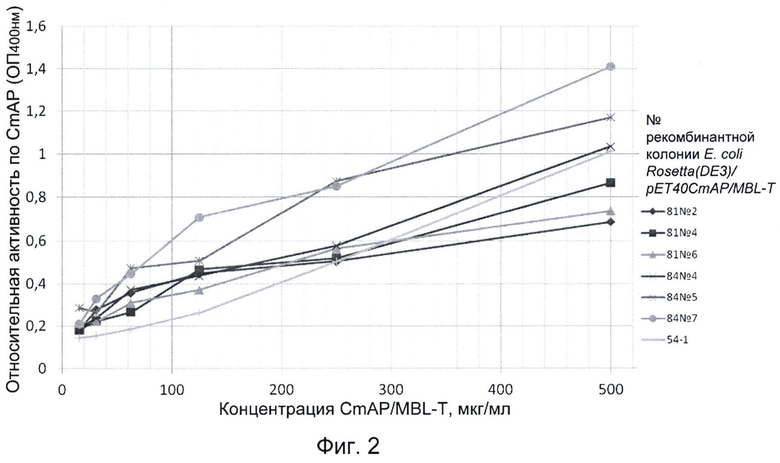
На фиг.2 представлены результаты иммуно-ферментного анализа (ИФА), проведенного на микропланшете, сенсибилизированном муцином, с применением гибридного бифункционального полипептида CmAP/MBL-T, полученного от разных колоний трансгенного штамма E.coli Rosetta(DE3)/pET40 CmAP/MBL-T. Уровень аффинности рекомбинантного гибридного бифункционального полипептида CmAP/MBL-T определяли по концентрации пектин-связанных комплексов с муцином (по оси X). Визуализацию лектин-связанных комплексов осуществляли методом измерения фосфатазной активности рекомбинантного гибридного бифункционального полипептида CmAP/MBL-T (по оси Y).
Существенными преимуществами заявляемого способа получения гибридного бифункционального полипептида CmAP/MBL-T являются:
использование рекомбинантного штамма-продуцента E.coli Rosetta(DE3)/pET40CmAP/MBL-T, что позволяет получать при биосинтезе большое количество высокоактивного бифункционального гибридного белка CmAP/MBL-T;
использование несложной трехстадийной хроматографической очистки рекомбинантного белка, что позволяет получить чистый гибридный полипептид CmAP/MBL-T за короткое время и с малыми потерями.
Способ получения функционально-активного гибридного полипептида CmAP/MBL-T на основе использования химерного гена, кодирующего щелочную фосфатазу морской бактерии CmAP и маннан-связывающий лектин С-типа дальневосточного трепанга MBL-T, иллюстрируется следующими примерами.
Пример 1. Конструирование плазмиды pET40CmAP/MBL-T.
Рекомбинантную плазмиду pET40CmAP/MBL-T, содержащую химерный ген, кодирующий полноразмерную щелочную фосфатазу CmAP и полноразмерный маннан-связывающий лектин С-типа MBL-T, соединяющиеся через гибкий линкер (G)4S(G)4S(G)4SEL, фланкированный сайтами рестрикции NcoI и SalI, конструируют на основе коммерческой плазмиды pET-40b(+) (Novagen).
Фрагмент ДНК, содержащий химерный ген гибридного полипептида CwAP/MBL-Т, получают в два этапа. На первом этапе проводят полимеразную цепную реакцию с использованием плазмиды 40Pho в качестве матрицы для получения гена щелочной фосфатазы СтАР и праймеров X-PhoN_F и Pho40X-SacI-R, где X-PhoN_F - праймер, специфичный по отношению к N-концевой последовательности CmAP, включающий сайт для рестриктазы NcoI; Pho40X-SacI-R - обратный праймер, специфичный по отношению к С-концевой последовательности CmAP, включающий полинуклеотид, кодирующий линкер (G)4S(G)4S(G)4SEL и сайт рестрикции SacI:
X-PhoN_F: 5'-TATTCCATGGCAGAGATCAAGAATGTCATTCTGAT-3'
Pho40X-SacI-R: -5'-TTAAGAGCTCAGAACCACCACCACCAGAACCACCACCACCAGAACCACCACCACC CTTCGCTACCACTGTCTTCAGATACTGTCCT-3'.
Данную реакцию проводят в следующих условиях: 10х Encycio буфер, 50х смесь полимераз Encyclo («Encyclo PCR kit», Евроген, Москва), 50х смесь dNTP (10 mM каждого), смесь праймеров (5 µМ каждого), 20 нг ДНК. Процесс амплификации состоит из следующих стадий: 30 циклов ПЦР (15 с - 95°С, 1 мин 30 с - 72°С) и инкубация 10 мин при 72°С. После амплификации ПЦР-продукт очищают электрофоретически в 1% агарозном геле. Фрагмент (1 мкг) обрабатывают рестриктазами NcoI и SacI в оптимальном буфере (Fermentas) в течение 3 часов, затем ферменты удаляют из реакционной среды по стандартной методике фенолом (1:1) [10]. В водную фракцию, содержащую фрагмент, добавляют 1/10 объема 0,3 М ацетата Na, pH 5,2 и 1/2 объема изопропанолового спирта и оставляют на -20°С в течение 30 мин. Затем центрифугируют при 14000 об/мин в течение 20 мин, осадок промывают 75% этанолом и высушивают при комнатной температуре. Осадок растворяют в 20 мкл деионизованной воды.
2 мкг плазмидной ДНК рЕТ-40b(+) обрабатывают рестриктазами NcoI и SacI в соответствии с методикой, описанной выше, и из полученного гидролизата выделяют векторную часть плазмиды в 1% геле легкоплавкой агарозы.
Полученный фрагмент гена CmAP и векторную часть плазмиды рЕТ-40b(+) сшивают при помощи лигазной реакции в 50 мкл буфера для лигирования согласно инструкции (Fermentas). 10 мкл реакционной смеси используют для трансформации компетентных клеток E.coli Rosetta(DE3). Трансформанты высевают на LB-агар, содержащий 25 мкг/мл канамицина. После инкубирования в течение 16 ч при 37°С клоны отсевают, выделяют плазмидную ДНК и анализируют на наличие мутаций при помощи автоматического секвенирования. Отбирают плазмидную ДНК pET40CmAP, содержащую последовательность CmAP с линкером (G)4S(G)4S(G)4SEL на С-концевой части.
На втором этапе проводят амплификацию гена MBL-T с использованием к-ДНК дальневосточного трепанга и пары праймеров Lect-X-dir и Lect-X-rev, несущими сайты для рестриктаз SacI и SalI:
Lect-X-dir: 5'-AGCTGAGCTCTGTCTGACGGCTTGTCCGGAGTTTTG-3
Lect-X-rev: 5'-CAGTGTCGACCTCCAAATGATACTCGATACAGGGAAG-3'
Для создания конструкции pET40CmAP/MBL-T полученный ген маннан-связывающего пектина С-типа MBL-T и 2 мкг плазмидной ДНК pET40CmAP обрабатывают рестриктазами SacI и SalI в соответствии с методикой, описанной выше, и очищают в 1% геле легкоплавкой агарозы. Очищенные ПЦР-фрагменты MBL-T и векторную часть плазмиды pET40CmAP сшивают при помощи лигазной реакции в 50 мкл буфера для лигирования согласно инструкции (Fermentas). 10 мкл реакционной смеси используют для трансформации компетентных клеток E.coli Rosetta(DE3). Трансформанты высевают на LB-агар, содержащий 25 мкг/мл канамицина. После инкубирования в течение 16 ч при 37°С клоны отсевают, выделяют плазмидную ДНК и анализируют на наличие мутаций при помощи автоматического секвенирования. Отбирают ДНК, содержащую необходимые последовательности генов CmAP и MBL-T, представляющую собой плазмиду pET40CmAP/MBL-T размером 8194 п.о. (фиг.1).
Пример 2. Получение рекомбинантного штамма E.coli Rosetta(DE3)/pET40CmAP/MBL-T - продуцента гибридного бифункционального полипептида CmAP/MBL-T.
Рекомбинантный штамм-продуцент E.coli Rosetta(DE3)/pET40CmAP/MBL-T получают путем трансформации клеток штамма E.coli Rosetta(DE3) рекомбинантной плазмидой pET40CmAP/MBL-T. Ночную культуру (0,5 мл LB) рекомбинантного штамма-продуцента гибридного бифункционального полипептида CmAP/MBL-T выращивают в литровой колбе в жидкой среде LB, содержащей на литр 10 г бакто-триптона, 5 г бакто-дрожжевого экстракта и 10 г NaCl, 25 мг/мл канамицина, рН 7,7, на шейкере при 200 об/мин при температуре 37°С в течение 2 часов до оптической плотности 0,6-0,8 (OD600), затем добавляют индуктор экспрессии IPTG до конечной концентрации 0,2 мМ и инкубируют далее при 16°С в течение 12 часов.
Для определения продуктивности штамма клеточные водные экстракты анализируют электрофорезом в 12,5% полиакриламидном геле с додецилсульфатом натрия. Гель окрашивают Кумасси R-250 по стандартной методике и определяют относительное количество белка в полосе целевого продукта. Содержание рекомбинантного белка в растворимой клеточной фракции составляет не менее 30% от всех белков этой фракции.
Пример 3. Выделение и характеристика гибридного бифункционального полипептида CmAP/MBL-T.
Рекомбинантный штамм-продуцент гибридного бифункционального полипептида CmAP/MBL-T - E.coli Rosetta(DE3)/pET40CmAP/MBL-T инкубируют в литровой колбе в жидкой среде LB, содержащей на литр 10 г бакто-триптона, 5 г бакто-дрожжевого экстракта и 10 г NaCl, 0,5 мМ IPTG, 25 мг/мл канамицина, рН 7,7, на шейкере при 200 об/мин в течение 12 часов при 16°С. Бактериальные клетки осаждают на проточной центрифуге при 5000 об/мин в течение 10 мин. Суспензию клеток дезинтегрируют в 20 мл буфера А (0,05 М трис-HCl, рН 8,6, 0.01% NaN3) в течение 5×30 с, охлаждая во льду. Затем центрифугируют при 10000 об/мин в течение 30 мин. Надосадочную жидкость собирают и помещают на колонку с ДЕАЕ-52-целлюлозой (Whatman). Элюцию белка проводят градиентом концентрации NaCl (0,05 М-0,380 М) в буфере А. Активные фракции собирают и помещают на колонку с металлоаффинной смолой (Qiagen), предварительно уравновешенную буфером А. Элюцию белка проводят буфером В (50 мМ Tris-HCl, рН 8,6, 50 мМ EDTA, 0,01% NaN3). Активные фракции собирают, обессоливают и концентрируют на колонке с ДЕАЕ-Toyopearl 650М (Тоуо Soda), затем инкубируют с энтерокиназой (Invitrogen) при комнатной температуре в течение 12 часов. Затем раствор белка наносят на колонку для гель-фильтрации с Superdex 200 (Sigma). Выход рекомбинантного белка составляет 10 мг с 1 литра культуры.
Полученный рекомбинантный полипептид определяют по первым 10 аминокислотам на автоматическом секвенаторе. Проведенное секвенирование препарата рекомбинантного белка, выделенного из клеток штамма E.coli Rosetta(DE3)/pET40CmAP/MBL-T, выявило аминокислотную последовательность А1а-Glu-Ile-Lys-Asn-Val-Ile-Leu-Met-Ile, соответствующую первым 10 аминокислотам щелочной фосфатазы CmAP, являющейся N-концевой составляющей химерного белка CmAP/MBL-T.
Ферментативную функциональность гибридного полипептида CmAP/MBL-T проверяют по активности щелочной фосфатазы, которую определяют по расщеплению паранитрофенилфосфата (п-НФФ). Стандартная инкубационная смесь в объеме 500 мкл содержит 15 мМ п-НФФ, 1 М диэтаноламина (ДЭА), рН 10,3 и фермент либо 2 мМ п-НФФ, 0,1 М трис-HCl, 0.2 М KCl, рН 9,5-10,0. После 30 мин инкубации при 37°С реакцию останавливают добавлением 2 мл 0,5 М NaOH. Количество образовавшегося в процессе ферментативной реакции п-нитрофенола (п-НФ) определяют спектрофотометрически при 400 нм. За единицу активности щелочной фосфатазы принимают количество фермента, катализирующего освобождение 1 мкМ п-НФ (ε400 нм = 18600) в течение 1 мин инкубации. Удельную активность выражают в единицах активности фермента на 1 мг белка. Концентрацию белка в растворе определяют по методу Брэдфорда.
Лектинную функциональность гибридного полипептида CmAP/MBL-T проверяют по уровню аффинности к муцину. На сенсибилизированный муцином полистирольный микропланшет вносят раствор (0,0015-0,1 мг/мл) гибридного полипептида CmAP/MBL-T и инкубируют 1,5 часа при комнатной температуре. Лектин-связанные комплексы отмывают буфером 10 мм трис-HCl, рН 9,0, 0,15 М NaCl, 0,05% Тритон Х-100, 20 мМ CaCl2 по 200 мкл в каждую лунку не менее 10 раз. Затем в лунки микропланшета добавляют буфер для активности щелочной фосфатазы с субстратом, как описано выше, для визуализации связавшихся комплексов (фиг.2).
Полученные данные по характеристике и функциональной активности продукта экспрессии искусственного химерного гена гибридного бифункционального полипептида CmAP/MBL-T в клетках рекомбинантного штамма E.coli Rosetta(DE3)/pET40CmAP/MBL-T свидетельствуют о соответствии исследуемого полипептида его природному аналогу - пектину MBL-T, применяемому в лектин-иммуноферментном методе ранней дифференциальной диагностики рака шейки матки [8].
Как следует из приведенных примеров, заявляемая группа изобретений позволяет получать активный рекомбинантный гибридный бифункциональный полипептид CmAP/MBL-T со свойствами высокоактивной щелочной фосфатазы морской бактерии CmAP и высокоспецифичного маннан-связывающего лектина дальневосточного трепанга С-типа MBL-T с высоким выходом при относительно простой и надежной технологии.
Заявленное изобретение позволяет:
- с помощью использования рекомбинантного штамма-продуцента E.coli Rosetta(DE3)/pET40CmAP/MBL-T получать путем биосинтеза большое количество активного гибридного бифункционального полипептида CmAP/MBL-T;
- использование ионообменной, металлоаффинной и гель-фильтрационной хроматографий при очистке рекомбинантного белка из водного экстракта клеток рекомбинантного штамма-продуцента позволяет получать гибридный бифункциональный полипептид CmAP/MBL-T с чистотой более 98% в качестве аналога маннан-связывающего лектина С-типа MBL-T, конъюгированного с ферментом, применяемого для проведения иммуноферментного анализа.
Литература
1. Чиссов В.И., Старинский В.В., Сотникова Е.Н. Ранняя диагностика онкологических заболеваний. М.: 1994. С.193.
2. Davina J.H.М., Stadhouders А.М., van Haelst U.J.G.М., Lamers G.E.М., Kenemans P. Concanavalin A Peroxidase labeling in cervical exfoliative cytopathology. Gynecologic Oncology, 1985. - Vol.22. - I.2. - P.212-223.
3. Reddi A. L., Sankaranarayanan K., Arulraj H. S., Devaraj N., Devaraj Enzime-linked PNA lectin-binding assay of serum T-antigen in patient with SCC of the uterine cervix. Cancer letters - 2000. - Vol.149, - P.207-211.
4. A.A. Bulgakov, M.G. Eliseikina, I.Yu. Petrova, E.L. Nazarenko, S.N. Kovalchuk Isolation and properties of a mannan-bind ing lectin from the holothurian Apostichopus japonicus. Glycobiology 2007, V.17, №12, P.1284-1298.
5. Aoyagi Y., Suzuki Y., Isemura М., Nomoto М., Sekini C., Igarashi K., Ichida F. The fucosylation of alfa-fetoprotein and its usefulness in the early diagnosis of hepatocellular carcinoma. Cancer, 1988. - Vol.61. - N.4. P.769-774.
6. 24. Yuan C.C, Wang P.H., Ng H.T., Tsai L.C., Juang C.M., Chiu L.M. Both TPA and SCC-Ag levels are prognostic even in high-risk stage Ib-IIa cervical carcinoma as determined by a stratification analysis. Eur. J. Gynaecol Oncol. 2002; 23(1):17-20.
7. Chi-Mou Juang M.D., Peng-Hui Wang M.D., Ming-Shien Yen M.D., Chiung-Ru Lai M.D., Heung-Tat Ng M.D. and Chiou-Chung Yuan M.D. Application of Tumor Markers CEA, TPA, and SCC-Ag in Patients with Low-Risk FIGO Stage IB and IIA Squamous Cell Carcinoma of the Uterine Cervix. Gynecologic Oncology. 2000; 76(1):103-106.
8. RU 2343485 C1, 10.01.2009.
9. RU 2447151 C1, 10.04.2012.
10. Sambrook J., Fritsch E.F., Maniatis Т. // Molecular Cloning. A. Laboratory Manual. 2bd ed. Cold Spring Harbor, NY, 1989.
Перечень нуклеотидных и аминокислотных последовательностей приведен в конце описания.


Изобретение относится к биотехнологии и представляет собой плазмиду pET40CmAP/MBL-T, определяющую синтез гибридного бифункционального полипептида CmAP/MBL-T со свойствами высокоактивной щелочной фосфатазы морской бактерии Cobetia marina (CmAP) и маннан-связывающего лектина С-типа дальневосточного трепанга Apostichopus japonicus (MBL-T). Плазмида включает NcoI/SalI - фрагмент плазмиды рЕТ-40b(+) (Novagen) и фрагмент ДНК размером 2034 пар оснований, который является химерным геном, кодирующим структурные гены щелочной фосфатазы CmAP и маннан-связывающего лектина С-типа MBL-T, соединенных между собой полинуклеотидом, кодирующим аминокислотную последовательность линкера (G)4S(G)4S(G)4SEL. Описан рекомбинантный штамм E.coli Rosetta(DE3)/pET40CmAP/MBL-T, трансформированный указанной плазмидой, - продуцент гибридного бифункционального белка CmAP/MBL-T. Предложен также способ получения гибридного бифункционального белка CmAP/MBL-T c использованием заявленного штамма. Изобретение позволяет получать высокоочищенный препарат гибридного белка CmAP/MBL-T со свойствами рекомбинантной высокоактивной щелочной фосфатазы CmAP и высокоспецифичного маннан-связывающего лектина С-типа MBL-T по отношению к углеводным компонентам гликопротеинов раковых клеток шейки матки и может быть использован для высокочувствительного лектин-иммунноферментного метода ранней дифференциальной диагностики рака шейки матки.3 н.п. ф-лы, 2 ил., 3 пр.
1. Плазмида pET40CmAP/MBL-T размером 8194 пар оснований (п.о.), определяющая синтез рекомбинантного гибридного бифункционального полипептида CmAP/MBL-T и характеризующаяся наличием следующих фрагментов: NcoI/SalI-фрагмента плазмиды pET-40b(+) (Novagen) и фрагмента ДНК размером 2034 п.о., содержащего химерный ген, состоящий из структурной части гена щелочной фосфатазы CmAP, включая линкер (G)4S(G)4S(G)4SEL, и структурной части гена маннан-связывающего лектина С-типа MBL-T (SEQ ID N 1).
2. Рекомбинантный штамм E.coli Rosetta(DE3)/pET40CmAP/MBL-T, трансформированный плазмидой pET40CmAP/MBL-T по п.1, - продуцент гибридного бифункционального полипептида CmAP/MBL-T.
3. Способ получения рекомбинантного гибридного бифункционального полипептида CmAP/MBL-T, характеризующийся тем, что штамм-продуцент по п.2 инкубируют в жидкой питательной среде LB в течение 12 ч при 16°С, затем бактериальные клетки осаждают центрифугированием, суспензию клеток дезинтегрируют в буфере, далее экстракт центрифугируют, затем надосадочную жидкость помещают на колонку с ионообменной смолой, далее элюируют белок, затем белковый элюат помещают на колонку с металлоаффинной смолой, далее активные фракции концентрируют на ионообменной смоле и выделяют целевой продукт гель-фильтрацией.
| БРОНЕВАЯ СТАЛЬ | 2011 |
|
RU2447181C1 |
| Электроакустический резонансный фильтр | 1934 |
|
SU42221A1 |
| Машина для уборки и переворачивания кускового торфа | 1950 |
|
SU92772A1 |
| US 20020082209, 27.06.2002 | |||
Авторы
Даты
2015-01-10—Публикация
2013-09-11—Подача