Область изобретения
Данное изобретение относится в целом к области вакцин и, в частности, к адъювантным композициям для усиления иммунного ответа в ветеринарии. В частности, изобретение относится к применению субмикронной эмульсии «масло в воде» в качестве адъюванта вакцины для усиления иммуногенности антигенов. Настоящее изобретение относится к композициям субмикронной эмульсии «масло в воде», композициям вакцины, содержащим антиген, включенный в такие эмульсии, а также способам получения эмульсий и вакцин.
Предшествующий уровень техники
Бактериальные, вирусные, паразитарные и микоплазменные инфекции широко распространены в ветеринарии, например, у крупного рогатого скота, свиней и домашних животных. Заболевания, вызванные этими инфекционными агентами, часто устойчивы к противомикробным фармацевтическим средствам, не оставляя эффективных средств лечения. Следовательно, вакцины все чаще используют для борьбы с инфекционными заболеваниями у таких животных. Полноразмерный инфекционный патоген можно сделать пригодным для применения в композиции вакцины после химической инактивации или соответствующего генетического воздействия. Альтернативно, белковая субъединица патогена может экспрессироваться в рекомбинантной системе экспрессии и быть очищена для применения в композиции вакцины.
Адъювант, как правило, относится к любому веществу, который увеличивает гуморальный и/или клеточный иммунный ответ на антиген. Обычные вакцины состоят из неочищенного препарата убитых патогенных микроорганизмов, и примеси, связанные с культурами патологических микроорганизмов, могут действовать в качестве адъюванта для усиления иммунного ответа. Однако когда в качестве антигенов для вакцинации применяются однородные препараты патологических микроорганизмов или очищенных белковых субъединиц, то иммунитет, вызванный такими антигенами, слабый, и таким образом необходимо добавление к ним определенных экзогенных веществ в качестве адъюванта. Кроме того, производство синтетических и субъединичных вакцин дорогостоящее. Поэтому благодаря адъюванту может потребоваться меньшая доза антигена для стимуляции иммунного ответа, что таким образом сэкономит производственные затраты вакцин.
Известно, что адъюванты действуют различными путями для усиления иммунного ответа. Многие адъюванты модифицируют цитокиновую сеть, связанную с иммунным ответом. Эти иммуномодуляторные адъюванты могут оказывать свой эффект даже без антигена. В целом, иммуномодуляторные адъюванты стимулируют регуляцию определенных цитокинов и параллельно подавляют регуляцию других цитокинов, что приводит к клеточному Th1 и/или гуморальному Th2 ответу.
Некоторые адъюванты способны сохранять конформационную целостность антигена, и такие антигены могут быть эффективно представлены соответствующим иммунным эффекторным клеткам. В результате такого сохранения антигенной конформации адъювантной композицией, вакцина имела бы более продолжительный срок хранения, например такой, как у иммуностимулирующих комплексов (ISCOM). Ozel M., et. al.; Quarternary Structure of the Immunestimmulating Complex (Iscom), J. of Ultrastruc. and Molec. Struc. Res. 102, 240-248 (1989).
Некоторые адъюванты обладают свойством удерживать антиген в виде депо в месте инъекции. В результате, антиген не так быстро выводится печеночным клиренсом. Соли алюминия и эмульсии «вода в масле» действуют посредством эффекта депо кратковременно. Например, можно, используя полный адъювант Фрейнда (FCA), который представляет собой эмульсию «вода в масле», получить долгосрочное депо. FCA обычно остается в месте инъекции до своей биодеградации, которая обеспечит удаление антигена антиген-презентирующими клетками.
По своей физической природе адъюванты могут быть разделены на две широкие категории, а именно адъюванты в виде частиц и адъюванты, не состоящие из частиц. Адъюванты в виде частиц существуют в форме микрочастиц. Иммуноген способен либо включаться, либо связываться с микрочастицами. Соли алюминия, эмульсии «вода в масле», эмульсии «масло в воде», иммуностимулирующие комплексы, липосомы и нано- и микрочастицы являются примерами адъювантов в виде частиц. Адъюванты, не состоящие из частиц, представляют собой как правило иммуномодуляторы, и они как правило используются в сочетании с адъювантами в виде частиц. Мурамилдипептид (адъювантно-активный компонент пептидогликана, экстрагированного из микобактерий), не ионные блок-сополимеры, сапонины (сложная смесь тритерпеноидов, экстрагированных из коры дерева Quillaja saponaria), липид А (дисахарид глюкозамина с двумя фосфатными группами и 5 или 6 цепями жирных кислот, в целом длиной от С12 до С16), цитокины, углеводородные полимеры, производные полисахариды и бактериальные токсины, такие как холерный токсин и лабильный токсин E.coli (LT) являются примерами адъювантов, не состоящих из частиц.
Некоторые из наиболее известных адъювантов представляют собой комбинацию иммуномодуляторов, не состоящих из частиц, и частиц, которые могут придать эффект депо адъювантной композиции. Например, FCA сочетает в себе иммуномодуляторные свойства компонентов Mycobacterium tuberculosis наряду с кратковременным эффектом депо масляных эмульсий.
Масляные эмульсии использовались в качестве адъювантов вакцин долгое время. Le Moignic и Pinoy обнаружили в 1916 г., что суспензия убитой Salmonella typhimurium в минеральном масле повышала иммунный ответ. Затем в 1925 г. Ramon описал крахмальное масло в качестве одного из веществ, усиливающих антитоксический ответ на дифтерийный токсоид. Однако масляные эмульсии не были популярными до 1937 г., пока Фрейнд не предложил адъювантную композицию, в настоящее время известную как полный адъювант Фрейнда (FCA). FCA представляет собой эмульсию «вода в масле», состоящую из минерального (парафинового) масла, смешанного с убитой микобактерией и Artacel A. Artacel A главным образом представляет собой моноолеат маннида и применяется в качестве эмульгирующего агента. Хотя FCA великолепно индуцирует антителогенез, он вызывает сильную боль, образование абсцесса, лихорадку и грануломатозное воспаление. Во избежание нежелательных побочных реакций, был разработан неполный адъювант Фрейнда (IFA). IFA аналогичен FCA по его составу, за исключением отсутствия микобактериальных компонентов. IFA действует посредством образования депо на месте инъекции и медленно высвобождает антиген, стимулируя антиген прогнозирующие клетки.
Другой подход к усовершенствованию FCA был основан на том принципе, что замещение минерального масла биологически совместимым маслом могло бы устранить реакции, связанные с FCA, в месте инъекции. Также предполагали, что эмульсия должна представлять собой эмульсию «масло в воде», а не эмульсию «вода в масле», так как последняя создает долгосрочное депо на месте инъекции. Hilleman et al. описали адъювант на масляной основе “Adjuvant 65”, состоящий из 86% арахисового масла, 10% Arlacel A, в качестве эмульгатора, и 4% моностеарата алюминия, в качестве стабилизатора. Hilleman, 1966, Prog. Med. Virol. 8: 131-182; Hilleman and Beale, 1983, in New Approaches to Vaccine Development (Eds. Bell, R. and Torrigiani, G.), Schawabe, Basel. Для людей Adjuvant 65 был безопасным и активным, но проявлял меньшую адъювантность, чем IFA. Тем не менее, применение Adjuvant 65 у людей было прекращено вследствие реактогенности определенных количеств вакцины и сокращения адъювантности, при использовании очищенного или синтетического эмульгатора вместо Arlacel A. В патентах США №№ 5718904 и 5690942 сообщается, что минеральное масло в эмульсии «масло в воде» можно заменить метаболическим маслом с целью улучшения свойств безопасности.
Кроме адъювантности и безопасности, физические признаки эмульсии также являются коммерчески важными. Физические признаки зависят от стабильности эмульсии. Расслоение эмульсии, образование осадка и слипание являются показателями нестабильной эмульсии. Расслоение эмульсии происходит, когда масляная и водная фазы эмульсии имеют различный удельный вес. Расслоение эмульсии также происходит, когда капли имеют большой исходный размер, когда у них нет броуновского движения. Когда капли больше, тогда наблюдается межповерхностный разрыв, и капли слипаются в крупные частицы. Стабильная устойчивость эмульсии определяется рядом факторов, таких как природа и количество используемого эмульгатора, величина капель в эмульсии и разность плотности между фазами масло и вода.
Эмульгаторы способствуют стабилизации диспергированных капель, снижая межповерхностную свободную энергию и создавая физический и электростатический барьер для слипания капель. В качестве эмульгаторов использовали неионные, а также ионные детергенты. Неионные эмульгаторы находятся на поверхности раздела и образуют относительно объемные структуры, что ведет к пространственному предупреждению образования диспергированных капель. Анионные или катионные эмульгаторы вызывают образование электрического двойного слоя, притягивая противоионы; отталкивающие силы двойного слоя вызывают отталкивание капель друг от друга при их сближении.
Кроме использования эмульгаторов, стабильность эмульсии можно также достичь за счет уменьшения размера капель эмульсии механическими способами. Обычно для изготовления эмульсий используют пропеллерные миксеры, турбинные роторы, коллоидные мельницы, гомогенизаторы и устройства для обработки ультразвуком. Микрофлюидизация представляет собой другой путь увеличения однородности размера капель в эмульсии. Микрофлюидизация может создавать высококачественную, физически стабильную эмульсию с однородным размером частиц в субмикронном диапазоне. Кроме повышения стабильности эмульсии, способ микрофлюидизации обеспечивает заключительную фильтрацию, которая представляет собой предпочтительный путь стерилизации конечного продукта. Более того, субмикронные частицы масла могут поступать из места инъекции в лимфатические сосуды, а затем в лимфатические узлы дренажной сети, кровь и селезенку. Это снижает вероятность образования масляного депо в месте инъекции, которое может вызвать местное воспаление и значительную реакцию на месте инъекции.
Микрофлюидизаторы в настоящее время коммерчески доступны. Образование эмульсии происходит в микрофлюидизаторе по мере того как два флюидизированных потока взаимодействуют на высоких скоростях внутри камеры взаимодействия. Микрофлюидизатор приводится в действие воздухом или азотом и может работать при величинах внутреннего давления, превышающих 20000 фунтов/кв.дюйм. В патенте США № 4908154 сообщается об использовании микрофлюидизатора для получения эмульсий, по существу свободных от каких-либо эмульгирующих агентов.
Ряд субмикронных адъювантных композиций в виде эмульсии «масло в воде» были описаны в литературе. В патенте США № 5376369 сообщается о субмикронной адъювантной композиции в виде эмульсии «масло в воде», известной как адъювантная композиция Syntax (SAF). SAF содержит сквален или сквалан в качестве масляного компонента, образующее эмульсию количество блок-сополимера Pluronic L121 (полиоксипропилен-полиоксиэтилен) и иммунопотенцирующее количество мурамилдипептида. Сквален представляет собой линейный углеводородный предшественник холестерина, обнаруживаемый во многих тканях, особенно в печени акул и у других рыб. Сквалан получают гидрированием сквалена, и он является полностью насыщенным. И сквален, и сквалан могут метаболизироваться, и было проведено достаточное количество их токсикологических исследований. Эмульсии сквалена или сквалана использовали в противораковых вакцинах людей и имели незначительные побочные эффекты и желательную эффективность (см., например, Anthony C. Allison, 1999, Squalene an Squalane emulsions as adjuvants, Methods 19:87-93).
В патенте США № 6299884 и Международной патентной публикации WO 90/14837 сообщалось, что полиокси-пропилен-полиоксиэтилен блок сополимеры не существенны для образования субмикронной эмульсии «масло в воде». Более того, в этих ссылках указывается использование нетоксичного метаболического масла, и явно исключается использование минерального масла и токсичных масел, получаемых в результате перегонки нефти, в таких эмульсионных композициях.
В патенте США № 5961970 описана еще одна субмикронная эмульсия «масло в воде», которая может использоваться как адъювант вакцины. В эмульсии, описанной в этом патенте, гидрофобный компонент выбран из группы, включающий среднецепочечное триглицеридное масло, растительное масло и их смеси. Поверхностно-активное вещество, включенное в эту эмульсию, может представлять собой природное, биологически совместимое поверхностно-активное вещество, такое как фосфолипид (например, лецитин) или фармацевтически приемлемое неприродное поверхностно-активное вещество, такое как TWEEN-80. В этом патенте также описано включение антигена в эмульсию в процессе образования эмульсии, в отличие от смешивания антигена с эмульсией после независимого и косвенного получения эмульсии.
В патенте США № 5084269 сообщается о том, что адъювантная композиция, содержащая лецитин в комбинации с минеральным маслом, уменьшает раздражение в организме животного-хозяина и одновременно усиливает системный иммунитет. Адъювантная композиция, полученная в патенте США № 5084269, промышленно используется в вакцинах, используемых в ветеринарии под торговым названием AMPHIGEN®. Композиция AMPHIGEN® изготавливается из капель мицелл-масла, окруженных лецитином. Эти мицеллы обеспечивают сцепление большого количества цельноклеточных антигенов по сравнению с традиционными адъювантами на масляной основе. Более того, композиции вакцины на основе AMPHIGEN® содержат низкое количество масла, содержащее от 2,5 до 5% минерального масла, по сравнению с другими композициями вакцины, содержащими масляные адъюванты, которые обычно содержат от 10% до 20% масла. Низкое содержание масла в композиции вакцины на основе адъюванта вызывает меньшее раздражение тканей на месте инъекции, что приводит к меньшему числу повреждений и снижает количество обрезок при обработке туш скота на бойне. Кроме того, лецитиновое покрытие, окружающее масляные капли, также уменьшает реакции на месте инъекции, что приводит к получению вакцины, которая является и безопасной, и эффективной.
Композиция AMPHIGEN® используется в качестве адъюванта в ряде вакцин, используемых в ветеринарии, но существует необходимость в поддержании физических признаков вакцины в течение короткого временного и длительного хранения, а также при растворении перед инъекцией. Кроме того, лиофилизированный антиген смешивают с предварительно полученной адъювантной композицией непосредственно перед инъекцией. Это не всегда гарантирует равномерное распределение антигена внутри эмульсии «масло в воде», и признаки эмульсии могут быть нежелательными. Более того, после отстаивания в гомогенизированной эмульсии может возникать фазовое разделение. Поэтому существует необходимость в стабильной адъювантной композиции, в которой не происходит фазового разделения при длительном хранении. Одним из путей предотвращения фазового разделения является уменьшение размера капель и увеличение однородности частиц в эмульсии. Хотя способ микрофлюидизации метаболических композиций в виде эмульсий на масляной основе был описан, микрофлюидизация эмульсий «масло в воде», таких как композиция AMPHIGEN®, еще не осуществлялась.
В настоящем изобретении микрофлюидизация использовалась для обеспечения субмикронного размера окруженных лецитином капель минерального масла. Неожиданно заявителями было обнаружено, что микрофлюидизация композиций вакцины с эмульсией «масло в воде», состоящей из смеси лецитина и масла, не только улучшает физические признаки композиций, но также усиливает иммунизирующее действие композиций. Микрофлюидизированные композиции также отличаются повышенными свойствами безопасности.
Краткое изложение сущности изобретения
Заявители неожиданно обнаружили, что адъювантную активность и свойства безопасности неметаболических эмульсий «масло в воде» на масляной основе можно улучшить посредством микрофлюидизации. Антигены, введенные в микрофлюидизированные эмульсии, стабильны даже тогда, когда антигены вводят перед микрофлюидизацией.
Соответственно, в одном из вариантов осуществления настоящее изобретение относится к композиции в виде субмикронных эмульсий «масло в воде», которую можно использовать в качестве адъюванта вакцины. Композиции в виде субмикронных эмульсий «масло в воде» по настоящему изобретению состоят из неметаболического масла, по меньшей мере, одного поверхностно-активного вещества и водного компонента, где масло диспергировано в водном компоненте со средним размером капель масла в субмикронном диапазоне. Предпочтительно, неметаболическим маслом является легкое минеральное масло. Предпочтительными поверхностно-активными веществами являются лецитин, Tween-80 и SPAN-80.
Предпочтительная эмульсия «масло в воде» по настоящему изобретению состоит из композиции AMPHIGEN®.
Эмульсии «масло в воде» по настоящему изобретению могут содержать дополнительные компоненты, которые целесообразны и желательны, включая консерванты, осмотические агенты, молекулы биологического клеящего вещества и иммуностимулирующие молекулы. Предпочтительные иммуностимулирующие молекулы включают в себя, например, Quil-A, холестерин, GPI-0100, бромид диметилдиоктадециламмония (DDA).
В другом варианте осуществления настоящее изобретение относится к способу получения субмикронной эмульсии «масло в воде». В соответствии с настоящим изобретением, различные компоненты эмульсии, включая масло, одно или несколько поверхностно-активных веществ, водный компонент и любой другой компонент, целесообразный для использования в эмульсии, смешиваются вместе. Смесь подвергают процессу первичного эмульгирования с образованием эмульсии «масло в воде», которую затем пропускают через микрофлюидизатор с получением эмульсии «масло в воде» с каплями менее 1 мкм в диаметре, предпочтительно, со средним размером капель менее чем 0,5 мкм.
В еще одном варианте осуществления настоящее изобретение относится к композициям вакцины, которые содержат антиген и описанную выше субмикронную эмульсию «масло в воде». Антиген вводят либо до, либо после получения эмульсии, предпочтительно до получения.
Антиген, который может быть включен в композицию вакцины по настоящему изобретению, может представлять собой бактериальный, грибковый или вирусный антиген или их комбинацию. Антиген может принимать форму инактивированной, цельной или частичной клетки или вирусного препарата или образовывать антигенные молекулы, полученные обычной очисткой белка, способами генной инженерии или химическим синтезом.
Еще в одном варианте осуществления настоящее изобретение относится к способам получения композиций вакцины, содержащих антиген или антигены, комбинированные с субмикронной эмульсией «масло в воде».
При получении композиций вакцины настоящего изобретения антиген(ы) можно вводить либо до (например, перед микрофлюидизацией), либо после образования эмульсии (например, после микрофлюидизации) с компонентами эмульсии «масло в воде». Предпочтительно, антиген комбинируют с компонентами эмульсии «масло в воде».
В еще одном варианте осуществления настоящее изобретение относится к композициям вакцины, которые содержат микроинкапсулированный антиген и описанную выше субмикронную эмульсию «масло в воде», где микроинкапсулированный антиген комбинируют с эмульсией после получения.
Краткое описание чертежей
На фиг.1 изображен способ получения в виде партии немикрофлюидизированных композиций вакцины. При этом способе различные компоненты вакцины добавляют в сосуд для добавления слева и, в конечном счете, закачиваются в сосуд для смешивания, где компоненты смешивают вместе простыми механическими способами.
На фиг. 2 изображен способ получения микрофлюидизированных композиций вакцины, содержащих до получения эмульсии включенный антиген. Различные компоненты вакцины добавляют в сосуд для добавления и переносят в блок предэмульсионного перемешивания для смешивания простыми механическими способами. Затем эмульсию пропускают через микрофлюидизатор и собирают в пост-микрофлюидизационную камеру.
На фиг. 3 изображено распределение размера капель вакцины на основе немикрофлюидизированной композиции AMPHIGEN®, вакцины на основе микрофлюидизированной композиции AMPHIGEN® и препарата вакцины, смешанной в газогенераторной печи.
На фиг. 4 показано отсутствие фазового разделения в препарате микрофлюидизированной вакцины.
На фиг. 5 изображено сравнение устойчивости антигенов, введенных до получения эмульсии в препарат вакцины на основе микрофлюидизированной композиции AMPHIGEN® (А907505) и трех контролей, препаратов вакцины на основе микрофлюидизированной композиции AMPHIGEN® (А904369, А904370 и А904371). Все четыре препарата вакцин хранились при 4°С в течение 2 лет. В различные моменты времени в процессе хранения (0, 6, 12 или 24 мес.) все четыре композиции использовали для вакцинации трехмесячных телят. Вакцинацию проводили в 0 и 21 день 2 мл дозами вакцины, и сыворотку брали через 2 недели после второй вакцинации. В каждом из образцов сыворотки определяли титр нейтрализующих антител к вирусу BVD II типа (вирусной диареи крупного рогатого скота). Данные показаны в виде среднего геометрического для 5 животных.
На фиг. 6 показана минимальная средняя квадратическая ректальной температуры у крупного рогатого скота перед и после введения микрофлюидизированной и немикрофлюидизированной вакцин. Т01: Группа плацебо - однократная доза; Т02: Группа плацебо - двойная доза; Т03: Немикрофлюидизированная композиция - однократная доза; Т04: Немикрофлюидизированная композиция - двойная доза; Т05: Микрофлюидизированная композиция - однократная доза; Т06: Микрофлюидизированная композиция - двойная доза.
На фиг. 7 изображены минимальные средние квадратические объемов реакции в месте инъекции, наблюдавшиеся у крупного рогатого скота после введения микрофлюидизированной и немикрофлюидизированной композиций вакцины. Т03: Немикрофлюидизированная композиция - однократная доза; Т04: Немикрофлюидизированная композиция - двойная доза; Т05: микрофлюидизированная композиция - однократная доза; Т06: микрофлюидизированная композиция - двойная доза.
На фиг. 8 показано среднее геометрическое титров IgG для рекомбинантного антигена PauA из Streptococcus aureus после вакцинации различными композициями вакцины, содержащими и рекомбинантный антигена PauA, и антиген цельных клеток E.coli.
На фиг. 9 показано среднее геометрическое титров антигена цельных клеток E.coli из Streptococcus aureus после вакцинации различными композициями вакцины, содержащими и рекомбинантный антигена PauA, и антиген цельных клеток E.coli.
На фиг.10А и 10В изображено распределение размера частиц микрофлюидизированной композиции AMPHIGEN при исходной продукции (фиг. 10А) и через 22 мес. после продукции (фиг. 10В).
Подробное описание изобретения
Авторы настоящего изобретения неожиданно обнаружили, что микрофлюидизация композиций вакцины с добавкой эмульсии «масло в воде», состоящей из смеси лецитина и минерального масла, не только улучшает физические параметры композиций вакцины, но также усиливает иммунизирующее действие композиций вакцины. Микрофлюидизированные композиции вакцины также характеризуются улучшенными свойствами безопасности.
На основании этого обнаружения, настоящее изобретение относится к субмикронным эмульсиям «масло в воде», которые можно использовать в качестве добавки к композициям вакцины. Изобретение также относится к способам получения этих субмикронных эмульсий «масло в воде» с помощью микрофлюидизатора. Кроме того, настоящее изобретение относится к субмикронным композициям вакцины, в которых антиген комбинирован с субмикронной эмульсией «масло в воде». Настоящее изобретение также относится к способам получения таких композиций вакцины. Настоящее изобретение, кроме того, относится к композициям вакцины, содержащим микроинкапсулированные антигены, в сочетании с субмикронной эмульсией «масло в воде», и к способам получения таких вакцин.
Для ясности описания, но не для ограничения, подробное описание изобретения разделено на следующие подразделы, которые описывают или иллюстрируют определенные признаки, варианты осуществления или применение по изобретению.
Субмикронные эмульсии «масло в воде»
В одном из вариантов осуществления настоящее изобретение относится к композициям в виде субмикронной эмульсии «масло в воде», которые можно использовать в качестве добавки к вакцине. Субмикронные эмульсии «масло в воде» по настоящему изобретению усиливают иммуногенность антигенов в композициях вакцины, безопасны при введении животным и стабильны во время хранения.
Субмикронные эмульсии «масло в воде» по настоящему изобретению состоят из неметаболического масла, по меньшей мере, одного поверхностно-активного вещества и водного компонента, где масло диспергировано в водном компоненте со средним размером капель в субмикронном диапазоне.
Под «субмикронным» подразумевается, что капли имеют размер менее чем 1 мкм (микрон), а средний или нормальный размер частиц составляет менее чем 1 мкм. Предпочтительно, средний размер капель эмульсии составляет менее чем 0,8 мкм; предпочтительнее, менее чем 0,5 мкм а еще предпочтительнее, менее чем 0,4 мкм или примерно 0,1-0,3 мкм.
Под «средним размером капель» понимают размер частиц в виде среднего диаметра объема (VMD). VMD рассчитывается умножением диаметра каждой частицы на объем всех частиц этого размера и сложением. Затем эта величина делится на общий объем всех частиц.
Используемый в настоящем описании термин «неметаболическое масло» относится к маслам, которые не могут метаболизироваться организмом животного-индивидуума, которому вводится эмульсия.
Используемые в настоящем описании термины «животное» и «животное-индивидуум» относятся ко всем животным, включая, например, крупный рогатый скот, овец и свиней, не относятся к человеку.
Неметаболические масла, которые можно использовать в виде эмульсии по настоящему изобретению, включают алканы, алкины и другие соответствующие кислоты и спирты, их простые и сложные эфиры и их смеси. Предпочтительно, отдельные соединения масла представляют собой легкие углеводородные соединения, то есть такие компоненты содержат от 6 до 30 атомов углерода. Масло может быть получено синтетически или очищено из нефтяных продуктов. Предпочтительные неметаболические масла, которые могут использоваться в эмульсиях по настоящему изобретению, включают, например, минеральное масло, парафиновое масло и циклопарафины.
Термин «минеральное масло» относится к смеси жидких углеводородов, полученных из нефти путем перегонки. Этот термин является синонимом термина «сжиженный парафин», «вазелиновое масло», то есть масло, которое получают аналогичным образом перегонкой петролатума, но которое имеет несколько более низкую удельную массу, чем белое минеральное масло. См., например, Remington's Pharmaceutical Sciences, 18th Edition (Easton, Pa.: Mack Publishing Company, 1990, at pages 788 and 1323). Минеральное масло может быть получено из различных коммерчески доступных источников, например, J.T.Baker (Phillipsburg, PA), USB Corporation (Cleveland, OH). Предпочтительно, минеральное масло представляет собой легкое минеральное масло, коммерчески доступное под торговым названием DRAKEOL®.
Обычно масляный компонент субмикронных эмульсий по настоящему изобретению присутствует в количестве от 1% до 50% об., предпочтительно, в количестве от 10% до 45%, предпочтительнее, в количестве от 20% до 40%.
Эмульсии «масло в воде» по настоящему изобретению обычно содержат, по меньшей мере, одно (то есть одно или несколько) поверхностно-активное вещество. Вещества, обозначаемые терминами «поверхностно-активные вещества» и «эмульгаторы», которые используются в настоящем описании взаимозаменяемо, представляют собой вещества, которые стабилизируют поверхность масляных капель и поддерживают масляные капли в пределах желательного размера.
Поверхностно-активные вещества, которые могут использоваться в эмульсиях по настоящему изобретению, включают природные биологически совместимые поверхностно-активные вещества и неприродные синтетические поверхностно-активные вещества. Биологически совместимые поверхностно-активные вещества включают фосфолипидные соединения или смесь фосфолипидов. Предпочтительными фосфолипидами являются фосфатидилхолины (лецитин), такие как соевый или яичный лецитин. Лецитин может быть получен в виде смеси фосфатидов и триглицеридов промыванием водой неочищенных растительных масел и разделением и сушкой полученных гидрированных смол. Очищенный продукт может быть получен фракционированием смеси на нерастворимые в ацетоне фосфолипиды и гликолипиды, остающиеся после удаления триглицеридов и растительного масла при промывании ацетоном. Альтернативно, лецитин может быть получен из различных коммерческих источников. Другие подходящие фосфолипиды включают фосфатидилглицерин, фосфатидилинозит, фосфатидилсерин, фосфатидовую кислоту, кардиолипин и фосфатидилэтаноламин. Фосфолипиды могут быть выделены из природных источников или синтезировать обычным путем.
Неприродные синтетические поверхностно-активные вещества, подходящие для использования в субмикронных эмульсиях по настоящему изобретению, включают неионные поверхностно-активные вещества на основе сорбитана, например поверхностно-активные вещества с сорбитаном, замещенным жирной кислотой (коммерчески доступные под названием SPAN® или ARLECEL®), сложные эфиры жирных кислот полиэтоксилированного сорбита (TWEEN®), сложные эфиры жирных кислот полиэтиленгликоля из таких источников как касторовое масло (EMULFOR); полиэтоксилированную жирную кислоту (например, стеариновую кислоту, имеющуюся под названием SIMULSOL M-53), полимер полиэтоксилированного изооктила/формальдегида (TYLOXAPOL), простые эфиры жирных спиртов полиоксиэтилена (BRIJ®); простые не фениловые эфиры полиоксиэтилена (TRITON®N), простые изооктилфениловые эфиры полиоксиэтилена (TRITON®X). SPAN® и TWEEN® являются предпочтительными синтетическими поверхностно-активными веществами.
Предпочтительные поверхностно-активные вещества для использования в эмульсиях «масло в воде» по настоящему изобретению включают лецитин, Twen-80 и SPAN-80.
Обычно количество поверхностно-активного вещества или комбинации поверхностно-активных веществ при использовании двух или более поверхностно-активных веществ, присутствующих в эмульсии, составляет от 0,01% до 10% об., предпочтительно, от 0,1% до 6,0%, предпочтительнее, от 0,2% до 5,0%.
Водный компонент составляет дисперсионную фазу эмульсии и может представлять собой воду, буферный солевой раствор или любой другой подходящий водный раствор.
Эмульсии «масло в воде» по настоящему изобретению могут содержать дополнительные компоненты, которые являются подходящими и желательными, включая консерванты, осмотические агенты, биоадгезивные молекулы и иммуностимулирующие молекулы.
Полагают, что биоадгезивные молекулы могут усиливать доставку и прикрепление антигенов на мишеневой слизистой поверхности, вызывая иммунный ответ. Примеры подходящих биоадгезивных молекул включают кислые, неприродные полимеры, такие как полиакриловая кислота и полиметакриловая кислота (например, CARBOPOL®, CARBOMER); кислотные синтетически модифицированные природные полимеры, такие как карбоксиметилцеллюлоза; нейтральные синтетически модифицированные естественные полимеры, такие как (гидроксипропил)метилцеллюлоза; основные несущие амин полимеры, такие как хитосан; кислотные полимеры, получаемые из природных источников, такие как альгиновая кислота, гиалуроновая кислота, пектин, смола трагаканта и смола карайя; и нейтральные неприродные полимеры, такие как поливиниловый спирт, или их сочетания.
Используемая в настоящем описании фраза «иммуностимулирующие молекулы» относится к тем молекулам, которые усиливают защитный иммунный ответ, индуцированный антигенным компонентом вакцинными композициями. Подходящие иммуностимулирующие вещества включают компоненты стенки бактериальной клетки, например производные N-ацетилмурамил-L-аланил-D-изоглутаминовой кислоты, такие как мурабутид, треонил-MDP и мурамилтрипептид; сапониновые гликозиды и их производные, например, Quil-A, QS 21 и GPI-0100; холестерин; и соединения четвертичного аммония, например бромид диметилдиоктадециламмония (DDA) и N,N-диоктадецил-N,N-бис(2-гидроксиэтил)пропандиамин («авридин»).
Сапонины представляют собой гликозидные соединения, которые продуцируются в качестве вторичных метаболитов у большого количества видов растений. Химическая структура сапонинов придает широкий диапазон фармакологической и биологической активности, включая некоторую мощную и эффективную иммунологическую активность.
Структурно, сапонины состоят из любого агликона, присоединенного с одной или несколькими сахарными цепями. Сапонины можно классифицировать в соответствии с составом их агликонов: тритерпеновые гликозиды, стероидные гликозиды и стероидные алкалоидные гликозиды.
Сапонины можно выделить из коры Quillaja saponaria. В течение длительного времени сапонины были известны как иммуностимуляторы. Dalsgaard, K., “Evaluation of its adjuvant activity with a special reference to the application in the vaccination of cattle against foot-and-mouth disease”, Acta. Vet. Scand. 69: 1-40 1978. Неочищенные экстракты растений, содержащие сапонины, усиливали активность вакцин против ящура. Однако неочищенные экстракты вызывали неблагоприятные побочные эффекты при использовании в вакцинах. В последующем, Dalsgaard частично очистил активный компонент, обладающий свойствами адъюванта, от сапонинов путем диализа, ионнообменной и гель-фильтрационной хроматографией. Dalsgaard, K., et al., “Saponin adjuvants III. Isolation of a substance from Quillaja saponaria Morina with adjuvant activity in foot-and-mouth disease vaccines”, Arch. Gesamte. Virusforsch. 44: 243-254, 1974. Активный компонент, со свойствами адъюванта, очищенный таким путем, известен как «Quil-A». В весовом отношении Quil-A продемонстрировал повышенную активность и сниженные местные реакции по сравнению с сапонинами. Quil-A широко используется в вакцинах, используемых в ветеринарии.
Последующий анализ Quil-A с помощью высокоэффективной жидкостной хроматографии (ВЭЖХ) выявил неоднородную смесь близко родственных сапонинов и привел к открытию QS 21, который является мощным адъювантом со сниженной или минимальной токсичностью. Kensil C.R. et al., “Separation and characterization of saponins with adjuvant activity from Quillaja saponaria Molina cortex”, J.Immunol. 146: 431-437, 1991. В отличие от других иммуностимуляторов, QS 21 растворим в воде, и его можно использовать в вакцинах, содержащих композиции по типу эмульсий или несодержащих. Было показано, что QS 21 вызывает Th1 реакцию у мышей, стимулируя продукцию антител IgG2a и IgG2b и индуцирует антиген-специфические CD8+CTL (MHC класса I) в ответ на субъединичные антигены. Клинические исследования людей доказали его адъювантные свойства и приемлемый токсикологический профиль. Kensil, C.R. et al., “Structural and immunological characterization of the vaccine adjuvant QS-21. In Vaccine Design: the subunit and Adjvuant Approach, ”Eds.Powell, M.F. and Newman, M.J.Plenum Publishing Corporation, New York. 1995, pp. 525-541.
В патенте США № 6080725 описаны способы получения и применения конъюгата сапонин-липофил. В конъюгате сапонин-липофил, липофильная часть, например липид, жирная кислота, полиэтиленгликоль или терпен, ковалентно связана с неацетилированным или дезацетилированным тритерпеновым сапонином через карбоксигруппу, присутствующую на 3-О-глюкуроновой кислоте тритерпенового сапонина. Присоединение липофильной части к 3-О-глюкуроновой кислоте сапонина, такого как дезациклосапонин Quillaja, люциосид Р или сапонин из Gypsophia, saponaria и Acanthophyllum, усиливает их адъювантные свойства на гуморальный и клеточный иммунитет. Кроме того, присоединение липофильной части к остатку 3-О-глюкуроновой кислоты не- или дезацетилсапонина дает аналог сапонина, который легче очистить, является менее токсичным, химически более устойчив и обладает равными или лучшими адъювантными свойствами, чем первоначальный сапонин.
GPI-0100 представляет собой конъюгат сапонин-липофил, описанный в патенте США № 6080725. GPI-0100 получают путем добавления алифатического амина к дезацилспорину через карбоксильную группу глюкуроновой кислоты.
Соединения четвертичного аммония. Ряд алифатических азотистых оснований был предложен для использования в качестве иммунологических адъювантов, включая амины, соединения четвертичного аммония, гуанидины, бензамидины и тиоуронии. Конкретные соединения включают в себя бромид диметилдиоктадециламмония (DDA) и N,N-диоктадецил-N,N-бис(2-гидроксиэтил)пропандиамин («авридин»).
В патенте США № 5951988 описана адъювантная композиция, содержащая соли четвертичного аммония, например, DDA в сочетании с масляным компонентом. Эту композицию можно использовать в сочетании с хорошо известными иммунологическими веществами, например, вирусными или бактериальными антигенами в композиции вакцины, для усиления антигенного ответа. Композицию также можно использовать без включенного антигена в качестве неспецифической иммуностимулирующей композиции.
В патенте США № 4310550 описано применение N,N-высшего алкил-N,N'-бис(2-гидроксиэтил)пропандиамина и N,N-высших алкил-ксилилендиаминов, входящих в состав композиции с жировой или липидной эмульсией, в качестве адъюванта вакцины. Способ индукции или усиления антигенного ответа антигена у человека или животного посредством парентерального введения адъювантной композиции описан в патенте США № 4310550.
В предпочтительном варианте осуществления настоящее изобретение относится к субмикронной эмульсии «масло в воде», которая состоит из композиции AMPHIGEN® с каплями размером менее чем 1 мкм и средним размером капель примерно 0,25 мкм.
Используемый в настоящем описании термин «композиция AMPHIGEN®» относится к раствору, получаемому при смешивании раствора лецитинового масла DRAKEOL® (Hydronics, Lincoln, NE) с солевым раствором в присутствии TWEEN® 80 и SPAN® 80. Обычная композиция AMPHIGEN® содержит 40% об. легкого минерального масла (об./об.), примерно 25% масс./об. лецитина, примерно 0,18% об. TWEEN 80 (об./об.) и примерно 0,08% об. Span 80 (об./об.).
Способы получения субмикронных эмульсий «масло в воде»
Еще в одном варианте осуществления настоящее изобретение относится к способам получения описанных выше субмикронных эмульсий «масло в воде».
В соответствии с настоящим изобретением, различные компоненты эмульсии, включая масло, одно или несколько поверхностно-активных веществ, водный компонент и любой другой компонент, подходящий для использования в эмульсии, объединяют и смешивают.
Полученную смесь подвергают процессу эмульгирования, обычно пропуская один или несколько раз через один или несколько гомогенизаторов или эмульгаторов с образованием эмульсии «масло в воде», которая имеет однородный вид и средний размер капель примерно 0,5 мкм. Для этой цели можно использовать любой имеющийся в продаже гомогенизатор или эмульгатор, например эмульгатор Ross (Hauppauge, NY), гомогенизатор Gaulin (Everett, MA).
Полученную таким образом эмульсию затем подвергают микрофлюидизации, доводя размер капель до субмикронного диапазона. Микрофлюидизация может быть осуществлена, используя промышленный микрофлюидизатор, такой как модель № 110Y, доступная от Microfluidics, Newton, Mass; Gaulin Model 30CD (Gaulin, Inc., Everett, Mass.) и Rainnie Minilab Type 8.30H (Miro Atomizer Food and Diary, Inc., Hudson, Wis.). Действие микрофлюидизаторов заключается в принудительном пропускании жидкости через маленькие отверстия под высоким давлением, так что два потока жидкости взаимодействуют на высоких скоростях в камере взаимодействия с образованием эмульсий с каплями субмикронного размера.
Размер капель можно определить различными способами, известными в данной области, например лазерной дифракцией, использованием коммерчески доступных приборов, устанавливающих размер. Размер может изменяться в зависимости от типа используемого поверхностно-активного вещества, соотношения между поверхностно-активным веществом и маслом, рабочего давления, температуры и тому подобных факторов. Специалист в данной области может определить желательную комбинацию этих параметров для получения эмульсий с желательным размером капель без чрезмерного экспериментирования. Диаметр капли эмульсий по настоящему изобретению составляет менее чем 1 мкм, предпочтительно, со средним размером капель менее чем 0,8 мкм, а предпочтительнее, со средним размером капель менее чем 0,5 мкм, а еще предпочтительнее, со средним размером капель менее чем 0,3 мкм.
В предпочтительном варианте осуществления настоящего изобретения раствор лецитинового масла DRAKEOL, коммерчески доступный от компании Hydronics (Lincoln, NE) и содержит 25% лецитина в легком минеральном масле, объединяют и смешивают с солевым раствором, а также с поверхностно-активными агентами TWEEN® 80 и SPAN® 80 для образования «раствора AMPHIGEN®» или «композиции AMPHIGEN®». Затем раствор AMPHIGEN® эмульгируют эмульгатором Ross® (Hauppauge, NY 11788) примерно при 3400 об/мин до образования эмульсии «масло в воде». Затем эмульсию однократно пропускают через микрофлюидизатор, работающий примерно при 4500±500 фунтов/кв.дюйм. Размер капель микрофлюидизированной эмульсии «масло в воде» составляет менее 1 мкм при среднем размере капель примерно 0,25 мкм.
Композиции вакцины, содержащие антигены, включенные в субмикронные эмульсии «масло в воде»
В другом варианте осуществления настоящее изобретение относится к композициям вакцины, которые содержат антиген(ы) и описанную выше субмикронную эмульсию «масло в воде». Эти композиции вакцины обладают повышенным антигенным ответом и улучшенными физическими признаками (например, после длительного периода хранения не наблюдается фазовое разделение). Кроме того, композиции вакцины по настоящему изобретению безопасны для введения животным.
В соответствии с настоящим изобретением, антиген можно комбинировать с эмульсией либо до, либо после ее получения, предпочтительно, до ее получения. Термин «до получения эмульсии» относится к способу, при котором антиген вводят в эмульсию перед стадией микрофлюидизации. Термин «после получения эмульсии» относится к способу, при котором антиген добавляется к эмульсии после того, как эмульсия была микрофлюидизирована. Антиген, добавленный в эмульсию после ее получения, может быть свободным антигеном, или он может быть инкапсулирован в микрочастицы, как далее описано ниже в настоящем описании.
Используемый в настоящем описании термин «антиген» относится к любой молекуле, соединению или композиции, которые являются антигенными у животного, и которые введены в композицию вакцины для того, чтобы вызвать защитную иммунную реакцию у животного, которому вводят композицию вакцины.
Термин «антигенный» или «иммуногенный», используемый в связи с антигеном, относится к способности антигена вызывать иммунную реакцию у животного против антигена. Иммунный ответ может быть клеточным иммунным ответом, опосредованным в первую очередь цитотоксическими Т-клетками, или гуморальным иммунным ответом, опосредованным в первую очередь Т-хелперами, который в свою очередь активирует В-клетки, приводя к продукции антител.
«Защитная иммунная реакция» определяется как любой иммунный ответ, опосредованный либо антителами, либо клетками, или ими обоими, возникающий у животного, который либо предотвращает, либо явно уменьшает частоту возникновения, либо устраняет, либо явно снижает тяжесть, либо явно замедляет скорость прогрессирования расстройства или заболевания, вызванного антигеном, или патогеном, содержащим антиген.
Антигены, которые могут быть введены в композицию вакцины по настоящему изобретению, включают антигены, полученные из патогенных бактерий, таких как Mycoplasma hyopneumoniae, Haemophilus somnus, Haemophilus parasuis, Bordetella bronchiseptica, Actinobacillus pleuropneumonie, Pasteurella multocida, Manheimia hemolytica, Mycoplasma bovis, Mycoplasma galanacieum, Mycobacterium bovis, Mycobacterium paratuberculosis, виды Clostridial, Streptococcus uberis, Streptococcus suis, Staphylococcus aureus, Erysipelothrix rhusopathiae, виды Campylobacter, Fusobacterium necrophorum, Escherichia coli, серологические варианты Salmonella enterica, виды Leptospira; патогенных грибов, таких как Candida; простейших, таких как Cryptosporidium parvum, Neospora canium, Toxoplasma gondii, виды Eimeria; гельминтов, таких как Ostertagia, Cooperia, Haemonchus, Fasciola, или в форме инактивированного цельного, или частичного клеточного препарата, или в форме антигенных молекул, полученных обычной очисткой белка, методиками генной инженерии или химического синтеза. Дополнительные антигены включают патогенные вирусы, такие как с-вирусы герпеса крупного рогатого скота-1,3,6, вирус вирусной диареи крупного рогатого скота (BVDV) типов 1 и 2, вирус парагриппа крупного рогатого скота, респираторный синцитиальный вирус, вирус коровьего лейкоза, вирус чумы крупного рогатого скота, вирус ящура, бешенства, вирус свиной лихорадки, вирус африканской свиной лихорадки, свиной парвовирус, вирус PRRS, свиной цирковирус, вирус гриппа, вирус везикулярной болезни свиней, вирус лихорадки Techen, вирус ложного бешенства, или в форме инактивированного цельного, или частичного клеточного препарата, или в форме антигенных молекул, полученных обычной очисткой белка, методиками генной инженерии или химического синтеза.
Количество антигена должно быть таким, чтобы антиген, который находится в сочетании с эмульсией «масло в воде», был бы эффективен для индукции защитной иммунной реакции у животного. Точное эффективное количество антигена зависит от природы, активности и чистоты антигена, и его может определить специалист в данной области.
Количество эмульсии «масло в воде», присутствующее в композициях вакцины, должно быть достаточным для усиления иммуногенности антигена(ов) в композициях вакцины. Когда это является подходящим и желательным, дополнительные количества поверхностно-активного вещества (веществ) или дополнительное поверхностно-активное вещество (вещества) можно добавить в композицию вакцины кроме поверхностно-активного вещества (веществ), находящегося в эмульсии «масло в воде». Обобщая, масляный компонент присутствует в конечном объеме композиции вакцины в количестве от 1,0% до 20% об.; предпочтительно, в количестве от 1,0% до 10%; предпочтительнее, в количестве от 2,0% до 5,0%. Поверхностно-активное вещество или комбинация поверхностно-активных веществ, если используются два или более поверхностно-активных веществ, присутствует в конечном объеме композиции вакцины в количестве от 0,1% до 20% об., предпочтительно, от 0,15% до 10%, предпочтительнее, от 0,2% до 6,0%.
Кроме антигена (антигенов) и эмульсии «масло в воде» композиция вакцины может включать другие компоненты, которые могут быть подходящими и желательны, такие как консерванты, осмотические агенты, молекулы биологического клеящего вещества и иммуностимулирующие молекулы (например, Quil-A, холестерин, GPI-0100, бромид диметилдиоктадециламмония (DDA), как описано выше в связи с эмульсией «масло в воде».
Композиции вакцин по настоящему изобретению могут также включать приемлемый в ветеринарии носитель. Термин «приемлемый в ветеринарии носитель» включает в себя любой и все растворители, дисперсионные среды, покрытия, адъюванты, стабилизирующие агенты, разбавители, консерванты, антибактериальные и противогрибковые средства, изотонические вещества, вещества, задерживающие всасывание, и им подобные. Разбавители могут включать воду, солевой раствор, декстрозу, этанол, глицерин и им подобные. Изотонические вещества, наряду с другими, могут включать хлорид натрия, декстрозу, манит, сорбит и лактозу. Стабилизаторы, наряду с другими, включают альбумин.
В предпочтительном варианте осуществления настоящее изобретение относится к композиции вакцины, которая включает, по меньшей мере, антиген BVDV типа I или BVDV типа II, введенный перед получением эмульсии «масло в воде», размер капель которой составляет менее, чем 1 мкм, предпочтительно, средний размер капель составляет менее чем 0,8 мкм; предпочтительнее, менее чем 0,5 мкм, а еще предпочтительнее, средний размер капель составляет примерно 0,5 мкм. Антиген BVDV типа I и/или II представлен предпочтительно в форме инактивированного вирусного препарата. Субмикронная эмульсия «масло в воде» предпочтительно включает в свой состав композицию AMPHINOGEN® (то есть композиции, которая содержит легкое минеральное масло, лецитин, TWEEN® 80 и SPAN® 80). Композиция вакцины предпочтительно также включает Quil-A, холестерин и тимеросол.
В другом предпочтительном варианте осуществления настоящее изобретение предоставляет композицию вакцины, которая включает в себя лептоспирозный антиген и, по меньшей мере, один из антигенов BVDV типа I или BVDV типа II в эмульсии «масло в воде». Антигены, предпочтительно, в форме инактивированной клетки или вирусного препарата, вводят перед получением эмульсии «масло в воде», размер капель составляет менее чем 1 мкм, предпочтительно, средний размер капель составляет менее чем 0,8 мкм; предпочтительнее, менее чем 0,5 мкм, а еще предпочтительнее, средний размер капель составляет примерно 0,5 мкм. Субмикронная эмульсия «масло в воде» предпочтительно включает в свой состав композицию AMPHINOGEN (то есть композиции, которая содержит легкое минеральное масло, лецитин, TWEEN® 80 и SPAN® 80). Композиция вакцины, предпочтительно, также включает в себя одну или несколько иммуностимулирующих молекул, выбранных из Quil-A, холестерина, DDA, GPI-100 и гидроокиси алюминия.
В еще одном предпочтительном варианте осуществления настоящее изобретение относится к композиции вакцины, которая включает, по меньшей мере, один бактериальный антиген, например белок рекомбинантного Streptococcus uberis PauA или клеточный препарат E. Coli или комбинацию их обоих в эмульсии «масло в воде». Антиген(ы) вводят перед получением эмульсии «масло в воде», размер капель составляет менее чем 1 мкм, предпочтительно, средний размер капель составляет менее чем 0,8 мкм; предпочтительнее, менее чем 0,5 мкм, а еще предпочтительнее, средний размер капель составляет примерно 0,25 мкм. Субмикронная эмульсия «масло в воде» предпочтительно включает в свой состав композицию AMPHINOGEN® (то есть композиции, которая содержит легкое минеральное масло, лецитин, TWEEN® 80 и SPAN® 80). Композиция вакцины, предпочтительно, также включает в себя одну или несколько иммуностимулирующих молекул, выбранных из Quil-A, DDA и GPI-100.
Композиции вакцины по настоящему изобретению можно вводить животному известными путями, включая пероральный, интраназальный, слизистый, местный, трансдермальный и парентеральный (например, внутривенный, внутрибрюшинный, интрадермальный, подкожный или внутримышечный) путь. Введение можно осуществлять сразу несколькими путями, например, первое введение осуществлять парентеральным путем, а последующее введение - через слизистые оболочки.
Способы получения композиций вакцины
Еще в одном варианте осуществления настоящее изобретение относится к способам получения композиций вакцины, содержащих антиген или антигены и субмикронную эмульсию «масло в воде».
При получении композиций вакцины настоящего изобретения антиген(ы) может вводиться либо до, либо после получения эмульсии «масло в воде». Предпочтительно, антиген смешивают с компонентами эмульсии «масло в воде» перед ее получением.
Антиген можно смешивать с различными компонентами эмульсии, включая масло, одно или несколько поверхностно-активных веществ, водный компонент и любой другой целесообразный компонент, для образования смеси. Смесь подвергают процессу первичного смешивания, обычно пропусканием один или несколько раз через один или несколько гомогенизаторов или эмульгаторов с образованием «масло в воде», содержащей антиген. Для этой цели можно использовать любой имеющийся в продаже гомогенизатор или эмульгатор, например эмульгатор Ross (Hauppauge, NY), гомогенизатор Gaulin (Everett, MA) или Microfluidics (Newton, MA). Альтернативно, различные компоненты эмульсионного адъюванта, включая масло, одно или несколько поверхностно-активных веществ и водный компонент, можно сначала комбинировать для образования эмульсии «масло в воде» использованием гомогенизатора или эмульгатора, а затем антиген добавляют к этой эмульсии. Средний размер капель эмульсии «масло в воде» после первичного смешивания составляет приблизительно 1,0-1,2 мкм.
Эмульсию, содержащую антиген, затем подвергают микрофлюидизации для доведения размера капель до субмикронного диапазона. Микрофлюидизацию можно осуществлять с помощью промышленного микрофлюидизатора, такого как модель № 110Y, изготавливаемая Microfluidics, Newton, Mass; Gaulin Model 30CD (Gaulin, Inc., Everett, Mass.) и Rainnie Minilab Type 8.30H (Miro Atomizer Food and Diary, Inc., Hudson, Wis.).
Размер капель можно определить различными способами, известными в данной области, например лазерной дифракцией, использованием имеющихся в продаже аппаратов для определения размера. Размер может изменяться в зависимости от типа используемого поверхностно-активного вещества, соотношения между поверхностно-активным веществом и маслом, рабочего давления, температуры и им подобных факторов. Можно определить желательную комбинацию этих параметров для получения эмульсий с желательным размером капель. Капли эмульсий по настоящему изобретению имеют диаметр менее чем 1 мкм. Предпочтительно средний размер капель составляет менее чем 0,8 мкм. Предпочтительнее, средний размер капель составляет менее чем 0,5 мкм. Еще предпочтительнее, средний размер капель составляет примерно 0,3 мкм.
В предпочтительном варианте осуществления настоящего изобретения раствор лецитинового масла DRAKEOL®, который содержит 25% лецитина в легком минеральном масле, объединяют и смешивают с поверхностно-активными агентами TWEEN® 80 и SPAN® 80 и солевым раствором с образованием смеси, которая содержит 40% светлого минерального масла, лецитин, 0,18% TWEEN® 80 и 0,08% SPAN® 80. Затем смесь эмульгируют эмульгатором Ross® (Hauppauge, NY 11788) примерно при 3400 об/мин с образованием эмульсионного продукта, который также именуется «композицией AMPHINOGEN®» или «раствор AMPHINOGEN®». В последующем желательный(ые) антиген(ы) комбинируются с раствором AMPHINOGEN® и любыми другими подходящими компонентами (например, иммуностимулирующими молекулами) с помощью эмульгатора, например гомогенизатора Ross, с образованием эмульсии «масло в воде», содержащей антиген(ы). Такую эмульсию однократно пропускают через микрофлюидизатор, работающий примерно при 10000 ± 500 фунтов/кв.дюйм. Микрофлюидизированная эмульсия «масло в воде» имеет капли размером менее чем 1 мкм при среднем размере капель примерно 0,25 мкм.
Композиции вакцины, содержащие микроинкапсулированные антигены в субмикронной эмульсии «масло в воде» и способы получения
В другом варианте осуществления настоящее изобретение относится к композициям вакцины, которые содержат антиген, инкапсулированный в микрочастицы (или «микроинкапсулированный антиген»), причем микроинкапсулированный антиген вводят перед получением описанной выше субмикронной эмульсии «масло в воде».
Способы поглощения или захвата антигенов в носители в виде частиц известны в данной области (см., например, Pharmaceutical Particulate Carriers: Therapeutic Applications (Justin Hanes, Masatoshi Chiba and Robert Lander. Polymer microspheres for vaccine delivery. In: Vaccine design. The subunit and adjuvant approach. Eds.Michael F.Powell and Mark J.Newman, 1995 Plenum Press, New York and London). Носители в виде частиц представляют множественные копии выбранного антигена иммунной системе у животного-индивидуума и содействуют захвату и удерживанию антигенов в локальных лимфатических узлах. Частицы могут быть фагоцитированы макрофагами и могут усиливать представление антигена посредством высвобождения цитокинов. Носители в виде частиц были также описаны в данной области и включают, например, носители, полученные из полимеров полиметилметакрилата, а также носители, полученные из поли(лактидов) и поли(лактид-согликолидов), известных как PLG. Полиметилметакрилатные полимеры не являются биодеградируемыми, тогда как частицы PLG могут подвергаться биодеградации случайным неферментативным гидролизом сложноэфирных связей с молочной и гликолевой кислотами, которые поступают обычными метаболическими путями.
Биодеградируемые микросферы также используют для достижения контролируемого высвобождения вакцин. Например, можно достичь непрерывного высвобождения антигена в течение продолжительного периода. В зависимости от молекулярной массы полимера и соотношения между молочной и гликолевой кислотами в полимере, полимер PLGA может иметь скорость гидролиза от нескольких дней или недель до нескольких месяцев или года. Медленное, контролируемое высвобождение может привести к образованию высоких уровней антител, аналогичных антителам, наблюдавшимся после множественных инъекций. Альтернативно, пульсирующее высвобождение антигенов вакцины может быть достигнуто выбором полимеров с различными скоростями гидролиза. Скорость гидролиза полимера обычно зависит от молекулярной массы полимера и соотношением между молочной и гликолевой кислотами в полимере. Микрочастицы, полученные из двух или нескольких различных полимеров, с изменяющимися скоростями высвобождения антигена обеспечивают пульсирующее высвобождение антигенов и имитируют схемы вакцинации множественными дозами.
В соответствии с настоящим изобретением, антиген, включающий любой из антигенов, описанных выше, может быть абсорбирован на полимерный носитель в виде частиц, предпочтительно, полимер PLG, с помощью любого способа, известной в данной области (такой как способ, проиллюстрированный в примере 17), с образованием препарата микроинкапсулированного антигена. Затем препарат микроинкапсулированного антигена смешивают с описанной выше субмикронной эмульсией «масло в воде» и диспергируют в ней с образованием композиции вакцины.
В предпочтительном варианте осуществления настоящее изобретение относится к композиции вакцины, которая содержит антиген, инкапсулированный в полимер PLG, причем микроинкапсулированный антиген вводят в микрофлюидизированную эмульсию «масло в воде» перед ее получением и эмульсия состоит из легкого минерального масла, лецитина, TWEEN-80, SPAN-80 и солевого раствора, и имеет средний размер капель менее чем 1,0 мкм.
Ниже приведены примеры конкретных вариантов осуществления настоящего изобретения. Примеры представлены только в иллюстративных целях и ни в коей мере не предназначены для ограничения объема настоящего изобретения.
ПРИМЕР 1
Получение композиции AMPHIGEN®
Композицию AMPHIGEN® получают способом из двух стадий. На первой стадии 80 л лецитинового масляного раствора Drakeol, 116 л солевого раствора столбнячного анатоксина, 1,2 л SPAN-80 и 2,8 л Tween-80 смешивают вместе и эмульгируют, используя эмульгатор Ross. Лецитиновый масляный раствор Drakeol содержит 25% соевого лецитина и 75% минерального масла. Эмульгированный продукт рециркулируют через эмульгатор Ross для пропускания минимум 5 объемов или минимум в течение 10 мин. Эмульгированный продукт хранят при 2-7°С в течение максимум 24 ч для дальнейшей переработки. Эмульсию из резервуара эмульгатора Ross переносят в гомогенизатор Gaulin и гомогенизируют в течение 20 мин при давлении 4500 фунтов/кв.дюйм. Полученный 40% лецитиновый масляный раствор Drakeol (далее именуемый «композиция AMPHINOGEN®» или «раствор AMPHINOGEN®») затем подают в стерильные карбоксипропиленовые контейнеры. Подачу выполняют внутри колпачка подачи класса 100, расположенного в регулируемой среде класса 10000. Контейнеры хранят при 2-7°С. При отсутствии других указаний, композицию AMPHINOGEN® используют в описанных ниже экспериментах.
ПРИМЕР 2
Первичное смешивание гомогенизацией мгновенным испарительным смешиванием вакцины BVD
Устройство, используемое для этого способа гомогенизации, показано на фиг.1. Используя асептическую методику или паровые трехходовые клапаны, бутыль, содержащую антиген BVD типа I (препарат инактивированного вируса BVD типа I), присоединяют к нижнему боковому отверстию на сосуде для смешивания. После завершения переноса требуемого объема антигена BVD типа I, бутыль с BVD типа I заменяют бутылью, содержащей препарат инактивированного вируса BVD типа II (препарат инактивированного вируса BVD типа I). После того, как перенос требуемого количества антигена BVD типа II завершен, гомогенизатор Ross присоединяют к портативному сосуду и начинают рециркуляцию при максимальной скорости вращения (3300 об/мин). Перемешивание содержимого сосуда поддерживают на средней скорости.
Используя асептическую методику или паровые трехходовые клапаны, бутыль, содержащую Quil-A в концентрации 50 мг/мл, присоединяют к впускному отверстию гомогенизатора на сосуде для смешивания. Требуемое количество раствора Quil-A пропускают в сосуд посредством разрежения в магистрали. После завершения переноса раствора Quil-A бутыль удаляют. Таким же образом требуемое количество холестерина в растворе этанола (18 мг/мл) переносят в сосуд для перемешивания. В последующем требуемое количество композиции AMPHINOGEN®, 10% раствора тимеросола и наполняющих растворов основной модифицированной среды Игла (“BME”) добавляют в сосуд для перемешивания.
После завершения всех добавлений, смешивание продолжают в течение еще 15 мин. Полученную композицию делят на аликвотные дозы по 2 мл, и она представляет вакцину BVD на основе не микрофлюидизированной композиции AMPHINOGEN®. Каждая доза вакцины содержит 500 мкг Quil-A, холестерин, 2,5% композиции AMPHINOGEN® и 0,009% тимеросола. Концентрацию антигена для двух различных штаммов BVD определяют с точки зрения титра ELISA (иммуноферментного анализа) для gp53.
ПРИМЕР 3
Вторичное смешивание микрофлюидизацией
На фиг.2 показан способ, используемый для вторичного смешивания посредством микрофлюидизации. Микрофлюидизатор подвергают паровой стерилизации. Сначала вспомогательную камеру модуля переработки вставляют в блок и контрольную камеру вставляют во второе положение камеры. Сосуд, содержащий полностью снабженную адъювантами вакцину BVD, полученную как описано в примере 2, соединяют с микрофлюидизатором присоединением магистрали передачи от выпускного клапана сосуда подачи к впускному отверстию микрофлюидизатора. Резервуар с газообразным азотом подсоединяют к впускному отверстию воздушного фильтра сосуда подачи, и установку давления в сосуде регулируют до уровня 20±5 футов/кв.дюйм. Выпускной клапан сосуда для сбора присоединяют к магистрали передачи от выпускного отверстия микрофлюидизатора. После осуществления всех необходимых соединений клапаны открывают и микрофлюидизацию начинают при рабочем давлении 10000±500 футов/кв.дюйм. Всю содержащуюся вакцину пропускают через микрофлюидизатор 1 раз и собирают в камеру после микрофлюидизации. Препарат делят на аликвотные дозы по 2 мл, и он представляет вакцину BVD на основе микрофлюидизированной композиции AMPHINOGEN®.
ПРИМЕР 4
Получение композиции вакцины посредством смешивания в газогенераторной печи
Композицию AMPHINOGEN®, полученную как описано в примере 1, разводят до 2,5% добавлением антигенов BVD и наполнителя. Полученный раствор смешивают в газогенераторной печи с использованием бруска для перемешивания вместо использования гомогенизатора. Конечный препарат содержит следующую композицию: антигены BVD типа 1 и типа 2, 2,5% композиции AMPHINOGEN® (которая содержит масло, лецитин, SPAN® и TWEEN®, как описано в примере 1) и солевой раствор. TWEEN-80 и SPAN-80 присутствуют в конечном препарате вакцины соответственно в количестве 0,18% и 0,08% об.
ПРИМЕР 5
Сравнение распределения размера капель между
препаратами вакцины на основе не микрофлюидизированной
и микрофлюидизированной композиции AMPHINOGEN®
Вакцину на основе не микрофлюидизированной композиции AMPHINOGEN®, полученную как описано в примере 2, вакцину микрофлюидизированной композиции на основе композиции AMPHINOGEN®, полученную как описано в примере 3, и препарат, полученный смешиванием в газогенераторной печи, как описано в примере 4, используют для сравнения размера частиц препаратов вакцины. 2 мл образца из каждого препарата добавляют в измеритель лазерной дифракции Malvern 2000 и определяют распределение размера капель. Как показано на фиг.3, результаты указывают на то, что препарат вакцины микрофлюидизированной композиции на основе композиции AMPHINOGEN® имеет максимальный объем частиц около 0,1 мкм, тогда как препарат вакцины не микрофлюидизированной композиции на основе композиции AMPHINOGEN® имеет распределение максимального объема частиц около 1 мкм.
ПРИМЕР 6
Снижение фазового разделения вакцины
Три различных препарата вакцины: вакцину на основе не микрофлюидизированной композиции AMPHINOGEN®, полученную как описано в примере 2, вакцину микрофлюидизированной композиции на основе композиции AMPHINOGEN®, полученную как описано в примере 3, и вакцину, полученную посредством смешивания в газогенераторной печи, как описано в примере 4, сравнивают бок о бок для определения их свойств фазового разделения при длительном хранении. Всем этим препаратам давали возможность стоять при 4°С примерно в течение 1 мес., и фазовое разделение контролируют с точки зрения внешнего вида кремового слоя поверх препаратов вакцины. Как показано на фиг.4, при сравнении с другими двумя препаратами, в препарате на основе не микрофлюидизированной композиции AMPHINOGEN® не было фазового разделения.
ПРИМЕР 7
Получение микрофлюидизированной и не микрофлюидизированной вакцины для крупного рогатого скота против вируса вирусной диареи крупного рогатого скота
Антиген вируса вирусной диареи крупного рогатого скота вводят до получения эмульсии в композицию AMPHINOGEN® посредством микрофлюидизации. Термин «включают до получения эмульсии» относится к способу, посредством которого антиген добавляют к композиции AMPHINOGEN® перед микрофлюидизацией. Антиген повергают воздействию физических сил процесса микрофлюидизации наряду с компонентами адъювантной композиции. В контрольной не микрофлюидизированной группе препарат антигена диспергируют в композиции AMPHINOGEN® посредством смешивания.
Конечная композиция и контрольного, и микрофлюидизированного препаратов имеет следующий состав:
BVD типа I с титром ELISA после инактивации 2535 КЕ/дозу для gp53, BVD типа II с титром ELISA после инактивации 3290 КЕ/дозу для gp53, Quil-A в концентрации 1,25 мг/дозу, холестерин в концентрации 1,25 мг/дозу, композицию AMPHINOGEN® в конечной концентрации 2,5% и тимеросол в конечной концентрации 0,009%. Доза вакцины составляет 5 мл.
ПРИМЕР 8
Длительная устойчивость включенных после получения
эмульсии вирусных антигенов BVD в препарате вакцины
на основе микрофлюидизированной композиции AMPHINOGEN®
Эксперимент проводят для определения устойчивости включенного до получения эмульсии антигена в течение длительного хранения. Вирусный антиген BVD типа II включают до получения эмульсии в композицию AMPHINOGEN® во время процесса микрофлюидизации для получения препарата микрофлюидизированной вакцины (А907505). Три других препарата вакцины, содержащие тот же антиген в не микрофлюидизированной композиции AMPHINOGEN® (А904369, А904370 и А904371), служат в качестве контроля. В не микрофлюидизированных препаратах антиген смешивают с композицией AMPHINOGEN® и смешивают посредством перемешивания с использованием гомогенизатора Ross. Все четыре препарата вакцины хранили при 4°С в течение двух лет. В различные точки времени во время хранения (0, 6, 12 или 24 мес.) все четыре композиции используют для вакцинации трехмесячных телят.
На 0 и 21-й день трехмесячных телят вакцинируют посредством подкожного пути введения 2 мл композиции вакцины. Сыворотку от вакцинированных животных собирают на 35-й день, и серологическую реакцию на вакцину измеряют с точки зрения титра антител посредством ELISA BVDV-E2. Как показано на фиг.5, препарат микрофлюидизированной вакцины проявляет более высокий титр антител во все испытанные точки времени (0, 6, 12 и 24 мес.), свидетельствуя о том, что устойчивость препарата антигена не потеряна в течение включения антигена до получения эмульсии во время процесса микрофлюидизации. Более того, было обнаружено, что препарат микрофлюидизированной вакцины вызывает иммунную реакцию во все точки времени.
ПРИМЕР 9
Снижение вызванного вакциной увеличения
ректальной температуры после микрофлюидизации
Препараты микрофлюидизированной и не микрофлюидизированной вакцины, изготовленные, как описано в примере 7, используют для вакцинации крупного рогатого скота в нулевой день, и ректальную температуру контролируют в течение периода от одного дня перед вакцинацией до четырех дней после вакцинации. Доза вакцины составляет 2 мл. Группы вакцинируют или однократной, или двойной дозой вакцины. Величины ректальной температуры измеряют и регистрируют ежедневно с 1-го по 4-й день включительно. Величины ректальной температуры в 0 день измеряют перед введением испытуемого изделия.
Как показано на фиг.6, результаты указывают на то, что имеется крутой подъем ректальной температуры примерно через 24 ч после вакцинации у животных, которые были вакцинированы или однократной, или двойной дозой композиции вакцины. Однако у животных, вакцинированных микрофлюидизированными формами вакцины, подъем ректальной температуры после вакцинации был лишь минимальным и значительно ниже, чем у животных, вакцинированных не микрофлюидизированной композицией (фиг.6).
ПРИМЕР 10
Объем реакции в месте инъекции рассасывался
быстрее при вакцинации микрофлюидизированными
композициями вакцины
Препараты микрофлюидизированной и не микрофлюидизированной вакцины, изготовленные, как описано в примере 7, использовали для вакцинации крупного рогатого скота в нулевой день. Животные, включенные в это исследование, представляли собой гибридный мясной крупный рогатый скот. Было по три животных в каждой из группы лечения плацебо (Т01 и Т02). В каждой из групп с Т03 по Т06 было по шесть животных. Доза вакцины составляла 2 мл, и группы вакцинировали или одной, или двумя дозами вакцины в нулевой день. В нулевой день испытуемое изделие вводили в правую часть шеи. Животные, получавшие двойную дозу (4 мл) испытуемого изделия (Т02, Т04 и Т06), получали полную двойную дозу в виде одной инъекции в одну сторону. Наблюдения участков инъекции, включая оценку размера реакции в месте инъекции, проводили с правой стороны шеи с 0-го по 4-й день включительно, и в 6-й, 9-й и 14-й дни. В 0-й день участки инъекции наблюдали перед введением испытуемых изделий. У групп, вакцинированных одной или двумя дозами плацебо, не проявилось какое-либо значимое увеличение объема реакции участка инъекции, и поэтому эти данные не показаны на фиг.7. В случае не микрофлюидизированной композиции вакцины, наблюдалось пропорциональное увеличение объема реакции участка инъекции между вакцинацией одной дозой и двумя дозами. С другой стороны, в случае микрофлюидизированной композиции вакцины, хотя одна доза вызывала больший объем реакции участка инъекции, инъекция второй дозы не вызывала какого-либо дальнейшего увеличения. Более того, в случае инъекции животным микрофлюидизированной композиции вакцины, объем реакции участка инъекции рассасывался быстрее, в сравнении с таковым у животных, которым инъецировали не микрофлюидизированную композицию вакцины. Эти результаты показаны на фиг.7.
ПРИМЕР 11
Получение препаратов вакцины на основе микрофлюидизированной композиции AMPHIGEN® с включенными до получения эмульсии вирусными BVD и лептоспирозными антигенами и иммуностимулирующими молекулами, такими как Quil-A и DDA
Инактивированный формалином штамм CSL Leptospira hardjo-bovis включали в композицию с соответствующим адъювантом в количестве примерно 1,4×109 организмов/5 мл. Инактивированный формалином штамм Т262 Leptospira Pomona включали в композицию в количестве примерно 2400 нефелометрических единиц/5 мл дозу. Нефелометрические единицы рассчитывали на основании нефелометрического измерения предварительно переработанной ферментационной жидкости. Вирус BVD типа I включали в композицию при титре Elisa E2 примерно 3000 относительный единиц/5 мл дозу. Вирус BVD типа II включали в композицию при титре Elisa E2 примерно 3500 относительный единиц/5 мл дозу. Относительную единицу рассчитывали на основании титра ELISA E2 общего количества жидкости перед составлением композиции после инактивации. И Quil-A, и холестерин использовали в концентрации 0,5 мг на 1 дозу. Тимеросол и композицию AMPHINOGEN® использовали при конечной концентрации соответственно 0,009% и 2,5%. Гидроокись алюминия (Rehydragel LV) использовали при конечной концентрации 2,0%. Когда DDA использовали в качестве иммуномодулятора, DDA включали внутрь композиции AMPHINOGEN®. Композиция AMPHINOGEN® (то есть 40% маточный раствор Drakeol-лецитина) содержал 1,6 мг/мл DDA, и, при целесообразности, был разведен, конечный препарат вакцины содержал 2,5% композиции AMPHINOGEN® и 0,1 мг/мл DDA.
При получении различных композиций вакцины фракции BVD, Leptos, Quil-A, холестерин, тимеросол, композицию AMPHINOGEN® и солевой раствор в качестве наполнителя добавляли в гомогенизатор Silverson и смешивали в течение 15 мин при 10000±500 об/мин. Затем компоненты микрофлюидизировали через сетчатый фильтр 200 мкм при 10000 фунтах/кв.дюйм.
Когда композиция вакцины содержала гидроокись алюминия, микрофлюидизацию проводили без гидроокиси алюминия. После завершения микрофлюидизации добавляли гидроокись алюминия и смешивали бруском мешалки в течение ночи при 4°С.
ПРИМЕР 12
Получение вирусной вакцины BVD для исследований
контрольного заражения
Препарат вакцины, использованный в этом эксперименте, содержал антигены и из вируса BVD типа 1, и из вируса BVD типа 2. Антиген BVD1-5960 использовали при титре ELISA после инактивации 2535 КЕ/дозу для gp53. Антиген BVD2-890 использовали при титре ELISA после инактивации 3290 КЕ/дозу для gp53. Quil-A и холестерин использовали в концентрации 0,5 мг/мл. Тимерсол и композицию AMPHINOGEN® использовали в конечной концентрации соответственно 0,009% и 2,5%. Когда DDA использовали в качестве иммуномодулятора, DDA включали внутрь композиции AMPHINOGEN®. Композиция маточного раствора AMPHINOGEN® (40% раствор Drakeol-лецитина) содержал меняющиеся количества DDA, и, при целесообразности, был разведен, конечный препарат вакцины содержал 2,5% композиции AMPHINOGEN® и DDA в концентрации в диапазоне от 0,5 мг/дозу до 2,0 мг/дозу. Алюминиевый гель (Rehydragel-LV) использовали в конечной концентрации 2%. GPI-0100 использовали в диапазоне от 2, 3 и 5 мг/дозу.
Все компоненты добавляли в гомогенизатор Silverson и смешивали в течение 15 мин при 10500 об/мин, а затем микрофлюидизировали пропусканием через камеру 200 мкм при 10000 фунтах/кв.дюйм. Когда препарат вакцины содержал гидроокись алюминия, микрофлюидизацию проводили без гидроокиси алюминия. После завершения микрофлюидизации добавляли гидроокись алюминия и смешивали бруском мешалки в течение ночи при 4°С.
ПРИМЕР 13
Защита против контрольного заражения лептоспирами после вакцинации микрофлюидизированной композицией вакцины
Amphinogen с лептоспирозными антигенами
В таблице 1 показан состав адъювантных композиций в препаратах вакцины, испытанных в этом исследовании. Препараты вакцины получали, как описано в примере 11. В каждой группе было шесть животных. В этом исследовании использовали гибридных телок в возрасте примерно 6-7 мес. Вакцинацию проводили в 0 и 21-й день подкожным путем объемом вакцины 5 мл. Контрольное заражение штаммом L. hardjo-bovis из NADC (Национального центра болезней сельскохозяйственных животных). Контрольное заражение производили в течение 57-59-го дней инокулятом 1 мл. Контрольное заражение осуществляли конъюнктивальным введением в глаз и вагинально. Материал контрольного заражения содержал 5,0×106 лептоспир/мл. Мочу брали еженедельно для получения культуры лептоспир, FA (флюоресцентного анализа) и PCR (полимеразной реакции синтеза цепи). Ткань почек брали в течение 112 и 113 дней.
В таблице 2 показаны данные исследования контрольного заражения лептоспирами. При определении процентной доли инфекции лептоспирами у подвергнутых контрольному заражению животных использовали следующие критерии. Если почечная культура была положительной только по одному образцу, то животное считалось положительным по лептоспирам. Если животное является положительным только в одной пробе, по данным FA или PCR, то животное считается отрицательным. Если выборка является положительной по данным и FA, и PCR, только в одном образце, то ее считали положительной по лептоспирам.
Результаты, показанные в таблице 2, указывают на то, что имелась значимо более короткая длительность выделения лептоспир в мочу во всех группах вакцин на основании всех трех анализов. Что касается колонизации мочи и почек, то эффективность композиций, содержащих QAC и DDA без AlOH, были сравнимы. AlOH не улучшал и даже снижал эффективность вакцин, содержащих QAC и DDA в исследовании контрольного заражения.
Серологические реакции против обоих лептоспирозных антигенов в композиции вакцины были выявлены у вакцинированных животных, и максимальная реакция отмечалась на 35-й день. Не было корреляции между серологической реакцией и защитой против контрольного заражения. Присутствие алюминиевого геля в композиции вакцины снижало уровень защиты, хотя серологическая реакция усиливалась присутствием алюминиевого геля в вакцине.
ПРИМЕР 14
Иммунная реакция, вызванная на вирусный антиген BVD,
и защита против контрольного заражения вирусом BVD
типа 2 после иммунизации препаратом микрофлюидизированной вакцины, содержащей композицию AMPHIGEN® и DDA
В этом эксперименте использовали 4-7-месячных серонегативных телят. Было шесть различных групп, и в каждой группе было десять животных (таблица 4). В 0-й и 21-й день каждое животное получало одну дозу вакцины или плацебо 2 мл подкожно в боковую поверхность шеи приблизительно посредине между лопаткой и затылком.
Дозу 5 мл препарата вируса для контрольного заражения (приблизительно 2,5 мл на ноздрю) вводили интраназально на 44-й день исследования. Не цитопатический вирус BVD типа 2, изолят #24515 (штамм Ellis), лот #46325-70 использовали в этом исследовании в качестве штамма контрольного заражения. Удержанные образцы материала контрольного заражения титровали (2 повторения на титрование) во время, когда начиналось контрольное заражение, и сразу после его завершения. Средний титр живого вируса на дозу 5 мл составил 5,3 log10 FAID50/5 мл перед контрольным заражением и 5,43 log10 FAID50/5 мл после контрольного заражения (FAID представляет собой эквивалент TCID50, средней цитопатогенной дозы).
Животных контролировали ежедневно с 3-го по 58-ой день. Балльные оценки клинического заболевания 0, 1, 2 или 3 на основании клинических признаков, которые можно было отнести на счет инфекции BVD 2, определяли для каждого животного с 42-го по 58-ой день. Балльные оценки на 44-й день регистрировали перед контрольным заражением. Образцы крови (в 2 пробирки емкостью 13 мл для отделения сыворотки, SST) брали у каждого животного в 0-й, 21-й, 35-й, 44-й и 58-й день для определения сывороточных титров антител, нейтрализующих вирус BVD типа 1 и BVD типа 2.
Образцы крови брали у каждого животного с 42-го по 58 день включительно и определяли присутствие вируса BVD в клетках лейкоцитарной пленки. На 44-й день образцы получали перед контрольным заражением.
Для определения лейкоцитарной формулы образцы крови (одна пробирка 4 мл ЭДТА) брали у каждого заболевания с 42-го по 58 день включительно. На 44-й день образцы получали перед контрольным заражением.
Лейкопению определяли как снижение на 40% или более количества лейкоцитов, по сравнению с исходным уровнем (среднее количество лейкоцитов перед контрольным заражением по двум дням перед контрольным заражением и дню контрольного заражения).
Балльные оценки клинического заболевания использовали для определения болезненного состояния следующим образом: если балльная оценка составляет ≤1, то заболевания=нет; если балльная оценка составляет >2, то заболевание=да.
Как показано в таблицах 5 и 6, у групп, вакцинированных вакцинами, содержащими вирусные антигены BVD, наряду с микрофлюидизированной композицией AMPHINOGEN®, Quil-A или DDA, происходило серопревращение со значительной нейтрализацией титров вируса в сыворотке для вирусов и BVD типа 1, BVD типа 2. У этих групп было также значимое снижение процентной доли животных, проявляющих виремию после контрольного заражения, хотя в контрольной группе 100% животных имели виремию (таблица 7). Кроме того, у этих вакцинированных групп частота заболеваний была также значимо снижена (таблица 8). Аналогичным образом, процентная доля животных, проявляющих лейкопению, была также снижена в группах вакцины, и снижение лейкопении было более значимым в группе, содержащей DDA, чем группа, содержащая Quil-A (таблица 9). В контрольной группе было значительное падение прибавки массы тела, при сравнении с вакцинированными группами (таблица 10).
Серология
Перед вакцинацией в 0-й день животные в исследовании были серонегативными (SVN<1:2) для антител к вирусу BVD типа 1 и 2 (данные не показаны). Через 14 день после второй вакцинации (35-й день) все животные, которым вводили плацебо (Т01), оставались серонегативными в отношении антител к вирусу BVD типа 1 и 2; а все животные, вакцинированные ITA (исследовательским тестовым антигеном) (Т02, Т03, Т04, Т05 и Т06),были серопозитивными (SVN≥1:8) в отношении антител к вирусу BVD типа 1 и 2. У одного животного, которому вводили вакцину с добавками композиции AMPHINOGEN® в количестве 2 мг/дозу DDA, на 35-й день титр SVN антител к вирусу BVD типа 1 и 2 составил 3 (таблицы 11 и 12).
Перед контрольным заражением на 44-й день, все контроли (Т01), за исключением одного, были серонегативными (SVN<1:2) в отношении антител к вирусу BVD типа 1 и 2 (данные не показаны). Один контроль (#2497) был серопозитивным (SVN=10) в отношении антител к вирусу BVD типа 1 и серонегативным в отношении антител к вирусу BVD типа 2. Через 14 дней после контрольного заражения все животные в исследовании были серопозитивными в отношении антител к вирусу BVD типа 1 и 2.
вируса BVD типа 1 в сыворотке
вируса BVD типа 2 в сыворотке
вания
встречаемости (%) животных с виремией
после контрольного заражения
мости (%) животных с заболева-
нием
людений
вой
раст-
вор
ген Quil-A
ген 0,5 мг DDA, Al
ген 0,5 мг DDA
ген 1,0 мг DDA
ген 2,0 мг DDA
Выделение вируса
По данным, представленным в таблице 13, во время периода контрольного заражения (с 44-го по 58-й день) у всех животных в контроле (Т01) была виремия (вирус BVD был выделен в 1 или более дней). У групп, которым вводили ITA, частота выявления виремии у животных составляла 1, 0, 3, 2 и 2 в каждой группе из 10 животных (соответственно Т02, Т03, Т04, Т05 и Т06). Различие между контролем и группами, которым вводили ITA, было статистически значимым (P≤0,05). Минимальная средняя квадратическая величина дней виремии была также значимо больше (10,4 дня) в контроле по сравнению с группами, которым вводили ITA (от 0,0 до 0,5 дня).
Клиническое заболевание
Животные с балльными оценками клинических признаков 2 или 3 считались проявляющими признаки заболевания, вызванного BVD. Как показано в таблице 14, частота выявления животных с клиническими признаками заболевания, вызванного BVD, составляла 9 из 10 в контроле (Т01) и 1, 2, 0, 0 и 0 из 10 в каждой из групп, которым вводили ITA (соответственно Т02, Т03, Т04, Т05 и Т06). Различие между контролем и группами, которым вводили ITA, было статистически значимым (P≤0,05).
Лейкопения
Как показано в таблице 15, во время периода контрольного заражения (с 44-го по 58-й день) у всех 10 животных в контроле (Т01) была лейкопения (снижение на 40% количества лейкоцитов по сравнению с исходным уровнем перед контрольным заражением, 42-й-44-й дни). Количество животных с лейкопенией составило 6, 2, 4, 3 и 2 из 10 животных в каждой из групп, которым вводили ITA (соответственно Т02, Т03, Т04, Т05 и Т06). Различие между контролем и группой, которой вводили вакцину, которая имела добавки композиции AMPHINOGEN® в количестве 0,5 мг/дозу и гидроокиси алюминия (Т03), было статистически значимым (P≤0,05). Минимальная средняя квадратическая величина дней лейкопении была значимо больше (7,8 дня) в контроле по сравнению с группами, которым вводили ITA (от 0,2 до 1,2 дня).
ПРИМЕР 15
Иммунная реакция, вызванная на вирусный антиген BVD,
и защита против контрольного заражения вирусом BVD
типа 2 после иммунизации микрофлюидизированной
композицией вакцины, содержащей GPI-0100
Соблюдали набор экспериментальных условий, как описано в примере 14, и проводили прямое сравнение между Quil-A и GPI-01000. Как показано в таблицах 11 и 12, у животных, вакцинированных антигенами BVD в препарате на основе микрофлюидизированной композиции AMPHINOGEN®, содержащей или Quil-A, или GPI-01000, имелся значительный титр антител и к вирусу BVD типа 1, и к вирусу BVD типа 2. Титр антител к вирусу BVD типа 1 был гораздо выше, чем к вирусу BVD типа 2. Однако последующее контрольное заражение вирусом BVD типа 2 показало сильную защиту, и частота заболевания была значительно снижена у телят, вакцинированных микрофлюидизированным препаратом вакцины на основе композиции AMPHINOGEN®, содержащим GPI-01000.
после контрольного заражения
во (%) животных с заболева-
нием
чест
во наб-
людений
В заключение, безопасность каждой вакцины была продемонстрирована отсутствием побочных реакций у вакцинированных животных. Активность каждой вакцины была продемонстрирована серопревращением (SVN титров антител к BVD-1 и BVD-2>1:8) у 100% вакцинированных животных. Удовлетворительная устойчивость к контрольному заражению была продемонстрирована вакциной с добавкой только 2 мг GPI-0100.
ПРИМЕР 16
Препарат вакцины, содержащий микроинкапсулированный
антиген, в микрофлюидизированной эмульсии «масло в воде»
3 г Трегалозы (Fluka) добавляют к воде для получения маточного раствора, содержащего 333 мг/мл раствора трегалозы. Рекомбинантный антиген PauA, солюбилизированный в 0,8% растворе SDS (додецилсульфата натрия) (SDS/rPauA) добавляют к трегалозе для получения конечной концентрации 494 мкг rPauA/мл. На следующей стадии 10 г полилактидгликолевой кислоты (PLG-Resomer RE 503H, Boeringher Ingelheim) растворяют в 200 мл хлорида метилена (MeCl2). Полученный раствор PLG/MeCl2 объединяют с раствором SDS-rPauA/трегалозы, полученным на первой стадии. Объединенный раствор подвергают микрофлюидизации, используя микрофлюидизатор (Microfluidics, модель М110ЕН), и микрофлюидизированный препарат сушат распылением, используя устройство Temco Spray Dryer, модель SD-05. Высушенный распылением материал собирают, используя сетчатый фильтр 500 мкм.
Концентрацию rPauA в этом высушенном распылением материале количественно определяют анализом вестерн-блоттинга. 1,04 мг высушенного распылением материала растворяют в 50 мкл ацетона и центрифугируют при 13200 об/мин при комнатной температуре в течение 10 мин. Надосадочную жидкость удаляют. Надосадочную и полученную после центрифугирования осадочную фракции сушат в вытяжном колпаке биологической безопасности в течение 2,5 ч. Осадок после центрифугирования ресуспендируют в 47,43 мкл раствора образца (25 мкл буфера образца + 10 мкл восстанавливающего вещества + 65 мкл воды). Высушенную надосадочную фракцию ресуспендируют 20 мкл раствора образца. В анализе вестерн-блоттинга очищенный PauA используют в качестве стандарта для количественного определения содержания rPauA в высушенном распылением материале.
Маточный раствор 20% маннита получают растворением 100 г маннита (Sigma) в 500 мл воды для инъекций (WFI). Раствор нагревают до 40°С горячей пластиной/мешалкой и охлаждают до 30°С. Раствор подвергают стерилизационной фильтрации через стерильный фильтр 0,22 мкм (Millipore). 2,5% раствор карбоксиметилцеллюлозы готовят растворением 12,5 г карбоксиметилцеллюлозы (Sigma) в 500 мл WFI и смешивают в течение ночи при 4°С. Раствор автоклавируют при 121°С.
Порошок, полученный в результате сушки распылением, растворяют в растворе, содержащем 5% маннит, 0,3% карбоксиметилцеллюлозу и 1:5000 тимеросола. Конечный раствор делят на аликвотные количества во флакончики по 3 мл и лиофилизируют, используя лиофилизатор (USIFROID). Лиофилизированный порошок представляет микроинкапсулированный rPauA. Микроинкапсулированный субъединичный белковый антиген ресуспендируют в 2 мл микрофлюидизированной эмульсии «масло в воде», содержащей композицию AMPHINOGEN® (такую как микрофлюидизированная эмульсия, описанная в примере 20), и используют в качестве вакцины.
ПРИМЕР 17
Получение микрофлюидизированной композиции вакцины, содержащей
и антиген цельной бактериальной клетки, и рекомбинантный белковый антиген в эмульсии «масло в воде»
Изготавливали два препарата вакцины, которые содержали и рекомбинантный белок PauA Streptococcus uberis, и бактериальные клетки Escherishia coli, добавленные до получения эмульсии «масло в воде», как описано в примерах 2 и 3. Рекомбинантный антиген PauA присутствовал в концентрации 100 мкг на 1 дозу, а клетки E. coli находились в конечном количестве 4×109 на 1 дозу. Эмульсионные адъювантные составы двух композиций вакцин показаны в таблице 16.
ПРИМЕР 18
Иммунная реакция на микрофлюидизированную вакцину,
содержащую rPauA и бактериальные антигены цельной клетки
в эмульсии «масло в воде»
В этом эксперименте использовали половозрелых молочных коров. Во время включения в исследование у животных был конец их первой или второй лактации. 2 мл каждой композиции вакцины вводили подкожно 3 раза, 1 раз во время запускания коров (D-0), через 28 дней (D=28) и снова через 4-10 дней после отела (С+4-С+10). Первую и третью дозу вводили в левую сторону шеи, а вторую дозу вводили в правую сторону шеи. Кровь брали перед каждой вакцинацией и приблизительно через 14 дней и 32 дня после третьей вакцинации. Титр антител к E.coli и к антигену rPauA определяли с помощью ELISA. Как показано на фиг.8, результаты указывают на то, что титр антител к rPauA был выше в группе, вакцинированной композицией вакцины, содержащей GPI-0100 в качестве иммуностимулятора, и он достигал пика на 70-й день после первоначальной вакцинации. Титр антител к антигену E.coli показан на фиг.9. Титр антител к антигену E.coli был сравним у обеих композиций вакцины, хотя присутствие GPI-0100 в качестве иммуностимулятора вызывало относительно более высокий титр антител по сравнению с композицией с DDA в качестве иммуностимулятора.
ПРИМЕР 19
Анализ вирицидной активности микрофлюидизированных
препаратов вакцины на основе композиции AMPHINOGEN®
Для определения того, инактивирует ли вирус микрофлюидизация, определяли вирицидную активность трех микрофлюидизированных препаратов вакцины на основе композиции AMPHINOGEN®. Эти три препарата содержали три различных инфекционных вируса крупного рогатого скота, а именно вирус герпеса крупного рогатого скота (BHV), вирус 3 парагриппа (PI3) и респираторный синцитиальный вирус крупного рогатого скота (BRSV).
Выявление вирицидной активности трех препаратов вакцины проводили в соответствии с требованиями положений USDA 9CFR.113.35.
Результаты, показанные в таблице 17, указывают на то, что микрофлюидизация препаратов вакцины на основе композиции AMPHINOGEN® не вызывает какую-либо значимую инактивацию препарата вакцины.
А = Холестерин, добавленный в концентрации 650 мл/мин
В = Холестерин, добавленный в концентрации 28 мл/мин
С = Холестерин, добавленный в концентрации 5 мл/мин
М200 = Микрофлюидизирована сетчатым фильтром 200 мкм
М75 = Микрофлюидизирована сетчатым фильтром 75 мкм
М75@37C = Жидкости, нагретые до 37°С перед микрофлюидизацией
Величина выше 0,7 является показанием вирицидного эффекта.
ПРИМЕР 20
Получение микрофлюидизированной композиции AMPHINOGEN®
Композицию AMPHINOGEN® получали объединением раствора лецитинового масла DRAKEOL (светлого минерального масла с 25% лецитина) и TWEEN-80 (при конечной концентрации 0,18%) и Span-80 (при конечной концентрации 0,08%) при смешивании в течение 8-22 ч при 36±1°С. Затем смесь добавляли к солевому раствору с помощью эмульгатора Ross® (Hauppauge, NY 11788) приблизительно при 3400 об/мин. В последующем смесь пропускали однократно через микрофлюидизатор с камерой взаимодействия 200 мкм при 4500±500 фунтов/кв.дюйм. На фиг.10А и 10В показана устойчивость микрофлюидизированной композиции AMPHINOGEN®. Распределение размера частиц, по данным измерения лазерной дифракции, в начале, в исходной точке времени (фиг.10А) было почти идентичным распределению размера частиц через 22 месяца хранения при 4°С (фиг.10В).
| название | год | авторы | номер документа |
|---|---|---|---|
| МИКРОФЛЮИДИЗИРОВАННЫЕ ЭМУЛЬСИИ ТИПА "МАСЛО В ВОДЕ" И ВАКЦИННЫЕ КОМПОЗИЦИИ | 2005 |
|
RU2347586C2 |
| НОВЫЕ АДЪЮВАНТНЫЕ КОМПОЗИЦИИ | 2009 |
|
RU2510280C2 |
| АДЪЮВАНТЫ НА МАСЛЯНОЙ ОСНОВЕ | 2014 |
|
RU2730011C2 |
| АДЪЮВАНТЫ НА МАСЛЯНОЙ ОСНОВЕ | 2014 |
|
RU2816849C2 |
| ЛИПОСОМАЛЬНЫЕ АДЪЮВАНТНЫЕ КОМПОЗИЦИИ | 2016 |
|
RU2736642C2 |
| КОМБИНИРОВАННАЯ ВАКЦИНА PCV/MYCOPLASMA HYOPNEUMONIAE | 2013 |
|
RU2615443C2 |
| КОМБИНИРОВАННАЯ ВАКЦИНА PCV/MYCOPLASMA HYOPNEUMONIAE/PRRS (PCV/MYCOPLASMA HYOPNEUMONIAE/PRRS COMBINATION VACCINE) | 2013 |
|
RU2644256C2 |
| ВАКЦИНА MYCOPLASMA HYOPNEUMONIAE | 2013 |
|
RU2644254C2 |
| ВАКЦИНЫ И СПОСОБЫ ЛЕЧЕНИЯ СОБАЧЬЕГО ГРИППА | 2006 |
|
RU2396976C2 |
| ВАКЦИНА ПРОТИВ ИНФЕКЦИОННОГО БРОНХИТА | 2017 |
|
RU2781143C2 |
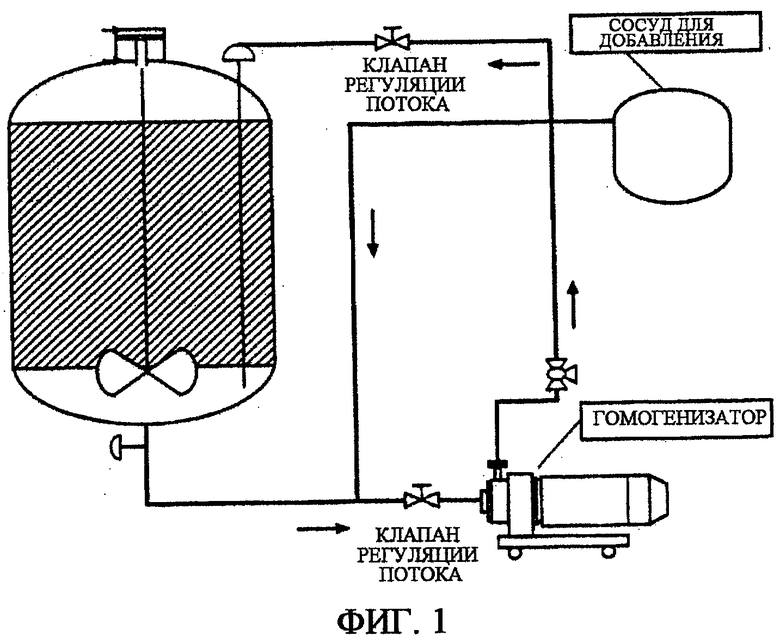
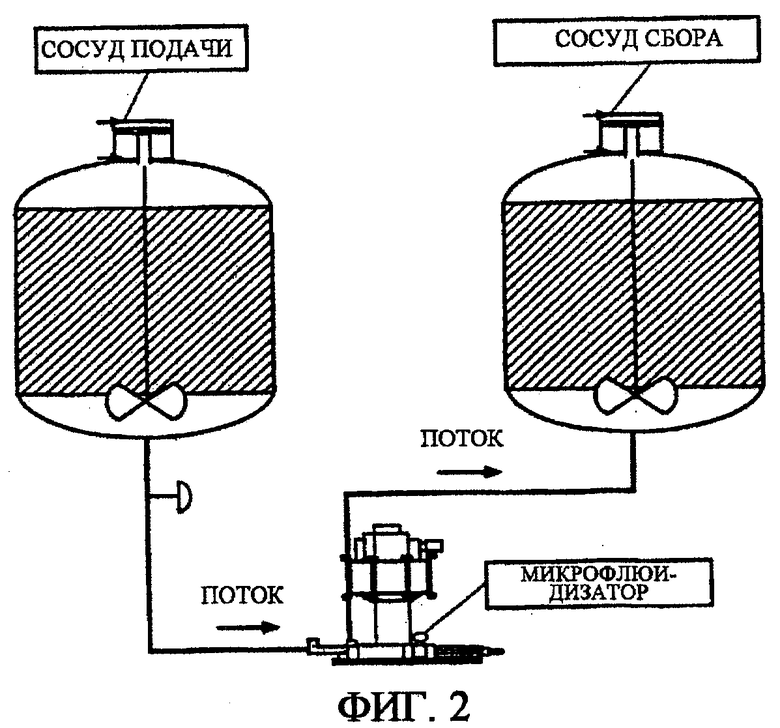
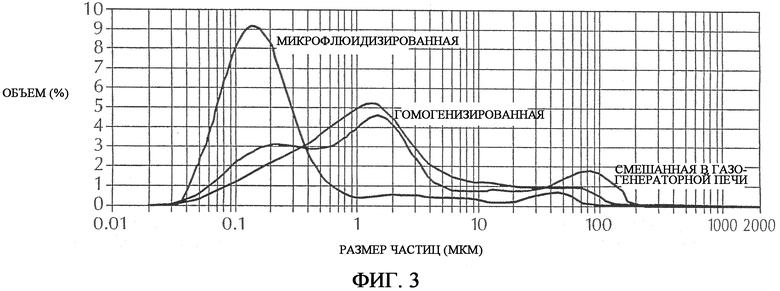

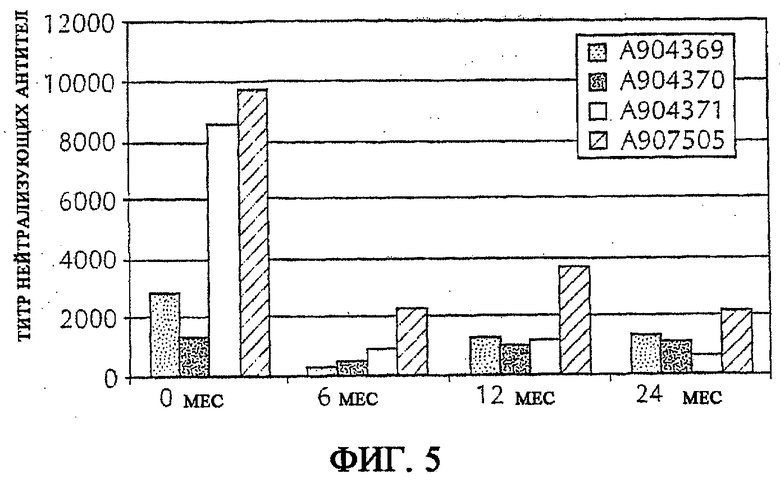
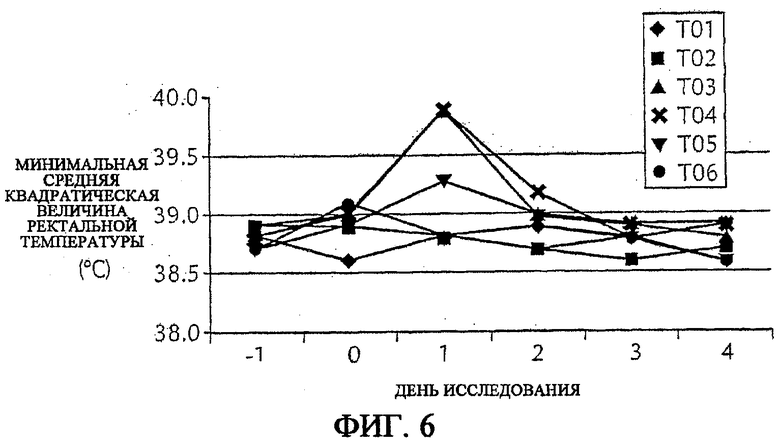
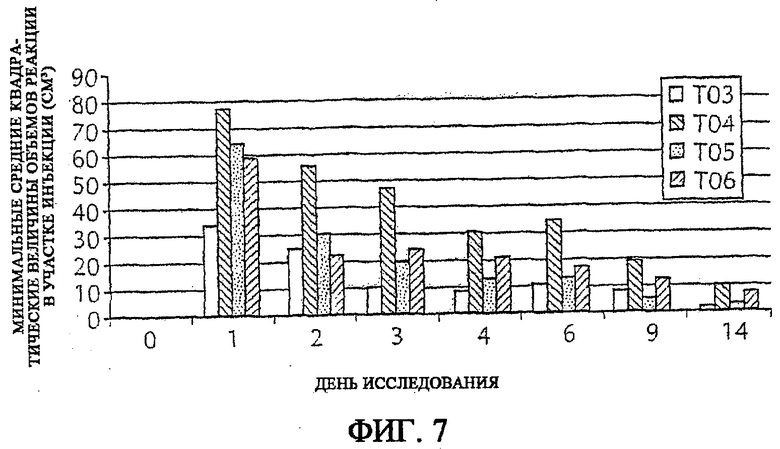
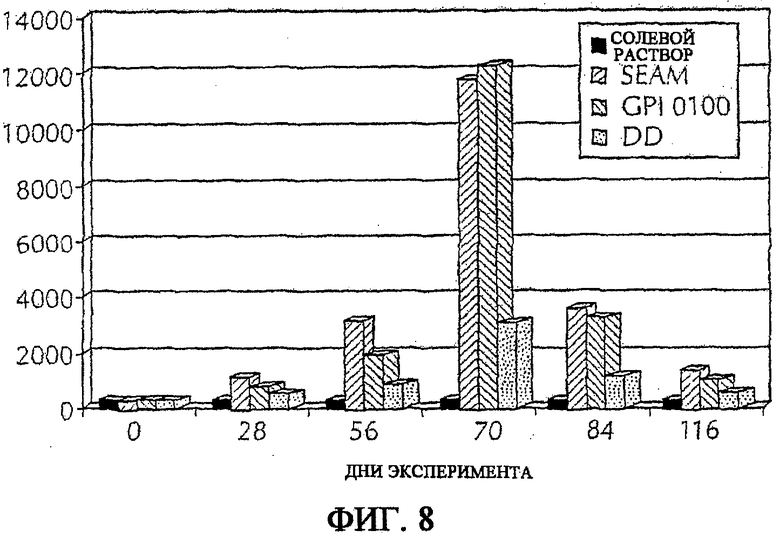
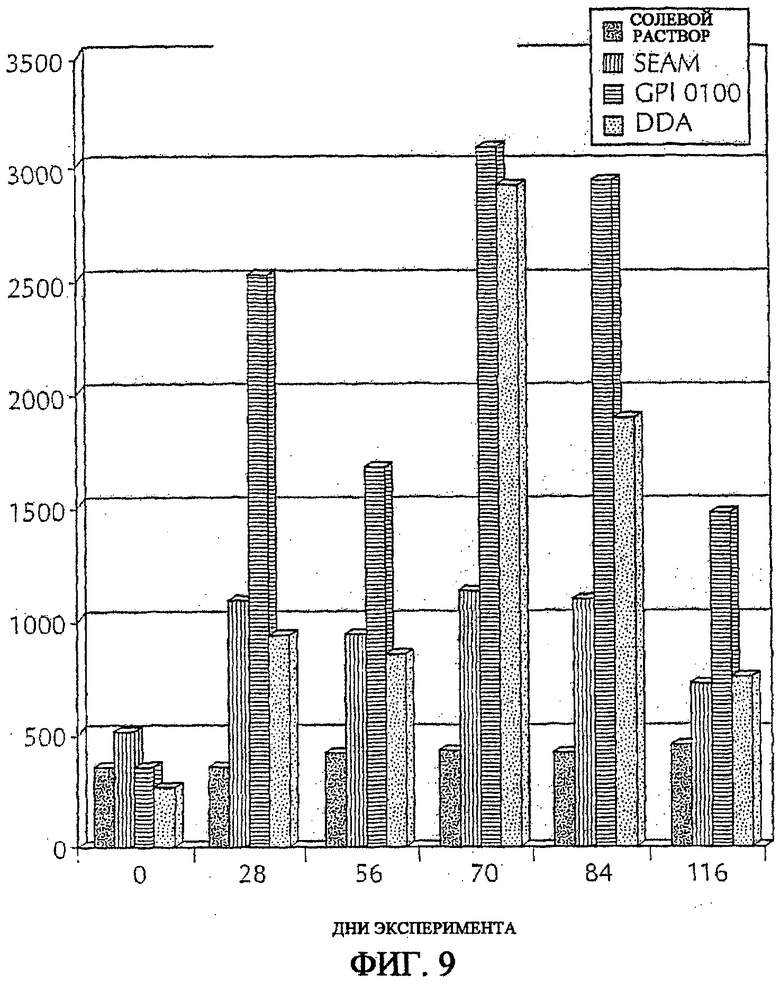
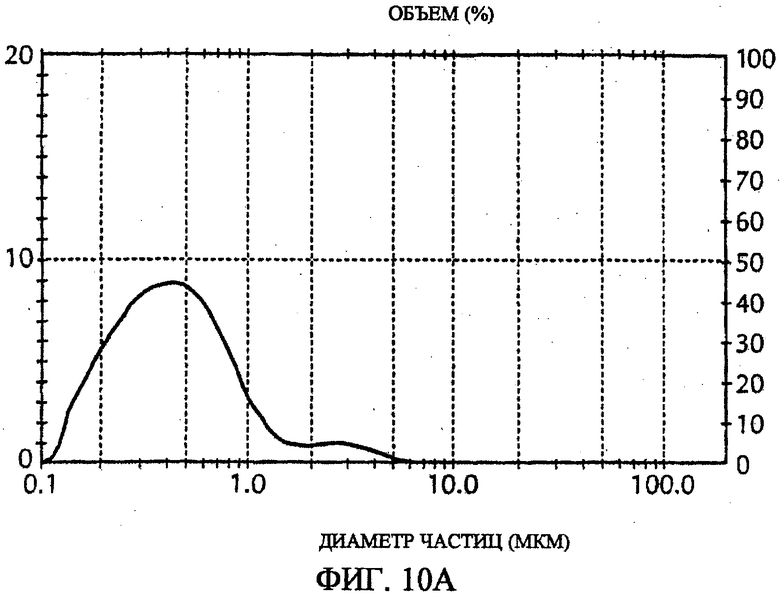
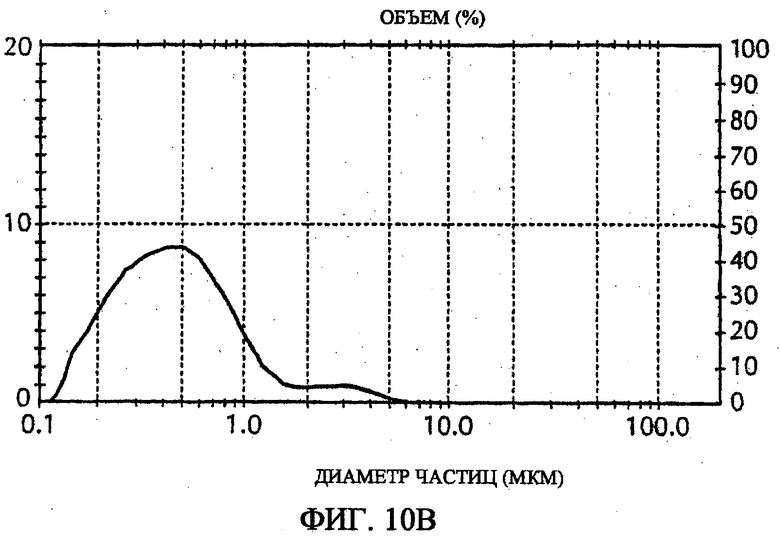
Изобретение относится к фармацевтике и представляет собой композицию вакцины для индукции иммунного ответа у животных. Композиция содержит антиген и 40% эмульсию «масло в воде», разведенную до 2,5%, где указанная 40% эмульсия «масло в воде» содержит 30% об./об. легкого углеводородного неметаболического масла, 10% об./об. лецитина, 0,6% об./об. сорбитана моноолеата, 1,4% об./об. полиоксиэтиленсорбитана моноолеата, причем масляный компонент диспергирован в водном компоненте путем эмульгирования, а композиция вакцины получена с помощью микрофлюидизатора. Средний размер капель в композиции составляет менее 0,3 мкм. Композиция обладает улучшенными физическими признаками, усиленным иммунизирующим действием, а также повышенной безопасностью. 3 н. и 7 з.п. ф-лы, 20 пр., 17 табл., 11 ил.
1. Композиция вакцины для индукции иммунного ответа у животных, где указанная композиция содержит антиген и 40% эмульсию «масло в воде», разведенную до 2,5%, где указанная 40% эмульсия «масло в воде» содержит:
a) 30% об./об. легкого углеводородного неметаболического масла;
b) 10% об./об. лецитина;
c) 0,6% об./об. сорбитана моноолеата (SPAN),
d) 1,4% об./об. полиоксиэтиленсорбитана моноолеата,
где масляный компонент диспергирован в водном компоненте путем эмульгирования,
где композиция вакцины получена с помощью микрофлюидизатора и имеет средний размер капель меньше 0,3 мкм.
2. Композиция вакцины по п.1, дополнительно содержащая солевой раствор столбнячного анатоксина и где максимальный размер частиц масла составляет 0,1 мкм.
3. Композиция вакцины по п.1, где указанный антиген представляет собой вирусный антиген или бактериальный антиген.
4. Композиция вакцины по п.3, где указанный вирусный антиген включает в себя убитый вирус диареи крупного рогатого скота типа 1 или типа 2, и где указанный бактериальный антиген включает, по меньшей мере, один компонент, выбранный из инактивированного бактерина Leptospira, рекомбинантного белка Streptococcus uberis PauA или препарата клеток E.coli.
5. Способ получения композиции вакцины по п.1, включающий:
(а) получение смеси объединением легкого углеводородного неметаболического масла, поверхностно-активного вещества и водного компонента;
(b) добавление антигена к смеси, полученной в стадии (а);
(c) процесс первичного эмульгирования смеси, содержащей указанный антиген, который получен в стадии (b) с получением эмульсии «масло в воде», со средним размером капель масла от 1,0 мкм до 1,1 мкм; и
(d) микрофлюидизация эмульсии, полученной в стадии (с) с получением указанной композиции вакцины, где средний размер капель композиции составляет менее чем 0,3 мкм.
6. Способ по п.5, где композиция дополнительно содержит солевой раствор столбнячного анатоксина и где максимальный размер частиц масла составляет 0,1 мкм.
7. Способ по п.5, где указанный антиген представляет собой вирусный антиген или бактериальный антиген.
8. Способ по п.7, где указанный вирусный антиген включает убитый вирус диареи крупного рогатого скота типа 1 или типа 2, и где указанный бактериальный антиген включает, по меньшей мере, один компонент, выбранный из группы инактивированного бактерина Leptospira, рекомбинантного белка Streptococcus uberis PauA или препарата клеток E.coli.
9. Композиция вакцины для индукции иммунного ответа у животных, включающая микроинкапсулированный антиген и 40% эмульсию «масло в воде», разведенную до 2,5%, где указанная 40% эмульсия «масло в воде» содержит:
а) 30% об./об. легкого углеводородного неметаболического масла;
b) 10% об./об. лецитина;
c) 0,6% об./об. сорбитана моноолеата (SPAN),
d) 1,4% об./об. полиоксиэтиленсорбитана моноолеата,
где масляный компонент диспергирован в водном компоненте путем эмульгирования,
где композиция вакцины получена с помощью микрофлюидизатора и имеет средний размер капель меньше 0,3 мкм,
где указанный микроинкапсулированный антиген диспергирован в указанной эмульсии.
10. Композиция вакцины по п.9, где композиция дополнительно содержит солевой раствор столбнячного анатоксина и где максимальный размер частиц масла составляет 0,1 мкм.
| EP 1023904 A2, 02.08.2000 | |||
| ЦЕНТРАЛЬНЫЙ ФОТОЗАТВОР | 0 |
|
SU315153A1 |
| WO 9511700 A1, 04.05.1995 | |||
| WO 9930737 A1, 24.06.1999 | |||
| RU 2058154 C1, 20.04.1996 | |||
Авторы
Даты
2015-02-20—Публикация
2004-03-22—Подача