Изобретение относится к фармацевтике, фармацевтической промышленности и может быть использовано при лечении гельминтного заболевания описторхоза, вызываемого Opistorchis felineus.
У человека зарегистрировано 364 вида гельминтов. Гельминтозы распространены от арктических широт до экватора. Гельминтами заражено более миллиарда человек. По числу больных заражение кишечными гельминтами занимает третье место в мире. По данным ВОЗ общее число заболеваний и смертей от кишечных гельминтозов выше, чем от бактериальных, вирусных инфекций и других паразитарных болезней, вместе взятых. Пораженность населения России кишечными гельминтозами составляет в среднем около 2%, в южных районах страны она достигает 7-10%. В частности, пораженность описторхозом в Западной Сибири составляет не менее 30-60%, на Урале - 20-40% населения. В ряде случаев лечение паразитарных инвазий недостаточно эффективно и приводит к тяжелым последствиям - истощению иммунной системы и возникновению вторичного иммунодефицита, нарушениям механизмов гомеостаза, возникновениям аритмий, нарушениям психики, образованиям опухолей, в том числе злокачественных.
Албендазол является популярным антигельминтным средством, обладающим активностью также в отношении патогенных простейших. Действует на кишечные и тканевые формы паразитов; активен в отношении яиц, личинок и взрослых гельминтов. Противоглистное действие албендазола обусловлено угнетением полимеризации тубулина, приводящим к нарушению метаболизма и гибели гельминтов. Албендазол активен в отношении кишечных паразитов, включая нематоды - Ascaris lumbricoides, Trichuris trichiura, Enterobius vermicularis, Ancylostoma duodenale, Necator americanus, Strongyloides stercoralis, Cutaneous Larva Migrans; цестоды - Hymenolepsis nana (карликовый цепень), Taenia solium (свиной цепень), Taenia saginata (бычий цепень); простейшие - Giardia lamblia. Албендазол активен в отношении тканевых паразитов, включая цистный эхинококкоз и альвеолярный эхинококкоз, вызываемые инвазией Echinococcus granulosus и Echinococcus multilocularis соответственно. Эффективен при лечении нейроцистицеркоза, вызываемого инвазией личинок свиного цепня Т. solium, капилляриоза, вызываемого Capillaria philippinensis, и гнатостомоза, вызываемого инвазией Gnathostoma spinigerum.
Однако активность албендазола в отношении трематод - Opisthorchis felineus и О. viverrini недостаточна, кроме того, этот препарат обладает гепатотоксичностью.
Албендазол применяли для лечения людей от описторхоза, вызванного заражением О. felineus. После курса лечения албендазолом у 68% пациентов остались симптомы заболевания описторхозом, подтвердилась инфекция О. felineus, и были необходимы дополнительные курсы лечения (1. Armignacco О, Ferri F, Gomez-Morales MA, Caterini L, Pozio E. Cryptic and asymptomatic Opisthorchis felineus infections. Am J Trop Med Hyg. 2013; 88(2): P. 364-366.). Албендазол применяли также для лечения описторхоза у людей, вызванного О. viverrini (Pungpark S., Bunnag D., Harinasuta T., Albendazole in the treatment of opisthorchiasis and concomitant intestinal helminthic infections. Southeast Asian J. Trop.Med. Public Health 1984. 15, P. 44-50). Курс албендазола в течение 7 дней приводил к снижению количества яиц гельминтов у 63% пациентов, однако оптимальные результаты полного излечивания не были достигнуты.
Ближайшим аналогом нашего изобретения являются результаты исследования антипаразитарного действия албендазола на хомяках, предварительно зараженных О. viverrini. В результате было показано, что количество гельминтов у животных было снижено на 81,5% (Bhaibulaya M, Punthuprapasa P. Treatment of Opisthorchiasis viverrini in hamsters with albendazole. Southeast Asian J Trop Med Public Health). Вероятной причиной этого является низкая биодоступность албендазола (менее 5%) при оральном приеме. Вследствие этого при лечении гельминтозов, вызванных Opisthorchis felineus и viverrini преимущественно применяется препарат празиквантель, эффективность которого тоже весьма ограничена.
Аналогом нашего изобретения является работа (3. N. Kohri, Y. Yamayoshi, K. Iseki, N. Sato, S. Todot. K. Mmiyazaki. Effect of Gastric pH on the Bioavailability of Albendazole in Rabbits // Pharm. Pharmacol. Commun. - 1998. - V4. - p.267-270), в которой показано возрастание биодоступности албендазола за счет увеличения кислотности желудочной среды. Однако такой путь физиологически неприемлем, так как высокая кислотность среды ЖКТ вызывает нарушение процесса пищеварения, изжогу, способствует эрозивным повреждениям стенки желудка.
Также аналогом нашего изобретения является работа (4. F.K. Alanazi, M. El-Badry, M.O. Ahmed. LA. Improvement of Albendazole Dissolution by Preparing Microparticles Using Spray-Drying Technique // Sci. Pharm. - 2007. - V. 75. - p. 63-79), где описано получение путем распылительной сушки твердых дисперсий албендазола с различными полимерами - гидроксипропилметилцеллюлозой, поливиниловым спиртом, поливинилпирролидоном.
Недостатком этого аналога является небольшая величина увеличения растворимости - до ~5 раз, а также довольно сложный процесс получения твердых дисперсий.
Известно техническое решение (С. Moriwaki, G.L. Costa, С.N. Ferracini, F.F. de Moraes, G.M. Zanin, E.A. G. Pineda and G. Matioli. Enhancement of solubility of albendazole by complexation with cyclodextrin // Brazilian Journal of Chemical Engineering - 2008. - Vol. 25, No. 02/ - p. 255-267.), где описано получение и исследование биодоступности водорастворимых межмолекулярных комплексов албендазола с бета-циклодекстрином. Несмотря на значительное достигнутое увеличение водорастворимости (до ~53 раз) и биодоступности, фармацевтическое применение описываемого технического решения практически затруднено вследствие действующих ограничений по величине рекомендованных/разрешенных для приема человеком доз циклодекстрина - не более 5 мг/кг (http://www.accessdata.fda.gov/scripts/fcn/gras_notices/214655 A.PDF).
Также аналогом нашего изобретения является (S.S. Khalikov, A.V. Dushkin, M.S. Khalikov and others (2011) Mechanochemical modification of properties of anthelmintic preparations // Chemistry for Sustainable Development. 19(6): 699-703), где было обнаружено явление повышения водорастворимости малорастворимых лекарственных веществ, в частности албендазола за счет образования межмолекулярных комплексов лекарственных молекул с полисахаридом арабиногалактаном при механической обработке их смесей интенсивными механическими воздействиями.
Однако в данной работе не исследовалась антигельминтная и тем более противоописторхозная активность получаемых композиций.
Следует отметить, что известные препараты албендазола в дозах, применяющихся для лечения тканевых паразитозов, обладают гепатотоксичностью и могут вызывать гидропическую дистрофию, дисплазию и множественные некрозы гепатоцитов (J.I.M.Zuluaga, А.Е.M.Castro, J.C.P.Cadavid, and J.C.R.Gutierrez, Albendazole-induced granulomatous hepatitis: a case report // Journal of Medical Case Reports, 2013, 7:201, http: //www.jmedicalcasereports.com/content/7/1/201; Arief A Suriawinata, MD, Swan N. Thung, MD // Liver Pathology: An Atlas and Concise Guide, Demos Medical Publishing, NY, 2011, 378p). Однако ни в одном из вышеуказанных аналогов нашего изобретения не определялась гепатотоксичность описываемых препаратов албендазола. При этом вполне логично предположить, что увеличение биодоступности албендазола должно усиливать этот нежелательный побочный эффект.
По сравнению с аналогами заявляемое техническое решение обладает новизной, поскольку именно заявляемый состав композиции обеспечивает высокую фармакологическую противоописторхозную активность и пониженную гепатотоксичность. Проведенный патентный поиск позволил установить, что аналогичных составов композиций, обладающих повышенной фармакологической противоописторхозной активностью и пониженной гепатотоксичностью, не обнаружено, что позволяет сделать вывод о соответствии заявляемого технического решения критерию «изобретательский уровень».
Заявляемая композиция легко может смешиваться с равным количеством или избытком вспомогательных веществ из классов фармакологически нейтральных моно-, ди- и полисахаридов для облегчения смачиваемости при суспендировании в водных растворах для последующего перорального приема.
Задачей заявляемого изобретения является создание композиции на основе албендазола, которая может быть использована для эффективного лечения паразитозов, вызванных трематодами - Opisthorchis felineus, и при этом не вызывать поражений печени.
Поставленная задача решается благодаря тому, что состав композиции включает субстанции албендазола и полисахарида арабиногалактана (АГ) из лиственницы сибирской или Гмелина при массовых соотношениях компонентов албендазол арабиногалактан, составляющих 1:5-20.
Размеры частиц компонентов композиции преимущественно не должны превышать 20 мкм.
Частицы компонентов предпочтительно состоят из агломератов размерами 10-30 мкм.
Композиция включает вспомогательные вещества из классов фармакологически нейтральных моно-, ди- и полисахаридов.
Арабиногалактан (Е.Н. Медведева, В.А. Бабкин, Л.А. Остроухова. Арабиногалактан лиственницы - свойства и перспективы развития (обзор), Химия растительного сырья, 1 (2003), с. 27-37) является полисахаридным метаболитом эндемиков сибирской лесной флоры лиственницы сибирской (Larix sibirica), лиственницы Гмелина (Larix Gmelinii), лиственницы американской (Larix laricina), лиственницы западной (Larix occidentalis) и легко выделяется из древесины указанных деревьев. Содержание арабиногалактана составляет до 15% от веса сухой древесины. Химически арабиногалактан представляет собой полисахарид гребенчатого строения с м.м. - 18 кДа. Главная цепь состоит из звеньев галактозы, боковые цепи - из звеньев арабинозы и галактозы. Эта особенность строения способствует образованию прочных межмолекулярных комплексов лекарственных препаратов, молекулы которых вероятнее всего связываются межмолекулярными водородными и Ван-дер-Ваальсовыми связями в пространстве, образованном боковыми цепями. Согласно рекомендациям Роспотребнадзора (Методические рекомендации МР2.3.1.1915-04 "Рекомендуемые уровни потребления пищевых и биологически активных веществ" (утв. Федеральной службой по надзору в сфере защиты прав потребителей и благополучия человека 2 июля 2004 г. ) разрешенная адекватная/максимальная суточная доза арабиногалактана составляет 10/20 г. Это означает, что может применяться его большой массовый избыток по отношению к лекарственному веществу - албендазолу.
Целесообразность использования массовых соотношений албендазола и арабиногалактана от 1: 5 до 1: 20 обусловлена следующим:
- при увеличении относительного содержания албендазола (>1:5) в композиции достигаемое увеличение растворимости за счет образования водорастворимых комплексов недостаточно для усиления биологической активности;
- при понижении относительного содержания албендазола (<1:20) - композиция оказывается «перегружена» вспомогательным веществом (арабиногалактаном), что приводит к нежелательному увеличению массы дозы препарата, а также к увеличению его себестоимости.
Для получения композиции используют механохимический подход, заключающийся в обработке смеси твердых компонентов интенсивными механическими воздействиями - давлением и сдвиговыми деформациями, реализуемыми преимущественно в мельницах различного типа, осуществляющих ударно-истирающие воздействия на вещества. Смесь субстанций албендазола и арабиногалактана подвергается механической обработке в шаровых мельницах. При этом параллельно происходят три процесса, обеспечивающие повышение растворимости албендазола:
1. Измельчение частиц субстанций албендазола и арабиногалактана. Учитывая, что размеры частиц исходных субстанций находятся в пределах 100-500 мкм, желательно, чтобы частицы сырья измельчались преимущественно до размеров менее 20 мкм;
2. Образование частиц - агрегатов разрушенных частиц исходных субстанций албендазола и арабиногалактана размером 10-30 мкм благодаря образованию контактов этих частиц способствует более эффективному образованию водорастворимых комплексов молекул албендазола и арабиногалактана при гидратации получаемой композиции.
В аналоге нашего изобретения (S.S. Khalikov, A.V. Dushkin, M.S. Khalikov and others (2011) Mechanochemical modification of properties of anthelmintic preparations // Chemistry for Sustainable Development. 19(6):699-703) не исследовалась антигельминтная и тем более противоописторхозная активность получаемых препаратов. Таким образом,
улучшение водорастворимости и биодоступности, описанные в этой работе, не обеспечивали повышения фармакологической - антигельминтной активности и снижения токсичности.
Техническим результатом нашего изобретения является получение композиции на основе албендазола с противоописторхозным фармакологическим действием.
Предлагаемое техническое решение иллюстрируется нижеследующими электронными микрофотографиями: на фиг. 1 изображена субстанция арабиногалактана; на фиг. 2 - субстанция албендазола; на фиг. 3 - композиция состава албендазол: арабиногалактан в массовых соотношениях 1: 10, полученная при обработке смесей исходных компонентов на мельнице ВМ-1 в течение 4 часов.
Морфологические и гранулометрические характеристики порошков композиций составов албендазол: арабиногалактан в массовых соотношениях 1:5 и 1:20 аналогичны составу 1:10.
Полученная нами композиция имеет более высокую водорастворимость по сравнению с исходной субстанцией албендазола (см. пример 1).
Заявленная композиция именно при данном соотношении компонентов обеспечивает повышение фармакологической - антигельминтной активности, и понижение гепатотоксичности, что показано в экспериментах - in vitro на выделенных гельминтах Opistorchis felineus и in vivo на зараженных паразитами Opisthorchis felineus лабораторных животных (см. примеры 2, 3, 4). Полученные фармакологические результаты заявляемого технического решения - противоописторхозное действие (против Opisthorchis felineus) - не следовали с очевидностью из ранее опубликованных материалов - аналогов и прототипа - и таким образом отвечают критерию новизны.
Настоящее изобретение подтверждается следующими примерами:
Пример 1. Получение и физико-химические свойства композиций.
Смеси субстанций албендазола с арабиногалактаном, взятые в весовых соотношениях 1:5, 1:10 и 1:20, были подвергнуты обработке ударно-истирающими воздействиями в шаровой ротационной/валковой мельнице ВМ-1, в течение 2-24 часов (механическая активация). Затем были определены водорастворимость албендазола из полученных твердых дисперсий и получены электронные микрофотографии порошка композиций. Для исследования водорастворимости 0,6 г навески исследуемого материала суспендировали в 10 мл дистиллированной воды при +25°С на орбитальном шейкере (170 об/мин) в течение 4 часов. Концентрация албендазола в растворе определялась хроматографированием на хроматографе Agilent 1200 (колонка Zorbax Eclipse XDB-C18, 4.6×50 мм; температура колонки 30°С, элюент - система ацетонитрил/вода 1/1, скорость
потока 1 мл/мин, объем пробы 5 мкл, детектирование на длинах волн 230,8 и 290,8 нм) относительно приготовленных калибровочных образцов спиртовых растворов.
Электронные микрофотографии порошкообразных субстанций и композиций получали на микроскопе HITACHI ТМ-1000.
Полученные физико-химические данные композиций приведены в Таблице 1.
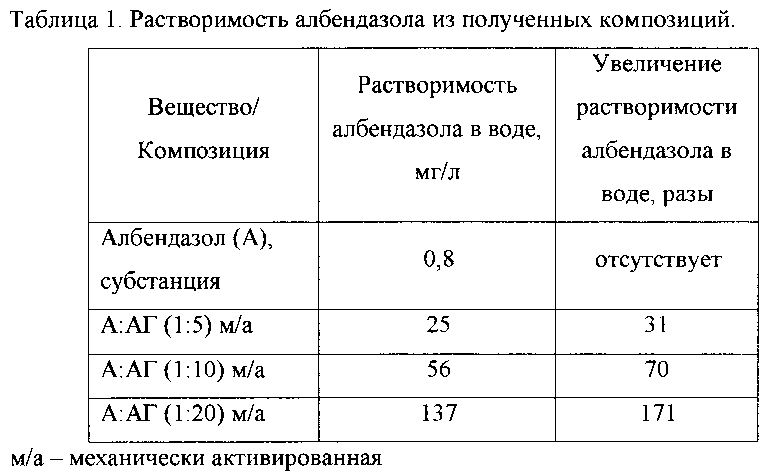
Электронные микрофотографии (Фиг. 1-3) демонстрируют уменьшение размеров частиц исходных субстанций до размеров менее 20 мкм, а также образование частиц-агрегатов с размерами 5-30 мкм. Во всех случаях имеет место увеличение водорастворимости албендазола по сравнению с исходной субстанцией в 31-171 раз. Эти характеристики композиций доказывают образование межмолекулярных комплексов молекул албендазола с макромолекулами полисахарида арабиногалактана в водных растворах, которые и обеспечивают противоописторхозное действие заявляемых композиций (см. примеры реализации 2-4).
Для улучшения суспендирования полученных композиций (см. Таблица 1) в водной среде при пероральном приеме перед применением возможно ее смешение с легко растворимыми пищевыми фармакологически нейтральными ди- и моносахаридами - глюкозой, лактозой, фруктозой, сахарозой и пр. Введение таких углеводов не влияет на параметры комплексообразования албендазол:АГ и на заявляемые фармакологические свойства. Могут использоваться любые массовые соотношения полученных композиций и углеводов.
Пример 2. Исследование противоописторхозной активности in vitro
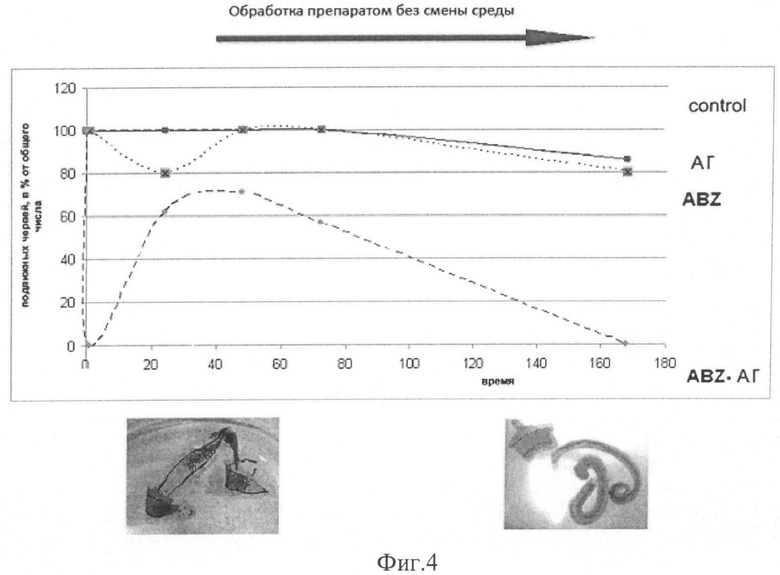
Проведен первый этап сравнительного тестирования албендазола (А) и заявляемых композиций с арабиногалактаном (А:АГ, см. Пример 1, Таблица 1). Проводили тестирование препаратов in vitro на живых интактных паразитах Opisthorchis felineus (Фиг. 4) с использованием насыщенных растворов исследуемых препаратов в инкубационной среде. В процессе тестирования применяли тесты на подвижность, а также использовали морфологические методы оценки жизнеспособности паразитов. Албендазол влиял на подвижность червей в ограниченной степени, при этом полностью не ограничивал подвижность. Подвижность червей полностью восстанавливалась до контрольного уровня уже через 3 суток. В отличие от них использование заявляемых композиций албендазола с арабиногалактаном (А:АГ, см. Пример 1, Таблица 1) приводило сначала к полному обездвиживанию паразитов уже через 1 час обработки и затем через 2 суток обнаруживались необратимые морфологические нарушения, в частности разрывы оболочки, что в итоге приводило к 100% гибели червей.
Оценка эффективности препаратов проводилась с использованием тестов на подвижность червей (Keiser J., Manneck Т., Vargas M. Interactions of mefloquine with praziquantel in the Schistosoma mansoni mouse model and in vitro. Journal of Antimicrobial Chemotherapy. 2011. doi:10.1093/jac/dkrl78.). На каждую точку брали 7-14 марит Opisthorchis felineus.
Пример 3. Исследование противоописторхозной активности in vivo.
В исследовании использовали хомяков M. auratus, предварительно зараженных 100 метацеркариями О. felineus за 2 месяца до проведения эксперимента. Водные суспензии исследуемых композиций вводили перорально через зонд, который позволял вводить препараты в пищевод, минуя глотку. Для облегчения суспендирования антигельминтные композиции смешивались с нейтральным гидрофильным наполнителем - фруктозой - в массовом соотношении 1:1. Хомяков M. auratus обрабатывали однократно, либо несколько дней подряд один раз в сутки в зависимости от выбранной схемы введения. Животных в группах было от 3 и до 11 особей. Через 3 недели от начала эксперимента определяли количество червей в желчных протоках печени животных (Табл. 2).
Таблица 2. Исследование антигельминтного действия албендазола (А) и его композиции с арабиногалактаном (АГ) в массовых соотношениях 1:5, 1:10 и 1:20 in vivo на модели экспериментального описторхоза золотистых хомяков M. auratus, вызванного заражением O. felineus.
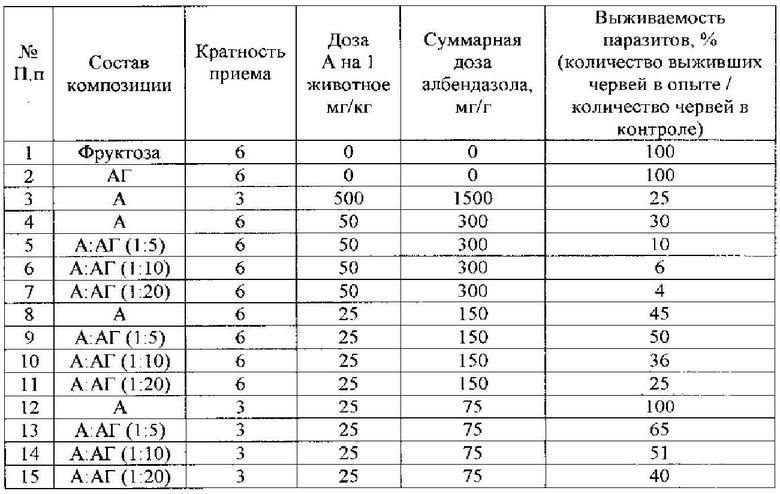
В качестве положительного контроля была выбрана высокая трехкратная доза албендазола (500 мг/кг веса), для того, чтобы достигнуть максимальной эффективности действия этого препарата (суммарно 1500 мг/кг). Однако оказалось, что этой дозы недостаточно для того, чтобы полностью излечить животных от описторхоза. Выживаемость червей в этом случае была 25%.
Было показано, что увеличение кратности введения сказывается на эффективности лекарства значительное существеннее, чем величина однократной дозы (см. Таблица 2). Так, доза 100 мг/кг при однократном введении уничтожала только 16% паразитов, тогда как при трехкратном ежедневном введении по 100 мг/кг уничтожала уже 70% паразитов.
Наиболее выраженные различия между албендазолом и его композициями А-АГ были получены при исследовании суммарной дозы препарата 300 мг/кг, вводимой животным 6 дней подряд, при ежедневном введении по 50 мг/кг (Таблица 2, группы 4-7), а также суммарной дозы препарата 75 мг/кг, вводимой животным 3 дня подряд, при ежедневном введении по 25 мг/кг (Таблица 2, группы 12-15). Выживаемость паразитов при приеме заявляемых композиций А-АГ в дозах 6X50 мг/кг составила 4-10%, при этом многие животные оказались полностью излечены от описторхозной инвазии, тогда как использование исходного албендазола приводило к уничтожению только 70% паразитов (выживаемость 30%). Выживаемость паразитов при приеме заявляемых композиций в дозе 3X25 мг/кг составила 60-35%, тогда как исходный албендазол в этой дозе был абсолютно неэффективен. Полученные результаты указывают, что по параметру выживаемости паразитов (группы 6-7 таблицы) заявляемое техническое решение имеет многократное (в 3-5 раз) преимущество по сравнению с ближайшим аналогом.
Таким образом, мы показали, что эффективность действия заявляемых композиций А-АГ была существенно выше, чем албендазола, и эти композиции могут быть использованы для лечения описторхозной инвазии, поскольку в большинстве случаев приводят к полному излечиванию животных.
Пример 4.
Гистоморфологическое исследование антигельминтного и гепатотоксического действия албендазола (А) и его композиции с арабиногалактаном (АГ) в массовом соотношении 1:10.
Препарат вводили перорально в водной суспензии через зонд, который позволял вводить препараты в пищевод, минуя глотку. В исследовании использовали хомяков, предварительно зараженных 100 метацеркариями О. felineus за 2 месяца до проведения эксперимента. Хомякам вводили препараты албендазола (А) и композицию с арабиногалактаном А-АГ (1:10) в дозе 6×50 мг/кг веса один раз в сутки в течение 6 дней (см. Пример 3). Через 15 дней после окончания эксперимента животных забивали и определяли гистоморфологическую картину в образцах печени.
На фоне описторхозной инвазии у животных в паренхиме выявляются обширные очаги пролиферации желчных капилляров с признаками тканевого и клеточного атипизма, инфильтрированные лимфоцитами и эозинофилами. Стенки желчных протоков резко утолщены за счет интраканаликулярного фиброза, выстланы активно пролиферирующим высоким призматическим эпителием. В частности, в контрольной группе выявляется мелкоочаговая гидропическая дистрофия гепатоцитов, единичные фокальные и моноцеллюлярные некрозы в паренхиме (Фиг. 5), признаки гемосидероза, свидетельствующие о нарушении пигментного обмена и наличии холестаза.
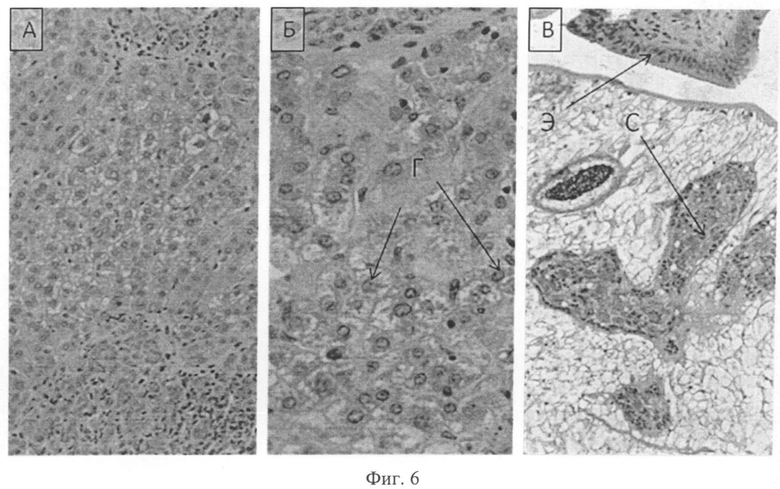
У животных, получавших албендазол (доза 6×50 мг/кг), выражены признаки токсического поражения печени, а именно крупноочаговая гидропическая дистрофия, дисплазия и множественные некрозы гепатоцитов (Фиг. 6). В теле гельминтов, найденных в желчных протоках, отмечаются деструктивные процессы в органах размножения в виде их расширения, вакуолизации и некроза (Фиг. 6), что свидетельствует о необратимых повреждениях репродуктивной системы гельминта.
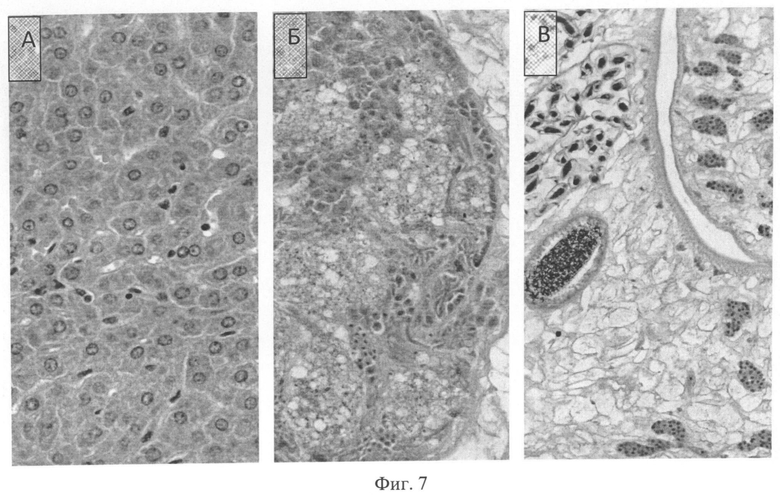
В отличие от группы, обработанной албендазолом, животные, получившие композицию албендазола и арабиногалактана (А:АГ 1:10) в той же дозе (6×50 мг/кг), не обнаруживают признаков токсического поражения гепатоцитов. Гепатоциты характеризуются однородностью, дисплазия и деструктивные процессы не выражены (Фиг. 7). В синусоидах выявляется большое количество купферовских клеток с признаками повышенной активности. У гельминтов в желчных протоках видны более выраженные деструктивно-некротические изменения в органах размножения по сравнению с животными, обработанными только албендазолом. Репродуктивные органы гельминтов гипертрофированы, очаги размножения в них сочетаются с некрозами клеток, ярко выражен отек (Фиг. 7), что свидетельствует о большей фармакологической активности композиции А:АГ, чем исходного албендазола в отношении паразитов печени O. felineus.
Таким образом, при сравнительном исследовании албендазола и его композиции с арабиногалактаном (1:10) in vivo на модели экспериментального описторхоза на хомяках M. auratus на основании проведенного гистоморфологического анализа можно сделать заключение, что композиция А:АГ (1:10) не вызывает токсического повреждения гепатоцитов в отличие от албендазола (А). Кроме того, композиция А:АГ проявляет более высокую фармакологическую активность, чем албендазол по отношению к взрослой особи Opisthorchis felineus.
Таким образом, примеры реализации изобретения подтверждают физико-химические и фармакологические характеристики заявляемой композиции, а также то, что заявленная композиция соответствует критерию «промышленная применимость».
| название | год | авторы | номер документа |
|---|---|---|---|
| Композиция на основе празиквантеля для лечения описторхоза | 2017 |
|
RU2681649C1 |
| Средство, обладающее противоописторхозной активностью | 2019 |
|
RU2702733C1 |
| ПРОТИВОПАРАЗИТАРНОЕ СРЕДСТВО НА ОСНОВЕ АЛЬБЕНДАЗОЛА И СПОСОБ ЕГО ИСПОЛЬЗОВАНИЯ ДЛЯ ЛЕЧЕНИЯ ГЕЛЬМИНТОЗОВ МЛЕКОПИТАЮЩИХ | 2014 |
|
RU2546535C1 |
| ВОДОРАСТВОРИМАЯ ЛЕКАРСТВЕННАЯ КОМПОЗИЦИЯ И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 2006 |
|
RU2337710C2 |
| КОМПОЗИЦИЯ НА ОСНОВЕ ДИПРОПИОНАТА БЕТУЛИНА | 2013 |
|
RU2541153C1 |
| РЕКОМБИНАНТНАЯ ПЛАЗМИДНАЯ ДНК pMALTEV-legumain, КОДИРУЮЩАЯ ПОЛИПЕПТИД, ОБЛАДАЮЩИЙ АНТИГЕННЫМИ СВОЙСТВАМИ БЕЛКА ЛЕГУМАИН Opisthorchis felineus, И ШТАММ E.coli BL 21(DE3)pLysS-pMALTEV-legumain - ПРОДУЦЕНТ РЕКОМБИНАНТНОГО ПОЛИПЕПТИДА, ОБЛАДАЮЩЕГО АНТИГЕННЫМИ СВОЙСТВАМИ БЕЛКА ЛЕГУМАИН Opisthorchis felineus | 2012 |
|
RU2496876C1 |
| Средство для профилактики заражения описторхозом | 2018 |
|
RU2703296C1 |
| КОМПОЗИЦИЯ НА ОСНОВЕ ДИАЦЕТАТА БЕТУЛИНА | 2013 |
|
RU2517157C1 |
| ЛЕКАРСТВЕННОЕ СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ АРТЕРИАЛЬНОЙ ГИПЕРТЕНЗИИ И НАРУШЕНИЯ РИТМА СЕРДЦА | 2008 |
|
RU2391980C1 |
| Противопаразитарное средство и способ терапии овец при паразитарных инвазиях | 2022 |
|
RU2815424C1 |




Изобретение относится к композиции на основе албендазола. Указанная композиция состоит из субстанции албендазола и полисахарида арабиногалактана из лиственницы сибирской или Гмелина при массовых соотношениях компонентов албендазол : арабиногалактан 1:5-20. Заявленное изобретение обладает более высокой противоописторхозной фармакологической активностью, чем албендазол, а также не вызывает токсического повреждения гепатоцитов. 2 з.п. ф-лы, 7 ил., 2 табл., 4 пр.
1. Композиция на основе албендазола с повышенной противоописторхозной фармакологической активностью и пониженной гепатотоксичностью, состоящая из субстанции албендазола и полисахарида арабиногалактана из лиственницы сибирской или Гмелина при массовых соотношениях компонентов албендазол:арабиногалактан соответственно 1:5-20.
2. Композиция по п. 1, отличающаяся тем, что размеры частиц компонентов композиции не превышают 20 мкм.
3. Композиция по п. 1, отличающаяся тем, что частицы компонентов образуют агломераты размерами 10-30 мкм.
| BHAIBULAYA M | |||
| "Treatment of Opisthorchiasis viverrini in hamsters with albendazole", Southeast Asian J | |||
| Trop | |||
| Med | |||
| Public Health, 1984, N15 | |||
| KHALIKOV M | |||
| S., "Mechanochemical modification of properties of antihelminthic preparations", Chemistry for sustainable development, 2011, N19, стр.653-657 | |||
| ВОДОРАСТВОРИМАЯ ЛЕКАРСТВЕННАЯ КОМПОЗИЦИЯ И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 2006 |
|
RU2337710C2 |
| Электрический подвесной изолятор шарнирного типа | 1928 |
|
SU14689A1 |
Авторы
Даты
2015-04-10—Публикация
2013-10-03—Подача