Изобретение относится к биологически активным соединениям, используемым в медицине и фармацевтической промышленности. Средство представляет собой 3-оксо-8-гидрокси-1,5,7б,4,8в(Н)-гвай-10(14),11(13)-диен-12,6-олид, выделенный из надземной части василька шероховатого (Centaurea scabiosa L., семейство Asteraceae). Новое средство обладает противоописторхозной активностью.
В комплексной терапии описторхоза применяются синтетические лекарственные средства: препарат празиквантел (бильтрицид) и его аналог – азинокс. Перечисленные препараты имеют ряд побочных эффектов и противопоказаний, что весьма ограничивает область их применения [1].
Известна композиция с противоописторхозной фармакологической активностью, на основе субстанции албендазола и полисахарида арабиногалактана из лиственницы сибирской или Гмелина [2]. Использование албендазола в сочетании с арабиногалактаном обусловлено тем, что индивидуальный албендазол недостаточно эффективен при лечении описторхоза и обладает гепатотоксичностью (наличие в композиции арабиногалактана повышает эффективность лечения и снижает вероятность негативных токсических эффектов). Поскольку данный аналог не является индивидуальным химическим веществом и проявил в эксперименте меньшую фармакологическую активность, то он уступает заявляемому решению.
Описано средство, обладающее противоописторхозным действием, на основе этанольного экстракта растений рода Centaurea семейства Asteraceae: Centaurea scabiosa L. (василек шероховатый) или Centaurea pseudomaculosa Dobrocz. (василек ложнопятнистый) или Centaurea jacea L. (василек луговой) [3]. Данный аналог уступает предлагаемому решению, поскольку представляет собой условно-стандартизуемую смесь экстрактивных веществ различных классов биологически активных соединений, большинство из которых не вносят вклад в общий противоописторхозный эффект. Кроме того, сопоставимая фармакологическая активность данного аналога достигается при использовании в дозах, примерно в пять раз превышающих дозу средства, предлагаемого в заявляемом решении.
Кроме того, существует способ получения средства, обладающего противолямблиозным и противоописторхозным действием, на основе этанольного экстракта из надземной части соссюреи иволистной (Saussurea salicifolia L.) [4]. Данный аналог так же уступает предлагаемому решению, поскольку представляет собой условно-стандартизуемый экстрактивный комплекс, состоящий из биологически активных веществ различных классов, большинство из которых не проявляют целевого противоописторхозного эффекта. При этом авторы изобретения не приводят данные по фармакологическим свойствам данного аналога.
Таким образом, взятые в качестве прототипов средства, наиболее близкие к предлагаемому решению, уступают заявляемому средству.
Новая техническая задача – расширение арсенала противоописторхозных средств, на основе индивидуальных веществ растительного происхождения, обладающих более высокой активностью и меньшей токсичностью.
Поставленную задачу решают применением в качестве противоописторхозного средства индивидуального сесквитерпенового лактона 3-оксо-8-гидрокси-1,5,7б,4,8в(Н)-гвай-10(14),11(13)-диен-12,6-олида, выделенного из василька шероховатого ранее разработанным способом [5].
Отличительные признаки проявили в заявляемой совокупности новые свойства – впервые установлено, что в качестве средства, обладающего противоописторхозной активностью, используют 3-оксо-8-гидрокси-1,5,7б,4,8в(Н)-гвай-10(14),11(13)-диен-12,6-олид, выделенный из надземной части василька шероховатого. Таким образом, предлагаемое техническое решение соответствует критериям изобретения, а именно – «новизна», «изобретательский уровень» и «промышленная применимость».
Фармакологические испытания
Противоописторхозная активность 3-оксо-8-гидрокси-1,5,7α,4,8β(Н)-гвай-10(14),11(13)-диен-12,6-олида исследована на моделях in vitro и in vivo в соответствии с общепринятыми методиками. В качестве референтного препарата во всенх типах исследования использован празиквантел (Praziquantel, CAS no: 55268-74-1).
Изучение специфической противоописторхозной активности на модели in vitro базируется на оценке жизнеспособности изолированных марит описторхов при их инкубировании в питательной среде, содержащей различные концентрации 3-оксо-8-гидрокси-1,5,7α,4,8β(Н)-гвай-10(14),11(13)-диен-12,6-олида. Оценку проводят через 24, 48 и 72 часа культивирования по величине двигательной активности марит описторхов, оцениваемой визуально под микроскопом с двадцатикратным увеличением. При этом отмечают движения ротовой присоски, движения тела на сгибание/скручивание, а также перистальтику внутренних органов. Используют общепринятую шкалу для оценки двигательной активности марит Opisthorchis felineus [6] (табл. 1). При оценке данных, полученных при фармакологических испытаниях в условиях in vitro, качественные данные описывали с помощью абсолютной частоты и в процентном отношении [7].
Изучение специфической противоописторхозной активности на модели in vivo, согласно Руководству по проведению доклинических исследований лекарственных средств [8], базируется на оценке влияния 3-оксо-8-гидрокси-1,5,7α,4,8β(Н)-гвай-10(14),11(13)-диен-12,6-олида на значение интенс-эффективности (ИЭ), рассчитываемое как процент отошедших из гепатобилиарной системы марит Opisthorchis felineus в результате лечения. ИЭ вычисляют, сравнивая среднее число гельминтов у экспериментальных животных в леченой и контрольной группах, в соответствии с формулой: ИЭ = К–О / К × 100 %, где К – среднее число гельминтов в контрольной группе, О – среднее число гельминтов в леченой группе.
При оценке данных, полученных при фармакологических испытаниях в условиях in vivo, использовали методы статистического описания и проверки статистических гипотез [7, 9]. Статистическая обработка результатов выполнена в программе SPSS (IBM, США). Данные представлены в виде медианы (Ме), отражающей центральную тенденцию, и верхнего и нижнего квартилей, характеризующие разброс значений показателя у 50 % образцов (Q1 — Q3), где Q1 — 25 % перцентиль, Ме – 50 % перцентиль, Q3 — 75 % перцентиль. Проверка на соответствие выборок нормальному закону распределения проводилась критерием Шапиро-Вилка. Для проверки достоверности различий нескольких групп независимых количественных данных использовали непараметрический критерий Краскала-Уоллиса, с последующим использованием непараметрического U-критерий Манна-Уитни для попарного сравнения исследуемых групп. Для исключения ошибки множественных сравнений использовали поправку Бенджамини-Хохберга (FDR). Показатели считали статистически значимыми при p<0,05.
В условиях in vitro доказано прямое действие 3-оксо-8-гидрокси-1,5,7α,4,8β(Н)-гвай-10(14),11(13)-диен-12,6-олида на жизнеспособность марит Opisthorchis felineus в сравнении с референтным препаратом празиквантелем. 3-оксо-8-гидрокси-1,5,7α,4,8β(Н)-гвай-10(14),11(13)-диен-12,6-олид и референтный препарат празиквантел исследовались в концентрациях 10, 15, 20, 25, 50 и 100 мкг/мл в среде инкубации марит Opisthorchis felineus. В качестве критерия жизнеспособности использовали характеристики двигательной активности марит Opisthorchis felineus, оцениваемые визуально с использованием общепринятой шкалы, через 24, 48 и 72 часа инкубации. Качественные характеристики двигательной активности описывали с помощью абсолютной частоты, а также величины процентного отношения.
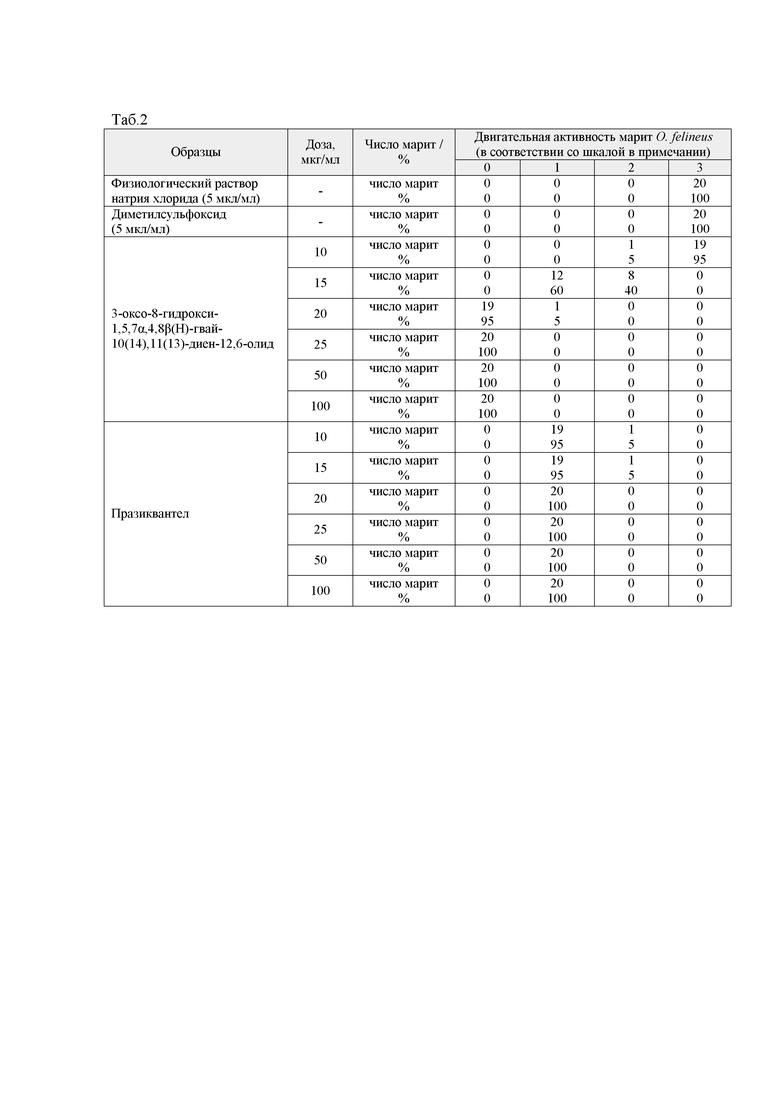
3-оксо-8-гидрокси-1,5,7α,4,8β(Н)-гвай-10(14),11(13)-диен-12,6-олид через 24 часа инкубации в дозах 25, 50 и 100 мкг/мл вызывал 100% гибель марит O. felineus. В концентрации 20 мкг/мл 3-оксо-8-гидрокси-1,5,7α,4,8β(Н)-гвай-10(14),11(13)-диен-12,6-олид приводил к гибели 95% марит O. felineus (табл. 2). В дозе 10 мкг/мл 3-оксо-8-гидрокси-1,5,7α,4,8β(Н)-гвай-10(14),11(13)-диен-12,6-олид редуцировал двигательную активность 5% марит O. felineus (оценка по шкале – 2), а в дозе 15 мкг/мл – оказывал более выраженное редуцирующее действие на двигательную активность (60% марит O. felineus оценка по шкале – 1, 40% марит O. felineus – оценка 2) (табл. 2).
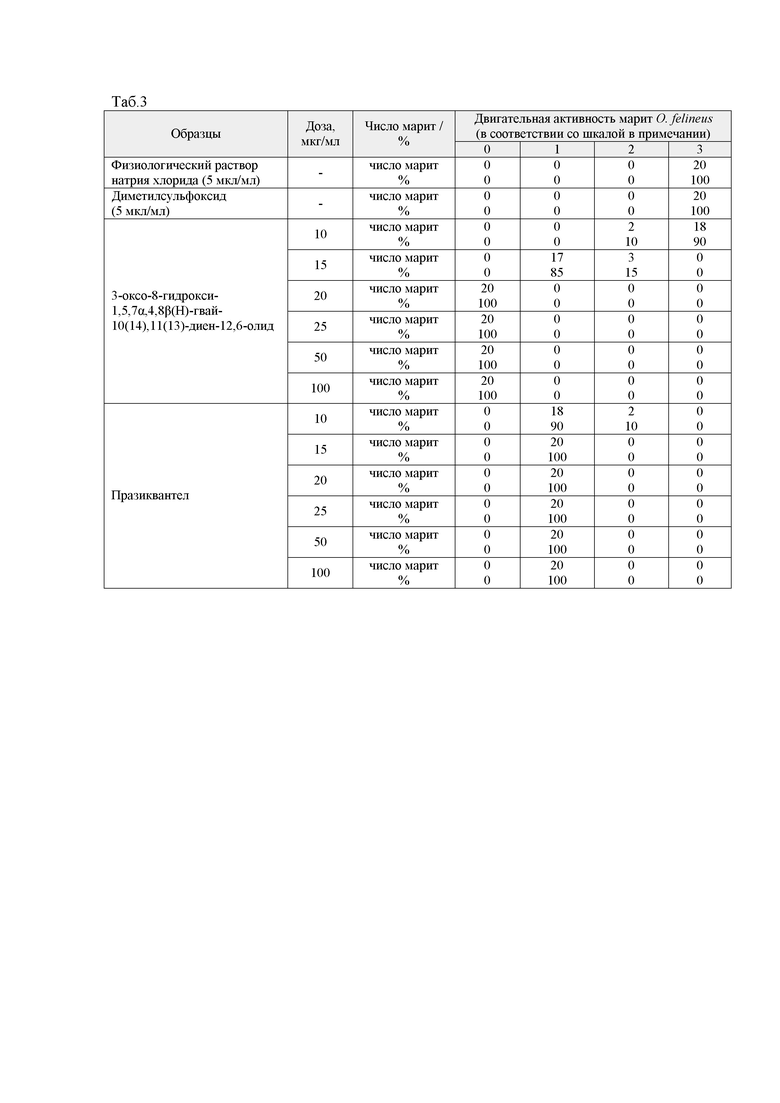
3-оксо-8-гидрокси-1,5,7α,4,8β(Н)-гвай-10(14),11(13)-диен-12,6-олид в дозах 20, 25, 50 и 100 мкг/мл через 48 часов инкубации вызывал 100% гибель марит O. felineus (табл. 3). В дозе 10 мкг/мл 3-оксо-8-гидрокси-1,5,7α,4,8β(Н)-гвай-10(14),11(13)-диен-12,6-олид через 48 часов инкубации редуцировал двигательную активность 10% марит O. felineus (оценка по шкале – 2), а в дозе 15 мкг/мл – оказывал более выраженное редуцирующее действие на двигательную активность (85% марит O. felineus оценка по шкале – 1, 15% марит O. felineus – оценка 2) (табл. 3).
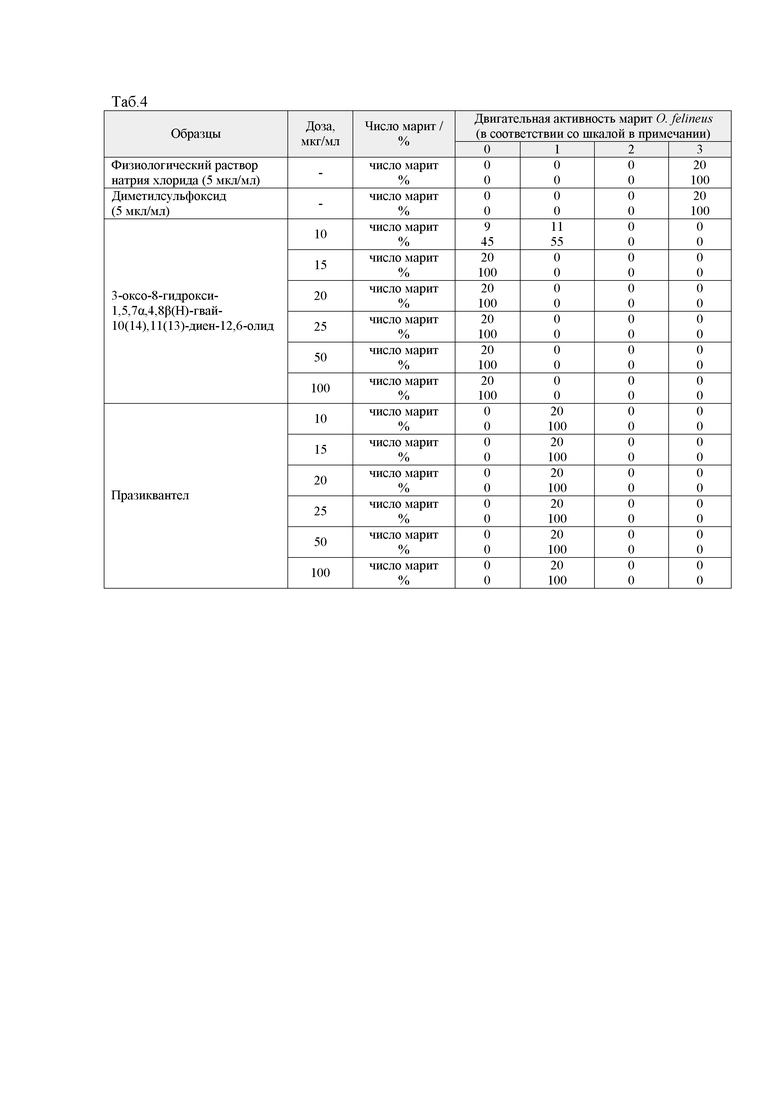
3-оксо-8-гидрокси-1,5,7α,4,8β(Н)-гвай-10(14),11(13)-диен-12,6-олида в дозах 15, 20, 25, 50 и 100 мкг/мл через 72 часа инкубации приводил к 100% гибели марит O. felineus (табл. 4). В дозе 10 мкг/мл 3-оксо-8-гидрокси-1,5,7α,4,8β(Н)-гвай-10(14),11(13)-диен-12,6-олид через 72 часа инкубации вызывал гибель 45% марит, а у 55% марит отмечалась очень слабая двигательная активность (оценка по шкале – 1) (табл. 4).
В результате эксперимента установлено, что добавление физиологического раствора натрия хлорида и растворителя диметилсульфоксида в количестве 5 мкл/мл среды инкубации (группы контроля растворителей) не приводило к изменению характеристик двигательной активности и гибели марит O. felineus при инкубации в течение 24, 48 и 72 часов (табл. 2-4).
Референтный препарат празиквантел проявил специфическую активность во всех исследованных концентрациях (10-100 мкг/мл инкубационной среды). Празиквантел приводил к параличу мышечной ткани марит O. felineus, редуцируя до минимальных значений их двигательную активность (оценка по шкале – 1, очень слабая двигательная активность), но сохраняя их жизнеспособность в течение 72 часов экспозиции. Через 24 часа инкубации 95% марит O. felineus характеризовались очень слабой двигательной активностью при добавлении в инкубационную среду празиквантела в концентрациях 10 и 15 мкг/мл. В более высоких концентрациях очень слабая двигательная активность наблюдалась у 100% марит O. felineus (табл. 2). Через 48 часов инкубации марит O. felineus с празиквантелем в концентрации 15, 20, 25, 50 и 100 мкг/мл очень слабая двигательная активность наблюдалась у 100% марит (табл. 3). В концентрации 10 мкг/мл очень слабая двигательная активность отмечалась у 90% марит и у 10% - сниженная двигательная активность (оценка по шкале – 2) (табл. 3). Через 72 часа инкубации марит O. felineus с празиквантелем во всех исследуемых концентрациях (10-100 мкг/мл инкубационной среды) отмечалась очень слабая двигательная активность (табл. 4).
На основании полученных экспериментальных данных показано прямое действие 3-оксо-8-гидрокси-1,5,7α,4,8β(Н)-гвай-10(14),11(13)-диен-12,6-олида на жизнеспособность марит Opisthorchis felineus и определена степень его активности при добавлении в среду культивирования, которая составила 20-25 мкг/мл инкубационной среды.
В результате экспериментов in vivo, с использованием золотистых хомяков с хронической фазой описторхозной инвазии, установлено, что 3-оксо-8-гидрокси-1,5,7α,4,8β(Н)-гвай-10(14),11(13)-диен-12,6-олид в дозах 40 и 80 мг/кг при четырехкратном введении в день в течение 5-ти суток проявляет сопоставимую с препаратом сравнения празиквантелем противоописторхозную активность. Величина ИЭ антигельминтного эффекта в этих дозах для 3-оксо-8-гидрокси-1,5,7α,4,8β(Н)-гвай-10(14),11(13)-диен-12,6-олида составила 71,28 и 69,59%, соответственно (табл. 5). Величина ИЭ празиквантела в условиях хронической фазы описторхозной инвазии составила 64,53 %.
Эффективная терапевтическая доза 3-оксо-8-гидрокси-1,5,7α,4,8β(Н)-гвай-10(14),11(13)-диен-12,6-олида в хронической фазе описторхозной инвазии при четырехкратном введении в течение 5-ти суток составила 40 мг/кг. При этом его эффективность в данной дозе сопоставима с эффективностью препарата сравнения празиквантела (в дозе 20 мг/кг).
Таким образом, фармакологические исследования противоописторхозной активности 3-оксо-8-гидрокси-1,5,7α,4,8β(Н)-гвай-10(14),11(13)-диен-12,6-олида на моделях in vitro и in vivo позволяют считать его перспективным лекарственным кандидатом для лечения описторхоза, имеющим ряд преимуществ перед применяющимся в настоящее время празиквантелем. Обладая сопоставимым уровнем эффективности, 3-оксо-8-гидрокси-1,5,7α,4,8β(Н)-гвай-10(14),11(13)-диен-12,6-олид не имеет признаков выраженных побочных эффектов в эксперименте.
Источники информации
1. Бронштейн, М. А. Трематодозы печени: описторхоз, клонорхоз / А. М. Бронштейн, В. И. Лучшев // Русский медицинский журнал. – 1998. – Т. 6, - № 3. – С. 17-27.
2. Душкин А. В., Метелева Е. С., Ляхов Н. З., Чистяченко Ю. С., Халиков С. С., Толстикова Т. Г., Хвостов М. В., Баев Д. С., Жукова Н. А., Мордвинов В. А., Катохин А. В., Пахарукова М. Ю. Композиция на основе албендазола с противоописторхозной фармакологической активностью / Пат. № 2545797 РФ.
3. Краснов Е. А., Кадырова Т. В., Каминский И. П. Средство, обладающее противоописторхозным действием, и способ его получения / Пат. № 2519666 РФ.
4. Буркова В. Н., Боев С. Г., Мозжелина Т. К., Чекрыгин В. Н. Способ получения средства, обладающего противоописторхозным действием / Пат. № 2162701 РФ.
5. Каминский И. П., Белоусов М. В., Кадырова Т. В., Юсубов М. С., Гурьев А. М. Российская Федерация. Способ выделения 3-оксо-8-гидрокси-1,5,7α,4,8β(Н)-гвай-10(14),11(13)-диен-12,6-олида / Пат. № 2665975 РФ.
6. Duthaler, U. In Vivo and In Vitro Sensitivity of Fasciola hepatica to triclabendazole Combined with Artesunate, Artemether, or OZ78./ U. Duthaler, T. Smith , J. Keiser // Antimicr. Ag. and Chemotherapy. – 2010. - №54. - P. 4596-4604.
7. Гланц, С. Медико – биологическая статистика / С. Гланц. – Пер. с англ. – М. : Практика, 1998. – 459 с.
8. Миронов А.Н., Бунятян Н.Д., Васильев А.Н. и др. Руководство по проведению доклинических исследований лекарственных средств. Часть первая. – Москва, 2013, с. 605-626.
9. Гмурман, В. Е. Теория вероятности и математическая статистика / В. Е. Гмурман. – Москва : Высшая школа, 2006. – 284 с.
| название | год | авторы | номер документа |
|---|---|---|---|
| Композиция на основе празиквантеля для лечения описторхоза | 2017 |
|
RU2681649C1 |
| КОМПОЗИЦИЯ НА ОСНОВЕ АЛБЕНДАЗОЛА С ПРОТИВООПИСТОРХОЗНОЙ ФАРМАКОЛОГИЧЕСКОЙ АКТИВНОСТЬЮ | 2013 |
|
RU2545797C1 |
| Средство для профилактики заражения описторхозом | 2018 |
|
RU2703296C1 |
| СПОСОБ ВЫДЕЛЕНИЯ 3-ОКСО-8-ГИДРОКСИ-1,5,7А,4,8В(Н)-ГВАЙ-10(14),11(13)-ДИЕН-12,6-ОЛИДА | 2017 |
|
RU2665975C1 |
| РЕАГЕНТ ДЛЯ ИММУНОФЕРМЕНТНОГО АНАЛИЗА И СПОСОБ ИММУНОФЕРМЕНТНОГО ТЕСТИРОВАНИЯ СПЕЦИФИЧЕСКИХ АНТИТЕЛ ПРИ ОПИСТОРХОЗЕ, ВЫЗЫВАЕМОМ ПЕЧЕНОЧНОЙ ТРЕМАТОДОЙ OPISTHORHIS FELINEUS | 2001 |
|
RU2197736C1 |
| СРЕДСТВО ДЛЯ ХИМИОПРОФИЛАКТИКИ ОПИСТОРХОЗА | 1989 |
|
RU2033181C1 |
| СПОСОБ НАГРУЗКИ ДЕНДРИТНЫХ КЛЕТОК АНТИГЕНОМ ИНФЕКЦИОННОГО ПРОИСХОЖДЕНИЯ Opisthorchis felineus | 2011 |
|
RU2486238C1 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ ПРОТИВООПИСТОРХОЗНЫМ ДЕЙСТВИЕМ, И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2008 |
|
RU2366443C1 |
| СРЕДСТВО ДЛЯ ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ ГЕЛЬМИНТОЗОВ, В ЧАСТНОСТИ ОПИСТОРХОЗА | 2011 |
|
RU2493864C2 |
| СПОСОБ КОМПЛЕКСНОГО ЛЕЧЕНИЯ БОЛЬНЫХ ПАРАЗИТАРНЫМИ ЗАБОЛЕВАНИЯМИ | 2011 |
|
RU2491936C2 |


Изобретение относится к медицине и фармацевтической промышленности. Предложено применение 3-оксо-8-гидрокси-1,5,7б,4,8в(Н)-гвай-10(14),11(13)-диен-12,6-олида качестве средства лечения и профилактики описторхоза. Средство выделено из надземной части василька шероховатого (Centaurea scabiosa L., семейство Asteraceae). Технический результат: средство растительного происхождения обладает более высокой активностью и меньшей токсичностью по сравнению с празиквантелом. 5 табл.
Применение 3-оксо-8-гидрокси-1,5,7α,4,8β(Н)-гвай-10(14),11(13)-диен-12,6-олида в качестве средства лечения и профилактики описторхоза.
Авторы
Даты
2019-10-10—Публикация
2019-02-13—Подача