Изобретение относится к области биотехнологии, а именно генной инженерии, и касается рекомбинантной вакцины для профилактики папилломавирусной инфекции, содержащей в своем составе в качестве активного компонента рекомбинантный капсидный белок L1 вируса папилломы человека типа 16 и 18, и/или 56, полученный путем культивирования рекомбинантных клеток дрожжей Hansenula polymorpha, а также способа получения вакцины.
Вирус папилломы человека (HPV - Human Papilloma Virus), поражая эпителиальные клетки, вызывает различные заболевания у человека. В зависимости от типа инфицирующего вируса, который на основании данных о гомологии последовательности ДНК классифицирован более чем в 70 типов, папилломавирусная инфекция проявляется в виде образования доброкачественных бородавок, незлокачественных кондилом или папиллом на слизистой половых органов или дыхательных путей. Вирус папилломы человека типа 16 и 18 вызывает эпителиальную дисплазию слизистой половых органов, именно эти типы вируса папилломы ассоциированы с большей частью преинвазивных и инвазивных карцином аногенитальной сферы (рак шейки матки, влагалища, вульвы и анального канала), из которых рак шейки матки - один из самых распространенных и опасных видов новообразований у женщин. В исследовании, проведенном на территории РФ, показано, что у женщин с высокой степенью плоскоклеточного интраэпителиального поражения и раком шейки матки наряду с HPV типа 16 обнаруживается HPV типа 56, причем в случаях мультиинфекции этот тип вируса преобладает (VII Всероссийская научно-практическая конференция с международным участием «Молекулярная диагностика - 2010», Сб. трудов п/ред. Академика РАМН В.И. Покровского, т.3, с.373-409). По данным ВОЗ ежегодно раком шейки матки заболевают около 500 тысяч женщин во всем мире, причем более половины этих случаев заканчиваются летальным исходом. Клинические проявления рака шейки матки не обнаруживаются длительное время, в то же время ранняя диагностика папилломавирусной инфекции довольно сложна. Именно поэтому в борьбе с распространением такого тяжелого заболевания предпочтение отдается профилактике папилломавирусной инфекции, в частности путем индуцирования иммунного ответа у человека при вакцинации.
Вирус папилломы относится к семейству паповирусов (Papoviridae), имеет диаметр 40-50 нм. Капсид вируса образован из 72 белковых капсомеров, состоящих из основного белка L1 и минорного белка L2. Геном вируса представлен в виде кольцевой двуцепочечной ДНК, которая содержит 8 ранних генов (Е1-Е7) и два поздних гена, кодирующих белки капсида L1 и L2. Главный белок L1 (55-60 кДа) способен сам собираться в вирусоподобные частицы (VLP, virus-like particles), сходные по строению с вирионами, но не содержащие вирусную ДНК. Белок L1 обладает высокой иммуногенностью и индуцирует образование антител, нейтрализующих инфекционный вирус.
В настоящее время рекомбинантные белки L1 HPV представляют собой перспективные иммуногенные компоненты для создания профилактических вакцин, направленных против опасных типов папилломавируса. Такие рекомбинантные вакцины безопасны, поскольку не содержат потенциально онкогенного вирусного генома. Экспрессируемый в эукариотической клетке рекомбинантный белок L1 способен к самосборке в капсидоподобную структуру, в основном отражающую VLP, морфологически и антигенно эквивалентную аутентичным вирионам. Иммунизация подобными VLP способствует продукции антител, нейтрализующих вирус, что приводит к защите против HPV инфекции.
Затруднения, возникающие при создании эффективных папилломавирусных вакцин, прежде всего связаны с разработкой оптимальных экспрессионных систем для продукции рекомбинантных белков HPV, обладающих иммуногенными свойствами природных белков HPV L1, способных к образованию конформационно правильных VLP.
Известно получение белков L1 и L2 HPV типа 16 путем культивирования клеток CV-1 млекопитающих, инфицированных рекомбинантным вектором вируса коровьей оспы [Zhou J et al. Virology v.185, p.251-257, 1991]. Известна экспрессия папилломавирусного белка L1, способного агрегировать в вирусоподобные частицы (VLP) и обладающего иммуногенностью, в эукариотической системе на основе культивируемых клеток насекомых, бакуловирусная система [Kimbauer R. et al. Proc. Natl. Acad. Sci USA, v.89, p.12180-12184, 1992]. В научной и патентной литературе представлены примеры использования для получения рекомбинантных белков HPV системы экспрессии на основе дрожжей Saccharomyces cerevisiae, которым отдается предпочтение благодаря международно признанной безопасности дрожжей, способности к наработке больших количеств белка в нативной конформации. Так, Петров Р.M. и др. [WO 2006/065166 A1, 2006] получали капсидные белки L1 вирусных серотипов 16, 18, 31 HPV, вызывающих наиболее агрессивные формы заболеваний у человека, из рекомбинантных штаммов дрожжей. Эти штаммы получали трансформацией дрожжевых клеток S. cerevisiae плазмидами с генами, кодирующими белки L1 указанных серотипов. Фрагменты ДНК, кодирующие эти белки, были выделены из клинического материала. Созданные дрожжевые продуценты при культивировании были способны экспрессировать белки L1 в виде вирусоподобных частиц. Белки L1 использовали для приготовления профилактических и терапевтических вакцин.
Известно использование метилотрофных дрожжей Pichia pastoris для получения HPV16-L1 [Bazan S.B. et al., Arch. Virol. 2009, 154(10), 1609-17]. В геном Р. pastoris был введен ген, кодирующий HPV16-L1, под контролем регулируемого метанолом промотора. Этот ген имел оптимизированный кодоновый состав. Очистку белка L1 выполняли с использованием гепарин-сефарозной хроматографии с последующей стадией сборки вирусоподобных частиц. Образование биологически активных VLP подтверждали методами иммуноэлектронной микроскопии и гемагглютинации.
В патентах RU 2445357, 2012 и RU 2445358, 2012 описаны рекомбинантные штаммы-продуценты капсидного белка L1 HPV типа 16 - Pichia angusta BKM Y-2988D и типа 18 - Pichia angusta Y-2989D. Штаммы получены путем интеграции в геном экспрессионной плазмиды, содержащей фрагмент ДНК с рекомбинантным геном, кодирующим L1 HPV типа 16 или 18, соответственно, под контролем промотора DAK (дигидроксиацетон киназа) Н. polymorpha, и селективный маркер (ген LEU2 Н. polymorpha). Описанные рекомбинантные штаммы-продуценты, имея высокую продуктивность, тем не менее не обеспечивают получение антигена, обладающего оптимальной для использования в вакцине иммуногенностью. Для повышения продуктивности штамма-продуцента экспрессионная кассета рекомбинантного белка вводится в геном реципиентного штамма в большом количестве копий. Однако в некоторых копиях экспрессионной кассеты в ходе получения и культивирования штамма могут возникать мутации, изменяющие свойства целевого белка. При этом контроль за возникновением мутаций в случае высокой копийности гена практически невозможен. Более того, при превышении определенного уровня синтеза может нарушаться процесс укладки целевого белка, что приводит к снижению его выхода, ухудшению биологической активности и усложняет процесс очистки.
Известна вакцина для создания иммунного ответа против папилломавируса человека, включающая вирусоподобные частицы HPV 16, HPV 18 и, по меньшей мере, одного из типов HPV31, HPV45, HPV52 (RU 2420313, 2010). VLP получали путем экспрессии в клетках Trichoplusia ni, инфицированных рекомбинантным бакуловирусом, кодирующим соответствующий ген LI HPV. После очистки каждый тип VLP независимо адсорбировали на гидроокиси алюминия с получением адсорбированных концентрированных моновалентов, которые затем смешивали в нужном соотношении. Дозировка компонентов вакцины варьирует в зависимости от состояния, пола, возраста, массы индивидуума, пути введения и может составлять 1-100 мкг каждой VLP.
Что касается капсидного белка LI HPV56, то из уровня техники известно получение капсомеров указанного белка (US 6,165,471, 26.12.2000) рекомбинантным путем с использованием бакуловирусной системы экспрессии. Известно также включение белка LI HPV56 в состав поливалентной вакцины, направленной против папилломавирусной инфекции (US 7,709,010, 04.05.2010). VLP LI HPV экспрессировали в рекомбинантных клетках дрожжей S. cerevisiae. Выделенные и очищенные VLP адсорбировали на алюминиевом адъюванте и адъюванте ISCOM-типа.
Большая часть известных из уровня техники вакцин для профилактики папилломавирусной инфекции еще не прошла необходимые клинические испытания. В настоящее время существуют две вакцины, разрешенные к применению: квадривалентная профилактическая вакцина Гардасил производства компании Merck Sharp & Dohme B.V. и бивалентная вакцина Церварикс производства компании Glaxo SmithKline Biologicals S.A.
Гардасил (ЛС-002293, 24.11.06) - рекомбинантная квадривалентная вакцина, состоящая из вирусоподобных частиц HPV 6, 11, 16, 18 типов. VLP получены путем экспрессии вирусных капсидных белков L1 в дрожжевых клетках Saccharomyces cerevisiae, очищены и адсорбированы на алюминиевом адъюванте (аморфный гидроксифосфатсульфат алюминия). Каждая доза вакцины (0,5 мл) содержит рекомбинантные антигены: тип 6-20 мкг, тип 11-40 мкг, тип 16-40 мкг, тип 18-20 мкг, а также 225 мкг алюминиевого адъюванта и буферный раствор. Рекомендуемый курс вакцинации состоит из трех доз (0-2-6).
Церварикс (ЛСР - 006423/08, 11.08.08) - рекомбинантная бивалентная вакцина, состоящая из вирусоподобных частиц HPV 16 и 18 типов. VLP получены с использованием рекомбинантных бакуловирусов на культуре клеток Trichoplusia ni. Каждая доза вакцины (0,5 мл) содержит рекомбинантные антигены: тип 16-20 мкг, тип 18-20 мкг, МФЛ (3-0-дезацил-4-монофосфорил липид А) - 50 мкг, алюминия гидроксид - 0,5 мг.
Несмотря на то, что указанные вакцины уже используются, остается еще много неизученных вопросов, связанных с их применением. Так, не исследованы отдаленные результаты вакцинации, отсутствуют данные о корреляции образующихся антител с защитным эффектом. Отмечается также, что при вакцинации продуцируется большое число специфичных антител, однако не все антитела способны нейтрализовать вирус папилломы. К недостаткам вакцин можно отнести реактогенность, побочные явления, ограничения в применении, дороговизну.
Ближайшим аналогом является патент RU 2206608, 2003, C12N 7/00, в котором описывается способ получения вирусоподобных частиц белка L1 HPV или L2 HPV разных типов, в том числе HPV 16 и 18. Способ включает конструирование экспрессионного плазмидного дрожжевого вектора, содержащего последовательность ДНК, кодирующую соответствующий полипептид, под контролем промотора GAL10 и трансформирование им клетки Saccharomyces cerevisiae, культивирование трансформированной клетки, сбор VLP из трансформированной клетки и очистку VLP с помощью хроматографии. Способность рекомбинантных клеток S. cerevisiae экспрессировать белки L1 или L2 HPV анализировали иммуноблотингом. Для создания вакцины против папилломавирусной инфекции очищенные VLP смешивали с фармацевтически приемлемым носителем, стабилизатором или адъювантом. Вакцина содержит 0,1-100 мкг, предпочтительно 1-20 мкг активного антигена. К недостаткам использования системы экспрессии на основе Saccharomyces cerevisiae можно отнести нестабильность рекомбинантных клеток, связанную с относительно высокой частотой потерь автономной плазмиды при делении клеток. При культивировании штамма в неселективных для плазмиды условиях это приводит к накоплению клеток, не содержащих плазмиды и неспособных к синтезу целевого белка. Это существенно осложняет культивирование рекомбинантного штамма и увеличивает себестоимость целевого продукта. Для индукции экспрессии рекомбинантных белков используется достаточно дорогой реагент - галактоза, что увеличивает себестоимость целевого продукта.
Задачей изобретения является создание высокоиммуногенной, нетоксичной, не обладающей побочными эффектами рекомбинантной вакцины для профилактики папилломавирусной инфекции, содержащей в качестве антигена L1 VLP HPV типа 16 и 18, и/или 56, а также способ ее получения. Задача решена за счет создания рекомбинантных клеток дрожжей Н. Polymorpha, стабильно и эффективно продуцирующих главный капсидный белок вируса папилломы человека типа 16, 18, 56, соответственно, обладающий необходимыми биологическими свойствами (правильная конформация, иммуногенность, чистота) и низкой себестоимостью. Полученные дрожжевые рекомбинантные клетки должны обеспечивать возможность контролировать отсутствие мутаций в экспрессируемом чужеродном гене, иметь контролируемый уровень экспрессии рекомбинантного гена, чтобы обеспечить высокую эффективность укладки синтезируемого полипептида с образованием природной конформации получаемого продукта, иметь достаточно высокий выход целевого белка, обеспечивающий экономическую целесообразность использования продуцента.
Согласно изобретению, для получения рекомбинантных дрожжевых клеток, продуцирующих главный капсидный белок LI HPV16, в геном реципиентных клеток Н. polymorpha последовательно интегрируют две экспрессионные кассеты, содержащие по одной копии нужного гена. Первая кассета содержит фрагмент ДНК с рекомбинантным геном, кодирующим HPV16-L1, под контролем промотора гена МОХ (метанол оксидаза) и селективный маркер (ген TRP3 Н. polymorpha). Вторая экспрессионная кассета содержит аналогичный ген HPV16-L1, но под контролем промотора гена DAK (дигидроксиацетон киназа) дрожжей Н. polymorpha и селективный маркер (ген LEU2 S. cerevisiae). В результате трансформации получают рекомбинантные клетки, содержащие одну копию гена HPV16-L1 под контролем DAK-промотора и одну копию гена HPV16-L1 под контролем МОХ-промотора. При этом искусственные гены интегрированы непосредственно в геном рекомбинантных клеток, т.е. находятся в составе хромосом дрожжей Н. polymorpha. Это обеспечивает высокую митотическую стабильность клеток, давая возможность оптимизировать условия культивирования без учета риска накопления клеток, потерявших способность синтезировать чужеродный белок. Кроме того, наличие только одной копии рекомбинантного гена в каждой экспрессионной кассете с уникальной промоторной и терминальной областью позволяет контролировать отсутствие мутаций этого гена в процессе его введения в геном и при культивировании. Контроль за отсутствием мутаций осуществляют путем анализа нуклеотидной последовательности продуктов полимеразной цепной реакции с использованием праймеров, уникальных к специфическим последовательностям в кодирующей области каждой экспрессионной кассеты.
Преимуществом предложенного изобретения также является возможность получения стабильно высокого уровня синтеза целевого белка без нарушения эффективности его укладки. Использование экспрессионных кассет с двумя разными промоторами (МОХ и DAK), максимальная активность которых достигается при разных условиях культивирования, обеспечивает большую равномерность синтеза продукта в процессе культивирования. При этом не превышается уровень синтеза белка, который может привести к возможному нарушению эффективности укладки и, как следствие, снижению продуктивности штамма.
В качестве реципиентных дрожжевых клеток при трансформации используют клетки штамма Н. polymorpha DLT2, происходящего из DL1 (АТСС26012), или Н. polymorpha CBS4732 (АТСС34438), выделенного из почвы Бразилии. Указанные штаммы имеют независимое происхождение.
В результате отбора клонов, способных синтезировать белок HPV16-L1, были выделены трансформанты, наиболее отвечающие требуемым свойствам. Полученные рекомбинантные клетки позволяют выделять белок HPV16-L1 в виде VLP с правильной конформацией, обладающий необходимыми антигенными и иммуногенными свойствами, с достаточно высоким выходом. Образование VLP подтверждали с использованием метода гель-фильтрационной хроматографии.
Аналогичным образом были получены рекомбинантные дрожжевые клетки, продуцирующие VLP HPV18-L1, и рекомбинантные дрожжевые клетки, продуцирующие VLP HPV56-L1.
Полученные рекомбинантные дрожжевые клетки, продуцирующие главный капсидный белок разных типов HPV, культивировали раздельно в условиях, подходящих для экспрессии главного капсидного белка HPV. После выделения и очистки рекомбинантные антигены использовали в составе вакцины для профилактики папилломавирусной инфекции человека. Рекомбинантная вакцина содержит в виде VLP L1 типа 16 и 18, или L1 типа 16 и 18, и 56, или L1 типа 16 и 56 в эффективном количестве, адьювант, физиологически приемлемый разбавитель и может содержать мертиолят в качестве консерванта. Очищенные VLP адсорбировали на адъюванте (гидроокись алюминия) и смешивали в нужном соотношении, или очищенные VLP первоначально смешивали в нужном соотношении, а затем адсорбировали на адъюванте. Под эффективным количеством понимается такое количество активного начала настоящего изобретения, которое достаточно для защиты от инфекции HPV. Точное количество будет зависеть от конкретных обстоятельств и может быть оценено специалистом в данной области с использованием известных методик.
Технический результат предложенного изобретения заключается в повышении иммунногенности вакцины (улучшении биологических свойств: антигенность, иммуногенность, правильная сборка VLP), снижении себестоимости, а также в создании вакцины, направленной против распространенных на территории РФ типов HPV 16, 18, 56.
Изобретение может быть проиллюстрировано следующими примерами.
В приводимых примерах все генно-инженерные операции производили согласно стандартным методикам и инструкциям компаний производителей ферментов и наборов для манипуляций с ДНК in vitro. Трансформацию клеток Escherichia coli и Hansenula polymorpha осуществляли согласно ранее описанным методам (Inoue et al., 1990, Gene, 96:23-28 и Bogdanova et al., 1995, Yeast 11:343-353, соответственно). Синтез фрагментов ДНК, а также определение последовательности нуклеотидов производились ЗАО "Евроген", г. Москва. Были использованы синтетические фрагменты ДНК, нуклеотидные последовательности которых приведены в Списке последовательностей.
Пример 1. Получение плазмидного вектора рАМ547, содержащего рекомбинантный ген DAK-HPV16-L1 и селективный маркер ген LEU2 S. cerevisiae.
Фрагмент ДНК DAK-HPV16 (SEQ ID NO:1) и препарат плазмиды AMIpSLI (Agaphonov et al., 1999, Yeast 15:541-551), содержащей ген LEU2 S. cerevisiae в качестве дрожжевого селективного маркера, был гидролизован рестриктазами BsrGI и HindIII. Полученные препараты фрагмента ДНК с рекомбинантным геном и линеаризованной плазмиды AMIpSLI внесли в реакционную смесь для проведения лигирования в концентрации 30 нг/мкл. После инкубации с Т4 ДНК лигазой в течение 2 часов, 2 мкл реакционной смеси использовали для трансформации штамма Escherichia coli DH5α. Из нескольких выросших трансформантов выделили плазмидную ДНК. На основании рестрикционного анализа была отобрана плазмида, содержащая фрагмент DAK-HPV16. Определение последовательности нуклеотидов этой плазмиды подтвердило, что она содержит ген, кодирующий HPV16-L1 под контролем промотора DAK H. polymorpha. Полученную плазмиду обозначили рАМ547.
Пример 2. Получение плазмидного вектора рКАМ539А, содержащего рекомбинантный ген MOX-HPV16-L1 и неполный ген TRP3 H. polymorpha в качестве селективного маркера.
Фрагмент ДНК MOX-HPV16 (SEQ ID NO: 2) и препарат плазмиды pTZ-MOX (Agaphonov et al., 1995, Yeast, 11:1241-1247), содержащей неполный ген TRP3 H. polymorpha в качестве дрожжевого селективного маркера, были гидролизованы рестриктазами BglII и Xhol. Продукт гидролиза фрагмента MOX-HPV16 и продукт гидролиза плазмиды pTZ-MOX длиной 4.3 т.п.н. были выделены после электрофоретического разделения в агарозном геле. Полученные препараты ДНК внесли в реакционную смесь для проведения лигирования в концентрации 30 нг/мкл. После инкубации с ДНК лигазой Т4 в течение 2 часов 2 мкл реакционной смеси использовали для трансформации штамма Escherichia coli DH5α. Из нескольких выросших трансформантов выделили плазмидную ДНК. На основании рестрикционного анализа была отобрана плазмида, содержащая фрагмент MOX-HPV16. Определение последовательности нуклеотидов этой плазмиды подтвердило, что она содержит ген, кодирующий HPV16-L1 под контролем промотора МОХ Н. polymorpha. Полученную плазмиду обозначили рКАМ539А.
Пример 3. Получение рекомбинантных клеток Н. polymorpha, содержащих экспрессионную кассету HPV16-L1 с промотором МОХ.
Штамм Н. polymorpha DLT2 (Agaphonov et al., 1994, Yeast, v.10, pp.509-513; коллекция штаммов лаборатории молекулярной генетики РКНПК МЗ РФ) трансформировали плазмидой рКАМ539А, гидролизованной рестриктазами Ес1136П и Xhol. Трансформантов отбирали на среде, содержащей 6,7 г/л смеси солей и витаминов "Yeast Nitrogen Base" (Difco), 20 г/л D-глюкозы, 20 г/л агара и 60 мг/л лейцина. Среди полученных трансформантов были отобраны клоны, способные продуцировать HPV16-L1. Один из таких трансформантов был обозначен DLT2/pKAM539(2).
Пример 4. Получение рекомбинантных клеток Н. polymorpha, содержащих две экспрессионные кассеты HPV16-L1, одна из которых с промотором МОХ, а другая с промотором DAK.
Клетки DLT2/pKAM539(2) трансформировали плазмидой рАМ547, гидролизованной рестриктазой BsrGI. Трансформантов отбирали на среде, содержащей 6,7 г/л смеси солей и витаминов "Yeast Nitrogen Base" (Difco), 20 г/л D-глюкозы и 20 г/л агара, и подтверждали наличие интактного гена DAK-HPV16 (см. пример 5) и интактного гена MOX-HPV16 (см. пример 6).
Пример 5. Определение наличия интактного гена DAK-HPV16 в геноме трансформантов Н. polymorpha.
Из анализируемых клонов получали препараты геномной ДНК и использовали в качестве матрицы для проведения полимеразной цепной реакции (ПЦР) с олигонуклеотидами dakFwl (SEQ ID NO:3) и AMI20 (SEQ ID NO:4) в качестве праймеров. ПЦР проводили с использованием полимеразы Pfu (Fermentas). При наличии в геноме гена DAK-HPV16 образовывался продукт ПЦР длиной 1714 п.н. Для подтверждения интактности этого гена определяли последовательность нуклеотидов полученного продукта ПЦР.
Пример 6. Определение наличия интактного гена MOX-HPV16 в геноме трансформантов Н. polymorpha.
Из анализируемых клонов получали препараты геномной ДНК и использовали в качестве матрицы для проведения полимеразной цепной реакции (ПЦР) с олигонуклеотидами МОХ20 (SEQ ID NO:5) и MOX3′TRP3 (SEQ ID NO:6) в качестве праймеров. ПЦР проводили с использованием полимеразы Pfu (Fermentas). При наличии в геноме гена MOX-HPV16 образовывался продукт ПЦР длиной 1711 п.н. Для подтверждения интактности этого гена определяли последовательность нуклеотидов полученного продукта ПЦР.
Пример 7. Культивирование рекомбинантных клеток Н. polymorpha, содержащих две экспрессионные кассеты HPV16-L1, одна из которых с промотором МОХ, а другая с промотором DAK.
Ферментацию рекомбинантных клеток дрожжей Н. polymorpha осуществляли в два этапа. На первом этапе в режиме фед-бэтч при температуре 30°С наращивали биомассу в культуральной среде, содержащей 4% дрожжевого экстракта, 2% бакто-пептона и 4% глицерина. Когда плотность сырой биомассы достигала 150 г/л (примерно через 28-32 часа ферментации), добавляли индуктор до концентрации 0.5-0.8% и поддерживали на этом уровне в течение 48-72 часов.
Пример 8. Выделение и очистка рекомбинантного белка HPV16-L1 из клеток Н. polymorpha.
После ферментации рекомбинантных клеток белок HPV16-L1 (SEQ ID NO:11) выделяли согласно опубликованной методике [Kim H.J. et al., Protein Expression and Purification, v.70, p.68-74, 2010] с небольшими изменениями. Клетки из культуральной жидкости осаждали центрифугированием при 4000 g в течение 15 минут при 4°С. Осажденную биомассу ресуспендировали до концентрации 380 г влажных клеток на литр суспензии в буфере для экстракции: PBS (рН 7.2) с добавлением 1.7 mM EDTA, 2 mM PMSF, 0.01% Tween-80. Далее клетки разрушали в мельнице Dyno-МШ типа KDL, используя стеклянные шары диаметром 0.5-0.7 мм. Для удаления основной массы нецелевых белков и выделения антигена полученный экстракт насыщали сульфатом аммония до 45% от насыщения и осажденные белки отделяли центрифугированием при 12000g в течение 30 минут. Осадок разводили в минимальном объеме буфера PBS (рН 7.2)+0.01% Tween-80 и диализовали в этот же буфер в течение 24 часов при комнатной температуре для осаждения части оставшихся примесных белков, которые затем отделяли центрифугированием при 12000g в течение 30 минут. Полученный супернатант диализовали в буфер для связывания: PBS (рН 7.0), содержащий 0.33М NaCl и 0.01% Tween-80 с последующей адсорбцией на сорбент Heparin Sepharose CL-6B (GE Healthcare, USA). После промывки сорбента тем же буфером для связывания белок HPV16-L1 элюировали линейным градиентом от 0.33 до 1.5 М NaCl. Объединенные фракции, содержащие антиген (по иммуноблоту и SDS-PAGE), концентрировали ультрафильтрацией в тангенциальном потоке на мембране 500 KDa и разделяли при помощи зонального ультрацентрифугирования (Beckman Coulter, USA) в градиенте глицерин/сахароза. Фракции, содержащие целевой белок, объединяли, а затем очищали гельфильтрацией на сорбенте Toyopearl HW-65 (ToyoSoda Corp., Japan). Чистоту полученного таким образом рекомбинантного белка HPV-L1 определяли методом SDS-PAGE электрофореза. Если чистота белка была недостаточна (менее 95%), производили дополнительную очистку при помощи катионобменной хроматографии на сорбенте Toyopearl SP-650M. Выход целевого белка составлял не менее 50 мг с 1 л культуральной жидкости.
Получение рекомбинантных дрожжевых клеток Н. polymorpha, продуцирующих VLP HPV18-L1 (SEQ ID NO:12), осуществляли аналогично примерам 1-4 с использованием фрагментов ДНК DAK-HPV18 (SEQ ID NO:7) и MOX-HPV18 (SEQ ID NO:8). Наличие интактного гена DAK-HPV18 в полученных клетках подтверждали согласно примеру 5 образованием ПЦР продукта длиной 1739 п.н. Наличие интактного гена MOX-HPV18 в полученных клетках подтверждали согласно примеру 6 образованием ПЦР продукта длиной 1717 п.н.
Получение рекомбинантных клеток Н. polymorpha, продуцирующих VLP HPV56-L1 (SEQ ID NO:13), осуществляли аналогично примерам 1-4 с использованием фрагментов ДНК DAK-HPV56 (SEQ ID NO:9) и MOX-HPV56 (SEQ ID NO:10). Наличие интактного гена DAK-HPV56 в полученных клетках подтверждали согласно примеру 5 образованием ПЦР продукта длиной 1819 п.н. Наличие интактного гена MOX-HPV56 в полученных клетках подтверждали согласно примеру 6 образованием ПЦР продукта длиной 1797 п.н.
Культивирование рекомбинантных клеток, продуцирующих VLP HPV18-L1 и VLP HPV56 -L1, соответственно, осуществляли аналогично примеру 7. Выделение и очистку VLP HPV18 и VLP HPV56 осуществляли аналогично примеру 8. Выход целевых белков составляет не менее 20%.
Получение рекомбинантных клеток Н. polymorpha, продуцирующих VLP HPV16-L1, VLP HPV18-L1, VLP HPV56-L1, соответственно, с использованием в качестве реципиентных клеток дрожжевых клеток Н. polymorpha CBS4732, а также их культивирование, выделение и очистку продуцируемых рекомбинантных белков осуществляли аналогично вышеприведенным примерам.
Пример 9. Анализ рекомбинантного HPV16-L1, HPV18-L1, HPV56-L1
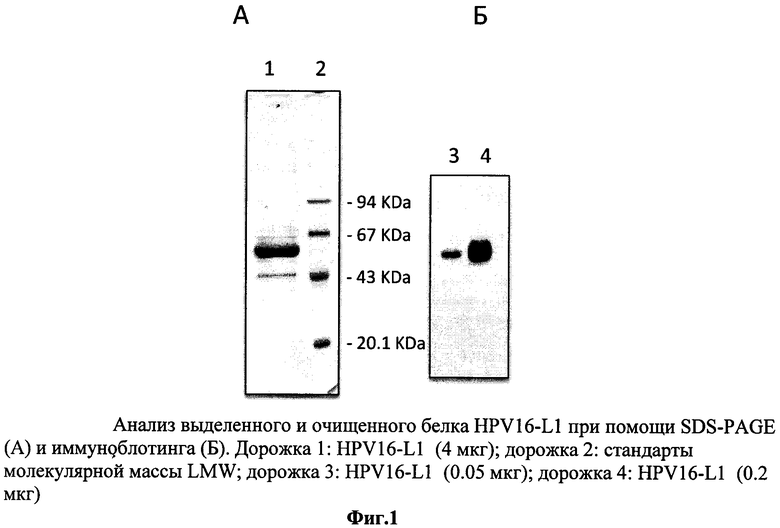
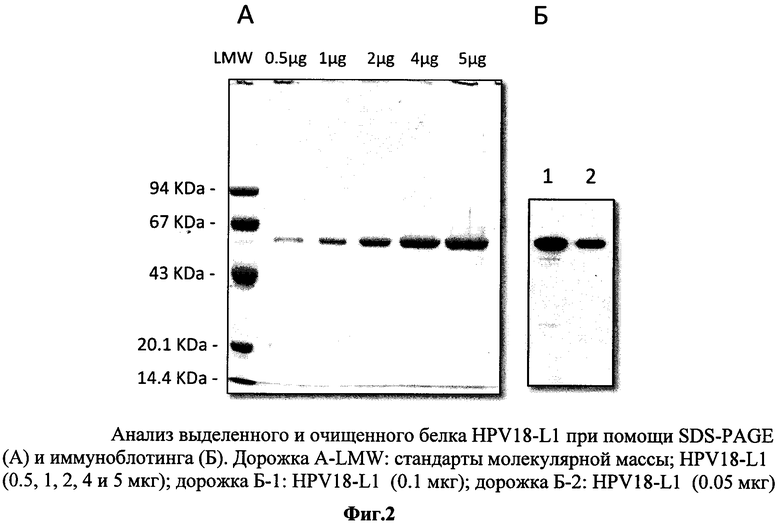
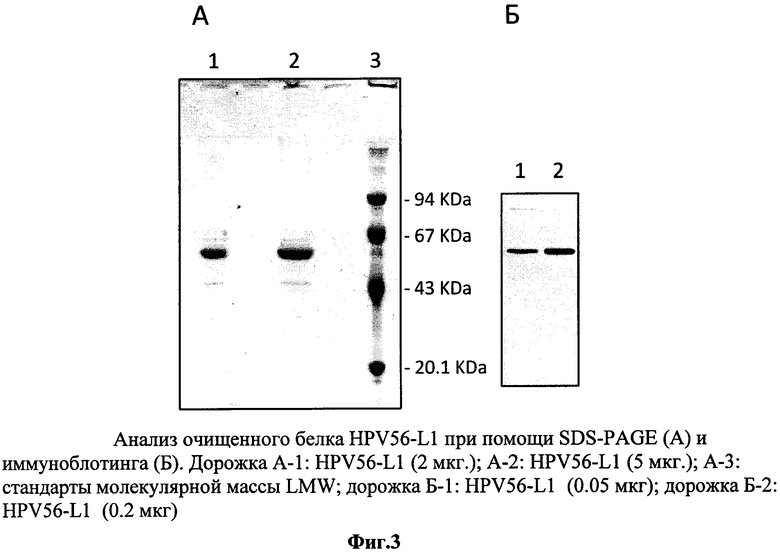
1. Чистота рекомбинантного HPV-L1 определяется электрофорезом в полиакриламидном геле в восстанавливающих условиях (SDS-PAGE) путем окрашивания с Coomassie Brilliant Blue R-250 и анализа интенсивности полос отсканированных гелей посредством компьютерной программы NIH Image. Чистота выделенных рекомбинантных белков HPV-L1 составляет не менее 95% (фиг.1А, 2А, 3А).
2. Иммуноспецифичность рекомбинантного HPV16-L1, HPV18-L1, HPV56-L1 определяют методом иммуноблотинга. Первичными моноклональными антителами к белку HPV-L1 серотипа 16, 18, 56 (Camvir-1, AbCam, UK), соответственно, окрашивают иммуноблот с последующей визуализацией при помощи специфических антител к иммуноглобулинам мыши, конъюгированными с пероксидазой хрена, по методике улучшенной хемилюминесценции ECL (Amersham, UK). Рекомбинантные антигены HPV16-L1, HPV18-L1, HPV56-L1 представлены в виде полосы мономера белка размером 55-60 кДа (фиг.1Б, 2Б, 3Б).
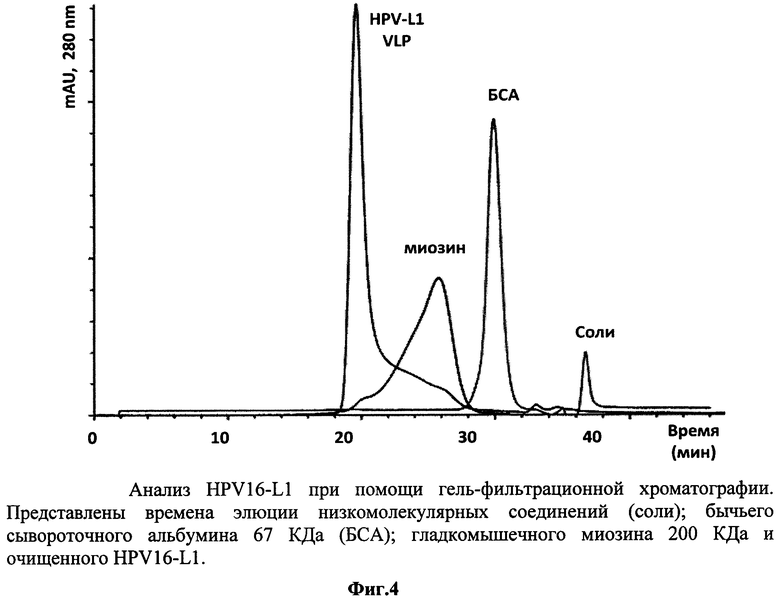
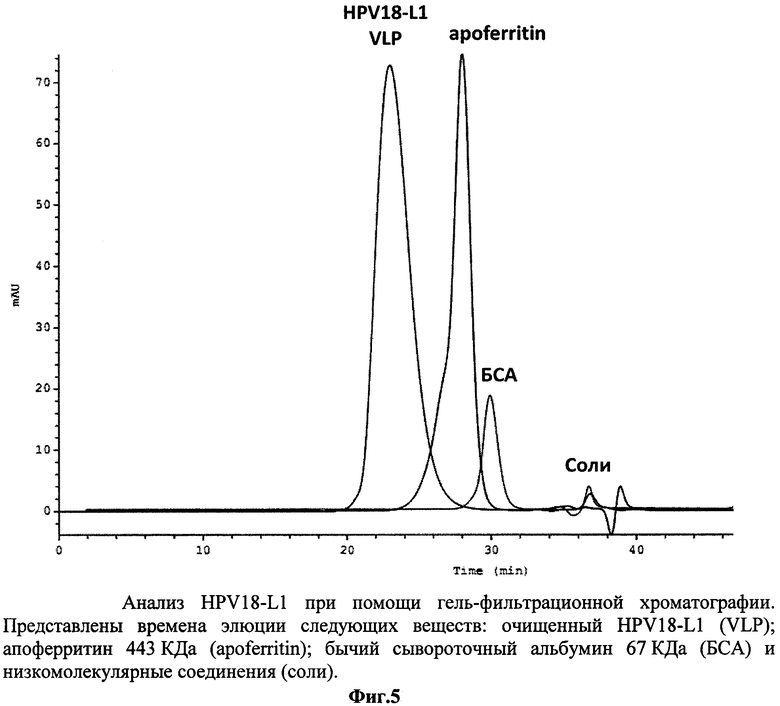
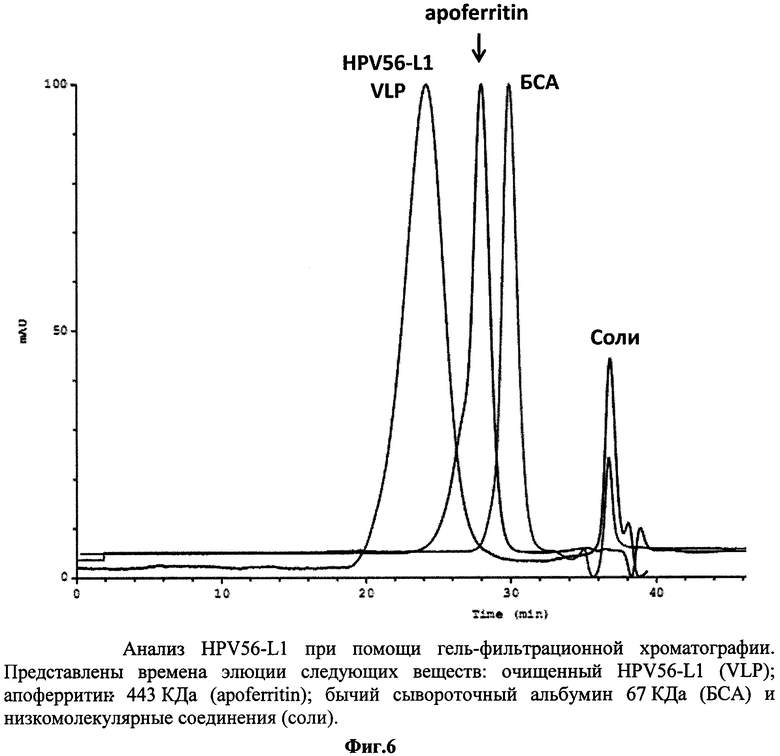
3. Образование VLP рекомбинантного белка HPV16-L1, HPV18-L1, HPV56-L1 подтверждали методом гель-фильтрационной хроматографии на полимерной колонке фирмы TosoHaas TSK G5000PW диаметром 7.5 мм и длиной 60 см, соединенной с предколонкой PrePW диаметром 7.5 мм и длиной 7.5 см. Размер пор сорбента составляет 1000 Å, что позволяет отделить правильно собранные VLP от мономеров белка L1. Разделение проводили в буфере 10 mM KH2PO4 (рН7.2), 0.03% Tween-20 при скорости потока 0.6 мл/мин. Мониторинг процесса осуществляли по поглощению на 280 нм. Время элюции белка L1 соответствует времени элюции вирусоподобных частиц (фиг.4, 5, 6).
4. Иммуногенность рекомбинантных белков определяли в тесте на мышах линии Balb/c с массой 12-14 г после однократной вакцинации белком, сорбированным на гидроокиси алюминия. Значение ED/50 (доза антигена, вызывающая сероконверсию у 50% мышей), рекомбинантного HPV16-L1, HPV18-L1, HPV56-L1 составляет не более 100 нг, что является хорошим показателем иммуногенных свойств рекомбинантного белка.
Культурально-морфологические особенности рекомбинантных клеток H. polymorpha: клетки округлой формы, небольшие по размеру, на агаризованной среде YPD образуют крупные круглые колонии с выраженной выпуклой серединой.
Хранение - при -70°С в виде суспензии клеток в стерильном 30-50%-ном растворе глицерина.
Генетические особенности: рекомбинантные клетки не являются зоопатогенными или фитопатогенными.
Способ, условия и состав сред для размножения рекомбинантных клеток: инкубирование прокачиванием при 30°С в питательной среде состава: 2% пептона, 1% дрожжевого экстракта, 2% глюкозы.
Условия и состав среды для ферментации: прокачивание при 30°С и рН 5,0-5,5 в питательной среде, содержащей до 4% глицерина.
Способ определения активности: в осветленном гомогенизате клеток методом иммуноблотинга или иммуноферментного анализа. Активность рекомбинантных клеток, продуцирующих VLP HPV16-L1 и HPV18-L1, - не менее 50 мг/л культуральной жидкости и не менее 15 мг/л для продуцента VLP HPV56-L1.
Выделенные и очищенные VLP HPV16-L1, HPV18-L1, HPV56-L1 используют для создания на их основе вакцины для профилактики папилломавирусной инфекции.
Полученные вакцинные композиции представлены в следующих вариантах:
1) Вакцина содержит VLP HPV16-L1, HPV18-L1, адъювант и физиологически приемлемый разбавитель;
2) Вакцина содержит VLP HPV16-L1, HPV56-L1, адъювант и физиологически приемлемый разбавитель;
3) Вакцина содержит VLP HPV16-L1, HPV18-L1, HPV56-L1 адъювант и физиологически приемлемый разбавитель;
4) Вакцина вариантов 1, 2, 3 дополнительно содержит консервант - мертиолят.
Конкретные примеры композиций вакцин для профилактики папилломавирусной инфекции:
1. Вакцина для профилактики папилломавирусной инфекции содержит:
20 мкг VLP HPV16-L1, полученного путем культивирования рекомбинантных клеток дрожжей H. polymorpha,
20 мкг VLP HPV18-L1, полученного путем культивирования рекомбинантных клеток дрожжей H. polymorpha,
0.5 мг геля гидроокиси алюминия,
до 0.5 мл фосфатно-солевого буфера (ФСБ), представленного 50 mM Na-фосфатного буфера, рН 6.8 и 0.13 М NaCl.
2. Вакцина для профилактики папилломавирусной инфекции содержит:
20 мкг VLP HPV16-L1, полученного путем культивирования рекомбинантных клеток дрожжей H. polymorpha,
20 мкг VLP HPV56-L1, полученного путем культивирования рекомбинантных клеток дрожжей H. polymorpha, 0.5 мг геля гидроокиси алюминия,
до 0.5 мл фосфатно-солевого буфера (ФСБ), представленного 50 mM Na-фосфатного буфера, рН 6.8 и 0.13 М NaCl.
3. Вакцина для профилактики папилломавирусной инфекции содержит:
20 мкг VLP HPV16-L1, полученного путем культивирования рекомбинантных клеток дрожжей H. polymorpha,
20 мкг VLP HPV18-L1, полученного путем культивирования рекомбинантных клеток дрожжей H. polymorpha,
20 мкг VLP HPV56-L1, полученного путем культивирования рекомбинантных клеток дрожжей H. polymorpha,
0.75 мг геля гидроокиси алюминия,
до 0.5 мл фосфатно-солевого буфера (ФСБ), представленного 50 mM Na-фосфатного буфера, рН 6.8 и 0.13 М NaCl.
4. Вакцина для профилактики папилломавирусной инфекции содержит:
20 мкг VLP HPV16-L1, полученного путем культивирования рекомбинантных клеток дрожжей H.polymorpha,
20 мкг VLP HPV18-L1, полученного путем культивирования рекомбинантных клеток дрожжей H.polymorpha,
20 мкг VLP HPV56-L1, полученного путем культивирования рекомбинантных клеток дрожжей H.polymorpha,
60 мкг мертиолята, 0.75 мг геля гидроокиси алюминия,
до 0.5 мл фосфатно-солевого буфера (ФСБ), представленного 50 mM Na-фосфатного буфера, рН 6.8 и 0.13 М NaCl.
Согласно изобретению вакцины для профилактики папилломавирусной инфекции можно получать как с введением в их состав консерванта - мертиолята, так и без него. Отсутствие в вакцине консерванта не сказывается на ее качестве.
Иммуногенность рекомбинантных вакцин, определенная в тесте на мышах линии Balb/c с массой 12-14 г в расчете на ED/50 (доза антигена, вызывающая сероконверсию у 50% мышей), составляет не более 100 нг.
Для сравнения была определена иммуногенность квадривалентной вакцины Гардасил (коммерчески доступная вакцина). Полученные данные показали, что относительная потенция (отношение дозы, выраженной в ED/50, аналога к ED/50 испытуемой вакцины) вакцины по изобретению в сравнении с аналогом составляет не менее 1.0.
Токсичность вакцины определяли путем введения белым мышам 0.5 мл (60 мкг) вакцины внутрибрюшинно и 0.5 мл (60 мкг) вакцины морским свинкам подкожно. Наблюдение в течение 7 суток показало, что вакцина не токсична.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения рекомбинантной вакцины для профилактики папилломавирусной инфекции человека, рекомбинантная вакцина | 2018 |
|
RU2681174C1 |
| РЕКОМБИНАНТНЫЙ ШТАММ ДРОЖЖЕЙ Hansenula polymorpha - ПРОДУЦЕНТ ГЛАВНОГО КАПСИДНОГО БЕЛКА L1 ВИРУСА ПАПИЛЛОМЫ ЧЕЛОВЕКА ТИПА 56 | 2014 |
|
RU2546240C1 |
| РЕКОМБИНАНТНЫЙ ШТАММ ДРОЖЖЕЙ Hansenula polymorpha - ПРОДУЦЕНТ ГЛАВНОГО КАПСИДНОГО БЕЛКА L1 ВИРУСА ПАПИЛЛОМЫ ЧЕЛОВЕКА ТИПА 18 | 2014 |
|
RU2546242C1 |
| РЕКОМБИНАНТНЫЙ ШТАММ ДРОЖЖЕЙ Hansenula polymorpha - ПРОДУЦЕНТ ГЛАВНОГО КАПСИДНОГО БЕЛКА L1 ВИРУСА ПАПИЛЛОМЫ ЧЕЛОВЕКА ТИПА 16 | 2014 |
|
RU2546241C1 |
| Рекомбинантный штамм дрожжей Hansenula polymorpha - продуцент главного капсидного белка L1 вируса папилломы человека типа 11 | 2018 |
|
RU2676160C1 |
| Рекомбинантный штамм дрожжей Hansenula polymorpha - продуцент главного капсидного белка L1 вируса папилломы человека типа 6 | 2018 |
|
RU2675471C1 |
| РЕКОМБИНАНТНЫЙ ШТАММ ДРОЖЖЕЙ PICHIA ANGUSTA - ПРОДУЦЕНТ КАПСИДНОГО БЕЛКА L1 ВИРУСА ПАПИЛЛОМЫ ЧЕЛОВЕКА ТИПА 18 | 2011 |
|
RU2445358C1 |
| РЕКОМБИНАНТНЫЙ ШТАММ ДРОЖЖЕЙ PICHIA ANGUSTA - ПРОДУЦЕНТ КАПСИДНОГО БЕЛКА L1 ВИРУСА ПАПИЛЛОМЫ ЧЕЛОВЕКА ТИПА 16 | 2011 |
|
RU2445357C1 |
| ОПТИМИЗИРОВАННАЯ ЭКСПРЕССИЯ HPV 58 L1 В ДРОЖЖАХ | 2004 |
|
RU2370538C2 |
| ОПТИМИЗИРОВАННАЯ ЭКСПРЕССИЯ HPV 52 L1 В ДРОЖЖАХ | 2005 |
|
RU2373219C2 |



Изобретения относятся к биотехнологии, а именно генной инженерии. Предложена рекомбинантная вакцина для профилактики папилломавирусной инфекции человека и способ ее получения. Вакцина создана на основе VLP главного капсидного белка LI HPV типов 16, 18, 56, полученных путем культивирования рекомбинантных клеток дрожжей Hansenula polymorpha. Рекомбинантные клетки были получены путем введения в геном клетки дрожжей одной копии последовательности ДНК, кодирующей капсидный белок L1 HPV типа 16, или 18, или 56 под контролем промотора ДАК и одной копии последовательности ДНК, кодирующей капсидный белок L1 HPV типа 16, или 18, или 56, под контролем промотора МОХ. Вакцина содержит эффективное количество VLP HPV16-L1, и HPV18-L1, и/или HPV56-L1, в равных долях, адъювант и физиологически приемлемый разбавитель. Предложенный способ позволяет получать высокоиммуногенную, нетоксичную, не обладающую побочными эффектами вакцину. 2 н. и 2 з.п. ф-лы, 6 ил., 9 пр.
1. Рекомбинантная вакцина для профилактики папилломавирусной инфекции человека, содержащая эффективное количество антигена HPV, адъювант и физиологически приемлемый разбавитель, отличающаяся тем, что в качестве антигена HPV рекомбинантная вакцина содержит в равных долях смесь VLP HPV16-L1, полученной путем культивирования клетки дрожжей Hansenula polymorpha, содержащей интегрированный в геном фрагмент ДНК, кодирующий HPV16-L1, под контролем промотора гена DAK (SEQ ID NO:1), и фрагмент ДНК, кодирующий HPV16-L1, под контролем промотора МОХ (SEQ ID NO:2), и VLP HPV18-L1, полученной путем культивирования клетки дрожжей Hansenula polymorpha, содержащей интегрированный в геном фрагмент ДНК, кодирующий HPV18-L1, под контролем промотора гена DAK (SEQ ID NO:7), и фрагмент ДНК, кодирующий HPV18-L1, под контролем промотора МОХ (SEQ ID NO:8), и/или VLP HPV56-L1, полученной путем культивирования клетки дрожжей Hansenula polymorpha, содержащей интегрированный в геном фрагмент ДНК, кодирующий HPV56-L1, под контролем промотора гена DAK (SEQ ID NO:9), и фрагмент ДНК, кодирующий HPV56-L1, под контролем промотора МОХ (SEQ ID NO:10).
2. Рекомбинантная вакцина для профилактики папилломавирусной инфекции по п. 1, отличающаяся тем, что дополнительно содержит мертиолят.
3. Способ получения вакцины для профилактики папилломавирусной инфекции человека, включающий трансформацию дрожжевой клетки молекулой ДНК, кодирующей L1 HPV, раздельное культивирование полученных рекомбинантных клеток, продуцирующих VLP HPV-L1 разных типов, в подходящих условиях, выделение и очистку VLP HPV-L1, смешивание эффективного количества VLP HPV-L1 разных типов с адъювантом и физиологически приемлемым разбавителем и получение целевого продукта, отличающийся тем, что дрожжевую клетку Hansenula polymorpha трансформируют последовательно экспрессионной кассетой, содержащей фрагмент ДНК, кодирующий HPV16-L1, под контролем промотора гена МОХ (SEQ ID NO:2) и неполный ген TRP3 Н. polymorpha, и экспрессионной кассетой, содержащей фрагмент ДНК, кодирующий HPV16-L1, под контролем промотора гена DAK (SEQ ID NO:1) и селективный маркер ген LEU2 S. cerevisiae, выделяют и очищают VLP HPV16-L1, дрожжевую клетку Hansenula polymorpha трансформируют последовательно экспрессионной кассетой, содержащей фрагмент ДНК, кодирующий HPV18-L1, под контролем промотора гена МОХ (SEQ ID NO:8) и неполный ген TRP3 Н. polymorpha, и экспрессионной кассетой, содержащей фрагмент ДНК, кодирующий HPV18-L1, под контролем промотора гена DAK (SEQ ID NO:7) и селективный маркер ген LEU2 S. cerevisiae, выделяют и очищают VLP HPV18-L1, дрожжевую клетку Hansenula polymorpha трансформируют последовательно экспрессионной кассетой, содержащей фрагмент ДНК, кодирующий HPV56-L1, под контролем промотора гена МОХ (SEQ ID NO:10) и неполный ген TRP3 Н. Polymorpha, и экспрессионной кассетой, содержащей фрагмент ДНК, кодирующий HPV56-L1, под контролем промотора DAK (SEQ ID NO:9) и селективный маркер ген LEU2 S. cerevisiae, выделяют и очищают VLP HPV56-L1, при этом выделенные и очищенные VLP HPV16-L1 и VLP HPV18-L1, и/или VLP HPV56-L1 смешивают в равных долях.
4. Способ по п. 3, отличающийся тем, что дополнительно добавляют мертиолят.
| ПАПИЛЛОМАВИРУСНЫЕ ВАКЦИНЫ | 1995 |
|
RU2206608C2 |
| МОЛЕКУЛА НУКЛЕИНОВОЙ КИСЛОТЫ, КОДИРУЮЩАЯ HPV31 L1, ЭКСПРЕССИРУЮЩИЙ ВЕКТОР, КЛЕТКА-ХОЗЯИН, ВИРУСОПОДОБНАЯ ЧАСТИЦА И СПОСОБ ЕЕ ПОЛУЧЕНИЯ, ВАКЦИНА, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ И СПОСОБЫ С ИХ ИСПОЛЬЗОВАНИЕМ | 2004 |
|
RU2356943C2 |
| WO 2011077371 A1, 30.06.2011 | |||
| US 20080248062 A1, 09.10.2008 | |||
Авторы
Даты
2015-04-10—Публикация
2014-02-13—Подача