Область техники, к которой относится изобретение
Данное изобретение относится к иммунологии, биотехнологии и медицине, а именно к области противоопухолевых лекарственных препаратов на основе моноклональных антител, и может быть использовано в медицине для лечения онкологических заболеваний.
Предшествующий уровень техники
Онкологические заболевания стоят на втором месте по смертности в мире после сердечно-сосудистых заболеваний [1]. За последние 10 лет число заболевших онкологическими заболеваниями, по разным данным, возросло на 15%. Ежегодно в России регистрируется более 490 тысяч новых пациентов, 2,5 миллиона находятся под наблюдением и более 290 тысяч больных ежегодно умирает от различных форм рака. Ввиду этого целесообразны разработка и создание безопасных, эффективных и доступных противоопухолевых препаратов.
Одним из типов противоопухолевых препаратов являются продукты биотехнологического синтеза - моноклональные антитела (Mab). Известен ряд фармакологических решений, в их числе Mab к рецептору эпидермального фактора роста, вазоэндотелиальному фактору роста, которые имеют доказанное значение для жизнедеятельности опухолевых клеток и малозначимы для функционирования нормальных клеток различных тканей организма [2].
В настоящее время в мире зарегистрировано и производится около десяти противоопухолевых препаратов на основе моноклональных антител, в частности Ритуксимаб (Mab к рецептору CD20), Трастузумаб (мишенью является рецептор HER2neu), Бевацизумаб (VEGF), Цетуксимаб и Панитумумаб (EGFR). Зарегистрированных препаратов, мишенью которых является поверхностный антиген синдекан-1 (CD138), в настоящее время не существует.
Белок синдекан-1 (CD138) [4] является перспективной мишенью противоопухолевой терапии моноклональными антителами: доказана важная роль данной молекулы в жизнедеятельности опухолевых клеток и показана ее малая значимость для функционирования нормальных клеток различных тканей организма [5].
Данная молекула обеспечивает межклеточные взаимодействия и взаимодействия между клетками и матриксом, адгезию и миграцию. Гиперэкспрессия CD138 была продемонстрирована в большинстве (около 90%) клеток различных опухолей, включая рак молочной железы, толстой кишки и желудка, предстательной железы и других эпителиальных злокачественных опухолей [6, 7]. Также описано такое явление, как потеря синдекана-1 с поверхности миеломных клеток с накоплением его в строме, как правило, в участках фиброза [8]. Показано, что при потере синдекана-1 миеломные клетки вступают в TRAIL - индуцированный апоптоз [9]. Функционально Синдекан-1 связан со способностью опухолевых клеток к инвазивному росту и метастазированию. В аспекте лечения злокачественных опухолей активность CD138 сопряжена с теми свойствами опухолевых клеток, которые практически не поддаются существующей терапии.
Показана локализация CD138 на поверхности опухолевых клеток в форме, доступной для узнавания антителами [10]. Более того, имеются данные об эффективности вакцинации с использованием в качестве антигена CD138 [11].
Известны мышиные антитела к синдекану-1 - В-В4 (IgG1) [13], В-В2 (IgG2b), а также химерные [8, 14] - МП5 (IgG1κ) и конъюгаты таковых с метками [12] [3]. Такие соединения используют в исследовательских или диагностических целях, причем антитело выполняет лишь функцию нацеливания [8, 14]. Цитотоксическую функцию выполняют эффекторные молекулы, как правило, конъюгированные с антителом [16, 17, 18]. Мышиные и кроличьи Mab иммунная система человека воспринимает как чужеродные, за счет различий в константной части антител (СН, CL), и запускает против них иммунный ответ. Для применения у людей разрабатывают химерные антитела, константная часть которых - человека, а вариабельная (VH, VL) - мыши. С использованием данной модификации удается получить более безопасные Mab.
Известно рекомбинантное антитело к синдекану-1 (OC-46F2), созданное в результате in vitro селекции библиотеки для фагового дисплея (ETH-2-Gold) человеческих антител на клетках меланомы человека и дальнейшей экспрессии полученных генов в клетках млекопитающих [26]. Показано, что данное антитело ингибирует созревание сосудов и опухолевый рост в экспериментальной модели человеческой меланомы (на мышах), а также эффективно в терапевтическом плане в отношении экспериментальной модели человеческой карциномы рака яичника.
OC-46F2 представляет собой одноцепочечный вариабельный фрагмент (scFv) - гибридный белок из вариабельных фрагментов тяжелой (VH) и легкой (VL - лямбда) цепи иммуноглобулинов, соединенных коротким линкерным пептидом.
Данное соединение не содержит константные фрагменты антитела, вариабельные фрагменты молекулы обеспечивают только связывание с антигеном, что обуславливает показанное авторами сдерживающее действие. Однако для элиминации опухоли необходимо использование дополнительных действующих веществ, возможно, создание конъюгатов. Наблюдаем тот же недостаток, что и при использовании химерного антитела.
Прототипом предлагаемого изобретения является химерное моноклональное антитело к CD138 подкласса IgG4 [15]. Однако данное Mab обеспечивает лишь нацеливание цитотоксического агента, конъюгированного с ним (DM4).
Таким образом, описанные на сегодняшний день мышиные антитела к CD138 непригодны для применения у людей ввиду высокой иммуногенности, их используют для лабораторных целей, химерные MAb не обладают самостоятельным терапевтическим действием - их используют только в качестве нацеливающего агента, а также могут быть иммуногенны. Нельзя исключать и индивидуальную реакцию пациента на то или иное Mab. Кроме того, действующий агент, который нацеливают с использованием антитела, или продукты его распада, могут являться стрессорным фактором для организма, ввиду их структуры, возможности и периода распада данного вещества, характера соединений, на которое он распадается. Точная структура природных моноклональных антител человека к синдекану-1 не установлена.
Учитывая функциональную роль синдекана-1 в инвазивном росте и метастазировании опухолей, создание антител к нему, обладающих самостоятельной высокой цитотоксичностью, наряду с более высокой аффинностью и более низкой иммуногенностью, является актуальной задачей.
Данная задача решена предложенным изобретением.
Технический результат от использования предлагаемого антитела к CD138 выражается, как минимум, в увеличении спектра MAb к CD138, используемых в терапии опухолевых заболеваний, что позволяет проводить им лечение при индивидуальной непереносимости или плохой переносимости аналогов.
Технический результат от использования предлагаемого антитела к CD138 выражается в увеличении аффинности к антигену, и, соответственно, эффективности антитела. Указанный технический результат достигается гуманизацией антитела: использование каркасных участков человеческого антитела позволяет более точно сориентировать гипервариабельные участки, что увеличивает соответствие эпитопа и паратопа и, соответственно, аффинность.
Технический результат от использования предлагаемого антитела к CD138 также выражается в индукции цитотоксичности. Указанный технический результат достигается тем, что в константный фрагмент тяжелой цепи антитела типа IgG4 введены участки цепей IgG3, опосредующие антитело- и комплемент-зависимую цитотоксичность.
Технический результат от использования предлагаемого антитела к CD138 также выражается в уменьшении иммуногенности за счет гуманизации антитела.
Технический результат от использования предлагаемого антитела к CD138 также выражается в уменьшении стрессорного воздействия на организм противоопухолевого препарата, за счет того что действующим веществом является сама молекула моноклонального антитела - по природе белок, который впоследствии деградирует до аминокислот, т.е. при его использовании исключаются какие-либо последствия возможного невыведения из организма в течение какого-либо времени действующего агента (химического вещества небелковой природы), либо продуктов его распада.
Технический результат от использования предлагаемого антитела к CD138 также выражается в увеличении срока полужизни антитела, что достигается введением аминокислотных замен на С-конце константной части тяжелой цепи. Это позволяет уменьшать дозировки, осуществлять меньшее количество введений антитела, что может снизить стоимость лечения.
Также техническим результатом является получение высокого уровня экспрессии антитела в клетках млекопитающих за короткий срок за счет кодонной оптимизации кодирующих последовательностей, а также введенной сигнальной секреторной последовательности на N-конце тяжелой и легкой цепи, что позволяет удешевить и ускорить производство.
Сущность изобретения
Задачей данного изобретения являлось создание универсального моноклонального антитела - к CD138, приемлемого для терапии опухолевых заболеваний, обладающего высокой аффинностью к антигену (к CD138), низкой иммуногенностью и высокой цитотоксичностью, а также длительным периодом полужизни, которое можно получать в больших количествах за короткий промежуток времени.
Данная задача решена тем, что предложено моноклональное гуманизированное антитело к синдекану-1 (CD138), на основе IgG4, с введенными в CH фрагмент антитела участками IgG3, обуславливающими формирование антитело-зависимой и комплемент-зависимой цитотоксичности, с введенной сигнальной секреторной последовательностью на N-конце тяжелой и легкой цепи, отщепляющейся после секреции белков из клеток-продуцентов, а также аминокислотными заменами, увеличивающими период полужизни данного антитела; имеющее последовательность тяжелой цепи SEQ ID ΝΟ:1 и легкой цепи SEQ ID NO:2, закодированную в нуклеотидных последовательностях SEQ ID NO:3 и SEQ ID NO:4, кодонно оптимизированных для увеличенной экспрессии в клетках млекопитающих (СНО).
Предложенное гуманизированное антитело к CD138 высокоаффинно связывается с гиперэкспрессированным на опухолевых клетках синдеканом-1 за счет гуманизации вариабельных фрагментов. Гипервариабельные участки полученных самостоятельно в результате иммунизации синдеканом-1 моноклональных антител мыши перенесены в наиболее структурно гомологичные по ключевым позициям акцепторные антитела человека, каркасные участки которых позволяют более точно сориентировать гипервариабельные участки в пространстве, что увеличивает соответствие эпитопа и паратопа и, соответственно, обеспечивает более высокую по сравнению с химерными антителами аффинность к мишени. На N-конце тяжелой и легкой цепей введена сигнальная секреторная последовательность, отщепляющаяся после секреции белков из клеток-продуцентов.
Конструкция предлагаемого антитела способна обеспечить его самостоятельный цитотоксический эффект по антитело-зависимому и комплемент-зависимому механизмам за счет оптимизации последовательности константного фрагмента (IgG4-IgG3 shifting), что обеспечивает привлечение клеток иммунной системы. Это позволяет отказаться от использования цитотоксического агента, т.е. от процедур выбора характера его использования в совокупности с Mab (присоединения или совместного использования), процедуры его конъюгации с антителом, поддержания активности обоих компонентов и других вытекающих последствий.
Антитела IgG4 не активируют комплемент, в то время как IgG3 способны активировать каскад протеолитических реакций, осуществляемых системой комплемента.
Предложенное моноклональное антитело к синдекану-1 (CD138) содержит участки IgG3 - введены аминокислотные замены в тяжелой цепи, что обеспечивает индукцию антитело-зависимой и комплемент-зависимой цитотоксичности, а также аминокислотные замены для увеличения периода полужизни антитела на С-конце константной части тяжелой цепи.
Кодонная оптимизация нуклеотидных последовательностей (SEQ ID NO:3, SEQ ID NO:4), кодирующих антитело согласно изобретению (тяжелые и легкие цепи), наряду с введением сигнальной секреторной последовательности, позволила получить до 2 грамм целевого белка на литр при трех днях культивирования клеток млекопитающих - продуцентов(СНО).
Полученное гуманизированное моноклональное антитело характеризуется значением Kd: 8,0*10-9.
Для испытания моноклонального антитела использовали мышей BALB/C Nude, у которых аллергическая реакция может быть более выражена, чем у стандартных лабораторных мышей. Однако аллергическая реакция не наблюдалась, что позволяет предполагать, что разработанный препарат будет достаточно безопасен с точки зрения побочных аллергических эффектов.
Результаты испытания препарата на моделях in vivo показали, что у лабораторных животных наблюдался регресс опухоли, отсутствие метастазирования; животные, получавшие препарат, имели большую продолжительность жизни.
Результаты данных испытаний препарата можно интерпретировать как предварительные данные по токсичности.
Способность индукции антипролиферативной и противометастазной активности показана на клетках линии А431.
Таким образом, предложенное гуманизированное антитело к CD138 обладает противоопухолевым эффектом за счет блокирования опосредованных синдеканом-1 функций (адгезия, миграция опухолевых клеток) и индукции цитотоксического иммунного ответа, т.е. не только сдерживает рост опухоли и миграцию клеток, но и способствует их элиминации естественным путем.
Таким образом, появляется возможность не только диагностики, но и терапии онкологических заболеваний моноклональным антителом к CD138, заявленным в изобретении за счет индукции антитело- и комплемент-зависимой цитотоксичности в отношении опухолей, в которых гиперэкспрессирован синдекан-1, благодаря внесению соответствующих аминокислотных замен в константные участки антитела человека (IgG4-IgG3 shifting). При использовании данного изобретения достигается высокая эффективность терапии, за счет увеличения аффинности антиген-связывающего участка моноклонального антитела к синдекану-1. За счет внесения соответствующих аминокислотных замен увеличено также время полужизни антитела после введения в организм пациента. Кодонная оптимизация тяжелой и легкой цепей, а также введение сигнальной секреторной последовательности на N-конце тяжелой и легкой цепей позволяет получать антитело в больших количествах за малые сроки в клетках млекопитающих.
Предлагаемое Mab является безопасным для человека с точки зрения побочных аллергических эффектов благодаря гуманизации.
Краткое описание графических материалов
Фигура 1. Электрофореграмма, показывающая экспрессию гена, кодирующего синдекан-1, в используемой клеточной линии миеломы SP 2.0
1) контроль качества синтеза кДНК, результат проведения ПЦР с праймерами KG3PDH;
2) положительный контроль, ПЦР с праймерами, специфическими к последовательности ДНК, кодирующей CD138, с использованием в качестве матрицы плазмидной ДНК, содержащей клонированный ген синдекана-1;
3) ПЦР на кДНК из клеток миеломы с использованием праймеров, специфических к ДНК, кодирующей синдекан-1;
4) контроль экспрессии - ПЦР с использованием праймеров, специфических к ДНК, кодирующей синдекан-1, на тотальной РНК из клеток миеломы;
5) маркер молекулярного веса 1 кb DNA Ladder (Fermentas).
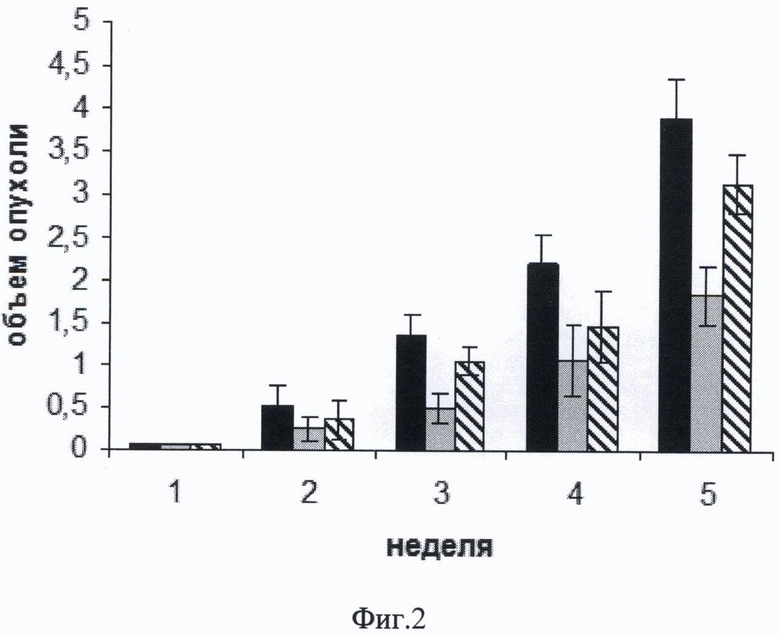
Фигура 2. Динамика развития миеломы SP 2.0 в мышах BALB/C в трех группах животных. Черный столбик - показатели контрольной группы, серый - группы мышей, которым вводили 1 мг препарата гуманизированного моноклонального антитела, заштрихованный - группы мышей, которым вводили 0,1 мг препарата гуманизированного моноклонального антитела.
ПРИМЕРЫ ОСУЩЕСТВЛЕНИЯ ИЗОБРЕТЕНИЯ
Пример 1. Получение моноклонального гуманизированного антитела к синдекану-1.
1.1. Получение синдекана-1
Ген, кодирующий синдекан-1, был синтезирован посредством химико-ферментативного синтеза [20] соответствующего гена двуступенчатым методом. Полученный ген был клонирован в векторе pET151/D-TOPO, обеспечивающем высокий уровень синтеза рекомбинантного белка, сшитого с полигистидиновой последовательностью, для удобства дальнейшей очистки с помощью металлохелатной хроматографии, в результате которой можно получить белок в виде отдельной аминокислотной последовательности, без полигистидина и каких-либо других примесей, благодаря наличию сайта для TEV-протеазы, в клетках E.coli BL21(DE3)Star, которые содержат мутированный ген rne (rne131), кодирующий усеченную форму РНКазы Е, что уменьшает внутриклеточное разрушение мРНК, приводя к увеличению ее ферментативной стабильности и, соответственно, продукции белка. Получили экспрессию данного гена в клетках E.coli BL21(DE3)Star.
Рекомбинантный белок выделяли из клеток штамма BL21[DE3]Star pET151sind-1, растворив клетки в лизирующем буфере. Проводили очистку синдекана-1 с помощью металлохелатной хроматографии.
Препарат рекомбинантного белка имел чистоту 95-97% и был использован для получения гибридомы, продуцирующей моноклональные антитела мыши к синдекану-1 и тестирования полученных моноклональных антител.
1.2. Иммунизация мышей линии Balb/c синдеканом-1
Была проведена иммунизация мышей линии Balb/c, в качестве антигена использовали очищенный рекомбинантный белок синдекан-1. При первичной иммунизации мышам вводили подкожно 50 мкг антигена в полном адъюванте Фрейнда (ПАФ). Через 28 дней анализировали уровень иммунного ответа на введенный антиген, оценивая титр специфических сывороточных антител с помощью иммунноферментного анализа (ИФА). Животным с максимальным значением иммунного ответа повторно вводили подкожно 30 мкг антигена в неполном адъюванте Фрейнда (НАФ) и оценивали уровень вторичного иммунного ответа через 21 день, затем за 4-5 дней до проведения соматической гибридизации вводили 30 мкг антигена в физиологическом растворе (ФР) внутрибрюшинно.
1.3. Получение гибридомы, синтезирующей моноклональные антитела, специфичные к синдекану-1
В качестве партнеров по слиянию использовали спленоциты иммунизированных мышей с титром сывороточных антител к белку синдекан-1 примерно 1:30000 и клетки мышиной миеломы sp2/0-Ag14 (АТСС, CRL-1581) в соотношении 2:1. Гибридизацию проводили с использованием раствора полиэтиленгликоля (Sigma) в соответствии со стандартной методикой. Селекцию стабильных гибридных клеток проводили путем культивирования на среде IMDM (Iscove-s Modified Dulbecco Medium, Sigma), содержащей 10% сыворотки FCI (HyClone) и HAT (Gibco). Отбор клонов гибридных клеток, секретирующих антитела, специфичные к заданным антигенам, проводили с помощью иммуноферментного анализа (ИФА). В результате первичного скрининга было отобрано 10 клонов гибридных клеток, продуцирующих моноклональные антитела к синдекану-1. После проведения пяти клонирований было получено 4 стабильных продуцирующих клона. Из каждой из клеточных линий была выделена мРНК, кодирующая тяжелые и легкие цепи антитела к синдекану-1.
1.4. Получение нуклеотидных последовательностей тяжелых и легких цепей гуманизированного антитела к синдекану-1
Из стабильных клонов гибридных клеток, продуцирующих мышиные моноклональные антитела к синдекану-1, была выделена РНК с использованием набора «TRI Reagent» производства фирмы «Sigma», США, по инструкции изготовителя. На 5-10х106 клеток использовали 1 мл лизирующего раствора «TRI Reagent». Синтез кДНК проводили с помощью набора Revert Aid® First Strand cDNA Synthesis Kit (производства фирмы «Fermentas», Литва).
Амплификацию генов, кодирующих вариабельные фрагменты мышиных антител, проводили методом ПЦР с использованием специфических праймеров (5' вырожденных праймеров для отжига на неизвестных VH и VL участках) и в качестве матрицы синтезированной кДНК. Наработку фрагментов ДНК для клонирования проводили методом ПЦР с использованием высокоточной, термоустойчивой ДНК-полимеразы Pfx. Полученные ПЦР-продукты были клонированы в векторе pGMT-easy с использованием набора Fast Ligation Kit, Fermentas и секвенированы ферментативным методом по Сенгеру.
Результаты секвенирования были использованы для получения гуманизированного моноклонального антитела.
Гуманизацию антитела проводили методом переноса выявленных (вычисленных с использованием компьютерных алгоритмов на полученных нуклеотидных последовательностях) гипервариабельных участков (CDR) вариабельного фрагмента мышиных антител, отвечающих за комплементарность антигену, на вариабельный фрагмент человека, помещали CDR между соответствующими каркасными участками, по результатам анализа баз данных и биоинформатического моделирования структурного сходства (аналогии) между антителами. Полученное гуманизированное антитело обладает специфичностью материнского мышиного антитела, но повышенной аффинностью за счет более подходящего пространственного расположения CDR, обусловленного каркасными участками.
Для молекулярной графики использовали программы: Insight II; Accelrys, СА. Моделирование конформационной гомологии между донорным мышиным антителом и человеческим акцепторным антителом проводили с использованием WAM (http://antibody.bath.ac.uk), SWISS-MODEL (http://www.expasy.org), INSIGHT-HOMOLOGY (Accelrys), COMPOSER (Tripos, МО) и GCG Wisconsin Package. Последовательности вариабельных фрагментов мышиных антител были аннотированы и пронумерованы с использованием баз данных Kabat и Chothia.
Информация о структуре вариабельных фрагментов учитывается в нумерации, разработанной Chothia [21], однако в данной нумерации не рассматриваются остатки аминокислот в вариабельных фрагментах антител. В соответствии с указанными выше данными для нумерации и аннотирования вариабельных фрагментов использовался модифицированный Kabat и Chothia алгоритм Abhinandan KR и Martin АС [22, 23]. При нумерации при этом учитывались не только исправленные данные множественных выравниваний последовательностей антител по Kabat и данные о структуре CDR по Chothia с учетом структуры FR, но и данные о VH/VL углах складывания в донорных и акцепторных антителах. Для автоматического аннотирования использовались программы с интерактивным web-интерфейсом: SeqTest (AbCheck) http://www.bioinf.org.uk/abs/seqtest.html, Abnum http://www.bioinf.org.uk/abs/abnum/, ручная корректировка и проверка проводились с использованием локальной версии базы данных Kabat http://www.kabatdatabase.com/index.html и программы KabatMan http://www.bioinf.org.uk/abs/simkab.html, средств IMGT http://imgt.cines.fr/ и данных множественного выравнивания последовательностей вариабельных фрагментов антител с использованием MUSCULE http://www.ebi.ac.uk/Tools/muscle/index.html и пакета программ FASTA http://fasta.bioch.virginia.edu/fasta_www2/fasta_http://down.shtml, структуры которых представлены в PDB на 2012 год, а также разработанных авторами изобретения нескольких Perl скриптов для автоматизации анализа данных. VH/VL углы складывания были рассчитаны и предсказаны исходя из алгоритма, предложенного Abhinandan [22]. Все необходимые расчеты, связанные с моделированием структуры белковых молекул, проводили с использованием Modeller и Swiss-Model.
Следующим шагом в гуманизации антител был выбор акцепторных вариабельных фрагментов антител человека для переноса. Правильный выбор акцепторного антитела человека практически на 100% гарантирует успешную гуманизацию антител, с Kd, достаточной для высокопрочного связывания с антигеном. С использованием методов молекулярного моделирования и описанных выше подходов была построена структурная модель вариабельного фрагмента мышиного моноклонального антитела против синдекана-1. С использованием полученных трехмерных моделей были определены наиболее гомологичные (особенно по ключевым позициям) последовательности акцепторных антител человека, при этом использовались только антитела со значением коэффициента «человечности» Н>1 (что потенциально может уменьшить НАНА ответ). На основании полученной модели рассчитали аминокислотные и, соответственно, нуклеотидные последовательности вариабельных фрагментов тяжелой и легкой (каппа) цепей антитела.
1.5. Получение гуманизированных моноклональных антител к синдекану-1
Для получения искомых свойств антител в константный фрагмент тяжелой цепи вводили участки IgG3, который обладает самой высокой степенью активации системы комплемента из всех изотипов, а также высокой аффинностью по отношению к связыванию с Fc рецептором фагоцитирующих клеток, в структуру константного фрагмента IgG4, что сообщило антителу способность индукции антитело-зависимой и комплемент-зависимой цитотоксичности. Также ввели аминокислотные замены 1M252Y, S254T, Т256Е, Н433К, N434F в область С-конца константного фрагмента IgG4 - для увеличения периода полужизни антитела.
Соединили последовательности вычисленных вариабельного и константного фрагментов тяжелой цепи в одну аминокислотную последовательность, добавив на N-конце сигнальную секреторную последовательность (SEQ ID NO:1). Соединили последовательности вычисленных вариабельного и константного фрагментов легкой каппа цепи в одну аминокислотную последовательность, добавив на N-конце сигнальную секреторную последовательность (SEQ ID NO:2).
Перевели аминокислотные последовательности белка в нуклеотидные, оптимизировав последние для увеличения продукции данного антитела в клетках млекопитающих (СНО) с помощью программы на сайте http://www.encorbio.com/protocols/Codon.htm.
В результате был получен окончательный вариант нуклеотидных последовательностей (SEQ ID NO:3, SEQ ID NO:4), кодирующих гуманизированное моноклонального антитело к синдекану-1 (SEQ ID NO:1, SEQ ID NO:2), и синтезировали их с использованием химического синтеза. Синтезированные фрагменты клонировали в плазмидный вектор pUC57 для наработки, затем переклонировали в вектор pcDNA3.1+ для трансфекции клеток млекопитающих.
Трансфекцию клеток млекопитающих созданными плазмидами проводили методом кальций-фосфатного осаждения.
Для проведения трансформации клеток млекопитающих (СНО) плазмидными ДНК клетки высевали в 12-луночные планшеты (Costar, США) с плотностью посева 5×104 кл/см2. На следующий день для синхронизации клеточных делений культуральную среду заменяли. Через три часа к клеткам добавляли плазмидную ДНК, осажденную фосфатом кальция. Для приготовления осадка 250 мкл раствора, содержащего 50 мкг ДНК в 250 мМ CaCl2, медленно смешивали с 250 мкл раствора (1,64% NaCl, 1,13% HEPES рН 7,12 и 0,04% Na2HPO4). После 24 часов инкубации при 37°С в атмосфере 5% СО2 среду заменяли на аналогичную, но содержащую 2 антибиотика: 80 мкг/мл зеоцин и 2 мкг/мл бластицидин S для селекции клонов, содержащих обе трансформированные плазмиды и, следовательно, экспрессирующих полноразмерные гуманизированные антитела, селекцию проводили в течение 20 суток, в лунках, содержащих живые клетки, меняли среду (при этом предыдущую культуральную среду не выливали, а использовали для определения количества секретируемых антител методом ИФА), а еще через сутки клетки снимали с подложки и проводили анализ на экспрессию трансформированных генов. Анализ эффективности трансфекции проводили на проточном цитофлуориметре EPICS XL Beckman Coulter (Beckman Coulter, США).
Уровень гуманизированных антител в культуральной среде полученных стабильных трансфектом линии СНО оценивали с использованием стандартного твердофазного ИФА.
В результате 6 клонирований были получены стабильные трансфектомы СНО, которые накапливали для криоконсервирования и наработки опытной партии антител. Продуктивность созданных трансфектом СНО, экспрессирующих антитела к синдекану-1, составила 500 мкг/107 клеток/день.
1.6. Культивирование клеток-продуцентов гуманизированного моноклонального антитела к синдекану-1
Культивирование клеток-продуцентов осуществляли с использованием биореакторов BIOSTAT® Bplus и автоклавированной среды IMDM с добавлением 45 г DFBS (0,5%) и 25,8 г (100 мМ) сульфата цинка семиводного (ZnSO4 x 7H2O) на 9 л среды. Задавали рабочий режим: температура 37ºC, pH 6,9-7,2, концентрация кислорода 50% насыщения воздуха. После достижения заданного режима производили засев биореактора, для чего в асептичных условиях в него вводили посевной материал. Время культивирования составляло 3 суток.
По окончании культивирования культуральную жидкость фильтровали через стерильную капсулу «Sartopure» («Sartorius», Германия), с диаметром пор 1,2 мкм, со скоростью 1 л/мин. Затем осветленную жидкость концентрировали на системе Viva Flow 200 («Sartorius», Германия) с использованием фильтра на 50 кДа. Концентрирование проводили до достижения общего объема - 200 мл.
1.7. Очистка полученного гуманизированного моноклонального антитела к синдекану-1
Хроматографическую очистку проводили в два этапа с использованием стерильных растворов. На первом этапе использовали систему BioLogic DuoFlow Pathfinder (Bio-Rad) с автоматическим коллектором фракций BioFrac и полупрепаративную хроматографическую колонку YMC TriArt, 250х4,6 мм, сорбент С18. Перед началом работы колонку уравновешивали с помощью 200 мл буфера (1 кг воды для инъекций и 1 г кислоты трифторуксусной) в ручном режиме через насос хроматографа на скорости 2 мл/мин.
Подготовленный материал в объеме 200 мл вносили в хроматограф через насос хроматографа на скорости 0,5 мл/мин. Элюцию производили буфером (2 кг ацетонитрила, 2 г кислоты трифторуксусной) со скоростью 0,5 мл в минуту. Собирали фракцию в максимуме поглощения при 260 нм. Объем фракции составил примерно 500 мл.
Второй этап очистки выполняли с использованием гель-хроматографической колонки BioSil SEC 125-5, 300x7,8 мм. Предварительно колонку уравновешивали 0,02 М PBS-буфером. Полученный материал вносили в хроматограф через насос хроматографа на скорости 0,5 мл/мин. Элюцию производили буфером (0,6 М раствор NaCl) с градиентом концентрации от 0,1 до 0,6 М. Собирали фракцию, имеющую поглощение при А280 нм не менее 3.4 оптических единиц. Фракцию собирали во флаконы. Объем получаемого раствора составил примерно 1 л с концентрацией антитела 2 мг на 1 мл.
Было проведено измерение Kd полученного антитела, изучено его влияние на модельные клеточные линии (антипролиферативная активность) и ксенографтные опухолевые модели (ингибирование развития опухоли). Оказалось, что созданное антитело обладает достаточно большой аффинностью (Kd =8,0*10-9).
Пример 2. Изучение противоопухолевого эффекта гуманизированного моноклонального антитела к синдекану-1 на модели миеломы Sp2.0
В качестве модели использовали клеточную линию миеломы SP2.0, сингенную с мышами BALB/C, предварительно показав в ней экспрессию гена, кодирующего синдекан-1 (Фиг.1). Для этого из культуры клеток была выделена РНК и проведен синтез и анализ кДНК.
Мышам линии BALB/c NUDE прививались клетки опухоли SP2.0: подкожно в нижнюю часть спины было введено 500 000 клеток опухоли SP2.0 на одно животное. Использовалось 3 группы животных: 2 опытные и 1 контрольная.
После животным вводили моноклональное антитело 1 раз в неделю в течение 5 недель в дозе 1 мг и 0,1 мг начиная с 6 дня после введения опухолевых клеток, когда размер опухоли составил >200+/-23 мм3. Размер опухоли (шарообразной формы) определяли дважды в неделю в течение 36 дней с использованием штангенциркуля по формуле: V(опухоли)=π/6*длина*ширина2, где длина>ширина.
Получили следующие результаты: при введении гуманизированного моноклонального антитела к синдекану-1 мышам с привитыми клетками миеломы Sp2.0 происходит достоверное подавление роста опухоли (Фиг.2). Использование препарата моноклонального антитела к синдекану-1 позволило снизить объем опухоли на 50% на 5 неделю эксперимента.
Пример 3. Изучение противоопухолевого эффекта гуманизированного моноклонального антитела к синдекану-1 на примере изучения цитотоксичности на клетках человека линии А431
Изучали противоопухолевый эффект гуманизированного моноклонального антитела к синдекану-1. Мышам линии BALB/c NUDE подкожно в области бока было введено 107 (300 мкл) человеческих клеток линии А431. После животным было введено моноклональное антитело в дозе 50 мг/кг веса и контрольное моноклональное антитело против овальбумина в дозе 50 мг/кг веса.
Моноклональное антитело вводилось дважды в неделю внутрибрюшинно в объеме 200 мкл начиная с 6 дня после введения опухолевых клеток, когда размер опухоли составил >250+/-23 мм3. Размер опухоли (шарообразной формы) определяли дважды в неделю в течение 36 дней с использованием штангенциркуля по формуле: V(опухоли)=π/6*длина*ширина2, где длина>ширина. Также оценивалась выживаемость животных, составляющая процент выживших животных относительно изначального размера группы на данную временную точку.
Получили следующие показатели: активация моноклональным антителом комплемент-зависимого цитолиза клеток линии А431 происходит в концентрации 0,3 мкг/мл, что является хорошим показателем, а максимальная антипролиферативная активность на клетках линии А431 осуществляется в концентрации 0,2 мкг/мл.
Литература
1. World Health Statistics 2012, http://www.who.int/healthinfo/EN_WHS2012_Full.pdf.
2. Жуков Н.В., Тюляндин С.А. Целевая терапия в лечении солидных опухолей; практика противоречит теории / Биохимия 2008, Т.73, вып.5, с751-768.
3. Gattei V, Godeas С, Degan M, Rossi FM, Aldinucci D, Pinto A. Characterization of anti-CD138 monoclonal antibodies as tools for investigating the molecular polymorphism of syndecan-1 in human lymphoma cells. Br J Haematol. 1999 Jan;104(l):152-62.
4. Wijdenes J, Dore JM, Clement C, Vermot-Desroches С (2003). "CD138". J. Biol. Regul. Homeost. Agents 16 (2): 152-5.
5. W. Wu 2007.
6. Rousseau et al. EJNMMI Research 2011.
7. Bayer-Garner I.B., Sanderson R.D., Dhodapkar M.V. et al. Syndecan-1 (CD138) immunoreactivity in bone marrow biopsies of multiple myeloma: shed syndecan-1 accumulates in fibrotic regions. Mod Pathol 2001;14:1052-8.
8. Байков B.B.. ТРУДНОСТИ МОРФОЛОГИЧЕСКОЙ ДИАГНОСТИКИ МНОЖЕСТВЕННОЙ МИЕЛОМЫ. Москва, ОНКОГЕМАТОЛОГИЯ 2'2007, стр.10-15
9. Wu YH, Yang С Y, Chien WL, Lin KI, Lai MZ. Removal of syndecan-1 promotes TRAIL-induced apoptosis in myeloma cells. J Immunol. 2012 Mar 15;188(6):2914-21. Epub 2012 Feb 3.
10. Wu W. с соавторами в 2010.
11. Bae J, Tai YT, Anderson КС, Munshi NC. 2011.
12. Clinical Trials. gov identifier: NCT01296204.
13. Wijdenes J., Vooijs W.C., Clement C. et al. A plasmacyte selective monoclonal antibody (B-B4) recognizes syndecan-1. Br J Haematol 1996; 94:318-23.
14. Ковригина A.M., Пробатова Н.А. ДИФФЕРЕНЦИАЛЬНАЯ ДИАГНОСТИКА НЕХОДЖКИНСКИХ В-КЛЕТОЧНЫХ ЛИМФОМ. Москва, ОНКОГЕМАТОЛОГИЯ 2'2007, стр.6.
15. WO 2009080829 (A1) - AGENTS TARGETING CD138 AND USES THEREOF (23.12.2008).
16. WO 2009080832 (A1) - METHODS AND AGENTS FOR IMPROVING TARGETING OF CD138 EXPRESSING TUMOR CELLS (23.12.2008).
17. WO 2009080830 (A1) - IMMUNOCONJUGATES TARGETING CD138 AND USES THEREOF (23.12.2008).
18. WO 2010128087 (A2) - USES OF IMMUNOCONJUGATES TARGETING CD138 (5.05.2010).
19. Sato Ν, Kinbara M, Kuroishi Τ, Kimura К, Iwakura Y, Ohtsu H, Sugawara S, Endo Y Clin. Lipopolysaccharide promotes and augments metal allergies in mice, dependent on innate immunity and histidine decarboxylase. Exp Allergy: 2007, May; 37(5): 743-751.
20. Young L, Dong Q., Two step total gene synthesis method. Nucleic Acid Research: 32, e59, 2004.
21. Chothia C, Lesk AM. Canonical structures for the hypervariable regions of immunoglobulins. J Mol Biol. 1987 Aug 20; 196(4): 901-17.
22. Abhinandan К R and Martin A C. Analysis and Prediction of VH/VL Packing in Antibodies, Protein Engineering Design and Selection. 2010.
23. Abhinandan KR, Martin AC. Analysis and improvements to Kabat and structurally correct numbering of antibody variable domains. Mol Immunol. 2008 Aug; 45(14): 3832-9.
24. Jason et al. 2009.
25. Points to Consider in the Manufacture and Testing of Monoclonal Antibody Products for Human Use, FDA, 1997, Guidance for Industry for the Submission of Chemistry, Manufacturing and Controls Information for a Therapeutic Recombinant DNA-derived Product or a Monoclonal Antibody Product for In Vivo Use, CBER/CDER, FDA, August, 1996, International Conference on Harmonisation; Final Guideline on Stability Testing of Biotechnological/Biological Products, July 10, 1996.
26. Orecchia P, Conte R, Balza E, Petretto A, Mauri P, Mingari MC, Carnemolla B. A novel human anti-syndecan-1 antibody inhibits vascular maturation and tumour growth in melanoma. Eur J Cancer. 2013 May; 49(8):2022-33. doi: 10.1016/j.ejca.2012.12.019. Epub 2013 Jan 24.




| название | год | авторы | номер документа |
|---|---|---|---|
| Гуманизированное моноклональное антитело, специфичное к синдекану-1 | 2015 |
|
RU2611685C2 |
| ГУМАНИЗИРОВАННОЕ МОНОКЛОНАЛЬНОЕ АНТИТЕЛО, СПЕЦИФИЧНОЕ К ЛЕГУМАИНУ | 2013 |
|
RU2574203C2 |
| АНТИТЕЛО К GD2-O-АЦЕТИЛИРОВАННОМУ ГАНГЛИОЗИДУ С ПРОАПОПТОЗНОЙ АКТИВНОСТЬЮ | 2014 |
|
RU2679715C1 |
| АГЕНТЫ ПРОТИВ КЛЕТКИ-МИШЕНИ, НАЦЕЛЕННЫЕ НА CD138, И ИХ ПРИМЕНЕНИЕ | 2008 |
|
RU2537265C2 |
| АНАЛЬГЕТИЧЕСКОЕ СРЕДСТВО НА ОСНОВЕ ПЛАЗМИДНОЙ ДНК, КОДИРУЮЩЕЙ HNP-1, ЛИБО HNP-2, ЛИБО HNP-3 (ВАРИАНТЫ) | 2014 |
|
RU2597789C2 |
| АНТИТЕЛА К HER3 И ИХ ПРИМЕНЕНИЯ | 2010 |
|
RU2560583C2 |
| ИММУНОКОНЪЮГАТЫ, НАПРАВЛЕННЫЕ НА CD138, И ИХ ПРИМЕНЕНИЕ | 2008 |
|
RU2547939C2 |
| Гуманизированные антитела к LIV-1 и их применение для лечения рака | 2011 |
|
RU2608646C2 |
| МОНОКЛОНАЛЬНЫЕ АНТИТЕЛА ЧЕЛОВЕКА К БЕЛКУ ПРОГРАММИРУЕМОЙ СМЕРТИ 1 (PD-1) И СПОСОБЫ ЛЕЧЕНИЯ РАКА С ИСПОЛЬЗОВАНИЕМ АНТИ-PD-1-АНТИТЕЛ САМОСТОЯТЕЛЬНО ИЛИ В КОМБИНАЦИИ С ДРУГИМИ ИММУНОТЕРАПЕВТИЧЕСКИМИ СРЕДСТВАМИ | 2013 |
|
RU2599417C2 |
| МОНОКЛОНАЛЬНЫЕ АНТИТЕЛА ЧЕЛОВЕКА К БЕЛКУ ПРОГРАММИРУЕМОЙ СМЕРТИ 1 (PD-1) И СПОСОБЫ ЛЕЧЕНИЯ РАКА С ИСПОЛЬЗОВАНИЕМ АНТИ-PD-1-АНТИТЕЛ САМОСТОЯТЕЛЬНО ИЛИ В КОМБИНАЦИИ С ДРУГИМИ ИММУНОТЕРАПЕВТИЧЕСКИМИ СРЕДСТВАМИ | 2006 |
|
RU2494107C2 |

Данное изобретение относится к иммунологии, биотехнологии и медицине, а именно к области противоопухолевых лекарственных препаратов на основе моноклональных антител, и может быть использовано в медицине для лечения онкологических заболеваний. Предложено гуманизированное моноклональное антитело (MAb), специфичное к синдекану-1 (CD138), охарактеризованное аминокислотными и нуклеотидными последовательностями. Антитело по настоящему изобретению принадлежит изотипу IgG4 каппа, при этом константные фрагменты полностью человеческие и модифицированы введением участков IgG3, придающих антителу самостоятельную антитело-зависимую и комплемент-зависимую цитотоксичность, и аминокислотных замен, позволяющих увеличить время полужизни антитела. Вариабельные области представлены мышиными гипервариабельными и человеческими каркасными участками, обеспечивающими увеличение аффинности связывания с лигандом. Каждая цепь дополнительно содержит сигнальную секреторную последовательность на N-конце, отщепляющуюся при секреции из клеток-продуцентов. Нуклеотидные последовательности оптимизированы для увеличения продукции антитела в клетках млекопитающих. Настоящее изобретение может найти дальнейшее применение в терапии заболеваний, ассоциированных с CD138, в том числе злокачественных опухолей (рака). 1 з.п. ф-лы, 2 ил., 3 пр.
1. Моноклональное антитело изотипа IgG4, специфичное к синдекану-1 (CD138), представленное двумя тяжелыми и двумя легкими цепями, каждая из которых содержит вариабельный фрагмент и константный фрагмент, для терапии опухолевых заболеваний, отличающееся тем, что содержит участки IgG3 в константном фрагменте, вариабельный фрагмент представлен мышиными, гипервариабельными, участками и человеческими, каркасными, участками, константный фрагмент полностью человеческий и содержит аминокислотные замены на С-конце для увеличения времени полужизни, каждая цепь дополнительно содержит сигнальную секреторную последовательность на N-конце, отщепляющуюся при секреции из клеток-продуцентов, тяжелая цепь представлена аминокислотной последовательностью SEQ ID NO:1, закодированной нуклеотидной последовательностью SEQ ID NO:3, легкая цепь - каппа и представлена аминокислотной последовательностью SEQ ID NO:2, закодированной нуклеотидной последовательностью SEQ ID NO:4, причем нуклеотидные последовательности кодонно оптимизированы для экспрессии в клетках млекопитающих, антитело используют в качестве самостоятельного действующего вещества.
2. Антитело по п. 1, отличающееся тем, что обладает самостоятельной антитело-зависимой и комплемент-зависимой цитотоксичностью.
| Колосоуборка | 1923 |
|
SU2009A1 |
| ORECCHIA P | |||
| et al | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| GATTEI V et al., "Characterization of anti-CD138 monoclonal antibodies as tools for investigating the molecular polymorphism of syndecan-1 in | |||
Авторы
Даты
2015-05-20—Публикация
2013-08-26—Подача