Данное изобретение относится к антителам, связывающимся с человеческим HER3 (анти-HER3-антителам), к способам их производства, к фармацевтическим композициям, содержащим указанные антитела, и к их применениям.
Уровень техники
Человеческий HER3 (ErbB-3, ERBB3, с-erbB-3, с-erbB3, тирозин-киназный рецептор erbB-3, SEQ ID №17) кодирует рецептор эпидермального фактора роста (EGFR), член семейства тирозинкиназных рецепторов, которое также включает HER1 (также известный как EGFR), HER2 и HER4 (Kraus, M.H. et al, PNAS 86 (1989) 9193-9197; Plowman, G.D. et al, PNAS 87 (1990) 4905-4909; Kraus, M.H. et al, PNAS 90 (1993) 2900-2904). Как и прототипичный рецептор эпидермального фактора роста, трансмембранный рецептор HER3 состоит из внеклеточного лиганд-связывающего домена (ECD, extracellular ligand-binding domain), домена димеризации с ECD, трансмембранного домена, внутриклеточного домена тирозинкиназного белка (TKD) и C-концевого фосфорилированного домена. Этот связанный с мембраной белок имеет херегулин (HRG)-связывающий домен HER3 во внеклеточном домене, но не имеет активного киназного домена. Таким образом, он может связывать этот лиганд, но не передает сигнал внутрь клетки через фосфорилирование белка. Тем не менее, он формирует гетеродимеры с другими членами HER-семейства, которые обладают киназной активностью. Гетеродимеризация приводит к активации рецептор-опосредованного сигнального пути и трансфосфорилированию его внутриклеточного домена. Образование димеров между членами HER-семейства расширяет возможности передачи сигнала HER3 и является средством не только распределения сигнала, но и усиления сигнала. Например, гетеродимер HER2/HER3 индуцирует один из наиболее важных митогенных сигналов через путь PI3K и AKT среди членов семейства HER (Sliwkowski M.X., et al, J. Biol. Chem. 269 (1994) 14661-14665; Alimandi M, et al, Oncogene. 10 (1995) 1813-1821; Hellyer, N.J., J. Biol. Chem. 276 (2001) 42153-4261; Singer, E., J. Biol. Chem. 276 (2001) 44266-44274; Schaefer, K.L, Neoplasia 8 (2006) 613-622).
Амплификация этого гена и/или сверхэкспрессия его белка были обнаружены при многих раковых заболеваниях, в том числе при опухолях предстательной железы, мочевого пузыря и молочной железы. Были охарактеризованы транскрипционные варианты альтернативного сплайсинга, кодирующие различные изоформы. У одной изоформы отсутствует межмембранная область, и эта изоформа секретируется за пределы клетки. Эта форма действует путем модуляции активности формы, связанной с мембраной. Также сообщалось о дополнительных вариантах сплайсинга, но они не были детально описаны.
WO 97/35885 относится к HER3-антителам. WO 2003/013602 относится к ингибиторам HER-активности, включая HER-антитела. WO 2007/077028 и WO 2008/100624 также относятся к HER3-антителам.
Сущность изобретения
Изобретение включает антитело, которое связывается с человеческим HER3, характеризующееся тем, что вариабельный домен тяжелой цепи содержит CDR3H-область SEQ ID №1, CDR2H-область SEQ ID №2, CDR1H-область SEQ ID №3, а вариабельный домен легкой цепи содержит CDR3L-область SEQ ID №4, CDR2L-область SEQ ID №5, CDR1L-область SEQ ID №6 или CDR1L-область SEQ ID №7.
Кроме того, изобретение включает антитело в соответствии с изобретением, которое характеризуется тем, что вариабельный домен тяжелой цепи VH представляет собой SEQ ID №8; а вариабельный домен легкой цепи VL представляет собой SEQ ID №9, либо вариабельный домен легкой цепи VL представляет собой SEQ ID №10, либо вариабельный домен легкой цепи VL представляет собой SEQ ID №11; или ее гуманизированную версию.
Кроме того, изобретение включает антитело, включающее вариабельный домен тяжелой цепи, содержащий CDR3H-область SEQ ID №1, CDR2H-область SEQ ID №2, CDR1H-область SEQ ID №3, и вариабельный домен легкой цепи, содержащий CDR3L-область SEQ ID №4, CDR2L-область SEQ ID №5 и CDR1L-область SEQ ID №6.
Кроме того, изобретение включает антитело, включающее вариабельный домен тяжелой цепи VH SEQ ID №8 и вариабельный домен легкой цепи VL SEQ ID №9 или SEQ ID №11.
Кроме того, изобретение включает антитело, включающее вариабельный домен тяжелой цепи, содержащий CDR3H-область SEQ ID №1, CDR2H-область SEQ ID №2 и CDR1H-область SEQ ID №3, и вариабельный домен легкой цепи, содержащий CDR3L-область SEQ ID №4, CDR2L-область SEQ ID №5 и CDR1L-область SEQ ID №7.
Кроме того, изобретение включает антитело, включающее вариабельный домен тяжелой цепи VH SEQ ID №8 и вариабельный домен легкой цепи VL SEQ ID №10.
Другой аспект изобретения предусматривает антитело, которое связывается с человеческим HER3 и которое состоит из вариабельного домена тяжелой цепи VH, имеющего по меньшей мере 95% идентичность последовательности с SEQ ID №8, и вариабельного домена легкой цепи VL, имеющего по меньшей мере 95% идентичность последовательности с SEQ ID №9, SEQ ID №10 или SEQ ID №11.
В одном воплощении антитело в соответствии с изобретением характеризуется тем, что оно является моноклональным.
В одном воплощении антитело в соответствии с изобретением характеризуется тем, что оно является гуманизированным.
В одном воплощении антитело в соответствии с изобретением характеризуется тем, что оно относится к подклассу IgG1 или IgG4.
Кроме того, изобретение включает фармацевтическую композицию, которая характеризуется тем, что содержит антитело в соответствии с изобретением.
Кроме того, изобретение включает антитело в соответствии с изобретением для лечения рака.
Кроме того, изобретение включает применение антитела в соответствии с изобретением для изготовления лекарственного препарата для лечения рака.
Кроме того, изобретение включает способ лечения пациента, страдающего от рака, который характеризуется введением пациенту антитела в соответствии с изобретением.
Другой аспект изобретения предусматривает нуклеиновую кислоту, кодирующую тяжелую и легкую цепь анти-HER3-антитела по изобретению. В одном воплощении антитело состоит из вариабельного домена тяжелой цепи VH, имеющего по меньшей мере 95% идентичность последовательности с SEQ ID №8, и вариабельного домена легкой цепи VL, имеющего по меньшей мере 95% идентичность последовательности с SEQ ID №9, SEQ ID №10 или SEQ ID №11.
Кроме того, изобретение включает нуклеиновую кислоту, кодирующую тяжелую и легкую цепи антитела, связывающегося с человеческим HER3, которая характеризуется тем, что указанное антитело состоит из вариабельного домена VH SEQ ID №8 и вариабельного домена легкой цепи VL SEQ ID №8, SEQ ID №10 или SEQ ID №11; или ее гуманизированной версии.
Кроме того, изобретение включает экспрессионный вектор, который характеризуется тем, что включает нуклеиновую кислоту в соответствии с изобретением для экспрессии антитела в соответствии с изобретением в прокариотической или эукариотической клетке-хозяине.
Кроме того, изобретение включает прокариотическую или эукариотическую клетку-хозяина, содержащую вектор в соответствии с изобретением.
Кроме того, изобретение включает способ производства рекомбинантного антитела в соответствии с изобретением, который характеризуется экспрессией нуклеиновой кислоты в соответствии с изобретением в прокариотической или эукариотической клетке-хозяине и восстановлением указанного антитела из указанной клетки или клеточного культурального супернатанта.
Неожиданно было установлено, что антитела в соответствии с изобретением обладают весьма ценными свойствами, такими как сильное торможение роста раковых клеток, экспрессирующих HER3, сильное торможение HER3-опосредованной передачи сигнала (такой как, например, HER3-фосфорилирование и AKT-фосфорилирование), что связано с пролиферацией раковых клеток, высокой аффинностью к HER3 или превосходными фармакокинетическими свойствами (например, долгим временем полужизни и т.д.).
Подробное описание изобретения
Изобретение включает антитело, которое связывается с человеческим HER3, характеризующееся тем, что вариабельный домен тяжелой цепи содержит CDR3H-область SEQ ID №1, CDR2H-область SEQ ID №2 и CDR1H-область SEQ ID №3, а вариабельный домен легкой цепи содержит CDR3L-область SEQ ID №4, CDR2L-область SEQ ID №5, CDR1L-область SEQ ID №6 или CDR-IL-область SEQ ID №7.
Кроме того, изобретение включает антитело в соответствии с изобретением, которое характеризуется тем, что вариабельный домен тяжелой цепи VH представляет собой SEQ ID №8; а вариабельный домен легкой цепи VL представляет собой SEQ ID №9, либо вариабельный домен легкой цепи VL представляет собой SEQ ID №10, либо вариабельный домен легкой цепи VL представляет собой SEQ ID №11, либо ее гуманизированную версию.
Кроме того, изобретение включает антитело в соответствии с изобретением, которое характеризуется тем, что вариабельный домен тяжелой цепи VH представляет собой SEQ ID №8; а вариабельный домен легкой цепи VL представляет собой SEQ ID №9, либо вариабельный домен легкой цепи VL представляет собой SEQ ID №10, либо вариабельный домен легкой цепи VL представляет собой SEQ ID №11.
В одном воплощении антитело в соответствии с изобретением характеризуется тем, что включает вариабельный домен тяжелой цепи, содержащий CDR3H-область SEQ ID №1, CDR2H-область SEQ ID №2 и CDR1H-область SEQ ID №3, и вариабельный домен легкой цепи, содержащий CDR3L-область SEQ ID №4, CDR2L-область SEQ ID №5 и CDR1L-область SEQ ID №6.
В одном воплощении антитело в соответствии с изобретением характеризуется тем, что вариабельный домен тяжелой цепи VH представляет собой SEQ ID №8, а вариабельный домен легкой цепи VL представляет собой SEQ ID №9, либо вариабельный домен легкой цепи VL представляет собой SEQ ID №11.
В одном воплощении антитело в соответствии с изобретением характеризуется тем, что включает в качестве вариабельного домена тяжелой цепи CDR3H-область SEQ ID №1, CDR2H-область SEQ ID №2, CDR1H-область SEQ ID №3, а вариабельный домен легкой цепи содержит CDR3L-область SEQ ID №4, CDR2L-область SEQ ID №5 и CDR1L-область SEQ ID №7.
В одном воплощении антитело в соответствии с изобретением характеризуется тем, что вариабельный домен тяжелой цепи VH представляет собой SEQ ID №8, а вариабельный домен легкой цепи VL представляет собой SEQ ID №10.
В одном воплощении антитело в соответствии с изобретением является моноклональным. В одном воплощении антитело в соответствии с изобретением является гуманизированным или человеческим. В одном воплощении антитело в соответствии с изобретением относится к подклассу IgG1 и IgG4. В одном воплощении антитело в соответствии с изобретением представляет собой моноклональное гуманизированное антитело подкласса IgG1. В одном воплощении антитело в соответствии с изобретением характеризуется тем, что указанное антитело является гликозилированным с сахарной цепочкой на Asn297, где количество фукозы в указанной сахарной цепочке составляет 65% или ниже.
Изобретение включает гуманизированные антитела Mab 205.10.1, Mab 205.10.2 и Mab 205.10.3 с их соответствующими VH и VL или CDR.
В одном воплощении такие антитела содержат константные области человеческого происхождения, например, SEQ ID №12-16, предпочтительно SEQ ID №12-13.
Термин «антитело» включает различные формы структур антитела, в том числе, но не ограничиваясь ими, целые антитела и фрагменты антител. Антитело в соответствии с изобретением предпочтительно представляет собой человеческое антитело, гуманизированное антитело, химерное антитело или антитело, полученное путем генной инженерии, до тех пор, пока сохраняются их характерные свойства в соответствии с изобретением.
«Фрагменты антитела» включают часть антитела полной длины, предпочтительно, его вариабельную область или по меньшей мере антиген-связывающий сайт. Примеры фрагментов антитела включают двойные антитела, одноцепочечные молекулы антител и полиспецифические антитела, сформированные из фрагментов антител. Например, scFv-антитела описаны в Huston, J.S., Methods in Enzymol. 203 (1991) 46-88. Кроме того, фрагменты антител включают одноцепочечные полипептиды, имеющие характеристики домена VH, a именно возможность объединяться с доменом VL, или характеристики домена VL, связывающего HER3, а именно возможность объединяться с доменом VH для формирования функционального антиген-связывающего сайта и, таким образом, обеспечивать свойства антитела в соответствии с изобретением.
Используемые в данном документе термины «моноклональное антитело» или «композиция с монокпональным антителом» относятся к препарату молекул антитела единого аминокислотного состава.
Термин «химерное антитело» относится к моноклональному антителу, содержащему вариабельную область, т.е. связывающую область, от мыши и по меньшей мере часть константной области, полученной из другого источника или вида, как правило полученному с помощью методик рекомбинантной ДНК. Особенно предпочтительными являются химерные антитела, содержащие мышиную вариабельную область и человеческую константную область. Такие мышиные/человеческие химерные антитела являются продуктом экспрессированных генов иммуноглобулинов, содержащих сегменты ДНК, кодирующие вариабельные области мышиного иммуноглобулина, и сегменты ДНК, кодирующие константные области человеческого иммуноглобулина. Другими формами «химерных антител», охватываемыми данным изобретением, являются те, в которых класс или подкласс был модифицирован или изменен по сравнению с исходным антителом. Такие «химерные» антитела также называют «антителами с переключением класса». Способы получения химерных антител включают обычные методики рекомбинантной ДНК и генной трансфекции, в настоящее время хорошо известные в данной области. См., например, Morrison, S.L, et al., Proc. Natl. Acad Sci. USA 81 (1984) 6851-6855; патенты США 5202238 и 5204244.
Термин «гуманизированное антитело» или «гуманизированная версия антитела» относится к антителам, в которых были изменены каркасные области или «области, определяющие комплементарность» (CDR) так, чтобы они содержали CDR иммуноглобулина другой специфичности, отличной от родительского иммуноглобулина. В предпочтительном воплощении мышиный CDR из VH или VL прививают каркасной области человеческого антитела для получения «гуманизированного антитела». См., например, Riechmann, L, et al., Nature 332 (1988) 323-327; и Neuberger, M.S., et al., Nature 314 (1985) 268-270. Каркасные вариабельные области тяжелой и легкой цепей могут быть получены из одной или разных человеческих последовательностей антител. Последовательности человеческого антитела могут быть последовательностями природных человеческих антител. Каркасные вариабельные области тяжелой и легкой цепей перечислены, например, в Lefranc, M.-P., Current Protocols in Immunology (2000) - Appendix 1P A.1P.1-A.1P.37, и доступны через IMGT, международную информационную систему иммуногенетики ImMunoGeneTics® (http://imgt.cines.fr) или через сайт http://vbase.mrc-cpe.cam.ac.uk. Каркасная область может быть дополнительно модифицирована путем дальнейших мутаций. Особенно предпочтительные CDR соответствуют тем, которые представляют последовательности, распознающие антигены, отмеченные выше для химерных антител. Предпочтительно такая гуманизированная версия химеризована с человеческой константной области (см., например, последовательности SEQ ID №12-16). Термин «гуманизированное антитело», используемый в данном документе, включает также такие антитела, которые были модифицированы в константной области для создания свойств в соответствии с изобретением, особенно в отношении C1q-связывания и/или FcR-связывания, например, путем «переключения класса», т.е. путем изменения или мутации Fc-частей (например, из IgG1 в IgG4 и/или мутация IgG1/IgG4).
Термин «человеческое антитело», используемый в данном документе, включает антитела с вариабельными и константными областями, полученными из человеческих зародышевых последовательностей иммуноглобулина. Человеческие антитела хорошо известны в данной области (van Dijk, M.A., and van de Winkel, J.G., Curr. Opin. Pharmacol. 5 (2001) 368-374). Человеческие антитела могут быть также получены на трансгенных животных (например, мышах), которые способны после иммунизации продуцировать полный репертуар или выборку человеческих антител в отсутствие эндогенной продукции иммуноглобулина. Перенос совокупности человеческих зародышевых последовательностей иммуноглобулина в такую мышь, мутантную по зародышевой линии, приведет к продукции человеческих антител в ответ на антигенную стимуляцию (см., например, Jakobovits, A., et al., Proc. Natl. Acad. Sci. USA 90 (1993) 2551-2555; Jakobovits, A., et al., Nature 362 (1993) 255-258; Brueggemann, M.D., et al., Year Immunol. 7 (1993) 33-40). Человеческие антитела могут быть также получены в библиотеках фагового дисплея (Hoogenboom, H.R„ and Winter, G., J. Mol. Biol. 227 (1992) 381-388; Marks, J.D., et al., J. Mol. Biol. 222 (1991) 581-597). Методики Cole, A., et al. и Boerner, P., et al. также доступны для изготовления человеческих моноклональных антител (Cole, A., et al., Monoclonal Antibodies and Cancer Therapy, Liss, A.L, p.77 (1985); и Boerner, P., et al., J. Immunol. 147 (1991) 86-95). Как уже было упомянуто по отношению к гуманизированным антителам в соответствии с изобретением, термин «человеческое антитело», используемый в данном документе, включает также такие антитела, которые были модифицированы в константной области для создания свойств в соответствии с изобретением, особенно в отношении C1q-связывания и/или FcR-связывания, например, путем «переключения класса», т.е. путем изменения или мутации Fc-частей (например, из IgG1 в IgG4 и/или мутации IgG1/IgG4).
Термин «рекомбинантное человеческое антитело», используемый в данном документе, охватывает все человеческие антитела, которые получают, экспрессируют, создают или выделяют с помощью рекомбинантных средств, например, антитела, выделенные из клетки-хозяина, такой как клетка NSO или СНО, или животного (например, мыши), которое является трансгенным для человеческих генов иммуноглобулинов или антител, экспрессируемых с помощью рекомбинантного экспрессионного вектора, трансфицированного в клетку-хозяина. Такие рекомбинантные человеческие антитела имеют вариабельные и константные области в перегруппированной форме. Рекомбинантные человеческие антитела в соответствии с изобретением подвергали соматическому гипермутированию in vivo. Таким образом, аминокислотные последовательности областей VH и VL рекомбинантных антител являются последовательностями, которые, будучи полученными из и связанными с человеческими зародышевыми последовательностями VH и VL, не могут естественным образом существовать в репертуаре человеческих зародышевых антител in vivo.
Используемые в данном документе термины «связывающийся с человеческим HER3», или «специфически связывающийся с человеческим HER3», или «анти-HER3-антитело» являются взаимозаменяемыми и относятся к антителу, специфически связывающемуся с человеческим HER3-антигеном с аффинностью связывания, которая имеет значение KD 1×10-8 моль/л или ниже при 25°С, в одном воплощении имеет значение KD 1×10-9 моль/л или ниже при 25°С. Аффинность связывания определяют в стандартном анализе связывания при 25°С, таком как методика поверхностного плазменного резонанса (BIAcore®, GE-Healthcare, Упсала, Швеция). Способ определения значения KD аффинности связывания описан в примере 2b). Таким образом, термин «антитело, связывающееся с человеческим HER3», используемый в данном документе, относится к антителу, специфически связывающемуся с человеческим HER3-антигеном с аффинностью связывания со значением KD 1×10-8 моль/л или ниже (предпочтительно 1×10-8 моль/л - 1,0×10-12 моль/л) при 25°С.
Человеческий HER3 (ErbB-3, ERBB3, c-erbB-3, с-erbB3, тирозин-киназный рецептор erbB-3, SEQ ID №17) кодирует рецептор эпидермального фактора роста (EGFR), член семейства тирозинкиназных рецепторов, которое также включает HER1 (также известный как EGFR), HER2 и HER4 (Kraus, M.H. et al, PNAS 86 (1989) 9193-9197; Plowman, G.D. et al, PNAS 87 (1990) 4905-4909; Kraus, M.H. et al, PNAS 90 (1993) 2900-2904). Как и прототипичный рецептор эпидермального фактора роста, трансмембранный рецептор HER3 состоит из внеклеточного лиганд-связывающего домена (ECD), домена димеризации с ECD, трансмембранного домена, внутриклеточного домена тирозинкиназного белка (TKD) и C-концевого фосфорилированного домена. Этот связанный с мембраной белок имеет херегулин (HRG)-связывающий домен HER3 во внеклеточном домене, но не имеет активного киназного домена. Таким образом, он может связывать этот лиганд, но не передает сигнал внутрь клетки через фосфорилирование белка. Тем не менее, он формирует гетеродимеры с другими членами HER-семейства, которые обладают киназной активностью. Гетеродимеризация приводит к активации рецептор-опосредованного сигнального пути и трансфосфорилированию его внутриклеточного домена. Образование димеров между членами HER-семейства расширяет возможности передачи сигнала HER3 и является средством не только распределения сигнала, но и усиления сигнала. Например, гетеродимер HER2/HER3 индуцирует один из наиболее важных митогенных сигналов через путь PI3K и AKT среди членов семейства HER (Sliwkowski M.X., et at, J. Biol. Chem. 269 (1994) 14661-14665; Alimandi M, etal, Oncogene. 10 (1995) 1813-1821; Hellyer, N.J., J. Biol. Chem. 276 (2001) 42153-4261; Singer, E., J. Biol. Chem. 276 (2001) 44266-44274; Schaefer, K.L, Neoplasia 8 (2006) 613-622).
HER3-антитела Mab205.10.1, Mab205.10.2 и Mab205.10.3 показали конкурентное с лигандом херегулином (HRG) связывание с HER3.
Амплификация этого гена и/или сверхэкспрессия его белка были обнаружены при многих раковых заболеваниях, в том числе при опухолях предстательной железы, мочевого пузыря и молочной железы. Были охарактеризованы транскрипционные варианты альтернативного сплайсинга, кодирующие различные изоформы. У одной изоформы отсутствует межмембранная область, и эта изоформа секретируется за пределы клетки. Эта форма действует путем модуляции активности формы, связанной с мембраной. Также сообщалось о дополнительных вариантах сплайсинга, но они не были детально описаны.
Термин «эпитоп» включает любую полипептидную детерминанту, способную специфически связываться с антителом. В некоторых воплощениях эпитопная детерминанта включает химически активные поверхностные группировки молекул, такие как аминокислоты, сахарные боковые цепочки, фосфорил или сульфонил, а в некоторых воплощениях может иметь специфические трехмерные структурные характеристики и/или специфические характеристики заряда. Эпитоп является областью антигена, которая связывается антителом.
Термин «вариабельный домен антитела в соответствии с изобретением» (вариабельный домен легкой цепи (VL), вариабельный домен тяжелой цепи (VH)), используемый в данном документе, означает каждую пару доменов легкой и тяжелой цепей, которые непосредственно участвуют в связывании антитела с антигеном. Вариабельные домены легкой и тяжелой цепей имеют одинаковую общую структуру, и каждый домен содержит четыре каркасные области (framework region, FR), последовательности которых в значительной степени консервативны, соединенные тремя «гипервариабельными областями» (или областями, определяющими комплементарность, CDR). Каркасные области принимают конформацию β-скпадчатости, а CDR могут образовывать петли, связывающие β-складчатую структуру. CDR в каждой цепи удерживаются в их трехмерной структуре с помощью каркасных областей и образуют вместе с CDR из другой цепи антигенсвязывающий сайт. CDR3-области тяжелой и легкой цепи антитела играют особенно важную роль в специфичности связывания/аффинности антител в соответствии с изобретением и, следовательно, обеспечивают дальнейший предмет изобретения.
Термин «антигенсвязывающая часть антитела», используемый в данном документе, относится к аминокислотным остаткам антитела, которые отвечают за связывание антигена. Антигенсвязывающая часть антитела содержит аминокислотные остатки из «областей, определяющих комплементарность», или «CDR». Термин «антигенсвязывающая часть» антитела изобретения включает шесть областей, определяющих комплементарность (CDR), которые в разной степени способствуют аффинности сайта связывания с антигеном. Существует три CDR вариабельного домена тяжелой цепи домена (CDRH1, CDRH2 и CDRH3) и три CDR вариабельного домена легкой цепи (CDRL1, CDRL2 и CDRL3). Термин «CDRH1» означает CDR1-область вариабельной области тяжелой цепи, рассчитанной по Кабату. CDRH2, CDRH3, CDRL1, CDRL2 и CDRL3 означают соответствующие области тяжелой (Н) или легкой (L) цепей. Протяженность CDR и каркасных областей (FR) определяют путем сравнения с собранной базой данных аминокислотных последовательностей, в которых эти области определены в соответствии с вариабельностью среди последовательностей по Kabat, et al., Sequences of Proteins of Immunological Interest, 5th Ed. Public Health Service, National Institutes of Health, Bethesda, MD. (1991)).
«Fc-часть» антитела непосредственно не участвует в связывании антитела с антигеном, но проявляет различные эффекторные функции. «Fc-часть антитела» является термином, хорошо известным специалистам в данной области, и определяется на основе расщепления антител папаином. В зависимости от аминокислотной последовательности константной области их тяжелых цепей антитела или иммуноглобулины делятся на классы: IgA, IgD, IgE, IgG и IgM, и некоторые из них могут быть разделены на подклассы (изотипы), например, IgG1, IgG2, IgG3 и IgG4, IgA1 и IgA2. В соответствии с константными областями тяжелой цепи различные классы иммуноглобулинов называются α, δ, ε, γ и µ, соответственно. Fc-часть антитела непосредственно участвует в ADCC (антитело-зависимой клеточной цитотоксичности) и CDC (комплемент-зависимой цитотоксичности), которые основаны на активации комплемента, C1q-связывании и Fc-рецепторном связывании. Термин «комплемент-зависимая цитотоксичность (CDC)» означает процесс, начинающийся при связывании фактора комплемента C1q с Fc-частью большинства подклассов IgG-антител. Связывание C1q с антителом обусловлено определенными белок-белковыми взаимодействиями в так называемом сайте связывания. Такие сайты связывания известны в настоящее время и описаны, например, Boackle, R.J., et al., Nature 282 (1979) 742-743, Lukas, T.J., et al., J. Immunol. 127 (1981) 2555-2560, Brunhouse, R., and Cebra, J.J., Mol. Immunol. 16 (1979) 907-917, Burton, D.R., et al., Nature 288 (1980) 338-344, Thommesen, J.E., et al., Mol. Immunol. 37 (2000) 995-1004, Idusogie, E.E., et al., J. lmmunol. 164 (2000) 4178-4184, Hezareh, M., et al., J. Virology 75 (2001) 12161-12168, Morgan, A., et al., Immunology 86 (1995) 319-324, EP 0307434. Такими сайтами связывания являются, например, L234, L235, D270, N297, Е318, K320, K322, Р331 и Р329 (нумерация в соответствии с EU индексом Кабата, см. ниже). Антитела подклассов IgG1, IgG2 и IgG3 обычно демонстрируют активацию комплемента и связывание C1q и С3, в то время как IgG4 не активируют систему комплемента и не связывают C1q и С3.
В одном воплощении антитело в соответствии с изобретением содержит Fc-часть человеческого происхождения и, предпочтительно, все другие части из человеческих константных областей. Используемый в данном документе термин «Fc-часть человеческого происхождения» означает Fc-часть, которая является либо Fc-частью человеческого антитела подкласса IgG1, IgG2, IgG3 или IgG4, например, Fc-частью человеческого антитела подкласса IgG1, мутированной Fc-частью из человеческого антитела подкласса IgG1 (предпочтительно с мутацией L234A+L235A), Fc-частью человеческого антитела подкласса IgG4, либо мутированной Fc-частью человеческого подкласса IgG4 (предпочтительно с мутацией S228P). Предпочтительными являются человеческие константные области тяжелой цепи SEQ ID №13 (человеческий подкласс IgG1), SEQ ID №14 (человеческий подкласс IgG1 с мутациями L234A и L235A).
В одном воплощении антитело в соответствии с изобретением относится к человеческому антителу подкласса IgG1 или человеческому антителу подкласса IgG3. В одном воплощении антитело в соответствии с изобретением относится к человеческому антителу подкласса IgG1.
В одном воплощении антитело в соответствии с изобретением характеризуется тем, что константные цепи имеют человеческое происхождение. Такие константные цепи хорошо известны в настоящее время и описаны, например, Kabat, Е.А., (см., например, Johnson, G. and Wu, T.T., Nucleic Acids Res. 28 (2000) 214-218). Например, используемая человеческая константная область тяжелой цепи состоит из аминокислотной последовательности SEQ ID №13. Например, используемая человеческая константная область легкой цепи состоит из аминокислотной последовательности константной области легкой цепи каппа SEQ ID №12.
Термин «аминокислота», используемый в данной заявке, обозначает группу природных карбокси-α-аминокислот, включающую аланин (трехбуквенный код: ala, однобуквенный код: А), аргинин (arg, R), аспарагин (asn, N), аспарагиновую кислоту (asp, D), цистеин (cys, С), глутамин (gln, Q), глутаминовую кислоту (glu, E), глицин (gly, G), гистидин (his, Н), изолейцин (ile, I), лейцин (leu, L), лизин (lys, K), метионин (met, М), фенилаланин (phe, F), пролин (pro, Р), серин (ser, S), треонин (thr, Т), триптофан (trp, W), тирозин (tyr, Y) и валин (val, V).
Термин «нуклеиновая кислота» или «нуклеиновокислотная молекула», используемый в данном документе, включает молекулы ДНК и молекулы РНК. Нуклеиновокислотная молекула может быть одноцепочечной или двуцепочечной, но предпочтительной является двуцепочечная ДНК. Нуклеиновая кислота является «функционально связанной», когда она находится в функциональной взаимосвязи с другой нуклеиновой кислотой. Например, ДНК предпоследовательности или секреторной лидерной последовательности функционально связана с ДНК полипептида, если она экспрессируется как пребелок, который участвует в секреции полипептида; промотор или энхансер функционально связан с кодирующей последовательностью, если он влияет на транскрипцию последовательности; или сайт связывания рибосомы функционально связан с кодирующей последовательностью, если он расположен так, чтобы облегчить трансляцию. Как правило, «функционально связан» означает, что последовательности ДНК, будучи линейными, являются коллинеарными, и в случае секреторного лидера смежными и одной рамке считывания. Тем не менее, энхансеры не обязаны быть смежными. Связь осуществляется путем лигирования подходящих сайтов рестрикции. Если таких сайтов не существует, в соответствии с обычной практикой используются синтетические олигонуклеотидные адаптеры или линкеры. Используемые в данном документе выражения «клетка», «клеточная линия» и «клеточная культура» используются как синонимы, и все такие обозначения включают потомство. Таким образом, слова «трансформанты» и «трансформированные клетки» включают первичную клетку-объект и культуры, полученные из нее, независимо от количества переносов. Также понятно, что все потомство может не быть точно идентичным по содержанию ДНК из-за преднамеренных или случайных мутаций. Подразумевается вариантное потомство, которое имеет такие же функции или биологическую активность, как и у исходной трансформированной клетки.
Антитело в соответствии с изобретением предпочтительно характеризуется тем, что константные цепи имеют человеческое происхождение. Такие константные цепи хорошо известны в настоящее время и описаны, например, Kabat et al., Sequences of Proteins of Immunological Interest, 5th ed., Public Health Service, National Institutes of Health, Bethesda, MD (1991). Например, используемая константная область человеческой легкой цепи включает аминокислотную последовательность константной области легкой цепи каппа SEQ ID №12. Например, используемая константная область человеческой тяжелой цепи включает SEQ ID №13-16.
Другое воплощение изобретения представляет собой нуклеиновую кислоту, кодирующую тяжелую и легкую цепи антитела в соответствии с изобретением.
Антитела в соответствии с изобретением включают, кроме того, такие антитела, которые имеют «консервативные модификации последовательности» (вариантные антитела), модификации нуклеотидной и аминокислотной последовательностей, которые не влияют или изменяют указанные выше характеристики антитела в соответствии с изобретением. Модификации могут быть внесены с помощью стандартных методик, известных в данной области, таких как сайт-направленный мутагенез и ПЦР-опосредованный мутагенез. Консервативные аминокислотные замены включают те, при которых аминокислотный остаток заменен аминокислотным остатком с аналогичной боковой цепью. Семейства аминокислотных остатков, имеющих сходные боковые цепи, определены в данной области. Эти семейства включают аминокислоты с основными боковыми цепями (например, лизин, аргинин, гистидин), кислыми боковыми цепями (например, аспарагиновую кислоту, глутаминовую кислоту), незаряженными полярными боковыми цепями (например, глицин, аспарагин, глутамин, серин, треонин, тирозин, цистеин, триптофан), неполярными боковыми цепями (например, аланин, валин, лейцин, изолейцин, пролин, фенилаланин, метионин), бета-разветвленными боковыми цепями (например, треонин, валин, изолейцин) и ароматическими боковыми цепями (например, тирозин, фенилаланин, триптофан, гистидин). Таким образом, предсказанный заменимый аминокислотный остаток в человеческом анти-HER3-антителе может быть предпочтительно заменен другим аминокислотным остатком из семейства с такой же боковой цепью. Таким образом, «вариантное» анти-HER3-антитело в данном документе относится к молекуле, аминокислотная последовательность которой отличается от аминокислотной последовательности «родительского» анти-HER3-антитела на десять, предпочтительно от двух до пяти, добавлений, удалений и/или замен в одной или более чем одной вариабельной области родительского антитела. Аминокислотные замены могут быть выполнены путем мутагенеза на основании молекулярного моделирования, как описано в Riechmann, L, et al., Nature 332 (1988) 323-327 и Queen, С., et al., Proc. Natl. Acad. Sci. USA 86 (1989) 10029-10033.
В другом аспекте анти-НЕР3-антитело в соответствии с изобретением содержит последовательность вариабельного домена тяжелой цепи (VH), имеющую по меньшей мере 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% идентичность последовательности с аминокислотной последовательностью SEQ ID №8. В некоторых воплощениях последовательность VH, имеющая по меньшей мере 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичность, содержит замены (например, консервативные замены), вставки или удаления по сравнению с референсной последовательностью, но анти-HER3-антитело, включающее эту последовательность, сохраняет способность связываться с HER3. В некоторых воплощениях в SEQ ID №8 было заменено, вставлено и/или удалено в общей сложности от 1 до 10 аминокислот. В некоторых воплощениях замены, вставки или удаления произведены в областях за пределами CDR (т.е., в FR). Возможно, анти-HER3-антитело включает VH-последовательность SEQ ID №8, в том числе посттрансляционные модификации этой последовательности. В конкретном воплощении VH состоит из одной, двух или трех CDR, выбранных среди: (a) CDR1H, содержащей аминокислотную последовательность SEQ ID №3, (б) CDR2H, содержащей аминокислотную последовательность SEQ ID №2; и (в) CDR3H, содержащей аминокислотную последовательность SEQ ID №1.
В другом аспекте анти-HER3-антитело в соответствии с изобретением включает вариабельный домен легкой цепи (VL), имеющий по меньшей мере 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% идентичность последовательности с аминокислотной последовательностью SEQ ID №9, SEQ ID №10 или SEQ ID №11. В некоторых воплощениях VL-последовательность, имеющая по меньшей мере 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичность, содержит замены (например, консервативные замены), вставки или удаления по сравнению с референсной последовательностью, но анти-HER-антитело, включающее эту последовательность, сохраняет способность связываться с HER. В некоторых воплощениях в SEQ ID №9, SEQ ID №10 ил SEQ ID №11 было заменено, вставлено и/или удалено в общей сложности от 1 до 10 аминокислот. В некоторых воплощениях замены, вставки или удаления произведены в областях за пределами CDR (т.е., в FR). Возможно, анти-HER3-антитело включает VL-последовательность SEQ ID №9, SEQ ID №10 или SEQ ID №11, в том числе посттрансляционные модификации этой последовательности. В конкретном воплощении VL состоит из одной, двух или трех CDR, выбранных среди: (a) CDR1L, содержащей аминокислотную последовательность SEQ ID №6 или SEQ ID №7; (б) CDR2L, содержащей аминокислотную последовательность SEQ ID №5; и (в) CDR3L, содержащей аминокислотную последовательность SEQ ID №4.
В другом аспекте предложено анти-HER3-антитело, которое содержит VH, как в любом из воплощений, приведенных выше, и VL, как в любом из воплощений, приведенных выше. В одном воплощении антитело содержит VH- и VL-последовательности SEQ ID №8 и SEQ ID №10, соответственно, в том числе посттрансляционные модификации этих последовательностей; а также обладает одним или более чем одним из следующих свойств (определяемых в анализах, описанных в примере 3 и 2):
- анти-HER3-антитело ингибирует HER3-фосфорилирование в опухолевых клетках, таких как клетки MCF7, клетки FaDu или клетки Mel-Juso (в одном воплощении анти-HER3-антитело демонстрирует ингибирование HER3-фосфорилирования в клетках MCF7 по меньшей мере на 80% (в одном воплощении по меньшей мере на 90%) в концентрации 1,0 мкг/мл; в одном воплощении анти-HER3-антитело демонстрирует ингибирование HER3-фосфорилирования в клетках FaDu по меньшей мере на 80% (в одном воплощении по меньшей мере на 90%) в концентрации 0,1 мкг/мл; в одном воплощении анти-HER3-антитело демонстрирует ингибирование HER3-фосфорилирования в клетках в Mel-Juso по меньшей мере на 60% (в одном воплощении по меньшей мере на 70%) в концентрации 0,1 мкг/мл).
- анти-HER3-антитело ингибирует AKT-фосфорилирование в опухолевых клетках, таких как клетки Mel-Juso (в одном воплощении анти-HER3-антитело ингибирует AKT-фосфорилирование в клетках Mel-Juso со значением IC50 менее 0,50 мкг/мл, в одном воплощении со значением IC50 менее 0,35 мкг/мл).
- анти-HER3-антитело ингибирует пролиферацию опухолевых клеток, таких как клетки MDA-MB-175 (в одном воплощении анти-HER3-антитело ингибирует пролиферацию клеток MDA-MB-175 со значением IC50 менее 10 мкг/мл)
- анти-HER3-антитело связывается с HER3 со значением KD менее 5,0×10-9 М, в одном воплощении со значением KD менее 3,0×10-9 М.
- В другом аспекте анти-HER3-антитело в соответствии с изобретением включает последовательность вариабельного домена тяжелой цепи (VH), имеющего по меньшей мере 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% идентичность последовательности с аминокислотной последовательностью SEQ ID №8, и включает вариабельный домен легкой цепи (VL), имеющий по меньшей мере 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% идентичность последовательности с аминокислотной последовательностью SEQ ID №9, SEQ ID №10 или SEQ ID №11; и обладает одним или более чем одним из следующих свойств (определяемых в анализах, описанных в примере 3 и 2):
- анти-HER3-антитело ингибирует HER3-фосфорилирование в опухолевых клетках, таких как клетки MCF7, клетки FaDu или клетки Mel-Juso (в одном воплощении анти-HER3-антитело демонстрирует ингибирование HER3-фосфорилирования в клетках MCF7 по меньшей мере на 80% (в одном воплощении по меньшей мере на 90%) в концентрации 1,0 мкг/мл; в одном воплощении анти-HER3-антитело демонстрирует ингибирование HER3-фосфорилирования в клетках FaDu по меньшей мере на 80% (в одном воплощении по меньшей мере на 90%) в концентрации 0,1 мкг/мл; в одном воплощении анти-HER3-антитело демонстрирует ингибирование HER3-фосфорилирования в клетках в Mel-Juso по меньшей мере на 60% (в одном воплощении по меньшей мере на 70%) в концентрации 0,1 мкг/мл).
- анти-HER3-антитело ингибирует AKT-фосфорилирование в опухолевых клетках, таких как клетки Mel-Juso (в одном воплощении анти-HER3-антитело ингибирует AKT-фосфорилирование в клетках Mel-Juso со значением IC50 менее 0,50 мкг/мл, в одном воплощении со значением IC50 по меньшей мере 0,35 мкг/мл).
- анти-HER3-антитело ингибирует пролиферацию опухолевых клеток, таких как клетки MDA-MB-175 (в одном воплощении анти-HER3-антитело ингибирует пролиферацию клеток MDA-MB-175 со значением IC50 менее 10 мкг/мл)
- анти-HER3-антитело связывается с HER3 со значением KD менее 5,0×10-9 М, в одном воплощении со значением KD менее 3,0×10-9 М.
Одно из воплощений изобретения представляет собой антитело, которое связывается с человеческим HER3 и состоит из вариабельного домена тяжелой цепи VH, имеющего по меньшей мере 95% идентичность последовательности с SEQ ID №8, и вариабельного домена легкой цепи VL, имеющего по меньшей мере 95% идентичность последовательности с SEQ ID №9, SEQ ID №10 или SEQ ID №11.
Одно из воплощений изобретения представляет собой такое антитело, в котором вариабельный домен легкой цепи VL имеет по меньшей мере 95% идентичность последовательности с SEQ ID №9.
Одно из воплощений изобретения представляет собой такое антитело, в котором вариабельный домен легкой цепи VL имеет по меньшей мере 95% идентичность последовательности с SEQ ID №10.
Одно из воплощений изобретения представляет собой такое антитело, в котором вариабельный домен легкой цепи VL имеет по меньшей мере 95% идентичность последовательности с SEQ ID №11.
Одно из воплощений изобретения представляет собой антитело, которое связывается с человеческим HER3 и состоит из вариабельного домена тяжелой цепи VH, имеющего по меньшей мере 95% идентичность последовательности с SEQ ID №8, и вариабельного домена легкой цепи VL, имеющего по меньшей мере 95% идентичность последовательности с SEQ ID №9, SEQ ID №10 или SEQ ID №11, и обладает одним или более чем одним из следующих свойств (определяемых в анализах, описанных в примере 3 и 2):
- анти-HER3-антитело ингибирует HER3-фосфорилирование в опухолевых клетках, таких как клетки MCF7, клетки FaDu или клетки Mel-Juso (в одном воплощении анти-HER3-антитело демонстрирует ингибирование HER3-фосфорилирования в клетках MCF7 по меньшей мере на 80% (в одном воплощении по меньшей мере на 90%) в концентрации 1,0 мкг/мл; в одном воплощении анти-HER3-антитело демонстрирует ингибирование HER3-фосфорилирования в клетках FaDu по меньшей мере на 80% (в одном воплощении по меньшей мере на 90%) в концентрации 0,1 мкг/мл; в одном воплощении анти-HER3-антитело демонстрирует ингибирование HER3-фосфорилирования в клетках в Mel-Juso по меньшей мере на 60% (в одном воплощении по меньшей мере на 70%) в концентрации 0,1 мкг/мл).
- анти-HER3-антитело ингибирует AKT-фосфорилирование в опухолевых клетках, таких как клетки Mel-Juso (в одном воплощении анти-HER3-антитело ингибирует AKT-фосфорилирование в клетках Mel-Juso со значением IC50 менее 0,50 мкг/мл, в одном воплощении со значением IC50 по меньшей мере 0,35 мкг/мл).
- анти-HER3-антитело ингибирует пролиферацию опухолевых клеток, таких как клетки MDA-MB-175 (в одном воплощении анти-HER3-антитело ингибирует пролиферацию клеток MDA-MB-175 со значением IC50 менее 10 мкг/мл)
- анти-HER3-антитело связывается с HER3 со значением KD менее 5,0×10-9 М, в одном воплощении со значением KD менее 3,0×10-9 М.
Идентичность или гомология по отношению к последовательности определяется здесь как процент аминокислотных остатков в кандидатной последовательности, которые идентичны с родительской последовательностью, после выравнивания последовательностей и введения пробелов, если это необходимо, для достижения максимального процента идентичности последовательностей. Ни N-концевые, ни C-концевые, ни внутренние расширения, удаления или вставки в последовательность антитела не должны толковаться как влияющие на идентичность или гомологию последовательности. Вариант сохраняет способность связываться с вариабельным доменом человеческого HER3 и, предпочтительно, обладает свойствами, которые превосходят такие свойства у родительского антитела. Например, вариант может иметь меньшие побочные эффекты во время лечения.
Типичное «родительское» антитело включает CDR-области антитела Mab 205.10.2 и предпочтительно используется для изготовления варианта. Предпочтительно, родительское антитело имеет человеческую каркасную область и, если они присутствуют, константные домены человеческого антитела. Например, родительское антитело может быть гуманизированным или человеческим антителом.
Термин «антитело-зависимая клеточная цитотоксичность (ADCC)» относится к лизису человеческих клеток-мишеней антителом в соответствии с изобретением в присутствии эффекторных клеток. ADCC предпочтительно измеряют путем обработки препарата HER3-экспрессирующих клеток антителом в соответствии с изобретением в присутствии эффекторных клеток, таких как свежевыделенные МКПК или очищенные эффекторные клетки из лейкоцитной пленки, такие как моноциты или натуральные киллеры (NK) или постоянно растущая клеточная линия NK.
Опосредованные клетками эффекторные функции моноклональных антител, такие как ADCC, могут быть усилены путем инженерии их олигосахаридного компонента, как описано в Umana, P., et al., Nature Biotechnol. 17 (1999) 176-180 и патенте США 6602684. Антитела типа IgG1, наиболее часто используемые терапевтические антитела, являются гликопротеинами, которые имеют консервативный N-связанный сайт гликозилирования на Asn297 в каждом СН2-домене. Два сложных двухантенных олигосахарида, присоединенные к Asn297, скрыты между СН2-доменами, образуя обширные контакты с полипептидной основой, и их присутствие имеет важное значение для антитела, чтобы опосредовать эффекторные функции, такие как антитело-зависимую клеточную цитотоксичность (ADCC) (Lifely, M.R., et al., Glycobiology 5 (1995) 813-822; Jefferis, R., et al., Immunol. Rev. 163 (1998) 59-76; Wright, A, and Morrison, S.L, Trends Biotechnol. 15 (1997) 26-32). В Umana, Р., et al. Nature Biotechnol. 17 (1999) 176-180 и WO 99/54342 показано, что сверхэкспрессия в клетках яичника китайского хомячка (СНО) β(1,4)-N-ацетилглюкозаминилтрансферазы III («GnTIII»), гликозилтрансферазы, катализирующей формирование олигосахаридов с симметричным разветвлением, значительно увеличивает in vitro ADCC-активность антител. Изменения в составе Asn297-углевода или его ликвидация также влияет на связывание с FcγR и C1q (Umana, P., et al., Nature Biotechnol. 17 (1999) 176-180; Davies, J., et al., Biotechnol. Bioeng. 74 (2001) 288-294; Mimura, Y., et al., J. Biol. Chem. 276 (2001) 45539-45547; Radaev, S, et al, J. Biol. Chem. 276 (2001) 16478-16483; Shields, R.L, et al., J. Biol. Chem. 276 (2001) 6591-6604; Shields, R.L, et al., J. Biol. Chem. 277 (2002) 26733-26740; Simmons, L.C, et al., J. Immunol. Methods 263 (2002) 133-147).
Способы усиления опосредованных клетками эффекторных функций моноклональных антител через гликотехнологию приведены, например, в WO 2005/044859, WO 2004/065540, W02007/031875, Umana, P., et al., Nature Biotechnol. 17 (1999) 176-180, WO 99/154342, WO 2005/018572, WO 2006/116260, WO 2006/114700, WO 2004/065540, WO 2005/011735, WO 2005/027966, WO 1997/028267, США 2006/0134709, США 2005/0054048, США 2005/0152894, WO 2003/035835 и WO 2000/061739 или, например, в Niwa, R, et al., J. Immunol. Methods 306 (2005) 151-160; Shinkawa, Т., et al, J Biol Chem, 278 (2003) 3466-3473; WO 03/055993 и США 2005/0249722.
В одном воплощении изобретения антитело в соответствии с изобретением является нефукозилированным, что означает, что антитело гликозилировано (если оно включает Fc-часть антитела подкласса IgG1 или IgG3) сахарной цепочкой на Asn297, при этом количество фукозы в указанной сахарной цепочке составляет 80% или ниже (нумерация в соответствии с Кабатом), например, от 80% до 1%. В другом воплощении количество фукозы в указанной сахарной цепочке составляет 65% или ниже, в одном воплощении от 5% до 65%, и в одном воплощении количество фукозы в указанной сахарной цепочке равно 0%. Такие антитела называются в последующем «нефукозилированными антителами» или «афукозилированными антителами». Такие нефукозилированные антитела демонстрирует повышенную ADCC, в то время как другие свойства антитела остаются в основном неизменными.
В другом воплощении в указанной сахарной цепочке количество N-гликолилнейраминовой кислоты (NGNA) составляет 1% или меньше, и/или количество N-концевой альфа-1,3-галактозы составляет 1% или меньше. Сахарная цепочка предпочтительно демонстрирует характеристики N-связанных гликанов, присоединенных к Asn297 антитела, рекомбинантно экспрессированного в клетке СНО.
«Asn297» в соответствии с изобретением означает аминокислоту аспарагиновую кислоту, расположенную примерно в позиции 297 в Fc-области. На основании незначительных изменений последовательности антител Asn297 также может быть расположен на несколько аминокислот (обычно не более чем ±3 аминокислоты) раньше или позже позиции 297, т.е. между позициями 294 и 300.
Термин «сахарные цепочки демонстрируют характеристики N-связанных гликанов, присоединенных к Asn297 антитела, рекомбинантно экспрессированного в клетке СНО» означает, что сахарная цепочка на Asn297 родительского антитела полной длины в соответствии с изобретением имеет ту же структуру и последовательность сахарного остатка, за исключением остатков фукозы, что и у того антитела, которое экспрессировано в немодифицированных клетках СНО, например, как сообщено в WO 2006/103100.
Термин «NGNA», используемый в данной заявке, обозначает сахарный остаток N-гликолил-нейраминовую кислоту.
Гликозилирование человеческого IgG1 или IgG3 происходит на Asn297 как гликозилирование сердцевинного фукозилированного двухантенного сложного олигосахарида, заканчивающегося двумя остатками Gal. Человеческие константные области тяжелой цепи подклассов IgG1 или IgG3 подробно описаны Kabat, Е. A., et al., Sequences of Proteins of Immunological Interest, 5th Ed. Public Health Service, National Institutes of Health, Bethesda, MD. (1991), и Brueggemann, M., et al., J. Exp. Med. 166 (1987) 1351-1361; Love, T.W, et al., Methods Enzymol. 178 (1989) 515-527. Эти структуры обозначаются как G0-, G1- (α-1,6- или α-1,3-), или G2-гликанановые остатки в зависимости от количества концевых Gal-остатков (Raju, T.S., Bioprocess Int. 1 (2003) 44-53). Тип гликозилирования Fc-частей антитела в СНО описан, например, Routier, F.H., Glycoconjugate J. 14 (1997) 201-207. Антитела, которые рекомбинантно экспрессируются в негликомодифицированных клетках-хозяевах СНО, обычно фукозилированы на Asn297 в количестве по меньшей мере 85%. Модифицированные олигосахариды родительского антитела полной длины могут быть гибридными или сложными. Предпочтительно олигосахариды с симметричным разветвлением, редуцированные/нефукозилированные, являются гибридными. В другом воплощении олигосахариды с симметричным разветвлением, редуцированные/нефукозилированные, являются сложными.
В соответствии с изобретением «количество фукозы» означает количество указанного сахара в сахарной цепочке на Asn297, связанное с суммой всех гликоструктур, присоединенных к Asn297 (например, сложных, гибридных и высоко маннозных структур), которое измеряется масс-спектрометрией MALDI-TOF (например, в системе LC/MS) и рассчитывается как среднее значение (см., например, WO 2008/077546). Относительное количество фукозы представляет собой процент фукозосодержащих структур, связанных со всеми гликоструктурами, выявленными в образце, обработанном N-гликозидазой F (например, сложной, гибридной и олиго- и высокоманнозной структурами, соответственно) на MALDI-TOF.
Антитела в соответствии с изобретением предпочтительно получают рекомбинантными средствами. Такие способы широко известны в данной области и включают экспрессию белка в прокариотических и эукариотических клетках с последующим выделением полипептида антитела и, обычно, очисткой до фармацевтически приемлемой чистоты. Для экспрессии белков нуклеиновые кислоты, кодирующие легкие и тяжелые цепи или их фрагменты, вставляют в экспрессионные векторы с помощью стандартных способов. Экспрессию осуществляют в соответствующих прокариотических или эукариотических клетках-хозяевах, таких как клетки СНО, клетки ns0, клетки SP2/0, клетки HEK293, клетки COS, дрожжевые клетки или клетки Е.coli, и из клеток выделяют антитело (из супернатанта или после лизиса клеток). Рекомбинантная продукция антител хорошо известна в данной области и описана, например, в обзоре статей Makrides, S.C., Protein Expr. Purif. 17 (1999) 183-202; Geisse, S., et al., Protein Expr. Purif. 8 (1996) 271-282; Kaufman, R.J., Mol. Biotechnol. 16 (2000) 151-161; Werner, R.G., Drug Res. 48 (1998) 870-880. Антитела могут находиться в целых клетках, в клеточном лизате, в частично очищенном или существенно чистом виде. Очистку проводят с целью устранения других клеточных компонентов или других загрязняющих веществ, например, других клеточных нуклеиновых кислот или белков, с помощью стандартных методик, в том числе колоночной хроматографии и других хорошо известных в данной области методик (см. Ausubel, F., et al., ed. Current Protocols in Molecular Biology, Greene Publishing and Wiley Interscience, New York (1987)). Экспрессия в клетках ns0 описана, например, в Barnes, L.M., et al., Cytotechnology 32 (2000) 109-123; Barnes, L.M., et al., Biotech. Bioeng. 73 (2001) 261-270. Транзиентная экспрессия описана, например, в Durocher, Y., et al., Nucl. Acids. Res. 30 (2002) E9. Клонирование вариабельных доменов описано в Orlandi, R., et al., Proc. Natl. Acad. Sci. USA 86 (1989) 3833-3837; Carter, P., et al., Proc. Natl. Acad. Sci. USA 89 (1992) 4285-4289; Norderhaug, L, et al., J. Immunol. Methods 204 (1997) 77-87. Предпочтительная система транзиентной экспрессии (HEK 293) описана Schlaeger, E.-J. Christensen, K., в Cytotechnology 30 (1999) 71-83, и Schlaeger, E.-J, J. Immunol. Methods 194 (1996) 191-199. Моноклональные антитела подходят для выделения из культуральной среды путем обычных процедур очистки иммуноглобулинов, таких как, например, с помощью белка А-сефарозы, гидроксиапатитной хроматографии, гель-электрофореза, диализа или аффинной хроматографии. ДНК и РНК, кодирующие моноклональные антитела, можно легко выделить и секвенировать с помощью обычных процедур. Гибридомные клетки могут служить источником таких ДНК и РНК. После выделения ДНК может быть вставлена в экспресионные векторы, которыми затем трансфицируют клетки-хозяева, например, клетки HEK 293, клетки СНО или клетки миеломы, которые в противном случае не производят иммуноглобулиновый белок, чтобы получить синтез рекомбинантных моноклональных антител в клетках-хозяевах. Антитела, получаемые из указанных клеточных линий, являются предпочтительными воплощениями изобретения. Нефукозилированные антитела предпочтительно получают с помощью гликотехнологии, как описано выше.
Варианты аминокислотных последовательностей анти-HER3-антитела получают путем введения соответствующих нуклеотидных замен в ДНК, кодирующую антитело, или путем пептидного синтеза. Тем не менее, такие изменения могут быть выполнены только в очень ограниченном диапазоне, например, как описано выше. Например, изменения не влияют на указанные выше характеристики антител, такие как IgG-изотип и связывание эпитопа, но могут повышать выход рекомбинантной продукции, стабильность белка или могут облегчать очистку. Любой остаток цистеина, не участвующий в поддержании требуемой конформации анти-HER3-антитела, может быть заменен, как правило, на серин для улучшения устойчивости молекулы к окислению и для предотвращения аберрантного сшивания. С другой стороны, цистеиновая связь(связи) может быть добавлена в антитело для улучшения стабильности (особенно когда антитело представляет собой фрагмент антитела, такой как Fv-фрагмент). Другой тип аминокислотного варианта антитела изменяет оригинальный профиль гликозилирования антитела. Под «изменением» понимается удаление одной или более чем одной углеводной группировки, содержащейся в антителе, и/или добавление одного или более чем одного сайта гликозилирования, который не присутствует в антителе. Гликозилирование антител, как правило, является N-связанным. Понятие «N-связанный» относится к присоединению углеводной группировки к боковой цепи остатка аспарагина, Трипептидные последовательности аспарагин-Х-серин и аспарагин-Х-треонин, где Х является любой аминокислотой, кроме пролина, являются последовательностями распознавания для ферментативного присоединения углеводной группировки к боковой цепи аспарагина. Таким образом, наличие любой из этих трипептидных последовательностей в полипептиде создает потенциальный сайт гликозилирования. Добавление сайтов гликозилирования в антитело удобно осуществлять путем изменения аминокислотной последовательности, так что она будет содержать одну или более чем одну из описанных выше трипептидных последовательностей (для N-связанных сайтов гликозилирования).
Нуклеиновокислотные молекулы, кодирующие варианты аминокислотной последовательности анти-HER3-антитела, получают с помощью различных способов, известных в данной области. Эти способы включают, но не ограничиваясь ими, выделение из природного источника (в случае природных вариантов аминокислотной последовательности) или получение путем опосредованного олигонуклеотидом (или сайт-направленного) мутагенеза, ПЦР-мутагенеза и кассетного мутагенеза полученной ранее вариантной или невариантной версии гуманизированного анти-HER3-антитела.
Другой тип ковалентной модификации антитела включает связывание антитела с одним из множества небелковых полимеров, например, полиэтиленгликолем, полипропиленгликолем или полиоксиалкиленами, способом, изложенным в патентах США №№4640835, 4496689, 4301144, 4670417, 4791192, 4179337.
Вариабельные домены тяжелой и легкой цепи в соответствии с изобретением комбинированы с последовательностями промотора, инициации трансляции, константной области, 3'-нетранслируемой области, полиаденилирования и терминации транскрипции для формирования экспрессионных векторных конструкций. Экспрессионные конструкции с тяжелыми и легкими цепями могут быть объединены в единый вектор, котрансфицированы, поочередно трансфицированы или отдельно трансфицированы в клетки-хозяева, которые затем подвергают слиянию для образования единой клетки, экспрессирующей обе цепи.
Одним аспектом данного изобретения является фармацевтическая композиция, содержащая антитело в соответствии с изобретением. Другим аспектом изобретения является применение антитела в соответствии с изобретением для производства фармацевтической композиции. Еще одним аспектом изобретения является способ изготовления фармацевтической композиции, содержащей антитело в соответствии с изобретением. В другом аспекте данное изобретение предусматривает композицию, например, фармацевтическую композицию, содержащую антитело в соответствии с данным изобретением, собранное вместе с фармацевтическим носителем.
Кроме того, анти-HER3-антитела в соответствии с изобретением оказались особенно полезными для лечения рака.
Поэтому одним из аспектов изобретения является указанная фармацевтическая композиция для лечения рака.
Другим аспектом изобретения является антитело в соответствии с изобретением для лечения рака.
Другим аспектом изобретения является применение антитела в соответствии с изобретением для изготовления лекарственного средства для лечения рака.
Другим аспектом изобретения является способ лечения пациента, страдающего от рака, путем введения антитела в соответствии с изобретением указанному пациенту, который нуждается в таком лечении.
Упоминаемый в данном документе «фармацевтический носитель» включает любые и все растворители, дисперсные среды, покрытия, антибактериальные и противогрибковые агенты, изотонические и задерживающие абсорбцию агенты и т.п., которые являются физиологически совместимыми. Предпочтительно, носитель подходит для внутривенного, внутримышечного, подкожного, парентерального, спинномозгового или эпидермального введения (например, путем инъекции или инфузии).
Композиция данного изобретения может быть введена различными способами, известными в данной области. Как будет понятно специалисту, путь и/или режим введения будет варьировать в зависимости от желаемого результата. Для введения соединения изобретения определенным путем может потребоваться покрытие соединения или одновременное введение соединения с материалом, предотвращающим его инактивацию. Например, соединение может быть введено субъекту в соответствующем носителе, например, в липосомах или разбавителе. Фармацевтически приемлемые разбавители включают физиологический раствор и водные буферные растворы. Фармацевтические носители включают стерильные водные растворы или дисперсии и стерильные порошки для приготовления стерильных растворов для инъекций или дисперсий непосредственно перед применением. Применение таких сред и агентов для фармацевтически активных веществ известно в данной области.
Фразы «парентеральное введение» и «вводят парентерально», используемые в данном документе, означают способы введения, отличные от энтерального и местного применения, как правило, путем инъекций, и включают, но не ограничиваясь ими, внутривенные, внутримышечные, внутриартериальные, интратекальные, внутрикапсулярные, интраорбитальные, внутрисердечные, внутрикожные, внутрибрюшинные, транстрахеальные, подкожные, субкутикулярные, внутрисуставные, субкапсулярные, субарахноидальные, спинномозговые, эпидуральные и интрастенальные инъекции и инфузии.
Термин «рак», используемый в данном документе, может представлять собой, например, рак легкого, немелкоклеточный рак легкого (NSCL), бронхиолоальвеолярный рак легкого, рак кости, рак поджелудочной железы, рак кожи, рак головы или шеи, кожную или внутриглазную меланому, рак матки, рак яичников, рак прямой кишки, рак анальной области, рак желудка, рак толстой кишки, рак молочной железы, рак матки, карциному фаллопиевых труб, карциному эндометрия, карциному шейки матки, карциному влагалища, карциному вульвы, болезнь Ходжкина, рак пищевода, рак тонкой кишки, рак эндокринной системы, рак щитовидной железы, рак паращитовидной железы, рак надпочечника, саркому мягких тканей, рак уретры, рак полового члена, рак предстательной железы, рак мочевого пузыря, рак почек или мочеточников, почечно-клеточную карциному, карциному почечной лоханки, мезотелиому, гепатоцеллюлярный рак, рак желчного пузыря, опухоли центральной нервной системы (ЦНС), опухоли спинного мозга, глиому головного мозга, мультиформную глиобластому, астроцитомы, шванномы, эпендимомы, медуллобластомы, менингиомы, плоскоклеточные карциномы, аденому гипофиза, лимфому, лимфобластный лейкоз, включая рефракторные версии любого из вышеперечисленных видов рака, или комбинацию одного или более чем одного из вышеперечисленных видов рака. Предпочтительно такой рак представляет собой рак молочной железы, рак легкого, рак головы или шеи или рак поджелудочной железы, предпочтительно рак легкого, рак головы или шеи или рак поджелудочной железы. Предпочтительно такой рак также характеризуется экспрессией или сверхэкспрессией HER3, более предпочтительно сверхэкспрессией HER3.
Эти композиции также могут содержать вспомогательные вещества, такие как консерванты, смачивающие агенты, эмульгаторы и диспергирующие агенты. Профилактика наличия микроорганизмов может быть обеспечена как за счет стерилизации, как сказано выше, так и за счет включения различных антибактериальных и противогрибковых препаратов, например, парабенов, хлорбутанола, фенола, сорбиновой кислоты и т.п. Также может быть целесообразным включение в композиции изотонических агентов, таких как сахар, хлорид натрия и т.п. Кроме того, удлиненную абсорбцию инъекционной лекарственной формы можно получить путем включения агентов, которые задерживают всасывание, таких как моностеарат алюминия и желатин.
Независимо от выбранного пути введения соединения данного изобретения, которые могут быть использованы в подходящей гидратированной форме, и/или фармацевтические композиции данного изобретения составляют в фармацевтически приемлемых лекарственных формах с помощью традиционных способов, известных специалистам в данной области.
Фактические уровни доз активных ингредиентов в фармацевтических композициях данного изобретения могут быть изменены таким образом, чтобы получить количество активного ингредиента, эффективное для достижения желаемого терапевтического эффекта для конкретного пациента, композиции и способа введения, но не токсичное для пациента. Выбранный уровень доз будет зависеть от ряда фармакокинетических факторов, включая активность конкретных используемых композиций данного изобретения, путь введения, время введения, скорость выведения конкретного используемого соединения, продолжительность лечения, другие препараты, соединения и/или материалы, используемые в сочетании с конкретными используемыми композициями, возраст, пол, вес, состояние, общее состояние здоровья и историю болезни пациента, подлежащего лечению, и т.п. факторов, хорошо известных в медицине.
Композиция должна быть стерильной и жидкой при условии, что она доставляется с помощью шприца. Кроме воды, предпочтительным носителем является изотонический буферный солевой раствор.
Соответствующая текучесть может быть обеспечена, например, путем использования покрытий, таких как лецитин, путем поддержания требуемого размера частиц в случае дисперсии и путем применения поверхностно-активных веществ. Во многих случаях в композицию предпочтительно включать изотонические агенты, например, сахара, многоатомные спирты, такие как маннит или сорбит, и хлорид натрия.
Далее приведены примеры, список последовательностей и графические материалы, чтобы помочь пониманию данного изобретения, истинные рамки которого изложены в формуле изобретения. Понятно, что в изложенных процедурах могут быть сделаны изменения без отступления от сущности изобретения.
Описание списка последовательностей
SEQ ID №1 тяжелая цепь CDR3H, Mab 205.10
SEQ ID №2 тяжелая цепь CDR2H, Mab 205.10
SEQ ID №3 тяжелая цепь CDR1H, Mab 205.10
SEQ ID №4 легкая цепь CDR3L, Mab 205.10
SEQ ID №5 легкая цепь CDR2L, Mab 205.10
SEQ ID №6 легкая цепь CDR1L (вариант 1), Mab 205.10
SEQ ID №7 легкая цепь CDR1L (вариант 2), Mab 205.10
SEQ ID №8 вариабельный домен тяжелой цепи VH, Mab 205.10
SEQ ID №9 вариабельный домен легкой цепи VL, Mab 205.10.1
SEQ ID №10 вариабельный домен легкой цепи VL, Mab 205.10.2
SEQ ID №11 вариабельный домен легкой цепи VL, Mab 205.10.3
SEQ ID №12 константная область человеческой легкой цепи каппа
SEQ ID №13 константная область человеческой тяжелой цепи, полученная из IgG1
SEQ ID №14 константная область человеческой тяжелой цепи, полученная из IgG1 с мутациями L234A и L235A
SEQ ID №15 константная область человеческой тяжелой цепи, полученная из IgG4
SEQ ID №16 константная область человеческой тяжелой цепи, полученная из IgG4 с мутацией S228P
SEQ ID №17 человеческий HER3
Описание графических материалов
Фиг.1А и В: Процент (%) ингибирования анти-HER3-антителами в различных концентрациях фосфорилирования рецептора в клетках MCF7
Фиг.1C Процент (%) ингибирования анти-HER3-антителами в различных концентрациях фосфорилирования рецептора в клетках Mel-Juso
Фиг.2 Введение Mab 205 (10 мг/кг q7dx3, внутрибрюшинно) привело к остановке опухолевого роста трансплантированных ксенотрансплантатов FaDu SCCHN
Фиг.3 Введение Mab 205 (10 мг/кг q7d, внутрибрюшинно) привело к остановке опухолевого роста трансплантированных ксенотрансплантатов рака молочной железы MAXF449
Фиг.4 Введение Mab 205 (25 мг/кг q7d, внутрибрюшинно) привело к остановке опухолевого роста трансплантированных ксенотрансплантатов 7177 NSCLC
Примеры
Пример 1
Иммунизация
Мышей NMRI иммунизировали hHER3-ECD (собственным) и бустировали hu-HER3-ECD. Иммунный ответ контролировали путем тестирования образцов сыворотки в HER1/2/3- ECD-ИФА. Клетки селезенки от мышей с достаточными титрами анти-HER3-иммуноглобулина замораживали для дальнейшей иммортализации путем слияния с мышиной миеломной клеточной линией Р3Х63 Ag8.653. Проводили одно слияние и гибридомные супернатанты скринировали с помощью HER1/2/-ECD-ИФА, который показывал отсутствие перекрестной реактивности, но связывание с HER3-ECD, и были отобраны анти-HER3 селективные гибридомы. Соответствующие гибридомы клонировали путем FACS-сортировки отдельных клеток. Клоны отдельных клеток из разных гибридом культивировали in vitro для продукции антитела в тканевой культуральной среде для характеризации. Антитела отбирали путем определения их способности ингибировать HER3-фосфорилирование, AKT-фосфорилирование и пролиферацию опухолевых клеток MDA-MB-175 (см. примеры ниже). Из полученных антител одно затем гуманизировали для получения следующих антител Mab 205.10.1, Mab 205.10.2 и Mab 205.10.3 с их соответствующими VH и VL или CDR.
В одном воплощении такие антитела получали с использованием константных областей человеческого происхождения, например, SEQ ID №12-13.
Пример 2
Анализ связывания
а) Антиген-специфический ИФА на связывание человеческого HER3 ECD
Растворимый человеческий внеклеточный домен HER3, слитый со стрептавидин-связывающим белком (SBP) захватывали на стрептовидиновый планшет. Для определения оптимального связывания антитела с SPB-CDCP1 384-луночные полистироловые планшеты (NUNC, покрытые стрептавидином), поставляемые MicroCoat, Бернрид, Германия (ID-№1734776-001) покрывали чистым и поэтапно разведенным супернатантом HER293 (в BSA/IMDM-буфере: 100 мг/мл BSA фракции V, Roche 10735078001, растворенного в среде Дульбекко, модифицированной по способу Исков). Используя мышиную калибровочную кривую химерных антител 205, в связи со способностью микротитровальных планшетов связывать стрептавидин, был определен оптимальный коэффициент разведения супернатанта HEK293. Для стандартного покрытия HEK293-супернатант, содержащий SBP-HER3, разводили (между 1:15 и 1:40) и инкубировали в течение ночи при 28°С (25 мкл на лунку). Для удаления оставшегося несвязанного SBP-HER3 необходимо интенсивное промывание микротитровального планшета.
Антитела в соответствии с изобретением тестировали либо неразведенными, либо с использованием 12-этапного разведения. 12,5 мкл каждого образца на лунку инкубировали в течение 90 мин при комнатной температуре. После интенсивного промывания с помощью PBS-T (0,1% Твин-20 в PBS) добавляли 25 мкл козьих античеловеческих IgG-антител, связанных с HRP (Jackson ImmunoResearch, кодовый №109-036-098, разведение 1:10000), для человеческих антител и инкубировали в течение 1 часа. После интенсивного промывания выявляли связывание антител с помощью таблеток ABTS (Roche Diagnostics GmbH, кат. №1112422). Поглощение при 405 нм/492 нм измеряли с помощью стандартного фотометра.
В таблице показаны соотношения относительного связывания различных антител.
б) Характеризация связывания анти-НЕР3-антител с фрагментом внеклеточным доменом (ECD) человеческого HER3 с помощью анализов Biacore:
Для измерения аффинности 30 мкг/мл анти-Fcγ-антител (козлиных, от Jackson Immuno Research) связывали с поверхностью сенсорного чипа СМ-5 путем стандартного аминного связывания связью и химии блокирования на инструменте SPR (Biacore Т100). После конъюгации анти-НЕР3-антитела вводили при 25°С со скоростью потока 5 мкл/мин с последующим введением серии разведении (от 0 нМ до 1000 нМ) человеческого HER3 ECD со скоростью 30 мкл/мин. Для эксперимента по связыванию использовали рабочий буфер PBS/0,1% BSA. Затем чип регенерировали с помощью 60 с импульсов раствором 10 мМ глицин-HCl, рН 2,0.
Расчет термодинамических параметров (KD, константа связывания с HER3) проводили с использованием модели связывания Ленгмюра 1:1.
В анализе конкурентного связывания (Biacore) Mab205.10.1, Mab205.10.2 и Mab205.10.3 продемонстрировали связывание с одним и тем же эпитопом. Анти-HER3-антитела U1-7, U-53 и U1-59, описанные в WO 2007/077028, и Ab №6, описанный в WO 2008/100624, исследовали в таком анализе и выявили связывание с эпитопами, отличными от антител Mab205.10.1, Mab205.10.2 и МаЬ205.10.3.
Пример 3
а) Ингибирование НЕР3-фосфорилирования в клетках MCF7, FaDu и Mel-Juso
Анализы проводили в клетках MCF7 и FaDu в соответствии со следующим протоколом: сеяли клетки в концентрации 500000 клеток/лунка в 6-луночном планшете, покрытом поли-D-лизином в среде RPMI 1640 с 10% FCS. Инкубировали в течение 24 часов. Удаляли среду путем аспирации, инкубировали в течение ночи с 500 мкл/лунка RPMI 1640 с 0,5% FCS. Добавляли антитела в 500 мкл RPMI 1640 с 0,5% FCS. Инкубировали в течение 1 часа. Добавляли HRG-1b (конечная концентрация 500 нг/мл) на 10 мин. Для лизиса клеток удаляли среду и добавляли 80 мкл ледяного буфера для лизиса клеток Triton-X-100 и инкубировали в течение 5 минут на льду. После переноса лизата в 1,5 мл реакционную пробирку и центрифугирования со скоростью 14000 оборотов в минуту в течение 15 мин при 4°С супернатант переносили в новые реакционные пробирки. Образцы, содержащие равные количества белка в загрузочном буфере SDS, разделяли на SDS-PAGE и определяли с помощью полусухого Вестерн-блоттинга на нитроцеллюлозных мембранах. Мембраны блокировали 1× NET-буфером + 0,25% желатина в течение 1 часа и выявляли pHER3 с помощью антитела α-фосфо-HER3/ErbB3 (Tyr1289) (21D3), Cell Signaling, №4791, и HER3 с помощью антитела αErbB3 (С-17), Santa Cruz, № SC-285, соответственно. После отмывки и выявления сигналов с помощью POD-связанного вторичного антитела, бэнды исследовали денситометрически. Были исследованы анти-HER3-антитела Mab205.10.1, Mab205.10.2 и Mab205.10.3, а также анти-HER3-антитела U1-7, U-53 и U1-59, описанные в WO 2007/077028, и Ab №6, описанное в WO 2008/100624. Процент (%) ингибирования анти-HER3-антителами фосфорилирования рецептора на клетках MCF7 показан ниже и на фиг.1А.
% Ингибирования HER3-фосфорилирования в клетках MCF7
В другом эксперименте были исследованы анти-HER3-антитело Mab205.10.2, а также анти-HER3-антитело 8B8.2D9, описанное в WO 97/35885, и 1В4С3 и 2D1D12, описанные в WO 2003/013602. Процент (%) ингибирования анти-НЕР3-антителами фосфорилирования рецептора в клетках MCF7 показан ниже и на фиг.1В.
% ингибирования HER3-фосфорилирования в клетках MCF7
Процент (%) ингибирования анти-HER3-антителами фосфорилирования рецептора в клетках FaDu показан ниже.
% ингибирования HER3-фосфорилирования в клетках FaDu
В другом эксперименте были исследованы анти-HER3-антитело Mab205.10.2, а также анти-HER3-антитело 8B8.2D9, описанное в WO 97/35885, и 1В4С3 и 2D1D12, описанные в WO 2003/013602 и 105.5 (от Millipore, кат. №05-47, названный α-HERECD в WO 2003/013602) в клетках Mel-Juso. Анализы в клетках Mel-Juso осуществляли в соответствии с упомянутым выше протоколом для клеток MCF7 и FaDu. Количества клеток и объемы сред были адаптированы для 12-луночных планшетов. Процент (%) ингибирования анти-HER3-антителами фосфорилирования рецепторов в клетках Mel-Juso показан ниже и на фиг.1C.
% ингибирования HER3-фосфорилирования в клетках Mel-Juso
б) AKT-фосфорилирование (ИФА)
Анализы проводили в клетках MCF7 в соответствии со следующим протоколом: сеяли клетки MCF7 в концентрации 30000 клеток/лунка в 96-луночном планшете, покрытом поли-D-лизином, в среде RPMI 1640 с 10% FCS и инкубировали в течение 24 часов. Удаляли среду путем постукивания по чистому бумажному полотенцу, осторожно промывали 200 мкл бессывороточной среды, инкубировали в течение ночи с 100 мкл/лунка RPMI 1640 с 0,5% FCS. Удаляли среду, как описано выше; добавляли антитела в 100 мкл RPMI 1640 с 0,5% FCS и инкубировали в течение 1,5 часов. Добавляли HRG-1b (конечная концентрация 5 нг/мл) на 10 мин. Удаляли среду, как описано выше. Для лизиса клеток добавляли 100 мкл ледяного буфера для лизиса клеток и ресуспендировали путем пипетирования примерно 5 раз. Центрифугировали планшет со скоростью 3000 оборотов в минуту в течение 10 мин при 4°С и переносили 80 мкл супернатанта (или аликвот) в новый полипропиленовый планшет и подвергали шоковой заморозке в жидком азоте. Хранили при -80°С до анализа.
Набор для анализа AKT1.2 (phospho-Ser473) EIA Kit Assay Designs №900-162: Образцы (разведение 1:10) добавляли к планшету, покрытому мышиным МКА, специфическим для N-конца AKT. Инкубировали в течение 1 часа при комнатной температуре со встряхиванием. Промывали 5 раз, инкубировали с биотинилированным анти-фосфо-AKT(Ser473) в течение 1 часа при комнатной температуре со встряхиванием. Промывали 5 раз, инкубировали с конъюгатом стрептавидин-HRP в течение 30 минут при комнатной температуре со встряхиванием. Промывали 5 раз, инкубировали с ТМВ в течение 30 минут при комнатной температуре со встряхиванием. Останавливали реакцию и регистрировали при 450 нм.
Mab 205.10.2 продемонстрировало ингибирование AKT-фосфорилирования с IC50 0,06 мкг/мл.
При pAKT-ИФА в клетках Mel-Juso, проводимом, как описано для клеток MCF7, Mab 205.10.2 продемонстрировало ингибирование AKT-фосфорилирования с IC50 0,28 мкг/мл, все другие анализируемые антитела продемонстрировали IC50 выше (>) 50.
% ингибирования AKT-фосфорилирования в клетках Mel-Juso
в) Ингибирование пролиферации опухолевых клеток
Оценивали противоопухолевую эффективность HER3-антител Mab205.10.1, Mab205.10.2 и Mab205.10.3 в анализе пролиферации клеток с помощью клеток MDA-MB-175 (клетки карциномы молочной железы человека VII, каталоговый № АТСС НТВ-25). 20000 клеток на лунку высевали в стерильные 96-луночные планшеты для культивирования тканей с культуральной клеточной средой DMEM/F12, содержащей 10% FCS, и инкубировали при 37°С±1°C с 5%±1% CO2 в течение одного дня. Клетки были медленно растущими с временем удвоения примерно 1,5 суток. Анти-HER3-антитела добавляли в серии разведении и затем инкубировали в течение 6 дней. Жизнеспособность клеток оценивали с помощью индикатора alamarBlue®. Если жизнеспособность клеток была снижена более чем на 50% по сравнению с контролем, значения IC50 рассчитывали с использованием тройных повторов для каждой концентрации антитела; в противном случае, если % ингибирования жизнеспособности клеток при самой высокой концентрации был ниже 50%, то IC50 не рассчитывали и указывали, что IC50 [мкг/мл] выше (>) самой высокой концентрации. Кроме того, были исследованы анти-HER3-антитело U1-59, описанное в WO 2007/077028, и АВ №6, описанное в WO 2008/100624.
В другом эксперименте были исследованы анти-HER3-антитело 8B8.2D9, описанное в WO 97/35885, и 1В4С3, описанное в WO 2003/013602.
Пример 5
ADCC in vitro в опухолевых клетках KPL4 при специфическом лизисе 1 мкг/мл
Клетки-мишени KPL4 (ADCC), карциномы молочной железы, культивированные в RPMI1640+2 мМ L-аланин-L-глутамина+10% FCS), собирали с помощью трипсина/ЭДТА (Gibco №25300-054) в экспоненциальной фазе роста. После этапа промывания и оценки количества и жизнеспособности клеток, необходимую аликвоту метили в течение 30 минут при 37°С в камере инкубатора с кальцеином (Invitrogen № С3100МР; 1 флакон ресуспендировали в 50 мкл ДМСО на 5 млн клеток в 5 мл среды). Затем клетки промывали три раза средой AIM-V, оценивали число и жизнеспособность клеток, и число клеток доводили до 0,3 млн/мл.
Между тем, МКПК (мононуклеарные клетки периферической крови) как эффекторные клетки получали путем центрифугирования в градиенте плотности (Histopaque-1077, Sigma №Н8889) в соответствии с протоколом производителя (1х этап промывания при 400g и 2× этап промывания при 350g по 10 минут каждый). Оценивали число и жизнеспособность клеток, и число клеток доводили до 15 млн/мл.
В круглодонные 96-луночные планшеты высевали 100 мкл меченых кальцеином клеток-мишеней, добавляли 50 мкл разведенного нефукозилированного антитела (Mab205.10.1, Mab205.10.2, Mab205.10.3, приготовление см. ниже) и 50 мкл эффекторных клеток. В некоторых экспериментах клетки-мишени смешивали с Redimune® NF Liquid (ZLB Behring) в концентрации 10 мг/мл Redimune.
Контролем служил спонтанный лизис, который определяли путем совместного культивирования мишеней и эффекторных клеток без антител, и максимальный лизис, который определяли путем лизиса клеток-мишеней только 1% Triton X-100. Планшеты инкубировали в течение 4 часов при 37°С во влажной камере инкубатора.
Убийство клеток-мишеней оценивали, измеряя высвобождение ЛДГ (лактатдегидрогеназы) из поврежденных клеток с помощью набора для обнаружения цитотоксичности Cytotoxicity Detection kit (LDH Detection Kit, Roche №1 644793) в соответствии с инструкцией производителя. Вкратце, 100 мкл супернатанта из каждой лунки смешивали со 100 мкл субстрата из набора в прозрачном плоскодонном 96-луночном планшете. Значения Vmax цветной реакции субстрата определяли в ИФА при 490 нм в течение по меньшей мере 10 минут. Процент специфического опосредованного антителом убийства рассчитывали следующим образом: ((А-SR)/(MR-SR)×100, где А представляет собой среднее значение Vmax с определенной концентрацией антитела, SR представляет собой среднее значение Vmax спонтанного высвобождения, a MR представляет собой среднее значение Vmax максимального высвобождения.
В качестве дополнительного индикатора оценивали сохранение кальцеина интактными клетками-мишенями путем лизиса сохранившихся клеток-мишеней в боратном буфере (5 мМ борат натрия+0,1% Triton) и измерения флуоресценции кальцеина на флуоресцентном планшетном ридере. Mab205.10.1, Mab205.10.2, Mab205.10.3 демонстрировали ADCC [KPL-4] при специфическом лизисе 1 мкг/мл примерно 40-60%.
Нефукозилированное антитело (Mab205.10.1, Mab205.10.2, Mab205.10.3) получали путем котрансфекции четырьмя плазмидами, две для экспрессии антитела, одна для экспрессии гибридного полипептида GnTIII (экспрессионный вектор GNT-III) и одна для экспрессии маннозидазы II (экспрессионный вектор маннозидазы II аппарата Гольджи) в соотношении 4:4:1:1, соответственно, в клетках HEK293 или СНО.
ДНК-последовательности тяжелой и легкой цепи полного антитела субклонировали в экспрессионные векторы для клеток млекопитающих (по одному для легкой и тяжелой цепей) под контролем промотора MPSV и перед синтетическим полиА-сайтом, при этом каждый вектор нес последовательности EBV OriP. Антитела получали путем котрансфекции клеток HEK293-EBNA или клеток СНО экспрессионными векторами с тяжелой и легкой цепями антитела, используя подход трансфекции с помощью фосфата кальция. Экспоненциально растущие клетки HEK293-EBNA трансфицировали способом с фосфатом кальция. Для продукции глико-инженерного антитела клетки котрансфицировали четырьмя плазмидами, две для экспрессии антитела, одна для экспрессии гибридного полипептида GnTIII (экспрессионный вектор GnT-III) и одна для экспрессии маннозидазы II (экспрессионный вектор маннозидазы II аппарата Гольджи) в соотношении 4:4:1:1, соответственно. Клетки выращивали как прикрепленные однослойные культуры в Т-образных колбах с использованием культуральной среды DMEM с добавлением 10% FCS, и трансфицировали, когда их комфлюентность составляла от 50 до 80%. Для трансфекции в колбу Т150 15 миллионов клеток высевали за 24 часа до трансфекции в 25 мл культуральной среды DMEM с FCS (конечная концентрация по объему 10%), и клетки помещали в инкубатор с температурой 37°С и с 5% CO2-атмосферой на ночь. Для каждого антитела, которое нужно было получить, раствор ДНК, CaCl2 и воды получали путем смешивания 188 мкг общей плазмидной векторной ДНК (четыре плазмиды, две для экспрессии антитела (одна легкая цепь и одна тяжелая цепь), одна для экспрессии гибридного полипептида GnTIII (экспрессионный вектор GnT-III) и одна для экспрессии маннозидазы II (экспрессионный вектор маннозидазы II аппарата Гольджи) в соотношении 4:4:1:1, соответственно), с водой до конечного объема 938 мкл и с 938 мкл 1М раствора CaCl2. К этому раствору добавляли 1876 мкп 50 мМ HEPES, 280 мМ NaCl, 1,5 мМ раствора Na2HPO4 с рН 7,05, немедленно перемешивали в течение 10 секунд и оставляли при комнатной температуре на 20 секунд. Суспензию разводили 46 мл DMEM с добавлением 2% FCS и делили на две колбы Т150, заменяя ею существующую среду.
Клетки инкубировали при 37°С, 5% СО2 в течение 17-20 часов, после чего среду заменяли 25 мл DMEM, 10% FCS. Кондиционированную культуральную среду собирали через 7 дней после трансфекции путем центрифугирования в течение 15 минут при 210 g, раствор стерилизовали путем фильтрации (через фильтр с размером пор 0,22 мкм) и добавляли азид натрия в конечной концентрации 0,01% w/v и сохраняли при 4°С.
Очищали секретированные нефукозилированные антитела и анализировали олигосахариды, прикрепленные к Fc-области антител, например, с помощью MALDI/TOF-MS (как описано, например, в WO 2008/077546). Для этого анализа олигосахариды ферментативно высвобождали из антител путем расщепления PNGaseF, при этом антитела либо были иммобилизованы на мембране PVDF, либо находились в растворе. Полученный в результате расщепления раствор, содержащий высвобожденные олигосахариды, либо непосредственно подготавливали для анализа MALDI/TOF-MS, либо далее расщепляли с помощью гликозидазы EndoH перед подготовкой образца для анализа MALDI/TOF-MS. Анализируемое количество фукозы в сахарной цепочке на Asn297 составляло 50-20%.
Пример 6
Противоопухолевая эффективность in vivo
Противоопухолевая эффективность in vivo антител Mab205.10.1, Mab205.10.2, Mab205.10.3 может быть обнаружена на моделях опухолей различного происхождения (например, рака легких, SCCHN (сквамозноклточной карциномы головы и шеи), рака молочной железы и рака поджелудочной железы), основанных на трансплантации клетки или фрагмента мышам SCID/beige или nude (голым). В качестве примера приведены данные для модели ксенотрансплантата SCCHN на FaDu (основанной на клеточной линии), модели рака молочной железы на MAXF449 (основанной на фрагменте) и модели NSCLC (немелкоклеточного рака легких) на 7177 (основанной на фрагменте).
Испытание агентов
Нефукозилированное Mab205.10.2 (обозначенное как Mab 205 на фиг.2, 3, 4) было предоставлено в виде стокового раствора от Roche, Пенцберг, Германия. Буфер для антитела включал гистидин. Перед инъекциями стоковый раствор антитела разводили соответствующим образом в буфере.
Клеточные линии и условия культивирования
Человеческие клетки FaDu HNSCC изначально были получены из АТСС. Опухолевую клеточную линию культивировали стандартным образом в среде Игла MEM Eagle с 10% эмбриональной телячьей сыворотки, 2 мМ L-глутамина, 1 мМ пирувата натрия и 0,1 мм NEAA при 37°С в насыщенной водными парами атмосфере с 5% CO2. Культуральные пассажи выполняли путем расщепления 1× трипсином/ЭДТА каждые три дня.
Фрагменты опухоли
Опухолевые фрагменты изначально получали от пациентов и трансплантировали подкожно голым мышам-донорам. Впоследствии опухолевые фрагменты серийно пассировали in vivo. Для доклинического исследования небольшие фрагменты опухоли получали от мышей-доноров и помещали подкожно другим голым мышам (MAXF449, 7177).
Животные
Самок мышей SCID/beige или nude приобретали у производителя (например, Charles River, Зюльцфельд, Германия) и содержали в условиях, свободных от специфических патогенов, с ежедневными циклами 12 часов света/12 часов темноты в соответствии с руководящими принципами (GV-Solas; Felasa; TierschG). Протокол экспериментального исследования был рассмотрен и одобрен местными властями. После получения животных содержали в карантинной части приспособления для животных в течение одной недели, чтобы они привыкли к новой среде обитания и для наблюдения. Постоянный мониторинг здоровья проводили на регулярной основе. Диетическое питание (Provimi Kliba 3337) и воду (подкисленную до рН 2,5-3) предоставляли без ограничения.
Мониторинг
Животных контролировали ежедневно на предмет клинических симптомов и для выявления побочных эффектов. Для мониторинга в течение всего эксперимента фиксировали массу тела животных.
Лечение животных
Лечение животных начали после рандомизации животных после трансплантации клеток или фрагмента, когда средний размер опухоли составлял примерно 100-150 мм3. Антитело вводили в виде единственного агента в количестве 10-25 мг/кг внутрибрюшинно по схеме q7d (раз в неделю) в течение 3-6 недель в зависимости от модели. Соответствующий носитель вводили в те же дни.
Эффективность антитела
A) Ксенотрансплантат FaDu HNSCC
Мышам с ксенотрансплантатом FaDu HNSCC вводили антитело Mab205.10.2 со дня исследования 14 по 35. В результате введение антитела Mab205.10.2 показало значительную противоопухолевую эффективность с остановкой опухолевого роста при подкожном FaDu-ксенотрансплантате. Ингибирование роста опухоли (TGI, Tumor Growth Inhibition) было рассчитано как 98%.
Введение Маб 205 (10 мг/кг, схема q7dx3, внутрибрюшинно) привело к остановке опухолевого роста трансплантированных ксенотрасплантатов FaDu HNSCC (см. фиг.2).
B) Ксенотрансплантат рака молочной железы MAXF449
Мышам с ксенотрансплантатом рака молочной железы MAXF449 вводили антитело Mab205.10.2 со дня исследования 64 по 91. В результате введение антитела Mab205.10.2 показало значительную противоопухолевую эффективность с остановкой опухолевого роста ксенотрансплантатов MAXF449. Ингибирование роста опухоли (TGI) составляло более 100%.
Введение Маб 205 (10 мг/кг, схема q7d, внутрибрюшинно) привело к остановке опухолевого роста трансплантированных ксенотрасплантатов MAXF449 (см. фиг.3).
C) Ксенотрансплантат 7177 NSCLC
Мышам с ксенотрансплантатом 7177 NSCLC вводили антитело Mab205.10.2 со дня исследования 28 по 56. В результате введение антитела Mab205.10.2 показало значительную противоопухолевую эффективность с остановкой опухолевого роста ксенотрансплантатов NSCLC. Ингибирование роста опухоли (TGI) составляло более 100%.
Введение Маб 205 (25 мг/кг, схема q7d, внутрибрюшинно) привело к остановке опухолевого роста трансплантированных ксенотрасплантатов NSCLC (см. фиг.4).
| название | год | авторы | номер документа |
|---|---|---|---|
| НЕКОНКУРЕНТНЫЕ В ОТНОШЕНИИ НЕЙРЕГУЛИНА АЛЛОСТЕРИЧЕСКИЕ АНТИТЕЛА ПРОТИВ ЧЕЛОВЕЧЕСКОГО HER3 И ИХ ПРИМЕНЕНИЯ | 2013 |
|
RU2704228C2 |
| БИСПЕЦИФИЧЕСКИЕ АНТИТЕЛА | 2011 |
|
RU2573588C2 |
| СВЯЗЫВАЮЩИЕ МОЛЕКУЛЫ, СПЕЦИФИЧНЫЕ ПО ОТНОШЕНИЮ К HER3, И ИХ ПРИМЕНЕНИЯ | 2012 |
|
RU2620068C2 |
| АНТИГЕНСВЯЗЫВАЮЩИЕ БЕЛКИ | 2012 |
|
RU2607038C2 |
| ТРИСПЕЦИФИЧНЫЕ СВЯЗЫВАЮЩИЕ МОЛЕКУЛЫ, КОТОРЫЕ СПЕЦИФИЧЕСКИ СВЯЗЫВАЮТ АНТИГЕНЫ МНОЖЕСТВА ЗЛОКАЧЕСТВЕННЫХ ОПУХОЛЕЙ, И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2015 |
|
RU2718692C2 |
| АНТИТЕЛА ПРОТИВ IL2 | 2006 |
|
RU2425054C2 |
| АНТИТЕЛО ПРОТИВ РЕЦЕПТОРА ЭПИДЕРМАЛЬНОГО ФАКТОРА РОСТА | 2013 |
|
RU2652880C2 |
| Антитела к PD-1 и способы их применения | 2015 |
|
RU2701797C2 |
| АНТИТЕЛА, ОБЛАДАЮЩИЕ СПЕЦИФИЧНОСТЬЮ К BTN2, И ИХ ПРИМЕНЕНИЕ | 2018 |
|
RU2794996C2 |
| АНТИ-ICOS АНТИТЕЛА | 2017 |
|
RU2764548C2 |

















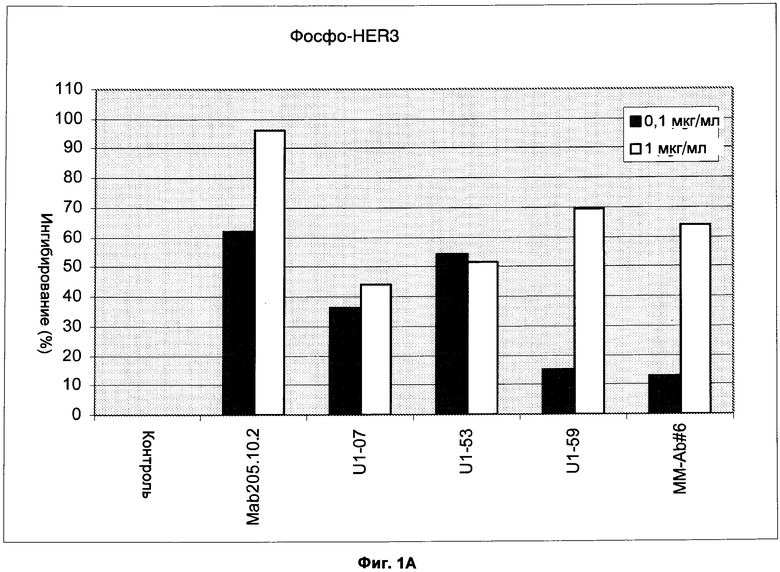
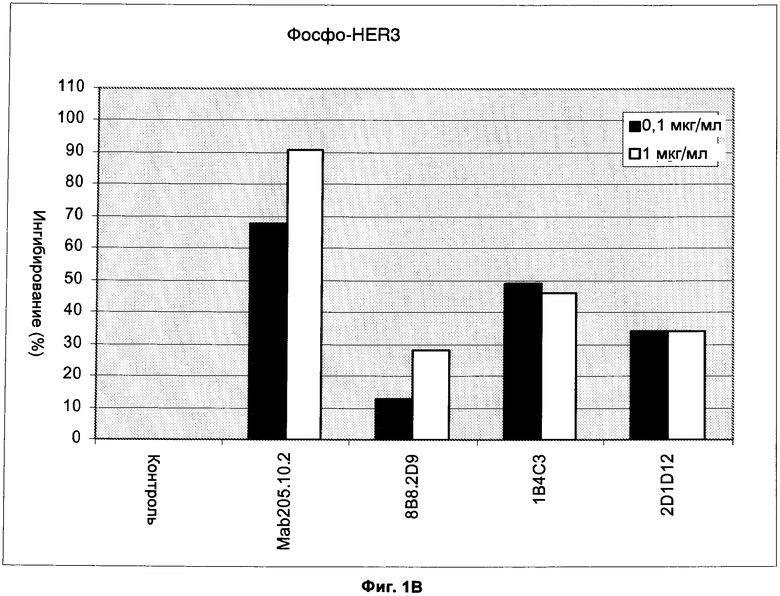
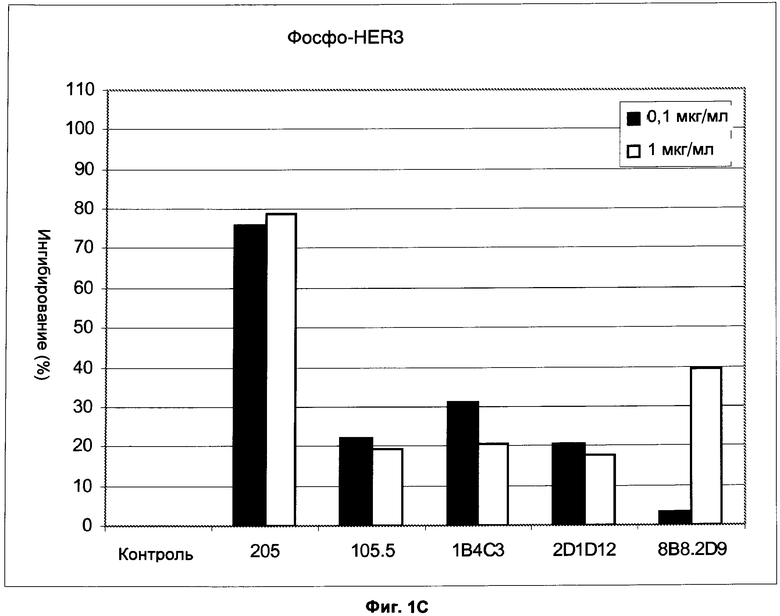
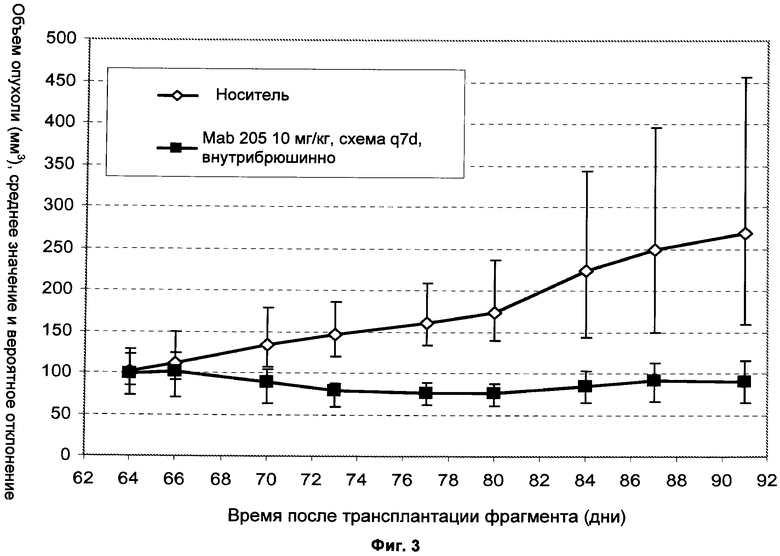
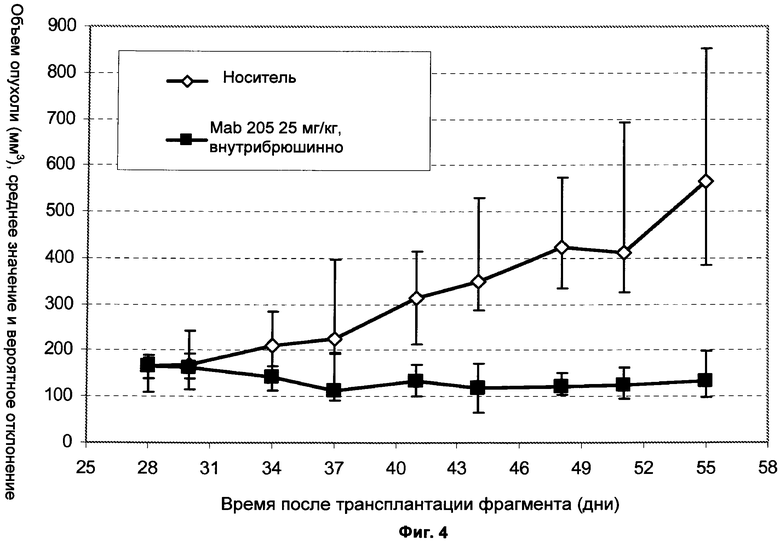
Изобретение относится к области биохимии, в частности к антителам, которые связываются с человеческим HER3, к способу их производства, к фармацевтическим композициям, содержащим указанные антитела, и к их применению для лечения рака. Изобретение позволяет эффективно тормозить рост раковых клеток, экспрессирующих HER3, и HER3-опосредованную передачу сигнала. 7 н. и 7 з.п. ф-лы, 6 ил., 13 табл., 6 пр. 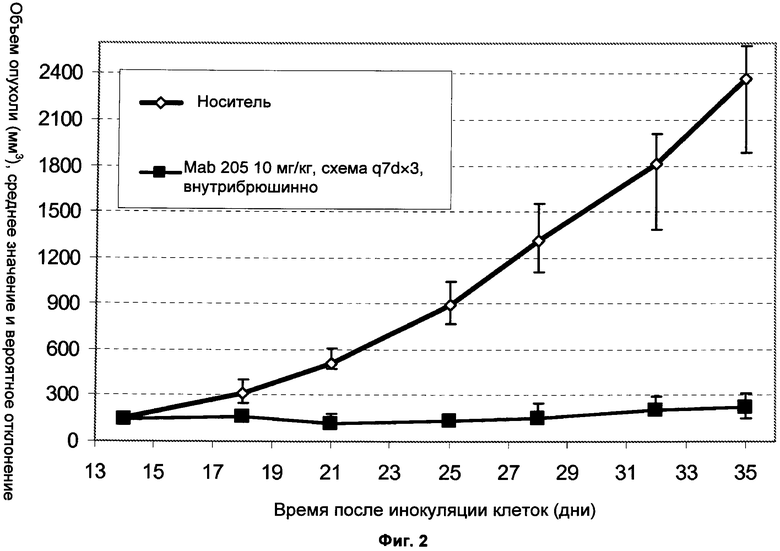
1. Антитело, которое связывается с человеческим HER3, характеризующееся тем, что вариабельный домен тяжелой цепи VH представляет собой SEQ ID NO:8; а вариабельный домен легкой цепи VL представляет собой SEQ ID NO:9, или вариабельный домен легкой цепи VL представляет собой SEQ ID NO:10, или вариабельный домен легкой цепи VL представляет собой SEQ ID NO:11.
2. Антитело по п.1, характеризующееся тем, что вариабельный домен тяжелой цепи VH представляет собой SEQ ID NO:8; а вариабельный домен легкой цепи VL представляет собой SEQ ID NO:10.
3. Антитело по п.1, характеризующееся тем, что вариабельный домен тяжелой цепи VH представляет собой SEQ ID NO:8; а вариабельный домен легкой цепи VL представляет собой SEQ ID NO:9, или вариабельный домен легкой цепи VL представляет собой SEQ ID NO:11.
4. Антитело по пп.1-3, характеризующееся тем, что оно является моноклональным.
5. Антитело по пп.1-4, характеризующееся тем, что оно относится к подклассу lgG1.
6. Антитело по пп.1-5, характеризующееся тем, что оно гликозилировано сахарной цепочкой на Asn297, при этом количество фукозы в указанной сахарной цепочке составляет 65% или ниже.
7. Антитело по п. 6, где количество фукозы в указанной сахарной цепочке составляет от 5% до 65%.
8. Фармацевтическая композиция, обладающая активностью связывания с HER-3, которая характеризуется тем, что содержит антитело по пп.1-7 в эффективном количестве.
9. Антитело по пп.1-7 для лечения рака.
10. Применение антитела по пп.1-7 для изготовления лекарственного средства для лечения рака.
11. Нуклеиновая кислота, кодирующая тяжелую и легкую цепь антитела, которое связывается с человеческим HER3, характеризующаяся тем, что антитело представляет собой антитело по любому из пп.1-7.
12. Экспрессионный вектор, который характеризуется тем, что содержит нуклеиновую кислоту по п.11 для экспрессии антитела по пп.1-7 в прокариотической или эукариотической клетке-хозяине.
13. Прокариотическая или эукариотическая клетка-хозяин для экспрессии антитела по любому из пп.1-7, содержащая вектор по п.12.
14. Способ производства рекомбинантного антитела по пп.1-7, который характеризуется экспрессией нуклеиновой кислоты по п.11 в прокариотической или эукариотической клетке-хозяине и восстановлением указанного антитела из указанной клетки или клеточного культурального супернатанта.
| Электрическое сопротивление для нагревательных приборов и нагревательный элемент для этих приборов | 1922 |
|
SU1997A1 |
| Способ и приспособление для нагревания хлебопекарных камер | 1923 |
|
SU2003A1 |
| Пресс для выдавливания из деревянных дисков заготовок для ниточных катушек | 1923 |
|
SU2007A1 |
| EDWARD HTUN VAN DER HORST ET AL., Anti-HER-3 MAbs inhibit HER-3-mediated signaling in breast cancer cell lines resistant to anti-HER-2 antibodies, International Journal of Cancer, 2005,Vol.115 Issue 4, pp.519-527 | |||
| EA 200801621 A1, 30.12.2008 | |||
| ГЕРШТЕЙН Е.С., | |||
Авторы
Даты
2015-08-20—Публикация
2010-12-17—Подача