Изобретение относится к медицинской микробиологии, может быть использовано для культивирования и идентификации урогенитальных микоплазм, в частности Mycoplasma hominis и Ureaplasma urealyticum, для лабораторной диагностики урогенитальных микоплазмозов путем выявления микоплазм в клиническом материале, для полуколичественного определения титра возбудителя, а также для определения их антибиотикочувствительности.
В последние годы отмечается рост урогенитальных инфекций. Наряду с возбудителями «классических» инфекций, передаваемых половым путем (ИППП), таких как гонорея, сифилис, трихомониаз, урогенитальный хламидиоз, возрастает удельный вес заболеваний, вызванных условно-патогенными микроорганизмами, в том числе урогенитальными микоплазмами.
Согласно данным современных исследователей, более чем у 40% больных с воспалительными заболеваниями органов малого таза выявляются урогенитальные микоплазмы, при этом наибольшее клиническое значение имеют три вида микоплазм: Mycoplasma genitalium, Mycoplasma hominis и Ureaplasma urealyticum.
Mycoplasma hominis и Ureaplasma urealyticum могут являться причиной ряда заболеваний урогенитального тракта: негонококковых уретритов, неспецифических вагинитов, простатитов и эпидермитов, развитием цервицитов и кольпитов, в том числе эндометритов и сальпингитов. Mycoplasma hominis и Ureaplasma urealyticum могут являться этиологическим фактором невынашивания беременности, преждевременных родов, нарушения репродуктивной функции, случаев мертворождения. Частота колонизации урогенитальными микоплазмами нижних отделов мочеполовой системы у детей, по данным различных исследований, варьирует от 2,9 до 22% для Mycoplasma hominis, от 8,3 до 30,4% для Ureaplasma urealyticum. Таким образом, очевидна необходимость специального обследования всех беременных женщин для выявления случаев урогенитального микоплазмоза и последующей санации.
Для выявления Mycoplasma hominis и Ureaplasma urealyticum пользуются различными лабораторными диагностическими методами. Наиболее надежным и простым является культуральный метод диагностики урогенитальных инфекций, в том числе для выявления Mycoplasma hominis и Ureaplasma urealyticum на селективной жидкой питательной среде. Использование этого метода позволяет осуществлять выявление и идентификацию Mycoplasma hominis и Ureaplasma urealyticum, а также проводить полуколичественную оценку титра. Последнее особенно важно для клинической оценки этиологии воспалительных процессов, так как для микоплазменной инфекции этиологическим значением считается концентрация Mycoplasma hominis и Ureaplasma urealyticum в исследуемом материале не менее 10000 КОЕ/мл. Культуральным методом можно определять чувствительность выделенных культур к антибиотикам, что выгодно отличает культуральный метод от других методов диагностики урогенитальных микоплазмозов (полимеразной цепной реакции (ПЦР) и реакции иммунофлюоресценции (РИФ)).
Для реализации культурального метода диагностики Mycoplasma hominis и Ureaplasma urealyticum используются различные наборы реагентов.
Наиболее близким к заявляемому набору реагентов является набор реагентов Mycoplasma IST 2 для диагностики урогенитального микоплазмоза: культивирования, идентификации, полуколичественной оценки титра, определения чувствительности к антибиотикам возбудителей урогенитального микоплазмоза Ureaplasma spp. и Mycoplasma hominis (bioMerieux SA, France, Ref. 42 505, wwwhttp://www.biomerieux.com), состоящий из транспортной лиофилизированной среды Mycoplasma R1 для подготовки исследуемых проб, лиофилизированного мочевино-аргининового бульона Mycoplasma R2 и стрипов с сорбированными в них субстратами (феноловый красный - контроль, феноловый красный и линкомицин - тест на Ureaplasma spp., эритромицин - тест на Mycoplasma hominis) и антибиотиками для определения чувствительности Ureaplasma spp. и Mycoplasma hominis (доксициклин, джозамицин, офлоксацин, эритромицин, тетрациклин, ципрофлоксацин, азитромицин, кларитромицин - в двух концентрациях, пристинамицин - в одной концентрации). Однако данный набор реагентов не позволяет одновременно определить антибиотикочувствительность к каждому возбудителю (Mycoplasma hominis, либо Ureaplasma urealyticum) в случае микс-инфекции.
Изобретение направлено на создание набора реагентов для лабораторной диагностики урогенитальных микоплазмозов, вызываемых Mycoplasma hominis и/или Ureaplasma urealyticum, при этом обеспечен следующий технический результат - одновременное выявление Mycoplasma hominis и Ureaplasma urealyticum, оценка их титра и определение чувствительности к различному спектру антибиотиков.
Набор содержит лиофилизированную транспортную среду для хранения исследуемых проб, лиофилизированную питательную среду для выявления Mycoplasma hominis и/или Ureaplasma urealyticum и стрипы для идентификации Mycoplasma hominis и Ureaplasma urealyticum, для полуколичественного определения титра возбудителя и для определения чувствительности Mycoplasma hominis и Ureaplasma urealyticum к антибиотикам.
Отличительной особенностью набора является то, что он содержит три вида стрипов. Первый вид стрипов предназначен для идентификации Mycoplasma hominis и Ureaplasma urealyticum, а также для полуколичественного определения их титра. Часть лунок первого вида стрипов, которые предназначены для выявления и определения титра Mycoplasma hominis, содержат аргинин, бриллиантовый синий и кларитромицин, другая часть лунок этого стрипа, которые предназначены для выявления и определения титра Ureaplasma urealyticum, содержат мочевину и линкомицин. Второй вид стрипов предназначен для определения антибиотикочувствительности Mycoplasma hominis, содержит специфические реагенты для выявления Mycoplasma hominis - аргинин, бриллиантовый синий и кларитромиц, а также восемь антибиотиков - доксициклин, джозамицин, мидекамицин, офлоксацин, ципрофлоксацин, спарфлоксацин, моксифлоксацин, клиндамицин, сорбированных в лунки стрипов в одной концентрации. Третий вид стрипов предназначен для определения антибиотикочувствительности Ureaplasma urealyticum, содержит специфические реагенты для выявления Ureaplasma urealyticum - мочевина и линкомицин, а также восемь антибиотиков - доксициклин, джозамицин, кларитромицин, эритромицин, рокситромицин, азитромицин, офлоксацин и спарфлоксацин, сорбированных в лунки стрипов в одной концентрации.
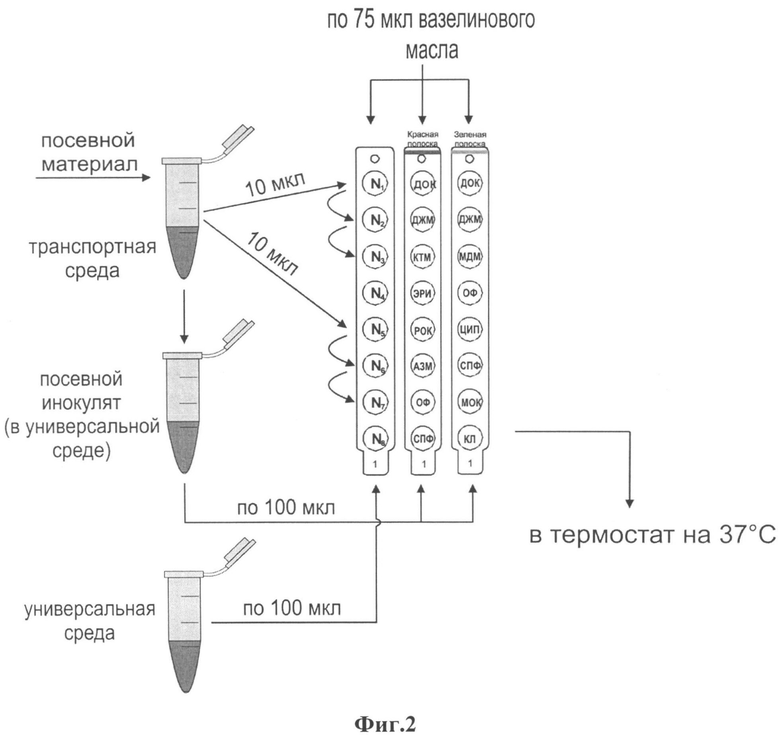
Сущность изобретения поясняется чертежами, где на фиг.1 представлена схема расположения сред, реагентов и проб в лунках стрипов, на фиг.2 представлен способ анализа инфекций, вызываемых Mycoplasma hominis и Ureaplasma urealyticum.
Изобретение реализуется следующим образом.
Пример 1. Приготовление лиофилизированной питательной среды для выявления Mycoplasma hominis и/или Ureaplasma urealyticum.
Селективная универсальная питательная среда для выявления Mycoplasma hominis и Ureaplasma urealyticum содержит питательную основу, стимуляторы роста, селективные компоненты, лошадиную сыворотку, рН-индикатор и дистиллированную воду. В качестве питательной основы служит пептон ферментативный, плацентарный бульон, PPLO бульон и натрий хлористый, в качестве стимуляторов роста - дрожжевой экстракт, и в качестве селективных добавок - антибиотики и противогрибковый препарат.
Плацентарный бульон готовят из свежей плаценты, промытой водопроводной водой и тщательно измельченной. Плаценту помещают в кастрюлю, заливают двойным количеством дистиллированной воды и кипятят в течение 30 мин. Полученный бульон осветляют и стерилизуют автоклавированием.
Дрожжевой экстракт готовят из свежих хлебопекарных дрожжей (ООО «Дю-Ле», Яст Болагет, Швеция, кат. № 00462, 2014 г). Дрожжи помещают в кастрюлю в кипящую дистиллированную воду из расчета 250 г/л, кипятят в течение 40 мин. Полученный экстракт осветляют и стерилизуют автоклавированием.
Содержание питательной среды имеет следующее соотношение ингредиентов (оптимальное), г/л:
Питательная среда содержит селективные добавки - антибиотики и противогрибковый препарат, при следующем соотношении ингредиентов, г/л:
Для приготовления основы питательной среды в 600 мл дистиллированной воды добавляют плацентарный бульон - 160,00 мл, растворяют пептон ферментативный (HiMedia Laboratories Pvt. Limited, Индия, RM 1892, 2014 г.) - 3,20 г, натрий хлористый (хч, Нева Реактив, ГОСТ 4233-77, 2014 г.) - 1,60 г, PPLO бульон б/кф (Pronadisa, Laboratories CONDA, ЗАО «ДиаКон», кат. №1262, 2014 г.) - 10,08 г, феноловый красный (Нева Реактив, PANREAC-131615, 2014 г.) - 0,06 г. Полученную основу среды стерилизуют автоклавированием.
Для приготовления среды в стерильных условиях смешивают основу питательной среды с дрожжевым экстрактом - 100,00 мл, лошадиной сывороткой (ООО «БиолоТ», код: 1.1.5., 2014 г.) - 100,00 мл. Смесь тщательно перемешивают, затем добавляют цефтриаксон - 0,064 г, амоксиклав (амоксициллин натриевая соль / клавулановая кислота калиевая соль) - 0,016 г, ванкомицина гидрохлорид - 0,0020 г, флуконазол - 0,020 г. Устанавливают pH 6,25-6,45, добавляя по каплям 1N соляную кислоту.
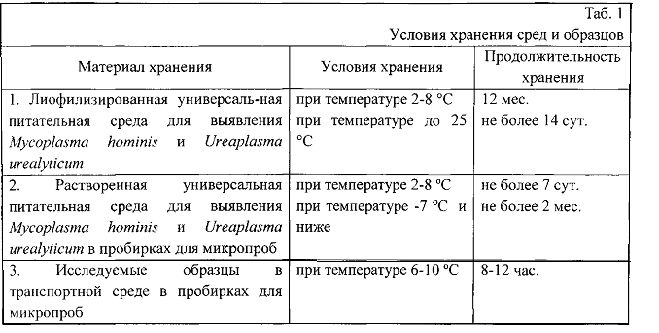
Питательную среду разливают в 50 мл флаконы по 15 мл и лиофильно сушат. Перед использованием флакон с лиофилизированной селективной универсальной питательной средой для выявления Mycoplasma hominis и Ureaplasma urealyticum растворяют 15 мл дистиллированной воды. Условия хранения питательной среды см. таб. 1.
В предложенном составе питательной среды представлено оптимальное количественное соотношение компонентов, концентраций антибиотиков и индикаторного красителя.
Данная питательная среда дает возможность проведения идентификации на сорбированных специфическими реагентами и антибиотиками стрипах выделенных культур микоплазм и оценки их количества (титра) в образцах.
Селективная питательная среда для выявления Mycoplasma hominis и Ureaplasma urealyticum при ее использовании в стрипах, сорбированных специфическими реагентами и антибиотиками, обеспечивает оптимальные условия для роста данного возбудителя при подавлении роста других микоплазм, дрожжеподобных грибов и большинства представителей бактериальной флоры, потенциально содержащихся в исследуемом образце. Наличие в среде pH-индикатора позволяет проводить визуальную оценку результатов исследования по изменению цвета питательной среды в процессе культивирования Mycoplasma hominis и Ureaplasma urealyticum на стрипах за счет проявления ферментативной активности.
Пример 2. Приготовление стрипов, сорбированных специфическими реагентами и антибиотиками.
В используемых вместе с селективной универсальной питательной средой для выявления Mycoplasma hominis и/или Ureaplasma urealyticum стрипах сорбированы специфические реагенты и антибиотики (см. фиг.1). В качестве специфических реагентов в лунках стрипов для выявления и определения антибиотикочувствительности Mycoplasma hominis служат аргинин, бриллиантовый синий и кларитромицин (для подавления роста других видов микоплазм). В качестве специфических реагентов в лунках стрипов для выявления и определения антибиотикочувствительности Ureaplasma urealyticum служат мочевина и линкомицин (для подавления роста других видов микоплазм).
Содержание лунок стрипов, предназначенных для выявления и определения антибиотикочувствительности Mycoplasma hominis, имеет следующее соотношение специфических реагентов и антибиотиков, г/л:
Содержание лунок стрипов, предназначенных для выявления и определения антибиотикочувствительности Ureaplasma urealyticum, имеет следующее соотношение специфических реагентов и антибиотиков, г/л:
Для сорбирования стрипов специфическими реагентами и антибиотиками готовят два раствора. Первый раствор содержит следующие реагенты из расчета концентрации на одну лунку: мочевину (SERVA Feinbiochemica, кат. 39305.01, 2014 г.) - 5,00 г/л, линкомицина гидрохлорид - 0,080 г/л, а второй - L-аргинина гидрохлорид (имп, НТК «Диаэм», кат. № 1119-34-2, 2014 г.) - 50,00 г/л, бриллиантовый синий (Нева Реактив, ACROS-22973, 2014 г.) - 0,15 г/л и кларитромицин - 0,020 г/л. Затем сорбируют по 20 мкл с помощью Labsystems Multidrop в лунки, предназначенные для выявления Ureaplasma urealyticum, первый раствор, а в лунки, предназначенные для выявления Mycoplasma hominis, второй раствор.
Затем в стрипы, предназначенные для определения антибиотикочувствительности Ureaplasma urealyticum, сорбируют по 20 мкл растворы антибиотиков, при этом их концентрации в лунках следующие: доксициклина гидрохлорид - 0,010 г/л, джозамицина - 0,010 г/л, кларитромицина - 0,0050 г/л, эритромицина - 0,0050 г/л, рокситромицина - 0,010 г/л, азитромицина - 0,0050 г/л, офлоксацина - 0,020 г/л, спарфлоксацина 0,0050 г/л. В стрипы, предназначенные для определения антибиотикочувствительности Mycoplasma hominis, сорбируют по 20 мкл растворы антибиотиков, при этом их концентрации в лунках следующие: доксициклина гидрохлорид - 0,010 г/л, джозамицина - 0,010 г/л, мидекамицина - 0,040 г/л, офлоксацина - 0,020 г/л, ципрофлоксацина лактат - 0,010 г/л, спарфлоксацина - 0,0025 г/л, моксифлоксацина - 0,0025 г/л, клиндамицина - 0,010 г/л.
Пример 3. Способ диагностики инфекций, вызываемых Mycoplasma hominis и Ureaplasma urealyticum, с помощью предложенного набора реагентов.
Селективная питательная среда должна обеспечивать рост Mycoplasma hominis и Ureaplasma urealyticum в лунках стрипов, сорбированных специфическими реагентами и антибиотиками, который сопровождается изменением цвета среды с желтого на красный или красно-малиновый в лунках, предназначенных для выявления Ureaplasma urealyticum, за счет проявления уреазной активности, а также изменением цвета среды с зеленого на фиолетовый в лунках, предназначенных для выявления Mycoplasma hominis, за счет проявления ферментативной активности, и тормозить рост сопутствующих микроорганизмов (грамположительных и грамотрицательных бактерий, грибов).
Диагностика инфекций, вызываемых Mycoplasma hominis и Ureaplasma urealyticum, с помощью предложенного набора реагентов включает введение универсальной питательной среды в лунки стрипов с сорбированными в них специфическими реагентами и антибиотиками, исследуемого материала и вещества, создающего анаэробные условия, и анализ изменения цвета питательной среды (см. фиг. 2).
Набор реагентов прост в постановке, не требует специального оборудования, позволяет проводить как выявление возбудителей, так и полуколичественное определение титра и чувствительности к различным антибактериальным препаратам. Использование предложенного набора позволяет повысить скорость, точность и экономичность диагностики микоплазменной инфекции.
Диагностика инфекций, вызываемых Mycoplasma hominis и Ureaplasma urealyticum, с помощью предложенного набора:
1. В лиофилизированную универсальную питательную среду для выявления Mycoplasma hominis и Ureaplasma urealyticum добавляют 15 мл дистиллированной воды и перемешивают до полного растворения (в течение 1 мин).
2. Полученную прозрачную среду желтого цвета разливают по 0,85 мл в пробирки для микропроб (для приготовления инокулятов на антибиотикочувствительность Mycoplasma hominis и Ureaplasma urealyticum) и по 0,8 мл в пробирки для микропроб (для контролей), закрывают и хранят до применения при температуре 2-8°С не более 7 сут или при температуре минус 7°C и ниже не более 2 мес. Перед проведением анализа пробирки со средой выдерживают при комнатной температуре (18-25°C) в течение 1 ч.
3. Анализ состоит из двух этапов:
3.1. Выделение и идентификация урогенитальных микоплазм.
В лунки первого стрипа (без полоски), содержащего различные специфические реагенты, вносят по 90 мкл раствора из пробирки, содержащей 0,8 мл селективной универсальной питательной средой без пробы. При этом среда в лунках, предназначенных для обнаружения, идентификации и полуколичественной оценки титра Ureaplasma urealyticum, окрашивается в желтый цвет, а среда в лунках, предназначенных для обнаружения, идентификации и полуколичественной оценки титра Mycoplasma hominis, окрашивается в зеленый цвет.
Затем из пробирки, содержащей транспортную среду с исследуемой пробой, вносят 10 мкл в лунку N1 и 10 мкл в лунку N5, и делают два последовательных разведения исследуемой пробы с шагом 10. Переносят 10 мкл раствора из лунки N1 в лунку N2 (разведение в 10 раз) и перемешивают пипетированием, затем переносят 10 мкл раствора из лунки N2 в лунку N3 (разведение в 100 раз) и перемешивают пипетированием. После переносят 10 мкл из лунки N5 в лунку N6 (разведение в 10 раз) и перемешивают пипетированием, затем переносят 10 мкл раствора из лунки N6 в лунку N7 (разведение в 100 раз) и перемешивают пипетированием.
3.2. Определение антибиотикочувствительности.
Готовят два инокулята добавлением по 85 мкл раствора из пробирки, содержащей транспортную среду с исследуемой пробой, в две пробирки с селективной универсальной питательной средой для выявления Mycoplasma hominis и Ureaplasma urealyticum (0,85 мл).
Во все лунки стрипов с красной и зеленой полосками (стрипы с антибиотиками) вносят по 100 мкл двух приготовленных инокулятов. Оба стрипа осторожно перемешивают встряхиванием до растворения сорбированных субстратов.
4. Во все лунки стрипов добавляют по 2-3 капли (50-75 мкл) вазелинового масла и стрипы помещают в термостат при температуре 37±1°C.
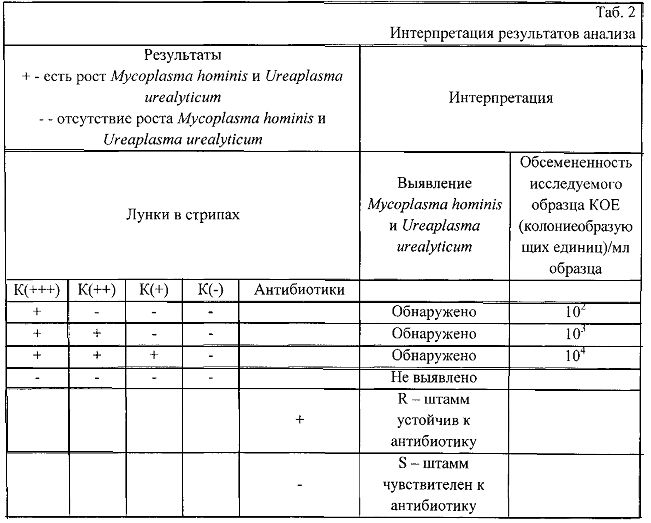
5. Учет результатов проводят через 24 ч для Ureaplasma urealyticum (лунки N1-4) и для Mycoplasma hominis (лунки N5-8). Окончательный учет результатов проводят через 48 ч для Ureaplasma urealyticum (лунки N1-4) и через 72 ч для Mycoplasma hominis (лунки N5-8). Интерпретацию результатов анализа см. таб.2.
5.1. Интерпретация качественного анализа.
В процессе роста микоплазм образуются продукты метаболизма, которые приводят к изменению pH сред. Визуально это проявляется в изменении цвета сред.
Появление красной или красно-малиновой окраски среды (без помутнения) в одной или нескольких лунках N1, N2, и N3 с положительными контролями K(+++), K(++) и K(+) при сохранении исходной желтой окраски среды в контрольной лунке N4 с K(-) свидетельствует о том, что в исследуемой пробе присутствует Ureaplasma urealyticum, т.е. результат является положительным «+».
Отсутствие изменений окраски среды (без помутнения) в лунках N1, N2 и N3 с положительными контролями K(+++), K(++) и K(+) при сохранении исходной желтой окраски среды в контрольной лунке N4 с K(-) свидетельствует о том, что в исследуемой пробе отсутствует Ureaplasma urealyticum, т.е. результат является отрицательным «-».
Появление фиолетовой окраски среды (без помутнения) в одной или нескольких лунках N5, N6 и N7 с положительными контролями K(+++), K(++) и K(+) при сохранении исходной зеленой окраски среды в контрольной лунке N8 с K(-) свидетельствует о том, что в исследуемой пробе присутствует Mycoplasma hominis, т.е. результат является положительным «+».
Отсутствие изменений окраски среды (без помутнения) в лунках N5, N6 и N7 при сохранении исходной зеленой окраски среды в контрольной лунке N8 с K(-) свидетельствует о том, что в исследуемой пробе отсутствуют Mycoplasma hominis, т.е. результат является отрицательным «-».
5.2. Интерпретация полуколичественного анализа.
Изменение окраски среды только в лунке N1 (или N5) с K(+++) при отсутствии изменений в окраске среды в лунках N2, N3 и N4 (или N6, N7 и N8) с K(++), K(+) и K(-) указывает на то, что титры соответствующих возбудителей составляют не более 102 колониеобразующих единиц в мл (КОЕ/мл).
Изменение окраски среды только в лунках N1, N2 (или N5, N6) с K(+++) и K(++) при отсутствии изменений в окраске среды в лунке N3 и N4 (или N7 и N8) с K(+) и K(-) указывает на то, что титры соответствующих возбудителей составляют не более 103 (КОЕ/мл).
Изменение окраски среды в лунках N1, N2, N3 (или N5, N6, N7) с K(+++), K(++) и K(+) при отсутствии изменения в окраске среды в лунке N4 (или N8) с K(-) указывает на то, что титры соответствующих возбудителей составляют не менее 104 (КОЕ/мл).
5.3. Определение антибиотикочувствительности.
В лунках других двух стрипов сорбированы антибиотики. После внесения в эти лунки инокулята сорбированные антибиотики растворяются. При изменении цвета среды «+» в лунках стрипа с антибиотиками (красная полоска) штамм Ureaplasma urealyticum расценивается как резистентный (R). При отсутствии изменения цвета среды «-» - как чувствительный (S).
При изменении цвета среды «+» в лунках стрипа с антибиотиками (зеленая полоска) штамм Mycoplasma hominis расценивается как резистентный (R). При отсутствии изменения цвета среды «-» - как чувствительный (S).
5.3. Примечание.
В исследуемой пробе могут одновременно обнаруживаться Ureaplasma urealyticum и Mycoplasma hominis, что свидетельствует о смешенной инфекции или носительстве.
Помутнение среды (при изменении или без изменения окраски) в какой-либо из лунок свидетельствует о росте посторонней микрофлоры. Результаты исследований таких проб учету не подлежат и требуют повторного проведения анализа или дополнительного посева образца на плотную питательную среду Ureaplasma urealyticum и (или) Mycoplasma hominis.
В качестве транспортной среды используют среду при следующем соотношении ингредиентов,: г/л:
Для проведения диагностики используется следующий клинический материал:
- соскоб клеток влагалища, цервикального канала, слизистой уретры;
- секрет предстательной железы (0,50-0,10 мл), эякулят (0,50-0,10 мл);
- первая порция утренней мочи (осадок, полученный центрифугированием 10 мл первой порции утренней мочи).
Для достоверной диагностики возбудителей урогенитальных уреаплазмозов необходимо стандартное взятие исследуемого материала и соблюдение условия его хранения:
1. Процедура взятия материала должна быть стандартной. Забор проб осуществлять с помощью ложки Фолькмана или одноразового тампона (щетки);
2. Не использовать при взятии материала местных антисептиков;
3. Необходимо брать материал до начала проведения антибактериальной терапии;
4. Важно получить достаточное количество клеток, поскольку уреаплазма является микроорганизмом, колонизирующим клеточную поверхность;
5. Необходимо тщательное удаление слизи из цервикального канала;
6. Взятие уретральных образцов следует проводить не ранее чем через 2-3 часа после мочеиспускания;
7. Получение секрета предстательной железы и эякулята проводить непосредственно после мочеиспускания;
8. Исследуемый материал помещать в специальную транспортную среду, наилучшим образом обеспечивающую сохранение жизнеспособности микоплазм.
9. Пробирки с пробами в транспортной среде закрыть, промаркировать и доставить в лабораторию. Время и условия транспортировки исследуемых образцов см. таб. 1.
| название | год | авторы | номер документа |
|---|---|---|---|
| Тест-система для определения ферментативной активности бактерий по аммиаку | 2018 |
|
RU2715405C1 |
| ЛИОФИЛИЗИРОВАННАЯ ПИТАТЕЛЬНАЯ СРЕДА ДЛЯ ВИЗУАЛЬНОГО ВЫЯВЛЕНИЯ MYCOPLASMA HOMINIS | 2014 |
|
RU2553549C1 |
| ЛИОФИЛИЗИРОВАННАЯ ПИТАТЕЛЬНАЯ СРЕДА ДЛЯ ВИЗУАЛЬНОГО ВЫЯВЛЕНИЯ Ureaplasma urealyticum | 2014 |
|
RU2568062C1 |
| РЕКОМБИНАНТНАЯ ПСЕВДОАДЕНОВИРУСНАЯ ЧАСТИЦА, ПРОДУЦИРУЮЩАЯ МОДИФИЦИРОВАННЫЕ НАНОАНТИТЕЛА, УЗНАЮЩИЕ МИКОПЛАЗМУ M.HOMINIS, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ЕЕ ОСНОВЕ И СПОСОБ ЕЕ ИСПОЛЬЗОВАНИЯ ДЛЯ ТЕРАПИИ МИКОПЛАЗМОЗОВ | 2013 |
|
RU2562158C2 |
| Система олигонуклеотидных праймеров и зонда для выявления ДНК Mycoplasma bovigenitalium | 2019 |
|
RU2732626C1 |
| СПОСОБ ПОЛУЧЕНИЯ ТАРГЕТНОЙ ДНК УРОГЕНИТАЛЬНЫХ МИКОПЛАЗМ, ВЫРАЩЕННЫХ НА СЕЛЕКТИВНОЙ ПИТАТЕЛЬНОЙ СРЕДЕ, ДЛЯ ПОЛНОГЕНОМНОГО СЕКВЕНИРОВАНИЯ | 2019 |
|
RU2715692C1 |
| СПОСОБ ДИФФЕРЕНЦИАЦИИ ШТАММОВ БАКТЕРИЙ ПО ГЕНУ РИБОСОМАЛЬНОЙ РНК | 2008 |
|
RU2386695C1 |
| СПОСОБ ДИФФЕРЕНЦИАЦИИ ШТАММОВ БАКТЕРИЙ Mycoplasma hominis ПО ГЕНУ РИБОСОМАЛЬНОЙ РНК | 2008 |
|
RU2386699C2 |
| Набор синтетических олигонуклеотидов для количественного определения ДНК Ureaplasma parvum, Ureaplasma urealyticum и Mycoplasma hominis в слизистой оболочке влагалища | 2017 |
|
RU2663453C1 |
| Способ оценки морфофункциональных нарушений плаценты при мико- и уреаплазменных инфекциях | 2022 |
|
RU2805830C1 |

Изобретение относится к медицинской микробиологии. Изобретение представляет собой набор для лабораторной диагностики инфекций, вызываемых урогенитальными микоплазмами Mycoplasma hominis и Ureaplasma urealyticum, содержащий лиофилизированную транспортную среду для хранения исследуемых проб, лиофилизированную питательную среду для выявления Mycoplasma hominis и/или Ureaplasma urealyticum и стрипы для идентификации Mycoplasma hominis и Ureaplasma urealyticum, для полуколичественного определения титра возбудителя и для определения чувствительности Mycoplasma hominis и Ureaplasma urealyticum к антибиотикам, который содержит три вида стрипов, первый из которых предназначен для идентификации Mycoplasma hominis и Ureaplasma urealyticum и для полуколичественного определения их титра, причем часть лунок первого вида стрипов, которые предназначены для выявления и определения титра Mycoplasma hominis, содержат аргинин, бриллиантовый синий и кларитромицин, другая часть лунок этого стрипа, которые предназначены для выявления и определения титра Ureaplasma urealyticum, содержат мочевину и линкомицин, второй вид стрипов предназначен для определения антибиотикочувствительности Mycoplasma hominis, содержит специфические реагенты для выявления Mycoplasma hominis - аргинин, бриллиантовый синий и кларитромицин, а также восемь антибиотиков - доксициклин, джозамицин, мидекамицин, офлоксацин, ципрофлоксацин, спарфлоксацин, моксифлоксацин, клиндамицин, сорбированных в лунки стрипов в одной концентрации, третий вид стрипов предназначен для определения антибиотикочувствительности Ureaplasma urealyticum, содержит специфические реагенты для выявления Ureaplasma urealyticum - мочевина и линкомицин, а также восемь антибиотиков - доксициклин, джозамицин, кларитромицин, эритромицин, рокситромицин, азитромицин, офлоксацин и спарфлоксацин, сорбированных в лунки стрипов в одной концентрации. Использование набора позволяет одновременно выявлять Mycoplasma hominis и Ureaplasma urealyticum, оценивать их титр и определять чувствительность к различному спектру антибиотиков, причем для Mycoplasma hominis и для Ureaplasma urealyticum используют разные антибиотики. 2 ил., 2 табл., 3 пр.
Набор для лабораторной диагностики инфекций, вызываемых урогенитальными микоплазмами Mycoplasma hominis и Ureaplasma urealyticum, содержащий лиофилизированную транспортную среду для хранения исследуемых проб, лиофилизированную питательную среду для выявления Mycoplasma hominis и/или Ureaplasma urealyticum и стрипы для идентификации Mycoplasma hominis и Ureaplasma urealyticum, для полуколичественного определения титра возбудителя и для определения чувствительности Mycoplasma hominis и Ureaplasma urealyticum к антибиотикам, отличающийся тем, что он содержит три вида стрипов, первый из которых предназначен для идентификации Mycoplasma hominis и Ureaplasma urealyticum и для полуколичественного определения их титра, причем часть лунок первого вида стрипов, которые предназначены для выявления и определения титра Mycoplasma hominis, содержат аргинин, бриллиантовый синий и кларитромицин, другая часть лунок этого стрипа, которые предназначены для выявления и определения титра Ureaplasma urealyticum, содержат мочевину и линкомицин, второй вид стрипов предназначен для определения антибиотикочувствительности Mycoplasma hominis, содержит специфические реагенты для выявления Mycoplasma hominis - аргинин, бриллиантовый синий и кларитромицин, а также восемь антибиотиков - доксициклин, джозамицин, мидекамицин, офлоксацин, ципрофлоксацин, спарфлоксацин, моксифлоксацин, клиндамицин, сорбированных в лунки стрипов в одной концентрации, третий вид стрипов предназначен для определения антибиотикочувствительности Ureaplasma urealyticum, содержит специфические реагенты для выявления Ureaplasma urealyticum - мочевина и линкомицин, а также восемь антибиотиков - доксициклин, джозамицин, кларитромицин, эритромицин, рокситромицин, азитромицин, офлоксацин и спарфлоксацин, сорбированных в лунки стрипов в одной концентрации.
| РОКА ВИЛЬЧЕС ВАШИНГТОН, Разработка тест-систем для идентификации и определения антибиотикочувствительности возбудителей микоплазмоза: Mycoplasma hominis и Ureaplasma urealyticum, диссертация, Санкт-Петербург, 2005, с.5,8, 43-48, с.63-112, 129 | |||
| БЕЗРУКОВ ВЛАДИСЛАВ МИХАЙЛОВИЧ, Изучение, разработка и стандартизация микротест-системы для выявления и идентификации уреаплазм, диссертация, Москва, 2006, с.22-29, с.65-81, 153 |
Авторы
Даты
2015-06-20—Публикация
2014-04-11—Подача