Настоящее изобретение касается биоразлагаемых нерастворимых в воде гидрогелей на основе полиэтиленгликоля. Настоящее изобретение также касается конъюгатов таких биоразлагаемых гидрогелей с аффинными лигандами или хелатирующими группами или ионообменными группами, связанных с носителем пролекарств, в которых биоразлагаемый гидрогель по настоящему изобретению является носителем, и их фармацевтических композиций, а также их применения в качестве лекарственного средства.
Гидрогели на основе поли(этиленгликоля) (PEG) представляют интерес для таких фармацевтических применений, как ушивание ран, тканевая инженерия и доставка лекарств. Гидрогели на основе PEG представляют собой трехмерные сщитые молекулярные сетки, которые могут поглощать большое количество воды. Гидрогели на основе PEG обычно имеют высокий процент содержания поли(этиленгликолевых) цепочек. Гидрогели на основе PEG известны в данной области техники.
Гидрогель на основе PEG в отсутствие заметных количеств не-PEG-полимеров описан в WO-A 99/14259. В данном документе описаны гидрогели на основе PEG, обладающие контролируемым временем полураспада.
Биоразлагаемые гидрогели на основе PEG обладают преимуществами для многих областей применений in vivo. В особенности из соображений безопасности, является очень предпочтительным придание PEG-гидрогелям способности к биоразложению, если планируется их применение в отношении человека. Способность к биоразложению можно придавать гидрогелю путем введения в него сложноэфирных связей, которые претерпевают спонтанный или ферментативный гидролиз в водной среде in vivo.
Для осуществления самой стадии полимеризации можно применять различные типы реакций, и выбор химии полимеризации предопределяет структуру исходных макромерных соединений. Например, радикальная полимеризация широко использовалась для производства полимеров на основе PEG и для создания биосовместимых гидрогелей (см., например ЕР-А 0627911). Также использовались реакции присоединения в полимеризации гидрогелей из макромеров на основе PEG (WO-A 2008/125655).
Альтернативно, для полимеризации гидрогеля описано применение реакций конденсации или сшивки, в основе которых лежит образование сложного эфира, карбамата, карбоната или имина. Перечисленные связующие фрагменты могут использоваться для придания гидрогелю способности к биоразложению за счет лабильных ароматических карбаматов (WO-A 01/47562) или карбонатов (US-A 2003/0023023), сложных эфиров или иминов (WO-A 99/14259).
В отличие от образования гидролитически лабильных связей во время стадии полимеризации, гидрогелям на основе PEG можно придавать способность к биоразложению за счет наличия гидролитически лабильных сложноэфирных связей в одном из исходных макромерных соединений. В случае применения таких макромеров, содержащих сложноэфирные группы, эффективной реакцией для формирования гидрогеля является реакция образования амидной связи. Таким образом, гидрогель формируется путем реакций конденсации между активированными карбоксильными и аминными функциональными группами, что приводит к созданию трехмерной сетки, образованной устойчивыми к гидролизу амидными связями. Биоразложение затем может происходить посредством гидролиза сложноэфирных групп, наличие которых обеспечивает, по меньшей мере, одно из исходных соединений, входящих в состав сетки гидрогеля.
Биоразлагаемые гидрогели на основе PEG, сформированные посредством образования амидных связей, можно получать из двух разных макромерных исходных соединений, при этом макромер, имеющий более двух аминных функциональных групп, может использоваться в качестве реагента основной цепи, а другой макромер, обычно называемый поперечносшивающим реагентом, имеет по меньшей мере две активированные карбоксильные функциональные группы. Биоразлагаемые сложноэфирные связи могут входить в состав одного из макромеров, например поперечносшивающего реагента. В такой системе кинетику разложения гидрогеля можно фиксировать в виде графика высвобождения неразлагаемого фрагмента макромера из гидрогеля с течение времени. Само собой разумеется, что высвобождаемый неразлагаемый макромер будет конъюгирован через амидные связи с группами, остающимися после разрушения разлагаемого макромера, содержащего сложноэфирные группы, индуцированного гидролизом сложноэфирных групп.
В статье Zhao and Harris et al., J. Pharmaceutical Sciences 87 (1998) 1450-1458, описана кинетика разложения гидрогелей на основе PEG. Для формирования гидрогеля в качестве одного макромера использовались реагирующие с аминами PEG-производные, содержащие сложноэфирные группы, а в качестве второго неразлагаемого макромера применялись разветвленные PEG-амины или белки. На Фиг. 3 в статье Zhao и Harris изображен график высвобождения флуоресцентно-меченого макромера на основе альбумина бычьей сыворотки из разлагаемых гидрогелей на основе PEG. В данном исследовании, в качестве прекурсора использовался меченый альбумин бычьей сыворотки, вместе с 4-разветвленным PEG-тетраамином, или 8-разветвленным PEG-октаамином, или альбумином человеческой сыворотки. Профили разложения фиксировались в буферном растворе (при рН 7, при 37°С) с течением времени, и характеризовались «всплеском» на поздней стадии разложения. Во время стадии всплеска, от 40% до 60% неразлагаемого макромера высвобождалось в течение очень короткого времени, т.е. в течение нескольких часов, в то время как предшествующая фаза задержки разложения гидрогеля составляла от 100 до 400 часов. В настоящем исследовании усилия были сфокусированы на создание такого гидрогеля, для которого не наблюдалось бы «нежелательного всплеска на поздней стадии». Усилия авторов настоящего изобретения увенчались успехом благодаря сокращению времени гелеобразования при формировании гидрогеля, и был достигнут профиль с почти нулевым порядком высвобождения неразлагаемого макромера.
Однако, такой профиль разложения гидрогеля не является предпочтительным в области доставки пролекарств, вследствие продолжительного времени фрагментации гидрогеля во время высвобождения лекарства пролекарством, имеющим в своей основе такие гидрогели.
Поэтому одной задачей настоящего изобретения является разработка гидрогелей, имеющих более удобный профиль разложения, чем у известных биоразлагаемых гидрогелей.
Данная задача решена посредством биоразлагаемого нерастворимого в воде гидрогеля на основе полиэтиленгликоля, содержащего фрагменты основной цепи, которые соединены гидролитически разрушаемыми связями, при этом указанные фрагменты основной цепи дополнительно содержат реакционноспособные функциональные группы, где указанный нерастворимый в воде гидрогель дополнительно отличается тем, что соотношение периода времени, необходимого для полного разложения гидрогеля посредством гидролиза разлагаемых связей на водорастворимые продукты разложения, содержащие один или более фрагментов основной цепи, и периода времени, необходимого для высвобождения первых 10 мол.% водорастворимых продуктов разложения, содержащих один или более фрагментов основной цепи, исходя из общего количества фрагментов основной цепи в гидрогеле, больше 1 и меньше или равно 2, предпочтительно больше 1 или меньше или равно 1.5.
Было обнаружено, что, особенно в области доставки лекарств, желательно, чтобы материал полимерного носителя не присутствовал намного дольше, чем требуется для высвобождения количества лекарства, необходимого для достижения желаемого терапевтического эффекта. Например, если PEG-гидрогели используются в качестве полимерных носителей для связанных с носителем пролекарств, желательно отщепить гидрогель от лекарства до того, как произойдет разрушение материала гидрогеля. Вследствие этого, будет в высшей степени предпочтительно использовать гидрогели, демонстрирующие ярко выраженный эффект всплеска в разложении гидрогеля, поскольку такие гидрогели демонстрируют описанный выше профиль разложения, характеризующийся тем, что период времени, необходимого для полного разложения гидрогеля путем гидролиза разрушаемых связей на водорастворимые продукты разложения, содержащие один или более фрагментов основной цепи, не более чем в два раза (или менее) превосходит период времени, необходимый для высвобождения первых 10 мол.% реакционноспособных функциональных групп, исходя из общего количества реакционноспособных функциональных групп в гидрогеле.
Авторы неожиданно обнаружили, что реакционноспособные биоразлагаемые PEG-гидрогели могут быть сконструированы таким образом, что высвобождение фрагментов основной цепи, несущих функциональные группы (90% или больше) происходит в течение очень короткого промежутка времени в сравнении с предшествующей фазой задержки, в течение которой высвобождаются первые 10% фрагментов основной цепи.
Термин «гидрогель» относится к трехмерной, гидрофильной или амфифильной полимерной сетке, способной поглощать большие количества воды. Такая сетка может состоять из гомополимеров или сополимеров и является нерастворимой из-за наличия ковалентных химических или физических (ионные, гидрофобные взаимодействия, переплетения) сшивок. Сшивки обуславливают структуру сетки и физическую целостность. Гидрогели обладают термодинамической совместимостью с водой, которая позволяет им набухать в водных средах. Цепочки в сетке соединены таким образом, что имеются поры, и значительная часть этих пор имеют размер между 1 нм и 1000 нм.
Термины «гидролитически разрушаемый», "биоразлагаемый" или "гидролитически расщепляемый", "расщепляемый", "авторасщепляемый", или "саморасщепление", "саморасщепление", "обратимый", "неустойчивый" или "временный" в контексте настоящего изобретения относятся к связям и связкам, являющимся неферментативно гидролитически разрушаемым или расщепляемым в физиологических условиях (водный буфер при рН 7.4, 37°С), имеющим время полужизни в диапазоне от одного часа до трех месяцев, включая (но не ограничиваясь только ими) аконитилы, ацетали, амиды, ангидриды карбоновых кислот, сложные эфиры, имины, гидразоны, полуамиды малеиновой кислоты, ортоэфиры, фосфамиды, сложные эфиры фосфорной кислоты, фосфосилиловые эфиры, силиловые эфиры, сложные эфиры сульфокислот, ароматические карбаматы, их комбинации и т.д.
При наличии в гидрогеле по настоящему изобретению в качестве разрушаемой соединяющей функциональной группы, предпочтительными биоразлагаемыми связками являются сложные эфиры карбоновых кислот, карбонаты, сложные эфиры фосфорных кислот и сложные эфиры сульфокислот, и наиболее предпочтительны сложные эфиры карбоновых кислот или карбонаты.
Понятно, что для испытаний in vitro в практических целях могут применяться условия ускоренных испытаний, такие как, например, рН 9, 37°С, водный буфер, При проведении двух последовательных испытаний, в которых изменяется только значение рН (рН 7.4 или рН 9, соответственно), можно вычислить коэффициент, который можно применять в дальнейших испытаниях, проводимых при рН 9, для вычисления эквивалентной кинетики реакции для эксперимента, проводимого при рН 7.4.
Стабильные (долговечные) связки являются неферментативно гидролитически разрушаемыми в физиологических условиях (водный буфер при рН 7.4, 37°С) и имеют времена полужизни от шести месяцев и больше, такие как, например, амиды.
Термин «реагент» относится к промежуточным и исходным соединениям, используемым в процессе сборки с получением биоразлагаемых гидрогелей, конъюгатов и пролекарств по настоящему изобретению.
Термин «химическая функциональная группа» относится к карбоновым кислотам и активированным производным, аминам, малеимиду, тиолам и их производным, сульфоновым кислотам и их производным, карбонатам и их производным, карбаматам и их производным, гидрокси-соединениям, альдегидам, кетонам, гидразинам, изоцианатам, изотиоцианатам, фосфорным кислотам и их производным, фосфоновым кислотам и их производным, галогенацетильным соединениям, алкилгалогенидам, акрилоильным соединениям и другим альфа-бета-ненасыщенным акцепторам Михаэля, арилирующим агентам, таким как арилфториды, гидроксиламину, дисульфидам, таким как пиридил дисульфид, винилсульфонам, винилкетонам, диазоалканам, диазоацетильным соединениям, оксиранам и азиридинам.
Если химическая функциональная группа связывается с другой химической функциональной группой, получаемая химическая структура называется «связкой». Например, реакция амино-группы с карбоксильной группой дает амидную связку.
"Реакционноспособные функциональные группы" представляют собой химические функциональные группы фрагмента основной цепи, которые соединены со сверхразветвленным фрагментом.
«Функциональная группа» - это объединенный термин, используемый в отношении терминов «реакционноспособная функциональная группа», «разрушаемая соединяющая функциональная группа» или «конъюгирующая функциональная группа».
"Разрушаемая соединяющая функциональная группа" представляет собой связку, содержащую биоразлагаемую связь, которая с одной стороны присоединена к спейсерному фрагменту, соединенному с фрагментом основной цепи, а с другой стороны присоединена к поперечносшивающему фрагменту. Термины "разрушаемая соединяющая функциональная группа", "биоразлагаемая соединяющая функциональная группа", "соединяющая биоразлагаемая функциональная группа" и "соединяющая функциональная группа" используются как синонимы.
"Конъюгирующая функциональная группа" содержит аффинный лиганд или хелатирующую группу или ионообменную группу, и стабильную связку, соединяющую указанный аффинный лиганд или хелатирующую группу со сверхразветвленным фрагментом фрагмента основной цепи.
Термины "блокирующая группа" или "концевая группа" используются как синонимы и относятся к фрагментам, которые необратимо (в особенности, стабильно) связываются с реакционноспособными функциональными группами, делая невозможным их дальнейшую реакцию с, например, химическими функциональными группами.
Термин «защитная группа» относится к фрагментам, которые обратимо связываются с реакционноспособными функциональными группами, делая невозможным их реакцию с, например, другими химическими функциональными группами
Термин "сшивающая функциональная группа" относится к химическим функциональным группам, которые принимают участие в реакции радикальной полимеризации и являются частью поперечносшивающего реагента или реагента основной цепи.
Термин "полимеризуемая функциональная группа" относится к химическим функциональным группам, которые принимают участие в реакции сшивающей полимеризации и являются частью поперечносшивающего реагента или реагента основной цепи.
Фрагмент основной цепи может содержать спейсерный фрагмент, который одним концом соединен с фрагментом основной цепи, а другим концом - с поперечносшивающим фрагментом.
Термин "производные" относится к химическим функциональным группам, надлежащим образом замещенным защитными и/или активирующими группами, или к активированным формам соответствующих химических функциональных групп, известным квалифицированным специалистам в данной области. Например, активированные формы карбоксильных групп включают (но не ограничиваются только ими) активные сложные эфиры, такие как эфиры сукцинимида, эфиры бензотриазола, нитрофениловые эфиры, пентафторфениловые эфиры, эфиры азабензотриазола, ацилгалогениды, смешанные или симметричные ангидриды, ацилимидазолы.
Термин "неферментативно разрушаемый линкер" относится к линкерам, гидролитически разрушаемым в физиологических условиях без действия ферментов.
"Небиологически активный линкер" означает линкер, не оказывающий фармакологического действия лекарства (D-H), являющегося производным биологически активного фрагмента.
Термины "спейсер", "спейсерная", "спейсерная молекула" и "спейсерный фрагмент" используются взаимозаменяемо и относятся к любому фрагменту, подходящему для соединения двух блоков, такому как C1-50 алкил, C2-50 алкенил или C2-50 алкинил, и указанные фрагменты необязательно могут включать в состав своей цепочки одну или более групп, выбранных из -NH-, -N(C1-4 алкил)-, -O-, -S-, -С(O)-, -C(O)NH-, -C(O)N(C1-4 алкил)-, -О-С(О)-, -S(O)-, -S(O)2-, 4-7-членного гетероциклила, фенила или нафтила.
Термины «терминальный», «конец» или «дальний конец» относятся к положению функциональной группы или связки в молекуле или фрагменте, в силу чего такая функциональная группа может быть химической функциональной группой, и связка может быть разрушаемой или представлять собой стабильную связку, и характеризоваться расположением рядом или в составе связки между двумя блоками, или на конце олигомерной или полимерной цепи.
Термины «лекарственное средство», «лекарственный фрагмент», «биологически активная молекула», "биологически активный фрагмент", "биологически активное средство" и т.п. используются как синонимы и означают любое вещество, которое может оказывать влияние на любые физические или биохимические свойства биологического организма, включая (но не ограничиваясь только ими) вирусы, бактерии, грибы, растения, животные и людей. В частности, при использовании в настоящем тексте, биологически активные молекулы включают любое вещество, предназначенное для диагностики, лечения, смягчения, излечения или профилактики заболевания у людей или других животных, или для улучшения физического или умственного здоровья людей или животных каким-то иным образом. Примеры биологически активных молекул включают (но не ограничиваются только ими) пептиды, белки, ферменты, низкомолекулярные лекарственные средства (например, небелковые лекарственные средства), красители, липиды, нуклеозиды, олигонуклеотиды, полинуклеотиды, нуклеиновые кислоты, клетки, вирусы, липосомы, микрочастицы и мицеллы. Классы биологически активных средств, которые пригодны для применения по настоящему изобретению, включают (но не ограничиваются только ими) антибиотики, фунгициды, противовирусные средства, противовоспалительные средства, противоопухолевые средства, сердечно-сосудистые средства, успокаивающие средства, гормоны, факторы роста, стероидные средства и т.п.
Выражения «в связанной форме» или «фрагмент» относятся к подструктурам, являющимся частью большей по размеры молекулы. Выражение «в связанной форме» применяется для упрощения обозначения фрагментов путем приведения названия или составления списка реагентов, исходных соединений или гипотетических исходных соединений, хорошо известных в данной области техники, и где выражение «в связанной форме» означает, что, например, один или более радикалов водорода (-Н), или одна или более активирующих или защитных групп, имеющихся в реагентах или исходных соединениях, не присутствует во фрагменте.
Понятно, что все реагенты и фрагменты, содержащие полимерные фрагменты, относятся к макромолекулярным структурам, которые, как известно, варьируются по молекулярному весу, длине цепочки или степени полимеризации, или числу функциональных групп.Структуры, приведенные для реагентов основной цепи, фрагментов основной цепи, поперечносшивающих реагентов и поперечносшивающих фрагментов, таким образом, являются только репрезентативными примерами.
Термин "водорастворимый" относится к продуктам разложения биоразлагаемого гидрогеля по изобретению, отделяемого от нерастворимых в воде продуктов разложения путем фильтрования.
Реагент или фрагмент может быть линейным или разветвленным. Если реагент или фрагмент имеет две терминальные группы, его называют линейным реагентом или фрагментом. Если реагент или фрагмент имеет больше двух терминальных групп, его рассматривают как разветвленный или мульти-функциональный реагент или фрагмент.
Исходные соединения
Биоразлагаемые гидрогели по настоящему изобретению могут полимеризоваться посредством радикальной полимеризации, ионной полимеризации или реакций сшивания.
В случае, если биоразлагаемый гидрогель по настоящему изобретению образуется посредством радикальной или ионной полимеризации, по меньшей мере два исходных соединения для биоразлагаемого гидрогеля по настоящему изобретению представляют собой поперечносшивающие макромономеры или поперечносшивающие мономеры - которые называют поперечносшивающими реагентами, и мульти-функциональный макромономер, который называют реагентом основной цепи. Поперечносшивающий реагент несет по меньшей мере две сшивающие функциональные группы, и реагент основной цепи несет по меньшей мере одну сшивающую функциональную группу и по меньшей мере одну химическую функциональную группу, которая не участвует в стадии полимеризации. Дополнительные разбавляющие мономеры могут присутствовать или отсутствовать.
Подходящие сшивающие функциональные группы включают (но не ограничиваются только ими) радикально полимеризуемые группы, такие как винил, винил-бензол, акрилат, акриламид, метакрилат, метакриламид, и ионно полимеризуемые группы, такие как оксетан, азиридин и оксиран.
В альтернативном способе получения биоразлагаемый гидрогель по настоящему изобретению получают реакцией химического связывания. В таких реакциях, исходным соединением является, по меньшей мере, одно макромолекулярное исходное соединение, имеющее комплементарные функциональные группы, которые вступают в такие реакции, как реакция конденсации или присоединения. В одном альтернативном варианте используется всего одно макромолекулярное исходное соединение, которое представляет собой гетеромультифункциональный реагент основной цепи, содержащий некоторое число полимеризуемых функциональных групп.
Альтернативно, в случае двух или более макромолекулярных исходных соединений, одно из этих исходных соединений представляет собой поперечносшивающий реагент, имеющий по меньшей мере две одинаковые полимеризуемые функциональные группы, а другое исходное соединение представляет собой гомомультифункциональный или гетеромультифункциональный реагент основной цепи, также содержащий несколько полимеризуемых функциональных групп.
Подходящие полимеризуемые функциональные группы, имеющиеся в поперечносшивающем реагенте, включают первичные и вторичные амины, карбоновые кислоты и их производные, малеимид, тиол, гидроксил и другие альфа-бета-ненасыщенные акцепторы Михаэля, такие как винилсульфоновые группы, предпочтительно терминальные первичные и вторичные амины, карбоновые кислоты и их производные, малеимид, тиол, гидроксил и другие альфа-бета-ненасыщенные акцепторы Михаэля, такие как винилсульфоновые группы. Подходящие полимеризуемые функциональные группы, имеющиеся в реагенте основной цепи, включают (но не ограничиваются только ими) первичные и вторичные амины, карбоновые кислоты и их производные, малеимид, тиол, гидроксил и другие альфа-бета-ненасыщенные акцепторы Михаэля, такие как винилсульфоновые группы.
Предпочтительно, фрагмент основной цепи отличается наличием разветвляющегося ядра, от которого отходят, по меньшей мере, три полимерных цепочки на основе PEG. Соответственно, в предпочтительном аспекте настоящего изобретения, реагент основной цепи содержит разветвляющееся ядро, от которого отходят, по меньшей мере, три полимерных цепочки на основе PEG. Такие разветвляющиеся ядра могут состоять из поли- или олигоспиртов в связанной форме, предпочтительно пентаэритритола, трипентаэритритола, гексаглицерина, сахарозы, сорбита фруктозы, маннита, глюкозы, целлюлозы, амилозы, крахмалов, гидроксиалкил-крахмалов, поливиниловых спиртов, декстранов, гиалурононанов, или разветвляющиеся ядра могут состоять из поли- или олигоаминов, таких как орнитин, диаминомасляная кислота, трилизин, тетрализин, пентализин, гексализин, гептализин, октализин, нонализин, декализин, ундекализин, додекализин, тридекализин, тетрадекализин, пентадекализин или олиголизины, полиэтиленимины, поливиниламины.
Предпочтительно, от разветвляющегося ядра отходят 3-16 полимерных цепочек на основе PEG, более предпочтительно 4-8. Предпочтительные разветвляющиеся ядра могут содержать пентаэритритол, трилизин, тетрализин, пентализин, гексализин, гептализин или олиголизин, низкомолекулярные полиэтиленимины, гексаглицерин, трипентаэритритол в связанной форме. Предпочтительно, от разветвляющегося ядра отходят 3-16 полимерных цепочек на основе PEG, более предпочтительно 4-8. Предпочтительно, полимерная цепь на основе PEG представляет собой подходящим образом замещенное производное поли(этиленгликоля).
Термин "полимерная цепь на основе поли(этиленгликоля)" или "цепь на основе PEG" относится к олиго- или полимерной молекулярной цепи.
Предпочтительно, такая полимерная цепь на основе поли(этиленгликоля) присоединена к разветвляющемуся ядру, она представляет собой линейную поли(этиленгликольную) цепь, один конец которой присоединен к разветвляющемуся ядру, а другой - к сверхразветвленному фрагменту. Понятно, что цепь на основе PEG может заканчиваться или прерываться алкильными или арильными группами, необязательно замещенными гетероатомами и химическими функциональными группами.
Если термин "полимерная цепь на основе поли(этиленгликоля)" применяется в отношении поперечносшивающего реагента, он относится к поперечносшивающему фрагменту или цепи, содержащей по меньшей мере 20 мас.% этиленгликольных фрагментов.
Предпочтительные структуры, содержащие полимерные цепочки на основе PEG, отходящие от разветвляющегося ядра, подходящие для реагентов основной цепи, представляют собой мульти-разветвленные PEG-производные, такие как, например, описанные в списке товаров JenKem Technology, USA (доступен для скачивания с www.jenkemusa.com на 28 июля 2009 г), 4-разветвленные PEG-производные (пентаэритритольное ядро), 8-разветвленные PEG-производные (гексаглицериновое ядро) и 8-разветвленные PEG-производные (трипентаэритритольное ядро). Наиболее предпочтительными являются 4-разветвленный PEG-амин (пентаэритритольное ядро) и 4-разветвленный PEG-карбоксил (пентаэритритольное ядро), 8-разветвленный PEG-амин (гексаглицериновое ядро), 8-разветвленный PEG-карбоксил (гексаглицериновое ядро), 8-разветвленный PEG-амин (трипентаэритритольное ядро) и 8-разветвленный PEG-карбоксил (трипентаэритритольное ядро). Предпочтительные молекулярные веса для таких мульти-разветвленных PEG-производных в реагенте основной цепи составляют от 1 кДа до 20 кДа, более предпочтительно от 1 кДа до 15 кДа, и еще более предпочтительно от 1 кДа до 10 кДа. Понятно, что терминальные амино-группы дополнительно конъюгированы, давая соединяющие и реакционноспособные функциональные группы в фрагменте основной цепи.
Термины "разветвляющееся ядро" и "ядро" используются взаимозаменяемо.
Сверхразветвленный дендритный фрагмент имеет полимеризуемые функциональные группы. Предпочтительно, каждый дендритный фрагмент имеет молекулярный вес от 0.4 кДа до 4 кДа, более предпочтительно от 0.4 кДа до 2 кДа. Предпочтительно, каждый дендритный фрагмент содержит, по меньшей мере, 3 разветвления и, по меньшей мере, 4 полимеризуемые функциональные группы, и максимально 63 разветвления и 64 полимеризуемые функциональные группы, предпочтительно, по меньшей мере, 7 разветвлений и, по меньшей мере, 8 полимеризуемых функциональных групп, и максимально 31 разветвление и 32 полимеризуемые функциональные группы.
Примерами таких дендритных фрагментов являются трилизин, тетрализин, пентализин, гексализин, гептализин, октализин, нонализин, декализин, ундекализин, додекализин, тридекализин, тетрадекализин, пентадекализин, гексадекализин, гептадекализин, октадекализин, нонадекализин, орнитин и диаминомасляная кислота. Примерами таких предпочтительных дендритных фрагментов являются трилизин, тетрализин, пентализин, гексализин, гептализин, наиболее предпочтительны трилизин, пентализин или гептализин в связанной форме.
Поперечносшивающий реагент может представлять собой линейную или разветвленную молекулу, и предпочтительно представляет собой линейную молекулу. Если поперечносшивающий реагент содержит две полимеризуемые функциональные группы, его называют "линейный поперечносшивающий реагент"; если поперечносшивающий реагент содержит более двух полимеризуемых функциональных групп, он рассматривается как "разветвленный поперечносшивающий реагент".
Поперечносшивающий реагент имеет на концах две полимеризуемые функциональные группы и может не содержать биоразлагаемую группу или может содержать по меньшей мере одну биоразлагаемую связь. Предпочтительно, поперечносшивающий реагент содержит, по меньшей мере, одну биоразлагаемую связь.
В одном варианте выполнения поперечносшивающий реагент состоит из полимера. Предпочтительно, поперечносшивающие реагенты имеют молекулярный вес в диапазоне от 60 Да до 5 кДа, более предпочтительно от 0.5 кДа до 4 кДа, еще более предпочтительно от 1 кДа до 4 кДа, еще более предпочтительно от 1 кДа до 3 кДа.
Помимо олигомерных или полимерных поперечносшивающих реагентов, могут использоваться низкомолекулярные поперечносшивающие реагенты, особенно когда гидрофильные высокомолекулярные фрагменты основной цепи применяются для формирования биоразлагаемого гидрогеля.
В одном варианте выполнения поперечносшивающий реагент содержит мономеры, соединенные биоразлагаемыми связями, т.е. поперечносшивающий реагент сформирован из мономеров, соединенных биоразлагаемыми связями. Такие полимерные поперечносшивающие реагенты могут содержать до 100 биоразлагаемых связей или более, в зависимости от молекулярного веса поперечносшивающего реагента и молекулярного веса мономерных единиц. Примеры таких поперечносшивающих реагентов могут содержать полимеры на основе поли(молочной кислоты) или поли(гликолевой кислоты).
Предпочтительно, поперечносшивающие реагенты имеют в своей основе PEG, предпочтительно представлены только одной молекулярной цепью на основе PEG. Предпочтительно, поперечносшивающие реагенты на основе поли(этиленгликоля) представляют собой углеводородные цепочки, содержащие соединенные единицы этиленгликоля, где поперечносшивающие реагенты на основе поли(этиленгликоля) содержат каждый, по меньшей мере, m единиц этиленгликоля, и где m представляет собой целое число в диапазоне от 3 до 100, предпочтительно от 10 до 70. Предпочтительно, поперечносшивающие реагенты на основе поли(этиленгликоля) имеют молекулярный вес в диапазоне от 0.5 кДа до 5 кДа.
Пример упрощенного реагента основной цепи изображен на Фиг. 1 для иллюстрации использующейся терминологии. От центрального разветвляющегося ядра (©) отходят четыре полимерные цепочки на основе PEG (тонкая черная линия), по концам которых присоединены сверхразветвленные дендритные фрагменты ("Hyp"; овалы). Сверхразветвленные дендритные фрагменты несут полимеризуемые функциональные группы (маленькие белые кружки), из которых показана только часть, т.е. сверхразветвленный дендритный фрагмент содержит больше реакционноспособных функциональных групп, чем показано на Фиг. 1.
На Фиг. 2 показаны четыре примера поперечносшивающих реагентов. Помимо их полимеризуемых функциональных групп (маленькие белые кружки), поперечносшивающие реагенты могут содержать одну или более биоразлагаемых связок (белые стрелки), которые содержат биоразлагаемую связь.
Поперечносшивающий реагент 2А не содержит биоразлагаемой связи. Если такие поперечносшивающие реагенты используются для синтеза биоразлагаемого гидрогеля, образуются биоразлагаемые связки по реакции полимеризуемой функциональной группы поперечносшивающего реагента с полимеризуемой функциональной группой реагента основной цепи.
Поперечносшивающий реагент 2В содержит одну биоразлагаемую связку, поперечносшивающий реагент 2С содержит две биоразлагаемые связки, и Поперечносшивающий реагент 2D содержит четыре биоразлагаемые связки.
Участок между полимеризуемой группой и первой биоразлагаемой связью называется спейсер и обозначается в различных поперечносшивающих фрагментах звездочками, где это применимо.
Реакционноспособный биоразлагаемый гидрогель
Реакционноспособный биоразлагаемый гидрогель по настоящему изобретению представляет собой мульти-функционализованный материал, то есть содержит реакционноспособные функциональные группы и соединяющие функциональные группы в виде трехмерной сшитой матрицы, набухающей в воде.
Реакционноспособный биоразлагаемый гидрогель состоит из фрагментов основной цепи, связанных гидролитически разрушаемыми связями, и фрагменты основной цепи могут быть соединены посредством поперечносшивающих фрагментов.
В одном варианте выполнения фрагменты основной цепи реакционноспособного биоразлагаемого гидрогеля могут быть соединены напрямую, т.е. без поперечносшивающих фрагментов. Сверхразветвленные дендритные фрагменты двух фрагментов основной цепи такого реакционноспособного биоразлагаемого гидрогеля могут быть напрямую связаны через соединяющую функциональную группу, соединяющую два сверхразветвленных дендритных фрагмента. В альтернативном случае, два сверхразветвленных дендритных фрагмента двух разных фрагментов основной цепи могут быть соединены через два спейсерных фрагмента, разделенных соединяющим функциональным фрагментом.
Предпочтительно, реакционноспособный биоразлагаемый гидрогель состоит из фрагментов основной цепи, связанных гидролитически разрушаемыми связями, и фрагменты основной цепи соединены посредством поперечносшивающих фрагментов.
Термин биоразлагаемая или гидролитически разрушаемая связь описывает связки, которые являются неферментативно гидролитически разрушаемыми в физиологических условиях (водный буфер при рН 7.4, 37°С), времена их полужизни находятся в диапазоне от одного часа до трех месяцев, они включают (но не ограничиваются только ими), аконитилы, ацетали, ангидриды карбоновых кислот, сложные эфиры, имины, гидразоны, полуамиды малеиновой кислоты, ортоэфиры, фосфамиды, сложные эфиры фосфорной кислоты, фосфосилиловые эфиры, силиловые эфиры, сложные эфиры сульфокислот, ароматические карбаматы, их комбинации и т.д. Предпочтительные биоразлагаемые связки представляют собой сложные эфиры, карбонаты, сложные эфиры фосфорной кислоты и сложные эфиры сульфокислот, а наиболее предпочтительными являются сложные эфиры или карбонаты.
В реакционноспособных биоразлагаемых гидрогелях по настоящему изобретению, скорость гидролиза биоразлагаемых связей между фрагментами основной цепи и поперечносшивающими фрагментами определяется числом и типом соединенных атомов в спейсерных фрагментах между сверхразветвленным фрагментом и соединяющими функциональными группами. Например, выбирая из янтарной, адипиновой или глутаровой кислот для формирования поперечносшивающего PEG-сложного эфира, можно варьировать время полужизни реакционноспособного биоразлагаемого гидрогеля.
Каждый поперечносшивающий фрагмент имеет на концах, по меньшей мере, две гидролитически разрушаемые связи. Помимо концевых биоразлагаемых связей, поперечносшивающие фрагменты могут содержать дополнительные биоразлагаемые связи. Таким образом, каждый конец поперечносшивающего фрагмента, связанный с фрагментом основной цепи, содержит гидролитически разрушаемую связь, и в поперечносшивающем фрагменте необязательно могут присутствовать дополнительные биоразлагаемые связи.
Реакционноспособный биоразлагаемый гидрогель может содержать один или более различных типов поперечносшивающих фрагментов, предпочтительно один, поперечносшивающий фрагмент может представлять собой линейную или разветвленную молекулу, и предпочтительно представляет собой линейную молекулу. В предпочтительном варианте выполнения настоящего изобретения, поперечносшивающий фрагмент связан с фрагментами основной цепи, по меньшей мере, двумя биоразлагаемыми связями.
Предпочтительно, поперечносшивающие фрагменты имеют молекулярный вес в диапазоне от 60 Да до 5 кДа, более предпочтительно, от 0.5 кДа до 4 кДа, еще более предпочтительно от 1 кДа до 4 кДа, еще более предпочтительно от 1 кДа до 3 кДа. В одном варианте выполнения поперечносшивающий фрагмент состоит из полимера.
Альтернативно, могут применяться низкомолекулярные поперечносшивающие фрагменты, особенно когда для формирования реакционноспособного биоразлагаемого гидрогеля применяются гидрофильные высокомолекулярные фрагменты основной цепи.
В одном варианте выполнения изобретения мономеры, составляющие полимерные поперечносшивающие фрагменты, соединены биоразлагаемыми связями. Такие полимерные поперечносшивающие фрагменты могут содержать до 100 биоразлагаемых связей или более, в зависимости от молекулярного веса поперечносшивающего фрагмента и молекулярного веса мономерных единиц. Примерами таких поперечносшивающих фрагментов являются полимеры на основе поли(гликолевой кислоты). Понятно, что такая цепь на основе поли(молочной кислоты) или поли(гликолевой кислоты) может заканчиваться или прерываться алкильными или арильными группами, необязательно замещенными гетероатомами и химическими функциональными группами
Предпочтительно, поперечносшивающие фрагменты имеют в своей основе PEG, предпочтительно представлены только одной молекулярной цепью на основе PEG. Предпочтительно, поперечносшивающие реагенты на основе поли(этиленгликоля) представляют собой углеводородные цепочки, содержащие единицы этиленгликоля, необязательно содержащие дополнительные химические функциональные группы, где поперечносшивающие фрагменты на основе поли(этиленгликоля) содержат каждый, по меньшей мере, m единиц этиленгликоля, где m представляет собой целое число в диапазоне от 3 до 100, предпочтительно от 10 до 70. Предпочтительно, поперечносшивающие фрагменты на основе поли(этиленгликоля) имеют молекулярный вес в диапазоне от 0,5 кДа до 5 кДа.
Если термин "на основе PEG" применяется в отношении поперечносшивающего фрагмента или полимерной цепи на основе PEG, присоединенной к разветвляющемуся ядру, он относится к поперечносшивающему фрагменту или полимерной цепи на основе PEG, содержащей, по меньшей мере, 20 мас.% этилен гликольных фрагментов.
Понятно, что полимерная цепь на основе PEG может заканчиваться или прерываться алкильными или арильными группами, необязательно замещенными гетероатомами и химическими функциональными группами.
В предпочтительном варианте выполнения настоящего изобретения, поперечносшивающий фрагмент состоит из PEG, который симметрично присоединен через сложноэфирные связи к двум альфа, омега-алифатическим дикарбоновым спейсерам фрагментов основной цепи, соединенных со сверхразветвленным дендритным фрагментом посредством стабильных амидных связей.
Дикарбоновые кислоты спейсерных фрагментов состоят из 3 - 12 атомов углерода, наиболее предпочтительно из 5 - 8 атомов углерода, и могут быть замещены по одному или более атомам углерода. Предпочтительные заместители представляют собой алкильные группы, гидроксильные группы или амидные группы или замещенные аминогруппы. Одна или более из метиленовых групп алифатических дикарбоновых кислот может необязательно быть замещена на О или NH или алкил-замещенный N. Предпочтительный алкил представляет собой линейный или разветвленный алкил, содержащий от 1 до 6 атомов углерода.
Предпочтительно, фрагмент основной цепи отличается наличием разветвляющегося ядра, от которого отходят, по меньшей мере, три полимерные цепочки на основе PEG. Соответственно, в предпочтительном аспекте настоящего изобретения фрагмент основной цепи содержит разветвляющееся ядро, от которого отходят по меньшей мере три полимерные цепочки на основе PEG. Такие разветвляющиеся ядра могут состоять из поли- или олигоспиртов в связанной форме, предпочтительно пентаэритритол, трипентаэритритол, гексаглицерин, сахарозу, сорбит, фруктозу, маннит, глюкозу, целлюлозу, амилозы, крахмалы, гидроксиалкил-крахмалы, поливиниловые спирты, декстраны, гиалурононаны, или разветвляющиеся ядра могут содержать в связанной форме поли- или олигоамины, такие как трилизин, тетрализин, пентализин, гексализин, гептализин, октализин, нонализин, декализин, ундекализин, додекализин, тридекализин, тетрадекализин, пентализин или олиголизины, полиэтиленимины, поливиниламины.
Предпочтительно, от разветвляющегося ядра отходят 3-16 полимерных цепочек на основе PEG, более предпочтительно 4-8. Предпочтительные разветвляющиеся ядра могут содержать пентаэритритол, орнитин, диаминомасляную кислоту, трилизин, тетрализин, пентализин, гексализин, гептализин или олиголизин, низкомолекулярные полиэтиленимины, гексаглицерин, трипентаэритритол в связанной форме. Предпочтительно, от разветвляющегося ядра отходят 3-16 полимерных цепочек на основе PEG, более предпочтительно 4-8. Предпочтительно, полимерная цепь на основе PEG представляет собой подходящим образом замещенное производное поли(этиленгликоля).
Предпочтительно, такая полимерная цепь на основе PEG, присоединенная к разветвляющемуся ядру, представляет собой линейную поли(этиленгликольную) цепочку, в которой один конец присоединен к разветвляющемуся ядру, а другой - к сверхразветвленному дендритному фрагменту. Понятно, что цепь на основе PEG может заканчиваться или прерываться алкильными или арильными группами, необязательно замещенными гетероатомами и химическими функциональными группами.
Предпочтительные структуры, содержащие полимерные цепочки на основе PEG, отходящие от разветвляющегося ядра, подходящие для фрагментов основной цепи, представляют собой мульти-разветвленные PEG-производные, такие как, например, описанные в списке товаров JenKem Technology, USA (доступен для скачивания с www.jenkemusa.com на 28 июля 2009 г), 4-разветвленные PEG-производные (пентаэритритольное ядро), 8-разветвленные PEG-производные (гексаглицериновое ядро) и 8-разветвленные PEG-производные (трипентаэритритольное ядро). Наиболее предпочтительными являются 4-разветвленный PEG-амин (пентаэритритольное ядро) и 4-разветвленный PEG-карбоксил (пентаэритритольное ядро), 8-разветвленный PEG-амин (гексаглицериновое ядро), 8-разветвленный PEG-карбоксил (гексаглицериновое ядро), 8-разветвленный PEG-амин (трипентаэритритольное ядро) и 8-разветвленный PEG-карбоксил (трипентаэритритольное ядро). Предпочтительные молекулярные веса для таких мульти-разветвленных PEG-производных в реагенте основной цепи составляют от 1 кДа до 20 кДа, более предпочтительно от 1 кДа до 15 кДа, и еще более предпочтительно от 1 кДа до 10 кДа. Понятно, что терминальные амино-группы описанных выше мульти-разветвленных молекул присутствуют в связанной форме в фрагменте основной цепи, давая дополнительные соединяющие функциональные группы и реакционноспособные функциональные группы в фрагменте основной цепи.
Такие дополнительные функциональные группы могут предоставляться дендритными фрагментами. Предпочтительно, каждый дендритный фрагмент имеет молекулярный вес от 0,4 кДа до 4 кДа, более предпочтительно от 0,4 кДа до 2 кДа. Предпочтительно, каждый дендритный фрагмент имеет, по меньшей мере, 3 разветвления и, по меньшей мере, 4 реакционноспособные функциональные группы, и, по большей мере, 63 разветвления и 64 реакционноспособные функциональные группы, предпочтительно, по меньшей мере, 7 разветвлений и, по меньшей мере, 8 реакционноспособных функциональных групп, и, по большей мере, 31 разветвление и 32 реакционноспособные функциональные группы.
Примеры таких дендритных фрагментов включают трилизин, тетрализин, пентализин, гексализин, гептализин, октализин, нонализин, декализин, ундекализин, додекализин, тридекализин, тетрадекализин, пентадекализин, гексадекализин, гептадекализин, октадекализин, нонадекализин в связанной форме. Примеры таких предпочтительных дендритных фрагментов включают трилизин, тетрализин, пентализин, гексализин, гептализин, наиболее предпочтительны трилизин, пентализин или гептализин в связанной форме.
Предпочтительно, чтобы общее число соединяющих функциональных групп и реакционноспособных функциональных групп фрагмента основной цепи было равномерно поделено между несколькими полимерными цепочками на основе PEG, отходящими от разветвляющегося ядра. Например, если имеется 32 соединяющие функциональные группы и реакционноспособные функциональные группы, по 8 групп может быть предоставлено каждой из четырех полимерных цепочек на основе PEG, отходящих от ядра, предпочтительно посредством дендритных фрагментов, присоединенных к концу каждой полимерной цепи на основе PEG. Альтернативно, по 4 группы может быть предоставлено каждой из восьми полимерных цепочек на основе PEG, отходящих от ядра, или по 2 группы может быть предоставлено каждой из шестнадцати полимерных цепочек на основе PEG.
Если число полимерных цепочек на основе PEG, отходящих от разветвляющегося ядра, не допускает равномерного распределения, предпочтительно, чтобы отклонение от среднего числа суммы соединяющих функциональных групп и реакционноспособных функциональных групп для каждой полимерной цепи на основе PEG сводилось к минимуму.
Реакционноспособные функциональные группы могут играть роль точек присоединения для прямого или опосредованного связывания с аффинным лигандом, хелатирующей группой, ионообменной группой, лекарственным средством, пролекарством, связанным с носителем пролекарством, блокирующей группой, концевой группой или тому подобными.
В идеале, реакционноспособные функциональные группы равномерно распределены во всем объеме реакционноспособного биоразлагаемого гидрогеля, и могут присутствовать или не присутствовать на поверхности реакционноспособного биоразлагаемого гидрогеля. Неограничивающие примеры таких реакционноспособных функциональных групп включают (но не ограничиваются только ими) следующие химические функциональные группы, присоединенные к сверхразветвленному дендритному фрагменту:
карбоновые кислоты и активированные производные, амины, малеимид, тиолы и их производные, сульфоновые кислоты и их производные, карбонаты и их производные, карбаматы и их производные, гидрокси-соединения, альдегиды, кетоны, гидразины, изоцианаты, изотиоцианаты, фосфорные кислоты и их производные, фосфоновые кислоты и их производные, галогенацетилы, алкилгалогениды, акрилоильные соединения и другие альфа-бета-ненасыщенные акцепторы Михаэля, арилирующие агенты, такие как арилфториды, гидроксиламин, дисульфиды, такие как пиридил дисульфид, винилсульфоны, винилкетоны, диазоалканы, диазоацетильные соединения, оксиран и азиридин. Предпочтительные реакционноспособные функциональные группы включают тиолы, малеимид, амины, карбоновые кислоты и производные, карбонаты и их производные, карбаматы и их производные, альдегиды и галогенацетилы. Предпочтительно, реакционноспособные функциональные группы представляют собой первичные амино-группы или карбоновые кислоты, наиболее предпочтительно - первичные аминогруппы.
Такие реакционноспособные функциональные группы характеризуются тем, что их можно хемоселективно вводить в присутствии других функциональных групп, и также характеризуются тем, что концентрация реакционноспособных функциональных групп в таких реакционноспособных биоразлагаемых гидрогелях практически стабильна в первую половины времени, необходимого для полного разложения реакционноспособного биоразлагаемого гидрогеля.
"Практически стабильная" весовая концентрация указанных реакционноспособных функциональных групп означает, что она не опускается ниже 90% изначальной концентрации в первую половину времени, необходимого для полного разложения реакционноспособного биоразлагаемого гидрогеля.
Реакционноспособные функциональные группы могут завершаться подходящими защитными реагентами.
Наиболее предпочтительно, реакционноспособный биоразлагаемый гидрогель по настоящему изобретению характеризуется тем, что фрагмент основной цепи имеет четвертичный атом углерода в формуле С(А-Нур)4, где каждый А независимо представляет собой полимерную цепь на основе поли(этиленгликоля), терминально присоединенную к четвертичному атому углерода стабильной ковалентной связью, и дистальный конец полимерной цепи на основе PEG ковалентно связан с дендритным фрагментом Hyp, каждый дендритный фрагмент Hyp содержит по меньшей мере четыре функциональные группы, представляющие собой соединяющие и реакционноспособные функциональные группы.
Предпочтительно, каждый А независимо выбран из формулы -(CH2)n1(OCH2CH2)nX-, где n1 равен 1 или 2; n представляет собой целое число в диапазоне от 5 до 50; и Х представляет собой химическую функциональную группу, ковалентно связывающую А и Hyp.
Предпочтительно, А и Hyp ковалентно связаны амидной связкой.
Предпочтительно, дендритный фрагмент Hyp представляет собой сверхразветвленный полипептид. Предпочтительно, сверхразветвленный полипептид состоит из остатков лизина в связанной форме. Предпочтительно, каждый дендритный фрагмент Hyp имеет молекулярный вес от 0.4 кДа до 4 кДа. Понятно, что фрагмент основной цепи С(А-Нур)4 может состоять из одинаковых или разных дендритных фрагментов Hyp, и что каждый Hyp может быть выбран независимо. Каждый фрагмент Hyp состоит из 5-32 лизинов, предпочтительно по меньшей мере из 7 лизинов, т.е. каждый фрагмент Hyp состоит из 5-32 лизинов в связанной форме, предпочтительно по меньшей мере из 7 лизинов в связанной форме. Наиболее предпочтительно, Hyp состоит из гептализинила.
Предпочтительно, имеется стабильная амидная связь между сверхразветвленным дендритным фрагментом и спейсерным фрагментом.
Предпочтительно, С(А-Нур)4 имеет молекулярный вес от 1 кДа до 20 кДа, более предпочтительно от 1 кДа до 15 кДа, и еще более предпочтительно от 1 кДа до 10кДа.
В реакционноспособном биоразлагаемом гидрогеле по настоящему изобретению, фрагмент основной цепи характеризуется числом функциональных групп, состоящим из соединяющих биоразлагаемых групп и реакционноспособных функциональных групп. Предпочтительно, сумма соединяющих биоразлагаемых групп и реакционноспособных функциональных групп больше или равна 16, предпочтительно 16-128, предпочтительно 20-100, также предпочтительно 20-40, более предпочтительно 24-80, также более предпочтительно 28-32, еще более предпочтительно 30-60; наиболее предпочтительно 30-32. Понятно, что помимо соединяющих функциональных групп и реакционноспособных функциональных групп могут также присутствовать защитные группы.
На Фиг. 3 представлен схематичный обзор различных способов, которыми два фрагмента основной цепи могут быть соединены в реакционноспособный биоразлагаемый гидрогель по настоящему изобретению. Сверхразветвленный дендритный фрагмент ("Hyp", овал) содержит несколько реакционноспособных функциональных групп (черные точки) и стабильную связку (белый ромб). Понятно, что каждый Сверхразветвленный фрагмент содержит больше реакционноспособных функциональных групп и стабильных связок, чем показано на Фиг. 3, и что Фиг. 3 приведена исключительно в иллюстративных целях.
Спейсерные фрагменты указаны звездочками, соединяющие функциональные группы представлены в виде белых стрел. Пунктирные линии указывают место присоединения к большему фрагменту, который не показан.
Фиг. 3а иллюстрирует участок реакционноспособного биоразлагаемого гидрогеля, в котором отдельные фрагменты основной цепи соединены напрямую через соединяющую функциональную группу, содержащую биоразлагаемую связь.
На Фиг. 3b сверхразветвленные дендритные фрагменты двух разных фрагментов основной цепи соединены через две соединяющие функциональные группы, разделенные спейсерным фрагментом.
На Фиг. 3с сверхразветвленные дендритные фрагменты двух разных фрагментов основной цепи соединены через два спейсерных фрагмента и одну соединяющую функциональную группу.
На Фиг. 3d и 3е изображен участок реакционноспособного биоразлагаемого гидрогеля, в котором два сверхразветвленных дендритных фрагмента соединены через поперечносшивающие фрагменты, обозначенные символом "#". Поперечносшивающие фрагменты могут содержать или не содержать по меньшей мере одну соединяющую функциональную группу (см. Фиг. 3d и 3е, соответственно).
Тонкие черные линии обозначают полимерные цепочки на основе PEG, отходящие от разветвляющегося ядра (не показано).
Модифицированный реакционноспособный биоразлагаемый гидрогель
Другой аспект настоящего изобретения представляет собой конъюгат, содержащий модифицированный реакционноспособный биоразлагаемый гидрогель по настоящему изобретению, отличающийся тем, что он состоит из фрагментов основной цепи, связанных гидролитически разрушаемыми связями, и дополнительно несущих стабильные связки к спейсерным молекулам, блокирующим группам, защитным группам или мульти-функциональным фрагментам.
Реакционноспособные функциональные группы фрагментов основной цепи реакционноспособных биоразлагаемых гидрогелей служат точками присоединения для спейсерных молекул, блокирующих групп, защитных групп или мульти-функциональных фрагментов.
Защитные группы известны в данной области и применяются для обратимой защиты химических функциональных групп в процессе синтеза. Подходящей защитной группой для амино-групп является fmoc-группа.
Понятно, что может применяться один тип защитной группы или две или более разных защитных групп, так чтобы обеспечить независимую защиту, т.е. разные защитные группы могут быть удалены в разных условиях.
Модифицированный реакционноспособный биоразлагаемый гидрогель по настоящему изобретению можно функционализировать с помощью спейсера, несущего такую же реакционноспособную функциональную группу. Например, амино-группы можно ввести в модифицированный реакционноспособный биоразлагаемый гидрогель сочетанием с гетеробифункциональным спейсером, таким как надлежащим образом активированный COOH-(EG)6-NH-fmoc (EG=этиленгликоль), и удалением fmoc-защитной группы. Такой реакционноспособный биоразлагаемый гидрогель можно далее соединить со спейсером, несущим другую функциональную группу, такую как малеимидная группа. Соответствующим образом модифицированный реакционноспособный биоразлагаемый гидрогель можно далее конъюгировать с лекарство-линкер реагентами, которые имеют реакционноспособную тиольную группу в линкерном фрагменте.
В таком модифицированном реакционноспособном биоразлагаемом гидрогеле, все оставшиеся реакционноспособные функциональные группы могут быть заблокированы подходящими блокирующими реагентами.
В альтернативном варианте выполнения настоящего изобретения, мульти-функциональные фрагменты вступают в реакцию сочетания с реакционноспособными функциональными группами полимеризованного реакционноспособного биоразлагаемого гидрогеля для увеличения числа реакционноспособных функциональных групп, что позволяет, например, увеличить загрузку лекарственного средства в биоразлагаемый гидрогель по настоящему изобретению. Такие мульти-функциональные фрагменты могут состоять из лизина, дилизина, трилизина, тетрализина, пентализина, гексализина, гептализина или олиголизина, низкомолекулярных полиэтилениминов в связанной форме. Предпочтительно, мульти-функциональный фрагмент состоит из лизинов в связанной форме. Необязательно, такой мульти-функциональный фрагмент может быть защищен защитными группами.
В таком модифицированном реакционноспособном биоразлагаемом гидрогеле, все оставшиеся реакционноспособные функциональные группы могут быть заблокированы подходящими блокирующими реагентами.
На Фиг. 4 показано схематическое изображение участка модифицированного реакционноспособного биоразлагаемого гидрогеля. Сверхразветвленный фрагмент (овал, "Hyp") содержит несколько реакционноспособных функциональных групп, модифицированных спейсерными молекулами или блокирующими группами (черные точки с полулунными структурами). Тонкие черные линии изображают полимерные цепи на основе PEG, отходящие от разветвляющегося ядра (не показано), жирная черная линия изображает спейсерный фрагмент, присоединенный к сверхразветвленному фрагменту стабильной связью (белый ромб). Белые стрелы обозначают соединяющие функциональные группы.
Пунктирные линии указывают место присоединения к большему фрагменту, который для упрощения не изображен полностью.
Биоразлагаемые гидрогели, содержащие конъюгатные функциональные группы
Другой аспект настоящего изобретения представляет собой конъюгат, содержащий биоразлагаемый гидрогель по настоящему изобретению, отличающийся тем, что он состоит из фрагментов основной цепи, связанных гидролитически разрушаемыми связями, и дополнительно несущих стабильные связки с конъюгатными функциональными группами, содержащими, например, лиганды или хелатирующие группы или ионообменные группы. Соответственно, биоразлагаемый гидрогель, содержащий конъюгатные функциональные группы по настоящему изобретению, содержит фрагменты основной цепи, соединенные гидролитически разрушаемыми связями и дополнительно несущие стабильные связки с конъюгатными функциональными группами, содержащими, например, лиганды или хелатирующие группы или ионообменные группы.
Реакционноспособные функциональные группы фрагментов основной цепи реакционноспособных биоразлагаемых гидрогелей и модифицированных реакционноспособных биоразлагаемых гидрогелей служат точками присоединения для прямого или непосредственного связывания аффинных лигандов или хелатирующих групп или ионообменных групп или их комбинации. В идеале, лиганды или хелатирующие группы или ионообменные группы равномерно распределены по всему объему гидрогеля по настоящему изобретению, и могут присутствовать или не присутствовать на поверхности гидрогеля по настоящему изобретению.
Оставшиеся реакционноспособные функциональные группы, которые не соединены с аффинными лигандами или хелатирующими или ионообменными группами, могут быть заблокированы подходящими блокирующими реагентами.
Такие аффинные лиганды или хелатирующие группы или ионообменные группы отличаются тем, что концентрация аффинных лигандов или хелатирующих групп или ионообменных групп в таких гидрогелях по настоящему изобретению практически стабильна на протяжении первой половины времени, необходимого для полного разложения гидрогеля по настоящему изобретению.
"Практически стабильная" весовая концентрация указанных аффинных лигандов или хелатирующих групп или ионообменных групп означает, что она не опускается ниже 90% изначальной концентрации в первую половину времени, необходимого для полного разложения гидрогеля по настоящему изобретению.
В гидрогеле, несущем аффинные лиганды или хелатирующие группы или ионообменные группы по настоящему изобретению, фрагмент основной цепи характеризуется числом функциональных групп, в которое входят соединяющие функциональные группы и конъюгатные функциональные группы, содержащие аффинные лиганды или хелатирующие группы или ионообменные группы. Предпочтительно, сумма соединяющих функциональных групп и конъюгатных функциональных групп, несущих аффинные лиганды или хелатирующие группы или ионообменные группы, равна 16-128, предпочтительно 20-100, более предпочтительно 24-80, и наиболее предпочтительно 30-60. Понятно, что, помимо соединяющих функциональных групп и реакционноспособных функциональных групп, могут также присутствовать блокирующие группы.
Предпочтительно, чтобы общее число соединяющих функциональных групп и конъюгатных функциональных групп, несущих аффинные лиганды или хелатирующие группы или ионообменные группы, в фрагменте основной цепи было равномерно поделено между несколькими полимерными цепочками на основе PEG, отходящими от разветвляющегося ядра. Например, если имеется 32 соединяющих функциональных групп и конъюгатных функциональных групп, несущих аффинные лиганды или хелатирующие группы или ионообменные группы, по 8 групп может быть предоставлено каждой из четырех полимерных цепочек на основе PEG, отходящих от ядра, предпочтительно посредством дендритных фрагментов, присоединенных к концу каждой полимерной цепи на основе PEG. Альтернативно, по 4 группы может быть предоставлено каждой из восьми полимерных цепочек на основе PEG, отходящих от ядра, или по 2 группы может быть предоставлено каждой из шестнадцати полимерных цепочек на основе PEG. Если число полимерных цепочек на основе PEG, отходящих от разветвляющегося ядра, не допускает равномерного распределения, предпочтительно, чтобы отклонение от среднего числа суммы соединяющих функциональных групп и конъюгатных функциональных групп, несущих аффинные лиганды или хелатирующие группы или ионообменные группы, для каждой полимерной цепи на основе PEG сводилось к минимуму.
Также предпочтительно, чтобы общее число соединяющих биоразлагаемых функциональных групп и стабильных связок с конъюгатными функциональными группами, несущими аффинные лиганды или хелатирующие группы или ионообменные группы, или, необязательно, спейсерные молекулы, или блокирующие группы, было больше или равно 16, предпочтительно 20-40, более предпочтительно 28-32, и наиболее предпочтительно 30-32.
В простейшем случае, гидрогель, несущий ионообменные группы, идентичен реакционноспособному биоразлагаемому гидрогелю.
Подходящие лиганды, присутствующие в связанной форме в биоразлагаемом гидрогеле, содержащем конъюгатные функциональные группы по настоящему изобретению, представляют собой, например, аффинные лиганды, такие как биотин. Другие лиганды представляют собой, например аффинные лиганды, такие как: 4-аминобензамидин, 3-(2'-аминобензгидрилокси)тропан, ε-аминокапроил-п-хлорбензиламид, 1-амино-4-[3-(4,6-дихлортриазин-2-иламино)-4-сульфофениламино]антрахинон-2-сульфоновая кислота, 2-(2'-амино-4'-метилфенилтио)-N,N-диметилбензиламин дигидрохлорид, ангиопоэтин-1, аптамеры, аротиноидная кислота, авидин, биотин, калмодулин, кокаэтилен, цитоспорон В, N,N-дигексил-2-(4-фторфенил)индол-3-ацетамид, N,N-дипропил-2-(4-хлорфенил)-6,8-дихлор-имидазо[1,2-а]пиридин-3-ацетамид, 5-фтор-2'-деоксиуридин 5'-(п-аминофенил) монофосфат, S-гексил-L-глутатион, (S,S)-4-фенил-α-(4-фенилоксазолидин-2-илиден)-2-оксазолидин-2-ацетонитрил, Pro-Leu-Gly гидроксамат, 2-(4-(2-(трифторметил)фенил)пиперидин-1-карбоксамидо)бензойная кислота, триметил(м-аминофенил)аммония хлорид, урокортин III, кофакторы, такие как аденозин трифосфат, s-аденозил метионин, аскорбиновая кислота, кобаламин, коэнзим А, коэнзим В, коэнзим М, коэнзим Q, коэнзим F420, цитидин трифосфат, флавин мононуклеотид, флавин аденин динуклеотид, глутатион, гем, липоамид, менахинон, метанофуран, метилкобаламин, молибдоптерин, НАД+, НАДФ+, нуклеотидные сахара, 3'-фосфоаденозин-5'-фосфосульфат, пиридоксаль фосфат, полигистидины, пирролохинолин хинон, рибофлавин, стрептавидин, тетрагидробиоптерин, тетрагидрометаноптерин, тетрагидрофолиевая кислота, белок-переносчик биотин-карбоксила (ВССР), хитин-связывающий белок, FK506 связывающие белки (FKBP), FLAG метка, зеленый флуоресцентный белок, глутатион-S-трансфераза, гемагглютинин (НА), мальтоза-связывающий белок, myc метка, NusA, белок С эпитоп, S-метка, стреп-метка, тиоредоксины, триазины (предпочтительно 2,4,6-тризамещенные триазины), аффинные каркасные белки, такие как фрагменты антител.
Подходящими хелатирующими группами, присутствующими в связанной форме в биоразлагаемом гидрогеле, содержащем конъюгатные функциональные группы, по настоящему изобретению являются, например ионные группы, способные взаимодействовать с субстратом по типу ионообменного вещества. Другими примерами хелатирующих групп являются комплексообразующие группы. Различными типами хелатирующих групп являются, например, 2,2'-бипиридил, 1,2-бис(2-аминофенокси)этан-N,N,N',N'-тетрауксусная кислота, дефероксамин мезилат, деферриферрихром, диэтилентриамин, 2,3-димеркапто-1-пропанол, димеркаптоянтарная кислота, диметилглиоксин, 2,2'-дипиридил, Этилендиамин, этилендиаминтетра(метиленфосфоновая кислота), 1,2-бис(2-амино-5-бромфенокси)этан-N,N,N',N'-тетрауксусная кислота, 8-гидроксихинолин, иминодиацетат, иминоди(метиленфосфоновая кислота), L-мимозин, нитрилотриацетат, оксалат, 1,10-фенантролин, фитиновая кислота, тартрат, 1,4,7,10-тетраазациклододекан-1,4,7,10-тетраацетат, N,N,N',N'-тетракис(2-пиридилметил)этилендиамин, триаминотриэтиламин, иминодиуксусная кислота, тиомочевина, 2-пиколиламин.
Ионообменные группы, присутствующие в связанной форме в биоразлагаемом гидрогеле, содержащем конъюгатные функциональные группы, по настоящему изобретению, представляют собой обычно используемые химические функциональные группы, присоединенные к ионообменным смолам, такие как сильно кислые группы, например сульфоновые кислотные группы, например пропилсульфоновая кислота; сильно основные группы, такие как четвертичные амино-группы, например триметиламмониевые группы, например пропилтриметиламмония хлорид; слабокислые группы, например алкилкарбоновые кислоты; или слабоосновные группы, такие как первичные, вторичные и/или третичные алкиламино-группы.
На Фиг. 5 показано схематическое изображение участка гидрогеля, содержащего конъюгатные функциональные группы. Сверхразветвленный фрагмент (овал, "Hyp") содержит несколько стабильных связей (белые ромбы) с конъюгатами, такими как аффинные лиганды или хелатирующие группы (черные овалы) или спейсерный фрагмент (жирная черная линия). Звездочки обозначают the спейсерный фрагмент; # обозначает поперечносшивающие фрагменты; пунктирные линии указывают место присоединения к большему фрагменту, который не показан. Тонкая черная линия обозначает полимерную цепь на основе PEG, отходящую от разветвляющегося ядра (не показано).
Пролекарства на базее гидрогеля
Другой аспект настоящего изобретения представляет собой связанное с носителем пролекарство, содержащее биоразлагаемый гидрогель по настоящему изобретению в качестве носителя, где имеется несколько стабильных связок фрагментов основной цепи с временным линкером пролекарства, к которому ковалентно присоединен биологически активный фрагмент.
"Пролекарство" это любое соединение, претерпевающее биотрансформацию перед тем, как проявить свое фармакологическое действие. Таким образом, Пролекарства можно рассматривать как лекарства, содержащие специальные нетоксичные защитные группы, применяемые в качестве временного средства для изменения или устранения нежелательных свойств родительской молекулы. Очевидно, это также включает усиление желаемых свойств лекарственного средства и подавление нежелательных свойств.
Термины "связанное с носителем пролекарство", "пролекарство на носителе" относится к пролекарству, которое содержит временную связку определенного действующего вещества с группой временного носителя, которая дает улучшение физико-химических или фармакокинетических свойств, и которая легко удаляется in vivo, обычно путем гидролитического расщепления.
Реакционноспособные функциональные группы реакционноспособного биоразлагаемого гидрогеля или модифицированного реакционноспособного биоразлагаемого гидрогеля служат местом присоединения для непосредственного связывания через упомянутые ранее стабильные связки с лекарственным средством, конъюгатом лекарство-линкер, пролекарством, связанным с носителем пролекарством и т.п.. В идеале, связанные с гидрогелем конъюгаты лекарство-линкер распределены в гидрогеле равномерно, и могут присутствовать или не присутствовать на поверхности гидрогеля по настоящему изобретению.
Оставшиеся реакционноспособные функциональные группы, не соединенные с временным линкером пролекарства или со спейсером, присоединенным к временному линкеру пролекарства, могут быть заблокированы подходящими блокирующими реагентами.
Предпочтительно, ковалентные связывания, формируемые между реакционноспособными функциональными группами, предоставляемыми фрагментами основной цепи, и линкером пролекарства, представляют собой стабильные связи. Подходящие функциональные группы для присоединения линкера пролекарства к гидрогелю по настоящему изобретению, включают (но не ограничиваются только ими) карбоновые кислоты и их производные, карбонаты и их производные, гирокси-группы, гидразин, гидроксиламин, полуамид малеиновой кислоты и его производные, кетоны, амины, альдегиды, тиолы и дисульфиды.
В гидрогеле, несущем конъюгаты лекарство-линкер по настоящему изобретению, фрагмент основной цепи отличается наличием нескольких гидрогель-соединенных конъюгатов лекарство-линкер; функциональных групп, содержащих биоразлагаемые соединяющие функциональные группы; и, необязательно, концевых групп. Предпочтительно, общее число биоразлагаемых соединяющих функциональных групп, конъюгатов лекарство-линкер и концевых групп равно 16-128, предпочтительно 20-100, более предпочтительно 24-80 и наиболее предпочтительно 30-60.
Предпочтительно, общее число соединяющих функциональных групп, гидрогель-соединенных конъюгатов лекарство-линкер и концевых групп в фрагменте основной цепи равномерно распределено среди полимерных цепочек на основе PEG, отходящих от разветвляющегося ядра. Например, если имеется 32 соединяющие функциональные группы, гидрогель-соединенных конъюгатов лекарство-линкер и концевых групп, по восемь групп может быть присоединено к каждой из четырех полимерных цепочек на основе PEG, отходящих от ядра, предпочтительно посредством дендритных фрагментов, присоединенных к концу каждой полимерной цепочки на основе PEG. Альтернативно, по четыре функциональные группы может быть присоединено к каждой из восьми полимерных цепочек на основе PEG, отходящих от ядра, или по две функциональные группы - к каждой из шестнадцати полимерных цепочек на основе PEG. Если число полимерных цепочек на основе PEG, отходящих от разветвляющегося ядра, не допускает равномерного распределения, предпочтительно, чтобы отклонение от среднего числа суммы соединяющих функциональных групп, гидрогель-соединенных конъюгатов лекарство-линкер и концевых групп для каждой полимерной цепи на основе PEG сводилось к минимуму.
Для таких связанных с носителем пролекарств по настоящему изобретению желательно, чтобы почти все высвобождение лекарственного средства (>90%) происходило до того, как произойдет высвобождение заметного количества фрагментов основной цепи (<10%). Это достигается регулировкой времени полужизни связанного с носителем пролекарства относительно кинетики разложения гидрогеля.
Для линкерного агент предпочтительно образование обратимого связывания с биологически активным фрагментом, предпочтительно таким образом, чтобы после расщепления линкера биологически активный фрагмент высвобождался в немодифицированной форме. Различные линкерные агенты или линкерные группы, которые могут применяться для этой цели, описаны в работе B. Testa и др. (В. Testa, J. Mayer, Hydrolysis in Drug и Prodrug Metabolism, Wiley-VCH, 2003).
Термины "линкер", "линкерная группа", "линкерная структура" или "линкерный агент" отностся к фрагменту, который одним своим концом присоединен к лекарственному фрагменту через обратимую связку, а другим концом присоединен стабильной связью к спейсерной молекуле, стабильным образом присоединенной к сверхразветвленному дендритному фрагменту, или напрямую присоединен стабильной связью к сверхразветвленному дендритному фрагменту.
Также предпочтительно, чтобы большинство линкерных структур оставалось присоединенными к гидрогелю по настоящему изобретению после расщепления биоразлагаемой связки с биологически активным фрагментом. Если линкер представляет собой каскадный линкер пролекарства, предпочтительно, чтобы активирующая группа оставалась устойчиво связанной с гидрогелем по настоящему изобретению.
Предпочтительно, временный линкер пролекарства соединен с биологически активным фрагментом посредством саморасщепляемой функциональной группы. Предпочтительно, линкер обладает способностью к саморасщеплению, и, как следствие, гидрогель-линкер-лекарство представляет собой связанное с носителем пролекарство, способное высвобождать лекарственное средство из конъюгата таким образом, что высвобождение зависит главным образом от саморасщепления линкера.
Термины "саморасщепляемый" или "гидролитически разрушаемый" используются как синонимы.
Предпочтительно, связка между линкером пролекарства и биоактивным фрагментом гидролитически разрушаема в физиологических условиях (водный буфер при рН 7.4, 37°С), при этом время полужизни находится в диапазоне от одного часа до трех месяцев, и включает (но не ограничиваются только ими): аконитилы, ацетали, амиды, ангидриды карбоновых кислот, сложные эфиры, имины, гидразоны, полуамиды малеиновой кислоты, ортоэфиры, фосфамиды, сложные эфиры фосфорной кислоты, фосфосилиловые эфиры, силиловые эфиры, сложные эфиры сульфокислот, ароматические карбаматы, их комбинации и т.д. Предпочтительные биоразлагаемые связки между линкером пролекарства и биоактивными фрагментами, образующиеся не через первичные или ароматические амино-группы, представляют собой сложные эфиры, карбонаты, сложные эфиры фосфорной кислоты и сложные эфиры сульфокислот, а наиболее предпочтительны сложные эфиры или карбонаты. Предпочтительные биоразлагаемые связки между линкером пролекарства и биоактивными фрагментами, образующиеся через первичные или ароматические амино-группы, представляют собой амиды или карбаматы.
"Саморасщепляемая функциональная группа" содержит гидролитически разрушаемую связь.
Если саморасщепляемая связка формируется с участием первичной или ароматической амино-группы биологически активного фрагмента, предпочтительными являются карбаматная или амидная группа.
После присоединения конъюгата лекарство-линкер к гидрогелю по настоящему изобретению, содержащему малеимидную группу, все оставшиеся функциональные группы блокируются подходящими блокирующими реагентами для предотвращения нежелательных побочных реакций.
На Фиг. 6 представлено схематическое изображение участка гидрогеля по настоящему изобретению, содержащего стабильные связки фрагментов основной цепи с временным линкером пролекарства, к которому ковалентно присоединен биологически активный фрагмент. Сверхразветвленный фрагмент (овал, "Hyp") содержит стабильные связи (белые ромбы) с временным линкером пролекарства (черная стрелка) или спейсерным фрагментом (жирная черная линия). Тонкая черная линия изображает полимерную цепь на основе PEG, отходящую от разветвляющегося ядра (не показано). Пунктирные линии указывают место присоединения к большему фрагменту, который не изображен полностью
На Фиг. 6а показано прямое связывание временного линкера пролекарства со сверхразветвленным фрагментом, тогда как на Фиг. 6b показано непрямое связывание временного линкера пролекарства со сверхразветвленным фрагментом. На Фиг. 6b временный линкер пролекарства соединен со сверхразветвленным фрагментом через спейсерный фрагмент (жирная серая линия), который связан с временным линкером пролекарства через стабильную связь (белый ромб). В каждом случае, лекарственный фрагмент (большой белый круг) соединен с временным линкером пролекарства через биоразлагаемую связку (белая стрелка).
Деграданты - водорастворимые продукты разложения Разложение гидрогеля по настоящему изобретению представляет собой многостадийную реакцию, в ходе которой расщепляется множество разрушаемых связей, давая продукты разложения, которые могут быть водорастворимыми или нерастворимыми в воде. Однако, нерастворимые в воде продукты разложения могут содержать разрушаемые связи, так что они могут расщепляться таким образом, что образуются водорастворимые продукты разложения. Эти водорастворимые продукты разложения могут содержать один или более фрагментов основной цепи. Понятно, что высвобождаемые фрагменты основной цепи могут, например, быть стабильно конъюгированы со спейсерными или блокирующими или линкерными группами, или аффинными группами и/или продуктами разложения линкера пролекарства, и также что водорастворимые продукты разложения могут содержать разрушаемые связи.
Структуры разветвляющегося ядра, полимерных цепочек на основе PEG, сверхразветвленных дендритных фрагментов и фрагментов, присоединенных к сверхразветвленным дендритным фрагментам, можно понять из соответствующих определений, данных в разделах, описывающих различные гидрогели по настоящему изобретению. Понятно, что структура деграданта зависит от типа гидрогеля по настоящему изобретению, претерпевающего разложение.
Общее количество фрагментов основной цепи можно измерить в растворе после полного разложения гидрогеля по настоящему изобретению, и во время разложения, фракции растворимых продуктов разложения в виде основных цепей можно отделять от нерастворимого гидрогеля по настоящему изобретению и количественно охарактеризовать без перекрывания с другими растворимыми продуктами разложения, высвобождаемыми из гидрогеля по настоящему изобретению. Гидрогельный объект можно отделить от избытка воды буфера, имеющего физиологическое значение осмоляльности, методом седиментации или центрифугирования. Центрифугирование можно проводить таким образом, что надосадочный раствор составляет по меньшей мере 10% от объема набухшего гидрогеля по настоящему изобретению. Растворимые продукты разложения гидрогеля после такой стадии седиментации или центрифугирования остаются в водном надосадочном растворе.
Предпочтительно, водорастворимые продукты разложения можно отделить от нерастворимых в воде продуктов разложения фильтрованием через фильтры с диаметром пор 0,45 мкм, после которого водорастворимые продукты разложения находятся в фильтрате.
Водорастворимые продукты разложения можно отделить от нерастворимых в воде продуктов разложения комбинацией стадий центрифугирования и фильтрования.
Водорастворимые продукты разложения, содержащие один или более фрагментов основной цепи, можно детектировать, анализируя аликвоты такого надосадочного раствора подходящими методами разделения и/или анализа. Например, фрагменты основной цепи могут нести группы, обладающие УФ-поглощением при длинах волн, при которых другие продукты разложения не проявляют УФ-поглощения. Такие селективно УФ-поглощающие группы могут быть структурными компонентами фрагмента основной цепи, такими как амидные связи, или могут вводиться в каркас присоединением к его реакционноспособным функциональным группам посредством ароматических циклических систем, таких как индолильные группы.
На Фиг. 7 представлено схематическое изображение разных продуктов разложения. Пример продукта разложения, изображенный на Фиг. 7а, является результатом разложения биоразлагаемого гидрогеля, несущего конъюгатные функциональные группы. От центрального разветвляющегося ядра (©) отходят четыре полимерные цепочки на основе PEG (тонкие черные линии), к концам которых присоединены сверхразветвленные дендритные фрагменты ("Hyp"; овалы). Указанные сверхразветвленные дендритные фрагменты содержат несколько стабильных связок (белые ромбы) со спейсерными фрагментами (звездочка) или с конъюгатами, такими как аффинные лиганды или хелатирующие группы (черные овалы). Пунктирные линии указывают место присоединения к большему фрагменту, который не показан.
Пример продукта разложения, изображенный на Фиг. 7b, является результатом разложения биоразлагаемого гидрогеля, несущего пролекарства. От центрального разветвляющегося ядра (©) отходят четыре полимерные цепочки на основе PEG (тонкие черные линии), к концам которых присоединены сверхразветвленные дендритные фрагменты ("Hyp"; овалы). Указанные сверхразветвленные дендритные фрагменты содержат несколько стабильных связок (белые ромбы) со спейсерными фрагментами (звездочка) или со спейсерными фрагментами (белый прямоугольник), которые соединены с временным линкером пролекарства (черная стрелка). Понятно, что указанный спейсерный фрагмент является опциональным и зависит от гидрогельного продукта. Пунктирные линии указывают место присоединения к большему фрагменту, который не показан.
Понятно, что сверхразветвленные дендритные фрагменты продуктов разложения содержат больше стабильных связок с спейсерными фрагментами, конъюгатами или временными линкерами пролекарств, чем показано на Фиг. 7а и 7b.
Краткое описание чертежей
На Фиг. 1 показан пример реагента основной цепи. ©: разветвляющееся ядро; тонкая черная линия: полимерная цепь на основе PEG; "Нур"/овал: сверхразветвленный дендритный фрагмент; маленький белый круг: полимеризуемые функциональные группы; пунктирные линии указывают место присоединения к большему фрагменту, который не показан.
На Фиг. 2 показаны примеры поперечносшивающих реагентов. Маленький белый круг: полимеризуемая функциональная группа; белая стрелка: биоразлагаемая связка; звездочка: спейсерный фрагмент, связанный с фрагментом основной цепи, и связанный с другой стороны со поперечносшивающим фрагментом.
На Фиг. 3 показан схематический обзор различных способов, которыми два фрагмента основной цепи могут быть соединены в реакционноспособном биоразлагаемом гидрогеле. "Нур"/овал: сверхразветвленный дендритный фрагмент; черная точка: реакционноспособная функциональная группа; белый ромб: стабильная связка; звездочка: спейсерный фрагмент, связанный с фрагментом основной цепи, и связанный с другой стороны со поперечносшивающим фрагментом; белые стрелки: соединяющие функциональные группы; #: поперечносшивающий фрагмент фрагмент; тонкая черная линия: полимерная цепь на основе PEG; пунктирные линии указывают место присоединения к большему фрагменту, который не показан.
На Фиг. 4 представлено схематическое изображение модифицированного реакционноспособного биоразлагаемого гидрогеля. "Нур"/овал: сверхразветвленный дендритный фрагмент; черная точка полулунной структуры: реакционноспособные функциональные группы, модифицированные спейсерными молекулами, блокирующими группами или защитными группами; белая стрелка: соединяющая функциональная группа; тонкая черная линия: полимерная цепь на основе PEG; белая стрелка: соединяющая функциональная группа; звездочка: спейсерный фрагмент, связанный с фрагментом основной цепи, и связанный с другой стороны со поперечносшивающим фрагментом; #: поперечносшивающий фрагмент фрагмент; пунктирные линии указывают место присоединения к большему фрагменту, который не показан.
На Фиг. 5 представлено схематическое изображение гидрогеля по настоящему изобретению, содержащего конъюгатные функциональные группы. "Нур"/овал: сверхразветвленный дендритный фрагмент; черный овал: конъюгатная функциональная группа; белый ромб: стабильные связи; звездочка: спейсерный фрагмент, связанный с фрагментом основной цепи, и связанный с другой стороны со поперечносшивающим фрагментом; #: поперечносшивающий фрагмент фрагмент; тонкая черная линия: полимерная цепь на основе PEG; пунктирные линии указывают место присоединения к большему фрагменту, который не показан.
На Фиг. 6 представлено схематическое изображение гидрогеля, содержащего стабильные связки с временными линкерами пролекарств, напрямую (Фиг. 6а) или опосредованно через спейсерный фрагмент (Фиг. 6b). "Нур"/овал: сверхразветвленный дендритный фрагмент; белый ромб: стабильная связь; звездочка: спейсерный фрагмент, связанный с фрагментом основной цепи, и связанный с другой стороны со поперечносшивающим фрагментом; белый прямоугольник: спейсер; белая стрелка: соединяющая функциональная группа; черная стрелка: линкер; большой белый круг: лекарственное средство; #: поперечносшивающий фрагмент фрагмент; пунктирные линии указывают место присоединения к большему фрагменту, который не показан.
На Фиг. 7 представлено схематическое изображение продуктов разложения, являющихся результатом либо разложения биоразлагаемого гидрогеля, содержащего конъюгатные функциональные группы (Фиг. 7а), либо разложения пролекарства на основе гидрогеля (Фиг. 7b). ©: разветвляющееся ядро; тонкая черная линия: полимерная цепь на основе PEG; "Нур"/овал: сверхразветвленный дендритный фрагмент; белый ромб:
стабильная связь; звездочка: спейсерный фрагмент, связанный с фрагментом основной цепи, и связанный с другой стороны со поперечносшивающим фрагментом; черный овал: конъюгатная функциональная группа; белый прямоугольник: спейсер; черная стрелка: линкер; пунктирные линии указывают место присоединения к большему фрагменту, который не показан.
На Фиг. 8 показана кинетика высвобождения in vitro для соединения 9 при рН 7.4 и 37°С.
На Фиг. 9 показана кинетика разложения in vitro для соединения 15 при рН 9 и 37°С.
На Фиг. 10 показана кинетика разложения (в двух повторах) in vitro для соединения 15 при рН 7.4 и 37°С.
На Фиг. 11 показана кинетика разложения in vitro для соединения 5 при рН 9 и 37°С.
На Фиг. 12 показана кинетика разложения in vitro для соединения 19а при рН 9 и 37°С.
На Фиг. 13 показана фармакокинетика соединения 19с в крысах.
На Фиг. 14 показана фармакокинетика соединения 19е в крысах.
На Фиг. 15 изображен график зависимости силы от потока при использовании иглы 30 G. Точки на графике: черные квадраты = этиленгликоль; черные треугольники = вода; черные точки = пролекарство инсулина на основе гидрогеля.
В настоящем изобретении описаны биоразлагаемые нерастворимые в воде гидрогели на основе поли(этиленгликоля) (PEG). Термин "на основе PEG" в тексте настоящего изобретения означает, что массовая доля PEG-цепочек в гидрогеле по настоящему изобретению составляет по меньшей мере 10% по весу, предпочтительно по меньшей мере 25%, из расчета на общий вес гидрогеля по настоящему изобретению. Остаток составляют другие полимеры. Термин "полимер" описывает молекулу, состоящую из повторяющихся структурных единиц, соединенных химическими связями линейно, в виде кольца, в виде разветвленных структур, сшитых структур или дендримеров, или в виде комбинации перечисленных способов, которая может иметь синтетическое или биологическое происхождение, или иметь комбинированное происхождение. Примеры включают (но не ограничиваются только ими): поли(акриловые кислоты), поли(акрилаты), поли(акриламиды), поли(алкилокси) полимеры, поли(амиды), поли(амидоамины), поли(аминокислоты), поли(ангидриды), поли(аспартамид), поли(масляная кислота), поли(капролактон), поли(карбонаты), поли(цианоакрилаты), поли(диметилакриламид), поли(сложные эфиры), поли(этилен), поли(этиленгликоль), поли(этиленоксид), поли(этилоксазолин), поли(гликолевая кислота), поли(гидроксиэтилакрилат), поли(гидроксиэтилоксазолин), поли(гидроксипропилметакриламид), поли(гидроксипропилметакрилат), поли(гидроксипропилоксазолин), поли(иминокарбонаты), поли(N-изопропилакриламид), поли(молочная кислота), поли(молочная-со-гликолевая кислота), поли(метакриламид), поли(метакрилаты), поли(метилоксазолин), поли(пропиленфумарат), поли(органофосфазены), поли(ортоэфиры), поли(оксазолины), поли(пропиленгликоль), поли(силоксаны), поли(уретаны), поливиниловые спирты), поли(виниламины), поли(винилметиловый эфир), поли(винилпирролидон), силиконы, рибонуклеиновые кислоты, дезоксинуклеиновые кислоты, альбумины, антитела и их фрагменты, белки плазмы крови, коллагены, эластин, фасцин, фибрин, кератины, полиаспартаты, полиглютаматы, проламины, трансферрины, цитохромы, флавопротеины, гликопротеины, гемопротеины, липопротеины, металлопротеины, фитохромы, фосфопротеины, опсины, агар, агароза, альгинат, арабинаны, арабиногалантаны, каррагенаны, целлюлоза, карбометил целлюлоза, гидроксипропил метилцеллюлоза и другие углеводные полимеры, хитозан, декстран, декстрин, желатин, гиалуроновая кислота и ее производные, маннан, пектины, рамногалактуронаны, крахмал, гидроксиалкил крахмал, ксилан и их сополимеры и функционализированные производные.
Если полимер присутствует в качестве профрагмента в пролекарстве, его можно называть термином «носитель».
Кроме того, термин "нерастворимый в воде" относится к набухаемой трехмерно сшитой молекулярной сетке, формирующей гидрогель по настоящему изобретению. Гидрогель по настоящему изобретению при суспендировании в большом избытке воды или водного буфера, имеющего физиологическое значение осмоляльности, может поглощать значительное количество воды, например, превосходящее его собственный вес до 10 раз, и поэтому является набухающим, но после удаления избытка воды сохраняет физическую устойчивость геля и форму. Такая форма может иметь любую геометрию, и понятно, что такой индивидуальный гидрогельный объект по настоящему изобретению следует рассматривать как отдельную молекулу, состоящую из компонентов, каждый из которых связан с другими компонентами химическими связями.
Исходные материалы
Биоразлагаемые гидрогели по настоящему изобретению могут быть полимеризованы посредством радикальной полимеризации, ионной полимеризации или реакций связывания.
В случае, если биоразлагаемый гидрогель по настоящему изобретению образуется посредством радикальной или ионной полимеризации, по меньшей мере два исходных соединения для биоразлагаемого гидрогеля по настоящему изобретению представляют собой поперечносшивающие макромономеры или поперечносшивающие мономеры - которые называют поперечносшивающими реагентами, и мульти-функциональный макромономер, который называют реагентом основной цепи. Поперечносшивающий реагент несет по меньшей мере две сшивающие функциональные группы, и реагент основной цепи несет по меньшей мере одну сшивающую функциональную группу и по меньшей мере одну химическую функциональную группу, которая не участвует в стадии полимеризации. Могут присутствовать или отсутствовать дополнительные разбавляющие мономеры.
Подходящие сшивающие функциональные группы включают (но не ограничиваются только ими) радикально полимеризуемые группы, такие как винил, винил-бензол, акрилат, акриламид, метакрилат, метакриламид и ионно полимеризуемые группы, такие как оксетан, азиридин и оксиран.
В альтернативном методе получения, биоразлагаемый гидрогель по настоящему изобретению получают реакцией химического связывания. В таких реакциях, исходным соединением является по меньшей мере одно макромолекулярное исходное соединение, имеющее комплементарные функциональные группы, которые вступают в такие реакции, как реакция конденсации или присоединения. В одном альтернативном варианте, используется всего одно макромолекулярное исходное соединение, которое представляет собой гетеромультифункциональный реагент основной цепи, содержащий некоторое число полимеризуемых функциональных групп.
Альтернативно, в случае двух или более макромолекулярных исходных соединений, одно из этих исходных соединений представляет собой поперечносшивающий реагент, имеющий по меньшей мере две одинаковые полимеризуемые функциональные группы, а другое исходное соединение представляет собой гомомультифункциональный или гетеромультифункциональный реагент основной цепи, также содержащий несколько полимеризуемых функциональных групп.
Подходящие полимеризуемые функциональные группы, имеющиеся в поперечносшивающем реагенте, включают первичные и вторичные амины, карбоновые кислоты и их производные, малеимид, тиол, гидроксил и другие альфа-бета-ненасыщенные акцепторы Михаэля, такие как винилсульфоновые группы, предпочтительно терминальные первичные и вторичные амины, карбоновые кислоты и их производные, малеимид, тиол, гидроксил и другие альфа-бета-ненасыщенные акцепторы Михаэля, такие как винилсульфоновые группы. Подходящие полимеризуемые функциональные группы, имеющиеся в реагенте основной цепи, включают (но не ограничиваются только ими) первичные и вторичные амины, карбоновые кислоты и их производные, малеимид, тиол, гидроксил и другие альфа-бета-ненасыщенные акцепторы Михаэля, такие как винилсульфоновые группы.
Предпочтительно, фрагмент основной цепи отличается наличием разветвляющегося ядра, от которого отходят по меньшей мере три полимерных цепочки на основе PEG. Соответственно, в предпочтительном аспекте настоящего изобретения, реагент основной цепи содержит разветвляющееся ядро, от которого отходят по меньшей мере три полимерных цепочки на основе PEG. Такие разветвляющиеся ядра могут состоять из поли- или олигоспиртов в связанной форме, предпочтительно пентаэритритола, трипентаэритритола, гексаглицерина, сахарозы, сорбита, фруктозы, маннита, глюкозы, целлюлозы, амилозы, крахмалов, гидроксиалкил-крахмалов, поливиниловых спиртов, декстранов, гиалурононанов, или разветвляющиеся ядра могут состоять из поли- или олигоаминов в связанной форме, таких как орнитин, диаминомасляная кислота, трилизин, тетрализин, пентализин, гексализин, гептализин, октализин, нонализин, декализин, ундекализин, додекализин, тридекализин, тетрадекализин, пентадекализин или олиголизины, полиэтиленимины, поливиниламины.
Предпочтительно, от разветвляющегося ядра отходят 3-16 полимерных цепочек на основе PEG, более предпочтительно 4-8. Предпочтительные разветвляющиеся ядра могут состоять из пентаэритритола, трилизина, тетрализина, пентализина, гексализина, гептализина или олиголизина, низкомолекулярных полиэтилениминов, гексаглицерина, трипентаэритритола в связанной форме. Предпочтительно, от разветвляющегося ядра отходят 3-16 полимерных цепочек на основе PEG, более предпочтительно 4-8. Предпочтительно, полимерная цепь на основе PEG представляет собой подходящим образом замещенное производное поли(этиленгликоля).
Предпочтительно, такая полимерная цепь на основе PEG, присоединенная к разветвляющемуся ядру, представляет собой линейную поли(этиленгликольную) цепь, один конец которой присоединен к разветвляющемуся ядру, а другой - к сверхразветвленному фрагменту. Понятно, что цепь на основе PEG может заканчиваться или прерываться алкильными или арильными группами, необязательно замещенными гетероатомами и химическими функциональными группами.
Если термин "на основе PEG" применяется в отношении поперечносшивающего реагента или полимерной цепи на основе PEG, присоединенной к разветвляющемуся ядру, он относится к поперечносшивающему фрагменту или полимерной цепи на основе PEG, содержащей по меньшей мере 20 мас.% этиленгликольных фрагментов.
Предпочтительные структуры, содержащие полимерные цепочки на основе PEG, отходящие от разветвляющегося ядра, подходящие для реагентов основной цепи, представляют собой мульти-разветвленные PEG-производные, такие как, например, описанные в списке товаров JenKem Technology, USA (доступен для скачивания с "www.jenkemusa.com на 28 июля 2009 г), 4-разветвленные PEG-производные (пентаэритритольное ядро), 8-разветвленные PEG-производные (гексаглицериновое ядро) и 8-разветвленные PEG-производные (трипентаэритритольное ядро). Наиболее предпочтительными являются 4-разветвленный PEG-амин (пентаэритритольное ядро) и 4-разветвленный PEG-карбоксил (пентаэритритольное ядро), 8-разветвленный PEG-амин (гексаглицериновое ядро), 8-разветвленный PEG-карбоксил (гексаглицериновое ядро), 8-разветвленный PEG-амин (трипентаэритритольное ядро) и 8-разветвленный PEG-карбоксил (трипентаэритритольное ядро). Предпочтительные молекулярные веса для таких мульти-разветвленных PEG-производных в реагенте основной цепи составляют от 1 кДа до 20 кДа, более предпочтительно от 1 кДа до 15 кДа, и еще более предпочтительно от 1 кДа до 10 кДа. Понятно, что терминальные амино-группы дополнительно конъюгированы, давая соединяющие и реакционноспособные функциональные группы в фрагменте основной цепи.
Термины "разветвляющееся ядро" и "ядро" используются взаимозаменяемо.
Сверхразветвленный дендритный фрагмент имеет полимеризуемые функциональные группы. Предпочтительно, каждый дендритный фрагмент имеет молекулярный вес от 0.4 кДа до 4 кДа, более предпочтительно от 0.4 кДа до 2 кДа. Предпочтительно, каждый дендритный фрагмент содержит по меньшей мере 3 разветвления и по меньшей мере 4 полимеризуемые функциональные группы, и максимально 63 разветвления и 64 полимеризуемые функциональные группы, предпочтительно по меньшей мере 7 разветвлений и по меньшей мере 8 полимеризуемых функциональных групп, и максимально 31 разветвление и 32 полимеризуемые функциональные группы.
Примерами таких дендритных фрагментов являются трилизин, тетрализин, пентализин, гексализин, гептализин, октализин, нонализин, декализин, ундекализин, додекализин, тридекализин, тетрадекализин, пентадекализин, гексадекализин, гептадекализин, октадекализин, нонадекализин, орнитин и диаминомасляная кислота. Примерами таких предпочтительных дендритных фрагментов являются трилизин, тетрализин, пентализин, гексализин, гептализин, наиболее предпочтительны трилизин, пентализин или гептализин, орнитин, диаминомасляная кислота в связанной форме.
Поперечносшивающий реагент может представлять собой линейную или разветвленную молекулу, и предпочтительно представляет собой линейную молекулу. Если Поперечносшивающий реагент содержит две полимеризуемые функциональные группы, его называют "линейный поперечносшивающий реагент"; если поперечносшивающий реагент содержит более двух полимеризуемых функциональных групп, он рассматривается как "разветвленный поперечносшивающий реагент".
Поперечносшивающий реагент имеет на концах две полимеризуемые функциональные группы и может не содержать биоразлагаемую группу или может содержать по меньшей мере одну биоразлагаемую связь. Предпочтительно, поперечносшивающий реагент содержит по меньшей мере одну биоразлагаемую связь.
В одном варианте выполнения, поперечносшивающий реагент состоит из полимера. Предпочтительно, поперечносшивающие реагенты имеют молекулярный вес в диапазоне от 60 Да до 5 кДа, более предпочтительно, от 0,5 кДа до 4 кДа, еще более предпочтительно от 1 кДа до 4 кДа, еще более предпочтительно от 1 кДа до 3 кДа.
Помимо олигомерных или полимерных поперечносшивающих реагентов, могут использоваться низкомолекулярные поперечносшивающие реагенты, особенно когда гидрофильные высокомолекулярные фрагменты основной цепи применяются для формирования биоразлагаемых гидрогелей по настоящему изобретению.
В одном варианте выполнения, поперечносшивающий реагент содержит мономеры, соединенные биоразлагаемыми связями. Такие полимерные поперечносшивающие реагенты могут содержать до 100 биоразлагаемых связей или более, в зависимости от молекулярного веса поперечносшивающего реагента и молекулярного веса мономерных единиц. Примеры таких поперечносшивающих реагентов могут содержать полимеры на основе поли(молочной кислоты) или поли(гликолевой кислоты).
Предпочтительно, поперечносшивающие реагенты имеют в своей основе PEG, предпочтительно представлены только одной молекулярной цепью на основе PEG. Предпочтительно, поперечносшивающие реагенты на основе поли(этиленгликоля) представляют собой углеводородные цепочки, содержащие фрагменты этиленгликоля, где поперечносшивающие реагенты на основе поли(этиленгликоля) содержат каждый по меньшей мере m единиц этиленгликоля, и где m представляет собой целое число в диапазоне от 3 до 100, предпочтительно от 10 до 70. Предпочтительно, поперечносшивающие реагенты на основе поли(этиленгликоля) имеют молекулярный вес в диапазоне от 0,5 кДа до 5 кДа.
Пример упрощенного реагента основной цепи изображен на Фиг. 1 для иллюстрации использующейся терминологии. От центрального разветвляющегося ядра (©) отходят четыре полимерные цепочки на основе PEG (тонкая черная линия), по концам которых присоединены сверхразветвленные дендритные фрагменты ("Hyp"; овалы). Сверхразветвленные дендритные фрагменты несут полимеризуемые функциональные группы (маленькие белые кружки), из которых показана только часть, т.е. сверхразветвленный дендритный фрагмент содержит больше реакционноспособных функциональных групп, чем показано на Фиг. 1.
На Фиг. 2 показаны четыре примера поперечносшивающих реагентов. Помимо их полимеризуемых функциональных групп (маленькие белые кружки), поперечносшивающие реагенты могут содержать одну или более биоразлагаемых связок (белые стрелки), которые содержат биоразлагаемую связь.
Поперечносшивающий реагент 2А не содержит биоразлагаемой связи. Если такие поперечносшивающие реагенты используются для синтеза биоразлагаемого гидрогеля, образуются биоразлагаемые связки по реакции полимеризуемой функциональной группы поперечносшивающего реагента с полимеризуемой функциональной группой реагента основной цепи.
Поперечносшивающий реагент 2В содержит одну биоразлагаемую связку, поперечносшивающий реагент 2С содержит две биоразлагаемые связки, и Поперечносшивающий реагент 2D содержит четыре биоразлагаемые связки.
Участок между полимеризуемой группой и первой биоразлагаемой связью называется спейсерный фрагмент, связанный с фрагментом основной цепи и связанный с другой стороны со поперечносшивающим фрагментом, и обозначается в различных поперечносшивающих фрагментах звездочками, где это применимо.
Реакционноспособный биоразлагаемый гидрогель
В одном варианте выполнения, гидрогель по настоящему изобретению представляет собой мульти-функционализованный материал, то есть биоразлагаемый гидрогель, содержащий реакционноспособные функциональные группы и соединяющие функциональные группы в виде трехмерной сшитой матрицы, набухающей в воде. Такой гидрогель также называют реакционноспособным биоразлагаемым гидрогелем. Реакционноспособные функциональные группы служат точками присоединения для прямого или опосредованного связывания с аффинным лигандом, хелатирующей группой, ионообменной группой, лекарственным средством, пролекарством, связанным с носителем пролекарством, блокирующей группой, концевой группой и т.п.
В идеале, реакционноспособные функциональные группы равномерно распределены в гидрогеле по настоящему изобретению, и могут присутствовать или не присутствовать на поверхности реакционноспособного биоразлагаемого гидрогеля. Неограничивающие примеры таких реакционноспособных функциональных групп включают (но не ограничиваются только ими) следующие химические функциональные группы, связанные со сверхразветвленным дендритным фрагментом:
карбоновые кислоты и их активированные производные, амины, малеимид, тиол и его производные, сульфоновые кислоты и их производные, карбонаты и их производные, карбаматы и их производные, гидрокси-соединения, альдегиды, кетоны, гидразины, изоцианаты, изотиоцианаты, фосфорные кислоты и их производные, фосфоновые кислоты и их производные, галогенацетильные соединения, алкилгалогениды, акрилоильные соединения и другие альфа-бета-ненасыщенные акцепторы Михаэля, арилирующие агенты, такие как арилфториды, гидроксиламин, дисульфиды, такие как пиридил дисульфид, винилсульфон, винилкетон, диазоалканы, диазоацетильные соединения, оксиран и азиридин. Предпочтительные реакционноспособные функциональные группы включают тиолы, малеимид, амины, карбоновые кислоты и производные, карбонаты и их производные, карбаматы и их производные, альдегиды и галогенацетилы. Предпочтительно, реакционноспособные функциональные группы представляют собой первичные амино-группы или карбоновые кислоты, наиболее предпочтительно - первичные амино-группы.
Такие реакционноспособные функциональные группы отличаются тем, что их можно хемоселективно вводить в реакции в присутствии других функциональных групп, и также отличаются тем, что концентрация реакционноспособных функциональных групп в таких реакционноспособных биоразлагаемых гидрогелях практически стабильна в первую половину времени, необходимого для полного разложения гидрогеля по настоящему изобретению.
"Практически стабильная" весовая концентрация указанных реакционноспособных функциональных групп означает, что она не опускается ниже 90% изначальной концентрации в первую половину времени, необходимого для полного разложения реакционноспособного биоразлагаемого гидрогеля.
Реакционноспособные функциональные группы можно заблокировать с помощью подходящих защитных реагентов.
Согласно настоящему изобретению, гидрогель состоит из фрагментов основной цепи, связанных гидролитически разрушаемыми связями, и фрагменты основной цепи могут быть соединены посредством поперечносшивающих фрагментов.
Предпочтительно, фрагмент основной цепи имеет молекулярный вес от 1 кДа до 20 кДа, более предпочтительно от 1 кДа до 15 кДа, и еще более предпочтительно от 1 кДа до 10 кДа. Фрагменты основной цепи предпочтительно также имеют в своей основе PEG, содержат одну или более цепей PEG.
Понятно, что полимерная цепь на основе PEG может заканчиваться или прерываться алкильными или арильными группами, необязательно замещенными гетероатомами и химическими функциональными группами.
В реакционноспособном биоразлагаемом гидрогеле по настоящему изобретению, фрагмент основной цепи отличается наличием некоторого числа функциональных групп, состоящего из соединяющих биоразлагаемых функциональных групп и реакционноспособных функциональных групп. Предпочтительно, общее число соединяющих биоразлагаемых функциональных групп и реакционноспособных функциональных групп больше или равно 16, предпочтительно 16-128, предпочтительно 20-100, также предпочтительно 20-40, более предпочтительно 24-80, также более предпочтительно 28-32 еще более предпочтительно 30-60; наиболее предпочтительно 30-32. Понятно, что помимо соединяющих функциональных групп и реакционноспособных функциональных групп, также могут присутствовать защитные группы.
Предпочтительно, фрагмент основной цепи отличается наличием разветвляющегося ядра, от которого отходят по меньшей мере три полимерных цепочки на основе PEG. Соответственно, в предпочтительном аспекте настоящего изобретения, реагент основной цепи содержит разветвляющееся ядро, от которого отходят по меньшей мере три полимерных цепочки на основе PEG. Такие разветвляющиеся ядра могут состоять из поли- или олигоспиртов в связанной форме, предпочтительно пентаэритритола, трипентаэритритола, гексаглицерина, сахарозы, сорбита, фруктозы, маннита, глюкозы, целлюлозы, амилозы, крахмалов, гидроксиалкил-крахмалов, поливиниловых спиртов, декстранов, гиалурононанов, или разветвляющиеся ядра могут состоять из поли- или олигоаминов в связанной форме, таких как орнитин, диаминомасляная кислота, трилизин, тетрализин, пентализин, гексализин, гептализин, октализин, нонализин, декализин, ундекализин, додекализин, тридекализин, тетрадекализин, пентадекализин или олиголизины, полиэтиленимины, поливиниламины.
Предпочтительно, от разветвляющегося ядра отходят 3-16 полимерных цепочек на основе PEG, более предпочтительно 4-8. Предпочтительные разветвляющиеся ядра могут состоять из пентаэритритола, трилизин, тетрализин, пентализин, гексализин, гептализин или олиголизин, низкомолекулярные полиэтиленимины, гексаглицерин, трипентаэритритол в связанной форме. Предпочтительно, от разветвляющегося ядра отходят 3-16 полимерных цепочек на основе PEG, более предпочтительно 4-8. Предпочтительно, полимерная цепь на основе PEG представляет собой подходящим образом замещенное производное поли(этиленгликоля).
Предпочтительно, от разветвляющегося ядра отходят 3-16 полимерных цепочек на основе PEG, более предпочтительно 4-8. Предпочтительные разветвляющиеся ядра могут содержать пентаэритритол, орнитин, диаминомасляную кислоту, трилизин, тетрализин, пентализин, гексализин, гептализин или олиголизин, низкомолекулярные полиэтиленимины, гексаглицерин, трипентаэритритол в связанной форме. Предпочтительно, от разветвляющегося ядра отходят 3-16 полимерных цепочек на основе PEG, более предпочтительно 4-8. Предпочтительно, полимерная цепь на основе PEG представляет собой линейную поли(этиленгликоль) цепочку, один конец которой соединен с разветвляющимся ядром, а другой - со сверхразветвленным дендритным фрагментом. Понятно, что полимерная цепь на основе PEG может заканчиваться или прерываться алкильными или арильными группами, необязательно замещенными гетероатомами и химическими функциональными группами. Предпочтительно, полимерная цепь на основе PEG представляет собой подходящим образом замещенное производное полиэтиленгликоля (на основе PEG).
Предпочтительные структуры для соответствующих полимерных цепочек на основе PEG, отходящих от разветвляющегося ядра, содержащегося в фрагменте основной цепи, представляют собой мульти-разветвленные PEG-производные, такие как, например, описанные в списке товаров JenKem Technology, USA (доступен для скачивания с www.jenkemusa.com на 28 июля 2009 г), 4-разветвленные PEG-производные (пентаэритритольное ядро), 8-разветвленные PEG-производные (гексаглицериновое ядро) и 8-разветвленные PEG-производные (трипентаэритритольное ядро). Наиболее предпочтительными являются 4-разветвленный PEG-амин (пентаэритритольное ядро) и 4-разветвленный PEG-карбоксил (пентаэритритольное ядро), 8-разветвленный PEG-амин (гексаглицериновое ядро), 8-разветвленный PEG-карбоксил (гексаглицериновое ядро), 8-разветвленный PEG-амин (трипентаэритритольное ядро) и 8-разветвленный PEG-карбоксил (трипентаэритритольное ядро). Предпочтительные молекулярные веса для таких мульти-разветвленных PEG-производных в фрагменте основной цепи составляют от 1 кДа до 20 кДа, более предпочтительно от 1 кДа до 15 кДа, и еще более предпочтительно от 1 кДа до 10 кДа. Понятно, что терминальные амино-группы дополнительно конъюгированы, давая соединяющие и реакционноспособные функциональные группы в фрагменте основной цепи.
Предпочтительно, чтобы общее число соединяющих функциональных групп и реакционноспособных функциональных групп в фрагменте основной цепи было равномерно распределено между несколькими полимерными цепочками на основе PEG, отходящими от разветвляющегося ядра. Если число полимерных цепочек на основе PEG, отходящих от разветвляющегося ядра, не допускает равномерного распределения, предпочтительно, чтобы отклонение от среднего числа суммы соединяющих и реакционноспособных функциональных групп для каждой полимерной цепи на основе PEG сводилось к минимуму.
Более предпочтительно, чтобы общее число соединяющих и реакционноспособных функциональных групп в фрагменте основной цепи было равномерно распределено между несколькими полимерными цепочками на основе PEG, отходящими от разветвляющегося ядра. Например, если имеется 32 соединяющих функциональных групп и реакционноспособных функциональных групп, по 8 групп может быть предоставлено каждой из четырех полимерных цепочек на основе PEG, отходящих от ядра, предпочтительно посредством дендритных фрагментов, присоединенных к концу каждой полимерной цепи на основе PEG. Альтернативно, по 4 группы может быть предоставлено каждой из восьми полимерных цепочек на основе PEG, отходящих от ядра, или по 2 группы может быть предоставлено каждой из шестнадцати полимерных цепочек на основе PEG.
Такие дополнительные функциональные группы могут предоставляться дендритными фрагментами. Предпочтительно, каждый дендритный фрагмент имеет молекулярный вес от 0.4 кДа до 4 кДа, более предпочтительно от 0.4 кДа до 2 кДа. Предпочтительно, каждый дендритный фрагмент имеет по меньшей мере 3 разветвления и по меньшей мере 4 реакционноспособные функциональные группы, и макисмально 63 разветвления и 64 реакционноспособные функциональные группы, предпочтительно по меньшей мере 7 разветвлений и по меньшей мере 8 реакционноспособных функциональных групп, и максимально 31 разветвление и 32 реакционноспособные функциональные группы.
Примеры таких дендритных фрагментов включают трилизин, тетрализин, пентализин, гексализин, гептализин, октализин, нонализин, декализин, ундекализин, додекализин, тридекализин, тетрадекализин, пентадекализин, гексадекализин, гептадекализин, октадекализин, нонадекализин в связанной форме. Примеры таких предпочтительных дендритных фрагментов включают трилизин, тетрализин, пентализин, гексализин, гептализин в связанной форме, наиболее предпочтительны трилизин, пентализин или гептализин, орнитин, диаминомасляная кислота в связанной форме.
Наиболее предпочтительно, реакционноспособный биоразлагаемый гидрогель по настоящему изобретению отличается тем, что фрагмент основной цепи имеет четвертичный атом углерода в формуле С(А-Нур)4, где каждый А независимо представляет собой полимерную цепь на основе поли(этиленгликоля), терминально присоединенную к четвертичному атому углерода стабильной ковалентной связью, и дистальный конец полимерной цепи на основе PEG ковалентно связан с дендритным фрагментом Hyp, каждый дендритный фрагмент Hyp содержит по меньшей мере четыре функциональные группы, представляющие собой соединяющие функциональные группы и реакционноспособные функциональные группы.
Предпочтительно, каждый А независимо выбран из формулы -(CH2)n1(OCH2CH2)nX-, где n1 равен 1 или 2; n представляет собой целое число в диапазоне от 5 до 50; и Х представляет собой химическую функциональную группу, ковалентно связывающую А и Hyp.
Предпочтительно, А и Hyp ковалентно связаны амидной связкой.
Предпочтительно, дендритный фрагмент Hyp представляет собой сверхразветвленный полипептид. Предпочтительно, сверхразветвленный полипептид состоит из остатков лизина в связанной форме. Предпочтительно, каждый дендритный фрагмент Hyp имеет молекулярный вес от 0.4 кДа до 4 кДа. Понятно, что фрагмент основной цепи С(А-Нур)4 может состоять из одинаковых или разных дендритных фрагментов Hyp, и что каждый Hyp может быть выбран независимо. Каждый фрамгент Hyp состоит из 5-32 лизинов, предпочтительно по меньшей мере из 7 лизинов, т.е. каждый фрагмент Hyp состоит из 5-32 лизинов в связанной форме, предпочтительно по меньшей мере из 7 лизинов в связанной форме. Наиболее предпочтительно, Hyp состоит из гептализинила.
Реакция полимеризуемых функциональных групп реагента основной цепи, более конкретно - реакция Hyp с полимеризуемыми функциональными группами поперечносшивающих реагентов на основе полиэтиленгликоля - приводит к образованию стабильной амидной связи.
Предпочтительно, С(А-Нур)4 имеет молекулярный вес от 1 кДа до 20 кДа, более предпочтительно от 1 кДа до 15 кДа, и еще более предпочтительно от 1 кДа до 10 кДа.
Один предпочтительный фрагмент основной цепи изображен ниже, пунктирные линии означают соединяющие биоразлагаемые связки со поперечносшивающими фрагментами, и n представляет собой целое число от 5 до 50:
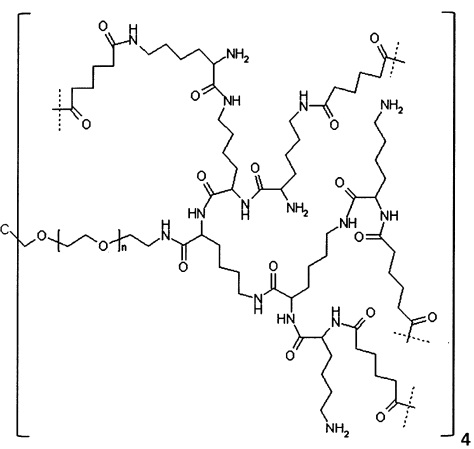
Способность гидрогелей по настоящему изобретению к биоразложению достигается введением гидролитически разрушаемых связей.
Термины «гидролитически разрушаемый», "биоразлагаемый" или "гидролитически расщепляемый", "авторасщепляемый", или "саморасщепление", "саморасщепляемый", "обратимый" или "временный" в контексте настоящего изобретения относятся к связям и связкам, являющимся не-энзиматически гидролитически разрушаемым или расщепляемым в физиологических условиях (водный буфер при рН 7.4, 37°С), имеющим время полужизни в диапазоне от одного часа до трех месяцев, включая (но не ограничиваясь только ими) аконитилы, ацетали, амиды, ангидриды карбоновых кислот, сложные эфиры, имины, гидразоны, полуамиды малеиновой кислоты, ортоэфиры, фосфамиды, сложные эфиры фосфорной кислоты, фосфосилиловые эфиры, силиловые эфиры, сложные эфиры сульфокислот, ароматические карбаматы, их комбинации и т.д.
При наличии в гидрогеле по настоящему изобретению в качестве разрушаемой соединяющей функциональной группы, предпочтительными биоразлагаемыми связками являются сложные эфиры карбоновых кислот, карбонаты, сложные эфиры фосфорных кислот и сложные эфиры сульфокислот, и наиболее предпочтительны сложные эфиры карбоновых кислот или карбонаты.
Стабильные связки не являются неферментативно гидролитически разрушаемыми в физиологических условиях (водный буфер при рН 7.4, 37°С) и имеют времена полужизни от шести месяцев и больше, такие как, например, амиды.
Для введения гидролитически расщепляемых связей, фрагменты основной цепи можно напрямую связывать друг с другом биоразлагаемыми связями.
В одном варианте выполнения, фрагменты основной цепи реакционноспособного биоразлагаемого гидрогеля могут быть соединены напрямую, т.е. без поперечносшивающих фрагментов. Сверхразветвленные дендритные фрагменты двух фрагментов основной цепи такого реакционноспособного биоразлагаемого гидрогеля могут быть напрямую связаны через соединяющую функциональную группу, соединяющую два сверхразветвленных дендритных фрагмента. Альтернативно, два сверхразветвленных дендритных фрагмента двух разных фрагментов основной цепи могут быть соединены через два спейсерных фрагмента, присоединенных к фрагменту основной цепи, а вторым концом присоединенных к поперечносшивающему фрагменту, разделенные соединяющими функциональными группами.
Альтернативно, фрагменты основной цепи могут быть соединены посредством поперечносшивающих фрагментов, каждый поперечносшивающий фрагмент фрагмент имеет на концах по меньшей мере две гидролитически разрушаемые связи. Помимо концевых разрушаемых связей, поперечносшивающие фрагменты могут содержать дополнительные биоразлагаемые связи. Так, каждый конец поперечносшивающего фрагмента, связанный с фрагментом основной цепи, содержит гидролитически разрушаемую связь, и при желании в поперечносшивающем фрагменте могут присутствовать дополнительные биоразлагаемые связи.
Предпочтительно, реакционноспособный биоразлагаемый гидрогель состоит из фрагментов основной цепи, связанных гидролитически разрушаемыми связями, и фрагменты основной цепи соединены посредством поперечносшивающих фрагментов.
Реакционноспособный биоразлагаемый гидрогель может содержать один или более разных типов поперечносшивающих фрагментов, предпочтительно один. поперечносшивающий фрагмент фрагмент может представлять собой линейную или разветвленную молекулу, и предпочтительно представляет собой линейную молекулу. В предпочтительном варианте выполнения настоящего изобретения, поперечносшивающий фрагмент фрагмент соединен с фрагментами основной цепи по меньшей мере двумя биоразлагаемыми связями.
Термин «биоразлагаемая связь» описывает связки, неферментативно гидролитически разрушаемые в физиологических условиях (водный буфер при рН 7.4, 37°С), времена полужизни которых составляют от одного часа до трех месяцев, включающие (но не ограничивающиеся только ими):
аконитилы, ацетали, ангидриды карбоновых кислот, сложные эфиры, имины, гидразоны, полуамиды малеиновой кислоты, ортоэфиры, фосфамиды, сложные эфиры фосфорной кислоты, фосфосилиловые эфиры, силиловые эфиры, сложные эфиры сульфокислот, ароматические карбаматы, их комбинации и т.д. Предпочтительные биоразлагаемые связки представляют собой сложные эфиры, карбонаты, сложные эфиры фосфорной кислоты и сложные эфиры сульфокислот, а наиболее предпочтительными являются сложные эфиры или карбонаты.
Предпочтительно, поперечносшивающие фрагменты имеют молекулярный вес в диапазоне от 60 Да до 5 кДа, более предпочтительно от 0,5 кДа до 4 кДа, еще более предпочтительно от 1 кДа до 4 кДа, еще более предпочтительно от 1 кДа до 3 кДа. В одном варианте выполнения, поперечносшивающий фрагмент фрагмент состоит из полимера.
Помимо олигомерных или полимерных поперечносшивающих фрагментов, могут применяться низкомолекулярные поперечносшивающие фрагменты, особенно когда для формирования биоразлагаемого гидрогеля по настоящему изобретению используются гидрофильные высокомолекулярные фрагменты основной цепи.
Предпочтительно, поперечносшивающие фрагменты на основе поли(этиленгликоля) представляют собой углеводородные цепочки, содержащие соединенные единицы этиленгликоля, необязательно содержащие другие химические функциональные группы, где поперечносшивающие реагенты на основе поли(этиленгликоля) содержат каждый по меньшей мере m единиц этиленгликоля, и где m представляет собой целое число в диапазоне от 3 до 100, предпочтительно от 10 до 70. Предпочтительно, поперечносшивающие фрагменты на основе поли(этиленгликоля) имеют молекулярный вес в диапазоне от 0,5 кДа до 5 кДа.
При использовании в отношении поперечносшивающего фрагмента или полимерной цепи на основе PEG, соединенной с разветвляющимся ядром, термин "на основе PEG" относится к поперечносшивающему фрагменту или полимерной цепи на основе PEG, содержащим по меньшей мере 20 мас.% фрагментов этиленгликоля.
В одном варианте выполнения, мономеры, составляющие полимерные поперечносшивающие фрагменты, соединены биоразлагаемыми связями. Такие полимерные поперечносшивающие фрагменты могут содержать до 100 биоразлагаемых связей или более, в зависимости от молекулярного веса поперечносшивающего фрагмента и молекулярного веса мономерных единиц. Примерами таких поперечносшивающих фрагментов являются поли(молочная кислота) или полимеры на основе поли(гликолевой кислоты). Понятно, что такие цепочки на основе поли(молочной кислоты) или поли(гликолевой кислоты) могут заканчиваться или прерываться алкильными или арильными группами, и что они необязательно могут быть замещены гетероатомами и химическими функциональными группами.
Предпочтительно, поперечносшивающие фрагменты имеют в своей основе PEG, предпочтительно представлены только одной молекулярной цепью на основе PEG. Предпочтительно, поперечносшивающие фрагменты на основе поли(этиленгликоля) представляют собой углеводородные цепочки, содержащие единицы этиленгликоля, необязательно содержащие дополнительные химические функциональные группы, где поперечносшивающие фрагменты на основе поли(этиленгликоля) содержат каждый по меньшей мере m единиц этиленгликоля, где m представляет собой целое число в диапазоне от 3 до 100, предпочтительно от 10 до 70. Предпочтительно, поперечносшивающие фрагменты на основе поли(этиленгликоля) имеют молекулярный вес в диапазоне от 0,5 кДа до 5 кДа.
В предпочтительном варианте выполнения настоящего изобретения, поперечносшивающий фрагмент фрагмент состоит из PEG, который симметрично связан через сложноэфирные связи с двумя альфа, омега-алифатическими дикарбоксильными спейсерами, предосталвяемыми фрагментами основной цепи, связанными со сверхразветвленным дендритным фрагментом стабильными амидными связями.
Дикарбоновые кислоты в спейсерных фрагментах, связанные с фрагментом основной цепи, а по другому концу связанные с поперечносшивающим фрагментом, содержат 3-12 атомов углерода, наиболее предпочтительно 5-8 атомов углерода, и могут быть замещены по одному или более атомам углерода. Предпочтительные заместители представляют собой алкильные группы, гидроксильные группы или амидные группы или замещенные амидные группы. Одна или более из метиленовых групп алифатической дикарбоновй кислоты может необязательно быть замещена О или NH или алкил-замещенным N. Предпочтительный алкил представляет собой линейный или разветвленный алкил, содержащий 1-6 атомов углерода.
Предпочтительно, имеется стабильная амидная свзь между сверхразветвленным дендритным фрагментом и спейсерным фрагментом, связанным с фрагментом основной цепи, а по другому концу связанным со поперечносшивающим фрагментом.
Один предпочтительный поперечносшивающий фрагмент изображен ниже; пунктирные линии означают соединяющие биоразлагаемые связки с фрагментами основной цепи:
 ,
,
где n представляет собой целое число от 5…50.
В реакционноспособных биоразлагаемых гидрогелях, скорость гидролиза биоразлагаемых связей между фрагментами основной цепи и поперечносшивающими фрагментами определяется числом и типом соединенных атомов, соседствующих с карбоксильной группой фрагмента PEG-сложный эфир. Например, выбирая из янтарной, адипиновой или глутаровой кислот для формирования фрагмента PEG-сложный эфир, можно варьировать время полужизни биоразлагаемого гидрогеля по настоящему изобретению.
В реакционноспособном биоразлагаемом гидрогеле присутствие реакционноспособных функциональных групп можно оценить количественно в соответствии с методиками, хорошо известными в данной области техники, например, применяющимися в твердофазном пептидном синтезе. Такое присутствие реакционноспособных функциональных групп в нерастворимом в воде гидрогеле можно количественно оценить как количество моль функциональных групп на грамм реакционноспособного биоразлагаемого гидрогеля.
Содержание амино-групп в гидрогеле можно определить посредством сочетания fmoc-аминокислоты со свободными амино-группами гидрогеля и последующей оценкой содержания fmoc-групп, как описано в работе Gude, М., J. Ryf, et al. (2002) Letters in Peptide Science 9(4): 203-206.
Для определения содержания малеимидных групп, можно лиофилизовать и взвесить аликвоту гидрогельных бусин. Другую аликвоту гидрогеля можно ввести в реакцию с избытком меркаптоэтанола (в 50 мМ натрий-фосфатном буфере, 30 мин при комнатной температуре), и количество вступившего в реакцию меркаптоэтанола можно определить по тесту Эллмана (Ellman, G. L. et al., Biochem. Pharmacol., 1961, 7, 88-95).
Предпочтительно, в реакционноспособном биоразлагаемом гидрогеле загрузка составляет от 0.02 до 2 ммоль/г, более предпочтительно до 0.05 моль/г реакционноспособного биоразлагаемого гидрогеля.
На Фиг. 3 представлен схематичный обзор различных способов, которыми два фрагмента основной цепи могут быть соединены в реакционноспособный биоразлагаемый гидрогель по настоящему изобретению. Сверхразветвленный дендритный фрагмент ("Hyp", овал) содержит несколько реакционноспособных функциональных групп (черные точки) и стабильную связку (белый ромб). Понятно, что каждый сверхразветвленный фрагмент содержит больше реакционноспособных функциональных групп и стабильных связок, чем показано на Фиг. 3, и что Фиг. 3 приведена исключительно в иллюстративных целях.
Сспейсерные фрагменты, связанные с фрагментом основной цепи, а другим концом связанные со поперечносшивающим фрагментом, обозначены звездочками, соединяющие функциональные группы представлены в виде белых стрел. Пунктирные линии указывают место присоединения к большему фрагменту, который не показан.
Фиг. 3а иллюстрирует участок реакционноспособного биоразлагаемого гидрогеля, в котором отдельные фрагменты основной цепи соединены напрямую через соединяющую функциональную группу, содержащую биоразлагаемую связь.
На Фиг. 3b сверхразветвленные дендритные фрагменты двух разных фрагментов основной цепи соединены через две соединяющие функциональные группы, разделенные спейсерным фрагментом.
На Фиг. 3с сверхразветвленные дендритные фрагменты двух разных фрагментов основной цепи соединены через два спейсерных фрагмента, связанные с фрагментом основной цепи, а другим концом связанные со поперечносшивающим фрагментом, и одну соединяющую функциональную группу.
На Фиг. 3d и 3е изображен участок реакционноспособного биоразлагаемого гидрогеля, в котором два сверхразветвленных дендритных фрагмента соединены через поперечносшивающие фрагменты, обозначенные символом "#". поперечносшивающие фрагменты могут содержать или не содержать по меньшей мере одну соединяющую функциональную группу (см. Фиг. 3d и 3е, соответственно).
Тонкие черные линии обозначают полимерные цепочки на основе PEG, отходящие от разветвляющегося ядра (не показано).
Модифицированный реакционноспособный биоразлагаемый гидрогель
Другой аспект настоящего изобретения представляет собой конъюгат, содержащий гидрогель по настоящему изобретению, отличающийся тем, что он состоит из фрагментов основной цепи, связанных гидролитически разрушаемыми связями, и дополнительно несущих стабильные связки к спейсерным молекулам, блокирующим группам, защитным группам или мульти-функциональным фрагментам.
Реакционноспособные функциональные группы фрагментов основной цепи реакционноспособных биоразлагаемых гидрогелей служат точками присоединения для спейсерных молекул, блокирующих групп, защитных групп или мульти-функциональных фрагментов.
Защитные группы известны в данной области и применяются для обратимой защиты химических функциональных групп в процессе синтеза. Подходящей защитной группой для амино-групп является fmoc-группа.
Понятно, что может применяться один тип защитной группы или две или более разных защитных групп, так чтобы обеспечить независимую защиту, т.е. разные защитные группы могут быть удалены в разных условиях.
Модифицированный реакционноспособный биоразлагаемый гидрогель по настоящему изобретению можно функционализировать с помощью спейсера, несущего такую же реакционноспособную функциональную группу. Например, амино-группы можно ввести в модифицированный реакционноспособный биоразлагаемый гидрогель сочетанием с гетеробифункциональным спейсером, таким как надлежащим образом активированный COOH-(EG)6-NH-fmoc (EG=этиленгликоль), и удалением fmoc-защитной группы. Такой реакционноспособный биоразлагаемый гидрогель можно далее соединить со спейсером, несущим другую функциональную группу, такую как малеимидная группа. Соответствующим образом модифицированный реакционноспособный биоразлагаемый гидрогель можно далее конъюгировать с лекарство-линкер реагентами, которые имеют реакционноспособную тиольную группу в линкерном фрагменте.
В таком модифицированном реакционноспособном биоразлагаемом гидрогеле, все оставшиеся реакционноспособные функциональные группы могут быть заблокированы подходящими блокирующими реагентами.
В альтернативном варианте выполнения настоящего изобретения, мульти-функциональные фрагменты вступают в реакцию сочетания с реакционноспособными функциональными группами полимеризованного реакционноспособного биоразлагаемого гидрогеля для увеличения числа реакционноспособных функциональных групп, что позволяет, например, увеличить загрузку лекарственного средства в биоразлагаемый гидрогель по настоящему изобретению. Такие мульти-функциональные фрагменты могут состоять из лизина, дилизина, трилизина, тетрализина, пентализина, гексализина, гептализина или олиголизина, низкомолекулярных полиэтилениминов в связанной форме. Предпочтительно, мульти-функциональный фрагмент состоит из лизинов в связанной форме. Необязательно, такой мульти-функциональный фрагмент может быть защищен защитными группами.
В таком модифицированном реакционноспособном биоразлагаемом гидрогеле, все оставшиеся реакционноспособные функциональные группы могут быть заблокированы подходящими блокирующими реагентами.
На Фиг. 4 показано схематическое изображение участка модифицированного реакционноспособного биоразлагаемого гидрогеля. Сверхразветвленный фрагмент (овал, "Hyp") содержит несколько реакционноспособных функциональных групп, модифицированных спейсерными молекулами или блокирующими группами (черные точки с полулунными структурами). Тонкие черные линии изображают полимерные цепи на основе PEG, отходящие от разветвляющегося ядра (не показано), жирная черная линия изображает часть спейсерного фрагмента, связанного с фрагментом основной цепи, а другим концом связанного со поперечносшивающим фрагментом, который присоединен к сверхразветвленному фрагменту стабильной связью (белый ромб). Белые стрелы обозначают соединяющие функциональные группы.
Пунктирные линии указывают место присоединения к большему фрагменту, который для упрощения не изображен полностью.
Биоразлагаемые гидрогели, содержащие конъюгатные функциональные группы
Другой аспект настоящего изобретения представляет собой конъюгат, содержащий биоразлагаемый гидрогель по настоящему изобретению, отличающийся тем, что он состоит из фрагментов основной цепи, связанных гидролитически разрушаемыми связями, и дополнительно несущих стабильные связки с конъюгатными функциональными группами, содержащими, например, лиганды или хелатирующие группы или ионообменные группы. Соответственно, биоразлагаемый гидрогель, содержащий конъюгатные функциональные группы по настоящему изобретению, содержит фрагменты основной цепи, соединенные гидролитически разрушаемыми связями и дополнительно несущие стабильные связки с конъюгатными функциональными группами, содержащими, например, лиганды или хелатирующие группы или ионообменные группы.
Реакционноспособные функциональные группы фрагментов основной цепи реакционноспособных биоразлагаемых гидрогелей и модифицированных реакционноспособных биоразлагаемых гидрогелей служат точками присоединения для прямого или опосредованного связывания аффинных лигандов или хелатирующих групп или ионообменных групп или их комбинации. В идеале, лиганды или хелатирующие группы или ионообменные группы равномерно распределены по всему объему гидрогеля по настоящему изобретению, и могут присутстовать или не присутствовать на поверхности гидрогеля по настоящему изобретению.
Оставшиеся реакционноспособные функциональные группы, которые не соединены с аффинными лигандами или хелатирующими или ионообменными группами, могут быть заблокированы подходящими блокирующими реагентами.
Такие аффинные лиганды или хелатирующие группы или ионообменные группы отличаются тем, что концентрация аффинных лигандов или хелатирующих групп или ионообменных групп в таких гидрогелях по настоящему изобретению практически стабильна на протяжении первой половины времени, необходимого для полного разложения гидрогеля.
"Практически стабильная" весовая концентрация указанных аффинных лигандов или хелатирующих групп или ионообменных групп означает, что она не опускается ниже 90% изначальной концентрации в первую половину времени, необходимого для полного разложения гидрогеля по настоящему изобретению.
По настоящему изобретению, биоразлагаемый гидрогель, содержащий конъюгированные функциональные группы, состоит из фрагментов основной цепи, связанных гидролитически разрушаемыми связями.
В гидрогеле, несущем аффинные лиганды или хелатирующие группы или ионообменные группы по настоящему изобретению, фрагмент основной цепи характеризуется числом функциональных групп, в которое входят соединяющие биоразлагаемые функциональные группы и конъюгатные функциональные группы, содержащие аффинные лиганды или хелатирующие группы или ионообменные группы. Предпочтительно, сумма соединяющих биоразлагаемых функциональных групп и конъюгатных функциональных групп, несущих аффинные лиганды или хелатирующие группы или ионообменные группы, равна 16-128, предпочтительно 20-100, более предпочтительно 24-80, и наиболее предпочтительно 30-60. Понятно, что, помимо соединяющих функциональных групп и реакционноспособных функциональных групп, могут также присутствовать блокирующие группы.
Предпочтительно, общее число соединяющих функциональных групп и конъюгатных функциональных групп, несущих аффинные лиганды или хелатирующие группы или ионообменные группы, в фрагменте основной цепи равномерно поделено между несколькими полимерными цепочками на основе PEG, отходящими от разветвляющегося ядра. Например, если имеется 32 соединяющие функциональные группы и конъюгатные функциональные группы, несущие аффинные лиганды или хелатирующие группы или ионообменные группы, по 8 групп может быть предоставлено каждой из четырех полимерных цепочек на основе PEG, отходящих от ядра, предпочтительно посредством дендритных фрагментов, присоединенных к концу каждой полимерной цепи на основе PEG. Альтернативно, по 4 группы может быть предоставлено каждой из восьми полимерных цепочек на основе PEG, отходящих от ядра, или по 2 группы может быть предоставлено каждой из шестнадцати полимерных цепочек на основе PEG. Если число полимерных цепочек на основе PEG, отходящих от разветвляющегося ядра, не допускает равномерного распределения, предпочтительно, чтобы отклонение от среднего числа суммы соединяющих функциональных групп и конъюгатных функциональных групп, несущих аффинные лиганды или хелатирующие группы или ионообменные группы, для каждой полимерной цепи на основе PEG сводилось к минимуму.
Также предпочтительно, чтобы общее число соединяющих биоразлагаемых функциональных групп и стабильных связок с конъюгатными функциональными группами, несущими лиганды или хелатирующие группы или ионообменные группы, или, необязательно, спейсерные молекулы, или блокирующие группы, было больше или равно 16, предпочтительно 20-40, более предпочтительно 28-32, и наиболее предпочтительно 30-32.
В простейшем случае, гидрогель, несущий ионообменные группы, идентичен реакционноспособному биоразлагаемому гидрогелю.
Предпочтительно, каждый дендритный фрагмент фрагмента основной цепи биоразлагаемого гидрогеля, содержащего конъюгатные функциональные группы, имеет по меньшей мере 3 разветвления и мо меньше мере 4 биоразлагаемые и/или стабильные связки, более предпочтительно 5 разветвлений и 6 биоразлагаемых и/или стабильных связок, наиболее предпочтительно 7 разветвлений и 8 биоразлагаемых и/или стабильных связок, или, необязательно, 15 разветвлений и 16 биоразлагаемых и/или стабильных связок.
Подходящие лиганды, присутствующие в связанной форме в биоразлагаемом гидрогеле, содержащем конъюгатные функциональные группы по настоящему изобретению, представляют собой, например, аффинные лиганды, такие как биотин. Другие лиганды представляют собой, например аффинные лиганды, такие как: 4-аминобензамидин, 3-(2'-аминобензгидрилокси)тропан, ε-аминокапроил-п-хлорбензиламид, 1-амино-4-[3-(4,6-дихлортриазин-2-иламино)-4-сульфофениламино]антрахинон-2-сульфоновая кислота, 2-(2'-амино-4'-метилфенилтио)-N,N-диметилбензиламин дигидрохлорид, ангиопоэтин-1, аптамеры, аротиноидная кислота, авидин, биотин, калмодулин, кокаэтилен, цитоспорон В, N,N-дигексил-2-(4-фторфенил)индол-3-ацетамид, N,N-дипропил-2-(4-хлорфенил)-6,8-дихлор-имидазо[1,2-а]пиридин-3-ацетамид, 5-фтор-2'-деоксиуридин 5'-(п-аминофенил) монофосфат, S-гексил-L-глутатион, (S,S)-4-фенил-α-(4-фенилоксазолидин-2-илиден)-2-оксазолидин-2-ацетонитрил, Pro-Leu-Gly гидроксамат, 2-(4-(2-(трифторметил)фенил)пиперидин-1-карбоксамидо)бензойная кислота, триметил(м-аминофенил)аммония хлорид, урокортин III, кофакторы, такие как аденозин трифосфат, s-аденозил метионин, аскорбиновая кислота, кобаламин, коэнзим А, коэнзим В, коэнзим М, коэнзим Q, коэнзим F420, цитидин трифосфат, флавин мононуклеотид, флавин аденин динуклеотид, глутатион, гем, липоамид, менахинон, метанофуран, метилкобаламин, молибдоптерин, НАД+, НАДФ+, нуклеотидные сахара, 3'-фосфоаденозин-5'-фосфосульфат, пиридоксаль фосфат, полигистидины, пирролохинолин хинон, рибофлавин, стрептавидин, тетрагидробиоптерин, тетрагидрометаноптерин, тетрагидрофолиевая кислота, белок-переносчик биотин-карбоксила (ВССР), хитин-связывающий белок, FK506 связывающие белки (FKBP), FLAG метка, зеленый флуоресцентный белок, глутатион-S-трансфераза, гемагглютинин (НА), мальтоза-связывающий белок, myc метка, NusA, белок С эпитоп, S-метка, стреп-метка, тиоредоксины, триазины (предпочтительно 2,4,6-тризамещенные триазины), аффинные каркасные белки, такие как фрагменты антител.
Подходящими хелатирующими группами, присутствующими в связанной форме в биоразлагаемом гидрогеле, содержащем конъюгатные функциональные группы, по настоящему изобретению являются, например ионные группы, способные взаимодействовать с субстратом по типу ионообменного вещества. Другими примерами хелатирующих групп являются комплексообразующие группы. Различными типами хелатирующих групп являются, например, 2,2'-бипиридил, 1,2-бис(2-аминофенокси)этан-N,N,N',N'-тетрауксусная кислота, дефероксамин мезилат, деферриферрихром, диэтилентриамин, 2,3-димеркапто-1-пропанол, димеркаптоянтарная кислота, диметилглиоксин, 2,2'-дипиридил, Этилендиамин, этилендиаминтетра(метиленфосфоновая кислота), 1,2-бис(2-амино-5-бромфенокси)этан-N,N,N',N'-тетрауксусная кислота, 8-гидроксихинолин, иминодиацетат, иминоди(метиленфосфоновая кислота), L-мимозин, нитрилотриацетат, оксалат, 1,10-фенантролин, фитиновая кислота, тартрат, 1,4,7,10-тетраазациклододекан-1,4,7,10-тетраацетат, N,N,N',N'-тетракис(2-пиридилметил)этилендиамин, триаминотриэтиламин, иминодиуксусная кислота, тиомочевина, 2-пиколиламин.
Ионообменные группы, присутствующие в связанной форме в биоразлагаемом гидрогеле, содержащем конъюгатные функциональные группы, по настоящему изобретению, представляют собой обычно используемые химические функциональные группы, присоединенные к ионообменным смолам, такие как сильно кислые группы, например сульфоновые кислотные группы, например пропилсульфоновая кислота; сильно основные группы, такие как четвертичные амино-группы, например триметиламмониевые группы, например пропилтриметиламмония хлорид; слабокислые группы, например алкилкарбоновые кислоты; или слабоосновные группы, такие как первичные, вторичные и/или третичные алкиламино-группы.
На Фиг. 5 показано схематическое изображение участка гидрогеля, содержащего конъюгатные функциональные группы, Сверхразветвленный фрагмент (овал, "Hyp") содержит несколько стабильных связей (белые ромбы) с конъюгатами, такими как аффинные лиганды или хелатирующие группы (черные овалы) или спейсерный фрагмент, связанный с фрагментом основной цепи, и связанный с другой стороны со поперечносшивающим фрагментом (жирная черная линия). Звездочки обозначают спейсерные фрагменты, связанные с фрагментом основной цепи, и связанные с другой стороны со поперечносшивающим фрагментом; # обозначает поперечносшивающие фрагменты; пунктирные линии указывают место присоединения к большему фрагменту, который не показан. Тонкая черная линия обозначает полимерную цепь на основе PEG, отходящую от разветвляющегося ядра (не показано).
Пролекарства на базе гидрогеля
Другой аспект настоящего изобретения представляет собой связанное с носителем пролекарство, содержащее биоразлагаемый гидрогель по настоящему изобретению в качестве носителя, где имеется несколько стабильных связок фрагментов основной цепи с временным линкером пролекарства, к которому ковалентно присоединен биологически активный фрагмент.
"Пролекарство" это любое соединение, претерпевающее биотрансформацию перед тем, как проявить свое фармакологическое действие. Таким образом, пролекарства можно рассматривать как лекарства, содержащие специальные нетоксичные защитные группы, применяемые в качестве временного средства для изменения или устранения нежелательных свойств родительской молекулы. Очевидно, это также включает усиление желаемых свойств лекарственного средства и подавление нежелательных свойств.
Термины "связанное с носителем Пролекарство", "Пролекарство на носителе" относятся к пролекарству, которое содержит временную связку определенного действующего вещества с группой временного носителя, которая дает улучшение физико-химических или фармакокинетических свойств, и которая легко удаляется in vivo, обычно путем гидролитического расщепления.
Реакционноспособные функциональные группы реакционноспособного биоразлагаемого гидрогеля или модифицированного реакционноспособного биоразлагаемого гидрогеля служат местом присоединения для непосредственного связывания через упомянутые ранее стабильные связки с лекарственным средством, конъюгатом лекарство-линкер, пролекарством, связанным с носителем пролекарством и т.п.. В идеале, связанные с гидрогелем конъюгаты лекарство-линкер распределены в гидрогеле по настоящему изобретению равномерно, и могут присутствовать или не присутствовать на поверхности гидрогеля по настоящему изобретению.
Оставшиеся реакционноспособные функциональные группы, не соединенные с временным линкером пролекарства или со спейсером, присоединенным к временному линкеру пролекарства, могут быть заблокированы подходящими блокирующими реагентами.
Предпочтительно, ковалентные связывания, формируемые между реакционноспособными функциональными группами, предоставляемыми фрагментами основной цепи, и линкером пролекарства, представляют собой стабильные связи. Подходящие функциональные группы для присоединения линкера пролекарства к гидрогелю по настоящему изобретению, включают (но не ограничиваются только ими) карбоновые кислоты и их производные, карбонаты и их производные, гидрокси-группы, гидразин, гидроксиламин, полуамид малеиновой кислоты и его производные, кетоны, амины, альдегиды, тиолы и дисульфиды.
После загрузки конъюгата лекарство-линкер на гидрогель, содержащий малеимидные группы, все остальные функциональные группы блокируют подходящими блокирующими реагентами для предотвращения нежелательных побочных реакций.
Согласно настоящему изобретению, биоразлагаемый гидрогель по настоящему изобретению состоит из фрагментов основной цепи, связанных гидролитически разрушаемыми связями.
В гидрогеле, несущем конъюгаты лекарство-линкер по настоящему изобретению, фрагмент основной цепи отличается наличием нескольких функциональных групп, включающих соединяющие биоразлагаемые функциональные группы и гидрогель-соединенные конъюгаты лекарство-линкер, и, необязательно, концевые группы. Это означает, что фрагмент основной цепи отличается наличием нескольких гидрогель-соединенных конъюгатов лекарство-линкер; функциональных групп, включая соединяющие биоразлагаемые функциональные группы; и, необязательно, концевые группы. Предпочтительно, общее число соединяющих биоразлагаемых функциональных групп и конъюгатов лекарство-линкер и концевых групп равно 16-128, предпочтительно 20-100, более предпочтительно 24-80, и наиболее предпочтительно 30-60.
Предпочтительно, общее число соединяющих функциональных групп, гидрогель-соединенных конъюгатов лекарство-линкер и концевых групп в фрагменте основной цепи равномерно распределено среди полимерных цепочек на основе PEG, отходящих от разветвляющегося ядра. Например, если имеется 32 соединяющие функциональные группы, гидрогель-соединенных конъюгатов лекарство-линкер и концевых групп, по восемь групп может быть присоединено к каждой из четырех полимерных цепочек на основе PEG, отходящих от ядра, предпочтительно посредством дендритных фрагментов, присоединенных к концу каждой полимерной цепочки на основе PEG. Альтернативно, по четыре функциональные группы может быть присоединено к каждой из восьми полимерных цепочек на основе PEG, отходящих от ядра, или по две функциональные группы - к каждой из шестнадцати полимерных цепочек на основе PEG. Если число полимерных цепочек на основе PEG, отходящих от разветвляющегося ядра, не допускает равномерного распределения, предпочтительно, чтобы отклонение от среднего числа суммы соединяющих функциональных групп, гидрогель-соединенных конъюгатов лекарство-линкер и концевых групп для каждой полимерной цепи на основе PEG сводилось к минимуму.
Для таких связанных с носителем пролекарств по настоящему изобретению желательно, чтобы почти все высвобождение лекарственного средства (>90%) происходило до того, как произойдет высвобождение заметного количества фрагментов основной цепи (<10%). Это достигается регулировкой времени полужизни связанного с носителем пролекарства относительно кинетики разложения гидрогеля по настоящему изобретению.
Термины "линкер", "линкерная группа", "линкерная структура" или "линкерный агент" относятся к фрагменту, который одним своим концом присоединен к лекарственному фрагменту через обратимую связку, а другим концом присоединен стабильной связью к спейсерной молекуле, стабильным образом присоединенной к сверхразветвленному дендритному фрагменту, или напрямую присоединен стабильной связью к сверхразветвленному дендритному фрагменту.
Для линкерного агент предпочтительно образование обратимого связывания с биологически активным фрагментом, предпочтительно таким образом, чтобы после расщепления линкера биологически активный фрагмент высвобождался в немодифицированной форме. Различные линкерные агенты или линкерные группы, которые могут применяться для этой цели, описаны в работе B. Testa и др. (В. Testa, J. Mayer, Hydrolysis in Drug и Prodrug Metabolism, Wiley-VCH, 2003).
Также предпочтительно, чтобы большинство линкерных структур оставалось присоединенными к гидрогелю по настоящему изобретению после расщепления биоразлагаемой связки с биологически активным фрагментом. Если линкер представляет собой каскадный линкер пролекарства, предпочтительно, чтобы активирующая группа оставалась устойчиво связанной с гидрогелем по настоящему изобретению.
Предпочтительно, временный линкер пролекарства соединен с биологически активным фрагментом посредством саморасщепляемой функциональной группы. Предпочтительно, линкер обладает способностью к саморасщеплению, и, как следствие, гидрогель-линкер-лекарство представляет собой связанное с носителем пролекарство, способное высвобождать лекарственное средство из конъюгата таким образом, что высвобождение зависит главным образом от саморасщепления линкера.
Термины "саморасщепляемый" или "гидролитически разрушаемый" используются как синонимы.
"Саморасщепляемая функциональная группа" содержит гидролитически разрушаемую связь.
Если саморасщепляемая связка формируется с участием первичной или ароматической амино-группы биологически активного фрагмента, предпочтительными являются карбаматная или амидная группа.
Примеры таких биологически активных соединений или лекарственных средств выбраны из группы, состоящей из средств, оказывающих действие на центральную нервную систему, противоинфекционых, противоаллергических, иммуномодулирующих средств, средств против ожирения, антикоагулянтов, противодиабетических средств, противоопухолевых средств, антибактериальных средств, противогрибковых средств, анальгетиков, противозачаточных средств, противовоспалительных средств, стероидов, сосудорасширяющих, сосудосуживающих и сердечно-сосудистых средств. Примеры включают (но не ограничиваются только ими): АСТН, аденозин деаминаза, агалзидаза, альбумин, альфа-1 антитрипсин (ААТ), альфа-1 протеиназы ингибитор (API), алглюкозидаза, алтеплаза, антистреплаза, анкрод серин протеаза, антитела (моноклональные или поликлональные и фрагменты или гибриды), антитромбин III, антитрипсины, апротинины, аспарагиназы, бифалин, костно-морфогенетические белки, кальцитонин (лосося), коллагеназа, DNаза, эндорфины, энфувиритид, энцефалины, эритропоетины, фактор VIIa, фактор VIII, фактор VIIIa, фактор IX, фибринолизин, гибридные белки, фолликуло-стимулирующие гормоны, гранулоцитарный колониестимулирующий фактор (Г-КСФ), галактозидаза, глюкагон, глюкагоноподобные пептиды типа GLP-1, глюкоцереброзидаза, гранулоцитарный-моноцитарный колониестимулирующий фактор (GM-CSF), хорионический гонадотропин (hCG), гемоглобины, вакцины гепатита В, гирудин, гиалуронидазы, идурнонидаза, иммуноглобулины, вакцины против простуды, интерлейкины (1 альфа, 1 бета, 2, 3, 4, 6, 10, 11, 12), антагонист рецептора IL-1 (rhIL-1ra), инсулины, интерфероны (альфа 2а, альфа 2b, альфа 2с, бета 1а, бета 1b, гамма 1а, гамма 1b), фактор роста кератиноцитов (KGF), лактаза, левпролид, левотироксин, лютеинизирующий гормон, вакцина Лайма, натрийуретические пептиды, панкрелипазы, папаин, паращитовидный гормон, PDGF, пепсин, фосфолипаза-активирующий белок (PLAP), тромбоцит-активирующий фактор ацетилгидролаза (PAF-AH), пролактин, белок С, октреотид, секретин, серморелин, пероксидисмутаза (SOD), соматропины (гормон роста), соматостатин, стерптокиназа, сукраза, фрагмент тетанотоксина, тилактаза, тромбины, тимозин, тиреостимулирующий гормон, тиротропин, трансформирующие факторы роста, фактор некроза опухолей (TNF), TNF рецептор-IgG Fc, тканевой активатор плазминогена (tPA), трансферрин, TSH, уратоксидаза, урокиназа, вакцины, растительные белки, такие как лектины и рицины, акарбоза, ацивицин, алапроклат, алендронат, амантадин, амбрисентан, амикацин, аминептин, аминоглютетимид, амисулприд, амлодипин, амотосален, амоксапен, амоксициллин, амфетамин, амфотерицин В, ампициллин, ампренавир, ампринон, анагрелид, анилерунид, антибиотики, апраклонидин, апрамицин, мышьяк(III)-оксид, атикаин, атенолол, атомоксетин, авизафон, баклофен, беназеприл, бенсеразид, бензокаин, бетаин безводный, бетаксолол, блеомицин, босентан, бромфенак, брофаромин, бусульфан, кальфитонин, карведилол, катин, катинон, карбутамид, цефалексин, целекоксиб, ципрофлоксацин, кладрибин, клинафлоксацин, клофарабин, дасатиниб, дефероксамин, делавирдин, дезипрамин, даунорубицин, дексметилфенидат, дексметилфенидат, диафенилсульфон, дизоцилпин, допамин, добутамин, дорзоламид, доксорубицин, дулоксетин, эфлорнитин, эналаприл, эпинефрин, эпирубицин, эрголин, эртапенем, эсмолол, эноксацин, этамбутол, фенфлурамин, фенолдопам, фенотерол, финголимод, флекаинид, флувоксамин, фолиевая кислота, фосампренавир, фловатриптан, фуросемид, флуоэксетин, габапентин, гатифлоксацин, гемифлокацин, гентамицин, грепафлоксацин, гексилкаин, гидралазан, гидрохлоротиазид, икофунгипен, идарубицин, имиквимод, инверсин, изопротеренол, исрадипин, канамицин А, кетамин, лабеталол, ламивудин, левобунолол, леводопа, левотироксин, лизиноприл, ломефлоксацин, лоракарбеф, мапротилин, мефлохин, мелфалан, мемантин, меропенем, месалазин, мескалин, метилдопа, метилендиоксиметамфетамин, метопролол, милнаципран, митоксантрон, моксифлоксацин, норэпинефрин, норфлоксацин, нортриптилин, неомицин В, нистатин, олсетамивир, памидроновая кислота, пароксетин, пазуфлоксацин, пеметрексед, периндоприл, фенметразин, фенелзин, прегабалин, прокаин, превдоэфедрин, протриптилин, ребоксетин, ритодрин, сабарубицин, салбутамол, серотонин, сертралин, ситаглиптин, соталол, спектиномицин, сульфадиазин, сульфамеразин, сертралин, спректиномицин, сульфален, сульфаметоксазол, такрин, тамсулозин, тербуталин, тимолол, тирофибан, тобрамицин, токаинид, тосуфлоксацин, трандолаприл, транексамовая кислота, транилципромин, тримерексат, тровафлоксацин, валацикловир, валганцикловир, ванкомицин, виомицин, вилоксазин, витамины и залцитабин.
Предпочтительно, связка между линкером пролекарства и биоактивным фрагментом гидролитически разрушаема в физиологических условиях (водный буфер при рН 7.4, 37°С), при этом время полужизни находится в диапазоне от одного часа до трех месяцев, и включает (но не ограничивается только ими): аконитилы, ацетали, амиды, ангидриды карбоновых кислот, сложные эфиры, имины, гидразоны, полуамиды малеиновой кислоты, ортоэфиры, фосфамиды, сложные эфиры фосфорной кислоты, фосфосилиловые эфиры, силиловые эфиры, сложные эфиры сульфокислот, ароматические карбаматы, их комбинации и т.д. Предпочтительные биоразлагаемые связки представляют собой сложные эфиры, карбонаты, сложные эфиры фосфорной кислоты и сложные эфиры сульфокислот, а наиболее предпочтительны сложные эфиры или карбонаты в случае биологически активных фрагментов или лекарственных средств, стабильным образом связанных через первичные или ароматические амино-группы.
Если саморасщепляемая связка сформирована совместно с первичной или ароматической амино-группой биологически активного фрагмента, предпочтительна карбаматная или амидная группа.
Предпочтительное временное пролекарство описано в WO-A 2005/099768 и, таким образом, выбрано из общих формул (I) и (II):
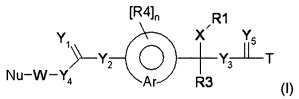
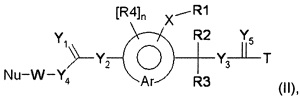
где X, Y1, Y2, Y3, Y4, Y5, R1, R2, R3, R4, Nu, W, n, и Т в формуле (I) и (II) имеют следующие значения:
Т представляет собой амин-содержащий биологически активный фрагмент, который присоединен к остальной части структур, представленных на формуле (I) и (II), путем образования связки -O-(C=O)-N-; -O-(C=S)-N-; -S-(C=O)-N-; или -S-(C=S)-N-;
X представляет собой спейсерный фрагмент;
Y1 и Y2 каждый независимо представляют собой О, S или NR6;
Y3 представляет собой О или S;
Y4 представляет собой О, NR6 или -C(R7)(R8)-;
Y5 представляет собой О или S;
Y4 представляет собой О, NR6 или -C(R7)(R8);
R3 представляет собой фрагмент, выбранный из группы, состоящей из атома водорода, замещенных или незамещенных линейных, разветвленных или циклических алкильных или гетероалкильных групп, арилов, замещенных арилов, замещенных или незамещенных гетероарилов, циано-групп, нитро-групп, галогенов, карбокси-групп, карбоксиалкильных групп, алкилкарбонильных групп или карбоксамидоалкильных групп;
R4 представляет собой фрагмент, выбранный из группы, состоящей из атома водорода, замещенных или незамещенных линейных, разветвленных или циклических алкилов или гетероалкилов, арилов, замещенных арилов, замещенных или незамещенных гетероарилов, замещенных или незамещенных линейных, разветвленных или циклических алкокси-групп, замещенных или незамещенных линейных, разветвленных или циклических гетероалкокси-групп, арилокси-групп или гетероарилокси-групп, циано-групп и галогенов;
R7 и R8 каждый независимо выбраны из группы, состоящей из атома водорода, замещенных или незамещенных линейных, разветвленных или циклических алкилов или гетероалкилов, арилов, замещенных арилов, замещенных или незамещенных гетероарилов, карбоксиалкильных групп, алкилкарбонильных групп, карбоксамидоалкильных групп, циано-групп и галогенов;
R6 представляет собой группу, выбранную из атома водорода, замещенных или незамещенных линейных, разветвленных или циклических алкилов или гетероалкилов, арилов, замещенных арилов и замещенных или незамещенных гетероарилов;
R1 представляет собой биоразлагаемый гидрогель по настоящему изобретению;
W представляет собой группу, выбранную из замещенных или незамещенных линейных, разветвленных или циклических алкилов, арилов, замещенных арилов, замещенных или незамещенных линейных, разветвленных или циклических гетероалкилов, замещенных или незамещенных гетероарилов;
Nu представляет собой нуклеофил;
n равен нулю или целому положительному числу; и
Ar представляет собой мульти-замещенный ароматический углеводород или мульти-замещенный ароматический гетероцикл.
Другое предпочтительное пролекарство по настоящему изобретению описано в WO-A 2006/136586. Соответственно, предпочтительными являются следующие структуры, выбранные из общих формул (III), (IV) и (V):
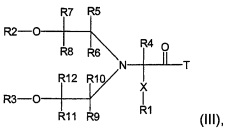
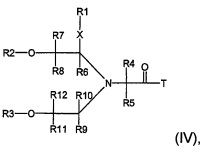
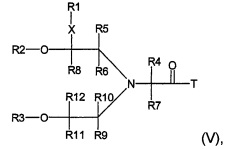
где R1, R2, R3, R4, R5, R6, R7, R8, R9, R10, R11, R12, X, и Т в формулах (III), (IV) и (V) имеют следующие значения:
Т представляет собой биологически активный фрагмент;
Х представляет собой спейсерный фрагмент, такой как R13-Y1;
Y1 представляет собой О, S, NR6, сукцинимид, малеимид, ненасыщенные углерод-углеродные связи или любой гетероатом, содержащий свободную пару электронов, или отсутствует;
R13 выбран из замещенных или незамещенных линейных, разветвленных или циклических алкилов или гетероалкилов, арилов, замещенных арилов, замещенных или незамещенных гетероарилов;
R2 и R3 независимо выбраны из атома водорода, ацильных групп или защитных групп для гидрокси-групп;
R4-R12 независимо выбраны из атома водорода, замещенных или незамещенных линейных, разветвленных или циклических алкилов или гетероалкилов, арилов, замещенных арилов, замещенных или незамещенных гетероарилов, циано-групп, нитро-групп, галогенов, карбокси-групп, карбоксамидных групп;
R1 представляет собой биоразлагаемый гидрогель по настоящему изобретению.
В другом предпочтительном варианте выполнения, предпочтительная структура для пролекарства по настоящему изобретению представляет собой пролекарственый конъюгат D-L, в котором
- D представляет собой биологически активный фрагмент; и
- L представляет собой
небиологически активный линкерный фрагмент -L1, представленный формулой (VI),
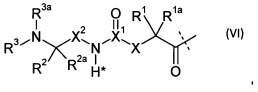
где пунктирная линия означает соединение с первичной или вторичной амино-группой аминосодержащего биологически активного фрагмента D посредством образования амидной связи; и где X, X1, X2, R1, R1a, R2, R2a, R3, и R3a в формуле (VI) имеют следующие значения:
X представляет собой C(R4R4a); N(R4); О; C(R4R4a)-C(R5R5a); C(R5R5a)-C(R4R4a); C(R4R4a)-N(R6); N(R6)-C(R4R4a); C(R4R4a)-O или O-C(R4R4a);
X1 представляет собой С или S(O);
X2 представляет собой C(R7, R7a) или C(R7, R7a)-C(R8, R8a);
R1, R1a, R2, R2a, R3, R3a, R4, R4a, R5, R5a, R6, R7, R7a, R8, R8a независимо выбраны из группы, состоящей из Н и С1-4 алкила; или
необязательно, одна или более из пар R1a/R4a, R1a/R5a, R4a/R5a, R4a/R5a, R7a/R8a образуют химическую связь;
необязательно, одна или более из пар R1/R1a, R2/R2a, R4/R4a, R5/R5a, R7/R7a, R8/R8a объединены вместе с атомом, с которым они соединены, с образованием С3-7 циклоалкила или 4-7-членного гетероциклила;
необязательно, одна или более из пар R1/R4, R1/R5, R1/R6, R4/R5, R7/R8, R2/R3 объединены вместе с атомами, с которыми они соединены, с образованием цикла А;
необязательно, R3/R3a объединены вместе с атомом азота, с которым они соединены, с образованием 4-7-членного гетероцикла;
А выбран из группы, состоящей из фенила; нафтила; инденила; инданила; тетралинила; С3-10 циклоалкила; 4-7-членного гетероциклила и 9-11-членного гетеробициклила; и
где L1 замещен одной группой L2-Z и необязательно дополнительно замещен, при условии, что атом водорода, помеченный звездочкой в формуле (VI), не заменен на заместитель;
где
L2 представляет собой одинарную химическую связь или спейсер; и
Z это заместитель по настоящему изобретению.
Пролекарственные конъюгаты данного типа описаны в European Patent application EP-A 08150973.
"Алкил" означает линейную или разветвленную углеродную цепочку. Каждый атом водорода у алкильного атома углерода может быть заменен на заместитель.
"C1-4 алкил" означает алкильную цепочку, содержащую 1-4 атомов углерода, например, в случае концевого расположения в молекуле: метил, этил, н-пропил, изопропил, н-бутил, изобутил, втор-бутил, трет-бутил, или, например, -СН2-, -СН2-СН2-, -СН(СН3)-, -СН2-СН2-СН2-, -CH(C2H5)-, -С(СН3)2-, когда два фрагмента молекулы соединены алкильной группой. Каждый атом водорода у C1-4 алкильного атома углерода может быть заменен на заместитель.
"C1-6 алкил" означает алкильную цепочку, содержащую 1-6 атомов углерода, например, в случае концевого расположения в молекуле: С1-4 алкил, метил, этил, н-пропил, изопропил, н-бутил, изобутил, втор-бутил, трет-бутил, н-пентил, н-гексил, или, например, -СН2-, -СН2-СН2-, -СН(СН3)-, -СН2-СН2-СН2-, -СН(С2Н5)-, -С(СН3)2-, когда два фрагмента молекулы соединены алкильной группой. Каждый атом водорода у C1-6 алкильного атома углерода может быть заменен на заместитель.
Соответственно, "C1-18 алкил" означает алкильную цепочку, содержащую 1-18 атомов углерода, и "C8-18 алкил" означает алкильную цепочку, содержащую 8-18 атомов углерода. Соответственно, "C1-50 алкил" означает алкильную цепочку, содержащую 1-50 атомов углерода.
"C2-50 алкенил" означает разветвленную или неразветвленную алкенильную цепочку, содержащую 2-50 атомов углерода, например, в случае концевого расположения в молекуле: -СН=СН2, -СН=СН-СН3, -СН2-СН=СН2, -СН=СН-СН2-СН3, -СН=СН-СН=СН2, или например -СН=СН-, когда два фрагмента молекулы соединены алкенильной группой. Каждый атом водорода у 62-50 алкенильного атома углерода может быть заменен на заместитель, определение которому дается дополнительно. Соответственно, термин "алкенил" относится к углеродной цепочке, содержащей по меньшей мере одну углерод-углеродную двойную связь. Необязательно может содержаться одна или более тройных связей.
"C2-50 алкинил" означает разветвленную или неразветвленную алкинильную цепочку, содержащую 2-50 атомов углерода, например, в случае концевого расположения в молекуле: -С≡СН, -СН2-С≡СН, СН2-СН2-С≡СН, СН2-С≡С-СН3, или например -С≡С-, когда два фрагмента молекулы соединены алкинильной группой. Каждый атом водорода у C2-50 алкинильного углерода может быть заменен на заместитель, определение которому дается дополнительно. Соответственно, термин "алкинил" относится к углеродной цепочке, содержащей по меньшей мере одну углерод-углеродную тройную связь. Необязательно может содержаться одна или более двойных связей "С3-7 циклоалкил" или "С3-7 циклоалкильное кольцо" означает циклическую алкильную цепь, содержащую 3-7 атомов углерода, в которой могут находиться углерод-углеродные двойные связи, которая является по меньшей мере частично насыщенной, например циклопропил, циклобутил, циклопентил, циклогексил, циклогексенил, циклогептил. Каждый атом водорода у циклоалкильного атома углерода может быть заменен на заместитель. Термин "С3-7 циклоалкил" или "С3-7 циклоалкильное кольцо" также включает мостиковые бициклы, такие как норборнан или норборнен. Соответственно, "С3-5 циклоалкил" означает циклоалкил, содержащий 3-5 атомов углерода, а С3-10 циклоалкил - циклоалкил, содержащий 3-10 атомов углерода.
Соответственно, "С3-10 циклоалкил" означает циклический алкил, содержащий 3-10 атомов углерода, например С3-7 циклоалкил; циклопропил, циклобутил, циклопентил, циклогексил, циклогексенил, циклогептил, циклооктил, циклононил, циклодецил. Термин "С3-10 циклоалкил" также включает по меньшей мере частично насыщенные карбомоно- и -бициклы.
Термин "галоген" означает фтор, хлор, бром или иод. В целом предпочтительно, чтобы галоген представлял собой фтор или хлор.
"4-7-членный гетероциклил" или "4-7-членный гетероцикл" означает цикл, имеющий 4, 5, 6 или 7 атомов в цикле, который может содержать до максимального числа двойных связей (ароматическое или неароматическое кольцо, полностью, частично или ненасыщенное) где от по меньшей мере одного атома в цикле до 4 атомов в цикле заменены на гетероатом, выбранный из группы, состоящей из серы (включая -S(O)-, -S(O)2-), кислорода и азота (включая =N(O)-), и где цикл связан с остальной частью молекулы через атом углерода или азота. Примерами 4-7-членных гетероциклов являются азетидин, оксетан, тиетан, фуран, тиофен, пиррол, пирролин, имидазол, имидазолин, пиразол, пиразолин, оксазол, оксазолин, изоксазол, изоксазолин, тиазол, тиазолин, изотиазол, изотиазолин, тиадиазол, тиадиазолин, тетрагидрофуран, тетрагидротиофен, пирролидин, имидазолидин, пиразолидин, оксазолидин, изоксазолидин, тиазолидин, изотиазолидин, тиадиазолидин, сульфолан, пиран, дигидропиран, тетрагидропиран, имидазолидин, пиридин, пиридазин, пиразин, пиримидин, пиперазин, пиперидин, морфолин, тетразол, тризол, тризолидин, тетразолидин, диазепан, азепин или гомопиперазин.
"9-11-членный гетеробициклил" или "9-11-членный гетеробицикл" означает гетероциклическую систему из двух циклов, содержащую 9-11 атомов в цикле, в которой по меньшей мере один атом в цикле является общим для обоих циклов, и которая может содержать до максимального числа двойных связей (ароматическое или неароматическое кольцо, полностью, частично или ненасыщенное) где от по меньшей мере одного атома в цикле до 6 атомов в цикле заменены на гетероатом, выбранный из группы, состоящей из серы (включая -S(O)-, -S(O)2-), кислорода и азота (включая =N(O)-), и где цикл связан с остальной частью молекулы через атом углерода или азота. Примерами 9-11-членного гетеробицикла являются индол, индолин, бензофуран, бензотиофен, бензоксазол, бензизоксазол, бензотиазол, бензизотиазол, бензимидазол, бензимидазолин, хинолин, хиназолин, дигидрохиназолин, хинолин, дигидрохинолин, тетрагидрохинолин, декагидрохинолин, изохинолин, декагидроизохинолин, тетрагидроизохинолин, дигидроизохинолин, бензазепин, пурин или птеридин. Термин «9-11-членный гетеробицикл» также включает спиро-структуры из двух циклов, такие как 1,4-диокса-8-азаспиро[4.5]декан или мостиковые гетероциклы, такие как 8-аза-бицикло[3.2.1]октан.
Предпочтительно, один или более дополнительных необязательных заместителей независимо выбраны из группы, состоящей из галогена; CN; COOR9; OR9; C(O)R9; C(O)N(R9R9a); S(O)2N(R9R9a); S(O)N(R9R9a); S(O)2R9; S(O)R9; N(R9)S(O)2N(R9aR9b); SR9; N(R9R9a); NO2; OC(O)R9; N(R9)C(O)R9a; N(R9)S(O)2R9a; N(R9)S(O)R9a; N(R9)C(O)OR9a; N(R9)C(O)N(R9aR9b); OC(O)N(R9R9a); T; C1-50 алкила; C2-50 алкенила или C2-50 алкинила, где Т; C1-50 алкил; C2-50 алкенил и C2-50 алкинил необязательно замещены одним или более R10, которые являются одинаковыми или разными, и где C1-50 алкил;
C2-50 алкенил и C2-50 алкинил необязательно включают в состав своей цепи одну или более групп, выбранных из группы, состоящей из Т, -С(O)O-; -O-; -С(O)-; -C(O)N(R11)-; -S(O)2N(R11)-; -S(O)N(R11)-; -S(O)2-; -S(O)-; -N(R11)S(O)2N(R11a)-; -S-; -N(R11)-; -OC(O)R11; -N(R11)C(O)-; -N(R11)S(O)2-; -N(R11)S(O)-; -N(R11)C(O)O-; -N(R11)C(O)N(R11a)- и -OC(O)N(R11R11a);
R9, R9a, R9b независимо выбраны из группы, состоящей из Н; Т; и C1-50 алкила; C2-50 алкенила или C2-50 алкинила, где Т; C1-50 алкил; C2-50 алкенил и C2-50 алкинил необязательно замещены одним или более R10, которые являются одинаковыми или разными, и где C1-50 алкил; C2-50 алкенил и C2-50 алкинил необязательно включают в состав своей цепи одну или более групп, выбранных из группы, состоящей из Т, -С(O)O-; -O-; -С(O)-; -C(O)N(R11)-; -S(O)2N(R11)-; -S(O)N(R11)-; -S(O)2-; -S(O)-; -N(R11)S(O)2N(R11a)-; -S-; -N(R11)-; -OC(O)R11; -N(R11)C(O)-; -N(R11)S(O)2-; -N(R11)S(O)-; -N(R11)C(O)O-; -N(R11)C(O)N(R11a)- и –OC(O)N(R11R11a);
Т выбран из группы, состоящей из фенила; нафтила; инденила; инданила; тетралинила; С3-10 циклоалкила; 4-7-членного гетероциклила или 9-11-членного гетеробициклила, где Т необязательно замещен одним или более R10, которые являются одинаковыми или разными;
R10 представляет собой галоген; CN; оксо (=O); COOR12; OR12; C(O)R12; C(O)N(R12R12a); S(O)2N(R12R12a); S(O)N(R12R12a); S(O)2R12; S(O)R12; N(R12)S(O)2N(R12aR12b); SR12; N(R12R12a); NO2; OC(O)R12; N(R12)C(O)R12a; N(R12)S(O)2R12a; N(R12)S(O)R12a; N(R12)C(O)OR12a; N(R12)C(O)N(R12aR12b); OC(O)N(R12R12a); или C1-6 алкил, где C1-6 алкил необязательно замещен одним или более галогенами, которые являются одинаковыми или разными;
R11, R11a, R12, R12a, R12b независимо выбраны из группы, состоящей из Н или C1-6 алкила, где C1-6 алкил необязательно замещен одним или более галогенами, которые являются одинаковыми или разными.
Термин "включают в состав своей цепи" означает, что группа находится между двумя атомами углерода или на конце углеродной цепочки между атомами углерода и водорода.
L2 представляет собой одинарную химическую связь или спейсер. В случае, если L2 представляет собой спейсер, он предпочтительно соответствует определению одного или более необязательных заместителей, определение которых дано выше, при условии что L2 имеет заместитель Z.
Соответственно, когда L2 отличен от одинарной химической связи, L2-Z представляет собой COOR9; OR9; C(O)R9; С(О)N(R9R9a); S(O)2N(R9R9a); S(O)N(R9R9a); S(O)2R9; S(O)R9; N(R9)S(O)2N(R9R9a); SR9; N(R9R9a); OC(O)R9; N(R9)C(O)R9a; N(R9)S(O)2R9a; N(R9)S(O)R9a; N(R9)C(O)OR9a; N(R9)C(O)N(R9aR9b); ОС(O)N(R9aR9b); Т; C1-50 алкил; C2-50 алкенил или C2-50 алкинил, где Т; C1-50 алкил; C2-50 алкенил и C2-50 алкинил необязательно замещены одним или более R10, которые являются одинаковыми или разными, и где C1-50 алкил; C2-50 алкенил и C2-50 алкинил необязательно включают в состав своей цепи одну или более групп, выбранных из группы, состоящей из -Т-, -С(O)O-; -O-; -С(O)-; -C(O)N(R11)-; -S(O)2N(R11)-; -S(O)N(R11)-; -S(O)2-; -S(O)-; -N(R11)S(O)2N(R11a)-; -S-; -N(R11)-; -OC(O)R11; -N(R11)C(O)-; -N(R11)S(O)2-; -N(R11)S(O)-; -N(R11)C(O)O-; -N(R11)C(O)N(R11a)- и -OC(O)N(R11R11a);
R9, R9a, R9b независимо выбраны из группы, состоящей из Н; Z; Т; и C1-50 алкила; C2-50 алкенила или C2-50 алкинила, где Т; C1-50 алкил; C2-50 алкенил и C2-50 алкинил необязательно замещены одним или более R10, которые являются одинаковыми или разными, и где C1-50 алкил; C2-50 алкенил и C2-50 алкинил необязательно включают в состав своей цепи одну или более групп, выбранных из группы, состоящей из Т, -С(O)O-; -O-; -С(O)-; -C(O)N(R11)-; -S(O)2N(R11)-; -S(O)N(R11)-; -S(O)2-; -S(O)-; -N(R11)S(O)2N(R11a)-; -S-; -N(R11)-; -OC(O)R11; -N(R11)C(O)-; -N(R11)S(O)2-; -N(R11)S(O)-; -N(R11)C(O)O-; -N(R11)C(O)N(R11a)- и -OC(O)N(R11R11a);
Т выбран из группы, состоящей из фенила; нафтила; инденила; инданила; тетралинила; С3-10 циклоалкила; 4-7-членного гетероциклила или 9-11-членного гетеробициклила, где t необязательно замещен одним или более R10, которые являются одинаковыми или разными;
R10 представляет собой Z; галоген; CN; оксо (=O); COOR12; OR12; C(O)R12; C(O)N(R12R12a); S(O)2N(R12R12a); S(O)N(R12R12a); S(O)2R12; S(O)R12; N(R12)S(O)2N(R12aR12b); SR12; N(R12R12a); NO2; OC(O)R12; N(R12)C(O)R12a; N(R12)S(O)2R12a; N(R12)S(O)R12a; N(R12)C(O)OR12a; N(R12)C(O)N(R12aR12b); OC(O)N(R12R12a) или C1-6 алкил, где C1-6 алкил необязательно замещен одним или более галогенами, которые являются одинаковыми или разными;
R11, R11a, R12, R12a, R12b независимо выбраны из группы, состоящей из Н; Z или C1-6 алкила, где С1-6 алкил необязательно замещен одним или более галогенами, которые являются одинаковыми или разными;
при условии, что один из R9, R9a, R9b, R10, R11, R11a, R12, R12a, R12b представляет собой Z.
Предпочтительные структуры для формулы (VI) выбраны из группы, состоящей из
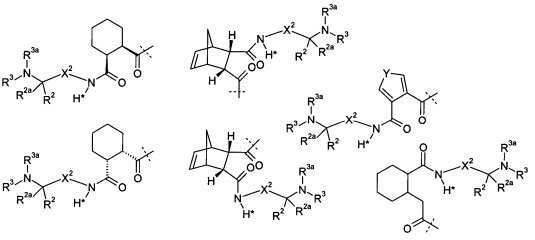

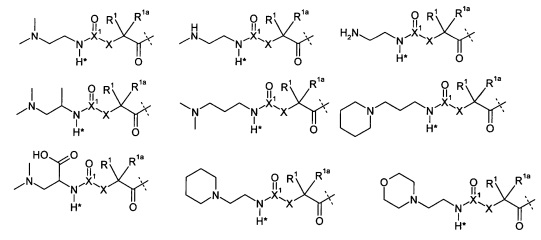
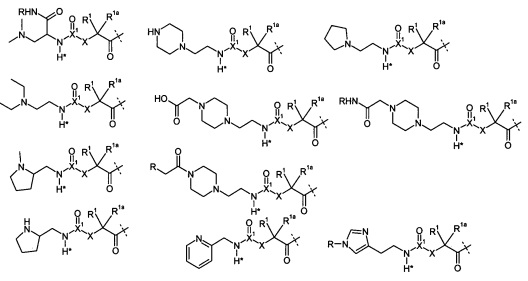
где R представляет собой Н или C1-4 алкил; Y представляет собой NH; О или S; и R1, R1a, R2, R2a, R3, R3a, R4, X, X1, X2 имеют указанные выше значения.
Еще более предпочтительные структуры для формулы (VI) выбраны из группы, состоящей из
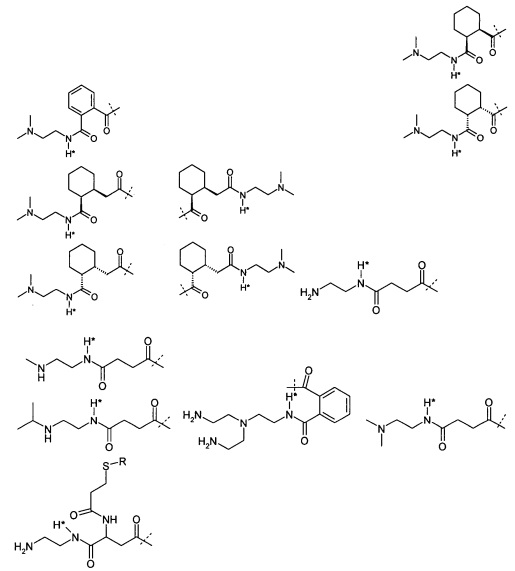
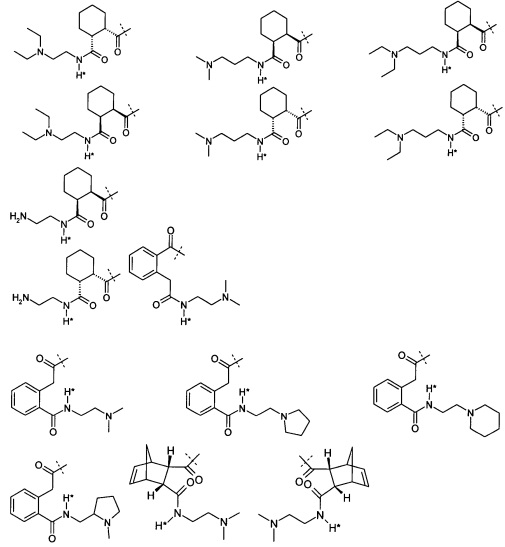

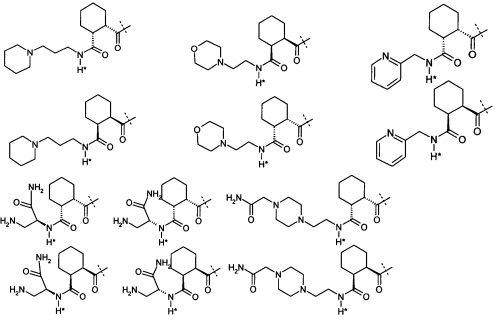
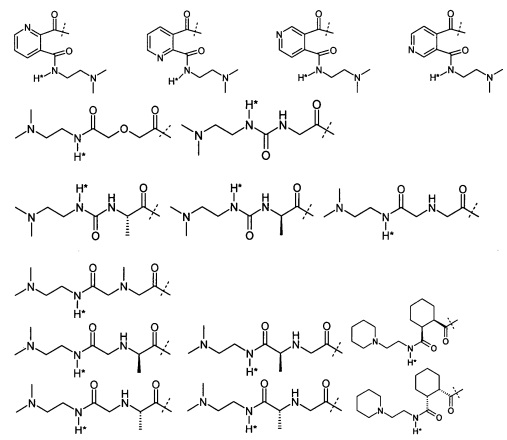
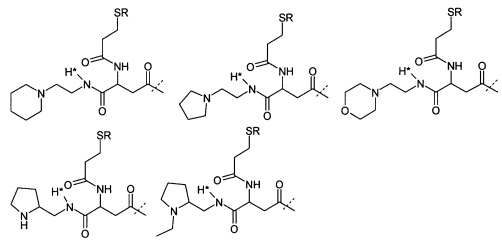
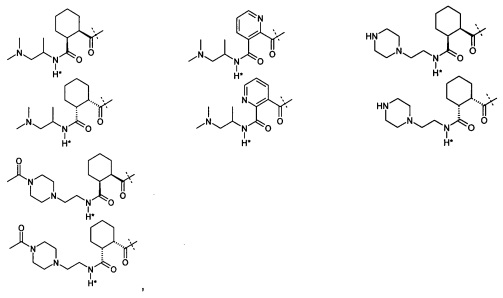
где R имеет указанное выше значение.
Другие предпочтительные пролекарства по настоящему изобретению представлены конъюгатом лекарство-линкер D-L, в котором
D представляет собой биологически активный фрагмент, содержащий ароматический амин; и
L представляет собой небиологически активный линкер, содержащий
i) фрагмент L1, представленный формулой (VII),
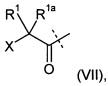
где пунктирная линия означает присоединение L1 к ароматической амино-группе в D с образованием амидной связи; и где X, R1, и R1a в формуле (VII) имеют следующие значения:
Х представляет собой Н или C1-50 алкил, необязательно включающий в состав своей цепи одну или более групп, выбранных из -NH-, -C(C1-4 алкил)-, -O-, -С(O)- или -С(O)NH-;
R1 и R1a независимо выбраны из группы, состоящей из Н и C1-C4 алкила; необязательно, L1 имеет дополнительные заместители.
ii) фрагмент L2, который представляет собой химическую связь или спейсер, и L2 связаны с группой-носителем Z, представляющей собой гидрогель по настоящему изобретению, где L1 замещен одним фрагментом L2.
Более предпочтительно, Х в формуле (VII) включает один из представленных далее фрагментов, где пунктирная линия справа показывает присоединение L1 к D путем образования амидной связи с ароматической амино-группой в D, и пунктирная линия слева показывает присоединение к остальной части X, и где L1 необязательно имеет дополнительные заместители:
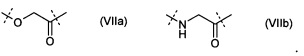
Более предпочтительно, Х в формуле (VII) включает один из представленных далее фрагментов, где пунктирная линия справа отражает присоединение L1 к D путем образования амидной связи с ароматической амино-группой в D, и пунктирная линия слева отражает присоединение к остальной части X:
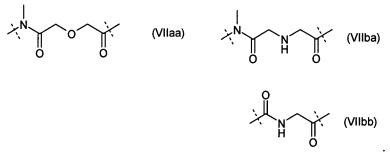
Более предпочтительно, L представляет собой небиологически активный линкер, содержащий
i) фрагмент L1, представленный формулой (VIII),
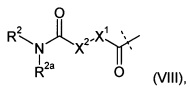
где пунктирная линия означает присоединение L1 к ароматической амино-группе в D с образованием амидной связи; и где X1, X2, R2, и R2a имеют следующие значения:
X1 представляет собой C(R1R1a) или циклический фрагмент, выбранный из С3-7 циклоалкила, 4-7-членного гетероциклила, фенила, нафтила, инденила, инданила, тетралинила, или 9-11-членного гетеробициклила;
X2 представляет собой химическую связь или выбран из
C(R3R3a), N(R3), О, C(R3R3a)-C(R4R4a), C(R3R3a)-N(R4), N(R3)-C(R4R4a), C(R3R3a)-O или О-С(R3R3a),
где в случае, если X1 представляет собой циклический фрагмент, X2 представляет собой химическую связь, C(R3R3a), N(R3) или О;
необязательно, в случае, если X1 представляет собой циклический фрагмент и X2 представляет собой C(R3R3a), порядок расположения фрагмента X1 и фрагмента X2 в составе L1 может поменяться;
R1, R3 и R4 независимо выбраны из группы, состоящей из Н, C1-4 алкила и –N(R5R5a);
R1a, R2, R2a, R3a, R4a и R5a независимо выбраны из группы, состоящей из Н и C1-4 алкила;
необязательно, одна из пар R2a/R2, R2a/R3a, R2a/R4a объединены с образованием 4-7-членного по меньшей мере частично насыщенного гетероцикла;
R5 представляет собой C(O)R6;
R6 представляет собой C1-4 алкил;
необязательно, одна из пар R1a/R4a, R3a/R4a или R1a/R3a образуют химическую связь;
необязательно, L1 имеет дополнительные заместители.
ii) фрагмент L2, который представляет собой химическую связь или спейсер, и L2 связан с группой-носителем Z, представляющей собой гидрогель по настоящему изобретению,
где L1 замещен одним фрагментом L2;
необязательно, L имеет дополнительные заместители.
Более предпочтительно, фрагмент L1 выбран из
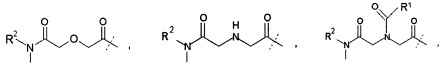
Предпочтительно, в формуле (VIII), R1a, R2, R2a, R3a, R4a и R5a независимо выбраны из группы, состоящей из Н и C1-4 алкила.
В другом предпочтительном варианте выполнения, L представляет собой небиологически активный линкер, содержащий
i) фрагмент L1, представленный формулой (IX),
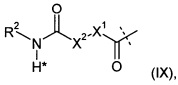
где пунктирная линия означает присоединение L1 к ароматической амино-группе в D с образованием амидной связи; и где X1, X2, и R2 в формуле (IX) имеют следующие значения:
X1 представляет собой C(R1R1a) или циклический фрагмент, выбранный из С3-7 циклоалкила, 4-7-членного гетероциклила, фенила, нафтила, инденила, инданила, тетралинила, или 9-11-членного гетеробициклила,
где в случае, если X1 представляет собой циклический фрагмент, данный циклический фрагмент встроен в состав L1 через два соседних атома в цикле, и атом цикла в X1, соседний с атомом углерода амидной связи, также представляет собой атом углерода;
X2 представляет собой химическую связь или выбран из C(R3R3a), N(R3), О, C(R3R3a)-C(R4R4a), C(R3R3a)-N(R4), N(R3)-C(R4R4a), C(R3R3a)-O или O-C(R3R3a),
где в случае, если X1 представляет собой циклический фрагмент, X2 представляет собой химическую связь, С(R3R3a), N(R3) или О;
необязательно, в случае, если X1 представляет собой циклический фрагмент и X2 представляет собой С(R3R3a), порядок расположения фрагмента X1 и фрагмента X2 в составе L1 может поменяться, и циклический фрагмент встроен в состав L1 через два соседних атома в цикле;
R1, R3 и R4 независимо выбраны из группы, состоящей из Н, C1-4 алкила и -N(R5R5a);
R1a, R2, R3a, R4a и R5a независимо выбраны из группы, состоящей из Н и C1-4 алкила;
R5 представляет собой C(O)R6;
R6 представляет собой C1-4 алкил;
необязательно, одна из пар R1a/R4a, R3a/R4a или R1a/R3a образуют химическую связь;
ii) фрагмент L2, который представляет собой химическую связь или спейсер, и L2 связан с группой-носителем Z, представляющей собой гидрогель по настоящему изобретению,
где L1 замещен одним фрагментом L2, при условии что атом углерода, помеченный звездочкой в формуле (IX), не заменен на L2;
необязательно, L имеет дополнительные заместители.
Более предпочтительно, фрагмент L1 выбран из
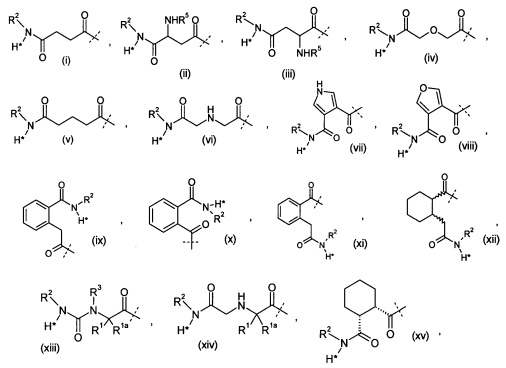
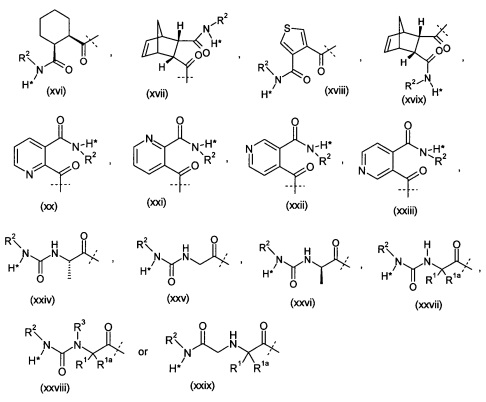
"Биологически активный фрагмент D, содержащий ароматический амин" означает часть (участок или фрагмент) конъюгата лекарство-линкер D-L, который образуется после расщепления в лекарстве D-H (действующее вещество), обладающую (известной) биологической активностью. Кроме того, подтермин "содержащий ароматический амин" означает, что соответствующий фрагмент D и, аналогично, соответствующее лекарственное средство D-H содержит по меньшей мере один ароматический фрагмент, замещенный по меньшей мере одной аминогруппой.
Амино-заместитель в ароматическом фрагменте в составе D образует совместно с карбонильным фрагментом (-С(О)-) на правой стороне L1 (как изображено в формуле (I)) амидную связь в составе конъюгата лекарство-линкер D-L. Вследствие этого, две части D и L конъюгата лекарство-линкер D-L соединены (химически связаны) амидным фрагментом общей структуры Y1-C(O)-N(R)-Y2. Y1 означает остальные части фрагмента L1, а Y2 означает ароматический фрагмент в D. R представляет собой заместитель, такой как С1-4 алкил или, предпочтительно, атом водорода. Например, указанная амидная связь изображена в формуле (I) пунктирной линией, диагонально добавленной по данной связи.
"Небиологически активный линкер" означает линкер, который не оказывает фармакологического действия лекарства (D-H), получаемого из биологически активного фрагмента.
Как указано выше, фрагмент X1 в фрагменте L1, представленном формулой (IX), может также представлять собой циклический фрагмент, такой как С3-7 циклоалкил, фенил или инданил. В случае, если X1 представляет собой такой циклический фрагмент, соответствующий циклический фрагмент включен в L1 через два соседних атома в цикле (указанного циклического фрагмента). Например, если X1 представляет собой фенил, фенильный фрагмент в L1 связан с фрагментом X2 в составе L1 через первый атом (фенильного) цикла, находящийся в α-положении (соседнем) ко второму атому (фенильного) цикла, который сам связан с атомом углерода карбонильного фрагмента на правой стороне L1 в соответствии с формулой (IX) (карбонильный фрагмент, который вместе с ароматической амино-группой в составе D образует амидную связь).
"Алкил" означает линейную или разветвленную углеродную цепочку (незамещенный алкил). Необязательно, каждый атом водорода у алкильного атома углерода может быть заменен на заместитель.
"C1-4 алкил" означает алкильную цепочку, содержащую 1-4 атомов углерода (незамещенный С1-4 алкил), например, в случае концевого расположения в молекуле: метил, этил, н-пропил, изопропил, н-бутил, изобутил, втор-бутил, трет-бутил, или, например, -СН2-, -CH2-CH2-, -СН(СН3)-, -СН2-СН2-СН2-, -СН(С2Н5)-, -С(СН3)2-, когда два фрагмента молекулы соединены алкильной группой. Необязательно, каждый атом водорода у C1-4 алкильного атома углерода может быть заменен на заместитель. Соответственно, "C1-50 алкил" означает алкильную цепочку, содержащую от 1 до 50 атомов углерода.
"C2-50 алкенил" означает разветвленную или неразветвленную алкенильную цепочку, содержащую 2-50 атомов углерода (незамещенный C2-50 алкенил), например, в случае концевого расположения в молекуле: -СН=СН2, -СН=СН-СН3, -СН2-СН=СН2, -СН=СН-СН2-СН3, -СН=СН-СН=СН2, или например -СН=СН-, когда два фрагмента молекулы соединены алкенильной группой. Необязательно, каждый атом водорода у C2-50 алкенильного атома углерода может быть заменен на заместитель, определение которому дается дополнительно. Соответственно, термин "алкенил" относится к углеродной цепочке, содержащей по меньшей мере одну углерод-углеродную двойную связь. Необязательно может содержаться одна или более тройных связей.
"C2-50 алкинил" означает разветвленную или неразветвленную алкинильную цепочку, содержащую 2-50 атомов углерода (незамещенный C2-50 алкинил), например, в случае концевого расположения в молекуле: -С≡СН, -СН2-С≡СН, СН2-СН2-С≡СН, СН2-С≡С-СН3, или например -С≡С-, когда два фрагмента молекулы соединены алкинильной группой. Необязательно, каждый атом водорода у C2-50 алкинильного углерода может быть заменен на заместитель, определение которому дается дополнительно. Соответственно, термин "алкинил" относится к углеродной цепочке, содержащей по меньшей мере одну углерод-углеродную тройную связь. Необязательно может содержаться одна или более двойных связей
"С3-7 циклоалкил" или "С3-7 циклоалкильное кольцо" означает циклическую алкильную цепь, содержащую 3-7 атомов углерода, в которой могут находиться углерод-углеродные двойные связи, которая является по меньшей мере частично насыщенной (незамещенный С3-7 циклоалкил), например циклопропил, циклобутил, циклопентил, циклогексил, циклогексенил, циклогептил. Необязательно, каждый атом водорода у циклоалкильного атома углерода может быть заменен на заместитель. Термин "С3-7 циклоалкил" или "С3-7 циклоалкильное кольцо" также включает мостиковые бициклы, такие как норборнан (норборнанил) или норборнен (норборненил). Соответственно, "С3-5 циклоалкил" означает циклоалкил, содержащий 3-5 атомов углерода.
Термин "галоген" означает фтор, хлор, бром или иод. В целом предпочтительно, чтобы галоген представлял собой фтор или хлор.
"4-7-членный гетероциклил" или "4-7-членный гетероцикл" означает цикл, имеющий 4, 5, 6 или 7 атомов в цикле, который может содержать до максимального числа двойных связей (ароматическое или неароматическое кольцо, полностью, частично или ненасыщенное), где от по меньшей мере одного атома в цикле до 4 атомов в цикле заменены на гетероатом, выбранный из группы, состоящей из серы (включая -S(O)-, -S(O)2-), кислорода и азота (включая =N(O)-), и где цикл связан с остальной частью молекулы через атом углерода или азота (незамещенный 4-7-членный гетероциклил). Для полноты указано, что, например, в случае, если X1 представляет собой 4-7-членный гетероциклил, необходимо рассматривать соответствующие дополнительные требования X1. Это означает, что в случае, если соответствующий 4-7-членный гетероциклил включен в L1 через два соседних атома цикла, то атом цикла в указанном 4-7-членном гетероциклиле, соседний с атомом углерода амидной связи, также представляет собой атом углерода.
Примерами 4-7-членных гетероциклов являются азетидин, оксетан, тиетан, фуран, тиофен, пиррол, пирролин, имидазол, имидазолин, пиразол, пиразолин, оксазол, оксазолин, изоксазол, изоксазолин, тиазол, тиазолин, изотиазол, изотиазолин, тиадиазол, тиадиазолин, тетрагидрофуран, тетрагидротиофен, пирролидин, имидазолидин, пиразолидин, оксазолидин, изоксазолидин, тиазолидин, изотиазолидин, тиадиазолидин, сульфолан, пиран, дигидропиран, тетрагидропиран, имидазолидин, пиридин, пиридазин, пиразин, пиримидин, пиперазин, пиперидин, морфолин, тетразол, тризол, тризолидин, тетразолидин, диазепан, азепин или гомопиперазин. Необязательно, каждый атом водорода в 4-7-членном гетероциклиле может быть заменен на заместитель.
"9-11-членный гетеробициклил" или "9-11-членный гетеробицикл" означает гетероциклическую систему из двух циклов, содержащую 9-11 атомов в цикле, в которой по меньшей мере один атом в цикле является общим для обоих циклов, и которая может содержать до максимального числа двойных связей (ароматическое или неароматическое кольцо, полностью, частично или ненасыщенное), где от по меньшей мере одного атома в цикле до 6 атомов в цикле заменены на гетероатом, выбранный из группы, состоящей из серы (включая -S(O)-, -S(O)2-), кислорода и азота (включая =N(O)-), и где цикл связан с остальной частью молекулы через атом углерода или азота (незамещенный 9-11-членный гетеробициклил). Для полноты указано, что, например, в случае, если X1 представляет собой 9-11-членный гетеробициклил, необходимо рассматривать соответствующие дополнительные требования X1. Это означает, что в случае, если соответствующий 9-11-членный гетеробициклил включен в L1 через два соседних атома цикла, то атом цикла в указанном 9-11-членном гетеробициклиле, соседний с атомом углерода амидной связи, также представляет собой атом углерода.
Примерами 9-11-членного гетеробицикла являются индол, индолин, бензофуран, бензотиофен, бензоксазол, бензизоксазол, бензотиазол, бензизотиазол, бензимидазол, бензимидазолин, хинолин, хиназолин, дигидрохиназолин, хинолин, дигидрохинолин, тетрагидрохинолин, декагидрохинолин, изохинолин, декагидроизохинолин, тетрагидроизохинолин, дигидроизохинолин, бензазепин, пурин или птеридин. Термин «9-11-членный гетеробицикл» также включает спиро-структуры из двух циклов, такие как 1,4-диокса-8-азаспиро[4.5]декан или мостиковые гетероциклы, такие как 8-аза-бицикло[3.2.1]октан.
Необязательно, каждый атом водорода у 9-11-членный гетеробициклил может быть заменен на заместитель.
Небиологически активный линкер L содержит фрагмент L1, представленный формулой (IX), как описано и определено выше. Предпочтительно, фрагмент L1 соответствует следующим определениям.
X1 представляет собой C(R1R1a), циклогексил, фенил, пиридинил, норборненил, фуранил, пирролил или тиенил,
где в случае, если X1 представляет собой циклический фрагмент, указанный циклический фрагмент включен в L1 через два соседних атома цикла;
X2 представляет собой химическую связь или выбран из C(R3R3a), N(R3), О, C(R3R3a)-O или C(R3R3a)-C(R4R4a);
R1, R3 и R4 независимо выбраны из Н, C1-4 алкила или –N(R5R5a);
R1a, R3a, R4a и R5a независимо выбраны из Н или С1-4 алкила;
R2 представляет собой C1-4 алкил;
R5 представляет собой C(O)R6;
R6 представляет собой C1-4 алкил;
Более предпочтительно, фрагмент L1 выбран из
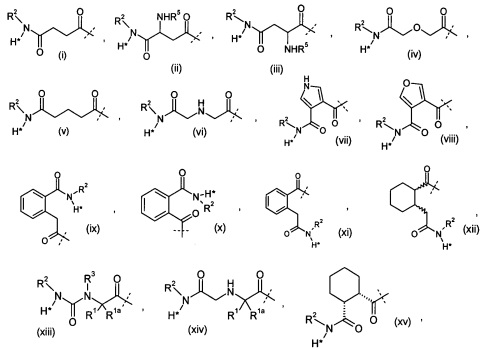
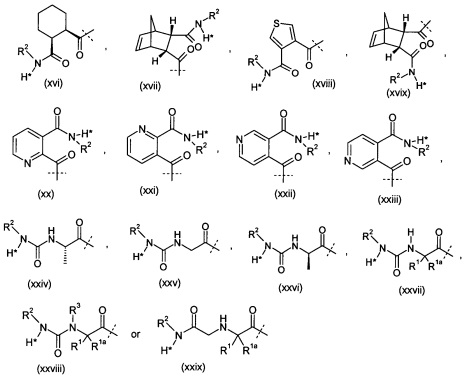
где
R5 представляет собой C(O)R6;
R1, R1a, R2, R3 и R6 независимо друг от друга представляют собой С1-C4 алкил;и
L1 замещен одним фрагментом L2, предпочтительно R2 замещен одним фрагментом L2, т.е. замещение в составе L1 предпочтительно происходит в R2.
В другом предпочтительном варианте выполнения, предпочтительная структура пролекарства по настоящему изобретению представляет собой пролекарство-конъюгат
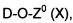
где
D представляет собой содержащий гидроксильную группу биологически активный фрагмент, который соединен с фрагментом Z0 через кислород гидроксильной группы; и где Z0 в формуле (X) имеет следующее значение:
Z0 представляет собой C(O)-X0-Z1; C(O)O-X0-Z1; S(O)2-X0-Z1; C(S)-X0-Z1; S(O)2O-X0-Z1; S(O)2N(R1)-X0-Z1; CH(OR1)-X0-Z1; C(OR1)(OR2)-X0-Z1; C(O)N(R1)-X0-Z1; P(=O)(OH)O-X0-Z1; P(=O)(OR1)O-X0-Z1; P(=O)(SH)O-X0-Z1; P(=O)(SR1)O-X0-Z1; P(=O)(OR1)-X0-Z1; P(=S)(OH)O-X0-Z1; P(=S)(OR1)O-X0-Z1; P(=S)(OH)N(R1)-X0-Z1; P(=S)(OR1)N(R2)-X0-Z1; P(=O)(OH)N(R1)-X0-Z1 или P(=O)(OR1)N(R2)-X0-Z1;
R1, R2 независимо выбраны из группы, состоящей из С1-6 алкила; или
R1, R2 вместе образуют C1-6 алкиленовую мостиковую группу;
Х0 представляет собой (X0A)m1-(X0B)m2;
m1; m2 независимо равны 0 или 1;
X0A представляет собой Т0;
X0B представляет собой разветвленную или неразветвленную C1-10 алкиленовую группу, которая является незамещенной или замещена одним или более R3, которые являются одинаковыми или разными;
R3 представляет собой галоген; CN; C(O)R4; C(O)OR4; OR4; C(O)R4; C(O)N(R4R4a); S(O)2N(R4R4a); S(O)N(R4R4a); S(O)2R4; S(O)R4; N(R4)S(O)2N(R4aR4b); SR4; N(R4R4a); NO2; OC(O)R4; N(R4)C(O)R4a; N(R4)SO2R4a; N(R4)S(O)R4a; N(R4)C(O)N(R4aR4b); N(R4)C(O)OR4a; OC(O)N(R4R4a) или Т0;
R4, R4a, R4b независимо выбраны из группы, состоящей из Н; Т0; С1-4 алкила; C2-4 алкенила и C2-4 алкинила, где C1-4 алкил; C2-4 алкенил и С2-4 алкинил необязательно замещены одним или более R5, которые являются одинаковыми или разными;
R5 представляет собой галоген; CN; C(O)R6; C(O)OR6; OR6; C(O)R6; С(O)N(R6R6a); S(O)2N(R6R6a); S(O)N(R6R6a); S(O)2R6; S(O)R6; N(R6)S(O)2N(R6aR6b); SR6; N(R6R6a); NO2; OC(O)R6; N(R6)C(O)R6a; N(R6)SO2R6a, N(R6)S(O)R6a; N(R6)C(O)N(R6aR6b); N(R6)C(O)OR6a; OC(O)N(R6R6a);
R6, R6a, R6b независимо выбраны из группы, состоящей из Н; С1-6 алкила; С2-6 алкенила и C2-6 алкинила, где C1-6 алкил; C2-6 алкенил и С2-6 алкинил необязательно замещены одним или более галогенами, которые являются одинаковыми или разными;
Т0 представляет собой фенил; нафтил; азуленил; инденил; инданил; С3-7 циклоалкил; 3-7-членный гетероциклил или 8-11-членный гетеробициклил, где Т0 необязательно замещен одним или более R7, которые являются одинаковыми или разными;
R7 представляет собой галоген; CN; COOR8; OR8; C(O)R8; C(O)N(R8R8a); S(O)2N(R8R8a); S(O)N(R8R8a); S(O)2R8; S(O)R8; N(R8)S(O)2N(R8aR8b); SR8; N(R8R8a); NO2; OC(O)R8; N(R8)C(O)R8a; N(R8)S(O)2R8a; N(R8)S(O)R8a; N(R8)C(O)OR8a; N(R8)C(O)N(R8aR8b); OC(O)N(R8R8a); оксо (=O), где цикл является по меньшей мере частично насыщенным; С1-6 алкил; C2-6 алкенил или С2-6 алкинил, где C1-6 алкил; С2-6 алкенил и С2-6 алкинил необязательно замещены одним или более R9, которые являются одинаковыми или разными;
R8, R8a, R8b независимо выбраны из группы, состоящей из Н; C1-6 алкила; С2-6 алкенила и С2-6 алкинила, где С1-6 алкил; С2-6 алкенил и С2-6 алкинил необязательно замещены одним или более R10, которые являются одинаковыми или разными;
R9, R10 независимо выбраны из группы, состоящей из галогена; CN; C(O)R11; C(O)OR11; OR11; C(O)R11; C(O)N(R11R11a); S(O)2N(R11R11a); S(O)N(R11R11a); S(O)2R11; S(O)R11; N(R11)S(O)2N(R11aR11b); SR11; N(R11R11a); NO2; OC(O)R11; N(R11)C(O)R11a; N(R11)SO2R11a; N(R11)S(O)R11a; N(R11)C(O)N(R11aR11b); N(R11)C(O)OR11a и OC(O)N(R11R11a);
R11, R11a, R11b независимо выбраны из группы, состоящей из Н; C1-6 алкила; C2-6 алкенила и С2-6 алкинила, где С1-6 алкил; C2-6 алкенил и С2-6 алкинил необязательно замещены одним или более галогенами, которые являются одинаковыми или разными;
Z1 представляет собой биоразлагаемый гидрогель по настоящему изобретению, который ковалентно присоединен к X0.
Такой гидроксил-содержащий биологически активный фрагмент D может представлять собой, например, палиперидон.
Предпочтительно, Z0 представляет собой C(O)-X0-Z1; C(O)O-X0-Z1 или S(O)2-X0-Z1. Более предпочтительно, Z0 представляет собой C(O)-X0-Z1 или C(O)O-X0-Z1. Еще более предпочтительно, Z0 представляет собой С(O)-Х0-Z1.
Предпочтительно, Х0 незамещенный.
Предпочтительно, m1 равен 0 и m2 равен 1.
Предпочтительно, X0-Z0 представляет собой C(R1R2)CH2-Z0, где R1, R2 независимо выбраны из группы, состоящей из Н и C1-4 алкила, при условии, что по меньшей мере один из R1, R2 отличен от Н; или (CH2)n-Z0, где n равно 3, 4, 5, 6, 7 или 8.
Предпочтительно, носитель Z1 ковалентно присоединен к Х0 через амидную группу.
В другом предпочтительном варианте выполнения, L представляет собой небиологически активный линкер, содержащий
i) фрагмент L1, представленный формулой (XI),
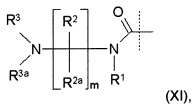
где пунктирная линия означает присоединение L1 к ароматической гидроксильной группе лекарства D путем образования карбаматной группы; и где R1, R2, R2a, R3, R3a и m в формуле (XI) имеют следующие определения:
R1 выбран из группы, состоящей из С1-4 алкила; гетероалкила; С3-7 циклоалкила; и
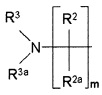 ;
;
R2, R2a, R3, R3a независимо выбраны из атома водорода, замещенного или незамещенного линейного, разветвленного или циклического С1-4 алкила или гетероалкила;
m независимо равен 2, 3 или 4;
ii) фрагмент L2, который представляет собой химическую связь или спейсер, и L2 связан с гидрогелем по настоящему изобретению,
где L1 замещен одним фрагментом L2,
необязательно, L имеет дополнительные заместители.
В другом предпочтительном варианте выполнения, L представляет собой небиологически активный линкер, содержащий
i) фрагмент L1, представленный формулой (XII),
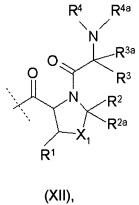
где пунктирная линия означает присоединение L1 к алифатической амино-группе лекарства D путем образования амидной связи; и где X1, R1, R2, R2a, R3, R3a, R4 и R4a в формуле (XII) имеют следующие значения:
X1 выбран из О, S или CH-R1a,
R1 и R1a независимо выбраны из Н, ОН, СН3
R2, R2a, R4 и R4a независимо выбраны из Н и C1-4 алкила,
R3, R3a независимо выбраны из Н, C1-4 алкила и R5
R5 выбран из
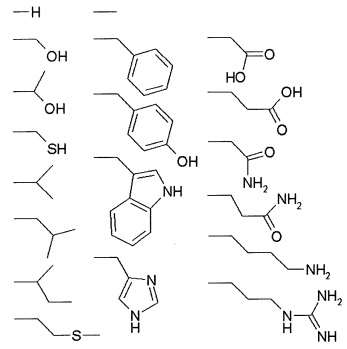
Предпочтительно, один из пары R3/R3a представляет собой Н, а другой выбран из R5.
Предпочтительно, один из R4/R4a представляет собой Н.
Необязательно, одна или более из пар R3/R3a, R4/R4a, R3/R4 может независимо образовывать один или более циклических фрагментов, выбранных из С3-7 циклоалкила, 4-7-членный гетероциклила или 9-11-членного гетеробициклила.
Необязательно, R3, R3a, R4 и R4a имеют дополнительные заместители; подходящими заместителями являются алкил (такой как C1-6 алкил), алкенил (такой как С2-6 алкенил), алкинил (такой как C2-6 алкинил), арил (такой как фенил), гетероалкил, гетероалкенил, гетероалкинил, гетероарил (такой как ароматический 4-7-членный гетероцикл) или галоген.
ii) фрагмент L2, который представляет собой химическую связь или спейсер, и L2 связан с гидрогелем по настоящему изобретению,
где L1 замещен одним фрагментом L2, необязательно, L имеет дополнительные заместители.
Подходящими заместителями являются алкил (такой как C1-6 алкил), алкенил (такой как C2-6 алкенил), алкинил (такой как С2-6 алкинил), арил (такой как фенил), гетероалкил, гетероалкенил, гетероалкинил, гетероарил (такой как ароматический 4-7-членный гетероцикл) или галоген.
В другом предпочтительном варианте выполнения, L представляет собой небиологически активный линкер, содержащий
i) фрагмент L1, представленный формулой (XIII),
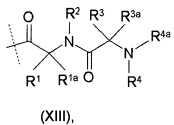
где пунктирная линия означает присоединение L1 к ароматической амино-группе лекарства D путем образования амидной связи; и где R1, R1a, R2, R2a, R3, R3a, R4 и R4a в формуле (XIII) имеют следующие определения:
R1, R1a, R2, R3, R3a, R4 и R4a независимо выбраны из Н и C1-4 алкила,
необязательно, любые два из R1, R1a, R2, R3, R3a, R4 и R4a могут независимо образовывать один или более циклических фрагментов, выбранных из С3-7 циклоалкила, 4-7-членного гетероциклила, фенила, нафтила, инденила, инданила, тетралинила или 9-11-членного гетеробициклила,
необязательно, R1, R1a, R2, R3, R3a, R4 и R4a имеют дополнительные заместители; подходящими заместителями являются алкил, такой как C1-6 алкил; алкен, такой как C2-6 алкен; алкин, такой как C2-6 алкин; арил, такой как фенил; гетероалкил; гетероалкен; гетероалкин; гетероарил, такой как ароматический 4-7-членный гетероцикл; или галоген.
ii) фрагмент L2, который представляет собой химическую связь или спейсер, и L2 связан с гидрогелем по настоящему изобретению,
где L1 замещен одним фрагментом L2, необязательно, L имеет дополнительные заместители;
Подходящими заместителями являются алкил (такой как C1-6 алкил), алкенил (такой как C2-6 алкенил), алкинил (такой как С2-6 алкинил), арил (такой как фенил), гетероалкил, гетероалкенил, гетероалкинил, гетероарил (такой как ароматический 4-7-членный гетероцикл) или галоген.
Предпочтительно, один из R4 или R4a представляет собой Н.
Другой предпочтительный линкер пролекарства описан в US patent No 7585837. Такой линкер L представляет собой небиологически активный линкер, содержащий
i) фрагмент L1, представленный формулой (XIV),
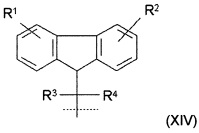
где пунктирная линия означает присоединение L1 к функциональной группе лекарства D, где такая функциональная группа выбрана из амино-группы, карбоксила, фосфата, гидроксила и меркапто-группы; и где R1, R2, R3 и R4 в формуле (XIV) имеют следующие определения:
R1 и R2 независимо выбраны из группы, состоящей из атома водорода, алкила, алкокси-группы, алкоксиалкила, арила, алкарила, аралкила, галогена, нитро-группы, -SO3H, -SO2NHR5, амино-группы, аммониевой группы, карбоксила, РО3Н2 и ОРО3Н2;
R3, R4, и R5 независимо выбраны из группы, состоящей из атома водорода, алкила и арила;
ii) фрагмент L2, который представляет собой химическую связь или спейсер, и L2 связан с гидрогелем по настоящему изобретению,
где L1 замещен одним фрагментом L2, необязательно, L имеет дополнительные заместители;
Другой предпочтительный линкер пролекарства описан в международной заявке под номером WO-A 2002/089789. Такой линкер L представляет собой изображенный на формуле (XV):
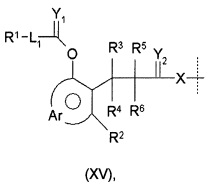
где пунктирная линия означает присоединение L к функциональной группе лекарства D; и где X, Ar, L1, Y1, Y2, R1, R2, R3, R4, R5, R6 в формуле (XV) имеют следующие определения:
R1 представляет собой гидрогель по настоящему изобретению;
L1 представляет собой бифункциональную линкерную группу;
Y1 и Y2 независимо представляют собой О, S или NR7;
R1-7 независимо выбраны из группы, состоящей из атома водорода, C1-6 алкилов, C3-12 разветвленных алкилов, С3-8 циклоалкилов, C1-6 замещенных алкилов, С3-8 замещенных циклоалкилов, арилов, замещенных арилов, аралкилов, С1-6 гетероалкилов, замещенных C1-6 гетероалкилов, C1-6 алкокси-групп, фенокси-групп и С1-6 гетероалкокси-групп;
Ar представляет собой фрагмент, который при включении в формулу XI образует полизамещенный ароматический углеводород или полизамещенную гетероциклическую группу;
Z представляет собой химическую связь или фрагмент, который активно транспортируется в целевую клетку, гидрофобный фрагмент, или их комбинацию.
Другой предпочтительный линкер пролекарства для применения с полинуклеотидными лекарственными средствами, такими как олигонуклеотиды, описан в WO-A 2008/034122. Такой линкер L показан на формуле (XVI):
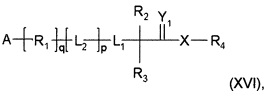
где A, R1, R2, R3, R4, L1, L2, Y1, X, q и р в формуле (XVI) имеют следующие определения:
А представляет собой концевую группу или
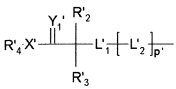 ,
,
R1 представляет собой гидрогель по настоящему изобретению;
L1 и L'1 представляют собой независимо выбранные спейсеры, имеющие неподеленную пару электронов, расположенную на расстоянии 4-10 атомов от C(=Y1) или C(=Y'1), предпочтительно на расстоянии от около 4 до около 8, и наиболее предпочтительно на расстоянии от около 4 до около атомов от C(=Y1) или C(=Y'1);
L2 и L'2 представляют собой независимо выбранные бифункциональные линкеры;
Y1 и Y'1 независимо представляют собой О, S или NR5;
Х и X' независимо представляют собой О или S;
R2, R'2, R3, R'3 и R5 независимо выбраны из атома водорода, C1-6 алкила, С2-6 алкенила, С2-6 алкинила, C3-19 разветвленного алкила, С3-8 циклоалкила, C1-6 замещенного алкила, C2-6 замещенного алкенила, С2-6 замещенного алкинила, С3-8 замещенного циклоалкила, арила, замещенного арила, гетероарила, замещенного гетероарила, C1-6 гетероалкила, замещенного С1-6 гетероалкила, C1-6 алкокси-группы, арилокси-группы, C1-6 гетероалкокси-группы, гетероарилокси-группы, C2-6 алканоила, арилкарбонила, С2-6 алкоксикарбонила, арилоксикарбонила, С2-6 алканоилокси-группы, арилкарбонилокси-группы, C2-6 замещенного алканоила, замещенного арилкарбонила, С2-6 замещенной алканоилокси-группы, замещенного арилоксикарбонила, С2-6 замещенной алканоилокси-группы и замещенной арилкарбонилокси-группы, или R2 вместе с R3 и R'2 вместе с R'3 независимо формируют замещенный или незамещенный неароматический циклоуглеводород, содержащий по меньшей мере три атома углерода;
R4 и R'4 представляют собой независимо выбранные полинуклеотиды и их производные;
(р) и (р') независимо равны нулю или положительному целому числу, предпочтительно нулю или целому числу от около 1 до около 3, более предпочтительно нулю или 1; и
(q) и (q') независимо равны нулю или 1,
при условии что R3 представляет собой замещенный или незамещенный углеводород, содержащий по меньшей мере три атома углерода, когда R2 представляет собой Н, и также при условии, что L1 не такой же, как С(R2)(R3).
Другой предпочтительный линкер пролекарства для применения с амино-содержащими лекарственными средствами описан в WO-A 2001/47562. Такой L показан на формуле формуле (XVII):
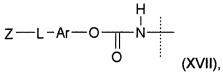
где пунктирная линия означает присоединение линкера L к аминогруппе лекарственного средства D; и где Z, L и Ar в формуле (XVII) имеют следующие значения:
Z представляет собой гидрогель по настоящему изобретению;
L представляет собой ковалентную связку, предпочтительно гидролитически устойчивую связку;
Ar представляет собой ароматическую группу;
Другой предпочтительный линкер пролекарства для применения с биологически активными фрагментами, содержащими гетероароматический амин, описан в US-patent 7393953 В2. Такой линкер L показан на формуле (XVIII):
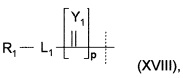
где пунктирная линия означает присоединение линкера L к гетероароматической амино-группе лекарственного средства D; и где R1, L1, Y1, и р в формуле (XVIII) имеют следующие значения:
R1 представляет собой гидрогель по настоящему изобретению;
Y1 представляет собой О, S или NR2;
р равен 0 или 1
L1 представляет собой бифункциональный линкер, такой как, например,
-NH(CH2CH2O)n(CH2)nNR3-,
-NH(CH2CH2O)nC(O)-,
-NH(CR4R5)nOC(O)-,
-C(O)(CR4R5)nNHC(O)(CR8R7)qNR3-,
-C(O)O(CH2)nO-
-C(O)(CR4R5)nNR3-,
-C(O)NH(CH2CH2O)n(CH2)nNR3-,
-C(O)O-(CH2CH2O)nNR3-,
-C(O)NH(CR4R5)nO-,
-C(O)O(CR4R5)nO-,
-C(O)NH(CH2CH2O)n-,
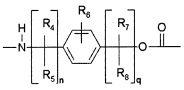 ,
,
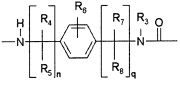 ;
;
R2, R3, R4, R5, R7 и R8 независимо выбраны из группы, состоящей из атома водорода, C1-6 алкилов, С3-12 разветвленных алкилов, С3-8 циклоалкилов, C1-6 замещенных алкилов, С3-8 замещенных циклоалкилов, арилов, замещенных арилов, аралкилов, C1-6 гетероалкилов, замещенных С1-6 гетероалкилов, C1-6 алкокси-групп, фенокси-групп и С1-6 гетероалкокси-групп;
R6 выбран из группы, состоящей из атома водорода, C1-6 алкилов, С3-12 разветвленных алкилов, С3-8 циклоалкилов, C1-6 замещенных алкилов, С3-8 замещенных циклоалкилов, арилов, замещенных арилов, аралкилов, C1-6 гетероалкилов, замещенных C1-6 гетероалкилов, C1-6 алкокси-групп, фенокси-групп и C1-6 гетероалкокси-групп, NO2, галогеналкилов и галогенов;
n и q выбраны независимо друг от друга, и каждый представляет собой положительное целое число.
Упомянутые выше линкеры подходят для применения с рядом биологически активных фрагментов. Подходящие биологически активные фрагменты представляют собой полипептиды, белки, олигонуклеотиды или низкомолекулярные биологически активные фрагменты. Биологически активный фрагмент может содержать аминную, гидроксильную, карбоксильную, фосфатную или меркапто-группу.
Биологически активные фрагменты могут быть конъюгированы с временным линкером пролекарства посредством связки, образованной амином, таким как алифатический или ароматический амин; гидроксилом, таким как алифатический или ароматический гидроксил; карбоксилом; фосфатной или меркапто-группой, предоставляемой биологически активным фрагментом.
Подходящие содержащие ароматический амин биологически активные фрагменты D представляют собой, например, (-)-Карбовир, (±)-Хименин, (±)-Норцисаприд, (±)-Пикуметерол, (R)-Аминоглютетимид, (R)-Кленбутерол, (S)-Аминоглютетимид, (S)-Кленбутерол, [6-р-аминофенилаланин]-ангиотензин II, 10'-Деметоксистрептонигрин, 17-Аминогелданамицин, 1-Аминоакридин, 1-Деазааденин, 1-NA-PP 1, 1-NM-РР 1, 2,7-Диаминоакридин, 2,7-Диметилпрофлавин, 2-Амино-6(5Н)-фенантридинон, 2-Аминоакридин, 2-амино-Карбанилид, 2-Аминогистамин, 2-Аминоперимидин, 2'-АМР, 2-ХлорАденозин, 2'-Деоксиксилотуберцидин, 2-Сульфаниламидоимидазол, 3,4-Диаминокумарин, 3'-Амино-4'-метоксифлавон, 3-Аминоакридин, 3-Аминопиколиновая кислота, 3- Деазагуанин, 4'-Аминофлавон, 4-Аминопиридин, 5'-ADP, 5-Аминоакридин, 5-амино-DLТриптофан, 5-Аминоникотинамид, 5'-АМР, 5'-АТР, 5-Хлордеоксицитидин, 5'-СМР, 5-Диметиламилорид, 5'-GDP, 5'-GMP, 5'-GTP, 5-Йодотуберцидин, 5-Метилцитозин, 6-Аминофлавон, 6-Аминофенантридин, 6-Аминотимин, 6-Бензилтиогуанин, 6-Хлортакрин, 6-Йодоамилорид, 7,8-Дигидронеоптерин, 7-Аминониметазепам, 7-Метокситакрин, 7-Метилтакрин, 9-Деазагуанин, 9-Фенетиладенин, Абакавир, Акадезин, Ацедиасульфон, Ацефуртиамин, Ацетил коэнзим А, Ацикловир, Актимид, Актиномицин, Ацикловир, Адефовир, Аденаллен, Аденин, Аденофостин А, Аденозин, Аденозин монофосфат, Аденозин трифосфат, Аденозилгомоцистеин, Адитерен, Афлоквалон, Аламифовир, Албофунгин, Альфузозин, Аллитиамин, Алпироприд, Аманозин, Амбасилид, Амбукаин, Амдоксовир, Амелтолид, Аметоптерин, Амфенак, Амфлутизол, Амициклин, Амидапсон, Амифампридин, Амилорид, Аминакрин, Аминоакридин, Аминоантипирин, Аминобензоат, Аминогенистеин, Аминоглютетимид, Аминогиппурат, Аминоизатин, Аминометрадин, Аминониметазепам, Аминофенилаланин, Аминопотентидин, Аминоптерин, Аминопурваланол А, Аминохинурид, Аминосалициловая кислота, Амифеназол, Амифенозин, Амисометрадин, Амисулприд, Амитерол, Амлексанокс, Аммелин, Амонафид, Амоксекаин, Амфенидон, Амфетинил, Амфоталид, Ампренавир, Ампурин, Амринон, АМТ, Амтамин, Амтизол, Ангустмицин А, Анилеридин, Ападеносон, Апраклонидин, Априцитабин, Арафлуороцитозин, Арамин, Аразид, Аристеромицин, Арприноцид, Аскамицин, Асцензил, Аспикуламицин, Атулид, Азабон, Азацитидин, Азалин В, Азамулин, Азанидазол, Азепексол, Азтреонам, Бахилоприм, Баседол, Батаноприд, b-D-Аденозин, Бемитрадин, Бенфотиамин, Бентиамин, Бензамил, Бензокаин, Бетоксикаин, Биноденозон, Биоптерин, Бисбентиамин, Бластицидин, Блеомицин, Блеомицин А1, Блеомицин А2, Блеомицин А5, Блеомицин А6, Блеомицин ДМА2, Бродимоприм, Бромфенак, Бромбутерол, Бромоприд, Бропиримин, Буцикловир, Буназозин, Бутирилтиамин дисульфид, Кадегуомицин, сАМР, Кандицидин, Кападеносон, Карбанилид, Карбодин, Карбовир, Карбутамид, Карумонам, CDP-дипалмитин, Цефкапенепивоксил, Цефклидин, Цефдалоксим, Цефдинир, Цефдиторен, Цефемпидон, Цефепим, Цефетамет, Цефетекол, Цефиксим, Цефлупренам, Цефматилен, Цефменоксим, Цефодизим, Цефоселис, Цефотаксим, Цефотиам, Цефозозопран, Цефподоксим, Цефквином, Цефром, Цефтазидим, Цефтерам, Цефтибутен, Цефтиофур, Цефтиолен, Цефтиоксид, Цефтизоксим, Цефтобипрол, Цефтриаксон, Цефузонам, Центазолон, Цетотиамин, cGMP, Хлорпрокаин, Цидофовир, Цифостодин, Ципамфиллин, Цисаприд, Кладрибин, Клафанон, Клафоран, Клебоприд, Кленбутерол, Кленпроперол, Клофарабин, Клорсулон, Коелентерамин, Коэнзим А, Колхицамид, Кумарин 10, Ковирацил, Кротонозид, Циклобут А, Циклобут G, Циклокленбутерол, Цикотиамин, Циталлен, Цитарабин, Цитаразид, Цитидин, Цитидин дифосфат, Цитидолин, ЦитозинD-(+)-Неоптерин, Дактиномицин, D-Аметоптерин, dAMP, Дамвар, Данихидон, Дапсон, Даптомицин, Дараприм, Дарунавир, DATHF, Дазоприд, dCMP, dCTP, Дебромохимениалдизин, Децитабин, Деклопрамид, Деизопропилгидроксиатразин, Делафлоксацин, Делфантрин, Денавир, Деоксиаденозин, Деокси-АТР, Деоксицитидин, Деоксигуанозин, Дефосфокоэнзим А, Деквалиниум, Десбутилбуметанид, Десцикловир, Дезоксиминоксидил, dGMP, dGTP, Диацетиамин, Диаминоакридин, Диаверидин, 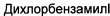 , Дихлорметотрексат, Дихлорфенарсин, Дидеоксицитидин, Дигидробиоптерин, Дигидрофолиевая кислота, Диметиалиум, Диметокаин, Диметил метотрексат, Диналин, DL-5,6,7,8-Тетрагидофолиевая кислота, DL-Метотрексат, Добуприд, Довитиниб, Доксазозин, Драфлазин, Эдатрексат, Эльпетригин, Элвуцитабин, Эмтрицитабин, Энтекавир, Энвираден, Эпцитабин, Эпироприм, Эритаденин, Этантерол, Этакридин, Этаден, Этилизопропиламилорид, Этоприн, Этоксазен, Этравирин, Этрицигуат, FAD, Фамцикловир, Фазарабин, Фенамол, Фепрацет, Фиацитабин, Флуцитозин, Флудара, Флударабин, Флуцитозин, Фолиевая кислота, Формицин А, Фосампренавир, Фуралазин, Фурсултиамин, Фурилтриазин, Ганцикловир, Ганцикловир, Гастрацид, Гемцитабин, Гиракодазол, Глоксимонам, Глибутиазол, GSK 3В Ингибитор XII, GSK3BИнгибиторХII, Гуанин, Гуанин арабинозид, Гуанозин, Гексил пара-аминобензойная ксилота, Гидрокси метил кленбутерол, Гидроксипрокаин, Гидрокситриамтерен сульфат, Ибацитабин, Иклаприм, Иманиксил, Имиквимод, Инданоцин, Иобензамовая кислота, Иоцетамовая кислота, Иомегламовая кислота, Иомегламовая кислота, Ипидакрин, Ирамин, Ирсогладин, Изаторибин, Изобутамбен, Исоритмон, Изосепиаптерин, Кетокленбутерол, Кетотрексат, Копексил, Ламивудин, Ламотригин, Ламотригин, Ламитидин, Лаппаконин, Лавендамицин, L-Цитидин, Леналидомид, Лейцинокаин, Лейковорин, L-g-Метилен-10-деазааминоптерин, Линифаниб, Линтоприд, Лисадимат, Лобукавир, Лоденозин, Ломегуатриб, Лометрексол, Локсорибин, L-S- Аденозилметионин, Мабутерол, Медейол, Меларсеноксид, Меларсопрол В, Мезалазин, Метабутетамин, Метабутоксикаин, Метагексамид, Метазоцин, Метиоприм, Метотрексат, Метилантранилат, Метиоприм, Метоклопрамид, Метоприн, Миноксидил, Мирабегрон, Митомицин, Мивобулин, Моцетиностат, Монокаин, Мосаприд, Мутамицин, N-(п-Аминофенетил)спироперидол, N6-[2-(4-аминофенил)этил]аденозин Role, NAD+, NADH, NADH2, NADP+, NADPH2, Наепаин, Наминтерол, Наретин, Небидразин, 5'-N-этилкрабоксамидаденозин (NECA), Неларабин, Нелзарабин, Неоламин, Неотропин, Непафенак, Неризопам, Нейрофорт, Нифупразин, Нимустин, Нитрин, N-Метилтетрагидрофолиевая кислота, Нолатрексед, Номифензин, Норцисаприд, N-Пропионилпрокаинамид, N-Сульфанилнорфлоксацин, о-Аминофенилаланин, Октотиамин, Оламуфлоксацин, Орметоприм, Ортокаин, Оксимонам, Оксибупрокаин, п-Аминоантипирин, п-Аминобензоат, п-Амино-D-фенилаланин, Панкоприд, Парсалмид, Пасдразид, Патоцидин, Пелитрексол, Пеметрексед, Пенцикловир, Пепломицин, Пералоприд, Фенамил, Феназон, Феназопиридин, Фенил п-аминобензоат, Фенил-PAS-Тебамин, Флеомицин D1, Пибутидин, Пикуметерол, Пиразмонам, Пиридокаин, Пиритрексим, Порфиромицин, Плататрексат, Прамипексол, Празобинд, Празоцин, Преладенант, Прокаинамид, Прокаин, Профлавин, Пропаракаин, Пропоксикаин, Просултиамин, Прукалоприд, Псевдоизоцитидин, Псикофуранин, Птеридоксамин, Птероилтриглютаминовая кислота, Пирамин, Пириметамин, Квестиомицин, хинелоран, Рацивир, Регаденосон, Реноквид, Рензаприд, Резиквимод, Резорцеин, Ретигабин, Реверсет, Рилузол, Роцикловир, Руфокромомицин, S-Аденозилметионин, Сангивамицин, Сапроптерин, S-Доксазозин, Сепиаптерин, Серебра сульфадиазин, Синефунгин, Сипатригин, Спарфлоксацин, Спарсомицин, Стеарил-СоА, Стеарилсульфамид, Стрептонигрин, Сукцисульфон, Сульфамонометоксин, Суламсерод, Сульфабромометазин, Сульфацетамид, Сульфахлорпиридазин, Сульфахризоидин, Сульфакломид, Сульфаклоразол, Сульфаклозин, Сульфацитин, Сульфадиасульфон, Сульфадиазин, Сульфадикрамид, Сульфадиметоксин, Сульфадимидин, Сульфадоксин, Сульфаэтоксипиридазин, Сульфагуанидин, Сульфагуанол, Сульфален, Сульфамеразин, Сульфаметазин, Сульфаметизол, Сульфаметоксазол, Сульфаметоксидиазин, Сульфаметоксипиридазин, Сульфаметомидин, Сульфаметопиразин, Сульфаметрол, Сульфаниламид, Сульфаниламидомидазол, Сульфанилилглицин, Сульфаперин, Сульфафеназол, Сульфапроксилин, Сульфапиразол, Сульфапиридин, Сульфасомизол, Сульфасимазин, Сульфатиадиазол, Сульфатроксазол, Сульфатрозол, Сульфизомидин Сульфизоксазол, Тацединалин, Такрин, Талампанел, Талипексол, Тализомицин А, Тенофовир, Тенофовир дизопроксил, Теразоцин, Тетрагидробиоптерин, Тетрагидрофолиевая кислота, Тетроксоприм, Тезацитабин, Тиамин, Тиазосульфон, Тиогуанин, Тиамиприн, Тигемонам, Тимирдин, Тиноридин, Тиодазоцин, Тирапазамин, Тивицикловир, Токладизин, Транкопал, Триакантин, Триамтерен, Триапин, Трицирибин, Тримазоцин, Триметоприм, Триметрексат, Тритоквалин, Троксацитабин, Туберцидин 5'-дифосфат, Туватидин, Тирфостин AG 1112, Валацикловир, Валганцикловир, Валопицитабин, Валторцитабин, Велнакрин, Венгицид, Верадолин, Видарабин, Вироксим, Витаберин, Залцитабин, Женггуангмицин В2, Зинвироксим, Зорбамицин, Зоксазоламин, (±)-Закситоксин, 2-Аминоперимидин, 6-Формилптерин, 8-13-Нейротензин, 8-Тиогуанозин, 9-Деазагуанозин, 9-Дезаргинин-Брадикинин, а4-10-Кортикотропин, Афамеланотид, Агматин, Аларелин, Амбазон, Амилорид, Аминоптерин, Ампиримин, Ангиотензин, Ангиотензин I, Ангиотензин II, Антибиотик O-129, Антипаин, Аргинин, Аргипрестоцин, Астрессин, Атриопептин III, Авиптадил, Бензилизотиомочевина, Бетациамин, Бисиндолилмалеимид IX, Бивалирудин, Бластицидин S, Блеомицин В2, Бомбезин 14, Буформин, Камостат, Карипорид, Карперитид, Цекропин Р 1, Цетрореликс, Циленгитид, Креапур, Цианогинозин LR, Циановиридин RR, Даларгин, Дамвар, Деазааминоптерин, Дефензин HNP 1, Деслорелин, Десмопрессин, Дезагуанин, Дихлорметотрексат, Дигидрострептомицин, Димаприт, Диметиламилорид, Диминазен, DL-Метотрексат, D- Метотрексат, Эбротидин, Эдатрексат, Тирокальцитонин угря, Эластатиналь, Элкатонин, Энтеростатин, Энвиомицин, Эптифибатид, Этилизопропиламилорид, Этиламид, Этоприн, Фамотидин, Флупиртин, Фуртерен, Галанин, Галегин, Грелин, Глюкагон, Гонадолиберин А, Гуанетидин, Гуанфацин, Гуаноксан, Гуанилтиомочевина, Гусперимус, Гексамидин, Гистатин 5, Гистрелин, Гомоаргинин, Икатибант, Иметит, Инсулинотропин, Изокарамидин, Калидин 10, Кемптид, Кетотрексат, Киоторфин, Лактоферрицин, Ламифибан, L-Брадикинин, Лейковерин, Лейковерин А, Лейпептин, Левпролид, Лометрексол, Лутрелин, м-Хлорфенилбигуанид, Мелагатран, Меланотан II, Меланотропин, Мелиттин, Метформин, Метотрексата диметиловый эфир, Метотрексат моногидрат, Метокстрексат, Метилизотиомочевина, Метоприн, Миакальцин, Мета-иодбензилгуанидин, Миноксидил, Митогуазон, Мивобулин, Мивобулин изетионат, Мороксидин, Нафарелин, Неотин, Несиритид, Нетропсин, Нейротензин, N-Метилтетрагидрофолат, Ноцицептин, Нолатрексед, Новастан, Панамидин, Патоцидин, Пебак, Пелдезин, Пелитрексол, Пеметрексед, Пентамидин, Перамивир, Фенформин, Фенилбигуанид, Свиной галанин, Пимагедин, Пиритрексим, Питрессин, Свиной ангиотензиноген, Свиной гастрин-высвобождающий гормон, Свиной нейропетид Y, Свиной PHI, Пралатрексат, Протеин человеческий, Ингибитор протеиназы Е 64, Пириметамин, Хинеспар, Крысиный атриопептин, Крысиный атриопептин, Резиквимод, Рибамидин, Риморфин, Саралазин, Сакситоксин, Серморелин, S-Этилизотиомочевина, Спантид, Сталлимицин, Стилбамидин, Стрептомицин А, Вещество Р в виде свободной кислоты, Сульфагуанидин, Синтетический рилизинг-фактор лютеинизирующего гормона (LHRH), Таллимустин, Тепротид, Тетракозактид, Тетрагидробиоптерин, Тетрагидрофолиевая кислота, Тромбин рецептор-активирующий пептид-14, Тимопентин, Тиогуанин, Тиотидин, Тирапазамин, Триамтерен, Триметрексат, Трипторелин, Туберактиномицин В, Тафцин, Urepearl, Виомицидин, Випровекс, Витамин М, Ксенопсин, Занамивир, Зеоцин, Зиконотид, Золадекс.
, Дихлорметотрексат, Дихлорфенарсин, Дидеоксицитидин, Дигидробиоптерин, Дигидрофолиевая кислота, Диметиалиум, Диметокаин, Диметил метотрексат, Диналин, DL-5,6,7,8-Тетрагидофолиевая кислота, DL-Метотрексат, Добуприд, Довитиниб, Доксазозин, Драфлазин, Эдатрексат, Эльпетригин, Элвуцитабин, Эмтрицитабин, Энтекавир, Энвираден, Эпцитабин, Эпироприм, Эритаденин, Этантерол, Этакридин, Этаден, Этилизопропиламилорид, Этоприн, Этоксазен, Этравирин, Этрицигуат, FAD, Фамцикловир, Фазарабин, Фенамол, Фепрацет, Фиацитабин, Флуцитозин, Флудара, Флударабин, Флуцитозин, Фолиевая кислота, Формицин А, Фосампренавир, Фуралазин, Фурсултиамин, Фурилтриазин, Ганцикловир, Ганцикловир, Гастрацид, Гемцитабин, Гиракодазол, Глоксимонам, Глибутиазол, GSK 3В Ингибитор XII, GSK3BИнгибиторХII, Гуанин, Гуанин арабинозид, Гуанозин, Гексил пара-аминобензойная ксилота, Гидрокси метил кленбутерол, Гидроксипрокаин, Гидрокситриамтерен сульфат, Ибацитабин, Иклаприм, Иманиксил, Имиквимод, Инданоцин, Иобензамовая кислота, Иоцетамовая кислота, Иомегламовая кислота, Иомегламовая кислота, Ипидакрин, Ирамин, Ирсогладин, Изаторибин, Изобутамбен, Исоритмон, Изосепиаптерин, Кетокленбутерол, Кетотрексат, Копексил, Ламивудин, Ламотригин, Ламотригин, Ламитидин, Лаппаконин, Лавендамицин, L-Цитидин, Леналидомид, Лейцинокаин, Лейковорин, L-g-Метилен-10-деазааминоптерин, Линифаниб, Линтоприд, Лисадимат, Лобукавир, Лоденозин, Ломегуатриб, Лометрексол, Локсорибин, L-S- Аденозилметионин, Мабутерол, Медейол, Меларсеноксид, Меларсопрол В, Мезалазин, Метабутетамин, Метабутоксикаин, Метагексамид, Метазоцин, Метиоприм, Метотрексат, Метилантранилат, Метиоприм, Метоклопрамид, Метоприн, Миноксидил, Мирабегрон, Митомицин, Мивобулин, Моцетиностат, Монокаин, Мосаприд, Мутамицин, N-(п-Аминофенетил)спироперидол, N6-[2-(4-аминофенил)этил]аденозин Role, NAD+, NADH, NADH2, NADP+, NADPH2, Наепаин, Наминтерол, Наретин, Небидразин, 5'-N-этилкрабоксамидаденозин (NECA), Неларабин, Нелзарабин, Неоламин, Неотропин, Непафенак, Неризопам, Нейрофорт, Нифупразин, Нимустин, Нитрин, N-Метилтетрагидрофолиевая кислота, Нолатрексед, Номифензин, Норцисаприд, N-Пропионилпрокаинамид, N-Сульфанилнорфлоксацин, о-Аминофенилаланин, Октотиамин, Оламуфлоксацин, Орметоприм, Ортокаин, Оксимонам, Оксибупрокаин, п-Аминоантипирин, п-Аминобензоат, п-Амино-D-фенилаланин, Панкоприд, Парсалмид, Пасдразид, Патоцидин, Пелитрексол, Пеметрексед, Пенцикловир, Пепломицин, Пералоприд, Фенамил, Феназон, Феназопиридин, Фенил п-аминобензоат, Фенил-PAS-Тебамин, Флеомицин D1, Пибутидин, Пикуметерол, Пиразмонам, Пиридокаин, Пиритрексим, Порфиромицин, Плататрексат, Прамипексол, Празобинд, Празоцин, Преладенант, Прокаинамид, Прокаин, Профлавин, Пропаракаин, Пропоксикаин, Просултиамин, Прукалоприд, Псевдоизоцитидин, Псикофуранин, Птеридоксамин, Птероилтриглютаминовая кислота, Пирамин, Пириметамин, Квестиомицин, хинелоран, Рацивир, Регаденосон, Реноквид, Рензаприд, Резиквимод, Резорцеин, Ретигабин, Реверсет, Рилузол, Роцикловир, Руфокромомицин, S-Аденозилметионин, Сангивамицин, Сапроптерин, S-Доксазозин, Сепиаптерин, Серебра сульфадиазин, Синефунгин, Сипатригин, Спарфлоксацин, Спарсомицин, Стеарил-СоА, Стеарилсульфамид, Стрептонигрин, Сукцисульфон, Сульфамонометоксин, Суламсерод, Сульфабромометазин, Сульфацетамид, Сульфахлорпиридазин, Сульфахризоидин, Сульфакломид, Сульфаклоразол, Сульфаклозин, Сульфацитин, Сульфадиасульфон, Сульфадиазин, Сульфадикрамид, Сульфадиметоксин, Сульфадимидин, Сульфадоксин, Сульфаэтоксипиридазин, Сульфагуанидин, Сульфагуанол, Сульфален, Сульфамеразин, Сульфаметазин, Сульфаметизол, Сульфаметоксазол, Сульфаметоксидиазин, Сульфаметоксипиридазин, Сульфаметомидин, Сульфаметопиразин, Сульфаметрол, Сульфаниламид, Сульфаниламидомидазол, Сульфанилилглицин, Сульфаперин, Сульфафеназол, Сульфапроксилин, Сульфапиразол, Сульфапиридин, Сульфасомизол, Сульфасимазин, Сульфатиадиазол, Сульфатроксазол, Сульфатрозол, Сульфизомидин Сульфизоксазол, Тацединалин, Такрин, Талампанел, Талипексол, Тализомицин А, Тенофовир, Тенофовир дизопроксил, Теразоцин, Тетрагидробиоптерин, Тетрагидрофолиевая кислота, Тетроксоприм, Тезацитабин, Тиамин, Тиазосульфон, Тиогуанин, Тиамиприн, Тигемонам, Тимирдин, Тиноридин, Тиодазоцин, Тирапазамин, Тивицикловир, Токладизин, Транкопал, Триакантин, Триамтерен, Триапин, Трицирибин, Тримазоцин, Триметоприм, Триметрексат, Тритоквалин, Троксацитабин, Туберцидин 5'-дифосфат, Туватидин, Тирфостин AG 1112, Валацикловир, Валганцикловир, Валопицитабин, Валторцитабин, Велнакрин, Венгицид, Верадолин, Видарабин, Вироксим, Витаберин, Залцитабин, Женггуангмицин В2, Зинвироксим, Зорбамицин, Зоксазоламин, (±)-Закситоксин, 2-Аминоперимидин, 6-Формилптерин, 8-13-Нейротензин, 8-Тиогуанозин, 9-Деазагуанозин, 9-Дезаргинин-Брадикинин, а4-10-Кортикотропин, Афамеланотид, Агматин, Аларелин, Амбазон, Амилорид, Аминоптерин, Ампиримин, Ангиотензин, Ангиотензин I, Ангиотензин II, Антибиотик O-129, Антипаин, Аргинин, Аргипрестоцин, Астрессин, Атриопептин III, Авиптадил, Бензилизотиомочевина, Бетациамин, Бисиндолилмалеимид IX, Бивалирудин, Бластицидин S, Блеомицин В2, Бомбезин 14, Буформин, Камостат, Карипорид, Карперитид, Цекропин Р 1, Цетрореликс, Циленгитид, Креапур, Цианогинозин LR, Циановиридин RR, Даларгин, Дамвар, Деазааминоптерин, Дефензин HNP 1, Деслорелин, Десмопрессин, Дезагуанин, Дихлорметотрексат, Дигидрострептомицин, Димаприт, Диметиламилорид, Диминазен, DL-Метотрексат, D- Метотрексат, Эбротидин, Эдатрексат, Тирокальцитонин угря, Эластатиналь, Элкатонин, Энтеростатин, Энвиомицин, Эптифибатид, Этилизопропиламилорид, Этиламид, Этоприн, Фамотидин, Флупиртин, Фуртерен, Галанин, Галегин, Грелин, Глюкагон, Гонадолиберин А, Гуанетидин, Гуанфацин, Гуаноксан, Гуанилтиомочевина, Гусперимус, Гексамидин, Гистатин 5, Гистрелин, Гомоаргинин, Икатибант, Иметит, Инсулинотропин, Изокарамидин, Калидин 10, Кемптид, Кетотрексат, Киоторфин, Лактоферрицин, Ламифибан, L-Брадикинин, Лейковерин, Лейковерин А, Лейпептин, Левпролид, Лометрексол, Лутрелин, м-Хлорфенилбигуанид, Мелагатран, Меланотан II, Меланотропин, Мелиттин, Метформин, Метотрексата диметиловый эфир, Метотрексат моногидрат, Метокстрексат, Метилизотиомочевина, Метоприн, Миакальцин, Мета-иодбензилгуанидин, Миноксидил, Митогуазон, Мивобулин, Мивобулин изетионат, Мороксидин, Нафарелин, Неотин, Несиритид, Нетропсин, Нейротензин, N-Метилтетрагидрофолат, Ноцицептин, Нолатрексед, Новастан, Панамидин, Патоцидин, Пебак, Пелдезин, Пелитрексол, Пеметрексед, Пентамидин, Перамивир, Фенформин, Фенилбигуанид, Свиной галанин, Пимагедин, Пиритрексим, Питрессин, Свиной ангиотензиноген, Свиной гастрин-высвобождающий гормон, Свиной нейропетид Y, Свиной PHI, Пралатрексат, Протеин человеческий, Ингибитор протеиназы Е 64, Пириметамин, Хинеспар, Крысиный атриопептин, Крысиный атриопептин, Резиквимод, Рибамидин, Риморфин, Саралазин, Сакситоксин, Серморелин, S-Этилизотиомочевина, Спантид, Сталлимицин, Стилбамидин, Стрептомицин А, Вещество Р в виде свободной кислоты, Сульфагуанидин, Синтетический рилизинг-фактор лютеинизирующего гормона (LHRH), Таллимустин, Тепротид, Тетракозактид, Тетрагидробиоптерин, Тетрагидрофолиевая кислота, Тромбин рецептор-активирующий пептид-14, Тимопентин, Тиогуанин, Тиотидин, Тирапазамин, Триамтерен, Триметрексат, Трипторелин, Туберактиномицин В, Тафцин, Urepearl, Виомицидин, Випровекс, Витамин М, Ксенопсин, Занамивир, Зеоцин, Зиконотид, Золадекс.
Предпочтительно, подходящие лекарственные средства с ароматическими амино-группами могут быть выбраны из списка, содержащего (-)-Драфлазин, (-)- Индокарбазостатин В, (+)-(R)-Прамипексол, (R)-(+)-Теразоцин, (R)-Ганцикловир Циклический Фосфонат, (R)-Суфинозин, (R)-Закоприд, (S)-Суфинозин, (S)-Закоприд Гидрохлорид, 17-Аминогелданамицин, 2-Аминоаристеромицин, 2-Аминонепланоцин А, 3-Хлорпрокаинамид, 3-Деазааденозин, 4-Аминосалициловая кислота, 4-Хлорфенилтио-DADME-Иммуциллин-А, 5'-Гомонепланоцин А, 5-Аминосалициловая кислота, 9-Аминокамптотецин, Абакавир Сукцинат, Абакавир Сульфат, Абаноквил Мезилат, Акадезин, Акрифлавин, Ацикловир, Ацикловир Элаидат, Ацикловир Олеат, Адефовир, Адефовир Дипивоксил, Адеметионин Тозилат Сульфат, Аденаллен, Аденофостин А, Аденофостин В, Аденозин, Афлоквалон, Агелиферин Диацетат, Агелиферин Дигидрохлорид, Аламифовир, Афлузоцин Гидрохлорид, Амбасилид, Амброксол Нитрат, Амдоксовир, Амелтолид, Амезиниум Метилсульфат, Амфенак Натрия, Амилорид Гидрохлорид, Аминоглютетимид, Амисулприд, Амоксанокс, Ампренавир, Ампидин, Амринон, Амселамин Гидробромид, Амтамин, Анакинра, Ападеносон, Аплонидин Гидрохлорид, Априцитабин, Азацитидин, Азаланстат, Азтреонам, Азтреонам L-Лизин, Балапиравир Гидрохлорид, Батрацилин, Белактин А, Бензокаин, Биноденосон, Блеомицин А2 Сульфат, Бродимоприм, Бромфенак Натрия, Бромгексин Гидрохлорид, Буназоцин Гидрохлорид, Кападеносон, Капесерод Гидрохлорид, Карбовир, Карбоксиамидотриазол, Карумонам Натрия, Цефкапен Пивоксил Гидрохлорид, Цефдалоксим, Цефдалоким Пентексил Тозилат, Цефдинир, Цефдиторен Пивоксил, Цефепим, Цефетамет Пивоксил, Цефетекол, Цефиксим, Цефлупренам, Цефматилен Гидрохлорид Гидрат, Цефменоким Гидрохлорид, Цефодизим, Цефодизим Натрия, Цефоселис Сульфат, Цефотаксим Натрия, Цефотиам Гексетил, Цефотиам Гексетил Гидрохлорид, Цефотиам Гидрохлорид, Цефозопран, Цефозопран Гидрохлорид, Цефпиром, Цефподоксим Проксетил, Цефквином, Цефтаролин, Цефтазидим, Цефтерам Пивоксил, Цефтибутен, Цефтобипрол, Цефтобипрол Медоркарил, Цефтразонал Бопентил, Цефтразонал Натрия, Цефтриаксон Натрия, Центанамицин, Цибростатин 1, Цидофовир, Циматерол, Цинитаприд Гидротартрат, Ципамфиллин, Цисаприд Гидрат, Цитиколин, Кладрибин, Клитоцин, Клофарабин, Клопидогрел Сульфат, Цикаллен, Циклический Цидофовир, Цигаловир, Цистазоцин, Цитарабин, Цитарабин Окфостат, Цитарамицин, Цитохлор, Дакциномицин, DADME-Иммуциллин-G, Дапроптерин Дигидрохлорид, Дапсон, Дарбуфелон Мезилат, Дарунавир, Делафлоксацин, Денуфозол Тетранатрия, Деоксивариолин В, Дезацитилвинбластингидразид/Фолат Конъюгат, Детивицикловир Диацетат, Декселвуцитабин, Дезоцитидин, Диаденозин Тетрафосфат, Диаверидин, Дихлорбензоприм, Диклогуамин Малеат, Дидеоксицитидин, DI-VAL-L-DC, Докозил Цидофовир, Довитиниб Лактат, Доксазоцин Мезилат, Драфлазин, DTPA-Аденозилкобаламин, Эценофлоксацин Гидрохлорид, Эйкозил Цидофовир, Элацитарабин, Элпетригин, Элвуцитабин, Эмтрицитабин, Энтекавир, Энтиностат, Эпинастин Гидрохлорид, Эпироприм, Эпофолат, Этилтио-DADME-Иммуциллин-А, Этинилцитидин, Этравирин, Этрицигуат, Фамцикловир, Филаризон, Флуцитозин, Флударабин Фосфат, Фторбензилтриамтерен, Фторминоксидил, Фторнепланоцин А, Флупиритин Малеат, Фолиновая Кислота, Фосампренавир Кальция, Фосампренавир Натрия, Фреселестат, Ганцикловир, Ганцикловир Элаидиновая Кислота, Ганцикловир Монофосфат, Ганцикловир Натрия, Гемцитабин, Гемцитабин Элаидат, Гиродазол, Гепавир В, Гептаминол Аденозинмонофосфат Амидат, Гексадецил Цидофовир, Гексадецилоксипропил-Цидофовир, Гидроксиакалон, Иклаприм, Имиквимод, Иммунозин, Инданоцин, Изобацеллин А, Изобацеллин В, Изобацеллин С, Изобацеллин D, Ламивудин, Ламотригин, Леналидомид, Лейцеттамин А, Лейковорин Кальция, Леволейковорин Кальция, Либломицин, Линифаниб, Линтоприд, Лирексаприд, Лобукавир, Лоденозин, Ломегуатриб, Лометрексол, Локсорибин, L-Симексонил Гомоцистеин, Лимфостин, Мабутерол Гидрохлорид, Макалувамин А, Макалувамин А, Макалувамин В, Макалувамин С, Манаглинат Диаланетил, Мериолин-3, Метазоцин, Метотрексат, Метилтио-DADME-Иммуциллин-А, Метоклопрамид Гидрохлорид, Мидориамин, Миноксидил, Мирабегрон, Митомицин, Мивобулин Изетионат, Моцетиностат Дигидробромид, Мосаприд Цитрат, Мозенавир Мезилат, Нелдазоцин, Нелзарабин, Непафенак, Нолатрексид Гидрохлорид, NO-Мезаламин, Нораристеромицин, O6-Бензилгуанин, Оламуфлоксацин, Оламуфлоксацин Мезилат, Омацикловир, Оксифенарсин, Палауамин, Панкоприд, Пелдезин, Пелитрексол, Пеметрексед Динатрия, Пенцикловир, Пеницилин G Прокаин, Пепломицин, Пикумитерол Фумарат, Пимелоиланилид O-Аминоанилид, РМЕО-5-МЕ-DAPY, Пралатрексат, Прамипексол Гидрохлорид, Празозин Гидрохлорид, Префолик А, Преладенант, Прокаинамид Гидрохлорид, Прокаин Гидрохлорид, Прукалоприд, Прукалоприд Гидрохлорид, Прукалоприд Сукцинат, Пириферон, Пириметамин, Хинелоран Гидрохлорид, Разаксабан Гидрохлорид, Регаденозон, Резиквимод, Ретигабин Гидрохлорид, Рилузол, Риоцигуат, Роцикловир, Румицин 1, Румицин 2, Сампиртин, Секобацеллин А, Секобацеллин В, Серебро Сульфадиазин, Сипатригин, Сонеденозон, Сотиримод, Спарфлоксацин, Стилогуанидин, Суфинозин, Сурфен, Синаденол, Сингуанол, Тацединалин, Такрин Гидрохлорид, Талампанел, Талипексол Дигидрохлорид, Талоптерин, Тенофовир, Тенофовир DF, Теразозин Гидрохлорид, Тетракозил Цидофовир, Тезацитабин, TGP, Тимиридин Диэтансульфонат, Торцитабин, Трантинтерол Гидрохлорид, Трихомицин А, Тримазозин Гидрохлорид, Триметрексат Глукуронат, Троксацитабин, Трибизин Гидрохлорид, Валацикловир, Валганцикловир Гидрохлорид, Валомацикловир Стеарат, Валопицитабин, Велнакрин Малеат, Ксилоцидин.
Подходящие лекарственные средства с амино-группой могут быть выбраны из группы, состоящей из следующих средств: Афидиколин Глицинат, Цетрореликс Ацетат, Пикуметерол Фумарат, (-)-Драфлазин, (-)-Индокарбазостатин В, (+)-(23,24)-Дигидродискодермолид, (+)-(R)-Прамипексол, (R)-(+)-Амлодипин, (R)-(+)-Теразоцин, (R)-Ганцикловир Циклический Фосфонат, (R)-Суфиноцин, (R)-Закоприд, (S)-(-)-Норкетамин, (S)-Оксирацетам, (S)-Суфиноцин, (S)-Закоприд Гидрохлорид, [90Y]-DOTAGA-Вещество Р, [ARG(Me)9] MS-10, [D-TYR1,ARG(Me)9] MS-10, [D-TYR1,AzaGLY7,ARG(Me)9] MS-10, [D-TYR1] MS-10, [Psi(CH2NH)TPG4]Ванкомицин Агликон, [TRP19] MS-10, 111IN-Пентетреотид, 13-Деоксиадриамицин Гидрохлорид, 17-Аминогелданамицин, 19-O-Метилгелданамицин, 1-Метил-D-Триптофан, 21-Аминоэпотилон В, 2-Аминоаристеромицин, 2-Аминонепланоцин А, 3-Хлорпрокаинамид, 3-Деазааденозин, 3-Матида, 4-Аминосалициловая кислота, 4-Хлорфенилтио-DADME-Иммуциллин-А, 5,4'-Диэпиарбекацин, 5'-Гомонепланоцин А, 5-Аминосалициловая Кислота, 8(R)-Фторидарубицин Гидрохлорид, 99MTC-C(RGDFK*)2Hynic, 9-Аминокамптотецин, А-42867 Псевдоагликон, Абакавир Сукцинат, Абакавир Сульфат, Абаноквил Мезилат, Абареликс, Акадезин, Акрифлавин, Ацикловир, Ацикловир Элаидат, Ацикловир Олеат, Ацилин, Адефовир, Адефовир Дипивоксил, Адеметионин Тозилат Сульфат, Аденаллен, Аденофостин А, Аденофостин В, Аденозин, Аэротрицин 1, Аэротрицин 16, Аэротрицин 41, Аэротрицин 45, Аэротрицин 5, Аэротрицин 50, Аэротрицин 55, Афлоквалон, Агелиферин Диацетат, Агелиферин Дигидрохлорид, Аладапцин, Аламифовир, Алатрофлоксацин Мезилат, Натриевая Соль Алендроновой Кислоты, Алестрамустин, Афлузоцин Гидрохлорид, Алискирен Фумарат, Алоглиптин Бензоат, Альфа-Метилнорэпинефрин, Альфа-Метилтриптофан, Алтемецидин, Алвеспимицин Гидрохлорид, Амантадин Гидрохлорид, Амбасилид, Амбазон, Амброксол Нитрат, Амдоксовир, Амелтолид, Амелубант, Амезиниум Метилсульфат, Амфенак Натрия, Амидокс, Амифостин Гидрат, Амикацин, Амилорид Гидрохлорид, Аминокандин, Аминоглютетимид, Аминогуанидин, Гексиловый Эфир Аминолевулиновой Кислоты, Метиловый Эфир Аминолевулиновой Кислоты, Амисулприд, Амлодипин, Амлодипин Безилат, Амоксанокс, Амоксициллин Pulsys, Амфотерицин В, Ампициллин Натрия, Ампренавир, Ампидин, Амринон, Амрубицин Гидрохлорид, Амселамин Гидробромид, Амтамин, Анакинра, Анаморелин Гидрохлорид, Анатибант Мезилат, Ангиопептин Ацетат, Анисперимус, Антагонист-G, Антид, Антид-1, Антид-2, Антид-3, Антилейкинат, Ападеносон, Апиксабан, Аплонидин Гидрохлорид, Апоптозол 1, Апоптозол 2, Апоптозол 3, Априцитабин, Арбекацин, Арбекацин Сульфат, Арборкандин А, Арборкандин В, Арборкандин С, Арборкандин D, Арборкандин Е, Арборкандин F, Аргатробан Моногидрат, Аргимесна, Аргинин Бутират, Аргиотоксин-636, Армодафинил, Аротинолол Гидрохлорид, Артеролан Малеат, Аспоксициллин, Атенолол, Атосибан, Атрелейтон, Аворелин, Азацитидин, Азаланстат, Азаромицин SC, Азелнидипин, Азетирелин, Азодикарбонамид, Азоксибацилин, Азтреонам, Азтреонам L-Лизин, Азумамид А, Баклофен, Бактоболин, Балапиравир Гидрохлорид, Балхимицин, Барусибан, Батрацилин, Белактин А, Белактоцин А, Белактоцин С, Бенаномицин В, Бенексат Циклодекстрин, Бензокаин, Бесифлоксацин Гидрохлорид, Бета-Амилоид (12-20), Биноденосон, Блеомицин А2 Сульфат, Боцепревир, Богорол А, Бохолмицин, Бразиликардин А, Бремеланотид, Бриваниб Аланинат, Бриварацетам, Бродимоприм, Бромфенак Натрия, Бромгексин Гидрохлорид, Бросталлицин Гидрохлорид, Буназоцин Гидрохлорид, Бусерелин Ацетат, Бутабиндин, Бутамидин, Бутеранол, Кабин 1, Кальций-Подобный Пептид 1, Кальций-Подобный Пептид 2, Камбресцидин 800, Камбресцидин 816, Камбресцидин 830, Камбресцидин 844, Камостат, Канфосамид Гидрохлорид, Кападеносон, Капесерод Гидрохлорид, Каправирин, Капразамицин А, Капразамицин В, Капразамицин С, Капразамицин Е, Капразамицин F, Капроморелин, Карафибан Малеат, Карбахол, Карбамазепин, Карбетоцин, Карбовир, Карбоксиамидотриазол, Карипорид Гидрохлорид, Карисбамат, Карпипрамин, Карумонам Натрия, Каспофунгин Ацетат, Цефаклор, Цефканел Далоксат Гидрохлорид, Цефкапен Пивоксил Гидрохлорид, Цефдалоксим, Цефдалоксим Пентексил Тозилат, Цефдинир, Цефдиторен Пивоксил, Цефепим, Цефатамет Пивоксил, Цефетекол, Цефиксим, Цефлупренам, Цефматилен Гидрохлорид Гидрат, Цефменоксим Гидрохлорид, Цефминокс Натрия, Цефодизим, Цефодизим Натрия, Цефоселис Сульфат, Цефотаксим Натрия, Цефотетан Динатрия, Цефотиам Гексетил, Цефотиам Гексетил Гидрохлорид, Цефотиам Гидрохлорид, Цефокситин, Цефозопран, Цефозопран Гидрохлорид, Цефпиром, Цефподоксим Проксетил, Цефпрозил, Цефпрозил Моногидрат, Цефквином, Цефтаролин, Цефтазидим, Цефтерам Пивоксил, Цефтибутен, Цефтобипрол, Цефтобипрол Медоркарил, Цефтразонал Бопентил, Цефтразонал Натрия, Цефтриаксон Натрия, Цефтризоксим Алапивоксил, Цефуроксим, Цефуроксим Аксетил, Цефуроксим Пивоксетил, Центанамицин, Цефалексин Моногидрат, Церанаприл, Церулетид Диэтиламин, Цетефлоксацин, Хлорфузин, Хлорориентицин А, Хлорориентицин В, Хлортетаин, Цибростатин 1, Цидофовир, Циластатин Натрия, Циленгитид, Циматерол, Цинитаприд Гидротартрат, Ципамфиллин, Цирцинамид, Цисаприд Гидрат, Циспентацин, Цитиколин, Цитруллимицин А, Кладрибин, Цитоцин, Клофарабин, Клопидогрел Сульфат, Соединение 301029, Кумамидин Гамма1, Кумамидин Гамма2, Кромогликат Лизетил Гидрохлорид, Цикаллен, Циклил-Цидофовир, Циклосерин, Циклотеонамид А, Циклотиалидин, Цигаловир, Ципемицин, Цисметинил, Цистамидин А, Цистамин, Цистазоцин, Цистоцин, Цитарабин, Цитарабин Окфосфат, Цитарамицин, Цитохлор, Цитомодулин, Дабигатран, Дабигатран Этексилат, Дакопафант, Дактимицин, Дактиномицин, Дактилоциклин А, Дактилоциклин В, DADME-Иммуциллин-G, Даларгин, Данегаптид Гидрохлорид, Дапроптерин Дигидрохлорид, Дапсон, Дарбуфелон Мезилат, Дарифенацин Гидробромид, Даринапарсин, Дарунавир, Даунорубицин, Давасаицин, Давунетид, Дебризохин Сульфат, Декагидромоэномицин А, Декапланин, Дефероксамин, Дегареликс Ацетат, Делафлоксацин, Гидрохлорид Дельта-Аминолевулиновой Кислоты, Делтибант, Денаглиптин Гидрохлорид, Денибулин Гидрохлорид, Денуфозол Тетранатрия, Деоксиметилспергуалин, Деоксинегамицин, Деоксивариолин В, Дезацетилвинбластингидразид/Фолат Конъюгат, Дез-F-Ситаглиптин, Дезглугастрин Трометамин, Деслорелин, Десмопрессин Ацетат, Детивицикловир Диацетат, Декселвуцитабин, Дексибупрофен Лизин, Декстроамфетамин Сульфат, Дезинамид, Дезоцитидин, Диаденозин Тетрафосфат, Диаверидин, Дихлорбензоприм, Диклогуамин Малеат, Дидемнин X, Дидемнин Y, Дидеоксицитидин, Дифуразон, Дилевалол, Дилевалол Гидрохлорид, Дисермолид, Дизопирамид Фосфат, DI-VAL-L-DC, Докозил Цидофовир, Доластатин 14, Доластатин С, Донитриптан Гидрохлорид, Донитриптан Мезилат, Довитиниб Лактат, Доксазоцин Мезилат, Доксорубицин Гидрохлорид, Доксициклин Гиклат, D-Пеницилламин, Драфлазин, Дроксидопа, DTPA-Аденозилкобаламин, Эбротидин, Эценофлоксацин Гидрохлорид, Эфегатран Сульфат Гидрат, Эфлорнитин Гидрохлорид, Эглумегад Гидрат, Эйкозил Цидофовир, Элацитарабин, Эластатинал В, Эластатинал С, Элпетригин, Элвуцитабин, Эмтрицитабин, Эналкирен, Энигмол, Энипорид Мезилат, Энтекавир, Энтиностат, Эпинастин Гидрохлорид, Эпироприм, Эпирубицин Гидрохлорид, Эпиталон, Эпофолат, Эпостатин, Эпсилон-аминокапроновая Кислота, Эремомицин, Эрибулин Мезилат, Эрукамид, Эсафлоксацин Гидрохлорид, Эсликарбазепин Ацетат, Этаквин, Этаноламин, Этилтио-DADME-Иммуциллин-А, Этинилцитидин, Этравирин, Этрицигуат, Эксаламид, Эксаморелин, Эксатекан Мезилат, Эзатиостат Гидрохлорид, Фамцикловир, Фамотидин, Фамотидин Висмут Цитрат, Фавипиравир, Феглимицил, Фелбамат, Фенлейтон, Фидарестат, Фидексабан, Филаминаст, Филаризон, Финголимод Гидрохлорид, Флуцитозин, Флударабин Фосфат, Фторбензилтриамтерен, Фторминоксидил, Фторнепланоцин А, Флупиритин Малеат, Флувируцин В2, Флувоксамин Малеат, Фолиновая Кислота, Фортимицин А, Фосампренавир Кальция, Фосампренавир Натрия, Фосфомицин Трометамол, Фрадафибан, Фрезелестат, Фроватриптан, Фудостеин, Фурамидин, G1 Пептид, Габадур, Габапентин, Габексат Мезилат, Галарубицин Гидрохлорид, Галмик, Галнон, Ганцикловир, Ганцикловир Элаидиновая Кислота, Ганцикловир Монофосфат, Ганцикловир Натрия, Ганиреликс, Ганиреликс Ацетат, Гаромефрин Гидрохлорид, Гемцитабин, Гемцитабин Элаидат, Гемифлоксацин Мезилат, Гилатид, Гиродазол, Гласпимод, Глюкозамин Сульфат, Глудопа, Глутатион Моноэтиловый эфир, Глутатион Моноизопропиловый эфир, Глицин-Пролин-Мелфалан, Глицопин, Гликотиогексид альфа, Голотимод, Госерелин, Антагонист-116 Фактора Роста, Гормон Роста-высвобождающий Пептид 2, Гуанабенз Ацетат, Гуанадрел Сульфат, Гуанетидин Моносульфат, Гуанфацин Гидрохлорид, Гусперимус Гидрохлорид, Галовир А, Галовир В, Галовир С, Галовир D, Галовир Е, Хаюмицин В, Хаюмицин С1, Хаюмицин С2, Хаюмицин D, Гелвекардин А, Гелвекардин В, Гепавир В, Гептаминол АМФ Амидат, Гекса-D-Аргинин, Гексадецил Цидофовир, Гексадецилоксипропил- Цидофовир, Гистамин Дигидрохлорид, Гистапродифен, Гистрелин, Гистрелин Ацетат, Человеческий Ангиотензин II, Гидростатин А, Гидроксиакалон, Гидроксимочевина, Гипептин, Ибутаморен Мезилат, Икатибант Ацетат, Иклаприм, Икофунгипен, Идарубицин Гидрохлорид, Илатреотид, Илонидап, Иметит, Имидафенацин, Имидазенил, Имиквимод, Иммуноцин, Импентамин, Инциклинид, Инданоцин, Индантадол Гидрохлорид, Индексам, Иногатран, Интрифибан, Иобенгуан[131I], Иодорубидазон (Р), Иотризид, Изепамицин Сульфат, Изобацеллин А, Изобацеллин В, Изобацеллин С, Изобацеллин D, Изобутирамид, Изодоксорубицин, Изопропамид Иодид, Испинезиб Мезилат, Истароксим, Янтиномицин А, Янтиномицин В, Янтиномицин С, Яспин В, Кахалалид F, Каитоцефалин, Канамицин, Карнамицин В1, Катаноцин А, Катаноцин В, Кистамицин А, L-4-Оксализин, Лабеталол Гидрохлорид, Лабрадимил, Лагатид, Ламифибан, Ламивудин, Ламотригин, Ланицемин 2(S)-Гидроксисукцинат, Ланицемин Гидрохлорид, Ланомицин, Ларазотид Ацетат, Лазабемид Гидрохлорид, L-Допа Метиловый Эфир Гидрохлорид, L-Допамид, Лекирелин, Леналидомид, Ленампициллин Гидрохлорид, Лейцеттамин А, Лейковорин Кальция, Левпролид Ацетат, Лейрубицин, Лейстродуксин А, Лейстродуксин В, Лейстродуксин С, Лейстродуксин Н, Леветирацетам, Леводопа, Леводопа 3-O-Глюкозид, Леводопа 4-O-Глюкозид, Леволейковорин Кальция, L-Гистидинол, L-Гомотиоцитруллин, Либломицин, Линаглиптин, Линифаниб, Линтоприд, Лирексаприд, Лиримиласт, Лизиноприл, L-Лизин-D-Амфетамин Димезилат, Лобофорин А, Лобукавир, Лоденозин, Лолоатин В, Ломегуатриб, Лометрексол, Лонафарниб, Лоракарбеф Гидрат, Ловирид, Локсорибин, L-Симексонил Гомоцистеин, L-Тиоцитруллин, Лимфостин, Лизобактин, Мабутерол Гидрохлорид, Макалувамин А, Макалувамин А, Макалувамин В, Макалувамин С, Манаглинат Диаланетил, Матристатин А2, Мелагатран, Меланотан II, Мемантин Гидрохлорид, Мемно-Пептид А, Мепробамат, Мериолин-3, Мерсацидин, Метараминол, Метазоцин, Метформин Гидрохлорид, Метотрексат, Метил Бестатин, Метилдопа, Метилтио-DADME-Иммуциллин-А, Метоклопрамид Гидрохлорид, Метирозин, Мексилетин Гидрохлорид, Микафунгин Натрия, Мидаксифиллин, Мидепланин, Мидориамин, Милакаинид Тартрат, Миласемид-[2Н], Милнаципран Гидрохлорид, Минаместан, Миноциклин Гидрохлорид, Миноксидил, Мирабегрон, Митомицин, Мивазерол, Мивобулин Изетионат, Мизорибин, Моцетиностат Дигидробромид, Модафинил, Модафинил Сульфон, Моэномицин А Хлорид Висмутовая Соль, Мофегилин, Мофегилин Гидрохлорид, Монамидоцин, Моноданзил Кадаверин, Монтирелин Тетрагидрат, Мосаприд Цитрат, Моксилубант, Моксилубант Малеат, Мозенавир Мезилат, M-Фенилен Этинилен, Мураминомицин А, Мураминомицин В, Мураминомицин С, Мураминомицин D, Мураминомицин Е1, Мураминомицин Е2, Мураминомицин F, Мураминомицин G, Мураминомицин Н, Мураминомицин I, Мураминомицин Z1, Мураминомицин Z2, Мураминомицин Z3, Мураминомицин Z4, Мурамил Дипептид С, Муреидомицин А, Муреидомицин В, Муреидомицин С, Муреидомицин D, Мицестерицин Е, Мириоцин, Нафамостат Мезилат, Нафарелин Ацетат, Нагливан, Намитекан, Напсагатран, Небостинел, Небрацетам Фумарат, Нелдазоцин, Нелзарабин, Немоноксацин, Неомицин В-Гексааргинин Конъюгат, Неомицин-Акридин, Непафенак, Непикастат Гидрохлорид, Нерамексан Гидрохлорид, Неридроновая Кислота, Нетамифтид Трифторацетат, Нетилмицин Сульфат, Нокатиацин I, Нокатиацин II, Нокатиацин III, Нокатиацин IV, NO-Габапентин, Нолатрексед Гидрохлорид, NO-Мезаламин, Нораристеромицин, Нуванил, O6-Бензилгуанин, Оцимумозид А, Октакозамицин А, Октакозамицин В, Октреотер, Октреотид Ацетат, Оглуфанид Динатрия, Оламуфлоксацин, Оламуфлоксацин Мезилат, Олцегепант, Олрадипин Гидрохлорид, Омацикловир, Омбрабулин, Обмбрабулин Гидрохлорид, Оннамид А, Опиорфин, Орбофибан Ацетат, Ориентицин А, Ориентицин В, Ориентицин С, Ориентицин D, Оритаванцин, Оселтамивир Карбоксилат, Оселтамивир Фосфат, Отамиксабан, Отенабант Гидрохлорид, Овотиол А, Оксазофурин, Окскарбазепин, Оксиглутатион Натрия, Оксирацетам, Оксолид, Оксинор, Оксифенарсин, Озареликс, Pachymedusa Dacnicolor Триптофиллин-1, Пециламинол, Пафурамидин Малеат, Палауамин, Палдимицин В, Памидронат Натрия, Панкоприд, Папуамид А, Папуамид В, Папуамид С, Папуамид D, Паразин I, Паромомицин, Пасиреотид, Пауломицин, Пауломицин А2, Пауломицин В, Пауломицин С, Пауломицин D, Пауломицин Е, Пауломицин F, Пазуфлоксацин, Пазуфлоксацин Мезилат, PEG-Ванкомицин, Пелагиомицин С, Пелдезин, Пелитрексол, Пеметрексед Динатрия, Пенцикловир, Пеницилин G Прокаин, Пентамидин Глюконат, Пентамидин Изетионат, Пентамидин Лактат, Пепломицин, Перамивир, Перфаназин 4-Аминобутират, Факеллистатин 5, PHE-ARG-Бета-Нафтиламид, Фентермин, Фортресс, Фосфолин, Пибутидин Гидрохлорид, Пимелоиланилид O-Аминоанилид, Пирацетам, Пирарубицин, Пивампициллин, Пиксантрон Малеат, Плурафлавин А, Плурафлавин В, Плюсбацин А1, Плюсбацин А2, Плюсбацин A3, Плюсбацин А4, Плюсбацин В1, Плюсбацин В2, Плюсбацин В3, Плюсбацин В4, PMEO-5-ME-DAPY, Пневмокандин А0, Пневмокандин В0, Пневмокандин В0 2-Фосфат, Пневмокандин D0, Полапрецинк, Полидискамид А, Связанный с Полимером Ингибитор лейкоцит-эластазы человека, Постстатин, PPI17-24, Прадимицин Е, Прадимицин FA-2, Пралатрексат, Прамипексол Гидрохлорид, Пранедипин Тартрат, Празоцин Гидрохлорид, Префолик А, Прегабалин, Преладенант, Примахин Фосфат, Пробестин, Прокаинамид Гидрохлорид, Прокаин Гидрохлорид, Про-Диазепам, Простатин, Прукалоприд, Прукалоприд Гидрохлорид, Прукалоприд Сукцинат, Псевдомицин А', Псевдомицин В', Пилорицидин В, Пирадизомицин, Пиразинамид, Пиразиноилгуанидин, Пириферон, Пириметамин, Хинелоран Гидрохлорид, R-(+)-Аминоиндан, Ралфинамид, Рамопланин А'1, Рамопланин А'2, Рамопланин А'3, Рамореликс, Равидомицин N-оксид, Разаксабан Гидрохлорид, Ребластатин, Регаденосон, Релковаптан, Ремацемид Гидрохлорид, Резиквимод, Рестриктицин, Ретаспимицин Гидрохлорид, Ретигабин Гидрохлорид, Родопептин С1, Родопептин С2, Родопептин С3, Родопептин С4, Родострептомицин А, Родострептомицин В, Рибавирин, Рибавирин Эйкозенат цис, Рибавирин Эйкозенат транс, Рибавирин Элаидат, Рибавирин Олеат, Рилмазафон Гидрохлорид Дигидрат, Рилузол, Римакалиб Гидрохлорид, Римепорид Гидрохлорид, Риоцикват, Ритипенем Акоксил, Робалзотан Гидрохлорид, Робалзотан Тартрат Гидрат, Роцикловир, Ромуртид, Ротигаптид, Роксифибан Ацетат, Рубоксил, Руфинамид, Румицин 1, Румицин 2, Сабарубицин Гидрохлорид, Сабипорид Мезилат, Сафинамид Мезилат, Сафингол, Сагамацин, Сампатрилат, Сампиртин, Сапризартан, Саквинавир, Саквинавир Мезилат, Сардомизид Гидрохлорид, Сардомозид, Сауссурамин С, Саксаглиптин, Секобацеллин А, Секобацеллин В, Сеглитид, Селанк, Селетрацетам, Семапимод Гидрохлорид, Сеникапок, Сепимостат Мезилат, Сепроксетин, Сераспенид, Севеламер Карбонат, Севеламер Гидрохлорид, Шефердин, Сибрафибан, Силодозин, Серебра Сульфадиазин, Сипатригин, Ситафлоксацин Гидрат, Ситаглиптин Фосфат Моногидрат, S-Нитрозоглутатион, Софигатран, Сонедоносон, Сотиримод, Спарфлоксацин, Сперабиллин А, Сперабиллин В, Сперабиллин С, Сперабиллин D, Сфингофунгин F, Спинорфин, Списулоцин, Скваламин Лактат, Стрептомицин, Стилогуанидин, Вещество Р(8-11), Суфиноцин, Сулцефалоспорин, Сулфостин, Сульфазоцин, Сультамициллин Тозилат, Sunflower Трипсин Ингибитор-1, Сурфен, Синаденол, Сингуанол, Табиморелин, Тацединалин, Такрин Гидрохлорид, Тагефлар, Талабостат, Талаглуметад Гидрохлорид, Талампанель, Талипексол Дигидрохлорид, Таллимустин Гидрохлорид, Талоптерин, Талтирелин, Танеспимицин, Таногитран, Таргинин, Технеций (99МТС) Депреотид, Тейкопланин-А2-1, Тейкопланин-А2-2, Тейкопланин-А2-3, Тейкопланин-А2-3, Тейкопланин-А2-5, Телаванцин Гидрохлорид, Телинавир, Темозоломид, Темуртид, Тенидап, Тенидап Натрия, Тенофовир, Тенофовир DF, Теразоцин Гидрохлорид, Тетракозил Цидофовир, Тетрациклин Гидрохлорид, Тетрафибрицин, Тексеномицин А, Тезацитабин, TGP, Тиоацет, Тиотио, Тразарин, Тимоктонан, Тимопентин, Тиамдипин, Тигециклин, Тиларгинин Гидрохлорид, Тимирдин Диэтансульфонат, Тимодепрессин, Типифарниб, Ингибитор TNF-Альфа Протеазы, Тобрамицин, Токаинид Гидрохлорид, Токарамид А, Томопенем, Топостатин, Торцитабин, Тозуфлоксацин, Тозуфлоксацин Тозилат, Транексамовая Кислота, Трантинтерол Гидрохлорид, Транилципромин Сульфат, Трелансерин, Тресперимус Трифлутат, Трихомицин А, Трицирибин, Трицирибин Фосфат, Триэнтин Гидрохлорид, Тримазоцин Гидрохлорид, Триметрексат Глюкуронат, Тримексаутид, Тримидокс, Тровафлоксацин, Тровафлоксацин Гидрат, Тровафлоксацин Гидрохлорид Мезилат, Тровафлоксацин Мезилат, Троксацитабин, Трибизин Гидрохлорид, Тубастрин, Туфцин, Тиросерватид, Тирфостин 47, Убенимекс, Валацикловир, Валганцикловир Гидрохлорид, Валнемулин, Валомацикловир Стеарат, Валономицин А, Валопицитабин, Валпромид, Валросемид, Вамикамид, Ванкомицин Гидрохлорид, Ванкорезмицин, Вапитадин Гидрохлорид, Вареспладиб, Вареспладиб Метил, Вареспладиб Мофетил, Велнакрин Малеат, Венорфин, Вигабатрин, Вилазодон Гидрохлорид, Виндезин, Вирамидин Гидрохлорид, Виранамицин-В, Витамин В3, W Пептид, Ксемилофибан, Ксилоцидин, Занамивир, Зилеутон, Зонипорид Гидрохлорид, Зорубицин Гидрохлорид.
Подходящие биологически активные фрагменты, содержащие вторичный амин, могут быть выбраны из группы, состоящей из следующих представителей: (-)-3-О-Ацетилспекталин Гидрохлорид, (-)-3-О-трет-Вос-спекталин Гидрохлорид, (-)-Циклопролол, (-)-Норхлор-[18F]фтор-гомоэпибатидин, (-)-Салбутамол Гидрохлорид, (-)-Сальметерол, (+)-(S)-Гидроксихлорохин, (+)-Изамолтан, (+)-R-Прамипексол, (R)-(+)-Амлодипин, (R)-Клевидипин, (R)-NSP-307, (R)-Телудипин, (R)-Тионизоксетин, (S)-Клевидипин, (S)-N-Десметилтримебутин, (S)-Норемопамил, [99Тс]Демобезин 4, [Glu10, Nle17, Nle30]-Панкреатический полипептид(2-36), [Nle17, Nle30]-Панкреатический полипептид(2-36), [psi[CH2NH]Tpg4]Ванкомицин Агликон, 15bбeтa-Метоксиардеемин, 3-Бромметкатинон, 4,5-Дианилинофталимид, 4-Гидроксиатомоксетин, 5-Метилурапидил, 7-Оксостауроспорин, 99mTc-c(RGDfK*)2HYNIC, A-42867 псевдоагликон, Абакавир Сукцинат, Абакавир Сульфат, Абареликс, Акарбоза, Ацебутолол Гидрохлорид, Ацеклофенак, Ацилин, Адафостин, Адапролол Малеат, Адапролол оксалат, Адеципенол, Адроголид Гидрохлорид, Аглаястатин С, Алхемикс, Алинидин, Альказар-18, Алминопрофен, Алнидитан, альфа-Метилэпинефрин, Алпрафенон Гидрохлорид, Алпренолол Гидрохлорид, Алпреноксим Гидрохлорид, Альтромицин А, Альтромицин С, Алвеспимицин Гидрохлорид, Амброксол нитрат, Амфебутамон Гидрохлорид, Амибегрон Гидрохлорид, Амифостин Гидрат, Аминептин, Аминокандин, Аминохинол, Амтивир, Амлодипин, Амлодипин бесилат, Амокарзин, Амодиахин, Амозулалол Гидрохлорид, Амоксапин, Амсакрин, Анабазин Гидрохлорид, Анисперимус, Антид-1, Аранидипин, Арапрофен, Арбутамин Гидрохлорид, Ардеемин, Арформотерол Тартрат, Аргатробан моногидрат, Аргиопин, Аротинолол Гидрохлорид, Асперлицин Е, Атенолол, Атевирдин Мезилат, Азатиоприн, Азелнидипин, Азепиностатин, Баламапимод, Балхимицин, Балофлоксацин, Балофлоксацин дигидрат, Бамбутерол, Бамирастин Гидрат, Баноксантрон, Баогонгтенг А, Бариксибат, Барнидипин Гидрохлорид, Батопразин, Бацеллин А, Бацеллин В, Бацеллин С, Бекампанел, Бедероцин, Бедорадрин Сульфат, Бефунолол Гидрохлорид, Белактин В, Белотекан Гидрохлорид, Беназеприл Гидрохлорид, Бендрофлуметиазид, Бенидипин Гидрохлорид, Берлафенон Гидрохлорид, Бетаксолол Гидрохлорид, Бевантолол Гидрохлорид, Биэмнидин, Бифемелан Гидрохлорид, Биноспирон Мезилат, Биоксаломицин альфа 1, Бис(7)-когнитин, Бисантрен Гидрохлорид, Биснафид Мезилат, Бисопролол Фумарат, Битолтерол Мезилат, Блеомицин А2 Сульфат, Бохолмицин, Бопиндолол, Бозутиниб, Бриназарон, Бринзоламид, Булаквин, Буметанид, Бутеранол, Бутофилолол, Кадрофлоксацин Гидрохлорид, Калдарет Гидрат, Калиндол Дигидрохлорид, Капридин бета, Кармотерол Гидрохлорид, Картеолол Гидрохлорид, Карведилол, Каспофунгин Ацетат, Цефтаролин фозамил Ацетат, Цефтизоксим Натрия, Цефтобипрол, Целипролол Гидрохлорид, Цереброкраст, Церулетид диэтиламин, Цевипабулин, Хиноин-169, Хлорптоцин, Хлордиазэпоксид Гидрохлорид, Хлорориентицин А, Хлорориентицин В, Цилазарпил, Цилнидипин, Цилупревир, Циматерол, Цинакальцет Гидрохлорид, Циннамицин, Ципрофлоксацин Гидрохлорид, Ципрофлоксацина серебряная соль, Клевидипин бутират, Клитоцин, Клопенфендиоксан, Клоранолол Гидрохлорид, Клозапин, Конантокин-R, Конофиллин, Криснатол Мезилат, Кронидипин, Дабелотин Мезилат, Дабигатран, Дабигатран этексилат, Далбаванцин, Дапивирин, Дапроптерин Дигидрохлорид, Дасантафил, Дебромошермиламин, Декапланин, Дегареликс Ацетат, Делаприл Гидрохлорид, Делавирдин Мезилат, Делфапразин Гидрохлорид, Делуцемин Гидрохлорид, Деметилаллосамидин, Демексиптилин Гидрохлорид, Денопамин, Деоксиметилспергуалин, Деоксиспергуалин Гидрохлорид, Дезацетилвинблатсингидразид/фолат Конъюгат, Дезбутил бенфлуметол, Дезбутилгалофантрин Гидрохлорид, Десферри-сальмицин А, Десферри-сальмицин В, Десферри-сальмицин С, Десферри-сальмицин D, Дезипрамин Гидрохлорид, Дезлоратадин, Дексфенфлурамин Гидрохлорид, Декскетопрофен меглумин, Дексметилфенидат Гидрохлорид, Декснигулдипин Гидрохлорид, Декссоталол, Диазепиномицин, Дихлорбензоприм, Диклофенак калия, Диклофенак Натрия, Диклофенак цинковая соль, Диэтилнорспермин, Дигидрексидин, Дилевалол, Дилевалол Гидрохлорид, Динапсолин, Диноксилин, Дипивефрин Гидрохлорид, Дискодермид, Дискодермид Ацетат, Дискорабдин D, Дискорабдин Р, Дискорабдин S, Дискорабдин Т, Дискорабдин U, Добутамин Гидрохлорид, Добутамин Фосфат, Допексамин, Допексамин Гидрохлорид, Дорипенем, Дорзоламид Гидрохлорид, d-Псевдоэфедрин Гидрохлорид, Дроксинавир, Дулоксетин Гидрохлорид, Дуокармицин А, Дуокармицин В1, Дуокармицин В2, Дуокармицин С1, Дуокармицин С2, Динемицин А, Динемицин С, Эбаниклин, Эктеинасцидин 1560, Эктеинасцидин 722, Эктеинасцидин 729, Эктеинасцидин 736, Эктеинасцидин 745, Эктеинасцидин 770, Эктеинасцидин 875, Эфароксан, Эфегатран Сульфат Гидрат, Эфепристин, Эфонидипин Гидрохлорид этанол, Элаголикс Натрия, Эланзолид С1, Эларофибан, Элбанизин, Элгодипин Гидрохлорид, Элинафид Мезилат, Элиногрел калия, Элнадипин, Эналаприл Малеат, Эналаприл нитрат, Эналаприлат, Эназадрем, Энкастин (D), Энкастин (D), Энкастин (D), Энкастин AD, Энкастин АЕ, Энкастин ID, Энкастин IE, Энкастин VD, Энкастин VE, Эноксацин, Эпибатидин, Эпостатин, Эремомицин, Эрсентилид, Эрсентилид Гидрохлорид, Эртапенем Натрия, Эскулеогенин А, Эскулозид А, Эсмолол Гидрохлорид, Эсперамицин А1, Этамзилат, Этокси-идазоксан, Эугенодилол, Эзлопитант, Фалнидамол, Фарглитазар, Фасобегрон Гидрохлорид, Фасудил Гидрохлорид, Фелодипин, Фенолдопам Мезилат, Фенотерол Гидробромид, Фепрадинол, Ферроквин, Ферулинолол, Финафлоксацин Гидрохлорид, Флекаинид Ацетат, Флорбетабен, Флорбетапир F 18, Флуфеноксин, Флумезапин, Флуодипин, Флуоксетин Гидрохлорид, Флупароксан, Флупиртин Малеат, Фоэтидин 1, Фоэтидин 2, Фолиновая кислота, Формотерол Фумарат, Фородезин Гидрохлорид, Фосапрепитант димеглумин, Фозопамин, Фроватриптан, Фурнидипин, Фуросемид, Габоксадол, Гадобеновой кислоты димеглуминовая соль, Гадопентетат димеглумин, Гадотерат меглумин, Галактомицин I, Галактомицин II, Гареноксацин Мезилат, Гатифлоксацин, Гефитиниб, Глюкоаланомицин, Глутапирон, Госоглиптин Гидрохлорид, Грепафлоксацин Гидрохлорид, Гипсетин, Галофугинон Гидробромид, Гелвекардин А, Гелвекардин В, Эрквилин В, Гесперидин, Гимастатин, Гиспидоспермидин, Гомоэпибатидин, Гидрохлортиазид, Гидрофлуметиазид, Гидроксихлорохин Сульфат, Ибопамин, Идазоксан Гидрохлорид, Иганидипин Гидрохлорид, Имидаприл, Имидаприл Гидрохлорид, Имидазоакридинон, Имисопасем марганца, Иммепип, Иммепир, Инкадронат, Индакатерол, Индантадол Гидрохлорид, Инделоксазин Гидрохлорид, Индолмицин, Инотагран, Интоплицин, Иофетамин Гидрохлорид I-123, Иптакалим Гидрохлорид, Исавуконазониум хлорид Гидрохлорид, Изепамицин Сульфат, Изофагомин Тартрат, Изохин, Испрониклин, Исрадипин, Итуреликс, Каитоцефалин, Кетамин Гидрохлорид, Копсинин, Корупенсамин А, Корупенсамин В, Корупенсамин С, Козиностатин, Лабедипинедилол А, Лабедипинедилол В, Лабеталол Гидрохлорид, Лабрадимил, Лацидипин, Ладастен, Ладостигил Тартрат, Лагатид, Ландиолол, Лапатиниб дитозилат, Ленапенем Гидрохлорид, Ленапенем Гидрохлорид Гидрат, Лерисетрон, Лейковорин кальция, Левобетаксолол Гидрохлорид, Левобунолол Гидрохлорид, Леволейковорин кальция, Левонебиволол, Либломицин, Линапразан, Лизиноприл, Литоксетин, Лобензарит Натрия, Лодамин, Лофексидин Гидрохлорид, Ломефлоксацин Гидрохлорид, Лоркасерин, Лотрафибан, Ловирид, Лубазодон Гидрохлорид, Люмиракоксиб, Мабутерол Гидрохлорид, Макалувамин D, Макалувамин Е, Макалувамин F, Макалувон, Манидипин Гидрохлорид, Манифаксин Гидрохлорид, Манзамин В, Манзамин D, Мапротилин Гидрохлорид, Маропитант, Мазнидипин Гидрохлорид, Мекамиламин Гидрохлорид, Меклофенамат Натрия, Мефенамовая кислота, Мефлохин Гидрохлорид, Мелагатран, Мелоглиптин, Мелуадрин, Мелуадрин Тартрат, Мемоквин, Мепиндолол Сульфат, чрезкожный пластырь с Мепиндололом, Меропенем, Метамфетамин Гидрохлорид, Метоктрамин, Метилклотиазид, Метилгистапродифен, Метилфенидат Гидрохлорид, Метипранолол, Метолазон, Метопролол Фумарат, Метопролол Сукцинат, Метопролол Тартрат, Мезакоприд, Мичеламин В, Микроцин J25, Микрономицин Сульфат, Мидафотел, Милацемид-[2Н], Минаприн Гидрохлорид, Мирабегрон, Митомицин, Митоксантрон Гидрохлорид, Мивобулин изетионат, Модипафант, Моэксиприл Гидрохлорид, Моэксиприлат, Монтирелин тетрагидрат, Моранолин, Мотесаниб дифосфат, Моксифлоксацин Гидрохлорид, Моксонидин Гидрохлорид Гидрат, Мураминомицин I, Муреидомицин Е, Муреидомицин F, Муреидомицины, N1,N8-Биснорцимсерин, Надолол, Напроксен пиперазин, Напсамицин А, Напсамицин В, Напсамицин С, Напсамицин D, Нардетерол, N-деметилированный силденафил, Небиволол, Немонаприд, Неомицин-акридин, Нератиниб, Нетилмицин Сульфат, Никардипин Гидрохлорид, Нифедепин, Нифекалант Гидрохлорид, Нигулдипин Гидрохлорид, Нилвадипин, Нимодипин, Нипрадилол, Нисолдипин, Нитракрин Дигидрохлорид Гидрат, Нитрендипин, Нитрофенак, Нитрозо-нифедипин, Ноберастин, Ноберастин цитрат, NO-ципрофлоксацин, N-Октил-бета-валиенамин, Ноломирол Гидрохлорид, Норфлоксацин, Норсеголин, Нортопиксантрон Гидрохлорид, Нортиптилин Гидрохлорид, N-трет-бутилизохин, Оберадилол, Оберадилол моноэтилмалеат, Оданакатиб, Оланзапин, Оланзапин памоат, Олрадипин Гидрохлорид, Онтазоласт, ОРС-17083, Орбифлоксацин, Орципреналин сульфат, Ориентицин А, Ориентицин В, Ориентицин С, Оритаванцин, Осемозотан Гидрохлорид, Осутидин, Отенабант Гидрохлорид, Овотиол В, Окспренолол Гидрохлорид, Озеноксацин, Пафенолол, Палау-амин, Палиндор Фумарат, Панобиностат, Пародилол гемифумарат, Парогрелил Гидрохлорид, Пароксетин, Пароксетин аскорбат, Пароксетин камзилат, Пароксетин Гидрохлорид, Пароксетин Мезилат, Пазеллиптин тригидрохлорид, Пазеллиптин тригидрохлорид моногидрат, Пелитиниб, Пелитрексол, Пенбутолол Сульфат, Пентостатин, Пепломицин, Периндоприл, Перцинфотел, Фендиоксан, Пибутидин Гидрохлорид, Пикуметерол Фумарат, Пиндолол, Пирбутерол Гидрохлорид, Pittsburgh Compound В, Пиксантрон Малеат, Плериксафор Гидрохлорид, Полиглутамат камптотецин, Позаниклин Гидрохлорид, Прадимицин А, Прадимицин В, Прадимицин D, Прадимицин FA-1, Прадимицин FL, Прадимицин FS, Прадимицин L, Прадимицин S, Прадофлоксацин, Прамипексол Гидрохлорид, Пранедипин Тартрат, Пранедипин, Префолик А, Премафлоксацин, Премафлоксацин Гидрохлорид, Премафлоксацин магния, Примахин Фосфат, Призотинол, Прокатерол Гидрохлорид Гемигидрат, Пропафенон Гидрохлорид, Пропранолол Гидрохлорид, Протриптилин Гидрохлорид, Проксодолол, Пумапразол, Пириндамицин А, Пириндамицин В, Хинаприл Гидрохлорид, Хинпрамин, рац-Дебромфлустрамин Е, Радезолид, Рафабегрон, Ралфинамид, Рамиприл, Расагилин Мезилат, Разупенем, Ребоксетин Мезилат, Репинотан, Репинотан Гидрохлорид, Репротерол Гидрохлорид, Ретаспимицин Гидрохлорид, Ретигабин Гидрохлорид, Родострептомицин А, Родострептомицин В, Рифабутин, Рилменидин дигидрофосфат, Римотерол Гидробромид, Ризотилид, Риваниклин, Робенакоксиб, Ролапитант Гидрохлорид, Сафинамид Мезилат, Сагандипин, Салбостатин, Салбутамол нитрат, Салбутамол Сульфат, Сальматерол, Сальметерол ксинафоат, Саризотан Гидрохлорид, Сауссурамин С, Сазетидин-А, Селоденосон, Сертралин, Сертралин Гидрохлорид, Сетазиндол, Сезоламид Гидрохлорид, Шишиймицин А, Шишиймицин В, Шишиймицин С, Сибаномицин, Сибенадет Гидрохлорид, Силодозин, Ситамахин Гидрохлорид, Сивелестат Натрия Гидрат, Софиниклин, Солабегрон Гидрохлорид, Солпекаинол Гидрохлорид, Сорапразан, Соталол Гидрохлорид, Спарфлоксацин, Спермин диальдегид, Спираприл, Спирохиназолин, Скваламин Лактат, Стрептомицин, Стрессин1-А, Суманирол Малеат, Супрофенак 1, Супрофенак 2, Супрофенак 3, Суфронакрин Малеат, Тафамидис меглумин, Тафенохин Сукцинат, Таларозол, Талибегрон, Талибегрон Гидрохлорид, Талнифлумат, Талотрексин, Талтобулин, Талудипин Гидрохлорид, Тамсулозин Гидрохлорид, Танеспимицин, Таногитран, Тауропирон, Тазопсин, Текалцет Гидрохлорид, Текастемизол, Технеций (99mTc) апцитид, Технеций (99mTc) бицизат, Телатиниб, Телаванцин Гидрохлорид, Темакразин Мезилат, Темафлоксацин Гидрохлорид, Темокаприл Гидрохлорид, Тербуталин Сульфат, Теродилин Гидрохлорид, Тертатолол Гидрохлорид, Тетракаин Гидрохлорид, Тетрагидродерцитин 1, Тетриндол, Тезампанел, Тиамет-G, Тиофедрин, Тиамдипин, Тиаменидин, Тианептин Натрия, Тиапафант, Тиеноксолол Гидрохлорид, Тигециклин, Тилизолол Гидрохлорид, Тимолол гемигидрат, Тимолол Малеат, Тиназолин гидрохлорид, Тирофибан Гидрохлорид, Тизанидин Гидрохлорид, Тоборинон, Толфенамовая кислота, Томатин, Томоксетин Гидрохлорид, Топиксантрон Гидрохлорид, Торасемид, Трабектедин, Трандолаприл, Трандолаприлат, Трантинтерол Гидрохлорид, Трепростинил диэтаноламин, Тресперимус трифлутат, Триацетил динемицин С, Триентин Гидрохлорид, Трифлупроксим, Триметазидин, Триметрексат глюкуронат, Тромбодипин, Троксипид, Тулатромицин А, Тулатромицин В, Тулобутерол Гидрохлорид, Уфенамат, Улифлоксацин, Улиморелин, Унциаламицин, Урапидил, Утибаприл, Утибаприлат, Вабикасерин Гидрохлорид, Ванкомицин Гидрохлорид, Вандетаниб, Ванидипинедилол, Ванинолол, Вапитадин Гидрохлорид, Варениклин Тартрат, Варлитиниб, Ваталаниб Сукцинат, Ватанидипин, Ватанидипин Гидрохлорид, Вестипитант Мезилат, Виценистатин, Вилдаглиптин, Вилоксазин Гидрохлорид, Вофопитант Гидрохлорид, Воглибоз, Ворелоксин, Ксамотерол Фумарат, Ксимелагатран, Иттрий-90 эдотреотид, Забициприл Гидрохлорид, Забициприлат Гидрохлорид (), Забофлоксацин Гидрохлорид, Занапезил Фумарат, Зеландопам Гидрохлорид, Зилпатерол, Золмитриптан.
Подходящие амин-содержащие биологически активные фрагменты могут также быть выбраны из группы, состоящей из следующих представителей: Fab (фрагмент, связывающийся с антигеном), F(ab)2 фрагменты, Fc (фрагмент, кристаллизующийся), pFc' фрагмент, Fv (фрагмент, варьирующийся), scFv (одноцепочечный варьирующийся фрагмент), di-scFv/diabodies, би-специфический активатор Т-клеток, CDR (определяющие комплементарность области), однодоменные антитела (sdABs/нанотела), тяжелые цепи (α, δ, ε, γ, μ) или фрагменты тяжелых цепей, легкие цепи (λ, κ) или фрагменты легких цепей, VH фрагменты (вариабельный участок тяжелой цепи), VL фрагменты (вариабельный участок легкой цепи), VHH фрагменты, VNAR фрагменты, фрагменты антител акулы и аффинные каркасные белки, аффинные каркасные белки на основе домена Куница, центириновые аффинные каркасные белки, убиквитиновые аффинные каркасные белки, липокалиновые аффинные каркасные белки, анкириновые аффинные каркасные белки, Versabodies (обогащенные дисульфидными фрагментами аффинные каркасные белки), фибронектиновые аффинные каркасные белки, камелоидные фрагменты антител и аффинные каркасные белки, лламовые фрагменты антител и аффинные каркасные белки, трансферриновые аффинные каркасные белки, Squash-type ингибиторы протеаз Squash-типа с имеющими цистеиновый узел скаффолдными аффинными каркасными белками.
Подходящие лекарства, содержащие ароматические гидроксильные группы, представляют собой, напрмиер, (-)-цис-Резорциклид, (-)-Индокарбазостатин В, (-)-Сальметерол, (-)-Субериновая кислота, (+)-альфа-Виниферин, (+)-Эторфин, (+)-Индокарбазостатин, (+)-SCH-351448, (R)-Госсипол, (S)-(+)-Куркуфенол, (S)-Метилналтрексон бромид, [8]-Джинджерол, [Arg(Me)9] MS-10, [D-Tyr1,Arg(Ме)9] MS-10, [D-Tyr1,AzaGly7,Arg(Me)9] MS-10, [D-Tyr1] MS-10, [psi[CH2NH]Tpg4]Ванкомицин Агликон, [Trp19] MS-10, 13-Деоксиадриамицин Гидрохлорид, 14-Метоксиметопон, 14-Фенилпропоксиметопон, 18,19-Дегидробупренорфин Гидрохлорид, 2,12-Диметилевротинон, 2'-Гидроксиматтеуценол, 2-метоксиэстрадиол, 2-Метилевротинон, 3,5-Дикаффеоилхиновая кислота, 3-Бромдиосметин, 3-Бромдиосмин, 3-Хлордиосметин, 3-Хлордиосмин, 4',7,8-Тригидроксиизофлавон, 4-Аминосалициловая кислота, 4-Гидроксиатомоксетин, 4-Йодпропофол, 5-Йодфредерикамицин A, 5Z-7-Оксозеаенол, 6-Карбоксигенистеин, 6-O-mPEG4-Налбуфин, 6-O-mPEG5-Налбуфин, 7-Метилкапилларизин, 8(R)-Фторидарубицин Гидрохлорид, 8',9'-Дегидроаскохлорин, 8-Карбокси-изо-иантеран А, 8-парадол, 8-Пренилапигенин, 8-Прениларингенин, 9-Гидроксикрисамицин А, А-42867 псевдоагликон, Абареликс, Акацетин, Акларубицин, Аколбифен Гидрохлорид, Акотиамид Гидрохлорид Гидрат, Акровестон, Актинопланон А, Актинопланон В, Акулеацин Агамма, Адафостин, Адаротен, Адксантромицин А, Аэротрицин 1, Аэротрицин 16, Аэротрицин 41, Аэротрицин 45, Аэротрицин 50, Аэротрицин 55, Аюлемовая кислота, Алхемикс, Алдифен, альфа-Мангостин, альфа-Метилэпинефрин, альфа-Метилнорэпинефрин, Альфа-Пелтатин, Алтромицин А, Алтромицин В, Алтромицин С, Алтромицин D, Алтромицины, Апвимопан Гидрат, Альвоцидиб Гидрохлорид, Амамистатин А, Амамистатин В, Амарогентин, Амелубант, Амидокс, Аминокандин, Амодиахин, Амоксициллин тригидрат, Амрубицин Гидрохлорид, Амурензин Н, Ангиллоспорал, Анидулафунгин, Анкиномицин, Аннамицин, Аннулин С, Антимицин А11, Антимицин А12, Антимицин А13, Антимицин А14, Антимицин А15, Антимицин А16, Апикуларен А, Апикуларен В, Апигенин, Апомин, Ароморфин Гидрохлорид, Арбидол, Арбутамин Гидрохлорид, Арформотерол Тартрат, Артепиллин С, Арзоксифен Гидрохлорид, Аспоксициллин, Аталафиллидин, Аталафиллинин, Атраровая кислота, Аворелин, Акситиром, Азарезвератрол, Азатоксин, Азепиностатин, Байкалеин, Байкалин, Балхимицин, Балсалазид динатрия, Баноксантрон, Базедоксифен Ацетат, Базедоксифен Гидрохлорид, Бедорадрин Сульфат, Бенадростин, Бенаномицин А, Бенаномицин В, Бенастатин А, Бенастатин В, Бенастатин С, Бенастатин D, Бензбромарон, Берефрин, Берупипам Малеат, бета-Мангостин, Биемнидин, Биоханин А, Биоксаломицин альфа 1, Биоксаломицин альфа2, Субсалицилат висмута, Бисфенол, Бикс, Бизелесин, Богорол А, Брандисианин А, Брандисианин В, Брандисианин С, Бразиликардин А, Бревифолин карбоновая кислота, Брейнин А, Брейнин В, Бромтопсентин, Буфломедил пиридоксалфосфат, Бупренорфин Гидрохлорид, Бусерелин Ацетат, Бутеин, Бутеранол, Буторфан, Буторфанол Тартрат, Калебин А, Калокумарин А, Калопорозид D, Калопорозид Е, Калопорозид F, Калфостин А, Калфостин В, Калфостин С, Калфостин D, Калфостин I, Капилларизин, Капсазепин, Карбазомадурин А, Карбазомадурин В, Карбетоцин, Карбидопа, Кармотерол Гидрохлорид, Каспофунгин Ацетат, Кассигалол А, Цефетекол, Цефоперазон Натрия, Цефпирамид Натрия, Цефпрозил, Цефпрозил моногидрат, Цетрореликс Ацетат, Хетоатрозин А, Хафурозид, Хлорориентицин А, Хлорориентицин В, Хондрамид А, Хондрамид В, Хондрамид С, Циннатриацетин А, Циннатриацетин В, цис-6-Шогаол, Цитпрессин I, Цитреамицин-Альфа, Цитреамицин-эта, Цитрусинин-I, Клаусенамин А, Комбретастатин А-1, Комбретастатин А-2, Комбретастатин А-3, Комбретастатин В-1, Комбретастатин В-2, Комбретастатин В-3, Комбретастатин В-4, Комбретастатин D-1, Комбретастатин D-2, Комплестатин, Конифероовый спирт, Конофиллин, Коринекандин, Козалан, Крисамицин С, Кробенетин, Кробенетин Гидрохлорид, Куртизиан А, Куртизиан В, Куртизиан D, Цианидин Хлорид Моногидрат, Циклокоммунол, Циклопропарадицикол, Циклотеонамид А, Циклотиалидин, Циртоминетин, Цитогенин, Цитоспорон В, Цитотриенин I, Цитотриенин II, Дактилоциклин А, Дактилоциклин В, Даларгин, Далбаванцин, Дамунакантал, Дафнодорин А, Дафнодорин В, Дафнодорин С ((-)-энантиомер), Дарбуфелон, Дарбуфелон Мезилат, Даунорубицин, Даурихроменовая кислота, Давидигенин, Деацетил Моксисилит Гидрохлорид, Декапланин, Децил галлат, Деферазирокс, Дегидрозингерон, Дельфинидин, Денопамин, Деоксимуландокандин, Дерсалазин, Дезацетилравидомицин N-оксид, Дезглугастрин трометамин, Деслорелин, Десмопрессин Ацетат, Дезвенлафаксин Сукцинат, Дексанабинол, Декстрорфан, Дексилозилбенаномицин А, D-Флувиабактин, Диазафилоновая кислота, Диазепиномицин, Диэкол, Дифлунизал, Дигидрексидин, Дигидроавенантрамид D, Дигидрогранатацин В, Дигидрохонокиол В, Дигидроралоксифен, Дилевалол, Дилевалол Гидрохлорид, Динапсолин, Диноксилин, Дионкохинон А, Дионкохинон В, Дикалия Госсиполат, Добутамин Гидрохлорид, Добутамин Фосфат, Допексамин, Допексамин Гидрохлорид, Досмалфат, Доксорубицин Гидрохлорид, Доксорубицин, Морфолинил, ДоксоТам 12, Доксициклин гиклат, Дронабинол, Дроксидопа, Дуокармицин В1, Дуокармицин В2, Дуокармицин С1, Дуокармицин С2, Дутомицин, Динемицин А, Динемицин С, Эконазол Сульфосалицилат, Экопипам, Эктеинасцидин 1560, Эктеинасцидин 722, Эктеинасцидин 729, Эктеинасцидин 736, Эктеинасцидин 745, Эктеинасцидин 757, Эктеинасцидин 770, Эктеинасцидин 875, Эдотекарин, Эдотреотид иттрия, Эфлуцимиб, Эфлумаст, Эланзолид С1, Элдацимиб, Эллаговая кислота-4-галлат, Эллиптиниум Ацетат, Элсибукол, Элтромбопаголамин, Эмодин, Эназадрем, Энофеласт, Энтакарпон, энт-Эстриол, Эпидоксоформ, Эпигаллокатехин-3-галлат, Эпирубицин Гидрохлорид, Эпливансерин, Эпливансерин Фумарат, Эпливансерин Мезилат, Эпокарбазолин А, Эпокарбазолин В, Эпротиром, Эптазоцин Гидробромид, Эрабуленол А, Эрабуленол В, Эремомицин, Эстетрол, Эстрадиол, Эстриол, Эталоциб Натрия, Этамзилат, Этинилэстрадиол, Этилгаллат, Этопозид, Еуротинон, Эуксантон, Эвернимицин, Эксифон, Эзетимиб, Фадолмидин Гидрохлорид, Феглимицин, Фенолдопам Мезилат, Фенотерол Гидробромид, Фидаксомицин, Фидексабан, Флуостатин А, Флуостатин В, Фоэтидин 1, Фоэтидин 2, Фолипастатин, Формобактин, Формотерол Фумарат, Фозопамин, Фредерин, Фулвестрант, Фурахиноцин А, Фурахиноцин В, Фузакандин А, Фузакандин В, Фузидиенол, Галактомицин I, Галактомицин II, Галарубицин Гидрохлорид, Галоцитабин, Гамбоговая кислота, гамма-Мангостин, гамма-Токотриенол, Ганиреликс, Ганиреликс Ацетат, Гарвалон С, Гарвеатин Е, Гарвеатин F, Генистеин-7-Фосфат, Гигантол, Гилвусмицин, Глюкопиерицидинол А1, Глюкопиерицидинол А2, Глюдопа, Гликотиогексид альфа, Госерелин, Гранатицин В, Гризеусин С, Хатомарубигин А, Хатомарубигин В, Хатомарубигин С, Хатомарубигин D, Хаюмицин А, Хаюмицин В, Хаюмицин С1, Хаюмицин С2, Хаюмицин D, Хеликвиномицин, Гелвекардин А, Гелвекардин В, Герицинал А, Герицинал В, Герицинал С, Гидросмин, Гистрелин, Гистрелин Ацетат, Хонгокверцин А, Хонгокверцин В, Хонокиол диэпоксид, Хонокиол диэпоксид, Человеческий ангиотензин II, Гидроморфон метиодид, Гименистатин 1, Гипептин, Гиперицин, Гиперозид, Икариин, Идарубицин Гидрохлорид, Идроноксил, Ифенпродил, Имидазоакридинон, Инциклинид, Индакатерол, Инданоцин, Интеграции А, Интеграцин В, Интеграции С, Интеграмицин, Интеграстатин А, Интеграстатин В, Интоплицин, Иодосхлоргидроксихин, Йододифлунисал, Иодорубидазон (р), Иолоприд (123I), Иоксиприд, Иралукаст, Иралукаст Натрия, Ирциниастатин А, Ирциниастатин В, Исалмадол, Изобавахалькон, Изодоксорубицин, Изо-иантеран А, Изоликвиритигенин, Изомолпан Гидрохлорид, Изохин, Изованихуперцин А, Ядомицин В, Джасплакинолид, Кадсуфилин С, Каитоцефалин, Кампанол А, Кампанол В, Канглемицин А, Капуримицин А1, Капуримицин A3, Капуримицин A3, Кехокорин D, Кехокорин Е, Кигамицин А, Кигамицин В, Кигамицин С, Кигамицин D, Кигамицин Е, Кигамициноп, Кистамицин А, Клаинетин А, Клаинетин В, Кодаистатин А, Кодаистатин В, Кодаистатин С, Кодаистатин D, Корупенсамин А, Корупенсамин В, Корупенсамин С, Корупенсамин D, Козиностатин, Лабеталол Гидрохлорид, Лаккаридион А, Лактонамицин, Лактосилфенил тролокс, Ладирубицин, Ламелларин альфа 20-Сульфата Натриевая соль, Ламифибан, Ланреотид Ацетат, Лазофоксифен, Лазофоксифен Тартрат, Латамоксеф Натрия, L-Цикориевая кислота, L-Допамид, Лецирелин, Ледазерол, Левпролид Ацетат, Леврубицин, Левалбутерол Гидрохлорид, Леводопа, Леводопа 3-O-глюкозид, Леводопа 4-O-глюкозид, Леворфанол Тартрат, L-Флувиабактин, Липиармицин В3, Липиармицин В4, Ликвиритин апиозид, Литоспермовой кислоты В магниевая соль, Лобатамид С, Лобатамид F, Лолоатин В, Люминиацин D, Лутеолин, Макрокарпин А, Макрокарпин В, Макалувамин D, Макалувамин Е, Малонобен, Малтолил п-кумарат, Маннопептимицин бета, Манзамин F, Маринопиррол А, Мармелин, Масопрокол, Мастпром, Маттеуориента А, Маттеуориенат В, Маттеуориенат С, Медикарпин, Мелеводопа Гидрохлорид, Меллеин, Мелуадрин, Мелуадрин Тартрат, Мемно-пептид А, Мептазинол Гидрохлорид, Месалазин, Метараминол, Метанобактин, Метил галлат, Метилдопа, Метилнатрексон бромид, Метирозин, Микакоцидин А, Микакоцидин В, Микафунгин Натрия, Мичелламин В, Мидепланин, Мимопезил, Миноциклин Гидрохлорид, Мипроксифен, Митоксантрон Гидрохлорид, Мивазерол, Модекаинид, Моллугин, Моногидроксиэтилрутозид, Морфин Глюкуронид, Морфин Гидрохлорид, Морфин Сульфат, Моксифетин Гидромалеат, Мумбаистатин, Муреидомицин А, Муреидомицин В, Муреидомицин С, Муреидомицин D, Муреидомицин Е, Муреидомицин F, Муреидомицин, Микофенолят Мофетил, Микофеноловой кислоты натриевая соль, Мирциацитрин I, Мирциацитрин II, Мирциафенон В, Мирицеровая кислота А, Митолбилин, Митолбилиновая кислота, Митолбилиновой кислоты метиловый эфир, Митолбилинол, Наамидин А, Набилон, N-Ацетилколхинол, Нафарелин Ацетат, Налбуфин Гидрохлорид, Налфурафин Гидрохлорид, N-Аллилсекоболдин, Налмефен, Налоксон Гидрохлорид, Налтрексон Гидрохлорид, Налтриндол, Напсамицин А, Напсамицин В, Напсамицин С, Напсамицин D, Нардетерол, N-Циклопентил-тазопсин, Небикапон, Нелфинавир Мезилат, Неморубицин, Непаренсинол А, Непаренсинол В, Непаренсинол С, Нерфилин I, Никанартин, Нитекапон, Нокардион А, Нокатиацин I, Нокатиацин III, Нокатиацин IV, NO-Месаламин, Нордамунаканталь, Ностоциклопептид М1, Нотрамицин, N-трет-бутилизохин, Обелмицин Н, Охромицинон, Октил галлат, Одапипам Ацетат, O-Деметилхлортрицин, O-Деметилмюррейафалин А, Энотеин В, Окиценон, Оланзапин памоат, Олцегепант, Олсалазин Натрия, Онжиксантон I, Онжиксантон II, Оолонгомобисфлаван А, Оолонгомобисфлаван С, Орципреналин сульфат, Ориентицин А, Ориентицин В, Ориентицин С, Ориентицин D, Оритаванцин, Орниплабин, Ортосомицин А, Ортосомицин В, Ортосомицин С, Ортосомицин D, Ортосомицин Е, Ортосомицин F, Ортосомицин G, Ортосомицин Н, Осутидин, Оксимидин III, Оксиметазолин Гидрохлорид, Оксиморфазол Дигидрохлорид, Оксиморфон Гидрохлорид, Оксифенарсин, Озареликс, Пецилохинин А, Пецилохинин D, Пецилохинон В, Пецилохинон D, Панкратистатин-3,4-Циклического фосфата натриевая соль, Паннорин, Папуамид А, Папуамид В, Папуамид С, Папуамид D, Парацетамол, Парвиспорин В, PEG-ванкомицин, Пенициллид, Пентазоцин Гидрохлорид, Пептициннамин Е, Фаффиаол, Факеллистатин 7, Факеллистатин 8, Факеллистатин 9, Фенохалазин А, Фентоламин Мезилат, Флорофукофуроэкол, Фомопсихалазин, Фталасцидин, Физостигмин салицилат, Пицеатаннол, Пидобензон, Пиноцембрин, Пипендоксифен, Пирарубицин, Pittsburgh Compound В, Платенцин, Платенсимицин, Плурафлавин А, Плурафлавин В, Плурафлавин Е, Пневмокандин А0, Пневмокандин В0, Пневмокандин В0 2-Фосфат, Пневмокандин D0, Полиэстрадиол Фосфат, Поликетомицин, Попологуанон Е, Прадимицин А, Прадимицин В, Прадимицин D, Прадимицин Е, Прадимицин FA-1, Прадимицин FA-2, Прадимицин FL, Прадимицин FS ((+)-энантиомер), Прадимицин L, Прадимицин Q, Прадимицин S, Прадимицин Т1, Прадимицин Т2, Принаберел, Пробукол, Прокатерол Гидрохлорид Гемигидрат, Пропофол, Пропил галлат, Протокатеховая кислота, Протокатеховый альдегид, Псевдогиперицин, Пурпуромицин, Пириндамицин А, Пириндамицин В, Кверцетин-3-О-Метиловый эфир, Квинаголид Гидрохлорид, Хинобен, рац-Апогоссиполон, рац-Толтеродин, Ралоксифен Гидрохлорид, Рамопланин А'1, Рамопланин А'2, Рамопланин А'3, Рамореликс, Равидомицин N-оксид, Равсонол, Ребластатин, Репротерол Гидрохлорид, Резобен, Резортиомицин, Ретаспимицин Гидрохлорид, Родиоцианозид В, Рододаурихромановая кислота А, Рифабутин, Рифалазил, Рифамексил, Рифампицин, Рифапентин, Рифаксимин, Римотерол Гидробромид, Риодоксол, Рогитукин, Ротигаптид, Ротиготин, Роксиндол Мезилат, Рубоксил, Руфигаллол, Румицин 1, Румицин 2, Руссуфелин А, Сабарубицин Гидрохлорид, Саинтопин, Саинтопин Е, Сакиомицин А, Сакиомицин Е, Салазопиридазин, Салбутамол нитрат, Салбутамол Сульфат, Салкапрозовой кислоты натриевая соль, Салицилазобензойная кислота, Салицилгаламид А, Салицилгаламид В, Салифенилгаламид, Сальматерол, Сальметерол ксинафоат, Салоксин, Сальвианоловая кислота L, Сампатрилат, Санглифехрин А, Санглифехрин В, Санглифехрин С, Санглифехрин D, Саптомицин D, Сапуримицин, Сарикандин, Секоизоларицирезинол диглюкозид, Сеглитид, Семорфон Гидрохлорид, Шишийимицин А, Шишийимицин В, Шишийимицин С, Сибенадет Гидрохлорид, Силихристин, Синоменин, Сивифен, Сивенмицин, Соотепенсеон, Спинорфин, Спиносульфат А, Спиносульфат В, Спироксимицин, Стахибоцин А, Стахибоцин В, Стахибоцин С, Стахиботрин С, Стахиботридиаль, Стаплабин, Стеренин А, Стеренин С, Стеренин D, Стрептопиррол, Сукцинобукол, Сульфасалазин, Сульфазоцин, Сусалимод, Симбиоимин, Сириакузин А, Сириакузин В, Сириакузин С, Тагефлар, Тайваньгомофлавон А, ТАР-доксорубицин, Тапентадол Гидрохлорид, Тараманон А, Тазофелон, Тазопсин, Тебуфелон, Технеций Tc 99m депреотид, Тейкопланин-А2-1, Тейкопланин-А2-2, Тейкопланин-А2-3, Тейкопланин-А2-3, Тейкопланин-А2-5, Телаванцин Гидрохлорид, Темопорфин, Тенипозид, Тенуифолизид А, Тенуифолизид В, Тенуифолизид С, Тербуталин Сульфат, Терпренин, Тетрациклин Гидрохлорид, Тетрагаллоилхиновая кислота, Тетрагидрокуркумин, Тетрагидроэхинокандин В, Тетрагидросвертианолин, Тенорфин, Теофиллин рутозид, Тиазинотриеномицин В, Тиазинотриеномицин F, Тиазинотриеномицин G, Тиелавин G, Тиелоцин В3, Тимопентин, Тигециклин, Типелукаст, Токотриенол, Токарамид А, Толкапон, Толтеродин Тартрат, Топотекан Ацетат, Топотекан Гидрохлорид, Топсентин В1, Трабектедин, транс-Ресвератрол, Траксопродил, Траксопродил Мезилат, Тримидокс, Трифендиол, Троглитазон, Тубастрин, Тубулизин А, Тубулизин В, Тубулизин С, Тукаресол, Тиропептин А10, Тиропептин А6, Тиропептин А9, Тиросерватид, Тирфостин 47, Ункариновая кислота А, Ункариновая кислота В, Унциаламицин, Валрубицин, Ванкомицин Гидрохлорид, Вейнамитол, Венорфин, Вертициллатин, Вексибинол, Виалинин В, Винаксантон, W Пептид, Видендиол А, Видендиол В, Вудуриен, Ксамотерол Фумарат, Ксантоангелол Е, Ксантофалвин, Ксантомегнин, Ксипамид, Ятакемицин, Зеландопам Гидрохлорид, Зорубицин Гидрохлорид.
Подходящие лекарственные средства с гидроксильной группой могут быть выбраны из группы, состоящей из следующих представителей: (-)-(2R*,3R*,11bS*)-Дигидротетрабеназин, (-)-(2R*,3S*,11bR*)-Дигидротетрабеназин, (-)-2-(2-Бромгексадеканоил)паклитаксел, (-)-4',5'-Дидеметоксипикроподофиллин, (-)-4'-Деметоксипикроподофиллин, (-)-9-Дегидрогалантаминия бромид, (-)-Калихемицинон, (-)-Циклопролол, (-)-цис-Резорцилид, (-)-Индокарбазостатин В, (-)-Кендомицин, (-)-Колавенол, (-)-Сальметерол, (-)-Субериновая кислота, (+)-(2R*,3R*,11bS*)-Дигидротетрабеназин, (+)-(2R*,3S*,11bR*)-Дигидротетрабеназин, (+)-(S)-Гидроксихлорохин, (+)-23,24-Дигидродискодермолид, (+)-Алмугептолид А, (+)-альфа-Виниферин, (+)-Азакаланолид А, (+)-Дигидрокаланолид А, (+)-Эторфин, (+)-Индокарбазостатин, (+)-Изамолтан, (+)-SCH-351448, (+)-Соталол, (Е)-п-Кумароилхиновая кислота, (R)-Алмокалант, (R)-Диксиразин Дигидрохлорид, (R)-Госсипол, (R)-Сульфинозин, (S)-(+)-Куркуфенол, (S)-Алмокалант, (S)-Метилналтрексон бромид, (S)-Оксирацетам, (S)-Сульфинозин, (Z)-Инденапрост, [8]-Джинджерол, [Arg(Me)9] MS-10, [D-Tyr1,Arg(Ме)9] MS-10, [D-Tyr1,AzaGly7,Arg(Me)9] MS-10, [D-Tyr1] MS-10, [N-MeIle4]-циклоспорин, [psi[CH2NH]Tpg4]Ванкомицин Агликон, [Trp19] MS-10, 111ln-Пентетреотид, 11-Гидроксиэпотилон D, 11-Кето-Бета-Босвелловая Кислота, 13-Деоксиадриамицин Гидрохлорид, 14альфа-Липоил андрографолид, 14бета-Гидроксидоцетаксел-1,14-ацетонид, 14бета-Гидрокситаксотер, 14-Деметилмикотицин А, 14-Гидроксикларитромицин, 14-Изобутаноиландрографолид, 14-Метоксиметопон, 14-Фенилпропоксиметопон, 14-Пивалоиландрографолид, 15-Метилэпотилон В, 16-Метилоксазоломицин, 17-Аминогелданамицин, 17бета-Гидроксивортманнин, 18,19-Дегидробупренорфин Гидрохлорид, 18-Гидроксикоронаридин, 19-O-Деметилсцитофицин С, 19-O-Метилгелданамицин, 1альфа,25-Дигидроксивитамин D3-23,26-лактон, 1альфа-Гидроксивитамин D4, 1-Оксорапамицин, 2,12-Диметилеуротинон, 21-Аминоэпотилон В, 22-Ен-25-оксавитамин D, 22-Оксакальцитриол, 24(S)-Окотиллол, 24-Деоксиаскомицин, 25-Ангидроцимигенол-3-O-бета-D-ксилопиранозид, 26-Фторэпотилон, 2-Аминоаристеромицин, 2-Аминонепланоцин А, 2'-Гидроксиматтеуцинол, 2-Метоксиэстрадиол, 2-Метилэуротинон, 2'-Пальмитоилпаклитаксел, 3,5-Дикаффеоилхиновая кислота, 3,7а-Диэпиалексин, 36-Дигидроизороллиниастатин 1, 3- Аллилфарнезол, 3-Бромдиосметин, 3-Бромдиосмин, 3-Хлордиосметин, 3-Хлордиосмин, 3-Деазааденозин, 3-Эпимаксакальцитол, 4,6-диен-Cer, 4',7,8-Тригидроксиизофлавон, 41-Деметилгомоолигомицин В, 44-Гомоолигомицин В, 4-Аминосалициловая кислота, 4-Хлорфенилтио-DADMe-Иммуциллин-А, 4-Деметилэпотилон В, 4-Деметилпенкломедин. 4'-Этинилставудин, 4-Гидроксиатомоксетин, 4''-Гидроксимевастатин лактон, 4-Иодопропофол, 5(R)-Гидрокситриптолид, 5,4'-Диэпиарбрекацин, 5,6-Дегидроаскомицин, 5'-Эпиэквизетин, 5-Этилтиорибоза, 5-Йодфредерикамицин А, 5-N-Ацетил-15bальфа-гидроксиардеэмин, 5-Фенилтиоациклоуридин, 5-Тиаэпотилон, 5Z-7-Оксозеаенол, 6альфа-7-Эпипаклитаксел, 6альфа-Фторурсодеоксихолевая кислота, 6-Карбоксигенистеин, 6'-Гомонепланоцин А, 6-Гидроксисцитофицин В, 6-O-mPEG4-Налбупин, 6-O-mPEG5-Налбуфин, 7,7а-Диэпиалексин, 7-Хлоркинуреновая кислота, 7-Деокситаксол, 7-Метилкапилларизин, 8(R)-Фторидарубицин Гидрохлорид, 8',9'-Дегидроаскохлорин, 8-Карбокси-изо-иантеран А, 8-Парадол, 8-Пренилапигенин, 8-Прениларингенин, 9,11-Дегидрокортексолон 17альфа-бутират, 9,9-Дигидротаксол, 9-[18F]Фторпропил-(+)-дигидротетрабеназин, 99mTc-c(RGDfK*)2HYNIC, 9-Аминокампотецин, 9-Гидроксикрисамицин А, 9-Гидроксирисперидон, А-42867 псевдоагликон, Абакавир Сукцинат, Абакавир Сульфат, Абаперидон Гидрохлорид, Абареликс, Абиетахинон метид, Абиратерон, Акацетин, Акадезин, Акарбоза, Акатерин, Ацебутолол Гидрохлорид, Ацеманнан, Аценейраминовой кислоты натриевая соль, Ацикловир, Акларубицин, Аколбифен Гидрохлорид, Акотиамид Гидрохлорид Гидрат, Акровестон, Актинопланон А, Актинопланон В, Акулеацин Агамма, Ацилин, Адамантил глоботриаозилкерамид, Адафостин, Адапролол Малеат, Адапролол Оксалат, Адаротен, Адеципенол, Аделмидрол, Адеметионин Тозилат Сульфат, Аденофостин А, Аденофостин В, Аденозин, Адлупулон, Адксантромицин А, Аэротрицин 1, Аэротрицин 41, Аэротрицин 45, Аэротрицин 5, Аэротрицин 50, Аэротрицин 55, Афелетекан Гидрохлорид, Агеласфин 517, Агеласфин 564, Аглаиастатин А, Аглаиастатин В, Аюлемовая кислота, Албаконазол, Албифиллин, Албитиазолия бромид, Албоциклин K3, Алхемикс, Алклометазон дипропионат, Алкурония хлорид, Алдекалмицин, Алдифен, Алемцинал, Альфакальцидол, Алисамицин, Алискирен Фумарат, Альказар-18, Алликсин, Алмокалант, Алоглиптин бензоат, альфа-С-Галактозилкерамид, альфа-Галактозилкерамид, альфа-Галактозилкерамид-BODIPY, альфа-Лактозилкерамид, альфа-Мангостин, альфа-Метилэпинэфрин, альфа-Метилнорэпинефрин, Альфа-Пелтатин, альфа-Пирон I, Алпрафенон Гидрохлорид, Алпренолол Гидрохлорид, Алпростадил, Алтемицидин, Алториртин С, Алтромицин А, Алтромицин В, Алтромицин С, Алтромицин D, Алтромицин, Алвеспимицин Гидрохлорид, Алвимопан Гидрат, Алвоцидиб Гидрохлорид, Амамистатин А, Амамистатин В, Амарогентин, Амброксол нитрат, Амдоксовир, Амелометазон, Амелубант, Амибегрон Гидрохлорид, Амидокс, Амикацин, Аминокандин, Амлексанокс, Аммоцидин А, Амодиахин, Амозулалол Гидрохлорид, Амоксициллин тригидрат, Амфидинолид Е, Амфидинолид Т1, Амфинидин А, Амфотерицин В, Ампренавир, Амрубицин Гидрохлорид, Амурензин Н, Амиколамицин, Амикомицин, Анандамид, Анденаллен, ANDREA-1, Андростанолон, Ангиллоспорал, Ангиномицин С, Ангиномицин D, Анидулафунгин, Анкиномицин, Аннамицин, Аннохеримолин, Аннулин С, Антелиатин, Антид, Антид-1, Антид-2, Антид-3, Антифламмин-1, Антифламмин-3, Антимицин А11, Антимицин А12, Антимицин А13, Антимицин А14, Антимицин А15, Антимицин А16, Ападеносон, Апалциллин Натрия, Апазиквон, Афидиколин, Афидиколин Глицинат, Апикуларен А, Апикуларен В, Апигенин, Аплавирок Гидрохлорид, Апомин, Ароморфин Гидрохлорид, Априцитабин, Арагустерол А, Арагустерол С, Аранорозин, Аранорозинол А, Аранорозинол В, Араноза, Арбекацин, Арбекацин Сульфат, Арбидол, Арборкандин А, Арборкандин В, Арборкандин С, Арборкандин D, Арборкандин Е, Арборкандин F, Арбутамин Гидрохлорид, Архазолид А, Архазолид В, Арформотерол Тартрат, Аргиотоксин-636, Аримокломол Малеат, Арисостатин А, Аришугацин А, Аротинолол Гидрохлорид, Артепиллин С, Артилид Фумарат, Арундифунгин, Арзоксифен Гидрохлорид, Аскостерозид, Азиатская кислота, Азиатикозид, Азимадолин, Асперлицин В, Асперлицин Е, Аспоксициллин, Ассамицин I, Ассамицин II, Астромицин Сульфат, Аталафиллидин, Аталафиллинин, Атазанавир Сульфат, Атенолол, Атиглифлозин, Аторвастатин, Аторвастатин кальция, Аторвастатин-Алискирен, Атосибан, Атоваквон, Атраровая кислота, Атринозитол, Ауристатин Е, Ауротиоглюкоза, Аустарлифунгин, Аустралин, Авиценол А, Авицехинон А, Авицин D, Авицин G, Аворелин, Акситиром, Азацитидин, Азарезвератрол, Азаромицин SC, Азатоксин, Азеластин эмбонат, Азепиностатин, Азитромицин, Азитромицин Медный Комплекс, Бактоболин, Бафиломицин А1, Бафиломицин С1, Байкалеин, Байкалин, Балхимицин, Балофлоксацин, Балофлоксацин дигидрат, Балсалазид динатрия, Бамбутерол, Баноксантрон, Баогонгтенг А, Бариксибат, Барусибан, Базедоксифен Ацетат, Базедоксифен Гидрохлорид, Бекатекарин, Беципарсил, Беклометазон дипропионат, Бекокальцидиол, Бедорадрин Сульфат, Бефлоксатон, Бефунолол Гидрохлорид, Бегацестат, Белактин В, Белотекан Гидрохлорид, Бенадростин, Бенаномицин А, Бенаномицин В, Бенастатин А, Бенастатин В, Бенастатин С, Бенастатин D, Бенексат циклодекстрин, Бенгазол А, Бенгазол В, Бензбромарон, Берапрост Натрия, Берефрин, Берупипам Малеат, Бервастатин, Бесифлоксацин Гидрохлорид, Бета-Босвеллевая Кислота, бета-Мангостин, Бетаметазон бутират пропионат, Бетаметазон дипропионат, Бета-Сиалозилхолестерол натриевая соль, Бетаксолол Гидрохлорид, Бевантолол Гидрохлорид, Биапенем, Биемнидин, Биматопрост, Бимокломол, Бимокломол 1-оксид, Бимосиамоза, Бинфлоксацин, Биноденосон, Биоханин А, Биоксаломицин альфа 1, Биоксаломицин альфа2, Бипранол Гидрохлорид, Бисабосквал В, Бисабосквал D, Висмута субсалицилат, Бисопролол Фумарат, Бисфенол, Битолтерол Мезилат, Бикс, Бизелезин, Блеомицин А2 Сульфат, Богорол А, Богемин, Бохолмицин, Болинахинон, Боррелидин, Бозентан, Брандисианин А, Брандисианин В, Брандисианин С, Бразиликардин А, Бразилинолид А, Бразилинолид В, Бреканавир, Брефлат, Бревифолин карбоновая кислота, Брейнин А, Брейнин В, Бриваниб, Бривудин, Бромотопсентин, Бриостатин 1, Бриостатин 10, Бриостатин 11, Бриостатин 12, Бриостатин 13, Бриостатин 9, Будесонид, Буфломедил пиридоксалфосфат, Бунгеоловая кислота, Бупренорфин Гидрохлорид, Бусерелин Ацетат, Буталактин, Бутеин, Бутеранол, Бутиксокорт, Бутофилолол, Буторфан, Буторфанол Тартрат, Биссохламизол, Кабазитаксел, Кабин 1, Кадралазин, Кадрофлоксацин Гидрохлорид, Каффеин цитрат, Каланолид А, Каланолид В, Калбистрин А, Калбистрин В, Калбистрин С, Калбистрин D, Кальципотриол, Кальцитриол, Кальций-подобный пептид 1, Калебин А, Калокумарин А, Калопорозид В, Калопорозид С, Калопорозид D, Калопорозид Е, Калопорозид F, Калфостин А, Калфостин В, Калфостин С, Калфостин D, Калфостин I, Калтеридол кальция, Камбресцидин 800, Камбресцидин 816, Камбресцидин 830, Камбресцидин 844, Камиглибоза, Кампестанол аскорбил Фосфат, Канадензол, Канаглифозин, Канделалид В, Канделалид С, Кангрелор тетранатрия, Канвентол, Кападенозон, Капецитабин, Капилларизин, Капразамицин А, Капразамицин В, Капразамицин С, Капразамицин Е, Капразамицин F, Капридин бета, Капсазепин, Караберсат, Карбазомадурин А, Карбазомадурин В, Карбетоцин, Карбидопа, Карбовир, Карбаэозид, Карисбамат, Кармотерол Гидрохлорид, Карпестерол, Каркиностатин А, Карсатрин, Картеолол Гидрохлорид, Картерамин А, Карвастатин, Карведилол, Каспофунгин Ацетат, Кассигалол А, Кастаноспермин, Цефбуперазон Натрия, Цефканел, Цефетекол, Цефоницид Натрия, Цефоперазон Натрия, Цефоселис Сульфат, Цефпирамид Натрия, Цефпрозил, Цефпрозил моногидрат, Целгозивир, Целикалим, Целипролол Гидрохлорид, Цефалостатин 1, Цефалостатин 2, Цефалостатин 3, Цефалостатин 4, Цефалостатин 7, Цефалостатин 8, Цефалостатин 9, Церамидастин, Цереброзид А, Цереброзид В, Цереброзид С, Цереброзид D, Церивастатин Натрия, Церулетид диетиламин, Цетефлоксацин, Цетромицин, Цетрореликс Ацетат, Хакол, Хетоатрозин А, Хафурозид, Хенодеоксихолевая кислота, Хетоцин, Хиноин-169, Хлоптозин, Хлоразикомицин, Хлорофузин, Хлорогетизилхинон, Хлорориентицин А, Хлорориентицин В, Холеры автовозбудитель-1, Холин альфоскерат, Хондрамид А, Хондрамид В, Хондрамид С, Циклезонид, Циклетанин, Цидофовир, Циматерол, Циметропия бромид, Цинатрин А, Цинатрин В, Цинатрин С1, Цинатрин С2, Циннабарамид А, Циннатриацетин А, Циннатриацетин В, Цинолазепам, Ципрофлоксацин Гидрохлорид, Ципрокирен, цис-6-Шогаол, Цитиколин, Цитпрессин I, Цитреамицин-Альфа, Цитреамицин-эта, Цитропептин, Цитруллимицин А, Цитрусинин-1, Кладрибин, Кларитромицин, Кпаусенамин А, Клаваровая кислота, Клаваринон, Клавуланат калия, Клазосентан, Клевудин, Клиндамицин Гидрохлорид, Цитоцин, Клобенозид, Клофарабин, Клопитерин, Клоранолол Гидрохлорид, Кокозитол, Колабомицин А, Коленейрамид, Колеофомон В, Колестимид, Колфорсин, Колфорсин дапроат Гидрохлорид, Коллетоевая кислота, Колупулон, Комбретастатин А-1, Комбретастатин А-2, Комбретастатин А-3, Комбретастатин В-1, Комбретастатин В-2, Комбретастатин В-3, Комбретастатин В-4, Комбретастатин D-1, Комбретастатин D-2, Комплестатин, Конагенин, Конифероловый спирт, Кониосетин, Конокурвон, Конофиллин, Контигнастерол, Контулакин G, Кортексолон 17альфа-пропионат, Коринекандин, Козалан, Козитекан, Костатолид, Кумамидин Гамма1, Кумамидин Гамма2, Крассикаулин А, Крелластатин А, Крисамицин С, Криснатол Мезилат, Кробенетин, Кробенетин Гидрохлорид, Кромакалим, Кроссоптин А, Кроссоптин В, Куртисиан А, Куртисиан В, Куртисиан D, Курвуларол, Цианидин Хлорид Моногидрат, Цикламенол, Цикланделат, Циклипостин А, Циклокоммунол, Циклогександиол, Цикломарин А, Циклооктатин, Циклоплатам, Циклопропарадицикол, Циклоспорин А, Циклоспорин J, Циклотеонамид А, Циклотиалидин, Цигаловир, Ципемицин, Циртоминетин, Цистоцин, Цистотиазол С, Цистотиазол D, Цистотиазол F, Циталлен, Цитарабин, Цитарамицин, Цитобластин, Цитохалазин В, Цитохлор, Цитогенин, Цитоспоровая кислота, Цитоспорон В, Цитостатин, Цитотриенин I, Цитотриенин II, Цитотриенин III, Цитотриенин IV, Цитоксазон, DACH-Pt(II)-бис-аскорбат, Дациностат, Дактимицин, Дактилфунгин А, Дактилфунгин В, Дактилоциклин А, Дактилоциклин В, Дактилорин В, DADMe-Иммуциллин-G, DADMe-Иммуциллин-Н, Даларгин, Далбаванцин, Далфопристин Мезилат, Далвастатин, Дамунаканталь, Данофлоксацин, Дапаглифозин, Дафнодорин А, Дафнодорин В, Дафнодорин С ((-)-энантиомер), Дапроптерин Дигидрохлорид, Дарбуфелон, Дарбуфелон Мезилат, Дарунавир, Дасантафил, Дасатиниб, Даунорубицин, Даурихроменовая кислота, Давидигенин, Давунетид, Диацетил моксисилит Гидрохлорид, Декагидромоеномицин А, Декапланин, Декарестриктин С, Декарестриктин D, Декатромицин А, Декатромицин В, Децитабин, Декурсинол, Децил галлат, Деферазирокс, Деферипрон, Дефлазакорт, Дефоролимус, Дегареликс Ацетат, Дегиделон, Дегидродоластатин-13, Дегидрозингерон, Делафлоксацин, Деламиномицин А, Деламиномицин В, Деламиномицин С, Делимотекан Натрия, Дельфинидин, дельта-Токоферол глюкозид, Делтибант, Деметиммуномицин, Деметомицин, Деметилаллозамидин, Деметиластеррихинон В-1, Денопамин, Денуфозол тетранатрия, Деоксиэнтероцин, Деоксилаидломицин, Деоксимулундокандин, Деоксинойиримицин, Деоксиспергуалин Гидрохлорид, Депродон пропионат, Дерсалазин, Дезацетилэлеутеробин, Дезацетилравидомицин N-оксид, Дезацетилвинбластингидразид, Дезацетилвинбластингидразид/фолат Конъюгат, Дезбутил бенфлуметол, Дезбутилгалофантрин Гидрохлорид, Десферри-даноксамин, Десферри-норданоксамин, Десферри-сальмицин А, Десферри-сальмицин В, Десферри-сальмицин С, Десферри-сальмицин D, Дезглугастрин трометамин, Дезизобутирилциклезонид, Деслорелин, Десметилэлеутеробин, Десмин-370, Десмопрессин Ацетат, Дезоксиэпотилон В, Дезоксиэпотилон F, Дезоксилаулималид, Дезвенлафаксин Сукцинат, Дексаметазон, Дексаметазон белоксил, Дексаметазон ципецилат, Дексаметазон пальмитат, Дексаметазон Натрия Фосфат, Дексанабинол, Декселвуцитабин, Декстрорфан, Дексилозилбенаномицин А, D-Флувиабактин, DHA-паклитаксел, Диаденозин тетрафосфат, Диазафилоновая кислота, Диазепиномицин, Дикумарол, Диктиостатин 1, Дидемнин X, Дидемнин Y, Дидеоксиинозин, Диэкол, Диэпоксин-сигма, Дифломотекан, Дифлунисал, Дигалактозилдиацилглицерол, Дигоксин, Дигетеропептин, Дигидрексидин, Дигидроавенантрамид D, Дигидрокостатолид, Дигидроэпонемицин, Дигидрогранатицин В, Дигидрогептапренол, Дигидрохонокиол В, Дигидроизостевиол, Дигидроралоксифен, Дилевалол, Дилевалол Гидрохлорид, Дилмапимод, Димеламол, Диметандролон, Диметилкуркумин, ди-mPEG5-Атазанавир, Динафин, Динапсолин, Диноксилин, Дионкохинон А, Дионкохинон В, Диоксолан тимин нуклеозид, Дипивефрин Гидрохлорид, Дикалия Госсиполат, Дипиридамол, Дипиридамол бета-циклодекстрин комплекс, Диквафозол тетранатрия, Диритромицин, Дискодермид, Дискодермид Ацетат, Дисермолид, Динатрия кромпроксат, Динатрия леттусат, Дизоразол Е1, Добутамин Гидрохлорид, Добутамин Фосфат, Доцетаксел, Докозанол, Докозил Цидофовир, Дофеквидар Фумарат, Доластатин 13, Допексамин, Допексамин Гидрохлорид, Докваласт, Дорамектин, Доранидазол, Доретинел, Дорипенем, Дорригоцин А, Дорригоцин В, Досмалфат, Довитиниб Лактат, Доксефазепам, Доксеркальциферол, Доксифлуридин, Доксорубицин Гидрохлорид, Доксорубицин, Морфолинил, ДоксоТам 12, Доксициклин гиклат, Дридокаинид, Дронабинол, Дроксидопа, Дроксинавир, DTPA-аденозилсобаламин, Дуокармицин В1, Дуокармицин В2, Дуокармицин С1, Дуокармицин С2, Дурамицин, Дутомицин, Динемицин А, Динемицин С, Экдистерон, Эценофлоксацин Гидрохлорид, Экомустин, Эконазол Сульфосалицилат, Экопипам, Экрапрост, Эктеинасцидин 1560, Эктеинасцидин 722, Эктеинасцидин 729, Эктеинасцидин 736, Эктеинасцидин 745, Эктеинасцидин 757, Эктеинасцидин 770, Эктеинасцидин 875, Эдотекарин, Эдотреотид иттрия, Эфепристин, Эфлуцимиб, Эфлумаст, Эйкозил Цидофовир, Элацитарабин, Эланзолид С1, Элдацимиб, Элдекальцитол, Элеутеробин, Элеутерозид В, Элипродил, Элизаптерозин В, Эллаговой кислоты-4-галлат, Эллиптиния Ацетат, Элокальцитол, Эломотекан Гидрохлорид, Элсибукол, Элтанолон, Элтромбопаголамин, Элвитегравир, Элвуцитабин, Эмакалим, Эмбелин, Эместрин С, Эмодин, Эмтрицитабин, Эналкирен, Эназадрем, Энфумафунгин, Энглерин А, Энигмол, Энкастин (D), Энкастин AD, Энкастин АЕ, Энкастин ID, Энкастин IE, Энкастин VD, Энкастин VE, Эноцитабин, Энофеласт, Энолоксон, Эноксацин, Энпростил, Энразентан, Энрофлоксацин, Энтакапон, Энтекавир, энт-Эстриол, Эперезолид, Эперезолид N-оксид, Эпервудин, Эпикохлиохинон А, Эпидоксоформ, Эпигаллокатехин-3-галлат, Эпирубицин Гидрохлорид, Эписпонгиадиол, Эпливансерин, Эпливансерин Фумарат, Эпливансерин Мезилат, Эпокарбазолин А, Эпокарбазолин В, Эпофолат, Эпонемицин, Эпопростенол Натрия, Эпотилон А, Эпотилон А N-оксид, Эпотилон В N-оксид, Эпотилон Е, Эпоксомицин, Эпоксивибсанин В, Эпротиром, Эпталопрост, Эптастатин Натрия, Эптастигмин Тартрат, Эптазоцин Гидробромид, Эрабуленол А, Эрабуленол В, Эректумин А, Эремомицин, Эремофиллен А, Эрибулин Мезилат, Эриокаликсин В, Эриторан тетранатрия, Эрсентилид, Эрсентилид Гидрохлорид, Эртапенем Натрия, Эрилозид А, Эрилозид F, Эритритол, Эритродиол, Эритромицин, Эритромицин Ацистрат, Эритромицин салнацедин, Эритромицин стинопрат, Эсафлоксацин Гидрохлорид, Эскулеогенин А, Эскулозид А, Эсмолол Гидрохлорид, Эспатропат Гидрат, Эсператруцин, Эстетрол, Эстрадиол, Эстрадиол Ацетат, Эстрен, Эстриол, Эталоциб Натрия, Этамзилат, Этаноламин, Этинилэстрадиол, Этилгаллат, Этилтио-DADMe-Иммуциллин-А, Этинилцитидин, Этипреднол диклоцетат, Этопозид, Этопозид Фосфат динатриевая соль, Эугенодилол, Эугеноседин А, Эуфодендроидин D, Эуротинон, Эуксантнон, Эвернимицин, Эверолисмус, Эксатекан Мезилат, Эксифон, Эзетимиб, Эзетимиб глюкуронид, Фадолмидин Гидрохлорид, Ферифунгин А, Ферифунгин В, Фандофлоксацин Гидрохлорид, Фаропенем медоксомил, Фаропенем Натрия, Фасобегрон Гидрохлорид, Фэттивирацин А1, Фавипиравир, Фебрадинол, Фебупрол, Феглимицин, Фенолдопам Мезилат, Фенотерол Гидробромид, Ферпифозат Натрия, Ферулинолол, Фезотиродин Фумарат, Фексофенадин Гидрохлорид, Фидаксомицин, Фидексабан, Филибувир, Фимбригал Р, Финафлоксацин Гидрохлорид, Финголимод Гидрохлорид, Финрозол, Флероксацин, Фломоксеф Натрия, Флопристин, Флоксуридин, Флударабин Фосфат, Флуделон, Флудеоксиглюкоза (18F), Флунизолид, Флунопрост, Флуоцинонид, Фториндолокарбазол А, Фториндолокарбазол В, Фториндолокарбазол С, Фторнепланоцин А, Флуостатин А, Флуостатин В, Флупентиксол Гидрохлорид, Флуфеназин Гидрохлорид, Флуритромицин, Флутиказон фуроат, Флутиказон пропионат, Флувастатин Натрия, Флувируцин В2, Фоэтидин 1, Фоэтидин 2, Фолиновая кислота, Фолипастатин, Фондапаринакс Натрия, Формамицин, Форместан, Формобактин, Формозин А, Формотерол Фумарат, Фородезин Гидрохлорид, Фозопамин, Фостеабин Натрия Гидрат, Фредерин, Фукоксантин, Фудостеин, Фуладектин компонент A3, Фуладектин компонент А4, Фулвестрант, Фумагалон, Фурахиноцин А, Фурахиноцин В, Фузакандин А, Фузакандин В, Фускозид В, Фузидат серебра, Фузидиенол, Габоксадол, Габусектин, Габусектина Метиловый эфир, Гадобутрол, Гадоколетовой кислоты тринатриевая соль, Гадомелитол, Гадотерат меглумин, Гадотеридол, Галактомицин I, Галактомицин II, Галактосиллактоза, Галамустин Гидрохлорид, Галантамин Гидробромид, Галарубицин Гидрохлорид, Галоцитабин, Гамбоговая кислота, гамма-Мангостин, гамма-Токотриенол, Ганцикловир, Ганцикловир Элаидиновая кислота, Ганцикловир Монофосфат, Ганцикловир Натрия, Ганефромицин Альфа, Ганефромицин Бета, Ганглиозид GM1, Ганиреликс, Ганиреликс Ацетат, Ганодеровая кислота X, Гареноксацин Мезилат, Гаромефрин Гидрохлорид, Гарвалон С, Гарвеатин Е, Гарвеатин F, Гатифлоксацин, Гемцитабин, Гемцитабин Элаидат, Гемепрост, Гемифлоксацин Мезилат, Генипин, Генистеин-7-Фосфат, Гигантол, Гилатид, Гилвусмицин, Гиместат, Гиродазол, Глаукокаликсин А, Глемансерин, Гленвастатин, Глидобактин PF-1, Глюкаролактам калий, Глюколаномицин, Глюколипсин А, Глюколипсин В, Глюкопирицидинол А1, Глюкопирицидинол А2, Глюкозамин Сульфат, Глюдопа, Глуфосфамид, Гликопин, Гликотиогексид альфа, Глицирризиновая кислота, Гомфостенин, Гудиэрозид А, Гудиэрозид В, Горалатид, Госерелин, Гранатицин В, Грепафлоксацин Гидрохлорид, Грисеузин С, Галистатин 1, Галистатин 2, Галистатин 3, Галобетазол пропионат, Галофантрин Гидрохлорид, Галофугинон Гидробромид, Галометазон, Галопредон Ацетат, Галовир А, Галовир В, Галовир С, Галовир D, Галовир Е, Халксазон, Хаперфорин В1, Хатомамицин, Хатомарубигин А, Хатомарубигин В, Хатомарубигин С, Хатомарубигин D, Хатталин, Хаюмицин А, Хаюмицин В, Хаюмицин С1, Хаюмицин С2, Хаюмицин D, Хедерахолкизид Е, Хелихиномицин, Гелвекардин А, Гелвекардин В, Гептаминол AMP Амидат, Хериценал А, Хериценал В, Хериценал С, Гексадецил Цидофовир, Гексадецилоксипропил-Цидофовир, Гексафторкальцитриол, Гидросмин, Химатстатин, Гистрелин, Гистрелин Ацетат, Хонгокверцин А, Хонгокверцин В, Хонокиол диэпоксид, Человеческий ангиотензин II, Гиалуронат Натрия, Гидрокортизон Ацепонат, Гидроморфон метиодид, Гидростатин А, Гидроксиакалон, Гидроксихлорохин Сульфат, Гидроксимикотриенин А, Гидроксимикотриенин В, Гидроксифослактомицин В, Гидроксизин Гидрохлорид, Гименистатин 1, Гипептин, Гиперицин, Гиперозид, Гипохоламид, Гипохоларид, Ибутилид Фумарат, Икариин, Икатибант Ацетат, Идарубицин Гидрохлорид, Идебенон, Идремцинал, Идроноксил, Ифенпродил, Илатреотид, Илипарцил, Илонидап, Илопрост, Имидазоакридинон, Имипенем, Иммунозин, Имплитапид, Инциклинид, Индакатерол, Инданапрост (S), Инданоцин, Индинавир Сульфат, Индометацин-Симвастатин, Индинапрост, Ингенол мебутат, Инофиллум В, Инофиллум Р, Иносиплекс, Интеграцид А, Интеграцид В, Интеграции А, Интеграции В, Интеграции С, Интеграмицин, Интеграстатин А, Интеграстатин В, Интоплицин, Иобитридол, Иодиксанол, Иодхлоргидрохин, Йододифлунисал, Иодорубидазон (р), Иофратол, Иогексол, Иолоприд (123I), Иомепрол, Иопамидол, Иопентол, Иопромид, Иотризид, Иотрол, Иоверсол, Иоксилан, Иоксиприд, Ипратория бромид, Иралукаст, Иралукаст Натрия, Ирциниастатин А, Ирциниастатин В, Иринотекан Гидрохлорид, Ирофулвен, Исалмадол, Изепамицин Сульфат, Изобавахалькон, Изодоксорубицин, Изоэлеутеробин А, Изофагомин Тартрат, Изофлокситепин, Изогомохалихондрин В, Изо-иантеран А, Изоликвиритигенин, Изомолпан Гидрохлорид, Изохин, Изосорбид 5-мононитрат, Изоспонгиадиол, Изованихуперцин А, Изоксазолидхиделон, Изоксазолфлуделон, Итавастатин кальция, Итроцинонид, Иксабепилон, Ядомицин В, Янтиномицин А, Янтиномицин В, Янтиномицин С, Джасплакинолид, Йорумицин, Кадсуфилин С, Кахалалид F, Каитоцефалин, Кампанол А, Кампанол В, Канамицин, Канглемицин А, Кансуинин В, каппа-Контоксин Р VIIA, Капуримицин А1, Капуримицин A3, Каралицин, Карнамицин В1, Катаноцин А, Катаноцин В, Кехокорин D, Кехокорин Е, Хафрефунгин, Кифунезин, Кигамицин А, Кигамицин В, Кигамицин С, Кигамицин D, Кигамицин Е, Кигамицинон, Кижимицин, Кинсенозид, Кистамицин А, Клаинетин А, Клаинетин В, Кобифуранон В, Кобиин, Кодаистатин А, Кодаистатин В, Кодаистатин С, Кодаистатин D, Корупенсамин А, Корупенсамин В, Корупенсамин С, Корупенсамин D, Козиностатин, Кюхнеромицин А, Курасоин В, Киностатин-227, Киностатин-272, Лабедипинедилол А, Лабедипинедилол В, Лабеталол Гидрохлорид, Лабрадимил, Лаккаридион А, Лактонамицин, Лактозилфенил тролокс, Ладирубицин, Лагатид, Лахеррадурин, Ламелларин альфа 20-Сульфата Натриевая соль, Ламифибан, Ламивудин, Ландиолол, Ланреотид Ацетат, Лантиопептин, Ларотаксел дигидрат, Лазинавир, Лазофоксифен, Лазофоксифен Тартрат, Лазонолид А, Латамоксеф Натрия, Латанопрост, Латрункулин S, Лавандахиноцин, L-Цикориевая кислота, L-Допамид, Лецирелин, Ледазерол, Лейнамицин, Лемутепорфин, Ленапенем Гидрохлорид, Ленапенем Гидрохлорид Гидрат, Лептофуранин А, Лептофуранин В, Лерсивирин, Лестауртиниб, Левпролид Ацетат, Лейрубицин, Лейстродуксин А, Лейстродуксин В, Лейстродуксин С, Лейстродуксин Н, Левалбутерол Гидрохлорид, Левобетаксолол Гидрохлорид, Левобуналол Гидрохлорид, Леводопа, Леводопа 3-O-глюкозид, Леводопа 4-O-глюкозид, Леводропропизин, Левофлоксацин, Левонадифлоксацин аргининовая соль, Левонбиволол, Леворфанол Тартрат, Лексакальцитол, L-Флувиабактин, L-Гистидинол, Либломицин, Лакричный-сапонин С2, Лифицигват, Лимапрост альфадекс, Линапразан, Линопристин, Липиармицин В3, Липиармицин В4, Ликвиритин апиозид, Лизофиллин, Литоспермовой кислоты В магниевая соль, Лобатамид С, Лобатамид F, Лобофорин А, Лобофорин В, Лобукавир, Лоденафил, Лоденозин, Лолоатин В, Ломефлоксацин Гидрохлорид, Лометрексол, Лонгестин, Лопинавир, Лоразепам, Лорметазепам, Лорноксикам, Лозартан, Лозартан калия, Лозигамон, Лотепреднол Этабонат, Ловастатин, Локсорибин, L-треитол керамид, L-трео-С6-пиридиний-керамид-бромид, Лубелузол, Люмефантрин, Люминацин D, Лупулон, Луртотекан, Лутеолин, Lu-Tex бис(глюконат), Лизобактин, Мабутерол Гидрохлорид, Макваримицин В, Макрокарпин А, Макрокарпин В, Макролактин М, Мадекассоновая кислота, Мадекассозид, Макалувамин D, Макалувамин Е, Малонобен, Малтолил п-кумарат, Манитимус, Маннопептимицин альфа, Маннопептимицин бета, Маннопептимицин дельта, Маннопептимицин эпсилон, Маннопептимицин гамма, Маноалид, Манумицин А, Манумицин В, Манумицин С, Манумицин Е, Манумицин F, Манумицин G, Манзамин F, Марбофлоксацин, Марибавир, Маримастат, Маринопиррол А, Мармелин, Маслиновая кислота, Масопрокол, Мастпром, Маттеуориенат А, Маттеуориенат В, Маттеуориенат С, Мазокалим, Медикарпин, Мефлохин Гидрохлорид, Меговалицин А, Меговалицин В, Меговалицин С, Меговалицин D, Меговалицин G, Меговалицин Н, Мелеводопа Гидрохлорид, Меллеин, Мелоксикам, Мелуадрин, Мелуадрин Тартрат, Мемно-пептид А, Мепиндолол Сульфат, Мепиндолол в составе чрезкожного пластыря, Мептазинол Гидрохлорид, Меропенем, Месалазин, Метараминол, Метезинд глюкуронат, Метанобактин, Метоксатон, Метскополамин бромид, Метил бестатин, Метил галлат, Метилдопа, Метилналтрексон бромид, Метилпреднизолон, Метилпреднизолон ацепонат, Метилпреднизолон сулептанат, Метилтио-DADMe-Иммуциллин-А, Метисергид Малеат, Метилдигоксин, Метипранолол, Метирозин, Метопролол Фумарат, Метопролол Сукцинат, Метопролол Тартрат, Метрифонат, Метронидазол, Микакоцидин А, Микакоцидин В, Микафунгин Натрия, Мичелламин В, Мичигазон, Микробиспорицин А2, Микроколин А, Микрономицин Сульфат, Мидекамицин Ацетат, Мидепланин, Мигитол, Миглустат, Милатаксел, Милбемицин альфа-9, Милринон Лактат, Мимопезил, Минервал, Миноциклин Гидрохлорид, Мипорамицин, Мипрагозид, Мипроксифен, Мирабегрон, Мироденафил Гидрохлорид, Мисакинолид, Мисопростол, Митемцинал Фумарат, Митоксантрон Гидрохлорид, Мивазерол, Мизорибин, Модекаинид, Модитромицин, Моеномицин А хлорида висмутовая соль, Моллугин, Мометазон фуроат, Момордин Ic, Монамидоцин, Монлицин А, Моногалактозилдиацилглицерин, Моногидроксиэтилрутозид, Монофосфорил липид А, Монтелукаст Натрия, Морфин Глюкуронид, Морфин Гидрохлорид, Морфин Сульфат, Мотексафин гадолиния, Мотексафин лютеция, Моксидектин, Моксифетин гидромалеат, Моксифлоксацин Гидрохлорид, Мозенавир Мезилат, Мультифоризин А, Мумбайстатин, Мупироцин, Мураминомицин А, Мураминомицин В, Мураминомицин С, Мураминомицин D, Мураминомицин Е1, Мураминомицин Е2, Мураминомицин F, Мураминомицин G, Мураминомицин Н, Мураминомицин I, Мураминомицин Z1, Мураминомицин Z2, Мураминомицин Z3, Мураминомицин Z4, Мурамил дипептид С, Муреидомицин А, Муреидомицин В, Муреидомицин С, Муреидомицин D, Муреидомицин Е, Муреидомицин F, Муреидомицин, Микаламид А, Мицестирицин Е, Миколактон А, Миколактон В, Микофенолят Мофетил, Микофеноловой кислоты натриевая соль, Мирциацитрин I, Мирциацитрин II, Мирциафенон В, Мирицеровая кислота А, Митолбилин, Митобилиновая кислота, Метиловый эфир Митобилиновой кислоты, Митолбилинол, N4-Гексадецил-dC-AZT, N-9-Оксадецил-6-Метил-DGJ, Наамидин А, Набилон, N-Ацетилколхинол, N-Ацетилсперамицин А1, N-Ацетилсперамицин А1В, N-Ацетилсперамицин А2, Надифлоксацин, Надолол, Нафарелин Ацетат, Нафтопидил, Нафуредин, Нафуредин-гамма, Нагстатин, Налбуфин Гидрохлорид, Налфурафин Гидрохлорид, N-Аллилсекоболдин, Налмефен, Налоксон Гидрохлорид, Налтрексон Гидрохлорид, Налтриндол, Намитекан, Напсамицин А, Напсамицин В, Напсамицин С, Напсамицин D, Нардетерол, Наропарцил, Навуридин, N-Циклопентил-тазопсин, Небикапон, Небиволол, Нектризин, Нелдазоцин, Нелфинавир Мезилат, Неливаптан, Нелзарабин, Немифитид дитрифлутат, Немоноксацин, Неморубицин, Неоцимицигенозид А, Неоцимицигенозид В, Неолаулималид, Неомицин В-аргинин Конъюгат, Неомицин-акридин, Непадутант, Непаренсинол А, Непаренсинол В, Непаренсинол С, Нерфилин I, Неристатин 1, Несбувир, Нетилмицин Сульфат, Нетивудин, Neu5Ac2en, Нгерхеумицин А, Нгерхеумицин В, N-гексакозанол, Никанартин, Нифекалант Гидрохлорид, Нилепрост бета-циклодекстрин клатрат, Нипрадолол, Нитекапон, Нитроправастатин, N-Нонил-деоксигалактогиримицин, Нокардион А, Нокатиацин I, Нокатиацин II, Нокатиацин III, Нокатиацин IV, N-Октил-бета-валиенамин, NO-гидрокартизон, Ноладиновый эфир, NO-Месаламин, Нооглютил, Нораристеромицин, Нордамунакантал, Норфлоксацин, Норфлоксацин сукцинил, Нортопиксантрон Гидрохлорид, Ностоциклопептид М1, Нотрамицин, NO-Урсодезоксихолевая кислота, N-Ретиноил-D-глюкозамин, N-трет-бутилизохин, Нубиотик 2, Нутлин-2, Обелмицин Н, Оберадилол, Оберадилол Моноэтил Малеат, Обетихолевая кислота, Охромицинон, Оцимумозид А, Оцимумозид В, Октакозамицин А, Октакозамицин В, Октреотид Ацетат, Октил галлат, Одапипам Ацетат, O-Деметилхлотрицин, O-Деметилмуррейафолин А, Одипарцил, Оенотеин В, Офлоксацин, Окиценон, Оламуфлоксацин, Оламуфлоксацин Мезилат, Оланзапин памоат, Олцегепант, Олеанолевая кислота, Олеоил-L-Валинол амид, Олсалазин Натрия, Омацикловир, Омбрабулин, Омбрабулин Гидрохлорид, Онжиксантон I, Онжиксантон II, Оннамид А, Оолонгомобистафлаван А, Оолонгомобистафлаван С, ОРС-17083, Опиорфин, Опипрамол Гидрохлорид, Орбифлоксацин, Орципреналин сульфат, Ориентицин А, Ориентицин В, Ориентицин С, Ориентицин D, Оритаванцин, Орниплабин, Орнопростил, Ортатаксел, Ортосомицин А, Ортосомицин В, Ортосомицин С, Ортосомицин D, Ортосомицин Е, Ортосомицин F, Ортосомицин G, Ортосомицин Н, Оспемифен, Осутидин, Оксаспирол А, Оксаспирол В, Оксазепам, Оксазофурин, Оксеклоспорин, Оксимидин III, Оксирацетам, Окситропия бромид, Оксолид, Окспренолол Гидрохлорид, Оксиметазолин Гидрохлорид, Оксиметацил, Оксиморфазол Дигидрохлорид, Оксиморфон Гидрохлорид, Оксинор, Оксифенарсин, Озареликс, Озеноксацин, Пахастриссамин, Pachymedusa dacnicolor Триптофиллин-1, Пацифоргин, Паклитаксел, Паклитаксел церибат, Пециламинол, Пецилохинин А, Пецилохинин D, Пецилохинин В, Пецилохинин D, Пафенолол, Палауамин, Палдимицин В, Палинавир, Палмидрол, Памапимод, Памаквезид, Панкратистатин динатрия Фосфат, Панкратистатин-3,4-Циклического Фосфата Натриевая соль, Панипенем, Паннорин, Пантетин, Папуамид А, Папуамид В, Папуамид С, Папуамид D, Паквинимод, Парацетамол, Паразин I, Парикальцитол, Пародилол Гемифумарат, Паромомицин, Парвиспорин В, Пателлазол А, Пателлазол В, Пателлазол С, Патупилон, Пауломицин, Пауломицин А2, Пауломицин В, Пауломицин С, Пауломицин D, Пауломицин Е, Пауломицин F, Пазуфлоксацин, Пазуфлоксацин Мезилат, Пефлоксацин, PEG40000-Паклитаксел, PEG5000-Паклитаксел, PEG-Конъюгированный камптотецин, PEG-ванкомицин, Пелитрексол, Пелорузид А, Пенастерол, Пенбутолол Сульфат, Пенцикловир, Пеницеллид, Пентазоцин Гидрохлорид, Пентостатин, Пепломицин, Пептициннамин Е, Перамивир, Перцихиннин, Перициазин, Периллиловый спирт, Перфеназин, Персии, Петрозаспонгиолид М, PG-камптотецин, Фаффиаол, Факеллистатин 7, Факеллистатин 8, Факеллистатин 9, Фазеолинон, Фенохалазин А, Фенпрокумон, Фентоламин Мезилат, Филинопсид А, Флорофукофуроэкол, Фомактин А, Фомактин В, Фомоидрид А, Фомопсихалазин, Форбоксазол А, Форбоксазол В, Фосфолин, Фталасцидин, Физостигмин салицилат, Пицеатаннол, Пикуметерол Фумарат, Пидобензон, Пимекролимус, Пимилпрост, Пиндолол, Пинитол, Пиноцембрин, Пипендоксифен, Пипотиазин, Пирарубицин, Пирбутерол Гидрохлорид, Пирфеноксон, Пиродомаст, Пиронетин, Пироксикам, Pittsburgh Compound В, Пладиенолид А, Пладиенолид В, Пладиенолид С, Пладиенолид D, Пладиенолид Е, Плантагозид, Платенцин, Платенсимицин, Плаунотол, Плевитрексед, Плитидепсин, Плурафлавин А, Плурафлавин В, Плурафлавин Е, Плюсбацин А1, Плюсбацин А2, Плюсбацин A3, Плюсбацин А4, Плюсбацин В1, Плюсбацин В2, Плюсбацин В3, Плюсбацин В4, Пневмокандин А0, Пневмокандин В0, Пневмокандин В0 2-Фосфат, Пневмокандин D0, Подофиллотоксин, Полиэстрадиол Фосфат, Поликетомицин, связанный с полимером ингибитор эластазы лейкоцитов человека, Поналрестат, Попологуанон Е, Посаконазол, Посизолид, Калия эмбелат, Прадимицин А, Прадимицин В, Прадимицин D, Прадимицин Е, Прадимицин FA-1, Прадимицин FA-2, Прадимицин FL, Прадимицин FS ((+)-энантиомер), Прадимицин L, Прадимицин Q, Прадимицин S, Прадимицин Т1, Прадимицин Т2, Прадофлоксацин, Прастерон, Предникарбат, Преднизолон, Преднизолон Ацетат, Преднизолон фарнезилат, Преднизон, Префолик А, Премафлоксацин, Премафлоксацин Гидрохлорид, Преуссин, Принаберел, Присотинол, Пристинамицин IA, Пристинамицин IIA, Проамипид, Пробестин, Пробукол, Прокатерол Гидрохлорид гемигидрат, Пролилмеридамицин, Пропафенон Гидрохлорид, Пропептин Т, Пропофол, Пропранолол Гидрохлорид, Пропил галлат, Простанит, Простатин, Простратин, Пиротокатеховая кислота, Протокатеховый альдегид, Проксодолол, Прулифлоксацин, Прулифлоксацин Гидрохлорид, Прулифлоксацин Мезилат, Псевдоэфедрин Гидрохлорид, Псевдогиперицин, Псевдомицин А', Псевдомицин В', Пурпуромицин, Пурваланол А, Пикнантухинон А, Пикнантухинон В, Пилорицидин В, Пиридавон, Пириндамицин А, Пириндамицин В, Пирипиропен А, Пирипиропен В, Пирипиропен С, Пирипиропен D, Пирролоспорин А, Кватромицин А1, Кватромицин А2, Кватромицин A3, Кватромицин D1, Кватромицин D2, Кватромицин D3, Кверцетин-3-О-Метиловый эфир, Кветиапин Фумарат, Хинаголид Гидрохлорид, Хинидин, Хинобен, Хиноксапептин С, Хинупристин Мезилат, рац-Апогоссиполон, рац-Толтеродин, Рафабегрон, Ралоксифен Гидрохлорид, Ралтитрексед, Ралуридин, Рамесваларид, Рамопланин А'1, Рамопланин А'2, Рамопланин А'3, Рамореликс, Ранимустин, Ранолазин, Рапамицин, Равидомицин N-оксид, Равсонол, Разупенем, Ребамипид висмута цитрат тетраметилдамин, Ребластатин, Регаденозон, Ремикирен Мезилат, Ремипростол, Ремоглифлозин этабонат, Репандиол, Репротерол Гидрохлорид, Резобен, Резортиомицин, Ретапамулин, Ретаспимицин Гидрохлорид, Реватропат, Реверомицин А, Родиоцианозид А, Родиоцианозид В, Рододаурихромановая кислота А, Родострептомицин А, Родострептомицин В, Рибавирин, Рибавирин эйкозенат цис, Рибавирин эйкозенат транс, Рибавирин Элаидат, Рибавирин Олеат, Рифабутин, Рифалазил, Рифамексил, Рифампицин, Рифапентин, Рифаксимин, Рилмакалим гемигидрат, Римексолон, Римотерол Гидробромид, Риодоксол, Ритипенем акоксил, Ритонавир, Ривастигмин Тартрат, Ривенпрост, Рокаглоевая кислота, Рокурония бромид, Рофлепонид, Рофлепонид пальмитат, Рогитукин, Рокитамицин, Роллиниастатин 1, Ромуртид, Роквинимекс, Розапростол Натрия, Росковитин, Роселипин 1А, Роселипин 1В, Роселипин 2А, Роселипин 2В, Ростафуроксин, Розувастатин кальция, Розувастатин Натрия, Ротигаптид, Ротиготин, Роксатидин висмута цитрат, Роксиндол Мезилат, Рокситромицин, Рубигинон А1, Рубигинон А2, Рубигинон В1, Рубигинон С1, Рубитекан, Рубоксил, Руфигаллол, Руфлоксацин Глюконат, Руфлоксацин Гидрохлорид, Румицин 1, Румицин 2, Руссуфелин А, Сабарубицин Гидрохлорид, Сафингол, Саинтопин, Саинтопин Е, Саишин N, Сакиомицин А, Сакиомицин Е, Салазопиридазин, Салбостатин, Салбутамол нитрат, Салбутамол Сульфат, Салкапрозовой кислоты натриевая соль, Салицилазобензойная кислота, Салицилигаламид А, Салицилигаламид В, Салинамид А, Салиноспорамид А, Салифенилгаламид, Сальматерол, Сальметерол ксинафоат, Салоксин, Сальвианоловая кислота L, Самадерин X, Сампатрилат, Санфетринем, Санфетринем цилексетил, Санфетринем Натрия, Санглиферин А, Санглиферин В, Санглиферин С, Санглиферин D, Сапацитабин, Саптомицин D, Сапуримицин, Саквинавир, Саквинавир Мезилат, Саркофитол А, Саркофитол В, Сарикандин, Сауссуреамин D, Сауссуреамин Е, Сазетидин-А, Скопинаст Фумарат, Скополамин, Скифостатин, Секалциферол, Секобацеллин А, Секобацеллин В, Секоизоларисирезинол диглюкозид, Секуриозид А, Секуриозид В, Сеглитид, Селамектин, Селанк, Селоденозон, Семагацестат, Семдурамицин, Семорфон Гидрохлорид, Сеокальцитол, Сеприлоз, Серглифлозин этабонат, Серофендовая кислота, Сессилозид, Сетамицин, Сетазиндол, Шеферидин, Шишиимицин А, Шишиимицин В, Шишиимицин С, Сиалозилхолестерин-Альфа Натриевая Соль, Сибаномицин, Сибенадет Гидрохлорид, Сибискозид, Силденафил цитрат, Силодозин, Силтензепин, Силихристин, Симотаксел, Симвастатин, Синоменин, Ситафлоксацин Гидрат, Ситостанол аскорбил Фосфат, Сивифен, Сивенмицин, Сизофиран, Смилагенин, Сокорромицин, Натрия хромгликат, Натрия оксибат, Солабегрон Гидрохлорид, Солпекаинол Гидрохлорид, Сонеденозон, Сутепензеон, Сорапразан, Сорбициллактон А, Соривудин, so-Симвастатин-6-он, Соталол Гидрохлорид, Спарфлоксацин, Спароксомицин А1, Спароксомицин А2, Сперабиллин А, Сперабиллин В, Сперабиллин С, Сперабиллин D, Сфингофунгин F, Спинорфин, Спиносульфат А, Спиносульфат В, Спирокардин А, Спирокардин В, Спироксимицин, Спирухостатин А, Спирухостатин В, Списулозин, Спонгиадиол, Спонгистатин 1, Спонгистатин 3, Спонгистатин 4, Спонгистатин 5, Спонгистатин 6, Спонгистатин 7, Спонгистатин 8, Спонгистатин 9, Спореамицин А, Спореамицин В, Скваламин Лактат, Сквалестатин I, Стахибоцин А, Стахибоцин В, Стахибоцин С, Стахиботрин С, Стахиботридиал, Стаплабин, Старризин, Ставудин, Стеллерамакрин А, Стеллерамакрин В, Стеренин А, Стеренин С, Стеренин D, Стрептомицин, Стрептопиррол, Стилогуанидин, Суберозенол А, Сукцинобукол, Сугаммадекс Натрия, Сульфасалазин, Сульфинозин, Сульфирцин С, Сулопенем, Сулопенем этзадроксил, Сульфазоцин, Сульфохиновозилдиацилглицерин, Сульпростон, Сулукаст, Sunflower трипсин ингибитор-1, Суплатаст Тозилат, Суронакрин Малеат, Сусалимод, Свифтиапрегнин, Симбиоимин, Синаденол, Сингуанол, Свифтиапрегнин А, Сириакузин В, Сириакузин С, Сизигиол, Такальцитол, Такапенем Пивоксил, Таккалонолид Е, Такролимус, Тафлупрост, Тагефлар, Тайваньгомофлавон А, Таканаваен А, Таканаваен В, Таканаваен С, Талибегрон, Талибегрон Гидрохлорид, Талнетант, Тамандарин А, Тамандарин В, Тамоларизин Гидрохлорид, Танеспимицин, ТАР-доксорубицин, Тапентадол Гидрохлорид, Тараманон А, Тасквинимод, Таурогиодеоксихолевая кислота, Таутомицин, Таксуюннанин, Тазофелон, Тазопсин, Тебипенем, Тебипенем цилексетил, Тебипенем Пивоксил, Тебуфелон, Текаденосон, Технеций Tc 99m депреотид, Тейкопланин-А2-1, Тейкопланин-А2-2, Тейкопланин-А2-3, Тейкопланин-А2-5, Телаванцин Гидрохлорид, Телбивудин, Телинавир, Телитромицин, Темафлоксацин Гидрохлорид, Темазепам, Темопорфин, Темпол, Темсиролимус, Темуртид, Тенидап, Тенипозид, Теноксикам, Тенуифолизид А, Тенуифолизид В, Тенуифолизид С, Тенуифолизид D, Тербуталин Сульфат, Терестигмин Тартрат, Терфенадин, Терифлуномид, Терлакирен, Тернатин, Терпренин, Терреулактон А, Терреулактон В, Терреулактон С, Терреулактон D, Тертатолол Гидрохлорид, Тезетаксел, Тестостерон глюкозид, Тетракозил Цидофовир, Тетрациклин Гидрохлорид, Тетрафибрицин, Тетрагаллоилхиновая кислота, Тетрагидрокортизол, Тетрагидрокуркумин, Тетрагидроэхинокандин В, Тетрагидросвертианолин, Тетрагидроксихинон, Тетромицин А, Тетромицин В, Тетронотиодин, Тексеномицин А, Тезацитабин, Тезосентан, Тезосентан динатрия, Тенорфин, Теопедерин D, Теоперидин Е, Теофиллин рутозид, Термозимоцидин, Тиамет-G, Тиамфеникол, Тиарубрин Е, Тиарубрин F, Тиарубрин G, Тиарубрин Н, Тиазинотриеномицин В, Тиазинотриеномицин F, Тиазинотриеномицин G, Тиазогалостатин, Тиелавин G, Тиелоцин В3, Тиофедрин, Тиомаринол, Тиомаринол В, Тиомаринол С, Тиомаринол D, Тиомаринол Е, Тиомаринол F, Тиовиридамид, Тиоксамицин, Тразарин, Тималлен, Тимектацин, Тимопентин, Тидемберсат, Тиеноксолол Гидрохлорид, Тигециклин, Тилизолол Гидрохлорид, Тимолол гемигидрат, Тимолол Малеат, Типелукаст, Типранавир, Тиквесид, Тисокальцитат, Тиксокортол бутират пропионат, Тоборинон, Тобрамицин, Токотриенол, Токарамид А, Толкапон, Толоксатон, Толтеродин Тартрат, Толваптан, Толитоксин, Томатин, Томегловир, Тонаберсат, Топиксантрон Гидрохлорид, Топотекан Ацетат, Топотекан Гидрохлорид, Топовал, Топсентин В1, Торцитабин, Торезолид, Тоседостат, Тосуфлоксацин, Тосуфлоксацин Тозилат, Трабектедин, Традекамид, транс-Ресвератрол, Трантинтерол Гидрохлорид, Травопрост, Траксопродил, Траксопродил Мезилат, Трекадрин, Трецетилид Фумарат, Трепростинил диэтаноламин, Трепростинил Натрия, Триамцинолон ацетонид, Триамцинолон гексацетонид, Триходимерол, Трихомицин А, Трихостатин D, Трициферол, Трицирибин, Трицирибин Фосфат, Трифлуридин, Трилостан, Тримегестон, Тримидокс, Тримопростил, Трифендиол, Триптерин, Триптолид, Троглитазон, Тровафлоксацин, Тровафлоксацин Гидрат, Тровафлоксацин Гидрохлорид Мезилат, Тровафлоксацин Мезилат, Троксацитабин, Цукубамицин А, Тубастрин, Тубелактомицин А, Туберактомицин В, Туберактомицин D, Туберактомицин Е, Тубингензин В, Тубулизин А, Тубулизин В, Тубулизин С, Тукаресол, Туфцин, Тулатромицин А, Тулатромицин В, Тулобутерол Гидрохлорид, Турбостатин 1, Турбостатин 2, Турбостатин 3, Турбостатин 4, Тиропептин А10, Тиропептин А6, Тиропептин А9, Тиросерватид, Тирфостин 47, Убенимекс, Украин, Улифлоксацин, Ункариновая кислота А, Ункариновая кислота В, Унциаламицин, Унопростон, Унопростон изопропиловый эфир, Урсодеоксихолиевая кислота, Устилипид А, Устилипид В, Устилипид С, Увалол, Вадимезан, Валганцикловир Гидрохлорид, Валнемулин, Валономицин А, Валопицитабин, Валрубицин, Ванкомицин Гидрохлорид, Ванкорезмицин, Ванидипинедилол, Ванинолол, Вариапептин, Вебуфлоксацин, Вейнамитол, Велнакрин Малеат, Велусетраг, Венорфин, Вермиспорин, Вернакалант Гидрохлорид, Вертициллатин, Вексибинол, Виалинин В, Виценистатин, Винаксантон, Виндезин, Винфосилтин Сульфат, Винлейцинол, Виниламицин, Виквидацин, Вирамидин Гидрохлорид, Виранамицин-А, Виранамицин-В, Вискозин, Витилевуамид, Воклоспорин, Воглибоз, Волинансерин, Волпристин, Ворелоксин, W Пептид, Видендиол А, Видендиол В, Вудурин, Ксамотерол Фумарат, Ксантоангелол Е, Ксантофульвин, Ксантомегнин, Ксеновулен А, Ксипамид, Ксилоцидин, Ятакемицин, Йохимбин, Забофлоксацин Гидрохлорид, Захавин В, Залцитабин, Зампанолид, Занамивир, Занкирен, Сарагосовая кислота D3, Зеландопам Гидрохлорид, Z-Элеутеробин, Зенарестат, Зидовудин, Зиласкорб (2Н), Зилпатерол, Зонампанель, Зорубицин Гидрохлорид, Зосуквидар тригидрохлорид, Зотаролимус, Зотиказон пропионат, Зуклопентиксол Гидрохлорид.
Подходящие леакрственные средства с карбоксильными группам могут быть выбраны из списка, содержащего следующие представители: (-)-Суберсиновая кислота, (+)-Деоксоартелиновая кислота, (+)-Гемипальмитоилкарнитин, (+)-Индобуфен, (+)-SCH-351448, (Е)-п-Кумароилхиновая кислота, (Z)-Инденапрост, [111In-DTPA-Pro1,Tyr4]бомбезин, [90Y]-DOTAGA-вещество Р, [пси[CH2NH]Tpg4]Ванкомицин Агликон, 111In-Пентетреотид, 11-Кето-Бета-Босвеллевая Кислота, 15-Метоксипинусолидная кислота, 1-Метил-D-триптофан, 3,5-Дикаффеоилхиновая кислота, 3-MATIDA, 3-O-Ацетилолеанолевая кислота, 4-Аминосалициловая кислота, 6альфа-Фторурсодеоксихолевая кислота, 6-Карбоксигенистеин, 7-Хлоркинуреновая кислота, 8-Карбокси-изо-иантеран А, 99mTc-c(RGDfK*)2HYNIC, A-42867 псевдоагликон, Ацеклофенак, Ацеметацин, Аценейраминовой кислоты Натриевая соль, Ацетил-11-Кето-Бета-Босвеллевая Кислота, Ацетил-Бета-Босвеллевая Кислота, Ацетилцистеин, Ахимиловые Кислоты, Аципимокс, Ацитазаноласт, акривастин, Актарит, Адапален, Адаротен, Адеметионин Тозилат Сульфат, Адксантромицин А, Аюлемовая кислота, Алацеприл, Аладапцин, Алеглитазар, Алитретиноин, Алминопрофен, Алоглиптин бензоат, альфа-Линоленовая кислота, альфа-Липоевая кислота, альфа-Метилтриптофан, Аппростадил, Алтемицидин, Алутаценовая кислота В, Апвимопан Гидрат, Амиглюмид, Аминептин, Аминокапроновая кислота, Аминолевулиновой кислоты Гидрохлорид, Амлексанокс, Амоксициллин тригидрат, Амфотерицин В, Амсиларотен, Анакинра, Антифламмин-1, Антифламмин-2, Антифламмин-3, Апалциллин Натрия, Аплавирок Гидрохлорид, Аргатробан моногидрат, Аргимесна, Артелинат, Артепиллин С, Артесунат, Арундифунгин, Аскостерозид, Азиатовая кислота, Аспирин, Аспоксициллин, Ассамицин I, Ассамицин II, Аталурен, Аторвастатин, Аторвастатин кальция, Атрасентан, Азаромицин SC, Азеловая Кислота, Азепиностатин, Азилсартан, Азоксибацилин, Азтреонам, Азтреонам L-лизин, Азумамид Е, Баклофен, Бафиломицин С1, Баикалин, Балхимицин, Балофлоксацин, Балофлоксацин дигидрат, Балсалазид динатрия, Бамирастин Гидрат, Белактоцин А, Белактоцин С, Бенаномицин А, Бенаномицин В, Бенастатин А, Бенастатин В, Беназеприл Гидрохлорид, Бентоцианин А, Бепотастин безилат, Берапрост Натрия, Бесифлоксацин Гидрохлорид, Бета-Босвеллевая Кислота, бета-Гидрокси бета-Метилбутират, Бетамипрон, Бета-Сиалозилхолестерина натриевая соль, Бевиримат, Бексаротен, Безафибрат, Биапенем, Биластин, Бимосиамоза, Биндарит, Бинфлоксацин, Бифенил-инданон А, Вос-Белактоцин А, Боррелидин, Бразиликардин А, Бразилинолид А, Бремеланотид, Бревифолин карбоновая кислота, Буцилламин, Буметанид, Бунгеоловая кислота, Бупренорфин гемиадипат, Бупренорфин -Val-карбамат, Бутибуфен, Бутоктамид гемисукцинат, Бутизамид, Кабин 1, Кадрофлоксацин Гидрохлорид, Калбистрин А, Калбистрин В, Калбистрин С, Калбистрин D, Кальций-подобный пептид 1, Кальций-подобный пептид 2, Калопорозид В, Калопорозид С, Калопорозид D, Калопорозид Е, Калопорозид F, Калпинактам, Калтеридол кальция, Кампрофен, Кандесартан, Кандоксатрил, Кандоксатрилат, Канфосфамид Гидрохлорид, Канреноат калия, Капразамицин А, Капразамицин В, Капразамицин С, Капразамицин Е, Капразамицин F, Каптоприл, Карбидопа, Кармоксирол Гидрохлорид, Карпрофен, Цефаклор, Цефалексин моногидрат, Цефбуперазон Натрия, Цефканел, Цефдалоксим, Цефдинир, Цефетекол, Цефиксим, Цефматилен Гидрохлорид Гидрат, Цефменоксим Гидрохлорид, Цефминокс Натрия, Цефодизим, Цефоницид Натрия, Цефоперазон Натрия, Цефоселис Сульфат, Цефотиам Гидрохлорид, Цефокситин, Цефпимизол Натрия, Цефпирамид Натрия, Цефпрозил, Цефпрозил моногидрат, Цефтаролин фозамил Ацетат, Цефтазидим, Цефтибутен, Цефтобипрол, Цефуроксим, Церанаприл, Церивастатин Натрия, Церулетид диэтиламин, Цетефлоксацин, Цетиризин Гидрохлорид, Хенодеоксихолевая кислота, Хиноин-169, Хлорамбуцил, Хлорориентицин А, Хлорориентицин В, Холин фенофибрат, Холин тиоктат, Хролактомицин, Циластатин Натрия, Цилазаприл, Циленгитид, Циломиласт, Цилупревир, Цинацикват, Циналукаст, Цинатрин А, Цинатрин В, Цинатрин С1, Цинатрин С2, Цинатрин С3, Циннатриацетин А, Циннатриацетин В, Ципрофибрат, Ципрофлоксацин Гидрохлорид, Цирцинамид, Циспентацин, Цитруллимицин А, Клаваровая кислота, Кпавуланат калия, Клинофибрат, Клопидогреля Сульфат, Коллетовая кислота, Комплестатин, Конагенин, Козалан, Креатин Фосфат, Циклокреатин, Циклоплатам, Циклотиалидин, Цитомодулин, Цитоспоровая кислота, Дабигатран, Даглутрил, Даларгин, Далбаванцин, Данегаптид Гидрохлорид, Данофлоксацин, Даринапарсин, Дарусентан, Даурихроменовая кислота, Давунетид, Декагидромоеномицин А, Декапланин, Декатромицин А, Декатромицин В, Деферазирокс, Делафлоксацин, Делаприл Гидрохлорид, Делтибант, Деоксилаидломицин, Деоксинегамицин, Дерсалазин, Дезацетилвинбластингидразид/фолат Конъюгат, Десферри-даноксамин, Десферри-норданоксамин, Дезглугастрин трометамин, Десмин-370, Дексибупрофен, Дексибупрофен лизин, Декскетопрофен, Декскетопрофен холин, Декскетопрофен D,L-лизин, Декскетопрофен лизин, Декскетопрофен меглумин, Декскетопрофен трометамол, Декслоксиглумид, Декспемедолак, декстро-Ципрофибрат, Дексилозилбенаномицин А, Диацереин, Диазафилоновая кислота, Ди-Кальцифор, Дифеноксин, Дифлунизал, Дигидроавенантрамид D, Дигидрогранатицин В, Дигидроизостевиол, Дигидролипоевая кислота, Дисалазин, Дисила-бексаротен, Динатрия кромпроксат, Динатрия леттузат, Докваласт, Дорипенем, Дормитробан, Дорригоцин А, Дорригоцин В, Дроксидопа, DTPA-аденозилкобаламин, Дурамицин, Динемицин А, Экабет Натрия, Эценофлоксацин Гидрохлорид, Эконазол Сульфосалицилат, Эдетовая кислота, Эдотреотид иттрия, Эфлетиризин, Эфлорнитин Гидрохлорид, Эглуметад Гидрат, Эланзолид С1, Эларофибан, Эластатинал В, Эластатинал С, Элсибукол, Элтромбопаг оламин, Элвитегравир, Эмрикасан, Эналаприл Малеат, Эналаприл нитрат, Эналаприлат, Энфумафунгин, Энкастин (D), Энкастин AD, Энкастин АЕ, Энкастин ID, Энкастин IE, Энкастин VD, Энкастин VE, Энолоксон, Эноксацин, Энрасентан, Энрофлоксацин, Эпалрестат, Эпидиоксиманадовая кислота А, Эпидиоксиманадовая кислота В, Эпиталон,Эпофолат, Эпопростенол Натрия, Эпостатин, Эпристерид, Эпросартан Мезилат, Эпротиром, Эпталопрост, Эпластатин Натрия, Эптастигмин Тартрат, Эптифибатид, Эрдостеин, Эремомицин, Эртапенем Натрия, Эртипротафиб, Эрилозид F, Эсафлоксацин Гидрохлорид, Эзонаримод, Этакриновая кислота, Эталоциб Натрия, Этодолак, Этретин, Эватанепаг, Эвернимицин, Эксисулинд, Эзетимиб глюкуронид, Фандофлоксацин Гидрохлорид, Фаранокси, Фарглитазар, Фаропенем Натрия, Фасобегрон Гидрохлорид, Фебуксостат, Феглимицин, Фелбинак, Фелбинак Лизиновая Соль, Фенбуфен, Фексофенадин Гидрохлорид, Фидексабан, Финафлоксацин Гидрохлорид, Флероксацин, Флобуфен, Фломоксеф Натрия, Флунопрост, Флуноксапрофен, Флурбипрофен, Флувастатин Натрия, Фолиновая кислота, Фондапаринукс Натрия, Фосфосал, Фрадафибан, Фрусемид, Фудостеин, Фурпрофен, G1 пептид, Габадур, Габапентин, Габапентин энакарбил, Габусектин, Гадобеновой кислоты димеглуминовая соль, Гадобутрол, Гадоколетовой кислоты тринатриевая соль, Гадодентерат, Гадомелитол, Гадопентетат димеглумин, Гадотерат меглумин, Гадотеридол, Гамбоговая кислота, Гамендазол, Гамма-Линоленовая Кислота, Ганефромицин Альфа, Ганефромицин Бета, Ганглиозид GM1, Ганодеровая кислота X, Гареноксацин Мезилат, Гастразол, Гатифлоксацин, Гемфиброзил, Гемифлоксацин Мезилат, Гемопатрилат, Гилатид, Гиматекан, Гирипладиб, Гласпимод, Глюкаролактам калия, Глудопа, Глутатиона Моноэтиловый Эфир, Глутатиона Моноизопропиловый Эфир, Глицин-пролин-Мелфалан, Гликопин, Глицирризиновая кислота, Голотимод, Гудиерозид В, Горалатид, Грепафлоксацин Гидрохлорид, GS-143, Гатерумадиоксин А, Гатерумадиоксин В, Гелвекардин А, Гелвекардин В, Гептелидовой кислоты хлоргидрин, Гериценал А, Гериценал В, Гериценал С, Гомоинданомицин, Хонгокверцин А, Хонгокверцин В, Человеческий ангиотензин II, Гиалуронат Натрия, Гидростатин А, Ибупрофен, Икатибант Ацетат, Икофунгипен, Идраприл, Ифетробан, Илепатрил, Илопрост, Имидаприл, Имидаприл Гидрохлорид, Имиглитазар, Имипенем, Инданапрост (S), Инданомицин, Индеглитазар, Индобуфен, Индол-3-пропионовая кислота, Индометацин, Индометацин трометамол, Индоксам, Индинапрост, Иногатран, Иносиплекс, Йододифлунизал, Иодофилтовая кислота-[123I], Иодстеариновая Кислота, Иралукаст, Иралукаст Натрия, Изалстеин, Изобонгкрековая кислота, Изотретиноин, Итавастатин кальция, Итриглумид, Каитоцефалин, Канглемицин А, Капуримицин А1, Капуримицин A3, Кетопрофен, Кетопрофен лизин, Кеторолак, Кеторолак трометамин, Кафрефунгин, Кижимицин, Кистамицин А, L-4-Охализин, Лабрадимил, Ламектацин, Ламифибан, Лантиопептин, Лапаквистат Ацетат, Ларазотид Ацетат, Ларопирант, Латамоксеф Натрия, L-Цикориевая кислота, Ленапенем Гидрохлорид, Ленапенем Гидрохлорид Гидрат, Левокабастин Гидрохлорид, Левоцетиризин Дигидрохлорид, лево-Ципрофибрат, Леводопа, Леводопа 3-O-глюкозид, Леводопа 4-O-глюкозид, Левофлоксацин, Левонадифлоксацина аргининовая соль, L-Гомотиоцитруллин, Ликофелон, Лакрица-сапонин С2, Лидорестат, Лимапрост альфадекс, Лимазоцик, Линолевая кислота 18:2w6-цис,9-цис, Линотробан, Линтитрипт, Липогексин, Лизиноприл, Лития Сукцинат, Литоспермовой кислоты В магниевая соль, Лолоатин В, Ломефлоксацин Гидрохлорид, Лометрексол, Лонгестин, Лонидамин, Лоракарбеф Гидрат, Лорглумид, Лотрафибан, Локсиглумид, L-Симексонил Гомоцистеин, L-Тиоцитруллин, Лубипростон, Люмиракоксиб, Lu-Tex бис(глюконат), Лизинированная-бетулоновая кислота, Лизина ацетилсалицилат, Макрокарпин В, Мадекассоновая кислота, Мараценин А1, Мараценин А2, Мараценин В1, Мараценин В2, Мараценин С1, Мараценин С2, Мараценин D1, Мараценин D2, Марбофлоксацин, Маслиновая кислота, Матристатин А1, Матристатин А2, Маттеуориенат А, Маттеуориенат В, Маттеуориенат С, Меброфенин, Меклинертант, Мефенамовая кислота, Мелагатран, Мемно-пептид А, Мептазинол-Val-карбамат, Меропенем, Мерсацидин, Месалазин, Метезинд глюкуронат, Метанобактин, Метотрексат, Метоксатин, Метилдопа, Метиленолактоцин, Метилгомоиндономицин, Метиаприл, Метирозин, Микакоцидин А, Микакоцидин В, Мидафотел, Мидориамин, Милринон Лактат, Минервал, Мипитробан, Миспировая кислота, Миксанприл, Моеномицин А хлорида висмутовая соль, Моэксиприл Гидрохлорид, Моэксиприлат, Мофезолак, Момордин Ic, Монамидоцин, Моноэтаноламина Олеат, Монтелукаст Натрия, Морфин Глукуронид, Моксифлоксацин Гидрохлорид, Мумбаистатин, Мупироцин, Мураглитазар, Мураминомицин А, Мураминомицин В, Мураминомицин С, Мураминомицин D, Мураминомицин Е1, Мураминомицин Е2, Мураминомицин F, Мураминомицин G, Мураминомицин Н, Мураминомицин I, Мураминомицин Z1, Мураминомицин Z2, Мураминомицин Z3, Мураминомицин Z4, Муреидомицин А, Муреидомицин В, Муреидомицин С, Муреидомицин D, Муреидомицин Е, Муреидомицин F, Муреидомицин, Микапероксид А, Микапероксид В, Мицестерисин Е, Микофеноловой кислоты Натриевая соль, Мирицеровая кислота А, Митолбилиновая кислота, Надифлоксацин, Нафагрел Гидрохлорид, Нафагрел Гидрохлорид гемигидрат, Нагстатин, Напиримус, Напсагатран, Напсамицин А, Напсамицин В, Напсамицин С, Напсамицин D, Натеглинид, Навеглитазар, Небостинел, Немоноксацин, Neu5Ac2en, Ниацин, Ниглизин, Нилепрост бета-циклодекстрин клатрат, Нооглютил, Норфлоксацин, Норфлоксацин сукцинил, Обетихолевая кислота, Октакозамицин А, Октакозамицин В, O-Деметилхлоротрицин, Офлоксацин, Оламуфлоксацин, Оламуфлоксацин Мезилат, Оланзапин памоат, Олеанолевая кислота, Олмесартан, Олопатадин Гидрохлорид, Олсалазин Натрия, Омапатрилат, ОннамидА, ОРС-17083, Опиорфин, Орбифлоксацин, Орегановая кислота, Ориентицин А, Ориентицин В, Ориентицин С, Ориентицин D, Оритаванцин, Орниплабин, Осельтамивир карбоксилат, Овотиол А, Овотиол В, Овотиол С, Оксапрозин, Оксеглитазар, Оксиглутатион Натрия, Оксиморфон-Val-карбамат, Оксинор, Озагрел Гидрохлорид, Озеноксацин, Пактимиб, Падопорфин, Пецилохинон В, Пецилохинон D, Палдимицин В, Паловаротен, Панипенем, Паразин I, Паринаровая кислота, Пауломицин, Пауломицин А2, Пауломицин В, Пауломицин С, Пауломицин D, Пауломицин Е, Пауломицин F, Пазуфлоксацин, Пазуфлоксацин Мезилат, Пефлоксацин, PEG-ванкомицин, Пелагиомицин С, Пелиглитазар, Пелитрексол, Пелретин, Пенастерол, Пеницилламин, Перамивир, Периндоприл, PG-камптотецин, Фомалленовая кислота С, Фомоидрид А, Фомоидрид В, Фосфиновый циклокреатин, Фосфозалсалат, Физостигмин салицилат, Пибаксизин, Пидотимод, Пираксостат, Пиретанид, Пирфеноксон, Пирпрофен, Пивагабин, Пиксантрон Малеат, Плакотенин, Платенцин, Платенсимицин, Плевитрексед, Плурафлавин Е, Плюсбацин А1, Плюсбацин А2, Плюсбацин A3, Плюсбацин А4, Плюсбацин В1, Плюсбацин В2, Плюсбацин В3, Плюсбацин В4, Полиалтидин, Помисартан, Поналрестат, Постстатин, PPI17-24, Прадимицин А, Прадимицин В, Прадимицин D, Прадимицин Е, Прадимицин FA-1, Прадимицин FA-2, Прадимицин FL, Прадимицин FS ((+)-энантиомер), Прадимицин L, Прадимицин Q, Прадимицин S, Прадимицин Т1, Прадимицин Т2, Прадофлоксацин, Пралатрексат, Пранопрофен, Префолик А, Прегабалин, Премафлоксацин, Премафлоксацин Гидрохлорид, Презатид меди ацетат, Проамипид, Пробенецид, Пробестин, Процистеин, Проглумид, Пропагерманиум, Пропофол гемисукцинат, Простатин, Простратин Сукцинат, Протокатеховая кислота, Протопорфирин IX галлия(III) комплекс, Прулифлоксацин, Прулифлоксацин Гидрохлорид, Прулифлоксацин Мезилат, Псевдомицин А', Псевдомицин В', Пикнантухинон А, Пикнантухинон В, Пилорицидин В, Пиридазомицин, Пирролоспорин А, Хифлапон Натрия, Хинаприл Гидрохлорид, Хинлукаст, Рафабегрон, Рагаглитазар, Ралтитрексед, Раматробан, Рамиприл, Раксофеласт, Разупенем, Ребамипид висмута цитрат тетраметиледамин, Ребамипид висмута L-Тартрат тетраметиледамин, Репаглинид, Резобен, Реверомицин А, Рододаурихромановая кислота А, Ридогрел, Робенацоксиб, Рокаглоевая кислота, Ролафагрел, Ромазарит, Ромуртид, Розапростол Натрия, Розувастатин кальция, Розувастатин Натрия, Руфлоксацин Глюконат, Руфлоксацин Гидрохлорид, Румицин 1, Румицин 2, Салазопиридазин, Салкапрозовой кислоты натриевая соль, Салицилазобензойная кислота, S-Аллилмеркаптокаптоприл, Салмистеин, Сальвианоловая кислота L, Самиксогрел, Сампатрилат, Санфетринем, Санфетринем Натрия, Сапуримицин, Сарпогрелат Гидрохлорид, Сауссурамин А, Сауссурамин В, Сауссурамин С, Сауссурамин D, Сауссурамин Е, Скабронин G, Скопадульцевая кислота В, Секуриозид А, Секуриозид В, Селанк, Семдурамицин, Сеокальцитол, Сератродаст, Серофендовая кислота, Сессилозид, Шефердин, Сиалозилхолестерин-Альфа Натрия Соль, Ситафлоксацин Гидрат, S-Нитрозокаптоприл, S-Нитрозоглутатион, Соделглитазар, Натрия хромогликат, Натрия оксибат, Софалкон, Солабегрон Гидрохлорид, Сорбициллактон А, Спарфлоксацин, Сфингофунгин F, Спинорфин, Спираприл, Спирипростил, Спироглумид, Спироксимицин, Сквалестатин I, Стахибоцин А, Стахибоцин В, Стахибоцин С, Стаплабин, Старризин, Стеренин D, Субтилопентадекановая кислота, Сукцинобукол, Суфотидин висмута цитрат, Шугаммадекс Натрия, Сульфасалазин, Сулиндак, Сулопенем, Сулукаст, ингибитор-1 трипсина подсолнечника, Сусалимод, Тафамидис меглумин, Тагефлар, Талаглуметад Гидрохлорид, Талибегрон, Талибегрон Гидрохлорид, Талоптерин, Талтобулин, Тамибаротен, Таногитран, Таномастат, ТАР-доксорубицин, Таренфлурбил, Таргинин, Тазаротеновая Кислота, Тебипенем, Тейкопланин-А2-1, Тейкопланин-А2-2, Тейкопланин-А2-3, Тейкопланин-А2-5, Телаванцин Гидрохлорид, Телместеин, Телмисартан, Темафлоксацин Гидрохлорид, Темокаприл Гидрохлорид, Темуртид, Теносал, Тербогрел, Терестигмин Тартрат, Терикалант Фумарат, Тезаглитазар, Тетомиласт, Тетрадецилселеноуксусная кислота, Тетрафибрицин, Тетрагаллоилхиновая кислота, Тетрагидроэхинокандин В, Тетронотиодин, Тезампанел, Термозимоцидин, Тиазогалостатин, Тиелавин G, Тиелоцин, Тиелоцин В3, Тиофоскарнет, Тиоксамицин, Тразарин, гуморальный фактор тимуса гамма-2, Тимопентин, Тиагабин Гидрохлорид, Тибенеласт, Тиколубант, Тиларгинин Гидрохлорид, Тилихинатин, Тимодепрессин, Типелукаст, Типлазинин, Тирофибан Гидрохлорид, Тисартан, Толфенамовая кислота, Толметин, Толрестатин, Томопенем, Тосуфлоксацин, Тосуфлоксацин Тозилат, Трандолаприл, Трандолаприлат, Транексамовая кислота, Траниласт, Трепростинил диэтаноламин, Трепростинил Натрия, Третиноин, Триацетилшикимовая кислота, Трихомицин А, Трифлузал, Тримексаутид, Тримопростил, Триптерин, Тропезин, Тровафлоксацин, Тровафлоксацин Гидрат, Тровафлоксацин Гидрохлорид Мезилат, Тровафлоксацин Мезилат, Тубелактомицин А, Туберактомицин D, Туберактомицин Е, Тубулизин А, Тубулизин В, Тубулизин С, Тукаресол, Туфцин, Турбинаровая кислота, Тиросерватид, Убенимекс, Улифлоксацин, Ункариновая кислота А, Ункариновая кислота В, Унопростон, Урсодеоксихолевая кислота, Фосфат Урсоловой кислоты, Утибаприл, Утибаприлат, Вадимезан, Валономицин А, Неполный вальпроат натрия, Вальпроевая кислота, Валсартан, Ванкомицин Гидрохлорид, Вареспладиб, Вебуфлоксацин, Ведапрофен, Велифлапон, Верлукаст, Винаксантон, Вихидацин, Виранамицин-А, Вискозин, Витилевуамид, Ворелоксин, W Пептид, Ксантофульвин, Забициприл Гидрохлорид, Забициприлат Гидрохлорид, Забофлоксацин Гидрохлорид, Залтопрофен, Занамивир, Сарагосовая кислота D3, Зенарестат, Зофеноприлат, Зофеноприлат аргинин, Золасартан, Зонампанел.
Подходящие лекарственные средства с фосфатной группой могут быть выбраны из группы, состоящей из следующих представителей: Аденофостин А, Аденофостин В, Атринозитол, Буфломедил пиридоксалфосфат, Цитостатин, Флударабин Фосфат, Фосфлуконазол, Фосфонохлорин, Фосфосал, Фосопамин, Фосквидон, Фостаматиниб, Ганцикловир Монофосфат, Генистеин-7-Фосфат, Гидроксифослактомицин В, Лейстродуксин А, Лейстродуксин В, Лейстродуксин С, Лейстродуксин Н, Мангафодипир тринатрия, Менадиол Натрия дифосфат, Мипроксифен Фосфат, Монофосфорил липид А, Фосфолин, Фосфозалсалат, Пневмокандин В0 2-Фосфат, Тафлупозид, Трицирибина Фосфат, Урсоловой кислоты Фосфат.
Подходящие лекарственные средства с тиольной группой могут быть выбраны из группы, состоящей из следующих представителей: Ацетилцистеин, Антилейкинат, Аргимесна, Буцилламин, Бутиксокорт, Каптоприл, Дигидролипоевая кислота, Гемопатрилат, Глутатиона моноэтиловый эфир, Глутатиона моноизопропиловый эфир, Мидориамин, Омапатрилат, Овотиол А, Овотиол В, Овотиол С, Пеницилламин, Ребимастат, Шефердин, Зофеноприлат, Зофеноприлат аргинин.
На Фиг. 6 представлено схематическое изображение участка гидрогеля, содержащего стабильные связки фрагментов основной цепи с временным линкером пролекарства, к которому ковалентно присоединен биологически активный фрагмент. Сверхразветвленный фрагмент (овал, "Hyp") содержит стабильные связи (белые ромбы) с временным линкером пролекарства (черная стрелка) или спейсерным фрагментом, связанным с фрагментом основной цепи, и связанным с другой стороны со поперечносшивающим фрагментом (жирная черная линия). Тонкая черная линия изображает полимерную цепь на основе PEG, отходящую от разветвляющегося ядра (не показано). Пунктирные линии указывают место присоединения к большему фрагменту, который не изображен полностью
На Фиг. 6а показано прямое связывание временного линкера пролекарства со сверхразветвленным фрагментом, тогда как на Фиг. 6b показано непрямое связывание временного линкера пролекарства со сверхразветвленным фрагментом. На Фиг. 6b временный линкер пролекарства соединен со сверхразветвленным фрагментом через спейсерный фрагмент (жирная серая линия), который связан с временным линкером пролекарства через стабильную связь (белый ромб). В каждом случае, лекарственный фрагмент (большой белый круг) соединен с временным линкером пролекарства через биоразлагаемую связку (белая стрелка).
Разложение гидрогеля
Разложение гидрогеля по настоящему изобретению представляет собой многостадийную реакцию, в ходе которой расщепляется множество разрушаемых связей, давая продукты разложения, которые могут быть водорастворимыми или нерастворимыми в воде. Однако нерастворимые в воде продукты разложения могут содержать разрушаемые связи, так что они могут расщепляться таким образом, что образуются водорастворимые продукты разложения. Эти водорастворимые продукты разложения могут содержать один или более фрагментов основной цепи. Понятно, что высвобождаемые фрагменты основной цепи могут, например, быть стабильно конъюгированы со спейсерными или блокирующими или линкерными группами, или аффинными группами и/или продуктами разложения линкера пролекарства, и также что водорастворимые продукты разложения могут содержать разрушаемые связи.
Структуры разветвляющегося ядра, полимерных цепочек на основе PEG, сверхразветвленных дендритных фрагментов и фрагментов, присоединенных к сверхразветвленным дендритным фрагментам, можно понять из соответствующих определений, данных в разделах, описывающих различные гидрогели по настоящему изобретению. Понятно, что структура деграданта зависит от типа гидрогеля по настоящему изобретению, претерпевающего разложение.
Общее количество фрагментов основной цепи можно измерить в растворе после полного разложения гидрогеля по настоящему изобретению, и во время разложения фракции растворимых продуктов разложения в виде основных цепей можно отделять от нерастворимого гидрогеля по настоящему изобретению и количественно охарактеризовать без перекрывания с другими растворимыми продуктами разложения, высвобождаемыми из гидрогеля по настоящему изобретению. Гидрогельный объект можно отделить от избытка воды буфера, имеющего физиологическое значение осмоляльности, методом седиментации или центрифугирования. Центрифугирование можно проводить таким образом, что надосадочный раствор составляет по меньшей мере 10% от объема набухшего гидрогеля по настоящему изобретению. Растворимые продукты разложения гидрогеля после такой стадии седиментации или центрифугирования остаются в водном надосадочном растворе, и водорастворимые продукты разложения, содержащие один или более фрагментов основной цепи, можно детектировать, анализируя аликвоты такого надосадочного раствора подходящими методами разделения и/или анализа.
Предпочтительно, водорастворимые продукты разложения можно отделить от нерастворимых в воде продуктов разложения фильтрованием через фильтры с диаметром пор 0.45 мкм, после которого водорастворимые продукты разложения находятся в фильтрате. Водорастворимые продукты разложения можно отделить от нерастворимых в воде продуктов разложения комбинацией стадий центрифугирования и фильтрования.
Например, фрагменты основной цепи могут нести группы, обладающие УФ-поглощением при длинах волн, при которых другие продукты разложения не проявляют УФ-поглощения. Такие селективно УФ-поглощающие группы могут быть структурными компонентами фрагмента основной цепи, такими как амидные связи, или могут вводиться в каркас присоединением к его реакционноспособным функциональным группам посредством ароматических циклических систем, таких как индолильные группы.
На Фиг. 7 представлено схематическое изображение разных продуктов разложения. Пример продукта разложения, изображенный на Фиг. 7а, является результатом разложения биоразлагаемого гидрогеля, несущего конъюгатные функциональные группы. От центрального разветвляющегося ядра (©) отходят четыре полимерные цепочки на основе PEG (тонкие черные линии), к концам которых присоединены сверхразветвленные дендритные фрагменты ("Hyp"; овалы). Указанные сверхразветвленные дендритные фрагменты содержат несколько стабильных связок (белые ромбы) со спейсерными фрагментами, соединенными с фрагментом основной цепи, а с другой стороны соединенными со поперечносшивающим фрагментом (звездочка), или с конъюгатами, такими как аффинные лиганды или хелатирующие группы (черные овалы). Пунктирные линии указывают место присоединения к большему фрагменту, который не показан.
Пример продукта разложения, изображенный на Фиг. 7b, является результатом разложения биоразлагаемого гидрогеля, несущего пролекарства. От центрального разветвляющегося ядра (©) отходят четыре полимерные цепочки на основе PEG (тонкие черные линии), к концам которых присоединены сверхразветвленные дендритные фрагменты ("Hyp"; овалы). Указанные сверхразветвленные дендритные фрагменты содержат несколько стабильных связок (белые ромбы) со спейсерными фрагментами, присоединенными к фрагменту основной цепи, а другим концом присоединенными к поперечносшивающему фрагменту (звездочка), или со спейсерными фрагментами (белый прямоугольник), которые соединены с временным линкером пролекарства (черная стрелка). Понятно, что указанный спейсерный фрагмент является опциональным и зависит от типа гидрогеля по настоящему изобретению. Пунктирные линии указывают место присоединения к большему фрагменту, который не показан.
Понятно, что сверхразветвленные дендритные фрагменты продуктов разложения содержат больше стабильных связок со спейсерными реагентами, присоединенными к фрагменту основной цепи, а другим концом присоединенными к поперечносшивающему фрагменту, конъюгатами или временными линкерами пролекарств, чем показано на Фиг. 7а и 7b.
Синтез биоразлагаемых реакционноспособных гидрогелей
Биоразлагаемые реакционноспособные гидрогели можно получить несколькими различными методами. Такие методы описаны, например WO-A 2006/003014. В основе одного частного процесса синтеза, основанного на радикальной или ионной полимеризации, лежит применение поперечносшивающего макромономера или поперечносшивающего мономера - так называемых поперечносшивающих реагентов, - несущих по меньшей мере две сшивающие функциональные группы и функционального макромономера - так называемого реагента основной цепи. Реагенты основной цепи несут по меньшей мере одну сшивающую функциональную группу и по меньшей мере одну химическую функциональную группу, которая не участвует в стадии полимеризации. Могут присутствовать или отсутствовать дополнительные мономеры-разбавители. Сополимеризация перечисленных компонентов дает гидрогель по настоящему изобретению содержащий реакционноспособные функциональные группы, предоставляемые фрагментом основной цепи. Чтобы гарантировать, что реакционноспособная функциональная группа доступна для реакций по окончании полимеризации, условия соединяющей полимеризации выбирают таким образом, чтобы реакционноспособные функциональные группы не модифицировались. Альтернативно, реакционноспособные функциональные группы можно защитить с помощью обратимых защитных групп, известных квалифицированным специалистам в данной области, которые после полимеризации удаляют. Подходящие сшивающие функциональные группы включают (но не ограничиваются только ими) радикально полимеризуемые группы, такие как винильные, винил-бензольные, акрилатные, акриламидные, метакрилатные, метакриламидные, и ионно-полимеризуемые группы, такие как оксетановая, азиридиновая и оксирановая.
В альтернативном способе получения, биоразлагаемый гидрогель по настоящему изобретению получают реакциями химического сшивания. В одном альтернативном способе, исходным материалом является одно макромолекулярное исходное соединение с комплементарными функциональными группами, которые претерпевают реакцию, такую как реакция конденсации или присоединения, которое представляет собой гетеромультифункциональный реагент основной цепи, содержащий несколько полимеризуемых функциональных групп.
Альтернативно, биоразлагаемый гидрогель по настоящему изобретению может быть сформирован из двух или более макромолекулярных исходных соединений с комплементарными функциональными группами, которые претерпевают реакцию, такую как реакция конденсации или присоединения. Один из данных исходных материалов представляет собой поперечносшивающий реагент, содержащий по меньшей мере две одинаковые полимеризуемые функциональные группы, а другой исходный материал представляет собой гомомультифункциональный или гетеромультифункциональный реагент основной цепи, также содержащий несколько полимеризуемых функциональных групп.
Подходящие полимеризуемые функциональные группы, имеющиеся в поперечносшивающем реагенте, включают терминальные первичные и вторичные амины, карбоновые кислоты и их производные, малеимид, тиол, гидроксил и другие альфа-бета-ненасыщенные акцепторы Михаэля, такие как винилсульфоновые группы. Подходящие полимеризуемые функциональные группы, имеющиеся в реагенте основной цепи, включают (но не ограничиваются только ими) первичные и вторичные амины, карбоновые кислоты и их производные, малеимид, тиол, гидроксил и другие альфа-бета-ненасыщенные акцепторы Михаэля, такие как винилсульфоновые группы.
Если полимеризуемая функциональные группы поперечносшивающего реагента используются в количестве меньше стехиометрического относительно полимеризуемых функциональных групп реагента основной цепи, получаемый биоразлагаемый гидрогель по настоящему изобретению будет представлять собой реакционноспособный биоразлагаемый гидрогель со свободными реакционноспособными функциональными группами, присоединенными к структуре основной цепи, т.е. к фрагментам основной цепи.
Синтез пролекарств на основе гидрогеля
Пролекарство на основе гидрогеля по настоящему изобретению можно получить исходя из реакционноспособного биоразлагаемого гидрогеля или модифицированного реакционноспособного биоразлагаемого гидрогеля по настоящему изобретению обычными способами, известными в данной области техники. Квалифицированному специалисту понятно, что существует несколько способов. Например, упомянутый выше линкер пролекарства, к которому ковалентно присоединен биологически активный фрагмент, можно ввести в реакцию с реакционноспособными функциональными группами гидрогеля по настоящему изобретению, который уже несет или не несет активный фрагмент, частично или полностью.
Необязательно, линкер пролекарства можно сначала конъюгировать с биологически активным фрагментом, и полученный конъюгат биологически активный линкерный фрагмент пролекарства можно затем вводить в реакцию с реакционноспособными функциональными группами биоразлагаемого гидрогеля. Альтернативно, после активирования одной из реакционноспособных функциональных групп линкера пролекарства, конъюгат линкер-гидрогель можно вводить в контакт с биологически активным фрагментом во второй стадии, и избыток биологически активного фрагмента (например, избыток лекарственного средства) можно удалить промывкой и фильтрованием после конъюгирования биологически активного фрагмента с гидрогель-связанным линкером пролекарства. Несмотря на большой размер пор гидрогеля по настоящему изобретению, биологически активный фрагмент остается связанным внутри биоразлагаемого гидрогеля по настоящему изобретению посредством ковалентного соединения подходящей химической функциональной группы, имеющейся в биологически активном фрагменте, со второй химической функциональной группой в линкере пролекарства.
Предпочтительно, ковалентное связывание, формирующееся между реакционноспособными функциональными группами, предоставляемыми фрагментами основной цепи, и химическими функциональными группами линкера пролекарства, представляет собой стабильные связи. Подходящие реакционноспособные функциональные группы для связывания линкера пролекарства с реакционноспособным биоразлагаемым гидрогелем включают (но не ограничиваются только ими) карбоновые кислоты и их производные, карбонаты и их производные, гидроксил, гидразин, гидроксиламин, полуамид малеиновой кислоты и его производные, кетон, амино-группу, альдегид, тиол и дисульфид.
Предпочтительным способом получения пролекарства по настоящему изобретению является описанный далее:
Предпочтительное исходное соединение для синтеза реагента основной цепи представляет собой 4-разветвленный PEG тетра-амин или 8-разветвленный PEG окта-амин, при этом PEG-реагент имеет молекулярный вес в диапазоне от 2000 до 10000 дальтон, наиболее предпочтительно от 2000 до 5000 дальтон. К таким мульти-разветвленным PEG-производным последовательно присоединяют остатки лизина с образованием сверхразветвленного реагента основной цепи. Понятно, что остатки лизина могут быть частично или полностью защищены защитными группами во время стадий присоединения, и что конечный реагент основной цепи также может содержать защитные группы. Предпочтительным строительным блоком является бис-boc-лизин.
Альтернативно, вместо последовательного добавления остатков лизина, можно сначала ввести дендритный поли-лизиновый фрагмент, и затем связать его с 4-разветвленным PEG тетра-амином или 8-разветвленным PEG окта-амином. Желательно получить реагент основной цепи, несущий 32 амино-группы, следовательно, по семь остатков лизина должно быть присоединено к каждому разветвлению 4-разветвленного PEG, или по пять остатков лизина должно быть присоединено к каждому разветвлению 8-разветвленного PEG.
В другом варианте выполнения, мульти-разветвленное PEG производное представляет собой тетра- или окта-карбокси PEG. В этом случае дендритные фрагменты могут генерироваться из глютаминовой или аспарагиновой кислоты, и получаемый реагент основной цепи несет 32 карбокси-группы. Понятно, что все или часть реакционноспособных функциональных групп реагента основной цепи могут присутствовать в свободной форме, в виде солей или быть связаны с защитными группами. Понятно, что по практическим соображениям число остатков лизина в реагенте основной цепи на каждое PEG-разветвление будет составлять между 6 и 7, более предпочтительно примерно 7.
Предпочтительный реагент основной цепи показан ниже:
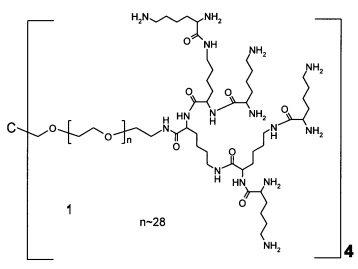
Синтез поперечносшивающего реагента начинается с линейного PEG, имеющего молекулярный вес в диапазоне от 0.2 до 5 кДа, более предпочтительно от 0.6 до 2 кДа, который этерифицируют полуэфиром дикарбоновой кислоты, наиболее предпочтительно адипиновой кислоты или глутаровой кислоты. Предпочтительной защитной группой для образования полуэфира является бензильная группа. Полученные бис-полуэфиры PEG и дикарбоновой кислоты превращают в более реакционноспособные карбокси-соединения, такие как ацилхлориды или активные сложные эфиры, например пентафторфенильные или N-гидроксисукцинимидные сложные эфиры, наиболее предпочтительно N-гидроксисукцинимидные сложные эфиры, предпочтительная структура которых показана ниже.
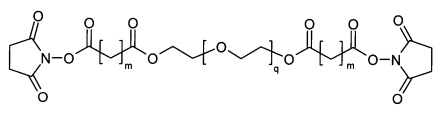 ,
,
где каждый m независимо равен целому числу в диапазоне от 2 до 4, и
q представляет собой целое число от 3 до 100.
Более предпочтительна следующая структура:
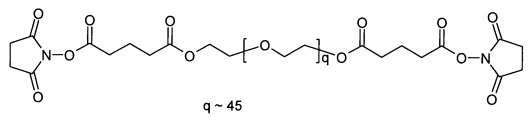 ,
,
Альтернативно, бис-полуэфиры PEG и дикарбоновой кислоты можно активировать в присутствии каплинг-агента, такого как ДЦК или HOBt или РуВОР.
В альтернативном варианте выполнения, реагент основной цепи несет карбоксильные группы, а соответствующий поперечносшивающий реагент выбирают из содержащих сложноэфирные группы PEG-цепочек с аминогруппами в терминальном положении.
Реагент основной цепи и поперечносшивающий реагент можно полимеризовать с образованием гидрогеля по настоящему изобретению, применяя обращенную полимеризацию в эмульсии. После выбора желаемого стехиометрического соотношения между полимеризуемыми функциональными группами агента основной цепи и пеперечносшивающего агента, агент основной цепи и поперечносшивающий агенты растворяют в ДМСО и применяют подходящий эмульгатор с нужным значением показателя гидрофильно-липофильного баланса (HLB), предпочтительно Arlacel P135, для формирования обращенной эмульсии с помощью механической мешалки и контроля скорости перемешивания. Полимеризацию инициализируют добавлением подходящего основания, предпочтительно N,N,N',N'-тетраметилендиамина. После перемешивания в течение необходимого времени, реакцию гасят добавлением кислоты, такой как уксусная кислота, и воды. Собирают гранулы, промывают и фракционируют по размеру частиц путем механического просеивания. Необязательно, на данной стадии можно удалить защитные группы.
В альтернативном варианте выполнения настоящего изобретения, мульти-функциональные фрагменты соединяют с реакционноспособными функциональными группами полимеризованного реакционноспособного биоразлагаемого гидрогеля для увеличения числа реакционноспособных функциональных групп, что позволяет увеличить загрузку лекарственного средства в биоразлагаемом гидрогеле по настоящему изобретению. Такие мульти-функциональные фрагменты могут предоставляться подходящим образом замещенными производными лизина, дилизина, трилизина, тетрализина, пентализина, гексализина, гептализина или олиголизина, низкомолекулярными полиэтилениминами, орнитином, диаминомасляной кислотой. Предпочтительно, указанный мульти-функциональный фрагмент представляет собой лизин.
Кроме того, такой гидрогель по настоящему изобретению можно функционализировать спейсером, несущим такую же реакционноспособную функциональную группу, например, амино-группы можно ввести в модифицированный реакционноспособный биоразлагаемый гидрогель сочетанием с гетеробифункциональным спейсером, таким как надлежащим образом активированный COOH-(EG)6-NH-fmoc, и удаление защитной fmoc-группы.
В одном варианте выполнения, лекарственное соединение может напрямую вступать в реакцию с реакционноспособным биоразлагаемым гидрогелем с образованием ковалентной временной связки, давая пролекарство на основе гидрогеля по настоящему изобретению. Такой временной связкой между лекарственным средством и биоразлагаемым гидрогелем по настоящему изобретению предпочтительно является карбамат, сложный эфир, амид или карбонат.
В другом варианте выполнения, лекарственное соединение сначала конъюгируют со спейсером таким образом, что связка между лекарственным соединением и спейсером представляет собой ковалентную временную связку, такую как карбаматная, сложноэфирная, амидная или карбонатная связка, и затем реагирует с реакционноспособным биоразлагаемым гидрогелем, формируя пролекарство по настоящему изобретению.
В другом варианте выполнения, лекарственное соединение сначала конъюгируют с линкером таким образом, что связка между лекарственным соединением и линкером представляет собой ковалентную временную связку, такую как карбаматная, сложноэфирная, амидная или карбонатная связка, и затем реагирует с реакционноспособным биоразлагаемым гидрогелем, формируя пролекарство по настоящему изобретению.
Кроме того, такой биоразлагаемый гидрогель по настоящему изобретению можно функционализировать спейсером, несущим другую реакционноспособную функциональную группу, отличающуюся от таковой, предоставляемой биоразлагаемым гидрогелем по настоящему изобретению. Например, малеимидные реакционноспособные функциональные группы можно ввести в гидрогель по настоящему изобретению сочетанием подходящего гетеробифункционального спейсера, такого как Mal-(EG)6-NHS, с биоразлагаемым гидрогелем по настоящему изобретению. Такой модифицированный реакционноспособный биоразлагаемый гидрогель можно затем конъюгировать с реагентами лекарство-линкер, несущими реакционноспособную тиольную группу в линкерном фрагменте, образуя связанные с носителем пролекарства по настоящему изобретению.
После загрузки конъюгата лекарство-линкер на функционализированный модифицированный реакционноспособный биоразлагаемый гидрогель, несущий малеимидные группы, все оставшиеся реакционноспособные функциональные группы блокируют подходящими блокирующими реагентами, такими как меркаптоэтанол, для предотвращения нежелательных побочных реакций.
В предпочтительном варианте выполнения настоящего изобретения, конъюгаты лекарство-линкер, в которых лекарственный фрагмент содержит дисульфидную (-S-S-) связку, и в которых свободная тиольная группа соединена с линкерным фрагментом, вводят в реакцию с малеимид-функционализированным гидрогелем при температурах от комнатной до 4°С, более предпочтительно при комнатной температуре, в водном буферном растворе, имеющем значение рН 2-5, предпочтительно рН 2.5-4.5, более предпочтительно рН 3.0-4.0. Затем полученный конъюгат лекарство-линкер-гидрогель обрабатывают низкомолекулярным соединением, содержащим тиольную группу, предпочтительно с тиол- содержащим соединением весом 34-500 Да, наиболее предпочтительно с меркаптоэтанолом, при температурах от комнатной до 4°С, более предпочтительно при комнатной температуре, в водном буферном растворе, имеющем значение рН 2-5, предпочтительно рН 2.5-4.0, более предпочтительно рН 2.5-3.5.
В другом предпочтительном варианте выполнения настоящего изобретения, конъюгаты лекарство-линкер, в которых лекарственный фрагмент содержит дисульфидную (-S-S-) связку, и в которых малеимидная группа соединена с линкерным фрагментом, вводят в реакцию с тиол-функционализированным гидрогелем по настоящему изобретению при температурах от комнатной до 4°С, более предпочтительно при комнатной температуре, в водном буферном растворе, имеющем значение рН 2-5, предпочтительно рН 2.5-4.5, более предпочтительно рН 3.0-4.0. Затем полученный конъюгат лекарство-линкер-гидрогель обрабатывают низкомолекулярным соединением, содержащим малеимидную группу, предпочтительно с малеимид-содержащим соединением весом 100-300 Да, например с N-этил-малеимидом, при температурах от комнатной до 4°С, более предпочтительно при комнатной температуре, в водном буферном растворе, имеющем значение рН 2-5, предпочтительно рН 2.5-4.0, более предпочтительно рН 2.5-3.5.
В другом предпочтительном варианте выполнения настоящего изобретения, конъюгаты лекарство-линкер, в которых свободная тиольная группа соединена с линкерным фрагментом, вводят в реакцию с малеимид-функционализированным гидрогелем при температурах от комнатной до 4°С, более предпочтительно при комнатной температуре, в водном буферном растворе, имеющем значение рН 5.5-8, предпочтительно рН 6.5-7.5. Затем полученный конъюгат лекарство-линкер-гидрогель обрабатывают низкомолекулярным соединением, содержащим тиольную группу, предпочтительно с тиол-содержащим соединением весом 34-500 Да, наиболее предпочтительно с меркаптоэтанолом, при температурах от комнатной до 4°С, более предпочтительно при комнатной температуре, в водном буферном растворе, имеющем значение рН 5.5-8, предпочтительно рН 6.5-7.5.
В другом предпочтительном варианте выполнения настоящего изобретения, конъюгаты лекарство-линкер, в которых малеимидная группа соединена с линкерным фрагментом, вводят в реакцию с тиол-функционализированным гидрогелем по настоящему изобретению при температурах от комнатной до 4°С, более предпочтительно при комнатной температуре, в водном буферном растворе, имеющем значение рН 5.5-8, предпочтительно рН 6.5-7.5. Затем полученный конъюгат лекарство-линкер-гидрогель обрабатывают низкомолекулярным соединением, содержащим малеимидную группу, предпочтительно с малеимид-содержащим соединением весом 100-300 Да, например с N-этил-малеимидом, при температурах от комнатной до 4°С, более предпочтительно при комнатной температуре, в водном буферном растворе, имеющем значение рН 5.5-8, предпочтительно рН 6.5-7.5.
Особенно предпочтительный способ получения пролекарства по настоящему изобретению включает стадии
(a) реакция соединения формулы С(А'-Х1)4, где А'-Х1 представляет собой А до его связывания с Hyp или прекурсором Hyp, и X1 представляет собой подходящую химическую функциональную группу, с соединением формулы Нур'-Х2, где Нур'-Х2 представляет собой Hyp до его связывания с А или прекурсор Hyp, и X2 представляет собой подходящую химическую функциональную группу для реакции с Х1;
(b) необязательно, превращение полученного соединения со стадии (а) по одной или более дополнительных стадий с получением соединения формулы С(А-Нур)4, имеющего по меньшей мере четыре химические функциональные группы;
(c) реакция по меньшей мере четырех химических функциональных групп полученного соединения со стадии (b) с реагентом-прекурсором линкера на основе поли(этиленгликоля), где реагент-прекурсор линкера используется в субстехиометрическом количестве относительно общего числа функциональных групп в С(А-Нур)4, с получением гидрогеля по настоящему изобретению;
(d) реакция оставшихся непрореагировавших реакционноспособных функциональных групп (представляющих собой реакционноспособные функциональные группы каркаса, содержащиеся в реакционноспособном биоразлагаемом гидрогеле по настоящему изобретению) в каркасе гидрогеля со стадии (с) с ковалентным конъюгатом биологически активного фрагмента и временного линкера пролекарства, или сначала реакция непрореагировавших реакционноспособных функциональных групп с временным линкером пролекарства и затем с биологически активным фрагментом;
(e) необязательно, блокирование оставшихся непрореагировавших реакционноспособных функциональных групп с получением пролекарства по настоящему изобретению.
Конкретнее, гидрогели по настоящему изобретению получают описанным далее образом:
Для объемной полимеризации, реагент основной цепи и поперечносшивающий реагент смешивают в соотношении амин/активный сложный эфир от 2:1 до 1.05:1.
Реагент основной цепи и поперечносшивающий реагент растворяют в ДМСО, получая раствор с концентрацией от 5 до 50 г на 100 мл, предпочтительно от 7.5 до 20 г на 100 мл, и наиболее предпочтительно от 10 до 20 г на 100 мл.
Для осуществления полимеризации добавляют от 2 до 10% (об.) N,N,N',N'-тетраметилэтилендиамина (TMEDA) к раствору в ДМСО, содержащему поперечносшивающий реагент и реагент основной цепи, и полученную смесь встряхивают от 1 до 20 секунд и оставляют стоять. Смесь затвердевает меньше чем за 1 минуту.
Такой гидрогель по настоящему изобретению предпочтительно измельчают механически такими способами, как перемешивание, разбивание, режущая прессовка или размалывание, и при необходимости просеивают.
При полимеризации в эмульсии реакционная смесь состоит из диспергированной фазы и диспергирующей фазы.
Для получения диспергированной фазы реагент основной цепи и поперечносшивающий реагент смешивают в соотношении амин/активный сложный эфир от 2:1 до 1.05:1 и растворяют в ДМСО, получая раствор с концентрацией от 5 до 50 г на 100 мл, предпочтительно от 7.5 до 20 г на 100 мл, и наиболее предпочтительно от 10 до 20 г на 100 мл.
Диспергирующей фазой является любой растворитель, который не смешивается с ДМСО, не является основным, апротонный и с вязкостью ниже 10 Па*с. Предпочтительно, растворитель не смешивается с ДМСО, не является основным, апротонный и имеет вязкость ниже 2 Па*с, и не токсичен. Более предпочтительно, растворитель представляет собой насыщенный линейный или разветвленный углеводород, содержащий 5-10 атомов углерода. Наиболее предпочтительно, растворитель представляет собой н-гептан.
Для образования эмульсии диспергированной фазы в диспергирующей фазе, эмульгатор добавляют в диспергирующую фазу до добавления диспергированной фазы. Количество эмульгатора составляет от 2 до 50 мг на мл диспергированной фазы, более предпочтительно от 5 до 20 мг на мл диспергированной фазы, наиболее предпочтительно 10 мг на мл диспергированной фазы.
Эмульгатор имеет значение HLB от 3 до 8. Предпочтительно, эмульгатор представляет собой триэфир сорбита и жирной кислоты или конъюгат поли(гидрокси-жирная кислота)-поли(этиленгликоль). Более предпочтительно, эмульгатор представляет собой конъюгат поли(гидрокси-жирная кислота)-полиэтиленгликоль, где на каждом конце цепи расположен линейный поли(этиленгликоль) с молекулярным весом в диапазоне от 0,5 кДа до 5 кДа и единицы поли(гидрокси-жирной кислоты) с молекулярным весом в диапазоне от 0,5 кДа до 3 кДа. Наиболее предпочтительно, эмульгатор представляет собой поли(этиленгликоль) диполигидрокси стеарат, Cithrol DPHS (Cithrol DPHS, бывший Arlacel P135, Croda International  ).
).
Капли диспергированной фазы генерируют перемешиванием осевой крыльчаткой, имеющей геометрию, сходную с такими мешалками, как Isojet, Intermig, Propeller (EKATO 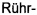 und Mischtechnik GmbH, Germany)), наиболее предпочтительно сходную с Isojet, имеющей диаметр от 50 до 90% от диаметра реактора. Предпочтительно, перемешивание начинают перед добавлением диспергированной фазы. Скорость мешалки устанавливают равной 0.6-1.7 м/с. Диспергированную фазу добавляют при комнатной температуре, и концентрация диспергированной фазы составляет от 2% до 70%, предпочтительно от 5 до 50%, более предпочтительно от 10 до 40%, и наиболее предпочтительно от 20 до 35% от общего объема реакционной смеси. Смесь диспергированной фазы, эмульгатора и диспергирующей фазы перемешивают 5-60 минут перед добавлением основания для начала полимеризации.
und Mischtechnik GmbH, Germany)), наиболее предпочтительно сходную с Isojet, имеющей диаметр от 50 до 90% от диаметра реактора. Предпочтительно, перемешивание начинают перед добавлением диспергированной фазы. Скорость мешалки устанавливают равной 0.6-1.7 м/с. Диспергированную фазу добавляют при комнатной температуре, и концентрация диспергированной фазы составляет от 2% до 70%, предпочтительно от 5 до 50%, более предпочтительно от 10 до 40%, и наиболее предпочтительно от 20 до 35% от общего объема реакционной смеси. Смесь диспергированной фазы, эмульгатора и диспергирующей фазы перемешивают 5-60 минут перед добавлением основания для начала полимеризации.
Добавляют 5-10 эквивалентов (относительно каждой формирующейся амидной связи) основания в смесь диспергированной и диспергирующей фазы. Основание апротонное, ненуклеофильное и растворимое в диспергированной фазе. Предпочтительно, основание апротонное, ненуклеофильное, хорошо растворимое в как диспергированной фазе, так и в ДМСО. Более предпочтительно, основание апротонное, ненуклеофильное, хорошо растворимое в как диспергированной фазе, так и в ДМСО, представляет собой амин и нетоксично. Наиболее предпочтительно, основание представляет собой N,N,N',N'-тетраметилэтилендиамин (TMEDA). Перемешивание в присутствии основания продолжают в течение 1-16 h.
Во время перемешивания капли диспергированной фазы затвердевают, становясь гранулами сшитого гидрогеля по настоящему изобретению, которые можно собрать и фракционировать по размеру на вибрационных ситах с размерами пор 75 мкм и 32 мкм, получая микрочастицы гидрогеля по настоящему изобретению.
Биоразлагаемые гидрогели по настоящему изобретению получают описанным выше способом в форме микрочастиц. В предпочтительном варианте выполнения настоящего изобретения, реакционноспособный биоразлагаемый гидрогель представляет собой формованное изделие, такое как покрытие, сетка, стент или микрочастица. Наиболее предпочтительно, биоразлагаемые гидрогели, содержащие конъюгатные функциональные группы, или соединенные с гидрогелем пролекарственные конъюгаты лекарство-линкер формуют в микрочастицы-гранулы, которые можно вводить инъекцией подкожно или внутримышечно стандартным шприцом. Такие мягкие гранулы имеют диаметр 1-500 микрометров. Предпочтительно, такие биоразлагаемые гидрогели, содержащие конъюгатные функциональные группы, или соединенные с биоразлагаемым гидрогелем пролекарственные конъюгаты лекарство-линкер имеют диаметр 10-100 микрометров, если они суспендированы в изотоническом водном буфере, наиболее предпочтительно имеют диаметр 20-100 микрометров, наиболее предпочтительно 25-80 микрометров.
Предпочтительно, такие гранулированные биоразлагаемые гидрогели, содержащие конъюгатные функциональные группы, или соединенные с биоразлагаемым гидрогелем пролекарственные конъюгаты лекарство-линкер можно вводить инъекцией через иглу с внутренним диаметром меньше 0.6 мм, предпочтительно через иглу с внутренним диаметром меньше 0.3 мм, более предпочтительно через иглу с внутренним диаметром меньше 0.25 мм, еще более предпочтительно через иглу с внутренним диаметром меньше 0.2 мм, и наиболее предпочтительно через иглу с внутренним диаметром меньше 0.16 мм.
Понятно, что термины "можно вводить инъекционно", "инъецируемый" или "возможность вводить инъекционно" относятся к комбинации факторов, таких как конкретная сила, прикладываемая к поршню шприца, содержащего биоразлагаемый гидрогель по настоящему изобретению, набухший в жидкости при определенной концентрации (вес/об) и при определенной температуре, игла указанного диаметра соединена с выпускным отверстием такого шприца, и время, необходимое для выдавливания определенного объема биоразлагаемого гидрогеля по настоящему изобретению из шприца через такую иглу.
Для обеспечения возможности инъекционного введения, объем в 1 мл биоразлагаемого гидрогеля по настоящему изобретению, набухшего в воде до концентрации по меньшей мере 5% (вес/об) и содержащегося в шприце, имеющем поршень диаметром 4.7 мм, должен выдавливаться при комнатной температуре в течение 10 секунд при приложении силы менее 50 Ньютон.
Предпочтительно, возможность инъекционного введения достигается для биоразлагаемого гидрогеля по настоящему изобретению, набухшего в воде до концентрации около 10% (вес/об).
Другой аспект настоящего изобретения представляет собой фармацевтическую композицию, содержащую пролекарство на основе гидрогеля по настоящему изобретению или его фармацевтически приемлемую соль вместе с фармацевтически приемлемым наполнителем.
Другой аспект настоящего изобретения представляет собой пролекарство на основе гидрогеля по настоящему изобретению или фармацевтическую композицию по настоящему изобретению для применения в лекарственном средстве.
В случае, если пролекарства на основе гидрогеля по настоящему изобретению содержат одну или более кислотных или основных групп, настоящее изобретение включает также их соответствующие фармацевтически или токсикологически приемлемые соли, в частности их фармацевтически применимые соли. Так, пролекарства на основе гидрогеля по настоящему изобретению, содержащие кислотные группы, могут применяться по настоящему изобретению, например, в виде солей щелочных металлов, солей щелочно-земельных металлов или аммониевых солей. Более конкретные примеры таких солей включают соли натрия, соли калия, соли кальция, соли магния или соли аммония или с органическими аминами, такими как, например, этиламин, этаноламин, триэтаноламин или аминокислоты. Пролекарства на основе гидрогеля по настоящему изобретению, содержащие одну или более основных групп, т.е. групп, которые могут быть протонированы, могут присутствовать и использоваться по настоящему изобретению в форме их солей с неорганическими или органическими кислотами. Примеры подходящих кислот включают хлорид водорода, бромид водорода, фосфорную кислоту, серную кислоту, азотную кислоту, метансульфокислоту, п-толуолсульфокислоту, нафталинсульфокислоту, щавелевую кислоту, уксусную кислоту, винную кислоту, молочную кислоту, салициловую кислоту, бензойную кислоту, муравьиную кислоту, пропионовую кислоту, пивалоиловую кислоту, диэтилуксусную кислоту, малоновую кислоту, янтарную кислоту, пимелиновую кислоту, фумаровую кислоту, малеиновую кислоту, яблочную кислоту, сульфаминовую кислоту, фенилпропионовую кислоту, глюконовую кислоту, аскорбиновую кислоту, изоникотиновую кислоту, лимонную кислоту, адипиновую кислоту и другие кислоты, известные квалифицированным специалистам в данной области. Если пролекарства на основе гидрогеля по настоящему изобретению одновременно содержат кислотные и основные группы в молекуле, настоящее изобретение включает также, помимо упомянутых солевых форм, внутренние соли или бетаины (цвиттерионы). Соответствующие соли могут быть получены обычными методами, известными квалифицированным специалистам в данной области, как, например, взаимодействием с органической или неорганической кислотой или основанием в растворителе или дисперсанте, или анионным обменом или катионным обменом с другими солями. Настоящее изобретение также включает все соли пролекарств, которые следствие низкой физиологической совместимости не пригодны непосредственно для применения в фармацевтических продуктах, но которые могут использоваться, например, как промежуточные продукты для химических реакций или для получения фармацевтически приемлемых солей.
Термин «фармацевтически приемлемый» означает одобренный надзорным органом, таким как ЕМЕА (Европа) и/или FDA (США) и/или любым другим национальным надзорным органом для применения в отношении животных, предпочтительно человека.
"Фармацевтическая композиция" означает одно или более действующих веществ, и один или более инертных ингредиентов, а также любой продукт, который получается, напрямую или опосредованно, при комбинации, комплексообразовании или агрегации любых двух или более из данных ингредиентов, или при диссоциации одного или более из данных ингредиентов, или при других типов реакций или взаимодействий одного или более из данных ингредиентов. Соответственно, фармацевтические композиции по настоящему изобретению охватывают любую композицию, полученную смешиванием соединения по настоящему изобретению и фармацевтически приемлемого наполнителя (фармацевтически приемлемого носителя).
Термин "наполнитель" относится к разбавителю, вспомогательному средству или носителю, совместно с которым вводится терапевтическое средство. Такой фармацевтический наполнитель может представлять собой стерильную жидкость, такую как вода и масла, включая жидкости нефтяного, животного, растительного или синтетического происхождения, включая (но не ограничиваясь только ими) арахисовое масло, соевое масло, минеральное масло, сезамовое масло и т.п.. Вода является предпочтительным наполнителем, когда фармацевтическая композиция вводится перорально. Раствор поваренной соли и раствор декстрозы являются предпочтительными наполнителями, когда фармацевтическая композиция вводится внутривенно. Растворы соли и водные растворы декстрозы и глицерина предпочтительно применяются в качестве жидких наполнителей для инъецируемых растворов. Подходящие фармацевтические наполнители включают крахмал, глюкозу, лактозу, сахарозу, маннит, трегалозу, желатин, солод, рис, муку, мел, силикагель, стеарат натрия, глицерин моностеарат, тальк, хлорид натрия, сухое молоко, глицерин, пропиленгликоль, воду, этанол и т.п.. Композиция при желании может содержать также небольшие количества увлажняющих или эмульгирующих средств, рН-буферных средств, таких как, например, ацетат, сукцинат, трис, карбонат, фосфат, HEPES (4-(2-гидроксиэтил)-1-пиперазинэтансульфокислота), MES (2-(N-морфолин)этансульфокислота) или может содержать детергенты, такие как Tween, полоксамеры, полоксамины, CHAPS, Igepal, или аминокислоты, такие как, например, глицин, лизин или гистидин. Такие композиции могут иметь вид растворов, суспензий, эмульсий, таблеток, пилюль, капсул, порошков, препаратов с замедленным высвобождением и т.п. Композиция может иметь вид суппозитория, с традиционными связующими средствами и наполнителями, такими как триглицериды. Препарат для перорального введения может содержать стандартные наполнители, такие как фармацевтические категории маннита, лактозы, крахмала, стеарата магния, сахарина натрия, целлюлоза, карбонат магния и т.д. Примеры подходящих фармацевтических наполнителей описаны в "Remington's Pharmaceutical Sciences" by E.W. Martin. Такие композиции содержат терапевтически эффективное количество терапевтического средства (лекарство или действующее вещество), предпочтительно в очищенной форме, вместе с подходящим количеством наполнителя, так чтобы получилась готовая форма для введения пациенту. Готовая форма должна соответствовать способу введения.
Другой аспект настоящего изобретения представляет собой способ лечения, контроля, замедления или профилактики у млекопитающего, предпочтительно у человека, нуждающегося в лечении, одного или более состояний, включающий введение указанному пациенту терапевтически эффективного количества пролекарства на основе гидрогеля по настоящему изобретению или фармацевтической композиции по настоящему изобретению или его фармацевтически приемлемой соли.
Примеры
Материалы и методы
Материалы: Exendin-4 с защищенной боковой цепью (J. Eng et al., J. Biol.Chem. 1992, 267(11), 7402-7405) на амидной смоле Ринка получали от Peptide Specialty Laboratories GmbH, Гейдельберг, Германия. Человеческий инсулин получали от Biocon Ltd., Бангалор, Индия..
Амино 4-разветвленный PEG5000 получали от JenKem Technology, Пекин, Китай). Амино 4-разветвленный PEG2000 получали от CreativePEGWorks, Winston Salem, Северная Каролина, США.
N-(3-малеимидопропил)-21-амино-4,7,10,13,16,19-гексаоксагеникозановой кислоты N-гидроксисукцинимидный эфир (Mal-PEG6-NHS) получали от Celares GmbH, Берлин, Германия.
2-Хлортритил хлоридную смолу, HATU и аминокислоты покупали в Merck Biosciences GmbH, Schwalbach/Ts, Германия, если не указано иное. Fmoc-Asp(OH)-OMe получали от Bachem AG, Бубендорф, Швейцария. S-Тритил-6-меркаптогексановую кислоту (Trt-MHA) получали от PolyPeptide (France).
Все остальные реагенты закупали в Sigma-ALDRICH Chemie GmbH, Тауфкирхен, Германия.
Твердофазный синтез проводили на 2-хлортритил хлоридной (TCP) смоле с загрузкой 1.3 ммоль/г. В качестве реакционных сосудов использовали шприцы, оснащенные полипропиленовыми фильтрами.
Загрузка первой аминокислоты на смолы осуществлялась в соответствии с инструкциями производителя.
Удаление защитной fmoc-группы:
Для удаления защитной fmoc-группы, смолу перемешивали со смесью 2/2/96 (об/об/об) пиперидин/DBU/ДМФА (дважды, по 10 минут каждый раз) и промывали ДМФА (десять раз).
Удаление защитной Mmt-группы:
Для удаления защитной Mmt-группы, смолу обрабатывали смесью гексафторизопропанол/ДХМ 1/9 (об/об) (15 раз, по 1 минуте каждый раз) и промывали ДХМ (десять раз).
Стандартные условия сочетания для кислот:
Сочетание кислот (алифатических кислот, Fmoc-аминокислот) со свободными амино-группами на смоле осуществляли, перемешивая смол с 3 экв. кислоты, 3 экв. РуВОР и 6 экв. DIEA относительно количества свободных амино-групп на смоле (вычислено исходя из теоретической загрузки смолы) в ДМФА при комнатной температуре. Через 1 час смолу промывали ДМФА (10 раз).
Методика отщепления от 2-хлортритил хлоридной смолы:
По окончании синтеза смолу промывали ДХМ, сушили в вакууме и дважды обрабатывали по 30 минут смесью 6/4 (об/об) ДХМ/гексафторизопропанол. Элюаты объединяли, летучие компоненты удаляли в токе азота, и продукт очищали методом обращенно-фазовой ВЭЖХ. ВЭЖХ-фракции, содержащие продукт, объединяли и лиофилизовали.
Амино-содержащие продукты, полученные в виде солей с ТФУК, превращали в соответствующие соли с HCl с помощью ионообменной смолы (Discovery DSC-SAX, Supelco, США). Эту стадию осуществляли в тех случаях, если остаточная ТФУК могла помешать, например, последующим реакциям сочетания.
Очистка методом обращенно-фазовой ВЭЖХ:
Обращенно-фазовую ВЭЖХ проводили на колонке 100×20 мм и 100×40 мм С18 ReproSil-Pur 300 ODS-3 5 мкм (Dr. Maisch, Аммербух, Германия), в составе ВЭЖХ-системы Waters 600 HPLC System и с детектором поглощения Waters 2487. Применяли линейный градиент раствора А (0.1% ТФУК в Н2О) и раствора В (0.1% ТФУК в ацетонитриле). ВЭЖХ-фракции, содержащие продукт, лиофилизовали.
Для гранул гидрогеля шприцы, оснащенные полипропиленовыми фильтрами, использовали в качестве реакционных сосудов или для стадий промывки.
Аналитика:
Масс-спектрометрию с ионизацией электрораспылением (ESI-MS) проводили на приборе Thermo Fisher Orbitrap Discovery, оснащенном системой сверхэффективной жидкостной хроматографии Waters Acquity UPLC System.
В МС-спектрах PEG-продуктов наблюдали серии (CH2CH2O)n фрагментов вследствие полидисперсности PEG-исходных соединений. Для простоты интерпретации в примерах приведено только по одному репрезентативному сигналу m/z.
Метод эксклюзионной хроматографии (SEC) проводили на системе Amersham Bioscience AEKTAbasic, оснащенной колонкой Superdex200 5/150 GL (Amersham Bioscience/GE Healthcare), имеющей фильтр 0.45 мкм на входе, если не указано иное. В качестве подвижной фазы применяли 20 мМ раствор фосфата натрия, 140 мМ NaCl, pH 7.4.
Пример 1
Синтез реагента основной цепи 1g и 1h
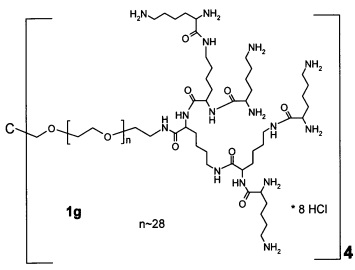
Реагент основной цепи 1g был получен из амино 4-разветвленного PEG5000 1а согласно следующей схеме:
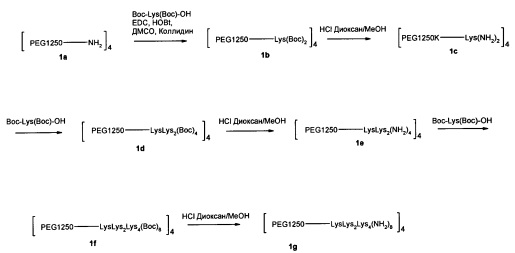
Для синтеза соединения 1b, 4-разветвленный-PEG5000 тетраамин 1а (мол. вес около 5200 г/моль, 5.20 г, 1.00 ммоль, HCl соль) растворяли в 20 мл ДМСО (безводн.). Добавляли Boc-Lys(Boc)-OH (2.17 г, 6.25 ммоль) в 5 мл ДМСО (безводн.), EDC HCl (1.15 г, 6.00 ммоль), HOBt⋅H2O (0.96 г, 6.25 ммоль) и коллидин (5.20 мл, 40 ммоль). Реакционную смесь перемешивали в течение 30 мин при комнатной температуре.
Реакционную смесь разбавляли добавлением 1200 мл дихлорметана и промывали 600 мл 0,1н. раствора H2SO4 (2х), насыщенным раствором поваренной соли (1 х), 0.1 М NaOH (2х), и 1/1 (об/об) смесью насыщенного раствора поваренной соли и воды (4х). Водные слои снова экстрагировали 500 мл ДХМ. Органические фазы сушили над Na2SO4, фильтровали и упаривали, получая 6.3 г неочищенного продукта 1b в виде бесцветного масла. Соединение 1b очищали методом обращенно-фазовой ВЭЖХ.
Выход 3.85 г (59%) бесцветного стекловидного продукта 1b.
МС: m/z 1294.4=[М+5Н]5+ (вычислено=1294.6).
Соединение 1с получали перемешиванием 3.40 г соединения 1b (0.521 ммоль) в 5 мл метанола и 9 мл 4н. раствора HCl в диоксане при комнатной температуре в течение 15 мин. Летучие компоненты удаляли в вакууме. Полученный продукт использовали в следующей стадии без дополнительной очистки.
МС: m/z 1151.9=[М+5Н]5+ (вычислено=1152.0).
Для синтеза соединения 1d, 3.26 г соединения 1с (0.54 ммоль) растворяли в 15 мл ДМСО (безводн.). Добавляли 2.99 г Boc-Lys(Boc)-OH (8.64 ммоль) в 15 мл ДМСО (безводн.), 1.55 г EDC HCl (8.1 ммоль), 1.24 г HOBt⋅H2O (8.1 ммоль) и 5.62 мл коллидина (43 ммоль). Реакционную смесь перемешивали в течение 30 мин при комнатной температуре.
Реакционную смесь разбавляли добавлением 800 мл ДХМ и промывали 400 мл 0.1н. раствора H2SO4 (2х), насыщенным раствором поваренной соли (1 х), 0.1 М NaOH (2х) и 1/1 (об/об) смесью насыщенного раствора поваренной соли и воды (4х). Водные слои снова экстрагировали 800 мл ДХМ. Органические фазы сушили над Na2SO4, фильтровали и упаривали, получая стекловидный неочищенный продукт.
Полученный продукт растворяли в ДХМ и высаживали охлажденным (-18°С) диэтиловым эфиром. Эту процедуру повторяли дважды, и осадок сушили в вакууме.
Выход: 4.01 г (89%) бесцветного стекловидного продукта 1d, который использовали в следующей стадии без дополнительной очистки.
МС: m/z 1405.4=[М+6Н]6+ (вычислено=1405.4).
Соединение 1е получали перемешиванием раствора соединения 1d (3.96 г, 0.47 ммоль) в 7 мл метанола и 20 мл 4н. раствора HCl в диоксане при комнатной температуре в течение 15 мин. Летучие компоненты удаляли в вакууме. Полученный продукт использовали в следующей стадии без дополнительной очистки.
МС: m/z 969.6=[М+7Н]7+ (вычислено=969.7).
Для синтеза соединения 1f, соединение 1е (3.55 г, 0.48 ммоль) растворяли в 20 мл ДМСО (безводн.). Добавляли Boc-Lys(Boc)-OH (5.32 г, 15.4 ммоль) в 18.8 мл ДМСО (безводн.), EDC HCl (2.76 г, 14.4 ммоль), HOBt⋅H2O (2.20 г, 14.4 ммоль) и 10.0 мл коллидина (76.8 ммоль). Реакционную смесь перемешивали в течение 60 мин при комнатной температуре. Реакционную смесь разбавляли добавлением 800 мл ДХМ и промывали 400 мл 0,1 н. раствора H2SO4 (2х), насыщенным раствором поваренной соли (1 х), 0,1 М NaOH (2х) и 1/1 (об/об) смесью насыщенного раствора поваренной соли и воды (4х). Водные слои снова экстрагировали 800 мл ДХМ. Органические фазы сушили над H2SO4, фильтровали и упаривали, получая неочищенный продукт 1f в виде бесцветного масла.
Полученный продукт растворяли в ДХМ и высаживали охлажденным (-18°С) диэтиловым эфиром. Данную стадию повторяли дважды и сушили осадок в вакууме.
Выход 4.72 г (82%) бесцветного стекловидного продукта 1f, который использовали в следующей стадии без дополнительной очистки.
МС: m/z 1505.3=[M+8H]8+ (вычислено=1505.4).
Реагент основной цепи 1g получали перемешиванием раствора соединения 1f (мол. вес около 12035 г/моль, 4.72 г, 0,39 ммоль) в 20 мл метанола и 40 мл 4н. раствора HCl в диоксане при комнатной температуре в течение 30 мин. Летучие компоненты удаляли в вакууме.
Выход 3.91 г (100%), стекловидный реагент основной цепи 1g.
МС: m/z 977.2=[М+9Н]9+ (вычислено=977.4).
Синтез реагента основной цепи 1h
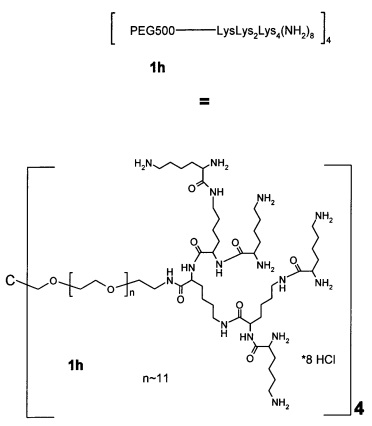
Реагент основной цепи 1h был синтезирован, как описано для 1g, за исключением того, что был использован 4-разветвленный PEG2000 вместо 4-разветвленного PEG5000.
МС: m/z 719.4=[М+8Н]8+ (вычислено=719.5).
Пример 2.
Синтез поперечносшивающих реагентов 2d, 2e, 2f и 2g
Поперечносшивающий реагент 2d получали из монобензилового эфира адипиновой кислоты (English, Arthur R. et al., Journal of Medicinal Chemistry, 1990, 33(1), 344-347) и PEG2000 согласно следующей схеме:
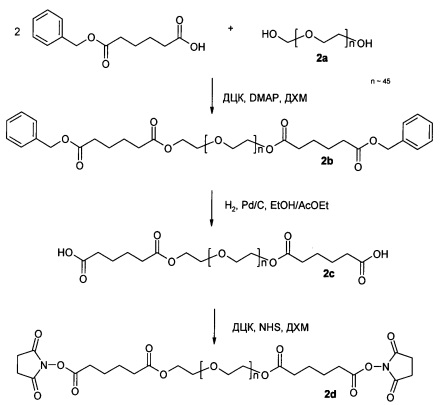
Раствор PEG2000 (2а) (11.0 г, 5.5 ммоль) и бензиладипатного полуэфира (4.8 г, 20.6 ммоль) в дихлорметане (90.0 мл) охлаждали до 0°С. Добавляли дициклогексилкарбодиимид (4.47 г, 21.7 ммоль), затем каталитическое количество DMAP (5 мг), раствор перемешивали и оставляли нагреваться до комнатной температуры на ночь (12 ч). Колбу выдерживали при +4°С в течение 5 ч. Твердый осадок отфильтровывали, и полностью удаляли растворитель отгонкой в вакууме. Остаток растворяли в 1000 мл 1/1 (об/об) смеси эфир/этилацетат и выдерживали при комнатной температуре в течение 2 часов, в течение которых образовывалось небольшое количество пушистого осадка. Осадок удаляли фильтрованием через слой целита (Celite®). Раствор выдерживали в плотно закрытой колбе при -30°С в морозильнике в течение 12 часов до окончания кристаллизации. Кристаллический продукт отфильтровывали через стеклянный фильтр и промывали охлажденным эфиром (-30°С). Отфильтрованный осадок сушили в вакууме. Выход: 11.6 г (86%) 2b в виде бесцветного твердого вещества. Полученный продукт был использован в следующей стадии без дополнительной очистки.
МС: m/z 813.1=[М+3Н]3+ (вычислено=813.3)
В стеклянном автоклаве объемом 500 мл растворяли PEG2000-бис-адипиновой кислоты-бис-бензиловый эфир 2b (13.3 г, 5.5 ммоль) в этилацетате (180 мл) и добавляли 10%-ный палладий на угле (0.4 г). Раствор гидрировали при 6 бар, 40°С до окончания поглощения водорода (5-12 ч). Катализатор удаляли фильтрованием через слой целита (Celite®) и упаривали растворитель в вакууме. Выход: 12.3 г (количественный) 2с в виде желтоватого масла. Полученный продукт был использован в следующей стадии без дополнительной очистки.
МС: m/z 753.1=[М+3Н]3+ (вычислено=753.2)
Раствор PEG2000-бис-адипиновой кислоты полуэфира 2с (9.43 г, 4.18 ммоль), N-гидроксисукцинимида (1.92 г, 16.7 ммоль) и дициклогексилкарбодиимида (3.44 г, 16.7 ммоль) в 75 мл ДХМ (безводн.) перемешивали в течение ночи при комнатной температуре. Реакционную смесь охлаждали до 0°С и отфильтровывали осадок. ДХМ упаривали, и остаток перекристаллизовывали из ТГФ.
Выход: 8.73 г (85%) поперечносшивающего реагента 2d в виде бесцветного твердого вещества.
MC: m/z 817.8=[М+3Н]3+ (вычислено=817.9).
Синтез 2е
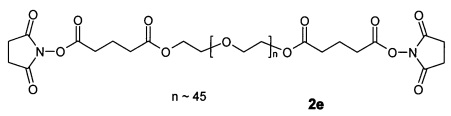
2е был синтезирован, как описано для 2d, за исключением того, что была использована глутаровая кислота вместо адипиновой кислоты.
MC: m/z 764.4=[М+3Н]3+ (вычислено=764.5).
Схема 2f
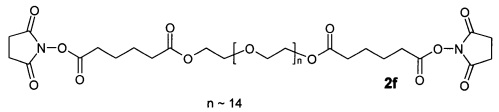
2f был синтезирован, как описано для 2d, за исключением того, что был использован PEG600 вместо PEG2000
MC: m/z 997.5=[М+H]+ (вычислено=997.8)
Синтез 2g
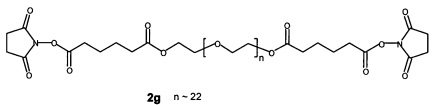
2g был синтезирован, как описано для 2d, за исключением того, что был использован PEG1000 вместо PEG2000
МС: m/z 697.4=[M+2H]2+ (вычислено=697.3)
Пример 3
Получение гидрогельных гранул 3а, 3b, 3с, 3d и 3е, содержащих свободные амино-группы
Раствор 275 мг 1g и 866 мг 2d в 14 мл ДМСО добавляли к раствору 100 мг Arlacel P135 (Croda International  ) в 60 мл гептана. Смесь перемешивали при 700 об/мин обычной металлической мешалкой в течение 10 мин при комнатной температуре, получая суспензию. Добавляли 1.0 мл N,N,N',N'-тетраметилендиамина (TMEDA) для осуществления полимеризации. Через 2 часа скорость вращения мешалки уменьшали до 400 об/мин, и смесь перемешивали еще 16 ч. Добавляли 1.5 мл уксусной кислоты, и затем через 10 мин добавляли 50 мл воды. Через 5 мин мешалку останавливали и сливали водную фазу.
) в 60 мл гептана. Смесь перемешивали при 700 об/мин обычной металлической мешалкой в течение 10 мин при комнатной температуре, получая суспензию. Добавляли 1.0 мл N,N,N',N'-тетраметилендиамина (TMEDA) для осуществления полимеризации. Через 2 часа скорость вращения мешалки уменьшали до 400 об/мин, и смесь перемешивали еще 16 ч. Добавляли 1.5 мл уксусной кислоты, и затем через 10 мин добавляли 50 мл воды. Через 5 мин мешалку останавливали и сливали водную фазу.
Для фракционирования гранул по размеру, суспензию вода-гидрогель просеивали во влажном состоянии на металлических ситах с размером отверстий 75, 50, 40, 32 и 20 мкм. Фракции гранул, оставшихся на ситах с размером отверстий 32, 40 и 50 мкм, объединяли и промывали 3 раза водой; 10 раз этанолом, и сушили 16 часов при 0.1 мбар, получая 3а в виде белого твердого порошка.
3b получали, как описано для 3а, за исключением того, что было использовано 300 мг 1g, 900 мг 2d, 10.8 мл ДМСО, 1.1 мл TMEDA и 1.6 мл уксусной кислоты.
3с получали, как описано для 3а, за исключением того, что было использовано 322 мг 1h, 350 мг 2f, 2.9 мл ДМСО, 1.6 мл TMEDA, 2.4 мл уксусной кислоты и скорость перемешивания 1000 об/мин.
3d получали, как описано для 3а, за исключением того, что было использовано 300 мг 1g, 810 мг 2е, 6.3 мл ДМСО, 1.1 мл TMEDA, 1.6 мл уксусной кислоты и скорость перемешивания 1000 об/мин.
3е получали, как описано для 3а, за исключением того, что было использовано 1200 мг 1g, 3840 мг 2d, 28.6 мл ДМСО, 425 мг Arlacel P135, 100 мл гептана и 4.3 мл TMEDA. При обработке добавляли 6.6 мл уксусной кислоты, и затем через 10 мин добавляли 50 мл воды и 50 мл насыщенного водного раствора хлорида натрия.
Содержание амино-групп в гидрогеле определяли посредством сочетания fmoc-аминокислоты со свободными амино-группами гидрогеля и последующей оценкой содержания fmoc-групп, как описано в работе Gude, М, J. Ryf, et al. (2002) Letters in Peptide Science 9(4): 203-206.
Определение содержания амино-групп для различных гидрогелей дало значения между 0.13 и 1.1 ммоль/г.
Пример 4
Получение гранул малеимид-функционализированного гидрогеля 4а, 4b, 4с и 4d, и определение степени замещения малеимидом
Раствор 600 мг Mal-PEG6-NHS (1.0 ммоль) в 4.5 мл 2/1 (об/об) смеси ацетонитрил/вода добавляли к 200 мг сухих гранул гидрогеля 3а. Добавляли 500 мкл натрийфосфатного буфера (рН 7.4, 0.5 М), и суспензию перемешивали 30 мин при комнатной температуре. Гранулы 4а промывали по пять раз смесью 2/1 (об/об) ацетонитрил/вода, метанолом и 1/1/0.001 (об/об/v/) ацетонитрил/вода/ТФУК.
Для определения содержания малеимида аликвоту гранул гидрогеля 4а лиофилизовали и взвешивали. Другую аликвоту гранул гидрогеля 4а вводили в реакцию с избытком меркаптоэтанола (в 50 мМ натрийфосфатном буфере, 30 мин при комнатной температуре), и поглощение меркаптоэтанола определяли по тесту Эллмана (Ellman, G. L. et al., Biochem. Pharmacol., 1961, 7, 88-95). Содержание малеимида составило 0.13 ммоль/г сухого гидрогеля.
4b и 4 с и 4d получали, как описано выше, за исключением того, что был использован 3b и 3с и 3е, соответственно.
Загрузка 4b: 0.14 ммоль/г
Загрузка 4 с: 0.9 ммоль/г
Загрузка 4d: 0.13 ммоль/г
Пример 5
Получение меченого индолуксусной кислотой гидрогеля 5
Раствор 15 мг 3-индолуксусной кислоты (87 мкмоль), 14 мкл N,N'-диизопропилкарбодиимида (87 мкмоль) и 27 мг 1-гидроксибензотриазол гидрата (174 мкмоль) в 0.4 мл ДМФА добавляли к 15 мг сухих гранул гидрогеля 3d в шприце, снабженном стеклянным фильтром. Суспензию перемешивали 1 час при комнатной температуре. 5 промывали пять раз ДМФА и инкубировали 5 мин с раствором 0.05 мл пиперидина в 1 мл ДМФА при комнатной температуре. 5 промывали пять раз ДМФА, пять раз дихлорметаном, пять раз этанолом и сушили в вакууме.
Пример 6
Получение дезтиобиотин-конъюгированного гидрогеля 6
Дезтиобиотин-конъюгированный гидрогель 6 получали из 3b и дезтиобиотина как описано для 5, за исключением того, что был использован дезтиобиотин и 3b вместо индолуксусной кислоты и 3а.
Пример 7
Синтез линкерного реагента 7
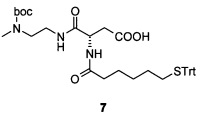
Fmoc-Asp(OMe)OH (150 мг, 0.41 ммоль), H2N-(СН2)2-N(СН3)-boc (36 мкл, 0.34 ммоль), HATU (156 мг, 0.41 ммоль) и DIEA (214 мкл, 1.23 ммоль) растворяли в 1 мл ДМФА. Смесь перемешивали в течение 1.5 ч при комнатной температуре, подкисляли добавлением АсОН (100 мкл) и очищали методом обращенно-фазовой ВЭЖХ.
Выход: 119 мг (0.23 ммоль).
MS Fmoc-Asp(OMe)CO(NH(CH2)2N(CH3)-boc): m/z 548.4=[M+Na]+ (вычислено=548.3).
Fmoc-Asp(OMe)CO(NH(CH2)2N(CH3)-boc) (119 мг, 0.23 ммоль) растворяли в ДМФА (1.0 мл), добавляли пиперидин (50 мкл) и DBU (15 мкл), и смесь перемешивали в течение 45 мин при комнатной температуре. Добавляли АсОН (100 мкл) и очищали NH2-Asp(ОМе)СО(NH(СН2)2N(СН3)-boc) методом обращенно-фазовой ВЭЖХ.
Выход: 73 мг (0.18 ммоль, ТФУК соль).
MS NH2-Asp(OMe)CO(NH(CH2)2N(CH3)-boc): m/z 326.2=[M+Na]+ (вычислено=326.2).
6-Тритилмеркаптогексановую кислоту (102 мг, 0.26 ммоль), (PfpO)2CO (103 мг, 0.26 ммоль) и коллидин (170 мкл, 1.31 ммоль) растворяли в ДМСО (1 мл). Смесь перемешивали в течение 1 ч и добавляли к раствору NH2-Asp(ОМе)СО(NH(СН2)2N(СН3)-boc) (73 мг, 0.18 ммоль) в ДМФА (1.0 мл). Смесь перемешивали в течение 1 ч, подкисляли добавлением АсОН (100 мкл) и очищали TrtS(CH2)5CONH-Asp(OMe)CO(NH(CH2)2N(CH3)-boc) методом обращенно-фазовой ВЭЖХ.
Выход: 61 мг (0.09 ммоль).
MS TrtS(CH2)5CONH-Asp(OMe)CO(NH(CH2)2N(CH3)-boc): m/z 698.5=[M+Na]+ (вычислено=698.3).
TrtS(CH2)5CONH-Asp(OMe)CO(NH(CH2)2N(CH3)-boc) (61 мг, 0.09 ммоль) растворяли в смеси 9:1 диоксан/H2O (1.0 мл), добавляли LiOH (4.3 мг, 0.18 ммоль), и смесь перемешивали при 60°С в течение 1 ч. Добавляли АсОН (50 мкл) и очищали 7 методом обращенно-фазовой ВЭЖХ.
Выход: 53 мг (0.08 ммоль).
MS 7: m/z 684.4=[M+Na]+ (вычислено=684.3 г/моль).
Пример 8
Синтез конъюгата 8 линкер-эксендин
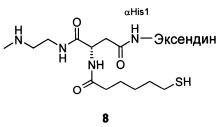
7 (22 мг, 33 мкмоль), РуВОР (23 мг, 44 мкмоль) и DIEA (31 мкл, 0.18 ммоль) растворяли в ДМФА (600 мкл) и немедленно добавляли к 220 мг (22 мкмоль) связанного с полимером эксендина с защищенной боковой цепью и свободным N-концом. После инкубирования в течение 1.5 ч при комнатной температуре, полимер промывали 10х ДМФА, 10х ДХМ и сушили в вакууме. Продукт отщепляли от полимера и очищали методом обращенно-фазовой ВЭЖХ.
Выход: 15.2 мг.
MS 8: m/z 1496.7=[М+3Н]3+ (вычислено=1497).
Пример 9
Получение эксендин-линкер-пролекарство на основе гидрогеля 9
Гидрогель 4b (600 мкл, суспендированный в смеси ацетонитрил/вода/ТФУК 1/1/0.001 (об/об/об), 7.3 мкмоль малеимидных групп) добавляли к раствору эксендин-линкер-тиола 8 (15.2 мг, 3.4 мкмоль) в 500 мкл смеси ацетонитрил/вода/ТФУК 1/1/0.001 (об/об/об). Добавляли фосфатный буфер (300 мкл, рН 7.4, 0.5 М), и образец инкубировали при комнатной температуре в течение 15 мин. Тест Эллмана подтвердил полное отсутствие тиольных групп. Добавляли меркаптоэтанол (10 мкл, 146 мкмоль), и образец инкубировали при комнатной температуре в течение 10 мин. Гидрогель 9 промывали (10 раз) смесью ацетонитрил/вода1/1 (об/об) и хранили в 0.1%-ной АсОН при 4°С.
Пример 10
Синтез линкерного реагента 10d
Линкерный реагент 10d синтезировали согласно следующей схеме:
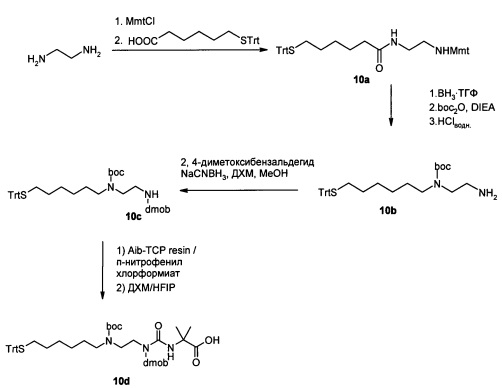
Синтез промежуточного продукта 5а для линкерного реагента:
4-Метокситритилхлорид (3 г, 9.71 ммоль) растворяли в ДХМ (20 мл) и прикалывали к раствору этилендиамина (6.5 мл, 97.1 ммоль) в ДХМ (20 мл). Через 2 часа раствор выливали в диэтиловый эфир (300 мл) и промывали три раза смесью 30/1 (об/об) насыщенный раствор поваренной соли/0.1 М NaOH (50 мл каждого) и один раз насыщенным раствором поваренной соли (50 мл). Органическую фазу сушили над Na2SO4, и летучие компоненты удаляли при пониженном давлении, получая Mmt-защищенный промежуточный продукт (3.18 г, 9.56 ммоль).
Mmt-защищенный промежуточный продукт (3.18 г, 9.56 ммоль) растворяли в безводном ДХМ (30 мл). Добавляли 6-(тритилмеркапто)гексановую кислоту (4.48 г, 11.47 ммоль), РуВОР (5.67 г, 11.47 ммоль) и DIEA (5.0 мл, 28.68 ммоль), и полученную смесь перемешивали в течение 30 мин при комнатной температуре. Раствор разбавляли добавлением диэтилового эфира (250 мл) и три раза промывали смесью 30/1 (об/об) насыщенный раствор поваренной соли/0.1 М NaOH (50 мл каждого) и один раз насыщенным раствором поваренной соли (50 мл). Органическую фазу сушили над Na2SO4, и летучие компоненты удаляли при пониженном давлении. 10а очищали методом флэш-хроматографии.
Выход: 5.69 г (8.09 ммоль).
МС: m/z 705.4=[M+H]+ (вычислено=705.0).
Синтез промежуточного продукта 10b для линкерного реагента:
К раствору 10а (3.19 г, 4.53 ммоль) в безводном ТГФ (50 мл) добавляли ВН3⋅ТГФ (1 м раствор, 8.5 мл, 8.5 ммоль), полученный раствор перемешивали в течение 16 часов при комнатной температуре. Добавляли еще ВН3⋅ТГФ (1 м раствор, 14 мл, 14 ммоль), и перемешивали в течение 16 часов при комнатной температуре. Реакцию гасили добавлением метанола (8.5 мл), добавляли N,N-диметилэтилендиамин (3 мл, 27.2 ммоль), раствор нагревали до кипения и перемешивали три часа. Смесь разбавляли добавлением этилацетата (300 мл) при комнатной температуре, промывали насыщенным водным раствором Na2CO3 (2×100 мл) и насыщенным водным раствором NaHCO3 (2×100 мл). Органическую фазу сушили над Na2SO4 и упаривали летучие компоненты при пониженном давлении, получая неочищенный аминный промежуточный продукт (3.22 г).
Аминный промежуточный продукт растворяли в ДХМ (5 мл), добавляли Boc2O (2.97 г, 13.69 ммоль), растворенный в ДХМ (5 мл) и DIEA (3.95 мл, 22.65 ммоль), и полученную смесь перемешивали при комнатной температуре в течение 30 мин. Смесь очищали методом флэш-хроматографии, получая неочищенный Boc- и Mmt-защищенный промежуточный продукт (3 г).
МС: m/z 791.4=[М+Н]+, 519.3=[M-Mmt+H]+ (вычислено=791.1).
0.4 м водный раствор HCl (48 мл) добавляли к раствору Boc- и Mmt-защищенного промежуточного продукта в ацетонитриле (45 мл). Смесь разбавляли добавлением ацетонитрила (10 мл) и перемешивали один час при комнатной температуре. Затем значение рН реакционной смеси доводили до 5.5 добавлением 5 м NaOH, удаляли ацетонитрил при пониженном давлении, и водный раствор экстрагировали дихлорметаном (4×100 мл). Объединенные органические фазы сушили над Na2SO4 и удаляли летучие компоненты при пониженном давлении. Сырой 5b использовали без дополнительной очистки.
Выход: 2.52 г (3.19 ммоль).
МС: m/z 519.3=[M+H]+ (вычислено=519.8 г/моль).
Синтез промежуточного продукта 10с для линкерного реагента:
10b (780 мг, 0.98 ммоль, ~65% чистота) и NaCNBH3 (128 мг, 1.97 ммоль) растворяли в безводном метаноле (13 мл). Добавляли раствор 2,4-диметоксибензальдегида (195 мг, 1.17 ммоль) в ДХМ (2 мл), и смесь перемешивали в течение 2 ч при комнатной температуре. Растворители упаривали при пониженном давлении, полученный неочищенный продукт растворяли в ДХМ и промывали насыщенным раствором Na2CO3. Водную фазу экстрагировали три раза ДХМ, и объединенные органические фазы промывали насыщенным раствором поваренной соли, сушили над MgSO4 и упаривали при пониженном давлении. 10с очищали методом флэш-хроматографии, используя ДХМ и МеОН как элюенты.
Выход: 343 мг (0.512 ммоль).
МС: m/z 669.37=[М+Н]+, (вычислено=669.95).
Синтез линкерного реагента 10d:
С Fmoc-Aib-загруженного TCP полимера (980 мг, ~0.9 ммоль) снимали защиту смесью ДМФА/пиперидин, промывали ДМФА (5 раз) и ДХМ (6 раз) и сушили в вакууме. Полимер обрабатывали раствором п-нитрофенилхлорформиата (364 мг, 1.81 ммоль) и коллидина (398 мкл, 3.0 ммоль) в безводном ТГФ (6 мл) и встряхивали в течение 30 мин. Раствор реагента удаляли фильтрованием, и полимер промывали тетрагидрофураном (5 раз) перед добавлением раствора амина 5с (490 мг, 0.7 ммоль) и DIEA (1.23 мл, 7.1 ммоль) в безводном ТГФ (6 мл). После встряхивания в течение 18 ч при комнатной температуре, раствор реагента удаляли фильтрованием, и полимер промывали дихлорметаном (5 раз). Линкер отщепляли от полимера и очищали методом обращенно-фазовой ВЭЖХ. Фракции, содержащие продукт, доводили до рН 6 добавлением насыщенного водного раствора NaHCO3 и упаривали при пониженном давлении. Полученную суспензию разделяли между насыщенным водным раствором NaCl и ДХМ, и водный слой экстрагировали дихлорметаном. Объединенные органические фракции упаривали досуха, получая линкерный реагент 10d.
Выход: 230 мг, (0.29 ммоль).
МС: m/z 798.41=[M+H]+, (вычислено=798.41).
Пример 11
Синтез αA1-конъюгированного инсулин-линкер конъюгата 11b
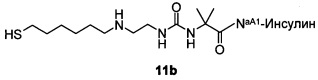
Синтез защищенного инсулин-линкер конъюгата 11а
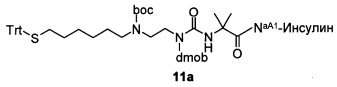
Линкерный реагент 10d растворяли в ДХМ (20 мг/мл) и активировали карбодиимид-привитым полимером (1.9 ммоль/г, 10 экв.) в течение 1 ч. Раствор активированного линкерного реагента добавляли к раствору инсулина (1.2 экв.) и DIEA (3.5 экв.) в ДМСО (100 мг инсулин/мл), и полученную смесь встряхивали при комнатной температуре в течение 45 мин. Раствор подкисляли добавлением уксусной кислоты, ДХМ упаривали при пониженном давлении, и NαA1-конъюгированный защищенный инсулин-линкер конъюгат 11а очищали методом обращенно-фазовой ВЭЖХ.
Лиофилизованный 11а обрабатывали смесью 90/10/2/2 (об/об/об/об) гексафторизопропанол/ТФУК/вода/триэтилсилан (2 мл/100 мг 11а) в течение 45 мин при комнатной температуре. Реакционную смесь разбавляли добавлением воды, и удаляли все летучие компоненты в токе азота. NαA1-конъюгированный инсулин-линкер конъюгат 11b очищали методом обращенно-фазовой ВЭЖХ.
Выход: 139 мг (0.023 ммоль) из 62 мг (0.078 ммоль) линкера 10d.
МС: m/z 1524.45=[М+4H]4+ (вычислено=1524.75).
Пример 12
Получение инсулин-линкер-пролекарства на основе гидрогеля 12
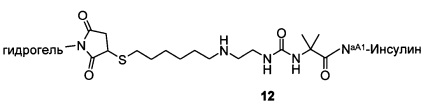
Сухой малеимид-функционализированный гидрогель 4а (82 мг, 10.3 мкмоль малеимидных групп) помещали в шприц, оснащенный фильтром. Добавляли раствор инсулин-линкер-тиол 11b (27.8 мг, 4.6 мкмоль) в 1.0 мл смеси ацетонитрил/вода/ТФУК 1/1/0.001 (об/об/об), и полученную суспензию инкубировали в течение 5 мин при комнатной температуре. Добавляли ацетатный буфер (0.4 мл, рН 4.8, 1.0 М), и образец инкубировали при комнатной температуре в течение 1 ч. Расход тиола отслеживали по тесту Эллмана. Гидрогель промывали 10 раз смесью 1/0.43/0.001 (об/об/об) ацетонитрил/вода/ТФУК и 2 раза смесью 1/1/0.2/0.25 (об/об/об/об) 1.0 М раствор саркозина рН 7.4/ацетонитрил/0.5 М фосфатный буфер рН 7.4/вода. Наконец, гидрогель суспендировали в растворе саркозина и инкубировали в течение 2 ч при комнатной температуре.
Инсулин-линкер-гидрогель 12 промывали 10 раз смесью ацетонитрил/вода/ТФУК 1/1/0.001 (об/об/об) и хранили при 4°С.
Загрузка инсулина в 12: 175 мг инсулина/г инсулин-линкер-гидрогеля.
Пример 13
Синтез прамипексол-линкер конъюгата 13b
Синтез прамипексол-глицинового промежуточного продукта 13а
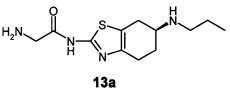
Boc-Gly-OH (659 мг, 3.76 ммоль), РуВОР (2.35 г, 4.51 ммоль) и N-метилморфолин (4.14 мл, 37.6 ммоль) растворяли в ДМСО (20 мл). Добавляли прамипексола дигидрохлорид (2.14 г, 7.52 ммоль), и смесь перемешивали в течение 1 ч. По окончании реакции раствор разбавляли добавлением 300 мл 1 м раствора NaOH, насыщали добавлением NaCl, и экстрагировали дихлорметаном (8×70 мл). Объединенные органические фазы сушили над MgSO4, растворитель упаривали при пониженном давлении, и остаток очищали методом обращенно-фазовой ВЭЖХ. После лиофилизации получали 721 мг (1.49 ммоль, ТФУК соль) Вос-защищенного производного.
МС: m/z 369.2=[М+Н]+, 737.4=[2М+Н]+ (вычислено=369.5 г/моль).
Для снятия boc-защиты промежуточный продукт растворяли в 3 м метанольном растворе HCl (10 мл), добавляли концентрированный водный HCl (400 мкл), и полученную смесь перемешивали в течение 4 ч. Растворитель удаляли при пониженном давлении и сушили 13а в вакууме.
Выход: 490 мг (1.44 ммоль, двойная HCl соль).
МС: m/z 269.1=[M+H]+ (вычислено=269.4).
Синтез 13b

6-(Тритилмеркапто)гексан-1-амин (1.21 г, 3.22 ммоль) и п-нитрофенилхлорформиат (0.78 г, 3.86 ммоль) суспендировали в сухом ТГФ (15 мл). Добавляли DIEA (841 мкл, 4.83 ммоль), и полученный раствор перемешивали при комнатной температуре в течение 2 ч. После подкисления уксусной кислотой, растворитель упаривали при пониженном давлении, и остаток очищали методом обращенно-фазовой ВЭЖХ. 1.21 г (2.25 ммоль) п-нитрофенилкарбамата было получено после лиофилизации.
Полученный карбамат (801 мг, 1.48 ммоль) растворяли в ДМСО (4.4 мл) и прикалывали к перемешиваемому раствору 13а (490 мг, 1.44 ммоль) и DIEA (800 мкл, 4.60 ммоль) в ДМСО (7 мл) в течение 30 мин. Смесь перемешивали в течение 4.5 ч при комнатной температуре. По окончании реакции, раствор разбавляли добавлением 0.5 м раствора NaOH (300 мл) и экстрагировали дихлорметаном (6×70 мл). Объединенные органические фазы сушили над MgSO4, растворитель упаривали при пониженном давлении, и конъюгат очищали методом обращенно-фазовой ВЭЖХ, получая 254 мг (0.323 ммоль, ТФУК соль) тритил-защищенного промежуточного продукта.
МС: m/z 670.3=[М+Н]+ (вычислено=670.0 г/моль).
Для снятия защиты, промежуточный продукт (248 мг, 0.32 ммоль) инкубировали в гексафторизопропаноле (6 мл) и триэтилсилане (240 мкл) в течение 30 мин при комнатной температуре. Упаривали летучие компоненты, и 13b очищали методом обращенно-фазовой ВЭЖХ.
Выход: 167 мг (0.31 ммоль, ТФУК соль).
МС: m/z 428.2=[М+Н]+ (вычислено=428.6 г/моль).
Пример 14
Синтез гидрогель-линкер-прамипексол конъюгата 14а и 14b
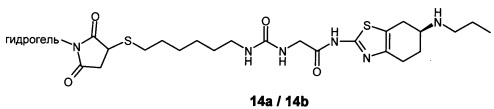
Малеимид-функционализированные микрочастицы гидрогеля 4а (100 мкл. загрузка 30 мкмоль/мл, 3 мкмоль) вводили в реакцию с соединением 13b (2.3 мг, 4.3 мкмоль) в смеси 1/1 ацетонитрил/вода(420 мкл) и 0.5 м фосфатного буфера рН 7.4 (52 мкл) в течение 10 мин при комнатной температуре. Гидрогель промывали 20 раз смесью 1/1 ацетонитрил/вода. Оставшиеся малеимидные фрагменты вводили в реакцию с 2-меркаптоэтанолом (34 мкл, 0.48 ммоль) в смеси 1/1 ацетонитрил/вода (3 мл) и 0.5 м фосфатного буфера рН 7.4 (0.4 мл) в течение 10 мин при комнатной температуре. Загруженный гидрогель промывали 20 раз смесью 1/1 ацетонитрил/вода, 20 раз фосфатным буфером рН 7.4 и инкубировали в том же буфере (1.5 мл) при 37°С.
Загрузка прамипексола в 14а: 27 мг/г.
Прамипексол-линкер гидрогель 14b с высокой загрузкой получали как описано выше, за исключением того, что было использовано 88 мг 13b и 100 мг 4с.
Загрузка прамипексола в 14b: 152 мг/г.
Пример 15
Получение гранул меркаптоэтанол-блокированного малеимид-функционализированного гидрогеля 15
2 мл раствора меркаптоэтанола (0.7 М в смеси 1/1/0.001 ацетонитрил/вода/ТФУК (об/об/об)) добавляли к 100 мг 4b, суспендированного в смеси 1/1/0.001 ацетонитрил/вода/ТФУК (об/об/об). Раствор доводили до рН 7.0 добавлением фосфатного буфера (рН 7.4, 0.5 М), и полученную смесь перемешивали в течение 30 мин при комнатной температуре. 15 промывали смесью ацетонитрил/вода/ТФУК 1/1/0.001 (10 раз).
Пример 16
Кинетика высвобождения in vitro
Лекарство-линкер-гидрогель 9, 12 и 14а, соответственно, (содержащие примерно 1 мг лекарственного средства) суспендировали в 2 мл 60 мМ раствора фосфата натрия, 3 мМ EDTA, 0.01% Tween-20, pH 7.4, и инкубировали при 37°С. Суспензии центрифугировали через определенные промежутки времени, и анализировали надосадочный раствор методом обращенно-фазовой ВЭЖХ с детектированием при 215 нм и методом ESI-MS (для 9 и 12), или измерением поглощения при 263 нм (для 14а). УФ-сигналы, соответствующие высвобожденному лекарственному средству, интегрировали (9 и 12) или использовали напрямую (14а) и строили график зависимости от времени инкубирования. Применяли программу аппроксимации кривой для оценки соответствующего времени полувысвобождения.
Для 9, 12 и 14а были определены времена полужизни in vitro, равные соответственно 14 дней, 18 дней и 8 дней. Кинетика высвобождения in vitro для 9 при pH 7.4 и 37°С представлена на Фиг. 8.
Пример 17
In vitro разложение 15 при pH 9 и 37°С
Ускоренный гидролиз гранул гидрогеля 15 осуществляли путем инкубирования 5 мг 15 в 2.0 мл 0.5 М натрий-боратного буфера, pH 9.0 при 37°С. Через определенные промежутки времени отбирали пробы и анализировали их методом эксклюзионной хроматографии. УФ-сигналы, соответствующие высвобождаемым из гидрогеля водорастворимым продуктам разложения, содержащим один или более фрагментов основной цепи (соответствующих реакционноспособным функциональным группам), интегрировали и строили график зависимости от времени инкубирования, см. Фиг. 9.
Время полного разложения гидрогеля вследствие гидролиза разрушаемых связей на водорастворимые продукты разложения, содержащие один или более фрагментов основной цепи, составило 94 часа, что в 1.45 раза дольше времени высвобождения первых 10 мол. % водорастворимых продуктов разложения, содержащих один или более фрагментов основной цепи (что соответствует в данном гидрогеле первым 10 мол. % реакционноспособных функциональных групп), которое составляет 65 часов.
Пример 18
In vitro разложение 15 при рН 7.4 и 37°С
Гидролиз гранул гидрогеля 15 осуществляли путем инкубирования 5 мг 15 в 2.0 мл 100 мМ раствора фосфата натрия, рН 7.4 при 37°С. Через определенные промежутки времени отбирали пробы и анализировали их методом эксклюзионной хроматографии (см. Материалы и Методы). УФ-сигналы, соответствующие высвобождаемым из гидрогеля водорастворимым продуктам разложения, содержащим один или более фрагментов основной цепи (соответствующих реакционноспособным функциональным группам), интегрировали и строили график зависимости от времени инкубирования, см. Фиг. 10.
Время полного разложения гидрогеля вследствие гидролиза разрушаемых связей на водорастворимые продукты разложения, содержащие один или более фрагментов основной цепи, составило 117 дней, что в 1.43 раза дольше времени высвобождения первых 10 мол.% водорастворимых продуктов разложения, содержащих один или более фрагментов основной цепи (что соответствует в данном гидрогеле первым 10 мол. % реакционноспособных функциональных групп), которое составляет 82 дня.
Коэффициент 1.43 практически равен значению 1.45 (см. пример 17) для условий ускоренного гидролиза при рН 9, что иллюстрирует возможность использования условий ускоренного гидролиза для анализа разложения образцов гидрогеля.
Пример 19
In vitro разложение 5 при рН 9 и 37°С
Гидролиз гранул гидрогеля 5 осуществляли путем инкубирования 5 мг 5 в 2.0 мл 0.5 М натрий-боратного буфера, рН 9.0 при 37°С. Через определенные промежутки времени отбирали пробы и анализировали их методом эксклюзионной хроматографии (см. Материалы и Методы). УФ-сигналы при 280 нм, соответствующие высвобождаемым из гидрогеля водорастворимым продуктам разложения, содержащим индол-ацетил меченые реакционноспособные функциональные группы, интегрировали и строили график зависимости от времени инкубирования, см. Фиг. 11.
Время полного разложения гидрогеля вследствие гидролиза разрушаемых связей на водорастворимые продукты разложения, содержащие индол-ацетил меченые реакционноспособные функциональные группы, составило 75 часов, что в 1.44 раза дольше времени высвобождения первых 10 мол.% индол-ацетил меченых реакционноспособных функциональных групп, которое составляет 52 часа (Фиг. 11).
Пример 20
Синтез полуэфиров палиперидона с дикарбоновыми кислотами
Общая методика синтеза эфиров палиперидона:
Палиперидон (1 экв) растворяли в сухом ДХМ и триэтиламине (4.4 экв), затем добавляли каталитическое количество DMAP и нужного циклического ангидрида (4 экв). Затем реакционную смесь перемешивали 1 час при комнатной температуре. Летучие компоненты удаляли и полученную смесь разбавляли добавлением смеси ацетонитрил/вода 1/1 + 0.1% ТФУК, и подкисляли примерно до значения рН 4. Соответствующий продукт очищали методом обращенно-фазовой ВЭЖХ и лиофилизовывали ВЭЖХ-фракции, содержащие продукт.
Синтез промежуточного продукта (16а):

16а синтезировали согласно описанной общей методике для синтеза эфиров палиперидона из 50 мг палиперидона и адипинового ангидрида, получая белое твердое вещество.
Выход: 68 мг (0.102 ммоль, 87%, ТФУК соль).
МС: m/z 555.3=[М+Н]+. (вычислено=555.6).
Синтез промежуточного продукта (16b):
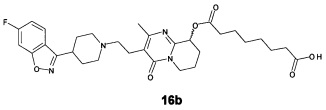
16b был получен из 130 мг палиперидона и суберинового ангидрида согласно общей методике, в виде белого твердого вещества.
Выход: 93 мг (0.133 ммоль, 43%, ТФУК соль).
МС: m/z 583.3=[M+H]+ (вычислено=583.7).
Синтез промежуточного продукта (16с):
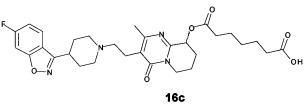
16с был получен из 500 мг палиперидона и пимелинового ангидрида в виде белого твердого вещества.
Выход: 483 мг (0.799 ммоль, 68%, HCl соль).
МС: m/z 569.3=[М+Н]+ (вычислено=569.7).
Пример 21
Получение гранул гидрогеля (17а), (17b) и (17с), содержащего свободные амино-группы.
Раствор 720 мг 1g и 1180 мг 2d в 7.3 мл ДМСО добавляли к раствору 300 мг Arlacel P135 (Croda International  ) в 60 мл гептана. Смесь перемешивали при 1200 об/мин стандартной металлической мешалкой в течение 10 мин при комнатной температуре, получая суспензию. Добавляли 2.6 мл N,N,N',N'-тетраметилендиамина (TMEDA) для осуществления полимеризации. Через 2 часа скорость вращения мешалки уменьшали до 500 об/мин, и смесь перемешивали еще 16 ч. Добавляли 4 мл уксусной кислоты, и затем через 10 мин добавляли 50 мл воды. Через 5 мин мешалку останавливали и сливали водную фазу.
) в 60 мл гептана. Смесь перемешивали при 1200 об/мин стандартной металлической мешалкой в течение 10 мин при комнатной температуре, получая суспензию. Добавляли 2.6 мл N,N,N',N'-тетраметилендиамина (TMEDA) для осуществления полимеризации. Через 2 часа скорость вращения мешалки уменьшали до 500 об/мин, и смесь перемешивали еще 16 ч. Добавляли 4 мл уксусной кислоты, и затем через 10 мин добавляли 50 мл воды. Через 5 мин мешалку останавливали и сливали водную фазу.
Для фракционирования гранул по размеру, суспензию вода-гидрогель просеивали во влажном состоянии на металлических ситах с размером отверстий 75, 50, 40, 32 и 20 мкм. Фракции гранул, оставшихся на ситах с размером отверстий 32, 40 и 50 мкм, объединяли и промывали 3 раза водой; 10 раз этанолом, и сушили 16 часов при 0.1 мбар, получая 17а в виде белого твердого порошка.
17b получали, как описано для 17а, за исключением того, что было использовано 900 мг 1g, 886 мг 2g, 6.7 мл ДМСО, 3.2 мл TMEDA, 5.0 мл уксусной кислоты и скорость перемешивания 1500 об/мин.
17с получали как описано для 17а, за исключением того, что было использовано 1200 мг 1h, 1300 мг 2f, 9.9 мл ДМСО, 6.1 мл TMEDA, 9.4 мл уксусной кислоты и скорость перемешивания 1000 об/мин.
Пример 22
Синтез Ado-модифицированных гидрогелей (18а), (18b) и (18с), и Lys-модифицированного гидрогеля (18d):
Ado-модифицированные гидрогели (18а, 18b, 18с):
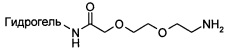
Гидрогель 17а, 17b и 17с, соответственно, в шприце, снабженном полипропиленовым фильтром, промывали 1%-ным раствором диизопропилэтиламина в ДМФА и десять раз диметилформамидом.
Затем проводили сочетание с fmoc-Ado-OH, перемешивая 17а, 17b и 17с, соответственно, с 3.5 экв. fmoc-Ado-OH, 3.5 экв. РуВОР и 8.75 экв. DIPEA в ДМФА (концентрация fmoc-Ado-OH 0.2 ммоль/мл). Через 45 мин гидрогель промывали ДМФА (10 раз), затем ДХМ (10 раз).
Удаление fmoc-защитной группы осуществляли перемешиванием гидрогеля дважды с раствором состава 96/2/2 ДМФА/пиперидин/DBU (об/об) по 5 минут каждый раз. 18а, 18b и 18с, соответственно, затем промывали диметилформамидом (10 раз) и этанолом (10 раз), и наконец, сушили в вакууме.
Lys-модифицированный гидрогель (18d):
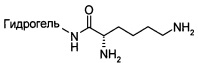
Гидрогель 17а в шприце, снабженном полипропиленовым фильтром, промывали 1%-ным раствором диизопропилэтиламина в ДМФА и десять раз диметилформамидом.
Затем проводили сочетание с fmoc-Lys(Fmoc)-OH, перемешивая 17а с 3.5 экв. fmoc-Lys(Fmoc)-OH, 3.5 экв. РуВОР и 8.75 экв. DIPEA в ДМФА (концентрация fmoc-Lys(Fmoc)-OH 0.2 ммоль/мл). Через 45 мин гидрогель промывали ДМФА (10 раз), затем ДХМ (10 раз).
Удаление fmoc-защитной группы осуществляли перемешиванием гидрогеля дважды с раствором состава 96/2/2 ДМФА/пиперидин/DBU (об/об) по 5 минут каждый раз. 18d затем промывали диметилформамидом (10 раз) и этанолом (10 раз), и наконец, сушили в вакууме.
Пример 23
Синтез палиперидон-линкер-гидрогеля (19а), (19b), (19с), (19d), (19e), (19f) и (19g):

Общая методика сочетания палиперидона с линкером:
18с (содержание амина 1 экв.) взвешивали и переносили в шприц, снабженный полипропиленовым фильтром, и перемешивали с 3 экв. палиперидон-эфира 16а, 3 экв. РуВОР и 7.5 экв. DIPEA в сухом ДМФА (концентрация палиперидон-эфира 16а 0.2 ммоль/мл) в течение 2 ч. Палиперидон-линкер-гидрогель 19а промывали ДМФА (8 раз), затем раствором состава 96/2/2 об/об ДМФА/пиперидин/DBU (10 раз), затем снова промывали ДМФА (10 раз) и в конце смесью ацетонитрил/вода 1/1 + 0.1% ТФУК (10 раз).
Загрузку палиперидона определяли полным гидролизом образцов палиперидон-линкер-гидрогеля при рН 12 в течение 4 ч при 37°С и количественным определением высвободившегося палиперидона методом сверхэффективной жидкостной хроматографии (UPLC), с детектированием при 280 нм по калибровочной кривой для палиперидона.
19b, 19с, 19d, 19e, 19f и 19g, соответственно, синтезировали по описанной выше методике, за исключением того, что был использован гидрогель 18с, 18а, 18b, 18а, 18d и 18d, соответственно, и палиперидон-эфир 16b, 16а, 16а, 16с, 16а и 16с, соответственно.
Загрузка в различных конъюгатах палиперидон-линкер-гидрогель приведена в Таблице 1:

Палиперидон-линкер гидрогель суспендировали в PBS буфере.
Концентрация палиперидона в суспензии палиперидон-линкер гидрогеля (вес/об):
19f: 100 мг/мл.
19g: 112 мг/мл.
Пример 24
Кинетика высвобождения in vitro
Изучение высвобождения in vitro при рН 7.4:
Образцы палиперидон-линкер-гидрогеля (19а-19g, соответственно) (в двух повторах), содержащие примерно 0.85 мг палиперидона, промывали три раза фосфатным буфером с рН 7.4 (60 мМ, 3 мМ EDTA, 0.01% Tween-20) и доводили до объема 1.5 мл тем же буфером. Образцы инкубировали при 37°С и анализировали аликвоты надосадочного раствора через различные промежутки времени методом сверхэффективной жилкостной хроматографии (UPLC) при детектировании при 280 нм. Интегрировали пики, соответствующие высвобожденному палиперидону, и вычисляли количество палиперидона сравнением с калибровочной кривой. Строили график зависимости количества высвободившегося палиперидона от времени и определяли времена полу-высвобождения с помощью программы аппроксимации кривой, считая кинетику высвобождения соответствующей первому порядку.
Кинетика высвобождения 19а in vitro показана на Фиг. 12.
Времена полужизни для других гидрогельных линкеров, перечисленных в Таблице 1, приведены в следующей далее таблице (Таблица 2):

Пример 25
Исследование фармакокинетики палиперидона в крысах
Фармакокинетику 19с изучали путем измерения концентрации палиперидона в плазме крови после подкожного введения однократной дозы крысам.
Одна группа из пяти самцов крыс Wistar (200-250 г) использовалась для изучения концентрации палиперидона в плазме крови в течение 28 дней. Каждому животному делали одну подкожную инъекцию 500 мкл суспензии 19с в ацетатном буфере с рН 5, содержащей 7 мг палиперидона (14 мг палиперидона/мл). Подъязычно отбирали по 200 мкл крови у животного через определенные промежутки времени для получения 100 мкл Li-Heparin плазмы. Пробы брали до введения и через 4 ч, 2, 4, 7, 11, 14, 18, 21, 25 и 28 дней после инъекции. Образцы плазмы замораживали в течение 15 минут после забора крови и хранили при -80°С до проведения анализа.
Количественное определение концентраций палиперидона в плазме крови проводили с помощью Waters Acquity UPLC в комплексе с масс-спектрометром Thermo LTQ Orbitrap Discovery на ESI детекторе, и с аналитической колонкой Waters ВЕН С18 (50×2.1 мм внутр. диаметр, размер частиц 1.7 мкм) (подвижная фаза А: 10 мМ формиат аммония с рН 4.0, подвижная фаза В: ацетонитрил, Т=45°С). Градиент составлял линейный градиент от 10% В до 50% В в течение 4 минут, фазу изократической промывки 95%-ным В (1.5 мин), и фазу восстановления (2.5 мин) с низкой скоростью потока 0.25 мл/мин. Детектирование ионов проводили в режиме контроля селективных реакций (SRM), отслеживая переходы пар ионов с m/z 427.2 (предшественник) в m/z 207.1 (продукт) для палиперидона, и ионов с m/z 376.1 (предшественник) в m/z 165.1 (продукт) для взятого в качестве внутреннего стандарта (IS) галоперидола.
Пробы крови после подкожного введения гидрогель-палиперидона собирали в гепаринизированные пробирки через разные интервалы времени. Плазму отделяли центрифугированием крови и хранили при -80°С до проведения анализа. После добавления водного раствора NaOH (50 мкл, 0.5 М NaOH), в оттаявшие образцы плазмы (~ 95 мкл) добавляли 220 пг галоперидола (10 мкл водного раствора галоперидола с концентрацией с=22 пг/мкл) и экстрагировали диэтиловым эфиром (2×500 мкл). Водный слой замораживали в бане из жидкого азота, а органический слой переносили в отдельную пробирку. Растворитель из объединенных органических фаз удаляли в токе азота при 40°С, и остаток сушили в вакууме. Остатки, полученные через разные интервалы времени, растворяли в смеси подвижной фазы А : подвижной фазы В = 7:3 (об/об) (100 мкл) и вводили аликвоты (15 мкл) в ВЭЖХ-МС систему.
Калибровочную кривую строили, откладывая на графике зависимость площади пика палиперидона от номинального количества калибровочных стандартов. Результаты обрабатывали методом линейно-регрессионного анализа с использованием 1/Х2 как весового коэффициента.
Площади пиков палиперидона в количественных экспериментах в различные моменты времени пересчитывали в соответствии с коэффициентом «средняя площадь пика внутреннего стандарта/площадь пика внутреннего стандарта». Полученные значения площади пиков использовали для вычисления концентрации палиперидона в плазме крови крыс (нг мл-1).
Не отмечалось всплеска уровня палиперидона, и наблюдали замедленное высвобождение палиперидона в течение 28 дней.
Результаты представлены на Фиг. 13.
Фармакокинетику 19е изучали так же, как описано для 19 с. Результаты представлены на Фиг. 14.
Пример 26
Альтернативный путь синтеза 1g
Для синтеза соединения 1b, к нагретой до 45°С суспензии 4-разветвленного-PEG5000 тетраамина (1а) (50.0 г, 10.0 ммоль) в 250 мл iPrOH (безводн.) добавляли boc-Lys(boc)-OSu (26.6 г, 60.0 ммоль) и DIEA (20.9 мл, 120 ммоль), и смесь перемешивали в течение 30 мин.
Затем добавляли, н-пропиламин (2.48 мл, 30.0 ммоль). Через 5 минут раствор разбавляли добавлением 1000 мл МТБЭ и хранили в течение ночи при -20°С без перемешивания. Примерно 500 мл надосадочного раствора декантировали и отбрасывали. Добавляли 300 мл холодного МТБЭ, и после 1 минуты встряхивания собирали продукт фильтрованием через стеклянный фильтр, и промывали 500 мл холодного МТБЭ. Полученный продукт сушили в вакууме в течение 16 ч.
Выход: 65.6 г (74%) 1b в виде белого комковатого твердого вещества.
МС: m/z=937.4=[М+7H]7+ (вычислено=937.6).
Соединение 1с получали перемешиванием полученного на предыдущей стадии соединения 1b (48.8 г, 7.44 ммоль) в 156 мл 2-пропанола при 40°С.
Добавляли смесь 196 мл 2-пропанола и 78.3 мл ацетилхлорида при перемешивании в течение 1-2 мин. Раствор перемешивали при 40°С в течение 30 мин и охлаждали до -30°С в течение ночи без перемешивания. Добавляли 100 мл холодного МТВЕ, суспензию встряхивали в течение 1 мин и охлаждали в течение 1 ч при -30°С. Собирали продукт фильтрованием через стеклянный фильтр и промывали 200 мл холодного МТБЭ. Полученный продукт сушили в вакууме в течение 16 ч.
Выход: 38.9 г (86%) 1с в виде белого твердого порошка.
МС: m/z=960.1 [М+6Н]6+ (вычислено=960.2).
Для синтеза соединения 1d, к нагретой до 45°С суспензии полученного на предыдущей стадии соединения 1с (19.0 г, 3.14 ммоль) в 80 мл 2-пропанола добавляли boc-Lys(boc)-OSu (16.7 г, 37.7 ммоль) и DIEA (13.1 мл, 75.4 ммоль), и смесь перемешивали в течение 30 мин при 45°С. Затем добавляли н-пропиламин (1.56 мл, 18.9 ммоль). Через 5 минут раствор осаждали добавлением 600 мл холодного МТБЭ и центрифугировали (3000 мин-1, 1 мин). Осадок сушили в вакууме в течение 1 ч и растворяли в 400 мл ТГФ. Добавляли 200 мл диэтилового эфира, и продукт охлаждали до -30°С в течение 16 ч без перемешивания. Суспензию фильтровали через стеклянный фильтр и промывали 300 мл холодного МТБЭ. Полученный продукт сушили в вакууме в течение 16 ч.
Выход: 21.0 г (80%) 1d в виде белого твердого вещества.
МС: m/z 1405.4=[М+6Н]6+ (вычислено=1405.4).
Соединение 1е получали растворением полученного на предыдущей стадии соединения 1d (15.6 г, 1.86 ммоль) в 3н. растворе HCl в метаноле (81 мл, 243 ммоль) и перемешиванием в течение 90 мин при 40°С. Добавляли 200 мл МеОН и 700 мл iPrOH, и полученную смесь выдерживали 2 дня при -30°С. Для полноты кристаллизации добавляли 100 мл МТБЭ, и суспензию выдерживали при -30°С в течение ночи. Добавляли 250 мл холодного МТБЭ, суспензию встряхивали в течение 1 мин, фильтровали через стеклянный фильтр и промывали 100 мл холодного МТБЭ. Полученный продукт сушили в вакууме.
Выход: 13.2 г (96%) 1е в виде белого твердого порошка.
МС: m/z=679.1=[М+10Н]10+ (вычислено=679.1).
Для синтеза соединения 1f, к нагретой до 45°С суспензии полученного на предыдущей стадии соединения 1е (8.22 г, 1.12 ммоль) в 165 мл 2-пропанола добавляли boc-Lys(boc)-OSu (11.9 г, 26.8 ммоль) и DIEA (9.34 мл, 53.6 ммоль), и смесь перемешивали в течение 30 мин. Затем добавляли н-пропиламин (1.47 мл, 17.9 ммоль). Через 5 минут раствор охлаждали до -18°С в течение 2 ч, затем добавляли 165 мл холодного МТБЭ, суспензию встряхивали в течение 1 мин и фильтровали через стеклянный фильтр. После этого осадок на фильтре промывали 4×200 мл холодной смеси МТБЭ/iPrOH 4:1 и 1×200 мл холодным МТБЭ. Полученный продукт сушили в вакууме в течение 16 ч.
Выход: 12.8 г, MW (90%) 1f в виде бледно-желтого комковатого твердого вещества.
МС: m/z 1505.3=[М+8H]8+ (вычислено=1505.4).
Реагент основной цепи 1g получали растворением 4-разветвленного-PEG 5кДа(-LysLys2Lys4(boc)8)4 (1f) (15.5 г, 1.29 ммоль) в 30 мл МеОН и охлаждением до 0°С. Добавляли 4н. раствор HCl в диоксане (120 мл, 480 ммоль, охлажден до 0°С) в течение 3 минут и убирали ледяную баню. Через 20 мин добавляли 3н. раствор HCl в метаноле (200 мл, 600 ммоль, охлажденный до 0°С) в течение 15 мин, и полученный раствор перемешивали в течение 10 мин при комнатной температуре. Раствор продукта осаждали добавлением 480 мл холодного МТБЭ и центрифугировали при 3000 об/мин в течение 1 мин. Осадок сушили в вакууме в течение 1 ч и снова рстворяли в 90 мл МеОН, осаждали добавлением 240 мл холодного МТБЭ, и суспензию еще раз центрифугировали при 3000 об/мин в течение 1 мин. Полученный продукт сушили в вакууме.
Выход: 11.5 г (89%) в виде бледно-желтых хлопьев.
МС: m/z=1104.9[M+8H]8+ (вычислено=1104.9).
Пример 27
Методика дериватизации мульти-амино функционализированных PEG, включая 1g для анализа методом обращенно-фазовой ВЭЖХ.
Амино-функционализированные PEG-производные с несколькими аминогруппами трудно анализировать методом обращенно-фазовой ВЭЖХ, поскольку они обычно элюируются быстро, дают широкие пики и имеют очень слабое поглощение в УФ-диапазоне. Поэтому чистоту таких PEG-производных невозможно напрямую проанализировать методом обращенно-фазовой ВЭЖХ, поскольку в типичном случае примеси не отделяются от пика основного вещества. Дериватизация с помощью 3-метокси-4-нитробензойной кислоты дает ароматические амиды, имеющие более узкие пики и лучшее разрешение в условиях анализа методом обращенно-фазовой ВЭЖХ. Кроме того, УФ-детектирование при длине волны 340 нм позволяет напрямую количественно оценить содержание амино-групп, имеющихся в амино-функционализированном PEG-производном.
3-метокси-4-нитробензойной кислоты N-сукцинимидиловый эфир был получен из 3-метокси-4-нитробензойной кислоты, N-гидроксисукцинимида и дициклогексилкарбодиимида в дихлорметане и очищен методом обращенно-фазовой ВЭЖХ.
PEG-раствор: 10 мг мульти-амино функционализированного PEG растворяли в 90 мкл раствора модифицирующего агента в ДМСО: 5 мг 3-метокси-4-нитробензойной кислоты N-сукцинимидилового эфира растворяли в 65 мкл ДМСО.
К 25 мкл PEG-раствора добавляли раствор модифицирующего агента (2 экв. на свободную амино-группу) и диизопропилэтиламина (3 экв. на свободную амино-группу), и полученную смесь встряхивали в течение 15 мин. Добавляли 500 мкл ацетонитрила и затем 800 мкл 0.1н. раствора NaOH, и полученную смесь встряхивали еще 60 минут. 10 мкл полученного раствора подкисляли добавлением 5 мкл уксусной кислоты и разбавляли добавлением 100 мкл смеси ацетонитрил/вода/трифторуксусная кислота (ТФУК) 90:10:0.1 (об/об/об), анализировали методом обращенно-фазовой UPLC (элюент: 0.05% ТФУК в воде / 0.04% ТФУК в ацетонитриле).
Пример 28
Синтез парацетамол-конъюгата 20
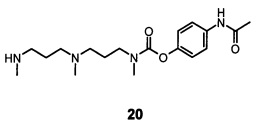
Парацетамол (1 ммоль) растворяли в 10 мл ТГФ и добавляли нитрофенил-хлорформиат (1.1 ммоль) и DIEA (1.1 ммоль). Через 30 минут добавляли N,N-бис[3-(метиламино)пропил]метиламин (2 ммоль), и реакционную смесь перемешивали при комнатной температуре в течение 30 мин. 20 очищали методом обращенно-фазовой ВЭЖХ.
Выход 83 мг (14%).
МС: m/z=351.26 [М+Н]+.
Пример 29
Синтез конъюгата 21 линкер-парацетамол
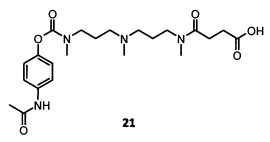
К раствору 20 (17 мкмоль) в ДМФА (300 мкл) добавляли твердый янтарный ангидрид (65 мкмоль) и DIEA (173 мкмоль), и смесь перемешивали при 60°С в течение 50 мин. 21 очищали методом обращенно-фазовой ВЭЖХ.
Выход: 7.7 мг (79%).
Пример 30
Синтез конъюгата 22 гидрогель-парацетамол
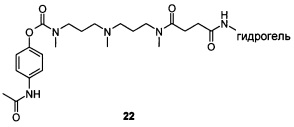
100 мг амино-функционализированного гидрогеля 3е (0.13 ммоль амина/г сухого гидрогеля) суспендировали в ДМФА. Добавляли раствор 21 (6 мкмоль), РуВОР (22 мкмоль) и DIEA (31 мкмоль) в ДМФА (0.5 мл), и полученную смесь встряхивали при 22°С в течение 2 ч. Полученный загруженный гидрогель промывали ДМФА (10 раз), дихлорметаном (10 раз) и этанолом (5 раз), и сушили в вакууме.
Пример 31
Синтез конъюгата 23 линкер-парацетамол
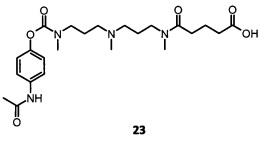
К раствору 20 (17 мкмоль) в ДМФА (300 мкл) добавляли твердый глутаровый ангидрид (79 мкмоль) и DIEA (173 мкмоль), и смесь перемешивали при 60°С в течение 50 мин. 23 очищали методом обращенно-фазовой ВЭЖХ.
Выход: 6.4 мг (64%).
Пример 32
Синтез конъюгата 24 гидрогель-парацетамол
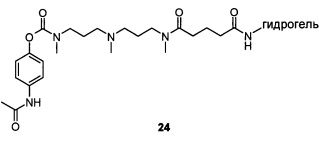
80 мг амино-функционализированного гидрогеля 3е (0.13 ммоль амина/г сухого гидрогеля) суспендировали в ДМФА. Добавляли раствор 23 (5 мкмоль), РуВОР (19 мкмоль) и DIEA (27 мкмоль) в ДМФА (0.5 мл), и полученную смесь встряхивали при 22°С в течение 3 ч. Полученный загруженный гидрогель промывали ДМФА (10 раз), дихлорметаном (10 раз) и этанолом (5 раз) и сушили в вакууме.
Пример 33
Высвобождение парацетамола in vitro
Гидрогель-парацетамол конъюгаты 22 и 24 растворяли в 60 мМ растворе фосфата натрия, рН 7.4, и инкубировали при 37°С. Аликвоты надосадочного раствора анализировали методом обращенно-фазовой ВЭЖХ при длине волны 242 нм и на масс-детекторе на предмет высвобождаемого парацетамоле. МС показал высвобождение немодифицированного парацетамола.
t1/2(22)=19 дней.
t1/2(24)=15 дней.
Пример 34
Синтез цетиризин-эфира 25
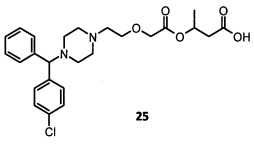
3-Гидроксимасляную кислоту (0.56 ммоль) загружали на 2-хлортритил полимер (0.35 ммоль) согласно методике производителя.
Полимер промывали дихлорметаном (7 раз), ДМФА (7 раз) и дихлорметаном (7 раз). Добавляли к полимеру раствор цетиризина дигидрохлорида (1.25 ммоль), DIC (1.46 ммоль), HOSu (1.39 ммоль) и DIEA (3.13 ммоль) в дихлорметане (3 мл) и инкубировали в течение 15 ч. Промежуточный продукт 25 отщепляли от полимера добавлением раствора гексафторизопропанола (2 мл) в дихлорметане (3 мл) и инкубированием 10 мин. Данную стадию повторяли еще раз, и все летучие компоненты удаляли из объединенных элюатов в токе азота. Продукт 25 (выход 2%) очищали методом обращенно-фазовой ВЭЖХ и анализировали методом обращенно-фазовой ВЭЖХ-МС.
Пример 35
Синтез конъюгата 26 цетиризин-гидрогель
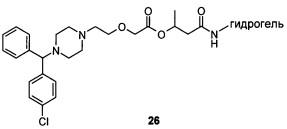
100 мг амино-функционализированного гидрогеля 3е (0.13 ммоль амина/г сухого гидрогеля) суспендировали в ДМФА (0.6 мл). В суспензию гидрогеля добавляли раствор 25 (7.1 мкмоль), РуВОР (23 мкмоль) и DIEA (28 мкмоль) в ДМФА (0.6 мл), и полученную смесь инкубировали в течение 3 ч. Раствор отбрасывали и промывали гидрогель ДМФА (7 раз) и этанолом (5 раз), и сушили в вакууме.
Пример 36
Высвобождение цетиризина in vitro
Высвобождение цетиризина из 26 осуществляли гидролизом в 60 мМ натрийфосфатного буфера при рН 7.4 и 37°С. Немодифицированный цетиризин высвобождался и анализировался методом обращенно-фазовой ВЭЖХ/МС.
t1/2=31 ч.
Пример 37
Синтез линкерного реагента 27f.
Линкерный реагент 27f синтезировали согласно следующей методике:
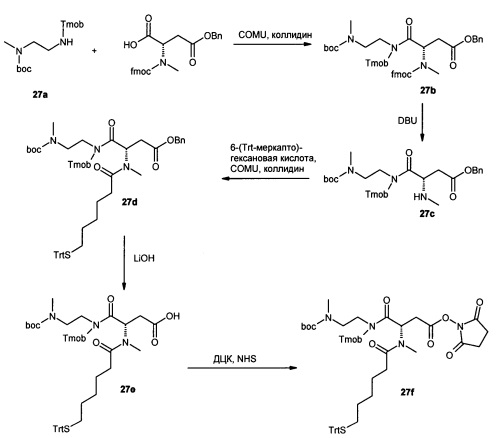
К раствору N-метил-N-boc-этилендиамина (2 г, 11.48 ммоль) и NaCNBH3 (819 мг, 12.63 ммоль) в МеОН (20 мл) порциями добавляли 2,4,6-триметоксибензальдегид (2.08 мг, 10.61 ммоль). Смесь перемешивали при комнатной температуре в течение 90 мин, подкисляли добавлением 3 М HCl (4 мл) и перемешивали еще 15 мин. Реакционную смесь выливали в насыщенный раствор NaHCO3 (200 мл) и экстрагировали 5 раз дихлорметаном. Объединенные органические фазы сушили над Na2SO4 и упаривали растворители в вакууме. Полученный N-метил-N-boc-N'-tmob-этилендиамин (27a) сушили в высоком вакууме и использовали в следующей стадии без дополнительной очистки.
Выход: 3.76 г (11.48 ммоль, 89% чистота, 27a: дважды Tmob-защищенный продукт = 8:1)
MC: m/z 355.22=[M+H]+, (вычислено=354.21).
К раствору 27а (2 г, 5.65 ммоль) в CH2Cl2 (24 мл) добавляли COMU (4.84 г, 11.3 ммоль), N-Fmoc-N-Me-Asp(OBn)-OH (2.08 г, 4.52 ммоль) и коллидин (2.65 мл, 20.34 ммоль). Реакционную смесь перемешивали в течение 3 ч при комнатной температуре, разбавляли дихлорметаном (250 мл) и промывали три раза 0.1 М раствором H2SO4 (100 мл) и три раза насыщенным раствором поваренной соли (100 мл). Водную фазу снова экстрагировали дихлорметаном (100 мл). Объединенные органические фазы сушили над Na2SO4, фильтровали, и остаток упаривали до объема 24 мл. 27b очищали методом флэш-хроматографии.
Выход: 5.31 г (148%, 6.66 ммоль).
MC: m/z 796.38=[M+H]+, (вычислено=795.37).
К раствору 27b [5.31 г, макс.4.51 ммоль N-Fmoc-N-Me-Asp(OBn)-OH] в ТГФ (60 мл) добавляли DBU (1.8 мл, 3% об/об). Раствор перемешивали в течение 12 мин при комнатной температуре, разбавляли дихлорметаном (400 мл) и промывали три раза 0.1 М раствором H2SO4 (150 мл) и три раза насыщенным раствором поваренной соли (150 мл). Водную фазу снова экстрагировали дихлорметаном (100 мл). Объединенные органические фазы сушили над Na2SO4 и фильтровали. 27с получали после упаривания растворителя и использовали в последующей реакции без дополнительной очистки.
MC: m/z 574.31=[M+H]+, (вычислено=573.30).
27с (5.31 г, 4.51 ммоль, неочищенный) растворяли в MeCN (26 мл) и добавляли COMU (3.87 г, 9.04 ммоль), 6-тритилмеркаптогексановую кислоту (2.12 г, 5.42 ммоль) и коллидин (2.35 мл, 18.08 ммоль). Реакционную смесь перемешивали в течение 4 ч при комнатной температуре, разбавляли дихлорметаном (400 мл) и промывали три раза 0.1 М раствором H2SO4 (100 мл) и три раза насыщенным раствором поваренной соли (100 мл). Водную фазу снова экстрагировали дихлорметаном (100 мл). Объединенные органические фазы сушили над Na2SO4, фильтровали и получали 7i упариванием растворителя. Продукт 27d очищали методом флэш-хроматографии.
Выход: 2.63 г (62%, 94% чистота).
МС: m/z 856.41=[M+H]+, (вычислено=855.41).
К раствору 27d (2.63 г, 2.78 ммоль) в i-PrOH (33 мл) и H2O (11 мл) добавляли LiOH (267 мг, 11.12 ммоль), и реакционную смесь перемешивали в течение 70 мин при комнатной температуре. Смесь разбавляли добавлением CH2Cl2 (200 мл) и промывали три раза 0.1 М раствором H2SO4 (50 мл) и три раза насыщенным раствором поваренной соли (50 мл). Водную фазу снова экстрагировали дихлорметаном (100 мл). Объединенные органические фазы сушили над Na2SO4, фильтровали и получали 27е упариванием растворителя. Продукт 27е очищали методом флэш-хроматографии.
Выход: 2.1 г (88%).
МС: m/z 878.4=[M+Na]+, (вычислено=878.40).
К раствору 27е (170 мг, 0.198 ммоль) в безводном ДХМ (4 мл) добавляли DCC (123 мг, 0.59 ммоль) и каталитическое количество DMAP. Через 5 мин добавляли N-гидрокси-сукцинимид (114 мг, 0.99 ммоль), и реакционную смесь перемешивали при комнатной температуре в течение 1 ч. Реакционную смесь фильтровали, растворитель удаляли в вакууме, и остаток растворяли в смеси ацетонитрила (90%) и 0.1%-ного раствора ТФУК (3.4 мл). Сырой продукт очищали методом обращенно-фазовой ВЭЖХ. Содержащие продукт фракции нейтрализовывали 0.5 М рН 7.4 фосфатным буфером и упаривали. Оставшуюся водную фазу экстрагировали дихлорметаном и получали 27f после упаривания растворителя.
Выход: 154 мг (81%).
МС: m/z 953.4=[M+H]+, (вычислено=953.43).
Пример 38
Синтез NεB29-инсулин линкерного конъюгата 28.
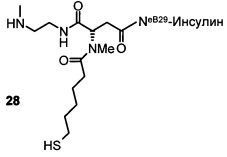
Инсулин (644 мг, 0.111 ммоль) растворяли в 6.5 мл ДМСО. Добавляли 3 мл охлажденного (4°С) 0.5 М натрий-боратного буфера (рН 8.5) и 27f (70 мг, 0.073 ммоль) в 2.5 мл ДМСО, и смесь перемешивали в течение 5 мин при комнатной температуре. Добавляли 400 мкл АсОН и очищали защищенный инсулиновый конъюгат методом обращенно-фазовой ВЭЖХ.
Выход: 172 мг (0.025 ммоль).
МС: m/z 1662.27=[М+4Н]4+ (вычислено=1662.48).
Удаление защитных групп проводили путем обработки лиофилизованных фракций, содержащих продукт, добавлением 6 мл смеси 90/10/2/2 (об/об/об/об) гексафторизопропанол/ТФУК/TES/вода в течение 1 часа при комнатной температуре. NεB29-конъюгированный инсулин-линкер конъюгат 28 очищали методом обращенно-фазовой ВЭЖХ.
Выход: 143 мг (0.023 ммоль).
МС: m/z 1531.46=[М+4Н]4+ (вычислено=1531.71).
Пример 39
Получение инсулин-линкер-гидрогеля 29.
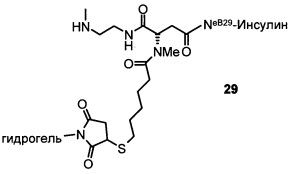
29 получали следующим образом: Суспензию малеимид-функционализированного гидрогеля 4d в рН 2.5 HCl, 0.01% Tween-20 (58.3 мл, 958 мкмоль малеимидных групп) помещали в реактор для твердофазного синтеза. Раствор инсулин-линкер-тиола 28 (117 мл, 460 мкмоль) в 2.5 HCl, 0.01% Tween-20 добавляли к 4d. Полученную суспензию инкубировали при комнатной температуре в течение 5 мин. Добавляли сукцинатный буфер (4.8 мл, рН 4.0, 150 мМ; 1 мМ EDTA, 0.01% Tween-20), достигая значения рН 3.6, и суспензию инкубировали при комнатной температуре в течение 90 мин.
Поглощение тиола отслеживали по тесту Эллмана. Гидрогель промывали 10 раз сукцинатным буфером (рН 3.0, 50 мМ; 1 мМ EDTA, 0.01% Tween-20) и 2 раза сукцинатным буфером (рН 3.0, 50 мМ; 1 мМ EDTA, 0.01% Tween-20), содержащим 10 мМ меркаптоэтанол. Наконец, гидрогель суспендировали в меркаптоэтанол-содержащем буфере и инкубировали 3 часа при комнатной температуре.
Инсулин-линкер-гидрогель 29 промывали 10 раз сукцинатным буфером (рН 3.0, 50 мМ; 1 мМ EDTA, 0.01% Tween-20) и 6 раз сукцинат/Tris буфером (рН 5.0, 10 мМ; 85 г/л трегалозы, 0.01% Tween-20).
Загрузка инсулина в 29: 18.7 мг инсулин/мл суспензии инсулин-линкер-гидрогель.
Пример 40
Инъецируемость инсулин-линкер-пролекарства на основе гидрогеля 29.
5 мл инсулин-линкер-пролекарства на основе гидрогеля 29 (распределение гранул по размеру 32-75 мкм, 18 мг инсулина/мл суспензии инсулин-линкер-пролекарства на основе гидрогеля) подвергали обмену в буфере с рН 5.0 янтарная кислота/трис (10 мМ, 40 г/л маннита; 10 г/л трегалозы дигидрата; 0.05% TWEEN-20). Суспензией инсулин-линкер-пролекарства на основе гидрогеля заполняли шприц объемом 1 мл (длина 57 мм) через игру 20 g. Иглу 20 g заменяли на иглу 30 g, помещали в узел для шприца (Aqua Computer GmbH&Co. KG) и начинали измерения при скорости движения поршня 172 мм/мин (соответствует 50 мкл/сек) (силовой испытательный стенд: Multitest 1-d, Программа записи данных: EvaluatEmperor Lite, Version 1.16-015, Forge Gauge: BFG 200 N (все производства Mecmesin Ltd., UK). Эксперименты с увеличивающейся скоростью движения поршня, проиллюстрированные в приведенной ниже таблице, проводили с новым образцом инсулин-линкер-пролекарства на основе гидрогеля. Аналогично проводили эксперименты с водой и этиленгликолем. Для всех экспериментов использовали такую же иглу 30 G. График зависимости силы от скорости потока при использовании иглы 30 g изображен на Фиг. 16.
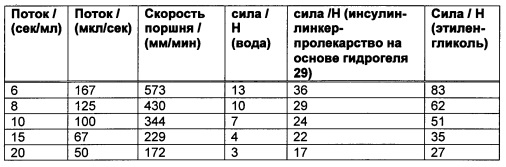
Пример 41
Получение гранул гидрогеля (30) и (30а), содержащего свободные амино-группы.
Раствор 275 мг 1g и 866 мг 2d в 14 мл ДМСО добавляли к раствору 100 мг Arlacel P135 (Croda International  ) в 60 мл гептана. Смесь перемешивали при 700 об/мин стандартной металлической мешалкой в течение 10 мин при 25°С, получая суспензию. Добавляли 1.0 мл N,N,N',N'-тетраметилэтилендиамина для осуществления полимеризации. Через 2 часа скорость вращения мешалки уменьшали до 400 об/мин, и смесь перемешивали еще 16 ч. Добавляли 1.5 мл уксусной кислоты, и через 10 мин добавляли 50 мл воды. Через 5 мин мешалку останавливали и сливали водную фазу.
) в 60 мл гептана. Смесь перемешивали при 700 об/мин стандартной металлической мешалкой в течение 10 мин при 25°С, получая суспензию. Добавляли 1.0 мл N,N,N',N'-тетраметилэтилендиамина для осуществления полимеризации. Через 2 часа скорость вращения мешалки уменьшали до 400 об/мин, и смесь перемешивали еще 16 ч. Добавляли 1.5 мл уксусной кислоты, и через 10 мин добавляли 50 мл воды. Через 5 мин мешалку останавливали и сливали водную фазу.
Для фракицонирования гранул по размеру, суспензию вода-гидрогель просеивали во влажном состоянии на металлических ситах с размером отверстий 75, 50, 40, 32 и 20 мкм. Фракции гранул, удерживаемые на ситах 32, 40 и 50 мкм, объединяли и промывали 3 раза водой, 10 раз этанолом и сушили в течение 16 ч при 0.1 мбар, получая 30 в виде белого твердого порошка.
30а получали, как описано для 30, за исключением того, что было использовано 1200 мг 1g, 3840 мг 2d, 28.6 мл ДМСО, 425 мг Arlacel P135, 100 мл гептана и 4.3 мл TMEDA. При обработке добавляли 6.6 мл уксусной кислоты и затем, через 10 минут, добавляли 50 мл воды и 50 мл насыщенного водного раствора хлорида натрия.
Содержание амино-групп в гидрогеле определяли конъюгированием fmoc-аминокислоты со свободными амино-группами гидрогеля и последующим количественным определением содержания fmoc, как описано в статье Gude, M., J. Ryf, et al. (2002) Letters in Peptide Science 9(4): 203-206.
По результатам определения, содержание амино-групп в 30 и 30а составило между 0.11 и 0.16 ммоль/г.
Сокращения:



| название | год | авторы | номер документа |
|---|---|---|---|
| ПРОЛЕКАРСТВА, СОДЕРЖАЩИЕ КОНЪЮГАТ ЭКСЕНДИН-ЛИНКЕР | 2011 |
|
RU2593774C2 |
| ПРОЛЕКАРСТВА, СОДЕРЖАЩИЕ КОНЪЮГАТ ИНСУЛИНА И ЛИНКЕРА | 2010 |
|
RU2574667C2 |
| СТЕРИЛИЗАЦИЯ БИОРАЗЛАГАЕМЫХ ГИДРОГЕЛЕЙ | 2010 |
|
RU2558847C9 |
| ПРОЛЕКАРСТВА НА ОСНОВЕ ГИДРОГЕЛЯ | 2013 |
|
RU2647729C2 |
| ДИАГНОСТИКА, ПРОФИЛАКТИКА И ЛЕЧЕНИЕ БОЛЕЗНЕЙ СУСТАВОВ | 2013 |
|
RU2682676C2 |
| ПРОЛЕКАРСТВА, СОДЕРЖАЩИЕ КОНЬЮГАТ ГИАЛУРОНОВОЙ КИСЛОТЫ, ЛИНКЕРА И ДВОЙНОГО АГОНИСТА GLP-1/ГЛЮКАГОНА | 2016 |
|
RU2719482C2 |
| VEGF-НЕЙТРАЛИЗУЮЩИЕ ПРОЛЕКАРСТВА ДЛЯ ЛЕЧЕНИЯ ОФТАЛЬМОЛОГИЧЕСКИХ ЗАБОЛЕВАНИЙ | 2013 |
|
RU2673881C2 |
| ГЛИЦЕРИН-СВЯЗАННЫЕ ПЭГИЛИРОВАННЫЕ САХАРА И ГЛИКОПЕПТИДЫ | 2007 |
|
RU2460543C2 |
| СИСТЕМЫ ДОСТАВКИ С ЗАМЕДЛЕННЫМ ВЫСВОБОЖДЕНИЕМ, СОДЕРЖАЩИЕ БЕССЛЕДНЫЕ ЛИНКЕРЫ | 2018 |
|
RU2772690C2 |
| КОМПОЗИЦИЯ ИНСУЛИНА ДЛИТЕЛЬНОГО ДЕЙСТВИЯ | 2010 |
|
RU2556340C2 |
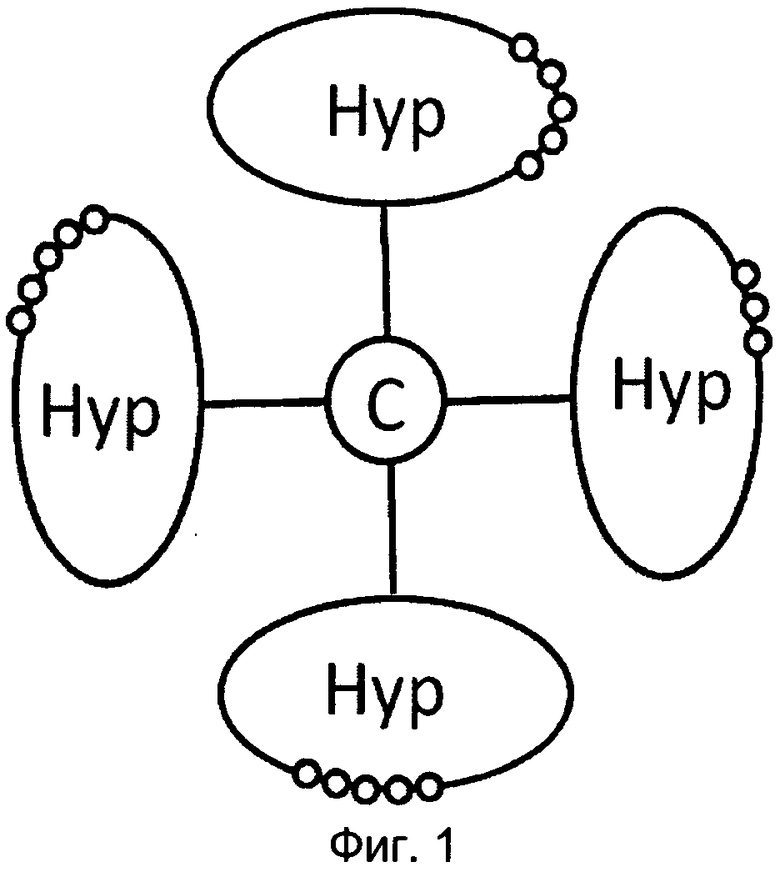
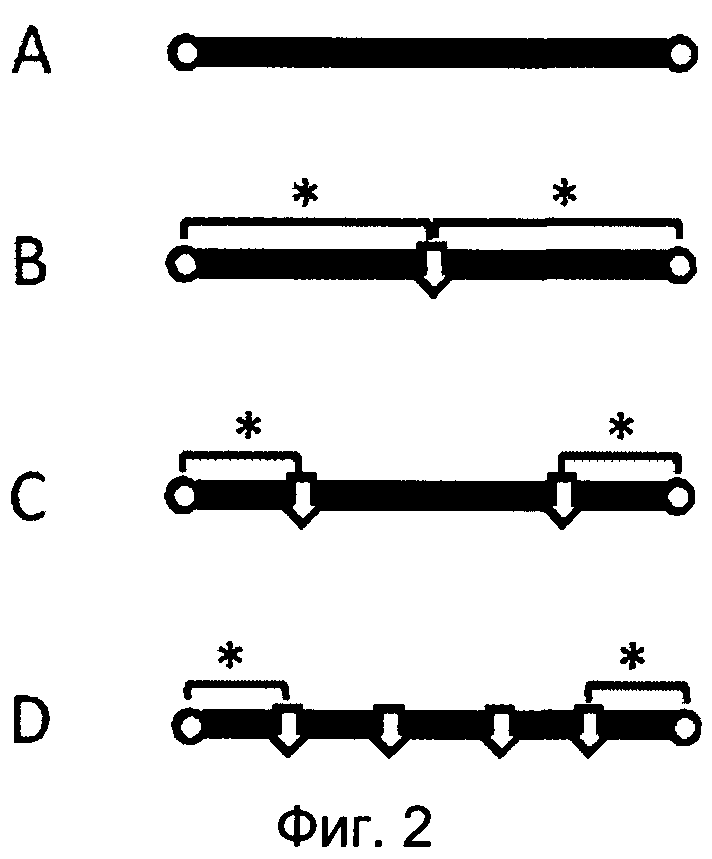

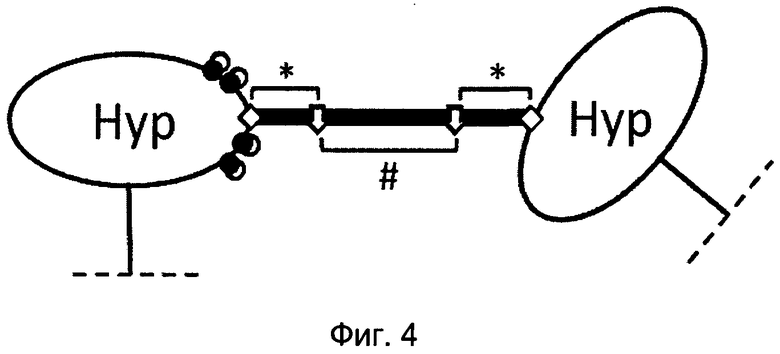
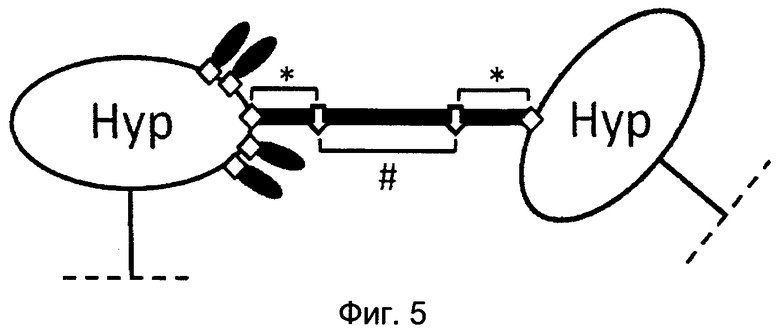
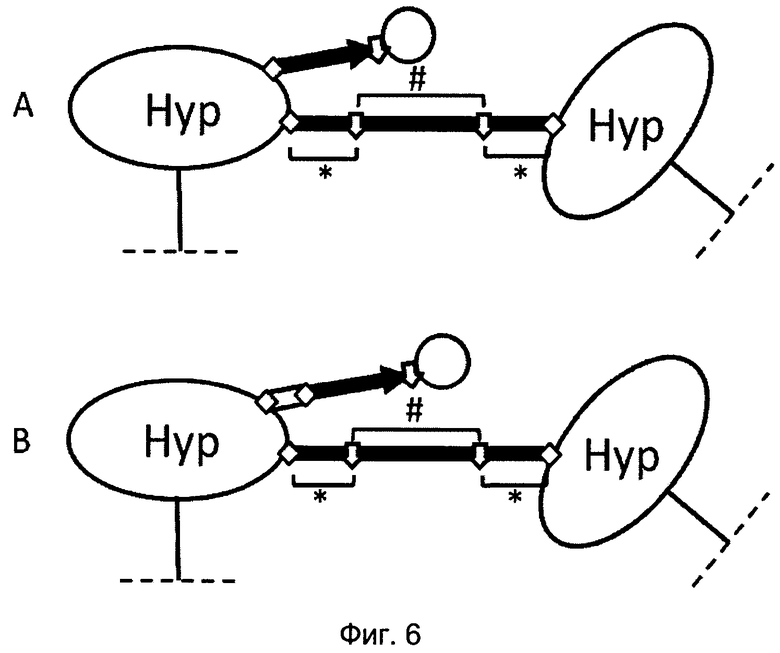
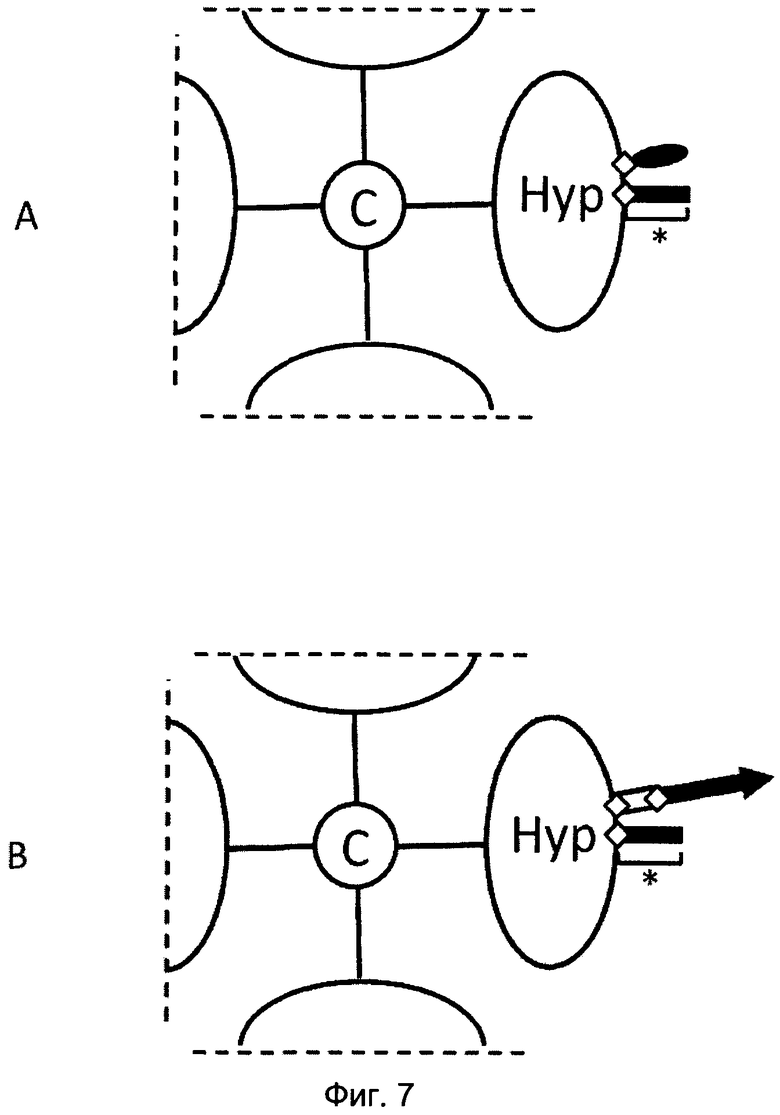
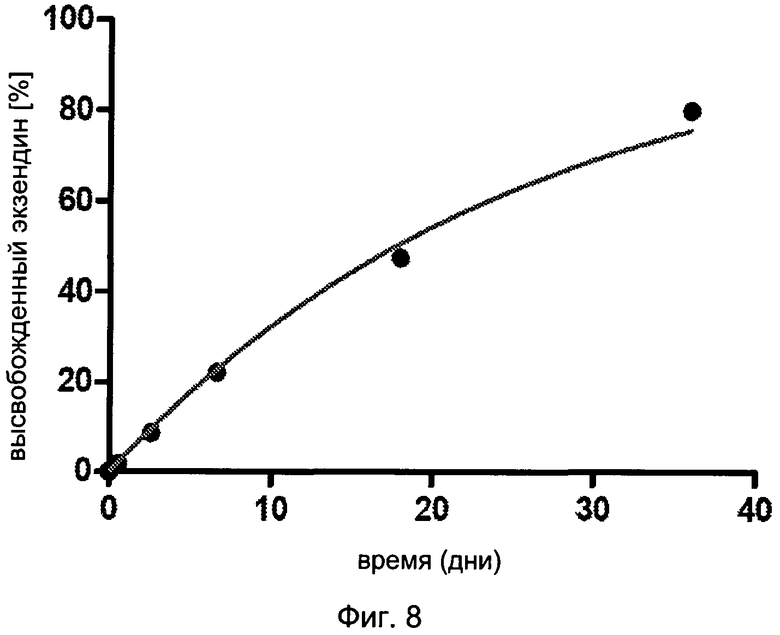
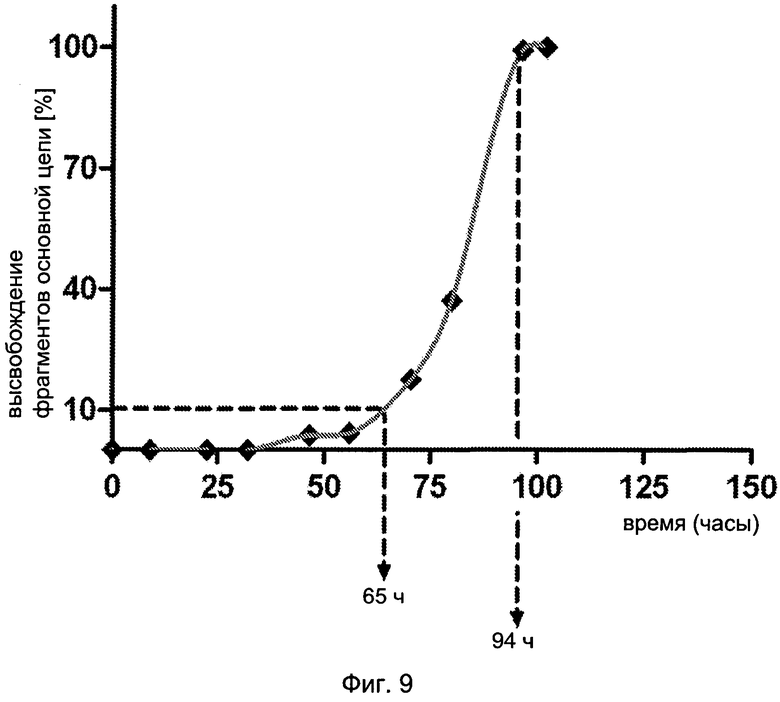
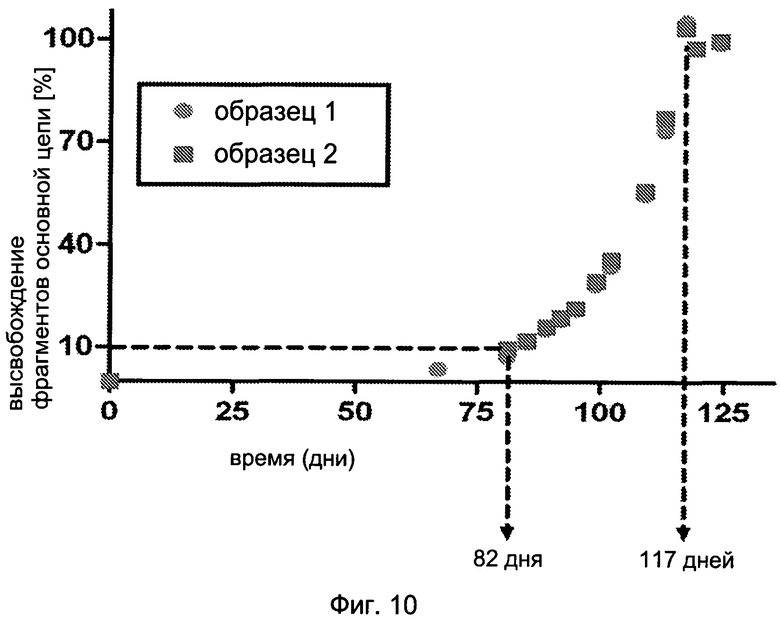
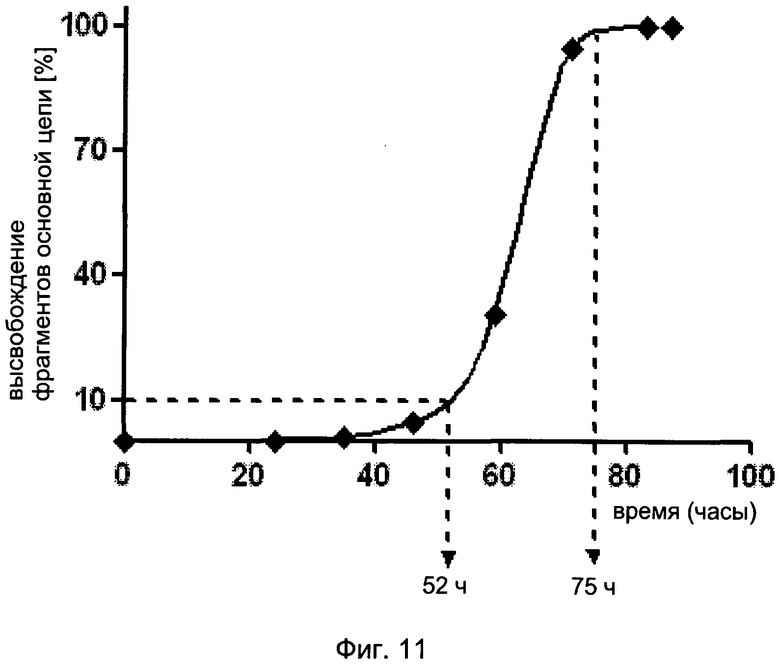
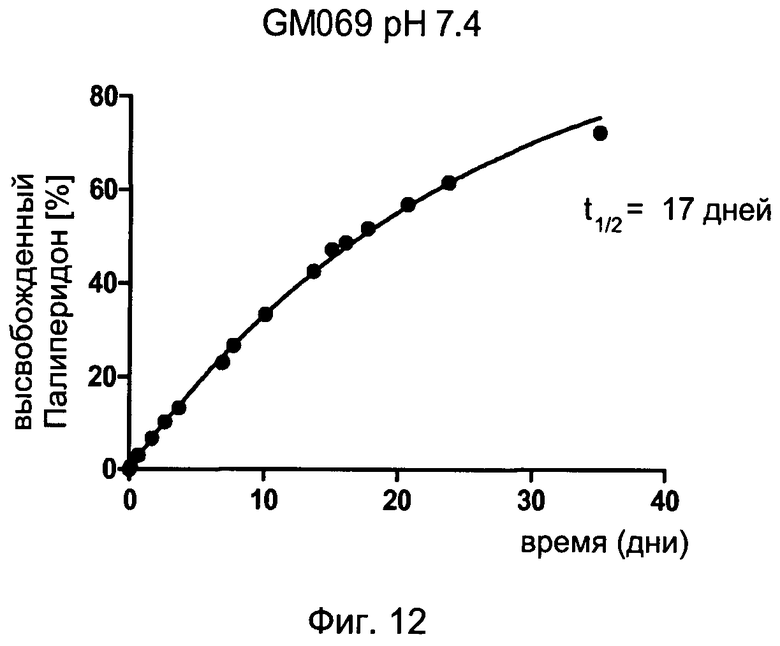
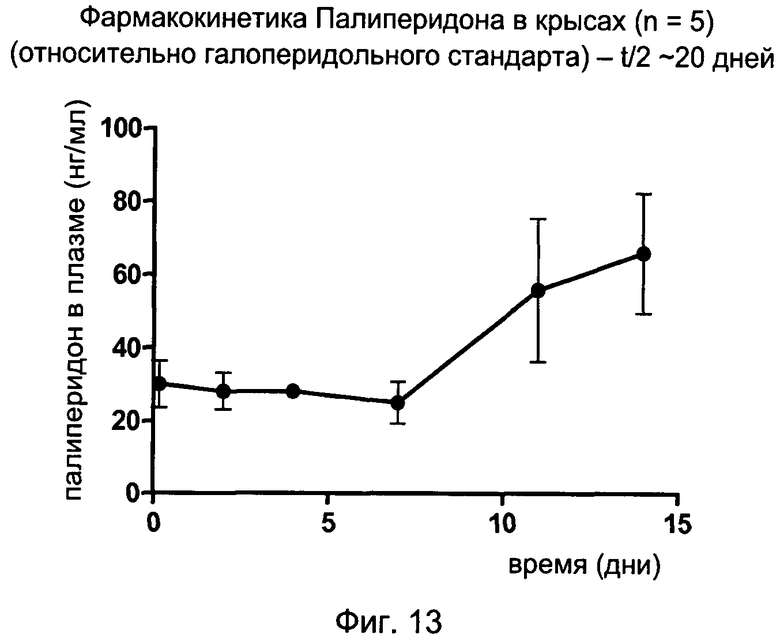
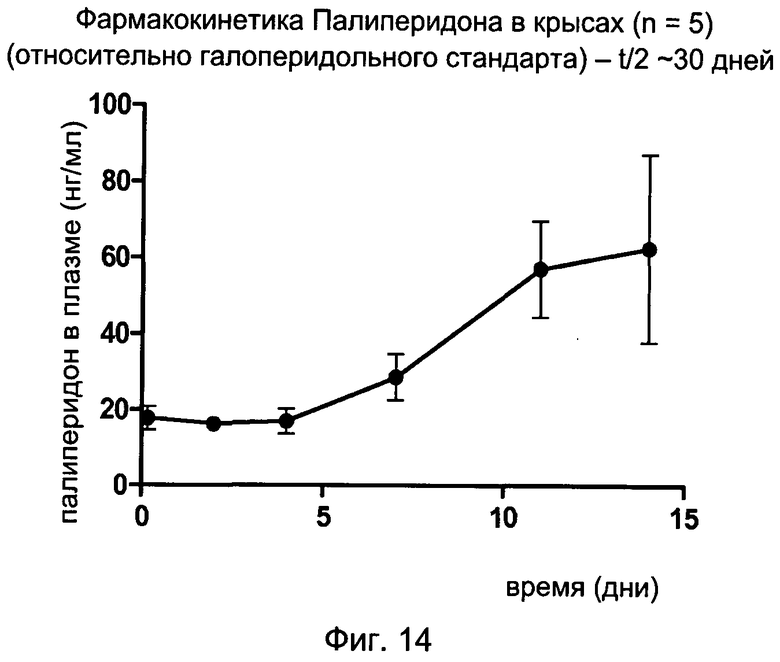
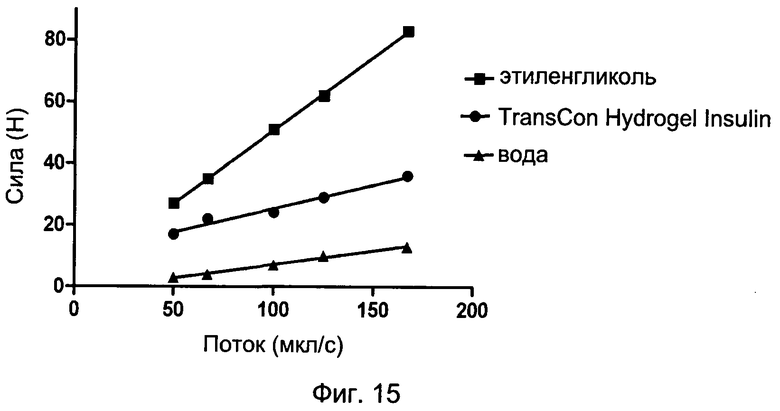
Настоящее изобретение касается биоразлагаемых нерастворимых в воде гидрогелей на основе полиэтиленгликоля. Настоящее изобретение также касается конъюгатов таких биоразлагаемых гидрогелей с аффинными лигандами или хелатирующими группами или ионообменными группами, связанных с носителем пролекарств, в которых биоразлагаемый гидрогель по настоящему изобретению является носителем, и их фармацевтических композиций, а также их применения в качестве лекарственного средства. Описан биоразлагаемый нерастворимый в воде гидрогель на основе поли(этиленгликоля), содержащий фрагменты основной цепи, которые соединены гидролитически разрушаемыми связями, причем фрагменты основной цепи характеризуются молекулярным весом в диапазоне от 1 кДа до 20 кДа и имеют структуру С*-(А-Нур)x, где С* представляет собой разветвляющееся ядро, А представляет собой полимерную цепь на основе поли(этиленгликоля), Hyp представляет собой сверхразветвленный дендритный фрагмент, x представляет собой целое число от 3 до 16; и где сверхразветвленный дендритный фрагмент дополнительно содержит реакционно-способные функциональные группы и соединяющие функциональные группы, причем фрагменты основной цепи соединены вместе посредством поперечносшивающих фрагментов, причем каждый поперечносшивающий фрагмент имеет на конце по меньшей мере две гидролитически разрушаемые связи. Описаны также конъюгат и связанное с носителем пролекарство, содержащие указанный биоразлагаемый гидрогель; применение пролекарства в лекарственном средстве. Также описаны способ получения вышеуказанного гидрогеля, включающий стадию (а) вступления в реакцию реагента основной цепи, и гидрогель, получаемый данным способом в форме покрытия, сетки, стента или микрочастицы, получаемый измельчением механическими способами, такими как перемешивание, разбивание, режущая прессовка или размалывание, и при необходимости просеиванием. Раскрываются способы получения пролекарства, способ получения инъецируемого через иглу пролекарства и пролекарство, полученное данным способом. 16 н. и 22 з.п. ф-лы, 41 пр., 15 ил.
1. Биоразлагаемый нерастворимый в воде гидрогель на основе поли(этиленгликоля), содержащий фрагменты основной цепи, которые соединены гидролитически разрушаемыми связями, причем фрагменты основной цепи характеризуются молекулярным весом в диапазоне от 1 кДа до 20 кДа и имеют структуру С*-(А-Нур)x, где
С* представляет собой разветвляющееся ядро,
А представляет собой полимерную цепь на основе поли(этиленгликоля),
Hyp представляет собой сверхразветвленный дендритный фрагмент,
x представляет собой целое число от 3 до 16;
и где сверхразветвленный дендритный фрагмент дополнительно содержит реакционноспособные функциональные группы и соединяющие функциональные группы,
причем фрагменты основной цепи соединены вместе посредством поперечносшивающих фрагментов, причем каждый поперечносшивающий фрагмент имеет на конце по меньшей мере две гидролитически разрушаемые связи.
2. Биоразлагаемый гидрогель по п. 1, в котором поперечносшивающие фрагменты имеют молекулярный вес в диапазоне от 0,5 кДа до 5 кДа.
3. Биоразлагаемый гидрогель по п. 1, в котором каждый поперечносшивающий фрагмент имеет в своей основе PEG.
4. Биоразлагаемый гидрогель по п. 3, в котором каждый поперечносшивающий фрагмент представляет собой одну полимерную цепь на основе поли(этиленгликоля).
5. Биоразлагаемый гидрогель по одному из пп. 1-4, в котором каждый фрагмент основной цепи содержит в сумме по меньшей мере 16 соединяющих биоразлагаемых и реакционноспособных функциональных групп.
6. Биоразлагаемый гидрогель по п. 5, в котором фрагмент основной цепи имеет четвертичный атом углерода формулы
С(А-Нур)4,
где каждый А независимо представляет собой полимерную цепь на основе поли(этиленгликоля), терминально присоединенную к четвертичному атому углерода стабильной ковалентной связью, и дистальный конец полимерной цепи ковалентно связан с дендритным фрагментом Hyp, причем каждый дендритный фрагмент Hyp имеет по меньшей мере четыре функциональные группы, представляющие собой соединяющие и реакционноспособные функциональные группы
7. Биоразлагаемый гидрогель по п. 6, в котором фрагменты основной цепи содержат разветвляющееся ядро следующей формулы:
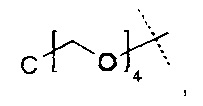
где пунктирная линия означает присоединение к остальной части фрагмента основной цепи.
8. Биоразлагаемый гидрогель по п. 7, в котором фрагменты основной цепи содержат структуру следующей формулы:
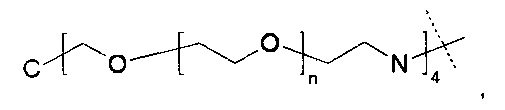
где n представляет собой целое число от 5 до 50, и пунктирная линия означает присоединение к остальной части молекулы.
9. Биоразлагаемый гидрогель по п. 7, в котором фрагмент основной цепи содержит сверхразветвленный фрагмент Hyp следующей формулы:
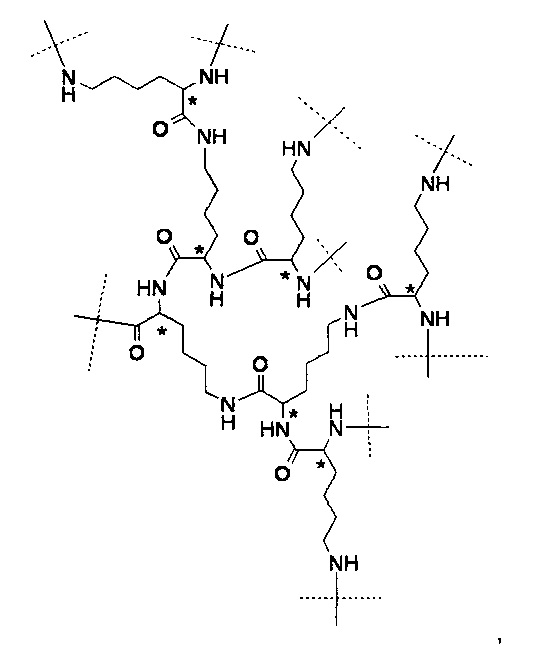
где пунктирные линии означают присоединение к остальной части молекулы, и помеченные звездочкой атомы углерода имеют S-конфигурацию.
10. Биоразлагаемый гидрогель по п. 7, в котором фрагменты основной цепи содержат по меньшей мере один спейсер следующей формулы:
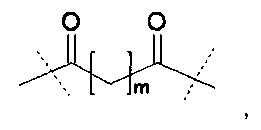
где одна из пунктирных линий означает присоединение к сверхразветвленному фрагменту Hyp, а вторая пунктирная линия означает присоединение к остальной части молекулы; и
где m представляет собой целое число от 2 до 4.
11. Биоразлагаемый гидрогель по одному из пп. 7-10, в котором фрагменты основной цепи соединены посредством поперечносшивающих фрагментов, содержащих следующую структуру
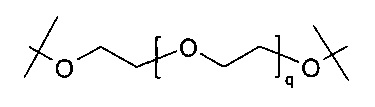
где
q представляет собой целое число от 3 до 100.
12. Конъюгат, содержащий гидрогель по одному из пп. 1-11, в котором гидрогель состоит из фрагментов основной цепи, связанных гидролитически разрушаемыми связями и дополнительно несущих стабильные связки со спейсерными молекулами или блокирующими группами, или их комбинациями.
13. Конъюгат, содержащий гидрогель по одному из пп. 1-11, в котором гидрогель состоит из фрагментов основной цепи, связанных гидролитически разрушаемыми связями и дополнительно несущих стабильные связки с лигандами или хелатирующими группами.
14. Связанное с носителем пролекарство, содержащее биоразлагаемый гидрогель по одному из пп. 1-11 в качестве носителя, в котором имеется несколько стабильных связок фрагментов основной цепи с временным линкером пролекарства L, к которому ковалентно присоединен биологически активный фрагмент D, причем биологически активный фрагмент D представляет собой полипептид, белок или низкомолекулярный биологически активный фрагмент.
15. Связанное с носителем пролекарство по п. 14, в котором биологически активный фрагмент D содержит аминную, гидроксильную, карбоксильную или меркапто-группу, и временный линкер пролекарства L, будучи небиологически активным линкером, образует вместе с аминной, гидроксильной, карбоксильной, фосфатной или меркапто-группой конъюгат D-L.
16. Связанное с носителем пролекарство по п. 14 или 15, в котором связка между D и L представляет собой карбаматную, карбонатную, амидную или сложноэфирную связку.
17. Связанное с носителем пролекарство по п. 16, в котором биологически активный фрагмент D содержит ароматический амин, и в котором временный линкер пролекарства L представляет собой небиологически активный линкер L, содержащий
i) фрагмент L1, представленный формулой (VIII),
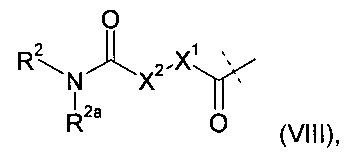
где пунктирная линия означает присоединение L1 к ароматической амино-группе биологически активного фрагмента D путем образования амидной связи;
X1 представляет собой C(R1R1a) или циклический фрагмент, выбранный из С3-7 циклоалкила, 4-7-членного гетероциклила, фенила, нафтила, инденила, инданила, тетралинила или 9-11-членного гетеробициклила;
X2 представляет собой химическую связь или выбран из C(R3R3a), N(R3), О, C(R3R3a)-C(R4R4a), C(R3R3a)-N(R4), N(R3)-C(R4R4a), C(R3R3a)-O или O-C(R3R3a),
где в случае, если X1 представляет собой циклический фрагмент, X2 представляет собой химическую связь, C(R3R3a), N(R3) или О;
необязательно, в случае, если X1 представляет собой циклический фрагмент и X2 представляет собой C(R3R3a), порядок расположения фрагмента X1 и фрагмента X2 в составе L1 может поменяться;
R1, R3 и R4 независимо выбраны из группы, состоящей из Н, C1-4 алкила и -N(R5R5a);
R1a, R2, R2a, R3a, R4a и R5a независимо выбраны из группы, состоящей из H и С1-4 алкила;
необязательно, одна из пар R2a/R2, R2a/R3a, R2a/R4a объединена с образованием 4-7-членного, по меньшей мере частично насыщенного гетероцикла;
R5 представляет собой C(O)R6;
R6 представляет собой С1-4 алкил;
необязательно, одна из пар R1a/R4a, R3a/R4a или R1a/R3a образует химическую связь;
необязательно, L1 дополнительно замещен;
ii) фрагмент L2 представляет собой химическую связь или спейсер, и L2 связан с группой-носителем Z, представляющей собой гидрогель по одному из пп. 1-5,
где L1 замещен одним фрагментом L2, при условии, что атом водорода, помеченный звездочкой в формуле (VIII), не заменен на L2;
необязательно, L имеет дополнительные заместители.
18. Связанное с носителем пролекарство по п. 16, в котором биологически активный фрагмент D содержит первичный или вторичный алифатический амин, и предпочтительная структура для пролекарства по настоящему изобретению представляет собой пролекарственный конъюгат D-L, где
D представляет собой биологически активный фрагмент, содержащий первичный или вторичный алифатический амин; и
L представляет собой небиологически активный линкерный фрагмент -L1, представленный формулой (VI),
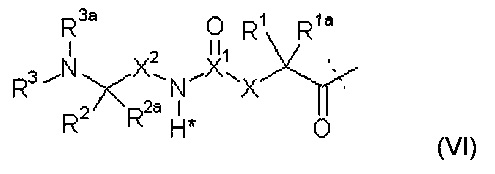
в котором пунктирная линия означает соединение с первичной или вторичной алифатической амино-группой биологически активного фрагмента путем образования амидной связи;
X представляет собой C(R4R4a); N(R4); О; C(R4R4a)-C(R5R5a); C(R5R5a)-C(R4R4a); C(R4R4a)-N(R6); N(R6)-C(R4R4a); C(R4R4a)-O или O-C(R4R4a);
X1 представляет собой С или S(O);
X2 представляет собой C(R7,R7a) или C(R7,R7a)-C(R8,R8a);
R1, R1a, R2, R2a, R3, R3a, R4, R4a, R5, R5a, R6, R7, R7a, R8, R8a независимо выбраны из группы, состоящей из H и С1-4 алкила; или
необязательно, одна или более из пар R1a/R4a, R1a/R5a, R4a/R5a, R4a/R5a, R7a/R8a образуют химическую связь;
необязательно, одна или более из пар R1/R1a, R2/R2a, R4/R4a, R5/R5a, R7/R7a, R8/R8a объединены с атомом, с которым они соединены, образуя С3-7 циклоалкил или 4-7-членный гетероциклил;
необязательно, одна или более из пар R1/R4, R1/R5, R1/R6, R4/R5, R7/R8, R2/R3 объединены с атомами, с которыми они соединены, образуя цикл А;
необязательно, R3/R3a объединены вместе с атомом азота, с которым они соединены, с образованием 4-7-членного гетероцикла;
А выбран из группы, состоящей из фенила; нафтила; инденила; инданила; тетралинила; С3-10 циклоалкила; 4-7-членного гетероциклила и 9-11-членного гетеробициклила; и
где L1 замещен одной группой L2-Z и необязательно дополнительно замещен, при условии, что атом водорода, помеченный звездочкой в формуле (VI), не заменен на заместитель; где
L2 представляет собой одинарную химическую связь или спейсер; и
Z представляет собой гидрогель по одному из пп. 1-5.
19. Связанное с носителем пролекарство по п. 16, в котором биологически активный фрагмент D содержит ароматическую гидроксильную группу, и в котором временный линкер пролекарства L представляет собой небиологически активный линкер L, содержащий
i) фрагмент L1, представленный формулой (XI),
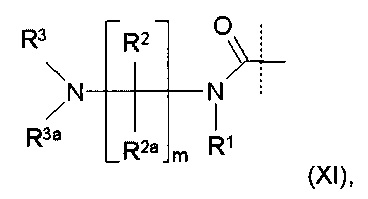
где пунктирная линия означает присоединение L1 к ароматической гидроксильной группе биологически активного фрагмента D путем образования карбаматной группы;
R1 выбран из группы, состоящей из С1-4 алкила; гетероалкила; С3-7 циклоалкила и
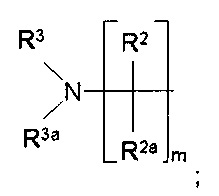
R2, R2a, R3, R3a независимо выбраны из атома водорода, замещенного или незамещенного линейного, разветвленного или циклического С1-4 алкила или гетероалкила;
m независимо равен 2, 3 или 4;
ii) фрагмент L2, который представляет собой химическую связь или спейсер, и L2 связан с гидрогелем по одному из пп. 1-5,
где L1 замещен одним фрагментом L2;
необязательно, L имеет дополнительные заместители.
20. Связанное с носителем пролекарство по одному из пп. 17-19, в котором L2 присоединен к Z через терминальную группу, имеющую следующую структуру
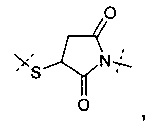
в котором пунктирные линии означают присоединение к L2 и Z, соответственно.
21. Пролекарство по одному из пп. 14-20 для применения в лекарственном средстве.
22. Способ получения гидрогеля по п. 1, включающий стадию
(а) вступления в реакцию реагента основной цепи, имеющего формулу
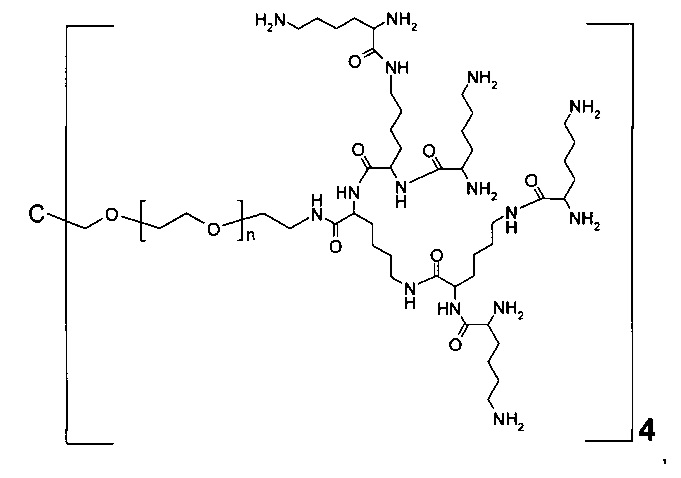
где n представляет собой целое число от 3 до 100;
с поперечносшивающим реагентом следующей формулы
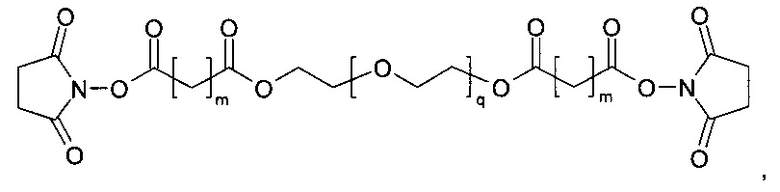
где
q представляет собой целое число от 3 до 100;
каждый m независимо представляет собой целое число от 2 до 4;
в соотношении амин/активный сложный эфир от 2:1 до 1,05:1, предпочтительно дающего загрузку гидрогеля от 0,02 до 2 ммоль амина на грамм гидрогеля; и где реагенты растворяются в апротонном растворителе в присутствии подходящего основания.
23. Способ по п. 22, в котором апротонный растворитель представляет собой ДМСО, а основание представляет собой N,N,N',N'-тетраметилэтилендиамин.
24. Способ по п. 22, в котором реагенты диспергированы в алифатическом углеводороде в присутствии подходящего эмульгатора.
25. Способ по п. 24, в котором алифатический углеводород представляет собой н-гептан, и эмульгатор представляет собой поли(этиленгликоль) 30 диполигидроксистеарат.
26. Способ по одному из пп. 22-25, дополнительно включающий стадии отделения микрочастиц, промывки и фракционирования по размеру частиц посредством механического просеивания.
27. Гидрогель по п. 1 или получаемый способом по п. 22 или 23 в форме покрытия, сетки, стента или микрочастицы, получаемый измельчением механическими способами, такими как перемешивание, разбивание, режущая прессовка или размалывание, и при необходимости просеиванием.
28. Способ получения пролекарства по одному из пп. 14-20, включающий стадии:
(a) реакция биологически активного фрагмента с гидрогелем, получаемым способом по пп. 22 или 23, с формированием временной связки, и удаление непрореагировавшего биологически активного фрагмента промывкой и фильтрованием;
(b) необязательно, блокирование непрореагировавших реакционноспособных функциональных групп подходящим блокирующим реагентом и удаление непрореагировавшего блокирующего реагента промывкой и фильтрованием.
29. Способ получения пролекарства по одному из пп. 14-20, включающий стадии:
(a) соединение спейсерного реагента с биологически активным фрагментом, дающее конъюгат биологически активный спейсерный фрагмент;
(b) реакция конъюгата биологически активный спейсерный фрагмент со стадии (а) с реакционноспособными функциональными группами гидрогеля, получаемого способом по пп. 22 или 23, и удаление непрореагировавшего конъюгата биологически активный спейсерный фрагмент промывкой и фильтрованием;
(c) необязательно, блокирование непрореагировавших реакционноспособных функциональных групп подходящим блокирующим реагентом и удаление непрореагировавшего блокирующего реагента промывкой и фильтрованием.
30. Способ получения пролекарства по одному из пп. 14-20, включающий стадии:
(a) соединение линкерного реагента с биологически активным фрагментом, дающее конъюгат биологически активный линкерный фрагмент;
(b) реакция конъюгата биологически активный линкерный фрагмент со стадии (а) с реакционноспособными функциональными группами гидрогеля, получаемого способом по пп. 22 или 23, и удаление непрореагировавшего конъюгата биологически активный линкерный фрагмент промывкой и фильтрованием;
(c) необязательно, блокирование непрореагировавших реакционноспособных функциональных групп подходящим блокирующим реагентом и удаление непрореагировавшего блокирующего реагента промывкой и фильтрованием.
31. Способ получения пролекарства по одному из пп. 14-20, включающий стадии:
(a) дериватизация гидрогеля, получаемого способом по п. 22 или 23, реакцией указанного гидрогеля с N-гидроксисукцинимидным эфиром N-(3-малеимидопропил)-21-амино-4,7,10,13,16,19-гексаоксагеникозановой кислоты, дающая малеимид-функционализированный гидрогель, и удаление непрореагировавшего N-гидроксисукцинимидного эфира N-(3-малеимидопропил)-21-амино-4,7,10,13,16,19-гексаоксагеникозановой кислоты промывкой и фильтрованием;
(b) соединение линкерного реагента с биологически активным фрагментом, дающее конъюгат биологически активный линкерный фрагмент, в котором линкер содержит свободную тиольную группу (-SH);
(c) реакция конъюгата биологически активный линкерный фрагмент со стадии (b) с малеимид-функционализированным гидрогелем со стадии (а) при температурах в диапазоне от комнатной температуры до 4°С в водном буферном растворе, имеющем рН в диапазоне от 5,5 до 8, и удаление непрореагировавшего конъюгата биологически активный линкерный фрагмент промывкой и фильтрованием;
(d) блокирование непрореагировавших реакционноспособных функциональных групп тиол-содержащим соединением, имеющим молекулярный вес 34-500 Да, и удаление непрореагировавшего блокирующего реагента промывкой и фильтрованием.
32. Способ получения пролекарства по одному из пп. 14-20, включающий стадии:
(а) дериватизация гидрогеля, получаемого способом по п. 22 или 23, реакцией указанного гидрогеля с N-гидроксисукцинимидным эфиром N-(3-малеимидопропил)-21-амино-4,7,10,13,16,19-гексаоксагеникозановой кислоты, дающая малеимид-функционализированный гидрогель, и удаление непрореагировавшего N-гидроксисукцинимидного эфира N-(3-малеимидопропил)-21-амино-4,7,10,13,16,19-гексаоксагеникозановой кислоты промывкой и фильтрованием;
(b) соединение линкерного реагента с биологически активным фрагментом, дающее конъюгат биологически активный линкерный фрагмент, в котором линкер содержит свободную тиольную группу (-SH), и в котором биологически активный фрагмент содержит дисульфидную (-S-S-) связку;
(c) реакция конъюгата биологически активный линкерный фрагмент со стадии (b) с малеимид-функционализированным гидрогелем со стадии (а) при температурах в диапазоне от комнатной температуры до 4°С в водном буферном растворе, имеющем рН в диапазоне от 2 до 5, в котором линкер соединен с тиольной группой и биологически активный фрагмент содержит дисульфидную (-S-S-) связку, и удаление непрореагировавшего конъюгата биологически активный линкерный фрагмент промывкой и фильтрованием;
(d) блокирование непрореагировавших реакционноспособных функциональных групп тиол-содержащим соединением, имеющим молекулярный вес 34-500 Да, и удаление непрореагировавшего блокирующего реагента промывкой и фильтрованием.
33. Способ получения пролекарства по одному из пп. 14-20, включающий стадии:
(a) дериватизация гидрогеля, получаемого способом по п. 22 или 23, реакцией указанного гидрогеля с низкомолекулярным спейсерным реагентом, содержащим защищенную тиольную группу, дающая тиол-функционализированный гидрогель, в котором тиольная группа связана с защитной группой, и удаление непрореагировавшего спейсерного реагента промывкой и фильтрованием;
(b) снятие защиты с тиол-функционализированного гидрогеля со стадии (а); и удаление снятой защитной группы промывкой и фильтрованием;
(c) соединение линкерного реагента с биологически активным фрагментом, дающее конъюгат биологически активный линкерный фрагмент, в котором линкер содержит малеимидный фрагмент;
(d) реакция конъюгата биологически активный линкерный фрагмент со стадии (с) с тиол-функционализированным гидрогелем со стадии (b) при температурах в диапазоне от комнатной температуры до 4°С в водном буферном растворе, имеющем рН в диапазоне от 5.5 до 8, и удаление непрореагировавшего конъюгата биологически активный линкерный фрагмент промывкой и фильтрованием;
(e) блокирование непрореагировавших реакционноспособных функциональных групп малеимид-содержащим соединением, имеющим молекулярный вес 100-300 Да, и удаление непрореагировавшего блокирующего реагента промывкой и фильтрованием.
34. Способ получения пролекарства по одному из пп. 14-20, включающий стадии:
(a) дериватизация гидрогеля, получаемого способом по п. 22 или 23, реакцией указанного гидрогеля с низкомолекулярным спейсерным реагентом, содержащим защищенную тиольную группу, дающая тиол-функционализированный гидрогель, в котором тиольная группа связана с защитной группой, и удаление непрореагировавшего спейсерного реагента промывкой и фильтрованием;
(b) снятие защиты с тиол-функционализированного гидрогеля со стадии (а); и удаление снятой защитной группы промывкой и фильтрованием;
(c) соединение линкерного реагента с биологически активным фрагментом, дающее конъюгат биологически активный линкерный фрагмент, в котором линкер содержит малеимидный фрагмент, и в котором биологически активный фрагмент содержит дисульфидную (-S-S-) связку;
(d) реакция конъюгата биологически активный линкерный фрагмент со стадии (b) с тиол-функционализированным гидрогелем со стадии (а) при температурах в диапазоне от комнатной температуры до 4°С в водном буферном растворе, имеющем рН в диапазоне от 2 до 5, в котором линкер соединен с тиольной группой, и биологически активный фрагмент содержит дисульфидную (-S-S-) связку, и удаление непрореагировавшего конъюгата биологически активный линкерный фрагмент промывкой и фильтрованием;
(е) блокирование непрореагировавших реакционноспособных функциональных групп малеимид-содержащим соединением, имеющим молекулярный вес 100-300 Да, и удаление непрореагировавшего блокирующего реагента промывкой и фильтрованием.
35. Способ получения инъецируемого через иглу пролекарства, включающий стадии:
(a) получение пролекарства способом по одному из пп. 28-34 в форме микрочастиц;
(b) просеивание микрочастиц;
(c) отбор фракции с диаметром гранул пролекарства между 25 и 80 мкм;
(d) суспендирование отобранной фракции гранул со стадии (с) в водном буферном растворе, пригодном для инъекции.
36. Пролекарство, полученное способом по п. 35, которое можно инъецировать через иглу с внутренним диаметром меньше 300 мкм.
37. Пролекарство по п. 36, которое можно инъецировать через иглу с внутренним диаметром меньше 225 мкм.
38. Пролекарство по п. 36, которое можно инъецировать через иглу с внутренним диаметром меньше 175 мкм.
| WO9914259 A1, 25.03.1999US2008293827 A1, 27.11.2008WO2009134336 A1, 05.11.2009US2008187568 A1, 07.08.2008WO2007082088 A2, 19.07.2007WO2006003014 A2, 12.01.2006WO2005099768 A2, 27.10.2005EA 11351 B1, 27.02.2009. |
Авторы
Даты
2015-06-27—Публикация
2010-07-30—Подача