Настоящее изобретение относится к пролекарствам на основе двойного агониста GLP-1/глюкагона, фармацевтическим композициям, содержащим указанные пролекарства, а также к их применению в качестве лекарственного препарата для лечения или предупреждения заболеваний или нарушений, которые можно вылечить посредством двойного агониста GLP-1/глюкагона, например, в лечении нарушений метаболического синдрома, в том числе диабета и ожирения, а также для снижения чрезмерного потребления пищи.
ПРЕДПОСЫЛКИ ИЗОБРЕТЕНИЯ
Агонисты GLP-1
Эксендин-4 представляет собой пептид из 39 аминокислот, выделенный из секрета слюнных желез аризонского ядозуба (Heloderma suspectum). Он обладает неким сходством последовательностей с некоторыми членами семейства глюкагоноподобных пептидов, при этом наиболее высокая гомология в 53% предполагается с амидом глюкагоноподобного пептида-1[7-36] (GLP-1). Эксендин-4 выступает в качестве агониста рецептора GLP-1 и обладает действием усиления секреции GLP-1-подобного инсулина в выделенных островковых клетках крысы. Эксендин-4 является высокоактивным агонистом, а амид усеченного агониста GLP-1-(9-39) представляет собой антагонист рецептора амида глюкагоноподобного пептида 1-(7-36) у секретирующих инсулин бета-клеток (см., например, J. Biol. Chem. 268(26):19650-19655). Эксендин-4 («эксенатид») недавно был утвержден в США и Европе для улучшения гликемического контроля у пациентов с диабетом 2 типа, принимающих метформин и/или сульфонилмочевину, но он не способен обеспечивать достаточный гликемический контроль.
Аминокислотная последовательность эксендина-4 представлена в виде SEQ ID NO: 1
HGEGTFTSDLSKQMEEEAVRLFIEWLKNGGPSSGAPPPS-NH2
Аминокислотная последовательность GLP-1(7-36)-амида представлена в виде SEQ ID NO: 2
HAEGTFTSDVSSYLEGQAAKEFIAWLVKGR-NH2
Глюкагон представляет собой пептид из 29 аминокислот, который высвобождается в кровоток при низком уровне циркулирующей в крови глюкозы. Аминокислотная последовательность глюкагона представлена в виде SEQ ID NO 3:
HSQGTFTSDYSKYLDSRRAQDFVQWLMNT-OH
При гипогликемии, когда уровни глюкозы в крови опускаются ниже нормальных, глюкагон сигнализирует печени о необходимости расщепления гликогена и высвобождения глюкозы, в результате чего уровни глюкозы в крови повышаются, достигая нормального уровня. Гипогликемия является распространенным побочным эффектом у пациентов, получающих инсулин в связи с гипергликемией (повышенные уровни глюкозы в крови), вызванной диабетом. Таким образом, наиболее преобладающая роль глюкагона в регуляции глюкозы заключается в противодействии действию инсулина и поддержании уровней глюкозы в крови.
Holst (Holst, J. J. Physiol. Rev. 2007, 87, 1409) и Meier (Meier, J. J. Nat. Rev. Endocrinol. 2012, 8, 728) описывают, что агонисты рецепторов GLP-1, такие как GLP-1, лираглутид и эксендин-4, оказывают 3 основных вида фармакологического действия, позволяющего улучшить гликемический контроль у пациентов с T2DM за счет понижения уровня глюкозы натощак и после приема пищи (FPG и PPG): (i) повышение глюкозозависимой секреции инсулина (улучшенные первая и вторая фазы), (ii) действие, направленное на подавление глюкагона в условиях гипергликемии, (iii) снижение скорости опорожнения желудка, что приводит к замедленному всасыванию поступившей с пищей глюкозы.
Агонисты GLP-1/глюкагона (Glc)
У Pocai с соавт. (Obesity. 2012;20:1566-1571; Diabetes 2009, 58, 2258) и Day с соавт. (Nat Chem Biol 2009;5:749) описано, что двойная активация рецепторов GLP-1 и глюкагона, например, путем объединения действий GLP-1 и глюкагона в одной молекуле, приводит к терапевтическому принципу с противодиабетическим действием и выраженным эффектом снижения веса.
Пептиды, которые связываются как с рецептором глюкагона, так и с рецептором GLP-1 и стимулируют их (Hjort et al. Journal of Biological Chemistry, 269, 30121-30124,1994; Day J.W. et al, Nature Chem Biol, 5: 749-757, 2009), а также сдерживают прибавление в весе и уменьшают потребление пищи, описаны в заявках на патенты WO 2008/071972, WO 2008/101017, WO 2009/155258, WO 2010/096052, WO 2010/096142, WO 2011/075393, WO 2008/152403, WO 2010/070251, WO 2010/070252, WO 2010/070253, WO 2010/070255, WO 2011/160630, WO 2011/006497, WO 2011/152181, WO 2011/152182, WO 2011/117415, WO 2011/117416 и WO 2006/134340, содержания которых включены в данный документ с помощью ссылки.
Кроме того, тройные коагонисты-пептиды, которые не только активируют рецептор GLP-1 и рецептор глюкагона, но также и рецептор GIP (желудочный ингибиторный полипептид), описаны в WO 2012/088116 и VA Gault с соавт. (Biochem Pharmacol, 85, 16655-16662, 2013; Diabetologia, 56, 1417-1424, 2013).
Bloom с соавт. (WO 2006/134340) раскрывают, что пептиды, которые связываются как с рецептором глюкагона, так и с рецептором GLP-1 и стимулируют их, можно создавать в виде гибридных молекул из глюкагона и эксендина-4, где N-концевая часть (например, остатки 1-14 или 1-24) происходит из глюкагона, а C-концевая часть (например, остатки 15-39 или 25-39) происходит из эксендина-4.
Otzen с соавт. (Biochemistry, 45, 14503-14512, 2006) раскрывают, что N- и C-концевые гидрофобные участки вовлечены в фибрилляцию глюкагона, что связано с гидрофобностью и/или высокой склонностью к образованию β-складчатой структуры нижележащих остатков.
В WO2014/056872 раскрываются пептиды, которые связываются как с рецептором глюкагона, так и с рецептором GLP-1 и стимулируют их, и которые получены из эксендина-4, где по меньшей мере аминокислота в положении 14 содержит боковую цепь для более длительного периода полураспада.
Пептиды, применяемые в настоящем изобретении, представляют собой аналоги пептида эксендина-4, содержащие лейцин в положении 10 и глютамин в положении 13, и описаны в WO2015/086731, WO2015/086732, WO2015/086733.
Пептиды, также применяемые в настоящем изобретении, представляют собой аналоги пептида эксендина-4, содержащие бета-аланин в положении 28, и описаны в EP15305899.5.
Дополнительно в настоящем изобретении применяют пептид, который представляет собой аналог пептида эксендина-4, содержащий глютамин в положении 3, бета-аланин в положении 28 и D-аланины в положении 29 и 34.
Пептиды, применяемые в данном изобретении, предпочтительно являются растворимыми не только при нейтральном рН, но и также при рН 4,5. Кроме того, химическая стабильность при значениях pH от 4,5 до 5 является важным критерием для продукта, являющегося пролекарством длительного действия. Пролекарство предпочтительно составляют в данном диапазоне pH, чтобы добиться срока годности по меньшей мере 6 месяцев при 4°C.
Агонисты GLP-1/глюкагона длительного действия
В идеальном варианте пептид составляют таким образом, чтобы обеспечить длительное поддержание уровня в плазме человека в течение по меньшей мере одной недели после применения к организму человека, что обеспечивает в результате частоту введения раз в неделю или реже.
Распространенным терапевтическим средством, содержащим агонисты GLP-1 длительного действия, является Bydureon®, которое представляет собой эксендин-4 в суспензии-депо на основе сополимера гликолевой и молочной кислот для введения с помощью инъекции раз в неделю с использованием иглы 23 калибра.
В WO2012/173422 описан агонист GLP-1/глюкагона, конъюгированный к Fc-области иммуноглобулина, для еженедельного введения, где пептид получен из оксинтомодулина.
Связанные с носителем пролекарства
Для усиления физико-химических или фармакокинетических свойств лекарственного средства in vivo, например, периода его полураспада, такое лекарственное средство может быть конъюгировано с носителем. Если лекарственное средство временно соединено с носителем и/или линкером, то такие системы обычно называют связанными с носителем пролекарствами. В соответствии с определениями, представленными IUPAC (как указано в http://www.chem.qmul.ac.uk/iupac.medchem, доступном от 22 июля 2009 г.), связанное с носителем пролекарство представляет собой пролекарство, которое содержит временную связь, образованную между данным активным веществом и переходной группой носителя, которая обеспечивает улучшенные физико-химические или фармакокинетические свойства, и которая может быть легко удалена in vivo, обычно посредством гидролитического расщепления.
Линкеры, использованные в таких связанных с носителем пролекарствах, могут быть временными, а это означает, что они являются неферментативно гидролитически разрушаемыми (расщепляемыми) в физиологических условиях (водный буфер при pH 7,4, 37°C) с периодами полураспада в диапазоне от, например, одного часа до трех месяцев. Подходящими носителями являются полимеры и они могут быть либо непосредственно конъюгированы с линкером, либо посредством нерасщепляемого спейсера.
Временная конъюгация полимера посредством бесследных линкеров пролекарства объединяет преимущества более длительного времени пребывания в связи с присоединением полимера и восстановления первоначальных фармакологических свойств исходного пептида после высвобождения из полимерного конъюгата.
При использовании конъюгатов полимера и линкерного пептида исходный неизмененный пептид медленно высвобождается после применения в отношении пациента, что регулируется только кинетическими характеристиками высвобождения линкера и фармакокинетическими свойствами полимерного носителя. В идеальном варианте кинетические характеристики высвобождения не будут зависеть от присутствия в биологических жидкостях ферментов, таких как протеазы или эстеразы, что гарантирует достоверную и одинаковую схему высвобождения.
WO2008/148839, WO2009/095479 и WO2012/035139 относятся к пролекарствам, содержащим конъюгаты лекарственного средства и линкера, где линкер ковалентно соединен посредством расщепляемой связи с биологически активным фрагментом, например, GLP 1-агонистом эксендином-4. Биологически активный фрагмент высвобождается из пролекарства при циклизации-активации посредством образования циклического амида. Кинетика высвобождения зависит от значения pH и является минимальной при хранении пролекарства при значениях pH от 4,5 до 5 и достигает ее предполагаемой скорости высвобождения при физиологическом pH около 7,4-7,5. Описано пролекарство на основе агониста GLP-1, в котором линкер основан на L-аланине, и полимерный носитель представляет собой гидрогель на основе PEG-лизина. Не описаны пролекарства на основе двойного агониста GLP-1/глюкагона.
Гиалуроновая кислота (HA)
Dhal с соавт. (Journal of Biomedical Nanotechnology, vol 9, 2013, 1-13) сообщают о гиалуроновой кислоте в качестве подходящего носителя для конъюгатов лекарственных средств. Kong с соавт. (Biomaterials 31 (2010), 4121-4128) сообщают о конъюгате эксендина-4 и гиалуроновой кислоты, который продемонстрировал эффект снижения уровня глюкозы у мышей за 3 дня. Применяемая HA представляла собой линейный полимер с загрузкой лекарственного средства в диапазоне от приблизительно 2,4 до 12%.
В настоящем изобретении гидрогели из сшитой гиалуроновой кислоты выбраны в связи с их более длительным временем пребывания в качестве местного депо в месте применения, чем у растворимой HA.
Важным критерием для применения гиалуроновой кислоты (HA) в качестве полимера-носителя является достижимая загрузка лекарственного средства в конечном лекарственном препарате, которую определяют по загрузке лекарственного средства на самом полимере и концентрации конечных раствора/суспензии. Следует учитывать тот факт, что объем инъекционного раствора для подкожных лекарственных депо практически ограничен до объема меньше/равного 1 мл, предпочтительно меньше/равного 0,6 мл.
Чем более концентрированные полимерные растворы/суспензии HA, тем более вязким является состав, что негативно сказывается на возможности введения через шприц состава пролекарства. Для вязких растворов требуются инъекционные иглы большего диаметра, чтобы ограничить силу, прикладываемую к поршню, и с которой нажимают на шприц. Кроме того, время инъекции является более длительным.
Целью настоящего изобретения является обеспечение пролекарства на основе агониста GLP-1/глюкагона для введения в качестве подкожного депо, которое высвобождает агонист GLP-1/глюкагона в активной форме в течение периода времени между введениями по меньшей мере 6 дней и которое можно инъецировать через иглы 26 калибра или даже через иглы с меньшим внутренним диаметром для лучшего соблюдения пациентом схемы лечения.
Целью настоящего изобретения является пролекарство или его фармацевтически приемлемая соль, содержащие конъюгат лекарственного средства и линкера формулы (I)
Z - L1 -L2 - L - Y - R20 (I),
где Y представляет собой пептидный фрагмент, характеризующийся формулой (II),
His-X2-X3-Gly-Thr-Phe-Thr-Ser-Asp-Leu-Ser-Lys-Gln-Leu-Asp-Glu-Gln-X18-Ala-X20-X21-Phe-Ile-Glu-Trp-Leu-Ile-X28-Gly-Gly-Pro-X32-Ser-Gly-Ala-Pro-Pro-Pro-Ser (II),
причем X2 представляет собой аминокислотный остаток, выбранный из Ser, D-Ser и Aib,
X3 представляет собой аминокислотный остаток, выбранный из Gln и His,
X18 представляет собой аминокислотный остаток, выбранный из Arg и Lys,
X20 представляет собой аминокислотный остаток, выбранный из Lys, Gln и His,
X21 представляет собой аминокислотный остаток, выбранный из Asp и Glu,
X28 представляет собой аминокислотный остаток, выбранный из Ser и Ala,
X32 представляет собой аминокислотный остаток, выбранный из Ser и Val,
или где Y представляет собой пептидный фрагмент, характеризующийся формулой (III),
His-X2-X3-Gly-Thr-Phe-Thr-Ser-Asp-Leu-Ser-Lys-Gln-Leu-Asp-Glu-Gln-X18-Ala-X20-X21-Phe-Ile-Glu-Trp-Leu-Ile-X28-Gly-Gly-Pro-X32-Ser-Gly-Ala-Pro-Pro-Pro-Ser (III),
причем X2 представляет собой аминокислотный остаток, выбранный из Ser, D-Ser и Aib,
X3 представляет собой аминокислотный остаток, выбранный из Gln и His,
X18 представляет собой аминокислотный остаток, выбранный из Leu и His,
X20 представляет собой аминокислотный остаток, выбранный из His, Arg, Lys и Gln,
X21 представляет собой аминокислотный остаток, выбранный из Asp и Glu,
X28 представляет собой аминокислотный остаток, выбранный из Lys, Ser и Ala,
X32 представляет собой аминокислотный остаток, выбранный из Ser и Val,
или
где Y представляет собой пептидный фрагмент, характеризующийся формулой (IV),
His-X2-X3-Gly-Thr-Phe-Thr-Ser-Asp-Leu-Ser-Lys-Leu-Leu-Asp-Glu-Gln-X18-Ala-Lys-Asp-Phe-Ile-Glu-Trp-Leu-Ile-Ala-Gly-Gly-Pro-X32-Ser-Gly-Ala-Pro-Pro-Pro-Ser (IV),
причем X2 представляет собой аминокислотный остаток, выбранный из Ser, D-Ser и Aib,
X3 представляет собой аминокислотный остаток, выбранный из Gln и His,
X18 представляет собой аминокислотный остаток, выбранный из Arg и Leu,
X32 представляет собой аминокислотный остаток, выбранный из Ser и Val,
или
где Y представляет собой пептидный фрагмент, характеризующийся формулой (IVa),
H2N-His-Aib-His-Gly-Thr-Phe-Thr-Ser-Asp-Leu-Ser-Lys-Gln-Leu-X15-Glu-Gln-Leu-Ala-Arg-Asp-Phe-Ile-Glu-Trp-Leu-Ile-Bal-X29-Gly-X31-X32-Ser-X34-X35-Pro-Pro-Pro-X39-R20 (IVa),
причем X15 представляет собой аминокислотный остаток, выбранный из Asp и Glu (предпочт. Asp),
X29 представляет собой аминокислотный остаток, выбранный из Gly, D-Ala и Pro (предпочт. Gly, D-Ala),
X31 представляет собой аминокислотный остаток, выбранный из Pro, His и Trp (предпочт. Pro),
X32 представляет собой аминокислотный остаток, выбранный из Ser, His, Pro и Arg (предпочт. Ser, His, Pro),
X34 представляет собой аминокислотный остаток, выбранный из Gly и D-Ala,
X35 представляет собой аминокислотный остаток, выбранный из Ala, Pro и Lys (предпочт. Ala, Pro),
X39 представляет собой Ser или Pro-Pro-Pro,
или
где Y представляет собой пептидный фрагмент, характеризующийся формулой (IVb),
H2N-His-Aib-Gln-Gly-Thr-Phe-Thr-Ser-Asp-Leu-Ser-Lys-Leu-Leu-Glu-Glu-Gln-Arg-Ala-Arg-Glu-Phe-Ile-Glu-Trp-Leu-Ile-Bal-D-Ala-Gly-Pro-Pro-Ser-D-Ala-Ala-Pro-Pro-Pro-Ser-R20;
или его соль или сольват;
R20 представляет собой ОН или NH2;
L представляет собой линкер формулы (Ia),
 Ia,
Ia,
где пунктирная линия указывает на присоединение к N-концу Y посредством образования амидной связи;
X представляет собой C(R4R4a), N(R4);
R1, R1a независимо выбраны из группы, состоящей из H и C1-4алкила;
R2, R2a независимо выбраны из группы, состоящей из H и C1-4алкила;
R4, R4a независимо выбраны из группы, состоящей из H и C1-4алкила;
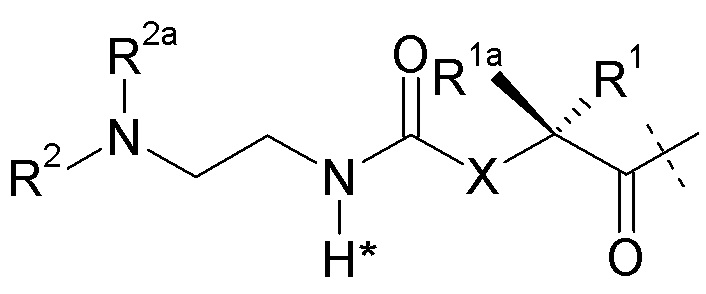
где R2, R2a, R4 или R4a замещен одной группой L2-L1-Z; где
L2 представляет собой одинарную химическую связь или представляет собой C1-20алкильную цепь, которая необязательно прервана одной или несколькими группами, независимо выбранными из -O- и C(O)N(R3aa), и необязательно замещена одной или несколькими группами, независимо выбранными из OH и C(O)N(R3aaR3aaa), где R3aa и R3aaa независимо выбраны из группы, состоящей из H и C1-4алкила; и
L2 прикреплен к L1 посредством концевой группы, выбранной из группы, состоящей из
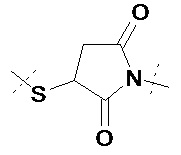 ,
,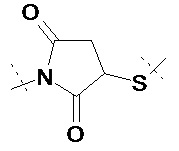 ,
,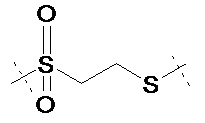 ,
, 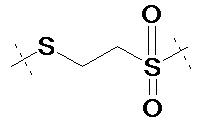 ,
, 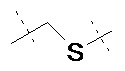 ,
, 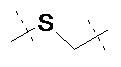 ,
, 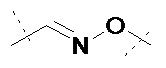 ,
, 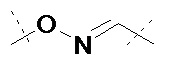 ,
, 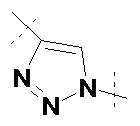 ,
, 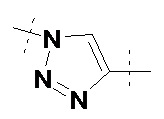 ,
, 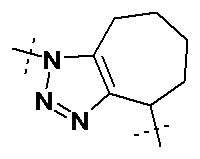 ,
,  ,
,  и
и  ;
;
где L2 прикреплен в одном положении, отмеченном пунктирной линией, и L1 прикреплен в положении, отмеченном другой пунктирной линией; и
L1 представляет собой C1-20алкильную цепь, которая необязательно прервана одной или несколькими группами, независимо выбранными из -O- и C(O)N(R5aa), и необязательно замещена одной или несколькими группами, независимо выбранными из OH и C(O)N(R5aaR5aaa), где R5aa и R5aaa независимо выбраны из группы, состоящей из H и C1-4алкила; и
L1 прикреплен к Z посредством концевой аминогруппы, образующей амидную связь с карбоксильной группой бета-1,3-D-глюкуроновой кислоты гиалуроновой кислоты из Z;
Z представляет собой гидрогель на основе сшитой гиалуроновой кислоты, в котором
от 0,05 до 20% мономерных дисахаридных звеньев сшиты посредством сшивателя; и от 0,2 до 8,5% мономерных дисахаридных звеньев содержат группы L1-L2-L-Y-R20.
Настоящее изобретение относится к пролекарству, которое обеспечивает высвобождение агониста GLP-1/глюкагона из подкожного депо в активной форме в течение периода времени по меньшей мере 6 дней между введениями.
Это помогает сократить частоту введения инъекционного раствора пациентам, при этом поддерживая оптимальный контроль уровней агониста GLP-1/глюкагона в плазме и, следовательно, уровней глюкозы в крови.
Дополнительные преимущества носителя сшитой гиалуроновой кислоты по настоящему изобретению заключаются в хорошей способности к введению посредством инъекции через иглу 26 калибра или даже иглу с меньшим внутренним диаметром.
ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
На фигуре 1a, фигуре 1a/2, фигуре 1b, фигуре 1b/2, фигуре 1c, фигуре 1c/2, фигуре 1c/3, фигуре 1c/4 показаны различные сшивающие химические структуры для синтеза гидрогелей на основе гиалуроновой кислоты.
Фигура 2a. Магнитно-резонансные (MR) томограммы гидрогеля на основе HA в месте инъекции, полученные в разные моменты времени.
Фигура 2b. Магнитно-резонансные (MR) томограммы полимерной суспензии, содержащей смесь 1:1 (вес/вес) гидрогеля на основе HA и растворимой HA, 800 кДа, в месте инъекции, полученные в разные моменты времени.
Фигура 3. Кинетические характеристики высвобождения in vitro двойного агониста эксендина-4 под Seq ID No. 26 с линкером из гидрогеля на основе HA в течение недели (пример 18). Период полураспада составляет 5 дней.
Фигура 4. Эффект конъюгата гидрогеля на основе HA и двойного агониста (Seq ID No. 26) in vivo на уровень глюкозы в крови мышей db/db не натощак: показано различие уровней глюкозы в крови в ммоль/л в зависимости от продолжительности лечения животных различными дозами.
Фигура 4b. Эффект конъюгата гидрогеля на основе HA и двойного агониста (Seq ID No. 26) in vivo на уровень глюкозы в крови мышей db/db не натощак: показано различие уровней глюкозы в крови в ммоль/л в зависимости от продолжительности лечения животных с помощью различных конструкций гидрогеля: на основе растворимой и сшитой гиалуроновой кислоты.
Фигура 4с. Эффект конъюгатов гидрогеля на основе HA и двойных агонистов (Seq ID No. 45, 46 и 48) in vivo на уровень глюкозы в крови мышей db/db не натощак: показан уровень глюкозы в крови в ммоль/л в зависимости от продолжительности лечения животных.
Фигура 4d. Эффект конъюгата гидрогеля на основе HA и двойного агониста (Seq ID No. 49) in vivo на уровень глюкозы в крови мышей db/db не натощак: показан уровень глюкозы в крови в ммоль/л в зависимости от продолжительности лечения животных.
Фигура 5. Исследование способности к введению посредством инъекции: сила выталкивания, прикладываемая к поршню шприца, для гидрогелей на основе HA с различной загрузкой пептида.
Результаты силы выталкивания: Эффект загрузки пептида
Подробное описание
Аминокислотные последовательности по настоящему изобретению содержат обычные однобуквенные и трехбуквенные коды для встречающихся в природе аминокислот, а также общепринятые трехбуквенные коды для других аминокислот, таких как Aib (α-аминоизомасляная кислота).
Более того, следующий код, который использовали для аминокислоты, представлен в нижеприведенной таблице.
Агонист GLP-1/глюкагона, связанный с линкером, называется «фрагмент агониста GLP-1/глюкагона».
"Защитные группы" относятся к фрагменту, который временно защищает химическую функциональную группу молекулы в ходе синтеза с обеспечением хемоселективности в последующих химических реакциях. Защитными группами для спиртов являются, например, бензил и тритил, защитными группами для аминов являются, например, трет-бутилоксикарбонил, 9-фторенилметилоксикарбонил и бензил, а для тиолов примерами защитных групп являются 2,4,6-триметоксибензил, фенилтиометил, ацетамидометил, п-метоксибензилоксикарбонил, трет-бутилтио, трифенилметил, 3-нитро-2-пиридилтио, 4-метилтритил.
"Защищенные функциональные группы" означают химическую функциональную группу, защищенную защитной группой.
"Ацилирующее средство" означает фрагмент структуры R-(C=O)-, обеспечивающий ацильную группу в реакции ацилирования, необязательно соединенную с уходящей группой, например, хлорангидрид, N-гидроксисукцинимид, пентафторфенол и пара-нитрофенол.
"Алкил" означает прямую или разветвленную углеродную цепь. Каждый атом водорода при алкильном атоме углерода может быть заменен заместителем.
"Арил" относится к любому заместителю, полученному из моноциклического, или полициклического, или конденсированного ароматического кольца, в том числе гетероциклических колец, например, фенила, тиофена, индолила, нафтила, пиридила, которые могут необязательно быть дополнительно замещены.
"Ацил" означает химическую функциональную группу структуры R-(C=O)-, где R представляет собой алкил или арил.
"C1-4алкил" означает алкильную цепь, содержащую 1-4 атома углерода, например, если присутствует в конце молекулы: метил, этил, н-пропил, изопропил, н-бутил, изобутил, втор-бутил, трет-бутил, или, например -CH2-, -CH2-CH2-, -CH(CH3)-, -CH2-CH2-CH2-, -CH(C2H5)-, -C(CH3)2-, если два фрагмента молекулы соединены алкильной группой. Каждый атом водорода при атоме углерода C1-4алкила может быть заменен заместителем.
"C1-6алкил" означает алкильную цепь, содержащую 1-6 атомов углерода, например, если присутствует в конце молекулы: C1-4алкил, метил, этил, н-пропил, изопропил, н-бутил, изобутил, втор-бутил; трет-бутил, н-пентил, н-гексил, или, например, -CH2-, -CH2-CH2-, -CH(CH3)-, -CH2-CH2-CH2-, -CH(C2H5)-, -C(CH3)2-, если два фрагмента молекулы соединены алкильной группой. Каждый атом водорода при атоме углерода C1-6алкила может быть заменен заместителем.
Соответственно, "C1-18алкил" означает алкильную цепь, содержащую 1-18 атомов углерода, а "C8-18алкил" означает алкильную цепь, содержащую 8-18 атомов углерода. Соответственно, "C1-50алкил" означает алкильную цепь, содержащую 1-50 атомов углерода.
"Галоген" означает фтор, хлор, бром или йод. В целом, предпочтительно, чтобы галоген представлял собой фтор или хлор.
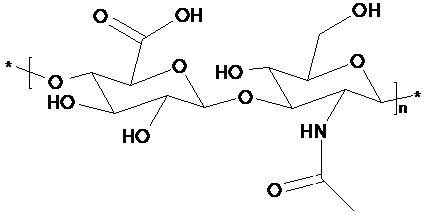
"Гиалуроновая кислота" означает полимер дисахарида, состоящий из бета-1,3-D-глюкуроновой кислоты, и бета-1,4-N-ацетил-D-глюкозамина, и их соответствующих натриевых солей. Данные полимеры являются линейными
 .
.
"Дисахаридное звено" означает дисахарид, состоящий из бета-1,3-D-глюкуроновой кислоты, и бета-1,4-N-ацетил-D-глюкозамина, и их соответствующих натриевых солей, и представляет собой мономерную структурную единицу для HA.
"Сшитая гиалуроновая кислота" означает полимер гиалуроновой кислоты, где разные цепи HA ковалентно связаны сшивателем, образуя 3-мерную полимерную сетку. Степень сшивания зависит от молярного отношения дисахаридных звеньев к звеньям сшивателя в полимерной сетке.
Сшитая гиалуроновая кислота может быть получена разными способами. Реакция HA со сшивателем, реакция модифицированной (активированной) HA со сшивателем, реакция двух разных модифицированных HA со сшивателем. Примеры могут быть описаны в Oh et al, Journal of Controlled Release 141 (2010), 2-12. В примере 11 описано сшивание немодифицированной HA с дивинилсульфоном. Дополнительные способы получения сшитой HA также изображены на фигуре 1a, фигуре 1b и фигуре 1c: восстановительное аминирование альдегида (окисление диола) и последующего амина, опосредованное гидроксилом алкилирование, реакция образования амида, сопряженное присоединение по Михаэлю (тиол - малеимид), диол-эпоксидная химия и другие.
"Сшиватель" может представлять собой линейную или разветвленную молекулу или химическую группу, предпочтительно представляет собой линейную молекулу с по меньшей мере химическими функциональными группами на каждом из дистальных концов.
"Функционализированная гиалуроновая кислота" означает полимер гиалуроновой кислоты, где HA химически модифицирована с помощью группы L1, которая содержит химическую функциональную группу на ее дистальном конце. Степень функционализации зависит от молярного отношения дисахаридных звеньев к звеньям L1 в полимере.
Термин "химическая функциональная группа" относится без ограничения к карбоновой кислоте и активированным производным, амино, малеимиду, тиолу и производным, сульфоновой кислоте и производным, карбонату и производным, карбамату и производным, гидроксилу, альдегиду, кетону, гидразину, изоцианату, изотиоцианату, фосфорной кислоте и производным, фосфоновой кислоте и производным, галогенацетилу, алкилгалогенидам, акрилоилу и другим альфа-бета-ненасыщенным акцепторам Михаэля, арилирующим средствам, подобным арилфторидам, гидроксиламину, дисульфидам, подобным пиридилдисульфиду, винилсульфону, винилкетону, диазоалканам, диазоацетиловым соединениям, оксирану и азиридину.
Если химическая функциональная группа соединена с другой химической функциональной группой, то образованная в результате химическая структура называется "связь". Например, реакция аминогруппы с карбоксильной группой обеспечивает в результате амидную связь.
"Реакционноспособные функциональные группы" представляют собой химические функциональные группы фрагмента каркаса, которые соединены со сверхразветвленным фрагментом.
"Функциональная группа" является общим термином, применяемым в отношении "реакционноспособной функциональной группы", "разрушаемой связанной функциональной группы" или "сопряженной функциональной группы".
Термины "блокирующая группа" или "кэпирующая группа" применяются синонимично и относятся к фрагментам, которые необратимо связываются с реакционноспособными функциональными группами, делая невозможной их дальнейшую реакцию с, например, химическими функциональными группами.
Термины "защищающая группа" или "защитная группа" относятся к фрагменту, который обратимо связывается с реакционноспособными функциональными группами, делая невозможной их дальнейшую реакцию с, например, другими химическими функциональными группами при конкретных условиях.
Термин "производные" относится к химическим функциональным группам, соответствующим образом замещенным защитными и/или активирующими группами, или к активированным формам соответствующей химической функциональной группы, которые известны квалифицированному специалисту в данной области. Например, активированные формы карбоксильных групп включают без ограничения активные сложные эфиры, например, сложный эфир сукцинимидила, сложный эфир бензотриазила, сложный эфир нитрофенила, сложный эфир пентафторфенила, сложный эфир азабензотриазила, ацилгалогениды, смешанные или симметричные ангидриды, ацилимидазол.
Термин "неферментативно расщепляемый линкер" относится к линкерам, которые гидролитически разрушаются в физиологических условиях без ферментативной активности.
Термины "спейсер", "спейсерная группа", "спейсерная молекула" и "спейсерный фрагмент" применяются взаимозаменяемо, и если применяются для описания фрагмента, присутствующего в гидрогеле-носителе по настоящему изобретению, то относятся к любому фрагменту, пригодному для соединения двух фрагментов, такому как C1-50алкил, участок которого необязательно прерван одной или несколькими группами, независимо выбранными из -NH-, -N(C1-4алкила)-, -O-, -S-, -C(O)-, -C(O)NH-, -C(O)N(C1-4алкила)-, -O-C(O)-, -S(O)-, -S(O)2-.
Термины "концевой", "конец" или "дистальный конец" относятся к положению функциональной группы или связи в молекуле или фрагменте, в силу чего такая функциональная группа может быть химической функциональной группой, а связь может быть разрушаемой или стабильной связью, и характеризоваться расположением вблизи или в пределах связи между двумя фрагментами или в конце олигомерной или полимерной цепи.
Фразы "в связанной форме" или "фрагмент" относятся к подструктурам, которые являются частью большей молекулы. Фраза "в связанной форме" применяется для упрощения обозначения фрагментов путем присвоения названия или перечисления реагентов, исходных материалов или предполагаемых исходных материалов, хорошо известных в данной области техники, и в силу чего "в связанной форме" означает, что, например, один или несколько водородных радикалов (-H), или одна или несколько активирующих или защитных групп, присутствующих в реагентах или исходных материалах, отсутствуют во фрагменте.
Понятно, что все реагенты и фрагменты, содержащие полимерные фрагменты, относятся к макромолекулярным структурам, которые, как известно, демонстрируют вариабельность в отношении молекулярного веса, длины цепей, или степени полимеризации, или числа функциональных групп. Структуры, приведенные для сшивающих реагентов и сшивающих фрагментов, таким образом, являются лишь иллюстративными примерами.
Реагент или фрагмент могут быть линейными или разветвленными. Если реагент или фрагмент имеет две концевые группы, то его называют линейным реагентом или фрагментом. Если реагент или фрагмент имеет больше двух концевых групп, то его считают разветвленным или многофункциональным реагентом или фрагментом.
Линкеры, использованные в таких связанных с носителем пролекарствах, являются временными, а это означает, что они являются неферментативно гидролитически разрушаемыми (расщепляемыми) в физиологических условиях (водный буфер с pH 7,4, 37°C), при этом их периоды полураспада находятся в диапазоне от, например, одного часа до трех месяцев.
Термин "пролекарство на основе агониста GLP-1/глюкагона и гидрогеля" относится к связанным с носителем пролекарствам из агониста GLP-1/глюкагона, где носитель представляет собой гидрогель. Термины "пролекарство на основе гидрогеля" и "связанное с гидрогелем пролекарство" относятся к пролекарствам из биологически активных средств, временно связанным с гидрогелем, и применяются взаимозаменяемо.
"Гидрогель" может быть определен как трехмерная гидрофильная или амфифильная полимерная сетка, способная поглощать большие количества воды. Такие сетки состоят из гомополимеров или сополимеров и являются нерастворимыми в связи с наличием ковалентных химических или физических (ионные, гидрофобные взаимодействия, переплетения) поперечных связей. Поперечные связи обеспечивают структуру сетки и физическую целостность. Гидрогели демонстрируют термодинамическую совместимость с водой, которая позволяет им набухать в водных средах. Цепи в сетке соединены таким образом, что имеются поры, и при этом значительная доля данных пор имеет размеры от 1 нм до 1000 нм.
"Свободная форма" лекарственного средства относится к лекарственному средству, в частности, к агонисту GLP-1/глюкагона, в его немодифицированной, фармакологически активной форме, например, после высвобождения из полимерного конъюгата.
Термины "лекарственное средство", "биологически активная молекула", "биологически активный фрагмент", "биологически активное средство", "активное средство" применяют синонимично, и они относятся к агонисту GLP-1/глюкагона, либо в связанной, либо в свободной форме.
"Терапевтически эффективное количество" агониста GLP-1/глюкагона, применяемое в данном документе, означает количество, достаточное для лечения, ослабления или частичного прекращения клинических проявлений данного заболевания и его осложнений. Количество, достаточное для осуществления этого, определяется как "терапевтически эффективное количество". Эффективные количества для каждой цели будут зависеть от тяжести заболевания или травмы, а также веса и общего состояния субъекта. Следует понимать, что определение соответствующей дозировки может быть достигнуто с использованием обычных экспериментов, посредством построения матрицы значений и тестирования различных точек в матрице, все из которых находятся в пределах обычных навыков квалифицированного специалиста.
"Стабильный" и "стабильность" означают, что в течение указанного времени хранения конъюгаты гидрогеля остаются конъюгированными и не гидролизуются в значительной степени, при этом демонстрируют приемлемый профиль примесей относительно агониста GLP-1/глюкагона. Композицию считают стабильной, если она содержит менее 5% лекарственного средства в свободной форме.
Термин "фармацевтически приемлемый" означает одобренный регуляторным органом, например, EMEA (Европа), и/или FDA (США), и/или любым другим национальным регуляторным органом для применения в отношения животных, предпочтительно, людей.
"Фармацевтическая композиция" или "композиция" означает один или несколько активных ингредиентов и один или несколько инертных ингредиентов, а также любой продукт, который образуется, прямо или косвенно, в результате объединения, образования комплекса или агрегации двух или более ингредиентов, или в результате диссоциации одного или нескольких ингредиентов, или в результате других типов реакций или взаимодействий одного или нескольких ингредиентов. Соответственно, фармацевтические композиции по настоящему изобретению охватывают любую композицию, полученную посредством смешивания соединения по настоящему изобретению и фармацевтически приемлемого вспомогательного вещества (фармацевтически приемлемого носителя).
"Сухая композиция" означает, что композиция пролекарства на основе агониста GLP-1/глюкагона и гидрогеля представлена в сухой форме в контейнере. Подходящими способами для высушивания являются, например, сушка распылением и лиофилизация (сублимационная сушка). Такая сухая композиция пролекарства на основе агониста GLP-1/глюкагона и гидрогеля характеризуется остаточным содержанием воды максимум 10%, предпочтительно менее 5% и более предпочтительно менее 2% (определено в соответствии с методом Карла Фишера). Предпочтительным способом высушивания является лиофилизация. "Лиофилизированная композиция" означает, что композицию полимерного пролекарства на основе агониста GLP-1/глюкагона и гидрогеля вначале замораживали, а затем подвергали уменьшению содержания воды посредством пониженного давления. Данная терминология не исключает дополнительные стадии высушивания, которые осуществляют в способе производства перед заполнением конечного контейнера композицией.
"Лиофилизация" (сублимационная сушка) представляет собой процесс обезвоживания, характеризующийся замораживанием композиции, а затем снижением давления окружающей среды и, необязательно, добавлением нагрева, что позволяет замороженной воде в композиции сублимироваться непосредственно из твердой фазы в газ. Как правило, сублимированную воду собирают посредством десублимации.
"Восстановление" означает добавление жидкости к сухой композиции для приведения ее в форму жидкой или суспендированной композиции. Следует понимать, что термин "восстановление" не ограничено добавлением воды, а относится к добавлению любой жидкости, в том числе, например, буферов или других водных растворов.
"Раствор для восстановления" относится к жидкости, применяемой для восстановления сухой композиции пролекарства на основе агониста GLP-1/глюкагона и гидрогеля перед введением пациенту, который в этом нуждается.
"Контейнер" означает любой контейнер, в котором содержится композиция пролекарства на основе агониста GLP-1/глюкагона и гидрогеля и может храниться до восстановления.
"Буфер" или "буферное средство" относится к химическим соединениям, которые поддерживают pH в необходимом диапазоне. Физиологически допустимыми буферами являются, например, фосфат, сукцинат натрия, гистидин, бикарбонат, цитрат и ацетат, пируват натрия. Также можно применять антациды, например, Mg(OH)2 или ZnCO3. Буферную способность можно регулировать для соответствия условиям, наиболее чувствительным к стабильности pH.
"Вспомогательные вещества" относятся к соединениям, которые вводят совместно с терапевтическим средством, например, буферные средства, модификаторы изотоничности, консерванты, стабилизаторы, антиадсорбционные средства, средства защиты от окисления или другие вспомогательные средства. Тем не менее, в некоторых случаях, одно вспомогательное вещество может выполнять двойные или тройные функции.
"Лиопротектор" представляет собой молекулу, которая при соединении с белком, представляющим интерес, в значительной степени предупреждает или снижает химическую и/или физическую нестабильность белка при высушивании в целом и, в частности, в ходе лиофилизации и последующего хранения. Иллюстративные лиопротекторы включают сахара, например, сахарозу или трегалозу; аминокислоты, например, аргинин, глицин, глютамат или гистидин; метиламины, например, бетаин; лиотропные соли, например, сульфат магния; полиолы, например, трехатомные или более высокого порядка сахарные спирты, например, глицерин, эритрит, глицерол, арабит, ксилит, сорбит и маннит; этиленгликоль; пропиленгликоль; полиэтиленгликоль; плюроники; гидроксиалкильные крахмалы, например, гидроксиэтиловый крахмал (HES), и их комбинации.
"Поверхностно-активное вещество" относится к смачивающим средствам, которые снижают поверхностное натяжение жидкости.
"Модификаторы изотоничности" относятся к соединениям, которые сводят к минимуму боль, которая возникает в результате повреждения клеток в связи с разностью осмотического давления в инъекционном депо.
Термин "стабилизаторы" относится к соединениям, применяемым для стабилизации полимерного пролекарства. Стабилизация достигается посредством усиления стабилизирующих белок сил, дестабилизации денатурированного состояния или прямого связывания вспомогательных веществ с белком.
"Антиадсорбционные средства" относятся в основном к ионным или неионным поверхностно-активным веществам, или другим белкам, или растворимым полимерам, применяемым для покрытия внутренней поверхности контейнера с композицией или адсорбции к ней по принципу первенства. Выбранная концентрация и тип вспомогательного вещества зависят от эффекта, которого следует избежать, но, как правило, монослой поверхностно-активного вещества образуется на границе раздела при концентрации чуть выше значения CMC.
"Средства защиты от окисления" относятся к антиоксидантам, таким как аскорбиновая кислота, эктоин, глутатион, метионин, монотиоглицерин, морин, полиэтиленимин (PEI), пропилгаллат, витамин E, хелатирующие средства, такие как лимонная кислота, EDTA, гексафосфат, тиогликолевая кислота.
"Противомикробный" относится к химическому веществу, которое уничтожает микроорганизмы или ингибирует их развитие, например, бактерий, грибов, дрожжей, простейших, и/или обезвреживает вирусы.
"Закупоривание контейнера" означает, что контейнер закрывают таким образом, чтобы он был герметичным, тем самым обеспечивая отсутствие газообмена между наружной частью и внутренней частью и сохранение стерильности содержимого.
Термин "реагент" или "вещество-предшественник" относится к промежуточному соединению или исходному материалу, применяемому в процессе сборки, который обеспечивает пролекарство по настоящему изобретению.
Целью настоящего изобретения является пролекарство или его фармацевтически приемлемая соль, содержащие конъюгат лекарственного средства и линкера формулы (I)
Z - L1 -L2 - L - Y - R20 (I),
где Y представляет собой пептидный фрагмент, характеризующийся формулой (II),
His-X2-X3-Gly-Thr-Phe-Thr-Ser-Asp-Leu-Ser-Lys-Gln-Leu-Asp-Glu-Gln-X18-Ala-X20-X21-Phe-Ile-Glu-Trp-Leu-Ile-X28-Gly-Gly-Pro-X32-Ser-Gly-Ala-Pro-Pro-Pro-Ser (II),
причем X2 представляет собой аминокислотный остаток, выбранный из Ser, D-Ser и Aib,
X3 представляет собой аминокислотный остаток, выбранный из Gln и His,
X18 представляет собой аминокислотный остаток, выбранный из Arg и Lys,
X20 представляет собой аминокислотный остаток, выбранный из Lys, Gln и His,
X21 представляет собой аминокислотный остаток, выбранный из Asp и Glu,
X28 представляет собой аминокислотный остаток, выбранный из Ser и Ala,
X32 представляет собой аминокислотный остаток, выбранный из Ser и Val,
или где Y представляет собой пептидный фрагмент, характеризующийся формулой (III),
His-X2-X3-Gly-Thr-Phe-Thr-Ser-Asp-Leu-Ser-Lys-Gln-Leu-Asp-Glu-Gln-X18-Ala-X20-X21-Phe-Ile-Glu-Trp-Leu-Ile-X28-Gly-Gly-Pro-X32-Ser-Gly-Ala-Pro-Pro-Pro-Ser (III),
причем X2 представляет собой аминокислотный остаток, выбранный из Ser, D-Ser и Aib,
X3 представляет собой аминокислотный остаток, выбранный из Gln и His,
X18 представляет собой аминокислотный остаток, выбранный из Leu и His,
X20 представляет собой аминокислотный остаток, выбранный из His, Arg, Lys и Gln,
X21 представляет собой аминокислотный остаток, выбранный из Asp и Glu,
X28 представляет собой аминокислотный остаток, выбранный из Lys, Ser и Ala,
X32 представляет собой аминокислотный остаток, выбранный из Ser и Val,
или
где Y представляет собой пептидный фрагмент, характеризующийся формулой (IV),
His-X2-X3-Gly-Thr-Phe-Thr-Ser-Asp-Leu-Ser-Lys-Leu-Leu-Asp-Glu-Gln-X18-Ala-Lys-Asp-Phe-Ile-Glu-Trp-Leu-Ile-Ala-Gly-Gly-Pro-X32-Ser-Gly-Ala-Pro-Pro-Pro-Ser (IV),
причем X2 представляет собой аминокислотный остаток, выбранный из Ser, D-Ser и Aib,
X3 представляет собой аминокислотный остаток, выбранный из Gln и His,
X18 представляет собой аминокислотный остаток, выбранный из Arg и Leu,
X32 представляет собой аминокислотный остаток, выбранный из Ser и Val,
или его соль или сольват;
или его соль или сольват;
R20 представляет собой ОН или NH2,
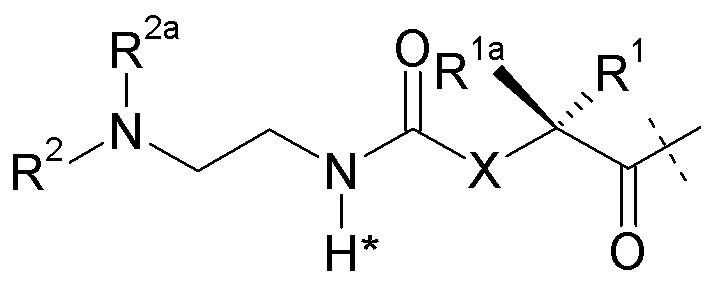
L представляет собой линкер формулы (Ia),
 Ia,
Ia,
где пунктирная линия указывает на присоединение к N-концу Y посредством образования амидной связи;
X представляет собой C(R4R4a), N(R4);
R1, R1a независимо выбраны из группы, состоящей из H и C1-4алкила;
R2, R2a независимо выбраны из группы, состоящей из H и C1-4алкила;
R4, R4a независимо выбраны из группы, состоящей из H и C1-4алкила;
где R2, R2a, R4 или R4a замещен одной группой L2-L1-Z; где
L2 представляет собой одинарную химическую связь или представляет собой C1-20алкильную цепь, которая необязательно прервана одной или несколькими группами, независимо выбранными из -O- и C(O)N(R3aa), и необязательно замещена одной или несколькими группами, независимо выбранными из OH и C(O)N(R3aaR3aaa), где R3aa и R3aaa независимо выбраны из группы, состоящей из H и C1-4алкила; и
L2 прикреплен к L1 посредством концевой группы, выбранной из группы, состоящей из
 ,
, ,
, ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  и
и  ;
;
где L2 прикреплен в одном положении, отмеченном пунктирной линией, и L1 прикреплен в положении, отмеченном другой пунктирной линией; и
L1 представляет собой C1-20алкильную цепь, которая необязательно прервана одной или несколькими группами, независимо выбранными из -O- и C(O)N(R5aa), и необязательно замещена одной или несколькими группами, независимо выбранными из OH и C(O)N(R5aaR5aaa), где R5aa и R5aaa независимо выбраны из группы, состоящей из H и C1-4алкила; и
L1 присоединен к Z посредством концевой аминогруппы, образующей амидную связь с карбоксильной группой бета-1,3-D-глюкуроновой кислоты гиалуроновой кислоты из Z;
Z представляет собой гидрогель на основе сшитой гиалуроновой кислоты, в котором
от 0,05 до 20% мономерных дисахаридных звеньев сшиты посредством сшивателя; и от 0,2 до 8,5% мономерных дисахаридных звеньев содержат группы L1-L2-L-Y-R20.
Дополнительные варианты осуществления L, L1, L2, Z и Y.
В другом варианте осуществления
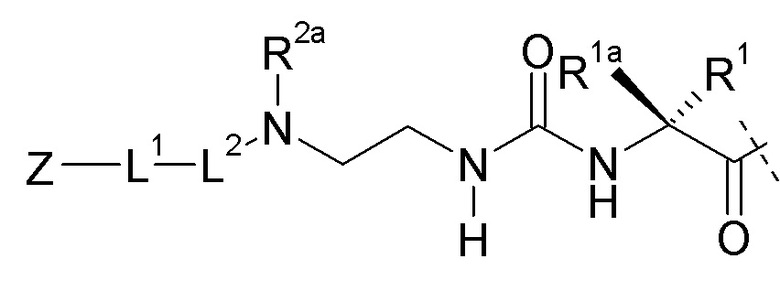
L представляет собой линкерный фрагмент формулы (Ib),
 (Ib),
(Ib),
где пунктирная линия указывает на присоединение к Y посредством образования амидной связи;
R1, R1a, R2a независимо выбраны из группы, состоящей из H и C1-4алкила;
L2-L1-Z определен, как описано выше.
В другом варианте осуществления
L представляет собой линкерный фрагмент формулы (Ib), где
R1 представляет собой CH3;
R1a представляет собой H;
R2a представляет собой H; и
L2-L1-Z определен, как описано выше.
В другом варианте осуществления
L представляет собой линкерный фрагмент формулы (Ib), где
R1 представляет собой H;
R1a представляет собой CH3;
R2a представляет собой H; и
L2-L1-Z определен, как описано выше.
В другом варианте осуществления
L представляет собой линкерный фрагмент формулы (Ib), где
R1 представляет собой CH3;
R1a представляет собой CH3;
R2a представляет собой H; и
L2-L1-Z определен, как описано выше.
В другом варианте осуществления
L представляет собой линкерный фрагмент -L формулы (Ic),
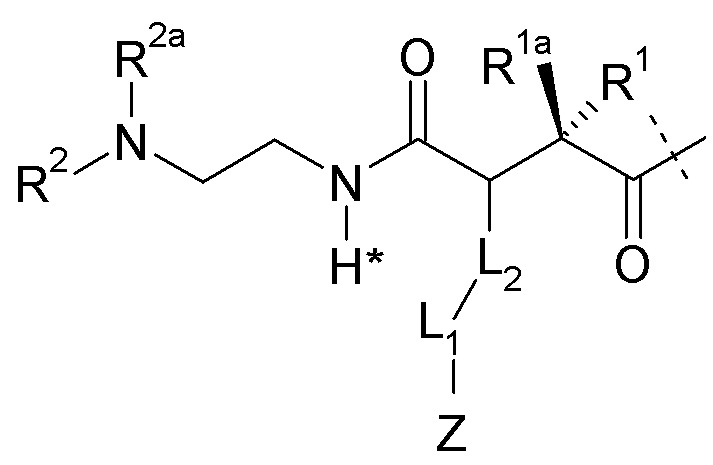 (Ic),
(Ic),
где пунктирная линия указывает на присоединение к Y посредством образования амидной связи;
R1 выбран из H или C1-4алкила, предпочтительно H;
R1a выбран из H или C1-4алкила, предпочтительно H;
R2, R2a независимо выбраны из группы, состоящей из H и C1-4алкила;
где L2-L1-Z определен, как описано выше.
В другом варианте осуществления
L представляет собой линкерный фрагмент -L формулы (Ic),
 (Ic),
(Ic),
где пунктирная линия указывает на присоединение к Y посредством образования амидной связи;
R1 и R1a представляют собой H;
R2, R2a независимо выбраны из группы, состоящей из H и CH3;
где L2-L1-Z определен, как описано выше.
В другом варианте осуществления
L представляет собой линкерный фрагмент -L формулы (Ic), где
R1 и R1a представляют собой H;
R2 представляет собой H, и R2a представляет собой CH3;
где L2-L1-Z определен, как описано выше.
В другом варианте осуществления
L2 представляет собой C1-10алкильную цепь, которая необязательно прервана одной или двумя группами, независимо выбранными из -O- и C(O)N(R3aa), и где R3aa независимо выбран из группы, состоящей из H и C1-4алкила; и
L2 прикреплен к L1 посредством концевой группы, выбранной из группы, состоящей из
 ,
, ,
, ,
, ,
,  ,
,  ,
,  ,
,  ,
,
где L2 прикреплен в одном положении, отмеченном пунктирной линией, и L1 прикреплен в положении, отмеченном другой пунктирной линией; и
в другом варианте осуществления
L2 представляет собой C1-6алкильную цепь, которая необязательно прервана одной группой, выбранной из -O- и C(O)N(R3aa), и где R3aa независимо выбран из группы, состоящей из H и C1-4алкила; и
L2 прикреплен к L1 посредством концевой группы, выбранной из группы, состоящей из
 и
и  ;
;
где L2 прикреплен в одном положении, отмеченном пунктирной линией, и L1 прикреплен в положении, отмеченном другой пунктирной линией.
В другом варианте осуществления
L2 представляет собой -CH2-CH2-CH2-CH2-CH2-C(O)NH- или -CH2-CH2-CH2-CH2-CH2-CH2- и
прикреплен к L1 посредством концевой группы
 ;
;
где L2 прикреплен к атому серы, отмеченному пунктирной линией, и L1 прикреплен к атому азота, отмеченному пунктирной линией.
В другом варианте осуществления
L1 представляет собой C1-10алкильную цепь с аминогруппой на одном дистальном конце, которая необязательно прервана одной или двумя группами, независимо выбранными из -O- и C(O)N(R5aa), и где R5aa независимо выбран из группы, состоящей из H и C1-4алкила.
Следующий вариант осуществления относится к пролекарствам, где
Z представляет собой гидрогель на основе сшитой гиалуроновой кислоты, в котором
от 0,05 до 15% мономерных дисахаридных звеньев сшиты посредством сшивателя.
Следующий вариант осуществления относится к пролекарствам, где
Z представляет собой гидрогель на основе сшитой гиалуроновой кислоты, в котором
от 1 до 10% мономерных дисахаридных звеньев сшиты посредством сшивателя.
Следующий вариант осуществления относится к пролекарствам, где
Z представляет собой гидрогель на основе сшитой гиалуроновой кислоты, в котором
от 0,2 до 8,5% мономерных дисахаридных звеньев содержат группы L1-L2-L-Y-R20.
Следующий вариант осуществления относится к пролекарствам, где
Z представляет собой гидрогель на основе сшитой гиалуроновой кислоты, в котором
от 0,2 до 6% мономерных дисахаридных звеньев содержат группы L1-L2-L-Y-R20.
Следующий вариант осуществления относится к пролекарствам, где
Z представляет собой гидрогель на основе сшитой гиалуроновой кислоты, в котором
от 0,2 до 5% мономерных дисахаридных звеньев содержат группы L1-L2-L-Y-R20.
Следующий вариант осуществления относится к пролекарствам, где
Z представляет собой гидрогель на основе сшитой гиалуроновой кислоты, в котором
от 0,4 до 4% мономерных дисахаридных звеньев содержат группы L1-L2-L-Y-R20.
В другом варианте осуществления пролекарство на основе агониста GLP-1/глюкагона имеет структуру, представленную формулой (V)
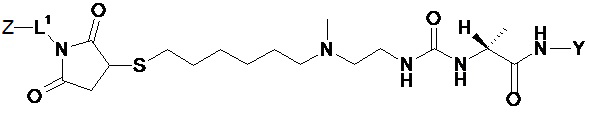 (V).
(V).
В другом варианте осуществления пролекарство на основе агониста GLP-1/глюкагона имеет структуру, представленную формулой (VI) (Aib-линкер)
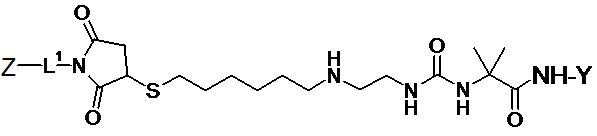 (VI).
(VI).
В другом варианте осуществления пролекарство на основе агониста GLP-1/глюкагона имеет структуру, представленную формулой (VII)
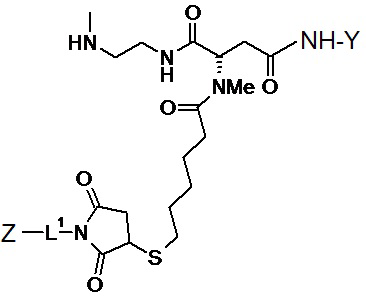 (VII).
(VII).
Следующий вариант осуществления относится к группе пролекарств, содержащих пептидный фрагмент Y формулы (II), где
X2 представляет собой аминокислотный остаток, выбранный из Ser, D-Ser и Aib,
X3 представляет собой аминокислотный остаток, выбранный из Gln и His,
X18 представляет собой Arg,
X20 представляет собой аминокислотный остаток, выбранный из Lys, Gln и His,
X21 представляет собой аминокислотный остаток, выбранный из Asp и Glu,
X28 представляет собой аминокислотный остаток, выбранный из Ser и Ala,
X32 представляет собой аминокислотный остаток, выбранный из Ser и Val.
Следующий вариант осуществления относится к группе пролекарств, содержащих пептидный фрагмент Y формулы (II), где
X2 представляет собой D-Ser,
X3 представляет собой His,
X18 представляет собой Arg,
X20 представляет собой Lys,
X21 представляет собой аминокислотный остаток, выбранный из Asp и Glu,
X28 представляет собой аминокислотный остаток, выбранный из Ser и Ala,
X32 представляет собой аминокислотный остаток, выбранный из Ser и Val.
Следующий вариант осуществления относится к группе пролекарств, содержащих пептидный фрагмент Y формулы (II), где
X2 представляет собой D-Ser,
X3 представляет собой аминокислотный остаток, выбранный из Gln и His,
X18 представляет собой Arg,
X20 представляет собой Lys,
X21 представляет собой аминокислотный остаток, выбранный из Asp и Glu,
X28 представляет собой Ala,
X32 представляет собой аминокислотный остаток, выбранный из Ser и Val.
Следующий вариант осуществления относится к группе пролекарств, содержащих пептидный фрагмент Y формулы (II), где
X2 представляет собой аминокислотный остаток, выбранный из Ser, D-Ser и Aib,
X3 представляет собой His,
X18 представляет собой Arg,
X20 представляет собой Lys,
X21 представляет собой Asp,
X28 представляет собой Ala,
X32 представляет собой аминокислотный остаток, выбранный из Ser и Val.
Следующий вариант осуществления относится к группе пролекарств, содержащих пептидный фрагмент Y формулы (II), где
X2 представляет собой аминокислотный остаток, выбранный из Ser, D-Ser и Aib,
X3 представляет собой аминокислотный остаток, выбранный из Gln и His,
X18 представляет собой аминокислотный остаток, выбранный из Arg и Lys,
X20 представляет собой Lys,
X21 представляет собой аминокислотный остаток, выбранный из Asp и Glu,
X28 представляет собой аминокислотный остаток, выбранный из Ser и Ala,
X32 представляет собой аминокислотный остаток, выбранный из Ser и Val.
Следующий вариант осуществления относится к группе пролекарств, содержащих пептидный фрагмент Y формулы (II), где
X2 представляет собой аминокислотный остаток, выбранный из Ser, D-Ser и Aib,
X3 представляет собой аминокислотный остаток, выбранный из Gln и His,
X18 представляет собой аминокислоту, выбранную из Arg и Lys,
X20 представляет собой аминокислотный остаток, выбранный из Lys, Gln и His,
X21 представляет собой Asp,
X28 представляет собой аминокислотный остаток, выбранный из Ser и Ala,
X32 представляет собой аминокислотный остаток, выбранный из Ser и Val.
Следующий вариант осуществления относится к группе пролекарств, содержащих пептидный фрагмент Y формулы (II), где
X2 представляет собой аминокислотный остаток, выбранный из Ser, D-Ser и Aib,
X3 представляет собой аминокислотный остаток, выбранный из Gln и His,
X18 представляет собой аминокислоту, выбранную из Arg и Lys,
X20 представляет собой аминокислотный остаток, выбранный из Lys, Gln и His,
X21 представляет собой аминокислотный остаток, выбранный из Asp и Glu,
X28 представляет собой аминокислотный остаток, выбранный из Ser и Ala,
X32 представляет собой Ser.
Следующий вариант осуществления относится к группе пролекарств, содержащих пептидный фрагмент Y формулы (II), где
X2 представляет собой аминокислотный остаток, выбранный из Ser, D-Ser и Aib,
X3 представляет собой аминокислотный остаток, выбранный из Gln и His,
X18 представляет собой Arg,
X20 представляет собой Lys,
X21 представляет собой аминокислотный остаток, выбранный из Asp и Glu,
X28 представляет собой Ala,
X32 представляет собой Val.
Следующий вариант осуществления относится к группе пролекарств, содержащих пептидный фрагмент Y формулы (III), где
X2 представляет собой аминокислотный остаток, выбранный из Ser, D-Ser и Aib,
X3 представляет собой аминокислотный остаток, выбранный из Gln и His,
X18 представляет собой Leu,
X20 представляет собой аминокислотный остаток, выбранный из His, Arg, Lys и Gln,
X21 представляет собой аминокислотный остаток, выбранный из Asp и Glu,
X28 представляет собой аминокислотный остаток, выбранный из Lys, Ser и Ala,
X32 представляет собой аминокислотный остаток, выбранный из Ser и Val.
Следующий вариант осуществления относится к группе пролекарств, содержащих пептидный фрагмент Y формулы (III), где
X2 представляет собой Aib,
X3 представляет собой аминокислотный остаток, выбранный из Gln и His,
X18 представляет собой аминокислотный остаток, выбранный из His и Leu,
X20 представляет собой аминокислотный остаток, выбранный из His, Arg, Lys и Gln,
X21 представляет собой аминокислотный остаток, выбранный из Asp и Glu,
X28 представляет собой аминокислотный остаток, выбранный из Lys, Ser и Ala,
X32 представляет собой аминокислотный остаток, выбранный из Ser и Val.
Следующий вариант осуществления относится к группе пролекарств, содержащих пептидный фрагмент Y формулы (III), где
X2 представляет собой Aib,
X3 представляет собой His,
X18 представляет собой Leu,
X20 представляет собой Lys,
X21 представляет собой аминокислотный остаток, выбранный из Asp и Glu,
X28 представляет собой аминокислотный остаток, выбранный из Ser и Ala,
X32 представляет собой аминокислотный остаток, выбранный из Ser и Val.
Следующий вариант осуществления относится к группе пролекарств, содержащих пептидный фрагмент Y формулы (III), где
X2 представляет собой аминокислотный остаток, выбранный из Ser, D-Ser и Aib,
X3 представляет собой His,
X18 представляет собой аминокислотный остаток, выбранный из His и Leu,
X20 представляет собой аминокислотный остаток, выбранный из His, Arg, Lys и Gln,
X21 представляет собой аминокислотный остаток, выбранный из Asp и Glu,
X28 представляет собой аминокислотный остаток, выбранный из Lys, Ser и Ala,
X32 представляет собой аминокислотный остаток, выбранный из Ser и Val.
Следующий вариант осуществления относится к группе пролекарств, содержащих пептидный фрагмент Y формулы (III), где
X2 представляет собой аминокислотный остаток, выбранный из Ser, D-Ser и Aib,
X3 представляет собой Gln,
X18 представляет собой Leu,
X20 представляет собой Lys,
X21 представляет собой аминокислотный остаток, выбранный из Asp и Glu,
X28 представляет собой Ala,
X32 представляет собой Ser.
Следующий вариант осуществления относится к группе пролекарств, содержащих пептидный фрагмент Y формулы (III), где
X2 представляет собой аминокислотный остаток, выбранный из Ser, D-Ser и Aib,
X3 представляет собой аминокислотный остаток, выбранный из Gln и His,
X18 представляет собой аминокислотный остаток, выбранный из His и Leu,
X20 представляет собой Lys,
X21 представляет собой аминокислотный остаток, выбранный из Asp и Glu,
X28 представляет собой аминокислотный остаток, выбранный из Lys, Ser и Ala,
X32 представляет собой аминокислотный остаток, выбранный из Ser и Val.
Следующий вариант осуществления относится к группе пролекарств, содержащих пептидный фрагмент Y формулы (III), где
X2 представляет собой аминокислотный остаток, выбранный из Ser, D-Ser и Aib,
X3 представляет собой аминокислотный остаток, выбранный из Gln и His,
X18 представляет собой аминокислотный остаток, выбранный из His и Leu,
X20 представляет собой аминокислотный остаток, выбранный из His, Arg, Lys и Gln,
X21 представляет собой Asp,
X28 представляет собой аминокислотный остаток, выбранный из Lys, Ser и Ala,
X32 представляет собой аминокислотный остаток, выбранный из Ser и Val.
Следующий вариант осуществления относится к группе пролекарств, содержащих пептидный фрагмент Y формулы (III), где
X2 представляет собой Aib,
X3 представляет собой аминокислотный остаток, выбранный из Gln и His,
X18 представляет собой Leu,
X20 представляет собой аминокислотный остаток, выбранный из Lys и Gln,
X21 представляет собой Glu,
X28 представляет собой Ala,
X32 представляет собой Ser.
Следующий вариант осуществления относится к группе пролекарств, содержащих пептидный фрагмент Y формулы (III), где
X2 представляет собой аминокислотный остаток, выбранный из Ser, D-Ser и Aib,
X3 представляет собой аминокислотный остаток, выбранный из Gln и His,
X18 представляет собой аминокислотный остаток, выбранный из His и Leu,
X20 представляет собой аминокислотный остаток, выбранный из His, Arg, Lys и Gln,
X21 представляет собой аминокислотный остаток, выбранный из Asp и Glu,
X28 представляет собой Ala,
X32 представляет собой аминокислотный остаток, выбранный из Ser и Val.
Следующий вариант осуществления относится к группе пролекарств, содержащих пептидный фрагмент Y формулы (III), где
X2 представляет собой аминокислотный остаток, выбранный из Ser, D-Ser и Aib,
X3 представляет собой аминокислотный остаток, выбранный из Gln и His,
X18 представляет собой аминокислотный остаток, выбранный из His и Leu,
X20 представляет собой аминокислотный остаток, выбранный из His, Arg, Lys и Gln,
X21 представляет собой аминокислотный остаток, выбранный из Asp и Glu,
X28 представляет собой аминокислотный остаток, выбранный из Lys, Ser и Ala,
X32 представляет собой аминокислотный остаток, выбранный из Ser и Val.
Следующий вариант осуществления относится к группе пролекарств, содержащих пептидный фрагмент Y формулы (II) или (III), где
X2 представляет собой аминокислотный остаток, выбранный из Aib и D-Ser,
X3 представляет собой His,
X18 представляет собой аминокислотный остаток, выбранный из Asp и Glu,
X28 представляет собой аминокислотный остаток, выбранный из Leu и Arg,
X20 представляет собой Lys,
X21 представляет собой аминокислотный остаток, выбранный из Asp и Glu,
X28 представляет собой аминокислотный остаток, выбранный из Ser и Ala,
X32 представляет собой аминокислотный остаток, выбранный из Ser и Val.
Следующий вариант осуществления относится к группе пролекарств, содержащих пептидный фрагмент формулы (IV), где
X2 представляет собой D-Ser,
X3 представляет собой аминокислотный остаток, выбранный из Gln и His,
X18 представляет собой аминокислотный остаток, выбранный из Arg и Leu,
X32 представляет собой аминокислотный остаток, выбранный из Ser и Val.
Следующий вариант осуществления относится к группе пролекарств, содержащих пептидный фрагмент формулы (IV), где
X2 представляет собой аминокислотный остаток, выбранный из Ser, D-Ser и Aib,
X3 представляет собой His,
X18 представляет собой аминокислотный остаток, выбранный из Arg и Leu, в частности, Leu,
X32 представляет собой аминокислотный остаток, выбранный из Ser и Val.
Следующий вариант осуществления относится к группе пролекарств, содержащих пептидный фрагмент формулы (IV), где
X2 представляет собой D-Ser,
X3 представляет собой Gln,
X18 представляет собой Arg,
X32 представляет собой аминокислотный остаток, выбранный из Ser и Val.
Следующий вариант осуществления относится к группе пролекарств, содержащих пептидный фрагмент формулы (IV), где
X2 представляет собой аминокислотный остаток, выбранный из Ser, D-Ser и Aib,
X3 представляет собой аминокислотный остаток, выбранный из Gln и His,
X18 представляет собой аминокислотный остаток, выбранный из Arg и Leu,
X32 представляет собой Ser.
Следующий вариант осуществления относится к группе пролекарств, содержащих пептидный фрагмент формулы (IVa),
H2N-His-Aib-His-Gly-Thr-Phe-Thr-Ser-Asp-Leu-Ser-Lys-Gln-Leu-X15-Glu-Gln-Leu-Ala-Arg-Asp-Phe-Ile-Glu-Trp-Leu-Ile-Bal-X29-Gly-X31-X32-Ser-X34-X35-Pro-Pro-Pro-X39-R20 (IVa),
где
X15 представляет собой аминокислотный остаток, выбранный из Asp и Glu (предпочт. Asp),
X29 представляет собой аминокислотный остаток, выбранный из Gly, D-Ala и Pro (предпочт. Gly, D-Ala),
X31 представляет собой аминокислотный остаток, выбранный из Pro, His и Trp (предпочт. Pro),
X32 представляет собой аминокислотный остаток, выбранный из Ser, His, Pro и Arg (предпочт. Ser, His, Pro),
X34 представляет собой аминокислотный остаток, выбранный из Gly и D-Ala,
X35 представляет собой аминокислотный остаток, выбранный из Ala, Pro и Lys (предпочт. Ala, Pro),
X39 представляет собой Ser или Pro-Pro-Pro,
или его соль или сольват.
Следующий вариант осуществления относится к группе пролекарств, содержащих пептидный фрагмент формулы (IVa), где
X15 представляет собой Asp,
X29 представляет собой аминокислотный остаток, выбранный из Gly, D-Ala и Pro,
X31 представляет собой аминокислотный остаток, выбранный из Pro, His и Trp,
X32 представляет собой аминокислотный остаток, выбранный из Ser, His, Pro и Arg,
X34 представляет собой аминокислотный остаток, выбранный из Gly и D-Ala,
X35 представляет собой аминокислотный остаток, выбранный из Ala, Pro и Lys,
X39 представляет собой Ser.
Следующий вариант осуществления относится к группе пролекарств, содержащих пептидный фрагмент формулы (IVa), где
X15 представляет собой аминокислотный остаток, выбранный из Asp и Glu,
X29 представляет собой Gly,
X31 представляет собой аминокислотный остаток, выбранный из Pro, His и Trp,
X32 представляет собой аминокислотный остаток, выбранный из Ser, His, Pro и Arg,
X34 представляет собой аминокислотный остаток, выбранный из Gly и D-Ala,
X35 представляет собой аминокислотный остаток, выбранный из Ala, Pro и Lys,
X39 представляет собой Ser или Pro-Pro-Pro.
Следующий вариант осуществления относится к группе пролекарств, содержащих пептидный фрагмент формулы (IVa), где
X15 представляет собой аминокислотный остаток, выбранный из Asp и Glu,
X29 представляет собой Gly,
X31 представляет собой Pro,
X32 представляет собой аминокислотный остаток, выбранный из Ser, His и Pro,
X34 представляет собой Gly,
X35 представляет собой Ala,
X39 представляет собой Ser.
Следующий вариант осуществления относится к группе пролекарств, содержащих пептидный фрагмент формулы (IVa), где
X15 представляет собой Asp,
X29 представляет собой D-Ala,
X31 представляет собой Pro,
X32 представляет собой Pro,
X34 представляет собой D-Ala,
X35 представляет собой аминокислотный остаток, выбранный из Ala и Pro,
X39 представляет собой Ser или Pro-Pro-Pro.
Следующий вариант осуществления относится к группе пролекарств, содержащих пептидный фрагмент формулы (IVa), где
X15 представляет собой аминокислотный остаток, выбранный из Asp и Glu,
X29 представляет собой аминокислотный остаток, выбранный из Gly, D-Ala и Pro,
X31 представляет собой Pro,
X32 представляет собой аминокислотный остаток, выбранный из Ser, His, Pro и Arg,
X34 представляет собой аминокислотный остаток, выбранный из Gly и D-Ala,
X35 представляет собой аминокислотный остаток, выбранный из Ala, Pro и Lys,
X39 представляет собой Ser или Pro-Pro-Pro.
Следующий вариант осуществления относится к группе пролекарств, содержащих пептидный фрагмент формулы (IVa), где
X15 представляет собой Asp,
X29 представляет собой Gly,
X31 представляет собой His,
X32 представляет собой Pro,
X34 представляет собой Gly,
X35 представляет собой аминокислотный остаток, выбранный из Ala и Lys,
X39 представляет собой Ser.
Следующий вариант осуществления относится к группе пролекарств, содержащих пептидный фрагмент формулы (IVa), где
X15 представляет собой Asp,
X29 представляет собой аминокислотный остаток, выбранный из Gly и Pro,
X31 представляет собой Pro,
X32 представляет собой Ser,
X34 представляет собой Gly,
X35 представляет собой Ala,
X39 представляет собой Ser.
Следующий вариант осуществления относится к группе пролекарств, содержащих пептидный фрагмент формулы (IVa), где
X15 представляет собой аминокислотный остаток, выбранный из Asp и Glu,
X29 представляет собой аминокислотный остаток, выбранный из Gly, D-Ala и Pro,
X31 представляет собой аминокислотный остаток, выбранный из Pro, His и Trp,
X32 представляет собой Pro,
X34 представляет собой аминокислотный остаток, выбранный из Gly и D-Ala,
X35 представляет собой аминокислотный остаток, выбранный из Ala, Pro и Lys,
X39 представляет собой Ser или Pro-Pro-Pro.
Следующий вариант осуществления относится к группе пролекарств, содержащих пептидный фрагмент формулы (IVa), где
X15 представляет собой Asp,
X29 представляет собой аминокислотный остаток, выбранный из Gly и Pro,
X31 представляет собой Pro,
X32 представляет собой His,
X34 представляет собой Gly,
X35 представляет собой Ala,
X39 представляет собой Ser.
Следующий вариант осуществления относится к группе пролекарств, содержащих пептидный фрагмент формулы (IVa), где
X15 представляет собой аминокислотный остаток, выбранный из Asp и Glu,
X29 представляет собой аминокислотный остаток, выбранный из Gly, D-Ala и Pro,
X31 представляет собой аминокислотный остаток, выбранный из Pro, His и Trp,
X32 представляет собой аминокислотный остаток, выбранный из Ser, His, Pro и Arg,
X34 представляет собой Gly,
X35 представляет собой аминокислотный остаток, выбранный из Ala, Pro и Lys,
X39 представляет собой Ser или Pro-Pro-Pro.
Следующий вариант осуществления относится к группе пролекарств, содержащих пептидный фрагмент формулы (IVa), где
X15 представляет собой Asp,
X29 представляет собой D-Ala,
X31 представляет собой Pro,
X32 представляет собой аминокислотный остаток, выбранный из Ser и Pro,
X34 представляет собой D-Ala,
X35 представляет собой аминокислотный остаток, выбранный из Ala и Pro,
X39 представляет собой Ser или Pro-Pro-Pro.
Следующий вариант осуществления относится к группе пролекарств, содержащих пептидный фрагмент формулы (IVa), где
X15 представляет собой аминокислотный остаток, выбранный из Asp и Glu,
X29 представляет собой аминокислотный остаток, выбранный из Gly, D-Ala и Pro,
X31 представляет собой аминокислотный остаток, выбранный из Pro, His и Trp,
X32 представляет собой аминокислотный остаток, выбранный из Ser, His, Pro и Arg,
X34 представляет собой аминокислотный остаток, выбранный из Gly и D-Ala,
X35 представляет собой Ala,
X39 представляет собой Ser.
Следующий вариант осуществления относится к группе пролекарств, содержащих пептидный фрагмент формулы (IVa), где
X15 представляет собой Asp,
X29 представляет собой Gly,
X31 представляет собой аминокислотный остаток, выбранный из Pro и His,
X32 представляет собой Pro,
X34 представляет собой Gly,
X35 представляет собой Lys,
X39 представляет собой Ser.
Следующий вариант осуществления относится к группе пролекарств, содержащих пептидный фрагмент формулы (IVa), где
X15 представляет собой Asp,
X29 представляет собой аминокислотный остаток, выбранный из Gly и D-Ala,
X31 представляет собой Pro,
X32 представляет собой Pro,
X34 представляет собой аминокислотный остаток, выбранный из Gly и D-Ala,
X35 представляет собой Pro,
X39 представляет собой Pro-Pro-Pro.
Следующий вариант осуществления относится к группе пролекарств, содержащих пептидный фрагмент формулы (IVa), где
X15 представляет собой аминокислотный остаток, выбранный из Asp и Glu,
X29 представляет собой аминокислотный остаток, выбранный из Gly, D-Ala и Pro,
X31 представляет собой аминокислотный остаток, выбранный из Pro, His и Trp,
X32 представляет собой аминокислотный остаток, выбранный из Ser, His, Pro и Arg,
X34 представляет собой аминокислотный остаток, выбранный из Gly и D-Ala,
X35 представляет собой аминокислотный остаток, выбранный из Ala, Pro и Lys,
X39 представляет собой Ser.
В одном варианте осуществления Y относится к агонисту GLP-1/глюкагона под SEQ ID NO: 60.
В одном варианте осуществления Y относится к агонисту GLP-1/глюкагона, выбранному из последовательностей под SEQ ID NO: 4-60.
В одном варианте осуществления Y относится к агонисту GLP-1/глюкагона, выбранному из последовательностей под SEQ ID NO: 4-44.
В одном варианте осуществления Y относится к агонисту GLP-1/глюкагона, выбранному из последовательностей под SEQ ID NO: 4-22.
В одном варианте осуществления Y относится к агонисту GLP-1/глюкагона, выбранному из последовательностей под SEQ ID NO: 23-39.
В одном варианте осуществления Y относится к агонисту GLP-1/глюкагона, выбранному из последовательностей под SEQ ID NO: 40-44.
В одном варианте осуществления Y относится к агонисту GLP-1/глюкагона, выбранному из последовательностей под SEQ ID NO: 45-59.
В одном варианте осуществления Y относится к агонисту GLP-1/глюкагона, выбранному из последовательностей под SEQ ID NO: 18, 21 и 26.
В одном варианте осуществления Y относится к агонисту GLP-1/глюкагона, выбранному из последовательностей под SEQ ID NO: 18, 21, 26, 45, 48, 49 и 60.
Таблица 1
Другим вариантом осуществления является пептид под SEQ ID NO: 60 и его применение в качестве фармацевтического средства.
В случае, если пролекарства на основе агониста GLP-1/глюкагона, содержащие соединения формулы (I), содержат одну или несколько кислотных или основных групп, настоящее изобретение также включает их соответствующие фармацевтически или токсикологически приемлемые соли, в частности, их фармацевтически пригодные соли. Таким образом, пролекарства на основе агониста GLP-1/глюкагона, содержащие соединения формулы (I), которые содержат кислотные группы, можно применять в соответствии с настоящим изобретением, например, в качестве солей щелочных металлов, солей щелочноземельных металлов или в качестве аммонийных солей. Более точные примеры таких солей включают соли натрия, соли калия, соли кальция, соли магния или соли с аммиаком или органическими аминами, такими как, например, этиламин, этаноламин, триэтаноламин или аминокислоты. Пролекарства на основе агониста GLP-1/глюкагона, содержащие соединения формулы (I), которые содержат одну или несколько основных групп, т. е. группы, которые могут быть протонированы, могут присутствовать, и их можно применять в соответствии с настоящим изобретением в форме их солей присоединения неорганических или органических кислот. Примеры пригодных кислот включают хлористый водород, бромистый водород, фосфорную кислоту, серную кислоту, азотную кислоту, метансульфоновую кислоту, п-толуолсульфоновую кислоту, нафталиндисульфоновые кислоты, щавелевую кислоту, уксусную кислоту, винную кислоту, молочную кислоту, салициловую кислоту, бензойную кислоту, муравьиную кислоту, пропионовую кислоту, пивалиновую кислоту, диэтилуксусную кислоту, малоновую кислоту, янтарную кислоту, пимелиновую кислоту, фумаровую кислоту, малеиновую кислоту, яблочную кислоту, сульфаминовую кислоту, фенилпропионовую кислоту, глюконовую кислоту, аскорбиновую кислоту, изоникотиновую кислоту, лимонную кислоту, адипиновую кислоту и другие кислоты, известные специалисту в данной области. Если пролекарства на основе агониста GLP-1/глюкагона, содержащие соединения формулы (I), одновременно содержат кислотные и основные группы в молекуле, то настоящее изобретение также включает, помимо упомянутых солевых форм, внутренние соли или бетаины (цвиттерионы). Соответствующие соли в зависимости от пролекарств на основе агониста GLP-1/глюкагона, содержащих соединения формулы (I), могут быть получены обычными способами, известными специалисту в данной области, как, например, путем приведения их в контакт с органическими или неорганическими кислотой или основанием в растворителе или диспергирующем средстве, или путем анионного обмена или катионного обмена с другими солями. Настоящее изобретение также включает все соли пролекарств на основе агониста GLP-1/глюкагона, содержащих соединения формулы (I), которые, в связи с низкой физиологической совместимостью, непригодны для непосредственного применения в фармацевтических препаратах, но которые можно применять, например, в качестве промежуточных соединений для химических реакций или для получения фармацевтически приемлемых солей.
Процесс получения
Пептиды Y могут быть получены с помощью обычных способов, известных в данной области.
Линкеры L получают с помощью способов, описанных в примерах и раскрытых в WO2009/095479, WO2011/012718 и WO2012/035139.
Связанное с гидрогелем пролекарство на основе агониста GLP-1/глюкагона по настоящему изобретению может быть получено путем синтеза активированного структурными единицами гидрогеля на основе гиалуроновой кислоты Z-L1* и активированного конъюгата пептида и линкера L2*-L-Y.
Активированные группы L1* и L2* применяют для конъюгирования пептида с полимерами.
На схеме 1 показаны различные типы связывающих химических структур, которые можно применять для конъюгирования пептида с помощью саморасщепляющихся линкеров с полимером. Таким образом, помимо химической структуры тиол-малеимид, можно применять другие биортогональные химические структуры. На схеме 1 пунктирные линии указывают на положения, где присоединены L1 и L2.
После загрузки конъюгата агониста GLP-1/глюкагона и линкера в гидрогель на основе функционализированной гиалуроновой кислоты все оставшиеся функциональные группы необязательно блокируются подходящим блокирующим реагентом для предупреждения нежелательных побочных реакций.
В случае гидрогеля на основе HA, содержащей функционализированную малеимидную группу, подходящим блокирующим средством является тиолсодержащее соединение, например, меркаптоэтанол.
Схема 1
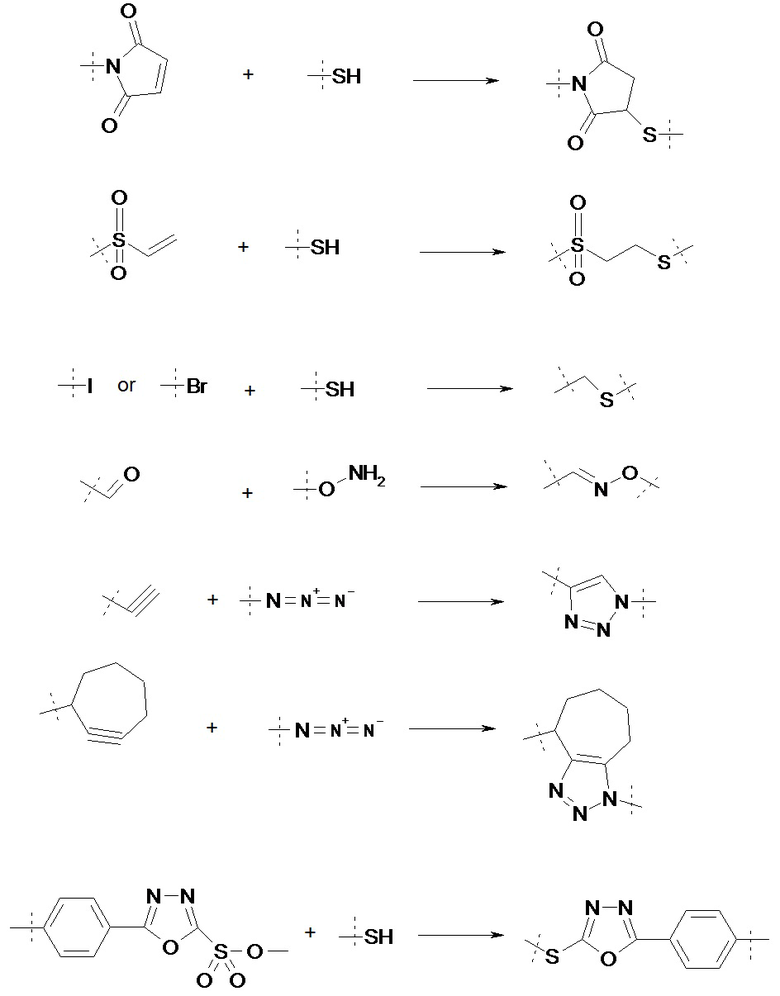
Другим аспектом настоящего изобретения являются функционализированные промежуточные соединения, содержащие конъюгат агониста GLP-1/глюкагона и линкера L2*-L-Y.
В одном варианте осуществления конъюгат агониста GLP-1/глюкагона и линкера L2*-L-Y содержит тиольную функциональную группу, в результате чего получают формулу
HS-L2-L-Y,
где L2, L и Y имеют значения, описанные выше.
Одним вариантом осуществления тиол-функционализированного конъюгата агониста GLP-1/глюкагона и линкера L2*-L-Y является конъюгат агониста GLP-1/глюкагона и линкера формулы (VIII)
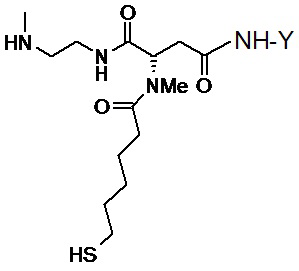 (VIII).
(VIII).
Одним вариантом осуществления тиол-функционализированного конъюгата агониста GLP-1/глюкагона и линкера L2*-L-Y является конъюгат агониста GLP-1/глюкагона и линкера формулы (IX)
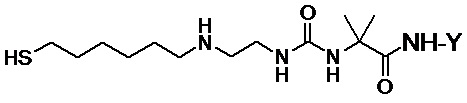 (IX).
(IX).
Одним вариантом осуществления тиол-функционализированного конъюгата агониста GLP-1/глюкагона и линкера L2*-L-Y является конъюгат агониста GLP-1/глюкагона и линкера формулы (X)
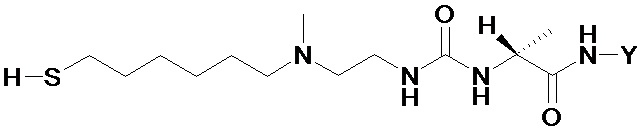 (X).
(X).
Фармацевтическая композиция
Другой аспект настоящего изобретения представляет собой фармацевтическую композицию, содержащую пролекарство по настоящему изобретению или его фармацевтически приемлемую соль вместе с фармацевтически приемлемым вспомогательным веществом. Фармацевтическая композиция дополнительно описана в нижеследующих абзацах.
Композиция пролекарства на основе агониста GLP-1/глюкагона и гидрогеля может быть представлена в виде суспендированной композиции или в виде сухой композиции. В одном варианте осуществления фармацевтическая композиция пролекарства на основе агониста GLP-1/глюкагона и гидрогеля представляет собой сухую композицию. Подходящими способами высушивания являются, например, сушка распылением и лиофилизация (сублимационная сушка). Предпочтительно, фармацевтическую композицию пролекарства на основе агониста GLP-1/глюкагона и гидрогеля высушивают посредством лиофилизации.
В другом варианте осуществления фармацевтическая композиция пролекарства на основе агониста GLP-1/глюкагона и гидрогеля представляет собой готовую к применению суспензию.
В другом варианте осуществления фармацевтическая композиция пролекарства на основе агониста GLP-1/глюкагона и гидрогеля представляет собой готовую к применению суспензию, где пролекарство набухает в воде/буфере до концентрации от 0,5 до 8% (вес/об.).
В другом варианте осуществления фармацевтическая композиция пролекарства на основе агониста GLP-1/глюкагона и гидрогеля представляет собой готовую к применению суспензию, где пролекарство набухает в воде/буфере до концентрации от 1 до 4% (вес/об.).
В другом варианте осуществления фармацевтическая композиция пролекарства на основе агониста GLP-1/глюкагона и гидрогеля представляет собой готовую к применению суспензию, где пролекарство набухает в воде/буфере до концентрации от 1,5 до 3% (вес/об.).
Предпочтительно, доза пролекарства на основе агониста GLP-1/глюкагона и гидрогеля в композиции является достаточной для обеспечения терапевтически эффективного количества агониста GLP-1/глюкагона в течение по меньшей мере трех дней за одно применение. Более предпочтительно, одно применение пролекарства на основе агониста GLP-1/глюкагона и гидрогеля является достаточным в течение одной недели.
Фармацевтическая композиция пролекарства на основе агониста GLP-1/глюкагона и гидрогеля по настоящему изобретению содержит одно или несколько вспомогательных веществ.
Вспомогательные вещества, применяемые в композициях для парентерального введения, могут быть отнесены к категории буферных средств, модификаторов изотоничности, консервантов, стабилизаторов, антиадсорбционных средств, средств защиты от окисления, загустителей/средств увеличения вязкости или других вспомогательных средств. В некоторых случаях данные ингредиенты могут обладать двойными или тройными функциями. Композиции пролекарств на основе агониста GLP-1/глюкагона и гидрогеля по настоящему изобретению содержат одно или больше одного вспомогательного средства, выбранного из групп, состоящих из следующего.
(i) Буферные средства: физиологически допустимые буферы для поддержания pH в требуемом диапазоне, например, фосфат, бикарбонат, сукцинат натрия, гистидин, цитрат и ацетат, сульфат, нитрат, хлорид, пируват натрия. Также можно применять антациды, например, Mg(OH)2 или ZnCO3. Буферную способность можно регулировать для соответствия условиям, наиболее чувствительным к стабильности pH.
(ii) Модификаторы изотоничности: для сведения к минимуму боли, которая возникает в результате повреждения клеток в связи с разностью осмотического давления в инъекционном депо. Примерами являются глицерин и хлорид натрия. Эффективные концентрации могут быть определены посредством осмометрии с использованием предполагаемой осмоляльности 285-315 мОсмоль/кг для сыворотки.
(iii) Консерванты и/или противомикробные средства: многодозовые препараты для парентерального введения требуют добавления консервантов в достаточной концентрации для сведения к минимуму риска инфицирования пациентов при инъекции, и были установлены соответствующие регуляторные требования. Типичные консерванты включают м-крезол, фенол, метилпарабен, этилпарабен, пропилпарабен, бутилпарабен, хлорбутанол, бензиловый спирт, нитрат фенилртути, тимеросал, сорбиновая кислота, сорбат калия, бензойная кислота, хлоркрезол и бензалкония хлорид.
(iv) Стабилизаторы: стабилизация достигается путем усиления стабилизирующих белок сил посредством дестабилизации денатурированного состояния или посредством прямого связывания вспомогательных веществ с белком. Стабилизаторы могут представлять собой аминокислоты, например, аланин, аргинин, аспарагиновую кислоту, глицин, гистидин, лизин, пролин, сахара, например, глюкозу, сахарозу, трегалозу, полиолы, например, глицерин, маннит, сорбит, соли, например, фосфат калия, сульфат натрия, хелатирующие средства, например, EDTA, гексафосфат, лиганды, например, ионы двухвалентных металлов (цинка, кальция и т. д.), другие соли или органические молекулы, например, фенольные производные. Кроме того, можно применять олигомеры или полимеры, например, циклодекстрины, декстран, дендримеры, PEG, или PVP, или протамин, или HSA.
(v) Антиадсорбционные средства: для покрытия внутренней поверхности контейнера с композицией или адсорбции к ней по принципу первенства в основном применяют ионные или неионные поверхностно-активные вещества, или другие белки, или растворимые полимеры. Например, полоксамер (Pluronic F-68), PEG додециловый эфир (Brij 35), полисорбат 20 и 80, декстран, полиэтиленгликоль, PEG-полигистидин, BSA, и HSA, и желатины. Выбранная концентрация и тип вспомогательного вещества зависит от эффекта, которого следует избежать, но, как правило, монослой поверхностно-активного вещества образуется на границе раздела сразу при концентрации чуть выше значения CMC.
(vi) Лио- и/или криопротекторы: в ходе сублимационной или распылительной сушки вспомогательные вещества могут противодействовать дестабилизирующим эффектам, вызванным разрывом водородной связи и удалением воды. Для данной цели можно применять сахара и полиолы, но соответствующие положительные эффекты также могут наблюдаться в случае поверхностно-активных веществ, аминокислот, неводных растворителей и других пептидов. Трегалоза является особенно эффективной при агрегации, вызванной снижением содержания влаги, а также улучшает термическую стабильность, потенциально вызванную воздействием гидрофобных групп белка на воду. Также можно применять маннит и сахарозу, либо в качестве отдельного лио/криопротектора, либо в комбинации друг с другом, где более высокие отношения маннит:сахароза, как известно, повышают физическую стабильность лиофилизированного осадка. Маннит также можно объединять с трегалозой. Трегалозу также можно объединять с сорбитом или сорбитом, применяемым в качестве единственного протектора. Также можно применять крахмал или производные крахмала.
(vii) Средства защиты от окисления: антиоксиданты, например, аскорбиновая кислота, эктоин, метионин, глутатион, монотиоглицерин, морин, полиэтиленимин (PEI), пропилгаллат, витамин E, хелатирующие средства, например, лимонная кислота, EDTA, гексафосфат, тиогликолевая кислота.
(viii) Загустители или средства увеличения вязкости: замедляют осаждение частиц во флаконах и шприце и применяются для облегчения смешивания, ресуспендирования частиц и получения суспензии, которую проще инъецировать (т. е. малое усилие на поршень шприца). Подходящими загустителями или средствами увеличения вязкости являются, например, карбомерные загустители, например, Carbopol 940, Carbopol Ultrez 10, производные целлюлозы, например, гидроксипропилметилцеллюлоза (гипромеллоза, HPMC) или диэтиламиноэтилцеллюлоза (DEAE или DEAE-C), коллоидный силикат магния (Veegum) или силикат натрия, гель гидроксиапатита, гель трикальция фосфата, ксантаны, каррагинаны, например, Satia gum UTC 30, алифатические поли(гидроксикислоты), например, поли(D,L- или L-молочная кислота) (PLA) и полигликолевая кислота (PGA) и их сополимеры (PLGA), терполимеры D,L-лактида, гликолида и капролактона, полоксамеры, гидрофильные поли(оксиэтиленовые) блоки и гидрофобные поли(оксипропиленовые) блоки для составления трехблочного поли(оксиэтилен)-поли(оксипропилен)-поли(оксиэтилена) (например, Pluronic®), сополимер полиэфира, содержащего сложноэфирные группы, например, сополимер полиэтиленгликоля терефталата/полибутилена терефталата, ацетат сахарозы изобутирата (SAIB), декстран или его производные, комбинации декстранов и PEG, полидиметилсилоксан, коллаген, хитозан, поливиниловый спирт (PVA) и производные, полиалкилимиды, сополимер акриламида и диаллилдиметиламмония (DADMA)), поливинилпирролидон (PVP), гликозаминогликаны (GAG), например, дерматансульфат, хондроитинсульфат, кератансульфат, гепарин, гепарансульфат, гиалуронан, ABA триблок или AB блок-сополимеры, состоящие из гидрофобных A-блоков, например, полилактид (PLA) или сополимер лактида и гликолида (PLGA), и гидрофильные B-блоки, например, полиэтиленгликоль (PEG) или поливинилпирролидон. Такие блок-сополимеры, а также упомянутые выше полоксамеры могут демонстрировать свойства обратного теплового гелеобразования (состояние жидкости при комнатной температуре для облегчения введения и гелеобразное состояние при температуре выше температуры перехода золь-гель при температуре тела после инъекции).
(ix) Средство, усиливающее растекание, или диффундирующее средство: модифицирует проницаемость соединительной ткани посредством гидролиза компонентов внеклеточного матрикса в интерстициальном пространстве, например, без ограничения, гиалуроновая кислота, полисахарид, обнаруженный в межклеточном пространстве соединительной ткани. Средство, усиливающее растекание, например, без ограничения гиалуронидаза, временно снижает вязкость внеклеточного матрикса и обеспечивает диффузию инъецируемых лекарственных средств.
(x) Другие вспомогательные средства: например, смачивающие средства, модификаторы вязкости, антибиотики, гиалуронидаза. Кислоты и основания, например, хлористоводородная кислота и гидроксид натрия, являются вспомогательными средствами, необходимыми для регулирования pH в ходе производства.
В одном варианте осуществления композиция пролекарства на основе агониста GLP-1/глюкагона и гидрогеля содержит один или больше одного загустителя и/или модифицирующего вязкость средства.
В другом варианте осуществления композиция пролекарства на основе агониста GLP-1/глюкагона и гидрогеля содержит гиалуроновую кислоту в качестве загустителя и/или модифицирующего вязкость средства.
В другом варианте осуществления композиция пролекарства на основе агониста GLP-1/глюкагона и гидрогеля содержит гиалуроновую кислоту в качестве загустителя и/или модифицирующего вязкость средства в концентрации от 5 до 30 вес. %.
В другом варианте осуществления композиция пролекарства на основе агониста GLP-1/глюкагона и гидрогеля содержит гиалуроновую кислоту в качестве загустителя и/или модифицирующего вязкость средства с молекулярным весом от 200 кДа до 6 миллионов кДа.
В другом варианте осуществления композиция пролекарства на основе агониста GLP-1/глюкагона и гидрогеля содержит гиалуроновую кислоту в качестве загустителя и/или модифицирующего вязкость средства с молекулярным весом от 500 кДа до 3 миллионов кДа.
Термин "вспомогательное вещество" предпочтительно относится к разбавителю, адъюванту или среде-носителю, с которыми вводят терапевтическое средство. Таким фармацевтическим вспомогательным веществом могут быть стерильные жидкости. Если фармацевтическую композицию вводят перорально, то предпочтительным вспомогательным веществом является вода. Солевой раствор и водный раствор декстрозы являются предпочтительными вспомогательными веществами, если фармацевтическую композицию вводят внутривенно. Солевые растворы, водный раствор декстрозы и растворы глицерина являются предпочтительными для использования в качестве жидких носителей для инъекционных растворов.
Подходящие фармацевтические вспомогательные вещества включают крахмал, глюкозу, лактозу, сахарозу, желатин, солод, рис, муку, мел, силикагель, стеарат натрия, глицерина моностеарат, тальк, хлорид натрия, сухое обезжиренное молоко, глицерин, пропилен, гликоль, воду, этанол и т. п. Композиция, при необходимости, также может содержать незначительные количества смачивающих или эмульгирующих средств, или буферных средств для регуляции pH. Данные композиции могут принимать форму растворов, суспензий, эмульсий, таблеток, пилюль, капсул, порошков, составов с замедленным высвобождением и т. п. Такие композиции будут содержать терапевтически эффективное количество терапевтического средства, предпочтительно в очищенной форме, вместе с подходящим количеством вспомогательного вещества, чтобы обеспечить форму для соответствующего введения пациенту. Состав должен соответствовать способу введения.
В общем варианте осуществления фармацевтическая композиция по настоящему изобретению, либо в сухой форме, либо в виде суспензии, или в другой форме может быть представлена в виде композиции с разовой дозой или несколькими дозами.
В одном варианте осуществления настоящего изобретения сухая композиция пролекарства на основе агониста GLP-1/глюкагона и гидрогеля представлена в виде разовой дозы, а это означает, что контейнер, в котором ее поставляют, содержит одну дозу фармацевтического средства.
Таким образом, в другом аспекте настоящего изобретения композиция представлена в виде композиции с разовой дозой.
В другом аспекте настоящего изобретения композиция содержится в контейнере. В одном варианте осуществления контейнер представляет собой двухкамерный шприц. В частности, в первой камере двухкамерного шприца предусмотрена сухая композиция по настоящему изобретению, а раствор для восстановления предусмотрен во второй камере двухкамерного шприца.
Перед применением сухой композиции пролекарства на основе агониста GLP-1/глюкагона и гидрогеля в отношении пациента, нуждающегося в этом, сухую композицию восстанавливают. Восстановление может происходить в контейнере, в котором представлена сухая композиция пролекарства на основе агониста GLP-1/глюкагона и гидрогеля, например, во флаконе, шприце, двухкамерном шприце, ампуле и картридже. Восстановление осуществляют путем добавления предварительно определенного количества раствора для восстановления к сухой композиции. Растворы для восстановления представляют собой стерильные жидкости, например, воду или буфер, которые могут содержать дополнительные добавки, например, консерванты и/или противомикробные средства. Если композиция пролекарства на основе агониста GLP-1/глюкагона и гидрогеля представлена в виде разовой дозы, раствор для восстановления может содержать один(одно) или несколько консервантов и/или противомикробных средств. Предпочтительно, раствор для восстановления представляет собой стерильную воду.
Дополнительный аспект настоящего изобретения относится к способу введения восстановленной композиции пролекарства на основе агониста GLP-1/глюкагона и гидрогеля. Композицию пролекарства на основе агониста GLP-1/глюкагона и гидрогеля можно вводить посредством способов инъекции или инфузии, в том числе внутрикожной, подкожной, внутримышечной, внутривенной, внутрикостной и внутрибрюшинной.
Дополнительный аспект представляет собой способ получения восстановленной композиции, содержащей терапевтически эффективное количество пролекарства на основе агониста GLP-1/глюкагона и гидрогеля и необязательно одно или несколько фармацевтически приемлемых вспомогательных веществ, где агонист GLP-1/глюкагон временно связан с гидрогелем, при этом способ включает стадию
- приведения в контакт композиции по настоящему изобретению с раствором для восстановления.
Другой аспект представляет собой восстановленную композицию, содержащую терапевтически эффективное количество пролекарства на основе агониста GLP-1/глюкагона и гидрогеля и необязательно одно или несколько фармацевтически приемлемых вспомогательных веществ, где агонист GLP-1/глюкагона временно связан с гидрогелем, получаемым согласно вышеизложенному способу.
Другой аспект настоящего изобретения представляет собой способ получения сухой композиции пролекарства на основе агониста GLP-1/глюкагона и гидрогеля. В одном варианте осуществления такую суспендированную композицию получают следующим образом:
(i) смешиванием пролекарства на основе агониста GLP-1/глюкагона и гидрогеля с одним или несколькими вспомогательными веществами,
(ii) переносом эквивалентных разовой или многократной дозе количеств в подходящий контейнер,
(iii) высушиванием композиции в указанном контейнере и
(iv) закупориванием контейнера.
Подходящими контейнерами являются флаконы, шприцы, двухкамерные шприцы, ампулы и картриджи.
Другим аспектом является набор элементов. Если устройство для введения представляет собой просто шприц для подкожных введений, то набор может включать шприц, иглу и контейнер, содержащий сухую композицию пролекарства на основе агониста GLP-1/глюкагона и гидрогеля для применения с помощью шприца, и второй контейнер, содержащий раствор для восстановления. В более предпочтительных вариантах осуществления устройство для инъекции отличается от простого шприца для подкожных введений, следовательно, отдельный контейнер с восстановленным пролекарством на основе агониста GLP-1/глюкагона и гидрогеля приспособлен так соприкасаться с устройством для инъекции, чтобы при использовании жидкая композиция в контейнере находилась в жидкостном соединении с выпускным отверстием устройства для инъекции. Примеры устройств для введения включают без ограничения шприцы для подкожного введения и устройства, представляющие собой инжекторы типа шприц-ручка. Особенно предпочтительными устройствами для инъекции являются инжекторы типа шприц-ручка, при этом контейнер представляет собой картридж, предпочтительно одноразовый картридж.
Предпочтительный набор элементов содержит иглу и контейнер, содержащий композицию по настоящему изобретению и необязательно дополнительно содержащий раствор для восстановления, при это контейнер приспособлен для применения при помощи иглы. Предпочтительно, контейнер представляет собой двухкамерный шприц.
В другом аспекте в настоящем изобретении представлен картридж, содержащий композицию пролекарства на основе агониста GLP-1/глюкагона и гидрогеля, как описано выше в данном документе, для применения с устройством, представляющим собой инжектор типа шприц-ручка. Картридж может содержать разовую дозу или несколько доз агониста GLP-1/глюкагона.
В одном варианте осуществления настоящего изобретения суспендированная композиция пролекарства на основе агониста GLP-1/глюкагона и гидрогеля включает в себя не только пролекарство на основе агониста GLP-1/глюкагона и гидрогеля и одно или больше одного вспомогательного вещества, но также другие биологически активные средства, либо в их свободной форме, либо в виде пролекарств. Предпочтительно, такие дополнительные одно или несколько биологически активных средств представляют собой пролекарство, более предпочтительно пролекарство на основе гидрогеля. Такие биологически активные средства включают без ограничения соединения нижеперечисленных классов.
Способность к введению посредством инъекции
Предпочтительно, состав можно вводить посредством инъекции через иглу с внутренним диаметром, меньшим чем 0,26 мм (26 калибр), еще более предпочтительно через иглу с внутренним диаметром, меньшим чем 0,18 мм (28 калибр), и наиболее предпочтительно через иглу с внутренним диаметром, меньшим чем 0,16 мм (30 калибр).
Следует понимать, что термины "может быть введен посредством инъекции", "инъецируемый" или "способность к введению посредством инъекции" относятся к комбинации таких факторов, как определенная сила, приложенная к поршню шприца, содержащего биоразлагаемый гидрогель HA по настоящему изобретению, набухший в жидкости с конкретной концентрацией (вес/об.) и при конкретной температуре, игла с данным внутренним диаметром, соединенная с выпускным отверстием такого шприца, и время, необходимое для вытеснения конкретного объема биоразлагаемого гидрогеля по настоящему изобретению из шприца через иглу.
Для обеспечения введения посредством инъекции, пролекарства на основе агониста GLP-1/глюкагона по настоящему изобретению объемом 1 мл, набухшие в воде и содержащиеся в шприце (удерживающем поршень с диаметром 4,7 мм), могут быть вытеснены при комнатной температуре за 10 секунд путем приложения силы равной/меньше 20 Н через иглу 26 калибра.
Предпочтительная способность к введению посредством инъекции представляет собой объем пролекарств на основе агониста GLP-1/глюкагона по настоящему изобретению, равный 1 мл, набухших в воде и содержащихся в шприце (удерживающем поршень с диаметром 4,7 мм), который может быть вытеснен при комнатной температуре за 10 секунд путем приложения силы равной/меньшей 20 Н через иглу 30 калибра.
Неожиданно было обнаружено, чем больше загрузка пептида в полимере, тем меньшая сила требуется для введения посредством инъекции носителя HA по настоящему изобретению (фиг. 5).
Для обеспечения введения посредством инъекции, пролекарства на основе агониста GLP-1/глюкагона по настоящему изобретению объемом 1 мл, набухшие в воде/буфере с концентрацией по меньшей мере 1,5% (вес/об.) и помещенные в шприц, содержащий поршень с диаметром 4,7 мм, можно вытеснять при комнатной температуре в течение 10 секунд путем приложения силы меньше 30 Н через иглу 30 калибра.
Более предпочтительно, введение посредством инъекции достигается для пролекарства на основе агониста GLP-1/глюкагона по настоящему изобретению, набухшего в воде/буфере до концентрации по меньшей мере 2% (вес/об.), посредством прикладывания силы меньше 30 Н через иглу 30 калибра.
Наиболее предпочтительно, ведение посредством инъекции достигается для пролекарства на основе агониста GLP-1/глюкагона по настоящему изобретению, набухшего в воде/буфере до концентрации по меньшей мере 2% (вес/об.) посредством прикладывания силы меньше 20 Н через иглу 30 калибра.
Важной характеристикой пролекарства является образование стабильного депо, которое остается в месте его введения. Распад полимера должен начинаться после высвобождения лекарственного средства.
Комбинированная терапия
Пролекарства по настоящему изобретению, двойные агонисты рецепторов GLP-1 и глюкагона, можно сочетать со многими другими фармакологически активными соединениями, такими как все лекарственные средства, упомянутые в Rote Liste 2015, например, со всеми средствами, снижающими вес тела или подавляющими аппетит, упомянутыми в Rote Liste 2015, главе 1, со всеми гиполипидемическими средствами, упомянутыми в Rote Liste 2015, главе 58, со всеми гипотензивными средствами и нефропротективными средствами, упомянутыми в Rote Liste 2015, или со всеми диуретиками, упомянутыми в Rote Liste 2015, главе 36.
Комбинации активных ингредиентов можно использовать, в частности, для синергического улучшения активности. Их можно применять либо путем раздельного введения активных ингредиентов пациенту, либо в форме комбинированных продуктов, где в одном фармацевтическом препарате присутствует множество активных ингредиентов. Если активные ингредиенты вводят путем раздельного введения активных ингредиентов, то это можно выполнять одновременно или последовательно.
Большинство активных ингредиентов, упомянутых в данном документе далее, раскрыты в словаре USAN и Международных наименованиях лекарственных средств Фармакопеи США, Фармакопея США, Rockville 2011.
Другие активные вещества, которые являются подходящими для таких комбинаций, включают в частности те, которые, например, усиливают терапевтический эффект одного или нескольких активных веществ по отношению к одному из упомянутых показаний к применению, и/или которые позволяют уменьшать дозировку одного или нескольких активных веществ.
Терапевтические средства, которые подходят для комбинаций, включают, например, противодиабетические средства, такие как:
инсулин и производные инсулина, например: гларгин/Lantus®, 270-330 ЕД/мл инсулина гларгин (EP 2387989 A), 300 ЕД/мл инсулина гларгин (EP 2387989 A), глулизин/Apidra®, детемир/Levemir®, лизпро/Humalog®/Liprolog®, деглюдек/деглюдек плюс, аспарт, базальный инсулин и аналоги (например, LY-2605541, LY2963016, NN1436), пэгилированный инсулин лизпро, Humulin®, линджета, SuliXen®, NN1045, инсулин плюс симлин, PE0139, инсулины быстрого действия и короткого действия (например, линджета, PH20, NN1218, HinsBet), с гидрогелем (APC-002), пероральные, ингаляционные, трансдермальные и сублингвальные инсулины (например, Exubera®, Nasulin®, афрезза, трегопил, TPM 02, капсулин, Oral-lyn®, пероральный инсулин Cobalamin®, ORMD-0801, NN1953, NN1954, NN1956, VIAtab, пероральный инсулин ошади). Также дополнительно включены такие производные инсулина, которые связаны с альбумином или другим белком с помощью бифункционального линкера.
GLP-1, аналоги GLP-1 и агонисты рецептора GLP-1, например: ликсисенатид/AVE0010/ZP10/ликсумия, эксенатид/эксендин-4/биетта/бидуреон/ITCA 650/AC-2993, лираглутид/виктоза, семаглутид, таспоглютид, синкриа/албиглутид, дулаглутид, rExendin-4, CJC-1134-PC, PB-1023, TTP-054, лангленатид/HM-11260C, CM-3, GLP-1 элиген, ORMD-0901, NN-9924, NN-9926, NN-9927, нодексен, виадор-GLP-1, CVX-096, ZYOG-1, ZYD-1, GSK-2374697, DA-3091, MAR-701, MAR709, ZP-2929, ZP-3022, TT-401, BHM-034. MOD-6030, CAM-2036, DA-15864, ARI-2651, ARI-2255, эксентатид-XTEN и глюкагон-Xten.
Ингибиторы DPP-4, например: алоглиптин/несина, тражента/линаглиптин/BI-1356/ондеро/тражента/траджента/трайента/традзента, саксаглиптин/онглиза, ситаглиптин/янувия/кселевия/тесаве/янумет/вельметиа, галвус/вилдаглиптин, анаглиптин, гемиглиптин, тенелиглиптин, мелоглиптин, трелаглиптин, DA-1229, омариглиптин/MK-3102, KM-223, эвоглиптин, ARI-2243, PBL-1427, пиноксацин.
Ингибиторы SGLT2, например: инвокана/канаглифозин, форксига/дапаглифлозин, ремоглифлозин, серглифлозин, эмпаглифлозин, ипраглифлозин, тофоглифлозин, лузеоглифлозин, LX-4211, эртуглифлозин/PF-04971729, RO-4998452, EGT-0001442, KGA-3235/DSP-3235, LIK066, SBM-TFC-039,
Бигуаниды (например, метформин, буформин, фенформин), тиазолидиндионы (например, пиоглитазон, ривоглитазон, розиглитазон, троглитазон), двойные агонисты PPAR (например, алеглитазар, мураглитазар, тезаглитазар), сульфонилмочевины (например, толбутамид, глибенкламид, глимепирид/амарил, глипизид), меглитиниды (например, натеглинид, репаглинид, митиглинид), ингибиторы альфа-глюкозидазы (например, акарбоза, миглитол, воглибоза), амилин и аналоги амилина (например, прамлинтид, симлин).
Агонисты GPR119 (например, GSK-263A, PSN-821, MBX-2982, APD-597, ZYG-19, DS-8500), агонисты GPR40 (например, фазиглифам/TAK-875, TUG-424, P-1736, JTT-851, GW9508).
Другие подходящие компоненты для комбинаций представляют собой следующие: циклосет, ингибиторы 11-бета-HSD (например, LY2523199, BMS770767, RG-4929, BMS816336, AZD-8329, HSD-016, BI-135585), активаторы глюкокиназы (например, TTP-399, AMG-151, TAK-329, GKM-001), ингибиторы DGAT (например LCQ-908), ингибиторы протеин-тирозинфосфатазы 1 (например, тродусквемин), ингибиторы глюкозо-6-фосфатазы, ингибиторы фруктозо-1,6-бисфосфатазы, ингибиторы гликогенфосфорилазы, ингибиторы фосфоенолпируваткарбоксикиназы, ингибиторы киназы гликогенсинтазы, ингибиторы киназы пируватдегидрогеназы, альфа-2-антагонисты, антагонисты CCR-2, ингибиторы SGLT-1 (например LX-2761).
В качестве партнеров для комбинаций подходящими являются также одно или несколько гиполипидемических средств, таких как, например: ингибиторы HMG-CoA-редуктазы (например, симвастатин, аторвастатин), фибраты (например, бензафибрат, фенофибрат), никотиновая кислота и ее производные (например, ниацин),
агонисты или модуляторы PPAR-(альфа, гамма или альфа/гамма) (например, алеглитазар),
агонисты PPAR-дельта, ингибиторы ACAT (например, авазимиб), ингибиторы абсорбции холестерина (например, эзетимиб), вещества, связывающие желчные кислоты (например, холестирамин, холесевелам), ингибиторы транспорта желчных кислот в подвздошной кишке, ингибиторы MTP или модуляторы PCSK9.
Соединения, повышающие уровень HDL, такие как: ингибиторы CETP (например, торцетрапиб, анацетрапид, дальцетрапид, эвацетрапид, JTT-302, DRL-17822, TA-8995) или регуляторы ABC1.
Другие подходящие компоненты для комбинаций представляют собой одно или несколько активных веществ для лечения ожирения, таких как, например: сибутрамин, тезофензин, орлистат, антагонисты каннабиноидного рецептора 1 типа, антагонисты рецептора MCH-1, агонисты рецептора MC4, антагонисты NPY5 или NPY2 (например, велнеперит), бета-3-агонисты, лептин или лептиномиметики, агонисты рецептора 5HT2c (например, лоркасерин) или комбинации бупропион/налтрексон, бупропион/зонисамид, бупропион/фентермин или прамлинтид/метрелептин.
Другие подходящие партнеры для комбинаций представляют собой:
дополнительные желудочно-кишечные пептиды, такие как пептид YY 3-36 (PYY3-36) или его аналоги, панкреатический полипептид (PP) или его аналоги.
Агонисты или антагонисты рецептора глюкагона, агонисты или антагонисты рецептора GIP, антагонисты или обратные агонисты грелина, ксенин и его аналоги.
Кроме того, комбинации с лекарственными средствами для воздействия на высокое кровяное давление, хроническую сердечную недостаточность или атеросклероз, такие как, например: антагонисты рецепторов ангиотензина II (например, телмисартан, кандесартан, валсартан, лозартан, эпросартан, ирбесартан, олмесартан, тазосартан, азилсартан), ингибиторы ACE, ингибиторы ECE, диуретики, бета-блокаторы, антагонисты кальция, средства против гипертензии центрального действия, антагонисты альфа-2-адренергического рецептора, ингибиторы нейтральной эндопептидазы, ингибиторы агрегации тромбоцитов и другие или их комбинации, также являются подходящими.
Применение
В другом аспекте данное изобретение относится к применению пролекарства согласно данному изобретению или его физиологически приемлемой соли в комбинации по меньшей мере с одним из активных веществ, описанных выше, в качестве компонента комбинации, для получения лекарственного препарата, который подходит для лечения или предупреждения заболеваний или состояний, на которые можно воздействовать путем связывания с рецепторами GLP-1 и глюкагона и путем модуляции их действия.
Указанные композиции предназначены для применения в способе лечения или предупреждения заболеваний или нарушений, известных для агонистов GLP-1/глюкагона и GLP-1/глюкагона, например, для лечения и предупреждения гипергликемии и для лечения и предупреждения сахарного диабета любого типа, например инсулинзависмого сахарного диабета, неинсулинзависимого саарного диабета, преддиабета или гестационного сахарного диабета, для предупреждения и лечения метаболического синдрома и/или ожирения и/или нарушений питания, синдрома инсулиновой резистентности, снижения уровня липидов в плазме, снижения сердечного риска, снижения аппетита, снижения веса тела и т.д.
Соединения по настоящему изобретению пригодны для лечения или предупреждения гепатостеатоза, предпочтительно неалкогольной жировой болезни печени (NAFLD) и неалкогольного стеатогепатита (NASH).
Применение пролекарств согласно настоящему изобретению или их физиологически приемлемой соли в комбинации с одним или несколькими активными веществами может происходить одновременно, по отдельности или последовательно.
Применение пролекарства согласно настоящему изобретению или его физиологически приемлемой соли в комбинации с другим активным веществом может происходить одновременно или со сдвигом во времени, но в частности в течение короткого промежутка времени. Если их вводят одновременно, то два активных вещества дают пациенту вместе; если их применяют со сдвигом во времени, то два активных вещества дают пациенту в течение периода, меньшего или равного 12 часам, но, в частности, меньшего или равного 6 часам.
Следовательно, в другом аспекте настоящее изобретение относится к лекарственному препарату, который содержит пролекарство согласно настоящему изобретению или физиологически приемлемую соль такого соединения и по меньшей мере одно из вышеописанных активных веществ в качестве партнеров для комбинации, необязательно вместе с одним или несколькими инертными носителями и/или разбавителями.
Соединение согласно настоящему изобретению или его физиологически приемлемая соль или сольват и дополнительное активное вещество, подлежащее объединению с ними, могут оба присутствовать в одном составе, например, в суспензии, или отдельно в двух одинаковых или разных составах, например, в форме так называемых составных наборов.
Еще один аспект настоящего изобретения представляет собой способ лечения, контроля, задержки или предупреждения у пациента-млекопитающего, предпочтительно у человека, требующего лечения одного или нескольких состояний, включающий введение указанному пациенту терапевтически эффективного количества пролекарства по настоящему изобретению, или фармацевтической композиции по настоящему изобретению, или его фармацевтически приемлемой соли.
ПРИМЕРЫ
Материалы и способы
Использовали следующие сокращения:
AA аминокислота
AcOH уксусная кислота
AcOEt этилацетат
cAMP циклический аденозинмонофосфат
Bn бензил
Boc трет-бутилоксикарбонил
BOP гексафторфосфат (бензотриазол-1-илокси)трис(диметиламино)фосфония
BSA бычий сывороточный альбумин
tBu третичный бутил
DBU 1,3-диазабицикло[5.4.0]ундецен
DCC N,N-дициклогексилкарбодиимид
DCM дихлорметан
Dde 1-(4,4-диметил-2,6-диоксоциклогексилиден)этил
ivDde 1-(4,4-диметил-2,6-диоксоциклогексилиден)3-метил-бутил
DIC N,N'-диизопропилкарбодиимид
DIPEA N,N-диизопропилэтиламин
DMAP диметиламино-пиридин
DMEM среда Игла, модифицированная по Дульбекко
DMF диметилформамид
DMSO диметилсульфоксид
DTT DL-дитиотреитол
EDC 1-этил-3-(3-диметиламинопропил)карбодиимид
EDT этандитиол
EDTA - этилендиаминтетрауксусная кислота
экв. стехиометрический эквивалент
EtOH этанол
FBS фетальная бычья сыворотка
Fmoc флуоренилметилоксикарбонил
HATU O-(7-азабензотриазол-1-ил)-N,N,N′,N′-тетраметилурония гексафторфосфат
HBSS сбалансированный солевой раствор Хенкса
HBTU гексафторфосфат 2-(1H-бензотриазол-1-ил)-1,1,3,3-тетраметилурония
HEPES 2-[4-(2-гидроксиэтил)пиперазин-1-ил]этансульфоновая кислота
HOBt 1-гидроксибензотриазол
HOSu N-гидроксисукцинимид
HPLC высокоэффективная жидкостная хроматография
HTRF гомогенная флуоресценция с временным разрешением
IBMX 3-изобутил-1-метилксантин
LC/MS жидкостная хроматография/масс-спектрометрия
Mal 3-малеимидопропил
Mal-PEG6-NHS N-(3-малеимидопропил)-21-амино-4,7,10,13,16,19-гексаокса-генэйкозановой кислоты NHS сложный эфир
Me метил
MeOH метанол
Mmt 4-метокситритил
MS масс-спектр/масс-спектрометрия
MTBE метил-трет-бутиловый эфир
MW молекулярная масса
NHSN-гидроксисукцинимид
Palm пальмитоил
iPrOH 2-пропанол
PBS фосфатно-солевой буферный раствор
PEG полиэтиленгликоль
PK фармакокинетический
PyBOP бензотриазол-1-ил-окси-трис-пирролидино-фосфония гексафторфосфат
Phth фталимидо
RP-HPLC обращенно-фазовая высокоэффективная жидкостная хроматография
об/мин оборотов в минуту
RT: комнатная температура
SEC эксклюзионная хроматография
TCEP трис(2-карбоксиэтил)фосфина гидрохлорид
TES триэтилсилан
TFA трифторуксусная кислота
THF тетрагидрофуран
TMEDA N,N,N'N'-тетраметилэтилендиамин
Tris трис(гидроксиметил)аминометан
Trt тритил
UPLC сверхэффективная жидкостная хроматография
UV ультрафиолет
V объем
Пример 1
Общий синтез пептидных соединений
Материалы
Различные амидные смолы Ринка (4-(2',4'-диметоксифенил-Fmoc-аминометил)-феноксиацетамидо-норлейциламинометильная смола, Merck Biosciences; 4-[(2,4-диметоксифенил)(Fmoc-амино)метил]феноксиацетамидометильная смола, Agilent Technologies) использовали для синтеза пептидных амидов с нагрузками в диапазоне 0,3-0,4 ммоль/г.
Природные аминокислоты, защищенные Fmoc, приобретали у Protein Technologies Inc., Senn Chemicals, Merck Biosciences, Novabiochem, Iris Biotech, Nagase или Bachem. В ходе синтеза использовали следующие стандартные аминокислоты: Fmoc-L-Ala-OH, Fmoc-L-Arg(Pbf)-OH, Fmoc-L-Asn(Trt)-OH, Fmoc-L-Asp(OtBu)-OH, Fmoc-L-Cys(Trt)-OH, Fmoc-L-Gln(Trt)-OH, Fmoc-L-Glu(OtBu)-OH, Fmoc-Gly-OH, Fmoc-L-His(Trt)-OH, Fmoc-L-Ile-OH, Fmoc-L-Leu-OH, Fmoc-L-Lys(Boc)-OH, Fmoc-L-Met-OH, Fmoc-L-Phe-OH, Fmoc-L-Pro-OH, Fmoc-L-Ser(tBu)-OH, Fmoc-L-Thr(tBu)-OH, Fmoc-L-Trp(Boc)-OH, Fmoc-L-Tyr(tBu)-OH, Fmoc-L-Val-OH.
Кроме того, следующие конкретные аминокислоты приобретали у тех же поставщиков, которые указаны выше: Fmoc-L-Lys(ivDde)-OH, Fmoc-Aib-OH, Fmoc-D-Ser(tBu)-OH, Fmoc-D-Ala-OH, Boc-L-His(Boc)-OH (доступна в виде сольвата толуола) и Boc-L-His(Trt)-OH, Fmoc-L-Nle-OH, Fmoc-L-Met(O)-OH, Fmoc-L-Met(O2)-OH, Fmoc-(S)MeLys(Boc)-OH, Fmoc-(R)MeLys(Boc)-OH, Fmoc-(S)MeOrn(Boc)-OH и Boc-L-Tyr(tBu)-OH.
Твердофазный синтез пептидов проводили, например, на синтезаторе пептидов Prelude (Protein Technologies Inc.) или аналогичном автоматическом синтезаторе с применением стандартной Fmoc-химии и активации HBTU/DIPEA. В качестве растворителя применяли DMF. Снятие защиты: 20% пиперидин/DMF 2×2,5 мин. Промывания: 7 x DMF. Присоединение 2:5:10 200 мМ AA/500 мМ HBTU/2M DIPEA в DMF 2 x по 20 мин. Промывания: 5 x DMF.
Все синтезированные пептиды отщепляли от смолы с использованием смеси Кинга для расщепления, состоящей из 82,5% TFA, 5% фенола, 5% воды, 5% тиоанизола, 2,5% EDT. Затем неочищенные пептиды осаждали в диэтиловом или диизопропиловом простом эфире, центрифугировали и лиофилизировали. Пептиды анализировали с помощью аналитической HPLC и проверяли с помощью масс-спектрометрии ESI. Неочищенные пептиды очищали с помощью стандартной процедуры очистки с помощью препаративной HPLC.
Аналитическая HPLC/UPLC
Способ A: обнаружение при 215 нм
колонка: Aeris Peptide, 3,6 мкм, XB-C18 (250×4,6 мм) при 60°C;
растворитель: H2O+0,1% TFA: ACN+0,1% TFA (поток 1,5 мл/мин);
градиент: от 90:10 (0 мин) до 90:10 (3 мин), до 10:90 (43 мин), до 10:90 (48 мин), до 90:10 (49 мин), до 90:10 (50 мин).
Способ B: обнаружение при 220 нм
колонка: Zorbax, 5 мкм, C18 (250×4,6 мм) при 25°C;
растворитель: H2O+0,1% TFA: 90% ACN+10% H2O +0,1%TFA (поток 1,0 мл/мин);
градиент: от 100:0 (0 мин) до 98:2 (2 мин), до 30:70 (15 мин), до 5:95 (20 мин), до 0:100 (25 мин), до 0:100 (30 мин), до 98:2 (32 мин), до 98:2 (35 мин).
Способ C1: обнаружение при 210-225 нм, необязательно в сочетании с масс-анализатором Waters LCT Premier, режим электрораспыления положительно заряженных ионов
колонка: Waters ACQUITY UPLC® BEH™ C18 1,7 мкм (150×2,1 мм) при 50°C;
растворитель: H2O+1% FA: ACN+1% FA (поток 0,5 мл/мин);
градиент: от 95:5 (0 мин) до 95:5 (1,80 мин), до 80:20 (1,85 мин), до 80:20 (3 мин), до 60:40 (23 мин), до 25:75 (23,1 мин), до 25:75 (25 мин), до 95:5 (25,1 мин), до 95:5 (30 мин).
Способ C2: обнаружение при 210-225 нм, необязательно в сочетании с масс-анализатором Waters LCT Premier, режим электрораспыления положительно заряженных ионов
колонка: Waters ACQUITY UPLC® BEH™ C18 1,7 мкм (150×2,1 мм) при 50°C;
растворитель: H2O+1% FA: ACN+1% FA (поток 0,6 мл/мин);
градиент: от 95:5 (0 мин) до 95:5 (1 мин), до 65:35 (2 мин), до 65:35 (3 мин), до 45:55 (23 мин), до 25:75 (23,1 мин), до 25:75 (25 мин), до 95:5 (25,1 мин), до 95:5 (30 мин).
Способ C3: обнаружение при 210-225 нм, необязательно в сочетании с масс-анализатором Waters LCT Premier, режим электрораспыления положительно заряженных ионов
колонка: Waters ACQUITY UPLC® BEH™ C18 1,7 мкм (150×2,1 мм) при 50°C;
растворитель: H2O+1% FA: ACN+1% FA (поток 1 мл/мин);
градиент: от 95:5 (0 мин) до 95:5 (1 мин), до 65:35 (2 мин), до 65:35 (3 мин), до 45:55 (20 мин), до 2:98 (20,1 мин), до 2:98 (25 мин), до 95:5 (25,1 мин), до 95:5 (30 мин).
Способ C4:
обнаружение при 210-225 нм, необязательно в сочетании с масс-анализатором Waters LCT Premier, режим электрораспыления положительно заряженных ионов
колонка: Waters ACQUITY UPLC® BEH™ C18 1,7 мкм (150×2,1 мм) при 50°C;
растворитель: H2O+1% FA: ACN+1% FA (поток 1 мл/мин);
градиент: от 95:5 (0 мин) до 95:5 (1,80 мин), до 80:20 (1,85 мин), до 80:20 (3 мин), до 60:40 (23 мин), до 2:98 (23,1 мин), до 2:98 (25 мин), до 95:5 (25,1 мин), до 95:5 (30 мин).
Способ D: обнаружение при 214 нм
колонка: Waters X-Bridge C18 3,5 мкм 2,1×150 мм;
растворитель: H2O+0,5% TFA: ACN (поток 0,55 мл/мин);
градиент: от 90:10 (0 мин) до 40:60 (5 мин), до 1:99 (15 мин).
Способ E: обнаружение при 210-225 нм, необязательно в сочетании с масс-анализатором Waters LCT Premier, режим электрораспыления положительно заряженных ионов
колонка: Waters ACQUITY UPLC® BEH™ C18 1,7 мкм (150×2,1 мм) при 50°C;
растворитель: H2O+1% FA: ACN+1% FA (поток 0,9 мл/мин);
градиент: от 95:5 (0 мин) до 95:5 (2 мин), до 35:65 (3 мин), до 65:35 (23,5 мин), до 5:95 (24 мин), до 95:5 (26 мин), до 95:5 (30 мин).
Общая процедура очистки с помощью препаративной HPLC.
Неочищенные пептиды очищали либо на системе для очистки Äkta или на системе полупрепаративной HPLC Jasco. Препаративные колонки RP-C18-HPLC различных размеров и с различными скоростями потока использовали в зависимости от количества неочищенного пептида, подлежащего очистке. В качестве элюентов использовали ацетонитрил+0,05-0,1% TFA (B) и воду+0,05-0,1% TFA (A). В качестве альтернативы применяли буферную систему, состоящую из ацетонитрила и воды с незначительными количествами уксусной кислоты. Фракции, содержащие продукт, собирали и лиофилизировали с получением очищенного продукта, как правило в виде TFA или ацетатной соли.
Испытания на растворимость и стабильность производных эксендина-4
До начала испытаний партии пептида на растворимость и стабильность определяли его содержание. Таким образом, исследовали два параметра: его чистоту (HPLC-UV) и количество загруженной соли в партии (ионообменная хроматография).
Пример 2
Для испытания на растворимость целевая концентрация чистого соединения составляла 1,0 мг/мл. Таким образом, растворы из твердых образцов готовили в разных буферных системах с концентрацией соединения, составляющей 1,0 мг/мл, на основе предварительно определенного содержания. HPLC-UV проводили после 2 ч. легкого перемешивания с надосадочной жидкостью, которую получали центрифугированием при 4000 об/мин в течение 20 мин.
Затем определяли растворимость путем сравнения с площадями УФ-пиков, полученных с исходным раствором пептида в концентрации, составляющей 2 мг/мл, в чистой воде или переменным количеством ацетонитрила (визуальный контроль, что все соединения растворились). Данный анализ служил также в качестве исходной точки (t0) для испытаний на стабильность.
Пример 3
Для испытаний на стабильность аликвоту надосадочной жидкости, полученной для испытания на растворимость, хранили в течение 7 дней при 25°C или 40°C. По истечении данного периода времени образец центрифугировали в течение 20 мин. при 4000 об/мин и надосадочную жидкость анализировали с помощью HPLC-UV.
Для определения количества оставшегося пептида сравнивали площади пиков целевого соединения в моменты времени t0 и t7, получая "% оставшегося пептида", исходя из уравнения:
% оставшегося пептида=[(площадь пика пептида в t7) x 100]/площадь пика пептида в t0.
Количество растворимых продуктов распада рассчитывали за счет сравнения суммы площадей пиков всех наблюдаемых примесей, сокращенной на сумму площадей пиков, наблюдаемых в t0 (т. е. для определения количества вновь образованных связанных с пептидами видов). Данное значение было приведено в процентном отношении к исходному количеству пептида в t0, исходя из уравнения:
% растворимых продуктов распада={[(сумма площадей пиков примесей в t7) - (сумма площадей пиков примесей в t0)] x 100}/площадь пика пептида в t0
Потенциальная разность 100% и суммы "% оставшегося пептида" и "% растворимых продуктов распада" отражает количество пептида, который не остается растворимым в стрессовых условиях, исходя из уравнения:
% осадка=100-([% оставшегося пептида]+[% растворимых продуктов распада]).
Этот осадок включает нерастворимые продукты распада, полимеры и/или волокна, которые были удалены в результате проведения анализа путем центрифугирования.
Химическая стабильность выражается как "% оставшегося пептида".
Анионная хроматография
Прибор: Dionex ICS-2000, пред-колонка: Ion Pac AG-18 2×50 мм (Dionex)/AS18 2×250 мм (Dionex), элюент: водный раствор гидроксида натрия, поток: 0,38 мл/мин.; градиент: 0-6 мин.: 22 мМ KOH, 6-12 мин.: 22-28 мМ KOH, 12-15 мин.: 28-50 мМ KOH, 15-20 мин.: 22 мМ KOH, подавитель: ASRS 300 2 мм, обнаружение: проводимость.
В качестве способа HPLC/UPLC применяли способ D или E.
Пример 4. Данные in vitro в отношении рецептора GLP-1 и глюкагона.
Эффективность пептидных соединений по отношению к рецепторам GLP-1 и глюкагона определяли путем воздействия на клетки, экспрессирующие рецептор глюкагона человека (hGlucagon R) или рецептор GLP-1 человека (hGLP-1 R), перечисленными соединениями с возрастающими концентрациями и измерения образовавшегося cAMP, как описано в примере 27.
Результаты представлены в таблице 2.
Таблица 2. Значения EC50 производных эксендина-4 для рецепторов GLP-1 и глюкагона (указано в пМ).
Синтез линкера
Пример 5
Синтез линкерного реагента 5c
Линкерный реагент 5c синтезировали в соответствии со следующей схемой:
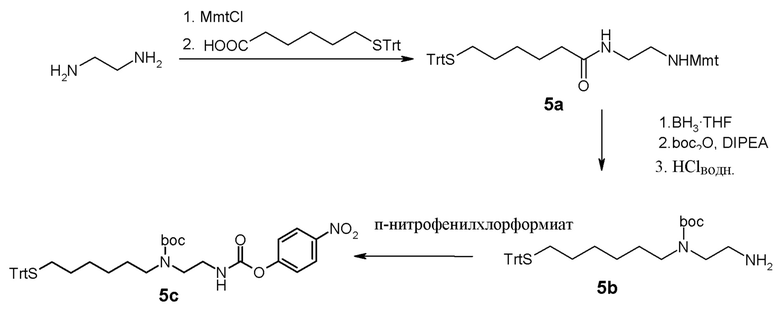
Синтез промежуточного соединения линкерного реагента 5a.
m-Метокситритилхлорид (3 г, 9,71 ммоль) растворяли в DCM (20 мл) и по капле добавляли к раствору этилендиамина (6,5 мл, 97,1 ммоль) в DCM (20 мл). Через два часа раствор выливали в диэтиловый эфир (300 мл) и промывали трижды с помощью 30/1 (об./об.) солевого раствора/0,1 М раствора NaOH (каждый 50 мл) и один раз с помощью солевого раствора (50 мл). Органическую фазу высушивали над Na2SO4 и удаляли летучие вещества при пониженном давлении. Mmt-защищенное промежуточное соединение (3,18 г, 9,56 ммоль) применяли на следующей стадии без дополнительной очистки.
Mmt-защищенное промежуточное соединение (3,18 г, 9,56 ммоль) растворяли в безводном DCM (30 мл). Добавляли 6-(S-тритилмеркапто)гексановую кислоту (4,48 г, 11,47 ммоль), PyBOP (5,67 г, 11,47 ммоль) и DIPEA (5,0 мл, 28,68 ммоль) и смесь перемешивали в течение 30 мин. при RT. Раствор разбавляли диэтиловым эфиром (250 мл) и промывали трижды с помощью 30/1 (об./об.) солевого раствора/0,1 M раствора NaOH (каждый 50 мл) и один раз солевым раствором (50 мл). Органическую фазу высушивали над Na2SO4 и удаляли летучие вещества при пониженном давлении. 5a очищали посредством флэш-хроматографии.
Выход: 5,69 г (8,09 ммоль).
MS: масса/заряд 705,4=[M+H]+ (расчетное значение MW=705,0).
Синтез промежуточного соединения линкерного реагента 5b.
К раствору 5a (3,19 г, 4,53 ммоль) в безводном THF (50 мл) добавляли BH3⋅THF (1 М раствор, 8,5 мл, 8,5 ммоль) и раствор перемешивали в течение 16 ч. при RT. Добавляли дополнительное количество BH3⋅THF (1 М раствор, 14 мл, 14 ммоль) и перемешивали в течение 16 ч. при RT. Реакционную смесь гасили добавлением метанола (8,5 мл). Добавляли N,N-диметил-этилендиамин (3 мл, 27,2 ммоль), раствор нагревали до температуры возврата флегмы и перемешивали в течение трех часов. Реакционную смесь оставляли для охлаждения до комнатной температуры и затем разбавляли этилацетатом (300 мл), промывали насыщенным водным раствором Na2CO3 (2×100 мл) и насыщенным водным раствором NaHCO3 (2×100 мл). Органическую фазу высушивали над Na2SO4 и удаляли летучие вещества при пониженном давлении с получением неочищенного промежуточного соединения в виде амина (3,22 г).
Промежуточное соединение в виде амина (3,22 г) растворяли в DCM (5 мл). Boc2O (2,97 г, 13,69 ммоль) растворяли в DCM (5 мл), добавляли DIPEA (3,95 мл, 22,65 ммоль) и смесь перемешивали при RT в течение 30 мин. Смесь очищали посредством флэш-хроматографии с получением неочищенного Boc- и Mmt-защищенного промежуточного соединения (3,00 г).
MS: масса/заряд 791,4=[M+H]+, 519,3=[M-Mmt+H]+ (расчетное значение MW=791,1).
0,4 М водный раствор HCl (48 мл) добавляли к раствору Boc- и Mmt-защищенного промежуточного соединения в ацетонитриле (45 мл). Смесь разбавляли ацетонитрилом (10 мл) и перемешивали в течение 1 ч. при RT. Затем значение pH реакционной смеси регулировали до 5,5 путем добавления 5 М раствора NaOH. Ацетонитрил удаляли при пониженном давлении и водный раствор экстрагировали с помощью DCM (4×100 мл). Объединенные органические фазы высушивали над Na2SO4 и удаляли летучие вещества при пониженном давлении. Неочищенный продукт 5b использовали на следующем этапе без дополнительной очистки.
Выход: 2,52 г (3,19 ммоль).
MS: масса/заряд 519,3=[M+H]+ (расчетное значение MW=519,8 г/моль).
Синтез линкерного реагента 5c.
Промежуточное соединение 5b (985 мг, 1,9 ммоль) и п-нитрофенилхлорформиат (330 мг, 2,5 ммоль) растворяли в безводном THF (10 мл). Добавляли DIPEA (0,653 мл, 3,7 ммоль) и смесь перемешивали в течение 2 ч. при RT. Раствор подкисляли путем добавления уксусной кислоты (1 мл). 5c очищали посредством RP-HPLC.
Выход: 776 мг (1,13 ммоль).
MS масса/заряд 706,3=[M+Na]+ (расчетное значение MW=706,3).
Синтез пептидного линкерного реагента
a) Синтез пептидов
Способы твердофазного синтеза пептидов проводили, например, на синтезаторе пептидов Prelude (Protein Technologies Inc.) или аналогичном автоматическом синтезаторе с применением стандартной Fmoc-химии и активации HBTU/DIPEA. В качестве растворителя применяли DMF. Снятие защиты: 20% пиперидин/DMF 2×2,5 мин. Промывания: 7 x DMF. Присоединение 2:5:10 200 мМ AA/500 мМ HBTU/2M DIPEA в DMF 2 x по 20 мин. Промывания: 5 x DMF.
b) N-концевое удлинение за счет D-Ala
0,9 ммоль связанного со смолой пептида (что эквивалентно 4 г смолы), синтезированного как описано на стадии a, со свободной аминогруппой на N-конце разделяли на пять равных частей. Каждую часть суспендировали в 15 мл DMF, а затем добавляли 2,5 экв. Fmoc-D-Ala-OH, 2,5 экв. HATU, 2,5 экв. HOAt и 2,5 экв. DIPEA. Смесь перемешивали в течение 16 ч. при температуре окружающей среды. Затем реакционную смесь удаляли посредством фильтрации и смолу промывали 3 раза с помощью 18 мл DMF, 18 мл DCM, 18 мл изопропанола, 18 мл диэтилового эфира. Оставшиеся растворители удаляли in vacuo.
c) Снятие Fmoc-защиты, присоединение и отщепление линкера
0,37 ммоль связанного со смолой пептида (что эквивалентно 1,6 г смолы), синтезированного как описано на стадии b, со свободной аминогруппой на N-конце разделяли на две равные части. Каждую часть суспендировали в 12 мл 20% раствора пиперидина в DMF и перемешивали в течение 5 мин. Растворитель удаляли и процедуру повторяли дважды.
Связанный со смолой пептид промывали 5 раз с помощью 12 мл DMF.
Затем смолу суспендировали в 10 мл DMF и добавляли 2,5 экв. трет-бутил(2-(((4-нитрофенокси)карбонил)амино)этил)(6-(тритилтио)гексил)карбамата 5c и 2,5 экв. DIPEA. Смесь перемешивали в течение 16 ч. при температуре окружающей среды. Затем реакционную смесь удаляли посредством фильтрации и смолу промывали 3 раза с помощью 15 мл DMF, 15 мл DCM, 15 мл изопропанола, 15 мл диэтилового эфира. Оставшиеся растворители удаляли in vacuo. Реакцию тестировали в отношении завершения посредством Kaisertest.
Затем добавляли смесь TFA/DTT/TIS/H2O/тиоанизол/Bu4NBr (100/3/2/3/1/0,05) и смесь перемешивали в течение 3,5 ч. Смесь фильтровали и смолу промывали с помощью 1 мл TFA. Объединенные фильтраты добавляли к 100 мл охлажденного диэтилового эфира. Осадок выделяли посредством центрифугирования и его промывали 2 раза с помощью 100 мл диэтилового эфира.
Неочищенный продукт очищали посредством препаративной HPLC на колонке Waters (XBridge, BEH130, Prep С18 5 мкм) с помощью градиента ацетонитрил/вода (оба буфера с 0,1% TFA). Очищенное промежуточное соединение сразу же лиофилизировали и хранили в атмосфере Ar или применяли непосредственно на следующей стадии.
Пример 6
Синтез линкерного реагента 6d агониста GLP-1/глюкагона (Ala-линкер)
Линкерный реагент агониста GLP-1/глюкагона 6d синтезировали в соответствии со следующей схемой:
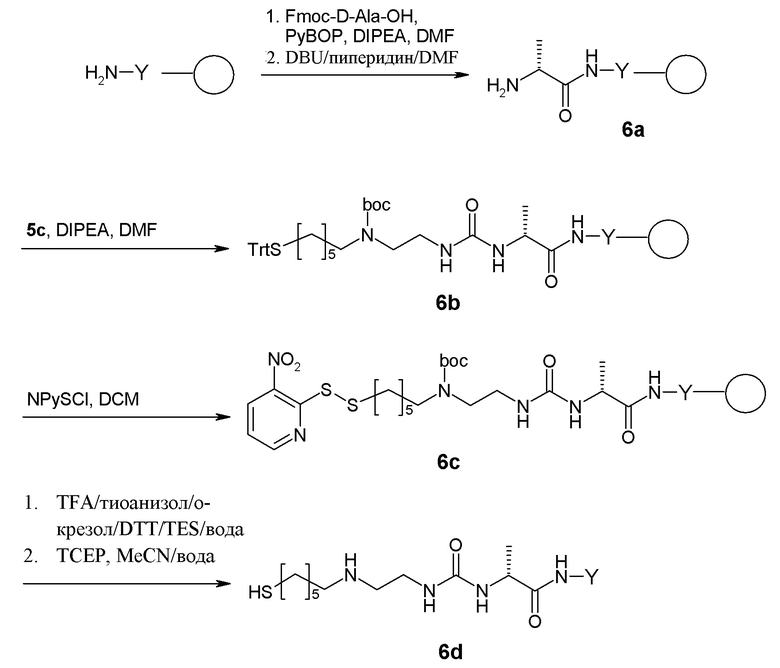
Синтез промежуточного соединения линкерного реагента агониста GLP-1/глюкагона 6a:
Агонист GLP-1/глюкагона с полностью защищенной боковой цепью и со свободным N-концом на смоле (2,00 г, 0,2 ммоль, загрузка примерно 0,1 ммоль/г) переносили в 20 мл шприц, оснащенный фильтровальной фриттой. В шприц набирали 8 мл безводного DMF и шприц встряхивали (600 об/мин) в течение 15 мин. для предварительного набухания смолы. Растворитель сливали и раствор Fmoc-D-аланин-OH (187 мг, 0,6 моль), PyBOP (312 мг, 0,6 ммоль) и DIPEA (174 мкл, 1,0 ммоль) в безводном DMF (4 мл) набирали в шприц. Шприц встряхивали при RT и 600 об/мин в течение 60 мин. Раствор сливали и смолу промывали десять раз с помощью DMF.
Снятие Fmoc-защиты осуществляли, как описано выше.
Синтез промежуточного соединения линкерного реагента агониста GLP-1/глюкагона 6b
Раствор 5c (137 мг, 0,4 ммоль) в безводном DMF (3 мл) добавляли к смоле 6a (0,2 ммоль), а затем добавляли раствор DIPEA (80 мкл, 0,46 ммоль) в безводном DMF (4,5 мл) и реакционную смесь встряхивали (600 об/мин) при 22°C в течение 15 часов.
Смолу промывали десять раз с помощью DMF и десять раз с помощью DCM и высушивали in vacuo.
Синтез промежуточного соединения линкерного реагента агониста GLP-1/глюкагона 6c
3-Нитро-2-пиридин-сульфенилхлорид (48 мг, 0,25 ммоль) набирали в шприц, содержащий 6b (0,05 ммоль, 0,5 г). Безводный DCM (4 мл) набирали в шприц и смесь встряхивали (600 об/мин) при RT. Через 2 ч. раствор сливали, смолу промывали 14 раз с помощью DCM и высушивали in vacuo.
Синтез промежуточного соединения линкерного реагента агониста GLP-1/глюкагона 6d
В круглодонной колбе o-крезол (1,5 мл), тиоанизол (1,5 мл), DTT (1,125 г), TES (1,125 мл) и воду (1,5 мл) растворяли в TFA (37,5 мл). 6c (0,15 ммоль, 1,5 г) добавляли к перемешиваемому (250-350 об/мин) раствору при RT с целью получения гомогенной суспензии. Перемешивание продолжали в течение 45 мин. Раствор отделяли от гранул смолы посредством фильтрации, гранулы промывали с помощью TFA дважды (каждый раз по 2 мл) и промывочные растворы объединяли с фильтратом. TFA удаляли из объединенных растворов в потоке азота.
Неочищенное 6d осаждали из концентрированного раствора (прибл. 10 мл) путем добавления диэтилового эфира (30 мл) и энергичного перемешивания. После центрифугирования (2 мин, 5000 об/мин) надосадочную жидкость сливали и осадок промывали диэтиловым эфиром дважды (каждый раз 20 мл).
Высушенный осадок растворяли в растворе TCEP (114 мг, 0,39 ммоль) в 30 мл смеси ацетонитрил/вода 1/19 (об./об.), содержащей 0,01% TFA (об./об.). Смесь инкубировали в течение 15 минут при RT. 6d очищали посредством RP-HPLC, как описано в материалах и способах, с использованием колонки 150×30 мм Waters XBridgeTM BEH300 C18 10 мкм и потока 40 мл/мин.
В колонку загружали не более 12 мл смеси. Элюирование осуществляли с использованием линейного градиента от 5% до 30% растворителя B (5 мин) с последующим линейным градиентом от 30% до 35% растворителя B (40 мин). Фракции, содержащие продукт 6d, соединяли и лиофилизировали. Чистота: 86% (215 нм).
Выход: 85,2 мг (19,2 мкмоль, начиная с 2,00 г смолы).
MS масса/заряд 1486,7=[M+3H]3+, (расчетное значение MW=4460,0 г/моль).
Пример 7 (Asn-линкер)
Синтез линкерного реагента 7f
Линкерный реагент 7f синтезировали в соответствии со следующей схемой:
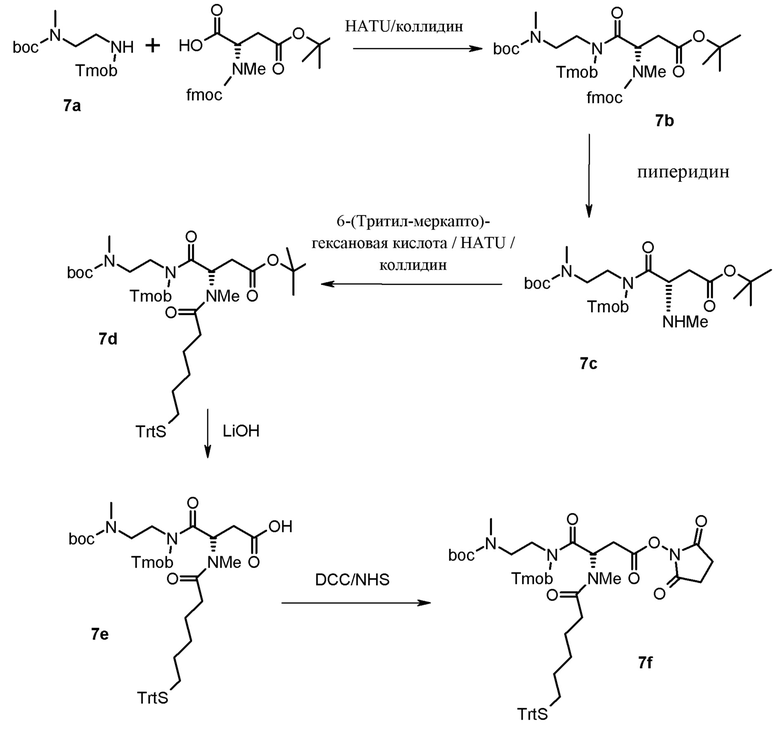
К охлажденному (0°C) раствору N-метил-N-boc-этилендиамина (0,5 мл, 2,79 ммоль) и NaCNBH3 (140 мг, 2,23 ммоль) в MeOH (10 мл) и уксусной кислоте (0,5 мл) добавляли раствор 2,4,6-триметоксибензальдегида (0,547 мг, 2,79 ммоль) в EtOH (10 мл). Смесь перемешивали при RT в течение 2 ч., подкисляли с помощью 2 M HCl (1 мл) и нейтрализовали с помощью насыщенного водного раствора Na2CO3 (50 мл). Выпаривание всех летучих веществ, экстракция DCM из полученной водной суспензии и концентрирование органических фракций давали на выходе N-метил-N-boc-N'-tmob-этилендиамин (7a) в виде неочищенного масла, которое очищали посредством RP-HPLC.
Выход: 593 мг (1,52 ммоль).
MS: масса/заряд 377,35=[M+Na]+, (расчетное значение=377,14).
N-Fmoc-N-Me-Asp(OtBu)-OH (225 мг, 0,529 ммоль) растворяли в DMF (3 мл) и 7a (300 мг, 0,847 ммоль), добавляли HATU (201 мг, 0,529 ммоль), и коллидин (0,48 мл, 3,70 ммоль). Смесь перемешивали при RT в течение 2 часов с получением 7b. Для снятия fmoc-защиты добавляли пиперидин (0,22 мл, 2,16 ммоль) и перемешивание продолжали в течение 1 ч. Добавляли уксусную кислоту (1 мл) и 7c очищали посредством RP-HLPC.
Выход: 285 мг (0,436 ммоль в виде соли TFA).
MS: масса/заряд 562,54=[M+Na]+, (расчетное значение=562,67).
6-Тритилмеркаптогексановую кислоту (0,847 г, 2,17 ммоль) растворяли в безводном DMF (7 мл). Добавляли HATU (0,825 г, 2,17 ммоль), и коллидин (0,8 мл, 6,1 ммоль), и 7c (0,78 г, 1,44 ммоль). Реакционную смесь перемешивали в течение 60 мин. при RT., подкисляли с помощью AcOH (1 мл) и очищали посредством RP-HPLC. Фракции продукта нейтрализовали с помощью насыщенного водного раствора NaHCO3 и концентрировали. Оставшуюся водную фазу экстрагировали с помощью DCM и 7d выделяли при выпаривании растворителя.
Выход: 1,4 г (94%).
MS: масса/заряд 934,7=[M+Na]+, (расчетное значение=934,5).
К раствору 7d (1,40 мг, 1,53 ммоль) в MeOH (12 мл) и H2O (2 мл) добавляли LiOH (250 мг, 10,4 ммоль) и реакционную смесь перемешивали в течение 14 ч. при 70°C. Смесь подкисляли с помощью AcOH (0,8 мл) и 7e очищали посредством RP-HPLC. Фракции продукта нейтрализовали с помощью насыщенного водного раствора NaHCO3 и концентрировали. Водную фазу экстрагировали с помощью DCM и 7e выделяли при выпаривании растворителя.
Выход: 780 мг (60%).
MS: масса/заряд 878,8=[M+Na]+, (расчетное значение=878,40).
К раствору 7e (170 мг, 0,198 ммоль) в безводном DCM (4 мл) добавляли DCC (123 мг, 0,59 ммоль) и N-гидрокси-сукцинимид (114 мг, 0,99 ммоль) и реакционную смесь перемешивали при RT в течение 1 ч. Смесь фильтровали, фильтрат подкисляли с помощью 0,5 мл AcOH и 7f очищали посредством RP-HPLC. Фракции продукта нейтрализовали с помощью насыщенного водного раствора NaHCO3 и концентрировали. Оставшуюся водную фазу экстрагировали с помощью DCM и 7f выделяли при выпаривании растворителя.
Выход: 154 мг (0,161 ммоль).
MS: масса/заряд 953,4=[M+H]+, (расчетное значение=953,43).
В качестве альтернативы, линкерный реагент 7f синтезировали в соответствии со следующей процедурой.
Альтернативная схема реакции:
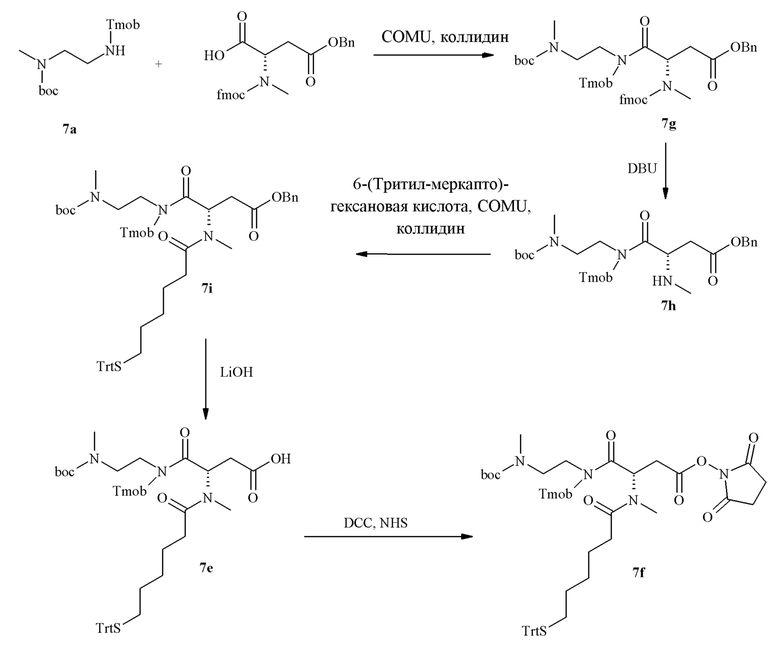
К раствору N-метил-N-boc-этилендиамина (2 г, 11,48 ммоль) и NaCNBH3 (819 мг, 12,63 ммоль) в MeOH (20 мл) порциями добавляли 2,4,6-триметоксибензальдегид (2,08 мг, 10,61 ммоль). Смесь перемешивали при RT в течение 90 мин, подкисляли с помощью 3 M HCl (4 мл) и дополнительно перемешивали в течение 15 мин. Реакционную смесь добавляли к насыщенному раствору NaHCO3 (200 мл) и экстрагировали 5 x с помощью CH2Cl2. Объединенные органические фазы высушивали над Na2SO4 и растворители выпаривали in vacuo. Полученный в результате N-метил-N-boc-N'-tmob-этилендиамин (7a) полностью высушивали в высоком вакууме и применяли на следующей стадии реакции без дополнительной очистки.
Выход: 3,76 г (11,48 ммоль, чистота 89%, 7a: дважды Tmob-защищенный продукт=8:1).
MS: масса/заряд 355,22=[M+H]+, (расчетное значение=354,21).
К раствору 7a (2 г, 5,65 ммоль) в CH2Cl2 (24 мл) добавляли COMU (4,84 г, 11,3 ммоль), N-Fmoc-N-Me-Asp(OBn)-OH (2,08 г, 4,52 ммоль) и коллидин (2,65 мл, 20,34 ммоль). Реакционную смесь перемешивали в течение 3 ч. при RT, разбавляли CH2Cl2 (250 мл) и промывали 3 x с помощью 0,1 M H2SO4 (100 мл) и 3 x с помощью солевого раствора (100 мл). Водные фазы повторно экстрагировали с помощью CH2Cl2 (100 мл). Объединенные органические фазы высушивали над Na2SO4, фильтровали и остаток концентрировали до объема 24 мл. Очищали 7g с применением флэш-хроматографии.
Выход: 5,31 г (148%, 6,66 ммоль).
MS: масса/заряд 796,38=[M+H]+, (расчетное значение=795,37).
К раствору 7g [5,31 г, макс. 4,51 ммоль относительно N-Fmoc-N-Me-Asp(OBn)-OH] в THF (60 мл) добавляли DBU (1,8 мл, 3% об./об.). Раствор перемешивали в течение 12 мин. при RT, разбавляли CH2Cl2 (400 мл) и промывали 3 x с помощью 0,1 M H2SO4 (150 мл) и 3 x с помощью солевого раствора (150 мл). Водные фазы повторно экстрагировали с помощью CH2Cl2 (100 мл). Объединенные органические фазы сушили над Na2SO4 и фильтровали. 7h выделяли при выпаривании растворителя и применяли на следующей стадии без дополнительной очистки.
MS: масса/заряд 574,31=[M+H]+, (расчетное значение=573,30).
7h (5,31 г, 4,51 ммоль, неочищенный) растворяли в ацетонитриле (26 мл) и COMU (3,87 г, 9,04 ммоль), добавляли 6-тритилмеркаптогексановую кислоту (2,12 г, 5,42 ммоль) и коллидин (2,35 мл, 18,08 ммоль). Реакционную смесь перемешивали в течение 4 ч. при RT, разбавляли CH2Cl2 (400 мл) и промывали 3 x с помощью 0,1 M H2SO4 (100 мл) и 3 x с помощью солевого раствора (100 мл). Водные фазы повторно экстрагировали с помощью CH2Cl2 (100 мл). Объединенные органические фазы высушивали над Na2SO4, фильтровали и 7i выделяли при выпаривании растворителя. Продукт 7i очищали с применением флэш-хроматографии.
Выход: 2,63 г (62%, чистота 94%).
MS: масса/заряд 856,41=[M+H]+, (расчетное значение=855,41).
К раствору 7i (2,63 г, 2,78 ммоль) в i-PrOH (33 мл) и H2O (11 мл) добавляли LiOH (267 мг, 11,12 ммоль) и реакционную смесь перемешивали в течение 70 мин. при RT. Смесь разбавляли CH2Cl2 (200 мл) и промывали 3x с помощью 0,1 M H2SO4 (50 мл) и 3x с помощью солевого раствора (50 мл). Водные фазы повторно экстрагировали с помощью CH2Cl2 (100 мл). Объединенные органические фазы высушивали над Na2SO4, фильтровали и 7e выделяли при выпаривании растворителя. 7j очищали с применением флэш-хроматографии.
Выход: 2,1 г (88%).
MS: масса/заряд 878,4=[M+Na]+, (расчетное значение=878,40).
К раствору 7e (170 мг, 0,198 ммоль) в безводном DCM (4 мл) добавляли DCC (123 мг, 0,59 ммоль) и каталитическое количество DMAP. Через 5 мин. добавляли N-гидрокси-сукцинимид (114 мг, 0,99 ммоль) и реакционную смесь перемешивали при RT в течение 1 ч. Реакционную смесь фильтровали, растворитель удаляли in vacuo и остаток помещали в 90% ацетонитрил плюс 0,1% TFA (3,4 мл). Неочищенную смесь очищали посредством RP-HPLC. Фракции продукта нейтрализовали с помощью 0,5 M фосфатного буфера, pH 7,4, и концентрировали. Оставшуюся водную фазу экстрагировали с помощью DCM и 7f выделяли при выпаривании растворителя.
Выход: 154 мг (81%).
MS: масса/заряд 953,4=[M+H]+, (расчетное значение=953,43).
Пример 8
Синтез линкерного реагента 8e
Линкерный реагент 8e синтезировали в соответствии со следующей схемой:
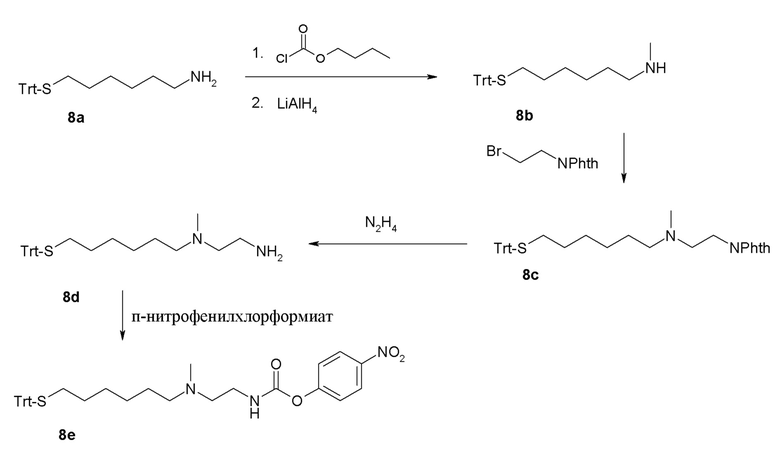
Синтез промежуточного соединения линкерного реагента 8b осуществляли в атмосфере азота. Раствор амина 8a (1,69 г, 4,5 ммоль, для получения см. WO-A 2009/133137) в 30 мл THF (сухой, молекулярное сито) охлаждали до 0°C. Добавляли бутилхлорформиат (630 мкл, 4,95 ммоль) в 3 мл THF (сухой, молекулярное сито) и DIPEA (980 мкл, 5,63 ммоль). Смесь перемешивали в течение 10 мин. при 0°C, охлаждение прекращали и смесь перемешивали в течение дополнительных 20 мин при RT. Добавляли 1 M LiAlH4 в THF (9 мл, 9 ммоль) и смесь нагревали с обратным холодильником в течение 1,5 ч. Реакцию гасили путем медленного добавления метанола (11 мл) и 100 мл насыщ. раствора Na/K тартрата. Смесь экстрагировали с помощью этилацетата, органический слой высушивали над Na2SO4 и растворитель выпаривали при пониженном давлении. Неочищенный продукт 8b (1,97 г) применяли на следующей стадии без дополнительной очистки.
MS: масса/заряд 390,2=[M+H]+ (расчетное значение MW=389,6).
Раствор неочищенного продукта 8b (1,97 г), N-(бромэтил)-фталимид (1,43 г, 5,63 ммоль) и K2CO3 (1,24 г, 9,0 ммоль) в 120 мл ацетонитрила нагревали с обратным холодильником в течение 6 ч. Добавляли 60 мл насыщ. раствора NaHCO3 и смесь экстрагировали 3 x с помощью этилацетата. Объединенные органические вещества высушивали (Na2SO4) и растворитель удаляли при пониженном давлении. Фталимид 8c очищали на диоксиде кремния с использованием гептана (содержащего 0,02% NEt3) и возрастающего количества этилацетата (содержащего 0,02% NEt3) в качестве элюентов.
Выход: 0,82 г (1,46 ммоль).
MS: масса/заряд 563,3=[M+H]+ (расчетное значение MW=562,8).
Фталимид 8c (819 мг, 1,46 ммоль) растворяли в 35 мл этанола и добавляли гидразина гидрат (176 мкл, 3,64 ммоль). Смесь нагревали с обратным холодильником в течение 3 ч. Осадок отфильтровывали. Растворитель удаляли при пониженном давлении и остаток обрабатывали с помощью 15 мл дихлорметана. Осадок отфильтровывали и дихлорметан удаляли при пониженном давлении. Остаток очищали посредством RP HPLC. pH соединенных HPLC-фракций регулировали до 7 путем добавления NaHCO3 и экстрагировали несколько раз с помощью дихлорметана. Объединенные органические вещества высушивали (Na2SO4) и растворитель удаляли при пониженном давлении с получением амина 8d.
Выход: 579 мг (1,34 ммоль).
MS: масса/заряд 433,3=[M+H]+ (расчетное значение MW=432,7).
Пара-нитрофенилхлорформиат (483 мг, 2,40 ммоль) растворяли в 10 мл дихлорметана (сухой, молекулярное сито). Добавляли раствор амина 8d (1,00 г, 2,31 ммоль) в 5 мл дихлорметана (сухой, молекулярное сито) и 1,8 мл сим-коллидина и смесь перемешивали при комнатной температуре в течение 40 мин. Дихлорметан удаляли при пониженном давлении, остаток подкисляли уксусной кислотой и очищали посредством RP-HPLC с получением пара-нитрофенилкарбамата 8e.
Выход: 339 мг (0,57 ммоль).
MS: масса/заряд 598,3=[M+H]+ (расчетное значение MW=597,8).
Синтез полимерных конъюгатов пептида и линкера
Пример 9
Синтез тиольного линкера 1 агониста GLP/глюкагона проводили в соответствии со следующей схемой:
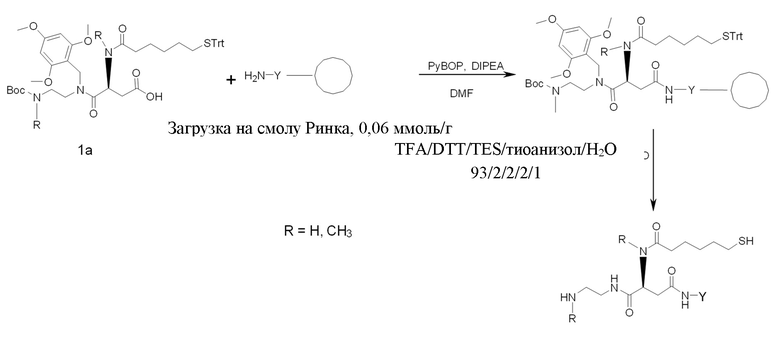
К 400 мг связанного со смолой Fmoc-защищенного эксендина-4 под Seq. ID 26 на смоле Ринка в сосуде для пептидного синтеза добавляли 4 мл 20% пиперидина в DMF и реакционную смесь перемешивали в течение 5 минут. Процесс повторяли трижды. Связанный со смолой пептид затем трижды промывали 4 мл DMF.
К 80 мг (2,5 экв.) линкера 1a и 60 мг (3,0 экв.) PyBOP добавляли 5 мл безводного DMF. К данному раствору добавляли 16 мкл (3,0 экв.) диизопропилдиэтиламина (DIPEA). Полученный в результате раствор добавляли к обработанной ранее смоле на основе связанного со смолой эксендина-4 под Seq ID. 3126. Реакцию в смеси продолжали в течение 18 ч. при 25°C. По истечении этого времени смолу фильтровали и промывали безводным DMF (5 мл x 5), дихлорметаном (5 мл x 5), изопропанолом (5 мл x 5) и диэтиловым эфиром (5 мл x 5).
Вышеприведенный конъюгат связанного со смолой пептида и линкера обрабатывали с помощью 10 мл раствора, содержащего трифторуксусную кислоту (TFA)/триэтилсилан (TES)/дитиотреитол (DTT)/тиоанизол/воду (100/2/3/1/2). Реакционную смесь встряхивали при 25°C в течение 3 ч. В конце реакции растворитель отфильтровывали и смолу промывали дихлорметаном (5×10 мл). Фильтрат концентрировали при пониженном давлении. Остаток выливали в 50 мл ледяного простого эфира. Осаждением отделяли белое твердое вещество. Смесь центрифугировали и декантировали. Твердое вещество промывали диэтиловым эфиром (2×20 мл). Пептид-линкер очищали посредством обращенно-фазовой HPLC (колонка 30×100 мм C18, 25-40% AcCN/H2O w/0,1% TFA в течение 20 мин). Соответствующие фракции собирали и выпаривали до сухости с получением 16 мг необходимого продукта в виде белого твердого вещества. Продукт определяли путем масс-спектрометрии (молекулярный ионный пик, масса/заряд 1469, z=3).
Пример 10
Тиольный линкер 2 GLP/глюкагона синтезировали в соответствии со следующей схемой:
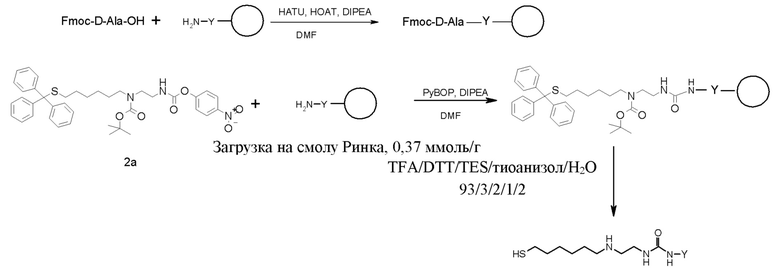
К 1,8 г связанного со смолой Fmoc-защищенного эксендина-4 под Seq ID. 26 на смоле Ринка в сосуде для пептидного синтеза добавляли 20 мл 20% пиперидина в DMF и реакционную смесь перемешивали в течение 5 минут. Процесс повторяли трижды. Связанный со смолой пептид затем трижды промывали 20 мл DMF.
К 163 мг (2,5 экв.) Fmoc-D-Ala-OH, 199 мг (2,5 экв.) HATU и 71 мг (2,5 экв.) HOAt добавляли 15 мл безводного DMF. К данному раствору добавляли 92 мкл (2,5 экв.) диизопропилдиэтиламина (DIPEA). Полученный в результате раствор добавляли к обработанной ранее смоле на основе связанного со смолой эксендина-4 под Seq ID. 26. Реакцию в смеси продолжали в течение 16 ч. при 25°C. По истечении этого времени смолу фильтровали и промывали безводным DMF (20 мл x 5), дихлорметаном (20 мл x 5), изопропанолом (20 мл x 5) и диэтиловым эфиром (20 мл x 5).
К приведенному выше связанному со смолой Fmoc-защищенному D-Ala-эксендину-4 под Seq ID. 26 на смоле Ринка в сосуде для пептидного синтеза добавляли 15 мл 20% пиперидина в DMF и реакционную смесь перемешивали в течение 5 минут. Процесс повторяли трижды. Связанный со смолой пептид затем трижды промывали 15 мл DMF.
К 352 мг (2,5 экв.) линкера 2a добавляли 15 мл безводного DMF. К данному раствору добавляли 92 мкл (2,5 экв.) диизопропилдиэтиламина (DIPEA). Полученный в результате раствор добавляли к обработанной ранее смоле на основе связанного со смолой D-Ala-эксендина-4 под Seq ID. 26. Реакцию в смеси продолжали в течение 16 ч. при 25°C. По истечении этого времени смолу фильтровали и промывали безводным DMF (15 мл x 5), дихлорметаном (15 мл x 5), изопропанолом (15 мл x 5) и диэтиловым эфиром (15 мл x 5).
Приведенный выше конъюгат связанного со смолой пептида и линкера обрабатывали с помощью 40 мл раствора, содержащего трифторуксусную кислоту (TFA)/триэтилсилан (TES)/дитиотреитол (DTT)/тиоанизол/воду (100/2/3/1/2). Реакционную смесь встряхивали при 25°C в течение 1 ч. В конце реакции растворитель отфильтровывали. Фильтрат выливали в 400 мл ледяного простого эфира. Осаждением отделяли белое твердое вещество. Смесь центрифугировали и декантировали. Твердое вещество промывали диэтиловым эфиром (2 X 200 мл). Пептид-линкер очищали посредством обращенно-фазовой HPLC (колонка 30×100 мм C18, 25-40% AcCN/H2O w/0,1% TFA в течение 20 мин). Соответствующие фракции собирали и выпаривали до сухости с получением 104 мг необходимого продукта в виде белого твердого вещества. Продукт определяли путем масс-спектрометрии (молекулярный ионный пик, масса/заряд 1465,3, z=3 и масса/заряд 1099,2, z=4).
Синтез гидрогелей на основе гиалуроновой кислоты
Пример 11.
Сшитую дивинилсульфоном гиалуроновую кислоту синтезировали в соответствии со следующей схемой:
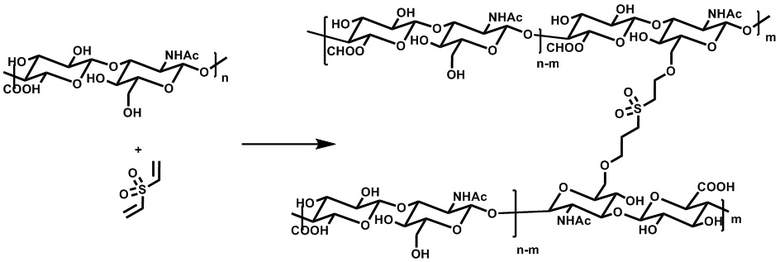
Пример 11a
К 0,2 M гидроксида натрия (168,9 г) добавляли хлорид натрия (23,4 г) при перемешивании до растворения. К раствору при быстром механическом перемешивании добавляли гиалуронат натрия (25,4 г, 400-500 кДа) и так продолжали в течение 2 ч. Полученный в результате раствор полимера имел концентрацию ~ 12% вес/вес. Готовили раствор дивинилсульфона (0,41 мл, 0,48 г) в изопропаноле (1,6 мл) и добавляли (5×0,4 мл) в течение ~ 30 с. Смесь перемешивали в течение дополнительных 2 мин, выливали в 23×28×6,5 см стеклянную кювету и закрывали пластиковой крышкой. После отстаивания при RT в течение 4 ч. гель переносили как единое целое к раствору 1 M хлористоводородной кислоты (100,1 г) в 0,9% солевом растворе (3 кг). Его аккуратно перемешивали при RT. Через 24 ч. pH раствора составлял 2,28. Раствор сливали, оставляя гель (416,2 г). Затем к гелю добавляли 0,9% солевой раствор (3 кг) и его аккуратно перемешивали при RT в течение 18 ч. К смеси добавляли 1 M гидроксид натрия (9,7 мл) через 0, 2, 4, 6 и 8 ч. Гель аккуратно перемешивали в течение еще 24 ч. при RT, во время чего pH геля составлял 6,65. Гель хранили при 2-8°C в течение 120 ч., а затем добавляли 10 мМ раствор фосфата натрия с pH 7,4 (2 л). Гель перемешивали в течение дополнительных 21 ч. и смывы сливали, оставляя гель (1036,2 г) с конечной концентрацией полимера 2,4%.
Пример 11b. Альтернативный синтез сшитой дивинилсульфоном гиалуроновой кислоты
К 35 г гиалуроната натрия добавляли 946 мл стерильной воды. Реакционную смесь выдерживали при 2-8°C в течение 7 дней, и в течение этого времени образовывался прозрачный раствор. К данному раствору добавляли 1 M 111 мл 1,0 M раствора гидроксида натрия и полученную в результате реакционную смесь энергично перемешивали в течение 5 мин. Реакционную смесь выдерживали при 2-8°C в течение 90 мин. Затем суспензию 6,7 мл дивинилсульфона в 10 мл стерильной воды добавляли к раствору полимера и полученную в результате реакционную смесь энергично перемешивали в течение 5 минут. Затем реакционную смесь хранили при 2-8°C в течение 150 минут, а затем в течение 90 минут при 25°C. Полимерный гель, образованный таким образом, промывали с помощью 0,9% стерильного солевого раствора в течение четырех дней. pH суспензии регулировали до 7,0 с помощью либо 1 M NaOH, либо 1,0 M HCl. Конечная концентрация гелевой суспензии составляла 0,58%.
Пример 12
Синтез 1-(трет-бутоксикарбонил)амино-3-(3-малеимидопропил)аминопропана.
В 250 мл круглодонную колбу отбирали 3,0 г 1-(трет-бутоксикарбонил)амино-3-аминопропана и 100 мл безводного хлороформа. Реакционную смесь перемешивали при 25°C, пока раствор не станет прозрачным. К данному раствору добавляли N-сукцинимидил-3-малеимидопропионат (5,05 г) при перемешивании до растворения, а затем 3,42 мл диизопропилэтиламина. Полученную в результате реакционную смесь перемешивали при 25°C в течение 18 ч. Раствор промывали с помощью 1 M хлористоводородной кислоты (50 мл), 10% солевого раствора (50 мл), насыщенного раствора бикарбоната натрия (50 мл), полунасыщенного солевого раствора (50 мл). Органическую фазу выделяли и высушивали над безводным сульфатом натрия. После удаления сульфата натрия посредством фильтрации, раствор концентрировали при пониженном давлении и остаток очищали посредством колоночной хроматографии на силикагеле с применением градиента этилацетат:гексаны в качестве подвижной фазы. Удаление растворителя при пониженном давлении с последующим высушиванием в вакууме обеспечивало необходимый продукт в виде грязно-белого твердого вещества (4,03 г).
Пример 13.
Синтез 1-(трет-бутилоксикарбонил)амино-8-(3-малеимидопропил)амино-3,6-диоксаоктана.
В 100 мл круглодонную колбу отбирали 1-(трет-бутилоксикарбонил)амино-8-амино-3,6-диоксаоктан (1,007 г) и 25 мл безводного ацетонитрила (25 мл). Реакционную смесь перемешивали в атмосфере азота до растворения. К данному раствору добавляли N-сукцинимидил-3-малеимидопропионат (1,302 г) и реакционную смесь перемешивали в атмосфере азота при 25°C в течение 6 ч. По истечению данного времени растворитель удаляли при пониженном давлении. Остаток очищали посредством колоночной хроматографии на силикагеле с использованием дихлорметана, содержащего 2-6% метанола. После удаления растворителя при пониженном давлении и высушивания остатка в вакууме получали 1,08 г необходимого продукта в виде грязно-белого твердого вещества.
Пример 14.
Синтез 3-(3-малеимидо-пропил)аминопропан-функционализированной гиалуроновой кислоты.
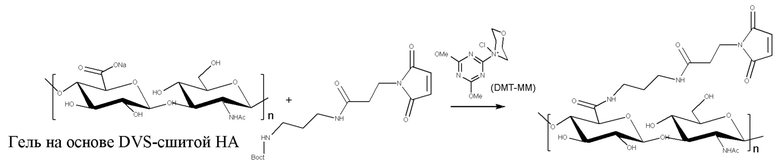
К 15 г сшитой дивинилсульфоном суспензии (пример 1) добавляли 45 мл деионизированной (DI) воды и полученную в результате суспензию перемешивали при 25°C в течение 10 минут. После добавления 45 мл этанола к суспензии ее перемешивали в течение дополнительных 60 мин. За этим следовало добавление 60 мл этанола и перемешивание в течение 10 минут. К данной суспензии добавляли 0,24 г 4-(4,6-диметокси-1,3,5-триазин-2-ил)-4-метилморфолиния хлорид (DMT-MM), растворенный в 5 мл этанола. Полученную в результате реакционную смесь перемешивали при 25°C в течение 60 мин. К 70 мг 1-(трет-бутоксикарбонил)амино-3-(3-малеимидопропил)аминопропана (пример 2), растворенного в 2 мл безводного дихлорметана, добавляли 2 мл трифторуксусной кислоты. Полученную в результате реакционную смесь перемешивали при комнатной температуре в течение 2 часов. Раствор концентрировали при пониженном давлении. Полученный в результате остаток обрабатывали 3 мл метанола и выпаривали до сухости. После повторения данного процесса еще один раз, остаток растворяли в этаноле (5 мл) и pH регулировали до 6-6,5 с помощью 10% N-метилморфолина в этаноле. Полученный в результате раствор добавляли к приведенной выше суспензии на основе гиалуроновой кислоты. Флакон ополаскивали этанолом (5 мл) и добавляли к взвеси. После перемешивания в течение 18 ч. при 25°C к реакционной смеси добавляли насыщенный солевой раствор (2 мл). Суспензию обрабатывали этанолом (3×30 мл, 2×15 мл) для осаждения полимерного геля. Реакционную смесь центрифугировали при 4000 об/мин и надосадочную жидкость декантировали. Остаток гидратировали в DI воде (20 мл) в течение ~ 20 мин. и осаждали из этанола (4×10 мл). Способ исследования на глюкозамин предполагает, что степень замещения составляет 19 мол. %.
Пример 15.
Синтез 3-(3-малеимидо-пропил)аминопропан-функционализированной гиалуроновой кислоты.
К 20 г сшитой дивинилсульфоном суспензии (пример 1) добавляли 60 мл деионизированной (DI) воды и полученную в результате суспензию перемешивали при 25°C в течение 10 минут. После добавления 60 мл этанола к суспензии ее перемешивали в течение дополнительных 60 мин. За этим следовало добавление 60 мл этанола и перемешивание в течение 10 минут. К данной суспензии добавляли 0,325 г DMT-MM, растворенного в 10 мл этанола. Полученную в результате реакционную смесь перемешивали при 25°C в течение 60 мин. К 0,38 г 1-(трет-бутоксикарбонил)амино-3-(3-малеимидопропил)аминопропана (пример 2), растворенного в 2,5 мл безводного дихлорметана, добавляли 2,5 мл трифторуксусной кислоты. Полученную в результате реакционную смесь перемешивали при комнатной температуре в течение 2 часов. Раствор концентрировали при пониженном давлении. Полученный в результате остаток обрабатывали 3 мл метанола и выпаривали до сухости. После повторения данного процесса еще один раз, остаток растворяли в этаноле (5 мл) и pH регулировали до 6-6,5 с помощью 10% N-метилморфолина в этаноле. Полученный в результате раствор добавляли к приведенной выше суспензии на основе гиалуроновой кислоты. Флакон ополаскивали этанолом (5 мл) и добавляли к взвеси. После перемешивания в течение 18 ч. при 25°C к реакционной смеси добавляли насыщенный солевой раствор (2 мл). Суспензию обрабатывали этанолом (3×30 мл, 2×15 мл) для осаждения полимерного геля. Реакционную смесь центрифугировали при 4000 об/мин и надосадочную жидкость декантировали. Остаток гидратировали в DI воде (20 мл) в течение ~ 20 мин. и осаждали из этанола (4×10 мл). Способ исследования на глюкозамин предполагает, что степень замещения составляет 24 мол. %.
Пример 16a
Общий способ синтеза гидрогеля на основе 3-(3-малеимидо-пропил)аминопропан-функционализированной HA
К соответствующему количеству суспензии на основе сшитой дивинилсульфоном HA (пример 11b) добавляли стерильный солевой раствор с получением геля с концентрацией ~1% вес/об. Полученную в результате суспензию перемешивали при 25°C в течение 15-30 минут. Смешиваемый с водой органический растворитель (предпочтительно этанол) добавляли к суспензии и полученную в результате суспензию перемешивали в течение дополнительных 30-60 мин. К данной суспензии добавляли соответствующее количество этанольного раствора 4-(4,6-диметокси-1,3,5-триазин-2-ил)-4-метилморфолиния хлорида (DMT-MM). Контейнер, содержащий раствор DMT-MM, дважды ополаскивали этанолом и смывы добавляли к вышеупомянутой суспензии. Полученную в результате реакционную смесь перемешивали при 25°C в течение 90 минут. Соответствующее количество 1-(трет-бутоксикарбонил)амино-3-(3-малеимидопропил)аминопропана растворяли в дихлорметане. К данному раствору добавляли трифторуксусную кислоту с получением раствора 1:1 (об./об.). После перемешивания при комнатной температуре в течение 60-90 минут, реакционную смесь выпаривали до сухости при пониженном давлении. Остаток растворяли в этаноле и добавляли к вышеприведенной суспензии. Контейнер, содержащий производное малеимида, дважды ополаскивали этанолом и смывы добавляли к суспензии. pH суспензии регулировали до pH 6,4-6,6 с использованием органического или неорганического основания (например, 10% N-метилморфолина в этаноле). После перемешивания в течение 16-20 ч. при 25°C суспензию обрабатывали этанолом до объема 60-65% об./об. Растворитель удаляли из реакционной смеси либо путем центрифугирования при 120 G с последующим декантированием надосадочной жидкости, либо путем применения небольшого избыточного давления газа N2 к системе и фильтрования через стеклянную фритту или мембрану фильтра. Затем остаток обрабатывали стерильным 20 мМ сукцинатным солевым раствором (0,9%) с pH 3,8 в течение ~ 15-20 мин. и осаждали путем добавления этанола до объема 60-65% об./об. Растворитель удаляли из реакционной смеси посредством приведенной выше процедуры. Данную процедуру повторяли еще один раз.
Пример 16b
Синтез гидрогелей на основе 3-(3-малеимидо-пропил)аминопропан-функционализированной HA со степенью замещения 20 мол. %.
К 5,65 г суспензии гидрогеля на основе HA (пример 11b) добавляли 7,5 мл стерильного солевого раствора и полученную в результате суспензию аккуратно перемешивали в течение 15 минут. К данной суспензии добавляли 3 мл этанола и полученную в результате реакционную смесь аккуратно перемешивали в течение 60 мин. К данной суспензии добавляли 94 мг DMT-MM, растворенного в 3 мл этанола. Флакон, содержащий DMT-MM, промывали этанолом (2×1 мл) и смывы добавляли к суспензии. Реакционную смесь оставляли аккуратно перемешиваться при температуре окружающей среды в течение 90 минут. К 21,7 мг 1-(трет-бутоксикарбонил)амино-3-(3-малеимидопропил)аминопропана добавляли 0,25 мл дихлорметана и реакционную смесь аккуратно смешивали, пока раствор не станет прозрачным. К данному раствору добавляли 0,25 мл трифторуксусной кислоты и аккуратно смешивали при температуре окружающей среды в течение 75 мин. Затем раствор выпаривали до сухости. Остаток растворяли в 3 мл этанола и полученный в результате раствор добавляли к вышеприведенной суспензии гидрогеля. Флакон, содержащий малеимидный реагент, промывали этанолом (2×1 мл) и смывы добавляли к реакционной смеси. pH реакционной смеси затем регулировали до 6,41 с использованием 10% об./об. N-метилморфолина в этаноле и полученную в результате реакционную смесь аккуратно встряхивали в течение 18 часов при температуре окружающей среды. По истечению данного времени pH реакционной смеси регулировали до pH 3,89 путем обработки 1,0 M HCl. Гель осаждали путем добавления этанола (4×3,5 мл). Суспензию центрифугировали при 120 G в течение 2 мин. при 20°C и надосадочную жидкость осторожно удаляли с использованием пипетки. Остаток повторно гидратировали в 12 мл 20,0 мМ SBS-буфера (pH 3,8) путем аккуратного встряхивания/смешивания в течение 15 минут. Суспензию подвергали дополнительной обработке этанолом (4×5 мл, 1×4 мл). После каждой обработки этанолом суспензию центрифугировали при 120 G в течение 2 мин. при 20°C с последующим осторожным удалением надосадочной жидкости. В заключение флакон переворачивали, оставляли для слива на 15 минут и надосадочную жидкость декантировали с получением 0,8876 г влажного геля.
Пример 16c
Синтез 3-(3-малеимидо-пропил)аминопропан-функционализированной гиалуроновой кислоты.
К 10 г сшитой дивинилсульфоном суспензии (пример 11а) добавляли 40 мл деионизированной (DI) воды и полученную в результате суспензию перемешивали при 25°C в течение 10 минут. После добавления 30 мл этанола к суспензии ее перемешивали в течение дополнительных 60 минут. За этим следовало добавление 60 мл этанола и перемешиванием в течение 10 минут. К данной суспензии добавляли 0,162 г DMT-MM, растворенного в 7,5 мл этанола. Полученную в результате реакционную смесь перемешивали при 25°C в течение 60 мин. К 29 мг 1-(трет-бутоксикарбонил)амино-3-(3-малеимидопропил)аминопропана (пример 2), растворенного в 0,5 мл безводного дихлорметана, добавляли 0,5 мл трифторуксусной кислоты. Полученную в результате реакционную смесь перемешивали при комнатной температуре в течение 2 часов. Раствор концентрировали при пониженном давлении. Полученный в результате остаток обрабатывали 2 мл метанола и выпаривали до сухости. После повторения данного процесса еще один раз, остаток растворяли в этаноле (7,5 мл) и 9,5 мкл N-метилморфолина. Раствор добавляли к вышеприведенной суспензии на основе гиалуроновой кислоты и pH регулировали до 7,1 с помощью N-метилморфолина. Флакон ополаскивали этанолом (5 мл) и добавляли к взвеси. После перемешивания в течение 21 ч. при 25°C добавляли насыщенный солевой раствор (2 мл) и гель осаждали путем добавления этанола (4×15 мл). Взвесь оставляли для осаждения в течение 15 мин. и надосадочную жидкость декантировали. Гидрогель гидратировали в 20 мМ PBS с pH 5 (35 мл) и осаждали путем добавления этанола (5×15 мл). Процесс повторяли, образец центрифугировали при 2500 об/мин в течение 1,5 мин. и надосадочную жидкость декантировали. Способ исследования на глюкозамин предполагает, что степень замещения составляет 24 мол. %.
Пример 17
Синтез 8-(3-малеимидопропил)амино-3,6-диоксаоктан-функционализированной гиалуроновой кислоты.
В 250 мл круглодонную колбу отбирали 0,5 г лиофилизированной HA (пример 11a) и 50 мл 0,9% солевого раствора. Реакционную смесь оставляли аккуратно перемешиваться при 25°C в течение одного часа. К данной суспензии добавляли 40 мл этанола и суспензию перемешивали в течение 5 мин. В 10 мл флакон отбирали 0,35 г DMT-MM и 5 мл этанола. Раствор добавляли к суспензии на основе HA. Флакон промывали 5 мл этанола и добавляли к суспензии. Полученную в результате реакционную смесь перемешивали при 25°C в течение 1 ч. Затем добавляли туда 86 мг 1-(трет-бутилоксикарбонил)амино-8-(3-малеимидопропил)амино-3,6-диоксаоктана, растворенного в 0,5 мл безводного дихлорметана и обработанного 0,5 мл трифторуксусной кислоты. Раствор перемешивали при комнатной температуре в течение 1 ч. Раствор концентрировали при пониженном давлении, растворяли в 2 мл этанола и выпаривали до сухости при пониженном давлении. Обработку этанолом повторяли дважды. Остаток растворяли в 5 мл этанола/воды (1:1) и pH раствора регулировали до 6,5 с использованием N-метилморфолина (60 мкл). Полученный в результате раствор добавляли к вышеприведенной суспензии. После перемешивания в течение 4 ч. при 25°C, pH суспензии регулировали до 3,75 с помощью 0,1 M HCl и гель осаждали путем добавления этанола (7×25 мл). Взвесь оставляли для осаждения в течение 30 мин. и 80% надосадочной жидкости удаляли декантированием. Оставшуюся суспензию центрифугировали при 1500 об/мин в течение 5 мин. После удаления растворителя остаток обрабатывали 0,9% солевым раствором и осаждали из этанола (7×15 мл). Остаток высушивали посредством лиофилизации. Степень замещения, определяемая посредством анализа на глюкозамин, оказалась равной 7,3 мол.%.
Пример 18
Синтез гиалуроновой кислоты, содержащей группу 2-пиридилдитиола.
К быстро перемешиваемому раствору 200 мг гиалуроната натрия (молекулярный вес=500 кДа), растворенного в 24 мл деионизированной воды, по капле добавляли 16 мл ацетонитрила. После завершения добавления ацетонитрила, к реакционной смеси добавляли 17,6 мг хлордиметокситриазина в 2 мл воды/ацетонитрила (1:1), а затем 20μл N-метилморфолина. Реакционную смесь перемешивали при 25°C в течение 1 ч. Затем добавляли 26,8 мг 2-((3-нитропиридин-2-ил)тио)этанимина гидрохлорида, растворенного в 1 мл деионизированной воды. Реакционную смесь оставляли перемешиваться в течение 18 ч. pH реакционной смеси доводили до 6,0 путем добавления 1 М HCl. К полученной в результате реакционной смеси добавляли 15 мл предварительно промытого Amberlite® CG-120 (Na+ форма) и реакционную смесь перемешивали в течение 20 минут. Смолу отфильтровывали и промывали деионизированной водой (2×5 мл). Процесс обработки с помощью Amberlite® CG-120 (Na+ форма) повторяли дважды. Раствор разбавляли водой с образованием раствора, содержащего 20 об. % ацетонитрила. Раствор фильтровали с помощью вращающегося фильтра с использованием центрифужных устройств Macrosep® (отсечение по молекулярной массе 30K). Ретентат промывали деионизированной водой (5×200 мл). Ретентаты объединяли и лиофилизировали с получением 120 мг продукта в виде грязно-белого твердого вещества. Степень модификации составляла 10%. Другую гиалуроновую кислоту, содержащую группу 2-пиридилдитиола, синтезировали с использованием гиалуроната натрия с молекулярным весом 70 кДа, следуя подобной процедуре.
Пример 19.
Синтез растворимой малеимид-функционализированной HA
В 100 мл колбу отбирали 200 мг гиалуроновой кислоты, натриевой соли (мол. вес=500 кДа) и 24 мл DI воды. Смесь перемешивали, пока раствор не станет прозрачным. К быстро перемешиваемому раствору HA добавляли 16 мл этанола. 4-(4,6-Диметокси-1,3,5-триазин-2-ил)-4-метилморфолиния хлорид (55 мг, 0,2 ммоль) в воде/этаноле добавляли вместе с N-метилморфолином (20μмкл, 0,2 ммоль) и реакционную смесь перемешивали в течение одного часа. Добавляли водный раствор 1-(2-(2-аминоэтокси)этил)-1H-пиррол-2,5-дион⋅трифторацетатной соли (60 мг, 0,2 ммоль). Реакционную смесь оставляли на ночь. pH регулировали до слегка кислотного, добавляли к реакционной смеси предварительно промытый Amberlite® CG-120, Na+ форма (≥15 мл), и перемешивали в течение 20 минут. Смолу отфильтровывали и промывали водой. К фильтрату снова добавляли предварительно промытый Amberlite® CG-120, Na+ форма (≥15 мл), и следовали описанной выше процедуре. Весь цикл повторяли еще раз. Раствор разбавляли водой с получением водного раствора, содержащего <20% этанола. Раствор фильтровали с помощью вращающегося фильтра с использованием центрифужных устройств Macrosep® от PALL, отсечение по молекулярной массе 30K (5000 об/мин, время вращения 15 минут). Мембрану каждый раз очищали путем аккуратного удара по ней лопаткой и активного встряхивания закрытого устройства. Ретентат промывали несколько раз деионизированной водой (>200 мл). Полученные в результате концентраты модифицированной HA объединяли и лиофилизировали. Восстановление составляло 50-75%. Степень модификации составляла ~ 20% согласно ЯМР.
Пример 20
Оценка содержания малеимида в гидрогелях на основе гиалуроновой кислоты.
Оценку малеимидных групп, включенных в гидрогели на основе HA, осуществляли посредством способа колориметрического анализа. 5-Тио-2-нитробензойную кислоту получали посредством восстановления 5,5'-дитиобис-(2-нитробензойной кислоты) трис-(2-карбоксиэтил)фосфина гидрохлоридом (TCEP) в PBS-буфере с pH 7,5. Для предотвращения побочных реакций с TCEP применяли 20 мол.% избыток 5,5'-дитиобис-(2-нитробензойной кислоты). Предварительно определенное количество малеимид-функционализированного гидрогеля суспендировали в 20 мМ сукцинатном буферном растворе (SBS) с pH 3,5. Вышеприведенный раствор 5-тио-2-нитробензойной кислоты добавляли к суспензии гидрогеля и реакционную смесь смешивали интенсивным перемешиванием (2×10 секунд), а затем аккуратно перемешивали при 25°C в течение 45 мин. Затем суспензию центрифугировали при 25°C в течение 10 мин. и отбирали аликвоту надосадочной жидкости. Поглощающую способность надосадочной жидкости измеряли при 412 нм. Концентрацию 5-тио-2-нитробензойной кислоты в растворе оценивали с использованием калибровочной кривой. Концентрация малеимида в гидрогелях эквивалентна количеству молей тиола, вступивших в реакцию, при этом ее рассчитывают по разности между количеством добавленной 5-тио-2-нитробензойной кислоты и количеством, присутствующим в надосадочной жидкости.
Пример 21.
Синтез конъюгированного с флуоресцирующим в ближнем ИК-диапазоне красителем (IRDye800CW) гидрогеля на основе HA.
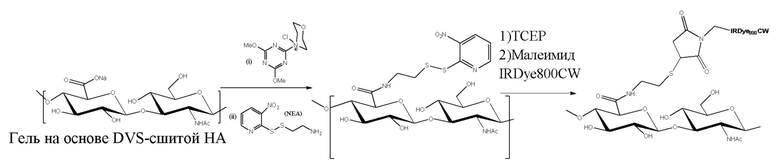
Пример 21 a. Синтез конъюгированной с 3-нитро-2-(2'-амино-этилдисульфанил)пиридина гидрохлоридом (NEA) сшитой дивинилсульфоном гиалуроновой кислоты.
Суспензию, содержащую 5,1 г (23 мг/г воды) гидрогеля на основе сшитой дивинилсульфоном гиалуроновой кислоты (пример 5) и 20 мл стерильной воды аккуратно перемешивали при 25°C в течение 15 мин. К данной суспензии добавляли этанол (20 мл) и полученную в результате реакционную смесь перемешивали при 25°C в течение одного часа. К данной суспензии добавляли 0,081 г DMT-MM, растворенного в 5 мл этанола. Флакон, содержащий раствор DMT-MM, промывали 2,5 мл этанола и смывы добавляли к суспензии. Реакционную смесь перемешивали при 25°C в течение 1 ч., а затем добавляли 0,017 г NEA. После перемешивания реакционной смеси в течение 22 ч. при 25°C к гелю добавляли 2 мл солевого раствора. Растворитель удаляли путем центрифугирования, остаток промывали посредством нескольких обработок этанолом (4×10 мл, 1×5 мл). Суспензию центрифугировали при 2500 об/мин в течение 5 мин, а затем при 5000 об/мин в течение 5 мин. (температуру центрифуги поддерживали на 5°C). Надосадочную жидкость декантировали и остаток оставляли для достижения равновесия на 20 мин. в стерильной воде (20 мл). Затем ее подвергали двум обработкам этанолом (4×10 мл). Суспензию оставляли для осаждения на 30 мин. и надосадочную жидкость декантировали. Процесс обработки этанолом повторяли еще раз и влажный гель хранили при 2°C до следующей стадии.
Пример 21b. Синтез гидрогеля на основе конъюгированной с NIR-красителем HA.
В асептических условиях отбирали 0,224 г NEA-модифицированной гиалуроновой кислоты (пример 15a) и 13 мл стерильной воды в 50 мл стерильный реакционный сосуд и обеспечивали аккуратное встряхивание смеси в течение 15 мин. при 25°C. К данной суспензии добавляли 20 мл этанола и суспензию перемешивали в течение 1 ч. при 25°C. Затем к суспензии добавляли 14 мг TCEP и реакционную смесь перемешивали в течение 16 ч. при 25°C. В конце реакции к реакционной смеси добавляли 2 мл солевого раствора. Затем гель подвергали 5 циклам обработки этанолом (5 мл) и центрифугированию (5000 об/мин, 5 мин, 5°C). После удаления надосадочной жидкости остаток обрабатывали 10 мл 0,9% стерильного солевого раствора, а затем следовало 5 циклов обработки этанолом (5 мл) и центрифугирование, как указано выше. Остаток суспендировали в 10 мл стерильного 0,9% солевого раствора. К данной суспензии добавляли 1,8 мг малеимид-функционализированного IRDye800CW, растворенного в стерильном 0,9% солевом растворе (3 мл), с использованием стерильного дегидрирующего фильтра. Фильтр промывали 5 мл этанола и смесью этанол/солевой раствор 1:1 (2×5 мл) и смывы добавляли к реакционной смеси. Реакционный сосуд аккуратно перемешивали в темноте в течение 2 ч. при 25°C и выдерживали при 2°C в течение 66 ч. Затем 11,5 мг N-метилмалеимида, растворенного в 3 мл этанола, добавляли к реакционной смеси и суспензию аккуратно встряхивали в течение дополнительных 3 ч при 25°C. В конце реакции суспензию центрифугировали (5000 об/мин, 5°C, 2×15 мин) и удаляли 20 мл надосадочной жидкости. Оставшуюся суспензию осаждали из этанола (5×5 мл), дополнительно центрифугировали (5000 об/мин, 5°C, 5 мин) и надосадочную жидкость декантировали. К остатку добавляли 10 мл 0,9% стерильного солевого раствора, а затем 5 мл этанола. Суспензию центрифугировали (5000 об/мин, 5 мин, 5°C) и надосадочную жидкость декантировали. Обработку этанолом и процесс центрифугирования повторяли еще 4 раза. Остаток обрабатывали 10 мл стерильного 0,9% солевого раствора и хранили при 2°C в темноте, обернув флакон алюминиевой фольгой.
Конъюгация линкерных тио-пептидов с гидрогелем на основе малеимид-функционализированной HA
Пример 22
Общая процедура для пептидов, несущих следовый линкер с концевой тиольной группой, и гидрогелей на основе малеимид-функционализированной HA.
В стерильный и депирогенизированный реактор с фриттой или фильтром средней пористости отбирали соответствующее количество гидрогеля на основе малеимид-модифицированной HA (примеры 6, 7 и 8). Затем соответствующее количество фильтрованного в стерильных условиях SB-буфера, 20 ммоль (содержащего 15% об./об. пропиленгликоля и 0,01% вес/об. Tween 20, pH 3,8), добавляли к реакционной смеси таким образом, чтобы концентрация полученной в результате суспензии составляла ~ 1% вес/вес. Суспензию оставляли смешиваться в течение 30-90 минут при аккуратном встряхивании. По истечению данного времени соответствующее количество пептида, несущего следовый линкер с концевой тиольной группой, причем растворенного в фильтрованном в стерильных условиях SB-буфере, 20 ммоль (содержащем 15% об./об. пропиленгликоля и 0,01% вес/об. Tween 20, pH 3,8), добавляли в реактор и обеспечивали аккуратное встряхивание полученной в результате реакционной смеси при температуре окружающей среды в течение 1,5-24 часов. В конце реакции надосадочную жидкость удаляли посредством фильтрации с применением незначительного избыточного давления азота или путем центрифугирования суспензии. Остаток обрабатывали фильтрованным в стерильных условиях 20 мМ SBS-буфером (содержащим 15% об./об. пропиленгликоля и 0,01% вес/об. Tween 20, pH 3,0) с получением суспензии 0,7% вес/об., встряхивали в течение 3 минут, центрифугировали и удаляли надосадочную жидкость путем декантирования. Данный процесс повторяли пять раз. Остаток обрабатывали 10 мМ раствором 1-гидрокси-2-меркаптоэтана, растворенного в фильтрованном в стерильных условиях 20 мМ SBS-буфере (содержащем 15% об./об. пропиленгликоля и 0,01% вес/об. Tween 20, pH 3,0) с получением ~1 вес. % суспензии, и оставляли аккуратно перемешиваться в течение 30 мин. с аккуратным встряхиванием/смешиванием. Растворитель удаляли путем центрифугирования с последующим декантированием, как указано выше. Данный процесс обработки 1-гидрокси-2-меркаптоэтаном повторяли четыре раза. Остаток суспендировали в фильтрованном в стерильных условиях 20 мМ SBS-буфере (содержащем 15% об./об. пропиленгликоля и 0,01% вес/об. Tween 20, pH 3,0) с получением суспензии с концентрацией ~0,5 вес. % и смешивали в течение 3 минут с последующим удалением путем центрифугирования и декантирования. Полученный в результате остаток суспендировали в 20 мМ SBS-буфере (содержащем 15% об./об. пропиленгликоля и 0,01% вес/об. Tween 20, pH 6,5) с получением 0,7 вес. % суспензии, перемешивали в течение 20 минут и фильтровали. После повторения данного процесса еще раз, остаток переносили в 20 мМ SBS-буфер (содержащий 15% об./об. пропиленгликоля и 0,01% вес/об. Tween 20, pH 4,5) с получением 0,5 вес.% суспензии, перемешивали в течение 15 минут и фильтровали. Данный процесс повторяли один раз. Остаток суспендировали в стерильной воде (pH 4,5), перемешивали в течение 5 минут и фильтровали. Данный процесс повторяли пять раз. Остаток фильтровали в асептических условиях с использованием стерильного мембранного фильтра и лиофилизировали до сухости.
В таблице 3 обобщены результаты синтеза различных конъюгатов гидрогеля на основе HA с пептидами двойных агонистов, полученных при различных условиях реакций и природе бесследного линкера.
Таблица 3b. Конъюгаты, полученные согласно описанному в примерах 14-22
Конъюгация линкера 7, содержащего тиол-функционализированный эксендин-4 под Seq ID No. 26, с малеимид-функционализированной гиалуроновой кислотой.
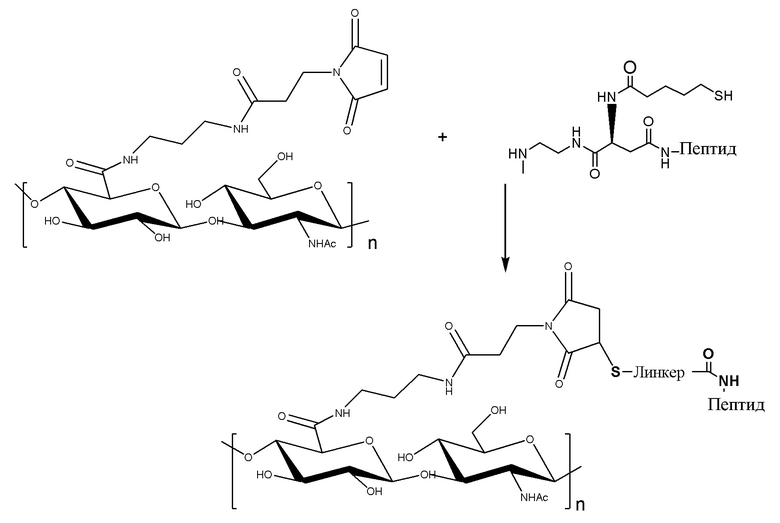
К 53 мг гидрогеля на основе 3-(3-малеимидопропил)аминопропан-модифицированной DVS-HA (пример 15) добавляли 7 мл 20 мМ SBS, содержащего 0,01 вес. % Tween® 20, пропиленгликоль (15% об./об.). pH буфера составлял 3,8. Суспензию аккуратно перемешивали при 25°C в течение 90 мин. К данной суспензии добавляли 2,1 мг тиол-функционализированного эксендина-4 под Seq ID 26 с линкером из примера 7, растворенным в 1 мл вышеприведенного буфера. Сосуд с пептидом промывали буфером (2×0,5 мл) и смывы добавляли к суспензии. Реакционную смесь аккуратно перемешивали при 25°C в течение 18 ч. Затем суспензию центрифугировали при 1750 об/мин в течение 2 мин. и надосадочную жидкость осторожно декантировали. Гидрогель суспендировали в 10 мл 20 мМ SBS-буфера, содержащего 0,01 вес. % Tween® 20, 15% об./об. пропиленгликоля, pH 3, перемешивали в течение 2 мин, центрифугировали при 1750 об/мин в течение 2 мин. и растворитель декантировали. Данный процесс повторяли еще 4 раза. Остаток обрабатывали 2 мл 10 мМ 1-гидрокси-2-меркаптоэтана, растворенного в 20 мМ SBS, pH 3, и обеспечивали протекание реакции в течение 30 мин. Реакционную смесь центрифугировали при 2000 об/мин в течение 2 мин. и растворитель декантировали. Данный способ повторяли еще три раза. Остаток суспендировали в 10 мл 20 мМ SBS, содержащего 0,01 вес. % Tween® 20, pH 3, перемешивали в течение 2 мин, центрифугировали при 2000 об/мин в течение 2 мин. и растворитель декантировали. Затем остаток суспендировали в 10 мл подкисленной стерильной воды (pH 3,5), содержащей 0,01 вес. % Tween® 20, перемешивали в течение 10 мин, центрифугировали при 5000 об/мин в течение 5 мин. и растворитель декантировали. Данный процесс повторяли с 8, 7 и 6 мл вышеприведенной подкисленной стерильной воды. Образец лиофилизировали с получением 78 мг гидрогеля на основе HA, конъюгированного с пептидом, в виде грязно-белого твердого вещества с 4 вес. % загрузкой пептида в гидрогеле.
Пример 23
Конъюгация линкера, содержащего тиол-функционализированный эксендин-4 под Seq ID No. 26, с малеимид-функционализированной гиалуроновой кислотой.
Реакцию и выделение продукта осуществляли с использованием безкислородных буферов и в атмосфере азота. К 36 мг гидрогеля на основе 3-(3-малеимидопропил)аминопропан-модифицированной DVS-HA (пример 15) добавляли 6 мл 20 мМ SBS (содержащего 0,01 вес. % Tween® 20, 10% об./об. пропиленгликоля). pH среды регулировали до 6. Суспензию аккуратно встряхивали при 25°C в течение 30 мин. К данной суспензии добавляли 2,4 мг тиол-функционализированного эксендина-4 под Seq ID 26 с линкером (пример 7), растворенным в 1 мл вышеприведенного буфера (pH 6). Сосуд с пептидом промывали буфером (2×0,5 мл) и смывы добавляли к суспензии. Реакционную смесь аккуратно встряхивали при 25°C в течение 90 мин. Затем суспензию центрифугировали при 4000 об/мин в течение 2 мин и надосадочную жидкость осторожно декантировали. Гидрогель суспендировали в 10 мл 20 мМ SBS при pH 3 (содержащего 0,01 вес. % Tween® 20 и 10 об./об.% пропиленгликоля), смешивали в течение 2 мин, центрифугировали при 3005 G в течение 2 мин. и растворитель декантировали. Данный процесс повторяли еще четыре раза. Остаток обрабатывали 2 мл 10 мМ 1-гидрокси-2-меркаптоэтана в 20 мМ SBS, pH 3, в течение 30 мин, центрифугировали при 4000 об/мин в течение 2 мин. и растворитель декантировали. Данный способ повторяли еще три раза. Остаток суспендировали в 10 мл 20 мМ SBS, содержащего 0,01 вес. % Tween® 20 (pH 3), смешивали в течение 2 мин, центрифугировали при 4000 об/мин в течение 2 мин и растворитель декантировали. Данный процесс повторяли еще четыре раза. Остаток суспендировали в подкисленной (pH 3,5) стерильной воде, содержащей 0,01 вес. % Tween® 20, смешивали в течение 10 мин, центрифугировали при 5000 об/мин в течение 5 мин и растворитель декантировали. Данный процесс повторяли с использованием 8, 7 и 6 мл вышеприведенной стерильной воды. Остаток лиофилизировали с получением 31 мг HA. конъюгированной с пептидом, в виде грязно-белого твердого вещества с загрузкой пептида 2,4 вес. % в гидрогеле.
Пример 24.
Процедура оценки загрузки пептида в конъюгатах гидрогеля и пептида.
Предварительно определенное количество конъюгата гидрогеля на основе HA и пептида суспендировали в CHES-буфере (pH 9,5) и суспензию оставляли аккуратно перемешиваться при 70°C. Суспензию центрифугировали и аликвоту анализировали в отношении содержания пептида посредством способа HPLC. Способ HPLC включает применение колонки q C-18 Kinetics (внутренний диаметр=4,6 мм и длина=100 мм, размер частиц 2,6 мкм, Phenomenex) с использованием Agilent 1100 LC. Композиция подвижной фазы A представляет собой 90% воды/10% ацетонитрила/0,1% трифторуксусной кислоты (TFA), а подвижной фазы B представляет собой 10% ацетонитрила/90% воды/0,09% TFA. Градиент представляет собой подвижную фазу от 25% B до 55% B за 8 минут. Скорость потока поддерживали на уровне 1 мл/мин. Чистые пептиды применяли в качестве стандартов для оценки высвобожденного из гидрогеля пептида.
Пример 25
Определение времени пребывания in vivo гидрогеля на основе HA.
Время пребывания гидрогелей in vivo в подкожном пространстве исследовали посредством магнитно-резонансной (MR) томографии. Интенсивность контраста протонов воды внутри гидрогеля применяли для оценки времени пребывания гидрогелей in vivo. Для этих целей в качестве животных применяли мышей CAnN.Cg-Foxn1nu/Crl. Гидрогель инъецировали с использованием иглы 31 G, следуя всем одобренным протоколам защиты животных. MR-томограмму места инъекции получали регулярно в течение некоторого периода времени. В одной группе вводили с помощью инъекции гидрогель, а в другой группе применяли суспензию, содержащую смесь 1:1 (вес/вес) гидрогеля и растворимой HA, 800000 Да. В случае чистого гидрогеля гель проявлялся в течение 3 недель с медленным уменьшением интенсивности (фиг. 2). Что же касается смеси, содержащей растворимую HA, то MR-сигнал, который был интенсивным в день 1, значительно снизился ко дню 4 (2). Это свидетельствует о том, что для улучшения времени пребывания полимерного носителя, его необходимо сшивать для достижения очень высокого молекулярного веса.
Фигура 2a. MR-томограмма гидрогеля на основе HA в месте инъекции в зависимости от времени.
Фигура 2b. MR-томограмма полимерной суспензии, содержащей смесь 1:1 (вес/вес) гидрогеля на основе HA и растворимой HA, 800 кДа, в месте инъекции в зависимости от времени.
Пример 26
Кинетические характеристики высвобождения in vitro
Аликвоту гидрогеля 8 с линкером и агонистом GLP-1/глюкагона (0,5 мг агониста GLP-1/глюкагона) переносили в шприц, оснащенный фильтровальной фриттой, и промывали 5 раз с помощью фосфатного буфера с pH 7,4 (60 мМ, 3 мМ EDTA, 0,01% Tween-20). Гидрогель суспендировали в том же буфере и инкубировали при 37°C. В определенные моменты времени (каждый раз через 1-7 дней инкубации) надосадочную жидкость заменяли и определяли количество выделенного агониста GLP-1/глюкагона посредством RP-HPLC при 215 нм. UV-сигналы, коррелирующие с выделенным агонистом GLP-1/глюкагона, интегрировали и откладывали на графике относительно времени инкубации.
Программное обеспечение для построения кривых применяли для оценки соответствующего периода полувыведения.
Фигура 3. Кинетические характеристики высвобождения in vitro двойного агониста эксендина-4 под Seq ID 26 с линкером из гидрогеля на основе HA (пример 23). Период полувыведения составляет ~ 5 дней.
Пример 27
Клеточные анализы in vitro в отношении эффективности рецептора GLP-1, рецептора глюкагона и рецептора GIP
Агонизм пептидов в отношении рецепторов определяли с помощью функциональных анализов, в ходе которых измеряли ответ cAMP клеточных линий НЕК-293, стабильно экспрессирующих рецепторы GIP, GLP-1 или глюкагона человека.
Содержание cAMP в клетках определяли с использованием набора от Cisbio Corp. (№ по кат. 62AM4PEC) на основе HTRF (гомогенная флуоресценция с временным разрешением). В целях подготовки клетки распределяли по культуральным флаконам T175 и выращивали в течение ночи практически до конфлюентности в среде (DMEM/10% FBS). Среду затем удаляли и клетки промывали PBS, не содержащим кальция и магния, с последующей обработкой протеиназой совместно с аккутазой (Sigma-Aldrich, № по кат. A6964). Отдельные клетки промывали и ресуспендировали в буфере для анализа (1 x HBSS; 20 мМ HEPES, 0,1% BSA, 2 мМ IBMX) и определяли плотность клеток. Затем их разбавляли до 400000 клеток/мл и вносили аликвоты по 25 мкл в лунки 96-луночных планшетов. Для проведения измерения в лунки добавляли 25 мкл испытуемого соединения в буфере для анализа с последующей инкубацией в течение 30 минут при комнатной температуре. После добавления реагентов HTRF, разбавленных в лизирующем буфере (компоненты набора), планшеты инкубировали в течение 1 часа с последующим измерением соотношения интенсивности флуоресценции при 665/620 нм. Эффективность агонистов in vitro количественно оценивали путем определения концентраций, которые вызывали 50% активацию максимального ответа (EC50).
Пример 28
Снижение уровня глюкозы у самок мышей dbdb с диабетом
В начале исследования задействовали самок мышей dbdb с диабетом (BKS.CG-m +/+ Lepr(db)/J) возрастом 24-27 недель. Мышей, поступивших в возрасте 10-13 недель, адаптировали к корму и условиям содержания в течение по меньшей мере 1 недели, затем их задействовали в первом исследовании и после периода отмывки в течение по меньшей мере 2 недель, наконец, повторно задействовали в настоящем исследовании. За 19 дней до начала исследования определяли отдельные значения HbA1c для стратификации и, соответственно, распределения животных на 4 группы с N=8 на группу для получения групп с как можно более равными средними значениями HbA1c. Животные получали избыток пищи и воды ad libitum в течение всего периода исследования. В первый день исследования уровень глюкозы в крови, взятой из надреза на кончике хвоста, определяли непосредственно перед одной подкожной обработкой и через 4 часа после этого (08:00-09:00 утра) либо средой-носителем (стерильный сукцинатный буфер), либо HA-конъюгатом агониста GLP-1/глюкагона под Seq. ID 26 из примера 23 в дозах 50, 100 и 200 нмоль/кг, разбавленными в среде-носителе. Затем проводили каждодневные измерения уровня глюкозы в крови в течение следующих 16 дней в одно и то же время (08:00-09:00 утра) за исключением дней 11 и 12 (выходные). Кроме того, ежедневно наблюдали за потреблением пищи и воды. Данные о глюкозе анализировали посредством двухфакторного дисперсионного анализа повторных измерений, а затем посредством апостериорного критерия Дунетта с уровнем значимости p<0,05. AUC-анализ глюкозы осуществляли с использованием однофакторного дисперсионного анализа, а затем посредством апостериорного критерия Дунетта с уровнем значимости p<0,05.
На фиг. 4 показана концентрация глюкозы в крови относительно исходного уровня в зависимости от времени после одной инъекции различных доз конъюгата агониста HA-GLP-1/глюкагона под Seq. ID 26.
Пример 28b. Эффекты снижения уровней глюкозы у самок мышей dbdb с диабетом
Самки мышей db/db с ожирением и диабетом (BKS.CG-m +/+ Lepr(db)/J и здоровые худые контроли (BKS.Cg-m +/+ Lepr(db)/J) поступали в возрасте 10-11 недель, и их адаптировали к условиям питания и условиям вивария. В возрасте 12-13 недель определяли отдельные значения HbA1c для стратификации и распределения животных в различные группы с N=8 на группу. Целью было получение групп с наиболее равными средними значениями HbA1c. В возрасте 13-14 недель 2 группы мышей db/db получали подкожно единичную дозу в 100 нмоль/кг массы тела конъюгата под Seq. ID 26 либо растворимой, либо сшитой HA. В то же время и во второй раз, в день 7, третья группа мышей db/db и здоровые худые контроли получали подкожную инъекцию сукцинатного буфера и растворимой HA в отношении 1:1. Во всех группах инъецировали общий объем 5 мл/кг массы тела. Концентрации глюкозы в крови после утреннего кормления определяли непосредственно перед обработкой (между 08:00 и 09:00 часами утра) и через четыре часа после этого, а затем ежедневно между 08:00 и 09:00 часами утра. Кровь отбирали из надрезов на кончике хвоста и определяли концентрации посредством ручного глюкометра (Accu Check). В течение всего периода исследования животные получали избыток пищи и воды ad libitum.
На фиг. 4b показана концентрация глюкозы в крови относительно исходного уровня в зависимости от времени после одной инъекции конъюгата сшитой и растворимой HA-GLP-1/глюкагона-агониста под Seq. ID 26.
Пример 28c
Эффекты снижения уровня глюкозы у самок мышей dbdb с диабетом
После поступления, самок мышей db/db с диабетом и ожирением (BKS.CG-m +/+ Lepr(db)/J) адаптировали к условиям питания и условиям вивария, и в начале исследования их возраст составлял 12 недель. Отдельные значения HbA1c определяли в день 10 фазы перед использованием препарата для стратификации и распределения животных по различным группам с N=8 на группу. Целью было получение групп с наиболее равными средними значениями HbA1c. В день 1 фазы дозирования мыши db/db получали подкожно разовую дозу в 12,75 мг/кг массы тела конъюгата с Seq ID 45, 46, 48 и 49. Животные db/db из группы, обработанной средой-носителем, получали подкожную инъекцию PBS. Во всех группах инъецировали общий объем 10 мл/кг массы тела. Концентрации глюкозы в крови после утреннего кормления определяли непосредственно перед обработкой (между 08:00 и 09:00 часами утра) и через четыре часа после этого в день 1 фазы дозирования, а затем ежедневно между 08:00 и 09:00 часами утра. Кровь отбирали из надрезов на кончике хвоста и определяли концентрации посредством ручного глюкометра (Accu Check). В течение всего периода исследования животные получали избыток пищи и воды ad libitum.
На фиг. 4с показана концентрация глюкозы в крови относительно исходного уровня в зависимости от времени после одной инъекции различных доз конъюгата агониста HA-GLP-1/глюкагона под Seq. ID 45 (треугольники), 46 (квадраты), 48 (круги).
На фиг. 4d показана концентрация глюкозы в крови относительно исходного уровня в зависимости от времени после одной инъекции различных доз конъюгата агониста HA-GLP-1/глюкагона под Seq. ID 49 (круги).
Пример 29
Исследование способности к введению посредством инъекции
Суспензию 3,75% (мг/мл) конъюгата HA и пептида получали путем диспергирования соответствующего количества пептидного конъюгата в 20 мМ сукцинатном буферном солевом растворе (SBS) при pH 4,5. В другом флаконе 2% (мг/мл) раствор исходного полимера HA получали путем растворения лиофилизированной HA в 20 мМ SBS при pH 4,5. Оба образца оставляли для гидратации в течение от 24 до 48 часов при 2-8°C. Флаконы доводили до комнатной температуры. После достижения равновесия при комнатной температуре 1 мл суспензии конъюгата пептида и гидрогеля на основе HA и HA отбирали в 3 мл шприц. К данной суспензии добавляли 0,25 мл раствора растворимой HA. Полученную в результате суспензию подвергали 20-кратному возвратно-поступательному смешиванию между двумя 3 мл шприцами. Примерно 220 мкл данной суспензии набирали в 1 мл шприц. К данному шприцу прикрепляли ½-дюймовую иглу 30G. Следует убедиться, что игла не была заполнена тестовым материалом. Шприц, содержащий суспензию, помещали в крепление для шприца оборудования Instron и головку Instron совмещали с поршнем шприца. Скорость головки регулировали до достижения целевой скорости инъекции. Начинали тестирование. Для каждого образца проводили три измерения и представленный результат является средним значением этих измерений. Результаты силы введения с помощью инъекции для различных конъюгатов пептида и гидрогеля на основе HA показаны в таблице 4.
Таблица 4. Эффект модификации HA на среднее значение силы, с которой производится инъекция*
(вес. %) (мол. %)
*n=3 на группу; скорость инъекции=12 мкл/с
На фиг. 5 показано среднее значение силы экструзии при выдавливании жидкости через 30 G иглу длиной 2,5 см, прикрепленную к 1 мл шприцу. Очевидно, что большая загрузка пептида в гидрогеле на основе HA приводит к более низким силам экструзии и, следовательно, повышает способность к введению посредством инъекции.
Пример 29b
Исследование способности к введению посредством инъекции у HA-конъюгата с Seq. ID No. 45, Aib-линкер
1 мл шприц Luer-Lock (BD шприц, внутренний диаметр 4 мм) заполняли примерно 500 мкл (460 мкл по шкале шприца) раствора образца и прикрепляли иглу 29 G x 12,7 мм. Измерение проводили в динамометре LF Plus от Lloyed Instruments. На шток поршня надавливали до появления небольшой капли на кончике иглы 29 G. Шприц помещали в крепление для шприца и динамометр двигали таким образом, чтобы он касался штока поршня.
Параметры измерения были следующими: сила прекращения 50 Н и скорость впрыска 5,8 мм/с (что равняется 100 мкл/с в данном случае).
Измерение начинали и автоматически прекращали, когда шток поршня достигал дна шприца (шприц пуст), или в ходе измерения сила достигала уровня более 50 Н.
В таблице 5 показаны максимальные силы впрыска конъюгатов с различными концентрациями при различных соотношениях в смеси с растворимой HA (sHA).
Таблица 5
20 мг/мл
sHA 20 мг/мл
Силы впрыска чистого раствора 20 мг/мл 600 кДа sHA составляли 13,3 Н, а для 2600 кДа sHA - 18,8 Н.
| название | год | авторы | номер документа |
|---|---|---|---|
| ОСНОВАННЫЕ НА АМИДАХ ПРОЛЕКАРСТВА ПЕПТИДОВ ГЛЮКАГОНОВОГО НАДСЕМЕЙСТВА | 2009 |
|
RU2550696C2 |
| ДВОЙНЫЕ АГОНИСТЫ GLP1/GIP ИЛИ ТРОЙНЫЕ АГОНИСТЫ GLP1/GIP/ГЛЮКАГОНА | 2013 |
|
RU2652783C2 |
| ТЕРАПЕВТИЧЕСКОЕ ПРИМЕНЕНИЕ КОНЪЮГАТА ТРОЙНОГО АГОНИСТА ДЛИТЕЛЬНОГО ДЕЙСТВИЯ, ОБЛАДАЮЩЕГО АКТИВНОСТЯМИ В ОТНОШЕНИИ ВСЕХ ИЗ РЕЦЕПТОРОВ ГЛЮКАГОНА /GLP-1/GIP, ДЛЯ ЛЕЧЕНИЯ ЗАБОЛЕВАНИЯ ЛЕГКОГО | 2020 |
|
RU2829342C1 |
| АЦИЛИРОВАННЫЕ ДВОЙНЫЕ АГОНИСТЫ GLP-1/GLP-2 | 2017 |
|
RU2753193C2 |
| МУЛЬТИРЕЦЕПТОРНЫЙ АГОНИСТ И ЕГО МЕДИЦИНСКОЕ ПРИМЕНЕНИЕ | 2020 |
|
RU2816492C2 |
| АНАЛОГИ ГЛЮКАГОНА, ОБЛАДАЮЩИЕ ПОВЫШЕННОЙ РАСТВОРИМОСТЬЮ И СТАБИЛЬНОСТЬЮ В БУФЕРАХ С ФИЗИОЛОГИЧЕСКИМИ ЗНАЧЕНИЯМИ Ph | 2009 |
|
RU2560254C2 |
| ПРИМЕНЕНИЕ ДОЛГОДЕЙСТВУЮЩИХ ПЕПТИДОВ GLP-1 | 2013 |
|
RU2657573C2 |
| ПЕПТИДЫ ГЛЮКАГОНОВОГО СУПЕРСЕМЕЙСТВА, ОБЛАДАЮЩИЕ АКТИВНОСТЬЮ ОТНОСИТЕЛЬНО ЯДЕРНЫХ ГОРМОНАЛЬНЫХ РЕЦЕПТОРОВ | 2011 |
|
RU2604067C2 |
| КОНЪЮГАТЫ ИНСУЛИН-ИНКРЕТИН | 2014 |
|
RU2678134C2 |
| ЛЕЧЕНИЕ НЕВРОЛОГИЧЕСКИХ ЗАБОЛЕВАНИЙ | 2017 |
|
RU2755997C2 |

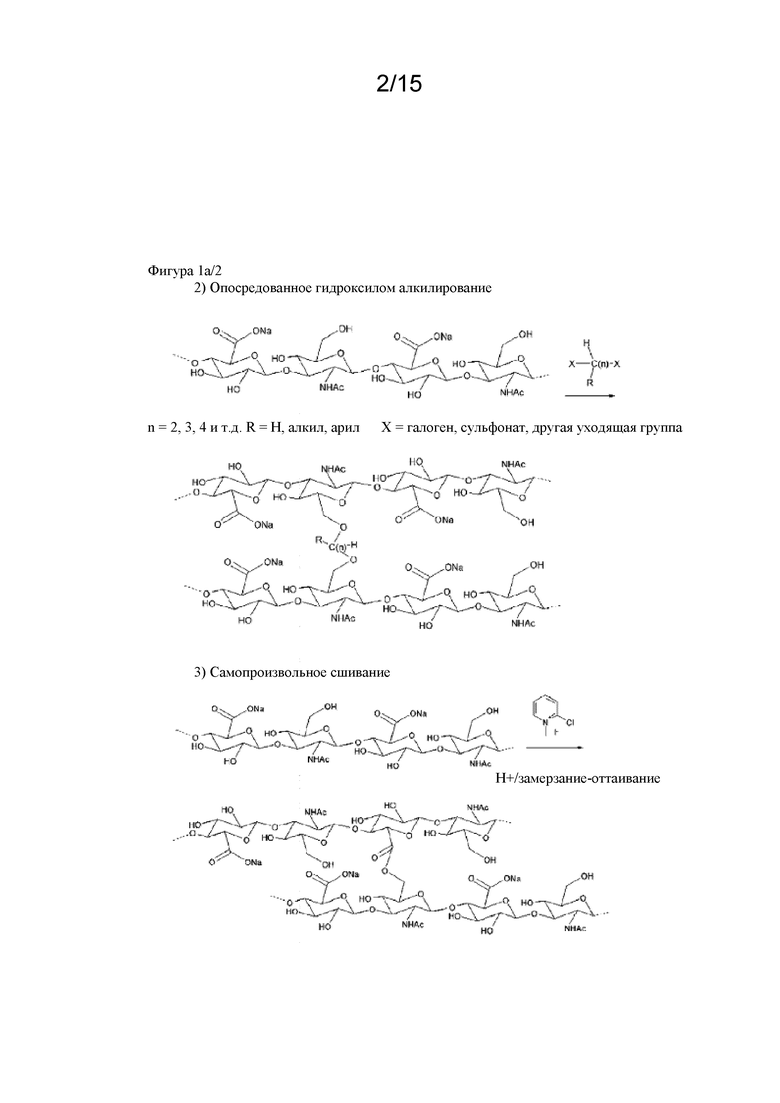
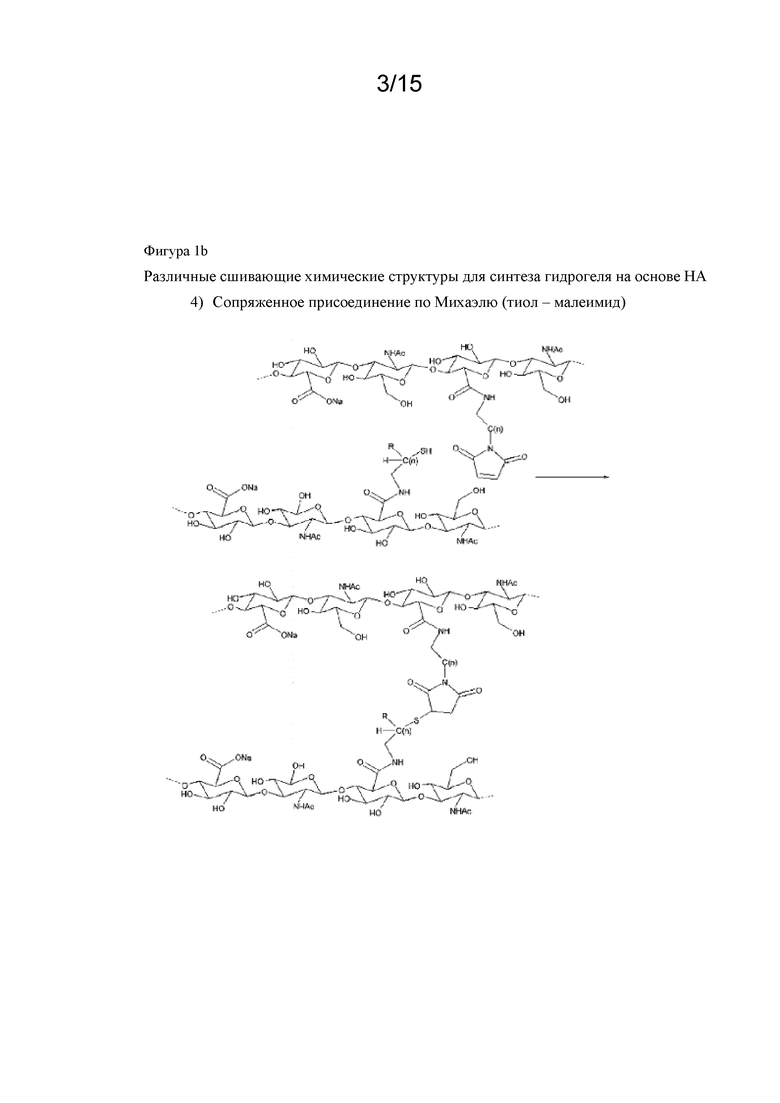
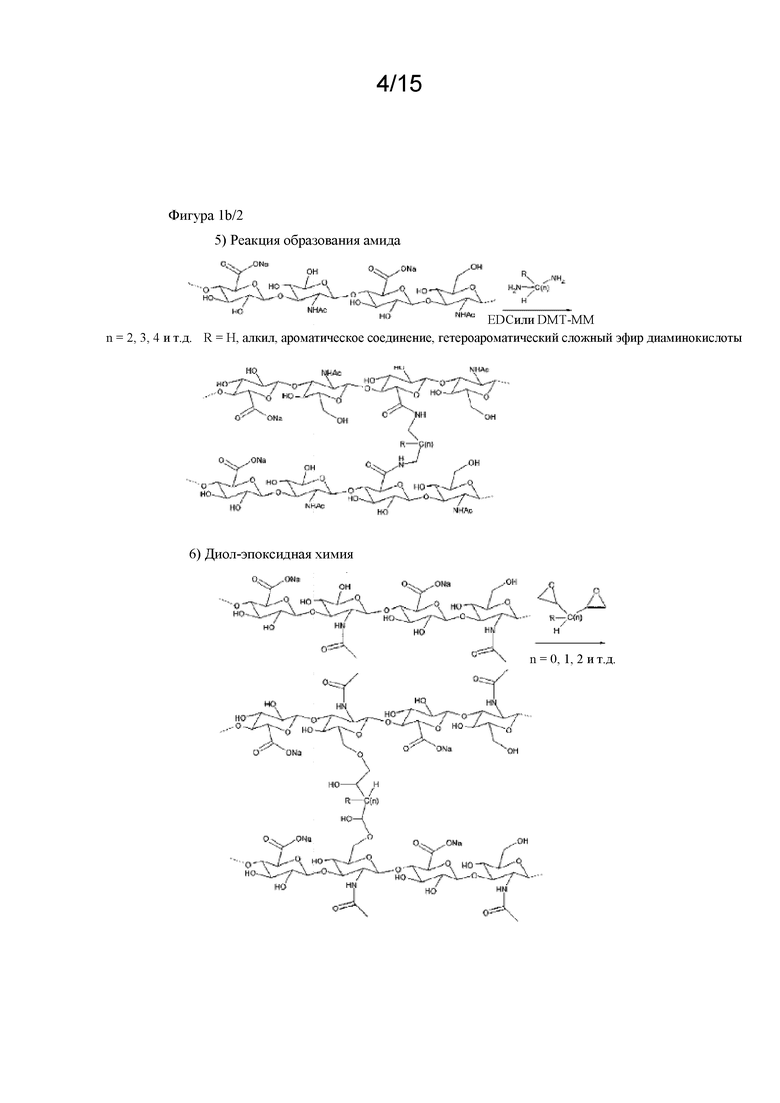
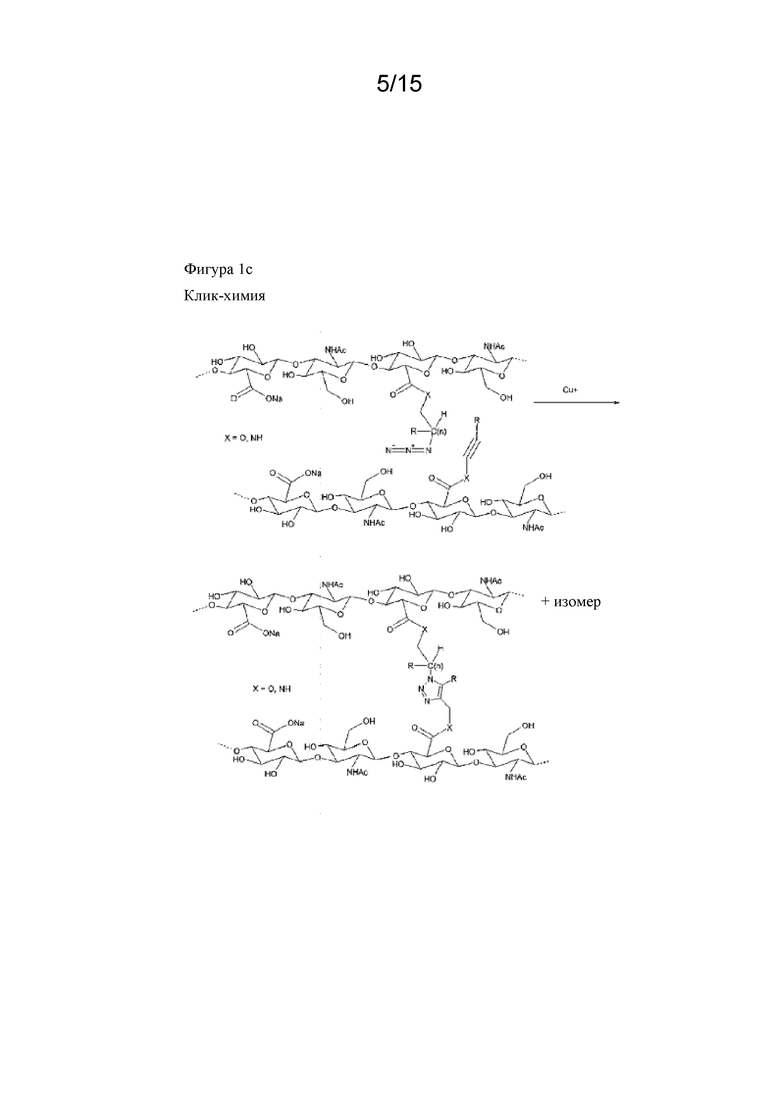
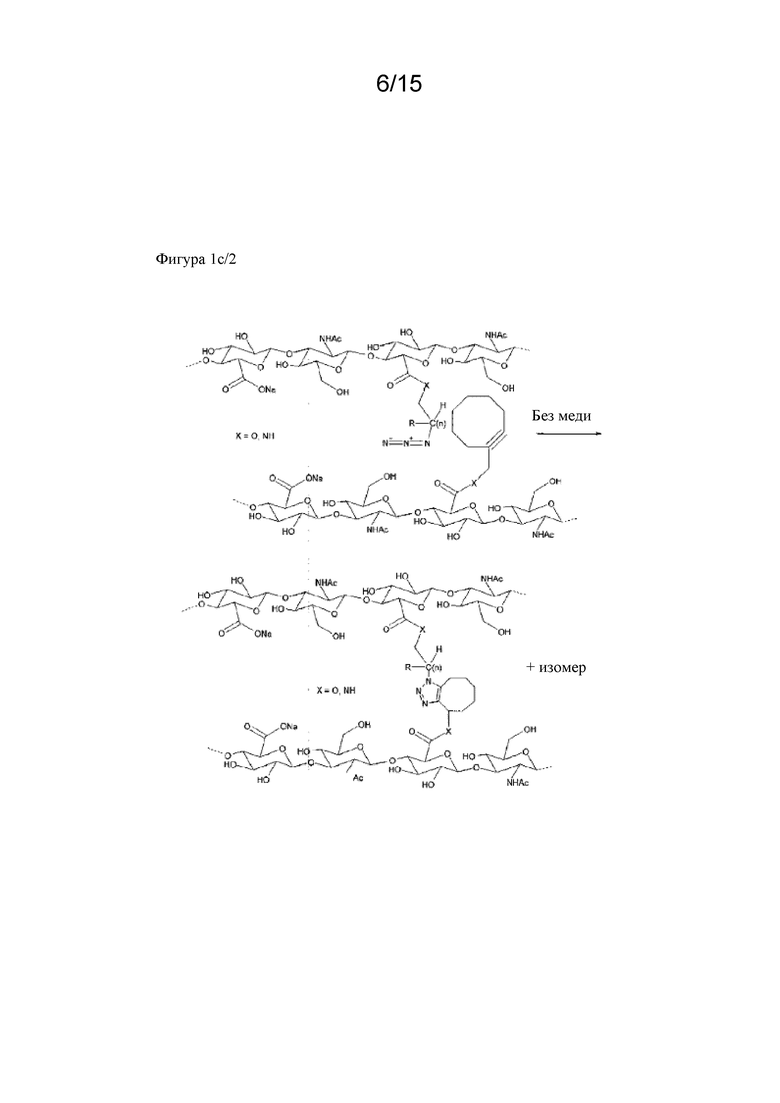
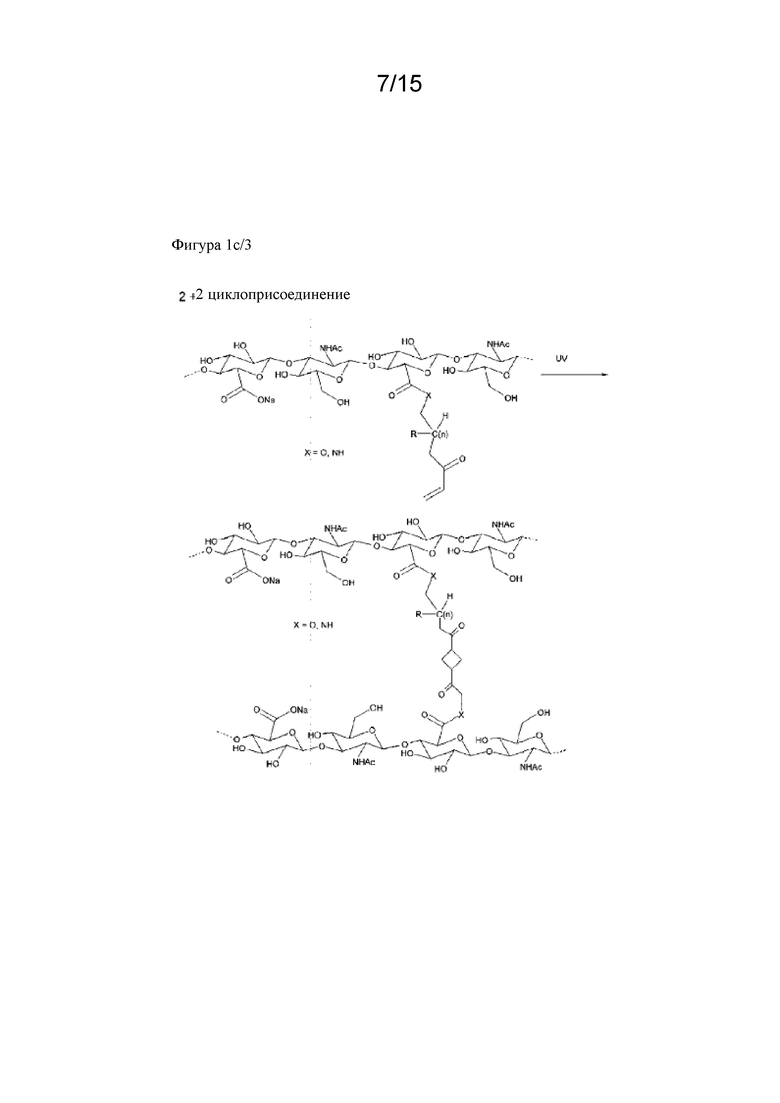
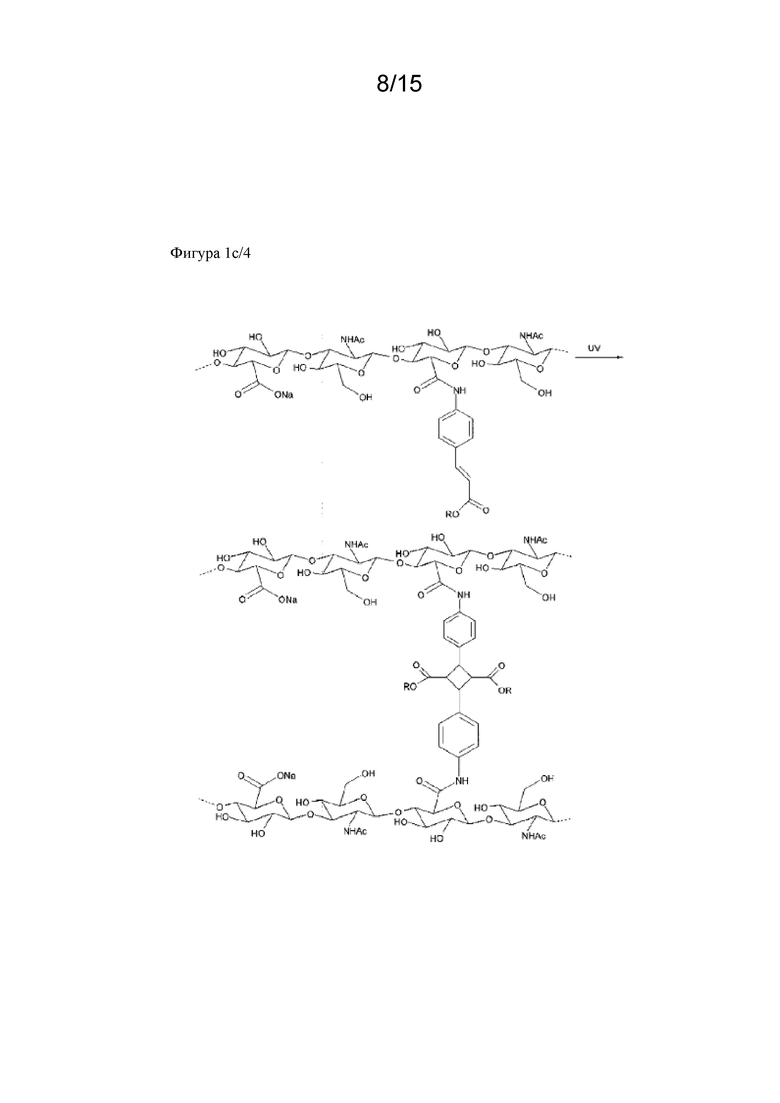
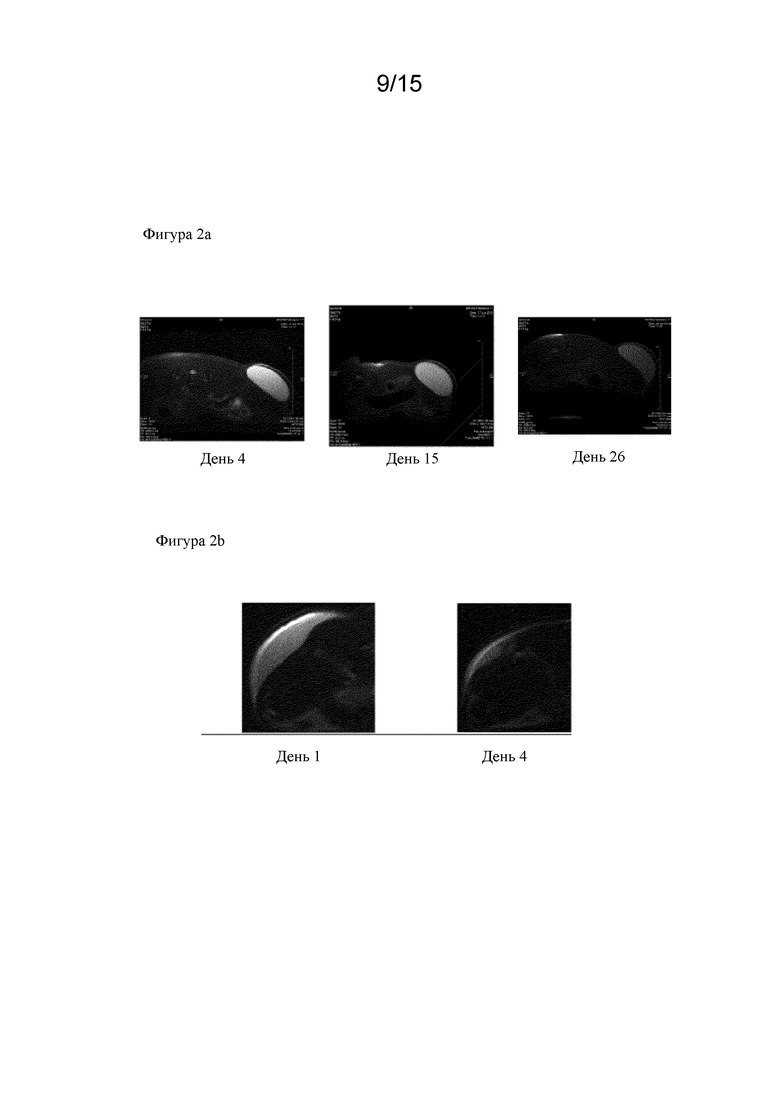
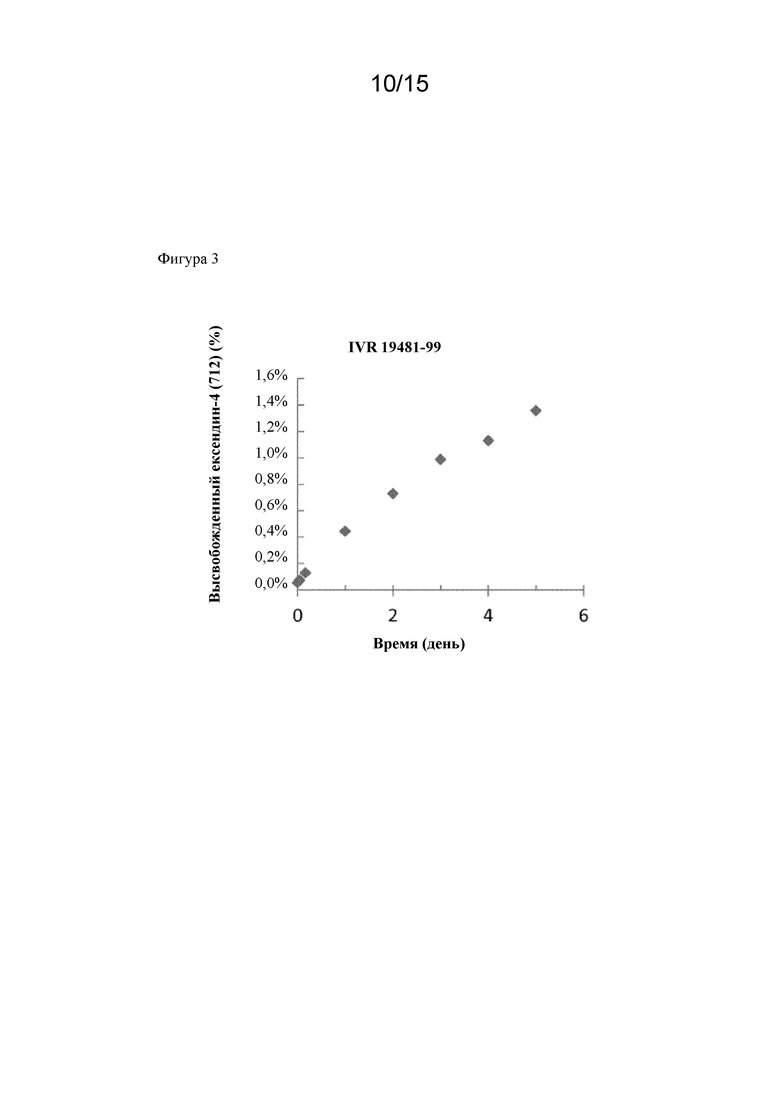

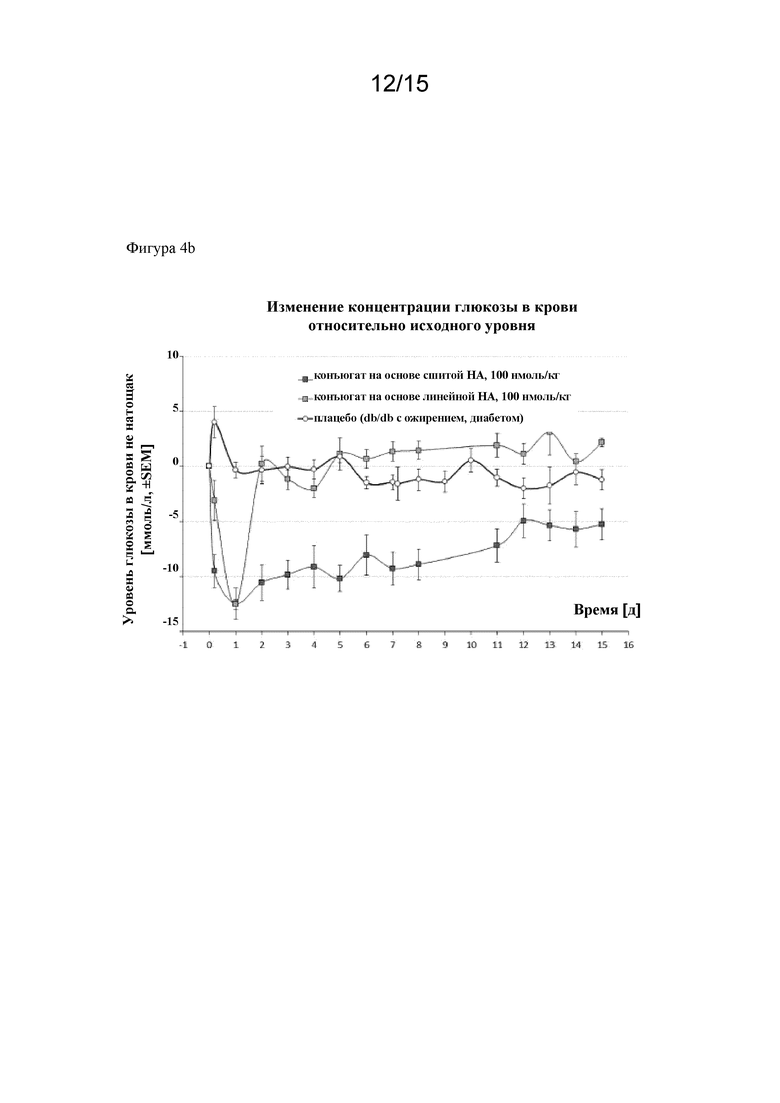


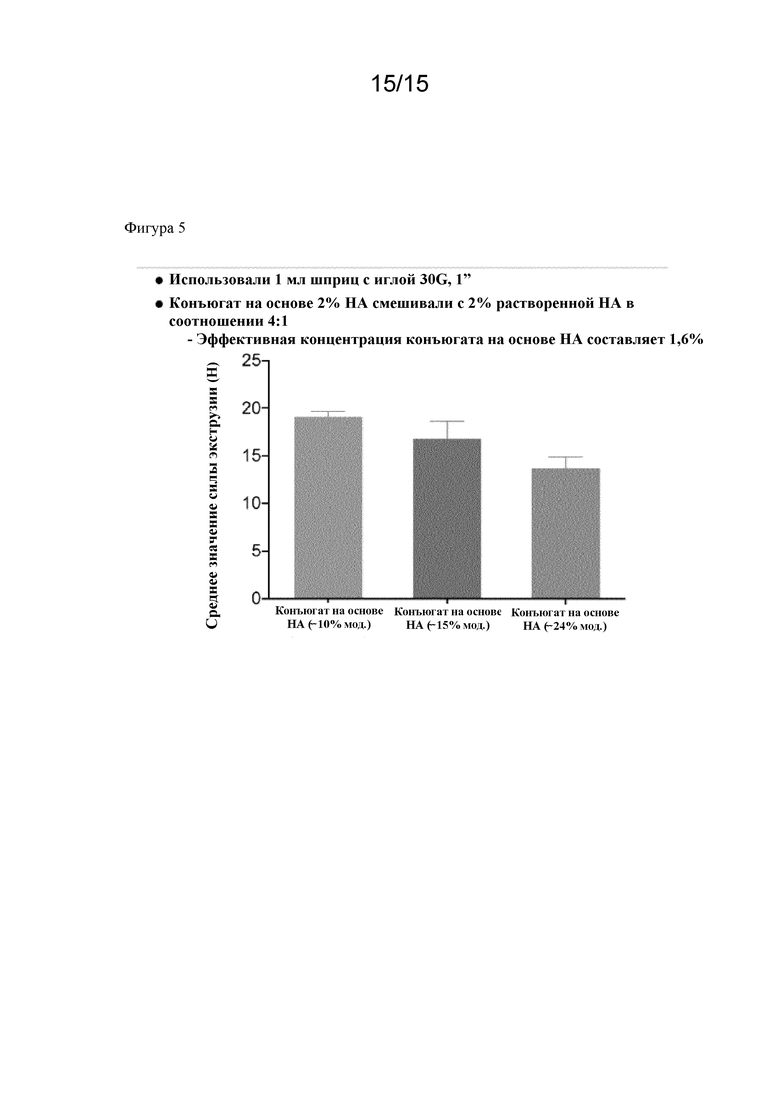
Изобретение относится к пролекарству или его фармацевтически приемлемой соли, содержащим конъюгат агониста GLP-1/глюкагона и линкера Z-L1-L2-L-Y-R20, где Y представляет собой фрагмент агониста GLP-1/глюкагона; и -L представляет собой линкерный фрагмент формулы (Ib) или фрагмент формулы (Ic), где пунктирная линия указывает на присоединение к одной из аминогрупп фрагмента агониста GLP-1/глюкагона за счет образования амидной связи, а Z представляет собой гидрогель на основе сшитой гиалуроновой кислоты, в котором от 0,05 до 20% мономерных дисахаридных звеньев сшиты посредством сшивателя; и от 0,2 до 8,5% мономерных дисахаридных звеньев содержат группы L1-L2-L-Y-R20. Настоящее изобретение дополнительно относится к фармацевтическим композициям, содержащим указанные пролекарства, а также к их применению в качестве лекарственного препарата для лечения или предупреждения заболеваний или нарушений, которые можно вылечить посредством агониста GLP-1/глюкагона. 6 н. и 15 з.п. ф-лы, 5 ил., 5 табл., 29 пр.
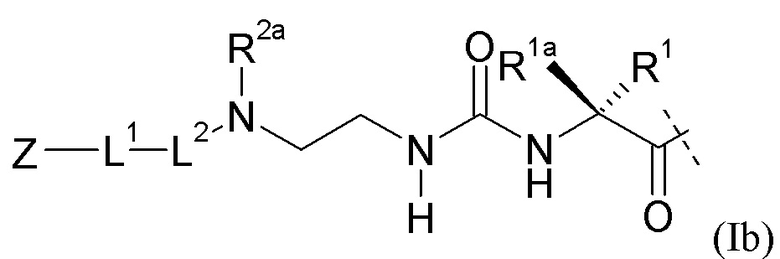
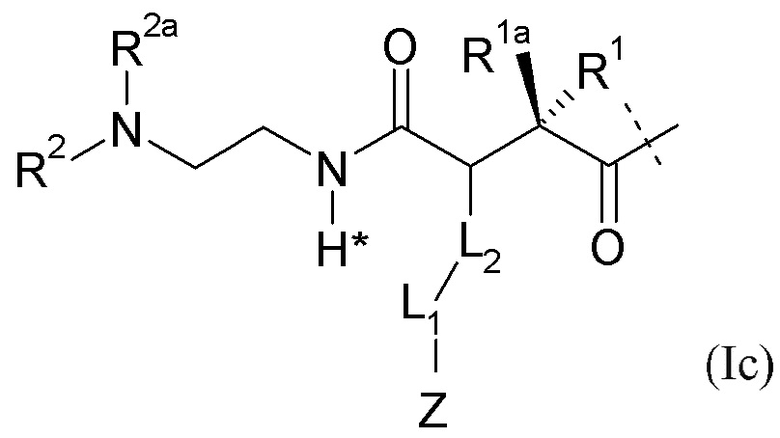
1. Пролекарство или его фармацевтически приемлемая соль, содержащие конъюгат лекарственного средства и линкера формулы (I)
Z - L1 -L2 - L - Y - R20 (I),
где Y представляет собой агонист GLP-1/глюкагона, выбранный из последовательностей SEQ ID NO: 4-60;
R20 представляет собой ОН или NH2,
L представляет собой линкер формулы (Ib)
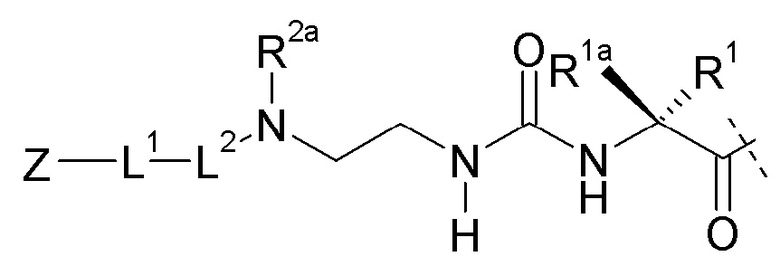 (Ib)
(Ib)
или линкер формулы (Ic)
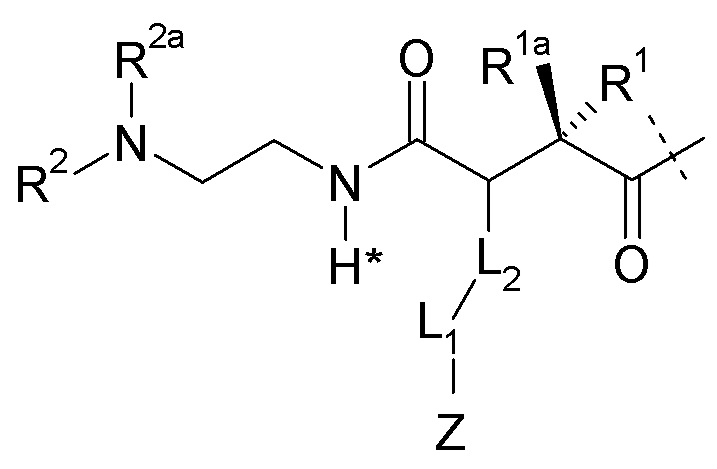 (Ic),
(Ic),
где пунктирная линия указывает на присоединение к N-концу Y посредством образования амидной связи;
где R1, R1a независимо выбраны из группы, состоящей из H и C1-4алкила;
R2, R2a независимо выбраны из группы, состоящей из H и C1-4алкила;
L2 представляет собой C1-20алкильную цепь, которая необязательно прервана одной или несколькими группами, независимо выбранными из C(O)N(R3aa), где R3aa независимо выбрана из группы, состоящей из C1-4алкила; и
L2 присоединен к L1 посредством концевой группы, выбранной из группы, состоящей из
 и
и  ;
;
где L2 присоединен в одном положении, отмеченном пунктирной линией, и L1 присоединен в положении, отмеченном другой пунктирной линией; и
L1 представляет собой C1-20алкильную цепь, которая необязательно прервана одной или несколькими группами, независимо выбранными из C(O)N(R5aa), где R5aa представляет собой H; и
L1 присоединен к Z посредством концевой аминогруппы, образующей амидную связь с карбоксильной группой бета-1,3-D-глюкуроновой кислоты гиалуроновой кислоты из Z;
Z представляет собой гидрогель на основе сшитой гиалуроновой кислоты, в котором
от 0,05 до 20% мономерных дисахаридных звеньев сшиты посредством сшивателя; и от 0,2 до 8,5% мономерных дисахаридных звеньев содержат группы L1-L2-L-Y-R20.
2. Пролекарство по п. 1, где
L представляет собой линкерный фрагмент формулы (Ib)
 (Ib),
(Ib),
где пунктирная линия указывает на присоединение к Y посредством образования амидной связи;
R1, R1a, R2a независимо выбраны из группы, состоящей из H и C1-4алкила;
L2-L1-Z определена в п. 1.
3. Пролекарство по п. 1, где
L представляет собой линкерный фрагмент -L формулы (Ic)
 (Ic),
(Ic),
где пунктирная линия указывает на присоединение к Y посредством образования амидной связи;
R1 и R1a представляют собой H;
R2, R2a независимо выбраны из группы, состоящей из H и CH3;
где L2-L1-Z определена в п. 1.
4. Пролекарство по любому из пп. 1-3, где
L2 представляет собой C1-6алкильную цепь, которая необязательно прервана одной группой C(O)N(R3aa), при этом R3aa представляет собой C1-4алкил; и
L2 присоединен к L1 посредством концевой группы, выбранной из группы, состоящей из
 и
и  ;
;
где L2 присоединен в одном положении, отмеченном пунктирной линией, и L1 присоединен в положении, отмеченном другой пунктирной линией.
5. Фармацевтическая композиция, обладающая агонистической активностью в отношении GLP-1/глюкагона, содержащая пролекарство по любому из пп. 1-4 или его фармацевтическую соль вместе с по меньшей мере одним фармацевтически приемлемым вспомогательным веществом.
6. Фармацевтическая композиция, обладающая агонистической активностью в отношении GLP-1/глюкагона, содержащая пролекарство по любому из пп. 1-4 или его фармацевтическую соль вместе с по меньшей мере одним фармацевтически приемлемым вспомогательным веществом и модификатором вязкости.
7. Фармацевтическая композиция по п. 6, где модификатор вязкости представляет собой гиалуроновую кислоту.
8. Фармацевтическая композиция по любому из пп. 5-7 в виде инъекционного состава.
9. Фармацевтическая композиция по любому из пп. 5-8 в виде суспензии.
10. Фармацевтическая композиция по любому из пп. 5-9 в виде суспензии, где пролекарство по любому из пп. 1-4 имеет концентрацию 0,5-8% вес/объем.
11. Фармацевтическая композиция по любому из пп. 5-9 в виде суспензии, где пролекарство по любому из пп. 1-4 имеет концентрацию 1,5-3% вес/объем.
12. Композиция по любому из пп. 5-11, где доза пролекарства в композиции является достаточной для обеспечения терапевтически эффективного количества агониста GLP1/глюкагона в течение по меньшей мере 6 дней за одно применение.
13. Композиция по любому из пп. 5-12, представляющая собой композицию с разовой дозой.
14. Пролекарство по любому из пп. 1-4 или фармацевтическая композиция по любому из пп. 5-13 для применения в способе лечения или предупреждения диабета.
15. Пролекарство по любому из пп. 1-4 или фармацевтическая композиция по любому из пп. 5-13 для применения в способе лечения или предупреждения дислипидемии.
16. Пролекарство по любому из пп. 1-4 или фармацевтическая композиция по любому из пп. 5-11 для применения в способе лечения или предупреждения метаболического синдрома.
17. Пролекарство по любому из пп. 1-4 или фармацевтическая композиция по любому из пп. 5-13 для применения в способе лечения или предупреждения гепатостеатоза, предпочтительно неалкогольной жировой болезни печени (NAFLD) и неалкогольного стеатогепатита (NASH).
18. Промежуточное соединение на основе конъюгата агониста GLP-1/глюкагона и линкера L2*-L-Y формулы (VIII)
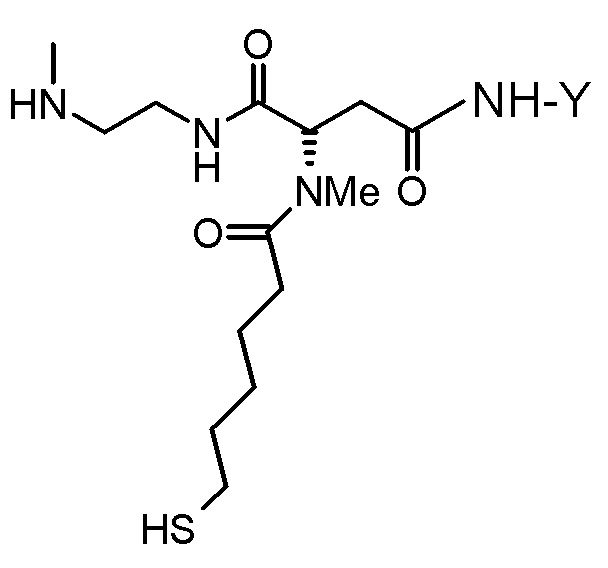 (VIII),
(VIII),
где Y представляет собой пептид под SEQ ID NO: 4-60.
19. Промежуточное соединение на основе конъюгата агониста GLP-1/глюкагона и линкера L2*-L-Y формулы (IX)
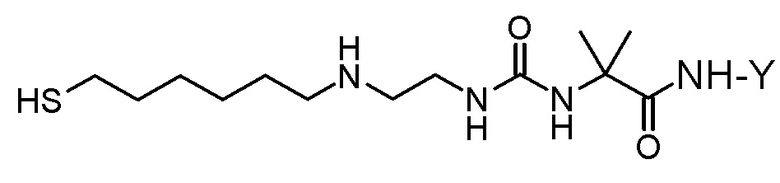 (IX),
(IX),
где Y представляет собой пептид под SEQ ID NO: 4-60.
20. Промежуточное соединение на основе конъюгата агониста GLP-1/глюкагона и линкера L2*-L-Y формулы (X)
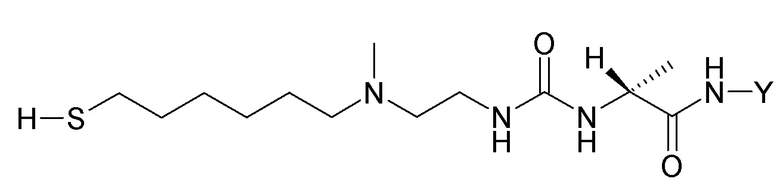 (X),
(X),
где Y представляет собой пептид под SEQ ID NO: 4-60.
21. Композиция по п. 13, где суспензию пролекарства можно вводить посредством инъекции через иглу с внутренним диаметром менее 0,26 мм.
| ПРОЛЕКАРСТВА, СОДЕРЖАЩИЕ КОНЪЮГАТ ЭКСЕНДИН-ЛИНКЕР | 2011 |
|
RU2593774C2 |
| WO 2009095479 A2, 06.08.2009 | |||
| WO 2007047922 A2, 26.04.2007. | |||
Авторы
Даты
2020-04-17—Публикация
2016-06-02—Подача