Изобретение относится к способу получения производных карбоновых кислот, в частности к новому способу получения амидов карбоновых кислот общей формулы

которые находят применение в качестве полупродуктов в синтезе аминов, нитрилов и гетероциклических соединений, применяется в качестве растворителей.
Известен способ получения амидов, заключающийся в переамидировании амида карбоновой кислоты при повышенной температуре [Bon Ε.D., Bigg С.H., Bertrand G.. Aluminum chloride promoted transamidation reactions // J. Org. Chem., V.59, 1994, p.4035-4036]. Недостатком этого способа является необходимость нагрева не ниже 180°C и невозможность использования в качестве исходных веществ термически нестабильных соединений.
Известен ряд способов переамидирования амидов карбоновых кислот аминами с использованием катализаторов - AlCl3, Sc(OTf)3 [Eldred S.Ε., Stone D.Α., Gellman S.H., Stahl S.S.. Catalytic transamidation under moderate conditions // J. Am. Chem. Soc, V.125, 2003, p.3422-3423], Ti(NMe2)4 [Eldred S.E., Stone D.A, Gellman S.H., Stahl S.S. Transamidation Catalyzed by a Recoverableand Reusable PolyDMAP-Based Hafnium Chloride and Montmorillonite // Chem. Soc, V. 125, 2003, p.3422-3423], способных переамидировать амиды карбоновых кислот аминами в среде толуола при 100°C в течение 20-24 часов. Также для катализа реакции переамидирования вторичных карбоксамидов первичными алкиламинами применялся комплекс Al2(NMe2)6 в среде толуола при 90°C [Hoerter J.M., Otte K.M., Gellman S.H., Stahl S.S. Mechanism of Al(III)-catalyzed transamidation of unactivated secondary carboxamides // Journal of the American Chemical Society, V.128, №15, 2006, p.5177-5183]. Вторичные или третичные амиды синтезировали взаимодействием первичных карбоксамидов с первичными или вторичными аминами в присутствии каталитических количеств гидрохлорида гидроксиламина [Allen С.L., Atkinson В.N., Williams J.M.. Transamidation of primary amides with amines using hydroxylamine hydrochloride as an inorganic catalyst // Angewandte Chemie-International Edition, V.51, №6, 2012, p.1383-1386]. Недостатком этих способов является использование труднодоступных катализаторов или соединений, обладающих сильнокислыми свойствами, ограничивающими выбор исходных реагентов для реакции и затрудняющих выделение продуктов реакции.
Известен способ получения амидов переамидированием первичных карбоксамидов с использованием в качестве катализаторов трифлата скандия и хлорида циркония [Dineen Т.Α., Zajac M.A, Myers A.G.. Efficient Transamidation of Primary Carboxamides by in Situ Activation with N,N-Dialkylformamide Dimethyl Acetais // Journal of the American Chemical Society, V.128, 2006, p.16406-16409]. Недостатком этого способа является использование труднодоступных катализаторов.
Известен способ переамидирования амидов с применением в качестве катализаторов L-пролина [Rao S.Ν., Mohan D.С, Adimurthy S.. L-Proline: An Efficient Catalyst for Transamidation of Carboxamides with Amines // Organic Letters, V.15, №7, 2013, p.1496-1499], реакция протекает в течение 36 часов. Недостатком этих способов является использование трудноотделимого от реакционной массы и достаточно дорогостоящего катализатора.
Известен способ переамидирования диметилформамида при катализе B(OCH2CF3)3 [Lanigan R.M., Starkov P., Sheppard T.D. Direct Synthesis of Amides from Carboxylic Acids and Amines by Using Heterogeneous Catalysts: Evidence of Surface Carboxylates as Activated Electrophilic Species // Chem. Cat. Chem., V.5, №10, 2013, p.2832-2834]. Недостатком способа является то, что применение данного соединения накладывает ограничение на выбор первичных амидов.
Известен способ переамидирования амидов в циклогексане при 80°C в течение 5-24 часов в присутствии каталитических количеств цирконоцендихлорида (Cp2ZrCl2). Для низших амидов реакцию проводят при температуре до 30°C [Atkinson В.N., Chhatwal A.R., Lomax H.V., Walton J.W., Williams J.M.. Transamidation of primary amides with amines catalyzed by zirconocene dichloride // Chem. Commun, V.48, №95, 2012, p.11626-11628]. Недостатком этого способа является использование труднодоступного и дорогостоящего катализатора.
Известен способ переамидирования амидов широким рядом аминов при катализе оксидом церия при 160°С, при этом получают соответствующие N-алкиламиды без использования растворителя [Masazumi Tamura, Takuya Tonomura, Ken-ichi Shimizu and Atsushi Satsuma. Transamidation of amides with amines under solvent-free conditions using a CeO2 catalyst // Green Chem., V.14, 2012, p.717-724]. Недостатком этого способа является использование труднодоступного и дорогостоящего катализатора.
Наиболее близким аналогом предлагаемого изобретения является способ переамидирования амидов при 140-160°C аминами (мольное соотношение 1:2 соответственно) при катализе мезопористыми сферами оксида ниобия (5% мол.) в течение 8-24 часа. Эту реакцию можно проводить без растворителя, и она применима к широкому ряду первичных амидов и аминов. Катализатор обладает высокой стабильностью и для повторного использования [Ghosh Subhash Chandra, Li Cheng Chao, Hua Chun Zeng, Anqi Chen. Mesoporous Niobium Oxide Spheres as an Effective Catalyst for the Transamidation of Primary Amides with Amines // Advanced Synthesis & Catalysis, V.356, №3, 2014, p.475-484]. Недостатками этого способа являются использование труднодоступного и дорогостоящего катализатора, достаточно высокие температуры процесса, его высокая длительность. В ряде случаев продукты образуются с невысокими выходами.
Задачей заявляемого способа является разработка технологичного способа получения амидов карбоновых кислот с высоким выходом.
Техническим результатом является упрощение способа переамидирования амидов карбоновых кислот.
Поставленный результат достигается в способе переамидирования амидов карбоновых кислот, заключающемся во взаимодействии амида карбоновой кислоты с амином при нагревании в присутствии катализатора, при этом в качестве амида карбоновой кислоты используют формамид, ацетамид, диметилформамид или изовалерамид, в качестве амина - циклогексиламин, пиперидин, морфолин или 2-аминоэтанол, а в качестве катализатора - наночастицы меди и процесс протекает при мольном соотношении амид карбоновой кислоты : амин : катализатор, равном 1:1-1.2:0.02-0.05, при температуре 20-100°C в течение 0.5-3 часов.
Сущность изобретения заключается в получении амидов карбоновых кислот по реакции переамидирования карбоксамидов аминами.

При этом в качестве катализатора применяется либо заранее приготовленные наночастицы меди, либо коллоидный раствор меди может быть приготовлен в самой реакционной массе in situ реакцией обмена хлорида меди (II) и безоболочечного стального магнитного элемента магнитной мешалки, вращение которого и неводная среда предотвращают образование крупных частиц меди.
Способ осуществляется следующим образом. Плоскодонную колбу на магнитной мешалке с амидом карбоновой кислоты, амином и катализатором, загруженных исходя из мольного соотношения амид карбоновой кислоты: амин: катализатор, равном 1:1-1.2:0.02-0.05, нагревают при температуре 20-100°C в присутствии катализатора. При этом выделяется аммиак или диметиламин. По окончании выделения аммиака (диметиламина) через 0.5-3 часа отгоняют избыток исходного амина, остаток перегоняют.
При использовании в качестве исходного вещества формамида реакция начинается уже при 20°C, интенсивное выделение аммиака происходит при 40°C. Для переамидирования ацетамида и других замещенных амидов требуется повышение температуры до 40-100°C.
Протекание реакции диметилацетамида и формамида с анилином даже при температурах выше 100°C осуществить не удалось. Таким образом, на скорость протекания реакции переамидирования по этому методу оказывает сильное влияние основность использованного амина.
Изобретение иллюстрируется следующими примерами.
Пример 1
Циклогексилформамид 
В плоскодонную колбу на магнитной мешалке загружают смесь 5 г (0,11 моль) формамида и 0.9 г (0,0055 моль) CuCl2·2H2O и перемешивают стальным магнитным элементом без оболочки в течение 30 минут. После этого при температуре 20°C добавляют 10,7 мл (0,11 моль) циклогексиламина. В течение 30 минут при температуре 20°C происходит выделение аммиака, после чего продукт перегоняют, собирая фракцию с т.кип. 115-116°C/30 мм рт.ст. Получают 12,7 г (0,089 моль, 90%) циклогексилформамида, т.пл. 35-38°C (лит. т.пл. 36-41°C).
Спектр ЯМР 1Н, δ, м.д.: 1,11-1,81 м (10Н, 5CH3), 3.60-3.69 м (III, CN), 7,67 д (1Н, ΝΗ, J=6,6 Гц), 7,88 с (1Н, СНО).
Пример 2
Циклогексилформамид 
В плоскодонную колбу на магнитной мешалке загружают 0,13 г (0,002 моль) наночастиц меди и 5 мл (0,11 моль) формамида, затем добавляют 11.9 г (0,12 моль) циклогексиламина и выдерживают при перемешивании 30 минут при 20-40°C (до прекращения выделения аммиака). Затем избыток циклогексиламина отгоняют, остаток перегоняют. Получают 12,7 г (0,1 моль, 90,9%) циклогексилформамида.
Спектр ЯМР 1H, δ, м.д.: 1,11-1,81 м (10Н, 5СН3), 3.60-3.69 м (1Н, CN), 7,67 д (1Н, NH, J=6,6 Гц), 7,88 с (1Н, СНО).
Пример 3
Циклогексилацетамид 
В плоскодонную колбу на магнитной мешалке загружают 5 г (0,085 моль) ацетамида, 0.44 г CuCl2·2H2O (0,0026 моль) и 8,2 г (0,085 моль) циклогексиламина и перемешивают при 60°C в течение 1 часа до прекращения выделения аммиака. Затем продукт перегоняют, получают 10,3 г (0,073 моль, 86%) циклогексилацетамида, т.кип. 289-292°C (лит. т.кип. 291-293°C).
Пример 4
Формилморфолин 
В плоскодонную колбу на магнитной мешалке загружают смесь 5 г (0,11 моль) формамида, 0.9 г (0,0055 моль) CuCl2·2H2O и перемешивают стальным магнитным элементом без оболочки течение 30 минут. После этого при температуре 20°C добавляют 9,6 г (0,11 моль) морфолина и перемешивают при той же температуре в течение 30 минут до прекращения выделения аммиака. Затем продукт перегоняют, получают 10,7 г (0,094 моль, 85%) формилморфолина, т.кип. 238-241°C (лит. т.кип. 239-241°C, т.пл. 20-23°C).
Спектр ЯМР 1Н, δ, м.д.: 3.34 д т (4Н, 2CH2N, J1=9.3 Гц, J2=15.6 Гц), 3.51 д т (4Н, 2CH2O, J1=9.3 Гц, J2=15.8 Гц), 7,89 с (1Н, СНО).
Пример 5
Формилморфолин 
В плоскодонную колбу на магнитной мешалке загружают 5 г (0,067 моль) диметилформамида, 0.51 г (0,003 моль) CuCl2·2H2O и 5,8 г (0,067 моль) морфолина и нагревают смесь до 60°C в течение 1 часа, при этом выделяется диметиламин. Затем продукт перегоняют, получают 6,9 г (0,061 моль, 91%) формилморфолина, т.кип. 239-241°C. Спектр ЯМР 1Н, δ, м.д.: 3.34 д т (4Н, 2CH2N, J1=9.3 Гц, J2=15.6 Гц), 3.51 д т (4Н, 2CH2O, J1=9.3 Гц, J2=15.8 Гц), 7,89 с (1Н, СНО).
Пример 6
Формилпиперидин
В плоскодонную колбу на магнитной мешалке загружают 5 г (0,11 моль) формамида, 0,25 г (0,004 моль) наночастиц меди и 11 г (0,13 моль) пиперидина и выдерживают смесь при перемешивании при 20-40°C в течение 30 минут, при этом выделяется аммиак. Затем отгоняют избыток пиперидина, остаток перегоняют, получают 11,9 г (0,103 моль, 94%) формилпиперидина, т.кип. 222°C (лит т.кип. 222°C).
Спектр ЯМР 1H δ, м.д.: 1.46-1.66 м (6Н, 3СН2), 3.31 д т (4Н, 2CH2N, J1=11 Гц, J2=26 Гц), 7,80 с (1H, СНО).
Пример 7
2-Гидроксиэтилформамид 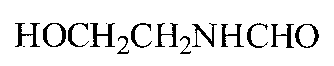
В плоскодонную колбу на магнитной мешалке загружают 5 г (0,11 моль) формамида, 0,25 г (0,004 моль) наночастиц меди и 6,8 г (0,12 моль) 2-аминоэтанола и выдерживают смесь при перемешивании при 20-40°C в течение 1 часа, при этом выделяется аммиак. Затем отгоняют избыток 2-аминоэтанола, остаток перегоняют, получают 8,1 г (0,091 моль, 83%) 2-гидроксиэтилформамида, т.кип. 347-350°C (лит. т.кип. 349.5°C).
Пример 8
Пиперидид 3-метилбутановой кислоты 
В плоскодонную колбу на магнитной мешалке загружают 5 г (0,05 моль) амида 3-метилбутановой кислоты, 0.06 г (0,001 моль) наночастиц меди и 4,2 г (0,05 моль) пиперидина и выдерживают смесь при перемешивании при 80-100°C в течение 3 часов, при этом выделяется аммиак. Затем продукт перегоняют, получают 7,3 г (0,043 моль, 85%) пиперидида 3-метилбутановой кислоты, т.кип. 142-145°C/20 мм рт.ст.
Спектр ЯМР 1Н, δ, м.д.: 0,87 м (6Н, 2СН3), 1,59 с (2Н, СН2), 1,58 д (2Н, СН2, J=4,2 Гц), 2,06 м (2Н, СН2СО); 3,38 д т (4Н, (CH2)2N, J1=27.2 Гц, J2=9.6 Гц).
Таким образом, разработан новый способ синтеза амидов карбоновых кислот, заключающийся в переамидировании амидов карбоновых кислот в присутствии наночастиц меди и протекающий в мягких условиях с высоким выходом.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ АМИДОВ КАРБОНОВЫХ КИСЛОТ | 2014 |
|
RU2565059C1 |
| СПОСОБ ПОЛУЧЕНИЯ ЦИКЛОАЛКИЛАМИНОВ | 2010 |
|
RU2425828C1 |
| Способ получения бензанилида | 2019 |
|
RU2712053C1 |
| Способ получения ароматических амидов 1-адамантанкарбоновой кислоты | 2019 |
|
RU2698193C1 |
| СПОСОБ ПОЛУЧЕНИЯ АНИЛИНА ИЛИ ЕГО ПРОИЗВОДНЫХ | 2010 |
|
RU2433116C1 |
| СПОСОБ ПОЛУЧЕНИЯ ТРЕТИЧНЫХ АМИНОВ | 2012 |
|
RU2499793C1 |
| СПОСОБ ПОЛУЧЕНИЯ ВТОРИЧНЫХ АМИНОВ | 2013 |
|
RU2523456C1 |
| СПОСОБ ПОЛУЧЕНИЯ НАСЫЩЕННЫХ КАРБОНОВЫХ КИСЛОТ | 2013 |
|
RU2529026C1 |
| СПОСОБ ПОЛУЧЕНИЯ АРИЛХЛОРСУЛЬФОНИЛБЕНЗАМИДОВ ИЗ БЕНЗОЙНЫХ КИСЛОТ | 2006 |
|
RU2298548C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПЕРВИЧНЫХ ИЛИ ВТОРИЧНЫЙ СПИРТОВ | 2013 |
|
RU2519950C1 |
Изобретение относится к способу получения производных карбоновых кислот, в частности к новому способу переамидирования амидов карбоновых кислот. Способ осуществляют путем взаимодействия амида карбоновой кислоты с амином при нагревании в присутствии катализатора - наночастицы меди. В качестве амида карбоновой кислоты используют формамид, ацетамид, диметилформамид или изовалерамид, в качестве амина - циклогексиламин, пиперидин, морфолин или 2-аминоэтанол. Процесс протекает при мольном соотношении амид карбоновой кислоты : амин : катализатор, равном 1:1-1.2:0.02-0.05, при температуре 20-100°C в течение 0.5-3 часов. Технический результат - упрощение способа переамидирования амидов карбоновых кислот за счет использования более дешевого катализатора и проведения процесса в более мягких условиях. 8 пр.
Способ переамидирования амидов карбоновых кислот, заключающийся во взаимодействии амида карбоновой кислоты с амином при нагревании в присутствии катализатора, отличающийся тем, что в качестве амида карбоновой кислоты используют формамид, ацетамид, диметилформамид или изовалерамид, в качестве амина - циклогексиламин, пиперидин, морфолин или 2-аминоэтанол, а в качестве катализатора - наночастицы меди и процесс протекает при мольном соотношении амид карбоновой кислоты : амин : катализатор, равном 1:1-1.2:0.02-0.05, при температуре 20-100°C в течение 0.5-3 часов.
| GHOSH SUBHASH CHANDRA et al., Mesoporous Niobium Oxide Spheres as an Effective Catalyst for the Transamidation of Primary Amides with Amines, Advanced Synthesis & Catalysis, 2014, vol.356, no.3, p.475-484 | |||
| ПОПЛАВКОВЫЙ РЕГУЛЯТОР ПЛОТНОСТИ | 0 |
|
SU271093A1 |
| US 7154004 B2, 26.12.2006 | |||
| СПОСОБ ПОЛУЧЕНИЯ ЦИКЛОАЛКИЛАМИНОВ | 2010 |
|
RU2425828C1 |
Авторы
Даты
2015-08-10—Публикация
2014-07-22—Подача