Изобретение относится к химии аминов или их производных, а именно новому способу получения анилина и его производных общей формулы
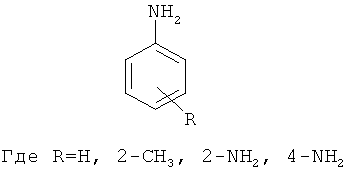
которые используются в качестве полупродуктов в органическом синтезе.
Известен способ получения анилина восстановлением нитробензола водородом под давлением в присутствии гетерогенного катализатора [Патент США 5616806, С07С 209/22, опубл. 1997; Патент США 4265834, С07С 85/11, опубл. 1981].
Недостатком этого метода является использование достаточно сложных технологических условий, неприменимых в лабораторных условиях.
Известен способ получения производных анилина восстановлением производных нитробензола полиметилгидросилоксаном в присутствии соединений родия или палладия в качестве катализатора [Ronald J. Rahaim, Robert E. Maleczka. Pd-Catalyzed Silicon Hydride Reductions of Aromatic and Aliphatic Nitro Groups // Org. Lett., Vol.7, No.22, - 2005, - pp.5087-5090], протекающий при температуре 25-70°C в течение 1-2 часов с выходами целевых продуктов 30-100%.
Недостатком этого метода является использование дорогостоящих катализаторов и малораспространенных реагентов.
Известен способ получения галогенсодержащих производных анилина восстановлением галогенированных производных нитробензола гидразингидратом на никеле Ренея, протекающий при температуре 60-70°С с выходом производных анилина 70-93% [В.Е.Leggetter, R.K.Brown. Reduction of monohalogenated nitrobenzenes with hydrazine and raney nickel. a convenient preparation of halogenated anilines // Can. J. Chem. Vol.38 - 1960. - p. 2363-2366].
Недостатком данного метода является то, что необходимо использование в качестве катализатора никеля Ренея, который готовится непосредственно перед синтезом из сплава никеля и алюминия, изготовление которого в лабораторных условиях невозможно.
Известен способ получения производных анилина восстановлением производных динитробензола гидразингидратом на никеле Ренея, протекающий при температуре 50-60°С с выходом производных анилина от 0,5 до 100% [Nagaraj Ayyangar, Uttam R. Kalkote, Ananda G. Lugade, Pandurang V. Nikrad, Vasant K. Sharma. Partial Reduction of Dinitroarenes to Nitroanilines with Hydrazine Hydrate // Bull. Chem. Soc. Jpn., 56, - 1983. - pp.3159-3164].
Недостатком данного метода является то, что необходимо использование в качестве катализатора никеля Ренея, который готовится непосредственно перед синтезом из сплава никеля и алюминия, изготовление которого в лабораторных условиях невозможно.
Наиболее близким к предлагаемому изобретению является способ получения соединений аналогичной структуры по реакции восстановления нитробензола и его производных гидразингидратом на никеле Ренея, протекающей при температуре 25-100°С. Выходы производных анилина 80-99% [Reductions with Hydrazine Hydrate Catalyzed by Raney Nickel. I. Aromatic Nitro Compounds to Amines. / D.Balcom, A.First // J. Am. Chem. Soc. Vol 57, p.4334].
Недостатком данного метода является то, что необходимо использование в качестве катализатора никеля Ренея, который готовится непосредственно перед синтезом из сплава никеля и алюминия, изготовление которого в лабораторных условиях невозможно. Кроме того, данный катализатор пирофорен при контакте с воздухом и дезактивируется при многократном использовании, а также в водной, кислой и щелочной среде.
Задачей предлагаемого изобретения является разработка технологичного метода синтеза анилина или его производных, протекающего с высоким выходом по исходному нитробензолу или его производному в мягких условиях с использованием доступных реагентов.
Техническим результатом является упрощение метода получения соединений заявляемой структурной формулы.
Поставленный технический результат достигается в новом способе получения анилина или его производных общей формулы

заключающемся в восстановлении нитробензола или его производного гидразингидратом в присутствии катализатора с последующим выделением, отличающемся тем, что в качестве производного нитробензола используют 2-нитротолуол, 2-нитроанилин, 4-нитроанилин, причем восстановление проводят в среде изопропилового спирта, а в качестве катализатора используют наночастицы металлов переменной валентности из ряда: железо, кобальт, никель или медь и процесс проводят при мольном соотношении наночастицы металлов переменной валентности:гидразингидрат:нитробензол или его производное 1:35÷170:10÷42, при температуре 20-80°С в течение 20-60 минут, при этом наночастицы железа, кобальта, или никеля получают в реакционной среде in situ восстановлением гидразингидратом их хлоридов или нитратов в щелочной среде, а наночастицы меди получают предварительно восстановлением хлорида меди II железом при перемешивании в системе растворителей формамид - вода при массовом соотношении CuCl2·2H2O:формамид:вода, равном 1:4:1.5.
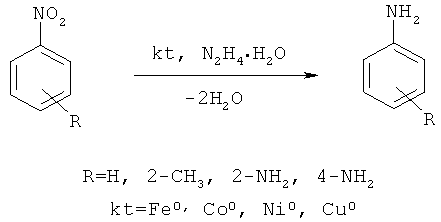
Сущностью метода является реакция получения анилина и его производных по реакции восстановления гидразингидратом нитробензола или его производных из ряда: 2-нитротолуол, 2-нитроанилин, 4-нитроанилин в среде изопропилового спирта в присутствии наночастиц металлов переменной валентности из ряда: железо, кобальт или никель, получаемых in situ из их хлоридов или нитратов гидразингидратом в щелочной среде, или в присутствии предварительно полученных наночастиц меди.
Способ осуществляется следующим образом.
В плоскодонную колбу, снабженную магнитной мешалкой и обратным холодильником, загружают рассчитанное количество водного раствора NaOH, изопропиловый спирт и требуемое количество гидразингидрата и нагревают смесь до 60-80°С, после чего порциями при интенсивном перемешивании прибавляют раствор соответствующего количества хлорида или нитрата металла переменной валентности из ряда железо, кобальт или никель в водном изопропиловом спирте с такой скоростью, чтобы избежать чрезмерно сильного кипения реакционной массы. По окончании полученный раствор выдерживают при кипении 10-30 мин. Возможно также использование каталитического количества предварительно приготовленной коллоидной меди. Приготовление проводят в плоскодонной колбе на магнитной мешалке с использованием железного (стального) магнитного элемента без оболочки. В колбу загружают формамид и водный раствор CuCl2×2H2O, соблюдая массовое соотношение CuCl2×2H2O:формамид:вода, равное 1:4:1.5, и нагревают реакционную смесь до 80-100°С при перемешивании 2-3 часа до прекращения образования тонкодисперсного осадка меди. Масса реагирующего железного (стального) магнитного элемента должна быть достаточной для завершения реакции обмена. По окончании реакции смесь при необходимости разбавляют небольшим количеством воды и фильтруют на воронке Бюхнера с бумажным фильтром, добиваясь прозрачности фильтрата. Осадок красного или рыжего цвета промывают водой для удаления формамида, отсасывают для удаления избыточной влаги. Полученная коллоидная медь используется для проведения реакции немедленно или может храниться достаточно долго в закрытой емкости.
После приготовления катализатора в реакционную смесь по каплям прибавляют рассчитанное количество нитробензола или его производного, не допуская бурного кипения и вспенивания реакционной смеси. При бурном протекании реакции рекомендуется снизить температуру ее проведения. По окончании прибавления нитробензола или его производного реакционную массу выдерживают при кипении 10-15 минут, фильтруют от механических примесей, отгоняют изопропанол, отделяют водный слой, органический слой перегоняют при атмосферном давлении или в вакууме водоструйного насоса, или перекристаллизовывают из изопропанола. Выходы продуктов заявляемой структурной формулы составляют 65-97.5%. Свойства синтезированного анилина и его производных соответствуют литературным данным.
Восстановление с использованием наночастиц никеля проводилось при постепенном прибавлении нитробензола или его гомологов к суспензии наночастиц никеля в смеси гидразингидрата и изопропанола при температуре 20-80°С. При повышенных температурах (60-80°С) восстановление нитробензола протекает практически мгновенно с интенсивным экзотермическим эффектом, при этом побочного алкилирования образующегося анилина или его производных изопропанолом не происходит. Выход анилина приближается к количественному, потери продукта обусловлены процессом перегонки. Содержание анилина в перегнанном продукте по данным ГЖХ составляет 100%, причем цветность анилина низкая и не увеличивается несколько дней при стоянии в светлой прозрачной емкости.
Обнаружено, что стабилизации коллоидных растворов наночастиц металлов не требуется, что значительно упрощает и удешевляет предлагаемый способ восстановления. Полученные суспензии могут использоваться в качестве катализатора восстановления без выделения наночастиц. Так как и при синтезе катализатора, и восстановлении нитробензола или его гомологов используются одинаковые условия, весь процесс сводится к одностадийному синтезу, при котором катализатор образуется in-situ из доступных солей железа, кобальта или никеля.
Обнаружено, что оптимальным мольным соотношением нитробензол или его производное:гидразингидрат является 35÷170:10÷42, при этом обеспечивается как восстановление солей металлов переменной валентности до наночастиц соответствующих металлов, так и последующее полное гидрирование нитрогруппы нитробензола или его производного. Снижение мольного избытка гидразингидрата приводит к неполной конверсии нитробензола или его производного и снижению выхода и чистоты получаемых продуктов. Дальнейшее увеличение избытка гидразингидрата не влияет на выход анилина или его производных и является нецелесообразным.
Найдено, что массовое соотношение нитробензол или его производное:катализатор в разработанном способе достигает 42:1, что выгодно отличается от способа с использованием никеля Ренея (≈10:1). Дальнейшее увеличение данного соотношения нецелесообразно, так как значительно замедляется процесс восстановления, снижается конверсия нитробензола или его производного, ухудшается качество получаемых продуктов. Снижение соотношения нитробензол или его производное:катализатор менее 10:1 нецелесообразно, так как указанное соотношение является достаточным для проведения процесса восстановления.
Поскольку коллоидный раствор нестабилен при стоянии и наночастицы скапливаются в кластеры и оседают в виде хлопьевидного осадка, их можно отделить от реакционной массы фильтрованием. Обнаружено, что данный катализатор может быть использован многократно без существенной потери активности, если исключить возможность его контакта с воздухом. Отличием данного катализатора является также способность работать в водно-щелочной среде, дезактивирующей никель Ренея при длительном контакте. Контактирующие с воздухом коллоидные растворы наночастиц металлов в отличие от никеля Ренея не пирофорны.
Процесс восстановления при использовании наночастиц железа также характеризуется значительным тепловым эффектом и завершается в течение нескольких минут при температуре 40-80°С. Выход анилина составил 96%, но очевидно может быть повышен при оптимизации процесса выделения продукта.
Обнаружено, что в отличие от никеля и железа, при катализе наночастицами кобальта обнаружено образование наряду с анилином побочного N-фенилгидроксиламина, легко отделимого от анилина вследствие его низкой растворимости в изопропаноле. Свойства данного кристаллического вещества соответствуют литературным данным.
Обнаружено, что восстановление нитробензола коллоидным раствором меди характеризуется меньшим тепловым эффектом, чем в случае никеля и кобальта, и приводит к получению анилина с выходом 92%.
Повышение температуры реакции при катализе наночастицами никеля или кобальта нецелесообразно в связи с высокой скоростью восстановления и интенсивным экзотермическим эффектом.
Изобретение иллюстрируется следующими примерами.
Пример 1.
Анилин 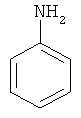
В плоскодонную колбу, снабженную магнитной мешалкой и обратным холодильником, загружают 0.4 г NaOH, 1 мл воды, 50 мл изопропилового спирта и 46 г (0.92 моль) гидразингидрата и нагревают до 60-80°С, после чего порциями при интенсивном перемешивании прибавляют раствор 1,25 г (0.0054 моль) NiCl2×6H2O или 1.55 г (0.0054 моль) Ni(NO3)2×6H2O в водном изопропиловом спирте с такой скоростью, чтобы избежать чрезмерно сильного кипения реакционной массы. По окончании полученный черный раствор выдерживают при кипении 10 мин, охлаждают и по каплям при температуре 20-60°С прибавляют 30 г (0.244 моль) нитробензола (мольное соотношение соль металла:гидразингидрат:нитробензол 1:170:42), не допуская бурного кипения и вспенивания смеси. При бурном протекании реакции рекомендуется снизить температуру ее проведения до 20°С. По окончании прибавления нитробензола реакционную массу выдерживают при кипении 20 минут, фильтруют от механических примесей, отгоняют изопропиловый спирт, отделяют водный слой, органический слой перегоняют при атмосферном давлении, получая 22.2 г (0.238 моль, 97.5%) анилина, т.кип. 183-184°С,  1.5860, лит. т.кип. 184°С,
1.5860, лит. т.кип. 184°С, 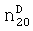 1.5863 [Alfa Aesar. Research Chemicals, Metals and Materials. 2006-2007. - 2766 p.].
1.5863 [Alfa Aesar. Research Chemicals, Metals and Materials. 2006-2007. - 2766 p.].
Пример 2.
Анилин 
Аналогично примеру 1, за 30-40 минут при 40-70°С из 0.5 г NaOH, 1 мл воды, 50 мл изопропилового спирта, 30 г (0.6 моль) гидразингидрата и 2.7 г (0.01 моль) FeCl3×6H2O получают коллоидный раствор железа, прикапывают 20 г (0.163 моль) нитробензола (мольное соотношение соль металла:гидразингидрат:нитробензол 1:60:16.3) и после выделения получают 14.5 г (0.156 моль, 96%) анилина, т.кип. 182-184°С, 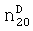 1.5862, лит.т.кип. 184°С,
1.5862, лит.т.кип. 184°С, 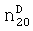 1.5863 [Alfa Aesar. Research Chemicals, Metals and Materials. 2006-2007. - 2766 p.].
1.5863 [Alfa Aesar. Research Chemicals, Metals and Materials. 2006-2007. - 2766 p.].
Пример 3.
Анилин 
Аналогично примеру 1, за 60 минут при 70-80°С из 0.5 г NaOH, 1 мл воды, 40 мл изопропилового спирта 17,5 г (0,35 моль) гидразингидрата и 2.4 г (0.01 моль) CoCl2×6H2O получают коллоидный раствор кобальта и прикапывают 12.3 г (0.1 моль) нитробензола (мольное соотношение соль металла:гидразингидрат:нитробензол 1:35:10). По окончании реакции реакционную массу охлаждают до 20°С, фильтруют, из фильтрата выделяют анилин аналогично примеру 1, т.кип. 183-185°С, 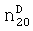 1.5865, лит. т.кип. 184°С,
1.5865, лит. т.кип. 184°С, 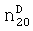 1.5863 5863 [Alfa Aesar. Research Chemicals, Metals and Materials. 2006-2007. - 2766 р.]. Выход 6.1 г (0.065 моль, 65%).
1.5863 5863 [Alfa Aesar. Research Chemicals, Metals and Materials. 2006-2007. - 2766 р.]. Выход 6.1 г (0.065 моль, 65%).
Отфильтрованный осадок дважды экстрагируют 20 мл кипящего изопропилового спирта, из фильтрата при охлаждении выпадает 3 г (0.028 моль) N-фенилгидроксиламина в виде бесцветных кристаллов, желтеющих при стоянии, т.пл. 81-83°С, лит. т.пл. 81°С [The Hydrogenating Activity of an Iridium Catalyst / K.Taya, // Chem. Commun., (14) 1966, p.464-465].
Пример 4.
Анилин 
Смесь 4 г (0.0233 моль) CuCl2×2H2O, 16 г формамида и 6 мл воды (массовое соотношение CuCl2×2H2O:формамид:вода, равном 1:4:1.5) помещают в плоскодонную колбу, снабженную стальным магнитным элементом массой 2.5 г и нагревают при интенсивном перемешивании до 100°С 2-3 часа. Наблюдается изменение цвета с синего на коричневый и далее в красноватый, после чего из пересыщенного коллоидного раствора начинает выпадать мелкодисперсный оранжево-красный осадок меди. По окончании реакции реакционную массу охлаждают и фильтруют на воронке Бюхнера через бумажный фильтр, промывают осадок небольшим количеством воды.
Аналогично примерам 1-3, за 60 минут при 80°С из 0.5 г (0.0078 моль) предварительно полученных наночастиц меди, 18 г (0.38 моль) гидразингидрата в 30 мл изопропилового спирта и 12.3 г (0.1 моль) нитробензола (мольное соотношение катализатор:гидразингидрат:нитробензол 1:46:12.8) получают 8.6 г (0.092 моль, 92%) анилина, т.кип. 182-184°С, 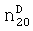 1.5862, лит. т.кип. 184°С,
1.5862, лит. т.кип. 184°С, 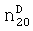 1.5863 [Alfa Aesar. Research Chemicals, Metals and Materials. 2006-2007. - 2766 p.].
1.5863 [Alfa Aesar. Research Chemicals, Metals and Materials. 2006-2007. - 2766 p.].
Пример 5.
2-Толуидин 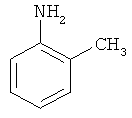
Аналогично примеру 1, за 40 минут при 50-80°С из 0.5 г NaOH, 1 мл воды, 30 мл изопропилового спирта, 17.5 г (0.35 моль) гидразингидрата и 2.4 г (0.01 моль) NiCl2×6H2O и 13.7 г (0.1 моль) 2-нитротолуола (мольное соотношение соль металла:гидразингидрат:2-нитротолуол 1:35:10) получают 6.55 г (0.061 моль, 83%) о-толуидина, т.кип. 197-200°С, 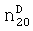 1.5717, лит. т.кип. 199-200°С,
1.5717, лит. т.кип. 199-200°С, 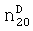 1.5720 5863 [Alfa Aesar. Research Chemicals, Metals and Materials. 2006-2007. - 2766 p.].
1.5720 5863 [Alfa Aesar. Research Chemicals, Metals and Materials. 2006-2007. - 2766 p.].
Пример 6.
о-Фенилендиамин 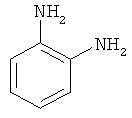
Аналогично примеру 1, за 50 минут при 60-80°С из 0.5 г NaOH, 1 мл воды, 30 мл изопропилового спирта, 17,5 г (0.35 моль) гидразингидрата и 0.8 г (0.0028 моль) Ni(NO3)2×6H2O и 13.8 г (0.1 моль) 2-нитроанилина (мольное соотношение соль металла:гидразингидрат:2-нитроанилин 1:125:35.7) получают 8.4 г (0.0775 моль, 77.5%) о-фенилендиамина, т.пл. 99-101°С, лит. т.пл. 100-102°С [Alfa Aesar. Research Chemicals, Metals and Materials. 2006-2007. - 2766 p.].
Пример 7.
п-Фенилендиамин 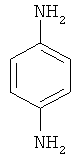
Аналогично примеру 1, за 45 минут при 60-80°С из 0.5 г NaOH, 1 мл воды, 30 мл изопропилового спирта, 17,5 г (0.35 моль) гидразингидрата и 0.8 г (0.0028 моль) Ni(NO3)2×6H2O и 13.8 г (0.1 моль) 4-нитроанилина (мольное соотношение соль металла:гидразингидрат:4-нитроанилин 1:125:35.7) получают 8.8 г (0.082 моль, 82%) п-фенилендиамина, т.пл. 138-140°С, лит. т.пл. 139-140°С 5863 [Alfa Aesar. Research Chemicals, Metals and Materials. 2006-2007. - 2766 p.].
Таким образом, вышеизложенные сведения свидетельствуют о выполнении при использовании заявленного изобретения следующей совокупности условий:
- средство, воплощающее заявленное изобретение при его осуществлении, предназначено для применения в различных отраслях промышленности;
- для заявленного изобретения в том виде, как оно охарактеризовано в независимом пункте нижеизложенной формулы изобретения, подтверждена возможность его осуществления с помощью вышеописанных в заявке или известных до даты приоритета средств и методов;
- средство, воплощающее заявленное изобретение при его осуществлении, способно обеспечить достижение технического результата.
Следовательно, заявленное изобретение соответствует требованию "промышленная применимость".
Выводы
Разработан новый способ получения анилина и его производных, протекающий с высоким выходом по исходному нитробензолу или его производным, сущностью которого является реакция восстановления гидразингидратом нитробензола или его производных из ряда: 2-нитротолуол, 2-нитроанилин, 4-нитроанилин в среде изопропилового спирта в присутствии наночастиц металлов переменной валентности из ряда: железо, кобальт или никель, получаемых in situ из их хлоридов или нитратов гидразингидратом в щелочной среде, или в присутствии предварительно полученных наночастиц меди. Свойства синтезированных соединений соответствуют литературным данным.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ЦИКЛОАЛКИЛАМИНОВ | 2010 |
|
RU2425828C1 |
| СПОСОБ ПОЛУЧЕНИЯ НАСЫЩЕННЫХ КАРБОНОВЫХ КИСЛОТ | 2013 |
|
RU2529026C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ НОРБОРНАНА | 2011 |
|
RU2456262C1 |
| СПОСОБ СЕЛЕКТИВНОГО ПОЛУЧЕНИЯ N-МЕТИЛ-ПАРА-ФЕНЕТИДИНА | 2011 |
|
RU2471771C1 |
| СПОСОБ СЕЛЕКТИВНОГО ПОЛУЧЕНИЯ N-МЕТИЛ-ПАРА-АНИЗИДИНА | 2011 |
|
RU2472774C1 |
| СПОСОБ СЕЛЕКТИВНОГО ПОЛУЧЕНИЯ N-МЕТИЛ-ПАРА-АНИЗИДИНА | 2012 |
|
RU2508288C1 |
| ПОЛУЧЕНИЕ АМИНОНИТРИЛОВ (ВАРИАНТЫ) | 1999 |
|
RU2220132C2 |
| СПОСОБ ПОЛУЧЕНИЯ АРОМАТИЧЕСКИХ ДИАМИНОВ, ТРИАМИНОВ ИЗ АРОМАТИЧЕСКИХ НИТРОСОЕДИНЕНИЙ | 2013 |
|
RU2549618C1 |
| СПОСОБ ПОЛУЧЕНИЯ АРОМАТИЧЕСКИХ АМИНОВ ВОССТАНОВЛЕНИЕМ СООТВЕТСТВУЮЩИХ НИТРОСОЕДИНЕНИЙ | 2001 |
|
RU2207335C2 |
| СПОСОБ ПОЛУЧЕНИЯ N-МЕТИЛАНИЛИНА | 2003 |
|
RU2240308C1 |
Изобретение относится к способу получения анилина и его производных общей формулы (I). Способ осуществляют путем восстановления нитробензола или его производного гидразингидратом в присутствии катализатора с последующим выделением продуктов. В качестве производного нитробензола используют 2-нитротолуол, 2-нитроанилин, 4-нитроанилин, причем восстановление проводят в среде изопропилового спирта, а в качестве катализатора используют наночастицы металлов переменной валентности из ряда: железо, кобальт, никель или медь. Процесс проводят при мольном соотношении наночастицы металлов переменной валентности:гидразингидрат:нитробензол или его производное 1:35÷170:10÷42, при температуре 20-80°С в течение 20-60 минут. При этом наночастицы железа, кобальта или никеля получают in situ восстановлением гидразингидратом их хлоридов или нитратов в щелочной среде, а наночастицы меди получают предварительно восстановлением хлорида меди II железом при перемешивании в системе растворителей формамид - вода при массовом соотношении CuCl2·2H2O:формамид:вода, равном 1:4:1.5. Технический результат - повышение выхода производных анилина. 2 з.п. ф-лы.
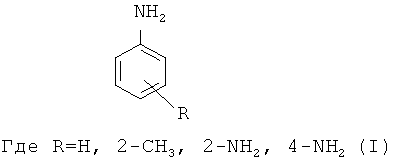
1. Способ получения анилина или его производных общей формулы
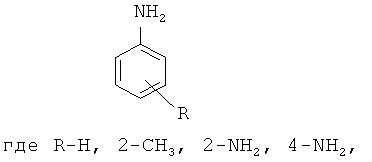
заключающийся в восстановлении нитробензола или его производного гидразингидратом в присутствии катализатора с последующим выделением, отличающийся тем, что в качестве производного нитробензола используют 2-нитротолуол, 2-нитроанилин, 4-нитроанилин, причем восстановление проводят в среде изопропилового спирта, а в качестве катализатора используют наночастицы металлов переменной валентности из ряда: железо, кобальт, никель или медь и процесс проводят при мольном соотношении наночастицы металлов переменной валентности : гидразингидрат : нитробензол или его производное 1 : 35÷170 : 10÷42, при температуре 20-80°С в течение 20-60 мин.
2. Способ по п.1, отличающийся тем, что наночастицы железа, кобальта или никеля получают в реакционной среде in situ восстановлением гидразингидратом их хлоридов или нитратов в щелочной среде.
3. Способ по п.1, отличающийся тем, что наночастицы меди получают предварительно восстановлением хлорида меди II железом при перемешивании в системе растворителей формамид - вода при массовом соотношении CuCl2·2H2O : формамид : вода, равном 1 : 4 : 1,5.
| D | |||
| BALCOM, A | |||
| FIRST: "Reduction witch Hydrazine Hydrate Catalyzed by Raney Nickel | |||
| I | |||
| Aromatic Nitro Compounds to Amines" JOURNAL OF THE AMERICAN CHEMICAL SOCIETY | |||
| US, 1953, v | |||
| Фальцовая черепица | 0 |
|
SU75A1 |
| HAN, ВYUNG НЕЕ; SHIN, DAE HYUN; LEE, HYUN RO: "Reduction of aromatic nitro group by activated Cu-Zn-NHNH.HO in | |||
Авторы
Даты
2011-11-10—Публикация
2010-05-06—Подача