Настоящее изобретение относится к новому полиморфу - агонисту вазопрессина V2, к фармацевтической композиции, содержащей его, и к его применению в терапии.
Нейрофизеальные гормоны вазопрессин (VP) и окситоцин (OT) представляют собой циклические нонапептиды, секретируемые задней долей гипофиза. Известны три подтипа рецепторов VP, и они обозначаются как V1a, V1b и V2 рецепторы. До сих пор хорошо охарактеризован только один OT рецептор.
V1a, V1b и V2, также как и OT рецепторы, представляют собой члены суперсемейства семи трансмембранных рецепторов, известных как сопряженные с G-белком рецепторы. Вазопрессин воздействует на кровеносные сосуды, где он является эффективным сосудосужающим средством, и на почки, где он промотирует обратный захват воды, приводя к противодиуретическому эффекту. Клеточные рецепторы, которые опосредуют указанные два действия, были охарактеризованы, и было показано, что они отличаются. Противодиуретическое действие опосредовано рецептором вазопрессина типа-2, обычно называемым V2 рецептором. Агенты, которые могут взаимодействовать с V2 рецептором и активировать его таким же образом, как вазопрессин, называют агонистами V2 рецептора (или просто агонистами V2). Такие агенты обладают противодиуретическим действием. Если указанные агенты селективно взаимодействуют с V2 рецептором, а не с другими подтипами рецепторов вазопрессина, тогда они не будут обладать гипертензивным действием вазопрессина. Это свойство было бы важным с точки зрения безопасности и сделало бы такие агенты привлекательными для лечения болезненных состояний человека, характеризующихся полиурией (что в рассматриваемом описании означает избыточное выделение мочи).
Существует необходимость в селективных агонистах рецептора вазопрессина V2, которые можно было бы применять в медицине. Известны как пептидные, так и непептидные агонисты V2. Примером пептидного агониста V2 является десмопрессин (известный также как [1-десамино, D-Arg8], вазопрессин, Minirin™, DDAVP™), который представляет собой пептидный аналог вазопрессина. Примеры непептидных аналогов агонистов вазопрессина V2 раскрыты, например, в международных патентных заявках WO 97/22591, WO 99/06403, WO 99/06409, WO 00/46224, WO 00/46225, WO 00/46227, WO 00/46228, WO 02/00626 и в статье Yea et al. в Journal of Medicinal Chemistry (2008), 51(24), 8124-8134.
Помимо его антидиуретических действий, десмопрессин применяют для повышения концентрации в крови коагуляционных белков, известных как фактор VIII и фактор фон Виллебранда. С клинической точки зрения это делает десмопрессин полезным при лечении гемофилии A и болезни фон Виллебранда. Аналогичные применения были бы возможны для других агонистов V2.
При приготовлении фармацевтических композиций важно, чтобы активное соединение было бы в форме, в которой им удобно манипулировать и обрабатывать его для получения коммерчески применимого процесса изготовления. Соответственно, важными факторами являются химическая стабильность и физическая стабильность активного соединения. Активное соединение и содержащие его композиции должны быть способны эффективно храниться в течение приемлемого промежутка времени, без проявления каких-либо заметных изменений в физико-химических характеристиках (например, в химическом составе, плотности, гигроскопичности и растворимости) активного соединения.
Кроме того, если активное соединение подлежит включению в лекарственную форму для перорального введения, такую как таблетки, желательно, чтобы активное соединение можно было легко измельчать, получая порошки с хорошими свойствами сыпучести, что способствовало бы процессу изготовления.
Известно, что приготовление конкретной твердой формы фармацевтического ингредиента может влиять на многие аспекты характеристик его твердого состояния и предоставлять преимущества с точки зрения растворимости, скорости растворения, химической стабильности, механических свойств, технической осуществимости, возможностей обработки, фармакокинетики и биодоступности. Некоторые из них раскрыты в "Handbook of Pharmaceutical Salts; Properties, Selection and Use", P. Heinrich Stahl, Camille G. Wermuth (Eds.) (Verlag Helvetica Chimica Acta, Zurich). Способы приготовления форм в твердом состоянии раскрыты также в "Practical Process Research and Development", Neal G. Anderson (Academic Press, San Diego) и в "Polymorphism: In the Pharmaceutical Industry", Rolf Hilfiker (Ed) (Wiley VCH). Полиморфизм в фармацевтических кристаллах раскрыт Byrn (Byrn, S.R., Pfeiffer, R.R., Stowell, J.G., "Solid-State Chemistry of Drugs", SSCI Inc., West Lafayette, Indiana, 1999), Brittain, H.G., "Polymorphism in Pharmaceutical Solids", Marcel Dekker, Inc., New York, Basel, 1999) или Bernstein (Bernstein, J., "Polymorphism in Molecular Crystals", Oxford University Press, 2002).
В международной патентной заявке WO 2001/049682 (PCT/GB 2001/000023) раскрыт новый класс агонистов вазопрессина, которые демонстрируют высокую селективную эффективность в отношении V2 рецептора. Один из таких агонистов вазопрессина, раскрытый в PCT/GB 2001/000023, представляет собой 1-(2-метил-4-(2,3,4,5-тетрагидро-1-бензазепин-1-илкарбонил)бензилкарбамоил)-L-пролин-N,N-диметиламид [CAS 347887-36-9]. Получение 1-(2-метил-4-(2,3,4,5-тетрагидро-1-бензазепин-1-илкарбонил)бензилкарбамоил)-L-пролин-N,N-диметиламида, раскрытое в PCT/GB 2001/000023, приводит к получению аморфного твердого вещества, которое, как было обнаружено, является гигроскопичным по данным гравиметрического парофазного сорбционного анализа (GVA).
Использование сканирующей электронной микрографии (SEM) для указанной аморфной формы показывает, что она состоит из нерегулярных, главным образом крупных (>5 мкм в диаметре) агрегатов. Такие свойства указанной аморфной формы делают ее менее подходящей для использования в процессе изготовления.
Заявители использовали различные способы, известные специалистам и раскрытые в (WO 2001/049682, WO 2002/000626 и у Yea et al, "New Benzylureas as a Novel Series of Potent, Non-peptidic Vasopressin V2 Receptor Agonists", Journal of Medicinal Chemistry (2008), 51(24), 8124-8134) в применении к синтезу 1-(2-метил-4-(2,3,4,5-тетрагидро-1-бензазепин-1-илкарбонил)бензилкарбамоил)-L-пролин-N,N-диметиламида, но все они приводили к получению аморфного твердого вещества (называемого здесь и далее "аморфной формой"). В свете указанных исследований кажется крайне маловероятным, что когда-либо может быть получена кристаллическая форма 1-(2-метил-4-(2,3,4,5-тетрагидро-1-бензазепин-1-илкарбонил)бензилкарбамоил)-L-пролин-N,N-диметиламида.
Однако неожиданно было обнаружено, что можно получить стабильную кристаллическую твердую форму 1-(2-метил-4-(2,3,4,5-тетрагидро-1-бензазепин-1-илкарбонил)бензилкарбамоил)-L-пролин-N,N-диметиламида (здесь и далее именуемую как "кристаллическая форма"), которая обладает благоприятными физико-химическими свойствами, например, в отношении химической стабильности, гигроскопичности, возможностей обработки, морфологии и технической осуществимости.
Способ, используемый для получения кристаллической формы, является необычным. Если 1-(2-метил-4-(2,3,4,5-тетрагидро-1-бензазепин-1-илкарбонил)бензилкарбамоил)-L-пролин-N,N-диметиламид растворяют в системе растворителя, из которого он должен кристаллизоваться, например в смеси ацетон/вода, он демонстрирует неожиданное и удивительное поведение, которое обычно было бы связано с поведением неионного поверхностно- активного агента. Поведение, характерное для поверхностно- активного агента, обычно наблюдают у молекул, которые окружены гидратной оболочкой при более низких температурах, что способствует их полной растворимости. Повышение температуры вызывает разрыв водородных связей, и растворимость соединений быстро снижается, что приводит к выделению соединения из раствора в виде масла. Применяя терминологию, используемую для поверхностно активных агентов, такое разделение фаз и неожиданное помутнение при повышении температуры известно как "температура помутнения".
Несмотря на тот факт, что строение 1-(2-метил-4-(2,3,4,5-тетрагидро-1-бензазепин-1-илкарбонил)бензилкарбамоил)-L-пролин-N,N-диметиламида значительно отличается от хорошо известных ионных поверхностно-активных агентов, таких как, например, Triton X-100, "температура помутнения" примерно при 38°C наблюдается, если нагревают раствор 1-(2-метил-4-(2,3,4,5-тетрагидро-1-бензазепин-1-илкарбонил)бензилкарбамоил)-L-пролин-N,N-диметиламида в смеси ацетон/вода (20/80). По аналогии с прецедентом для поверхностно-активных агентов, но не связываясь с какой-либо конкретной теорией, можно предположить, что гидратная оболочка, окружающая соединение, будет восстанавливаться ниже температуры помутнения, и предположить, что такое повышение молекулярной организации становится важной структурной прелюдией к кристаллизации гидрата. Утрата гидратной оболочки будет стимулировать разделение фаз и нарушение молекулярной организации, что станет интуитивно препятствовать образованию кристаллического гидрата. Такое поведение является необычным, и его нельзя было ожидать от соединения, такого как 1-(2-метил-4-(2,3,4,5-тетрагидро-1-бензазепин-1-илкарбонил)бензилкарбамоил)-L-пролин-N,N-диметиламид. Типичное поведение неионных поверхностно-активных агентов раскрыто в публикациях, таких как M. Alauddin, T. Parvin & T. Begum, Journal of Applied Sciences, (2009), 9, 2301-2306; P. Huibers, D. Shah & A. Katritzky, Journal of Colloid and Interface Science, (1997), 193, 132-136; T. Inoue, H. Ohmura & D. Murata, Journal of Colloid and Interface Science, (2003), 258, 374-382; T. Iwanaga & H. Kunieday, Journal of Colloid and Interface Science, (2000), 227, 349-355; H. Schott, Colloids and Surfaces A, (2001), 186, 129-136; и D. Myers, 2005, Surfactant Science and Technology, 3rd Edition, Oxford University Press, New York, ISBN:978-0-471-68024-6.
Далее раскрыт ряд преимуществ, связанных с кристаллической формой. Исследования кристаллической формы с помощью сканирующей электронной микроскопии (SEM) демонстрирует тот факт, что она обладает регулярной прямоугольной морфологией. Такая стабильная морфология позволяет обеспечить лучший контроль за процессом получения и упростить процесс изготовления таблеток. Например, таблетки, содержащие кристаллическую форму, можно получить, используя простой процесс прямого таблетирования. Попытки получения таблеток из аморфной формы оказываются неудачными.
К преимуществам кристаллической формы относится то, что она гораздо менее гигроскопична, чем аморфная форма. На фиг.9 представлена GVA изотерма сорбции/десорбции воды для кристаллической формы, и на фиг.10 представлена кинетика сорбции/десорбции воды. Представленные результаты свидетельствуют о том, что не происходит заметного захвата воды в интервале значений 40% относительной влажности (RH) и 90% RH (приблизительно 0,3% масс./масс.) кристаллической формой. Также не происходит никаких изменений в твердой форме на протяжении всего интервала времени поглощения воды. Аналогичные результаты, представленные на фиг.7 и 8, свидетельствуют о том, что аморфная форма высоко гигроскопична и поглощает воду в объеме образца при хранении в условиях выше 30% RH (полное количество 14% в равновесном состоянии при 90% RH). Дополнительная демонстрация преимуществ отсутствия гигроскопичности у кристаллических форм представлена результатами изучения стабильности, представленными далее.
Кристаллические формы более стабильны, чем аморфные формы. Если оба вещества хранят в течение 6 месяцев при температуре 40°C и 75% относительной влажности, кристаллическая форма остается в виде белого порошка без изменений в содержании воды (3,8% по данным анализа Карла Фишера). Кроме того, отсутствует заметное разложение по данным измерений суммы примесей, которое возрастает всего лишь с 0,9% до 1,0% (ВЭЖХ). Однако аморфная форма становится стекловидной по внешнему виду и приобретает желтый цвет. Показано также увеличение содержания влаги с 1,3% до 5,7% по данным анализа Карла Фишера и более быстрое разложение с повышенными количествами содержания примесей с 1,5% до 3,7% (ВЭЖХ).
Было обнаружено, что аморфная форма захватывает органический растворитель, что затрудняет высушивание. Это является проблемой, так как, если соединение содержит слишком высокий уровень остаточного растворителя, это может сделать его непригодным для фармацевтического применения. Напротив, кристаллическая форма не захватывает органический растворитель, что означает, что его можно легко высушить, используя стандартные процедуры.
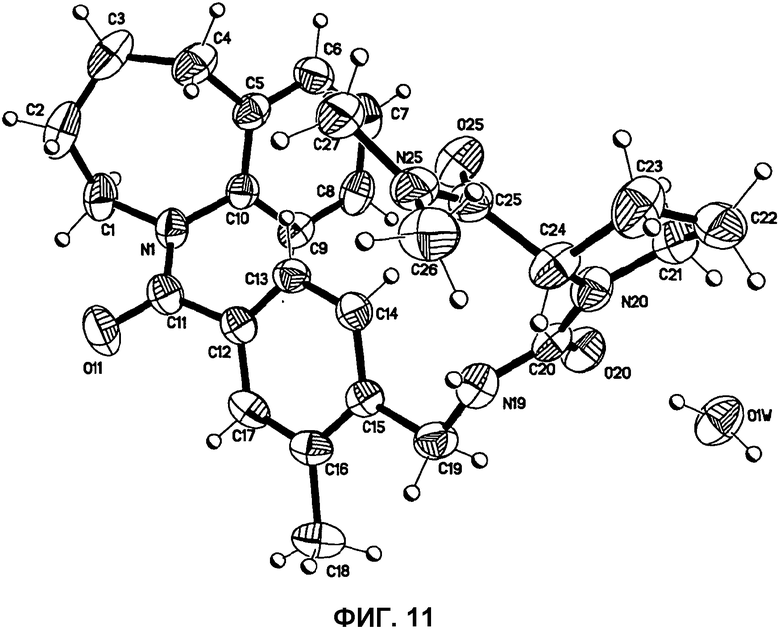
Кристаллическую форму выделили в виде монокристалла и провели рентгеноскопическое определение его кристаллической структуры. Результат представлен на фиг.11. Кроме подтверждения структуры указанного в заголовке соединения результаты рентгеноскопического исследования показывают, что кристаллическая решетка содержит одну молекулу воды на молекулу активного вещества, т.е. кристаллическая форма настоящего изобретения может существовать в виде гидрата, в частности моногидрата.
Таким образом, в соответствии с настоящим изобретением предложен кристаллический полиморф 1-(2-метил-4-(2,3,4,5-тетрагидро-1-бензазепин-1-илкарбонил)бензилкарбамоил)-L-пролин-N,N-диметиламида. В рассматриваемой заявке указанный полиморф может называться 'кристаллической формой'.
Название 1-(2-метил-4-(2,3,4,5-тетрагидро-1-бензазепин-1-илкарбонил)бензилкарбамоил)-L-пролин-N,N-диметиламид соответствует структуре, представленной формулой:
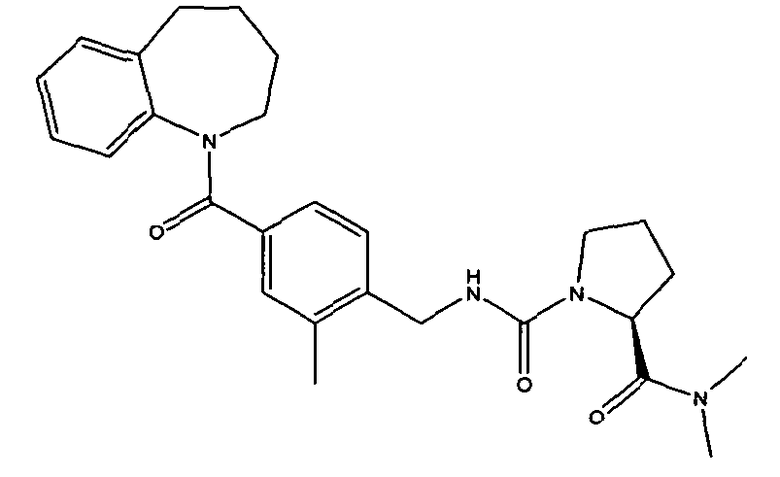
Настоящее изобретение включает сольваты (например, гидраты) кристаллической формы 1-(2-метил-4-(2,3,4,5-тетрагидро-1-бензазепин-1-илкарбонил)бензилкарбамоил)-L-пролин-N,N-диметиламида.
В одном из вариантов соединение настоящего изобретения обладает кристаллическими свойствами и является, предпочтительно, по меньшей мере на 50%, 60%, 70%, 80% или на 90% кристаллическим. В другом варианте соединение настоящего изобретения является на >95% кристаллическим. Кристалличность можно оценить, используя обычные методы рентгеновской дифрактометрии или дифференциальной сканирующей калориметрии.
До настоящего времени был выделен и охарактеризован один кристаллический полиморф соединения настоящего изобретения, который здесь именуют как 'форма 1'. В рассматриваемом описании пики на порошковой рентгеновской дифрактограмме (выраженные в градусах 2θ) измерены с использованием рентгеновского излучения меди с длиной волны 1,5406 Å (альфа1) и 1,5444 Å (альфа2).
В настоящем изобретении предложена кристаллическая форма (форма 1) 1-(2-метил-4-(2,3,4,5-тетрагидро-1-бензазепин-1-илкарбонил)бензилкарбамоил)-L-пролин-N,N-диметиламида, которая демонстрирует по меньшей мере следующие характеристические пики на порошковой рентгеновской дифрактограмме (Cu Kα излучение, выражено в градусах 2θ) на приблизительно:
(1) 5,5, 10,9, 14,2, 21,9 и 24,0, или
(2) 5,5, 10,6, 10,9, 14,2, 18,8, 21,9 и 24,0, или
(3) 5,5, 10,6, 10,9, 14,2, 15,1, 15,6, 18,8, 21,9 и 24,0.
Термин "приблизительно" в данном контексте означает, что существует некоторая неопределенность в измерениях градусов 2θ порядка ±0,2 (выражено в градусах 2θ).
В настоящем изобретении также предложена кристаллическая форма (форма 1) 1-(2-метил-4-(2,3,4,5-тетрагидро-1-бензазепин-1-илкарбонил)бензилкарбамоил)-L-пролин-N,N-диметиламида, характеристические пики которого на порошковой рентгеновской дифрактограмме (выражено в градусах 2θ), расположены на приблизительно 5,5, 10,6, 10,9, 14,2, 15,1, 15,6, 18,8, 21,9, 24,0, 26,0, 26,4 и 26,8.
В настоящем изобретении также предложена кристаллическая форма (форма 1) 1-(2-метил-4-(2,3,4,5-тетрагидро-1-бензазепин-1-илкарбонил)бензилкарбамоил)-L-пролин-N,N-диметиламида, порошковая рентгеновская дифрактограмма которого демонстрирует по меньшей мере следующие характеристические d-пространственные значения (Å) на приблизительно:
(1) 16,14, 8,11, 6,25, 4,72, 4,06 и 3,71, или
(2) 16,14, 8,37, 8,11, 6,25, 4,72, 4,06 и 3,71, или
(3) 16,14, 8,37, 8,11, 6,25, 5,86, 5,69, 4,72, 4,06 и 3,71.
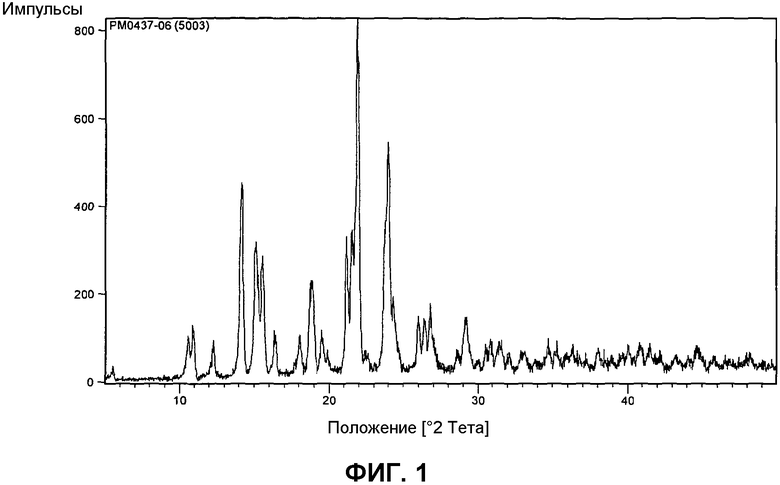
На фиг.1 представлена порошковая рентгеновская дифрактограмма формы 1 1-(2-метил-4-(2,3,4,5-тетрагидро-1-бензазепин-1-илкарбонил)бензилкарбамоил)-L-пролин-N,N-диметиламида. В настоящем изобретении также предложена кристаллическая форма (форма 1) 1-(2-метил-4-(2,3,4,5-тетрагидро-1-бензазепин-1-илкарбонил)бензилкарбамоил)-L-пролин-N,N-диметиламида, порошковая рентгеновская дифрактограмма которой по существу совпадает с представленной на фиг.1.
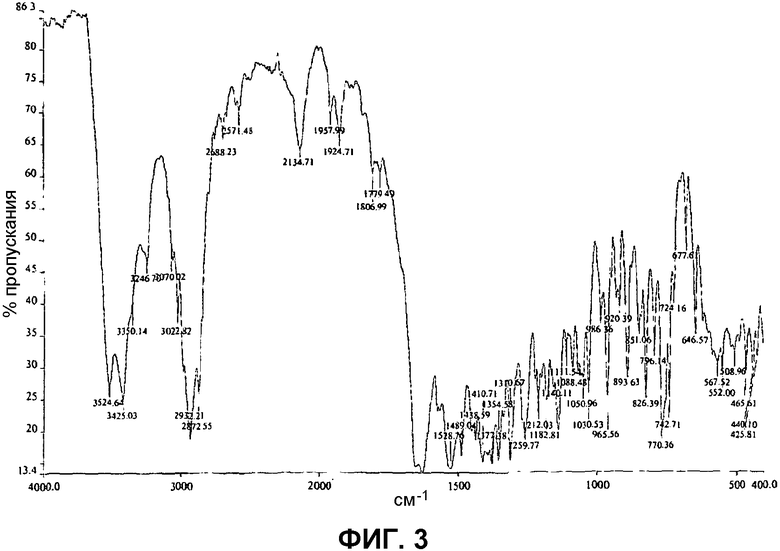
На фиг.3 представлен ИК спектр формы 1 1-(2-метил-4-(2,3,4,5-тетрагидро-1-бензазепин-1-илкарбонил)бензилкарбамоил)-L-пролин-N,N-диметиламида. В настоящем изобретении также предложена кристаллическая форма (форма 1) 1-(2-метил-4-(2,3,4,5-тетрагидро-1-бензазепин-1-илкарбонил)бензилкарбамоил)-L-пролин-N,N-диметиламида, которая охарактеризована по ИК спектру, характеристические пики которого, выраженные в см-1, расположены приблизительно на 3525, 3425, 2932, 2873, 2135, 1958, 1925, 1631, 1529, 1489, 1439, 1377, 1355, 1311, 1260, 770, 743 см-1.
Термин "приблизительно" в данном контексте означает, что значения, выраженные в см-1, могут отличаться, например, на вплоть до ±1 см-1. Кроме того, в настоящем изобретении предложена кристаллическая форма (форма 1) 1-(2-метил-4-(2,3,4,5-тетрагидро-1-бензазепин-1-илкарбонил)бензилкарбамоил)-L-пролин-N,N-диметиламида, ИК спектр которого по существу совпадает со спектром, представленным на фиг.3.
Кристаллическая форма настоящего изобретения может существовать как в несольватированной, так и в сольватированной формах. Термин 'сольват' используют в рассматриваемом описании для описания молекулярного комплекса, включающего соединение настоящего изобретения и некоторое количество одного или более из фармацевтически приемлемых растворителей, например, этанола. Термин 'гидрат' используют, если растворителем является вода.
Настоящее изобретение также включает способ получения кристаллической формы соединения настоящего изобретения, причем указанный способ включает кристаллизацию указанной кристаллической формы из раствора 1-(2-метил-4-(2,3,4,5-тетрагидро-1-бензазепин-1-илкарбонил)бензилкарбамоил)-L-пролин-N,N-диметиламида (полученного способом, раскрытым в PCT/GB 2001/000023) в растворителе, содержащем воду. В одном из аспектов настоящего изобретения растворителем является вода.
Способы осуществления настоящего изобретения могут также включать добавление кристаллической затравки кристаллической формы настоящего изобретения.
В одном из аспектов в настоящем изобретении предложена кристаллическая форма настоящего изобретения, полученная по способу настоящего изобретения.
Как было указано ранее, кристаллическая форма настоящего изобретения имеет ряд терапевтических применений, особенно при лечении заболеваний или состояний, опосредованных вазопрессином V2.
Соответственно, в настоящем изобретении предложена кристаллическая форма 1-(2-метил-4-(2,3,4,5-тетрагидро-1-бензазепин-1-илкарбонил)бензилкарбамоил)-L-пролин-N,N-диметиламида или его фармацевтически приемлемого сольвата, как определено ранее, для применения в терапии.
В настоящем изобретении также предложено использование кристаллической формы 1-(2-метил-4-(2,3,4,5-тетрагидро-1-бензазепин-1-илкарбонил)бензилкарбамоил)-L-пролин-N,N-диметиламида или его фармацевтически приемлемого сольвата, как здесь определено, при приготовлении лекарственного средства для лечения заболевания или состояния, опосредованного рецепторами вазопрессина V2.
В настоящем изобретении также предложена кристаллическая форма 1-(2-метил-4-(2,3,4,5-тетрагидро-1-бензазепин-1-илкарбонил)бензилкарбамоил)-L-пролин-N,N-диметиламида или его фармацевтически приемлемого сольвата, как здесь определено, для применения для лечения заболевания или состояния, опосредованного рецепторами вазопрессина V2.
В настоящем изобретении также предложен способ лечения заболевания или состояния, опосредованного рецепторами вазопрессина V2, причем указанный способ включает введение нуждающемуся в таком лечении млекопитающему терапевтически эффективного количества кристаллической формы 1-(2-метил-4-(2,3,4,5-тетрагидро-1-бензазепин-1-илкарбонил)бензилкарбамоил)-L-пролин-N,N-диметиламида или его фармацевтически приемлемого сольвата, как здесь определено.
В одном из аспектов заболевание или состояние, опосредованное рецепторами вазопрессина V2, выбирают из ночного энуреза, ночной полиурии, полиурии, вызванной центральным несахарным диабетом, недержания мочи и заболеваний, связанных с кровотечениями.
В одном из аспектов заболеванием или состоянием, опосредованным рецепторами вазопрессина V2, является ночная полиурия.
В контексте настоящего изобретения, встречающиеся ссылки на "лечение" включают ссылки на целительное, паллиативное и профилактическое лечение, если нет указаний на противоположное. Термины "терапия", "терапевтический" и "терапевтически" следует рассматривать аналогичным образом.
Кристаллическую форму настоящего изобретения можно вводить отдельно или в комбинации с одним или более из других лекарственных средств. Обычно ее вводят в виде композиции в ассоциации с одним или более из фармацевтически приемлемых эксципиентов. Термин "эксципиент" используют здесь для описания любого ингредиента, отличающегося от соединения (соединений) настоящего изобретения, который может придать композиции или функциональные (то есть контролирующие скорость выделения) и/или нефунциональные (т.е. вспомогательное технологическое вещество или разбавитель) свойства. Выбор эксципиента в значительной степени зависит от таких факторов, как конкретный способ введения, влияние эксципиента на растворимость и стабильность и природа лекарственной формы.
Фармацевтические композиции, пригодные для доставки кристаллической формы настоящего изобретения, и способы их получения будут совершенно очевидны специалистам в данной области. Такие композиции и способы их получения можно найти, например, в Remington's Pharmaceutical Sciences, 19th Edition (Mack Publishing Company, 1995).
Для введения пациентам-людям полная дневная доза кристаллической формы настоящего изобретения обычно находится в интервале значений 0,01 мг и 1000 мг, или между 0,1 мг и 250 мг, или между 1 мг и 50 мг в зависимости, естественно, от способа введения. Полную дневную дозу можно вводить в виде одной дозы или в виде разделенных доз, и она может, по предписанию врача, выходить за рамки типичных доз, представленных здесь. Указанные дозы основаны на примере среднего человека массой около 60-70 кг. Врач может легко определить дозы для субъектов, масса которых находится вне указанного интервала, для таких как дети и пациенты более старшего возраста.
Соответственно, в настоящем изобретении предложена фармацевтическая композиция, включающая кристаллическую твердую форму 1-(2-метил-4-(2,3,4,5-тетрагидро-1-бензазепин-1-илкарбонил)бензилкарбамоил)-L-пролин-N,N-диметиламида или его фармацевтически приемлемого сольвата, как здесь определено, и фармацевтически приемлемый носитель, разбавитель или эксципиент.
Фармацевтические композиции можно вводить местно (например, на кожу или в легкие и/или дыхательные пути) в форме, например, кремов, растворов, суспензий, аэрозолей гептафторалкана (HFA) и композиций сухого порошка; или системно, например, путем перорального введения в форме таблеток, капсул, сиропов, порошков или гранул; или путем парэтерального введения в форме растворов или суспензий; или путем подкожного введения; или путем ректального введения в форме суппозиториев; или трансдермально.
В одном из вариантов настоящего изобретения активный ингредиент вводят перорально. Пероральное введение может включать заглатывание, при котором соединение попадает в желудочно-кишечный тракт, и/или буккальное введение, лингвальное или сублингвальное введение, в результате которого соединение попадает в поток крови непосредственно изо рта.
Композиции, пригодные для перорального введения, включают твердые прессованные формы, твердые микрочастицы, полутвердые и жидкие формы (включая множественные фазы или диспергированные системы), такие как таблетки; мягкие или твердые капсулы, содержащие мульти- или наночастицы, жидкости, эмульсии или порошки; пастилки (включая заполненные жидкостью пастилки); жевательные таблетки; гели; быстро диспергируемые лекарственные формы; пленки; суппозитории; спреи; и защечные/мукоадгезивные пластыри.
Можно также создать композиции, пригодные для перорального введения, для доставки кристаллической формы способом, предусматривающим немедленное выделение или выделение с равномерной скоростью, в которых профиль выделения может быть замедленным, импульсным, контролируемым, непрерывным, или замедленным и непрерывным, или непрерывным, или модифицированным таким образом, чтобы оптимизировать терапевтическую эффективность указанной кристаллической формы. Средства доставки соединений с непрерывной скоростью выделения известны специалистам в данной области и включают полимеры, обеспечивающие медленное выделение, с которыми можно получить композиции с указанными соединениями, обеспечивающие контролируемое их выделение.
Примеры полимеров, обеспечивающих непрерывное выделение, включают разлагаемые и неразлагаемые полимеры, которые можно использовать для выделения указанных соединений за счет диффузии или комбинации диффузии и эрозии полимеров. Примеры полимеров, обеспечивающих непрерывное выделение, включают гидроксипропилметилцеллюлозу, гидроксипропилцеллюлозу, метилцеллюлозу, этилцеллюлозу, натрнийкарбоксиметилцеллюлозу, поливиниловый спирт, поливинилпирролидон, ксантамгам, полиметакрилаты, полиэтиленоксид и полиэтиленгликоль.
Жидкие (включая многофазные и дисперсные системы) композиции включают эмульсии, суспензии, растворы, сиропы и эликсиры. Такие композиции могут быть представлены в виде наполнителей мягких или твердых капсул (полученных, например, из желатина или гидроксипропилметилцеллюлозы) и обычно включают носитель, например, воду, этанол, полиэтиленгликоль, пропиленгликоль, метилцеллюлозу или подходящее масло, и один или более из эмульгирующих агентов и/или суспендирующих агентов. Жидкие композиции можно также получить путем восстановления твердого вещества, например, из саше.
Кристаллическую форму настоящего изобретения можно также использовать в быстрорастворимых, быстродиспергируемых лекарсвенных формах, таких как те, что раскрыты Liang and Chen, Expert Opinion in Therapeutic Patents, 2001, 11 (6), 981-986.
Получение таблеток обсуждается в Pharmaceutical Dosage Forms: Tablets, Vol. 1, by H. Lieberman and L. Lachman (Marcel Dekker, New York, 1980).
Далее изобретение будет проиллюстрировано следующими нелимитирующими примерами. В указанных примерах использованы следующие фигуры:
Фиг.1: Порошковая рентгеновская дифрактограмма формы 1 1-(2-метил-4-(2,3,4,5-тетрагидро-1-бензазепин-1-илкарбонил)бензилкарбамоил)-L-пролин-N,N-диметиламида.
Фиг.2: Полученные с помощью SEM (сканирующая электронная микроскопия) изображения формы 1 1-(2-метил-4-(2,3,4,5-тетрагидро-1-бензазепин-1-илкарбонил)бензилкарбамоил)-L-пролин-N,N-диметиламида.
Фиг.3: ИК спектр формы 1 1-(2-метил-4-(2,3,4,5-тетрагидро-1-бензазепин-1-илкарбонил)бензилкарбамоил)-L-пролин-N,N-диметиламида.
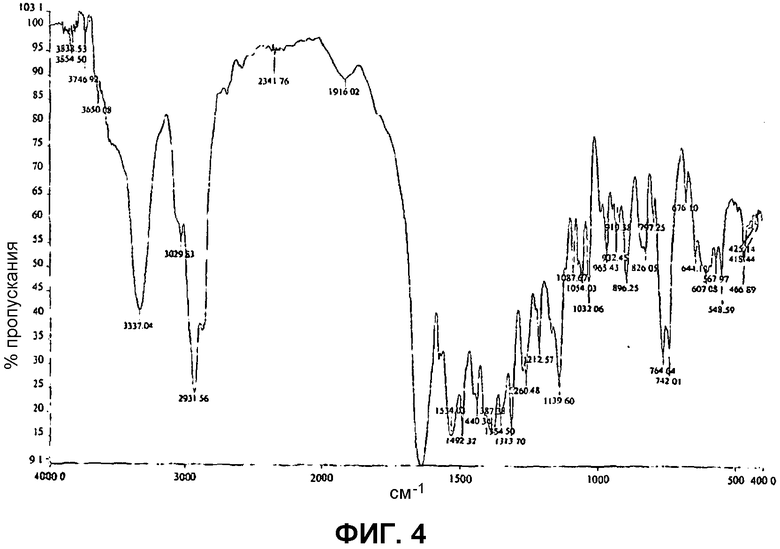
Фиг.4: ИК спектр аморфного 1-(2-метил-4-(2,3,4,5-тетрагидро-1-бензазепин-1-илкарбонил)бензилкарбамоил-L-пролин-N,N-диметиламида.
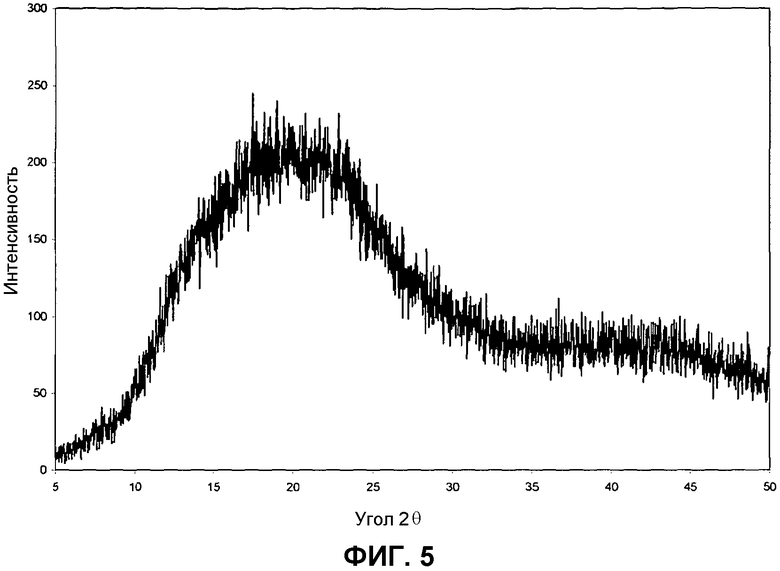
Фиг.5: Порошковая рентгеновская дифрактограмма аморфного 1-(2-метил-4-(2,3,4,5-тетрагидро-1-бензазепин-1-илкарбонил)бензилкарбамоил)-L-пролин-N,N-диметиламида.
Фиг.6: SEM изображения аморфного 1-(2-метил-4-(2,3,4,5-тетрагидро-1-бензазепин-1-илкарбонил)бензилкарбамоил)-L-пролин-N,N-диметиламида.
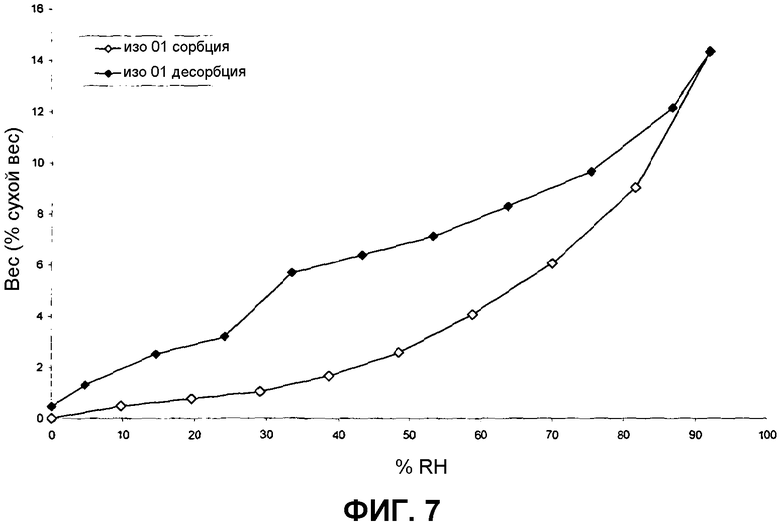
Фиг.7: GVA изотерма сорбции/десорбции воды для аморфного 1-(2-метил-4-(2,3,4,5-тетрагидро-1-бензазепин-1-илкарбонил)бензилкарбамоил)-L-пролин-N,N-диметиламида.
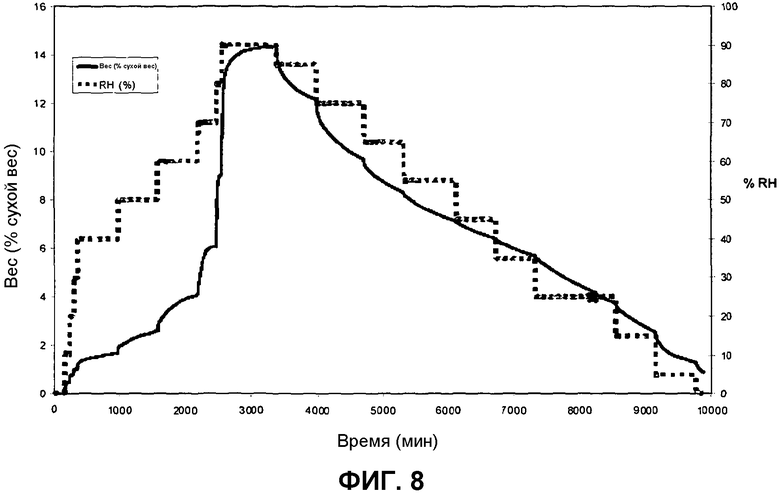
Фиг.8: GVA кинетическая изотерма сорбции/десорбции воды для аморфного 1-(2-метил-4-(2,3,4,5-тетрагидро-1-бензазепин-1-илкарбонил)бензилкарбамоил)-L-пролин-N,N-диметиламида.
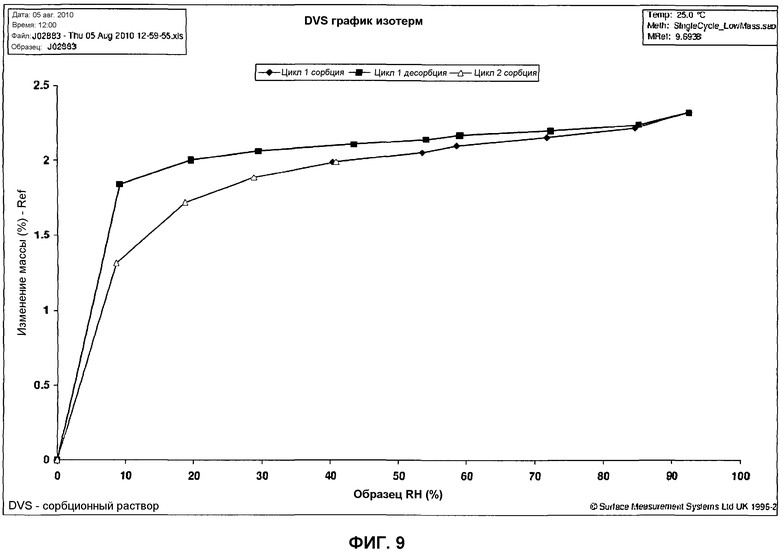
Фиг.9: GVA изотерма сорбции/десорбции воды для формы 1 1-(2-метил-4-(2,3,4,5-тетрагидро-1-бензазепин-1-илкарбонил)бензилкарбамоил)-L-пролин-N,N-диметиламида.
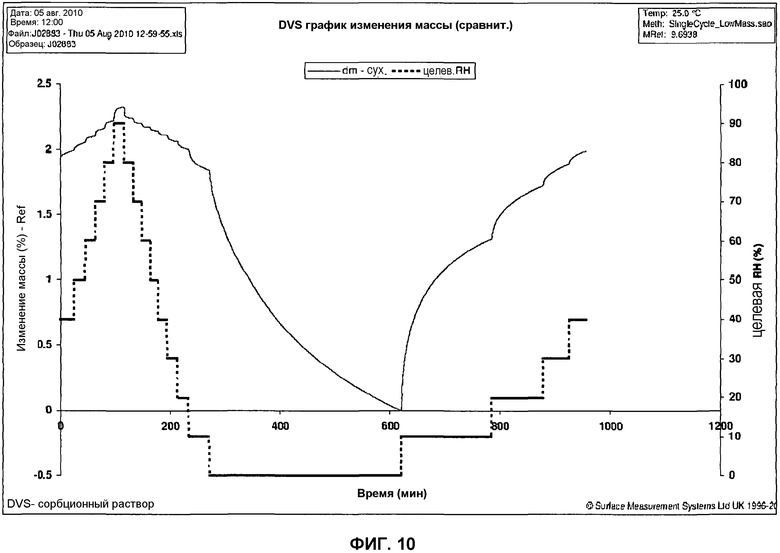
Фиг.10: GVA кинетическая изотерма сорбции/десорбции воды для формы 1 1-(2-метил-4-(2,3,4,5-тетрагидро-1-бензазепин-1-илкарбонил)бензилкарбамоил)-L-пролин-N,N-диметиламида.
Фиг.11: Рентгеновская структура монокристалла формы 1 1-(2-метил-4-(2,3,4,5-тетрагидро-1-бензазепин-1-илкарбонил)бензилкарбамоил)-L-пролин-N,N-диметиламида.
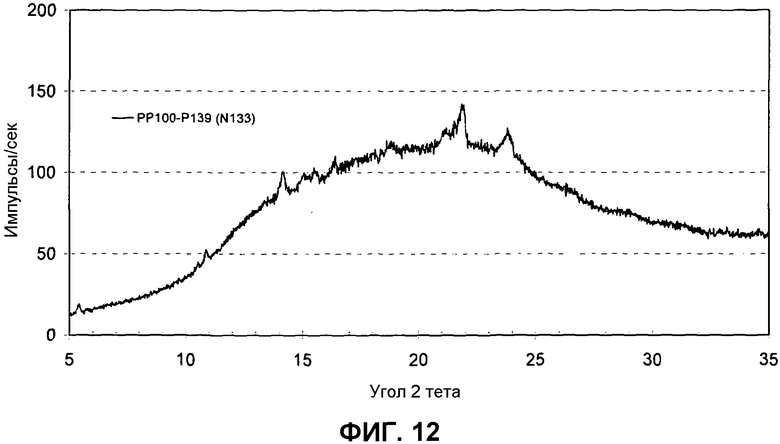
Фиг.12: Порошковая рентгеновская дифрактограмма смеси 95% аморфного 1-(2-метил-4-(2,3,4,5-тетрагидро-1-бензазепин-1-илкарбонил)бензилкарбамоил)-L-пролин-N,N-диметиламида и 5% формы 1 1-(2-метил-4-(2,3,4,5-тетрагидро-1-бензазепин-1-илкарбонил)бензилкарбамоил)-L-пролин-N,N-диметиламида.
Общие детали экспериментов
Все растворители и коммерческие реагенты используют в том виде, как они получены.
Определение содержания влаги по методу Карла Фишера осуществляют, используя волюметрический аппарат Карла Фишера Metrohm 795 KFT. Размер образцов составляет приблизительно 100 мг, и определение осуществляют в двух параллельных опытах.
Гравиметрический анализ сорбции паров (Gravimetric Vapour Sorption Analysis (GVA)) осуществляют, используя приблизительно 20 мг образца, помещенного в соответствующий держатель образца, такой как проволочное сито чашки весов для определения сорбции паров. Его помещают или в IGAsorp (Аналитический прибор Хайдена), или в DVS Intrinsic (Surface Measurement Systems) и баланс сорбции паров поддерживают при 25+/-0,1°C. Затем образец сушат, поддерживая влажность окружающей среды 0%, до тех пор, пока не регистрируют отсутствие дальнейшего изменения веса (до постоянного веса) (альтернативно, цикл сорбции/десорбции начинают в условиях типичной относительной влажности окружающей среды 40%). Затем относительную влажность образца повышают вплоть до 90%, используя инкременты относительной влажности в 10%, выдерживая образец на каждой стадии до достижения равновесия (99,5% ступень завершения). После достижения равновесия относительную влажность в аппарате повышают до следующей ступени и повторяют процедуру установления равновесия. После завершения цикла сорбции образец сушат, используя ту же процедуру. Изменение веса на протяжении циклов сорбция/десорбция регистрируют, определяя в результате характер гигроскопичности образца.
Результаты ВЭЖХ получают, используя колонку Zorbax Extend C18, 2,1×150 мм, 5 мкм диаметр частиц. Скорость потока составляет 0,3 мл/мин. Инжектируемый объем составляет 10 мкл, детектирование на длине волны 220 нм, и температура колонки 40°C. Элюент A представляет собой 10 мМ водный раствор ацетата аммония, pH 5,0. Элюент B представляет собой 20:80 об./об. 10 мМ водный раствор ацетата аммония:ацетонитрил. Программа для градиентного элюирования представлена далее:
Дифференциальная сканирующая калориметрия (DSC)
Образец массой приблизительно от 1 до 3 мг тщательно взвешивают в алюминиевой DSC чашке и закрывают, используя негерметичную крышку. Затем образец помещают в прибор Mettler 12E DSC, снабженный Julabo F25 охлаждающим устройством. Образцы нагревают с 50 до 200°C со скоростью 10°C/мин и регистрируют изменения в реакции теплового потока. Прибор предварительно калибруют, используя двойную калибровку, используя индий и свинец в качестве стандартов по мере необходимости.
Гипердифференциальная сканирующая калориметрия: образец массой приблизительно от 1 до 3 мг тщательно взвешивают в алюминиевой DSC чашке и закрывают, используя негерметичную крышку. Затем образец помещают в прибор Diamond DSC (Perkin-Elmer Instruments, US), снабженный охлаждающим устройством с использованием жидкого азота, и охлаждают до 0°C. После достижения стабильной базовой линии образцы нагревают с 0 до 200°C со скоростью 200°C/мин и регистрируют реакцию теплового потока. Поток гелия пропускают со скоростью 20 мл/мин для улучшения процесса теплопередачи с образца на термопару и окончательного повышения чувствительности. Перед анализами прибор калибруют по температуре и потоку тепла, используя в качестве сравнительного стандарта индий.
Инфракрасные спектры получают, используя конфигурацию системы диффузного отражения, образцы приготавливают в бромиде калия и сканирование осуществляют в диапазоне частот от 4000 см-1 до 400 см-1.
Рентгеновские порошковые дифрактограммы (X-Ray Powder Diffraction (XRPD)) получают, используя образцы массой приблизительно 2-10 мг, которые осторожно прессуют на наискось срезанном XRPD держателе образца с нулевым фоном из двуокиси кремния. Затем образец помещают в дифрактометр Philips X-Pert MPD и осуществляют анализ, используя следующие условия эксперимента:
Анодная трубка: Cu
Напряжение генератора: 40 кВ
Ток в трубке: 40 мА
Длина волны альфа 1: 1,5406 Å
Длина волны альфа 2: 1,5444 Å
Начальный угол [2θ]: 5
Конечный угол [2θ]: 50
Пошаговое время: 2,5 секунды (X-Pert MPD) или 31 секунда (X-Pert Pro).
Снимки, полученные с помощью сканирующего электронного микроскопа, получают, покрывая исследуемый материал тонким слоем золота (покрытие наносят методом напыления), и исследуют, используя сканирующий электронный микроскоп FEI-Philips XL30. Для анализа используют ускоряющее напряжение 10 кВ. Все снимки получают, используя присоединенную CCD камеру (полупроводниковая камера с зарядовой связью) с компьютерным управлением.
Раман микроскопию осуществляют, используя миниатюрный Раман-спектрометр BWTEK BTR-111 с длиной волны возбуждения на 785 нм и диапазоном измеряемых частот от 3000 см-1 до 100 см-1.
1-(2-метил-4-(2,3,4,5-тетрагидро-1-бензазепин-1-илкарбонил)бензилкарбамоил)-L-пролин-N,N-диметиламид (форма 1)
Способ A
1-(2-метил-4-(2,3,4,5-тетрагидро-1-бензазепин-1-илкарбонил)бензилкарбамоил)-L-пролин-N,N-диметиламид (15,0 г; полученный способом, раскрытым в PCT/GB 2001/000023), суспендируют в воде (1000 мл) и перемешивают в течение 12 дней. Полученную смесь фильтруют и твердую часть промывают ледяной водой. Твердую часть сушат при 60°C до постоянного веса, получая кристаллическое твердое вещество в виде белого порошка.
Способ B
1-(2-метил-4-(2,3,4,5-тетрагидро-1-бензазепин-1-илкарбонил)бензилкарбамоил)-L-пролин-NN-диметиламид (300 мг; полученный способом, раскрытым в PCT/GB 2001/000023), суспендируют в смеси ацетон/вода 20/80 (1 мл) и нагревают при 50°C, получая эмульсию. Полученную эмульсию охлаждают до 30°C и перемешивают, получая непрозрачный раствор при 30°C. Температуру снижают до 28°C, получая прозрачный раствор. Перемешивание продолжают в течение 18 часов, получая суспензию, и перемешивают в течение дополнительных 30 часов. Твердую часть удаляют фильтрованием, промывают смесью ацетон/вода 20/80, сушат воздухом в течение 10 минут и затем сушат дальше в эксикаторе в течение 1 часа, получая кристаллическую твердую форму в виде порошка белого цвета (выход 76%).
Способ C
1-(2-метил-4-(2,3,4,5-тетрагидро-1-бензазепин-1-илкарбонил)бензилкарбамоил)-L-пролин-N,N-диметиламид (200 г; полученный способом, раскрытым в PCT/GB2001/000023,) добавляют к смеси ацетон/вода (20/80) (500 мл) и перемешивают при 15°C в течение 5 минут. Полученную смесь нагревают до 50°C в течение 15 минут, получая эмульсию, которую перемешивают при 50°C в течение 10 минут и охлаждают до 27°C в течение 38 минут, получая прозрачный раствор. "Температуру помутнения" отмечают приблизительно при 38°C при охлаждении. Затравку кристаллического 1-(2-метил-4-(2,3,4,5-тетрагидро-1-бензазепин-1-илкарбонил)бензилкарбамоил)-L-пролин-N,N-диметиламида (форма 1) (10 г) суспендируют в смеси ацетон/вода (20/80) (25 мл) и добавляют к реакционной смеси. Дополнительное количество смеси ацетон/вода (20/80) (25 мл) используют для смывания остаточной суспензии затравки в смесь. Полученную суспензию оставляют при перемешивании при 27°C до тех пор, пока полное время эксперимента не достигает 46 часов. Суспензию охлаждают до 20°C в течение 1 часа и перемешивают в течение дополнительно 42 часов при 20°C. Полученную суспензию фильтруют и твердую часть сушат на воздухе приблизительно в течение 30 минут. Твердую часть промывают смесью ацетон/вода (5/95, 3×100 мл) и сушат на воздухе приблизительно в течение 3 часов. Твердую часть сушат далее при 45°C в вакууме, получая кристаллическую твердую форму в виде порошка белого цвета, выход 166 г (76%).
XRPD дифрактограмма 1-(2-метил-4-(2,3,4,5-тетрагидро-1-бензазепин-1-илкарбонил)бензилкарбамоил)-L-пролин-N,N-диметиламида (форма 1) представлена на фиг.1.
Таблица положения пиков:
[°2θ]
[°2θ]
[Å]
SEM анализ (анализ с использованием растрового электронного микроскопа)
SEM изображения демонстрируют прямоугольную морфологию кристаллов формы 1 (см. фиг.2). При сравнении, SEM изображения аморфной формы свидетельствуют о том, что исследованные образцы состоят из преимущественно крупных (>5 мкм в диаметре) агрегатов (см. фиг.6).
Инфракрасная спектроскопия; спектр содержит пики на частотах приблизительно 3524,6, 3425,0, 2932,2, 2872,6, 2134,7, 1958,0, 1924,7, 1630,7, 1528,8, 1489,0, 1438,6, 1377,4, 1354,6, 1310,7, 1259,8, 770,4, 742,7 см-1 . Спектр представлен на фиг.3.
DSC (дифференциальная сканирующая калориметрия): начало приблизительно 109,9°C.
Гипер DSC: начало приблизительно 114°C.
Анализ Карла Фишера свидетельствует о содержании влаги 3,8%, что эквивалентно стехиометрическому количеству воды и согласуется с выделением гидрата.
Гигроскопическое тестирование
Аморфная форма является гигроскопичной по данным гравиметрического парофазного сорбционного анализа (Gravimetric Vapour Sorption Analysis (GVA)). Изотермы сорбции/десорбции воды представлены на фиг.7 и 8.
Результаты GVA свидетельствуют о том, что аморфная форма высоко гигроскопична, абсорбируя воду в объеме образца при хранении при RH (относительной влажности) выше примерно 30% (всего примерно 14% в равновесном состоянии при 90% RH). Аморфное состояние остается стабильным при перекристаллизации во всем исследованном интервале сорбции воды, однако степень изменения физической формы наблюдается при прохождении образцом температуры перехода в стеклообразное состояние. Напротив, не наблюдается заметного поглощения воды в интервале от 40% RH до 90% RH (приблизительно 0,3% масс./масс.) для кристаллической твердой формы (изотермы сорбции/десорбции воды представлены на фиг.9 и 10). Не происходит никаких изменений в форме твердого состояния во всем интервале сорбции воды.
Тестирование стабильности
Кристаллическая твердая форма более стабильна, чем аморфная форма. Когда оба вещества хранят в течение 6 месяцев при 40°C и 75% относительной влажности, кристаллическая форма сохраняется как порошок белого цвета без изменения содержания воды (3,8% по данным анализа Карла Фишера). Не происходит также заметного разложения по данным измерения суммы примесей, которая увеличивается только с 0,9% до 1,0% (ВЭЖХ). Однако аморфная форма демонстрирует увеличение содержания влаги с 1,3% до 5,7% по данным анализа Карла Фишера. Аморфная форма также демонстрирует более быстрое разложение при увеличении количества примесей с 1,5% до 3,7% (ВЭЖХ). Вначале аморфная форма имеет вид порошка белого цвета, но при хранении становится стекловидной и приобретает желтый цвет.
Определение небольших количеств кристаллической формы (формы 1) в образце аморфной формы
XRPD измерения осуществляют, используя усовершенствованный порошковый рентгеновский дифрактометр Bruker D8 и Cu Kα излучение в Брэгг-Брентано геометрии отражения.
Обычно точность значений 2θ определяют с ошибкой ±0,1-0,2°. Относительные интенсивности пиков могут значительно отличаться для различных образцов одной и той же кристаллической формы из-за различных предпочтительных ориентаций кристаллов. Образцы приготавливают без какой-либо специальной обработки помимо приложения небольшого давления для создания плоской поверхности. Используют силиконовый держатель для образца в виде монокристалла глубиной 1,0 мм и с диаметром полости 12 мм. Напряжение на трубке и сила тока составляют 40 кВ и 40 мА, соответственно. Рентгеновский дифрактометр снабжен детектором LynxEye. Используют щель переменной ширины с окном в 3°. Величина шага составляет 0,02° 2θ и время шага 37 секунд. В процессе измерений образец вращают со скоростью 0,5 об/сек.
На фиг.12 представлена XRPD картина для смеси, состоящей на 95% из аморфной формы и на 5% из кристаллической формы (форма 1), причем небольшие пики на рентгеновской дифрактограмме перечислены далее.
Перечисление XRPD пиков для угла 2θ (для пиков, представленных на фиг.12).
Образец должен быть по меньшей мере на 5% кристаллическим, чтобы были заметны XRPD пики при разумном соотношении сигнал/шум.
Оценка фракции кристаллической формы 1 с помощью DSC
Приблизительную оценку содержания кристаллической формы по сравнению с содержанием аморфной формы можно получить, используя дифференциальную сканирующую калориметрию. Измерения с помощью дифференциальной сканирующей калориметрии проводят на приборе Perkin Elmer DSC-7. Образцы помещают в золотые тигли, открытый контейнер с образцом помещают в поток азота на 3 минуты и герметизируют в атмосфере азота. Измерения осуществляют при скорости повышения температуры 40°C в минуту в интервале температур от -50°C до 200°C.
Количества образцов обычно составляют 4 мг, и интегрирование площадей пиков осуществляют в интервале от около 80°C до около 130°C.
Образцы, содержащие по меньшей мере 50% кристаллической формы, демонстрируют энтальпию плавления выше, чем приблизительно 30 Джоуль/г. Образцы, содержащие по меньшей мере 70% кристаллической формы, демонстрируют энтальпию плавления выше, чем приблизительно 45 Джоуль/г. Образцы, содержащие по меньшей мере 90% кристаллической формы, демонстрируют энтальпию плавления выше, чем приблизительно 58 Джоуль/г, и образцы, содержащие по меньшей мере 95% кристаллической формы, демонстрируют энтальпию плавления выше, чем приблизительно 62 Джоуль/г.
Получение таблеток
Активное вещество пропускают через мельницу U3 Comil® (Quadro Engineering), снабженную ситом с размером ячеек 457 микрон, и отвешивают в контейнер из нержавеющей стали. Добавляют моногидрат лактозы и полученную смесь перемешивают и пропускают через 600 микронное сито. Микрокристаллическую целлюлозу пропускают через 600 микронное сито, добавляют и перемешивают. Стеарат магния пропускают через 600 микронное сито, добавляют и перемешивают. Сердцевину таблеток прессуют, используя подходящее устройство для таблетирования. Приготавливают суспензию материала кроющей пленки, содержащего гипромеллозу, тальк, диоксид титана, полиэтиленгликоль и натрийсахарин в очищенной воде, и распределяют суспензию на сердечники таблеток в устройстве для нанесения покрытия в псевдоожиженном слое. Воду удаляют в процессе получения.
Биологическая активность
Способность кристаллической формы настоящего изобретения подавлять рецепторы вазопрессина V2 можно определить, используя анализ in vivo, раскрытый в PCT/GB2001/000023.
При тестировании в указанном анализе 1-(2-метил-4-(2,3,4,5-тетрагидро-1-бензазепин-1-илкарбонил)бензилкарбамоил)-L-пролин-N,N-диметиламид демонстрирует 82% ингибирования выделения мочи (за 1 час) при введении в дозе 1 мг/кг.
Рентгеноскопическое определение структуры монокристалла
Приготовление кристаллов
Приготавливают суспензию (15 мл) аморфного 1-(2-метил-4-(2,3,4,5-тетрагидро-1-бензазепин-1-илкарбонил)бензилкарбамоил)-L-пролин-N,N-диметиламида (полученного способом, раскрытым в PCT/GB 2001/000023), в концентрации 387 мг/мл в смеси н-пропилацетата и воды (81:19) и нагревают при 80°C в течение 10 минут, получая почти прозрачный раствор. Полученную смесь охлаждают со скоростью 1°C в минуту до 10°C и снова нагревают до 40°C. Добавляют кристаллическую затравку 1-(2-метил-4-(2,3,4,5-тетрагидро-1-бензазепин-1-илкарбонил)бензилкарбамоил)-L-пролин-N,N-диметиламида (форма 1) (приблизительно 50 мг) и полученную смесь охлаждают со скоростью 0,5°C в минуту до 38°C. Смесь снова нагревают до 39°C и добавляют дополнительное количество кристаллической затравки 1-(2-метил-4-(2,3,4,5-тетрагидро-1-бензазепин-1-илкарбонил)бензилкарбамоил)-L-пролин-N,N-диметиламида (форма 1) (приблизительно 50 мг). Полученную смесь перемешивают при 39°C в течение 6 часов, затем охлаждают до 35°C со скоростью 0,1°C в минуту. Полученную смесь перемешивают при 35°C в течение 6 часов, затем охлаждают до 30°C со скоростью 0,1°C в минуту. Затем полученную смесь перемешивают в течение трех дней при 30°C. Выясняется, что реактор содержит суспензию и некоторое количество относительно крупных кристаллов на стенках реактора. Суспензию удаляют и фильтруют, и полученный фильтрат используют для смывания более крупных кристаллов со стенок реактора, которые выделяют в виде суспензии. Суспензию крупных кристаллов хранят в запаянном реакторе при комнатной температуре в течение двух недель, что приводит к растворению кристаллов. Дальнейшее хранение образца в герметизированном реакторе в течение 10 дней приводит к перекристаллизации с образованием кристаллов, пригодных для рентгеновского определения структуры монокристалла. DSC и Раман спектры отфильтрованных кристаллов свидетельствуют о том, что твердое вещество состоит из формы 1, причем нет никаких указаний на то, что присутствует какая-нибудь другая кристаллическая форма.
Определение структуры
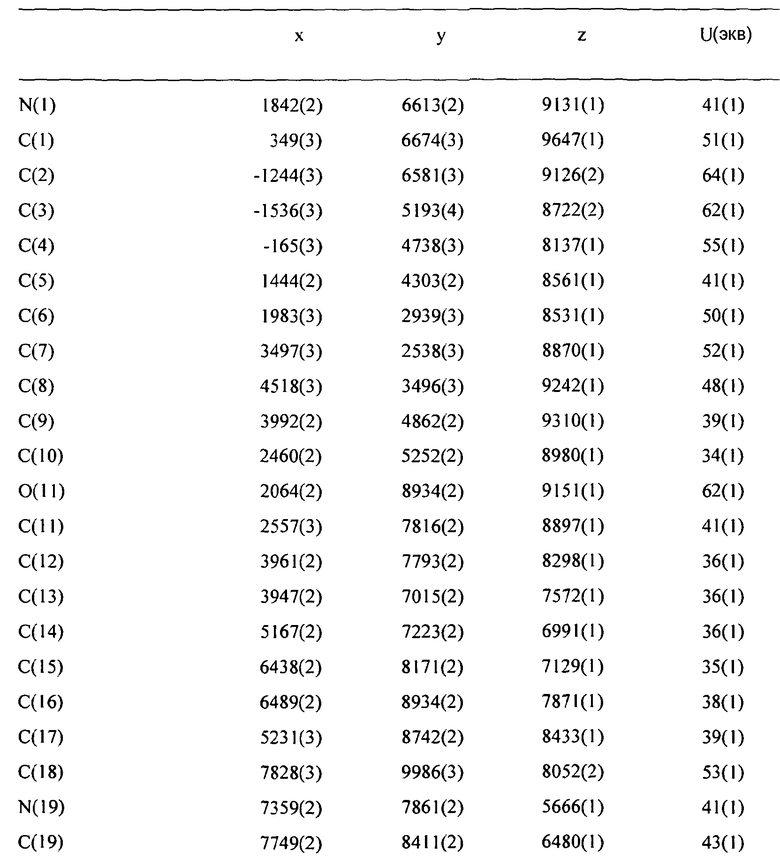
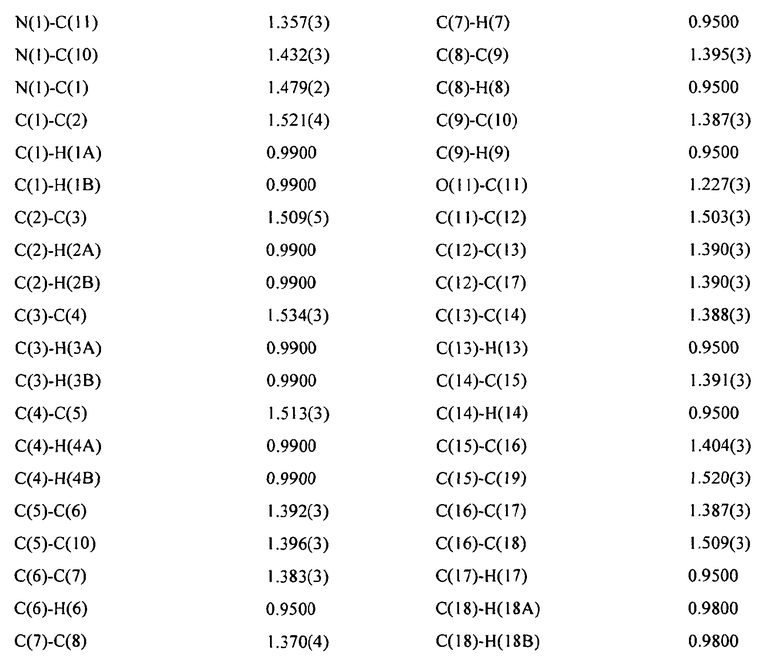
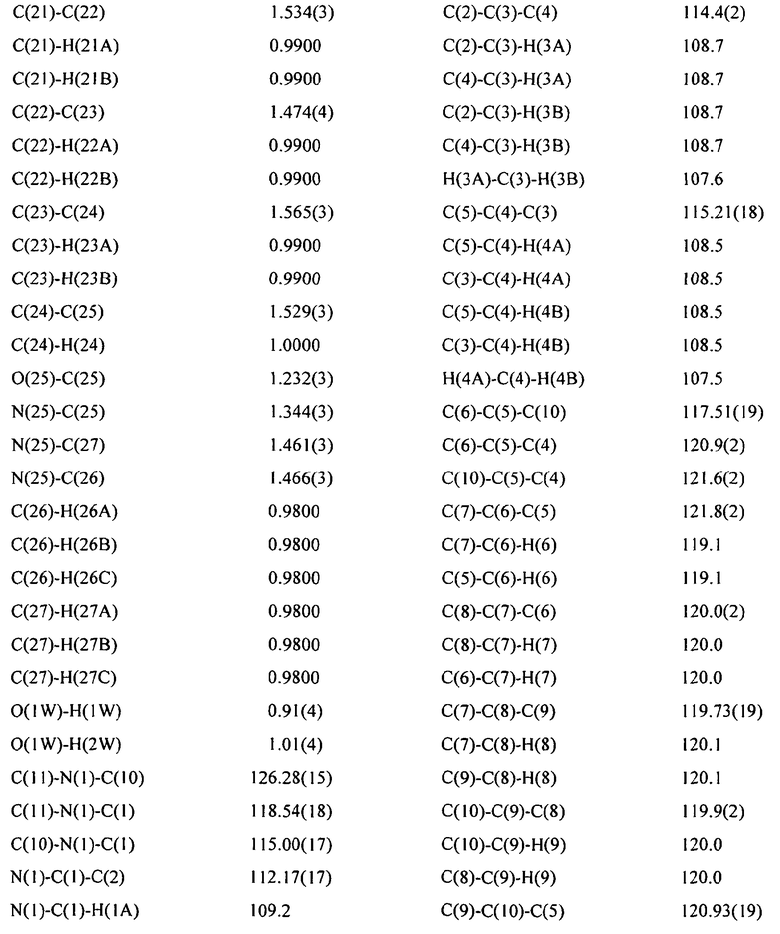
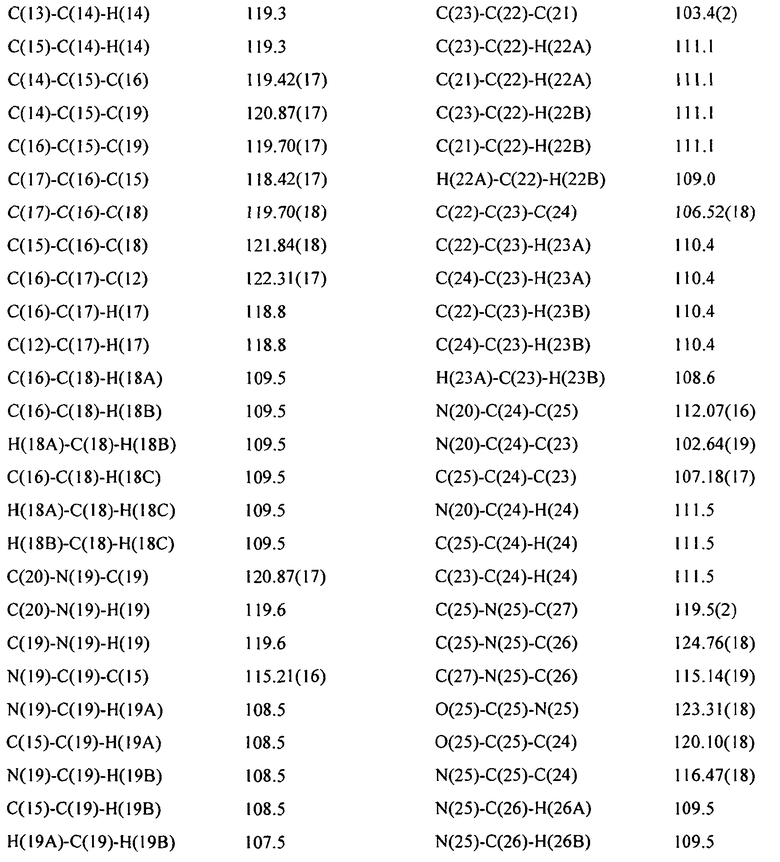
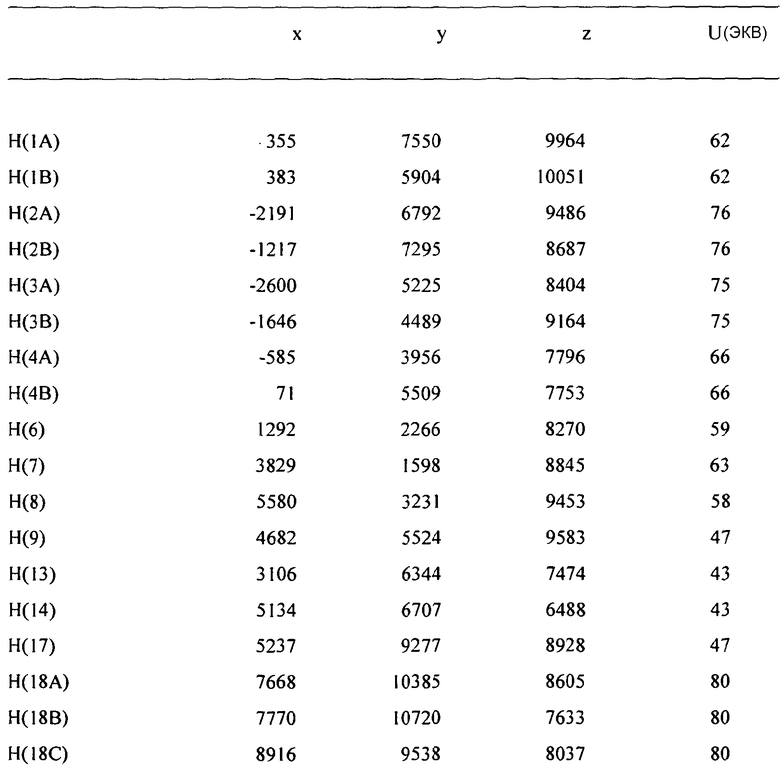
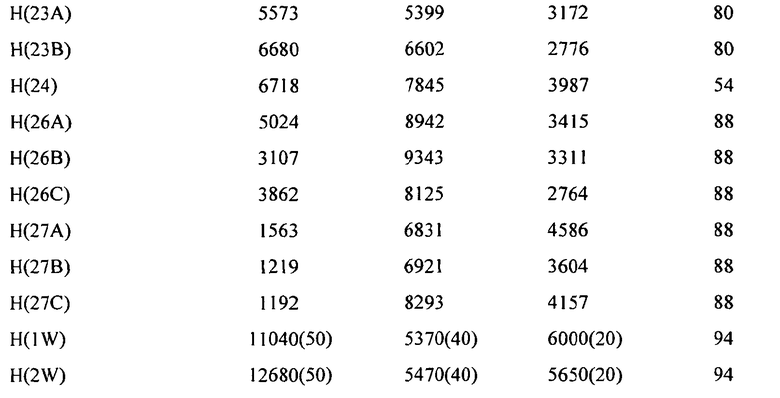
Кристаллографические исследования осуществляют, используя монокристальный дифрактометр Nonius Kappa CCD (Bruker). Абсолютную структуру определяют, исходя из известной конфигурации исходного материала (L-пролиндиметиламида, см. PCT/GB 2001/000023). Было определено расположение атомов водорода воды, и их положения были уточнены удовлетворительно. 2356 пар Фриделя были усреднены для уточнения. Полученная рентгеновская структура монокристалла представлена на фиг.11. Итоговый отчет о рентгеновском определении структуры монокристалла представлен далее и в таблицах 1-5.
Элементарная ячейка
Для уточнения элементарной ячейки используют 7436 отражений при 1,00°<тета<28,70° (разрешение между 20,40 Å и 0,74 Å)
Сбор данных
Результаты
Экспериментальные условия
Сканирование
Скейлинг с помощью Scalepack
Исключенные наблюдения
Сумма окончательных результатов
b=9,6869(2) Å, β=91,268(1)°.
c=16,0886(4) Å, γ=90°.






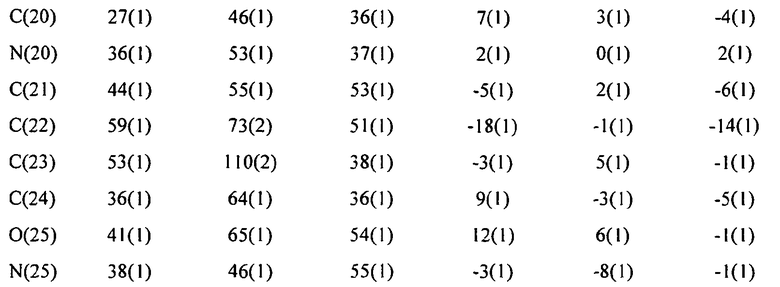




Изобретении относится к новому полиморфу, а именно к твердой форме 1-(2-метил-4-(2,3,4,5-тетрагидро-1-бензазепин-1-илкарбонил)бензилкарбамоил)-L-пролин-N,N-диметиламида, содержащим его фармацевтическим композициям и его применению для лечения заболевания или состояния, опосредованного рецепторами вазопрессина V2. 3 н. и 7 з.п. ф-лы, 14 табл., 12 ил.
1. Твердая форма 1-(2-метил-4-(2,3,4,5-тетрагидро-1-бензазепин-1-илкарбонил)бензилкарбамоил)-L-пролин-N,N-диметиламида, которая демонстрирует по меньшей мере следующие характеристические пики на рентгеновской порошковой дифрактограмме (Cu Кα излучение, выражено в градусах 2θ) на приблизительно 5,5, 10,9, 14,2, 21,9 и 24,0.
2. Твердая форма по п. 1, порошковая рентгеновская дифрактограмма которой по существу совпадает с представленной на фиг. 1.
3. Твердая форма по п. 1, которая характеризуется ИК спектром, положения пиков которого, выраженные в см-1, расположены приблизительно на 3525, 3425, 2932, 2873, 2135, 1958, 1925, 1631, 1529, 1489, 1439, 1377, 1355, 1311, 1260, 770, 743 см-1.
4. Твердая форма по п. 3, ИК спектр которой по существу совпадает с представленным на фиг. 3.
5. Твердая форма по любому из пп. 1-4, которая представляет собой гидрат.
6. Твердая форма по п. 5, где гидрат представляет собой моногидрат.
7. Фармацевтическая композиция для лечения заболевания или состояния, опосредованного рецепторами вазопрессина V2, включающая твердую форму по любому из пп. 1-6 или ее сольват, в смеси с фармацевтически приемлемым адъювантом, разбавителем или носителем.
8. Применение твердой формы по любому из пп. 1-6 или ее
сольвата для лечения заболевания или состояния, опосредованного рецепторами вазопрессина V2.
9. Применение по п. 8, где заболевание или состояние, опосредованное рецепторами вазопрессина V2, выбирают из ночного энуреза, ноктурии, полиурии в результате центрального несахарного диабета, недержания мочи и нарушений, связанных с кровотечениями.
10. Применение по п. 8, где заболевание или состояние, опосредованное рецепторами вазопрессина V2, представляет собой ноктурию.
| WO 0149682 A1 12.07.2001 | |||
| 0 |
|
SU200626A1 | |
| Cristopher M | |||
| Yea at al, New Benzylureas as a Novel Series of Potent, Nonpeptidic Vasopressin V2 Reteptor Agonists, J.Med | |||
| Chem., 2008,v.51,p.8124-8134 | |||
| КОНДЕНСИРОВАННЫЕ АЗЕПИНЫ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СОДЕРЖАЩАЯ ИХ, СПОСОБ ЛЕЧЕНИЯ С ИСПОЛЬЗОВАНИЕМ УКАЗАННОЙ КОМПОЗИЦИИ | 2001 |
|
RU2259367C2 |
Авторы
Даты
2015-08-10—Публикация
2011-03-31—Подача