Изобретение относится к области медицины, фармации, к лекарственным средствам и может быть использовано в качестве средства, обладающего адсорбционной и детоксикационной активностью при эндотоксикозе, вызванном химическими и бактериальными агентами.
Известны энтеросорбенты, обладающие аналогичным действием, и в настоящее время их можно объединить в следующие группы [1].
1. По структурно-сорбционным характеристикам энтеросорбенты разделяют на:
- высокодисперсные порошки с высокой (до 1000 м2/г) площадью поверхности;
- пористые сорбенты, которые включают материалы, содержащие поверхностные поры (угольные сорбенты), и сорбенты со структурой глобулярной матрицы.
2. По консистенции (агрегатному состоянию):
- твердые порошкообразные сорбенты;
- субстанции, набухающие в воде;
- гидро- и лиогели;
- взвеси-суспензии в растворах.
3. По химической структуре:
- углеродные адсорбенты на основе активированного угля (карболен, карбоктин, гастросорб, марки СКН - сферический карбонит насыщенный) и углеволокнистых материалов (ваулен, актилен, «Днепр»), углеродминерального препарата (СУМС-1);
- ионообменные материалы или смолы (кайексилит, холестирамин);
- энтеросорбенты на основе лигнина (полифепан, лигносорб, полифан), гидролизатного лигнина (фильтрум, лактофильтрум);
- производные поливинилпирролидона (энтеродез, энтеросорб);
- природные пищевые волокна (отруби злаковых культур, целлюлоза), альгинаты (детоксал, кальций альгинат), пектины (полисорбовит-50, полисорбовит-95);
- энтеросорбенты на основе высокодисперсного кремнезема (полисорб, аэросил, энтеросгель);
- энтеросорбенты различной химической природы (алюминия гидроокись, неоинтестопан, смекта, алмагель, гастал, сукральфат, энтеросан).
4. По физико-химическим свойствам поверхности:
- гидрофильные энтеросорбенты, обладающие высоким сродством к воде за счет расположенных на поверхности кислородсодержащих групп;
- гидрофобные энтеросорбенты, имеющие сродство к неполярным органическим соединениям за счет расположенных на поверхности радикалов гидрофобного характера;
- смешанные гидрофильно-гидрофобные энтеросорбенты, поверхность которых сформирована кислородсодержащими группами и неполярными радикалами.
5. По лекарственной форме:
- гранулы (СКН, СКТ - сферический карбонит торфяной);
- порошки (энтеросорб, холестирамин, полифепан);
- таблетки (карболен, АУВ «Днепр», гастросорб);
- пасты, гели, взвеси, коллоиды (энтеродез);
- инкапсулированные формы (энтеросгель);
6. По механизмам сорбции:
- адсорбенты;
- абсорбенты;
- ионообменные материалы;
- комплексообразующие материалы;
- сорбенты с сочетанными механизмами взаимодействия;
- сорбенты, обладающие каталитическими свойствами.
7. По селективности:
- селективные монофункциональные;
- селективные би- и полифункциональные;
- неселективные.
Сорбционная активность является относительной количественной характеристикой функциональных параметров сорбентов, определяемой по модельным веществам-маркерам. При исследовании вновь разрабатываемых энтеросорбентов используют различные маркеры, отличающиеся структурой молекулы, ее зарядом, размерами и другими свойствами.
Так, метиленовый синий является катионным маркером, метиловый оранжевый - анионным. Белок связующую активность определяют по связыванию с белками (желатином, бычьим сывороточным альбумином и альбумином человеческим сывороточным).
Известны лекарственные средства, представляющие уголь активированный и полисорб МП.
Активированный уголь представляет собой гидрофобный адсорбент, структурированный микро-, мезо- и макропорами, размер которых отличается более чем в 100 раз. Адсорбционная активность угля по метиленовому синему должна составлять не менее 225 мг/г, метиловому оранжевому - 210 мг/г (ГОСТ 4453-74 «Уголь активный осветляющий порошкообразный») [2].
Полисорб МП - полимерный высокодисперсный кремния диоксид, имеющий непористую структуру. Его адсорбционная активность по желатину в пересчете на сухое вещество должна иметь значения не менее 220 мг/г (ФС 42-3731-99 «Полисорб МП»).
Однако уголь активированный имеет побочные эффекты при применении в течение длительного времени - раздражающий эффект на желудочно-кишечный тракт, вызывает аллергические реакции, кровотечения. Следует отметить, что уголь активированный адсорбирует вещества катионного и анионного характера.
Наиболее близким к предлагаемому является энтеросорбент (патент РФ №2391998 от 20.06.2010) [8]. Энтеросорбент представляет собой гранулы, содержащие Sphagnum fuscum, полученные путем измельчения высушенной дерновины Sphagnum fuscum до размера частиц 0,1-0,3 мм, с последующим смешиванием с 10% водным медицинским низкомолекулярным поливинилпирролидоном, гранулированием, сушкой и повторным гранулированием, при этом остаточная влажность сухих гранул не более 30-35%.
Однако недостатками известного средства является ограниченная область применения, обусловленная тем, что он обладает адсорбционной активностью только по катионному маркеру и недостаточно высокой адсорбционной и детоксикационной активностью по отношению к пулу веществ среднемолекулярной массы [3].
Компоненты пула веществ среднемолекулярной массы обладают нейротоксичным действием, вызывают вторичную иммунодепрессию, ингибируют тканевое дыхание, эритропоэз, биосинтез белка и нуклеотидов, усиливают проницаемость мембран и перекисное окисление липидов, оказывают цитотоксическое действие, нарушают баланс электролитов, микроциркуляции крови и лимфы. Все эти вещества носят название эндогенных токсичных субстанций: нейротензины, нейрокинины, эндорфины, токсины (бактериальные, ожоговые, кишечные), мочевина, креатинин, холестерин, билирубин и другие.
Новая техническая задача - расширение арсенала средств растительного происхождения, обладающих детоксикационной активностью, и области их применения.
Для решения поставленной задачи применяют порошок дерновины сфагнумов, полученный путем измельчения высушенной дерновины сфагнумов до размера 0,01-0,3 мм в качестве средства для введения, обладающего детоксикационной активностью при эндотоксикозах.
В качестве объектов испытаний использовали высушенную дерновину сфагнумов: S. girgensohnii Russ, S. capillifolium (Ehrh.) Hedw, S. fimbriatum Wils. in Wils. et Hook. f., S. fuscum (Schimp.) Klinggr, S. russowii Warnst., S. rubellum Wils., S. aongstroemii C. Hartm., S. centrale C. Jens, ex H. Arnell et C. Jens, S. magellanicum Brid, S. palustre L., S. papillosum Lindb, S. squarrosum Crome., S. angustifolium (Russ. ex Russ.) C. Jens., S. balticum (Russ.) Russ. ex C. Jens, S. cuspidatum Ehrh ex Hoffm., S. lindbergii Schimp. ex Lindb, S. lenense H. Lindb. ex Savicz., S. majus (Russ.) C. Jens, S. flexuosum Dozy et Molk., S. fallax (Klinggr.) Klinggr., S. obtusum Warnst., S. riparium Aongstr., S. jensenii H. Lindb., S. wulfianum Girg. Собранные образцы высушивали в проветриваемом помещении до воздушно-сухого состояния. Высушенное сырье измельчали при помощи аналитической мельницы JKAA-11 basik, шаровой мельницы М-01 и планетарной мельницы АГО-2С.
В качестве маркеров, позволяющих определять эффективность действия сорбентов в отношении среднемолекулярных токсинов, являющихся основным биохимическим субстратом ЭТ, использовали краситель метиленовый синий, метиловый оранжевый, желатин.
Определение адсорбционной активности объектов по метиленовому синему (МС), метиловому оранжевому (МО) и желатину проводили согласно методике, описанной в работе В.И. Решетникова [3].
Методика определения адсорбционной активности по МС: около 0,15 г (точная навеска) образца помещали в коническую колбу вместимостью 200 мл, прибавляли 50 мл раствора рабочего стандартного образца (РСО) метиленового синего, закрывали пробкой и взбалтывали на встряхивающем аппарате в течение 20 минут. Затем раствор переносили в пробирки для центрифугирования и центрифугировали в течение 15 минут при 3000 оборотов в минуту. Далее осторожно отбирали 5 мл надосадочного раствора, переносили в мерную колбу вместимостью 50 мл и доводили объем раствора водой до метки (испытуемый раствор).
Оптическую плотность (D0) испытуемого раствора определяли на спектрофотометре СФ-2000 при длине волны 396 нм в кювете с толщиной поглощающего слоя 10 мм.
Параллельно определяли оптическую плотность (D1) раствора рабочего стандартного образца первого (PCO1) метиленового синего. В качестве раствора сравнения использовали воду очищенную. Адсорбционную активность МС в миллиграммах на один грамм образца (X) вычисляли по формуле (I):
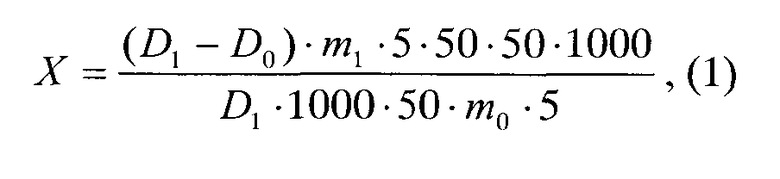
где: D0 - оптическая плотность испытуемого раствора; D1 - оптическая плотность раствора PCO1 метиленового синего; m0 - масса навески испытуемого образца, г; m1 - масса навески МС для приготовления РСО, г.
Методика определения адсорбционной активности по МО: около 0,2 г (точная навеска) образца помещали в коническую колбу вместимостью 100 мл, прибавляли 25 мл раствора РСО метилового оранжевого, закрывали пробкой и взбалтывали на аппарате для встряхивания в течение 20 минут. Полученную суспензию переносили в пробирки и центрифугировали в течение 15 минут при 3000 оборотов в минуту. Отбирали пипеткой 1 мл надосадочного раствора, переносили в мерную колбу вместимостью 100 мл и доводили объем раствора водой очищенной до метки (испытуемый раствор).
Оптическую плотность (D0) испытуемого раствора определяли на спектрофотометре СФ-2000 при длине волны 481 нм в кювете с толщиной поглощающего слоя 10 мм.
Параллельно определяли оптическую плотность (D1) раствора PCO1 метилового оранжевого. В качестве раствора сравнения использовали воду очищенную. Адсорбционную активность метилового оранжевого в миллиграммах на один грамм образца (X) вычисляли по формуле (2):

где: D0 - оптическая плотность испытуемого раствора; D1 - оптическая плотность раствора PCO1 метилового оранжевого; m0 - масса навески испытуемого образца, г; m1 - масса навески МО для приготовления РСО, г.
Методика определения адсорбционной активности по желатину: около 0,2 г (точная навеска) образца помещали в коническую колбу вместимостью 100 мл, прибавляли 25 мл 0,6% раствора желатина (раствор А), и встряхивали на аппарате для встряхивания в течение 30 минут. Далее суспензию переносили в пробирки для центрифугирования и центрифугировали в течение 20 минут при 3000 оборотов в минуту. Отбирали пипеткой 5 мл надосадочной жидкости, переносили в мерную колбу вместимостью 25 мл и доводили объем раствора биуретовым реактивом до метки, перемешивали (испытуемый раствор).
Через 30 минут определяли оптическую плотность (D1) испытуемого раствора на спектрофотометре СФ-2000 при длине волны 560 нм в кювете с толщиной поглощающего слоя 10 мм.
Параллельно определяли оптическую плотность (D0) раствора желатина (раствора Б). В качестве раствора сравнения использовали биуретовый реактив в разведении с водой очищенной в соотношении 4:1. Адсорбционную активность в мг на 1 г образца (X) вычисляли по формуле (4):
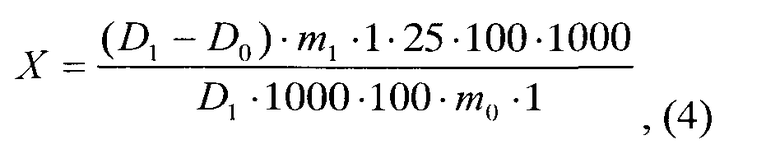
где: D0 - оптическая плотность раствора желатина (раствора Б); D1 - оптическая плотность испытуемого раствора; m0 - масса навески желатина для приготовления РСО, г; m1 - масса навески образца, г.
В результате проведенных экспериментальных исследований была определена роль дисперсности ПДС в обеспечении сорбционной активности исследуемых сфагнумов.
Полученные результаты представлены в таблице 1 и свидетельствуют, что с увеличением дисперсности сырья до 0,1 мм способность дерновины поглощать метиленовый синий увеличивается. Дальнейшее уменьшение размеров частиц дерновины не приводит к росту ее адсорбционной активности. Это может быть связано с разрушением структур растительной ткани, ответственных за обеспечение основных механизмов сорбционного эффекта. Оптимальная дисперсность сырья 0,01-0,3 мм.
Одним из путей решения и создания многофункционального сорбента является использование маркеров, проявляющих сорбционную активность к веществам различной природы (табл. 2).
Анализ результатов испытаний адсорбционной активности по метиловому оранжевому показал отсутствие выраженного сорбционного эффекта у исследуемых видов ПДС и полисорба МП. Адсорбционная активность по желатину у ПДС оказалась в 2 раза, а у активированного угля - в 6 раз ниже, чем у полисорба МП. Способность связывать метиленовый синий у полисорба МП оказалась в 3 раза ниже адсорбционной активности активированного угля.
Результаты исследований детоксикационных свойств порошка дерновины сфагнумов.
Многообразие причин, первичных очагов, пусковых механизмов возникновения и развития ЭТ в клинике предполагает использование достаточно широкого набора моделей при его изучении в эксперименте. Анализ литературных данных показывает, что в качестве индикаторов тяжести патологического процесса можно применять биохимические показатели сыворотки и морфофункциональные изменения в органах и тканях.
Детоксикационные свойства исследуемого порошка дерновины сфагнумов (ПДС) и энтеросорбентов изучали на моделях острого эндотоксикоза (ОЭТ) и хронического эндотоксикозов (ХЭТ) по В.В. Новочадову [4]. Эксперименты проводили в соответствии с «Руководством по экспериментальному (доклиническому) изучению новых фармакологических веществ», 2005 [6].
ОЭТ индуцировали внутрижелудочным введением тетрахлорметана (ТХМ) в масляном растворе (1:1) в дозе 1 мл/кг ежедневно в течение 6-ти дней, на 7-й день липополисахарид S. thyphi (ЛПС) внутрибрюшинно. Животным ХЭТ вводили внутрижелудочно ТХМ в масляном растворе (1:1) 1 мл/кг веса животного в течение 20 дней через день, на 6, 13, 20 день - ЛПС в дозе 20 мг/кг внутрибрюшинно. Контрольные животные получали эквиобъемное количество растворителей.
Животным 3-5 групп вводили внутрижелудочно ТХМ в масляном растворе (1:1) в дозе 1 мл/кг ежедневно в течение 6-ти дней, с третьего дня ежедневно в дозе 500 мг/кг порошок угля активированного, 500 мг/кг ПДС, 450 мг/кг - Полисорб МП в водных растворах в течение 4-х дней. На 7-й ЛПС внутрибрюшинно в дозе 20 мг/кг.
Крысам 8-10 групп вводили внутрижелудочно ТХМ в масляном растворе (1:1) в дозе 1 мл/кг через день в течение 20-ти дней, с третьего дня ежедневно в дозе 500 мг/кг порошок угля активированного, 500 мг/кг ПДС, 450 мг/кг - Полисорб МП в водных растворах ежедневно в течение 21 дня. На 7, 14, 21-й день ЛПС внутрибрюшинно в дозе 20 мг/кг.
Степень развития интоксикации оценивали по активности аланинаминотрансферазы (АЛТ), аспартатаминотрансферазы (ACT), определяемых кинетическим методом с помощью наборов фирмы "ChronolabAG" (Швейцария), содержанию мочевины, общего белка, измеряемого биуретовым методом с использованием набора "Ольвекс диагностикум" (г. Санкт-Петербург) и уровню малонового диальдегида (МДА) по методу К. Jagi [9].
Печень, почки, легкие и сердце животных подлежали гистологическому исследованию. Микропрепараты просматривали в проходящем свете на микроскопе Axioskop 40 (Karl Zeiss, Germany). Для количественной оценки изменений вычисляли объемные доли основных гистологических компонентов исследуемых органов.
Статистическую обработку полученных данных проводили с использованием программ Statistica 6.0 для Windows. Статистическую значимость различий в сравниваемых группах определяли по непараметрическому U-критерию Манна-Уитни. Различия между группами полагали статистическими значимыми на уровне статистической значимости p<0,05. Средние величины представлены в виде (М±m), где М - среднее арифметическое, a m - стандартная ошибка среднего значения.
Введение крысам ТХМ и ЛПС в условиях острого эксперимента приводило к существенному повышению в сыворотке крови активностей АЛТ и ACT (в 3,1 и 2,7 раза соответственно, (p<0,01), увеличению уровня МДА в 2,1 раза (p<0,01), а также снижению содержания белка на 34% (p<0,01) и мочевины на 76% (p<0,01) по сравнению с аналогичными показателями контрольной группы экспериментальных животных (табл. 3).
В препаратах печени животных с ОЭТ наблюдали диффузный мелкоочаговый некроз гепатоцитов, характеризующийся наличием лизирующихся и безъядерных клеток. Регистрировались признаки диссеминированной крупнокапельной жировой дистрофии печени, отдельные гепатоциты приобретали вид перстневидных клеток. Отмечалась гиперемия синусоидных капилляров и части центральных вен, незначительное расширение вен портальных трактов. При окраске по Ван Гизону небольшое количество соединительной ткани выявлялось только вдоль портальных трактов (Фиг. 1в).
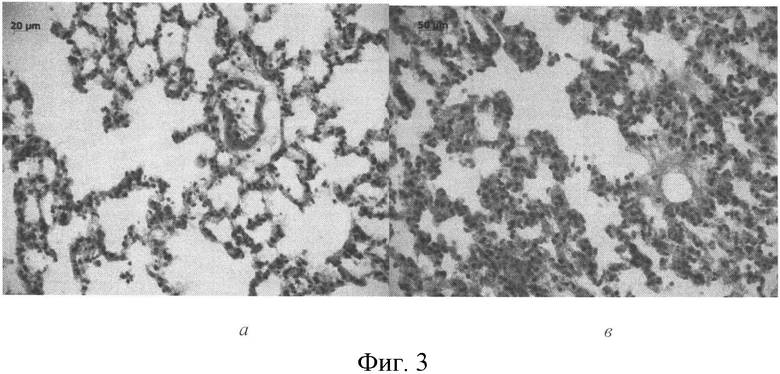
В препаратах легкого крыс с ОЭТ по сравнению со срезами этого органа у контрольной группы животных наблюдали гиперемию сосудов межальвеолярных перегородок, спазм более крупных сосудов и плазматическое пропитывание их стенок (Фиг. 3в).
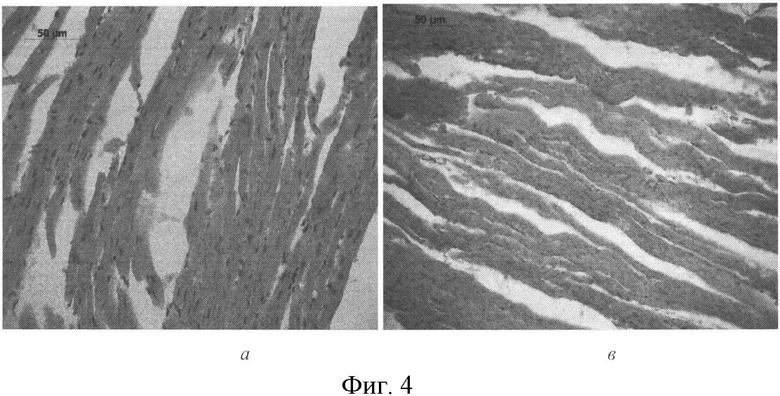
Кардиомиоциты у животных с ОЭТ не отличались от клеток сердца контрольной группы, был виден спазм мелких вен - их просвет уменьшался, эндотелий становился похожим на кубический (Фиг. 4в).
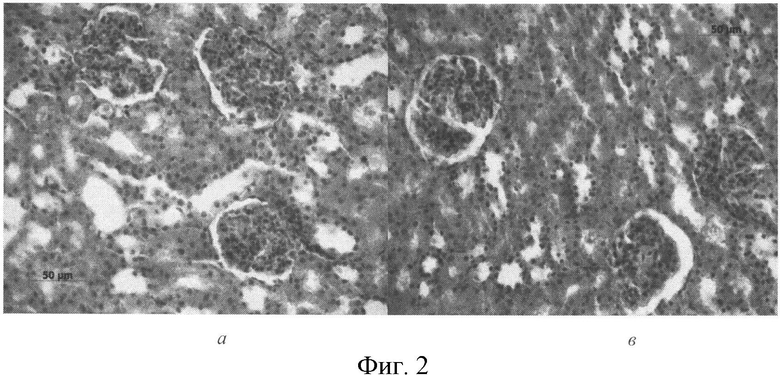
В сердце животных, получавших ТХМ и ЛПС, наблюдали выраженный отек - инстерстицию. У животных с ОЭТ не зарегистрировано существенных изменений структуры почек по сравнению с морфологической картиной органа контрольной группы (Фиг. 2в).
Полученные данные свидетельствует о развитии выраженной эндотоксической реакции, связанной с нарушением структуры и функций клеток печени, легких и сердца.
В эксперименте у животных с ОЭТ введение сорбентов ограничивало выход в кровяное русло АЛТ: активность фермента под влиянием УА снижалась на 20%, Полисорба МП - на 36,5%, ПДС - почти на 40% в сравнении с аналогичными показателями у животных, получавших ТХМ и бактериальный ЛПС (p<0,01). Активность ACT в сыворотке крови крыс, которым вводили УА, полисорб МП и ПДС, уменьшалась на 32%, 44% и 41% соответственно (p<0,01) (табл. 3).
Уменьшение выхода ферментов из клеток под действием сорбентов может быть связано с ингибированием интенсивности ПОЛ, о чем свидетельствовало снижение в сыворотке крови уровня МДА: у животных, получавших УА - на 35%, Полисорб МП - на 42%, ПДС - на 40% в сравнении с соответствующим показателем крыс с ОЭТ, не подвергавшихся лечению энтеросорбентами (p<0,01) (табл. 3).
Введение УА животным с ОЭТ препятствовало снижению содержания мочевины в сыворотке крови на 38% (p<0,01). Полисорб МП и ПДС оказывали более выраженный фармакотерапевтический эффект и предотвращали индуцированное ТХМ и ЛПС уменьшение концентрации мочевины на 46% и 51% (р<0,01), соответственно, в сравнении с аналогичными показателями у животных с ОЭТ (табл. 3).
В эксперименте с ОЭТ все исследуемые сорбенты ограничивали снижение уровня общего белка. При этом ПДС оказывал более выраженный эффект, чем УА и полисорб МП, о чем свидетельствует более высокий уровень исследуемого показателя в сравнении с концентрацией белка в сыворотке крови у животных, получавших только ТХМ и бактериальный ЛПС (p<0,01) (табл. 3).
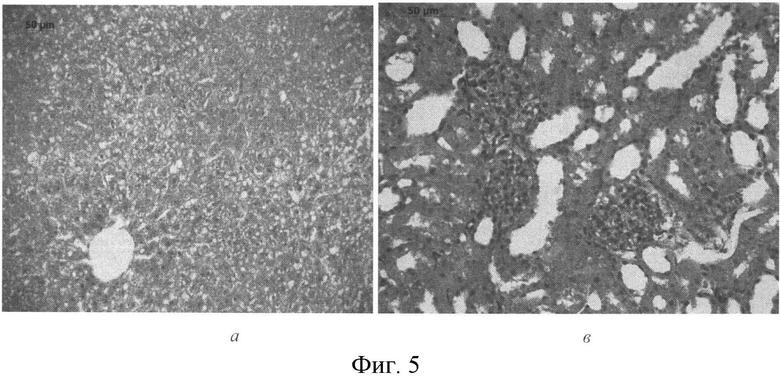
В микропрепаратах животных с ОЭТ, получавших ПДС, гистологическая картина печени в целом была сходна с таковой в контрольной группе крыс, однако встречались гепатоциты с крупнокапельной жировой дистрофией. Также наблюдали признаки регенерации - много крупных гепатоцитов с крупными ядрами. Очаги некрозов отсутствовали, регистрировался слабо выраженный макрофагально-лимфоцитарный инфильтрат вдоль портальных трактов. При окраске по Ван Гизону коллагеновые волокна соединительной ткани располагались по ходу портальных трактов и контурировали центральные вены (Фиг. 5а).
В препаратах почек животных, леченых энтеросорбентами, основная масса почечных телец сохраняла нормальную структуру, но встречались отдельные клубочки с расширенной капсулой Шумлянского-Боумена. В отличие от срезов органа контрольной группы крыс и животных с ОЭТ в гистопрепаратах крыс, получавших ПДС, наблюдали расширение проксимальных и дистальных извитых канальцев с уплощением их эпителия. При этом признаки дистрофии и некроза в эпителии не обнаруживались. Вокруг сосудов регистрировались признаки небольшого отека. При окраске по Ван Гизону расположение соединительной ткани соответствовало нормальному (Фиг. 5в).
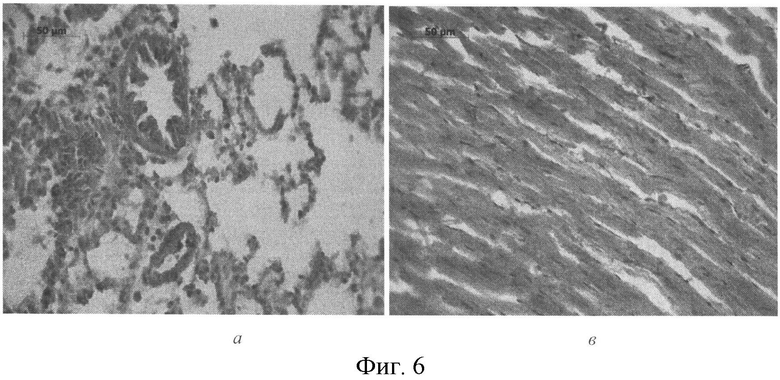
Изучение микропрепаратов сердца и легкого у животных, получавших ПДС, не выявило патологических изменений исследуемых органов (Фиг. 6а, в).
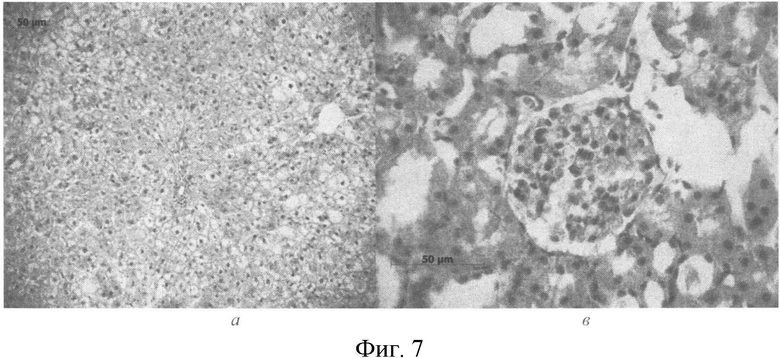
В микропрепаратах группы животных, получавших УА, гистологическая картина печени в целом соответствовала таковой в группе крыс, получавших ПДС, но жировая дистрофия приобретала более выраженный характер - дистрофически измененные гепатоциты располагались не диффузно, а преимущественно вокруг центральных вен. При окраске по Ван Гизону на срезах печени обращали на себя внимание более выраженная, чем в группе с ПДСБ, соединительная ткань по ходу портальных трактов, а также наличие коллагеновых волокон вокруг гепатоцитов с жировой дистрофией (Фиг. 7а).
В препаратах почек крыс при ОЭТ, получавших УА, выявленные изменения такие же, как и в препаратах животных, получавших ПДС, только расширение дистальных извитых канальцев было более выражено (Фиг. 7в)
Гистологическая картина легкого в целом соответствовала таковой в группе получавших ПДС, но менее выраженными эмфизематозными расширениями, при этом в стенках мелких бронхов обнаруживались единичные гранулемы. Изучение микропрепаратов сердца не выявило патологических изменений в миокарде.
Изучение микропрепаратов группы животных, получавших полисорб МП, выявило наличие морфологических изменений печени и почек, аналогичные изменениям в группе животных, получавших УА (Фиг. 8а и в).
Изменения в легких соответствуют морфологической картине органов животных, получавших ПДС, но дополнительно наблюдали ярко выраженную гиперемию сосудов, при этом гранулемы в стенках мелких бронхов не просматривались. В микропрепаратах миокарда патологические изменения не обнаружены.
Для количественной оценки морфофункциональных изменений в печени, почках, легких и сердце крыс с ОЭТ, индуцированных ТХМ и бактериальным ЛПС, и коррекции их препаратами вычисляли объемные доли (мкм3/мкм3) основных гистологических компонентов изученных органов (табл. 4).
При ОЭТ развивался жировой гепатоз и явления гепатофиброза. Количественными характеристиками этого процесса стали увеличение объемных долей гепатоцитов с жировой дистрофией, некрозов центральных вен, соединительной ткани.
На фоне лечения энтеросорбентами в ОЭТ выявлено, что у крыс, получавших ПДС, количество гепатоцитов с жировой дистрофией снижалось в 2 раза, некротизированных клеток - в 3 раза по сравнению с аналогичными показателями у крыс, леченных УА и Полислирбом МП (табл.4). Сравнение результатов в группах показало, что эффективность протекторного действия энтеросорбентов в отношении паренхимы печени на модели ОЭТ убывала в ряду: ПДС > УА > Полисорб МП.
В эксперименте с ОЭТ наблюдали нарушение канальцевой реабсорбции в почках, усиление гемодинамических нарушений в микрососудах всех исследованных органов паренхемы почек. Полисорб МП и ПДС практически полностью нормализовали содержание просвета канальцев, соединительной ткани и капилляров клубочек в опытах с ОЭТ. УА проявлял меньшую терапевтическую активность (табл.4). Эффективность протекторного действия энтеросорбентов в отношении почечной паренхимы при ОЭТ убывала в ряду: Полисорб МП>ПДС>УА.
Введение крысам ТХМ и ЛПС в условиях хронического эксперимента приводило к достоверному повышению в сыворотке крови активностей АЛТ и ACT в 2,1 и 1,7 раза соответственно, увеличению уровня МДА в 2,5 раза, а также снижению содержания белка на 36% и мочевины на 40% по сравнению с аналогичными показателями контрольной группы животных (табл. 5).
У животных с ХЭТ введение сорбентов ограничивало выход в кровяное русло АЛТ: под влиянием УА - на 12%, Полисорба МП - на 19%, ПДС - на 28% в сравнении с аналогичными показателями крыс, получавших ТХМ и бактериальный ЛПС (p<0,05). Активность ACT в сыворотке крови животных, которым вводили УА и Полисорба МП, уменьшалась на 15%, ПДС - на 20% (p<0,05) (табл.5).
Уменьшение активности ферментов под действием сорбентов может быть связано с ингибированием интенсивности ПОЛ, о чем свидетельствовало снижение в сыворотке крови уровня МДА: у животных, получавших УА и Полисорба МП, - на 40%, ПДС - на 30% в сравнении с соответствующим показателем крыс с ХЭТ, не подвергавшихся лечению энтеросорбентами (p<0,05) (табл.5).
Введение исследуемых препаратов препятствовало снижению содержания мочевины в сыворотке крови, ее уровень под влиянием Полисорба МП был на 12,5, УА - на 23 и ПДС - 17% выше, чем аналогичный показатель у животных с ХЭТ (табл.1). Концентрация белка повышалась на 20, 31 и 26% соответственно (р<0,05) (табл.5).
Развитие выраженной эндотоксической реакции под влиянием ТХМ и ЛПС на модели хронического эндотоксикоза (ХЭТ) подтверждалось выраженными нарушениями структуры клеток печени и почек.
На срезах печени границы долек определялись слабо, центральные вены и синусоиды незначительно и неравномерно расширены. В портальных трактах наблюдали увеличение просвета и переполнение эритроцитами части междольковых вен, клеточный детрит сдавливал центральную вену, затрудняя ее визуализацию. По ходу портальных трактов присутствовала лимфоцитарная инфильтрация. Часть гепатоцитов имела признаки жировой дистрофии или была некротизирована. Гибель гепатоцитов регистрировали преимущественно в центральной части дольки. Обнаруживались клетки с признаками гипертрофии, размер которых превышал обычные в 2-3 раза (Фиг. 9а).
В микропрепаратах животных с ХЭТ, получавших ПДС, Полисорб МП и УА, гистологическая картина печени в целом была сходна с таковой в группе животных с эндотоксикозом, однако присутствующие признаки жировой дистрофии и некроза гепатоцитов выражены значительно слабее (Фиг. 9в, г, д).
Количественными характеристиками этого процесса стало увеличение объемных долей гепатоцитов с жировой дистрофией, некрозов, центральных вен, соединительной ткани (табл. 6).
На фоне лечения ПДС количество клеток печени с жировой дистрофией снижалось в 2 раза, некрозов - в 3 раза по сравнению с аналогичными показателями у крыс, получавших УА и Полисорб МП. Сравнение результатов измерений показало, что эффективность протекторного действия энтеросорбентов в отношении паренхимы печени на модели ХЭТ убывала в ряду: ПДС > Полисорб МП > АУ.
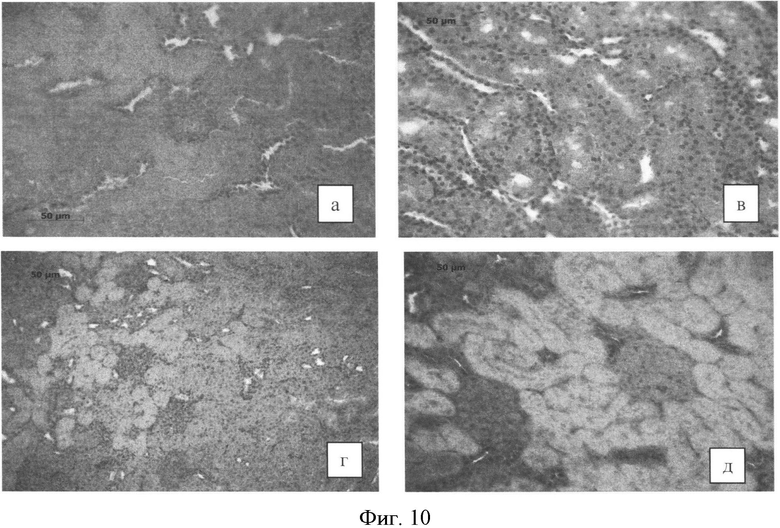
При ХЭТ в паренхиме почек крыс развивалась выраженная дисметаболическая нефропатия, признаками которой являлись сосудистые нарушения, отек и инфильтрация ткани, дистрофия и некроз эпителия канальцев, развитие очагового нефросклероза (рис. 10а). Количественными критериями развития ЭТ стал прирост объемной доли соединительной ткани и пространства клубочков и пространства капсул Боумена. В паренхиме почек животных, получавших УА, наблюдали снижение количества капилляров клубочек в 2 раза, эпителия канальцев - 1,7 раз и увеличение пространства капсул Баумена и сосудов в 2 раза (табл.6). У всех животных, леченых энтеросорбентами, отмечали выраженный некроз ткани почек. У крыс, получавших ПДС, проявлялись более выраженные повреждения канальцев почек (Фиг. 10в, г, д).
Эффективность протекторного действия энтеросорбентов в отношении почечной паренхимы на модели ХЭТ убывала в ряду: Полисорб МП>АУ>ПДС.
Таким образом, на основании проведенных исследований можно сделать вывод о том, что порошок, полученный из высушенной дерновины сфагнумов (ПДС) S. girgensohnii Russ, S. capillifolium (Ehrh.) Hedw, S. fimbriatum Wils. in Wils.et Hook. f., S. fuscum (Schimp.) Klinggr, S. russowii Warnst., S. rubellum Wils., S. aongstroemii C. Hartm., S. centrale C. Jens, ex H. Arnell et C. Jens, S. magellanicum Brid, S. palustre L., S. papillosum Lindb, S. squarrosum Crome., S. angustifolium (Russ. ex Russ.) C. Jens., S. balticum (Russ.) Russ. ex C. Jens, S. cuspidatum Ehrh ex Hoffm., S. lindbergii Schimp. ex Lindb, S. lenense H. Lindb. ex Savicz., S. majus (Russ.) C. Jens, S. flexuosum Dozy et Molk., S. fallax (Klinggr.) Klinggr., S. obtusum Warnst., S. riparium Aongstr., S. jensenii H. Lindb., S. wulfianum Girg., можно использовать в качестве средства, обладающего адсорбционными и детоксикационными свойствами.
1 - p<0,01 по сравнению с эндотоксикозом, вызванным ТХМ+ЛПС,
2 - p<0,01 по сравнению с контрольной группой.
1 - p≤0,01 по сравнению с контрольной группой,
2 - p≤0,05 по сравнению с группой ОЭТ.
1 - р<0,05 по сравнению с эндотоксикозом, вызванным ТХМ+ЛПС,
2 - р<0,05 по сравнению с контрольной группой.
1 - p≤0,01 по сравнению с контрольной группой,
2 p≤0,05 по сравнению с группой ХЭТ.
Источники информации, принятые во внимание при составлении описания
1. Гаев, П.А. Энтеросорбция как метод эфферентной терапии: учебное пособие / П.А. Гаев, О.Ф. Калев, А.В. Коробкин. - Челябинск: ЧелГМА, 2001. - 56 с.
2. ГОСТ-4453-74 Уголь активный осветляющий древесный порошкообразный.
3. Марупов, А.М. Эндотоксикоз при острых экзогенных отравлениях / А.М. Марупов, Е.А. Лужников, Ю.С. Гольдфарб // Токсикологический вестник. - 2004. - №5 - С.2-8.
4. Новочадов, В. В. Эндотоксикоз: Моделирование и органопатология: монография / В.В. Новочадов, В.Б. Писарев. - Волгоград: Изд-во ВолГМУ, 2005. - 240 с.
5. Решетников, В.И. Оценка адсорбционной способности энтеросорбентов и их лекарственных форм / В.И. Решетников // Химико-фармацевтический журнал. - 2003. - Т.37, №5. - С.28-32.
6. Руководство по экспериментальному (доклиническому) изучению новых фармакологических веществ / под ред. Р.У. Хабриева. - 2-е изд., испр. и доп. - М.: Медицина, 2005. - 832 с.
7. Хотимченко, Ю.С.Применение энтеросорбентов в медицине / Ю.С. Хотимченко, А.В. Кропотов // Тихоокеанский медицинский журнал. - 1999. - №2. - с. 84-89.
8. Энтеросорбент растительного происхождения и способ его получения: пат. 2391998 Рос. Федерация, МПК7 A61K 36/902, A61P 1/04 / Дмитрук С.Е., Бабешина Л.Г., Келус Н.В.; заявитель и патентообладатель ГОУ ВПО «Сибирский государственный университет» Росздрава. - №2008147659/15; заявл. 02.12.2008; опубл. 20.06.2010, Бюл. №17.
9. Yagi, К.A simple fluorometric assay for lipoperoxide in blood plasma / K. Yagi // Biochem. Med. - 1976. - V.12, №2. - P.212-216.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ СРЕДСТВА, ОБЛАДАЮЩЕГО АНТИОКСИДАНТНЫМ, ЖЕЛЧЕГОННЫМ, ГЕПАТО-, РАДИО- И НЕФРОПРОТЕКТОРНЫМ, АНТИРАДИКАЛЬНЫМ, РАНОЗАЖИВЛЯЮЩИМ ДЕЙСТВИЕМ | 2007 |
|
RU2355412C1 |
| НУКЛЕОПРОТЕКТОРНОЕ, КЛЕТОЧНОСБЕРЕГАЮЩЕЕ СОРБЦИОННОЕ СРЕДСТВО | 2007 |
|
RU2347610C1 |
| ПЕРОРАЛЬНАЯ ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ЛЕЧЕНИЯ ВОСПАЛИТЕЛЬНЫХ ЗАБОЛЕВАНИЙ ЖЕЛУДОЧНО-КИШЕЧНОГО ТРАКТА | 2010 |
|
RU2445965C2 |
| ЭНТЕРОСОРБЕНТ ДЛЯ НАПРАВЛЕННОЙ СОРБЦИИ ХОЛЕРНОГО ЭКЗОТОКСИНА, ЛЕКАРСТВЕННАЯ ФОРМА ЭНТЕРОСОРБЕНТА ДЛЯ НАПРАВЛЕННОЙ СОРБЦИИ ХОЛЕРНОГО ЭКЗОТОКСИНА | 2015 |
|
RU2611356C2 |
| СПОСОБ КОРРЕКЦИИ ГЕПАТОТОКСИЧЕСКИХ РЕАКЦИЙ, ИНДУЦИРОВАННЫХ ИЗОНИАЗИДОМ | 2015 |
|
RU2601919C1 |
| ПОРИСТЫЙ СОРБЕНТ С ГЕПАТОПРОТЕКТОРНЫМИ СВОЙСТВАМИ | 2006 |
|
RU2329864C2 |
| СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ АЛКОГОЛЬНЫХ ТОКСИКОЗОВ | 2011 |
|
RU2493867C2 |
| КОМПОЗИЦИОННЫЙ ВЕТЕРИНАРНЫЙ ПРЕПАРАТ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2011 |
|
RU2477125C1 |
| КОМПОЗИЦИЯ В ВИДЕ СИРОПА ДЛЯ ДЕТОКСИКАЦИИ ОРГАНИЗМА | 2018 |
|
RU2716223C2 |
| КОМПОЗИЦИЯ, ОБЛАДАЮЩАЯ ДЕТОКСИКАЦИОННОЙ И СПАЗМОЛИТИЧЕСКОЙ АКТИВНОСТЬЮ | 2018 |
|
RU2694227C1 |



Изобретение относится к фармацевтической промышленности, а именно к средству, обладающему детоксикационной активностью при эндотоксикозе. Применение порошка дерновины сфагнумов, полученного путем измельчения высушенной дерновины сфагнумов до определенного размера, в качестве средства для введения, обладающего детоксикационной активностью при эндотоксикозах. Вышеописанное средство обладает выраженной детоксикационной активностью при эндотоксикозах при введении. 10 ил., 6 табл.
Применение порошка дерновины сфагнумов, полученного путем измельчения высушенной дерновины сфагнумов до размера 0,01-0,3 мм, в качестве средства для введения, обладающего детоксикационной активностью при эндотоксикозах.
| КЕЛУС Н.В | |||
| и др | |||
| Разработка проекта фармакопейной статьи на субстанцию сфагнума бурого (Sphagnum fuscum L.) // Бюллетень сибирской медицины, N5, 2011, стр.121-125 | |||
| КЕЛУС Н.В | |||
| и др | |||
| Адсорбционная активность сырья водно-болотных растений Западной Сибири //Бюллетень сибирской медицины, N4, 2009, стр.37-41 | |||
| ЭНТЕРОСОРБЕНТ РАСТИТЕЛЬНОГО ПРОИСХОЖДЕНИЯ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2008 |
|
RU2391998C1 |
| Технология гранул | |||
Авторы
Даты
2015-08-20—Публикация
2013-10-17—Подача