Область техники
Приоритет
Настоящая заявка утверждает преимущество предварительной заявки США № 61/217133, поданной 26 мая 2009 года, которая включена в данное описание в полном объеме посредством ссылки.
Настоящее изобретение относится к области биологической науки, в частности, к области терапии онкологических заболеваний. В частности, изобретение относится к новым пептидам, которые чрезвычайно эффективны в качестве противораковых вакцин и лекарственных средств для лечения и предупреждения опухолей.
Предпосылки изобретения
Рак легких представляет собой самую распространенную форму рака, составляющую 1,35 млн. из 10,9 млн. новых случаев рака в год. Он также является основной причиной смерти от связанного с раком заболевания, что составляет 1,18 млн. из 6,7 млн. смертей, связанных с раком, во всем мире (непатентная литература, NPL 1). Несмотря на недавние улучшения в системной терапии, как например, химиотерапия и молекулярно-адресная терапия, прогноз для пациентов с раком легких в поздней стадии остается весьма неутешительным (NPL 2). Рак легких рецидирует у 50% пациентов после операции, и менее 25% пациентов реагирует на системную химиотерапию. В связи с этим, крайне необходимы более эффективные способы лечения, и иммунотерапия представляет один из перспективных подходов для лечений рака легких в будущем (NPL 3-5).
Успех терапевтических противораковых вакцин может основываться, в конечном счете, на идентификации иммуногенных антигенов, которые сверхэкспрессируются в опухолях по сравнению с нормальными тканями. Эффективная индукция цитотоксических Т-лимфоцитов (ЦТЛ) опухолеспецифическими антигенами (ОСА) продемонстрировала многообещающие результаты (NPL 6-7). В последнее время развитие технологии кДНК-микрочипов, наряду с геномной информацией, предоставило исчерпывающие профили экспрессии генов в злокачественных клетках, которые затем можно сравнивать с таковыми в нормальных клетках (NPL 8). Получение профилей экспрессии генов при помощи технологий кДНК-микрочипов представляет собой эффективный подход для выявления новых ОСА, полезных для диагностики рака и иммунотерапии (NPL 9-12).
Несмотря на то, что официально сообщалось о некоторых кандидатах в ОСА, экспрессируемых при раке легких (NPL 13-14), важно идентифицировать разнообразные ОСА, сверхэкспрессирующиеся при данном раке, для разработки более эффективной противораковой иммунотерапии, опосредованной Т-клетками (NPL 15).
CDC45L (cell division cycle 45-like) представляет собой жизненно важный клеточный белок, который функционирует как в инициации, так и в элонгации при репликации ДНК для обеспечения репликации хромосомной ДНК только один раз за клеточный цикл (NPL 16-19). CDC45L является высоко консервативным среди всех эукариотов, и направленное разрушение этого гена приводит к эмбриональной летальности у мышей (NPL 20). У взрослых людей подавляющее большинство клеток является дифференцированными и прекратило клеточное деление, и только небольшая популяция клеток пролиферируется в некоторых самообновляющийся тканях (NPL 21). Таким образом, в то время как CDC45L отсутствует в покоящихся в течение длительного времени, окончательно дифференцированных и стареющих клетках человека, он присутствует в пролиферирующих раковых клетках на протяжении всего клеточного цикла (NPL 18). Соответственно, экспрессия CDC45L тесно связана с пролиферирующими популяциями клеток, и, таким образом, CDC45L считается перспективным кандидатом в качестве нового маркера пролиферации в клеточной биологии рака (NPL 18, 22). Однако пригодность CDC45L в качестве мишени для иммунотерапии рака еще не была полностью исследована.
Список ссылок
Непатентная литература

Краткое описание изобретения
Настоящее изобретение основывается, по крайней мере частично, на открытии пептидов, которые могут служить в качестве мишеней иммунотерапии. Открытие соответствующих мишеней является чрезвычайно важным, поскольку ОСА иногда воспринимаются иммунной системой как «свои» и, вследствие этого, часто не обладают иммуногенностью. Как отмечалось выше, CDC45L (типичные аминокислотная последовательность и генная последовательность приведены в SEQ ID NO: 18 и SEQ ID NO: 17, соответственно, и последовательности также доступны из GenBank под номером NM_003504) был идентифицирован как активированный при раках, неограничивающие примеры которых включают опухоль яичка, рак поджелудочной железы, рак мочевого пузыря, немелкоклеточный рак легкого, мелкоклеточный рак легкого, рак молочной железы, рак пищевода, рак предстательной железы, хронический миелоидный лейкоз (ХМЛ), опухоль мягких тканей, рак желудка, гепатобилиарный рак и рак прямой кишки. Таким образом, CDC45L является кандидатом в качестве мишени иммунотерапии рака/опухолей.
Настоящее изобретение также относится к идентификации специфических эпитопных пептидов генного продукта CDC45L, которые обладают способностью индуцировать ЦТЛ, специфичные для CDC45L. Как подробно обсуждается ниже, мононуклеарные клетки периферической крови (PBMC), полученные от здоровых доноров, стимулировали при помощи связывающихся с HLA-A*2402 или HLA-A*0201 пептидов-кандидатов, полученных из CDC45L. Затем были образованы линии ЦТЛ со специфической цитотоксичностью в отношении HLA-А24- или HLA-A2-положительных клеток-мишеней, подвергнутых импульсному воздействию каждым из пептидов-кандидатов. Данные результаты показывают, что эти пептиды представляют собой HLA-А24- или HLA-A2-рестриктированные эпитопные пептиды, которые могут индуцировать сильные и специфические иммунные ответы в отношении клеток, экспрессирующих CDC45L. Кроме того, полученные результаты показывают, что CDC45L является сильным иммуногеном и его эпитопы представляют собой эффективные мишени для иммунотерапии рака/опухолей.
Соответственно, предметом по настоящему изобретению является предоставление выделенных пептидов, связывающихся с HLA-антигеном, в особенности таких, которые получены из CDC45L (SEQ ID NO: 18), или их иммунологически активных фрагментов. Предполагается, что эти пептиды обладают способностью индуцировать ЦТЛ и поэтому могут быть использованы для индуцирования ЦТЛ ex vivo, или их можно вводить субъекту для индукции иммунного ответа против раков, таких как опухоль яичка, рак поджелудочной железы, рак мочевого пузыря, немелкоклеточный рак легкого, мелкоклеточный рак легкого, рак молочной железы, рак пищевода, рак предстательной железы, хронический миелоидный лейкоз (ХМЛ), опухоль мягких тканей, рак желудка, гепатобилиарный рак, рак прямой кишки и т.д. Предпочтительно, пептиды представляют собой нонапептиды или декапептиды и более предпочтительно имеют последовательность аминокислот, выбранную из SEQ ID NO: 1-16. Среди них пептиды, имеющие последовательность аминокислот, выбранную из SEQ ID NO: 2, 3, 4, 7 и 12, демонстрировали сильную способность индуцировать ЦТЛ и, таким образом, являются наиболее предпочтительными.
Пептиды по настоящему изобретению включают такие, у которых одна, две или несколько аминокислот заменены, удалены или добавлены, при условии, что полученные модифицированные пептиды сохраняют исходную способность индуцировать ЦТЛ.
Настоящее изобретение также предоставляет выделенные полинуклеотиды, кодирующие любой из пептидов по настоящему изобретению. Эти полинуклеотиды можно использовать для индуцирования антигенпредставляющих клеток (АПК) со способностью индуцировать ЦТЛ, и можно вводить субъекту для стимулирования иммунного ответа против рака подобно настоящим пептидам.
При введении субъекту настоящие пептиды предпочтительно представлены на поверхности АПК, чтобы индуцировать ЦТЛ, нацеливающие соответствующие пептиды. Соответственно, еще одним объектом по настоящему изобретению является предоставление композиций или веществ, которые индуцируют ЦТЛ, где такие композиции или вещества включают один или несколько пептидов или полинуклеотидов по настоящему изобретению. Настоящее изобретение также рассматривает композиции или вещества, включающие один или несколько пептидов или полинуклеотидов по настоящему изобретению, составленные для лечения и/или профилактики раковых заболеваний, а также предупреждения их послеоперационных рецидивов, таких видов рака, в качестве неограничивающих примеров, как опухоль яичка, рак поджелудочной железы, рак мочевого пузыря, немелкоклеточный рак легкого, мелкоклеточный рак легкого, рак молочной железы, рак пищевода, рак предстательной железы, хронический миелоидный лейкоз (ХМЛ), опухоль мягких тканей, рак желудка, гепатобилиарный рак и рак прямой кишки. Таким образом, настоящее изобретение также предоставляет фармацевтические композиции или вещества для лечения и/или профилактики рака и/или предупреждения его послеоперационных рецидивов, где такие фармацевтические композиции или вещества включают один или несколько пептидов или полинуклеотидов по настоящему изобретению. В дополнение к и/или вместо вышеупомянутых пептида или полинуклеотида, фармацевтические композиции или вещества по настоящему изобретению могут необязательно включать, в качестве активных ингредиентов, АПК или экзосомы, которые представляют один или несколько представленных пептидов по настоящему изобретению.
Пептиды и полинуклеотиды по настоящему изобретению могут индуцировать АПК, которые представляют на своей поверхности комплекс HLA-антигена и настоящего пептида, например, путем контактирования АПК, полученных от субъекта, с пептидом по настоящему изобретению или путем введения полинуклеотида, кодирующего такой пептид, в АПК. Такие АПК обладают высокой способностью индуцировать ЦТЛ в отношении пептидов-мишеней и находят применение в иммунотерапии рака. Таким образом, настоящее изобретение охватывает способы индуцирования АПК со способностью индуцировать ЦТЛ, и АПК, полученные с помощью таких способов.
Настоящее изобретение также предоставляет способ индуцирования ЦТЛ, который включает стадию совместного культивирования CD8-положительных клеток с АПК или экзосомами, представляющими пептид по настоящему изобретению на своей поверхности. Альтернативно, способ может включать стадию введения гена, который содержит полинуклеотид, кодирующий субъединицу Т-клеточного рецептора (ТКР), способную связываться с пептидом по настоящему изобретению. ЦТЛ, полученные с помощью таких способов, могут найти применение при лечении и/или предупреждении раковых заболеваний, неограничивающие примеры которых включают опухоль яичка, рак поджелудочной железы, рак мочевого пузыря, немелкоклеточный рак легкого, мелкоклеточный рак легкого, рак молочной железы, рак пищевода, рак предстательной железы, хронический миелоидный лейкоз (ХМЛ), опухоль мягких тканей, рак желудка, гепатобилиарный рак и рак прямой кишки. Таким образом, настоящее изобретение охватывает ЦТЛ, полученные при помощи настоящих способов.
Еще одним предметом по настоящему изобретению является предоставление способов индуцирования иммунного ответа против рака у нуждающегося в этом субъекта, где такие способы включают стадию введения композиций или веществ, содержащих полипептиды CDC45L по настоящему изобретению или их иммунологически активные фрагменты, полинуклеотиды, кодирующие полипептиды CDC45L по настоящему изобретению, или экзосомы или АПК, представляющие такие полипептиды CDC45L.
В частности, настоящее изобретение представляет следующие [1]-[22]:
[1] Выделенный пептид, связывающийся с HLA-антигеном и обладающий способностью индуцировать цитотоксические Т-лимфоциты (ЦТЛ), где пептид получен из полипептида, состоящего из аминокислотной последовательности SEQ ID NO: 18, или иммунологически активного фрагмента,
[2] Выделенный пептид по [1], где HLA-антиген представляет собой HLA-А24 или HLA-А2,
[3] Выделенный пептид по [1] или [2], где указанный пептид содержит аминокислотную последовательность, выбранную из группы, состоящей из:
(a) SEQ ID NO: 4, 2, 3, 7 и 12; и
(b) SEQ ID NO: 4, 2, 3, 7 и 12, где 1, 2 или несколько аминокислот заменены, встроены, удалены и/или добавлены:
[4] Выделенный пептид по любому из [1]-[3], где пептид обладает одной или обеими из следующих характеристик:
(a) вторая аминокислота с N-конца представляет собой или модифицирована, чтобы представлять собой аминокислоту, выбранную из группы, состоящей из фенилаланина, тирозина, метионина и триптофана; и
(b) C-концевая аминокислота представляет собой или модифицирована, чтобы представлять собой аминокислоту, выбранную из группы, состоящей из фенилаланина, лейцина, изолейцина, триптофана и метионина.
[5] Выделенный пептид по любому из [1]-[3], где пептид обладает одной или обеими из следующих характеристик:
(a) вторая аминокислота с N-конца представляет собой или модифицирована, чтобы представлять собой аминокислоту, выбранную из группы, состоящей из лейцина и метионина; и
(b) C-концевая аминокислота представляет собой или модифицирована, чтобы представлять собой аминокислоту, выбранную из группы, состоящей из валина и лейцина,
[6] Выделенный пептид по любому из [1]-[5], где пептид представляет собой нонапептид или декапептид,
[7] Выделенный полинуклеотид, кодирующий пептид по любому из [1]-[6],
[8] Композиция для индуцирования ЦТЛ, где композиция содержит один или несколько из пептидов, описанных в любом из [1]-[6], или один или несколько из полинуклеотидов, описанных в [7],
[9] Фармацевтическая композиция для лечения и/или профилактики рака и/или предупреждения его послеоперационных рецидивов, где композиция содержит один или несколько из пептидов, описанных в любом из [1]-[6], или один или несколько из полинуклеотидов, описанных в [7],
[10] Фармацевтическая композиция по [9], составленная для введения субъекту, чей HLA-антиген представляет собой HLA-А24 или HLA-A2,
[11] Фармацевтическая композиция по [9] и [10], составленная для лечения рака,
[12] Способ индуцирования антигенпредставляющих клеток (АПК) со способностью индуцировать ЦТЛ, включающий стадию, выбранную из группы, состоящей из следующего:
(a) контактирование АПК с пептидом по любому из [1]-[6] in vitro, ex vivo и in vivo, и
(b) введение полинуклеотида, кодирующего пептид по любому из [1]-[6], в АПК,
[13] Способ индуцирования ЦТЛ, где способ включает стадию, выбранную из группы, состоящей из:
a) совместное культивирование CD8-положительных Т-клеток с АПК, которые представляют на своей поверхности комплекс HLA-антигена и пептида по любому из [1] до [6];
(b) совместное культивирование CD8-положительных Т-клеток с экзосомами, которые представляют на своей поверхности комплекс HLA-антигена и пептида по любому из [1]-[6]; и
(c) введение гена, который содержит полинуклеотид, кодирующий полипептид субъединицы Т-клеточного рецептора (ТКР), способный связывать пептид по любому из [1]-[6], в Т-клетки,
[14] Выделенная АПК, которая представляет на своей поверхности комплекс HLA-антигена и пептида по любому из [1]-[6],
[15] АПК по [14], которую индуцируют при помощи способа по [12],
[16] Выделенный ЦТЛ, который нацелен на любой из пептидов по [1]-[6],
[17] ЦТЛ по [16], который индуцируют при помощи способа по [13],
[18] Способ индуцирования иммунного ответа против рака у субъекта, где способ включает введение субъекту композиции, содержащей один или несколько пептидов по [1]-[6], один или несколько их иммунологически активных фрагментов или один или несколько полинуклеотидов, кодирующих пептид или фрагмент,
[19] Антитело или его фрагмент против любого из пептидов по [1]-[6],
[20] Вектор, включающий нуклеотидную последовательность, кодирующую любой из пептидов по [1]-[6],
[21] Клетка-хозяин, трансформированная или трансфицированная экспрессионным вектором по [20], и
[22] Диагностический набор, содержащий любой из пептидов по [1]-[6], нуклеотид по [7] или антитело по [19].
Применимость настоящего изобретения распространяется на любое число заболеваний, связанных с или являющихся результатом сверхэкспрессии CDC45L, таких как рак, неограничивающие примеры которого включают опухоль яичка, рак поджелудочной железы, рак мочевого пузыря, немелкоклеточный рак легкого, мелкоклеточный рак легкого, рак молочной железы, рак пищевода, рак предстательной железы, хронический миелоидный лейкоз (ХМЛ), опухоль мягких тканей, рак желудка, гепатобилиарный рак и рак прямой кишки.
В дополнение к вышесказанному, другие предметы и признаки изобретения станут в более полной степени очевидными после прочтения следующего подробного описания в сочетании с сопутствующими фигурами и примерами. Однако необходимо понимать, что как предшествующее краткое описание настоящего изобретения, так и нижеследующее подробное описание представляют собой иллюстративные варианты осуществления и не являются ограничивающими настоящее изобретение или другие альтернативные варианты осуществления настоящего изобретения. В частности, хотя изобретение и описывается в настоящем документе с учетом ряда конкретных вариантов осуществления, следует принять во внимание, что описание является иллюстрацией изобретения и не построено как ограничение изобретения. Различные модификации и приложения могут быть определены тем, кто специализируется в рассматриваемой области, без отступления от сущности и объема изобретения, как описано в прилагаемых пунктах формулы изобретения. Аналогичным образом, другие объекты, признаки, достоинства и преимущества настоящего изобретения будут понятны из этого краткого описания и конкретных вариантов осуществления, описанных ниже, и будут совершенно очевидны тем, кто специализируется в рассматриваемой области. Такие предметы, признаки, достоинства и преимущества будут очевидны из вышесказанного в сочетании с прилагаемыми примерами, данными, фигурами и всеми разумными заключениями, вытекающими из этого, сами по себе или с учетом ссылок, включенных в настоящий документ.
Краткое описание чертежей
Различные аспекты и приложения по настоящему изобретению станут очевидными специалисту в рассматриваемой области после рассмотрения краткого описания фигур и подробного описания настоящего изобретения и его предпочтительных вариантов осуществления, которые следуют.
[Фиг. 1a-d] Фигура 1 состоит из серий фотографий, от A до F, описывающих результаты анализов экспрессии мРНК CDC45L человека в нормальных тканях, раковых клеточных линиях и раковых тканях. Части A, B: RT-PCR и Нозернблот-анализ мРНК CDC45L, экспрессируемых в различных нормальных тканях. Часть C: Анализ при помощи ПЦР в реальном времени мРНК CDC45L, экспрессируемых в различных раковых линиях клеток. Часть D: Анализ при помощи RT-PCR мРНК CDC45L, экспрессируемых в раковых тканях легких и прилегающих нормальных тканях легких.
[Фиг. 1e-f] Часть E: Анализ при помощи RT-PCR мРНК CDC45L, экспрессируемых в различных раковых линиях клеток, полученных из рака желудка, гепатобилиарного рака, рака молочной железы, рака поджелудочной железы и колоректального рака. Часть F: Иммуногистохимический анализ белка CDC45L, экспрессируемого в аденокарциноме, плоскоклеточной карциноме, мелкоклеточной карциноме, нормальных легких, яичке и нормальной коже (первоначальное увеличение - 400-кратное). Сигналы положительного окрашивания выглядят, как коричневые. Масштаб линейки 50 мкм.
[Фиг. 2] На фигуре 2 представлен протокол индукции CDC45L-специфичных ЦТЛ из PBMC. PBMC были выделены из доноров, и Т-клетки CD8+ и клетки CD14+ выделяли при помощи микробус, покрытых анти-CD8 mAb или анти-CD14 mAb, соответственно, из PBMC HLA-А24-положительных здоровых доноров и пациентов с раком легких. DC (дендритные клетки) были получены из клеток CD14+, глубокой культуры в присутствии GM-CSF и IL-4 в течение 5 дней. DC подвергали импульсному воздействию HLA-А24-связывающихся пептидов в присутствии бета-2-микроглобулина в течение 2 ч при 37 градусах C. Эти подвергнутые импульсному воздействию пептидов DC затем облучали и смешивали в соотношении 1:20 с аутологичными Т-клетками CD8+ для образования пептид-реактивных ЦТЛ. Клетки культивировали с IL-7 в AIM-V с добавлением 2% аутосыворотки в день 0, и к этим культурам добавляли IL-2 на 2-ой день. Две дополнительные еженедельные стимуляции нагруженными пептидами аутологичными PHA-бластными клетками проводили на 7-ой и 14-ый день. INF-гамма ELISPOT, CD107a-мобилизацию и тесты по высвобождению 51Cr проводили на 6-ые дни после третьего раунда пептидного стимулирования Т-клеток CD8+.
[Фиг. 3] Фигура 3 состоит из серий гистограмм А-C, представляющих ЦТЛ-ответ у здоровых доноров на пептиды, полученные из CDC45L. Части A, B, C: анализ ELISPOT CDC45L пептид-реактивных ЦТЛ, образованных из PBMC HLA-А24-положительных здоровых доноров (A, C - здоровый донор-1; В - здоровый донор-4). Т-клетки CD8+ стимулировали аутогенными DC, полученными из моноцитов, (день 0) и аутогенными PHA-бластными клетками (7-ой и 14-ый день), подвергнутыми импульсному воздействию смеси 4 из 16 пептидов-кандидатов (SEQ ID NO: от 1 до 16). ЦТЛ собирали на 20-ый день, и ЦТЛ, продуцирующие IFN-гамма, детектировали при помощи анализа ELISPOT. Столбцы указывают на количество точек IFN-гамма, когда линии ЦТЛ повторно стимулировали клетками C1R-A2402, подвергнутых импульсному воздействию пептидами, полученными из CDC45L, (открытый столбец) или посторонним пептидом HIV-А24 (закрытый столбец). Соотношение эффекторов к клеткам-мишеням составляет 10:1. Данные представлены как среднее +/- SD из трех повторностей. Для каждого донора приведен образец двух независимых экспериментов с похожими результатами.
[Фиг. 4] Фигура 4 состоит из серии панелей, представляющих уровень CD107a, экспонированных на поверхности CD8+ Т-клеток после стимуляции антигеном. Все пептиды были использованы в конечной концентрации 1 мкг/мл. Представленные события являются окнами для CD8+ Т-клеток. Верхняя и средняя панели: стимулировали родственными пептидами, полученными из CDC45L. Нижняя панели: стимулировали посторонним пептидом HIV-А24. Числа внутри графиков показывают процент клеточной популяции с квадрантной характеристикой (CD8+ CD107a+ Т-лимфоциты). Каждая линия является представителем двух независимых экспериментов с похожими результатами.
[Фиг. 5-c] Фигура 5 состоит из серии графиков A-D, представляющих индукцию CDC45L-специфических ЦТЛ человека из PBMC HLA-А24-положительных пациентов с раком легких. Часть A: анализ ELISPOT ЦТЛ, индуцированных от пациентов с раком легких, культивируемых совместно с клетками-мишенями, подвергнутых импульсному воздействию CDC45L-А24-9-109-2(SEQ ID NO: 2), CDC45L-А24-9-294-3(SEQ ID NO: 3), CDC45L-А24-9-556-4(SEQ ID NO: 4), CDC45L-А24-9-370-7(SEQ ID NO: 7) или пептида CDC45L-А24-10-556-12(SEQ ID NO: 12). Продуцирование IFN-гамма клетками C1R-А*2402, стимулированных импульсным воздействием пептидов, было значительно большим, чем клетками C1R-А*2402, стимулированными импульсным воздействием HIV-пептида. Столбцы указывают на число точек IFN-гамма, когда образованные линии ЦТЛ были повторно стимулированы клетками C1R-A2402, подвергнутых импульсному воздействию пептидов, полученных из CDC45L (открытый столбец), или постороннего пептида HIV-А24 (закрытый столбец). Соотношение эффектор:клетки-мишени составляет 10:1. Данные представлены как среднее +/- SD трех повторностей. Часть B: Цитотоксичность ЦТЛ против клеток C1R-A2402, подвергнутых импульсному воздействию родственных пептидов, полученных из CDC45L (белый треугольник; CDC45L-А24-9-109-2(SEQ ID NO: 2), CDC45L-А24-9-294-3(SEQ ID NO: 3), CDC45L-А24-9-556-4(SEQ ID NO: 4), CDC45L-А24-9-370-7(SEQ ID NO: 7) или CDC45L-А24-10-556-12(SEQ ID NO: 12), и клеток C1R-A2402, подвергнутых импульсному воздействию постороннего пептида HIV-А24 (черный треугольник), в тесте по высвобождению 51Cr. Каждое значение представляет собой процент от специфического лизиса, рассчитанное на основе средних значений из трех повторностей. Часть C: Вестерн-блот-анализ суммарных лизатов клеток, полученных из клеток Lu99 (левая панель, линия 1), клеток Lu99, трансфицированных siRNA CDC45L (левая панель, линия 2) или контрольной siRNA GFP (левая панель, линия 3) и клеток ЕВС-1 (правая панель, линия 1), клеток EBC-1, трансфицированных siRNA CDC45L (правая панель, линия 2) или контрольной siRNA GFP (правая панель, линия 3), с использованием антитела anti-CDC45L. Бета-актин служил в качестве внутреннего контроля.
[Фиг. 5d] Часть D: Аннулирование CDC45L-специфической цитотоксической активности ЦТЛ путем понижающей регуляции белка CDC45L в клетках-мишенях Lu99 и EBC-1 (CDC45L*, HLA-A*2402+). Цитотоксические активности ЦТЛ в отношении Lu99, EBC-1, CDC45L siRNA Lu99, CDC45L siRNA EBC-1, GFP siRNA Lu99, GFP siRNA EBC-1 или A549 анализировали при помощи теста по высвобождению 51Cr. Каждое значение представляет процент специфического лизиса, рассчитанный на основе средних значений трех повторностей.
[Фиг. 6] Фигура 6 состоит из серии графиков, представляющих ингибирование ответов CDC45L-реактивных ЦТЛ при помощи mAb против HLA класса I. После инкубации клеток-мишеней Lu99 с mAb против HLA класса I (W6/32, IgG2a) или контрольными mAb против HLA класса II (IgG2a) в течение 1 ч клетки Lu99 культивировали совместно с ЦТЛ, образованными от CD8+ Т-клеток здоровых доноров или пациентов с раком легких путем стимуляции с пептидами CDC45L-А24-9-109-2(SEQ ID NO: 2), CDC45L-А24-9-294-3(SEQ ID NO: 3), CDC45L-А24-9-556-4(SEQ ID NO: 4) или CDC45L-А24-9-370-7(SEQ ID NO: 7). Показаны продуцирование IFN-гамма (Часть А) и цитотоксичность (Часть Б), обусловленная ЦТЛ. Белый кружок, Lu99; черный кружок, Lu99+W6/32; белый квадрат, Lu99+контрольное mAb. Данные представлены как среднее +/- SD трех повторностей. Статистически существенные различия отмечены звездочками (*P<0,05).
[Фиг. 7] Фигура 7 состоит из серии графиков А-C, представляющих индукцию как HLA-А24(А*2402)-, так и HLA-A2(*0201)-рестриктированных ЦТЛ путем стимуляции пептидом CDC45L-A2-9-556-4(SEQ ID NO: 4, также упоминаемый в настоящем документе как CDC45L-А24-9-556-4), 556KFLDALISL564. Часть A: анализ IFN-гамма ELISPOT ЦТЛ, индуцированных от HLA-A*0201-положительного здорового донора, совместно культивируемых с клетками T2, подвергнутых импульсному воздействию пептида CDC45L-A2-9-556-4(SEQ ID NO: 4). Данные представлены как среднее +/- SD из трех повторностей. Часть B: Цитотоксическая активность ЦТЛ против клеток T2, подвергнутых импульсному воздействию пептида CDC45L-A2-9-556-4(SEQ ID NO: 4) (белый треугольник), клеток T2, подвергнутых импульсному воздействию пептида HIV-A2 (черный треугольник), и клеток C1R-A2402, подвергнутых импульсному воздействию пептида CDC45L-A2-9-556-4(SEQ ID NO: 4) (черный ящик), анализируемая в тесте по высвобождению 51Cr. Часть C: Ингибирование ответов CDC45L-реактивных ЦТЛ при помощи mAb против HLA класса I, анализируемая в тесте по высвобождению 51Cr. После инкубирования клеток-мишеней Panc1 (CDC45L+, HLA-A2+ и HLA-А24-) с mAb против HLA класса I (W6/32, IgG2a) или контрольным mAb против HLA класса II (IgG2a), в течение 1 ч, клетки Panc1 культивировали совместно с ЦТЛ, образованными от CD8+ Т-клеток HLA-A*0201-положительного здорового донора путем стимуляции пептидом CDC45L-A2-9-556-4(SEQ ID NO: 4). Белый кружок, клетки Panc1; черный кружок, Panc1+W6/32; белый квадрат, Panc1+контрольное mAb. Каждое значение представляет собой процент от специфического лизиса, рассчитанный на основе средних значений из трех повторностей. Представлены репрезентативные данные трех независимых экспериментов с похожими результатами.
[Фиг. 8а-b] Фигура 8 состоит из серии графиков А-D, представляющих противоопухолевую активность in vivo CDC45L-реактивных ЦТЛ человека у мышей NOD/SCID. Части A, B, C: Пептид-специфическая цитотоксическая активность ЦТЛ человека, образованных от двух здоровых доноров путем стимуляции смесью из трех полученных из CDC45L пептидов. Часть A: анализ IFN-гамма ELISPOT ЦТЛ, культивируемых совместно с клетками C1R-A2402, подвергнутых импульсному воздействию либо пептидом CDC45L-А24-9-109-2(SEQ ID NO: 2), CDC45L-А24-9-294-3(SEQ ID NO: 3) либо пептидом CDC45L-А24-9-556-4(SEQ ID NO: 4). Часть B: CDC45L-специфическая цитотоксичность ЦТЛ против Lu99 (CDC45L+, HLA-А24+) в случае отсутствия (белый кружок) или наличия mAb против HLA класса I (W6/32, черный кружок) или контрольного mAb против HLA класса II (белый квадрат), анализируемая в тесте по высвобождению 51Cr.
[Фиг. 8c-d] Часть C: Цитотоксическая активность ЦТЛ в отношении клеток C1R-A2402, подвергнутых импульсному воздействию одного из трех полученных из CDC45L пептидов (белый кружок, CDC45L-А24-9-109-2(SEQ ID NO: 2); белый квадрат, CDC45L-А24-9-294-3(SEQ ID NO: 3); белый треугольник, CDC45L-А24-9-556-4(SEQ ID NO: 4) и посторонний пептид HIV-А24 (черный кружок), анализируемая в тесте по высвобождению 51Cr. Часть D: Опухоли у мышей NOD/SCID, привитых внутривенно CDC45L-индуцированными ЦТЛ (черный квадрат, n=5), контрольные CD8+ Т-клетки (белый ромб, n=5) или один PBS (белый кружок, n=5). Когда размер опухоли достигал примерно 25 мм2 на 7 день после подкожной имплантации опухоли, внутривенно прививали ЦТЛ человека (4×106), реагирующие на смесь из трех CDC45L-пептидов. Прививку ЦТЛ повторяли на 14 день. Контрольные CD8+ Т-клетки, стимулированные посторонним HLA-А24-рестриктированным HIV-пептидом, также прививали мышам в качестве контроля. Размер опухоли выражался в квадратных миллиметрах. Каждый символ представляет средние размеры опухоли в каждой группе мышей, отрезки показывают SD. Двусторонний t-теста Стьюдента применяли для определения значимости различий между двумя группами на 42 день.
Описание вариантов осуществления
Несмотря на то, что любые способы и материалы, аналогичные или эквивалентные тем, которые описаны в настоящем документе, могут быть использованы в практике или выполнении вариантов осуществления по настоящему изобретению, сейчас описываются предпочтительные способы, приборы и материалы. При этом перед описанием настоящих материалов и способов следует понимать, что настоящее изобретение не ограничивается конкретными размерами, формами, величинами, материалами, методиками, протоколами и т.п., описанными в рассматриваемом документе, поскольку они могут меняться в соответствии с определенным режимом проведения экспериментов и/или оптимизацией. Следует также понимать, что терминология, используемая в описании, служит лишь для характеристики конкретных версий или вариантов осуществления и не предназначена для ограничения сферы применения настоящего изобретения, которая ограничивается только прилагаемыми пунктами формулы изобретения.
Раскрытие каждой публикации, патента или патентной заявки, упомянутых в данной спецификации, специально включено здесь в качестве ссылки в полном объеме. При этом ничто в настоящем документе не может быть истолковано в качестве признания того, что изобретение не дает права датировать более ранним числом такое раскрытие на основании изобретения или до изобретения.
I. Определения
Формы единственного числа, как используется здесь, означают «по крайней мере, один», если иное специально не указано.
Термины «полипептид», «пептидные» и «белок» используются взаимозаменяемо в данном документе по отношению к полимеру из аминокислотных остатков. Термины относятся к аминокислотным полимерам, в которых один или несколько аминокислотных остатков представляет собой модифицированный остаток или не встречающийся в природе остаток, такой как рассматриваемый химический миметик соответствующей аминокислоты естественного происхождения, а также к аминокислотным полимерам естественного происхождения.
Термин «аминокислоты», как используется здесь, относится к аминокислотам естественного происхождения и синтетическим аминокислотам, а также к аналогам аминокислот и миметикам аминокислот, которые функционируют аналогично аминокислотам естественного происхождения. Аминокислоты могут быть как L-, так и D-аминокислотами. Аминокислоты естественного происхождения представляют собой аминокислоты, кодируемые генетическим кодом, а также аминокислоты, модифицированные после трансляции в клетках (например, гидроксипролин, гамма-карбоксиглутаминовая кислота и О-фосфосерин). Выражение «аминокислотный аналог» относится к соединениям, которые обладают той же основной химической структурой (альфа-углеродный атом, связанными с водородом, карбоксильная группа, аминогруппа и R-группа), что и у аминокислоты естественного происхождения, но имеет модифицированную R-группу или модифицированный каркас (например, гомосерин, норлейцин, метионин, сульфоксид, метионинметилсульфоний). Выражение «миметик аминокислоты» относится к химическим соединениям, которые имеют отличные структуры, но аналогичные с обычными аминокислотами функции.
Аминокислоты могут называться здесь их широко известными трехбуквенными символами или однобуквенными символами, рекомендованными Биохимической номенклатурной комиссией IUPAC-IUB.
Термины «ген», «полинуклеотиды», «нуклеотиды» и «нуклеиновые кислоты» используются взаимозаменяемо здесь, и, если специально не указано, сходно с аминокислотами их называют по общепринятым однобуквенным кодам.
Термин «композиция», используемый в настоящем документе, предназначен для охватывания продукта, включающего определенные ингредиенты в определенных количествах, а также любого продукта, который образуется, прямо или косвенно, от комбинации определенных ингредиентов в определенных количествах. Такой термин по отношению к «фармацевтической композиции» предназначен для охватывания продукта, включающего активный ингредиент(ты), и любого инертного ингредиента(ов), которые составляют носитель, а также любого продукта, который образуется, прямо или косвенно, от комбинации, комплексообразования или агрегации двух или нескольких ингредиентов, или от диссоциации одного или нескольких ингредиентов, или от других типов реакций и взаимодействий одного или нескольких ингредиентов. Соответственно, в контексте настоящего изобретения выражение «фармацевтическая композиция» охватывает любую композицию, изготовленную путем смешивания соединения по настоящему изобретению и фармацевтически или физиологически приемлемого носителя. Выражение «фармацевтически приемлемый носитель» или «физиологически приемлемый носитель», как используется в настоящем документе, означает фармацевтически или физиологически приемлемый материал, композицию, вещество или средство доставки, включая, в качестве неограничивающих примеров, жидкий или твердый наполнитель, растворитель, связующее средство, растворитель или инкапсулирующий материал, принимающий участие в переносе или транспортировке активного ингредиента(ов) от одного органа или части тела к другому органу или части тела.
Если иное не определено, термин «рак» относится к ракам и опухолям, в которых сверхэкспрессируется ген CDC45L, неограничивающих примеры которых включают опухоль яичка, рак поджелудочной железы, рак мочевого пузыря, немелкоклеточный рак легкого, мелкоклеточный рак легкого, рак молочной железы, рак пищевода, рак предстательной железы, хронический миелоидный лейкоз (ХМЛ), опухоль мягких тканей, рак желудка, гепатобилиарный рак и рак прямой кишки.
Если не определено иначе, термины «цитотоксический Т-лимфоцит», «цитотоксическая Т-клетка» и «ЦТЛ» используются взаимозаменяемо в настоящем документе и, если иное специально не указано, относятся к подгруппе Т-лимфоцитов, которые способны распознавать «не свои» клетки (например, опухолевые клетки, инфицированные вирусом клетки) и индуцировать гибель таких клеток.
Если иное не определено, термины «HLA-А24» относятся к типу HLA-А24, содержащему подтипы, такие как HLA-A*2402.
Если иное не определено, термин «HLA-А2», как используется в настоящем документе, репрезентативно относится к подтипам, таким как HLA-A*0201 и HLA-A*0206.
Если иное не определено, термин «набор», как используется в настоящем документе, применяется по отношению к комбинации реактивов и других материалов. Предполагается в настоящем документе, что набор может включать микрочип, чип, маркер и так далее. Не подразумевается, что термин «набор» ограничивается конкретным сочетанием веществ и/или материалов.
В пределах того, что способы и композиции по настоящему изобретению находят применение в контексте «лечения» рака, лечение считается «эффективным», если это приводит к клиническому преимуществу, такому как уменьшение экспрессии гена CDC45L или уменьшение размера, распространенности или метастатического потенциала рака у субъекта. В случае, когда лечение применяется профилактически, «эффективное» означает, что оно замедляет или предотвращает образование рака или предотвращает или ослабляет клинический симптом рака. Эффективность определяется в связи с каким-либо известным способом диагностики или лечения конкретного типа опухоли.
В пределах того, что способы и композиции по настоящему изобретению находят применение в контексте «предупреждения» и «профилактики» рака, такие термины взаимозаменяемо используются в настоящем документе для обозначения любой активности, которая снижает бремя смертности или процент смертности, связанной с заболеванием. Предупреждение и профилактика могут происходить «на первичном, вторичном и третичном уровнях предупреждения». В то время как первичное предупреждение и профилактика предотвращают развитие заболевания, вторичный и третичный уровни предупреждения и профилактики охватывают мероприятия, направленные на предупреждение и профилактику прогрессирования заболевания и появления симптомов, а также на уменьшение негативного воздействия уже существующего заболевания путем восстановления функций и уменьшения осложнений, связанных с заболеванием. Альтернативно, предупреждение и профилактика могут включать широкий спектр профилактических терапий, направленных на смягчение тяжести конкретного расстройства, например, снижение пролиферации и метастазирования опухолей.
В контексте настоящего изобретения лечение и/или профилактика рака и/или предупреждение его послеоперационных рецидивов включают любые из следующих стадий, как, например, хирургическое удаление раковых клеток, подавление роста злокачественных клеток, уменьшение или регрессия опухоли, индукция ремиссии и пресечения возникновения рака, регрессия опухоли и сокращение или подавление метастазов. Эффективное лечение и/или профилактика рака уменьшает смертность и улучшает прогноз для индивидуумов, имеющих рак, снижает уровни онкомаркеров в крови и облегчает обнаруживаемые симптомы, сопутствующие раку. Например, уменьшение или улучшение симптомов составляет эффективное лечение и/или профилактику, включающие 10%, 20%, 30% и более уменьшение или стабильное заболевание.
В контексте настоящего изобретения термин «антитело» относится к иммуноглобулинам и их фрагментам, которые специфически реагируют на указанный белок или пептид этого. Антитело может включать антитела человека, приматизированные антитела, химерные антитела, биспецифические антитела, гуманизированные антитела, антитела, соединенные с другими белками или радиоизотопными метками, и фрагменты антител. Кроме того, антитело в настоящем документе используется в широком смысле и, в частности, охватывает интактные моноклональные антитела, поликлональные антитела, поливалентные антитела (например, биспецифические антитела), образованные, по меньшей мере, из двух интактных антител, и фрагменты антител, при условии, что они проявляют необходимую биологическую активность. «Антитело» указывает на все классы (например, IgA, IgD, IgE, IgG и IgM).
Если иное не определено, все технические и научные термины, используемые в настоящем документе, имеют такой же смысл, как это обычно понимается любым специалистом в области, к которой настоящее изобретение относится.
II. Пептиды
Для демонстрации того, что пептиды, полученные из CDC45L, действуют в качестве антигена, распознаваемого ЦТЛ, пептиды, полученные из CDC45L (SEQ ID NO: 18), анализировали для определения того, представляют ли они собой антигенные эпитопы, рестриктированные по HLA-А24 или А2, которые являются часто встречающимися HLA-аллелями (Date Y et al., Tissue Antigens 47: 93-101, 1996; Kondo A et al., J Immunol 155: 4307-12, 1995; Kubo RT et al., J Immunol 152: 3913-24, 1994).
Кандидаты из HLA-А24-связывающихся пептидов, полученных из CDC45L, определяли по их аффинности связывания с HLA-А24. Следующие пептиды представляют собой пептиды-кандидаты для иммунотерапии:

Кроме того, после стимуляции Т-клеток in vitro дендритными клетками (DC), подвергнутыми импульсному взаимодействию с (нагруженными) этими пептидами, были успешно образованы ЦТЛ с использованием каждого из следующих пептидов:

Эти образованные ЦТЛ продемонстрировали сильную специфическую ЦТЛ-активность в отношении клеток-мишеней, подвергавшихся импульсному взаимодействию с соответствующими пептидами. Результаты в настоящем документе показывают, что CDC45L представляет собой антиген, распознаваемый ЦТЛ, и что проверенные пептиды являются эпитопными пептидами CDC45L, рестриктированными по HLA-А24.
Среди этих пептидов CDC45L-А24-9-556-4(SEQ ID NO: 4) был также определен в качестве HLA-A2-связывающего пептида-кандидата. Здесь, CDC45L-А24-556-4(SEQ ID NO: 4) также называется CDC45L-A2-9-556-4(SEQ ID NO: 4) в контексте HLA-A2-рестриктированных пептидов. С помощью этого пептида были успешно образованы ЦТЛ против клеток-мишеней, которые экспрессируют CDC45L и HLA-A2. Таким образом, CDC45L-A2-9-556-4(SEQ ID NO: 4) представляет собой не только эпитопный пептид, рестриктированный по HLA-А24, но также и эпитопный пептид, рестриктированный по HLA-А2.
Поскольку ген CDC45L сверхэкспрессируется в раковых клетках и тканях, включая, например, клетки и ткани опухоли яичка, рака поджелудочной железы, рака мочевого пузыря, немелкоклеточного рака легкого, мелкоклеточного рака легкого, рака молочной железы, рака пищевода, рака предстательной железы, хронического миелоидного лейкоза (ХМЛ), опухоли мягких тканей, рака желудка, гепатобилиарного рака и рака прямой кишки, и не экспрессируется в большинстве нормальных органов, он представляет собой хорошую мишень для иммунотерапии рака. Таким образом, настоящее изобретение предоставляет нонапептиды (пептиды, состоящие из девяти аминокислотных остатков) и декапептиды (пептиды, состоящие из десяти аминокислотных остатков), соответствующие ЦТЛ-распознаваемым эпитопам CDC45L. Альтернативно, настоящее изобретение предоставляет выделенные пептиды, которые связываются с HLA-антигенами и индуцируют цитотоксические Т-лимфоциты (ЦТЛ), где пептид имеет аминокислотную последовательности SEQ ID NO: 18 или является иммунологически активным фрагментом. Особенно предпочтительные примеры по настоящему изобретению включают те пептиды, которые имеют SEQ ID NO: 2, 3, 4, 7 и 12.
Как правило, программы системы программного обеспечения, доступные в настоящее время, например, в Интернете, такие как описано в Parker KC et al., J Immunol 1994 Jan 1, 152(1): 163-75 и Nielsen M et al., Protein Sci 2003; 12: 1007-17, могут быть использованы для расчета аффинностей связывания между различными пептидами и HLA-антигенами in silico. Аффинность связывания с HLA-антигенами можно определить, как описано, например, в Parker KC et al., J Immunol 1994 Jan 1, 152(1): 163-75, Kuzushima K et al., Blood 2001, 98(6): 1872-81, Larsen MV et al. BMC Bioinformatics. 2007 Oct 31; 8: 424, Buus S et al. Tissue Antigens., 62: 378-84, 2003, Nielsen M et al., Protein Sci 2003; 12: 1007-17, и Nielsen M et al. PLoS ONE 2007; 2: e796, которые кратко изложены, например, в Lafuente EM et al., Current Pharmaceutical Design, 2009, 15, 3209-3220. Способы определения аффинности связывания описаны, например, в Journal of Immunological Methods, 1995, 185: 181-190 and Protein Science, 2000, 9: 1838-1846. Поэтому с помощью таких программ системы программного обеспечения можно выбрать фрагменты, полученные из CDC45L, которые обладают высокой аффинностью связывания с HLA-антигенами. Таким образом, настоящее изобретение охватывает пептиды, состоящие из любых фрагментов, полученных их CDC45L, которые связываются с HLA-антигенами, в соответствии с такими известными программами. Кроме того, такие пептиды могут включать пептид, состоящий из полноразмерного CDC45L.
Нонапептиды и декапептиды по настоящему изобретению можно фланкировать дополнительными аминокислотными остатками, при условии, что полученный пептид сохраняет свою способность индуцировать ЦТЛ. Дополнительные аминокислотные остатки могут состоять из аминокислот любого вида, при условии, что они не ослабляют способность индуцировать ЦТЛ исходного пептида. Таким образом, настоящее изобретение охватывает пептиды с аффинностью связывания с HLA-антигенами, в том числе пептиды, полученные из CDC45L. Такие пептиды состоят, например, из менее чем примерно 40 аминокислот, часто менее чем примерно 20 аминокислот и, как правило, меньше, чем примерно 15 аминокислот.
В большинстве случаев модификация одной или нескольких аминокислот в пептиде не влияет на функции пептида, а в некоторых случаях даже усиливает нужную функцию исходного белка. В самом деле, известно, что модифицированные пептиды (т.е., пептиды, состоящие из последовательности аминокислот, в которых один, два или несколько аминокислотных остатков были модифицированы (т.е., заменены, добавлены, удалены и/или встроены), по сравнению с исходной контрольной последовательностью) сохраняют биологическую активность исходного пептида (Mark et al., Proc Natl Acad Sci USA 1984, 81: 5662-6; Zoller and Smith, Nucleic Acids Res 1982, 10: 6487-500; Dalbadie-McFarland et al., Proc Natl Acad Sci USA 1982, 79: 6409-13). Таким образом, в одном варианте осуществления пептиды по настоящему изобретению обладают как способностью индуцировать ЦТЛ, так и имеют аминокислотную последовательность, выбранную из SEQ ID NO: 2, 3, 4, 7 и 12, где одна, две или даже больше аминокислот добавлены, удалены и/или заменены.
Специалисты в рассматриваемой области должны признать, что отдельные добавления, удаления или замены в последовательности аминокислот, которые изменяют одну аминокислоту или небольшой процент аминокислот, имеют тенденцию к сохранению свойств боковой цепи исходной аминокислоты. Как таковые, они часто называются «консервативными заменами» или «консервативными модификациями», где изменение белка приводит к образованию модифицированного белка, имеющего функции, аналогичные функциям исходного белка. Таблицы консервативных замен, предоставляющие функционально сходные аминокислоты, хорошо известны в рассматриваемой области. Примеры особенностей боковых цепей аминокислот, которые предпочтительно являются консервативными, включают, например: гидрофобные аминокислоты (A, I, L, M, F, P, W, Y, V), гидрофильные аминокислоты (R, D, N, C, E, Q, G, H, K, S, T) и боковые цепи, имеющие следующие функциональные группы или общие характеристики: алифатическая боковая цепь (G, A, V, L, I, P); боковая цепь, содержащая гидроксильную группу (S, T, Y); боковая цепь, содержащая атом серы (C, M); боковая цепь, содержащая карбоновую кислоту и амид (D, N, E, Q); боковая цепь, содержащая основание (R, K, H); и боковая цепь, содержащая ароматическую группу (H, F, Y, W). Кроме того, каждая из следующих восьми групп содержит аминокислоты, которые в рассматриваемой области принимаются в качестве консервативных замен друг для друга:
1) Аланин (А), Глицин (G);
2) Аспарагиновая кислота (D), Глутаминовая кислота (E);
3) Аспарагин (N), Глутамин (Q);
4) Аргинин (R), Лизин (K);
5) Изолейцин (I), Лейцин (L), Метионин (M), Валин (V);
6) Фенилаланин (F), Тирозин (Y), Триптофан (W);
7) Серин (S), Треонин (T); и
8) Цистеин (C), Метионин (М) (см., например, Creighton, Proteins 1984).
Такие консервативно модифицированные пептиды рассматриваются также как пептиды по настоящему изобретению. При этом пептиды по настоящему изобретению не ограничиваются этим и могут включать неконсервативные модификации, при условии, что модифицированный пептид сохраняет способность индуцировать ЦТЛ исходного пептида. Более того, модифицированные пептиды не должны исключать ЦТЛ-индуцирующих пептидов полиморфных вариантов, межвидовых гомологов и аллелей CDC45L.
Чтобы сохранить необходимую способность индуцировать ЦТЛ, можно изменять (вставлять, удалять, добавлять и/или заменять) небольшое число (например, 1, 2 или несколько) или небольшой процент аминокислот. В настоящем документе термин «несколько» означает 5 или меньше аминокислот, например, 4, 3 или меньше. Доля аминокислот, подлежащих модифицированию, составляет предпочтительно 20% или меньше, более предпочтительно 15% или меньше, даже более предпочтительно 10% или меньше, или от 1% до 5%.
При использовании в контексте противораковой иммунотерапии, пептиды по настоящему изобретению должны быть представлены на поверхности клетки или экзосомы, предпочтительно в качестве комплекса с HLA-антигеном. Поэтому, предпочтительно выбирать пептиды, которые не только индуцируют ЦТЛ, но также обладают высокой аффинностью связывания HLA-антигенов. С этой целью пептиды можно модифицировать путем замены, вставки и/или добавления аминокислотных остатков, чтобы получить модифицированный пептид с увеличенной аффинностью связывания. В дополнение к пептидам, которые обнаруживаются в природе, поскольку закономерность последовательностей пептидов, обнаруживаемых путем связывания с HLA-антигенами, уже известна (J Immunol 1994, 152: 3913; Immunogenetics 1995, 41: 178; J Immunol 1994, 155: 4307), то модификации, основанные на такой закономерности, можно вводить в иммуногенные пептиды по настоящему изобретению.
Например, для увеличения HLA-А24-связывания может быть желательна замена второй с N-конца аминокислоты фенилаланином, тирозином, метионином или триптофаном, и/или аминокислоты на C-конце фенилаланином, лейцином, изолейцином, триптофаном или метионином. Таким образом, пептиды, имеющие аминокислотные последовательности, выбранные из группы, состоящей из SEQ ID NO: 2, 3, 4, 7 и 12, где вторая аминокислота с N-конца аминокислотной последовательности заменена фенилаланином, тирозином, метионином или триптофаном, и/или где C-конец заменен фенилаланином, лейцином, изолейцином, триптофаном или метионином, охватываются настоящим изобретением.
Кроме того, предпочтительной может быть замена второй с N-конца аминокислоты лейцином или метионин, и/или аминокислоты на C-конце валином или лейцином для увеличения аффинности связывания с HLA-A2. Таким образом, пептиды, имеющие аминокислотную последовательность, выбранную из SEQ ID NO: 4, где вторая с N-конца аминокислота заменена на лейцин или метионин, и/или где аминокислота на C-конце заменена на валин или лейцин, охватываются настоящим изобретением.
Замены можно вводить не только в концевые аминокислоты, но также в положение потенциального распознавания Т-клеточного рецептора (ТКР) пептидов. Несколько исследований продемонстрировали, что пептид с аминокислотными заменами может обладать такой же или улучшенной функцией по сравнению с исходным, например, CAP1, р53(264-272), her-2/neu(369-377) или gp100(209-217) (Zaremba et al. Cancer Res. 57, 4570-4577, 1997, T. K. Hoffmann et al. J Immunol. (2002) Feb 1; 168(3): 1338-47., S. O. Dionne et al. Cancer Immunol immunother. (2003) 52: 199-206 и S. O. Dionne et al. Cancer Immunology, Immunotherapy (2004) 53, 307-314).
Настоящее изобретение также предусматривает добавление одной, двух или нескольких аминокислот к N- и/или C-концу настоящих пептидов. Такие модифицированные пептиды, обладающие высокой аффинностью связывания с HLA-антигеном и сохраненной способностью индуцировать ЦТЛ, также включены в настоящее изобретение.
Однако в случае, когда пептидная последовательность идентична части аминокислотной последовательности эндогенного или экзогенного белка, имеющего отличные функции, могут индуцироваться такие побочные эффекты, как аутоиммунные расстройства и/или аллергические симптомы в отношении определенных веществ. Поэтому, предпочтительно сначала провести поиск гомологий с использованием имеющихся баз данных, чтобы избежать ситуации, в которой последовательности пептидов соответствует последовательности аминокислот другого белка. Когда из поиска гомологий становится ясно, что не существует пептид даже с различиями в 1 или 2 аминокислоты по сравнению с реальным пептидом, реальный пептид можно модифицировать в целях увеличения его аффинности связывания с HLA-антигенами и/или увеличения его способности индуцировать ЦТЛ без какого-либо риска таких побочных эффектов.
Несмотря на то, что ожидается, что пептиды, обладающие высокой аффинностью связывания с HLA-антигенами, как описано выше, будут высокоэффективными, пептиды-кандидаты, которые выбираются в зависимости от наличия в качестве индикатора высокой аффинности связывания, в дальнейшем проверяют на присутствие способности индуцировать ЦТЛ. В настоящем документе выражение «способность индуцировать ЦТЛ» указывает на способность пептида индуцировать ЦТЛ, в случае представленности на антигенпредставляющих клетках (АПК). Кроме того, «способность индуцировать ЦТЛ» включает способность пептида индуцировать активацию ЦТЛ, пролиферацию ЦТЛ, способствовать ЦТЛ-лизису клеток-мишеней и увеличивать продуцирование ЦТЛ гамма-интерферона.
Подтверждение способности индуцировать ЦТЛ достигается путем индуцирования АПК, несущих ГКГС-антигены человека (например, B-лимфоцитов, макрофагов и дендритных клеток (ДК)), или, более конкретно, ДК, полученных из мононуклеарных лейкоцитов периферической крови человека, и после стимуляции пептидами, смешивания с CD8-положительными клетками, а затем измерения гамма-интерферона, продуцированного и высвобожденного цитотоксическими Т-лимфоцитами против клеток-мишеней. В качестве реакционной системы можно использовать трансгенных животных, которые были выведены для экспрессии HLA-антигена человека (например, таких, которые описаны в BenMohamed L, Krishnan R, Longmate J, Auge C, Low L, Primus J, Diamond DJ, Hum Immunol 2000 Aug, 61(8): 764-79, родственные статьи, книги, Linkout Induction of CTL response by a minimal epitope vaccine in HLA A*0201/DR1 transgenic mice: dependent on MHC (HLA) class II restricted T(H) response). Например, клетки-мишени можно метить радиоактивным изотопом 51Cr и подобным, и цитотоксическую активность можно рассчитать по радиоактивности, высвобожденной из клетки-мишени. Альтернативно, способность индуцировать ЦТЛ можно оценивать путем определения гамма-интерферона, продуцированного и высвобожденного ЦТЛ в присутствии АПК, которые несут иммобилизованные пептиды, и визуализации зоны ингибирования на среде с помощью моноклональных антител против IFN-гамма.
В результате проверки способности пептидов индуцировать ЦТЛ, как описано выше, было обнаружено, что нонапептиды или декапептиды, выбранные из пептидов, состоящих из аминокислотных последовательностей, представленных в SEQ ID NO: 2, 3, 4, 7 и 12, демонстрировали чрезвычайно высокую способность индуцировать ЦТЛ, а также высокую аффинность связывания с HLA-антигеном. Таким образом, эти пептиды являются примером предпочтительного варианта осуществления настоящего изобретения.
Более того, результаты анализа гомологий показали, что эти пептиды не имеют значительной гомологии с пептидами, полученными от любых других известных генных продуктов человека. Соответственно, снижается возможность неизвестных или нежелательных иммунных реакций в случае применения для иммунотерапии. В силу вышесказанного и с данной точки зрения эти пептиды находят применение для вызывания иммунитета против CDC45L у больных раком. Таким образом, пептиды по настоящему изобретению, предпочтительно, пептиды, имеющие последовательность аминокислот, выбранную из группы, состоящей из SEQ ID NO: 2, 3, 4, 7 и 12,.
В дополнение к описанным выше модификациям пептиды по настоящему изобретению также могут быть соединены с другими пептидами, при условии, что образующийся соединенный пептид сохраняет необходимую способность индуцировать ЦТЛ исходного пептида. Примеры подходящих пептидов включают: пептиды по настоящему изобретению или ЦТЛ-индуцирующие пептиды, полученные из других ОСА. Подходящие межпептидные линкеры хорошо известны в рассматриваемой области и включают, например, AAY (P. M. Daftarian et al., J Trans Med 2007, 5: 26), AAA, NKRK (R. P. M. Sutmuller et al., J Immunol. 2000, 165: 7308-7315) или K (S. Ota et al., Can Res. 62, 1471-1476, K. S. Kawamura et al., J Immunol. 2002, 168: 5709-5715).
Например, пептиды отличных от CDC45L опухолеспецифических антигенов также можно в основном одновременно использовать для повышения иммунного ответа с помощью HLA класса I и/или класса II. Хорошо известно, что раковые клетки могут экспрессировать более одного опухолеспецифического гена. Таким образом, в рамках применения обычных экспериментов для любого специалиста в рассматриваемой области является определение того, экспрессирует ли конкретный субъект дополнительные опухолеспецифические гены, а затем включить HLA класса I- и/или HLA класса II-связывающиеся пептиды, полученные из продуктов экспрессии таких генов, в CDC45L-композиции или вакцины по настоящему изобретению.
Примеры HLA класса I- и HLA класса II-связывающих пептидов известны специалистам в рассматриваемой области (см., например, Coulie, Stem Cells 13: 393-403, 1995) и могут быть использованы в изобретении таким же образом, как раскрыто в настоящем документе. Таким образом, любой специалист в рассматриваемой области может легко подготовить полипептиды, включающие один или несколько CDC45L-пептидов и один или несколько из пептидов, отличных от CDC45L-пептидов, или нуклеиновых кислот, кодирующих такие полипептиды, используя стандартные методики молекулярной биологии.
Такие упомянутые выше соединенные пептиды называются в этом документе как «политопы», т.е. группы из двух или нескольких потенциально иммуногенных или стимулирующих иммунный ответ пептидов, которые могут быть соединены вместе в различных конфигурациях (например, сцепленных, перекрывающихся). Политоп (или нуклеиновую кислоту, кодирующую политоп) можно вводить в стандартный протокол иммунизации, например, животных, для проверки эффективности политопа в стимулировании, усилении и/или вызывании иммунной реакции.
Пептиды можно соединять вместе непосредственно или посредством использования фланкирующих последовательностей в виде политопов, а также использования политопов в качестве вакцин, как известно в рассматриваемой области (см., например, Thomson et al., Proc. Natl. Acad. Sci USA 92(13): 5845-5849, 1995; Gilbert et al., Nature Biotechnol. 15(12): 1280-1284, 1997; Thomson et al., J Immunol. 157(2): 822-826, 1996; Tarn et al., J Exp. Med. 171(l): 299-306, 1990). Политопы, содержащие различное число и различные комбинации эпитопов, можно подготовить и протестировать на распознавание ЦТЛ и на эффективность увеличения иммунного ответа.
Пептиды по настоящему изобретению также могут быть связаны с другими веществами, при условии, что образующийся связанный пептид сохраняет необходимую способность индуцировать ЦТЛ исходного пептида. Примеры подходящих веществ включают, например, белки, пептиды, липиды, сахара и цепи сахаров, ацетильные группы, природные и синтетические полимеры и др. Пептиды могут содержать модификации, такие как гликозилирование, окисление боковой цепи и/или фосфорилирование; при условии, что модификации не уничтожают биологическую активность исходного пептида. Такого рода модификации можно выполнять для предоставления дополнительных функций (например, функции мишени и функции доставки) и/или стабилизации полипептида.
Например, в рассматриваемой области известно, что для увеличения полипептидной стабильности in vivo встраиваются D-аминокислоты, миметики аминокислот или ненатуральные аминокислоты; эта концепция также может быть адаптирована для настоящих полипептидов. Стабильность полипептида можно определять рядом способов. Например, для проверки устойчивости могут быть использованы пептидазы и различные биологические среды, такие как плазма и сыворотка человека (см., например, Verhoef et al., Eur J Drug Metab Pharmacokin 1986, 11: 291-302).
Кроме того, как отмечалось выше, среди модифицированных пептидов, у которых заменены, удалены и/или добавлены один, два или несколько аминокислотных остатков, можно скринировать или отобрать такие, которые обладают такой же или более высокой активностью по сравнению с исходными пептидами. Вследствие этого настоящее изобретение также предоставляет способ скрининга или отбора модифицированных пептидов, обладающих такой же или более высокой активностью по сравнению с исходными. Иллюстративный способ может включать следующие стадии:
а: замена, удаление или добавление, по крайней мере, одного аминокислотного остатка у пептида по настоящему изобретению, и
b: определение активности пептида, полученного на стадии а,
c: отбор пептида, обладающего такой же или более высокой активностью по сравнению с исходным.
В настоящем документе активность, которую следует определить, может включать активность связывания с MHC, способность индуцировать АПК или ЦТЛ и цитотоксическую активность. Предпочтительно, активность, которую следует определить, представляет собой способность индуцировать ЦТЛ, и такую активность можно определять при помощи способов, описанных в разделе «ПРИМЕРЫ».
В настоящем документе пептиды по настоящему изобретению также могут описываться как «пептид(ы) CDC45L» или «полипептид(ы) CDC45L».
III. Подготовка пептидов CDC45L
Пептиды по настоящему изобретению можно подготовить с использованием известных способов. Например, пептиды можно подготовить синтетически, с помощью технологии рекомбинантных ДНК или химического синтеза. Пептиды по настоящему изобретению можно синтезировать по отдельности или в качестве больших полипептидов, состоящих из двух или нескольких пептидов. Затем пептиды можно выделить, т.е. очистить или отделить так, чтобы в существенной степени освободить от других природных белков клеток-хозяев и их фрагментов, или каких-либо других химических веществ.
Пептиды по настоящему изобретению могут содержать модификации, как, например, гликозилирование, окисление боковой цепи и фосфорилирование, при условии, что модификации не уничтожают биологической активности исходного пептида. Другие иллюстративные модификации включают встраивание D-аминокислот или других аминокислотных миметиков, которые можно использовать, например, для увеличения времени полужизни пептидов.
Пептид по настоящему изобретению можно получить путем химического синтеза на основе выбранной последовательности аминокислот. Примеры традиционных способов пептидного синтеза, которые можно применить для синтеза, включают:

Альтернативно, настоящие пептиды можно получить, применяя любые известные генно-инженерные способы для получения пептидов (например, Morrison J, J Bacteriology 1977, 132: 349-51; Clark-Curtiss & Curtiss, Methods in Enzymology (eds. Wu et al.) 1983, 101: 347-62). Например, во-первых, подготавливают подходящий вектор, несущий полинуклеотид, кодирующий реальный пептид в экспрессируемой форме (например, ниже регуляторной последовательности, соответствующей промоторной последовательности), и трансформируют соответствующую клетку-хозяин. Такие векторы и клетки-хозяева также представлены настоящим изобретением. Клетку-хозяин затем культивируют для продуцирования представляющего интерес пептида. Пептид также можно продуцировать in vitro, используя систему трансляции in vitro.
IV. Полинуклеотиды
Настоящее изобретение также предоставляет полинуклеотиды, которые кодируют любые из вышеупомянутых пептидов по настоящему изобретению. Они включают полинуклеотиды, полученные из гена CDC45L природного происхождения (номер GenBank Accession NM_003504 (SEQ ID NO: 17)), а также полинуклеотиды, имеющие консервативно их модифицированные нуклеотидные последовательности. В настоящем документе выражение «консервативно модифицированная нуклеотидная последовательность» относится к последовательностям, которые кодируют идентичные или в существенной степени идентичные аминокислотные последовательности. Из-за вырожденности генетического кода любой заданный белок кодирует большое количество функционально идентичных нуклеиновых кислот. Например, каждый из кодонов GCA, GCC, GCG и GCU кодирует аминокислоту аланин. Поэтому в каждом положении, где аланин точно определяется кодоном, кодон может быть заменен любым из соответствующих кодонов, записанных без изменения закодированного полипептида. Такие варианты нуклеиновых кислот представляют собой «молчащие варианты», которые являются одним из видов консервативно модифицированных вариантов. Каждая последовательность нуклеиновых кислот в настоящем документе, которая кодирует пептид, также описывает каждый возможный молчащий вариант нуклеиновой кислоты. Любой специалист в рассматриваемой области признает, что каждый кодон в нуклеиновой кислоте (за исключением AUG, который обычно является единственным кодоном для метионина, и TGG, который обычно является единственным кодоном для триптофана) можно модифицировать для получения функционально идентичной молекулы. Соответственно, каждый молчащий вариант нуклеиновой кислоты, которая кодирует пептид, в неявном виде описывается в каждой раскрытой последовательности.
Полинуклеотид по настоящему изобретению может состоять из ДНК, РНК и их производных. Как известно в рассматриваемой области, молекула ДНК состоит из оснований, таких как основания естественного происхождения A, T, C, и G, и T заменяется на U в РНК. Любой специалист признает, что основания, не встречающиеся в природе, равным образом включаются в полинуклеотиды.
Полинуклеотид по настоящему изобретению может кодировать несколько пептидов по настоящему изобретению с присутствием встраиваемых аминокислотных последовательностей или без таковых. Например, встраиваемая аминокислотная последовательность может обеспечивать участок расщепления (например, последовательность распознавания ферментом) полинуклеотида или транслированных пептидов. Более того, полинуклеотид может включать любые дополнительные последовательности для кодирующей последовательности, кодирующей пептид по настоящему изобретению. Например, полинуклеотид может представлять собой рекомбинантный полинуклеотид, который включает регуляторные последовательности, необходимые для экспрессии пептида, или может представлять собой экспрессионный вектор (плазмиду) с маркерными генами и т.д. В большинстве случаев такие рекомбинантные полинуклеотиды можно подготовить путем манипуляции с полинуклеотидами с помощью обычных рекомбинантных методик, используя, например, полимеразы и эндонуклеазы.
Для получения полинуклеотидов по настоящему изобретению можно применять способы как рекомбинантного, так и химического синтеза. Например, полинуклеотид можно продуцировать путем встраивания в соответствующий вектор, который может экспрессироваться при трансфекции в компетентные клетки. Альтернативно, полинуклеотид можно амплифицировать с помощью методик ПЦР или экспрессии в соответствующих хозяевах (см., например, Sambrook et al., Molecular Cloning: A Laboratory Manual, Cold Spring Harbor Laboratory, New York, 1989). Кроме того, полинуклеотид можно синтезировать с использованием твердофазных способов, как описано в Beaucage SL & Iyer RP, Tetrahedron 1992, 48: 2223-311; Matthes et al., EMBO J 1984, 3: 801-5.
V. Экзосомы
Настоящее изобретение дополнительно предоставляет внутриклеточные везикулы, называемые экзосомами, которые представляют комплексы, образуемые на их поверхности между пептидами по настоящему изобретению и HLA-антигенами. Экзосомы можно подготовить, например, с помощью способов, подробно изложенных в патентной заявке Японии Kohyo Publications NO. Hei 11-510507 и WO99/03499, и можно подготовить с использованием АПК, полученных от пациентов, которые являются субъектами лечения и/или профилактики. Экзосомы по настоящему изобретению можно прививать в качестве вакцины, подобно пептидам по настоящему изобретению.
Тип HLA-антигенов, содержащихся в комплексах, должен соответствовать таковому субъекта, нуждающегося в лечении и/или профилактике. Например, среди японского населения наиболее распространенными являются HLA-А24 и HLA-A2, в особенности HLA-A*-2402 и HLA-A*0201 и HLA-A*0206, и вследствие этого они были бы подходящими для лечения японского пациента. Использование типов А24 и А2, которые высоко экспрессируются среди японцев и европейцев, является благоприятным для получения эффективных результатов, и также находят применение подтипы, такие как А*2402, А*0201 и А*0206. Как правило, в клиниках заранее исследуют тип HLA-антигена пациента, нуждающегося в лечении, что дает возможность соответствующей селекции пептидов, обладающих высоким уровнем аффинности связывания с определенным антигеном или обладающих способностью индуцировать ЦТЛ путем представления антигена. Кроме того, в целях получения пептидов, обладающих как высокой аффинностью связывания, так и способностью индуцировать ЦТЛ, можно осуществлять замещение, удаление, встраивание и/или добавление 1, 2 или нескольких аминокислот на основе аминокислотной последовательности частичного пептида природного CDC45L.
При использовании HLA-антигена типа А24 для экзосомы по настоящему изобретению находят применение пептиды, имеющие последовательность любой из SEQ ID NO: 2, 3, 4, 7 и 12.
Альтернативно, при использовании HLA-антигена типа A2 для экзосомы по настоящему изобретению находит применение пептид, имеющий последовательность SEQ ID NO: 4.
VI. Антигенпредставляющие клетки (АПК)
Настоящее изобретение также предоставляет выделенные антигенпредставляющие клетки (АПК), которые представляют комплексы, образованные на их поверхности между HLA-антигенами и пептидами по настоящему изобретению. АПК можно получать от пациентов, которые являются субъектами лечения и/или профилактики, и можно вводить в качестве вакцины сами по себе или в комбинации с другими лекарственными средствами, включая пептиды по настоящему изобретению, экзосомы или ЦТЛ.
АПК не ограничиваются определенным видом клеток и включают дендритные клетки (DC), клетки Лангерганса, макрофаги, В-лимфоциты и активированные Т-клетки, которые, как известно, представляют белковоподобные антигены на своей клеточной поверхности так, чтобы они распознавались лимфоцитами. Поскольку ДК являются представляющими АПК, которые обладают самой сильной ЦТЛ-индуцирующей активностью среди АПК, ДК находят применение в качестве АПК по настоящему изобретению.
Например, АПК по настоящему изобретению можно получить путем индуцирования DC из моноцитов периферической крови и затем контактирования (стимулирования) их с пептидами по настоящему изобретению in vitro, ex vivo и in vivo. Когда пептиды по настоящему изобретению вводят субъектам, АПК, которые представляют пептиды по настоящему изобретению, индуцируются в организме субъекта. Выражение «индуцирование АПК» включает контактирование (стимулирование) клетки с пептидами по настоящему изобретению или нуклеотидами, кодирующими пептиды по настоящему изобретению, для представления комплексов, образующихся на клеточной поверхности между HLA-антигенами и пептидами по настоящему изобретению. Таким образом, АПК по настоящему изобретению можно получить путем сбора АПК от субъекта после введения пептидов по настоящему изобретению субъекту. Альтернативно, АПК по настоящему изобретению можно получить путем контактирования АПК, полученных от субъекта, с пептидом по настоящему изобретению.
АПК по настоящему изобретению можно вводить субъекту отдельно или в комбинации с другими лекарственными средствами, включая пептиды, экзосомы или ЦТЛ по настоящему изобретению, для индукции у субъекта иммунного ответа против рака. Например, введение ex vivo может включать следующие стадии:
а: сбор АПК от первого субъекта,
b: контактирование АПК со стадии а) с пептидом и
c: введение АПК со стадии b) второму субъекту.
Первый субъект и второй субъект могут являться одним и тем же индивидуумом, или это могут быть разные индивидуумы. АПК, полученные на стадии b, могут применяться в качестве вакцины для лечения и/или предупреждения рака, неограничивающие примеры которого включают опухоль яичка, рак поджелудочной железы, рак мочевого пузыря, немелкоклеточный рак легкого, мелкоклеточный рак легкого, рак молочной железы, рак пищевода, рак предстательной железы, хронический миелоидный лейкоз (ХМЛ), опухоль мягких тканей, рак желудка, гепатобилиарный рак и рак прямой кишки.
Настоящее изобретение представляет изготовление фармацевтической композиции, включающей такие антигенпредставляющие клетки, индуцированные пептидами по настоящему изобретению.
В соответствии с аспектом настоящего изобретения, АПК обладают высоким уровнем способности индуцировать ЦТЛ. В термине «высокий уровень способности индуцировать ЦТЛ» высокий уровень сравнивается с уровнем таковой для АПК, не контактирующей с пептидом или контактирующей с пептидами, которые не могут индуцировать ЦТЛ. Такие АПК, обладающие высоким уровнем способности индуцировать ЦТЛ, можно подготовить при помощи способа, который включает стадию передачи полинуклеотида, кодирующего пептид по настоящему изобретению, АПК в условиях in vitro, а также способов, упомянутых выше. Введенные гены могут быть в виде ДНК или РНК. Примеры способов введения включают, без особых ограничений, различные способы, традиционно осуществляемые в этой области, такие как липофекция, электропорация и кальцийфосфатный способ. А именно, их можно выполнить, как описано в Cancer Res 1996, 56: 5672-7; J Immunol 1998, 161: 5607-13; J Exp Med 1996, 184: 465-72; опубликованный японский перевод международных публикаций № 2000-509281. В результате переноса гена в АПК ген в клетке претерпевает транскрипцию, трансляцию и т.д., а затем полученный белок процессируется ГКГС Класса I или Класса II, и проходит через путь представления для представления частичных пептидов.
В предпочтительных вариантах осуществления АПК по настоящему изобретению могут представлять собой такие АПК, которые представляют комплексы, образованные на их поверхности между HLA-А24-антигеном, таким как HLA-A*2402, и пептидом по настоящему изобретению. Альтернативно, АПК по настоящему изобретению могут представлять комплексы, образованные на их поверхности между HLA-A2-антигеном, таким как HLA-A*0201, и пептидом с SEQ ID NO: 4 или модифицированным пептидом.
VII. Цитотоксические Т-лимфоциты (ЦТЛ)
ЦТЛ, индуцированный в отношении любого из пептидов по настоящему изобретению, усиливает иммунную реакцию в отношении раковых клеток in vivo и, поэтому, может быть использован в качестве вакцин, по виду похожих на пептиды как таковые. Таким образом, настоящее изобретение также предоставляет выделенные ЦТЛ, которые специфически индуцируются или активируются при помощи любого из настоящих пептидов.
Такие ЦТЛ можно получить путем (1) введения пептида(ов) по настоящему изобретению субъекту или (2) контактирования (стимулирования) полученных от субъекта АПК и CD8-положительных клеток, или мононуклеарных лейкоцитов периферической крови in vitro с пептидом(ами) по настоящему изобретению, или (3) контактирования CD8-положительных клеток или мононуклеарных лейкоцитов периферической крови in vitro с АПК или экзосомами, представляющими на своей поверхности комплекс HLA-антигенов и настоящего пептида, или (4) введения гена, включающего полинуклеотид, кодирующий субъединицу Т-клеточного рецептора (ТКР), способную связываться с пептидом по настоящему изобретению. Такие АПК и экзосомы можно подготовить с помощью способов, описанных выше, и подробности способа (4) подробно описаны ниже в разделе «VIII. Т-клеточный рецептор (ТКР)».
ЦТЛ по настоящему изобретению можно получать от пациентов, которые являются субъектами лечения и/или профилактики, и можно вводить сами по себе или в комбинации с другими лекарственными средствами, в том числе с пептидами по настоящему изобретению или экзосомами с целью регулирования воздействий. Полученные ЦТЛ действуют специфически в отношении клеток-мишеней, представляющих пептиды по настоящему изобретению, например, те же пептиды, что использовались для индукции. Клетки-мишени могут представлять собой клетки, которые эндогенно экспрессируют CDC45L, такие как раковые клетки или клетки, трансфицированные геном CDC45L; и клетки, которые представляют пептид по настоящему изобретению на поверхности клеток за счет стимуляции пептидом, также могут служить в качестве мишени для атаки активированных ЦТЛ.
VIII. Т-клеточный рецептор (ТКР)
Настоящее изобретение также предоставляет композицию, содержащую нуклеиновые кислоты, кодирующие полипептиды, которые способны образовывать субъединицы T-клеточного рецептора (ТКР), и способы ее применения. Субъединицы ТКР по настоящему изобретению обладают способностью образовывать ТКР, которые придают специфичность Т-клеткам в отношении опухолевых клеток, представляющих CDC45L. С помощью известных в данной области способов можно идентифицировать нуклеиновые кислоты альфа- и бета-цепей, которые составляют ТКР-субъединицы ЦТЛ, индуцированных одним или несколькими пептидами по настоящему изобретению (WO2007/032255 и Morgan et al., J Immunol, 171, 3288 (2003)). Например, способ ПЦР является предпочтительным для анализа нуклеотидных последовательностей, кодирующих ТКР-субъединицы. ПЦР-праймеры для анализа могут представлять собой, например, праймеры 5'-R (5'-gtctaccaggcattcgcttcat-3') в качестве праймеров с 5'-стороны (SEQ ID NO: 23) и праймеры 3-ТRа-С (5'-tcagctggaccacagccgcagcgt-3'), специфические для C-области альфа-цепи ТКР (SEQ ID NO: 24), праймеры 3-ТRb-C1 (5'-tcagaaatcctttctcttgac-3'), специфические для C1-области бета-цепи ТКР (SEQ ID NO: 25) или праймеры 3-TRbeta-C2 (5'- ctagcctctggaatcctttctctt-3'), специфические для C2-области бета-цепи ТКР (SEQ ID NO: 26), в качестве праймеров с 3'-стороны, но без ограничения. Производные ТКР могут с высокой авидностью связывать клетки-мишени, представляющие пептид CDC45L, и необязательно опосредовать эффективное уничтожение клеток-мишеней, представляющих пептид CDC45L, in vivo и in vitro.
Нуклеиновые кислоты, кодирующие субъединицы ТКР, могут быть включены в соответствующие векторы, например, ретровирусные векторы. Эти векторы хорошо известны в рассматриваемой области. Нуклеиновые кислоты или векторы, содержащие их, можно эффективно передавать в Т-клетки, например, в Т-клетки пациента. Предпочтительно, настоящее изобретение предоставляет готовую к использованию композицию, позволяющую быстро модифицировать собственные Т-клетки пациента (или таковые другого млекопитающего) для того, чтобы быстро и легко продуцировать модифицированные Т-клетки, имеющие превосходные свойства уничтожать раковые клетки.
Специфический ТКР представляет собой рецептор, способный специфически распознавать комплекс пептида по настоящему изобретению и молекулы HLA, придающий Т-клетке специфическую активность по отношению к клетке-мишени в случае, когда ТКР находится на поверхности Т-клетки. Специфическое распознавание вышеупомянутого комплекса можно подтвердить любыми известными способами, предпочтительные неограничивающие примеры которых включают анализ HLA-мультимерного окрашивания с использованием молекул HLA и пептидов по настоящему изобретению и анализ ELISPOT. Проведением анализа ELISPOT можно подтвердить, что T-клетка, трансдуцированная нуклеиновой кислотой, кодирующей субъединицы ТКР, распознает клетку, экспрессирующую молекулы HLA и CDC45L, и сигнал передается интрацеллюлярно. Также можно подтвердить, могут ли субъединицы ТКР, введенные в Т-клетку, придавать T-клеткам цитотоксическую активность при помощи известных в рассматриваемой области способов. Предпочтительные способы включают, например, анализ высвобождения хрома с использованием HLA-A2-положительных и CDC45L-сверхэкспрессирующих клеток в качестве клеток-мишеней.
Кроме того, настоящее изобретение представляет ЦТЛ, которые подготавливают путем передачи нуклеиновых кислот, кодирующих полипептиды ТКР-субъединиц, которые связываются с пептидом CDC45L, например, SEQ ID NO: 4 в контексте HLA-A2, а также с пептидами с SEQ ID NO: 2, 3, 4, 7 и 12 в контексте HLA-А24.
Трансдуцированные ЦТЛ способны направляться к раковым клеткам in vivo, и их можно наращивать при помощи известных способов культивирования in vitro (см., Kawakami et al., J Immunol., 142, 3452-3461 (1989)). ЦТЛ по настоящему изобретению можно применять для формирования иммуногенной композиции, полезной для лечения и/или предупреждения рака у пациента, нуждающегося в терапии или защите (см. WO2006/031221, содержание которого включено настоящим документом в качестве ссылки).
IX. Фармацевтические вещества или композиции
Поскольку экспрессия CDC45L специфически увеличена при раках, неограничивающие примеры которых включают опухоль яичка, рак поджелудочной железы, рак мочевого пузыря, немелкоклеточный рак легкого, мелкоклеточный рак легкого, рак молочной железы, рак пищевода, рак предстательной железы, хронический миелоидный лейкоз (ХМЛ), опухоль мягких тканей, рак желудка, гепатобилиарный рак и рак прямой кишки, по сравнению с нормальной тканью, пептиды по настоящему изобретению и полинуклеотиды, кодирующие такие пептиды, находят применение при лечении и/или профилактике рака, и/или предупреждения послеоперационных рецидивов этого. Таким образом, настоящее изобретение предоставляет фармацевтическое средство или композицию для лечения и/или предупреждения рака и/или для профилактики его послеоперационных рецидивов, такое фармацевтическое средство или композицию, которые включают, в качестве активного ингредиента, один или несколько из пептидов или полинуклеотидов по настоящему изобретению. Альтернативно, настоящие пептиды можно экспрессировать на поверхности любой из вышеупомянутых экзосом или клеток, таких как АПК, для применения в качестве фармацевтических средств или композиций. Кроме того, вышеупомянутые ЦТЛ, которые нацелены на любой из пептидов по настоящему изобретению, также может использовать в качестве активного ингредиента настоящих фармацевтических средств или композиций.
Фармацевтические вещества или композиции (т.е., «фармацевтические вещества») по настоящему изобретению также находят применение в качестве вакцин. В контексте настоящего изобретения выражение «вакцина» (также именуемая как «иммуногенная композиция») означает вещество, которое имеет функцию индуцирования противоопухолевого иммунитета после прививки животным.
Фармацевтические вещества или композиции по настоящему изобретению можно использовать для лечения и/или предупреждения онкологических заболеваний и/или профилактики их послеоперационных рецидивов у субъектов или пациентов, включая человека и любое другое млекопитающее, включая, в качестве неограничивающих примеров, мышь, крысу, морскую свинку, кролика, кошку, собаку, овцу, козу, свинью, крупный рогатый скот, лошадь, обезьяну, бабуина и шимпанзе, в частности, коммерчески важных животных или домашних животных.
В другом варианте осуществления настоящее изобретение также предоставляет применение активного ингредиента, выбранного из:
(a) пептида по настоящему изобретению;
(b) нуклеиновой кислоты, кодирующей такой пептид, как раскрыто в настоящем документе, в экспрессируемой форме;
(c) АПК или экзосомы, представляющей пептид по настоящему изобретению на своей поверхности; и
(d) цитотоксической Т-клетки по настоящему изобретению
в изготовлении фармацевтической композиции или вещества для лечения и/или предупреждения рака или опухоли.
Альтернативно, настоящее изобретение дополнительно предоставляет активный ингредиент, выбранный из:
(a) пептида по настоящему изобретению;
((b) нуклеиновой кислоты, кодирующей такой пептид, как раскрыто в настоящем документе, в экспрессируемой форме;
(c) АПК или экзосомы, представляющей пептид по настоящему изобретению на своей поверхности; и
(d) цитотоксической Т-клетки по настоящему изобретению
для применения при лечении и/или предупреждении рака или опухоли.
Альтернативно, настоящее изобретение дополнительно предоставляет способ или процесс изготовления фармацевтической композиции или вещества для лечения и/или предупреждения рака или опухоли, где способ или процесс включает стадию составления рецептуры фармацевтически или физиологически приемлемого носителя с активным ингредиентом, выбранным из:
(a) пептида по настоящему изобретению;
((b) нуклеиновой кислоты, кодирующей такой пептид, как раскрыто в настоящем документе, в экспрессируемой форме;
(c) APC или экзосомы, представляющей пептид по настоящему изобретению на своей поверхности; и
(d) цитотоксической Т-клетки по настоящему изобретению
в качестве активных ингредиентов.
В другом варианте осуществления, настоящее изобретение также предоставляет способ или процесс изготовления фармацевтической композиции или вещества для лечения и/или предупреждения рака или опухоли, где способ или процесс включает стадии смешивания активного ингредиента с фармацевтически или физиологически приемлемым носителем, где активный ингредиент выбирают из:
(a) пептида по настоящему изобретению;
((b) нуклеиновой кислоты, кодирующей такой пептид, как раскрыто в настоящем документе, в экспрессируемой форме;
(c) APC или экзосомы, представляющей пептид по настоящему изобретению на своей поверхности; и
(d) цитотоксической Т-клетки по настоящему изобретению.
В соответствии с настоящим изобретением, оказалось, что пептиды, обладающие любой аминокислотной последовательностью из SEQ ID NO: 2, 3, 4, 7 и 12, представляют собой HLA-А24-рестриктированные эпитопные пептиды или пептиды-кандидаты, которые могут индуцировать сильный и специфический иммунный ответ. Вследствие этого настоящие фармацевтические вещества или композиции, которые включают любые из этих пептидов, обладающих аминокислотными последовательностями SEQ ID NO: 2, 3, 4, 7 и 12, особенно подходят для введения субъектам, чей HLA-антиген представляет собой HLA-А24. Было также обнаружено, что пептид, имеющий аминокислотную последовательность SEQ ID NO: 4, представляет собой HLA-A2-рестриктированный эпитопный пептид. Таким образом, фармацевтические вещества и композиции, которые включают пептид с аминокислотной последовательности SEQ ID NO: 4, также подходят для введения субъектам, чей HLA-антиген представляет собой HLA-A2, в дополнение к субъектам, чей HLA-антиген представляет собой HLA-А24. То же относится и к фармацевтическим веществам или композициям, которые содержат полинуклеотиды, кодирующие любой из этих пептидов (т.е., полинуклеотиды по настоящему изобретению).
Онкологические заболевания, подвергаемые лечению фармацевтическими веществами или композициями по настоящему изобретению, не ограничены и включают любой рак, в котором задействован CDC45L (например, сверхэкспрессирован), в том числе, например, опухоль яичка, рак поджелудочной железы, рак мочевого пузыря, немелкоклеточный рак легкого, мелкоклеточный рак легкого, рак молочной железы, рак пищевода, рак предстательной железы, хронический миелоидный лейкоз (ХМЛ), опухоль мягких тканей, рак желудка, гепатобилиарный рак и рак прямой кишки.
Настоящие фармацевтические вещества и композиции могут содержать, в дополнение к вышеупомянутым активным ингредиентам, другие пептиды, которые имеют способность индуцировать ЦТЛ в отношении злокачественных клеток, другие полинуклеотиды, кодирующие другие пептиды, другие клетки, которые представляют другие пептиды, или подобное. В настоящем документе другие пептиды, которые обладают способностью индуцировать ЦТЛ в отношении злокачественных клеток, иллюстрируются раковыми специфическими антигенами (например, идентифицированными ОСА), но не ограничиваются этим.
Если необходимо, фармацевтические вещества или композиции по настоящему изобретению могут дополнительно включать другие терапевтические вещества в качестве активного ингредиента, при условии, что вещество не ингибирует противоопухолевый эффект активного ингредиента, например, любого из настоящих пептидов. Например, составы могут включать противовоспалительные вещества, обезболивающие, вещества для химиотерапии и подобное. Дополнительно к включению других терапевтических веществ в лекарственный препарат как таковой, лекарственные препараты по настоящему изобретению можно также применять последовательно или одновременно с одним или несколькими другими фармакологическими веществами или композициями. Количества лекарственного препарата и фармакологического вещества зависят, например, от типа применяемого фармакологического вещества(в) или композиции(ий), подлежащего лечению заболевания и графика и способов введения.
Следует понимать, что в дополнение к ингредиентам, подробно упомянутым здесь, фармацевтические вещества или композиции по настоящему изобретению могут включать и другие вещества или композиции, общепринятые в данной области, с учетом типа рассматриваемого состава.
В одном варианте осуществления настоящего изобретения, настоящие фармацевтические вещества или композиции могут быть включены в готовые изделия и наборы, содержащие материалы, полезные для лечения патологических состояний подлежащего лечению заболевания, например, рака. Готовое изделие может включать контейнер любого из настоящих фармацевтических веществ или композиций с этикеткой. Соответствующие контейнеры включают бутылки, флаконы и пробирки. Контейнеры могут быть образованы из различных материалов, таких как стекло или пластик. Надпись на контейнере должна указывать, что композиция применяется для лечения или предупреждения одного или нескольких состояний заболевания. Этикетки могут также содержать предписание по введению и так далее.
В дополнение к контейнеру, описанному выше, набор, включающий фармацевтическое вещество или композицию по настоящему изобретению, может также необязательно включать второй контейнер, размещающий фармацевтически приемлемый разбавитель. Он может дополнительно включать другие материалы, желательные с коммерческой точки зрения и с точки зрения пользователя, включая другие буферы, разбавители, фильтры, иглы, шприцы и вкладыши с инструкцией по применению.
Фармацевтические композиции, при желании, представляются в упаковке или дозаторном устройстве, которое может содержать одну или несколько единичных лекарственных форм, содержащих активный ингредиент. Упаковка может, например, включать металлическую или пластиковую фольгу, такую как блистерная упаковка. Упаковка или дозаторное устройство может сопровождаться инструкциями для введения.
(1) Фармацевтические вещества или композиции, содержащие пептиды в качестве активного ингредиента
Пептиды по настоящему изобретению можно вводить непосредственно в качестве фармацевтического вещества или композиции, или, при необходимости, чтобы они были составлены при помощи общепринятых способов подбора составов. В последнем случае, в дополнение к пептидам по настоящему изобретению, носители, наполнители и подобное, которые обычно используются для лекарственных средств, могут быть включены как соответствующие без особых ограничений. Примерами таких носителей являются стерилизованная вода, физиологический раствор, фосфатный буфер, культуральная жидкость и подобное. Более того, фармацевтические вещества или композиции могут при необходимости содержать стабилизаторы, суспензии, консерванты, сурфактанты и подобное. Фармацевтические вещества или композиции по настоящему изобретению можно применять для противоопухолевых назначений.
Для индуцирования ЦТЛ in vivo пептиды по настоящему изобретению можно подготовить в виде комбинации, состоящей из двух или нескольких пептидов по настоящему изобретению. Пептидная комбинация может быть в виде смеси или может соединяться друг с другом с помощью стандартных методик. Например, пептиды могут быть химически связаны или экспрессироваться в качестве единой слитой полипептидной последовательности, которая может иметь одну или несколько аминокислот в качестве линкера (например, лизиновый линкер: K. S. Kawamura et al. J. Immunol. 2002, 168: 5709-5715). Пептиды в комбинации могут быть одинаковыми или различными. При введении пептидов по настоящему изобретению пептиды с высокой плотностью представляются при помощи HLA-антигенов на АПК, затем индуцируются ЦТЛ, которые специфически реагируют на комплекс, образовавшийся между представленным пептидом и HLA-антигеном. Альтернативно, у субъектов отбирают АПК (например, ДК), а затем стимулируют пептидами по настоящему изобретению для получения АПК, которые представляют любой из пептидов по настоящему изобретению на своей клеточной поверхности. Эти АПК повторно вводят субъектам для индуцирования ЦТЛ у субъектов, и, как следствие, агрессивность по отношению к опухолеспецифическому эндотелию может увеличиться.
Фармацевтические вещества или композиции для лечения и/или предупреждения рака, которые содержат пептид по настоящему изобретению в качестве активного ингредиента, также могут включать адъювант для, как известно, эффективного индуцирования клеточного иммунитета. Альтернативно, фармацевтические вещества или композицию можно вводить с другими активными ингредиентами или вводить при помощи составов в гранулах. Адъювантом называется любое соединение, вещество или композиция, которое усиливает иммунный ответ в отношении белка при введении одновременно (или последовательно) с белком, обладающим иммунологической активностью. Адъюванты, рассматриваемые здесь, включают такие, которые описаны в литературе (Clin Microbiol Rev 1994, 7: 277-89). Неограничивающие примеры подходящих адъювантов включают фосфат алюминия, гидроокись алюминия, квасцы, холерный токсин, токсин сальмонеллы, неполный адъювант Фрейнда (IFA), полный адъювант Фрейнда (CFA), ISCOMatrix, GM-CSF, CpG, эмульсию масло-в-воде и подобные, но не ограничиваются этим.
Более того, можно удобно использовать липосомные составы, гранулированные составы, в которых пептид связывается с бусинами диаметром несколько микрометров, и составы, в которых липид связывается с пептидом.
В другом варианте осуществления настоящего изобретения, пептиды по настоящему изобретению можно также вводить в виде фармацевтически приемлемой соли. Предпочтительные примеры солей включают соли щелочных металлов, соли металлов, соли на органической основе, соли органических кислот и соли неорганических кислот.
В некоторых вариантах осуществления фармацевтические вещества или композиции по настоящему изобретению могут дополнительно включать компонент, который праймирует ЦТЛ. Липиды были определены в качестве веществ, способных праймировать ЦТЛ in vivo в отношении вирусных антигенов. Например, остатки пальмитиновой кислоты можно присоединять к эпсилон- и альфа- аминогруппе остатка лизина, а затем присоединять к пептиду по настоящему изобретению. Липидированный пептид затем можно либо вводить непосредственно в мицеллу или частицу, включенную в липосому, либо эмульгировать в адъюванте. В качестве другого примера липидного праймирования ЦТЛ-ответов, можно использовать липопротеины E. coli, такие как, например, трипальмитоил-S-глицерилцистеинил-серил-серин (P3CSS), для праймирования ЦТЛ в случае ковалентного присоединения к соответствующему пептиду (см., например, Deres et al., Nature 1989, 342: 561-4).
Способ введения может быть пероральным, внутрикожным, подкожным, при помощи внутривенной инъекции или подобным, и системным введением или местным введением поблизости от участков-мишеней. Введение можно осуществлять посредством единичного введения или поддерживать с помощью нескольких введений. Дозу пептидов по настоящему изобретению можно соответствующим образом корректировать в зависимости от подлежащего лечению заболевания, возраста пациента, массы, способа введения и подобного, и она обычно составляет от 0,001 мг до 1000 мг, например, от 0,001 мг до 1000 мг, например, от 0,1 мг до 10 мг, и может вводиться от одного раза в несколько дней до одного раза в несколько месяцев. Любой специалист в рассматриваемой области может соответствующим образом подобрать подходящую дозу.
(2) Фармацевтические вещества или композиции, содержащие полинуклеотиды в качестве активного ингредиента
Фармацевтические вещества или композиции по настоящему изобретению также могут содержать нуклеиновые кислоты, кодирующие описанные в настоящем документе пептиды в экспрессируемой форме. В настоящем документе выражение «в экспрессируемой форме» означает, что полинуклеотид в случае введения в клетку будет экспрессироваться in vivo в качестве полипептида, который индуцирует противоопухолевый иммунитет. В типичном варианте осуществления последовательности нуклеиновых кислот представляющего интерес полинуклеотида включают регуляторные элементы, необходимые для экспрессии полинуклеотида. Полинуклеотид(ы) можно приспособить таким образом, чтобы получить стабильную вставку в геном клетки-мишени (см., например, Thomas KR & Capecchi MR, Cell 1987, 51: 503-12 для описания векторов с кассетами для гомологичной рекомбинации. См. также, например, Wolff et al., Science 1990, 247: 1465-8; патенты США №№ 5580859; 5589466; 5804566; 5739118; 5736524; 5679647 и WO 98/04720). Примеры технологий доставки на основе ДНК включают «голую ДНК», облегченную (бупивакаин, полимеры, пептид-опосредованная) доставку, катионные липидные комплексы, и опосредованную частицами («генной пушки») или опосредованную давлением доставку (см., например, патент США № 5922687).
Пептиды по настоящему изобретению можно также экспрессировать при помощи вирусных или бактериальных векторов. Примеры экспрессионных векторов включают ослабленных вирусных хозяев, таких как вакцинный вирус или вирус чумы птиц. Этот подход предполагает использование вакцинного вируса, например, в качестве вектора для экспрессии нуклеотидных последовательностей, кодирующих пептид. После введения в хозяина рекомбинантный вакцинный вирус экспрессирует иммуногенный пептид, и, посредством этого, вызывает иммунный ответ. Вакцинные векторы и способы пригодны для протоколов иммунизации, как описано, например, в патенте США № 4722848. Другим вектором является БЦЖ (бацилла Кальметта-Герена). Векторы БЦЖ описаны в Stover et al., Nature 1991, 351: 456-60. Наблюдается широкое разнообразие других векторов, пригодных для терапевтического введения или иммунизации, например, аденовирусные и связанные с аденовирусными векторы, ретровирусные векторы, векторы Salmonella typhi, векторы на основе обезвреженного токсина сибирской язвы и подобные. См., например, Shata et al., Mol Med Today 2000, 6: 66-71; Shedlock et al., J Leukoc Biol 2000, 68: 793-806; Hipp et al., In Vivo 2000, 14: 571-85.
Доставка полинуклеотида в организме субъекта может являться либо непосредственной, и в этом случае субъект непосредственно подвергается действию вектора, несущего полинуклеотид, или опосредованной, в случае чего клетки сначала трансформируют in vitro представляющим интерес полинуклеотидом, а затем клетки трансплантируют субъекту. Эти два подхода известны, соответственно, как генные терапии in vivo и ex vivo.
Для общего обзора способов генной терапии см. Goldspiel et al., Clinical Pharmacy 1993, 12: 488-505; Wu and Wu, Biotherapy 1991, 3: 87-95; Tolstoshev, Ann Rev Pharmacol Toxicol 1993, 33: 573-96; Mulligan, Science 1993, 260: 926-32; Morgan & Anderson, Ann Rev Biochem 1993, 62: 191-217; Trends in Biotechnology 1993, 11(5): 155-215). Способы, широко известные в области технологии рекомбинантной ДНК, также могут быть использованы для настоящего изобретения. См., например, Ausubel et al., Current Protocols in Molecular Biology, John Wiley & Sons, NY, 1993; и Krieger, Gene Transfer и Expression, A Laboratory Manual, Stockton Press, NY, 1990.
Способ введения может быть пероральным, внутрикожным, подкожным, при помощи внутривенной инъекцией или подобным, и системным введением или местным введением поблизости от участков-мишеней. Введение можно осуществлять посредством единичного введения или поддерживать с помощью нескольких введений. Дозу пептидов по настоящему изобретению можно соответствующим образом корректировать в зависимости от подлежащего лечению заболевания, возраста пациента, массы, способа введения и подобного, и она обычно составляет от 0,001 мг до 1000 мг, например, от 0,001 мг до 1000 мг, например, от 0,1 мг до 10 мг, и может вводиться от одного раза в несколько дней до одного раза в несколько месяцев. Любой специалист в рассматриваемой области может соответствующим образом подобрать подходящую дозу.
X. Способы применения пептидов, экзосом, АПК и ЦТЛ
Пептиды и полинуклеотиды по настоящему изобретению можно использовать для индуцирования АПК и ЦТЛ. Экзосомы и АПК по настоящему изобретению также можно использовать для индуцирования ЦТЛ. Пептиды, полинуклеотиды, экзосомы и АПК можно использовать в комбинации с любыми другими соединениями, при условии, что соединения не ингибируют их способность индуцирования ЦТЛ. Таким образом, любое из вышеупомянутых фармацевтических веществ или композиций по настоящему изобретению можно применять для индуцирования ЦТЛ, и дополнительно к этому, те, которые включают пептиды и полинуклеотиды, можно также применять для индуцирования АПК, как обсуждается и описывается ниже.
(1) Способ индуцирования антигенпредставляющих клеток (АПК)
Настоящее изобретение предоставляет способы индуцирования АПК с высокой способностью индуцировать ЦТЛ при помощи пептидов или полинуклеотидов по настоящему изобретению. Способы по настоящему изобретению включают стадию контактирования АПК с пептидами по настоящему изобретению in vitro, ex vivo и in vivo. Например, способ контактирования АПК с пептидами ex vivo может включать следующие стадии:
a: сбор АПК от субъекта, и
b: контактирование АПК со стадии а) с пептидом.
АПК не ограничиваются определенным видом клеток и включают ДК, клетки Лангерганса, макрофаги, В-клетки и активированные Т-клетки, которые, как известно, представляют белковоподобные антигены на своей клеточной поверхности так, чтобы они распознавались лимфоцитами. ДК могут предпочтительно использоваться из-за их самой сильной среди АПК способности индуцировать ЦТЛ. Любые пептиды по настоящему изобретению можно использовать сами по себе или в комбинации с другими пептидами по настоящему изобретению.
С другой стороны, когда пептиды по настоящему изобретению вводятся субъекту, АПК контактируют с пептидами in vivo, вследствие этого в организме субъекта возникают АПК с высокой способностью индуцировать ЦТЛ. Таким образом, в настоящее изобретение включает введение субъекту пептидов по настоящему изобретению. Аналогичным образом, когда полинуклеотиды по настоящему изобретению в экспрессируемой форме вводят субъекту, пептиды по настоящему изобретению экспрессируются и контактируют с АПК in vivo, вследствие этого в организме субъекта возникают АПК с высокой способностью индуцировать ЦТЛ. Таким образом, настоящее изобретение также может включать введение субъекту полинуклеотидов по настоящему изобретению. Выражение «экспрессируемая форма» определено выше в разделе «IX. Фармацевтические вещества или композиции,(2) Фармацевтические вещества или композиции, содержащие полинуклеотиды в качестве активного ингредиента».
Настоящее изобретение также может включать стадию введения полинуклеотида по настоящему изобретению в АПК, чтобы индуцировать АПК со способностью индуцировать ЦТЛ. Наглядный пример такого способа может включать следующие стадии:
а: сбор АПК от субъекта, и
b: введение полинуклеотида, кодирующего пептид по настоящему изобретению.
Стадию b можно выполнять, как описано выше в разделе «VI. Антигенпредставляющие клетки».
Альтернативно, настоящее изобретение предоставляет способ подготовки антигенпредставляющей клетки (АПК), которая специфически индуцирует активность ЦТЛ в отношении CDC45L, где способ включает одну из следующих стадий:
(a) контактирование АПК с пептидом по настоящему изобретению in vitro, ex vivo или in vivo; и
(b) введение полинуклеотида, кодирующего пептид по настоящему изобретению, в АПК.
(2) Способ индуцирования ЦТЛ
Более того, настоящее изобретение предоставляет способы индуцирования ЦТЛ с помощью пептидов, полинуклеотидов, экзосом или АПК по настоящему изобретению.
Настоящее изобретение также предоставляет способы индуцирования ЦТЛ с помощью полинуклеотида, кодирующего полипептид, который способен образовывать субъединицу Т-клеточного рецептора (ТКР), распознающую комплекс пептидов по настоящему изобретению и HLA-антигенов. Предпочтительно, способы индуцирования ЦТЛ включают, по крайней мере, одну стадию, выбранную из группы, состоящей из следующего:
а) контактирование CD8-положительных Т-клеток с антигенпредставляющей клеткой и/или экзосомой, которая представляет на своей поверхности комплекс HLA-антигена и пептида по настоящему изобретению; и
b) введение полинуклеотида, кодирующего полипептид, который способен образовывать ТКР-субъединицу, распознающую комплекс пептида по настоящему изобретению и HLA-антигена в CD8-положительных клетках.
В случае, когда пептиды, полинуклеотиды, АПК или экзосомы по настоящему изобретению вводят субъекту, в организме субъекта индуцируются ЦТЛ, и возрастает сила иммунного ответа, нацеленного на раковые клетки. Таким образом, способы по настоящему изобретению включают стадию введения субъекту пептидов, полинуклеотидов, АПК или экзосом по настоящему изобретению.
Альтернативно, можно также индуцировать ЦТЛ путем их использования ex vivo или in vitro, и после индуцирования ЦТЛ активированные ЦТЛ можно возвратить субъекту. Например, способ может включать следующие стадии:
а) сбор АПК от субъекта;
б) контактирование АПК со стадии а) с пептидом; и
c) совместное культивирование АПК со стадии b) с CD8-положительными клетками.
АПК, совместно культивируемые с CD8-положительными клетками в вышеприведенной стадии c, также можно подготовить путем передачи гена, который включает полинуклеотид по настоящему изобретению, в АПК, как описано выше в разделе «VI. Антигенпредставляющие клетки», хотя настоящее изобретение не ограничивается этим и, следовательно, может включать любые АПК, которые эффективно представляют на своей поверхности комплекс HLA-антигена и пептида по настоящему изобретению.
Вместо таких АПК можно также использовать экзосомы, которые представляют на своей поверхности комплекс HLA-антигена и пептида по настоящему изобретению. А именно, настоящее изобретение может включать стадию совместного культивирования экзосом, представляющих на своей поверхности комплекс HLA-антигена и пептида по настоящему изобретению. Такие экзосомы можно подготовить при помощи способов, описанных выше в разделе «V. Экзосомы».
Более того, ЦТЛ можно индуцировать введением гена, который включает полинуклеотид, кодирующий субъединицу ТКР, связывающуюся с пептидом по настоящему изобретению в CD8-положительных клетках. Такую передачу можно осуществлять, как описано выше в разделе «VIII. Т-клеточный рецептор (ТКР)».
Кроме того, настоящее изобретение предоставляет способ или процесс изготовления фармацевтического вещества или композиции, индуцирующей ЦТЛ, где способ включает стадию смешивания или составления рецептуры пептида по настоящему изобретению с фармацевтически приемлемым носителем.
(3) Способ индукцирования иммунного ответа
Более того, настоящее изобретение предоставляет способы индукцирования иммунного ответа в отношении заболеваний, связанных с CDC45L. Подходящие заболевания включают рак, неограничивающие примеры которого включают опухоль яичка, рак поджелудочной железы, рак мочевого пузыря, немелкоклеточный рак легкого, мелкоклеточный рак легкого, рак молочной железы, рак пищевода, рак предстательной железы, хронический миелоидный лейкоз (ХМЛ), опухоль мягких тканей, рак желудка, гепатобилиарный рак и рак прямой кишки.
Способы по настоящему изобретению могут включать стадию введения вещества(в) или композиции(й), содержащих любой из пептидов по настоящему изобретению или полинуклеотидов, кодирующих их. Способы по изобретению также предусматривают введение экзосом или АПК, представляющих любой из пептидов по настоящему изобретению. Более подробно см. в разделе «IX. Фармацевтические вещества или композиции», особенно в части, описывающей применение фармацевтических веществ или композиций по настоящему изобретению в качестве вакцин. Кроме того, экзосомы и АПК, которые можно использовать в настоящих способах для индуцирования иммунного ответа, подробно описаны в пунктах разделов «V. Экзосомы», «VI. Антигенпредставляющие клетки (АПК)» и (1) и (2) раздела «X. Способы применения пептидов, экзосом, АПК и ЦТЛ», см. выше.
Настоящее изобретение также предоставляет способ или процесс изготовления фармацевтического вещества или композиции, индуцирующей иммунный ответ, где способ включает стадию смешивания или составления рецептуры пептида по настоящему изобретению с фармацевтически приемлемым носителем.
Альтернативно, способ по настоящему изобретению может включать стадию введения вакцины или фармацевтического вещества или композиции, которая содержит:
(a) пептид по настоящему изобретению;
(b) нуклеиновую кислоту, кодирующую такой пептид, как раскрыто здесь, в экспрессируемой форме;
(c) APC или экзосому, представляющую пептид по настоящему изобретению на своей поверхности; или
(d) цитотоксическую Т-клетку по настоящему изобретению.
В контексте настоящего изобретения рак, сверхэкспрессирующий CDC45L, можно лечить с помощью этих активных ингредиентов. Неограничивающие примеры таких раков включают опухоль яичка, рак поджелудочной железы, рак мочевого пузыря, немелкоклеточный рак легкого, мелкоклеточный рак легкого, рак молочной железы, рак пищевода, рак предстательной железы, хронический миелоидный лейкоз (ХМЛ), опухоль мягких тканей, рак желудка, гепатобилиарный рак и рак прямой кишки. Соответственно, перед введением вакцин или фармацевтических веществ или композиций, содержащих активные ингредиенты, желательно убедиться в том, увеличен ли уровень экспрессии CDC45L в подлежащих лечению клетках или тканях по сравнению с нормальными клетками того же органа. Таким образом, в одном варианте осуществления настоящее изобретение предоставляет способ лечения рака, (сверх)экспрессирующего CDC45L, который может включать следующие стадии:
i) определение уровня экспрессии CDC45L в клетках или ткани(ях), полученных от субъекта с подлежащим лечению раком;
ii) сравнение уровня экспрессии CDC45L с уровнем нормального контроля; и
iii) введение, по крайней мере, одного компонента, выбранного из группы, состоящей из (a)-(d), описанной выше, субъекту с раком, сверхэкспрессирующим CDC45L по сравнению с нормальным контролем.
Альтернативно, настоящее изобретение может предоставлять вакцину или фармацевтическое вещество или композицию, которая содержит, по крайней мере, один компонент, выбранный из группы, состоящей из (a)-(d), описанной выше, для применения при введении субъекту с раком, сверхэкспрессирующим CDC45L. Иными словами, настоящее изобретение дополнительно предоставляет способ идентификации субъекта, подлежащего лечению полипептидом CDC45L по настоящему изобретению, включающий стадию определения уровня экспрессии CDC45L в полученных от субъекта клетках или ткани(ях), где увеличение уровня по сравнению с нормальным контрольным уровнем гена указывает на то, что субъект может иметь рак, который можно лечить полипептидом CDC45L по настоящему изобретению. Способ лечения рака по настоящему изобретению будет описан более подробно ниже.
Любая полученная от субъекта клетка или ткань может быть использована для определения экспрессии CDC45L, при условии, что она содержит реальный продукт транскрипции или трансляции CDC45L. Неограничивающие примеры подходящих образцов включают ткани и жидкости организма, такие как кровь, слюна и моча. Предпочтительно, чтобы полученный от субъекта клеточный или тканевый образец содержал популяцию клеток, включающую эпителиальные клетки, более предпочтительно злокачественные эпителиальные клетки или эпителиальные клетки, полученные из тканей с подозрением на злокачественность. Далее, если необходимо, клетка может быть очищена от полученных тканей и жидкостей организма, а затем использована в качестве образца, полученного от субъекта.
В контексте настоящего изобретения, контрольный уровень, определенный для биологического образца, о котором известно, что он не является злокачественным, называется «нормальный контрольный уровень». С другой стороны, если контрольный уровень определяется для злокачественного биологического образца, его называют «злокачественным контрольным уровнем». Различие между уровнем экспрессии для образца и контрольным уровнем можно нормировать на уровень экспрессии контрольных нуклеиновых кислот, например, генов «домашнего хозяйства», для которых известно, что их уровни экспрессии не отличаются в зависимости от того, является ли состояние клетки злокачественным или незлокачественным. Типичные контрольные гены включают, в качестве неограничивающих примеров, гены бета-актина, глицеральдегид-3-фосфатдегидрогеназы и рибосомального белка P1.
Подлежащий лечению при помощи настоящего способа субъект предпочтительно является млекопитающим. Типичные млекопитающие включают, в качестве неограничивающих примеров, человека, отличного от человека примата, мышь, крысу, собаку, кошку, лошадь и корову.
В соответствии с настоящим изобретением, можно определить уровень экспрессии CDC45L в клетках или тканях, полученных от субъекта. Уровень экспрессии можно определить на уровне продукта транскрипции (нуклеиновой кислоты), используя способы, известные в рассматриваемой области. Например, мРНК CDC45L можно количественно определить с помощью зондов при помощи способов гибридизации (например, Нозерн-гибридизации). Определение можно проводить при помощи чипа, эррея или подобного. Использование эррея является предпочтительным для определения уровня экспрессии CDC45L. Специалисты в рассматриваемой области могут подготовить такие зонды, используя информацию о последовательности CDC45L. Например, в качестве зондов можно использовать кДНК CDC45L. При необходимости, зонды можно пометить с помощью подходящей метки, такой как красители, флуоресцентные вещества и изотопы, и уровень экспрессии гена можно детектировать по интенсивности гибридизованных меток.
Более того, продукт транскрипции CDC45L (например, SEQ ID NO: 17) можно количественно определять при помощи праймеров с использованием способов на основе амплификации (например, ПЦР в режиме реального времени). Такие праймеры можно также подготовить на основе имеющейся информации о последовательности гена.
В конкретном плане, зонд или праймер, используемый в настоящем способе, гибридизуется при жестких, умеренно жестких или нежестких условиях с мРНК CDC45L. Как используется в настоящем документе, выражение «жесткие условия (гибридизации)» означает условия, при которых зонд или праймер будет гибридизоваться со своей последовательностью-мишенью, но не с другой последовательностью. Жесткие условия зависят от последовательности и будут разными при различных условиях. При более высоких температурах наблюдается специфическая гибридизация более длинных последовательностей, чем более коротких последовательностей. Как правило, температуру при жестких условиях выбирают приблизительно на 5 градусов С ниже, чем тепловая температура плавления (Tm) для конкретной последовательности, при определенной ионной силе и pH. Tm представляет собой температуру (при определенной ионной силе, pH и концентрации нуклеиновых кислот), при которой 50% зондов, комплементарных своей последовательности-мишени, равновесно гибридизуются с последовательностью-мишенью. Поскольку последовательность-мишень, как правило, присутствует в избытке, при Tm 50% зондов находятся в равновесии. Как правило, жесткими являются условия, при которых концентрация соли составляет менее чем около 1,0 М ионов натрия, как правило, от около 0,01 до 1,0 М ионов натрия (или других солей) при рН от 7,0 до 8,3, и температура составляет, по крайней мере, около 30 градусов C для коротких зондов или праймеров (например, от 10 до 50 нуклеотидов) и, по крайней мере, около 60 градусов С для более длинных зондов или праймеров. Жесткие условия также можно достичь добавлением дестабилизирующих веществ, таких как формамид.
Альтернативно, для диагностики по настоящему изобретению можно детектировать продукт трансляции. Например, можно определить количество белка CDC45L (SEQ ID NO: 18) или его фрагмента, подлежащего иммунологическому определению. Способы определения количества белка как продукта трансляции включают способы иммуноанализа, в которых используется антитело, специфически распознающее белок. Антитело может являться моноклональным или поликлональным. Более того, для детектирования можно использовать любой фрагмент или модификацию (например, химерное антитело, scFv, Fab, F(ab')2, Fv и т.д.) антитела, при условии, что фрагмент или модифицированное антитело сохраняет способность связывания с белком CDC45L. Способы подготовки этих видов антител для детектирования белков известны в рассматриваемой области, и любой способ можно использовать по настоящему изобретению для подготовки таких антител и их эквивалентов.
В качестве еще одного способа детектирования уровня экспрессии гена CDC45L, основанного на его продукте трансляции, интенсивность окраски можно определять при помощи иммуногистохимического анализа с использованием антител против белка CDC45L. То есть, при этом определении сильное окрашивание указывает на увеличенное присутствие белка/увеличенный уровень белка и, в то же время, на высокий уровень экспрессии гена CDC45L.
Уровень экспрессии гена-мишени, например гена CDC45L, в раковых клетках можно определить как увеличенный, если уровень превышает контрольный уровень (например, уровень в нормальных клетках) гена-мишени, например, на 10%, 25% или 50%, или увеличен до более чем в 1,1 раза, более чем в 1,5 раза, более чем в 2,0 раза, более чем в 5,0 раз, более чем в 10,0 раз или более.
Контрольный уровень можно определять одновременно с раковыми клетками, используя предварительно собранные и сохраненные образец(ы) от субъекта(ов), чей(чьи) статус(сы) заболевания (злокачественное и доброкачественное) известен. Кроме того, в качестве нормального контроля можно использовать нормальные клетки, полученные из нераковых участков органа, который имеет подлежащий лечению рак. Альтернативно, контрольный уровень можно определить при помощи статистического способа на основании результатов, полученных путем анализа ранее определенного(ых) уровня(ней) экспрессии гена CDC45L в образцах, полученных от субъектов, чей статус заболевания известен. Кроме того, контрольный уровень можно получать из базы данных паттернов экспрессий в ранее проверенных клетках. Более того, в соответствии с аспектом данного изобретения, уровень экспрессии гена CDC45L в биологическом образце можно сравнивать с несколькими контрольными уровнями, которые определяются из нескольких эталонных образцов. Предпочтительным является использование контрольного уровня, определенного по эталонному образцу, полученному из тканей того же типа, что биологический образец, полученный от субъекта. Более того, предпочтительно использовать стандартное значение уровней экспрессии гена CDC45L в популяции с известным статусом заболевания. Стандартное значение можно получить любым способом, известным в рассматриваемой области. Например, диапазон среднее +/-2 S.D. или среднее +/-3 S.D. можно использовать в качестве стандартного значения.
В случае, когда уровень экспрессии гена CDC45L увеличен по сравнению с нормальным контрольным уровнем или сходен/эквивалентен злокачественному контрольному уровню, субъекту может быть диагностирован подлежащий лечению рак.
Настоящее изобретение также предоставляет способ (i) диагностики того, имеет ли предполагаемый субъект подлежащий лечению рак, и/или (ii) выбора субъекта для лечения рака, где способ включает следующие стадии:
а) определение уровня экспрессии CDC45L в раковых клетках или ткани(ях), полученных от субъекта, у которого подозревается подлежащий лечению рак;
б) сравнение уровня экспрессии CDC45L с нормальным контрольным уровнем;
c) диагностика субъекта, как имеющего подлежащий лечению рак, на предмет того, увеличен ли уровень экспрессии CDC45L по сравнению с нормальным контрольным уровнем; и
d) выбор субъекта для лечения рака, если субъект диагностируется как имеющий подлежащий лечению рак, на стадии c).
Альтернативно, такой способ включает следующие стадии:
а) определение уровня экспрессии CDC45L в раковых клетках или ткани(ях), полученных от субъекта, у которого подозревается подлежащий лечению рак;
б) сравнение уровня экспрессии CDC45L со злокачественным контрольным уровнем;
c) диагностика субъекта, как имеющего подлежащий лечению рак, на предмет того, увеличен ли уровень экспрессии CDC45L по сравнению со злокачественным контрольным уровнем; и
d) выбор субъекта для лечения рака, если субъект диагностируется как имеющий подлежащий лечению рак, на стадии c).
Настоящее изобретение также предоставляет диагностический набор для диагностики или определения субъекта, который страдает или предполагается страдающим раком, которого можно лечить полипептидом CDC45L по настоящему изобретению, который также может найти применение при оценке прогноза рака и/или мониторинга эффективности и применимости конкретной противораковой терапии, особенно противораковой иммунотерапии. Иллюстративные неограничивающие примеры подходящих раков включают опухоль яичка, рак поджелудочной железы, рак мочевого пузыря, немелкоклеточный рак легкого, мелкоклеточный рак легкого, рак молочной железы, рак пищевода, рак предстательной железы, хронический миелоидный лейкоз (ХМЛ), опухоль мягких тканей, рак желудка, гепатобилиарный рак и рак прямой кишки. Конкретнее, набор предпочтительно включает, по крайней мере, один реактив для детектирования экспрессии гена CDC45L в полученной от субъекта клетке, такой как реактив, выбранный из группы:
(a) реактив для детектирования мРНК гена CDC45L;
(b) реактив для детектирования белка CDC45L или иммунологически активного фрагмента; и
(c) реактив для детектирования биологической активности белка CDC45L.
Примеры реактивов, пригодных для детектирования мРНК гена CDC45L, могут включать нуклеиновые кислоты, которые специфически связываются с или идентифицируют мРНК CDC45L, такие как олигонуклеотиды, которые имеют последовательность, комплементарную части мРНК CDC45L. Эти виды олигонуклеотидов являются примером праймеров и зондов, которые являются специфическими для мРНК CDC45L. Эти виды олигонуклеотидов можно подготовить, основываясь на способах, известных в рассматриваемой области. Если необходимо, реактив для детектирования мРНК CDC45L можно иммобилизовать на твердой основе. Более того, в набор может быть включен более чем один реактив для детектирования мРНК CDC45L.
С другой стороны, примеры реактивов, подходящих для детектирования белка CDC45L или иммунологически активного фрагмента, могут включать антитела к белку CDC45L или иммунологически активному фрагменту. Антитело может являться моноклональным и поликлональным. Более того, можно использовать любой фрагмент или модификацию (например, химерное антитело, scFv, Fab, F(ab')2, Fv и т.д.) антитела в качестве реактива, при условии, что фрагмент или модифицированное антитело сохраняет способность связывания с белком CDC45L. Способы подготовки этих видов антител для детектирования белков известны в рассматриваемой области, и любой способ можно использовать по настоящему изобретению для подготовки таких антител и их эквивалентов. Кроме того, антитела могут быть мечены молекулами, генерирующими сигнал, при помощи непосредственного присоединения или методик опосредованного мечения. Метки и способы мечения антител и детектирования связывания антител со своими мишенями известны в рассматриваемой области, и для настоящего изобретения можно использовать любые метки и способы. Кроме того, в набор может быть включен более чем один реактив для детектирования белка CDC45L.
Набор может содержать более чем один из вышеупомянутых реактивов. Набор может дополнительно включать твердую основу и реактив для связывания зонда к гену CDC45L или антитела против пептида CDC45L, среду и контейнер для культивирования клеток, реактивы для положительного и отрицательного контроля, и вторичное антитело для детектирования антитела против пептида CDC45L. Например, образцы тканей, полученные от субъектов без рака или страдающих раком, могут служить в качестве полезных контрольных реактивов. Набор по настоящему изобретению может дополнительно включать другие материалы, желательные с коммерческой точки зрения и точки зрения потребителя, включая буферы, разбавители, фильтры, иглы, шприцы и вкладыши (например, напечатанные, кассета, CD-ROM и т.д.) с инструкцией по применению. Эти реактивы и подобные можно сохранять в контейнере с этикеткой. Соответствующие контейнеры могут включать бутылки, флаконы и пробирки. Контейнеры могут быть оформлены из различных материалов, таких как стекло или пластик.
В качестве варианта осуществления настоящего изобретения, когда реактивом является зонд к мРНК CDC45L, реактив может быть иммобилизован на твердой основе, как, например, пористая полоска, для образования, по крайней мере, одного участка детекции. Область измерения или детекции пористой полоски может включать несколько участков, каждый из которых содержит нуклеиновую кислоту (зонд). Индикаторная полоска может также содержать участки для отрицательного и/или положительного контролей. Альтернативно, контрольный участок может быть расположен на полоске, отделенной от индикаторной полоски. Необязательно, различные участки детекции могут содержать разное количество иммобилизованных нуклеиновых кислот, то есть большее количество на первом участке детекции и меньшие количества на последующих участках. После добавления тестируемого образца ряд участков, отображающих детектируемый сигнала, обеспечивает количественную индикацию количества мРНК CDC45L, присутствующей в образце. Участки детекции можно скомпоновать в любой подходящей детектируемой форме, и, как правило, они представлены в форме полосы или точки, перекрывающей в ширину индикаторную полоску.
Набор по настоящему изобретению может дополнительно включать образец положительного контроля или стандартный образец CDC45L. Образец положительного контроля по настоящему изобретению можно подготовить путем сбора CDC45L-положительных образцов, а затем анализа в них уровней CDC45L. Альтернативно, очищенный белок CDC45L или полинуклеотид можно добавлять к клеткам, которые не экспрессируют CDC45L, для образования положительного образца или стандартного образца CDC45L. В настоящем изобретении очищенный CDC45L может являться рекомбинантным белком. Уровень CDC45L в образце положительного контроля составляет, например, больше, чем малозначимая величина.
В одном варианте осуществления настоящее изобретение дополнительно предоставляет диагностический набор, включающий белок или частичный белок, способный к специфическому распознаванию антителом по настоящему изобретению, или иммуногенный фрагмент.
Примеры частичных пептидов и иммуногенных фрагментов белков по настоящему изобретению, предусмотренных в настоящем документе, включают полипептиды, состоящие из, по меньшей мере, 8, предпочтительно 15, и наиболее предпочтительно 20 смежных аминокислот в аминокислотной последовательности белка по настоящему изобретению. Рак можно диагностировать путем детектирования антитела в образце (например, крови, ткани), используя белок или пептид (полипептид) по настоящему изобретению. Способы подготовки пептида или белка по настоящему изобретению представляют собой описанные выше.
Способ диагностики рака по настоящему изобретению можно осуществлять путем определения различия между количеством антитела против CDC45L и таковым в соответствующем контрольном образце, как описано выше. Предполагается, что субъект страдает раком, если клетки или ткани субъекта содержат антитела против продуктов экспрессии гена (CDC45L), и количество антитела против CDC45L, как определяется, превышает по уровню малозначимую величину, по сравнению с таковым в нормальном контроле.
В другом варианте осуществления диагностический набор по настоящему изобретению может включать пептид по настоящему изобретению и связанную с ним HLA-молекулу. Уже создан подходящий способ детекции антиген-специфических ЦТЛ с помощью антигенных пептидов и HLA-молекул (например, Altman JD et al., Science. 1996, 274(5284): 94-6). Таким образом, комплекс пептида по настоящему изобретению и HLA-молекулы может применяться в способе детекции для выявления ЦТЛ, специфичных к опухолевым антигенам, тем самым давая возможность раннего выявления рака, рецидивов и/или метастазов рака. Кроме того, он может быть использован для выбора субъектов, пригодных для применения лекарственных препаратов, включая пептид по настоящему изобретению в качестве активного ингредиента, или оценки терапевтического эффекта лекарственных препаратов.
В частности, в соответствии с известным способом (см., например, Altman JD et al., Science. 1996, 274(5284): 94-6), можно подготовить олигомерный комплекс, такой как тетрамер, радиоактивно меченной HLA-молекулы и пептида по настоящему изобретению. Комплекс может быть использован для количественного определения антиген-пептид специфических ЦТЛ в лимфоцитах периферической крови, полученных от субъекта, предположительно страдающего раком.
Настоящее изобретение дополнительно предоставляет способы и диагностические вещества для оценки иммунологической реакции у субъекта с использованием пептидных эпитопов, как описано в настоящем документе. В одном варианте осуществления изобретения HLA-рестриктированные пептиды, как описано в настоящем документе, могут использоваться в качестве реактивов для оценки и прогнозирования иммунного ответа у субъекта. Иммунный ответ, который следует оценить, можно вызвать при помощи контактирования иммуногена с иммунокомпетентными клетками в условиях in vitro или in vivo. В определенных вариантах осуществления вещества или композиции, применяемые в качестве реактива, могут представлять собой любое вещество или композицию, которые могут приводить к продуцированию антиген-специфических ЦТЛ, которые распознают и связывают пептидный эпитоп(ы). Пептидные реактивы не следует использовать в качестве иммуногена. Системы тестирования, которые используются для такого анализа, включают сравнительно недавние технические разработки, такие как тетрамеры, окрашивание на внутриклеточные лимфокины и тесты по высвобождению интерферона, или анализы ELISPOT. В предпочтительном варианте осуществления иммунокомпетентные клетки, предназначенные для контактирования с пептидным реактивом, могут представлять собой антигенпредставляющие клетки, включая дендритные клети.
Например, пептиды по настоящему изобретению можно использовать в тестах по тетрамерному окрашиванию для оценки мононуклеарных клеток периферической крови на присутствие антиген-специфических ЦТЛ после воздействия на опухолевые клетки антиген или иммуногена. HLA-тетрамерный комплекс можно применять для непосредственной визуализации антиген-специфических ЦТЛ (см., например, Ogg et al., Science 279: 2103-2106, 1998; и Altman et al., Science 174: 94-96, 1996) и определения частоты популяции антиген-специфических ЦТЛ в образце мононуклеарных клеток периферической крови. Тетрамерный реактив можно получить с использованием пептидов по изобретению, как описано ниже.
Пептид, который связывается с HLA-молекулой, повторно сворачивается в присутствии соответствующей тяжелой цепи HLA и бета-2-микроглобулина с образованием тримолекулярного комплекса. В комплексе карбокси-конец тяжелой цепи биотинилируется по сайту, который был заранее сконструирован в белке. Затем к комплексу добавляют стрептавидин для образования тетрамера, состоящего из тримолекулярного комплекса и стрептавидина. С помощью флуоресцентно меченного стрептавидина тетрамер может быть использован для окрашивания антиген-специфических клеток. Клетки затем можно идентифицировать, например, при помощи способа проточной цитометрии. Такой анализ может использоваться для диагностических и прогностических целей. Клетки, идентифицированные при помощи этой методики, также можно использовать в терапевтических целях.
Настоящее изобретение также предоставляет реактивы для оценки иммунных анамнестических реакций (см., например, Bertoni et al., J. Clin. Invest. 100: 503-513, 1997 и Penna et al., J Exp. Med. 174: 1565-1570, 1991), в том числе пептиды по настоящему изобретению. Например, образцы PBMC от индивидуумов с подвергаемым лечению раком можно проанализировать на присутствие антиген-специфических ЦТЛ с помощью специфичных пептидов. Образец крови, содержащий мононуклеарные клетки, можно оценить путем культивирования PBMC и стимулирования клеток пептидом по изобретению. После соответствующего периода культивирования размноженную клеточную популяцию можно проанализировать, например, на активность ЦТЛ.
Пептиды также можно использовать в качестве реактивов для оценки эффективности вакцины. PBMC, полученные от пациента, вакцинированного иммуногеном, можно проанализировать с помощью, например, любого из способов, описанных выше. Пациент является HLA-типированным, и реактивы пептидных эпитопов, которые распознают аллель-специфические молекулы, присутствующие в пациенте, отбирают для анализа. Иммуногенность вакцины может быть показана присутствием эпитоп-специфических ЦТЛ в образце PBMC. Пептиды по изобретению могут также использоваться для изготовления антител, используя известные в рассматриваемой области методики (см., например, CURRENTPROTOCOLSINIMMUNOLOGY, Wiley/Greene, NY; and Antibodies A Laboratory Manual, Harlow и Lane, Cold Spring Harbor Laboratory Press, 1989), которые могут найти применение в качестве реактивов для диагностики, определения или мониторинга рака. Такие антитела могут включать антитела, которые распознают пептиды в контексте HLA-молекулы, т.е. антитела, которые связываются с комплексом пептид-MHC.
Пептиды и композиции по настоящему изобретению имеют ряд дополнительных применений, некоторые из которых описаны в этом документе. Например, настоящее изобретение предоставляет способ диагностики или детектирования заболевания, характеризующегося экспрессией иммуногенного полипептида CDC45L. Такие способы включают определение экспрессии HLA-связывающегося пептида CDC45L, или комплекса HLA-связывающегося пептида CDC45L и молекулы HLA класса I в биологическом образце. Экспрессию пептида или комплекса пептида и молекулы HLA класса I можно определить или детектировать путем тестирования с партнером по связыванию для пептида или комплекса. В предпочтительном варианте осуществления партнером по связыванию для пептида или комплекса может быть антитело, распознающее и специфически связывающееся с пептидом. Экспрессия CDC45L в биологическом образце, таком как биопсия опухоли, также может быть проверена посредством протоколов стандартной ПЦР-амплификации с помощью CDC45L-праймеров. Пример экспрессии в опухоли представлен в настоящем документе, и дальнейшее раскрытие типичных условий и праймеров для амплификации CDC45L можно найти в WO2003/27322.
Предпочтительные способы диагностики предусматривают контактирование биологического образца, выделенного из субъекта, с веществом, характерным для HLA-связывающегося пептида CDC45L, чтобы обнаружить присутствие HLA-связывающегося пептида CDC45L в биологическом образце. Как используется в настоящем документе, «контактирование» означает размещение биологического образца в достаточной близости от вещества и в соответствующих условиях, например, концентрации, температуры, времени, ионной силы, чтобы обеспечить специфическое взаимодействие между веществом и HLA-связывающимся пептидом CDC45L, которые присутствуют в биологическом образце. В большинстве случаев условия для контактирования вещества с биологическим образцом являются условиями, известными специалистам в рассматриваемой области, для облегчения специфического взаимодействия молекулы и узнаваемого ею (например, белка и узнаваемого им рецептора, антитела и узнаваемого им белкового антигена, нуклеиновой кислоты и узнаваемой ею комплементарной последовательности) в биологическом образце. Типичные условия для облегчения специфического взаимодействия между молекулой и узнаваемого ею описаны в патенте США № 5108921, опубликованном Low et al.
Способы диагностики по настоящему изобретению можно выполнять либо in vivo, либо in vitro, либо и тем, и другим. Соответственно, биологический образец может быть расположен in vivo или in vitro в настоящем изобретении. Например, биологический образец может представлять собой ткань in vivo, и вещество, специфическое для иммуногенного полипептида CDC45L, можно использовать для детектирования присутствия этих молекул в ткани. Альтернативно, биологический образец можно собрать или выделить in vitro (например, анализ крови, биопсия опухоли, экстракт ткани). В особенно предпочтительном варианте осуществления, биологический образец может представлять собой образец, содержащий клетки, более предпочтительно образец, содержащий опухолевые клетки, полученные от подвергаемого диагностике или лечению субъекта.
Альтернативно, диагностику можно выполнять при помощи способа, который позволяет непосредственно количественно оценивать антиген-специфические Т-клетки путем окрашивания меченных флуоресцеином HLA-мультимерных комплексов (например, Altman, J. D. et al., 1996, Science 274: 94; Altman, J. D. et al., 1993, Proc. Natl. Acad. Sci. USA 90: 10330). Также были предусмотрены окрашивание внутриклеточных лимфокинов и тесты по высвобождению интерферона-гамма или анализы ELISPOT. Оказалось, что каждый из этих способов - окрашивание мультимеров, окрашивание внутриклеточных лимфокинов и анализы ELISPOT - являются, по меньшей мере, в 10 раз более чувствительными, чем более традиционные тесты (Murali-Krishna, K. et al., 1998, Immunity 8: 177; Lalvani, A. et al., 1997, J. Exp. Med. 186: 859; Dunbar, P. R. et al., 1998, Curr. Biol. 8: 413). Также можно использовать пентамеры (например, США 2004-209295A), декстрамеры (например, WO 02/072631) и стрептамеры (например, Nature medicine 6. 631-637 (2002)).
XI. Антитела
Настоящее изобретение дополнительно предоставляет антитела, которые связываются с пептидами по настоящему изобретению. Предпочтительные антитела специфически связываются с пептидами по настоящему изобретению и не связываются (или слабо связываются) с пептидом, не являющимся пептидом по настоящему изобретению. Альтернативно, антитела связываются с пептидами по изобретению, а также с их гомологами. Антитела против пептидов по изобретению могут найти применение в диагностических и прогностических тестах на рак и методиках обработки изображений. Аналогичным образом, такие антитела могут найти применение в лечении, диагностике и/или прогнозе других видов рака, в той мере, что CDC45L также экспрессируется или сверхэкспрессируется у больного раком. Кроме того, экспрессируемые интрацеллюлярно антитела (например, одноцепочечные антитела) могут терапевтически найти применение при лечении раков, в которых задействована экспрессия CDC45L, неограничивающие примеры которых включают опухоль яичка, рак поджелудочной железы, рак мочевого пузыря, немелкоклеточный рак легкого, мелкоклеточный рак легкого, рак молочной железы, рак пищевода, рак предстательной железы, хронический миелоидный лейкоз (ХМЛ), опухоль мягких тканей, рак желудка, гепатобилиарный рак и рак прямой кишки.
Настоящее изобретение также предоставляет различные иммунологические тесты для детекции и/или количественной оценки белка CDC45L (SEQ ID NO: 18) или его фрагментов, в том числе полипептида, состоящего из аминокислотных последовательностей, выбранных из группы, состоящей из SEQ ID NO: 2, 3, 4, 7 и 12. Такие тесты могут включать одно или несколько антител против CDC45L, способных распознавать и связываться с белком CDC45L или фрагментами этого, в зависимости от ситуации. В контексте настоящего изобретения антитела против CDC45L, связывающиеся с полипептидом CDC45L, предпочтительно распознают полипептид, состоящий из аминокислотных последовательностей, выбранных из группы, состоящей из SEQ ID NO: 2, 3, 4, 7 и 12. Специфичность связывания антитела можно подтвердить при помощи анализа ингибирования. То есть, показано, что в случае, когда связывание между антителом, которое следует проанализировать, и полноразмерным полипептидом CDC45L ингибируется в присутствии любых фрагментарных полипептидов, состоящих из аминокислотной последовательности SEQ ID NO: 2, 3, 4, 7 и 12, это антитело специфически связывается с фрагментом. В контексте настоящего изобретения такие иммунологические тесты выполняются в рамках различных форматов иммунологического анализа, хорошо известных в рассматриваемой области, включая, в качестве неограничивающих примеров, различные виды радиоиммуноанализов, иммуно-хроматографических методик, твердофазных иммуноферментных анализов (ELISA), иммуноферментных флуоресцентных анализов (ELIFA) и тому подобное.
Связанные иммунологические тесты, но отличные от тестов с использованием антител, по изобретению также могут включать тесты Т-клеточной иммуногенности (ингибирующие или стимулирующие), а также тесты по ГКГС-связыванию. Кроме того, настоящее изобретение предусматривает иммунологические способы визуализации, позволяющие детектировать рак по экспрессии CDC45L, неограничивающие примеры которых включают радиосцинтиграфические способы визуализации с использованием меченых антител по настоящему изобретению. Такие анализы находят клиническое применение для обнаружения, мониторинга и прогнозирования CDC45L-экспрессирующих раков, неограничивающие примеры которых включают опухоль яичка, рак поджелудочной железы, рак мочевого пузыря, немелкоклеточный рак легкого, мелкоклеточный рак легкого, рак молочной железы, рак пищевода, рак предстательной железы, хронический миелоидный лейкоз (ХМЛ), опухоль мягких тканей, рак желудка, гепатобилиарный рак и рак прямой кишки.
Настоящее изобретение также предоставляет антитела, которые связываются с пептидами по изобретению. Антитело по изобретению можно использовать в любой форме, например, как моноклональное или поликлональное антитело, и может также включать антисыворотку, полученную путем иммунизации животных, таких как кролик, пептидом по изобретению, все классы поликлональных и моноклональных антител, антитела человека и гуманизированные антитела, полученные путем генетической рекомбинации.
Пептид по изобретению, используемый в качестве антигена для получения антитела, можно получать из любых видов животных, но предпочтительно получать из млекопитающих, таких как человек, мышь или крыса, более предпочтительно из человека. Полученный из человека пептид можно получить из нуклеотидных или аминокислотных последовательностей, раскрытых в настоящем документе.
В соответствии с настоящим изобретением, пептид, предназначенный для использования в качестве антигена для иммунизации, может представлять собой полный белок или частичный пептид белка. Частичный пептид может включать, например, амино(N)-концевой или карбокси(C)-концевой фрагмент пептида по настоящему изобретению.
В настоящем документе, антитело определяется как белок, который реагирует либо с полноразмерным пептидом CDC45L, либо с его фрагментом. В предпочтительном варианте осуществления антитело по настоящему изобретению может распознавать фрагментарные пептиды CDC45L, состоящие из последовательности аминокислот, выбранной из группы, состоящей из SEQ ID NO: 2, 3, 4, 7 и 12. Способы синтеза олигопептидов известны в рассматриваемой области. После синтеза пептиды могут быть необязательно очищены перед использованием в качестве иммуногена. В контексте настоящего изобретения олигопептид (например, 9- или 10-мер) может быть соединен или связан с носителями для усиления иммуногенности. Гемоцианин лимфы улитки (KLH) хорошо известен в качестве носителя. Способ соединения KLH и пептида также хорошо известен в рассматриваемой области.
Альтернативно, ген, кодирующий пептид по изобретению или его фрагмент, можно встраивать в известный экспрессионный вектор, который затем используется для трансформации клетки-хозяина, как описано в настоящем документе. Нужный пептид или фрагмент можно извлечь из клеток-хозяев или внеклеточной среды любым стандартным способом, и впоследствии можно использовать в качестве антигена. Альтернативно, целые клетки, экспрессирующие пептид, или их лизаты или химически синтезированные пептиды можно использовать в качестве антигена.
Любое животное-млекопитающее может быть иммунизировано антигеном, но предпочтительно следует учитывать совместимость с родительскими клетками, используемыми для слияния клеток. В большинстве случаев можно использовать животных из семейств грызунов, зайцеобразных или приматов. Животные семейства грызунов включают, например, мышь, крысу и хомячка. Животные семейства зайцеобразных включают, например, кролика. Животные семейства приматов включают, например, обезьяну катаррини (обезьяна восточного полушария), такую как Macaca fascicularis, макака-резус, священного бабуина и шимпанзе.
Способы иммунизации животных антигенами известны в рассматриваемой области. Внутрибрюшинная инъекция или подкожная инъекция антигенов представляет собой стандартный способ иммунизации млекопитающих. Конкретнее, антигены могут быть разбавлены и суспендированы в соответствующем количестве в забуференном фосфатом солевом растворе (PBS), физиологическом растворе и др. При желании, суспензию антигена можно смешать с соответствующим количеством стандартного адъюванта, такого как полный адъювант Фрейнда, изготовить в виде эмульсии, а затем ввести в животных-млекопитающих. Предпочтительно, за этим следует несколько введений антигена, смешанного с соответствующим количеством неполного адъювантна Фрейнда, каждые 4-21 день. Соответствующий носитель также можно использовать для иммунизации. После проведения иммунизации, как описано выше, сыворотку можно проверить стандартным способом для увеличения количества нужных антител.
Поликлональные антитела против пептидов по настоящему изобретению можно подготовить путем сбора крови от иммунизированного млекопитающего, проверенного на увеличение уровня нужного антитела в сыворотке крови, и путем отделения сыворотки от крови при помощи любого обычного способа. Поликлональные антитела могут включать сыворотку, содержащую поликлональные антитела, а фракцию, содержащую поликлональные антитела, также можно отделить от сыворотки. Можно подготовить иммуноглобулин G или M из фракции, которая распознает только пептид по настоящему изобретению, используя, например, аффинную колонку с пептидом по настоящему изобретению, и в дальнейшем очищать эту фракцию с помощью колонки с протеином A или протеином G.
Для подготовки моноклональных антител иммунные клетки получают от млекопитающих, которые иммунизированы антигенами и у которых проверено увеличение уровня желаемых антител в сыворотке крови, как описано выше, и подвергают слиянию клеток. Иммунные клетки, используемые для слияния клеток, можно предпочтительно получить из селезенки. Другие предпочтительные родительские клетки, предназначенные для слияния с вышеописанными иммуноцитами, включают, например, миеломные клетки млекопитающих, и более предпочтительно, миеломные клетки, имеющие приобретенные свойства для отбора слившихся клеток при помощи лекарственных средств.
Вышеописанные иммуноциты и миеломные клетки можно сливать в соответствии с известными способами, например, способом Milstein et al. (Galfre and Milstein, Methods Enzymol 73: 3-46 (1981)).
Образованные гибридомы, полученные путем слияния клеток, можно селектировать путем их культивирования в стандартной селективной среде, такой как среда HAT (среда, содержащая гипоксантин, аминоптерин и тимидин). Культура клеток, как правило, поддерживается на среде HAT в течение от нескольких дней до нескольких недель, времени, достаточного для того, чтобы дать возможность погибнуть всем остальным клеткам (неслившимся клеткам), за исключением нужной гибридомы. Затем можно провести стандартное предельное разведение для скринирования и клонирования гибридомных клеток, продуцирующих необходимое антитело.
В дополнение к вышеописанному способу, в котором отличное от человека животное иммунизируют антигеном для подготовки гибридомы, лимфоциты человека, например, инфицированные вирусом EB, можно иммунизировать пептидом, экспрессирующими пептид клетками или их лизатами in vitro. Затем иммунизированные лимфоциты сливают с полученными от человека миеломными клетками, способными неограниченно делиться, такими как U266, чтобы получить гибридому, продуцирующую нужное антитело человека, способное связываться с пептидом (непроверенная опубликованная японская патентная заявка № Sho 63-17688).
Полученные гибридомы затем пересаживают в брюшную полость мыши и извлекают асциты. Полученные моноклональные антитела можно очистить, например, при помощи осаждения сульфатом аммония, колонки с протеином А и протеином G, ДЕАЕ-ионообменной хроматографии или аффинной колонки, к которой присоединен пептид по настоящему изобретению. Антитело по настоящему изобретению можно использовать не только для очистки и детекции пептида по настоящему изобретению, но также в качестве кандидата в агонисты и антагонисты пептида по настоящему изобретению.
Альтернативно, иммунная клетка, как, например, иммунизированный лимфоцит, продуцирующий антитела, может стать бессмертной при помощи онкогена и использоваться для подготовки моноклональных антител.
Моноклональные антитела, полученные таким образом, также можно подготовить рекомбинантно с использованием способов генной инженерии (см., например, Borrebaeck and Larrick, Therapeutic Monoclonal Antibodies, published in the United Kingdom by MacMillan Publishers LTD (1990)). Например, ДНК, кодирующая антитела, может быть клонирована из иммунной клетки, такой как гибридома или иммунизированный лимфоцит, продуцирующий антитело, встроена в соответствующий вектор и введена в клетку-хозяин, чтобы подготовить рекомбинантное антитело. Настоящее изобретение также предоставляет рекомбинантные антитела, подготовленные так, как описано выше.
Кроме того, антитело по настоящему изобретению может представлять собой фрагмент антитела или модифицированного антитела, при условии, что он связывается с одним или несколькими из пептидов на изобретению. Например, фрагмент антитела может представлять собой Fab, F(ab')2, Fv или одноцепочечный Fv (scFv), в котором Fv-фрагменты из H- и L-цепей связаны соответствующим линкером (Huston et al., Proc Natl Acad Sci USA 85: 5879-83 (1988)). Конкретнее, фрагмент антитела можно получить путем обработки антитела ферментом, как, например, папаин или пепсин. Альтернативно, можно сконструировать ген, кодирующий фрагмент антитела, встроить в экспрессионный вектор и экспрессировать в соответствующей клетке-хозяине (см., например, Co et al., J Immunol 152: 2968-76 (1994); Better and Horwitz, Methods Enzymol 178: 476-96 (1989); Pluckthun and Skerra, Methods Enzymol 178: 497-515 (1989); Lamoyi, Methods Enzymol 121: 652-63 (1986); Rousseaux et al., Methods Enzymol 121: 663-9 (1986); Bird and Walker, Trends Biotechnol 9: 132-7 (1991)).
Антитело можно модифицировать путем конъюгации с различными молекулами, такими как полиэтиленгликоль (ПЭГ). Настоящее изобретение предоставляет такие модифицированные антитела. Модифицированное антитело можно получить путем химической модификации антитела. Эти способы модификации являются общепринятыми в данной области.
Альтернативно, антитело по настоящему изобретению можно получить как химерное антитело, между вариабельной областью, полученной из антитела, отличного от антитела человека, и константной областью, полученной из антитела человека, или как гуманизированное антитело, включающее гипервариабельный участок (CDR), полученный из антитела, отличного от антитела человека, каркасную область (FR) и константную область, полученную из антитела человека. Такие антитела можно подготовить в соответствии с известной технологией. Гуманизацию можно осуществить путем замены последовательности CDR или последовательностей CDR грызунов на соответствующие последовательности антитела человека (см., например, Verhoeyen et al., Science 239: 1534-1536 (1988)). Соответственно, такие гуманизированные антитела представляют собой химерные антитела, где существенно меньший, чем интактный, вариабельный домен человека был заменен соответствующей последовательностью из видов, отличных от человека.
Также можно использовать полностью человеческие антитела, включающие вариабельные области человека в дополнение к каркасной и константной областям человека. Такие антитела можно изготовить с использованием различных методик, известных в рассматриваемой области. Например, способы in vitro предполагают использование рекомбинантных библиотек фрагментов антител человека, представленных на бактериофагах (например, Hoogenboom & Winter, J. Mol. Biol. 227: 381 (1991)). Аналогичным образом, человеческие антитела можно изготовить путем введения локусов иммуноглобулинов человека в трансгенных животных, например, мышей, у которых гены эндогенных иммуноглобулинов были частично или полностью инактивированы. Этот подход описан, например, в патентах США №№ 6150584, 5545807, 5545806, 5569825, 5625126, 5,633425, 5661016.
Антитела, полученные, как описано выше, могут быть очищены до гомогенности. Например, разделение и очистку антитела можно выполнять в соответствии со способами разделения и очистки, используемыми для обычных белков. Например, антитела можно отделять и выделять при помощи специально выбранного и комбинированного использования колоночных хроматографий, как, например, аффинная хроматография, фильтрация, ультрафильтрация, высаливание, диализ, электрофорез в полиакриламидном геле в присутствии додецилсульфата натрия и изоэлектрическое фокусирование (Antibodies: A Laboratory Manual. Ed Harlow and David Lane, Cold Spring Harbor Laboratory (1988)), но не исчерпываются этим. Колонку с протеином А и колонку с протеином G можно использовать в качестве аффинной колонки. Типичные колонки с протеином А для использования включают, например, Hyper D, POROS and Sepharose F.F. (Pharmacia).
Типичная хроматография, кроме аффинной, включает, например, ионообменную хроматографию, гидрофобную хроматографию, гель-фильтрацию, обращенно-фазовую хроматографию, адсорбционную хроматографию и т.п. (Strategies for Protein Purification and Characterization: A Laboratory Course Manual. Ed Daniel R. Marshak et al., Cold Spring Harbor Laboratory Press (1996)). Хроматографические процедуры могут осуществлять при помощи жидкостной хроматографии, как, например, ВЭЖХ и жидкостная хроматография быстрого разрешения.
Например, определение оптической плотности, иммуноферментный твердофазный анализ (ELISA), иммуноферментный анализ (ИФА), радиоиммуноанализ (РИА) и/или иммунофлюоресценцию можно использовать для определения антигенсвязывающей активности антитела по изобретению. В ELISA антитело по настоящему изобретению иммобилизовано на планшете, пептид по изобретению добавляют к планшету, а затем добавляют образец, содержащий нужное антитело, такой как культуральный супернатант продуцирующих антитело клеток или очищенные антитела. Затем добавляют вторичное антитело, которое распознает первичное антитело и которое маркировано ферментом, например, щелочной фосфатазой, и планшет инкубируют. Далее, после промывки к планшету добавляют ферментный субстрат, такой как п-нитрофенилфосфат, и измеряют оптическую плотность для оценки антигенсвязывающей активности образца. Фрагмент пептида, такой как С-концевой или N-концевой фрагмент, можно использовать в качестве антигена для оценки связывающей активности антитела. BIAcore (Pharmacia) можно использовать для оценки активности антитела в соответствии с настоящим изобретением.
Приведенные выше способы позволяют детектировать или измерять пептид по изобретению путем выдерживания антитела по изобретению с образцом, предположительно содержащим пептид по изобретению, и детектирования или определения иммунного комплекса, образованного антителом и пептидом.
Поскольку способом детектирования или определения пептида по изобретению можно специфически детектировать и определять пептид, способ может найти применение в различных экспериментах, в которых пептид используется.
XII. Векторы и клетки-хозяева
Настоящее изобретение также предоставляет вектор и клетку-хозяин, в которые вводится нуклеотид, кодирующий пептид по настоящему изобретению. Вектор по настоящему изобретению можно использовать для поддержания нуклеотида, особенно ДНК, по настоящему изобретению в клетке-хозяине, чтобы экспрессировать пептид по настоящему изобретению, или вводить нуклеотид по настоящему изобретению для генной терапии.
Когда E. coli является клеткой-хозяином и вектор амплифицируется и продуцируется в большом количестве в E. coli (например, JM109, DH5-α, HB101 или XL1-Blue), вектор должен иметь «ori», чтобы амплифицироваться в E. Coli, и маркерный ген, отвечающий за селекцию трансформированной E. coli (например, ген устойчивости к лекарственному средству, выбранному, например, из ампициллина, тетрациклина, канамицина, хлорамфеникола и т.п.). Например, можно использовать векторы серий M13, векторы серий pUC, pBR322, pBluescript, pCR-Script и др. Кроме того, можно использовать pGEM-T, pDIRECT и pT7 для субклонирования и экстрагирования кДНК, а также описанные выше векторы. Когда вектор используется для продуцирования белка по настоящему изобретению, могут найти применение экспрессионные векторы. Например, экспрессионный вектор для экспрессии в E. coli должны иметь вышеупомянутые характеристики для амплификации в E. coli. Когда E. coli, как, например, JM109, DH5-α, HB101 или XL1-Blue, используются в качестве клетки-хозяина, вектор должен иметь промотор, например, промотор lacZ (Ward et al., Nature 341: 544-6 (1989); FASEB J 6: 2422-7 (1992)), промотор araB (Better et al., Science 240: 1041-3 (1988)), промотор T7 или подобный, который позволяет эффективно экспрессировать нужный ген в E. coli. В этом отношении, вместо вышеприведенных векторов можно использовать, например, pGEX-5X-1 (Pharmacia), «QIAexpress system» (Qiagen), pEGFP и pET (в этом случае хозяином предпочтительно является BL21, экстрессирующая РНК-полимеразу Т7). Кроме того, вектор также может содержать сигнальную последовательность для секреции пептида. Типичная сигнальная последовательность, которая направляет пептид для секреции в периплазму E. Coli, является сигнальная последовательность pelB (Lei et al., J Bacteriol 169: 4379 (1987)). К средствам для введения векторов в хозяйскую клетку-мишень относятся, например, способ с использованием хлорида кальция и способ электропорации.
В дополнение к E. coli, для производства полипептида по настоящему изобретению можно использовать, например, экспрессионные векторы, полученные из млекопитающих (например, pcDNA3 (Invitrogen) и pEGF-BOS (Nucleic Acids Res 18(17): 5322 (1990)), pEF, pCDM8), экспрессионные векторы, полученные из клеток насекомых (например, «Bac-to-BAC baculovirus expression system» (GIBCO BRL), pBacPAK8), экспрессионные векторы, полученные из растений (например, рMH1, pMH2), экспрессионные векторы, полученные из вирусов животных (например, рHSV, pMV, pAdexLcw), экспрессионные векторы, полученные из ретровирусов (например, PZIpneo), экспрессионные векторы, полученные из дрожжей (например, «Pichia Expression Kit» (Invitrogen), pNV11, SP-Q01), и экспрессионные векторы, полученные из Bacillus subtilis (например, рPL608, pKTH50).
Для того чтобы экспрессировать вектор в животных клетках, таких как клетки СНО, COS или NIH3T3, вектор должен иметь промотор, необходимый для экспрессии в таких клетках, например, промотор SV-40 (Mulligan et al., Nature 277: 108 (1979)), промотор MMLV-LTR, промотор EF1-альфа (Mizushima et al., Nucleic Acids Res 18: 5322 (1990)), промотор CMV и подобные, и предпочтительно маркерный ген, отвечающий за селекцию трансформантов (например, ген лекарственной устойчивости, отобранный при помощи антибиотика (например, неомицин, G418)). Примеры известных векторов с этими характеристиками включают, например, pMAM, pDR2, pBK-RSV, pBK-CMV, pOPRSV и pOP13.
Несмотря на то, что способы и материалы, аналогичные или эквивалентные тем, которые описаны в настоящем документе, могут быть использованы в практике или проверке настоящего изобретения, подходящие материалы и способы описаны. Все публикации, заявки на патенты, патенты и другие документы, указанные в настоящем документе, включены в качестве ссылки в полном объеме. В случае конфликта настоящая спецификация, включая определения, является регулирующей. Кроме того, материалы, способы и примеры приведены только для иллюстрации и не должны рассматриваться в качестве ограничивающих.
Следующие примеры приведены для иллюстрации данного изобретения и помощи специалистам в рассматриваемой области при его изготовлении и применении. В любом случае, примеры не предназначены для ограничения каким-либо образом сферы применения изобретения.
Примеры
Материалы и способы
Анализы с использованием кДНК-микрочипов.
Профили экспрессии генов были образованы путем анализа с использованием кДНК-микрочипов, как описано ранее (Nakamura T et al., Oncogene 2004; 23: 2385-400, Taniwaki M et al., Int J Oncol 2006; 29: 567-75). Необработанные данные анализа с использованием микрочипов доступен по запросу у профессора Ю. Накамура (университет Токио, Inst. Med. Sci.). Образцы тканей рака легких и прилегающих незлокачественных нормальных тканей легких были получены из хирургических образцов, и все пациенты предоставили свое письменное информационное согласие на участие в этом исследовании.
Мыши.
Шестинедельные неполные страдающие диабетом (NOD)/тяжелым комбинированным иммунодефицитом (SCID) самки мышей были приобретены от Charles River Laboratories Japan. Мыши поддерживались в Центре ресурсов животного мира и развития университета Кумамото, и с ними обращались в соответствии с рекомендациями по уходу за животными университета Кумамото.
Линии клеток и экспрессия HLA.
CDC45L- и HLA-A*2402-положительные клеточные линии рака легких человека EBC-1 и Lu99 были любезно предоставлены Банком научно-исследовательских ресурсов медицинских наук (Цукуба, Япония). Клетки C1R-A2402, HLA-A*2402-трансфектанты B-лимфобластоидной клеточной линии C1R человека, экспрессирующие следовое количество естественной молекулы HLA класса I (Karaki S, Kariyone A, Kato N, Kano K, Iwakura Y, Takiguchi M. HLA-B51 transgenic mice as recipients for production of polymorphic HLA-A, B-specific antibodies. Immunogenetics 1993; 37: 139-42)26, были любезно предоставлены доктором Masafumi Takiguchi (Университет Кумамото, Кумамото, Япония). CDC45L-положительные клетки линии рака поджелудочной железы человека PANC1 (HLA-A*0201+ и HLA-A*2402) и ТАР-дефицитные и HLA-A*0201-положительные клеточные линии T2 были приобретены в Банке клеток Riken. Экспрессию HLA-A2 и HLA-А24 изучали способом проточной цитометрии при помощи моноклонального антитела anti-HLA-A2 (mAb) BB7.2 (One Lambda, Inc., Канога-Парк, Калифорния) и anti-HLA-А24 mAb (One Lambda, Inc.), соответственно, для того чтобы выбрать HLA-А24- и HLA-A2-положительных доноров крови для анализов. Эти клетки поддерживались in vitro в среде RPMI 1640 с добавлением 10% FCS в атмосфере 5% СО2 при 37 градусах С.
Пациенты, образцы крови и опухолевые ткани.
Протокол исследования для сбора и использования PBMC от доноров была утверждена Контрольной комиссией при университете Кумамото. Образцы крови или злокачественные ткани и прилегающие незлокачественные ткани получены от пациентов в госпитале университета Кумамото во время обычных диагностических процедур после получения письменного информационного согласия. Образцы крови были также получены от здоровых доноров после получения их письменного информационного согласия. Все образцы были случайным образом закодированы, чтобы замаскировать их идентичность, и образцы крови хранились при -80 градусов C до использования.
Ревертазо-полимеразная цепная реакция и Нозерн-блот анализ.
Анализ при помощи ревертазо-полимеразной цепной реакции (RT-PCR) клеточных линий и нормальных и раковых тканей был выполнен, как описано ранее (Nakatsura T et al., Biochem Biophys Res Commun 2001; 281: 936-44). Последовательности CDC45L-праймера представляли собой 5'-CTGGTGTTGCACAGGCTGTCATGG-3' (SEQ ID NO: 19) (смысловой) и 5'-CGCACACGGTTAGAAGAGGAG-3' (SEQ ID NO: 20) (антисмысловой). После нормирования на мРНК бета-актина в качестве контроля, авторы сравнили экспрессию мРНК CDC45L в тканях и клеточных линиях. Нозерн-блот анализ выполняли, как описано ранее, используя кДНК зонд, специфический для гена CDC45L (соответствующий парам нуклеотидов от 1245 до 1867) (Nakatsura T et al., Biochem Biophys Res Commun 2003; 306: 16-25).
Иммуногистохимическое окрашивание.
Иммуногистохимическое исследование CDC45L человека выполняли, как описано ранее, с некоторыми модификациями (Nakatsura T et al., Biochem Biophys Res Commun 2001; 281: 936-44). Вкратце, после депарафинизации и регидратации срезов тканей эндогенную перекись гасили 0,3% перекисью водорода в метаноле в течение 15 мин, и неспецифическое связывание уменьшали путем инкубации с белковым блокирующим бессывороточным реактивом (Dako) в течение 10 мин. После промывки буферным раствором (0,1% Tween 20 и 0,5 М NaCl в 0,05 М Трис-HCl-буфере) первичное антитело (антитело против CDC45L человека, полученные от кролика, разведение 1:100, HPA000614, аффинно очищенное, Sigma-Aldrich), разведенное в Can Get Signal (R) immuNOtain Solution A (Toyobo Co., Осака, Япония), инкубируют с образцами в течение ночи при 4 градусах C. После этого срезы тщательно промывали буферным раствором и инкубировали с вторичным антителом (анти-мышиное, меченное полимером-HRP и анти-кроличье антитело, Dako) при комнатной температуре. После трех промывок буферным раствором проводили реакцию окрашивания путем инкубации с раствором 3,3'-диаминобензидина (Liquid DAB+ Substrate Chromogen System, Dako). Слайды были затем слегка контрастно окрашивали гематоксилином, обезвоженным в этаноле, и проясняли в ксилоле. Срезы яичек, для которых известно, что они экспрессируют CDC45L, использовали в качестве положительного контроля для антитела против CDC45L человека. Для отрицательного контроля авторы заменили первичное антитело нормальным IgG кролика.
Пептиды.
Пептиды, полученные из CDC45L человека, несущие мотивы связывания с HLA-A*2402-кодируемыми молекулами, были отобраны с помощью программного обеспечения BIMAS (Bioinformatics and Molecular Analysis Section, Center for Information Technology, NIH, Bethesda, MD), и были синтезированы 16 пептидов (10 нонамеров и 6 декамеров, с чистотой >95%) (AnyGen, Кванджу, Корея) (Таблица 1). Пептиды растворяли в диметилсульфоксиде в концентрации 20 мкг/мл и хранили при -80 градусов С. Два HIV-пептида, HLA-А24-рестриктированный RYLRDQQLL (SEQ ID NO: 21) пептид (HIV-А24) и HLA-A2-рестриктированный SLYNTYATL (SEQ ID NO: 22) пептид (HIV-А2), были использованы в качестве отрицательного контроля (Komori H et al., Clin Cancer Res 2006; 12: 2689-97).

Образование ЦТЛ, реагирующих на CDC45L человека, и проверка ЦТЛ-ответов.
PBMC выделяли из HLA-А24- или HLA-A2-положительных японских здоровых доноров и пациентов с раком легких, и образовывали дендритные клетки (DC), полученные из моноцитов периферической крови, как описано ранее (Harao M et al., Int J Cancer 2008; 123: 2616-25, Naito K et al., Int J Oncol 2006; 28: 1481-9). DC подвергали импульсному воздействию 20 мкг/мл пептидов-кандидатов в присутствии 4 мкг/мл бета 2-микроглобулина (Sigma-Aldrich) в течение 2 ч при 37 градусах С в AIM-V (Invitrogen) с добавлением 2% инактивированной теплом аутологичной плазмы. Клетки затем облучали (40 Гр) и инкубировали с выделенными CD8+ Т-клетками, как описано ранее (Imai K et al., Clin Cancer Res 2008; 14: 6487-95, Harao M et al., Int J Cancer 2008; 123: 2616-25). Две дополнительных стимуляции с нагруженными пептидами аутологичными PHA-бластами проводили на 7 и 14 день. PHA-бласты образовывали, как описано ранее (Inoue M et al., Immunol Lett 2009; 126: 67-72), и эти PHA-бласты (5×105) подвергали импульсному воздействию 20 мкг/мл пептидов в течение 3 ч, облучали (100 Гр) и культивировали с 2×106 CD8+ Т-клеток в присутствии 10 нг/мл рекомбинантного IL-7 человека (Wako, Осака, Япония). После 2 дней в культуры добавляли 20 МЕ/мл рекомбинантного IL-2 человека (PeproTec, Inc.).
Через шесть дней после последней стимуляции были исследованы антиген-специфические ответы индуцированных ЦТЛ. Две дополнительные еженедельные стимуляции с нагруженными пептидами аутологичными PHA-бластами проводили на 7 и 14 день. Аутологичные CD14-CD8-клетки, обогащенные CD4+ Т-клетками, культивировали с РНА (2 мкг/мл) и рекомбинантным IL-2 человека (100 МЕ/Мл) в течение 2 дней, и клетки промывали PBS и культивировали с рекомбинантным IL-2 человека (100 МЕ/Мл) в течение еще трех дней. Эти PHA-бласты (5×105) были подвергнуты импульсному воздействию 50 мкг/мл пептидов течение 2 часов при 37 градусов C в AIM-V (Invitrogen) с добавлением 2% инактивированной теплом аутологичной плазмы. Клетки затем облучали (100 Гр) и инкубировали с 2×106 CD8+ Т-клеток. Эти культуры помещали в 24-луночные планшеты с использованием среды с добавлением 5 нг/мл рекомбинантных IL-7, IL-2 и IL-15 человека. Через шесть дней после последней стимуляции, антиген-специфические ответы индуцированных ЦТЛ исследовали при помощи INF-гамма анализа ELISPOT, анализа CD107a-мобилизации и анализа высвобождения 51Cr, как описано ранее (Komori H et al. Clin Cancer Res 2006; 12: 2689-97) и далее.
Анализ CD107a-мобилизации.
Для идентификации дегранулированных CD8+ Т-лимфоцитов, стимулированных эпитопными пептидами, CD107a, экспонированные на поверхности клетки, анализировали способом проточной цитометрии (Rubio V et al., Nat Med 2003; 9: 1377-82, Betts MR et al., J Immunol Methods 2003; 281: 65-78). Анализ CD107a-мобилизации выполняли с использованием immunocyte CD107a detection kit (MBL, Нагоя, Япония) в соответствии с инструкциями изготовителя. Индуцированные ЦТЛ суспендировали в конечной концентрации 2×106 клеток/мл в AIM-V с добавлением 2% инактивированной теплом аутологичной плазмы, и 150 мкл клеточной суспензии добавляли в каждую лунку 96-луночного круглодонного микропланшета. В качестве стимулятора добавляли пептид, полученный из CDC45L, или контрольный HIV-пептид (1 мкг/мл), и FITC-меченные mAb против CD107a человека или FITC-меченные изотипные контрольные IgG1 мыши и монензин добавляли в каждую лунку. Клетки культивировали в течение 5 ч при 37 градусов С. После культивирования клетки окрашивали с PE-коньюгированными антителами против CD8a человека (Biolegend) и анализировали способом проточной цитометрии (FACScan; BD Biosciences).
Образование клеток с подавленной экспрессией CDC45L.
Для подавления экспрессии CDC45L в клетках рака легких, малые интерферирующие (si) РНК к CDC45L (siRNA к Cdc45 человека, sc-35044: пул из трех мишень-специфических siRNA длиной 20-25 нуклеотидов, Santa Cruz) добавляли в конечной концентрации 150 нМ к клеткам, слившимся на 40-60%. Липофектамин (TM) 2000 (Invitrogen) использовали для трансфекции siRNA в клетки, в соответствии с инструкциями изготовителя. siRNA к GFP были использованы в качестве постороннего контроля. Обработанные клетки промывались один раз с PBS, и прикрепленные клетки собирали через 72 ч после трансфекции и использовали в качестве клеток-мишеней для анализа высвобождения 51Cr. Для исследования способности siRNA подавлять экспрессию CDC45L был проведен Вестерн-блот анализ, как описано ранее (Nakatsura T et al., Biochem Biophys Res Commun 2003; 306: 16-25). Раковые клетки промывались один раз PBS через 48 ч после трансфекции, и прикрепленные клетки собирали и лизировали для анализа уровня экспрессии CDC45L по сравнению с таковым для клеток отрицательного контроля. Бета-актин был использован в качестве внутреннего контроля. Поликлональное антитело кролика, реагирующее с CDC45L (sc-20685, Santa Cruz Biotechnology), использовали в качестве первичного антитела.
Ответы ЦТЛ человека в отношении линий раковых клеток.
Частоту клеток, продуцирующих интерферон (INF)-гамма на 1×105 ЦТЛ после стимуляции клетками Lu99 (1×104/лунку) или подвергнутыми импульсному воздействию пептидов клетками C1R-A2402 и T2 (1×104/лунку), анализировали при помощи анализа ELISPOT (Human IFN-gamma ELISPOT kit, BD Biosciences), как было описано ранее (Komori H et al., Clin Cancer Res 2006; 12: 2689-97, Bourgault VI et al., Cancer Res 2004; 64: 8761-6). ЦТЛ совместно культивировали с раковыми клетками или подвергнутыми импульсному воздействию пептидов клетками C1R-A2402 и T2 в качестве клеток-мишеней (5×103/лунку) с указанным соотношением эффектора-к-мишени, и стандартный анализ высвобождения 51Cr выполняли, как описано ранее (Yokomine K et al., Int J Cancer 2009; 126: 2153-63, Monji M et al., Clin Cancer Res 2004; 10: 6047-57). Блокирование HLA класса I при помощи mAb против HLA класса I человека, W6/32 (IgG2a, Santa Cruz Biotechnology) или mAb HLA-DR против HLA класса II человека (IgG2a, BD Biosciences), было выполнено так, как описано ранее (Komori H et al., Clin Cancer Res 2006; 12: 2689-97, Makita M et al., Clin Cancer Res 2002; 8: 2626-31).
Модель адоптивной иммунотерапии.
Экспериментальная адоптивная иммунотерапия была выполнена, как описано ранее (Imai K et al., Clin Cancer Res 2008; 14: 6487-95, Komori H et al., Clin Cancer Res 2006; 12: 2689-97). Вкратце, клетки Lu99 (3×106 клеток/мышь), положительные как по эндогенному CDC45L, так и по HLA-А24, подкожно прививали в правый бок мышам NOD/SCID. Когда размеры опухоли достигли примерно 25 мм2 на 7 день, CDC45L-специфические линии ЦТЛ, индуцированные от двух здоровых доноров in vitro-стимуляцией смесью пептидов CDC45L-А24-9-109-2(SEQ ID NO: 2), CDC45L-А24-9-294-3(SEQ ID NO: 3) и CDC45L-А24-9-556-4(SEQ ID NO: 4) или линии ЦТЛ, индуцированные стимуляцией посторонним HLA-А24-рестриктированным HIV-пептидом, суспендировали в 100 мкл PBS и инъецировали внутривенно (4×106 клеток/мышь). Внутривенную инъекцию ЦТЛ повторяли на 14 день. Размер опухолей оценивали два раза в неделю с помощью штангенциркуля, измеряя два перпендикулярных диаметра.
Статистический анализ.
Двусторонний t-теста Стьюдента был использован для оценки статистической значимости различий в данных ELISPOT и размерами опухоли между группами лечения. Значения P менее 0,05 считались статистически значимыми. Статистический анализ проводили с использованием коммерческого статистического программного пакета (StatView 5.0, Abacus Concepts, Калабасас, Калифорния).
Результаты
Идентификация сверхэкспрессиии гена CDC45L в раке легких по тестам на основе кДНК-микрочипов.
Охватывающий геном кДНК-микрочип, содержащий 27648 генов, был использован для изучения профилей экспрессии генов 18 тканей рака легких и прилегающих к ним нормальных аналогов. Анализ кДНК-микрочипов показал заметное увеличение экспрессии гена CDC45L в тканях рака легких у каждого из 12 пациентов с мелкоклеточным раком легких (среднее относительное соотношение экспрессии: 163,087; диапазон: 81,204-369,309) и у 4 из 6 пациентов с немелкоклеточным раком легких (среднее относительное соотношение экспрессии: 15,170; диапазон: 0,08-40,131) (Таблица 2). Вследствие этого CDC45L был выбран, чтобы быть охарактеризованы как новый ОСА от рака легких. Уровень экспрессии гена CDC45L также был улучшен в большинстве нескольких других злокачественных новообразований, в том числе рака простаты, молочной железы и мочевого пузыря, на основе анализа кДНК-микрочипов (Таблица 2).

Экспрессия мРНК CDC45L в нормальных тканях, раковых клеточных линиях и раковых тканях легких.
Экспрессия гена CDC45L в нормальных тканях на уровне мРНК анализировали с помощью RT-PCR и Нозерн-блот анализа. Полуколичественный RT-PCR-анализ CDC45L в нормальных тканях выявил, что он слабо экспрессировался только в семенниках и молочной железе (Фиг. 1А). Нозерн-блот анализ в нормальных тканях с использованием кДНК CDC45L в качестве зонда показал, что он не экспрессировался в двадцати двух жизненно важных органах, за исключением семенника (Фиг. 1B), в соответствии с результатами RT-PCR-анализа. Напротив, экспрессия гена CDC45L была обнаружена во всех девяти клеточных линиях рака легких с помощью RT-PCR-анализа (Фиг. 1C). Впоследствии, экспрессию гена CDC45L анализировали с помощью RT-PCR-анализа в раковых тканях легких. У 7 из 8 больных НМКРЛ в раковых тканях сильно экспрессировалась мРНК CDC45L (Фиг. 1D верхний). Кроме того, экспрессию гена CDC45L анализировали с помощью RT-PCR-анализа в раковых тканях и прилегающих к ним нормальных аналогах, которые вырезали хирургически. Экспрессия гена CDC45L была обнаружена в каждой из 4 раковых тканей легких, но в их нормальных аналогах была обнаружена слабая экспрессия (Фиг. 1 нижний). Кроме того, RT-PCR-анализ различных раковых клеточных линий, полученных из рака желудка, гепатобилиарного рака, рака молочной железы, рака предстательной железы и колоректального рака, показал, что ген CDC45L также экспрессируется во многих из этих раковых клеточных линий (Фиг. 1E).
Для изучения экспрессии CDC45L на уровне белка был выполнен иммуногистохимический анализ раковых тканей легких и нормальных тканей. Было изучено 26 образцов раковых тканей легких, состоящих из 12 аденокарцином (7 из 12 представляли собой бронхоальвеолярный рак), 8 - плоскоклеточный рак и 6 - мелкоклеточная карцинома. Все 26 образцов проявляли сильное ядерное окрашивание на CDC45L и слабое окрашивание цитоплазмы (Фиг. 1F). Отсутствие окрашивания или очень слабое окрашивание наблюдалось в нормальных прилегающих тканях легких (Фиг. 1F). CDC45L экспрессировался в семенниках, однако, отсутствие окрашивания или очень слабое окрашивание наблюдалось в других видах нормальных тканей взрослого человека, включая ткани головного мозга, сердца, печени, почек, желудка, тонкого кишечника, толстой кишки, поджелудочной железы, кожи, селезенки, вилочковой железы (Фиг. 1F и данные не показаны). Далее, уровни экспрессии белка CDC45L в раках легких человека были, по-видимому, гораздо выше, чем в нормальных тканях взрослого организма, за исключением семенников. Эти результаты согласуются с результатами RT-PCR и Нозерн-блот анализа (Фиг. 1A, B и D).
Идентификация полученных из CDC45L и HLA-А24-рестриктированных ЦТЛ-эпитопов у здоровых доноров.
Для определения HLA-А24-рестриктированных и полученных из CDC45L ЦТЛ-эпитопов 16 пептидов-кандидатов, которые, по предсказанию, имеют высокую аффинность связывания с HLA-А24, были выбраны в соответствии с прогнозированием HLA-пептидного связывания на основе программного обеспечения, предоставляемого NIH BIMAS (Таблица 1). Для проверки того, какой пептид может индуцировать реагирующие на пептид ЦТЛ, CD8+ Т-клетки, отсортированные из PBMC здоровых доноров, инкубировали с аутологичными, полученными из моноцитов DC, подвергнутыми импульсному воздействию смеси из четырех пептидов, выбранных из этих 16 CDC45L-пептидов. После двух дополнительных еженедельных стимуляций нагруженными пептидами аутологичными PHA-бластами, цитотоксическая активность против подвергнутых импульсному воздействию клеток C1R-*2402 проверяли при помощи INF-гамма ELISPOT-анализа (Фиг. 2). CD8+ Т-клетки, отсортированные из PBMC двух HLA-А24 положительных здоровых доноров, стимулировали с аутологичными, полученными из моноцитов DC, подвергнутыми импульсному воздействию смеси 4 из 16 CDC45L-пептидов. Частота CD8+ Т-клеток, специфичных для полученных из CDC45L пептидов, в образованных линиях ЦТЛ проверяли при помощи INF-гамма ELISPOT-анализа (Фиг. 3). Фоновые контроли стимулировали клетками C1R-A2402, подвергнутыми импульсному воздействию посторонним HIV-А24 пептидом. Образованные линии ЦТЛ воспроизводимо продуцировали большое количество INF-гамма после стимуляции клетками C1R-A2402, подвергнутыми импульсному воздействию пептидами CDC45L-А24-9-109-2(SEQ ID NO: 2), 109VYNDTQIKL117, CDC45L-А24-9-294-3(SEQ ID NO: 3), 294SYТТАRFKL302, CDC45L-А24-9-556-4(SEQ ID NO: 4), 556KFLDALISL564, CDC45L-А24-9-370-7(SEQ ID NO: 7), 370KFLASDVVF378 или CDC45L-А24-10-556-12(SEQ ID NO: 12), 556KFLDALISLL565. Данные результаты свидетельствуют о том, что эти пять полученных из CDC45L пептидов являются иммуногенными.
Для дальнейшего анализа ЦТЛ-стимулирующей способности этих пяти иммуногенных пептидов, был проведен анализ CD107a-мобилизации для оценки антиген-специфической секреции содержания цитолитических гранул ЦТЛ (Rubio V et al., Nat Med 2003; 9: 1377-82, Betts MR et al. J Immunol Methods 2003; 281: 65-78). Существенно большее соотношение CD8+ Т-клеток окрашивалось mAb против CD107a в случае, когда линии ЦТЛ, образованные стимуляцией одним из этих пяти иммуногенных пептидов, были повторно стимулированы их родственными пептидами, по сравнению с повторной стимуляцией посторонним HIV-А24 пептидом (Фиг. 4).
Создание линий ЦТЛ, специфичных для полученных из CDC45L пептидов у пациентов с раком легких.
CDC45L-специфические ЦТЛ были образованы из PBMC пациентов с раком легких, положительных по HLA-А24, путем стимуляции пептидами CDC45L-А24-9-109-2(SEQ ID NO: 2), CDC45L-А24-9-294-3(SEQ ID NO: 3), CDC45L-А24-9-556-4(SEQ ID NO: 4), CDC45L-А24-9-370-7(SEQ ID NO: 7) или CDC45L-А24-10-556-12(SEQ ID NO: 12). Эти линии ЦТЛ продуцировали значительно большее количество INF-гамма в ответ на полученные из CDC45L пептиды в IFN-гамма ELISPOT-анализах (Фиг. 5A). Кроме того, эти линии ЦТЛ проявляли цитотоксическую активность в отношении клеток C1R-A2402, подвергнутых импульсному воздействию пятью полученными из CDC45L пептидами, но не в отношении клеток C1R-A2402, подвергнутых импульсному воздействию посторонним HIV-А24-пептидом, в тестах по высвобождению 51Cr (Фиг. 5B). Данные результаты показывают, что эти ЦТЛ обладают пептид-специфической цитотоксической активностью.
Естественный процессинг ЦТЛ-эпитопов CDC45L в раковых клетках.
Проверялась способность этих ЦТЛ уничтожать клеточные линии рака легких человека, которые естественно экспрессировали CDC45L и HLA-А24. Клетки Lu99 и EBC-1 (CDC45L+, HLA-А24+), клетки Lu99 и EBC-1, трансфицированные CDC45L-специфическими siRNA (CDC45L-, HLA-А24+), клетки Lu99 и EBC-1, трансфицированные контрольными GFP-siRNA (CDC45L+, HLA-А24+) (Фиг. 5C) и клетки A549 (CDC45L+, HLA-А24-) были использованы в качестве клеток-мишеней. Как показано на Фиг. 5D, линии ЦТЛ, образованные от здорового донора-4 (нижняя панель, слева) и пациента-18 с раком легких (нижняя панель, справа) путем стимуляции пептидами CDC45L-А24-9-109-2(SEQ ID NO: 2) и CDC45L-А24-9-556-4(SEQ ID NO: 4), соответственно, проявляли цитотоксичность в отношении клеток Lu99 и клеток Lu99, трансфицированных контрольными GFP-siRNA, но не в отношении клеток Lu99, трансфицированных CDC45L-специфическими siRNAs (нижняя панель), и клеток A549 (нижняя панель, слева). Аналогичным образом, ЦТЛ, образованные от пациента-1 с раком легких путем стимуляции пептидом CDC45L-А24-9-294-3(SEQ ID NO: 3), проявляли цитотоксичность для клеток EBC-1 и EBC-1, трансфицированных GFP-siRNAs, но не для клеток EBC-1, трансфицированных с CDC45L-специфическими siRNA, и клеток A549 (верхняя панель, слева). Кроме того, ЦТЛ, образованные от пациентов 3 и 8 с раком легких, стимулированных и пептидом CDC45L-А24-9-370-7(SEQ ID NO: 7), проявляли цитотоксичность для клеток EBC-1 и ЕВС-1, трансфицированных GFP-siRNA, но не для клеток EBC-1, трансфицированных CDC45L-специфическими siRNA, и клеток A549 (верхняя панель, в центре, справа). Среди пяти иммуногенных, полученных из CDC45L пептидов, три, CDC45L-А24-9-109-2(SEQ ID NO: 2), CDC45L-А24-9-294-3(SEQ ID NO: 3) и CDC45L-А24-9-556-4(SEQ ID NO: 4), вызывали CDC45L-специфические ЦТЛ, которые могли эффективно лизировать клетки рака легких, которые естественно экспрессировали CDC45L и HLA-А24. Данные результаты свидетельствуют о том, что эти три полученные из CDC45L пептида могут быть естественным образом процессированы и представлены в контексте HLA-А24-молекул в раковых клетках.
Для подтверждения того, что ЦТЛ, специфичные для трех полученных из CDC45L пептидов, распознают клетки-мишени HLA класса I-рестриктированным образом, mAb, специфичное для HLA класса I (W6/32), было использовано для блокировки распознавания ЦТЛ. Продукция IFN-гамма и цитотоксичности значительно ингибировались при помощи блокирования mAb против HLA класса I, но не при помощи контрольного mAb против HLA класса II (Фигуры 6A и B). Данные результаты ясно показывают, что эти индуцированные ЦТЛ рспознают клетки-мишени, экспрессирующие эндогенный CDC45L, HLA класса I-рестриктированным образом.
Пептид CDC45L-9-556-4(SEQ ID NO: 4), 556KFLDALISL564, может индуцировать ЦТЛ, рестриктированные как HLA-A2 (А*0201), так и HLA-А24 (А*2402)
Пептид CDC45L-A2-9-556-4(SEQ ID NO: 4, также упоминаемый в настоящем документе как CDC45L-А24-9-556-4), 556KFLDALISL564, как предсказано, обладал высокой аффинностью связывания не только с HLA-А24 (А*2402), но и с HLA-A2 (А*0201), в соответствии с программным обеспечением SYFPEITHI (Институт Иммунологии, Университет Тюбингена, Тюбинген, Германия, www.syfpeithi.de/) для предсказания связывания HLA с пептидами. HLA-A*2402 является наиболее распространенной аллелью HLA класса I среди японского населения, и HLA-A*0201 является одной из наиболее обычных аллелей HLA в различных этнических группах, включая азиатов, африканцев, афро-американцев и европейцев (Browning M et al. Immunol Today 1996; 17: 165-70). Таким образом, была выдвинута гипотеза о том, что пептид CDC45L-A2-9-556-4(SEQ ID NO: 4) является обычным ЦТЛ=эпитопом-кандидатом, рестриктированным как HLA-A2, так и HLA-А24. Для того чтобы определить, может ли пептид CDC45L-A2-9-556-4(SEQ ID NO: 4) связываться с молекулами HLA-A2, был проведен анализ стабилизации HLA-A2 с клетками T2, как описано ранее (Yokomine K et al., Int J Cancer 2009; 126: 2153-63). Пептид CDC45L-A2-9-556-4(SEQ ID NO: 4) связывался с молекулами HLA-A2 с улучшенной способностью стабилизации HLA-A2 по сравнению с пептидом HIV-A2, который использовался в качестве положительного контроля (данные не приведены). Таким образом, было подтверждено действительное связывание пептида с HLA-A2.
Далее, CDC45L-A2-9-556-4(SEQ ID NO: 4)-специфические ЦТЛ из PBMC здорового донора, положительного по HLA-A2 (А*0201), были образованы путем стимуляции пептидом CDC45L-A2-9-556-4(SEQ ID NO: 4). Линии ЦТЛ, образованные от HLA-A2-положительного здорового донора, продуцировали IFN-гамма конкретно в ответ на повторное стимулирование клетками T2, подвергнутых импульсному воздействию пептидом (Фиг. 7A). Кроме того, образованные линии ЦТЛ проявляли цитотоксичность в отношении клеток T2, подвергнутых импульсному воздействию пептида CDC45L-A2-9-556-4(SEQ ID NO: 4), но не в отношении клеток T2, нагруженных посторонним пептидом HIV-A2, или клеток C1R-A2402, нагруженных пептидом CDC45L-A2-9-556-4(SEQ ID NO: 4) (Фиг. 7B). Данные результаты показывают, что эти ЦТЛ обуславливали пептид-специфическую цитотоксичность HLA-A2-рестриктированным образом. Кроме того, образованные линии ЦТЛ могли эффективно лизировать клетки Panc1, которые экспрессировали эндогенные молекулы CDC45L и HLA-A2 А0201), но не HLA-А24, и цитотоксичность значительно подавлялась путем блокирования mAb против HLA класса I (W6/32), но не контрольным mAb против HLA класса II, как определено путем анализа высвобождения 51Cr (Фиг. 7C).
Эти результаты ясно показывают, что пептид CDC45L-A2-9-556-4(SEQ ID NO: 4) естественным образом процессировался из белка CDC45L и был представлен не только в контексте HLA-А24, но и в контексте HLA-A2 для распознавания ЦТЛ, индуцированных пептидом CDC45L-A2-9-556-4(SEQ ID NO: 4) (Фиг. 5, 6 и Фиг. 7). Таким образом, CDC45L-A2-9-556-4(SEQ ID NO: 4) является обычным ЦТЛ-эпитопом, рестриктированным как HLA-A2, так и HLA-А24, и этот пептид будет применяться для иммунотерапии более чем 80% японских пациентов с раком, экспрессирующим CDC45L.
Противоопухолевая активность in vivo ЦТЛ человека, реагирующих на CDC45L, у мышей NOD/SCID.
Для оценки терапевтической эффективности прививки ЦТЛ, реагирующих на CDC45L, в иммунодефицитных мышах, имплантированных CDC45L-положительными клетками рака легких человека, клетки Lu99 подкожно прививали мышам NOD/SCID. После 7 дней, когда размеры опухоли достигали примерно 5×5 мм, мышам внутривенно вводили ЦТЛ человека, образованные стимулированием CD8+Т-клеток с помощью аутологичных DC, полученных из моноцитов, (день 0) и аутологичных PHA-бластов (дни 7 и 14), подвергнутых импульсному воздействию смеси пептидов CDC45L-А24-9-109-2(SEQ ID NO: 2), CDC45L-А24-9-294-3(SEQ ID NO: 3) и CDC45L-А24-9-556-4(SEQ ID NO: 4) или постороннего пептида HIV-А24. Перед вакцинацией мышам ЦТЛ оценивали пептид-специфическую цитотоксическую активность ЦТЛ (Фиг. 8). Линии ЦТЛ, образованные от двух здоровых доноров, которые были HLA-А24 положительными, продуцировали IFN-гамма конкретно в ответ на повторную стимуляцию клетками C1R-A2402, подвергнутых импульсному воздействию пептидов, за исключением пептида CDC45L-А24-9-294-3(SEQ ID NO: 3) в здоровом доноре-5 (Фиг. 8A). Кроме того, смесь пептидов CDC45L вызывала ЦТЛ, которые могли эффективно лизировать клетки Lu99, и цитотоксичность значительно подавлялась путем блокирования mAb, специфичным для HLA класса I в анализе высвобождения 51Cr (Фиг. 8B). С другой стороны, линии ЦТЛ проявляли специфический лизис в отношении C1R-A2402, подвергнутых импульсному воздействию пептидом CDC45L-А24-9-109-2(SEQ ID NO: 2), но не в отношении C1R-A2402, подвергнутых импульсному воздействию пептидами CDC45L-А24-9-294-3(SEQ ID NO: 3), CDC45L-А24-9-556-4(SEQ ID NO: 4) или посторонним пептидом HIV-А24 у обоих здоровых доноров-4 и -5 (Фиг. 8C).
Опухоли у мышей, привитых CDC45L-стимулированными ЦТЛ (n=5; среднее+/-стандартное отклонение [SD], 108+/-65 мм2), были значительно меньше, чем у мышей, привитых CD8+Т-клетками, индуцированными контрольным HIV-пептидом (n=5; среднее +/ SD, 271+/-94 мм2) или одним PBS (n=5; среднее +/- SD, 297+/-44 мм2) на 42 день после прививки от клеток Lu99 (двусторонний t-тест Стьюдента, *P<0,05, **P<0,01; Фиг. 8D). Результаты ясно указывают на эффективность трансфертной терапии CDC45L-специфических ЦТЛ человека в отношении CDC45L-положительных опухолей человека у мышей NOD/SCID.
В заключение, предлагается, что антиген CDC45L является высокоиммуногенной и перспективной мишенью для основанной на пептидах иммунотерапии рака легких без вызывания аутоиммунных явлений.
Обсуждение
В текущем исследовании с помощью анализа на основе кДНК-микрочипов рака легких был идентифицирован новый ОСА, Cell division cycle 45-like (CDC45L). Данные микрочипов показали, что CDC45L сверхэкспрессировался в раке предстательной железы, молочной железы и мочевого пузыря, а также в раке легкого. В соответствии с данными, полученными из анализа на основе кДНК-микрочипов экспрессии гена CDC45L в раковых тканях легких, экспрессия гена CDC45L была обнаружена в каждой из 4 раковых тканях легких, но не в их нормальных аналогах. Кроме того, экспрессия CDC45L была едва различима во многих жизненно важных органах, за исключением семенников, в анализах RT-PCR и Нозерн-блот нормальных тканей. Эти результаты свидетельствуют о том, что нацеливание на CDC45L может представлять собой новый иммунотерапевтический подход для этих раковых заболеваний, без вызывания аутоиммунных расстройств.
Также было установлено, что полученные из CDC45L иммуногенные пептиды CDC45L-А24-9-109-2, CDC45L-А24-9-204-3 и CDC45L-А24-9-556-4 могли индуцировать эпитоп-специфические ЦТЛ у мышей BALB/c, иммунизированных пептидами, эмульгированными в неполном адъюванте Фрейнда (данные не представлены). Мыши BALB/c, иммунизированные полученными из CDC45L и H2-Kd-рестриктированными пептидами CDC45L-А24-9-109-2 и CDC45L-А24-9-204-3, не проявляли патологических изменений, таких как инфильтрация лимфоцитов или разрушение тканей, и не обладали никакими признаками аутоиммунных заболеваний, такими как потеря массы, диарея и кожные нарушения, в течение долговременного периода наблюдения (неопубликованные данные). Эти результаты также показали, что полученные из CDC45L пептиды могли индуцировать in vivo реагирующие на пептид ЦТЛ без вызывания аутоиммунных расстройств у мышей.
Хорошо известно, что CDC45L играет важную роль в стадиях инициации и элонгации при репликации ДНК, поэтому потери CDC45L с трудом происходят в раковых клетках. В предыдущем исследовании Pollok et al. показали, что уровень белка CDC45L был стабильно выше у клеток человека, полученных из рака, по сравнению с первичными клетками человека, и экспрессия CDC45L тесно связана с пролиферирующими клеточными популяциями (Pollk S, et al. FEBS J 2007; 274: 3669-3684.). Дополнительные предыдущие исследования позволили предположить, что активация CDC45L зависит от степени дисплазии и состояния лимфатических узлов (Li JN, et al. BMC Cancer 2008, 395: 1-8). Кроме того, Feng с сотрудниками недавно сообщили, что подавление экспрессии гена CDC45L специфической si-RNA заметно сдерживало рост раковых линий клеток, таких как клетки Hela и HepG2, что позволило предположить, что CDC45L является пригодной мишенью для противоопухолевой терапии (Feng D, et al. Cancer Res 2003; 63: 7356-7364). В недавнем докладе было обобщено, что реальная скорость ответа противораковой вакцины в клинических испытаниях была низкой (2,6%) (Rosenberg S A, et al. Nat Med 2004; 10: 909-15). Одна из возможных причин состоит в том, что иммунное избежание раковых клеток, относящееся к делетированию, мутированию или подавлению ОСА, возникает как следствие терапевтически направляемой иммунной селекции. На основе той точки зрения, что опухолевые клетки не могут утратить антигены, которые необходимы для онкогенеза, CDC45L рассматривается в качестве возможного ОСА-кандидата, пригодного для противоопухолевой иммунотерапии. В настоящем изобретении было выявлено пять HLA-А24-рестриктированных CDC45L-эпитопных пептидов, CDC45L-А24-9-109-2, CDC45L-А24-9-294-3, CDC45L-А24-9-556-4, CDC45L-А24-9-370-7 и CDC45L-А24-10-556-12, которые могли образовывать HLA-А24-рестриктированные ЦТЛ человека из PBMC путем in vitro-стимуляции пептидами. Кроме того, было обнаружено, что CDC45L-реактивные ЦТЛ также могут образовываться из PBMC, выделенных из пациентов с раком легких, путем стимулирования этими 5 пептидами. Для четырех CDC45L-эпитопных пептидов, CDC45L-А24-9-109-2, CDC45L-А24-9-294-3, CDC45L-А24-9-556-4 и CDC45L-А24-9-370-7, пептид-индуцированные ЦТЛ могли уничтожать не только клетки C1R-А*2402, подвергнутые импульсному воздействию родственным пептидом, но и раковые линии клеток, экспрессирующие CDC45L HLA-А24-рестриктированным образом. Эти данные позволяют предположить, что такие CDC45L-пептиды естественным образом процессируются из белка CDC45L в раковых клетках и представляются на поверхности клеток в контексте HLA-А24-молекул, чтобы быть распознанными ЦТЛ. HLA-А24 (А*2402), как известно, является одной из наиболее обычных HLA-аллелей у японского населения, с частотой встречаемости антигена, по оценкам, 60%, и также встречается у европейцев, с частотой встречаемости антигена, по оценкам, 10%. Также было предложено определение HLA-А24-рестриктированных и полученных из CDC45L ЦТЛ-эпитопов для применения при иммунотерапии многих пациентов с раком легких, во всем мире, особенно в Азии (Date, Y., et al. Tissue Antigens, 1996; 47: 93-101).
В заключение, результаты, раскрытые в настоящем документе, предполагают, что CDC45L представляет собой новый ОСА, эпитопные пептиды которого могут вызывать ЦТЛ, которые могут уничтожать раковые клетки, экспрессирующие как CDC45L, так и HLA-А24. Поскольку CDC45L сильно экспрессируется в нескольких видах злокачественных новообразований человека, в том числе в раковых опухолях легких, предстательной железы, молочной железы и мочевого пузыря, то было высказано предложение, что CDC45L является перспективной мишенью основанной на пептидах иммунотерапии злокачественных заболеваний, описанных выше, без вызывания каких-либо аутоиммунных явлений.
Промышленная применимость
Настоящее изобретение представляет новые ОСА, в особенности полученные из CDC45L, которые могут индуцировать сильные и специфические противоопухолевые иммунные ответы и имеют применимость для широкого спектра типов раковых опухолей. Такие ОСА могут найти применение в качестве пептидных вакцин против заболеваний, связанных с CDC45L, например, рака, неограничивающие примеры которого включают опухоль яичка, рак поджелудочной железы, рак мочевого пузыря, немелкоклеточный рак легкого, мелкоклеточный рак легкого, рак молочной железы, рак пищевода, рак предстательной железы, хронический миелоидный лейкоз (ХМЛ), опухоль мягких тканей, рак желудка, гепатобилиарный рак и рак прямой кишки.
Все патенты, патентные заявки и публикации, цитируемые в настоящем документе, включены в качестве ссылки в полном объеме.
Кроме того, несмотря на то, что настоящее изобретение подробно описано в настоящем документе и с учетом конкретных вариантов его осуществления, следует понимать, что вышеприведенное описание носит примерный и разъяснительный характер и предназначено для иллюстрации настоящего изобретения и его предпочтительных вариантов осуществления. Путем проведения рутинных экспериментов любой специалист в рассматриваемой области без труда признает, что различные изменения и модификация могут быть сделаны без отступления от духа и области применения настоящего изобретения, пределы и границы которого определены в прилагаемых пунктах формулы изобретения.
| название | год | авторы | номер документа |
|---|---|---|---|
| МОДИФИЦИРОВАННЫЕ ПЕПТИДЫ MELK И СОДЕРЖАЩИЕ ИХ ВАКЦИНЫ | 2011 |
|
RU2580035C2 |
| ПЕПТИДЫ FOXM1 И ВАКЦИНЫ, СОДЕРЖАЩИЕ ИХ | 2010 |
|
RU2560431C2 |
| CDCA1 ЭПИТОП-ПЕПТИДЫ И СОДЕРЖАЩИЕ ИХ ВАКЦИНЫ | 2009 |
|
RU2502740C2 |
| ПЕПТИДЫ HJURP И СОДЕРЖАЩИЕ ИХ ВАКЦИНЫ | 2011 |
|
RU2570560C2 |
| ЭПИТОПНЫЕ ПЕПТИДЫ RAB6KIFL/KIF20A И СОДЕРЖАЩИЕ ИХ ВАКЦИНЫ | 2009 |
|
RU2532105C2 |
| CDH3-ПЕПТИД И ВКЛЮЧАЮЩЕЕ ЕГО ЛЕКАРСТВЕННОЕ СРЕДСТВО | 2008 |
|
RU2483078C2 |
| ПЕПТИДЫ ТОРК И СОДЕРЖАЩИЕ ИХ ВАКЦИНЫ | 2012 |
|
RU2633503C2 |
| HLA-A*3303-РЕСТРИКТИРОВАННЫЙ ПЕПТИД WT1 И СОДЕРЖАЩАЯ ЕГО ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 2007 |
|
RU2435782C2 |
| ПЕПТИД, ПОЛУЧЕННЫЙ ИЗ URLC10, И СОДЕРЖАЩАЯ ЕГО ВАКЦИНА | 2015 |
|
RU2700881C2 |
| ПЕПТИД, ПОЛУЧЕННЫЙ ИЗ KOC1, И СОДЕРЖАЩАЯ ЕГО ВАКЦИНА | 2015 |
|
RU2699542C2 |









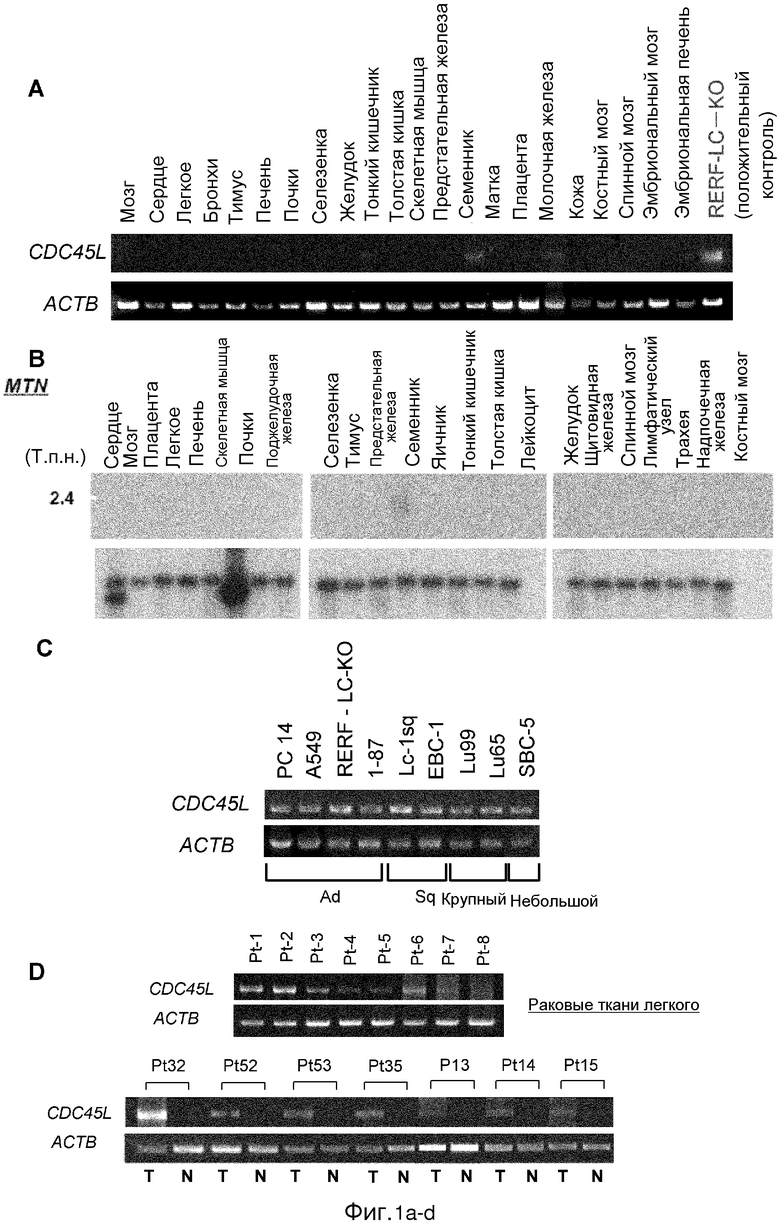

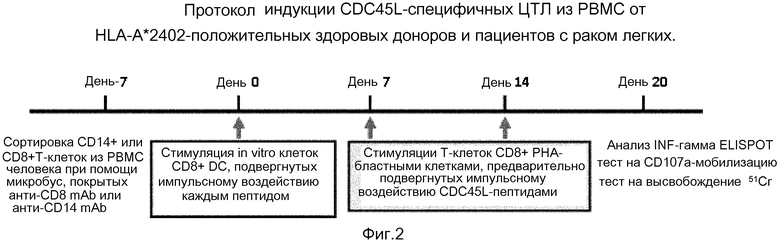


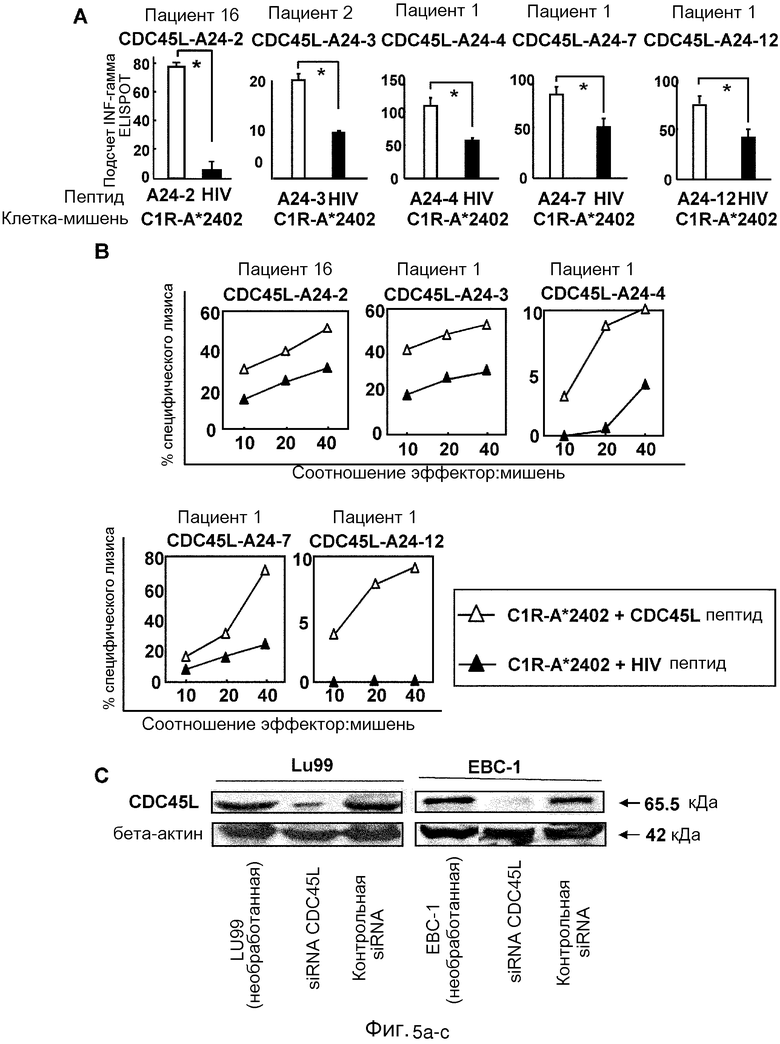
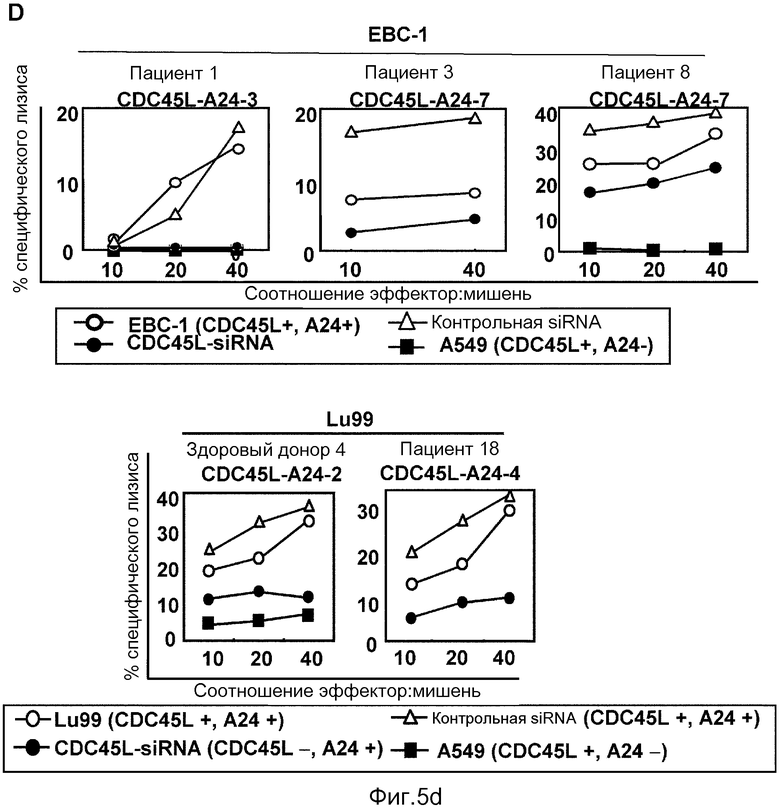




Настоящее изобретение относится к области иммунологии. Предложен выделенный пептид, представляющий собой фрагмент белка CDC45L и обладающий способностью индуцировать цитотоксические Т-лимфоциты в форме комплекса с молекулой HLA-A*2402 или HLA-A*0201. Также рассмотрены полинуклеотид, кодирующий пептид по изобретению; композиция для индуцирования цитотоксического лимфоцита (CD8-положительной Т-клетки, ЦТЛ) в присутствии антигенпредставляющей клетки (АПК); фармацевтическая композиция для лечения и/или профилактики CDC45L-экспрессирующих раков и/или предупреждения их послеоперационных рецидивов; способы индуцирования АПК и ЦТЛ; выделенная АПК, которая представляет на своей поверхности комплекс HLA-антигена и пептида по изобретению; способ индуцирования иммунного ответа против CDC45L-экспрессирующего рака у субъекта; вектор для экспрессирования пептида по изобретению и трансформированная или трансфицированная им клетка-хозяин; а также применение пептида по изобретению и АПК в изготовлении фармацевтической композиции для лечения или предупреждения CDC45L-экспрессирующего рака. Данное изобретение может найти дальнейшее применение в терапии онкологических заболеваний. 14 н. и 2 з.п. ф-лы, 8 ил., 2 табл.
1. Выделенный пептид, обладающий способностью индуцировать цитотоксические Т-лимфоциты, где данный пептид выбран из группы, состоящей из
(a) пептида, состоящего из аминокислотной последовательности SEQ ID NO: 2, 3, 7 или 12, и
(b) пептида, состоящего из аминокислотной последовательности SEQ ID NO: 4,
причем если указанный пептид представляет собой (а), то данный пептид обладает способностью индуцировать ЦТЛ в форме комплекса с HLA-A*2402, а если указанный пептид представляет собой (b), то данный пептид обладает способностью индуцировать ЦТЛ в форме комплекса с HLA-A*2402 или HLA-A*0201.
2. Выделенный пептид, обладающий способностью индуцировать ЦТЛ в форме комплекса с HLA-A*2402, где указанный пептид состоит из аминокислотной последовательности, обладающей одной или обеими из следующих характеристик:
(a) вторая аминокислота с N-конца аминокислотной последовательности SEQ ID NO: 4, 2, 3, 7 или 12 модифицирована, чтобы представлять собой аминокислоту, выбранную из группы, состоящей из фенилаланина, тирозина, метионина и триптофана, и
(b) С-концевая аминокислота аминокислотной последовательности SEQ ID NO: 4, 2, 3, 7 или 12 модифицирована, чтобы представлять собой аминокислоту, выбранную из группы, состоящей из фенилаланина, лейцина, изолейцина, триптофана и метионина.
3. Выделенный пептид, обладающий способностью индуцировать ЦТЛ в форме комплекса с HLA-А*0201, где указанный пептид состоит из аминокислотной последовательности, обладающей одной или обеими из следующих характеристик:
(a) вторая аминокислота с N-конца аминокислотной последовательности SEQ ID NO: 4 модифицирована, чтобы представлять собой аминокислоту, выбранную из группы, состоящей из лейцина и метионина; и
(b) С-концевая аминокислота аминокислотной последовательности SEQ ID NO: 4 модифицирована, чтобы представлять собой аминокислоту, выбранную из группы, состоящей из валина и лейцина.
4. Выделенный полинуклеотид, кодирующий пептид по любому из пп.1-3.
5. Композиция для индуцирования ЦТЛ в присутствии антигенпредставляющей клетки (АПК), экспрессирующей HLA-антиген, где композиция содержит 0,001-1000 мг одного или нескольких пептида(ов), описанных в любом из пп.1-3, в которой если указанный пептид представляет собой (а) по п.1 или 2, указанный HLA-антиген представляет собой HLA-A*2402; если указанный пептид представляет собой (b) по п.1, указанный HLA-антиген представляет собой HLA-A*2402 или HLA-A*0201; и если указанный пептид представляет собой пептид по п.3, указанный HLA-антиген представляет собой HLA-A*0201.
6. Фармацевтическая композиция для лечения и/или профилактики CDC45L-экспрессирующих раков и/или предупреждения их послеоперационных рецидивов, где фармацевтическая композиция содержит 0,001-1000 мг одного или нескольких пептида(ов), описанных в любом из пп.1-3, в которой указанная фармацевтическая композиция составлена для введения субъекту, чей HLA-антиген представляет собой HLA-A*2402, если указанный пептид представляет собой (а) по п.1 или 2; составлена для введения субъекту, чей HLA-антиген представляет собой HLA-A*2402 или HLA-A*0201, если указанный пептид представляет собой (b) по п.1; и составлена для введения субъекту, чей HLA-антиген представляет собой HLA-A*0201, если указанный пептид представляет собой пептид по п.3.
7. Фармацевтическая композиция по п.6, составленная для лечения рака.
8. Способ индуцирования антигенпредставляющих клеток (АПК) со способностью индуцировать ЦТЛ, где способ включает стадию, выбранную из группы, состоящей из следующего:
(a) контактирование АПК с пептидом по любому из пп.1-3 in vitro, ex vivo и in vivo, и
(b) введение полинуклеотида, кодирующего пептид по любому из пп.1-3 в экспрессируемой форме, в АПК,
где указанная АПК экспрессирует HLA-A*2402, если указанный пептид представляет собой (а) по п.1 или 2; экспрессирует HLA-А*2402 или HLA-A*0201, если указанный пептид представляет собой (b) по п.1; и экспрессирует HLA-A*0201, если указанный пептид представляет собой пептид по п.3.
9. Способ индуцирования ЦТЛ, где способ включает стадию, выбранную из группы, состоящей из следующего:
а) совместное культивирование CD8-положительных Т-клеток с АПК, которые представляют на своей поверхности комплекс HLA-антигена и пептида по любому из пп.1-3, и
(b) совместное культивирование CD8-положительных Т-клеток с экзосомами, которые представляют на своей поверхности комплекс HLA-антигена и пептида по любому из пп.1-3,
где указанная АПК или экзосома экспрессирует HLA-A*2402, если указанный пептид представляет собой (а) по п.1 или 2; экспрессирует HLA-A*2402 или HLA-A*0201, если указанный пептид представляет собой (b) по п.1; и экспрессирует HLA-A*0201, если указанный пептид представляет собой пептид по п.3.
10. Выделенная АПК, которая представляет на своей поверхности комплекс HLA-антигена и пептида по любому из пп.1-3, где указанный HLA-антиген представляет собой HLA-A*2402, если указанный пептид представляет собой (а) по п.1 или 2; HLA-А*2402 или HLA-A*0201, если указанный пептид представляет собой (b) по п.1; и HLA-A*0201, если указанный пептид представляет собой пептид по п.3.
11. АПК по п.10, которая индуцирована при помощи способа по п.8.
12. Способ индуцирования иммунного ответа против CDC45L-экспрессирующего рака у субъекта, где способ включает введение субъекту композиции, содержащей один или несколько пептидов по любому из пп.1-3, в котором указанный рак экспрессирует HLA-А*2402, если указанный пептид представляет собой (а) по п.1 или 2; HLA-A*2402 или HLA-A*0201, если указанный пептид представляет собой (b) по п.1; и HLA-A*0201, если указанный пептид представляет собой пептид по п.3.
13. Вектор для экспрессирования пептида по любому из пп.1-3, содержащий нуклеотидную последовательность, кодирующую пептид по любому из пп.1-3.
14. Клетка-хозяин для поддержания вектора по п.13 или экспрессирования пептида по любому из пп.1-3, трансформированная или трансфицированная экспрессионным вектором по п.13.
15. Применение пептида по любому из пп.1-3 в изготовлении фармацевтической композиции для лечения или предупреждения CDC45L-экспрессирующего рака, где указанная АПК и рак экспрессируют HLA-A*2402, если указанный пептид представляет собой (а) по п.1 или 2; HLA-A*2402 или HLA-A*0201, если указанный пептид представляет собой (b) по п.1; и HLA-A*0201, если указанный пептид представляет собой пептид по п.3.
16. Применение АПК, представляющей пептид по любому из пп.1-3 на своей поверхности, в изготовлении фармацевтической композиции для лечения или предупреждения CDC45L-экспрессирующего рака, где указанная АПК и рак экспрессируют HLA-A*2402, если указанный пептид представляет собой (а) по п.1 или 2; HLA-A*2402 или HLA-А*0201, если указанный пептид представляет собой (b) по п.1; и HLA-A*0201, если указанный пептид представляет собой пептид по п.3.
| SHAIKH T.H | |||
| et al | |||
| Железобетонный фасонный камень для кладки стен | 1920 |
|
SU45A1 |
| Пресс для выдавливания из деревянных дисков заготовок для ниточных катушек | 1923 |
|
SU2007A1 |
| SAHA P | |||
| et al., "The human homolog of Saccharomyces cerevisiae CDC45", Journal of Biological Chemistry, 1998; 273(29): 18205-18209 | |||
| KOMORI H | |||
| et | |||
Авторы
Даты
2015-09-10—Публикация
2010-05-25—Подача