Изобретение относится к технологии переработки химических концентратов природного урана, включающей выщелачивание (растворение) химических концентратов природного урана азотной кислотой, экстракционный аффинаж нитрата уранила, химическую денитрацию нитрата уранила через осаждение аммиаком полиуранатов аммония с получением маточника, содержащего нитрат аммония, термическое разложение полиуранатов аммония до триоксида урана, его восстановление, гидрофторирование до тетрафторида урана и фторирование до гексафторида урана. Химические концентраты природного урана (ХКПУ), в основном, представлены соединениями урана: UO2, U3O8, UO3, Na2U2O7, (NH4)2U2O7 и UO4.
Недостаток данной технологии состоит в том, что нитрату аммония - продукту химической денитрации нитрата уранила, из-за опасности его загрязнения ураном невозможно найти применения в гражданских отраслях промышленности.
Для проведения процесса экстракционного аффинажа ХКПУ предварительно растворяют в азотной кислоте по реакциям:
3UO2+8HNO3=3UO2(NO3)2+2NO+4H2O
UO2+4HNO3=UO2(NO3)2+2NO2+2H2O
3U3O8+20HNO3=9UO2(NO3)2+3NO+10H2O
UO3+2HNO3=UO2(NO3)2+H2O
Na2U2O7+6HNO3=2UO2(NO3)2+2NaNO3+3H2O
(NH4)2U2O7+6HNO3=2UO2(NO3)2+2NH4NO3+3H2O
UO4+2HNO3=UO2(NO3)2+H2O+1/2O2
В результате растворения уран, находящийся в ХКПУ в виде различных соединений, переходит в нитрат уранила.
После экстракционной очистки нитрата уранила проводят аммиачное осаждение полиуранатов аммония по реакции:
UO2(NO3)2+2NH4OH=0,5(NH4)2U2O7+2NH4NO3+H2O
Задача состоит в использовании нитрата аммония, появляющегося в процессе аммиачного осаждения, для нитрования химических концентратов природного урана с получением нитрата уранила.
Известен способ переработки облученного ядерного топлива [патент РФ №2366012, МПК G21F 9/28, опубл. 27.08.2009, бюл. №24], по которому UO2 обрабатывается диоксидом азота с добавлением стехиометрического (из расчета получения гексагидрата нитрата уранила) количества воды. В этом процессе U(IV) окисляется и переходит в нитрат. Достоинство способа состоит в проведении нитрования UO2 нитрующим агентом без использования азотной кислоты.
Недостаток способа состоит в том, что нет рентабельной технологии получения диоксида азота из нитрата аммония.
Известна твердофазная реакция [Meera Keskar, Vittal Rao T.V., Sali S.K. Solid state reactions of UO2, ThO2 and (U, Th)O2 with ammonium nitrate // Thermo-chimica Acta, 20 October 2010, V. 510, I. 1-2, P. 68-74] (прототип) между UO2 и нитратом аммония, в результате которой UO2 нитруется с образованием двойных солей нитрата уранила с нитратом аммония:
5UO2+22NH4NO3=5(NH4)2UO2(NO3)4+N2+12NH3
5UO2+17NH4NO3=5NH4UO2(NO3)3+N2+12NH3
Для нитрования UO2 спекали с NH4NO3 в различных соотношениях, повышая температуру до 400°C на воздухе. Конечные продукты при 400°C были определены как U3O8 и UO3. В процессе твердофазной реакции были идентифицированы промежуточные продукты в виде двойных солей (NH4)2UO2(NO3)4 и NH4UO2(NO3)3, образовавшихся при 180 и 220°C.
Достоинство способа, взятого за прототип, состоит в использовании нитрата аммония в качестве нитрующего агента при нитровании диоксида урана для получения нитрата уранила в виде двойной соли.
Недостаток данного способа состоит во взрывоопасности реагента - безводной соли нитрата аммония и низком выходе UO2 в нитрат уранила.
Задачей изобретения является снижение взрывоопасности процесса и увеличение выхода нитрата уранила.
Поставленную задачу решают тем, что в способе получения нитрата уранила, включающем нитрование соединений урана нитрующим агентом, соединения урана, такие как: оксиды урана, полиуранаты натрия, полиуранаты аммония или пероксид урана переводят в нитрат уранила обработкой водным раствором нитрата аммония и спеканием полученных смесей в интервале температур 200-350°C.
Используют водный раствор нитрата аммония концентрацией 2-9 моль/л.
Полученную смесь оксидов урана и нитрата уранила растворяют в азотной кислоте или в азотнокислых рафинатах от экстракционного аффинажа урана.
Известно, что «…влажная соль, содержащая более 3% воды, не взрывается даже при взрыве детонатора…» [Позин М.Е., Технология минеральных солей (удобрений, пестицидов, промышленных солей, окислов и кислот). Л.: Химия, 1974, ч. 2, с. 1183]. Однако неизвестно, как пойдет нитрование ХКПУ, если парогазовая фаза кроме продуктов термического разложения будет содержать пары воды.
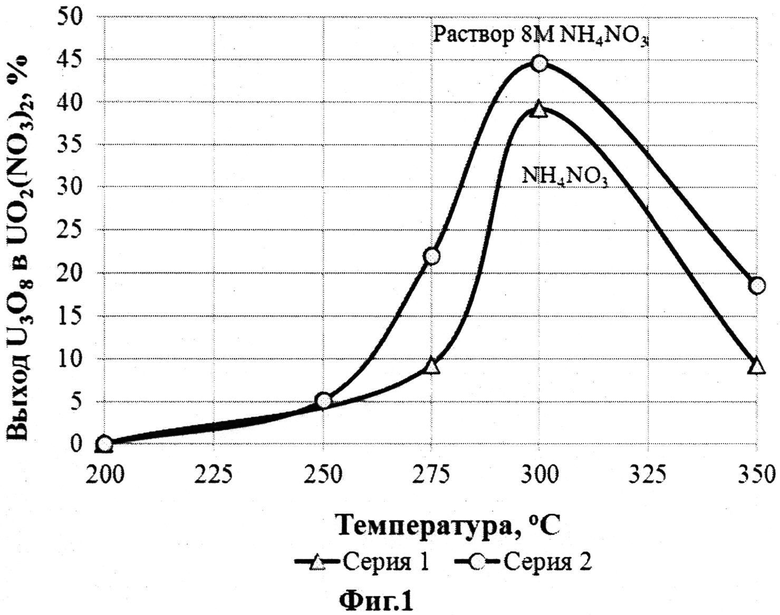
На фигуре 1 представлена зависимость выхода U3O8 в UO2(NO3)2 от агрегатного состояния нитрата аммония.
Способ осуществляют следующим образом.
Пример 1.
Известно, что октаоксид триурана в химических реакциях ведет себя как смесь оксидов UO2 и UO3 [Технология урана: учебное пособие / А.А. Маслов, Г.В. Каляцкая, Г.Н. Амелина, А.Ю. Водянкин, Н.Б. Егоров - Томск: Издательство Томского политехнического университета, 2007. - С. 17]. Поэтому для интегральной оценки результатов реакции с нитратом аммония сразу UO2 и UO3 в качестве исходного оксида был взят U3O8.
К U3O8 добавляли NH4NO3 в стехиометрическом соотношении, рассчитанном из уравнения нитрования:
U3O8+6,4NH4NO3+3,2H2O=3UO2(NO3)2+0,2N2+6,4NH4OH.
Было поставлено две серии опытов. В первой серии NH4NO3 вводили в виде соли (как в прототипе), во второй серии NH4NO3 вводили в виде водного раствора с [NH4NO3]=8 моль/л.
Смеси выдерживали при заданной температуре. Охлажденные спеки полностью растворяли в 3,0 М HNO3 с расходом 1,0 л на 0,2 кг U3O8.
По содержанию азотной кислоты в полученных растворах рассчитывали выход урана в нитрат уранила. Полученные результаты представлены на фиг.1.
Из зависимости на фиг.1 видно, что нитрование U3O8 прошло в обеих сериях. UO2(NO3)2 начинает появляться, начиная с температуры спекания 200°C. Выход U3O8 в UO2(NO3)2 достигает максимума при температуре 300°C и при дальнейшем увеличении температуры снижается.
Из сравнения результатов нитрования двух серий видно, что выход U3O8 в UO2(NO3)2 выше во второй серии, в которой нитрат аммония использовался в виде 8M раствора.
Таким образом, результаты нитрования U3O8 показали, что замена соли на раствор увеличивает выход U3O8 в UO2(NO3)2. Кроме того, раствор является взрывобезопасным.
Пример 2.
Провели нитрование разных соединений урана, входящих в состав химических концентратов природного урана, растворяемых в процессе аффинажа урана: триоксида урана, полиуранатов аммония и натрия, пероксида урана.
Нитрование провели 8M раствором NH4NO3. Расход соответствовал стехиометрическому: на 1 моль урана вводили 2 моля NH4NO3.
Результаты нитрования сведены в таблицу 1.
Из таблицы 1 видно, что ХКПУ нитруются 8M раствором NH4NO3, при этом нитрование ХКПУ начинается со 150-200°C. Максимальный выход урана в UO2(NO3)2 наблюдается при температуре 300°C.
В дополнительных опытах было установлено, что изменение концентрации нитрата аммония в растворе в интервале 2-9 моль/л несущественно сказывается на выходе урана в UO2(NO3)2, но приводит к изменению концентрации аммиака в конденсате, который может быть рециклирован для повторного использования при химической денитрации нитрата уранила.
Кроме того, было установлено, что UO2(NO3)2 можно растворять в азотнокислых рафинатах от экстракционного аффинажа химических концентратов природного урана.
Таким образом, предложенный способ нитрования соединений урана позволяет увеличить выход оксидов урана в нитрат уранила, позволяет провести нитрование полиуранатов натрия и аммония и пероксида урана, что позволяет утилизировать нитрат аммония, появляющийся в процессе химической денитрации нитрата уранила, и использовать рафинат от экстракционного аффинажа урана. Кроме того, данный способ позволил отказаться от применения взрывоопасной соли нитрата аммония, заменив ее на взрывобезопасный водный раствор.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ЭКСТРАКЦИОННОГО АФФИНАЖА УРАНА | 2013 |
|
RU2554830C2 |
| СПОСОБ ЭКСТРАКЦИОННОГО АФФИНАЖА УРАНА | 2005 |
|
RU2295168C1 |
| СПОСОБ ПОЛУЧЕНИЯ ОКСИДОВ УРАНА | 2015 |
|
RU2603359C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПОРОШКА ДИОКСИДА УРАНА | 2013 |
|
RU2542317C2 |
| СПОСОБ ПЕРЕРАБОТКИ УРАН-МОЛИБДЕНОВОЙ КОМПОЗИЦИИ | 2009 |
|
RU2395857C1 |
| СПОСОБ ПОЛУЧЕНИЯ ОКСИДОВ УРАНА | 2013 |
|
RU2554636C1 |
| СПОСОБ ПЕРЕРАБОТКИ УРАНСОДЕРЖАЩИХ РАСТВОРОВ | 1999 |
|
RU2174492C2 |
| СПОСОБ ПОЛУЧЕНИЯ СМЕШАННОГО ТОПЛИВА, СОДЕРЖАЩЕГО УРАН И ПО МЕНЬШЕЙ МЕРЕ, ОДИН АКТИНИД И/ИЛИ ЛАНТАНИД С ИСПОЛЬЗОВАНИЕМ КАТИОНООБМЕННОЙ СМОЛЫ | 2009 |
|
RU2516282C2 |
| СПОСОБ КОНТРОЛЯ ОКСИДОВ УРАНА UO И UO НА ПРИМЕСИ | 2015 |
|
RU2605456C1 |
| СПОСОБ ПОЛУЧЕНИЯ СМЕСИ ПОРОШКООБРАЗНЫХ ОКСИДОВ МЕТАЛЛОВ ИЗ НИТРАТОВ МЕТАЛЛОВ В ЯДЕРНОЙ ПРОМЫШЛЕННОСТИ | 1996 |
|
RU2175643C2 |
Изобретение относится к технологии переработки химических концентратов природного урана. Способ получения нитрата уранила включает обработку водным раствором нитрата аммония соединений урана таких как: оксиды урана, полиуранаты натрия, полиуранаты аммония или пероксид урана, и спекание полученных смесей в интервале температур 200-350°C. Изобретение обеспечивает увеличение выхода нитрата уранила и снижение взрывоопасности процесса. 2 з.п. ф-лы, 1 ил., 1 табл., 1 пр.
1. Способ получения нитрата уранила, включающий нитрование соединений урана нитрующим агентом, отличающийся тем, что соединения урана, такие как: оксиды урана, полиуранаты натрия, полиуранаты аммония или пероксид урана переводят в нитрат уранила обработкой водным раствором нитрата аммония и спеканием полученных смесей в интервале температур 200-350°C.
2. Способ по п. 1, отличающийся тем, что используют водный раствор нитрата аммония концентрацией 2-9 моль/л.
3. Способ по п. 1 или 2, отличающийся тем, что полученную смесь оксидов урана и нитрата уранила растворяют в азотной кислоте или в азотнокислых рафинатах от экстракционного аффинажа урана.
| СПОСОБ ПОЛУЧЕНИЯ НИТРАТОВ АКТИНИДОВ (ВАРИАНТЫ) | 2005 |
|
RU2295789C1 |
| СПОСОБ ПЕРЕРАБОТКИ ОБЛУЧЕННОГО ЯДЕРНОГО ТОПЛИВА | 2007 |
|
RU2366012C2 |
| СПОСОБ ЭКСТРАКЦИОННОГО АФФИНАЖА УРАНА | 2005 |
|
RU2295168C1 |
| US 4405567 A, 20.09.1983 | |||
Авторы
Даты
2015-09-20—Публикация
2013-10-08—Подача