УРОВЕНЬ ТЕХНИКИ
(а) Область техники
[001] Настоящее изобретение относится к биоразлагаемым и биоабсорбируемым блок-сополимерам в виде твердого порошка или воскообразного порошка, которые можно легко превратить в водный раствор полимера и которые обладают способностью к обратимому термическому гелеобразованию при воздействии повышенных температур, например при воздействии температуры тела непосредственно перед введением или после него. Предложенные полимеры преимущественно используют, например, при парентеральном введении лекарственных средств.
(b) Описание уровня техники
[002] Биоразлагаемые блок-сополимеры, способные к обратимому термическому гелеобразованию, описаны в патентах США № 6201072, 6117949 и 6004573 на имя Rathi с соавторами и в патенте 5702717 на имя Cha с соавторами. Указанные полимерные композиции при низких температурах существуют в виде жидкого раствора, затем обратимо образуют гели при физиологически релевантных температурах и обеспечивают хорошие характеристики высвобождения лекарственных средств. Такие композиции включают биоразлагаемые блок-сополимеры типа ABA или ВАВ со средней молекулярной массой примерно от 2000 до 4990 и содержат примерно от 51 до 83% по массе гидрофобного полимерного блока А, содержащего биоразлагаемый сложный полиэфир, и примерно от 17 до 49% по массе гидрофильного полимерного блока В, образованного полиэтиленгликолем. В патентах США № 7018645 и 7135190 на имя Piao с соавторами описаны смеси триблок-сополимеров, проявляющих аналогичные свойства обратимого термического гелеобразования.
[003] Указанные полимеры для доставки лекарственного средства проявляют свойства обратимого термического гелеобразования, но, как было обнаружено, с большим трудом образуют водные композиции для доставки лекарственного средства или восстанавливаются с образованием таких композиций. Трудность восстановления указанных композиций требует проведения на предприятии-изготовителе стадии восстановления с целью получения водного продукта для доставки лекарственного средств. После восстановления указанные водные продукты для доставки лекарственного средств, способные к обратимому термическому гелеобразованию, обычно хранят в виде замороженного водного полимерного раствора вплоть до применения. При комнатной температуре водные растворы таких способных к обратимому термическому гелеобразованию полимеров начинают разлагаться. Соответственно, указанные водные композиции для доставки лекарственного средств приходится перевозить и хранить в охлажденном или замороженном состоянии. Ранее известные способные к обратимому термическому гелеобразованию композиции для доставки лекарственного средств, такие как композиции, описанные Rathi с соавторами, демонстрируют хорошую стабильность при хранении и перевозке в замороженной форме. При применении для доставки лекарственного средств полимеры, описанные Rathi с соавторами, можно хранить и перевозить в предварительно заполненных шприцах, готовых для инъекции, или ампулах с продуктом (обычных или двойных). Перед инъекцией шприцы и ампулы размораживают, что занимает от 24 до 48 часов.
[004] Другие триблок-сополимеры типа ABA содержали капролактон и гликолевую кислоту, включенные в гидрофобные блоки наряду с индивидуальными гидрофильными полимерами. См. опубликованную заявку на патент Китая CN 1958074 А. Однако способы синтеза, описанные в этой заявке, не подходят для получения композиции триблок-сополимера с требуемой молекулярной массой и полимерными свойствами. Например, способы синтеза, описанные в указанной заявке, основаны на применении коммерчески доступного мономера полиэтиленгликоля с номинальной молекулярной массой (т.е. 1540 дальтон). Хотя полиэтиленгликоли с удельными номинальными молекулярными массами, отличными от 1540, являются доступными, было обнаружено, что три блока, состоящих из одного полиэтиленгликолевого компонента с одной и той же средней молекулярной массой, не обладают наиболее желательным сочетанием характеристик восстановления, высвобождения лекарственного средства, набухания и растворения для ряда применяемых лекарственных средств и показателей, важных для систем контролируемого высвобождения.
[005] Авторы настоящего изобретения обнаружили, что характеристики высвобождения лекарственного средства, разложения, набухания и растворения значительно зависят от состава термообратимого блок-сополимера. В частности, было обнаружено, что точное регулирование длины гидрофильного полимера, а также состава гидрофобного полимера, является решающим для достижения требуемых характеристик восстановления, высвобождения лекарственного средства, набухания и растворения. Как было обнаружено, известные блок-сополимеры, проявляющие свойства обратимого термического гелеобразования, имеют неудовлетворительные характеристики восстановления, высвобождения лекарственного средства, набухания и/или растворения.
Соответственно, в данной области техники существует потребность в водной биоразлагаемой полимерной композиции для доставки лекарственного средства, способной к обратимому термическому гелеобразованию, которую можно хранить при комнатной температуре и которую можно легко получить или восстановить непосредственно перед применением в течение минимального количества времени, обладающей желаемыми характеристиками высвобождения лекарственного средства, набухания и растворения.
КРАТКОЕ ОПИСАНИЕ ПРЕДПОЧТИТЕЛЬНЫХ ВАРИАНТОВ РЕАЛИЗАЦИИ ИЗОБРЕТЕНИЯ
[006] Были разработаны новые способные к восстановлению блок-сополимеры в форме твердого порошка или порошкообразного парафина, обладающие способностью к термически обратимому гелеобразованию после восстановления. Форма полимеров в виде неводного твердого порошка или воскообразного порошка обеспечивает повышенную стабильность по сравнению с композициями в известном уровне техники и не требует замораживания и/или охлаждения. Такая стабильность позволяет осуществлять хранение при комнатной температуре, что преимущественно исключает необходимость в охлаждении с момента производства до применения продукта. Способные к восстановлению полимеры согласно настоящему изобретению обеспечивают улучшенную технологическую обработку и совместимость с нестабильными и требующими осторожного обращения лекарственными средствами.
[007] Способные к восстановлению полимеры могут быть получены в водной форме непосредственно перед применением и не требуют добавок или нагревания свыше 60°C для их получения в водной форме. Например, способные к восстановлению полимеры можно перевести в водную форму, подходящую для парентерального или внутриопухолевого введения, непосредственно перед применением врачом. Полимеры можно восстановливать непосредственно перед применением путем взбалтывания, например путем перемешивания и/или встряхивания полимера вместе с водой или буфером при слабом нагревании (т.е. ниже 60°C). При необходимости, лекарственное средство можно включить в композицию для доставки лекарственного средств перед восстановлением, во время или после него. Кроме того, лекарственное средство можно включать как часть сухой порошковой композиции.
[008] Уникальные способы синтеза, описанные в настоящей заявке, позволяют точно регулировать физико-химические свойства полимера, такие как температура гелеобразования. Например, температуру гелеобразования восстановленного полимера
можно точно регулировать в диапазоне от 26 до 35°C. Указанный полимер можно получить таким образом, чтобы он имел требуемые характеристики набухания и высвобождения лекарственного средства. Например, при необходимости, набухание полимера может составлять менее чем 5% после 30 дней воздействия водой, при этом полимер может высвобождать примерно от 10 до 15% паклитаксела в течение пяти дней и от 15% до 20% паклитаксела в течение 20 дней. В то время как предшествующие способы синтеза опирались на применение одного коммерчески доступного гидрофильного полимера в качестве строительного блока для блок-сополимеров, некоторые варианты реализации согласно настоящему изобретению позволяют получить высококачественные полимеры на основе применения новых способов синтеза. Как более подробно описано ниже, такие новые способы включают применение двух или более гидрофильных полимеров для получения блок-сополимеров. Авторы изобретения обнаружили, что можно добиться превосходных характеристик восстановления, высвобождения, разложения, набухания и/или растворения при применении в реакции двух гидрофильных полимерных предшественников с различными средними молекулярными массами. Например, в реакции с биоразлагаемыми полиэфир-образующими мономерами можно одновременно использовать первую полимерную композицию полиэтиленгликоля с номинальной молекулярной массой, составляющей 1000 дальтон, и вторую полимерную композицию полиэтиленгликоля с номинальной молекулярной массой, составляющей 1450 дальтон, при различных соотношениях. Рассмотрены и другие комбинации гидрофильных полимерных предшественников. Как показано на прилагаемых чертежах, указанные-уникальные способы синтеза позволяют получить биоразлагаемые полимерные композиции для доставки лекарственного средств, проявляющие способность к обратимому термическому гелеобразованию, которые можно хранить при комнатной температуре и которые можно легко получить или восстановить непосредственно перед применением в течение минимального количества времени, имеющие требуемые характеристики высвобождения лекарственного средства, набухания и растворения.
[009] Способные к восстановлению полимеры согласно настоящему изобретению можно вводить при комнатной температуре, что обеспечивает их универсальное применение в больницах, клиниках или в домашних условиях. Способные к восстановлению полимеры можно подвергать гамма-стерилизации без неблагоприятных эффектов, возникающих в результате разложения или свободнорадикальных реакций. Продукт также можно удобно поставлять в виде комплекта из двух или трех флаконов, заполненных продуктом, в зависимости от применения. Задача настоящего изобретения состоит в обеспечении низкомолекулярных блок-сополимерных систем для доставки
лекарственного средства, которые распределены в стабильной твердой форме, но все еще образуют биоразлагаемые, биоабсорбируемые полимерные растворы при комнатной температуре. Полимерные растворы проявляют свойства обратимого термического гелеобразования, а именно, существуют в виде жидкого раствора при низких температурах, обратимо образуют гели при физиологически релевантных температурах и обеспечивают хорошие характеристики высвобождения лекарственного средства. Полимеры согласно настоящему изобретению могут иметь температуру гелеобразования, которая ниже или соответствует температуре тела, так что после инъекции образуется гель, или полимер можно адаптировать таким образом, чтобы он образовывал гель перед введением.
[0010] Еще одна задача настоящего изобретения заключается в обеспечении системы доставки лекарственного средств для парентерального или внутриопухолевого введения гидрофильных и гидрофобных лекарственных средств, пептидных и белковых лекарственных средств, гормонов, генов/нуклеиновых кислот, олигонуклеотидов и противораковых агентов. Классы противораковых агентов включают, например, алкилирующие агенты, антиметаболиты, антибиотики, гормональные средства, противоваскуляризационные средства или нитрозомочевины.
[0011] Эти и другие задачи выполнимы с помощью блок-сополимерной композиции типа АВ, ABA или ВАВ, при этом блок-сополимер включает по меньшей мере первый блок-сополимерный компонент типа АВ, ABA или ВАВ, содержащий первый гидрофобный А-блок и первый гидрофильный В-блок, причем первый гидрофобный А-блок представляет собой биоразлагаемый сложный полиэфир, содержащий по меньшей мере 60% капролактона и по меньшей мере один второй полиэфир-образующий мономер, и первый гидрофильный В-блок имеет первую среднюю молекулярную массу и содержит полиэтиленгликоль; по меньшей мере второй блок-сополимерный компонент типа АВ, ABA или ВАВ, содержащий второй гидрофобный А-блок и второй гидрофильный В-блок, при этом второй гидрофобный А-блок представляет собой биоразлагаемый сложный полиэфир и второй гидрофильный В-блок имеет вторую среднюю молекулярную массу и содержит полиэтиленгликоль, причем вторая средняя молекулярная масса отличается от первой средней молекулярной массы; при этом общая средняя молекулярная масса блок-сополимерной композиции составляет от 1500 до 10000 дальтон, общее содержание А-блока в композиции составляет примерно от 60 до 85% по массе и общее содержание В-блока в композиции составляет примерно от 15% до 40% по массе, причем общая средняя молекулярная масса В-блока в композиции составляет от 300 до 2000 дальтон, при этом блок-сополимерная композиция при комнатной температуре является порошкообразной или воскообразной, способна к обратимому термическому гелеобразованию при получении в виде водного полимерного раствора и способна превращаться в водный полимерный раствор в течение менее чем тридцати минут при взбалтывании без применения добавок или нагревания свыше 60°C.
[0012] Настоящее изобретение также включает новые формы введения в теплокровное животное по меньшей мере одного лекарственного средства в форме с контролируемым высвобождением. Указанные новые способы включают (1) обеспечение блок-сополимерной композиции типа АВ, ABA или ВАВ, являющейся при комнатной температуре порошкообразной или воскообразной, способной к обратимому термическому гелеобразованию при получении в виде водного полимерного раствора и способной превращаться в водный полимерный раствор в течение менее чем тридцати минут при взбалтывании без применения добавок или нагревания свыше 60°C; (2) получение водного раствора указанной порошкообразной или воскообразной композиции путем смешивания сополимера с водой без воздействия нагревания, превышающего 60°C; и (3) введение указанной композиции указанному теплокровному животному в виде гелевого депо.
[0013] Кроме того, изобретение включает способы получения порошкообразных или воскообразных блок-сополимерных композиций. Такие способы включают (1) обеспечение блок-сополимерной композиции типа ABA, содержащей: i) примерно от 60 до 85% по массе биоразлагаемого, гидрофобного А-блока, представляющего собой биоразлагаемый сложный полиэфир, при этом указанный А-блок включает по меньшей мере 60% капролактона и по меньшей мере один второй полиэфир-образующий мономер; и ii) примерно от 15 до 40% по массе биоразлагаемого, гидрофильного В-блока, содержащего полиэтиленгликоль, при этом молекулярная масса В-блока составляет от 300 до 2000 дальтон, (2) лиофильную сушку указанного блок-сополимера с получением порошкообразной или воскообразной блок-сополимерной композиции, при этом порошкообразная или воскообразная блок-сополимерная композиция является твердой при комнатной температуре, способна к обратимому термическому гелеобразованию при получении в виде водного полимерного раствора и способна превращаться в водный полимерный раствор в течение менее чем тридцати минут при взбалтывании без применения добавок или нагревания свыше 60°C.
[0014] Эти и другие задачи можно осуществить с помощью блок-сополимера типа ABA, содержащего: i) примерно от 60 до 85% по массе биоразлагаемого, гидрофобного А-блока, представляющего собой биоразлагаемый сложный полиэфир, при этом указанный А-блок включает по меньшей мере 85% капролактона и по меньшей мере один второй полиэфир-образующий мономер; и ii) примерно от 15 до 40% по массе биоразлагаемого, гидрофильного В-блока, содержащего полиэтиленгликоль, причем молекулярная масса В-блока составляет от 1000 до 1450 дальтон; при этом блок-сополимерная композиция при комнатной температуре является порошкообразной или воскообразной, способна к обратимому термическому гелеобразованию при получении в виде водного полимерного раствора и способна превращаться в водный полимерный раствор в течение менее чем тридцати минут при взбалтывании без применения добавок или нагревания свыше 60°C. Более предпочтительно, содержание А-блока в АВА-блок-сополимере составляет от 65 до 80% и содержание В-блока в указанном сополимере составляет от 20 до 35% и, наиболее предпочтительно, содержание А-блока составляет от 67 до 75% и содержание В-блока составляет от 25 до 33%. Второй мономер сложного полиэфира предпочтительно содержит остаток по меньшей мере одного из соединений: D,L-лактида, D-лактида, L-лактида, D,L-молочной кислоты, D-молочной кислоты, L-молочной кислоты, гликолида, гликолевой кислоты, ε-гидроксигексановой кислоты, γ-бутиролактона, γ-гидроксимасляной кислоты, δ-валеролактона, δ-гидроксивалериановой кислоты, гидроксимасляных кислот, яблочной кислоты или их сополимеров и, более предпочтительно, второй мономер сложного полиэфира содержит остатки лактида или гликолида или их сополимеров и, наиболее предпочтительно, второй мономер сложного полиэфира содержит остатки гликолида. Предпочтительно, А-блок содержит по меньшей мере 85% капролактона, более предпочтительно, биоразлагаемый сложный полиэфир А-блока содержит по меньшей мере 90 мольных % капролактона и, наиболее предпочтительно, биоразлагаемый сложный полиэфир А-блока содержит приблизительно от 90 до 95% капролактона. Предпочтительно, средняя молекулярная масса В-блока в АВА-блок-сополимере составляет от 800 до 1800 дальтон, более предпочтительно, средняя молекулярная масса В-блока составляет от 1000 до 1600 дальтон и, более предпочтительно, средняя молекулярная масса В-блока составляет от 1200 до 1500 дальтон. Предпочтительно, общая средняя молекулярная масса блок-сополимерной композиции составляет от 4000 до 8000 дальтон и, более предпочтительно, общая средняя молекулярная масса составляет от 5500 до 7500 дальтон. АВА-блок-сополимер предпочтительно представляет собой порошкообразную или воскообразную композицию, которая образует водный полимерный раствор в течение менее чем 30 минут без воздействия дополнительных агентов или температур, превышающих 60°C, способна к набуханию, составляющему менее чем 5% после 30 дней воздействия водой, и способна высвобождать примерно от 10 до 15% паклитаксела в течение пяти дней и от 15% до 20% паклитаксела в течение 20 дней.
[0015] Эти и другие задачи также можно осуществить с помощью блок-сополимера типа АВ, содержащего: i) примерно от 60 до 85% по массе биоразлагаемого, гидрофобного А-блока, представляющего собой биоразлагаемый сложный полиэфир, при этом указанный А-блок включает по меньшей мере 85% капролактона и по меньшей мере один второй полиэфир-образующий мономер; и ii) примерно от 15 до 40% по массе биоразлагаемого, гидрофильного В-блока, содержащего полиэтиленгликоль, причем молекулярная масса В-блока составляет от 300 до 2000 дальтон; при этом блок-сополимерная композиция при комнатной температуре является порошкообразной или воскообразной, способна к обратимому термическому гелеобразованию при получении в виде водного полимерного раствора и способна превращаться в водный полимерный раствор в течение менее чем тридцати минут при взбалтывании без применения добавок или нагревания свыше 60°C. Более предпочтительно, содержание А-блока в АВ-блок-сополимере составляет от 65 до 80% и содержание В-блока в указанном сополимере составляет от 20 до 35% и, наиболее предпочтительно, содержание А-блока составляет от 67 до 75% и содержание В-блока составляет от 25 до 33%. Второй мономер сложного полиэфира предпочтительно содержит остаток по меньшей мере одного из соединений: D,L-лактида, D-лактида, L-лактида, D,L-молочной кислоты, D-молочной кислоты, L-молочной кислоты, гликолида, гликолевой кислоты, ε-гидроксигексановой кислоты, γ-бутиролактона, γ-гидроксимасляной кислоты, δ-валеролактона, δ-гидроксивалериановой кислоты, гидроксимасляных кислот, яблочной кислоты или их сополимеров и, более предпочтительно, второй мономер сложного полиэфира содержит остатки лактида или гликолида или их сополимеров и, более предпочтительно, второй мономер сложного полиэфира содержит остатки гликолида. Предпочтительно, А-блок содержит по меньшей мере 85% капролактона, более предпочтительно, биоразлагаемый сложный полиэфир А-блока содержит по меньшей мере 90 мольных % капролактона и, более предпочтительно, биоразлагаемый сложный полиэфир А-блока содержит приблизительно от 90 до 95% капролактона. Средняя молекулярная масса В-блока в АВ-блок-сополимере предпочтительно составляет от 300 до 800 дальтон, более предпочтительно, средняя молекулярная масса В-блока составляет от 500 до 750 дальтон. Предпочтительно, общая средняя молекулярная масса блок-сополимерной композиции составляет от 1500 до 4500 дальтон и, более предпочтительно, общая средняя молекулярная масса составляет от 2000 до 4000 дальтон. Блок-сополимер типа АВ предпочтительно является порошкообразной или воскообразной композицией, которая образует водный полимерный раствор в течение менее чем 30 минут без воздействия дополнительных агентов или температур, превышающих 60°C, способна к набуханию, составляющему менее чем 5% после 30 дней воздействия водой, и способна высвобождать примерно от 10 до 15% паклитаксела в течение пяти дней и от 15% до 20% паклитаксела в течение 20 дней.
[0016] Эти и другие задачи можно осуществить с помощью блок-сополимера типа ВАВ, содержащего: i) примерно от 60 до 85% по массе биоразлагаемого, гидрофобного А-блока, представляющего собой биоразлагаемый сложный полиэфир, при этом указанный А-блок включает по меньшей мере 85% капролактона и по меньшей мере один второй полиэфир-образующий мономер; и ii) примерно от 15 до 40% по массе биоразлагаемого, гидрофильного В-блока, содержащего полиэтиленгликоль, при этом молекулярная масса В-блока составляет от 300 до 2000 дальтон; причем блок-сополимерная композиция при комнатной температуре является порошкообразной или воскообразной, способна к обратимому термическому гелеобразованию при получении в виде водного полимерного раствора и способна превращаться в водный полимерный раствор в течение менее чем тридцати минут при взбалтывании без применения добавок или нагревания свыше 60°C. Более предпочтительно, содержание А-блока в ВАВ-блок-сополимере составляет от 65 до 80% и содержание В-блока в указанном сополимере составляет от 20 до 35% и, наиболее предпочтительно, содержание А-блока составляет от 67 до 75% и содержание В-блока составляет от 25 до 33%. Второй мономер сложного полиэфира предпочтительно содержит остаток по меньшей мере одного из соединений: D,L-лактида, D-лактида, L-лактида, D,L-молочной кислоты, D-молочной кислоты, L-молочной кислоты, гликолида, гликолевой кислоты, ε-гидроксигексановой кислоты, γ-бутиролактона, γ-гидроксимасляной кислоты, δ-валеролактона, δ-гидроксивалериановой кислоты, гидроксимасляных кислот, яблочной кислоты или их сополимеров и, более предпочтительно, второй мономер сложного полиэфира содержит остатки лактида или гликолида или их сополимеров и, более предпочтительно, второй мономер сложного полиэфира содержит остатки гликолида. Предпочтительно, А-блок содержит по меньшей мере 85% капролактона, более предпочтительно, биоразлагаемый сложный полиэфир А-блока содержит по меньшей мере 90 мольных % капролактона и, наиболее предпочтительно, биоразлагаемый сложный полиэфир А-блока содержит приблизительно от 90 до 95% капролактона. Средняя молекулярная масса ВАВ-сополимера предпочтительно составляет от 300 до 800 дальтон для каждого В-блока в ВАВ-сополимере и, более предпочтительно, средняя молекулярная масса составляет от 500 до 750 дальтон для каждого В-блока в ВАВ-сополимере. Предпочтительно, общая средняя молекулярная масса блок-сополимерной композиции типа ВАВ составляет от 4000 до 8000 дальтон и, более предпочтительно, общая средняя молекулярная масса составляет от 5500 до 7500 дальтон. Блок-сополимер типа ВАВ предпочтительно является порошкообразной или воскообразной композицией, которая образует водный полимерный раствор в течение менее чем 30 минут без воздействия дополнительных агентов или температур, превышающих 60°C, способна к набуханию, составляющему менее чем 5% после 30 дней воздействия водой и способна высвобождать примерно от 10 до 15% паклитаксела в течение пяти дней и от 15% до 20% паклитаксела в течение 20 дней.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
[0017] Вышеописанные и другие задачи, особенности и преимущества изобретения будут очевидны из следующего подробного описания и прилагаемых чертежей:
[0018] Фиг. 1 представляет собой диаграмму фазового состояния, иллюстрирующую влияние композиции мономера на процесс гелеобразования водных растворов блок-сополимера, изученный при различных концентрациях и температурах.
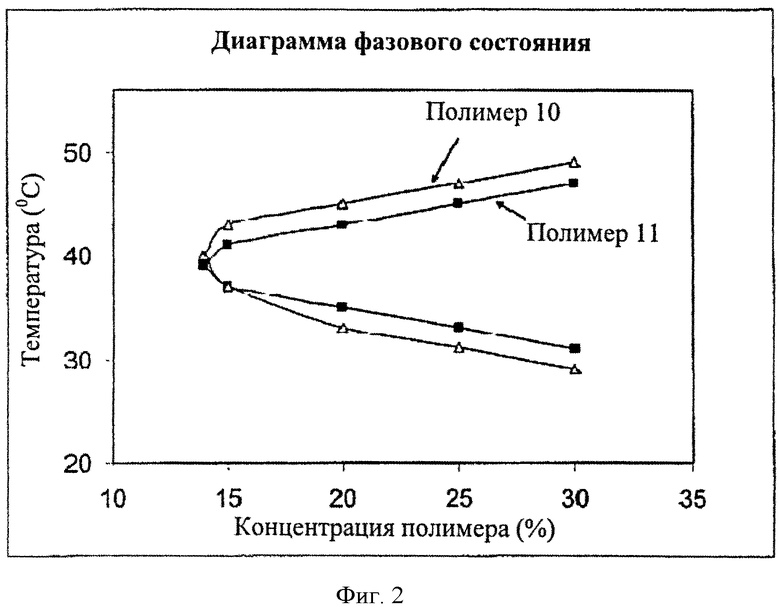
[0019] Фиг. 2 представляет собой диаграмму фазового состояния, иллюстрирующую влияние гидрофобности полимера на процесс гелеобразования водных растворов блок-сополимера, изученный при различных концентрациях и температурах.
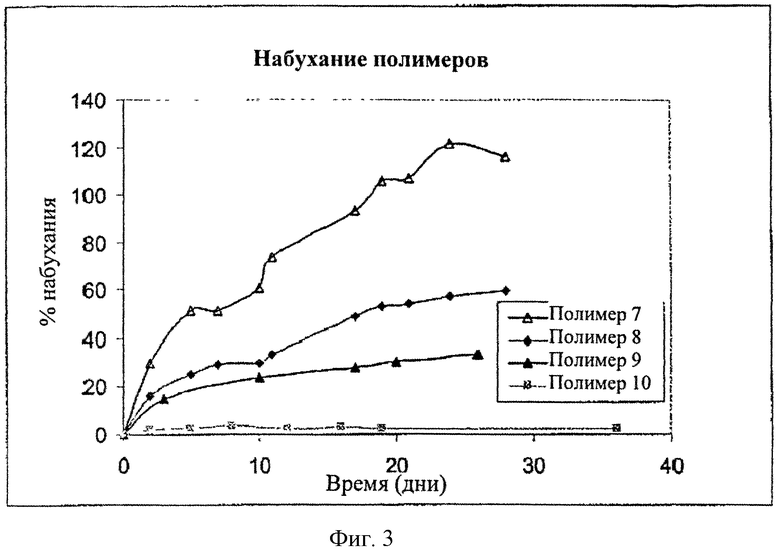
[0020] Фиг. 3 представляет собой график, иллюстрирующий набухание в процентах блок-сополимерного термического геля в течение нескольких дней для различных блок-сополимерных композиций.
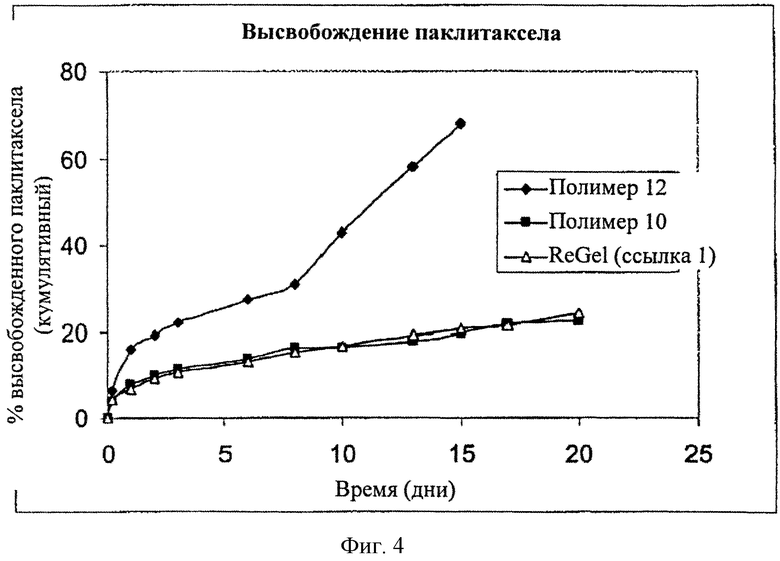
[0021] Фиг. 4 представляет собой профиль высвобождения паклитаксела из блок-сополимерного состава, способного к термическому гелеобразованию, показывающий кумулятивное контролируемое высвобождение паклитаксела в течение приблизительно 20 дней для различных блок-сополимерных композиций.
ПОДРОБНОЕ ОПИСАНИЕ ПРЕДПОЧТИТЕЛЬНЫХ ВАРИАНТОВ РЕАЛИЗАЦИИ ИЗОБРЕТЕНИЯ
[0022] Дополнительные задачи и преимущества настоящего изобретения будут очевидны из приведенного ниже подробного описания различных вариантов реализации настоящего изобретения. В настоящей заявке следующие термины будут иметь данные значения:
[0023] "Парентеральное" включает внутримышечное, внутрибрюшинное, интраабдоминальное, подкожное, внутриопухолевое, внутричерепное (или в полость резецированной опухоли), внутрисуставное, глазное и, при наличии возможности, внутривенное и внутриартериальное введение.
[0024] "Температура гелеобразования" означает температуру, при которой биоразлагаемый блок-сополимер подвергается обратимому термическому гелеобразованию, т.е. температуру, ниже которой блок-сополимер растворим в воде и
выше которой блок-сополимер подвергается фазовому переходу с увеличением вязкости или образованием полутвердого геля.
[0025] Термины "температура гелеобразования" и "температура обратимого термического гелеобразования" или т.п. следует применять взаимозаменяемо, подразумевая температуру гелеобразования.
[0026] "Полимерный раствор", "водный раствор" и т.п., при применении со ссылкой на биоразлагаемый блок-сополимер, содержащийся в таком растворе, означает раствор на основе воды, содержащий указанный блок-сополимер, растворенный в этом растворе при функциональной концентрации и сохраняющий свою форму при температуре ниже температуры гелеобразования блок-сополимера.
[0027] Полиэтиленгликоль (PEG) также иногда называют поли(этиленоксидом) (РЕО) или поли(оксиэтиленом), при этом для целей настоящего изобретения указанные термины можно использовать взаимозаменяемо.
[0028] "Обратимое термическое гелеобразование" представляет собой процессы, посредством которых раствор блок-сополимера самопроизвольно увеличивает вязкость и во многих случаях превращается в полутвердый гель, когда температура раствора возрастает выше температуры гелеобразования сополимера. Для целей настоящего изобретения, термин "гель" включает как полутвердое гелеобразное состояние, так и высоковязкое состояние, которое существует при температурах выше температуры гелеобразования. При охлаждении ниже температуры гелеобразования гель самопроизвольно возвращается в прежнее состояние и повторно образует раствор с более низкой вязкостью. Такое чередование между раствором и гелем можно повторять до бесконечности, поскольку переход раствор/гель не включает какого-либо изменения химического состава полимерной системы. Все взаимодействия, приводящие к образованию геля, имеют физическую природу и не затрагивают образование или разрушение ковалентных связей.
[0029] "Жидкость для доставки лекарственного средств" или "жидкость для доставки лекарственного средства со свойствами обратимого термического гелеобразования" означает полимерный раствор, содержащий лекарственное средство (лекарственное средство само по себе может находиться в растворенной или коллоидной форме), подходящий для введения теплокровному животному, который образует желеобразное депо для лекарственного средства при повышении температуры до температуры гелеобразования блок-сополимера или выше.
[0030] "Депо" означает жидкость для доставки лекарственного средства после введения в теплокровное животное, которая образовала гель после повышения
температуры до температуры гелеобразования или выше.
[0031] "Гель" означает полутвердую фазу, возникающую самопроизвольно при повышении температуры "полимерного раствора" или "жидкости для доставки лекарственного средства" до температуры гелеобразования блок-сополимера или выше. В некоторых случаях, образовавшийся гель может терять или поглощать воду из окружающей среды и становиться более плотным или набухшим, такие гели также подпадают под объем настоящего изобретения.
[0032] "Водная полимерная композиция" означает либо жидкость для доставки лекарственного средств, либо гель, состоящий из водной фазы, содержащей равномерно распределенное в ней лекарственное средство и биоразлагаемый блок-сополимер. При температурах ниже температуры гелеобразования сополимер может растворяться в водной фазе, при этом указанная композиция будет представлять собой раствор. При температурах, равных или выше температуры гелеобразования, сополимер будет затвердевать с образованием геля с водой фазой, при этом композиция будет представлять собой гель или полутвердое вещество.
[0033] "Биоразлагаемый" означает, что блок-сополимер может разрушаться или разлагаться в теле химическим способом с образованием нетоксичных компонентов. Скорость разложения может быть равной скорости высвобождения лекарственного средства или отличаться от нее.
[0034] "Лекарственное средство" означает любое органическое или неорганическое соединение или вещество, обладающее биоактивностью и адаптированное или применяемое для терапевтической цели. Белки, гормоны, противораковые агенты, олигонуклеотиды, ДНК, РНК и генные терапии включены в более широкое определение лекарственного средства.
[0035] Термины "пептид", "полипептид", "олигопептид" и "белок" следует применять взаимозаменяемо по отношению к пептидным или белковым лекарственным средствам и не следует ограничивать какой-либо определенной молекулярной массой, последовательностью или длиной пептида, областью биоактивности или терапевтического применения, если это не указано специально. Такие терапевтические применения могут включать, например, алкилирующие агенты, антиметаболиты, антибиотики, гормональные средства, противоваскуляризационные средства или нитрозомочевины.
[0036] "Поликапролактон-со-(лактид-со-гликолид)" или "PCLGA" означает сополимер, образованный в результате конденсационной сополимеризации капроновой кислоты, молочной кислоты и гликолевой кислоты, или путем полимеризации с раскрытием кольца предшественников α-гидроксикислот, таких как капролактон, лактид
или гликолид. "Поликапролактон-со-гликолид" или "PCGA" означает сополимер, полученный в результате конденсационной полимеризации капроновой кислоты и гликолевой кислоты или путем полимеризации с раскрытием кольца предшественников α-гидроксикислот, таких как капролактон или гликолид. Термины "капролактон и капроновая кислота" используют взаимозаменяемо, "лактид" и "лактат или молочная кислота" используют взаимозаменяемо и термины "гликолид" и "гликолят или гликолевая кислота" используют взаимозаменяемо.
[0037] "Поли(лактид)" или "PLA" означает полимер, полученный в результате конденсации молочной кислоты или путем полимеризации с раскрытием кольца лактида. Термины "лактид" и "лактат или молочная кислота" используют взаимозаменяемо.
[0038] "Биоразлагаемые сложные полиэфиры" относятся к любым биоразлагаемым сложным полиэфирам, которые предпочтительно синтезированы из по меньшей мере одного из соединений: D,L-лактида, D-лактида, L-лактида, D,L-молочной кислоты, D-молочной кислоты, L-молочной кислоты, гликолида, гликолевой кислоты, ε-капролактона, ε-гидроксигексановой кислоты, γ-бутиролактона, γ-гидроксимасляной кислоты, δ-валеролактона, δ-гидроксивалериановой кислоты, гидроксимасляных кислот, яблочной кислоты или их сополимеров.
[0039] "Способный к восстановлению" или "восстановление" означает твердый полимер, который можно легко превратить в водный полимерный раствор без необходимости добавления других веществ за период времени, составляющий менее чем тридцать минут. Термины "способный к восстановлению" или "восстановление" не подразумевают, что полимерная композиция остается одинаковой как перед существованием в твердой полимерной форме, так и после него, или что полимерная композиция имеет одинаковые свойства как перед существованием в твердой полимерной форме, так и после него. Термины "способный к восстановлению" или "восстановление" включают водные полимерные растворы, образованные из твердых порошков впервые, даже если твердый порошок ранее не существовал в виде водного полимерного раствора.
[0040] Авторы изобретения обнаружили, что некоторые блок-сополимеры типа АВ, ABA и ВАВ при получении согласно способам, описанным в настоящей заявке, обладают уникальными полезными свойствами восстанавливаться и по-прежнему проявлять способность к обратимому термическому гелеобразованию. Предшествующие полимерные растворы, способные к обратимому термическому гелеобразованию, образуются только в предельных условиях, включающих применение добавок, избыточное тепло (>60 градусов Цельсия) или продолжительное взбалтывание. Такие свойства делали нецелесообразным восстановление предшествующих композиций с образованием полимерного раствора непосредственно перед применением. Поэтому предшествующие композиции перевозили в охлажденной или замороженной форме, чтобы избежать их разложения перед применением конечным пользователем. Полимеры, описанные в настоящей заявке, преодолели некоторые или все из указанных недостатков за счет обеспечения способного к восстановлению блок-сополимера типа АВ, ABA или ВАВ в виде твердого порошка или воскообразного порошка.
[0041] Блок-сополимеры, описанные в настоящей заявке, содержат гидрофобные сегменты или сегменты "А" блока и гидрофильные сегменты или сегменты "В" блока. В общем, блок-сополимер будет представлять собой блок-сополимер типа АВ, ABA или ВАВ. Однако блок-сополимер может также представлять собой многоблочный сополимер, содержащий повторяющиеся звенья ВА или АВ, образующие сополимеры А(ВА)n или В(АВ)n, где n представляет собой целое число от 2 до 5.
[0042] Как было обнаружено, твердые порошкообразные или воскообразные порошковые блок-сополимеры соответствуют критериям, которые обобщены в таблице 1, а именно, имеют композиционный состав в пределах указанных диапазонов. Для целей описания параметров молекулярной массы, все приведенные значения молекулярной массы основаны на измерениях с применением аналитических методов ЯМР или ГПХ (гель-проникающей хроматографии). Приведенные средневесовые молекулярные массы и среднечисловые молекулярные массы были определены посредством ГПХ и ЯМР, соответственно. Приведенные соотношения капролактона и лактида/гликолида были рассчитаны на основе данных ЯМР. Анализ методом ГПХ был выполнен с применением комбинации Phenogel, смешанного слоя и Phenogel, колонок 500 Angstrom, калиброванных с применением стандартов PEG путем использования рефрактометрического детектирования и тетрагидрофурана в качестве элюента. Спектры ЯМР были получены в CDCl3 на приборе Bruker 200 MHz.

[0043] Блок-сополимеры типа АВ, ABA и ВАВ можно синтезировать путем полимеризации с раскрытием кольца или конденсационной полимеризации согласно общим реакционным схемам, описанным в патентах США № 5702717, 6004573, 6117949 и 6201072, тем самым включенным в настоящим документ посредством ссылки в полном объеме. Например, блоки типа B(PEG) можно соединять с А-блоками (сложными полиэфирами) за счет эфирных или уретановых связей и т.п. Можно использовать методы конденсационной полимеризации и полимеризации с раскрытием кольца, которые позволяют связать монофункциональный гидрофильный В-блок с любым концом бифункционального гидрофобного А-блока в присутствии связующих агентов, таких как изоцианаты. Кроме того, реакции связывания могут сопровождать активацию функциональных групп активирующими агентами, такими как карбонилдиимидазол, янтарный ангидрид, N-гидроксисукцинимид и р-нитрофенил хлорформиат и т.п.
[0044] Гидрофильный В-блок образуется из PEG с подходящими молекулярными массами. PEG был выбран в качестве гидрофильного, водорастворимого блока благодаря его уникальным свойствам биосовместимости, нетоксичности, гидрофильности, солюбилизации и быстрому клиренсу из тела пациента. Согласно предпочтительному варианту реализации изобретения PEG компонент можно выбрать из смеси PEG с различными средними молекулярными массами. Авторы изобретения обнаружили, что при применении полимерной смеси с более чем одной молекулярной массой PEG можно добиться лучшего регулирования свойств образующихся композиций. Хотя применение мономера с более чем одной молекулярной массой PEG обеспечивает эластичность, следует понимать, что не существует ограничения на количество мономеров с различными молекулярными массами PEG, которые можно применять в настоящем изобретении. Например, указанных преимуществ настоящего изобретения можно добиться, используя три или более мономеров с различными молекулярными массами PEG.
[0045] Гидрофобные А-блоки используют вследствие их способности к биоразложению, биосовместимости и солюбилизирующих свойств. Разложение in vitro и in vivo таких гидрофобных, биоразлагаемых полиэфирных А-блоков хорошо изучено, при этом продукты разложения имеют природное происхождение (или имеют свойства, эквивалентные свойствам природных продуктов) или представляют собой биосовместимые соединении, которые легко усваиваются и/или элиминируются телом пациента.
[0046] Концентрацию, при которой блок-сополимеры растворимы при температурах ниже температуры гелеобразования, можно рассматривать как функциональную концентрацию. В целом, можно применять концентрации блок-сополимеров, составляющие минимум 3% и до примерно 50% по массе, которые все еще являются функциональными. Однако предпочтительными являются концентрации в диапазоне примерно от 5 до 40%, а наиболее предпочтительны концентрации в диапазоне примерно от 10 до 30% по массе. Чтобы обеспечить практически осуществимый переход в гелевую фазу с помощью сополимера, необходима определенная минимальная концентрация, например, 3% по массе. При более низких функциональных концентрациях образующийся гель будет жидким и может произойти разделение фаз. При более высоких концентрациях полимера может образоваться гораздо более прочная полимерная сетка.
[0047] Смесь биоразлагаемого сополимера и пептидных/белковых лекарственных средств и/или других видов лекарственных средств можно приготовить в виде водного раствора сополимера при температуре ниже температуры гелеобразования с получением жидкости для доставки лекарственного средств, в которой лекарственное средство может быть частично или полностью растворено. Когда лекарственное средство частично растворено или когда лекарственное средство по существу нерастворимо, указанное средство существует в коллоидном состоянии, таком как суспензия или
эмульсия. Описанные полимеры преимущественно применяют при парентеральном введении, таком как внутримышечное или подкожное, внутриопухолевое, внутричерепное (или в полость резецированной опухоли), внутрисуставное, глазное, топическое, трансдермальное, вагинальное, буккальное, чресслизистое, пульмональное, трансуретральное, ректальное, назальное, пероральное или ушное введение, после которого полимеры будут подвергаться обратимому термическому гелеобразованию, поскольку температура тела будет выше температуры гелеобразования.
[0048] Такая система будет иметь минимальную токсичность и вызывать минимальное механическое раздражение окружающей ткани благодаря биосовместимости материалов, эластичности геля и точному регулированию характеристик набухания на физиологических участках, где набухание может привести к повреждению окружающей ткани. Кроме того, полиэфирные блоки в описанной системе будут также полностью биоразлагаться в пределах определенного временного интервала с образованием капроновой кислоты, молочной кислоты, гликолевой кислоты и других соответствующих мономеров. Полиэтиленгликолевые блоки удаляются из тела посредством экскреции. Высвобождение лекарственного средства, прочность геля, температуру гелеобразования и скорость разложения можно регулировать с помощью подходящей конфигурации и способов получения различных сополимерных блоков, а именно, за счет модификаций весового процентного содержания А-блоков и В-блоков, мольных концентраций капролактона, лактата и гликолята и молекулярной массы и полидисперсности блок-сополимеров типа ABA или ВАВ. Высвобождение лекарственного средства также можно контролировать путем регулирования концентрации полимера в жидкости для доставки лекарственного средств.
[0049] Лекарственную форму, состоящую из раствора блок-сополимера, содержащего либо растворенное лекарственное средство, либо лекарственное средство в виде суспензии или эмульсии, вводят в тело. Далее, при повышении температуры состава до температуры тела указанный состав самопроизвольно превращается в гель благодаря способности блок-сополимера к обратимому термическому гелеобразованию с созданием депо, содержащим лекарственное средство. Единственным ограничением в отношении того, как много лекарственного средства можно ввести в состав, является одно из функциональных свойств. А именно, содержание лекарственного средства можно увеличивать до тех пор, пока свойства термического гелеобразования сополимера не ухудшатся до недопустимой степени, способность к высвобождению лекарственного средства не изменится неблагоприятным образом или пока свойства состава не ухудшатся до такой степени, что сделает введение состава недопустимо сложным. В целом, предполагают, что в большинстве случаев содержание лекарственного средства будет составлять примерно от 0,01 до 20% по массе состава, при этом наиболее распространенные диапазоны включают примерно от 0,01 до 10%. Указанные диапазоны концентраций лекарственного средства не являются ограничивающими для данного изобретения. Предусмотренные функциональные возможности сохраняются, концентрации лекарственного средства в пределах указанных диапазонов находятся в рамках настоящего изобретения.
[0050] Явное преимущество композиций, описанных в настоящей заявке, заключается в способности блок-сополимера увеличивать растворимость многих лекарственных веществ. Комбинация гидрофобного А-блока (блоков) и гидрофильного В-блока (блоков) придает блок-сополимеру амфифильность за счет разных гидрофильных и гидрофобных доменов, которые стабилизируют и солюбилизируют гидрофобные лекарственные средства. В этом отношении, блок-сополимер функционирует почти как мыло или поверхностно-активное вещество, поскольку обладает как гидрофильными, так и гидрофобными свойствами. Это является особенным преимуществом при солюбилизации гидрофобных или плохо растворимых в воде лекарственных средств, таких как циклоспорин и паклитаксел. Что вызывает удивление, так это степень солюбилизации большинства, если не всех, лекарственных средств, поскольку основным компонентом блок-сополимера является содержание гидрофобного А-блока. Однако, как уже обсуждалось, хотя гидрофобный полимерный блок (блоки) является основным компонентом, блок-сополимер растворим в воде и было обнаружено, что имеет место дополнительное увеличение растворимости лекарственного средства при комбинировании блок-сополимера в водной фазе.
[0051] Еще одно преимущество композиций, описанных в настоящей заявке, заключается в способности блок-сополимера увеличивать химическую стабильность многих лекарственных веществ, например паклитаксела. Как было экспериментально обнаружено, различные механизмы разложения лекарственных средств, которые приводят к их химической нестабильности, ингибированы, когда лекарственное средство находится в присутствии блок-сополимера. Например, паклитаксел по существу стабилизирован в водной полимерной композиции согласно настоящему изобретению по сравнению с некоторыми водными растворами таких же лекарственных средств в присутствии органических сорастворителей. Такое стабилизирующее действие на паклитаксел иллюстрирует эффект, которого можно добиться со многими другими лекарственными веществами.
[0052] В некоторых случаях полимер, содержащий лекарственное средство, можно ввести в гелеобразном состоянии, а не в виде раствора. Гелеобразование может быть результатом повышения температуры полимерного раствора, содержащего лекарственное средство, выше температуры гелеобразования полимера перед введением или может быть вызвано повышением концентрации полимера в растворе выше концентрации насыщения при температуре введения, или может быть вызвано включением в полимерный раствор добавок, что приводит к превращению раствора в гель. В любом случае, образованный таким образом гель можно ввести парентеральным путем, таким как внутримышечное или подкожное, внутриопухолевое, внутричерепное (или в полость резецированной опухоли), внутрисуставное, глазное, топическое, трансдермальное, вагинальное, буккальное, чресслизистое, пульмональное, трансуретральное, ректальное, назальное, пероральное или ушное введение лекарственных средств.
[0053] Настоящее изобретение применимо к биоактивным агентам и лекарственным средствам всех типов, включая нуклеиновые кислоты, гормоны, противораковые агенты и в нем предложен необычайно эффективный способ доставки полипептидов и белков. Многие неустойчивые пептидные и белковые лекарственные средства могут быть включены в блок-сополимеры согласно изобретению и могут извлечь пользу из процесса обратимого термического гелеобразования, описанного в настоящей заявке. Хотя они специально не ограничены следующим перечнем, примерами фармацевтически применяемых полипептидов и белков могут являться эритропоэтин, окситоцин, вазопрессин, адренокортикотропный гормон, эпидермальный фактор роста, тромбоцитарный фактор роста (PDGF), пролактин, люлиберин, рилизинг-фактор лютеинизирующего гормона (LHRH), агонисты LHRH, антагонисты LHRH, гормон роста (человеческий, свиной, бычий и т.п.), фактор, стимулирующий выделение гормона роста, инсулин, соматостатин, глюкагон, интерлейкин-2 (IL-2), интерферон-α, β или γ, гастрин, тетрагастрин, пентагастрин, урогастрон, секретин, кальцитонин, энкефалины, эндорфины, ангиотензины, гормон, высвобождающий тиреотропен (TRH), фактор некроза опухолей (TNF), фактор роста нервов (NGF), гранулоцитарный колониестимулирующий фактор (G-CSF), гранулоцитарно-макрофагальный колониестимулирующий фактор (GM-CSF), макрофагальный колониестимулирующий фактор (M-CSF), гепараназа, костный морфогенетический белок (BMP), hANP, глюкагоноподобный пептид (GLP-1), интерлейкин-11 (IL-11), ренин, брадикинин, бацитрацины, полимиксины, колистины, тироцидин, грамицидины, циклоспорины или их синтетические аналоги, модификации и фармакологически активные фрагменты, ферменты, цитокины, антитела или вакцины.
[0054] Единственным ограничением в отношении полипептидного или белкового лекарственного средства, который можно использовать согласно изобретению,
является одно из функциональных свойств. В некоторых случаях, функциональность или физическая стабильность полипептидов и белков может также возрастать при введении различных добавок в твердые порошки или воскообразные порошки блок-сополимеров типа АВ, ABA или ВАВ согласно изобретению перед образованием твердой формы или после него. Добавки также можно ввести в водные растворы или суспензии полипептидного или белкового лекарственного средства. Такие добавки, как полиолы (в том числе, сахара), аминокислоты, поверхностно-активные вещества, полимеры, другие белки и некоторые соли можно применять для стабилизации самих лекарственных средств без изменения свойств композиции для доставки лекарственного средств. Указанные добавки можно легко ввести в блок-сополимеры, которые сохранят способность к восстановлению вследствие обратимого термического гелеобразования.
[0055] Разработки в области белковой инженерии могут обеспечить возможность повышения собственной стабильности пептидов или белков. Несмотря на то, что такие полученные сконструированные или модифицированные белки можно рассматривать как новые соединения в отношении регуляторных последствий, это не изменяет их пригодность для применения в настоящем изобретении. Одним из типичных примеров модификации является пегилирование, когда стабильность полипептидных лекарственных средств можно значительно улучшить путем связывания с помощью ковалентных связей водорастворимых полимеров, таких как полиэтиленгликоль, с полипептидом. Еще один пример представляет собой модификацию аминокислотной последовательности в зависимости от идентичности или расположения одного или более аминокислотных остатков путем терминального и/или внутреннего добавления, делеции или замещения. Любое улучшение стабильности позволяет непрерывно высвобождать терапевтически эффективный полипептид или белок в течение продолжительного периода времени после одного введения пациенту жидкости для доставки лекарственного средств.
[0056] Наряду с ранее перечисленными лекарственными средствами на основе пептидов или белков, можно использовать другие лекарственные средства из всех терапевтических и пригодных в медицине категорий лекарств. Эти лекарственные средства описаны в таких хорошо известных литературных источниках, как Merck Index, the Physicians Desk Reference и The Pharmacological Basis of Therapeutics. Краткий перечень конкретных средств приведен только с иллюстративными целями и не должен рассматриваться как ограничивающий: противораковые агенты, такие как актиномицин D, анастрозол, азацитидин, бевацизумаб, бикалутамид, блеомицин, BCNU, бортезомиб, камптотецин, капецитабин, карбоплатин, цетуксимаб, даунорубицин, дазатиниб, доцетаксел, доксорубицин, эпирубицин, эрлотиниб, эксеместан, гефитиниб, гемцитабин,
гозерелин, иматиниб, STI-571, иринотекан, лапатиниб, летрозол, лейпрорелин, метотрексат, митомицин, оксалиплатин, паклитаксел, пеметрексед, ритуксимаб, зорафениб, сунитиниб, тамоксифен, таксотер, тегафур-урацил, темозоломид, трастузумаб, трипторелин, винорелбин; антипсихотические средства, такие как оланзапин и ципразидон; антибактериальные средства, такие как цефокситин; противоглистные средства, такие как ивермектин; противовирусные средства, такие как ацикловир; иммунодепрессанты, такие как циклоспорин А (циклический агент полипептидного типа), стероиды и простагландины. Дополнительные противораковые агенты включают поркабацин, дакарбацин, альтретамин, дисплатин, меркаптопурин, тиогуанин, флударабина фосфат, кладрибин, пентостатин, флуороурацил, цитарабин, азацитидин, винбластин, винкристин, этопозид, тенипозид, топотекан, дактиномицин, идарубинцин, пликамицин, флутамид, лейпрорелин, гозерелин, аминоглутетимид, амзакрин, гидроксимочевину, аспарагиназу, митоксатрон, митотан, производное ретиноевой кислоты, факторы роста костного мозга, амифостин, кармустин, ломустин, семустин, противо-VEGF (эндотелиальный фактор роста сосудов) и т.п.
[0057] Чтобы проиллюстрировать предпочтительные варианты реализации настоящего изобретения, был выполнен синтез различных низкомолекулярных блок-сополимеров типа ABA, содержащих от 60 до 85% по массе гидрофобных А-блоков (сложных полиэфиров) и от 15 до 40% по массе гидрофильного В-блока (полиэтиленгликоль "PEG"). Задача состояла в получении блок-сополимеров типа АВ, ABA или ВАВ со средними молекулярными массами примерно от 1500 до 10000, включающими А-блок, содержащий по меньшей мере 60% ε-капролактона и другой мономер, и В-блок, содержащий полиэтиленгликоль (PEG), при этом молекулярная масса В-блока составляет от 300 до 2000 дальтон. В случае триблок-сополимеров, средневесовая молекулярная масса полимеров более предпочтительно составляет от 4000 до 8000 дальтон и, наиболее предпочтительно, молекулярная масса составляет от 5500 до 7500. В случае диблок-полимеров типа АВ, диапазон молекулярной массы полимеров составляет более предпочтительно от 1500 до 4500, и, наиболее предпочтительно, от 2000 до 4000. Блок-сополимер представляет собой твердый порошок или воскообразную порошковую композицию, которая при переходе в водный раствор способна к обратимому термическому гелеобразованию. Ниже приведены примеры, иллюстрирующие предпочтительные варианты реализации изобретения, но, как подразумевают, рассмотрены исключительно с репрезентативными целями.
Пример 1
Синтез триблок-сополимера PCLG-PEG-PCLG типа ABA путем полимеризации с раскрытием кольца
[0058] 20 г полиэтиленгликоля с номинальной молекулярной массой 1000, которая, как указано на сертификате анализа, составляет 981, сушили под вакуумом (<1 мм Hg) при 120°C в течение 3 часов. Добавляли в реакционную колбу 43,13 г ε-капролактона и 4,87 г D,L-лактида и/или гликолида. Когда температура реакционной смеси достигала 80°C, инициировали полимеризацию путем добавления в реакционную смесь 27 мг октоата двухвалентного олова. Реакционную смесь нагревали при 155°C в течение дополнительных восьми часов. Непрореагировавшие мономеры удаляли с применением вакуума (<1 мм Hg) в течение 1 часа при 140°C и оставшийся полимер растворяли в воде. Непрореагировавший PEG, водорастворимые низкомолекулярные полимеры и мономеры удаляли путем осаждения полимерного раствора в горячей водяной бане (70°C). Избыток воды удаляли с помощью лиофильной сушки и получали белый твердый порошкообразный или воскообразный порошковый полимер. Молекулярную массу и состав полученного блок-сополимера определяли с помощью гель-проникающей хроматографии, используя стандарты PEG, и ЯМР, соответственно.
Пример 2
Синтез диблок-полимера MPEG-PCG путем сополимеризации с раскрытием кольца
[0059] Следуют общей процедуре, описанной в Примере 1, синтезировали диблок-сополимеры, используя смесь полиэтиленгликоль - монометиловый эфир с номинальными средними молекулярными массами, равными 550 и 750, и осуществляя реакцию указанной смеси с ε-капролактоном и гликолидом с получением АВ-блок-сополимера. Средняя молекулярная масса PEG в АВ-блок-сополимере составляла 590 из расчета средневзвешенных молекулярных масс PEG 550 и PEG 750, применяемых при получении АВ-блок-сополимера.
Пример 3
Синтез триблок-сополимера MPEG-PCG-PEGM типа ВАВ
[0060] Диблок-сополимер из Примера 2 (25 г; 12,7 ммоль.) добавляли к 170 мл безводного толуола. Оставшуюся воду, адсорбированную в полимере, удаляли путем азеотропной перегонки до достижения конечного объема 125 мл. К раствору добавляли HMDI (би (4-изоцианатоциклогексил)метан) (1,25 г; 6,35 ммоль) и октоат двухвалентного олова (0,11 г; 0,27 ммоль), перемешивали при 60°C в течение 10 часов и при 130°C в течение 6 часов в атмосфере сухого азота. Толуол в растворе удаляли посредством дистилляции до достижения конечного объема 70 мл. Реакционную смесь два раза осаждали в 300 мл диэтилового эфира. Оставшийся растворитель удаляли путем высушивания под высоким вакуумом при 100°C, получая триблок-сополимер типа ВАВ.
Пример 4
[0061] Следуя общей процедуре, описанной Примерах 1-3, синтезировали другие блок-сополимеры типа АВ, ABA и ВАВ. Композиции 2, 4-5 и 11-13 синтезировали с применением PEG с номинальными молекулярными массами 550, 1000 и 1450, не смешивая PEG с различной молекулярной массой. Композиции 1, 3 и 6-10 синтезировали с применением PEG с более чем одной молекулярной массой, выбранной из 550, 750, 1000 и 1450. Например, полимер 1 синтезировали, смешивая PEG 550 с PEG 750 перед проведением реакции, аналогичной реакции, описанной в Примере 1. Подобным образом, композиции 3 и 6-10 синтезировали с применением PEG 1000 и PEG 1450 при различных соотношениях. Молекулярные массы PEG, перечисленные ниже в таблице II, для полимеров 1, 3 и 6-10 представляют собой средневзвешенные значения для PEG полимеров, используемых при синтезе. В таблице II также показано различное содержание ε-капролактона, D,L-лактида и гликолида в каждом из блок-сополимеров. Значения молекулярных масс, приведенные в таблице III, являются приближенными значениями вследствие нормальной и ожидаемой вариации между номинальной молекулярной массой и молекулярной массой, указанной на соответствующем сертификате анализа.

Пример 5
Восстановление полимера
[0062] Все синтезированные блок-сополимеры были способны к восстановлению и обладали свойствами обратимого термического гелеобразования. В 20 мл флаконе взвешивали 1,15 г твердого полимера и 3,85 г воды и помещали флакон в 60°C водяную баню при слабом перемешивании на протяжении примерно 1 минуты. Флакон
встряхивали в течение нескольких секунд с последующим перемешиванием в прохладном помещении при 4°C. Через 20 минут мутный полимерный раствор превращался в прозрачный свободно текучий раствор. Температуры гелеобразования восстановленных полимеров (23%, по весу) представлены в таблице III.

Пример 6
Диаграмма фазового состояния
[0063] Было изучено поведение водного раствора различных блок-сополимеров при термическом гелеобразовании. Следуя процедуре, описанной в Примере 5, были получены водные растворы полимера в воде (от 10 до 30% во весу). Прослеживали изменение вязкости как функцию температуры в диапазоне от 10 до 60°C. Результаты, представленные на Фиг. 1 и 2, ясно демонстрируют влияние гидрофобного состава на поведение при термическом гелеобразовании.
Пример 7
Характер набухания полимера
[0064] Модуляции набухания блок-сополимерных систем, способных к обратимому термическому гелеобразованию, добивались путем изменения содержания гидрофобного мономера и длины цепи. Приготавливали 23% (по весу) водные растворы блок-сополимеров 7, 8, 9 и 10 в соответствии с процедурой, описанной в Примере 5. Помещали 3 мл аликвоты четырех указанных полимерных растворов в 20 мл сцинтилляционные флаконы. После образования геля (37°C, 20 минут) в каждый флакон добавляли 5 мл воды (37°C) и инкубировали в инкубаторе-встряхивателе при 37°C. Периодически удаляли слой воды и определяли массу геля. Водный слой заменяли свежей водой и рассчитывали % набухания полимера. Результаты представлены на Фиг. 3. Набухание сополимеров с одинаковой молекулярной массой PEG (полимеры 8, 9 и 10) зависело от гидрофобного состава полимера. Полимер с более высоким содержанием ε-капролактона демонстрировал гораздо меньшее набухание, чем полимер с более низким содержанием ε-капролактона. При одинаковых молекулярной массе PEG и содержании ε-капролактона полимер с более длиной гидрофобной цепью проявлял более низкое набухание, чем полимер с более короткой гидрофобной цепью. Как показано на Фиг. 3, набухание блок-сополимерной композиции с составом №10 составляет менее чем 10% после 5 дней воздействия водой и менее чем 5% после 30 дней воздействия водой.
Пример 8
Повышение растворимости лекарственных средств
[0065] Паклитаксел представляет собой гидрофобное лекарственное средство, практически нерастворимое в воде (растворимость составляет приблизительно 4 мкг/мл в воде). Однако это лекарственное средство проявляло значительно более высокую растворимость в водном растворе сополимеров (ε-капролактон-со-гликолид)-PEG-(ε-капролактон-со-гликолид). В 23% по весу водном растворе сополимера паклитаксел растворим вплоть до 12 мг/мл. Скорость солюбилизации была гораздо выше по сравнению с ранее синтезированным полимером (см. Rami с соавторами, патент США №6004573, описанный выше). Для исследования солюбилизации рассчитанное количество паклитаксела добавляли к водному раствору блок-полимеров (полученных согласно Примеру 5) и перемешивали в течение 10-20 минут при комнатной температуре или 4°C. Суспензия полимер-паклитаксел превращалась в чистый раствор через 20 минут и могла быть отфильтрована через фильтр с размером пор, составляющим 0,2 мкм. Растворимость паклитаксела в отфильтрованном полимерном растворе была подтверждена с помощью ВЭЖХ анализа. Указанный эксперимент продемонстрировал ~3000-кратное увеличение растворимости паклитаксела. Было достигнуто аналогичное повышение растворимости других гидрофобных лекарственных средств.
Пример 9
Высвобождение лекарственного средства
[0066] В настоящем примере продемонстрирован профиль высвобождения паклитаксела (модельное лекарственное средство) из геля полимера (ε-капролактон-со-гликолид)-PEG-(ε-капролактон-со-гликолид). Паклитаксел (30 мг) растворяли в 4,97 г 23% (по весу) полимерном водном растворе, как описано в Примере 5. Тест на растворение выполняли с применением модифицированного аппарата для исследования растворения USP-II. Исследовали высвобождение паклитаксела из 1,0 г депо, содержащего лекарственное средствои полимер, при 37°C с применением 138 мМ NaCl, 2,7 мМ KCl, 0,2% (масс/об.) NaN3 и 10 мМ фосфатного буфера, pH 7,4 (содержащего 4% (масс/об.) Cremophor EL и 2,4% (масс/об.) Tween-80) в качестве среды растворения. Содержание высвобожденного паклитаксела анализировали с применением ВЭЖХ. Результаты представлены на Фиг. 4. Содержание ε-капролактона в полимере ясно продемонстрировало влияние на высвобождение лекарственного средства при требуемых свойствах восстановления. В частности, композиция №10 высвобождала примерно от 10 до 15% паклитаксела в течение пяти дней и от 15% до 20% паклитаксела в течение 20 дней. Как показано на Фиг. 4, способные к восстановлению полимеры согласно настоящему изобретению могут проявлять характеристики высвобождения, подобные характеристикам предшествующих композиций для высвобождения лекарственного средства, не способных к восстановлению, таких как ReGel (т.е. требуют применение добавок или длительного взбалтывания для перехода в водную форму, способную к обратимому термическому гелеобразованию).
Повышение стабильности лекарственных средств
[0067] Паклитаксел является крайне нестабильным в водных растворах сорастворителей (например, в растворах вода/ацетонитрил). После 30 дней хранения (от 2 до 8°C и 37°C)>90% паклитаксела, содержащегося в 23% по массе водных растворах триблок-сополимера (ε-капролактон-со-гликолид)-PEG-(ε-капролактон-со-гликолид) (т.е. ниже температуры гелеобразования сополимера) или в гелях (т.е. выше температуры гелеобразования сополимера), находилось в неизменном виде, тогда как>50% паклитаксела в растворе сорастворителей подверглось разложению через менее чем одну неделю при 37°C.
[0068] Приведенное выше описание позволит специалисту в данной области техники синтезировать блок-сополимеры типа АВ, ABA или ВАВ, находящиеся в виде твердого порошка или воскообразного порошка, которая после восстановления превращается в водные растворы, обладающие свойствами обратимого термического гелеобразования, и применять указанные сополимеры в области доставки лекарственного средств. Хотя контролируемая доставка паклитаксела проиллюстрирована на приведенных выше примерах с целью демонстрации функциональных возможностей гидрогелей, полученных из водных растворов блок-сополимеров, подразумевают, что указанное описание не содержит исчерпывающее перечисление всех лекарственных средств, которые можно использовать и вводить в биоразлагаемые блок-сополимеры. Безусловно, другие многочисленные лекарственные средства из различных классов терапевтических агентов хорошо подходят для доставки из водных композиций блок-сополимеров, как описано в настоящей заявке. Также специально не показаны все блок-сополимеры, которые могут быть получены и которые демонстрируют важнейшее свойство термического гелеобразования. Однако специалисту в данной области техники будет сразу же очевидна возможность выполнения различных модификации без выхода за рамки настоящего изобретения, которое ограничено только приведенными ниже пунктами формулы изобретения и их функциональными эквивалентами.

Настоящее изобретение относится к биоразлагаемым и биоабсорбируемым блок-сополимерам в виде твердого порошка или воскообразного порошка. Описана композиция блок-сополимера типа АВ, ABA или ВАВ для введения лекарственного средства, при этом указанный блок-сополимер содержит: по меньшей мере первый блок-сополимерный компонент типа АВ, ABA или ВАВ, содержащий первый гидрофобный А-блок и первый гидрофильный В-блок, причем первый гидрофобный А-блок представляет собой биоразлагаемый сложный полиэфир, содержащий по меньшей мере 60% капролактона и по меньшей мере один второй полиэфир-образующий мономер, при этом указанный первый гидрофильный В-блок имеет первую среднюю молекулярную массу и содержит полиэтиленгликоль; по меньшей мере второй блок-сополимерный компонент типа АВ, ABA или ВАВ, содержащий второй гидрофобный А-блок и второй гидрофильный В-блок, при этом второй гидрофобный А-блок содержит биоразлагаемый сложный полиэфир, а второй гидрофильный В-блок имеет вторую среднюю молекулярную массу и содержит полиэтиленгликоль, причем вторая средняя молекулярная масса отличается от первой средней молекулярной массы; при этом общая средневесовая молекулярная масса блок-сополимерной композиции составляет от 1500 до 10000 Дальтон, общее содержание А-блока в композиции составляет примерно от 60 до 85% по массе, а общее содержание В-блока в композиции составляет примерно от 15 до 40% по массе, причем общая средневесовая молекулярная масса В-блока в композиции составляет от 300 до 2000 Дальтон, при этом указанная композиция блок-сополимера является твердой при комнатной температуре, способна к обратимому термическому гелеобразованию при получении в виде водного полимерного раствора и способна превращаться в водный полимерный раствор менее чем за тридцать минут при перемешивании без применения добавок или нагревания свыше 60°C. Также описан способ введения теплокровному животному по меньшей мере одного лекарственного средства в форме с контролируемым высвобождением, включающий: (1) обеспечение композиции блок-сополимера типа АВ, ABA или ВАВ указанной выше, (2) получение водного полимерного раствора указанной твердой композиции путем объединения сополимера с водой без воздействия температуры свыше 60°C; и (3) введение указанного водного полимерного раствора указанному теплокровному животному. Описан способ получения указанной выше композиции. Технический результат - получение композиций для введения лекарственного средства, обладающих улучшенной стабильностью, имеющих требуемые характеристики высвобождения лекарственного средства, набухания и растворения. 3 н. и 12 з.п. ф-лы, 4 ил., 3 табл., 9 пр.
1. Композиция блок-сополимера типа АВ, ABA или ВАВ для введения лекарственного средства, при этом указанный блок-сополимер содержит:
по меньшей мере первый блок-сополимерный компонент типа АВ, ABA или ВАВ, содержащий первый гидрофобный А-блок и первый гидрофильный В-блок,
причем первый гидрофобный А-блок представляет собой биоразлагаемый сложный полиэфир, содержащий по меньшей мере 60% капролактона и по меньшей мере один второй полиэфир-образующий мономер, при этом указанный первый гидрофильный В-блок имеет первую среднюю молекулярную массу и содержит полиэтиленгликоль;
по меньшей мере второй блок-сополимерный компонент типа АВ, ABA или ВАВ, содержащий второй гидрофобный А-блок и второй гидрофильный В-блок, при этом второй гидрофобный А-блок содержит биоразлагаемый сложный полиэфир, а второй гидрофильный В-блок имеет вторую среднюю молекулярную массу и содержит полиэтиленгликоль, причем вторая средняя молекулярная масса отличается от первой средней молекулярной массы;
при этом общая средневесовая молекулярная масса блок-сополимерной композиции составляет от 1500 до 10000 Дальтон, общее содержание А-блока в композиции составляет примерно от 60 до 85% по массе, а общее содержание В-блока в композиции составляет примерно от 15 до 40% по массе, причем общая средневесовая молекулярная масса В-блока в композиции составляет от 300 до 2000 Дальтон,
при этом указанная композиция блок-сополимера является твердой при комнатной температуре, способна к обратимому термическому гелеобразованию при получении в виде водного полимерного раствора и способна превращаться в водный полимерный раствор менее чем за тридцать минут при перемешивании без применения добавок или нагревания свыше 60°C.
2. Композиция блок-сополимера по п. 1, отличающаяся тем, что указанная композиция блок-сополимера представляет собой водный полимерный раствор, подходящий для парентерального введения.
3. Композиция блок-сополимера по п. 1, отличающаяся тем, что общее содержание А-блока в композиции составляет от 65 до 80%, а общее содержание В-блока в композиции составляет от 20 до 35%.
4. Композиция блок-сополимера по п. 1, отличающаяся тем, что общее содержание А-блока в композиции составляет от 67 до 75%, а общее содержание В-блока в композиции составляет от 25 до 33%.
5. Композиция блок-сополимера по п. 1, отличающаяся тем, что второй сложнополиэфирный мономер содержит остатки по меньшей мере одного из D,L-лактида, D-лактида, L-лактида, D,L-молочной кислоты, D-молочной кислоты, L-молочной кислоты, гликолида, гликолевой кислоты, ε-гидроксигексановой кислоты, γ-бутиролактона, γ-гидроксимасляной кислоты, δ-валеролактона, δ-гидроксивалериановой кислоты, гидроксимасляных кислот, яблочной кислоты или их сополимеров.
6. Композиция блок-сополимера по п. 1, отличающаяся тем, что биоразлагаемый сложный полиэфир первого А-блока содержит по меньшей мере 85% капролактона.
7. Композиция блок-сополимера по п. 1, отличающаяся тем, что общая средняя молекулярная масса В-блока в композиции составляет от 1200 до 1500 дальтон.
8. Композиция блок-сополимера по п. 1, отличающаяся тем, что указанная твердая порошкообразная композиция блок-сополимера способна образовывать указанный водный полимерный раствор менее чем за 30 минут без воздействия дополнительных агентов или температур, превышающих 60°C, способна к набуханию, составляющему менее чем 5% после 30 дней воздействия воды, и способна высвобождать примерно от 10 до 15% паклитаксела в течение пяти дней и от 15 до 20% паклитаксела в течение 20 дней.
9. Композиция блок-сополимера по п. 8, отличающаяся тем, что содержание лекарственного средства в указанной композиции составляет примерно от 0,01 до 20% по массе.
10. Способ введения теплокровному животному по меньшей мере одного лекарственного средства в форме с контролируемым высвобождением, включающий:
(1) обеспечение композиции блок-сополимера типа АВ, ABA или ВАВ для введения лекарственного средства по п. 1,
(2) получение водного полимерного раствора указанной твердой композиции путем объединения сополимера с водой без воздействия температуры свыше 60°C; и
(3) введение указанного водного полимерного раствора указанному теплокровному животному.
11. Способ по п. 10, отличающийся тем, что указанный водный полимерный раствор подходит для парентерального введения.
12. Способ по п. 10, отличающийся тем, что указанный сополимер образует гель после введения указанному теплокровному животному.
13. Способ по п. 10, отличающийся тем, что указанный водный полимерный раствор содержит лекарственное средство.
14. Способ по п. 13, отличающийся тем, что содержание лекарственного средства в указанном водном полимерном растворе составляет примерно от 0,01 до 20% по массе.
15. Способ получения твердой композиции блок-сополимера, включающий:
(1) обеспечение композиции блок-сополимера типа АВ, ABA или ВАВ для введения лекарственного средства по п. 1,
(2) лиофильную сушку указанного блок-сополимера с получением композиции блок-сополимера, при этом указанная композиция блок-сополимера является твердой при комнатной температуре, способна к обратимому термическому гелеобразованию при получении в виде водного полимерного раствора и способна превращаться в водный полимерный раствор менее чем за тридцать минут при перемешивании без применения добавок или нагревания свыше 60°C.
| US 7135190 B2, 14.11.2006 | |||
| US 7018645 B1, 28.03.2006 | |||
| БИОРАЗРУШАЕМЫЕ ТРЕХБЛОЧНЫЕ СОПОЛИМЕРЫ СЛОЖНОГО ПОЛИЭФИРА И ПОЛИЭТИЛЕНГЛИКОЛЯ, ИМЕЮЩИЕ НИЗКУЮ МОЛЕКУЛЯРНУЮ МАССУ И ОБРАТИМЫЕ ТЕРМИЧЕСКИЕ ЖЕЛАТИНИРУЮЩИЕ СВОЙСТВА | 1999 |
|
RU2232779C2 |
| US 6117949 A, 12.09.2000 | |||
| Способ приготовления мыла | 1923 |
|
SU2004A1 |
| Jin Woo Lee, Feng-jun Hua, Doo Sung Lee "Thermoreversible gelation of biodegradable poly(e-caprolactone) and poly(ethylene glycol) multiblock copolymers in aqueous solutions" Journal of Controlled Released 73 (2001), p.315-327 | |||
Авторы
Даты
2015-10-20—Публикация
2010-09-20—Подача