Настоящая заявка относится к способам и системам для планирования лучевой терапии. Настоящая заявка применима, в частности, для идентификации анатомических особенностей на медицинских изображениях и введения в них лучевой терапии.
Лучевая терапия является распространенным терапевтическим методом в онкологии, при котором дозу высокоэнергетического гамма (γ) излучения, пучка частиц или другого излучения вводят в тело пациента для достижения терапевтического эффекта, т.е. ликвидации злокачественной ткани. Множество томографических пучков излучения или единственный пучок излучения модулируют по интенсивности с использованием многостворчатых коллиматоров или элементов для формирования пучка, чтобы с высокой точностью облучать объем мишени, например, злокачественной ткани, с ограничением при этом облучения чувствительных соседних органов с повышенным риском. Сеанс(ы) лучевой терапии планируют перед облучением, на основании по меньшей мере одного планировочного объемного изображения, например, компьютерного томографического (КТ) изображения или подобного изображения опухоли и окружающей ткани. Компьютеризированная система планирования автоматически или полуавтоматически сегментирует границы объема мишени и здоровой окружающей ткани, некоторая часть которой является чувствительными органами с повышенным риском, которые не должны пересекаться пучком излучения. С помощью информации о границах, система планирования оптимизирует параметры модуляции интенсивности, чтобы подавать излучение, главным образом, внутри контуров, соответствующих объемам злокачественных опухолей, при ограничении дозы облучения внутри контуров, соответствующих органов с повышенным риском. Чтобы обеспечить полное облучение мишени, вокруг полученного контура объема мишени определяют постоянную граничную область для учета неопределенностей, например, движения органа и положения пациента. А именно, мишень увеличивают на постоянную граничную область во всех направлениях, чтобы повысить вероятность того, что мишень облучают точно. Применение постоянной граничной области к неопределенности может приводить к ненадлежащему облучению рака, излишнему лучевому поражению окружающей ткани или тому и другому.
Например, при планировании лечения рака предстательной железы, предстательную железу оконтуривают и идентифицируют как объем мишени, а такие органы, как мочевой пузырь, прямая кишка, головки бедренной кости и т.д., оконтуривают и идентифицируют как органы с повышенным риском, лучевую нагрузку на которые следует ограничить. Поскольку упомянутые органы находятся в определенной непосредственной близости, то обычное решение добавления постоянной граничной области к объему мишени представляет риск в отношении упомянутых чувствительных органов. Отказ от добавления граничной области представляет риск, что рак не будет полностью ликвидирован.
Настоящая заявка предлагает новые и усовершенствованные способ и устройство для планирования лучевой терапии, которые решают вышеупомянутые и другие проблемы.
В соответствии с одним аспектом, предлагается способ сегментации изображений анатомических особенностей. Способ содержит этап идентификации контура поверхности по меньшей мере одного интересующего объекта в наборе многомерных данных и этап определения непостоянной граничной области на основании идентифицированного контура поверхности, при этом к идентифицированному контуру поверхности добавляют непостоянный контур.
В соответствии с еще одним аспектом, предлагается способ лучевой терапии. Способ содержит этап сбора набора многомерных данных объекта лечения и этап реконструкции набора многомерных данных в по меньшей мере одно представление изображения по меньшей мере одной анатомической особенности объекта лечения. Представление изображения сегментируют в соответствии со способом сегментации изображений.
В соответствии с еще одним аспектом, предлагается система лучевой терапии. Система лучевой терапии содержит сканер диагностического изображения, систему введения излучения и процессор для планирования лучевой терапии, запрограммированный для выполнения способа сегментации изображений анатомических особенностей.
В соответствии с еще одним аспектом, предлагается устройство для обработки изображений. Устройство для обработки изображений содержит блок сегментации, который идентифицирует контур поверхности по меньшей мере одного интересующего объекта в наборе многомерных данных, и блок маскирования, который определяет непостоянную граничную область на основании идентифицированного контура поверхности и добавляет полученную определением непостоянную граничную область к идентифицированному контуру поверхности.
В соответствии с еще одним аспектом, предлагается система лучевой терапии. Система лучевой терапии содержит сканер диагностического изображения, который собирает набор многомерных данных объекта лечения и формирует по меньшей мере одно представление изображения интересующего объекта из набора многомерных данных, и устройство обработки изображений.
Одно из преимуществ заключается в том, что снижают лучевую нагрузку на здоровую ткань.
Дополнительные преимущества настоящего изобретения станут очевидными специалистам со средним уровнем компетентности в данной области техники после прочтения и изучения нижеследующего подробного описания.
Изобретение может принимать форму различных компонентов и схем расположения компонентов, и различных этапов и схем расположения этапов. Чертежи предназначены только для иллюстрации предпочтительных вариантов осуществления и не подлежат истолкованию в смысле ограничения изобретения.
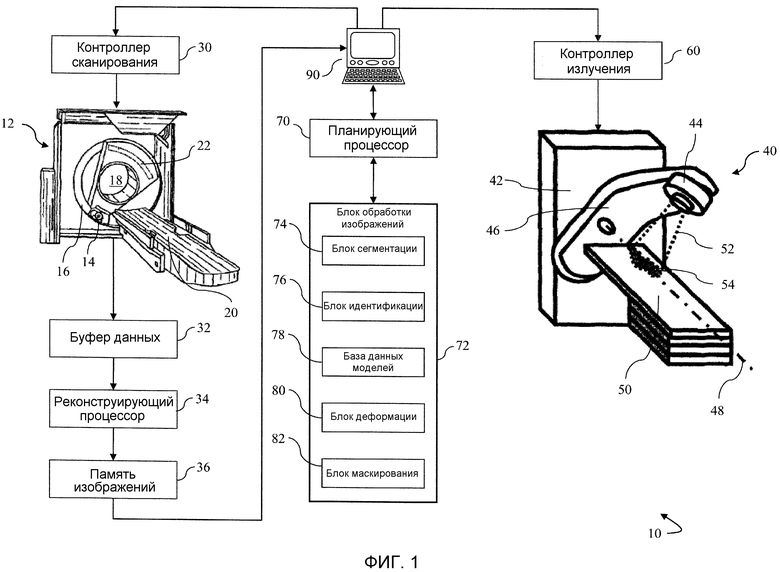
Фиг. 1 - схематическое изображение системы лучевой терапии с блоком обработки изображений для определения непостоянной граничной области;
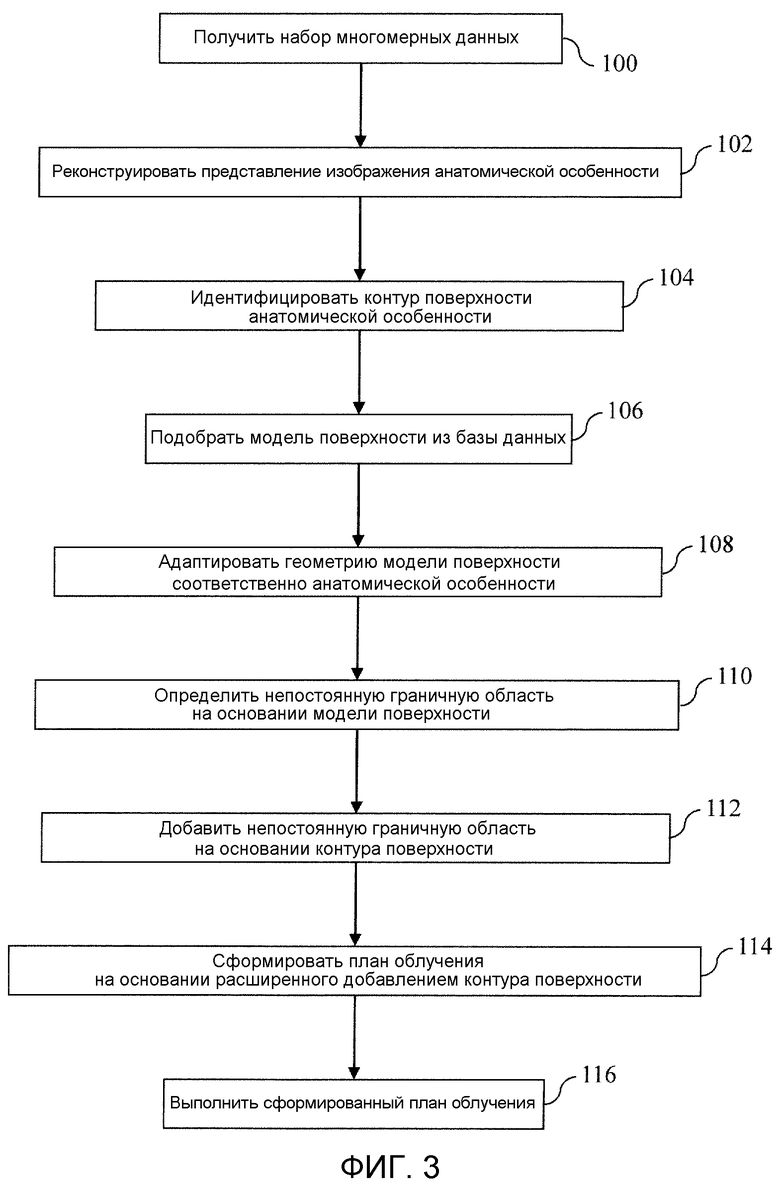
Фиг. 2 - двумерный аксиальный срез интересующего объекта и добавленная непостоянная граничная область; и
Фиг. 3 - блок-схема последовательности операций способа сегментации изображений для определения непостоянной граничной области.
Как показано на Фиг. 1, система 10 терапии, например, система лучевой терапии, содержит сканер 12 для диагностической визуализации, например, компьютерный томографический (КТ) сканер, МРТ-сканер (сканер для магнитно-резонансной томографии) или сходное устройство для получения диагностических изображений для применения при планировании протокола лучевой терапии. КТ-сканер 12 содержит рентгеновский источник 14, смонтированный на поворотном гентри 16. Рентгеновский источник 14 формирует рентгеновское излучение, проходящее сквозь область 18 исследования, в которой рентгеновское излучение взаимодействует с зоной мишени в объекте лечения (не показанном), размешенном на опоре 20, которая позиционирует зону мишени внутри области 18 исследования. Матрица 22 детекторов рентгеновского излучения расположена с возможностью приема рентгеновского пучка после того, как он проходит сквозь область 18 исследования, в которой рентгеновское излучение взаимодействует с объектом лечения и частично поглощается последним. Следовательно, детектированное рентгеновское излучение содержит информацию, относящуюся к объекту.
КТ-сканер 12 работает с управлением от контроллера 30 для выполнения выбранных последовательностей визуализации выбранной зоны мишени объекта лечения, который подлежит лечению методом лучевой терапии. Последовательности визуализации получают набор многомерных данных диагностической визуализации зоны мишени и прилегающей ткани. Набор данных диагностической визуализации сохраняется в буфере 32 данных. Реконструирующий процессор 34 реконструирует 3-мерные представления изображения из полученных данных визуализации, и реконструированные представления изображений сохраняются в памяти 36 диагностических изображений. В совокупности, КТ-сканер 12, контроллер 30 и реконструирующий процессор 34 образуют средство для формирования диагностического изображения.
Вышеописанная система диагностической визуализации является всего лишь примером. Специалистам в данной области техники должно быть очевидно, что КТ-сканер 12, по желанию, замещают сканерами для диагностической визуализации других типов, например, сканером для магнитно-резонансной томографии (МРТ-сканером), сканером для позитронной эмиссионной томографии (ПЭТ-сканером), сканером для однофотонной эмиссионной компьютерной томографии (ОФЭКТ-сканером) или сходным устройством.
В показанном варианте осуществления, устройство 12 для диагностической визуализации разделено с системой 40 введения терапии, однако данное устройство и данная система могут быть объединены в одном корпусе. Система введения терапии может быть внешней системой введения лучевой терапии или внутренней системой введения лучевой терапии, например, брахитерапии. По желанию, перед диагностической визуализацией, на объект лечения наносят метки, которые остаются в заданном месте для последующей лучевой терапии, чтобы обеспечивать совмещение диагностических изображений с введением лучевой терапии. Предполагаются также другие способы пространственного совмещения получения диагностических изображений и лучевой терапии, например, использование собственных анатомических меток. Предполагается также возможность объединения сканера для диагностической визуализации с устройством лучевой терапии, чтобы уменьшать несовмещение диагностической визуализации и лучевой терапии.
Система 40 введения излучения содержит устройство 42 введения излучения, которое содержит источник 44 излучения, например, линейный ускоритель, сфокусированный рентгеновский источник или что-то подобное, смонтированный на поворотном гентри 46. Гентри 46 поворачивает или пошагово перемещает источник 44 излучения вокруг оси 48 поворота. Опора 50 жестко позиционирует объект лечения с зоной мишени, облучаемой модулированным по интенсивности пучком 52 излучения, формируемым источником 44 излучения. Опора 50 позиционирует и перемещает объект лечения в то время, как гентри 46 поворачивает источник 44 излучения вокруг объекта лечения. Пучок 52 излучения имеет зону 54 поперечного сечения с регулируемой интенсивностью и/или периметром. Пучок 52 излучения может подаваться непрерывно или может импульсно включаться и выключаться в течение терапии. По желанию, на стороне пациента, противоположной источнику, расположена система детектирования излучения для контроля интенсивностей излучения, пересекающего пациента. Данные из детектора могут быть реконструированы в изображение проекций с низкой разрешающей способностью, чтобы контролировать совмещение пучка и мишени и дозу. Система 40 введения излучения работает с управлением от контроллера 60 излучения для выполнения выбранного протокола излучения, назначенного планирующим процессором 70. В совокупности, система 40 введения излучения, контроллер 60 излучения и планирующий процессор 70 образуют средство для введения лучевой терапии.
Планирующий процессор 70, который образует средство для планирования лучевой терапии, определяет план лучевой терапии на основании диагностических представлений изображений интересующего объекта и клинических органов, полученных из устройства 12 визуализации. Интересующий объект может быть злокачественной опухолью или патологическим изменением, которое должно получить лучевую терапию от системы 40 введения излучения. Критические структуры включают в себя здоровую или чувствительную ткань, которую следует сберегать в максимальной возможной степени или считать более приоритетной по сравнению с некритической тканью, например, спинной мозг или подобную ткань. Обычно, после того, как интересующий объект локализован и идентифицирован, то к контуру поверхности интересующего объекта добавляют изотропную граничную область, чтобы расширить область облучения, что повышает вероятность того, что весь интересующий объект подвергнут облучению, т.е. анатомические структуры, соответствующие добавленной граничной области, получат одинаковую дозу облучения. Граничная область учитывает неопределенность движения, связанную с движением в течение сеанса лечения, например, дыхательным движением, движением сердца и т.п., или даже движением между сеансами лечения, например, позиционированием пациента, наполнением прямой кишки или мочевого пузыря и т.п. Недостаток добавления изотропной граничной области состоит в том, что, если интересующий объект претерпевает движение только в одном направлении или даже двух направлениях, то изотропная граничная область предполагает движение во всех направлениях равным образом, что приведет к излишнему облучению здоровой ткани.
Как также показано на Фиг. 1, блок 72 обработки изображения, который связан с планирующим процессором 70, а также образует средство для обработки изображений, определяет анизотропную или непостоянную граничную область на основании характеристик интересующего объекта и/или критических структур, проекций движения и источников потенциальной ошибки. Блок обработки изображений содержит блок 74 сегментации, который образует средство для сегментации, которое автономно или полуавтономно определяет границы контура поверхности интересующего объекта и критических структур по полученному диагностическому представлению изображения. Предполагается возможность применения любого из известных способов сегментации, например, кластеризации, выделения признаков, на основе модели и т.п. Блок 76 идентификации, который образует средство для идентификации, сопоставляет выделенный контур поверхности с опорными данными. Опорные данные содержат базу 78 данных моделей поверхностей, соответствующих различным органам и/или типам тканей, из которых подбирают подходящую модель поверхности соответственно выделенному контуру интересующего объекта. Методы подбора могут содержать алгоритмы оценивания по максимуму правдоподобия, нейронные сети и т.п.
С каждой моделью поверхности связана непостоянная граничная область. Например, модель поверхности содержит множество областей, при этом каждая область имеет связанную с ней ширину граничной области. Ширина граничной области в отдельных областях модели поверхности может зависеть от ряда факторов. Факторы содержат морфологию интересующего объекта, например, является ли поверхность гладкой, неравномерной, содержащей выступы в виде усиков и т.п. Неопределенность положения границы обусловлено движением в по меньшей мере одном направлении, например, злокачественная опухоль легких может претерпевать движение во фронтальном направлении из-за дыхания; и, поэтому, области модели поверхности, которые перпендикулярны среднему направлению перемещения, имеют более широкие соответствующие граничные области. Учитывается также физиологическая функция ткани, подлежащей облучению, или функция соседних структур, как критических, так и некритических, и близость к критическим структурам. Факторы могут зависеть от системы 40 введения излучения, например, ширины пучка, интенсивности пучка, рассеяния пучка, скорости гентри, колебаний или вибраций гентри и т.п. В дополнение к ширине граничной области, каждая область модели поверхности может также иметь весовой коэффициент, соответствующий интенсивности пучка лучевой терапии, вводимого в анатомическую структуру, соответствующую данной области. В одном варианте осуществления, весовой коэффициент является постоянным, так что соответствующая граничная область работает как ступенчатая функция. В другом варианте осуществления, весовой коэффициент является нелинейной, например, градиентной функцией, в соответствии с которой интенсивность пучка возрастает/снижается к краю граничной области, противоположному интересующему объекту. Например, весовой коэффициент можно также выбирать для введения излучения по схеме, которая устанавливает границы назначенной дозы по краевым зонам мишени с выбираемой достоверностью, например, вероятностью 99%, что назначенная доза вводится во все части мишени, или вероятностью 95%.
Блок 80 деформации, который образует средство для деформирования, адаптирует поверхность модели поверхности, чтобы обеспечить соответствие геометрии контура поверхности интересующему объекту. Блок 82 маскирования, который образует средство для маскирования, добавляет непостоянную граничную область к интересующему объекту, и планирующий процессор 70 формирует карту интенсивностей на основании расширенного добавлением контура поверхности интересующего объекта и контуров критических структур. На Фиг. 2 изображен пример аксиального 2-мерного среза модели 84 поверхности интересующего объекта с добавленной непостоянной граничной областью 86. Результирующее перемещение интересующего объекта происходит в z-направлении, следовательно, непостоянная граничная область 86 в данном направлении шире, для учета неопределенностей положения поверхностей, перпендикулярных или, по существу, перпендикулярных направлению перемещения. Поверхности, по существу, параллельные направлению перемещения, т.е. y-направлению в показанном варианте осуществления, имеют суженную, соответствующую им непостоянную граничную область 86. Карта интенсивности размечает траектории, геометрические параметры и/или интенсивность терапевтического пучка для контроллера излучения, чтобы управлять системой 40 введения излучения. Планирующий процессор выдает карту интенсивности на пульт 90. Пульт 90 содержит графический пользовательский интерфейс, а также содержит устройство пользовательского ввода, которое врач может использовать для управления контроллером 30 сканера или контроллером 60 излучения, чтобы выбирать, соответственно, последовательности или протоколы сканирования и схемы или дозы лечения в соответствии со сформированной картой интенсивности. Пульт представляет диагностические изображения, экранные инструменты сегментации, модели поверхности, непостоянные граничные области и т.п. В совокупности, блок 74 сегментации, блок 76 идентификации, база 78 данных, блок 80 деформации и блок 82 маскирования образуют средство для формирования непостоянной граничной области.
Пульт 90 содержит графический пользовательский интерфейс, а также содержит устройство пользовательского ввода, которое врач может использовать для управления контроллером 30 сканера или контроллером 60 излучения, чтобы выбирать, соответственно, последовательности или протоколы сканирования и схемы или дозы лечения. Пульт представляет диагностические изображения, экранные инструменты сегментации, карты интенсивности, модели поверхности и т.п.
Как показано на Фиг. 3, планирующий процессор 70 содержит процессор, запрограммированный компьютерной программой, при этом компьютерная программа хранится на машиночитаемом носителе, чтобы выполнять способ лучевой терапии и способ сегментации изображений. Машиночитаемый носитель может содержать оптическую память, магнитную память или твердотельную память, например, компакт-диски (CD), универсальные цифровые диски (DVD), флэш-память, микросхемы оперативной памяти (RAM) или подобные устройства.
Способ сегментации изображений и лучевой терапии, как показано на блок-схеме последовательности операций способа, содержит этап 100 сбора набора многомерных данных, например, данных изображения или проекций из сканера диагностического изображения. Набор данных реконструируют на этапе 102 в представление изображения анатомической особенности, которая подлежит исследованию. На этапе 104 идентифицируют контур поверхности анатомической особенности. Например, может быть сегментирована и выделена граница опухоли. На этапе 106 подбирают модель поверхности соответственно контуру поверхности. Подбор основан на морфологии, положении, движении, результатах предварительного лечения, функциональности интересующего объекта и т.п. На этапе 108, модель поверхности подгоняют к геометрии анатомической особенности. Каждая модель поверхности имеет непостоянную граничную область, соответствующую данной модели. На этапе 110, для анатомической особенности определяют непостоянную граничную область на основании модели поверхности и соответствующего непостоянной граничной области вместе с другими факторами, изложенными ранее. Соответствующую непостоянную граничную область корректируют или оптимизируют на основании факторов, которые обычно являются специфическими для пациента. На этапе 112, непостоянную граничную область добавляют к контуру поверхности анатомической особенности, и на этапе 114, с учетом вышеизложенного, формируют план лучевой терапии. План лучевой терапии исполняют на этапе 116, например, вводят гамма-излучение в анатомическую особенность пациента, соответствующую расширенной добавлением модели поверхности.
В другом варианте осуществления, моделируют последующие контрольные представления изображений, например, методами Монте-Карло или подобными методами, с использованием расширенной добавлением модели поверхности и статистических данных, описывающих вероятность деформации и/или функциональных изменений анатомической особенности. Для множества планов лучевой терапии, сформированных по последующим контрольным представлениям изображений, определяют вероятность обезвреживания опухоли (TCP) и вероятность осложнений в нормальной ткани (NTCP). Планы лучевой терапии классифицируют по отношению TCP/NTCP и наилучший план выбирают.
В другом варианте осуществления, толщина граничной области является равномерной для органа. При нормальной клинической практике, статистические данные и разброс положения и функциональных характеристик органа отсутствуют или требуют большого объема вычислений для использования. Для повседневного применения, определяют границы органов, и некоторые интересующие области (ROI) согласуют с предварительно заданной моделью, после чего упомянутые области используют в целевых функциях. Определяют границы интересующей области (ROI). Соответствующие контуры интересующей области (ROI) согласуют с моделью. Поверхность каждой модели имеет разные зоны, для каждой зоны задают расстояние до фактической границы и весовой коэффициент. Контуры модели поверхности расширяют. Целевые функции, которые используют контуры органов, определяют вместе с расширенными контурами с их весовыми коэффициентами. С помощью коллекции планов с (искусственными) последующими контрольными изображениями, определяется расстояние до фактической границы и весовой коэффициент для каждой зоны модели. Объединение зон в одну целевую функцию определяется функциональной архитектурой (последовательной или параллельной) органа и типом используемой целевой функции (биологическим или физическим ограничением).
В другом варианте осуществления, планирующий процессор 70 формируют на перспективу адаптивный план лучевой терапии на основании добавленного непостоянной граничной области. КТ-сканер 12 получает планировочное изображение интересующего объекта, и по данному изображению определяется непостоянная граничная область с использованием средства для формирования непостоянной граничной области. Планирующий процессор формирует план лучевой терапии соответственно расширенному добавлением интересующему объекту. Сформированный план терапии содержит множество сеансов воздействия излучением, при этом, перед каждым сеансом, КТ-сканер 12 или другое средство для диагностической визуализации получает вспомогательное изображение интересующего объекта для совмещения пациента и для контроля за развитием лечения. Планирующий процессор сравнивает морфологию, положение и т.п. текущего интересующего объекта с ранее найденными значениями, например, из планировочного изображения или ранее полученных вспомогательных изображений. Если разность удовлетворяет предварительно выбранному порогу, то непостоянная граничная область корректируется в соответствии с текущим контуром поверхности. Таким образом, планирующий процессор адаптивно корректирует непостоянную граничную область в процессе плана терапии. Соответственно, текущий сеанс лечения и/или остающийся план лучевой терапии корректируется для учета изменений расширенного добавлением интересующего объекта. Аспекты, которые корректируются, содержат дозу облучения, траекторию пучка, геометрию пучка и/или график сеансов лечения; однако, предполагается также наличие других аспектов.
Выше изобретение описано со ссылкой на предпочтительные варианты осуществления. После прочтения и изучения вышеприведенного подробного описания, специалистами могут быть созданы модификации и внесены изменения. Предполагается, что изобретение следует интерпретировать как включающее в себя все упомянутые модификации и изменения в той мере, насколько они содержатся в объеме притязаний прилагаемой формулы изобретения или ее эквивалентов.
Изобретение относится к области планирования лучевой терапии. Техническим результатом является снижение лучевой нагрузки на здоровую ткань за счет того, что к идентифицированному контуру поверхности добавляют непостоянную граничную область. Способ содержит этапы, на которых идентифицируют контур поверхности по меньшей мере одного интересующего объекта в наборе многомерных данных и определяют непостоянную граничную область на основании идентифицированного контура поверхности и по меньшей мере одного из морфологии поверхности интересующего объекта и анизотропного движения поверхности интересующего объекта, при этом непостоянная граничная область шире в направлении, перпендикулярном направлению движения, чем в направлении, параллельном направлению движения; причем к идентифицированному контуру поверхности добавляют непостоянную граничную область. 4 н. и 10 з.п. ф-лы, 3 ил.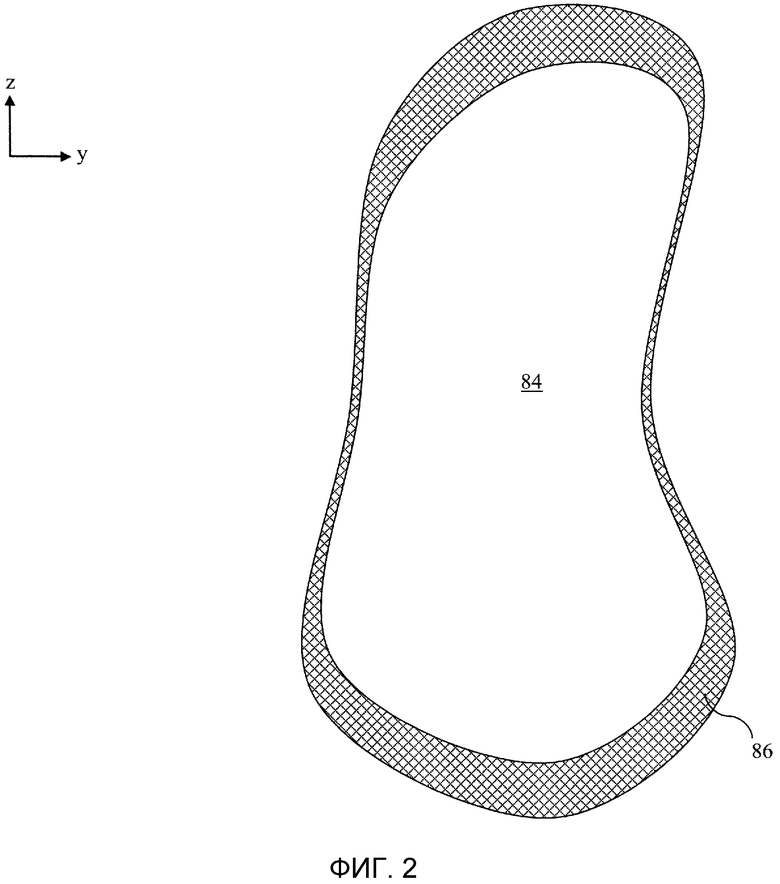
1. Способ сегментации изображений анатомических особенностей, при этом способ содержит этапы, на которых:
идентифицируют контур поверхности по меньшей мере одного интересующего объекта в наборе многомерных данных; и
определяют непостоянную граничную область на основании идентифицированного контура поверхности и по меньшей мере одного из морфологии поверхности интересующего объекта и анизотропного движения поверхности интересующего объекта, при этом непостоянная граничная область шире в направлении, перпендикулярном направлению движения, чем в направлении, параллельном направлению движения;
причем к идентифицированному контуру поверхности добавляют непостоянную граничную область.
2. Способ по п. 1, дополнительно включающий в себя этапы, на которых:
идентифицируют модель поверхности на основании контура поверхности; и
определяют непостоянную граничную область на основании модели поверхности.
3. Способ по п. 2, в котором модель поверхности включает в себя множество элементов поверхности, которые определяют поверхность модели поверхности, при этом каждый элемент поверхности описывает ширину и весовой коэффициент участка непостоянной граничной области, соответствующего данному элементу поверхности.
4. Способ по любому из пп. 2 и 3, в котором этап идентификации модели поверхности дополнительно содержит этапы, на которых:
подбирают модель поверхности соответственно контуру поверхности по меньшей мере одного интересующего объекта; и
адаптируют поверхность модели поверхности так, чтобы она соответствовала геометрии контура поверхности по меньшей мере одного интересующего объекта.
5. Способ по п. 4, в котором подбор модели поверхности соответственно контуру поверхности по меньшей мере одного интересующего объекта основан по меньшей мере на одном из положения, морфологии, движения или функциональности интересующего объекта.
6. Машиночитаемый носитель данных, содержащий компьютерную программу, которая управляет процессором для выполнения способа по любому из пп. 1-5.
7. Система (10) лучевой терапии, содержащая:
сканер (12) для диагностической визуализации;
систему (40) введения излучения и
процессор (70) для планирования лучевой терапии, запрограммированный для выполнения способа по пп. 1-5.
8. Устройство (72) обработки изображений, содержащее:
блок (74) сегментации, который идентифицирует контур поверхности по меньшей мере одного интересующего объекта в наборе многомерных данных; и
блок (82) маскирования, который определяет непостоянную граничную область на основании идентифицированного контура поверхности и добавляет определенную непостоянную граничную область к идентифицированному контуру поверхности.
9. Устройство (72) обработки изображений по п. 8, дополнительно содержащее:
блок (76) идентификации, который идентифицирует модель поверхности, выбираемую из базы (78) данных моделей поверхности, на основании идентифицированного контура поверхности.
10. Устройство (72) обработки изображений по любому из пп. 8 и 9, в котором непостоянная граничная область основана по меньшей мере на одном из анизотропного движения, морфологии поверхности, неопределенности положения, близости к другим органам и вероятности распределения дозы.
11. Устройство (72) обработки изображений по п. 9, в котором модель поверхности включает в себя множество элементов поверхности, которые определяют поверхность модели поверхности, при этом каждый элемент поверхности описывает ширину и весовой коэффициент участка непостоянной граничной области, соответствующего данному элементу поверхности.
12. Устройство (72) обработки изображений по п. 9, дополнительно включающее в себя:
блок (80) деформации, который подбирает модель поверхности соответственно контуру поверхности по меньшей мере одного интересующего объекта и адаптирует поверхность модели поверхности так, чтобы она соответствовала геометрии контура поверхности по меньшей мере одного интересующего объекта.
13. Устройство (72) обработки изображений по п. 12, в котором подбор модели поверхности соответственно контуру поверхности по меньшей мере одного интересующего объекта основан по меньшей мере на одном из положения, морфологии, движения или функциональности интересующего объекта.
14. Устройство (72) обработки изображений по любому из пп. 11-13, в котором модель поверхности является сеточной моделью поверхности и каждый элемент поверхности является многоугольным сеточным элементом.
| US20050111621 A1, 26.05.2005 | |||
| US200900226060 A1, 10.09.2009 | |||
| WO2009095837 A2, 06.08.2009 | |||
| РЕНТГЕНОВСКИЕ СРЕДСТВА ДЛЯ ОПРЕДЕЛЕНИЯ МЕСТОПОЛОЖЕНИЯ И ЛУЧЕВОЙ ТЕРАПИИ ЗЛОКАЧЕСТВЕННЫХ НОВООБРАЗОВАНИЙ | 2000 |
|
RU2209644C2 |
Авторы
Даты
2015-10-27—Публикация
2010-11-18—Подача