Изобретение относится к области биотехнологии, микробиологической, комбикормовой и перерабатывающей промышленности и может быть использовано для получения питательных сред, используемых в процессах выращивания посевных культур микроорганизмов.
Целлюлозосодержащее сырье имеется практически в неограниченных количествах в виде древесины, соломы, отходов переработки сельхозпродукции. Однако его эффективное превращение в биологически усвояемые сахара является сложной задачей. Проблема использования ресурсов целлюлозосодержащего сырья осложняется тем, что существующие традиционные технологии гидролиза растительного сырья с применением сильных кислот и щелочей связаны с образованием значительного количества побочных продуктов, ингибирующих рост микроорганизмов и биосинтез ими ряда целевых веществ. Поэтому важнейшей задачей является разработка оптимального способа приготовления питательных сред для выращивания биомассы микроорганизмов на основе гидролизатов целлюлозосодержащего сырья, например пшеничной соломы.
Известен способ получения питательного субстрата для производства кормовых дрожжей, включающий гидролиз растительного сырья концентрированной серной кислотой, инверсию, нейтрализацию гидролизата натронным щелоком до рН 4,5-6,0 и отделение лигнина от субстрата, субстрат после отделения от лигнина упаривают в 2-3 раза, осаждают сульфат натрия (А.с. СССР №973612, C12N 1/22, 1982).
К недостаткам известного способа относится необходимость нейтрализации остаточного количества кислоты щелочами, что приводит к образованию в гидролизате дополнительных количеств минеральных солей в виде сульфатов. Также к недостаткам данного аналога можно отнести высокие расходы гидролизующих агентов, большую длительность процесса, сложность аппаратурного оформления, высокую трудоемкость и фондоемкость производства.
Известен способ быстрого кислотного гидролиза лигноцеллюлозного материала минеральными кислотами с одновременным десорбированием части продуктов гидролиза (патент РФ 2189996, С08Н 5/04, D21C 3/20, D21C 3/04, D21C 7/00, C07G 1/00, B01J 19/24, 2002). Известный способ включает непрерывный кислотный гидролиз с одновременной делигнификацией и осахариванием в одном реакционном цикле с использованием растворяющего лигнин органического растворителя и сильной неорганической кислоты с выделением высококонцентрированного сахара.
К недостаткам данного способа относится то, что сахаросодержащие гидролизаты загрязняются продуктами распада лигнина. Кроме того, применение органических растворителей (сорбентов) при рабочих температурах гидролиза создает повышенную пожароопасность.
Известен способ гидролиза и фракционирования биомассы, основанный на новых видах кинетики углеводородного гидролиза, предусматривающий подачу твердой исходной биомассы или твердой частично фракционированной лигноцеллюлозной биомассы, по крайней мере, в один проточный реактор непрерывного действия со сжимающимся слоем (патент RU 2194078, С13К 1/00, 2002).
К недостаткам данного способа относится то, что при этом способе непрерывно вводится разбавленная минеральная кислота в объеме, превышающем объем аппарата в 2 раза. Эта операция приводит к повышенному расходу кислоты и разбавлению гидролизата, что ограничивает его применение в микробиологических синтезах или требует дополнительных затрат энергии на упаривание.
Известен способ приготовления питательной среды для выращивания дрожжей, включающий гидролиз смеси измельченных соломы и отрубей сернистой кислотой сначала при температуре 120-130°С в течение 60-90 минут, затем при температуре 165-190°С в течение 25-40 минут с последующей отгонкой остаточного количества сернистого газа с абсорбцией его водой. Гидролизат разделяют центрифугированием, и осветленный гидролизат используют для приготовления питательной среды (патент РФ №2510842, МПК C12N 1/22, C12N 1/16, 2014).
Недостатками данного способа являются необходимость проведения отгонки остаточного количества сернистого газа, проведение нескольких стадий гидролиза и большая продолжительность процесса.
Известен способ получения гидролизата для ферментационной среды, в котором жом сахарного тростника гидролизуют фосфорной кислотой в течение 300 минут при температуре 122°С и концентрации фосфорной кислоты в гидролизуемой массе 4 масс. % (Study of the hydrolysis of sugar cane bagasse using phosphoric acid / S. Gamez [and ets.] // Journal of Food Engineering. - 2006. - №74. - P. 78-88). Затем от полученного гидролизата отделяют твердую фазу. Доля сахаров (редуцирующих веществ) от содержания растворимых веществ в растворимых продуктах гидролиза составляет не менее 55 масс. %. Данный способ выбран в качестве прототипа.
К недостаткам прототипа относятся большая продолжительность процесса, что вызывает образование побочных токсичных продуктов, таких как уксусная кислота, фурфурол и гидроксиметилфурфурол, что требует очистки полученного гидролизата, и перерасход гидролизующего агента, приводящий к высокому остаточному количеству фосфорной кислоты в конечном продукте, что снижает скорость роста микроорганизмов.
Задачей заявляемого технического решения является снижение расхода фосфорной кислоты и уменьшение продолжительности процесса гидролиза.
Поставленная задача решается тем, что в способе получения гидролизата для приготовления питательной среды для выращивания микроорганизмов, включающем гидролиз измельченного растительного сырья фосфорной кислотой, отделение твердой фазы, согласно изобретению гидролизу подвергают солому при концентрации фосфорной кислоты в гидролизуемой массе 1 масс. % и гидролиз проводят при температуре 180-190°С в течение 20 минут.
Техническим результатом предлагаемого изобретения является снижение расхода гидролизующего агента и сокращение продолжительности процесса гидролиза при увеличении выхода редуцирующих веществ (РВ).
В предлагаемом способе гидролизу подвергают солому. Это доступное сырье, имеющееся в больших количествах и содержащее до 70% полисахаридов. Гидролиз осуществляют при температуре 180-190°С. Применение более высоких температур гидролиза по сравнению с прототипом позволяет сократить расход фосфорной кислоты. Достаточной является концентрация фосфорной кислоты в гидролизуемой массе 1,0 масс. %. При этом остаточное количество фосфатов в полученном нейтрализованном гидролизате соответствует потребности микроорганизмов, культивируемых на гидролизных средах, и в 3-4 раза меньше, чем в прототипе. При концентрации фосфорной кислоты менее 1,0 масс. % увеличивается продолжительность процесса гидролиза. Повышение концентрации кислоты более 1 масс. % приводит к образованию побочных продуктов и снижению доли РВ в гидролизате, и концентрация фосфатов в получаемых средах будет избыточной.
Известно, что при высоких температурах гидролиза ускоряются реакции разрушения и карамелизация сахаров, полученных при гидролизе полисахаридов, однако воздействие высокой температуры в предлагаемом способе кратковременно и составляет 20 минут, при этом разрушение сахаров незначительно, не более 0,1-0,2 масс. %. Снижение температуры процесса гидролиза ниже 180°С приводит к увеличению его продолжительности, а увеличение температуры выше 190°С даже при уменьшении продолжительности процесса приводит к образованию побочных продуктов, вызывающих потемнение гидролизата, и, следовательно, к уменьшению доли РВ в гидролизате.
Заявляемые режимные условия проведения гидролиза в совокупности обеспечивают достижение концентрации редуцирующих веществ в гидролизате не менее 2,5 масс. %, что соответствует оптимальной концентрации для роста микроорганизмов.
Изобретение поясняется следующими конкретными примерами выполнения способа.
Во всех примерах использовали пшеничную солому 17% влажности. Измельченное сырье предварительно высушивали до постоянного веса.
Пример 1.
Навески сырья 3,3 г помещали в просушенные капсулы, добавляли 15,2 г воды и 4 г фосфорной кислоты с концентрацией 5,65 масс. % (концентрация кислоты в гидролизуемой массе - 1 масс. %). Общая масса загрузки каждой капсулы составила 22,5 г. Капсулы закрывали, помещали в прогретую до температуры 180°С ванну термостата. Проводили процесс гидролиза при данной температуре в течение 20 минут. Затем капсулы быстро охлаждали и отделяли негидролизованный осадок центрифугированием. В полученном гидролизате определяли содержание редуцирующих веществ по методу Бертрана (Емельянова И.З. Химико-технологический контроль гидролизных производств / И.З. Емельянова. - М.: Лесная промышленность, 1976. - 405 с.).
Примеры 2-5 аналогичны примеру 1, режимные условия приведены в таблице.
Анализ табличных данных показывает, что доля редуцирующих веществ от растворимых веществ гидролизата в заявляемом способе составляет 64,45 масс. %, а в прототипе - 55 масс. %. При этом общее содержание полисахаридов в пшеничной соломе и жоме сахарного тростника отличается незначительно и составляет 62-71% и 65-80% соответственно (). Следовательно, по сравнению с прототипом, предлагаемый способ, при уменьшении продолжительности процесса и снижении расхода гидролизующего агента, позволяет увеличить выход РВ.
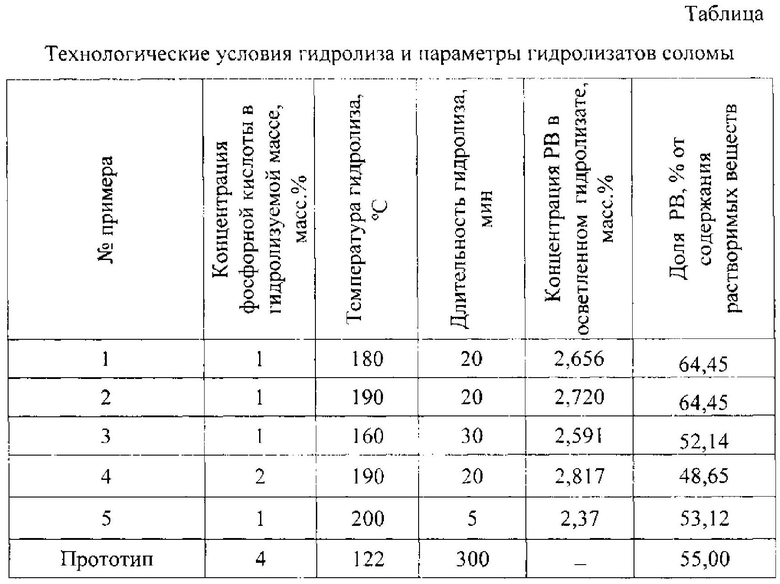
Как видно из табличных данных, снижение температуры гидролиза ниже 180°С (пример 3) приводит к увеличению продолжительности процесса в 1,5 раза и снижению выхода РВ, а увеличение температуры свыше 190°С (пример 5) даже при значительном снижении продолжительности процесса гидролиза приводит к образованию побочных продуктов, вызывающих потемнение гидролизата, что снижает выход РВ.
Повышение концентрации кислоты (пример 4) также приводит к образованию побочных продуктов, поэтому доля РВ в гидролизате снижается.
В предлагаемом способе расход фосфорной кислоты в 5 раз меньше и продолжительность процесса гидролиза в 15 раз меньше, чем в прототипе, а доля РВ в сухих веществах полученного гидролизата на 14% больше. При этом остаточного количества фосфатов в гидролизате достаточно для обеспечения потребности в фосфоре микроорганизмов, культивируемых на гидролизных средах.
Получаемый по заявляемому способу гидролизат может быть использован для приготовления на его основе питательной среды для выращивания посевных культур сахаромицетов, кормовых дрожжей и других аэробных микроорганизмов и их ассоциаций. При этом нет необходимости подачи фосфатов в питательную среду.
Таким образом, предлагаемый способ получения гидролизата для приготовления питательной среды для выращивания микроорганизмов по сравнению с прототипом позволяет снизить расход гидролизующего агента и сократить продолжительность процесса гидролиза при увеличении выхода редуцирующих веществ.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения гидролизата для приготовления питательной среды для выращивания микроорганизмов | 2024 |
|
RU2831194C1 |
| СПОСОБ ПРИГОТОВЛЕНИЯ ПИТАТЕЛЬНОЙ СРЕДЫ ДЛЯ ВЫРАЩИВАНИЯ ДРОЖЖЕЙ | 2012 |
|
RU2510842C2 |
| Способ приготовления питательной среды для выращивания дрожжей | 1988 |
|
SU1606532A1 |
| СПОСОБ ПОЛУЧЕНИЯ БЕЛКОВО-ВИТАМИННОГО КОРМА | 2007 |
|
RU2391859C2 |
| Питательная среда для выращивания дрожжей | 1985 |
|
SU1317019A1 |
| СПОСОБ ПОЛУЧЕНИЯ ОСНОВЫ ПИТАТЕЛЬНЫХ СРЕД ДЛЯ КУЛЬТИВИРОВАНИЯ МИКРООРГАНИЗМОВ | 1994 |
|
RU2061038C1 |
| СПОСОБ ПРИГОТОВЛЕНИЯ ПИТАТЕЛЬНОГО СУБСТРАТА ДЛЯ ВЫРАЩИВАНИЯ КОРМОВЫХ ДРОЖЖЕЙ | 1991 |
|
RU2022009C1 |
| СПОСОБ ПОЛУЧЕНИЯ БИОЭТАНОЛА ИЗ ЦЕЛЛЮЛОЗОСОДЕРЖАЩЕГО СЫРЬЯ | 2018 |
|
RU2701643C1 |
| СПОСОБ ПОЛУЧЕНИЯ БИОЭТАНОЛА ИЗ ЛИГНОЦЕЛЛЮЛОЗНОГО СЫРЬЯ | 2015 |
|
RU2581799C1 |
| Способ получения фурфурола и кормовых дрожжей | 1984 |
|
SU1330155A1 |
Изобретение относится к области биотехнологии. Предложен способ получения гидролизата для приготовления питательной среды для выращивания микроорганизмов. Способ включает гидролиз измельченной соломы фосфорной кислотой при температуре 180-190°С в течение 20 минут и при концентрации фосфорной кислоты в гидролизуемой массе 1 мас.%. Затем проводят отделение твердой фазы. Преимуществом изобретения является снижение расхода гидролизующего агента и сокращение продолжительности процесса гидролиза при увеличении выхода редуцирующих веществ. 1 табл., 5 пр.
Способ получения гидролизата для приготовления питательной среды для выращивания микроорганизмов, включающий гидролиз измельченного растительного сырья фосфорной кислотой, отделение твердой фазы, отличающийся тем, что гидролизу подвергают солому при концентрации фосфорной кислоты в гидролизуемой массе 1 мас.% и гидролиз проводят при температуре 180-190°C в течение 20 минут.
| S | |||
| GAMEZ et al | |||
| Study of the hydrolysis of sugar cane bagasse using phosphoric acid // Journal of Food Engineering, 2006, p | |||
| Парный автоматический сцепной прибор для железнодорожных вагонов | 0 |
|
SU78A1 |
| СПОСОБ ПРИГОТОВЛЕНИЯ ПИТАТЕЛЬНОЙ СРЕДЫ ДЛЯ ВЫРАЩИВАНИЯ ДРОЖЖЕЙ | 2012 |
|
RU2510842C2 |
| СПОСОБ ПРИГОТОВЛЕНИЯ ПИТАТЕЛЬНОЙ СРЕДЫ ДЛЯ ПОЛУЧЕНИЯ ЛАБОРАТОРНОЙ ЗАКВАСКИ БИФИДОБАКТЕРИЙ | 1988 |
|
SU1515430A1 |
Авторы
Даты
2015-11-20—Публикация
2014-12-30—Подача