Изобретение относится к области медицины, а именно челюстно-лицевой хирургии, и направленно на создание многокомпонентного остеогенного трансплантата, применяемого при хирургическом лечении врожденных и приобретенных дефектов кости челюстей. Известен способ восстановления дефекта костной ткани (Jose R. Perez, Dimitrios Kouroupis, Deborah J. Li, Thomas M. Best, Lee Kaplan and Diego Correa. Tissue Engineering and Cell-Based Therapies for Fractures and Bone Defects. Front. Bioeng. Biotechnol., 31 July 2018. doi.org/10.3389/fbioe.2018.00105), при использовании которого осуществляют хирургический доступ к дефекту, заполняют дефект биотрансплантатом и закрывают раневую поверхность. В качестве биотрансплантата использовали трехмерный остеотрансплантат, полученный в результате направленной остеогенной дифференцировки трехмерного хондротрансплантата из культивированных хондробластов и межклеточного матрикса. В частности, заполнение дефекта остеотрансплантатом осуществляют таким образом, чтобы остеотрансплантат примыкал к краям дефекта по всей поверхности полости дефекта.
Недостатком известного способа является неконтролируемое изменение объема остеогенного трансплантата в послеоперационном периоде.
Известен способ расчета объема костного дефекта и объема костнопластического материала, проведенного на основании полученных из спиральных томографов объемных биомоделей кости путем точного определения объема дефекта, требующего выполнить процедуру регенерации кости, и обоснованного использования полученных биореплик для расчета объема костнопластического материала перед планированием операции по восстановлению кости. Для получения высококачественной биореплики проводится компьютерная аксиальная томография (КТ) с использованием медицинской спирально-конической лучевой машины без контрастных фильтров или реконструкции полученного регистра, затем изображения восстанавливали из необработанного формата DICOM. Гранулированную фракцию костнопластического материала подвергают композиционному порошковому формованию по технологии быстрого прототипирования, путем литья физического объекта в трех измерениях методом агглютинации последовательности слоев порошка. После того, как получили модель в порошке, ее инфильтрировали для придания модели окончательных физических свойств, таких как твердость, температурный допуск и т.д. Инфильтрация - заключительный этап процесса состоит из инфильтрации модели одним из материалов, выбранных в соответствии с требованиями готового продукта. Эти материалы проникают вглубь полученного блока и связывают гранулы и затвердевают в композитное порошковое тело (
 Calvo-Guirado,
Calvo-Guirado, 
 Rafael Delgado-Ruiz, Maria-Piedad
Rafael Delgado-Ruiz, Maria-Piedad 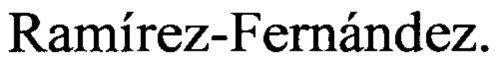 Calculation of bone graft volume using 3D reconstruction system. MedOralPatolOralCirBucal. 2011. Marl; 16(2):e260-doi: 10.4317/medoral. 16.e260 ttp://dx.doi.org/doi: 10.4317/medoral. 16.e260).
Calculation of bone graft volume using 3D reconstruction system. MedOralPatolOralCirBucal. 2011. Marl; 16(2):e260-doi: 10.4317/medoral. 16.e260 ttp://dx.doi.org/doi: 10.4317/medoral. 16.e260).
Ключевыми недостатками данного метода являются:
- в результате спекания гранул удаляется сквозная пористость трансплантата, что препятствует прорастанию сосудов, миграции клеточных элементов крови и остеобластов из краев дефекта в толщу трансплантата и делает невозможным его биодеградацию и биотрансформацию в оптимальные сроки послеоперационного периода;
- костнопластический блок не содержит аутологичных структур мезенхимально-стромальной фракции, тробоцитарной массы и факторов роста сосудов, не содержит дентальный имплантат.
- невозможно провести одномоментную установку дентального имплантата из-за хрупкости костнопластического блока, полученного таким способом, что отмечено самими авторами способа.
Наиболее близким к заявляемому способу (прототипом) является «Способ наращивания объема костной ткани в зонах дефекта альвеолярного отростка челюсти» (патент RU 2570034 С1). Сущность способа заключается в наращивании объема костной ткани в зонах дефекта альвеолярного отростка челюсти и включает забор из передней брюшной стенки методом липосакции жировой ткани, последующую ее ферментацию с добавлением коллагеназы, центрифугирование и получение стромально-васкулярной фракции, при этом в качестве остеокондуктивного материала используют пористые никелид-титановые гранулы, которые насыщают клетками полученным из стромально-васкулярной фракции и размещают в зоне дефекта, с последующим приданием требуемого объема восстанавливаемой костной ткани с помощью ксеногенного костного матрикса, который также укладывают в зону дефекта с последующим ушиванием раны.
В заявленном техническом решении после проведения ферментной обработки жировой ткани из нее получают клетки стромально-васкулярной фракции (СВФ).
Сущность прототипа заключается в том, что полученные клетки стромально-васкулярной фракции жировой ткани (далее СВФЖТ) доставляют в зону дефекта альвеолярного отростка с помощью никелид-титановых гранул с приданием требуемого объема, с последующим закрытием области дефекта ксеногенным костным матриксом (мембраной) и ушиванием раны. При этом в качестве остеокондуктивного материала использован никелид-титановый порошок (в виде гранул), пропитанный стромально-васкулярной фракцией (полученной из жировой ткани), и ксеногенный костный матрикс (мембрана). Таким образом, заявленное техническое решение разработано с целью наращивания объема костной ткани альвеолярного отростка челюсти в качестве подготовительного этапа для последующей операции дентальной имплантации.
Недостатки прототипа:
- при планировании костной пластики дефекта не учитывается высокий коэффициент естественного уплотнения гранул никелид-титана, опускающихся в нижнюю часть дефекта в послеоперационном периоде, это препятствует костеобразованию и делает крайне затруднительным, а порой невозможным, выполнение второй операции дентальной имплантации, когда формирование фрезами ложа имплантата при прохождении через металлические гранулы приводит к перегреву этой области, выкрашиванию гранул никелид-титана и нарушению формирования необходимого диаметра под ложе имплантата.
- смешивание титановой крошки и клеток мезенхимально-стромальной фракции сразу после центрифугирования противоречит протоколу применения клеточных структур, что неоднократно продемонстрировано в научной литературе;
- клеточная масса мезенхимально-стромальной фракции сразу после ферментации и центрифугирования представляет собой дезорганизованную клеточную массу жидкой консистенции, клетки которой находятся в стрессе и не в состоянии фиксироваться к любым поверхностям, они не могут пропитывать металлические гранулы, как утверждают авторы способа, ввиду отсутствия физической способности металла к насыщению жидкостью, даже имея поры, это препятствует фиксации клеток на гранулах никелид-титана и, соответственно, использоваться в таком виде в качестве костнопластического элемента не может;
- не проводится специальная подготовка ксеногенного материала (мембраны) перед внесением в рану.
Задачей настоящего изобретения является устранение указанных недостатков.
Поставленная задача решается за счет того, что известные компоненты объединяются в новую совокупность связей с новыми количественными и качественными характеристиками - многокомпонентный остеогенный трансплантат, который включает: аутологичный клеточный пул стромально-васкулярной фракции (Компонент №1-10%), тромбоцитарную массу (Компонент №2-5%), фибриноген аутологичной плазмы крови пациента (Компонент №3-20%), гранулированный остеокондуктивный костнопластический материал животного происхождения (Компонент №4-55%) и дентальный имплантат (Компонент №5-10%).
Техническим результатом способа изготовления многокомпонентного остеогенного трансплантата при хирургическом устранении дефектов кости челюстей является ряд стадий, направленных на изготовление многокомпонентного остеогенного трансплантата.
Суть способа изготовления многокомпонентного остеогенного трансплантата. Приступают к приготовлению пропорциональных объемов Компонентов №1, 2, 3. Для приготовления Компонента №1 методом туменисцентной липоаспирации производится забор 200 мл жировой ткани из области передней брюшной стенки, жировая ткань многократно отмывается фосфатно-солевым раствором, подвергается ферментативной обработке раствором коллагеназы 1 типа, после чего выделяются клетки стромально-васкулярной фракции, которые помещаются в стерильные культуральные чашки Петри с ростовой средой, а затем ставятся в газовый CO2 инкубатор для культивирования при температуре +37°С и содержании CO2 - 5% на 7-14 дней до достижения монослоя, после чего клетки 2-3-кратно пассируют до достижения 50 млн клеток; в день готовности к операции трансплантации у пациента производится пункция кубитальной вены, забор периферической крови в объеме 40 мл в 4-е пробирки с К2 ЭДТА для приготовления Компонентов №2 и №3, пробирки центрифугируются двукратно: первоначально с целью оседания эритроцитов и лейкоцитов, затем отбирается плазма крови из 4 пробирок в пробирку для получения Компонента №3, при втором центрифугировании получаем 6 мл Компонента №2, в день операции к 2 мл Компонента №3 добавляется Компонент №4.
Компонент №4 проходит стадию дегазации. Перед объединением, для увеличения свободной площади внутренних поверхностей трансплантата, заполненных воздухом, Компонент №4 проходит стадию дегазации путем погружения в физиологический раствор при +37°С по 20 минут в термостате двукратно (Рисунок 1). Опытным путем установлено, что при погружении компонента №4 в течение 20 минут в физраствор при 37 градусах происходит вытеснение воздуха из всех полостей и каналов Компонента №4. Температура 37 градусов взята, так как она совпадает с температурой инкубатора клеток для подготовки компонентов 1, 2, 3 и для снижения испытания стресса клетками при их объединении и размещении в реципиентном ложе. Физиологический раствор использован для дегазации так его как парциальное давление (0,9) соответствует парциальному давлению сыворотки крови. Дегазацию проводят двукратно потому, что первоначально удаляют воздух и мелкие частицы материала, а затем удаляют остатки газов, в результате чего поры и каналы становятся доступными для клеточных элементов компонентов 1, 2, 3 и прорастания сосудов из реципиентного ложа. Это позволяет увеличить площадь контакта с внутренними поверхностями трансплантата и увеличить коэффициент поглощения костнопластическим материалом тканевой жидкости, клеточных элементов и сыворотки крови, мигрирующих с периферии реципиентного ложа в трансплантат. Увеличенный таким образом внутренний объем трансплантата, за счет вытеснения воздушных пузырей, становится доступным для большей диффузии Компонентами №1, 2, 3. Этап подготовки материала с помощью вышеописанной дегазации является новым по сравнению с описанными аналогами и прототипом и позволяет достигнуть нового результата: улучшения биотрансформации костнопластического материала в полноценную кость и сохранения расчетного объема реставрируемой кости, что позволяет избежать послеоперационных осложнений, повторных хирургических вмешательств и оптимизировать сроки лечения.
После проведения дегазации Компонента №4 в него вносится Компонент №1 в объеме 15 млн клеток, затем вносится Компонент №2, затем добавляется 200 мкл стерильного раствора глюконата кальция, после чего проводят инкубацию полученной смеси при температуре +37 градусов 5-15 минут, до формирования фибринового сгустка, флакон с многокомпонентным остеогенным костнопластическим трансплантатом стерильно упаковывается, маркируется, транспортируется до операционной в термоконтейнере при комнатной температуре, в операционной за 40 минут до операции трансплантации Компонент №5 вносится во флакон с фракцией остеогенного костнопластического трансплантата (Компоненты: №1; №2; №3; №4) для смачивания и фиксации Компонентами №2 и 3 поверхности Компонента №5, пациент готовится к операции, раскрывается костный дефект, изучается визуально, подготовленный таким образом Компонент №5 устанавливается в дефект кости, затем окутывая Компонент №5, укладываются рассчитанные объемы компонентов №1; 2; 3; 4 и моделируются параболоидно поверх Компонента №5 с перекрытием его тела и заглушки по лекалу профильного шаблона, в результате чего вновь объединяются все пять компонентов в многокомпонентный остеогенный трансплантат. Трансплантат укрывается изолирующей мембраной, которая фиксируется поверх трансплантата, далее производится поэтажный раскрой слизисто-надкостничного лоскута, рана ушивается наглухо, пациент наблюдается четыре месяца, затем проводится контрольная визуализация остеогенной биотрансформации многокомпонентного трансплантата, раскрывается и извлекается заглушка Компонента №5, на ее место устанавливается формирователь десны, затем через три недели устанавливаются слепочные трансферы и снимаются оттиски челюстей, далее в зуботехнической лаборатории изготавливается зубная коронка на импланте, коронка фиксируется на абатмент, установленный на Компонент №5, лечение закончено.
Изобретение иллюстрируется изображениями, где
на фиг. 1 - КЛКТ верхней челюсти пациентки, в аксиальной А и фронтальной Б проекциях. Определение проектируемых границ размещения трансплантируемого костно-пластического материала,
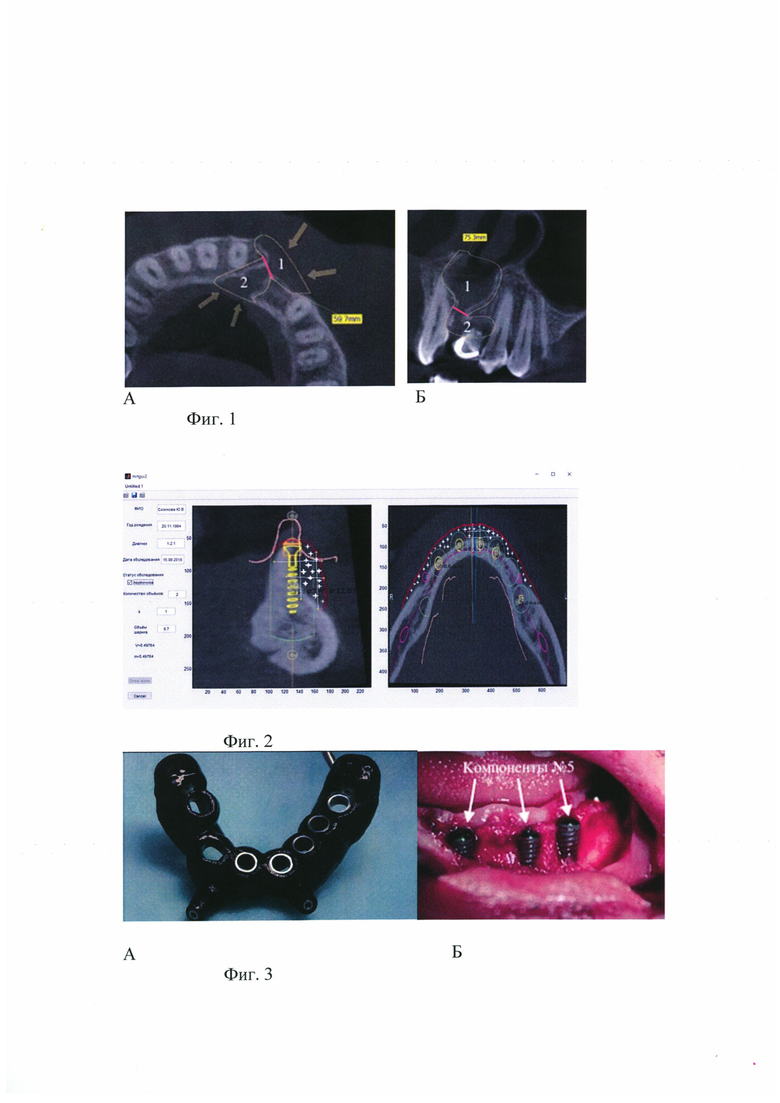
на фиг. 2 - Вид окна программы для ЭВМ с расстановкой имплантов и дизайном границ многокомпонентного остеогенного трансплантата на этапе расчета объема дефекта и количества материала,
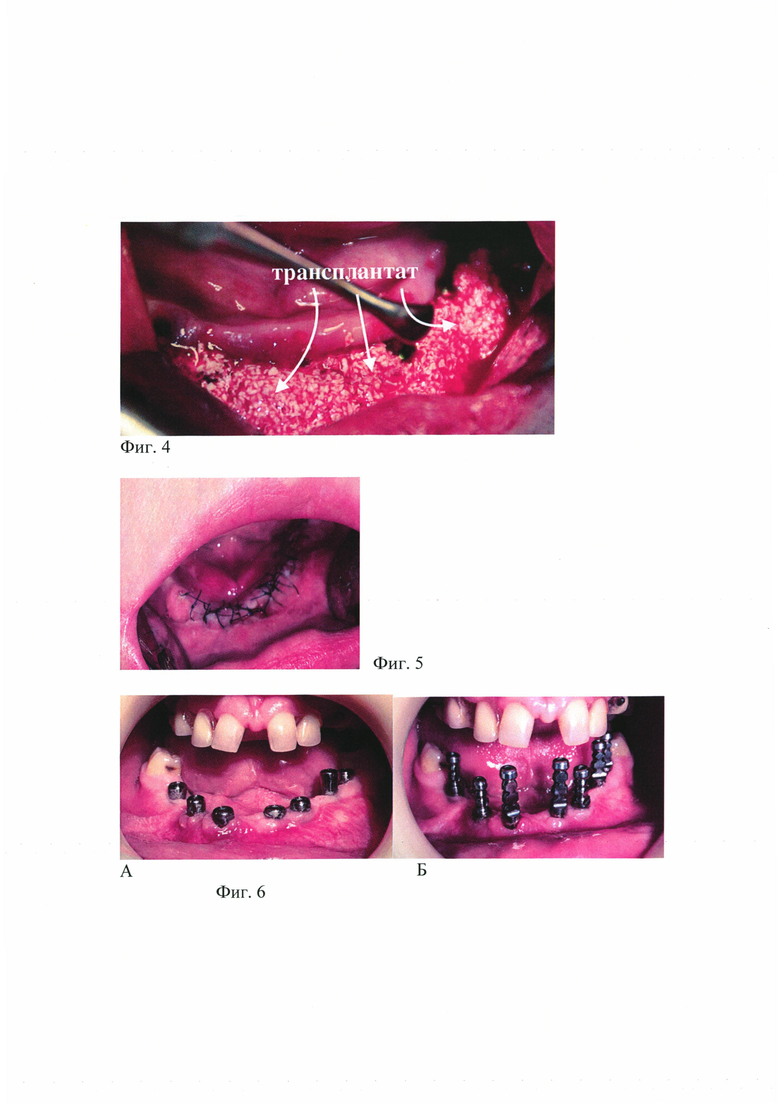
на фиг. 3 - А - Навигационный шаблон. Б - Компоненты №5 многокомпонентного остеогенного трансплантата установлены в костную ткань дефекта,
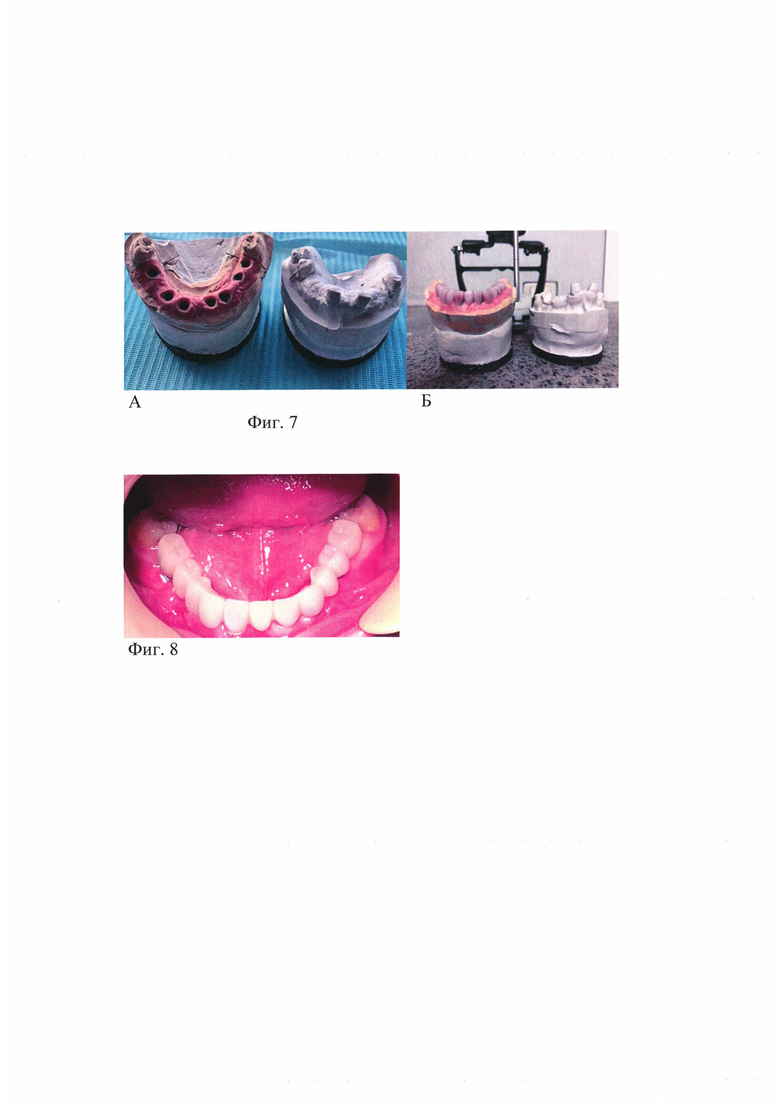
на фиг. 4 - Многокомпонентный остеогенный трансплантат уложен в реципиентное ложе,
на фиг. 5 - Многокомпонентный остеогенный трансплантат укрыт мембраной и слизисто-надкостничным лоскутом, наложены швы, рана ушита наглухо. Вид раневой поверхности на вторые сутки после устранения врожденного дефекта,
на фиг. 6 - А. Формирователи установлены на Компоненты №5. Б. На Компоненты №5 установлены трансферы для снятия слепка с нижней челюсти,
на фиг. 7 - А - вид гипсовой модели с аналогами Компонентов №5. Б - вид конструкций из воска,
на фиг. 8 - Зубные протезы установлены на Компоненты №5 трансплантата. Слизистая оболочка бледно-розового цвета, зубные протезы адекватно прилегают к слизистой оболочке, не травмируя ее.
Предлагаемое изобретение реализовано в клиническом примере.
Клинический пример. Пациентка С., 32-х лет, обратилась с жалобами на отсутствие зубов на нижней челюсти, возникшее после смены молочного прикуса. Диагноз: врожденная первичная адентия нижней челюсти в пределах 3.6 4.6, нефиксированная высота прикуса, нестабильная окклюзия.
4.6, нефиксированная высота прикуса, нестабильная окклюзия.
Разработанный план лечения пациентки включал три этапа: 1. Этап планирования: 3D расчет объема дефекта и прорисовка дизайна планируемых границ элиминации внутреннего и аугментации наружного сегментов дефекта; 2. Этап: прогностический расчет требуемого количества компонентов трансплантата; 3. Этап приготовления требуемого объема многокомпонентного остеогенного трансплантата.
В программе для ЭВМ по 3D рентгенологическому изображению костей черепа проводится определение топографии и дизайна сложного дефекта кости челюсти в аксиальной, фронтальной и сагиттальной плоскости, затем сложный дефект разбиваем на два геометрически простых сегмента: №1 - наружный, расположенный по наружному рельефу кости, и №2 - внутренний, полый и щелевидный (Фиг. 1).
На фиг. 1 - КЛКТ верхней челюсти пациентки С., в аксиальной А и фронтальной Б проекциях. Определение проектируемых границ размещения трансплантируемого костно-пластического материала.
Полый сегмент №2 планируют устранить методом элиминации, а наружный №1 - аугментации. Проектируют контуры элиминации и аугментации сегментов и профильный шаблон наружного рельефа реконструкции. В объеме дефекта учитывают объем дентального импланта, объем которого рассчитывают, как объем цилиндра (Фиг. 2). На фиг. 2 показан вид окна программы для ЭВМ с расстановкой имплантов и дизайном границ многокомпонентного остеогенного трансплантата на этапе расчета объема дефекта и количества материала.
Ввиду различного естественного уплотнения костнопластического материала в полом и наружном дефекте для определения требуемого количества костнопластического материала раздельно рассчитывают данные для элиминации сегмента №2, имеющего несколько костных стенок, и аугментации сегмента №1, с одной костной стенкой, применяя коэффициент уплотнения. Согласно расчету объем сегмента №1 равен 2,85 см3, а сегмента №2 равен 2,40 см3. В результате экспериментов установлены коэффициент уплотнения и коэффициент насыщения жидкостью для материала "Cerabone", который использован в качестве Компонента №4. Объем сегмента №1-2,85 см3 умножают на коэффициент 1,25 и получают, что для его аугментации необходимо 3,56 см3 костнопластического материала, затем объем сегмента №2-2,40 см3 умножают на коэффициент 1,15 и получают, что для его аугментации необходимо 2,76 см3 костнопластического материала, складывая полученные объемы и определяют, что для устранения костного дефекта в 5,25 см3 необходимо использовать 6,32 см3 Компонента №4. Затем фракция Компонента №4-6,32 см3 объединяется с Компонентами №1, 2, 3.
За 40 минут до операции дентальный имплантат (Компонент №5) для фиксации на его поверхности плазмы сыворотки крови вносится во флакон с фракцией Компонентов №1; №2; №3; №4 остеогенного костнопластического трансплантата. Таким образом, все компоненты, в указанных выше соотношениях и согласно полученным объемам, объединяются в новую совокупность связей с новыми количественными и качественными характеристиками - многокомпонентный остеогенный тканеспецифичный трансплантат: аутологичный клеточный пул стромально-васкулярной фракции (Компонент №1), тромбоцитарная масса (Компонент №2), фибриноген аутологичной сыворотки крови пациента (Компонент №3), остеокондуктивный костнопластический материал животного происхождения (Компонент №4) и дентальный имплантат (Компонент №5). Пациент готовится к операции известным способом, раскрывается костный дефект, изучается визуально, на зубной ряд накладывается навигационный шаблон для установки Компонентов №5, последние извлекаются из многокомпонентной фракции и устанавливаются в кость дефекта (Фиг. 3). На фиг. 3 показаны: А - Навигационный шаблон, Б - Компоненты №5 многокомпонентного остеогенного трансплантата установлены в костную ткань дефекта.
Затем, окутывая дентальный имплантат, порционно укладывается весь рассчитанный объем фракции многокомпонентного остеогенного трансплантата и моделируется параболоидно поверх имплантата с перекрытием его тела и заглушки по границам профильного шаблона, в результате чего все пять составляющих многокомпонентного остеогенного трансплантата размещены в реципиентном ложе, согласно профилю наружного рельефа реконструкции (Фиг. 4).
На фиг. 4. Показано. Как многокомпонентный остеогенный трансплантат уложен в реципиентное ложе.
Трансплантат укрывается изолирующей мембраной, которая фиксируется известным способом, далее производится поэтажный раскрой слизисто-надкостничного лоскута на несколько подвижных лепестков: надкостницы, подслизистого слоя и слизистой оболочки, которые поочередно укладываются, перекрывая первым лепестком периферию трансплантата и изолирующей мембраны, вторым лепестком перекрывается изолирующая мембрана от края до центра, третьим лепестком перекрывается вся область трансплантации, рана ушивается наглухо (фиг. 5). На фиг. 5 - Многокомпонентный остеогенный трансплантат укрыт мембраной и слизисто-надкостничным лоскутом, наложены швы, рана ушита наглухо. Вид раневой поверхности на вторые сутки после устранения врожденного дефекта.
После четырех месяцев наблюдения на контрольных томограммах определена хорошая биотрансформация трансплантата в костную ткань альвеолярного отростка нижней челюсти без потери объема костнопластического материала. Затем проводится раскрытие заглушек Компонента №5, извлекаются заглушки и в Компоненты №5 устанавливаются формирователи десны, через три недели снимаются слепки с трансферами (фиг. 6). Положение трансферов подтверждает правильное расположение имплантов, полное закрытие их костью и слизистой оболочкой. На фиг. 6 показано: А. - Формирователи установлены на Компоненты №5, Б. - На Компоненты №5 установлены трансферы для снятия слепка с нижней челюсти.
По слепкам в зуботехнической лаборатории известным способом изготавливаются модели челюстей, в которые загипсовываются аналоги Компонентов №5 (Фиг. 7, А). На аналоги устанавливаются абатменты, проводится их параллелометрия и фрезеровка. На абатментах моделируются провизорные конструкции из воска и переносятся для примерки в полость рта. Выстраиваются сагиттальная и аксиальная плоскости, проверяется качество кривой Шпее и угла Беннета, моделируются фронтальная и клыковая направляющие. Затем в лаборатории припасованные восковые шаблоны известным способом переводятся в постоянные конструкции (Фиг. 7, Б).
На фиг.7: А - вид гипсовой модели с аналогами Компонентов №5, Б - вид конструкций из воска.
Изготовленные зубные коронки припасовываются и устанавливаются на абатменты имплантов в полости рта пациентки. Получено хорошее положение зубов и расположение языка, восстановлено полноценное питание, фонетика и эстетический оптимум средней зоны лица. Лечение закончено (Фиг. 8). Слизистая оболочка бледно-розового цвета, зубные протезы адекватно прилегают к слизистой оболочке, не травмируя ее.
Таким образом, основанная на прогностическом расчете новая совокупность физических и биологических связей, возникающая при изготовлении многокомпонентного остеогенного трансплантата, наделяет его новыми качественными и количественными свойствами, что исключает неконтролируемое изменение формы и объема трансплантата в реципиентном ложе в послеоперационном периоде. Это позволяет на этапе планировании операции трансплантации просчитать и устранить риски осложнения лечения, снизить материальные затраты и оптимизировать сроки реабилитации пациента.
Технологическими и клиническими результатами использования предлагаемого способа являются:
- изготовление требуемого количества трансплантата производится не только по геометрическим данным, а по совокупности изменений в послеоперационном периоде физических и биологических показателей, используемого костнопластического материала, которые учитывают характер изменения физических и биологических свойств фракций трансплантата в послеоперационном периоде;
- предлагаемый способ изготовления трансплантата предотвращает неконтролируемое изменение формы и объема трансплантата при устранении наружных (не проникающих в губчатое вещество кости), внутренних (проникающих и сквозных) и сочетанных костных дефектов костей лицевого черепа сложной геометрической формы с восстановлением анатомической формы органа;
- обеспечение предсказуемого поведения трансплантата в проектных границах реципиентного ложа, как при элиминации внутренних, так и при аугментации наружных дефектов кости;
- включение в трансплантат дентального импланта позволяет исключить проведение второй операции и предотвратить нарушение васкуляризации регенерирующей кости в области устраняемого дефекта, что обеспечивает полноценную биотрансформацию костнопластического материала и предсказуемый клинический результат, снижение материальных затрат и психоэмоционального дискомфорта пациента.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ предотвращения неконтролируемого изменения объёма остеогенного трансплантата в послеоперационном периоде после устранении врождённых и приобретённых дефектов кости челюстей | 2021 |
|
RU2778352C2 |
| Многокомпонентный остеогенный трансплантат для хирургического устранения врождённых и приобретённых дефектов кости челюстей | 2021 |
|
RU2766978C1 |
| Способ укладки и стабилизации гранулированных костнопластических материалов в реципиентном ложе при устранении сложных дефектов костей челюстей | 2021 |
|
RU2766977C1 |
| СПОСОБ НАРАЩИВАНИЯ ОБЪЕМА КОСТНОЙ ТКАНИ В ЗОНАХ ДЕФЕКТА АЛЬВЕОЛЯРНОГО ОТРОСТКА ЧЕЛЮСТИ | 2014 |
|
RU2570034C1 |
| Способ определения объёма остеогенного трансплантата при устранении врождённых и приобретённых дефектов кости сложной геометрической формы | 2021 |
|
RU2754190C1 |
| Способ наращивания объема костной ткани гребня альвеолярного отростка челюсти | 2016 |
|
RU2645963C2 |
| СПОСОБ ПЛАСТИКИ АЛЬВЕОЛЯРНОЙ КОСТИ АУТОТКАНЯМИ ЗУБОВ | 2021 |
|
RU2768970C1 |
| Блок имплантата для реконструкции дефектной части кости и способ реконструкции дефектной части кости | 2014 |
|
RU2620494C2 |
| СПОСОБ ВОССТАНОВЛЕНИЯ КОСТИ АЛЬВЕОЛЯРНОГО ГРЕБНЯ ЧЕЛЮСТИ И ТКАНЕЙ ПАРОДОНТА С РЕДУЦИРОВАННЫМ РЕГЕНЕРАТОРНЫМ ПОТЕНЦИАЛОМ | 2006 |
|
RU2320285C2 |
| Способ увеличения объема костной ткани челюсти | 2023 |
|
RU2806519C1 |
Изобретение относится к медицине, а именно челюстно-лицевой хирургии, и может быть использовано для изготовления многокомпонентного остеогенного трансплантата при хирургическом устранении врожденных и приобретенных дефектов кости челюстей. Готовят аутологичный клеточный пул стромально-васкулярной фракции следующим образом: методом туменисцентной липоаспирации производится забор 200 мл жировой ткани из области передней брюшной стенки, жировая ткань отмывается фосфатно-солевым раствором, подвергается ферментативной обработке раствором коллагеназы 1 типа, после чего выделяются клетки стромально-васкулярной фракции, которые помещаются в стерильные культуральные чашки Петри с ростовой средой, а затем ставятся в газовый CO2 инкубатор для культивирования при температуре +37°C и содержании CO2 - 5% на 7-14 дней до достижения монослоя, после чего клетки 2-3 кратно пассируют до достижения 50 млн клеток; у пациента производится пункция кубитальной вены, забор периферической крови в объеме 40 мл в 4-е пробирки с К2 ЭДТА, после чего готовят фибриноген аутологичной плазмы крови пациента и тромбоцитарную массу следующим образом: пробирки центрифугируются двукратно: первоначально с целью оседания эритроцитов и лейкоцитов, затем отбирается плазма крови из 4 пробирок в отдельную пробирку с получением фибриногена аутологичной плазмы крови пациента, далее вновь центрифугируют пробирку с получением 6 мл тромбоцитарной массы, к 2 мл фибриногена аутологичной плазмы крови пациента добавляется остеокондуктивный костнопластический материал животного происхождения, полученная смесь проходит стадию дегазации путем погружения в физиологический раствор при +37°С двукратно по 20 минут каждый в термостате, далее вносится аутологичный клеточный пул стромально-васкулярной фракции в объеме 15 млн клеток, затем вносится тромбоцитарная масса, добавляется 200 мкл стерильного раствора глюконата кальция, после чего проводится инкубация полученной смеси при температуре +37 градусов 15 минут, до формирования фибринового сгустка, с дальнейшей упаковкой в стерильный флакон, маркировкой и транспортировкой до операционной в термоконтейнере при комнатной температуре, в операционной за 40 минут до использования с целью хирургического устранения врожденных и приобретенных дефектов кости челюстей во флакон с указанной выше смесью вносится дентальный имплантат, при этом многокомпонентный остеогенный трансплантат включает: дентальный имплант - 10 об.%, аутологичный клеточный пул стромально-васкулярной фракции - 10 об.%, тромбоцитарная масса - 5 об.%, фибриноген аутологичной плазмы крови пациента - 20 об.%, гранулированный остеокондуктивный костнопластический материал животного происхождения - 55 об.%. Способ обеспечивает устранение рисков осложнения лечения, снижение материальных затрат и сокращение сроков реабилитации пациента за счет исключения неконтролируемого изменение формы и объема трансплантата в реципиентном ложе в послеоперационном периоде. 8 ил.
Способ изготовления многокомпонентного остеогенного трансплантата при хирургическом устранении врожденных и приобретенных дефектов кости челюстей,
отличающийся тем, что
готовят аутологичный клеточный пул стромально-васкулярной фракции следующим образом: методом туменисцентной липоаспирации производится забор 200 мл жировой ткани из области передней брюшной стенки, жировая ткань отмывается фосфатно-солевым раствором, подвергается ферментативной обработке раствором коллагеназы 1 типа, после чего выделяются клетки стромально-васкулярной фракции, которые помещаются в стерильные культуральные чашки Петри с ростовой средой, а затем ставятся в газовый CO2 инкубатор для культивирования при температуре +37°C и содержании CO2 - 5% на 7-14 дней до достижения монослоя, после чего клетки 2-3-кратно пассируют до достижения 50 млн клеток; у пациента производится пункция кубитальной вены, забор периферической крови в объеме 40 мл в 4-е пробирки с К2 ЭДТА, после чего готовят фибриноген аутологичной плазмы крови пациента и тромбоцитарную массу следующим образом: пробирки центрифугируются двукратно: первоначально с целью оседания эритроцитов и лейкоцитов, затем отбирается плазма крови из 4 пробирок в отдельную пробирку с получением фибриногена аутологичной плазмы крови пациента, далее вновь центрифугируют пробирку с получением 6 мл тромбоцитарной массы, к 2 мл фибриногена аутологичной плазмы крови пациента добавляется остеокондуктивный костнопластический материал животного происхождения, полученная смесь проходит стадию дегазации путем погружения в физиологический раствор при +37°С двукратно по 20 минут каждый в термостате, далее вносится аутологичный клеточный пул стромально-васкулярной фракции в объеме 15 млн клеток, затем вносится тромбоцитарная масса, добавляется 200 мкл стерильного раствора глюконата кальция, после чего проводится инкубация полученной смеси при температуре +37 градусов 15 минут, до формирования фибринового сгустка, с дальнейшей упаковкой в стерильный флакон, маркировкой и транспортировкой до операционной в термоконтейнере при комнатной температуре, в операционной за 40 минут до использования с целью хирургического устранения врожденных и приобретенных дефектов кости челюстей во флакон с указанной выше смесью вносится дентальный имплантат, при этом многокомпонентный остеогенный трансплантат включает:
дентальный имплант - 10 об.%,
аутологичный клеточный пул стромально-васкулярной фракции - 10 об.%,
тромбоцитарная масса - 5 об.%,
фибриноген аутологичной плазмы крови пациента - 20 об.%,
гранулированный остеокондуктивный костнопластический материал животного происхождения - 55 об.%.
| СПОСОБ НАРАЩИВАНИЯ ОБЪЕМА КОСТНОЙ ТКАНИ В ЗОНАХ ДЕФЕКТА АЛЬВЕОЛЯРНОГО ОТРОСТКА ЧЕЛЮСТИ | 2014 |
|
RU2570034C1 |
| Способ наращивания объема костной ткани гребня альвеолярного отростка челюсти | 2016 |
|
RU2645963C2 |
| СПОСОБ СОЗДАНИЯ ПЕРСОНАЛИЗИРОВАННОГО ГЕН-АКТИВИРОВАННОГО ИМПЛАНТАТА ДЛЯ РЕГЕНЕРАЦИИ КОСТНОЙ ТКАНИ | 2015 |
|
RU2597786C2 |
| Способ пластики альвеолярного отростка челюсти | 2015 |
|
RU2616337C1 |
| WO 2010092001 A1, 19.08.2010 | |||
| Franceschi RT | |||
| Biological approaches to bone regeneration by gene therapy | |||
| J Dent Res | |||
| Способ обработки целлюлозных материалов, с целью тонкого измельчения или переведения в коллоидальный раствор | 1923 |
|
SU2005A1 |
Авторы
Даты
2022-08-17—Публикация
2021-01-13—Подача