Изобретение относится к выявлению циркулирующих опухолевых клеток, микроэмбол и апоптотических телец в крови больных онкологическими заболеваниями, в частности раком легкого человека с помощью аптамеров.
Для неинвазивной диагностики и мониторинга терапии онкологических заболеваний может использоваться оценка уровня и характеристики опухолевых клеток, микроэмбол и апоптотических телец в крови пациентов (Punnoose E.А. Endpoints in a Phase II Clinical Trial of Pertuzumab and Erlotinib Small Cell Lung Cancer: Association with Clinical - in Non Evaluation of Circulating Tumor Cells and Circulating Tumor DNA / E.A. Punnoose // Clinical Cancer Research. - 2012. - №18. - P.2391-2401).
В ходе развития злокачественных новообразований трансформированные клетки претерпевают ряд преобразований и могут попадать в кровяное русло (Paterlini-Brechot, P. Circulating tumor cells (CTC) detection: Clinical impact and future directions / P. Paterlini-Brechot, N.L. Benali // Cancer Letters. - 2007. - №253. - P.180-204), экспериментально показано, что один грамм опухолевой ткани может высвобождать в кровь около миллиона клеток в сутки (Chang Y.S. Mosaic blood vessels in tumors: frequency of cancer cells in contact with flowing blood / Y.S. Chang, E. di Tomaso, D.M. McDonald, R. Jones, R.K. Jain. L.L. Munn // Proceedings of the national academy of sciences of the United States of America. - 2000. - №97. - P. 14608-14613). Большая часть (85%) опухолевых клеток, попавших в кровоток, погибает, превращаясь в апоптотические тельца; выжившие в кровотоке клетки меняют свои гемодинамические и метаболические свойства и могут обнаруживаться в крови в виде единичных циркулирующих клеток, а также в виде циркулирующих опухолевых микроэмбол - трех или более опухолевых клеток, циркулирующих в крови, объединенных вместе и имеющих пролиферативный потенциал (Ковалев А.А. Гетерогенность циркулирующих опуолевых клеток / А.А. Ковалев, Т.В. Грудинская, Т.П. Кузнецова, К.А. Ковалев // Онкология. - 2012. - Т.14. - №2. - С.126-129).
В настоящее время для неинвазивного выявления циркулирующих опухолевых клеток в образцах периферической крови широко применяются различные коммерческие системы.
Существуют системы ISET (Isolation by Size of Epithelial Tumor Cells, дословно: «отделение эпителиальных опухолевых клеток по размеру», позволяющие отделять в образцах крови с помощью микрофильтров клетки более 11 мкм, эритроциты в которых были заранее разрушены с помощью лизирующего раствора (Metagenex, Paris France; www.metagenex.fr). Использование фильтров позволяет выделять из крови циркулирующие опухолевые клетки, размер которых превышает 10 мкм, а также микроэмболы, размер которых может варьировать от 20 до 130 мкм (Krebs M.G. Evaluation and prognostic significance of circulating tumor cells in patients with non-small-cell lung cancer / M.G. Krebs, R. Sloane, L. Priest, L. Lancashire, J.M. Hou, A. Greystoke, T.H. Ward, R. Ferraldeschi, A. Hughes, G. Clack, M. Ranson, C. Dive, F.H. Blackhall // Journal of clinical oncology. - 2011. - V.29. - №12. - P.1556-1563). Однако данные системы не позволяют улавливать апоптотические тельца, размер которых составляет 0,5-2 мкм (Kosaka N. Circulating microRNA in body fluid: a new potential biomarker for cancer diagnosis and prognosis / N. Kosaka, H. Iguchi, T. Ochiya // Cancer science. - 2010. - V.101. - №10. - P.2087-2092).
В системах Oncoquick реализована сепарация клеток крови с помощью раствора, позволяющего отделять эритроциты и лейкоциты от опухолевых клеток, эпителиальных клеток, тромбоцитов и лейкоцитов низкой плотности (Rosenberg R. Comparison of two density gradient centrifugation systems for the enrichment of disseminated tumor cells in blood / Rosenberg, R. Gertler, J. Friederichs, K. Fuehrer; M. Dahm. R. Phelps. S. Thorban, H. Nekarda, J.R. Siewert // Cytometry. - 2002. - V.49. - №12. - P.150-158). Образцы крови в определенном соотношении осторожно наслаивают на находящийся в пробирке раствор, затем центрифугируют на низких оборотах. В результате образуется несколько отдельных фракций клеток, содержащих эритроциты, лейкоциты и клетки, имеющие низкую плотность - опухолевые и эпителиальные клетки, лейкоциты низкой плотности и тромбоциты. Выделенные фракции клеток, содержащие циркулирующие опухолевые клетки, пропускаются через фильтр, диаметр пор которого составляет 8 мкм и исследуются с помощью цитопатологических, иммунологических, молекулярных методов исследования; ограничения этого подхода включают потерю небольших циркулирующих опухолевых клеток и апоптотических телец и удержание конгломератов лейкоцитов (Gertler R. Detection of circulating tumor cells in blood using an optimized density gradient centrifugation / R. Gertler, R. Rosenberg, K. Fuehrer. M. Dahm, H. Nekarda, J.R. Siewert // Cancer Researh. - 2003. - V.162. - P.149-155).
Системы CellSearch® system основаны на иммуномагнитной сепарации циркулирующих клеток с помощью антител к таким антигенам как, например, EpCAM (молекулы клеточной адгезии) и Cytokeratin (цитокератин); для уменьшения количества ложноположительных результатов в таких методах может использоваться идентификация лимфоцитов в образцах крови с помощью антител к Cd45 (Allard W.J. Tumor cells circulate in the peripheral blood of all major carcinomas but not in healthy subjects or patients with nonmalignant diseases / W.J. Allard, J. Matera, M.C. Miller, M. Repollet, M.C. Connelly, C. Rao, A.G. Tibbe, J.W. Uhr, L.W. Terstappen // Clinical cancer research. - 2004. - №10. - P.6897-6904).
Цитокератин и ЕрСАМ относятся к эпителиальным антигенам, в результате чего специфичные для них антитела могут связываться с эпителиальными клетками неопухолевой природы, которые могут попадать в кровоток в результате воспалительных процессов или после хирургических вмешательств. Кроме того, в ходе развития злокачественной опухоли трансформированные клетки претерпевают ряд преобразований, в которые входит потеря клетками эпителиальных антигенов, в результате чего часть клеток может не быть детектирована. Вследствие этого использование антител к цитокератинам и молекулам клеточной адгезии может снизите точность диагностики онкологических заболеваний.
Наиболее близким аналогом заявляемого изобретения является способ выявления циркулирующих опухолевых клеток в крови с помощью моноклональных антител (Marrinucci D. Fluid biopsy in patients with metastatic prostate, pancreatic and breast cancers / D. Marrinucci, K. Bethel, A. Kolatkar, M.S. Luttgen, M. Malchiodi, F. Baehring, K. Voigt, D. Lazar, J. Nieva, L. Bazhenova, A.H. Ko, M. Korn, E. Schram, M. Coward, X. Yang, T. Metzner, R. Lamy, M. Honnatti, C. Yoshioka, J. Kunken, Y. Petrova, D. Sok, D. Nelson, P. Kuhn//Physical biology. - 2012. - №9. - P.1-9).
Поиск циркулирующих раковых клеток по известному способу осуществляли в периферической крови пациентов с диагнозами рака молочной железы, простаты и панкреатического рака с использованием флуоресцентно меченых моноклональных антител. Для этого образцы периферической крови перемешивали в течение 5 минут на качалке, после чего эритроциты частично разрушали раствором хлорида аммония. Образцы центрифугировали, ядерные клетки ресуспензировали в фосфатном буфере, содержащем Са2+ и Mg2+, и наносили на предметные стекла для микроскопии. Одно такое стекло при этом вмещало до 3 млн. ядерных клеток. Стекла замораживали и хранили при температуре -80°С. После размораживания клетки фиксировали 2% формальдегидом, пермиабилизовали холодным метанолом, не специфические сайты связывания антител блокировали козьей сывороткой. Полученные мазки окрашивали антителами к цитокератинам и Cd45. инкубировали с DAPI для придания контрастности и фиксировали закрепляющим раствором.
Поскольку количество циркулирующих опухолевых клеток и микроэмбол в 10 мл крови онкологического больного составляет около 10 на 100 миллионов лейкоцитов и 50 биллионов эритроцитов (Paterlini-Brechot, P. Circulating tumor cells (CTC) detection: Clinical impact and future directions / P. Paterlini-Brechot, N. L. Benali // Cancer Letters. - 2007. - №253. - P.180-204), то даже при частичном разрушении эритроцитов, что предусмотрено в известном способе, для получения достоверного результата необходимо исследовать не менее 20 предметных стекол, содержащих фиксированные окрашенные клетки, для каждого пациента, что является достаточно трудоемкой процедурой.
Кроме того, осуществление детекции циркулирующих опухолевых клеток, микроэмбол и апоптотических телец в крови с помощью антител к цитокератинам не всегда дает точный (достоверный) результат, так как известно, что в некоторых типах опухолей, в том числе в злокачественных опухолях легкого, экспрессия молекулярных маркеров (цитокератинов) может быть снижена (Paterlini-Brechot. P. Circulating tumor cells (CTC) detection: Clinical impact and future directions / P. Paterlini-Brechot, N. L. Benali // Cancer Letters. - 2007. - №253. - P.180-204).
Задачей настоящего изобретения является повышение специфичности способа выявления циркулирующих опухолевых клеток, микроэмбол и апоптотических телец в образцах крови больных раком легкого человека при уменьшении трудовых и временных затрат.
Поставленная задача решается тем, что в способе выявления циркулирующих опухолевых клеток, микроэмбол и апоптотических телец в крови больных раком легкого человека образец периферической крови больных раком легкого человека центрифугируют, отделяют плазму, концентрированный клеточный осадок инкубируют с гипотоническим раствором хлорида аммония для разрушения эрритроцитов, ядерные клетки ресуспензируют в фосфатном буфере, содержащем Са2+ и Mg2+, образец микроскопируют на предметных стеклах, согласно изобретению перед стадией ресуспензирования оставшиеся после разрушения эритроцитов клетки осаждают центрифугированием и путем добавления гипотонического раствора хлорида натрия частично разрушают лейкоциты, далее образец центрифугируют и снимают надосадок, осадок, содержащий неразрушенные клетки, ресуспензируют для восстановления объема оставшихся клеток в фосфатном буфере, содержащем Са2+ и Mg2+, после чего клетки концентрируют для уменьшения общего объема образца, полученную клеточную суспензию инкубируют с маскирующей ДНК. Затем добавляют аптамеры, специфичные к раку легкого меченые флуоресцентной меткой, полученные образцы исследуются с помощью методов микроскопии, позволяющих регистрировать флуоресцентные метки.
Для выявления циркулирующих опухолевых клеток, микроэмбол и апоптотических телец в крови больных раком легкого в заявляемом способе используют аптамеры, специфичные к опухолевым тканям легкого человека, полученные в процессе селекции, имеющие установленную нуклеотидную последовательность, отраженную как SEQ ID NO 1 - SEQ ID NO 34.
В способе выявления циркулирующих опухолевых клеток, микроэмбол и апоптотических телец в крови больных раком легкого для подтверждения принадлежности детектируемых опухолевых клеток к клеткам эпителиального происхождения после стадии инкубации клеточной суспензии с маскирующей ДНК, одновременно с аптамерами добавляют моноклональные антитела, меченые флуоресцентной меткой, специфичные к антигенам эпителиальных клеток.
Способ выявления циркулирующих опухолевых клеток, микроэмбол и апоптотических телец в крови больных раком легкого может быть осуществлен путем микроскопирования мазка, полученного в результате распределенного по предметному стеклу осадка от центрифугирования полученного образца для исследования, зафиксированного в метиловом спирте и окрашенного по Романовскому-Гимзе.
Уменьшение количества лейкоцитов в образцах крови больных позволяет сократить количество анализируемых проб на порядок, по сравнению с наиболее близким аналогом, что значительно упрощает мониторинг редких опухолевых клеток и продуктов их распада. Использование пула специфичных аптамеров повышает специфичность и чувствительность диагностики заболевания.
Способ иллюстрируется фотографиями микроскопии, сделанными при исследовании образцов, полученных при реализации способа.
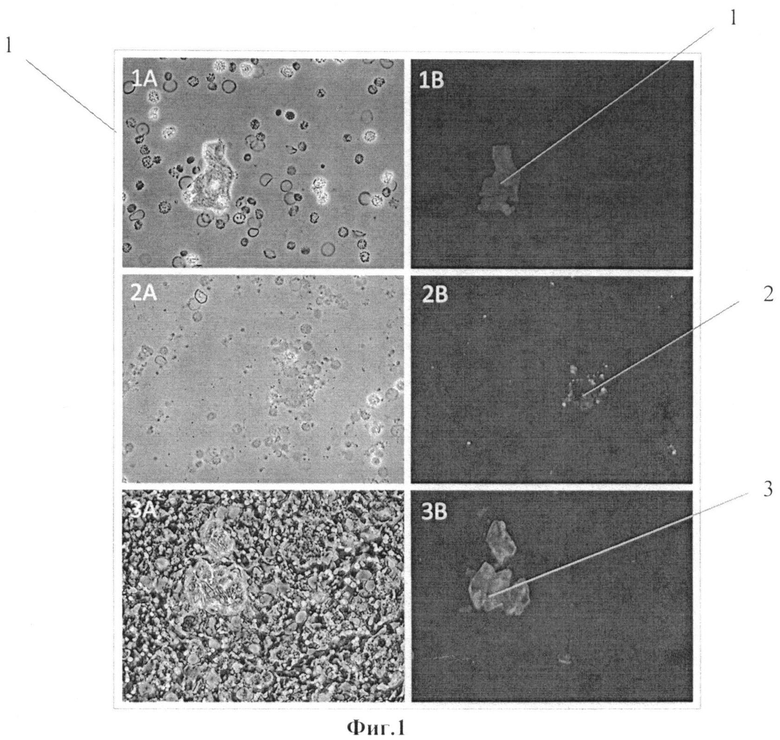
на фиг.1 приведены фотографии, полученные при исследовании образцов крови больного аденокарциномой легкого человека с помощью световой микроскопии и флуоресцентной микроскопии (инкубирование образца с аптамерами);
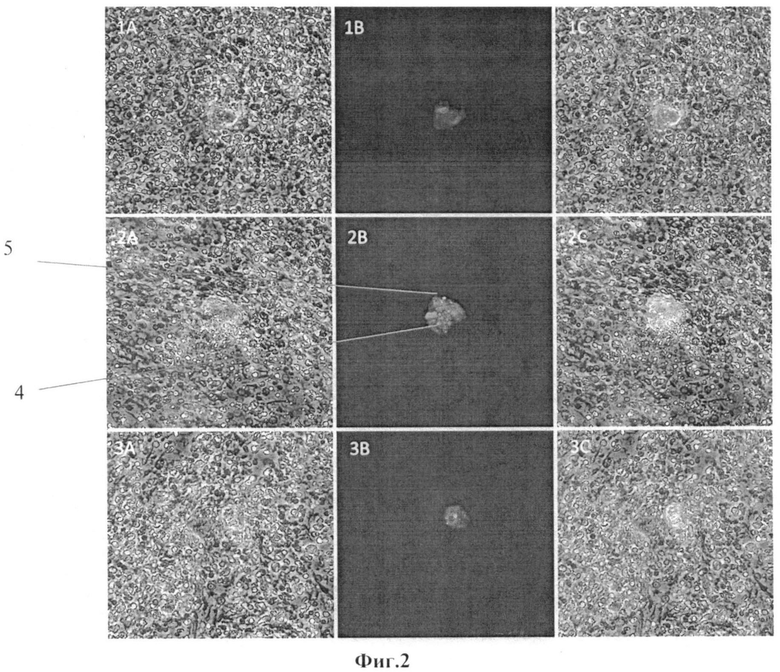
на фиг.2 приведены фотографии, полученные при исследовании образцов крови больного плоскоклеточным раком легкого человека с помощью конфокальной микроскопии в разных режимах;
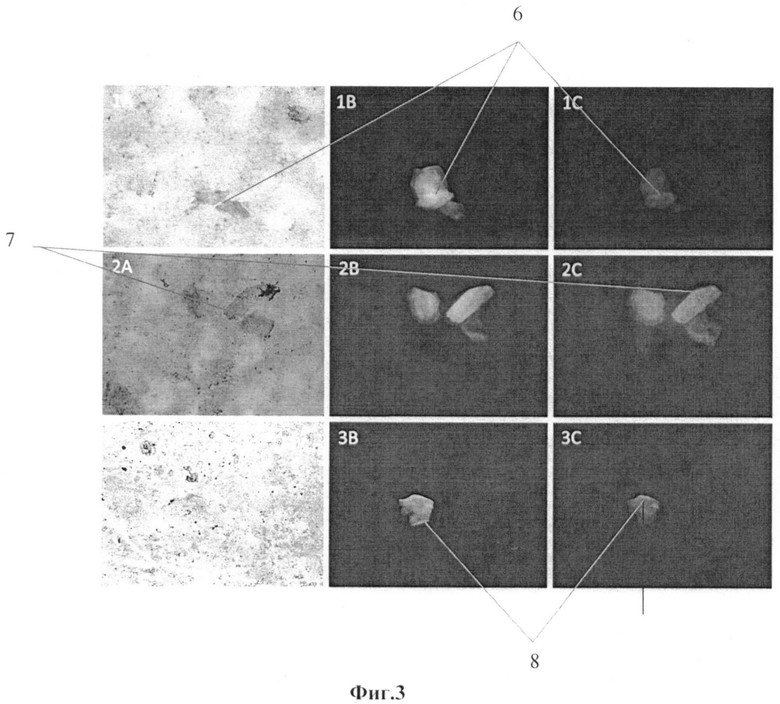
на фиг.3 приведены фотографии, полученные при исследовании образцов мазков крови больных аденокарциномой легкого человека и железисто-плоскоклеточным раком легкого человека с помощью световой микроскопии и флуоресцентной микроскопии;
на фиг.4 приведены фотографии, полученные при исследовании образцов крови больного плоскоклеточным раком легкого человека с помощью световой микроскопии и флуоресцентной микроскопии (инкубирование образца с аптамерами и моноклональными антителами);
на фиг.5 приведены фотографии, полученные при исследовании образцов мазков крови больного плоскоклеточным раком легкого человека с неразрушенными лейкоцитами с помощью световой микроскопии и флуоресцентной микроскопии.
Способ выявления циркулирующих опухолевых клеток, микроэмбол и апоптотических телец в крови больных раком легкого осуществляют следующим образом.
Для осуществления способа используют следующие расходные материалы и реактивы:
1. Фосфатный буфер, содержащий Са2+ и Mg2+
2. Раствор хлорида аммония
3. Раствор хлорида натрия
4. Маскирующая ДНК
5. Аптамеры, специфичные к клеткам рака легкого человека
Образцы периферической крови больных (4 мл) центрифугируют в течение 5 минут при 3000 об/мин, после чего плазму убирают и к 1 мл концентрированных клеток добавляют 0,42% раствор хлорида аммония в соотношении 1:5 для разрушения эритроцитов, затрудняющих анализ. Оставшиеся клетки осаждают центрифугированием в течение 5 мин при 3000 об/мин, после чего добавляют 3 мл 0,2% раствора хлорида натрия для частичного разрушения лейкоцитов. По истечении 1 часа образец центрифугируют и снимают надосадок. Осадок, содержащий неразрушенные клетки, ресуспензируют в 500 мкл фосфатного буфера, содержащего Са2+ и Mg2+, для восстановления объема оставшихся клеток в течение 30 минут. После чего клетки концентрируют для уменьшения общего объема образца в 50 мкл фосфатного буфера, содержащего Са2+ и Mg2+. Клеточную суспензию инкубируют с маскирующей ДНК в течение 30 минут, затем добавляют аптамеры, в частности, имеющие установленную нуклеотидную последовательность, отраженную как SEQ ID NO 1 - SEQ ID NO 34, меченые флуоресцентной меткой. Дополнительно для подтверждения принадлежности детектируемых опухолевых клеток к клеткам эпителиального происхождения допускается окрашивание образца моноклональными антителами, специфичными к антигенам эпителиальных клеток.
Полученные образцы исследуют с помощью методов микроскопии, позволяющих регистрировать флуоресцентные метки.
При этом выявление циркулирующих опухолевых клеток, микроэмбол и апоптотических телец может быть осуществлено как непосредственно в полученных в результате реализации способа образцах для исследования, в этом случае, каплю образца наносят на предметное стекло, накрывают покровным стеклом и микроскопируют; так и по мазкам, полученным из образцов для исследования, которые центрифугируют в течение 5 минут при 3000 об/мин, после чего снимают надосадок. Осадок равномерно наносят на предметное стекло. Мазки фиксируют в метиловом спирте в течение 5 минут, затем окрашивают с помощью краски Романовского-Гимза.
Приготовленные таким образом мазки могут храниться до нескольких месяцев в темном сухом месте.
Способ диагностики рака легкого иллюстрируется примерами, описывающими выявление циркулирующих опухолевых клеток, микроэмбол и апоптотических телец в крови больных плоскоклеточным раком легкого человека, аденокарциномой легкого человека и железисто-плоскоклеточным раком легкого человека.
Пример 1.
Для осуществления примера использовали периферическую кровь больного аденокарциномой легкого человека (с подтвержденным диагнозом).
Образец периферической крови для исследования, забиравшейся из вены с добавлением антикоагулянта, был предоставлен Красноярским краевым клиническим онкологическим диспансером имени А.И. Крыжановского.
Образец периферической крови больного центрифугировали, плазму убирали и добавляли 0,42% раствор хлорида аммония в соотношении 1:5 для разрушения эритроцитов, затрудняющих анализ. Затем добавляли 3 мл 0,2% раствора хлорида натрия для частичного разрушения лейкоцитов. По истечении 1 часа оставшиеся неразрушенными клетки ресуспензировали в 500 мкл фосфатного буфера, содержащего Са2+ и Mg2+, для восстановления объема оставшихся клеток. После чего клетки концентрировали для уменьшения общего объема образца в 50 мкл буфера. Клеточную суспензию инкубировали с маскирующей ДНК в конечной концентрации 1 нг/мкл в течение 30 минут, затем добавляли аптамеры, меченые флуоресцентной меткой Cy′3 (красный) в конечной концентрации 50 нМ.
Образцы исследовали с помощью световой и флуоресцентной микроскопии (микроскоп Olympus BX51). Результаты, полученные с помощью световой микроскопии - первый столбец (квадраты 1А, 2А, 3А) и флуоресцентной микроскопии - второй (1В, 2В, 3В), представлены на фотографиях с увеличением 100Х, приведенных на Фиг.1. Во втором столбце представлены фотографии флуоресцентной микроскопии образцов крови человека, больного аденкарциномой легкого, окрашенного с помощью аптамеров меченых флуоресцентной меткой Cy′3 (1В, 2В, 3В). На фотографии позицией 1 показана флуоресценция аптамера, связавшегося с мишенью, то есть с циркулирующей опухолевой клеткой, аптамеры также связались с апоптотическими тельцами 2, присутствующими в крови больного, а также с циркулирующей опухолевой микроэмболой 3. Таким образом, аптамеры позволили выявить в крови больного аденокарциномой легкого человека все виды присутствующих в ней опухолевых элементов, а именно: циркулирующую опухолевую клетку, апоптотическое тельце и циркулирующую опухолевую микроэмболу. Это позволяет говорить о том, что с помощью аптамеров возможно выявлять упомянутые опухолевые элементы в крови больных раком легкого при их наличии.
Данные, полученные с помощью флуоресцентной микроскопии, показали, что применение заявляемого способа подтвердило поставленный диагноз.
Пример 2.
Для осуществления примера использовали кровь больного плоскоклеточным раком легкого человека (с подтвержденным диагнозом).
Образец крови для исследования, забиравшейся из вены с добавлением антикоагулянта, был предоставлен Красноярским краевым клиническим онкологическим диспансером имени А.И. Крыжановского.
Образец крови больного центрифугировали в течение 5 минут при 3000 об/мин, после чего плазму убирали и к 1 мл концентрированных клеток добавляли 0,42% раствор хлорида аммония в соотношении 1:5 для разрушения эритроцитов, затрудняющих анализ. Оставшиеся клетки осаждали центрифугированием в течение 5 мин при 3000 об/мин, после чего к ним добавляли 3 мл 0,2% раствора хлорида натрия для частичного разрушения лейкоцитов. По истечении 1 часа образец центрифугировали и оставшиеся неразрушенными клетки ресуспензировали в 500 мкл фосфатного буфера, содержащего Са2+ и Mg2+, для восстановления объема оставшихся клеток. После чего клетки концентрировали для уменьшения общего объема образца в 50 мкл буфера. Клеточную суспензию инкубировали с маскирующей ДНК в конечной концентрации 1 нг/мкл в течение 30 минут, затем добавляли аптамеры, меченые флуоресцентной меткой Cy′3 (красный) в конечной концентрации 50 нМ и моноклональные антитела к цитокератинам 4, 5, 6, 8, 10, 13, 18 с флуоресцентной меткой FITC (зеленый) (Sigma Aldrich, USA) и инкубировали в течение еще 30 минут.
Образец исследовали с помощью конфокального микроскопа Olympus Fluoview 10vi (Olympus Optical Co., Япония) в режиме фазового контраста для поиска мишеней и режиме флуоресценции (красный и зеленый каналы) для идентификации опухолевых клеток, связавшихся с аптамерами мечеными флуоресцентной меткой Cy′3 (красный) и моноклональными антителами к цитокератинам с флуоресцентной меткой FITC (зеленый).
Результаты конфокальной микроскопии представлены на фотографиях, приведенных на фиг.2.
В первом столбце (квадраты 1А, 2А, 3А) представлены фотографии опухолевых клеток, полученных в режиме фазового контраста. Поскольку у людей, больных онкологическими заболеваниями, эритроциты являются более осмотически устойчивыми, и часть из них не подвергается воздействию гипотонического раствора хлорида аммония, помимо опухолевых клеток в образце присутствуют неразрушенные эритроциты.
Во втором столбце фиг.2 (квадраты 1В, 2В, 3В) представлены фотографии, полученные в режиме флуоресценции при наложении зеленого и красного каналов, видно, что присутствующие в крови клетки, связались с антителами к цитокератинам 4, что говорит об их эпителиальной природе и с аптамерами 5, что говорит об их опухолевой природе.
В третьем столбце 1 (квадраты 1C, 2С, 3С) видны циркулирующие опухолевые клетки, полученные в режиме фазового контраста с наложением флуоресценции, что также позволяет видеть опухолевые клетки, окрашенные аптамерами и антителами к цитокератинам.
Таким образом, приведенный пример реализации заявляемого способа позволил подтвердить поставленный диагноз.
Пример 3.
Для осуществления примера использовали кровь больного железисто-плоскоклеточным раком легкого (с подтвержденным диагнозом).
Образец крови для исследования, забиравшейся из вены с добавлением антикоагулянта, был предоставлен Красноярским краевым клиническим онкологическим диспансером имени А.И. Крыжановского.
Способ осуществляли в условиях примера 1, далее полученные окрашенные образцы центрифугировали в течение 5 минут при 3000 об/мин, после чего снимали надосадок. Осадок равномерно наносили на предметное стекло. Мазки фиксировали в метиловом спирте в течение 5 минут, затем окрашивали с помощью краски Романовского-Гимза.
Всего было приготовлено по 2 мазка образца, полученного из крови больного железисто-плоскоклеточным раком легкого.
Образцы исследовали с помощью световой и флуоресцентной микроскопии (микроскоп Olympus BX51).
На фиг.3 представлены результаты световой и флуоресцентной микроскопии мазков, полученных из образца крови больного железисто-плоскоклеточным раком легкого. В первом столбце (1А, 2А, 3А) приведены фотографии образцов, полученные с помощью световой микроскопии; во втором столбце (1В, 2В, 3В) фотографии образцов крови, окрашенных с помощью антител к цитокератинам, меченых флуоресцентной меткой FITC, полученные с помощью флуоресцентной микроскопии; в третьем столбце (1C, 2С, 3С) фотографии образцов крови, окрашенных с помощью аптамеров, меченых флуоресцентной меткой Cy′3, полученные с помощью флуоресцентной микроскопии. Увеличение 100Х.
Из полученных фотографий видно, что аптамер связывался с цитокератин-положительными опухолевыми клетками 6, 7 присутствующими в крови больного железисто-плоскоклеточным раком легкого. Опухолевые клетки, присутствующие в крови больных, окрашенные краской Романовского-Гимза, отчетливо видны и при световой микроскопии.
Мишень, присутствующая в крови больного 8, связавшаяся с аптамерами и с антителами к цитокератинам, не окрасилась краской Романовского-Гимза и не просматривается при световой микроскопии (фиг.3, 3А). Это может означать, что связавшаяся мишень являлась, скорее всего, апоптотическим тельцем.
Результаты анализов мазков крови показали, что в исследованных образцам больного присутствовали циркулирующая опухолевая клетка легкого, циркулирующая опухолевая микроэмбола и апоптотическое тельце.
Таким образом, использование заявляемого метода позволило подтвердить поставленный диагноз.
Пример 4.
Для осуществления примера использовали кроль больного плоскоклеточным раком легкого человека (с подтвержденным диагнозом).
Образец крови для исследования, забиравшейся из вены с добавлением антикоагулянта, был предоставлен Красноярским краевым клиническим онкологическим диспансером имени А.И. Крыжановского.
Образец периферической крови больного центрифугировали в течение 5 минут при 3000 об/мин, плазму убирали и добавляли 0,42% раствор хлорида аммония для разрушения эритроцитов, затрудняющих анализ. Затем добавляли 0,2% раствор хлорида натрия для частичного разрушения лейкоцитов. По истечении 1 часа оставшиеся неразрушенными клетки ресуспензировали в 500 мкл фосфатного буфера, содержащего Ca2+ и Mg2+ для восстановления объема оставшихся клеток и инкубировали в течение 30 минут. Затем образец центрифугировали и к осадку добавляли 50 мкл фосфатного буфера, содержащего Са2+ и Mg2+, для уменьшения общего объема образца. Клеточную суспензию инкубировали с маскирующей ДНК в конечной концентрации 1 нг/мкл в течение 30 минут, затем добавляли аптамеры, меченые флуоресцентной меткой Cy′3 (красный) в конечной концентрации 50 нМ и моноклональные антитела к цитокератинам 4, 5, 6, 8, 10, 13, 18 с флуоресцентной меткой FITC (зеленый) (Sigma Aldrich, USA) и инкубировали в течение еще 30 минут.
Образец исследовали с помощью конфокального микроскопа Olympus Fluoview 10vi (Olympus Optical Co., Япония) в режиме фазового контраста для поиска мишеней и режиме флуоресценции (красный и зеленый каналы) для идентификации опухолевых клеток, связавшихся с аптамерами мечеными флуоресцентной меткой Cy′3 (красный) и моноклональными антителами к цитокератинам с флуоресцентной меткой FITC (зеленый).
Результаты конфокальной микроскопии представлены на фотографиях, приведенных на фиг.4
В квадрате 1А представлена фотография опухолевой клетки, полученной в режиме фазового контраста. В квадрате 1В представлена фотография, полученная в режиме флуоресценции при наложении зеленого и красного каналов. Видно, что циркулирующая опухолевая клетка связалась с аптамерами, мечеными флуоресцентной меткой Cy′3 (красный) 9; отсутствие свечения в зеленом диапазоне говорит о том, что антитела к цитокератинам, меченые флуоресцентной меткой FITC (зеленый,) не связались с циркулирующей опухолевой клеткой 9.
В квадрате 1C представлена циркулирующая опухолевая клетка, полученная в режиме фазового контраста с наложением флуоресценции, где также видно, что циркулирующая опухолевая клетка, связавшаяся с аптамерами, флуоресцирует в красном диапазоне 10.
Таким образом, по результатам анализа конфокальной микроскопии можно заключить, что в образце присутствовала циркулирующая опухолевая клетка, что и позволило подтвердить поставленный диагноз, используя аптамеры, меченые флуоресцентной меткой, тогда как с помощью моноклональных антител к цитокератинам, меченых флуоресцентной меткой, поставленный диагноз - плоскоклеточный рак легкого человека - подтвердить не удалось.
Пример 5.
Для осуществления примера использовали кровь больного плоскоклеточным раком легкого человека (с подтвержденным диагнозом).
Образец крови для исследования, забиравшейся из вены с добавлением антикоагулянта, был предоставлен Красноярским краевым клиническим онкологическим диспансером имени А.И. Крыжановского.
Образец крови больного центрифугировали в течение 5 минут при 3000 об/мин, после чего плазму убирали и к 1 мл концентрированных клеток добавляли раствор хлорида аммония в конечной концентрации 0,42% в соотношении 1:5 для разрушения эритроцитов, затрудняющих анализ, при этом лейкоциты в образцах крови не подвергались разрушению. Оставшиеся клетки осаждали центрифугированием в течение 5 мин при 3000 об/мин, оставшиеся неразрушенными клетки ресуспензировали в 500 мкл фосфатного буфера, содержащего Са2+ и Mg2+, для восстановления объема оставшихся клеток. После чего клетки концентрировали для уменьшения общего объема образца в 50 мкл фосфатного буфера, содержащего Са2+ и Mg2+. Клеточную суспензию инкубировали с маскирующей ДНК в конечной концентрации 1 нг/мкл в течение 30 минут, затем добавляли аптамеры, меченые флуоресцентной меткой Cy′3 (красный) в конечной концентрации 50 нМ, и моноклональные антитела к цитокератинам 4, 5, 6, 8, 10, 13, 18 с флуоресцентной меткой FITC (зеленый) (Sigma Aldrich, USA) и инкубировали в течение еще 30 минут. Для осуществления примера готовились мазки.
Для этого приготовленные окрашенные образцы центрифугировали в течение 5 минут при 3000 об/мин, после чего надосадок снимался. Осадок равномерно наносили на предметное стекло. Мазки фиксировались в метиловом спирте в течение 5 минут, затем окрашивались с помощью краски Романовского-Гимза.
Было приготовлено 23 мазка образца полученного из крови больного плоскоклеточным раком легкого.
Мазки исследовали с помощью световой и флуоресцентной микроскопии (микроскоп Olympus BX51). Увеличение 100Х.
На фиг.5 представлены результаты световой и флуоресцентной микроскопии мазков, полученных из образцов крови человека, больного плоскоклеточным раком легкого.
При просмотре 23 стекол с образцами только в 1 из них были обнаружены циркулирующие опухолевые клетки.
В квадрате 1А представлена световая микроскопия циркулирующей опухолевой клетки 11, окрашенной краской Романовского-Гимза. В квадрате 1В представлена флуоресцентная микроскопия циркулирующей опухолевой клетки, наличие флуоресценции показывает, что клетка связалась с антителами к цитокератинам, мечеными флуоресцентной меткой 12. В квадрате 1C видна флуоресценция этой же циркулирующей опухолевой клетки, связавшейся с аптамерами, мечеными флуоресцентной меткой 13. Результаты анализа также подтвердили поставленный диагноз.
Таким образом, заявляемый способ обладает большей специфичностью, чем способ по прототипу к опухолевым элементам, характерным для рака легкого человека и позволяет выявлять циркулирующие опухолевые клетки, микроэмболы и апоптотические тельца в образцах крови больных раком легкого человека разных типов. При этом значительно сокращаются затраты времени на подтверждение диагноза, вследствие уменьшения количества просматриваемых образцов, а соответственно и трудовые затраты.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ выявления опухолеспецифичных мишеней в гистологических срезах тканей больных раком легкого человека | 2015 |
|
RU2639238C2 |
| АПТАМЕР, СПЕЦИФИЧНЫЙ К ОПУХОЛЕВЫМ ТКАНЯМ ЛЕГКОГО ЧЕЛОВЕКА | 2012 |
|
RU2528870C2 |
| СПОСОБ СЕЛЕКЦИИ АПТАМЕРОВ К ЗАДАННЫМ БЕЛКОВЫМ МИШЕНЯМ НА ПОВЕРХНОСТИ КЛЕТОК | 2012 |
|
RU2518368C1 |
| Способ визуализации глиобластомы человека | 2015 |
|
RU2654665C2 |
| Аптамеры для интраоперационного окрашивания глиобластомы и способ их применения | 2023 |
|
RU2826956C1 |
| Способы детектирования 5Т4-положительных циркулирующих опухолевых клеток и способы диагностики 5Т4-положительного рака у млекопитающего | 2013 |
|
RU2646498C2 |
| Способ выявления мишеней, ассоциированных с определенным диагнозом, в крови пациентов на основе ДНК-аптамеров | 2017 |
|
RU2685936C2 |
| Аптамер, проходящий через гематоэнцефалический барьер головного мозга мыши | 2016 |
|
RU2711912C2 |
| АНАЛИЗ ЦИРКУЛИРУЮЩИХ ОПУХОЛЕВЫХ КЛЕТОК | 2007 |
|
RU2429486C2 |
| Способ определения циркулирующих опухолевых клеток у больных раком молочной железы | 2021 |
|
RU2770284C1 |













Изобретение относится к способу выявления циркулирующих опухолевых, микроэмбол и апоптотических телец в крови больных онкологическими заболеваниями, в частности раком легкого с помощью аптамеров. Способ выявления циркулирующих опухолевых клеток, микроэмбол и апоптотических телец в крови больных раком легкого включает центрифугирование образца периферической крови больных раком легкого, отделение плазмы, инкубацию концентрированного клеточного осадка с гипотоническим раствором хлорида аммония для разрушения эритроцитов, разрушение лейкоцитов хлоридом натрия, ресуспензирование осадка в фосфатном буфере. Полученную клеточную суспензию инкубируют с маскирующей ДНК, затем добавляют аптамеры, специфичные к раку легкого меченые флуоресцентной меткой, полученные образцы исследуются с помощью методов микроскопии, позволяющих регистрировать флуоресцентные метки. Способ позволяет повысить специфичность выявления опухолевых клеток при разных типах рака легкого человека, сократить время диагностики 3 з.п. ф-лы, 5 ил., 5 пр.
1. Способ выявления циркулирующих опухолевых клеток, микроэмбол и апоптотических телец в крови больных раком легкого человека, включающий центрифугирование образца периферической крови больных раком легкого, отделение плазмы крови, инкубацию концентрированного клеточного осадка с гипотоническим раствором хлорида аммония с разрушением эритроцитов, ресуспензирование оставшихся клеток в фосфатном буфере, микроскопирование образца на предметных стеклах, отличающийся тем, что перед стадией ресуспензирования оставшиеся после разрушения эритроцитов клетки осаждают центрифугированием и путем добавления гипотонического раствора хлорида натрия частично разрушают лейкоциты, далее образец центрифугируют и снимают надосадок, осадок, содержащий неразрушенные клетки, ресуспензируют в фосфатном буфере, содержащем Ca2+ и Mg2+, для восстановления объема оставшихся клеток, после чего клетки концентрируют для уменьшения общего объема образца, полученную клеточную суспензию инкубируют с маскирующей ДНК, затем добавляют аптамеры, специфичные к раку легкого, меченые флуоресцентной меткой, полученные образцы исследуют с помощью методов микроскопии, позволяющих регистрировать флуоресцентные метки.
2. Способ, по п.1, отличающийся тем, что используют аптамеры, специфичные к опухолевым тканям легкого человека, полученные в процессе селекции, имеющие установленную нуклеотидную последовательность, отраженную как SEQ ID NO 1 - SEQ ID NO 34.
3. Способ, по п.1, отличающийся тем, что после стадии инкубации клеточной суспензии с маскирующей ДНК одновременно с аптамерами добавляют моноклональные антитела, меченые флуоресцентной меткой, специфичные к антигенам эпителиальных клеток.
4. Способ по п.1, отличающийся тем, что выявление циркулирующих опухолевых клеток, микроэмбол и апоптотических телец в крови больных раком легкого человека осуществляют путем микроскопирования мазка, полученного в результате распределенного по предметному стеклу осадка от центрифугирования полученного образца для исследования, зафиксированного в метиловом спирте и окрашенного по Романовскому-Гимзе.
| Т.Н | |||
| ЗАМАЙ и др | |||
| Метод диагностики рака легкого человека с помощью одноцепочечных днк-олигонуклеотидов | |||
| Известия Самарского научного центра Российской академии наук, том 14, N5(2), 2012 | |||
| Устройство для преобразования движения поршня двигателя во вращательное движение вала | 1922 |
|
SU452A1 |
| WO2012070970 A1, 31.05.2012 | |||
| WO2009012140 A3, 05.03.2009 | |||
| MIKULOVA V | |||
| et al | |||
| Methods for Detection of Circulating Tumour Cells and Their Clinical Value | |||
Авторы
Даты
2015-12-20—Публикация
2013-09-26—Подача