Предлагаемое изобретение относится к области синтеза соединений с биологической активностью, конкретно к способу получения 3-[1-(1-адамантил)этил]-1,5,3-дитиазепана (1) на основе каталитической реакции α-метил-1-адамантилметиламина с 1-окса-3,6-дитиациклогептаном. Соединение (1), in vitro полностью подавляющее развитие Rhizoctonia solani, может быть использовано для борьбы с болезнями сельскохозяйственных растений, вызываемыми этим фитопатогенным грибом
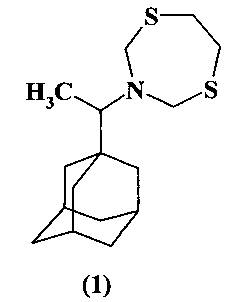
Известен способ (Η.Н. Махмудиярова, К.И. Прокофьев, Л.В. Мударисова, А.Г. Ибрагимов, У.М. Джемилев. ЖОрХ, 2013, 5, 658) получения 3-гетарил-1,5,3-дитиазепанов (2) реакцией Ν,Ν-бис(метоксиметил)гетариламинов с 1,2-этандитиолом под действием катализатора CuCl2
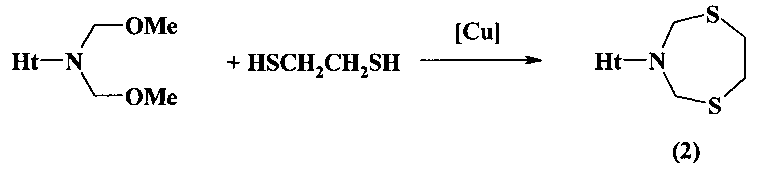
Известным способом не может быть получен 3-[1-(1-адамантил)этил]-1,5,3-дитиазепан (1).
Известен способ (U. Wellmar. J. Heterocyclic Chem. 1998, 35, 1531) получения 3-(трет-бутил)пергидро-1,5,3-дитиазепина (3) взаимодействием 5-(трет-бутил)-2-оксогексагидро-1,3,5-триазина с 1,2-этандитиолом в присутствии BF3 ·2CH3COOH.
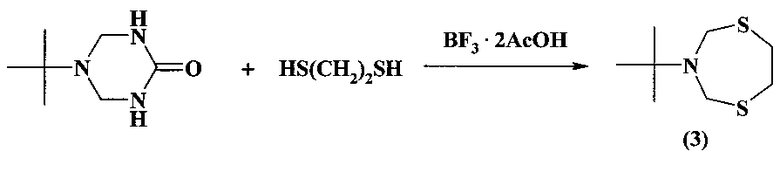
Известным способом не может быть получен 3-[1-(1-адамантил)этил]-1,5,3-дитиазепан (1).
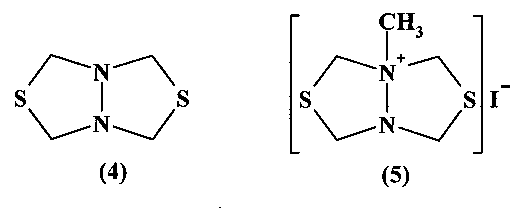
Известны (Akhmetova, V.R., Murzakova, Ν.Ν., Khabibullina, G.R., Galimzyanova, N.F. Russ. J. Appl. Chem., 2011, 84, 2, 225-229) фунгицидные средства для борьбы с грибковыми заболеваниями растений на основе 1,3,4-тиадиазолидинового бицикла (4) и его аддукта с CH3I (5), которые подавляют развитие таких фитопатогенных грибов, как Bipolaris sorokiniana, Fusarium oxysporum, Aspergillus fumigatus, Aspergillus niger и Paecilomyces variotii
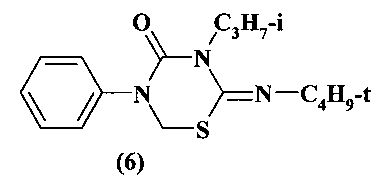
Известен (H Kanno. Pure&Appl. Chem. 1987. Vol. 59. №8. P. 1027-1032) фунгицид бупрофезин (6), предназначенный для борьбы с грибковыми заболеваниями сельскохозяйственных культур. Производство известного фунгицида (6) осуществляется 2-стадийным синтезом и базируется на использовании труднодоступных исходных реагентов.
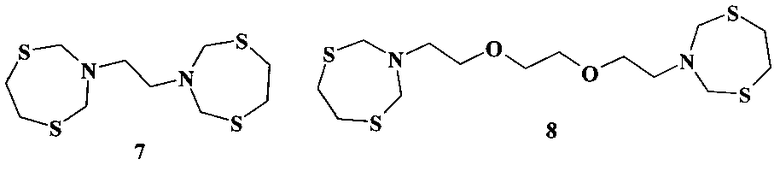
Известна фунгицидная активность бис-(1,5,3-дитиазепан-3-ил)этана (7) и 3,3′-(3,6-диоксаоктан-1,8-диил)бис-1,5,3-дитиазепана (8) в отношении фитопатогенных грибов Botrytis cinerea (Е.Б. Рахимова, Р.А. Исмагилов, Р.А. Зайнуллин, Н.Ф. Галимзянова, А.Г. Ибрагимов. Журнал прикладной химии, 2013, 86, 10, 1547).
Синтезы указанных соединений или многостадийны или базируются на использовании дорогостоящих исходных реагентов.
Предлагается новый способ получения 3-[1-(1-адамантил)этил]-1,5,3-дитиазепана (1) в одну препаративную стадию из доступных исходных реагентов. Соединение формулы (1) может быть использовано в качестве средства с фунгицидной активностью.
Сущность способа заключается во взаимодействии α-метил-1-адамантилметиламина (лекарственное средство «Римантадин») с 1-окса-3,6-дитиациклогептаном в присутствии катализатора SmCl3·6H2O, взятых в мольном соотношении α-метил-1-адамантилметиламин:1-окса-3,6-дитиациклогептан:SmCl3·6H2O = 1:1:(0.03-0.07), предпочтительно 1:1:0.05, в среде этанол-хлороформ (1:1, объемные) в течение 2.5-3.5 ч при комнатной температуре (~20°C) и атмосферном давлении. Выход 3-[1-(1-адамантил)этил]-1,5,3-дитиазепана (1) составляет 64-72%. Реакция протекает по схеме
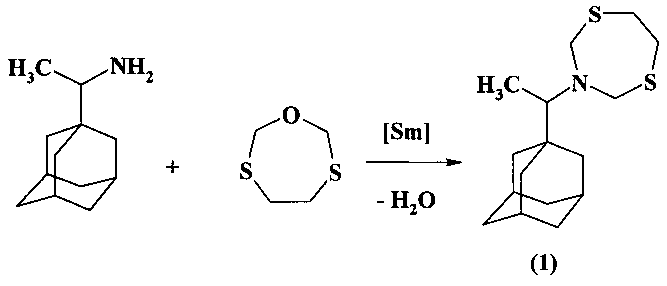
3-[1-(1-Адамантил)этил]-1,5,3-дитиазепан (1) образуется только лишь с участием α-метил-1-адамантилметиламина и 1-окса-3,6-дитиациклогептана, взятых в мольном соотношении 1:1 (стехиометрические количества). При другом соотношении исходных реагентов снижается выход целевого продукта (1).
Без катализатора реакция идет с выходом, не превышающим 10%. Проведение указанной реакции в присутствии катализатора SmCl3·6H2O больше 7 мол.% не приводит к существенному увеличению выхода целевого продукта (1). Использование катализатора SmCl3·6H2O менее 3 мол.% снижает выход (1), что связано, возможно, со снижением каталитически активных центров в реакционной массе. Реакции проводили при комнатной температуре ~20°C. При температуре выше 20°C (например, 60°C) увеличиваются энергозатраты, а при температуре ниже 20°C (например, при 0°C) снижается скорость реакции. Опыты проводили в среде растворителей этанол-хлороформ, т.к. в них хорошо растворяются исходные соединения.
Выявление фунгицидной активности осуществлено с использованием микроскопического гриба Rhizoctonia solani. Rhizoctonia solani - фитопатогенный гриб, возбудитель бурой и сухой гнили (ризоктониоза), поражающий 230 видов сельскохозяйственных растений (картофель, томат, капуста, редис, свекла, фасоль, чечевица, люцерна, лен и др.). (Микроорганизмы-возбудители болезней растений. // Под ред. Билай В.И. - Киев: Наукова думка, 1988, 552 с.). Микроскопические грибы поддерживаются в коллекции микроорганизмов Института биологии УНЦ РАН. Для испытаний использовали растворы (1) в ДМФА. Растворитель ДМФА не оказывал негативного воздействия на развитие Rhizoctonia solani.
Общая методика оценки фунгицидной активности соединения (1).
Оценку фунгицидной активности проводили методом диффузии в агар (Практикум по микробиологии. // Под ред. Егорова Н.С. - М.: Изд-во МГУ, 1976, 307 с.). Поверхность питательной среды (картофельно-глюкозный агар), разлитой по 15 мл в чашки Петри d 70 мм, засевали суспензией спор тест-культур грибов. Затем в среде сверлом диаметром 10 мм вырезали 3 лунки, в которые помещали по 100 мкл испытываемых растворов. Фунгицидную активность оценивали по диаметру зоны подавления роста микромицетов, а также наблюдая за развитием тест-культур с использованием светового микроскопа Leica DM 1000 при увеличении ×10. Повторность трехкратная. Контролем служило развитие гриба на питательной среде. Время инкубации 7 суток при 28°C.
Раствор 3-[1-(1-адамантил)этил]-1,5,3-дитиазепана (1) в концентрации 0.1% оказывал фунгистатическое действие, а в концентрации 0.2% полностью подавлял развитие Rhizoctonia solani (таблица 1).

Таким образом, 3-[1-(1-адамантил)этил]-1,5,3-дитиазепан (1) в концентрации 0.2% проявляет фунгицидный эффект по отношению к Rhizoctonia solani.
Существенные отличия предлагаемого способа
В известном способе для получения 1,5,3-дитиазепана (2) в качестве исходных реагентов применяются N,N-бис(метоксиметил)гетариламины и 1,2-этандитиол. Реакция осуществляется в присутствии катализатора CuCl2.
В предлагаемом способе исходными реагентами являются α-метил-1-адамантилметиламин и 1-окса-3,6-дитиациклогептан. Реакция осуществляется в присутствии катализатора SmCl3·6Н2О. В отличие от известного, предлагаемый способ позволяет получать 3-[1-(1-адамантил)этил]-1,5,3-дитиазепан (1) с фунгицидной активностью.
Способ поясняется примерами.
Пример 1. В сосуд Шленка, установленный на магнитной мешалке, в атмосфере аргона при температуре ~20°C помещают 0.14 г (1 ммоль) 1-окса-3,6-дитиациклогептана в 10 мл хлороформа и 0.018 г (0.05 ммоль) SmCl3·6Н2О, затем по каплям добавляют 0.18 г (1 ммоль) α-метил-1-адамантилметиламина в 10 мл этанола. Реакционную смесь перемешивают при температуре ~20°C в течение 3 ч, очищают колоночной хроматографией на SiO2 и выделяют 3-[1-(1-адамантил)этил]-1,5,3-дитиазепинан с выходом 67%.
Другие примеры, подтверждающие способ, приведены в таблице 2.
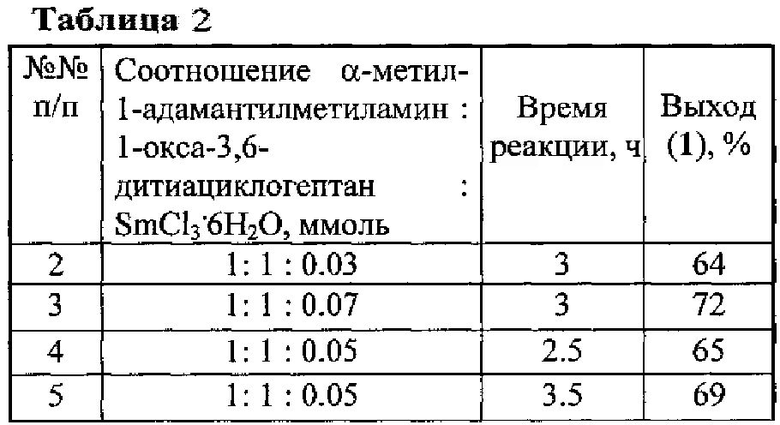
Все опыты проводили в среде этанол-хлороформ (1:1, объемные) при комнатной температуре (~20°C).
Спектральные характеристики 3-[1-(1-адамантил)этил]-1,5,3-дитиазепинана1 (1Контроль реакции осуществляли методом ТСХ на пластинах Silufol W-254, проявляли парами I2. Для колоночной хроматографии использовали силикагель КСК (100-200 мкм). Температура плавления определена на приборе РНМК 80/2617. Спектры ЯМР 1D (1Н, 13C) и 2D (COSY, NOESY, HSQC, НМВС) сняты на спектрометре Bruker Avance 400 (100.62 МГц для 13C и 400.13 МГц для 1H) по стандартным методикам фирмы Bruker, внутренний стандарт Me4Si, растворитель - CDCl3. Масс-спектры получены на приборе MALDI TOF/TOF AUTOFLEX III фирмы Bruker.):
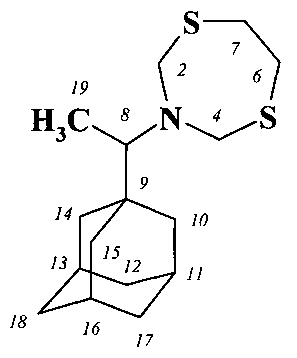
Т. пл. 90-92°C. Элюент гексан: этилацетат (4:3), Rf 0.5. Спектр ЯМР 1Н, δ, м.д.: 1.16 (д, 3H, CH3 (19)); 1.43 (д, 3H, Ha (12, 17, 18)); 1.58-1.63 (м, 6H, CH2 (10, 14, 15)); 1.70 (д, 3H, Hb (12, 17, 18)); 2.04 (уш.с, 3H, CH (11, 13, 16)); 2.35-2.45 (м, 1H, CH (8)); 2.83-2.93 (м, 2Н, Ha (6, 7)); 3.13-3.22 (м, 2H, Hb (6, 7)); 4.27-4.35 (м, 4H, СН2 (2, 4)). Спектр ЯМР 13С, δ, м.д.: 9.6 (С-19), 28.5 (С-11, С-13, С-16), 36.8 (С-6, С-7), 37.2 (С-10, С-14, С-15), 38.9 (С-12, С-17, С-18), 59.2 (С-2, С-4), 67.0 (С-8). MALDI TOF, m/z: 296.292 [М-H]+. C16H27NS2. Μ 297.524.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ 3-(1-АДАМАНТИЛ)-1,5,3-ДИТИАЗЕПАНА И ЕГО ПРИМЕНЕНИЕ В КАЧЕСТВЕ СРЕДСТВА С ФУНГИЦИДНОЙ АКТИВНОСТЬЮ | 2014 |
|
RU2584692C2 |
| СПОСОБ ПОЛУЧЕНИЯ 5-(1,5,3-ДИТИАЗЕПАН-3-ИЛ)-ХИНОЛИНА И ЕГО ПРИМЕНЕНИЕ В КАЧЕСТВЕ СРЕДСТВА С ФУНГИЦИДНОЙ АКТИВНОСТЬЮ | 2014 |
|
RU2565783C1 |
| СПОСОБ ПОЛУЧЕНИЯ N-АДАМАНТИЛ-1,5,3-ДИТИАЗЕПАНОВ | 2015 |
|
RU2605447C1 |
| СПОСОБ ПОЛУЧЕНИЯ N-ЦИКЛОГЕКСИЛЗАМЕЩЕННЫХ 1,5,3-ДИТИАЗЕПАНОВ | 2014 |
|
RU2574074C1 |
| СПОСОБ ПОЛУЧЕНИЯ (1,5,3-ДИТИАЗЕПАН-3-ИЛ)-АЛКАНДИОЛОВ | 2013 |
|
RU2559359C2 |
| СПОСОБ ПОЛУЧЕНИЯ N-ЦИКЛОПЕНТИЛЗАМЕЩЕННЫХ 1,5,3-ДИТИАЗЕПАНОВ | 2014 |
|
RU2565790C1 |
| СПОСОБ ПОЛУЧЕНИЯ N-ЦИКЛОАЛКИЛЗАМЕЩЕННЫХ 1, 5, 3-ДИТИАЗЕПАНОВ | 2015 |
|
RU2601313C1 |
| СПОСОБ ПОЛУЧЕНИЯ БИС-(1,5,3-ДИТИАЗЕПИНАН-3-ИЛ)ЭТАНА И ЕГО ПРИМЕНЕНИЕ В КАЧЕСТВЕ СРЕДСТВА С ФУНГИЦИДНОЙ АКТИВНОСТЬЮ | 2013 |
|
RU2541791C2 |
| СПОСОБ ПОЛУЧЕНИЯ 3-(1-АДАМАНТИЛ)- И 3-[1-(1-АДАМАНТИЛ)ЭТИЛ]-1,5,3-ДИТИАЗЕПИНАНОВ | 2013 |
|
RU2551668C1 |
| СПОСОБ ПОЛУЧЕНИЯ МЕТИЛ 2-(1,5,3-ДИТИАЗЕПАН-3-ИЛ)АЛКАНОАТОВ | 2015 |
|
RU2605448C1 |
Изобретение относится к области синтеза соединений с биологической активностью, конкретно к способу получения 3-[1-(1-адамантил)этил]-1,5,3-дитиазепана, обладающего фунгицидной активностью против Rhizoctonia solani. Сущность способа заключается во взаимодействии α-метил-1-адамантилметиламина с 1-окса-3,6-дитиациклогептаном в присутствии катализатора SmCl3·6H2O при мольном соотношении α-метил-1-адамантилметиламин:1-окса-3,6-дитиациклогептан:SmCl3·6H2O=1:1:(0.03-0.07) при температуре ~20°С и атмосферном давлении в течение 2.5-3.5 ч. Выход 3-[1-(1-адамантил)этил]-1,5,3-дитиазепана (1) составляет 64-72%. 2 н. и 1 з.п. ф-лы, 2 табл., 1 пр.
1. Способ получения 3-[1-(1-адамантил)этил]-1,5,3-дитиазепана (1)
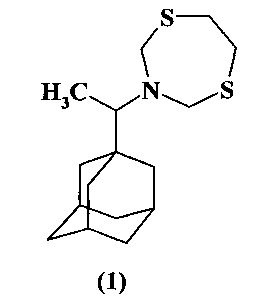
отличающийся тем, что α-метил-1-адамантилметиламин подвергают взаимодействию с 1-окса-3,6-дитиациклогептаном в среде этанол-хлороформ в присутствии катализатора SmCl3·6H2O при мольном соотношении α-метил-1-адамантилметиламин:1-окса-3,6-дитиациклогептан:SmCl3·6H2O=1:1:(0.03-0.07) при комнатной температуре (~20°C) и атмосферном давлении в течение 2.5-3.5 ч.
2. Способ по п.1, отличающийся тем, что реакцию проводят в среде этанол-хлороформ при объемном соотношении компонентов равном 1:1.
3. Применение 3-[1-(1-адамантил)этил]-1,5,3-дитиазепана (1) в качестве средства с фунгицидной активностью для борьбы с заболеваниями сельскохозяйственных культур, вызываемыми грибами Rhizoctonia solani.
| Рахимова Е.Б., Васильева И.В., Халилов Л.М | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| НИВЕЛЛИР | 1923 |
|
SU1132A1 |
| Мурзакова Н., Прокофьев К.И., Тюмкина Т.В., Ибрагимов А.Г | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
Авторы
Даты
2016-02-10—Публикация
2014-07-22—Подача