Перекрестные ссылки на родственные заявки
По данной заявке испрашивается приоритет по предварительной заявке США № 61/143049, поданной 7 января 2009 года, которая включена в настоящее описание в качестве ссылки в полном объеме.
Область изобретения
Изобретение относится в основном к молекулярной биологии, к композициям и способам для увеличения устойчивости растений к гербицидам, ингибирующим синтазу ацетогидроксикислот, и композициям и способам для борьбы с сорными растениями.
Предпосылки изобретения
Соя (Glycine max) является важной сельскохозяйственной культурой, которая произрастает на многих посевных площадях мира. По отношению к сое уже применяли биотехнологические способы с целью улучшения агротехнических характеристик и качества продукта. Одной из таких агротехнических характеристик, важной при получении сои, является устойчивость к гербицидам, в частности, устойчивость к гербициду глифосату. Так как возросло применение устойчивой к глифосату сои, появлялись сорняки, которые являются устойчивыми к глифосату. Таким образом, при борьбе с сорными растениями существует необходимость в растениях сои, которые обладают устойчивостью к гербицидам, отличным от глифосата.
Фенотипическую экспрессию трансгена (такого как те, которые обеспечивают устойчивость к гербицидам) в растении, таком как соя, затрагивают как посредством структуры самого гена, так и посредством участка его интеграции в геном растения. Наряду с этим присутствие трансгена (в чужеродной ДНК) в различных участках генома будет различными способами оказывать влияние на фенотип растения в целом. Агротехнически или промышленно успешное введение в растение представляющего коммерческий интерес признака посредством генетического воздействия может представлять собой длительную процедуру, зависящую от различных факторов. Существующие способы трансформации и регенерации генетически трансформированных растений являются первыми в серии стадий селекции, где стадии включают интенсивную генетическую характеризацию, разведение и оценку в полевых условиях, что приводит в итоге к отбору элитного объекта.
Возможность однозначно определять и/или распознавать конкретные трансгенные события становится все более важной вследствие возросшего применения генетической модификации для повышения урожайности культуры, для улучшения интрогрессии трансгенов в коммерческие сорта, для разделения продуктов с ГМО и без ГМО, и идентификации запатентованного материала. Для определения конкретных трансгенных событий сохраняется необходимость в разработке способов, которые являются как быстрыми, так и простыми, не нуждаются в большом количестве лабораторного оборудования. Кроме того, способы определения конкретного события были бы полезными для согласования с нормативными актами, что требуется для проверки продукции до выпуска на рынок сбыта и маркировки продуктов, полученных из рекомбинантных сельскохозяйственных культур или для применения при контроле за состоянием окружающей среды, контроле признаков сельскохозяйственных культур, произрастающих в поле или контроле продуктов, полученных из собранного урожая сельскохозяйственных культур, а также для применения в целях обеспечения соответствия партий согласно регуляторным или договорным условиям.
Сущность изобретения
В одном из вариантов осуществления настоящее изобретение относится к способам борьбы с сорняками на посевной площади, где способы включают: применение эффективного количества неселективного гербицида на посевной площади с растением соей, содержащим молекулу нуклеиновой кислоты события 127.
В другом варианте осуществления настоящее изобретение относится к способам борьбы на посевных площадях с сорняками, устойчивыми к глифосату, где способы включают: применение эффективного количества ингибирующего AHAS гербицида на посевных площадях с растением соей, содержащим молекулу нуклеиновой кислоты события 127.
В другом варианте осуществления настоящее изобретение относится к выделенной молекуле нуклеиновой кислоты с последовательностью нуклеиновых кислот от положения 1312 до положения 6069 в SEQ ID NO:1.
В другом варианте осуществления настоящее изобретение также относится к трансгенным растениям сои, имеющим гетерологичную молекулу нуклеиновой кислоты с последовательностью нуклеотидов от положения 1302 до положения 6079 в SEQ ID NO:1.
Настоящее изобретение также относится к выделенной паре нуклеиновокислотных праймеров, содержащих: первую и вторую выделенную молекулу нуклеиновой кислоты, которые обеспечивают амплификацию молекулы нуклеиновой кислоты события 127.
В другом варианте осуществления настоящее изобретение относится к набору для идентификации молекулы нуклеиновой кислоты события 127 в биологическом образце, содержащему: первый и второй нуклеиновокислотный праймер, где первый и второй нуклеиновокислотный праймер обеспечивают амплификацию молекулы нуклеиновой кислоты события 127.
Настоящее изобретение также относится к способам идентификации растения сои события 127, где способы включают: (a) получение смеси, включающей биологический образец, содержащий ДНК сои, и первый и второй нуклеиновокислотный праймер, обеспечивающие амплификацию молекулы нуклеиновой кислоты, специфичную для события 127; (b) проведение реакции в смеси в условиях, которые позволяют первому и второму нуклеиновокислотным праймерам обеспечивать амплификацию молекулы нуклеиновой кислоты, специфичной для события 127; и (c) определение наличия амплифицированного фрагмента молекулы нуклеиновой кислоты, где наличие молекулы нуклеиновой кислоты, специфичной для события 127 сои, показывает, что растение соя представляет собой растение сою события 127.
В другом дополнительном варианте осуществления изобретения, настоящее изобретение относится к способам идентификации растения сои с молекулой нуклеиновой кислоты события 127, где способы включают: (a) получение смеси, включающей биологический образец, содержащий ДНК сои, и молекулу нуклеиновокислотного зонда, который способен гибридизоваться с молекулой нуклеиновой кислоты, специфичной для события 127; (b) проведение реакции в смеси в условиях, которые позволяют молекуле нуклеиновокислотного зонда гибридизоваться с молекулой нуклеиновой кислоты, специфичной для события 127; и (c) детекцию гибридизации зонда с ДНК, где наличие гибридизации молекулы нуклеиновокислотного зонда с ДНК сои показывает наличие молекулы нуклеиновой кислоты события 127.
Настоящее изобретение дополнительно относится к способам повышения урожая растений сои, содержащих молекулу нуклеиновой кислоты события 127, где способ включает: применение эффективного количества ингибирующего AHAS гербицида на одном или нескольких растениях сои, содержащих молекулу нуклеиновой кислоты события 127, и на окружающих площадях, где ингибирующий AHAS гербицид уменьшает рост сорняков на окружающей площади; и сбор семян от одного или нескольких растений сои.
В другом варианте осуществления настоящее изобретение относится к способам разведения растений сои, устойчивых к ингибирующему AHAS гербициду, где способ включает: (a) скрещивание растения сои, содержащего молекулу нуклеиновой кислоты события 127, со вторым растением сои; (b) получение семян из растения, полученного в результате скрещивания на стадии (a); (c) получение образца ДНК из семян; и (d) детекцию наличия молекулы нуклеиновой кислоты события 127 в образце, где наличие молекулы нуклеиновой кислоты события 127 показывает, что семена способны производить растение сои, устойчивое к ингибирующему AHAS гербициду.
Настоящее изобретение также относится к семенам растения сои, содержащим молекулу нуклеиновой кислоты события 127.
В другом варианте осуществления настоящее изобретение относится к способам детекции наличия молекулы нуклеиновой кислоты события 127 в биологическом образце, где способы включают: (a) получение смеси, включающей биологический образец, содержащий ДНК, и первый и второй нуклеиновокислотный праймер, обеспечивающие амплификацию молекулы нуклеиновой кислоты, специфичной для события 127; (b) проведение реакции в смеси в условиях, которые позволяют первому и второму нуклеиновокислотным праймерам обеспечивать амплификацию молекулы нуклеиновой кислоты, содержащей молекулу нуклеиновой кислоты, специфичную для события 127; и (c) детекцию наличия амплифицированной молекулы нуклеиновой кислоты, где присутствие молекулы нуклеиновой кислоты, специфичной для события 127, показывает, что образец содержит молекулу нуклеиновой кислоты события 127.
В другом варианте осуществления настоящее изобретение относится к способам детекции молекулы нуклеиновой кислоты события 127 в биологическом образце, где способ включает: (a) получение смеси, включающей биологический образец, содержащий ДНК, и нуклеиновокислотный зонд, способный гибридизоваться с молекулой нуклеиновой кислоты, специфичной для события 127; (b) проведение реакции в смеси в условиях, которые позволяют зонду гибридизоваться с молекулой нуклеиновой кислоты, специфичной для события 127; и (c) детекцию наличия гибридизованной молекулы нуклеиновой кислоты, где присутствие молекулы нуклеиновой кислоты, специфичной для события 127, показывает, что образец содержит молекулу нуклеиновой кислоты события 127.
Настоящее изобретение также относится к способам детекции наличия встроенной молекулы нуклеиновой кислоты события 127 в биологическом образце, где способ включает: (a) получение смеси, включающей биологический образец, содержащий ДНК, и первый и второй праймеры, способствующие амплификации встроенной молекулы нуклеиновой кислоты события 127; (b) проведение реакции в смеси в условиях, которые позволяют первому и второму нуклеиновокислотным праймерам обеспечивать амплификацию молекулы нуклеиновой кислоты, содержащей встроенную молекулу нуклеиновой кислоты события 127; и (c) детекцию наличия амплифицированной молекулы нуклеиновой кислоты, где присутствие встроенной молекулы нуклеиновой кислоты события 127 показывает, что образец содержит встроенную ДНК события 127.
В еще одном варианте осуществления настоящее изобретение относится к способам детекции наличия встроенной молекулы нуклеиновой кислоты события 127 в биологическом образце, где способы включают: (a) получение смеси, включающей биологический образец, содержащий ДНК, и первый праймер, способный к отжигу с участком встроенной молекулы нуклеиновой кислоты события 127, и второй праймер, способный к отжигу с фланкирующей молекулой нуклеиновой кислоты в геноме клетки-хозяина; (b) проведение реакции в смеси в условиях, которые позволяют первому и второму нуклеиновокислотным праймерам производить амплифицированную молекулу нуклеиновой кислоты, содержащую фрагмент встроенной молекулы нуклеиновой кислоты события 127; и (c) детекцию наличия молекулы нуклеиновой кислоты, где присутствие фрагмента встроенной молекулы нуклеиновой кислоты события 127 показывает, что образец содержит встроенную ДНК события 127.
В другом варианте осуществления настоящее изобретение относится к способам выращивания растений сои, где способ включает: (a) получение семян сои, содержащих молекулу нуклеиновой кислоты события 127; (b) посев семян для получения сои в среде для выращивания в условиях, которые обеспечивают прорастание семян, для выращивания растения сои, содержащего молекулу нуклеиновой кислоты события 127; и (c) взаимодействие среды для выращивания, семян или растений с гербицидной композицией, содержащей по меньшей мере один компонент, выбранный из группы, состоящей из гербицидов на основе имидазолинона, сульфонилкарбамида, их комбинации друг с другом, и их комбинации по меньшей мере с другим одним активным ингредиентом.
В другом варианте осуществления настоящее изобретение относится к способам детекции полипептида события 127 в образце, где способы включают: получение биологического образца из растения сои; и проведение по меньшей мере одного иммунологического анализа образца, где в результате проведения анализа возможна детекция полипептида события 127.
Настоящее изобретение также относится к устройствам для применения в детекции биологических молекул, где устройства включают: твердую подложку с поверхностью; и по меньшей мере одну диагностическую молекулу для события 127, присоединенную к поверхности твердой подложки.
Краткое описание фигур
На фиг.1A представлено схематическое изображение плазмиды pAC321. На фиг.1B представлено схематическое изображение фрагмента PvuII pAC321, содержащего AHASL 5' UTR, кодирующую последовательность csr1-2 и AHASL 3' UTR, который использован для трансформации. Показаны участки рестрикции ферментов (NcoI, XbaI, SpeI), используемые для анализа блоттинг по Саузерну для определения числа копий, проверки отсутствия векторной конструкции и стабильности в поколениях.
На фиг.2 предоставлено схематическое изображение истории разведения на примере одного растения сои события 127.
На фиг.3 предоставлено схематическое изображение выравнивания фрагмента трансформации PvuII pAC321 со вставкой события 127 сои.
На фиг.4A-4C представлены результаты блот-гибридизации по Саузерну для определения числа копий вставки на одном примере для растения сои события 127, как описано в примере 3. На фиг.4D представлено схематическое изображение взаимного расположения зондов, используемых в экспериментах по гибридизации.
На фиг.5 предоставлены результаты блот-гибридизации по Саузерну, показывающие отсутствие последовательности векторной конструкции в одном примере растения сои события 127, как описано в примере 3. На фиг.5A представлены результаты с использованием зонда VP1, а на фиг.5B представлены результаты с использованием зонда VP2. На фиг.5C представлено схематическое изображение взаимного расположения участков гибридизации на последовательности события 127.
На фиг.6 предоставлены результаты блот-гибридизации по Саузерну анализа стабильности наследования в поколениях последовательности события 127. На фиг.6A представлены результаты с использованием зонда 5' UTR. На фиг.6B представлены результаты с использованием зонда AHAS. На фиг.6C представлены результаты с использованием зонда 3' UTR. На фиг.6D представлено схематическое изображение участков гибридизации соответствующих зондов на последовательности события 127.
На фиг.7 предоставлена схема вставки и фланкирующей последовательности на одном примере растения сои события 127. Также показано шесть ампликонов, используемых для секвенирования, как описано в примере 3.
На фиг.8 предоставлены полноразмерные последовательности нуклеиновокислотной вставки события 127 и фланкирующей области в геноме сои (SEQ ID NO:1). Положения 1-1311 соответствуют 5' фланкирующей ДНК, положения 1312-6069 соответствуют кодирующей модифицированный белок AHASL вставке ДНК, а положения 6070-10656 соответствуют 3'фланкирующей ДНК.
На фиг.9 предоставлен электрофорез в геле с результатами транскрипции посредством анализа ОТ-ПЦР γ субъединицы AtSec61 в одном примере растения сои события 127, как описано в примере 3.
На фиг.10 предоставлен электрофорез в геле с результатами транскрипции посредством анализа ОТ-ПЦР открытой рамки считывания (ORF) размером 501 п.н., образованной посредством встраивания дупликации кодирующей последовательности csr1-2 размером 376 п.н. в участок соединения с 3' фланкирующей последовательностью, на одном примере растения сои события 127, как описано в примере 3.
На фиг.11 предоставлен электрофорез в геле с результатами примеров способов ПЦР-детекции, специфичной к событию 127, как описано в примере 3.
На фиг.12 предоставлена ДНК, используемая для получения события 127, т.е. фрагмент PvuII размером 6156 п.н. из конструкта pAC321 (SEQ ID NO:4).
Подробное описание
Настоящее изобретение относится к растениям сои, которые демонстрируют устойчивость к ингибирующим AHAS гербицидам, таким как гербициды на основе имидазолинона, сульфонилкарбамида, триазолопиримидинсульфоанилида и/или пиримидилоксибензоата. Растения сои по настоящему изобретению содержат встроенную молекулу нуклеиновой кислоты, которая располагается в охарактеризованном участке в геноме сои. Также предоставленными являются способы и композиции для применения по отношению к описанным растениям сои.
До более подробного описания изобретения предварительно будет дано определение следующим терминам.
I. Определения
Как применяют в настоящем документе, термины “соя” и “растения сои” обозначает растения Glycine max и включает все сорта растений, которые можно скрещивать с соей. Термин “растение соя” включает части растения. Как применяют в настоящем документе, термин “часть растения” включает растительные клетки, органы растения, протопласты растения, культуру ткани растительной клетки, из которой можно регенерировать растения, каллюсы растений, растительные массы и растительные клетки, которые являются интактными в растениях или частях растений, таких как зародыши, пыльца, семяпочки, семена, семянки, листья, цветки, ветви, плод, стебли, корни, концы корней, пыльники, семядоли, гипокотили и т.п. Зерно предназначено для обозначения зрелого семени, получаемого овощеводами для целей, отличных от цели разведения или воспроизведения сорта. Потомство, производные, варианты и мутанты регенерированных растений также включены в пределы объема изобретения, при условии, что эти части включают молекулу нуклеиновой кислоты события 127.
“Молекула нуклеиновой кислоты события 127” относится к молекуле нуклеиновой кислоты, которая содержит последовательность нуклеиновой кислоты в положениях от 1312 до 6069 в SEQ ID NO:1; ее вариант, полученный общепринятой селекцией растений, который предназначен для обеспечения экспрессии модифицированной формы фермента AHAS, имеющей белок AHASL, содержащий вместо природного серина (S653N) аспарагин в соответствующем положении 653, где модифицированная форма фермента AHAS демонстрирует устойчивость к ингибитору AHAS, который в норме ингибирует ферментативную активность фермента AHAS дикого типа; или дополнение любого из них. Молекула нуклеиновой кислоты события 127 может содержать дополнительные последовательности, которые фланкируют положения 1312-6069 SEQ ID NO:1 (или, для вариантов, дополнительные последовательности, которые фланкируют 5' и 3' положения).
“Участок события 127” относится к молекуле нуклеиновой кислоты, которая включает по меньшей мере фрагмент молекулы нуклеиновой кислоты события 127 и которая является показателем растения события 127. Участок события 127 может включать один или несколько из 5' и/или 3' участков соединения, вставку ДНК или участок соединения дупликации csr1-2 вставки ДНК с остальной последовательностью вставки ДНК. Также 5' и/или 3' фланкирующие последовательности ДНК могут быть дополнительно включены в настоящий документ.
Как применяют в настоящем документе, термин “молекула нуклеиновой кислоты, специфичная для события 127” относится к последовательности молекул нуклеиновой кислоты, которая отличительно идентифицирует или которая допускает отличительную идентификацию молекулы нуклеиновой кислоты события 127 в образце. Молекула нуклеиновой кислоты, специфичная для события 127, может включать участки соединения и уникальные мутации или дупликации во вставке ДНК, полученной в результате процесса трансформации. Например, применение в реакции ПЦР праймеров для ПЦР с последовательностью нуклеиновых кислот, представленных в SEQ ID NO:37 и 38, приводит к амплификации ампликона, который является показателем молекулы нуклеиновой кислоты события 127.
Термин “молекула события 127” относится к молекуле нуклеиновой кислоты, молекулам полипептида и другим биологическим молекулам, которые происходят из молекулы нуклеиновой кислоты события 127, получены из молекулы нуклеиновой кислоты события 127, или кодируются молекулой нуклеиновой кислоты события 127.
Термин “диагностическая молекула события 127” относится к молекулам, которые можно использовать для детекции, как прямой так и непрямой, молекулы нуклеиновой кислоты события 127. Диагностическая молекула события 127 включает молекулы нуклеиновой кислоты, такие как праймеры и зонды, антитела и их фрагменты с сохраненным участком связывания (например, Fv, Fab, Fab', F(ab') и антитела с делетированным доменом H), полипептиды и их производные, аналоги нуклеиновых кислот, аптамеры и т.п., которые можно использовать в способах детекции молекулы нуклеиновой кислоты события 127 или полипептидов, экспрессированных с такой молекулы нуклеиновой кислоты.
Как применяют в настоящем документе, “вставка ДНК” относится к гетерологичной ДНК, встроенной в материал растения посредством процесса трансформации и включает ДНК, которая отличается от исходной ДНК, используемой для такой трансформации, как объяснено в настоящем документе. “Вставка нуклеиновой кислоты события 127” и “вставка ДНК события 127” относится к молекуле нуклеиновой кислоты с последовательностью нуклеиновых кислот в положениях 1312-6069 SEQ ID NO:1 (которая отличается от ДНК, используемой для создания события 127, т.е. фрагмента PvuII длиной 6156 п.о. из конструкта pAC321, представленного на фиг.12 (SEQ ID NO:4)).
“Событие 127” растения, клетки, семени, части растения или ткани растения относится к любому растению, клетке, семени, части растения или ткани растения, которые содержат молекулу нуклеиновой кислоты события 127, и предпочтительно содержат по меньшей мере одну нуклеиновую кислоту, специфичную для события 127. Событие 127 растений включает Событие 127-9 растений сои, содержащее молекулу нуклеиновой кислоты с последовательностью SEQ ID NO:1, как, например, то, которое обозначают как BPS-CV127-9.
Термин “фланкирующая ДНК” относится к геномной ДНК, естественно существующей в организме, таком как растение, которая располагается непосредственно против хода транскрипции или по ходу транскрипции и смежно со встроенной молекулой нуклеиновой кислоты. “Фланкирующая область” или "фланкирующая последовательность”, как применяют в настоящем документе, относится к последовательности по меньшей мере из 10, 20, 50, 100, 200, 300, 400, 1000, 1500, 2000, 2500 или 5000 пар нуклеотидов или более, которая располагается или непосредственно против хода транскрипции (5') и смежна с молекулой исходной чужеродной ДНК-вставки или непосредственно по ходу транскрипции (3') и смежна с молекулой исходной чужеродной ДНК-вставки. Неограничивающие примеры фланкирующих областей события 127 представлены в SEQ ID NO:2 и 3, и варианты и их фрагменты, где SEQ ID NO:2 соответствует положениям 1-1311 в SEQ ID NO:1, а SEQ ID NO:3 соответствует положениям 6070-10656 в SEQ ID NO:1.
Способы трансформации, приводящие к встраиванию чужеродной ДНК-вставки случайным образом, приведут в результате к образованию индивидуальных трансформантов, содержащих различные фланкирующие области, характерные и уникальные для каждого трансформанта. Если рекомбинантную ДНК встраивают в растение посредством общепринятого скрещивания, ее фланкирующие области не будут, как правило, отличаться от фланкирующих областей исходного трансформанта. Индивидуальные трансформанты будут также содержать уникальные соединения между участком гетерологичной ДНК-вставки и геномной ДНК или двумя участками геномной ДНК или двумя участками гетерологичной ДНК.
“Точка соединения” представляет собой точку, где соединяются два специфичных фрагмента ДНК, например, где ДНК-вставка соединяется с фланкирующей ДНК. Точка соединения также присутствует в трансформированном организме, где два фрагмента ДНК соединяются вместе способом, представляющим модификацию того способа, который обнаружен в природном организме. Как применяют в настоящем документе, “ДНК-соединение” или “участок соединения” относится к ДНК, которая содержит точку соединения. Неограничивающие примеры точек соединения в ДНК сои события 127 включают последовательности, такие как представлены, например, в SEQ ID NO:5 и 6, где SEQ ID NO:5 представляет собой положения 1311-1312 в SEQ ID NO:1 и SEQ ID NO:6 представляет собой положения 6069-6070 в SEQ ID NO:1.
Следует понимать, что термин “трансгенный”, как применяют в настоящем документе, включает любую клетку, клеточную линию, каллюс, ткань, часть растения или растение, генотип которых изменен вследствие присутствия гетерологичной нуклеиновой кислоты, включающей первоначально измененные трансгенные события, а также те, которые получили посредством полового или бесполого размножения от первоначально регенерированного события. Как применяют в настоящем документе термин “трансгенный” не включает изменение генома (хромосомного или внехромосомного) посредством общепринятых способов разведения растений или посредством природных процессов, таких как перекрестное опыление случайным образом, нерекомбинантная вирусная инфекция, нерекомбинантная бактериальная трансформация, нерекомбинантная транспозиция или спонтанная мутация.
“Трансформация” относится к переносу фрагмента нуклеиновой кислоты в геном организма хозяина, что приводит к стабильному генетическому наследованию. Организмы хозяев, содержащие трансформированные фрагменты нуклеиновой кислоты, обозначают как “трансгенные” организмы. Примеры способов трансформации растений включают те, которые известны в данной области и описаны ниже.
“Трансгенное событие” получают посредством трансформации растительных клеток гетерологичным ДНК-конструктом(ами), включающим нуклеиновокислотную экспрессирующую кассету, которая содержит представляющий интерес трансген, регенерацией популяции растений, полученных в результате встраивания трансгена в геном растения, и селекцией конкретного регенерированного растения, характеризующегося наличием вставки в конкретном участке генома. Событие характеризуют фенотипически посредством экспрессии трансгена(ов). На генетическом уровне, событие является частью генома растения.
Как применяют в настоящем документе, “образец” включает любой образец, который содержит молекулы нуклеиновой кислоты или полипептиды и получен из растений, растительного материала или из продуктов, таких как, но не ограничиваясь этим, пищевые продукты или корма (свежие или подвергнутые обработке), которые содержат растительный материал или получены из растительного материала.
Термином “встраивание” или “встроенный” в контексте трансформации обозначают предоставление растению гетерологичной конструкции ДНК таким образом, что конструкт получает доступ к внутреннему содержимому клеток растения. Растения и способы по изобретению не зависят от конкретного способа встраивания нуклеиновокислотного конструкта в растение, за исключением только того, что нуклеиновокислотный конструкт получает доступ к внутреннему содержимому по меньшей мере одной клетки растения. Способы встраивания нуклеиновокислотных конструктов в растения известны в данной области, включая, в качестве неограничивающих примеров, способы для устойчивой трансформации, временной трансформации и способы, которые опосредованы вирусами.
Термин “потомство” относится к растениям, полученным с помощью полового размножения (например, аутокроссинг, самоопыление или возвратное скрещивание) между растением события 127 и другим сортом. Даже после повторных возвратных скрещиваний с реккурентным родителем, встроенная ДНК и/или фланкирующая ДНК из родителя события 127 присутствует в потомстве после скрещивания в том же положении на хромосоме и его можно идентифицировать, например, скринингом участков, специфичных для события 127.
Как применяют в настоящем документе, “гетерологичная” по отношению к молекуле нуклеиновой кислоты обозначает молекулу нуклеиновой кислоты, которая происходит из чужеродных видов, или, если из тех же самых видов, вследствие преднамеренного вмешательства человека в композиции и/или в геномный локус, представляет собой модификацию своей природной формы.
“Выделенная” или “очищенная” молекула нуклеиновой кислоты или ее биологически активная часть, представляет собой молекулу по существу или в основном свободную от компонентов, которые, как показано, сопутствуют молекуле нуклеиновой кислоты в ее природном окружении в норме или взаимодействуют с молекулой нуклеиновой кислоты. Таким образом, выделенная или очищенная молекула нуклеиновой кислоты является по существу свободной от остального клеточного материала или, в случае получения рекомбинантными способами, от среды для культивирования, или, будучи химически синтезированной, по существу свободной от химически синтезированных предшественников или других химических реагентов.
“Зонд” относится к выделенной молекуле нуклеиновой кислоты, к которой присоединяют детектируемую метку или репортерную молекулу, например, радиоактивный изотоп, лиганд, хемилюминесцентное средство, фермент и т.д. Такой зонд комплементарен к цепи целевой молекулы нуклеиновой кислоты, а в рассматриваемом случае к цепи ДНК, выделенной из биологического материала сои события 127, будь то из растения сои или из образца, который включает ДНК события. Зонды включают не только дезоксирибонуклеиновые или рибонуклеиновые кислоты, но также полиамиды и другие материалы для зонда, которые могут специфично определять наличие целевой последовательности ДНК.
Как применяют в настоящем документе, “праймеры” представляют собой выделенные молекулы нуклеиновой кислоты, которые способны к отжигу с комплементарной цепью целевой ДНК посредством гибридизации нуклеиновых кислот, с образованием гибрида между праймером и цепью целевой ДНК, который затем может удлиняться вдоль цепи целевой ДНК посредством полимеразы, например, ДНК-полимеразы. “Пары праймеров” относится к паре праймеров для применения в амплификации целевой молекулы нуклеиновой кислоты, например, посредством полимеразной цепной реакции (ПЦР) или другими общепринятыми способами нуклеиновокислотной амплификации. “Полимеразная цепная реакция” или “ПЦР” представляет собой способ, который используют для амплификации специфичных отрезков ДНК.
“Линия” или “штамм” представляет собой группу индивидуумов одинакового происхождения, которые, как правило, до некоторой степени инбредны и которые, как правило, являются изогенными или близко-изогенными.
Термин “скрещенный” или “скрещивание” в контексте по данному изобретению обозначают слияние гамет, например, в случае растений, посредством опыления для получения потомства (т.е. клеток, семян или растений). Термин включает как половое скрещивание (опыление одного растения другим) и в случае растений самооплодотворение (самоопыление, т.е. в случае, если пыльца и семяпочка представлены на одном и том же растении).
Термин “интрогрессия” относится к передаче желаемого аллеля генетического локуса из одного генетического фона в другой. В одном способе, желаемые аллели можно подвергать интрогрессии посредством полового скрещивания двух родителей, где по меньшей мере один из родителей имеет в своем геноме желаемый аллель.
II. Растения сои события 127
Предоставлены композиции и способы, относящиеся к трансгенным растениям сои, устойчивым к ингибитору AHAS. Такие композиции включают растения сои события 127. Растение сои события 127 получают модификацией дикого типа или нетрансформированного растения сои посредством встраивания или интрогрессии гена большой субъединицы синтазы ацетогидроксикислот, который отвечает за устойчивость к имидазолинону, из Arabidopsis thaliana (csr1-2) в геном сои, как определено в настоящем документе. В некоторых вариантах осуществления встраивание гена csr1-2 в геном сои обеспечивает экспрессию модифицированной формы фермента синтазы ацетогидроксикислот (AHAS), с белком AHASL, содержащим, вместо природного серина, аспарагин в соответствующем положении 653 (S653N). Фермент AHAS представляет собой фермент, важный для биосинтеза аминокислот с разветвленной цепью и ингибируется некоторыми гербицидами (ингибирующие AHAS гербициды). Модификация в гене AHAS позволяет преодолеть это ингибирование и, таким образом, обеспечивает устойчивость к широкому диапазону ингибирующих AHAS гербицидов. Таким образом, растение сои события 127 является устойчивым по меньшей мере к одному ингибирующему AHAS гербициду или является устойчивым к более широкому количеству по меньшей мере одного ингибирующего AHAS гербицида, по сравнению с растением соей, не имеющем молекулу нуклеиновой кислоты события 127.
Показано, что молекулу нуклеиновой кислоты, обеспечивающую устойчивость к ингибитору AHAS, можно встраивать в охарактеризованное положение в геноме сои и получать, тем самым, событие 127. Растение сои события 127, содержащее молекулу нуклеиновой кислоты события 127 в описанном хромосомном положении содержит, в одном из вариантов осуществления, один или несколько геномных/трансгенных соединений с по меньшей мере последовательностью молекул нуклеиновых кислот из SEQ ID NO:5 и/или 6. Характеристика геномного участка встраивания события 127 обеспечивает повышенную эффективность разведения и дает возможность применения молекулярных маркеров для слежения за встроенным трансгеном в популяции для разведения и их потомстве. В настоящем документе представлены различные способы и композиции для идентификации, детекции и применения растений сои события 127.
Экспрессирующая кассета csr1-2, фрагмент PvuII из плазмиды pAC321, интегрировали в один охарактеризованный генетический локус в геноме сои для получения события 127. В одном из вариантов осуществления в событии 127 встроенная кассета csr1-2 содержит три точечные мутации относительно исходного фрагмента трансформации из плазмиды pAC321, с одной мутацией в кодирующей AHAS последовательности и двумя другими мутациями по ходу транскрипции в 3'-нетранслируемой области AHASL (UTR). Такие мутации включают мутацию G на A в кодирующей последовательности, которая приводит к экспрессии полипептида AHAS с заменой аминокислоты R272 на K272. Анализ Саузерн-блоттинг и верификация последовательности на наличие точечной мутации показывают, что вставка является стабильной на протяжении по меньшей мере восьми поколений. В событии 127 встроенная ДНК также содержит дупликацию части кодирующей последовательности csr1-2 размером 376 пар нуклеотидов (п.н.) непосредственно перед 3' участком встраивания (дупликация соответствует положениям 5694-6069 в SEQ ID NO:1). Этот дуплицированный сегмент размером 376 п.н. приводит к образованию открытой рамки считывания (ORF) размером 501 п.н., которая распространяется на 3' фланкирующую последовательность. Результаты обратной транскрипции и полимеразной цепной реакции (ОТ-ПЦР) позволяют предположить, что данная ORF размером 501 п.н. не подвергается транскрипции. В некоторых вариантах осуществления молекула нуклеиновой кислоты события 127 также содержит большую часть генного локуса γ субъединицы SEC61 Arabidopsis (At3g48570), которая является компонентом фрагмента ДНК, используемого для трансформации. В других вариантах осуществления ген γ субъединицы SEC61 можно экспрессировать в растении сои события 127. Например, как описано более подробно в примерах ниже, результаты экспериментов ОТ-ПЦР показали, что ген γ субъединицы SEC61 Arabidopsis слабо транскрибируется в ткани листа растения события 127. В целом, секвенировали приблизительно 1,3 тысячу пар нуклеотидов (т.п.н.) 5' фланкирующей ДНК сои вместе с приблизительно 4,6 т.п.н. 3' фланкирующей ДНК сои. Информацию о фланкирующей последовательности можно использовать в разработке способа детекции на основе качественной ПЦР, специфичной к событию 127, в соответствии с настоящим изобретением. Другие характеристики молекулы нуклеиновой кислоты события 127, такие как идентифицированные точечные мутации и дупликации, также можно использовать в способах, предоставленных в настоящем документе для детекции растений события 127, включая потомство и его производные.
Растения события 127 по настоящему изобретению являются устойчивыми к применению ингибирующих AHAS гербицидов. Растения события 127 проявляют устойчивость или повышенную устойчивость к ингибирующим AHAS гербицидам, уровни применения которых включают количества, эквивалентные количеству применения гербицидов между 50 г д.в./га и приблизительно 500 г д.в./га, между 70 г д.в./га и приблизительно 400 г д.в./га и между 70 г д.в./га и приблизительно 300 г д.в./га. Такая устойчивость может также включать устойчивость к ингибирующим AHAS гербицидам, которые применяются на уровнях количеств в 1, 2, 3, 4, 5 раз или больших, чем коммерческие уровни применения гербицида.
Устойчивость к ингибирующему AHAS гербициду можно определять любым способом определения устойчивости к гербицидам. Например, растение сои события 127 может демонстрировать устойчивость к ингибирующему AHAS гербициду или другому химическому средству, если у растения наблюдают повреждение, которое, по сравнению с соответствующим контрольным растением, представлено менее, чем повреждение, наблюдаемое у контрольного растения, по меньшей мере, на 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 90%, 100%, 150%, 200%, 250%, 300%, 400%, 500%, 600%, 700%, 800%, 900% или 1000% или более. Таким образом, растение, которое является устойчивым к ингибирующему AHAS гербициду или другому химическому средству демонстрирует, по сравнению с соответствующим контрольным растением, “повышенную устойчивость”. Повреждение, полученное в результате действия гербицида или другого химического воздействия, определяет специалист в данной области, посредством оценки любого параметра роста растения или жизнеспособности, который считается подходящим. Повреждение можно оценивать визуальным осмотром и/или статистическим анализом подходящих параметров, полученных от индивидуальных растений или группы растений. Таким образом, повреждение можно определять оценкой параметров, например, таких как высота растения, масса растения, цвет листа, цветение, фертильность, урожайность, продукция семян и т.п. Повреждение можно также определять оценкой времени, которое затрачено на конкретную стадию развития (например, зрелость или цветение) или оценкой времени, прошедшего до того момента, как растение восстановилось после обработки конкретным химическим средством или и/или гербицидом.
Повреждение, вызванное ингибирующим AHAS гербицидом или другим химическим средством, можно определять в различные периоды времени после обработки или взаимодействия растения события 127 с гербицидом. Повреждение можно оценивать приблизительно в момент времени, в котором у контрольного растения наблюдают максимальное повреждение или позднее того момента времени, за которое контрольное растение, не обработанное гербицидом или другим химическим средством, значительно выросло и/или подверглось развитию, по сравнению с размером или стадией развития, в которой проводили обработку. Кроме того, повреждение можно определять в различные периоды времени, например, в 12 часов или на 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14 сутки или через три недели, четыре недели, или более, после того, как тестируемое растение обработали гербицидом. Любой временной период является подходящим для оценки при условии, что он позволяет определять различие в реакции на обработку у тестируемого и контрольного растений.
Настоящее изобретение дополнительно включает семена линии сои CV603 (также известной как “BPS-CV127-9”), содержащей молекулу нуклеиновой кислоты события 127 и которую депонировали как патентный депозит № 41603 NCIMB, и растения, растительные клетки и семена, полученные от этой линии. Заявитель(ли) депонировал по меньшей мере 2500 семян растений сои, содержащих молекулу нуклеиновой кислоты события 127, в Национальных коллекциях промышленных, пищевых и морских бактерий (NCIMB), 23 St. Machar Drive, Aberdeen AB2 1RY, Шотландия, Великобритания, 22 декабря 2008 года, и депозиту присвоен входящий номер № 41603 в NCIMB. Эти депозиты будут поддерживаться в соответствии с условиями Будапештского договора о международном признании депонирования микроорганизмов для целей патентной процедуры. Этот депозит предоставляется исключительно в качестве услуги для специалистов в данной области и не допускает того, чтобы депозит запрашивался по 35 U.S.C. § 112. Семена, депонированные в NCIMB 22 декабря 2008 года, были взяты из депозита, поддерживающегося Embrapa (Empresa Brasileira de Pesquisa Agropecuaria). Доступ к депозиту будет возможен, по запросу, в течение нахождения заявки на рассмотрении, для комиссаров по патентным ведомствам и товарным знакам и для лиц, определенных комиссаром уполномоченными для этой цели. При одобрении пунктов формулы изобретения в заявке, заявитель(ли) обеспечит публичную доступность, в соответствии с 37 C.F.R. § 1808, образца(ов) депозита, по меньшей мере, 2500 семян растений сои, содержащих молекулу нуклеиновой кислоты события 127, в Национальных коллекциях промышленных, пищевых и морских бактерий (NCIMB), 23 St. Machar Drive, Aberdeen AB2 1RY, Шотландия, Великобритания. Депозит семян линии сои CV603 будет поддерживаться в депозитарии NCIMB, который является общедоступным депозитарием, в течение периода времени 30 лет или 5 лет после последнего запроса, или в течение установленного срока действия патента, в зависимости от того, какой срок более длинный, и будет заменен, если станет нежизнеспособным в течение указанного периода. Дополнительно, заявитель(и) выполняет все требования 37 C.F.R. §§ 1801-1809, включая обеспечение условия жизнеспособности образца при депонировании. Заявитель(и) не имеет права отказываться от любых ограничений, установленных законом на передачу биологического материала или его перевозки в коммерческих целях. Заявитель(и) не отказывается от любого нарушения своих прав, предоставляемых настоящим патентом, или прав в области линии сои CV603 в силу Закона об охране сорта растений (7 USC 2321 et seq.). Незаконное размножение семян запрещено. Семена могут быть адаптированы.
Растения сои события 127 по настоящему изобретению также включают потомство, производные, варианты и мутанты исходного события трансформации, которое является источником возникновения растений сои события 127. Такие растения можно идентифицировать с использованием любого способа идентификации таких растений, включая, в качестве неограничивающих примеров, учет родословной, способы определения устойчивости к гербицидам, способы молекулярной детекции, способы, описываемые в настоящем документе и их комбинации.
Растения сои события 127 по настоящему изобретению являются устойчивыми по меньшей мере к одному гербициду, который затрагивает активность эндогенного фермента AHAS (ингибирующие AHAS гербициды), не имеющему мутацию S653N. Гербициды, которые затрагивают активность фермента AHAS, включают гербициды на основе имидазолинона, сульфонилкарбамида, триазолопиримидина, пиримидинилоксибензоата, сульфониламинокарбонилтриазолинона или их смеси или их комбинации. В одном из вариантов осуществления такие гербициды представляют собой гербицид на основе имидазолинона, сульфонилкарбамида или их смеси. Гербициды на основе имидазолинона включают, но не ограничиваются ими, PURSUIT® (имазетапир), CADRE® (имазапик), RAPTOR® (имазамокс), SCEPTER® (имазаквин), ASSERT® (имезатабенз), ARSENAL® (имазапир), производное любых указанных выше гербицидов и смесь или комбинацию двух или более указанных выше гербицидов, например, имазапир/имазамокс (ODYSSEY®). Гербицид на основе имидазолинона можно также выбрать, но не ограничиваясь ими, из 2-(4-изопропил-4-метил-5-оксо-2-имидиазолин-2-ил)никотиновой кислоты, [2-(4-изопропил)-4-][метил-5-оксо-2-имидазолин-2-ил)-3-хинолинкарбоновой] кислоты, [5-этил-2-(4-изопропил-]-4-метил-5-оксо-2-имидазолин-2-ил)никотиновой кислоты, 2-(4-изопропил-4-метил-5-оксо-2-имидазолин-2-ил)-5-(метоксиметил)никотиновой кислоты, [2-(4-изопропил-4-метил-5-оксо-2-]имидазолин-2-ил)-5-метилникотиновой кислоты и смеси метил[6-(4-изопропил-4-]метил-5-оксо-2-имидазолин-2-ил)-м-толуата и метил[2-(4-изопропил-4-метил-5-]оксо-2-имидазолин-2-ил)-п-толуата. В одном из вариантов осуществления из 5-этил-2-(4-изопропил-4-метил-5-оксо-2-имидазолин-2-ил)никотиновой кислоты и [2-(4-изопропил-4-метил-5-оксо-2-имидазолин-2-]ил)-5-(метоксиметил)никотиновой кислоты. В другом варианте осуществления используют [2-(4-изопропил-4-]метил-5-оксо-2-имидазолин-2-ил)-5-(метоксиметил)никотиновую кислоту.
Гербициды на основе сульфонилкарбамида, которые можно использовать в настоящем изобретении, включают, но не ограничиваются ими, хлорсульфурон, метсульфуронметил, сульфометуронметил, хлоримуронэтил, тифенсульфуронметил, трибенуронметил, бенсульфуронметил, никосульфурон, этаметсульфуронметил, римсульфурон, трифлюсульфуронметил, триасульфурон, примисульфуронметил, циносульфурон, амидосульфурон, флузасульфурон, имазосульфурон, пиразосульфуронэтил, галогенсульфурон, азимсульфурон, циклосульфурон, этоксисульфурон, флазасульфурон, флупирсульфуронметил, форамсульфурон, иодсульфурон, оксасульфурон, мезосульфурон, просульфурон, сульфосульфурон, трифлоксисульфурон, тритосульфурон, производное любого из указанных выше гербицидов и смесь двух или более указанных выше гербицидов. Гербициды на основе триазолопиримидина по изобретению включают, но не ограничиваются ими, хлорансулам, диклосулам, флорасулам, флуметсулам, метосулам и пеноксулам. Гербициды на основе пиримидинилоксибензоата (или пиримидинилкарбокси) по изобретению включают, но не ограничиваются ими, биспирибак, пиритиобак, пириминобак, пирибензоксим и пирифталид. Гербициды на основе сульфониламинокарбонилтриазолинона включают, но не ограничиваются ими, флукарбазон и пропоксикарбазон.
Установлено, что гербициды на основе пиримидинилоксибензоата относятся к гербицидам на основе пиримидинилтиобензоата и могут распространяться под названием гербицидов на основе пиримидинилтиобензоата, посредством американского общества исследователей сорных растений. Таким образом, гербициды по настоящему изобретению дополнительно включают гербициды на основе пиримидинилтиобензоата, включая, в качестве неограничивающих примеров, гербициды на основе пиримидинилоксибензоата, описанные выше.
III. Молекулы нуклеиновой кислоты
Настоящее изобретение также относится к выделенной молекуле нуклеиновой кислоты события 127. Как применяют в настоящем документе, применение термина “молекула нуклеиновой кислоты” не предназначено для ограничения молекулы нуклеиновой кислотой включением только ДНК, но также включает любые нуклеотиды, такие как рибонуклеотиды и комбинации рибонуклеотидов и дезоксирибонуклеотидов. Такие дезоксирибонуклеотиды и рибонуклеотиды включают как природные молекулы, так и синтетические аналоги. Молекулы нуклеиновой кислоты также включают все формы последовательности, включая, в качестве неограничивающих примеров, одноцепочечные формы, двухцепочечные формы, шпильки, структуры вида стебель-петля и т.п. В одном из вариантов осуществления молекула нуклеиновой кислоты события 127 включает молекулу нуклеиновой кислоты с последовательностью нуклеиновых кислот, располагающихся в положениях от 1312 до 6069 в SEQ ID NO:1. В другом варианте осуществления молекула нуклеиновой кислоты события 127 включает молекулу нуклеиновой кислоты с последовательностью нуклеотидов, располагающихся в положениях от 1302 до 6079 в SEQ ID NO:1.
Молекула нуклеиновой кислоты события 127 также включает фрагменты SEQ ID NO:1. “Фрагменты” нуклеотидной последовательности могут представлять собой фрагменты любой длины, такой как, например, по меньшей мере 7, 15, 20, 25, 30, 40, 60, 80, 100, 150, 200, 250, 300, 350, 400, 450, 550, 650, 700, 800, 900, 1000, 1200, 1400, 1600, 1800, 2000, 2200, 2400, 2600, 2800, 3000, 3500, 4000, 4500 или более нуклеотидов (нт) в длину. Эти фрагменты имеют обширное применение, которое включает, но не ограничивается ими, диагностические зонды и праймеры. Разумеется, что более длинные фрагменты, такие как те, длина которых 601-8000 нт, также являются пригодными по настоящему изобретению, поскольку представляют собой фрагменты, соответствующие большинству, если не всем, нуклеотидным последовательностям SEQ ID NO:1. Под фрагментами по меньшей мере 20 нт в длину подразумевают, например, фрагменты, которые включают 20 или более смежных оснований, например, из нуклеотидной последовательности SEQ ID NO:1.
Растение события 127 включает трансгенную экспрессирующую кассету с кодирующей последовательностью AHASL, которая имеет мутацию S653N, что обеспечивает невосприимчивость или устойчивость к ингибирующим гербицидам на основе имидазолинона. Кассета дополнительно включает 5' и 3' регуляторные последовательности, функционально связанные с кодирующей последовательностью AHASL. “Функционально связанный” предназначен для обозначения функциональной связи между двумя или более элементами. Например, функциональная связь между представляющей интерес молекулой нуклеиновой кислоты и регуляторной последовательностью (например, промотором) является функциональной связью, которая предусмотрена для экспрессии представляющей интерес молекулы нуклеиновой кислоты. Функционально связанные элементы могут являться смежными или не смежными. При использовании в отношении соединения двух кодирующих белок областей, под функционально связанными следует понимать, что кодирующие области располагаются в одной и той же рамке считывания.
Таким образом, экспрессирующая кассета в растении сои события 127 содержит в 5'-3' направлении транскрипции, область инициации транскрипции (например, промотор) и область инициации трансляции, кодирующую область AHASL S653N и области терминации транскрипции и трансляции, функционирующие в растениях. “Промотор” относится к нуклеотидной последовательности, способной регулировать экспрессию кодирующей последовательности или функциональной РНК. В основном кодирующая последовательность локализована с 3'-конца по отношению к промоторной последовательности. Последовательность промотора может включать проксимальные и более дистальные элементы, расположенные против хода транскрипции, последние элементы часто обозначают как энхансеры. Таким образом, “энхансер” представляет собой нуклеотидную последовательность, которая может стимулировать активность промотора и может являться внутренним элементом промотора или гетерологичным элементом, встроенным для увеличения уровня эффективности или тканеспецифичности промотора. Промоторы можно получать в полном объеме из природного гена или комбинированием различных элементов, полученных из различных промоторов, найденных в природе, или промотор даже содержит синтетические нуклеотидные сегменты. Специалистам в данной области будет понятно, что различные промоторы могут управлять экспрессией гена в различных тканях или типах клеток, или на различных стадиях развития или под действием различных условий окружающей среды. Промоторы, которые обуславливают экспрессию фрагмента нуклеиновой кислоты в большинстве типов клеток большую часть времени, обычно обозначают как “конститутивные промоторы”.
В одном из вариантов осуществления экспрессирующая кассета в растении сои события 127 содержит, в качестве функционально связанных компонентов, кодирующую последовательность AHASL с S653N, располагающуюся под контролем промотора csr1-2 Arabidopsis thaliana, и область терминации транскрипции csr1-2. Экспрессирующую кассету получают в виде фрагмента PvuII из нуклеиновокислотного конструкта pAC321. В одном из вариантов осуществления экспрессирующая кассета имеет последовательность SEQ ID NO:4.
Предоставляют выделенные молекулы нуклеиновой кислоты, которые можно использовать в различных способах для детекции и/или идентификации молекулы нуклеиновой кислоты события 127. В одном из вариантов осуществления, “выделенная” молекула нуклеиновой кислоты не имеет последовательностей (например, последовательностей, кодирующих белок), которые в природе фланкируют молекулу нуклеиновой кислоты (т.е. последовательности, расположенные на 5' и 3'-концах нуклеиновой кислоты) в геномной ДНК организма, из которой получена молекула нуклеиновой кислоты. Например, в различных вариантах осуществления, выделенная молекула нуклеиновой кислоты может содержать менее чем приблизительно 5 т.п.н., 4 т.п.н., 3 т.п.н., 2 т.п.н., 1 т.п.н., 0,5 т.п.н. или 0,1 т.п.н. в нуклеотидной последовательности, которая в природе фланкирует молекулу нуклеиновой кислоты в геномной ДНК клетки, из которой получена молекула нуклеиновой кислоты.
В некоторых вариантах осуществления молекулы нуклеиновой кислоты включают соединяющую последовательность ДНК, представленную в SEQ ID NO:5 и/или 6. В других вариантах осуществления молекулы нуклеиновой кислоты включают соединяющую последовательность ДНК, представленную в SEQ ID NO:5 и/или 6, или ее варианты и фрагменты. Фрагменты и варианты соединяющий последовательности ДНК являются подходящими для отличительной идентификации ДНК события 127. Как обсуждалось в другом месте настоящего документа, такие последовательности находят применение в качестве праймеров и/или зондов для применения при детекции в образце встроенной ДНК события 127.
В других вариантах осуществления предоставляют молекулы нуклеиновой кислоты, с помощью которых можно детектировать растения события 127, встроенную ДНК события 127 или молекулу нуклеиновой кислоты, специфичную для события 127. Такие последовательности включают любую молекулу нуклеиновой кислоты, содержащую молекулу нуклеиновой кислоты, представленную в SEQ ID NO:5 и/или 6, или их варианты или комплементарные им. В некоторых вариантах осуществления молекула нуклеиновой кислоты, использующаяся для детекции молекулы нуклеиновой кислоты события 127, включает последовательность, представленную в SEQ ID NO:5 и/или 6 или комплементарную им. Фрагменты и варианты молекул нуклеиновой кислоты, которые детектируют молекулу нуклеиновой кислоты события 127, встроенную ДНК события 127 или конкретный участок события 127, являются подходящими для отличительной идентификации растений события 127. Как обсуждалось в другом месте настоящего документа, такие последовательности нашли применение в качестве праймеров и/или зондов. Дополнительно представленными являются выделенные последовательности ДНК нуклеотидных праймеров, содержащие или состоящие из последовательности, представленной в SEQ ID NO:35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 47, 67, 68, 69, 70 или комплементарные им, или варианты и фрагменты SEQ ID NO:35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 47, 67, 68, 69, 70 или комплементарные им.
В одном из вариантов осуществления специфичная пара праймеров для применения по настоящему документу содержит прямые и обратные праймеры, представленные ниже (идентифицированное взаимное расположение в SEQ ID NO:1). Праймеры рассчитывали для получения полосы размером 327 пар оснований.
(SEQ ID NO:1)

Как применяют в настоящем документе, “варианты”, по отношению к последовательности нуклеиновой кислоты, относятся к по существу похожим последовательностям. Для молекул нуклеиновой кислоты, вариант содержит молекулу нуклеиновой кислоты с делециями (например, укорочения) с 5' и/или 3'-конца; делецию и/или вставку одного или нескольких нуклеотидов в одном или нескольких внутренних участках в природной молекуле нуклеиновой кислоты; и/или замену одного или нескольких нуклеотидов в одном или нескольких участках в природной молекуле нуклеиновой кислоты.
В настоящем изобретении можно использовать любую комбинацию праймеров, такую как те, которые описывают в настоящем документе, для детекции конкретной области события 127 (например, SEQ ID NO:35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 47, 67, 68, 69 и 70). Неограничивающие примеры пар праймеров включают SEQ ID NO:35 и 36; SEQ ID NO:37 и 38; SEQ ID NO:39 и 40; SEQ ID NO:41 и 42; SEQ ID NO:43 и 44, SEQ ID NO:67 и 68, SEQ ID NO:69 и 70. По настоящему изобретению можно также конструировать дополнительные праймеры и пары праймеров для применения в описанных способах.
Зонды и праймеры, для применения в предоставленных способах, имеют достаточную нуклеотидную длину для связывания с целевой последовательностью ДНК и специфичной детекции и/или идентификации молекулы нуклеиновой кислоты в биологическом образце, например, образцов, полученных из тестируемого растения. Установлено, что для достижения этого результата условия гибридизации или реакции может определить оператор. Длина зондов и праймеров может представлять собой любую длину, которая может быть полезной в выборе способа детекции, такую как 8, 10, 11, 14, 16, 18, 20, 22, 24, 26, 28, 30, 40, 50, 75, 100, 200, 300, 400, 500, 600, 700 нуклеотидов или более или приблизительно от 11-20, 20-30, 30-40, 40-50, 50-100, 100-200, 200-300, 300-400, 400-500, 500-600, 600-700, 700-800 или более нуклеотидов в длину. Такие зонды и праймеры можно специфично гибридизовать с целевой последовательностью в сильно “строгих условиях” гибридизации. Зонды и праймеры, по вариантам осуществления, могут иметь последовательность ДНК, полностью идентичную нуклеотидам, смежным с целевой последовательностью, хотя общепринятыми способами можно конструировать зонды, отличающиеся от целевой последовательности ДНК и которые сохраняют способность специфично детектировать и/или идентифицировать целевую последовательность ДНК. Таким образом, зонды и праймеры могут разделять приблизительно 80%, 85%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или больше идентичности последовательности или комплементарности к целевой молекуле нуклеиновой кислоты (например, SEQ ID NO:35, 36, 37, 38, 39, 40, 41, 42, 43, 44) или могут отличаться от целевой последовательности (например, SEQ ID NO:35, 36, 37, 38, 39, 40, 41, 42, 43, 44) за счет 1, 2, 3, 4, 5, 6 или более нуклеотидов. Зонды можно использовать в качестве праймеров, но, как правило, их конструируют для связывания с целевой ДНК или РНК и не используют в реакции амплификации.
В некоторых вариантах осуществления специфичные праймеры можно использовать для амплификации фрагмента ДНК события для получения ампликона, который можно использовать в качестве “специфичного зонда” или ампликона, который сам может быть детектирован для идентификации молекул нуклеиновой кислоты события 127 в биологических образцах. Альтернативно, зонд можно использовать в течение реакции ПЦР для обеспечения детекции амплифицированного события (например, зонд Taqman или зонд MGB) (так называемая ПЦР в реальном времени). Если зонд гибридизуют с молекулами нуклеиновой кислоты в биологическом образце в условиях, которые обеспечивают связывание зонда с образцом, это связывание можно детектировать, и это, таким образом, обеспечивает наличие показателя присутствия события 127 в биологическом образце. Такая идентификация связанного зонда описана в данной области. В одном из вариантов осуществления зонд представляет собой последовательность, которая, в оптимальных условиях, специфично гибридизуется с областью, включающей 5' или 3' фланкирующую область события, включая также часть встроенной ДНК, смежной с ней, таким образом, перекрывая область соединения. Специфичный зонд может содержать последовательность, по меньшей мере на 80%, между 80 и 85%, между 85 и 90%, между 90 и 95% и между 95 и 100% идентичную (или комплементарную) специфичному участку молекулы нуклеиновой кислоты события 127.
Как применяют в настоящем документе, “амплифицированная ДНК” или “ампликон” относится к продукту амплификации целевой молекулы нуклеиновой кислоты, которая является частью нуклеиновокислотной матрицы. Например, для определения того, содержит ли полученное в результате полового скрещивания растение сои молекулу нуклеиновой кислоты события 127, ДНК, полученную из ткани растения сои, можно подвергать способу амплификации молекул нуклеиновых кислот, используя пару праймеров из ДНК, которая включает первый праймер, полученный к фланкирующей последовательности, расположенной рядом с участком встраивания встроенной гетерологичной ДНК, а второй праймер получен к встроенной гетерологичной ДНК, для получения ампликона, который является диагностическим или является показателем наличия молекулы нуклеиновой кислоты события 127. Посредством “диагностического” для участка события 127 обозначают применение любого способа или анализа, который позволяет сделать различие между наличием или отсутствием участка события 127 в биологическом образе. Альтернативно, второй праймер можно получать к фланкирующей последовательности. В других вариантах осуществления пары праймеров можно получать к фланкирующим последовательностям, которые расположены по обеим сторонам встроенной ДНК, чтобы, таким образом, получить ампликон, который включает полную встроенную молекулу нуклеиновой кислоты экспрессирующей конструкции, а также последовательность, фланкирующую трансгенную вставку, например, SEQ ID NO:1. Ампликон имеет длину и последовательность, которая также является диагностической для события (например, содержит ДНК-соединение из участка события 127). Ампликон может варьировать в длину, от комбинированной длины пар праймеров и одной пары нуклеотидных оснований до любой длины ампликона, получаемой по протоколу амплификации ДНК. Представитель пары праймеров, полученный из фланкирующей последовательности, может быть расположен на расстоянии от встроенной последовательности ДНК, это расстояние может варьировать от одной нуклеотидной пары оснований вплоть до предельных величин реакции амплификации или приблизительно двадцати тысяч нуклеотидных пар оснований. В другом варианте осуществления пары праймеров можно конструировать для амплификации встроенной ДНК или фрагмента встроенной ДНК. Такие пары праймеров пригодны для детекции наличия в биологическом образце встроенной ДНК события 127. Применение термина “ампликон”, в частности, исключает димеры праймеров, которые могут образовываться в зависимой от температуры реакции амплификации ДНК.
В определенных вариантах осуществления пригодные пары праймеров будут включать один праймер, который перекрывает точку соединения встроенной ДНК и фланкирующих 5' или 3' последовательностей геномной ДНК. Такие праймеры можно конструировать к последовательности, располагающейся вблизи точки соединения 5' фланкирующей ДНК и встроенной ДНК (т.е. соединением между положениями 1311 и 1312 SEQ ID NO:1), а также вблизи точки соединения между встроенной ДНК и 3' фланкирующей ДНК (т.е. соединением между положениями 6069 и 6070 SEQ ID NO:1). Такие праймеры можно конструировать для гибридизации с приблизительно 10 нуклеотидами или из фланкирующей области или из встроенной ДНК, и по меньшей мере с 1 нуклеотидом, проходящим через точку соединения во встроенной ДНК или фланкирующей области. Таким образом, праймеры могут содержать, например, нуклеотидные последовательности, сконструированные для гибридизации с нуклеотидами, представленными по меньшей мере следующими положениями в SEQ ID NO:1: 1311-1321, 1302-1312, 6060-6070 и/или 6069-6079.
В других вариантах осуществления пригодные пары праймеров будут включать праймер, который перекрывает точку соединения 5′-конца дублированной части кодирующей последовательности csr1-2 во встроенной ДНК (в положении 5694 SEQ ID NO:1) и смежной встроенной ДНК (т.е. в положении 5693 SEQ ID NO:1). Такие праймеры можно конструировать для гибридизации с приблизительно 10 нуклеотидами или из дублированного участка, или из смежной встроенной ДНК и с по меньшей мере 1 нуклеотидом, проходящим через точку соединения (например, по меньшей мере 5693-5703 или по меньшей мере 5684-5694 в SEQ ID NO:1).
Способы получения и использования зондов и праймеров для применения в настоящем изобретении являются известными в данной области. Пары праймеров для ПЦР можно получать из известной последовательности, например, с использованием компьютерных программ, предназначенных для такой цели, таких как анализ праймеров для ПЦР в версии 6 программы Vector NTI (Informax Inc., Bethesda Md.); PrimerSelect (DNASTAR Inc., Madison, Wis.); и Primer (Version 0,5©, 1991, Whitehead Institute for Biomedical Research, Cambridge, Mass.). Дополнительно, последовательность можно визуально изучать, и идентифицировать праймеры вручную, используя руководства, известные специалисту в данной области.
IV. Способы разведения
Описанные растения сои события 127 можно использовать в программе разведения, используя способы разведения для получения дополнительных растений сои события 127, таких как растения-потомки. Такие способы разведения можно использовать для получения растений сои для применения, например, в коммерческом производстве в различных географических областях или для получения дополнительных популяций поколений сои.
Кроме того, растения сои события 127 можно использовать в программах разведения, используя способы разведения для получения растений сои с дополнительными представляющими интерес признаками, комбинированными с признаком устойчивости к ингибитору AHAS (также обозначаемых как “объединенные признаки” или “объединение признаков”), такие как комбинации невосприимчивости к другим гербицидам, таким как гербициды на основе глифосата, глуфосината и/или к гербициду дикамба. Кроме того, растения сои события 127 можно использовать в программе разведения, используя способы разведения для получения растений сои, с кодирующими последовательностями, обеспечивающими множественную невосприимчивость к ингибирующему AHAS гербициду. Описанные растения также можно использовать в программах разведения, используя способы разведения для получения растений с признаком устойчивости к ингибирующему AHAS гербициду, объединенному с другими агрономически важными признаками, включающими начальные признаки (такие как невосприимчивость к заболеваниям и патогенам, такие признаки, которые обеспечиваются геном Bt) и конечные признаки, такие как качество и количество масла и белка.
Описанные способы разведения растений сои, невосприимчивых к ингибирующему AHAS гербициду, включают стадии (a) скрещивание растения сои события 127 со вторым растением сои; и (b) получение, в результате скрещивания, семян. Полученные семена можно дополнительно подвергать скринингу для идентификации семян, которые содержат молекулу нуклеиновой кислоты события 127. В такие способы можно дополнительно включать получение образца ДНК из семян, полученных в результате скрещивания, и анализ образца на наличие или отсутствие молекулы нуклеиновой кислоты события 127. Альтернативно, семена можно подвергать скринингу на устойчивость к ингибирующему AHAS гербициду для идентификации семян или потомков, которые содержат ДНК события 127.
Растение сои события 127 можно размножать, используя любые способы разведения, доступные для растений сои. Например, растение сои события 127 можно размножать посредством первого полового скрещивания первого родительского растения сои, выросшего от трансгенного растения сои события 127 (или его потомства, полученного в результате трансформации экспрессирующими кассетами по варианту осуществления, которые придают устойчивость к гербицидам), и второго родительского растения сои, которое лишено фенотипа устойчивости к гербициду, с получением, таким образом, множества растений-потомков первого поколения; и дальнейший отбор растений потомков первого поколения, которые демонстрируют требуемую устойчивость к гербициду; и самоопыление растений-потомков первого поколения, с получением, таким образом, множества растений-потомков второго поколения; и дальнейший отбор растений-потомков второго поколения, которые демонстрируют требуемую устойчивость к гербицидам. Эти стадии могут дополнительно включать возвратное скрещивание растений-потомков первого поколения, устойчивых к гербицидам, или растений-потомков второго поколения, устойчивых к гербицидам, со вторым родительским растением сои или третьим родительским растением сои, с получением, тем самым, растения сои, которые демонстрируют требуемую невосприимчивость к гербицидам. Дополнительно показали, что анализ фенотипа потомства не требуется. Различные способы и композиции, которые описаны в другом месте настоящего документа, можно использовать для детекции и/или идентификации вставки события 127.
Также будет понятно, что различные трансгенные растения можно также подвергать половому скрещиванию для получения потомства, которое содержит два независимо добавленных сегрегирующих экзогенных гена. Самоопылением подходящих потомков можно получать растения, которые являются гомозиготными по обоим добавленным, экзогенным генам. Также предполагают возвратное скрещивание с родительским растением и аутокроссинг с нетрансгенным растением, также как и вегетативное размножение. Однако любой способ можно использовать для создания таких растений.
Можно выводить инбредные линии сои, содержащие молекулу нуклеиновой кислоты события 127, для применения в получении сортов сои и в качестве родительских растений в программах разведения, для создания новых и отличительных инбредных линий сои. Инбредные линии сои часто используют в качестве целевых линий для интрогрессии новых признаков, посредством общепринятых способов разведения и/или молекулярных способов интрогрессии. Доступными являются многие аналитические способы для определения гомозиготной и фенотипической стабильности инбредных линий.
В некоторых вариантах осуществления молекулу нуклеиновой кислоты, приводящую в результате к получению растения сои события 127 по изобретению, можно конструировать в молекулярной сцепке с молекулой нуклеиновой кислоты, которая придает свойство невосприимчивости ко второму гербициду, такому как глифосат. В других вариантах осуществления молекулярная сцепка дополнительно содержит по меньшей мере одну дополнительную молекулу нуклеиновой кислоты, которая придает свойство устойчивости к третьему гербициду. В одном из вариантов осуществления последовательность придает свойство устойчивости к глуфосинату, и в конкретном варианте осуществления последовательность включает pat.
В других вариантах осуществления растение сои события 127 по изобретению содержит один или несколько представляющих интерес признаков, и, в некоторых вариантах осуществления, для создания растений с требуемой комбинацией признаков, ДНК события 127 объединена с любой комбинацией последовательностей молекул нуклеиновой кислоты и/или представляющими интерес признаками. Признак, как применяют в настоящем документе, относится к фенотипу, полученному из конкретной последовательности или группы последовательностей. Например, молекулу нуклеиновой кислоты, обеспечивающую устойчивость к гербицидам, можно объединять с любыми другими молекулами нуклеиновой кислоты, кодирующими полипептиды с пестицидной и/или инсектицидной активностью, такие как токсические белки Bacillus thuringiensis (белки Bt), лектины и т.п. Полученные комбинации могут также включать множественные копии любых представляющих интерес молекул нуклеиновой кислоты.
В некоторых вариантах осуществления, для создания трансгенного растения по изобретению с дополнительными улучшенными свойствами, ДНК сои события 127 можно объединять с ДНК, обеспечивающими другие признаки устойчивости к гербицидам. Другие молекулы нуклеиновой кислоты, обеспечивающие устойчивость к гербицидам, которые можно использовать в таких вариантах осуществления, включают те, которые придают устойчивость к глифосату или к ингибиторам AHAS посредством других способов действия, таких как, например, ген, который кодирует фермент глифосатоксидоредуктазу. Другие признаки, которые можно комбинировать с ДНК сои события 127, включают те, которые получены из молекулы нуклеиновой кислоты, которая придает растению способность продуцировать на повышенном уровне 5-енолпирувилшикимат-3-фосфатсинтазу (EPSPS). Другие признаки, которые можно комбинировать с событием 127 сои, включают те признаки, которые придают устойчивость к сульфонилкарбамиду и/или имидазолинону.
В некоторых вариантах осуществления ДНК сои события 127 можно объединять, например, с гидроксифенилпируватдиоксигеназой, которые представляют собой ферменты, которые катализируют реакцию, в которой пара-гидроксифенилпируват (HPP) трансформируют в гомогентизат. Молекулы, которые ингибируют этот фермент и которые связываются с ферментом для ингибирования трансформации HPP в гомогентизат, являются пригодными в качестве гербицидов. Признаки, придающие растениям устойчивость к таким гербицидам, являются известными в данной области. Другие примеры подходящих признаков, обеспечивающих устойчивость к гербицидам, которые можно объединять с ДНК сои события 127, включают молекулы нуклеиновой кислоты, кодирующие арилоксиалканоатдиоксигеназу (которая, как сообщают, придает устойчивость к 2,4-D и другим гербицидам на основе феноксиауксина, а также к гербицидам на основе арилоксифеноксипропионата), и молекулы нуклеиновой кислоты, придающие устойчивость к гербициду дикамба.
Другие примеры признаков, придающие устойчивость к гербицидам, которые можно объединять с ДНК сои события 127, включают те признаки, которые обеспечиваются молекулами нуклеиновой кислоты, кодирующими экзогенную фосфинотрицинацетилтрансферазу. Растения, содержащие экзогенную фосфинотрицинацетилтрансферазу, могут проявлять повышенную устойчивость к гербицидам на основе глуфосината, которые ингибируют фермент глутаминсинтазу. Другие примеры признаков, придающих устойчивость к гербицидам, которые можно объединять с ДНК сои события 127, включают те признаки, которые обеспечиваются молекулами нуклеиновой кислоты, изменяющими активность протопорфириногеноксидазы (протокс). Растения, содержащие такие молекулы нуклеиновой кислоты, могут проявлять повышенную устойчивость к любой разновидности гербицидов, цель которых - фермент протокс (также обозначаемые как “ингибиторы протокса”).
Другие примеры признаков, придающих устойчивость к гербицидам, которые можно объединять с признаком устойчивости к гербицидам, ингибирующими AHAS, включают признаки, которые придают устойчивость по меньшей мере к одному гербициду у растения, такого как, например, растение сои. Растения сои, устойчивые к гербицидам, известны в данной области, поскольку являются растениями, которые различаются по своей устойчивости к конкретным гербицидам. Для получения растения по изобретению, а также для способов его применения можно комбинировать признак(и), ответственные за устойчивость к гербицидам, посредством разведения или посредством других способов, подходящих для растения сои события 127.
ДНК сои события 127 также можно комбинировать по меньшей мере с одним другим признаком, для получения растений по настоящему изобретению, которые дополнительно содержат ряд комбинаций требуемых признаков, включая, в качестве неограничивающих примеров, признаки, необходимые для корма для животных, такие как высокое содержание масла; композиция аминокислот, содержание белка, повышенная усвояемость или измененная композиция жирных кислот.
ДНК сои события 127 также можно комбинировать с другими необходимыми признаками, такими как, например, авирулентность и наличие генов, обеспечивающих признаки устойчивости к заболеваниям, таким как признаки невосприимчивости к цистообразующей нематоде сои, например, SCN, и признаки, требуемые для переработки или производства продуктов, такие как повышенное содержание масла или модифицированная композиция жирных кислот (например, гены десатуразы жирных кислот; и для полимеров или биопластиков (например, бета-кетотиолаза, полигидроксибутиратсинтаза и ацетоацетил-КоA-редуктаза), облегчающие экспрессию полигидроксиалканоатов (PHA)). Молекулы нуклеиновой кислоты, обеспечивающие устойчивость к гербицидам, можно также комбинировать с молекулами нуклеиновой кислоты, обеспечивающими любые агротехнические характеристики.
Объединенные комбинации можно создавать любым способом, включая, в качестве неограничивающих примеров, разведение растений любым известным способом или генетической трансформацией. Если последовательности объединяют посредством генетической трансформации растений, представляющие интерес последовательности молекул нуклеиновой кислоты можно комбинировать в любой период времени и в любом порядке. Признаки могут быть введены одновременно, в протоколе совместной трансформации с представляющими интерес молекулами нуклеиновой кислоты, при условии комбинации кассет для трансформации. Например, при введении двух последовательностей две последовательности могут содержаться в отдельных кассетах для трансформации (транс) или в одной и той же кассете для трансформации (цис). Экспрессию последовательностей можно получать под одним и тем же промотором или под различными промоторами. В некоторых случаях может быть желательным введение кассеты для трансформации, которая будет тормозить экспрессию представляющей интерес молекулы нуклеиновой кислоты. Это можно комбинировать с любой комбинацией других кассет для супрессии или сверхэкспрессирующих кассет для создания требуемой комбинации признаков у растения. Дополнительно показано, что молекулы нуклеиновой кислоты можно объединять в требуемом положении в геноме, используя систему сайт-специфической рекомбинации.
Также предоставленными являются способы разведения растений сои с ДНК события 127, где способ включает (a) скрещивание растения сои события 127 или его производных со вторым родительским растением сои; (b) получение семян в результате скрещивания; (c) получение образца ДНК из одного или нескольких семян; и (d) определение наличия молекулы нуклеиновой кислоты события 127.
V. Трансформированные растения
Растения сои, обладающие признаками, комбинированными с признаком наличия события 127, также можно получать посредством трансформации растительного материала или частей растения, полученных от растений сои события 127. Дополнительные признаки можно комбинировать в растениях сои события 127, используя любой способ трансформации, доступный для специалистов в данной области. Таким образом, растения сои события 127 можно использовать в качестве источника растительного материала для применения в способах трансформации для введения дополнительных гетерологичных молекул нуклеиновой кислоты в растение сои события 127. Например, векторы для трансформации можно получать для введения представляющих интерес генов в растения сои события 127 для получения растений сои, обладающих множественными введенными признаками.
Для применения в таких способах можно использовать векторы для трансформации для получения растений, трансформированных любым представляющим интерес геном, включая те, которые описаны в настоящем документе. Вектор для трансформации может включать селективный маркер, и подлежащий введению представляющий интерес ген, как правило, экспрессируется в трансформированном растении сои события 127. Такие селективные маркеры известны в данной области. Представляющие интерес гены по изобретению варьируют в зависимости от подлежащего введению требуемого признака. Например, различные изменения в фенотипе, которые могут представлять интерес, включают модифицированную композицию жирных кислот в растении, измененный аминокислотный состав растения, изменение насекомого у растения и/или механизмов защиты от патогенов и т.п. Этих результатов можно достичь обеспечением экспрессии гетерологичных продуктов или повышенной экспрессией эндогенных продуктов в растениях. Альтернативно, для снижения экспрессии одного или нескольких эндогенных продуктов, конкретно ферментов или кофакторов, результатов можно достичь посредством предоставления растению эндогенных продуктов. Эти изменения приводят к изменению фенотипа трансформированного растения.
В способах по настоящему изобретению можно использовать любой вектор для трансформации. Ряд векторов для трансформации растений и способы трансформации растений являются доступными. Способы трансформации можно использовать для объединения любого признака с признаком, обеспечивающим устойчивость к ингибирующему AHAS гербициду, который обеспечивается вставкой события 127, включая те признаки, которые описывают в настоящем документе.
VI. Способы детекции
Также предоставляют способы и композиции для идентификации и/или детекции в биологическом образце молекул нуклеиновой кислоты события 127, например, в образце, полученном из растения сои, включая его потомство и производные. Такие способы находят применение при идентификации и/или детекции участков события 127 или молекул нуклеиновой кислоты события 127 в любом биологическом материале. Такие способы включают, например, способы, которые доказывают однородность семян, и способы скрининга семян в партии семян на наличие молекулы нуклеиновой кислоты события 127. В одном из вариантов осуществления предоставляют способ для идентификации молекулы нуклеиновой кислоты со встроенным событием 127 в биологическом образце, где способ включает получение смеси из биологического образца и первого и второго нуклеиновокислотного праймеров, допускающих амплификацию молекулы нуклеиновой кислоты события 127; проведение реакции в смеси в условиях, которые позволяют первому и второму нуклеиновокислотным праймерам амплифицировать молекулу нуклеиновой кислоты события 127 сои; и, детекцию наличия или отсутствия амплифицированной молекулы нуклеиновой кислоты события 127. В некоторых вариантах осуществления молекула нуклеиновой кислоты события 127 является молекулой нуклеиновой кислоты, специфичной для события 127.
Также предоставленными являются способы идентификации молекулы нуклеиновой кислоты события 127 в биологическом образце, где способы включают получение смеси, содержащей биологический образец с ДНК сои и молекулу нуклеиновокислотного зонда, который способен гибридизоваться с молекулой нуклеиновой кислоты события 127 сои, проведение реакции в смеси в условиях, которые позволяют молекуле нуклеиновокислотного зонда гибридизоваться с молекулой нуклеиновой кислоты события 127, и детекцию того, произошла ли в образце гибридизация молекулы нуклеиновокислотного зонда с молекулой нуклеиновой кислоты события 127, где наличие гибридизации свидетельствует о присутствии молекулы нуклеиновой кислоты события 127.
Способы по настоящему изобретению также можно использовать для идентификации и/или детекции в биологическом образце молекулы нуклеиновой кислоты со встроенным событием 127. В одном из вариантов осуществления предоставляют способ идентификации молекулы нуклеиновой кислоты события 127 в биологическом образце, и способ включает получение смеси из биологического образца и первого и второго нуклеиновокислотного праймера, способных обеспечить амплификацию молекулы нуклеиновой кислоты со встроенным событием 127; проведение реакции в смеси в условиях, которые позволяют первому и второму нуклеиновокислотным праймерам обеспечивать амплификацию молекулы нуклеиновой кислоты со встроенным событием 127; и детекцию наличия или отсутствия амплифицированной молекулы нуклеиновой кислоты со встроенным событием 127.
Также предоставленными являются способы идентификации в биологическом образце молекул нуклеиновой кислоты события 127, где способы включают получение смеси, содержащей биологический образец с ДНК и молекулу нуклеиновокислотного зонда, который способен гибридизоваться с молекулой нуклеиновой кислоты события 127, реакцию в смеси в условиях, которые позволяют молекуле нуклеиновокислотного зонда гибридизоваться с молекулой нуклеиновой кислоты события 127, и детекцию того, произошла ли в образце гибридизация молекулы нуклеиновокислотного зонда с молекулой нуклеиновой кислоты события 127, где наличие гибридизации свидетельствует о присутствии молекулы нуклеиновой кислоты события 127.
Дополнительно представленными являются способы детекции в биологическом образце участков события 127. Участки события 127, которые можно детектировать, используя способы по настоящему изобретению, включают ДНК со встроенным событием 127, 5' участки соединения, 3' участки соединения, 5' фланкирующие области, 3' фланкирующие области, специфичные мутации или дупликации во встроенной ДНК, обусловленные трансформационным событием или их комбинацией и фрагментами любого из них.
Биологический образец может содержать любой образец, в котором желают определить присутствие молекулы нуклеиновой кислоты события 127. Например, биологический образец может включать любой материал растения или материал, содержащий материал растения или полученный из материала растения, такой как, но не ограничиваясь этим, пищевые продукты или корма. Как применяют в настоящем документе, “материал растения” относится к материалу, который получают или производят из растения или части растения. В конкретных вариантах осуществления, биологический образец включает ткань сои. В других вариантах осуществления биологический образец получают из ткани листьев сои. В других вариантах осуществления биологический образец получают из ткани семян сои.
Любую молекулу нуклеиновой кислоты, связанную с событием 127, можно детектировать и/или идентифицировать, используя способы по настоящему изобретению. Например, молекулы нуклеиновой кислоты, которые можно детектировать, включают в качестве неограничивающих примеров ДНК, мРНК, кДНК и т.п. В других вариантах осуществления, используя способы по настоящему изобретению, можно детектировать и/или идентифицировать полипептиды, кодируемые молекулой нуклеиновой кислоты события 127. Детектированные и/или идентифицированные молекулы нуклеиновой кислоты могут включать любой фрагмент ДНК со вставкой события 127, включая идентифицированные мутации во вставке ДНК, например, молекулы нуклеиновой кислоты, кодирующие полипептиды AHAS с S653N или R272K и т.п., последовательности промотора, терминирующие последовательности, фрагменты таких последовательностей и их комбинации.
Праймеры и зонды для применения в способах, описываемых в настоящем документе, можно использовать для подтверждения (и, если необходимо, для коррекции) описанных последовательностей посредством общепринятых способов, например посредством повторного клонирования и секвенирования таких последовательностей. Молекулы нуклеиновокислотных зондов и праймеров специфично детектируют целевую последовательность ДНК. Любой общепринятый способ нуклеиновокислотной гибридизации или амплификации можно использовать для детекции или идентификации в образце наличия молекулы нуклеиновой кислоты трансгенного события. Под “специфично определять” следует понимать, что молекулу нуклеиновой кислоты можно использовать или в качестве праймера для амплификации специфичного участка 127, или в качестве зонда, который гибридизуется в “строгих условиях” с молекулой нуклеиновой кислоты, имеющей специфичный участок события 127. Уровень или степень гибридизации, которые обеспечивают специфичную детекцию события 127 или специфичного участка события 127, являются достаточными для распознавания молекулы нуклеиновой кислоты со специфичным участком 127 и молекулы нуклеиновой кислоты без этого участка и обеспечивают, тем самым, отличительную идентификацию молекулы события 127. Под “разделять достаточную идентичность или комплементарность последовательности для обеспечения амплификации молекулы нуклеиновой кислоты события 127” подразумевают последовательность, которая разделяет по меньшей мере 80%, 85%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% идентичности или комплементарности с фрагментом молекулы нуклеиновой кислоты, обладающей молекулой нуклеиновой кислоты события 127, или с полноразмерной молекулой нуклеиновой кислоты, обладающей молекулой нуклеиновой кислоты события 127.
В отношении амплификации целевой молекулы нуклеиновой кислоты (например, посредством ПЦР) с использованием специфичной пары праймеров для амплификации, “строгие условия” представляют собой условия, которые позволяют паре праймеров гибридизоваться с целевой молекулой нуклеиновой кислоты, с которой будет связываться праймер, имеющий соответствующую последовательность дикого типа (или комплементарную ей), и позволяют предпочтительно получать, в зависящей от температуры реакции амплификации ДНК, поддающийся идентификации продукт амплификации (ампликон), имеющий молекулу нуклеиновой кислоты события 127. В способе ПЦР, олигонуклеотидные праймеры можно конструировать для применения в реакциях ПЦР для амплификации молекулы нуклеиновой кислоты события 127. Способы конструирования праймеров для ПЦР и ПЦР-клонирования, как правило, известны в данной области. Понятно, что ряд параметров в конкретных протоколах ПЦР можно по необходимости адаптировать к конкретным лабораторным условиям и можно незначительно модифицировать и, тем не менее, обеспечить набор похожих результатов. Эти поправки будут очевидны специалистам в данной области.
Для применения в описанных способах можно использовать праймеры для амплификации любой молекулы нуклеиновой кислоты события 127. Например, можно конструировать пары праймеров, которые способны обеспечить аплификацию участков, являющихся показателем растения, содержащего фрагмент молекулы нуклеиновой кислоты события 127. В одном из вариантов осуществления такие пары праймеров могут обеспечить амплификацию участка, содержащего один участок соединения, например, 5' участок соединения или 3' участок соединения. Такие пары праймеров включают один праймер, который способен обеспечить удлинение праймера от фланкирующего участка хромосомы (например, 5' или 3' фланкирующие области) в направлении вставки ДНК, тогда как второй праймер способен обеспечить удлинение праймера от вставки ДНК в направлении первого праймера во фланкирующем участке хромосомы. Такие пары праймеров амплифицируют молекулу нуклеиновой кислоты, которая включает участок соединения. В некоторых вариантах осуществления один из праймеров, использующихся в амплификационной паре, является способным к отжигу с участком, который охватывает один из участков соединения (например, 5', или 3' участки соединения) и способен обеспечивать амплификацию в направлении участка хромосомы или в направлении вставки. Праймеры к фланкирующему участку хромосомы для применения в таких способах могут являться способными к отжигу или с 5', или с 3' фланкирующими участками хромосомы и инициировать амплификацию в направлении вставки. В других вариантах осуществления можно конструировать пары праймеров, которые способны обеспечивать амплификацию двух участков соединения.
Для применения в таких способах можно конструировать другие примеры подходящих праймеров, способных к отжигу с 5' или 3' фланкирующими областями и которые могут включать, например, последовательности праймеров из от приблизительно 10 или 12 до приблизительно 40 нуклеотидов, способных к отжигу с молекулой нуклеиновой кислоты, представленной между положениями 1-1311 SEQ ID NO:1 или положениями от 6070 до 10656 SEQ ID NO:1.
Альтернативно, можно конструировать случайные праймеры, которые способны к отжигу на всем протяжении генома растения и которые можно использовать в комбинации со специфичным к последовательности вставки праймером для амплификации молекулы нуклеиновой кислоты, которая включает вставку ДНК и фрагмент фланкирующей последовательности. В некоторых вариантах осуществления праймер, специфичный к последовательности вставки, можно пометить, что позволяет осуществлять детекцию амплифицированного фрагмента, используя праймер, специфичный к последовательности вставки. В других вариантах осуществления для идентификации или детекции молекул нуклеиновой кислоты события 127 с мечеными зондами можно гибридизовать полученные в результате амплифицированные молекулы нуклеиновой кислоты.
В другом варианте осуществления можно конструировать пары праймеров, которые позволяют амплифицировать полную последовательность ДНК-вставки или часть последовательности вставки, которая является показателем наличия ДНК события 127. Например, в некоторых вариантах осуществления можно конструировать пары праймеров для амплификации полной последовательности ДНК-вставки, используя праймеры, которые располагаются вначале 5' и 3' фланкирующих областей вставки. Альтернативно, можно конструировать пары праймеров, которые способны обеспечивать амплификацию только участка вставки с событием 127 для идентификации наличия вставки. Например, для применения при детекции вставки в биологическом образце можно конструировать праймеры для амплификации любого участка в пределах фрагмента PvuII плазмиды pAC321. Такие праймеры включают праймеры, которые способны обеспечивать амплификацию любых участков ДНК-вставки, включая участок последовательности между положениями 1312 и 6069 SEQ ID NO:1. В некоторых вариантах осуществления можно конструировать пары праймеров, которые способны обеспечивать амплификацию кодирующей последовательности ДНК-вставки в Arabidopsis thaliana, мутантной по AHAS (например, от положений 2762 вплоть до 4774 или их фрагменты) или любой комбинации кодирующей и регуляторной последовательности вставки.
Амплифицированная молекула нуклеиновой кислоты (ампликон) может быть любой длины, которая позволяет осуществлять детекцию молекулы нуклеиновой кислоты события 127. Например, ампликон может составлять в длину приблизительно 10, 50, 100, 200, 300, 500, 700, 1000, 2000, 3000, 4000, 5000 нуклеотидов или более.
В некоторых вариантах осуществления можно детектировать один или несколько специфических участков молекулы нуклеиновой кислоты события 127.
В способах по настоящему изобретению можно применять любой праймер, который обеспечивает амплификацию и/или детекцию молекулы нуклеиновой кислоты события 127. В одном из вариантов осуществления праймеры содержат молекулу нуклеиновой кислоты события 127 или являются комплементарными молекуле нуклеиновой кислоты события 127, такой как, например, 8, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30 или более смежных нуклеотидов, соответствующих или комплементарных молекуле нуклеиновой кислоты с последовательностью SEQ ID NO:1. Например, в некоторых вариантах осуществления первый и второй праймеры содержат молекулу нуклеиновой кислоты из SEQ ID NO:35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 67, 68, 69 и 70, где первый или второй праймер разделяют достаточную идентичность или комплементарность последовательности с молекулой нуклеиновой кислоты, для амплификации молекулы нуклеиновой кислоты события 127. В дополнительных вариантах осуществления первый и второй праймер могут содержать любую одну или любую комбинацию последовательностей, представленных в SEQ ID NO:35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 67, 68, 69 и 70. Праймеры могут быть любой длины, достаточной для амплификации участка события 127 сои, включая, например, по меньшей мере 6, 7, 8, 9, 10, 15, 20, 15 или 30 или приблизительно 7-10, 10-15, 15-20, 20-25, 25-30, 30-35, 35-40, 40-45 нуклеотидов или более.
Как описано выше, в определенных вариантах осуществления пригодные пары праймеров будут включать один праймер, который перекрывает точку соединения между ДНК-вставкой и 5' или 3' фланкирующими последовательностями геномной ДНК. Такие праймеры можно конструировать к участку вблизи точки соединения между 5' фланкирующей ДНК и ДНК-вставкой (т.е. соединению между положениями 1311 и 1312 SEQ ID NO:1), а также к участку вблизи точки соединения между ДНК-вставкой и 3' фланкирующей ДНК (т.е. к соединению между положениями 6069 и 6070 SEQ ID NO:1). Такие праймеры можно конструировать для гибридизации с приблизительно 10 нуклеотидами или из фланкирующей области или из ДНК-вставки, по меньшей мере, с 1 нуклеотидом, проходящим через точку соединения в ДНК-вставке или фланкирующей области. Таким образом, праймеры могут включать, например, нуклеотидные последовательности, сконструированные для гибридизации с нуклеотидами, представленными следующими положениями в SEQ ID NO:1: 1311-1321, 1302-1312, 6060-6070 и/или 6069-6079.
В других вариантах осуществления пригодные пары праймеров будут включать один праймер, который перекрывает точку соединения между 5'-концом дуплицированного участка кодирующей последовательности csr1-2 ДНК-вставки (в положении 5694 SEQ ID NO:1) и 3'-концом смежного участка ДНК-вставки (т.е. в положении 5693 SEQ ID NO:1). Такие праймеры можно конструировать для гибридизации приблизительно с 10 нуклеотидами или из дуплицированного участка, или из смежной с ним ДНК-вставки и с по меньшей мере 1 нуклеотидом, проходящим через точку соединения (например, по меньшей мере 5693-5703 или по меньшей мере 5684-5694 SEQ ID NO:1).
Как обсуждалось в другом месте настоящего документа, можно применять любой способ ПЦР-амплификации молекул нуклеиновой кислоты события 127, включая, например, ПЦР в реальном времени.
Таким образом, в некоторых вариантах осуществления предоставляют способ детекции наличия молекул нуклеиновой кислоты события 127 в биологическом образце. Способ включает (a) выделение образца ДНК из биологического образца; (b) предоставление пары молекул праймеров к ДНК (например, любая комбинация SEQ ID NO:35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 67, 68, 69 и 70, где комбинация обеспечивает амплификацию участка события 127 сои), включая, в качестве неограничивающих примеров, i) последовательности SEQ ID NO:35 и SEQ ID NO:36, ii) SEQ ID NO:37 и SEQ ID NO:38, iii) SEQ ID NO:39 и SEO ID NO:40, iv) SEQ ID NO:41 и SEQ ID NO:42, v) SEQ ID NO:43 и SEQ ID NO:44, vi) SEQ ID NO:67 и SEQ ID NO:68 и vii) SEQ ID NO:69 и SEQ ID NO:70; (c) обеспечение условий, необходимых для реакции амплификации ДНК; (d) осуществление реакции амплификации ДНК, с получением, тем самым, молекулы ДНК-ампликона; и (е) детекцию молекулы ДНК-ампликона, где присутствие молекулы ДНК-ампликона в реакции амплификации ДНК указывает на присутствие в образце молекул нуклеиновой кислоты события 127. Для того чтобы молекула нуклеиновой кислоты служила в качестве праймера или зонда, она должна быть только комплементарной к последовательности, чтобы быть в состоянии сформировать стабильную двухцепочечную структуру в конкретно применяемых концентрациях раствора и соли.
В способах гибридизации можно применять всю или часть молекулы нуклеиновой кислоты, которая избирательно гибридизуется с целевой молекулой нуклеиновой кислоты события 127. Под “строгими условиями” или “строгими условиями гибридизации” в отношении условий, применяемых к молекуле нуклеиновокислотного зонда, подразумевают условия, в которых зонд будет гибридизоваться со своей целевой последовательностью в детектируемо большей степени, чем с другими последовательностями (например, по меньшей мере, с 2-кратным превышением фона). Относительно амплификации целевой молекулы нуклеиновой кислоты (например, посредством ПЦР), с использованием конкретной пары праймеров для амплификации, “строгие условия” представляют собой условия, которые позволяют паре праймеров гибридизоваться с целевой молекулой нуклеиновой кислоты, праймер для которой обладает соответствующей последовательностью дикого типа. Строгие условия зависят от последовательности и будут различными в различных условиях. Посредством контроля строгости условий гибридизации и/или промывки, можно идентифицировать целевые последовательности, которые являются на 100% комплементарными зонду (гомологичный зонд). Альтернативно, строгость условий можно регулировать, чтобы обеспечить в последовательности наличие некоторого количества неправильно спаренных оснований, с тем, чтобы детектировать более низкую степень идентичности (гетерологичный зонд). Как правило, зонд представляет собой менее чем приблизительно 1000 нуклеотидов в длину или менее чем 500 нуклеотидов в длину.
Как применяют в настоящем документе, по существу идентичная или комплементарная последовательность представляет собой молекулу нуклеиновой кислоты, которая будет специфично гибридизоваться с комплементарной молекулой нуклеиновой кислоты, с которой она сравнивается в условиях с высокой строгостью. Подходящие “строгие условия”, которые способствуют гибридизации ДНК, например, 6× хлорид натрия/цитрат натрия (SSC) при приблизительно 45°C, с последующей промывкой 2× SSC при 50°C, известны специалистам в данной области. Как правило, строгие условия для гибридизация и детекции будут представлять собой те, в которых концентрация соли составляет менее чем приблизительно 1,5 M ионов Na, как правило, от приблизительно 0,01 до 1,0 M концентрации ионов N (или других солей) при pH от 7,0 до 8,3, и температура составляет по меньшей мере приблизительно 30°C для коротких зондов (например, от 10 до 50 нуклеотидов) и по меньшей мере приблизительно 60°C для длинных зондов (например, больших чем 50 нуклеотидов). “Строгие условия” могут также достигаться добавлением дестабилизирующих средств, таких как формамид. Примеры условий “низкой строгости” включают гибридизацию с буферным раствором, содержащим от 30 до 35% формамида, 1 M NaCl, 1% SDS (додецилсульфат натрия) при 37°C, и промывкой в 1×-2× SSC (20× SSC=3,0 M NaCl/0,3 M трицитрата натрия) при температуре от 50 до 55°C. Примеры условий средней строгости включают гибридизацию в 40%-45% формамиде, 1,0 M NaCl, 1% SDS при 37°C, и промывку в 0,5×-1× SSC при температуре от 55 до 60°C. Примеры условий с высокой строгостью включают гибридизацию в 50% формамиде, 1 M NaCl, 1% SDS при 37°C и промывку в 0,1× SSC при температуре от 60 до 65°C. Необязательно, буферы для промывки могут содержать приблизительно от 0,1% до приблизительно 1% SDS. Продолжительность гибридизации составляет, как правило, менее чем приблизительно 24 часа, как правило, приблизительно от 4 до приблизительно 12 часов. Продолжительность времени промывки будет составлять, по меньшей мере, период времени, достаточный для достижения равновесия.
В реакциях гибридизации, специфичность является, как правило, функцией промывки после гибридизации, критические факторы представляют собой ионную силу и температуру конечного раствора для промывки. Для гибридов ДНК-ДНК, Tm можно вывести из уравнения Meinkoth и Wahl (1984) Anal. Biochem. 138:267-284: Tm=81,5°C + 16,6 (log M) + 0,41(% GC) - 0,61 (% форм.) - 500/л; где M представляет собой молярность одновалентных катионов, % GC представляет собой процент нуклеотидов гуанозина и цитозина в ДНК, % форм. представляет собой процент формамида в растворе для гибридизации, и L представляет собой длину гибрида в парах оснований. Tm представляет собой температуру (при определенной ионной силе и pH), при которой 50% комплементарной целевой последовательности гибридизуется с идеально подобранным зондом. Tm уменьшают приблизительно на 1°C для каждого 1% неправильно спаренных нуклеотидов; таким образом, Tm, гибридизация и/или условия промывки можно отрегулировать для гибридизации с последовательностью желаемой идентичности. Например, если необходимо отыскать последовательности с идентичностью ≥90%, Tm можно снизить на 10°C. Как правило, строгие условия выбираются, чтобы быть приблизительно на 5°C ниже, чем температура точки плавления (Tm) для специфической последовательности и комплементарной ей при определенной ионной силе и pH. Однако при очень строгих условиях гибридизацию и/или промывку можно проводить при 1, 2, 3 или 4°C ниже, чем температура точки плавления (Tm); при умеренно строгих условиях гибридизацию и/или промывку можно проводить при 6, 7, 8, 9 или 10°C ниже, чем температура плавления (Tm); в условиях низкой строгости гибридизацию и/или промывку можно проводить при 11, 12, 13, 14, 15 или 20°C ниже, чем температура точки плавления (Tm). Используя уравнение, гибридизацию и состав промывки и желаемую Tm, специалистам будет понятно, что различия в строгости условий гибридизации и/или растворах для промывки по существу описаны. Если желаемая степень несоответствия приводит к Tm менее чем 45°C (водный раствор) или 32°C (раствор формамида), предпочтительно увеличить концентрацию SSC таким образом, чтобы можно было использовать более высокую температуру. Гибридизацию зонда с целевой молекулой ДНК можно детектировать рядом способов, известных специалистам в данной области, эти способы могут включать, но не ограничиваются ими, флуоресцентные метки, радиоактивные метки, метки на основе антител и хемилюминесцентные метки.
Как указывают, молекула нуклеиновой кислоты является “комплементарной” другой молекуле нуклеиновой кислоты, если они демонстрируют комплементарность. Как применяют в настоящем документе, молекулы, как указывают, демонстрируют “полную комплементарность”, если каждый нуклеотид одной молекулы нуклеиновой кислоты является комплементарным нуклеотиду другой молекулы нуклеиновой кислоты. Как указывают, две молекулы являются “минимально комплементарными”, если молекулы могут гибридизоваться друг с другом с достаточной стабильностью, такой, которая позволяет им оставаться гибридизованными в общепринятых условиях “низкой строгости”. Аналогично, как указывают, молекулы являются "комплементарными”, если молекулы могут гибридизоваться друг с другом с достаточной стабильностью, такой, которая позволяет им оставаться гибридизованными в общепринятых условиях “высокой строгости”.
В других вариантах осуществления растения события 127 можно детектировать или идентифицировать детекцией экспрессированного полипептида AHAS Arabidopsis thanliana. В детекции полипептида AHAS можно использовать любой способ. Например, для детекции наличия экспрессии полипептида AHAS можно использовать антитела, индуцированные против встроенного белка AHAS.
Любой способ можно использовать для детекции молекулы нуклеиновой кислоты события 127 или ее ампликона, включая, в качестве неограничивающих примеров, генетический анализ в битовом представлении. В одном способе, конструируют ДНК олигонуклеотид, который перекрывает как смежную фланкирующую последовательность ДНК, так и встроенную последовательность ДНК. В других вариантах осуществления конструируют олигонуклеотидные ДНК-праймеры для обеспечения получения ампликона, специфичного для события 127. Олигонуклеотид иммобилизуют в лунках планшета для микротитрования. После осуществления ПЦР представляющего интерес участка, одноцепочечный продукт ПЦР можно гибридизовать с иммобилизованным олигонуклеотидом и использовать в качестве матрицы в реакции удлинения одного нуклеотида, с использованием ДНК-полимеразы и меченых ddNTP, специфичных для следующего предполагаемого основания. Представление данных может быть основано на флуоресценции или способе ELISA. Сигнал показывает наличие вставки/фланкирующей последовательности в результате успешной амплификации, гибридизации и реакции удлинения одного нуклеотида.
Другой способ детекции для применения в способах по настоящему изобретению представляет собой способ пиросеквенирования. В этом способе конструируют олигонуклеотид, который перекрывает соединение смежной ДНК и ДНК-вставки или используют пару олигонуклеотидов, которые могут амплифицировать участок, специфичный для события 127. Олигонуклеотид гибридизуют с одноцепочечным ПЦР-продуктом из представляющего интерес участка (один праймер к встроенной последовательности и один к фланкирующей последовательности) и инкубируют в присутствии ДНК-полимеразы, АТФ, сульфурилазы, люциферазы, апиразы, аденозин-5'-фосфосульфата и люциферина. dNTP добавляют индивидуально и включение приводит к образованию светового сигнала, который измеряют. Световой сигнал показывает наличие трансгенной вставки/фланкирующей последовательности вследствие успешной амплификации, гибридизации и реакции удлинения одного или нескольких нуклеотидов.
Для детекции ампликона по изобретению также можно использовать поляризацию флуоресценции. Используя этот способ, конструируют олигонуклеотид, который перекрывает точку соединения фланкирующей и встроенной ДНК, или используют пару олигонуклеотидов, которые позволяют амплифицировать специфичный участок события 127. Олигонуклеотид гибридизуют с ПЦР-продуктом из представляющего интерес участка (один праймер к встроенной ДНК и один к фланкирующей последовательности ДНК) и инкубируют в присутствии ДНК полимеразы и флуоресцентно меченных ddNTP. В результате реакции удлинения одного нуклеотида происходит встраивание ddNTP. Встраивание можно измерять как изменение в поляризации, используя флуориметр. Изменение поляризации показывает наличие трансгенной вставки/фланкирующей последовательности вследствие успешной амплификации, гибридизации и реакции удлинения одного нуклеотида.
Анализ экспрессии генов Taqman® (PE Applied Biosystems, Foster City, Calif.) также можно использовать для детекции и количественного определения наличия молекулы нуклеиновой кислоты события 127. В кратком изложении, конструируют олигонуклеотидный зонд FRET, который перекрывает точку соединения фланкирующей последовательности и ДНК-вставки, или используют пару олигонуклеотидов, которые обеспечивают амплификацию молекулы нуклеиновой кислоты события 127. Зонд FRET и праймеры ПЦР (один праймер во встроенной последовательности ДНК и один во фланкирующей геномной последовательности) участвуют в циклах реакции в присутствии термостабильной полимеразы и dNTP. Гибридизация зонда FRET приводит к расщеплению и высвобождению флуоресцентной группы, располагающейся на расстоянии от группы гашения флуоресценции на зонде FRET. Сигнал флуоресценции показывает наличие фланкирующей/трансгенной встроенной последовательности вследствие успешной амплификации и гибридизации.
В описанных способах можно также использовать способ Molecular Beacons. В кратком изложении, конструируют олигонуклеотидный зонд FRET, который перекрывает соединение фланкирующей ДНК и ДНК-вставки, или используют пару олигонуклеотидов, которые могут обеспечить амплификацию специфичного участка 127. Уникальная структура зонда FRET приводит к тому, что зонд содержит вторичную структуру, которая удерживает флуоресцентную группу и группу гашения флуоресценции в непосредственной близости. Зонд FRET и праймеры ПЦР (один праймер к последовательности ДНК-вставки и один к фланкирующей последовательности) участвуют в циклах реакции в присутствии термостабильной полимеразы и dNTP. Дальнейшая успешная ПЦР-амплификация, гибридизация зонда FRET с целевой последовательностью приводит в результате к разрушению вторичной структуры зонда и пространственному разделению флуоресцентной группы и группы гашения флуоресценции. В результате получают флуоресцентный сигнал. Флуоресцентный сигнал показывает наличие фланкирующей/трансгенной последовательности вставки вследствие успешной амплификации и гибридизации.
Реакция гибридизации с использованием зонда, специфичного к последовательности, расположенной в пределах ампликона, представляет собой еще один способ, используемый для детекции ампликона, получаемого реакцией ПЦР по настоящему изобретению.
В другом варианте осуществления молекулу нуклеиновой кислоты события 127 можно детектировать или идентифицировать способами детекции полипептидов, экспрессируемых молекулами нуклеиновой кислоты события 127. Например, продукт экспрессии гена csr-1AHAS можно детектировать, используя способы, описываемые в настоящем документе. Такие способы могут включать применение связывающих белков, которые являются способными связываться с полипептидами, экспрессируемыми встроенной молекулой нуклеиновой кислоты события 127. Такие способы включают в качестве неограничивающих примеров иммунологические анализы, такие как, ELISA (твердофазный иммуноферментный анализ), анализы на основе антигенов, иммуноокрашивание, иммуногистохимия, анализы на основе белковых чипов, радиоиммунопреципитационные анализы, высокочувствительные мембранные иммунохроматографические анализы и высокочувствительные иммунохроматографические анализы на основе тест-полосок (латеральные проточные тесты).
Способы, описываемые в настоящем документе, можно адаптировать для применения в высокопроизводительных способах, например, посредством присоединения диагностических молекул (таких как праймеры и/или зонды) на субстраты, для создания устройства, например, чипа или микроматриц, или многолуночных планшетов. Устройства можно предоставлять в любом пригодном формате, таком как чипы, предметные стекла, планшеты, мембраны, волокна, гранулы, полоски, тест-полоски, маты, решетки, стержни, сетки, стенки емкостей и т.п. Кроме того, субстраты можно сделать из любого доступного материала, такого как, стекло, керамика, гели (например, гидрогели, микрогели, псевдогели) и полимерные материалы (например, пластик, силикон, фторполимеры). Таким образом, субстраты для применения в устройствах и способах по настоящему изобретению включают, но не ограничиваются ими, чипы на основе диоксида кремния, нейлоновые мембраны, оптические волокна, многолуночные планшеты и т.п. Зонды или другую диагностическую молекулу к событию 127 можно присоединять к субстрату, используя любые доступные способы присоединения, такие как ковалентное связывание, координационное связывание и нековалентное связывание (например, ионное связывание, водородное связывание, липофильное взаимодействие).
Способ на основе биочипов для высокопроизводственной детекции, идентификации или контролирования экспрессии можно использовать для измерения мишеней для гибридизации - молекул нуклеиновой кислоты события 127. Этот способ на основе “чипа” включает использование микроматриц с молекулами нуклеиновой кислоты в качестве геноспецифичных мишеней для гибридизации, для количественного измерения экспрессии соответствующих генов. Единовременно можно устанавливать любой нуклеотид в большой последовательности. Гибридизацию можно использовать для эффективного анализа нуклеотидных последовательностей.
Любой доступный способ на основе микроматриц можно использовать в способах по настоящему изобретению. Например, способом на основе микроматриц можно сравнивать анализируемые последовательности, посредством гибридизации с набором олигонуклеотидов или молекул кДНК, представляющих все возможные последовательности. Во втором способе гибридизуют образец с биочипом олигонуклеотидов или кДНК-зондов. Биочип, состоящий из олигонуклеотидов или молекул кДНК, комплементарных последовательностям целевой последовательности события 127, можно использовать для определения идентичности целевой последовательности, измерения ее количества и определения различий между целевой и контрольной последовательностью. Микроматрицы с молекулами нуклеиновой кислоты можно также подвергать скринингу белковыми молекулами или их фрагментами для определения молекул нуклеиновой кислоты, которые специфично связывают белковые молекулы или их фрагменты. Другие диагностические способы на основе микроматриц для применения в способах по настоящему изобретению включают, например, те, которые описаны в публикации США № 2007/0298423.
Таким образом, молекулы нуклеиновой кислоты события 127 можно идентифицировать или детектировать в образце, используя любой доступный способ. Такие способы включают в качестве неограничивающих примеров способы разделения в геле, детекцию на основе блот-гибридизации нуклеиновых кислот (например, гибридизация по Саузерну, Нозерн-гибридизация), качественную, полуколичественную или количественную ПЦР, иммуноанализы (например, ELISA, анализы на основе тест-полосок (например, на основе тест-полосок для латерального проточного иммуноанализа), с использованием любых иммуноглобулинов, моноклональных антител, одноцепочечных антител или фрагментов антител с сохраненным участком связывания) для детекции экспрессии модифицированного AHASL и детекции на основе анализов микроматрицы или “микрочипа”. В других вариантах осуществления способы могут включать применение способов масс-спектрометрии или ядерного магнитного резонанса (ЯМР) для детекции или идентификации наличия молекул нуклеиновой кислоты события 127 в биологическом образце.
Устройства, пригодные в таких способах детекции, также предоставляют в различных вариантах осуществления изобретения устройства, включающие твердофазную подложку, имеющую поверхность; и присоединенную к ней по меньшей мере одну диагностическую молекулу к событию 127. Это могут быть устройства для гибридизационного анализа, устройства для иммуноанализа, устройства для анализа на основе связывания рецептора и лиганда, или любые другие известные в данной области.
VII. Наборы
Настоящее изобретение также относится к наборам для детекции растения события 127 или молекул нуклеиновой кислоты события 127, где набор включает первый и второй нуклеиновокислотный праймер, который является способным обеспечивать амплификацию молекулы нуклеиновой кислоты события 127. Полученные в результате амплифицированные молекулы нуклеиновой кислоты события 127 можно детектировать напрямую или использовать в качестве зондов для гибридизации в реакциях с биологическими образцами, содержащими ДНК.
Как применяют в настоящем документе, “набор” относится к комплекту реагентов, подобранному с целью осуществления способа вариантов осуществления, более конкретно, для идентификации и/или детекции события 127 в биологических образцах. Набор можно использовать и компоненты набора специфично подбирать в целях контроля качества (например, однородности партий семян), детекции молекул нуклеиновой кислоты события 127 в растительном материале или материале, содержащем материал растения или полученном из материала растения, такого как, но не ограничивающегося ими, пищевые продукты или корма.
В конкретных вариантах осуществления, предоставляют набор для идентификации молекул нуклеиновой кислоты события 127 в биологическом образце. Набор включает первый и второй праймер, где первый и второй праймер способны обеспечивать амплификацию молекулы нуклеиновой кислоты события 127. В дополнительных вариантах осуществления набор также включает молекулу нуклеиновой кислоты для детекции молекулы нуклеиновой кислоты события 127. Набор может включать, например, первый праймер и второй праймер, содержащие молекулу нуклеиновой кислоты с последовательностями SEQ ID NO:35, 36, 37, 38, 39, 40, 41, 42, 43 и 44, где первый или второй праймер разделяет достаточную гомологию последовательности или комплементарность с молекулой нуклеиновой кислоты, для амплификации молекулы нуклеиновой кислоты события 127. Например, в специфических вариантах осуществления, первый праймер или второй праймер включает фрагмент молекулы нуклеиновой кислоты с последовательностью SEQ ID NO:35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 67, 68, 69 и 70, где первый или второй праймер разделяет достаточную гомологию последовательности или комплементарность с молекулой нуклеиновой кислоты, для амплификации молекулы события 127. Пара праймеров может включать фрагмент молекулы нуклеиновой кислоты, обладающей последовательностью SEQ ID NO:5, и фрагмент молекулы нуклеиновой кислоты с последовательностью SEQ ID NO:6, или, альтернативно, пару праймеров можно выбирать из последовательностей i) SEQ ID NO:35 и SEQ ID NO:36, ii) SEQ ID NO:37 и SEQ ID NO:38, iii) SEQ ID NO:39 и SEQ ID NO:40, iv) SEQ ID NO:41 и SEQ ID NO:42, v) SEQ ID NO:43 и SEQ ID NO:44, vi) SEQ ID NO:67 и SEQ ID NO:68, и vii) SEQ ID NO:69 и SEQ ID NO:70. В дополнительных вариантах осуществления первый и второй праймер могут включать только одну последовательность или любую комбинацию последовательностей, представленную в SEQ ID NO:35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 67, 68, 69 и 70. Праймеры могут быть любой длины, достаточной для амплификации молекулы события 127, где длина включает, например, по меньшей мере 6, 7, 8, 9, 10, 15, 20, 15 или 30 или приблизительно 7-10, 10-15, 15-20, 20-25, 25-30, 30-35, 35-40, 40-45 нуклеотидов или более.
Дополнительно представленными являются наборы для детекции ДНК, включающие по меньшей мере одну молекулу нуклеиновой кислоты, которая может специфично детектировать участок события 127, где молекула нуклеиновой кислоты включает по меньшей мере одну молекулу ДНК достаточной длины из смежных нуклеотидов, которая гомологична или комплементарна SEQ ID NO:5 и/или 6. В некоторых вариантах осуществления набор для детекции ДНК включает молекулу нуклеиновой кислоты с SEQ ID NO:5 и/или 6 или включает последовательность, которая гибридизуется с последовательностями, которые специфично детектируют участок события 127, такие как те, которые выбраны из группы, состоящей из SEQ ID NO:5 и/или 6.
VIII. Способы борьбы с сорняками
Настоящее изобретение также относится к способам и композициям для борьбы с сорняками или нежелательными растениями. Способы, как правило, включают применение эффективного количества одного или нескольких неселективных гербицидов на посевной площади или занятом культурой поле, содержащим одно или несколько растений сои события 127. Хотя с любыми сорными растениями можно бороться описанными способами, в некоторых вариантах осуществления способы могут включать первоначальную идентификацию сорняков или нежелательных растений на площади или поле, чувствительных к ингибирующему AHAS гербициду.
Предоставлены способы для борьбы с сорняками на посевной площади, предотвращающие развитие или появление сорняков или нежелательных растений на посевной площади, где способы обеспечивают сельскохозяйственную культуру и повышенную сохранность сельскохозяйственной культуры. Термин “контролирование” и его производные, как, например, “борьба с сорняками”, относятся к одному или нескольким ингибирующим рост, прорастание, размножение и/или распространение сорняков; и/или к уничтожению, удалению, поражению, или иначе, уменьшению распространенности и/или активности сорняка и/или нежелательного растения.
Способы по изобретению могут контролировать сорняки или нежелательные растения на посевной площади на любое измеряемое количество, такое как уменьшение количества сорняков или нежелательных растений на посевной площади по меньшей мере на приблизительно 5%, 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90%, 95% по сравнению с площадью, которую не обрабатывали тем же количеством и видом гербицида. Контролирование сорняков или нежелательных растений можно измерять любыми воспроизводимыми способами измерения. В одном из вариантов осуществления контролирование сорняков или нежелательных растений измеряют, подсчитывая количество сорных или нежелательных растений, произрастающих на площади, обработанной гербицидом, и сравнивают с количеством сорных или нежелательных растений, произрастающих на необработанной гербицидом площади такого же размера.
Настоящее изобретение также относится к способам борьбы с сорняками или нежелательными растениями посредством подсчета семян растения сои события 127 до посева и/или после предварительного проращивания в присутствии ингибирующего AHAS гербицида. Способ может дополнительно включать посев семян, например, в подходящую среду для выращивания, такую как почву поля или в среду для горшечных растений в теплице. Способы находят конкретное применение в борьбе с сорняками и/или нежелательными растениями в непосредственной близости от семян.
Под сорными растениями подразумеваются, в самом широком смысле, все те растения, которые растут в местах, где их произрастание нежелательно.
Сорные растения, которые можно контролировать способами по настоящему изобретению включают, например, двудольные и однодольные сорные растения. Двудольные сорные растения, которые можно контролировать, используя описанные способы, включают, но не ограничиваются ими, сорняки вида: Sinapis, Lepidium, Galium, Stellaria, Matricaria, Anthemis, Galinsoga, Chenopodium, Urtica, Senecio, Amaranthus, Portulaca, Xanthium, Convolvulus, Ipomoea, Poligonum, Sesbania, Ambrosia, Cirsium, Carduus, Sonchus, Solanum, Rorippa, Rotala, Lindernia, Lamium, Veronica, Abutilon, Emex, Datura, Viola, Galeopsis, Papaver, Centaurea, Trifolium, Ranunculus и Taraxacum. Однодольные сорные растения, которые можно контролировать, используя описанные способы, включают, но не ограничиваются ими, сорняки вида: Echinochloa, Setaria, Panicum, Digitaria, Phleum, Poa, Festuca, Eleusine, Brachiaria, Lolium, Bromus, Avena, Cyperus, Sorghum, Agropyron, Cynodon, Monochoria, Fimbristyslis, Sagittaria, Eleocharis, Scirpus, Paspalum, Ischaemum, Sphenoclea, Dactyloctenium, Agrostis, Alopecurus и Apera. Конкретные сорные растения, которые можно контролировать способами по настоящему изобретению, включают, но не ограничиваются ими, сорняки важных сельскохозяйственных культур, такие как Ipomoea spp., Commelina spp., Tridax procumbens, Euphorbia spp., Sida spp., Bidens spp., Galinsoga spp., Solanum spp., Xanthium spp., Chenopodium spp., Spermacoce latifolia, Richardia brasiliensis, Sonchus oleraceous, Conyza spp., Amaranthus spp., Acanthospermum spp., Hyptis spp. Portulaca oleracea, Casia obtusifolia, и также включает контроль видов осоковых Cyperus spp., а также видов трав, включающих Brachiaria spp., Digitaria spp., Panicum spp., Setaria spp., Sorghum halepense, Echnochloa spp., Eleusine indica и Pennisetum spp. С применением неселективных гербицидов на основе имидазолинона, описанные способы являются выгодными для контроля сорных растений, трудно поддающихся контролированию, таких как Commelina spp., Conyza spp., Chamaesise hirta, Spermacoce latifolia, Richardia brasiliensis, Ipomoea spp., Euphorbia heterophylla, Echnochloa spp. и Casia obtusifolia.
Кроме того, сорные растения, с которыми можно бороться способами по настоящему изобретению, включают, например, нежелательные сельскохозяйственные культуры, которые растут в непредназначенных для них местах. Например, растение-самосев кукурузы, присутствующее на поле, которое преимущественно содержит растения сои события 127, может считаться сорным растением, если произрастание растения кукурузы нежелательно на поле с растениями сои.
Нежелательные растения, с которыми можно бороться способами по настоящему изобретению, включают те растения, которыми ранее засевали конкретное поле в предыдущем сезоне или высеивали на прилегающей площади, и включают сельскохозяйственные культуры, включающие сою, кукурузу, канолу, хлопок, подсолнечник и т.п. В некоторых аспектах, сельскохозяйственные культуры могут являться устойчивыми к гербицидам, таким как гербициды глифосат или глуфосинат, или могут быть устойчивыми к ингибирующим AHAS гербицидам.
Как применяют в настоящем документе, “площадь для посевов” или “посевная площадь” включают любую область, на которой желают вырастить одно или несколько растений, таких как растение сои события 127. Такие площади для посевов включают в качестве неограничивающих примеров поле, на котором культивируют растение сои события 127 (такие как поле, занятое культурой, поле для испытаний, и т.д.), теплицу, вегетационную камеру и т.д.
Способы включают засеивание посевной площади семенами сои события 127 или растениями сои, и в некоторых вариантах осуществления применение на сельскохозяйственных культурах, семени, сорном растении, нежелательном растении, почве или их посевной площади эффективного количества представляющего интерес гербицида. Гербицид можно применять в любой период культивирования растений сои с 127. Гербицид можно применять до или после того, как сельскохозяйственная культура посеяна на культивируемой площади. Такие способы применения гербицидов могут включать применение ингибирующего AHAS гербицида или их комбинации.
Термин “эффективное количество” обозначает количество гербицида, достаточного для контроля, с любой поддающейся измерению величиной, сорных или нежелательных растений на посевной площади. Эффективное количество ингибирующего AHAS гербицида может быть представлено в диапазоне приблизительно от 50 г д.в./га до приблизительно 500 г д.в./га, приблизительно от 50 г д.в./га и приблизительно 400 г д.в./га или приблизительно от 50 г д.в./га до приблизительно 300 г д.в./га. Эффективное количество ингибирующего AHAS гербицида может также составлять приблизительно 70 г д.в./га, 140 г д.в./га или 280 г д.в./га. На эффективные уровни применения ингибирующего AHAS гербицида в способах по настоящему изобретению может влиять много факторов, включая окружающую среду, и эффективные уровни необходимо определять в реальных условиях применения. Контроль над сорными или нежелательными растениями можно осуществлять посредством одного или нескольких применений ингибирующего AHAS гербицида на уровне, сходном или большем, чем используемое количество для такого контроля на площадях, на которых не произрастает соя с событием 127. Такие уровни применений включают те, которые составляют или эквивалентны 70 г д.в./га, 140 или 280 г д.в./га. Типичные коммерческие уровни применения ингибирующего AHAS гербицида составляют приблизительно 70 г д.в./га, также обозначаемого как IX уровень применения.
В некоторых вариантах осуществления эффективное количество может представлять собой количество ингибирующего AHAS гербицида, большее, чем количество, к которому сорные или нежелательные растения, подлежащие контролированию, являются устойчивыми. Например, в вариантах осуществления, в которых сорные или нежелательные растения являются устойчивыми к применению 70 г д.в./га, но являются чувствительными к применению 140 г д.в./га, эффективное количество гербицида составляет 140 г д.в./га.
Таким образом, настоящее изобретение относится к способам борьбы с ростом сорняков или нежелательных растений на посевной площади, включающим применение эффективного количества неселективного гербицида на посевной площади с одним или несколькими растениями сои события 127.
Также представленными являются способы контролирования устойчивых к глифосату сорняков или растений на посевной площади, где способы включают применение эффективного количества ингибирующего AHAS гербицида на посевной площади с одним или несколькими растениями сои события 127.
Также предоставленным является способ контролирования на посевной площади устойчивых к ингибирующему AHAS гербициду сорняков или растений, где способ включает применение эффективного количества ингибирующего AHAS гербицида на посевной площади с одним или несколькими растениями сои события 127. В таких вариантах осуществления эффективное количество ингибирующего AHAS гербицида применяют в количестве, достаточном для контроля сорняков, так как гербицид по существу не оказывает эффекта на растение сои события 127.
В некоторых вариантах осуществления сорные растения можно контролировать до посадки на поле семян сои события 127. Например, эффективное количество неселективных гербицидов, таких как ингибирующие AHAS гербициды, можно применять на поле до посадки, для уменьшения или удаления сорных растений на поле перед посевом семян. До посадки такое применение можно осуществлять в любой момент времени, эффективный для борьбы с сорными растениями, например, на 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14 или более суток до посадки. Кроме того, в таких способах можно применять любую комбинацию сельскохозяйственных композиций.
В других вариантах осуществления сорные растения можно контролировать после посадки семян сои события 127. Например, в количестве, эффективном для контролирования сорных растений, ингибирующие AHAS гербициды можно применять к растущим растениям сои, частям растений, среде для выращивания (такой как почва), окружающей растущее растение и соседнее с ним, или к площади, т.е. локальному окружению, на котором произрастает растение сои события 127 или растения. Растущее растение сои события 127 может быть на любой стадии развития. В некоторых таких вариантах осуществления, в момент применения гербицида растущая соя, по меньшей мере, представляет собой растение на стадии первого настоящего листа. Кроме того, любую комбинацию сельскохозяйственных композиций можно применять в таких способах.
Если в способах используют комбинации сельскохозяйственных композиций, то такие комбинации могут включать комбинации гербицидов, фунгицидов, бактерицидных средств, инсектицидов и т.п. Например, ингибирующий AHAS гербицид можно комбинировать с другими гербицидами, такими как гербициды, ингибирующие 5-енолпирувилшикимат-3-фосфатсинтазу (EPSPS), гербициды, ингибирующие глутаминсинтазу (GS), гербициды, ингибирующие протопорфириноген[IX]оксидазу (PPO), гербициды с ауксиновой активностью или их комбинации.
IX. Способы повышения урожайности
Также предоставленными являются способы повышения урожая растения или растений сои, где способы включают применение эффективного количества ингибирующего AHAS гербицида на посевной площади с одним или несколькими растениями сои события 127 и сбор семян растений сои. В некоторых вариантах осуществления повышение урожая растения или растений сои является результатом уменьшения количества сорных растений, произрастающих на локальной площади с растением или растениями сои, которые, как правило, конкурируют с растением или растениями сои.
Используя такие способы, урожай сои на поле можно увеличить, по сравнению с аналогичной площадью, не имеющей растений сои события 127. Урожай соевых растений можно увеличивать на любое количество, включая, в качестве неограничивающих примеров, на 5%, 6%, 7%, 8%, 9%, 10%, 11%, 12%, 13%, 14%, 15%, 20%, 25% или более, по сравнению с урожаем, полученным с аналогичной площади, не имеющей растений сои события 127, на которой применяют ингибирующий AHAS гербицид.
X. Химические композиции для сельского хозяйства
Настоящее изобретение также относится к сельскохозяйственным композициям для применения к описанным растениям сои события 127. Такие композиции могут включать гербициды, фунгицидные средства, бактерицидные средства, удобрения, и т.п. В одном из вариантов осуществления сельскохозяйственные композиции представляют собой гербицидные композиции, содержащие один или несколько гербицидов или комбинации одного или нескольких гербицидов с другой сельскохозяйственной композицией, такой как фунгицид, бактерициды, удобрение и т.п.
Любой гербицид можно применять к сельскохозяйственной культуре сои события 127, части сельскохозяйственной культуры или посевной площади, содержащей растение сои события 127. Классификация гербицидов (т.е. группирование гербицидов на классы и подклассы) является хорошо известной в данной области и включает классификации HRAC (Herbicide Resistance Action Committee) и WSSA (the Weed Science Society of America). Классификация HRAC является всемирно доступной, например, сокращенная версия классификации HRAC (с примечаниями относительно соответствующей группы WSSA) представлена на веб-сайте hracglobal.com/Publications/Classificationof HerbicideModeofAction/tabid/222/Default.aspx.
В некоторых вариантах осуществления настоящее изобретение относится к способам, которые включают использование по меньшей мере одного ингибирующего AHAS гербицида, выбранного из группы, состоящей из гербицидов на основе имидазолинона, гербицидов на основе сульфонилкарбамида, гербицидов на основе триазолопиримидина, гербицидов на основе пиримидинилоксибензоата, гербициды на основе сульфониламинокарбонилтриазолинона и их смеси. В этих способах, ингибирующий AHAS гербицид можно применять любым известным в данной области способом, включая, в качестве неограничивающих примеров, обработку семян, почвы и некорневую обработку.
В некоторых вариантах осуществления ингибирующий AHAS гербицид можно комбинировать с одной или несколькими дополнительными сельскохозяйственными композициями, такими как дополнительные гербициды, фунгициды, бактерициды, противовирусные композиции или их комбинации. Дополнительные гербициды для использования в комбинации включают любой гербицид, включая сульфамидные гербициды, органофосфатные гербициды и гербициды на основе бензотиадиазинона. Сульфамидные гербициды включают в качестве неограничивающих примеров сафлуфенацил. Органофосфатные гербициды включают в качестве неограничивающих примеров глифосат и глуфосинат. Гербициды на основе бензотиадиазинона включают в качестве неограничивающих примеров бентазон. Фунгициды для применения в таких комбинациях включают в качестве неограничивающих примеров пираклостробин.
Обработка комбинациями композиций ингибирующего AHAS гербицида и/или одной или несколькими композициями ингибирующего AHAS гербицида и одной или несколькими дополнительными сельскохозяйственными композициями можно осуществлять посредством применения смеси таких композиций, одновременного применения таких композиций, последовательного применения таких композиций или любой их комбинации.
В некоторых вариантах осуществления композиции ингибирующего AHAS гербицида включают по меньшей мере один A) ингибирующий AHAS гербицид и по меньшей мере одно дополнительное активное соединение, выбранное из B) гербицидов классов от b1) до b15):
b1) ингибиторы биосинтеза липидов;
b2) ингибиторы ацетолактатсинтазы (AHAS ингибиторы);
b3) ингибиторы фотосинтеза;
b4) ингибиторы протопорфириноген-IX оксидазы;
b5) отбеливающие гербициды;
b6) ингибиторы енолпирувилшикимат-3-фосфатсинтазы (EPSP ингибиторы);
b7) ингибиторы глутаминсинтазы;
b8) ингибиторы 7,8-дигидроптероатсинтазы (DHP ингибиторы);
b9) ингибиторы митоза;
b10) ингибиторы синтеза длинноцепочечных жирных кислот (ингибиторы VLCFA);
b11) ингибиторы биосинтеза целлюлозы;
b12) разобщающие гербициды;
b13) ауксиновые гербициды;
b14) ингибиторы транспорта ауксина;
b15) другие гербициды, выбранные из группы, состоящей из бензоилпропа, флампропа, флампроп-М, бромобутида, хлорфлуренола, цинметилина, метилдимурона, этобензанида, фосамина, метама, пирибутикарба, оксазикломефона, дазомета, триазифлама и метилбромида, и
сельскохозяйственно-приемлемые соли активного соединения B и сельскохозяйственно-приемлемые производные активных соединений B при условии, что они имеют карбоксильную группу.
В других случаях, такую комбинацию по меньшей мере одного A) ингибирующего AHAS гербицида и по меньшей мере одного гербицида B можно использовать в комбинации с средством защиты C (такие средства защиты также можно использовать в комбинации с по меньшей мере одним ингибирующим AHAS гербицидом). Средства защиты C можно выбрать из: беноксакора, клоквинтоцета, циометринила, дихлормида, дициклонона, диэтолата, фенхлоразола, фенклорима, флуразола, флуксофенима, фурилазола, изоксадифена, мефенпира, мефената, нафталевого ангидрида, 2,2,5-триметил-1-3-(дихлорацетил)-1,3-оксазолидина (R29148), 4-(дихлорацетил)-1-окса-4-азаспиро[4.5]декана (AD-67, MON 4640) и оксабетринила, сельскохозяйственно-приемлемых солей активных соединений C и сельскохозяйственно-приемлемых производных активных соединений C, при условии, что они имеют карбоксильную группу.
Примеры гербицидов B, которые можно использовать в комбинации с ингибирующими AHAS соединениями, представляют собой:
b1) из группы ингибиторов биосинтеза липидов: хлоразифоп, клодинафоп, клофоп, цигалофоп, диклофоп, феноксапроп, феноксапроп-П, фентиапроп, флуазифоп, флуазифоп-П, галоксифоп, галоксифоп-П, изоксапирифоп, метамифоп, пропаквизафоп, хизалофоп, хизалофоп-П, трифоп, аллоксидим, бутроксидим, клетодим, клопроксидим, циклоксидим, профоксидим, сетоксидим, тепралоксидим, тралкоксидим, бутилат, циклоат, диаллат, димепиперат, ЕРТС, эспрокарб, этиолат, изополинат, метиобенкарб, молинат, орбенкарб, пебулат, просульфокарб, сульфалат, тиобенкарб, тиокарбазил, триаллат, вернолат, бенфуресат, этофумесат и бенсулид:
b2) из группы ингибиторов AHAS: амидосульфурон, азимсульфурон, бенсульфурон, хлоримурон, хлорсульфурон, циносульфурон, циклосульфамурон, этаметсульфурон, этоксисульфурон, флазасульфурон, флупирсульфурон, форамсульфурон, галосульфурон, имазосульфурон, йодосульфурон, мезосульфурон, метсульфурон, никосульфурон, оксасульфурон, примисульфурон, просульфурон, пиразосульфурон, римсульфурон, сульфометурон, сульфосульфурон, тифенсульфурон, триасульфурон, трибенурон, трифлоксисульфурон, трифлусульфурон, тритосульфурон, имазаметабенз, имазамокс, имазапик, имазапир, имазаквин, имазетапир, клорансулам, диклосулам, флорасулам, флуметсулам, метосулам, пеноксулам, биспирибак, пириминобак, пропоксикарбазон, флукарбазон, пирибензоксим, пирифталид и пиритиобак;
b3) из группы ингибиторов фотосинтеза: атратон, атразин, аметрин, азипротрин, цианазин, цианатрин, хлоразин, ципразин, десметрин, диметаметрин, дипропетрин, эглиназин, ипазин, мезопразин, метометон, метопротрин, проциазин, проглиназин, прометон, прометрин, пропазин, себутилазин, секбуметон, симазин, симетон, симетрин, тербуметон, тербутилазин, тербутрин, триэтазин, аметридион, амибузин, гексазинон, изометиозин, метамитрон, метрибузин, бромацил, изоцил, ленацил, тербацил, бромпиразон, хлоридазон, димидазон, десмедифам, фенисофам, фенмедифам, фенмедифамэтил, бензтиазурон, бутиурон, этидимурон, изоурон, метабензтиазурон, моноизоурон, тебутиурон, тиазафлурон, анизурон, бутурон, хлорбромурон, хлоретурон, хлоротолурон, хлороксурон, дифеноксурон, димефурон, диурон, фенурон, флуометурон, флуотиурон, изопротурон, линурон, метиурон, метобензурон, метобромурон, метоксурон, монолинурон, монурон, небурон, парафлурон, фенобензурон, сидурон, тетрафлурон, тидиазурон, циперкват, диэтамкват, дифензокват, дикват, морфамкват, паракват, бромобонил, бромоксинил, хлороксинил, йодобонил, иоксинил, амикарбазон, бромофеноксим, флумезин, метазол, бентазон, пропанил, пентанохлор, пиридат и пиридафол;
b4) из группы ингибиторов протопорфириноген IX оксидазы: ацифлуорфен, бифенокс, хлометоксифен, хлорнитрофен, этоксифен, флуородифен, флуорогликофен, флуоронитрофен, фомесафен, фурилоксифен, галосафен, лактофен, нитрофен, нитрофторфен, оксифлуорфен, флуазолат, пирафлуфен, цинидон-этил, флумиклорак, флумиоксазин, флумипропин, флутиацет, тидиазимин, оксадиазон, оксадиаргил, азафенидин, карфентразон, сульфентразон, пентоксазон, бензфендизон, бутафенацил, пираклонил, профлуазол, флуфенпир, флупропацил, нипираклофен и этнипромид;
b5) из группы отбеливающих гербицидов: метфлуразон, норфлуразон, флуфеникан, дифлуфеникан, пиколинафен, бефлубутамид, флуридон, флурохлоридон, флуртамон, мезотрион, сулкотрион, изоксахлортол, изоксафлутол, бензофенап, пиразолинат, пиразоксифен, бензобициклон, амитрол, кломазон, аклонифен, 4-(3-трифторметилфенокси)-2-(4-трифторметилфенил)пиримидин и также 3-гетероциклил-замещенные производные бензоила формулы I:
в которой показатели от R8 до R13 такие, как определено ниже: R8, R10 представляют собой водород, галоген, C1-C6-алкил, C1-C6-галогеналкил, C1-C6-алкокси, C1-C6-галоалкокси, C1-C6-алкилтио, C1-C6-алкилсульфинил или C1-C6-алкилсульфонил; R9 представляет собой гетероциклический радикал, выбранный из группы, состоящей из: тиазол-2-ила, тиазол-4-ила, тиазол-5-ила, изоксазол-3-ила, изоксазол-4-ила, 10 изоксазол-5-ила, 4,5-дигидроизоксазол-3-ила, 4,5-дигидроизоксазол-4-ила и 4,5-дигидроизоксазол-5-ила, где девять упомянутых радикалов могут являться незамещенными или моно- или полизамещенными, например, моно-, ди-, три- или тетразамещенными, посредством галогена, С1-C4-алкила, C1-C4-алкокси, C1-C4-галогеналкила, C1-C4-галоалкокси или C1-C4-алкилтио; R11 представляет собой водород, галоген или C1-C6-алкил; R12 представляет собой C1-C6-алкил; R13 представляет собой водород или C1-C6-алкил.
b6) из группы ингибиторов EPSP синтазы: глифосат;
b7) из группы ингибиторов глутаминсинтазы: глуфозинат и биланафос;
b8) из группы ингибиторов DHP синтазы: асулам;
b9) из группы ингибиторов митоза: бенфлуралин, бутралин, динитрамин, эталфлуралин, флухлоралин, изопропалин, металпропалин, нитралин, оризалин, пендиметалин, продиамин, профлуралин, трифлуралин, амипрофосметил, бутамифос, дитиопир, триазопир, пропизамид, тебутам, хлортал, карбетамид, хлорбуфам, хлорпрофам и профам;
b10) из группы ингибиторов VLCFA: из группы ингибиторов VLCFA: ацетохлор, алахлор, бутахлор, бутенахлор, делахлор, диэтатил, диметахлор, диметенамид, диметенамид-П, метазахлор, метолахлор, С-метолахлор, претилахлор, пропахлор, пропизохлор, принахлор, тербухлор, тенилхлор, ксилахлор, аллидохлор, CDEA, эпроназ, дифенамид, напропамид, напроанилид, петоксамид, флуфенацет, мефенацет, фентразамид, анилофос, пиперофос, кафенстрол, инданофан и тридифан;
b11) из группы ингибиторов биосинтеза целлюлозы: дихлобенил, хлортиамид, изоксабен и флупоксам;
b12) из группы разобщающих гербицидов: динофенат, динопроп, диносам, диносеб, динотерб, DNOC, этинофен и мединотерб;
b13) из группы ауксиновых гербицидов: кломепроп, 2,4-D, 2,4,5-Т, МСРА, МСРА тиоэтил, дихлорпроп, дихлорпроп-П, мекопроп, мекопроп-П, 2,4-DB, MCPB, хлорамбен, дикамба, 2,3,6-ТВА, трикамба, квинклорак, квинмерак, клопиралид, флуроксипир, пиклорам, триклопир и беназолин;
b14) из группы ингибиторов транспорта ауксинов; напталам, дифлуфензопир;
b15) бензоилпроп, флампроп, флампроп-М, бромобутид, хлорфлуренол, цинметилин, метилдимрон, этобензанид, фосамин, метам, пирибутикарб, оксазикломефон, дазомет, триазифлам и метилбромид.
Активные соединения B групп b1)-b15) и активные соединения C являются известными гербицидами и средствами защиты, см., например, The Compendium of Pesticide Common Names (доступен повсеместно в сети интернет на сайте hclrss.demon.co.uk/index.html); Farm Chemicals Handbook 2000 Vol.86, Meister Publishing Company, 2000; B. Hock, C. Fedtke, R. R. Schmidt, Herbizide, Georg Thieme Verlag, Stuttgart 1995; W. H. Ahrens, Herbicide Handbook, 7th Edition, Weed Science Society of America, 1994; и K. K. Hatzios, Herbicide Handbook, Supplement to 7th Edition, Weed Science Society of America, 1998. 2,2,5-триметил-3-(дихлорацетил)-1,3-оксазолидин [CAS № 52836-31-4] также известен под названием R-29148. 4-(Дихлорацетил)-1-окса-4-азаспиро[4,5]декан [CAS № 71526-07-03] также известен под названием AD-67 и MON 4660. Отбеливающие гербициды формулы II раскрыты в WO 96/26202, WO 97/41116, WO 97/41117 и WO 97/41118.
В качестве активного соединения C, композиции могут включать по меньшей мере одно из соединений, перечисленных ниже: беноксакор, клоквинтоцет, дихлормид, фенхлоразол, фенклорим, флуксофеним, фурилазол, изоксадифен, мефенпир, 2,2,5-триметил-3-(дихлорацетил)-1,3-оксазолидин, 4-(дихлорацетил)-1-окса-4-азаспиро[4.5]декан и оксабетринил и/или их сельскохозяйственно-приемлемая соль и/или, в случае соединений, имеющих группу COOH, сельскохозяйственно-приемлемое производное.
Композиции, которые содержат комбинации активных ингредиентов, могут являться бинарными и тернарными композициями, которые включают по меньшей мере одно ингибирующее AHAS соединение в качестве активного соединения-A и по меньшей мере один гербицид, выбранный из классов b1)-b15), и, если необходимо, один или несколько сохраняющих средств C.
В бинарных композициях, которые включают по меньшей мере одно ингибирующее AHAS соединение в качестве компонента A и по меньшей мере один гербицид B, массовые отношения активных соединений A:B могут располагаться в диапазоне от 1:500 до 10:1, в диапазоне от 1:100 до 10:1, в диапазоне от 1:50 до 10:1, или в диапазоне от 1:25 до 5:1.
В бинарных композициях, которые содержат по меньшей мере одно ингибирующее AHAS соединение и по меньшей мере одно сохраняющее средство C, массовые отношения активных соединений A:C представлены, как правило, в диапазоне от 1:100 до 10:1, от 1:50 до 10:1 или в диапазоне от 1:25 до 5:1.
В тернарных композициях, которые включают ингибирующее AHAS соединение в качестве компонента A, по меньшей мере один гербицид B и по меньшей мере одно сохраняющее средство C, относительные массовые отношения компонентов A:B:C могут быть представлены в диапазоне от 10:1:1 до 1:500:10, от 10:1:1 до 1:100:10, от 10:1:1 до 1:50:1 или от 5:1:1 до 1:25:5.
В одном из вариантов осуществления в тернарных композициях массовое отношение гербицида B к сохраняющему средству C представлено в диапазоне от 50:1 до 1:10.
Смеси с гербицидной активностью, описанные в патенте США № 7375058 (включена в настоящий документ в качестве ссылки в полном объеме), также можно использовать при обработке растений сои события 127.
Гербициды, ингибирующие протопорфириноген[IX]оксидазу (PPO), также нашли применение в композициях по настоящему изобретению. Ингибирующие PPO гербициды известны в данной области и включают в качестве неограничивающих примеров гербициды на основе дифенилового эфира (включающие гербициды на основе нитрофенилового эфира), такие как ацифлуорфен (5-[2-хлор-4-(трифторметил)фенокси]-2-нитробензойная кислота), бифенокс (метил-5-(2,4-дихлорфенокси)-2-нитробензоат), DPEI (5-[2-хлор-4-(трифторметил)фенокси]-2-нитроацетофенон, оксим-o-(метиловый эфир уксусной кислоты)), DPEII (5-[2-хлор-4-(трифторметил)фенокси]-3-метоксифталид), этоксифен ((1S)-1-карбоксиэтил-2-хлор-5-[2-хлор-4-(трифторметил)фенокси]бензоат), фомесафен (5-[2-хлор-4-(трифторметил)фенокси]-N-(метилсульфонил)-2-нитробензамид), лактофен (этил-О-[5-(2-хлор-α,α,α-трифтор-п-толилокси)-2-нитробензоил]-DL-лактат), и оксифлуорфен (2-хлор-1-(3-этокси-4-нитрофенокси)-4-(трифторметил)бензол). Ингибирующие PPO гербициды также включают дикарбоксимидные гербициды, такие как N-фенил-фталимиды флумиклорак ([2-хлор-5-(циклогекс-1-ен-1,2-дикарбоксимидо)-4- фторфенокси]уксусная кислота), флумиоксазин (N-(7-фтор-3,4-дигидро-3-оксо-4-проп-2-инил-2H-1,4-бензоксазин-6-ил)циклогекс-1-ен-1,2-дикарбоксамид). Ингибирующие PPO гербициды дополнительно включают гербициды на основе триазолинона, такие как карфентразон (α,2-дихлор-5-[4-(дифторметил)-4,5-дигидро-3-метил-5-оксо-1H-1,2,4-триазол-1-ил]-4-фторбензолпропановая кислота) и сулфентразон (N-[2,4-дихлор-5-[4-(дифторметил)-4,5-дигидро-3-метил-5-оксо-1H-1,2,4-триазол-1-ил]фенил]метансульфонамид). Ингибирующие PPO гербициды также включают гербициды на основе фенилпиразола, включая, в качестве неограничивающих примеров, нипираклофен (1-[2,6-дихлор-4-(трифторметил)фенил]-4-нитро-1H-пиразол-5-амин) и пирафлуфен (2-хлор-5-(4-хлор-5-дифторметокси-1-метилпиразол-3-ил)-4-фторфеноксиуксусная кислота). Ингибирующие PPO гербициды также включают гербициды на основе оксадиазолона, такие как оксадиазон (3-[2,4-дихлор-5-(1-метилэтокси)фенил]-5-(1,1-диметилэтил)-1,3,4-оксадиазол-2(3H)-он) и оксадиаргил (5-трет-бутил-3-[2,4-дихлор-5-(проп-2-инилокси)фенил]-1,3,4-оксадиазол-2(3Н)-он). Ингибирующие PPO гербициды дополнительно включают гербициды на основе тиадиазолона, такие как флутиацет ([[2-хлор-4-фтор-5-[(тетрагидро-3-оксо-1H,3H-[1,3,4]тиадиазоло[3,4-α]пиридазин-1-илиден)амино]фенил]тио]уксусная кислота); а также те, которые описаны в разделе III. 4) в US 2008254985 Zagar и Sievernich (включенной в настоящий документ в качестве ссылки в полном объеме).
Ауксиновые гербициды также находят применение в композициях по настоящему изобретению. Ауксиновые гербициды включают те, которые включают гербицидные активные ингредиенты, которые по своему механизму действия имитируют ауксин или являются его ингибиторами (антиауксины). Примеры ауксиновых гербицидов включают в качестве неограничивающих примеров пиклорам (4-амино-3,5,6-трихлорпиколиновая кислота); дикамба (3,6-дихлор-2-метоксибензойная кислота); клофибриновая кислота ((п-хлорфенокси)изомасляная кислота); 2-(4-хлорфенокси)-2-метилпропановая кислота); беназолин (4-хлор-2-оксо-3-бензотиазолуксусная кислота; 4-хлор-2-оксобензотиазолин-3-ил-уксусная кислота); TIBA (2,3,5-трийодбензойная кислота); 2,3,6-TBA (2,3,6-трихлорбензойная кислота); триклопир (3,5,6-трихлор-2-пиридилоксиуксусная кислота); квинклорак (3,7-дихлорхинолин-8-карбоновая кислота); и имитирующие и блокирующие ауксин фенокси-гербициды, например, гербициды на основе феноксиуксусной кислоты, феноксипропионовой кислоты и феноксимасляной кислоты, включающие: 2,4-D((2,4-дихлорфенокси)уксусную кислоту), MCPA ((4-хлор-2-метилфенокси)уксусную кислоту), 2,4-DB (4-(2,4-дихлорфенокси)масляная кислота), 2,4-DEP (трис[2-(2,4-дихлорфенокси)этил]фосфат), 4-CPA (4-хлорфеноксиуксусную кислоту), 2,4,5-T ((2,4,5-трихлорфенокси)уксусную кислоту), дихлорпроп (2-(2,4-дихлорфенокси)пропановую кислоту), фенопроп (2-(2,4,5-трихлорфенокси)пропионовую кислоту) и мекопроп (2-(2-метил-4-хлорфенокси)пропановую кислоту).
Примеры комбинаций сельскохозяйственных композиций по настоящему изобретению включают: имазапир и имазапик; имазапир и бентазон; имазапир, имазапик и бентазон; имазапир и пираклостробин; имазапир, имазапик и пираклостробин; имазапир и сафлуфенацил; имазапир, имазапик и сафлуфенацил; имазапик, сафлуфенацил и глифосат; имазапир, имазапик, сафлуфенацил и глифосат; имазапик и глифосат; имазапир и глифосат; имазапир, сафлуфенацил и глифосат; и сафлуфенацил и глифосат.
Перед применением гербицид, такой как ингибирующий AHAS гербицид, можно преобразовать в привычные составы, например растворы, эмульсии, суспензии, пудру, порошки, пасты и гранулы. Форма применения зависит от конкретной намеченной цели; в любом случае она должна обеспечить хорошее и равномерное распределение соединения по изобретению.
Составы для применения в способах по настоящему изобретению можно получать любым известным способом, например, предоставляя активное соединение вместе с вспомогательными средствами, подходящими для агрохимических составов, такими как растворители и/или носители, при желании эмульгаторы, поверхностно-активные средства и дисперсанты, консерванты, противовспениватели, понижающие температуру замерзания средства, для составов для обработки семян также необязательно вместе с красителями, и/или связывающими средствами, и/или гелеобразующими средствами.
Примеры подходящих растворителей для применения в составах включают воду, ароматические растворители (например, продукты Solvesso, ксилол), парафины (например, фракции минерального масла), спирты (например, метанол, бутанол, пентанол, бензиловый спирт), кетоны (например, циклогексанон, гамма-бутиролактон), пирролидоны (NMP, NOP), ацетаты (диацетат гликоля), гликоли, диметиламиды жирных кислот, жирные кислоты и сложные эфиры жирных кислот. Также можно использовать смеси растворителей.
Примеры подходящих носителей для применения в составах по настоящему изобретению включают измельченные природные минералы (например, каолины, глина, тальк, мел) и измельченные синтетические минералы (например, высоко размельченные диоксид кремния, силикаты).
Подходящие эмульгаторы для применения в составах по настоящему изобретению включают неионные и анионные эмульгаторы (например, полиоксиэтиленовые эфиры жирных спиртов, алкилсульфонаты и арилсульфонаты).
Примеры дисперсантов для применения в составах по настоящему изобретению включают отработанный лигнинсульфитный щелок и метилцеллюлозу.
Подходящие поверхностно-активные вещества для применения в составах по настоящему изобретению включают щелочной металл, щелочноземельный металл и аммониевые соли лигносульфоновой кислоты, нафталинсульфоновой кислоты, фенолсульфоновой кислоты, дибутилнафталинсульфоновой кислоты, алкиларилсульфонаты, алкилсульфаты, алкилсульфонаты, сульфаты жирного спирта, гликолевые эфиры жирных кислот и сульфатированных жирных спиртов, кроме того конденсаты сульфированного нафталина и его производных с формальдегидом, конденсаты нафталина или нафталинсульфоновой кислоты с фенолом и формальдегидом, полиоксиэтиленовый эфир октилфенола, этоксилированный изооктилфенол, октилфенол, нонилфенол, алкилфенолполигликолевые эфиры, трибутилфенилполигликолевый эфир, тристеарилфенилполигликолевый эфир, алкиларилполиэфирные спирты и конденсаты жирного спирта и этиленоксида, этоксилированное касторовое масло, простые полиоксиэтиленалкиловые эфиры, этоксилированный полиоксипропилен, ацетат полигликолевого эфира лаурилового спирта, сложные сорбитовые эфиры, отработанный лигнинсульфитный щелок и метилцеллюлозу.
Средства, которые являются подходящими для получения непосредственно поддающихся разбрызгиванию растворов, эмульсий, паст или дисперсий в масле, представляют собой среднекипящие-высококипящие фракции нефтепродуктов, таких как керосин или дизельное масло, кроме того каменноугольный деготь и масла растительного или животного происхождения, алифатические, циклические и ароматические углеводороды, например, толуол, ксилол, парафин, тетрагидронафталин, алкилированные нафталины или их производные, метанол, этанол, пропанол, бутанол, циклогексанол, циклогексанон, изофорон, высокополярные растворители, например, диметилсульфоксид, N-метилпирролидон или вода.
Также к составу можно добавлять средства понижающие температуру замерзания, такие как глицерин, этиленгликоль, пропиленгликоль и бактерицидные средства.
Подходящие противовспениватели для применения в составах по настоящему изобретению включают, например, противовспениватели на основе силикона или стеарата магния.
Подходящие консерванты для применения в составах по настоящему изобретению включают, например, дихлорфенол и бензиловый спирт и геми-формальдегид.
По настоящему изобретению составы для протравливания семян могут дополнительно включать связывающие средства и необязательно красители.
Связывающие средства можно добавлять к описанным составам для семян для увеличения адгезии активных материалов на семенах после обработки. Подходящие связывающие средства представляют собой поверхностно-активные вещества блок-сополимеры EO/PO, а также поливиниловый спирт, поливинилпирролидоны, полиакрилаты, полиметакрилаты, полибутены, полиизобутилены, полистирол, полиэтиленамины, полиэтиленамиды, полиэтиленимины (Lupasol®, Polymin®), простые полиэфиры, полиуретаны, поливинилацетат, тилозу и сополимеры, полученные из этих полимеров.
Необязательно, в состав также можно включать красители. Подходящие красители или окрашивающие средства в составах для протравливания семян представляют собой родамин B, C.I. пигмент красный 112, C.I. растворимый красный 1, пигмент голубой 15:4, пигмент голубой 15:3, пигмент голубой 15:2, пигмент голубой 15:1, пигмент синий 80, пигмент желтый 1, пигмент желтый 13, пигмент красный 112, пигмент красный 48:2, пигмент красный 48:1, пигмент красный 57:1, пигмент красный 53:1, пигмент оранжевый 43, пигмент оранжевый 34, пигмент оранжевый 5, пигмент зеленый 36, пигмент зеленый 7, пигмент белый 6, пигмент коричневый 25, основной фиолетовый 10, основной фиолетовый 49, кислотный красный 51, кислотный красный 52, кислотный красный 14, кислотный синий 9, кислотный желтый 23, основной красный 10, основной красный 108.
Пример подходящего гелеобразующего средства представляет собой карраген (Satiagel®).
Порошки, препараты для опыливания и опудривания можно получать смешиванием или совместным измельчением активных средств с твердым носителем.
Гранулы, например, гранулы в оболочке, гранулы с пропиткой и гомогенные гранулы, можно получать посредством связывания активных соединений с твердыми носителями. Примеры твердых носителей представляют собой минералы почвы, такие как силикагели, силикаты, тальк, каолин, аттагель, известняк, известь, мел, железисто-известковую глину, лесс, глину, доломит, диатомовую землю, сульфат кальция, сульфат магния, оксид магния, измельченные синтетические минералы, удобрения, такие как, например, аммоний сульфат, аммоний фосфат, аммоний нитрат, мочевина и продукты растительного происхождения, такие как мука зерновых, мука из древесной коры, древесная мука и мука из ореховой скорлупы, целлюлозные порошки и другие твердые носители.
В основном составы включают от 0,01 до 95% по массе, предпочтительно от 0,1 до 90% по массе, гербицида, например, ингибирующего AHAS гербицида. Гербициды можно использовать с чистотой от 90% до 100% по массе, предпочтительно от 95% до 100% по массе (в соответствии со спектром ЯМР). В целях протравливания семян, соответствующие составы можно разводить в 2-10 раз, что приводит к концентрациям в готовых для применения препаратах от 0,01 до 60% по массе активного соединения, предпочтительно от 0,1 до 40% по массе.
Ингибирующий AHAS гербицид по настоящему изобретению можно использовать, по существу, в форме, в которой он находится в составах, или используя формы, полученные из него, например, в форме непосредственно разбрызгиваемых растворов, порошков, суспензий или дисперсий, эмульсий, масляных дисперсий, паст, продуктов для опыливания, материалов для распыления или гранул, посредством разбрызгивания, распыления, присыпания, разбрасывания или полива. Формы применения полностью зависят от заданных целей; они предназначены для обеспечения, в каждом случае, самого лучшего распределения ингибирующего AHAS гербицида по изобретению.
Водные формы применения можно получать из эмульсионных концентратов, паст или смачиваемых порошков (порошки для разбрызгивания, масляные дисперсии) при добавлении воды. Для получения эмульсий, паст или масляных дисперсий, вещества, могут быть сами по себе или растворенные в масле или растворителе, гомогенизированы в воде с помощью смачивающего средства, средства для повышения клейкости, дисперсанта или эмульгатора. Однако также возможно получать концентраты, состоящие из активного вещества, смачивающего средства, средства для повышения клейкости, дисперсанта или эмульгатора и, при необходимости, растворителя или масла, и такие концентраты являются подходящими для разведения водой.
Концентрации активного соединения в готовых к применению препаратах могут варьировать в широких пределах. В основном они составляют 0,0001 до 10%, предпочтительно от 0,01 до 1% по массе.
Ингибирующий AHAS гербицид по настоящему изобретению также можно успешно использовать способом “очень малого количества” (ULV), что делает возможным применение составов, содержащих выше 95% по массе активного соединения, или даже применять активное соединение без добавок.
Далее представлены примеры составов с ингибирующим AHAS гербицидом для использования в способах по настоящему изобретению:
1. Препараты для разведения водой для внекорневых обработок. С целью протравливания семян такие препараты можно применять разведенными или неразведенными.
A) Водорастворимые концентраты (SL, LS)
Десять массовых частей ингибирующего AHAS гербицида растворяют в 90 массовых частях воды или водорастворимого растворителя. Альтернативно добавляют смачивающие средства или другие вспомогательные средства. Ингибирующий AHAS гербицид растворяется при разведении водой, таким образом получают состав с 10% (масс./масс.) ингибирующего AHAS гербицида.
B) Диспергируемые концентраты (DC)
Двадцать массовых частей ингибирующего AHAS гербицида растворяют в 70 массовых частях циклогексанона с добавлением 10 массовых частей дисперсанта, например, поливинилпирролидона. Разведение водой приводит к образованию дисперсии, таким образом получают состав с 20% (масс./масс.) ингибирующего AHAS гербицида.
C) Эмульгируемые концентраты (EC)
Пятнадцать массовых частей ингибирующего AHAS гербицида растворяют в 7 массовых частях ксилола с добавлением додецилбензолсульфоната кальция и этоксилированного касторового масла (в каждом случае 5 массовых частей). Разведение водой дает эмульсию, таким образом получают состав с 15% (масс./масс.) ингибирующего AHAS гербицида.
D) Эмульсии (EW, EO, ES)
Двадцать пять массовых частей ингибирующего AHAS гербицида растворяют в 35 массовых частях ксилола с добавлением додецилбензолсульфоната кальция и этоксилированного касторового масла (в каждом случае 5 массовых частей). Эту смесь вводят в 30 массовых частей воды посредством прибора для эмульгирования (например, Ultraturrax) и переводят в гомогенную эмульсию. Разведение водой приводит к образованию эмульсии, таким образом получают состав с 25% (масс./масс.) ингибирующего AHAS гербицида.
E) Суспензии (SC, OD, FS)
В грануляторе с перемешиванием 20 массовых частей ингибирующего AHAS гербицида измельчают с добавлением 10 массовых частей дисперсантов, смачивающих средств и 70 массовых частей воды или органического растворителя для получения тонкодисперсной суспензии ингибирующего AHAS гербицида. Разведение водой приводит к образованию стабильной суспензии ингибирующего AHAS гербицида, таким образом получают состав с 20% (масс./масс.) ингибирующего AHAS гербицида.
F) Диспергируемые в воде гранулы и водорастворимые гранулы (WG, SG)
Пятьдесят массовых частей ингибирующего AHAS гербицида тонко измельчают с добавлением 50 массовых частей дисперсантов и смачивающих средств и получают в виде диспергируемых в воде или водорастворимых гранул посредством технических приспособлений (например, экструдирование, сушка распылением, псевдоожиженный слой). Разведение водой приводит к образованию стабильной дисперсии или раствора ингибирующего AHAS гербицида, таким образом получают состав с 50% (масс./масс.) ингибирующего AHAS гербицида.
G) Диспергируемые в воде и водорастворимые порошки (WP, SP, SS, WS)
Семьдесят пять массовых частей ингибирующего AHAS гербицида измельчают в мельнице с системой ротор/статор с добавлением 25 массовых частей дисперсантов, смачивающих средств и силикагеля. Разведение водой приводит к образованию стабильной дисперсии или раствора ингибирующего AHAS гербицида, таким образом получают состав с 75% (масс./масс.) ингибирующего AHAS гербицида.
H) Состав на основе геля (GF)
В грануляторе с перемешиванием, 20 массовых частей ингибирующего AHAS гербицида измельчают с добавлением 10 массовых частей дисперсантов, 1 массовой части гелеобразующих смачивающих средств и 70 массовых частей воды или органического растворителя для получения тонкодисперсной суспензии ингибирующего AHAS гербицида. Разведение водой приводит к образованию стабильной суспензии ингибирующего AHAS гербицида, таким образом получают состав с 20% (масс./масс.) ингибирующего AHAS гербицида. Такой гелевый состав является подходящим для применения при протравливании семян.
2. Препараты для внекорневой обработки, применяемые в неразведенном виде. В целях протравливания семян такие препараты можно применять разведенными.
A) Порошки для опыливания (DP, DS)
Пять массовых частей ингибирующего AHAS гербицида тонко измельчают и смешивают непосредственно с 95 массовыми частями тонкоизмельченного каолина. В результате получают препарат для опыливания с 5% (масс./масс.) ингибирующего AHAS гербицида.
B) Гранулы (GR, FG, GG, MG)
Половину массовой части ингибирующего AHAS гербицида тонко измельчают и связывают с 95,5 массовыми частями носителей, таким образом получают состав с 0,5% (масс./масс.) ингибирующего AHAS гербицида. Существующие способы представляют собой экструдирование, сушку распылением или псевдоожиженный слой. В результате получают гранулы, которые применяют для внекорневого использования неразведенными.
Общепринятые составы для протравливания семян включают, например, сыпучие концентраты FS, растворы LS, порошки для сухого протравливания DS, диспергируемые в воде порошки для протравливания взвесью WS, водорастворимые порошки SS и эмульсии ES и EC и состав на основе геля GF. Эти составы можно применять для обработки семян как разведенными, так и неразведенными. Обработку семян осуществляют непосредственно перед посевом или обрабатывают семена.
В одном из вариантов осуществления состав FS используют для протравливания семян. Как правило, состав FS может содержать 1-800 г/л активного ингредиента, 1-200 г/л поверхностно-активного вещества, от 0 до 200 г/л понижающего температуру замерзания средства, от 0 до 400 г/л связывающего средства, от 0 до 200 г/л пигмента и вплоть до 1 литра растворителя, предпочтительно воду.
Для протравливания семян, семена растения сои события 127 по настоящему изобретению обрабатывают гербицидами, такими как гербициды, выбранные из группы, состоящей из ингибирующих AHAS гербицидов, таких как амидосульфурон, азимсульфурон, бенсульфурон, хлоримурон, хлорсульфурон, циносульфурон, циклосульфамурон, этаметсульфурон, этоксисульфурон, флазасульфурон, флупирсульфурон, форамсульфурон, галосульфурон, имазосульфурон, йодосульфурон, мезосульфурон, метсульфурон, никосульфурон, оксасульфурон, примисульфурон, просульфурон, пиразосульфурон, римсульфурон, сульфометурон, сульфосульфурон, тифенсульфурон, триасульфурон, трибенурон, трифлоксисульфурон, трифлусульфурон, тритосульфурон, имазаметабенз, имазамокс, имазапик, имазапир, имазаквин, имазетапир, клорансулам, диклосулам, флорасулам, флуметсулам, метосулам, пеноксулам, биспирибак, пириминобак, пропоксикарбазон, флукарбазон, пирибензоксим, пирифталид, пиритиобак и их смеси, или в составе, содержащем ингибирующий AHAS гербицид.
Термин «протравливание семян» включает все подходящие способы протравливания семян, известные в данной области, такие как дезинфекция семян, удобрение семян, опудривание семян, замачивание семян и дражирование семян.
В соответствии с одним вариантом по настоящему изобретению, дополнительной задачей по изобретению является способ обработки почвы посредством применения в сеялке, в частности, одного из двух: гранулированного состава, содержащего ингибирующий AHAS гербицид в качестве композиции/состава (например, гранулированный состав, необязательно с одним или несколькими твердыми или жидкими сельскохозяйственно-приемлемыми носителями и/или необязательно с одним или несколькими сельскохозяйственно-приемлемыми поверхностно-активными веществами. Такой способ преимущественно применяют, например, на грядках с зерновыми культурами, кукурузой, хлопком и подсолнечником.
Настоящее изобретение также включает семена, покрытые составом для протравливания семян или содержащие состав для протравливания семян, включающий по меньшей мере один ингибирующий AHAS гербицид, выбранный из группы, состоящей из амидосульфурона, азимсульфурона, бенсульфурона, хлоримурона, хлорсульфурона, циносульфурона, циклосульфамурона, этаметсульфурона, этоксисульфурона, флазасульфурона, флупирсульфурона, форамсульфурона, галосульфурона, имазосульфурона, йодосульфурона, мезосульфурона, метсульфурона, никосульфурона, оксасульфурона, примисульфурона, просульфурона, пиразосульфурона, римсульфурона, сульфометурона, сульфосульфурона, тифенсульфурона, триасульфурона, трибенурона, трифлоксисульфурона, трифлусульфурона, тритосульфурона, имазаметабенза, имазамокса, имазапика, имазапира, имазаквина, имазетапира, клорансулама, диклосулама, флорасулама, флуметсулама, метосулама, пеноксулама, биспирибака, пириминобака, пропоксикарбазона, флукарбазона, пирибензоксима, пирифталида и пиритиобака.
Термин “семя” включает семена и все части растения, отвечающие за размножение, включая, в качестве неограничивающих примеров, истинные семена, часть семенного клубня, корневые ростки, клубнелуковицу, луковицы, плод, клубни, черенки, побеги и т.п. В предпочтительном варианте осуществления используют истинное семя. “Истинное семя” относится к созревшей семяпочке растения, содержащей зародыш, и заключенной внутри оболочки семени или семенной оболочки, а также заключенные в перикарпе или скорлупе, например, в виде зерновки или семянки в семяподобных репродуктивных структурах.
Термин “покрытый и/или содержащие”, обозначает, как правило, что активный ингредиент, в момент применения, представлен преимущественно на поверхности продукта распространения, хотя большая или меньшая часть ингредиента может проникать внутрь продукта распространения, в зависимости от способа применения. Если указанный продукт распространения посажен (пересажен), он может поглощать активный ингредиент.
Протравливание семян с применением ингибирующего AHAS гербицида или с составом, содержащим ингибирующий AHAS гербицид, осуществляют разбрызгиванием или опыливанием семян до посева растений и до прорастания растений.
При протравливании семян применяют соответствующие составы, протравливая семена эффективным количеством ингибирующего AHAS гербицида или составом, содержащим ингибирующий AHAS гербицид. В настоящем документе, дозы внесения составляют, как правило, от 0,1 г до 10 кг д.в. (или в смеси д.в. или в составе) на 100 кг семян, предпочтительно от 1 г до 5 кг на 100 кг семян, в частности от 1 г до 2,5 кг на 100 кг семян. Для конкретных сельскохозяйственных культур, таких как салат, доза внесения может быть выше.
Любой гербицидный состав, применяемый к растению сои события 127, можно получать в виде композиции “баковая смесь”. В таких вариантах осуществления каждый ингредиент или комбинацию ингредиентов можно хранить отдельно друг от друга. Затем, перед применением, ингредиенты можно смешать друг с другом. Как правило, такое смешивание осуществляют незадолго до применения. В способе баковой смеси каждый ингредиент перед смешиванием, как правило, находится в воде или подходящем органическом растворителе. Способы и руководства для получения таких составов известны в данной области.
Способы дополнительно предусматривают разработку гербицидной комбинации, которую используют с растениями сои события 127. В таких способах оценивают условия окружающей среды на посевной площади. Условия окружающей среды, которые можно оценивать, включают в качестве примеров, но не ограничиваются ими, проблемы, связанные с загрязнением почвы и вод наземных водоемов, предполагаемое применение сельскохозяйственной культуры, устойчивость сельскохозяйственной культуры, природный грунт, наличие сорняков на посевной площади, состав почвы, pH почвы, количество органических веществ в почве, применяемое оборудование и приемы механической обработки почвы. На сельскохозяйственной культуре, части сельскохозяйственной культуры, семенах сельскохозяйственной культуры или посевной площади эффективное количество комбинации гербицидов можно применять, исходя из оценки условий окружающей среды.
В некоторых вариантах осуществления гербицид, применяемый на растении сои события 127, предназначен для предупреждения начала роста чувствительных к гербициду сорных или нежелательных растений и/или способен вызвать повреждение сорных или нежелательных растений, которые произрастают на представляющей интерес площади. В некоторых вариантах осуществления гербицид или гербицидная смесь, которые проявляют подобное действие на сорных или нежелательных растениях, затрагивают сельскохозяйственные культуры, которые впоследствии растут на представляющей интерес площади (т.е. на поле или посевной площади). В способах гербицидную комбинацию не нужно применять в одно и то же время. При условии, что поле, на котором растет сельскохозяйственная культура, содержит детектируемые количества первого гербицида, и второй гербицид применяют в определенное время в период, в течение которого сельскохозяйственная культура произрастает на посевной площади, считают, что сельскохозяйственную культуру обработали смесью гербицидов по изобретению. Таким образом, предоставленные способы включают применение гербицидов, которые являются “предвсходовыми”, “послевсходовыми”, “для предпосадочного внесения” и/или которые вовлекают в протравливание семян до посадки.
Кроме того, представлены способы дражирования семян растений сои события 127. Способы включают покрытие семени эффективным количеством гербицида или комбинацией гербицидов (как описывается в другом месте настоящего документа). Семена затем можно выращивать на посевной площади. Дополнительно представленными являются семена растений события 127, имеющие оболочку, содержащую эффективное количество гербицида или комбинации гербицидов (как раскрыто в другом месте настоящего документа).
“Предвсходовый” относится к гербициду, который применяют на представляющей интерес площади (например, на поле или посевной площади) до видимого появления растения из почвы и/или до прорастания семян. “Послевсходовый” относится к гербициду, который применяют на площади после видимого появления растения из почвы. В некоторых случаях термины “предвсходовый” и “послевсходовый” используют в отношении присутствующих на представляющей интерес площади сорных или нежелательных растений, а в некоторых случаях эти термины используют в отношении растущей на представляющей интерес площади сельскохозяйственной культуры. При использовании в отношении сорных или нежелательных растений, эти термины можно применять только к конкретному представителю сорного растения или видам сорных или нежелательных растений, которые произрастают, или предполагается, что они произрастают на представляющей интерес площади. Тогда как какой-либо гербицид можно применять в предвсходовой и/или послевсходовой обработке, известно, что некоторые гербициды, будучи примененными или в предвсходовой обработке или послевсходовой обработке, являются более эффективными в борьбе с сорным или сорными растениями или нежелательными растениями. Например, римсульфурон обладает как предвсходовой, так и послевсходовой активностью, тогда как другие гербициды обладают преимущественно предвсходовой (метолахлор) или послевсходовой (глифосат) активностью. Эти свойства конкретных гербицидов известны в данной области и легко определяются специалистом в данной области. Дополнительно, специалист в данной области легко сможет выбрать подходящие гербициды и период их применения для использования на трансгенных растениях по изобретению и/или на площадях, на которых предназначено расти трансгенным растениям по изобретению. “Предвсходовое внесение” включает внесение соединений в почву до посадки.
Таким образом, предоставлены усовершенствованные способы выращивания сельскохозяйственной культуры и/или борьбы с сорняками или нежелательными растениями, такие как, например, “допосевное уничтожение”, когда посевную площадь до посева представляющей интерес сельскохозяйственной культуры обрабатывают одним или несколькими гербицидами, для лучшей борьбы с сорняками или нежелательными растениями. Дополнительно представленными являются способы возделывания сельскохозяйственной культуры и/или борьбы с сорняками или нежелательными растениями, где способы представляют собой “беспахотный” способ или способ “неглубокой вспашки” (также обозначаемый как “минимальное вспахивание”). В таких способах почву не обрабатывают или обрабатывают реже в течение цикла произрастания растений, по сравнению с традиционными способами; эти способы помогают снизить затраты, которые были бы иначе понесены вследствие дополнительной обработки почвы, включая трудовые ресурсы и затраты на топливо.
Способы включают использование способов одновременного и/или последовательного применения множества классов гербицидов. В некоторых вариантах осуществления способы включают обработку растения по изобретению и/или представляющей интерес площади (например, поля или посевной площади), и/или сорного растения, и/или нежелательного растения только одним гербицидом или другим химическим средством, таким как, например, гербицид имидазолинон.
Период, в котором применяют гербицид на представляющей интерес площади (и какому-либо растению на площади), может являться важным в оптимизации борьбы с сорными или нежелательными растениями. Период применения гербицида на представляющей интерес площади можно определить на основании размера растений и/или стадии роста, и/или развития растений, например, сельскохозяйственных культур или сорных растений, или нежелательных растений, произрастающих на площади. Стадии роста и/или развития растений известны в данной области. Например, растения сои, как правило, проходят через стадии вегетативного развития, известные как VE (прорастание), Vc (однолепестная), V1 (образование первого тройчатого листа), и от V2 до VN. Затем, в ответ на длину светового дня, соя переходит в фазу репродуктивного роста; репродуктивные стадии включают R1 (начало цветения), R2 (полное цветение), R3 (начало образования стручков), R4 (интенсивное образование стручков), R5 (начало образование семян), R6 (интенсивное семяобразование), R7 (начало созревания) и R8 (полная зрелость). Таким образом, например, период, в котором применяют гербицид или другое химическое средство на представляющей интерес площади, на которой произрастают растения, может представлять собой период, в течение которого на конкретной площади одно или все растения достигли, по меньшей мере, конкретного размера и/или стадии роста и/или развития, или период, в течение которого одно или все растения на конкретной площади еще не достигли конкретного размера или стадии роста и/или развития.
В некоторых вариантах осуществления растения сои события 127 демонстрируют повышенную устойчивость к послевсходовой обработке гербицидами. Например, растения события 127 могут являться устойчивыми к повышенным дозам гербицида, устойчивыми к широкому спектру гербицидов (т.е. устойчивость к большим химическим составам, содержащим ингибитор AHAS), и/или может являться устойчивым к дозам гербицида, примененного, по сравнению с соответствующим контрольным растением, в более ранний или более поздний период развития.
Различные химические средства, такие как гербициды, проявляют различные “остаточные действия”, т.е. демонстрируют различные периоды времени, в течение которых обработка химическим средством или гербицидом продолжает оказывать действие на растения, произрастающие на возделываемой площади. Такие действия могут являться желательными или нежелательными, в зависимости от будущей цели, которую желают достигнуть на возделываемой площади (например, поле или посевной площади). Таким образом, режим севооборота можно выбрать, основываясь на остаточных действиях обработки, которую будут использовать для каждой сельскохозяйственной культуры, и остаточном действии на сельскохозяйственную культуру, которую затем будут выращивать на той же самой площади. Специалист в данной области хорошо знает способы, которые можно использовать для оценки остаточного действия гербицида; например, гербициды, которые ингибируют AHAS, отличаются по уровням остаточной активности. Остаточная активность различных гербицидов в данной области известна, и также известно, что она изменяется в зависимости от различных факторов окружающей среды, таких как, например, уровни влажности почвы, температуры, pH и состава почвы (структура и органический материал). Растения сои события 127 находят конкретное применение в способах выращивания сельскохозяйственной культуры, где существенным является повышенная устойчивость к остаточной активности гербицида.
Кроме того, растения сои события 127 по настоящему изобретению обеспечивают повышенную устойчивость к обработке дополнительными химическими средствами, используемыми по отношению к сельскохозяйственным культурам, в комбинации с обработкой гербицидами, такими химическими средствами, как сохраняющие средства, адъюванты, такие как аммоний сульфонат и концентрат масла сельскохозяйственной культуры и т.п.
Кроме того, раскрытые способы могут включать применение ингибирующего AHAS гербицида или смеси гербицидов, а также один или несколько других инсектицидов, фунгицидов, нематоцидов, бактерицидных средств, акарицидов, регуляторов роста, химических стерилизаторов, химических сигнальных веществ, репеллентов, аттрактантов, феромонов, стимулирующих питательных веществ или других биологически активных соединений или энтомопатогенных бактерий, вирусов или грибов для создания многокомпонентной смеси, предоставляющей более широкий спектр для применения защитных средств в сельском хозяйстве. Примеры таких сельскохозяйственных защитных средств, которые можно использовать в способах включают: инсектициды, так как абамектин, ацефат, ацетамиприд, амидофлумет (S-1955), авермектин, азадирактин, азинфос-метил, бифентрин, бифеназат, бупрофезин, карбофуран, картап, хлорфенапир, хлорфлуазурон, хлорпирифос, хлорпирифос-метил, хромафенозид, клотианидин цифлуметофен, цифлутрин, бета-цифлутрин, цигалотрин, лямбда-цигалотрин, циперметрин, циромазин, дельтаметрин, диафентиурон, диазинон, диэльдрин, дифлубензурон, димефлутрин, диметоат, динотефуран, диофенолан, эмамектин, эндосульфан, эсфенвалерат, этипрол, фенотиокарб, феноксикарб, фенпропатрин, фенвалерат, фипронил, флоникамид, флубендиамид, флуцитринат, тау-флувалинат, флуфенерим (UR-50701), флуфеноксурон, фонофос, галофенозид, гексафлумурон, гидраметилнон, имидаклоприд, индоксакарб, изофенфос, луфенурон, малатион, метафлумизон, метальдегид, метамидофос, метидатион, метомил, метопрен, метоксихлор, метофлутрин, монокротофос, метоксифенозид, нитенпирам, нитиазин, новалурон, новифлумурон (XDE-007), оксамил, паратион, паратион-метил, перметрин, форат, фосалон, фосмет, фосфамидон, пиримикарб, профенофос, профлутрин, пиметрозин, пирафлупрол, пиретрин, пиридалил, пирипрол, пирипроксифен, ротенон, рианодин, спиносад, спиродиклофен, спиромезифен (BSN 2060), спиротетрамат, сулпрофос, тебуфенозид, тефлубензурон, тефлутрин, тербуфос, тетрахлорвинфос, тиаклоприд, тиаметоксам, тиодикарб, тиосултап-натрия, тралометрин, триазамат, трихлорфон и трифлумурон; фунгициды, такие как ацибензолар, алдиморф, амисульбром, азаконазол, азоксистробин, беналаксил, беномил, бентиаваликарб, бентиаваликарб-изопропил, биномиал, бифенил, битертанол, бластицидин-S, бордосская жидкость (трехосновный сульфат меди), боскалид/никобифен, бромуконазол, бупиримат, бутиобат, карбоксин, капропамид, каптафол, каптан, карбендазим, хлорнеб, хлорталонил, хлозолинат, клотримазол, оксихлорид меди, соли меди, такие как сульфат меди и гидроксид меди, циазофамид, цифлюнамид, цимоксанил, ципроконазол, ципродинил, дихлофлюанид, дикломет, дикломезин, диклоран, диетофенкарб, дифеноконазол, диметоморф, димоксистробин, диниконазол, диниконазол-М, динокап, дискостробин, дитианон, додеморф, додин, эконазол, этаконазол, эдифенпос, эпоксиконазол, этабоксам, этиримол, этридиазол, фамоксадон, фенамидон, фенаримол, фенбуконазол, фенкарамид, фенфурам, фенгексамид, феноксанил, фенпиклонил, фенпропидин, фенпропиморф, ацетат фентина, гидроксид фентина, фербам, ферфуразоат, феримзон, флуазинам, флудиоксинил, флуметовер, флуопиколид, флуоксастробин, флуквинконазол, флузилазол, флусульфамид, флутоланил, флутриафол, фолпет, фозетил-алюминий, фуберидазол, фуралаксил, фураметапир, гексаконазол, химексазол, гуазатин, имазалил, имибенконазол, иминоктадин, иодикарб, ипконазол, ипробенфос, ипродион, ипроваликарб, изоконазол, изопротиолан, казугамицин, крезоксим-метил, манкозеб, мандипропамид, манеб, мапанипирин, мефеноксам, мепронил, металаксил, метконазол, метасульфокарб, метирам, метоминустробин/феноминостробин, мепанипирим, метрафенон, миконазол, миклобутанил, нео-асозин (метанарсонат железа), нуаримол, октилинон, офурак, оризастробин, оксадиксил, оксолиновая кислота, окспоконазол, оксикарбоксин, паклобутразол, пенконазол, пенцикурон, пентиопирад, перфуразоат, фосфоновая кислота, фталид, пикобензамид, пикоксистробин, полиоксин, пробеназол, прохлораз, процимидон, пропамокарб, пропамокарб-гидрохлорид, пропиконазол, пропинеб, проквиназид, протиоконазол, пираклостробин, приазофос, пирифенокс, пириметанил, пирифенокс, пирролнитрин, пироквилон, квинконазол, квиноксифен, квинтозен, силтиофам, симеконазол, спироксамин, стрептомицин, сера, тебуконазол, техразен, теклофталам, текназен, тетраконазол, тиабендазол, тифлузамид, тиофанат, тиофанат-метил, тирам, тиадинил, толклофос-метил, толифлуанид, триадимефон, триадименол, триаримол, триазоксид, тридеморф, триморфамид трициклазол, трифлоксистробин, трифорин, тритиконазол, униконазол, валидамицин, винклозолин, зинеб, зирам и зохамид; нематоциды, такие как алдикарб, оксамил и фенамифос; бактерицидные средства, такие как стрептомицин; акарициды, такие как амитраз, хинометионат, хлорбензилат, цигексатин, дикофол, диенохлор, этоксазол, феназаквин, фенбутатина оксид, фенпропатрин, фенпироксимат, гекситиазокс, пропаргит, пиридабен и тебуфенпирад; и биологические средства, включающие энтомопатогенные бактерии, такие как Bacillus thuringiensis subsp. Aizawai, Bacillus thuringiensis subsp. Kurstaki и инкапсулированные дельта-эндотоксины Bacillus thuringiensis (например, Cellcap, MPV, MPVII); энтомопатогенные грибы, такие как гриб возбудитель заболевания “зеленая мускардина”; и энтомопатогенный вирус, включающий бакуловирус, нуклеополигедровирус (NPV), такой как HzNPV, AfNPV; и вирус гранулеза (GV), такой как CpGV. Массовые отношения таких различных компонентов, смешиваемых в других композициях (например, гербицидах), используемых в способах, как правило, представлены между 100:1 и 1:100 или между 30:1 и 1:30, между 10:1 и 1:10 или между 4:1 и 1:4.
Дополнительно представленными являются композиции, содержащие биологически эффективное количество представляющего интерес ингибирующего AHAS гербицида или смеси гербицидов и эффективное количество по меньшей мере одного дополнительного биологически активного соединения или средства, и могут дополнительно содержать по меньшей мере одно поверхностно-активное вещество, твердый разбавитель или жидкий разбавитель. Примеры таких биологически активных соединений или средств представляют собой: инсектициды, такие как абамектин, ацефат, ацетамиприд, амидофлумет (S-1955), авермектин, азадирактин, азинфос-метил, бифентрин, бифеназат, бупрофезин, карбофуран, хлорфенапир, хлорфлуазурон, хлорпирифос, хлорпирифос-метил, хромафенозид, клотианидин, цифлутрин, бета-цифлутрин, цигалотрин, лямбда-цигалотрин, циперметрин, циромазин, дельтаметрин, диафентиурон, диазинон, дифлубензурон, диметоат, диофенолан, эмамектин, эндосульфан, эсфенвалерат, этипрол, фенотиокарб, феноксикарб, фенпропатрин, фенвалерат, фипронил, флоникамид, флуцитринат, тау-флувалинат, флуфенерим (UR-50701), флуфеноксурон, фонофос, галофенозид, гексафлумурон, имидоклоприд, индоксакарб, изофенфос, луфенурон, малатион, метальдегид, метамидофос, метидатион, метомил, метопрен, метоксихлор, монокротофос, метоксифенозид, нитиазин, новалурон, новифлумурон (XDE-007), оксамил, паратион, паратион-метил, перметрин, форат, фосалон, фосмет, фосфамидон, пиримикарб, профенофос, пиметрозин, пиридалил, пирипроксифен, ротенон, спиносад, спиромезифен (BSN 2060), сулпрофос, тебуфенозид, тефлубензурон, тефлутрин, тербуфос, тетрахлорвинфос, тиаклоприд, тиаметоксам, тиодикарб, тиосултап-натрия, тралометрин, трихлорфон и трифлумурон; фунгициды, такие как ацибензолар, азоксистробин, беномил, бластицидин-С, бордосская жидкость (трехосновный сульфат меди), бромуконазол, карпропамид, каптафол, каптан, карбендазим, хлорнеб, хлорталонил, оксихлорид меди, соли меди, цифлуфенамид, цимоксанил, ципроконазол, ципродинил, (S)-3,5-дихлор-N-(3-хлор-1-этил-1-метил-2-оксопропил)-4-метилбензамид (RH 7281), диклоцимет (S-2900), дикломезин, дихлоран, дифеноконазол, (S)-3,5-дигидро-5-метил-2-(метилтио)-5-фенил-3-(фениламино)-4H-имидазол-4-он (RP 407213), диметоморф, димоксистробин, диниконазол, диниконазол-М, додин, эдифенфос, эпоксиконазол, фамоксадон, фенамидон, фенаримол, фенбуконазол, фенкарамид (SZX0722), фенпиклонил, фенпропидин, фенпропиморф, ацетат фентина, гидроксид фентина, флуазинам, флудиоксонил, флуметовер (RPA 403397), флуморф/флуморлин (SYP-L190), флуоксастробин (HEC 5725), флуквинконазол, флузилазол, флутоланил, флутриафол, фолпет, фозетил-алюминий, фуралаксил, фураметапир (S-82658), гексаконазол, ипконазол, ипробенфос, ипродион, изопротиолан, казугамицин, крезоксим-метил, манкозеб, манеб, мефеноксам, мепронил, металаксил, метконазол, метоминостробин/феноминостробин (SSF-126), метрафенон (AC375839), миклобутанил, нео-асозин (метанарсонат железа), никобифен (BAS 510), орисастробин, оксадиксил, пенконазол, пенцикурон, пробеназол, прохлораз, пропамокарб, пропиконазол, проквиназид (DPX-KQ926), протиоконазол (JAU 6476), пирифенокс, пираклостробин, пириметанил, пироквилон, квиноксифен, спироксамин, сера, тебуконазол, тетраконазол, тиабендазол, тифлузамид, тиофанат-метил, тирам, тиадинил, триадимефон, триадименол, трициклазол, трифлоксистробин, тритиконазол, валидамицин и винклозолин; нематоциды, такие как алдикарб, оксамил и фенамифос; бактерицидные средства, такие как стрептомицин; акарициды, такие как амитраз, хинометионат, хлорбензилат, цигексатин, дикофол, диенохлор, этоксазол, феназахин, фенбутатин оксид, фенпропатрин, фенпироксимат, гекситиазокс, пропаргит, пиридабен и тебуфенпирад; и биологические средства, включающие энтомопатогенные бактерии, такие как Bacillus thuringiensis subsp. Aizawai, Bacillus thuringiensis subsp. Kurstaki и инкапсулированные дельта-эндотоксины Bacillus thuringiensis (например, Cellcap, MPV, MPVII); энтомопатогенные грибы, такой как гриб возбудитель заболевания “зеленая мускардина”; и энтомопатогенный вирус, включающий бакуловирус, нуклеополигедровирус (NPV), такие как HzNPV, AfNPV; и вирус гранулеза (GV), такой как CpGV. Способы могут также включать применение растений, генетически трансформированных для экспрессии белков, токсичных для беспозвоночных вредителей (таких белков, как дельта-эндотоксины Bacillus thuringiensis). В таких вариантах осуществления действие применяемых извне соединений для борьбы с беспозвоночными вредителями может являться синергичным с экспрессируемыми белками-токсинами.
Таким образом, в способах можно применять ингибирующий AHAS гербицид или комбинацию ингибирующего AHAS гербицида, и способы могут дополнительно включать применение инсектицидов и/или фунгицидов, и/или других сельскохозяйственных химических средств, таких как удобрения. Применение такой комбинированной обработки может расширить спектр действия по отношению к дополнительным видам сорных растений и подавлять размножение любых устойчивых биотипов.
Варианты осуществления дополнительно характеризуют в следующих примерах. Следует понимать, что эти примеры предоставляют только для иллюстрации. Из обсуждения выше и примеров, специалист в данной области может определить основные характеристики, и, не отступая от сущности и объема изобретения, может произвести различные изменения и модификации вариантов осуществления изобретения, для его приспособления к различным способам применения и условиям. Таким образом, различные модификации вариантов осуществления изобретения, в дополнение к тем, которые представлены и описаны в настоящем документе, будут очевидны специалистам в данной области из приведенного выше описания. Такие модификации также предназначены для включения в объем прилагаемых пунктов формулы изобретения.
ПРИМЕРЫ
Пример 1: Получение трансгенных растений
Трансгенные растения сои (Glycine max L.) получали, используя линеаризованный фрагмент (PvuII) ДНК из плазмиды pAC321, содержащий мутантную последовательность, кодирующую большую субъединицу синтазы ацетогидроксикислот (AHASL), обеспечивающую устойчивость к гербицидам на основе имидазолинона. Плазмида pAC321 содержит мутантный ген AHASL Arabidopsis thaliana (csr1-2), кодирующий последовательность, содержащую вместо природного серина аспарагин в положении, соответствующем положению 653 (S653N). Кодирующая последовательность AHAS (S653N) расположена под контролем природной последовательности промотора AHAS A. thaliana и последовательности терминации транскрипции. См., например, публикацию U.S. № 2005/0034187, которая, таким образом, полностью включена в качестве ссылки. Фрагмент PvuII включает промотор AHASL Arabidopsis, придающую устойчивость к гербициду кодирующую последовательность AHASLl Arabidopsis (csr1-2) и терминатор AHASL Arabidopsis. Кассету с промотором, кодирующей последовательностью и терминатором в настоящем документе обозначают как кассета csr1-2.
Для биолистической трансформации использовали эмбриональную осевую ткань, полученную из апикальной меристемы отдельного семени сои коммерческого сорта «Conquista». Биолистическую трансформацию (бомбардировку микрочастицами или частицами) (Aragao, F. J. L., et al., Theor. Appl. Genet. 1996; 93:142-150) использовали для получения трансформационных событий сои, содержащих ген csr1-2. До бомбардировки, ДНК, содержащую фрагмент гена csr1-2, осаждали на микроскопических частицах золота. Осажденную ДНК и частицы затем помещали в пластиковый макроноситель и ускоряли до высокой скорости, такой, при которой останавливающий экран задерживал макроноситель. Частицам с ДНК позволяли продолжать свое движение и возможное проникновение и встраивание в клетки растения сои. Подвергнутые бомбардировке клетки переносили в селективную среду, содержащую эквивалент 50 г д.в./га имазапира, гербицида на основе имидазолинона, и рост продолжали только те клетки, которых трансформировали геном csr1-2. В результате этого процесса идентифицировали устойчивое растение T0 и обозначали его как соя события 127 (таблица 1).
Пример 2: Получение линии
Первоначальный трансформант сои события 127 поддерживали самооплодотворением ("самоопылением") до поколения T4, как представлено ниже в таблице 1.
Получение первых поколений сои события 127
Генетический анализ семян из девяти растений T3 (E01, E02, E03, E04, E05, E06, E07, E09 и E10) выявил, что трансгенная сегрегация не всегда следовала простым менделевским схемам, что указывает на присутствие более чем одного активного локуса. Потомство T4 от растений T3 (E09, E10 и E05), которое по устойчивости к имазапиру демонстрирует сегрегацию по Менделю и у которого имелся нормальный фенотип, скрещивали с нетрансгенным сортами (BRS137, Conquista и BR97-7066), для получения четырех популяций (таблица 2, фиг.2).
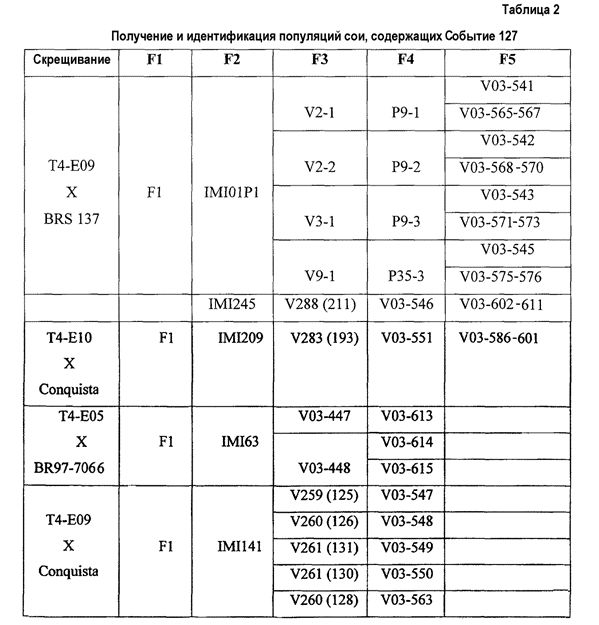
Среди поколений F2 и F3, в теплицу отбирали семейства и отдельные растения, которые имели нормальный фенотип и устойчивость к имазапиру. Схема сегрегации (38 устойчивых:13 не устойчивых) по устойчивости к имазапиру (100 г д.в./га) в популяции скрещивания F2 между трансгенной Conquista (T4-E10) × нетрансгенной Conquista показала, что устойчивость к имазапиру контролирует один доминантный ген в трансгенной линии V03-603 (CV-603), содержащей событие 127.
Последующие испытания в полевых условиях с использованием линий F4 и/или F5 от каждого из четырех скрещиваний (таблица 2) поддерживают выбор линии V03-603, содержащей событие 127, в качестве элитной соевой линии для последующего анализа и получения линии. Испытания в полевых условиях проводили путем засева четырех участков, с использованием рандомизированного полноблочного плана с трехкратным повторением и применением плана с расщепленными делянками. В табличных данных представлены целые делянки, а доза внесения имазапира (0, 70, 240 или 280 г д.в./га) представлена на подделянках. Растения обрызгивали спустя 18-21 сутки после посева, и результат оценивали через 14 суток после обработки. Растения оценивали в процентах повреждения (от 0 = в делянке нет погибших растений до 100 = в делянке погибли все растения). Дополнительно собранные данные включали высоту растения, урожай семян, размер семени, количество суток до цветения и количество суток до зрелости.
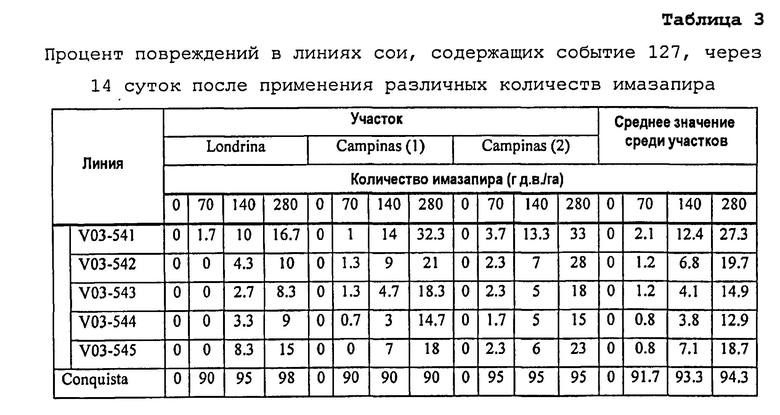
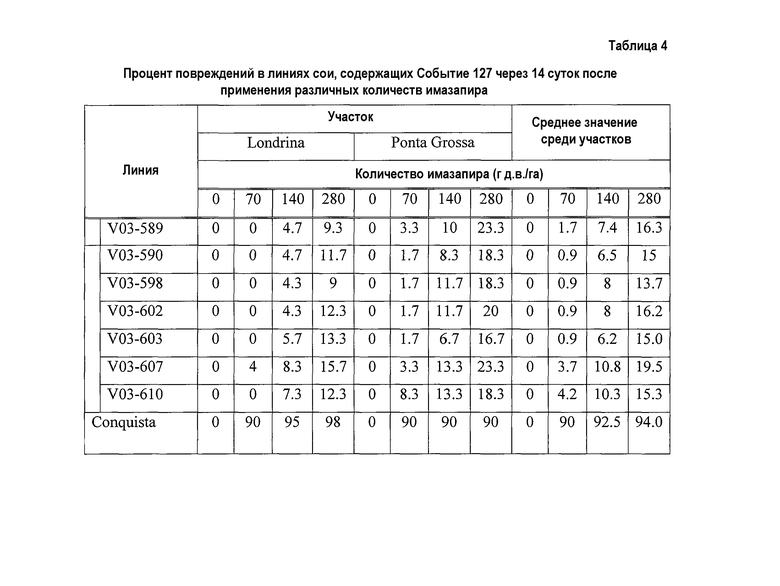

Пример 3: Молекулярное описание
A: Способы выделения и количественного анализа ДНК и РНК
ДНК выделяли из ткани листа сои посредством модифицированного способа CTAB (цетил-триметил аммония бромид) (Carlson et al., 1991). Высушенную силикагелем ткань листа замораживали в жидком азоте и измельчали Autogrinder (Autogen; Holliston, MA). Измельченную ткань инкубировали с предварительно нагретым буфером для экстракции, состоящим из 2% (масс./об.) CTAB, 100 мМ Tris-HCl, 1,4 М NaCl, 1% (масс./об.) поливинилпирролидона (PVP), 20 мМ этилендиаминтетрауксусной кислоты (ЭДТА), pH 9,5 (5 мл на 60 мг высушенной ткани листа) и β-меркаптоэтанола (10 мкл на мл буфера), при 74°C в течение 20 минут. После центрифугирования в 2440 ×g в течение 10 минут, супернатант дважды экстрагировали равным объемом хлороформа/изоамилового спирта (24:1). ДНК осаждали 0,7 объема изопропанола и растворяли в ТЕ буфере (10 мМ Tris-HCl, 1 мМ ЭДТА, pH 8,0) с РНКазой А 0,5 мг/мл (Invitrogen; Carlsbad, CA), добавленной до конечной концентрации приблизительно 500 нг/мкл. Выделенную ДНК количественно определяли красителем Хехст 33258 (Invitrogen) с ДНК тимуса теленка (Invitrogen), которую использовали в качестве ДНК-стандарта, на микропланшетном флуориметре Packard FluoroCount™ BF10000 (Packard Instrument Company; Meriden, CT), согласно руководству по использованию флуориметра.
Суммарную РНК экстрагировали из высушенных силикагелем молодых листьев, полученных из поколений F7 и F8 с событием 127, и из листьев нетрансгенной родительской сои сорта Conquista с набором Qiagen RNeasy Mini (Qiagen; Valencia, CA). Приблизительно 25 мг высушенной силикагелем ткани листа замораживали жидким азотом и измельчали Autogrinder. Процедуру выделения суммарной РНК выполняли по указаниям производителя. Расщепление ДНКазой на колонке выполняли с ДНКазой без примеси РНКазы (Qiagen), для удаления любой примеси геномной ДНК сои из препарата суммарной РНК, согласно руководству для пользователей набором RNeasy Mini. Выделенную РНК определяли количественно, измеряя оптическую плотность при 260 нм, используя спектрофотометр BioMate™ 3 (Thermo Electron Corporation; Waltham, MA).
B: Способы выделения и мечения зонда
Расположение фрагментов ДНК, используемых в качестве трансгенных зондов, указано на фиг.1B. Зонды к конструкции вектора указаны на фиг.5C. Праймеры для ПЦР, которые используют для получения идентифицированного трансгена, и зонды к вектору представлены ниже в таблице 3. Вместе эти 5 прекрывающихся зондов охватывают всю плазмиду. Конкретно зонд 1 охватывает область промотора AHASL, зонд 2 - кодирующую последовательность csr1-2, зонд 3 - область терминатора AHASL, а зонды 4 и 5 вместе охватывают полную конструкцию вектора (VB). Фрагменты ДНК-зонда получали ПЦР-амплификацией, используя в качестве матрицы плазмиду pAC321. Зонды (25-50 нг каждый) метили радиоактивным изотопом из расчета 50 мкКи (α-32P)-dCTP (3000 Ки/ммоль) (MP Biomedicals; Irvine, CA), используя систему для мечения ДНК Rediprime™ II (Amersham; Piscataway, NJ), согласно инструкциям производителя. Меченые зонды очищали с помощью центрифужных пробирок с фильтром Spin-X® (Corning Costar Corporation; Acton, MA).
Праймеры, используемые для получения зондов для анализа блоттинг по Саузерну
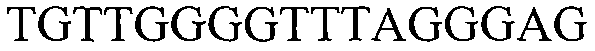
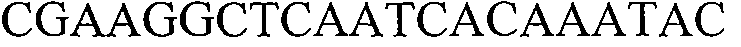

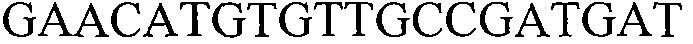
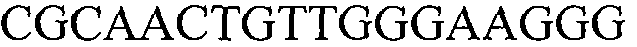

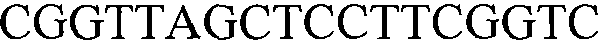


C: Число копий, сохранность и стабильность вставки
Блоттинг по Саузерну использовали для определения числа копий и сохранности экспрессионной кассеты csr1-2, а также для подтверждения отсутствия конструкции плазмиды в событии 127. Ферменты рестрикции NcoI, SpeI и XbaI использовали для расщепления геномной ДНК, полученной из растения события 127 и нетрансгенного контрольного растения Conquista. На фиг.3 выравнивают фрагмент трансформации PvuII из pAC321 со вставкой события 127 сои. Фрагмент PvuII из плазмиды pAC321, который использовали для трансформации сои, показан в верхней части фиг.3. Части этого фрагмента, которые не содержатся в пределах трансгенной вставки события 127 сои, указаны посредством прямоугольников, закрашенных диагональными полосами. Особенности трансгенной вставки ДНК и фланкирующей геномной ДНК сои события 127 показаны в нижней части фигуры. ДНК между вертикальными пунктирными линями, которые нанесены между картами фрагмента трансформации PvuII и областью трансгенной вставки, являются общими для обоих фрагментов ДНК. Указаны участки рестрикции, имеющие отношение к блоттингу по Саузерну. Система нумерации фрагмента трансформации PvuII соответствует системе нумерации карты плазмиды pAC321 на фиг.1. Система нумерации для вставки события 127 сои соответствуют таковому на фиг.8, где #1 представляет собой первый нуклеотид на 5' конце фланкирующей геномной последовательности сои (фланкирующие последовательности указаны посредством серых прямоугольников). Единственный участок рестрикции NcoI в кассете csr1-2 расположен на 5' конце кодирующей последовательности csr1-2, и при расщеплении геномной ДНК события 127 NcoI, как ожидали, получают два фрагмента, которые содержат ДНК из кассеты csr1-2. Оба фрагмента характеризуются посредством участка NcoI в кассете csr1-2 и ближайшими участками NcoI во фланкирующей геномной последовательности сои. Существует один участок рестрикции SpeI в 5' фланкирующей геномной последовательности сои и два участка рестрикции SpeI по ходу транскрипции относительно AHASL 3' UTR в событии 127. Участки рестрикции XbaI фланкируют полную экспрессионную кассету csr1-2. Число и размеры фрагментов ДНК, которые предположительно подлежат определению гибридизацией по Саузерну, перечислены ниже в таблице 7.
Число и размеры фрагментов ДНК, которые предположительно подлежат определению гибридизацией по Саузерну
b Зонд 5' UTR и зонд 3' UTR, каждый, перекрывают участок рестрикции XbaI и таким образом гибридизуются с обоими фрагментами XbaI плазмиды.
c Анализ последовательности вставки события 127 показывает, что небольшой участок кодирующей области csr1-2 дублирован в направлении против хода транскрипции сразу после 3' трансгенного участка интеграции, что подтверждает тождественность полосы в 800 п.н., представленной в таких анализах блоттинг по Саузерну.
Расчетные размеры фрагмента оценивают, исходя из клонированной вставки и фланкирующих последовательностей события 127 в геноме растений. Зонд 5' UTR и зонд 3' UTR, каждый, перекрывают участок XbaI и таким образом гибридизуются с обоими фрагментами XbaI из плазмиды pAC321 (отмечены точками на дорожке 11 на фиг.4A и 4C). Анализ последовательности участка события 127 показал, что небольшая часть кодирующего участка csr1-2 дублирована в направлении против хода транскрипции непосредственно перед 3' трансгенным участком интеграции, что подтверждает тождественность полосы в 800 п.н., идентифицированной в результатах анализа блоттинг по Саузерну.
Геномную ДНК (7 мкг) из поколения F8 с событием 127 и из нетрансгенного контрольного растения Conquista расщепляли в течение ночи в объеме 40 мкл с упомянутыми выше рестрикционными ферментами (8 единиц на мкг ДНК) в условиях, установленных изготовителями фермента (New England Biolabs; Ipswich, MA; или Amersham). Рестрикционные фрагменты разделяли электрофорезом в 0,8% агарозных гелях длиной 10 см. ДНК дополнительно фрагментировали, погружая гели в 0,25 HCl в течение приблизительно 20 минут, и денатурировали с 0,4 NaOH в течение приблизительно 30 минут. Гели промыли с 2× раствором NaCl/цитрат натрия (SSC), и денатурированную ДНК переносили на нейлоновую мембрану Hybond N+ (Amersham), используя 0,4 Н NaOH в качестве буфера для переноса. Гибридизацию по Саузерну выполняли согласно Sambrook et al. (1989). Мембраны предварительно гибридизовали при 65°C в течение 2-4 часов и гибридизовали при 65°C в течение ночи в 20-30 мл (приблизительно 0,2 мл/см2) буфера для гибридизации (2× SSC, 0,6% SDS, 50 мМ Na2HPO4, 1× раствор Денхардта, 2,5 мМ ЭДТА, 5% сульфат декстрана, pH 7,2) в Hybaid MAXI 14 Hybridization Oven (Thermo Electron Corporation). После гибридизации мембраны промывали 2× SSC, 0,5% SDS (1 мл/см2) при комнатной температуре в течение 15 минут, 2× SSC, 0,1% SDS (4 мл/см2) при 65°C в течение 30 минут, и в заключение с 0,1× SSC, 0,1% SDS (4 мл/см2) при 65°C в течение 15 минут. После промывки мембраны завернули в пластиковую упаковку и экспонировали с пленкой Hyperfilm™ MP (Amersham) при -80°C в кассетах с усиливающими экранами в течение 2-5 суток, в зависимости от интенсивности радиоактивного сигнала.
Анализы блоттинг по Саузерну также проводили, как описано выше, для контролирования стабильности вставки ДНК во множестве поколений. Материал растения получали из поколений T4, F4, F8 и F9 (фиг.2). Геномную ДНК из этих образцов расщепляли NcoI и SpeI (как описано выше) и выполняли анализ блоттинг по Саузерну, как описано выше.
Число копий вставки события 127 оценивали анализом блоттинг по Саузерну геномной ДНК из растений поколения F8 с событием 127, которую расщепляли ферментами рестрикции NcoI, SpeI и XbaI, используя способ, описанный выше.
Результаты анализов блоттинг по Саузерну приведены на фиг.4A, 4B и 4C. Геномную ДНК нетрансгенного сорта сои Conquista (дорожки 1, 5 и 9); Conquista, эквивалентную 1 копии генома (дорожки 2, 6 и 10); или эквивалентную 2 копиям генома pAC321 (дорожки 3, 7 и 11); и геномную ДНК события 127 сои из поколения F8 (дорожки 4, 8 и 12) расщепляли ферментами рестрикции NcoI (1-4), SpeI (5-8) и XbaI (9-12), как описано. Блоты гибридизовали с зондом 5' UTR (фиг.4A), зондом AHAS (фиг.4B) и зондом 3' UTR (фиг.4C). Первые и последние дорожки (помеченные M) содержат маркер длины λ/HindIII; размеры полосы указаны в т.п.н. На фиг.4D показаны области гомологии между зондами для гибридизации по Саузерну и вставкой события 127. Стрелка на фиг.4B показывает фрагмент SpeI, длиной приблизительно 885 п.н., содержащий дополнительный фрагмент длиной 376 п.н. csr1-2, представленный в событии 127 в 3' фланкирующей последовательности области соединения.
Нетрансгенная ДНК Conquista, расщепленная всеми тремя ферментами рестрикции и гибридизированная с тремя зондами, не показала какого-либо сигнала, что свидетельствует о том, что ни эндогенный ген сои AHASL, ни эндогенный ген γ субъединицы Sec61 сои не обнаружены в “строгих условиях” гибридизации, используемых при выполнении анализа блоттинг по Саузерну (фиг.4, дорожки 1, 5 и 9). Образцы ДНК из растений поколения F8 с событием 127, подвергнутые воздействию различных комбинаций ферментов и зондов, все показали по одной полосе (фиг.4A, B, и C, дорожки 4, 8 и 12), за исключением фрагмента расщепления SpeI, гибридизованного с зондом к кодирующей последовательности AHASL, для которого была выявлена дополнительная полоса небольшого размера приблизительно в 800 п.н. (фиг.4B, дорожка 8, показано стрелкой). Наличие этого продукта расщепления SpeI, размером в 800 п.н, гибридизующегося с зондом к AHASL, согласуется с наблюдением о том, что небольшой фрагмент кодирующей последовательности AHASL повторяется в событии 127 в участке соединения с 3' фланкирующей последовательностью (см. раздел “Полная последовательность”; пример 3E). Все основные полосы обладали интенсивностью сигнала, примерно равной эквиваленту 1 геномной копии pAC321.
Геномная ДНК из растения события 127, которую расщепляли NcoI и зондировали в области At AHASL 5' UTR, давала в результате полосу гибридизации размером приблизительно 4,5 т.п.н. Размер этой полосы согласуется с образованием одного фрагмента ДНК, который характеризуется участком NcoI в пределах вставки (2761 нт, фиг.4D) и участком NcoI, который располагается приблизительно через 4,5 т.п.н. против хода транскрипции в 5' геномной фланкирующей последовательности. Этот же продукт расщепления зондировали или в области кодирующей последовательности AtAHASL, или в области 3'UTR AtAHASL, получали полосу гибридизации размером приблизительно 9,0 т.п.н. Размер этой полосы соответствует одному фрагменту ДНК, который характеризуется участком расщепления NcoI во вставке ДНК (2761 нт, фиг.4D) и участком расщепления NcoI приблизительно через 9,0 т.п.н. по ходу транскрипции в 3' геномной фланкирующей последовательности сои.
Расщеплением геномной ДНК растения события 127 рестриктазой SpeI и зондированием области AtAHASL 5' UTR получали полосу гибридизации размером приблизительного 4,4 т.п.н. Это соответствует одному фрагменту ДНК, характеризующемуся участком SpeI во вставке (5620 нт, фиг.4D) и участком рестрикции SpeI, который располагается через приблизительно 4,4 т.п.н. против хода транскрипции в 5' фланкирующей последовательности ДНК генома сои (1268 нт, фиг.4D). Наличие против хода транскрипции такого участка расщепления SpeI подтверждали анализом 5' фланкирующей последовательности события 127 (см. раздел “Фланкирующие последовательности”; пример 3D). Тот же самый фрагмент подвергали зондированию или в области кодирующей последовательности AtAHASL, или в AtAHASL 3' UTR, в результате также получали полосу гибридизации размером в 4,4 т.п.н., соответствующую тому же самому фрагменту, описанному выше. Дополнительно, если продукт расщепления SpeI зондировали в области кодирующей последовательности AtAHASL, детектировали полосу гибридизации размером приблизительно 0,8 т.п.н., которая соответствует одному ДНК-продукту расщепления SpeI, содержащему сегмент гена csr1-2 в 3' фланкирующей последовательности участка соединения ДНК размером 376 п.н. Этот фрагмент, полученный в результате гибридизации, образован из участка SpeI во вставке ДНК и участка SpeI, который расположен через 0,8 т.п.н. по ходу транскрипции в геноме сои (5620-6505 нт, фиг.4D). Полосу гибридизации размером 0,8 т.п.н. не детектировали в результате гибридизации с зондом к AtAHASL 3' UTR, что свидетельствует о том, что ДНК AtAHASL 3' UTR не включена в фрагмент размером 0,8 т.п.н., а участок SpeI в положении 5620 нт во вставке ДНК соседствует с сегментом гена csr1-2 размером 376 п.н. Таким образом, участки расщепления фермента рестрикции SpeI в положениях 5622 нт и 5719 нт в линейном фрагменте PvuII плазмиды pAC321, используемом для трансформации (показано на фиг.1B), не включены во вставку ДНК в геноме с событием 127. Это подтверждали анализом последовательности ДНК вставки ДНК (см. раздел “Полная последовательность”; пример 3E). Наименьшие расчетные фрагменты размером 280 и 97 п.н, полученные в результате расщепления SpeI, внесенные в контроли к pAC321, с использованием этого способа давали бы сигнал ниже уровня детекции.
Геномная ДНК растения события 127 в случае расщепления XbaI и зондирования области AtAHASL 5' UTR показывает одну полосу гибридизации, размером приблизительного 10 т.п.н. Основываясь на расположении в линейной ДНК, используемой для трансформации (фиг.1B), участков рестрикции XbaI, рассчитывали получить полосу гибридизации размером приблизительно 5,7 т.п.н., образованную в результате расщепления во вставке ДНК в геноме с событием 127. Однако анализ последовательности ДНК вставки в геноме с событием 127 показал, что ни один из участков рестрикции XbaI в линейной трансформированной ДНК не был включен во вставку ДНК (см. раздел “Полная последовательность”; пример 3E). Таким образом, полосу гибридизации размером 10 т.п.н. получали в результате расщепления в участках рестрикции XbaI в пределах 5' и 3' фланкирующих последовательностей вставки ДНК (410 нт и 10652 нт, фиг.4D). Соответственно, тот же самый продукт расщепления зондировали или в области кодирующей последовательности AtAHASL, или AtAHASL 3' UTR, в результате получали аналогичную полосу гибридизации размером 10 т.п.н., соответствующую тому же самому фрагменту ДНК, описанному выше.
Анализ числа и размера всех полос гибридизации анализом блоттинга по Саузерну, который показан на фиг.4, соответствует интеграции одной вставки ДНК в геном сои события 127, содержащей одну функциональную копию гена csr1-2, а также кодирующие последовательности для белка SEC61γ на 5' конце гена csr1-2 и один фрагмент ДНК, содержащий сегмент гена csr1-2 размером 376 п.н. в 3' конце вставки ДНК.
Хотя трансформацию осуществляли фрагментом рестрикции PvuII из pAC321, который не включал ДНК конструкции вектора, выполняли исследования блоттинг по Саузерну для подтверждения отсутствия векторной ДНК плазмиды pAC321 в геноме с событием 127. Для определения того, была ли конструкция вектора интегрирована в геном с событием 127, тот же самый набор блотов, используемых для анализа блоттинг по Саузерну, описанного выше (фиг.4), гибридизовали с двумя зондами, специфичными к конструкции вектора (фиг.5). Как ожидалось, в дорожках, содержащих геномную ДНК нетрансгенной Conquista, не детектировали полос гибридизации. Геномная ДНК нетрансгенной Conquista, с внесенным одним или двумя эквивалентами геномной копии трансформированной плазмиды pAC321, показала полосы гибридизации расчетных размеров (таблица 7). Блот гибридизовали с зондом VP1 (фиг.5A) и зондом VP2 (фиг.5B). В ДНК растений поколения F8 с событием 127 не детектировали полос гибридизации, что в таком случае показывает, что ДНК векторной конструкции не интегрирована в геном сои с таким событием. На фиг.5C показаны положения зондов VP1 и VP2 относительно компонентов pAC321.
Для определения стабильности вставки в растении с событием 127, образцы ДНК растений четырех различных поколений T4, F4, F8 и F9 (фиг.2), подвергали анализу блоттинг по Саузерну. Образцы геномной ДНК расщепляли NcoI и SpeI и зондировали в области At AHASL 5' UTR, кодирующей последовательности AtAHASL или AtAHASL 3' UTR зондами, охватывающими весь фрагмент ДНК, используемый для трансформации (фиг.1B). Комбинация этих ферментов рестрикции и зондов обеспечивает уникальный анализ вставки ДНК в геноме с событием 127 способом геномных “отпечатков пальцев” (фингерпринт) (фиг.4). Геномную ДНК нетрансгенной Conquista использовали в качестве отрицательного контроля, а Conquista с внесенными одним и двумя эквивалентами геномной копии pAC321 использовали в качестве положительного контроля (фиг.6). Для всех трех зондов детектировали множество полос из ДНК растений поколения T4 с событием 127, расщепленную или NcoI или SpeI, что указывает, что поколение T4 содержит множество копий кассеты csr1-2. Однако ДНК из всех растений поколений F4, F8 и F9 продемонстрировали ту же самую картину, полученную в результате анализа блоттинг по Саузерну (фиг.6), ранее наблюдаемую в анализах на наличие вставки и подсчета числа копий (фиг.4). Этот результат показывает, что множество копий вставки в поколении T4 сегрегировало в потомстве, полученном в результате скрещивания между T4 и Conquista, и что в отобранном сегреганте сохранилась только одна копия. Кроме того, эта единственная копия устойчиво наследуется в следующих поколениях.
D: Геномная последовательность, фланкирующая 5' и 3' концы вставки ДНК
Для получения последовательности геномной ДНК сои, фланкирующей встроенную кассету csr1-2, использовали «инвертированную» ПЦР (Triglia et al., 1988). Геномную ДНК (1 мкг) из растения поколения F7 с событием 127 расщепляли 15 единицами XbaI, SpeI, HindIII, NcoI, EcoRI, BamHI или BglII в объеме реакции 20 мкл в течение 3 часов. Фрагменты расщепления XbaI, HindIII, NcoI и EcoRI инкубировали при 65°C в течение 20 минут, для инактивации ферментов, в то время как фрагменты расщепления BamHI и BglII подвергали осаждению c изопропанолом. T4 ДНК лигазу (800 единиц, New England Biolabs) добавляли непосредственно к каждой реакции расщепления. Также добавляли воду, для доведения объема реакции до 200 мкл. Реакционные смеси инкубировали при 16°C в течение ночи, кольцевую ДНК использовали непосредственно в качестве матрицы для «инвертированной» ПЦР. Трансгенные фланкирующие последовательности амплифицировали посредством набора для ПЦР GeneAmp® XL (Applied Biosystems; Foster City, CA). 100 мкл смеси для простой ПЦР содержали 1× поставляемый изготовителем буфер для ПЦР, 200 мкл каждого dNTP, 25 нг кольцевых геномных фрагментов ДНК, 1,2 мМ ацетата магния, 2 единицы ДНК-полимеразы XL rTth и 0,2 мкМ каждого праймера для простой ПЦР. 100 мкл смеси «гнездовой» ПЦР содержали те же самые компоненты, что и в простой ПЦР, за исключением того, что в качестве матрицы использовали 10 мкл разведенной 1:50 смеси простой ПЦР. Простые и «гнездовые» ПЦР выполняли на GeneAmp PCR System 9700 (Applied Biosystems). Последовательности праймеров для простой и «гнездовой» ПЦР приведены ниже в таблице 4. После начальной стадии денатурации в течение 1 минуты при 94°C, выполняли 30 циклов при 94°C в течение 15 секунд, 60°C в течение 8 минут и 72°C в течение 2 минут, с последующей финальной стадией удлинения в течение 10 минут при 72°C.
Праймеры, используемые для получения данных о фланкирующей последовательности ДНК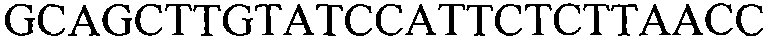
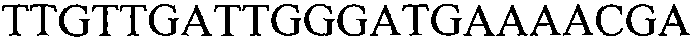
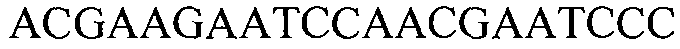
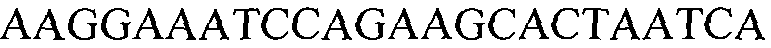

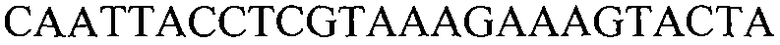
После завершения реакций ПЦР продукты реакций очищали посредством Zymo DNA Clean & Concentrator™-5 (Zymo Research; Orange, CA). Продукты реакций ПЦР или сразу секвенировали, или секвенировали после клонирования. Для получения полноразмерной последовательности, в случае если продукты реакций ПЦР или клонированные фрагменты были длиннее, чем 1 т.п.н., использовали “блуждающую” затравку. Для получения качества последовательности, большего, чем Phred 40 для каждого основания, секвенировали обе цепи ДНК. Секвенирование выполняли посредством набора для секвенирования BigDye™ Terminator v3.1 Ready Reaction Cycle и ABI 3730 DNA Analyzer от Applied Biosystems.
3' фланкирующий продукт ПЦР, амплифицированный на основе фрагмента расщепления XbaI, составил приблизительно 6 т.п.н., и эффективность амплификации была очень низкой для получения достаточного количества ДНК для секвенирования непосредственно сразу после ПЦР. Таким образом, продукты реакций ПЦР расщепляли SpeI, и полученные в результате фрагменты рестрикции, один приблизительно 800 п.н., а другие приблизительно 5,2 т.п.н., подвергали воздействию большого фрагмента ДНК полимеразы I (Кленова), (New England Biolabs), для получения тупых концов и клонировали в клонирующий вектор pCR®-Blunt II-TOPO (набор для клонирования Zero Blunt® TOPO® PCR; Invitrogen). Десять клонов каждого фрагмента проверяли рестриктазами и секвенировали посредством “блуждающей” затравки. Соединение фрагментов рестрикции подтверждали ПЦР-амплификацией и секвенированием последовательности, проходящей через соединение.
Фрагмент ДНК размером 3 т.п.н. амплифицировали посредством "инвертированной" ПЦР на основе внутримолекулярного кольцевого продукта расщепления NcoI геномной ДНК из растения поколения F7 c событием 127. Секвенирование обоих концов фрагмента показало, что фрагмент специфично амплифицировали с 5' конца трансгенной вставки. Фрагмент дополнительно секвенировали для получения 5' фланкирующей геномной последовательности сои размером 1,3 т.п.н. Фрагмент ДНК размером 6 т.п.н. амплифицировали "инвертированной" ПЦР на основе фрагмента расщепления рестриктазой XbaI геномной ДНК из растения поколения F7 с событием 127 и полностью секвенировали после субклонирования. Полученная последовательность показывает, что она фланкирует вставку на 3' конце. ПЦР анализ ДНК нетрансгенного сорта Conquista, с использованием праймеров к 5' и 3' фланкирующим участкам выполняли для подтверждения того, что фланкирующая последовательность являлась природной для генома растения (данные не представлены).
Полная последовательность трансгенной вставки в геноме сои события 127 с 5' и 3' фланкирующими последовательностями показана на фиг.8 (SEQ ID NO:1). Анализ BLAST 5' фланкирующей последовательности, с запросом общедоступных баз данных ДНК (все последовательности GenBank+EMBL+DDBJ+PDB) и запатентованной базы данных ДНК Plant Science BASF, выявил участок последовательности, идентичный с запатентованной экспрессируемой в сое маркерной последовательностью (EST), что подтверждает, что идентифицированная фланкирующая последовательность происходит из природной ДНК сои. Последовательность дополнительно анализировали на наличие предполагаемых открытых рамок считывания. Результаты показали, что существует ORF размером 315 п.н., из нуклеотидов от 941 до 1255 фланкирующей последовательности, которая располагается против хода транскрипции в 5' конце вставки. Выравнивание 5' фланкирующей последовательности с трансформированной последовательностью показало, что точка интеграции представлена нуклеотидом в положении 1312 (фиг.8; SEQ ID NO:1), который располагается через 60 п.н. от стоп-кодона предполагаемой ORF в направлении по ходу транскрипции.
Анализ 3' фланкирующей последовательности показал, что перед 3' точкой интегрирования представлен сегмент размером 376 п.н., последовательность которого отличается от части кодирующей последовательности csr1-2 только одним нуклеотидом (нуклеотиды 3768-4143 из фиг.8; SEQ ID NO:1). Вставка последовательности размером 376 п.н. в 3' фланкирующей последовательности соединения создавала ORF размером 501 п.н., которая простирается от трансгенной вставки до 3' фланкирующей последовательности. Потенциальную возможность транскрипции ORF исследовали ОТ-ПЦР. Анализ BLAST 3' фланкирующей последовательности с запросом общедоступных баз данных ДНК (все последовательности GenBank+EMBL+DDBJ+PDB) и запатентованных баз данных ДНК Plant Science BASF, выявил участок последовательности в проксимальной 3' фланкирующей последовательности, который подобен последовательности гену каталазы сои (входящий № Z12021). Однако точка интегрирования представлена приблизительно через 500 п.н. против хода транскрипции от потенциального гомолога гена, а предполагаемая кодирующая последовательность располагается приблизительно через 2,4 т.п.н. по ходу транскрипции от точки интегрирования. Таким образом, даже если возможный гомолог каталазы представляет собой активный ген, то маловероятно, что он подвергнется воздействию вставки. Кроме того, участок дистальной 3' фланкирующей последовательности разделяет идентичность последовательности с запатентованной EST сои.
Исследования проводили ПЦР-амплификацией участка интеграции с событием 127 в геноме нетрансгенного сорта Conquista. С наборами праймеров для ПЦР A и B для амплификации участка встраивания, где праймеры включают один праймер к 5' фланкирующей области, а второй праймер к 3' фланкирующей области, при использовании в качестве матрицы геномной ДНК нетрансгенного сорта Conquista амплифицированного ДНК-продукта не получали. С набором праймеров C, с праймером, специфичным к 3' фланкирующей последовательности, не получали амплифицированного продукта, при использовании ДНК нетрансгенного сорта Conquista, в то время как расчетный ампликон получали с геномной ДНК из растения события 127 (данные не представлены). Это демонстрирует, что фрагмент ДНК, амплифицированный посредством набора праймеров C, присутствует в событии 127, но не представлен в том же самом окружении в геноме Conquista, что предполагает, что в событии 127 произошла перестановка ДНК в участке встраивания. Это согласуется с идентификацией сегмента размером 376 п.н., дублированной последовательности из кодирующей области csr1-2, располагающейся вблизи соединения встроенной ДНК и геномной ДНК сои.
E. Полная последовательность встроенной ДНК
Шесть полученных в результате ПЦР ампликонов конструировали так, чтобы охватить полную последовательности вставки, а также последовательности соединения с соседними геномными последовательностями (фиг.7). Полную последовательность встроенной ДНК получали посредством ПЦР-амплификации шести таких перекрывающихся фрагментов с последующим анализом последовательности ДНК. Последовательности праймеров, используемых в ПЦР-амплификации, представлены в таблице 5. ПЦР-ампликоны, содержащие последовательность с несоответствиями по отношению к последовательности фрагмента трансформации, подвергали повторному амплифицированию с ДНК полимеразой XL rTth. ПЦР-продукты очищали Zymo ДНК Clean & Concentrator™-5, и проводили секвенирование обеих цепей до показателя качества Phred 40 посредством прямого секвенирования и “блуждающей” затравки. Секвенирование ДНК выполняли, как описано выше.
Праймеры, используемые для амплификации вставки ДНК события 127

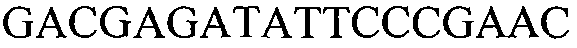
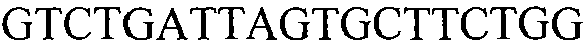
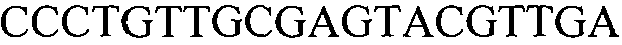


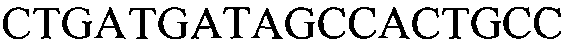
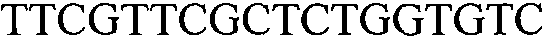
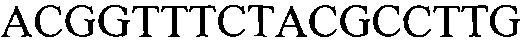
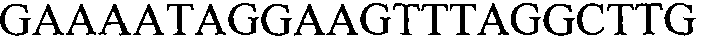
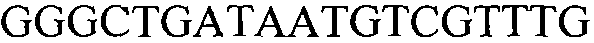
Хотя результаты анализа блоттинга по Саузерну позволяли предположить, что трансгенная вставка содержала полную экспрессирующую кассету csr1-2, клонирование и секвенирование вставки выполняли для подтверждения сохранности вставки. Полную последовательность встроенной ДНК получали посредством ПЦР-амплификации с ДНК полимеразой Taq шести перекрывающихся ампликонов (фиг.7). Полная последовательность вставки в растении сои события составляет 4758 п.н. в длину, и за исключением встраивания фрагмента размером 376 п.н. из csr1-2, который располагается в 3' точке интеграции, последовательность идентична последовательности фрагмента трансформации, за исключением трех точечных мутаций (фиг.8; SEQ ID NO:1). Одна из точечных мутаций представляет собой мутацию замены G на A мутация в кодирующей последовательности AHASL, что приводит к замене аминокислоты R272 на K272. Замена представляет собой консервативную замену аминокислот и не имеет влияния на свойство устойчивости к гербициду или ферментативные свойства белка At AHAS. Две другие мутации включают мутацию замены G на A и G на C, которые расположены по ходу транскрипции в 3'UTR гена csr1-2 и являются, таким образом, генетически “молчащими”.
Эксперименты выполняли для определения того, в какой точке, в процессе получения и селекции сои события 127, произошла мутация замены G на A в кодирующей последовательности AHASL. Первоначально, выполняли реакцию с ПЦР 4 (фиг.7), используемой для секвенирования вставки, используя в качестве матрицы как геномную ДНК от события 127 растений поколения T4, так и геномную ДНК от события 127 растений поколения F8, и секвенировали ПЦР-продукты. Последовательность от события 127 растения поколения T4 не отличалась от расчетной (pAC321) последовательности. Полагая, что поколение T4 содержит множество копий вставки, и продукт реакции с ПЦР 4, вероятно, представляет собой смесь последовательностей различных копий вставки, разрабатывали ПЦР, специфичную к локусу ампликона события 127 размером 2,5 т.п.н., используя прямой праймер (5'-GCCCTCCTTATTTATCCCCTTA-3'; SEQ ID NO:35) к 5' фланкирующей последовательности и обратный праймер (5'-ACAAACCTACCCAATTCATCGC-3'; SEQ ID NO:36) к кодирующей последовательности csr1-2. Продукты реакций ПЦР сразу секвенировали. Сравнение последовательности показало, что мутация замены G на A также присутствует в поколении T4 растений события 127, что показывает, что мутация произошла в какой-то момент, предшествующий получению поколения T4 (данные не показаны), и сохраняется в последующих восьми поколениях.
Начальная трансформированная последовательность содержит сегмент размером 2,5 т.п.н., который первоначально аннотировали как промотор AHASL и 5' UTR. Недавнее секвенирование показало, что этот сегмент последовательности также содержит ранее неаннотируемый ген Arabidopsis, кодирующий гамму субъединицу SEC61, мультимерного транспортного белка. Последовательность вставки события 127, содержит большую часть гена γ субъединицы AtSec61, включающую полную кодирующую последовательность. 5' UTR AtSec61γ, который аннотируется The Arabidopsis Information Resource, начинается через 18 нуклеотидов по ходу транскрипции от 5' трансгенного участка интеграции. Таким образом, маловероятно, что вставка содержит полный природный промотор гена AtSec61γ.
Возможную транскрипцию гена γ субъединицы AtSEC61 Arabidopsis, обнаруженного во вставке в геноме сои события 127, оценивали, используя ОТ-ПЦР. ОТ-ПЦР осуществляли, используя в качестве матрицы обработанную ДНКазой суммарную РНК, выделенную из поколения F7 сои события 127. Праймеры Iota и GmSec61 γ, специфичные для двух эндогенных генов сои, использовали в качестве положительного контроля для подтверждения качества РНК-матрицы. Суммарную РНК из листа Arabidopsis и тканей корня, не обработанную ДНКазой, также использовали в качестве положительного контроля. Результаты показали, что для обоих положительных контролей к эндогенным генам сои, Iota и GmSec61 γ представлена хорошая транскрипция в молодой ткани листа сои, в то время как ген γ субъединицы AtSEC61 в поколении F7 генома события 127 транскрибирован только в небольшом количестве. На фиг.9 стрелкой показан малопредставленный продукт реакции ОТ-ПЦР, соответствующий γ субъединице AtSEC61, амплифицированной с генома события 127. Представленная полосой с размером 393 п.н. амплифицированная ДНК γ субъединицы AtSEC61 из поколения F7 растения события 127 имеет тот же размер, что и полоса, соответствующая ДНК, амплифицированной из листьев и корней Arabidopsis (фиг.9). Ту же пару праймеров также использовали в амплификации для получения полосы с расчетным размером 965 п.н., для амплификации контаминирующей геномной ДНК, присутствующей в образцах листа и корня Arabidopsis. Для подтверждения идентичности продукта реакции ОТ-ПЦР события 127, продукт секвенировали и сравнивали с прогнозированной последовательностью мРНК γ субъединицы AtSEC61 (данные не представлены). Обе последовательности сочетались, что показывает, что γ субъединица AtSEC61 транскрибируется в листьях события 127 в небольшом количестве.
Вставка участка в 376 п.н. кодирующей последовательности csr1-2 около участка соединения с 3' фланкирующей последовательностью (фиг.7) создавала ORF размером 501 п.н. Возможную транскрипцию этой ORF исследовали анализом ОТ-ПЦР. ОТ-ПЦР выполняли с двумя различными количествами РНК-матрицы, 500 нг и 125 нг. Геномную ДНК из поколения F8 растения события 127 также использовали в реакции с праймерами, специфичными к ORF, в качестве положительного контроля. Праймеры, специфичные к Iota гену сои, использовали в реакциях положительного контроля для подтверждения качества матрицы РНК. Праймеры, специфичные к ORF, обеспечивают амплифицикацию фрагмента геномной ДНК генома события 127 размером 435 п.н. Однако при использовании в качестве матрицы суммарной РНК из ткани молодого листа детектируемого продукта реакции ОТ-ПЦР не наблюдали, что позволяет предположить, что ORF не экспрессируется в геноме события 127 (фиг.10).
F. Анализ ПЦР для качественной специфичной к событию детекции
Разрабатывали специфичную к событию ПЦР, используя информацию, полученную как из фланкирующей последовательности ДНК, так и из последовательности вставки. Конструировали четыре пары праймеров, где один праймер каждой пары представлял собой праймер к 5' фланкирующей последовательности генома сои, а другой представлял собой праймер к кассете csr1-2. Последовательности праймеров, которые использовали в специфичной к событию ПЦР, приведены ниже в таблице 10.
Праймеры, используемые для специфичной к событию ПЦР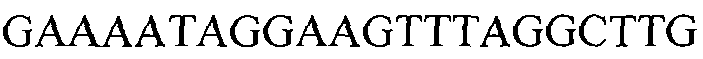
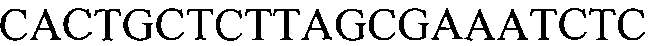
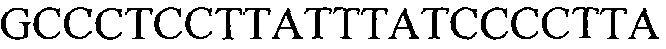



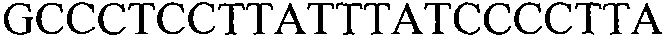
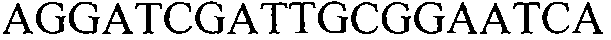
Разработали праймеры для амплификации продуктов реакции ПЦР размером приблизительно между 200 и 400 п.н. В качестве матрицы использовали геномную ДНК как из события 127, так и из нетрансгенного сорта Conquista. ПЦР выполняли в суммарном объеме 25 мкл с 25 нг матрицы ДНК, 200 мкМ каждого dNTP, 0,4 мкМ каждого праймера и 1 единицей ДНК-полимеразы Taq на реакцию. После начальной стадии денатурации в течение 4 минут при 94°C, выполняли 30 циклов при 94°C в течение 30 секунд, 60°C (ПЦР 1 и 3 к событию) или 66°C (ПЦР 2 и 4 к событию) в течение 30 секунд и 72°C в течение 45 секунд, с последующей финальной стадией удлинения в течение 10 минут при 72°C. По четыре растения сои события 127 и нетрансгенного сорта Conquista с шести засеянных участков анализировали качественной ПЦР, используя набор праймеров "ПЦР 3 к событию".
В результате всех четырех ПЦР получали продукты реакций расчетного размера, специфичного для генома сои события 127 (фиг.11A), что указывает на то, что любой из четырех наборов праймеров можно использовать для детекции в образце молекул нуклеиновой кислоты события 127. Продукт 3 специфичной к событию ПЦР дополнительно проверяли в образцах растений сои события 127 и нетрансгенного сорта Conquista, собранных с шести различных засеянных участков. Результаты показали, что продукт 3 реакции ПЦР специфично амплифицирован во всех 24 образцах сои события 127, но не представлен в контрольном нетрансгенном сорте Conquista (фиг.11B и C).
G. Анализ ПЦР для количественной специфичной к событию детекции
Специфичную к событию количественную ПЦР разрабатывали для детектирования и надежного и точного определения количества нуклеиновой кислоты события 127 в суммарной смеси семян, если нуклеиновая кислота сои события 127 представлена в образце в количестве между 0,08% и 5% от общего количества присутствующей в образце нуклеиновой кислоты. В этом способе используют две пары праймеров наряду с промежуточными зондами. Последовательности праймеров для использования в специфичной к событию ПЦР показаны ниже в таблице 11.
Праймеры, используемые для анализа Q-ПЦР





В этом анализе, основанном на применении Taq-Man, сравнивают уровень продукта реакции в специфичной к событию ПЦР и уровень продукта эндогенного контроля, в течение каждого цикла в двух различных реакционных смесях.
В формате анализа используют калибровочные кривые для каждой из двух систем ПЦР; каждая калибровочная кривая состоит из четырех стандартных точек, каждая из которых получена тройными измерениями. Стандарты получают посредством получения растворов с 20 нг/мкл суммарной геномной ДНК, содержащей 10% ДНК сои события 127 (стандарт 1), и последующего серийного разведения 1:5 буфером для разведения (стандарты 2-4). Три контрольных реакции на систему, в которых не добавлена матрица (NTC), выполняют для проверки чистоты реактивов. Каждый образец (неизвестный) анализируют из расчета 100 нг геномной ДНК на реакцию.
Зонды ПЦР к событию и эндогенному гену конъюгируют с FAM (возбуждение 495 нм; эмиссия 520 нм). Праймеры разработаны для получения коротких ампликонов длиной менее чем 100 п.н. Смесь геномной ДНК сои события 127 (10%) и Conquista (не является ГМ) (90%) разводили до 20 нг/мкл. Для калибровочной кривой смесь затем разводили 10 нг/мкл ДНК из спермы лосося до 20, 4 и 0,8 нг ДНК сои (объем в реакции составляет 5 мкл). Реакции ПЦР выполняли в объеме 25 мкл в 96-луночных планшетах, со всеми стандартными компонентами (TaqMan Universal PCR master mix с урацил-N-гликозилазой (AmpErase®UNG, ABI)). Для ПЦР к событию праймеры добавляли в концентрации 400 нМ, а зонды в концентрации 100 нМ. Для эндогенной ПЦР праймеры добавляли в концентрации 150 нМ, а зонды в концентрации 50 нМ. Анализы выполняли в системе для ПЦР в реальном времени модели Applied Biosystems 7500 Fast. После начальной стадии выполнения цикла в течение 2 минут при 50°C и в течение 10 минут при 95°C, выполняли 45 циклов при 95°C течение 15 секунд и при 60°C в течение 60 секунд. Три образца, которые представляют собой сою события 127 и нетрансгенного сорта Conquista по отдельности и их смесь, анализировали количественной ПЦР.
H. Анализ дупликации и гена SEC61
ОТ-ПЦР выполняли для определения того, подверглись ли транскрипции как дупликация части кодирующей последовательности csr1-2 размером 376 п.н., так и ген γ AtSec61 сои события 127. В качестве матрицы для ОТ-ПЦР использовали суммарные РНК, с использованием набора Qiagen OneStep RT-PCR (Qiagen). Для анализа ОТ-ПЦР кодирующей последовательности γ AtSec61, образцы суммарной РНК из листьев и корней Arabidopsis также использовали в качестве положительного контроля. Образцы суммарной РНК Arabidopsis получали с реактивом TRIzol (Invitrogen) без обработки ДНКазой. Реакции ОТ-ПЦР содержали 1× буфера для ОТ-ПЦР Qiagen OneStep, 400 мкМ каждого dNTP, 0,6 мкМ каждого праймера, 2 мкл смеси ферментов для ОТ-ПЦР OneStep Qiagen, и 500 нг или 125 нг суммарной РНК в суммарном объеме 50 мкл. ОТ-ПЦР проводили, используя систему ПЦР GeneAmp 9700. После выполнения стадии обратной транскрипции в течение 30 минут при 50°C выполняли амплификацию ПЦР со следующими условиями: одна стадия денатурации в течение 15 минут при 95°C; 30 циклов при 94°C в течение 30 секунд, при 64°C течение 30 секунд и при 72°C течение 1 минуты; одна стадия удлинения в течение 10 минут при 72°C. Последовательности праймеров, используемых для анализа ОТ-ПЦР, представлены в таблице 12.
Эндогенный ген γ субъединицы Sec61 сои и ген Iota использовали в качестве положительного контроля. Ген субъединицы Iota сои экспрессируется в сое конститутивно и повсеместно (Yamamoto and Knap, 2001).
Праймеры, используемые для анализа ОТ-ПЦР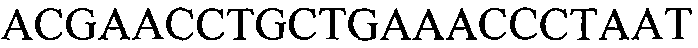
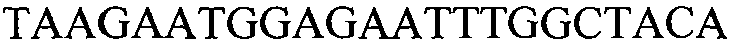

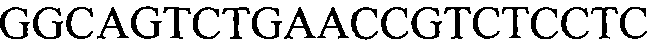


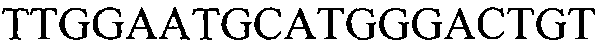

I. Анализ ПЦР участка интеграции
Три реакции ПЦР выполняли, для характеристики участка встраивания в нетрансгенном сорте сои Conquista. Праймеры ПЦР, используемые в этом исследовании, получали из последовательности ДНК, которую определяли для 5' и 3' геномных областей, фланкирующих новую экспрессионную кассету в геноме События 127.
Праймеры ПЦР для PCRA (см. таблицу 13 ниже) были разработаны таким образом, что прямой праймер будет связываться с 5' фланкирующей последовательностью, а обратный праймер будет связываться 3' фланкирующей последовательностью, сразу после 3' точки интегрирования. Праймеры для PCRB были разработаны таким образом, что прямой праймер свяжется с 5' фланкирующей последовательностью, в то время как обратный праймер свяжется с последовательностью, близкой к дистальному концу 3' фланкирующей последовательности. Оба праймера для PCRC были разработаны для связывания в пределах 3' фланкирующей последовательности.
Праймеры, используемые для анализа участка интеграции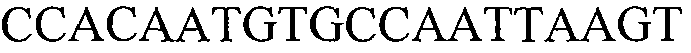
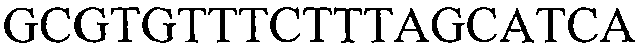

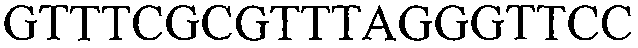
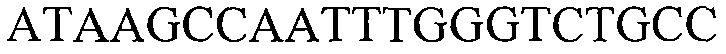
ПЦР A и ПЦР C выполняли с ДНК полимеразой Taq Qiagen и ПЦР 2 с набором для ПЦР GeneAmp® XL. Двадцать пять нг или ДНК События 127 или ДНК Conquista использовали во всех ПЦР-амплификациях. Для ПЦР с ДНК полимеразой Taq Qiagen, реакция содержала 1× Qiagen буфер ПЦР, 200 мкМ каждого dNTP, 0,4 мкМ каждого праймера и 1 единицу ДНК полимеразы Taq в суммарном объеме 25 мкл. После начальной стадии денатурации в течение 4 минут при 94°C, выполняли 30 циклов при 94°C в течение 30 секунд, при 66°C в течение 45 секунд и 72°C в течение 2 минут, с последующей финальной стадией удлинения в течение 10 минут при 72°C.
Для ПЦР с набором для ПЦР GeneAmp® XL, реакция содержала те же самые компоненты, как и использующиеся в клонировании фланкирующей последовательности за исключением матрицы ДНК. После начальной стадии денатурирования в течение 1 минуты при 94°C, выполняли 30 циклов при 94°C в течение 1 минуты и при 66°C в течение 10 минут, с последующей финальной стадией удлинения в течение 10 минут при 72°C.
J. Биоинформационный анализ
Сборку последовательности ДНК выполняли с Staden Pregap4 и Gap4 (Staden, 1996). Выравнивание клонированной последовательности и предполагаемой последовательности вставки осуществляли программным обеспечением LI-COR AlignIR (Licor Biotechnology; Lincoln, NE). Анализ BLAST фланкирующих последовательностей выполняли с запросом общедоступных баз данных ДНК (все последовательности GenBank+EMBL+DDBJ+PDB) и запатентованных баз данных ДНК Plant Science BASF (Altschul et al., 1997). Открытые рамки считывания 30 кодонов или более идентифицировали с функцией анализа ORF Vector NTI v9.0 (Invitrogen).
Основываясь на результатах этих экспериментов, геном сои события 127 содержит одну копию вставки размером 4758 п.н., которая включает полную экспрессионную кассету csr1-2, так же как 5' UTR, полную кодирующую последовательность и 3' UTR гена γ субъединицы AtSec61. Повтор кодирующей последовательности из гена csr1-2 размером 376 п.н. также интегрирован в участке соединения 3' фланкирующей последовательности. Векторную последовательность, интегрированную в геном сои, не обнаружили. Вставка устойчиво наследовалась в восьми поколениях скрещивания, демонстрируя, что вставка устойчиво интегрирована в геном сои. В экспрессионной кассете csr1-2 присутствуют три точечных мутации: одна консервативная мутация в кодирующей последовательности AHASL, которая не оказывает влияние на устойчивость к гербициду или ферментативные свойства мутантного белка AHASL, и две мутации по ходу транскрипции в 3' UTR. Выяснено, что перестановка геномной ДНК сои произошла в ДНК, фланкирующей 3' конец вставки, и это, наиболее вероятно, произошло во время процесса интеграции ДНК. Вставка содержит кодирующую последовательность гена γ субъединицы AtSec61, которую включили в используемый для трансформации фрагмент ДНК. Транскрипция этого гена представлена только в небольшом количестве. Фрагмент кодирующей последовательности csr1-2 размером 376 п.н. создал новую ORF размером 501 п.н. Эксперименты ОТ-ПЦР не показали детектируемой транскрипции этой ORF.
Пример 4: Борьба с сорным растением
A. Пример 4A: Послевсходовое применение
Три полевых испытания провели на трех различных участках в центральной области Бразилии: Станция сельскохозяйственных исследований (ARS) в Санто Антонио де Поссе, SP, Embrapa Rice и Beans (CNPAF) в Санто Антонио де Гояс, GO и Embrapa-Epamig (CTTP) в Убераба, МГ. Засорение сорными растениями в каждом участке представлено в таблице 13.
Засорение сорными растениями на каждом участке, период применения гербицидов - ранний послевсходовой период
CYPRO = Cyperus rotundus; BOILF = Spermacoce latifolia; COMBE = Commelina benghalensis; EPHHL = Euphorbia heterophylla; SIDRH = Sida rombifolia; RCHBR = Richardia brasiliensis; IPOGR = Ipomoea grandifolia.
Все процедуры от посева до сбора урожая являлись одинаковыми для всех трех участков. Гербициды применяли в ранний послевсходовый период, когда у сорных растений образовалось от 2 до 4 листов, а у культуры сои полностью раскрылся первый тройчатый лист. Использовали полностью рандомизированный блочный план с тройным повторением. Виды основных обработок представлены в таблице 15.
Виды основных обработок сорных растений, применяемые в ранний послевсходовый период:
Гербициды на основе имидазолинона применяли на устойчивой к имидазолинону сое, (полученной с событием 127), а глифосат применяли на сое Roundup Ready (Valiosa RR), высаженных рядом на одном участке. Гербициды на основе имидазолинона (имазапир и Kifix) применяли с неионным адъювантом - Dash - из расчета 0,25% об./об. Ранцевый опрыскиватель CO2 с распыливающим наконечником низкого давления 80015, обеспечивающий 170 л/га из расчета 190 КПа, использовали во всех случаях применения гербицидов. Все семена сои популяции из 380000 семян/га заделывали на глубину 5 см с расстоянием между рядами 50 см.
Повреждение сельскохозяйственной культуры оценивали через 15 и 30 суток после применения (DAA), основываясь на шкале от 0 до 100, где 0 соответствует состоянию, при котором нет повреждений, и 100 соответствует состоянию гибели растения. Эффективность гербицида оценивали через 15, 30 и 60 DAA, основываясь на шкалу от 0 до 100, где 0 обозначает, что гербицид не оказал никакого эффекта, и 100 обозначает полную эффективность гербицида.
В таблице 16 ниже представлена эффективность этих основных обработок сорных растений, произрастающих на площади в период применения гербицида. В соответствии с этими результатами, имазапир и комбинация имазапир+имазапик показала похожую эффективность. В 30 DAA оба препарата оказали большое воздействие на семь значимых сорных растений, произрастающих в Бразилии: CYPRO (87%), COMBE (87-90%), EPHHL (85-87%), IPOGR (90-91%), BOILF (82-83%), SIDRH (86-87%) и RCHBR (83%).
В 60 DAA, гербициды на основе имидазолинона превосходили глифосат по действию на CYPRO, COMBE, RCHBR и IPOGR, в случае послевсходового применения.
Эффективность имазапира, комбинации имазапир+имазапик и глифосата, примененных в послевсходовый период на площади с растениями сои (Событие 127 и RR)
Пример 4B: Применение до полного уничтожения
Три полевых испытания провели на трех различных участках в центральной области Бразилии: Станция сельскохозяйственных исследований (ARS) в Санто Антонио де Поссе, SP, Embrapa Rice и Beans (CNPAF) в Санто Антонио де Гояс, GO и Embrapa-Epamig (CTTP) в Убераба, МГ. Засорение сорными растениями в каждом участке представлено в таблице 17.
Сорные растения, засоряющие каждый участок в период применения гербицида - до полного уничтожения сорных растений
BRAPL = Brachiaria plantaginea; DIGHO = Digitaria horizontalis; CYPRO = Cyperus rotundus; COMBE = Commelina benghalensis; EPHHL = Euphorbia heterophylla; IPOGR = Ipomoea grandifolia; GASPA = Galinsoga parviflora; BIDPI = Bidens pilosa.
Все процедуры от посева до сбора урожая являлись одинаковыми для всех трех участков. Гербициды применяли до полного уничтожения сорных растений за пять суток до посева растений сои.
Использовали полностью рандомизированный блочный план с тройным повторением. Виды основных обработок представлены в таблице 18.
Основные способы обработки, примененные для полного уничтожения сорных растений - 5 суток до посева
Устойчивую к имидазолинону сою, полученную из события 127, заделывали на глубину 5 см в популяции 380000 семян/га с расстоянием между рядами 50 см. Гербициды на основе имидазолинона применяли с неионным адъювантом, Dash, из расчета 0,25% об./об. Ранцевый опрыскиватель CO2 с распыливающим наконечником низкого давления 80015, обеспечивающий 170 л/га из расчета 190 КПа, использовали во всех случаях применения гербицидов. (Таблица 18).
Повреждение сельскохозяйственной культуры оценивали через 15 и 30 суток после посева (DAP), основываясь на шкале от 0 до 100, где 0 соответствует состоянию, при котором нет повреждений, и 100 соответствует состоянию гибели сельскохозяйственной культуры. Эффективность гербицида оценивали через 15, 30 и 60 DAP, основываясь на шкале от 0 до 100, где 0 обозначает, что гербицид не оказал никакого эффекта, и 100 обозначает полную эффективность гербицида.
В таблице 19 представлена эффективность действия этих основных способов обработки сорных растений, произрастающих на площади в период применения гербицида до полного уничтожения сорных растений. Результаты на 30 и 60 DAA показали наличие остаточного действия гербицида на основе имидазолинона, по сравнению с глифосатом. На 30 DAA, эффект от действия комбинации имазапир + имазапик был немного лучше, чем имазапика, но оба способа обработки были эффективны по отношению к BRAPL (85%), DIGHO (95%), CYPRO (88%), COMBE (75-94%), EPHHL (95%), IPOGR (75%), GASPA (84-95%) и BIDPI (79-93%). Глифосат не обладал остаточной активностью и не оказал воздействия на перечисленные сорные растения в 30 и 60 DAA.
Эффективность (%) имазапика, комбинации имазапир + имазапик и глифосата, примененных для полного уничтожения основных сорных растений Бразилии
Пример 4C: Контролирование устойчивых к глифосату растений
Для определения того, можно ли использовать гербициды на основе имидазолинона для контролирования нежелательных устойчивых к глифосату сорных растений и сельскохозяйственных культур, произрастающих на посевной площади, проводили исследования в теплице. Семена невосприимчивых к глифосату растений высаживали в делянки размером 4,5 дюймов, используя смесь с названием metro mix для послевсходового применения и почву North Carolina для предвсходового применения с удобрением, медленно высвобождающимся на поверхность почвы. Растения оставляли в теплице с подвесным поливом.
Пять индивидуальных растений каждого вида невосприимчивых к глифосату растений сои, кукурузы и мелколепестника канадского опрыскивали глифосатом, имазапиром или имазапиком, которые применяли или в послевсходовый период, или в предвсходовый период. Опрыскивание в послевсходовый период выполняли в стадии 2 настоящих листов для кукурузы и сои и в стадии 9 настоящих листов для мелколепестника канадского. Глифосат применяли в количестве 774 г д.в./га, тогда как гербициды имазапир и имазапик применяли в количествах 20 г д.в./га, 40 г д.в./га, 80 г д.в./га, 160 г д.в./га и 240 г д.в./га. Степень общего повреждения в процентах визуально определяли через 14 суток после обработки (DAT) и через 25 суток после обработки (DAT). Необработанные контрольные растения не продемонстрировали видимых повреждений во всех исследованиях.
Результаты послевсходовых анализов суммированы в таблице 20, а результаты предвсходовых исследований суммированы в таблице 21. Результаты представлены как среднее, полученное от значений для 5 индивидуальных растений.
Степень повреждения после послевсходового применения глифосата и гербицидов на основе имидазолинона
Степень повреждения после предвсходового применения глифосата и гербицидов на основе имидазолинона
Эти результаты показывают, что гербициды на основе имидазолинона можно использовать для контроля устойчивых к глифосату сорных растений и сельскохозяйственных культур или в предвсходовый период, или в послевсходовый период. Одним преимуществом является способность использовать гербициды на основе имидазолинона на растениях события 127 для контроля невосприимчивых сорных и нежелательных растений, для контроля которых глифосат более не является эффективным.
Пример 4D: Повышенное получение сои с использованием события 127 сои
Полевые испытания проводили для оценки агрономических, фенотипических и фенологических характеристик трансгенной линии сои с устойчивостью к гербицидам на основе имидазолинона (событие 127) относительно нетрансгенной изогенной контрольной линии (ноль) и относительно других нетрансгенных (традиционных) сортов сои (проверочные испытания). С этой целью исследования проводили на полевых участках в Бразилии, которые представляют собой типичные площади для коммерческого получения сои и на которых адаптируют все генотипы.
Пять обработок повторяли четыре раза в полностью рандомизированном блочном плане на всех полевых участках (таблица 22). Каждая делянка состояла из шести грядок длиной 8 м с расстоянием между грядками 0,5 м на одной и той же делянке и 1,0 м между грядок соседней делянки. Фенотипические и агрономические параметры определяли на растениях в пределах 3-й и 4-й грядок.
Пять способов обработки, включенные в исследования по оценке, представляли комбинацию конкретных генотипов сои и гербицидных составов (гербициды на основе имидазолинона и неимидозалиноновые гербициды), необходимую для получения соответствующих данных для выполнения задач исследования.
Два способа гербицидной обработки использовали в этих анализах: 1) имазапир, распыленный в количестве 70 г д.в./га, и 2) Volt, комбинация бентазона (400 г д.в./га) и ацифлуорфена (170 г д.в./га), распыленного в количестве 570 г д.в./га. Различные соевые генотипы и гербицидные составы комбинировали для получения пяти способов обработки (таблица 22). Эти пять способов обработки (T1, T2, T3, T4, T5) представляли собой полную реплику в схеме опыта.
Способы экспериментальной обработки (табличные данные) включенные в каждое полевое испытание сои
Экспериментальные растения высевали на семи экспериментальных станциях в Бразилии (таблица 23). Станции расположены в областях, которые представляют собой типичные площади для получения сои, и площади, на которых адаптируют генотипы сои. Все участки имели сертификат качества биобезопасности (CQB), налаженную инфраструктуру, лабораторное оборудование и полевую аппаратуру, и персонал, с опытом работы в области исследований в сельском хозяйстве и владеющий основами биобезопасности.
Фенотипическое, фенологическое и агрономическое сходство видов растений события 127, изогенного контроля и проверочного испытания определяли посредством регистрации различных характеристик, обычно используемых для описания фенотипа и свойств генотипа сои. Характеристики регистрировали на всех делянках всех участков (если не указано иначе). Тест Тьюки использовали для сравнения значений среднего для источников изменчивости, определенных ANOVA для получения достоверного эффекта от конкретной характеристики.
В виде среднего среди участков, результаты для События 127 с имазапиром (T1) или с Volt (T2) и результаты для изогенной контрольной линии с имазапиром (T3) не значимо различались по всхожести, полной густоте слияния растений, зеленому стеблю, полеганию, суткам до цветения, суткам до созревания или по снятию урожая (таблица 24). T1 значимо отличались от T3 только по высоте растения и размеру семян, а T2 значимо отличался от T3 только по размеру семян. Кроме того, ни одно из различий в значениях среднего для способов обработки участков с T1 и T2 не являлись существенно значимыми (таблица 24).
Средние значения для способов обработки участка по каждому оцениваемому признаку
*T1 = BPS-CV-127-9, обработанный имазапиром, T2 = BPS-CV-127-9, обработанный Volt, T3 = контрольная изолинии, обработанная Volt, T4 = Monsoy 8001, обработанная Volt, T5 = Coodetec 217, обработанная Volt.
§ Средние значения с последующим обозначением таким символом с 5% вероятностью не отличаются значимо по тесту Тьюки.
Результаты этого исследования показывают, что линии сои, содержащие событие 127, можно использовать для сохранения урожайности после применения гербицидов на основе имидазолинона с остаточной активностью, на уровне, эквивалентном другим коммерческим сортам в отсутствие применения такого гербицида.
Пример 5: Основанный на электрофорезе в геле анализ ПЦР для качественной специфичной детекции события 127
Способ качественного анализа ПЦР, основанного на электрофорезе в геле, разработали для использования в детекции нуклеиновых кислот события 127 в образцах семени и зерна. Способом могли детектировать 0,05% ДНК сои события 127 в смеси с ДНК нетрансгенной сои.
Образцы семени и зерна измельчали в 25 мл в стакане для измельчения в течение 30 секунд при 30 Гц, используя мельницу с мешалкой ММ 400 (Retsch; Haan, Germany), для получения гомогенного порошка. Геномную ДНК экстрагировали из 0,1-1 г образцов измельченного зерна, используя буфер CTAB (цетил-триметил аммония бромид), с последующей экстракцией смесью хлороформ:октанол и спиртовым осаждением. Полученный в результате осадок растворяли, и оставшиеся ингибиторы удаляли анионообменной хроматографией, используя колонку с безнапорным течением Genomic-tip 20/G (Qiagen; Hilden, Germany).
Концентрацию и чистоту ДНК анализировали спектрофотометром Nanodrop ND-1000 (Peqlab Biotechnologie; Erlangen, Germany), определяя отношение поглощения света в образце на длине волны 260 и 280 нм (A260/280) и на 260 и 230 нм (A260/230). ДНК, имеющую значение отношения A260/280, близкое к 1,8, а значение отношения A260/230 выше, чем 1,8, отбирали для последующей ПЦР.
Другой набор праймеров получали для амплификации специфичного участка события 127, и ген, специфичный для генома сои, использовали в качестве эндогенного контроля. Специфичный к событию анализ ПЦР нацелен на уникальный для события 127 трансгенный участок соединения между вставкой и природной геномной ДНК сои. Все реакции ПЦР-амплификации выполняли в T1 Thermal Cycler (Biometra; Gottingen, Germany). Сто нанограмм геномной ДНК использовали в качестве матрицы в каждой из реакций ПЦР.
Специфичную к геному сои систему ПЦР для детектирования гена лектина (Lei) Glycine max (соя), (GenBank входящий номер № K00821) использовали в качестве калибровочной системы. Последовательности праймера и условия циклов ПЦР для реакции ПЦР гена лектина адаптировали Hird et al. (J. AOAC Int., 86:66-71 (2003)). Последовательности праймеров представляли собой SoyLec-F (5'-TGGTCGCGCCCTCTACTC) (SEQ ID NO:65) и SoyLec-R (5'-GGCGAAGCTGGCAACG) (SEQ ID NO:66). Праймеры разработали для амплификации фрагмента, специфичного к участку генома сои размером 70 пар нуклеотидов (п.н.).
Реакции ПЦР для эндогенных контролей выполняли в 20 мкл суммарного объема с 100 нг геномной ДНК, 200 мкМ dNTP, 2 мМ MgCl2, 500 нм каждого праймера и 1 единицей ДНК полимеразы Taq на реакцию. После начальной стадии денатурации в течение 2 минут при 94°C, выполняли 32 цикла при 94°C в течение 30 секунд, 60°C в течение 30 секунд и 72°C в течение 30 секунд, с последующей финальной стадией удлинения в течение 1 минуты при 72°C.
Реакции с использованием упомянутых выше праймеров и условий реакции проводили с отдельными образцами ДНК, полученными из риса (Oryza sativa), рапсового семени (Brassica napus), хлопка (Gossypium hirsutum, 2 различных линии), кукурузы (Zea mays), сои Conquista, сои события 127, и без добавления матрицы ДНК (в качестве контроля), и наносили на агарозный гель. Продукт в 70 пар нуклеотидов получали в образцах ДНК из растений сои (Conquista и событие 127), в то время как никаких продуктов амплификации не получали в других образцах. Таким образом, контрольные праймеры к эндогенному гену способны специфично детектировать геномную ДНК сои.
Специфичный к событию анализ для события 127 сои создан на основе участка соединения 5' вставки и геномной ДНК сои. Участок связывания прямого праймера расположен в пределах природной геномной ДНК сои (127-61F: 5'-GGGCAAACTAGTCTCGTAATATAT) (SEQ ID NO:67), а участок связывания с обратным праймером расположен на вставке 127 (127-176R: 5'-CGGAATTGGTAATCGAAATT) (SEQ ID NO:68). В реакции подвергается амплификации фрагмент размером 116 пар нуклеотидов (п.н.).
Специфичность праймеров, специфичных к событию (127-61F и 127-176R), определили, используя 100 нг геномной ДНК (из риса (Oryza sativa), рапсового семени (Brassica napus), хлопка (Gossypium hirsutum), кукурузы (Zea mays), сои GTS 40-3-2, сои 305423, сои 356043, сои A2704-12, сои Conquista, сои события 127, и контроль без добавления матрицы). Специфичные к событию реакции ПЦР выполняли в 20 мкл суммарного объема с 100 нг матрицы ДНК, 200 мкМ dNTP, 2 мМ MgCl2, 500 нм каждого праймера и 1 единицей ДНК полимеразы Taq на реакцию. После начальной стадии денатурации в течение 2 минут при 94°C, выполняли 32 цикла при 94°C в течение 30 секунд, 56°C в течение 30 секунд и 72°C в течение 30 секунд, с последующей финальной стадией удлинения в течение 1 минуты при 72°C.
Отсутствие или наличие события 127 сои в образцах определяли разделением амплифицированных фрагментов ПЦР размером 116 п.н., специфичных для события 127, в окрашенном бромистым этидием 4% агарозном геле.
Фрагмент ПЦР размером 116 п.н., специфичный для события 127, получали во всех реакциях, соответствующих образцам сои события 127, в то время как ни в одном из других образцов не получали фрагмента ПЦР, специфичного для события 127. Таким образом, праймеры, специфичные к событию, 127-61F и 127-176R, способны специфично детектировать ДНК из растений сои события 127. Поиск нуклеотидной последовательности с использованием специфичной для события амплифицированной последовательности ампликона с использованием анализа DNA-DNA Basic Local Alignment Search Tool (BLASTN) не идентифицировал 100% идентичных совпадений.
Для определения предела детекции в реакциях с использованием праймеров 127-61F и 127-176R разработали стандарты, содержащие определенное количество ДНК события 127 (100%, 1%, 0,5%, 0,1%, 0,05% и 0%), с последующим разведением ДНК события 127 ДНК Conquista. Для каждого разведения выполняли ПЦР-амплификации, с повторением 22 раза, используя условия, обсужденные выше. Для проверки чистоты реактивов выполняли по одному контролю на систему, без ДНК-матрицы (NTC).
Продукты реакции ПЦР, специфичной к событию 127 (фрагмент 116 п.н.), детектировали во всех разведениях, тестируемых в диапазоне от 0,05% до 100% ДНК события 127. Как и ожидалось, в специфичной к геному сои ПЦР-амплификации не детектировали специфичные полосы события 127 в нетрансгенных образцах сои или в контролях, не содержащих матрицу (NTC), хотя все образцы нетрансгенной сои показали наличие способной к амплификации ДНК посредством наличия расчетного ампликона. Самое меньшее количество ДНК события 127 в образце, которое можно достоверно детектировать, используя праймеры 127-61F и 127-176R, составляет 0,05%.
Специфичная к событию ПЦР с использованием праймеров 127-61F и 127-176R демонстрирует относительный LOD <0,1% с 95% достоверностью. Кроме того, праймеры 127-61F и 127-176R не способны амплифицировать какие-либо детектируемые ПЦР-продукты в значении 0% события 127 (100% нетрансгенная соя) или в контрольных реакциях без добавления матрицы.
Для определения влияния различных температур отжига в ПЦР-реакциях, четыре образца (0%, 0,05%, 1% и 100% ДНК события 127 сои, разведенная нетрансгенной соевой ДНК Conquista) анализировали в экспериментах с трехкратным повторением с температурами отжига 54°C и 58°C. Результаты показывают, что температуры отжига, отклоняющаяся от оптимальной температуры отжига на ±2°C, приводит к 100% правильной детекции специфичной ДНК события 127.
Для оценки влияния различных платформ ПЦР, три образца (0,05%, 1% и 100% ДНК события 127 сои, разведенная нетрансгенной соевой ДНК Conquista) анализировали в экспериментах с трехкратным повторением, используя систему для ПЦР в реальном времени ABI 7500 Fast (Applied Biosystems; Darmstadt, Germany). Образец с 0% события 127 (100% ДНК Conquista) и образец без добавления ДНК-матрицы включали в качестве контролей.
Результаты демонстрируют хорошее проведение специфичного к событию 127 анализа ПЦР с использованием праймеров 127-61F и 127-176R в различных приборах для проведения ПЦР. Относительный предел определения составил 0,05% во всех трех реакциях. Как и ожидалось, ПЦР-продуктов не обнаруживали в образцах, содержащих 0% ДНК события 127 в сопутствующей ДНК нетрансгенной сои, или контролях, не содержащих матрицу.
Для оценки воспроизводимости анализов в пределах лабораторий (междулабораторная взаимозаменяемость), в различных лабораториях проводили два независимых эксперимента. Различные образцы, содержащие от 0,05% до 100% количества ДНК события 127 в сопутствующей нетрансгенной ДНК сои, анализировали с двухкратным повторением в двух независимых экспериментах с использованием 100 нг геномной ДНК на реакцию в DNA Engine Dyad thermal cycler (BioRad; Мюнхен, Германия). Результаты показывают хорошую воспроизводимость анализа в пределах лабораторий (междулабораторная взаимозаменяемость). Результаты показали 100% положительные результаты в образцах со 100%, 1% и 0,5% количеством ДНК события 127. Кроме того, по меньшей мере 95% положительные результаты получали для образцов с 0,1% и 0,05% количеством ДНК события 127 (при условии, что относительный LOD≤0,05%), и не получали положительных результатов для образцов с 0% количеством ДНК события 127 или в контролях, не содержащих матрицу.
Качественный, специфичный к событию, основанный на электрофорезе в геле способ детекции посредством ПЦР с использованием праймеров 127-61F и 127-176R способен детектировать специфичную целевую последовательность события 127 в смеси с 0,05% ДНК события 127 в сопутствующей ДНК нетрансгенной сои. Ни в одном из образцов, содержащих только ДНК нетрансгенной сои или другие трансгенные события, не получали детектируемого ПЦР-продукта, специфичного для события 127, что тем самым экспериментально демонстрирует специфичность способа.
Пример 6: Улучшенная жизнеспособность растений с использованием события 127 сои с комбинацией имидазолинонов и стробилуринов
Растения сои события 127 обрабатывали (1) имидазолиноновым гербицидом или гербицидами, (2) фунгицидом на основе стробилурина и (3) комбинацией имидазолинонового гербицида или гербицидами вместе с фунгицидом на основе стробилурина.
Растения сои события 127 выращивали на делянках диаметром 25 см с 5 растениями на делянку. Различные варианты применения гербицид(ов) и/или фунгицида (описаны ниже в таблице X) имели место на 23 сутки после посева для способов обработки 1-16 и на 24 сутки после посева для способов обработки 17-32.
На 1, 7 и 14 сутки после применения (DAA), растения оценивали на фототоксичность, мощность, высоту растения, относительную величину фотосинтеза, относительную величину SPAD (т.е. относительный параметр листа хлорофилл/зеленость) и устьичную проводимость.
Как показано в таблице 26 ниже, добавление пираклостробина к различным способам обработки с имазапиком или имазапик плюс имазапир значительно увеличивает общий фотосинтез, увеличивает общее позеленение растений (относительная величина SPAD), и повышает устьичную проводимость относительно некоторых способов обработки без пираклостробина в некоторые моменты времени.
Это показывает, что комбинация пироклостробина с ингибирующим AHAS гербицидом (или гербицидами) обеспечивает неожиданное преимущество для растений сои события 127.
| название | год | авторы | номер документа |
|---|---|---|---|
| ДЕТЕКТИРОВАНИЕ AAD-12-СОБЫТИЯ 416 У СОИ | 2010 |
|
RU2573898C2 |
| УСТОЙЧИВЫЙ К НАСЕКОМЫМ-ВРЕДИТЕЛЯМ И ТОЛЕРАНТНЫЙ К ГЕРБИЦИДАМ СЕЛЕКЦИОННЫЙ ГИБРИД ТРАНСФОРМАНТА СОИ pDAB9582.814.19.1 и pDAB4468.04.16.1 | 2012 |
|
RU2627161C2 |
| ЛИНИИ ТРАНСГЕННОЙ СОИ, ГЕНЕТИЧЕСКОЕ СОБЫТИЕ 8264.42.32.1, УСТОЙЧИВОЕ К ГЕРБИЦИДАМ С ПАКЕТИРОВАННЫМИ ГЕНАМИ НА ЕГО ОСНОВЕ, И ИХ ДЕТЕКТИРОВАНИЕ | 2012 |
|
RU2636021C2 |
| ПАКЕТИРОВАННОЕ СОБЫТИЕ 8264.44.06.1 С УСТОЙЧИВОСТЬЮ К ГЕРБИЦИДАМ, СВЯЗАННЫЕ ТРАНСГЕННЫЕ ЛИНИИ СОИ И ИХ ДЕТЕКТИРОВАНИЕ | 2011 |
|
RU2608650C2 |
| ОБЪЕКТ СОИ 9582.814.19.1, ПРИДАЮЩИЙ УСТОЙЧИВОСТЬ К НАСЕКОМЫМ И УСТОЙЧИВОСТЬ К ГЕРБИЦИДАМ | 2012 |
|
RU2628099C2 |
| РЕЗИСТЕНТНЫЙ К НАСЕКОМЫМ И УСТОЙЧИВЫЙ К ГЕРБИЦИДАМ ТРАНСФОРМАНТ СОИ рDAB9582.816.15.1 | 2013 |
|
RU2650626C2 |
| ДЕТЕКЦИЯ AAD-1 ОБЪЕКТА DAS-40278-9 | 2010 |
|
RU2577143C2 |
| ТРАНСГЕННЫЙ ОБЪЕКТ СОИ MON 87708 И СПОСОБЫ ЕГО ПРИМЕНЕНИЯ | 2010 |
|
RU2624025C2 |
| ПОСЛЕДОВАТЕЛЬНОСТЬ НУКЛЕИНОВОЙ КИСЛОТЫ ДЛЯ ВЫЯВЛЕНИЯ РАСТЕНИЯ СОИ DBN8002 И СПОСОБ ЕЕ ВЫЯВЛЕНИЯ | 2019 |
|
RU2818368C2 |
| РАСТЕНИЕ КУКУРУЗЫ DBN9858, УСТОЙЧИВОЕ К ГЕРБИЦИДУ, И НУКЛЕОТИДНАЯ ПОСЛЕДОВАТЕЛЬНОСТЬ И СПОСОБ ДЛЯ ЕЕ ВЫЯВЛЕНИЯ | 2016 |
|
RU2712730C2 |




























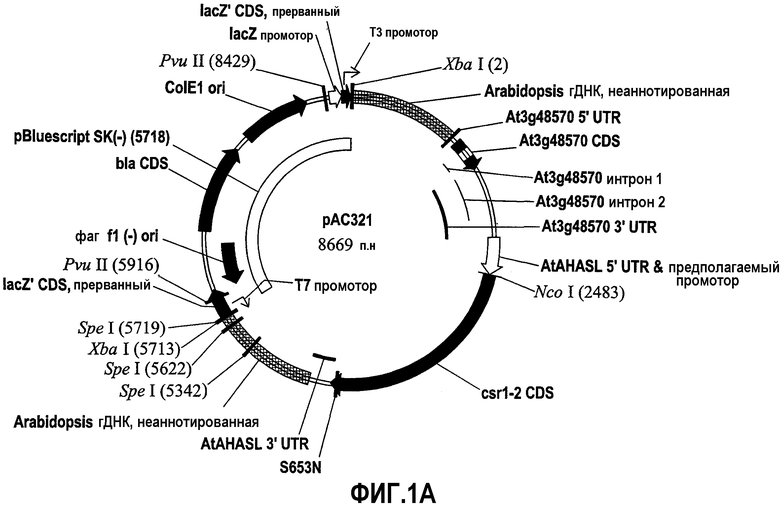
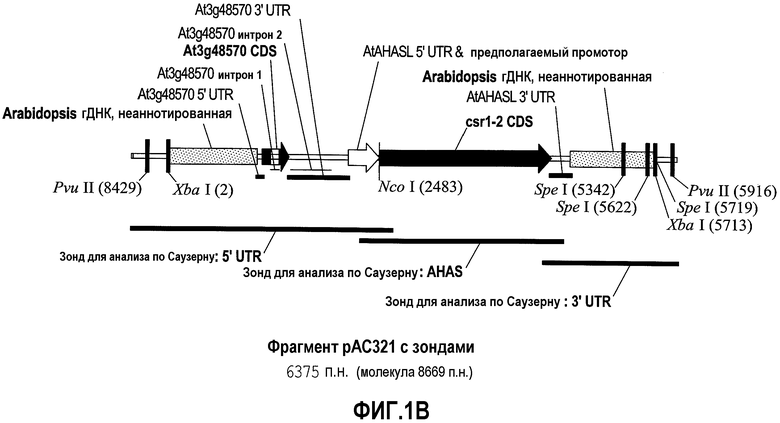
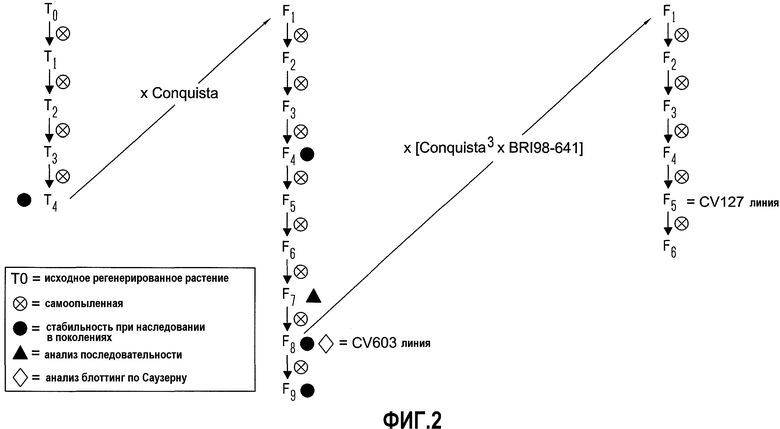



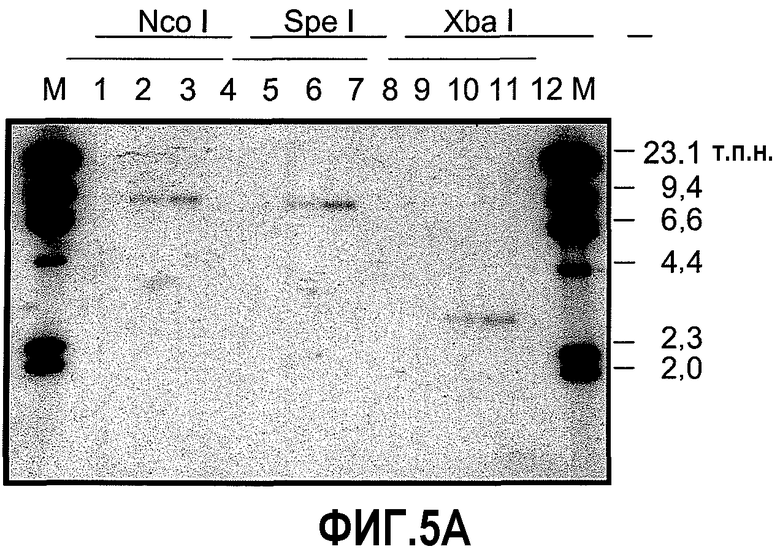
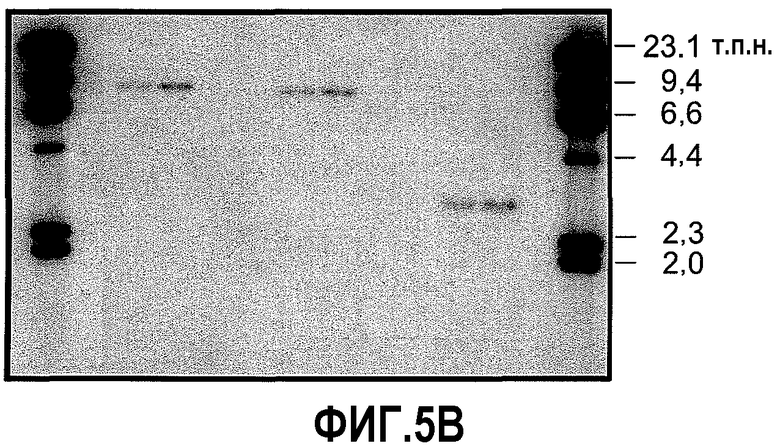
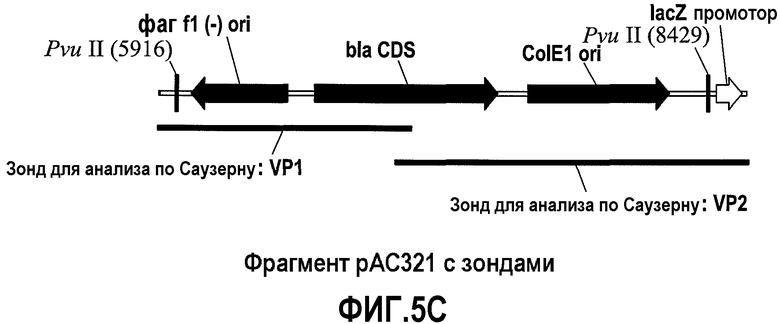
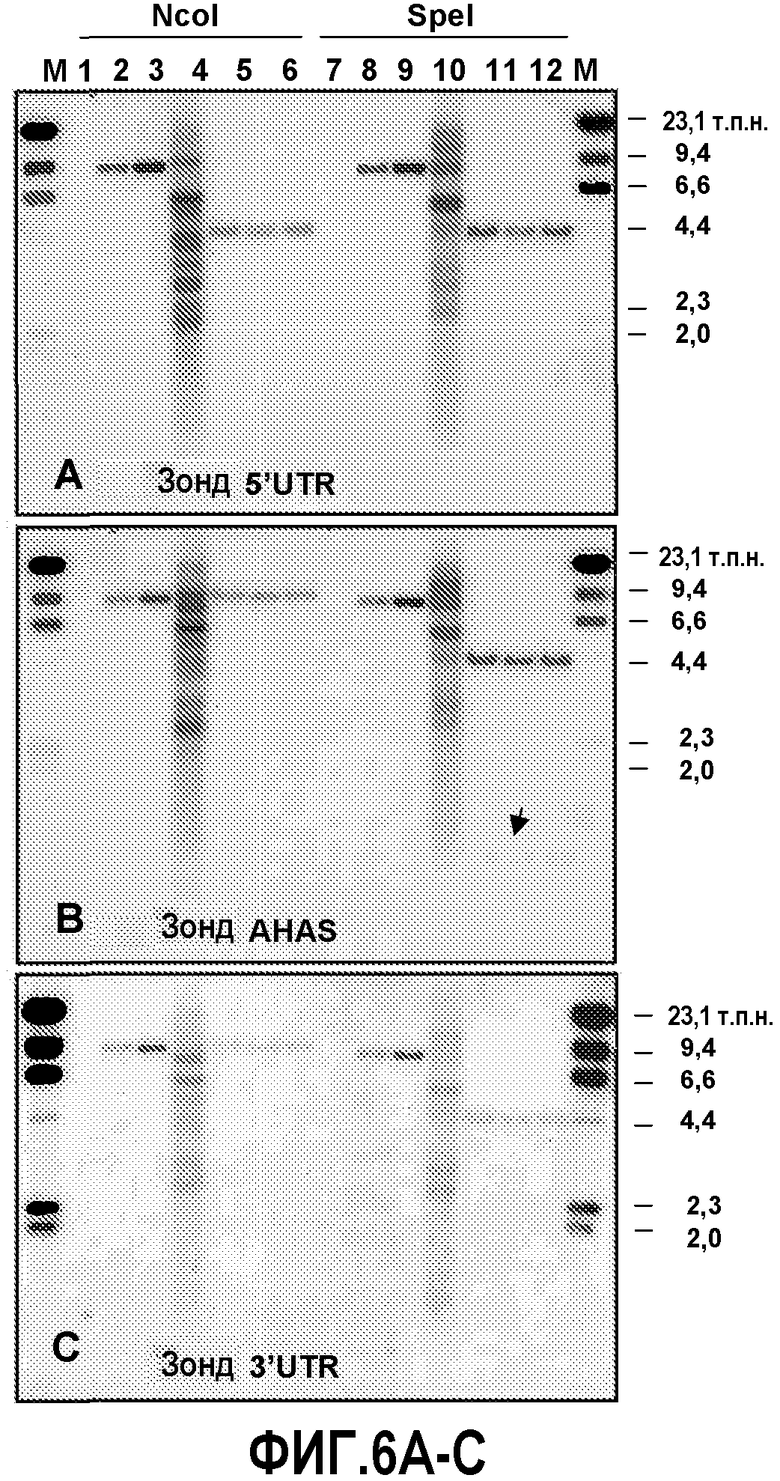
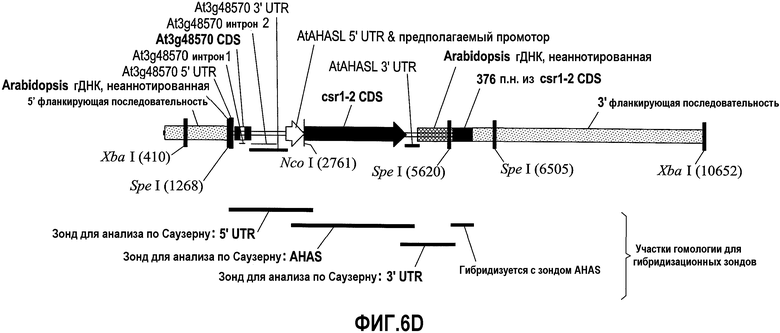
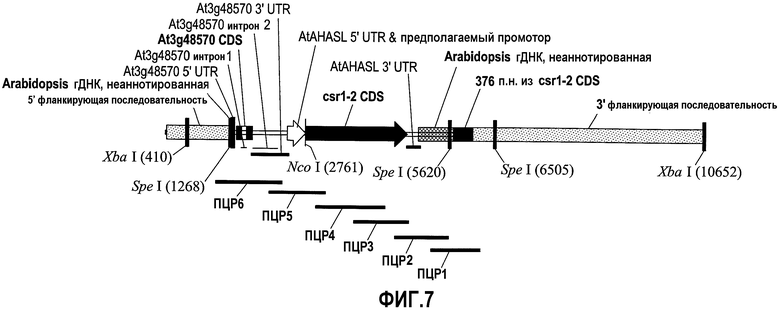




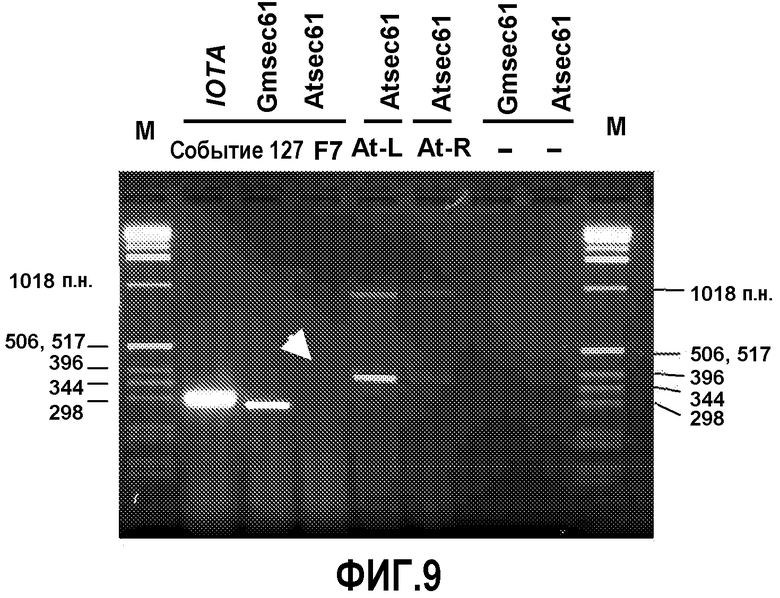
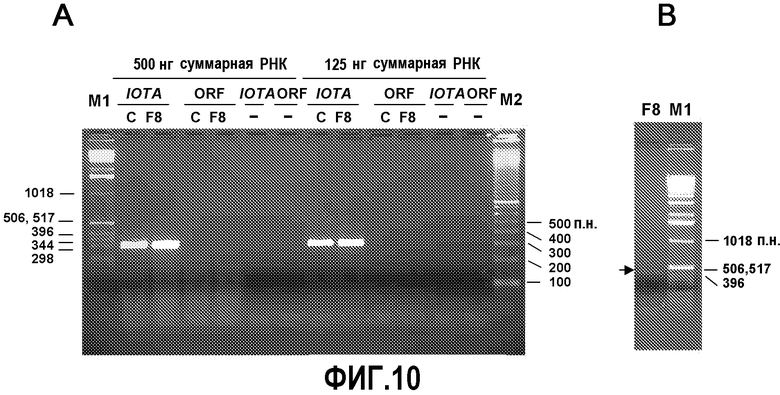



Изобретение относится к области биохимии, в частности к способу борьбы с сорными растениями на посевной площади, а также к способу борьбы с устойчивыми к глифосату сорными растениями на посевной площади, которые включают применение эффективного количества ингибирующего AHAS гербицида на посевной площади с произрастающим на ней растением сои. Также раскрыта выделенная молекула нуклеиновой кислоты, кодирующая модифицированную форму белка AHASL, содержащую замену серина на аспарагин в положении 653 (S653N), трансгенное растение сои, семя и часть растения, ее содержащие, выделенная пара нуклеиновокислотных праймеров для ее амплификации и способ выявления присутствия молекулы нуклеиновой кислоты с ее помощью. Раскрыта конструкция рекомбинантной нуклеиновой кислоты для получения растения, устойчивого к ингибирующему AHAS гербициду. Также раскрыт способ повышения урожайности растения сои на посевной площади, включающий применение эффективного количества ингибирующего AHAS гербицида на растениях сои. Изобретение позволяет эффективно бороться с устойчивыми к глифосату сорными растениями на посевной площади. 15 н. и 15 з.п. ф-лы, 12 ил., 26 табл., 6 пр.
1. Способ борьбы с сорными растениями на посевной площади, включающий:
применение эффективного количества ингибирующего AHAS гербицида на посевной площади с растением сои, содержащим молекулу нуклеиновой кислоты, которая характеризуется последовательностью нуклеиновой кислоты, представленной положениями 1312-6069 SEQ ID NO: 1, где эффективное количество ингибирует рост сорных растений и борется с ростом соевых растений дикого типа на посевной площади.
2. Способ по п. 1, где ингибирующий AHAS гербицид представляет собой гербицид на основе имидазолинона.
3. Способ по п. 2, где гербицид на основе имидазолинона представляет собой имазапир, имазапик или любую их комбинацию.
4. Способ по п. 1, дополнительно включающий применение на посевной площади эффективного количества гербицида, выбранного из группы, состоящей из ингибирующих EPSPS гербицидов, ингибирующих GS гербицидов, ингибирующих РРО гербицидов, ауксиновых гербицидов и их комбинаций.
5. Способ по п. 1, где сорные растения являются устойчивыми к глифосату.
6. Способ по п. 1, дополнительно включающий применение стробилурина на посевной площади.
7. Способ по п. 6, где стробилурин представляет собой пираклостробин.
8. Способ по п. 1, где применение эффективного количества ингибирующего AHAS гербицида включает применение эффективного количества гербицидной композиции, которая включает
имазапир;
имазапик;
или любое из следующего:
комбинация имазапира и имазапика;
комбинация имазапира, имазапика и бентазона;
комбинация имазапира, имазапика и пироклостробина;
комбинация имазапира, имазапика и сафлуфенацила;
комбинация имазапира, имазапика, сафлуфенацила и глифосата;
комбинация имазапира и бентазона;
комбинация имазапира и пироклостробина;
комбинация имазапира и сафлуфенацила;
комбинация имазапира, сафлуфенацила и глифосата;
комбинация имазапира и глифосата;
комбинация имазапика и глифосата; и
комбинация имазапика, сафлуфенацила и глифосата;
или дополнительно включает применение эффективного количества комбинации сафлуфенацила и глифосата.
9. Способ борьбы с устойчивыми к глифосату сорными растениями на посевной площади, включающий:
применение эффективного количества ингибирующего AHAS гербицида на посевной площади с произрастающим на ней растением сои, содержащим молекулу нуклеиновой кислоты, характеризуемую последовательностью нуклеиновой кислоты, представленной положениями 1312-6069 SEQ ID NO: 1.
10. Способ по п. 9, где ингибирующий AHAS гербицид представляет собой имазапир, имазапик или любую их комбинацию.
11. Способ по п. 9, где способ дополнительно включает применение стробилурина на посевной площади.
12. Выделенная молекула нуклеиновой кислоты, кодирующая модифицированную форму белка AHASL, содержащую замену серина на аспарагин в положении 653 (S653N), и характеризующаяся последовательностью нуклеиновой кислоты, представленной положениями 1312-6069 SEQ ID NO: 1.
13. Конструкция рекомбинантной нуклеиновой кислоты для получения растения, устойчивого к ингибирующему AHAS гербициду, содержащая молекулу нуклеиновой кислоты, характеризующуюся последовательностью нуклеиновой кислоты, представленной положениями 1312-6069 SEQ ID NO: 1, где молекула нуклеиновой кислоты кодирует модифицированную форму белка AHASL, где белок содержит замену серина на аспарагин в положении 653 (S653N).
14. Трансгенное растение сои, содержащее выделенную молекулу нуклеиновой кислоты по п. 12, где трансгенное растение сои является устойчивым к ингибирующему AHAS гербициду.
15. Трансгенное растение сои, содержащее гетерологичную молекулу нуклеиновой кислоты, характеризуемую последовательностью нуклеиновой кислоты, представленной нуклеотидами 1312-6069 SEQ ID NO: 1, где растение сои является устойчивым к ингибирующему AHAS гербициду.
16. Выделенная пара нуклеиновокислотных праймеров для применения в амплификации целевой молекулы нуклеиновой кислоты по п. 12, содержащая:
первую выделенную молекулу нуклеиновой кислоты, характеризующуюся фланкирующей областью генома сои последовательности нуклеиновой кислоты SEQ ID NO: 1, и вторую выделенную молекулу нуклеиновой кислоты, характеризующуюся областью обратной комплементарной последовательности нуклеиновой кислоты, представленной нуклеотидами с 1312 по 6069 SEQ ID NO: 1, где:
первая выделенная молекула нуклеиновой кислоты характеризуется последовательностью нуклеиновой кислоты SEQ ID NO: 37, и вторая выделенная молекула нуклеиновой кислоты характеризуется последовательностью нуклеиновой кислоты SEQ ID NO: 38;
первая выделенная молекула нуклеиновой кислоты характеризуется последовательностью нуклеиновой кислоты SEQ ID NO: 39, и вторая выделенная молекула нуклеиновой кислоты характеризуется последовательностью нуклеиновой кислоты SEQ ID NO: 40;
первая выделенная молекула нуклеиновой кислоты характеризуется последовательностью нуклеиновой кислоты SEQ ID NO: 41, и вторая выделенная молекула нуклеиновой кислоты характеризуется последовательностью нуклеиновой кислоты SEQ ID NO: 42;
первая выделенная молекула нуклеиновой кислоты характеризуется последовательностью нуклеиновой кислоты SEQ ID NO: 43, и вторая выделенная молекула нуклеиновой кислоты характеризуется последовательностью нуклеиновой кислоты SEQ ID NO: 44; или
первая выделенная молекула нуклеиновой кислоты характеризуется последовательностью нуклеиновой кислоты SEQ ID NO: 67, и вторая выделенная молекула нуклеиновой кислоты характеризуется последовательностью нуклеиновой кислоты SEQ ID NO: 68.
17. Выделенная пара нуклеиновокислотных праймеров по п. 16, где первая выделенная молекула нуклеиновой кислоты характеризуется последовательностью нуклеиновой кислоты SEQ ID NO: 41, и вторая выделенная молекула нуклеиновой кислоты характеризуется последовательностью нуклеиновой кислоты SEQ ID NO: 42.
18. Способ выявления присутствия молекулы нуклеиновой кислоты, характеризующейся последовательностью нуклеиновой кислоты, представленной положениями 1312-6069 SEQ ID NO: 1, в биологическом образце, включающий:
(а) получение смеси, содержащей биологический образец, который содержит ДНК сои, первый нуклеиновокислотный праймер, характеризующийся 5′ частью фланкирующей области сои, характеризующейся последовательностью нуклеиновой кислоты, представленной нуклеотидами 1-1311 SEQ ID NO: 1, и второй нуклеиновокислотный праймер, характеризующийся областью обратной комплементарной последовательности нуклеиновой кислоты, представленной нуклеотидами с 1312 по 6069 SEQ ID NO: 1, где:
первый нуклеиновокислотный праймер характеризуется последовательностью нуклеиновой кислоты SEQ ID NO: 37, и второй нуклеиновокислотный праймер характеризуется последовательностью нуклеиновой кислоты SEQ ID NO: 38;
первый нуклеиновокислотный праймер характеризуется последовательностью нуклеиновой кислоты SEQ ID NO: 39, и второй нуклеиновокислотный праймер характеризуется последовательностью нуклеиновой кислоты SEQ ID NO: 40;
первый нуклеиновокислотный праймер характеризуется последовательностью нуклеиновой кислоты SEQ ID NO: 41, и второй нуклеиновокислотный праймер характеризуется последовательностью нуклеиновой кислоты SEQ ID NO: 42;
первый нуклеиновокислотный праймер характеризуется последовательностью нуклеиновой кислоты SEQ ID NO: 43, и второй нуклеиновокислотный праймер характеризуется последовательностью нуклеиновой кислоты SEQ ID NO: 44; или
первый нуклеиновокислотный праймер характеризуется последовательностью нуклеиновой кислоты SEQ ID NO: 67, и второй нуклеиновокислотный праймер характеризуется последовательностью нуклеиновой кислоты SEQ ID NO: 68;
(b) проведение реакции в смеси в условиях, которые позволяют первому и второму нуклеиновокислотным праймерам амплифицировать молекулу нуклеиновой кислоты; и
(c) выявление наличия или отсутствия амплифицированной молекулы нуклеиновой кислоты, где наличие амплифицированной молекулы нуклеиновой кислоты указывает на то, что биологический образец содержит молекулу нуклеиновой кислоты, характеризующуюся последовательностью нуклеиновой кислоты, представленной положениями 1312-6069 SEQ ID NO: 1.
19. Способ выявления присутствия молекулы нуклеиновой кислоты, характеризующейся последовательностью нуклеиновой кислоты, представленной положениями 1312-6069 SEQ ID NO: 1, в биологическом образце, включающий:
(a) получение смеси, содержащей биологический образец, который содержит ДНК сои, и молекулу нуклеиновокислотного зонда, которая способна гибридизоваться с молекулой нуклеиновой кислоты, характеризующейся последовательностью нуклеиновой кислоты, представленной положениями 1312-6069 SEQ ID NO: 1;
(b) проведение реакции в смеси в условиях, которые позволяют молекуле нуклеиновокислотного зонда гибридизоваться с молекулой нуклеиновой кислоты, характеризующейся последовательностью нуклеиновой кислоты, представленной положениями 1312-6069 SEQ ID NO: 1; и
(c) выявление гибридизации зонда с ДНК, где наличие гибридизации молекулы нуклеиновокислотного зонда с ДНК сои указывает на присутствие в биологическом образце молекулы нуклеиновой кислоты, характеризующейся последовательностью нуклеиновой кислоты, представленной положениями 1312-6069 SEQ ID NO: 1.
20. Способ по любому из пп. 18 и 19, где указанный биологический образец содержит семена сои.
21. Способ по любому из пп. 18 и 19, где указанный биологический образец содержит часть растения сои.
22. Способ повышения урожайности растения сои на посевной площади, включающий:
применение эффективного количества ингибирующего AHAS гербицида на одном или нескольких растениях сои, содержащих молекулу нуклеиновой кислоты, характеризующейся последовательностью нуклеиновой кислоты, представленной положениями 1312-6069 SEQ ID NO: 1, и на посевной площади, где ингибирующий AHAS гербицид уменьшает рост сорных растений на посевной площади; и
сбор семян с одного или нескольких растений сои;
где повышение урожайности растения или растений сои является результатом уменьшенного роста сорняков на посевной площади, которые могли бы конкурировать с растением или растениями сои.
23. Способ разведения растения сои, устойчивого к ингибирующему AHAS гербициду, включающий:
(a) скрещивание растения сои, содержащего молекулу нуклеиновой кислоты, характеризующуюся последовательностью нуклеиновой кислоты, представленной положениями 1312-6069 SEQ ID NO: 1, со вторым растением сои;
(b) получение семян из скрещивания стадии (а);
(c) получение из семян образца ДНК;
(d) выявление наличия молекулы нуклеиновой кислоты, характеризующейся последовательностью нуклеиновой кислоты, представленной положениями 1312-6069 SEQ ID NO: 1 в образце, где наличие молекулы нуклеиновой кислоты, характеризующейся последовательностью нуклеиновой кислоты, представленной положениями 1312-6069 SEQ ID NO: 1, указывает на то, что из семени способно вырасти растение сои, устойчивое к ингибирующему AHAS гербициду; и
(e) выбор семян для дополнительного скрещивания, если молекула нуклеиновой кислоты выявлена в образце ДНК.
24. Семя трансгенного растения сои, содержащее молекулу нуклеиновой кислоты, кодирующую модифицированную форму белка AHASL, который содержит замену серина на аспарагин в положении 653 (S653N), где:
молекула нуклеиновой кислоты характеризуется последовательностью нуклеиновой кислоты, представленной положениями 1312-6069 SEQ ID NO: 1; и
семя трансгенного растения сои является устойчивым к ингибирующему AHAS гербициду.
25. Семя по п. 24, где молекула нуклеиновой кислоты характеризуется последовательностью нуклеиновой кислоты SEQ ID NO: 1.
26. Семя по п. 25, где указанное семя является семенем растения линии «BPS-CV127-9» или растения, являющегося его потомством, где типичный образец семени указанной линии депонирован под номером доступа NCIMB №41603.
27. Семя по п. 24, где семя обработано гербицидом, ингибирующим AHAS, или комбинацией гербицидов, ингибирующих AHAS.
28. Способ борьбы с сорными растениями на посевной площади, включающий:
нанесение эффективного количества ингибирующего AHAS гербицида на посевную площадь путем посадки семян по п. 27 на посевной площади, где эффективное количество будет препятствовать росту сорняков и будет контролировать рост растений сои дикого типа на посевной области.
29. Трансгенное растение сои, содержащее молекулу нуклеиновой кислоты, кодирующую модифицированную форму белка AHASL, содержащую замену серина на аспарагин в положении 653 (S653N), полученное посредством проращивания семени по п. 24, где:
молекула нуклеиновой кислоты характеризуется последовательностью нуклеиновой кислоты, представленной положениями 1312-6069 SEQ ID NO: 1; и
трансгенное растение сои является устойчивым к ингибирующему AHAS гербициду.
30. Часть трансгенного растения сои, содержащая молекулу нуклеиновой кислоты, кодирующую модифицированную форму белка AHASL, содержащую замену серина на аспарагин в положении 653 (S653N), полученная посредством проращивания семени по п. 24, где:
молекула нуклеиновой кислоты характеризуется последовательностью нуклеиновой кислоты, представленной положениями 1312-6069 SEQ ID NO: 1; и
часть трансгенного растения сои является устойчивой к ингибирующему AHAS гербициду.
| WO 2008124495 А2, 16.10.2008 | |||
| TAN S | |||
| et al., Herbicidal inhibitors of amino acid biosynthesis and herbicide-tolerant crops, Amino Acids, 2006, Volume 30, Issue 2, pp | |||
| Регулятор давления для автоматических тормозов с сжатым воздухом | 1921 |
|
SU195A1 |
| CHANG A.K | |||
| et al., Herbicide-resistant forms of Arabidopsis thaliana acetohydroxyacid synthase: characterization of the catalytic properties and sensitivity to inhibitors of | |||
Авторы
Даты
2016-02-10—Публикация
2010-01-06—Подача