Перекрестные ссылки на смежные заявки
Настоящая заявка представляет собой частичное продолжение заявки на патент США № 11/617346, поданной 28 декабря 2006 г., которая испрашивает приоритет по предварительной заявке на патент США № 60/754366, поданной 28 декабря 2005 г., содержание которых полностью включено в настоящий документ путем ссылки.
Область применения изобретения
Настоящее изобретение относится к области клеточной или регенеративной терапии для пациентов с заболеванием периферических сосудов, особенно пациентов с ишемией периферических сосудов. Более конкретно, в настоящем изобретении предложены клетки, полученные из ткани пуповины, обладающие способностью стимулировать и поддерживать ангиогенез, улучшать кровоток, регенерировать, восстанавливать и улучшать состояние скелетных мышц, поврежденных в результате периферического ишемического события, и защищать скелетные мышцы от ишемического повреждения.
Предпосылки создания изобретения
В настоящем описании цитируются различные публикации, включая патенты, опубликованные заявки на патенты, технические статьи и научные статьи. Каждая из этих цитируемых публикаций полностью включена в настоящий документ путем ссылки.
Заболевание периферических сосудов (ЗПС) может представлять собой результат атеросклеротической окклюзии кровеносных сосудов, особенно в конечностях и удаленных от сердца областях, приводящей к ухудшению кровотока и недостаточной перфузии кислорода в тканях рядом или ниже по току крови от места окклюзии. ЗПС часто проявляется в кровеносных сосудах подвздошной области, бедренных и подколенных кровеносных сосудах и подключичных кровеносных сосудах, и его эффекты могут дополнительно усугубляться тромбами, эмболами или травмами. Согласно оценкам, в США ЗПС страдают приблизительно от 8 до 12 миллионов человек, особенно люди пожилого возраста и с сахарным диабетом.
Распространенные симптомы ЗПС включают в себя судороги в верхних и нижних конечностях, кистях и стопах, онемение, слабость, мышечную усталость, боли в конечностях, кистях и стопах, гипотермию в конечностях, кистях и стопах, нарушение окраски кожи кистей и стоп, ощущение сухости или шелушение кожи и гипертензию. Самым распространенным симптомом являются хромота или ощущение боли, скованность и спастические боли в местах ниже по току крови от места окклюзии в кровеносном сосуде, которые проявляются при некоторых формах физической нагрузки, таких как ходьба, но проходят сами после периода отдыха.
В терминах патофизиологии окклюзия кровеносных сосудов приводит к ишемии ткани в месте окклюзии и рядом с ним. Эту ишемию по существу называют ишемией периферических сосудов, имея в виду, что она проявляется в местах, дистальных по отношению к сердцу. Степень тяжести ишемии определяется размером и количеством окклюзий, степенью близости места окклюзии к мышце или органу и наличием достаточной дублирующей сосудистой системы. В более тяжелых случаях ишемия приводит к отмиранию затронутых тканей и может привести к ампутации пораженных конечностей или даже смерти пациента.
Используемые в настоящее время способы лечения более тяжелых случаев ЗПС включают в себя курсы химиотерапии, ангиопластику, вставку стентов, восстановительную хирургию, установку обходных сосудистых шунтов, иссечение пораженной ткани или ампутацию. К сожалению, у многих пациентов такие вмешательства приводят лишь к частичному успеху, и многие пациенты испытывают ухудшение своего состояния или симптомов.
В настоящее время существует интерес к использованию либо стволовых клеток, которые способны делиться и дифференцироваться, либо мышечных клеток из других источников, включая клетки гладкой и скелетной мускулатуры, чтобы способствовать восстановлению или обращению повреждения ткани. Трансплантацию стволовых клеток можно использовать в качестве клинического инструмента для восстановления целевой ткани, восстанавливая посредством этого ее физиологическую и анатомическую функциональность. Область применения технологии стволовых клеток очень широка и включает в себя технологии культивирования тканей, доставку агентов генной терапии и клеточных терапевтических агентов, т.е. доставку биотерапевтических агентов в целевую область с использованием экзогенно вводимых живых клеток или клеточных компонентов, которые содержат или вырабатывают такие агенты (обзор приведен в работе Tresco, P. A. et al., (2000 г.) Advanced Drug Delivery Reviews, 42: 2-37). Обнаружение стволовых клеток способствовало появлению исследований, направленных на селективное получение конкретных типов клеток для восстановительной медицины.
Одним препятствием к реализации терапевтического потенциала технологии стволовых клеток является трудность получения достаточного количества стволовых клеток. Один источник стволовых клеток представляет собой эмбриональные ткани или ткани плода. Эмбриональные стволовые клетки и клетки-предшественники выделены из ряда видов млекопитающих, включая людей, и для нескольких типов таких клеток продемонстрирована способность к самообновлению и размножению, а также дифференцированию по нескольким различным клеточным линиям дифференцирования. Однако получение стволовых клеток из эмбриональных тканей или тканей плода породило множество этических и моральных вопросов, которые желательно избегать путем выявления других источников мультипотентных или плюрипотентных клеток.
Ткани из послеродового материала, такого как пуповина и плацента, привлекли к себе интерес в качестве альтернативного источника стволовых клеток. Например, описаны способы извлечения стволовых клеток путем перфузии плаценты или сбора из крови или ткани пуповины. Ограничения этих способов получения стволовых клеток заключались в неадекватном объеме крови пуповины или количества получаемых клеток, а также неоднородности или отсутствии характеризации популяций клеток, полученных из этих источников.
Надежный, хорошо охарактеризованный и обильный источник по существу однородных популяций таких клеток, способных к дифференцированию по различным линиям дифференцирования клеток скелетной мышечной ткани, периваскулярных клеток или васкулярных клеток, будет эффективным во множестве диагностических и терапевтических приложений для восстановления, регенерации и улучшения скелетной мускулатуры, для стимулирования и/или поддержки ангиогенеза и для улучшения кровотока после периферического ишемического события, особенно у пациентов с ЗПС.
Изложение сущности изобретения
В одном аспекте настоящего изобретения описан способ лечения пациента с заболеванием периферических сосудов, включающий введение пациенту клеток, полученных из ткани пуповины, в количестве, эффективном для лечения заболевания периферических сосудов, причем клетки, полученные из ткани пуповины, получены из ткани пуповины человека по существу без крови, и причем клетки способны к самообновлению и размножению в культуре и имеют потенциал для дифференцирования в клетки по меньшей мере фенотипов клеток скелетных мышц, клеток гладких мышц сосудов, периваскулярных клеток или клеток эндотелия сосудов; причем для роста клеткам необходим L-валин, и клетки могут расти в атмосфере с содержанием кислорода по меньшей мере приблизительно 5%; причем клетки дополнительно обладают по меньшей мере одной из следующих характеристик: (a) потенциал к по меньшей мере приблизительно 40 удвоениям в культуре; (b) закрепление и размножение на поверхности сосуда для культивирования ткани с покрытием или без покрытия, причем сосуд для культивирования с покрытием содержит покрытие из желатина, ламинина, коллагена, полиорнитина, витронектина или фибронектина; (c) выработка по меньшей мере одного из тканевого фактора, виментина и альфа-актина гладких мышц; (d) выработка по меньшей мере одного из CD10, CD13, CD44, CD73, CD90, PDGFr-альфа, PD-L2 и HLA-A,B,C; (e) отсутствие выработки по меньшей мере одного из CD31, CD34, CD45, CD80, CD86, CD117, CD141, CD178, B7-H2, HLA-G и HLA-DR,DP,DQ по результатам анализа с использованием проточной цитометрии; (f) экспрессия гена, которая, по сравнению с клеткой человека, представляющей собой фибробласт, мезенхимальную стволовую клетку или клетку костного мозга гребня подвздошной кости, повышена для по меньшей мере одного из генов, кодирующих: интерлейкин-8; ретикулон 1; CXCL1 (хемокиновый (мотив C-X-C) лиганд 1/стимулятор активности роста меланомы, альфа); CXCL6 (хемокиновый (мотив C-X-C) лиганд 6/белок хемотаксиса гранулоцитов 2); CXCL3 (хемокиновый (мотив C-X-C) лиганд 3); TNFAIP3 (индуцируемый фактором некроза опухоли альфа белок 3); (g) экспрессия гена, которая, по сравнению с клеткой человека, представляющей собой фибробласт, мезенхимальную стволовую клетку или клетку костного мозга гребня подвздошной кости, понижена для по меньшей мере одного из генов, кодирующих: SHOX2 (содержащий гомеобокс ген низкорослости 2); HSPB2 (27 кДа белок теплового шока 2); CXCL12 (хемокиновый (мотив C-X-C) лиганд 12/стромальный фактор 1); эластин (надклапанный аортальный стеноз, синдром Вильямса-Бойрена); мРНК Homo sapiens; кДНК DKFZp586M2022 (из клона DKFZp586M2022); Meox2 (содержащий мезенхимальный гомеобокс гена 2, содержащий гомеобокс блокировки роста ген); SIX1 (гомолог содержащего гомеобокс гена sine oculis 1) (Drosophila); кристаллин, альфа B; DAAM2 (ассоциированный с белком Disheveled активатор морфогенеза 2); белок DKFZP586B2420; аналог нейтралина 1; тетранектин (связывающийся с плазминогеном белок); STAC (ген, содержащий домен src-гомологии 3 (SH3) и богатый цистеином домен); холестерин-25-гидроксилазу; RUNX3 (связанный с карликовостью фактор транскрипции 3); рецептор интерлейкина-11, альфа; PCOLCE (усилитель проколлаген-C-эндопептидазы); FZD7 (гомолог frizzled 7) (Drosophila); гипотетический ген BC008967; коллаген, тип VIII, альфа 1; TNC (тенасцин C, гексабрахион); IRX5 (содержащий гомеобокс IRX белок 5); гефестин; интегрин, бета 8; SV2A (гликопротеин синаптического пузырька 2); NBL1 (нейробластома, ген подавления онкогенности 1); IGFBP2 (связывающийся с инсулиноподобным фактором роста белок 2, 36 кДа); кДНК Homo sapiens FLJ12280 fis, клон MAMMA1001744; CRLF1 (подобный цитокиновому рецептору фактор 1); KCNN4 (активируемый кальцием калиевый канал средней/низкой проводимости, подсемейство N, член 4); интегрин, бета 7; транскрипционный коактиватор с мотивом связывания с PDZ (TAZ); SIX2 (гомолог содержащего гомеобокс гена sine oculis 2) (Drosophila); белок KIAA1034; VAMP5 (везикуло-ассоциированный мембранный белок 5/миобревин); EFEMP1 (содержащий EGF фибулин-подобный белок внеклеточного матрикса 1); EGR3 (белок раннего ростового ответа 3); DLX5 (содержащий гомеобокс distal-less гена 5); гипотетический белок FLJ20373; AKR1C3 (альдокеторедуктаза семейства 1, член C3/3-альфа-гидроксистероиддегидрогеназа, тип II); бигликан; транскрипционный коактиватор с мотивом связывания с PDZ (TAZ); фибронектин 1; проэнкефалин; интегрин, бета-подобный 1 (с доменами EGF-подобных повторов); мРНК Homo sapiens, полноразмерная вставка кДНК, клон EUROIMAGE 1968422; EphA3; белок KIAA0367; NPR3 (рецептор натрийуретического пептида C/гуанилатциклаза C/рецептор атрионатрийуретического пептида C); гипотетический белок FLJ14054; мРНК Homo sapiens; кДНК DKFZp564B222 (из клона DKFZp564B222); BNIP3L (ген белка, подобного белку 3, взаимодействующему с BCL2/белком аденовируса E1B 19 кДа); AE-связывающий белок 1; COX7A1 (полипептид 1 субъединицы VIIa цитохром c оксидазы) (мышечный); аналог нейтралина 1; BTG1 (ген транслокации B-клеток 1); гипотетический белок FLJ23191; и DKFZp586L151, (h) секреция по меньшей мере одного из MCP-1, IL-6, IL-8, GCP-2, HGF, KGF, FGF, HB-EGF, BDNF, TPO, MIP1b, RANTES и TIMP1; и (i) отсутствие секреции по меньшей мере одного из TGF-бета2, ANG2, PDGFbb, MIP1a и VEGF по результатам ИФА.
В конкретном варианте осуществления заболевание периферических сосудов представляет собой ишемию периферических сосудов. В определенных вариантах осуществления перед введением пациенту клетки индуцируют in vitro для дифференцирования по линиям дифференцирования клеток скелетных мышц, клеток гладких мышц сосудов, периваскулярных клеток или клеток эндотелия сосудов. В других вариантах осуществления клетки модифицируют методами генной инженерии для выработки продукта гена, который способствует лечению заболевания периферических сосудов.
В некоторых вариантах осуществления способа клетки вводят с клетками по меньшей мере одного другого типа, которые могут включать в себя клетки скелетных мышц, клетки-предшественники клеток скелетных мышц, клетки гладких мышц сосудов, клетки-предшественники клеток гладких мышц сосудов, периваскулярные клетки, клетки эндотелия сосудов, клетки-предшественники клеток эндотелия сосудов или другие мультипотентные или плюрипотентные стволовые клетки. Клетки другого типа можно вводить одновременно либо до, либо после клеток, полученных из ткани пуповины.
В других вариантах осуществления клетки вводят по меньшей мере с одним другим агентом, который может представлять собой, например, антитромбогенный агент, противовоспалительный агент, иммуносупрессорный агент, иммуномодулирующий агент, проангиогенный агент или антиапоптозный агент. Другой агент можно вводить одновременно либо до, либо после клеток, полученных из ткани пуповины.
Клетки предпочтительно вводят непосредственно в месте или рядом с местом ишемического повреждения периферических сосудов, но их также можно вводить в местах, дистальных к местам ишемического повреждения периферических сосудов. Клетки можно вводить путем инъекции, инфузии, имплантации устройства пациенту, либо путем имплантации содержащих клетки матрицы или каркаса. Клетки могут оказывать трофическое действие, такое как пролиферация, на мышечную мускулатуру, гладкую мускулатуру сосудов или эндотелий сосудов пациента. Клетки могут индуцировать миграцию клеток скелетных мышц, клеток гладких мышц сосудов, клеток эндотелия сосудов, клеток-предшественников клеток скелетных мышц, периваскулярных клеток, клеток-предшественников клеток гладких мышц сосудов или клеток-предшественников клеток эндотелия сосудов к месту или местам заболевания периферических сосудов, такого как ишемия периферических сосудов.
В другом аспекте настоящего изобретения описаны фармацевтические композиции и наборы для лечения пациента с заболеванием периферических сосудов, содержащие фармацевтически приемлемый носитель и описанные выше клетки, полученные из ткани пуповины, или препараты из таких клеток, полученных из ткани пуповины. В некоторых предпочтительных вариантах осуществления такие препараты содержат FGF и HGF. Фармацевтические композиции и наборы разработаны и/или приготовлены для реализации на практике способов, составляющих предмет настоящего изобретения, как описано выше.
В соответствии с другим аспектом настоящего изобретения описанные выше способы можно применять на практике с использованием препарата, изготовленного из клеток, полученных из ткани пуповины, причем препарат содержит клеточный лизат клеток, полученных из ткани пуповины, внеклеточный матрикс клеток, полученных из ткани пуповины, или кондиционированную среду, в которой выращивали клетки, полученные из ткани пуповины. Такие препараты предпочтительно содержат FGF и HGF.
В других аспектах настоящего изобретения описаны фармацевтические композиции и наборы, в состав которых входят препараты, содержащие клеточные лизаты, внеклеточные матриксы или кондиционированную среду клеток, полученных из ткани пуповины.
Один вариант осуществления настоящего изобретения представляет собой способ лечения пациента с заболеванием периферических сосудов, включающий введение фармацевтической композиции, содержащей фибриновый клей и выделенную однородную популяцию клеток, полученных из ткани пуповины человека, в количестве, эффективном для лечения такого заболевания, причем ткань пуповины по существу свободна от крови, и причем выделенная однородная популяция клеток способна к самообновлению и размножению в культуре, имеет потенциал для дифференцирования и не экспрессирует CD117 и/или теломеразу. Выделенная популяция клеток также может обладать одной или более из следующих характеристик:
(a) экспрессирует рецептор окисленных липопротеинов низкой плотности 1, ретикулон, лиганд хемокинового рецептора 3 и/или гранулоцитарный хемотаксический белок;
(b) не экспрессирует CD31, CD34 или CD45;
(c) экспрессирует, по отношению к фибробластам, мезенхимальным стволовым клеткам или клеткам костного мозга гребня подвздошной кости человека, повышенные уровни интерлейкина-8 или ретикулона 1;
(d) имеет потенциал для дифференцирования в клетки по меньшей мере фенотипов клеток скелетных мышц, клеток гладких мышц сосудов, периваскулярных клеток или клеток эндотелия сосудов; и
(е) экспрессирует CD10, CD13, CD44, CD73 и CD90.
В одном варианте осуществления заболевание периферических сосудов представляет собой ишемию периферических сосудов. Фармацевтическую композицию вводят в местах ишемического повреждения периферических сосудов. В другом варианте осуществления фармацевтическую композицию вводят локально. В одном варианте осуществления фармацевтическую композицию вводят путем инъекции, инфузии, имплантации устройства пациенту либо путем имплантации матрицы или каркаса, содержащих фармацевтическую композицию. В альтернативном варианте осуществления фармацевтическую композицию вводят путем внутримышечной инъекции и инъекции в жировые депо в мышцах. В другом варианте осуществления фармацевтическую композицию вводят путем инъекции в интерстициальное пространство таким образом, чтобы композиция не попадала напрямую в кровоток. Выделенную популяцию клеток перед введением пациенту можно индуцировать in vitro для дифференцирования по линиям дифференцирования клеток скелетных мышц, клеток мышц сосудов, периваскулярных клеток или клеток эндотелия сосудов. Популяцию клеток также можно модифицировать методами генной инженерии для выработки продукта гена, который способствует лечению заболевания периферических сосудов. Композиция необязательно дополнительно содержит агент, выбранный из группы, состоящей из антитромбогенного агента, иммуносупрессорного агента, иммуномодулирующего агента, проангиогенного агента, антиапоптозного агента и их смесей. В альтернативном варианте осуществления композиция дополнительно содержит клетки по меньшей мере одного другого типа (такие как, например, клетки скелетных мышц, клетки-предшественники клеток скелетных мышц, клетки гладких мышц сосудов, клетки-предшественники клеток гладких мышц сосудов, периваскулярные клетки, клетки эндотелия сосудов, клетки-предшественники клеток эндотелия сосудов или другие мультипотентные или плюрипотентные стволовые клетки). В одном варианте осуществления фармацевтическая композиция оказывает трофическое действие (такое как, например, пролиферация клеток эндотелия сосудов). В другом варианте осуществления фармацевтическая композиция индуцирует миграцию клеток эндотелия сосудов и/или клеток-предшественников клеток эндотелия сосудов к местам заболевания периферических сосудов. В другом альтернативном варианте осуществления фармацевтическая композиция индуцирует миграцию клеток гладких мышц сосудов и/или клеток-предшественников клеток гладких мышц сосудов к местам заболевания периферических сосудов. В другом варианте осуществления фармацевтическая композиция индуцирует миграцию периваскулярных клеток к местам заболевания периферических сосудов. В одном варианте осуществления фибриновый клей содержит фибриноген и тромбин. В другом варианте осуществления фибриновый клей содержит от приблизительно 16 до приблизительно 24 МЕ/мл тромбина и от приблизительно 39,3 до приблизительно 60,7 мг/мл фибриногена.
Другой вариант осуществления настоящего изобретения представляет собой способ лечения пациента с заболеванием периферических сосудов, включающий введение фибринового клея (например, композиции, содержащей фибриноген и тромбин) и выделенной однородной популяции клеток, полученных из ткани пуповины человека, в количестве, эффективном для лечения такого заболевания, причем ткань пуповины по существу свободна от крови, и причем выделенная однородная популяция клеток способна к самообновлению и размножению в культуре, имеет потенциал для дифференцирования и не экспрессирует CD117 и/или теломеразу. Выделенная популяция клеток может обладать другими характеристиками, включая одну или более из следующих характеристик:
(a) экспрессирует рецептор окисленных липопротеинов низкой плотности 1, ретикулон, лиганд хемокинового рецептора 3 и/или гранулоцитарный хемотаксический белок;
(b) не экспрессирует CD31, CD34 или CD45;
(c) экспрессирует, по отношению к фибробластам, мезенхимальным стволовым клеткам или клеткам костного мозга гребня подвздошной кости человека, повышенные уровни интерлейкина-8 или ретикулона 1;
(d) имеет потенциал для дифференцирования в клетки по меньшей мере фенотипов клеток скелетных мышц, клеток гладких мышц сосудов, периваскулярных клеток или клеток эндотелия сосудов; и
(е) экспрессирует CD10, CD13, CD44, CD73 и CD90.
В одном варианте осуществления заболевание периферических сосудов представляет собой ишемию периферических сосудов, и фибриновый клей и популяцию клеток необязательно вводят в местах ишемического поражения периферических сосудов. Можно использовать различные пути введения, включая введение путем инъекции, инфузии, имплантации устройства пациенту либо путем имплантации содержащих клетки матрицы или каркаса. В одном варианте осуществления популяцию клеток и фибриновый клей вводят локально (например, путем внутримышечной инъекции и инъекции в жировые депо в мышцах). В другом варианте осуществления клетки и фибриновый клей вводят путем инъекции в интерстициальное пространство таким образом, чтобы они попадали напрямую в кровоток. Выделенную популяцию клеток перед введением пациенту необязательно индуцируют in vitro для дифференцирования по линиям дифференцирования клеток скелетных мышц, клеток мышц сосудов, периваскулярных клеток или клеток эндотелия сосудов. Популяцию клеток также можно модифицировать методами генной инженерии для выработки продукта гена, который способствует лечению заболевания периферических сосудов. В одном варианте осуществления способ дополнительно содержит введение агента, выбранного из группы, состоящей из антитромбогенного агента, иммуносупрессорного агента, иммуномодулирующего агента, проангиогенного агента, антиапоптозного агента и их смесей. В другом варианте осуществления способ дополнительно содержит введение клеток по меньшей мере одного другого типа (таких как, например, клетки скелетных мышц, клетки-предшественники клеток скелетных мышц, клетки гладких мышц сосудов, клетки-предшественники клеток гладких мышц сосудов, периваскулярные клетки, клетки эндотелия сосудов, клетки-предшественники клеток эндотелия сосудов или другие мультипотентные или плюрипотентные стволовые клетки). В одном варианте осуществления популяция клеток оказывает трофическое действие (такое как, например, пролиферация клеток эндотелия сосудов). Популяция клеток может индуцировать миграцию клеток эндотелия сосудов и/или клеток-предшественников клеток эндотелия сосудов к местам заболевания периферических сосудов. В альтернативном варианте осуществления популяция клеток может индуцировать миграцию клеток гладких мышц сосудов и/или клеток-предшественников клеток гладких мышц сосудов к местам заболевания периферических сосудов. Популяция клеток также может индуцировать миграцию периваскулярных клеток к местам заболевания периферических сосудов. Фибриновый клей может содержать фибриноген и тромбин. В одном варианте осуществления фибриновый клей вводят одновременно либо до, либо после введения выделенной однородной популяции клеток, полученных из ткани пуповины человека. В другом варианте осуществления фибриновый клей содержит от приблизительно 16 до приблизительно 24 МЕ/мл тромбина и от приблизительно 39,3 до приблизительно 60,7 мг/мл фибриногена.
Другой вариант осуществления настоящего изобретения представляет собой набор для лечения пациента с заболеванием периферических сосудов, содержащий фибриноген, тромбин и выделенную однородную популяцию клеток, полученных из ткани пуповины человека, в количестве, эффективном для лечения такого заболевания, причем ткань пуповины по существу свободна от крови, и причем указанная выделенная однородная популяция клеток способна к самообновлению и размножению в культуре, имеет потенциал для дифференцирования и не экспрессирует CD117 и/или теломеразу. Набор может дополнительно содержать инструкцию по применению. В одном варианте осуществления фибриноген и выделенная однородная популяция клеток представлены в виде композиции, к которой непосредственно перед использованием можно добавить тромбин. Выделенная популяция клеток может обладать другими характеристиками, включая одну или более из следующих характеристик:
(a) экспрессирует рецептор окисленных липопротеинов низкой плотности 1, ретикулон, лиганд хемокинового рецептора 3 и/или гранулоцитарный хемотаксический белок;
(b) не экспрессирует CD31, CD34 или CD45;
(c) экспрессирует по отношению к фибробластам, мезенхимальным стволовым клеткам или клеткам костного мозга гребня подвздошной кости человека повышенные уровни интерлейкина-8 или ретикулона 1;
(d) имеет потенциал для дифференцирования в клетки по меньшей мере фенотипов клеток скелетных мышц, клеток гладких мышц сосудов, периваскулярных клеток или клеток эндотелия сосудов; и
(е) экспрессирует CD10, CD13, CD44, CD73 и CD90.
В одном варианте осуществления набор содержит от приблизительно 16 до приблизительно 24 МЕ/мл тромбина и от приблизительно 39,3 до приблизительно 60,7 мг/мл фибриногена. В одном варианте осуществления набор содержит фибриногенный компонент, содержащий фибрин и фактор XII, и тромбиновый компонент, содержащий тромбин и кальций.
Другие характеристики и преимущества настоящего изобретения станут понятны после изучения следующего подробного описания и примеров.
Краткое описание чертежей
На фигуре 1 показан эффект клеток, полученных из ткани пуповины человека (hUTC), партия № 120304, мезенхимальных стволовых клеток (MSC) и фибробластов на пролиферацию клеток эндотелия. Клетки эндотелия высевали на дно 24-луночной чашки Петри с плотностью 5000 клеток/см2 (10000 клеток/лунку), и клетки hUTC (партия № 120304), клетки MSC или фибробласты высевали во вкладыши трансвел с плотностью 5000 клеток/см2 (1650 клеток/вкладыш) в среде для совместного культивирования (среда Хейфлика 80% + среда EGM-2MV 20% или среда Хейфлика 50% + среда EGM-2MV 50%). После 7 суток совместного культивирования клетки собирали и подсчитывали при помощи анализатора Guava®. Кроме того, клетки эндотелия также поддерживали в среде EGM-2MV в качестве положительного контроля. A, клетки HUVEC (клетки эндотелия пупочной вены человека). B, клетки HCAEC (клетки эндотелия коронарной артерии человека). C, клетки HIAEC (клетки эндотелия подвздошной артерии человека).
На фигуре 2 показан эффект клеток hUTC (партия № 120304) и нейтрализующих антител на пролиферацию клеток эндотелия. Клетки HUVEC или HCAEC высевали на дно 24-луночной чашки Петри с плотностью 5000 клеток/см2 (10000 клеток/лунку), и клетки hUTC (партия № 120304) высевали во вкладыши трансвел с плотностью 5000 клеток/см2 (1650 клеток/вкладыш) в среде для совместного культивирования (среда Хейфлика 50% + EGM-2MV 50%). В это же время также добавляли нейтрализующие антитела к FGF (7 мкг/мл), HGF (1 мкг/мл) или VEGF (1 мкг/мл). После 7 суток совместного культивирования клетки собирали и подсчитывали при помощи анализатора Guava®. Кроме того, клетки эндотелия также поддерживали в среде EGM-2MV в качестве положительного контроля. На фигуре показаны результаты для клеток, обработанных только фактором роста и фактором роста плюс нейтрализующие антитела. A и B, клетки HUVEC. C и D, клетки HCAEC.
На фигуре 3 показан эффект клеточного лизата клеток hUTC (партия № 120304) и нейтрализующих антител на пролиферацию клеток HUVEC. Клетки HUVEC высевали на дно 24-луночной чашки Петри с плотностью 5000 клеток/см2 (10000 клеток/лунку) в среде EGM-2MV на 8 часов. Затем клетки переводили в бессывороточную среду путем инкубации в течение ночи в 0,5 мл среды EGM-2MV, содержащей 0,5% FBS и не содержащей факторов роста. После этого добавляли FBS, свежеприготовленные клеточные лизаты клеток hUTC (партия № 120304) и нейтрализующие антитела к FGF (7 мкг/мл) или HGF (1 мкг/мл). После 4 суток культивирования клетки собирали и подсчитывали при помощи анализатора Guava®. Светло-серыми столбиками показаны результаты для контролей в чистой среде. Серыми столбиками показаны результаты для клеток HUVEC, инкубированных с лизатом, содержащим 62,5 мкг белка. Темно-серыми столбиками показаны результаты для клеток HUVEC, инкубированных с лизатом, содержащим 125 мкг белка.
На фигуре 4 показан эффект клеток hUTC и клеток MSC на миграцию клеток эндотелия. Клетки HUVEC или HCAEC высевали во вкладыши трансвел с плотностью 5000 клеток/см2 (23000 клеток/вкладыш), и клетки hUTC (партия № 120304) или клетки MSC высевали на дно 6-луночной чашки Петри с плотностью 5000 клеток/см2 (48000 клеток/лунку) в среде для совместного культивирования (среда Хейфлика 50% + EGM-2MV 50%). После 7 суток совместного культивирования клетки, оказавшиеся с нижней стороны вкладыша трансвел, собирали и подсчитывали при помощи анализатора Guava®. Кроме того, клетки эндотелия также поддерживали в среде EGM-2MV в качестве контроля. A, клетки HUVEC. B, клетки HCAEC.
На фигуре 5 показан эффект клеток hUTC (партия № 120304) и нейтрализующих антител на миграцию клеток эндотелия. Клетки HUVEC или HCAEC высевали во вкладыши трансвел с плотностью 5000 клеток/см2 (23000 клеток/вкладыш), и клетки hUTC (партия № 120304) высевали на дно 6-луночной чашки Петри с плотностью 5000 клеток/см2 (48000 клеток/лунку) в среде для совместного культивирования (среда Хейфлика 50% + EGM-2MV 50%). В это же время добавляли нейтрализующие антитела к FGF (7 мкг/мл) или HGF (1 мкг/мл). После 7 суток совместного культивирования клетки, оказавшиеся с нижней стороны вкладыша трансвел, собирали и подсчитывали при помощи анализатора Guava®. Кроме того, клетки эндотелия также поддерживали в среде EGM-2MV в качестве контроля. A, клетки HUVEC. B, клетки HCAEC.
На фигуре 6 показаны данные по перфузии, полученные с использованием лазерной доплеровской визуализации (LDI), из эксперимента с мышами линии NSG в исследовании, раскрытом в примере 5. Данные представлены в виде среднего значения ±СПС. Идентификация точек данных представлена в легенде. Цифры в скобках указывают на (1) P<0,001 по сравнению с соответствующим контролем; (2) P<0,05 по сравнению с клетками hUTC без фибрина.
На фигуре 7 показаны данные по перфузии, полученные с использованием лазерной доплеровской визуализации, из эксперимента с бестимусными мышами в исследовании, раскрытом в примере 5. Данные представлены в виде среднего значения ±СПС. Идентификация точек данных представлена в легенде. Цифры в скобках указывают на (1) P<0,001 по сравнению с соответствующим контролем; (2) P<0,05 по сравнению с клетками hUTC без фибрина.
На фигуре 8 показаны данные по перфузии, полученные с использованием лазерной доплеровской визуализации, для сравнения системной (внутривенной (в/в)), локальной (внутримышечной (в/м)) доставки и локальной доставки + фибриновый клей в исследовании, раскрытом в примере 6. Данные представлены в виде среднего значения ±СПС.
На фигуре 9 показаны данные по перфузии, полученные с использованием лазерной доплеровской визуализации, для различных доз клеток hUTC в фибриновом клее при локальной (в/м) доставке в исследовании, раскрытом в примере 6. Данные представлены в виде среднего значения ±СПС.
На фигуре 10 показаны данные по перфузии, полученные с использованием лазерной доплеровской визуализации, для сравнения системной (в/в), локальной (в/м) доставки и локальной доставки + фибриновый клей на 14 сутки после травмы в исследовании, раскрытом в примере 6. Для ясности данные представлены в виде средних значений.
На фигуре 11 показаны данные по перфузии, полученные с использованием лазерной доплеровской визуализации, для исследования, раскрытого в примере 7. Идентификация точек данных представлена в легенде. *, P<0,05; ***, P<0,001.
На фигуре 12 показана плотность капилляров в ишемизированных конечностях по сравнению с неишемизированными конечностями мышей, выживших на 21 сутки, для исследования, раскрытого в примере 7.
На фигуре 13 показана плотность артериол в ишемизированных конечностях по сравнению с неишемизированными конечностями мышей, выживших на 21 сутки, для исследования, раскрытого в примере 7.
Подробное описание изобретения
В приведенном ниже описании и формуле изобретения используются различные термины. Считается, что такие термины имеют общепринятое в данной области значение, если не указано иное. Другие специально определенные термины должны трактоваться согласно приведенным в настоящем документе определениям.
Стволовые клетки представляют собой недифференцированные клетки, определяющиеся по способности на уровне единичной клетки как самообновляться, так и дифференцироваться для получения клеток-потомков, включая самообновляющиеся клетки-предшественники, необновляющиеся клетки-предшественники и окончательно дифференцированные клетки. Стволовые клетки также характеризуются своей способностью дифференцироваться in vitro в функциональные клетки различных клеточных линий дифференцирования из множества зародышевых листков (эндодермы, мезодермы и эктодермы), а также после трансплантации давать начало тканям, происходящим от множества зародышевых листков, и способствовать образованию по существу большинства, если не всех, тканей после инъекции в бластоцисты.
По своему потенциалу развития стволовые клетки разделяются на: (1) тотипотентные; (2) плюрипотентные; (3) мультипотентные; (4) олигопотентные; и (5) унипотентные. Тотипотентные клетки способны преобразовываться во все типы эмбриональных и внеэмбриональных клеток. Плюрипотентные клетки способны преобразовываться во все типы эмбриональных клеток. Мультипотентные клетки включают в себя клетки, способные преобразовываться в подмножество клеточных линий дифференцирования, но только в пределах конкретной ткани, органа или физиологической системы. Например, гемопоэтические стволовые клетки (ГСК) могут порождать потомство, которое включает в себя ГСК (самообновление), рестриктированные олигопотентные клетки-предшественники клеток крови и все типы и элементы клеток (например, тромбоциты), представляющие собой стандартные компоненты крови. Клетки, которые являются олигопотентными, способны преобразовываться в более ограниченное подмножество клеточных линий дифференцирования, чем мультипотентные стволовые клетки. Клетки, которые являются унипотентными, способны преобразовываться в единственную клеточную линию дифференцирования (например, сперматогенные стволовые клетки).
Стволовые клетки также разделяются на категории по источнику их получения. Взрослая стволовая клетка по существу представляет собой мультипотентную недифференцированную клетку, присутствующую в ткани, содержащей множество дифференцированных типов клеток. Взрослая стволовая клетка способна к самообновлению. В нормальных условиях она также может дифференцироваться для получения специальных типов клеток ткани, в которой они находятся, а также, возможно, тканей других типов. Эмбриональная стволовая клетка представляет собой плюрипотентную клетку из внутренней клеточной массы эмбриона на стадии бластоцисты. Фетальная стволовая клетка представляет собой клетку, происходящую из тканей или мембран плода. Постнатальная стволовая клетка представляет собой мультипотентную или плюрипотентную клетку, происходящую по существу из доступной после родов внеэмбриональной ткани, а именно плаценты и пуповины. Известно, что эти клетки обладают признаками, характерными для плюрипотентных стволовых клеток, включая быструю пролиферацию и потенциал дифференцирования в клетки многих клеточных линий дифференцирования. Постнатальные стволовые клетки можно получить из крови (например, клетки, полученные из пуповинной крови) или не из крови (например, из отличных от крови тканей пуповины и плаценты).
Эмбриональную ткань, как правило, определяют как ткань, происходящую из эмбриона (что для человека обозначает срок развития от оплодотворения до приблизительно шести недель). Ткань плода обозначает ткань, происходящую из плода, что для человека обозначает срок развития от приблизительно шести недель до рождения. Внеэмбриональная ткань представляет собой ткань, связанную с эмбрионом или плодом, но не происходящую из них. Внеэмбриональные ткани включают в себя внеэмбриональные мембраны (хорион, амнион, желточный мешок и аллантоис), пуповину и плаценту (которая сама образуется из хориона и базальной отпадающей материнской плаценты).
Дифференцирование представляет собой процесс, при помощи которого неспециализированная («некоммитированная») или менее специализированная клетка приобретает характеристики специализированной клетки, например, такой как нервная клетка или мышечная клетка. Дифференцированная клетка представляет собой клетку, занявшую более специализированное («коммитированное») положение в линии дифференцирования клетки. Термин «коммитированный» применительно к процессу дифференцирования относится к клетке, в процессе дифференцирования дошедшей до момента, с которого в нормальных условиях она продолжит дифференцирование до конкретного типа клеток или подмножества типов клеток и не сможет в нормальных условиях дифференцироваться в другой тип клеток или вернуться к менее дифференцированному типу клеток. Дедифференцирование обозначает процесс, в ходе которого клетка возвращается к менее специализированному (или коммитированному) положению в линии дифференцирования клетки. В настоящем документе линия дифференцирования клетки определяет наследственность клетки, т.е. то, из каких клеток она произошла и каким клеткам она может дать начало. В линии дифференцирования клетка помещается в наследственную схему развития и дифференцирования.
В широком смысле клетка-предшественник представляет собой клетку, обладающую способностью образовывать клетки-потомки, которые будут более дифференцированными по сравнению с ней, и при этом сохраняющую способность к восполнению пула клеток-предшественников. Согласно этому определению, стволовые клетки также сами являются клетками-предшественниками, так же как и более близкие клетки-предшественники окончательно дифференцированных клеток. При описании клеток, составляющих предмет настоящего изобретения, как более подробно описано ниже, можно использовать это широкое определение клетки-предшественника. В более узком смысле клетку-предшественника часто определяют как клетку, которая является промежуточным звеном в процессе дифференцирования, т.е. она происходит из стволовой клетки и является промежуточным звеном в получении зрелого типа клеток или подмножества типов клеток. Клетки-предшественники этого типа по существу не способны к самообновлению. Таким образом, при отсылке к клетке этого типа в настоящем документе она будет называться «необновляющейся клеткой-предшественником» или «промежуточной клеткой-предшественником».
При использовании в настоящем документе фраза «дифференцируется по мезодермальной, эктодермальной или эндодермальной линии дифференцирования» относится к клетке, которая становится коммитированной конкретной мезодермальной, эктодермальной или эндодермальной линии дифференцирования соответственно. Примеры клеток, которые дифференцируются по мезодермальной линии дифференцирования или преобразуются в конкретные мезодермальные клетки, включают в себя, без ограничений, клетки, которые являются липогенными, хондрогенными, кардиогенными, дерматогенными, гемопоэтическими, гемангиогенными, миогенными, нефрогенными, урогенитогенными, остеогенными, перикардиогенными или стромальными. Примеры клеток, которые дифференцируются по эктодермальной линии дифференцирования, включают в себя, без ограничений, эпидермальные клетки, нейрогенные клетки и нейроглиагенные клетки. Примеры клеток, которые дифференцируются по эндодермальной линии дифференцирования, включают в себя, без ограничений, плеврогенные клетки, гепатогенные клетки, клетки, порождающие оболочку кишечника, и клетки, порождающие панкреогенные и спланхогенные клетки.
Клетки, используемые в настоящем изобретении, по существу называются клетками, полученными из ткани пуповины (клетки UTC или клетки hUTC). Они также могут иногда называться клетками, полученными из пуповины (клетки UDC). Кроме того, такие клетки могут быть описаны как клетки, являющиеся стволовыми клетками или клетками-предшественниками, причем последний термин используется в широком смысле. Термин «полученный из» используется для указания того, что клетки получены из их биологического источника и выращены или иным образом обработаны in vitro (например, культивированы в ростовой среде для размножения популяции и/или получения клеточной линии). Манипуляции in vitro с пуповинными стволовыми клетками и уникальные характеристики клеток, полученных из пуповины, составляющих предмет настоящего изобретения, более подробно описаны ниже.
Периваскулярные клетки, также известные в данной области как астроциты или перициты, представляют собой клетки, как правило, внедренные в базальную мембрану кровеносных микрососудов (Armulik A. et al. (2005 г.) Circ. Res. 97: 512-23), которые, помимо прочего, участвуют в коммуникации/передаче сигнала клеткам эндотелия, сужении и расширении сосудов, регуляции кровотока, формировании и развитии сети кровеносных сосудов, ангиогенезе и блокировании дифференцирования и роста эндотелия (Bergers G. et al. (2005 г.) Neuro-Oncology 7: 452-64).
Для описания клеток в процессе культивирования используются различные термины. Культура клеток по существу обозначает клетки, взятые из живого организма и выращенные в контролируемых условиях («в культуре» или «культивированные»). Первичная культура клеток обозначает культуру клеток, тканей или органов, взятых непосредственно из организма(ов) до первого пересева. Клетки размножают в культуре, когда их помещают в ростовую среду в условиях, облегчающих рост и/или деление клеток, что приводит к большей популяции клеток. При размножении клеток в культуре скорость пролиферации клеток иногда измеряют по количеству времени, которое необходимо клеткам для удвоения численности. Это время называют временем удвоения.
Клеточная линия представляет собой популяцию клеток, образованную одним или более пересевами из первичной культуры клеток. Каждый цикл пересева называют пассажем. Клетки, которые пересеивают, называются клетками, которые пассированы. Конкретная популяция клеток или клеточная линия иногда описывается или характеризуется числом выполненных с ней пассажей. Например, пассированная десять раз культивируемая популяция клеток может называться культурой P10. Первичная культура, т.е. первая культура после выделения клеток из ткани, обозначается P0. После первого пересева клетки описываются как вторичная культура (P1 или культура первого пассажа). После второго пересева клетки превращаются в третичную культуру (P2 или культура второго пассажа) и т.п. Специалист в данной области определит, что за промежуток времени между последовательными пассированиями популяция клеток может многократно удваиваться; следовательно, количество удвоений популяций в культуре больше номера пассажа. Степень размножения клеток (т.е. количество удвоений популяции) за период времени между пассированиями зависит от многих факторов, включая, без ограничений, плотность посева, тип субстрата, тип среды, условия роста и время между пассированиями.
Кондиционированная среда представляет собой среду, в которой культивировали и из которой затем удалили конкретную клетку или популяцию клеток. При культивировании в среде клетки могут секретировать клеточные факторы, которые обеспечивают трофическую поддержку для других клеток. Такие трофические факторы включают в себя, без ограничений, гормоны, цитокины, внеклеточный матрикс (ECM), белки, везикулы, антитела и гранулы. Среду, содержащую клеточные факторы, называют кондиционированной средой.
По существу трофический фактор определяют как вещество, стимулирующее выживаемость, рост, пролиферацию и/или созревание клетки или стимулирующее повышенную активность клетки.
При описании культивированных клеток позвоночных термин «старение» (также «репликативное старение» или «клеточное старение») обозначает свойство конечности клеточных культур, а именно их неспособность расти далее конечного количества удвоений популяции (иногда называется «пределом Хейфлика»). Хотя клеточное старение было впервые описано с использованием фибробластоподобных клеток, клеточное старение характерно для большинства нормальных типов клеток человека, которые можно успешно выращивать в культуре. Продолжительность жизни in vitro различных типов клеток варьируется, однако максимальная продолжительность жизни, как правило, не превышает 100 удвоений популяции (это количество удвоений, за которое все клетки в культуре состарятся, в результате чего культура полностью утратит способность к делению). Старение не зависит от хронологического времени, а измеряется количеством клеточных делений, или удвоений популяции, совершенных культурой. Таким образом, клетки, переведенные в фазу покоя путем удаления существенных факторов роста, могут возобновить свой рост и деление после обратного введения факторов роста в среду и затем могут выполнить то же количество удвоений, что и эквивалентные клетки, которые росли непрерывно. Аналогичным образом при заморозке в жидком азоте после варьируемого количества удвоений популяции и последующей разморозке и культивировании клетки совершают по существу то же количество удвоений, что и клетки, которые поддерживали в культуре в незамороженном состоянии. Старые клетки не являются мертвыми или умирающими клетками; на самом деле они устойчивы к запрограммированной смерти клетки (апоптозу) и успешно поддерживались в своем состоянии неделения до трех лет. Эти клетки совершенно живы и метаболически активны, но они не делятся. В настоящее время пока не найдено биологических, химических или вирусных агентов, способных обратить состояние неделения старых клеток.
При использовании в настоящем документе термин «ростовая среда» по существу относится к среде, достаточной для культивирования клеток, полученных из ткани пуповины. В частности, одной предпочтительной в настоящее время средой для культивирования клеток, составляющих предмет настоящего изобретения, является модифицированная по способу Дульбекко среда Игла (DMEM). Особенно предпочтительной является среда DMEM с низким содержанием глюкозы (DMEM-LG) (Invitrogen, г. Карлсбад, штат Калифорния). В среду DMEM-LG предпочтительно добавляют сыворотку, наиболее предпочтительно - фетальную бычью сыворотку или сыворотку человека. Как правило, добавляют 15% (об./об.) фетальной бычьей сыворотки (например, фетальной бычьей сыворотки определенного состава, Hyclone, г. Логан, штат Юта) вместе с антибиотиками/антимикотиками (предпочтительно 100 единиц/миллилитр пенициллина, 100 миллиграмм/миллилитр стрептомицина и 0,25 микрограмма/миллилитр амфотерицина B; Invitrogen, г. Карлсбад, штат Калифорния) и 0,001% (об./об.) 2-меркаптоэтанола (Sigma, г. Сент-Луис, штат Миссури). В некоторых случаях используют другие ростовые среды или добавляют в них другие компоненты, обычно они указаны в тексте в качестве добавок в ростовую среду. В определенных химически определенных средах клетки можно выращивать вообще без наличия сыворотки. В таких случаях клеткам могут потребоваться определенные факторы роста, которые можно добавить в среду для поддержки и подпитывания клеток. В настоящее время предпочтительные факторы для добавления при выращивании в бессывороточной среде включают в себя один или более из bFGF, EGF, IGF-I и PDGF. В более предпочтительных вариантах осуществления в бессывороточную или химически определенную среду добавляют два, три или все четыре фактора. В других вариантах осуществления для поддержания или улучшения роста клеток в бессывороточную среду добавляют фактор, ингибирующий лейкоз (LIF).
Также в описании настоящего изобретения термин «стандартные условия роста» обозначает культивирование клеток при температуре 37°C в стандартной атмосфере, содержащей 5% CO2. Относительную влажность поддерживают на уровне приблизительно 100%. Хотя описанные выше условия можно использовать при культивировании клеток, следует понимать, что специалист в данной области, принимая во внимание возможности культивирования клеток, известные в данной области, вполне может варьировать такие условия.
Термин «эффективное количество» относится к концентрации или количеству соединения, материала или композиции, как описано в настоящем документе, которое позволяет эффективно достигать определенного биологического результата. Такие результаты включают в себя, без ограничений, регенерацию, восстановление или улучшение скелетной ткани, улучшение кровотока и/или стимулирование и/или поддержку ангиогенеза у пациентов с ишемией периферических сосудов. Такую эффективную активность можно получить, например, путем введения пациентам с ишемией периферических сосудов клеток и/или композиций, составляющих предмет настоящего изобретения. В отношении клеток, полученных из ткани пуповины, которые вводят пациенту in vivo, эффективное количество может означать диапазон от нескольких сотен или менее до нескольких миллионов или более. В конкретных вариантах осуществления эффективное количество может находиться в диапазоне от 103 до 1011, более конкретно составлять по меньшей мере приблизительно 104 клеток. Следует понимать, что количество вводимых клеток будет варьироваться в зависимости от конкретного расстройства, лечение которого проводится, включая, без ограничений, размер или общий объем/площадь обрабатываемой поверхности и степень близости места введения к обрабатываемому участку, наряду с другими факторами, знакомыми медицинскому биологу.
Термины «лечить» или «лечение» относятся к любому успеху или признаку успеха в ослаблении симптомов или облегчении травмы, патологии или состояния, включая любые объективные или субъективные параметры, такие как ослабление боли, ремиссия, ослабление симптомов или перевод травмы, патологии или состояния в легче переносимую пациентом форму, замедление скорости развития дегенеративных изменений или угасания функции, перевод итоговой точки дегенеративных изменений в менее угнетающую для пациента форму, улучшение общего физического или умственного состояния пациента или продление выживаемости. Лечение или облегчение симптомов может основываться на объективных или субъективных параметрах, включая результаты врачебного осмотра, неврологического осмотра и/или психиатрической экспертизы.
В настоящем документе термины «эффективный период времени (или время)» и «эффективные условия» обозначают период времени или другие контролируемые условия (например, температуру, влажность для способов in vitro), необходимые или предпочтительные для получения предполагаемых результатов от применения агента или фармацевтической композиции.
Термины «пациент» или «субъект» в настоящем документе используются как взаимозаменяемые и относятся к животным, предпочтительно млекопитающим, более предпочтительно к человеку, на которого направлено лечение с использованием фармацевтических или терапевтических композиций или в соответствии со способами, описанными в настоящем документе.
«Ишемия» обозначает любое уменьшение или блокировку кровоснабжения любого органа, ткани или части тела, вызванное любым сужением или окклюзией кровеносной системы. В настоящем документе термины «ишемический эпизод» или «ишемическое событие» используются как взаимозаменяемые и относятся к любому временному или постоянному периоду ишемии. «Ишемия периферических сосудов» обозначает любое уменьшение или блокировку кровоснабжения любого органа, ткани или части тела, за исключением сердца, вызванное любым сужением или окклюзией кровеносной системы. «Заболевание периферических сосудов (ЗПС)» обозначает болезни кровеносных сосудов за пределами сердца и мозга. Часто оно принимает форму сужения кровеносных сосудов, обеспечивающих кровоснабжение конечностей, и является следствием двух типов нарушения кровообращения, а именно: (1) функционального заболевания периферических сосудов, при котором происходит кратковременный спазм, приводящий к сужению кровеносных сосудов; и (2) органического заболевания периферических сосудов, при котором происходят структурные изменения кровеносных сосудов, такие как, например, изменения, вызванные воспалением или жировой закупоркой сосудов. При использовании в настоящем документе ЗПС также охватывает болезнь Рейно, перемежающуюся хромоту и критическую ишемию конечностей.
Термин «фармацевтически приемлемый носитель» (или «среда»), который можно использовать взаимозаменяемо с термином «биологически совместимый носитель» (или «среда»), относится к реагентам, клеткам, соединениям, материалам, композициям и/или дозированным формам, которые не только совместимы с вводимыми в терапевтических целях клетками и другими агентами, но которые также, в рамках медицинского здравого смысла, можно использовать в контакте с тканями людей или животных, не вызывая чрезмерную токсичность, раздражение, аллергическую реакцию или другое осложнение, соразмерное с разумным соотношением пользы/риска от применения. Как более подробно описано в настоящем документе, фармацевтически приемлемые носители, подходящие для применения в настоящем изобретении, включают в себя жидкости, полутвердые (например, гели) и твердые материалы (например, клеточные каркасы и матрицы, трубки, листы и другие такие материалы, известные в данной области и более подробно описанные в настоящем документе). Эти полутвердые и твердые материалы могут быть выполнены с возможностью сопротивления разложению внутри тела (небиоразлагаемые) или могут быть выполнены с возможностью разложения внутри тела (биоразлагаемые, биоразрушаемые). Биоразлагаемый материал может дополнительно быть саморассасывающимся или биорассасывающимся, т.е. он может растворяться и всасываться биологическими жидкостями (одним из примеров являются водорастворимые имплантаты) или разлагаться и в конечном итоге выводиться из тела либо путем превращения в другие материалы, либо путем расщепления и выведения естественными путями. Скорость биоразложения может варьироваться в соответствии с необходимой скоростью высвобождения после имплантации в тело. Матрица также желательно выполняет функцию временного каркаса до ее замены вновь выросшей скелетной мышцей, периваскулярными клетками, гладкой мускулатурой сосудов или тканью эндотелия сосудов. Следовательно, в одном варианте осуществления матрица обеспечивает возможность замедленного высвобождения других агентов, используемых в сочетании с клетками, полученными из ткани пуповины, и может обеспечивать структуру для роста развивающейся ткани в теле пациента. В других вариантах осуществления матрица просто обеспечивает временный каркас для развивающейся ткани. Матрица может быть выполнена в форме отдельных частиц (макрочастицы с диаметром более 10 микрон или микрочастицы с диаметром менее 10 микрон), либо иметь форму структурно устойчивого трехмерного имплантата (например, каркаса). Например, такой имплантат может представлять собой куб, цилиндр, трубку, блок, параллелепипед, пленку, лист или иметь соответствующую анатомическую форму.
В настоящем документе для описания трансплантации клеток или тканей используется несколько терминов. В настоящем документе термины «аутогенный перенос», «аутогенная трансплантация», «аутогенный трансплантат» и т.п. относятся к трансплантации, в которой донор трансплантата также является и получателем трансплантата. В настоящем документе термины «аллогенный перенос», «аллогенная трансплантация», «аллогенный трансплантат» относятся к трансплантации, в которой донор трансплантата также является представителем того же биологического вида, что и получатель трансплантата, но не является получателем. Клеточный трансплантат, в котором клетки донора были подобраны с точки зрения гистосовместимости с телом получателя, иногда называют «сингенным переносом». В настоящем документе термины «ксеногенный перенос», «ксеногенная трансплантация», «ксеногенный трансплантат» и т.п. относятся к трансплантации, в которой донор трансплантата является представителем другого биологического вида по сравнению с получателем трансплантата.
В своих различных вариантах осуществления, описанных в настоящем документе, настоящее изобретение предлагает способы и фармацевтические композиции для лечения заболевания периферических сосудов, в которых применяются клетки-предшественники и популяции клеток, полученных из ткани пуповины. Такие способы и фармацевтические композиции выполнены с возможностью стимулирования и поддержания ангиогенеза, улучшения кровотока, регенерации, восстановления и улучшения скелетной мускулатуры, поврежденной в результате периферического ишемического события, и/или для защиты скелетной мускулатуры от ишемического повреждения. Клетки, популяции клеток и препараты, содержащие клеточные лизаты, кондиционированные среды и т.п., используемые в фармацевтических препаратах и способах, составляющих предмет настоящего изобретения, подробно описаны в публикациях патентов США №№ 2005/0058631 и 2005/0054098, а также ниже в настоящем документе.
Один вариант осуществления настоящего изобретения представляет собой способ лечения заболевания периферических сосудов с использованием клеток, полученных из ткани пуповины, как описано в настоящем документе. В одном варианте осуществления настоящего изобретения клетки являются частью фармацевтической композиции.
В другом варианте осуществления настоящего изобретения в способе лечения заболевания периферических сосудов используют фибриновый клей (также известный как фибриновый герметик). При использовании в настоящем документе термин «фибриновый клей» охватывает любое биологическое или синтетическое вещество, используемое для создания фибринового сгустка. В одном варианте осуществления фибриновый клей представляет собой каркас для имплантации клеток. В оптимальном варианте фибриновый клей способен противостоять разложению внутри тела в течение достаточного времени. В одном варианте осуществления фибриновый клей содержит фибриноген (фактор I), такой как, например, рекомбинантный фибриноген или фибриноген, выделенный из крови, и тромбин. В другом варианте осуществления фибриновый клей содержит фибриноген, тромбин, фактор XIII и необязательно один или более из кальция, апротинина, фибронектина и плазминогена. В другом варианте осуществления фибриновый клей содержит фибриноген, тромбин и необязательно один или более из фактора XIII, антифибринолитических агентов (например, транексамовую кислоту), стабилизаторов (например, гидрохлорид аргинина), кальция, апротинина, фибронектина и плазминогена. В альтернативном варианте осуществления фибриновый клей по существу свободен от добавленных ингибиторов протеаз. В другом варианте осуществления фибриновый клей содержит BAC2 (фибриноген) и тромбин. В альтернативном варианте осуществления фибриновый клей представляет собой фибриновый клей EVICEL® (EVICEL® Fibrin sealant (Human), Omrix Pharmaceuticals) (тромбин и BAC2 (фибриноген)). В одном варианте осуществления фибриновый клей может представлять собой многокомпонентную систему, которую смешивают перед применением, причем один компонент содержит фибрин (и необязательно фактор XIII) и другой компонент содержит тромбин (и необязательно кальций). В другом варианте осуществления фибриновый клей представляет собой каркас, как описано в предварительной заявке на патент США № 61/372929 (поданной 12 августа 2010 г.), описание которой полностью включено в настоящий документ путем ссылки в части, относящейся к описанию, характеристике и применению фибриновых каркасов.
Фибриновый клей можно вводить одновременно либо до, либо после клеток, полученных из ткани пуповины, как описано в настоящем документе (клетки, полученные из пуповины). В одном варианте осуществления фибриновый клей и клетки, полученные из пуповины, как описано в настоящем документе, представлены в форме композиции, такой как, например, фармацевтическая композиция. В одном варианте осуществления композицию вводят локально (например, путем внутримышечной инъекции или инъекции в жировые депо в мышцах). В другом варианте осуществления фибриновый клей и клетки, полученные из пуповины, как описано в настоящем документе, вводят локально (например, путем внутримышечной инъекции или инъекции в жировые депо в мышцах). В другом варианте осуществления композицию или клетки и фибриновый клей вводят путем инъекции в интерстициальные пространства таким образом, чтобы они не попадали напрямую в кровоток. В другом варианте осуществления способ включает обеспечение клеток в фибриногене, к которому непосредственно перед локальным введением добавляют тромбин. В одном варианте осуществления фибриновый клей содержит от приблизительно 16 до приблизительно 24 МЕ/мл, альтернативно от приблизительно 18 до 22 МЕ/мл тромбина и от приблизительно 39,3 до приблизительно 60,7 мг/мл, альтернативно от приблизительно 45 до приблизительно 60 мг/мл, альтернативно от приблизительно 40 до приблизительно 55 мг/мл, альтернативно от приблизительно 45 до приблизительно 55 мг/мл фибриногена (например, BAC2). В другом варианте осуществления фибриновый клей содержит приблизительно 16, 17, 18, 19, 20, 21, 22, 23 или 24 МЕ/мл тромбина и приблизительно 40, 43, 45, 48, 50, 52, 53, 58 или 60 мг/мл фибриногена. В одном варианте осуществления с фибриновым клеем используют приблизительно 1×106 клеток.
В соответствии со способами, описанными в настоящем документе, пуповину млекопитающего получают по завершении доношенной или недоношенной беременности, например, после отделения последа, или вскоре после этого. Ткань пуповины можно транспортировать с места родов в лабораторию в стерильном контейнере, таком как колба, лабораторный стакан, чашка для культивирования или пакет. Контейнер может содержать раствор или среду, включая, без ограничений, солевой раствор, такой как модифицированная по способу Дульбекко среда Игла (DMEM) (также известный как минимальная эссенциальная среда Игла) или фосфатно-буферный раствор (PBS), либо любой раствор, применяемый для транспортировки органов, используемых для трансплантации, такой как раствор, разработанный в Висконсинском университете, либо перфторированный раствор. В среду или буферный раствор можно добавить один или более антибиотиков и/или антимикотиков, включая, без ограничений, пенициллин, стрептомицин, амфотерицин B, гентамицин и нистатин. Ткань можно промыть в растворе антикоагулянта, таком как гепаринсодержащий раствор. До извлечения клеток, полученных из ткани пуповины, ткань предпочтительно следует хранить при температуре приблизительно 4-10°C. Еще более предпочтительно не замораживать ткань до извлечения клеток, полученных их ткани пуповины.
Выделение клеток, полученных из пуповины, предпочтительно происходит в асептических условиях. Пуповину можно отделить от плаценты с использованием средств, известных специалистам в данной области. Кровь и продукты распада клеток предпочтительно отделяют от ткани до выделения клеток, полученных из ткани пуповины. Например, ткань пуповины можно промыть в буферном растворе, включая, без ограничений, фосфатно-буферный раствор. Промывочный буфер может также содержать один или более антимикотиков и/или антибиотиков, включая, без ограничений, пенициллин, стрептомицин, амфотерицин B, гентамицин и нистатин.
Ткань пуповины, представляющую собой цельную пуповину или ее фрагмент или часть, механически измельчают (используя разрезающее или сдвиговое усилие). В предпочтительном в настоящее время варианте осуществления в процедуре выделения клеток также используют способ ферментативного расщепления. Специалистам в данной области известно множество ферментов, подходящих для использования при выделении отдельных клеток из сложных тканевых матриц для облегчения их выращивания в культуре. В продаже доступны следующие расщепляющие ферменты: от слабо расщепляющих (например, дезоксирибонуклеазы и диспаза (нейтральная протеаза)) до сильно расщепляющих (например, папаин и трипсин). Неограничивающий перечень ферментов, совместимых с целями настоящего изобретения, включает в себя ферменты с муколитической активностью, металлопротеазы, нейтральные протеазы, сериновые протеазы (такие как трипсин, химотрипсин или эластаза) и дезоксирибонуклеазы. В настоящее время предпочтительными являются ферменты с активностью, выбранные из металлопротеаз, нейтральных протеаз и ферментов с муколитической активностью. Например, известно, что коллагеназы подходят для выделения различных клеток из тканей. Дезоксирибонуклеазы могут расщеплять одноцепочечные ДНК и позволяют свести к минимуму агглютинацию клеток в процессе выделения. Предпочтительные способы включают ферментативную обработку, например, с использованием коллагеназы и диспазы, либо коллагеназы, диспазы и гиалуронидазы. В определенных вариантах осуществления на стадии диссоциации используют смесь коллагеназы и нейтральной протеазы (диспазы). В более конкретных вариантах осуществления применяют расщепление в присутствии по меньшей мере одной коллагеназы из Clostridium histolyticum и одного из ферментов с протеазной активностью, диспазы или термолизина. В других вариантах осуществления используют расщепление с использованием ферментов как с коллагеназной, так и диспазной активностью. Также используют способы, которые включают расщепление ферментом с гиалуронидазной активностью помимо ферментов с коллагеназной и диспазной активностью. Специалист в данной области определит, что известно множество способов таких ферментативных обработок для выделения клеток из различных тканей-источников. Например, в способах, составляющих предмет настоящего изобретения, можно применять ферментативные смеси для диссоциации тканей, доступные в продаже под торговым наименованием LIBERASE® (Roche, г. Индианаполис, штат Индиана). Известны и другие источники ферментов, и специалист в данной области также может получить такие ферменты непосредственно из их природных источников. Специалист в данной области также может оценивать возможности новых или дополнительных ферментов или комбинаций ферментов для выделения клеток, составляющих предмет настоящего изобретения. Предпочтительная продолжительность ферментативной обработки составляет 0,5, 1, 1,5 или 2 часа или более. В других предпочтительных вариантах осуществления ткань инкубируют при температуре 37°C в процессе ферментативной обработки на стадии диссоциации.
В некоторых вариантах осуществления настоящего изобретения ткань пуповины разделяют на части, содержащие различные аспекты ткани, такие как, например, неонатальный, неонатальный/материнский и материнский аспекты плаценты. Разделенные части затем диссоциируют с использованием механической и/или ферментативной диссоциации в соответствии со способами, описанными в настоящем документе. Клетки неонатальных или материнских линий можно идентифицировать любыми средствами, известными специалистам в данной области, например, путем анализа кариотипа или гибридизации in situ на Y-хромосому.
Выделенные клетки или ткань пуповины, из которой получают клетки, можно использовать для инициирования, или посева, клеточных культур. Выделенные клетки переносят в стерильные сосуды для культивирования ткани без покрытия или с покрытием внеклеточным матриксом или лигандами, такими как ламинин, коллаген (нативный, денатурированный или сшитый), желатин, фибронектин и другие белки внеклеточного матрикса. Клетки, полученные из ткани пуповины, культивируют в любой культуральной среде, способной поддерживать рост клеток, такой как, без ограничений, среда DMEM (с высоким или низким содержанием глюкозы), улучшенная среда DMEM, среда DMEM/MCDB 201, основная среда Игла, среда Хэма F10 (F10), среда Хэма F12 (F12), модифицированная по способу Искова среда Дульбекко, ростовая среда для мезенхимальных стволовых клеток (MSCGM), среда DMEM/F12, среда RPMI 1640 и среда, не содержащая сыворотку/субстрат, доступная в продаже под торговым наименованием CELL-GRO-FREE® (MediatechGRO, г. Херндон, штат Вирджиния). В культуральную среду можно дополнительно ввести один или более компонентов, включая, например, фетальную бычью сыворотку (FBS), предпочтительно в количестве приблизительно 2-15% (об./об.); сыворотку лошади (ES); сыворотку человека (HS); бета-меркаптоэтанол (BME или 2-ME), предпочтительно в количестве приблизительно 0,001% (об./об.); один или более факторов роста, например тромбоцитарный фактор роста (PDGF), эпидермальный фактор роста (EGF), фактор роста фибробластов (FGF), фактор роста эндотелия сосудов (VEGF), инсулиноподобный фактор роста-1 (IGF-1), фактор ингибирования лейкоцитов (LIF) и эритропоэтин (EPO); аминокислоты, включая L-валин; и один или более антибиотиков и/или антимикотиков для борьбы с микробактериальным заражением, таких как пенициллин G, сульфат стрептомицина, амфотерицин B, гентамицин и нистатин, либо индивидуально, либо в комбинации. Культуральная среда предпочтительно содержит ростовую среду, как описано в приведенных ниже примерах.
Клетки высевают в сосуды для культивирования с плотностью, позволяющей клеткам расти. В предпочтительном варианте осуществления клетки культивируют в атмосфере с содержанием CO2 от приблизительно 0 до приблизительно 5% об. В некоторых предпочтительных вариантах осуществления клетки культивируют в атмосфере с содержанием O2 от приблизительно 2 до приблизительно 25%, предпочтительно в атмосфере с содержанием O2 от приблизительно 5 до приблизительно 20%. Клетки предпочтительно культивируют при температуре от приблизительно 25 до приблизительно 40°C и более предпочтительно культивируют при температуре 37°C. Клетки предпочтительно культивируют в инкубаторе. Среда в сосуде для культивирования может быть неподвижной или перемешиваемой, например, с использованием биореактора. Клетки, полученные из ткани пуповины, предпочтительно выращивают в условиях низкого окислительного стресса (например, с добавлением глутатиона, витамина C, каталазы, витамина E, N-ацетилцистеина). При использовании в настоящем документе термин «условия низкого окислительного стресса» обозначают условия отсутствия или минимального свободнорадикального повреждения культивируемых клеток.
Способы выбора наиболее предпочтительной культуральной среды, подготовки среды и методик культивирования клеток хорошо известны в данной области и описаны в ряде источников, включая руководства Doyle et al., (ред.), 1995 г., Cell & Tissue Culture: Laboratory Procedures, John Wiley & Sons, Chichester; и Ho и Wang (ред.), 1991 г., Animal Cell Bioreactors, Butterworth-Heinemann, Boston, которые включены в настоящий документ путем ссылки.
После культивирования выделенных клеток или фрагментов ткани в течение достаточного периода времени клетки, полученные из ткани пуповины, прорастают в результате миграции из ткани пуповины или деления клеток, либо по обеим причинам. В некоторых вариантах осуществления настоящего изобретения клетки, полученные из ткани пуповины, пассируют или переносят в отдельный сосуд для культивирования, содержащий свежую среду того же типа или другого типа по сравнению с первоначально использованной, где популяцию клеток можно митотически размножить. Клетки, составляющие предмет настоящего изобретения, можно применять на любой стадии от пассажа 0 до старения. Клетки предпочтительно пассируют от приблизительно 3 до приблизительно 25 раз, более предпочтительно пассируют от приблизительно 4 до приблизительно 12 раз и предпочтительно пассируют 10 или 11 раз. Для подтверждения выделения клональной популяции клеток можно провести клонирование и/или субклонирование.
В некоторых аспектах настоящего изобретения различные типы клеток, присутствующие в ткани пуповины, фракционируют на субпопуляции, из которых можно выделить клетки, полученные из ткани пуповины. Фракционирования или отбора можно достигнуть с использованием стандартных методик разделения клеток, включая, без ограничений, ферментативную обработку для диссоциации ткани пуповины на составляющие ее клетки с последующим клонированием и отбором конкретных типов клеток, включая, без ограничений, отбор на основе морфологических и/или биохимических маркеров; выборочный рост необходимых клеток (положительный отбор), выборочное разрушение нежелательных клеток (отрицательный отбор); разделение на основе различной способности клеток в смешанной популяции к агглютинации, например, с соевым агглютинином; процедуры заморозки-разморозки; различие адгезионных характеристик клеток в смешанной популяции; фильтрование; стандартное и зональное центрифугирование; элютриационное центрифугирование (противоточное центрифугирование); разделение в тяжелой среде; противоточное распределение; электрофорез; и сортировку флуоресцентно-активированных клеток (FACS). Обзор методик клонального отбора и разделения клеток см. в руководстве Freshney, 1994 г., Culture of Animal Cells: A Manual of Basic Techniques, 3-е изд., Wiley-Liss, Inc., New York, которое включено в настоящий документ путем ссылки.
Культуральную среду меняют по необходимости, например, путем осторожного отсасывания среды из чашки, например, с помощью пипетки и добавления требуемого количества свежей среды. Инкубацию продолжают до накопления в чашке достаточного количества или плотности клеток. Исходные эксплантированные части ткани можно удалить и трипсинизировать оставшиеся клетки с помощью стандартных методик или с использованием скребка. После трипсинизации клетки собирают, переносят в свежую среду и инкубируют, как описано выше. В некоторых вариантах осуществления среду заменяют по меньшей мере один раз приблизительно через 24 часа после трипсинизации для удаления плавающих клеток. Оставшиеся в культуре клетки считают клетками, полученными из ткани пуповины.
Клетки, полученные из ткани пуповины, можно криоконсервировать. Соответственно, в предпочтительном варианте осуществления, более подробно описанном ниже, клетки, полученные из ткани пуповины, для аутогенного переноса (либо для матери, либо для ребенка) можно получить из соответствующих тканей пуповины после рождения ребенка и затем криоконсервировать их таким образом, чтобы после этого они были доступны в случае возникновения необходимости в трансплантации.
Клетки, полученные из ткани пуповины, можно охарактеризовать, например, по ростовым характеристикам (например, способности к удвоению популяции, времени удвоения, количеству пассажей до старения), анализу кариотипа (например, нормальный кариотип; материнская или неонатальная линия), проточной цитометрии (например, анализу FACS), иммуногистохимически и/или иммуноцитохимически (например, на обнаружение эпитопов), по профилю экспрессии генов (например, с использованием генных чипов; полимеразной цепной реакции (например, ПЦР с обратной транскриптазой, ПЦР в реальном времени и стандартной ПЦР)), по белковым чипам, по секреции белков (например, по анализу коагулирующей активности плазмы или анализу среды, кондиционированной плазмацитоидными дендритными клетками (ПДК), например, с использованием твердофазного иммуноферментного анализа (ИФА)), реакции смешанной культуры лимфоцитов (например, как меры стимуляции мононуклеарных клеток периферической крови (МКПК)) и/или другими способами, известными в данной области.
Примеры клеток, полученных из ткани пуповины, депонированы в коллекции American Type Culture Collection (ATCC, 10801 University Blvd., Manassas, VA) 10 июня 2004 г. под следующими номерами доступа ATCC: (1) штамму UMB 022803 (P7) присвоен номер доступа PTA-6067; и (2) штамму UMB 022803 (P17) присвоен номер доступа PTA-6068.
В различных вариантах осуществления клетки, полученные из ткани пуповины, обладают одной или более из следующих характеристик роста: (1) для роста в культуре клеткам необходим L-валин; (2) клетки способны расти в атмосфере с содержанием кислорода от приблизительно 5% до по меньшей мере приблизительно 20%; (3) клетки обладают потенциалом к по меньшей мере приблизительно 40 удвоениям в культуре до достижения старения; и (4) клетки закрепляются и размножаются на поверхности сосуда для культивирования с покрытием или без покрытия, причем сосуд для культивирования с покрытием содержит покрытие из желатина, ламинина, коллагена, полиорнитина, витронектина или фибронектина.
В определенных вариантах осуществления клетки, полученные из ткани пуповины, имеют нормальный кариотип, который сохраняется по мере пассирования клеток. Кариотипирование, в частности, подходит для идентификации и отличия неонатальных клеток от материнских клеток, полученных из плаценты. Способы кариотипирования доступны и известны специалистам в данной области.
В других вариантах осуществления клетки, полученные из ткани пуповины, можно охарактеризовать по выработке определенных белков, включая (1) выработку по меньшей мере одного из тканевого фактора, виментина и альфа-актина гладких мышц; и (2) выработку по меньшей мере одного из маркеров клеточной поверхности CD10, CD13, CD44, CD73, CD90, PDGFr-альфа, PD-L2 и HLA-A,B,C по результатам анализа с использованием проточной цитометрии. В других вариантах осуществления клетки, полученные из ткани пуповины, можно охарактеризовать по отсутствию выработки по меньшей мере одного из маркеров клеточной поверхности CD31, CD34, CD45, CD80, CD86, CD117, CD141, CD178, B7-H2, HLA-G и HLA-DR,DP,DQ по результатам анализа с использованием проточной цитометрии. Особенно предпочтительными являются клетки, которые вырабатывают по меньшей мере два из тканевого фактора, виментина и альфа-актина гладких мышц. Более предпочтительными являются клетки, которые вырабатывают все три из тканевого фактора, виментина и альфа-актина гладких мышц.
В других вариантах осуществления клетки, полученные из ткани пуповины, можно охарактеризовать по экспрессии гена, которая, по сравнению с клеткой человека, представляющей собой фибробласт, мезенхимальную стволовую клетку или клетку костного мозга гребня подвздошной кости, повышена для гена, кодирующего по меньшей мере один из интерлейкина-8; ретикулона 1; CXCL1 (хемокиновый (мотив C-X-C) лиганд 1/стимулятор активности роста меланомы, альфа); CXCL6 (хемокиновый (мотив C-X-C) лиганд 6/белок хемотаксиса гранулоцитов 2); CXCL3 (хемокиновый (мотив C-X-C) лиганд 3); и TNFAIP3 (индуцируемый фактором некроза альфа белок 3).
В других вариантах осуществления клетки, полученные из ткани пуповины, могут быть охарактеризованы по экспрессии гена, которая, по сравнению с клеткой человека, представляющей собой фибробласт, мезенхимальную стволовую клетку или клетку костного мозга гребня подвздошной кости, понижена для гена, кодирующего по меньшей мере один из следующих генов: SHOX2 (содержащий гомеобокс ген низкорослости 2); HSPB2 (27 кДа белок теплового шока 2); CXCL12 (хемокиновый (мотив C-X-C) лиганд 12/стромальный фактор 1); эластин (надклапанный аортальный стеноз, синдром Вильямса-Бойрена); мРНК Homo sapiens; кДНК DKFZp586M2022 (из клона DKFZp586M2022); Meox2 (содержащий мезенхимальный гомеобокс гена 2, содержащий гомеобокс блокировки роста ген); SIX1 (гомолог содержащего гомеобокс гена sine oculis 1) (Drosophila); кристаллин, альфа B; DAAM2 (ассоциированный с белком Disheveled активатор морфогенеза 2); белок DKFZP586B2420; аналог нейтралина 1; тетранектин (связывающийся с плазминогеном белок); STAC (ген, содержащий домен src-гомологии 3 (SH3) и богатый цистеином домен); холестерин-25-гидроксилаза; RUNX3 (связанный с карликовостью фактор транскрипции 3); рецептор интерлейкина-11, альфа; PCOLCE (усилитель проколлаген-C-эндопептидазы); FZD7 (гомолог frizzled 7) (Drosophila); гипотетический ген BC008967; коллаген, тип VIII, альфа 1; TNC (тенасцин C, гексабрахион); IRX5 (содержащий гомеобокс IRX белок 5); гефестин; интегрин, бета 8; SV2A (гликопротеин синаптического пузырька 2); NBL1 (нейробластома, ген подавления онкогенности 1); IGFBP2 (связывающийся с инсулиноподобным фактором роста белок 2, 36 кДа); кДНК Homo sapiens FLJ12280 fis, клон MAMMA1001744; CRLF1 (подобный цитокиновому рецептору фактор 1); KCNN4 (активируемый кальцием калиевый канал средней/низкой проводимости, подсемейство N, член 4); интегрин, бета 7; транскрипционный коактиватор с мотивом связывания с PDZ (TAZ); SIX2 (гомолог содержащего гомеобокс гена sine oculis 2) (Drosophila); белок KIAA1034; VAMP5 (везикуло-ассоциированный мембранный белок 5/миобревин); EFEMP1 (содержащий EGF фибулин-подобный белок внеклеточного матрикса 1); EGR3 (белок раннего ростового ответа 3); DLX5 (содержащий гомеобокс distal-less гена 5); гипотетический белок FLJ20373; AKR1C3 (альдокеторедуктаза семейства 1, член C3/3-альфа-гидроксистероиддегидрогеназа, тип II); бигликан; транскрипционный коактиватор с мотивом связывания с PDZ (TAZ); фибронектин 1; проэнкефалин; интегрин, бета-подобный 1 (с доменами EGF-подобных повторов); мРНК Homo sapiens, полноразмерная вставка кДНК, клон EUROIMAGE 1968422; EphA3; белок KIAA0367; NPR3 (рецептор натрийуретического пептида C/гуанилатциклаза C/рецептор атрионатрийуретического пептида C); гипотетический белок FLJ14054; мРНК Homo sapiens; кДНК DKFZp564B222 (из клона DKFZp564B222); BNIP3L (ген белка, подобного белку 3, взаимодействующему с BCL2/белком аденовируса E1B 19 кДа); AE-связывающий белок 1; и COX7A1 (полипептид 1 субъединицы VIIa цитохром c оксидазы) (мышечный).
В других вариантах осуществления клетки, полученные из ткани пуповины, можно охарактеризовать по секреции по меньшей мере одного из MCP-1, IL-6, IL-8, GCP-2, HGF, KGF, FGF, HB-EGF, BDNF, TPO, MIP1b, RANTES и TIMP1. В некоторых вариантах осуществления клетки, полученные из ткани пуповины, можно охарактеризовать по отсутствию секреции по меньшей мере одного из TGF-бета2, ANG2, PDGFbb, MIP1a и VEGF по результатам ИФА.
В некоторых предпочтительных вариантах осуществления клетки получают из ткани пуповины по существу без крови, клетки способны к самообновлению и размножению в культуре, требуют для роста L-валин, могут расти в атмосфере с содержанием кислорода по меньшей мере приблизительно 5% и обладают по меньшей мере одной из следующих характеристик: потенциал к по меньшей мере приблизительно 40 удвоениям в культуре; закрепление и размножение на поверхности сосуда для культивирования с покрытием или без покрытия, который содержит покрытие из желатина, ламинина, коллагена, полиорнитина, витронектина или фибронектина; выработка виментина и альфа-актина гладких мышц; выработка CD10, CD13, CD44, CD73 и CD90; и экспрессия гена, которая, по сравнению с клеткой человека, представляющей собой фибробласт, мезенхимальную стволовую клетку или клетку костного мозга гребня подвздошной кости, повышена для гена, кодирующего интерлейкин-8 и ретикулон 1. В некоторых вариантах осуществления такие клетки не вырабатывают CD45 и CD117. Описанные в данном абзаце клетки можно использовать в способах лечения пациента с заболеванием периферических сосудов, можно использовать в фармацевтических композициях для лечения заболевания периферических сосудов, например, там, где такие композиции содержат клетки с этими характеристиками и фармацевтически приемлемый носитель, и можно использовать в наборах для изготовления, использования и применения на практике таких способов и фармацевтических композиций, как описано и показано в примерах, представленных в настоящем документе. Кроме того, описанные в данном абзаце клетки можно использовать для получения кондиционированной клеточной культуральной среды или для изготовления препаратов, таких как клеточные экстракты и субклеточные фракции, которые можно использовать для изготовления, использования и применения на практике таких способов и фармацевтических композиций, как описано и показано в примерах, представленных в настоящем документе.
В предпочтительных вариантах осуществления клетки не экспрессируют теломеразу (hTert). Таким образом, один вариант осуществления настоящего изобретения представляет собой клетки, полученные из пуповины, которые не экспрессируют теломеразу (hTert) и которые обладают одной или более из характеристик, раскрытых в настоящем документе.
В одном варианте осуществления настоящего изобретения клетки выделяются из ткани пуповины человека по существу без крови, они способны к самообновлению и размножению в культуре и не вырабатывают CD117 и/или теломеразу. Клетки необязательно (i) экспрессируют рецептор окисленных липопротеинов низкой плотности 1, ретикулон, лиганд хемокинового рецептора 3 и/или гранулоцитарный хемотаксический белок; и/или (ii) не экспрессируют CD31, CD34 или CD45; и/или (iii) экспрессируют, по отношению к фибробластам, мезенхимальным стволовым клеткам или клеткам костного мозга гребня подвздошной кости человека, повышенные уровни интерлейкина-8 или ретикулона 1; и/или (iv) имеют потенциал для дифференцирования в клетки по меньшей мере фенотипов клеток скелетных мышц, клеток гладких мышц сосудов, периваскулярных клеток или клеток эндотелия сосудов; и/или (v) экспрессируют CD10, CD13, CD44, CD73 и CD90. В другом варианте осуществления настоящего изобретения клетки выделяются из ткани пуповины человека по существу без крови, они способны к самообновлению и размножению в культуре и не вырабатывают CD117, CD34, CD31 и/или теломеразу. В другом варианте осуществления настоящего изобретения клетки выделяются из ткани пуповины человека по существу без крови, они способны к самообновлению и размножению в культуре и не вырабатывают CD117, CD45, CD34, CD31 и/или теломеразу.
Среди клеток, которые в настоящее время предпочтительны для использования в целях настоящего изобретения в некоторых его аспектах, имеются клетки, полученные из ткани пуповины, обладающие описанными выше характеристиками, и, в частности, те из них, которые имеют нормальные кариотипы и поддерживают нормальные кариотипы при пассировании, и дополнительно те из них, которые экспрессируют каждый из маркеров CD10, CD13, CD44, CD73, CD90, PDGFr-альфа и HLA-A,B,C, причем клетки вырабатывают иммунологически детектируемые белки, соответствующие перечисленным маркерам. Еще более предпочтительны клетки, которые, в дополнение к описанному выше, не вырабатывают белки, соответствующие любому из маркеров CD31, CD34, CD45, CD117, CD141 или HLA-DR,DP,DQ по результатам анализа с использованием проточной цитометрии.
Определенные клетки, обладающие потенциалом к дифференцированию по линиям, ведущим к различным фенотипам, неустойчивы и, таким образом, могут спонтанно дифференцироваться. В настоящее время предпочтительны для использования в целях настоящего изобретения клетки, которые не дифференцируются спонтанно, например, в линиях миобластов, клеток скелетных мышц, клеток гладких мышц сосудов, периваскулярных клеток, гемангиогенных клеток, ангиогенных клеток, васкулогенных клеток или клеток эндотелия сосудов. Предпочтительные клетки, при их выращивании в ростовой среде, являются по существу устойчивыми по отношению к клеточным маркерам, вырабатываемым на их поверхности, и по отношению к схемам экспрессии различных генов, например, по результатам медицинского диагностического теста, доступного в продаже под торговым наименованием GENECHIP (Affymetrix, Inc., г. Санта-Клара, штат Калифорния). Клетки остаются по существу постоянными, например, в отношении характеристик маркеров клеточной поверхности при пассировании на протяжении множества удвоений популяции.
В другом аспекте настоящего изобретения описано использование популяций клеток, полученных из ткани пуповины, как описано выше. В некоторых вариантах осуществления популяция клеток является неоднородной. Неоднородная популяция клеток, составляющая предмет настоящего изобретения, может содержать по меньшей мере приблизительно 5%, 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90% или 95% клеток, полученных из ткани пуповины, составляющих предмет настоящего изобретения. Неоднородные популяции клеток, составляющие предмет настоящего изобретения, могут дополнительно содержать стволовые клетки или другие клетки-предшественники, такие как миобласты или другие клетки-предшественники мышечных клеток, гемангиобласты, или клетки-предшественники клеток кровеносных сосудов, или она может дополнительно содержать полностью дифференцированные клетки скелетных мышц, клетки гладких мышц сосудов, периваскулярные клетки или клетки эндотелия кровеносных сосудов. В некоторых вариантах осуществления популяция является по существу однородной, т.е. содержит по существу только клетки, полученные из ткани пуповины (предпочтительно по меньшей мере приблизительно 96%, 97%, 98%, 99% или более клеток, полученных из ткани пуповины). Однородная популяция клеток, составляющая предмет настоящего изобретения, может содержать клетки, полученные из пуповины или из плаценты. Однородные популяции клеток, полученных из пуповины, предпочтительно свободны от клеток материнской линии. Однородные популяции клеток, полученных из плаценты, могут принадлежать неонатальной или материнской линии. Однородности популяции клеток можно достичь при помощи любого способа, известного в данной области, например, путем сортировки клеток (например, с использованием проточной цитометрии) или путем клонального размножения в соответствии с известными способами. Таким образом, предпочтительные однородные популяции клеток могут содержать клонированную клеточную линию клеток, полученных из ткани пуповины. Такие популяции особенно подходят в тех случаях, когда выделен клеточный клон с крайне необходимыми характеристиками.
В настоящем документе также описано применение популяций клеток, инкубированных в присутствии одного или более факторов или в условиях, которые стимулируют дифференцирование стволовых клеток по линиям дифференцирования клеток гладких мышц сосудов, клеток эндотелия сосудов, периваскулярных клеток или клеток скелетных мышц. Такие факторы известны в данной области, и специалист определит, что подбор соответствующих условий для дифференцирования можно провести стандартными экспериментами. Оптимизацию таких условий можно получить путем статистического построения эксперимента и его анализа, например, методология поверхности отклика позволяет одновременно провести оптимизацию по множеству переменных, как, например, в биологической культуре. Предпочтительные в настоящее время факторы включают в себя, без ограничений, факторы роста или трофические факторы, хемокины, цитокины, клеточные продукты, деметилирующие агенты и другие стимулы, которые, как уже известно или как будет установлено позднее, стимулируют дифференцирование, например, стволовых клеток по путям или линиям дифференцирования ангиогенных клеток, гемангиогенных клеток, васкулогенных клеток, клеток скелетных мышц, клеток гладких мышц сосудов, периваскулярных клеток или клеток эндотелия сосудов.
Клетки, полученные из ткани пуповины, также можно генетически модифицировать для выработки терапевтически полезных продуктов генов, для выработки ангиогенных агентов для облегчения или поддержки формирования и роста дополнительных кровеносных сосудов либо для выработки факторов для привлечения клеток-предшественников клеток эндотелия в область ишемического повреждения. Клетки-предшественники клеток эндотелия способствуют развитию кровеносных сосудов и улучшают кровоток, особенно после ишемического события (Urbich C и Dimmeler S (2004 г.) Circ. Res. 95: 343-53). Факторы, участвующие в привлечении клеток эндотелия, включают в себя, без ограничений, VEGF, стромальный фактор-1 (SDF-1), эритропоэтин (EPO), G-CSF, статины, эстроген, PPARγ, CXCR4, FGF и HGF. Генетическую модификацию можно провести с использованием любого из ряда векторов, включая, без ограничений, интегрирующие вирусные векторы, например, ретровирусный вектор или векторы, связанные с аденовирусами; неинтегрирующие реплицирующиеся векторы, например, векторы вируса папилломы, векторы SV40, аденовирусные векторы; или вирусные векторы с нарушенной репликацией. Другие способы введения ДНК в клетки включают применение липосом, электропорации, генной пушки или прямую инъекцию ДНК.
Клетки-хозяева предпочтительно трансформируют или трансфицируют ДНК под контролем или в функциональной связи с одним или более соответствующими элементами управления экспрессией, такими как промоторные или усилительные последовательности, терминаторы транскрипции, сайты полиаденилирования и т.п., и селектируемым маркером. Для индуцирования экспрессии вставленного гена можно использовать любой промотор. Например, вирусные промоторы включают в себя, без ограничений, промотор/усилитель CMV, SV40, папилломавирус, вирус Эпштейна-Барра или промотор гена эластина. В некоторых вариантах осуществления управляющие элементы, используемые для контроля над экспрессией рассматриваемого гена, могут позволять осуществление регулируемой экспрессии гена таким образом, чтобы в условиях in vivo продукт синтезировался только в случае необходимости. При необходимости временной экспрессии предпочтительно используют конститутивные промоторы в неинтегрирующем векторе и/или векторе с нарушенной репликацией. В альтернативном варианте осуществления при необходимости для активации экспрессии вставленного гена можно использовать индуцируемые промоторы. Индуцируемые промоторы включают в себя, без ограничений, промоторы, связанные с металлотионеином и белками теплового шока.
После введения экзогенной ДНК клетки, полученные методами генной инженерии, можно оставить для роста в обогащенных средах и затем перевести в селективные среды. Селектируемый маркер в экзогенной ДНК придает устойчивость к селекции и позволяет клеткам стабильно интегрировать экзогенную ДНК, как, например, вводимую на плазмиде, в свои хромосомы и вырасти для образования очагов, которые затем можно клонировать и размножить в клеточные линии. Данный способ можно эффективно использовать для конструирования клеточных линий, экспрессирующих продукт гена.
Клетки, составляющие предмет настоящего изобретения, можно модифицировать методами генной инженерии для «выключения» или «выбивания» экспрессии факторов, стимулирующих воспаление или отторжение имплантата в месте введения. Ниже описаны методики отрицательной модуляции для снижения уровней экспрессии целевого гена или активности продукта целевого гена. При использовании в настоящем документе «отрицательная модуляция» обозначает снижение уровня и/или активности продукта целевого гена по отношению к уровню и/или активности продукта целевого гена в отсутствие модулирующей обработки. Экспрессию гена, нативного для клеток скелетных мышц, клеток гладких мышц сосудов, периваскулярных клеток, клеток эндотелия сосудов или их клеток-предшественников, можно понизить или выключить с использованием нескольких методов, включая, например, ингибирование экспрессии путем инактивации гена с использованием методики гомологичной рекомбинации. Как правило, экзон, кодирующий важный участок белка (или экзон в положении 5' к данному участку), прерывают положительно селектируемым маркером, например, neo, блокируя получение нормальной мРНК с целевого гена, что приводит к инактивации гена. Ген также можно инактивировать путем создания делеции в части гена или путем удаления всего гена. Использование конструкции с двумя участками гомологии к целевому гену, находящимися в геноме далеко от друга, позволяет вырезать соединяющие эти два участка последовательности (Mombaerts et al., 1991 г., Proc. Nat. Acad. Sci. U.S.A. 88: 3084-3087). Для снижения уровня активности целевого гена также можно использовать антисмысловые гены, ДНК-ферменты, рибозимы, малые интерферирующие РНК (миРНК) и другие такие молекулы, которые ингибируют экспрессию целевого гена. Например, показано, что молекулы антисмысловой РНК, ингибирующие экспрессию главных комплексов генов гистосовместимости (HLA), являются наиболее универсальными в отношении иммунных ответов. Кроме того, для снижения уровня активности целевого гена можно дополнительно использовать трехцепочечные молекулы. Эти методики подробно описаны в публикации L.G. Davis et al. (ред.), 1994 г., Basic Methods in Molecular Biology, 2-я ред., Appleton & Lange, Norwalk, CN.
В других аспектах в настоящем изобретении используют клеточные лизаты и растворимые фракции клеток, приготовленные из клеток, полученных из ткани пуповины, или однородные или неоднородные клеточные популяции, содержащие клетки, полученные из ткани пуповины, а также клетки, полученные из ткани пуповины, или их популяции, которые были генетически модифицированы или которые стимулировали для дифференцирования по линиям дифференцирования клеток скелетных мышц, клеток гладких мышц сосудов, периваскулярных клеток или клеток эндотелия сосудов. Такие лизаты и их фракции имеют множество применений. Использование растворимой фракции клеточного лизата (например, по существу свободной от мембран) in vivo, например, позволяет использовать полезное внутриклеточное вещество аллогенно для пациента без введения значительного количества белков клеточной поверхности, которые скорее всего могут спровоцировать отторжение или другие нежелательные иммунологические ответы. Способы лизиса клеток хорошо известны в данной области и включают в себя различные способы механического разрушения, ферментативного разрушения или химического разрушения или их комбинации. Такие клеточные лизаты можно приготовить из клеток непосредственно в их ростовой среде таким образом, чтобы они содержали секретированные факторы роста и т.п., либо их можно приготовить из отмытых от среды клеток, например, с использованием PBS или другого раствора. При необходимости отмытые клетки можно ресуспендировать в концентрациях, превышающих плотность исходной популяции.
В одном варианте осуществления получают цельноклеточные лизаты, например, путем разрушения клеток без последующего разделения клеточных фракций. В другом варианте осуществления фракцию клеточных мембран отделяют от растворимой клеточной фракции стандартными способами, известными в данной области, например центрифугированием, фильтрованием или аналогичными способами.
Клеточные лизаты или растворимые клеточные фракции, приготовленные из популяций клеток, полученных из ткани пуповины, можно использовать непосредственно, в дополнительно сконцентрированном виде, например, с использованием ультрафильтрации или лиофилизации, или даже в высушенном виде, частично высушенном виде, в сочетании с известными в данной области фармацевтически приемлемыми носителями или разбавителями или в сочетании с другими соединениями, такими как биологические соединения, например, фармацевтически эффективными белковыми композициями. Клеточные лизаты или их фракции можно использовать in vitro или in vivo, индивидуально или, например, вместе с аутогенными или сингенными живыми клетками. При использовании in vivo лизаты можно вводить локально в месте обработки или удаленно, например, чтобы обеспечить пациента необходимыми клеточными факторами роста.
В дополнительном варианте осуществления клетки, полученные из ткани пуповины, можно культивировать in vitro для выработки биологических продуктов с высоким выходом. Клетки, полученные из ткани пуповины, которые либо естественным образом вырабатывают конкретный рассматриваемый биологический продукт (например, трофический фактор), либо модифицируют методами генной инженерии для выработки биологического продукта, можно клонально размножать с использованием методик культивирования, описанных в настоящем документе. В альтернативном варианте осуществления клетки можно размножать в среде, которая индуцирует их дифференцирование по линиям дифференцирования клеток скелетных мышц, клеток гладких мышц сосудов, периваскулярных клеток или клеток эндотелия сосудов. В любом случае из кондиционированной среды можно легко выделить вырабатываемые клеткой и секретируемые в среду биологические продукты, используя стандартные методики разделения, такие как, например, дифференциальное осаждение белков, ионообменная хроматография, гельпроникающая хроматография, электрофорез, ВЭЖХ и т.п. Для реализации проточного способа питания, например, трехмерной культуры in vitro можно эффективно использовать «биореактор». По существу, по мере прохождения свежей среды через трехмерную культуру биологический продукт вымывается из культуры и затем может быть выделен из выходящего потока, как описано выше.
В альтернативном варианте осуществления рассматриваемый биологический продукт может оставаться внутри клеток, и, таким образом, для его сбора может потребоваться лизис клеток, как описано выше. Затем биологический продукт можно очистить с использованием любой одной или более из перечисленных выше методик.
В других вариантах осуществления в настоящем изобретении используется кондиционированная среда от культивированных клеток, полученных из ткани пуповины, для применения in vitro и in vivo, как описано ниже. Использование кондиционированной клетками среды позволяет использовать секретированные клетками, полученными из ткани пуповины, полезные трофические факторы аллогенно для пациента без введения интактных клеток, что может спровоцировать отторжение или другие нежелательные иммунологические ответы. Кондиционированную среду готовят путем культивирования клеток в культуральной среде и последующего удаления клеток из среды.
Кондиционированную среду, приготовленную из популяций клеток, полученных из ткани пуповины, можно использовать непосредственно, в дополнительно сконцентрированном виде, например, с использованием ультрафильтрации или лиофилизации, или даже в высушенном виде, частично высушенном виде, в сочетании с известными в данной области фармацевтически приемлемыми носителями или разбавителями или в сочетании с другими соединениями, такими как биологические соединения, например, фармацевтически эффективными белковыми композициями. Кондиционированную среду можно использовать in vitro или in vivo, индивидуально или, например, вместе с аутогенными или сингенными живыми клетками. При использовании in vivo кондиционированную среду можно вводить локально в месте обработки или удаленно, чтобы обеспечить пациента необходимыми клеточными факторами роста или трофическими факторами.
В другом варианте осуществления в качестве альтернативы имплантации живых клеток субъекту, нуждающемуся в восстановлении или замещении ткани, готовят, собирают и используют внеклеточный матрикс (ECM), полученный культивированием клеток, полученных из ткани пуповины, на жидких, твердых или полутвердых субстратах. Клетки, полученные из ткани пуповины, культивируют in vitro на трехмерном каркасе, как описано ниже в настоящем документе, в условиях, обеспечивающих секретирование необходимого количества ECM на каркас. Клетки, составляющие новую ткань, удаляют и ECM обрабатывают для последующего использования, например, в виде препарата для инъекции. С этой целью клетки на каркасе убивают и продукты распада клеток удаляют с каркаса. Этот процесс можно проводить несколькими различными способами. Например, живую ткань можно резко заморозить в жидком азоте без использования криопротектора, или ткань можно погрузить в стерильную дистиллированную воду таким образом, чтобы клетки лопнули под воздействием осмотического давления.
После гибели клеток клеточные мембраны можно разрушить и продукты распада клеток можно удалить путем обработки мягким моющим средством, таким как этилендиаминтетрауксусная кислота (ЭДТА), 3-[(3-холамидопропил)диметиламмонио]-1-пропансульфонат (CHAPS) или цвиттерионное моющее средство. В альтернативном варианте осуществления ткань можно ферментативно расщепить и/или экстрагировать реагентами, которые разрушают клеточные мембраны и позволяют провести извлечение содержимого клеток. Примеры таких ферментов включают в себя, без ограничений, гиалуронидазу, диспазу, протеазы и нуклеазы. Примеры моющих средств включают в себя неионные моющие средства, такие как, например, алкиларилполиэфирный спирт (TRITON X-100), октилфеноксиполиэтоксиэтанол (Rohm and Haas, г. Филадельфия, штат Пенсильвания), BRIJ-35, полиэтоксиэтаноллауриловый эфир (Atlas Chemical Co., г. Сан-Диего, штат Калифорния), полисорбат 20 (TWEEN 20), полиэтоксиэтанолсорбитанмонолаурат (Rohm and Haas, г. Филадельфия, штат Пенсильвания), полиэтиленлауриловый эфир (Rohm and Haas, г. Филадельфия, штат Пенсильвания); и ионные моющие средства, такие как додецилсульфат натрия, сульфатированные высшие алифатические спирты, сульфонированные алканы и сульфонированные алкиларены, содержащие от 7 до 22 атомов углерода в разветвленной или неразветвленной цепи.
Сбор ECM можно проводить различными способами в зависимости по меньшей мере частично от того, образована ли новая ткань на трехмерном каркасе, который является или не является биоразлагаемым, как в случае с металлами. Например, если каркас не является биоразлагаемым, ECM можно удалить обработкой каркаса ультразвуком, водяными струями высокого давления, механическим соскабливанием или мягкой обработкой моющими средствами или ферментами или любой комбинацией перечисленных выше способов.
Если каркас является биоразлагаемым, ECM можно собрать, например, позволив каркасу разложиться или раствориться в растворе. В альтернативном варианте осуществления, если биоразлагаемый каркас состоит из материала, который можно вводить пациенту вместе с ECM, каркас и ECM можно обрабатывать in toto для последующей инъекции. В альтернативном варианте осуществления ECM можно удалить с биоразлагаемого каркаса любым из описанных выше способов для сбора ECM с каркаса, который не является биоразлагаемым. Все процедуры сбора ECM предпочтительно составляют таким образом, чтобы не допустить денатурации ECM.
После сбора обработку ECM можно продолжить. Например, собранный ECM можно гомогенизировать до мелких частиц с использованием известных в данной области методик, таких как обработка ультразвуком, чтобы обеспечить возможность его прохождения по хирургической игле. При необходимости в компонентах ECM можно также провести поперечную сшивку полимеров гамма-облучением. Предпочтительно для стерилизации и поперечной сшивки ECM доза облучения ECM составляет от 0,25 до 2 мегарад. Также возможна, но по существу не является предпочтительной, химическая поперечная сшивка с использованием токсичных агентов, таких как глутаральдегид.
Количества и/или соотношения белков, таких как различные типы коллагена, присутствующего в ECM, можно корректировать путем смешивания ECM, выработанного клетками, составляющими предмет настоящего изобретения, с ECM одного или более других типов клеток. Кроме того, в ECM можно ввести биологически активные вещества, такие как белки, факторы роста и/или лекарственные средства. Примеры биологически активных веществ включают в себя тканевые факторы роста, такие как TGF-бета, и т.п., которые стимулируют заживление и восстановление ткани в месте введения. Такие дополнительные агенты можно использовать в любом из описанных выше в настоящем документе вариантах осуществления, например, с цельноклеточными лизатами, растворимыми клеточными фракциями или дополнительно очищенными компонентами и продуктами, выработанными клетками, полученными из ткани пуповины.
В другом аспекте в настоящем изобретении предложены фармацевтические композиции, в которых клетки, полученные из ткани пуповины, популяции клеток, полученных из ткани пуповины, компоненты и продукты клеток, полученных из ткани пуповины, используют в различных способах лечения травмы или повреждения, вызванного периферическим ишемическим эпизодом. Определенные варианты осуществления охватывают фармацевтические композиции, содержащие живые клетки (клетки, полученные из ткани пуповины, отдельно или в смеси с клетками других типов). Другие варианты осуществления охватывают фармацевтические композиции, содержащие клеточные компоненты клеток, полученных из ткани пуповины (например, клеточные лизаты, растворимые клеточные фракции, кондиционированную среду, ECM или компоненты любого из перечисленных элементов), или клеточные продукты (например, трофические и другие биологические факторы, вырабатываемые клетками, полученными из ткани пуповины, естественным образом или в результате генетической модификации, кондиционированная среда от культивирования клеток, полученных из ткани пуповины). В любом случае фармацевтическая композиция может дополнительно содержать другие известные в данной области активные агенты, такие как противовоспалительные агенты, антиапоптозные агенты, антиоксиданты, факторы роста, миотропные факторы или миорегенеративные или миопротекторные лекарственные средства.
Примеры других компонентов, которые можно добавить в фармацевтические композиции, включают в себя, без ограничений: (1) другие миостимулирующие или миопротекторные лекарственные средства либо ангиостимулирующие или ангиопротекторные лекарственные средства; (2) выбранные компоненты внеклеточного матрикса, такие как один или более известных в данной области типов коллагенов, и/или факторы роста, плазму с высоким содержанием тромбоцитов и лекарственные средства (в альтернативном варианте осуществления клетки, полученные из ткани пуповины, можно модифицировать методами генной инженерии для экспрессии и выработки факторов роста); (3) антиапоптозные агенты (например, эритропоэтин (EPO), миметические антитела EPO, тромбопоэтин, инсулиноподобные факторы роста IGF-I, IGF-II, фактор роста гепатоцитов, ингибиторы каспазы); (4) противовоспалительные соединения (например, ингибиторы p38 MAP-киназы, ингибиторы TGF-бета, статины, ингибиторы IL-6 и IL-1, Pemirolast, Tranilast, REMICADE® (Centocor, Inc., г. Малверн, штат Пенсильвания), Sirolimus и нестероидные противовоспалительные лекарственные средства (НПВС) (такие как Tepoxalin, Tolmetin и Suprafen); (5) иммуносупрессорные или иммуномодулирующие агенты, такие как ингибиторы кальциневрина, ингибиторы мишени рапамицина в клетках млекопитающих (mTOR), антипролиферативные агенты, кортикостероиды и различные антитела; (6) антиоксиданты, такие как пробукол, витамины C и E, кофермент Q-10, глутатион, L-цистеин и N-ацетилцистеин; (6) местные анестетики; (7) трофические факторы, такие как Agrin, VEGF, VEGF-B, VEGF-C, VEGF-D, NEGF-1, NEGF-2, PDGF, GDF, IGF1, IGF2, EGF и FGF; и (8) факторы, которые участвуют в привлечении и встраивании клеток-предшественников клеток эндотелия в ишемизированную ткань, такие как VEGF, SDF-1, EPO, G-CSF, статины, эстроген, PPARγ и CXCR4, а также многие другие.
Фармацевтические композиции, составляющие предмет настоящего изобретения, содержат клетки, полученные из ткани пуповины, их компоненты или продукты, включая препараты, изготовленные из клеток, полученных из ткани пуповины, в смеси с фармацевтически приемлемым носителем или средой. Подходящие для настоящего изобретения фармацевтически приемлемые носители включают в себя воду, солевой раствор (такой как раствор Рингера), спирты, масла, желатины, поливинилпирролидин, углеводы (такие как лактоза, амилоза или крахмал, эфиры жирных кислот) и гидроксиметилцеллюлозу. Такие препараты можно стерилизовать и при необходимости смешать со вспомогательными агентами, такими как смазывающие вещества, консерванты, стабилизаторы, смачивающие агенты, эмульгаторы, соли для коррекции осмотического давления, буферные растворы и красители. Подходящие для настоящего изобретения фармацевтические носители известны в данной области и описаны, например, в публикациях Pharmaceutical Sciences (17-е изд., Mack Pub. Co., Easton, PA) и международной заявке № WO 96/05309.
Как правило, хотя и не всегда, фармацевтические композиции, содержащие компоненты или продукты клеток, полученных из ткани пуповины, но не живые клетки, готовят в виде жидкостей (или в виде твердых таблеток, капсул и т.п. в случае приемлемости перорального введения). Такие композиции можно готовить для введения любым приемлемым путем, который, как известно в данной области, обеспечивает доставку лекарственных средств и биологических молекул в целевые ткани скелетной мускулатуры, ткани гладкой мускулатуры сосудов, периваскулярной ткани или ткани эндотелия сосудов, включая, без ограничений, пероральный, назальный, глазной и парентеральный пути, включая введение внутривенно. Конкретные пути парентерального введения включают в себя, без ограничений, внутримышечное, подкожное, внутрибрюшинное, подоболочечное или внутриполостное введение с использованием шприцов с иглами или катетеров с использованием или без использования нагнетающих устройств.
Фармацевтические композиции, содержащие живые клетки, полученные из ткани пуповины, как правило, готовят в виде жидкостей, полутвердых композиций (например, гелей (включая фибриновый клей)) или твердых композиций (например, матриц, каркасов и т.п. в соответствии с культивированием тканей сосудов или скелетной мускулатуры). Жидкие композиции готовят для введения любым приемлемым путем, который, как известно в данной области, обеспечивает доставку живых клеток в целевые ткани сосудов или скелетной мускулатуры. Как правило, такие пути включают в себя инъекцию или инфузию, либо диффузным образом, либо целевым образом для доставки в место периферической ишемической травмы, повреждения или нарушения, с использованием пути введения, который включает в себя, без ограничений, внутримышечное, внутривенное или внутриартериальное введение с использованием шприцов с иглами и/или катетеров с использованием или без использования нагнетающих устройств.
Фармацевтические композиции, содержащие живые клетки в полутвердом или твердом носителе, как правило, готовят для хирургической имплантации в месте ишемической травмы, повреждения или нарушения. Следует понимать, что жидкие композиции также можно вводить с использованием хирургических процедур. В конкретных вариантах осуществления полутвердые или твердые фармацевтические композиции могут представлять собой полупроницаемые гели, решетки, клеточные каркасы и т.п., которые могут быть биоразлагаемыми или биологически неразлагаемыми. Например, в определенных вариантах осуществления может оказаться желательно или уместно изолировать экзогенные клетки от их окружения, но при этом позволить клеткам секретировать и доставлять биологические молекулы (например, миотрофические факторы, ангиотрофические факторы или факторы привлечения клеток-предшественников клеток эндотелия) в окружающие клетки скелетной мускулатуры или сосудов. В таких вариантах осуществления клетки можно приготовить в виде автономных имплантатов, содержащих живые клетки, полученные из ткани пуповины, или клеточные популяции, содержащие клетки, полученные из ткани пуповины, окруженные неразлагаемым, селективно проницаемым барьером, который физически отделяет трансплантированные клетки от ткани-хозяина. Такие имплантаты иногда называются «иммунопротекторными», поскольку они обладают способностью не допускать, чтобы клетки и макромолекулы иммунной системы убивали трансплантированные клетки в отсутствие фармакологически индуцированной иммуносупрессии (обзор таких устройств и способов см., например, в работе P.A. Tresco et al., (2000 г.) Adv. Drug Delivery Rev., 42: 3-27).
В других вариантах осуществления для получения фармацевтических композиций, составляющих предмет настоящего изобретения, используют различные виды разлагаемых гелей и сеток. Например, разлагаемые материалы, особенно подходящие для получения составов с замедленным высвобождением, включают в себя биосовместимые полимеры, такие как полимолочная кислота, сополимер молочной и гликолевой кислот, метилцеллюлоза, гиалуроновая кислота, коллаген и т.п. Структура, выбор и применение разлагаемых полимеров в средах доставки лекарственных средств описаны в нескольких публикациях, включая публикацию A. Domb et al., 1992 г., Polymers for Advanced Technologies, 3: 279-292.
В других вариантах осуществления может оказаться желательно или уместно вводить клетки либо на биоразлагаемом, предпочтительно саморассасывающемся, либо биорассасывающемся каркасе или матрице. Такие биоматериалы, как правило, с трехмерной структурой содержат живые клетки, прикрепленные к каркасу, распределенные внутри каркаса или встроенные во внеклеточный матрикс, удерживаемый в каркасе. После имплантирования в целевой участок тела эти имплантаты интегрируются в ткань-хозяина, в которой постепенно укореняются трансплантированные клетки (см. например, работу Tresco, P.A., et al. (2000 г.) выше; см. также Hutmacher, D.W. (2001 г.) J. Biomater. Sci. Polymer Edn., 12: 107-174).
Биосовместимая матрица может состоять из природных, модифицированных природных или синтетических биоразлагаемых полимеров, включая гомополимеры, сополимеры и блок-полимеры, а также их комбинации. Следует отметить, что полимер по существу получает название на основе мономера, из которого он синтезируется.
Примеры подходящих биоразлагаемых полимеров или классов полимеров включают в себя фибрин, коллаген, эластин, желатин, витронектин, фибронектин, ламинин, тромбин, полиаминокислоту, окисленную целлюлозу, тропоэластин, шелк, рибонуклеиновые кислоты, дезоксирибонуклеиновые кислоты; белки, полинуклеотиды, восстановленные матрицы базальной мембраны, крахмалы, декстраны, альгинаты, гиалурон, хитин, хитозан, агарозу, полисахариды, гиалуроновую кислоту, полимолочную кислоту, полигликолевую кислоту, полиэтиленгликоль, децеллюляризованную ткань, самособирающиеся пептиды, полипептиды, гликозаминогликаны, их производные и их смеси. Как для гликолевой, так и для молочной кислоты перед полимеризацией, как правило, готовят и очищают промежуточный циклический димер. Эти промежуточные димеры называются гликолид и лактид соответственно. Другие подходящие биоразлагаемые полимеры или классы полимеров включают в себя, без ограничений, алифатические полиэфиры, полиалкиленоксалаты, поликарбонаты на основе тирозина, полииминокарбонаты, полиортоэфиры, полиоксаэфиры, полиамидоэфиры, полиоксаэфиры с аминными группами, полипропиленфумарат, полидиоксаноны, поликарбонаты, полиоксалаты, поли(альфа-гидроксикислоты), полиэфиры, полиуретаны, полиэфируретаны с простыми и сложными эфирами, полиангидриды, полиацетаты, поликапролактоны, полиортоэфиры, полиаминокислоты, полиамиды, а также их смеси и сополимеры. Дополнительные подходящие биоразлагаемые полимеры включают в себя, без ограничений, стереополимеры L- и D-молочной кислоты, сополимеры бис(пара-карбоксифенокси)пропана и себациновой кислоты, сополимеры себациновой кислоты, сополимеры капролактона, сополимеры молочной кислоты/гликолевой кислоты/полиэтиленгликоля, сополимеры полиуретана и молочной кислоты, сополимеры альфа-аминокислот, сополимеры альфа-аминокислот и капроновой кислоты, сополимеры альфа-бензилглутамата и полиэтиленгликоля, сополимеры сукцината и полигликолей, полифосфазен, полигидроксиалканоаты и их смеси. Также предусматривается возможность использования двойных и тройных систем.
В общем подходящий биоразлагаемый полимер для применения в качестве матрицы желательно выполнен с возможностью обеспечения механических свойств, удовлетворяющих требованиям планируемого применения, остается достаточно интактным до прорастания и заживления ткани, не вызывает воспалительных или токсических реакций, метаболизируется в теле после выполнения своей функции, легко обрабатывается для получения необходимого конечного продукта, имеет приемлемый срок хранения и легко стерилизуется.
В одном аспекте настоящего изобретения биосовместимый полимер, используемый для образования матрицы, имеет форму гидрогеля. В одном варианте осуществления настоящего изобретения гидрогель содержит фибриновый клей. По существу гидрогели представляют собой поперечносшитые полимерные материалы, которые могут впитывать более 20% от своего веса воды, сохраняя при этом заданную трехмерную структуру. Это определение включает в себя сухие поперечносшитые полимеры, которые разбухнут в водной среде, а также разбухшие в воде материалы. Гидрогели можно получить поперечной сшивкой гидрофильных полимеров, при этом полимер может быть биологического происхождения, полусинтетическим или полностью синтетическим. Гидрогель можно получить из синтетического полимерного материала. Такие синтетические полимеры можно получать с заданными свойствами и предсказуемой воспроизводимостью от партии к партии, и они представляют собой надежный источник материала, для которого по существу не стоит проблема иммуногенности. Матрицы могут включать в себя гидрогели, образованные из самособирающихся пептидов, например, таких, как описанные в патентах США №№ 5670483 и 5955343, опубликованной заявке на патент США № 2002/0160471 и публикации PCT № WO 02/062969.
Свойства, которые делают гидрогели ценными при доставке лекарственных средств, включают в себя равновесную степень разбухания, кинетику сорбции, проницаемость к растворенным веществам, а также их характеристики in vivo. Проницаемость к соединениям зависит частично от степени разбухания или содержания воды и скорости биоразложения. Поскольку механическая прочность геля падает прямо пропорционально его степени разбухания, в рамках настоящего изобретения также предусматривается, что гидрогель можно закрепить на субстрате таким образом, что полученная композитная система будет иметь повышенную механическую прочность. В некоторых вариантах осуществления гидрогель можно импрегнировать внутрь пористого субстрата с достижением механической прочности субстрата и полезных свойств гидрогеля как системы доставки.
Неограничивающие примеры каркаса или матрицы (иногда собирательно называемых «каркас»), которые можно использовать в настоящем изобретении, включают в себя текстильные структуры, такие как тканые материалы, вязаные материалы, плетеные материалы, сетки, нетканые материалы и скрученные вязаные материалы; пористые пеноматериалы, полупористые пеноматериалы, перфорированные пленки или листы, микрочастицы, гранулы и сферы, а также композитные структуры, представляющие собой комбинацию перечисленных выше структур. Например, нетканые маты можно образовать с использованием волокна, состоящего из синтетического разлагаемого сополимера гликолевой и молочной кислот (PGA/PLA), доступного в продаже под торговым наименованием нитей VICRYL (Ethicon, Inc., г. Сомервилл, штат Нью-Джерси). Также можно использовать пены, состоящие из, например, сополимера эпсилон-капролактона/гликолевой кислоты (PCL/PGA), сформированные с использованием таких процессов, как лиофильная сушка, или лиофилизация, как описано в патенте США № 6355699. Также можно использовать гидрогели, такие как самособирающиеся пептиды (например, RAD16). В целях настоящего изобретения также можно использовать образованные in situ разлагаемые сетки (см., например, Anseth, KS et al. (2002 г.) J. Controlled Release 78: 199-209; Wang, D. et al., (2003 г.) Biomaterials 24: 3969-3980; публикацию патента США № 2002/0022676, выданного He et al.). Эти образуемые in situ материалы готовят в виде подходящих для инъекции текучих сред, которые затем можно активировать различными способами, например, изменением температуры, pH или освещенности in situ или in vivo для образования гидрогеля.
В другом варианте осуществления каркас представляет собой войлок, который может состоять из мультифиламентной пряжи, изготовленной из биорассасывающегося материала, например, сополимеров или смесей PGA, PLA, PCL или гиалуроновой кислоты. Пряжу сваливают в войлок с использованием стандартных методик обработки текстильных материалов, состоящих из обжатия, нарезки, чесания и простегивания. В другом варианте осуществления клетки высевают на каркасы из пеноматериалов, которые могут представлять собой композитные структуры.
Во многих из указанных выше вариантов осуществления каркасу можно придать подходящую геометрическую форму, такую как форма кровеносного сосуда. Кроме того, следует понимать, что клетки, полученные из ткани пуповины, можно культивировать на заранее образованных неразлагаемых хирургических или имплантируемых устройствах, например, способом, соответствующим способу, применяемому для подготовки содержащих фибробласты внутрисосудистых разделяемых спиралей GDC (Marx, W.F. et al., (2001 г.) Am. J. Neuroradiol. 22: 323-333).
Перед посевом клеток матрицу, каркас или устройство можно обработать для улучшения клеточной адгезии. Например, перед посевом клеток нейлоновые матрицы можно обработать 0,1 молярным раствором уксусной кислоты и инкубировать в полилизине, PBS и/или коллагене для покрытия нейлона. Полистирол можно аналогичным образом обработать серной кислотой. Можно также модифицировать внешние поверхности каркаса для улучшения клеточной адгезии или роста клеток и дифференцирования ткани, используя, например, плазменное покрытие каркаса или добавление одного или более белков (например, коллагенов, эластичных волокон, ретикулярных волокон), гликопротеинов, гликозаминогликанов (например, гепаринсульфата, хондроитин-4-сульфата, хондроитин-6-сульфата, дерматансульфата, кератинсульфата), генетических материалов, таких как цитокины и факторы роста, клеточного матрикса и/или других материалов, включая, без ограничений, желатин, альгинаты, агар, агарозу и растительные камеди и т.п., помимо прочих факторов, влияющих на выживаемость и дифференцирование клеток.
Каркасы, содержащие клетки hUTC, готовят в соответствии со способами, известными в данной области. Например, клетки можно растить свободно в сосуде для культивирования до получения субконфлюентной или конфлюентной культуры, затем изъять из культуры и засеять на каркас. При необходимости в культуральную среду до, во время или после высевания клеток можно добавить факторы роста для инициирования дифференцирования клеток и формирования ткани. В альтернативном варианте осуществления сами каркасы можно модифицировать таким образом, чтобы улучшить рост клеток на них или снизить риск отторжения имплантата. Таким образом, в каркас можно добавить одно или более биологически активных соединений, включая, без ограничений, противовоспалительные соединения, иммуносупрессоры или факторы роста, для их местного высвобождения.
Клетки, полученные из ткани пуповины, части клеток, полученных из ткани пуповины, или клеточные популяции, содержащие клетки, полученные из ткани пуповины, или компоненты или продукты, вырабатываемые клетками, полученными из ткани пуповины, можно использовать различными способами для поддержания и облегчения восстановления, регенерации и улучшения состояния клеток и тканей скелетной мускулатуры, для улучшения кровотока и для стимулирования и/или поддержки ангиогенеза, особенно у пациентов с заболеванием периферических сосудов. Такие возможности охватывают способы in vitro, ex vivo и in vivo.
В одном варианте осуществления, как описано выше, клетки, полученные из ткани пуповины, можно культивировать in vitro для выработки биологических продуктов, которые либо вырабатываются клетками естественным образом, либо вырабатываются клетками после их индуцирования для дифференцирования по линиям дифференцирования клеток скелетных мышц, клеток гладких мышц сосудов, периваскулярных клеток или клеток эндотелия сосудов, либо вырабатываются клетками в результате их генетической модификации. Например, обнаружена секреция TIMP1, TPO, KGF, HGF, FGF, HBEGF, BDNF, MIP1-бета, MCP1, RANTES, I309, TARC, MDC и IL-8 клетками, полученными из пуповины и выращенными в ростовой среде. Кроме того, клетки, полученные из ткани пуповины, могут вырабатывать и секретировать в ростовую среду факторы для привлечения клеток-предшественников клеток эндотелия, таких как VEGF, SDF-1, EPO, G-CSF, статины, эстроген, PPARγ и CXCR4. Клетки, полученные из ткани пуповины, также могут вырабатывать и возможно секретировать в среду другие трофические факторы, пока не обнаруженные или не изученные, для использования при восстановлении и регенерации тканей сосудов или скелетной мускулатуры.
В связи с этим в другом варианте осуществления настоящего изобретения описано использование клеток, полученных из ткани пуповины, для выработки кондиционированной среды либо из недифференцированных клеток, полученных из ткани пуповины, либо из клеток, полученных из ткани пуповины, инкубированных в условиях, которые стимулируют их дифференцирование по линиям дифференцирования клеток скелетной мускулатуры или сосудов. Для таких кондиционированных сред предусматривается применение для культивирования in vitro или ex vivo клеток-предшественников клеток скелетных мышц, клеток гладких мышц сосудов, периваскулярных клеток или клеток эндотелия сосудов, или in vivo для поддержания трансплантированных клеток, содержащих однородные популяции клеток, полученных из ткани пуповины, или неоднородных популяций, содержащих клетки, полученные из ткани пуповины, и клетки-предшественники клеток скелетных мышц, клеток гладких мышц сосудов, периваскулярных клеток или клеток эндотелия, или, например, для привлечения клеток-предшественников клеток эндотелия к месту ишемической травмы.
Другой вариант осуществления содержит применение лизатов клеток hUTC, их растворимых клеточных фракций или компонентов, либо ECM или его компонентов в различных целях. Как указано выше, некоторые из этих компонентов можно применять в фармацевтических композициях. В других вариантах осуществления клеточный лизат или ECM используют для нанесения покрытия или другой обработки веществ или устройств, предназначенных для использования при выполнении хирургической операции или для имплантации, либо для целей ex vivo, для стимуляции заживления или повышения выживаемости клеток или тканей, с которыми производится контакт при выполнении таких процедур. В некоторых предпочтительных вариантах осуществления такие препараты, изготовленные из клеток, полученных из ткани пуповины, содержат FGF и HGF.
В другом варианте осуществления клетки, полученные из ткани пуповины, используют преимущественно при совместном культивировании in vitro для обеспечения трофической поддержки другим клеткам, более конкретно, клеткам скелетных мышц, клеткам-предшественникам клеток скелетных мышц, клеткам гладких мышц сосудов, клеткам-предшественникам клеток гладких мышц сосудов, периваскулярным клеткам, клеткам эндотелия сосудов или клеткам-предшественникам клеток эндотелия сосудов. В некоторых предпочтительных вариантах осуществления трофическая поддержка состоит в пролиферации клеток. При совместном культивировании для клеток, полученных из ткани пуповины, и других необходимых клеток может быть необходимо совместное культивирование в условиях, обеспечивающих контакт между клетками двух типов. Этого можно достичь, например, высевая клетки в культуральной среде или на подходящий культуральный субстрат в виде неоднородной популяции клеток. В альтернативном варианте осуществления можно сначала нарастить клетки, полученные из ткани пуповины, до конфлюентности культуры, которая затем будет служить субстратом для культивирования клеток второго необходимого типа клеток. В этом последнем варианте осуществления клетки можно дополнительно физически разделить, например, с помощью мембраны или аналогичного устройства таким образом, чтобы после периода совместного культивирования клетки другого типа можно было снять и использовать отдельно. Применение клеток, полученных из ткани пуповины, при совместном культивировании для стимулирования размножения и дифференцирования клеток скелетной мускулатуры или сосудов может найти применение в исследовательской и клинической/терапевтической практике. Например, совместное культивирование с клетками, полученными из ткани пуповины, можно использовать для облегчения роста и дифференцирования клеток скелетных мышц, клеток гладких мышц сосудов, периваскулярных клеток или клеток эндотелия сосудов в культуре для исследовательских целей или, например, для использования при скрининге лекарственных средств. Совместное культивирование с клетками, полученными из ткани пуповины, можно также использовать для размножения ex vivo клеток-предшественников клеток скелетных мышц, клеток гладких мышц сосудов, периваскулярных клеток или клеток эндотелия сосудов для последующего введения в терапевтических целях. Например, у пациента можно взять клетки-предшественники клеток скелетных мышц, клеток гладких мышц сосудов, периваскулярных клеток или клеток эндотелия сосудов, размножить их ex vivo при совместном культивировании с клетками, полученными из ткани пуповины, и затем вернуть их обратно тому же пациенту (аутогенный перенос) или другому пациенту (сингенный или аллогенный перенос). Следует понимать, что в этих вариантах осуществления после размножения ex vivo смешанную популяцию клеток, содержащую клетки, полученные из ткани пуповины, и клетки-предшественники клеток скелетных мышц, клеток гладких мышц сосудов, периваскулярных клеток или клеток эндотелия сосудов, можно ввести пациенту, нуждающемуся в лечении. В альтернативном варианте осуществления в ситуациях, когда уместен или желателен аутогенный перенос, совместно культивируемые популяции клеток можно при культивировании держать физически разделенными, что позволит отделить клетки-предшественники клеток скелетных мышц, клеток гладких мышц сосудов, периваскулярных клеток или клеток эндотелия сосудов для введения пациенту.
В патентных публикациях США №№ 2005/0058631, 2005/0054098 и 2005/0058630 показана эффективная трансплантация клеток, полученных из ткани пуповины, в тело и улучшение кровотока и снижение некроза ткани в общепринятой животной модели. Эти наблюдения вместе с открытиями, изложенными в настоящем изобретении, поддерживают предпочтительные варианты осуществления настоящего изобретения, в которых клетки, полученные из ткани пуповины, используют в клеточной терапии для лечения ишемической травмы или повреждения путем восстановления или регенерации ткани скелетной мускулатуры и/или сосудов у пациента с заболеванием периферических сосудов или путем улучшения кровотока или стимулирования и/или поддержания ангиогенеза у пациента с заболеванием периферических сосудов. В одном варианте осуществления клетки, полученные из ткани пуповины, трансплантируют в целевое место в теле, в частности, в место или рядом с местом ишемического эпизода, где клетки, полученные из ткани пуповины, могут дифференцироваться в клетки одного или более из фенотипов клеток скелетных мышц, клеток гладких мышц сосудов, периваскулярных клеток или клеток эндотелия сосудов, клетки, полученные из ткани пуповины, могут обеспечивать трофическую поддержку для клеток-предшественников клеток скелетных мышц, клеток гладких мышц сосудов, периваскулярных клеток или клеток эндотелия сосудов и/или клеток скелетных мышц, клеток гладких мышц сосудов, периваскулярных клеток или клеток эндотелия сосудов in situ, клетки, полученные из ткани пуповины, могут вырабатывать факторы для привлечения клеток-предшественников клеток эндотелия к месту ишемической травмы, или клетки, полученные из ткани пуповины, могут оказывать положительный эффект, помимо прочего, двумя или более из описанных способов. Клетки, полученные из ткани пуповины, секретируют трофические факторы, включая, без ограничений, GFGFm, IL-6, IL-8, HGF, IGF-1, TPO и т.п. Клетки, полученные из ткани пуповины, могут способствовать привлечению клеток-предшественников клеток сосудов, таких как ангиобласты, для стимулирования формирования новых кровеносных сосудов.
Клетки, полученные из ткани пуповины, могут оказывать трофический эффект в теле пациента, которому их вводят. Например, клетки, полученные из ткани пуповины, могут оказывать трофический эффект на клетки скелетных мышц, клетки гладких мышц сосудов, клетки эндотелия сосудов, периваскулярные клетки или на их клетки-предшественники. В некоторых предпочтительных вариантах осуществления трофический эффект состоит в пролиферации таких клеток. Клетки, полученные из ткани пуповины, также могут индуцировать миграцию клеток в теле пациента, которому их вводят. Такая миграция может облегчить восстановление, регенерацию и лечение заболевания периферических сосудов, такого как ишемия периферических сосудов. Например, клетки, полученные из ткани пуповины и вводимые в месте или рядом с местом заболевания периферических сосудов, могут индуцировать миграцию клеток к месту заболевания периферических сосудов для восстановления, регенерации или иной терапии пораженной ткани и ее окружения. Введенные таким образом клетки, полученные из ткани пуповины, могут индуцировать миграцию клеток скелетных мышц, клеток гладких мышц сосудов, клеток эндотелия сосудов, периваскулярных клеток или их клеток-предшественников. В предпочтительных вариантах осуществления клетки, полученные из ткани пуповины, индуцируют миграцию клеток-предшественников клеток эндотелия сосудов и/или клеток эндотелия сосудов к месту или по меньшей мере к окрестности места заболевания периферических сосудов. В некоторых вариантах осуществления миграция индуцируется или поддерживается FGF и/или HGF, предпочтительно FGF и HGF, которые экспрессируются клетками, полученными из ткани пуповины. Препараты, изготовленные из клеток, полученных из ткани пуповины, включая клеточные лизаты, субклеточные фракции и т.п., также можно использовать для лечения заболевания периферических сосудов. Такие препараты можно готовить в смеси с фармацевтически приемлемыми носителями, такими как описанные и проиллюстрированные в настоящем документе, и вводить пациентам в количествах, эффективных для лечения заболевания периферических сосудов. В предпочтительных вариантах осуществления препараты, изготовленные из клеток, полученных из ткани пуповины, содержат FGF и HGF.
Конкретные варианты осуществления настоящего изобретения направлены на непосредственное восстановление, регенерацию, замещение либо на поддержку восстановления, регенерации или замещения кровеносных сосудов для лечения периферической ишемической травмы или повреждения.
Клетки, полученные из ткани пуповины, можно вводить самостоятельно (например, в виде по существу однородных популяций) или в виде примесей с другими клетками. Как описано выше, клетки, полученные из ткани пуповины, можно вводить в составе фармацевтического препарата на основе матрицы или каркаса, либо в стандартных фармацевтически приемлемых носителях. При введении клеток, полученных из ткани пуповины, вместе с другими клетками их можно вводить одновременно или последовательно с другими клетками (перед другими клетками или после них). Клетки, которые можно вводить вместе с клетками, полученными из ткани пуповины, включают в себя, без ограничений, миоциты, клетки скелетных мышц, клетки-предшественники клеток скелетных мышц, клетки гладких мышц сосудов, клетки-предшественники клеток гладких мышц сосудов, периваскулярные клетки, клетки эндотелия сосудов или клетки-предшественники клеток эндотелия сосудов и/или другие мультипотентные или плюрипотентные стволовые клетки. Клетки других типов можно смешивать с клетками, полученными из ткани пуповины, непосредственно во время или незадолго перед введением, либо клетки можно совместно культивировать в течение некоторого периода времени перед введением.
Клетки, полученные из ткани пуповины, можно вводить вместе с другими благоприятными лекарственными средствами или биологическими молекулами, либо другими активными агентами, такими как противовоспалительные агенты, антиапоптозные агенты, антиоксиданты, факторы роста, ангиогенные факторы или миорегенеративные или миопротекторные лекарственные средства, известные в данной области. При введении клеток, полученных из ткани пуповины, совместно с другими агентами их можно вводить вместе в виде одной фармацевтической композиции или в отдельных фармацевтических композициях одновременно или последовательно с другими агентами (перед введением других агентов или после него). Другие агенты могут быть частью курса лечения, который начинают либо перед трансплантацией и затем продолжают на протяжении всего курса восстановления, либо начинают его в момент трансплантации, или даже после трансплантации, на усмотрение врача с опытом в данной области.
Примеры других соединений, которые можно вводить вместе с клетками, полученными из ткани пуповины, включают в себя, без ограничений: (1) другие ангиогенные факторы, ангиогенные лекарственные средства или миорегенеративные или миопротекторные факторы или лекарственные средства; (2) выбранные компоненты внеклеточного матрикса, такие как один или более известных в данной области типов коллагенов, и/или факторы роста, плазму с высоким содержанием тромбоцитов и лекарственные средства (в альтернативном варианте осуществления клетки, полученные из ткани пуповины, можно модифицировать методами генной инженерии для экспрессии и выработки факторов роста); (3) антиапоптозные агенты (например, эритропоэтин (EPO), миметические антитела EPO, тромбопоэтин, инсулиноподобные факторы роста IGF-I, IGF-II, фактор роста гепатоцитов, ингибиторы каспазы); (4) противовоспалительные соединения (например, ингибиторы p38 MAP-киназы, ингибиторы TGF-бета, статины, ингибиторы IL-6 и IL-1, Pemirolast, Tranilast, REMICADE® (Centocor, Inc., г. Малверн, штат Пенсильвания), Sirolimus и нестероидные противовоспалительные лекарственные средства (НПВС) (такие как Tepoxalin, Tolmetin и Suprafen); (5) иммуносупрессорные или иммуномодулирующие агенты, такие как ингибиторы кальциневрина, ингибиторы мишени рапамицина в клетках млекопитающих (mTOR), антипролиферативные агенты, кортикостероиды и различные антитела; (6) антиоксиданты, такие как пробукол, витамины C и E, кофермент Q-10, глутатион, L-цистеин и N-ацетилцистеин; и (6) местные анестетики и т.п.
В одном варианте осуществления клетки, полученные из ткани пуповины, вводят в виде недифференцированных клеток, т.е. в том виде, в котором их культивировали в ростовой среде. В альтернативном варианте осуществления клетки, полученные из ткани пуповины, можно вводить после их обработки в культуре в условия, которые стимулируют их дифференцирование в направление необходимых фенотипов клеток скелетных мышц, клеток гладких мышц сосудов, периваскулярных клеток или клеток эндотелия сосудов.
Клетки, составляющие предмет настоящего изобретения, можно имплантировать хирургическим путем, вводить шприцом, доставлять (например, с помощью катетера, шприца, шунта, стента, микрокатетера или насоса) или иным образом вводить напрямую или опосредованно в место ишемической травмы, повреждения или нарушения. Способы введения клеток, составляющих предмет настоящего изобретения, или содержащих их композиций включают в себя, без ограничений, внутривенный, внутримышечный, подкожный, интраназальный, подоболочечный, внутриполостной способ или способ введения с использованием шприцов с иглами или катетеров с помощью нагнетающих устройств или без них.
При введении клеток в составе полутвердых или твердых устройств подходящим средством введения, как правило, является хирургическая имплантация в определенное место в теле. Однако жидкие или текучие фармацевтические композиции можно вводить через кровь или непосредственно в пораженную мышечную ткань (например, по всей диффузно пораженной области, что имеет место при диффузной ишемической травме). Миграцию клеток, полученных из ткани пуповины, можно направлять с помощью химических сигналов, факторов роста или кальпаинов.
Клетки, полученные из ткани пуповины, или композиции и/или матрицы, содержащие клетки, полученные из ткани пуповины, можно вводить в необходимое место с помощью микрокатетера, интракатетеризации или через мини-насос. В качестве используемого эксципиента или носителя можно выбрать любой фармацевтически приемлемый для введения пациенту эксципиент или носитель, в частности, локально в месте, где будет проводиться индукция клеточного дифференцирования. Примеры включают в себя жидкие среды, например, модифицированную по способу Дульбекко среду Игла (DMEM), стерильный физиологический раствор, стерильный фосфатно-буферный раствор, среду Лейбовица (L15, Invitrogen, г. Карлсбад, штат Калифорния), раствор декстрозы в стерильной воде и любую другую физиологически приемлемую жидкость.
Другие варианты осуществления охватывают способы лечения периферической ишемической травмы или нарушения путем введения терапевтических композиций, содержащих фармацевтически приемлемый носитель и компоненты клеток, полученных из ткани пуповины (например, клеточные лизаты или их компоненты), либо их продукты (например, трофические и другие биологические факторы, вырабатываемые клетками, полученными из ткани пуповины, естественным образом или в результате их генетической модификации, кондиционированная среда от культивирования клеток, полученных из ткани пуповины) или ростовую среду клеток, полученных из ткани пуповины, либо продукты, выделенные из такой ростовой среды. В предпочтительных вариантах осуществления биологические факторы представляют собой FGF и HGF. Данные способы могут дополнительно содержать введение других активных агентов, таких как факторы роста, ангиогенные факторы, миорегенераторы или миопротекторы, известные в данной области.
Дозированные формы и режимы введения клеток, полученных из ткани пуповины, или любых других терапевтических или фармацевтических композиций, описанных в настоящем документе, разрабатывают в соответствии с надлежащей медицинской практикой, принимая во внимание состояние конкретного пациента, например, природу и степень травмы или повреждения в результате периферического ишемического события, возраст, пол, вес тела и общее состояние пациента, а также другие известные медицинским работникам факторы. Таким образом, эффективное количество фармацевтической композиции для введения пациенту определяется с учетом этих соображений, как известно в данной области.
Результаты показали, что клетки, полученные из ткани пуповины, не стимулируют аллогенные МКПК в реакции смешанной культуры лимфоцитов. Таким образом, в некоторых случаях допустима трансплантация с аллогенными или даже ксеногенными клетками, полученными из ткани пуповины. В некоторых вариантах осуществления клетки, полученные из ткани пуповины, сами обеспечивают иммуносупрессорный эффект, предотвращая посредством этого отторжение организмом-хозяином трансплантированных клеток, полученных из ткани пуповины. В таких случаях можно обойтись без фармакологического подавления иммунитета в ходе клеточной терапии.
Однако в других случаях может быть необходимо или уместно фармакологическое подавление иммунитета у пациента перед началом клеточной терапии. Этого можно достичь применением местных или системных иммуносупрессорных агентов, либо же этого можно достичь доставкой клеток в инкапсулированном устройстве, как описано выше. В данной области известны эти и другие способы снижения или устранения иммунного ответа на трансплантированные клетки. В качестве альтернативы клетки, полученные из ткани пуповины, можно генетически модифицировать для снижения их иммуногенности, как описано выше.
Выживаемость трансплантированных клеток, полученных из ткани пуповины, у живого пациента можно определить путем использования различных методик сканирования, например, с помощью исследования компьютерной аксиальной томографией (КАТ или КТ), магниторезонансной томографией (МРТ) или позитронно-эмиссионной томографией (ПЭТ). Определение выживаемости трансплантированных клеток можно также провести post mortem путем извлечения скелетной мышцы или сосудистой ткани и изучения ее визуально или с помощью микроскопа. В альтернативном варианте осуществления клетки можно обработать красителем, специфичным к клеткам скелетных мышц, клеткам гладких мышц сосудов, периваскулярным клеткам или клеткам эндотелия сосудов. Трансплантированные клетки также можно идентифицировать по предварительно введенным в них меткам-красителям, таким как микросферы, меченные родамином или флуоресцеином, быстрый голубой, микрочастицы железа, бисбензамид или продукты генетически встроенного репортерного гена, такие как бета-галактозидаза или бета-глюкуронидаза.
В другом аспекте в настоящем изобретении предложены наборы, в которых в различных способах используют клетки, полученные из ткани пуповины, популяции клеток, полученных из ткани пуповины, компоненты и продукты клеток, полученных из ткани пуповины, для стимулирования и/или поддержания ангиогенеза, для улучшения кровотока, для регенерации, восстановления и улучшения состояния скелетной мускулатуры, травмированной или поврежденной периферическим ишемическим событием, как описано выше. При использовании для лечения повреждения или травмы, вызванных ишемическим событием, или другого предписанного лечения наборы могут включать в себя одну или более клеточных популяций, включая по меньшей мере клетки, полученные из ткани пуповины, и фармацевтически приемлемый носитель (в жидком, полутвердом или твердом состоянии). Наборы также могут необязательно включать в себя средство для введения клеток, например, путем инъекции. Наборы могут дополнительно включать в себя инструкции по применению клеток. Наборы, приготовленные для использования в условиях полевого госпиталя, как, например, в условиях боевых действий, могут включать в себя полный комплект для проведения всей процедуры, включая каркасы тканей, хирургические нити и т.п., где клетки будут использоваться в сочетании с восстановлением острых поражений. Наборы для проведения анализов и способов in vitro, описанные в настоящем документе, могут содержать одни или более из (1) клеток, полученных из ткани пуповины, или компонентов или продуктов клеток, полученных из ткани пуповины; (2) реагентов для осуществления способа in vitro; (3) других клеток или популяций клеток, если это необходимо; и (4) инструкций по осуществлению способа in vitro.
Следующие примеры более подробно описывают настоящее изобретение. Эти примеры предназначены для дополнительного иллюстрирования, но не для ограничения, аспектов настоящего изобретения, описанных в настоящем документе.
Пример 1
Эффективность клеток, полученных из пуповины, в модели ишемии периферических сосудов задней конечности мыши
Материалы и способы
Культивирование и выделение клеток пуповины. Клетки, полученные из пуповины, (UDC) приготовили, как описано в патентных публикациях США №№ 2005/0058631 или 2005/0054098. Клетки культивировали до пассажа 10 или 11 (приблизительно от 20 до 25 удвоений популяции) и затем криоконсервировали.
Клеточная линия 2: U072804A p11
Подготовка образца для инъекции. Клетки размораживали непосредственно перед инъекцией (группы 3-5) или культивировали в течение 24-30 часов (группа 6). Клетки подсчитывали и определяли их жизнеспособность окрашиванием трипановым голубым и подсчитыванием на гемоцитометре. Всю дозу клеток или плазмиды (100 мкг) ресуспендировали в 100 мкл PBS и набирали в туберкулиновый шприц объемом 300 мкл с иглой 27 размера для инъекции мышам.
Хирургическая операция. На 0 сутки у бестимусных мышей хирургически индуцировали острую ишемию задней конечности путем одностороннего лигирования и вырезания левой подвздошно-бедренной артерии. Мышей разбивали на 6 групп, по меньшей мере n=8 животных в группе, для обработки клетками UDC или в качестве контролей. Мышей случайным образом распределяли по группам обработки 1-5. Поскольку группу 6 добавили позднее по ходу исследования, рандомизации не было. Кроме того, накладки в планировании не позволили провести микроКТ/ПЭТ одновременно с первичным исследованием. Этот анализ провели на группе из 8 дополнительных животных (4 контрольных и 4 с культивированными клетками линии 1), взятых после окончания исследования в течение 21 суток.
Инъекции клеток. Через сутки после хирургической операции мышей анестезировали для анализа подошвенного участка с использованием лазерной доплеровской визуализации. Все еще находящимся под воздействием анестезии мышам инъекционно ввели клетки в 5 местах левой (ишемизированной) конечности: (1) 20 мкл в переднюю большеберцовую мышцу; (2) 2×20 мкл в икроножную мышцу; и (3) 2×20 мкл в прямую мышцу бедра у четырехглавого узла.
Анализы. Анализ с использованием лазерной доплеровской визуализации проводили на 1, 4, 8, 14 и 21 сутки. На 21 сутки мышей умерщвляли, переднюю большеберцовую мышцу, икроножную мышцу и мышцы четырехглавого узла вырезали и криофиксировали для подготовки тонких срезов и иммуногистохимического окрашивания антителом к CD31. На 8 сутки проводили микроКТ/ПЭТ-анализ с использованием газообразного фторметана для определения перфузионного статуса мышц. Этих мышей умерщвляли сразу после анализа и обрабатывали мышцы задней конечности для гистохимического анализа к CD31 на криофиксированных тонких срезах.
Критерии исключения. Мышей с тяжелым некрозом большого пальца на 1 сутки после хирургической операции исключали из исследования перед проведением инъекций. Мышей также исключали из исследования в любой момент исследования при обнаружении тяжелой формы некроза (например, полного некроза ступни) или при выявлении значительной потери веса или проявлении иных признаков очень сильной боли.
Результаты
Целью данных экспериментов являлось определение того, защищают ли клетки UDC ткани от травмы в модели ишемии задней конечности у грызунов. Эту модель реализовывали путем создания травмы в бедренном пути кровотока и инъекции клеток в пораженную область приблизительно через 24 часа после травмы. Результаты анализировали путем оценки степени перфузии конечностей данных животных и сравнения ее с неповрежденной контралатеральной конечностью. Также по окончании исследования у данных животных забирали ткани для оценки степени развития системы сосудов и травмы у животных. Это исследование также проводили с клетками человека в бестимусных мышах во избежание ксеногенного отторжения имплантированных клеток.
Представленные на фигуре 1 результаты показывают, что клетки UDC оказали благоприятный эффект у мышей, поскольку у животных, обработанных культивированными клетками, наблюдали улучшенную перфузию на 4 и 8 сутки, а у животных, обработанных клетками партии № 120304, размороженными непосредственно перед введением, также наблюдали улучшенный кровоток на 8 сутки. Клетки партии № 072804A не продемонстрировали благоприятного эффекта ни в какой момент времени, что указывает на возможные различия между этими двумя партиями клеток. По существу у животных со временем наблюдалось улучшение состояния, что указывает на наличие определенной врожденной способности к восстановлению у этой линии животных. Эти животные также были относительно молоды, что могло сыграть свою роль в их внутреннем потенциале к регенерации.
В конце исследования забирали переднюю большеберцовую мышцу животных и ее срезы анализировали с использованием антитела к CD31 для выявления клеток эндотелия сосудов. Некоторые репрезентативные результаты приведены на фигуре 2. Результаты показывают, что у животных из контрольной группы с обработкой PBS наблюдали тяжелый некроз и ограниченное развитие системы кровеносных сосудов в ишемизированной конечности (например, мыши № 26 и № 43), тогда как в конечностях, обработанных клетками UDC, наблюдали более высокие относительные уровни по окрашиванию к CD31 и пониженный уровень некроза. Результаты также указывают, что у животных, обработанных культивированными клетками UDC, наблюдается более развитая система кровеносных сосудов по сравнению с контрольными животными (обработанные PBS животные и, в некоторых случаях, нормальная (нетравмированная) конечность). Повышение уровня окрашивания к CD31 наблюдали в ишемизированной, но обработанной конечности по сравнению с нормальной конечностью. Для животных, обработанных плазмидой VEGF и клетками партии Umb072804A, были получены такие же результаты, что и для контрольных животных с обработкой PBS.
Сводная информация
Эти результаты подтверждают, что клетки, полученные из пуповины, могут быть эффективны для улучшения кровотока и для снижения степени некроза ткани в модели ишемии задней конечности у грызунов. В исследовании использовали две разные партии клеток пуповины, которые размораживали непосредственно перед инъекцией, и полученные результаты указывают на возможное различие между двумя партиями. Клетки, демонстрировавшие активность, также культивировали перед инъекцией в течение приблизительно 48 часов и включили их в другую группу обработки. Эти клетки продемонстрировали максимальную эффективность, и это указывает на возможное изменение профиля активности клеток с культивированием. Гистологические результаты также подтверждают, что описываемая обработка может оказывать положительное действие. Эти результаты не дают достаточной информации относительно механизма, по которому клетки UDC оказывают свое действие. Без ограничения какой-либо конкретной теорией или механизмом действия считается, что клетки могут оказывать свое действие путем стимулирования роста новых кровеносных сосудов или защиты мышечной ткани от прогрессирования повреждения, например, путем защиты от апоптоза или привлечения эндогенных активных агентов. Для исследования точного механизма действия требуются дополнительные исследования.
Литература
1) Rehman, J. et al. (2004 г.) Circulation 109: 1292-1298.
Пример 2
Анализ формирования сети эндотелия
Для роста новой ткани необходим ангиогенез или формирование новой сосудистой системы. Индуцирование ангиогенеза является важной терапевтической целью при многих патологических состояниях. Для выявления потенциальной ангиогенной активности клеток, полученных из ткани пуповины, в анализах in vitro использовали хорошо отработанный способ высевания клеток эндотелия на культуральные планшеты, покрытые биологическим клеточным культуральным субстратом, доступным в продаже под торговым наименованием MATRIGEL (BD Discovery Labware, г. Бедфорд, штат Массачусетс), экстрактом базальной мембраны (Nicosia and Ottinetti (1990 г.) In vitro Cell Dev. Biol. 26(2): 119-28). Обработка клеток эндотелия на MATRIGEL (BD Discovery Labware, г. Бедфорд, штат Массачусетс) ангиогенными факторами стимулирует клетки к образованию сети, аналогичной капиллярам. Это представляет собой стандартный анализ in vitro для проверки стимуляторов и ингибиторов формирования кровеносных сосудов (Ito et al. (1996 г.) Int. J. Cancer 67(1): 148-52). В проводимых экспериментах использовали системы совместного культивирования, высевая клетки, полученные из ткани пуповины, на вкладыши в лунки для культивирования. Эти проницаемые вкладыши позволяют осуществлять пассивный обмен компонентов среды между средами для культивирования клеток эндотелия и клеток, полученных из ткани пуповины.
Способы и материалы
Клеточная культура
Клетки, полученные из ткани пуповины и плаценты. Получили пуповины и плаценту человека и выделили клетки, как описано выше (см. пример 1). Клетки культивировали в ростовой среде (модифицированная по способу Дульбекко среда Игла (DMEM; Invitrogen, г. Карлсбад, штат Калифорния), 15% (об./об.) фетальной бычьей сыворотки (Hyclone, г. Логан, штат Юта), 100 единиц/миллилитр пенициллина, 100 микрограмм/миллилитр стрептомицина (Invitrogen), 0,001% (об./об.) 2-меркаптоэтанола (Sigma, г. Сент-Луис, штат Миссури)) на покрытых желатином пластиковых культуральных сосудах. Культуры инкубировали при температуре 37°C в атмосфере с содержанием 5% CO2. Для экспериментов использовали клетки с пассажами между 4 и 12.
Активно растущие клетки трипсинизировали, подсчитывали и высевали на вкладыши для культивирования тканей COSTAR TRANSWELL диаметром 6,5 миллиметра (Corning, г. Корнинг, штат Нью-Йорк) в количестве 15000 клеток на вкладыш. Клетки культивировали на вкладышах в течение от 48 до 72 часов в ростовой среде при температуре 37°C в стандартных условиях роста.
Мезенхимальные стволовые клетки человека (hMSC). Клетки hMSC приобрели у компании Cambrex (г. Уолкерсвилл, штат Мэриленд) и культивировали в среде MSCGM (Cambrex). Культуры инкубировали в стандартных условиях роста.
Активно растущие клетки MSC трипсинизировали, подсчитывали и высевали на вкладыши для культивирования тканей COSTAR TRANSWELL диаметром 6,5 миллиметра (Corning, г. Корнинг, штат Нью-Йорк) в количестве 15000 клеток на вкладыш. Клетки культивировали на вкладышах в течение 48-72 часов в ростовой среде в стандартных условиях роста.
Клетки эндотелия пуповинной вены человека (HUVEC). Клетки HUVEC приобрели у компании Cambrex (г. Уолкерсвилл, штат Мэриленд). Клетки выращивали в отдельных культурах либо в среде EBM, либо в среде EGM для клеток эндотелия (Cambrex). Клетки выращивали на стандартном культивированном тканью пластике в стандартных условиях роста. Для анализов использовали клетки с пассажами между 4 и 10.
Клетки эндотелия коронарной артерии человека (HCAEC). Клетки HCAEC приобрели у компании Cambrex Incorporated (г. Уолкерсвилл, штат Мэриленд). Эти клетки также поддерживали в отдельных культурах в составе либо среды EBM, либо среды EGM. Клетки выращивали на стандартном культивированном тканью пластике в стандартных условиях роста. Для экспериментов использовали клетки с пассажами между 4 и 8.
Анализы формирования сети эндотелия (MATRIGEL). Культуральные планшеты покрывали препаратом MATRIGEL (BD Discovery Labware, г. Бедфорд, штат Массачусетс) в соответствии с указаниями производителя. Вкратце, MATRIGEL (BD Discovery Labware, г. Бедфорд, штат Массачусетс) размораживали при температуре 4°C и приблизительно 250 микролитров добавляли и равномерно распределяли по каждой лунке охлажденного 24-луночного культурального планшета (Corning). Затем планшет инкубировали при температуре 37°C в течение 30 минут, чтобы дать материалу затвердеть. Активно растущие культуры клеток эндотелия трипсинизировали и подсчитывали. Клетки дважды промывали в ростовой среде с добавлением 2% FBS путем центрифугирования, ресуспендирования и отсасывания супернатанта. Клетки высевали на покрытые лунки в количестве 20000 клеток на лунку в приблизительно 0,5 миллилитра ростовой среды с добавлением 2% (об./об.) FBS. Затем клетки инкубировали в течение приблизительно 30 минут, чтобы дать клеткам возможность осесть.
После этого культуры клеток эндотелия обрабатывали либо 10-наномолярным раствором bFGF человека (Peprotech, г. Роки-Хилл, штат Нью-Джерси), либо 10-наномолярным раствором VEGF человека (Peprotech, г. Роки-Хилл, штат Нью-Джерси) для подготовки положительного контроля для отклика клеток эндотелия. Затем в соответствующие лунки поместили вкладыши трансвел с высеянными клетками, полученными из ткани пуповины, добавив в камеры вкладышей ростовую среду с 2% FBS. Культуры инкубировали при температуре 37°C в атмосфере с содержанием 5% CO2 в течение приблизительно 24 часов. Затем планшет извлекли из инкубатора и при помощи инвертированного микроскопа Olympus (Olympus, г. Мелвилл, штат Нью-Йорк) получили изображения культур клеток эндотелия.
Результаты
В системе совместного культивирования с клетками, полученными из плаценты, или клетками, полученными из пуповины, клетки HUVEC образуют клеточные сети (данные не показаны). Клетки HUVEC образуют ограниченные клеточные сети в экспериментах по совместному культивированию с клетками hMSC и с 10-наномолярным раствором bFGF (данные не показаны). Клетки HUVEC без обработки практически или совсем не образовывали сети (данные не показаны). Данные результаты указывают, что клетки, полученные из ткани пуповины, секретируют ангиогенные факторы, которые стимулируют клетки HUVEC.
В системе совместного культивирования с клетками, полученными из плаценты, или клетками, полученными из пуповины, клетки CAEC образуют клеточные сети (данные не показаны).
В таблице 2-1 приведены уровни известных ангиогенных факторов, секретируемых клетками, полученными из плаценты и ткани пуповины, в ростовую среду. Клетки, полученные из плаценты и ткани пуповины, высевали на вкладыши, как описано выше. Клетки культивировали на вкладышах при температуре 37°C в атмосфере с содержанием кислорода в течение 48 часов, затем переносили в среду с добавлением 2% FBS и культивировали при температуре 37°C в течение 24 часов. Среду отделяли, немедленно замораживали и хранили при температуре -80°C, а также анализировали с использованием мультиплексного ИФА SearchLight (Pierce Chemical Company, г. Рокфорд, штат Иллинойс). Результаты представляют собой средние значения по повторным измерениям. Результаты показывают, что клетки, полученные из пуповины и плаценты, не секретируют определяемых уровней тромбоцитарного фактора роста-bb (PDGF-bb) или связывающегося с гепарином эпидермального фактора роста (HBEGF). Однако клетки секретируют измеримые количества тканевого ингибитора металлопротеиназ-1 (TIMP-1), ангиопоэтина 2 (ANG2), тромбопоэтина (TPO), фактора роста кератиноцитов (KGF), фактора роста гепатоцитов (HGF), фактора роста фибробластов (FGF) и фактора роста эндотелия сосудов (VEGF).
Потенциальные ангиогенные факторы, секретируемые клетками, полученными из пуповины и плаценты
(пг/мл)
(пг/мл)
(пг/мл)
(пг/мл)
(пг/мл)
(пг/мл)
(пг/мл)
(пг/мл)
Клетки, полученные из плаценты и пуповины, культивировали в течение 24 часов в среде с добавлением 2% FBS в атмосфере с естественным содержанием кислорода. Затем среду отделяли и анализировали с использованием мультиплексного ИФА SearchLight (Pierce). Результаты представляют собой средние значения по повторному анализу. Приведены концентрации в среде в единицах пикограмм на миллилитр культуральной среды. Плацента: клетки, полученные из плаценты. Пуповина: клетки, полученные из пуповины.
В таблице 2-2 приведены уровни известных ангиогенных факторов, секретируемых клетками, полученными из пуповины и плаценты. Клетки, полученные из пуповины и плаценты, высевали на вкладыши, как описано выше. Клетки культивировали на вкладышах в ростовой среде в атмосфере с содержанием кислорода 5% в течение 48 часов, затем переносили в среду с добавлением 2% FBS и культивировали в атмосфере с содержанием O2 5% в течение 24 часов. Среду отделяли, немедленно замораживали и хранили при температуре -80°C, а также анализировали с использованием мультиплексного ИФА SearchLight (Pierce Chemical Company, г. Рокфорд, штат Иллинойс). Результаты представляют собой средние значения по повторным измерениям. Результаты показывают, что клетки, полученные из пуповины и плаценты, не секретируют определяемых уровней тромбоцитарного фактора роста-bb (PDGF-bb) или связывающегося с гепарином эпидермального фактора роста (HBEGF). Однако клетки секретируют измеримые количества тканевого ингибитора металлопротеиназ-1 (TIMP-1), ангиопоэтина 2 (ANG2), тромбопоэтина (TPO), фактора роста кератиноцитов (KGF), фактора роста гепатоцитов (HGF), фактора роста фибробластов (FGF) и фактора роста эндотелия сосудов (VEGF).
Потенциальные ангиогенные факторы, секретируемые клетками, полученными из пуповины и плаценты
(пг/мл)
(пг/мл)
(пг/мл)
(пг/мл)
(пг/мл)
(пг/мл)
(пг/мл)
(пг/мл)
Клетки, полученные из плаценты и пуповины, культивировали в течение 24 часов в среде с добавлением 2% FBS в атмосфере с содержанием кислорода 5%. Затем среду отделяли и анализировали с использованием мультиплексного ИФА SearchLight (Pierce). Результаты представляют собой средние значения по повторному анализу. Приведены концентрации в среде в единицах пикограмм на миллилитр культуральной среды. Плацента: клетки, полученные из плаценты. Пуповина: клетки, полученные из пуповины.
Сводная информация
Результаты показывают, что клетки, полученные из пуповины и плаценты, могут стимулировать как клетки эндотелия пуповинной вены человека, так и клетки эндотелия коронарной артерии человека к образованию сетей в анализе in vitro с использованием препарата MATRIGEL (BD Discovery Labware, г. Бедфорд, штат Массачусетс). Данный эффект аналогичен эффекту, наблюдавшемуся в данной системе анализа с известными ангиогенными факторами. Данные результаты указывают на то, что клетки, полученные из пуповины и плаценты, подходят для стимулирования ангиогенеза in vivo.
Пример 3
Эффект клеток hUTC на пролиферацию и миграцию клеток эндотелия in vitro
Провели исследования для определения эффектов клеток, полученных из ткани пуповины человека, (hUTC) на пролиферацию и миграцию клеток эндотелия in vitro. Данные эффекты изучали путем совместного культивирования клеток hUTC и клеток эндотелия и путем инкубирования культур клеток эндотелия пуповинной вены человека (HUVEC) с лизатами клеток hUTC. Результаты показывают, что клетки hUTC индуцируют повышение пролиферации и миграции клеток эндотелия. Кроме того, данные указывают, что данные эффекты частично опосредуются фактором роста фибробластов (FGF) и фактором роста гепатоцитов (HGF).
Материалы и способы
Клеточная культура
Криоконсервированные клетки, полученные из ткани пуповины человека (hUTC) (партия № 120304), размораживали на пассаже 8-9, высевали на покрытые желатином колбы и культивировали в ростовой среде Хейфлика (среда DMEM с низким содержанием глюкозы (Gibco, номер по каталогу 11885-084), 15% об./об. фетальной бычьей сыворотки (FBS, Hyclone, номер по каталогу SH30070.03), 0,001 об./об. бета-меркаптоэтанола (Sigma, номер по каталогу M7154) и 50 ед./мл пенициллина и 50 микрограмм/мл стрептомицина (Gibco, номер по каталогу 3810-74-0)). Для описанных ниже исследований использовали клетки с пассажа 10 или 11. Клетки эндотелия пуповинной вены человека (HUVEC, номер по каталогу C2517A), клетки эндотелия коронарной артерии человека (HCAEC, номер по каталогу CC2585) и клетки эндотелия подвздошной артерии человека (HIAEC, номер по каталогу CC2545) приобрели у компании Cambrex и культивировали в ростовой среде для клеток эндотелия (среда EGM-2MV, номер по каталогу 3202) в соответствии с рекомендациями производителя. Мезенхимальные стволовые клетки человека (MSC, номер по каталогу PT-2501) также приобрели в компании Cambrex и поддерживали их в ростовой среде для мезенхимальных стволовых клеток (среда MSCGM, номер по каталогу PT-3001) в соответствии с рекомендациями производителя. Фибробласты кожи человека (линия CCD9) получили из коллекции ATCC и поддерживали их в среде DMEM/F12, содержащей 10% FBS и 1 ед./мл пенициллина-стрептомицина.
Для стандартного пассирования клетки один раз промывали фосфатно-буферным раствором (PBS, Invitrogen, номер по каталогу 14190) и отделяли трипсинизацией (0,25% трипсин-ЭДТА, Invitrogen, номер по каталогу 25200-056). Клетки подсчитывали с использованием анализатора Guava® (Guava Technologies, г. Хейуорд, штат Калифорния) и высевали с плотностью 5000 клеток/см2. Клетки стандартно пассировали каждые 3-4 суток.
Факторы роста и антитела
Рекомбинантный основной фактор роста фибробластов человека (bFGF, номер по каталогу 100-18B) и рекомбинантный фактор роста гепатоцитов человека (HGF, номер по каталогу 100-39) приобретали у компании Peprotech, а рекомбинантный фактор роста эндотелия сосудов человека (VEGF, номер по каталогу 293-VE) приобрели у компании R and D Systems. Антитела к bFGF (номер по каталогу ab11937), HGF (номер по каталогу ab10678) и VEGF (номер по каталогу ab9570) приобрели у компании Abcam (г. Кембридж, штат Массачусетс).
Подготовка клеточного лизата
Клеточные лизаты готовили из замороженной клеточной массы клеток hUTC (партия № 120304), взятой от предыдущих выращиваний. Вкратце, клетки hUTC (партия № 120304) культивировали в течение 4 суток, собирали трипсинизацией и осаждали центрифугированием. Затем клетки 3 раза промывали PBS и ресуспендировали в PBS в концентрации 1×107 клеток/мл. Аликвоты суспензии объемом 1 мл помещали в стерильные силиконизированные микроцентрифужные пробирки объемом 1,5 мл и центрифугировали при 300×g в течение 5 минут. PBS отсасывали и клеточный осадок хранили при температуре -80°C до дальнейшего применения.
Для получения клеточных лизатов пробирки с клеточным осадком погружали в жидкий азот (LN2) на 60 секунд и затем немедленно погружали в водяную баню с температурой 37°C на 60 секунд или до растаивания, но не более чем на 3 минуты. Данную стадию повторили 3 раза. После данной стадии образцы, прошедшие циклы заморозки и оттаивания, центрифугировали при 13000×g при температуре 4°C в течение 10 минут и затем помещали на лед. Супернатант осторожно отделяли и переносили его в чистую стерильную силиконизированную пробирку объемом 1,5 мл. Стадию центрифугирования повторили 3 раза и собранные супернатанты объединили вместе. Концентрацию белков определяли с использованием протокола микроанализа в наборе для анализа белков Quickstart Bradford (Bio-rad, номер по каталогу 500-0201).
Измерение пролиферации клеток
Клетки собирали и высевали непосредственно в указанный состав среды в концентрации 5000 клеток/см2. Для экспериментов с совместным культивированием использовали 24-луночные планшеты системы Transwell (Corning, номер по каталогу 3413), высевая клетки эндотелия в нижнюю часть лунки (10000 клеток/лунка), а клетки hUTC, MSC или фибробласты - внутрь вкладышей трансвел (1650 клеток/вкладыш трансвел). В указанные периоды времени вкладыши с клетками hUTC, MSC или фибробластами вынимали и утилизировали. Клетки эндотелия собирали путем добавления в каждую лунку 90 мкл трипсина. Клетки отделяли путем пипетирования вверх и вниз и затем переносили на чистый 96-луночный планшет. Трипсин ингибировали добавлением 90 мкл среды. Клетки окрашивали добавлением 20 мкл раствора для окрашивания (18 мкл среды + 1 мкл Guava Viacount Flex Reagent + 1 мкл DMSO) и подсчитывали с использованием анализатора Guava® (Guava Technologies, г. Хейуорд, штат Калифорния).
Для изучения эффекта клеточного лизата клеток hUTC (партия № 120304) на пролиферацию клеток HUVEC клетки HUVEC высевали на 24-луночные чашки Петри с плотностью 10000 клеток/лунка в среде EGM-2MV на 8 часов. Затем клетки переводили в бессывороточную среду путем инкубации в течение ночи в 0,5 мл среды EGM-2MV, содержащей 0,5% FBS и не содержащей факторов роста. Затем добавляли FBS, свежеприготовленный клеточный лизат клеток hUTC (партия № 120304), содержащий 62,5 мкг или 125 мкг белка, и нейтрализующие антитела к FGF (7 мкг/мл) или HGF (1 мкг/мл). После 4 суток культивирования клетки собирали и подсчитывали при помощи анализатора Guava®.
Для исследований потенциальных механизмов опосредованного клетками hUTC увеличения пролиферации клеток эндотелия в совместные культуры клеток HUVEC и HCAEC с клетками hUTC вводили нейтрализующие антитела к FGF (7 мкг/мл), HGF (1 мкг/мл) и VEGF (1 мкг/мл). Антитела добавляли в среду для культивирования клеток при первичном посеве клеток. После 7 суток совместного культивирования клетки собирали и подсчитывали при помощи анализатора Guava®.
Оценка миграции клеток
Для измерения миграции клеток использовали 6-луночную систему Transwell (Corning, номер по каталогу 3428). Клетки высевали непосредственно в указанный состав среды с плотностью 5000 клеток/см2. Клетки эндотелия высевали внутрь вкладышей трансвел (23000 клеток/вкладыш трансвел), а клетки hUTC (партия №120304) или клетки MSC высевали на дно лунки (48000 клеток/лунка). Миграцию оценивали после 7 суток совместного культивирования путем подсчета числа клеток на нижней стороне вкладыша трансвел. Вкратце, вкладыши трансвел переносили в чистую лунку и однократно промывали PBS. Клетки с нижней стороны лунки собирали путем добавления трипсина на дно лунки. Трипсин ингибировали добавлением полной ростовой среды и собирали клетки центрифугированием. Клетки затем ресуспендировали в 25 мкл среды и 20 мкл суспензии, которую использовали для определения числа клеток при помощи анализатора Guava®.
Для исследований потенциальных механизмов опосредованного клетками hUTC увеличения миграции клеток эндотелия в совместные культуры клеток HUVEC и HCAEC с клетками hUTC (партия № 120304) вводили нейтрализующие антитела к FGF (7 мкг/мл) и HGF (1 мкг/мл). Антитела добавляли в среду для культивирования клеток при первичном посеве клеток. После 7 суток совместного культивирования клетки, оказавшиеся с нижней стороны вкладыша трансвел, собирали и подсчитывали при помощи анализатора Guava®.
Результаты
Эффект клеток hUTC на пролиферацию клеток эндотелия
Для исследования эффектов клеток hUTC на пролиферацию клеток эндотелия использовали систему совместного культивирования. С данной целью использовали систему Transwell, высевая клетки эндотелия на дно 24-луночной чашки Петри и клетки hUTC внутри вкладышей трансвел. В данных экспериментах использовали два различных состава среды (составы среды указаны в разделе «Материалы и способы»): (1) среда Хейфлика 80% + среда EGM-2MV 20% (H80) или (2) среда Хейфлика 50% + среда EGM-2MV 50% (H50). После 6 или 7 суток совместного культивирования вкладыши трансвел извлекали, клетки эндотелия собирали трипсинизацией и подсчитывали при помощи анализатора Guava®.
Эффект клеток hUTC (партия № 120304) на пролиферацию клеток эндотелия при культивировании в среде H80 по сравнению со средой H50 показан на фигуре 1. Пролиферация клеток HUVEC, поддерживавшихся в среде H50, оказалась выше, чем у клеток, поддерживавшихся в среде H80 (фигура 1A), тогда как клетки HCAEC и HIAEC продемонстрировали аналогичный рост для данных составов среды для совместного культивирования (фигура 1B и фигура 1C). Для обоих составов среды совместное культивирование клеток эндотелия с клетками hUTC (партия № 120304) привело к существенному увеличению числа клеток после 7 суток. Все дальнейшие исследования по совместному культивированию клеток hUTC и клеток эндотелия проводили в среде следующего состава: среда Хейфлика 50% + среда EGM-2MV 50% (H50).
При совместном культивировании с клетками эндотелия клетки MSC и фибробласты также проверили относительно того, могут ли клетки других типов также оказывать влияние на пролиферацию клеток эндотелия. Как показано на фигуре 1A, не было обнаружено различия в пролиферации клеток HUVEC, которые находились в средах для совместного культивирования (H50 или H80), и клеток, которые совместно культивировали с клетками MSC или с фибробластами. Тот же результат был получен и для клеток HCAEC (фигура 1B) и клеток HIAEC (фигура 1C), когда совместное культивирование с клетками hUTC (партия № 120304) привело к увеличению пролиферации клеток, но различий в пролиферации для клеток, которые находились в средах для совместного культивирования (H50 или H80), и клеток, которые совместно культивировали с клетками MSC, обнаружено не было.
Для исследований потенциальных механизмов опосредованного клетками hUTC увеличения пролиферации клеток эндотелия в совместные культуры клеток HUVEC и HCAEC с клетками hUTC вводили нейтрализующие антитела к FGF (7 мкг/мл), HGF (1 мкг/мл) и VEGF (1 мкг/мл). Представленные на фигурах 2A-2D результаты показывают, что как для клеток HUVEC, так и для клеток HCAEC добавление нейтрализующих антител к FGF и HGF приводило к снижению увеличения числа клеток, индуцированного клетками hUTC (партия № 120304). При концентрациях, использованных в данных исследованиях, данные нейтрализующие антитела блокировали индуцированную факторами роста пролиферацию клеток HUVEC (фигуры 2A и 2B). Интересным является то, что нейтрализующее антитело к VEGF не имело существенного эффекта на пролиферацию клеток, индуцированную совместным культивированием как клеток HUVEC (фигуры 2A и 2B), так и клеток HCAEC (фигуры 2C и 2D) с клетками hUTC (партия № 120304). В отдельных исследованиях было обнаружено, что на пролиферацию клеток hUTC (партия № 120304) не оказывало влияние добавление в культуральную среду нейтрализующих антител к FGF и VEGF (данные не показаны).
Эффект клеточного лизата клеток hUTC (партия № 120304) на пролиферацию клеток HUVEC
Также провели исследования для определения эффекта клеточного лизата на пролиферацию клеток HUVEC. Клетки HUVEC высевали на 24-луночные планшеты в среде EGM-2MV на 8 часов с плотностью 5000 клеток/см2. Затем клетки переводили в бессывороточную среду путем инкубации в течение ночи в 0,5 мл среды EGM-2MV, содержащей 0,5% фетальной бычьей сыворотки (FBS) и не содержащей факторов роста. После инкубации добавляли различные концентрации свежеприготовленного клеточного лизата клеток hUTC (партия № 120304). В некоторых случаях также вводили FGF, HGF и нейтрализующие антитела. После 4 суток культивирования клетки HUVEC собирали и подсчитывали при помощи анализатора Guava®.
Как показано на фигуре 3, добавление клеточных лизатов приводило к увеличению числа клеток HUVEC по сравнению с клетками, которые поддерживали в сыворотке с низкой концентрацией (0,5% FBS), а увеличение числа клеток оказалось пропорционально количеству добавленного клеточного лизата. При более низкой концентрации клеточного лизата (62,5 мкг/мл) число клеток было сравнимо с числом клеток при их инкубации в условиях оптимального состава среды (10% FBS). Кроме того, добавление нейтрализующего антитела либо к FGF, либо к HGF понизило увеличение числа клеток, индуцированное 2 различными концентрациями клеточного лизата. Данные результаты сопоставимы с результатами, полученными при совместном культивировании клеток HUVEC с клетками hUTC (партия № 120304).
Эффект клеток hUTC на миграцию клеток эндотелия
Миграцию клеток эндотелия оценивали путем определения числа клеток, прошедших через мембрану вкладыша трансвел (размер пор: 8 микрон). Клетки-реципиенты (клетки эндотелия) высевали на 6-луночные вкладыши трансвел, а клетки hUTC высевали на дно лунки. После некоторого периода совместного культивирования клетки, оказавшиеся на нижней стороне вкладыша трансвел, собирали и подсчитывали. На фигуре 4A показана миграция клеток HUVEC, которые культивировали совместно с клетками hUTC и клетками MSC. Клетки hUTC (партия № 120304) индуцировали перемещение клеток HUVEC на нижнюю сторону вкладыша трансвел, тогда как клетки MSC такого эффекта не вызвали (фигура 4A). Такой же результат был получен у клеток HCAEC, где совместное культивирование с клетками hUTC (партия № 120304) привело к увеличению числа клеток, мигрирующих через вкладыш трансвел, по сравнению с контролем в среде (фигура 4B).
Эффект клеток hUTC (партия № 120304) на миграционное поведение клеток HUVEC и HCAEC дополнительно анализировали с использованием нейтрализующих антител к FGF и HGF. Как показано на фигуре 5A, данные антитела снизили миграцию клеток HUVEC, вызванную клетками hUTC (партия № 120304). В совместных культурах клеток HCAEC с клетками hUTC (партия № 120304) нейтрализующее антитело к HGF блокировало опосредованное клетками hUTC (партия № 120304) усиление клеточной миграции, тогда как нейтрализующее антитело к FGF такого эффекта не дало (фигура 5B).
Сводная информация
Изложенные выше результаты описывают эффекты клеток hUTC на пролиферативное и миграционное поведение клеток эндотелия in vitro. Исследование проводили с использованием совместных культур клеток hUTC (партия № 120304) и клеток эндотелия или путем непосредственного инкубирования клеток эндотелия с клеточным лизатом, приготовленным из клеток hUTC (партия № 120304).
Для исследований по пролиферации проверили эффекты клеток hUTC (партия № 120304), и в качестве иммунореактивных клеток использовали три типа клеток эндотелия из различных участков сосудистого русла. Совместное культивирование с клетками hUTC привело к усилению пролиферации клеток эндотелия. Совместное культивирование с клетками MSC или фибробластами обеспечило численность клеток, сравнимую с контролями для среды. Пролиферативный отклик клеток HUVEC на клетки hUTC (партия № 120304) подавлялся путем добавления нейтрализующих антител к FGF и HGF, но не подавлялся нейтрализующим антителом к VEGF. Это указывает на то, что вызываемая клетками hUTC (партия № 120304) индукция пролиферации опосредуется FGF и HGF. Следует отметить, что инкубация клеток HUVEC с лизатами клеток hUTC (партия № 120304) обеспечила тот же эффект, что и совместное культивирование.
Миграцию количественно характеризовали путем подсчета числа клеток, оказавшихся на нижней стороне вкладыша трансвел, и в качестве иммунореактивных клеток использовали как клетки HUVEC, так и клетки HCAEC. В отличие от исследований по пролиферации миграционный отклик данных клеток оказался несколько разным. Клетки hUTC (партия № 120304) индуцировали миграцию как клеток HUVEC, так и клеток HCAEC. Клетки MSC не индуцировали миграции клеток HUVEC, что указывает на специфичность данного отклика на клетки hUTC. Антитела к FGF и HGF компенсировали эффект клеток hUTC (партия № 120304) на миграцию клеток HUVEC, тогда как только антитело к HGF влияло на миграцию клеток HCAEC, что указывает на различия между двумя типами клеток эндотелия.
Таким образом, данные показывают, что клетки hUTC индуцируют пролиферацию и миграцию клеток эндотелия in vitro. Применение нейтрализующих антител указывает на возможное участие в данных наблюдаемых эффектах как FGF, так и HGF. Однако в пролиферативном и миграционном поведении клеток эндотелия могут также быть задействованы и другие факторы.
Пример 4
Экспрессия теломеразы в клетках, полученных из пуповины
Функция теломеразы состоит в синтезе теломерных повторов, которые защищают целостность хромосом и продлевают репликативно-активную жизнь клеток (Liu, K, et al., PNAS, 1999 г.; 96: 5147-5152). Теломераза состоит из двух компонентов - теломеразного РНК-шаблона (hTER) и теломеразной обратной транскриптазы (hTERT). Регулирование теломеразы определяется транскрипцией hTERT, но не hTER. Таким образом, полимеразная цепная реакция (ПЦР) в реальном времени для мРНК hTERT является общепринятым способом определения теломеразной активности клеток.
Выделение клеток. Для определения продукции теломеразы в клетках, полученных из ткани пуповины человека, проводили эксперименты с ПЦР в реальном времени. Клетки, полученные из ткани пуповины человека, подготовили в соответствии с описанными выше примерами. По существу, пуповины, полученные в Национальном центре по обмену материалами для исследования заболеваний (NDRI, г. Филадельфия, штат Пенсильвания) после нормально прошедших родов, промывали для удаления крови и продуктов распада клеток и механически диссоциировали. Затем ткань инкубировали с расщепляющими ферментами, включая коллагеназу, диспазу и гиалуронидазу, в культуральной среде при температуре 37°C. Клетки, полученные из ткани пуповины человека, культивировали в соответствии со способами, описанными в приведенных выше примерах. Мезенхимальные стволовые клетки и нормальные фибробласты дермы кожи (cc-2509 (партия № 9F0844)) приобретали у компании Cambrex, г. Уолкерсвилл, штат Мэриленд. Плюрипотентные клетки nTera-2 клеточной линии тестикулярной эмбриональной карциномы (тератомы) (NTERA-2 cl.Dl) (см. работу Plaia et al., Stem Cells, 2006 г.; 24(3): 531-546) приобрели из коллекции ATCC (г. Манассас, штат Вирджиния) и культивировали в соответствии с описанными выше способами.
Выделение общей РНК. РНК экстрагировали из клеток при помощи набора RNeasy® (Qiagen, г. Валенсия, штат Калифорния). РНК элюировали 50 микролитрами обработанной DEPC воды и хранили при температуре -80°C. Обратную транскрипцию РНК проводили с использованием случайных гексамеров, применяя реагенты для обратной транскрипции TaqMan® (Applied Biosystems, г. Фостер Сити, штат Калифорния) при температуре 25°C в течение 10 минут, температуре 37°C в течение 60 минут и температуре 95°C в течение 10 минут. Образцы хранили при температуре -20°C.
ПЦР в реальном времени. ПЦР проводили на образцах кДНК с использованием продуктов для экспрессии генов Assays-on-Demand™ компании Applied Biosystems (также известные как наборы для определения экспрессии генов TaqMan® Gene Expression Assays) в соответствии с инструкциями производителя (Applied Biosystems). Данный доступный в продаже набор широко используют для анализа клеток человека на теломеразу. Вкратце, hTert (ген теломеразы человека) (Hs00162669) и GAPDH человека (внутренний контроль) смешивали с кДНК и универсальным мастер-миксом для ПЦР TaqMan®, при этом использовали секвенатор 7000 с программным обеспечением ABI Prism 7000 SDS (Applied Biosystems). Использовали следующие условия термоциклирования: сначала 50°C в течение 2 минут и 95°C в течение 10 минут, затем 40 циклов при 95°C в течение 15 секунд и 60°C в течение 1 минуты. Данные ПЦР анализировали в соответствии с рекомендациями производителя.
Клетки, полученные из ткани пуповины человека (номер доступа ATCC PTA-6067), фибробласты и мезенхимальные стволовые клетки человека анализировали на hTert и 18S РНК. Как показано в таблице 4-1, hTert и, следовательно, теломеразу не обнаружили в клетках, полученных из ткани пуповины человека.
Проанализировали клетки, полученные из ткани пуповины человека (изолят 022803, номер доступа ATCC PTA-6067), и клетки nTera-2, и результаты показали отсутствие экспрессии теломеразы в двух партиях клеток, полученных из ткани пуповины человека, тогда как клеточная линия тератомы экспрессировала теломеразу на высоком уровне (таблица 4-2).
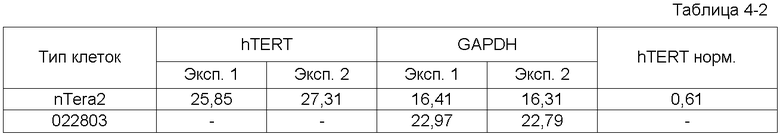
Следовательно, можно сделать вывод, что клетки, полученные из ткани пуповины человека, которые составляют предмет настоящего изобретения, не экспрессируют теломеразу.
Пример 5
Эффективность трансплантации клеток hUTC в мышиной модели ишемии задней конечности
Описанные выше данные показали, что системное введение клеток hUTC существенно улучшило кровоток у мышей с односторонней ишемией задней конечности на 5 и 10 сутки после обработки. Кроме того, прямое сравнительное исследование показало, что системная (внутривенная) инъекция клеток hUTC привела к более существенному восстановлению кровотока по сравнению с местной (внутримышечной) инъекцией.
В данном примере оценивали эффективность внутримышечной инъекции клеток hUTC и клеток hUTC в фибриновом клее в мышиной модели периферической ишемии задней конечности (модель односторонней ишемии задней конечности). Использовали линии бестимусных мышей с ослабленным иммунитетом и мышей линии NOD/scid IL2rγ-/- (NSG).
Описание животной модели
Для описываемых в настоящем примере исследований проводили сравнение между бестимусными мышами и мышами линии NSG.
Линия мышей NSG привлекала к себе интерес для исследований по ксенотрансплантации благодаря ее многочисленным иммунологическим дефектам, включая отсутствие зрелых лимфоцитов, T-клеток, B-клеток и NK-клеток. Данные животные выживают в течение более 6 месяцев без развития Т-клеточной лимфомы даже после сублетального облучения (Ito M. et al. (2002 г.) Blood. 100: 3175-82).
У данных мышей создавали модель односторонней ишемии задней конечности. Вкратце, животных анестезировали ингаляцией изофлурана. В средней части левой задней конечности делали разрез. Лигировали бедренную артерию и ее ветви, начиная от паховой связки и до бифуркации подкожной и подколенной артерий. Участки между лигатурами вырезали и разрезы зашивали шелковыми викриловыми нитями 5-0 (Ethicon).
Клетки и фибриновый клей
Замороженные суспензии клеток получили в сухой транспортной упаковке. После получения клетки перенесли в жидкий азот для долговременного хранения. Клетки размораживали непосредственно перед инъекцией. Клетки подсчитывали и определяли их жизнеспособность окрашиванием трипановым голубым и подсчитыванием на гемоцитометре. Всю дозу ресуспендировали в PBS и набирали в туберкулиновый шприц объемом 0,3 мл с иглой для инъекции 28 размера.
Для данных исследований использовали фибриновый клей (EVICEL® Fibrin sealant (Human), Omrix Pharmaceuticals). Компоненты размораживали перед использованием и разводили до конечной концентрации 16-24 МЕ/мл тромбина и 39,3-60,7 мг/мл BAC2 (фибриноген). Базовые растворы тромбина (концентрация базового раствора приблизительно 800-1200 МЕ/мл) и BAC2 (фибриноген) (концентрация базового раствора приблизительно 55-85 мг/мл) разводили 1:50 для тромбина и 1:1,4 для BAC2 соответственно.
Дизайн исследования
48 (сорок восемь) бестимусных мышей (возраст 6-8 недель) и 48 (сорок восемь) мышей линии NOG/SCID (NSG) (возраст 6-11 недель), согласованных по дате рождения, случайным образом распределили по группам, как указано ниже в таблице 5-1.
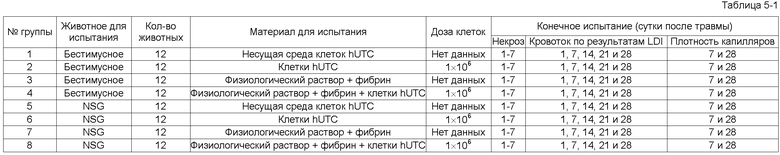
Конечное испытание проводили путем измерения следующих параметров:
оценка кровотока с использованием лазерной допплеровской визуализации на 1, 7, 14, 21 и 28 сутки; оценка плотности капилляров с использованием окрашивания на CD31 на 7 сутки (3 животных из каждой группы) и 28 сутки.
Способ
Через сутки после создания односторонней ишемии задней конечности в мышцу ишемизированной задней конечности вводили несущую среду, клетки hUTC в несущей среде, фибриновый клей или клетки hUTC в фибриновом клее.
При инъекциях клеток hUTC в мышцу ишемизированной задней конечности вводили указанное количество клеток hUTC в несущей среде или клеток hUTC в фибриновом клее. Проводили по три инъекции (3×20 мкл) в верхнюю часть конечности и две инъекции (2×20 мкл) в нижнюю часть конечности при полной дозе 100 мкл. Контрольным животным вводили несущую среду таким же образом, как и клетки.
Для каждой инъекции клеток hUTC в фибриновом клее клетки ресуспендировали в тромбине (конечная концентрация 16-24 МЕ/мл). В отдельную пробирку отбирали аликвоту BAC2 (фибриноген; конечная концентрация 39,3-60,7 мг/мл).
Непосредственно перед инъекцией клетки hUTC в тромбине переносили в пробирку, содержащую BAC2, перемешивали, набирали в туберкулиновый шприц объемом 0,3 мл (с иглой 28 размера) и вводили в заднюю конечность мыши. Дозу 100 мкл вводили пятью внутримышечными (в/м) инъекциями по 20 мкл - 3 инъекции в верхнюю часть конечности и 2 инъекции в нижнюю часть конечности. Контрольным животным вводили фибриновый клей таким же образом, как и клетки.
Статистический анализ
Данные представлены в виде среднего значения ± стандартная ошибка среднего значения. Сравнение между группами проводили с использованием двухстороннего t-критерия Стьюдента.
Оценка кровотока
Перфузию крови в задних конечностях мышей оценивали с использованием лазерной допплеровской визуализации на анализаторе компании Moor. Животных анестезировали ингаляцией изофлурана и помещали на подогреваемую платформу с установленной температурой 37°C. Для определения соответствующего ишемии фонового уровня получали данные по перфузии крови на подошвенном участке обеих задних конечностей через 24 часа после создания травмы. Последовательные оценки перфузии проводили на 7, 14, 21 и 28 сутки. Данные приведены в виде отношения величин перфузии в левой (ишемизированной) и правой (неишемизированной) конечностях.
Результаты и анализ
Оценка перфузии с использованием лазерной допплеровской визуализации
Полученные с использованием лазерной допплеровской визуализации данные по перфузии (выраженные в виде относительной величины в процентах перфузии в ишемизированной левой конечности по сравнению с неишемизированной контрольной правой конечностью) для мышей линии NSG представлены на фигуре 6 и в таблице 5-2 (ниже). Наибольший эффект от обработки был зафиксирован для клеток hUTC, вводимых в фибриновой матрице; относительная перфузия у таких мышей к 21 суткам практически вдвое превышала величину для контрольной группы с фибрином (40,3±2,43 и 22,6±2,34). На 21 и 28 сутки данный эффект был существенно больше, чем в обеих контрольных группах (P<0,001), а также в группах, получавших клетки hUTC только в несущей среде (P<0,05). Эффект клеток hUTC, вводимых в несущей среде, на относительную величину перфузии составил 27%-ое превышение над контролем на 28 сутки (P<0,05). В данный момент времени относительная перфузия в ишемизированной конечности мышей линии NSG, получивших клетки hUTC только в несущей среде, составила 30,0±2,3 по сравнению с 23,7±1,6 для мышей, получивших только несущую среду.
Средние значения ±СПС для относительных величин перфузии у мышей линии NSG
Данные по перфузии для бестимусных мышей приведены на фигуре 7 и в таблице 5-3. Введение клеток hUTC в фибрине значительно (P<0,05) повысило перфузию в ишемизированной конечности на 14 сутки (53,9±4,7) и 21 сутки (53,4±3,2) по сравнению с контролями, получавшими только фибрин (39,2±1,7 и 40,9±3,7 соответственно). Эффект введения клеток в фибрине имел тенденцию к повышению на 28 сутки (52,0±5,8) по сравнению с контролем (40,8±4,3), но не был значительным из-за больших отклонений в результатах измерения между животными. Местная доставка клеток hUTC только в несущей среде имела тенденцию к повышению перфузии на 21 сутки (64,0±6,3 и 43,7±7,4 для контроля) и значительно (P<0,05) улучшала перфузию на 28 сутки (52,0±3,5 и 40,8±4,9). Существенных отличий между эффектами от введения клеток hUTC в фибрине или только в несущей среде не выявлено.
Средние значения ±СПС для относительных величин перфузии у бестимусных мышей
Настоящие данные указывают на то, что как для мышей линии NSG, так и для бестимусных мышей местное введение клеток hUTC путем в/м инъекции обеспечивало ранний эффект при смешивании с фибриновым носителем. У мышей линии NSG долговременный эффект оказался существенно более выраженным, чем от введения клеток только в несущей среде.
Заключение
Непосредственное внутримышечное введение клеток hUTC через 1 сутки после создания ишемии улучшало реперфузию ишемизированных мышц как для мышей линии NSG, так и для бестимусных мышей. Введение клеток в фибриновой матрице мышам линии NSG дало более сильный видимый ответ, чем введение клеток только в несущей среде. Животные, которым непосредственно внутримышечно вводили клетки hUTC в мышиной модели периферической ишемии задней конечности, показали улучшение реперфузии ишемизированных конечностей как для мышей линии NSG, так и для бестимусных мышей. Однако среди мышей линии NSG животные, получавшие клетки hUTC в фибриновом клее, продемонстрировали более существенный и более долговременный эффект по сравнению с животными, получавшими клетки только в несущей среде.
Пример 6
Эффективность трансплантации клеток hUTC в модели периферической ишемии задней конечности у мышей линии NOD/scid IL2rγ-/-: исследование зависимости от дозировки и способа введения
В данном исследовании оценивали эффективность клеток hUTC в мышиной модели периферической ишемии задней конечности (модель односторонней ишемии задней конечности). Для данного исследования использовали мышей линии NOD/scid IL2rγ-/- (NSG). Эффект на восстановление кровотока оценивали при введении клеток hUTC (1) местно (внутримышечно) с несущей средой; (2) местно (внутримышечно) с фибриновым клеем; или (3) системно (внутривенно). В исследовании также оценивали эффект клеток hUTC, вводимых внутримышечно при различных дозах с фибриновым клеем или без него, на восстановление кровотока.
Материалы и способы
Описание животной модели
Использовали мышей линии NSG. Линия мышей NSG привлекала к себе интерес для исследований по ксенотрансплантации благодаря ее многочисленным иммунологическим дефектам, включая отсутствие зрелых лимфоцитов, T-клеток, B-клеток и NK-клеток. Данные животные выживают в течение более 6 месяцев без развития Т-клеточной лимфомы даже после сублетального облучения (Ito M. et al. (2002 г.) Blood. 100: 3175-82).
У данных мышей создавали модель односторонней ишемии задней конечности. Вкратце, животных анестезировали ингаляцией изофлурана. В средней части левой задней конечности делали разрез. Лигировали бедренную артерию и ее ветви, начиная от паховой связки и до бифуркации подкожной и подколенной артерий. Участок между лигатурами вырезали, и разрез зашивали шелковыми викриловыми нитями 5-0.
Клетки и фибриновый клей
Криоконсервированные клетки hUTC размораживали непосредственно перед инъекцией. Клетки подсчитывали и определяли их жизнеспособность окрашиванием трипановым голубым и подсчитыванием на гемоцитометре. Всю дозу ресуспендировали либо в несущей среде, либо в фибриновом клее и набирали в туберкулиновый шприц объемом 0,3 мл с иглой для инъекции 28 размера.
Использовали фибриновый клей (EVICEL® Fibrin sealant (Human), Omrix Pharmaceuticals). Компоненты размораживали перед использованием и разводили до конечной концентрации 16-24 МЕ/мл тромбина и 39,3-60,7 мг/мл для BAC2. Брали базовые растворы тромбина (концентрация базового раствора приблизительно 800-1200 МЕ/мл) и BAC2 (фибриноген) (концентрация базового раствора приблизительно 55-85 мг/мл) и разводили их 1:50 для тромбина и 1:1,4 для BAC2, соответственно.
Дизайн исследования
Мышей линии NSG (возраст 6-11 недель), согласованных по дате рождения, случайным образом распределили по группам, как указано ниже в таблице 6-1.
по результатам LDI
Через сутки после создания односторонней ишемии задней конечности системно или местно путем инъекции вводили клетки hUTC. При системных инъекциях через хвостовую вену вводили указанное количество клеток hUTC в 100 мкл несущей среды, используя инсулиновый шприц объемом 0,3 мл и иглу 28 размера. Клетки вводили на протяжении приблизительно 1 минуты. Контрольным животным вводили только несущую среду.
При местных инъекциях в мышцу ишемизированной задней конечности вводили указанное количество клеток hUTC в несущей среде или клеток hUTC в фибриновом клее. Инъекции проводили в 5 местах; в каждом месте внутримышечно (в/м) вводили по 20 мкл. Проводили по три инъекции (3×20 мкл) в верхнюю часть конечности и две инъекции (2×20 мкл) в нижнюю часть конечности при полной дозе 100 мкл. Контрольным животным вводили несущую среду таким же образом, как и клетки.
Для каждой инъекции клеток hUTC в фибриновом клее клетки ресуспендировали в тромбине (конечная концентрация 16-24 МЕ/мл). В отдельную пробирку отбирали аликвоту BAC2 (фибриноген; конечная концентрация 39,3-60,7 мг/мл). Непосредственно перед инъекцией клетки hUTC в тромбине переносили в пробирку, содержащую BAC2, перемешивали, набирали в туберкулиновый шприц объемом 0,3 мл (с иглой 28 размера) и вводили в заднюю конечность мыши. Дозу 100 мкл вводили пятью внутримышечными (в/м) инъекциями по 20 мкл - 3 инъекции в верхнюю часть конечности и 2 инъекции в нижнюю часть конечности. Контрольным животным вводили фибриновый клей таким же образом, как и клетки.
Оценка кровотока
Перфузию крови в задних конечностях мышей оценивали с использованием лазерной допплеровской визуализации на анализаторе компании Moor. Животных анестезировали ингаляцией изофлурана и помещали на подогреваемую платформу с установленной температурой 37°C. Для определения соответствующего ишемии фонового уровня получали данные по перфузии крови на подошвенном участке обеих задних конечностей через 24 часа после создания травмы. Последовательные оценки перфузии проводили на 7, 14, 21 и 28 сутки после травмы. Данные приведены в виде отношения величин перфузии в левой (ишемизированной) и правой (неишемизированной) конечностях.
Результаты
Средние (±СПС) величины для относительной перфузии в ишемизированных конечностях для каждой группы представлены в таблице 6-2 (ниже). Проводили двухпараметрический статистический анализ ANOVA на трех наборах данных (например, в/м (без фибрина), в/м с фибрином и в/в (без фибрина)) при уровне значимости 5%. Оценивали общие эффекты времени и типа обработки. Обнаружили значительный (P<0,01) эффект типа обработки и времени во всех группах. Провели пост-испытание по критерию Бонферрони для сравнения всех групп с контролем и друг с другом внутри каждого набора (например, в/м, в/м с фибрином и в/в).
Сводная информация по результатам анализа с использованием лазерной допплеровской визуализации. Приведены средние значения ± стандартные ошибки (СПС) для результатов измерения в указанные сутки (после травмы)
Явных различий в величине эффекта для 3 разных способов доставки не выявлено. Использование 1×106 клеток hUTC в фибрине привело к приблизительно 43,4% относительной перфузии на 28 сутки после травмы, тогда как введение только клеток hUTC привело к максимальной величине относительной перфузии 40,6% (см. фигура 8). При системной доставке клеток относительная перфузия в ишемизированных конечностях мышей, получавших клетки hUTC, была значительно выше контроля на 21 и 28 сутки после травмы (P<0,01).
Проверили две дозы клеток путем местного (в/м) введения. Большая доза дала статистически существенно отличный эффект (P<0,05) по сравнению с контролем на 21 и 28 сутки после травмы. Меньшая доза не дала статистически существенно отличного эффекта от контроля на любые сутки. Группы с большей и меньшей дозами в любой момент времени статистически существенно не отличались друг от друга (таблица 6-2).
Проверили четыре дозы клеток hUTC в фибриновом клее путем местного (в/м) введения. В группе, получавшей 1×106 клеток, относительная перфузия в ишемизированной конечности оказалась значительно выше, чем в контроле, на 21 сутки (P<0,05) и 28 сутки (P<0,01) после травмы. Относительная перфузия в группах, получавших 0,5, 0,25 и 0,125×106 клеток, во всех группах оказалась значительно выше, чем в контроле, на 21 сутки (P<0,001, P<0,01 и P<0,05, соответственно) после травмы. Все группы дозирования не отличались между собой (фигура 9).
Наблюдалась небольшая тенденция к большей реперфузии при повышении дозы, особенно заметная на 14 сутки после травмы (на фигуре 10 для ясности приведены данные без указания интервала ошибки).
Таким образом, животные, получавшие клетки hUTC любым из описанных трех способов введения, продемонстрировали повышенную реперфузию в ишемизированных конечностях. В данном исследовании не выявлено явного различия в величине получаемого эффекта при разных способах введения. Следует отметить, что для групп с максимальной дозировкой на 28 сутки после травмы относительная реперфузия оказалась значительно выше, независимо от способа доставки или количества клеток.
Пример 7
Оценка эффективности трансплантации клеток hUTC в мышиной модели ишемии периферических сосудов задней конечности: исследование способа введения
Целью данного исследования была оценка того, насколько введение клеток hUTC способно восстановить кровоток в мышиной модели ишемии периферических сосудов задней конечности (модель односторонней ишемии задней конечности). Провели сравнение двух способов введения - внутривенного и внутримышечного; в последнем случае также использовали суспензию клеток в фибриновой матрице.
Способы
Группы по типу обработки представлены ниже в таблице 7-1.
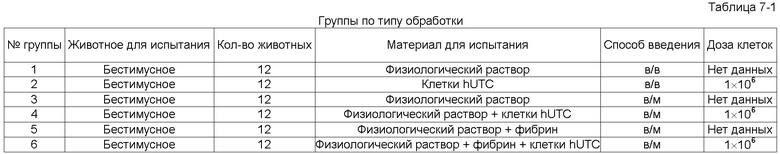
Составы композиций на основе фибринового клея для групп 5 и 6, в/м введение, представлены ниже в таблице 7-2.
Составы композиций на основе фибринового клея для групп 5 и 6, в/м введение
Тромбин = конечное разведение базового раствора 1:5000 (базовый раствор содержит 1,6 мкл тромбина (800-1200 МЕ/мл)) + 998,4 мкл PBS
Фибриноген = разведение 1:8 (базовый раствор содержит 55-85 мг/мл)
Самцам иммунотолерантных бестимусных мышей (возраст 8-10 недель) хирургически индуцировали одностороннюю ишемию задней конечности. Через 1 сутки после операции оценили кровоток в обеих задних конечностях с использованием лазерной допплеровской визуализации для оценки перфузии (LDPI). 6 группам мышей (N = 15/группа) ввели по однократной дозе (106) клеток hUTC или несущей среды для контроля, как указано в приведенной таблице 7-1. В качестве способа введения использовали либо в/в введение 100 мкл в хвостовую вену, либо в/м введение той же суммарной дозы отдельными инъекциями по 20 мкл в верхнюю (3 места) и нижнюю (2 места) скелетные мышцы ишемизированной конечности. В 2 группах с в/м введением также использовали фибриновую матрицу.
Последовательные анализы LDPI проводили на 1, 3, 7, 10, 14 и 21 сутки; последние сутки также были последними сутками исследования. За 3 суток до операции и затем еще раз через 10 суток после операции проводили оценку способности животного плавать. Считали, что мышь достигла своего предела по способности плавать, когда она не могла подняться на поверхность в течение 5 секунд после погружения. Сравнивали отношение времени плавания после ишемической травмы к средней выносливости до ишемической травмы. Взятые после умерщвления животного образцы ткани икроножной мышцы из ишемизированной и нормальной конечностей 5 мышей из каждой группы, достигших 21 суток исследования, обработали для проведения гистологического окрашивания на капилляры (CD31/PECAM-1) и артериолы (α-актин гладких мышц). Плотность сосудов количественно оценивали по оцифрованным изображениям иммуноокрашенных срезов.
Также оценивали степень приживления клеток и плотности сосудов в тканях, собранных на 7 сутки. Анализ плотности сосудов на 7 сутки сочли непригодным в связи с тем, что разделение средних значений относительной перфузии для в/в введения клеток и для контрольных групп значительно отличалось на 21 сутки. Анализ приживления клеток не проводили из-за технических трудностей со способами обнаружения клеток.
Оценка кровотока
Оценку кровотока в задних конечностях мышей проводили с использованием лазерной допплеровской визуализации на анализаторе компании Moor. Животных анестезировали ингаляцией изофлурана и помещали на подогреваемую платформу с установленной температурой 37°C. Для определения соответствующего ишемии фонового уровня получали данные по перфузии крови на подошвенном участке обеих задних конечностей через 24 часа после создания травмы. Последовательные оценки перфузии проводили на 5, 10, 15 и 20 сутки. Данные приводили в виде отношения величин перфузии в левой (ишемизированной) и правой (неишемизированной) конечностях.
Тест способности плавать
Мышей также проверяли на способность плавать или оставаться на плаву в камере для плавания. Для этого мышей обучали способности оставаться на плаву в камере для плавания. Мышей тренировали ежедневно в течение 3 суток. По окончании данного периода мышей оценивали по продолжительности времени, которое они могли продержаться на плаву до наступления усталости, определяемой как неспособность подняться к поверхности воды для вдоха за 7-10 сек (фоновый уровень, 3 суток). На 0 сутки мышам индуцировали одностороннее повреждение задней конечности и вводили клетки через 24 часа после травмы. Затем на 10 и 15 сутки у животных оценивали способность плавать/оставаться на плаву.
Результаты и анализ
Уровень отсева животных из-за некроза конечности был низким во всех группах. Весь отсев произошел за неделю 1. Количество животных, удаленных из исследования (показано в скобках), в каждой группе составило: группа 1 (2); группа 2 (1); группа 3 (2); группа 4 (2); группа 5 (1); и группа 6 (2).
Оценка перфузии с использованием лазерной допплеровской визуализации
Полученные с использованием лазерной допплеровской визуализации данные по перфузии (выраженные в виде относительной величины в процентах перфузии в ишемизированной левой конечности по сравнению с неишемизированной контрольной правой конечностью) представлены на фигуре 11 и в таблице 7-3. У мышей, получавших в/в клетки hUTC, наблюдалось улучшение относительной реперфузии по сравнению с контрольными животными, получавшими в/в физиологический раствор. Данный эффект был статистически существенным на 7, 10 и 21 сутки. Значительных различий между любыми другими группами по типу обработки и соответствующими контролями не выявлено. У всех животных контрольной группы наблюдался необъясненный максимум относительной перфузии на 14 сутки. К 21 суткам значения для контрольных животных снижались. Относительные величины перфузии на 14 сутки для 2 мышей в контрольной группе в/в введения исключили по причине относительных значений, превышавших 100%. Даже с учетом данных исключенных значений в данный момент времени не было обнаружено различий между группой с в/в введением клеток и контрольной группой.
Средние значения ±СПС для относительных величин перфузии
Плотности капилляров и артериол в обеих задних конечностях определяли в иммуногистологически окрашенных тонких срезах, полученных на 21 сутки. Корреляции между плотностью микрососудов и перфузией не выявлено. Относительная плотность капилляров между контрольными и обработанными группами (фигура 12) значительно не отличалась.
Отличия в плотности артериол между контрольными и обработанными животными не выявлены (фигура 13). Наблюдали некоторую тенденцию к снижению плотности артериол в мышцах, в которые вводили прямую инъекцию фибрина.
Оценивали способность мышей плыть против ламинарного течения перед операцией и затем снова на 10 сутки после операции. В каждом сеансе фиксировали и сравнивали общее время плавания перед индукцией ишемии. Значительного различия между контрольными и обработанными группами в данном функциональном анализе не выявлено.
Таким образом, результаты показывают, что внутривенное введение клеток hUTC приводит к восстановлению кровотока в ишемизированных мышцах на 3 сутки, 10 сутки и 21 сутки после травмы. В частности, внутривенное введение клеток hUTC через 1 сутки после создания ишемии привело к ускорению реперфузии ишемизированных мышц и более высокому уровню относительной перфузии в конце эксперимента (21 сутки). Другие варианты обработки не дали заметного эффекта по результатам любых измерений, использованных в данном исследовании. Механизм, по которому вводимые в/в клетки hUTC улучшали реперфузию, не был выяснен на основе анализа возобновления роста сосудов в ишемизированной области. Возможно, что наблюдаемые эффекты можно объяснить другими механизмами. Недавно было показано, что системно вводимые мезенхимальные стволовые клетки, полученные из костного мозга, захватываются в легких, где они стимулируют защиту на расстоянии путем секреции противовоспалительных факторов, которые могут снижать степень нанесенного ранее повреждения тканей (Lee et al. (2009 г.) Stem Cell. 5(1): 54-63).
Настоящее изобретение не ограничивается описанными и представленными выше вариантами осуществления. Существует возможность вариаций и модификаций в рамках объема прилагаемой формулы изобретения.
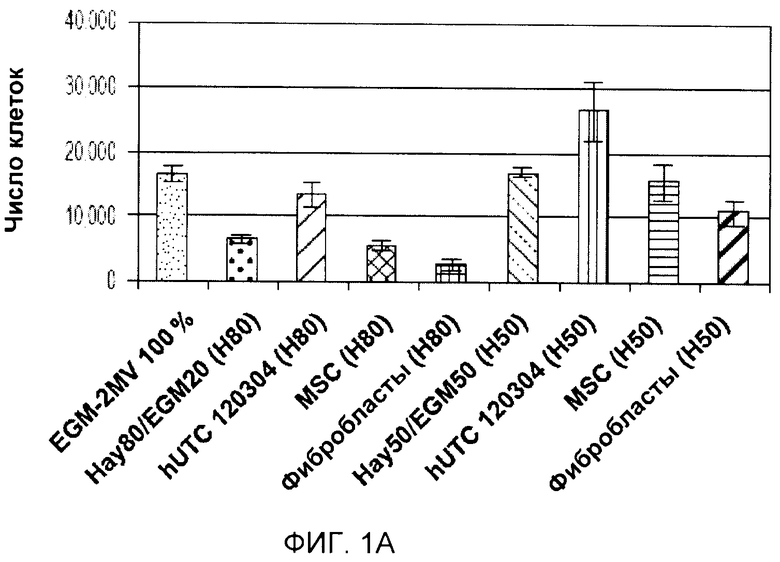
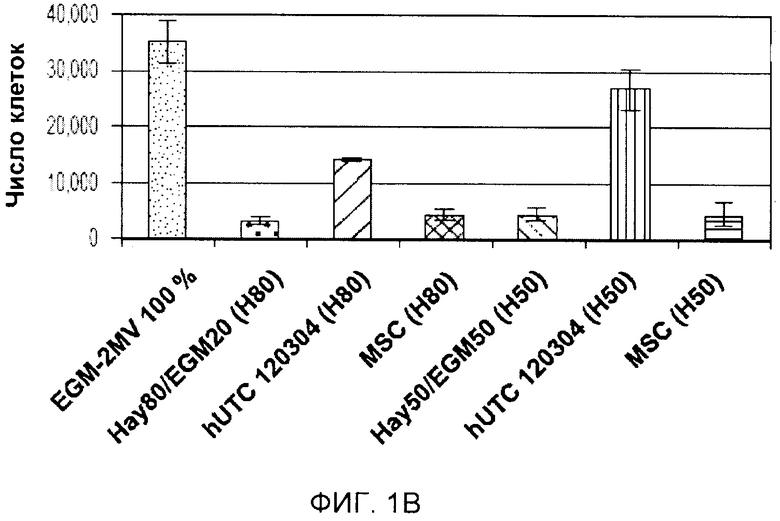
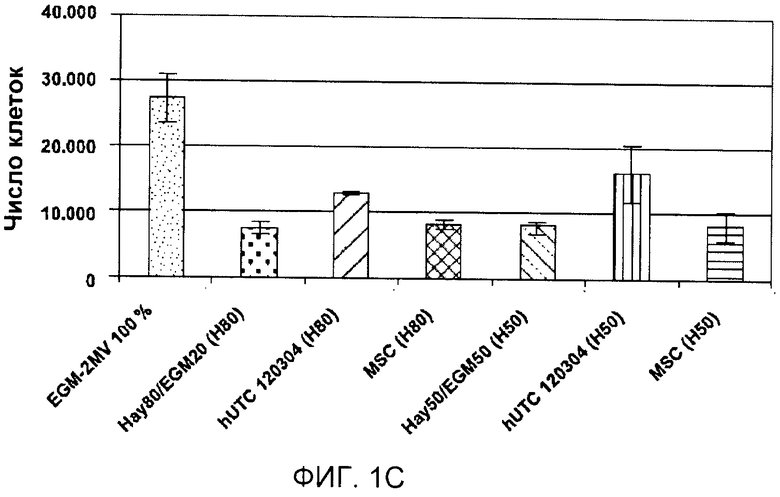
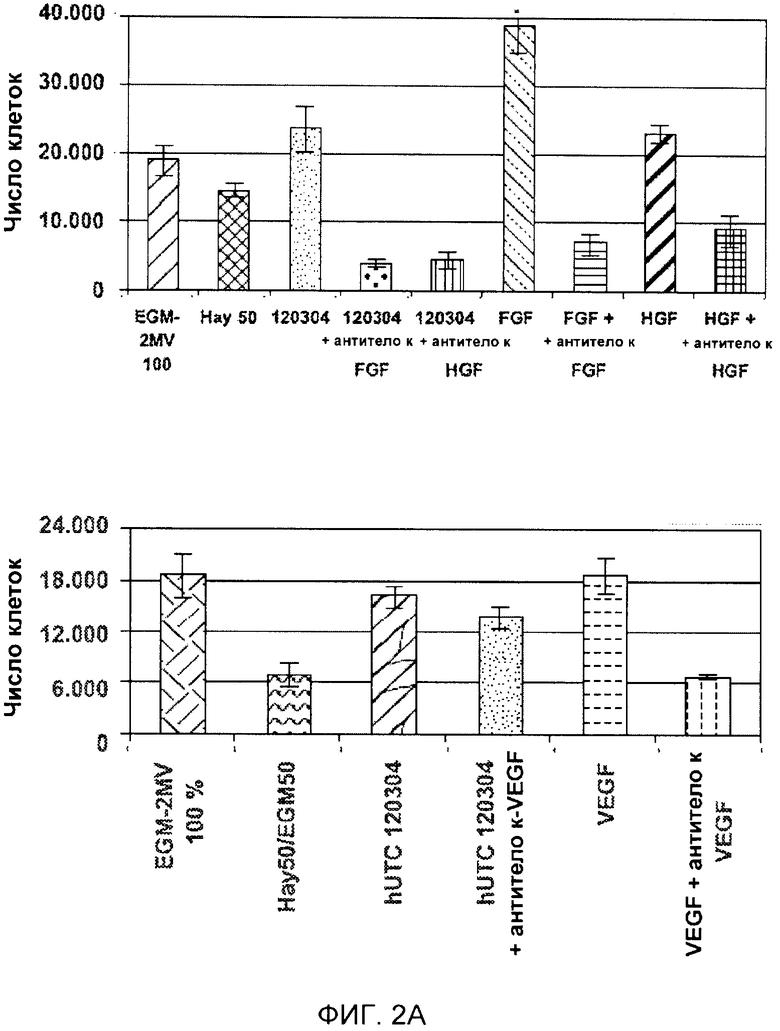

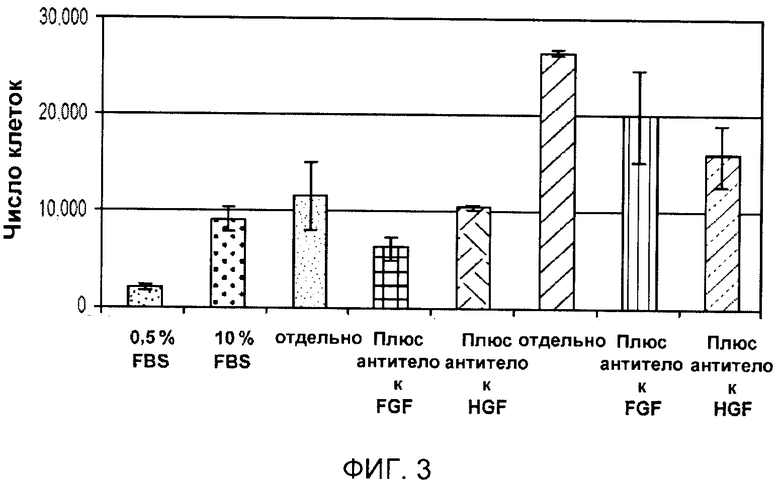
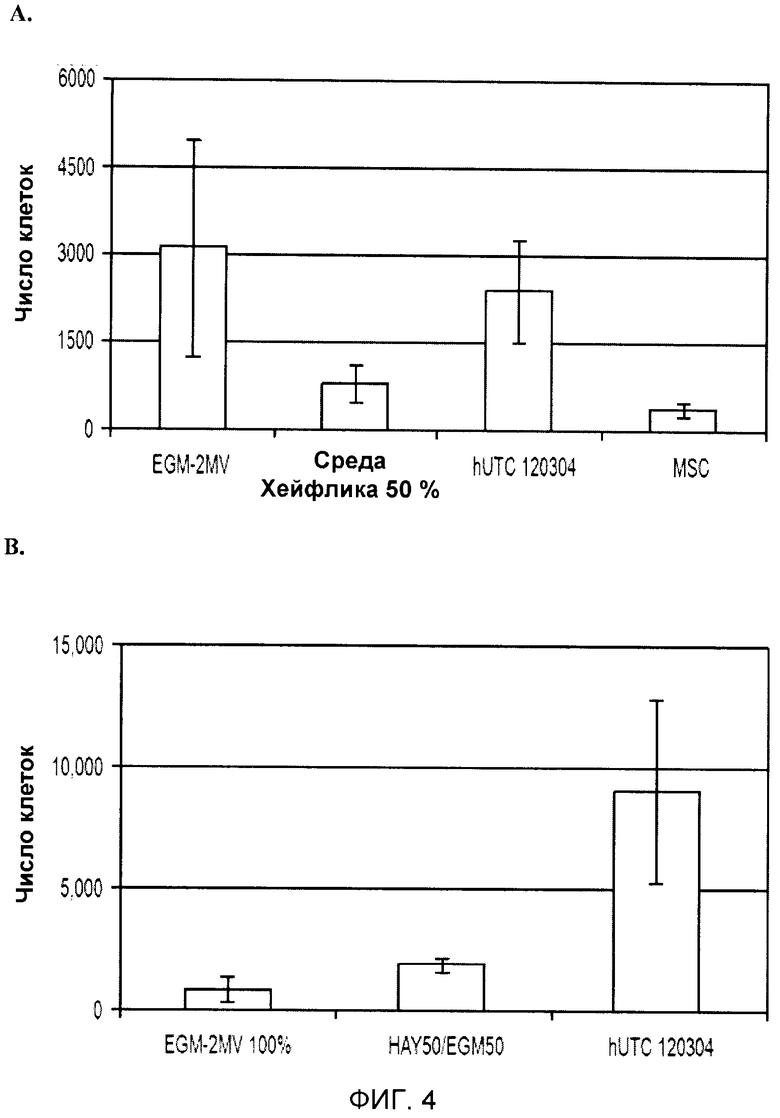
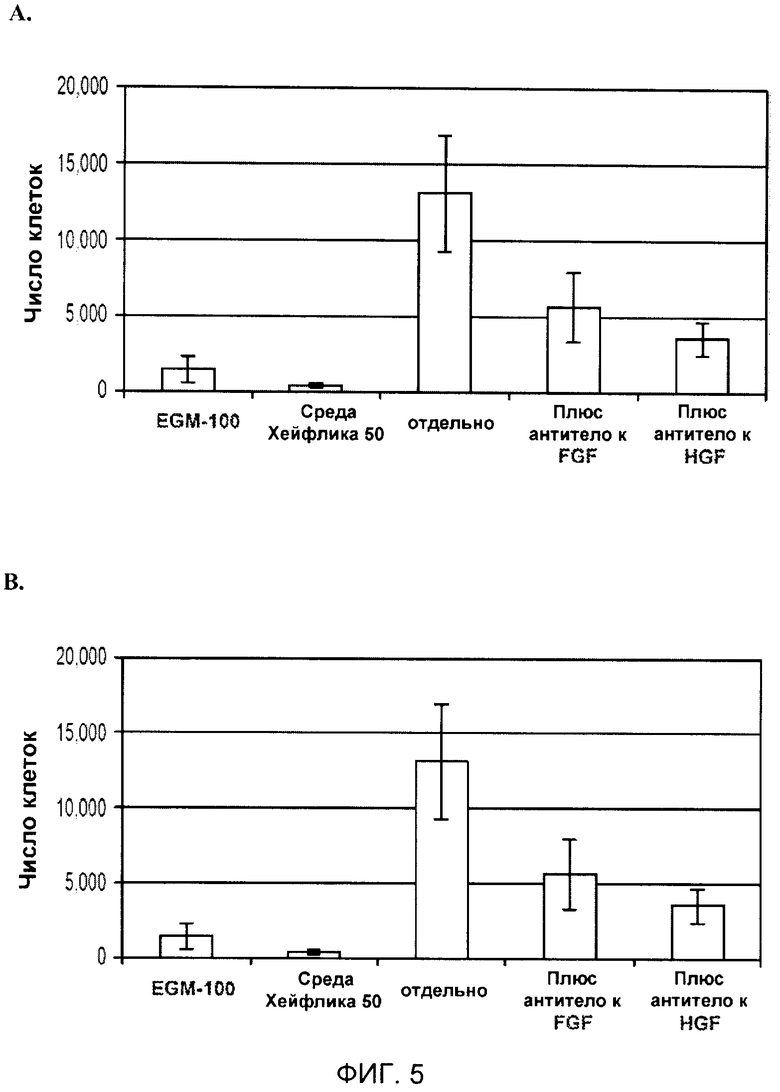

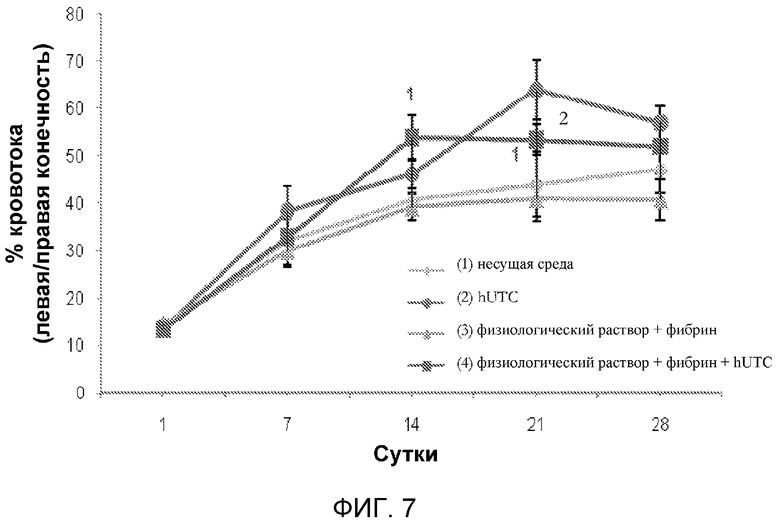

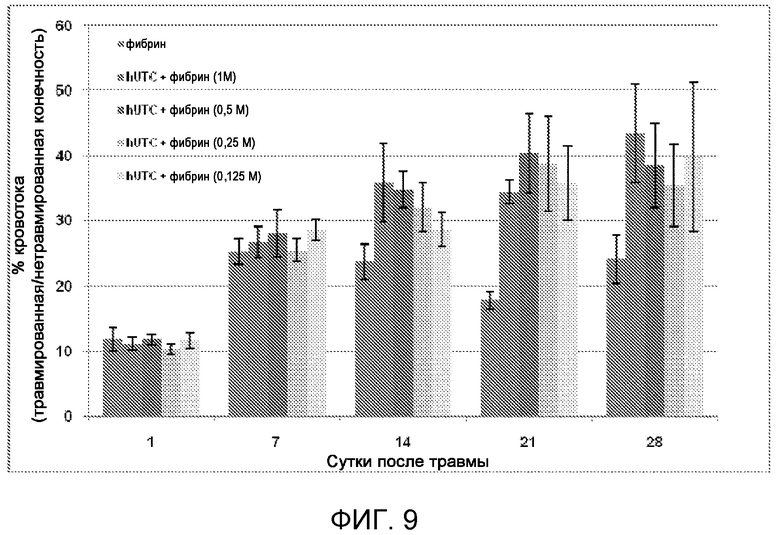
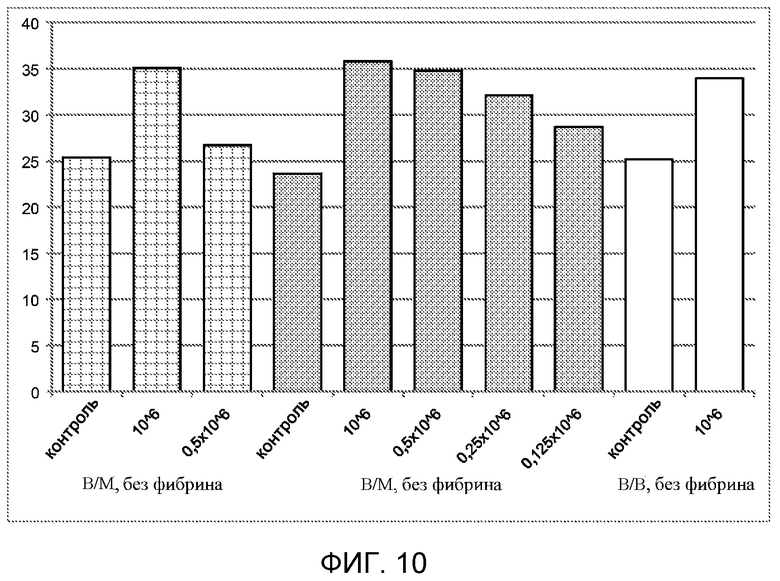
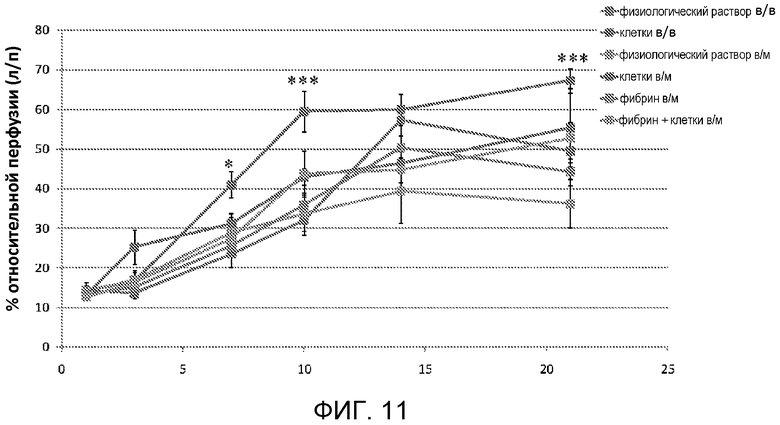
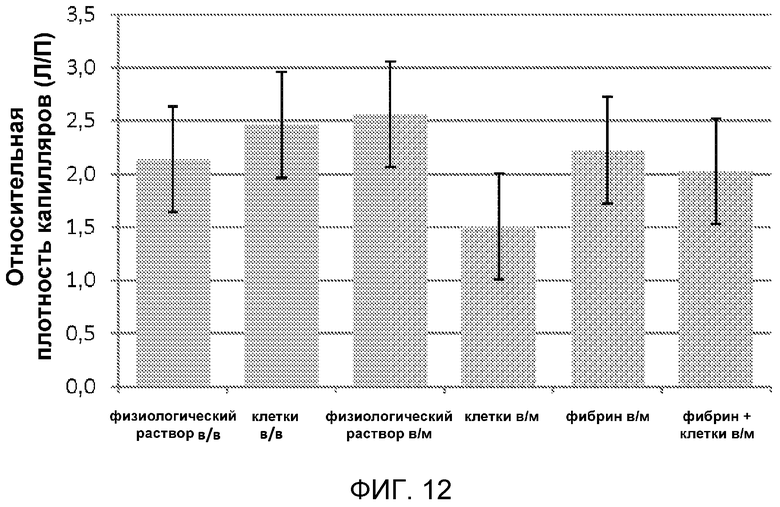
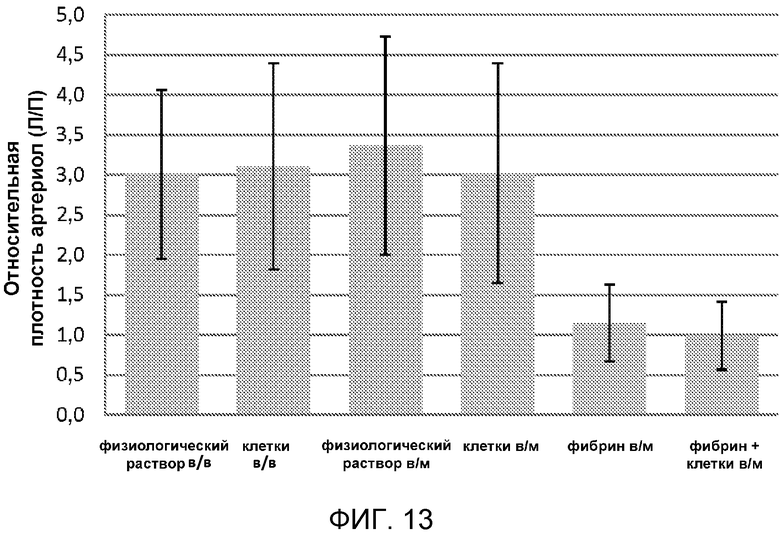
Группа изобретений относится к медицине, а именно к терапии, и может быть использована для повышения реперфузии у пациента, имеющего заболевание периферических сосудов. Для этого применяют местно фармацевтическую композицию, содержащую фибриновый клей и выделенную однородную популяцию клеток, полученных из ткани пуповины человека, в количестве, эффективном для лечения заболевания, причем ткань пуповины по существу свободна от крови. Указанная выделенная однородная популяция клеток способна к самообновлению и размножению в культуре, имеет потенциал для дифференцирования и не экспрессирует CD117 и/или теломеразу. Использование данных изобретений позволяет повысить реперфузию у пациента, имеющего заболевание периферических сосудов путем местного использования клеток ткани пуповины. 2 н. и 32 з.п. ф-лы, 7 пр., 13 ил., 7 табл.
1. Способ повышения реперфузии у пациента, имеющего заболевание периферических сосудов, включающий местное введение фармацевтической композиции, содержащей фибриновый клей и выделенную однородную популяцию клеток, полученных из ткани пуповины человека, в количестве, эффективном для лечения заболевания, причем ткань пуповины по существу свободна от крови, и причем указанная выделенная однородная популяция клеток способна к самообновлению и размножению в культуре, имеет потенциал для дифференцирования и не экспрессирует CD117 и/или теломеразу.
2. Способ по п. 1, в котором выделенная популяция клеток имеет одну или более из следующих характеристик:
(a) экспрессирует рецептор окисленных липопротеинов низкой плотности 1, ретикулон, лиганд хемокинового рецептора 3 и/или гранулоцитарный хемотаксический белок;
(b) не экспрессирует CD31, CD34 или CD45;
(c) экспрессирует, по отношению к фибробластам, мезенхимальным стволовым клеткам или клеткам костного мозга гребня подвздошной кости человека, повышенные уровни интерлейкина-8 или ретикулона 1;
(d) имеет потенциал для дифференцирования в клетки по меньшей мере фенотипов клеток скелетных мышц, клеток гладких мышц сосудов, периваскулярных клеток или клеток эндотелия сосудов; и
(e) экспрессирует CD10, CD13, CD44, CD73 и CD90.
3. Способ по п. 1, в котором заболевание периферических сосудов представляет собой ишемию периферических сосудов.
4. Способ по п. 3, в котором фармацевтическую композицию вводят в местах ишемии периферических сосудов.
5. Способ по п. 4, в котором фармацевтическую композицию вводят путем внутримышечной инъекции или инъекции в жировые депо в мышцах.
6. Способ по п. 1, в котором фармацевтическую композицию вводят путем инъекции, инфузии, имплантации устройства пациенту либо путем имплантации матрицы или каркаса, содержащих фармацевтическую композицию.
7. Способ по п. 1, в котором выделенную популяцию клеток перед введением индуцируют in vitro для дифференцирования по линиям дифференцирования клеток скелетных мышц, клеток мышц сосудов, периваскулярных клеток или клеток эндотелия сосудов.
8. Способ по п. 1, в котором популяцию клеток модифицируют методами генной инженерии для выработки продукта гена, который способствует лечению заболевания периферических сосудов.
9. Способ по п. 1, в котором композиция дополнительно содержит агент, выбранный из группы, состоящей из антитромбогенного агента, иммуносупрессорного агента, иммуномодулирующего агента, проангиогенного агента, антиапоптозного агента и их смесей.
10. Способ по п. 1, в котором композиция дополнительно содержит клетки по меньшей мере одного другого типа, выбранные из следующих: клетки скелетных мышц, клетки-предшественники клеток скелетных мышц, клетки гладких мышц сосудов, клетки-предшественники клеток гладких мышц сосудов, периваскулярные клетки, клетки эндотелия сосудов, клетки-предшественники клеток эндотелия сосудов или другие мультипотентные или плюрипотентные стволовые клетки.
11. Способ по п. 1, в котором фармацевтическая композиция обеспечивает трофический эффект.
12. Способ по п. 11, в котором трофический эффект представляет собой пролиферацию клеток эндотелия сосудов.
13. Способ по п. 1, в котором фармацевтическая композиция индуцирует миграцию клеток эндотелия сосудов и/или клеток-предшественников клеток эндотелия сосудов к местам заболевания периферических сосудов.
14. Способ по п. 1, в котором фармацевтическая композиция индуцирует миграцию клеток гладких мышц сосудов и/или клеток-предшественников клеток гладких мышц сосудов к местам заболевания периферических сосудов.
15. Способ по п. 1, в котором фармацевтическая композиция индуцирует миграцию периваскулярных клеток к местам заболевания периферических сосудов.
16. Способ по п. 1, в котором фибриновый клей содержит фибриноген и тромбин.
17. Способ по п. 16, в котором фибриновый клей содержит от приблизительно 16 до приблизительно 24 МЕ/мл тромбина и от приблизительно 39,3 до приблизительно 60,7 мг/мл фибриногена.
18. Способ повышения реперфузии у пациента, имеющего заболевание периферических сосудов, включающий местное введение фибринового клея и выделенной однородной популяции клеток, полученных из ткани пуповины человека, в количестве, эффективном для лечения заболевания, причем ткань пуповины по существу свободна от крови, и причем указанная выделенная однородная популяция клеток способна к самообновлению и размножению в культуре, имеет потенциал для дифференцирования и не экспрессирует CD117 и/или теломеразу.
19. Способ по п. 18, в котором выделенная популяция клеток имеет одну или более из следующих характеристик:
(a) экспрессирует рецептор окисленных липопротеинов низкой плотности 1, ретикулон, лиганд хемокинового рецептора 3 и/или гранулоцитарный хемотаксический белок;
(b) не экспрессирует CD31, CD34 или CD45;
(c) экспрессирует, по отношению к фибробластам, мезенхимальным стволовым клеткам или клеткам костного мозга гребня подвздошной кости человека, повышенные уровни интерлейкина-8 или ретикулона 1;
(d) имеет потенциал для дифференцирования в клетки по меньшей мере фенотипов клеток скелетных мышц, клеток гладких мышц сосудов, периваскулярных клеток или клеток эндотелия сосудов; и
(e) экспрессирует CD10, CD13, CD44, CD73 и CD90.
20. Способ по п. 18, в котором заболевание периферических сосудов представляет собой ишемию периферических сосудов.
21. Способ по п. 18, в котором клетки и фибриновый клей вводят в местах ишемии периферических сосудов.
22. Способ по п. 18, в котором популяцию клеток и фибриновый клей вводят путем инъекции, инфузии, имплантации устройства пациенту либо путем имплантации матрицы или каркаса, содержащих популяцию клеток.
23. Способ по п. 18, в котором выделенную популяцию клеток перед введением индуцируют in vitro для дифференцирования по линиям дифференцирования клеток скелетных мышц, клеток мышц сосудов, периваскулярных клеток или клеток эндотелия сосудов.
24. Способ по п. 18, в котором популяцию клеток модифицируют методами генной инженерии для выработки продукта гена, который способствует лечению заболевания периферических сосудов.
25. Способ по п. 18, дополнительно включающий введение агента, выбранного из группы, состоящей из антитромбогенного агента, иммуносупрессорного агента, иммуномодулирующего агента, проангиогенного агента, антиапоптозного агента и их смесей.
26. Способ по п. 18, дополнительно включающий введение клеток по меньшей мере одного другого типа, выбранных из следующих: клетки скелетных мышц, клетки-предшественники клеток скелетных мышц, клетки гладких мышц сосудов, клетки-предшественники клеток гладких мышц сосудов, периваскулярные клетки, клетки эндотелия сосудов, клетки-предшественники клеток эндотелия сосудов или другие мультипотентные или плюрипотентные стволовые клетки.
27. Способ по п. 18, в котором популяция клеток обеспечивает трофический эффект.
28. Способ по п. 27, в котором трофический эффект представляет собой пролиферацию клеток эндотелия сосудов.
29. Способ по п. 18, в котором популяция клеток индуцирует миграцию клеток эндотелия сосудов и/или клеток-предшественников клеток эндотелия сосудов к местам заболевания периферических сосудов.
30. Способ по п. 18, в котором популяция клеток индуцирует миграцию клеток гладких мышц сосудов и/или клеток-предшественников клеток гладких мышц сосудов к местам заболевания периферических сосудов.
31. Способ по п. 18, в котором популяция клеток индуцирует миграцию периваскулярных клеток к местам заболевания периферических сосудов.
32. Способ по п. 18, в котором фибриновый клей содержит фибриноген и тромбин.
33. Способ по п. 32, в котором фибриновый клей содержит от приблизительно 16 до приблизительно 24 МЕ/мл тромбина и от приблизительно 39,3 до приблизительно 60,7 мг/мл фибриногена.
34. Способ по п. 18, в котором фибриновый клей вводят одновременно либо до, либо после введения выделенной однородной популяции клеток, полученных из ткани пуповины человека.
| WO 2007076522 A2, 05.07.2007 | |||
| US 2010210013 А1, 19.08.2010 | |||
| WO 2010071862 А1, 24.06.2010 | |||
| ZHAO Q.H | |||
| Et al | |||
| Biological characteristics of human umbilical cord-derived mesenchymal stem cells and their differentiation into chondrogenic and osteogenic cells // Zhonghua Yi Xue Za Zhi | |||
| Способ приготовления лака | 1924 |
|
SU2011A1 |
Авторы
Даты
2016-03-10—Публикация
2011-08-10—Подача