Область применения изобретения
Настоящая заявка на патент относится к питательной обогащенной культурной среде для роста субстратзависимых клеток, например, клеток, извлеченных из ткани пуповины.
Предпосылки создания изобретения
Для аллогенного клеточного терапевтического продукта, клетки и ткани получают от донора, после чего подвергают их дальнейшей обработке до назначения пациентам. В целом, производственный процесс для не-гомологичного клеточного терапевтического продукта включает следующие стадии: размораживание флакона банка клеток и распределение клеток для посева в сосуд для производства; рост клеток в сосуде для производства; удаление нежелательных примесей, использованных во время роста клеток, таких как сыворотка и трипсин; концентрация клеток; формирование клеток в буфер финального формирования; и замораживание клеток. Подобные производственные процессы могут быть весьма сложными и дорогостоящими. Например, клетки для применения в клеточной терапии, как правило, культивируются и разрастаются в ростовой среде, обогащенной сывороткой. Стоимость производства для нужд клеточной терапии может быть очень высокой из-за высокой стоимости сыворотки, среды и прочих материалов, используемых в процессе. Многочисленные факторы могут ограничивать способность клеток к разрастанию до высокой клеточной плотности, в том числе ограничение в питательности, аккумуляция побочных продуктов клеток в культуре, физическая окружающая среда и т.д. Соответственно, желательно увеличить количество волюметрических клеток, произведенных во сосуде для выращивания путем выращивания клеток до высокой клеточной плотности.
Ранее было показано, что субстратзависимые клетки, такие как, к примеру, клетки, извлеченные из тканей человеческой пуповины (hUTC) могут разрастаться до высокой клеточной плотности путем замены среды выращивания клеток, содержащей 15% эмбриональной бычьей сыворотки (FBS) в день 3 процесса. Однако, подобная замена среды менее желательна из-за высокой стоимости сыворотки, высокого уровня использования сыворотки для производства и дополнительных операционных манипуляций. Таким образом, процесс с заменой среды не является коммерчески целесообразным.
Необходим новый способ для выращивания клеток без необходимости замены ростовой среды, который был бы коммерчески целесообразным.
Изложение сущности изобретения
Один из вариантов осуществления изобретения является культуральная среда для выращивания субстратзависимых клеток, которая содержит: (1) аминокислоты L-аргинин; L-цистин; L-цистеин; L-глютамин; глицин; L-гистидин; L-изолейцин; L-лейцин; L-лизин; L-метионин; L-фенилаланин; L-серин; L-треонин; L-триптофан; L-тирозин; L-валин; L-аланин; L-аспарагин, L-аспарагиновая кислота; L-глютаминовая кислота; L-пролин; и L-таурин; (2) витамины D-кальций пантотенат; холина хлорид; фолиевая кислота; I-инозитол; ниацинамид; пиридоксаль; рибофлавин; тиамин; d-биотин; пиридоксин; и витамин B12 (цианокобаламин); (3) соли кальция хлорид; калия хлорид; магнезии сульфат; натрия хлорид; и одна или несколько солей натрия фосфата; (4) нуклеозиды тимидин; аденозин; цитидин; уридин и гуанозин; (5) инсулин; (6) трансферрин; (7) липоевая кислота/тиоктовая кислота; (8) этаноламин; (9) натрия селенит; и (10) один или несколько источников энергии.
В одном варианте осуществления, культурная среда содержит:
по меньшей мере приблизительно 0,05 г/л L-аргинина; по меньшей мере приблизительно 0,02 г/л L-цистина; по меньшей мере приблизительно 0,2 г/л L-глютамина; по меньшей мере приблизительно 0,01 г/л глицина; по меньшей мере приблизительно 0,02 г/л L-гистидина; по меньшей мере приблизительно 0,09 г/л L-изолейцина; по меньшей мере приблизительно 0,09 г/л L-лейцина; по меньшей мере приблизительно 0,09 г/л L-лизина; по меньшей мере приблизительно 0,02 г/л L-метионина; по меньшей мере приблизительно 0,05 г/л L-фенилаланина; по меньшей мере приблизительно 0,03 г/л L-серина; по меньшей мере приблизительно 0,08 г/л L-треонина; по меньшей мере приблизительно 0,009 г/л L-триптофана; по меньшей мере приблизительно 0,08 г/л L-тирозина; по меньшей мере приблизительно 0,08 г/л L-валина; по меньшей мере приблизительно 0,005 г/л L-цистеина; по меньшей мере приблизительно 0,0004 г/л L-аланина; по меньшей мере приблизительно 0,01 г/л L-аспарагина; по меньшей мере приблизительно 0,006 г/л L-аспарагиновой кислоты; по меньшей мере 0,03 г/л L-глютаминовой кислоты; по меньшей мере приблизительно 0,005 г/л L-пролина; и по меньшей мере приблизительно 0,0003 г/л L-таурина;
от приблизительно 5×10-6 г/л до приблизительно 0,015 г/л каждого из витаминов;
по меньшей мере приблизительно 0,05 г/л кальция хлорида, обезвоженного, по меньшей мере приблизительно 0,1 г/л калия хлорида; по меньшей мере приблизительно 0,2 г/л магнезии сульфата; по меньшей мере приблизительно 0,08 г/л натрия фосфата, одноосновного, H2O и по меньшей мере приблизительно 0,0005 г/л натрия фосфата двухосновного гептагидрата (Na2HPO4.7H2O);
по меньшей мере приблизительно 0,0001 г/л тимидина и по меньшей мере приблизительно по 0,005 г/л аденозина, цитидина, уридина и гуанозина; и
по меньшей мере приблизительно 0,003 г/л инсулина; по меньшей мере приблизительно 0,05 г/л трансферрина; по меньшей мере приблизительно 5×10-6 г/л липоевой кислоты/тиоктовой кислоты; по меньшей мере приблизительно 0,05 г/л этаноламина и по меньшей мере приблизительно 0,00004 г/л натрия селенита.
Другим вариантом вариантов осуществления изобретения является не содержащий сыворотки питательный раствор для выращивания субстратзависимых клеток, который содержит:
аминокислоты L-аргинин; L-цистин; L-цистеин; глицин; L-гистидин; L-изолейцин; L-лейцин; L-лизин; L-метионин; L-фенилаланин; L-серин; L-треонин; L-триптофан; L-тирозин; L-валин; L-аланин; L-аспарагин, L-аспарагиновая кислота; L-глютаминовая кислота; L-пролин; и L-таурин;
витамины D-кальций пантотенат; холина хлорид; фолиевая кислота; I-инозитол; ниацинамид; пиридоксаль; рибофлавин; тиамин; d-биотин; пиридоксин; и витамин B12 (цианокобаламин);
соли натрия фосфата, одноосновная, и натрия фосфата двухосновный гептагидрат;
нуклеозиды аденозин; цитидин; уридин и гуанозин;
инсулин; трансферрин; липоевую кислоту/тиоктовую кислоту; этаноламин и натрия селенит.
Изобретение также представляет наборы для выращивания субстратзависимых клеток. Наборы содержат культурную среду и/или не содержащий сыворотки питательный раствор. Культурная среда, не содержащий сыворотки раствор и наборы могут применяться в способе выращивания субстратзависимых клеток (таких, к примеру, как клетки, извлеченные из тканей пуповины).
Соответственно, другой вариант осуществления изобретения представляет собой способ культивации изолированных клеток, полученных из ткани пуповины, который содержит:
выращивание клеток, извлеченных из тканей пуповины, высеянных на микроносители в культуральной среде, содержащей аминокислоты, витамины, соли, нуклеозиды, липоевую/тиоктовую кислоту, этаноламин, инсулин, трансферрин, натрия селенит, которая дополнена сывороткой на период времени, достаточный для достижения клетками желательной первоначальной плотности популяции;
добавление не содержащего сыворотки питательного раствора, который содержит аминокислоты, витамины, соли, инсулин, трансферрин, этаноламин, липоевую/тиоктовую кислоту, натрия селен, после того, как клетки достигли желательной первоначальной плотности популяции; и
выращивание клеток на протяжении достаточного периода времени, чтобы позволить клеткам достичь желательной финальной плотности популяции.
Способ может также содержать дополнительные стадии. В одном варианте осуществления способ также содержит посев клеток в микроносители. В другом варианте осуществления способ также содержит изоляцию клеток после культивации. В одном варианте осуществления желательная первоначальная плотность популяции достигается через 3-4 дня. Способ не требует замены среды. Способ может быть осуществлен в системе культуры в роллерном флаконе и микроносители могут обладать обработанной аминами поверхностью.
Используемые в данном способе клетки, выделенные из ткани пуповины человека, изолированы от ткани пуповины человека по существу свободными от крови, способны к самообновлению и размножению в культуре, обладающими потенциалом к дифференцированию, экспрессирующими CD13, CD90 и HLA-ABC, а также не экспрессирующими CD34, CD117 и HLA-DR. В одном варианте осуществления клетки не экспрессируют hTERT или теломеразу. Характеристики клеток до и после культивирования по существу одинаковы. В одном варианте осуществления характеристики клеток до и после культивирования по существу одинаковы.
В одном варианте осуществления, культурная среда, применяемая в способе, содержит:
аминокислоты L-аргинин; L-цистин; L-цистеин; L-глютамин; глицин; L-гистидин; L-изолейцин; L-лейцин; L-лизин; L-метионин; L-фенилаланин; L-серин; L-треонин; L-триптофан; L-тирозин; L-валин; L-аланин; L-аспарагин, L-аспарагиновая кислота; L-глютаминовая кислота; L-пролин; и L-таурин;
витамины D-кальций пантотенат; холина хлорид; фолиевая кислота; I-инозитол; ниацинамид; пиридоксаль; рибофлавин; тиамин; d-биотин; пиридоксин; и витамин B12 (цианокобаламин);
соли кальция хлорид; калия хлорид; магнезии сульфат; натрия хлорид; и одна или несколько солей натрия фосфата;
нуклеозиды тимидин, аденозин, цитидин, уридин и гуанозин;
инсулин; трансферрин; липоевая кислота/тиоктовая кислота; этаноламин; натрия селенит; и один или несколько источников энергии (таких как, к примеру, D-глюкоза и натрия пируват).
В другом варианте осуществления, культурная среда, применяемая в способе, содержит:
по меньшей мере приблизительно 0,05 г/л L-аргинина; по меньшей мере приблизительно 0,02 г/л L-цистина; по меньшей мере приблизительно 0,2 г/л L-глютамина; по меньшей мере приблизительно 0,01 г/л глицина; по меньшей мере приблизительно 0,02 г/л L-гистидина; по меньшей мере приблизительно 0,09 г/л L-изолейцина; по меньшей мере приблизительно 0,09 г/л L-лейцина; по меньшей мере приблизительно 0,09 г/л L-лизина; по меньшей мере приблизительно 0,02 г/л L-метионина; по меньшей мере приблизительно 0,05 г/л L-фенилаланина; по меньшей мере приблизительно 0,03 г/л L-серина; по меньшей мере приблизительно 0,08 г/л L-треонина; по меньшей мере приблизительно 0,009 г/л L-триптофана; по меньшей мере приблизительно 0,08 г/л L-тирозина; по меньшей мере приблизительно 0,08 г/л L-валина; по меньшей мере приблизительно 0,005 г/л L-цистеина; по меньшей мере приблизительно 0,0004 г/л L-аланина; по меньшей мере приблизительно 0,01 г/л L-аспарагина; по меньшей мере приблизительно 0,006 г/л L-аспарагиновой кислоты; по меньшей мере 0,03 г/л L-глютаминовой кислоты; по меньшей мере приблизительно 0,005 г/л L-пролина; и по меньшей мере приблизительно 0,0003 г/л L-таурина;
от приблизительно 5×10-6 г/л до приблизительно 0,015 г/л каждого из витаминов;
по меньшей мере приблизительно 0,05 г/л кальция хлорида, обезвоженного, по меньшей мере приблизительно 0,1 г/л калия хлорида; по меньшей мере приблизительно 0,2 г/л магнезии сульфата; по меньшей мере приблизительно 0,08 г/л натрия фосфата, одноосновного, H2O и по меньшей мере приблизительно 0,0005 г/л натрия фосфата двухосновного гептагидрата (Na2HPO4.7H2O);
по меньшей мере приблизительно 0,0001 г/л тимидина и по меньшей мере приблизительно по 0,005 г/л аденозина, цитидина, уридина и гуанозина; и
по меньшей мере приблизительно 0,003 г/л инсулина; по меньшей мере приблизительно 0,05 г/л трансферрина; по меньшей мере приблизительно 5×10-6 г/л липоевой кислоты/тиоктовой кислоты; по меньшей мере приблизительно 0,05 г/л этаноламина и по меньшей мере приблизительно 0,00004 г/л натрия селенита.
Культурная среда, использованная в способе, обогащена от 2 до 20% эмбриональной бычьей сыворотки. В одном варианте осуществления, культурная среда обогащена приблизительно 7,5%, приблизительно 10% или приблизительно 15 % эмбриональной бычьей сыворотки.
В одном варианте осуществления, не содержащая сыворотки культурная среда, применяемая в способе, содержит:
аминокислоты L-аргинин; L-цистин; L-цистеин; глицин; L-гистидин; L-изолейцин; L-лейцин; L-лизин; L-метионин; L-фенилаланин; L-серин; L-треонин; L-триптофан; L-тирозин; L-валин; L-аланин; L-аспарагин, L-аспарагиновая кислота; L-глютаминовая кислота; L-пролин; и L-таурин;
витамины D-кальций пантотенат; холина хлорид; фолиевая кислота; I-инозитол; ниацинамид; пиридоксаль; рибофлавин; тиамин; d-биотин; пиридоксин; и витамин B12 (цианокобаламин);
соли натрия фосфата, одноосновная, и натрия фосфата двухосновный гептагидрат;
микроэлементы меди (II) сульфат пентагидрат (CuSO4.5H2), цинка сульфат, гептагидрат (ZnSO4.7H2O);
нуклеозиды аденозин; цитидин; уридин и гуанозин;
инсулин; трансферрин; этаноламин, липоевая кислота/тиоктовая кислота и натрия селенит.
Культурная среда и не содержащий сыворотки питательный раствор могут также содержать другие компоненты. Например, культурная среда и/или не содержащий сыворотки питательный раствор могут далее содержать путресцин, стабилизатор и/или пенообразующий агент.
Другие характеристики и преимущества настоящего изобретения станут им понятны после изучения следующего подробного описания и примеров.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
В приведенном ниже подробном описании примерных вариантов осуществления содержатся ссылки на соответствующие рисунки, которые являются частью настоящего изобретения. Такие варианты осуществления описаны достаточно подробно, чтобы дать возможность специалистам в данной области практически использовать настоящее изобретение, и следует понимать, что могут использоваться и другие варианты осуществления и что логические структурные, механические, электрические и химические изменения можно вносить без отступления от сущности и объема настоящего изобретения. С тем чтобы исключить чрезмерную детализацию, которая не требуется для практического использования специалистами в данной области описанных в настоящем документе вариантов осуществления, в описании может быть опущена определенная информация, известная специалистам в данной области. Поэтому приведенное ниже подробное описание не следует рассматривать как ограничивающее.
В одном аспекте изобретение предоставляет собой процесс выращивания субстратзависимых клеток, таких как, например, клетки, извлеченные из ткани человеческой пуповины, («hUTC»), закрепленных на микроносителях, в содержащей сыворотку среде до высокой клеточной плотности без замены среды путем подпитки культуры не содержащим сыворотки питательным раствором в процессе выращивания. Процесс позволяет рост клеток до высокой клеточной плотности без воздействия на биологическую функцию клеток. Поскольку изобретение увеличивает урожайность производственного биореактора, изобретение предоставляет экономические и коммерческие преимущества.
В другом аспекте изобретение предоставляет культурную среду и питательные растворы, которые пригодны для выращивания субстратзависимых клеток в центрифужных пробирках, предпочтительно без необходимости замены среды.
В одном из вариантов осуществления, изобретение раскрывает композицию обогащенной среды и концентрированного не содержащего сыворотки питательного раствора для выращивания клеток hUTC до высокой плотности в центрифужных пробирках без замены среды. Этот способ снижает потребление сыворотки и увеличивает волюметрическую производительность для снижения стоимости производства. В частности, способ позволяет повысить удвоение популяции с заменой среды.
В другом варианте осуществления изобретение предоставляет не содержащий сыворотки питательный раствор, который содержит: аминокислоты (для восполнения потребленных аминокислот в культуре); витамины; соли (для достижения осмотического баланса в культуре); нуклеозиды; инсулин; трансферрин; и не обязательно, но желательно этаноламин; и натрия селений. Данное изобретение позволяет масштабировать процесс для крупномасштабных биореакторов. В еще одном варианте осуществления, изобретение предоставляет культурную среду, содержащую аминокислоты, витамины, соли, нуклеозиды, инсулин, трансферрин и не обязательно, но предпочтительно этаноламин и натрия селен. Перед применением данная культурная среда может быть дополнена сывороткой.
Другим аспектом изобретения является способ выращивания hUTC, подсоединенных к микроносителям, до высокой клеточной плотности во взвешенной культуре в центрифужных пробирках путем обогащения сыворотки, содержащей среду для выращивания с питательными веществами, и питание культуры не содержащими сыворотки питательными веществами также раскрыто. Этот способ ликвидирует необходимость замены среды для выращивания hUTC до высокой плотности.
В приведенном ниже описании и формуле изобретения применяются различные термины. Такие термины должны иметь смысл, который они обычно имеют в этой области, если только не указано иное. Другие явно определенные термины следует толковать согласно приведенным в настоящем документе определениям.
В одном из вариантов осуществления, клетки, применяемые в настоящем изобретении, обычно называют постнатальными клетками или клетками, полученными в постнатальный период (PPDC). Более конкретно, данные клетки являются «клетками, полученными из пупка», «клетками, полученными из пуповины» (UDC) или «клетками, полученными из ткани пуповины» (UTC). Кроме того, клетки могут быть описаны как являющиеся стволовыми клетками или клетками-предшественниками, причем последний термин применяется в широком смысле. Термин «полученный из» применяется для указания того, что клетки были получены из их биологического источника и были выращены или иным образом обработаны in vitro (например, культивированы в ростовой среде для размножения популяции и/или получения клеточной линии). Манипуляции in vitro с пуповинными стволовыми клетками и уникальные характеристики клеток, полученных из пуповины, составляющих предмет настоящего изобретения, более подробно описаны ниже.
Стволовые клетки представляют собой недифференцированные клетки, определяющиеся по способности на уровне единичной клетки как самообновляться, так и дифференцироваться для получения клеток-потомков, включая самообновляющиеся клетки-предшественники, необновляющиеся клетки-предшественники и окончательно дифференцированные клетки. Стволовые клетки также характеризуются своей способностью дифференцироваться in vitro в функциональные клетки различных клеточных линий из множества зародышевых листков (энтодермы, мезодермы и эктодермы), также как и давать начало тканям после трансплантации, и способствовать образованию по существу большинства, если не всех, тканей после инъекции в бластоцисты.
По своему потенциалу развития стволовые клетки разделяются на: (1) тотипотентные; (2) плюрипотентные; (3) мультипотентные; (4) олигопотентные; и (5) унипотентные. Тотипотентные клетки способны преобразовываться во все виды эмбриональных и внеэмбриональных клеток. Плюрипотентные клетки способны преобразовываться во все виды эмбриональных клеток. Мультипотентные клетки включают в себя клетки, способные преобразовываться в подмножество клеточных линий дифференцировки, но только в пределах конкретной ткани, органа или физиологической системы. Например, гемопоэтические стволовые клетки (HSC) могут порождать клетки-потомки, которые включают в себя HSC (самообновление), рестриктированные олигопотентные клетки-предшественники клеток крови и все типы и элементы клеток (например, тромбоциты), представляющие собой стандартные компоненты крови. Клетки, которые являются олигопотентными, способны преобразовываться в более ограниченное подмножество клеточных линий, чем мультипотентные стволовые клетки. Клетки, которые являются унипотентными, способны преобразовываться в единственную клеточную линию (например, сперматогенные стволовые клетки).
Стволовые клетки также классифицируются на основании источника их получения. Взрослая стволовая клетка как правило представляет собой мультипотентную недифференцированную клетку, присутствующую в ткани, содержащей множество дифференцированных видов клеток. Взрослая стволовая клетка способна к самообновлению. В нормальных условиях она также может дифференцироваться для получения специализированных типов клеток ткани, в которой они находятся, а также, возможно, тканей других типов. Эмбриональная стволовая клетка представляет собой плюрипотентную клетку из внутренней клеточной массы эмбриона на стадии бластоцисты. Фетальная стволовая клетка представляет собой клетку, происходящую из фетальных тканей или мембран. Постнатальная стволовая клетка является мультипотентной или плюрипотентной клеткой, которая по существу происходит из внеэмбриональной ткани, доступной после родов, а именно, из пуповины. Обнаружено, что данные клетки обладают признаками, характерными для плюрипотентных стволовых клеток, включая быструю пролиферацию и потенциал дифференцировки в клетки многих линий. Постнатальные стволовые клетки можно получить из крови (например, клетки, полученные из пуповинной крови) или не из крови (например, из отличных от крови тканей пуповины и плаценты).
Для описания клеток в культуре используются различные термины. «Культура клеток» по существу обозначает клетки, взятые из живого организма и выращенные в контролируемых условиях («в культуре» или «культивированные»). «Первичная культура клеток» обозначает культуру клеток, тканей или органов, взятых непосредственно из организма(ов) до первого пересева. Клетки «размножаются» в культуре, когда их помещают в питательную среду в условиях, способствующих росту и/или делению клеток, что приводит к увеличению популяции клеток. При размножении клеток в культуре скорость пролиферации клеток иногда измеряют по количеству времени, которое необходимо клеткам для удвоения численности. Данное время называют «временем удвоения».
Термин «клеточная линия» по существу относится к популяции клеток, полученной в результате одного или более пересевов первичной клеточной культуры. Каждый цикл пересева называют пассажем. Когда клетки пересеиваются, их называют «пассированными». Конкретная популяция клеток или клеточная линия иногда описывается или характеризуется количеством выполненных с ней пересеваний (пассажей). Например, пересеянная 10 раз культивируемая популяция клеток может описываться как культура десятого пассажа, или культура P10. Первичная культура, т.е. первая культура после изолирования клеток из ткани, обозначается P0. После первого пересева клетки описываются как вторичная культура (P1, или культура первого пассажа). После второго пересева клетки превращаются в третичную культуру (P2, или культура второго пассажа) и т.п. Специалист в данной области определит, что за промежуток времени между последовательными пассированиями популяция клеток может удваиваться многократно; поэтому количество удвоений популяций в культуре превышает количество пассажей. Степень размножения клеток (т.е. число удвоений популяции) за промежуток времени между пассированиями зависит от многих факторов, включая, без ограничений, плотность посева, тип подложки, тип среды, условия роста и продолжительность времени между пассированиями.
«Дифференцировка» представляет собой процесс, при помощи которого неспециализированная («некоммитированная») или малоспециализированная клетка приобретает свойства специализированной клетки, как, например, нервной или мышечной клетки. «Дифференцированная» клетка представляет собой клетку, занявшую более специализированное («коммитированное») положение в линии дифференцировки клетки. Термин «коммитированная» применительно к процессу дифференцирования относится к клетке, дошедшей в ходе процесса дифференцирования до стадии, с которой в нормальных условиях она продолжит дифференцироваться до конкретного типа клеток или подмножества типов клеток и не сможет в нормальных условиях дифференцироваться в иной тип клеток или вернуться к менее дифференцированному типу. «Дедифференцировка» обозначает процесс, в ходе которого клетка возвращается к менее специализированной (или коммитированной) позиции в клеточной линии дифференцировки. Используемый в настоящем документе термин «клеточная линия дифференцировки» определяет наследственность клетки, т.е. определяет, из какой клетки произошла данная клетка и каким клеткам она может дать начало. В клеточной линии дифференцировки клетка помещается в наследственную схему развития и дифференцировки.
В широком смысле «клетка-предшественник» представляет собой клетку, обладающую способностью образовывать клетки-потомки, которые будут более дифференцированы по сравнению с ней, и при этом сохраняющую способность к восполнению пула клеток-предшественников. По данному определению, сами стволовые клетки также являются прогениторными клетками, поскольку являются ближайшими предшественниками окончательно дифференцированных клеток. В отношении клеток из настоящего изобретения, которые более подробно описываются ниже, может использоваться это широкое значение клеток-предшественников. В более узком смысле клетку-предшественника часто определяют как клетку, которая является промежуточным предшественником в процессе дифференцировки, т.е. она происходит из стволовой клетки и является промежуточным звеном при выработке зрелого вида клеток или подмножества видов клеток. Клетки-предшественники этого типа по существу не способны к самообновлению. Соответственно, при отсылке к клетке данного типа в настоящем документе она будет называться «необновляющейся клеткой-предшественником» или «промежуточной клеткой-предшественником».
По существу, «трофический фактор» определяют как вещество, стимулирующее выживаемость, рост, пролиферацию и/или созревание клетки или стимулирующее повышенную активность клетки.
Применяемый в настоящем документе термин «стандартные условия роста» относится к культивированию клеток при 37°C в стандартной атмосфере, содержащей 5% CO2, и при относительной влажности приблизительно 100%. Хотя описанные выше условия можно применять при культивировании клеток, следует понимать, что специалист в данной области, принимая во внимание возможности культивирования клеток, известные в данной области, вполне может варьировать такие условия.
Применяемый в настоящем документе термин «выделенная» по существу относится к клетке, которая была отделена от ее естественной среды. Данный термин включает грубое физическое отделение от естественной среды, например, путем удаления у животного-донора. В предпочтительных вариантах осуществления выделенная клетка не находится в ткани, т.е. клетка отделена или разобщена с соседними клетками, с которыми она контактирует в нормальных условиях. Предпочтительно вводить клетки в виде клеточной суспензии. Применяемый в настоящем документе термин «клеточная суспензия» включает в себя клетки, которые контактируют со средой и были разобщены, например, путем осторожного измельчения фрагмента ткани.
Один из вариантов осуществления изобретения является способом культивирования изолированных субстратзависимых клеток с применением ростовой среды и не содержащего сыворотки питательного раствора данного изобретения. Способ культивирования изолированных субстратзависимых клеток (таких как, к примеру, клеток ткани пуповины) предполагает культивирование клеток на по меньшей мере одной частице-носителе, например, микроносителе. Микроноситель может состоять их материалов натурального или синтетического происхождения. Примерами являются микроносители на основе коллагена, декстрана, или целлюлозы, а также стекла, керамики, полимеров (таких как полистирол), или металлов. Микроноситель может не содержать белков или иметь белковое покрытие, например, из коллагена. В дополнительном аспекте микроноситель может состоять или иметь покрытие из соединений, улучшающих связывание клетки с микроносителем и улучшающих отделение клетки от микроносителя, включая, помимо прочего, такие соединения, как натрия гиалуронат, поли(моностеароилглицерид-ко-янтарная кислота), поли-D,L-лактид-ко-гликолид, фибронектин, ламинин, эластин, лизин, n-изопропилакриламид, витронектин и коллаген. Дальнейшие примеры включают микроносители, обладающие микротоком, такие как микроносители с частичной гальванической парой цинка и меди, которая производит низкие уровни биологически релевантного электричества; или микроносители, являющиеся парамагнетическими, такие как парамагнетические кальций-альгинатные микроносители. Эти способы можно осуществить в системе роллерных флаконов.
Необходимо понимать, что это изобретение не ограничивается конкретными способами, реагентами, соединениями, композициями или биологическими системами, которые, конечно, могут варьироваться. Следует также иметь в виду, что применяемые в настоящем документе термины используются только в целях описания конкретных вариантов осуществления настоящего изобретения и не носят ограничительного характера. При использовании в этом описании и в прилагаемой формуле изобретения, формы единственного числа включают и множественное число, если только содержание текста ясно не указывает на иное. Так, например, обозначение «клетка» включает в себя сочетание двух или более клеток, и подобное.
«Микроносителями» называются частицы, сферы или гранулы, которые могут использоваться для связывания и культивирования субстратзависимых клеток. Микроносители обладают следующими свойствами: (a) они имеют достаточно малые размеры, чтобы их можно было использовать в суспензионных культурах (при скорости перемешивания, не приводящей к заметным сдвиговым повреждениям микроносителей или клеток); (b) они являются цельными или имеют цельное ядро и пористое покрытие на поверхности; и (c) их поверхности (внешняя и внутренняя, в случае пористых носителей) могут иметь положительный или отрицательный заряд. В одном аспекте изобретения общий диаметр частицы находится в диапазоне от приблизительно 150 до 350мкм, а плотность положительного заряда - в диапазоне от приблизительно 0,8 до 2,0 мг-экв/г. Примеры используемых микроносителей включают Cytodex® 1, Cytodex® 2, или Cytodex® 3 (GE Healthcare Life Sciences).
В другом аспекте микроноситель представляет собой цельный носитель. Цельные носители хорошо подходят для адгезионных клеток, например, для субстратзависимых клеток. Частица носителя может также представлять собой пористый микроноситель. Дальнейшие примеры включают микроносители, обладающие микротоком, такие как микроносители с частичной гальванической парой цинка и меди, которая производит низкие уровни биологически релевантного электричества; или микроносители, являющиеся парамагнетическими, такие как парамагнетические кальций-альгинатные микроносители.
Термин «пористые микроносители» относится к частицам, которые могут использоваться для связывания и культивирования субстратзависимых клеток. Пористые микроносители обладают следующими свойствами: (a) они имеют достаточно малые размеры, чтобы их можно было использовать в суспензионных культурах (при скорости перемешивания, не приводящей к сдвиговым повреждениям микроносителей или клеток); (b) они имеют поры и внутренние лакуны, размеры которых достаточны для миграции клеток в лакуны; (c) их поверхности (внешняя и внутренняя) могут иметь положительный или отрицательный заряд. В одной серии вариантов осуществления носители: (a) имеют общий диаметр частицы от приблизительно 150 до 350μмкм; (b) имеют поры с диаметром отверстия от приблизительно 15 до приблизительно 40μмкм; (c) имеют плотность положительного заряда от приблизительно 0,8 до 2,0 мг-экв/г. В некоторых вариантах осуществления, группы DEAE (N, N,-диэтиламиноэтил) предоставляют положительный заряд. К применимым пористым микроносителям относятся, помимо прочего, Cytopore 1® и Cytopore 2® (GE Healthcare Life Sciences, Piscataway, Нью-Джерси, США).
«Субстратзависимыми клетками» являются клетки, в том числе клетки млекопитающих, которым необходимо сцепление с поверхностью, например, поверхностью сосуда для тканевой культуры или поверхностью частицы-микроносителя, для реплицирования в культуре ткани.
При использовании в настоящем документе, термин «приблизительно», когда он относится к измеряемому значению, такому как количество, длительность времени и тому подобное, означает колебания в пределах ±20% или ±10%, более предпочтительно ±5%, еще более предпочтительно ±1%, и еще более предпочтительно ±0,1% от указанного значения, в зависимости от того, какие колебания подходят для осуществления раскрываемых способов.
I. Культурная среда и не содержащий сыворотки питательный раствор
Данное изобретение представляет обогащенную среду и концентрированный питательный раствор, не содержащие сыворотки. Питательная среда и не содержащий сыворотки питательный раствор применяются для выращивания клеток до высокой плотности. В предпочтительном варианте осуществления среда и не содержащий сыворотки питательный раствор могут быть использованы для выращивания субстратзависимых клеток, таких как, например, hUTC, до высокой плотности в центрифужных пробирках при более низком потреблении сыворотки.
В одном из вариантов осуществления культурная среда и не содержащий сыворотки питательный раствор применяются для выращивания клеток, извлеченных из тканей пуповины человека. В другом варианте осуществления культурная среда и не содержащий сыворотку питательный раствор пригодны для выращивания прогениторных клеток, включая, но не ограничиваясь ими, мезенхимальные стволовые клетки, стволовые клетки костного мозга, клетки, извлеченные из плацентарной ткани, адгерентные клетки, извлеченные из не-костомозговых тканей, таких как, например, жировая ткань, мускульная ткань, клетки, извлеченные из кровеносных сосудов, в том числе из грудной артерии, клетки, извлеченные из дентальной пульпы зубов, клетки, извлеченные из амниотической жидкости и фибробласты, в том числе неонатальные фибробласты крайней плоти.
А. Культуральная среда
Одним из аспектов изобретения является культурная среда, содержащая аминокислоты, витамины, соли, нуклеозиды, инсулин, трансферрин, этаноламин и натрия селен, D-глюкоза и натрия пируват.
В одном из вариантов осуществления культуральная среда содержит общие L-аминокислоты. В другом варианте осуществления культуральная среда содержит следующие аминокислоты: L-аргинин; L-цистин; L-глютамин; глицин; L-гистидин; L-изолейцин; L-лейцин; L-лизин; L-метионин; L-фенилаланин; L-серин; L-треонин; L-триптофан; L-тирозин; L-валин; и не в обязательном порядке L-цистеин; L-аланин; L-аспарагин, L-аспарагиновая кислота; L-глютаминовая кислота; L-пролин; и L-таурин. В альтернативном варианте осуществления культуральная среда содержит от приблизительно 0,0006 г/л до приблизительно 0,1 г/л каждой из аминокислот.
В еще одном варианте осуществления культуральная среда включает по меньшей мере приблизительно 0,1 г/л L-аргинина; по меньшей мере приблизительно 0,05 г/л L-цистина; по меньшей мере приблизительно 0,3 г/л L-глютамина; по меньшей мере приблизительно 0,02 г/л глицина; по меньшей мере приблизительно 0,03 г/л L-гистидина; по меньшей мере приблизительно 0,08 г/л L-изолейцина; по меньшей мере приблизительно 0,08 г/л L-лейцина; по меньшей мере приблизительно 0,1 г/л L-лизина; по меньшей мере приблизительно 0,1 г/л L-метионина; по меньшей мере приблизительно 0,05 г/л L-фенилаланина; по меньшей мере приблизительно 0,03 г/л L-серина; по меньшей мере приблизительно 0,08 г/л L-треонина; по меньшей мере приблизительно 0,01 г/л L-триптофана; по меньшей мере приблизительно 0,09 г/л L-тирозина; по меньшей мере приблизительно 0,07 г/л L-валина; по меньшей мере приблизительно 0,007 г/л L-цистеина; по меньшей мере приблизительно 0,0005 г/л L-аланина; по меньшей мере приблизительно 0,02 г/л L-аспарагина; по меньшей мере приблизительно 0,006 г/л L-аспарагиновой кислоты; по меньшей мере 0,03 г/л L-глютаминовой кислоты; по меньшей мере приблизительно 0,01 г/л L-пролина; и по меньшей мере приблизительно 0,0006 г/л L-таурина.
В альтернативном варианте осуществления культуральная среда содержит приблизительно 0,09705 г/л L-аргинина; приблизительно 0,06779 г/л L-цистина; приблизительно 0,009224 г/л L-цистеина; приблизительно 0,584 г/л L-глютамина; приблизительно 0,031125 г/л глицина; приблизительно 0,048288 г/л L-гистидина; приблизительно 0,163713 г/л L-изолейцина; приблизительно 0,163713 г/л L-лейцина; приблизительно 0,16807 г/л L-лизина; приблизительно 0,036748 г/л L-метионина; приблизительно 0,073695 г/л L-фенилаланина; приблизительно 0,05145 г/л L-серина; приблизительно 0,108609 г/л L-треонина; приблизительно 0,018457 г/л L-триптофана; приблизительно 0,121813 г/л L-тирозина; приблизительно 0,111105 г/л L-валина; приблизительно 0,000668 г/л L-аланина; приблизительно 0,031978 г/л L-аспарагина; приблизительно 0,0080 г/л L-аспарагиновой кислоты; 0,054728 г/л L-глютаминовой кислоты; приблизительно 0,02403 г/л L-пролина; и приблизительно 0,000844 г/л L-таурина.
Культуральная среда далее содержит один или несколько витаминов. В одном из вариантов осуществления культуральная среда содержит по меньшей мере следующие витамины: D-кальций пантотенат; холина хлорид; фолиевая кислота; I-инозитол; ниацинамид; пиридоксаль; рибофлавин; тиамин; и не в обязательном порядке d-биотин; пиридоксин; и витамин B12 (цианокобаламин). Среда далее может содержать витамин С и витамин А. В другом варианте осуществления, культуральная среда содержит от приблизительно 5×10-6 г/л до приблизительно 0,015 г/л каждого из витаминов. В одном из вариантов осуществления культуральная среда содержит приблизительно 0,004338 г/л D-кальция пантотената; приблизительно 0,006094 г/л холина хлорида; приблизительно 0,004302 г/л фолиевой кислоты; приблизительно 0,009568 г/л I-инозитола; приблизительно 0,004302 г/л ниацинамида: приблизительно 0,004153 г/л пиридоксаля; приблизительно 0,000431 г/л рибофлавина; приблизительно 0,004304 г/л тиамина; приблизительно 3,75Е-05 г/л d-биотина; приблизительно 1,85Е-05 г/л пиридоксина и приблизительно 0,000102 г/л витамина B12 (цианокобаламин).
Культуральная среда далее включает одну или несколько неорганических солей. В одном из вариантов осуществления культуральная среда содержит кальция хлорид; калия хлорид; магнезии сульфат; натрия хлорид; и одну или несколько солей натрия фосфата. В другом варианте осуществления культуральная среда содержит кальция хлорид, обезвоженный, калия хлорид, магнезии сульфат обезвоженный, натрия фосфат одноосновный H2O и не в обязательном порядке натрия фосфат, двухосновный гептагидрат (Na2HPO4,7H2O). В зависимости от применяемой соли, культуральная среда может содержать от по меньшей мере приблизительно 0,005 г/л до по меньшей мере приблизительно 7 г/л солей. В одном из вариантов осуществления культуральная среда содержит по меньшей мере приблизительно 0,01 г/л кальция хлорида, обезвоженного, по меньшей мере приблизительно 0,1 г/л калия хлорида; по меньшей мере приблизительно 0,2 г/л магнезии сульфата; по меньшей мере приблизительно 0,08 г/л натрия фосфата, одноосновного, H2O и по меньшей мере приблизительно 0,0005 г/л натрия фосфата двухосновного гептагидрата (Na2HPO4.7H2O); В одном из вариантов осуществления культуральная среда содержит приблизительно 0,2 г/л кальция хлорида, обезвоженного, приблизительно 0,4 г/л калия хлорида; приблизительно 0,9767 г/л магнезии сульфата; по меньшей мере приблизительно 0,13 г/л натрия фосфата, одноосновного, H2O, приблизительно 6,4 г/л натрия хлорида и не в обязательном порядке по меньшей мере приблизительно 0,002 г/л натрия фосфата двухосновного гептагидрата (Na2HPO4.7H2O);
Культуральная среда также содержит нуклеозиды. В одном из вариантов осуществления культуральная среда содержит производные от нуклеиновой кислоты (нуклеозиды) тимидин, аденозин, уридин и гуанозин. В альтернативном варианте осуществления среда содержит от по меньшей мере 0,0001 г/л до по меньшей мере приблизительно 0,02 г/л каждого из нуклеозидов. В одном из вариантов осуществления среда содержит по меньшей мере приблизительно 0,0001 г/л тимидина и по меньшей мере приблизительно по 0,005 г/л аденозина, цитидина, уридина и гуанозина. В другом варианте осуществления среда содержит приблизительно 0,00045 г/л тимидина и приблизительно по 0,015 г/л аденозина, цитидина, уридина и гуанозина.
В одном из вариантов осуществления культуральная среда также содержит инсулин, трансферрин, этаноламин и натрия селенат. В другом варианте осуществления культуральная среда содержит по меньшей мере приблизительно 0,003 г/л инсулина. В другом варианте осуществления культуральная среда содержит приблизительно 0,01 г/л инсулина. В альтернативном варианте осуществления культуральная среда содержит по меньшей мере приблизительно 0,05 г/л трансферрина. В другом варианте осуществления культуральная среда содержит приблизительно 0,055 г/л трансферрина. В еще одном варианте осуществления культуральная среда содержит по меньшей мере приблизительно 0,01 г/л этаноламина. В альтернативном варианте осуществления культуральная среда содержит приблизительно 0,02 г/л этаноламина. В одном из вариантов осуществления культуральная среда содержит по меньшей мере приблизительно 0,00004 г/л натрия селенита. В другом варианте осуществления культуральная среда содержит приблизительно 0,000067 г/л натрия селенита. В еще одном варианте осуществления культуральная среда не содержит инсулина, трансферрина и этаноламина.
В одном из вариантов осуществления изобретения культуральная среда содержит:
аминокислоты: L-аргинин; L-цистин; L-цистеин; L-глютамин; глицин; L-гистидин; L-изолейцин; L-лейцин; L-лизин; L-метионин; L-фенилаланин; L-серин; L-треонин; L-триптофан; L-тирозин; L-валин; L-аланин; L-аспарагин, L-аспарагиновая кислота; L-глютаминовая кислота; L-пролин; и L-таурин; витамины: D-кальций пантотенат; холина хлорид; фолиевая кислота; I-инозитол; ниацинамид; пиридоксаль; рибофлавин; тиамин; d-биотин; пиридоксин; и витамин B12 (цианокобаламин); соли: кальция хлорид; калия хлорид; магнезии сульфат; натрия хлорид; и одну или несколько солей натрия фосфата; нуклеозиды (производные нуклеиновых кислот): тимидин, аденозин, цитидин, уридин и гуанозин; инсулин; трансферрин; этаноламин; натрия селенит; и один или несколько источников энергии. В одном из вариантов осуществления культуральная среда содержит от приблизительно 0,0006 г/л до приблизительно 0,1 г/л каждой из аминокислот. В другом варианте осуществления культуральная среда содержит по меньшей мере приблизительно 0,05 г/л L-аргинина; по меньшей мере приблизительно 0,02 г/л L-цистина; по меньшей мере приблизительно 0,2 г/л L-глютамина; по меньшей мере приблизительно 0,01 г/л глицина; по меньшей мере приблизительно 0,02 г/л L-гистидина; по меньшей мере приблизительно 0,09 г/л L-изолейцина; по меньшей мере приблизительно 0,09 г/л L-лейцина; по меньшей мере приблизительно 0,09 г/л L-лизина; по меньшей мере приблизительно 0,02 г/л L-метионина; по меньшей мере приблизительно 0,05 г/л L-фенилаланина; по меньшей мере приблизительно 0,03 г/л L-серина; по меньшей мере приблизительно 0,08 г/л L-треонина; по меньшей мере приблизительно 0,009 г/л L-триптофана; по меньшей мере приблизительно 0,08 г/л L-тирозина; по меньшей мере приблизительно 0,08 г/л L-валина; по меньшей мере приблизительно 0,005 г/л L-цистеина; по меньшей мере приблизительно 0,0004 г/л L-аланина; по меньшей мере приблизительно 0,01 г/л L-аспарагина; по меньшей мере приблизительно 0,006 г/л L-аспарагиновой кислоты; по меньшей мере 0,03 г/л L-глютаминовой кислоты; по меньшей мере приблизительно 0,005 г/л L-пролина; и по меньшей мере приблизительно 0,0003 г/л L-таурина. В альтернативном варианте осуществления культуральная среда содержит от приблизительно 5 x10-6 г/л до приблизительно 0,015 г/л каждого из витаминов. В одном из вариантов осуществления культуральная среда содержит по меньшей мере приблизительно 0,005 г/л кальция хлорида, обезвоженного, по меньшей мере приблизительно 0,1 г/л калия хлорида; по меньшей мере приблизительно 0,2 г/л магнезии сульфата; по меньшей мере приблизительно 0,1 г/л натрия фосфата, одноосновного, H2O и по меньшей мере приблизительно 0,0005 г/л натрия фосфата двухосновного гептагидрата (Na2HPO4.7H2O); В другом варианте осуществления среда содержит от по меньшей мере 0,0001 г/л до по меньшей мере приблизительно 0,02 г/л каждого из нуклеозидов. В одном из вариантов осуществления среда содержит по меньшей мере приблизительно 0,0001 г/л тимидина и по меньшей мере приблизительно по 0,005 г/л аденозина, цитидина, уридина и гуанозина. В одном из вариантов осуществления культуральная среда содержит по меньшей мере 0,005 г/л инсулина и как по меньшей мере 0,03 г/л трансферрина, по меньшей мере 0,01 г/л этаноламина и по меньшей мере приблизительно 0,00004 г/л натрия селенита. Одним или несколькими источниками энергии может быть D-глюкоза и натрия пируват.
В другом варианте осуществления, культуральная среда содержит: (1) аминокислоты L-аргинин; L-цистин; L-цистеин; L-глютамин; глицин; L-гистидин; L-изолейцин; L-лейцин; L-лизин; L-метионин; L-фенилаланин; L-серин; L-треонин; L-триптофан; L-тирозин; L-валин; L-аланин; L-аспарагин, L-аспарагиновая кислота; L-глютаминовая кислота; L-пролин; и L-таурин; (2) витамины D-кальций пантотенат; холина хлорид; фолиевая кислота; I-инозитол; ниацинамид; пиридоксаль; рибофлавин; тиамин; d-биотин; пиридоксин; и витамин B12 (цианокобаламин); (3) соли кальция хлорид; калия хлорид; магнезии сульфат; натрия хлорид; и одна или несколько солей натрия фосфата; (4) нуклеозиды тимидин; аденозин; цитидин; уридин и гуанозин; (5) инсулин; (6) трансферрин; (7) липоевая кислота/тиоктовая кислота; (8) этаноламин; (9) натрия селенит; и (10) один или несколько источников энергии.
В одном из вариантов осуществления изобретения культуральная среда содержит: аминокислоты: L-аргинин; L-цистин; L-цистеин; L-глютамин; глицин; L-гистидин; L-изолейцин; L-лейцин; L-лизин; L-метионин; L-фенилаланин; L-серин; L-треонин; L-триптофан; L-тирозин; L-валин; L-аланин; L-аспарагин, L-аспарагиновая кислота; L-глютаминовая кислота; L-пролин; и L-таурин; витамины: D-кальций пантотенат; холина хлорид; фолиевая кислота; I-инозитол; ниацинамид; пиридоксаль; рибофлавин; тиамин; d-биотин; пиридоксин; и витамин B12 (цианокобаламин); соли: кальция хлорид; калия хлорид; магнезии сульфат; натрия хлорид; и одна или несколько солей натрия фосфата; нуклеозиды (производные нуклеиновых кислот): тимидин, аденозин, цитидин, урилдин и гуанозин; липоевая/тиоктовая кислота; микроэлементы железа нитрат, меди сульфат, цинка сульфат; и один или несколько источников энергии. В одном из вариантов осуществления культуральная среда содержит от приблизительно 0,0006 г/л до приблизительно 0,1 г/л каждой из аминокислот. В другом варианте осуществления культуральная среда содержит по меньшей мере приблизительно 0,05 г/л L-аргинина; по меньшей мере приблизительно 0,02 г/л L-цистина; по меньшей мере приблизительно 0,2 г/л L-глютамина; по меньшей мере приблизительно 0,01 г/л глицина; по меньшей мере приблизительно 0,02 г/л L-гистидина; по меньшей мере приблизительно 0,09 г/л L-изолейцина; по меньшей мере приблизительно 0,09 г/л L-лейцина; по меньшей мере приблизительно 0,09 г/л L-лизина; по меньшей мере приблизительно 0,02 г/л L-метионина; по меньшей мере приблизительно 0,05 г/л L-фенилаланина; по меньшей мере приблизительно 0,03 г/л L-серина; по меньшей мере приблизительно 0,08 г/л L-треонина; по меньшей мере приблизительно 0,009 г/л L-триптофана; по меньшей мере приблизительно 0,08 г/л L-тирозина; по меньшей мере приблизительно 0,08 г/л L-валина; по меньшей мере приблизительно 0,005 г/л L-цистеина; по меньшей мере приблизительно 0,0004 г/л L-аланина; по меньшей мере приблизительно 0,01 г/л L-аспарагина; по меньшей мере приблизительно 0,006 г/л L-аспарагиновой кислоты; по меньшей мере 0,03 г/л L-глютаминовой кислоты; по меньшей мере приблизительно 0,005 г/л L-пролина; и по меньшей мере приблизительно 0,0003 г/л L-таурина. В альтернативном варианте осуществления культуральная среда содержит от приблизительно 5×10-6 г/л до приблизительно 0,015 г/л каждого из витаминов. В одном из вариантов осуществления культуральная среда содержит по меньшей мере приблизительно 0,1 г/л кальция хлорида, обезвоженного, по меньшей мере приблизительно 0,1 г/л калия хлорида; по меньшей мере приблизительно 0,2 г/л магнезии сульфата (обезвоженного), по меньшей мере приблизительно 0,01 г/л натрия фосфата, одноосновного, H2O и по меньшей мере приблизительно 0,005 г/л натрия фосфата двухосновного гептагидрата (Na2HPO4.7H2O). В другом варианте осуществления среда содержит от по меньшей мере 0,0001 г/л до по меньшей мере приблизительно 0,02 г/л каждого из нуклеозидов. В одном из вариантов осуществления среда содержит по меньшей мере приблизительно 0,0001 г/л тимидина и по меньшей мере приблизительно по 0,005 г/л аденозина, цитидина, уридина и гуанозина. Одним или несколькими источниками энергии может быть D-глюкоза и натрия пируват.
В дополнение к микроэлементу натрия селенит, в некоторых вариантах осуществления, культуральная среда также содержит один или более дополнительных микроэлементов. В одном из вариантов осуществления среда также содержит железа нитрат, меди сульфат и цинка сульфат. В одном из вариантов осуществления среда также содержит железа нитрат (9H2O), меди (II) сульфат пентагидрат (CuSO4.5H2O) и цинка сульфат, гептагидрат (ZnSO4,7H2O). Микроэлементы могут присутствовать в количествах, варьирующих от 5×10-8 г/л до приблизительно 3×10-4 г/л каждого из микроэлементов. В альтернативном варианте осуществления среда также содержит приблизительно 0,001 г/л железа нитрата (9H2O), приблизительно 9,33 Е-08 г/л меди (II) сульфата пентагидрата (CuSO4.5H2O) и 3,24 Е-05 г/л цинка сульфата, гептагидрата (ZnSO4,7H2O).
Далее, среда может содержать липоевую кислоту/тиоктовую кислоту, которая может содержать по меньшей мере приблизительно 5×10-6 г/л раствора. В одном из вариантов осуществления среда содержит приблизительно 0,000015 г/л липоевой кислоты/тиоктовой кислоты.
Не в обязательном порядке среда может содержать путресцин, альбумин, стабилизатор и/или пенообразующий агент. В одном из вариантов осуществления альбумин является альбумином бычьей сыворотки. В одном из вариантов осуществления альбумин бычьей сыворотки представлен в форме коммерчески доступного AlbuMAX® I (Gibco™ Cell Culture, Invitrogen Corporation, Карлсбад, Калифорния), который является богатым липидами альбумином бычьей сыворотки. В другом варианте осуществления среда также содержит коммерчески доступный стабилизатор/противовспенивающий агент Pluronic® F68 (Invitrogen Corporation, Карлсбад, Калифорния).
Примеры пригодных вариантов осуществления культуральной среды приведены в таблице ниже:
Количество (г/л)
Количество (г/л)
Количество (г/л)
Данная среда может далее содержать альбумин бычьей сыворотки (BSA), путресцин и Pluronic® F68. В частности, для варианта осуществления А, среда может содержать 3,02 E-05 г/л путресцина, 2,5 г/л BSA и 0,015 г/л Pluronic® F68. Аналогично, для варианта осуществления В, не содержащий сыворотки питательный раствор может содержать по меньшей мере 1 E-05 г/л путресцина, приблизительно 1 г/л BSA и по меньшей мере 0,005 г/л Pluronic® F68. В одном из вариантов осуществления среда содержит путресцин и Pluronic® F68, как, например, 3,02Е-05 г/л путресцина, 2,5 г/л BSA и 0,015 г/л Pluronic® F68.
Культуральная среда изобретения может далее содержать по меньшей мере 0,8 г/л D-глюкозы и по меньшей мере 0,1 г/л натрия пирувата. В одном из вариантов осуществления культуральная среда изобретения может далее содержать приблизительно 1 г/л D-глюкозы и приблизительно 0,11 г/л натрия пирувата.
В одном из вариантов осуществления изобретения культуральная среда дополнена сывороткой, такой как, например, эмбриональная бычья сыворотка (FBS) или сыворотка новорожденного теленка (NCS). Составляющая сыворотки может варьировать в концентрации от 0 (не содержащая сыворотки среда) до 20% общего объема среды. В одном из вариантов осуществления среда дополнена сывороткой (такой как, например, FBS) во время подготовки среды. В другом варианте осуществления среда дополнена прямо перед применением (например, путем добавления раствора, содержащего сыворотку (например, FBS)). В одном из вариантов осуществления предпочтительным дополнением культуральной среды является приблизительно от 2 до 15% (об/об) эмбриональной бычьей сыворотки, альтернативно от приблизительно 2 до приблизительно 10%, альтернативно от приблизительно 3 до приблизительно 12%, альтернативно от приблизительно 5 до приблизительно 15%, альтернативно от приблизительно 4% до приблизительно 10%. В избранных вариантах осуществления, культурная среда обогащена приблизительно 7,5%, приблизительно 10% или приблизительно 15% (об/об) эмбриональной бычьей сыворотки.
В. Не содержащие сыворотки питательные растворы
Другим аспектом изобретения предоставляет не содержащий сыворотки питательный раствор, который содержат: аминокислоты; витамины; соли; нуклеозиды; инсулин; трансферрин; этаноламин; и натрия селенит. Термин «не содержащий сыворотки», применяемый в данном документе относительно питательного раствора, обозначает, что питательный раствор не содержит сыворотки перед добавлением в культуральную среду. Если не указано иное, количества, указанные для компонентов не содержащего сыворотки раствора базируются на измерениях увеличения веса каждого компонента после добавления не содержащего сыворотки питательного раствора к культуре.
В одном из вариантов осуществления не содержащий сыворотки питательный раствор содержит 20 общих L-аминокислот. В другом варианте осуществления не содержащий сыворотки питательный раствор содержит аминокислоты L-аргинин; L-цистин; L-цистеин; глицин; L-гистидин; L-изолейцин; L-лейцин; L-лизин; L-метионин; L-фенилаланин; L-серин; L-треонин; L-триптофан; L-тирозин; L-валин; и не в обязательном порядке L-аланин; L-аспарагин, L-аспарагиновая кислота; L-глютаминовая кислота; L-пролин; и L-таурин. В одном из вариантов осуществления раствор содержит от по меньшей мере 0,0001 г/л до по меньшей мере приблизительно 0,03 г/л каждой из перечисленных аминокислот. В другом варианте осуществления не содержащий сыворотки питательный раствор содержит по меньшей мере приблизительно 0,005 г/л L-аргинина; по меньшей мере приблизительно 0,002 г/л L-цистина; по меньшей мере приблизительно 0,0003 г/л L-цистеина, по меньшей мере приблизительно 0,0005 г/л глицина; по меньшей мере приблизительно 0,002 г/л L-гистидина; по меньшей мере приблизительно 0,01 г/л L-изолейцина; по меньшей мере приблизительно 0,01 г/л L-лейцина; по меньшей мере приблизительно 0,008 г/л L-лизина; по меньшей мере приблизительно 0,002 г/л L-метионина; по меньшей мере приблизительно 0,002 г/л L-фенилаланина; по меньшей мере приблизительно 0,002 г/л L-серина; по меньшей мере приблизительно 0,003 г/л L-треонина; по меньшей мере приблизительно 0,0008 г/л L-триптофана; по меньшей мере приблизительно 0,005 г/л L-тирозина; по меньшей мере приблизительно 0,005 г/л L-валина; по меньшей мере приблизительно 0,0001 г/л L-аланина; по меньшей мере приблизительно 0,005 г/л L-аспарагина; по меньшей мере приблизительно 0,002 г/л L-аспарагиновой кислоты; по меньшей мере 0,01 г/л L-глютаминовой кислоты; по меньшей мере приблизительно 0,008 г/л L-пролина; и по меньшей мере приблизительно 0,008 г/л L-таурина.
В альтернативном варианте осуществления не содержащий сыворотки питательный раствор включает приблизительно 0,013 г/л L-аргинина, HCl; приблизительно 0,005 г/л L-цистина, 2HCl; приблизительно 0,009 г/л L-цистеина HCl H2O; приблизительно 0,001 г/л глицина; приблизительно 0,006 г/л L-гистидина HCl, H2O; приблизительно 0,059 г/л L-изолейцина; приблизительно 0,059 г/л L-лейцина; приблизительно 0,022 г/л L-лизина, HCl; приблизительно 0,007 г/л L-метионина; приблизительно 0,008 г/л L-фенилаланина; приблизительно 0,009 г/л L-серина; приблизительно 0,013 г/л L-треонина; приблизительно 0,002 г/л L-триптофана; приблизительно 0,018 г/л L-тирозина, 2Na, 2H2O ; приблизительно 0,018 г/л L-валина; приблизительно 0,001 г/л L-аланина; приблизительно 0,032 г/л L-аспарагина H2O; приблизительно 0,008 г/л L-аспарагиновой кислоты; 0,055 г/л L-глютаминовой кислоты; приблизительно 0,024 г/л L-пролина; и приблизительно 0,0008 г/л L-таурина. Предполагается, что аминокислоты помогут возместить потребленные в культуре аминокислоты.
Не содержащий сыворотки питательный раствор также содержит один или несколько витаминов. В одном из вариантов осуществления не содержащий сыворотки питательный раствор включает по меньшей мере следующие витамины: D-кальций пантотенат; холина хлорид; фолиевая кислота; I-инозитол; ниацинамид; пиридоксаль; рибофлавин; тиамин; d-биотин; пиридоксин; и витамин B12 (цианокобаламин). Раствор также может содержать витамин С и витамин А. В одном из вариантов осуществления, раствор содержит от приблизительно 5×10-6 г/л до приблизительно 0,001 г/л каждого из витаминов. В одном из вариантов осуществления не содержащий сыворотки питательный раствор содержит по меньшей мере приблизительно 0,0001 г/л D-кальций пантотената; по меньшей мере приблизительно 0,0008 г/л холина хлорида; как минимум приблизительно 0,0001 г/л фолиевой кислоты; по меньшей мере приблизительно 0,0008 г/л I-инозитола; по меньшей мере приблизительно 0,0001 г/л ниацинамида; по меньшей мере приблизительно 0,00005 г/л пиридоксаля; по меньшей мере приблизительно 1×10-5 g/L рибофлавина; по меньшей мере приблизительно 0,00001 г/л тиамина; по меньшей мере 1×10-5 г/л d-биотина; по меньшей мере приблизительно 1×10-5 г/л пиридоксина и по меньшей мере приблизительно 1×10-5 витамина В12 (цианокобаламин). В одном из вариантов осуществления не содержащий сыворотки питательный раствор содержит приблизительно 0,000338 г/л D-кальция пантотената; приблизительно 0,002094 г/л холина хлорида; приблизительно 0,000302 г/л фолиевой кислоты; приблизительно 0,002568 г/л I-инозитола; приблизительно 0,000302 г/л ниацинамида: приблизительно 0,000153 г/л пиридоксаля HCl; приблизительно 3,11T-05 г/л рибофлавина; приблизительно 0,000304 г/л тиамина HCl; приблизительно 3,75Е-05 г/л d-биотина; приблизительно 1,85Е-05 г/л пиридоксина HCl и приблизительно 0,000102 г/л витамина B12 (цианокобаламин).
Дополнительно не содержащий сыворотки питательный раствор содержит одну или несколько солей. В другом варианте осуществления раствор содержит от приблизительно 0,0005 г/л до приблизительно 0,001 г/л фосфатных солей. В альтернативном варианте осуществления раствор содержит фосфаты натрия, такие как натрия фосфат одноосновный и натрия фосфат двухосновный гептагидрат. В еще одном варианте осуществления раствор включает по меньшей мере приблизительно 0,005 г/л натрия фосфата одноосновного и по меньшей мере приблизительно 0,001 г/л натрия фосфата, двухосновного гептагидрата. В альтернативном варианте осуществления раствор включает приблизительно 0,008 г/л натрия фосфата одноосновного и приблизительно 0,002 г/л натрия фосфата, двухосновного гептагидрата.
Не содержащий сыворотки питательный раствор также содержит нуклеозиды. В одном из вариантов осуществления не содержащий сыворотки питательный раствор содержит производные от нуклеиновой кислоты тимидин, аденозин, уридин и гуанозин. В альтернативном варианте осуществления раствор содержит от по меньшей мере 0,0001 г/л до по меньшей мере приблизительно 0,005 г/л каждого из нуклеозидов. В одном из вариантов осуществления раствор содержит по меньшей мере приблизительно 0,0001 г/л тимидина и по меньшей мере приблизительно по 0,005 г/л аденозина, цитидина, уридина и гуанозина. В другом варианте осуществления раствор содержит приблизительно 0,0005 г/л тимидина и приблизительно по 0,015 г/л аденозина, цитидина, уридина и гуанозина.
Не содержащий сыворотки питательный раствор также содержит инсулин, трансферрин, этаноламин и натрия селенит. В одном из вариантов осуществления раствор содержит по меньшей мере 0,002 г/л, альтернативно приблизительно 0,01 г/л инсулина. В другом варианте осуществления раствор содержит по меньшей мере 0,01 г/л, альтернативно приблизительно 0,06 г/л трансферрина. В альтернативном варианте осуществления раствор содержит по меньшей мере 0,005 г/л, альтернативно приблизительно 0,02 г/л этаноламина. В еще одном варианте осуществления раствор содержит по меньшей мере 2×10-5 г/л, альтернативно приблизительно 7×10-5г/л натрия селенита.
В дополнение к микроэлементу натрия селенит, в некоторых вариантах осуществления, не содержащий сыворотки питательный раствор также содержит один или несколько дополнительных микроэлементов. В одном из вариантов осуществления раствор содержит от приблизительно 3×10-8 г/л до приблизительно 2×10-5 каждого из одного или нескольких дополнительных микроэлементов. В одном из вариантов осуществления раствор также содержит меди (II) сульфат пентагидрат (CuSO4.5H2O) и цинка сульфат, гептагидрат (ZnSO4,7H2O). В другом варианте осуществления раствор также содержит по меньшей мере приблизительно 3×10-8 г/л меди (II) сульфата пентагидрата (CuSO4.5H2O) и по меньшей мере приблизительно 5×10-6 г/л цинка сульфата, гептагидрата (ZnSO4.7H2O). В альтернативном варианте осуществления раствор также содержит приблизительно 9×10-8 г/л меди (II) сульфата пентагидрата (CuSO4.5H2O) и приблизительно = 3×10-5 г/л цинка сульфата, гептагидрата (ZnSO4.7H2O).
Подробнее, в дополнение к липидному этаноламину, не содержащий сыворотки питательный раствор может также содержать липоевую кислоту/тиоктовую кислоту, которая может содержать по меньшей мере приблизительно 1×10-5 г/л раствора.
В одном из вариантов осуществления изобретения не содержащий сыворотки питательный раствор содержит:
аминокислоты L-аргинин; L-цистин; L-цистеин; глицин; L-гистидин; L-изолейцин; L-лейцин; L-лизин; L-метионин; L-фенилаланин; L-серин; L-треонин; L-триптофан; L-тирозин; L-валин; L-аланин; L-аспарагин, L-аспарагиновая кислота; L-глютаминовая кислота; L-пролин; и L-таурин;
витамины D-кальций пантотенат; холина хлорид; фолиевая кислота; I-инозитол; ниацинамид; пиридоксаль; рибофлавин; тиамин; d-биотин; пиридоксин; и витамин B12 (цианокобаламин);
соли натрия фосфата, одноосновная, и натрия фосфата двухосновный гептагидрат;
нуклеозиды аденозин; цитидин; уридин и гуанозин;
инсулин; трансферрин; этаноламин и натрия селенит.
Этот не содержащий сыворотки раствор может не в обязательном порядке содержать меди (II) сульфат пентагидрат (CuSO4.5H2O) и цинка сульфат, гептагидрат (ZnSO4,7H2O). Дополнительно не содержащий сыворотки раствор может также не в обязательном порядке содержать липоевую кислоту/тиоктовую кислоту. В одном из вариантов осуществления, раствор содержит: (1) от приблизительно 0,0001 г/л до приблизительно 0,03 г/л каждой из аминокислот; (2) от приблизительно 0,00001 г/л до приблизительно 0,001 г/л каждого из витаминов; (3) по меньшей мере приблизительно 5×10-6 г/л натрия фосфата, одноосновного и по меньшей мере приблизительно 0,001 г/л натрия фосфата, двухосновного гептагидрата; (4) по меньшей мере приблизительно 0,0001 г/л тимидина и по меньшей мере приблизительно по 0,005 г/л аденозина, цитидина, уридина и гуанозина; (5) по меньшей мере 0,002 г/л инсулина; (6) по меньшей мере приблизительно 0,03 г/л трансферрина; (7) по меньшей мере приблизительно 0,005 г/л этаноламина и (8) по меньшей мере приблизительно 5×10-5 г/л натрия селенита. Не в обязательном порядке раствор также содержит (9) по меньшей мере приблизительно 7×10-8 г/л меди (II) сульфата пентагидрата (CuSO4.5H2O); (10) по меньшей мере приблизительно 5×10-6 г/л цинка сульфата, гептагидрата (ZnSO4.7H2O); и (11) по меньшей мере приблизительно 1×10-6 г/л липоевой кислоты/тиоктовой кислоты.
В другом варианте осуществления не содержащий сыворотки питательный раствор содержит аминокислоты, витамины, соли, нуклеозиды, меди (II) сульфат пентагидрат (CuSO4.5H2O), цинка сульфат, гептагидрат, (ZnSO4,7H2O) и липоевую/тиоктовую кислоту. В этом варианте осуществления, раствор содержит:
аминокислоты L-аргинин; L-цистин; L-цистеин; глицин; L-гистидин; L-изолейцин; L-лейцин; L-лизин; L-метионин; L-фенилаланин; L-серин; L-треонин; L-триптофан; L-тирозин; L-валин; L-аланин; L-аспарагин, L-аспарагиновая кислота; L-глютаминовая кислота; L-пролин; и L-таурин;
витамины D-кальций пантотенат; холина хлорид; фолиевая кислота; I-инозитол; ниацинамид; пиридоксаль; рибофлавин; тиамин; d-биотин; пиридоксин; и витамин B12 (цианокобаламин);
соли натрия фосфата, одноосновная, и натрия фосфата двухосновный гептагидрат; и
нуклеозиды тимидин, аденозин, цитидин, уридин и гуанозин.
В одном из вариантов осуществления не содержащий сыворотки питательный раствор содержит по меньшей мере приблизительно 0,005 г/л L-аргинина; по меньшей мере приблизительно 0,002 г/л L-цистина; по меньшей мере приблизительно 0,0003 г/л L-цистеина, по меньшей мере приблизительно 0,0005 г/л глицина; по меньшей мере приблизительно 0,002 г/л L-гистидина; по меньшей мере приблизительно 0,01 г/л L-изолейцина; по меньшей мере приблизительно 0,01 г/л L-лейцина; по меньшей мере приблизительно 0,008 г/л L-лизина; по меньшей мере приблизительно 0,002 г/л L-метионина; по меньшей мере приблизительно 0,002 г/л L-фенилаланина; по меньшей мере приблизительно 0,002 г/л L-серина; по меньшей мере приблизительно 0,003 г/л L-треонина; по меньшей мере приблизительно 0,0008 г/л L-триптофана; по меньшей мере приблизительно 0,005 г/л L-тирозина; по меньшей мере приблизительно 0,005 г/л L-валина; по меньшей мере приблизительно 0,0001 г/л L-аланина; по меньшей мере приблизительно 0,005 г/л L-аспарагина; по меньшей мере приблизительно 0,002 г/л L-аспарагиновой кислоты; по меньшей мере 0,01 г/л L-глютаминовой кислоты; по меньшей мере приблизительно 0,008 г/л L-пролина; и по меньшей мере приблизительно 0,008 г/л L-таурина. В одном из вариантов осуществления не содержащий сыворотки питательный раствор также содержит по меньшей мере приблизительно 0,0001 г/л D-кальций пантотената; по меньшей мере приблизительно 0,0008 г/л холина хлорида; как минимум приблизительно 0,0001 г/л фолиевой кислоты; по меньшей мере приблизительно 0,0008 г/л I-инозитола; по меньшей мере приблизительно 0,0001 г/л ниацинамида; по меньшей мере приблизительно 0,00005 г/л пиридоксаля; по меньшей мере приблизительно 1×10-5 g/L рибофлавина; по меньшей мере приблизительно 0,00001 г/л тиамина; по меньшей мере приблизительно 1×10-5 г/л d-биотина; по меньшей мере приблизительно 1×10-5 г/л пиридоксина и по меньшей мере приблизительно 1×10-5 витамина В12 (цианокобаламин). В альтернативном варианте осуществления этот раствор также содержит по меньшей мере приблизительно 0,0001 г/л тимидина и по меньшей мере приблизительно по 0,01 г/л аденозина, цитидина, уридина и гуанозина. В другом варианте осуществления раствор также содержит по меньшей мере приблизительно 3×10-8 г/л меди (II) сульфата пентагидрата (CuSO4.5H2O), приблизительно 5×10-5 г/л цинка сульфата, гептагидрата (ZnSO4.7H2O); и приблизительно 2×10-5 г/л липоевой кислоты/тиоктовой кислоты.
Не в обязательном порядке не содержащие сыворотки питательные растворы могут также содержать путресцин, альбумин бычьей сыворотки, стабилизатор и/или пенообразующий агент. В одном из вариантов осуществления альбумин бычьей сыворотки представлен в форме коммерчески доступного AlbuMAX® I (Gibco™ Cell Culture, Invitrogen Corporation, Карлсбад, Калифорния), который является богатым липидами альбумином бычьей сыворотки. В другом варианте осуществления не содержащий сыворотки питательный раствор содержит коммерчески доступный стабилизатор/противовспенивающий агент Pluronic® F68 (Invitrogen Corporation, Карлсбад, Калифорния).
Примеры пригодных вариантов осуществления не содержащего сыворотки питательного раствора приведены в таблице ниже:
Количество (г/л)
Количество (г/л)
Количество (г/л)
ФСША
Эти не содержащие сыворотки питательные растворы могут также содержать альбумин бычьей сыворотки (BSA), путресцин и Pluronic® F68. В частности, для варианта осуществления А, не содержащий сыворотки питательный раствор может также содержать 3,02 E-05 г/л путресцина, 2,5 г/л альбумина бычьей сыворотки и 0,015 г/л Pluronic® F68. Аналогично, для варианта осуществления В, не содержащий сыворотки питательный раствор может содержать по меньшей мере 1 E-05 г/л путресцина, приблизительно 1 г/л BSA и по меньшей мере 0,005 г/л Pluronic® F68. В одном из предпочтительных вариантов осуществления не содержащие сыворотки питательные растворы также содержат путресцин и Pluronic® F68.
В варианте осуществления не содержащий сыворотки питательный раствор содержит натрия селенат, этаноламин, инсулин, трансферрин, тимидин, аденозин, цитидин, уридин, гуанозин и альбумин сыворотки (например, альбумин бычьей сыворотки).
Не в обязательном порядке не содержащий сыворотки питательный раствор может также содержать один или несколько энергетических субстратов, таких как, например, глюкоза и/или пируват.
В одном из вариантов осуществления изобретения, культуральная среда и/или не содержащий сыворотки питательный раствор не содержат привнесенных извне факторов, стимулирующих рост недифференцированных клеток. В одном предпочтительном варианте осуществления культуральная среда и/или не содержащий сыворотки питательный раствор не содержат фибробластного фактора роста, такого как, например, базовый FGF или FGF-4.
II. Клетки, полученные из ткани пуповины человека (hUTC)
Как обсуждалось выше в некоторых вариантах осуществления изобретения, культуральная среда и не содержащие сыворотки питательные растворы могут применяться для выращивания изолированных клеток, полученных из ткани пуповины человека («hUTC» или «UTC»). Популяции UTC и UTC пригодны для применения с культуральной средой, не содержащим сыворотки раствором, оборудованием и способами настоящего изобретения, которые подробно описаны как ниже в настоящем документе, так и в патентах США № 7510873; 7524489 и опубликованной заявки на патент США № 2005/005863, которые включены в настоящий документ во всей полноте, поскольку они имеют отношение к описанию, выделению и характеристике hUTC.
A. Выделение и рост клеток, полученных из ткани пуповины
В соответствии со способами, описанными в настоящем документе, пуповину млекопитающего получают по завершении доношенной или недоношенной беременности, например, после отделения последа, или вскоре после этого. Ткань постнатального материала можно транспортировать с места родов в лабораторию в стерильном контейнере, например, в колбе, лабораторном стакане, чашке для культивирования или пакете. Контейнер может содержать раствор или среду, включая, без ограничений, солевой раствор, такой как модифицированная по способу Дульбекко среда Игла (DMEM) (также известный как минимальная эссенциальная среда Игла) или фосфатно-буферный раствор (PBS), либо любой раствор, применяемый для транспортировки органов, используемых для трансплантации, такой как раствор, разработанный в Висконсинском университете, либо перфторированный раствор. В среду или буферный раствор можно добавить один или более антибиотиков и/или антимикотиков, включая, без ограничений, пенициллин, стрептомицин, амфотерицин B, гентамицин и нистатин. Ткань постнатального материала можно промыть в растворе антикоагулянта, таком как гепаринсодержащий раствор. До экстрагирования UTC ткань предпочтительно поддерживать при температуре приблизительно 4–10°. Еще более предпочтительно не замораживать ткань до извлечения клеток UTC.
Выделение UTC предпочтительно проводить в асептических условиях. Пуповину можно отделить от плаценты с использованием средств, известных специалистам в данной области. В альтернативном варианте осуществления пуповину и плаценту используют без отделения. Перед выделением клеток UTC из ткани постнатального материала предпочтительно удалить кровь и продукты распада клеток. Например, ткань неонатального материала можно промыть в буферном растворе, включая фосфатно-буферный раствор, но не ограничиваясь им. Промывочный буфер может также содержать один или более антимикотиков и/или антибиотиков, включая, без ограничений, пенициллин, стрептомицин, амфотерицин B, гентамицин и нистатин.
Ткань неонатального материала, представляющую собой цельную пуповину или ее фрагмент или часть, механически измельчают (используя разрезающее или сдвиговое усилие). В предпочтительном в настоящее время варианте осуществления в процедуре выделения клеток также используют способ ферментативного расщепления. Специалистам в данной области известно множество ферментов, подходящих для использования при выделении отдельных клеток из сложных тканевых матриц для облегчения их выращивания в культуре. В продаже доступны расщепляющие ферменты от слабо расщепляющих (например, дезоксирибонуклеазы и нейтральная протеаза, диспаза) до сильно расщепляющих (например, папаин и трипсин). Неограничивающий перечень ферментов, совместимых с целями настоящего изобретения, содержит ферменты с муколитической активностью, металлопротеазы, нейтральные протеазы, серинпротеазы (такие как трипсин, химотрипсин или эластаза) и дезоксирибонуклеазы. В настоящее время предпочтительными являются ферменты с активностью, выбранные из металлопротеаз, нейтральных протеаз и ферментов с муколитической активностью. Например, известно, что коллагеназы подходят для выделения различных клеток из тканей. Дезоксирибонуклеазы могут расщеплять одноцепочечные ДНК и позволяют свести к минимуму агглютинацию клеток в процессе выделения. Предпочтительные способы содержат ферментативную обработку, например, с использованием коллагеназы и диспазы, либо коллагеназы, диспазы и гиалуронидазы. В определенных вариантах осуществления на стадии диссоциации используют смесь коллагеназы и нейтральной протеазы (диспазы). В более конкретных вариантах осуществления применяют расщепление в присутствии по меньшей мере одной коллагеназы из Clostridium histolyticum и одного из ферментов с протеазной активностью, диспазы и термолизина. В других вариантах осуществления используют расщепление с использованием ферментов как с коллагеназной, так и диспазной активностью. Также используют способы, которые включают в себя расщепление ферментом с гиалуронидазной активностью помимо ферментов с коллагеназной и диспазной активностью. Специалист в данной области определит, что известно множество способов таких ферментативных обработок для выделения клеток из различных тканей-источников. Например, в быстрых способах можно применять ферментативные смеси для диссоциации тканей, доступные в продаже под торговым наименованием LIBERASE (Roche, Индианаполис, штат Индиана). Известны и другие источники ферментов, и специалист в данной области также может получить такие ферменты непосредственно из их природных источников. Специалист в данной области также может оценивать возможности новых или дополнительных ферментов или комбинаций ферментов для выделения клеток, составляющих предмет настоящего изобретения. Предпочтительная продолжительность ферментативной обработки составляет 0,5, 1, 1,5 или 2 часа или более. В других предпочтительных вариантах осуществления ткань инкубируют при температуре 37°C в процессе ферментативной обработки на стадии диссоциации.
В некоторых вариантах осуществления настоящего изобретения ткань постнатального материала разделяют на части, содержащие различные аспекты ткани, такие как, например, неонатальный, неонатальный/материнский и материнский аспекты плаценты. Разделенные части затем диссоциируют с использованием механической и/или ферментативной диссоциации в соответствии со способами, описанными в настоящем документе. Клетки неонатальных или материнских линий можно определить любыми средствами, известными специалистам в данной области техники, например, с использованием анализа кариотипа или гибридизации in situ на Y-хромосому.
Выделенные клетки или ткань пуповины, из которой получают UTC, можно использовать для инициирования, или посева, клеточных культур. Выделенные клетки переносят в стерильные сосуды для культивирования ткани без покрытия или с покрытием внеклеточным матриксом или лигандами, такими как ламинин, коллаген (нативный, денатурированный или сшитый), желатин, фибронектин и другие белки внеклеточного матрикса. В дополнение к раскрытой в данном документе культуральной среде UTC можно культивировать в любой культуральной среде, которая способна поддерживать рост клеток, такой как, без ограничений, среда DMEM (с высоким или низким содержанием глюкозы), улучшенная среда DMEM, среда DMEM/MCDB 201, основная среда Игла, среда Хэма F10 (F10), среда Хэма F12 (F12), модифицированная по способу Искова среда Дульбекко, ростовая среда для мезенхимальных стволовых клеток (MSCGM), среда DMEM/F12, среда RPMI 1640 и среда, не содержащая сыворотку/субстрат, доступная в продаже под торговым наименованием CELL-GRO-FREE® (Mediatech, Inc., Херндон, штат Вирджиния). В культуральную среду можно дополнительно ввести один или более компонентов, включая, например, фетальную бычью сыворотку, предпочтительно приблизительно 2-15% (об/об); лошадиную сыворотку; человеческую сыворотку; фетальную телячью сыворотку; бета-меркаптоэтанол (BME или 2-ME), предпочтительно приблизительно 0,001% (об/об); один или более факторов роста, например, фактор роста тромбоцитов (PDGF), эпидермальный фактор роста (EGF), фактор роста фибробластов (FGF), фактор роста эндотелия сосудов (VEGF), инсулиноподобный фактор роста-1 (IGF-1), фактор ингибирования лейкоцитов (LIF) и эритропоэтин (ЕРО); аминокислоты, включая L-валин; и один или более антибиотиков и/или антимикотических агентов для контроля за микробным заражением, таких как, например, пенициллин G, стрептомицина сульфат, амфотерицин B, гентамицин и нистатин, по отдельности или в комбинации. Культуральная среда может содержать ростовую среду, которая описана в приведенных ниже примерах.
Клетки высевают в сосуды для культивирования с плотностью, позволяющей клеткам расти. В предпочтительном варианте осуществления клетки культивируются в атмосфере, содержащей от 0 до приблизительно 5% CO2 по объему. В некоторых предпочтительных вариантах осуществления клетки культивировались в атмосфере, содержащей в от приблизительно 2 до приблизительно 25% O2, предпочтительно от приблизительно 5 до приблизительно 20% O2. Предпочтительно, чтобы клетки культивировались при температуре от приблизительно 25 до приблизительно 40°C, предпочтительнее, чтобы они культивировались при 37°C. Предпочтительно, чтобы клетки культивировались в термостате. Среда в сосуде для культивирования может быть неподвижной или перемешиваемой, например, при помощи биореактора. Клетки UTC предпочтительно выращивают в условиях низкого окислительного стресса (например, с добавлением глутатиона, витамина C, каталазы, витамина E, N-ацетилцистеина). Термин «условия низкого окислительного стресса» обозначает условия отсутствия или минимального свободнорадикального повреждения культивируемых клеток.
Способы выбора наиболее предпочтительной культуральной среды, подготовки среды и способов культивирования клеток хорошо известны в данной области и описаны в ряде источников, включая руководства Doyle et al., (ред.), 1995 г., Cell & Tissue Culture: Laboratoty Procedures, John Wiley & Sons, Chilchester; и Ho and Wang (ред.), 1991 г., Animal Cell Bioreactors, Butterworth-Heinemann, Boston, которые включены в настоящий документ путем ссылки.
После культивирования выделенных клеток или фрагментов ткани в течение достаточного периода времени клетки UTC прорастают в результате миграции из ткани неонатального материала или деления клеток, либо по обеим причинам. В некоторых вариантах осуществления UTC пассируют или переносят в отдельный сосуд для культивирования, содержащий свежую среду того же типа или другого типа по сравнению с первоначально использованной, в которой популяцию клеток можно митотически размножить. Клетки настоящего изобретения можно применять на любой стадии от пассажа 0 до старения. Клетки предпочтительно пассируют от приблизительно 3 до приблизительно 25 раз, более предпочтительно пассируют от приблизительно 4 до приблизительно 12 раз и предпочтительно пассируют 10 или 11 раз. Для подтверждения выделения клональной популяции клеток можно провести клонирование и/или субклонирование.
В некоторых вариантах осуществления различные виды клеток, находящиеся в неонатальном материале, фракционируются в субпопуляции, из которых могут быть выделены клетки UTC. Фракционирование и разделение могут осуществляться с применением стандартных способов разделения клеток, включая без ограничений ферментативную обработку для диссоциации постнатальной ткани на клеточные компоненты, за которой следует клонирование и выбор конкретных типов клеток, например, без ограничений, выбор на основе морфологических и/или биохимических маркеров; выборочное выращивание требуемых клеток (положительный отбор), выборочное разрушение ненужных клеток (отрицательный отбор); разделение на основе различной способности к агглютинации клеток в смешанной популяции, например, с использованием соевого агглютинина; процедуры замораживания-оттаивания; различные адгезионные свойства клеток в смешанной популяции; фильтрацию; стандартное и зональное центрифугирование; элютриационное центрифугирование (центрифугирование в противотоке); разделение в поле тяжести; противоточное распределение; электрофорез; сортировку флуоресцентно-активированных клеток (FACS). Обзор способов клонального отбора и техники разделения клеток см. в руководстве Freshney, 1994 г., Culture of Animal Cells: A Manual of Basic Techniques, 3-е изд., Wiley-Liss, Inc., Нью-Йорк, которое включено в настоящий документ путем ссылки.
Культуральную среду меняют по необходимости, например, путем осторожной аспирации среды из чашки, например, с помощью пипетки, и добавления требуемого количества свежей среды. Инкубацию продолжают до накопления в чашке достаточного количества или плотности клеток. Исходные эксплантированные части ткани можно удалить и трипсинизировать оставшиеся клетки с помощью стандартных способов или с использованием скребка. После трипсинизации клетки собирают, переносят в свежую среду и инкубируют описанным выше способом. В некоторых вариантах осуществления среду заменяют по меньшей мере один раз приблизительно через 24 часа после трипсинизации для удаления плавающих клеток. Оставшиеся в культуре клетки считают клетками UTC.
Клетки UTC могут криоконсервироваться. Соответственно, клетки UTC для аутогенного переноса (либо для матери, либо для ребенка) можно получить из соответствующих послеродовых тканей после рождения ребенка, а затем криоконсервировать их таким образом, чтобы после этого они были доступны в случае возникновения необходимости в трансплантации.
B. Характеристики клеток, полученных из ткани пуповины
Клетки, полученные из ткани пуповины, можно характеризовать, например, по характеристикам роста (например, способность к удвоению популяции, время удвоения, число пассажей до старения), анализу кариотипа (например, нормальный кариотип; материнская или неонатальная линия), проточной цитометрией (например, анализ FACS), иммуногистохимически и/или иммуноцитохимически (например, на обнаружение эпитоп), по профилю экспрессии генов (например, с использованием генных чипов; полимеразной цепной реакцией (например, ПЦР с обратной транскриптазой, ПЦР в реальном времени и стандартный ПЦР)), белковым порядком, по секреции белков (например, по анализу коагулирующей активности плазмы или анализу PDC-кондиционированной среды, например, с использованием твердофазного иммуноферментного анализа (ИФА)), реакции смешанной культуры лимфоцитов (например, как меры стимуляции мононуклеарных клеток периферической крови) и/или другими известными специалистам способами.
Примеры клеток, полученных из ткани пуповины, хранятся в Американской коллекции клеточных культур (ATCC, 10801 Университетский бульвар, Манассас, штат Вирджиния, индекс 20110) с 10 июня 2004 г. под следующими номерами доступа ATCC: (1) определению натяжения UMB 022803 (P7) был присвоен номер доступа PTA-6067; и (2) определению натяжения UMB 022803 (P17) был присвоен номер доступа PTA-6068.
В различных вариантах осуществления клетки UTC обладают одной из более из следующих характеристик роста: (1) для роста в культуре им необходим L-валин; (2) они способны расти в атмосфере с содержанием кислорода от приблизительно 5% до по меньшей мере приблизительно 20%; (3) они обладают потенциалом к по меньшей мере приблизительно 40 удвоениям в культуре до достижения старения; и (4) они закрепляются и размножаются на поверхности сосуда для культивирования ткани с покрытием или без покрытия, причем поверхность сосуда для культивирования ткани с покрытием содержит покрытие из желатина, ламинина, коллагена, полиорнитина, витронектина или фибронектина.
В некоторых вариантах осуществления клетки UTC имеют нормальный кариотип, который сохраняется в процессе пассирования клеток во время культивирования. Способы кариотипирования хорошо разработаны и известны специалистам в данной области.
В других вариантах осуществления клетки тканей пуповины можно характеризовать по выработке определенных белков, включая (1) выработку по меньшей мере одного из тканевого фактора, виментина и альфа-актина гладких мышц; и (2) выработку по меньшей мере одного из белков CD10, CD13, CD44, CD73, CD90, PDGFr-альфа, PD-L2 и HLA-A,B,C, маркеров клеточной поверхности, определенную с помощью проточной цитометрии. В других вариантах осуществления клетки UTC можно охарактеризовать по отсутствию выработки по меньшей мере одного из маркеров клеточной поверхности CD31, CD34, CD45, CD80, CD86, CD117, CD141, CD178, B7-H2, HLA-G и HLA-DR, DP, DQ по результатам анализа с использованием проточной цитометрии. Особенно предпочтительными являются клетки, которые вырабатывают по меньшей мере два из тканевого фактора, виментина и альфа-актина гладких мышц. Более предпочтительными являются клетки, которые вырабатывают все три белка из тканевого фактора, виментина и альфа-актина гладких мышц.
В других вариантах осуществления клетки ткани пуповины можно охарактеризовать генной экспрессией, которая, относительно человеческой клетки, представляющей собой фибробласт, мезенхимальную стволовую клетку или клетку костного мозга гребня подвздошной кости, имеет повышенный уровень для гена, кодирующего по меньшей мере один из интерлейкина 8; ретикулона 1; хемокинового (мотив C-X-C) лиганда 1 (стимулятора активности роста меланомы, альфа); хемокинового (мотив C-X-C) лиганда 6 (гранулоцитарного хемотаксического белка 2); хемокинового (мотив C-X-C) лиганда 3; и опухолевого фактора некроза ткани, альфа-индцированного белка 3.
В других вариантах осуществления клетки имеют, по сравнению с клеткой человека, представляющей собой фибробласт, мезенхимальную стволовую клетку или клетку костного мозга гребня подвздошной кости, пониженный уровень экспрессии для гена, кодирующего по меньшей мере один из: SHOX2 (содержащий гомеобокс ген short stature 2); HSPB2 (27 кДа белок теплового шока 2); CXCL12 (хемокиновый (мотив C-X-C) лиганд 12/стромальный фактор 1); эластин (надклапанный аортальный стеноз, синдром Уильямса-Бойрена); мРНК Homo sapiens; кДНК DKFZp586M2022 (из клона DKFZp586M2022); Meox2 (содержащий мезенхимальный гомеобокс ген 2, содержащий гомеобокс блокировки роста ген); SIX1 (гомолог гомеобокс-содержащего гена sine oculis 1) (Drosophila); кристаллин, альфа B; DAAM2 (ассоциированный с белком Disheveled активатор морфогенеза 2); белок DKFZP586B2420; аналог нейтралина 1; тетранектин (связывающийся с плазминогеном белок); STAC (ген, содержащий домен src-гомологии 3 (SH3) и богатый цистеином домен); холестерин 25-гидроксилаза; RUNX3 (связанный с карликовостью фактор транскрипции 3); рецептор интерлейкина 11, альфа; PCOLCE (усилитель проколлаген-C-эндопептитазы); FZD7 (гомолог frizzled 7) (Drosophila); гипотетический ген BC008967; коллаген, тип VIII, альфа 1; тенацин C, TNC (гексабрахион); IRX5 (содержащий гомеобокс IRX белок 5); гефестин; интегрин, бета 8; SV2A (гликопротеин синаптического пузырька 2); NBL1 (нейробластома, ген подавления онкогенности 1); IGFBP2 (связывающийся с инсулинподобным фактором роста белок 2, 36 кДа); кДНК Homo sapiens FLJ12280 fis, клон MAMMA1001744; CRLF1 (подобный цитокиновому рецептору фактор 1); KCNN4 (активируемый кальцием канал средней/низкой проводимости, подсемейство N, член 4); интегрин, бета 7; транскрипционный коактиватор с мотивом связывания с PDZ (TAZ); SIX2 (гомолог гомеобокс-содержащего гена sine oculis 2) (Drosophila); белок KIAA1034; VAMP5 ( везикуло-ассоциированный мембранный белок 5/миобревин); EFEMP1 (содержащий EGF фибулин-подобный белок внеклеточного матрикса 1); EGR3 (белок раннего ростового ответа 3); DLX5 (содержащий гомеобокс distal-less ген 5); гипотетический белок FLJ20373; AKR1C3 (альдокеторедуктазы, семейство 1, член C3/3-альфагидроксистероид-дегидрогеназа, тип II); бигликан; транскрипционный коактиватор с мотивом связывания с PDZ (TAZ); фибронектин 1; проэнкефалин; интегрин, бета-подобный 1 (с EGF-подобными повторами); мРНК Homo sapiens, полноразмерная вставка, кДНК, клон EUROIMAGE 1968422; EphA3; белок KIAA0367; NPR3 (рецептор натрийуретического пептида C/гуанилатциклаза C/рецептор атрионатрийуретического пептида C); гипотетический белок FLJ14054; мРНК Homo sapiens ; кДНК DKFZp564B222 (из клона DKFZp564B222); BNIP3L (ген белка, подобного белку 3, взаимодействующему с BCL2/19 кДа белком аденовируса); AE-связывающий белок 1; и COX7A1 (полипептид 1 субъединицы VIIa цитохром c оксидазы) (мышечный).
В других вариантах осуществления клетки могут быть охарактеризованы при культивировании по секреции по меньшей мере одного из MCP-1, IL-6, IL-8, GCP-2, HGF, KGF, FGF, HB-EGF, BDNF, TPO, MIP1b, I309, MDC RANTES, и TIMP1. Дополнительно, клетки ткани пуповины во время культивирования можно характеризовать по отсутствию секреции по меньшей мере одного из белков TGF-бета2, ANG2, PDGFbb, MIP1A и VEGF по результатам ИФА.
В некоторых вариантах осуществления, клетки ткани пуповины выделены из ткани пуповины по существу свободными от крови, способны к самообновлению и росту в культуре, требуют L-валина для роста, могут расти при по меньшей мере приблизительно 5% кислорода и обладают по меньшей мере одной из следующих характеристик: потенциал к по меньшей мере приблизительно 40 удвоениям в культуре; закрепление и рост на поверхности сосуда для выращивания ткани как с покрытием, так и без покрытия, которое включает желатин, ламинин, коллаген, полиорнитин, витронектин или фибронектин; продуцирование виментина и альфа-актина гладкой мускулатуры: продуцирование CD10, CD13, CD44, CD73, и CD90; и генная экспрессия, которая относительно человеческой клетки, являющейся фибробластом, мезенхимальной стволовой клеткой или клеткой костного мозга гребня подвздошной кости, имеет повышенный уровень для гена, кодирующего интерлейкин 8 и ретикулон 1. В некоторых вариантах осуществления подобные клетки UTC не вырабатывают CD45 и CD117.
В предпочтительных вариантах осуществления клетка обладает двумя или более из перечисленных выше характеристик роста, выработки белков/маркеров клеточной поверхности, экспрессии генов или характеристик секреции веществ. Более предпочтительна клетка, обладающая тремя, четырьмя, пятью или более характеристиками. Еще более предпочтительна клетка UTC обладающая шестью, семью, восемью или более характеристиками. Еще более предпочтительны клетки, обладающие всеми вышеперечисленными характеристиками.
Среди клеток, которые в настоящее время предпочтительны для использования в целях настоящего изобретения в некоторых его аспектах, имеются постнатальные клетки, обладающие описанными выше характеристиками, и, в частности, те из них, которые имеют нормальные кариотипы и поддерживают нормальные кариотипы при пассировании, и дополнительно те из них, которые экспрессируют каждый из маркеров CD10, CD13, CD44, CD73, CD90, PDGFr-альфа и HLA-A,B,C, причем клетки вырабатывают иммунологически детектируемые белки, соответствующие перечисленным маркерам. Еще более предпочтительны клетки, которые, в дополнение к описанному выше, не вырабатывают белки, соответствующие любому из маркеров CD31, CD34, CD45, CD117, CD141 или HLA-DR,DP,DQ по результатам анализа с использованием проточной цитометрии.
В одном варианте осуществления клетки UTC выделены из ткани пуповины человека по существу свободными от крови, способными к самообновлению и размножению в культуре, обладающими потенциалом к дифференцированию, не вырабатывающими CD117 или CD45, и не экспрессирующими hTERT или теломеразу. Эти клетки UTC не в обязательном порядке экспрессируют оксидированный липопротеиновый рецептор 1 низкой плотности ретикулон лиганд 3 и/или гранулоцитарный хемотаксический белок; и/или не экспрессировать CD31 или CD34; и/или экспрессировать, по отношению к фибробластам, мезенхимальным стволовым клеткам или клеткам костного мозга гребня подвздошной кости человека, повышенные уровни интерлейкина 8 или ретикулона 1; и/или экспрессировать CD10, CD13, CD44, CD73 и CD90.
В другом варианте осуществления клетки UTC выделены из ткани пуповины человека по существу свободными от крови, способными к самообновлению и размножению в культуре, обладающими потенциалом к дифференцированию, экспрессирующими CD13 и CD90, а также не экспрессирующими CD34 и CD117. В необязательном порядке подобные клетки не экспрессируют hTERT или теломеразу. В еще одном варианте осуществления клетки также экспрессируют CD10, CD44 и CD43. В альтернативном варианте осуществления клетки также не экспрессируют CD45 и CD31. Эти клетки UTC не в обязательном порядке (i) экспрессируют оксидированный липопротеиновый рецептор 1 низкой плотности ретикулон, хемокиновый рецептор лиганд 3 и/или гранулоцитарный хемотаксический белок; и/или (іі) экспрессируют, по отношению к человеческим фибробластам, мезенхимальным стволовым клеткам или клеткам костного мозга гребня подвздошной кости человека, повышенные уровни интерлейкина 8 или ретикулона 1.
В другом варианте осуществления клетки UTC выделены из ткани пуповины человека по существу свободными от крови, способными к самообновлению и размножению в культуре, обладающими потенциалом к дифференцированию, экспрессирующими CD13, CD90 и HLA-ABC, а также не экспрессирующими CD34, CD117 и HLA-DR. В необязательном порядке подобные клетки также не экспрессируют hTERT или теломеразу. В одном варианте осуществления клетки также экспрессируют CD10, CD44 и CD43. В альтернативном варианте осуществления клетки также не экспрессируют CD45 и CD31. Эти клетки UTC не в обязательном порядке (i) экспрессируют оксидированный липопротеиновый рецептор 1 низкой плотности ретикулон, хемокиновый рецептор лиганд 3 и/или гранулоцитарный хемотаксический белок; и/или (іі) экспрессируют, по отношению к человеческим фибробластам, мезенхимальным стволовым клеткам или клеткам костного мозга гребня подвздошной кости человека, повышенные уровни интерлейкина 8 или ретикулона 1.
В другом варианте осуществления клетки UTC выделены из ткани пуповины человека по существу свободными от крови, способными к самообновлению и размножению в культуре, обладающими потенциалом к дифференцированию и следующими характеристиками: (1) экспрессия CD10, CD13, CD44, CD90 и HLA-ABC; (2) отсутствие экспрессии CD31, CD34, CD45, HLA-DR и CD117, а также (3) отсутствие экспрессии hTERT или теломеразы. В другом варианте осуществления клетки UTC выделены из ткани пуповины человека по существу свободными от крови, способными к самообновлению и размножению в культуре, обладающими потенциалом к дифференцированию и следующими характеристиками: (1) экспрессия CD10, CD13, CD44, CD90 и HLA-ABC; (2) отсутствие экспрессии CD31, CD34, CD45, HLA-DR и CD117; (3) отсутствие экспрессии hTERT или теломеразы; (4) экспрессия оксидированного липопротеинового рецептора 1 низкой плотности ретикулона, хемокинового рецептора лиганд 3, и/или гранулоцитового хемотактического белка; и (4) экспрессия, по отношению к человеческим фибробластам, мезенхимальным стволовым клеткам или клеткам костного мозга гребня подвздошной кости человека, повышенных уровней интерлейкина 8 или ретикулона 1.
В одном варианте осуществления клетки hUTC представлены популяцией клеток, которые могут быть однородными. В некоторых вариантах осуществления клеточная популяция может быть неоднородной. Неоднородная популяция клеток, составляющая предмет настоящего изобретения, может содержать по меньшей мере приблизительно 5%, 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90% или 95% клеток UTC, составляющих предмет настоящего изобретения. Неоднородные популяции клеток, составляющие предмет настоящего изобретения, могут дополнительно содержать стволовые клетки или другие клетки-предшественники, такие как миобласты или другие клетки-предшественники мышечных клеток, гемангиобласты, или клетки-предшественники клеток кровеносных сосудов, или она может дополнительно содержать полностью дифференцированные клетки скелетных мышц, клетки гладких мышц сосудов, периваскулярные клетки или клетки эндотелия кровеносных сосудов. В некоторых вариантах осуществления популяция является по существу однородной, т.е. содержит по существу только клетки UTC (предпочтительно по меньшей мере приблизительно 96%, 97%, 98%, 99% или более клеток UTC). Однородные популяции клеток настоящего изобретения содержат клетки, полученные из пуповины. Однородные популяции клеток, полученных из пуповины, предпочтительно свободны от клеток материнской линии дифференцировки. Однородность популяции клеток можно получить при помощи любого способа, известного в данной области, например, путем сортировки клеток (например, с использованием проточной цитометрии) или путем клонального размножения в соответствии с известными способами. Однородные популяции клеток UTC могут содержать клональную линию клеток из постнатально полученных клеток.
В одном из вариантов осуществления клетки hUTC после культивирования обладают по существу теми же характеристиками (например, маркерный профиль и/или профиль генной экспрессии), что и клетки hUTC перед культивированием. В альтернативном варианте осуществления клетки hUTC после культивирования обладают по существу теми же характеристиками (например, маркерный профиль и/или профиль генной экспрессии), что и клетки hUTC перед культивированием. В одном из вариантов осуществления клетки hUTC после культивирования обладают теми же характеристиками, что и клетки hUTC перед культивированием для по меньшей мере CD13, CD34, CD90 и CD117.
III. Прочие пригодные клетки
Как обсуждалось выше в некоторых вариантах осуществления изобретения, культуральная среда и не содержащие сыворотки питательные растворы могут применяться для выращивания изолированных клеток, полученных из ткани пуповины человека («hUTC» или «UTC»). В дополнение, культуральная среда и не содержащие сыворотки питательные растворы могут применяться для выращивания других субстратзависимых клеток.
В одном из вариантов воплощения настоящего изобретения культуральная среда и не содержащий сыворотки питательный раствор используются для выращивания других субстратзависимых клеток, таких как клетки, выделенные из плаценты. Примеры других субстратзависимых клеток включают, не ограничиваясь, мезенхимальные стволовые клетки, выделенные из костного мозга, прогениторы мезенхимальных стволовых клеток, выделенные из костного мозга, клетки, извлеченные не из костномозговых тканей, таких как адипозная ткань, мышечная ткань, клетки, выделенные из кровеносных сосудов, в том числе внутренней грудной артерии, клетки, извлеченные из дентальной пульпы зубов. Дополнительно, амниотическая жидкость оказалась очень богатым источником субстратзависимых стволовых клеток. Другим примером субстратзависимых клеток являются фибробласты, в том числе неонатальные фибробласты крайней плоти.
IV. Способы культивирования
Другим вариантом осуществления изобретения является способ культивирования клеток с применением кондиционированной среды и не содержащего сыворотки питательного раствора данного изобретения. Способы могут применять роллерные флаконы, центрифужные пробирки и/или микроносители. В предпочтительных вариантах осуществления, способы применяются для культивирования субстратзависимых клеток, таких как, например, клетки hUTC, и требуют микроносителей.
В предпочтительных вариантах осуществления способ включает культивирование клеток hUTC с кондиционированной средой и не содержащим сыворотку питательным раствором, описанными в данном изобретении, без необходимости заменять сыворотку. Как обсуждалось выше, клетки UTC могут выращиваться в различных видах культуральной среды. Способы настоящего изобретения оптимально снижают потребление сыворотки и повышают волюметрическую продуктивность для снижения стоимости производства композиций, содержащих субстратзависимые клетки, например, клетки, выделенные из пуповины человека. Более того, способ позволяет выращивать клетки (например, hUTC) без замены среды.
Примеры способов выращивания клеток в роллерных флаконах и микроносителях раскрыты в опубликованных в США приложении №№ 2007/0141700 и 2008/0166328 соответственно, которые включены в настоящий документ путем ссылки в полном объеме, насколько это относится к описанию роллер-флакона, микроносителей и культивированию на роллер-флаконах и микроносителях. Примеры подходящих роллер-флаконов, центрифужных пробирок, микроносителей, их характеристик и соответствующих параметров культур обсуждаются ниже.
А. Роллер-флаконы
Системы культивирования роллер-флаконов известны в области технологии клеточной культуры. При использовании в данном изобретении, культивационная система роллер-флаконов содержит по меньшей мере необходимую клеточную линию, ростовую среду, роллер-флаконы, аппаратуру для вращения флаконов и средства сбора клеток.
Культивационные системы роллер-флаконов как правило также содержат средства контроля температуры во время инкубации, так же как и средства для асептической обработки культур, например, во время первоначального засевания флаконов клетками, или во время последующих перемещений. Сбор клеток может быть осуществлен путем ферментной обработки, например с помощью трипсина, трипсина-EDTA, диспазы и коллагеназы, или другими ферменами, или комбинациями ферментов с другими компонентами или без них. Могут применяться и другие коммерческие продукты, такие как TrypLE™ Express (Gibco, Inc.), но не ограничиваясь ими. Клетки также могут быть собраны мануальным путем, включая, например, порционное центрифугирование, или же сбор может быть автоматизированным.
В одном из вариантов осуществления флаконы наполняются приблизительно 100-300 мл ростовой среды, в других вариантах осуществления используется приблизительно 100-200 мл. В альтернативном варианте осуществления во флаконы помещают приблизительно 100-120 мл или даже 105-115 мл. В других вариантах осуществления флаконы наполняются приблизительно 112 мл ростовой среды для достижения максимальных удвоений популяции. В одном из вариантов осуществления флаконы засеваются от приблизительно 2500 до приблизительно 10000 клеток/см2. В одном из вариантов осуществления используется нижний конец этой шкалы, например, осуществляется посев менее чем приблизительно 3000 клеток на квадратный сантиметр. Засеянные флаконы вращаются во время закрепления и роста. Скорость вращения может быть установлена между приблизительно 0,5 до 1 об/мин. Предпочтительно вращение на скорости между приблизительно 0,75 и 1 об/мин. Более предпочтительно вращение флаконов со скоростью между приблизительно от 0,8 до 1 об/мин.
В другом варианте осуществления флаконы наполняются приблизительно 100-300 мл ростовой среды, предпочтительно использование приблизительно 300 мл. Во флаконы засевают от приблизительно 2500 до приблизительно 10000 клеток на квадратный сантиметр. В одном из вариантов осуществления используется нижний конец этой шкалы, например, осуществляется посев менее чем приблизительно 3000 клеток на квадратный сантиметр. Более предпочтительны варианты осуществления, где плотность посева составляет приблизительно 2500 клеток/см2. Засеянные флаконы вращаются во время закрепления и роста. Скорость вращения устанавливают между приблизительно 0,5 до 1 об/мин. Предпочтительно вращение на скорости между приблизительно 0,75 и 1 об/мин. Более предпочтительно вращение флаконов со скоростью между приблизительно от 0,8 до 1 об/мин. В настоящий момент предпочитают скорость вращения приблизительно 0,9-1,0 об/мин, как показано на фигуре.
Наполненные и засеянные роллер-флаконы вращаются и инкубируются на протяжении приблизительно от 5 до 7 дней для получения максимального количества удвоений. В настоящий момент предпочитают инкубационный период от приблизительно 5,5 до приблизительно 6,5 дней.
Роллер-флаконы могут быть покрыты агентом, способствующим закреплению клеток на внутренней поверхности роллер-флаконов, таким как желатин, экстрацеллюлярные матриксные молекулы (такие как желатин, ламинин, витронектин, фибронектин, коллаген типов I, IV и VI) и т.п. Одним из примеров подобных коммерчески доступных флаконов с покрытием являются покрытые материалом CellBind (можно приобрести в компании Corning, номер в каталоге 3907). Можно предвидеть, что различные агенты для покрытия будут сочтены приемлемыми для закрепления и выращивания клеток в соответствии с представленными в настоящем документе способами.
В. Центрифужные пробирки
Системы культивирования центрифужных пробирок также известны в области технологии клеточной культуры. При использовании в данном изобретении, культивационная система центрифужных пробирок содержит по меньшей мере необходимую клеточную линию, ростовую среду, одну или несколько центрифужных пробирок, средства вращения одной или нескольких пробирок и средства сбора клеток.
Культивационные системы центрифужных пробирок как правило также содержат средства контроля температуры во время инкубации, так же как и средства для аспетической обработки культур, например, во время первоначального засевания пробирок клетками, или во время последующих перемещений. Сбор клеток может быть осуществлен путем ферментной обработки, например с помощью трипсина, трипсина-EDTA, диспазы и коллагеназы, или другими ферменами, или комбинациями ферментов с другими компонентами или без них. Могут применяться и другие коммерческие продукты, такие как TrypLE™ Express (Gibco, Inc.), но не ограничиваясь ими. Клетки также могут быть собраны мануальным путем, включая, например, порционное центрифугирование, или же сбор может быть автоматизированным.
В одном из вариантов осуществления скорость вращения установлена между от приблизительно 35 до приблизительно 65 об/мин, альтернативно между приблизительно 35 и 45 об/мин, альтернативно между приблизительно 40 и приблизительно 50 об/мин, альтернативно между приблизительно 45 и приблизительно 55 об/мин, альтернативно между приблизительно 55 и приблизительно 65 об/мин, альтернативно между приблизительно 50 и приблизительно 60 об/мин. В предпочтительном варианте осуществления поддерживается скорость вращения приблизительно 40 об/мин или 60 об/мин.
В одном из вариантов осуществления применяются центрифужные пробирки емкостью 3 л, которые можно запомнить приблизительно 3 л ростовой среды, эмбриональной бычьей сыворотки, не содержащего сыворотки питательного раствора, микроносителей и клеток. В том варианте осуществления скорость вращения может быть установлена между приблизительно 35 до 45 об/мин. Предпочтительно вращение на скорости приблизительно 40 об/мин.
В другом варианте осуществления применяются пробирки емкостью 125 мл. Эти пробирки могут быть заполнены приблизительно 100 мл раствора, содержащего ростовую среду, эмбриональную бычью сыворотку, микроносители и клетки. В одном из вариантов осуществления пробирки содержат приблизительно от 85 мл до 115 мл ростовой среды, эмбриональной бычьей сыворотки, не содержащего сыворотки питательного раствора, микроносителей и клеток. В том варианте осуществления скорость вращения может быть установлена между приблизительно 55 до 65 об/мин. Предпочтительно вращение на скорости приблизительно 50 об/мин.
В еще одном варианте осуществления применяются центрифужные пробирки емкостью 500 мл. Эти пробирки могут быть заполнены приблизительно 500 мл раствора, содержащего ростовую среду, эмбриональную бычью сыворотку, микроносители и клетки. В одном из вариантов осуществления пробирки содержат приблизительно от 450 мл до 500 мл ростовой среды, эмбриональной бычьей сыворотки, не содержащего сыворотки питательного раствора, микроносителей и клеток. В том варианте осуществления скорость вращения может быть установлена между приблизительно 55 до 65 об/мин. Предпочтительно вращение на скорости приблизительно 50 об/мин.
В альтернативном варианте осуществления применяются центрифужные пробирки емкостью 500 мл. Эти пробирки могут быть заполнены приблизительно 500 мл раствора, содержащего ростовую среду, эмбриональную бычью сыворотку, микроносители и клетки. В одном из вариантов осуществления пробирки содержат приблизительно от 450 мл до 500 мл ростовой среды, эмбриональной бычьей сыворотки, не содержащего сыворотки питательного раствора, микроносителей и клеток. В том варианте осуществления скорость вращения может быть установлена между приблизительно 35 до 45 об/мин. Предпочтительно вращение на скорости приблизительно 40 об/мин.
Пробирки засеваются от приблизительно 2500 до приблизительно 10000 клеток/см2. Клетки могут быть засеяны напрямую в пробирку, на поверхность пробирки или на микроноситель, помещенный внутрь пробирки. В предпочтительных вариантах осуществления производится посев от приблизительно 3000 до приблизительно 7500, альтернативно от приблизительно 3000 до приблизительно 7000, альтернативно от приблизительно 4000 до приблизительно 7000, альтернативно от приблизительно 3000 до приблизительно 5000, альтернативно от приблизительно 5000 до приблизительно 7000, альтернативно от приблизительно 3500 до приблизительно 5000, альтернативно от приблизительно 4500 до приблизительно 7500, альтернативно от приблизительно 3500 до приблизительно 5500 клеток/см2. Засеянные пробирки вращаются во время закрепления и роста. В одном из вариантов осуществления с целью максимизации уровня удвоения популяции, заполненные и засеянные пробирки вращаются и инкубируются на протяжении от приблизительно 5 до 7 дней, с предпочтительным периодом инкубации от приблизительно 5 до приблизительно 6 дней.
С. Микроносители
Культивирование на микроносителях представляет собой технологию, которая обеспечивает возможность получения высокого практического выхода в культуре субстратзависимых клеток, например, сусбтратзависимых постнатальных клеток. Микроносители специально разработаны для культивирования клеток, например, постнатальных клеток млекопитающих, при объемах культуры в диапазоне от нескольких миллилитров до более тысячи литров. Микроноситель является биологически инертным и является надежным, но не жестким субстратом для смешиваемых культур на микроносителях. Микроносители могут быть прозрачными, что позволяет проводить микроскопическое исследование прикрепленных клеток. Микроноситель Cytodex 3® (GE Healthcare Life Sciences, Piscataway N.J.) состоит из тонкого слоя денатурированного коллагена, химически связанного с матриксом из сшитого декстрана. Слой денатурированного коллагена на носителях Cytodex 3® может разлагаться различными протеазами, включая трипсин и коллагеназу, что дает возможность извлекать клетки из микроносителя, сохраняя максимальную жизнеспособность, функциональность и целостность клеток.
Для культивирования клеток могут использоваться микроносители, не содержащие белка. Например, сферические микроносители, предназначенные для производственного, лабораторного или исследовательского применения, предлагаемые под торговым наименованием HILLEX® (SoloHill Engineering, Inc., Мичиган, США), представляют собой модифицированные полистироловые сферы с закрепленными на поверхности катионами триметиламмония для придания поверхности микроносителя положительного заряда. Диаметр сфер может находиться в диапазоне от приблизительно 90 до приблизительно 200 микрон.
Способы культивирования клеток с использованием микроносителей дают много преимуществ, включая простоту дальнейшей технологической обработки во многих областях применения. Микроносители, как правило, имеют приблизительно сферическую форму и могут быть пористыми или цельными. Использование микроносителей для прикрепления к ним клеток упрощает использование смесительных сосудов и вспомогательных реакторов для выращивания субстратзависимых клеток. Клетки прикрепляются к микроносителями, легко образующим суспензию. Необходимость образования суспензии ограничивает физические характеристики микроносителей. Вследствие этого микроносители, как правило, имеют средний диаметр в диапазоне 50-2000 микрон. В некоторых областях применения цельные микроносители имеют диаметр от приблизительно 100 до приблизительно 250 микрон, а пористые микроносители - от приблизительно 250 до приблизительно 2500 микрон. Диапазоны размеров позволяют выбирать микроносители, достаточно крупные, чтобы на них прикреплялось много субстратзависимых клеток, и достаточно мелкие, чтобы образовывать суспензии со свойствами, подходящими для использования в смесительных реакторах.
При использовании микроносителей и аналогичных средств учитываются, помимо прочего, следующие факторы: эффективность прикрепления, иммуногенность, биосовместимость, возможность биологической деградации, время достижения конфлюэнтности, параметры роста прикрепившихся клеток, в том числе максимально достижимая плотность на единице поверхности, технологии отделения клеток (при необходимости) и эффективность отделения, масштабируемость условий культивирования, а также гомогенность культуры при увеличении масштабов производства, возможность успешного масштабирования процедур отделения клеток, а также будут ли микроносители использоваться для имплантации. На эти параметры могут влиять характеристики поверхности микроносителя, а также пористость, диаметр, плотность и свойства микроносителя при обработке.
Например, важным свойством является плотность частиц или сфер микроносителя. Слишком высокая плотность может приводить к оседанию микроносителей из суспензии или к скапливанию в нижней части сосуда для культивирования, что может приводить к плохому перемешиванию массы клеток, культуральной среды и газовых фаз в реакторе. С другой стороны, слишком низкая плотность может приводить к излишней плавучести микроносителя. Стандартной для многих сферических микроносителей является плотность 1,02-1,15 г/см3.
Малый диаметр микроносителей и количество частиц, добавляемых в реактор, позволяют получить значительную площадь поверхности, значительно превышающую площадь роллер-флаконов и другого оборудования для культивирования субстратзависимых клеток, например, планшет. Пористые микроносители обеспечивают еще большую площадь на единицу объема или массы. Пористые микроносители имеют большие лакуны, в которых могут расти субстратзависимые клетки. Такие лакуны значительно увеличивают площадь поверхности и могут защищать клетки от разрушительных механических влияний, например, при перемешивании или пропускании газа.
Поверхность микроносителя может быть рельефной для обеспечения лучшего прикрепления и пролиферации клеток. Рельеф на поверхности микроносителей может быть сформирован различными способами, включая, помимо прочего, прессовку, отливку, выщелачивание и травление. Размер элементов рельефа может измеряться нанометрами. Рельеф поверхности может использоваться для обеспечения специфического выравнивания клеток на поверхности микроносителя. Поверхность пор в пористых микроносителях также может быть рельефной для облегчения прикрепления и пролиферации клеток. Рельеф на поверхность пор может быть нанесен различными способами, включая, помимо прочего, прессовку, отливку, выщелачивание и травление.
Поверхность микроносителя может быть покрыта плазмой для придания ей заряда. Заряд может улучшать прикрепление и пролиферацию клеток.
В других вариантах осуществления микроносители состоят или имеют покрытие из термочувствительных полимеров, например, поли-N-изопропилакриламида, или имеют электромеханические свойства. Микроносители также могут обладать микротоком, например микроносители с частичной гальванической парой цинка и меди, которая биологически релевантное электричество низкого уровня. Микроносители могут быть парамагнетическими, например парамагнетические кальций-альгинатные микроносители.
В продаже есть как цельные, так и пористые типы микроносителей. Примеры коммерчески доступных цельных микроносителей включают Cytodex ® 1 и Cytodex® 3, которые относятся к микроносителям на декстрановой основе от компании GE Healthcare Life Sciences. Пригодные для применения коммерчески доступные пористые микроносители включают Cytoline™ и Cytopore™ от компании GE Healthcare Life Sciences, Biosilon (NUNC) и Cultispher® (Percell Biolytical).
В определенных вариантах осуществления способы и оборудование настоящего изобретения используют декстрановый сферический микроноситель, обладающий приблизительным размером частиц приблизительно 60-90 микрон и плотностью приблизительно 1,03 г/см3 при температуре 25ºC. В других вариантах осуществления способы и оборудование настоящего изобретения используют декстрановый сферический микроноситель, обладающий приблизительным размером частиц приблизительно 114-198 микрон и плотностью приблизительно 1,04 г/см3 при температуре 25ºC. В еще некоторых вариантах осуществления способы и оборудование настоящего изобретения используют декстрановый сферический микроноситель, обладающий приблизительным размером частиц приблизительно 60-87 микрон и плотностью приблизительно 1,04 г/см3 при температуре 25ºC. В альтернативном варианте осуществления способы и оборудование настоящего изобретения используют пористые микроносители. Эти пористые микроносители могут обладать диаметром частиц приблизительно 200-280 микрон, эффективную область поверхности приблизительно 1,1 м2/г в сухом виде и средний диаметр отверстия поры приблизительно 30 микрон. В других вариантах осуществления способы и оборудование настоящего изобретения используют микроносители, обладающие поверхностью, обработанной амином. В предпочтительных вариантах осуществления микроносители обладают обработанной амином поверхностью с размером частиц приблизительно 160-200 микрон, относительная плотность варьирует приблизительно 1,090-1,150, область поверхности приблизительно 515 см2/г. Такие микроносители могут быть представлены в растворах, содержащих 5,5×105 микроносителей/г.
Микроносители также могут содержать биологически активный агент. Частицы носителей могут также содержать биологически активный агент или фактор, который может регулировать рост или функционирование клеток или тканевой среды. Подходящие факторы включают, помимо прочего, факторы роста фибробластов, немопоэтический фактор, факторы роста эндотелия кровеносных сосудов, факторы роста тромбоцитов, костные морфогенические белки, трансформирующие факторы роста, факторы опухолевого некроза, факторы эпидермального роста и инсулиноподобные факторы роста. Могут использоваться как полные факторы, так и миметики или активные фрагменты этих факторов.
D. Способы
В целом, способы настоящего изобретения включают культивирование (например, выращивание) клеток в культуральной вреде настоящего изобретения, обогащенной сывороткой (например, эмбриональной бычьей сывороткой). После того, как клетки были выращены до желательной плотности (такой как, например, за период приблизительно 3-4 дней), добавляют не содержащий сыворотки питательный раствор. Клетки могут быть субстратзависимыми клетками, которые можно посеять на микроноситель. Эти способы культивации можно осуществить в системе культивации роллер-флаконов или центрифужных пробирок. При посеве субстратзависимых клеток на микроноситель предпочтительно применение культивационной системы центрифужных пробирок. Желательный период времени определяется такими параметрами, как, например, желательная плотность популяции, желательное удвоение(я) популяции или время. В некоторых вариантах осуществления клетки культивируются на протяжении 4-7 дней с добавлением не содержащего сыворотки питательного раствора приблизительно в день 3. В других вариантах осуществления клетки выращиваются на протяжении 1-2 удвоений популяции или до достижения желательной первоначальной плотности популяции перед добавлением не содержащего сыворотки питательного раствора. Как обсуждалось выше, способы позволяют выращивать клетки (например, hUTC) без замены среды.
1. Способы культивации изолированных субстратзависимых клеток
Одним из вариантов осуществления настоящего изобретения является способ культивации (например, выращивания) субстратзависимых клеток. Способ включает культивацию изолированных сустратзависимых клеток, посеянных на тканевую поверхность флакона, или, предпочтительно, микроноситель в культуральной среде настоящего изобретения, обогащенной сывороткой, и добавлением не содержащего сыворотки питательного раствора после выращивания клеток на протяжении периода времени, достаточного для достижения желательной первоначальной плотности популяции. В одном из вариантов осуществления клетки выращивают от приблизительно 3 до приблизительно 7 дней, альтернативно от приблизительно 3 до приблизительно 5 дней, альтернативно от приблизительно 4 дней до приблизительно 5 дней, перед добавлением не содержащего сыворотки питательного раствора. В одном из вариантов осуществления клетки выращиваются приблизительно 3 дней перед добавлением не содержащего сыворотки питательного раствора. В другом варианте осуществления клетки выращиваются до по меньшей мере одного или двух удвоений популяции перед добавлением не содержащего сыворотки питательного раствора. В предпочтительном варианте осуществления осуществляется посев клеток на любой из микроносителей, раскрытых в настоящем изобретении, и клетки выращиваются в центрифужных пробирках при условиях, описанных выше. В одном из вариантов осуществления способ включает размораживание флакона банка клеток, содержащего эти клетки, и выращивание клеток для посева в производственный сосуд. Другой вариант осуществления включает стадию изначального разделения клеток и затем посев разделенных клеток.
Как уже обсуждалось, среда, в том числе среда, применяемая в данных способах, может быть обогащена от приблизительно 2% до приблизительно 20% сыворотки (например, эмбриональной бычьей сыворотки, FBS). В одном из вариантов осуществления среда дополнена сывороткой (такой как, например, FBS) во время подготовки среды. В другом варианте осуществления среда дополнена прямо перед применением (например, путем добавления раствора, содержащего сыворотку (например, FBS)). В другом варианте осуществления предпочтительным дополнением культуральной среды является приблизительно от 2 до 15% (об/об) эмбриональной бычьей сыворотки, альтернативно от приблизительно 2 до приблизительно 10%, альтернативно от приблизительно 3 до приблизительно 12%, альтернативно от приблизительно 5 до приблизительно 15%, альтернативно от приблизительно 4% до приблизительно 10%. В избранных вариантах осуществления, культурная среда обогащена приблизительно 7,5%, приблизительно 10% или приблизительно 15% (об/об) эмбриональной бычьей сыворотки.
В другом варианте осуществления способ также включает посев субстратзависимых клеток. В то время как целевая плотность посева может варьировать, в определенных предпочтительных вариантах осуществления от приблизительно 5 000 до приблизительно 8 000, альтернативно от приблизительно 5 500 до приблизительно 7 500, альтернативно от приблизительно 6 000 до приблизительно 8 000, альтернативно от приблизительно 6 500 до приблизительно 7 500 жизнеспособных клеток/см2, засеваются при концентрации микроносителей от приблизительно 12 до приблизительно 30, альтернативно от приблизительно 12 до приблизительно 20, альтернативно от приблизительно 18 до приблизительно 25, альтернативно от приблизительно 15 до приблизительно 23 г/л.
2. Способы культивирования изолированных клеток, извлеченных из ткани пуповины
Один из вариантов осуществления изобретения представляет собой способ культивации клеток, полученных их ткани пуповины. В то время как данный способ в целом содержит стадии способа культивирования изолированных субстратзависимых клеток, описанного выше, возможны некоторые вариации. Соответственно, одним из вариантов осуществления настоящего изобретения является способ культивирования изолированных субстразависимых клеток hUTC, закрепленных на микроносителях, до высокой плотности популяции в суспензийной культуре в центрифужных пробирках путем обогащения ростовой среды не содержащим сыворотки питательным раствором. Этот способ оптимально ликвидирует необходимость в замене среды (например, в день 3) для бесперебойного выращивания клеток >20 000 клеток/см2. Более того, этот способ улучшает жесткость пассирования клеток hUTC. Этот способ использует культуральную среду и не содержащие сыворотку питательные растворы настоящего изобретения.
Способ включает культивирование изолированных клеток hUTC, высеянных на микроноситель в культуральной среде настоящего изобретения, обогащенной сывороткой (например, эмбриональной бычьей сывороткой) на протяжении периода времени, достаточного для достижения клетками желательно первоначальной плотности популяции. В определенных вариантах осуществления используются осуществления культуральной среды А, В или С. В некоторых вариантах осуществления клетки культивируются в роллер-флаконах и культивирование производится в системах роллер-флаконов. В предпочтительном варианте осуществления посев клеток осуществляется на микроносители в центрифужных пробирках и культивирование происходит в системах центрифужных пробирок. В одном из вариантов осуществления клетки инкубируются при температуре приблизительно 37ºC в атмосфере, содержащей менее 10% СО2.
В другом варианте осуществления флаконы вращаются со скоростью от приблизительно 55 до приблизительно 65 об/мин, альтернативно от приблизительно 55 об/мин до приблизительно 60 об/мин, альтернативно от приблизительно 58 об/мин до приблизительно 61 об/мин. В другом варианте осуществления флаконы вращаются со скоростью от приблизительно 35 об/мин до приблизительно 45 об/мин, альтернативно от приблизительно 38 об/мин до приблизительно 42 об/мин, альтернативно от приблизительно 40 об/мин до приблизительно 43 об/мин, альтернативно от приблизительно 36 об/мин до приблизительно 45 об/мин. В другом варианте осуществления плотность микроносителей колеблется между приблизительно от 11,0 до 13,0 г/л.
В одном из вариантов осуществления клетки hUTC культивируют при температуре приблизительно 37°C в атмосфере, содержащей менее 10% СО2 в пробирке емкостью 125 мл, которая вращается со скоростью от приблизительно 55 об/мин до приблизительно 65 об/мин (предпочтительно приблизительно 60 об/мин). В еще одном варианте осуществления клетки hUTC культивируют при температуре приблизительно 37°C в атмосфере, содержащей менее 10% СО2 в пробирке емкостью 500 мл, которая вращается со скоростью от приблизительно 55 об/мин до приблизительно 65 об/мин (предпочтительно приблизительно 60 об/мин). В другом варианте осуществления клетки hUTC культивируют при температуре приблизительно 37°C в атмосфере, содержащей менее 10% СО2 в пробирке емкостью 500 мл, которая вращается со скоростью от приблизительно 35 об/мин до приблизительно 45 об/мин (предпочтительно приблизительно 40 об/мин). В другом варианте осуществления клетки hUTC культивируют при температуре приблизительно 37°C в атмосфере, содержащей менее 10% СО2 в пробирке емкостью 3 л, которая вращается со скоростью от приблизительно 35 об/мин до приблизительно 45 об/мин (предпочтительно приблизительно 40 об/мин). В этих вариантах осуществления пробирки могут содержать от приблизительно 11,0 до приблизительно 13,0 г/л микроносителей в среде (предпочтительно приблизительно 12 г/л).
С целью максимизации плотности популяции, заполненные и засеянные пробирки, содержащие клетки hUTC, вращаются и инкубируются на протяжении от приблизительно 5 до 7 дней, с периодом инкубации от приблизительно 5 до приблизительно 6 дней. Приблизительно на срединной точке инкубации (т.е., после от приблизительно 2,5 до приблизительно 3,5 дней(предпочтительно 3 дней)) или когда клетки достигли желаемой первоначальной плотности, не содержащий сыворотки питательный раствор, описанный в настоящем изобретении, добавляется к культуре hUTC. В определенных вариантах осуществления используются осуществления не содержащих сыворотки питательных растворов А, В или С.
В предпочтительном варианте осуществления клетки выращиваются на протяжении достаточного для достижения клетками желательной первоначальной плотности популяции периода времени перед добавлением не содержащего сыворотки питательного раствора.
Таким образом в одном из вариантов осуществления способ включает выращивание клеток, полученных из ткани пуповины, посеянных на микроносители в культуральной среде настоящего изобретения на период времени, достаточный для достижения клетками желательной первоначальной плотности популяции; добавление не содержащего сыворотки питательного раствора, описанного в настоящем изобретении, после достижения клетками желательной первоначальной плотности популяции; и выращивание клеток на протяжении периода времени, достаточного для достижения клетками желательной финальной плотности популяции.
В другом варианте осуществления применяются осуществление культуральной среды А и осуществление не содержащего сыворотки питательного раствора А. В другом варианте осуществления применяются осуществление культуральной среды В и осуществление не содержащего сыворотки питательного раствора В. В одном из вариантов осуществления применяются осуществление культуральной среды С и осуществление не содержащего сыворотки питательного раствора С.
В одном из вариантов осуществления способ включает посев клеток hUTC на микроносители перед культивированием. Микроносители могут быть любыми из микроносителей, описанных выше. В некоторых вариантах осуществления микроносители обладают поверхностью, обработанной амином. В предпочтительных вариантах осуществления микроносители обладают обработанной амином поверхностью с размером частиц приблизительно 160-200 микрон, относительная плотность варьирует приблизительно 1,090-1,150, область поверхности приблизительно 515 см2/г. В одном варианте осуществления используется микроноситель Hillex® II Ultra.
В то время как целевая плотность посева может варьировать, в определенных вариантах осуществления от приблизительно 5 000 до приблизительно 8 000, альтернативно от приблизительно 5 500 до приблизительно 7 500, альтернативно от приблизительно 6 000 до приблизительно 8 000, альтернативно от приблизительно 6 500 до приблизительно 7 500 жизнеспособных клеток/см2, засеваются при концентрации микроносителей от приблизительно 15 до приблизительно 30, альтернативно от приблизительно 18 до приблизительно 25, альтернативно от приблизительно 15 до приблизительно 23 г/л. Посеянные клетки добавляются в пробирку. Альтернативно посев производится в пробирке. В одном из вариантов осуществления процесс посева включает размораживание криосохраненных клеток hUTC. В одном из вариантов осуществления способ также включает размораживание криосохраненных клеток hUTC и распределение клеток перед засеванием микроносителя. В одном из вариантов осуществления распределение клеток осуществляется на микроносителе.
В одном из вариантов осуществления культуральная среда, применяемая в способе для выращивания клеток hUTC, обогащена от приблизительно 2% до приблизительно 20% сыворотки (например, эмбриональной бычьей сыворотки). В одном из вариантов осуществления среда дополнена сывороткой (такой как, например, FBS) во время подготовки среды. В другом варианте осуществления среда дополнена прямо перед применением (например, путем добавления раствора, содержащего сыворотку (например, FBS)). В одном из вариантов осуществления предпочтительным дополнением культуральной среды является приблизительно от 2 до 15% (об/об) эмбриональной бычьей сыворотки, альтернативно от приблизительно 2 до приблизительно 10%, альтернативно от приблизительно 3 до приблизительно 12%, альтернативно от приблизительно 5 до приблизительно 15%, альтернативно от приблизительно 4% до приблизительно 10%, альтернативно от приблизительно 8% до приблизительно 15%, альтернативно от приблизительно 10% до приблизительно 15%. В избранных вариантах осуществления, культурная среда обогащена приблизительно 7,5%, приблизительно 10% или приблизительно 15% (об/об) эмбриональной бычьей сыворотки.
3. Прочие характеристики способов настоящего изобретения
Независимыми вариабельными характеристиками в способах настоящего изобретения, которые могут быть использованы для максимизации количества удвоений популяции, достижимого в культурах центрифужных пробирок или роллер-флаконов, без необходимости замены среды являются скорость вращения, плотность посева клеток во флаконы, количество микроносителей, время инкубации, тип культуральной среды, тип не содержащего сыворотки питательного раствора и объем культуральной среды, помещенной во флакон. Для подготовленного специалиста очевидно, что прочие значения за пределами протестированных диапазонов могут быть протестированы обычными путями с применением той же методологии, и эти значения могут доказать наличие приращения количества удвоений популяции. Максимальный ответ от зависимых вариабельных характеристик, в данном случае достигнутое количество удвоений популяции, измеряется как функция этих параметров, и варианты осуществления, не описанные в настоящем документе детально, следует считать частью данного раскрытия.
Клетки, культивированные в соответствии с представленными способами (такие как, к примеру, клетки hUTC) характеризуются как обладающие по существу таким же профилем маркера клеточной поверхности или профилем генной экспрессии, как и первоначальные клетки. В одном из вариантов осуществления клетки, культивированные в соответствии с представленными способами характеризуются как обладающие по существу таким же профилем маркера клеточной поверхности или профилем генной экспрессии, как и первоначальные клетки. Для многих вариантов применения клеточной терапии важно, чтобы клеточные характеристики не изменялись при масштабировании условий культивирования для увеличения количества. Например, морфология, маркеры клеточной поверхности и экспрессия уникальных характеристик генов, которые помогают отличить или обозначить терапевтические клетки, должны оставаться по существу не измененными, если не идентичными. Клетки, полученные в соответствии с настоящим изобретением и способами, изложенными в настоящем документе, по существу неизменны или, предпочтительно, идентичны в подобных характеристиках тем же клеткам, выращенным в лабораторных условиях и масштабе.
V.Наборы оборудования, содержащие культуральную среду и не содержащий сыворотки питательный раствор
Еще одним вариантом осуществления настоящего изобретения является набор оборудования для выращивания клеток, содержащий культуральную среду настоящего изобретения и не содержащий сыворотки питательный раствор. В одном варианте осуществления набор также содержит клетки. В одном из предпочтительный вариантов осуществления набор содержит клетки, выделенные из ткани человеческой пуповины. Набор может также содержать инструкцию по применению. Не в обязательном порядке набор может также содержать микроносители и сыворотку, такую как эмбриональная бычья сыворотка. В альтернативном варианте набор может также содержать систему роллер-флаконов.
Без более подробного описания предполагается, что любой специалист в данной области может, используя предыдущее описание и следующие иллюстративные примеры, реализовать и использовать настоящее изобретение и на применять на практике заявленные способы. Следующие рабочие примеры, в связи с этим, специально указывают на предпочтительные варианты осуществления настоящего изобретения, и не должны быть истолкованы как ограничивающие каким-либо образом остальную часть раскрытия.
Примеры
Пример 1
Выращивание и сбор клеток hUTC на микроносителях в центрифужных пробирках с обогащенной средой
В данном примере рассматривается выращивание и сбор клеток hUTC на микроносителях в центрифужных пробирках с различными видами обогащенной культуральной среды. Для исследования в данном примере клетки, полученные из ткани пуповины, были распространены из посева и затем выращены в ассортименте различных условий роста (Условия 1-9), в каждом из которых применялась другая культуральная среда, как описано ниже.
Микроносителями, использованными в процессе исследования, были Hillex® Ultra (Solohill Engineering, Ann Arbor, MI), обладающие областью поверхности 515 см2/г.
Применимо к данному примеру термин «пассаж» определяется как засевание сосуда, содержащего свежие микроносители, конфлюэнтными микроносителями из отдельного сосуда. Далее, применимо к данному примеру, термин «удвоение популяции» определяется как количество раз удвоения популяции клеток на протяжении данного времени, и рассчитывается следующим образом:
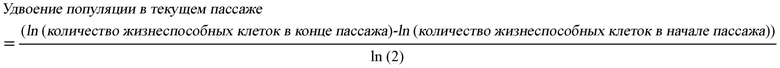
Процедура подсчета клеток
Подсчет клеток, как того требуют различные условия, был проведен в соответствии со следующей процедурой. 10 мл образца было извлечено из культуры и перенесено в 15 мл коническую пробирку в асептических условиях. Затем образец центрифугировали на 1600 об/мин в течение 5 минут. Супернатант был аккуратно удален; при этом следует удостовериться, что ни один из микроносителей не был удален. Затем к микроносителям добавили от 5 до 10 мл TrypLE™ Select (Gibco®), предварительно подогретого до температуры 37°C, и перемешивали в ротаторе от 15 до 30 минут. Содержимое центрифужной пробирки затем перенесли в 50 мл коническую пробирку через 40-микронный фильтр для удаления микроносителей и позволяя пройти только отделившимся клеткам. Было выполнено два промывания с помощью 1×PBS сквозь фильтр. Коническую пробирку емкостью 50 мл затем центрифугировали при 1600 об/мин в течение 5 минут. Супернатант был аккуратно удален без нарушения клеточных планшетов до тез пор, пока в пробирке не осталось приблизительно от 1 до 2 мл супернатанта. Этот оставшийся объем был измерен с помощью пипетки и клеток, повторно взвешенных в этом объеме. Полученная клеточная суспензия был подсчитана с помощью оборудования для подсчета клеток CEDEX (Innovatis), в котором применяется способ исключения трипанового синего. Основанная на клеточном подсчете CEDEX концентрация клеток в сосуде для культивации была рассчитана следующим образом:
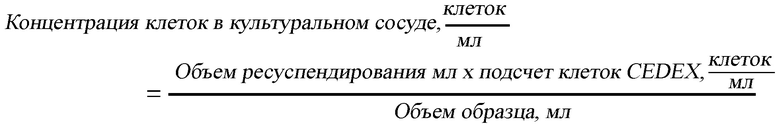

Процедура культивирования клеток
Емкости с замороженными клетками hUTC были разморожены и промыты свежей культуральной средой. Клеточную суспензию переместили в стеклянную центрифужную пробирку емкостью 125 мл, содержащую среду и микроноситель. Эти размороженные клетки были использованы для приготовления посевного материала.
Подготовка клеток для посева
Посевной материал был распределен путем многократных пассажей в контрольной среде, содержащей DMEM и 15% об/об эмбриональной бычьей сыворотки с 12 г/л концентрацией микроносителей, в стеклянные центрифужные пробирки (Corning, NY) различных размеров (125 мл, 500 мл и 3 л). Кумулятивное удвоение популяции клеток в посеве было менее 35. Критерии для пассажа и условия культивирования во время распределения посева указаны в таблице ниже. В целевой день пассажа был выполнен подсчет клеток и если целевая плотность для пассажа была достигнута, клетки были пассированы в новый сосуд, с целевой плотностью посева, основанной на новом сосуде. Если целевая плотность для пассажа не была достигнута, производилась 80% замена среды и клетки считались на следующий день. Для замены среды сосуд убрали с вращающейся платформы и микроносителям позволили осесть под влиянием гравитации на протяжении 5 минут, и 80% среды удалили асептическим путем (без удаления микроносителей) и добавили равное количество свежей культуральной, и сосуд был помещен обратно на вращающуюся платформу в инкубаторе.
Условия роста и параметры во время серийного пассирования для подготовки посевного материала описаны ниже в таблице 1-1.
Условия роста и параметры во время серийного пассирования для подготовки посевного материала
Различные условия роста, использованные в данном примере
Для каждого из условий с 1 по 9 день посева считается днем 0. Так же был выполнен подсчет клеток при посеве для каждого из условий.
Условие 1 (контроль): Целевой плотностью посева для данного условия было ~6000 жизнеспособных клеток/см2 при концентрации микроносителей ~18 г/л. Желательный объем посевного материала, основанный на подсчете клеток в инокулюмах, был добавлен в автоклавированную центрифужную пробирку емкостью 500 мл. Микроносителям позволили осесть под воздействием гравитации. Из инокулюма удаляли культуральную среду до тех пор, пока в пробирке не осталось ~100 мл. Затем добавили свежие микроносители, так что финальный вес микроносителей в пробирке составил ~9 г. Добавили свежую культуральную среду, содержащую DMEM и 15% (об/об) эмбриональной бычьей сыворотки, для увеличения объема до 500 мл. Пробирку поместили на вращающуюся платформу при 60 об/мин в инкубатор при температуре 37°C и 10% СО2. В день 3 осуществили замену 80% среды, применяя DMEM+15% эмбриональной бычьей сыворотки. Периодически производились подсчеты клеток в соответствии с вышеописанной процедурой. В день 3 и 5 в пробирку было добавлено 3 мл и 2,5 мл глюкозы соответственно. В день 3 добавили 2,5 мл 200 мкг L-глютамина.
Условие 2: Целевой плотностью посева для данного условия было ~6000 жизнеспособных клеток/см2 при концентрации микроносителей ~20 г/л. Желательный объем посевного материала, основанный на подсчете клеток в инокулюмах, был добавлен в автоклавированную центрифужную пробирку емкостью 500 мл. Микроносителям позволили осесть под воздействием гравитации. Из инокулюма удаляли культуральную среду до тех пор, пока в пробирке не осталось ~100 мл. Затем добавили свежие микроносители, так что финальный вес микроносителей в пробирке составил ~10 г. Добавили свежую культуральную среду, содержащую базальную среду M5 и 15% (об/об) эмбриональной бычьей сыворотки, для увеличения объема до 500 мл. Пробирку поместили на вращающуюся платформу при 60 об/мин в инкубатор при температуре 37°C и 10% СО2. В день 3 добавили питательный состав F5. Замена среды не производилась. Дополнительно, в день 3 было добавлено 2,5 мл глюкозы. Периодически выполнялись подсчеты клеток как пояснялось в разделе о подсчете клеток. В день 5 в пробирку добавили 5 мл 200 мкг L-глютамина.
Условие 3: Целевой плотностью посева для данного условия было ~7000 жизнеспособных клеток/см2 при концентрации микроносителей ~20 г/л. Желательный объем посевного материала, основанный на подсчете клеток в инокулюмах, был добавлен в автоклавированную центрифужную пробирку емкостью 500 мл. Микроносителям позволили осесть под воздействием гравитации. Из инокулюма удаляли культуральную среду до тех пор, пока в пробирке не осталось ~100 мл. Затем добавили свежие микроносители, так что финальный вес микроносителей в пробирке составил ~10 г. Добавили свежую культуральную среду, содержащую базальную среду M1 и 15% (об/об) эмбриональной бычьей сыворотки, для увеличения объема до 500 мл. Пробирку поместили на вращающуюся платформу при 45 об/мин в инкубатор при температуре 37°C и 10% СО2. В день 3 добавили питательный состав F1. Замена среды не производилась. Периодически выполнялись подсчеты клеток как пояснялось в разделе о подсчете клеток. В день 3 добавили 2,5 мл глюкозы. В день 4 в пробирку добавили 5 мл 200 мкг L-глютамина.
Условие 4: Целевой плотностью посева для данного условия было ~7000 жизнеспособных клеток/см2 при концентрации микроносителей ~20 г/л. Желательный объем посевного материала, основанный на подсчете клеток в инокулюмах, был добавлен в автоклавированную центрифужную пробирку емкостью 500 мл. Микроносителям позволили осесть под воздействием гравитации. Из инокулюма удаляли культуральную среду до тех пор, пока в пробирке не осталось ~100 мл. Затем добавили свежие микроносители, так что финальный вес микроносителей в пробирке составил ~10 г. Добавили свежую культуральную среду, содержащую базальную среду M2 и 15% (об/об) эмбриональной бычьей сыворотки, для увеличения объема до 500 мл. Пробирку поместили на вращающуюся платформу при 45 об/мин в инкубатор при температуре 37°C и 10% СО2. В день 3 добавили питательный состав F2. Замена среды не производилась. Периодически выполнялись подсчеты клеток как пояснялось в разделе о подсчете клеток. 2,5 мл глюкозы (водного раствора 220 г/л декстрозы моногидрата) добавили в день 3. В день 4 в пробирку добавили 5 мл 200 мкг L-глютамина.
Условие 5: Целевой плотностью посева для данного условия было ~7000 жизнеспособных клеток/см2 при концентрации микроносителей ~20 г/л. Желательный объем посевного материала, основанный на подсчете клеток в инокулюмах, был добавлен в автоклавированную центрифужную пробирку емкостью 500 мл. Микроносителям позволили осесть под воздействием гравитации. Из инокулюма удаляли культуральную среду до тех пор, пока в пробирке не осталось ~100 мл. Затем добавили свежие микроносители, так что финальный вес микроносителей в пробирке составил ~10 г. Добавили свежую культуральную среду, содержащую базальную среду M3 и 15% (об/об) эмбриональной бычьей сыворотки, для увеличения объема до 500 мл. Пробирку поместили на вращающуюся платформу при 45 об/мин в инкубатор при температуре 37°C и 10% СО2. В день 3 добавили питательный состав F3. Замена среды не производилась. Периодически выполнялись подсчеты клеток как пояснялось в разделе о подсчете клеток. 2,5 мл глюкозы (водного раствора 220 г/л декстрозы моногидрата) добавили в день 3. В день 4 в пробирку добавили 5 мл 200 мкг L-глютамина.
Условие 6: Целевой плотностью посева для данного условия было ~7000 жизнеспособных клеток/см2 при концентрации микроносителей ~20 г/л. Желательный объем посевного материала, основанный на подсчете клеток в инокулюмах, был добавлен в автоклавированную центрифужную пробирку емкостью 500 мл. Микроносителям позволили осесть под воздействием гравитации. Из инокулюма удаляли культуральную среду до тех пор, пока в пробирке не осталось ~100 мл. Затем добавили свежие микроносители, так что финальный вес микроносителей в пробирке составил ~10 г. Добавили свежую культуральную среду, содержащую базальную среду M4 и 15% (об/об) эмбриональной бычьей сыворотки, для увеличения объема до 500 мл. Пробирку поместили на вращающуюся платформу при 45 об/мин в инкубатор при температуре 37°C и 10% СО2. В день 3 добавили питательный состав F4. Замена среды не производилась. Периодически выполнялись подсчеты клеток как пояснялось в разделе о подсчете клеток. 2,5 мл глюкозы (водного раствора 220 г/л декстрозы моногидрата) добавили в день 3. В день 4 в пробирку добавили 5 мл 200 мкг L-глютамина.
Условие 7: Целевой плотностью посева для данного условия было ~7000 жизнеспособных клеток/см2 при концентрации микроносителей ~20 г/л. Желательный объем посевного материала, основанный на подсчете клеток в инокулюмах, был добавлен в автоклавированную центрифужную пробирку емкостью 500 мл. Микроносителям позволили осесть под воздействием гравитации. Из инокулюма удаляли культуральную среду до тех пор, пока в пробирке не осталось ~100 мл. Затем добавили свежие микроносители, так что финальный вес микроносителей в пробирке составил ~10 г. Добавили свежую культуральную среду, содержащую базальную среду M5 и 15% (об/об) эмбриональной бычьей сыворотки, для увеличения объема до 500 мл. Пробирку поместили на вращающуюся платформу при 45 об/мин в инкубатор при температуре 37°C и 10% СО2. В день 3 добавили питательный состав F5. Замена среды не производилась. Периодически выполнялись подсчеты клеток как пояснялось в разделе о подсчете клеток. 2,5 мл глюкозы (водного раствора 220 г/л декстрозы моногидрата) добавили в день 3. В день 4 в пробирку добавили 5 мл 200 мкг L-глютамина.
Условие 8: Целевой плотностью посева для данного условия было ~7000 жизнеспособных клеток/см2 при концентрации микроносителей ~20 г/л. Желательный объем посевного материала, основанный на подсчете клеток в инокулюмах, был добавлен в автоклавированную центрифужную пробирку емкостью 500 мл. Микроносителям позволили осесть под воздействием гравитации. Из инокулюма удаляли культуральную среду до тех пор, пока в пробирке не осталось ~100 мл. Затем добавили свежие микроносители, так что финальный вес микроносителей в пробирке составил ~10 г. Добавили свежую культуральную среду, содержащую базальную среду M6 и 15% (об/об) эмбриональной бычьей сыворотки, для увеличения объема до 500 мл. Пробирку поместили на вращающуюся платформу при 45 об/мин в инкубатор при температуре 37°C и 10% СО2. В день 3 добавили питательный состав F6. Замена среды не производилась. Периодически выполнялись подсчеты клеток как пояснялось в разделе о подсчете клеток. 2,5 мл глюкозы (водного раствора 220 г/л декстрозы моногидрата) добавили в день 3. В день 4 в пробирку добавили 5 мл 200 мкг L-глютамина.
Условие 9: Целевой плотностью посева для данного условия было ~7000 жизнеспособных клеток/см2 при концентрации микроносителей ~20 г/л. Желательный объем посевного материала, основанный на подсчете клеток в инокулюмах, был добавлен в автоклавированную центрифужную пробирку емкостью 500 мл. Микроносителям позволили осесть под воздействием гравитации. Из инокулюма удаляли культуральную среду до тех пор, пока в пробирке не осталось ~100 мл. Затем добавили свежие микроносители, так что финальный вес микроносителей в пробирке составил ~10 г. Добавили свежую культуральную среду, содержащую базальную среду M7 и 15% (об/об) эмбриональной бычьей сыворотки, для увеличения объема до 500 мл. Пробирку поместили на вращающуюся платформу при 45 об/мин в инкубатор при температуре 37°C и 10% СО2. В день 3 добавили питательный состав F7. Замена среды не производилась. Периодически выполнялись подсчеты клеток как пояснялось в разделе о подсчете клеток. 2,5 мл глюкозы (водного раствора 220 г/л декстрозы моногидрата) добавили в день 3. В день 4 в пробирку добавили 5 мл 200 мкг L-глютамина.
Сбор
На 6 день был собран урожай клеток из всех пробирок. Для сбора микроносителям позволили осесть под воздействием гравитации и удалили среду настолько, насколько это возможно без удаления микроносителей. В пробирку добавили 250-300 мл TrypLE™, предварительно подогретого до температуры 37°C, и поместили на вращающуюся платформу в инкубатор при температуре 37°C. Через 30 минут перемешивание остановили и взяли 25 мл образца из пробирки, и пропустили через 40 мкм фильтр. Микроносители, оставшиеся на фильтре, удалили в отходы, и произвели подсчет клеток путем прямого применения CEDEX к образцу. Добавили объем, основанный на TrypLE™, и полученный подсчет клеток, рассчитали общее количество клеток в сосуде и рассчитали плотность клеток (клетки/см2).
Композиция среды культивирования клеток
DMEM (с 1 г/л глюкозы, 4ммоль L-глютамина и 3,7 г/л натрия бикарбоната и без натрия пирувата и фенола красного) был базовой средой, использованной для условия 1 (контроля).
Несколько других базовых сред были также протестированы для идентификации некоторых компонентов, которые имеют критическое значение в ликвидации необходимости замены среды и, таким образом, снижении потребления сыворотки. Одним из компонентов, использованных в формулах является альбумин бычьей сыворотки, представленный в форме коммерчески доступного AlbuMAX® I (Gibco™ Cell Culture, Invitrogen Corporation, Карлсбад, Калифорния), который является богатым липидами альбумином бычьей сыворотки. Таблица 1-2 представляет формулу базовой среды (М1 - М7). Как базисная, так и питательная среда содержать коммерчески доступный стабилизатор клеточных мембран и противовспенивающий агент Pluronic® F68.
(г/л)
(г/л)
(г/л)
(г/л)
(г/л)
(г/л)
(г/л)
тиоктовая кислота
Как указывалось выше, в день 3 была произведена замена 80% среды в условии 1. Для остальных условий был добавлен питательный состав для ликвидации необходимости замены среды. Различные формулы питательных составов приведены в таблице 1-3. Количества, показанные в таблице 1-3, представляют увеличение в весе (г) компонента на литр (л) объема культуры при добавлении питательного состава.
(г/л)
(г/л)
(г/л)
(г/л)
(г/л)
(г/л)
(г/л)
7H2O)
тиоктовая кислота
Во все среды, использованные в условиях от 1 до 9 была добавлена эмбриональная бычья сыворотка. Компоненты эмбриональной бычьей сыворотки показаны ниже:
Профиль эмбриональной бычьей сыворотки (см. Price et al., In Vitro, 18:576-584 (1982))
Результаты
Результаты подсчета клеток из различных условий показаны в таблице 1-5 ниже. Результаты можно проанализировать в двух частях. При сравнении условий 1 и 2 очевидно, что комбинация среды М5 и питательного состава F5 в день 3 ликвидирует необходимость в замене среды. Это важно, поскольку резко понижает концентрацию сыворотки на более чем 44%. При сравнении условий от 3 до 9 очевидно, что следующие три условия дают самые низкие результаты в сравнении с остальными: условие 6, базовая среда М4+15% эмбриональной бычьей сыворотки с добавлением F4 в день 3; условие 8, базовая среда М6+15% эмбриональной бычьей сыворотки с добавлением F6 в день 3; и условие 9, базовая среда М7+15% эмбриональной бычьей сыворотки с добавлением F7 в день 3. Внимательное рассмотрение формул показывает, что ни одно из этих условий не имеет производных от нуклеиновых кислот в среде или питательном составе. Следовательно, можно заключить, что производные от нуклеиновых кислот имеют критическое значение для роста клеток hUTC. Этот пример демонстрирует, что клетки hUTC могут быть выращены за 6 дней без замены среды путем обогащения культуральной среды и внесения добавочных компонентов среды в день 3, и производные от нуклеиновых кислот имеют критическое значение при достижении относительного роста клеток.
Подсчет жизнеспособных клеток, клетки/см2 для культур hUTC, выращенных в условиях 1-9
Пример 2
Выращивание и серийное пассирование клеток hUTC на микроносителях и в центрифужных пробирках с обогащенной средой
Серийное пассирование клеток человеческой пуповины (hUTC), закрепленных на микроносителях в суспензийной культуре в центрифужных пробирках требует замены среды, если клетки не достигают предварительно определенной оптимальной клеточной плотности >20 000 клеток/см2 на день 3. Эта замена среды увеличивает количество манипуляций в процессе и усложняет прогнозирование расписания пассирования клеток. Следовательно, эта процедура для пассирования клеток является коммерчески нежелательной. Клетки hUTC могут выращиваться до высокой клеточной плотности путем замены клеточной ростовой среды, содержащей 15% эмбриональной бычьей сыворотки. Этот пример исследует альтернативный, более коммерчески желательный способ пассирования клеток hUTC. Клетки hUTC, закрепленные на микроносителе, были выращены до высокой клеточной плотности в суспензийной культуре в центрифужных пробирках путем обогащения ростовой среды не содержащими сыворотки питательными составами. Этот способ ликвидирует необходимость в замене среды в день 3 для бесперебойного выращивания клеток >20 000 клеток/см2. Этот способ улучшает жесткость пассирования клеток hUTC.
В настоящем исследовании было использованы следующие компоненты: DMEM (с 2 г/л глюкозы, 4 ммоль L-глютамина и 3,7 г/л натрия бикарбоната и без натрия пирувата и фенола красного); эмбриональный бычья сыворотка (15% об/об); базовая среда М5 (см. пример 1 выше); питательный состав F5 (см. пример 1 выше); и микроносители Hillex® Ultra (Solohill Engineering, Ann Arbor, MI).
Способ анализа поверхностного маркера
3% эмбриональной бычьей сыворотки в фосфатно-солевом буфере Дульбекко (DPBS) без кальция или магния было использовано в качестве красящего буфера. Шесть антител было использовано для идентификации поверхностных маркеров и два антитела были использованы в качестве контроля. Список антител и их растворов в красящем буфере для анализа представлен в таблице 2-1 ниже.
Список антител и растворов
Методология: Был выполнен подсчет клеток в образце и 2,5×106 были ресуспендированы в 10 мл среды DMEM+15% эмбриональной бычьей сыворотки. Затем клетки были центрифугированы, супернатант удален и ресуспендирован в красящем буфере для достижения концентрации клеток 1×106 клеток/мл. Эта клеточная суспензия была затем распределена по разным пробиркам, так, что каждая пробирка получила по 20000 клеток. Затем были добавлены соответствующие количества растворенных антител и красящего буфера, как показано выше в таблице 2-1. Затем образцы инкубировали в течение 30 минут при температуре 2-8°C. После инкубации было добавлено 3 мл DPBS и образцы центрифугировали. Супернатант был удален и клеточный планшет был ресуспендирован в 500 мкл DPBS. Образцы были затем обработаны на приборе Guava® PCA™, Millipore, MD, USA. Из шести поверхностных маркеров три являются положительными маркерами (CD13, CD90, HLA-ABC) и три являются отрицательными маркерами (CD34, CD117, HLA-DR).
Условия культивирования
Способы культивирования и серийного пассирования клеток hUTC были разъяснены в примере 1. Как уже упоминалось, в этом серийном пассировании использовалась в качестве культуральной среды DMEM с 15% эмбриональной бычьей сыворотки, и часто требовалась замена среды для соответствия критериям пассирования. В этом примере была предпринята попытка ликвидации необходимости частой замены среды во время серийного пассирования. Это было достигнуто путем использования модицифированной среды М5 (с 2 г/л глюкозы вместо 1 г/л) и 15% эмбриональной бычьей сыворотки (об/об). С применением этой модифицированной среды М5 с 15% эмбриональной бычьей сыворотки день пассирования был зафиксирован и ни одной замены среды не выполнялось на протяжении шести пассажей. Условия культивирования и критерии представлены ниже в таблице 2-2.
Условия культивирования
Клетки демонстрировали жесткий рост на протяжении шести пассажей как показано в таблице 2-3 ниже. В процессе при участии только DMEM+15% эмбриональной бычьей сыворотки клетки часто требовали замены среды в день перед пассажем с целью достижения удвоения популяции 1,5, таким образом увеличивая длительность пассажа на дополнительный день. С обогащенной средой, клетки стабильно обладали удвоением популяции по меньшей мере превышающим 1,5 через 3 дня (4 дня от размораживания сосуда) и не требовали никакой замены среды. Клетки сохраняли свою тождественность после семи пассажей в этой среде и затем растили эти клетки на протяжении 6 дней в этой среде с введением питательного состава F5 в день 3 6-дневной культуры. Анализ поверхностных маркеров этих клеток показан в таблице 2-4 ниже.
Результаты
(После размораживания сосуда)
Результаты поверхностных маркеров клеток, пассированных в среде М5 +15% эмбриональной бычьей сыворотки для 7 пассажей, за которыми следовало 6-дневное культивирование в среде М5+15% эмбриональной бычьей сыворотки и добавлением питательного состава F5 в день 3 6-дневной культуры
Пример 3
Выращивание клеток hUTC на микроносителях а среде с пониженным содержанием сыворотки в центрифужных пробирках
Клетки пуповины человека (hUTC) могут быть выращены до высокой клеточной плотности путем замены клеточной ростовой среды, содержащей 15% эмбриональной бычьей сыворотки на день 3 серии. Высокая концентрация сыворотки в среде и замена среды нежелательны с коммерческой точки зрения из-за высокой стоимости сыворотки, большого расхода сыворотки для производства и дополнительных операционных манипуляций. Этот пример раскрывает способ выращивания клеток hUTC, закрепленных на микроносителях в ростовой среде с пониженным содержанием сыворотки, и без замены среды при достижении высокой клеточной плотности.
Культуральной средой, использованной в примере, была базовая среда М5 (см. выше), с 2 г/л D-глюкозы вместо 1 г/л D-глюкозы, к которой была добавлена эмбриональная бычья сыворотка. Была использована среда с добавкой питательного состава F5. Глюкоза была представлена в виде водного раствора 220 г/л декстрозы моногидрата. Глютамин был представлен в виде раствора 200 ммоль. В данном примере были изучены различные условия роста. Эти условия описаны ниже. Применимо к данным условиям день посева считается днем 0. Далее, в каждом условии применялись микроносители Hillex® Ultra (Solohill Engineering, Ann Arbor, MI).
Условие 1 (15% эмбриональной бычьей сыворотки): При посеве был осуществлен подсчет клеток. Целевой плотностью посева для данного условия было ~6000 жизнеспособных клеток/см2 при концентрации микроносителей ~20 г/л. Желательный объем посевного материала, основанный на подсчете клеток в инокулюмах, был добавлен в автоклавированную центрифужную пробирку емкостью 500 мл. Микроносителям позволили осесть под воздействием гравитации. Из инокулюма удаляли культуральную среду до тех пор, пока в пробирке не осталось ~100 мл. Затем добавили свежие микроносители, так что финальный вес микроносителей в пробирке составил ~10 г. Добавили свежую культуральную среду, содержащую базальную среду M5 и 15% (об/об) эмбриональной бычьей сыворотки, для увеличения объема до 500 мл. Пробирку поместили на вращающуюся платформу при 60 об/мин в инкубатор при температуре 37°C и 10% СО2. В день 3 добавили питательный состав F5. Замена среды не производилась. Периодически выполнялись подсчеты клеток как пояснялось в разделе о подсчете клеток. 2,5 мл глюкозы было добавлено в день 3 и день 5. В день 4 в пробирку добавили 5 мл 200 мкг L-глютамина.
Условие 2 (10% эмбриональной бычьей сыворотки): При посеве был осуществлен подсчет клеток. Целевой плотностью посева для данного условия было ~6000 жизнеспособных клеток/см2 при концентрации микроносителей ~20 г/л. Желательный объем посевного материала, основанный на подсчете клеток в инокулюмах, был добавлен в автоклавированную центрифужную пробирку емкостью 500 мл. Микроносителям позволили осесть под воздействием гравитации. Из инокулюма удаляли культуральную среду до тех пор, пока в пробирке не осталось ~100 мл. Затем добавили свежие микроносители, так что финальный вес микроносителей в пробирке составил ~10 г. Добавили свежую культуральную среду, содержащую базальную среду M5 и 10% (об/об) эмбриональной бычьей сыворотки, для увеличения объема до 500 мл. Пробирку поместили на вращающуюся платформу при 60 об/мин в инкубатор при температуре 37°C и 10% СО2. В день 3 добавили питательный состав F5. Замена среды не производилась. Периодически выполнялись подсчеты клеток как пояснялось в разделе о подсчете клеток. 2,5 мл глюкозы было добавлено в день 3 и день 5. В день 4 в пробирку добавили 5 мл 200 мкг L-глютамина.
Условие 3 (7,5% эмбриональной бычьей сыворотки): При посеве был осуществлен подсчет клеток. Целевой плотностью посева для данного условия было ~6000 жизнеспособных клеток/см2 при концентрации микроносителей ~20 г/л. Желательный объем посевного материала, основанный на подсчете клеток в инокулюмах, был добавлен в автоклавированную центрифужную пробирку емкостью 500 мл. Микроносителям позволили осесть под воздействием гравитации. Из инокулюма удаляли культуральную среду до тех пор, пока в пробирке не осталось ~100 мл. Затем добавили свежие микроносители, так что финальный вес микроносителей в пробирке составил ~10 г. Добавили свежую культуральную среду, содержащую базальную среду M5 и 7,5% (об/об) эмбриональной бычьей сыворотки, для увеличения объема до 500 мл. Пробирку поместили на вращающуюся платформу при 60 об/мин в инкубатор при температуре 37ºC и 10% СО2. В день 3 добавили питательный состав F5. Замена среды не производилась. Периодически выполнялись подсчеты клеток как пояснялось в разделе о подсчете клеток. 2,5 мл глюкозы было добавлено в день 3 и день 5. В день 4 в пробирку добавили 5 мл 200 мкг L-глютамина.
Сбор: На 6 день был собран урожай клеток из обеих пробирок. Для сбора микроносителям позволили осесть под воздействием гравитации и удалили среду настолько, насколько это возможно без удаления микроносителей. В пробирку добавили 300 мл TrypLE™, предварительно подогретого до температуры 37°C, и поместили на вращающуюся платформу в инкубатор при температуре 37°C. Через 30 минут перемешивание остановили и взяли 25 мл образца из пробирки, и пропустили через 40 мкм фильтр. Микроносители, оставшиеся на фильтре, удалили в отходы, и произвели подсчет клеток путем прямого применения CEDEX к образцу. Добавили объем, основанный на TrypLE™, и полученный подсчет клеток, рассчитали общее количество клеток в сосуде и рассчитали плотность клеток (клетки/см2).
РЕЗУЛЬТАТЫ: Результаты подсчета клеток для трех условий с различной концентрацией эмбриональной бычьей сыворотки представлены в таблице ниже. В дополнение к результатам из этого примера, результаты из примера 1, условие 1 (DMEM+15% эмбриональной бычьей сыворотки с заменой среды в день 3) включены для сравнения. Таким образом, обогащенная среда не только ликвидирует необходимость в замене среды, но также моет снизить концентрацию сыворотки в среде, тем самым также минимизируя количество сыворотки, используемой в культуре.
Подсчет клеток, жизнеспособные клетки/см2
ПРИМЕР 4
Выделение клеток
Выделение клеток пуповины. Пуповины получили в Национальном центре по обмену материалами для исследования заболеваний (NDRI, г. Филадельфия, штат Пенсильвания). Ткани были получены после нормально прошедших родов. Протоколы выделения клеток проводили в асептических условиях в ламинарном боксе. Для удаления крови и продуктов распада клеток пуповины были промыты в фосфатно-буферном солевом растворе (PBS; Invitrogen, Карлсбад, Калифорния) в присутствии пенициллина в дозе 100 Ед/мл, стрептомицина в дозе 100 мг/мл и амфотерицина В в дозе 0,25 мкг/мл (Invitrogen, Карлсбад, Калифорния). Затем ткани механически диссоциировали в планшетах для культивирования тканей площадью 150 см2 в присутствии 50 миллилитров среды (среды DMEM с низким содержанием глюкозы или среды DMEM с высоким содержанием глюкозы; Invitrogen) до измельчения ткани в мелкую пульпу. Размельченные ткани перенесли в конические пробирки объемом 50 мл (приблизительно по 5 г ткани на пробирку).
Затем ткань была расщеплена в среде DMEM с низким содержанием глюкозы или среде DMEM с высоким содержанием глюкозы, каждая из которых содержала пенициллин в дозе 100 Ед/мл, стрептомицин в дозе 100 мг/мл, амфотерицин B в дозе 0,25 мкг/мл и расщепляющие ферменты. В некоторых экспериментах использовали ферментативную смесь коллагеназы и диспазы (C:D; коллагеназа (Sigma, г. Сент-Луис, штат Миссури), 500 единиц/миллилитр; и диспаза (Invitrogen), 50 единиц/миллилитр в среде DMEM c низким содержанием глюкозы). В других экспериментах использовали смесь коллагеназы, диспазы и гиалуронидазы (C:D:H = коллагеназа, 500 единиц/миллилитр; диспаза, 50 единиц/миллилитр; и гиалуронидаза (Sigma), 5 единиц/миллилитр, в среде DMEM c низким содержанием глюкозы). Конические пробирки, содержащие ткань, среду и расщепляющие ферменты, инкубировали при температуре 37°C на орбитальном шейкере (Environ, г. Бруклин, штат Нью-Йорк) при скорости 225 об/мин в течение 2 часов.
После расщепления ткани центрифугировали при 150×g в течение 5 минут и аспирировали супернатант. Осадок был ресуспендирован в 20 мл ростовой среды (DMEM с низким содержанием глюкозы (Invitrogen), 15% (об/об) эмбриональной бычьей сыворотки (FBS; выявленная эмбриональная бычья сыворотка; Lot #AND18475; Hyclone, Logan, UT), 0,001% (об/об) 2-меркаптоэтанол (Sigma), пенициллин в дозе 100 Ед/мл, стрептомицин в дозе 100 мкг/мл и амфотерицин В в дозе 0,25 мкг/мл (каждый от Invitrogen, Карлсбад, Калифорния)). Клеточную суспензию фильтровали через нейлоновый клеточный фильтр BD FALCON с размером поры 70 мкм (BD Biosciences, Сан-Хосе, штат Калифорния). Фильтр дополнительно промыли 5 мл ростовой среды. Затем клеточную суспензию пропустили через нейлоновый клеточный фильтр с размером пор 40 мкм (BD Biosciences, Сан-Хосе, штат Калифорния), после чего фильтр дополнительно промыли 5 мл ростовой среды.
Фильтрат ресуспендировали в ростовой среде (до общего объема 50 мл) и центрифугировали при 150×g в течение 5 минут. Супернатант аспирировали, а клетки ресуспендировали в 50 мл свежей ростовой среды. Описанную процедуру повторили еще дважды.
После последнего центрифугирования супернатант аспирировали, а клеточный сгусток ресуспендировали в 5 мл свежей ростовой среды. Число жизнеспособных клеток определили окрашиванием трипановым синим. Затем клетки культивировали в стандартных условиях.
Клетки, выделенные из ткани пуповины, высевали с плотностью 5000 клеток/см2 на покрытые желатином колбы T-75 (Corning Inc., г. Корнинг, штат Нью-Йорк) в ростовой среде. Через два дня из колб аспирировали использованную среду и незакрепившиеся клетки. Закрепившиеся клетки трижды промывали PBS для удаления продуктов распада клеток и клеток крови. Затем клетки снова заливали ростовой средой и давали культуре расти до конфлюентности (приблизительно 10 суток от пассажа 0 до пассажа 1). При последующих пассированиях (от пассажа 1 до пассажа 2 и т.д.) клетки достигали субконфлюентности (75–85% конфлюентности) за 4–5 суток. Для данных последующих пассирований клетки высевали с плотностью 5000 клеток/см2. Клетки выращивались во влажной камере с 5% углекислого газа при 37°C.
В некоторых вариантах осуществления клетки выделялись из тканей неонатального материала в среду DMEM с низким содержанием глюкозы после расщепления с использованием LIBERASE (2,5 мг/мл, Blendzyme 3; Roche Applied Sciences, Indianapolis, IN) и гиалуронидазы (5 Ед/мл, Sigma). Расщепление ткани и выделение клеток проводили описанным выше способом для расщепления с использованием других протеаз, при этом применяли смесь LIBERASE/гиалуронидазы вместо ферментативной смеси C:D или C:D:H. Расщепление ткани с использованием LIBERASE позволило выделить из тканей постнатального материала популяции клеток, которые легко размножались.
Сравнили между собой процедуры выделения клеток из пуповины с применением разных комбинаций ферментов. Ферменты, сравниваемые для расщепления, включали: i) коллагеназу; іі) диспазу; iii) гиалуронидазу; iv) смесь коллагеназы: диспазы (C: D): v) смесь коллагеназы: гиалуронидазы (C: H); vi) смесь диспазы: гиалуронидазы (D: H); и vii) смесь коллагеназы: диспазы: гиалуронидазы (C: D: H)/ При выделении клеток с использованием данных разных условий ферментативного расщепления наблюдались различия (см. таблицу 4-1).
Предпринимали другие попытки выделения пулов клеток из пуповины различными способами. В одном случае пуповину нарезали и промывали ростовой средой для отделения сгустков крови и студенистого материала. Смесь крови, студенистого материала и ростовой среды была собрата и центрифугирована при 150×g. Осадок был ресуспендирован и посеян в покрытые желатином пробирки в ростовую среду. Данные эксперименты позволили выделить популяцию клеток, которые легко размножались.
Клетки также выделили из образцов пуповинной крови, полученных из NDRI. Использовали протокол выделения, описанный в международной заявке на патент PCT/US2002/029971, авторы Ho et al. Образцы (объемом 50 миллилитров и 10,5 миллилитра соответственно) пуповинной крови (NDRI, г. Филадельфия, штат Пенсильвания) смешивали с лизирующим буфером (стерилизованный фильтрацией раствор 155 мМ хлорида аммония, 10 мМ бикарбоната калия, 0,1 мМ ЭДТА, буферизованный до pH 7,2 (все компоненты производства Sigma, г. Сент-Луис, штат Миссури)). Клетки лизировали при соотношении пуповинной крови к лизирующему буферному раствору 1:20. Полученную суспензию клеток в течение 5 секунд перемешивали вихревым способом и затем инкубировали в течение 2 минут при температуре окружающей среды. Лизат центрифугировали (10 минут при 200×g). Клеточный осадок ресуспендировали в полноценной минимальной питательной среде (Gibco, Карлсбад, штат Калифорния), содержащей 10% фетальной бычьей сыворотки (Hyclone, Логан, штат Юта), 4 мМ глутамина (Mediatech, Херндон, штат Виргиния), пенициллин в дозе 100 Ед/мл и стрептомицин в дозе 100 мкг/мл (Gibco, Карлсбад, штат Калифорния). Повторно растворенные клетки центрифугировали (10 минут при 200×g), супернатант аспирировали и клеточный осадок промыли в полной среде. Клетки высевали непосредственно либо в колбы T75 (г. Корнинг, штат Нью-Йорк) либо в покрытые ламинином колбы T75, либо в покрытые фибронектином колбы T175 (все колбы производства Becton Dickinson, г. Бедфорд, штат Массачусетс).
Чтобы определить возможность выделения популяций клеток в разных условиях и их размножения в различных условиях сразу после выделения клетки расщепляли в ростовой среде с добавлением или без добавления 0,001% (об/об) 2-меркаптоэтанола (Sigma, Сент-Луис, штат Миссури) с использованием комбинации ферментов C:D:H в соответствии с описанными выше процедурами. Все клетки выращивались в присутствии пенициллина в дозе 100 Ед/мл и стрептомицина в дозе 100 мкг/мл. Клетки закреплялись и хорошо размножались между пассажами 0 и 1 при всех исследуемых условиях (таблица 4-2). Для клеток при условиях 5–8 и 13–16 наблюдали хорошую пролиферацию вплоть до 4 пассажей после посева, после чего их криоконсервировали.
Комбинация ферментов C:D:H обеспечила наилучший выход клеток после выделения и дала клетки, которые размножались в культуре в течение большего количества поколений, чем при использовании других условий (таблица 4-1). При применении только коллагеназы или только гиалуронидазы не удавалось получить способную к размножению популяцию клеток. Попытки проверить, специфичен ли этот результат к конкретной исследуемой коллагеназе, не предпринимались.
Выделение клеток из ткани пуповины с использованием различных комбинаций ферментов
Клетки закреплялись и хорошо размножались между пассажами 0 и 1 при всех исследуемых условиях по ферментативному расщеплению и условиям роста (таблица 4-2). Для клеток при экспериментальных условиях 5–8 и 13–16 наблюдали хорошую пролиферацию вплоть до четырех пассажей после посева, после чего их криоконсервировали. Все клетки криоконсервировали для проведения дополнительного анализа.
Выделение и размножение в культуре клеток неонатального материала при различных условиях
Ядросодержащие клетки быстро закреплялись и росли. Данные клетки анализировали способом проточной цитометрии, и они оказались аналогичны клеткам, полученным способом ферментативного расщепления.
Препараты содержали эритроциты и тромбоциты. Ядросодержащие клетки не закреплялись и не делились в течение первых 3 недель. Среду заменили через 3 недели после посева, не наблюдали никакого закрепления и роста клеток.
Популяции клеток можно успешно выделять из ткани пуповины при помощи комбинации ферментов, содержащей коллагеназу (металлопротеазу), диспазу (нейтральную протеазу) и гиалуронидазу (фермент с муколитической активностью, который разрушает гиалуроновую кислоту). Также можно применять смесь LIBERASE, которая представляет собой смесь коллагеназы и нейтральной протеазы. Вместе с гиалуронидазой для выделения клеток также использовали смесь Blendzyme 3, которая представляет собой смесь коллагеназы (4 единицы Вунша/г) и термолизина (1714 единиц казеина/г). Данные клетки легко размножались на протяжении многих пассирований при культивировании в ростовой среде для размножения на покрытом желатином пластике.
Клетки также выделяли из остаточной крови в пуповинах, но не из пуповинной крови. Присутствие клеток в сгустках крови, смытых с ткани, которые закрепляются и растут в применяемых условиях, может быть обусловлено клетками, высвобожденными в процессе рассечения.
ПРИМЕР 5
Анализ кариотипа клеток
Применяемые в клеточной терапии клеточные линии предпочтительно должны быть однородными и свободными от любых примесей клеток других типов. Клетки человека, которые применяются в терапевтических целях, должны иметь нормальное количество (46) хромосом с нормальной структурой. Был проведен анализ кариотипов образцов клеток для определения линий полученных из пуповины клеток, однородных и свободных от клеток, происходящих не из ткани пуповины.
Клетки UTC, полученные из тканей неонатального материала новорожденного мальчика, культивировали в ростовой среде. Ткань постнатального материала новорожденного мальчика (X,Y) выбрали для возможности различения неонатальных клеток и материнских клеток (X,X). Клетки высевали с плотностью 5000 клеток на кв. сантиметр в ростовой среде в колбе T25 (Corning, г. Корнинг, штат Нью-Йорк) и размножали до степени конфлюентности 80%. Затем содержащую клетки колбу T25 заполнили по горлышко ростовой средой. Образцы доставили курьером в лабораторию клинической цитогенетики (оцениваемое время транспортировки из лаборатории в лабораторию составляет один час). Анализ хромосом был выполнен Центром человеческой и молекулярной генетики в медицинской школе Нью-Джерси, Ньюарк, Нью-Джерси. Клетки анализировали во время метафазы, когда хромосомы видны лучше всего. Из двадцати подсчитанных в метафазе клеток пять проанализировали на количество кариотипов для нормальной однородной популяции клеток (два). Образец клеток охарактеризовали как однородный при наблюдении двух кариотипов. Образец клеток охарактеризовали как неоднородный при наблюдении более двух кариотипов. При определении количества кариотипов (четыре), характерного для неоднородной популяции клеток, подсчитывали и анализировали дополнительные клетки в метафазе.
Все образцы клеток, отправленные для проведения хромосомного анализа, были интерпретированы персоналом цитогенетической лаборатории как нормальные. Три из шестнадцати проанализированных клеточных линий продемонстрировали неоднородный фенотип (XX и XY), указывающий на присутствие клеток как неонатального, так и материнского происхождения (Таблица 5-1). Каждый из образцов клеток был охарактеризован как однородный. (Таблица 5-1).
Результаты кариотипирования клеток hUTC
В результате хромосомного анализа идентифицировали клетки UTC, полученные из пуповины, кариотипы которых интерпретировали в лаборатории клинической цитогенетики как нормальные. В результате кариотипического анализа также идентифицировали клеточные линии, свободные от материнских клеток, что было определено по однородному кариотипу.
ПРИМЕР 6
Определение количества маркеров клеточной поверхности способом проточной цитометрии
Характеризацию белков, или «маркеров», клеточной поверхности способом проточной цитометрии можно применять для определения отличительных признаков клеточной линии. Стабильность экспрессии можно определить по множеству доноров и в клетках, которые культивировали и обрабатывали в разных условиях. Линии клеток постнатального материала, выделенных из пуповины, охарактеризовали способом проточной цитометрии, получив профиль экспрессии для установления отличительных признаков данных клеточных линий.
Клетки культивировали в ростовой среде в обработанных плазмой колбах для культивирования тканей T75, T150 и T225 (Corning, г. Корнинг, штат Нью-Йорк) до конфлюентности. Ростовые поверхности колб покрывали желатином инкубацией с 2% (в/об) раствором желатина (Sigma, г. Сент-Луис, штат Миссури) в течение 20 минут при комнатной температуре.
Закрепившиеся клетки в колбах промывали фосфатно-солевым буфером (PBS) (Gibco, г. Карлсбад, штат Калифорния) и отделяли с помощью трипсина/ЭДТА (Gibco). Клетки собирали, центрифугировали и ресуспендировали в 3% (об/об) ФБС в ФБР при концентрации 1x107/ мл. В соответствии с инструкциями производителя, добавляли антитело на рассматриваемый маркер клеточной поверхности (см. ниже) к 100 микролитрам клеточной суспензии и инкубировали смесь в темноте в течение 30 минут при температуре 4°C. После инкубации клетки промывали PBS и центрифугировали для удаления несвязавшихся антител. Клетки повторно суспендировали в 500 мкл ФБР и анализировали с использованием проточной цитометрии. Анализ способом проточной цитометрии проводили на анализаторе FACS calibur (Becton Dickinson, Сан-Хосе, штат Калифорния).
Применяли следующие антитела на маркеры клеточной поверхности.
Антитела, примененные в характеризации маркеров клеточной поверхности клеток UDC
Клетки, полученные из пуповины, анализировали на пассажах 8, 15 и 20.
Для сравнения различий доноров друг с другом сравнивались клетки, полученные из ткани пуповины, от различных доноров. Клетки, полученные из пуповины, культивировавшиеся на покрытых желатином колбах, также сравнили с клетками, полученными из пуповины, культивировавшимися на непокрытых колбах.
Сравнили результаты четырех процедур выделения и подготовки клеток. Клетки, полученные из ткани неонатального материала путем обработки: 1) коллагеназы; 2) коллагеназы/диспазы; 3) коллагеназы/гиалуронидазы; и 4) коллагеназы/гиалуронидазы/диспазы, сравнивались между собой.
Все проанализированные способом проточной цитометрии клетки, полученные из пуповины, на пассажах 8, 15 и 20 экспрессировали CD10, CD13, CD44, CD73, CD 90, PDGFr-альфа и HLA-A, B, C, на что указывают повышенные значения флуоресценции по сравнению с используемым в качестве контроля IgG. Данные клетки были отрицательными в отношении CD31, CD34, CD45, CD117, CD141 и HLA-DR, DP, DQ, на что указывают значения флуоресценции, согласующиеся с величинами для используемого в качестве контроля IgG.
Все проанализированные способом проточной цитометрии клетки, полученные из пуповины и выделенные у разных доноров, показали положительную выработку CD10, CD13, CD44, CD73, CD 90, PDGFr-альфа и HLA-A, B, C, на что указывают повышенные значения флуоресценции по сравнению с используемым в качестве контроля IgG. Данные клетки были отрицательными в отношении выработки CD31, CD34, CD45, CD117, CD141 и HLA-DR, DP, DQ, на что указывают значения флуоресценции, согласующиеся с величинами для используемого в качестве контроля IgG.
Все проанализированные способом проточной цитометрии клетки, полученные из ткани пуповины и размножаемые на покрытых желатином и на непокрытых колбах, были положительными в отношении выработки CD10, CD13, CD44, CD73, CD 90, PDGFr-альфа и HLA-A, B, C, при этом значения флуоресценции были повышены по сравнению с используемым в качестве контроля IgG. Данные клетки были отрицательными в отношении выработки CD31, CD34, CD45, CD117, CD141 и HLA-DR, DP, DQ, на что указывают значения флуоресценции, согласующиеся с величинами для используемого в качестве контроля IgG.
Анализ клеток, полученных из пуповины, способом проточной цитометрии позволил установить отличительные особенности данных клеточных линий. Клетки, полученные из ткани пуповины, положительны для CD10, CD13, CD44, CD73, CD90, PDGFr-альфа и HLA-A,B,C; и отрицательны для CD31, CD34, CD45, CD117, CD141 и HLA-DR, DP, DQ. Данные отличительные признаки были стабильными при изменении различных переменных, включая донора, номер пассажа, покрытие поверхности сосуда для культивирования, расщепляющие ферменты и плацентарный слой. Наблюдаются некоторые вариации в средних значениях и диапазонах изменения кривых гистограмм значений флуоресценции, но все положительные кривые при всех исследуемых условиях имели нормальный вид и значения интенсивности флуоресценции, превышающие значения для используемого в качестве контроля IgG, тем самым подтверждая, что клетки представляют собой однородную популяцию с положительной экспрессией маркеров.
ПРИМЕР 7
Анализ клеток при помощи олигонуклеотидных чипов
Для сравнения профилей экспрессии генов клеток, полученных из пуповины и плаценты, с профилями экспрессии для фибробластов, мезенхимальных стволовых клеток человека и другой клеточной линии, полученной из костного мозга человека, применяли олигонуклеотидные чипы. Данный анализ позволил охарактеризовать полученные из постнатального материала клетки и идентифицировать уникальные молекулярные маркеры данных клеток.
Клетки, полученные из ткани постнатального материала. Пуповины и плаценту человека получили в Национальном центре по обмену материалами для исследования заболеваний (NDRI, Филадельфия, штат Пенсильвания) после нормально прошедших родов при доношенной беременности с согласия пациента. Ткани были получены, а клетки выделили способом, описанным в Примере 5, после расщепления смесью C:D:H. Клетки культивировали в ростовой среде на покрытых желатином пластиковых колбах для культивирования тканей. Культуры инкубировали при 37ºC в атмосфере с 5% CO2.
Фибробласты. Фибробласты дермы человека приобрели в компании Cambrex Incorporated (г. Уолкерсвилл, штат Мэриленд; партия № 9F0844) и ATCC CRL-1501 (CCD39SK). Обе линии культивировали в среде DMEM/F12 (Invitrogen, г. Карлсбад, штат Калифорния) с добавлением 10% (об/об) фетальной бычьей сыворотки (Hyclone) и пенициллина/стрептомицина (Invitrogen). Клетки растили на стандартном обработанном тканью пластике.
Мезенхимальные стволовые клетки человека (hMSC). Мезенхимальные стволовые клетки человека (hMSC) приобрели в компании Cambrex Incorporated (г. Уолкерсвилл, штат Мэриленд; партии № 2F1655, 2F1656 и 2F1657) и культивировали в соответствии с рекомендациями производителя в среде MSCGM (Cambrex). Клетки растили на стандартном культивированном тканью пластике при 37°C в атмосфере с 5% CO2.
Клетки костного мозга гребня подвздошной кости человека (ICBM). Костный мозг гребня подвздошной кости человека получили из NDRI с согласия пациента. Костный мозг обработали в соответствии со способом, описанном Ho et al. (международная заявка № WO03/025149). Костный мозг смешивали с лизирующим буферным раствором (155 мМ NH4Cl, 10 мМ KHCO3 и 0,1 мМ ЭДТА, pH 7,2) в соотношении 1 часть костного мозга к 20 частям лизирующего буферного раствора. Клеточная суспензия была перемешана вихревым способом, инкубирована на протяжении 2 минут при окружающей температуре, и центрифугирована на протяжении 10 минут при 500×g. Супернатант был отправлен в отходы и клеточный осадок был ресуспендирован в минимальной полной альфа-среде (Invitrogen), обогащенной 10% (об/об) эмбриональной бычьей сывороткой и 4 мМ глутамина. Клетки еще раз центрифугировали и клеточный осадок повторно суспендировали в свежей среде. Количество жизнеспособных мононуклеарных клеток определили тестом на вытеснение трипанового синего (Sigma, Сент-Луис, штат Миссури). Мононуклеарные клетки высевали в пластиковые колбы для культивирования тканей в количестве 5×104 клеток/см2. Клетки инкубировали при 37°C в атмосфере с 5% CO2 либо в условиях стандартной атмосферы O2, либо 5% O2. Клетки культивировали в течение 5 дней без замены среды. Среду и незакрепившиеся клетки удаляли после 5 дней культивирования. Закрепившиеся клетки поддерживали в культуре.
Активно растущие культуры клеток удаляли из колб при помощи скребка для клеток в холодный фосфатный буферный раствор (PBS). Повторно растворенные клетки центрифугировали (5 минут при 300 x g), супернатант удаляли и клеточный осадок промывали в свежем фосфатном буферном растворе и центрифугировали снова. Супернатант удаляли, а клеточный осадок немедленно замораживали и хранили при температуре -80°C. Клеточную мРНК экстрагировали и выполняли транскрипцию на кДНК. Затем кДНК транскрибировали в кРНК и пометили биотином. Меченую биотином кРНК гибридизировали с олигонуклеотидными чипами Affymetrix GENECHIP HG-U133A (Affymetrix, г. Санта-Клара, штат Калифорния). Гибридизации и сбор данных проводили в соответствии с техническими требованиями производителя. Анализ данных проводили при помощи программного обеспечения версии 1,21 «Достоверность микроматричных анализов» (SAM) (Tusher, V.G. et al., 2001 г., Proc. Natl. Acad. Sci. США 98: 5116-5121). Лицензии для аналитического программного обеспечения можно приобрести в Управлении лицензирования технологий Стэнфордского университета, а более подробную информацию можно получить во всемирной сети на веб-сайте профессора Тибширани с кафедры статистики Стэнфордского университета.
В рамках данного исследования анализу подвергли четырнадцать различных популяций клеток. В Таблице 7-1 перечислены клетки, информация о их пассировании, субстрат для культивирования и питательная среда для культивирования. Клеточные линии перечислены вместе со своими идентификационными номерами, сведениями о пассаже на момент анализа, субстратом для роста клеток и ростовой средой.
Клетки, проанализированные на микрочипах
Данные были оценены при помощи анализа главных компонентов с использованием программного обеспечения SAM описанным выше способом. В ходе анализа выявили 290 генов, которые экспрессировались в исследуемых клетках в различных сравнительных количествах. Данный анализ позволил провести сравнительное сопоставление популяций друг с другом.
В таблице 7-2 представлены евклидовы расстояния, рассчитанные для сравнения клеточных пар. Евклидовы расстояния были основаны на сравнении клеток на основе 290 генов, которые дифференциально экспрессировались в клетках разных типов. Евклидово расстояние обратно пропорционально схожести в экспрессии 290 генов. Евклидово расстояние рассчитывали для видов клеток при помощи 290 генов, которые по-разному экспрессируются в этих видах клеток. Схожесть клеток обратно пропорциональна евклидовому расстоянию.
Евклидовы расстояния для клеточных пар
В таблице 7-3, 7-4 и 7-5 показана экспрессия генов, повышенная в клетках, полученных из плаценты (таблица 7-3), повышенная в клетках, полученных из пуповины (таблица 7-4) и пониженная в клетках, полученных из пуповины и плаценты (таблица 7-5).
Гены со специфически повышенной экспрессией в клетках, полученных из плаценты, по сравнению с другими проанализированными клеточными линиями
Гены, экспрессия которых специфически повышена в клетках, полученных из пуповины, по сравнению с другими проанализированными клеточными линиями
Гены, экспрессия которых специфически снижена в клетках, полученных из пуповины и плаценты, по сравнению с другими проанализированными клеточными линиями
В таблице 7-6, 7-7 и 7-8 показана экспрессия генов, повышенная в фибробластах человека (таблица 7-6), клетках ICBM (таблица 7-7) и клетках MSC (таблица 7-8).
Гены, экспрессия которых повышена в фибробластах человека, по сравнению с другими проанализированными клеточными линиями
Гены, экспрессия которых повышена в клетках ICBM, по сравнению с другими проанализированными клеточными линиями
Гены, экспрессия которых повышена в клетках MSC, по сравнению с другими проанализированными клеточными линиями
Настоящее приблизительное исследование провели для получения молекулярной характеризации клеток, полученных из пуповины и плаценты. Анализ включал клетки, полученные из трех различных пуповин и трех различных плацент. Исследование также включало две различные линии фибробластов дермы, три линии мезенхимальных стволовых клеток и три линии клеток костного мозга гребня подвздошной кости. Экспрессируемую данными клетками мРНК подвергли анализу с использованием олигонуклеотидного чипа GENECHIP, который содержал олигонуклеотидные зонды для 22 000 генов.
Анализ позволил обнаружить транскрипты 290 генов, которые присутствуют в различных количествах в пяти различных видах клеток. Данные гены содержат десять генов, экспрессия которых специфически повышается в клетках, полученных из плаценты, и семь генов, экспрессия которых специфически повышается в клетках, полученных из пуповины. Было обнаружено пятьдесят четыре гена со специфически сниженными уровнями экспрессии в клетках, полученных из плаценты, и клетках, полученных из ткани пуповины.
ПРИМЕР 8
Иммуногистохимическая характеризация клеточных фенотипов
Провели иммуногистохимический анализ фенотипов клеток, обнаруженных в ткани пуповины человека.
Ткань человеческой пуповины была собрана и зафиксирована погружением в 4% (об/об) раствор параформальдегида в течение ночи при температуре 4°C; иммуногистохимический анализ проводили с использованием антител, направленных на следующие эпитопы (см. таблицу 8-1): виментин (1:500; Sigma, г. Сент-Луис, штат Миссури), дезмин (1:150, выработанные на кролика; Sigma; или 1:300, выработанные на мышь; Chemicon, г. Темекула, штат Калифорния), альфа-актин гладких мышц (SMA; 1:400; Sigma), цитокератин 18 (CK18; 1:400; Sigma), фактор фон Виллебранда (vWF; 1:200; Sigma) и CD34 (CD34 человека, класс III; 1:100; DAKOCytomation, г. Карпинтерия, штат Калифорния). Кроме того, проверили следующие маркеры: анти-человеческий GROальфа - PE (1:100; Becton Dickinson, г. Франклин Лейкс, штат Нью-Джерси), анти-человеческий GCP-2 (1:100; Santa Cruz Biotech, г. Санта-Круз, штат Калифорния), анти-рецептор 1 окисленных ЛПНП человека (ox-LDL R1; 1:100; Santa Cruz Biotech) и анти-человеческий NOGO-A (1:100; Santa Cruz Biotech). Зафиксированные образцы обрезали скальпелем и поместили в заливочный состав OCT (Tissue-Tek OCT; Sakura, г. Торранс, штат Калифорния) на баню из сухого льда с этанолом. Затем замороженные блоки нарезали на срезы толщиной 10 мкм с использованием стандартного криостата (Leica Microsystems) и установили на предметные стекла для окрашивания.
Иммуногистохимический анализ провели аналогично предыдущим исследованиям. (E.g., Messina et al., Exper. Neurol., 2003; 184: 816-829). Срезы тканей промывали фосфатно-солевым буфером (ФСБ) и обрабатывали белковым блокирующим раствором, содержащим ФСБ, 4% (об/об) козьей сыворотки (Chemicon, г. Темекула, штат Калифорния) и 0,3% (об/об) Тритона (Triton X-100; Sigma) в течение 1 часа для доступа к внутриклеточным антигенам. Когда рассматриваемый эпитоп находился на клеточной поверхности (CD34, ox-LDL R1), тритон исключали на всех стадиях процедуры, чтобы не допустить потери эпитопа. Кроме того, когда первичное антитело было выработано на козу (GCP-2, oкс-LDL R1, NOGO-A), в течение всей процедуры вместо козьей сыворотки применяли 3% (об/об) ослиную сыворотку. Затем срезы обрабатывали в течение 4 часов при комнатной температуре первичными антителами, разбавленными в блокирующем растворе. Растворы первичных антител удаляли и промывали культуры ФСБ перед добавлением растворов вторичных антител (1 час при комнатной температуре), содержащих блокирующий раствор вместе с конъюгатом козьего антимышиного IgG - Texas Red (1:250; Molecular Probes, г. Евген, штат Орегон) и (или) конъюгатом козьего антикроличьего IgG - Alexa 488 (1:250; Molecular Probes) или конъюгатом ослиного анти-козьего IgG – FITC (1:150; Santa Cruz Biotech). Культуры промывали и обрабатывали 10-микромолярным раствором DAPI (Molecular Probes) в течение 10 минут для визуализации клеточных ядер.
После иммунного окрашивания получали флуоресцентные изображения с использованием соответствующего фильтра для флуоресценции на инвертированном эпи-флуоресцентном микроскопе (Olympus, Мелвилл, штат Нью-Йорк). Положительное окрашивание представляло собой флуоресцентный сигнал выше сигнала окрашивания контроля. Показательные изображения получали с использованием цветной цифровой видеокамеры и программного пакета ImagePro (Media Cybernetics, Карлсбад, штат Калифорния). Для образцов с тройным окрашиванием каждое изображение получали с использованием только одного фильтра на эмиссию. Затем получали послойные монтажи с использованием программного обеспечения Adobe Photoshop (Adobe, г. Сан-Хосе, штат Калифорния).
Обзор примененных первичных антител
Маркеры виментин, дезмин, SMA, CK18, vWF и CD34 экспрессировались подмножеством клеток, присутствующих в пуповине (данные не приведены). В частности, экспрессия vWF и CD34 ограничивалась кровеносными сосудами, находящимися внутри пуповины. Клетки CD34+ находились на самом внутреннем слое (со стороны просвета). Экспрессию виментина обнаружили по всему матриксу и кровеносным сосудам пуповины. Экспрессия SMA ограничивалась матриксом и внешними стенками артерии и вены, но не проходила внутри самих сосудов. CK18 и дезмин наблюдали только внутри сосудов, причем экспрессия дезмина ограничивалась только средними и внешними слоями.
Ни один из данных маркеров не обнаружили в ткани пуповины (данные не приведены).
Маркеры виментин, дезмин, альфа-актин гладких мышц, цитокератин 18, фактор фон Виллебранда и CD 34 экспрессируются в клетках пуповины человека. На основании исследований, посвященных характеризации in vitro, было показано, что экспрессируются только виментин и альфа-актин гладких мышц, причем данные свидетельствуют о том, что текущий процесс выделения клеток из пуповины приводит к созданию субпопуляции клеток или что в выделенных клетках изменяется экспрессия маркеров, вследствие чего в клетках начинают экспрессироваться виментин и альфа-актин гладких мышц.
Пример 9
Секреция трофических факторов
Измерялась секреция выбранных трофических факторов в клетках UTC. Факторы были выбраны исходя из их ангиогенной активности, например, фактор роста гепатоцитов (HGF) (Rosen et al., Ciba Found. Symp., 1997 г.; 212:215-26), моноцитарный хемотаксический фактор 1 (MCP-1) (Salcedo et al., Blood, (2000 г.; 96:34-40), интерлейкин-8 (IL-8) ( Li et al., J. Immunol., 2003 г.; 170:3369-76), фактор роста кератиноцитов (KGF), основной фактор роста фибробластов (bFGF), фактор роста эндотелия сосудов (VEGF) (Hughes et al., Ann. Thorac. Surg. 2004 г., 77:812-8), тканевой ингибитор матриксной металлопротеазы 1 (TIMP1), ангиопоэтин 2 (ANG2), фактор роста тромбоцитов (PDGFbb), тромбопоэтин (TPO), связывающийся с гепарином эпидермальный фактор роста (HB-EGF),фактор стромального происхождения 1 альфа (SDF-1 альфа),факторы с известной нейротрофической/нейропротекторной активностью (нейротрофический фактор головного мозга (BDNF) (Cheng et al., Dev. Biol., 2003 г.; 258:319-33), интерлейкин-6 (IL-6), гранулоцитарный хемотаксический белок 2 (GCP-2), трансформирующий фактор роста бета 2(TGFbeta2); и ли факторы с известной хемокиновой активностью, такие как макрофагальный белок воспаления 1 альфа (MIP1alpha), макрофагальный белок воспаления 1 бета (MIP1beta), моноцитарный хемоатрактантный белок-1 (MCP-1), Rantes (хемокин, экспрессируемый и выделяемый нормальными T-клетками при активации), I309, выделяемый при активации хемокин тимуса (TARC), эотаксин, хемокин макрофагов (MDC), IL-8.
Клетки, полученные из ткани пуповины, а также фибробласты человека, полученные из неонатальной крайней плоти человека, культивировали в ростовой среде в покрытых желатином колбах T75. На пассаже 11 клетки криоконсервировали и замораживали в жидком азоте. После размораживания в клетки добавляли ростовую среду, переносили их в пробирку для центрифугирования объемом 15 мл и центрифугировали при 150×g в течение 5 минут. Клеточный осадок ресуспендировали в 4 миллилитрах ростовой среды, после чего клетки подсчитывали. Клетки высевали в количестве 5000 клеток/см2 в колбы T75, каждая из которых содержала 15 мл ростовой среды, и культивировали в течение 24 часов. Среду меняли на бессывороточную среду (DMEM с низким содержанием глюкозы (Gibco), 0,1% (масса/об) альбумин бычьей сыворотки (Sigma), пенициллин (50 Ед/мл) и стрептомицин (50 мкг/мл) (Gibco)) и культивировали в течение 8 часов. В конце инкубации кондиционированную бессывороточную среду собрали центрифугированием при 14000×g в течение 5 минут и хранили при температуре -20°C.
Для определения количества клеток в каждой колбе клетки были промыты в фосфатном буферном растворе (ФБР) и отделены при помощи 2 мл трипсина/ЭДТА (Gibco). Активность трипсина ингибировали добавлением 8 миллилитров ростовой среды. Клетки центрифугировали при 150×g в течение 5 минут. Супернатант удалили, а клетки ресуспендировали в 1 миллилитре ростовой среды. Количество клеток устанавливали при помощи гемоцитометра.
Клетки выращивали при температуре 37°C в присутствии 5% CO2 и атмосферной концентрации кислорода. Количество MCP-1, IL-6, VEGF, SDF-1-альфа, GCP-2, IL-8 и TGF-бета-2, вырабатываемое каждым образцом клеток, определяли способом твердофазного иммуноферментного анализа (ИФА) (R&D Systems, г. Миннеаполис, штат Миннесота). Все анализы проводили в соответствии с инструкциями производителя. Представленные значения выражены в пикограммах на мл на миллион клеток (n=2, сканирующая электронная микроскопия).
Хемокины (MIP1alpha, MIP1beta, MCP-1, RANTES, I309, TARC, Eotaxin, MDC, IL8), BDNF и ангиогенные факторы (HGF, KGF, bFGF, VEGF, TIMP1, ANG2, PDGFbb, TPO, HB-EGF) были измерены с помощью SearchLight Proteome Arrays (Pierce Biotechnology Inc.). Протеомные массивы представляют собой мультиплексные твердофазные иммуноферментные сэндвич-системы для количественного определения от 2 до 16 белков на лунку. Массивы получают, нанося матрицу 2×2, 3×3 или 4×4 разных антител захвата в каждую лунку 96-луночного планшета. После проведения процедуры сэндвич-ИФА снимают изображение всего планшета для получения сигнала хемилюминесценции, генерируемого в каждой точке матрицы в каждой лунке планшета. Сигнал, генерируемый в каждой точке матрицы, пропорционален количеству целевого белка в исходном стандартном или анализируемом образце.
MCP-1 и IL-6 секретировались клетками PPDC, полученными из ткани пуповины, и фибробластами дермы (таблица 9-1). SDF-1-альфа и GCP-2 секретировались фибробластами. GCP-2 и IL-8 секретировались клетками PPDC, полученными из ткани пуповины. При использовании анализа ИФА во всех видах клеток не обнаружили TGF-бета-2.
Результаты анализа ИФА: обнаружение трофических факторов
Мультиплексный анализ ИФА Searchlight™. TIMP1, TPO, KGF, HGF, FGF, HBEGF, BDNF, MIP1beta, MCP1, RANTES, I309, TARC, MDC и IL-8 секретировались клетками, полученными из пуповины (таблицы 9-2 и 9-3). Ang2, VEGF или PDGFbb не были обнаружены.
Результаты мультиплексного анализа ИФА Searchlight™
Результаты мультиплексного анализа ИФА Searchlight™
Клетки, полученные из пуповины, секретируют множество трофических факторов. Некоторые из данных трофических факторов, такие как HGF, bFGF, MCP-1 и IL-8, играют важную роль в ангиогенезе. Другие трофические факторы, такие как BDNF и IL-6, играют важную роль в регенерации или защите нервной ткани.
ПРИМЕР 10
Анализ теломеразной активности
Функция теломеразы состоит в синтезе теломерных повторов, которые защищают целостность хромосом и продлевают репликативно-активную жизнь клеток (Liu, et al., PNAS, 1999 г.; 96:5147-5152). Теломераза состоит из двух компонентов - теломеразного РНК-шаблона (hTER) и теломеразной обратной транскриптазы (hTERT). Регулирование теломеразы определяется транскрипцией hTERT, но не hTER. Таким образом, полимеразная цепная реакция (ПЦР) в реальном времени для мРНК hTERT является общепринятым способом определения теломеразной активности клеток.
Выделение клеток
Для определения выработки теломеразы в клетках, полученных из ткани пуповины человека, провели эксперименты по ПЦР в реальном времени. Клетки, полученные из ткани пуповины человека, были подготовлены в соответствии с приведенными выше примерами, а также примерами, изложенными в патенте США № 7510873. По существу, пуповины, полученные в Национальном центре по обмену материалами для исследования заболеваний (NDRI, г. Филадельфия, штат Пенсильвания) после нормально прошедших родов, промывали для удаления крови и продуктов распада клеток и механически диссоциировали. Ткань затем инкубировалась с расщеплением ферментов, включая коллагеназу, диспазу и гиалуронидазу в культуральной среде при температуре 37°C. Клетки, полученные из ткани пуповины человека были культивированы в соответствии с способами, описанными в примерах заявки '012. Мезенхимальные стволовые клетки и нормальные фибробласты дермы кожи (cc-2509 партия № 9F0844) получили от компании Cambrex, г. Уолкерсвилль, штат Мэриленд. Плюрипотентные клетки nTera-2 клеточной линии тестикулярной эмбриональной карциномы (тератомы) (NTERA-2 cl.Dl) (см. работу et al., Stem Cells, 2006 г.; 24(3): 531–546) приобрели из коллекции ATCC (г. Манассас, штат Вирджиния) и культивировали в соответствии с способами, описанными в патенте США №7510873.
Выделение всей РНК
РНК экстрагировали из клеток при помощи набора RNeasy® (Qiagen, г. Валенсия, штат Калифорния). РНК элюировали с 50 микролитрами обработанной DEPC воды и хранили при температуре –80°C. Обратную транскрипцию РНК проводили с использованием случайных гексамеров, применяя реагенты для обратной транскрипции TaqMan® (Applied Biosystems, г. Фостер Сити, штат Калифорния) при 25°C в течение 10 минут, при 37°C в течение 60 минут и при 95°C в течение 10 минут. Образцы хранились при -20°C.
ПЦР в реальном времени
ПЦР проводили на образцах кДНК с использованием продуктов для экспрессии генов Assays-on-Demand™ компании Applied Biosystems (также известные как наборы для определения экспрессии генов TaqMan®) в соответствии с инструкциями производителя (Applied Biosystems). Данный доступный в продаже набор широко применяют для анализа клеток человека на теломеразу. Вкратце, hTert (ген теломеразы человека) (Hs00162669) и GAPDH человека (внутренний контроль) смешивали с кДНК и универсальным мастер-миксом для ПЦР TaqMan®, при этом использовали секвенатор 7000 с программным обеспечением ABI Prism 7000 SDS (Applied Biosystems). Использовали следующие условия термоциклирования: сначала 50°C в течение 2 минут и 95°C в течение 10 минут, затем 40 циклов по 95°C в течение 15 секунд и 60°C в течение 1 минуты. Данные ПЦР анализировали в соответствии с рекомендациями производителя.
Клетки, полученные из ткани пуповины человека (номер доступа ATCC PTA-6067), фибробласты и мезенхимальные стволовые клетки анализировали на hTert и 18S РНК. Как показано в таблице 10-1, hTert и, следовательно, теломеразу не обнаружили в клетках, полученных из ткани пуповины человека.
Проанализировали клетки, полученные из ткани пуповины человека (изолят 022803, номер доступа ATCC PTA-6067), и клетки nTera-2, и результаты показали отсутствие экспрессии теломеразы в двух партиях клеток, полученных из ткани пуповины человека, тогда как клеточная линия тератомы экспрессировала теломеразу на высоком уровне (таблица 10-2).
Следовательно, можно сделать вывод о том, что клетки, полученные из ткани пуповины человека, которые составляют предмет настоящего изобретения, не экспрессируют теломеразу.
ПРИМЕР 11
Выращивание клеток UTC на микроносителя в импеллерном реакторе в центрифужных пробирках
Материалы и способы
Клетки. Клетки из партии CBAT lot# 050604B пассаж 8 были разморожены и посеяны в пробирку Т225 на один пассаж.
Микроносители
Шариковые микроносители Cytodex® 3 (GE Healthcare Life Sciences, номер в каталоге 17-0485) гидрировали в фосфатно-солевом растворе на протяжении по меньшей мере 3 часов и обработали в автоклаве.
Центрифужные пробирки
Центрифужные пробирки с системой внутренней вращающейся лопасти емкостью 100 мл и 250 мл (Bellco, Inc.).
Конфлюэнция
Конфлюэнция определена как приблизительно 90% микроносителей, наблюдаемых в репрезентативном поле микроносителей, у которых более чем приблизительно 60% поверхности покрыто клетками.
Пассаж
Пассаж определен как засевание центрифужной пробирки, содержащей свежие микроносители с аликвотой конфлюэнтых микроносителей, полученных из отдельной центрифужной пробирки с культурой.
Посев и культура
Клетки были собраны из пробирок Т225 с помощью трипсина и 4,0E+06 клеточных аликвот были добавлены к 330 мг шариковых микроносителй в 100 мл импеллерную или стеклянную палочковую центрифужную пробирку, содержащую 40 мл среды. Пробирки были промыты 5% CO2 газом на протяжении одной минуты перед инкубацией. Скорость/частота инокуляции составляла 30 об/мин на протяжении 2 минут каждые 30 минут на протяжении 8 часов. Через восемь часов объем среды был увеличен да 100 мл и скорость вращения была установлена на 45 об/мин постоянной ротации, инкубация проводилась при температуре 37°C.
Пассаж
Пассаж 1- (из пробирки емкостью 100 мл в 250 мл) клетки культивировали на протяжении восьми дней. Все микроносители из 100 мл пробирки собрали и позволили отделиться от среды под воздействием гравитации. Среда была аспирирована и микроносители были ресуспендированы в 10 мл свежей среды. После пипетирования для обеспечения равномерного распространения, 5 мл среды с микроносителями удалили и поместили в центрифужную пробирку емкостью 250 мл. Также добавили приблизительно 660 мг свежей гидрированных и обработанных в автоклаве микроносителей Cytodex® 3 и среды. Объем среды увеличили до 200 мл и промыли пробирки 5% СО2 газа в течение одной минуты перед инкубацией. Скорость центрифуги была установлена на 45 об/мин постоянного вращения, инкубация проводилась при температуре 37ºC. Оставшиеся клетки собрали путем трипсинизации и подсчитали с помощью прибора Guava PCA (Guava Technologies, Hayward, CA).
Пассаж 2- (из пробирки емкостью 250 мл в 250 мл) клетки культивировали на протяжении шести дней. Все микроносители из 250 мл пробирки собрали и позволили отделиться от среды под воздействием гравитации. Среда была аспирирована и микроносители были ресуспендированы в 25 мл свежей среды. После пипетирования для обеспечения равномерного распространения, 5 мл среды с микроносителями удалили и поместили в центрифужную пробирку емкостью 250 мл. Также добавили приблизительно 660 мг свежей гидрированных и обработанных в автоклаве микроносителей Cytodex® 3 и среды. Объем среды увеличили до 200 мл и промыли пробирки 5% СО2 газа в течение одной минуты перед инкубацией. Скорость центрифуги была установлена на 45 об/мин постоянного вращения, инкубация проводилась при температуре 37ºC. Оставшиеся клетки собрали путем трипсинизации и подсчитали с помощью прибора Guava PCA.
Замена среды
Центрифужные пробирки удалили из культуры и микроносителям позволили осесть под воздействием гравитации на дно пробирки. Приблизительно половина объема среды была удалена путем аспирации и заменена равным объемом свежей среды. Пробирки были промыты 5% CO2 газом на протяжении одной минуты и возвращены в культуру. Замена среды производилась в день 1 и день 4.
Проверка жизнеспособности путем окрашивания 1 мл аликвоты удалили из пробирки и микроносителям позволили осесть под воздействием гравитации. Среду удалили путем аспирации и заменили 1 мл живые/мертвые красящего раствора (Молекулярные Зонды, номер в каталоге L3224) и инкубировали на протяжении 15 минут при температуре 37°C. После инкубации 20 микролитров аликвоты поместили на стеклянный слайд для микроскопа и исследовали способом флуоресцентной микроскопии. Живые клетки окрашиваются в зеленый цвет, мертвые клетки окрашиваются в красный. Микроскопические поля были проанализированы вручную для оценки распространения и соотношения живых и мертвых клеток, закрепленных на микроносителях. Было оценено по меньшей мере три микроскопических поля и был осуществлен подсчет приблизительного процентного содержания жизнеспособных клеток.
Урожай клеток. Микроносители были собраны из центрифужных пробирок, три раза промыты фосфатно-солевым буфером и равномерно распределены между двумя коническими пробирками емкостью 50 мл. Каждая пробирка были инкубирована с 25 мл трипсина на протяжении 10 минут при температуре 37°C. Объем содержимого пробирок был дополнен до 50 мл фосфатно-солевым буфером и микроносителям позволили осесть под воздействием гравитации. Супернатант, содержащий клетки, был собран путем аспирации и перенесен в конические пробирки емкостью 50 мл, предварительно наполненных 2,5 мл эмбриональной бычьей сыворотки (введение 5% раствора эмбриональной бычьей сыворотки с целью инактивации трипсина). Этот процесс был повторен четыре раза, с каждой собранной фракцией отдельно. Все собранные клетки были центрифугированы, ресуспендированы в сыворотке, содержащей ростовую среду, и клетки были подсчитаны путем применения прибора Guava PCA.
Статичная культура в Т-пробирке
Клеточные аликвоты, собранные из пробирки Т225, были использованы для засева двух пробирок Т225 и инкубировались на протяжении четырех дней с применением способов, указанных в заявке на патент США № 10/877012. Клетки были собраны и проанализированы с помощью проточной цитометрии.
Проточная цитометрия
Собранные клетки были проанализированы способом проточной цитометрии с применением прибора Becton-Dickinson FACSCalibur™ (Becton Dickinson, ан-Хосе, Калифорния) для определения профиля поверхностного маркера клеток. Все антитела был приобретены в BD PharMingen (San Diego, CA).
Результаты
Урожай клеток
Таблица 11-1 показывает фракции урожая, образование клеток и жизнеспособность на пассаж от клеточной линии UTC 050604B, размножавшейся от пассажа 9 до пассажа 11 на микроносителях Cytodex® 3 в культурах центрифужных пробирок.
Урожай клеток
Клеточная кинетика
Таблица 11-2 показывает кинетику роста клеток клеточной линии UTC 050604B, размножавшейся от пассажа 9 до пассажа 11 на микроносителях Cytodex® 3 в культурах центрифужных пробирок. Таблица показывает, что общее удвоение составляло 7,48 и среднее количество часов на удвоение составляло 69,53 (± 17,52) часов.
Клеточная кинетика
Живые/мертвые окрашивание
Анализ живые/мертвые окрашенных аликвот микроносителей показывает, что большая часть поверхности микроносителей покрыта окрашенными в зеленый цвет (жизнеспособными) клетками с небольшим очагами окрашенных красным клеточных ядер (мертвых). Клетки демонстрируют морфологию, аналогичную морфологии клеток, культивированных в статических условиях.
Анализ способом проточной цитометрии: Таблица 11-3 показывает результаты («+ положительный» или «- отрицательный») для маркеров клеточной поверхности, экспрессированные клетками, извлеченными из пуповины человека (hUTC), собранными с микроносителей в центрифужных пробирках в сравнении с hUTC, собранным с культуры в статических Т-пробирках. Таблица показывает, что маркеры, экспрессированные клетками, произведенными двумя способами, были соответствующими.
Сравнение экспрессии клеточных поверхностных белков клетками Umb 050604B, размножавшихся в статичных Т-пробирках или на микроносителях Cytodex® 3 в центрифужных пробирках и проанализированных путем проточной цитометрии
Заключение: Клетки, извлеченные из тканей пуповины человека (hUTC) были культивированы на микроносителях Cytodex® 3 в импеллерных биореакторах с центрифужными пробирками. Клетки достигли 7,48 удвоений популяции на протяжении двадцати дней и обладали средним временем удвоения популяции 69 часов. Жизнеспособность клеток на пассаж варьировала от 94,4% до 99,7%. Анализ экспрессии тринадцати маркеров клеточной поверхности клеток hUTC, культивированных на микроносителях, соответствовал экспрессии маркеров клеточной поверхности hUTC, культивированных в Т-пробирках. Этот пример показывает, что микроносители могут использоваться для посева, размножения и сбора урожая клеток hUTC в биореакторных системах.
Пример 12
Выращивание размножающихся клеток hUTC на покрытых коллагеном микроносителях MGSA и PLGA в центрифужных пробирках
Была исследована способность клеток hUTC закрепляться на материалах, изготовленных из синтетических способных к рассасыванию биоматериалах с коллагенным покрытием, в том числе способность сохранения жизнеспособности в культуре в центрифужных пробирках и пролиферации при пересеве в статичную культуру. Размножившиеся клетки hUTC были посеяна на покрытые коллагеном или не покрытые поли-(D, L-лактид-ко-глюколид) (PLGA) и поли(моностеароилглицерид ко-янтарная кислота) (MGSA) микроносители. Микроносители с клетками были культивированы в центрифужных пробирках на протяжении пяти дней, собраны путем трипсинизации и пересеяны в статичные культуры.
Материалы и способы
Микроносители
Подготовка микроносителя. Увлажнение микроносителей - приблизительно по 1 мг микроносителей MGSA и PLGA были асептически суспендированы в 25 мл 70% этанола на 30 минут для увлажнения микроносителей. Этанол был удален путем аспирации и микроносители были затем промыты три раза фосфатно-солевым буфером и ресуспендированы в 25 мл фосфатно-буферном солевом растворе Дульбекко.
Покрытие коллагеном. Увлажненные микроносители были осажены путем центрифугирования, фосфатно-солевой буфер был удален путем аспирации и микроносители были ресуспендированы в 2,9% растворе коллагена (Vitrogen 1000, Cohesion, Inc. Palo Alto, CA). Микроносители инкубировали в коллагене в течение 30 минут. Остаточный коллаген был удален путем аспирации и покрытые коллагеном микроносители были промыты фосфатно-солевым буфером три раза.
Количества использованных микроносителей
Посев и культивирование Материалы, типы клеток, ростовая среда, центрифужные пробирки, посев и условия культивирования, замена среды, окрашивание жизнеспособных клеток и способы сбора урожая, примененные в примере 11, были применены в данном примере.
Результаты
Урожай клеток
Пересев урожая клеток Клетки, собранные с покрытых и непокрытых микроносителей MGSA и PLGA были повторно засеяны в пробирки Т225 с плотностью приблизительно 5000 клеток/см2. Через четыре дня после пересева клетки, собранные с обоих материалов, пролиферировали до свыше 50% конфлюэнции.
Размножившиеся клетки hUTC были высеяны на покрытые коллагеном микроносители PLGA и MGSA, культивированы в центрифужных пробирках на протяжении пяти дней, собраны путем трипсинизации и пересеяны в статичные культуры. Клетки, собранные с синтетических микроносителей, были жизнеспособны свыше 90%. Пересеянные клетки размножались в статичной культуре на протяжении четырех дней, демонстрируя сохранение способности к пролиферации. Этот пример демонстрирует возможность применения синтетических биоматериалов в качестве микроносителей в культуре центрифужных пробирок.
Пример 13
Размножение клеток hUTC на микроносителях в длительной культуре в центрифужных пробирках
Целью данного исследования было культивировать продолжительное время размножившиеся клетки hUTC, закрепленные на коммерческих микроносителях в центрифужных пробирках путем множественных удвоений популяции. Возможность размножать клетки hUTC на микроносителях путем множественных удвоений популяции послужит моделью системы для масштабирования до крупномасштабного производства клеток hUTC для применения в клеточной терапии. Оценивались два изолята клеток hUTC, 120304 - выделенные, размноженные и криосохраненные в условиях исследования и CNTO 2476 - выделенные, размноженные и криосохраненные в условиях GMP. Были также оценены коммерческие микроносители Cytodex® 1 или Hillex® II. Криосохраненные клетки были разморожены и сразу же использованы для инокуляции культур в центрифужные пробирки. Клетки длительное время культивировались с множественными пассажами до достижения клетками приблизительного удвоения популяции 30. Клетки hUTC также культивировались статично в пробирках Т225 в качестве контроля.
hUTC изолят 120304, криосохраненный на удвоении популяции 12,8 был способен к размораживанию и размножению на микроносителях Cytodex® 1 и Hillex® II до удвоения популяции 28,6 и 28,7 соответственно. Часы на удвоение популяции соответствовали от пассажа к пассажу, отмечая стабильный логарифмический рост и соответствовали кинетике роста в Т-пробирках. hUTC изолят CNTO 2476, криосохраненный на удвоении популяции 22,6 был способен к размораживанию и размножению на микроносителях Cytodex® 1 и Hillex® II до удвоения популяции 33,2 и 31,0 соответственно. Часы на удвоение популяции соответствовали от пассажа к пассажу, отмечая стабильный логарифмический рост и соответствовали кинетике роста в Т-пробирках. Статистический анализ путем одностороннего ANOA всех данных о часах на удвоение популяции указывает на отсутствие значимой разницы в кинетике роста hUTC во всех протестированных условиях. (p=0,988). Экспрессия белка клеточной поверхностью оставалась соответствующей при финальном сборе урожая для всех протестированных условий.
Этот пример демонстрирует способность клеток hUTC размножаться до приблизительно 30 удвоений популяции на микроносителях в стабильном, согласованном режиме, при котором остается неизменным фенотип белка клеточной поверхности.
Материалы и способы
Клетки
Были использованы криосохраненный размноженный hUTC изолят 12034, удвоение популяции (PD) 12 и hUTC CNTO 2476 лот 25126078 PD 22.
Ростовая среда
Модифицированная среда Игла Дульбекко (DMEM) с низким содержанием глюкозы (Gibco- Grand Island, NY), 15% эмбриональной бычьей сыворотки (HyClone- Logan UT), пенициллин/стрептомицин (P/S) (Gibco- Grand Island, NY), бетамеркаптоэтанол (BME) (Sigma- St. Louis, MO).
Микроносители
Микроносители Cytodex® 1 (GE Health Sciences- Piscataway, NJ) гидрировали в фосфатно-солевом буфере на протяжении по меньшей мере 3 часов и обработали в автоклаве. Микроносители Cytodex® 1 применялись в концентрации 3 г/л. Микроносители Hillex® II (SoloHill Engineering, Inc., Ann Arbor, MI) были гидрированы в деионизированной воде по меньшей мере 30 минут и обработаны в автоклаве. Микроносители Hillex® II применялись в концентрации 12 г/л.
Центрифужные пробирки
Применялись одноразовые центрифужные пробирки емкостью 100 мл и 500 мл (Corning, Inc.- Corning, NY).
Посев и культивирование в центрифужной пробирке емкостью 100 мл. Криосохраненные флаконы с клетками hUTC были разморожены, промыты и ресуспендированы в ростовой среде. 6,6×106 hUTC были добавлены к 3000 мг микроносителей Cytodex® 1 (5,0×103 клеток на см2) в центрифужной пробирке емкостью 100 мл, содержащей 100 мл среды и помещены в инкубатор тканевых культур при температуре 37°C, и инкубировались на протяжении от трех до четырех дней. Вращающаяся платформа была установлена на 60 об/мин непрерывного вращения. 3,1×106 hUTC были добавлены к 1,2 г микроносителей Hillex® II (5,0×103 клеток на см2) в центрифужной пробирке емкостью 100 мл, содержащей 100 мл среды и помещены на вращающуюся платформу, установленную на 60 об/мин непрерывного вращения. Вращающиеся платформы были помещены в 5% СО2.
Пассаж культуры из одной центрифужной пробирки емкостью 100 мл в одну центрифужную пробирку емкостью 500 мл. Центрифужная пробирка емкостью 100 мл была удалена с вращающейся платформы и микроносителям позволили осесть. Супернатант среды удалили путем аспирации. Оставшиеся микроносители с прикрепленными клетками были ресуспендированы в 20 мл свежей ростовой среды. Микроносители с прикрепленными клетками были затем перенесены пипеткой в асептических условиях в центрифужную пробирку емкостью 500 мл, содержащую 480 мл свежей ростовой среды и 4,8 микроносителей Hillex® II (6 г финальной составляющей микроносителей) или 1,2 г Cytodex® 1 (1,5 г финальной составляющей микроносителей). Затем центрифужную пробирку поместили на вращающуюся платформу, установленную на 60 об/мин непрерывного вращения. Вращающиеся платформы поместили в инкубаторы тканей при 5% CO2 и температуре 37ºC и инкубировали на протяжении от трех до четырех дней.
Пассаж культуры из одной центрифужной пробирки емкостью 500 мл в пять центрифужных пробирок емкостью 500 мл. Центрифужная пробирка емкостью 500 мл была удалена с вращающейся платформы и микроносителям позволили осесть. Супернатант среды удалили путем аспирации. Оставшиеся микроносители с прикрепленными клетками были ресуспендированы в 50 мл свежей ростовой среды. Пять отдельных аликвот по 10 мл микроносителей с прикрепленными клетками были затем перенесены пипеткой в асептических условиях в пять отдельных центрифужных пробирок емкостью 500 мл, каждая из которых содержит 490 мл свежей ростовой среды и 4,8 микроносителей Hillex® II (6 г финальной составляющей микроносителей) или 1,2 г Cytodex® 1 (1,5 г финальной составляющей микроносителей). Затем центрифужные пробирки поместили на вращающуюся платформу, установленную на 60 об/мин непрерывного вращения. Вращающиеся платформы поместили в инкубаторы тканей при 5% CO2 и температуре 37ºC и инкубировали на протяжении от трех до четырех дней.
Сбор клеток, прикрепленных к микроносителям Cytodex® 1 Центрифужная пробирка емкостью 500 мл была удалена с вращающейся платформы и микроносителям с прикрепленными клетками позволили осесть под воздействием гравитации. Супернатант среды удалили путем аспирации. В центрифужную пробирку добавили 500 мл фосфатно-солевого буфера и позволили микроносителям осесть под воздействием гравитации. Супернатант фосфатно-солевого буфера удалили путем аспирации. В центрифужную пробирку добавили 500 мл среды DMEM с низким содержанием глюкозы. Затем центрифужную пробирку инкубировали на вращающейся платформе на протяжении 20 минут при скорости вращения 60 об/мин. Центрифужная пробирка мл была удалена с вращающейся платформы и микроносителям позволили осесть под воздействием гравитации. Супернатант среды DMEM с низким содержанием глюкозы удалили путем аспирации. В центрифужную пробирку добавили 500 мл фосфатно-солевого буфера. Затем центрифужную пробирку инкубировали на вращающейся платформе на протяжении 20 минут при скорости вращения 60 об/мин. Центрифужная пробирка мл была удалена с вращающейся платформы и микроносителям позволили осесть под воздействием гравитации. Супернатант фосфатно-солевого буфера удалили путем аспирации. В центрифужную пробирку добавили 250 мл выборки TrypLE. Затем центрифужную пробирку инкубировали на вращающейся платформе на протяжении 10 минут при скорости вращения 60 об/мин. Центрифужная пробирка мл была удалена с вращающейся платформы и микроносителям позволили осесть под воздействием гравитации. Путем применения серологической пипетки емкостью 50 мл раствор микроносителей-выборки TrypLE™ был смешан путем пипетирования вверх и вниз ~10 раз для отделения остаточных прикрепленных клеток от микроносителей. Затем в центрифужную пробирку добавили 250 мл фосфатно-солевого буфера и позволили микроносителям осесть под воздействием гравитации. Супернатант, содержащий клетки, собирают путем повторного пипетирования и переносят в многочисленные конические пробирки, предварительно наполненные 5 мл эмбриональной бычьей сыворотки; в просвет пробирки помещен фильтр с размером ячеек 100 микрон. Пробирки ценрифугировали на протяжении 5 минут при 300 rcf, супернатант отцедили и клетки ресуспендировали в ростовой среде.
Сбор клеток, прикрепленных к микроносителям Hillex® II Центрифужная пробирка емкостью 500 мл была удалена с вращающейся платформы и микроносителям с прикрепленными клетками позволили осесть под воздействием гравитации. Супернатант среды удалили путем аспирации. В центрифужную пробирку добавили 500 мл фосфатно-солевого буфера и позволили микроносителям осесть под воздействием гравитации. В центрифужную пробирку добавили 100 мл выборки TrypLE. Затем центрифужную пробирку инкубировали на вращающейся платформе на протяжении 10 минут при скорости вращения 60 об/мин. Центрифужная пробирка мл была удалена с вращающейся платформы и микроносителям позволили осесть под воздействием гравитации. Путем применения серологической пипетки емкостью 25 мл раствор микроносилей-выборки TrypLE™ был смешан путем пипетирования вверх и вниз ~10 раз для отделения остаточных прикрепленных клеток от микроносителей. Супернатант, содержащий клетки, собирают путем повторного пипетирования и переносят в многочисленные конические пробирки, предварительно наполненные 5 мл эмбриональной бычьей сыворотки; в просвет пробирки помещен фильтр с размером ячеек 100 микрон. Пробирки ценрифугировали на протяжении 5 минут при 300 rcf, супернатант отцедили и клетки ресуспендировали в ростовой среде.
Проверка жизнеспособности путем окрашивания 1 мл аликвот среды и микроносителей перенесли в коническую пробирку емкостью 15 мл и микроносителям позволили отделиться под воздействием гравитации. Среду удалили путем аспирации и заменили 1 мл живые/мертвые красящего раствора (Молекулярные Зонды, номер в каталоге L3224) и инкубировали на протяжении 15 минут при температуре 37º C. После инкубации 20 микролитров аликвоты поместили на стеклянный слайд для микроскопа и исследовали способом флуоресцентной микроскопии. Живые клетки окрашиваются в зеленый цвет. Микроскопические поля были проанализированы вручную для оценки распространения живых клеток, закрепленных на микроносителях. Было оценено по меньшей мере три микроскопических поля и был осуществлен подсчет приблизительного процентного содержания жизнеспособных клеток.
Подсчет клеток внутри культуры - анализ высвобождения клеточных ядер 5 мл (центрифужная пробирка емкостью 100 мл) или 10 мл (центрифужная пробирка емкостью 500 мл) аликвот гомогенной суспензии микроносителей извлекли из центрифужной пробирки и перенесли в пробирку емкостью 15 мл. Микроносителями позволили отделиться под воздействием гравитации и супернатант удалили путем аспирации. Микроносители промыли один раз 10 мл фосфатно-солевого буфера, микроносителям позволили отделиться под воздействием гравитации и удалили супернатант фосфатно-солевого буфера путем аспирации. Микроносители инкубировали на протяжении одного часа при температуре 37°C в растворе, высвобождающем ядра (0,1М лимонной кислоты (Sigma- St. Louis, MO), содержащей 0,1% масса/объем кристаллвиолета (Sigma- St. Louis, MO)). После инкубации, 100 мкл аликвоты микроносителей, содержащей высвобождающий ядра раствор было добавлено к 100 мкл фосфатно-солевого буфера. 10 мкл аликвоты этого раствора затем поместили в гемоцитометр и подсчитали высвобожденные ядра.
Подсчет клеток внутри культуры - анализ TrypLE™. 5 мл (центрифужная пробирка емкостью 100 мл) или 10 мл (центрифужная пробирка емкостью 500 мл) аликвот гомогенной суспензии микроносителей извлекли из центрифужной пробирки и перенесли в пробирку емкостью 15 мл. Микроносителями позволили отделиться под воздействием гравитации и супернатант удалили путем аспирации. Микроносители промыли один раз 10 мл фосфатно-солевого буфера, микроносителям позволили отделиться под воздействием гравитации и удалили супернатант фосфатно-солевого буфера путем аспирации. Микроносители инкубировались на протяжении 10 минут при температуре 37°C в выборке TrypLE™. После инкубации добавили 5 мл фосфатно-солевого буфера и позволили микроносителям отделиться под воздействием гравитации. Супернатант, содержащий клетки, собирают путем повторного пипетирования и переносят в многочисленные конические пробирки, предварительно наполненные 1 мл эмбриональной бычьей сыворотки. Пробирки центрифугировали на протяжении 5 минут при 300 центробежном ускорении, супернатант отцедили, клетки ресуспендировали в ростовой среде, и аликвота была использована для определения клеточного подсчета с помощью прибора Guava PCA (Guava Technologies, Haywood, CA).
Статичная культура в Т-пробирке
Криосохраненные флаконы с клетками hUTC были разморожены, промыты и ресуспендированы в ростовой среде. Клетки культивировались статично в Т225 на протяжении многочисленных пассажей с применением способов, описанных в US2004877012A.
Проточная цитометрия
Собранные клетки были проанализированы способом проточной цитометрии с применением прибора Becton-Dickinson FACSCalibur™ (Becton Dickinson, ан-Хосе, Калифорния) для определения профиля поверхностного маркера клеток с применением способов, описанных в US2004877012A. Все антитела был приобретены в BD PharMingen (San Diego, CA).
Результаты
Продолжительное культивирование hUTC изолята 120304 на микроносителях Cytodex® 1
Продолжительное культивирование hUTC изолята 120304 на микроносителях Hillex® II
Продолжительное культивирование hUTC изолята CNTO 2476 на микроносителях Cytodex® 1
Продолжительное культивирование hUTC изолята CNTO 2476 на микроносителях Hillex® II
Продолжительное культивирование hUTC изолята 120304 в центрифужных пробирках Т225
Сравнение экспрессии белков клеточной поверхности клетками hUTC, размноженными на микроносителях и в Т-пробирках и проанализированных способом проточной цитометрии
hUTC изолят 120304, криосохраненный на удвоении популяции 12,8 был способен к размораживанию и размножению на микроносителях Cytodex® 1 и Hillex® II до удвоения популяции 28,6 и 28,7 соответственно. Часы на удвоение популяции соответствовали от пассажа к пассажу, отмечая стабильный логарифмический рост и соответствовали кинетике роста в Т-пробирках. hUTC изолят CNTO 2476, криосохраненный на удвоении популяции 22,6 был способен к размораживанию и размножению на микроносителях Cytodex® 1 и Hillex® II до удвоения популяции 33,2 и 31,0 соответственно. Часы на удвоение популяции соответствовали от пассажа к пассажу, отмечая стабильный логарифмический рост и соответствовали кинетике роста в Т-пробирках. Статистический анализ путем одностороннего ANOA всех данных о часах на удвоение популяции указывает на отсутствие значимой разницы в кинетике роста hUTC во всех протестированных условиях. (p=0,988). Кроме того, экспрессия белка клеточной поверхностью оставалась соответствующей при финальном сборе урожая для всех протестированных условий. Эти данные демонстрируют способность клеток hUTC размножаться до приблизительно 30 удвоений популяции на микроносителях в стабильном, согласованном режиме, при котором остается неизменным фенотип белка клеточной поверхности.
Хотя изобретение было описано и проиллюстрировано ссылками на различные конкретные материалы, процедуры и примеры, следует понимать, что изобретение не ограничивается конкретными комбинациями материалов и процедур, выбранными для этой цели. Многочисленные изменения, касающиеся таких деталей изобретения, будут очевидными для специалистов в данной области техники. Подразумевается, что все описания и примеры представлены только в качестве иллюстрации и находятся в пределах сущности и объема настоящего изобретения, что отражено в нижеприведенной формуле изобретения. Все ссылки, патенты и заявки на патенты, приведенные в этой заявке, полностью включены в этот документ путем отсылки.
Изобретение относится к области биохимии. Изобретение представляет собой способ культивирования выделенных клеток, полученных из ткани пуповины человека, в культуральной среде, содержащей аминокислоты, витамины, соли, нуклеозиды, инсулин, трансферрин, этаноламин и натрия селенит, где культуральная среда обогащена сывороткой. Способ включает добавление не содержащего сыворотки питательного раствора, содержащего аминокислоты, витамины, соли, нуклеотиды, инсулин, трансферрин, этаноламин и натрия селенит, выращивание клеток на протяжении достаточного периода времени, позволяющего клеткам достичь желаемой конечной плотности популяции, причем клетки, полученные из ткани пуповины человека, выделяют из ткани пуповины человека, по существу, не содержащими крови, способными к самообновлению и размножению в культуре, обладающими потенциалом к дифференцировке, экспрессирующими CD13, CD90 и HLA-ABC и не экспрессирующими CD34, CD117 и HLA-DR. Способ позволяет осуществить рост клеток, полученных из ткани пуповины человека. 17 з.п. ф-лы, 13 табл., 13 пр.
1. Способ культивирования выделенных клеток, полученных из ткани пуповины человека, включающий:
а) растущие клетки, полученные из ткани пуповины человека, засеянные на микроносителях в культуральную среду, содержащую аминокислоты, витамины, соли, нуклеозиды, липоевую кислоту/тиоктовую кислоту, этаноламин, инсулин, трансферрин, натрия селенит, причем в культуральную среду добавлена сыворотка, на протяжении достаточного периода времени, позволяющего клеткам достичь желаемой первоначальной плотности популяции;
b) добавление бессывороточного питательного раствора после достижения клетками желаемой первоначальной плотности популяции, причем бессывороточный питательный раствор содержит аминокислоты, витамины, соли, инсулин, трансферрин, этаноламин, липоевую кислоту/тиоктовую кислоту, натрия селенит; и
с) выращивание клеток на протяжении достаточного периода времени, позволяющего клеткам достичь желаемой конечной плотности популяции;
причем клетки, полученные из ткани пуповины человека, выделяют из ткани пуповины человека, по существу, не содержащими крови, способными к самообновлению и размножению в культуре, обладающими потенциалом к дифференцировке, экспрессирующими CD13, CD90 и HLA-ABC и не экспрессирующими CD34, CD117 и HLA-DR.
2. Способ по п.1, причем способ дополнительно включает посев клеток на микроносители.
3. Способ по п.1, причем способ дополнительно включает выделение клеток после стадии с).
4. Способ по п.1, причем способ не требует замены среды.
5. Способ по п.1, причем способ осуществляется в системе культивирования в центрифужных пробирках.
6. Способ по п.1, в котором характеристики клеток до и после культивирования по существу одинаковы.
7. Способ по п.6, в котором характеристики клеток до и после культивирования одинаковы.
8. Способ по п.1, в котором желаемая первоначальная плотность популяции достигается через 3–4 дня.
9. Способ по п.1, в котором микроносители имеют поверхность, обработанную амином.
10. Способ по п.1, в котором культуральная среда содержит:
аминокислоты L-аргинин, L-цистин, L-цистеин, L-глутамин, глицин, L-гистидин, L-изолейцин, L-лейцин, L-лизин, L-метионин, L-фенилаланин, L-серин, L-треонин, L-триптофан, L-тирозин, L-валин, L-аланин, L-аспарагин, L-аспарагиновую кислоту, L-глутаминовую кислоту, L-пролин и L-таурин;
витамины кальция D-пантотенат, холина хлорид, фолиевую кислоту, I-инозитол, ниацинамид, пиридоксаль, рибофлавин, тиамин, d-биотин, пиридоксин и витамин B12 (цианокобаламин);
соли кальция хлорид, калия хлорид, магния сульфат, натрия хлорид и одну или более солей натрия фосфата;
нуклеозиды тимидин, аденозин, цитидин, уридин и гуанозин; и
инсулин, трансферрин, липоевую кислоту/тиоктовую кислоту, этаноламин, натрия селенит и один или более энергетических субстратов.
11. Способ по п.10, в котором одним или более энергетическим субстратом являются D-глюкоза и натрия пируват.
12. Способ по п.10, в котором культуральная среда содержит:
по меньшей мере приблизительно 0,05 г/л L-аргинина, по меньшей мере приблизительно 0,02 г/л L-цистина, по меньшей мере приблизительно 0,2 г/л L-глутамина, по меньшей мере приблизительно 0,01 г/л глицина, по меньшей мере приблизительно 0,02 г/л L-гистидина, по меньшей мере приблизительно 0,09 г/л L-изолейцина, по меньшей мере приблизительно 0,09 г/л L-лейцина, по меньшей мере приблизительно 0,09 г/л L-лизина, по меньшей мере приблизительно 0,02 г/л L-метионина, по меньшей мере приблизительно 0,05 г/л L-фенилаланина, по меньшей мере приблизительно 0,03 г/л L-серина, по меньшей мере приблизительно 0,08 г/л L-треонина, по меньшей мере приблизительно 0,009 г/л L-триптофана, по меньшей мере приблизительно 0,08 г/л L-тирозина, по меньшей мере приблизительно 0,08 г/л L-валина, по меньшей мере приблизительно 0,005 г/л L-цистеина, по меньшей мере приблизительно 0,0004 г/л L-аланина, по меньшей мере приблизительно 0,01 г/л L-аспарагина, по меньшей мере приблизительно 0,006 г/л L-аспарагиновой кислоты, по меньшей мере 0,03 г/л L-глутаминовой кислоты, по меньшей мере приблизительно 0,005 г/л L-пролина и по меньшей мере приблизительно 0,0003 г/л L-таурина;
от приблизительно 5×10-6 г/л до приблизительно 0,015 г/л каждого из витаминов;
по меньшей мере приблизительно 0,05 г/л кальция хлорида безводного, по меньшей мере приблизительно 0,1 г/л калия хлорида, по меньшей мере приблизительно 0,2 г/л магния сульфата, по меньшей мере приблизительно 0,08 г/л натрия фосфата одноосновного, H2O и по меньшей мере приблизительно 0,0005 г/л натрия фосфата двухосновного гептагидрата (Na2HPO4⋅7H2O);
по меньшей мере приблизительно 0,0001 г/л тимидина и по меньшей мере приблизительно по 0,005 г/л аденозина, цитидина, уридина и гуанозина; и
по меньшей мере приблизительно 0,003 г/л инсулина, по меньшей мере приблизительно 0,05 г/л трансферрина, по меньшей мере приблизительно 5×10-6 г/л липоевой кислоты/тиоктовой кислоты, по меньшей мере приблизительно 0,05 г/л этаноламина и по меньшей мере приблизительно 0,00004 г/л натрия селенита.
13. Способ по п.10, в котором в культуральную среду добавляют от 2 до 20% ФБС.
14. Способ по п.10, в котором в культуральную среду добавляют приблизительно 7,5%, приблизительно 10% или приблизительно 15% ФБС.
15. Способ по п.10, в котором культуральная среда дополнительно содержит путресцин, стабилизатор и/или противовспенивающий агент.
16. Способ по п.1, в котором бессывороточный питательный раствор содержит:
аминокислоты L-аргинин, L-цистин, L-цистеин, глицин, L-гистидин, L-изолейцин, L-лейцин, L-лизин, L-метионин, L-фенилаланин, L-серин, L-треонин, L-триптофан, L-тирозин, L-валин, L-аланин, L-аспарагин, L-аспарагиновую кислоту, L-глутаминовую кислоту, L-пролин и L-таурин;
витамины кальция D-пантотенат, холина хлорид, фолиевую кислоту, I-инозитол, ниацинамид, пиридоксаль, рибофлавин, тиамин, d-биотин, пиридоксин и витамин B12 (цианокобаламин);
соли натрия фосфат одноосновный и натрия фосфат двухосновный гептагидрат;
микроэлементы меди (II) сульфат пентагидрат (CuSO4⋅5H2), цинка сульфат, гептагидрат (ZnSO4⋅7H2O);
нуклеозиды аденозин, цитидин, уридин и гуанозин; и
инсулин, трансферрин, этаноламин, липоевую кислоту/тиоктовую кислоту и натрия селенит.
17. Способ по п.16, в котором бессывороточный питательный раствор дополнительно содержит путресцин, стабилизатор и/или пенообразующий агент.
18. Способ по п.1, в котором в бессывороточном питательном растворе отсутствует энергетический субстрат.
| US 20040151709 A1, 05.08.2004 | |||
| WO 9110726 A1, 25.07.1991 | |||
| ШАМАНСКАЯ Т.В | |||
| и др | |||
| Культивирование мезенхимальных стволовых клеток ex vivo в различных питательных средах (обзор литературы и собственный опыт), Фундаментальные исследования в практической медицине на современном этапе | |||
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
Авторы
Даты
2018-05-08—Публикация
2013-12-12—Подача