Родственные заявки
Настоящая заявка испрашивает приоритет по дате подачи предварительной заявки на патент США №61/180,784, поданной 22 мая 2009 года, предварительной заявки на патент США №61/235,628, поданной 20 августа 2009, предварительной заявки на патент США №61/240,587, поданной 8 сентября 2009 года, предварительной заявки на патент США №61/240,626, поданной 8 сентября 2009 года, и предварительной заявки на патент США №61/305,918, поданной 18 февраля 2010 года. Содержание всех указанных заявок включено в настоящую заявку посредством ссылки.
I. Предпосылки создания изобретения
Вирус простого герпеса типа 2 (ВПГ-2) является основной причиной генитального герпеса. ВПГ-2 чаще всего передается половым путем, и инфицирование вирусом обычно приводит к повторным возникновениям очагов поражений на половых органах и перианальной области в сочетании с выделением вирусных частиц в половые пути. Распространение вируса (выделение) может происходить и в отсутствии герпетических поражений или других симптомов. ВПГ-2 также задерживается в латентном состоянии в чувствительных ганглиях. Инфекция ВПГ-2 вызывает физический дискомфорт и психосексуальные нарушения у пострадавших пациентов, и вносит дополнительный вклад в угрозу для здоровья. В частности, пациенты, инфицированные ВПГ-2, подвергаются повышенному риску инфицирования ВИЧ, и беременные матери, инфицированные ВПГ-2, могут вертикально передавать ВПГ-2 своему плоду. Для лиц с ослабленным иммунитетом или для новорожденных инфекция ВПГ-2 может быть фатальной. В настоящее время не существует способов лечения инфекции ВПГ-2.
Инфекция ВПГ-2 широко распространена, при этом в одном из исследований подсчитано, что около 20% населения во всем мире инфицированы (Looker et al., 2008, Bulletin of the World Health Organization, October 2008, 86(10)). Большее количество женщин, по сравнению с мужчинами, инфицировано, и распространенность заболевания увеличивается с возрастом. Большое количество подростков с диагнозом ВПГ-2 свидетельствует о том, что распространенность среди населения будет продолжать расти, поскольку инфекция ВПГ-2 является пожизненной.
Возможности лечения симптомов ВПГ-2 ограничены. Противовирусная терапия с использованием таких соединений, как фамцикловир, валацикловир или ацикловир ограничивает продолжительность проявления симптомов, а в некоторых случаях, ускоряет заживление повреждений и уменьшает частоту выделения вируса. Противовирусные препараты не являются лечебными, и не предотвращают повторного возникновения очагов поражений или не уничтожают вирус полностью. Кроме того, для применения противовирусных препаратов необходимо распознать симптомы инфекции ВПГ-2 у пациентов, затем получить подтверждающий диагноз, и, в конечном счете, приступить к противовирусной терапии. Такие требования могут быть несостоятельными в тех регионах мира, где противовирусные препараты не всегда доступны. Кроме того, пациенты часто не подозревают, что они инфицированы, либо потому что они у них не проявляются симптомы, либо потому что симптомы первичной инфекции ослабевают, позволяя пациентам думать, что произошло излечивание заболевания.
Для решения медицинских и социальных проблем, связанных с ВПГ-2, крайне желательно разработать фармацевтические композиции для ингибирования или противодействия инфекции ВПГ-2. Эффективную композицию можно применять для индукции усиленного иммунного ответа против ВПГ-2, который будет предотвращать первичную инфекцию, блокировать способность вируса задерживаться бессимптомно в чувствительных ганглиях, устранять повторное возникновение очагов повреждений и/или предотвращать распространение (выделение) вируса. Иммунная система, как известно, создает защиту против ВПГ-2, о чем свидетельствует тот факт, что рецидивирующие инфекции проявляются с меньшими, менее острыми симптомами и с меньшей частотой с течением времени.
Хотя конечной целью вакцины против ВПГ должна быть длительная защита от вирусных инфекций, ослабление симптомов заболевания также обеспечит значительные преимущества для здоровья. Одной из текущих задач как для профилактических, так и для терапевтических вакцин является снижение клинических эпизодов и выделения вируса при первичной и латентной инфекции. Существует три категории профилактических вакцин, прошедших клинические испытания с неудовлетворительными результатами, к ним относятся: I) вакцина на основе целого вируса, II) вакцина на основе белковых субъединиц и III), генная субъединичная вакцина (Stanberry et al., Clinical Infect. Dis., 30(3):549-566, 2000). В 1970-х годах был исследован ряд противовирусных вакцин на основе убитых вирусов, ни одна из которых не оказалась эффективной. Недавно было показано, что ослабленный ВПГ является слабо иммуногенным. Было проведено клиническое исследование субъединичных вакцин на основе двух рекомбинантных гликопротеинов в сочетании с различными адъювантами. Одна из таких вакцин, разработанная компанией Chiron, содержит укороченные формы как гликопротеина D (gD2), так и гликопротеина В (GB2) ВПГ-2, выделенные из трансфицированных клеток яичника китайского хомячка (СНО), и введенных в состав препарата вместе с адъювантом MF59. Другая вакцина, разработанная Glaxo-Smithkline (GSK), содержит укороченный gD2, введенный в состав препарата вместе с адъювантами квасцы- и 3-O-деацилированным монофосфориллипидом А (МФЛ). Обе вакцины оказались иммуногенными и хорошо переносимыми на 1/11 этапе испытаний. Однако на III этапе испытаний вакцина Chiron не показала общей эффективности против сероконверсии ВПГ-2, и работа была прекращена. Вакцина GSK показала значительную эффективность (73-74%) у ВПГ-1-, ВПГ-2-серонегативных женщин-добровольцев, но отсутствие эффективности у мужчин.
Хотя даже вакцина с ограниченной эффективностью оказалась бы полезной для пациентов с ВПГ, такого рода испытания позволяют протестировать только небольшое число возможностей вакцин. Причина этого состоит в том, что исследование вакцин не было систематическим. Создание вакцины на основе целого вируса предполагает, что презентация самого возбудителя иммунной системе будет индуцировать оптимальный иммунитет. Действительно, широта и продолжительность иммунного ответа на вакцины с целым возбудителем исторически были лучше, чем на субъединичные вакцины. Однако следует учитывать патогенность конкретного вакцинного штамма. Субъединичные вакцины на сегодняшний день выбраны для тестирования вакцин на основании их предполагаемого значения в патогенезе болезни и иммуногенности во время инфекции. Такие подходы позволили выявить одну вакцину-кандидат против ВПГ, демонстрирующую ограниченную эффективность в некоторых препаратах, но не эффективную в других препаратах. Таким образом, для защиты заболеваний вирусом герпеса необходимы новые и усовершенствованные способы разработки вакцин.
II. Краткое описание изобретения
Инфекция и передача ВПГ-2 является одной из основных проблем здравоохранения. Настоящее изобретение предусматривает, в частности, некоторые высокоэффективные вакцины против ВПГ-2. Такие вакцины можно применять либо в терапевтических, либо в профилактических целях. Настоящее изобретение также обеспечивает специфичные антигены и способы применения таких антигенов для запуска иммунного ответа против ВПГ-2.
В одном своем аспекте настоящее описание раскрывает препарат вакцины, который содержит фармацевтически приемлемый носитель и по меньшей мере один полипептид, который состоит из последовательности SEQ ID NO:2, 3, 4 и 5 или иммуногенного фрагмента указанной последовательности, и который также может дополнительно содержать последовательность SEQ ID NO:1 или ее иммуногенный фрагмент. Указанный препарат вакцины может содержать первый полипептид, который состоит из одной из вышеуказанных последовательностей (SEQ ID NO), и второй полипептид, который состоит из другой из вышеуказанных последовательностей (SEQ ID NO).
Другой аспект настоящего изобретения обеспечивает препарат вакцины, который содержит фармацевтически приемлемый носитель, адъювант, включающий одну и более очищенную фракцию сапонинов килайи, и по меньшей мере один полипептид, который включает любую из последовательностей SEQ ID NO:2, 3, 4 и 5 или ее иммуногенный фрагмент, и может дополнительно содержать последовательность SEQ ID NO:1 или ее иммуногенный фрагмент.
Другим аспектом настоящего изобретения является препарат вакцины, содержащий фармацевтически приемлемый носитель и полипептид, который состоит из последовательности SEQ ID NO:2 или ее иммуногенного фрагмента. Из SEQ ID NO:2 могут быть удалены некоторые остатки аминокислот. Полипептид может быть гликозилирован, или может быть не гликозилирован.
Еще в одном аспекте настоящее изобретение обеспечивает препарат вакцины, содержащий фармацевтически приемлемый носитель и полипептид, включающий последовательность SEQ ID NO:5, при этом в указанном полипептиде полностью отсутствует трансмембранный домен, состоящий из остатков 341-363, или его часть из по меньшей мере 8 последовательных аминокислотных остатков. Соответственно, один из аспектов настоящего изобретения обеспечивает препарат вакцины, содержащий фармацевтически приемлемый носитель и полипептид, включающий SEQ ID NO:4. Полипептид может быть гликозилирован или может быть не гликозилирован.
Еще один аспект настоящего изобретения обеспечивает препарат вакцины, содержащий фармацевтически приемлемый носитель и полипептид, включающий SEQ ID NO:5. Полипептид может быть гликозилирован или может быть не гликозилирован.
Еще одним аспектом настоящего изобретения обеспечивает препарат вакцины, содержащий фармацевтически приемлемый носитель и полипептид, включающий SEQ ID NO:3. Полипептид может быть гликозилирован или может быть не гликозилирован.
В некоторых вариантах реализации настоящего изобретения полипептиды в препаратах вакцины могут быть конъюгированы с иммуногенными носителями, например гемоцианином лимфы улитки. В других вариантах реализации препараты вакцины дополнительно содержат адъювант. Адъювант может представлять собой одну или более очищенную фракцию сапонинов килайи.
Изобретение обеспечивает способы лечения субъекта, инфицированного ВПГ-2 или восприимчивого к инфекции ВПГ-2, путем введения эффективного количества препарата вакцины, описанного в настоящей заявке. В некоторых вариантах реализации указанный способ приводит к ингибированию симптоматики ВПГ-2, например, путем уменьшения количества герпетических поражений, уменьшения количества дней, в течение которых у пациента присутствуют герпетические поражения, снижения степени инфицирования ВПГ-2 у неинфицированных субъектов, повышения титра IgG и/или Т-клеточного ответа против одного или более антигена ВПГ-2 и/или сокращения числа герпетических поражений на начальных стадиях инфекции ВПГ-2.
В другом аспекте настоящее изобретение описывает результаты, полученные с помощью системы с высокой пропускной способностью для скрининга библиотек эффективных Т-клеток для выявления их специфичных антигенов-мишеней из полного протеома ВПГ-2. Эта технология позволила идентифицировать отдельные антигены, которые могут быть эффективными in vivo либо в качестве профилактических, либо терапевтические композиций. С одной стороны в настоящей заявке предусмотрено несколько важных защитных Т-клеточных антигенов, которые могут быть включены в композиции на основе белков, запускающие иммунный ответ.
Один из аспектов настоящего изобретения обеспечивает фармацевтические композиции, содержащие два или более изолированные полипептида, выбранные из полипептидов, которые имеют аминокислотную последовательность, включающую по меньшей мере одну из последовательностей SEQ ID NO:1-38 или ее иммуногенный фрагмент.
В другом аспекте изобретение обеспечивает препараты вакцины, которые включают фармацевтически приемлемый носитель и полипептид, содержащий по меньшей мере одну из последовательностей SEQ ID NO:1-38 или ее иммуногенный фрагмент. В некоторых вариантах реализации указанный полипептид включает по меньшей мере одну из последовательностей SEQ ID NO:1-38.
В другом аспекте настоящего изобретения предусмотрен способ запуска иммунного ответа у субъекта, включающий введение указанному субъекту эффективного количества препарата вакцины или фармацевтической композиции, содержащих эффективное количество двух или более изолированных полипептидов, выбранных из полипептидов, которые имеют аминокислотную последовательность, соответствующую по меньшей мере одной из последовательностей SEQ ID NO:1-38, или ее иммуногенному фрагменту.
Еще один аспект настоящего изобретения относится к способу ослабления одного или более симптомов инфекции ВПГ-2 у субъекта, включающий введение указанному субъекту эффективного количества препарата вакцины или фармацевтической композиции, содержащих два или более изолированных полипептидов, выбранных из полипептидов, которые имеют аминокислотную последовательность, соответствующую по меньшей мере одной из последовательностей SEQ ID NO:1-38, или ее иммуногенному фрагменту. В некоторых вариантах реализации симптомы инфекции ВПГ-2 включают один или более следующего: образование очагов поражения, боль, раздражение, зуд, лихорадка, недомогание, головная боль, распространение вируса и признак, предшествующий началу заболевания.
Еще один из аспектов настоящего изобретения обеспечивает способ ингибирования возникновения инфекции ВПГ-2, включающий введение эффективного количества препарата вакцины или композиции, содержащих два или более изолированных полипептидов ВПГ, выбранных из полипептидов, которые имеют аминокислотную последовательность, соответствующую по меньшей мере одной из последовательностей SEQ ID NO:1-38, или ее иммуногенному фрагменту.
Заявители раскрывают еще один аспект настоящего изобретения, который обеспечивает способ ингибирования развития скрытой (латентной) инфекции ВПГ-2 у субъекта, инфицированного ВПГ-2, включающий введение эффективного количества препарата вакцины или композиции, содержащих два или более изолированных полипептидов ВПГ-2, выбранных из полипептидов, которые имеют аминокислотную последовательность, соответствующую по меньшей мере одной из последовательностей SEQ ID NO:1-38 или ее иммуногенному фрагменту.
В родственном аспекте настоящее изобретение предлагает способ снижения выделения вируса у субъекта, инфицированного ВПГ-2, включающий введение эффективного количества препарата вакцины или композиции, содержащих два или более изолированных полипептидов ВПГ-2, выбранных из полипептидов, которые имеют аминокислотную последовательность, соответствующую по меньшей мере одну из последовательностей SEQ ID NO:1-38, или ее иммуногенному фрагменту.
Кроме того, один из аспектов настоящего изобретения обеспечивает способ снижения повторного проявления вспышек заболевания у субъекта, инфицированного ВПГ-2, включающий введение эффективного количества препарата вакцины или композиции, содержащих два или более изолированных полипептидов ВПГ-2, выбранных из полипептидов, которые имеют аминокислотную последовательность, соответствующую по меньшей мере одной из последовательностей SEQ ID NO:1-38, или ее иммуногенному фрагменту.
Дополнительный аспект настоящего изобретения обеспечивает способ получения любой из фармацевтических композиций, описанных выше, включающий экспрессию указанных двух или более полипептидов и выделение указанных двух или более полипептидов.
Заявители также раскрывают аспект настоящего изобретения, обеспечивающий способ диагностики степени тяжести симптомов у субъекта, инфицированного ВПГ-2, включающий (I) оценку уровня активации Т-клеток в ответ на аутологичные антигенпрезентирующие клетки (АПК), на которые подействовали одним или более изолированным полипептидом ВПГ-2, выбранным из полипептидов, представленных SEQ ID NO:1-38, или его иммуногенным фрагментом, и (II) сравнение указанного уровня с контрольным (эталонным) уровнем, характерным для инфицированных субъектов с частыми вспышками заболевания, при этом значимое увеличение указанного уровня ответа, по сравнению с контрольным (референсным) уровнем, свидетельствует о том, что указанный субъект имеет меньшую степень тяжести симптомов (например, у субъекта отсутствуют симптомы). Значительное увеличение ответа может, например, включать увеличение в 1,5 раза или более, в 2 раза или более, в 3 раза или более, в 5 раз или более, в 10 раз или более, или даже в 20 раза или более.
Другой аспект настоящего изобретения относится к способу диагностики степени тяжести симптомов у субъекта, инфицированного ВПГ-2, включающему (I) оценку уровня активации Т-клеток у субъекта, инфицированного естественным путем или подвергшегося воздействию вируса, в ответ на АПК, презентирующие один или более изолированный полипептид ВПГ-2, выбранный из полипептидов, соответствующих SEQ ID NO:1-38, или его иммуногенный фрагмент, и (II) сравнение указанного уровня с контрольным (эталонным) уровнем, характерным для инфицированных субъекта с частыми вспышками заболевания, при этом значимое снижение указанного уровня активации, по сравнению с контрольным (эталонным) уровнем, свидетельствует о том, что указанный субъект имеет большую степень тяжести симптомов (например, более частые вспышки поражений).
Другой аспект настоящего изобретения обеспечивает фармацевтические композиции, содержащие антитело, которое связывается с одним или более изолированными полипептидами ВПГ, выбранными из списка, включающего последовательности SEQ ID NO:1-38 или иммуногенные фрагменты указанных последовательностей.
Кроме того, другой аспект настоящего изобретения обеспечивает способ идентификации иммуногенных композиций для ВПГ-2 путем тестирования двух или более полипептидов, выбранных из полипептидов с аминокислотной последовательностью, соответствующей одной из последовательностей SEQ ID NO: 1-38, или ее иммуногенному фрагменту, на способность индуцировать выработку цитокинов в Т-клетках млекопитающих, при этом указанная иммуногенная композиция представляет собой такую композицию, которая значительно повышает уровень цитокинов до более высокого уровня, по сравнению с уровнем цитокинов, продуцируемых нативными Т-клетками млекопитающих. Значительное увеличение уровня цитокинов, как правило, представляет собой увеличение по меньшей мере в 1,5 раза, в 2 раза, в 3 раза, в 5 раз, в 10 раз или даже в 20 раз, по сравнению с уровнем продукции в нативных клетках.
Еще один аспект настоящего изобретения обеспечивает способ обнаружения ВПГ-2 в образце, полученном от субъекта, при этом указанный способ включает: (I) осуществление контакта указанного образца с одним или более антителом к одному или более полипептиду, который имеет аминокислотную последовательность SEQ ID NO:1-38 или его иммуногенному фрагменту, и (II) обнаружение связывания указанного одного или более антитела с указанным один или более полипептидом ВПГ-2 из указанного образца.
Наконец, один из аспектов настоящего изобретения обеспечивает фармацевтические композиции, содержащие два или более изолированных полинуклеотида, из нуклеотидов, кодирующих SEQ ID NO:1-38, или фрагменты, кодирующие соответствующие иммуногенные пептиды.
III. Краткое описание графических материалов
Фигуры 1А и В представляют собой графики, показывающие, соответственно, ответ CD4+ и CD8+ Т-клеток после иммунизации полноразмерным белком gD2, gD2ΔTMR или укороченным gD2, лишенным участка непосредственно перед трансмембранным доменом (обозначен как 306t).
Фигуры 2А и В представляют собой графики, показывающие, соответственно, ответ CD4+ и CD8+ Т-клеток после иммунизации пулом перекрывающихся пептидов, охватывающих фрагменты GL2, ICP4.1 или ICP4, кодируемые RS1.1, RS1.3.1 и RS1.3.2.
Фигуры 3А и В представляют собой графики, показывающие, соответственно, ответ CD4+ и CD8+ Т-клеток после иммунизации gD2ΔTMR, или gD2ΔTMR и ICP4.2.
IV. Подробное описание изобретения
Настоящая заявка описывает вакцины и иммуногенные композиции, действующие против ВПГ-2. Препараты вакцины могут включать полипептид, который содержит последовательность из Таблицы 1, или его иммуногенный фрагмент, или комбинацию по меньшей мере двух полипептидов, содержащих последовательность из Таблицы 1 или их иммуногенных фрагментов. В некоторых вариантах реализации полипептид (полипептиды) в составе вакцины включает полную последовательность, соответствующую по меньшей мере одной из последовательностей SEQ ID NO:1-26, или состоит из полной последовательности, которая соответствует любой из последовательностей SEQ ID NO:1-26. Иммуногенные композиции могут включать в себя полипептид, включающий последовательность из Таблицы 1 и Таблицы 2, или ее иммуногенный фрагмент, или комбинацию по меньшей мере двух полипептидов, включающих последовательности из Таблицы 1 и Таблицы 2, или их иммуногенные фрагменты. В некоторых вариантах реализации полипептид (полипептиды) иммуногенной композиции содержат полную последовательность, соответствующую любой из последовательностей SEQ ID NO:1-38 или состоят из полной последовательности SEQ ID NO:1-38. Полипептиды в Таблицах 1 или 2, могут кодироваться последовательностями SEQ ID NO:39-46 и 117-134, как это указано, и/или последовательностями кДНК, публично доступными на сайте http://www.ncbi.nlm.nih.gov/sites/entrez. Последовательности кДНК и белков также могут быть получены из любого известного штамма ВПГ-2, в том числе HG52, 333 и штамма G. Таким образом, последовательность кДНК может быть доступна по названию гена или белка из геномной последовательности, соответствующей номеру NC_001798.1, и может иметь сходство (консервативность) приблизительно 97% с последовательностями, соответствующими NC_001798.1. Как описано в настоящей заявке, полипептид может упоминаться по названию белка, по номеру последовательности SEQ ID NO и/или по названию гена, кодирующего указанный белок.
Полипептиды могут быть получены с помощью различных систем для экспрессии. Подходящие системы для экспрессии включают системы экспрессии в Е.coli и системы на основе бакуловирусов (например, в клетках насекомых). Полипептиды, полученные с помощью экспрессии в Е.coli, как правило, являются полноразмерными и негликозилированными, хотя с помощью такой системы также могут быть получены укороченные варианты. В некоторых вариантах реализации такие укороченные варианты сохраняют сигнальный домен целиком или его часть. Полипептиды, полученные с применением системы на основе бакуловируса, как правило, лишены N-терминальной сигнальной последовательности, но они полностью или частично гликозилированы.
Название белка
ICP4
ICP4 внутренний фрагмент (ICP4.2)
gL2 цитоплазматический
gD2 внутренняя делеция (gDΔTMR)
gD2
ICP34.5
ICP0
ICP4 внутренние фрагменты
ICP4 внутренние фрагменты
ICP4 внутренние фрагменты
ICP4 внутренние фрагменты
ICP4 внутренние фрагменты
ICP4 внутренние фрагменты
ICP4 внутренние фрагменты
ICP4 внутренние фрагменты
ICP4 внутренние фрагменты
урацил ДНК-гликозилаза
миристилированный белок оболочки
gL2 секретируемый
VP5
VP5
ICP1/2
ICP1/2 внутренние фрагменты
ICP1/2 внутренние фрагменты
рибонуклеозид-редуктаза
ICP47
Название белка
gM2
белок для расщепления/упаковки ДНК
ICP35
ДНК-зависимая полимераза
комплекс ДНК геликазы/праймазы
комплекс ДНК геликазы/праймазы
неизвестный белок
белок для расщепления/упаковки
ICP1/2 фрагмент
ICP27
ассоциированный с мембраной белок вириона
gG2
А. Иммуногенные полипептиды ВПГ-2
Иммуногенные полипептиды или полинуклеотиды, указанные в Таблице 1 и/или Таблице 2, можно применять в фармацевтических композициях. Настоящее изобретение относится к фармацевтическим композициям, содержащим иммуногенные полипептиды или полинуклеотиды, кодирующие такие иммуногенные полипептиды, совместно с фармацевтическим носителем. Антигены ВПГ-2 могут быть идентифицированы путем скрининга клеток иммунной системы у пациентов, инфицированных ВПГ-2. Кратко, библиотеку антигенов ВПГ-2 экспрессируют в клетках бактерий, смешивают с антиген-презентирующими клетками (АПК). АПК, в свою очередь, процессируют и презентируют производные полипептидов ВПГ-2 для лимфоцитов, изолированных у пациентов, инфицированных ВПГ-2. Пациенты принадлежат к нескольким группам: (1) имевшие контакт с ВПГ-2, но серонегативные по данной инфекции, (2) инфицированные ВПГ-2, но не проявляющие симптомов, (3) инфицированные ВПГ-2 и редко проявляющие вспышки очагов поражений, (4) инфицированы ВПГ-2 и проявляющие частые вспышки, (5) нативные и (6) серонегативные по отношению к ВПГ-2 (ВПГ-2-), но содержащие антитела к ВПГ-1 (ВПГ-1+). Ответ лимфоцитов от каждой группы сравнивали на реактивность по отношению к ВПГ-2-производным полипептидам, и путем такого скрининга выявляли антигены, которые с большей частотой индуцировали реактивные лимфоциты в одной группе пациентов, по сравнению с другими. Инфицированные, но не проявляющие симптомы, и подвергшиеся действию вируса, но серонегативные пациенты могут иметь активированные защитные иммунные реакции, которые не активируются у пациентов, демонстрирующий частые вспышки очагов поражений, в частности, у подвергшихся действию вируса, но серонегативных пациентов, как предполагается, развит стерильный иммунитет к инфекции ВПГ-2. Предполагается, что у таких пациентов уникальный набор полипептидов активирует лимфоциты. Таким образом, настоящее изобретение предусматривает композиции из конкретных полипептидов ВПГ-2, которые активируют лимфоциты у инфицированных, но не проявляющих симптомы пациентов, у подвергшихся действию вируса, но серонегативных пациентов, или комбинацию таких полипептидов для подавления или противодействия инфекции ВПГ-2.
Антигены, которые были идентифицированы на основании их иммуногенности у инфицированных, но не проявляющих симптомы пациентов, и у подвергшихся действию вируса, но серонегативных пациентов, как ожидается, также будут иммуногенными у любого субъекта.
В некоторых вариантах реализации указанный полипептид может индуцировать врожденный иммунный ответ, гуморальный иммунный ответ или клеточный иммунный ответ. В клеточном иммунном ответе могут быть задействованы клетки TH1, и в некоторых вариантах реализации иммунный ответ с участием TH1 клеток представляет собой иммунный ответ, в котором активируются клетки TH1. В некоторых вариантах реализации иммуногенные полипептиды не индуцируют цитокины TH2. В некоторых вариантах реализации в клеточный иммунный ответ могут быть вовлечены клетки TH17, а в некоторых вариантах реализации иммунный ответ с участием клеток TH17 представляет собой иммунный ответ, в котором активируются клетки TH17.
Полипептиды (или их иммуногенные фрагменты) в композициях согласно настоящему изобретению могут индуцировать Т-клеточные реакции у многих индивидов, независимо от их HLA гаплотипа (Human Lymphocyte Antigens, антигены лейкоцитов человека). В частности, эпитопы в составе указанных полипептидов могут индуцировать Т-клеточные реакции у людей с одним или более из следующих супертипов HLA: HLA-А2, -A3, -А24, -А1, -В7, -В8, -В27, -В44, -В58, и В62, и HLA-DQB01, -DQB02, -DQB03, -DQB-04, и -DQB05. В некоторых вариантах реализации в составе композиции согласно настоящему изобретению обеспечены один или более, например, два, три, четыре или более полипептидов из Таблицы 1 и/или Таблицы 2 (или их иммуногенных фрагментов). В некоторых вариантах реализации композиция согласно настоящему изобретению содержит два полипептида из Таблицы 1 и/или Таблице 2. В других вариантах реализации композиция согласно настоящему изобретению содержит три полипептида из Таблицы 1 и/или Таблицы 2.
В некоторых вариантах реализации два, три, четыре или более полипептидов из Таблицы 1 и/или Таблицы 2 (или их иммуногенных фрагмента) обеспечивают вместе в виде конъюгата. В некоторых вариантах реализации два полипептида из Таблицы 1 и/или Таблицы 2 или три полипептида из Таблицы 1 и/или Таблицы 2, обеспечивают вместе в виде конъюгата. В некоторых вариантах реализации два, три, четыре или более полипептида из Таблицы 1 и/или Таблицы 2 ковалентно связаны друг с другом, например, в виде гибридного белка. В некоторых вариантах реализации два, три, четыре или более полипептида из Таблицы 1 и/или Таблицы 2 ковалентно связаны друг с другом, например, в виде гибридного белка. В некоторых вариантах реализации два полипептида из Таблицы 1 и/или Таблицы 2 или три полипептида из Таблицы 1 и/или Таблицы 2 ковалентно связаны друг с другом, например, в виде гибридного белка.
В некоторых вариантах реализации композиции содержат два или более полипептида, выбранных из группы, включающей SEQ ID №1-38, а также могут содержать или не содержать другие полипептиды ВПГ-2.
В некоторых вариантах реализации Заявители обеспечивают полипептиды, которые по меньшей мере на 70%, 80%, 90%, 95%, 96%, 97%, 98%, 99% или 100% идентичны полипептиду, кодируемому геном в Таблице 1 и/или Таблице 2, или части указанного полипептида. В некоторых вариантах реализации длина указанного гомологичного полипептида составляет по меньшей мере, 8, 10, 15, 20, 30, 40, 50, 60, 80, 100, 120, 140, 160, 180, 200, 220, 240, 260, 280, 300, 350, 400, 450, или 500 аминокислот. В некоторых вариантах реализации, таких, как только что описаны выше, длина указанного полипептида не превышает 300, 350, 400, 450, или 500 аминокислот.
Иммуногенная композиция может также содержать части указанных полипептидов и генов, например, делеционные мутантные варианты, укороченные мутантные варианты, олигонуклеотиды и пептидные фрагменты. В некоторых вариантах реализации часть указанного белка является иммуногенной.
Иммуногенность части белка или его гомолога можно легко определить с помощью тех же тестов, которые применяют для определения иммуногенности полноразмерного белка. В некоторых вариантах реализации часть белка имеет практически такую же иммуногенность, как полноразмерный белок. В некоторых вариантах реализации иммуногенность части белка снижена не более чем на 10%, 20%, 30%, 40%, или на 50%, по сравнению с полноразмерным белком. Белковые фрагменты могут быть, например, линейными, круговыми или разветвленными. В некоторых вариантах реализации белок или белковый фрагмент включает одну или более неприродную аминокислоту (например, аминокислоту, отличную от 20 обычно встречающихся в природных белках). Неприродная аминокислота может иметь атипичную боковую цепь. Кроме того, можно применять пептидомиметики; их применение может изменять пептидный остов.
Некоторые варианты реализации полипептидных композиций, описанных в настоящей заявке, включают иммуногенные полипептиды, которые содержат последовательность для транслокации через мембрану (membrane translocating sequence, MTS), облегчающую введение полипептидов в клетки млекопитающих и последующую стимуляцию клеточного иммунного ответа. Примеры последовательности для транслокации через мембрану включают гидрофобную область в сигнальной последовательности фактора роста фибробластов Капоши, MTS α-синуклеина, β-синуклеина или γ-синуклеина, третью спираль гомео домена Antennapedia, SN50, интегрин β3 h-области, Tat ВИЧ, pAntp, PR-39, абаецин, апидаецин, Вас5, Вас7, белок CS из Р. berghei белка, а также MTS, описанные в патентах США 6248558, 6432680 и 6248558.
В некоторых вариантах реализации указанные иммуногенные полипептиды конъюгированы (т.е. ковалентно связаны) с другой молекулой. Это может, например, увеличивать период полувыведения, растворимость, биодоступность или иммуногенность антигена. Молекулы, с которыми могут быть конъюгированы иммуногенные полипептиды, включают углеводы, биотин, полиэтиленгликоль (ПЭГ), полисиаловую кислоту, N-пропионилированную полисиаловую кислоту, нуклеиновые кислоты, полисахариды и PLGA (сополимер молочной и гликолевой кислоты). Существует много различных типов ПЭГ, молекулярный вес которых варьирует от менее 300 г/моль до более 10 миллионов г/моль. Цепи ПЭГ цепи могут быть линейными, разветвленными или с геометрией гребня или звезды.
В. Иммуногенные полипептиды и нуклеиновые кислоты ВПГ-2 для применения в вакцинах
В некоторых вариантах реализации один или более, например, два, три, четыре или более иммуногенных фрагментов или их варианты представлены в смеси. Например, препарат вакцины может включать в себя одну или более из последовательностей SEQ ID NO:1-26.
В некоторых вариантах реализации препарат вакцины может содержать любой один, два или три из следующих полипептидов: ICP4, ICP4.2, GL2, gD2ΔTMR и gD2 (SEQ ID NO:1-5), или их иммуногенных фрагментов (частей). В некоторых вариантах реализации комбинации содержат полипептиды или иммуногенные фрагменты только единого из ICP4 (SEQ ID NO 1) и ICP4.2 (SEQ ID NO 2). В других вариантах комбинация содержит полипептиды или иммуногенные фрагменты только одного из следующих пептидов: gD2ΔTMR (SEQ ID NO:4) и gD2 (SEQ ID NO:5). Примеры комбинаций ICP4, ICP4.2, GL2, gD2ΔTMR и gD2 включают:
Отдельные антигены и их комбинации, описанные выше, могут также включать дополнительные пептиды ВПГ-2 или полученные из ВПГ-2, например, полипептиды, включающие последовательности, выбранные из SEQ ID NO:6-26, или их иммуногенные фрагменты.
1. ICP4 (SEQ ID NO:1) кодируемый RS1
RS1 кодирует ICP4, транскрипционный трансактиватор, который может взаимодействовать с и рекрутировать специфические компоненты общей транскрипционной машины к вирусным промоторам и стабилизировать их формирование для инициации транскрипции. ICP4 содержит различные домены для трансактивации/фосфорилирования (примерно охватывает аминокислотные остатки 150-200 из SEQ ID NO:1), для связывания ДНК (примерно охватывает остатки 380-540 из SEQ ID NO:1), для ядерной локализации (примерно охватывает остатки 630-730 из SEQ ID NO:1), и для поздней регуляторной трансактивации (примерно охватывает остатки 1220-1319 из SEQ ID NO:1). Последовательности ДНК и белка RS1 можно обнаружить путем поиска RS1 в общедоступной базе данных, Entrez Gene (на интернет-сайте NCBI NIH, www.ncbi.nlm.nih.gov/sites/entrez?db=gene) в полном геноме вируса герпеса человека 2 типа.
В некоторых вариантах реализации вакцины против ВПГ-2 включают полипептид, содержащий не менее 20 последовательных аминокислотных остатков, выбранных из остатков 383-766 из ICP4 (SEQ ID NO:1), но не более 1000 аминокислот ICP4 (SEQ ID NO:1). Полипептид может также представлять собой вариант фрагмента из по меньшей мере 20 остатков.
В некоторых вариантах реализации полипептид включает в себя не более чем 950, 900, 850, 800, 750, 700, 650, 600, 550, 500, 450 или даже 400 последовательных аминокислот из ICP4. Примеры полипептидов, примерно соответствующих аминокислотным остаткам полноразмерного ICP4, являются следующими: 383-766 (RS1.2); 1-400 (RS1.1); 750-1024 (RS1.3.1); 1008-1319 (RS1.3.2); 750-1319 (RS1.3); 280-785 (RS1.4, включающий ДНК-связывающую область целиком); 680-1319 (RS1.5, включающий гликозилазу/C-концевую область); 208-1319 (RS1.6, который может также включать остаток Met на N-конце); 1-380 плюс 545-1319 (RS1.7, в котором удален участок, охватывающий примерно остатки 381-544, с удалением ДНК-связывающей области); 1-785 плюс 870-1319 (RS1.8, в котором удалена область, охватывающая примерно остатки 786-869 с удалением области ядерной локализации), или 1-766, 383-1318, 100-750,400-1300, 250-766, 383-900 из ICP4 (SEQ ID NO. 1) и т.п.
2. Внутренний фрагмент ICP4 - ICP4.2 (SEQ ID NO:2), кодируемый RS1.2
RS1.2 кодирует фрагмент из 384 аминокислот, соответствующий остаткам 383-766 ICP4 (или нуклеотидам 1150-2398 из последовательности RS1), обозначенный как ICP4.2. Последовательность ДНК и белка RS1.2 можно найти путем поиска RS1 в общедоступной базе данных Entrez Gene (на интернет-сайте NCBI NIH www.ncbi.nlm.nih.gov/sites/entrez?db=gene) в полном геноме вируса герпеса человека 2 типа.
В конкретных вариантах реализации вакцины против ВПГ-2 включают полипептид, содержащий от 50 до всех 384 аминокислотных остатков ICP4.2 (SEQ ID NO:2), например, от 100 до 384, от 200 до 384 или 250 до 350 остатков. В частных вариантах реализации полипептид включает весь ICP4.2 (SEQ ID NO:2) или представляет собой ICP4.2 (SEQ ID NO:2). Такие полипептиды могут, например, включать полноразмерный ICP4.2 или его фрагмент (SEQ ID NO:2), описанный в настоящей заявке, с аминокислотными остатками 1-382 или 767-1318 ICP4 (. SEQ ID NO 1) или его фрагмент, который в некоторых вариантах реализации представляет собой последовательные аминокислотные остатки ICP4.2. Примеры фрагментов, которые объединяют остатки SEQ ID NO:2 с выбранными остатками 1-382 или 767-1318 из SEQ ID NO:1, описаны выше.
Иммуногенный фрагмент ICP4.2 содержит по меньшей мере один иммуногенный участок, выявленный экспериментально или определенный с помощью алгоритма. Пептиды, идентифицированные с помощью таких способов, включают следующие:
GLAHVAAAV (SEQ ID NO:47)
FISGSVARA (SEQ ID NO:48)
QYALITRLL (SEQ ID NO:49)
RYDRAQKGF (SEQ ID NO:50)
GYAMAAGRF (SEQ ID NO:51)
PPHADAPRL (SEQ ID NO:52)
KPAAAAAPL (SEQ ID NO:53)
SEAAVAAV (SEQ ID NO:54)
FGWGLAHV (SEQ ID NO:55)
YALITRLLY (SEQ ID NO:56)
ALPRSPRLL (SEQ ID NO:57)
DLLFQNQSL (SEQ ID NO:58)
ADLLFQNQS (SEQ ID NO:59)
ARNSSSFIS (SEQ ID NO:60)
QACFRISGA (SEQ ID NO:61)
FVRDALVLM (SEQ ID NO:62)
FDGDLAAVP (SEQ ID NO:63)
GLGDSRPGL (SEQ ID NO:64)
WAPELGDAA (SEQ ID NO:65)
ECLAACRGI (SEQ ID NO:66)
RAWLRELRF (SEQ ID NO:67).
Таким образом, в некоторых аспектах настоящая заявка обеспечивает иммуногенный фрагмент ICP4.2. Фрагменты, в некоторых случаях, близки по размерам полноразмерному полипептиду. Например, в указанных фрагментах могут отсутствовать не более одной, двух, трех, четырех, пяти, десяти или двадцати аминокислот с одного конца или с обоих концов. В других вариантах реализации длина фрагмента составляет 100-384 аминокислот или 150-384, или 200-384, или 250-384 аминокислот. Другие примеры фрагментов представляют собой аминокислотные остатки 1-350, 1-300, 1-250, 1-200, 1-150, 1-100, 1-50, 50-384, 50-350, 50-300, 50-250, 50-200, 50-150, 50-100, 100-384, 100-350, 100-300, 100-250, 100-200, 100-150, 150-383, 150-350, 150-300, 150-250, 150-200, 200-383, 200-350, 200-300, 200-250, 250-383, 250-350, 250-300, 300-383 и 350-383. Фрагменты, описанные выше, или части указанных фрагментов (например, фрагменты из 8-50, 8-30 или 8-20 аминокислотных остатков) предпочтительно обладают одной из биологических активностей, описанных ниже, такой как усиление Т-клеточного ответа, по меньшей мере в 1,5 раза или 2 раза. Фрагмент можно применять в качестве полипептида в вакцинах, описанных в настоящей заявке, или можно объединять в виде гибридного белка с другим белком, фрагментом белка или полипептидом.
В некоторых аспектах настоящая заявка обеспечивает иммуногенные полипептиды, которые по меньшей мере на 90%, 95%, 97%, 98%, 99% или на 99,5% идентичны ICP4.2 или его иммуногенному фрагменту.
3. Гликопротеин L-2 (SEQ ID NO:3), кодируемый UL1
UL1 кодирует гликопротеин L-2 (Glycoprotein L-2, GL2), гетеродимерный гликопротеин, который необходим для слияния вирусной и клеточной мембраны, и который позволяет вирусу попасть в клетку-хозяина. Последовательность ДНК и белка UL1 можно найти при поиске в общедоступной базе данных Entrez Gene (на Интернет-сайте NCBI NIH www.ncbi.nlm.nih.gov/sites/entrez?db=gene) в полном геноме вируса герпеса человека 2 типа.
В некоторых вариантах реализации вакцины против ВПГ-2 включают полипептид, содержащий по меньшей мере 20 последовательных аминокислотных остатков, выбранных из остатков 1-224 в GL2 (SEQ ID NO:3), но не более 224 аминокислот последовательности GL2 (SEQ ID NO:3). Полипептид может также представлять собой вариант фрагмента по меньшей мере из 20 остатков.
В некоторых вариантах реализации такой полипептид по меньшей мере на 85% идентичен фрагменту из 200-250 аминокислот SEQ ID NO:3.
В некоторых вариантах реализации полипептид включает по меньшей мере 200 или 100 последовательных аминокислот из GL2. Примеры полипептидов представляют собой аминокислотные остатки 1-20, 21-40, 41-60, of 61-80, 81-100, 101-120, 121-140, 141-160, 161-180, 181-200, 201-221 GL2 (SEQ ID NO. 3) и т.п.
В других аспектах настоящая заявка обеспечивает иммуногенный фрагмент GL2. Иммуногенный фрагмент GL2 содержит по меньшей мере один иммуногенный участок, выявленный экспериментально или определенный с помощью алгоритма. Пептиды, идентифицированные с помощью таких способов, включают следующие:
AYLVNPFLF (SEQ ID NO:100)
PFLFAAGFL (SEQ ID NO:101)
TEYVLRSVI (SEQ ID NO:102)
GSQATEYVL (SEQ ID NO:103)
RIDGIFLRY (SEQ ID NO:104)
FLEDLSHSV (SEQ ID NO:105)
YVLRSVIAK (SEQ ID NO:106)
YVLRSVIAK (SEQ ID NO:107)
AYLVNPFLF (SEQ ID NO:108)
ETTTRRALY (SEQ ID NO:109)
RIDGIFLRY (SEQ ID NO:110)
YLVNPFLFA (SEQ ID NO:111)
FVCLFGLVV (SEQ ID NO:112)
LYKEIRDAL (SEQ ID NO:113)
GLDTFLWDR (SEQ ID NO:114)
RVSPTRGRR (SEQ ID NO:115)
YVLRSVIAK (SEQ ID NO:115)
GLDTFLWDR (SEQ ID NO:116)
DILRVPCMR (SEQ ID NO:117)
DRHAQRAYL (SEQ ID NO:118)
4. Гликопротеин D-2 (SEQ ID NO:118), кодируемый US6, и гликопротеин D-2 с внутренней делецией (SEQ ID NO:4), кодируемый D-2
US6 кодирует гликопротеин оболочки D-2 (glycoprotein D-2, GD2), гликопротеин оболочки, который связывается с «рецепторами проникновения» клетки-хозяина и может запускать слияние вируса с мембраной клетки-хозяина. Белок GD2 имеет несколько различных доменов, включая сигнальный домен (аминокислотные остатки 1-25), который отщепляется от зрелого белка, и трансмембранный домена (примерно соответствующий аминокислотным остаткам 340-363). Последовательность ДНК и белка US6 можно найти при поиске в общедоступной базе данных Entrez Gene (на интернет-сайте NCBI NIH www.ncbi.nlm.nih.gov/sites/entrez?db=gene) в полном геноме вируса герпеса человека 2 типа.
В некоторых вариантах реализации вакцины против ВПГ-2 содержат полипептид, включающий gD2, у которого отсутствует трансмембранный домен целиком или его часть (который примерно соответствует аминокислотным остаткам 340-363, включительно), а также сигнальную последовательность. В других вариантах реализации делегированный участок может дополнительно включать 5-10 аминокислот последовательности, фланкирующей трансмембранный домен. Делегированный участок может также включать часть трансмембранного домена, например, по меньшей мере три аминокислоты между остатками 340-363. В некоторых вариантах реализации по меньшей мере один остаток в трансмембранного домена модифицирован, удалены или замещен, например, таким образом, что трансмембранный домен перестает быть функциональным. Например, внутренняя делеция такого варианта начинается с аминокислотного остатка 336, 337, 338, 339, 340, 341, 342, 343, 344, 345 или 346 и заканчивается аминокислотным остатком 358, 359, 360, 361, 362, 363, 364, 365, 366, 367 или 368.
Конструкция, кодирующая gD2, лишенный аминокислотных остатков 341-363 (трансмембранного домена) называется US6ΔTMR (SEQ ID NO:40). ПМР (SEQ ID NO:4). Соответствующий белок обозначают как gD2ΔTMR. В других вариантах реализации иммуногенный фрагмент gD2 или gD2ΔTMR может включать делецию части трансмембранного домена и/или может включать делецию фланкирующих последовательностей вне трансмембранного домена.
В других аспектах настоящая заявка обеспечивает иммуногенный фрагмент gD2 или gD2ΔTMR. Иммуногенный фрагмент gD2 или gDΔTMR содержит по меньшей мере один иммуногенный участок, выявленный экспериментально или идентифицированный с помощью алгоритма. Пептиды, идентифицированные с помощью таких способов, включают следующие:
ALAGSTLAV (SEQ ID NO.68)
LLEDPAGTV (SEQ ID NO.69)
VIGGIAFWV (SEQ ID NO.70)
TVYYAVLER (SEQ ID NO.71)
KYALADPSL (SEQ ID NO.72)
AFETAGTYL (SEQ ID NO.73)
APSNPGLII (SEQ ID NO.74)
IPITVYYAV (SEQ ID NO.75)
APPSHQPLF (SEQ ID NO.76)
FLMHAPAFE (SEQ ID NO.77)
FSAVSEDNL (SEQ ID NO.78)
VYYAVLER (SEQ ID NO.79)
IGMLPRFI (SEQ ID NO.80)
YTECPYNKS (SEQ ID NO.81)
FLMHAPAFE (SEQ ID NO.82)
NLGFLMHAP (SEQ ID NO.83)
VIGGIAFWV (SEQ ID NO.84)
GIAFWVRRR (SEQ ID NO.85)
SEDNLGFLM (SEQ ID NO.86)
RTQPRWSYY (SEQ ID NO.87)
IAFWVRRRA (SEQ ID NO.88)
LVIGGIAFW (SEQ ID NO.89)
FWVRRRAQM (SEQ ID NO.90)
PYTSTLLPP (SEQ ID NO.91)
VGTAALLVV (SEQ ID NO.92)
TAALLVVAV (SEQ ID NO.93)
TSTLLPPEL (SEQ ID NO.94)
GTVSSQIPP (SEQ ID NO.95)
TAGTYLRLV (SEQ ID NO.96)
GVTVDSIGM (SEQ ID NO.97)
AFWVRRRAQ (SEQ ID NO.98)
RVYHIQPSL (SEQ ID NO.99)
Таким образом, в некоторых аспектах настоящая заявка обеспечивает иммуногенный фрагмент gD2 (SEQ ID NO:5) или gDΔTMR (SEQ ID NO:4). Такие фрагменты в некоторых случаях близки по размеру полноразмерному полипептиду. Например, они могут быть лишены не более одной, двух, трех, четырех, пяти, десяти или двадцати аминокислот с одного или обоих концов. В других вариантах реализации длина фрагмента составляет 100-384 аминокислот или 150-384, или 200-384, или 250-384 аминокислот. Другие примеры фрагментов представляют собой аминокислотные остатки 1-350, 1-300, 1-250, 1-200, 1-150, 1-100, 1-50, 50-384, 50-350, 50-300, 50-250, 50-200, 50-150, 50-100, 100-384, 100-350, 100-300, 100-250, 100-200, 100-150, 150-383, 150-350, 150-300, 150-250, 150-200, 200-383, 200-350, 200-300, 200-250, 250-383, 250-350, 250-300, 300-383 и 350-383. Фрагменты, описанные выше, или части указанных фрагментов (например, фрагменты из 8-50, 8-30, или 8-20 аминокислотных остатков) предпочтительно обладают одной из биологических активностей, описанных ниже, такой как усиление Т-клеточного ответа, по меньшей мере в 1,5 раза или 2 раза. Фрагмент можно применять в качестве полипептида в вакцинах, описанных в настоящей заявке, или он может быть объединен с образованием гибридного белка с другим белком, фрагментом белка или полипептида.
В других вариантах реализации указанный полипептид содержит всю последовательность SEQ ID NO:4 или SEQ ID NO:5, либо включает всю последовательность SEQ ID NO:4 или SEQ ID NO:5. В некоторых вариантах реализации иммуногенный фрагмент gD2 сохраняет целиком или часть сигнального домена (аминокислотные остатки 1-25) и/или трансмембранного домена (аминокислотные остатки 339-363).
В некоторых вариантах реализации полипептиды имеют менее 20%, 30%, 40%, 50%, 60% или 70% гомологии с аутоантигенами человека. Примеры таких аутоантигенов включают UL6 из ВПГ-1 и gK или UL53 из ВПГ-2.
В некоторых аспектах настоящая заявка обеспечивает иммуногенные полипептиды, которые по меньшей мере на 90%, 95%, 97%, 98%, 99% или 99,5% идентичны gDΔTMR или его иммуногенному фрагменту.
С. Дополнительные характеристики полипептидов ВПГ-2
Как правило, полипептиды, присутствующие в препаратах вакцины или фармацевтических композициях, описанные в настоящей заявке, являются иммуногенными, либо в отдельности, либо в виде варианта, включающего полипептиды, слитые с другим полипептидом с образованием гибридного полипептида или в смеси или в комплексе с адъювантом. Варианты включают также последовательность, которая менее чем 100% идентична последовательности, как описано в настоящей заявке. Кроме того, можно применять фрагменты, предшественники и аналоги, обладающие соответствующей иммуногенностью.
Такие полипептиды могут быть иммуногенными у млекопитающих, например, мышей, морских свинок или людей. Иммуногенный полипептид, как правило, представляет собой полипептид, способный вызывать значительный иммунный ответ в исследовании или у субъекта. Кроме того, иммуногенный полипептид может (I) индуцировать выработку антител, например, нейтрализующих антител, которые связываются с полипептидом (II) индуцировать иммунитет TH1, (III), активировать ответ CD8+ ЦТЛ, например, путем увеличения CD8+ Т-клеток и/или локального увеличения CD8+ Т-клеток в месте инфекции или реинфекции, (IV) индуцировать иммунитет TH17, и/или (V) активировать врожденный иммунитет. В некоторых вариантах реализации иммуногенный полипептид вызывает образование детектируемого количества антитела, специфичных к такому антигену.
В некоторых вариантах реализации полипептиды имеют менее 20%, 30%, 40%, 50%, 60% или 70% гомологии с аутоантигенами человека.
Полипептид может включать один или более иммуногенный участок и один или более неиммуногенный участок. Иммуногенные участки могут быть идентифицированы с помощью различных способов, в том числе с помощью белковых микрочипов, методов ELISPOT (метод иммуноферментных пятен) /ELISA (твердофазный ИФА) и/или специальных исследований на разных делеционных мутантах (например, фрагментов) исследуемого полипептида. Иммуногенные участки также могут быть определены с помощью компьютерных алгоритмов. Некоторые такие алгоритмы, как EpiMatrix (производства EpiVax), используют вычислительный матричный метод. Другие вычислительные средства для выявления антигенных эпитопов включают PEPVAC (Promiscuous EPitope-based VACcine, размещенный Институтом рака Дана-Фарбер (Dana Farber Cancer Institute) в Интернете на сайте immunax.dfci.harvard.edu/PEPVAC), MHCPred (который использует метод частных наименьших квадратов и размещен Институтом Дженнера в Интернете на сайте www.jenner.ac.uk / MHCPred) и Syfpeithi, размещенный в Интернете на сайте wwvv.syfpeithi.de/.
В некоторых вариантах реализации вакцина или фармацевтическая композиция может включать гибридный белок и/или гибридную конструкцию ДНК. Базовые последовательности ДНК, указанные выше, могут быть модифицированы без изменения последовательности белкового продукта. Например, может быть оптимизирован состав кодонов последовательности ДНК для улучшения экспрессии в клетках-хозяевах, таких как Е.coli или линия клеток насекомых (например, с применением бакуловирусной экспрессионной системы) и линия клеток млекопитающих (например, клетки яичника китайского хомячка). В конкретных вариантах реализации, например, при применении родственных пептидов меньших размеров, в том числе, имеющих молекулярную массу менее 5000 дальтон, например, от 1500 до 5000 дальтон, могут быть полезны модификации, направленные на запуск желаемого иммунного ответа. Например, полипептиды меньших размеров могут быть конъюгированы с соответствующим иммуногенными носителями, такими как белки из других патогенных организмов или вирусов (например, анатоксин столбняка), крупными белками (например, гемоцианин лимфы улитки) и т.п. Конъюгирование может быть прямым или опосредованным (например, через линкер). В других конкретных вариантах реализации гибридный белок может включать в себя полипептид, описанный выше, или его иммуногенный фрагмент или его вариант, и метку (tag). Метка может быть N-концевой или С-концевой. Например, метка может быть добавлена к нуклеиновой кислоте или полипептиду для облегчения очистки, детекции, растворимости или для обеспечения других желаемых характеристик белка или нуклеиновой кислоты. Например, метка для очистки может представлять собой пептид, олигопептид или полипептид, который может быть использован при аффинной очистке. Примеры включают His, GST, TAP, FLAG, myc, НА, МВР, VSV-G, тиоредоксин, V5, авидин, стрептавидин, ВССР, кальмодулин, Nus, S-теги, липопротеин D и β-галактозидазу. В некоторых вариантах реализации добавляемая в гибридный белок белковая часть является короткой. Таким образом, в некоторых случаях гибридный белок включает в себя не более чем 1, 2, 3, 4, 5, 10, 20 или 50 дополнительных аминокислот на одном или обоих концах полипептида, описанного выше, например, последовательных аминокислот из любого полипептида в Таблице 1.
В некоторых вариантах реализации метки, сигналы для секреции или другие сигнальные последовательности могут быть добавлены в C-концевой и/или N-концевой участок полипептида. Метку можно добавлять для облегчения очистки экспрессируемых полипептидов. Примеры меток включают НННННН (SEQ ID NO:130) и MSYYHHHHHH (SEQ ID NO:131). Сигналы для секреции могут быть оптимизированы для применения с клетками, полученными не от млекопитающих, такими как клетки насекомых. Примером сигнала для секреции является последовательность MKFLVNVALVFMVVYISYIYA (SEQ ID NO:132).
Метку для детекции можно применять для обнаружения метки и, следовательно, любой последовательности аминокислот, слитой с ней. Детектируемые метки включают флуоресцентные белки, белки, связывающиеся с флуоресцентной меткой, и белки, которые связываются с электронно-плотными молекулами. Примеры включают флуоресцентные белки DsRed, mRFP/YFP, GFP, CFP, BFP и Venus. Примером белка, который связывается с флуоресцентными или электронно-плотными метками, является Flash.
Еще один аспект, раскрытый в настоящей заявке, относится к препарату антитела, направленного к композиции настоящего изобретения (например, композиции, содержащей один или более или два или более полипептида, перечисленных в Таблице 1). Можно применять любые из различных антител. Такие антитела включают, например, поликлональные, моноклональные, рекомбинантные гуманизированные или частично гуманизированные, одноцепочечные антитела, Fab и их фрагменты и т.п. Антитела могут быть любого изотипа, например, IgA, IgG, различных изотипов IgG, таких как IgG1, IgG2, IgG2a, IgG2b, IgG3, IgG4, и т.д., и антитела могут быть получены из любого животного, которое производит антитела, в том числе козы, кролика, мыши, курицы или т.п. В некоторых вариантах реализации молекулы Fab экспрессируют и собирают в генетически трансформированной клетке-хозяине, например, Е.coli. Систему на основе вектора лямбда можно применять, таким образом, для экспрессии популяции молекул Fab с потенциальным разнообразием, равным или превышающим разнообразие при выработке антитела-предшественника субъектом. См. Huse et al. (1989), Science 246, 1275-81.
D. Компоненты вакцин и фармацевтических композиций
В некоторых вариантах реализации вакцины и фармацевтические композиции содержат один или более из полипептидов и нуклеиновых кислот, описанных выше, и один или более из следующих компонентов: адъювант, стабилизатор, буфер, поверхностно-активное вещество, компоненты для контролируемого высвобождения, соли, консерванты и антитела, специфичные к указанному антигену.
1. Адъюванты
Каждый из препаратов вакцины и каждая из фармацевтических композиций, описанных в настоящей заявке, может содержать адъювант. В целом адъюванты можно разделить на два класса в зависимости от их основного механизма действия: системы доставки вакцин и иммуностимулирующие адъюванты (см., например, Singh et al., Curr. HIV Res. 1:309-20, 2003). Системы доставки вакцин часто представляют собой дисперсные препараты, например, эмульсии, микрочастицы, иммуностимулирующие комплексы (ИСКОМ, англ. immune-stimulating complexes, ISCOM), которые могут быть в виде, например, частиц и/или матрикса и липосом. В противоположность этому, иммуностимулирующие адъюванты, которые иногда получают из возбудителей, могут представлять собой патоген-ассоциированные молекулярные паттерны (ПАМП), например, липополисахариды (ЛПС), монофосфорил липиды (МФЛ), или CpG-содержащую ДНК, которая активирует клетки иммунной системы.
Кроме того, адъюванты могут быть классифицированы как органические и неорганические. Неорганические адъюванты включают соли квасцов, такие как фосфат алюминия, аморфный гидроксифосфат-сульфат алюминия и гидроксид алюминия, которые обычно применяют при изготовления вакцин для человека. Органические адъюванты включают органические молекулы, в том числе макромолекулы. Примером органического адъюванта является холерный токсин.
Адъюванты можно также классифицировать на основании той реакции, которую они вызывают, при этом адъюванты могут активировать более одного типа ответа. В некоторых вариантах адъювант вызывает активацию CD4+ Т-клеток. Адъювант может вызвать активизацию TH1 - клеток и/или активацию TH17-клеток и/или активацию TH2-клеток. С другой стороны, адъювант может вызвать активацию TH1-клеток и/или TH17-клеток, но не активацию TH2-клеток, или наоборот. В некоторых вариантах адъювант вызывает активацию CD8+ Т-клеток. В других вариантах адъювант может вызывать активацию Т-клеток - натуральных киллеров (НКТ). В некоторых вариантах реализации адъювант вызывает активацию TH1-клеток или TH17-клеток или TH2-клеток. В других вариантах реализации адъювант вызывает активацию В-клеток. В других вариантах реализации адъювант вызывает активацию антигенпрезентирующих клеток. Указанные категории не являются взаимоисключающими, и в некоторых случаях адъювант активирует более одного типа клеток.
В некоторых вариантах реализации адъювант представляет собой вещество, которое увеличивает число или активность антигенпрезентирующих клеток, таких как дендритные клетки. В некоторых вариантах реализации адъювант способствует созреванию антигенпрезентирующих клеток, таких как дендритные клетки. В некоторых вариантах адъювант представляет собой или включает сапонин. Как правило, сапонин представляет собой тритерпеновый гликозид, такой как выделенный из коры дерева килайи Quillaja saponaria. Экстракт сапонина из биологического источника может быть в дальнейшем фракционирован (например, с помощью хроматографии) для получения частей экстракта с лучшей адъювантной активностью и с приемлемой токсичностью. Типичные фракции экстракта дерева Quillaja saponaria, которые применяют в качестве адъювантов, известны как фракции А и С. Примером адъюванта-сапонина является QS-21, который доступен у компании Antigenics. QS-21 представляет собой олигосахарид-конъюгированное низкомолекулярное соединение. При желании в QS-21 может быть добавлена примесь липида, такого как 3D-MPL или холестерин.
Особая форма сапонинов, которые можно применять в препаратах вакцины, описанных в настоящей заявке, представляет собой иммуностимулирующие комплексы (ИСКОМ). Иммуностимулирующие комплексы являются признанным в данной области классом адъювантов, который в целом включает фракции сапонина килайи и липиды (например, холестерин и фосфолипиды, такие как фосфатидилхолин). В некоторых вариантах ИСКОМ объединяют вместе с полипептидом или нуклеиновой кислотой, представляющей интерес. При этом различные фракции сапонинов можно применять в различных соотношениях. Кроме того, различные фракции сапонинов могут присутствовать вместе в одних и тех же частицах, или в одной частице может присутствовать по существу только одна фракция (например, таким образом, что указанное соотношение фракций А и С получают путем смешивания частиц различных фракций). В этом контексте, «по существу» относится к менее чем на 20%, 15%, 10%, 5%, 4%, 3%, 2% или даже 1%. Такие адъюванты могут включать фракцию А и фракцию С, смешанные в соотношении 70-95: 30-5 С, например от 70: 30 С до 75: 5 С, от 75: 5 С до 80: 20 С, от 80: 20 С до 85: 15 С, от 85: 15 С до 90: 10 С, от 90: 10 С до 95: 5 С или от 95: 5 С до 99: 1 С. ISCOMatrix, производства CSL, и AbISCO 100 и 300, выпускаемые Isconova представляют собой матрикс ИСКОМ, включающий сапонин, холестерин и фосфолипиды (липиды из клеточных мембран), которые образуют подобные клетке структуры обычно 40-50 нм в диаметре. Posintro, выпускаемый Nordic Vaccines, представляет собой матрикс ИСКОМ, в котором иммуноген связан с частицей с помощью различных механизмов, например, через электростатическое взаимодействие путем модификации заряда, включения хелатирующей группы или прямого связывания.
В некоторых вариантах адъювант представляет собой лиганд TLR (Toll-like receptor, Toll-подобный рецептор). TLR представляют собой белки, которые присутствуют на мембранах лейкоцитов и узнают чужеродные антигены (в том числе микробные антигены). Примером лиганда TLR является IC-31, который доступен у компании Intercell. IC31 включает антимикробный пептид, KLK и иммуностимулирующий олигодезоксинуклеотид, ODN1a. IC31 обладает агонистической активностью по отношению к TLR9. Другим примером является CpG-содержащая ДНК, при этом различные варианты CpG-содержащей ДНК доступны у Prizer (Coley): VaxImmune, представляющий собой CpG-7909 ((CpG)-содержащий олигодезоксинуклеотид), и Actilon, представляющий собой агонист TLR9, CpG 10101 ((CpG)-содержащий олигодезоксинуклеотид).
В некоторых вариантах реализации адъювант представляет собой наноэмульсию. Один из примеров адъюванта в виде наноэмульсии - Nanostat Vaccine, выпускаемый компанией Nanobio. Такая наноэмульсия представляет собой высокоэнергетическую эмульсию «масло-в-воде». Такая наноэмульсия, как правило, имеет размер 150-400 нанометров, и включает поверхностно-активные вещества для обеспечения стабильности. Более подробную информацию о Nanostat можно найти в патентах США 6015832, 6506803, 6559189, 6635676 и 7314624.
Адъюванты могут быть ковалентно связаны с антигенами (например, полипептидами, описанными выше). В некоторых вариантах адъювант может представлять собой белок, который индуцирует воспалительные реакции через активацию антигенпрезентирующих клеток (АПК). В некоторых вариантах реализации один или более из таких белков может быть слита с образованием рекомбинантного белка с выбранным антигеном, например, таким образом, что образующаяся гибридная молекула будет способствовать созреванию дендритных клеток, активировать дендритные клетки к выработке цитокинов и хемокинов, и в конечном счете, усиливает презентацию антигена Т-клеткам и инициацию Т-клеточных реакций (см. Wu et al., Cancer Res 2005; 65(11), pp 4947-4954). Другие примеры адъювантов, которые могут быть ковалентно связаны с антигенами, включают полисахариды, синтетические пептиды, липопептиды и нуклеиновые кислоты.
Адъювант можно применять в отдельности или в комбинации с двумя или более видами адъювантов. Адъюванты могут быть напрямую конъюгированы с антигенами. Адъюванты могут также быть объединены для увеличения силы иммунного ответа на антиген. Как правило, один и тот же адъювант или смесь адъювантов присутствует в каждой дозе вакцины. При желании, однако, адъювант можно вводить с первой дозой вакцины, но не с последующими дозами (т.е. бустер-доза). Кроме того, сильный адъювант может быть введен с первой дозой вакцины, а более слабый адъювант или более низкие дозы сильного адъюванта могут быть введены с последующими дозами. Адъювант можно вводить до введения антигена, одновременно с введением антигена или после введения антигена субъекту (иногда в течение 1, 2, 6 или 12 часов, иногда в течение 1, 2 или 5 дней). Некоторые адъюванты можно применять для человека, животных, отличных от человека, или для обоих вариантов.
2. Дополнительные компоненты вакцин и фармацевтических композиций
В дополнение к антигенам и адъювантам, описанным выше, препарат вакцины или фармацевтическая композиция может включать один или более дополнительный компонент.
В некоторых вариантах реализации препарат вакцины или фармацевтическая композиция может включать один или более стабилизатор, такой как сахар (например, сахароза, глюкоза или фруктоза), фосфат (например, натрия фосфат двузамещенный, калия фосфат однозамещенный, двухосновный фосфат калия, мононатрий фосфат), глутамат (например, мононатрия L-глутамат), желатин (например, обработанный желатин, гидролизованный желатин или свиной желатин), аминокислоту (например, аргинин, аспарагин, гистидин, L-гистидин, аланин, валин, лейцин, изолейцин, серии, треонин, лизин, фенилаланин, тирозин, и алкильные эфиры), инозин, или борат натрия.
В некоторых вариантах реализации препарат вакцины или фармацевтическая композиция включает один или более буфер, такой как смесь бикарбоната натрия и аскорбиновой кислоты. В некоторых вариантах препарат вакцины можно вводить в солевом растворе, например в фосфатно-солевом буферном растворе (ФСБ) или в дистиллированной воде.
В некоторых вариантах реализации препарат вакцины или фармацевтическая композиция включает одно или более поверхностно-активное вещество, например, полисорбат 80 (Твин 80), Тритон Х-100, полиэтилен гликоль трет-октилфенил эфир т-октилфеноксиполиэтоксиэтанол 4-(1,1,3,3-тетраметилбутил) фенил-полиэтиленгликоль (TRITON Х-100); полиоксиэтиленсорбитан монолаурат полиэтиленгликоль сорбитан монолаурат (Твин 20) и полимер 4-(1,1,3,3-тетраметилбутил)фенола с формальдегидом и оксираном (Тилоксапол). Поверхностно-активное вещество может быть ионным или неионным.
В некоторых вариантах реализации препарат вакцины или фармацевтическая композиция включает одну или более соль, такую как хлорид натрия, хлорид аммония, хлорид кальция или хлорид калия.
В некоторых вариантах реализации в состав вакцины входит консервант. В других вариантах реализации консервант не применяют. Консервант чаще всего применяют для вакцины в многодозовом флаконе, и реже во флаконе с однократной дозой. В некоторых вариантах реализации консервант представляет собой 2-феноксиэтанол, метил- и пропилпарабены, бензиловый спирт и/или сорбиновую кислоту.
В некоторых вариантах реализации препарат вакцины или фармацевтическая композиция представляет собой препарат с контролируемым высвобождением.
Е. ДНК-вакцины
В некоторых аспектах вакцина включает одну из нуклеиновых кислот, описанных в настоящей заявке. При введении пациенту вакцины в виде нуклеиновой кислоты соответствующий продукта гена (например, желаемый антиген) производится в организме пациента. В некоторых вариантах реализации векторы вакцины в виде нуклеиновой кислоты, включающие оптимизированный рекомбинантный полинуклеотид, могут быть доставлены в организм млекопитающего (включая человека) для индукции иммунного ответа с терапевтической или профилактической целью. Нуклеиновые кислоты могут представлять собой, например, ДНК, РНК или синтетические нуклеиновые кислоты. Нуклеиновые кислоты могут быть одноцепочечными или двухцепочечными.
Векторы вакцины в виде нуклеиновой кислоты (например, аденовирусы, липосомы, папилломы, ретровирусы и др.) можно вводить непосредственно млекопитающим для трансдукции клеток т vivo. Вакцины в виде нуклеиновой кислоты могут быть составлены в виде фармацевтических композиций для введения любым подходящим способом, в том числе путем парентерального введения.
При определении эффективного количества вектора для введения в лечении или профилактики инфекции или другого патологического состояния врач оценивает токсичность вектора, степень прогрессирования заболевания и продукцию антител к вектору, если это происходит. Часто дозовый эквивалент изолированной нуклеиновой кислоты вектора составляет примерно от 1 мкг до 1 мг на 70 кг веса у типичного пациента, и дозы векторов, применяемых для доставки нуклеиновой кислоты, рассчитывают для получения выхода эквивалентного количества терапевтической нуклеиновой кислоты. Введение может быть осуществлено в виде одной дозы или в виде разделенных доз. Токсичность и терапевтическую эффективность вектора вакцины на основе нуклеиновой кислоты можно определить с помощью стандартных фармацевтических процедур в клеточных культурах или на экспериментальных животных.
Вакцины на основе нуклеиновых кислот могут содержать ДНК, РНК, модифицированную нуклеиновую кислоту или их комбинации. В некоторых вариантах реализации вакцина содержит один или более вектор для клонирования или экспрессии, например, вакцина может содержать некоторое количество векторов для экспрессии, каждый из которых способен автономно экспрессировать кодирующую область в клетке млекопитающего для продуцирования по меньшей мере одного иммуногенного полипептида. Вектор для экспрессии часто включает последовательность эукариотического промотора, например, последовательность сильного эукариотического промотора, функционально связанного с одной или более кодирующей областью. Композиции и способы настоящего изобретения могут включать применение какого-либо конкретного эукариотического промотора, при этом известно широкое разнообразие таких промоторов, включая промотор CMV или RSV. Промотор может быть, но не обязательно должен быть, гетерологичным по отношению к клетке-хозяину. Применяемый промотор может быть конститутивным промотором.
Вектор, применяемый в настоящих композициях и способах, может быть кольцевым или линейным, одноцепочечным или двухцепочечным, и может представлять собой плазмиду, космиду или эписому. В подходящем варианте каждая кодирующая область находится в составе отдельного вектора, однако следует понимать, что одна или более кодирующая область может присутствовать в составе одного вектора, и эти кодирующие участки могут находиться под контролем одно или более промотора.
Многочисленные плазмиды можно применять для производства вакцины в виде нуклеиновой кислоты. В подходящих вариантах вакцин в виде нуклеиновой кислоты применяют в виде вектора конструкции с использованием плазмид VR1012 (Vical Inc., San Diego Calif.), pCMVI.UBF3/2 (S. Johnston, University of Texas) или pcDNA3.1 (InVitrogen Corporation, Carlsbad, Calif.). Кроме того, векторная конструкция может содержать иммуностимулирующую последовательность (ИСП), такую как неметилированный dCpG мотив, который стимулирует иммунную систему животного. Вакцины в виде нуклеиновых кислот также могут кодировать гибридный продукт, содержащий иммуногенный полипептид. Плазмидная ДНК также может быть доставлена с помощью системы доставки на основе ослабленных бактерий, способа, подходящего для ДНК-вакцины, вводимой перорально. Бактерии трансформируют с помощью независимо реплицируемой плазмиды, которая высвобождается в цитоплазму клетки-хозяина после гибели ослабленной бактерии в клетке-хозяине.
Альтернативный подход для доставки нуклеиновой кислоты в организм животного включает применение вирусных или бактериальных векторов. Примеры подходящих вирусных векторов включают аденовирус, вирус полиомиелита, вирусы оспы, например, альфавирусы, вирус коровьей оспы, вирус оспы канареек и оспы птиц, вирусы герпеса, в том числе вирус герпеса сома, аденовирус-ассоциированный вектор, и ретровирусы. Вирус-подобные векторы включают виросомы и вирус-подобные частицы. Примеры бактериальных векторов включают ослабленные формы Salmonella, Shigella, Edwardsiella ictaluri, Yersinia ruckerii и Listeria monocytogenes. В некоторых вариантах реализации нуклеиновая кислота представляет собой вектор, например плазмиду, способную аутологично экспрессировать нуклеотидную последовательность, кодирующую иммуногенный полипептид.
F. Применение вакцин
Вакцины, описанные в настоящей заявке, можно применять для профилактики и/или терапевтического лечения герпеса, в том числе ВПГ-1 и в особенности ВПГ-2. Субъект, получающий вакцинацию, может быть мужского или женского пола, может быть ребенком или взрослым. В некоторых вариантах реализации субъект, проходящий лечение, является человеком. В других вариантах реализации субъект представляет собой животное, отличное от человека.
1. Профилактическое применение
В профилактических вариантах реализации вакцину ВПГ-2 вводят субъекту для индукции иммунного ответа, который может помочь защитить организм от ВПГ-2.
В некоторых вариантах реализации композиции вакцины настоящего изобретения обеспечивают защитный иммунитет, благодаря которому у вакцинированных индивидов происходит более позднее проявление симптомов или уменьшение тяжести симптомов (например, снижение количества очагов повреждений при появлении инфекции), как результат воздействия вакцины на организм пациента (например, вторичный иммунный ответ). В некоторых вариантах реализации снижение тяжести симптомов составляет по меньшей мере 25%, 40%, 50%, 60%, 70%, 80% или даже 90%. Некоторые вакцинированные индивиды могут не проявлять симптомов при контакте с ВПГ-2, или даже могут не инфицироваться ВПГ-2. Защитный иммунитет, обычно, достигается за счет одного или нескольких из следующих механизмов: мукозный, гуморальный или клеточный иммунитет. Мукозный иммунитет обычно является результатом действия секреторных антител IgA (sIGA) на поверхности слизистых оболочек органов дыхания, желудочно-кишечного тракта и мочеполовых путей. Антитела sIGA образуются после ряда событий, опосредуемых клетками, процессирующими антиген, В и Т-лимфоцитами, которые приводят к выработке sIGA В-лимфоцитами на слизистой выстилке тканей тела. Гуморальный иммунитет, как правило, является результатом действия антител IgG и IgM в сыворотке крови. Например, титр IgG может быть повышен в 1,5 раза, в 2 раза, в 3 раза, в 4 раза, в 5 раз, в 10 раз, в 20 раз, в 50 раз или даже в 100 раз или более после введения препарата вакцины, описанного в настоящей заявке. Клеточный иммунитет может быть достигнут посредством цитотоксических Т-лимфоцитов или через гиперчувствительность замедленного типа, в которую вовлечены макрофаги и Т-лимфоциты, а также другие механизмы с участием Т-клеток без участия антител. В частности, клеточный иммунитет может быть опосредован TH1-клетками или TH17-клетками. Активацию TH1-клеток можно измерить с помощью секреции ИФН-γ, относительно уровня ИФН-γ, выделяемого в ответ на полипептид, который не индуцирует иммунный ответ. В некоторых вариантах реализации количество высвобождаемого ИФН-γ в 1,5 раза, в 2 раза, в 3 раза, в 4 раза, в 5 раз, в 10 раз, в 20 раз, в 50 раз или даже в 100 раз больше. Основным результатом защитного иммунитета является уничтожение вирусных частиц ВПГ-2 или подавление способности ВПГ-2 к репликации. В некоторых вариантах реализации защитный иммунитет, обеспеченный презентацией антигена до воздействия ВПГ-2, позволяет снизить вероятность сероконверсии к ВПГ-2-позитивному статусу.
Продолжительность защитного иммунитета предпочтительно является как можно более длительной. В некоторых вариантах реализации препараты вакцины вызывают защитный иммунитет продолжительностью шесть месяцев, один год, два года, пять лет, десять лет, двадцать лет или даже всю жизнь.
2. Терапевтическое применение
При терапевтическом применении вакцину, включающую полипептид или нуклеиновую кислоту согласно настоящему изобретению, можно вводить пациенту, страдающему заболеванием ВПГ-2, в количестве, достаточном для лечения пациента. Лечение пациента, в данном случае, может относиться к замедлению проявления или снижению выраженности симптомов ВПГ-2 у инфицированного индивида. В некоторых вариантах реализации лечение пациента относится к уменьшению длительности проявления поражения, снижение количества очагов поражений, уменьшению продолжительности симптомов в период вспышки заболевания и/или сокращению иным образом интенсивности проявления симптомов в период вспышки заболевания, В некоторых вариантах такая вакцина - снижает продолжительность и степени тяжести симптомов со слабым проявлением, а в некоторых вариантах вакцина снижает продолжительность и степень тяжести серьезных симптомов. В некоторых вариантах реализации вакцина снижает распространение вируса и, следовательно, способность к передаче ВПГ-2 от вакцинированных пациентов. В некоторых вариантах сокращение/уменьшение, описанное выше, составляет не менее 25%, 30%, 40%, 50%, 60%, 70%, 80% или даже 90%. В некоторых вариантах сокращение/уменьшение, описанное выше, включает полное подавление симптомов вируса и/или будущих вспышек (например, путем блокирования способности вируса задерживаться в латентном состоянии сенсорных ганглиях).
В терапевтических вариантах реализации вакцину против ВПГ-2 вводят индивидам после инфицирования. Вакцина против ВПГ-2 может быть введена вскоре после инфицирования, например, перед проявлением симптомов или может быть введена во время или после проявления симптомов. В некоторых вариантах реализации вакцина против ВПГ-2 может предотвратить эндогенную реактивацию ранней инфекции. В некоторых вариантах реализации постинфекционную вакцину можно вводить пациентам в группах высокого риска.
Продолжительность терапевтических эффектов препарата вакцины, описанного в настоящей заявке, предпочтительно является как можно более длительной. В некоторых вариантах реализации препараты вакцины обуславливают терапевтический эффект продолжительностью один месяц, два месяца, три месяца, шесть месяцев, один год, два года, пять лет, десять лет, двадцать лет или даже всю жизнь.
3. Исследование эффективности вакцинации
Эффективность вакцинации с помощью вакцин, описанных в настоящей заявке, может быть определена различными способами.
Эффективность вакцины моно проанализировать на различных модельных системах. Подходящие модельные системы для изучения ВПГ-2 включают модели на морских свинках и мышах, как описано в примерах ниже. Кратко, животных вакцинируют, и затем воздействуют на них ВПГ-2, или же вакцины вводят уже инфицированным животным. Реакцию животного на воздействие ВПГ-2 или вакцины затем сравнивают с контрольными животными, использованием измерений, описанных выше. Аналогичный анализ можно применять для клинических испытаний на человеке. Лечебный и профилактический эффекты, описанные выше, представляют собой дополнительные способы определения эффективности вакцины.
Кроме того, эффективность можно оценить при иммунизации in vitro нативных мононуклеарных клеток периферической крови (МКПК) человека, при этом на АПК воздействуют вакциной, а затем АПК кокультивируют с нативными Т-клетками от того же самого донора для оценки первичного ответа на иммунизацию в тестируемой пробирке. Активацию Т-клеток в 1,5 раза, в 2 раза, в 5 раз, в 10 раз, в 20 раз, в 50 раз или в 100 раз или более, по сравнению с активацией Т-клеток с помощью АПК, не подвергшихся воздействию вакцины, в некоторых вариантах реализации, считают адекватной реакцией.
Эффективность вакцины можно, кроме того, определить с помощью анализа нейтрализации вируса. Кратко, животных иммунизируют и собирают сыворотку в разные дни после иммунизации. Серийные разведения сыворотки преинкубируют с вирусом, во время этого антитела в сыворотке крови, специфичные по отношению к вирусу, связываются с вирусом. После этого смесь вирус/сыворотка добавляют в пермиссивные клетки для определения инфекционности с помощью анализа бляшкообразования. Если антитела в сыворотке крови нейтрализуют вирус, образуется меньшее количество бляшек, по сравнению с контрольной группой.
G. Применение фармацевтических композиций
1. Защита от инфекции ВПГ
Фармацевтические композиции согласно настоящему изобретению предназначены для запуска иммунного ответа против ВПГ-2. Композиции, описанные в настоящей заявке, могут стимулировать врожденный иммунный ответ, гуморальный иммунный ответ или клеточный иммунный ответ, или сочетание этих ответов у субъекта, которому вводят такие композиции. В некоторых вариантах реализации композиция стимулирует иммунные клетки в периферической зоне инфекции или в сенсорных ганглиях, такие как нейтрофилы, макрофаги и NK-клетки. Композиция настоящего изобретения может стимулировать инфильтрацию макрофагами, выработку противовирусных соединений, таких как оксид азота, TNF-α, интерферон (ИФН) и интерлейкин-12 (IL-12) нейтрофилами и/или стимулирует продукцию NK-клетками ИФН-γ. Выработка IL-2, ИФН-α и ИФН-β может также индуцироваться полипептидами в составе композиции настоящего изобретения, что, как полагают, способствует борьбе с инфекцией.
В некоторых вариантах реализации композиция содержит антигены, которые стимулируют выработку нейтрализующих антител. Нейтрализующие антитела могут быть направлены на гликопротеины вирусной оболочки, которые опосредуют взаимодействие вирионов с клеткой-хозяином и ответственны за присоединение, связывание и проникновение ВПГ-2 в клетки. Соответственно, типичная композиция включает один или более гликопротеин, описанный выше, или кодируемый нуклеиновой кислотой, описанной выше. Иммуногенные антигены и/или эпитопы, как описано в настоящей заявке, можно вводить отдельно, последовательно, а также в комбинации друг с другом.
В некоторых вариантах реализации композиция согласно настоящему изобретению запускает клеточный ответ, в который могут быть вовлечены CD4+ Т-клетки, CD8+ Т-клетки и/или выработка противовирусных цитокинов. Композиция настоящего изобретения может вызвать секрецию ИФН-γ, например, путем активации врожденного иммунного ответа, и опосредовать уничтожение вируса CD8+ Т-клетками. ИФН-γ также секретируется TH1-клетками, (TH17-клетками), TC-клетками, дендритными клетками и NK-клетками, и композиция настоящего изобретения может вызвать секрецию ИФН-γ любым из этих типов клеток. Такая активность CD8+ Т-клеток может быть цитолитической, или, как альтернатива, может регулироваться ингибирующими молекулами на поверхности нейронов, которые предотвращают киллинг нейронов. CD4+ и/или CD8+ Т-клетки могут играть роль в поддержании латентности вируса, таким образом, предотвращая реактивацию. В некоторых вариантах реализации композиция усиливает CD4+ Т-клеточный ответ и/или CD8+ Т-клеточный ответ, что предотвращает реактивацию вируса из его латентного состояния.
В некоторых вариантах реализации композиция блокирует способность ВПГ избегать иммунного ответа в организме хозяина, или, как альтернатива, усиливает иммунный ответ, от которого в норме уклоняется ВПГ. В некоторых вариантах композиция препятствует ВПГ-2 в смещении иммунологического баланса в сторону толерантности к антигенам ВПГ. ВПГ-2 может опосредовать толерантность через TH2-клетки. Во-первых, ВПГ-2 может индуцировать супрессорные Т-клетки, такие как CD4+ CD25+ клетки, и Tr1-клетки, которые секретируют IL-10, цитокины TH2. Цитокины TH2 подавляют костимулирующие молекулы и подавляют созревание и функции антигенпрезентирующих дендритных клеток. Кроме того, инфекция ВПГ-2 подавляет созревание и миграцию дендритных клеток, которые имеют существенное значение для эффективной активации ЦТЛ. Примечательно, что цитокины TH2 образуются в ходе рецидива инфекции ВПГ-2, в отличие от цитокинов TH1, которые вырабатываются в безрецидивный период. Таким образом, в некоторых вариантах реализации композиции настоящего изобретения подавляют супрессорные Т-клетки и/или индуцируют созревание и миграцию, или то и другое, дендритных клеток.
В некоторых вариантах реализации способы индукции иммунного ответа против ВПГ-2 у млекопитающего включают введение композиции, описанной выше. Композицию можно применять для индукции иммунного ответа в разные моменты времени, например, до воздействия ВПГ-2, после первичного инфицирования ВПГ-2, до или после ВПГ-2 установления латентного состояния, до или после распространения ВПГ-2, и/или до или после периодических вспышек очагов поражений. В некоторых вариантах реализации иммунный ответ против ВПГ-2 может быть вызван на одном или более из этапов, указанных выше. Композиция может вызвать ответ ТН1 и/или ответ TH17, но не ответ TH2, или может активировать такие ответы одновременно или в разное время.
В некоторых вариантах реализации введение композиции уменьшает симптомы, связанные с первичной инфекцией, латентностью или рецидивом инфекции ВПГ. Такая композиция может уменьшать частоту и/или степень тяжести поражений, ран, боль, раздражение, зуд, лихорадку, недомогание, головную боль, распространение вируса или признаки, предшествующие началу заболевания, связанные с инфекцией ВПГ или вспышки очагов поражений.
В некоторых вариантах реализации одно или более антитело к антигенам ВПГ-2 можно вводить индивидам с целью выработки пассивного иммунитета. Пассивный иммунитет представляет собой результат передачи активного гуморального иммунитета в виде готовых антител от одного человека к другому. Пассивную иммунизацию можно применять, когда существует высокий риск заражения и недостаточно времени для развития собственного иммунного ответа у организма или для уменьшения симптомов существующих или иммуносупрессорных заболеваний. Адоптивный перенос Т-клеток может обеспечить другой способ запуска иммунного ответа к антигенам ВПГ-2 у пациентов. В одном варианте расширяют специфичность действия аутологичных Т-клеток на АПК, презентирующие антигены, полученные на основе полипептидов, описанных выше. Впоследствии такие ВПГ-2-специфичные Т-клетки передают обратно в организм пациента, из которого получали исходные Т-клетки.
2. Диагностическое применение
Настоящая заявка обеспечивает, помимо прочего, быстрый, недорогой, чувствительный и специфичный способ выявления ВПГ-2 у пациентов. В этом отношении такой способ должен быть полезным для больниц и врачей, осматривающих и проводящих лечение с инфекцией ВПГ-2 или с риском такой инфекции. При использовании в настоящей заявке «пациент» обозначает индивида (например, человека), который либо инфицирован ВПГ-2 либо имеет угрозу инфицирования ВПГ-2.
В некоторых вариантах реализации можно применять антитела к одному из полипептидов, описанных в настоящей заявке, например, в Таблице 1 и/или Таблице 2, для обнаружения ВПГ-2 в человека. Настоящее изобретение также обеспечивает способ фенотипирования биологических образцов от пациентов с подозрением на инфекцию ВПГ-2, который включает: (а) подготовку биологического образца для иммунологического анализа, при необходимости, (б) обработку образца соответствующим ВПГ-2-специфичным антителом или его антиген-связывающим участком в условиях, делающих возможным связывание антитела или антиген-связывающей части с эпитопом ВПГ-2, и (в) определение того, присутствует ли в образце ВПГ-2 в сравнении с контрольной тканью; при этом, если анализ ткани пациента показывает наличие ВПГ-2, то такого пациента рассматривают как возможно инфицированного ВПГ-2.
Кроме того, можно применять полипептиды, в настоящей заявке, для выявления антител к ВПГ-2 у индивида. Настоящее описание также обеспечивает способ фенотипирования биологических образцов от пациентов с подозрением на инфекцию ВПГ-2, который включает: (а) подготовку биологического образца для аффинного анализа, такого как ИФА, в случае необходимости, (б) обработку образца ВПГ-2-специфичным антигеном или его частью в условиях, делающих возможным связывание антигена с любым антителом организма-хозяина, присутствующего в образце, а также (в) определение того, присутствует ли в образце ВПГ-2 в сравнении с контрольной тканью; при этом, если анализ ткани пациента показывает наличие ВПГ-2, то такого пациента рассматривают как возможно инфицированного ВПГ-2.
Вышеупомянутый тест может быть соответствующим образом скорректирован для выявления других вирусных инфекций, например, с помощью гомолога (из другого вида вируса) белков, описанных выше, например, в Таблице 1 и/или Таблице 2.
Ряд способов для оценки связывания антитела с антигеном, известных в данной области, в том числе твердофазный ИФА (твердофазный иммуноферментный анализ), Вестерн-блоттинга, анализ конкурентного связывания и спот-блот. Детекция может быть, например, хемилюминесцентной, флуоресцентной или колориметрической. Один из подходящих способов для оценки связывания антитела с белками представляет система Luminex xMAP, в которой пептиды конъюгированы с содержащей краситель микросферой. Некоторые системы, включая систему Xmap, предназначены для оценки различных маркеров в мультиплексе, и их можно применять для одновременного определения уровня антител. В некоторых вариантах реализации применяют другие системы для анализа множества маркеров в мультиплексе. Например, анализ спектра (профиля) можно осуществить с помощью любой из следующих систем: антигенные микрочипы, микрочипы с использованием микробусин, технологии нано-штрихкодов, микрочиповый анализ белков из экспрессионных библиотек кДНК, микрочиповый анализ белков in situ, микрочиповый анализ белков живых трансформантов, универсальный микрочиповый анализ белков, микрожидкостная технология «лаборатория на чипе» и технология «пептиды на булавке» (peptides on pins). Другой тип клинического анализа представляет собой хемилюминесцентный анализ для обнаружения антитела. В некоторых таких способах анализа, в том числе анализа VITROS Eci антител к ВПЧ-2, антитела связываются с твердой подложкой, сделанной в виде микрочастиц в жидкой суспензии, а поверхность флуорометра используется для количественной оценки ферментативного образования поколения флуоресцентного продукта.
В других вариантах реализации можно применять полипептиды, описанные выше, например, в Таблице 1 и/или в Таблице 2, для обнаружения Т-клеток, которые являются специфичными по отношению к ВПГ-2. Настоящая заявка обеспечивает способ фенотипирования биологических образцов от пациентов с подозрением на наличие инфекции ВПГ-2, включающий (а) подготовку биологического образца для анализа активации Т-клеток, в случае необходимости, (б) обработку образца ВПГ-2-специфичным полипептидом или его частью в условиях, делающих возможным процессинг полипептида в АПК, (в) оценку активации Т-клеток в ответ на ВПГ-2-специфичный полипептид; при этом усиление активации Т-клеток в образце, по сравнению с неинфицированными пациентами, указывает на наличие инфекции. Такой диагностический анализ предназначен для выявления присутствия ВПГ-2-специфичных Т-клеток у любых пациентов, включая пациентов, которые подверглись воздействию ВПГ-2, но не демонстрируют сероконверсию с образованием детектируемого уровня антител к ВПГ-2.
Активацию Т-клеток можно измерить с помощью различных способов анализа пролиферации, в том числе цитокин-специфичного ИФА, пролиферацию клеток измеряют по включению меченного тритием тимидина или встраивающегося в мембрану красителя (PKH-67) или цитоплазматического (CFSE) красителя, ELISPOT, проточной цитометрии, и микрочипового анализа с микрогранулами. Кроме того, можно измерять Т-клеточный ответ в Т-клеточных линиях или Т-клеточных гибридомах, полученных от мыши или человека, которые являются специфичными по отношению к антигенам. Показатели активированных Т-клеток включают пролиферацию, продукцию цитокинов, или индукция фермента, экспрессируемого гибридомой, при активации Т-клеток или Т-клеточной гибридомы в ответ на антиген. Например, активацию Т-клеточного ответа можно выявить с помощью Т-клеточной гибридомы, сконструированной таким образом, что она продуцирует β-галактозидазу. Активность β-галактозидазы может быть обнаружена с помощью колориметрических субстратов β-галактозидазы, таких как хлорфенил красный β-D галактопиранозид (CPRG).
Инфекция ВПГ-2 может быть острой или латентной. В некоторых вариантах реализации в случае, если биологический образец показывает наличие ВПГ-2, можно вводить пациенту терапевтически эффективное количество композиции и применять способы терапии, описанные в настоящей заявке. Биологический образец может включать, например, кровь, сперму, мочу, вагинальную жидкость, слизь, слюну, кал, мочу, спинномозговую жидкость или образец ткани. В некоторых вариантах реализации биологический образец представляет собой орган, предназначенный для трансплантации. В некоторых вариантах реализации перед стадией детекции биологический образец подлежит культивированию при условиях, способствующих росту ВПГ-2.
Диагностические тесты, приведенные в настоящей заявке, можно применять для выявления ВПГ-2 в различных образцах, в том числе образцах, взятых у пациентов, и образцах, полученных из других источников. Например, диагностические тесты можно применять для выявления ВПГ-2 на таких объектах, как медицинские инструменты. В некоторых вариантах реализации тесты, приведенные в настоящей заявке, можно проводить на образцах, взятых у животных, таких как сельскохозяйственные животные (коровы, свиньи, куры, козы, лошади и т.п.), домашние животные (собаки, кошки, птицы и т.п.) или дикие животные. В некоторых вариантах реализации тесты, описанные в настоящей заявке, можно проводить на образцах, взятых из культур клеток, таких как культуры клеток человека, продуцирующие терапевтические белки, культуры клеток бактерий, предназначенные для производства полезных биологических молекул, или культуры клеток, выращиваемые в исследовательских целях.
Изобретение также включает способ определения локализации инфекции ВПГ-2 у пациента, включающий: (а) введение пациенту фармацевтической композиции, содержащей меченое антитело к ВПГ-2 или его антиген-связывающую часть, (б) детекцию метки, и (в) определение того, присутствует ли у пациента ВПГ-2, по сравнению с контролем. В некоторых вариантах способ дополнительно включает в себя, если у пациента присутствует инфекция ВПГ-2, введение пациенту терапевтически эффективного количества композиции, описанной в настоящей заявке. Способ может дополнительно включать определение типов инфицированных клеток и/или объема ВПГ-2 у пациента. Такой способ можно применять для оценки распространения ВПГ-2 у пациента, и для определения того, целесообразно ли применение локальной терапии.
В некоторых вариантах реализации полипептиды, описанные в настоящей заявке, можно применять для прогнозирования развития инфекции. В некоторых вариантах реализации ответы Т-клеток или антител, специфичных по отношению к полипептидам настоящего изобретения, можно выявить в образце, взятом от больного. Если антитело или Т-клетки присутствуют на нормальном уровне, это означает, что у пациента индуцировался эффективный иммунный ответ против возбудителя. Если антитела или Т-клетки отсутствуют, или присутствуют на пониженном уровне, это означает, что у пациента не индуцировался достаточный ответ против возбудителя, и рекомендуется более агрессивные способы лечения. В некоторых вариантах реализации антитела или Т-клетки, присутствующие на пониженном уровне, относятся к ответам, которые присутствуют на уровне менее 50%, 20%, 10%, 5%, 2%, или 1% от типичного уровня у пациента с защитным иммунным ответом. Т-клеточный ответ может быть обнаружен с помощью способов, известных в данной области, таких как анализ Т-клеточной пролиферации, ELISPOT или ИФА, а антитела можно обнаружить на основании сродства к любому из антигенов, описанных в настоящей заявке, с помощью способов, известных в данной области, таких как ИФА.
В некоторых вариантах реализации обнаружение Т-клеток, специфичных по отношению к антигенам ВПГ-2, можно применять для прогнозирования развития и симптомов инфекции ВПГ-2 у пациента. После инфицирования ВПГ-2, некоторые пациенты не проявляют симптомов, хотя вирус может находиться в организме в латентном состоянии. Другие пациенты демонстрируют симптомы инфекции ВПГ-2, и могут периодически проявлять вспышки очагов поражений. Антигены ВПГ-2, обнаруживаемые у не проявляющих симптомы пациентов, могут отличаться от антигенов, присутствующих у пациентов, которые проявляют симптомы и/или периодическими вспышками очагов поражений. В соответствии с этим, способы детекции согласно настоящему изобретению можно применять, чтобы разлить данные подгруппы в популяции пациентов, инфицированных ВПГ-2. Подгруппы можно далее подразделить на тех пациентов, которые испытывают частые вспышки и пациентов, не испытывающих вспышки или редко испытывающих, или пациентов, у которых выделение вируса происходит на высоком уровне, и пациентов, у которых распространение вируса происходит на низком уровне или не происходит. Отнесение пациента к той или иной группе в зависимости от наличия и уровня Т-клеточных ответов на одни конкретные антигены ВПГ-2 антигенов, но не на другие антигены, может помочь практикующим врачам определить соответствующую схему лечения. Кроме того, различия в величине Т-клеточного ответа и/или различия в комбинации и уровня цитокинов, продуцируемых Т-клетками, также можно применять для прогнозирования хода и симптомов инфекции ВПГ-2 у пациента. Таким образом, инфицированному пациенту, у которого набор ВПГ-2 антигенов, на которые наблюдается ответ Т-клеток, прогнозирует тяжелые симптомы, частые вспышки и/или высокую степень выделения вируса, может потребоваться более интенсивная противовирусная терапия и/или длительный курс терапевтического лечения, чем пациенту, у которого набор антигенов к ВПГ-2 прогнозирует бессимптомную инфекцию.
Как очевидно специалистам в данной области, способы, описанные в настоящей заявке, не ограничиваются детекцией ВПГ-2. Другие варианты реализации включают детекцию родственных вирусов, включая вирусы, имеющие гомологичные белки, описанные выше, например, в Таблице 1 и/или в Таблице 2. К таким родственным вирусам относятся, например, другие представители семейства Herpesviridae. В зависимости от гомологии, к таким родственным вирусам могут также относиться вирусы, не являющиеся представителями семейства Herpesviridae.
3. Применение в группах с повышенным риском инфицирования ВПГ-2
По сути, любой человек имеет определенный риск заражения ВПГ-2. Тем не менее, некоторые группы населения имеют повышенный риск инфицирования. В некоторых вариантах реализации пациенты, получающие композицию для лечения ВПГ-2, представляют собой пациентов с ослабленным иммунитетом.
Иммунодефицитное состояние, возникающее вследствие медицинского лечения, с большой вероятностью может подвергнуть такого пациента более высокому риску инфицирования. Можно лечить инфекцию профилактически у индивидов с ослабленным иммунитетом до или во время лечения, вызывающего такое Иммунодефицитное состояние. Путем профилактического лечения антигена до или во время лечения, обуславливающего такое состояние, можно предотвратить последующее инфицирование или снизить у индивида риск инфицирования вследствие иммунодефицитного состояния. В случае, если индивид инфицировался, например, после лечения, ведущего к иммунодефицитному состоянию, также возможно лечения инфекции путем введения индивиду композиции антигена.
В некоторых вариантах реализации композиции вводят детям или взрослым пациентам. В других вариантах реализации композиции подходят для беременных женщин, которые были инфицированы до беременности, или которые были инфицированы во время беременности, например, для подавления инфекции плода или ребенка. Композиции можно также вводить новорожденным и младенцам, инфицированным внутриутробно или во время родов.
Н. Дозы и пути введения
1. Дозировка количества и сроков
Количество антигена в каждой дозе вакцины выбирают в виде эффективного количества, которое индуцирует профилактический или терапевтический ответ, как описано выше, либо в однократной дозе или виде нескольких доз. Предпочтительно, доза не вызывает существенных побочных эффектов в типичных вакцинах. Такое количество варьирует в зависимости от конкретного применяемого антигена. В целом, предполагается, что доза, например, составляет 1-1000 мкг белка, в некоторых случаях 2-100 мкг, например, 4-40 мкг. Оптимальное количество для конкретной вакцины может быть установлено путем стандартных исследований, связанных с наблюдением титра антитела, уровня активации Т-клеток, и других ответов у пациентов. В некоторых вариантах соответствующее количество вводимого антигена зависит от возраста, веса и состояния здоровья (например, иммунного статуса) субъекта. Если присутствует, адъювант добавляют, как правило, в количестве от 1 мкг до 250 мкг на дозу, например 50-150 мкг, 75-125 мкг или 100 мкг.
В некоторых вариантах реализации для достижения результатов, описанных выше, вводят только одну дозу вакцины. В других вариантах реализации после первичной вакцинации субъект получает одну или более повторную (бустер) вакцинацию, в общей сложности две, три, четыре или пять вакцинаций. Преимущественно, количество вакцинаций составляет три или менее. Повторную (бустер) вакцинацию можно проводить, например, в течение 1 месяца, 2 месяцев, 4 месяцев, 6 месяцев или 12 месяцев после первичной вакцинации, таким образом, что один режим вакцинации включает введение в течение 0, 0,5-2 и 4-8 месяцев. Может быть предпочтительно введение разделенных доз вакцин, которые можно вводить одним и тем же или различными способами.
Фармацевтические композиции, описанные в настоящей заявке, могут быть представлены в разнообразных лекарственных формах. В некоторых вариантах реализации композиция представлена в твердой форме или в порошковой (например, лиофилизированной) форме, композиция также может быть предоставлена в форме раствора. В некоторых вариантах реализации лекарственная форма представлена в виде дозы лиофилизированной композиции и по меньшей мере одного отдельного стерильного контейнера с разбавителем.
В некоторых вариантах реализации антиген вводят пациенту в количестве 1 мкмоль на дозу. В некоторых вариантах реализации антиген вводят в дозе от 10 нмоль до 100 нмоль на дозу. Соответствующее количество вводимого антигена может определить специалистов в данной области. В некоторых вариантах реализации соответствующее количество доставляемого антигена зависит от возраста, веса и состояния здоровья (например, иммунодефицитного статуса) субъекта.
Фармацевтические композиции, описанные в настоящей заявке, вводят (в некоторых вариантах) в количестве, достаточном для индукции выработки антител как части иммуногенного ответа. В некоторых вариантах композиция может быть составлена таким образом, что она содержит 5 мкг/0,5 мл или от 10 мкг/1 мл до 200 мкг/1 мл антигена. В других вариантах композиция может включать комбинацию антигенов. Каждый из антигенов может быть представлен в одной и той же концентрации, или антигены могут быть представлены в различных концентрациях.
В некоторых вариантах композицию вводят согласно схеме с увеличением дозы, таким образом, что последующие введения композиции содержат более высокую концентрацию композиции, по сравнению с предыдущими введениями. В некоторых вариантах реализации композицию вводят таким образом, что последующие введения композиции содержат более низкую концентрацию соединения, по сравнению с предыдущими введениями.
При терапевтическом применении композиции вводят пациенту, страдающему заболеванием, в количестве, достаточном для лечения или, по меньшей мере, частичного подавления развития заболевания и его осложнений.
Терапевтическое применение композиции, описанной в настоящей заявке, включает уменьшение трансмиссивности, замедление прогрессирования заболевания, уменьшение выделения вируса или устранение рецидивирующих инфекций у пациентов, которые были инфицированы ВПГ-2, например, на 90%, 80%, 70%, 60%, 50%, 40%, 30%, 20% или 10% от уровня, на котором они возникают у пациентов, не получавших лечения с помощью композиции настоящего изобретения. Композиция может также уменьшать степень распространения ВПГ-2 инфицированными пациентами, ингибировать экспрессию белков, необходимых для реактивации ВПГ-2 из латентной стадии у инфицированных пациентах, и/или подавлять репликацию ВПГ-2 в нейронах инфицированных пациентов, например, на 90%, 80%, 70%, 60%, 50%, 40%, 30%, 20%, или 10% от уровня, на котором они возникают у пациентов, не получавших лечения с помощью композиции настоящего изобретения.
При профилактическом применении композицию настоящего изобретения вводят человеку или другому млекопитающему для индукции иммунного ответа, который может препятствовать развитию инфекционного заболевания или другого патологического состояния. В некоторых вариантах реализации указанная композиция может частично препятствовать переходу вируса в латентное состояние или снижать эффективность, с которой вирус переходит в латентное состояние.
В некоторых вариантах реализации пациент получает только одну дозу (введение) композиции настоящего изобретения. В других вариантах реализации композицию вводят в различных дозах. В различных вариантах реализации композицию вводят один раз, два, три раза, или более трех раз. Количество вводимых субъекту доз зависит от антигена, степени заболевания или ожидаемого воздействия на заболевание, и реакции субъекта на композицию.
В некоторых вариантах композиции вводят в сочетании с противомикробными молекулами. Противомикробные молекулы могут включать противовирусные молекулы. Многие противовирусные молекулы известны в настоящее время в данной области, и они направленно воздействуют на одну или более стадию жизненного цикла вируса, в том числе прикрепление вируса к клеткам-хозяевам, высвобождение вирусных генов и/или ферментов в клетке-хозяине, репликации вирусных компонентов, с использованием аппарата клетки-хозяина, сборки вирусных компонентов в полные вирусные частицы, а также высвобождение вирусных частиц для заражения новых хозяев.
2. Способы введения
Вакцины и фармацевтические композиции настоящего изобретения можно вводить, как правило, посредством системного применения (например, внутривенного, внутрибрюшинного, внутримышечного, внутрикожного, подкожного, трансдермального, субдермального, внутричерепного, интраназального, мукозального, анального, вагинального, перорального, сублингвального, буккального способа введения, или посредством ингаляции), или их можно вводить посредством местного применения.
В некоторых вариантах реализации соединение можно вводить непосредственно в предполагаемые области заражения. Пациентам женского пола соединение можно наносить локально на слизистые оболочки или вводить вагинально или ректально с использованием приборов и способов, известных в данной области. Вагинальные и ректальные способы введения позволяют осуществить пролонгированную, непрерывную или импульсную доставку и введение дозированной композиции, и такая композиция может быть введена до или после контакта с ВПГ, в зависимости от применения профилактической или терапевтической композиции. У пациентов мужского пола соединение можно наносить местно на кожу или слизистые оболочки, или доставлять ректально. Обеим группам пациентов композицию можно также направленно доставлять в сенсорные ганглии.
Вакцину ВПГ-2 или фармацевтическую композицию часто вводят внутримышечно. Как правило, при таком пути введении вакцину вводят в доступную область мышечной ткани. Внутримышечные инъекции в некоторых вариантах реализации осуществляют в дельтовидную мышцу, в латеральную широкую мышцу бедра, в малую ягодичную (вентро-глютеально) или дорсо-глютеально. Инъекции, как правило, осуществляют под углом примерно 90° к поверхности кожи, таким образом, что вакцина проникает в мышцы.
Вакцину против ВПГ-2 можно также вводить подкожно. Такие инъекции, как правило, осуществляют под углом 45° к поверхности кожи, таким образом, что вакцину вводят в подкожный слой, а не в мышцы.
В некоторых вариантах реализации вакцину против ВПГ-2 вводят внутридермально. Внутридермальное введение похоже на подкожное введение, но инъекцию вводят не так глубоко, и целевым слоем кожи является дерма. Инъекцию, как правило, вводят под углом 10-15° к поверхности кожи, таким образом, что вакцина доставляется непосредственно под эпидермис.
3. Препараты
Препараты вакцины могут быть пригодны для введения человеку, и препарат вакцины может соответствовать стандартам FDA (USFDA). В некоторых вариантах реализации препарат вакцины подходит для введения животному, отличному от человека. В некоторых вариантах реализации вакцина по существу не содержит ни эндотоксинов, ни экзотоксинов. Эндотоксины включают пирогенны, такие как молекулы липополисахаридов (ЛПС). Вакцина может также по существу не содержать неактивных белковых фрагментов. В некоторых вариантах реализации пирогены содержатся в вакцине на более низком уровне, чем в промышленной воде, водопроводной воде или дистиллированной воде. Другие компоненты вакцины могут быть очищены с помощью методов, известные в данной области, например, ионообменной хроматографии, ультрафильтрации, или дистилляции. В других вариантах пирогены могут быть инактивированы или разрушены перед введением пациенту. Сырьевое вещество для вакцины, например, вода, буферы, соли и другие химические вещества можно также проверить и депирогенизировать. Все вещества, содержащиеся в вакцине, могут быть стерильными, и каждая партия вакцины может быть проверена на стерильность. Таким образом, в некоторых вариантах реализации уровень эндотоксинов в вакцине ниже уровня, установленного FDA США, например 0,2 эндотоксина (EU)/кг в препарате для интратекальной инъекции; 5 EU/кг в препарате для не интратекальной инъекции и 0,25-0,5 EU/мл для стерильной воды.
В некоторых вариантах вакцина, включающая полипептид, содержит менее 5%, 2%, 1%, 0,5%, 0,2%, 0,1% других нежелательных веществ (не полипептидов), по сравнению с количеством желаемых полипептидов. В некоторых вариантах реализации вакцина содержит менее 5%, менее 2%, менее 1%, менее 0,5%, менее 0,2%, или менее 0,1% ДНК и/или РНК.
Желательно, чтобы вакцина имела токсичность или бы не имела токсичности, с приемлемым соотношением риска и пользы.
Препараты, пригодные для включения фармацевтической композиции варьируют в зависимости от пути введения. Композиции, пригодные для парентерального введения, такого как, например, внутрисуставное введение, внутривенное, внутримышечное, внутрикожное, внутрибрюшинное, интраназальное и подкожное, включают водные и неводные, изотонические стерильные растворы для инъекций, которые могут содержать антиоксиданты, буферы, бактериостатические, и растворенные вещества, которые делают препарат изотоничным крови предполагаемого реципиента, а также водные и неводные стерильные суспензии, которые могут включать суспендирующие вещества, растворители, загустители, стабилизаторы и консерванты. Формулировки могут быть представлены в содержащих одну дозу или несколько доз герметичных контейнерах, таких как ампулы и флаконы.
Растворы для инъекций и суспензии могут быть приготовлены из стерильных порошков, гранул и таблеток описанного выше типа. Клетки, трансдуцированные с помощью упакованной нуклеиновой кислоты, также можно вводить внутривенно или парентерально.
Композиции, пригодные для перорального введения могут включать (а) жидкие растворы, например, эффективное количество полипептидов или упакованных нуклеиновых кислот, ресуспендированное в разбавителе, таком как вода, физиологический раствор или ПЭГ 400, (б) капсулы, саше или таблетки, каждая из которых содержит заданное количество активного ингредиента в виде жидкости, твердого вещества, гранулы или желатин; (в) суспензии в подходящей жидкости, и (г) подходящие эмульсии. Таблетки могут включать один или более из следующих компонентов: лактоза, сахароза, маннит, сорбит, фосфат кальция, кукурузный крахмал, картофельный крахмал, трагакант, целлюлоза микрокристаллическая, камедь, желатин, коллоидный диоксид кремния, кроскармеллоза натрия, тальк, стеарат магния, стеариновая кислота, а также другой эксципиент, краситель, наполнитель, связующее вещество, разбавитель, буферное вещество, увлажняющий агент, консервант, ароматизатор, краситель, разрыхлитель и фармацевтически совместимый носитель. Лекарственные формы в виде таблеток для рассасывания могут включать активный ингредиент вместе со вкусовой добавкой, как правило, сахарозой и камедью или трагакантовой камедью, кроме того в данной области техники известны пастилки, содержащие активный ингредиент в инертной основе, такой как желатин и глицерин или эмульсии сахарозы и камеди, гели и т.п., наряду с носителем. Фармацевтические композиции могут быть заключены, например, в липосомы, или в препарат, который обеспечивает медленное высвобождение активного ингредиента.
Антигены, отдельно или в. комбинации с другими соответствующими компонентами, могут входить в состав препарата в форме аэрозоля (например, они могут быть «распылены») для введения путем ингаляции. Аэрозольные препараты могут быть помещены в находящийся под давлением приемлемый пропеллент, такой как дихлордифторметан, пропан, азот и т.п.
К подходящим препаратам для вагинального или ректального применения относятся, например, суппозитории, включающие полипептиды или упакованные нуклеиновые кислоты с основой для суппозиториев. Подходящие основы для суппозиториев включают природные или синтетические триглицериды или парафиновые углеводороды. Кроме того, также можно применять желатиновые ректальные капсулы, которые включают полипептиды или упакованные нуклеиновые кислоты в комбинации с основой, в том числе, например, жидкими триглицеридами, полиэтиленгликолями и парафиновыми углеводородами. Препараты могут быть пригодны для введения человеку, и препарат вакцины может соответствовать стандартам FDA (USFDA). В некоторых вариантах реализации препарат вакцины подходит для введения животному, отличному от человека. В некоторых вариантах реализации композиция по существу не содержит ни эндотоксинов, ни экзотоксинов. Эндотоксины могут включать пирогены, такие как молекулы липополисахаридов (ЛПС). Композиция может также по существу не содержать неактивных белковых фрагментов, которые могут вызвать лихорадку или другие побочные эффекты. В некоторых вариантах композиция содержит менее 1%, менее 0,1%, менее 0,01%, менее 0,001%, или менее 0,0001% эндотоксинов, экзотоксинов и/или неактивных фрагментов белка. В некоторых вариантах реализации пирогены содержатся в вакцине на более низком уровне, чем в промышленной воде, водопроводной воде или дистиллированной воде. Другие компоненты вакцины могут быть очищены с помощью методов, известные в данной области, например, ионообменной хроматографии, ультрафильтрации, или дистилляции. В других вариантах пирогены могут быть инактивированы или разрушены перед введением пациенту. Сырьевое вещество для вакцины, например, вода, буферы, соли и другие химические вещества, можно также проверить и депирогенизировать. Все вещества, содержащиеся в вакцине, могут быть стерильными, и каждая партия вакцины может быть проверена на стерильность. Таким образом, в некоторых вариантах реализации уровень эндотоксинов в вакцине ниже уровня, установленного FDA США, например 0,2 эндотоксина (EU)/кг в препарате для интратекальной инъекции; 5 EU/кг в препарате для не интратекальной инъекции и 0,25-0,5 EU/мл для стерильной воды.
В некоторых вариантах реализация препарат включает менее 50%, 20%, 10% или 5% (на сухой вес) контаминирующего белка. В некоторых вариантах реализации желаемая молекула присутствует в препарате по существу с отсутствием других биологических макромолекул, таких как другие белки (в частности, другие белки, которые могут существенно маскировать, снижать, мешать или изменять характеристики белковых компонентов либо в виде очищенных препаратов или их функции в восстановленной смеси). В некоторых вариантах реализации в препарате присутствует по меньшей мере 80%, 90%, 95%, 99% или 99,8% (на сухой вес) биологических макромолекул одного и того же типа (кроме воды, буферов и других низкомолекулярных веществ, в частности молекул с молекулярным весом менее 5000).
Предпочтительно, композиция имеет низкую токсичность или совсем не токсична с приемлемым соотношением риска и пользы. В некоторых вариантах реализации композиция содержит ингредиенты в концентрациях, которые меньше показателей ЛД50 для животных, получающих композиции. Показатели ЛД50 могут быть оценены на мышах или в других экспериментальных модельных системах, и экстраполированы на людей и других животных. Методы оценки ЛД50 соединений в организме человека и других животных хорошо известны в данной области. Композиция и любой элемент внутри нее может иметь значение ЛД50 для крыс более 100 г/кг, более 50 г/кг, более 20 г/кг, более 10 г/кг, более 5 г/кг, более 2 г/кг, более 1 г/кг, более 500 мг/кг, более 200 мг/кг, более 100 мг/кг, более 50 мг/кг, более 20 мг/кг или более 10 мг/кг. В некоторых вариантах реализации терапевтический индекс композиции (измеренный как токсичная доза для 50% популяции (ТД50), разделенная на минимальную эффективную дозу для 50% популяции (ЭД50)), более 1, более 10 или более 100.
I. Подготовка и хранение препаратов вакцины и иммуногенных композиций
Вакцины против ВПГ-2, описанные в настоящей заявке, могут быть получены с помощью различных способов. Например, полипептид может быть получены с применением технологии рекомбинантной ДНК в подходящей клетке-хозяине. Подходящая клетка-хозяин может представлять собой бактериальную клетку, клетку дрожжей, млекопитающих или клетку другого типа. Клетки-хозяева могут быть модифицированы для экспрессии экзогенной копии одного из генов соответствующих полипептидов. Как правило, ген функционально связан с соответствующей регуляторной последовательностью, такой как сильный промотор и последовательность полиаденилирования. В некоторых вариантах реализации промотор является индуцибельным или репрессируемым. Также могут присутствовать другие регуляторные последовательности для секреции или выделения полипептида интереса или сохранения полипептида интереса в цитоплазме или в мембране, в зависимости от того, как будет происходить очистка полипептида. Ген может присутствовать в составе внехромосомной плазмиды или может быть интегрирован в геном хозяина. Специалисту в данной области очевидно, понятно, что не обязательно применение нуклеиновой кислоты, которая на 100% идентична природной последовательности. Скорее всего, в такую последовательность могут быть внесены изменения и они могут быть желательными. Так, например, нуклеиновые кислоты могут быть модифицированы с учетом вырожденности генетического кода, таким образом, что кодируемый полипептид останется неизменным. В некоторых вариантах последовательность гена оптимизируют по составу кодов для улучшения экспрессии в конкретной клетке-хозяине. Нуклеиновая кислота может быть получена, например, с помощью ПЦР или путем химического синтеза.
После продукции рекомбинантной клеточной линии полипептид может быть изолирован из нее. Выделение полипептида может быть осуществлено, например, с помощью методов аффинной очистки или физических методов разделения (например, по размеру на колонке).
Еще в одном аспекте настоящее изобретение обеспечивает способ изготовления, включающий смешивание одно или более полипептида или иммуногенного фрагмента или его варианта, с носителем и/или адъювантом. В некоторых вариантах реализации адъювант стимулирует TH1-клеточный ответ.
В некоторых вариантах реализации антигены для включения в композиции настоящего изобретения могут быть получены в культуре клеток. Один способ включает обеспечение одного или более вектора для экспрессии в клетках млекопитающих и клонирование нуклеотидов, кодирующих два или более полипептида, выбранных из полипептидов, имеющих аминокислотную последовательность, соответствующую одной из SEQ ID NO:1-38, с последующей экспрессией и выделением полипептида.
Иммуногенные полипептиды, описанные в настоящей заявке, и композиции из нуклеиновой кислоты, экспрессирующие полипептиды, могут быть упакованы в упаковки, дозирующие устройства, а также наборы для введения композиции из нуклеиновой кислоты в организм млекопитающего. Например, предусмотрены упаковки и устройства для дозирования, содержащие одну или более форм единичную дозированную форму. Как правило, в упаковке присутствует инструкции для применения соединений, вместе с подходящим указанием на этикетке на то, что соединение подходит для лечения указанного патологического состояния, такого, как описано в настоящей заявке.
V. Примеры
Пример 1. Идентификация антигенов ВПГ-2.
Получали библиотеку антигенов ВПГ-2 (из штамма ВПГ-2 G, парт. №7С0013, от Advanced Biotechnologies Inc, Maryland), и проводили ее скрининг с использованием мононуклеарных клеток периферической крови (МКПК) от донора-человека. Кратко, библиотеку антигенов ВПГ экспрессировали в клетках бактерий и смешивали с антигенпрезентирующими клетками (АПК). АПК, в свою очередь, презентировали пептиды ВПГ лимфоцитам, которые получали из организма пациента, инфицированного ВПГ-2. Пациенты относились к нескольким группам, как описано ниже. Ответы лимфоцитов из каждой группы сравнивали по реактивности по отношению к каждому экспрессируемому белку, и путем скрининга выявляли антигены, индуцирующие реактивные лимфоциты с большей частотой у одного пациента из группы, по сравнению с другими. У инфицированных пациентов, но не проявляющих симптомы, и пациентов, подвергшихся воздействию вируса, но серонегативных, могут активироваться защитные иммунные реакции, которые не активируются у пациентов, страдающих частыми вспышками заболеваний, в частности, у подвергшихся воздействию вируса, но серонегативных пациентов, как предполагается, сформировался стерилизующий иммунитет к инфекции ВПГ-2. Считается, что уникальный набор полипептидов активирует лимфоциты у таких пациентов.
Высвобождение ИФН-γ из CD4+ Т-клеток и CD8+ Т-клеток в каждой группе оценивали с помощью ИФА после воздействия антигенов-кандидатов. Антигены отбирали на основании кратного увеличения высвобождения ИФН-γ, по сравнению с уровнем ИФН-γ, высвобождаемого у пациентов с частыми рецидивами, которые испытывают более четырех вспышек в год.
А. Определение антигенов, кодируемых UL10, UL19, UL40, US4, US6, RS1 (RS1.1, RS1.2, RS1.3), UL 36 (UL36.3, UL36.4, UL36.5), UL32 и RL2
Лимфоциты получали от пациентов, относящихся к нескольким группам: не проявляющие симптомы (n=40), подвергшиеся воздействию вируса (n=40), проявляющие частые рецидивы, которые испытывают 4 или более вспышки в год (n=43), проявляющие менее частые рецидивы, которые испытывают менее 4 вспышек в год (n=19), нативные (n=10) и ВПГ-2-/ВПГ-1+ (n=10). В Таблице 3 представлен частотный анализ для тринадцати антигенов ВПГ-2, кодируемых UL10, UL19, UL40, US4, US6, RS1 (RS1.1, RS1.2, RS1.3), UL36 (UL36.3, UL 36.4, UL36.5), UL32, и RL2 у подвергшихся воздействию вируса пациентов, по сравнению с пациентами, демонстрирующими рецидивы с 2 и более вспышками в год.
В. Выявление антигенов, кодируемых UL1, UL49.5 и UL54
Лимфоциты получали от пациентов, относящихся к нескольким группам: не проявляющие симптомы (n=40), подвергшихся воздействию вируса (n=40), проявляющие частые рецидивы, которые испытывают 4 или более вспышки в год (n=43), проявляющие менее частые рецидивы, которые испытывают менее 4 вспышек в год (n=19), нативные (n=10) и ВПГ-2-/ВПГ-Г (n=10).
В Таблице 4 представлен частотный анализ для трех антигенов ВПГ-2, кодируемых UL1, UL49.5 и UL54 у подвергшихся воздействию вируса пациентов, по сравнению с пациентами, демонстрирующими рецидивы с 2 и более вспышками в год.
С. Выявление антигенов, кодируемых RL1, UL1 и UL11
Лимфоциты получали от пациентов, относящихся к нескольким группам: не проявляющие симптомы (n=40), подвергшихся воздействию вируса (n=40), проявляющие частые рецидивы, которые испытывают 4 или более вспышки в год (n=43), проявляющие менее частые рецидивы, которые испытывают менее 4 вспышек в год (n=19), нативные (n=10) и ВПГ-2-/ВПГ-Г (n=10).
В Таблице 5 представлен частотный анализ для трех антигенов ВПГ-2, кодируемых RL1, U11 и UL11 у подвергшихся воздействию вируса пациентов, по сравнению с пациентами, демонстрирующими рецидивы с 2 и более вспышками в год.
Пример 2. Данные, полученные in vivo
А. [Протокол А] Протокол терапевтической вакцинации морской свинки
Самкам морских свинок Hartley вводили интравагинально штамм MS ВПГ-2 при 5×105 БОЕ для инфицирования половых путей. Животных исследовали на наличие инфекции с помощью вагинального тампона на 1-й день после заражения, а также острого заболевания между 3 и 14 после инфекции. На 14-й день после развития основного заболевания животных случайны образом распределяли по группам по 12 особей и иммунизировали подкожно антигеном (полипептид ВПГ-2 в дозе 15 мкг) вместе с адъювантом (доза 50 мкг матрикс ИСКОМ со смесью 91:9 фракций сапонина килайи А и С). Каждая группа получила в общей, сложности 3 прививки в дни 14, 21 и 34 после инфекции. Генитальные мазки собирали во время периода вакцинации для контроля над распространением вируса, а также ежедневно фиксировали наблюдения. Симптомы оценивали по шкале от 0 до 4 на основании степени тяжести, 0 = отсутствие симптомов, 1 = покраснение или припухлость, 2 = небольшие пузырьки, 3 = нескольких крупных пузырьков, 4 = нескольких крупных пузырьков с мацерацией. Кроме того, животным с поражением промежуточной степени тяжести между указанными выше баллами присваивали баллы 0,5, 1,5, 2,5 или 3,5.
1. Результаты исследований терапевтической вакцинации с помощью ICP4.2, gD2ΔTMR и gD2
Результаты исследований представлены ниже в Таблицах 6-10. Титр IgG определяли на день 41 после инфицирования и 7 день после третьей иммунизации с использованием в среднем 4 из 12 животных в каждой группе. Средний балл для оценки рецидивирующих поражений и среднее количество дней проявления поражений определяли с 15 по 63 день после инфицирования. Баллы для оценки поражений представляют собой общую степень поражения для каждой группы с 15 по 60 день, после чего рассчитывали среднее значение. Среднее количество дней поражений представляет собой среднее число дней после инфицирования, в течение которых иммунизированные или не иммунизированные животные проявляли герпетические поражения. Образцы вагинальных мазков собирали ото всех животных в течение 12 дней между днями 20-59 после инфицирования и помещали на хранение при -80°С до анализа на титр выделения вируса с помощью количественной ПЦР в реальном времени.
В. [Протокол В] Протокол профилактической вакцинации мышей
Самок мышей C57BL/6 от 6 до 8 недель иммунизировали подкожно с помощью антигена (полипептид ВПГ-2) вместе с адъювантном (доза 12 мкг матрикса ИСКОМ со смесью 82:18 фракций А и С сапонина килайи) на день 0 и день 9. На 11-й день эстральные циклы синхронизировали с помощью депо-провера, после чего на 16 день мышам вводили интравагинально под наркозом 10-кратную ЛД50 штамма 333 ВПГ-2. Животных наблюдали на предмет заболеваемости (клиническая оценка) и смертности, и с 17 по 28 день после заражения оценивали массу тела и собирали мазки из влагалища,. Клинические оценки производили согласно следующей балловой шкале: 0 = отсутствие симптомов, 1 = вагинальная эритема, 2 = вагинальные эритема и отек, 3 = вагинальные герпетические поражения, 4 = односторонний паралич или тяжелая форма генитальных язв, и 5 = двусторонний паралич или смерть.
1. Результаты исследования профилактической вакцинации мышей с помощью ICP4.2, VPS, gD2ΔTMR и gD2ΔTMR и ICP4.2
В экспериментальной группе мышей иммунизированных подкожно с помощью либо 5 мкг или 10 мкг антигена вместе с адъювантом (доза 12 мкг матрикса ИСКОМ со смесью 82:18 фракций А и С сапонина килайи) на день 0 и день 9. Контрольным животным вводили только фосфатно-солевой буфер (ФСБ) или только адъювант.
Мыши, получавшие только ФСБ или только адъювант, все умерли к 9-му дню после заражения (нет выживших). В отличие от этого, мыши, получавшие антиген в значительной степени выжили к 9-му дню, и 20-75% дожили до 12-го дня после заражения. Тяжесть симптомов заболевания (генитальное и неврологическое заболевании) также оценивали на 9 или 10 день после заражения. Мыши, иммунизированные ICP4.2, VP5, gD2ΔTMR или gD2ΔTMR и ICP4.2 с адъювантом ИСКОМ, демонстрировали значительное уменьшение симптомов заболевания, по сравнению с группами мышей, которым вводили ФСБ или только адъювант.
С. [Протокол С] Протокол профилактической вакцинации морских свинок
Самок морских свинок Хартли от 250-350 грамм (вес) иммунизировали подкожно с помощью 15 мкг антигена плюс адъювант (доза 50 мкг матрицы ИСКОМ со смесью 91:9 фракций сапонина А и С из Quillaja) на день 0 и день 14-21. Сыворотку собирали путем отрезания ноготка через 2-3 недели после иммунизации, а после чего морским свинкам вводили интравагинально 5×105 БОЕ штамм MS ВПГ-2. Вагинальные мазки собирали со всех животных в дни 30 и 32, и помещали на хранение при -80°С до проведения анализа на титр вируса путем количественной ПЦР в реальном времени. Оценку состояния морских свинок проводили ежедневно (дни 1-14), и проводили количественную оценку первичного кожного заболевания половых органов с использованием балловой шкалы степени тяжести повреждений от 1 до 4. Балловые оценки соотносили с конкретными признаками заболевания следующим образом: 0, отсутствие заболевания; 1, покраснение или припухлость, 2, несколько мелких пузырьков, 3, несколько крупных пузырьков, 4, несколько крупных пузырьков с мацерацией. В конце исследования морских свинок подвергали эвтаназии, собирали дорсальные корешковые ганглии (ДКГ), помещали на хранение при -80°С до проведения количественного анализа с помощью ПЦР в реальном времени.
D. [Протокол D] Анализ иммуногенности I (стандартный)
Мышей иммунизировали подкожно в заднюю часть шеи путем 100 мкл инъекции 5 мкг антигена вместе с адъювантом (12 мкг доза матрикса ИСКОМ со смесью 82:18 фракций А и С сапонина килайи) в физиологическом растворе. Мыши получали одну или две инъекции с интервалом в 7 дней. Анализ иммуногенности инъекции проводили через 7 дней после последней инъекции.
Оценку иммуногенности проводили ex vivo путем анализа ИФН-γ методом иммуноферментных пятен (ELISPOT). CD4+ и CD8+ Т-клетки получали из селезенки и анализировали в отдельности. Для анализа с помощью ELISPOT на мембранный микропланшет наносили в течение ночи антитела для захвата и впоследствии заблокировали с помощью среды с добавками не менее 2 часов при температуре 37°С. Мышей подвергали эвтаназии, и собирали их селезенки. Затем получали Т-клетки посредством отбора CD4+ и CD8+ Т-клеток из спленоцитов с использованием магнитных бусин. Блокирующий раствор смывали с микропланшетов ELISPOT, и на блокированные микропланшеты наносили Т-клетки. Микропланшеты вновь помещали в инкубатор для адаптации Т-клеток. АПК получали путем активации нативных Т-обедненных спленоцитов с помощью антигена в течение 2 часов при температуре 37°С. Для анализа ELISPOT CD4+ АПК активировали целым белком. Для анализа ELISPOT CD8+ АПК активировали с помощью экспрессируемого в Е.coli белка вместе с cLLO (цитоплазматический листериолизип О). В контрольной среде АПК инкубировали в течение 2 часов при температуре 37°С без добавления антигена. Активированные АПК облучали, промывали и доводили их концентрацию до 2×106 клеток/мл. АПК добавляли в соответствующие лунки планшетов, содержащие Т-клетки. Затем в контрольные лунки добавляли форболмиристатацетат (ФМА) и иономицин в качестве положительного контроля. Планшеты инкубировали в течение 18 часов при 37°С при 5% СО2. После этого планшеты обрабатывали с использованием вторичных биотинилированных антител, пероксидазы хрена (ПХ) и субстрата 3-амино-9-этилкарбазол (АЭК) для проявления реакции.
1. Результаты анализа иммуногенности I с помощью ICP4.2
Анализ иммуногенности I показал выраженный иммуногенный ответ для вариантов обработки как с одной, так и с двумя инъекциями с помощью ICP4.2. Для варианта с одной инъекции количество пятен, соответствующих ИФН-γ, на 200000 Т-клеток составило 8 и 101 для CD4+ и CD8+ клеток, соответственно. Для варианта с двумя инъекциями выявлено 50 и 70 пятен, соответственно. В отличие от этого, менее 15 пятен было выявлено среды или адъюванта в отдельности, как для CD4+, так и для CD8+ клеток.
2. Результаты анализа иммуногенности I с использованием gD2ΔTMR и gD2
Результаты анализа иммуногенности I показаны на Фигуре 1А и В. Выраженный CD4+ и CD8+ Т-клеточный ответ был получен как для полноразмерного gD2, так и для gD2ΔTMR. В противоположность этому, антиген gD2, лишенный участка непосредственно перед трансмембранным доменом (обозначенный 306t на Фигуре 1) демонстрировал значительно сниженный ответ.
Е. [Протокол Е] Анализ иммуногенности II (быстрый)
В рекомбинантном штамме Е.coli из библиотеки Genocea, включающей ОРС (открытые рамки считывания) ВПГ-2, индуцировали экспрессию gL2 или фрагментов белка ICP4 (ICP4.2 и полипептиды, кодируемые RS1.1, RS1.3.1 и RS1.3.2). Белки оставались в бактериальных клетках. Бактерии затем фиксировали с помощью ПФА, тщательно промывали ФСБ, и помещали их на хранение при температуре -80°C до использования для иммунизации.
Трех мышей из группы иммунизировали с использованием 1х108 бактерий в ФСБ на мышь путем внутрибрюшинной инъекции. Мыши получали 1-2 дополнительные бустер-инъекции с интервалом в 1 неделю. Через семь дней после последней инъекции собирали сыворотку и анализировали с помощью ВПГ-2 нейтрализующего анализа. Получали пятикратные серийные разведения для образцов плазмы или сыворотки в 96-луночном круглодонном планшете, после чего в каждую лунку добавляли 50 БОЕ ВПГ-2 (штамм 333). Планшеты накрывали и инкубировали при 37°С в течение 1 часа. 200 мкл разведения вируса-сыворотки добавляли в двух повторениях к клеткам Vero, выращенных в 48-луночных культуральных планшетах, и инкубировали в течение 1 часа при 37°С. Затем в каждую лунку добавляли 300 мкл DMEM (модифицированной по способу Дульбекко среды Игла), содержащей 2% ЭТС, и планшеты инкубировали в течение 48 часов при 37°С. Для визуализации вирусных бляшек пластины окрашивали кристаллическим фиолетовым.
F. [Протокол F] Анализ иммуногенности III (перекрывающиеся пептидные пулы)
Мышей иммунизировали 2 мкг/мышь пулом перекрывающихся пептидов (ППП), охватывающих полную последовательность фрагментов gL2, ICP4, и ICP4, кодируемых RS 1.3.1 и RS1.3.2. ППП помещали в состав композиции вместе с адъювантом TiterMax (Alexis Biochemical) в общем объеме 100 мкл на мышь, при этом адъювант занимал 1/3 от дозы для подкожного введения. Мышей иммунизировали на день 0, вводили повторную бустер-инъекцию на 6 день, и 11-й день собирали селезенку и кровь. Из селезенки получали суспензию отдельных клеток, и лизировали эритроциты. Суспензию спленоцитов разделяли на две половины. Первую половину разделяли на АПК, CD4+ и CD8+ Т-клетки; наносили по 200000 Т-клеток в одну лунку планшета ELISPOT для анализа ИФН-гамма и стимулировали их с добавлением 100000 АПК и пула перекрывающихся пептидов (ППП), соответствующих иммунизации, несоответствующего пептида, положительного и отрицательного контроля. Клетки инкубировали на планшетах в течение ночи, после чего планшеты оставляли для проявления реакции и учитывали количество пятен на лунку. Вторую половину каждой суспензии прогоняли как неразделенные спленоциты (400000/лунка), активировали с помощью пептидов, и анализировали, как описано выше.
Результаты показаны на Фигуре 2А и В как величина ответа на иммунизацию в группе.
G. [Протокол G] Вакцинация с использованием по меньшей мере двух антигенов
Пример 1. Иммуногенность gD2ΔTMR u ICP4 или ICP4.2 у мышей C57BL/6
Очищенный белок смешивали с адъювантом и иммунизировали нативных мышей для оценки способности индуцировать CD4+ и CD8+ Т-клеточный ответ на белковые антигены. Кратко, антиген в отдельности (gD2ΔTMR (5 мкг)) или комбинации антигенов (gD2 gD2ΔTMR и ICP4.2 (10 мкг) смешивали с адъювантом (доза 12 мкг матрикса ИСКОМ со смесью 82:18 фракций сапонина А и С из килайи) и вводили мышам подкожно дважды с интервалом 9 дней. Через семь дней после второй иммунизации мышей подвергали эвтаназии и собирали их селезенки для анализа ex vivo IFNγ методом ELISPOT. CD4+ и CD8+ Т-клетки отделяли с помощью сортинга от популяции спленоцитов с помощью магнитных частиц, покрытых антителами, и затем кокультивировали на мембранах, покрытых специфичными к IFNγ антителами, в 96-луночных планшетах с нативными спленоцитами, которые были активированы с помощью специфичных или неспецифичных антигенов (как описано) и облучены рентгеновским излучателем. После 18 часов захваченный антителами IFNγ выявляли с помощью биотинилированных вторичных IFNγ-специфичных антител и визуализировали с помощью пероксидазы хрена и субстрата 3-амино-9-этилкарбазола. Данные представляли в виде количества единиц, образующих IFN-γ-специфичные пятна на 2×105 Т-клеток ± стандартное отклонение на основании анализа трех мышей в группе. На Фигуре 3 показано количество единиц, образующих IFN-γ-специфичные пятна на 2×105 CD4+ или CD8+ Т-клеток ± стандартное отклонение на основании анализа трех мышей в группе. Как видно на Фигурах 3А и В, количество единиц, образующих IFN-γ-специфичные пятна на 2×105 CD4+ или CD8+ Т-клеток, увеличено у мышей, иммунизированных с помощью антигена gD2ΔTMR в комбинации с ICP4.2, по сравнению с антигеном gD2ΔTMR в отдельности.
Пример 2. Иммунизация с использованием комбинации gD2 и ICP4.2 вместе с адъювантом снижает симптомы заболевания и смертность у мышей.
Способность запускать защитный иммунитет после иммунизации с помощью белка ICP4.2 в комбинации с gD2 вместе с адъювантом оценивали с использованием в качестве модели мышей, на которых воздействовали летальной дозой ВПГ-2. Кратко, восемь мышей C57BL/6 на группу иммунизировали либо с помощью gD2 (2 мкг) или ICP4.2 (10 мкг) вместе с адъювантом в отдельности или с помощью обоих антигенов вместе с адъювантом. Препараты вводили подкожно в заднюю часть шеи дважды с интервалом 9 дней. За 5 дней перед инфицированием вирусом эстральные циклы синхронизировали с помощью депо-провера, и через 7 дней после второй иммунизации животным вводили интравагинально 20-кратную ЛД50 штамма 333 ВПГ-2. После инфицирования оценивали степень тяжести симптомов у животных и их выживаемость. Клинические оценки производили согласно следующей балловой шкале: 0 = отсутствие симптомов, 1 = покраснения, 2 = покраснения и отек, 3 = герпетические поражения, 4 = тяжелая форма изъязвления или односторонний паралич, и 5 = двусторонний паралич или смерть.
Пример 3. Иммунизация с использованием комбинации gD2ΔTMR и ICP4.2 вместе с адъювантом снижает симптомы заболевания и смертность у мышей
Мыши, иммунизированные комбинацией антигенов gD2ΔTMR и ICP4.2, демонстрировали более низкий средний балл заболевания на десятый день после воздействия вируса, по сравнению с животными, получающими каждый из антигенов в отдельности вместе с адъювантом.
Пример 4. Иммунизация с помощью комбинации gD2 и ICP4.2 вместе с адъювантом снижает тяжесть рецидивирующих поражений при терапевтическом введении морским свинкам, инфицированным ВПГ-2
Оценивали способность терапевтической вакцинации с помощью антигенов вместе с адъювантом влиять на реактивацию ВПГ-2 у инфицированных морских свинок. Кратко, морских свинок инфицировали интравагинально с использованием 5×105 БОЕ штамма MS ВПГ-2, наблюдали за развитием первичного заболевания в течение 14 дней, и затем распределяли морских свинок по группам для иммунизации (N=15). Животных иммунизировали три раза подкожно на 14, 21 и 35 день после инфицирования с использованием антигена (15 мкг) вместе с адъювантом (50 мкг) или адъювантом в отдельности, или растворителем в качестве контроля, и ежедневно оценивали степень тяжести локального заболевания, день на местном тяжести заболевания. Балловая система оценки была следующей: 0 = отсутствие симптомов, 1 = покраснения, 2 = отдельные поражения, 3 = обильные и сплошные герпетические поражения, 4 = тяжелая форма изъязвления или односторонний паралич, и 5 = двусторонний паралич или смерть.
На Таблице 16 показаны данные в виде среднего балла рецидивирующих поражений для каждой недели после того, как морские свинки оправлялись от острого заболевания. Морские свинки, получавшие комбинацию антигенов gD2 и ICP4.2, демонстрировали снижение среднего балла поражений через 7 (день 42) и 14 (49 день) дней после их последней иммунизации, по сравнению с животными, получавших антигены в отдельности вместе с адъювантом.
| название | год | авторы | номер документа |
|---|---|---|---|
| ВАКЦИНЫ И КОМПОЗИЦИИ, НАПРАВЛЕННЫЕ ПРОТИВ STREPTOCOCCUS PNEUMONIAE | 2010 |
|
RU2580299C2 |
| ВАКЦИНЫ И КОМПОЗИЦИИ ПРОТИВ STREPTOCOCCUS PNEUMONIAE | 2012 |
|
RU2623174C2 |
| ИММУНОГЕННЫЕ КОМПОЗИЦИИ И СПОСОБЫ | 2008 |
|
RU2468034C2 |
| КОМПОЗИЦИИ И СПОСОБЫ ЛЕЧЕНИЯ ГРИБКОВЫХ И БАКТЕРИАЛЬНЫХ ПАТОГЕНОВ | 2014 |
|
RU2717306C2 |
| КОМПОЗИЦИИ И СПОСОБЫ ДЛЯ ЛЕЧЕНИЯ ЦИТОМЕГАЛОВИРУСА | 2012 |
|
RU2737530C1 |
| КОМПОЗИЦИИ И СПОСОБЫ ДЛЯ ЛЕЧЕНИЯ АКТИВНОЙ ИНФЕКЦИИ MYCOBACTERIUM TUBERCULOSIS | 2013 |
|
RU2659149C2 |
| ВАКЦИННЫЙ АНТИГЕН БАБЕЗИОЗА СОБАК | 2011 |
|
RU2599544C2 |
| ИММУНОГЕННЫЕ КОМПОЗИЦИИ ДЛЯ ИММУНИЗАЦИИ СВИНЕЙ ПРОТИВ ЦИРКОВИРУСА ТИПА 3 И СПОСОБЫ ИХ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЯ | 2016 |
|
RU2744193C2 |
| ИММУНОГЕНЫ ДЛЯ ВАКЦИНАЦИИ ПРОТИВ ВИЧ | 2013 |
|
RU2648791C2 |
| УКОРОЧЕННАЯ СЕКРЕТИРУЕМАЯ АСПАРТИЛ-ПРОТЕИНАЗА 2 | 2008 |
|
RU2493255C2 |
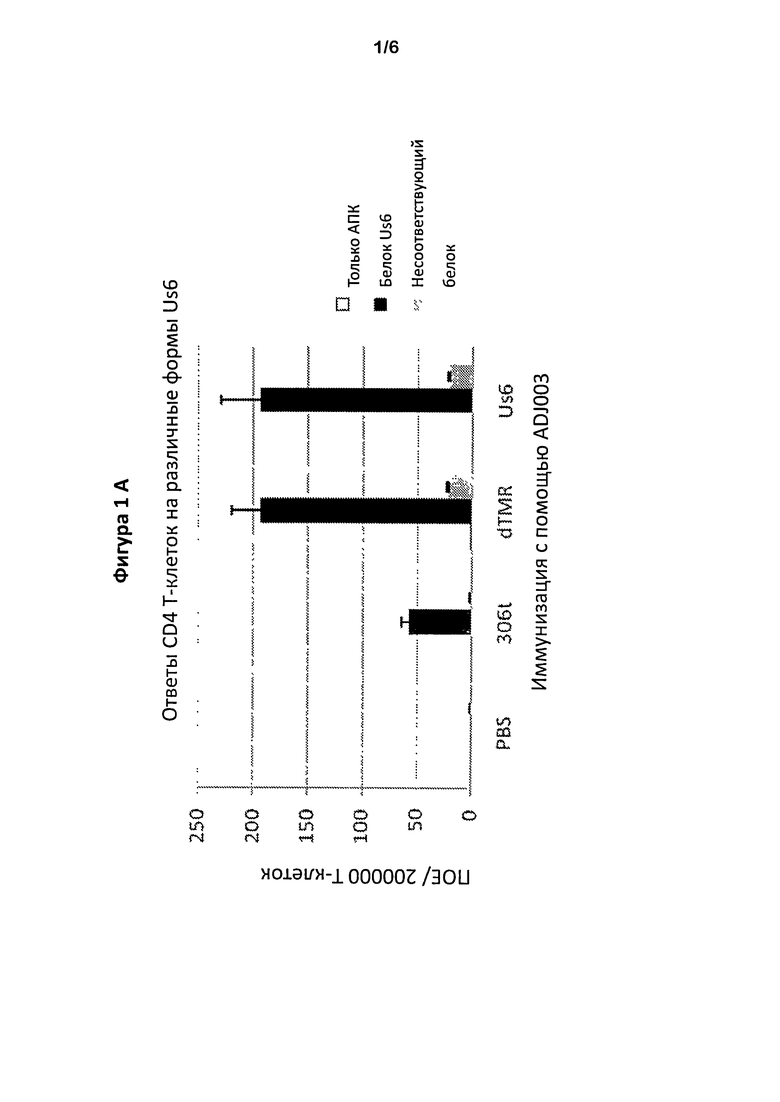
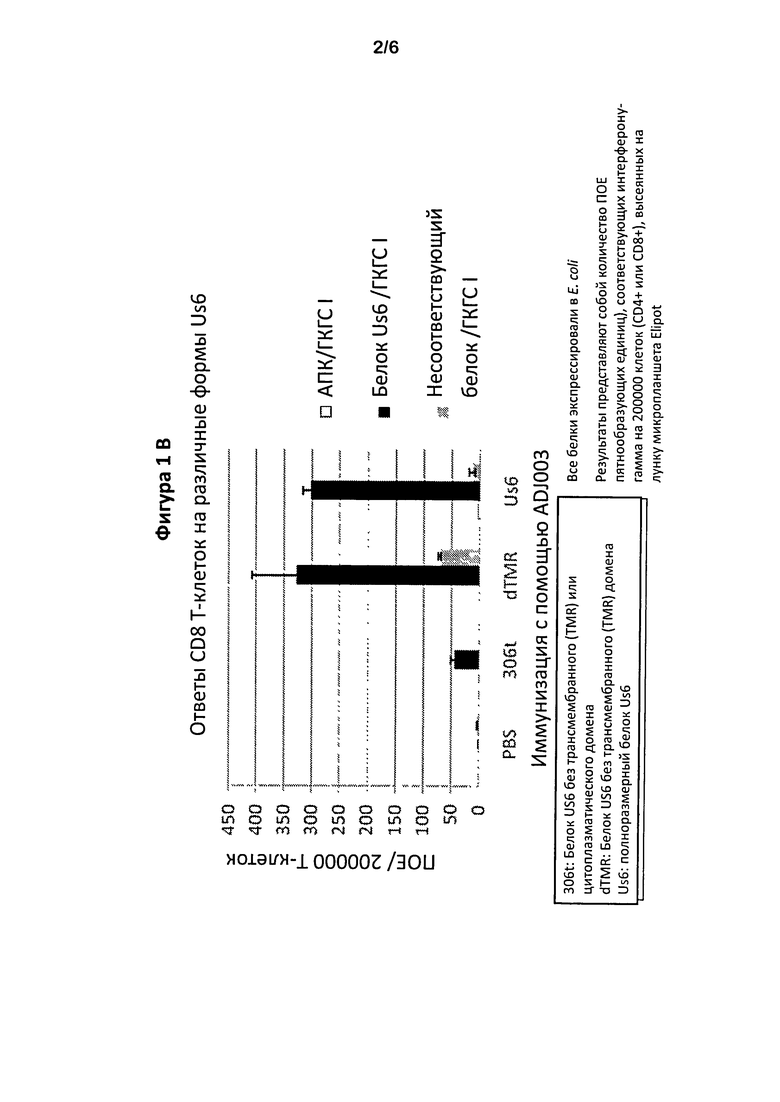
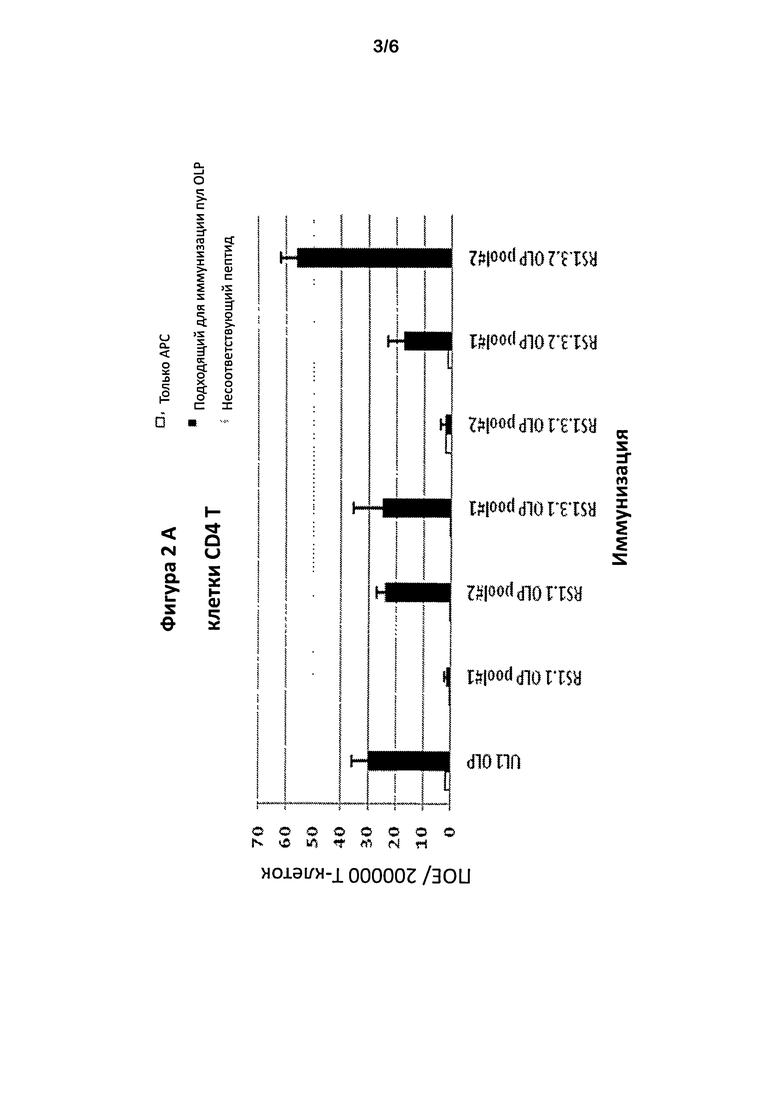
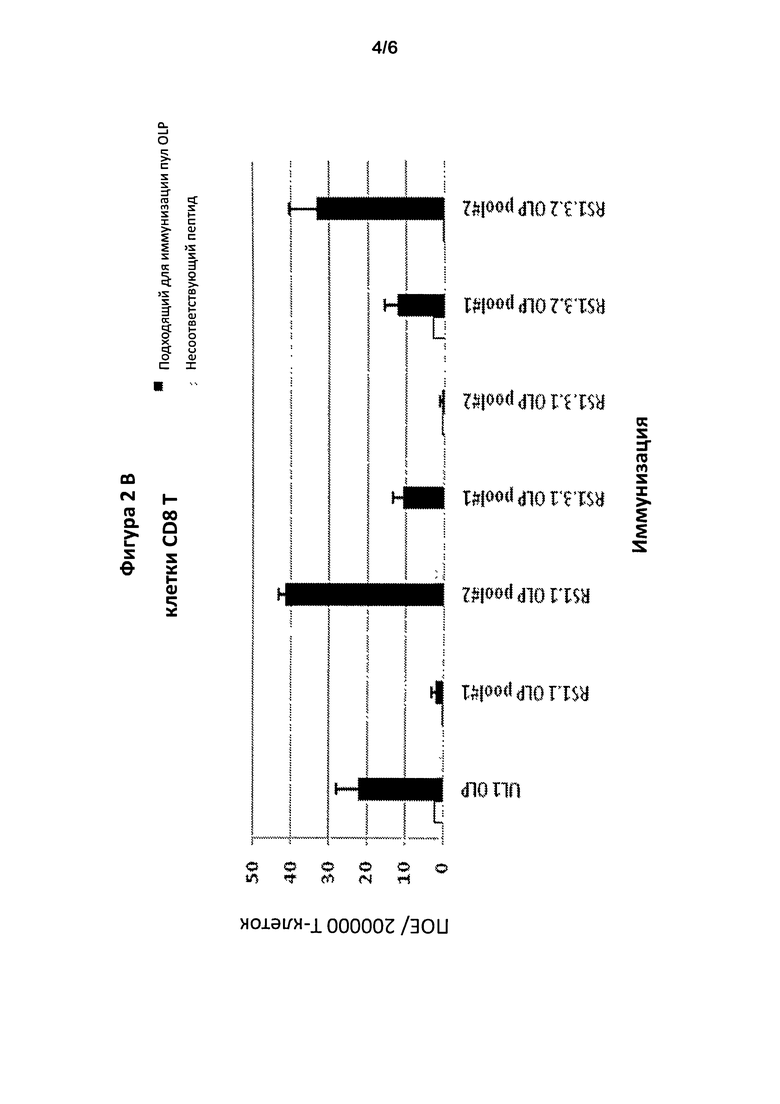
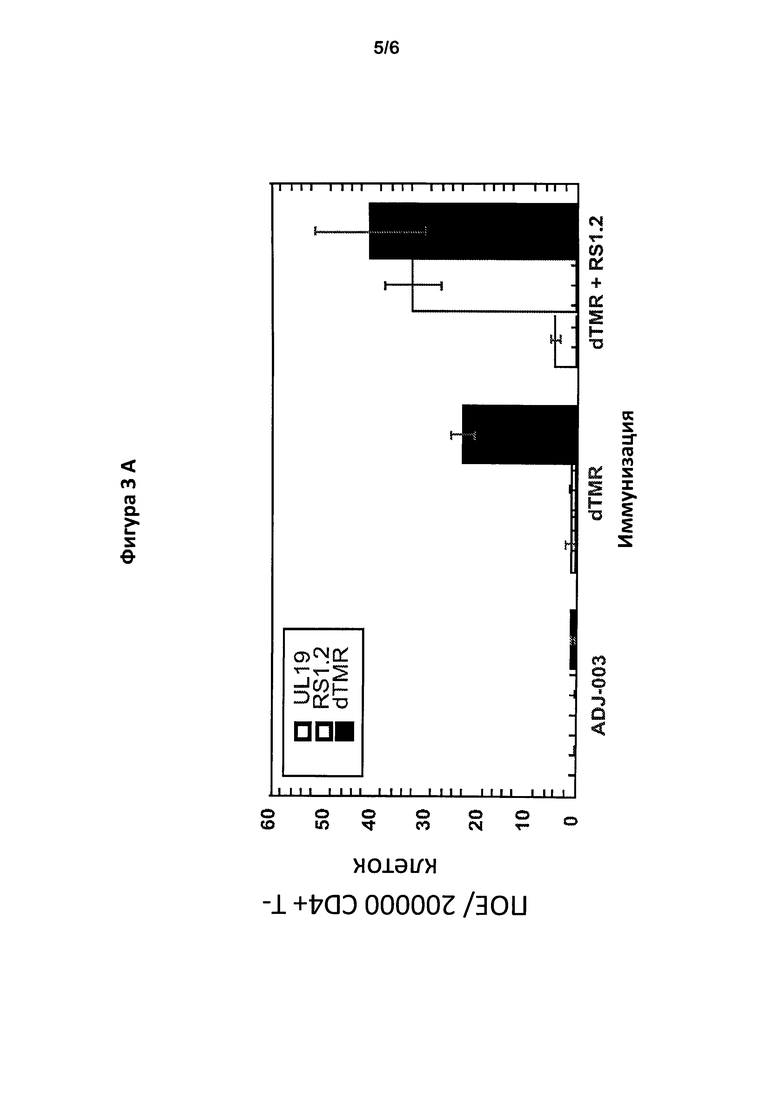
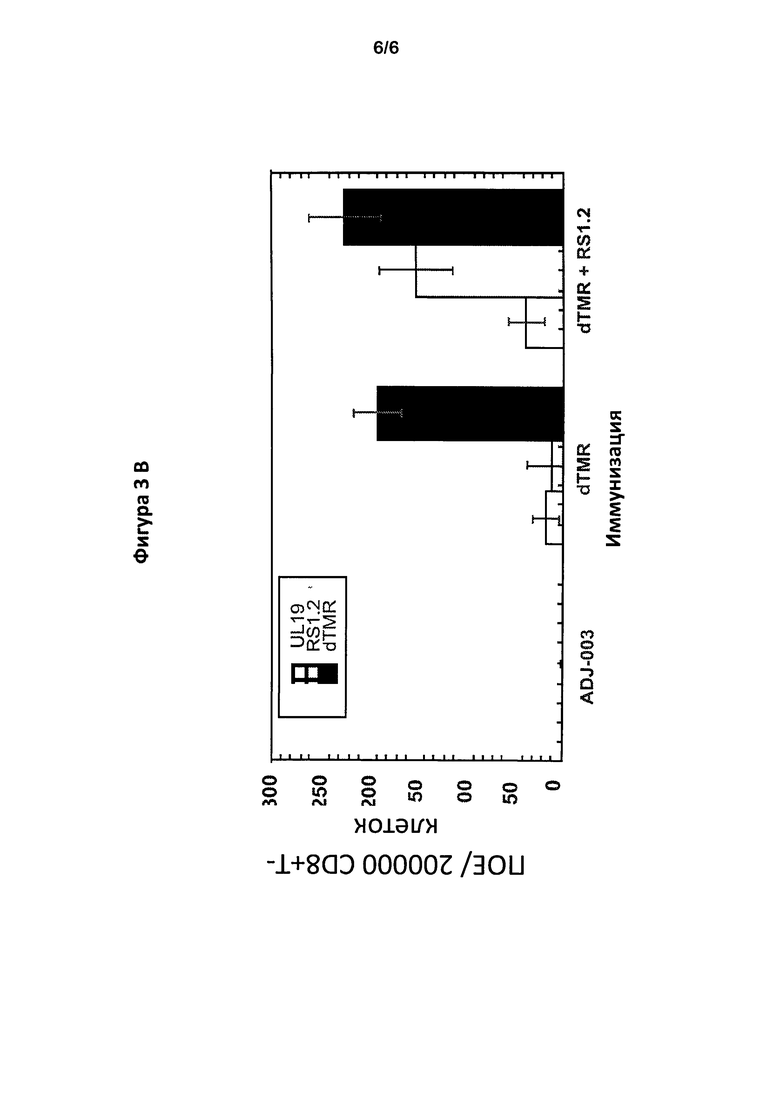







































































































































































Группа изобретений относится к медицине, а именно к иммунологии, и может быть использована для получения препарата вакцины против вируса простого герпеса (ВПГ). Препарат содержит фармацевтически приемлемый носитель и полипептид, содержащий аминокислотную последовательность SEQ ID NO: 2 или содержащий аминокислотную последовательность SEQ ID NO: 2, в которой отсутствует 1-20 аминокислот с N-конца, С-конца или с обоих концов. Группа изобретений относится также к применению изолированных полипептидов для получения лекарственного средства для лечения пациента от инфекции вируса простого герпеса. Использование данной группы изобретений позволяет применять выделенные полипептиды, представленные SEQ ID NO: 2 отдельно или в комбинации с SEQ ID NO: 4 и SEQ ID NO: 5 в качестве эффективной вакцины. 8 н. и 130 з.п. ф-лы, 16 табл., 6 ил.
1. Препарат вакцины против вируса простого герпеса (ВПГ), содержащий фармацевтически приемлемый носитель и полипептид, содержащий аминокислотную последовательность SEQ ID NO: 2 или содержащий аминокислотную последовательность SEQ ID NO: 2, в которой отсутствует 1-20 аминокислот с N-конца, С-конца или с обоих концов.
2. Препарат вакцины по п. 1, дополнительно содержащий полипептид gD2.
3. Препарат вакцины по п. 1, дополнительно содержащий полипептид gD2, в котором отсутствует трансмембранный домен и отсутствует цитоплазматический домен.
4. Препарат вакцины по п. 1, дополнительно содержащий полипептид gD2, в котором отсутствует трансмембранный домен.
5. Препарат вакцины по п. 1, дополнительно содержащий второй полипептид, который состоит из аминокислотной последовательности SEQ ID NO: 3, или SEQ ID NO: 4, или SEQ ID NO: 5.
6. Препарат вакцины по п. 1, дополнительно содержащий второй полипептид, который состоит из аминокислотной последовательности SEQ ID NO: 4 или SEQ ID NO: 5.
7. Препарат вакцины по п. 1, дополнительно содержащий второй полипептид, который состоит из аминокислотной последовательности SEQ ID NO: 4.
8. Препарат вакцины по п. 1, дополнительно содержащий второй полипептид, который состоит из аминокислотной последовательности SEQ ID NO: 3, и третий полипептид, который состоит из аминокислотной последовательности SEQ ID NO: 4.
9. Препарат вакцины по п. 1, дополнительно содержащий второй полипептид, который состоит из аминокислотной последовательности SEQ ID NO: 3, и третий полипептид, который состоит из аминокислотной последовательности SEQ ID NO: 5.
10. Препарат вакцины по п. 1, отличающийся тем, что указанный полипептид содержит аминокислотную последовательность SEQ ID NO: 2, в которой отсутствует 1-10 аминокислотных остатков с N-конца, С-конца или с обоих концов.
11. Препарат вакцины по п. 1, дополнительно содержащий второй полипептид, содержащий аминокислотную последовательность SEQ ID NO: 5, в которой отсутствуют все или по меньшей мере 8 последовательных аминокислотных остатков из остатков 340-363 SEQ ID NO: 5.
12. Препарат вакцины по п. 1, дополнительно содержащий второй полипептид, содержащий аминокислотную последовательность SEQ ID NO: 4 или аминокислотную последовательность SEQ ID NO: 4, в которой отсутствует 1-20 аминокислот с N-конца, С-конца или с обоих концов.
13. Препарат вакцины по п. 1, дополнительно содержащий второй полипептид, содержащий аминокислотную последовательность, которая по меньшей мере на 95% идентична SEQ ID NO: 4.
14. Препарат вакцины по п. 1, дополнительно содержащий второй полипептид, содержащий аминокислотную последовательность SEQ ID NO: 5 или аминокислотную последовательность SEQ ID NO: 5, в которой отсутствует 1-20 аминокислот с N-конца, С-конца или с обоих концов.
15. Препарат вакцины по п. 1, дополнительно содержащий второй полипептид, содержащий аминокислотную последовательность, которая по меньшей мере на 95% идентична SEQ ID NO: 5.
16. Препарат вакцины по любому из пп. 1-15, отличающийся тем, что по меньшей мере один полипептид не гликозилирован.
17. Препарат вакцины по п. 1, дополнительно содержащий второй полипептид, содержащий аминокислотную последовательность SEQ ID NO: 3 или аминокислотную последовательность SEQ ID NO: 3, в которой отсутствует 1-20 аминокислот с N-конца, С-конца или с обоих концов.
18. Препарат вакцины по любому из пп. 1-15, отличающийся тем, что указанный по меньшей мере один полипептид конъюгирован с иммуногенным носителем.
19. Препарат вакцины по любому из пп. 1-15, дополнительно содержащий адъювант.
20. Препарат вакцины по п. 19, отличающийся тем, что указанный адъювант представляет собой одну или больше очищенных фракций сапонинов килайи.
21. Препарат вакцины п. 20, отличающийся тем, что указанный адъювант включает фракцию сапонина А и фракцию сапонина С.
22. Препарат вакцины по п. 21, отличающийся тем, что указанный адъювант включает холестерин, фосфатидилхолин, фракцию сапонина А и фракцию сапонина С.
23. Препарат вакцины по п. 22, отличающийся тем, что указанный адъювант находится в форме частиц.
24. Препарат вакцины по п. 23, отличающийся тем, что частицы, включающие фракцию сапонина А, содержат менее 20%, 15%, 10%, 5%, 4%, 3%, 2% или 1% фракции сапонина С и частицы, включающие фракцию сапонина С, содержат менее 20%, 15%, 10%, 5%, 4%, 3%, 2% или 1% фракции сапонина А.
25. Препарат вакцины по п. 19, отличающийся тем, что указанный препарат вакцины содержит 5-200 мкг указанного полипептида или полипептидов и 5-200 мкг адъюванта.
26. Препарат вакцины по любому из пп. 1-15, отличающийся тем, что по меньшей мере один полипептид конъюгирован с меткой.
27. Препарат вакцины по любому из пп. 1-15, отличающийся тем, что после введения субъекту указанный препарат вакцины подавляет инфекцию вирусом ВПГ-1, ВПГ-2 или ВПГ-1 и ВПГ-2 у субъекта.
28. Препарат вакцины по любому из пп. 1-15, отличающийся тем, что после введения субъекту указанный препарат вакцины лечит инфекцию вирусом ВПГ-1, ВПГ-2 или ВПГ-1 и ВПГ-2 у субъекта.
29. Препарат вакцины по любому из пп. 1-15, отличающийся тем, что после введения субъекту указанный препарат вакцины обеспечивает лечение герпеса у субъекта.
30. Препарат вакцины по п. 29, отличающийся тем, что герпес представляет собой генитальный герпес.
31. Препарат вакцины по любому из пп. 1-15, отличающийся тем, что указанный препарат вакцины подавляет один или более симптомов герпеса.
32. Препарат вакцины по любому из пп. 1-15, отличающийся тем, что указанный препарат вакцины подавляет появление симптомов герпеса.
33. Препарат вакцины по любому из пп. 1-15, отличающийся тем, что указанный препарат вакцины снижает тяжесть симптомов герпеса.
34. Препарат вакцины по любому из пп. 1-15, отличающийся тем, что указанный препарат вакцины снижает повторное проявление симптомов герпеса.
35. Препарат вакцины по любому из пп. 1-15, отличающийся тем, что указанный препарат вакцины снижает частоту симптомов герпеса.
36. Препарат вакцины по любому из пп. 1-15, отличающийся тем, что указанный препарат вакцины снижает выделение вируса.
37. Препарат вакцины по п. 36, отличающийся тем, что указанный препарат вакцины снижает передачу вируса.
38. Препарат вакцины по любому из пп. 1-15, отличающийся тем, что указанный препарат вакцины снижает количество герпетических поражений.
39. Препарат вакцины по любому из пп. 1-15, отличающийся тем, что указанный препарат вакцины сокращает количество дней, в течение которых у субъекта присутствуют герпетические поражения.
40. Препарат вакцины по любому из пп. 1-15, отличающийся тем, что указанный препарат вакцины подавляет инфекцию ВПГ-2 у неинфицированного субъекта.
41. Препарат вакцины по любому из пп. 1-15, отличающийся тем, что указанный препарат вакцины увеличивает титр IgG на один или более антигенов ВПГ-2.
42. Препарат вакцины по любому из пп. 1-15, отличающийся тем, что указанный препарат вакцины индуцирует ответ антител на один или более антигенов ВПГ-2.
43. Препарат вакцины по любому из пп. 1-15, отличающийся тем, что указанный препарат вакцины активирует Т-клеточный ответ на один или более антигенов ВПГ-2.
44. Препарат вакцины по любому из пп. 1-15, отличающийся тем, что указанный препарат вакцины усиливает Т-клеточный ответ на один или более антигенов ВПГ-2.
45. Препарат вакцины по любому из пп. 1-15, отличающийся тем, что указанный препарат вакцины сокращает количество герпетических поражений в начале развития инфекции вирусом ВПГ-2.
46. Препарат вакцины по любому из пп. 1-15, отличающийся тем, что указанный препарат вакцины подавляет один или более симптомов ВПГ-2 или подавляет инфекцию вирусом ВПГ-2 в трех или менее дозах.
47. Препарат вакцины по любому из пп. 1-15, отличающийся тем, что указанный препарат вакцины лечит инфекцию вирусом ВПГ-1, ВПГ-2 или ВПГ-1 и ВПГ-2 в трех или менее дозах.
48. Препарат вакцины по любому из пп. 1-15, отличающийся тем, что указанный препарат вакцины вводят до, одновременно с или после лечения противовирусной молекулой.
49. Препарат вакцины по любому из пп. 1-15, отличающийся тем, что указанный препарат вакцины снижает риск ВИЧ-инфекции.
50. Препарат вакцины по п.1, отличающийся тем, что указанный полипептид, состоит из аминокислотной последовательности SEQ ID NO: 2, в которой отсутствует 1-20 аминокислот с N-конца, С-конца или с обоих концов.
51. Препарат вакцины против ВПГ, содержащий фармацевтически приемлемый носитель и полипептид, содержащий аминокислотную последовательность, которая по меньшей мере на 95% идентична SEQ ID NO: 2.
52. Препарат вакцины по п. 51, дополнительно включающий полипептид gD2.
53. Препарат вакцины по п. 51, дополнительно включающий полипептид gD2, у которого отсутствует трансмембранный домен и отсутствует цитоплазматический домен.
54. Препарат вакцины по п. 51, дополнительно включающий полипептид gD2, у которого отсутствует трансмембранный домен.
55. Препарат вакцины по п. 51, дополнительно включающий второй полипептид, состоящий из аминокислотной последовательности SEQ ID NO: 3, или SEQ ID NO: 4, или SEQ ID NO: 5.
56. Препарат вакцины по п. 51, дополнительно включающий второй полипептид, состоящий из аминокислотной последовательности SEQ ID NO: 4 или SEQ ID NO: 5.
57. Препарат вакцины по п. 51, дополнительно включающий второй полипептид, состоящий из аминокислотной последовательности SEQ ID NO: 4.
58. Препарат вакцины по п. 51, дополнительно включающий второй полипептид, состоящий из аминокислотной последовательности SEQ ID NO: 3, и третий полипептид, состоящий из аминокислотной последовательности SEQ ID NO: 4.
59. Препарат вакцины по п. 51, дополнительно включающий второй полипептид, состоящий из аминокислотной последовательности SEQ ID NO: 3, и третий полипептид, состоящий из аминокислотной последовательности SEQ ID NO: 5.
60. Препарат вакцины по п. 51, отличающийся тем, что указанный полипептид включает аминокислотную последовательность SEQ ID NO: 2, в которой отсутствует 1-10 аминокислотных остатков с N-конца, С-конца или с обоих концов.
61. Препарат вакцины по п. 51, дополнительно включающий второй полипептид, включающий аминокислотную последовательность SEQ ID NO: 5, в которой отсутствуют все или по меньшей мере 8 последовательных аминокислотных остатков из остатков 340-363 в SEQ ID NO: 5.
62. Препарат вакцины по п. 51, дополнительно включающий второй полипептид, включающий аминокислотную последовательность SEQ ID NO: 4 или аминокислотную последовательность SEQ ID NO: 4, в которой отсутствует 1-20 аминокислотных остатков с N-конца, С-конца или с обоих концов.
63. Препарат вакцины по п. 51, дополнительно включающий второй полипептид, включающий аминокислотную последовательность, которая по меньшей мере на 95% идентична SEQ ID NO: 4.
64. Препарат вакцины по п. 51, дополнительно включающий второй полипептид, включающий аминокислотную последовательность SEQ ID NO: 5 или аминокислотную последовательность SEQ ID NO: 5, в которой отсутствует 1-20 аминокислотных остатков с N-конца, С-конца или с обоих концов.
65. Препарат вакцины по п. 51, дополнительно включающий второй полипептид, включающий аминокислотную последовательность, которая по меньшей мере на 95% идентична SEQ ID NO: 5.
66. Препарат вакцины по любому из пп. 51-65, отличающийся тем, что по меньшей мере один полипептид не гликозилирован.
67. Препарат вакцины по п. 51, дополнительно включающий второй полипептид, включающий аминокислотную последовательность SEQ ID NO: 3 или аминокислотную последовательность SEQ ID NO: 3, в которой отсутствует 1-20 аминокислотных остатков с N-конца, С-конца или с обоих концов.
68. Препарат вакцины по любому из пп. 51-65, в котором по меньшей мере один полипептид конъюгирован с иммуногенным носителем.
69. Препарат вакцины по любому из пп. 51-65, дополнительно содержащий адъювант.
70. Препарат вакцины по п. 69, отличающийся тем, что указанный адъювант представляет собой одну или больше очищенных фракций сапонинов килайи.
71. Препарат вакцины по п. 70, отличающийся тем, что указанный адъювант включает фракцию сапонина А и фракцию сапонина С.
72. Препарат вакцины по п. 71, отличающийся тем, что указанный адъювант включает холестерин, фосфатидилхолин, фракцию сапонина А и фракцию сапонина С.
73. Препарат вакцины по п. 72, отличающийся тем, что указанный адъювант находится в форме частиц.
74. Препарат вакцины по п. 73, отличающийся тем, что частицы, включающие фракцию сапонина А, содержат менее 20%, 15%, 10%, 5%, 4%, 3%, 2% или 1% фракции сапонина С и частицы, включающие фракцию сапонина С, содержат менее 20%, 15%, 10%, 5%, 4%, 3%, 2% или 1% фракции сапонина А.
75. Препарат вакцины по п. 69, отличающийся тем, что указанный препарат вакцины содержит 5-200 мкг указанного полипептида или полипептидов и 5-200 мкг адъюванта.
76. Препарат вакцины по любому из пп. 51-65, отличающийся тем, что по меньшей мере один полипептид конъюгирован с меткой.
77. Препарат вакцины по любому из пп. 51-65, отличающийся тем, что после введения субъекту указанный препарат вакцины подавляет инфекцию вирусом ВПГ-1, ВПГ-2 или ВПГ-1 и ВПГ-2 у субъекта.
78. Препарат вакцины по любому из пп. 51-65, отличающийся тем, что после введения субъекту указанный препарат вакцины лечит инфекцию вирусом ВПГ-1, ВПГ-2 или ВПГ-1 и ВПГ-2 у субъекта.
79. Препарат вакцины по любому из пп. 51-65, отличающийся тем, что после введения субъекту указанный препарат вакцины лечит герпес у субъекта.
80. Препарат вакцины по п. 79, отличающийся тем, что герпес представляет собой генитальный герпес.
81. Препарат вакцины по любому из пп. 51-65, отличающийся тем, что указанный препарат вакцины подавляет один или более симптомов герпеса.
82. Препарат вакцины по любому из пп. 51-65, отличающийся тем, что указанный препарат вакцины подавляет появление симптомов герпеса.
83. Препарат вакцины по любому из пп. 51-65, отличающийся тем, что указанный препарат вакцины снижает тяжесть симптомов герпеса.
84. Препарат вакцины по любому из пп. 51-65, отличающийся тем, что указанный препарат вакцины снижает повторное появление симптомов герпеса.
85. Препарат вакцины по любому из пп. 51-65, отличающийся тем, что указанный препарат вакцины снижает частоту симптомов герпеса.
86. Препарат вакцины по любому из пп. 51-65, отличающийся тем, что указанный препарат вакцины снижает выделение вируса.
87. Препарат вакцины по п. 85, отличающийся тем, что указанный препарат вакцины снижает передачу вируса.
88. Препарат вакцины по любому из пп. 51-65, отличающийся тем, что указанный препарат вакцины снижает количество герпетических поражений.
89. Препарат вакцины по любому из пп. 51-65, отличающийся тем, что указанный препарат вакцины сокращает количество дней, в течение которых у субъекта присутствуют герпетические поражения.
90. Препарат вакцины по любому из пп. 51-65, отличающийся тем, что указанный препарат вакцины подавляет инфекцию вирусом ВПГ-2 у неинфицированного субъекта.
91. Препарат вакцины по любому из пп. 51-65, отличающийся тем, что указанный препарат вакцины увеличивает титр IgG на один или более антигенов ВПГ-2.
92. Препарат вакцины по любому из пп. 51-65, отличающийся тем, что указанный препарат вакцины индуцирует ответ антител на один или более антигенов ВПГ-2.
93. Препарат вакцины по любому из пп. 51-65, отличающийся тем, что указанный препарат вакцины активирует Т-клеточный ответ на один или более антигенов ВПГ-2.
94. Препарат вакцины по любому из пп. 51-65, отличающийся тем, что указанный препарат вакцины усиливает Т-клеточный ответ на один или более антигенов ВПГ-2.
95. Препарат вакцины по любому из пп. 51-65, отличающийся тем, что указанный препарат вакцины снижает количество герпетических поражений в начале развития инфекции вирусом ВПГ-2.
96. Препарат вакцины по любому из пп. 51-65, отличающийся тем, что указанный препарат вакцины подавляет один или более симптомов ВПГ-2 или подавляет инфекцию вирусом ВПГ-2 в трех или менее дозах.
97. Препарат вакцины по любому из пп. 51-65, отличающийся тем, что указанный препарат вакцины лечит инфекцию вирусом ВПГ-1, ВПГ-2 или ВПГ-1 и ВПГ-2 в трех или менее дозах.
98. Препарат вакцины по любому из пп. 51-65, отличающийся тем, что указанный препарат вакцины вводят до, одновременно с или после лечения противовирусной молекулой.
99. Препарат вакцины по любому из пп. 51-65, отличающийся тем, что указанный препарат вакцины снижает риск ВИЧ-инфекции.
100. Препарат вакцины против ВПГ, включающий фармацевтически приемлемый носитель и полипептид, содержащий аминокислотную последовательность SEQ ID NO: 2, конъюгированную с иммуногенным носителем, сигнальной последовательностью, или полипептидом из не более чем 20 аминокислот на N-конце или С-конце указанного полипептида.
101. Применение препарата вакцины по пп. 1-100 для получения лекарственного средства для лечения субъекта, страдающего от или восприимчивого к инфекции вирусом ВПГ-1, ВПГ-2 или ВПГ-1 и ВПГ-2.
102. Применение по п. 101, отличающееся тем, что указанное лечение подавляет инфекци вирусом ВПГ-1, ВПГ-2 или ВПГ-1 и ВПГ-2 у субъекта.
103. Применение по п. 101, отличающееся тем, что указанное лечение лечит инфекцию вирусом ВПГ-1, ВПГ-2 или ВПГ-1 и ВПГ-2 у субъекта.
104. Применение по п. 101, отличающееся тем, что указанное лечение лечит герпес у субъекта.
105. Применение по п. 104, отличающееся тем, что герпес представляет собой генитальный герпес.
106. Применение по п. 101, отличающееся тем, что указанное лечение подавляет один или более симптомов герпеса.
107. Применение по п. 101, отличающееся тем, что указанное лечение уменьшает количество герпетических поражений.
108. Применение по п. 101, отличающееся тем, что указанное лечение сокращает количество дней, в течение которых у субъекта присутствуют герпетические поражения.
109. Применение по п. 101, отличающееся тем, что указанное лечение подавляет появление симптомов герпеса.
110. Применение по п. 101, отличающееся тем, что указанное лечение снижает тяжесть симптомов герпеса.
111. Применение по п. 101, отличающееся тем, что указанное лечение снижает повторное появление симптомов герпеса.
112. Применение по п. 101, отличающееся тем, что указанное лечение снижает частоту симптомов герпеса.
113. Применение по п. 101, отличающееся тем, что указанное лечение подавляет инфекцию вирусом ВПГ-2 у неинфицированного субъекта.
114. Применение по п. 101, отличающееся тем, что указанное лечение индуцирует ответ антител на один или более антигенов ВПГ-2.
115. Применение по п. 101, отличающееся тем, что указанное лечение активирует Т-клеточный ответ на один или более антигенов ВПГ-2.
116. Применение по п. 101, отличающееся тем, что указанное лечение увеличивает титр IgG против одного или более антигенов ВПГ-2.
117. Применение по п. 101, отличающееся тем, что указанное лечение усиливает Т-клеточный ответ на один или более антигенов ВПГ-2.
118. Применение по п. 101, отличающееся тем, что указанное лечение сокращает количество герпетических поражений в начале развития инфекции вирусом ВПГ-2.
119. Применение по п. 101, отличающееся тем, что указанное лечение снижает выделение вируса.
120. Применение по п. 119, отличающееся тем, что указанное лечение снижает передачу вируса.
121. Применение по п. 101, отличающееся тем, что указанное лечение обеспечивает лечение субъекта при трехдозовом режиме.
122. Применение по п. 101, отличающееся тем, что указанное лечение осуществляют до, одновременно с или после лечения противовирусной молекулой.
123. Применение по п. 101, отличающееся тем, что указанное лечение снижает риск ВИЧ-инфекции.
124. Применение по п. 101, отличающееся тем, что указанный субъект представляет собой человека.
125. Фармацевтическая композиция против ВПГ, которая содержит первый полипептид, имеющий аминокислотную последовательность, которая по меньшей мере на 95% идентична SEQ ID NO: 2, и один или более дополнительных полипептидов, имеющих аминокислотную последовательность, которая по меньшей мере на 95% идентична любой из последовательностей SEQ ID NO: 1 и 3-38; содержащих SEQ ID NO: 4, в которой отсутствуют 1-20 аминокислот с N-конца, С-конца или обоих концов; или содержащих SEQ ID NO: 5, в которой отсутствуют все или по меньшей мере 8 последовательных аминокислотных остатков трансмембранного домена.
126. Фармацевтическая композиция по п. 125, отличающаяся тем, что указанные дополнительные полипептиды исключительно выбраны из любой из последовательностей SEQ ID NO: 27, 28, 20, 25, 29, 30, 38, 4, 5 и 7.
127. Фармацевтическая композиция по п. 125, отличающаяся тем, что указанные дополнительные полипептиды исключительно выбраны из любой из последовательностей SEQ ID NO: 31, 32, 33, 34, 22 и 35.
128. Фармацевтическая композиция по п. 125, отличающаяся тем, что указанные дополнительные полипептиды исключительно выбраны из любой из последовательностей SEQ ID NO: 3, 37 и 36.
129. Фармацевтическая композиция по п. 125, отличающаяся тем, что указанная фармацевтическая композиция вызывает секрецию ИФН-γ, по меньшей мере в 1,5 раза увеличенную по сравнению с уровнем ИФН-γ, высвобождаемым в ответ на полипептид, который не индуцирует иммунный ответ.
130. Фармацевтическая композиция по п. 125, дополнительно содержащая адъювант.
131. Применение двух и более изолированных полипептидов для получения лекарственного средства для индукции иммунного ответа у субъекта, где первый полипептид имеет последовательность аминокислот, по меньшей мере на 95% идентичную SEQ ID NO: 2, и один или более дополнительных полипептидов, выбранных из полипептидов, состоящих из аминокислотной последовательности, которая по меньшей мере на 95% идентична любой из последовательностей SEQ ID NO: 1 и 3-38; содержащих SEQ ID NO: 4, в которой отсутствуют 1-20 аминокислот на N-конце, С-конце или на обоих концах; или содержащих SEQ ID NO: 5, в которой отсутствуют все или по меньшей мере 8 последовательных аминокислотных остатков трансмембранного домена.
132. Применение по п. 131, отличающееся тем, что индукция включает введение указанного лекарственного средства два, три, четыре или пять раз.
133. Применение по п. 131, отличающееся тем, что индукция включает введение указанного лекарственного средства до контакта с вирусом простого ВПГ-1, ВПГ-2 или ВПГ-1 и ВПГ-2.
134. Применение по п. 131, отличающееся тем, что индукция включает введение указанного лекарственного средства после воздействия ВПГ-1, ВПГ-2 или ВПГ-1 и ВПГ-2.
135. Применение по п. 131, отличающееся тем, что указанное лекарственное средство вызывает ответ Th1.
136. Применение двух и более изолированных полипептидов для получения лекарственного средства для уменьшения выраженности одного или более симптомов инфекции вирусом ВПГ-2 у субъекта, где первый полипептид имеет последовательность аминокислот, по меньшей мере на 95% идентичную SEQ ID NO: 2, и один или более дополнительных полипептидов, выбранных из полипептидов, состоящих из аминокислотной последовательности, которая по меньшей мере на 95% идентична любой из последовательностей SEQ ID NO: 1 и 3-38; содержащих SEQ ID NO: 4, в которой отсутствуют 1-20 аминокислот с N-конца, С-конца или обоих концов; или содержащих последовательность SEQ ID NO: 5, в которой отсутствуют все или по меньшей мере 8 последовательных аминокислотных остатков трансмембранного домена.
137. Применение по п. 136, отличающееся тем, что указанные симптомы инфекции вирусом ВПГ-1, ВПГ-2 или ВПГ-1 и ВПГ-2 включают один или более из следующих симптомов: образование герпетических поражений, боль, раздражение, зуд, лихорадка, недомогание, головная боль, выделение вируса и признаки, предшествующие началу заболевания.
138. Применение двух и более изолированных полипептидов для получения лекарственного средства для ингибирования начала инфекции вирусом ВПГ-1, ВПГ-2 или ВПГ-1 и ВПГ-2, ингибирования развития латентной инфекции ВПГ-1, ВПГ-2 или ВПГ-1 и ВПГ-2 у субъекта, снижения выделения вируса у субъекта, инфицированного ВПГ-1, ВПГ-2 или ВПГ-1 и ВПГ-2, снижения рецидивирующих вспышек у субъекта, инфицированного ВПГ-1, ВПГ-2 или ВПГ-1 и ВПГ-2, где первый полипептид имеет последовательность аминокислот, по меньшей мере на 95% идентичную SEQ ID NO: 2, и один или более дополнительных полипептидов, выбранных из полипептидов, состоящих из аминокислотной последовательности, которая по меньшей мере на 95% идентична любой из последовательностей SEQ ID NO: 1 и 3-38; содержащих SEQ ID NO: 4, в которой отсутствуют 1-20 аминокислот с N-конца, С-конца или обоих концов; или содержащих последовательность SEQ ID NO: 5, в которой отсутствуют все или по меньшей мере 8 последовательных аминокислотных остатков трансмембранного домена.
| WO 03086308 A2, 23.10.2003 | |||
| WO 2005028496 A2, 31.03.2005. |
Авторы
Даты
2016-06-10—Публикация
2010-05-24—Подача