Настоящая заявка описывает способ для устранения органического соединения, имеющего один или несколько положительных зарядов, из водного раствора, который включает в себя стадии: a) подготовку водного раствора, содержащего органическое соединение, и гидрофобного органического раствора, включающего в себя жидкий катионообменник, причем жидкий катионообменник гидрофобен, b) приведение водного раствора в контакт с органическим раствором и c) отделение органического раствора от водного раствора, причем органическое соединение представляет собой соединение с формулой 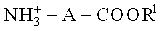
Фундаментальная проблема, имеющая место при биотехнологическом производстве из возобновляемого сырья химикатов высокой степени очистки, которые в обычном случае синтезируют из минеральных топлив, состоит в том, чтобы перевести полученный однажды продукт, обычно присутствующий в большом объеме водной фазы, в органическую фазу. Это перемещение осуществляют, с одной стороны, чтобы сконцентрировать готовый промежуточный или конечный продукт и чтобы при необходимости получить возможность синтетической переработки в органическом растворе на следующих этапах, а с другой стороны, чтобы повысить выход реакции в водном растворе путем устранения желательного продукта или же вообще создать возможность протекания реакции в имеющих технический смысл рамках. Прямое термическое сгущение (повышение концентрации) продукта, который часто присутствует в низких концентрациях, из крупных объемов водного раствора, как правило, неразумно.
Распределение некоторого соединения в двухфазной системе, включающей водную (гидрофильную) и органическую (гидрофобную) фазы, которые не смешиваются друг с другом, в значительной мере зависит от физико-химических свойств данного конкретного соединения. В то время как соединения с высокой долей незамещенных углеводородов, или же состоящие исключительно из таковых, собираются преимущественно в гидрофобной фазе, соединение с высокой долей полярных групп, как, например, функциональных групп, содержащих гетероатомы, а в особенности - соединения с зарядами, находятся преимущественно или практически исключительно в водной фазе, что осложняет перенос в органическую фазу.
Распределение соединения в указанной двухфазной системе после установления равновесия часто описывают с помощью коэффициента распределения, например, согласно уравнению Нернста
α=cфаза 1/cфаза 2,
Особенный коэффициент распределения - это Kow, также называемый показателем P, который характеризует равновесное распределение некоторого соединения между фазой октанола и водной фазой:
Kow=P=cв октаноле/Cв воде
Пример пользующегося большим спросом в промышленности органического соединения с положительным зарядом - это 12-аминолауриновая кислота (АЛК, ALS) и ее производные, в особенности метиловый эфир (МЭАЛК, ALSME). ALS - это важное исходное вещество при синтезе полимеров, например, для изготовления проводящих систем и нейлона. Обычно ALS изготавливают, исходя из минерального сырья, в процессе с низким выходом, через лауринлактам, который синтезируют путем тримеризации бутадиена, последующего гидрирования с образованием циклододекана, за которым следует окисление до циклододеканона, реакция с гидроксилаурином и последующее перераспределение по Бекману. Многообещающий путь к биотехнологическому производству ALS либо же ALSME описан в DE 10200710060705.
В уровне техники известна методика получения положительно заряженных органических соединений путем создания контакта водной реакционной смеси, включающей в себя биологическое действующее вещество, с органической фазой, включающей в себя органический растворитель. Так например в DE 10200710060705 описано получение продукта ALSME путем экстрагирования встряхиванием из водной реакционной смеси с помощью этилового эфира уксусной кислоты. Asano et al. (2008) публикуют сообщение об экстракции ALS толуолом из водного реакционного раствора, включающего в себя фермент, синтезирующий ALS.
Поэтому в основе настоящего изобретения лежит задача разработать способ удаления положительно заряженных органических соединений, в особенности ω-аминокарбоновых кислот, по меньшей мере с одним положительным зарядом, из водной реакционной смеси, причем желательно по возможности максимально выгодное положение равновесного распределения между реакционной смесью и используемой в качестве экстрагента гидрофобной органической фазой, т.е. равновесное распределение должно быть максимально смещено на сторону гидрофобной органической фазы.
Еще одна задача настоящего изобретения состоит в том, чтобы разработать способ для удаления органических соединений по меньшей мере с одним положительным зарядом, в особенности ω-аминокарбоновых кислот, из водного раствора, включающего в себя биологическое действующее вещество, с применением в качестве экстрагента гидрофобной органической фазы, при реализации которого равновесное распределение смещено максимально возможно далеко на сторону гидрофобной органической фазы.
Еще одна задача настоящего изобретения состоит в том, чтобы разработать способ для удаления органических соединений по меньшей мере с одним положительным зарядом, в особенности ω-аминокарбоновых кислот, из водного раствора с применением в качестве экстрагента гидрофобного органического раствора, который минимально препятствует росту важных для биотехнологии микроорганизмов, в особенности Escherichia coli, либо же замедляет его, и/или при этом по возможности в минимальной степени уменьшает число способных к делению, и/или жизнеспособных, и/или обладающих дыхательной активностью, и/или обладающих метаболической и синтетической активностью клеток.
Наконец, в основе изобретения лежит задача разработать способ для удаления органического соединения по меньшей мере с одним положительным зарядом, особенно ω-аминокарбоновых кислот, из водного раствора, включающего в себя биологическое действующее вещество, с применением гидрофобной органической фазы в качестве экстрагента, при реализации которого совокупность свойств, имеющих решающее значение для выхода, общего оборота и быстрой реализуемости базового процесса биотехнологического синтеза, в особенности токсичность органической фазы для биологического действующего вещества и поглощение соединения органическим экстрагентом, оптимизированы с точки зрения общего выхода или более быстрого протекания, или же - в случае непрерывного процесса - максимально возможной долгосрочной применимости биологического действующего вещества, особенно для того случая, когда органическое соединение по меньшей мере с одним положительным зарядом представляет собой продукт или промежуточный продукт синтетического процесса, синтезируемый с задействованием каталитической активности биологического действующего вещества.
Эту и другие задачи решают посредством предмета настоящей заявки, а в особенности также посредством предмета прилагаемых независимых пунктов формулы изобретения, причем формы исполнения следуют из зависимых пунктов.
Один из аспектов лежащей в основе изобретения задачи разрешают посредством способа для удаления органического соединения, несущего один или несколько положительных зарядов, из водного раствора, который включает в себя стадии
a) Подготовка водного раствора, содержащего органическое соединение и гидрофобного органического раствора, который включает в себя жидкий катионообменник,
причем жидкий катионообменник гидрофобен,
b) Контактирование водного раствора и органического раствора, и
c) Отделение органического раствора от водного раствора,
причем органическое соединение представляет собой соединение формулы I
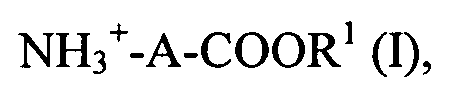
причем R1 представляет собой водород, метил, этил или отрицательный заряд, а A - незамещенную прямоцепочечную алкиленовую группу по меньшей мере с тремя, предпочтительно по меньшей мере восемью атомами углерода,
и причем жидкий катионообменник представляет собой жирную кислоту В первом варианте выполнения первого аспекта задачу решают посредством способа согласно одному из пунктов 1 формулы изобретения, причем температура на этапе b) составляет от 28 до 70, предпочтительно от 30 до 37°C.
Во втором варианте выполнения, который также представляет собой вариант выполнения первого варианта выполнения первого аспекта, задачу решают посредством способа согласно одному из пунктов 1-2 формулы изобретения, причем значение pH на этапе b) составляет от 6 до 8, предпочтительно от 6,2 до 7,2.
В третьем варианте выполнения, который также представляет собой вариант выполнения первого - второго варианта выполнения первого аспекта, проблему решают посредством способа, причем соотношение количества вещества жидкого катионообменника и органического соединения составляет по меньшей мере 1.
В третьем варианте выполнения, который также представляет собой вариант выполнения первого - третьего варианта выполнения первого аспекта, проблему решают посредством способа, причем соотношение объемов органического раствора и водного раствора составляет от 1:10 до 10:1.
В четвертом варианте выполнения, который также представляет собой форму исполнения первого - третьего варианта выполнения первого аспекта, проблему решают посредством способа, причем жидкий катионообменник представляет собой жирную кислоту более чем с 12, предпочтительно с 14-22, еще более предпочтительно с 16-18 атомами углерода.
В пятом варианте выполнения, который также представляет собой вариант выполнения первого - четвертого варианта выполнения первого аспекта, проблему решают посредством способа, причем жидкий катионообменник представляет собой ненасыщенную жирную кислоту, предпочтительно олеиновую кислоту или эруковую кислоту.
В шестом варианте выполнения, который также представляет собой вариант выполнения первого - пятого варианта выполнения первого аспекта, проблему решают посредством способа, причем водный раствор также включает в себя биологический агент с каталитической активностью.
В седьмом варианте выполнения, который также представляет собой вариант выполнения первого - шестого варианта выполнения первого аспекта, проблему решают посредством способа, причем биологический агент представляет собой клетку, предпочтительно бактериальную клетку, а клетка, что еще более предпочтительно рекомбинантную алканмонооксигеназу, рекомбинантную трансаминазу, а предпочтительно также сверх того по меньшей мере один фермент из группы, включающей в себя алкогольдегидрогеназу, аланиндегидрогеназу и продукт гена AlkL.
В восьмом варианте выполнения, который также представляет собой вариант выполнения первого - седьмого варианта выполнения первого аспекта, задачу решают посредством способа, причем присутствие органического соединения отрицательно сказывается на каталитической активности, предпочтительно посредством того, что органическое соединение представляет собой токсичное для клетки соединение.
В девятом варианте выполнения, который также представляет собой вариант выполнения первого - восьмого варианта выполнения первого аспекта, проблему решают посредством способа, причем органический раствор дополнительно содержит по меньшей мере один органический растворитель, предпочтительно жирную кислоту и/или сложный эфир жирной кислоты.
В десятом варианте выполнения, который также представляет собой вариант выполнения первого - девятого варианта выполнения первого аспекта, проблему решают посредством способа по пункту 12, причем органический раствор включает в себя в качестве жидкого катионообменника от 20 до 80 об.%, предпочтительно от 25 до 75 об.% олеиновой кислоты, а в качестве растворителя - метиловый эфир лауриновой кислоты, а органическое соединение представляет собой метиловый эфир 12-аминолауриновой кислоты, а в водном растворе присутствует бактериальная клетка, которая включает рекомбинантную алканмонооксигеназу, рекомбинантную трансаминазу, а предпочтительно также сверх того по меньшей мере один фермент из группы, включающей в себя алкогольдегидрогеназу, аланиндегидрогеназу и продукт гена AlkL.
В соответствии со вторым аспектом задачу, лежащую в основе изобретения, решают посредством реакционной смеси, включающей в себя водный раствор и гидрофобный органический раствор,
причем гидрофобный органический раствор включает в себя в качестве жидкого катионообменника жирную кислоту, более предпочтительно - жирную кислоту более чем с 12 атомами углерода, еще более предпочтительно - ненасыщенную жирную кислоту,
и причем водный раствор представляет собой соединение формулы (I)
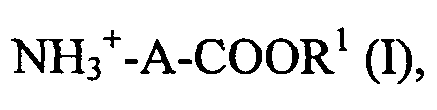
причем R1 представляет собой водород, метил, этил или отрицательный заряд, а A - незамещенную прямоцепочечную алкиленовую группу по меньшей мере с тремя, предпочтительно по меньшей мере восемью атомами углерода,
В одном из вариантов выполнения второго аспекта задачу, лежащую в основе изобретения, решают посредством реакционной смеси в соответствии с первым аспектом, причем водный раствор по-прежнему включает в себя клетку, которая включает рекомбинантную алканмонооксигеназу, рекомбинантную трансаминазу, а предпочтительно также сверх того по меньшей мере один фермент из группы, включающей в себя алкогольдегидрогеназу, аланиндегидрогеназу и продукт гена AlkL или его варианты.
Прочие варианты выполнения второго аспекта включают в себя все варианты выполнения первого аспекта.
Четвертый аспект лежащей в основе изобретения задачи разрешают посредством способа для удаления органического соединения, несущего один или несколько положительных зарядов, из водного раствора, который включает в себя стадии:
a) Подготовка водного раствора, содержащего органическое соединение, и гидрофобного органического раствора, который включает в себя жидкий катионообменник,
причем жидкий катионообменник гидрофобен,
и причем жидкий катионообменник содержит один или несколько отрицательных зарядов или общий отрицательный заряд.
b) Контактирование водного раствором и органического раствора и
c) Отделение органического раствора от водного раствора.
Во втором варианте выполнения четвертого аспекта настоящего изобретения, который также представляет собой форму выполнения первой формы исполнения настоящего изобретения, способ включает в себя этап:
d) дополнительная обработка органического раствора, предпочтительно путем обратной экстракции органического соединения еще в один водный раствор.
В третьем варианте выполнения четвертого аспекта настоящего изобретения, который также представляет собой вариант выполнения первого - второго варианта выполнения настоящего изобретения, температура на стадии b) способа согласно изобретению составляет от 28 до 70°C, предпочтительно от 30 до 37°C. В четвертом варианте выполнения четвертого аспекта настоящего изобретения, которая также представляет собой форму исполнения первой - третьей формы исполнения настоящего изобретения, значение pH на этапе b) способа согласно изобретению составляет от 3 до 8, предпочтительно от 6 до 8, особо предпочтительно от 6,2 до 7,2.
В пятом варианте выполнения четвертого аспекта настоящего изобретения, который также представляет собой вариант выполнения первого - четвертого варианта выполнения настоящего изобретения, отношение количества вещества жидкого катионообменника к органическому соединению при реализации способа составляет по меньшей мере 1.
В шестом варианте выполнения четвертого аспекта настоящего изобретения, который также представляет собой вариант выполнения первого - пятого варианта выполнения настоящего изобретения, отношение объемов органического раствора и водного раствора составляет от 1:10 до 10:1.
В седьмом варианте выполнения четвертого аспекта настоящего изобретения, который также представляет собой вариант выполнения первого - шестого варианта выполнения настоящего изобретения, у органического соединения имеется по меньшей мере один положительно заряженный заместитель формулы (I)
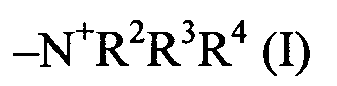
или - если по меньшей мере один заместитель из группы, включающей в себя R2, R3 и R4, представляет собой водород, его депротонированную форму,
причем R2, R3 и R4 независимо друг от друга выбирают из группы, включающей в себя водород, метил, этил, пропил, 2-пропил, бутил, трет.-бутил, пентил, гексил, бензил, гидроксил, замещенный или незамещенный и/или прямоцепочечный, или разветвленный, или циклический алкил или алкенил.
В восьмом варианте выполнения четвертого аспекта настоящего изобретения, который также представляет собой вариант выполнения первого - седьмого варианта выполнения настоящего изобретения, органическое соединение имеет формулу (II)
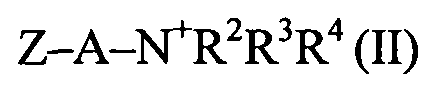
или - если по меньшей мере один заместитель из группы, включающей в себя R2, R3 и R4, представляет собой водород, его депротонированную форму.
причем R2, R3 и R4 независимо друг от друга выбирают из группы, включающей в себя водород, метил, этил, пропил, 2-пропил, бутил, трет.-бутил, пентил, гексил, бензил, гидроксил, замещенный или незамещенный и/или прямоцепочечный, или разветвленный, или циклический алкил или алкенил,
причем А представляет собой углеводородную цепь, включающую по меньшей мере три атома углерода, предпочтительно - незамещенную алкениловую группу,
и причем Z выбирают из группы, которая включает в себя -COOH, -COOR5, -COH, -CH2OH и их депротонированные формы,
причем R5 выбирают из группы, включающей в себя водород, метил, этил, пропил, 2-пропил, бутил, трет.-бутил, пентил, гексил, бензил, гидроксил, замещенный или незамещенный и/или прямоцепочечный, или разветвленный, или циклический алкил или алкенил.
В девятом варианте выполнения четвертого аспекта настоящего изобретения, который также представляет собой вариант выполнения первого - восьмого варианта выполнения настоящего изобретения, органическое соединение имеет формулу (III)
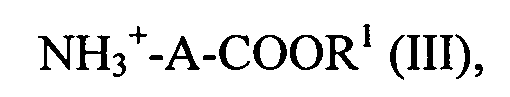
или его депротонированную форму, причем R1 представляет собой водород, метил или этил, а A - незамещенную, прямоцепочечную алкиленовую группу по меньшей мере с тремя атомами углерода.
В десятом варианте выполнения четвертого аспекта настоящего изобретения, который также представляет собой вариант выполнения первого - девятого варианта выполнения настоящего изобретения, жидкий катионообменник имеет по меньшей мере одну алкиловую или алкениловую группу по меньшей мере с шестью атомами углерода, а также концевой заместитель из группы, который включает в себя -COOH, -OSO2H, -OPO(OH)2- и -OPO(OH)O-, а также их депротонированные формы.
В одиннадцатом варианте выполнения четвертого аспекта настоящего изобретения, который также представляет собой вариант исполнения первого - десятого варианта выполнения настоящего изобретения, жидкий катионообменник представляет собой ненасыщенную жирную кислоту, предпочтительно олеиновую кислоту.
В двенадцатом варианте выполнения четвертого аспекта настоящего изобретения, который также представляет собой вариант выполнения первого - одиннадцатого варианта выполнения настоящего изобретения, водный раствор также включает в себя биологический агент с каталитической активностью.
В тринадцатом варианте выполнения четвертого аспекта настоящего изобретения, который также представляет собой вариант выполнения первого - двенадцатого варианта выполнения настоящего изобретения, биологический агент представляет собой клетку, предпочтительно бактериальную клетку.
В четырнадцатом варианте выполнения четвертого аспекта настоящего изобретения, который также представляет собой вариант выполнения первого - тринадцатого варианта выполнения настоящего изобретения, присутствие органического соединения отрицательно сказывается на каталитической активности. В пятнадцатом варианте выполнения четвертого аспект настоящего изобретения, который также представляет собой вариант выполнения первого - четырнадцатого варианта настоящего изобретения, органический раствор кроме того содержит по меньшей мере один органический растворитель, предпочтительно жирную кислоту и/или эфир жирной кислоты.
В шестнадцатом варианте выполнения четвертого аспекта настоящего изобретения, который также представляет собой вариант выполнения первого - пятнадцатого варианта настоящего изобретения, органический раствор включает в себя в качестве жидкого катионообменника 20-80% по объему, предпочтительно от 25-75% по объему, олеиновой кислоты, а в качестве растворителя - метиловый эфир лауриновой кислоты, и органическое соединение представляет собой метиловый эфир 12-аминолауриновой кислоты, а в водном растворе присутствует бактериальная клетка, которая обладает каталитической активностью, задействованной в синтезе метилового эфира 12-аминолауриновой кислоты.
В соответствии с пятым аспектом задачу, лежащую в основе изобретения, решают посредством биореактора, включающего в себя водный раствор, содержащий в себе биологический агент, а также гидрофобный органический раствор, содержащий в себе жидкий катионообменник. В предпочтительном варианте выполнения настоящего изобретения под термином «биореактор», использованном в этом тексте, подразумевают любой сосуд, в котором в контролируемых условиях культивируют пригодные к биотехнологическому использованию микроорганизмы, и/или их можно использовать для биотехнологического процесса, предпочтительно синтеза органического соединения.
Во втором варианте выполнения пятого аспекта, которая также представляет собой вариант выполнения первого варианта выполнения третьего аспекта настоящего изобретения, жидкий катионообменник представляет собой жирную кислоту, предпочтительно олеиновую кислоту.
В третьем варианте выполнения пятого аспекта, который также представляет собой вариант выполнения первого - второго варианта выполнения третьего аспекта настоящего изобретения, гидрофобный органический раствор также включает в себя эфир жирной кислоты, предпочтительно метиловый эфир лауриновой кислоты.
В четвертом варианте выполнения пятого аспекта, который также представляет собой вариант выполнения первого - третьего варианте выполнения второго аспекта настоящего изобретения, гидрофобный органический раствор включает в себя в качестве катионообменника олеиновую кислоту, а в качестве растворителя от 25 до 75 об.% метилового эфира лауриновой кислоты.
В пятом варианте выполнения, который также представляет собой вариант выполнения первого - четвертого варианта выполнения пятого аспекта настоящего изобретения, органическое соединение представляет собой соединение, соответствующее одному из вариантов выполнения первого аспекта изобретения.
В соответствии с шестым аспектом задачу, лежащую в основе изобретения, решают посредством способа синтеза органического соединения с одним или несколькими положительными зарядами, причем органическое соединение токсично для клеток, каковой способ включает в себя культивацию в водном растворе клеток, участвующих в синтезе органического соединения, предпочтительно клеток, которые катализируют по меньшей мере один этап синтеза, в присутствии гидрофобного органического раствора, включающего в себя жидкий катионообменник и в качестве опции органический растворитель.
Во втором варианте выполнения шестого аспекта настоящего изобретения органическое соединение представляет собой 12-аминолауриновую кислоту или метиловый эфир 12-аминолауриновой кислоты, а органический растворитель - метиловый эфир лауриновой кислоты.
Прочие формы исполнения четвертого, пятого и шестого аспекта охватывают все формы исполнения первого и второго аспектов настоящего изобретения.
Авторы настоящего изобретения (изобретатели) обнаружили, что эффективность удаления органического соединения с одним или несколькими положительными зарядами из водного раствора в гидрофобный органический раствор можно неожиданным образом повысить, если этот органический раствор включает в себя жидкий катионообменник. Не желая фиксироваться на какой-либо теории, авторы настоящего изобретения предполагают, что отрицательный заряд либо же отрицательные заряды жидкого катионообменника ионным способом взаимодействует(ют) с положительным зарядом или несколькими положительными зарядами органических соединений, и что это взаимодействие ведет к маскировке по меньшей мере одного положительного заряда, повышающей растворимость в органической фазе.
В предпочтительном варианте выполнения термин «жидкий катионообменник», применяемый в этом тексте, означает растворимое в гидрофобном органическом растворителе соединение, которое ввиду одного или нескольких постоянных отрицательных зарядов в состоянии осуществлять ионное взаимодействие по меньшей мере с одним катионом. Обычно жидкий катионообменник включает в себя по меньшей мере одну насыщенную или ненасыщенную углеводородную цепь, которая может быть прямой или разветвленной, а также отрицательно заряженную группу, например, карбоксигруппу. В предпочтительной форме исполнения жидкий ионообменник представляет собой жирную кислоту, в еще более предпочтительной форме исполнения - ненасыщенную жирную кислоту, например, олеиновую кислоту. В предпочтительной форме исполнения жидкий ионообменник является ди(2-этилгексил)фосфорной кислотой (также называемой DEHPA или D2EHPA).
В предпочтительной форме исполнения у жидкого ионообменника не только отрицателен совокупный заряд, но вообще отсутствует положительный заряд. В предпочтительной форме исполнения под термином «совокупный заряд» ионообменника или иной молекулы, как этот термин применен в настоящем тексте, подразумевают сумму зарядов всех функциональных групп, ковалентно связанных с молекулой. Например, у лауриновой кислоты при pH 7 совокупным зарядом является отрицательный заряд, независимо от присутствия других молекул или противоионов, таких как: ионов калия, которые присутствуют в водном растворе.
В предпочтительной форме исполнения настоящего изобретения под термином «приведение в контакт», применяемом в этом тексте, подразумевают, что две фазы подвергают экспозиции друг друга прямо, и в частности, без введения между ними какого-либо физического барьера, как, например, мембраны. В простейшем случае приведение в контакт осуществляют посредством того, что обе фазы помещают в один и тот же сосуд и надлежащим образом, например, путем перемешивания, смешивают друг с другом.
В предпочтительной форме исполнения органическое соединение несет положительный совокупный заряд. Еще в одной предпочтительной форме исполнения органическое соединение не имеет отрицательных зарядов. В предпочтительной форме исполнения органическое соединение представляет собой ω-аминокарбоновую кислоту.
В предпочтительной форме исполнения термин «имеет заряд», как его применяют в настоящем тексте, означает, что обозначенное таким образом соединение характеризуется соответствующим зарядом в водном растворе при pH от 0 до 14, предпочтительно от 2 до 12, от 2 до 6, от 8 до 12, от 3 до 10, от 6 до 8, а наиболее предпочтительно при pH 7. В предпочтительной форме исполнения речь идет о постоянно имеющемся заряде. Еще в одной предпочтительной форме исполнения термин «имеет заряд», как его применяют в настоящем тексте, означает, что соответствующая функциональная группа или соединение при pH 7 преимущественно представлена в виде с соответствующим зарядом, т.е. по меньшей мере на 50, предпочтительно на 90, а еще более предпочтительно на 99%.
В предпочтительном варианте выполнения термин «содержит» подразумевает «включает в себя», то есть не имеет окончательного значения. В этом смысле смесь, «содержащая А», может иметь помимо А и другие компоненты. Формулировка «один или несколько зарядов» означает по меньшей мере один заряд соответствующей природы.
В предпочтительном варианте выполнения под термином «гидрофобный», который применяют в настоящем тексте, подразумевают свойство жидкости формировать в присутствии водной фазы четко отграниченную от водной фазы собственную жидкую фазу. Последняя может представлять собой сплошную жидкую фазу или эмульсию. Еще в одной предпочтительной форме исполнения под термином «гидрофобный», который применяют в настоящем тексте, подразумевают свойство соединения по существу не растворяться в воде. Наконец, еще в одной предпочтительной форме исполнения термин, как его применяют здесь, подразумевает, что обозначенное таким образом соединение имеет показатель Р (J. Sangster, Octanol-Water Partition Coefficients: Fundamentals and Physical Chemistry, Vol.2 of Wiley Series in Solution Chemistry, John Wiley & Sons, Chichester, 1997), десятичный логарифм которого выше 0, более предпочтительно выше 0,5, еще более предпочтительно выше 1, а наиболее предпочтительно - больше 2.
Еще в одном из вариантов выполнения настоящего изобретения жидкий ионообменник не обладает токсическим воздействием на имеющие биотехнологическое значение микроорганизмы или обладает им лишь в умеренной степени. Под термином «токсическое воздействие», как его применяют в настоящем тексте, в предпочтительной форме исполнения подразумевают свойство соединения снижать скорость роста соответствующих микроорганизмов при контакте с ними, снижать активность их обмена веществ, повышать их энергопотребление, снижать их оптическую плотность или число способных к росту клеток и/или прямо вызывать их отмирание или лизис. В предпочтительном варианте выполнения по меньшей мере один из этих видов воздействия в случае токсического соединения проявляется (оказывается достигнут) уже в низкой концентрации, предпочтительно в концентрации 1000, более предпочтительно 100, еще более предпочтительно 50 или 25, а наиболее предпочтительно - 5 мг/л. Специалисту известны многочисленные применимые в рутинном порядке методы, посредством которых можно исследовать токсичность. К таковым относятся, например, измерение интенсивности дыхания соответствующих микроорганизмов с помощью кислородных электродов или сравнительный посев образцов микроорганизмов с последующим подсчетом колониеобразующих единиц (КОЕ). В предпочтительной форме исполнения под «умеренным токсическим действием» подразумевают, что микроорганизмы, находящиеся в фазе роста, в присутствии соединения продолжают расти и/или сохраняют метаболическую активность, но в меньшей степени, чем контрольные, которые инкубируют в тех же условиях в отсутствие соответствующего соединения, и/или характеризуются удлиненной фазой запаздывания.
Водный и органический растворы приводят в контакт друг с другом в надлежащих условиях, и в особенности на протяжении времени, которого хватает для достаточного перехода органического соединения из водной фазы в органическую фазу, в идеальном случае - даже для установления соответствующего равновесия. Эту длительность и эти условия специалист может определить в рамках экспериментирования.
В особо предпочтительном варианте выполнения органическое соединение, имеющее один или несколько положительных зарядов, представляет собой аминированную в концевом положении жирную кислоту, особо предпочтительно 12-аминолауриновую кислоту, или ее эфир, или смесь обоих соединений. Специалисту ясно, что эфир жирной кислоты в присутствии биологической системы, включающей в себя активность эстеразы, может частично находиться в форме соответствующей кислоты, и оба соединения в этом контексте следует, соответственно, рассматривать как эквивалентные. Соответственно, жирные кислоты или производные жирных кислот в особо предпочтительной форме исполнения, как этот термин применяется здесь, включают в себя также и соответствующие эфиры, предпочтительно метиловые эфиры, и наоборот.
В особо предпочтительной форме исполнения термин «алкиленовая группа», как его применяют в настоящем тексте, подразумевает группу формулы -(CH2)n-, т.е. алкан с двумя открытыми, предпочтительно концевыми заместителями. Два заместителя могут представлять собой, например, аминогруппу и карбоксигруппу. В предпочтительном варианте исполнения n равняется по меньшей мере 3, более предпочтительно по меньшей мере 6, а еще более предпочтительно 11. В случае «замещенной алкиловой цепи» по меньшей мере один атом водорода заменен заместителем, отличным от атома водорода, или алкиловым остатком, предпочтительно атомом, отличным от атома водорода. В особом варианте исполнения термин «незамещенная алкиленовая группа», как его применяют в настоящем тексте, напротив, означает углеводородную цепь формулы -(CH2)n- без подобных заместителей.
Температура на этапе b) зависит не только от свойств жидкого катионообменника, но (в особенности в том случае, когда контакт между водным и органическим раствором осуществляют при прохождении реакции в водной фазе) также и от температурных потребностей реакций, которые, возможно, проходят в водной фазе. В частности, в том случае, когда биологический агент, например, живая клетка, проявляет в водной фазе каталитическую активность, температура должна быть пригодна для поддержания этой активности. В предпочтительной форме исполнения температура на этапе b) составляет от 0 до 100°C, более предпочтительно от 20 до 80°C, от 28 до 70°C, от 30 до 37°C, от 35 до 40°C.
Значение pH на этапе b) также должно соответствовать потребностям реакций, которые, возможно, проходят одновременно, условиям стабильности исходных компонентов, продуктов, промежуточных продуктов или реагентов. В предпочтительном варианте выполнения значение pH составляет от 3 до 8, более предпочтительно от 6 до 8, а еще более предпочтительно от 6,2 до 7,2.
Чтобы по возможности полностью перевести органическое соединение из водной фазы в органическую, требуется достаточное количество жидкого катионообменника. В предпочтительной форме исполнения настоящего изобретения соотношение между жидким катионообменником и органическим соединением по количеству вещества по меньшей мере на одном этапе, при непрерывном процессе, суммарно по всему прохождению реакции составляет по меньшей мере 1, т.е. на молекулу органического соединения применяют по меньшей мере одну молекулу жидкого катионообменника. В еще более предпочтительном варианте выполнения это соотношение больше 2, 3, 5, 10, 15, или 20, предпочтительно оно составляет от 1,5 до 3.
Соотношение объемов органического раствора и водного раствора, вместе с соотношением по количеству вещества между катионообменником и органическим соединением, имеет значение для производительности способа. В особом варианте выполнения оно составляет от 100:1 до 1:100, более предпочтительно от 20:1 до 1:20, еще более предпочтительно от 10:1 до 1:10, от 4:1 до 1:4, от 3:1 до 1:3 или наиболее предпочтительно от 1:2 до 2:1.
В предпочтительном варианте выполнения настоящего изобретения в качестве жидкого катионообменника применяют жирную кислоту. В предпочтительном варианте выполнения настоящего изобретения под термином «жирная кислота», как его применяют здесь, подразумевают карбоновую кислоту, предпочтительно алкановую кислоту, по меньшей мере с 6, предпочтительно 8, еще более предпочтительно 10, наиболее предпочтительно 12 атомами углерода. В предпочтительном варианте выполнения речь идет о прямоцепочечных жирных кислотах, в другой форме исполнения - о разветвленных. В предпочтительном варианте выполнения речь идет о насыщенных жирных кислотах. В особо предпочтительном варианте выполнения речь идет о ненасыщенных жирных кислотах. Еще в одном предпочтительном варианте выполнения речь идет о прямоцепочечной жирной кислоте по меньшей мере с 12 атомами углерода, включающей в себя двойную связь, предпочтительно в положении 9. Еще в одном предпочтительном варианте выполнения речь идет об однократно ненасыщенной жирной кислоте, у которой двойная связь находится в положении 9 и/или 11. Еще в одном предпочтительном варианте исполнения жидкий катионообменник представляет собой ненасыщенную жирную кислоту, выбранную из группы, которую образуют олеиновая кислота, пальмитолеиновая кислота, гадолеиновая кислота и икозеновая кислота. В наиболее предпочтительной форме исполнения речь идет об олеиновой кислоте. В особо предпочтительной форме исполнения речь идет о жирной кислоте с 6, 7, 8 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30 атомами углерода, предпочтительно более чем с 12, еще более предпочтительно более чем с 14 атомами углерода, еще более предпочтительно с 14-28, 14-22, а наиболее предпочтительно - с 16-18 атомами углерода.
Еще в одной предпочтительной форме исполнения в качестве жидкого ионообменника применяют смесь различных жирных кислот, которая существует, например, в форме соевого масла или масла мордовника. По потребности, в том случае, когда жирные кислоты находятся в форме эфиров, это предусматривает предварительный гидролиз.
В особо предпочтительной форме исполнения настоящего изобретения применяют комбинацию двух жидких катионообменников, причем предпочтительно, чтобы по меньшей мере один из них был жирной кислотой.
Особое преимущество настоящего изобретения состоит в совместимости способа согласно изобретению с биотехнологическими методами и применяемыми в них биологическими агентами. В одной из форм исполнения настоящего изобретения под термином «биологический агент с каталитической активностью», как его применяют в этом тексте, подразумевают синтезируемый некоторой клеткой биокатализатор на всех этапах очистки - от цельной клетки до изолированной молекулы. В предпочтительной форме исполнения это клетка, экспрессирующая ферменты с каталитической активностью. Эти клетки могут быть прокариотами (в том числе археями) или эукариотами, предпочтительно из группы, включающей в себя Pseudomonas, Corynebacterium и Е.coli. В еще более предпочтительной форме исполнения агент представляет собой бактериальную клетку, еще более предпочтительно - грамотрицательную бактериальную клетку, наиболее предпочтительно - Е.coli. Еще в одной предпочтительной форме исполнения речь идет об эукариотической клетке, предпочтительно о грибковой клетке, еще более предпочтительно о дрожжевой клетке, а наиболее предпочтительно - о Saccharomyces или Candida, Pichia, в особенности Candida tropicalis. В особой форме исполнения в настоящей заявке термин «клетка» имеет то же значение, что и термин «микроорганизм», и эти термины используют как взаимозаменяемые. Кроме того, клетка может представлять собой изолированную клетку или смесь культур.
Клетка, применяемая как биологический агент, может быть жизнеспособной или представлять собой препарат, например, мембранную фракцию, или цитозольную фракцию, или же сырцовый экстракт клетки.
Если биологический агент означает изолированную молекулу на различных этапах очистки, то это могут быть все синтезируемые клеткой каталитически активные молекулы. В особо предпочтительной форме исполнения речь идет о молекуле из группы, включающей в себя пептиды, полипептиды, углеводы, нуклеиновые кислоты или смешанные формы. В еще более предпочтительной форме исполнения речь идет об обладающей каталитической активностью полипептиде. Еще в одной предпочтительной форме исполнения речь идет об иммобилизованной молекуле.
Каталитические функции, потребные для синтетических биотехнологических методов, разнообразны. В предпочтительной форме исполнения под термином «каталитическая активность», как его применяют в этом тексте, подразумевают синтетическую активность, то есть катализ химических реакций, включающих в себя формирование по меньшей мере одной новой ковалентной связи. Еще в одной предпочтительной форме исполнения речь идет о транспортной активности, то есть о способности молекулы обеспечить транспортировку другой молекулы из одного компартмента в другой, например, поглощение некоторого вещества из водной среды через клеточную мембрану во внутреннее пространство клетки.
В особо предпочтительной форме исполнения биологический агент представляет собой живую клетку, которую в присутствии жидкого катионообменника применяют для катализа, предпочтительно - чтобы синтезировать органическое соединение с одним или несколькими положительными зарядами, которое затем или одновременно выводят в гидрофобную органическую фазу посредством жидкого катионообменника.
В особо предпочтительной форме исполнения присутствие органического соединения отрицательно сказывается на каталитической активности. В одной из форм исполнения это может снизить величину имеющейся активности, выражаемую в смысле более низкого kcat фермента. Еще в одной форме исполнения может быть затронуто сродство обладающего каталитической активностью агента в смысле повышенной KM фермента.
Еще в одной форме исполнения может быть изменена специфичность каталитической активности, например, таким образом, что предпочтительно происходит преобразование (или предпочтительное преобразование) иной молекулы, нежели желательная молекула субстрата. Еще в одной форме исполнения органическое соединение оказывает токсическое воздействие на клетку как биологический агент.
Еще в одной форме исполнения органическое соединение представляет собой такое органическое соединение, которое снижает доступность эссенциального косубстрата или кофермента. Это может иметь место, например, в том случае, когда органическое соединение ингибирует соответствующую реакцию регенерации.
Помимо жидкого катионообменника гидрофобная органическая фаза может также содержать гидрофобный растворитель. Это может служить для того, чтобы повысить поглощающую способность жидкого катионообменника в гидрофобной фазе и воспрепятствовать нежелательным процессам, например, хлопьеобразованию. В предпочтительной форме исполнения растворитель представляет собой исходный компонент реакции, проходящей в водном растворе, наиболее предпочтительно - субстрат катализируемой ферментом реакции, проходящей в водном растворе. В предпочтительной форме исполнения речь идет об эфире жирной кислоты. В особо предпочтительной форме исполнения растворитель представляет собой эфир жирной кислоты, предпочтительно - метиловый эфир жирной кислоты, служащей жидким катионообменником.
Доля растворителя, если он присутствует, в гидрофобной органической фазе составляет в предпочтительном варианте выполнения от 1 до 99 об.%. В предпочтительной форме исполнения доля растворителя составляет от 10 до 90, еще более предпочтительно от 20 до 80, наиболее предпочтительно - от 25 до 75 об.%.
В наиболее предпочтительном варианте выполнения способа органическое соединение представляет собой 12-аминолауриновую кислоту и/или метиловый эфир 12-аминолауриновой кислоты, которую либо же который в водной фазе синтезирует штамм Е.coli путем пошагового окисления концевого атома углерода метилового эфира лауриновой кислоты, как это раскрыто в DE 10200710060705, а гидрофобная фаза включает в себя от 25 до 75% олеиновой кислоты в качестве жидкого катионообменника, растворенной в метиловом эфире лауриновой кислоты как субстрате реакции.
Реализовать теоретическое изложение настоящего изобретения можно не только с применением последовательностей аминокислот или нуклеиновых кислот, точно соответствующих описанным здесь биологическим макромолекулам, но и с применением вариантов таких макромолекул, которые можно получить делецией, добавлением или замещением одной или более чем одной аминокислот или нуклеиновых кислот. В предпочтительном варианте выполнения под термином «вариант» последовательности нуклеиновых кислот или аминокислот, в дальнейшем идентичным по значению и взаимозаменяемым в употреблении с термином «гомолог», как его применяют в настоящем тексте, подразумевают другую последовательность нуклеиновых кислот или аминокислот, которая применительно к соответствующей исходной последовательности нуклеиновых кислот или аминокислот дикого типа характеризуется гомологичностью (в данном случае имеет то же значение, что «идентичность») в 70, 75, 80, 85, 90, 92, 94, 96, 98, 99% или более процентов, причем предпочтительно, чтобы делеции или замещению (субституции) были подвергнуты другие аминокислоты, нежели таковые, образующие каталитически активный центр, или критически важные для структуры или складки, или же чтобы последние подвергались лишь консервативному замещению, например, глутамат вместо аспартата или лейцин вместо валина. На нынешнем техническом уровне описаны алгоритмы, которые можно применять, чтобы рассчитать степень гомологичности двух последовательностей, например, в книге Arthur Lesk (2008), Introduction to bioinformatics, 3rd edition. Еще в одной предпочтительной форме исполнения настоящего изобретения вариант последовательности аминокислот или нуклеиновых кислот характеризуется (предпочтительно в дополнение к вышеуказанной гомологичной последовательности) по существу той же ферментативной активностью, что и молекула дикого типа либо же исходная молекула. Например, вариант полипептида, имеющего ферментативную активность протеазы, обладает той же или по существу той же протеолитической активностью, что и полипептидный фермент, то есть, способностью катализировать гидролиз пептидной связи. В особенной форме исполнения формулировка (термин, понятие) «по существу та же ферментативная активность» означает активность по отношению к субстратам полипептида дикого типа, которая существенно превышает фоновую активность, или/и ее показатели KM- и/или kcat- менее чем на 3, более предпочтительно на 2, еще более предпочтительно на один порядок величины отличаются от таковых, которыми характеризуется полипептид дикого типа по отношению к тем же субстратам. Еще в одном предпочтительном варианте выполнения термин «вариант» последовательности нуклеиновых кислот или аминокислотной последовательности включает в себя по меньшей мере одну активную часть или фрагмент последовательности нуклеиновых кислот или аминокислотной последовательности. Еще в одной предпочтительной форме исполнения термин «активная часть», как его применяют в настоящем тексте, означает аминокислотную последовательность или последовательность нуклеиновых кислот, которая имеет длину, меньшую чем полная длина аминокислотной последовательности либо же кодирует меньшую длину, чем полная длина аминокислотной последовательности, причем аминокислотная последовательность или кодированная аминокислотная последовательность меньшей длины, чем у аминокислотной последовательности дикого типа, обладает по существу той же ферментативной активностью, что и полипептид дикого типа или его вариант, например, в качестве алкогольдегидрогеназы, монооксигеназы или трансаминазы. В особой форме исполнения термин «вариант» нуклеиновой кислоты включает в себя нуклеиновую кислоту, комплементарная нить которой, предпочтительно - в строжайших условиях, связывается с нуклеиновой кислотой дикого типа. Специалисту легко определить строгость реакции гибридизации; в общем случае она зависит от длины зонда, температур при отмывке и от концентрации солей. В общем случае более длинным зондам для гибридизации требуются более высокие температуры, а более короткие зонды, напротив, обходятся меньшими температурами. Произойдет ли гибридизация, в общем случае зависит от способности денатурированной ДНК присоединяться к комплементарным нитям, присутствующим в окружении, причем ниже температуры плавления строгость реакции гибридизации и соответствующие условия более подробно описаны в Ausubel et al. 1995. В предпочтительной форме исполнения термин «вариант» нуклеиновой кислоты, как его применяют в настоящем тексте, включает в себя произвольную последовательность нуклеиновой кислоты, которая кодирует ту же последовательность аминокислот, что и исходная нуклеиновая кислота, или же вариант этой аминокислотной последовательности в рамках вырожденности генетического кода.
Надлежащие полипептиды, которые можно использовать для синтеза органических соединений формулы (I) в особенности алканмонооксигеназы, AlkL, трансаминазы, альдегиддегидрогеназы и аланиндегидрогеназы описаны в уровне техники, например, в DE 10200710060705, европейском патенте ЕР 11004029 и в РСТ/ЕР 2011/053834.
В самой предпочтительной форме исполнения алканмонооксигеназа представляет собой алканмонооксигеназу типа AlkB. AlkB - это оксидоредуктаза из системы AlkBGT из Pseudomonas putida, которая известна своей гидролазной активностью. Она зависит от двух других полипептидов, AlkG и AlkT. AlkT характеризуют как ФАД-зависимую рубредоксин-редуктазу, которая передает электроны от НАД-Н на AlkG. AlkG - это рубредоксин, то есть железосодержащий окислительно-восстановительный белок, который играет роль непосредственного донора электронов для AlkB. В предпочтительной форме исполнения под формулировкой «Алканмонооксигеназа типа alkB», как его применяют в настоящем тексте, подразумевают расположенную на мембране алканмонооксидазу. Еще в одном предпочтительном варианте выполнения под тем же термином «Алканмонооксигеназа типа alkB» подразумевают (в порядке возрастания предпочтительности) полипептид с гомологичностью последовательности по меньшей мере в 75, 80, 85, 90, 92, 94, 96, 98 или 99% к последовательности AlkB из Pseudomonas putida Gpol (код банка данных САВ54050.1). Еще в одной предпочтительной форме исполнения под этим термином подразумевают цитохром-независимую монооксигеназу. Еще в одной предпочтительной форме исполнения под термином «Алканмонооксигеназа типа alkB» 5 подразумевают цитохром-независимую монооксигеназу, которая в качестве донора электронов использует по меньшей мере один рубредоксин или гомолог. В особо предпочтительной форме исполнения под этим термином подразумевают расположенную на мембране, цитохром-независимую алканмонооксигеназу с гомологичностью последовательности (в порядке возрастания предпочтительности) по меньшей мере в 75, 80, 85, 90, 92, 94, 96, 98 или 99% к последовательности AlkB из Pseudomonas putida Gpol, которой в качестве донора электронов необходим по меньшей мере AlkG (CAB54052.1), а предпочтительно - комбинация AlkG с редуктазой AlkT (CAB54063.1), причем alkG и/или alkT могут представлять собой гомолог соответствующего полипептида. Термин «последовательность», как его применяют в настоящем тексте, может относиться к аминокислотной последовательности некоторого полипептида и/или к кодирующей его последовательности нуклеиновой кислоты. Еще в одной предпочтительной форме исполнения «Алканмонооксигеназа типа alkB», как этот термин применяют в настоящем тексте, представляет собой цитохром-независимую оксидоредуктазу, т.е. оксидоредуктазу, которая не включает в себя в качестве кофактора цитохром.
Далее настоящее изобретение иллюстрируется нижеследующими фигурами и не налагающими ограничений примерами, дальнейшие признаки, варианты выполнения, варианты и преимущества которых можно извлечь из настоящего изобретения.
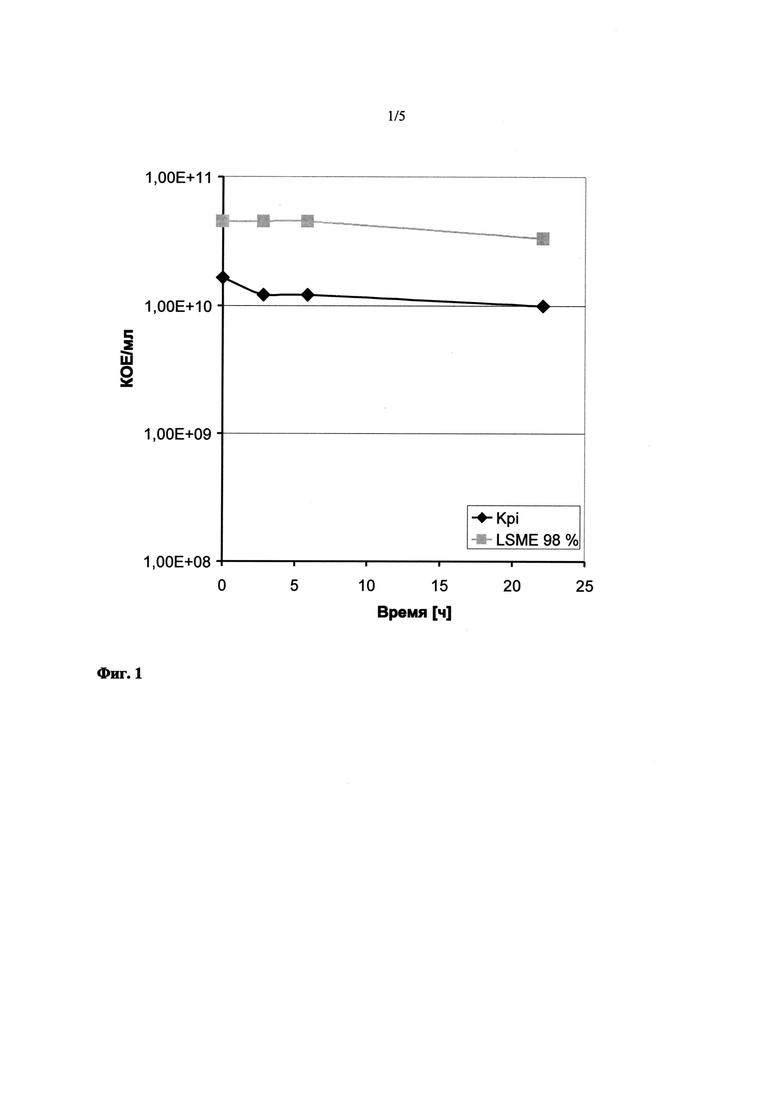
На Фиг.1 показан контрольный эксперимент для подтверждения того, что LSME не обладает токсическим действием, проведенный со штаммом Е.coli W3110 и с использованием для сравнения калиево-фосфатного буфера (Kpi) в качестве отрицательного контроля.
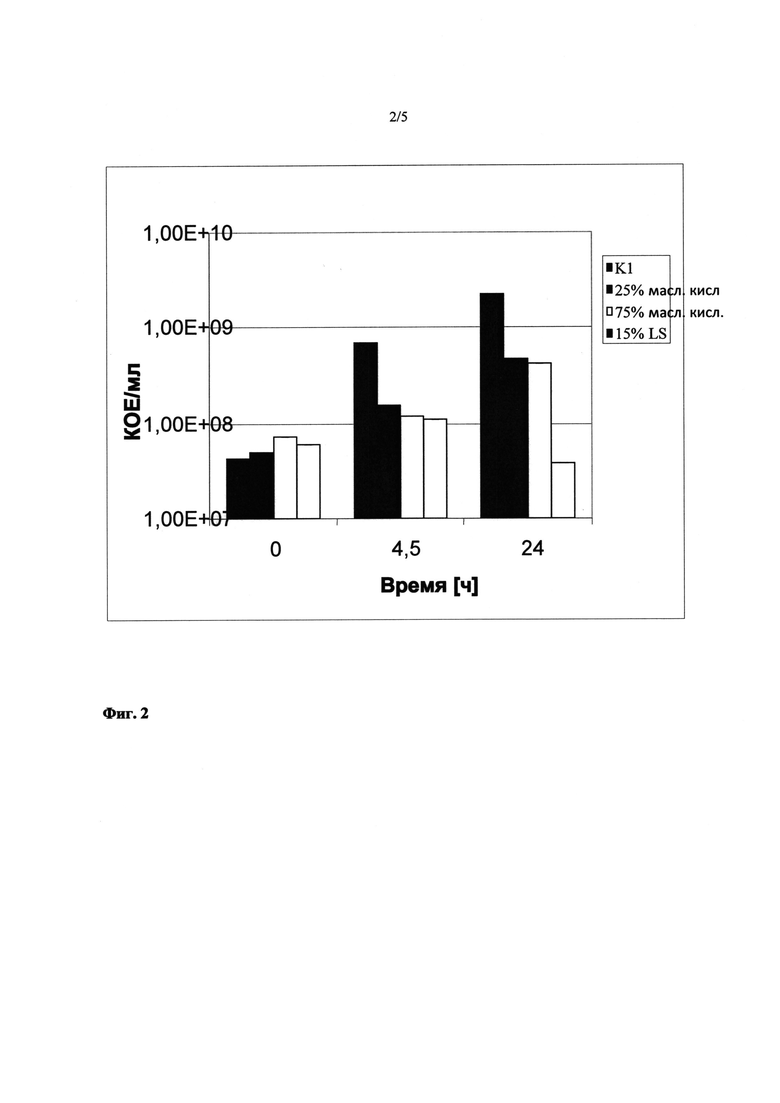
На Фиг.2 показана жизнеспособность штамма Е.coli W3110 в форме числа КОЕ, которые штамм способен сформировать в отсутствие жидкого катионообменника и в присутствии различных жидких катионообменников по прошествии 0 ч, 4 ч и 24 ч.
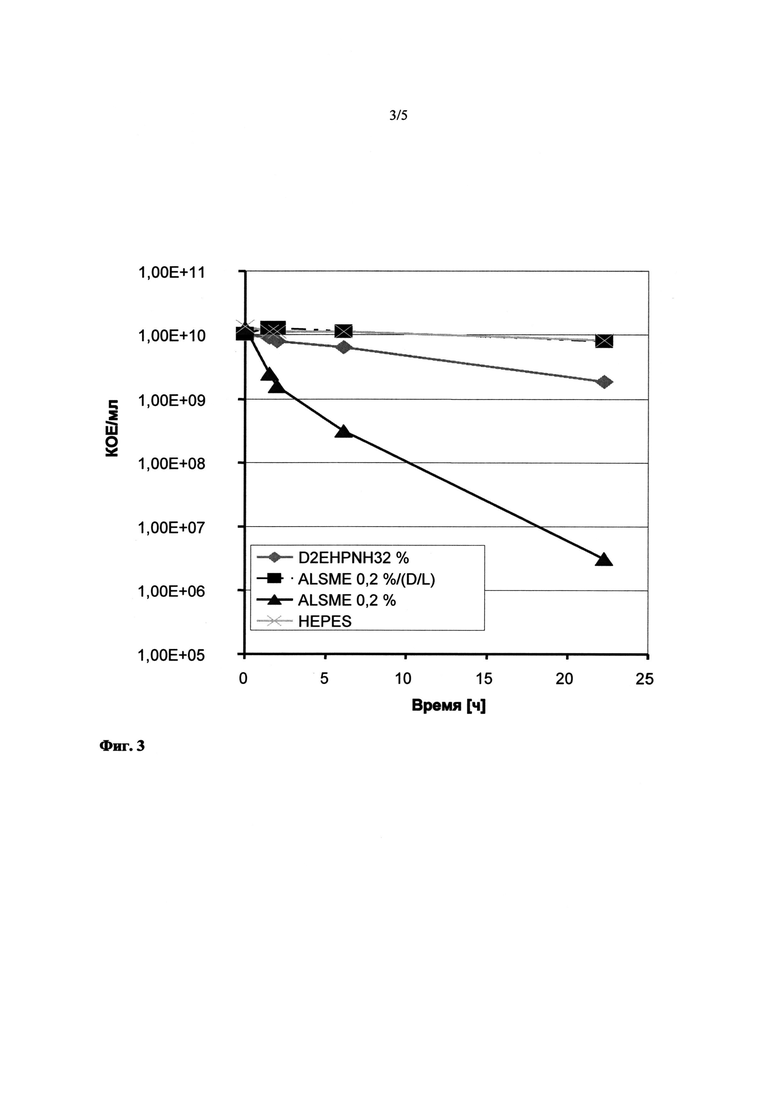
На Фиг.3 показано воздействие применения жидкого катионообменника на токсичность по изменению числа живых клеток штамма Е.coli - W3110 в присутствии ALSME 0,2%, доведенной аммиаком DEHPA („D2EHPNH3 2%″) либо же смеси DEHPA/LSME (2%/98%) („D/L″) в присутствии ALSME 0,2%.
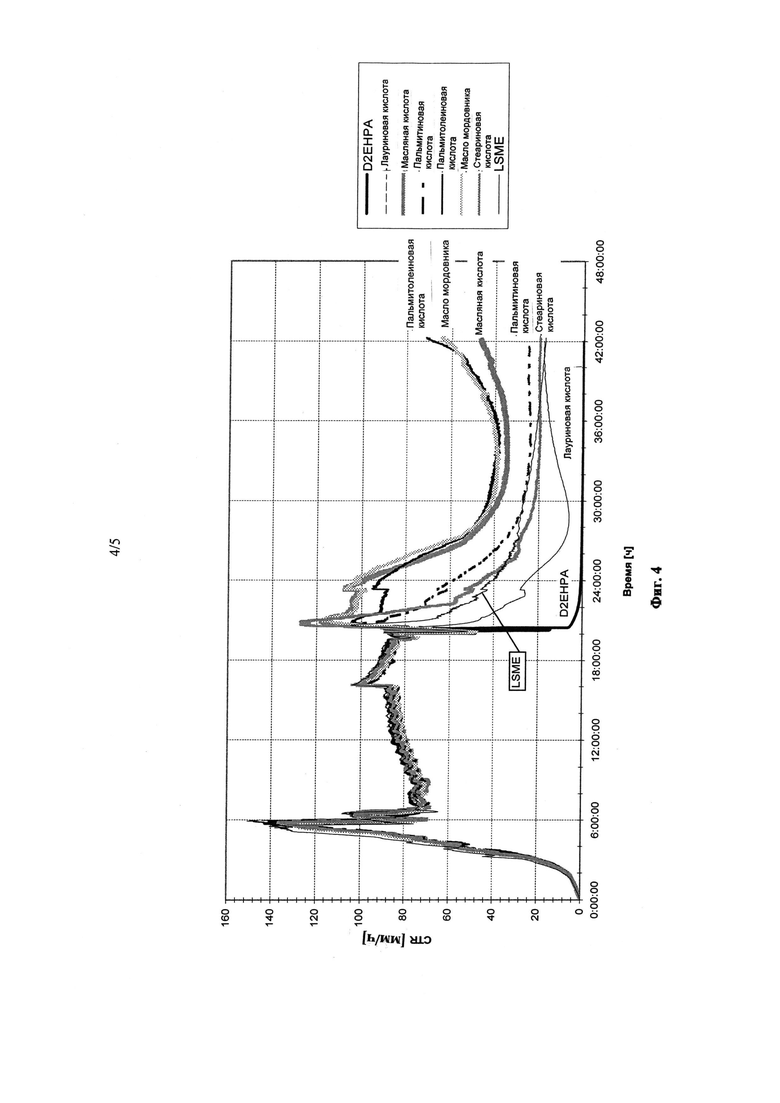
Фиг.4 демонстрирует воздействие различных жидких катионообменников на CTR штамма Е.coli, вырабатывающего метиловый эфир аминолауриновой кислоты. Эксперимент проводили так, как описано в примере 4.
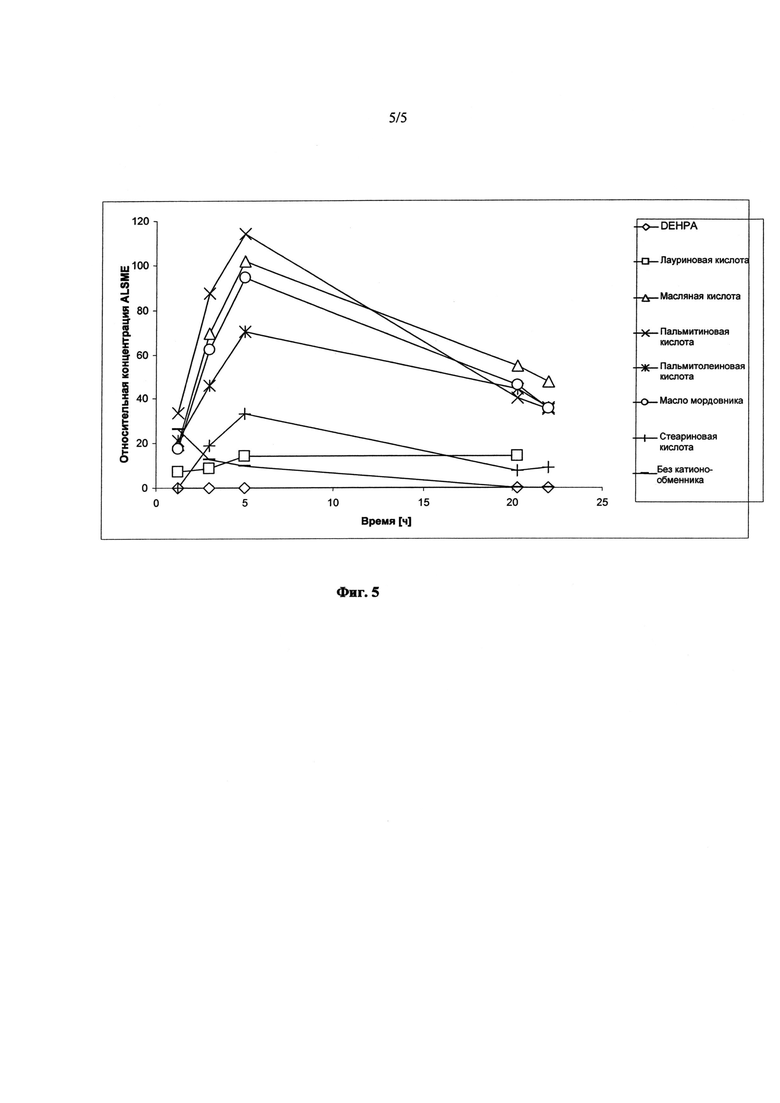
Фиг.5 демонстрирует влияние различных жидких катионообменников на выход метилового эфира аминолауриновой кислоты, который синтезирует штамм Е.coli с надлежащей генетической модификацией. Эксперимент проводили так, как описано в примере 4.
Пример 1: Исследование токсичности растворителя LSME (метиловый эфир лауриновой кислоты), который применяют в составах с жидкими катионообменниками.
В этом опыте продемонстрировали относительно низкую токсичность LSME в отношении имеющих биотехнологическое значение микроорганизмов, которая делает LSME подходящим органическим растворителем для способа согласно изобретению.
Прежде чем можно было провести определение КОЕ, на пластину LB (10 г/л пептона из казеина, 5 г/л экстракт дрожжей, 10 г/л NaCl) провели посев мазком Е.coli BW3110 и инкубировали 24 ч. Вечером следующего дня с этой пластины, на которую ранее сделали посев, привили предварительную культуру. Объем этой предварительной культуры составлял 50 мл среды LB, а инкубирование проводили на протяжении ночи - ок. 16 ч. На следующий день предварительную культуру, имеющую OD600 в 0,2 пересеяли в 200 мл среды М9 (Na2HPO4 6,79 г/л; KH2PO4 3,0 г/л; NaCl 0,5 г/л; NH4Cl 1 г/л; 1 мл/л раствор микроэлементов, pH 7,4. Раствор микроэлементов: HCl 37% (=455,8 г/л) 36,50 г/л; MnCl2*7H2O 1,91 г/л; ZnSO4*7H2O 1,87 г/л; Na-EDTA*2H2O (Titriplex III) 0,84 г/л; H3BO3 0,30 г/л; Na2MoO4*2H2O 0,25 г/л; CaCl2*2H2O 4,70 г/л; FeSO4*7H2O 17,80 г/л; CuCl2*2H2O 0,15 г/л) с 3% глюкозы (м/об.) и инкубировали ок. 20 ч. После инкубации основной культуры клетки собрали, центрифугировали их при 5258 G и 4°C в течение 10 мин. и ресуспендировали их при OD600, равной 30, в 10 мл 50 мМ Kpi-буфера при pH 7,4 (или 25 мМ буфера HEPES pH 7,4, если определение КОЕ проводили с ALSME). Оба использованных буферных раствора содержали 5% глюкозы (м/об.). Затем суспензию бактерий перенесли в колбы для встряхивания и добавили растворы соответствующих веществ. По завершении перемешивания путем качания колбы оттуда извлекали пипеткой 100 мкл суспензии и помещали в 900 мкл подготовленного стерильного солевого раствора. Это соответствовало пробоотбору в момент t0. Затем реакционные смеси инкубировали при 250 об/мин и 30°C. Число КОЕ определяли на протяжении периода в 22 ч. Сначала пробоотбор проводили в моменты t0, t3, t6 и t22. Для некоторых реакционных смесей добавили еще одну временную точку пробоотбора - t1,5, а кроме того высеяли еще один ряд разведении, чтобы минимизировать отклонения.
OD600 составляла 60. Клетки ресуспендировали в Kpi-буфере, а затем смешали в колбе с 5 мл LSME 98% (вес/вес). Высеяли по одной степени разведения на реакционную смесь. Число КОЕ/мл на оставалось постоянным на протяжении 6 ч. Через 22 ч отмечалось снижение числа живых клеток только на 30,3%.
Пример 2: Контрольные опыты по сравнению токсичности различных жидких катионообменников в отношении микроорганизмов, имеющих биотехнологическое значение
Этот пример демонстрирует более низкую токсичность неразветвленных жирных кислот по сравнению с другими жидкими катионообменниками, например, DEHPA, а также разветвленными и неразветвленными насыщенными жирными кислотами.
Сначала предварительную культуру, включающую в себя 20 мл среды LB в колбе с дефлектором емкостью 100 мл, привили криокультурой соответствующего штамма. В течение ночи проводили культивацию при 37°C на фоне встряхивания с интенсивностью 200 об/мин, а на следующий день культуру использовали для прививки той же главной культурой до OD в 0,2. Затем главные культуры (по 30 мл среды LB) продолжали инкубировать в тех же условиях. При оптической плотности OD 0,4-0,5 на главную культуру в каждом случае наслаивали тот же объем растворителя (30 мл), а затем продолжали инкубирование.
Для определения числа КОЕ (cfu - colony-forming units, колониеобразующих единиц) при последующих опытах отбирали пробы размером 0,1 мл и разбавляли их стерильным раствором 0,9% NaCl. Подходящие уровни разбавления высевали в чашки LB-агара. После инкубирования в течение ночи при 34°C подсчитывали образовавшиеся колонии и определяли число КОЕ.
Эксперимент 1: сравнение токсичности DE2HPA и насыщенной жирной кислоты в роли жидкого катионообменника
50% DEHPA либо же лауриновой кислоты (15%), в каждом случае растворенных в LSME и с эквимолярной либо же 25 моль-% нагрузкой ALSME, в качестве жидкого катионообменника приводили в контакт со штаммом Е.coli BL21 (DE3) и изучали влияние обоих этих соединений на способность штамм формировать колонии, выраженную в КОЕ. В предварительных опытах удалось показать, что метиловый эфир лауриновой кислоты (который ввиду недостающего заряда не может играть роль жидкого катионообменника) хорошо переносится используемыми штаммами.
Показано, что оба жидких катионообменника существенно снижают число КОЕ, но при использовании лауриновой кислоты (в отличие от DEHPA) все еще имеется некоторое количество жизнеспособных клеток, и поэтому насыщенная жирная кислота предпочтительна в качестве жидкого катионообменника.
Эксперимент 2: сравнение токсичности разветвленных насыщенных жирных кислот и различных количеств олеиновой кислоты в роли жидкого катионообменника
Для этого использовали две различные концентрации олеиновой кислоты и регулировали объем добавлением соответствующего количества LSME (метилового эфира лауриновой кислоты).
Показано, что при использовании ненасыщенной жирной кислоты (олеиновой кислоты) вместе с LSME число жизнеспособных клеток значительно выше, чем при использовании разветвленных насыщенных жирных кислот.
Эксперимент 3: сравнение токсичности неразветвленных насыщенных жирных кислот и ненасыщенных жирных кислот в роли жидкого катионообменника
В этом опыте сравнивали различные количества насыщенной жирной кислоты с ненасыщенной жирной кислотой с точки зрения их токсичности при использовании в качестве жидкого катионообменника.
Ввиду малой растворимости такой ненасыщенной жирной кислоты как лауриновая кислота ее применяли в малом количестве. Объемы различных катионообменников приравнивали к LSME. Число КОЕ определяли в начале, через 4,5 ч и через 24 ч.
Как видно на Фиг.2, добавление в качестве жидкого катионообменника насыщенной жирной кислоты, даже в меньшей концентрации, чем у ненасыщенной жирной кислоты, вызывает снижение числа КОЕ, в то время как в случае ненасыщенной жирной кислоты, напротив, обнаруживается увеличение числа КОЕ.
В целом токсичность различных исследованных жидких катионообменников снижается в следующем порядке: DEHPA > насыщенные жирные кислоты > ненасыщенные жирные кислоты.
Пример 3: Снижение токсичности органического соединения с положительным зарядом посредством создания контакта с жидким катионообменником.
Этот эксперимент демонстрирует, что благодаря присутствию жидкого катионообменника токсическое действие положительно заряженного органического соединения в водной фазе, которая представляет собой ферментационный бульон, можно снизить, если это соединение экстрагировать в органическую фазу.
Основные экспериментальные процедуры соответствовали таковым в примере 1.
Поскольку ALSME 0,2% (масс./об), будучи растворен в водных системах, оказывает бактерицидное действие, этот опыт повторно провели в комбинации с D2EHPNH3/LSME 2/98% (масс./масс.) в колбах для встряхивания, и D2EHPNH3 при этом означает загруженную аммонием D2EHPA.. Применение жидкого ионообменника улучшает переход ALSME в органическую фазу, благодаря чему его концентрация в жидкой фазе, в которой также находятся клетки, снижается. Чтобы снизить токсическое воздействие, обусловленное D2EHPA, применяли низкие концентрации в 2% (масс./масс.) D2EHPNH3.
Бактерии сначала ресуспендировали в 5 мл (соответствует половине объема буфера). К другим 5 мл буфера при необходимости добавляли 0,4% (масс./об) ALSME, а затем обрабатывали в вортексе (шейкер) в 5 мл D2EHPNH3/LSME 2/98% (масс./масс.) в течение 1 мин. при 3000 об/мин. Этот раствор добавили к предварительно помещенной в колбы для встряхивания суспензии бактерий и перемешали с ней. Затем отобрали первую пробу.
В начале экспериментов раствор обладал пенистой консистенцией, которая, однако, в обоих опытах исчезла ко второму пробоотбору. Сокращение ″D/L″ использовали для обозначения смеси D2EHPNH3 (нагруженная аммиаком D2EHPA)/LSME 2/98% (вес/вес). Между пробоотборами t0 и t1,5 ч число КОЕ/мл возросло на 34,3%. С момента пробоотбора (t1,5) до последнего пробоотбора (122) число КОЕ/мл снизилось на 54,9%.
По сравнению с реакционной смесью с D2EHPNH3/LSME 2/98% (масс./масс.) без добавления ALSME 0,2% (масс./об), число способных к размножению клеток через 22 ч было в 4,5 раза выше и незначительно ниже (на 3,4%), чем среднее значение контрольных реакционных смесей в буфере HEPES (см. Фиг.4). По сравнению с реакционной смесью с ALSME 0,2% (масс./об) в колбах для встряхивания без добавления органической фазы, число КОЕ/мл было в 2800 раз выше.
Показано, что присутствие жидкого катионообменника снижает токсичность положительно заряженного соединения, что в данном случае выражается в числе оставшихся КОЕ.
Пример 4: Контрольные эксперименты для сравнения токсичности различных жидких катионообменников по отношению к микроорганизму, вырабатывающему ω-аминолауриновую кислоту (ALS) и метиловый эфир (ALSME)
Биотрансформацию метилового эфира лауриновой кислоты в метиловый эфир аминолауриновой кислоты тестировали в системе 8-кратной параллельной ферментации производства DasGip с различными ионообменниками.
Для ферментации использовали реакторы емкостью 1 л. Зонды для pH калибровали по двум точкам с помощью эталонных растворов с pH 4,0 и pH 7,0. Реакторы заполнили 300 мл воды и автоклавировали их при 121°C в течение 20 минут, чтобы обеспечить стерильность. Затем зонды для определения р0з поляризовали на протяжении ночи (не менее 6 часов). На следующее утро воду удалили в условиях чистого помещения (бокса, Clean Bench) и заменили ее средой с высокой плотностью клеток с 50 мг/л канамицина и 34 мг/л хлорамфеникола. После этого зонды для pO2 откалибровали по одной точке (мешалка 600 об/мин, газ 10 сл/ч воздуха), а магистрали для питательного раствора, коррекционных средств и средств индукции очистили методом «по месту» (Clean-in-Place). Для этого шланги промыли 70%-ным этанолом, затем 1 М NaOH, потом стерильной полностью обессоленной водой, а в конце заполнили соответствующей средой.
Вырабатывающий ALS и ALSME штамм Е.coli BL21 (DE3) Tlr рВТ10 pACYC:Duet[TAcv] сначала выращивали на протяжении ночи как криокультуру в среде LB (25 мл в колбе с дефлектором емкостью 100 мл) с 50 мг/л канамицина и 34 мг/л хлорамфеникола, при 37°C и 200 об/мин на протяжении приблизительно 18 ч. Затем по 2 мл пересеяли в среду с высокой плотностью клеток (глюкоза 15 г/л (30 мл / л отдельно автоклавированного маточного раствора 500 г/л с 1% MgSO4·7H2O и 2,2% NH4Cl), (NH4)2SO4 1,76 г/л, K2HPO4 19,08 г/л, KH2PO4 12,5 г/л, экстракт дрожжей 6,66 г/л, тринатрия цитрата дигидрат 11,2 г, раствор цитрата железа аммония 17 мл/л отдельно автоклавированного 1%-ного маточного раствора, раствор микроэлементов 5 мл/л отдельно автоклавированного маточного раствора (HCl (37%) 36,50 г/л, MnCl2·4H2O 1,91 г/л, ZnSO4·7H2O 1,87 г/л, этилендиаминтетрауксусной кислоты дигидрат 0,84 г/л, H3BO3 0,30 г/л. Na2MoO4·2H2O 0,25 г/л, CaCl2·2H2O 4,70 г/л, FeSO4·7H2O 17,80 г/л, CuCl2·2H2O 0,15 г/л)) (3*25 мл в колбе с дефлектором емкостью 100 мл) 50 мг/л канамицина и 34 мг/л хлорамфеникола и инкубировали при 37°C/ 200 об/мин еще 6 ч.
Три культуры объединили в колбе для встряхивания и определили, что оптическая плотность составляет 7,2. Чтобы привить реакторы с оптической плотностью 0,1, в шприцы емкостью 5 мл набрали по 4,2 мл и привили реакторы иглой через перегородку.
Использовали следующую стандартную программу:
Проведенный эксперимент можно разделить на два этапа: выращивания, во время которого клетки должны были достичь определенной оптической плотности, и последующей биотрансформации, во время которого индуцировали экспрессию генов, необходимых для биотехнологического процесса синтеза ALSME. Значения pH односторонним образом доводили аммиаком (12,5%) до pH 6,8. Во время выращивания и биотрансформации уровень растворенного кислорода (DO, dissolved oxygen) в культуре поддерживали на уровне 30%, регулируя его скоростью вращения мешалки и скоростью подачи газа. Ферментацию осуществляли в периодическом режиме с подпиткой, причем старт подачи питания - 5 г/лч глюкозой (500 г/л глюкозы с 1% MgSO4·7H2O и 2,2% NH4Cl), обусловливался пиком DO. С началом подпитки температуру также снизили с 37°C до 30°C. Экспрессию трансаминазы индуцировали через 2 ч после начала подпитки посредством автоматического добавления ИПТГ (1 мМ). Индукцию генов alk вызывали ручным добавлением DCPR (0,025% об/об) через 10 ч после старта подпитки. До начала биотрансформации определяли оптическую плотность бульонов с культурой.
Фаза биотрансформации начиналась через 14 ч после старта подпитки. Для этого к ферментационному бульону в виде порции добавляли 150 мл смеси метилового эфира лауриновой кислоты и конкретного ионообменника (10% масс./масс.). В качестве ионообменников применяли ди-(2-этилгексил-)фосфорную кислоту (DEHPA), лауриновую кислоту, пальмитиновую кислоту, пальмитолеиновую кислоту, стеариновую кислоту и смесь свободных жирных кислот с омыления масла мордовника. Чтобы предоставить трансаминазе донор аминогрупп, одновременно с добавлением органической фазы к ферментационному бульону добавили 10,7 мл раствора аланина (125 г/л). Для пробоотбора из котла извлекали 2 мл ферментационного бульона и часть его разбавляли в соотношении 1/20 смесью ацетона и HCl (с(HCl)=0,1 моль/л) и экстрагировали ею же. Пробы отбирали из всех 8 реакторов через 1,25 ч, 3 ч, 5 ч, 20 ч, 22 ч и 25 ч после начала биотрансформации. Скорость оборота кислорода (OTR = oxygen transfer rate) и углерода (CTR = carbon transfer rate) во время ферментации определяли с помощью анализа отходящих газов систем DasGip. Ферментацию завершали через 22 ч после старта биотрансформации.
Количественное определение ALS, ALSME, DDS, DDSME, LS, LSME, HLS, HLSME, OLS и OLSME в ферментационных пробах осуществляли методом ЖХ-ИЭР/МС2 с помощью внешней калибровки для всех анализируемых веществ и с применением внутреннего стандарта аминоундекановой кислоты (AUD).
При этом использовали следующее оборудование:
- Установку ВЭЖХ системы 1260 (Agilent; Бёблинген) с автоматическим пробоотборником (G1367E), бинарным насосом (G1312B) и термостатом (нагревателем) для колонки (G1316A)
- Масс-спектрометр TripelQuad 6410 (Agilent; Бёблинген) с источником ИЭР (ESI)
- Колонка для ВЭЖХ: Kinetex С 18, 100×2,1 мм, размер частиц 2,6 мкм, размер пор 100 Å (Phenomenex, Ашаффенбург)
- Предколонка: KrudKatcher Ultra HPLC In-Line Filter; глубина фильтра 0,5 мкм, внутренний диаметр 0,004 мм (Phenomenex, Ашаффенбург)
Для подготовки образцов в реакционный сосуд (пробирку) емкостью 2 мл пипеткой помещали 1900 мкл растворителя (смесь ацетона и 0,1 N НС1 1:1) и 100 мкл образца. Смесь встряхивали на вортексе ок. 10 секунд, а затем центрифугировали при 13000 об/мин на протяжении 5 мин. Прозрачный супернатант отбирали пипеткой и после соответствующего разбавления (80% (об/об) ACN, 20% бидистиллированной H2O (об/об), + 0,1% муравьиной кислоты) проводили анализ К каждым 900 мкл образца добавляли пипеткой 100 мкл ISTD (10 мкл при объеме образца 90 мкл).
Разделение посредством ВЭЖХ осуществляли с помощью вышеуказанной колонки либо же предколонки. Объем впрыскивания составил 0,7 мкл, температура колонки 50°C, скорость потока 0,6 мл/мин. Подвижная фаза состояла из элюента А (0,1%-ный (об/об) водный раствор муравьиной кислоты) и элюента В (ацетонитрил с 0,1% (об/об) муравьиной кислоты). Использовали следующую конфигурацию градиента:
Анализ ИЭР-МС2 проводили в положительном режиме со следующими параметрами источника ИЭР:
- Температура газа 280°C
- Поток газа 11 л/мин
- Давление распылителя 50 psi
- Напряжение в капилляре 4000 В
Детектирование и количественное определение отдельных соединений осуществляли с использованием следующих параметров, причем в каждом случае один ион-продукт использовали как Qualifier (качественный индикатор), а один как Quantifier (количественный индикатор):
Результаты:
Если в качестве катионообменника используют DEHPA, как это изложено в уровне техники, то непосредственно после добавления соединения в культуру происходит падение OTR. За короткое время кривая падает до 0, что указывает на то, что в культуре не остается клеток с метаболической активностью. То есть, DEHPA оказывает на клетки сильное токсическое воздействие.
Если вместо DEHPA в качестве жидкого катионообменника применяют лауриновую кислоту, то, хотя падение OTR тоже имеет место, но оно не так сильно выражено, а за последующие 22 ч клетки оправляются и демонстрируют рост метаболической активности. Следовательно, лауриновая кислота заметно менее токсична, чем DEHPA.
Результаты, наблюдаемые при использовании насыщенных жирных кислот с более длинными углеродными цепями, еще существенно лучше. Если используют пальмитиновую и стеариновую кислоту, то падение кривой OTR значительно более ограничено, чем в случае применения лауриновой кислоты или тем более DEHPA. Из этого можно сделать вывод, что эти кислоты обладают значительно меньшим токсическим действием.
Применение ненасыщенных жирных кислот, например, пальмитолеиновой кислоты, омыленного масла мордовника (содержит в основном линолевую кислоту) и олеиновой кислоты неожиданным образом приводит к еще существенно лучшим результатам. Эти кислоты неожиданным образом демонстрируют еще меньшую токсичность, чем насыщенные жирные кислоты.
Источники литературы:
J. Sangster, Octanol-Water Partition Coefficients: Fundamentals and Physical Chemistry, («Коэффициенты распределения «октанол-вода» - основы и физическая химия») Vol.2 of Wiley Series in Solution Chemistry, John Wiley & Sons, Chichester, 1997
Asano, Y., Fukuta, y., Yoshida, Y., and Komeda, H. (2008): The Screening, Characterisation, and Use of w-Laurolactam Hydrolase: A New Enzymatic Synthesis of 12-Aminolauric Acid («Скрининг, характеристика и использование ω-лактам-гидролазы - новый ферментативный синтез 12-аминолауриновой кислоты»), Biosc. Biotechn. Biochem., 72 (8), 2141-2150
DE 10200710060705 (2007): ω-Aminocarbonsauren oder ihre Lactame, herstellende, rekombinante Zeilen («Рекомбинантные клетки, синтезирующие ω-аминокарбоновые кислоты или их лактамы»)
F.М. Ausubel (1995), Current Protocols in Molecular Biology («Действующие протоколы в молекулярной биологии»). John Wiley & Sons, Inc.
A.М. Lesk (2008), Introduction to Bioinformatics («Введение в биоинформатику»), 3rd Edition
| название | год | авторы | номер документа |
|---|---|---|---|
| РАПАМИЦИН ДЛЯ ЛЕЧЕНИЯ ЛИМФАНГИОЛЕЙОМИОМАТОЗА | 2014 |
|
RU2707285C2 |
| СОСТАВЫ И СПОСОБЫ, ПРИМЕНЯЕМЫЕ ДЛЯ УДАЛЕНИЯ ОБОЛОЧЕК ТАБЛЕТОК | 2014 |
|
RU2676474C2 |
| ПЕРОКСИДНЫЕ ДИСПЕРСИИ | 2014 |
|
RU2650394C2 |
| СТАБИЛИЗИРОВАННЫЕ ПО ОТНОШЕНИЮ К ПРОТЕАЗАМ АЦИЛИРОВАННЫЕ АНАЛОГИ ИНСУЛИНА | 2009 |
|
RU2571857C2 |
| ПЕРОКСИДНЫЕ ДИСПЕРСИИ | 2013 |
|
RU2663168C1 |
| ПЕРОКСИДНЫЕ ДИСПЕРСИИ | 2013 |
|
RU2631815C2 |
| КОРМОВАЯ ДОБАВКА, СОДЕРЖАЩАЯ ОЛИГОСАХАРИДЫ И СРЕДНЕЦЕПОЧЕЧНЫЕ ЖИРНЫЕ КИСЛОТЫ | 2011 |
|
RU2557588C2 |
| РАПАМИЦИН-СОДЕРЖАЩАЯ КОМПОЗИЦИЯ, ВВОДИМАЯ ПУТЕМ ИНГАЛЯЦИИ ДЛЯ ЛЕЧЕНИЯ ВОЗРАСТНЫХ ЗАБОЛЕВАНИЙ | 2015 |
|
RU2718583C2 |
| ИНГАЛЯЦИОННАЯ ЛЕКАРСТВЕННАЯ ФОРМА РАПАМИЦИНА ДЛЯ ЛЕЧЕНИЯ ЛЕГОЧНОЙ ГИПЕРТЕНЗИИ | 2015 |
|
RU2732908C2 |
| ЛИПИДНЫЙ ПРЕДКОНЦЕНТРАТ КАТИОННОГО ФАРМАКОЛОГИЧЕСКИ АКТИВНОГО ВЕЩЕСТВА С ДЛИТЕЛЬНЫМ ВЫСВОБОЖДЕНИЕМ И СОДЕРЖАЩАЯ ЕГО ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 2013 |
|
RU2649810C2 |
Изобретение относится к способу для удаления органического соединения из водного раствора. Способ включает стадии a)-c). На стадии a) осуществляют подготовку водного раствора, содержащего органическое соединение, и гидрофобного органического раствора, который включает в себя жидкий катионообменник, причем жидкий катионообменник является гидрофобным. На стадии b) происходит контактирование водного раствора и органического раствора. На стадии c) осуществляют отделение органического раствора от водного раствора. Органическое соединение представляет собой соединение формулы (I) 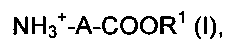 , где R1 представляет собой водород, метил, этил или отрицательный заряд, A - незамещенную прямоцепочечную алкиленовую группу по меньшей мере с тремя атомами углерода, а жидкий катионообменник представляет собой жирную кислоту. Предлагаемый способ позволяет достигнуть максимального смещения равновесного распределения в сторону гидрофобной органической фазы. Изобретение относится также к реакционной смеси для удаления органического соединения из водного раствора. 2 н. и 23 з.п. ф-лы, 5 ил., 2 табл., 4 пр.
, где R1 представляет собой водород, метил, этил или отрицательный заряд, A - незамещенную прямоцепочечную алкиленовую группу по меньшей мере с тремя атомами углерода, а жидкий катионообменник представляет собой жирную кислоту. Предлагаемый способ позволяет достигнуть максимального смещения равновесного распределения в сторону гидрофобной органической фазы. Изобретение относится также к реакционной смеси для удаления органического соединения из водного раствора. 2 н. и 23 з.п. ф-лы, 5 ил., 2 табл., 4 пр.
1. Способ для удаления органического соединения из водного раствора, включающий стадии:
a) подготовка водного раствора, содержащего органическое соединение, и гидрофобного органического раствора, который включает в себя жидкий катионообменник,
причем жидкий катионообменник является гидрофобным,
b) контактирование водного раствора и органического раствора, и
c) отделение органического раствора от водного раствора,
причем органическое соединение представляет собой соединение формулы (I)
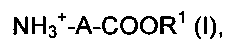
причем R1 представляет собой водород, метил, этил или отрицательный заряд, а A - незамещенную прямоцепочечную алкиленовую группу по меньшей мере с тремя, предпочтительно по меньшей мере с восемью, атомами углерода,
и причем жидкий катионообменник представляет собой жирную кислоту.
2. Способ по п.1, причем температура на стадии b) составляет от 28 до 70°C, предпочтительно от 30 до 37°C.
3. Способ по п.1, причем значение pH на стадии b) составляет от 6 до 8, предпочтительно от 6,2 до 7,2.
4. Способ по п.1, причем соотношение жидкого катионообменника и органического соединения по количеству вещества составляет по меньшей мере 1.
5. Способ по п.1, причем соотношение объемов органического раствора к водному раствору составляет от 1:10 до 10:1.
6. Способ по п.1, причем жидкий катионообменник представляет собой жирную кислоту более чем с 12 атомами углерода.
7. Способ по п.6, причем жидкий катионообменник представляет собой жирную кислоту с 14-22, особенно с 16-18 атомами углерода.
8. Способ по п.1, причем жидкий катионообменник представляет собой ненасыщенную жирную кислоту.
9. Способ по п.8, причем жидкий катионообменник представляет собой олеиновую кислоту или эруковую кислоту.
10. Способ по п.1, причем водный раствор дополнительно включает в себя биологический агент с каталитической активностью, причем биологический агент представляет собой клетку.
11. Способ по п.10, причем клетка представляет собой бактериальную клетку.
12. Способ по п.10, причем клетка представляет собой рекомбинантную алканмонооксигеназу или рекомбинантную трансаминазу.
13. Способ по п.10, причем клетка включает в себя по меньшей мере один фермент из группы, включающей в себя алкогольдегидрогеназу, аланиндегидрогеназу и продукт гена AlkL или их варианты.
14. Способ по п.10, причем присутствие органического соединения отрицательно сказывается на каталитической активности предпочтительно посредством того, что органическое соединение представляет собой токсичное для клетки соединение.
15. Способ по одному из пп.1-14, причем органический раствор дополнительно содержит по меньшей мере один органический растворитель.
16. Способ по п.15, причем органический растворитель - это жирная кислота и/или сложный эфир жирной кислоты.
17. Способ по п.15, причем органический раствор включает в себя в качестве жидкого катионообменника от 20 до 80 об.% олеиновой кислоты, а в качестве растворителя - сложный метиловый эфир лауриновой кислоты, а органическое соединение представляет собой сложный метиловый эфир 12-аминолауриновой кислоты.
18. Способ по п.17, причем в водном растворе присутствует бактериальная клетка, которая включает в себя рекомбинантную алканмонооксигеназу или рекомбинантную трансаминазу.
19. Способ по п.17, причем в водном растворе присутствует бактериальная клетка, которая включает в себя по меньшей мере один фермент из группы, включающей в себя алкогольдегидрогеназу, аланиндегидрогеназу и продукт гена AlkL или их варианты.
20. Реакционная смесь для удаления органического соединения из водного раствора, включающая водный раствор и гидрофобный органический раствор,
причем гидрофобный органический раствор включает в себя жирную кислоту в качестве жидкого катионообменника
и причем водный раствор представляет собой соединение формулы (I)
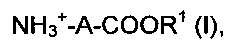
причем R1 представляет собой водород, метил, этил или отрицательный заряд, а A - незамещенную прямоцепочечную алкиленовую группу по меньшей мере с тремя атомами углерода.
21. Реакционная смесь по п.20, причем А представляет незамещенную прямоцепочечную алкиленовую группу по меньшей мере с восемью атомами углерода.
22. Реакционная смесь по п.20, причем жирная кислота содержит более 12 атомов углерода.
23. Реакционная смесь по п.20, причем жирная кислота представляет собой ненасыщенную жирную кислоту.
24. Реакционная смесь по одному из пп.20-23, причем водный раствор дополнительно включает клетку, которая содержит рекомбинантную алканмонооксигеназу или рекомбинантную трансаминазу.
25. Реакционная смесь по одному из пп.20-23, причем водный раствор дополнительно включает клетку, которая содержит по меньшей мере один фермент из группы, включающей алкогольдегидрогеназу, аланиндегидрогеназу и продукт гена AlkL или их варианты.
| Дорожная спиртовая кухня | 1918 |
|
SU98A1 |
| DE 19919490 A1, 23.11.2000 | |||
| D | |||
| M | |||
| TEMPLE ET AL., Liquid Ion-exchange Extraction of some Physiologically Active Amines, NATURE, 1966, Vol | |||
| Парный рычажный домкрат | 1919 |
|
SU209A1 |
| СПОСОБ ВЫДЕЛЕНИЯ ЛИЗИНА ИЗ КУЛЬТУРАЛЬНОЙ ЖИДКОСТИ | 1992 |
|
RU2056941C1 |
Авторы
Даты
2016-07-20—Публикация
2011-12-01—Подача