ПЕРЕКРЕСТНАЯ ССЫЛКА НА ДРУГИЕ ЗАЯВКИ
Данная заявка представляет собой заявку - частичное продолжение патентной заявки США 12/584448, поданной 4 сентября 2009 года, которая включена в данное описание изобретения со ссылками во всей ее полноте.
ОБЛАСТЬ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к новым химическим соединениям 5-амино- или замещенным амино-1,2,3-триазолам, а также к их замещенным производным (упоминаемым в данном описании изобретения как карбоксиамидотриазолы или CAI), к композициям 5-амино- или замещенных амино-1,2,3-триазол-оротатов, а также к их замещенным производным (с определенными соотношениями основание:кислота, СТО), к композициям 5-амино- или замещенных амино-1,2,3-триазол-оротатов, а также к их замещенным производным и оротовой кислоте (с определенными соотношениями основание:кислота, САО) и к более безопасным способам их получения с использованием стабильных, более эффективных и более безопасных исходных веществ для синтеза промежуточных азидных веществ, необходимых в процессе синтеза CAI и композиций оротата - СТО и САО. Более конкретно, изобретение относится к новым полиморфам 5-амино- или замещенных амино-1,2,3-триазолов, а также к их замещенным производным. Еще более конкретно, данное изобретение относится к новым 5-амино- или замещенным амино-1,2,3-триазол-оротатам (СТО с оптимальными соотношениями основание:кислота в диапазоне от 1:1 до 1:4), а также композициям 5-амино- или замещенных амино-1,2,3-триазолов, а также к их замещенным производным и оротовой кислоте (САО) в оптимальных соотношениях основание: кислота от 1:1 до 1:4 и к их применению в контроле и лечении заболеваний, включая, но без ограничения ими, солидные виды рака, дегенерацию желтого пятна, ретинопатию, хронический миелолейкоз, СПИД и заболевания, которые основаны на аберрантной сигнальной трансдукции и пролиферации.
ПРЕДШЕСТВУЮЩИЙ УРОВЕНЬ ТЕХНИКИ
Настоящее изобретение относится к области разработки новых полиморфов 5-амино- или замещенного амино-1,2,3-триазола (CAI), а также к их замещенным производным, оротатам 5-амино- или замещенных амино-1,2,3-триазолов, а также к их замещенным производным и к композициям 5-амино-или замещенных амино-1,2,3-триазолов, а также к их замещенным производным и оротовой кислоте (в оптимальных соотношениях основание:кислота). Целью является разработка новых полиморфов 5-амино- или замещенных амино-1,2,3-триазолов, а также их замещенных производных для улучшения химических, биологических, фармакокинетических и токсикокинетических свойств и улучшения терапевтических свойств, включая, но без ограничения ими, противораковую активность, антиметастатическую активность, опосредованную кальцием сигнальную трансдукцию, антиангиогенез, анти-Р13, анти-СОХ2, апоптоз, понижающую регуляцию белка BCR-ABL при хроническом миелолейкозе, регулирование транскрипции LTR (длинных концевых повторов) ВИЧ или анти-VEGFI свойства.
В 1986 было показано, что 5-амино- или замещенные амино-1,2,3-триазольные соединения, а также их замещенные производные обладают противококцидной активностью. В US 4590201, выданном R.J.Bochis et el., 1986, описан способ получения 5-амино-1-(4-[4-хлорбензоил]-3,5-дихлорбензил)-1,2,3-триазол-4-карбоксамида (L651582 или CAI), который включал использование азида натрия для синтеза одного из основных промежуточных соединений в пути синтеза, 3,5-дихлор-4-(4-хлорбензоил)бензилазида. Затем было показано, что L651582 или CAI ингибирует выборочные пути сигнальной трансдукции, включающие те, в которые вовлечен приток кальция, высвобождение арахидоновой кислоты и образование инозитолфосфатов. US 5359078, выданный Е.С.Kohn et а/, 1994. "L651582" при использовании в данном описании изобретения представляет собой L6515182, CAI, карбоксиамидотриазол, NSC 609974 или 99519-84-3, описанные в предшествующем уровне техники.
Затем в US 5912346, выданном F. Wehrmann, 1999 описаны неорганические и органические соли L651582 и, в частности, описан способ получения оротатных солей L651582. L651582 получали способом, описанным в патенте US 4590201. L651582: оротат находился в соотношении 2:1 (основание:кислота), как определено посредством протонной ЯМР, и имел точку плавления 234-235°С. Как описано выше, синтез промежуточного соединения 3-(4-хлорбензоил)-4-хлорбензил азида выполняли, используя промежуточное соединение 3-(4-хлорбензоил)-4-хлорбензоил бромид и азид натрия в этаноле. В US 5912346 описана улучшенная противоопухолевая активность оротата L651582 (CAI оротат, основание:кислота 2:1) по сравнению с противоопухолевой активностью эквивалентной дозы L651582 в крысиной модели андроген-независимого рака простаты Даннинга R-3227-AT-1.
Карбоксиамидотриазол, L651582, CAI, NSC 609974 или 99519-84-3, ингибитор опосредованной кальцием сигнальной трансдукции, является одним из первых открытых противораковых лекарственных средств, являющихся цитостатическими ингибиторами сигнала. Его испытывали на пациентах, страдающих от солидных видов рака в Фазе I, Фазе II и Фазе III клинических исследований в Национальном Институте Рака (NCI). Однако NCI остановило разработку L651582, так как он не продемонстрировал эффективность в испытаниях на людях и/или беспокоил вследствие недостаточной биодоступности, тяжелой желудочно-кишечной токсичности, нейротоксичности и проблем с переносимостью, которые мешали оптимальному дозированию для достижения терапевтического эффекта. Капсулы микронизированной композиции L651582 в PEG-400 использовали в клинических исследованиях для улучшения биодоступности лекарственного средства. Kohn EC et al., Clinical Cancer Res 7: 1600-1609 (2001); Bauer KS et al., Clinical Cancer Res 5: 2324-2329 (1999); Berlin J et al., J Clin One 15: 781-789 (1997); Berlin J et al., Clinical Cancer res 8: 86-94 (2002); Yasui H et al., J Bioi Chem 45:28762-28770 (1997); Alessandro Retal., J Cell Physiol 215: 111-121 (2008).
Следовательно, оротат L651582 (основание:кислота 2:1), описанный в US 5912346, представлял собой потенциальный путь спасения этого многообещающего лекарственного средства, L651582, посредством улучшения его эффективности, на основе доклинических исследований. Однако возникли проблемы в масштабировании способа получения оротата L651582 (соотношение 2:1) в больших количествах согласно способу, описанному в US 5912346.
Относительно применения оротовой кислоты в усилении обезболивающих эффектов лекарственных средств в US 4061741, выданном Wawretschek W et al, 1977, описано применение декстропропоксифена-HCl, левопропоксифена-HCl или салицилата натрия в комбинации с оротатом холина и сделан вывод, что препарат лекарственного средства в комбинации с оротатом холина обеспечивал наилучшие эффекты. Очевидно, что известный уровень техники представляет противоречивые учения о соотношениях и химической природе оротовой кислоты, связанной с химическими соединениями.
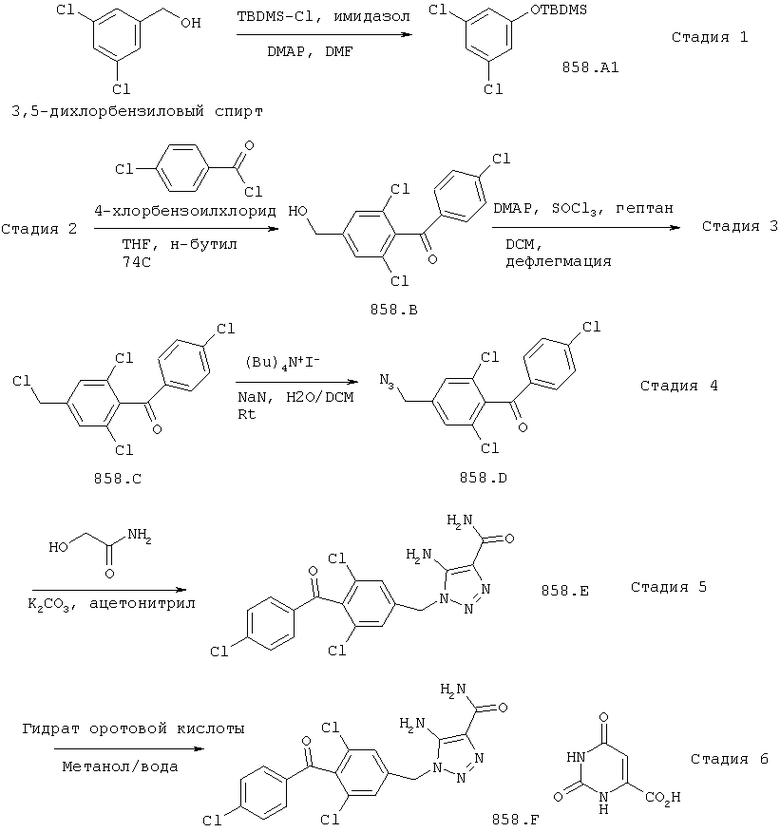
Схема синтеза, описанная в предшествующем уровне техники для оротата L651582, показана в Реакционной схеме I выше. 858 является идентификатором продукта, например 858A-858D представляют собой промежуточные соединения. 858Е представляет собой карбоксиамидотриазол (CAI). 858F представляет собой карбоксиамидотриазол: оротовую кислоту или карбоксиамидотриазол: оротат или СТО, как определено в данном описании изобретения.
В сведениях из предшествующего уровня техники предлагалось применение оротата холина в комбинации с лекарственным средством в качестве предпочтительного воплощения. К сожалению, это не относилось к проблемам масштабирования производства СТО для клинической разработки, встретившимся в настоящем изобретении. Было непонятно, является ли соотношение основание:кислота в оротате L651582 (2:1) оптимальной химической структурой лекарственного средства. Кроме того, возникли проблемы при масштабировании производства оротата L651582 (2:1) для изготовления больших количеств. Лишь некоторые производители имели оборудование и средства, необходимые для обработки больших количеств азида натрия, и подрядчиков, которые имели средства взимать большую плату за услуги.
После защиты спиртовой группы в 3,5-дихлорбензиловом спирте как стадии TBDMS (трет-бутилдиметилсилил) эфира (стадия 1) этот эфир взаимодействует с 4-хлорбензоилхлоридом с образованием замещенного бензофена (стадия 2). Бензофен обрабатывают тионилхлоридом (стадия 3) и затем азидом натрия (стадия 4) с образованием 3,5-дихлор-4-(4-хлорбензоил)бензилазида. В результате взаимодействия данного азида с цианоацетамидом получают L651582 (стадия 5). В результате взаимодействия L651582 с оротовой кислотой образуется оротат L651582 (2:1) (стадия 6).
Применение азида натрия в указанном выше способе в стадии 4 было серьезным недостатком при масштабировании получения оротата L6515182 в больших количествах. Обработка больших количеств азида натрия должна производиться в специальных чувствительных к давлению реакторах, так как азид натрия представляет собой взрывоопасное вещество с высоким содержанием энергии. Специальные удерживающие установки, требующиеся для обработки азида натрия, обычно увеличивают стоимость изготовления, так как лишь некоторые производители лекарственных средств имели возможность масштабировать процесс для больших количеств лекарственного средства. Это вызвано тем, что азид натрия является быстродействующим, потенциально смертоносным химическим веществом, которое существует в виде белого твердого вещества без запаха. При смешивании с водой или кислотой азид натрия быстро превращается в токсичный газ с едким запахом. Также он превращается в токсичный газ при контакте с твердыми металлами. Оставшиеся в живых после серьезного отравления азидом натрия могут иметь повреждения сердца и головного мозга, и Центр профилактики и контроля заболеваний немедленно консультирует пострадавших по своей «горячей линии» (CDC - Facts About Sodium Azide, 2009). Очевидно, что имелась необходимость разработать более безопасный, новый, доступный по цене и эффективный способ получения оротата 1.651582 без применения азида натрия. Конкурентное ценообразование при доступной цене было невозможным, так как азид натрия (Стадия 4) требовался в получении 3,5-дихлор-4-(4-хлорбензоил)бензилазида, промежуточного соединения, в синтезе оротата L651582, как показано выше. По этой причине было необходимо разрабатывать альтернативный, более безопасный, более эффективный способ получения оротатного лекарственного средства с оптимальной химической конфигурацией и соотношением основание:кислота. Настоящее изобретение стремится преодолеть эти недостатки.
Хотя и было показано, что оротат L651582 имеет значительно более высокую противоопухолевую активность в модели рака предстательной железы у крыс (патент US 5912346), отсутствовало указание или предположение относительно того, являются химические, фармакологические и биологические свойства оротата L65182 в соотношении основание:кислота 2:1 оптимальными или нет. Очевидно, что существует необходимость разработать новые полиморфы CAI и оротатное соединение CAI, которое проявляет оптимальные химические, биологические, фармакологические, терапевтические и токсикокинетических характеристики для обоснования клинической разработки.
Таким образом, главной целью изобретения являлась разработка оротатной композиции CAI (где соотношение основание:кислота находится в диапазоне от 1:1 до 1:4), обладающей улучшенной эффективностью, которая связана с ее биодоступностью, которая, в свою очередь, зависит от ее растворимости в жидкостях организма человека.
Другой целью изобретения являлась разработка более безопасного, более рентабельного способа производства больших количеств CAI, СТО (в виде оротата CAI) и САО (в виде композиции CAI, смешанного с оротовой кислотой).
Важной целью изобретения являлось изготовление более безопасного CAI при помощи использования более безопасных и менее токсичных ингредиентов для производства промежуточных соединений вместо использования азида натрия или азида калия, которые являются высокотоксичными при очень низких концентрациях. Было обнаружено, что CAI, полученный способами, описанными в предшествующем уровне техники, имеет серьезную нейротоксичность и вызывает токсические поражения желудка у пациентов. Следовательно, было важно использовать более безопасные ингредиенты, и улучшенный способ производства также приводил к получению новых полиморфов CAI и их оротатным композициям.
Релевантное содержание указанных выше ссылок специально включено в данное описание изобретения посредством ссылки во всей полноте.
КРАТКОЕ ИЗЛОЖЕНИЕ СУЩНОСТИ ИЗОБРЕТЕНИЯ
Настоящее изобретение стремится преодолеть недостатки, свойственные известному уровню техники путем предложения композиций новых полиморфов 5-амино- или замещенного амино-1,2,3-триазола, а также его замещенных производных (упоминаемых в данном описании изобретения как карбоксиамидотриазолы или CAI); препаратов 5-амино- или замещенных амино-1,2,3-триазол-оротатов, а также их замещенных производных (с определенными соотношениями основание:кислота, СТО); и препаратов 5-амино- или замещенных амино-1,2,3-триазол-оротатов, а также их замещенных производных и оротовой кислоты (с определенными соотношениями основание:кислота, САО).
В настоящем изобретении предлагаются более безопасные способы их получения посредством использования стабильных, более эффективных и безопасных исходных веществ для синтеза промежуточных азидных веществ, необходимых в синтезе CAI и оротатных препаратов - СТО и САО.
Более конкретно, данное изобретение относится к новым полиморфам 5-амино- или замещенных амино-1,2,3-триазолов (CAI), а также к их замещенным производным. CAI присутствует в нескольких полиморфных формах, включая, без ограничения ими, Форму 1 или Форму 2.
Еще более конкретно данное изобретение относится к новым 5-амино- или замещенным амино-1,2,3-триазол-оротатам (СТО с оптимальными соотношениями основание:кислота в диапазоне от 1,1 до 1:4), а также к композициям 5-амино- или замещенных амино-1,2,3-триазолов, а также их замещенных производных и оротовой кислоты (САО) с оптимальными соотношениями основание:кислота, к оротатам (СТО), а также к их замещенным производным.
В другом аспекте данное изобретение относится к способу получения промежуточных азидных веществ, необходимых в синтезе, с использованием стабильных, более безопасных и допустимых (по цене) исходных веществ, включая, без ограничения ими, дифенилфосфорилазид или триметилсилилазид, TMSN3 вместо азида натрия или азида калия.
Более конкретно, данное изобретение относится к новым полиморфам 5-амино- или замещенного амино-1,2,3-триазола, а также к их замещенным производным, их оротатным производным (СТО) (соотношение основание:кислота в диапазоне от 1:1 до 1:4) и их применению в лечении заболеваний, включая, без ограничения ими, солидные виды рака, дегенерацию желтого пятна, ретинопатию, хронический миелолейкоз, СПИД и заболевания, которые основаны на аберрантной сигнальной трансдукции и путях пролиферации, таких как не зависящий от напряжения блокатор кальциевых каналов, PI3, СОХ2, BCR-ABL, апоптоз, транскрипция LTR ВИЧ или VEGF1.
С учетом вышеуказанного состояния уровня техники, в настоящем изобретении предлагаются оротатные производные нового 5-амино- или замещенного амино-1,2,3-триазола или карбоксиамидотриазол-оротаты (СТО), содержащие в своей структуре химический органический фрагмент, который увеличивает их биодоступность, доставку к мишени, противоопухолевую эффективность и снижает токсичность. Конкретно, один класс карбоксиамидотриазолоротатов (СТО), имеющих ионную связь в соотношении в диапазоне от примерно 1:1 до 1:4 (триазол:оротовая кислота), представляет собой новые соединения по изобретению.
Кроме того, композиции 5-амино- или замещенного амино-1,2,3-триазола (CAI), а также их замещенные производные и оротовая кислота (с определенными соотношениями основание:кислота в диапазоне от 1:1 до 1:4, САО).
В другом аспекте изобретения предлагается способ получения азидного промежуточного соединения, 3,5-дихлор-4-(4-хлорбензоил)бензилазида, без использования азида натрия, но при использовании вместо него дифенилфосфорилазида (DPPA), или TMN3, или более безопасных азидных эквивалентов. DPPA значительно более безопасен, чем азид натрия, и использовался для превращения спиртов непосредственно в азиды и, следовательно, в синтезе СТО исключается одна стадия (стадия 3 в Схеме, изображенной выше).
Другой целью изобретения является повышение биодоступности СТО при введении перорально или другими путями человеку и другим млекопитающим и улучшение доставки СТО к мишени, например, посредством улучшения поглощения, доставки и транспорта через ткани, гематоэнцефалический барьер и комплекс сосудистая оболочка глаза-сетчатка.
Еще одной целью изобретения является уменьшение токсичности СТО и родственных соединений при введении в виде оротатных солей посредством увеличения клиренса лекарственного средства из крови, тканей и органов.
Кроме того, изобретение можно применять для снижения взаимодействия лекарственных средств и побочных эффектов, когда СТО или CAI вводят в виде композиции вместе с оротовой кислотой (САО).
Другой целью изобретения является предложение композиций СТО для лечения неоплазм человека и, в частности, первичных или метастатических опухолей, заболеваний, включающих неоваскуляризацию, таких как дегенерация желтого пятна, ретинопатия, диабетическая ретинопатия, хронического миелолейкоза, СПИД, и заболеваний, которые основаны на аберрантной сигнальной трансдукции, и путей пролиферации, таких как не зависящий от напряжения блокатор кальциевых каналов, PI3, СОХ2, BCR-ABL, апоптоз, транскрипция LTR ВИЧ или VEGFI, и снижения токсических вторичных эффектов лекарственного средства на 10%-100% по сравнению с введением L651582 или CAI путем снижения уровней лекарственного средства в нераковых тканях, которые являются объектами, чувствительными к токсичности лекарственного средства.
Предпочтительное воплощение изобретения содержит СТО в соотношении основание: кислота 1:1, более предпочтительное воплощение - в соотношение 1:2 и наиболее предпочтительное воплощение изобретения содержит композиции СТО (в соотношение примерно 0,7:1,3), полученные новым способом по изобретению, для лечения заболеваний, включая, но без ограничения ими, солидные виды рака, дегенерацию желтого пятна, ретинопатию, хронический миелолейкоз и модуляцию путей сигнальной трансдукции, таких как PI3, СОХ2, BCR-ABL, STATS, CrkL, апоптоз, транскрипция LTR ВИЧ, VEGF 1 или другие.
КРАТКОЕ ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
Фиг.1 иллюстрирует структуру СТО посредством ЯМР в виде CAI: оротовая кислота или CAI: оротат, где образец J02642 СТО имеет Форму 1 или Структуру 1 полиморфа CAI.
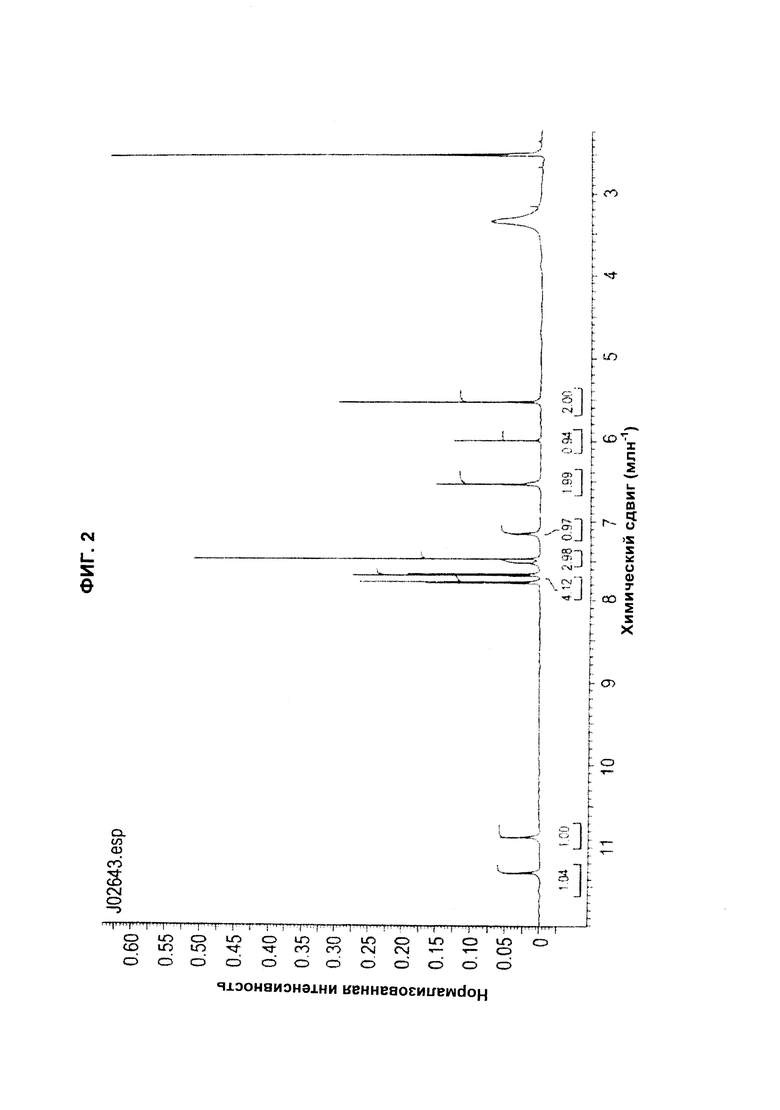
Фиг.2 иллюстрирует структуру СТО с помощью ЯМР в виде CAI: оротовая кислота или CAI: оротат, где образец J02643 СТО имеет Форму 2 или Структуру 2 полиморфа CAI.
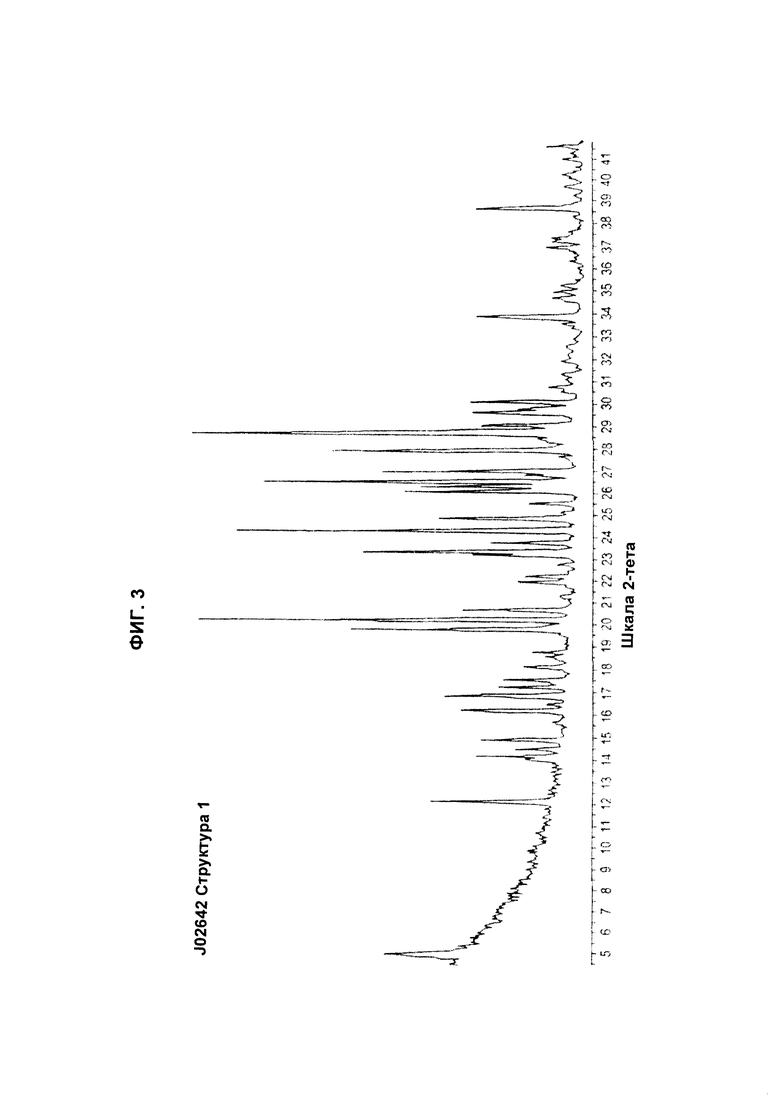
Фиг.3 иллюстрирует дифрактограмму высокого разрешения для образца J02642 СТО, имеющего Форму 1 или Структуру 1 полиморфа CAI.
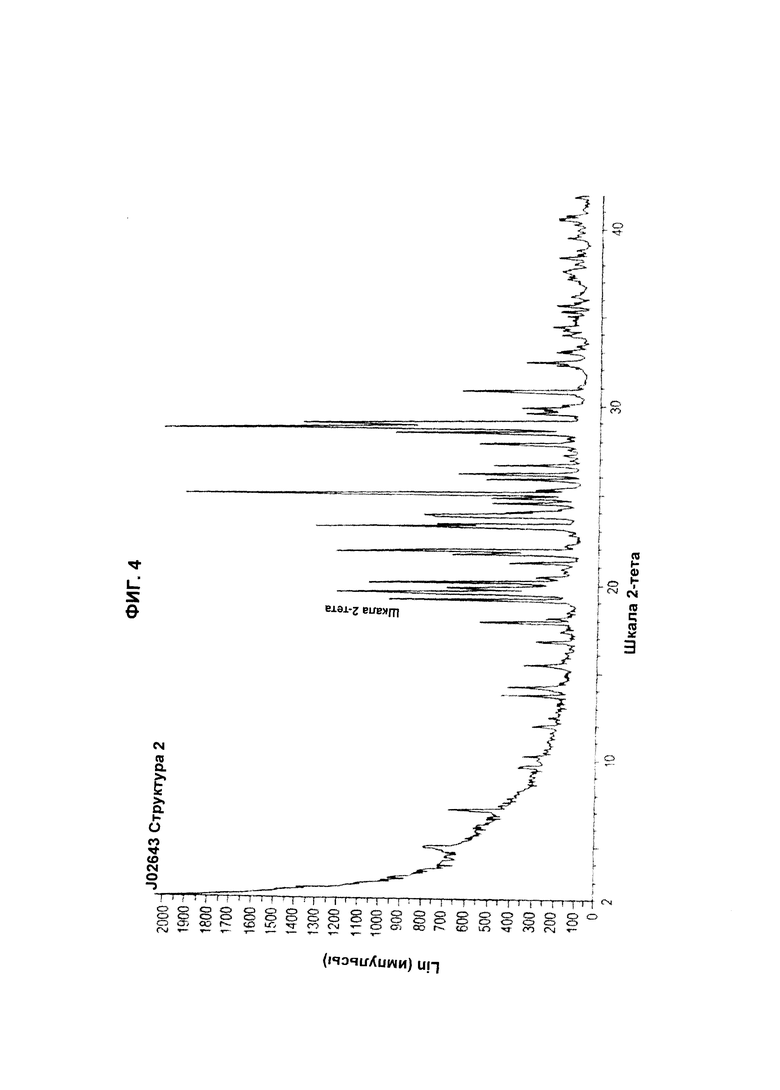
Фиг.4 иллюстрирует дифрактограмму высокого разрешения для образца J02643 СТО, имеющего Форму 2 или Структуру 2 полиморфа CAI.
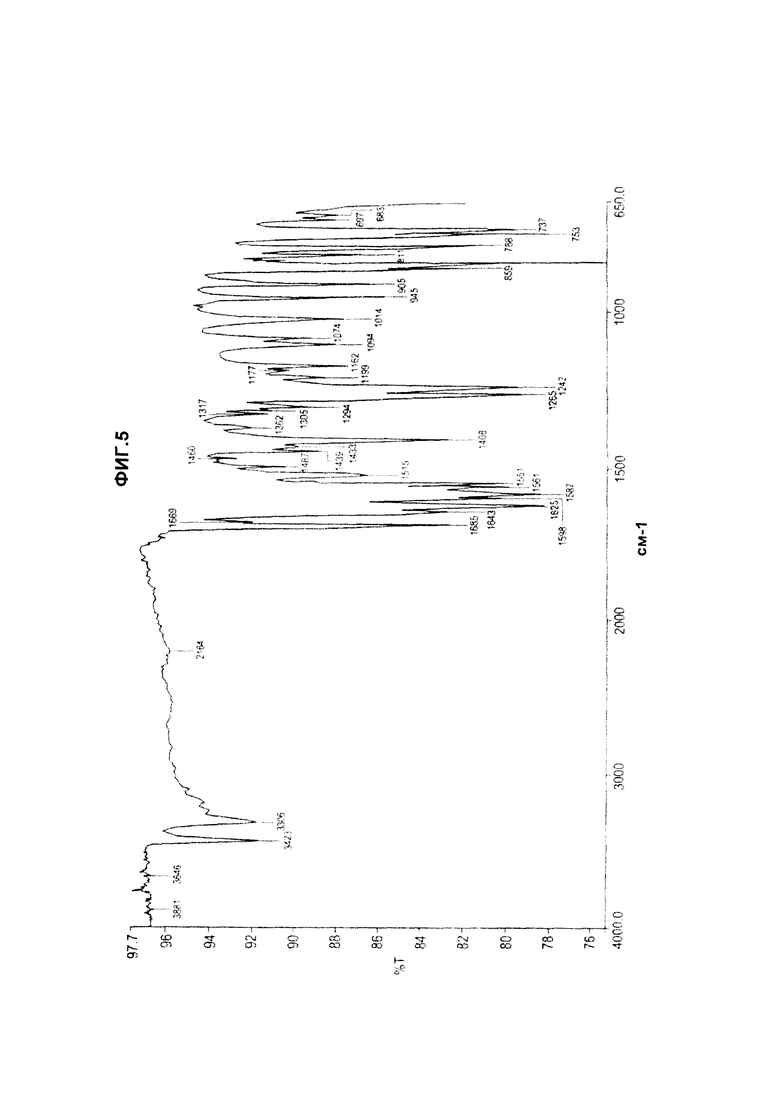
Фиг.5 иллюстрирует FT-IR (инфракрасную спектрометрию с преобразованием Фурье) для образца J02642 СТО, имеющего Форму 1 или Структуру 1 полиморфа CAI.
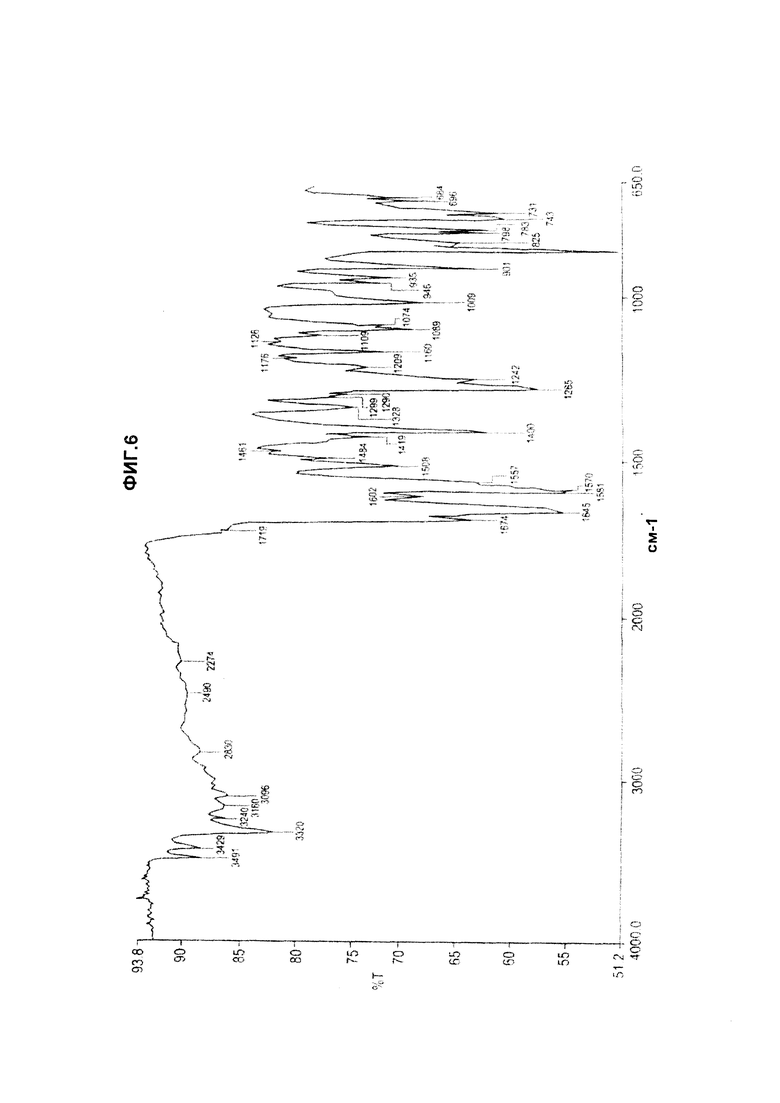
Фиг.6 иллюстрирует FT-IR для образца J02643 СТО, имеющего Форму 2 или Структуру 2 полиморфа CAI.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
В настоящем изобретении предложены новые полиморфы 5-амино- или замещенного амино-1,2,3-триазола или их замещенных амино-1,2,3-триазолов (CAI), полученные новым способом, и включен класс соединений формулы I. Новые полиморфы CAI включают, без ограничения ими, Форму 1 или Форму 2, которые охарактеризованы такими методами, как ЯМР, DSC (дифференциальной сканирующей калориметрией), FT-IR и XRDP (дифракция рентгеновских лучей на порошке).
Формула I
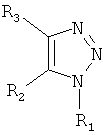
где R1 имеет формулу II, где
R1 представляет собой
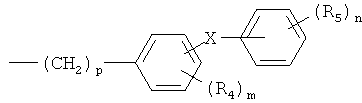
где р равен от 0 до 2; m равен от 0 до 4; и n равен от 0 до 5; Х представляет собой О, S, SO, SO2, CO, CHCN, СН2, или C=NR6, где R6 представляет собой водород, низший алкил, гидрокси, низший алкокси, амино, низший алкиламино, ди(низший алкил)амино или циано; и R4 и R5 независимо представляют собой галоген (F, Cl, Br), циано, трифторметил, низший алканоил, нитро, низший алкил, низший алкокси, карбокси, низший карбалкокси, трифторметокси, ацетамидо, низший алкилтио, низший алкилсульфинил, низший алкилсульфонил, трихлорвинил, трифторметилтио, трифторметилсульфинил или трифторметилсульфонил; R2 представляет собой амино, моно- или ди(низший алкил)амино, ацетамидо, ацетимидо, уреидо, формамидо, формимидо или гуанидино; и R3 представляет собой карбамоил, циано, карбазоил, амидино или N-гидроксикарбамоил; где низший алкил, низшие алкильные, содержащий низший алкил и низшие алканоильные группы, содержат от 1 до 3 атомов углерода.
5-Амино- или замещенное амино-1,2,3-триазольное соединение взаимодействует с оротовой кислотой с образованием оротатных соединений 5-амино- или замещенного амино-1,2,3-триазольного соединения с соотношением в диапазоне от 1:1 до 1:4 (основание:кислота) с помощью улучшенного и более безопасного способа по изобретению с образованием СТО для применения согласно способам по настоящему изобретению.
Кроме того, новые полиморфы CAI взаимодействуют с оротовой кислотой с образованием оротатных соединений из класса соединений формулы II:
Формула II

где оротовая кислота связана ионной связью с R2,
R1 представляет собой
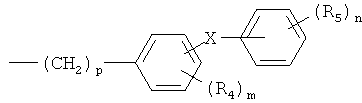
где р равен от 0 до 2; m равен от 0 до 4; и n равен от 0 до 5; Х представляет собой О, S, SO, SO2, СО, CHCN, CH2 или C=NR6, где R6 представляет собой водород, низший алкил, гидрокси, низший алкокси, амино, низший алкиламино, ди(низший алкил)амино или циано; и R4 и R5 независимо представляют собой галоген (F, Cl, Br), циано, трифторметил, низший алканоил, нитро, низший алкил, низший алкокси, карбокси, низший карбалкокси, трифторметокси, ацетамидо, низший алкилтио, низший алкилсульфинил, низший алкилсульфонил, трихлорвинил, трифторметилтио, трифторметилсульфинил или трифторметилсульфонил; R2 представляет собой амино, моно- или ди(низший алкил)амино, ацетамидо, ацетимидо, уреидо, формамидо, формимидо или гуанидино; и R3 представляет собой карбамоил, циано, карбазоил, амидино или N-гидроксикарбамоил; где низший алкил, низшие алкильные, содержащий низший алкил и низшие алканоильные группы, содержат от 1 до 3 атомов углерода.
Предпочтительные воплощения "СТО", как определено в данном описании изобретения, имеют эмпирическую формулу C22H16Cl3N7O6, молекулярную массу 580,76, два перехода с точками плавления 201°С и 236°С. СТО включает новые полиморфы CAI, связанные ионной связью с оротовой кислотой. CAI имеет много полиморфов, включая, без ограничения ими, Форму 1 (Структура 1) или Форму 2 (Структура 2). Два воплощения СТО имеют разные переходные точки плавления, например СТО (Форма I, Структура 1) имеет точки плавления примерно при 136°С, 194°С и 235°С; и СТО (Форма 2, Структура 2) имеет точки плавления примерно при 137°С и 234°С. Эти два воплощения СТО имеют спектр 1H ЯМР, соответствующий структуре CAI: оротовая кислота (Фиг.1 и Фиг.2 соответственно) и картины FT-IR, соответствующие Форме 1 и Форме 2 (Фиг.3 и Фиг.4 соответственно). СТО является кристаллическим, как показывает картина дифракции рентгеновских лучей на порошке для Формы 1 и Формы 2 (Фиг.5 и Фиг.6 соответственно).
Химические названия предпочтительного воплощения СТО включают:
5-амино-1-(4-(4-хлорбензоил)-3,5-дихлорбензил)-1,2,3-триазол-4-карбоксамид, соединение с оротовой кислотой; 5-амино-1-(3,5-дихлор-4-(4-хлорбензоил)бензил)-1Н-1,2,3-триазол-4-карбоксамид, соединение с оротовой кислотой; и 5-амино-1-{[3,5-дихлор-4-(4-хлорбензоил)фенил]метил}-1Н,1,2,3-триазол-4-карбоксамид, соединение с оротовой кислотой.
Более конкретно, химическая структура полиморфов СТО представляет собой:
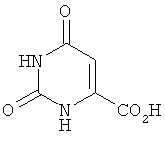
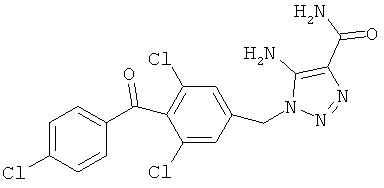
CAI: оротовая кислота
Дополнительное воплощение включает композицию разных полиморфов CAI и оротовой кислоты (САО). Новые полиморфы 5-амино- или замещенного амино-1,2,3-триазола (CAI) или 5-амино- или замещенных амино-1,2,3-триазолов смешивают с оротовой кислотой в диапазоне от 1:1 до 1:4 (основание:кислота) с получением композиций САО, используемой согласно способам по настоящему изобретению.
Новый способ:
Новый способ по изобретению с пятью (5) стадиями, где могут быть получены соединения по изобретению, показан на Реакционной схеме II ниже. Более конкретно, в новом способе используется дифенилфосфорилазид для взаимодействия с промежуточным соединением 858,В на стадии 3 вместо азида натрия. Это исключает стадию 3 в предшествующем уровне техники с образованием промежуточного соединения 858.С. Смотри Схему 1 выше (шесть стадий). Подробные способы описаны в Примерах. От 858.А до 858.F являются промежуточными продуктами и СТО, как обобщено ниже:
858.А представляет собой трет-бутилдиметилсилил-3,5-дихлорбензиловый эфир.
858.В представляет собой 3,5-дихлор-4-(4-хлорбензоил)бензиловый спирт.
858.С представляет собой 3,5-дихлор-4-(4'-хлорбензоил)бензилхлорид.
858.D представляет собой 3,5-дихлор-4-(4'-хлорбензоил)бензилазид.
858.Е представляет собой 5-амино-1-(4-(4-хлорбензоил)-3,5- дихлорбензил)-1,2,3-триазол-4-карбоксамид.
858.F представляет собой 5-амино-1-(4-(4-хлорбензоил)-3,5-дихлорбензил)-1,2,3-триазол-4-карбоксамид, соединение с оротовой кислотой, (CAI:оротовая кислота)(CAI:оротат) (СТО).
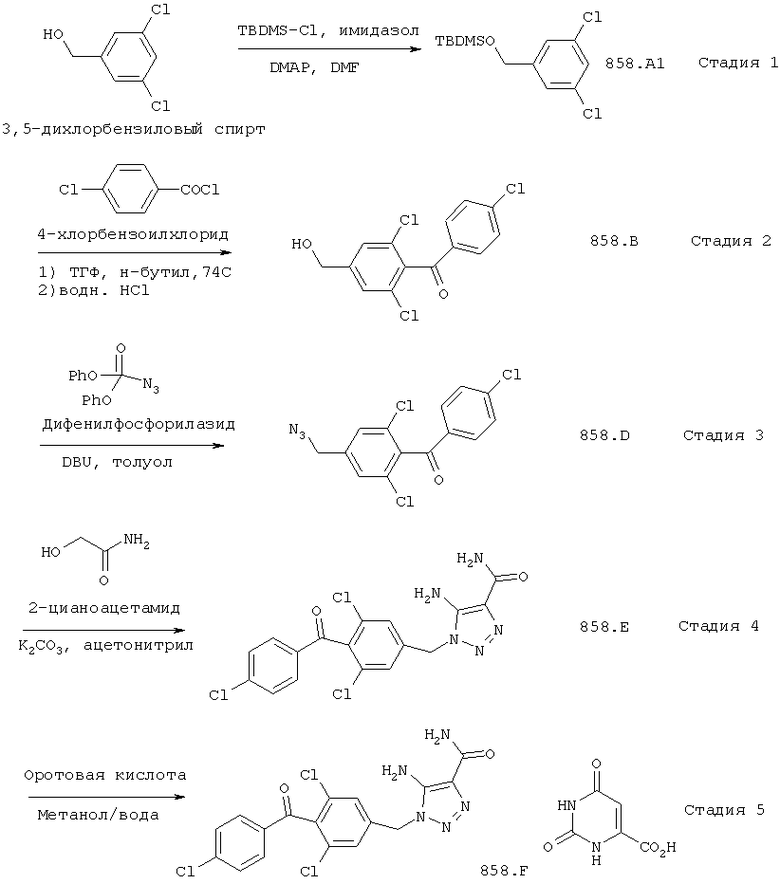
Как было отмечено, важно, что разные полиморфы CAI, СТО и САО, изготовленные указанным выше способом, демонстрируют меньшие поражения желудка и меньшую токсичность у грызунов по сравнению с CAI, который был синтезирован способами, описанными в предшествующем уровне техники. Это может быть связано с отсутствием использования токсичных ингредиентов, таких как азид натрия или азид калия.
Новый способ также приводит к получению новых полиморфов CAI, СТО и САО. Таким образом, соединения по изобретению включают молекулы, которые кристаллизуются в более чем одну различную кристаллическую структуру и проявляют разные химические свойства разных полиморфов CAI, охарактеризованных такими методами, как ЯМР, DSC, FT-IR и XRDP (Фиг.1-6).
Дозировка и композиция
5-амино- или замещенные амино-1,2,3-триазолы, а также их замещенные производные были изготовлены в разных полиморфных формах, имеющих химические и биологические свойства, которые преодолевают недостатки CAI, полученного способами, описанными в предшествующем уровне техники.
Кроме того, 5-амино" или замещенный амино-1,2,3-триазол, а также их замещенные производные химически взаимодействовали с оротовой кислотой с образованием оротатов (СТО) в соотношении от 1:1 до 1:4 (основание:кислота), имеющих исключительную биодоступность, фармакокинетические свойства, безопасность и эффективность.
Альтернативное воплощение включает полиморфы 5-амино- или замещенных амино-1,2,3-триазолов, а также их замещенные производные, смешанные с оротовой кислотой в соотношении от 1:1 до 1:4 (основание:кислота) с образованием композиций CAI и оротовой кислоты (САО).
Указанные выше фармацевтические композиции и препараты могут быть приготовлены в виде фармацевтических препаратов для введения млекопитающим для профилактики и лечения первичных и метастатических неоплазм, хронического миелолейкоза, дегенерации желтого пятна, ретинопатий и других клеточных пролиферативных заболеваний. Многие из триазол-оротатных соединений могут быть получены в виде солей органических кислот непосредственно или с фармацевтически совместимыми противоионами, в единственной форме, в которой они являются водорастворимыми. Соли обычно более растворимы в водных или других протонных растворителях, чем соответствующие формы свободных оснований. Терапевтические соединения или фармацевтические композиции можно вводить внутривенно, внутрибрюшинно, подкожно, внутримышечно, интратекально, перорально, ректально, местно или посредством аэрозоля.
Композиции, подходящие для перорального введения, включают твердые порошковые композиции, жидкие растворы активного соединения, растворенного в разбавителях, таких как физиологический раствор, вода или PEG 400; капсулы или таблетки, каждая из которых содержит заранее определенное количество активного агента в виде твердого вещества, порошка, гранул или желатина; суспензии в подходящей среде; и эмульсии.
Композиции, подходящие для парентерального введения, включают водные и неводные изотонические стерильные растворы, которые содержат буферы, антиоксиданты и консерванты. Композиции могут находиться в стандартной дозе или в многодозовых герметично закрытых контейнерах.
Дозировки пациенту для перорального введения СТО варьируются в пределах 0,25-500 мг/в сутки, как правило, 25-100 мг в сутки и обычно 50-400 мг/в сутки. В расчете на массу тела пациента обычная дозировка варьируется от 0,005 до 10 мг/кг/в сутки, как правило, от 0,5-2,0 мг/кг/в сутки, обычно от 1,0 до 8,0 мг/кг/в сутки. В расчете на площади поверхности тела пациента обычная дозировка варьируется от 0,1 до 300 мг/м2 /в сутки, как правило, от 20 до 250 мг/м2 /в сутки, обычно от 25 до 50 мг/м2 /в сутки. Величину дозировки и интервал можно регулировать индивидуально, чтобы обеспечить уровни активной группировки в плазме, которые являются достаточными для поддержания антипролиферативных, антиметастатических эффектов, антиангиогенезных эффектов или других терапевтических эффектов при заболеваниях, которые основаны на аберрантной сигнальной трансдукции и пролиферации.
Дозы можно регулировать в зависимости от пути введения, например для внутривенного, для ингаляционного/аэрозольного, для прямого внутрибрюшинного или подкожного, для местного или для интратекального введений.
Можно использовать разные системы доставки фармакологических соединений, включая, без ограничения ими, липосомы, наночастицы, суспензии и эмульсии. Фармацевтические композиции также могут содержать подходящие носители с твердой или гелевой фазой или эксципиенты. Примеры таких носителей или эксципиентов включают, без ограничения ими, карбонат кальция, фосфат кальция, различные сахара, крахмалы, производные целлюлозы, желатин и полимеры, такие как полиэтиленгликоли.
Кроме того, можно вводить лекарственное средство в нацеленную систему доставки лекарственного средства, например в липосому, покрытую опухолеспецифическим антителом, такую как наночастицы и другие формы. Липосомы или наночастицы могут быть нацелены на опухоль или другой объект заболевания и селективно ими захватываться.
Одним из наиболее трудных свойств для встраивания в недавно обнаруженную лидерную молекулу является нужный фармакокинетический профиль, особенно в случае перорально дозируемых соединений. "Наиболее опытные медицинские химики предпочли бы начинать в структурных сериях, которые имеют присущие им хорошие фармакокинетические свойства, хотя и с недостаточной активностью на целевом рецепторе, и затем начать улучшение активности на объекте, чем работать в другом направлении", "Organic Chemistry in Drugs Discovery, Drugs Discovery", Science 303: 1810-1813 (2004).
Улучшение биодоступности СТО, вводимого перорально
Настоящее изобретение относится в основном к способу увеличения пероральной биодоступности, доставки и клиренса СТО, уникального оротата L651582 с соотношением от 1:1: до 1:4 (основание:кислота). В настоящем изобретении предлагаются способы получения оротатных солей нерастворимых в воде лекарственных средств, имеющих ионизируемый центр, для улучшения пероральной биодоступности лекарственных средств, токсикологического профиля и эффективности. Предпочтительно СТО находится в соотношении 1:1, и более предпочтительно оно находится соотношении 1:2, и наиболее предпочтительно находится в соотношении 0,7:1,3.
Поглощение лекарственных средств пероральным путем является объектом интенсивного исследования в фармацевтической индустрии, так как хорошая биодоступность означает, что лекарственное средство способно достигать системного кровообращения через рот. На пероральное поглощение влияют как свойства лекарственного средства, так и физиология желудочно-кишечного тракта, включая растворение лекарственного средства из лекарственной формы, способ, которым лекарственное средство взаимодействует с водной средой и мембраной, проникновение через мембрану и необратимое удаление органами первого прохождения, такими как кишечник, печень и легкие. Некоторые фармацевтические агенты, которые проявляют низкую растворимость, показывают слабую биодоступность или не соответствующее требованиям поглощение, где на степень несоответствия оказывают воздействие такие факторы, как уровень дозы, статус питания пациента и физико-химические свойства лекарственного средства.
Большая часть поглощения лекарственного средства происходит в тонком кишечнике из-за большой площади поверхности, поскольку присутствие ворсинок и микроворсинок многократно увеличивает площадь поглощения. Кровообращение в кишечнике является уникальным, так как кишечник является передней или портальной тканью, которая регулирует поток субстратов в печень. Кишечная венозная кровь составляет примерно 75% притока крови к печени. Следовательно, для лекарственных средств, которые легко выводятся кишечником, вклад печени, почек или легких в метаболизм лекарственного средства уменьшается. Наоборот, для лекарственных средств, которые плохо выводятся кишечником, субстрат может достигать следующих органов, печени и легких, для удаления. Следовательно, концентрация лекарственного средства, поступающего в кишечник, и скорость потока в кишечнике изменяют скорость доставки лекарственного средства и влияют на скорости кишечного клиренса и клиренса посредством первого прохождения через печень.
"Биодоступность лекарственного средства" определена здесь как количество лекарственного средства, системно доступного в течение некоторого времени. В настоящем изобретении лекарственную биодоступность фармацевтических агентов увеличивают путем превращения их в оротатные соли. Это может быть достигнуто путем изменения гидрофильных и липофильных свойств лекарственного средства, так что это лекарственное средство проникает через стенку мембраны и скорость перфузии крови становится общей ограничивающей скорость стадией для поглощения, или путем ингибирования биотрансформации лекарственного средства в кишечнике и/или путем ингибирования активных систем обратного транспорта в кишечнике, которые уменьшают чистый перенос лекарственных средств через кишечную мембрану в кровоток. В любом случае, композиция, ответственная за повышенную биодоступность лекарственного средства, представляет собой оротатную соль фармацевтического агента. По причинам, которые не сразу стали очевидными, было обнаружено, что превращение нерастворимого в воде L651582 в СТО (основание:кислота, от 0,5:1 до 1:2) обеспечивает способ увеличения биодоступности фармацевтического агента, перорально вводимого млекопитающему, нуждающемуся в лечении.
Изменения в суммарных системных концентрациях с течением времени показывает площадь под кривой (AUC) или Смакс, оба параметра хорошо известные в данном уровне техники.
В настоящем изобретении предлагаются способы, где композиция обеспечивает увеличение биодоступности оротатной соли фармацевтического агента, при измерении посредством AUC, по меньшей мере 25%-100% относительно дозировки фармацевтического агента.
В изобретении предлагается композиция, которая увеличивает биодоступность оротатной соли фармацевтического агента, при измерении посредством Смакс, по меньшей мере от 50% до 100%.
"Побочные эффекты" или "токсичность" или "неблагоприятные реакции на лекарственное средство" химиотерапевтических агентов наблюдаются в острой фазе проведения химиотерапии и у пациентов, излеченных от рака, с субклиническим повреждением ткани. Существует более высокая степень распознавания побочных эффектов в ткани, связанных с лекарственным средством, которые могут быть довольно тяжелыми, инвалидизирующими и необратимыми. Врач должен быть осведомлен о возможных осложнениях в ткани/органе от химиотерапевтических агентов и где следует осуществить первоначальное исследования ткани до начала терапии.
"Клиренс" лекарственного средства имеет место при перфузии крови в органы выделения. "Выделение" относится к части лекарственного средства, направляемого в орган, которая необратимо удаляется (выделяется) или меняется на другую химическую форму (метаболизм).
В настоящем изобретении предлагается способ увеличения клиренса оротатных производных СТО из нераковых или нормальных тканей по меньшей мере 25%-100% относительно дозировки фармацевтического агента при оценке в фармакологических исследованиях.
"Биодоступность" лекарственного средства после перорального дозирования представляет собой степень, в которой, или скорость, при которой активная группировка лекарственного средства или метаболит поступает в большой круг кровообращения, получая, таким образом, доступ к месту действия. Физико-химические свойства лекарственного средства влияют на его абсорбционный потенциал и связывание с белками сыворотки. Эффективность лекарственного средства зависит от его взаимодействия с молекулярной мишенью. И вследствие этого от свойств лекарственной формы, которые частично зависят от ее химических характеристик и от способов изготовления лекарственного средства в больших количествах. Различия в биодоступности, эффективности, транспорте и клиренсе среди химических композиций данного лекарственного средства могут обладать клинической значимостью.
Важной является скорость "поглощения", так как даже при полном поглощении лекарственного средства, оно может абсорбироваться слишком медленно для достаточно быстрого получения терапевтического уровня в крови или так быстро, что высокие концентрации лекарственного средства, даваемые для достижения терапевтического уровня после каждой дозы, вызывают токсичность. Поглощение происходит одним из трех способов, или пассивной диффузией, активным транспортом или облегченным активным транспортом. Пассивная диффузия представляет собой просто прохождение молекул через слизистый барьер, пока концентрация молекул не достигнет осмотического равновесия по обе стороны мембраны. В активном транспорте молекулу активно накачивают через слизистую оболочку. В облегченном транспорте требуется носитель, в основном белок, чтобы переместить молекулу через мембрану для поглощения. В настоящем изобретении предлагаются соединения СТО в химических конфигурациях, которые позволяют успешно доставлять лекарственное средство в разные ткани и органы и даже через гематоэнцефалический барьер, чтобы достичь головного мозга.
Оротовая кислота, свободный пиримидин, является важной в синтезе уридилата (UPP), главного пиримидинового нуклеотида. Пиримидины играют главную роль в клеточной регуляции и метаболизме. Они являются субстратами для биосинтеза ДНК/РНК, регуляторами биосинтеза некоторых аминокислот и кофакторами в биосинтезе фосфолипидов, гликолипидов, сахаров и полисахаридов. Классический de novo биосинтетический путь пиримидина заканчивается синтезом UMP (уридин-монофосфат). Biochemistry, ed. Lubert Stryer, ed, W.H.Freeman & Co NY, 4th ed, 739-762 (1995). В настоящем изобретении предлагается класс СТО, которые подвергаются растворению с высвобождением лекарственного средства в виде заряженной молекулы и свободной оротовой кислоты, которая может предотвращать связывание лекарственного средства с белками и облегчать транспорт к мишени и быстрый клиренс.
В изобретении предлагаются воплощения, демонстрирующие увеличение эффективности СТО, оцениваемой по улучшению 1) эффективности СТО по сравнению с композицией эквивалентной дозы CAI+оротовая кислота, 2) биодоступности и клиренсе СТО, при приеме в виде инкапсулированного твердого СТО, по сравнению с СТО в PEG-400, 3) транспорта перорально введенного СТО в головной мозг через гематоэнцефалический барьер, 4) транспорта перорально введенного СТО в разные глазные ткани, включая комплекс сосудистая оболочка глаза-сетчатка и стекловидное тело у собак.
Важно, что доклиническую токсичность СТО определяли на собаках пероральным путем в количеством 175, 350, 1025 мг/кг/в сутки, и через 28 суток не было ни одной смерти.
ПРИМЕРЫ
Пример 1
4-Хлорбензоилхлорид
3,5-Дихлорбензиловый спирт (1 моль) обрабатывали трет-бутилдиметилсилилхлоридом (1,05 моль), имидазолом, 99% (2,44 моль), 4-диметиламинопиридином в N,N-диметилформамиде при пониженной температуре с получением трет-бутилдиметилсилил-3,5-дихлорбензилового эфира (858.А1) при выполнении экстракции.
Пример 2
3,5-Дихлор-4-(4-хлорбензоил)бензиловый спирт
Взаимодействие трет-бутилдиметилсилил-3,5-дихлорбензилового эфира (858.А1) (1 моль) с 1,6 М раствором н-бутиллития в гексане с последующим добавлением 4-хлорбензоилхлорида (1,01 моль) в тетрагидрофуране, пока они холодные, и обработка промежуточного соединения водной соляной кислотой с получением 3,5-дихлор-4-(4-хлорбензоил)бензилового спирта (858.В).
Пример 3
3,5-дихлор-4-(4-хлорбензоил)бензилазид
3,5-Дихлор-4-(4-хлорбензоил)бензиловый спирт (858.В) (1 моль) взаимодействует с дифенилфосфорилазидом (азид дифенилфосфоновой кислоты) (DPPA) (1,2 моль) и 1,8-диазабицикло[5.4.0]ундец-7-еном (синоним: DBU) (1,2 моль)) в толуоле при пониженной температуре с последующей обработкой водой и титрованием спиртом с получением 3,5-дихлор-4-(4'-хлорбензоил)бензилазида (858.D). DPPA представляет собой органическое соединение, которое используют в синтезе других органических соединений. Aust. J.Chem 26:191-1593 (1973). Стабильность DPPA к нагреванию показана посредством его дистилляции при 157°С и тем фактом, что не наблюдалось сильного выделения азота до достижения температуры 175°С.
Пример 4
5-Амино-1-(4-(4-хлорбензоил)-3,5-дихлорбензил)-1,2.3-триазол-4-карбоксамид (CAI)
3,5-Дихлор-4-(4'-хлорбензоил)бензилазид (858.D) (1 моль) взаимодействует с цианоацетамидом (1,69 моль) в горячем ацетонитриле и карбонатом калия (6,2 моль) с получением 5-амино-1-(4-(4-хлорбензоил)-3,5-дихлорбензил)-1,2,3-триазол-4-карбоксамида (858. Е).
Пример 5
5-Амино-1-(4-(4-хлорбензоил)-3,5-дихлорбензил)-1,2,3-триазол-4-карбоксамид, соединение с оротовой кислотой. (CAI:оротовая кислота)
5-Амино-1-(4-(4-хлорбензоил)-3,5-дихлорбензил)-1,2,3-триазол-4-карбоксамид (858.Е) (1 моль) взаимодействует с оротовой кислотой (1,03 моль) и смесью метанол/вода с получением 5-амино-1-(4-(4-хлорбензоил)-3,5-дихлорбензил)-1,2,3-триазол-4-карбоксамида, твердого соединения с оротовой кислотой, (CAI:оротовая кислота; 1:1) (СТО) (858.F), MM (молекулярная масса) 580,76 г, имеющего переходные точки плавления примерно 151°С, 238°С и 332°С, при измерении посредством дифференциальной сканирующей калориметрии. Картина XRPD показывает, что СТО состоит из кристаллического и аморфного (полиморфного) вещества.
Пример 6
Сравнение противораковой активности СТО (858. F) с CAI + оротовая кислота (1:1)
Эффект СТО с ММ 580,8 и CAI с ММ 424,6 + оротовая кислота с ММ 156,1 исследовали на бычьих ксенотрансплантатах подкожно имплантированной опухоли прямой кишки НТ29 человека у самцов бестимусных мышей NCr-nu/nu. Мышам в возрасте 6 недель имплантировали фрагменты НТ29 и через 13 суток их распределяли в 3 группы по десять особей. В течение следующих 14 суток (13-26 сутки) Группа 1, контроль (С), получала носитель; Группа 2=343 мг/кг/доза; Группа 3=240 мг/кг/в сутки CAI+103 мг/кг/в сутки оротовой кислоты. На 41 сутки измеряли средний объем опухоли (мм3), как показано ниже:
Группа 1 (контроль)=1436 мм3
Группа 2 (СТО 343 мг/кг/в сутки)=864 мм3 (р=0,0050, Гр.2 против Гр.1)
Группа 3 (CAI 250 мг/кг/в сутки + оротовая кислота 103 мг/кг/в сутки)=1268 мм3 (р=0,2706, Гр. 3 против Гр.1). Данные результаты свидетельствуют о том, что СТО является более эффективным в ингибировании роста опухоли, чем эквивалентное количество CAI и оротовой кислоты, которые химически не провзаимодействовали. Однако композиция CAI + оротовая кислота показала некоторое ингибирование опухоли.
Пример 7
Сравнение СТО, введенного перорально в виде твердого вещества в капсуле или в виде жидкости в PEG-400
Биодоступность СТО (основание:кислота, 0,7:1,3) определяли путем введения однократной дозы 685 мг/кг посредством капсулы (Группа 1) или перорального зонда в PEG400 (Группа 2). В каждой группе использовали двух собак (1 самка/1 самец). Образцы крови отбирали в 0, 1, 2, 4, 8, 12, 24, 48, 72 и 92 часа. CAI измеряли при помощи ВЭЖХ/МС.
Группа 1, получившая капсулу: концентрации в плазме через 1 ч составляли 155 и 174 нг/мл для самцов и самок собак. Смакс равнялась 5800 нг/мл в 12 ч для самцов и 7950 нг/мл в 24 ч для самок. Период полувыведения составлял 18 ч и 22,7 ч и значения AUC равнялись 326 и 277 нг/мл для самцов и самок соответственно.
Группа 2, получившая зондовое введение в PEG400: концентрации в плазме через 1 ч составляли 511 и 570 нг/мл для самцов и самок собак. Смакс равнялась 6634 нг/мл в 24 ч для самцов и 5350 нг/мл в 24 ч для самок. Биодоступность составляла 81,8% от биодоступности в Группе 1 (100%).
Эти результаты показывают, что СТО, введенный в виде твердого вещества в капсуле, имел лучшую картину поглощения и биодоступности, чем СТО в PEG400. На основании этих и дополнительных результатов СТО подлежит введению пациентам в виде твердого вещества в капсулах.
Пример 8
СТО, введенный мышам перорально, проходит гематоэнцефалический барьер.
СТО вводили перорально (в PEG400) мышам в возрасте шести недель, распределенным в две Группы по 6 особей. Были введены две дозы - Группа 1=513 мг/кг; Группа 2=342 мг/кг. Через восемь часов после обработки СТО мышей умерщвляли для измерения концентрации СТО (в виде CAI) в ткани головного мозга.
Полученные результаты: Группа 1 - уровни CAI составляли 15167±2372 нг/г ткани; Группа 2 - уровни CAI составляли 10950±1704 нг/г ткани, оба в терапевтическом диапазоне (6000 нг/мл). Так как СТО вводили перорально, данные результаты показывают, что СТО проходит гематоэнцефалический барьер и достигает органа-мишени, головного мозга.
Настоящее изобретение не ограничено объемом воплощения, раскрытого в примере, который предназначен для иллюстрации одного аспекта изобретения, и любые способы, которые являются функционально эквивалентными, входят в объем изобретения. Действительно, различные модификации изобретения, в дополнение к показанным и описанным в данном описании изобретения, станут очевидными специалисту в данной области техники из предшествующего описания. Такие модификации, как предполагается, подпадают под объем прилагаемой формулы изобретения.
Специалист в данной области техники идентифицирует или сможет установить, используя не более чем обычное экспериментирование, любые эквиваленты конкретных воплощений изобретения, описанных в данном описании изобретения. Такие эквиваленты, как предполагается, охвачены формулой изобретения.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ 1-ЗАМЕЩЕННЫХ-4-ЦИАНО-1,2,3-ТРИАЗОЛОВ И 4-ЦИАНО-1-(2,6-ДИФТОРБЕНЗИЛ)-1H-1,2,3-ТРИАЗОЛ | 1997 |
|
RU2177942C2 |
| ПРОИЗВОДНЫЕ ТРИАЗОЛКАРБОКСАМИДА | 2013 |
|
RU2637938C2 |
| ПРОИЗВОДНЫЕ ТРИАЗОЛО [4,5-d]ПИРИМИДИНА И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ АНТАГОНИСТОВ ПУРИНЕРГИЧЕСКОГО РЕЦЕПТОРА | 2002 |
|
RU2317084C2 |
| НОВЫЕ СОЕДИНЕНИЯ ТРИАЗОЛА | 2011 |
|
RU2588137C2 |
| СОЕДИНЕНИЯ ЗАМЕЩЕННОЙ ТРИАЗОЛБОРОНОВОЙ КИСЛОТЫ | 2013 |
|
RU2625801C2 |
| 5-ЗАМЕЩЕННЫЕ ИНДАЗОЛЫ В КАЧЕСТВЕ ИНГИБИТОРОВ КИНАЗЫ | 2008 |
|
RU2487873C2 |
| АМИД 8-АМИНО-[1.2.4]ТРИАЗОЛО-[1.5-А]ПИРИДИН-6-КАРБОНОВОЙ КИСЛОТЫ И СОДЕРЖАЩЕЕ ЕГО ЛЕКАРСТВЕННОЕ СРЕДСТВО | 2002 |
|
RU2296763C2 |
| АМИДНОЕ ПРОИЗВОДНОЕ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 1998 |
|
RU2185381C2 |
| НОВЫЕ ПРОТИВОМИКРОБНЫЕ СРЕДСТВА | 2009 |
|
RU2522582C2 |
| ПРОИЗВОДНЫЕ ТРИАЗОЛА В КАЧЕСТВЕ ЛИГАНДОВ РЕЦЕПТОРОВ ГАМК | 2011 |
|
RU2582337C2 |

Изобретение относится к полиморфным формам 1 и 2 5-амино-1-(4-(4-хлорбензоил)-3,5-дихлорбензил)-1,2,3-триазол-4-карбоксамида, связанным с оротовой кислотой, где оротовая кислота связана ионной связью при соотношении основание : кислота в диапазоне от 1:1 до 1:4. Изобретение также относится к способу получения 5-амино-1-(4-(4-хлорбензоил)-3,5-дихлорбензил)-1,2,3-триазол-4-карбоксамида и к способу получения 5-амино-1-(4-(4-хлорбензоил)-3,5-дихлорбензил)-1,2,3-триазол-4-карбоксамида, связанного с оротовой кислотой. Технический результат: получены новые полиморфные формы 5-амино-1-(4-(4-хлорбензоил)-3,5-дихлорбензил)-1,2,3-триазол-4-карбоксамида, связанного с оротовой кислотой, которые могут применяться в качестве лекарственного средства в лечении заболеваний, которые основаны на аберрантной сигнальной трансдукции и путях пролиферации, включающих PI3, СОХ2, BCR-ABL, ВИЧ или VEGF1. 4 н. и 6 з.п. ф-лы, 6 ил., 8 пр.
1. Полиморфная форма 1 5-амино-1-(4-(4-хлорбензоил)-3,5-дихлорбензил)-1,2,3-триазол-4-карбоксамида, связанная с оротовой кислотой, где оротовая кислота связана ионной связью при соотношении основание : кислота в диапазоне от 1:1 до 1:4, имеющая картину дифракции рентгеновских лучей на порошке (XRPD) по существу такую, как показано на Фиг. 3.
2. Полиморф по п. 1, где соединение представляет собой полиморфную форму 1 5-амино-1-(4-(4-хлорбензоил)-3,5-дихлорбензил)-1,2,3-триазол-4-карбоксамида, связанную с оротовой кислотой, имеющую картину дифракции рентгеновских лучей на порошке, содержащую пики при углах 2θ 4,9, 20,2, 24,3, 26,5 и 28,7.
3. Полиморф по п. 2, имеющий картину XRPD, дополнительно содержащую пики при 23,3, 28,0 и 27,0.
4. Полиморфная форма 2 5-амино-1-(4-(4-хлорбензоил)-3,5-дихлорбензил)-1,2,3-триазол-4-карбоксамида, связанная с оротовой кислотой, где оротовая кислота связана ионной связью при соотношении основание : кислота в диапазоне от 1:1 до 1:4, имеющая картину XRPD по существу такую, как показано на Фиг. 4.
5. Полиморф по п. 4, где соединение представляет собой полиморфную форму 2 5-амино-1-(4-(4-хлорбензоил)-3,5-дихлорбензил)-1,2,3-триазол-4-карбоксамида, связанную с оротовой кислотой, имеющую картину дифракции рентгеновских лучей на порошке, содержащую пики при углах 2θ 19,5, 23,2, 25, 28,7 и 29.
6. Полиморф по п. 5, имеющий картину XRPD, дополнительно содержащую пики при 21,9, 20,1 и 19,1.
7. Способ получения 5-амино-1-(4-(4-хлорбензоил)-3,5-дихлорбензил)-1,2,3-триазол-4-карбоксамида, включающий:
взаимодействие дифенилфосфорилазида с 3,5-дихлор-4-(4′-хлорбензоил)бензиловым спиртом с получением 3,5-дихлор-4-(4-хлорбензоил)бензилазида; и
взаимодействие 2-цианоацетамида с 3,5-дихлор-4-(4-хлорбензоил)бензилазидом с получением 5-амино-1-(4-(4-хлорбензоил)-3,5-дихлорбензил)-1,2,3-триазол-4-карбоксамида.
8. Способ получения 5-амино-1-(4-(4-хлорбензоил)-3,5-дихлорбензил)-1,2,3-триазол-4-карбоксамида, связанного с оротовой кислотой, где оротовая кислота связана ионной связью при соотношении основание : кислота в диапазоне от 1:1 до 1:4, включающий:
взаимодействие дифенилфосфорилазида с 3,5-дихлор-4-(4′-хлорбензоил)бензиловым спиртом с получением 3,5-дихлор-4-(4-хлорбензоил)бензилазида;
взаимодействие 2-цианоацетамида с 3,5-дихлор-4-(4-хлорбензоил)бензилазидом с получением 5-амино-1-(4-(4-хлорбензоил)-3,5-дихлорбензил)-1,2,3-триазол-4-карбоксамида; и
взаимодействие оротовой кислоты с 5-амино-1-(4-(4-хлорбензоил)-3,5-дихлорбензил)-1,2,3-триазол-4-карбоксамидом.
9. Полиморф по любому из пп. 1-6 для применения в качестве лекарственного средства в лечении заболеваний, которые основаны на аберрантной сигнальной трансдукции и путях пролиферации, включающих PI3, СОХ2, BCR-ABL, ВИЧ или VEGF1.
10. Полиморф по любому из пп. 1-6 для применения в лечении солидных видов рака, дегенерации желтого пятна, ретинопатии, хронического миелолейкоза или СПИД (синдром приобретенного иммунодефицита).
| Ian F | |||
| Cottrell et al | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| ДВУХБАРАБАННАЯ ЛЕБЕДКА С ДИСТАНЦИОННЫЛ1 ПЕРЕКЛЮЧЕНИЕМ БАРАБАНОВ | 0 |
|
SU304221A1 |
| Капкан для промыслового отлова диких животных | 1962 |
|
SU151529A1 |
| US 5861406 A, 19.01.1999 | |||
| US 5861406 A, 19.01.1999 | |||
| WO 9325536 A1, 23.12.1993 | |||
| US 20060189640 A1, 24.08.2006 | |||
| US 20060189640 A1, 24.08.2006 | |||
| 1998 |
|
RU2198167C2 | |
Авторы
Даты
2016-08-10—Публикация
2010-09-03—Подача