Изобретение относится к органической химии, конкретно к получению 1,4-диоксанкарбоксилатов, которые применяют в фармакологии в качестве биоактивных препаратов.
Известен способ получения 1,4-диоксанкарбоксилатов взаимодействием алкилдиазоацетатов с 1,3-диоксоланами при температуре 150°C в течение нескольких часов (Султанова P.M. Диазосоединения и их фосфазины в синтезе кислород-, азот- и серосодержащих гетероциклических соединений. // Дисс. … док. хим. наук. Уфа. 2013. 345 с.).
Недостатками известного способа являются длительность получения, низкий выход целевого продукта и протекание побочных процессов.
Задача, решение которой предлагается в настоящем изобретении, заключается в разработке способа получения 1,4-диоксанкарбоксилатов, отличающегося увеличением выхода целевого продукта.
Указанная задача решается тем, что способ получения 1,4-диоксанкарбоксилатов, реакцией расширения 1,3-диоксоланового кольца, согласно изобретению, проводят взаимодействием моно-, ди- и тризамещенных 1,3-диоксоланов с метилдиазоацетатом в условиях микроволнового излучения (230 Вт) в течение 0,5-1,5 часов.
Реакцию 1,3-диоксолана с метилдиазоацетатом проводят при следующем соотношении компонентов, мас. %: 1,3-диоксолан 0,006-0,012; метилдиазоацетат 5,48; CH2Cl2 94,514-94,508.
Способ осуществляется следующим образом.
Используемые в реакции 1,3-диоксоланы с количественным выходом образуются при взаимодействии пирокатехина с дигалогеналканами в присутствии основания в условиях межфазного катализа (Рахманкулов Д.Л., Зорин В.В., Латыпова Ф.Н., Мусавиров Р.С., Сираева И.Н. Методы синтеза 1,3-дигетероаналогов циклоалканов - Уфа: Реактив - 1998 - 254 с.).
Метилдиазоацетат получают по известной методике (Джемилев У.М., Поподько Н.Р., Козлова Е.В. Металлокомплексный катализ в органическом синтезе. - М.: Химия. - 1999. - 648 с.).
В качестве источника микроволнового излучения использовали бытовую микроволновую печь марки «Sanyo EM-S1073W», мощностью 600-800 Вт. Обратный холодильник и термометр вынесены из зоны микроволнового излучения.
Исходные реагенты должны соответствовать следующим требованиям:
- Метилен хлористый - ГОСТ 9968-86;
- Диэтиловый эфир - ТУ 2600-00143852015-05;
- Al2O3 - ГОСТ 8136-85.
К 1,3-диоксолану в хлористом метилене добавляют метилдиазоацетат (или этилдиазоацетат). Реакционную смесь интенсивно перемешивают и облучают микроволновым излучением (230 Вт) в течение 0,5-1,5 часов. Мольное соотношение 1,3-диоксолан : метилдиазоацетат (этилдиазоацетат) = 0,0015:1. По окончании реакции хлористый метилен отгоняют при атмосферном давлении, остаток растворяют в диэтиловом эфире и отфильтровывают через тонкий слой оксида алюминия. Затем диэтиловый эфир отгоняют при атмосферном давлении, остаток перегоняют в вакууме.
Пример 1.
К раствору 0,015 ммоль 1,3-диоксолана в 10 мл CH2Cl2 при интенсивном перемешивании добавили 0,01 моль метилдиазоацетата (этилдиазоацетата) в 3 мл CH2Cl2. Реакционную смесь перемешивали и облучали микроволновым излучением (230 Вт) в течение 0,5 часа. По окончании реакции растворитель упарили в вакууме водоструйного насоса, остаток растворили в 10 мл диэтилового эфира и отфильтровали через тонкий слой Al2O3, растворитель отогнали на роторном испарителе. Продукт подвергали вакуумной разгонке.
Выход метилового эфира 1,4-диоксан-2-карбоновой кислоты - 95%.
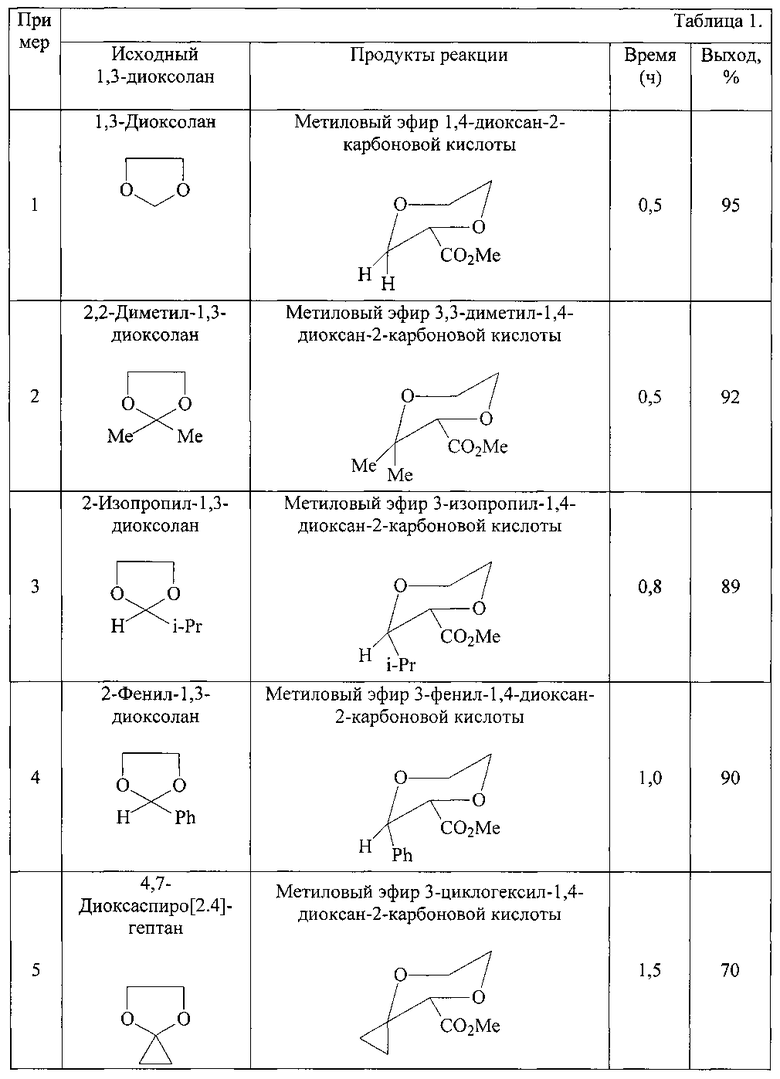
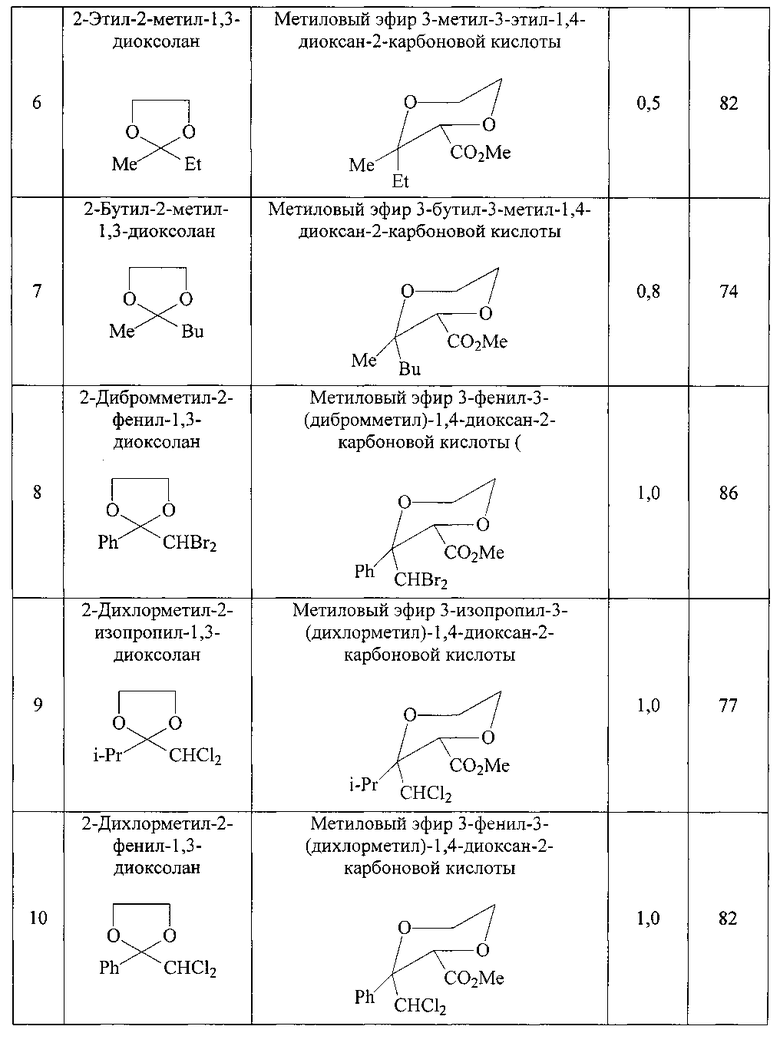
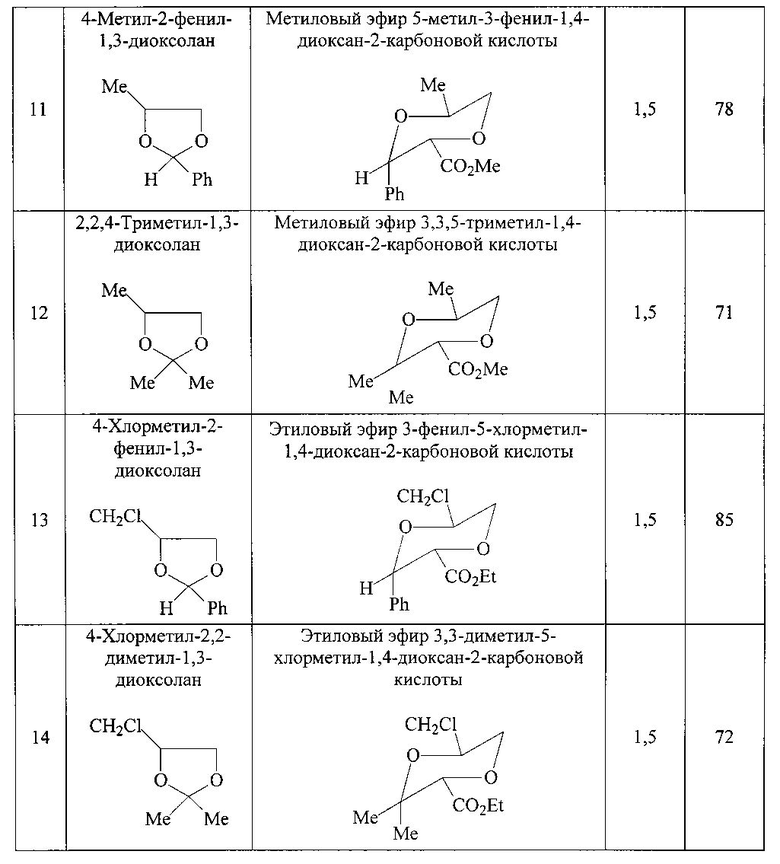
Результаты синтезов приведены в таблице 1, синтезы проведены аналогично примеру 1.
Из таблицы видно, что предлагаемый способ позволяет достигнуть выхода 1,4-диоксанкарбоксилатов 70-95% по сравнению с прототипом, где выход достигает 45%, что обеспечит широкое использование этих соединений в качестве лекарственных средств, обладающих широким спектром физиологического действия.
Спектральные характеристики 1,4-диоксанкарбоксилатов.
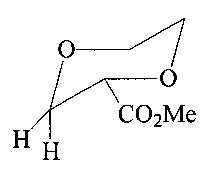
Спектр ЯМР 1H (CDCl3, δ, м.д., J/Гц): 3.05-3.18 (м, 2Н, СН2(4)); 3.76 (с, 3Н, OMe); 3.75-3.80 (м, 4Н, 2СН2); 4.28 (д.д, 1Н, СН(2), 3J=10.0, 3J=4.0). Спектр ЯМР 13С (δ, м.д.): 52.2 (OMe); 63.4 (С(6)); 67.1 (С(3)); 67.3 (С(5)); 73.4 (С(3)); 171.7 (CO2). Масс-спектр (ЭУ, 70 эВ), m/z (Ioтн, %): 145 [М]+; 116 (~1.0); 88; 75 (100); 59 (4.5).
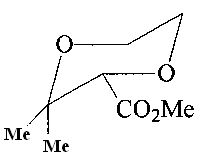
Спектр ЯМР 1Н (CDCl3, δ, м.д., J/Гц): 1.20 (с, 6Н, 2СН3); 3.76 (с, 3Н, OMe); 3.88-3.80 (м, 4Н, 2СН2); 4.26 (с, 1Н, НС(2)). Спектр ЯМР 13С (δ, м.д.): 21.5, 23.4 (2 Me); 53.1 (OMe); 62.7, 64.4 (С(5) и C(6)); 80.1 (С(2)); 82.1 (С(3)); 172.7 (CO). Масс-спектр (ЭУ, 70 эВ), m/z (Ioтн, %): 173 [М]+; 75 (100); 59 (5.0).
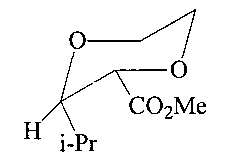
Спектр ЯМР 1Н (CDCl3, δ, м.д., J/Гц): 0.90-0.99 (д, 6Н, 2Ме, 3J=7.5); 1.68-1.96 (м, 1Н, -CH-, i-Pr); 3.20-3.31 (м(д.д), 1Н, НС(3), (3J=8.7, 3J=10.0)); 3.76 (с, 3Н, OCH3); 3.88-3.90 (м, 4Н, 2СН2); 4.60 (д, 1Н, НС(2), 3J=10.0). Спектр ЯМР 13C (δ, м.д.): 17.4, 19.3 (2 Me); 29.3 (С, i-Pr); 52.4 (OMe); 64.3, 64.9 (С(5) и C(6)); 73.4 (С(2)); 79.6 (С(3)); 168.6 (CO). Масс-спектр (ЭУ, 70 эВ), m/z (Ioтн, %): 187 [М]+; 116 (~1.0); 88 (4.0); 75 (100); 59 (3.0).
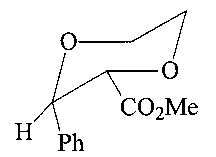
Спектр ЯМР 1Н (CDCl3, δ, м.д., J/Гц): 3.73 (с, 3Н, ОСН3); 4.25 (д, 1Н, НС(2), 3J=7.5); 3.87-3.95 (м, 4Н, 2СН2); 5.50 (д, 1Н, НС(3), 3J=7.5); 7.25-7.45 (м, 5Н, Ar). Спектр ЯМР 13С (δ, м.д.): 52.3 (OMe); 64.3, 65.9 (C(5) и C(6)); 75.7 (C(2)); 77.4 (C(3)); 124.2, 126.2, 127.3 (5Н, Ar), 136.7 (C, Ar); 168.6 (CO). Масс-спектр (ЭУ, 70 эВ), m/z (Ioтн, %): 221 [М]+; 116 (~1.0); 105 (4.0); 88; 77; 75 (100); 59 (3.0).
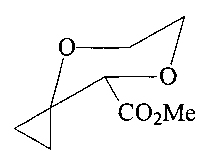
Спектр ЯМР 1Н (CDCl3, δ, м.д., J/Гц): 0.82-1.11, 1.39-1.68 (оба м, 10Н, (-CH2-)5); 3.12-3.40 (м, 2Н, Н2С(5)); 3.42-3.58 (м, 2Н, H2C(6)); 3.66 (с, 3Н, OMe); 4.74-4.81 (м, 1Н, НС(2)). Спектр ЯМР 13C (δ, м.д.): 24.1, 25.9, 32.2, 34.2 ((-CH2-)5); 53.1 (OMe); 63.7 (С(5)); 64.4 (С(6)); 77.1 (С(2)); 85.3 (С(3)); 172.0 (CO). Масс-спектр (ЭУ, 70 эВ), m/z (Ioтн, %): 213 [М]+; 75; 59.
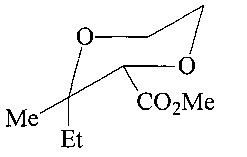
Спектр ЯМР 1Н (CDCl3, δ, м.д., J/Гц): 0.8 (т, 3Н, СН3(13), J=7.5); 1.07 (с, 3Н, СН3(12)); 1.12 (т, 3Н, СН3(10), J=7.1); 1.5 (к, 2Н, СН2(13), J=7.5); 3.3-3.6 (м, 4Н, СН2(5, 6)); 3.85 (с, Н, CHa(2)); 4.05 (к, 2Н, СН2(9), J=7.1). Спектр ЯМР 13С (CDCl3, δ, м.д.): 5.8 (Me); 15.7 (Me); 30.8 (СН2СН3); 52.9 (OMe); 59.8 (С(5)); 65.7 (С(6)); 72.7 (С(3)); 79.9 (С(2)); 167.7 (CO2). Масс-спектр (ЭУ, 70 эВ), m/z (Ioтн, %): 202 [М]+.
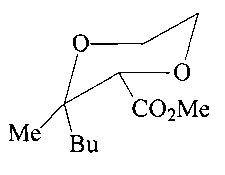
Спектр ЯМР 1Н (CDCl3, δ, м.д., J/Гц): 0.82 (т, 3Н, СН3(16), J=7.15); 1.1 (м, 2Н, СН2(15)); 1.15 (с, 3Н, СН3(12)); 1.2 (т, 3Н, СН3(10), J=7.22); 1.35 (м, 2Н, СН2(14)); 1.52 (т, 2Н, СН2(13), J=10.2); 3.4-3.7 (м, 4Н, СН2(5, 6)); 3.95 (с, Н, CHa(2)); 4.15 (к, 2Н, СН2(9), J=7.22). Спектр ЯМР 13С (CDCl3, δ, м.д.): 13.8 (Me); 16.9 (Me); 23.0 (СН2); 24.2 (СН2); 38.7 (СН2); 52.8 (OMe); 60.8 (С(5)); 66.5 (С(6)); 73.7 (С(3)); 80.7 (С(2)); 168.7 (CO2). Масс-спектр (ЭУ, 70 эВ), m/z (Ioтн, %): 230 [М]+.
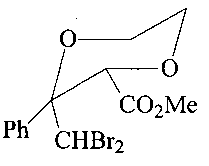
Спектр ЯМР 1Н (CDCl3, δ, м.д., J/Гц):3.76 (с, 3Н, OMe); 3.97-4.4 (м, 4Н, 2СН2);4.39 (с, 1Н, СН); 5.83 (с, 1Н, HCBr2); 7.33-7.60 (м, 5Н, Ar). Спектр ЯМР 13С (δ, м.д.): 53.1 (OMe); 56.3 (CHBr2); 63.7 (С(5)); 66.9 (С(6)); 80.2 (С(2)); 91.4 (С(3)); 123.4, 125.4, 127.2, 128.9, 132.1 (Ar); 172.8 (CO). Масс-спектр (ЭУ, 70 эВ), m/z (Ioтн, %): 393 [М]+; 116; 105; 88; 75; 77; 59.
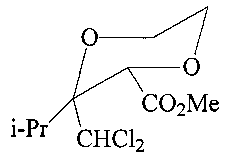
Спектр ЯМР 1H (CDCl3, δ, м.д., J/Гц): 1.00 (д, 6Н, 2СН3); 2.45-2.55 (м, 1Н, СН-изо.C3H7); 3.76 (с, 3Н, OCH3); 3.88-4.15 (м, 4Н, 2СН2); 4.39 (с, 1Н, -CH-CO2-); 5.88 (с, 1Н, HCCl2). Спектр ЯМР 13C (δ, м.д.): 18.2, 20.3 (2 Me); 32.3 (С, i-Pr); 53.3 (OMe); 63.8, 67.9 (С(5) и C(6)); 77.4 (С(2)); 91.6 (C(3)); 171.4 (CO). Масс-спектр (ЭУ, 70 эВ), m/z (Ioтн, %): 216 [М]+; 116; 88; 75; 59.
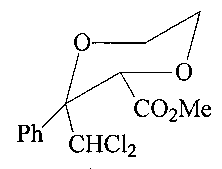
Спектр ЯМР 1Н (CDCl3, δ, м.д., J/Гц): 3.76 (с, 3Н, OCH3); 4.40 (с, 1Н, -CH-CO2-); 3.98-4.40 (м, 4Н, 2СН2); 5.88 (с, 1Н, CHCl2); 7.25-7.57 (м, 5Н, Ar). Спектр ЯМР 13С (δ, м.д.): 53.1 (OMe); 64.2 (С(5)); 67.9 (С(6)); 76.8 (CHCl2); 79.5 (С(2)); 89.7 (С(3)); 123.3, 125.4, 126.9, 127.5, 132.0 (Ar); 171.2 (CO). Масс-спектр (ЭУ, 70 эВ), m/z (Ioтн, %): 304 [М]+; 116; 105; 88; 75; 77; 59.
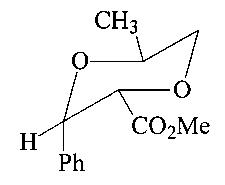
Спектр ЯМР 1Н (CDCl3, δ, м.д., J/Гц): 1.20 (д, 3Н, Me, 3J=6.40); 3.43 (д д, 1H, Н(6)а, 2J=-11.51, 3J=10.15); 3.47 (с, 3Н, Me); 3.90 (м, 1Н, Н(5)а); 3.95 (д д, Н, Н(6)е, 2J=-11.51, 3J=2.64); 4.04 (д, 1Н, Н(2)а, 3J=9.10); 4.68 (д, Н, Н(3)а); 7.20-7.35 (м, 5Н, Ph). Спектр ЯМР 13С (CDCl3, δ, м.д.): 16.7 (Me); 51.8 (Me); 71.4 (С(6)); 71.5 (С(5)); 80.1 (С(3)); 80.4 (С(2)); 136.6, 128.6, 127.1, 128.3 (Ph); 168.7 (CO2). Масс-спектр (ЭУ, 70 эВ), m/z (Ioтн, %): 236 [М]+.
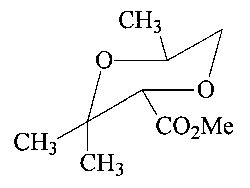
Спектр ЯМР 1Н (CDCl3, δ, м.д, J/Гц): 1.10 (д, 3Н, Me, 3J=6.15); 1.23 (с, 3Н, Me); 1.28 (с, 3Н, Me); 3.19 (д д, 1Н, Н(6)а, 2J=-11.80, 3J=11.20); 3.73 (с, 3Н, Me); 3.95 (д д, 1H, Н(6)е, 2J=-11.80, 3J=2.86); 3.97 (м, 1H, Н(5)а); 4.21 (с, 1Н, Н(2)а). Спектр ЯМР 13С (CDCl3, δ, м.д.): 16.9 (Me); 18.7 (Me); 26.7 (Me); 52.1 (Me); 64.1 (C(5)); 67.9 (C(3)); 72.4 (CH(6)); 81.9 (C(2)); 169.4 (CO2). Масс-спектр (ЭУ, 70 эВ), m/z (Ioтн, %): 188 [M]+.
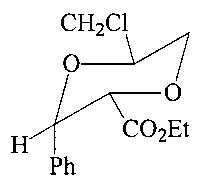
Спектр ЯМР 1H (CDCl3, δ, м.д., J/Гц): 0.94 (т, 3Н, Me, 3J=7.07); 3.56 (м, 2Н, СН2); 3.60 (д д, Н, Н(6)а, 2J=-10.8, 3J=9.9); 3.95 (к, 2Н, СН2, 3J=7.07); 4.03 (д, Н, С2На, 3J=9.11); 4.12 (м, Н, Н(5)а); 4.18 (д д, Н, Н(6)е, 3J=-10.8, 3J=2.6); 4.68 (д, Н, Н(3)а, 3J=9.11); 7.20-7.35 (м, 5Н, Ph). Спектр ЯМР 13С (CDCl3, δ, м.д.): 13.5 (Me); 42.5 (CH2); 60.9 (CH2); 68.2 (С(6)); 74.1 (С(5)); 80.2 (С(3)); 80.4 (C(2)); 136.0, 128.8, 128.3, 127.2 (Ph); 167.9 (CO2). Масс-спектр (ЭУ, 70 эВ), m/z (Ioтн, %): 285 [М]+.
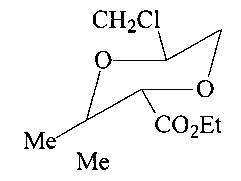
Спектр ЯМР 1Н (CDCl3, δ, м.д, J/Гц): 1.20 (м, 3Н, Me); 1.21 (с, 3Н, Me); 1.27 (с, 3Н, Me); 3.29 (д д, 1Н, Н(12)′, 2J=-13.4); 3.30 (т, Н, Н(6)а, 2J=-11.38, 3J=11.4); 3.40 (д д, Н, Н(12)′′, 3J=-13.4); 3.70 (м, Н, Н(6)е); 3.90 (с, 1Н, Н(2)); 4.00 (м, Н, Н(5)а); 4.20 (м, 2Н, СН2). Спектр ЯМР 13С (CDCl3, δ, м.д.): 13.9 (Me); 18.5 (Me); 26.3 (Me); 43.0 (СН2); 61.1 (СН2); 69.1 (С(5)); 70.4 (С(6)); 72.8 (С(3)); 81.9 (С(2)); 168.4 (CO2). Масс-спектр (ЭУ, 70 эВ), m/z (Ioтн, %): 236 [М]+.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ 3-(2-АЛКИНИЛ)-1,3-ОКСАЗОЛИДИНОВ | 2014 |
|
RU2565780C1 |
| СПОСОБ ПОЛУЧЕНИЯ N-АЛКИЛ-N,N-ДИ(АЛКАДИИНИЛ)АМИНОВ | 2015 |
|
RU2626008C2 |
| 4-ЗАМЕЩЕННЫЕ N-АРИЛ-1,8-НАФТАЛИМИДЫ, ПРОЯВЛЯЮЩИЕ СВОЙСТВА ФЛУОРЕСЦЕНТНЫХ СЕНСОРОВ НА КАТИОНЫ МЕТАЛЛОВ, И СПОСОБЫ ИХ ПОЛУЧЕНИЯ | 2012 |
|
RU2515195C1 |
| ЗАМЕЩЁННЫЕ ИЗОКСАЗОЛЫ, ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ НА ИХ ОСНОВЕ, ОБЛАДАЮЩИЕ ПРОТИВОВИРУСНОЙ АКТИВНОСТЬЮ, И СПОСОБ ИХ ПРИМЕНЕНИЯ | 2018 |
|
RU2733945C2 |
| Хиральные S-монотерпенилцистеины | 2018 |
|
RU2689381C1 |
| СПОСОБ ПОЛУЧЕНИЯ 1,3-ДИКАРБОНИЛЬНЫХ СОЕДИНЕНИЙ, СОДЕРЖАЩИХ ДИБЕНЗОСУБЕРЕНИЛЬНЫЙ ФРАГМЕНТ | 2014 |
|
RU2560727C1 |
| Четвертичные аммониевые соли на основе производных витамина В6 | 2015 |
|
RU2607522C1 |
| СИНТЕЗ НОВОГО КЛАССА ФТОРСОДЕРЖАЩИХ ЖИДКОКРИСТАЛЛИЧЕСКИХ СОЕДИНЕНИЙ С ИСПОЛЬЗОВАНИЕМ ХЛАДОНА 114В2 В КАЧЕСТВЕ ИСХОДНОГО СОЕДИНЕНИЯ | 2012 |
|
RU2505529C1 |
| (2R*,5R*)-2-Арил-5-гидрокси-8,8-диметил-3-фенил-2,3,5,7,8,9-гексагидро-2,5-метанобензо[f][1,3]оксазепин-4,6-дионы | 2023 |
|
RU2813548C1 |
| АНТИБАКТЕРИАЛЬНЫЕ СРЕДСТВА НА ОСНОВЕ ЧЕТВЕРТИЧНЫХ АММОНИЕВЫХ СОЛЕЙ | 2014 |
|
RU2561281C1 |
Изобретение относится к способу получению 1,4-диоксанкарбоксилатов, который заключается в том, что проводят расширение 1,3-диоксоланового кольца при взаимодействии моно-, ди- и тризамещенных 1,3-диоксоланов с метилдиазоацетатом в условиях микроволнового излучения (230 Вт) в течение 0,5-1,5 часов в среде хлористого метилена. Реакцию 1,3-диоксолана с метилдиазоацетатом проводят при следующем соотношении компонентов, мас.%: 1,3-диоксолан 0,006-0,012; метилдиазоацетат 5,48; CH2Cl2 94,514-94,508. Технический результат - увеличение выхода целевого продукта при повышении его качества. 1 з.п. ф-лы, 1 табл.
1. Способ получения 1,4-диоксанкарбоксилатов реакцией расширения 1,3-диоксоланового кольца, взаимодействием моно-, ди- и тризамещенных 1,3-диоксоланов с метилдиазоацетатом, отличающийся тем, что реакцию проводят при микроволновом излучении (230 Вт) в течение 0,5-1,5 часов в среде хлористого метилена.
2. Способ по п. 1, отличающийся тем, что процесс с моно-, ди- и тризамещенными 1,3-диоксоланами проводят при следующем соотношении компонентов, мас.%: 1,3-диоксолан 0,006-0,012; метилдиазоацетат 5,48; CH2Cl2 94,514-94,508.
| Султанова Р.М., "Диазосоединения и их фосфозаны в синтезе кислород-, азот- и серосодержащих гетероциклических соединений", Автореферат дисс | |||
| д.х.н., Уфа, 2013,стр.7-9 | |||
| US 20060122407 A1 08.06.2006 | |||
| СПОСОБ ПОЛУЧЕНИЯ ЭФИРОВ ДИОКСАНУКСУСНОЙ КИСЛОТЫ | 2003 |
|
RU2315761C2 |
Авторы
Даты
2016-09-10—Публикация
2015-07-20—Подача