Область техники
Изобретение относится к области медицины, может быть использовано в травматологии и ортопедии, челюстно-лицевой хирургии и хирургической стоматологии в рамках регенеративного подхода к лечению дефектов костной ткани как само по себе, так и в качестве материала - носителя лекарственных средств или в качестве материала несущей матрицы в конструкциях тканевой инженерии.
Уровень техники
Основными требованиями, предъявляемыми к материалам, используемым для заполнения костных дефектов, являются отсутствие токсического воздействия на организм, приемлемые механические характеристики и образование прочного контакта с окружающей костной тканью. Регенерационный подход к восстановлению утраченной костной ткани предполагает использование биорезорбируемых материалов, способных служить средой, стимулирующей образование новой костной ткани. Данный подход требует разработки материалов, обладающих таким функциональным свойством, как биорезорбируемость. Биорезорбируемость материала для костных имплантатов - это способность материала, постепенно растворяясь в среде организма, стимулировать рост природной костной ткани, являясь в это же время источником компонентов для ее строительства. Для реализации регенерации утраченной или поврежденной костной ткани наибольшей степени подходят и разработаны биорезорбируемые неорганические материалы на основе фосфатов кальция [Баринов С.М. Керамические и композиционные материалы на основе фосфатов кальция для медицины // Успехи химии, 2010. Т. 79, №1, с. 15-32]. Для формирования таких материалов используют технологию керамики, стекла или вяжущих [Путляев В.И., Сафронова Т.В. Новое поколение кальцийфосфатных биоматериалов: роль фазового и химического составов // Стекло и керамика, 2006. №3, с. 30-33]. Одним из преимуществ технологии вяжущих является формирование материала вследствие протекания реакций химического связывания при относительно низких температурах. Другое преимущество заключается в возможности широкого варьирования состава и свойств как матрицы, так и наполнителя композиционного материала, получаемого по технологии вяжущих материалов, в основе которой лежат процессы химического связывания, наиболее часто представленные кислотно-основным взаимодействием или гидролизом [Dorozhkin S.V. Calcium orthophosphate cements for biomedical application // J Mater Sci, 2008. V. 43, p. 3028-3057].
Продолжительность процесса биодеградации композиционного материала может сильно варьироваться, и зависит от фазового состава матрицы и наполнителя, а также от индивидуальных особенностей организма пациента и конкретных участков имплантации. Реакционно-связанные материалы на основе нестехиометричного гидроксипатита (соотношение Са/Р 1,5-1,66) обладают более высокой скоростью биодеградации по сравнению с материалами на основе синтетического стехиометрического гидроксиапатита и могут быть использованы в качестве резорбируемого материала, предназначенного для использования в регенерационной медицине. Биодеградации такого реакционно-связанного материала происходит приблизительно в течение 3-6 месяцев.
Способность к биорезорбированию существующих фосфатов кальция с мольным соотношением Са/Р в интервале 0,5-1,66 коррелирует с их растворимостью, которая в свою очередь определяется кристаллическим строением и значением соотношения Са/Р. При этом использование материалов на основе фосфатов кальция с соотношением Са/Р, выходящим за пределы указанного интервала недопустима в виду кислой реакции среды при Са/Р меньшим 0,5 или щелочной - при Са/Р большим 1,67. Повышение резорбируемости материалов, предназначенных для изготовления костных имплантатов, может также быть достигнуто применением неизовалентного катионного или анионного замещения в структуре фосфатов кальция, изменением фазового состава наполнителя при введении более резорбируемых биосовместимых фаз, а также при уменьшении размеров структурных элементов (зерен, прослоек аморфных фаз) микроструктуры материала. При этом варьирование фазового состава - это подход к заметному изменению резорбируемости (растворимости) материала. Внесение изменения в кристаллическую структуру замещающими ионами или варьирование размеров элементов микроструктуры позволяет осуществлять более тонкое регулирование глубиной и скоростью резорбирования материала. Растворимость соединений, используемых для получения материалов для костных имплантатов, возрастает в следующем ряду (таблицы 1, 2).
Реакционно-связанные материалы на основе фосфатов кальция могут содержать все упомянутые фазы или в качестве наполнителя, или в качестве матрицы. Некоторые из них формируются в результате реакций кислотно-основного взаимодействия (CaHPO4*2H2O), другие - в результате гидролиза (Са10(PO4)6(ОН)2, Ca9Na(HPO4)(PO4)5CO3). Фазы, формирующиеся вследствие протекания реакций химического связывания, сообщают материалу прочность, могут рассматриваться как матрица композиционного материала.
Другие фазы привносятся как наполнитель, и не претерпевают изменений в процессе получения материала. Варьирование состава и качества наполнителя - действенный инструмент управления свойствами материла. В таблице 3 представлены некоторые свойства биосовместимых фаз композиционных материалов, способных к биорезорбции. Растворимость, как свойство, коррелирующее с резорбируемостью, возрастает в ряду упомянутых соединений слева направо.
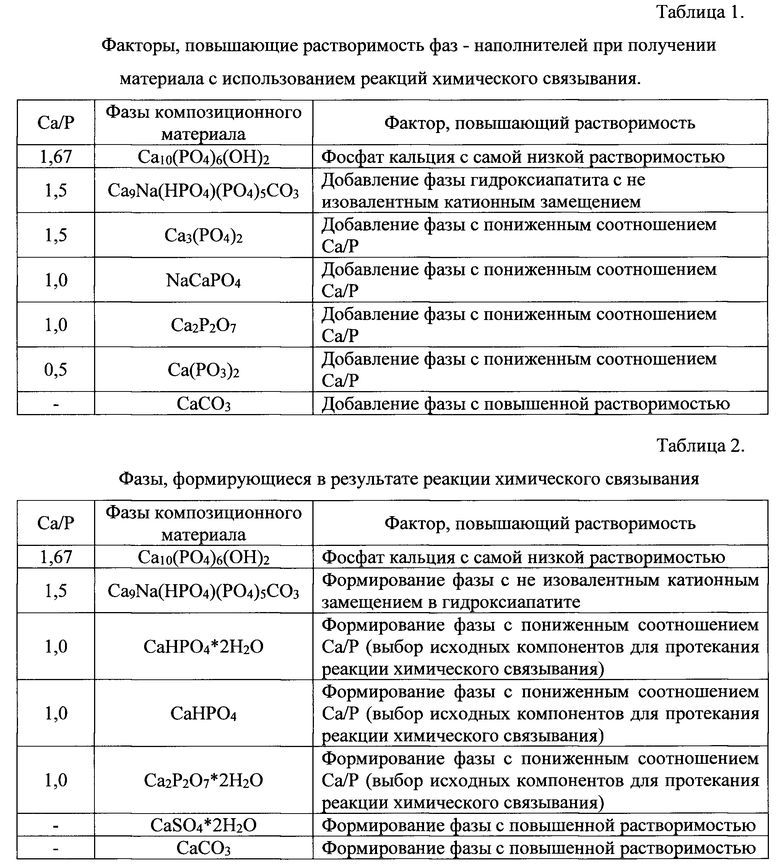
Материалы, полученные с использованием химического связывания и содержащие в качестве фазы, образующей матрицу, гидроксиапатит или его структурные аналоги (карбонатгидроксиапатит, Са-дефицитный гидроксиапатит) обладают наибольшей прочностью [Филиппов Я.Ю., Ларионов Д.С., Путляев В.И., Соколов А.В., Ковальков В.К., Агахи К.А., Селезнева И.И., Никонова Ю.А., Реакционно-связанные резорбируемые фосфатные биоматериалы: получение и испытания in vitro. // Стекло и керамика, 2013. №8, с. 35-40]. При этом данные, представленные в таблицах 1 и 3, указывают на то, что существует достаточно большой список фаз, которые могут быть использованы в качестве наполнителя композиционного материала, матрица которого сформирована в результате протекания реакций химического связывания.
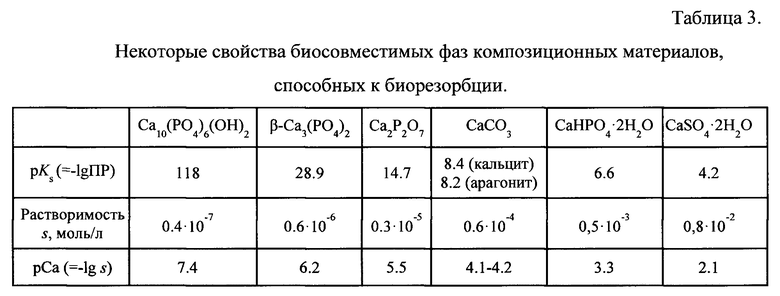
Следует отметить, что из всего списка соединений только карбонатгидроксиапатит и карбонат кальция содержат в своей структуре карбонат ионы, которые при растворении могут поступать в зону формирования костной ткани, поддерживая ее анаэробное дыхание и способствуя протеканию остеосинтеза [Gilbert SF. Developmental Biology. 6th edition. Sunderland (MA): Sinauer Associates; 2000. Osteogenesis: The Development of Bones. Available from: http://www.ncbi.nlm.nih.gov/books/NBK10056/].
В качестве материалов для костных имплантатов, способных поддерживать анаэробное дыхание, могли бы быть использованы материалы на основе природного карбоната кальция (коралла), а также и керамические материалы на основе синтетического карбоната кальция. Однако, природный коралл трудно доступен для широкого применения, а керамические материалы получают с использованием высокотемпературного обжига.
Материал на основе CaCO3, фазовый состав которого представлен различными модификациями карбоната кальция, был получен при использовании ватерита и арагонита в качестве наполнителя, аморфного карбоната кальция в качестве вяжущего компонента и изотонического раствора (0,9 мас. % NaCl в воде) в качестве жидкости затворения [Combes С., Miao Baoji, Bareille R., Rey С. Preparation, physical-chemical characterisation and cytocompatibility of calcium carbonate cements // Biomaterials, 2006. V. 27, p. 1945-1954]. Недостатком материала является его низкая прочность и отсутствие в составе фосфат-содержащих фаз, дающих при растворении необходимый для строительства новой костной ткани фосфат-ион.
Известны способы получения материала из порошковой смеси карбонита кальция в виде ватерита или арагонита и фосфатов кальция в виде брушита или аморфного фосфата кальция [Mirtchi А.А., Lqeumeasitre J., Munting E. Calcium phosphate cements: study of the β-tricalciumphosphate - dicalcium phosphate - calcite cements // Biomarenals, 1990. Vol 11, p. 83-88; Combes C., Bareille R., Rey C. Calcium carbonate-calcium phosphate mixed cement compositions for bone reconstruction // J Biomed Mater Res., 2006. V. 79A, p. 318-328]. В качестве жидкости затворения были использованы вода или изотонический раствор (0,9 мас. % NaCl в воде). К недостаткам этих материалов следует отнести низкую прочность (не выше 13 МПа на сжатие), а также использование для получения брушита и гидроксиапатита водных растворов нитрата кальция и гидрофосфата аммония. В результате взаимодействия нитрата кальция и гидрофосфата аммония кроме целевого фосфата кальция формируется агрессивный к живым тканям сопутствующий продукт - нитрат аммония, полное удаление которого промыванием невозможно.
Известен способ получения бифазного материала, содержащего гидроксиапатит и трикальцийфосфат, с использованием реакций химического связывания. В этом способе карбонат кальция используется в качестве компонента, участвующего в формировании микроструктуры при взаимодействии порошковой смеси карбоната кальция и Са(H2PO4)2·H2O с дистиллированной водой, используемой в качестве жидкости затворения [Chung-King Hsu The preparation of biphasic porous calcium phosphate by the mixture of Са(H2PO4)2·H2O and CaCO3 // Materials Chemistry and Physics, 2003. V. 80, p. 409-420]. Недостатком данного материала является низкая прочность, обусловленная пористостью, образовавшейся вследствие взаимодействия кислой соли и карбоната кальция, а также отсутствие в структуре цементного камня фазы карбоната кальция, способной не только повышать скорость резорбирования материала при имплантации, но и вносить заметный вклад в поддержание анаэробного дыхания костной ткани.
Известен способ, в котором композиция для производства композитных карбонизированных изделий включает в качестве наполнителя отходы добычи и обработки известняка-ракушечника, а в качестве вяжущего вещества - гашеную кальциевую известь [Патент RU 2549257, 20.04.2015]. Данное изобретение относится к области создания строительных материалов и не может быть использовано для создания материалов медицинского назначения.
Известен способ получения материала с использованием реакций химического связывания, в котором карбонат кальция используется в качестве наполнителя и в качестве компонента, участвующего в формировании матрицы из гидроксиапатита при взаимодействии с жидкостью затворения, в состав которой входят фосфорная кислота и NaOH или Na2HPO4 [Tas A. Cuneyt Porous, Biphasic CaCO3-Calcium Phosphate Biomedical Cement Scaffolds from Calcite (CaCO3) Powder // Int. J. Appl. Ceram. Technol., 2007. V. 4, №2, p. 152-163]. Недостатком данного способа является получения не прочного пористого материала, в котором пористость образуется вследствие вытеснения фосфорной кислотой СО2 из карбоната кальция.
Известен способ [Goldberg М.А., Smirnov V.V., Popov V.K., Popova A.V., Trofimov V.V., Fomin A.S., Fedotov A.Yu., Shvorneva L.I., Kutsev S.V., Barinov S.M. Hardening of calcium phosphate bone cement by supercritical carbon dioxide // Doklady Chemistry, 2013. V. 452, №2, p. 259-262] получения кальций фосфатного цемента из тетракальциевого фосфата с использованием в качестве жидкости затворения водного раствора дигидрофосфата натрия с последующей обработкой сформованных образцов жидкостью СО2 в сверхкритическом состоянии. О получении фазы карбоната кальция в настоящей работе не сообщается, однако отмечается повышение прочности (до 29,5 МПа на сжатие) кальцийфосфатного цемента, представляющего собой композит и содержащего брушит, гтдроксиапатит, тетракальциевый фосфат и в некоторых случаях фосфат натрия. Содержание в составе материала тетракальциевого состава приводит к установлению щелочных значений рН в зоне взаимодействия материала имплантата и тканей организма, что ограничивает применение подобного материала.
Известное взаимодействие кислого (СО2) и основного (СаО) оксидов находит свое применение в различных отраслях промышленности. Так, оксид кальция может быть эффективным сорбентом для поглощения CO2 при высоких температурах [Grasa G.S., Abanades J.С. CO2 capture capacity of СаО in long series of carbonation/calcination cycles // Industrial & Engineering Chemistry Research, 2006. T. 45, №. 26, c. 8846-8851]. Развитие ускоренной искусственной карбонизации рассматривается и как эффективный инновационный метод борьбы с глобальным потеплением [Любомирский Н., Воробьев Д. Современное состояние исследований искусственной карбонизации известковых систем // MOTROL, 2011. Т. 13, с. 165-176]. Еще в глубокой древности для скрепления кирпичной или каменной кладки использовали «известковый раствор» - смесь Са(ОН)2, SiO2 и воды. Постепенно реагируя с СО2 (из воздуха) и SiO2, гидроксид кальция образует очень прочную массу, состоящую из карбоната и силиката кальция. Процесс твердения идет медленно, что является недостатком «известкового раствора» [Карапетьянц М.Х., Дракин С.И. Общая и неорганическая химия. Учебное пособие для вузов. М.: Химия, 1981, 632 с., ил.: с. 323]. Известны технологии строительных материалов, базирующихся на процессах карбонизации извести углекислым газом, содержащимся в атмосфере [Любомирский Н. Влияние температуры на кинетику карбонизации извести // MOTROL, 2014. Т. 16, с. 65-74]. Однако при использование атмосферного CO2 процессы карбонизации требуют длительного времени. Процессы карбонизации извести могут протекать быстрее в потоке углекислого газа [Патент RU 2549258, 20.04.2015], но это потребует специального оборудования и предварительной подготовки СО2.
Известен способ получения кальцийфосфатного цемента с близким к природной костной ткани катион-анионным составом, который получают из смеси дикальциевого фосфата, тетракальциевого фосфата, бикарбоната натрия и окиси кальция путем затворения серной кислотой [Патент RU 2207106, 27.06.2003]. Недостатками материала, получаемого с использованием данного метода, невысокие прочностные характеристики, а также слишком кислая реакция среды, которая устанавливается при имплантировании этого материала.
Известен способ получения кальцийфосфатного цемента, который получают из порошковой смеси α-трехкальциевого фосфата, источника кальция (например, карбоната кальция) и фосфорной кислоты в присутствии гидрофосфата натрия [US 5571493, 05.11.1996] Недостатком данного метода являются невысокие прочностные характеристики.
В способе [Arief Cahyanto, Riki Toita, Kanji Tsuru, Kunio Ishikawa, Effect of Particle Size on Carbonate Apatite Cement Properties Consisting of Calcite (or Vaterite) and Dicalcium Phosphate Anhydrous // Key Engineering Materials, 2015. V. 631, p. 128-133] для получения цемента на основе карбонатзамещенного гидроксиапатита использовали порошковую смесь карбоната кальция и дикальциевого фосфата ангидрида в соотношении 40:60 по массе и 0.8М водный раствор Na2HPO4 в качестве жидкости затворения. Фазовый состав цементного камня после протекания реакции был представлен карбонатгидроксиапатитом и карбонатом кальция в виде кальцита или ватериата. Карбонат исходной смеси частично используется для формирования фазы матрицы композиционного материала, частично выступает в роли наполнителя. Недостатком данного метода также являются невысокие прочностные характеристики и отсутствие системы макропор.
Известно, что для формирования кальций фосфатного цементного камня используют в качестве исходных компонентов кальцийсодержащие компоненты и фосфат-содержащие компоненты. В список кальцийсодержащих компонентов включены оксид кальция и карбонат кальция. При этом предполагается, что в процессе формирования цементного камня в результате протекания реакций, обеспечивающих химическое связывание такие Са-содержащие компоненты будут полностью исчерпываться в результате образования фосфатов кальция [US 7175858, 13.02.2007].
Известен метод получения плотного композиционного материала, состоящего из фаз гидроксиапатита и α-трехкальциевого фосфата, который включает в себя стадию спекания смеси безводного порошка дикальцийфосфата и карбоната кальция при температуре 1200-1400°C с образованием монолитных блоков из α-трехкальциевого фосфата с последующим помещением их в водные растворы при температуре 10-50°C для преобразования его в нанокристаллический гидроксиапатит [Патент RU 2529802, 27.09.2014]. Недостатком данного материала является отсутствие в фазовом составе фазы с повышенной скоростью резорбции, такой, например, как карбонат кальция, а также недостаточная скорость биорезорбции и наличие значительной доли α-трехкальциевого фосфата, что, возможно, приводит заметному росту рН в области имплантации.
Таким образом, данные научной и патентной литературы свидетельствуют о том, что получение материала, содержащего одновременно карбонат кальция и фосфаты кальция, является актуальным. При этом карбонат кальция может быть использован в качестве или вяжущего компонента, или наполнителя, или одного из прекурсоров фосфатов кальция в материале. Введение карбоната кальция возможно непосредственно в виде различных модификаций карбоната кальция, которые в цементном камне или остаются без изменения или превращаются в кальцит. Образование карбоната кальция в цементном камне в виде кальцита возможно и вследствие взаимодействия СаО или Са(ОН)2 с углекислым газом в процессе воздушного твердения или в токе CO2. Все упомянутые способы позволяют получить содержащие карбонат кальция композиционные материалы или с низкой прочностью или не предназначенные для использования в медицине. Создание достаточно прочных композитов возможно при формировании матрицы композиционного материала, состоящей из гидроксиапатита или его более растворимых аналогов.
Наиболее близким к предполагаемому изобретению является способ получения композиционного материала для замещения костных дефектов [Филиппов Я.Ю., Ларионов Д.С., Путляев В.И., Соколов А.В., Ковальков В.К., Агахи К.А., Селезнева И.И., Никонова Ю.А., Реакционно-связанные резорбируемые фосфатные биоматериалы: получение и испытания in vitro. // Стекло и керамика, 2013. No 8, с. 35-40], включающий; подготовку порошковой смеси, содержащей порошок α-Са3(PO4)2; подготовку пасты при добавлении жидкости затворения в виде водного раствора, содержащего карбонат-ион; формование образцов из пасты; гидролитическую обработку изделия в водном растворе, содержащем карбонат-ион, и сушку.
Фазовый состав материала, полученного по этому способу, представлен карбонатгидроксиапатитом и трикальцийфосфатом. Данные фазы являются биорезорбируемыми. Однако скорость и степень резорбции недостаточны для использования таких материалов для создания пористой основы конструкций тканевой инженерии или для использования в регенеративных методиках лечения костных дефектов, когда от материала требуется более высокая скорость резорбции, обусловленная более высокой растворимостью. Кроме того, материал не содержит фазы, которая могла бы при биодеградации стать источником СО2, поддерживающего анаэробное дыхание костной ткани. Недостатком материала, получаемого в соответствии с этим способом является отсутствие в составе цементного камня фаз способных резорбироваться с достаточно высокой скоростью и поддерживать анаэробное дыхание костной ткани в процессе ее формирования, являясь при этом источником компонентов для формирования новой костной ткани, таких как Са2+ и CO3 2-.
Раскрытие изобретения
Была поставлена задача разработать способ получения композиционного материала для замещения костных дефектов с использованием гидролитической конверсии, обладающего достаточной прочностью и высокой скоростью биорезорбции в среде организма вследствие содержания резорбируемых фаз карбоната кальция, трикальцийфосфата и карбонатгидроксиапатита. Задача была решена настоящим изобретением.
Способ получения композиционного материала для замещения костных дефектов с использованием гидролитической конверсии, включает подготовку порошковой смеси, содержащей порошок α-Са3(PO4)2; подготовку пасты при добавлении жидкости затворения в виде водного раствора, содержащего карбонат-ион; формование образцов из пасты; гидролитическую обработку изделия в водном растворе, содержащем карбонат-ион, и сушку. Согласно изобретению, порошковая смесь дополнительно содержит оксид кальция при соотношении массы СаО к массе α-Са3(PO4)2 в интервале 0,11-0,43, концентрация [CO3 2-] в жидкости затворения составляет 0,9М-1,1М при соотношении «жидкость затворения/масса порошка» в интервале 0,8-1,0, давление прессования составляет 100-450 МПа, а гидролитическую конверсию проводят в водном растворе с концентрацией [CO3 2-] в интервале 0,9М-1,1М в течение 12-120 часов при температуре в интервале 30-60°C. При этом для образцов или изделий, изготовленных из 100 г порошковой смеси, для проведения гидролитической конверсии используют 800-1200 мл раствора, содержащего карбонат-ион, а в качестве растворимых соединений, являющихся источником карбонат-иона, используют гидрокарбонаты аммония, натрия и калия.
Подготовка компонентов исходной порошковой смеси.
Подготовка α-Ca3(PO4)2
Для получения порошка α-Ca3(PO4)2 используют твердофазный синтез при обжиге в интервале 1350-1450°C в течение 1-2 часов порошковой смеси, включающей CaHPO4 и CaCO3, рассчитывая количества исходных компонентов по реакции (1), после гомогенизации порошковой смеси в плантерной мельнице.

Обжиг при температуре ниже 1350°C и продолжительностью менее 1 часа не обеспечивает полной конверсии β-Ca3(PO4)2, образовавшегося в интервале 700-1125°C в α-Ca3(PO4)2. Термообработка при более высокой температуре, чем 1450°C в течение периода, превышающего 2 часа не целесообразна, поскольку конверсия уже завершена, а использование более продолжительной выдержки при более высоких температурах будет приводить к огрублению частиц порошка, что не желательно.
Для получения порошка CaHPO4 используют следующую последовательность реакций:
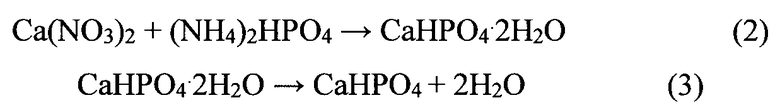
Реакцию (2) проводят при комнатной температуре, используя концентрированные водные растворы нитрата кальция и гидрофосфата аммония. Для увеличения выхода целевого продукта используют растворы с концентрацией 1-2М. Использование растворов с более низкой (менее 1М) концентрацией снижает выход целевого продукта, использование растворов с более высокой (более 2М) концентрацией может быть ограничена растворимостью используемых солей и возможными сложностями с обеспечением однородных условий синтеза по объему реактора. Полученный осадок отделяют от маточного раствора, промывают и сушат при температуре 250-270°C в течение 10-12 часов. Сушка при температуре менее 250°C продолжительностью менее 10 часов не обеспечивает полной конверсии брушита (CaHPO4·2H2O) в монетит (CaHPO4). Сушка при температуре выше 270°C продолжительностью более 12 часов не целесообразна, поскольку конверсия до этой температуры в течение указанного периода проходит полностью.
Подготовка СаО
Порошок оксида кальция получают термообработкой порошка карбоната кальция при температуре 1000-1100°C в течение 10-12 часов. При этом происходит превращение по реакции (4):
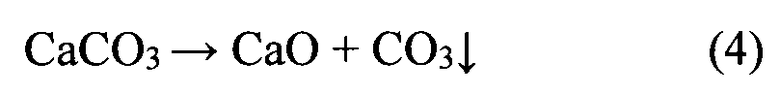
При проведении термообработки при температуре ниже 1000°C в течение периода продолжительностью менее 10 часов возможно не полное превращение карбоната кальция в оксид кальция. Термообработка при температуре выше 1100°C продолжительностью более 12 часов нецелесообразна, поскольку превращение завершено, а высокотемпературная продолжительная термообработка может приводить к огрублению порошков, т.е увеличению размера частиц его составляющих.
Подготовка жидкости затворения и жидкости для гидролитической конверсии
Жидкость затворения и жидкость для гидролитической конверсии представляют собой водный раствор гидрокарбонатов натрия, калия или аммония с концентрациями [CO3 2-], лежащей в интервале 0,9М-1,1М. Высокая концентрация (выше 0,9М) необходима для обеспечения протекания реакций формирования карбонатгидроксиапатита и карбоната кальция при достаточном содержании [CO3 2-], который расходуется в результате формирования новых фаз карбонатгидроксиапатита и карбоната кальция. Концентрация выше 1,1М не может быть превышена вследствие достижения предела растворимости одного из гидрокарбонатов.
Подготовка массы для формования.
Содержание СаО в смеси составляет 10-30 мас. % Соответственно, содержание α Ca3(PO4)2 в смеси составляет 90-70 мас. %, а соотношение массы СаО к массе α Ca3(PO4)2 меняется в интервале 0,11-0,43. Предварительно подготовленные порошки α-Ca3(PO4)2 и СаО смешивают посредством совместного помола в шаровой мельнице в течение 10-20 минут под слоем ацетона. Смешивание порошковых компонентов в течение периода времени меньшего 10 мин не обеспечивает необходимой степени гомогенизации. Смешивание порошковых компонентов в течение периода времени большего 20 мин избыточна, поскольку необходимая степень гомогенизации уже достигнута. После смешивания и удаления ацетона полученные порошковые смеси протирают через сито. К подготовленной таким образом порошковой смеси добавляют жидкость затворения при массовом соотношении «жидкость/твердое» в интервале 0,8-1,0 и тщательно перемешивают.
Подготовленная таким образом паста готова к последующей консолидации. Уменьшение соотношения «жидкость/твердое» менее 0,8 не позволяет достичь необходимой гомогенности пасты и сплошности массы, предназначенной для формования. Использование соотношения «жидкость/твердое» при значениях выше 1,0 существенным образом понижает вязкость формовочной массы и превращает ее в неустойчивую дисперсную систему, склонную к расслоению.
Консолидация и формирование конечного фазового состава.
Полученную пасту, содержащую α-Ca3(PO4)2 и СаО и жидкость затворения формуют при помощи разборной пресс-формы (либо нескольких пресс-форм) под давлением 100-400 МПа.
Вода, присутствующая в жидкости затворения реагирует с СаО, образуя Са(ОН)2 (реакция 5).

Присутствующие в жидкости затворения ионы принимают участие в нескольких одновременно протекающих процессах, которые могут быть отражены реакциями (6) и (7), где Z=Na, К, NH4.
В результате протекания реакций (5), (6) и (7) формируются целевые фазы резобируемого композиционного материала.
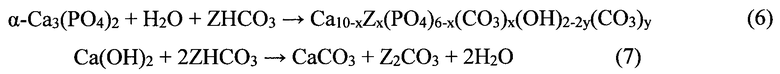
На стадии формования реакции (6) и (7) протекают лишь частично. Окончательное формирование заданного фазового состава материала происходит на стадии гидролитической конверсии.
Полученные прессовки сушат на воздухе в течение 20-24 часов, после чего помещают раствор, содержащий CO3 2-, полученный растворением гидрокарбоната натрия, калия или аммония. Раствор, в котором проводят гидролитическую конверсию, необходимо взять в количестве 800-1600 мл на 100 г исходной порошковой смеси. Образцы после формования и выдерживают при температуре 30-60°C в течение 12-120 часов.
Соотношение массы СаО к массе α-Ca3(PO4)2 (α-ТКФ) меняется в интервале 0,11-0,43. Содержание в смеси СаО при этом составляет 10-30 мас. %, что обеспечивает содержание фазы CaCO3 в 17-53 мас. % в материале после проведения стадии гидролитической конверсии. Соответственно, содержание α-Ca3(PO4)2 в смеси составляет 90-70 мас. %, который служит источником двух фаз карбонатгидроксиапатита и α Ca3(PO4)2. Поскольку, СаО является прекурсором фазы CaCO3 в композиционном материале, то снижение содержания СаО ниже 10 мас. % (соотношение СаО/α-ТКФ=0,11) отрицательно скажется на способности материала к растворению и биодеградации. Использование СаО в количестве меньшем 10 мас. % приведет к снижению содержания фазы карбоната кальция в целевом материале, а следовательно, и снижению общей способности материала к резорбированию. При взаимодействии α-Ca3(PO4)2 и компонентов жидкости затворения только часть этого компонента идет на формирование карбонатгидроксиапатита, который присутствует в материале в количестве 22-68 мас. %. С ростом содержания СаО в исходной смеси степень превращения α-ТКФ в карбонатгидроксиапатит снижается. Превышение содержания СаО в исходной смеси выше 30 мас. % (соотношение СаО/α-ТКФ=0,43) приведет к существенному снижению количества фазы карбонатгидроксиапатита, обеспечивающей прочность композита.
Раствор, содержащий карбонат-ионы и предназначенный для гидролитической конверсии фаз СаО и Ca3(PO4)2 в целевые фазы резорбируемого биосовместимого композита, содержит избыток карбонат-ионов, который необходим для достижения заданного фазового состава. При концентрации карбонат-ионов менее 0,9М при объеме 800 мл/100 г растворов, используемых в качестве жидкости затворения и раствора для гидролитической конверсии, и продолжительность стадии гидролитической конверсии менее 12 часов в материале может остаться не прореагировавший СаО, что не допустимо при создании материалов для имплантации. Концентрация карбонат-ионов более 1,1М при объеме 1600 мл/100 г растворов, используемых в качестве жидкости затворения и раствора для гидролитической конверсии, и продолжительность стадии гидролитической конверсии более 120 ч. избыточны, поскольку превращение Са(ОН)2 до граничных условий проходит полностью. Более низкая концентрация (0,9М) приводит к образованию слабо-замещенного гидроксиапатита, обладающего более низкой скоростью биорезорбции, а верхнее значение (1,1М) соответствует насыщенному раствору, когда процесс замещения наиболее эффективен. При проведении процесса гидролитической конверсии менее 12 часов глубина протекания реакции химического связывания невысока, кроме того, возможно наличие непрореагировавшего Са(ОН)2, что приводит к отторжению со стороны организмы вследствие высокого рН. Проводить процесс более 120 часов нецелесообразно, так как возможно протекание процессов перекристаллизации с укрупнением среднего размера частиц, что ухудшает прочностные и биологические характеристики.
Гидролитическую конверсию проводят при 30-60°C. Использование температур выше 60°C может привести к уменьшению содержания CO3 2- в растворе, предназначенном для гидролитической конверсии. Использование температур ниже 30°C замедляет скорость протекания гидролитической конверсии и увеличивает продолжительность операции, что не желательно.
Формирование фазового состава материала в процессе гидролитической конверсии может быть отражено реакциями (6) и (7).
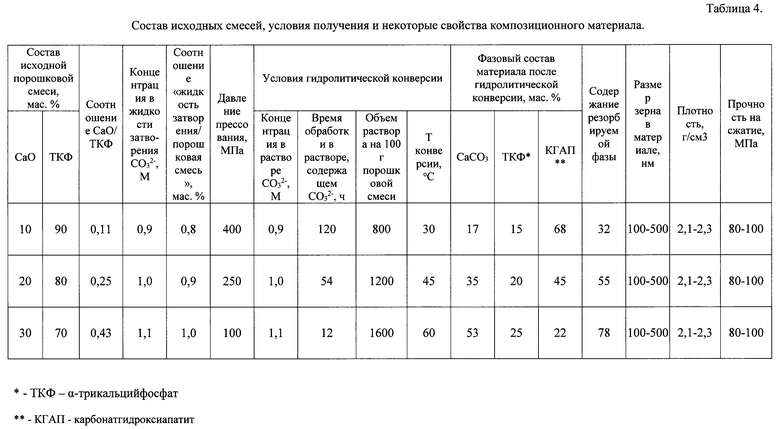
В результате протекания гидролитической конверсии предварительно сформованных из пасты образцов формируется материал, включающий фазы кальцита, α-трикальцийфосфта и карбонатгидроксиапатита (таблица 3, фигура 1).
Полученные в результате материалы извлекают из раствора, удаляют с их поверхности влагу и сушат при температуре 58-62°C в течение 10-12 часов. Сушка при температуре ниже 58°C будет проходить слишком медленно. Сушка при температуре выше 62°C может привести к растрескиванию образцов вследствие слишком быстрого удаления влаги. Сушка в течение периода продолжительностью менее 10 часов недостаточна, поскольку образцы не достигают постоянного значения массы. Сушка в течение периода продолжительностью более 12 часов уже не целесообразна, поскольку масса образцов вследствие удаления воды уже не изменяется.
Краткое описание чертежей (фигур)
На фигуре 1 приведены данные РФА материалов, содержавших в исходной порошковой смеси 10, 20, 30 мас. % СаО после гидролитической конверсии (а); штрих-диаграммы, соответствующие СаСО3-карточка PDF2 №5-586 (б); α-ТКФ (α-трикальцийфосфат) - карточка PDF2 №29-359 (в); ГАП (гидроксиапатит) - карточка PDF2 №9-432.
На фигуре 2 показана микроструктура материалов после гидролитической конверсии, содержавших в исходной порошковой смеси 10 мас. % СаО (а), и 30 мас. % СаО (б).
Осуществление изобретения
Пример 1. Подготовка компонентов исходной шихты
Для получения 100 г α-трехкальциевого фосфата (α-ТКФ) порошковую смесь, включающую безводный гидрофосфат кальция (43,87 г) и карбоната кальция (32,26 г), взятые в стехиометрическим соотношении, обжигают при температуре 1400°C в течение 1,5 часа. Безводный гидрофосфат кальция CaHPO4 в количестве 100 г получают из 126,46 г бушита CaHPO4·2H2O после сушки в течение 11 часов при температуре 260°C. Бушит CaHPO4 2Н2О в количестве 132,15 г получают при взаимодействии 0,5 л 1,5М водного раствора 4-х-водного нитрата кальция и 0,5 л 1,5М водного раствора гидрофосфата аммония. Для приготовления 0,5 л 1,5М водного раствора 4-х-водного нитрата кальция 177,11 г соли растворяют в 0,5 л дистиллированной воды. Для приготовления 0,5 л 1,5М водного раствора гидрофосфата аммония 99,05 г растворяют в 0,5 л дистиллированной воды. Полученные растворы смешивают при интенсивном перемешивании и доводят до состояния однородной массы. Полученную суспензию фильтруют для удаления маточного раствора и промывают дистиллированной водой. Полученную массу сушат для получения безводного гидрофосфата кальция.
Для получения 100 г оксида кальция 178,48 г порошка карбоната кальция прокаливают при температуре 1050°C в течение 11 часов, который затем хранили в эксикаторе.
Пример 2. Подготовка растворов гидрокарбоната натрия, калия и аммония, которые используют в качестве жидкости затворения и в качестве среды для проведения гидролитической конверсии
Для приготовления 1 л 0,9 М раствора 71,2 г гидрокарбоната аммония растворяют в необходимом количестве дистиллированной воды при постоянном перемешивании. Для приготовления 1 л 1 М раствора 79,1 г гидрокарбоната аммония растворяют в необходимом количестве дистиллированной воды при постоянном перемешивании. Для приготовления 1 л 1,1 М раствора 87,0 г гидрокарбоната аммония растворяют в необходимом количестве дистиллированной воды при постоянном перемешивании.
Для приготовления 1 л 0,9 М раствора 75,6 г гидрокарбоната натрия растворяют в необходимом количестве дистиллированной воды при постоянном перемешивании. Для приготовления 1 л 1 М раствора 84 г гидрокарбоната натрия растворяют в необходимом количестве дистиллированной воды при постоянном перемешивании. Для приготовления 1 л 1,1 М раствора 92,4 г гидрокарбоната натрия растворяют в необходимом количестве дистиллированной воды при постоянном перемешивании.
Для приготовления 1 л 0,9 М раствора 90,1 г гидрокарбоната калия растворяют в необходимом количестве дистиллированной воды при постоянном перемешивании. Для приготовления 1 л 1 М раствора 100,1 г гидрокарбоната калия растворяют в необходимом количестве дистиллированной воды при постоянном перемешивании. Для приготовления 1 л 1,1 М раствора 110,1 г гидрокарбоната калия растворяют в необходимом количестве дистиллированной воды при постоянном перемешивании.
Пример 3.
Для получения 100 г композиционного материала 10 г оксида кальция смешивают с 90 г порошка α-трехкальциевого фосфатата (см. пример 1) посредством совместного помола в шаровой мельнице в течение 15 минут под слоем ацетона. 80 мл 0,9 М раствора гидрокарбоната аммония (см. пример 2) добавляют к полученной порошковой смеси и перемешивают до получения однородной субстанции, после чего ее формуют в прессформе при удельном давлении прессования 400 МПа. Полученные прессовки сушат на воздухе в течение 24 часов, после чего помещают в 800 мл раствора гидрокарбоната аммония, после чего выдерживают при температуре 30°C в течение 120 часов. Полученные в результате материалы извлекают из раствора, удаляют с их поверхности влагу и сушат при температуре 58°C в течение 10 часов.
Пример 4
Для получения 100 г конечного материала 20 г. оксида кальция смешивают с 80 г порошка α-трехкальциевого фосфатата (см. пример 1) посредством совместного помола в шаровой мельнице в течение 15 минут под слоем ацетона. 90 мл 1 М раствора гидрокарбоната натрия (см. пример 2) добавляют к полученной порошковой смеси и перемешивают до получения однородной субстанции, после чего ее формуют при помощи разборной пресс-формы (либо нескольких пресс-форм) под давлением 250 МПа в течение 5 минут. Полученные прессовки сушат на воздухе в течение 24 часов, после чего помещают в 1200 мл раствора гидрокарбоната натрия, после чего выдерживают при температуре 45°C в течение 54 часов. Полученные в результате материалы извлекают из раствора, удаляют с их поверхности влагу и сушат при температуре 60°C в течение 11 часов.
Пример 5
Для получения 100 г конечного материала 30 г оксида кальция смешивают с 70 г порошка α-трехкальциевого фосфатата (см. пример 1) посредством совместного помола в шаровой мельнице в течение 15 минут под слоем ацетона. 100 мл 1,1 М раствора гидрокарбоната калия (см. пример 2) добавляют к полученной порошковой смеси и перемешивают до получения однородной субстанции, после чего ее формуют при помощи разборной пресс-формы (либо нескольких пресс-форм) под давлением 100 МПа в течение 5 минут. Полученные прессовки сушат на воздухе в течение 24 часов, после чего помещают в 1600 мл раствора гидрокарбоната калия, после чего выдерживают при температуре 62°C в течение 12 часов. Полученные в результате материалы извлекают из раствора, удаляют с их поверхности влагу и сушат при температуре 62°C в течение 12 часов.
Таким образом, экспериментальные данные показывают, что применение заявленного способа с использованием гидролитической конверсии позволяет получать композиционные материалы для замещения костных дефектов, фазовый состав которых представлен фазами, подверженными биорезобции. При этом карбоната кальция в составе материала при его резорбции является источником необходимых при регенерации костной ткани ионов Са2+ в качестве обязательных и CO3 2- в качестве модифицирующих структуру биогенного апатита, а также агентом, способным поддержать анаэробное дыхание в зоне образования новой костной ткани. Полученные материалы обладают плотностью 2,1-2,3 г/см3, прочностью на сжатие 80-100 МПа и размером зерен 100-500 нм (Фигура 2).
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ПОРОШКОВОГО МАТЕРИАЛА НА ОСНОВЕ КАРБОНАТГИДРОКСИАПАТИТА И БРУШИТА | 2014 |
|
RU2546539C1 |
| СПОСОБ ПОЛУЧЕНИЯ КЕРАМИЧЕСКОГО КОМПОЗИЦИОННОГО БИОДЕГРАДИРУЕМОГО МАТЕРИАЛА НА ОСНОВЕ ДВОЙНОГО ФОСФАТА КАЛИЯ КАЛЬЦИЯ | 2008 |
|
RU2395303C1 |
| СПОСОБ ПОДГОТОВКИ ШИХТЫ ДЛЯ ПОЛУЧЕНИЯ КЕРАМИЧЕСКОГО БИОДЕГРАДИРУЕМОГО МАТЕРИАЛА | 2010 |
|
RU2456253C2 |
| СПОСОБ ПОЛУЧЕНИЯ КЕРАМИЧЕСКОГО БИОДЕГРАДИРУЕМОГО МАТЕРИАЛА НА ОСНОВЕ ФОСФАТОВ КАЛЬЦИЯ И НАТРИЯ | 2007 |
|
RU2372891C2 |
| Самосхватывающаяся композиция для получения кальцийфосфатного матрикса для замещения костных дефектов опорно-двигательной системы человека и способ получения кальцийфосфатного матрикса на её основе | 2021 |
|
RU2756020C1 |
| Способ биомиметического синтеза Sr-содержащего карбонатгидроксилапатита, допированного брушитом | 2017 |
|
RU2650637C1 |
| Способ биомиметического синтеза Sr - содержащего карбонатгидроксилапатита, модифицированного брушитом | 2017 |
|
RU2640924C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПОРИСТОГО МАТЕРИАЛА НА ОСНОВЕ ФОСФАТА КАЛЬЦИЯ | 2008 |
|
RU2392007C2 |
| СПОСОБ ПОЛУЧЕНИЯ НАНОКРИСТАЛЛИЧЕСКОГО СИЛИКАТЗАМЕЩЕННОГО КАРБОНАТГИДРОКСИАПАТИТА | 2014 |
|
RU2555337C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПОРИСТОГО ПИРОФОСФАТА КАЛЬЦИЯ | 2012 |
|
RU2537615C2 |

Изобретение относится к медицине и биотехнологии. Описан способ получения композиционного материала для замещения костных дефектов, включающий: подготовку порошковой смеси, содержащей порошок альфа-Ca3(PO4)2; подготовку пасты при добавлении жидкости затворения в виде водного раствора, содержащего карбонат-ионы; формование образцов или изделий из пасты; гидролитическую обработку образцов или изделий в водном растворе, содержащем карбонат-ион, и сушку. Согласно изобретению порошковая смесь дополнительно содержит оксид кальция при соотношении массы СаО к массе альфа-Ca3(PO4)2 в интервале 0,11-0,43, концентрация [СО3 2-] в жидкости затворения составляет 0,9М-1,1М при соотношении жидкость затворения/масса порошка в интервале 0,8-1,0, формование осуществляют при давлении прессования 100-450 МПа, а гидролитическую конверсию проводят в водном растворе с концентрацией [СО3 2-] в интервале 0,9М-1,1М в течение 12-120 часов при температуре в интервале 30-60°C. В композиционном материале содержание кальцита, обладающего повышенной скоростью резорбции, составляет 17-53 мас. %, размер зерен в полученном материале 100-500 нм, плотность лежит в интервале 2,1-2,3 г/см3, а прочность составляет 80-100 МПа. 2 з. п. ф-лы, 2 ил., 4 табл., 5 пр.
1. Способ получения композиционного материала для замещения костных дефектов с использованием гидролитической конверсии, включающий подготовку порошковой смеси, содержащей порошок альфа-Ca3(PO4)2; подготовку пасты при добавлении жидкости затворения в виде водного раствора, содержащего карбонат-ионы; формование материала из пасты; гидролитическую обработку сформованного материала из пасты в водном растворе, содержащем карбонат-ион, и сушку, отличающийся тем, что порошковая смесь дополнительно содержит оксид кальция при соотношении массы CaO к массе альфа-Ca3(PO4)2 в интервале 0,11-0,43, концентрация [СО3 2-] в жидкости затворения составляет 0,9М-1,1М при соотношении «жидкость затворения/масса порошка» в интервале 0,8-1,0, формование осуществляют при давлении прессования 100-450 МПа, а гидролитическую конверсию проводят в водном растворе с концентрацией [СО3 2-] в интервале 0,9М-1,1М в течение 12-120 часов при температуре раствора в интервале 30-60°C.
2. Способ по п. 1, отличающийся тем, что для сформованного материала из пасты, изготовленного из 100 г порошковой смеси, для проведения гидролитической конверсии используют 800-1200 мл раствора, содержащего карбонат-ион.
3. Способ по п. 1, отличающийся тем, что в качестве растворимых соединений, являющихся источником карбонат-иона, используют гидрокарбонаты аммония, натрия, калия.
| ФИЛИППОВ Я.Ю | |||
| и др., Реакционно-связанные резорбируемые фосфатные биоматериалы: получение и испытания in vitro, Стекло и керамика, 2013, 8, с | |||
| Скоропечатный станок для печатания со стеклянных пластинок | 1922 |
|
SU35A1 |
| КОМПОЗИЦИОННЫЙ МАТЕРИАЛ ДЛЯ ЗАМЕЩЕНИЯ КОСТНОЙ ТКАНИ | 2004 |
|
RU2260402C1 |
| ФОСФАТНЫЙ ЦЕМЕНТ | 2002 |
|
RU2207106C1 |
Авторы
Даты
2016-10-10—Публикация
2015-07-29—Подача