Изобретение относится к химической технологии, а именно к способу очистки промышленных сточных вод от гипохлорит-иона, образующегося в процессе хлорирования гидрооксидов лития, натрия, кальция.
Известны способы очистки от гипохлорит-иона путем разложения гипохлорита с использованием реагентных восстановительных процессов и каталитических способов разложения гипохлорит-иона. Так, например, известен способ обезвреживания водного раствора гипохлорит-иона с использованием технического лигносульфоната - отхода производства целлюлозы, описанный в патенте РФ 2073637, кл. С01В 11/06, опубл. 20.02.97 г. Такие варианты осуществления процесса разложения требуют значительного расхода восстановителей. К недостаткам также можно отнести необходимость обезвреживания сточных вод от вторичных загрязнений.
Этих недостатков лишены каталитические способы разложения гипохлорита. Из каталитических процессов заслуживающим внимания является способ «Calcium aluminate cement based catalyst», Hancock, Frederick Ernest. United States Patent 6,020,285 Hancock February 1, 2000, в котором разложение гипохлорит-иона идет сферическими частицами алюминиевого цемента, на который нанесены оксиды никеля и кобальта. Такой катализатор показал большую активность. Однако определенные трудности представляет изготовление самого катализатора.
Известен способ [авт.св. СССР 311867, кл. С01В 11/06, опубл. 19.08.71], где обезвреживания растворов гипохлорита (гипохлорит-иона) ведут путем пропускания нагретого до температуры 80-100°С раствора через слой сыпучего материала, например кварцевого песка, в который введен катализатор - гидроксид никеля или кобальта. Однако, необходимость регулярной регенерации катализатора вызывает существенные трудности при организации непрерывного процесса.
Известен способ «Способ каталитического разложения гипохлорита» [патент RU 2091296 МПК С01В 11/06, C02F 1/70, 1997 г. ], заключающийся в каталитическом разложении гипохлорит-ионов в потоке жидкости, с выделением кислорода. Жидкость контактирует со слоем катализатора, расположенным в двух последовательно соединенных слоях, которые находятся в каскаде со стояками. Поток жидкости и выделяющийся в процессе разложения гипохлорит-иона кислород находятся в противотоке. Часовая объемная скорость потока жидкости, содержащей гипохлорит-ионы, который течет через слой катализатора, составляет 0,1-10 ч-1, температура процесса 10-90°С. В способе используют катализатор « Экструдат А» по ЕР 0397342. Катализатор содержит глиноземистый цемент и, по меньшей мере, один оксид металла группы VIII, выбранный из никеля и кобальта, в количестве 10 до 70% от массы оксида, при общей пористости от 15 до 35 нм. Использование отечественного никельсодержащего катализатора марки ГИПА-3-6Н сопровождается разрушением катализатора и уносом, что приводит к значительному расходу катализатора, кроме того, катализатор имеет небольшую скорость разложения гипохлорит-иона.
Наиболее близким по ряду технических приемов и достигаемому результату к предлагаемому способу является «Способ каталитического разложения гипохлорита» [патент RU №2203850, МПК С01В 11/06,C02F 1/72, 2001 г.]. Способ включает контактирование потока жидкости, содержащей гипохлорит-ионы, с катализатором в противотоке с выделяющимся в процессе разложения газообразным кислородом, при температуре 20-90°С. При этом поток жидкости после контактирования с катализатором дополнительно контактирует с зернистым фильтром, на котором задерживаются осколки частиц катализатора, образующиеся в ходе процесса. В качестве катализатора используют промышленный катализатор ГИАП-3-6Н или ГИАП-8 - оксид никеля, диспергированный на оксиде алюминия. В качестве зернистого фильтра используют речной песок зернением 0,2-2 мм. Недостатками вышеизложенного изобретения являются низкая скорость процесса разложения (время контактирования раствора с катализатором - до 16 часов), высокая температура (до 90°С) проведения процесса, кроме того, эти катализаторы ГИАП-3-6Н, ГИАП-8 постепенно разрушаются, что ведет к большому расходу катализатора.
Задачей настоящего изобретения является создание эффективного каталитического способа очистки от гипохлорит-ионов с достаточно большой скоростью разложения, при более низких температурах с техническим результатом - сокращение времени контактирования раствора гипохлорит-иона с катализатором, увеличение скорости разложения гипохлорит-ионов и упрощение процесса очистки (без дополнительного контактирования раствора с зернистым фильтром по прототипу) и при более низких температурах.
Поставленная задача достигается тем, что в способе каталитического разложения гипохлорит-иона, включающего контактирование раствора, содержащего гипохлорит-ионы с никельсодержащим катализатором в виде частиц, с выделением газообразного кислорода, при этом в качестве катализатора используют основной карбонат никеля, диспергированный на нанопористом углеродном композиционной материале, содержащем в качестве связующего фторопластовую суспензию при соотношении компонентов, мас. %: нанопористый углеродный композиционный материал 49-54, фторопластовая суспензия 5-9, основной карбонат никеля - остальное, разложение раствора гипохлорита лития ведут при температуре 32-67°С.
Отличительные признаки изобретения: катализатор, температура разложения.
Известный в настоящее время технологический процесс получения хлорида лития предполагает, что протекание процесса идет по реакции взаимодействия (1)
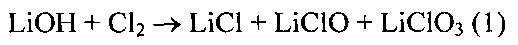
Допустимая концентрация оксихлоридов лития в технологическом растворе LiCl составляет не более 0.5% LiClO и менее 5% LiClO3. Для предотвращения образования LiClO3 в раствор LiCl добавляют катализатор, при котором реакция хлорирования гидроксида лития протекает с образованием LiClO (2) и последующим его разложением с выделением О2 (3).
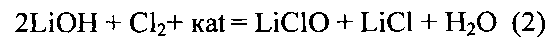
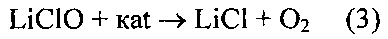
Периодически, с потерей катализатором активности, возникает необходимость его удаления путем фильтрации. Процесс фильтрации чрезвычайно медленный, если отработанный катализатор представляет собой мелкодисперсный или гелеобразный осадок.
В предлагаемом способе в качестве катализатора используют основной карбонат никеля, диспергированный на гранулированном нанопористом углеродном композиционной материале (НУМС), содержащем в качестве связующего фторопластовую суспензию (Ф4Д). НУМС представляет собой нанопористый углеродный композиционный материал (L.М. Levchenko and V.S. Golovizin Investigation of texture characteristics of the Technosorb carbon material in the oxidation process // Journal of Structural Chemistry, 2010, V. 51, Suppl. S. 92-95) [6], который характеризуется тем, что состоит из частиц размера 1-16 мм, с удельной поверхностью по адсорбции азота 300-600 м2/г, содержанием углерода 99.5%, имеющего характерное распределение пор с максимумом, приходящимся на поры с размером 4 нм. Развитая поверхность углеродного материала, преобладание нанопор, позволяет использовать НУМС в качестве матрицы для диспергирования основного карбоната никеля на развитой углеродной поверхности в каталитически достаточном количестве. Использование фторопластовой суспензии (Ф4Д) способствует обволакиванию частиц НУМС, защищая их от разрушения в процессе разложения гипохлорит-иона и прилипания частиц основного карбоната никеля на поверхность закрытых суспензией (обволоченных) частиц НУМС. Основной карбонат никеля не растворяется в среде гипохлорит-иона, что позволяет избегать попадания Ni2+ в раствор. Катализатор при этом хорошо фильтруется, так как состоит из гранулированных частиц, что важно при его фильтрации и его регенерации (восстановлении каталитической активности). Заявленное соотношение компонентов является оптимальным. Количество основного карбоната никеля ((NiOH)2СО3) определяется характеристикой НУМС, взятого в качестве основы, для диспергирования основного карбоната никеля и прилипанием его частиц на поверхности НУМС. Экспериментальные данные показали, что оптимальная температура процесса разложения гипохлорит-иона составляет 32-67°С (в прототипе 80-90°С и скорость разложения меньше).
Способ осуществляют следующим образом. Для исследований берут нанопористый углеродный композиционный материал (НУМС), имеющий фракцию 0,7-1,5 мм с диаметром пор 4 нм, удельной поверхностью 350 м2/г, пикнометрической плотностью 2,08 г/см3, объемом свободных пор 63,9 об.%. НУМС пропитывают фторопластовой разбавленной суспензией (Ф4Д), после полного поглощения материалом фторопластовой суспензии, материал сушат, затем вводят порошок основного карбоната никеля (сухой), перемешивают с массой углеродного материала НУМС, пропитанного фторопластовой суспензией (Ф4Д) до полного прилипания, так чтобы не было остатков неприлипшего основного карбоната никеля, и подсушивают в сушильном шкафу. В реактор с обогреваемой рубашкой заливают водно-щелочной раствор гипохлорита (гипохлорит-иона) вводят катализатор и разложение ведут при 32-67°С. Процесс контролируют по объему выделенного кислорода (по окончании его выделения). При этом процесс разложения можно вести в реакторе без противотока, так и в реакторе, обеспечивающем противоток раствора гипохлорит-иона потоку выделяющегося кислорода. Затем раствор фильтруют, катализатор хорошо фильтруется, т.к. катализатор находится в виде частиц и карбонат никеля не растворим в щелочной среде. Определяют титрованием тиосульфатом натрия концентрацию гипохлорит-иона в растворе на выходе из реактора.
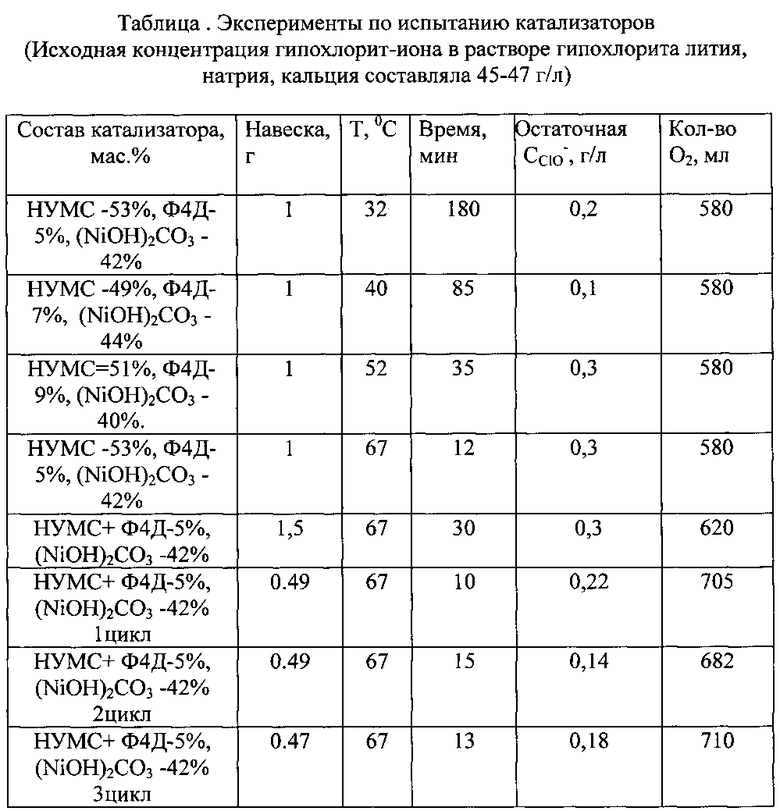
Экспериментальные данные по заявленному способу каталитического разложения гипохлорит-иона приведены в таблице, из которых видно, что каталитическая активность используемого катализатора при варьировании содержания (NiOH)2СО3 и Ф4Д в заявляемом интервале температур дает эффективную очистку от гипохлорит-ионов. Показано, что остаточная концентрация гипохлорит-иона в растворе после разложения катализатором составляет 0,1-0,3 г/л, что соответствует требованиям, предъявляемым химическим производством к процессу получения хлоридов щелочных металлов. Были проведены эксперименты по эффективности работы катализатора в циклах. Показано, что эффективность работы катализатора не изменилась при проведении 3-х циклов испытаний по разложению гипохлорит-иона в растворе.
Пример 1.
Берут 50 мл водно-щелочного раствора с содержанием 47 г/л гипохлорита лития заливают в химический реактор с обогреваемой рубашкой, вводят 1 г, приготовленного катализатора при соотношении, мас. %: НУМС - 53%, Ф4Д - 5%, основной карбонат никеля = 42% (по никелю = 11,7%). Разложение гипохлорит-иона проводят при температуре 67°С в течение 12 мин с выделением кислорода, который замеряют по объему в мл. Затем раствор фильтруют со скоростью 20,6*10-3 мл/мин*см2. Концентрацию гипохлорита лития в растворе на выходе из реактора определяют титрованием тиосульфатом натрия. Концентрация гипохлорита лития на выходе составляет 0,3 г/л, степень разложения гипохлорита составляет 99,4%.
Пример 2.
Берут 50 мл водно-щелочного раствора с содержанием 47 г/л гипохлорита лития заливают в химический реактор с обогреваемой рубашкой, вводят 1 г приготовленного катализатора при соотношении, мас. %: НУМС - 49%, Ф4Д - 7%, основной карбонат никеля = 44%. Разложение гипохлорит-иона проводят при температуре 40°С в течение 85 мин с выделением кислорода, который замеряют по объему в мл. Затем раствор фильтруют со скоростью 20,6*10-3 мл/мин*см2. Концентрацию гипохлорита лития в растворе на выходе из реактора определяют титрованием тиосульфатом натрия. Концентрация гипохлорита лития на выходе составляет 0,1 г/л, степень разложения гипохлорита составляет 99,8%.
Пример 3.
Берут 50 мл водно-щелочного раствора с содержанием 45 г/л гипохлорита лития заливают в химический реактор с обогреваемой рубашкой, вводят 1 г приготовленного катализатора при соотношении, мас. %: НУМС - 53%, Ф4Д - 5%, основной карбонат никеля = 42% (по никелю = 11,7%). Разложение гипохлорит-иона проводят при температуре 32°С в течение 180 мин с выделением кислорода, который замеряют по объему в мл. Концентрация гипохлорита лития на выходе составляет 0,2 г/л, степень разложения гипохлорита составляет 99,6%.
Пример 4.
Водно-щелочной раствор, содержанием 47 г/л гипохлорита лития. Берут 50 мл раствора, заливают в химический реактор с обогреваемой рубашкой, добавляют 1 г катализатора при соотношении, мас. %: НУМС=51%, Ф4Д=9%, основной карбонат никеля = 40%. Разложение гипохлорита проводят при температуре 52°С в течение 35 мин с выделением кислорода, который замеряется по объему в мл. Концентрация гипохлорита лития в растворе на выходе из реактора определялась титрованием тиосульфатом натрия и составила 0,3 г/л. Степень разложения гипохлорита 99,4%.
Пример 5.
Водно-щелочной раствор, содержанием 45 г/л гипохлорита натрия. Берут 50 мл раствора, заливают в химический реактор с обогреваемой рубашкой, добавляют 1 г катализатора при соотношении, мас. %: НУМС - 51%, Ф4Д - 9%, (NiOH)2CO3 - 40%. Разложение гипохлорита натрия проводят при температуре 52°С в течение 35 мин. Концентрация гипохлорита натрия в растворе на выходе из реактора определялась титрованием тиосульфатом натрия и составила 0,3 г/л. Степень разложения гипохлорита 99,4%.
Пример 6.
50 мл водно-щелочного раствора, содержащего 47 г/л гипохлорита кальция, заливают в химический реактор с обогреваемой рубашкой, добавляют 1,5 г катализатора при соотношении, мас. %: НУМС - 51%, Ф4Д - 9%, (NiOH)2CO3 - 40%. Разложение гипохлорита натрия проводят при температуре 52°С в течение 35 мин. Концентрация гипохлорита натрия в растворе на выходе из реактора определялась титрованием тиосульфатом натрия и составила 0,3 г/л. Степень разложения гипохлорита 99,4%.
Таким образом, в сравнении с прототипом при такой же концентрации гипохлорит-иона в заявляемом изобретении скорость разложение гипохлорит-иона выше, чем в прототипе в 1,5 раза при меньшем количестве катализатора (в 10 раз) и температуре разложения (в прототипе разложение при 80°С).
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ КАТАЛИТИЧЕСКОГО РАЗЛОЖЕНИЯ ГИПОХЛОРИТА | 2001 |
|
RU2203850C2 |
| СПОСОБ КАТАЛИТИЧЕСКОГО РАЗЛОЖЕНИЯ ГИПОХЛОРИТА | 1992 |
|
RU2091296C1 |
| СПОСОБ ПОЛУЧЕНИЯ КОМПОЗИТНОГО МАТЕРИАЛА СИСТЕМЫ УГЛЕРОД-НИКЕЛЬ | 2014 |
|
RU2570672C1 |
| СПОСОБ ПОЛУЧЕНИЯ ХЛОРИДА ЛИТИЯ | 1996 |
|
RU2114058C1 |
| СПОСОБ ПОЛУЧЕНИЯ ХЛОРИДА ЛИТИЯ | 2005 |
|
RU2300497C1 |
| СПОСОБ МОДИФИЦИРОВАНИЯ УГЛЕРОДНЫХ НАНОТРУБОК | 2012 |
|
RU2528985C2 |
| СПОСОБ ПОЛУЧЕНИЯ ПОЛИБУТАДИЕНА | 2007 |
|
RU2436802C2 |
| Катализатор для термолиза перхлората аммония в виде металл-оксид-углеродного композиционного материала | 2023 |
|
RU2808979C1 |
| Способ получения хлора и щелочи | 1980 |
|
SU1030424A1 |
| СЛОИСТЫЙ ГИДРОКСИД СО СТРУКТУРОЙ ГИДРОТАЛЬКИТА, СОДЕРЖАЩИЙ НИКЕЛЬ В СТЕПЕНИ ОКИСЛЕНИЯ +3, И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2013 |
|
RU2540402C1 |
Изобретение относится к химической технологии, а именно к способу очистки промышленных сточных вод от гипохлорит-ионов, образующихся в процессе хлорирования гидрооксидов лития, натрия, кальция. Способ каталитического разложения гипохлорит-иона включает контактирование раствора, содержащего гипохлорит-ионы, с никельсодержащим катализатором в виде частиц, при температуре 32-67°C, с выделением газообразного кислорода. При этом в качестве никельсодержащего катализатора используют основной карбонат никеля, диспергированный на нанопористом композиционном углеродном материале, содержащем в качестве связующего фторопластовую суспензию при соотношении компонентов, мас. %: нанопористый композиционный углеродный материал 49-54, фторопластовая суспензия 5-9, основной карбонат никеля - остальное. Изобретение обеспечивает эффективную очистку от гипохлорит-ионов с высокой скоростью разложения и при более низких температурах. 1 табл., 6 пр.
Способ каталитического разложения гипохлорит-иона, включающий контактирование раствора, содержащего гипохлорит-ионы, с никельсодержащим катализатором в виде частиц, с выделением газообразного кислорода, отличающийся тем, что в качестве катализатора используют основной карбонат никеля, диспергированный на нанопористом композиционном углеродном материале, содержащем в качестве связующего фторопластовую суспензию при соотношении компонентов, мас. %: нанопористый композиционный углеродный материал 49-54, фторопластовая суспензия 5-9, основной карбонат никеля - остальное, разложение раствора гипохлорит-иона ведут при температуре 32-67°C.
| СПОСОБ КАТАЛИТИЧЕСКОГО РАЗЛОЖЕНИЯ ГИПОХЛОРИТА | 2001 |
|
RU2203850C2 |
| СПОСОБ КАТАЛИТИЧЕСКОГО РАЗЛОЖЕНИЯ ГИПОХЛОРИТА | 1992 |
|
RU2091296C1 |
| 0 |
|
SU311867A1 | |
| СПОСОБ ОБЕЗВРЕЖИВАНИЯ ПУЛЬПЫ ГИПОХЛОРИТА КАЛЬЦИЯ | 1994 |
|
RU2073637C1 |
| US 6020285 A, 01.02.2000. | |||
Авторы
Даты
2016-11-10—Публикация
2015-06-16—Подача