Область техники, к которой относится изобретение
Изобретение относится к области биотехнологии и будет использовано в пищевой промышленности. Более конкретно, изобретение относится к штаммам микроорганизмов L. plantarum МСС1 и L. gasseri MCC2 и их применению для уменьшения аллергии на молоко и симптомов раздражения нижних мочевыводящих путей, сопутствующих доброкачественной гиперплазии предстательной железы, а также окислительного стресса и воспаления, ассоциированных с ними.
Уровень техники
Молочнокислые бактерии в течение долгого времени используются при производстве полезных для здоровья пищевых продуктов, например в качестве заквасочных культур. Наиболее распространенным способом является применение молочнокислых бактерий в функциональных пищевых продуктах. Функциональные пищевые продукты представляют собой пищевые продукты, которые в дополнение к обычной пищевой ценности содержат добавочные натуральные компоненты, которые оказывают полезное влияние на некоторые функции организма или снижают риск возникновения заболеваний.
Способы, включающие в себя применение специально биологически отобранных живых молочнокислых бактерий, которые на следующем технологическом этапе умерщвляют пастеризацией, менее широко использовались при приготовлении пищевых продуктов. Это означает, что конечный продукт не содержит живых молочнокислых бактерий, но при предварительной обработке, надлежащей технологической схеме и необходимых добавках созданный продукт имеет целенаправленный биологический эффект.
Аллергия на молоко и ее уменьшение
Инфекции, проблемы, связанные с воспалением, аллергией и окислительным стрессом, например пищевые аллергии, симптомы, связанные с мочеиспускательными путями (например, расстройства мочеиспускания, ассоциированные с заболеваниями предстательной железы), становятся все более экономически обременительными для общества. Например, до 4% населения страдает пищевыми аллергиями, и в США 100-200 случаев смерти напрямую связаны с пищевой аллергией. Пищевые аллергии (включая аллергическую реакцию на коровье молоко) представляют собой особенно серьезную проблему для детей. Применение молочных продуктов в детском питании необходимо для нормального роста и развития детей. Решение проблемы аллергенности пищи является очень сложным, поскольку невозможно создать продукты, которые абсолютно свободны от компонентов, вызывающих аллергическую реакцию, и при этом имеют очень высокий уровень хорошего биологического качества. Результатом недавних обсуждений в ООН, ВПО и ВОЗ стала следующая декларация: безаллергенность - время для ясности; тезис: не существует действующего законодательства, позволяющего декларировать полное отсутствие аллергенов. Таким образом, любые технологические идеи/решения, приводящие к созданию более гипоаллергенных продуктов, которые позволят уменьшить число случаев аллергических реакций у детей по меньшей мере на несколько процентов, будут иметь высокую ценность. Каждый процент, на который уменьшается число случаев аллергической реакции, очень важен в итоге/в долгосрочной перспективе, поскольку любой успех в области аллергологии, позволяющий снизить аллергенность пищевых продуктов, имеет значительные социально-экономические результаты (в том числе повышение качества жизни у детей и взрослых и снижение затрат на лечение).
Аллергенность молочных продуктов определяется белками, но выделение так называемого основного аллергена является затруднительным (Encyclopedia of Food Sciences and Nutrition (EFSN) AP, 2003, Wal J.M. (2004) Bovine Milk Allergenicity. Ann.Allergy Asthma Immunol., 93, S2-11). Тем не менее, аллергические реакции на равном уровне вызываются казеином и бета-лактоглобулином. Аллергия на коровье молоко связана главным образом с α-казеином и β-лактоглобулином (Host A. (2002). Frequency of cow′s milk allergy in childhood. Ann Allergy Immunol 89 (Suppl 1): 33-7; EFSN, 2003). У многих детей с аллергией на молоко наблюдается реакция на альфа-казеин (Hill D.J, Firer M.A, Shelton M.J et al. (1986) Manifestation of milk allergy in infancy: clinical and immunologic findings. J Pediatr 109: 270-6; EFSN, 2003, Vandenplas Y, Brueton M, Dupont C, Hill D, Isolauri E, Koletzko S, Oranje AP, Staiano A. (2007) Guidelines for the diagnosis and management of cow′s milk protein allergy in infants. Arch Dis Child. 92: 902-908).
Казеин состоит из следующих элементов: α-S1 (основной аллерген), α-S2, β- и κ-казеин, где преобладают α-S1 и β-казеин. Ферментный гидролиз молочных белков снижает их аллергенность. При частичном гидролизе молочных белков формируются длинные пептиды, а более полный гидролиз приводит к образованию смеси длинных и коротких пептидов и аминокислот. Даже глубокий пепсин-трипсиновый гидролиз не приводит к получению безаллергенных веществ, поскольку аллергическая реакция может быть вызвана незначительными количествами иммунореактивных компонентов нативного белка. Таким образом, лишь подход, основанный на глубоком гидролизе, обеспечил некоторые возможности, однако он не обеспечивает окончательного решения, даже в случае с гидролизатами белков молочной сыворотки (Businco L, Cantani A, Longhi MA, Giampietro PG (1989) Anaphylactic reactions to a cow′s milk whey protein hydrolysate (Alfa-Ré, Nestlé) in infants with a cow′s milk allergy. Ann Allergy. 62 (4): 333-5.; Sampson НА, James MJ, Bernhisel-Broadbent J. (1992) Safety of an amino-derived infant formula in children allergic to cow milk. Pediatrics. 90, 463-465). Таким образом, необходимы новые подходы к уменьшению аллергии на коровье молоко, в связи с чем перспективную тенденцию к значительному уменьшению проблем, связанных с аллергией, представляет направленный гидролиз вызывающих аллергию молочных белков штаммом(ами) микроорганизмов, придающих дополнительную ценность продуктам.
Гидролиз молочных белков при помощи молочнокислых бактерий и добавок уже описан ранее. В патенте ЕЕ 03424 (заявка на патент WO 9700078, Valio Oy) описано применение штамма L. rhamnosus ATCC 53103 (LGG) для приготовления препарата гидролизата белка, причем белки гидролизуют пепсином и трипсином. Применение LGG для снижения риска аллергии рассматривается в нескольких изобретениях Nestec SA. В патенте ЕР 1296694 описано применение LGG для снижения риска атопических заболеваний у детей. В заявке на патент WO 2008116907 описано применение бифидобактерий и LGG, L. rhamnosus CGMCC 1.3724, L. reuteri ATCC 55730 и L. paracasei CNCM I-2116 для снижения риска у грудных детей, рожденных при помощи кесарева сечения, и в том числе с применением частично (2-20%) гидролизованных белков. В патентной заявке WO 03099037 Nestec SA описана протеолитическая система молочнокислых бактерий и пищевого продукта, содержащего Bifidobacterium lactis ATCC 27536 для применения в том числе для уменьшения пищевой аллергии, в то время как бактерии могут быть инактивированы или мертвы. В патенте ЕЕ 04724 (заявка на патент WO 9929833, Arla Foods) описано применение L. paracasei subsp. paracasei, в том числе для устранения атопических проблем у детей. В патенте ЕР 1175156 (Bioferme OY) описан пастеризованный зерновой напиток, содержащий микроорганизмы. В заявке на патент CN 101427782 (Min Zhao) описан содержащий бифидобактерий кукурузный напиток, который производят с помощью ферментации, и в котором бактерии инактивируют в ферментированном продукте. В концентрате белка молочной сыворотки (WPC) максимальный достигнутый уровень гидролиза β-лактоглобулина составил 21% (M. Pescuma et al (2007), Hydrolysis of whey proteins by L. acidophilus, Streptococcus thermophilus and L. delbrueckii ssp. bulgaricus grown in a chemically defined medium, Journal of Appl Microbiol, 103, 5, 1738-1746). Гидролиз молочных белков (2-32%) двумя микроорганизмами с целью получения продукта с хорошими вкусовыми качествами описан в европейском патенте ЕР 1383394 (New Zealand Dairy Board), причем один предлагаемый микроорганизм представляет собой Macrococcus, Micrococcus, Enterococcus, Staphylococcus, Brevibacterium, Anthrobacker или Corynebacterium, предпочтительно Macrococcus caseolyticus, a другой микроорганизм представляет собой молочнокислую бактерию Lactococcus, Lactobacillus, Pediococcus или Leuconostoc, и ферментацию останавливают путем удаления или уничтожения микроорганизмов. В заявке на патент Японии JP 7203844 (Morinaga Milk Industry Co) описан частичный гидролиз молочной сыворотки (30%) с помощью фермента, получаемого от микроорганизма Bacillus subtilis, трипсина и папаина.
Проблемы с предстательной железой и их уменьшение
С предстательной железой может быть связано несколько проблем: нарушение проходимости мочевыводящих путей и раздражение и боль или дискомфорт в области малого таза. Проблемы с предстательной железой, в особенности связанные с мочеиспусканием, являются очень распространенными и снижают качество жизни у большого числа мужчин. По оценкам, гиперплазия предстательной железы (доброкачественная гиперплазия предстательной железы - ВРН) встречается приблизительно у половины мужчин в возрасте 50 лет и приблизительно у 70% мужчин старше 70 лет. Симптомы в области нижних мочевыводящих путей (LUTS), сопутствующие доброкачественной гиперплазии предстательной железы, включают в себя симптомы раздражения и непроходимости (связанные с опорожнением), которые оценивают по международной шкале простатических симптомов (IPSS). Любая возможность облегчения затрудненного мочеиспускания у мужчин нефармацевтическими средствами будет иметь значительную ценность, и наилучшей возможностью было бы создание нового пищевого продукта с таким эффектом.
Применение молочнокислых бактерий в терапевтических композициях для лечения и облегчения мочеполовых инфекций, в том числе инфекции предстательной железы, описано в нескольких заявках на патенты, причем описанные композиции содержат один или несколько видов молочнокислых бактерий (US 2008274162, Nessa Jeffrey Bryan et al., 2007).
Сочетание молочнокислых бактерий, одна из составляющих которого содержит L. crispatus, L. salivarius и L. casei, a другая составляющая содержит L. brevis, L. gasseri и L. fermentum, может быть использовано в качестве пищевой добавки или фармацевтической композиции для лечения и профилактики инфекций и воспалений, в том числе уретрита (ЕЕ 04620, Actial Farmaceutica Lda, 2000). Молочнокислые бактерии L. coprophilus PL 9001 (KCCM-10245) применялись для профилактики и лечения мочеполовых инфекций (KR 20040067161, PL BIO Co Ltd., 2003). Фармацевтические композиции, используемые в урологии для местного лечения, могут содержать в качестве активного вещества молочнокислые бактерии L. casei, L. gasseri (EP 353581, Silvana Tosi et al., 1993).
Вышесказанное показывает, что уменьшение аллергии на молоко и облегчение проблем с предстательной железой, в том числе с помощью частичного гидролиза и молочнокислых бактерий, исследовались в течение длительного времени.
Тем не менее, на рынке доступно недостаточное количество пищевых продуктов и пищевых добавок, которые уменьшают аллергию на молоко и облегчают проблемы с предстательной железой. Таким образом, существует потребность в приготовлении и применении надежных, проверенных испытаниями продуктов и пищевых добавок с полезными для здоровья свойствами.
Раскрытие изобретения
Настоящее изобретение относится к новым изолированным антиоксидантным штаммам микроорганизмов L. plantarum MCC1 DSM 23881 и L. gasseri MCC2 DSM 23882, композициям, содержащим один или оба упомянутых штамма, применению упомянутых микроорганизмов в качестве антиоксидантного протеолитического ингредиента для приготовления пищевого продукта и пищевой добавки, применению микроорганизмов для приготовления пищевого продукта и пищевой добавки, уменьшающих аллергию на молоко и симптомы воспаления нижних мочевыводящих путей, сопутствующие доброкачественному увеличению предстательной железы, и ассоциированный с ними окислительный стресс и воспаление, и к способу приготовления пищевого продукта и пищевой добавки, уменьшающих вышеупомянутые проблемы.
Молочнокислые бактерии, частично гидролизующие молочные белки, которые являются объектами настоящего изобретения, были обнаружены путем постепенной биоселекции. Цель состояла в нахождении штаммов с многовалентным биопотенциалом, многовалентность которого обеспечила бы возможность синергетического использования полезных биологических эффектов (большая степень гипоаллергенности, менее выраженные аллергические реакции, эффект уменьшения воспаления и окислительного стресса) для получения пищевых продуктов с желаемыми свойствами. Идея, лежащая в основе подхода согласно изобретению состоит не в достижении полного гидролиза белков. Попытки полного гидролиза предпринимались, но это создает новые проблемы, включая очень неприятные органолептические свойства продукта. Применение штаммов со множеством биологических потенциалов с требуемыми техническими процедурами и применение надлежащих полезных дополнительных сырых продуктов были выбраны в качестве идеологии настоящего изобретения. L. plantarum MCC1 и L. gasseri MCC2 имеют множество биологических потенциалов и обладают синергетическим эффектом - они способны целенаправленно (частично) гидролизовать молочные белки (казеины), они обладают значительной устойчивостью к окислению, они вырабатывают конъюгированную линолевую кислоту, NO и другие компоненты. Таким образом, изобретение обеспечивает возможность создания пищевых продуктов, обладающих потенциалом уменьшения аллергии на молоко и проблем с мочевыводящими путями, с помощью интегрального биотехнологического решения.
Описание L. plantarum MCC1 и L. gasseri MCC2
Объекты настоящего изобретения, L. plantarum MCC1 DSM 23881 и L. gasseri MCC2 DSM 23882, были изолированы из фекалий здорового ребенка во время эстонско-шведского сравнительного исследования микрофлоры у детей. Штамм L. plantarum MCC1 и штамм L. gasseri MCC2 были изолированы путем посева нескольких растворов фекалий ребенка в возрасте 1 года (10-2-10-7 в фосфатном буфере с 0,04% тиогликолевой кислотой, pH 7,2). Растворы были посеяны на свежеприготовленную культуральную среду агара MRS (Oxoid, Великобритания) и культивированы при 37°C в микроаэробной среде. Штаммы, которые являются объектами настоящего изобретения, были изолированы на основе колонии и морфологии клеток, характерной для Lactobacillus ssp. Затем была выполнена предварительная идентификация, а после этого и более точная идентификация, описанная ниже.
L. plantarum MCC1 и L. gasseri MCC2 были депонированы в коллекции культур Deutsche Sammlung von Mikroorganismen und Zellkulturen GmbH под номерами DSM 23881 и DSM 23882, соответственно, 5 августа 2010 г.
Культурально-морфологические характеристики
Культурально-морфологические характеристики определяли после культивации в средах агара MRS и бульона (Oxoid).
Для культивирования L. plantarum MCC1 в течение 24-48 часов в микроаэробной среде подходил бульон MRS, после чего в бульоне наблюдался равномерно плотный рост. После культивирования в течение 48 часов в культуральной среде агара MRS при 37°C в микроаэробной среде колонии L. plantarum MCC1 имели диаметр 2-2,5 мм, белый цвет, были выпуклыми, блестящими и с правильными границами. Клетки представляют собой короткие палочки в цепочке с частично параллельным расположением. Оптимальная температура роста клеток составляет 37°C; штамм также размножается при 15°C и 45°C. pH оптимальной среды роста клеток составляет 6,5. L. plantarum MCC1 является каталазотрицательной и оксидазотрицательной, при необходимости гетероферментативной, не гидролизует аргинин и не вырабатывает газ во время ферментации глюкозы.
L. plantarum MCC1 идентифицировали на основании тест-набора API 50CHL System (bioMérieux, Франция) в качестве L. plantarum (совпадение с типовым штаммом: отличное, ID %-99,9, Т-индекс 0,83).
Молекулярная идентификация L. plantarum MCC1 на основании последовательности 16S рРНК показала гомологичность с типовым штаммом L. plantarum Lp-01 (BLAST http://www.ncbi.nlm.nih.gov/guide/sequence-analysis/).
Характеристика ферментации углеводов L. plantarum MCC1 на основании API CHL 50 была следующей. Ферменты штамма: рибоза, галактоза, D-глюкоза, D-фруктоза, D-манноза, N-ацетилглюкозамин, амигдалин, арбутин, эскулин, салицин, целлобиоза, мальтоза, лактоза, сахароза, трегалоза, мелецитоза, D-рафиноза, L-арабиноза, метил-αD-маннопиранозид, D-тураноза, мелибиоза, сорбит и манит.
Согласно показаниям тест-набора API ZYM (bioMerieux, Франция) L. plantarum MCC1 характеризуется активностью лейцинариламидазы, валинариламидазы, α-глюкозидазы, β-глюкозидазы.
Для культивирования L. gasseri MCC2 в течение 24-48 часов в анаэробной среде подходил бульон MRS, после чего в бульоне наблюдался равномерно плотный рост. После культивирования в течение 48 часов в культуральной среде агара MRS при 37°C в анаэробной среде (CO2/H2/N2:5/5/90) колонии L. gasseri MCC2 имели диаметр 1,5-2 мм, беловатый цвет, были неровными и с неправильными краями. Клетки представляют собой палочки от коротких до кокковидных, со средней толщиной. Оптимальная температура роста клеток составляет 37°C; штамм также размножается при 45°C. pH оптимальной среды роста клеток составляет 6,5. L. gasseri MCC2 является каталазотрицательной и оксидазотрицательной, обязательно гомоферментативной (OHOL), не гидролизует аргинин и не вырабатывает газ при ферментации глюкозы.
L. gasseri MCC2 идентифицировали на основании тест-набора API 50CHL System (bioMérieux, Франция) в качестве L. delbrueckii ssp. delbrueckii (совпадение с типовым штаммом: хорошее, ID %-94,6, Т-индекс 0,35). Молекулярная идентификация L. gasseri MCC2 на основании последовательности 16S рРНК показала гомологичность с типовым штаммом L. gasseri IDCC 3102 (BLAST http://www.ncbi.nlm.nih.gov/guide/sequence-analysis/).
Характеристика ферментации углеводов L. gasseri MCC2 на основании API CHL 50 была следующей. Ферменты штамма: лактоза, сахароза, трегалоза и эскулин.
Согласно показаниям тест-набора API ZYM (bioMérieux, Франция) L. gasseri MCC2 характеризуется активностью лейцинариламидазы, валинариламидазы, α-глюкозидазы и β-глюкозидазы.
Безопасность
Происхождение штаммов микробов из пищеварительного тракта здорового ребенка подтверждает их статус GRAS (общепризнанно безопасный), или штаммы микробов безопасны для человека и подходят для перорального введения. Виды лактобактерий L. plantarum и L. gasseri были внесены EFSA в перечень таксономических единиц со статусом QPS (квалифицированная презумпция безопасности) (EFSA. Introduction of a Qualified Presumption of Safety (QPS) approach for assessment of selected microorganisms referred to EFSA. EFSA J 2007; 587, 1-16).
Гемолитическая активность
Методика: Гемолитическую активность L. plantarum MCC1 и L. gasseri MCC2 определяли после инкубации в микроаэробной среде на планшетах с кровяным агаром (Blood Agar Base №2, Oxoid +7% человеческой или лошадиной крови).
Результат. Штаммы L. plantarum MCC1 и L. gasseri MCC2 не проявили гемолитической активности.
Устойчивость к антибиотикам
Методика: Восприимчивость L. plantarum MCC1 и L. gasseri MCC2 к антибиотикам испытывали с помощью Е-теста (АВ Biodisk, Сольна). Минимальную ингибирующую концентрацию определяли в соответствии с эпидемиологическими контрольными значениями, рекомендованными Европейской комиссией.
Было показано, что L. plantarum MCC1 является устойчивой к цефокситину и ванкомицину в соответствии с показателями, установленными для лактобактерий Европейской комиссией (ЕС, 2002. Opinion of the Scientific Committee on Animal Nutrition on the criteria for assessing the safety of micro-organisms resistant to antibiotics of human clinical and veterinary importance. European Commission, Health and Consumer Protection Directorate General, Directorate C, Scientific Opinions, Brussels, Belgium. http://ec.europa.eu/food/fs/sc/scan/out64 en.pdf).
Известно, что несколько видов/штаммов лактобактерий обладают естественной устойчивостью к упомянутым антибиотикам, и таким образом при применении этого микроорганизма не ожидается горизонтальная передача генов, обуславливающих устойчивость к антибиотикам. Устойчивость к другим исследованным антибиотикам не проявлялась.
Штамм L. gasseri MCC2 не обладал устойчивостью к испытанным антибиотикам.
Функциональные свойства L. plantarum МСС1 и L. gasseri MCC2
Характеристика метаболитов
Методика: Характеристику метаболитов устанавливали путем газовой хроматографии (HP 6890) после 24 ч и 48 ч инкубации в микроаэробной среде роста (Таблица 2). Лактобактерий выращивали в течение 48 часов в культуральной среде агара MRS в атмосфере с 10% CO2, затем готовили суспензию в 0,9% растворе NaCl с плотностью 109 микроорганизмов/мЛ по МакФарланду (McFarland), и 1,0 мЛ полученной суспензии высевали в 9,0 мЛ жидкой культуральной среды MRS. Определяли количество метаболитов в ммоль/Л с использованием капиллярной колонки HP-INNOWax (15 м × 0,25 мм; 0,15 мкм). Температурная программа колонки 60°C 1 мин, 20°C/мин 120°C 10 мин; детектор (FID) 350°C.
Определение агрегации L. plantarum MCC1 и L. gasseri MCC2 и способности к свертыванию молока
Методика: Способность к свертыванию молока. Способность к свертыванию молока исследовали после инкубации штаммов в течение 48 ч в микроаэробных условиях в обезжиренном молоке UHT при температуре в 37°C. Способность к свертыванию оценивали в соответствии со следующей схемой:
1. Сильная (+) - молоко сворачивается в течение 24 часов,
2. Медленная (+/-) - молоко сворачивается в течение 48 часов,
3. Отсутствует (-) молоко не сворачивается.
Самоагрегация. Для оценки способности к самоагрегации штаммы, перед этим прокультивированные в течение 24 ч в культуральной среде агара MRS, суспендировали в физиологическом растворе. Полученную суспензию в течение 15 минут сохраняли при комнатной температуре. Способность к агрегации оценивали в соответствии со следующей схемой: 0 - отсутствует, суспензия равномерно плотная; 1 - некоторое количество хлопьев в растворе; 2 - большое количество хлопьев в суспензии, легкий осадок на дне тестовой пробирки; 3 - интенсивная, суспензия не развивается, осадок на дне, раствор почти прозрачный.
L. plantarum MCC1 и L. gasseri MCC2 свертывали молоко в течение 24 часов, имели сильные свойства самоагрегации (Таблица 3).
Способность пребиотиков к ферментации
Для оценки ферментации тагатозы (Arla Food Ingredients), рафтилозы Р95 (Beneo Orafti), рафтилозы Synergy 1 (Beneo Orafti) и рафтилозы L60/75 (Orafti) 0,05 мЛ 48-часовой испытываемой культуры Lactobacillus sp. высевали в культуральную среду MRS, которая содержала 0,5% сорбита, тагатозы или мелецитозы вместо глюкозы. В качестве индикатора в культуральную среду добавляли хлорофеноловый красный (0,004%). Ферментацию оценивали на основании изменения цвета (с красного на желтый) после 48 ч.
Противомикробная активность против патогенов
Методика: Для оценки противомикробных свойств использовали способ окрашенной струи (Hütt P, Shchepetova J, Loivukene K, Kullisaar Т, Mikelsaar M. Antagonistic activity of probiotic lactobacilli and bifidobacteria against entro- and uropathogens. J Appl Microbiol. 2006; 100 (6): 1324-32).
Для определения ингибирования патогенов измеряли зону отсутствия роста в мм. Аналогично методу Hütt et al (2006) вычисляли арифметическое среднее и стандартное отклонение на основании результатов для используемого образца, и оценивали антагонистическую активность штаммов (мм) во время инкубации при 37°C следующим образом: - слабая <9,7; средняя 9,7-12,2; сильная >12,2. Все пробы повторяли параллельно по меньшей мере три раза.
Противомикробная активность L. plantarum MCC1 в пробе способом окрашенной струи (умерщвленные клетки и эффект их экскретированных метаболитов) была сильной по отношению к большинству испытанных патогенов (кроме L. monocytogenes и S. enteritidis) в обеих средах.
L. gasseri MCC2 оказалась слабым антагонистом в обеих средах.
Общие протеолитические свойства
Общие протеолитические свойства L. plantarum MCC1 и L. gasseri MCC2 изучали на культуральной среде SMA (среда с обезжиренным молоком и агаром) и на Ca-казеинатном агаре, с посевом штрихом на испытательные культуральные среды штаммов, предварительно выращенных в течение 48 ч в бульоне MRS. Их инкубировали в течение 7 дней в микроаэробной среде при 37°C. Интенсивность протеолиза оценивали (6 проб, арифметическое среднее значение) на основании системы оценок: 4 - сильный, 3 - средний, 2 - слабый, 1 - очень слабый, 0 - отсутствует.
Результаты: L. plantarum MCC1 и L. gasseri MCC2 обладают достаточно хорошим протеолитическим эффектом (в 4-балльной системе у L. plantarum MCC1 было три балла, а у L. gasseri MCC2 - два балла).
Биоселекция на основании более специфичной способности к протеолизу (масс-спектрометрические исследования и исследования по технологии ВЭЖХ-ОФ для определения уровня протеолиза α-S1-казеина и β-казеина)
В отношении L. plantarum MCC1 и L. gasseri MCC2 не было известно, как они гидролизуют различные молочные белки. Поэтому сначала были уточнены изменения в спектрах молекулярных масс, получаемые при гидролизе, с использованием отдельных чистых молочных белков (β-лактоглобулина, α-S1-казеина, β-казеина) для последующего анализа изменений спектра белков необезжиренного молока. Молекулярные массы продуктов гидролиза молочных белков определяли на масс-спектрометре MALDI-TOF (матричном лазерном десорбционном ионизационном времяпролетном масс-спектрометре) (Marsilio, R. Catinella, S. Seraglia R. Traldi P. (1995) Matrix-assisted Laser-Desorption lonization Mass-Spectrometry for the Rapid Evaluation of Thermal-Damage in Milk. Rapid. Communications In Mass Spectrometry, 9, 550-552). Суспензию плотностью 109 КОЕ/мЛ по стандарту МакФарланда 4 приготовили из культур, помещенных в физиологический раствор KCl. 10 мкл молочной белковой фракции добавили в полученную суспензию. Выживаемость штаммов в растворах этих фракций определяли путем посева штрихом растворенных серий до и после испытания. Штаммы инкубировали в соответствующей среде белковой фракции в течение 2-6 дней при 37°C. Затем образцы центрифугировали и определяли характеристику белков на масс-спектрометре (Voyager DE Pro, Applied Biosystems) Фиг.1 и Фиг.2). Было установлено, что штаммы, которые являются объектами настоящего изобретения, способны адаптировать обмен веществ к среде, бедной питательными веществами. Например, в испытании единственным источником питательных веществ был либо α-S1-казеин, β-лактоглобулин, β-казеин, либо вещества, полученные из самих клеток штамма. Штаммы обнаруживались по окончании испытания во всех трех средах с белковыми фракциями (α-S1-казеином, β-лактоглобулином, β-казеином).
Затем протеолитические свойства штаммов исследовали в доступном на рынке молоке с содержанием жира 2,5% с помощью способа ВЭЖХ-ОФ {высокоэффективной жидкостной хроматографии на обращенной фазе). Уровень протеолиза α-S1-казеина и β-казеина измеряли на 2-й и 4-й день инкубации (Фиг.3). Для этого область пика хроматограммы ВЭЖХ-ОФ, соответствующую исследуемому молочному белку, сравнивали с начальным моментом (контроль, т.е. молоко до внесения лактобактерий, приравнивали к 100%) и вычисляли количество оставшегося молочного белка в процентах. Кроме того, проводили эксперименты с временем инкубации более 21 дня. Также исследовали сочетания штаммов, которые являются объектами настоящего изобретения, для повышения эффективности протеолиза и протеолитической активности также с молочной сывороткой (для уменьшения количества аллергенных казеинов) в случае с предварительно разведенным молоком. Приготовление образцов молока для анализа ВЭЖХ-ОФ и условия хроматографирования разрабатывали в соответствии с методическими указаниями, описанными в работе Bobe et al. (Bobe G, Beitz DC, Freeman AE, Lindberg GL. (1998) Separation and Quantification of Bovine Milk Proteins By reversed-Phase High-Performance Liquid Chromatography. J. Agric. Food Chem., 46, 458-463). Доступное на рынке молоко с содержанием жиров 2,5%, в которое добавляли 107 КОЕ/мЛ исследуемых штаммов и инкубировали их при 37°C, сравнивали с молоком без штаммов. Для разделения молочных белков использовали высокоэффективный жидкостный хроматограф (ВЭЖХ) (Hewlett Packard 1100) и колонку с обращенной фазой Zorbax 300SB-C18, заполненную пористым силикагелем. Подвижная фаза представляла собой элюирующую систему с изменяющимся градиентом, состоящую из: раствора А - ацетонитрил, вода, трифторуксусная кислота (TFA) в соотношении 900:100:1 (об/об/об); раствор В - ацетонитрил, вода, TFA в соотношении 100:900:1 (об/об/об). Градиент начинался с раствора В и пропорция раствора А начинала возрастать непосредственно после введения образца в систему. Во время фазы разделения, когда происходило разделение молочных белков, содержание раствора А возрастало на 0,47% в минуту. Полученные фракции идентифицировали путем сравнения времени удерживания со значениями времени удерживания согласно стандартам для основных молочных белков и определения молекулярной массы посредством масс-спектрометра MALDI-TOF. Молочные белки элюируют в следующей последовательности: κ-CN, αS2-CN, αS1-CN, β-CN, α-LA и β-LG. L. plantarum MCC1 и L. gasseri МСС2 оказывали надлежащие эффекты в отношении α-S1-казеина и β-казеина (см. итоговые данные на Фиг.1 и Фиг.2), причем количество белков, доминирующих при аллергической реакции на коровье молоко у детей, α-S1-казеина и β-казеина, уменьшилось на 2-й день. На основании анализа ВЭЖХ-ОФ лучшим средством направленного частичного протеолиза оказалась L. gasseri MCC2 (Фиг.3). При объединении вышеупомянутых лактобактерий протеолитический эффект в молоке был несколько снижен по сравнению с использованием тех же штаммов по отдельности. L. plantarum MCC1 также инкубировали в течение 4 дней в смеси, состоящей из 40% молока и 60% молочной сыворотки: содержание α-казеина на четвертый день составило 81%, а содержание β-казеина составило 83% по сравнению с начальным моментом.
Поставленная задача была решена: штаммы L. plantarum MCC1 и L. gasseri MCC2 и их сочетание уменьшали количество α-S1-казеина и/или β-казеина на 20-40% (т.е. происходил умеренный направленный гидролиз).
L. plantarum MCC1 и L. gasseri MCC2 гидролизуют белки, вызывающие аллергию на молоко, и они обладают хорошей общей протеолитической активностью. Их использование по отдельности или совместно снижает аллергенность молока и таким образом они могут быть использованы при приготовлении пищевого продукта, уменьшающего аллергию на молоко, и пищевой добавки с полезными для здоровья свойствами.
Биоселекция на основании выработки конъюгированной линолевой кислоты (КЛК)
КЛК означает группу изомеров жирной кислоты, линолевой кислоты (ЛК, cis-9, cis-12-18:2) с 18 атомами углерода, в которых двойные связи являются конъюгированными. КЛК образуется естественным путем при процессах биогидрогенации и окисления. Предполагается, что КЛК имеет антиадипогенный, антиканцерогенный, антидиабетогенный и противовоспалительный эффект, а также регулирующий эффект на иммунную систему, участвует в выработке цитокинов и иммуноглобулинов и обладает способностью модулировать экспрессию определенных генов непосредственно или опосредованно через конкретные транскрипционные факторы (Wahle, K. W. J., Heys, S.D. и Rotondo, D (2004). Conjugated linoleic acids: are they beneficial or detrimental to health? Prog. Lipid Res. 43: 553-587). Поскольку несколько видов молочнокислых бактерий способны преобразовывать линолевую кислоту в конъюгированную линолевую кислоту, то предполагается, что возможно повысить содержание КЛК в ферментированных молочных продуктах (Sieber, R., Collomb, M., Aeschlimann, A., Jelen, Р. и Eyer, H. (2004). Impact of microbial cultures on CLA in dairy products- a review. Int. Dairy J. 14: 1-15). Для этого следует проверить, какие молочнокислые бактерии являются производителями КЛК. Известно, что свободные жирные кислоты, присутствующие в средах роста микроорганизмов, обладают бактериостатическим эффектом, влияющим на рост микроорганизмов и проницаемость клеточной мембраны. Интенсивность эффекта зависит от жирной кислоты. Жирные кислоты с длинной цепочкой с более высоким уровнем насыщенности обладают более сильным противомикробным эффектом. Стереохимия двойных связей также влияет на противомикробную активность: жирная кислота с cis-конфигурацией является более сильным ингибитором, чем trans-форма (Kankaanpää, Р.Е., Salminen, S.J., Isolauri, E., Lee, Y. K. (2001). The influence of polyunsaturated fatty acids on probiotic growth and adhesion. FEMS Microbiol. Lett. 194: 149-153). Микроорганизмы обладают установленным защитным механизмом для противодействия веществу, ингибирующему его жизненные функции: полиненасыщенные кислоты изомеризуются в менее ингибирующие варианты, например линолевая кислота (ЛК) с более сильным бактериостатическим эффектом преобразуется в КЛК (Sieber, R., Collomb, M., Aeschlimann, A., Jelen, Р. и Eyer, Н. (2004). Impact of microbial cultures on conjugated linoleic acid in dairy products- a review. Int. Dairy J. 14: 1-15). Большинство образующейся КЛК остается в среде; одна часть добавляется к липидам клеточной мембраны. Было обнаружено, что КЛК может в небольших количествах находиться в клетке микроорганизма. Способность конъюгировать ЛК и другие жирные кислоты (олеиновую кислоту, рицинолевую кислоту) обнаружена у представителей нескольких видов микроорганизмов, включая Lactobacillus sp. Способность штаммов вырабатывать КЛК на основании линолевой кислоты, добавляемой в среду роста (MRS, обезжиренное молоко) количественно оценивали с использованием способа определения КЛК, разработанного нами. Стало ясно, что L. plantarum МСС1 и L. gasseri MCC2, которые обладали необходимым направленным протеолитическим эффектом, в значительной мере вырабатывали КЛК (Таблица 7). В то же время, эти штаммы не были практически подвержены бактериостатическому эффекту ЛК.
Биоселекция на основании устойчивости к окислению (антиоксидантности)
Были проведены исследования для определения того, обладают ли штаммы L. plantarum МСС1 и L. gasseri MCC2, имеющие конкретные свойства ограниченного протеолиза, а также способность вырабатывать КЛК, физиологически значимой устойчивостью к окислению. Устойчивость к окислению следует определять с использованием по меньшей мере двух способов.
Тест с линолевой кислотой (ЛК-тест), который позволяет определить способность клеточных суспензий лактобактерий ингибировать пероксидацию линолевой кислоты, использовали в качестве первого способа.
Доступный на рынке тест (общий антиоксидантный статус - TAS, Randox Laboratories Ltd., UK), основанный на ингибировании образования радикала феррил метмиоглобина, вырабатываемого перекисью водорода в клеточной суспензии лактобактерий, использовали в качестве второго способа (Rice-Evans и Miller, 1994). Значение TAS определяли в единицах тролокса (растворимая форма витамина Е) (ммоль/Л). Оба способа описаны в литературе (Kullisaar Т, Zilmer M, Mikelsaar M, Vihalemm Т, Annuk Н, Kairane С, Kilk А. (2002). Two antioxidative lactobacilli strains as promising probiotics. Int. J. Food Microblol. 72, 215-224; Kullisaar, Т., Songisepp, Е., Mikelsaar, M., Zilmer, K., Vihalemm, Т., Zilmer, M. (2003) Antioxidative probiotic fermented goats milk decreases oxidative stress-mediated atherogenicity in human subjects. British Journal of Nutrition 90, 449-456).
Для определения ТАА и TAS штаммы инкубировали в бульоне MRS (Oxoid) в течение 24 часов при 37°C. Клетки микроорганизмов центрифугировали при 4°C и 1500 об/мин в течение 10 минут, промывали изотоническим физиологическим раствором (4°C) и суспендировали в 1,15% KCl (Sigma, США). Плотность суспензии при OD260 1,1 составляла 109 клеток микроорганизмов/мЛ. L. plantarum МСС1 и L. gasseri MCC2 обладают физиологически значимой общей антиоксидантностью (Таблица 6).
Биоселекция на основании способности к выработке оксида азота и перекиси водорода
Для получения полезной информации предварительно выбранные штаммы (конкретные свойства ограниченного протеолиза, выработка КЛК, антиоксидантность) также исследовали в отношении выработки NO и H2O2. Согласно литературе, ранее не проводились исследования сопутствующей выработки NO и H2O2 штаммами микроорганизмов. Измерения выполняли для живых клеток с использованием электрохимического измерения (анализатор свободных радикалов Apollo 4000, WPI, Берлин, Германия), с использованием электродов типа ISO-HPO2 и ISO-NOP. Электроды помещали в культуру, выращиваемую в бульоне MRS (Oxoid), сигналы записывали одновременно в течение 5-7 минут и вычисляли среднюю интенсивность за время измерения. Каждую точку эксперимента измеряли в качестве 4 независимых параллелей и каждую параллель измеряли дважды. Концентрацию NO и H2O2 в исследуемом образце определяли путем сравнения сигнала для образца со стандартной кривой.
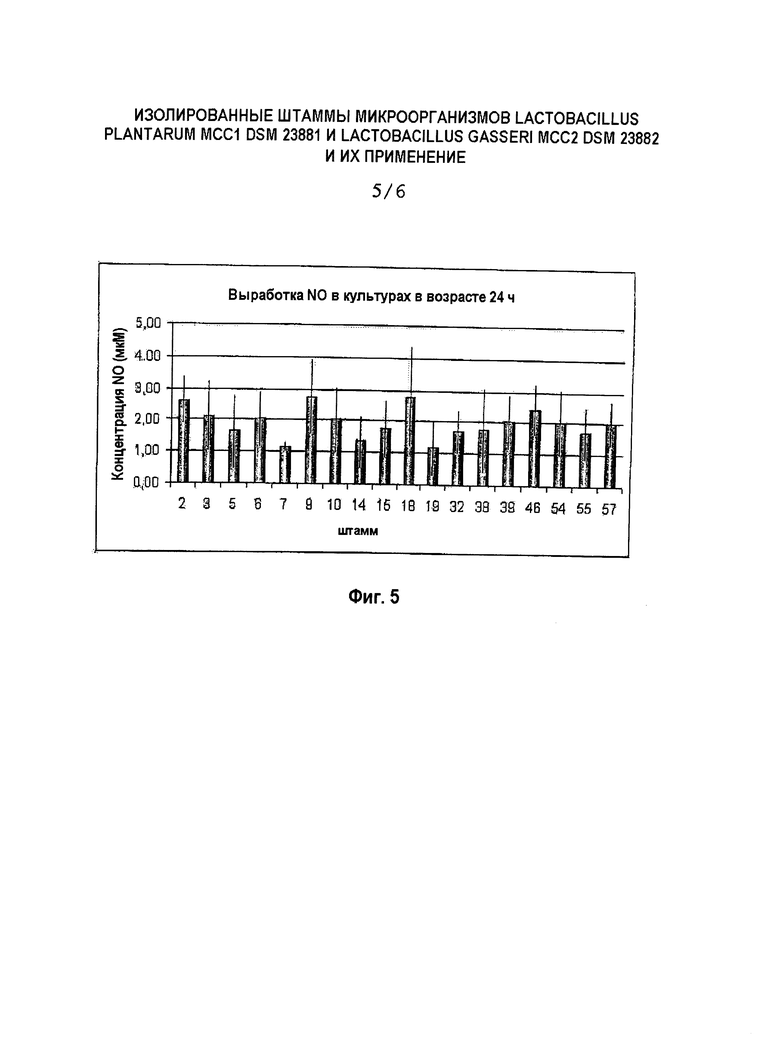
L. plantarum MCC1 обладает значительной способностью вырабатывать NO и перекись водорода, оба соединения также вырабатывались L. gassen MCC2 (Фиг.4 и 5).
Таким образом, штаммы L. plantarum MCC1 и L. gasseri MCC2 подходят в качестве антиоксидантных добавок для приготовления пищевого продукта и пищевой добавки.
В таблице 7 показан обзор функциональных свойств вышеупомянутых штаммов и их сочетания.
Приведенные выше сведения описывали штаммы микроорганизмов, которые являются объектами изобретения.
Следующими объектами изобретения являются композиции, содержащие один или оба штамма L. plantarum MCC1 и L. gasseri МСС2. Если композиция содержит только один штамм, содержание штамма находится в диапазоне от 0,8 до 1,2 объемных процента, при этом количество микроорганизмов штамма L. plantarum MCC1 составляет 0,25×108-4×108 КОЕ/мЛ, и количество микроорганизмов штамма L. gasseri МСС2 составляет 0,5×107-1×108 КОЕ/мЛ.
Когда используют один штамм, содержание штамма предпочтительно составляет 1,0 объемный процент, при этом количество микроорганизмов штамма L. plantarum MCC1 находится в диапазоне 0,4×108-4,8×108 КОЕ/мЛ, и количество микроорганизмов штамма L. gasseri МСС2 составляет 0,8×107-1,2×108 КОЕ/мЛ.
Если композиция содержит оба штамма L. plantarum MCC1 и L. gasseri МСС2, содержание обоих штаммов находится в диапазоне 0,4-0,6 объемных процента, при этом количество микроорганизмов штамма L. plantarum MCC1 находится в диапазоне 0,2×108-2,4×108 КОЕ/мЛ и количество микроорганизмов штамма L. gasseri МСС2 составляет 0,4×107-0,6×108 КОЕ/мЛ.
Когда используют оба штамма, содержание обоих штаммов предпочтительно составляет по меньшей мере 0,5 объемных процента, при этом количество микроорганизмов штамма L. plantarum MCC1 находится в диапазоне 0,25×108-2×108 КОЕ/мЛ, и количество микроорганизмов штамма L. gasseri МСС2 составляет 0,5×107-0,5×108 КОЕ/мЛ.
Вышеупомянутые штаммы могут быть живыми или умерщвленными.
Следующие объекты изобретения представляют собой применение упомянутых штаммов по отдельности или в сочетании
- в качестве антиоксидантного протеолитического ингредиента для приготовления пищевого продукта и/или пищевой добавки,
- для приготовления гипоаллергенного пищевого продукта и/или пищевой добавки, уменьшающей аллергию на молоко,
- для приготовления пищевого продукта и/или пищевой добавки, уменьшающих симптомы раздражения нижних мочевыводящих путей, связанные с доброкачественной гиперплазией предстательной железы, и окислительный стресс и воспаление, связанные с ними.
Следующий объект изобретения представляет собой способ приготовления пищевого продукта и/или пищевой добавки, уменьшающих аллергию на молоко и симптомы раздражения нижних мочевыводящих путей и окислительный стресс и воспаление, связанные с ними.
Способ согласно изобретению включает в себя этапы, на которых:
A) Исходную смесь, содержащую молочный белок, разогревают до 37+2°C;
B) Добавляют L. plantarum MCC1 и/или L. gasseri MCC2 или оба штамма вместе. Если используют только L. plantarum MCC1, то его добавят до 1,2 объемных процента, предпочтительно 1 объемный процент, с количеством микроорганизмов 0,4×108-4,8×108 КОЕ/мЛ. Если используют только L. gasseri MCC2, его добавят до 1,2 объемных процента, предпочтительно 1 объемный процент, с количеством микроорганизмов 0,8×107-1,2×108 КОЕ/мЛ. Когда используют оба вышеупомянутых штамма вместе, их добавят до 1,2 объемных процента, предпочтительно 1 объемный процент, причем L. plantarum MCC1 добавят 0,25×108-2×108 КОЕ/мЛ и L. gasseri MCC2 0,5×107-0,5×108 КОЕ/мЛ. Конечный уровень pH для ферментирования составляет 4,2±0,25.
C) Смесь ферментируют L. plantarum MCC1 или L. gasseri MCC2 или L. plantarum MCC1 + L. gasseri MCC2 при 37+2°C в течение по меньшей мере 18-26 часов.
D) Смесь пастеризуют в диапазоне 80-85°C (предпочтительно 82°C±2) в течение 30-35 минут (предпочтительно 30 минут) и охлаждали до температуры 20-30°C.
Е) Полученную смесь ароматизировали добавками и охлаждали до температуры 2-6°C.
F) Полученную смесь использовали для приготовления пищевого продукта и/или пищевой добавки. В случае пищевого продукта смесь разливают в бутылки, хранят (при 2-6°C) и выполняют все требуемые анализы (определение устойчивости к окислению и т.п.). Смесь также быть использована в форме порошка (капсул, пастилок, таблеток, пакетиков с порошком и т.п.) или жидкости (ампул) для производства пищевой добавки для розничной продажи.
При приготовлении пищевой добавки в форме порошка из смеси удаляют воду, например путем лиофилизации (сублимационной сушки), сушки распылением, сушки на мельнице или другим известным способом (до получения порошковой консистенции). При приготовлении жидкой пищевой добавки воду частично удаляют из продукта (до получения желаемой консистенции). Пищевая добавка может быть приготовлена с надлежащими добавками (например, антиоксидантами, подсластителями, пребиотиками) или без них.
В вышеупомянутом способе источником молочного белка является молоко, молочный порошок, концентрат молочного белка, молочная сыворотка или другой источник молочного белка. Подходящими добавками являются фруктовый или ягодный сок, концентрат фруктового или ягодного сока, сироп или напиток на основе сока или фруктовый или ягодный джем, предпочтительно облепиховый, черничный или малиновый сок или другой сок, сироп, концентрат.
Краткое описание чертежей
Фиг.1 - масс-спектрометрический анализ MALDI-TOF (иллюстративный примерный эксперимент). Бета-казеин через 30 минут после смешивания со штаммом L. gasseri MCC2.
Фиг.2 - масс-спектрометрический анализ MALDI-TOF (иллюстративный примерный эксперимент). После 48 часов инкубации со штаммом L. gasseri MCC2 пик масс-спектра бета-казеина 24,0 кДа был по существу устранен.
Фиг.3 - эффект штаммов L. plantarum MCC1 и L. gasseri MCC2 при 48- и 96-часовой инкубации на уровень бета-казеина (базовый уровень составлял 100%, на основании данных масс-спектрометрического анализа MALDI-TOF и анализа ВЭЖХ-ОФ).
Фиг.4 - выработка NO штаммами L. plantarum MCC1 и L. gasseri MCC2.
Фиг.5 - выработка H2O2 штаммами L. plantarum MCC1 и L. gasseri MCC2.
Фиг.6 - схема приготовления пищевого продукта и пищевой добавки.
Осуществление изобретения
Пример 1. Способ приготовления пищевого продукта и пищевой добавки с вышеупомянутыми полезными для здоровья свойствами, уменьшающих аллергические реакции на молоко и симптомы раздражения мочевыводящих путей и ассоциированный с ними окислительный стресс и воспаление, содержащих микроорганизмы L. plantarum MCC1 или L. gasseri MCC2 или их сочетание.
Ниже представлен предпочтительный вариант выполнения.
Для приготовления пищевого продукта и/или пищевой добавки, уменьшающих аллергические реакции на молоко и проблемы с мочевыводящими путями, использовались культуры микроорганизмов, которые были предварительно выращены в ферментаторе в течение 24 часов и затем лиофилизированы.
Для приготовления пищевого продукта лиофилизированные культуры микроорганизмов L. plantarum MCC1 и/или L. gasseri MCC2 активировали в небольшом количестве теплой (по меньшей мере 20°C) молочной сыворотки, молока или раствора, приготовленного из молочного порошка/концентрата молочного белка или другого источника молочного белка в течение по меньшей мере 4 часов.
Способ приготовления пищевого продукта или пищевой добавки с полезными для здоровья свойствами включал в себя следующие этапы (см. схему на Фиг.6):
a) Исходную смесь, содержащую молочный белок, сыворотку, полученную с производства сыра (физико-химические свойства представлены в таблице 8), в которой уменьшили жирную фазу путем разделения и удалили сырную пыль, нагревали до температуры ферментирования 37±2°C;
b) 1 объемный процент штамма L. plantarum MCC1 (с количеством микроорганизмов 0,5×108-4×108 КОЕ/мЛ) или штамма L. gasseri MCC2 (с количеством микроорганизмов 1×107-1×108 КОЕ/мЛ) или обоих штаммов вместе (по 0,5 объемных процента, содержащих живые клетки штамма L. plantarum MCC1 с плотностью в диапазоне 0,25-2×108 КОЕ/мЛ и живые клетки штамма L. gasseri MCC2 с плотностью в диапазоне 0,5×107-0,5×108 КОЕ/мЛ).
c) Смесь ферментировали в течение 18-26 часов при температуре 37±2°C, во время чего происходил частичный гидролиз молочного белка под действием штамма(ов) L. plantarum MCC1 и/или L. gasseri MCC2. Ферментация продолжалась до тех пор, пока кислотность не достигла значения pH 4,20±0,25;
d) Для инактивации (уничтожения) штамма(ов) L. plantarum MCC1 и/или L. gasseri MCC2 смесь пастеризовали при 82±2°C в течение 30-35 минут и охлаждали до температуры 20-30°C;
e) Полученную смесь ароматизировали выбранными добавками, которые могли быть фруктовым или ягодным соком или концентратом или сиропом, напитком на основе сока или фруктовым или ягодным джемом. Например, использовали 16-17 объемных процентов облепихового джема или 4,7-5 объемных процентов концентрированного вишневого напитка на основе сока и облепихового сока и 9,8-10,2 объемных процента концентрированного малиново-черничного напитка на основе сока.
f) Полученную смесь охлаждали до 2-6°C, пищевой продукт разливали по бутылкам, выполняли органолептический анализ и анализ устойчивости к окислению и сохраняли (2-6°C) и выполняли клинические исследования (см. ниже).
Для приготовления порошкообразной пищевой добавки удаляли воду из полученной смеси с использованием способов, известных в области технологии обработки пищевых продуктов (например, с помощью лиофилизации или сушки (сушки распылением, сушки на мельнице и т.п.)). В предпочтительном варианте для приготовления порошкообразной пищевой добавки использовали одноступенчатую распылительную сушилку (температура поступающего воздуха 160°C и температура выходящего воздуха 80°C).
В смесь, приготовленную вышеописанным способом, добавляли подходящий наполнитель, имеющий более высокую температуру плавления, чем лактоза, например мальтодекстрин (в соотношении 1:1 с сухим веществом молочной сыворотки).
В качестве другого варианта использовали отделение воды, сахара (лактозы) и соли путем ультрафильтрации, после чего выполняли концентрацию посредством вакуумной машины и сушку (сушку распылением), и таким образом получали порошкообразную пищевую добавку с низким содержанием лактозы и высоким содержанием белка.
В качестве третьего варианта для удаления воды использовали концентрацию посредством вакуумного устройства с последующей сушкой распылением. Окончательным результатом была порошкообразная пищевая добавка, содержащая лактозу.
Пищевые продукты FP-I - FP-V, содержащие микроорганизмы, которые являются объектом изобретения, и добавки готовили вышеупомянутым способом следующим образом:
Пищевой продукт I (или FP-I): Смесь, содержащая молочный белок + L. plantarum MCC1 + L. gasseri MCC2; добавка облепиховый сок (ВТ);
Пищевой продукт II (или FP-II): Смесь, содержащая молочный белок + L. plantarum MCC1; добавка - концентрированный напиток на основе малинового-черничного сока (RB).
Пищевой продукт III (или FP-III): Смесь, содержащая молочный белок + L. plantarum MCC1 + L. gasseri MCC2; добавка концентрированный напиток на основе черносмородинового-малинового сока (BR).
Пищевой продукт IV (или FP-IV): Смесь, содержащая молочный белок + L. plantarum MCC1; добавка - концентрат черники (В).
Пищевой продукт V (или FP-V): Смесь, содержащая молочный белок + L. plantarum MCC1; добавка - концентрированный напиток на основе брусничного сока (С).
Пищевая добавка I (или DS/FP-I): Смесь, содержащая молочный белок + L. plantarum MCC1 + L. gasseri MCC2; добавка - облепиховый сок (ВТ);
Пищевая добавка II (или DS/FP-II): Смесь, содержащая молочный белок + L. plantarum MCC1; добавка - концентрированный напиток на основе малинового-черничного сока (RB).
Пищевая добавка III (или DS/FP-III): Смесь, содержащая молочный белок + L. gasseri MCC2; добавка.
Пример 2. Добавки для приготовления пищевого продукта и пищевой добавки, уменьшающих аллергические реакции на молоко и симптомы раздражения мочевыводящих путей и ассоциированный с ними окислительный стресс и воспаление, содержащих микроорганизмы L. plantarum MCC1 или L. gasseri MCC2 или их сочетание.
В качестве добавок к продуктам использовали облепиховый сок (ВТ) (приготовленный из ягод облепихи, без консервантов, путем холодного отжима и с пастеризацией), напиток на основе малинового-черничного сока (состав: концентрированный малиновый-черничный сок (RB), сахар, регулятор кислотности лимонная кислота, консерватор сорбат калия, растворен 10-кратно), концентрированный напиток на основе брусники (С) и концентрат черники (В) (см. таблицу 10). Для добавок определяли антиоксидантность (исследования ТАА и DPPH) и содержание биоэлементов способом атомно-абсорбционной спектрофотометрии (AAS) Spektra AAFS и 220Z. (Varian, Австралия), содержание Cu, Zn, Fe, Mn определяли способом AAS в пламени, содержание K определяли эмиссионным способом в воздушно-ацетиленовой смеси. Органолептические испытания конечного продукта выполняли в соответствии с действительными требованиями на основании специальных опросников. Результаты представлены в таблице 10.
Пример 3. Клиническое испытание №1.
Безопасность и полезные эффекты продуктов, биохимические, клинические и органолептические испытания.
Путем использования мультипотентных штаммов, полученных многовариантной биоселекцией, а также добавок, и применения надлежащей технологической схемы (см. пример 1) получили пищевые продукты FP-1 (MCC1 + L. gasseri MCC2, ВТ) и FP-II (MCC1, RB). Затем провели клинические испытания (в соответствии с Хельсинкской декларацией Всемирной медицинской ассоциации, одобренной Комитетом по вопросам этики Университета Тарту) для выяснения уровня безопасности и полезных для здоровья эффектов пищевых продуктов FP-1 и FP-II.
Основная схема клинического испытания была следующей: 25 добровольцев (11 женщин, 14 мужчин) в возрасте 40-65 лет случайным образом распределили по двум группам на основании следующих критериев включения в исследование: лица без клинических проблем, хронических заболеваний, специальных диет, не принимающие витамины, минеральные препараты, участники не должны изменять свою физическую активность, обычный уровень употребления алкоголя, привычки к курению и пищевые привычки. До и после двухнедельного курса ежедневного приема 200 г FP-I (n=10) или FP-II (n=15) определяли следующие биохимические и клинические параметры: маркеры воспаления (высокочувствительный С-реактивный белок, миелопероксидаза, IL-6, IL-10), липидные и липопротеиновые маркеры (триглицериды, холестерин, холестерин ЛПНП, холестерин ЛПВП, малые плотные ЛПНП), иммуноглобулины (IgM, IgA, IgG, IgE), маркеры окислительного стресса (ОкС) (изопростаны, окЛПНП, ЛПНП-b2-гликопротеин), глюкоза в крови, артериальное давление и креатинин в моче.
Результаты
1) Безопасность
Научный анализ ежедневных опросников показал, что никто из субъектов не жаловался на дискомфорт или проблемы с кишечником во время двухнедельного курса применения, и не проявились какие-либо негативные симптомы. Применение FP-I или FP-II не оказало эффектов, которые вывели бы их биохимические и клинические параметры за пределы эндемических опорных значений. Они не повысили количество антител IgE - одного из важных маркеров аллергии, по сравнению с периодом до испытания, не вызвали воспалительную реакцию (высокочувствительный С-реактивный белок (hsCPB), окЛПНП, миелопероксидаза (МПО), IL-6) и не изменили значения содержания липидов в крови, липопротеинов (триглицеридов, ЛПНП, ЛПВП) и глюкозы и не повысили уровень ОкС в организме (изопростаны, окЛПНП, миелопероксидаза (МПО), малые плотные ЛПНП, b2-гликопротеин) (таблица 10) и не нарушили функции почек (креатинин в моче). Таким образом, FP-I и FP-II, полученные на основе принципа настоящего изобретения, не вызывают воспалительных реакций, общей аллергической сенсибилизации, ОкС и таким образом не наносят вред организму у здоровых лиц.
2) Полезные для здоровья эффекты
Анализы результатов клинического испытания показали, что применение FP-I или FP-II вызвало некоторые статистически достоверные и несколько различные положительные эффекты (Таблица 10). FP-I оказал эффект, состоящий в снижении системной нагрузки ОкС на весь организм (снижение уровня изопростанов в моче и уровня МПО в крови) и противовоспалительный эффект (снижение уровня МПО в крови). FP-II снизил системную нагрузку ОкС на весь организм (снижение уровня изопростанов в крови) и оказал противовоспалительный эффект (снижение уровня высокочувствительного С-реактивного белка и повышение уровня IL-10). В то же время применение обоих пищевых продуктов не изменило численных значений уровня иммуноглобулинов IgM, IgA и IgM.
Таким образом, первое клиническое испытание показало, что принцип изобретения (многовариантная целенаправленная биоселекция штаммов, биоселекция добавок и технологическое решение) привел к созданию пищевых продуктов, которые являются безопасными и более гипоаллергеннымии имеют несколько эффектов в отношении воспаления и окислительного стресса (вызывают меньше аллергических реакций по сравнению с коровьим молоком) и оказывают положительный эффект на биохимические и клинические параметры также у лиц с жалобами в отношении предстательной железы (включая расстройства мочеиспускания).
Пример 4. Клиническое испытание №2. Исследования аллергии на коровье молоко у детей
Реакции, вызываемые белком коровьего молока, проявляются у 5-15% детей (Host А. (2002). Frequency of cow′s milk allergy in childhood. Ann Allergy Immunol 89 (Suppi 1): 33-7), но аллергия на коровье молоко (СМРА) проявляется у 2-7,5% (Hill DJ, Firer MA, Shelton MJ et al. (1986) Manifestation of milk allergy in infancy: clinical and immunologic findings. J Pediatr 109: 270-6). СМРА может быть IgE-опосредованной и не-IgE-опосредованной. Как правило, ранние реакции представляют собой крапивницу, ангиоотек, рвоту или обострение атопического дерматита. Обострение атопического дерматита или жалобы, относящиеся к желудочно-кишечному тракту, проявляются в качестве поздних реакций (Vandenplas Y, Brueton M, Dupont С, Hill D, Isolauri E, Koletzko S, Oranje AP, Staiano A. (2007) Guidelines for the diagnosis and management of cow′s milk protein allergy in infants. Arch Dis Child. 92: 902-908). Ни одна из существующих диагностических проб не утверждает и не отрицает наличия или отсутствия СМРА у ребенка (Vanto Т, Juntunen-Backman K, Kalimo K et al. (1999) The patch test, skin prick test, and serum milk-specific IgE as diagnostic tools in cows′ milk allergy in infants. Allergy 54: 837-42). Таким образом, золотым стандартом диагностики СМРА является элиминационная диета с последующим провоцированием (Vandenplas Y, Brueton M, Dupont С, Hill D, Isolauri E, Koletzko S, Oranje AP, Staiano A. (2007) Guidelines for the diagnosis and management of cow′s milk protein allergy in infants. Arch Dis Child. 92: 902-908). В качестве протокола для провокационной пробы использовали всемирно признанную схему таких исследований, описанную Isolauri et al. (Isolauri E, Turjanmaa K. (1996) Combined skin prick and patch testing enhances identification of food allergy in infants with atopic dermatitis. J Allergy Clin Immunol; 97: 9-15; Sütas Y, Kekki O-M, Isolauri E. (2000) Late onset reactions to oral food challenge are linked to low serum interleukin-10 concentrations in patients with atopic dermatitis and food allergy. Clin Exp Allergy 30: 1121-8).
Методика
Открытую провокационную пробу с пищевыми продуктами FP-II и FP-I выполняли в Центре аллергических заболеваний Детской клиники Фонда клиники Университета Тарту (в соответствии с Хельсинкской декларацией Всемирной медицинской ассоциации, одобренной Комитетом по вопросам этики Университета Тарту). Пробу выполняли 20 раз (часть субъектов участвовала в испытаниях обоих пищевых продуктов) у детей в возрасте от 9 месяцев до 4 лет 8 месяцев (средний возраст 25,1 месяца). Обстановка перед исследованием была следующей: врачом в Центре аллергических заболеваний Детской клиники Фонда клиники Университета Тарту (проба на IgE к молоку, NTT к молоку) у всех детей была диагностирована аллергия на коровье молоко и/или непереносимость коровьего молока на основании анамнеза и дополнительных исследований. Все дети в экспериментальной группе были на безмолочной элиминационной диете. После применения молока у 9 детей развилась кожная сыпь, обычно наблюдалось обострение атопического дерматита, у одного ребенка развилась острая крапивница, у одного ребенка - диарея. У одного ребенка было затруднено дыхание и появилась кожная сыпь только после употребления продуктов из переработанного молока. У 3 детей была диагностирована конкурирующая астма, у одного из них также наблюдался аллергический ринит и у одного - сенная лихорадка (поллиноз). У одного ребенка были конкурирующие заболевания - астма и сенная лихорадка. Никто из детей не получал антигистаминное или кортикостероидное лечение. У трех детей конкурирующая астма была в стадии ремиссии, поэтому они не получали постоянного лечения по поводу астмы, когда была выполнена провокационная проба.
Открытая пероральная провокационная проба была выполнена на первый день исследования в Центре аллергических заболеваний Детской клиники TUCF. Ребенку вводили исследуемый продукт (FP-II или FP-I) в возрастающих количествах (каплю на нижнюю губу, 2 мЛ, 10 мЛ, 50 мЛ, 100 мЛ). После каждой введенной дозы оценивали состояние ребенка и развитие аллергической реакции в течение 20 минут. Если развивались сыпь, кашель, затрудненное дыхание или боль в животе/диарея, введение продукта немедленно прерывали. Если ребенок не проявлял реакции в первый день исследования после введения до 100 мЛ продукта, то ребенок получал исследуемый продукт дома по 100 мЛ в день на второй, третий и четвертый дни. Родителей просили оценивать развитие поздних реакций. Пробу считали положительной, если у ребенка проявлялась: a) ранняя реакция - на первый день провокационной пробы после введения небольшого количества продукта развивался зуд, сыпь, крапивница или рвота; b) поздняя реакция - развивались обостренный дерматит, рвота, боль в животе и диарея >24 часов после начала провокации с исследуемым продуктом. Открытая провокационная проба была отрицательной, если во время провокации (четыре дня) и в последующую неделю не развивалась реакция. Таким образом, у субъекта была переносимость к продукту.
Обзор результатов
Решение проблемы аллергенности пищи является очень сложным и невозможно создать продукты, аллергическая реакция на которые совершенно отсутствует, но при этом обладающие очень высокой биологической ценностью. Проблема становится более сложной, поскольку в настоящее время ребенок может проявлять аллергическую реакцию на несколько пищевых продуктов (но также и на другие общие факторы) одновременно. Это также наблюдалось в наших исследованиях (см. таблицу 5), из-за чего сложно исключить возможность возникновения сыпи, характеризующей положительную реакцию, в определенный момент под действием других причин. Поэтому исследование было сосредоточено на том, чтобы возникало меньше аллергических реакций, т.е. чтобы полученные пищевые продукты были более гипоаллергенными, чем коровье молоко. Каждый процент детей, не имеющих аллергии или имеющих менее выраженную аллергию на определенные пищевые продукты, увеличил бы число детей, которые получали бы достаточное количество пищи с высокой биологической ценностью для своего развития в наиболее важный период их биологического развития. Провокационная проба показала, что как продукт FP-II, так и FP-I были более гипоаллергенными, чем коровье молоко (таблица 5). По меньшей мере у 3-4 детей из 12 не развилась какая-либо аллергическая реакция после применения FP-I на основании провокационной пробы. У трех субъектов из восьми не развилась какая-либо аллергическая реакция после применения FP-II. Из пяти субъектов, у которых FP-I вызвал некоторую реакцию, три показали переносимость к FP-II (60%). Таким образом, с точки зрения этих случаев FP-II обладал еще большим уровнем гипоаллергенности, чем FP-I. Большинство детей также предпочли FP-II по его вкусовым свойствам.
Пример 5. Клиническое испытание №3. Эффект пищевых продуктов FP-I и FP-II на симптомы раздражения нижних мочевыводящих путей, сопутствующие доброкачественной гиперплазии предстательной железы, и на индикаторы окислительного стресса и воспаления.
Вышеупомянутые клинические испытания показали, что принцип изобретения (многовариантная целенаправленная биоселекция штаммов, биоселекция добавок и технологическое решение) привел к созданию пищевых продуктов FP-I и FP-II, которые безопасны для применения и являются более гипоаллергенными и обладают несколькими эффектами в отношении воспаления и окислительного стресса и обладают положительным эффектом на симптомы раздражения мочевыводящих путей и на индикаторы ОкС и воспаления.
Методика
В испытании участвовали 55 мужчин (получали FP-I) и 5 мужчин (получали FP-II), у которых были невысокие или средние показатели по шкале IPSS {международной шкале простатических симптомов) <8. Опросник IPSS содержит 3 вопроса для оценки симптомов раздражения нижних мочевыводящих путей и 4 вопроса для оценки непроходимости мочевыводящих путей (синдромов непроходимости). Также выполняли необходимые предварительные пробы (ПСА, секрет предстательной железы) для точного выбора экспериментальной группы. Это означает, что с помощью исследований секрета предстательной железы и опросника NIH-CPSI исключался простатит в активной фазе (воспаление предстательной железы), и с использованием пробы на ПСА и пальцевой пальпации исключалась клиническая возможность рака предстательной железы. Таким образом, мы включили в экспериментальную группу мужчин с невысоким или средним уровнем расстройств мочевыводящих путей, у которых были исключены другие источники жалоб (простатит, рак предстательной железы). Пациенты (с невысоким или средним уровнем расстройства мочеиспускания, без воспалительной реакции) принимали пищевой продукт FP-I или FP-II по 200 г ежедневно в течение двух недель.
Результаты
FP-I. Были проведены две серии исследований. В первой серии участвовали 23 пациента, и во второй (где также осуществлялся контроль с помощью плацебо) участвовали 32 пациента (таблица 13). В обоих случаях наблюдалось статистически достоверное снижение уровня воспалительного маркера - высокочувствительного С-реактивного белка (hsCPB) и маркера ОкС - изопростанов. Вторая серия исследований также указала на статистически положительные изменения уровней противовоспалительного IL-10 и маркера воспаления/ОкС - окЛПНП. В первой серии испытаний (n=23) также наблюдалась тенденция к положительным изменениям в уровне этого маркера. Во второй серии испытаний также определяли уровень гликированного гемоглобина, снижение которого было статистически достоверным.
Обзор результатов обеих серий испытаний (таблица 13) показал, что уровни hsCPB, изопростанов и окЛПНП статистически достоверно снизились, и наблюдалась положительная тенденция к снижению уровня IgE и статистически достоверное повышение IL-10. Наблюдалась корреляция между hsCPB и окЛПНП после применения FP-I. В контрольной группе не наблюдались статистически достоверные изменения какого-либо из упомянутых параметров.
FP-II. Была выполнена одна серия испытаний и определены следующие параметры: IgE кед./Л, окЛПНП, IL-10, 8-изопростаны, hsCPB и МПО. Было обнаружено, что в группе лиц, принимавших РР-II, имело место статистически достоверное уменьшение маркера воспаления и ОкС - МПО (до приема - 77±13, и после приема 53±9 нг/мЛ, p=0,0056) и снижение частоты расстройств мочеиспускания у более 40% лиц, принимавших продукт.
Обзор результатов
Применение FP-I, а также FP-II снизило уровень ОкС и воспаления у субъектов с умеренным уровнем проблем, связанных с нижними мочевыводящими путями (балл по IPSS<8) и ведущими симптомами раздражения. В случае FP-I у 66% мужчин из экспериментальной группы (55), имевших умеренный уровень проблем, связанных с нижними мочевыводящими путями (балл по IPSS<8) и ведущие симптомы воспаления, наблюдалось уменьшение уровня жалоб по меньшей мере на 20%, а у 30% участников экспериментальной группы наблюдалось уменьшение уровня жалоб в среднем на 40%. Клинические и биохимические параметры пациентов (hsCPB, IL-10, окЛПНП, 8-изопростаны) статистически достоверно улучшились. В контрольной группе изменений не произошло.
Пример 6. Эффект пищевой добавки (DS/FP-I) на симптомы раздражения нижних мочевыводящих путей, сопутствующие доброкачественной гиперплазии предстательной железы и на индикаторы окислительного стресса и воспаления.
В исследование были включены 10 мужчин, имевших невысокий или умеренный уровень расстройства мочеиспускания по IPSS (международной шкале простатических симптомов), при этом активный простатит был исключен на основании предварительных исследований секрета предстательной железы и опросника NIH-CPSI, а клинически значимая возможность рака предстательной железы была исключена с использованием пробы на ПСА и пальцевой пальпации. Пищевую добавку применяли по 45 г в день в течение 14 дней. Из всех 10 пациентов с невысоким (балл по IPSS 2-7) и умеренным (балл по IPSS 8-19) уровнем расстройств мочевыводящих путей, у 3/7, соответственно, на 50-60% улучшилось состояние в отношении расстройств мочевыводящих путей после приема пищевой добавки (p=0,003) по «международной шкале простатических симптомов», при этом было обнаружено, что значительные положительные изменения произошли в отношении потребности в мочеиспускании в ночное время (в среднем 87,5%).
Общий обзор всех клинических испытаний
Пищевые продукты и пищевые добавки, содержащие L. plantarum МСС1 и L. gasseri MCC2 являются гипоаллергенными, снижают уровень ОкС и обладают статистически достоверным эффектом на проблемы с предстательной железой у лиц с умеренным уровнем жалоб, связанных с нижними мочевыводящими путями, и с ведущими симптомами раздражения.





Группа изобретений относится к штаммам микроорганизмов Lactobacillus plantarum MCC1 DSM 23881 и Lactobacillus gasseri MCC2 DSM 23882 и их применению в качестве антиоксидантных протеолитических ингредиентов для приготовления пищевого продукта или пищевой добавки. Штаммы вырабатывают конъюгированную линолевую кислоту (CLA), пероксид водорода (H2O2) и монооксид азота (NO). Пищевые продукты и пищевые добавки, содержащие указанные штаммы вместе или по отдельности, являются гипоаллергенными, уменьшают аллергию на молоко и симптомы раздражения нижних мочевыводящих путей у мужчин зрелого возраста, сопутствующие доброкачественной гиперплазии предстательной железы, и ассоциированный с ними окислительный стресс и воспаление. Предложены также способы получения пищевого продукта или пищевой добавки. Группа изобретений относится к области биотехнологии и может быть использована в пищевой промышленности. 10 н. и 3 з.п. ф-лы, 6 ил., 13 табл., 6 пр.
1. Штамм микроорганизма Lactobacillus plantarum МСС1 DSM 23881, который вырабатывает конъюгированную линолевую кислоту (CLA), пероксид водорода (H2O2) и монооксид азота (NO) для применения в качестве антиоксидантного и протеолитического ингредиента пищевого продукта или пищевой добавки.
2. Штамм микроорганизма Lactobacillus gasseri МСС2 DSM 23882, который вырабатывает конъюгированную линолевую кислоту (CLA), пероксид водорода (H2O2) и монооксид азота (NO) для применения в качестве антиоксидантного и протеолитического ингредиента пищевого продукта или пищевой добавки.
3. Микроорганизм по п.1 или 2 в умерщвленной форме.
4. Композиция для приготовления пищевого продукта или пищевой добавки, содержащая два микроорганизма по пп.1-3, причем содержание обоих микроорганизмов находится в диапазоне 0,4-0,6 объемных процента, при этом количество микроорганизмов штамма Lactobacillus plantarum МСС1 находится в диапазоне 0,2×108-2,4×108 КОЕ/мл, а количество микроорганизмов штамма Lactobacillus gasseri МСС2 находится в диапазоне 0,4×107-0,6×108 КОЕ/мл.
5. Применение микроорганизма по п. 1 и/или 2 вместе или по отдельности в качестве антиоксидантного протеолитического ингредиента для приготовления пищевого продукта или пищевой добавки.
6. Применение микроорганизма по пп.1-3 вместе или по отдельности в качестве антиоксидантного протеолитического ингредиента для приготовления гипоаллергенного, уменьшающего аллергию на молоко пищевого продукта или пищевой добавки.
7. Применение микроорганизма по пп.1-3 вместе или по отдельности в качестве антиоксидантного протеолитического ингредиента для приготовления пищевого продукта или пищевой добавки, уменьшающих у мужчин зрелого возраста симптомы раздражения нижних мочевыводящих путей, сопутствующие доброкачественной гиперплазии предстательной железы, и ассоциированный с ними окислительный стресс и воспаление.
8. Способ приготовления пищевого продукта, уменьшающего аллергию на молоко, включающий в себя этапы, на которых:
A) нагревают исходную смесь, содержащую молочный белок (37±2°С);
B) в качестве протеолитического ингредиента добавляют 1 объемный процент микроорганизмов по п.1 с количеством микроорганизмов 0,4×108-4,8×108 КОЕ/мл и/или микроорганизмов по п.2 с количеством микроорганизмов 0,8×107-1,2×108 КОЕ/мл или микроорганизмов по п.1 и микроорганизмов по п.2 вместе соответственно по 0,25×108-2×108 КОЕ/мл и 0,5×107-0,5×108 КОЕ/мл;
C) полученную смесь ферментируют при температуре 37±2°С в течение 18-26 часов;
D) пастеризуют смесь при температуре 82±2°С в течение 30-35 минут и охлаждают до температуры 20-30°С;
E) ароматизируют смесь добавкой и охлаждают полученный пищевой продукт до 2-6°С.
9. Способ приготовления пищевой добавки, уменьшающей аллергию на молоко, включающий в себя этапы, на которых:
A) нагревают исходную смесь, содержащую молочный белок (37±2°С);
B) в качестве протеолитического ингредиента добавляют 1 объемный процент микроорганизмов по п.1 с количеством микроорганизмов 0,4×108-4,8×108 КОЕ/мл и/или микроорганизмов по п.2 с количеством микроорганизмов 0,8×107-1,2×108 КОЕ/мл или микроорганизмов по п.1 и микроорганизмов по п.2 вместе соответственно по 0,25×108-2×108 КОЕ/мл и 0,5×107-0,5×108 КОЕ/мл;
C) полученную смесь ферментируют при температуре 37±2°С в течение 18-26 часов;
D) пастеризуют смесь при температуре 82±2°С в течение 30-35 минут и охлаждают до температуры 20-30°С;
E) ароматизируют смесь добавкой и охлаждают полученный пищевой продукт до 2-6°С;
F) для приготовления порошкообразной пищевой добавки удаляют воду из смеси до получения порошкообразной консистенции, а для приготовления жидкой пищевой добавки частично удаляют воду из смеси до получения желаемой консистенции.
10. Способ приготовления пищевого продукта, уменьшающего проблемы с мочевыводящими путями у мужчин зрелого возраста и окислительный стресс и воспаление, ассоциированные с ними, включающий в себя этапы, на которых:
A) нагревают исходную смесь, содержащую молочный белок (37±2°С);
B) в качестве протеолитического ингредиента добавляют 1 объемный процент микроорганизмов по п.1 с количеством микроорганизмов 0,4×108-4,8×108 КОЕ/мл и/или микроорганизмов по п.2 с количеством микроорганизмов 0,8×107-1,2×108 КОЕ/мл или микроорганизмов по п.1 и микроорганизмов по п.2 вместе соответственно по 0,25×108-2×108 КОЕ/мл и 0,5×107-0,5×108 КОЕ/мл;
C) полученную смесь ферментируют при температуре 37±2°С в течение 18-26 часов;
D) пастеризуют смесь при температуре 82±2°С в течение 30-35 минут и охлаждают до температуры 20-30°С;
E) ароматизируют смесь добавкой и охлаждают полученный пищевой продукт до 2-6°С.
11. Способ приготовления пищевой добавки, уменьшающей проблемы с мочевыводящими путями у мужчин зрелого возраста и окислительный стресс и воспаление, ассоциированные с ними, включающий в себя этапы, на которых:
A) нагревают исходную смесь, содержащую молочный белок (37±2°С);
B) в качестве протеолитического ингредиента добавляют 1 объемный процент микроорганизмов по п.1 с количеством микроорганизмов 0,4×108-4,8×108 КОЕ/мл и/или микроорганизмов по п.2 с количеством микроорганизмов 0,8×107-1,2×108 КОЕ/мл или микроорганизмов по п.1 и микроорганизмов по п.2 вместе соответственно по 0,25×108-2×108 КОЕ/мл и 0,5×107-0,5×108 КОЕ/мл;
C) полученную смесь ферментируют при температуре 37±2°С в течение 18-26 часов;
D) пастеризуют смесь при температуре 82±2°С в течение 30-35 минут и охлаждают до температуры 20-30°С;
E) ароматизируют смесь добавкой и охлаждают полученный пищевой продукт до 2-6°С;
F) для приготовления порошкообразной пищевой добавки удаляют воду из смеси до получения порошкообразной консистенции, а для приготовления жидкой пищевой добавки частично удаляют воду из смеси до получения желаемой консистенции.
12. Способ по пп. 8, 9, 10 или 11, в котором добавка со стадии (Е) представляет собой фруктовый или ягодный сок, концентрат, сироп или напиток на основе сока или фруктовый или ягодный джем, предпочтительно облепиховый, черничный или малиновый сок.
13. Способ по пп. 8, 9, 10 или 11, в котором источником молочного белка исходной смеси на стадии (А) является молочная сыворотка, концентрированная молочная сыворотка, порошок молочной сыворотки, молоко, молочный порошок или концентрат молочного белка.
| WO 2006041930 A2, 20.04.2006 | |||
| EP 2000530 A1, 10.12.2008 | |||
| СПОСОБ ПРОИЗВОДСТВА ШВЕЛЛЕРОВ | 1999 |
|
RU2169050C2 |
| ПРОБИОТИЧЕСКИЕ ШТАММЫ Lactobacillus (ВАРИАНТЫ) И ИХ ПРИМЕНЕНИЕ | 2003 |
|
RU2316586C2 |
| Способ выделения волокон из лубовых растений | 1926 |
|
SU6037A1 |
Авторы
Даты
2016-11-20—Публикация
2012-02-23—Подача