Изобретение относится к рекомбинантному штамму вируса осповакцины (ВОВ), продуцирующему секретируемый гранулоцитарно-макрофагальный колониестимулирующий фактор (ГМ-КСФ) человека и онкотоксический белок лактаптин и обладающему онколитической активностью в отношении опухолей человека, и может быть использовано в биотехнологии, в частностиив генетической инженерии для разработки лекарственных средств нового поколения для борьбы с онкологическими заболеваниями, в частности раком молочной железы.
Конструирование рекомбинантных штаммов ВОВ с целью создания на их основе противоопухолевых препаратов является перспективным направлением биотехнологии. Ряд таких штаммов в настоящее время успешно проходят клинические испытания за рубежом (Parato, 2012 [1]). Наиболее изученным среди рекомбинантных ВОВ является штамм JX-594, (Jennerex Biotherapeutics, Inc.) полученный на основе американского вакцинного штамма Wyeth и несущий ген гранулоцито-макрофагального колониетимулирующего фактора (ГМ-КСФ) человека в структурной части гена вирусной тимидинкиназы (tk-ген) под контролем ранне-позднего синтетического промотора BOB (Mastrangelo, 2000 [2]). Кроме гена ГМ-КСФ в структурную часть tk-гена данного штамма встроен также ген β-галактозидазы E. coli под контролем природного промотора ВОВ р7.5К. Этот штамм разработан в американской компании Jennerex Biotherapeutics и французской компании Transgene и получил коммерческое название pexastimogene devacirepvec - Pexa-Vec. Первые клинические испытания Pexa-Vec были проведены Mastrangelo с соавторами в США при интратуморальном введении неоперабельным больным с меланомой (Mastrangelo, 2002 [3]). В этом исследовании была показана безопасность многократного интратуморального введения Pexa-Vec, функциональная активность ГМ-КСФ и регрессия опухолей. Дальнейшие исследования включали I и II фазы клинических испытаний как меланомы, так и солидных опухолей - гепатоцеллюлярной карциномы, которые продемонстрировали, что Pexa-Vec оказывает противоопухолевый эффект не только при интратуморальном, но также и при внутривенном введении, несмотря на наличие нейтрализующих антител у вакцинированных против оспы пациентов (Breitbach, 2011; Нео, 2013; Hwang, 2011; Park, 2008 [4-7]).
Pexa-Vec продемонстрировал способность реплицироваться в опухоли даже после девяти циклов интратуморального введения, несмотря на наличие высоких титров антител в крови (Hwang, 2011 [6]). У пациентов не было выявлено побочных эффектов при введении высоких доз вируса Pexa-Vec: 2×109 БОЕ (внутривенно) или 1×109 БОЕ (интратуморально). Напротив, наблюдался дозозависимый терапевтический эффект, который коррелировал с увеличением времени выживания пациентов. Внутривенное введение обеспечивало доставку вируса в метастазирующие опухоли, где он реплицировался и экспрессировал ГМ-КСФ дозозависимым образом, не затрагивая нормальные ткани, поскольку негативный по тимидинкиназе (ТК-) вирус преимущественно реплицируется в делящихся раковых клетках (Breitbach, 2011 [4]). Интратуморальное введение также приводило к выходу вируса в кровоток, что позволяло ему достигать отдаленных неинъецированных частей опухоли и метастазов (Breitbach, 2011 [4]; Park, 2008 [7]). Терапевтическая эффективность Pexa-Vec обуславливается его прямым онколитическим действием, ГМ-КСФ индуцированным усилением противоопухолевого иммунитета, а также антиваскулярным эффектом вируса в опухолевых узлах (Liu, 2008 [8]; Parato, 2012 [1]; Hou, 2014 [9]).
Однако проведенная недавно в США II фаза клинических испытаний Pexa-Vec на группе больных с гепатокарциномой не выявила ожидаемого противоопухолевого эффекта (Chan, 2014 [10]), что, возможно, связано с поздней стадией болезни пациентов, а также с недостаточной литической активностью штамма Wyeth ВОВ, на основе которого был сконструирован Pexa-Vec.
Из источников научно-технической информации известен другой подход к созданию онколитических ВОВ, основанный на использовании более вирулентных штаммов ВОВ, например WR, но при этом, кроме гена тимидинкиназы, делетируются и другие гены - факторы вирулентности. Показано, что сочетанное подавление генов тимидинкиназы и ростового фактора ВОВ приводит к практически полному отсутствию репликации вируса в неделящихся клетках (McCart, 2007 [11]), при этом эффективность разрушения раковых клеток такими двойными мутантами (VVdd) не отличалась от исходного штамма. Штамм VVdd показал более высокую онколитическую эффективность в доклинических исследованиях, чем Pexa-Vec (Thorne, 2007 [12]).
Однако этот штамм создан на основе высоковирулентного штамма ВОВ WR (Western Reserve), что осложняет его широкое использование в медицинской практике, особенно для иммунодефицитных раковых пациентов. Кроме того, штамм VVdd не содержит встроек трансгенов, которые способствовали бы усилению его адресной онколитической активности.
На основе VVdd был сконструирован штамм JX-963, в котором в районе делеции tk-гена проведена встройка гена ГМ-КСФ человека. Этот штамм также разработан в американской компании Jennerex Biotherapeutics и в настоящее время проходит I фазу клинических испытаний для пациентов с солидными опухолями (Russell, 2012 [13]). На основе VVdd создан еще один онколитический штамм vvDD-CDSR, в котором вместо гена вирусного ростового фактора (virus growth factor, VGF) встроен ген цитозиндезаминазы дрожжей. Этот фермент катализирует превращение пролекарства 5-фторцитозина в 5-фторурацил, который является токсичным для активно реплицирующихся клеток и широко используется при лечении многочисленных форм рака. Пролекарство 5-фторцитозин не оказывает нежелательных побочных токсических проявлений в нормальных тканях человека (Lee, 2010 [14]). Штамм vvDD-CDSR показал высокую эффективность в отношении педиатрических солидных опухолей и в настоящее время также проходит I фазу клинических испытаний в США в комбинации с химиотерапией (Lun, 2013 [15]).
Таким образом, создание противоопухолевого препарата целесообразно проводить на основе литически активного (вирулентного) штамма ВОВ с двойной делецией генов тимидинкиназы и ростового фактора, что обеспечит аттенуацию вируса и безопасность его использования для иммунодефицитных раковых больных. Для усиления противоопухолевой активности рекомбинантных ВОВ целесообразно также введение в качестве трансгена гена ГМ-КСФ и цитотоксических генов, обеспечивающих специфическую гибель раковых клеток.
Авторы настоящей заявки на изобретение в своей работе использовали средний по вирулентности штамм ВОВ Л-ИВП (Маренникова, Щелкунов, 1998 [16]), который широко применялся для вакцинации людей против оспы в России до 1980 года, когда такая вакцинация была прекращена вследствие ликвидации оспы на земном шаре. Таким образом, штамм Л-ИВП имеет хорошую многолетнюю медицинскую историю применения в России, что будет способствовать облегчению условий проведения клинических испытаний препаратов на его основе.
Наиболее близким аналогом (прототипом) является рекомбинантный штамм VV-GMCSF-S1/3 (заявка на изобретение №2013132993, МПК C12N 15/27, опубл. 27.01.2015 г.) [17], сконструированный на основе штамма Л-ИВП вируса осповакцины, содержащий встройку гена ГМ-КСФ человека, структура которого соответствует кДНК матричной РНК ГМ-КСФ человека, представленной в GenBank под номером M11220.1, в центральной части гена вирусной тимидинкиназы между позициями 83665 и 83696 п.н. (GenBank Аcc. DQ121394); ген ГМ-КСФ человека экспрессируется под контролем природного промотора р7.5K вируса осповакцины и продуцирует секретируемую форму биологически активного ГМ-КСФ человека в клетках млекопитающих на уровне 40 мкг на мл культуральной среды; штамм VV-GMCSF-S1/3 депонирован в Государственной коллекции Роспотребнадзора возбудителей вирусных инфекций, риккетсиозов ФБУН ГНЦ ВБ «Вектор» под номером V-631.
Однако рекомбинантный онколитический штамм-прототип не обеспечивает дополнительную аттенуацию (ослабление) вируса в отношении нормальных клеток и дополнительное усиление литической активности в отношении раковых клеток вследствие отсутствия в его конструкции цитотоксических генов, обеспечивающих дополнительную специфическую гибель раковых клеток.
Техническим результатом заявляемого изобретения является обеспечение дополнительной аттенуации (ослабления) рекомбинантного онколитического вируса ВОВ в отношении нормальных клеток и усиление его литической активности в отношении раковых клеток.
Указанный технический результат достигается созданием двойного рекомбинантного штамма VV-GMCSF-Lact, сконструированного на основе умеренно патогенного российского штамма Л-ИВП вируса осповакцины, содержащего делеции фрагментов генов вирусной тимидинкиназы и ростового фактора, в районы которых встроены: ген гранулоцитарно-макрофагального колониестимулирующего фактора (ГМ-КСФ) человека, структура которого соответствует кДНК матричной РНК ГМ-КСФ человека (GenBank Аcc. M11220.1), в центральной части гена вирусной тимидинкиназы между позициями 81277 и 81308 п.н. (GenBank Аcc. KP233807.1); ген ГМ-КСФ человека экспрессируется под контролем природного промотора Р7.5k вируса осповакцины и продуцирует секретируемую форму биологически активного ГМ-КСФ человека в клетках млекопитающих; ген лактаптина, кодирующий фрагмент каппа-казеина человека 23-134 а.о., в левом концевом районе вирусного генома между позициями 7770 и 8071 п.н. (GenBank Аcc. KP233807.1); ген лактаптина экспрессируется под контролем синтетического промотора вируса осповакцины P7.5synth и продуцирует онкотоксический рекомбинантный белок лактаптин; штамм VV-GMCSF-Lact обладает высокой онколитической активностью в отношении клеток рака молочной железы человека и депонирован в Государственной коллекции возбудителей вирусных инфекций и риккетсиозов ФБУН ГНЦ ВБ «Вектор» под номером V-688.
Встройка в качестве трансгена гена лактаптина в район делеции гена вирусного ростового фактора будет способствовать как дополнительной аттенуации (ослаблению) вируса в отношении нормальных клеток, так и усилению его литической (цитотоксической) активности в отношении клеток рака молочной железы.
Лактаптин является фрагментом каппа-казеина молока человека (23-134 а.о.), который специфически индуцирует гибель клеток рака молочной железы человека in vitro и in vivo (Koval, 2014 [18]). Встройка в качестве трансгена гена лактаптина в район делеции гена вирусного ростового фактора будет способствовать как дополнительной аттенуации (ослаблению) вируса в отношении нормальных клеток, так и усилению его литической (цитотоксической) активности в отношении раковых клеток, как было показано нами ранее при использовании другого апоптоз-индуцирующего белка - апоптина (Кочнева, 2013 [19]).
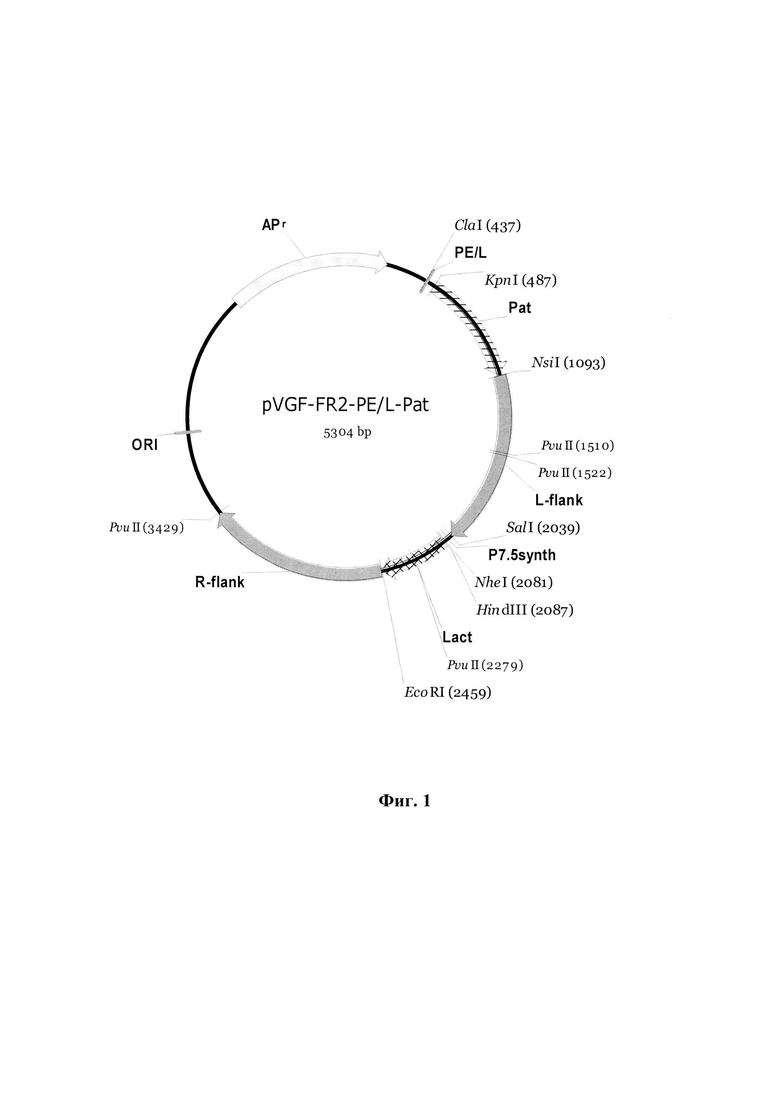
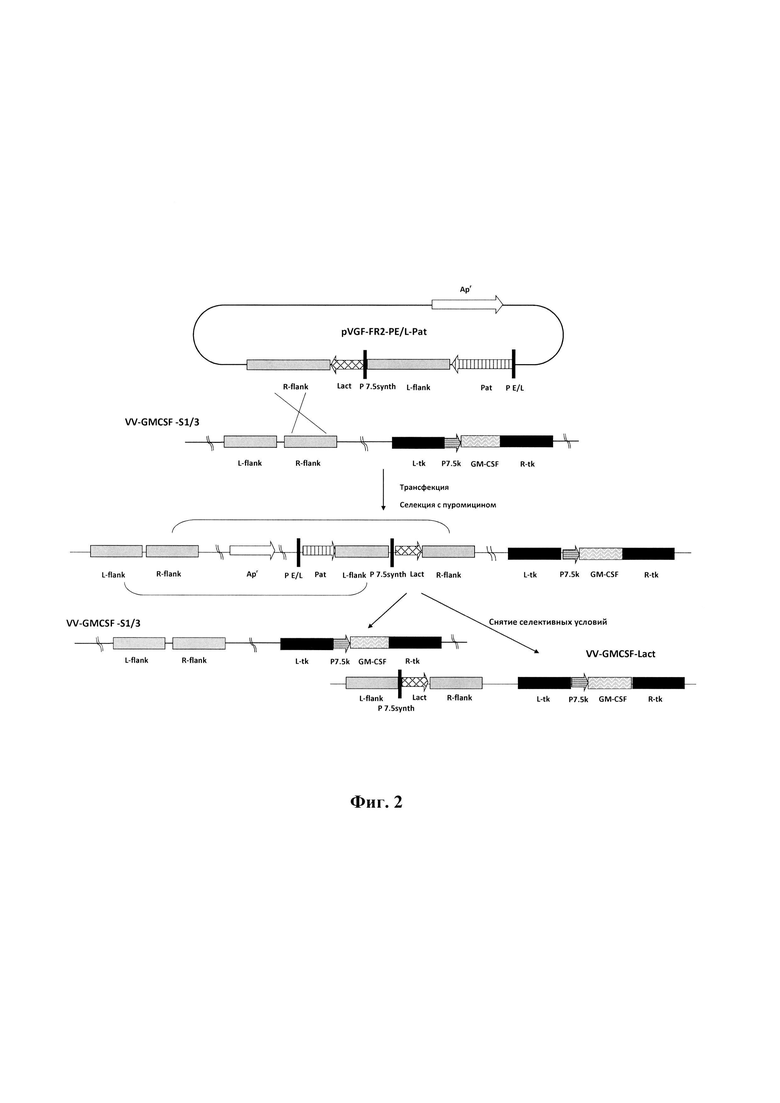
Штамм VV-GMCSF-Lact образуется за счет одиночного кроссинговера между ДНК штамма VV-GMCSF-S1/3 и плазмидной ДНК pVGF-FR2-PE/L-Pat (фиг. 1) в цитоплазме клеток CV-1, последующей селекции полученной нестабильной конструкции с добавлением в культуральную среду пуромицина за счет наличия в ней гена устойчивости к этому антибиотику (Pat) (Кочнева, 2013 [19]) и внутримолекулярной рекомбинации после снятия селективных условий (фиг. 2).
Штамм VV-GMCSF-Lact характеризуется следующими признаками:
Морфологические признаки. Штамм обладает свойствами типичного представителя ВОВ, но в отличие от векторного вируса имеет фенотип ТК- ГМКСФ+VGF-Lact+ (фиг. 3А). Показано, что при заражении клеток почки китайского хомячка ВНК штамм VV-GMCSF-Lact продуцирует ГМ-КСФ и лактаптин.
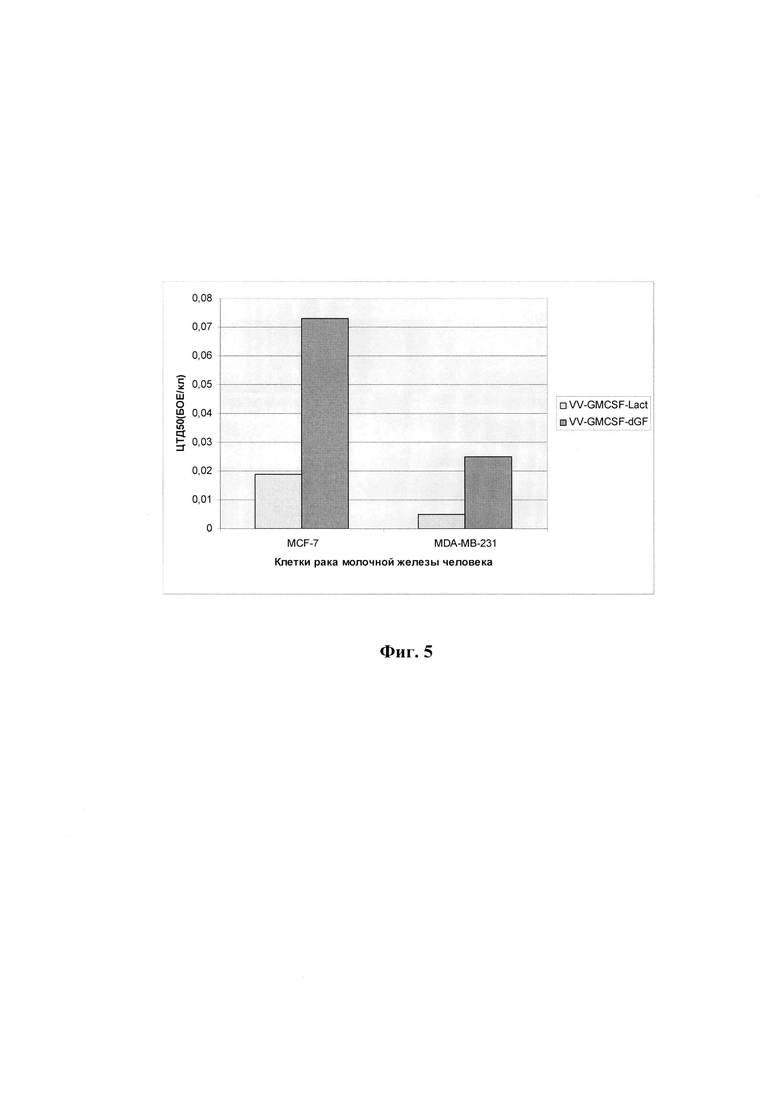
Физиолого-биохимические характеристики и культуральные свойства штамма. ДНК рекомбинантного ВОВ имеет длину около 200000 п.н. Наличие в его геноме дополнительной встройки оперона лактаптина длиной 414 п.н. и стабильность этой встройки при 20-кратном пассировании вируса на клетках CV-1 подтверждены с помощью метода ПЦР (фиг. 3Б). Экспрессия гена лактаптина подтверждена иммуногистохимическим анализом клеток почки китайского хомячка ВНК, инфицированных рекомбинантом VV-GMCSF-Lact. Для выявления лактаптина использовали моноклональные антитела anti-RL2 (Koval, 2014 [18]) (фиг. 4). Встройка гена лактаптина обеспечивает повышенную онкотоксическую активность штамма W-GMCSF-Lact в отношении клеток рака молочной железы человека MCF7 и MDA-MB-231 (фиг. 5). Для сравнения использовали специально сконструированный рекомбинант VV-GMCSF-dGF, в котором имеется встройка гена ГМ-КСФ человека в районе гена вирусной тимидинкиназы (аналогично VV-GMCSF-1/3) и делеция гена вирусного ростового фактора (аналогично ранее описанному варианту VVdGF2/6 (Кочнева, 2013 [19]), но отсутствует встройка гена лактаптина. Как следует из фиг. 5, цитотоксическая активность в отношении клеток рака молочной железы штамма VV-GMCSF-Lact в 4-5 раз выше (ЦТД50 0,019-0,005 БОЕ/кл.), чем штамма VV-GMCSF-dGF (ЦТД50 0,073-0,025 БОЕ/кл.).
Изобретение иллюстрируется следующими фигурами графических изображений:
- Фиг. 1. Физическая и генетическая карта плазмиды pVGF-FR2-PE/L-Pat. L-flank - ПЦР-фрагмент генома ВОВ штамма Л-ИВП длиной 944 п.н., соответствующий позициям нуклеотидов 6827-7770 депонированного в GenBank штамма L-IVP (Асс. KP233807.1), расположенный слева от гена VGF (ген VGF имеет длину 423 п.н. и соответствует позициям нуклеотидов 7801-8223 в GenBank Аcc. KP233807.1), и фланкированный сайтами узнавания эндонуклеаз рестрикции Nsil и SalI; R-flank - ПЦР-фрагмент генома ВОВ длиной 962 п.н., соответствующий позициям нуклеотидов 8071-9032 (GenBank Аcc. KP233807.1), расположенный справа от гена вирусного ростового фактора и фланкированный сайтами узнавания эндонуклеаз рестрикции EcoRI и PvuII; P7.5synth (36 п.н.) и PE/L (41 п.н.) - синтетические ранний и ранне-поздний промоторы BOB (Merchlinsky, 1997 [20]); Lact - фрагмент гена каппа-казеина (23-134 а.о.), содержащий лактаптин с добавлением последовательности, кодирующей Gly-Gly-Ser-6His и стоп-кодона на С-конце и ATG-кодона на N-конце, размер 366 п.н. (Semenov, 2010 [21]); Pat - ген пуромицин N-ацетилтрансферазы, определяющий устойчивость к пуромицину; APr - ген β-лактамазы, определяющий устойчивость к ампициллину; ORI - область начала репликации.
- Фиг. 2. Схема конструирования рекомбинантного штамма VV-GMCSF-Lact ВОВ методом временной доминантной селекции с использованием в качестве маркера гена устойчивости к пуромицину (Pat). L-flank и R-flank - фрагменты генома ВОВ, штамм Л-ИВП, фланкирующие ген VGF слева и справа соответственно (как на фиг. 1); Lact - ген лактаптина (как на фиг. 1); P7.5synth и PE/L - синтетические промоторы ВОВ (как на фиг. 1); Pv - природный промотор BOB; L-tk и R-tk - последовательности генома ВОВ штамм Л-ИВП, фланкирующие ген тимидинкиназы слева и справа соответственно; GM-CSF - ген ГМ-КСФ человека.
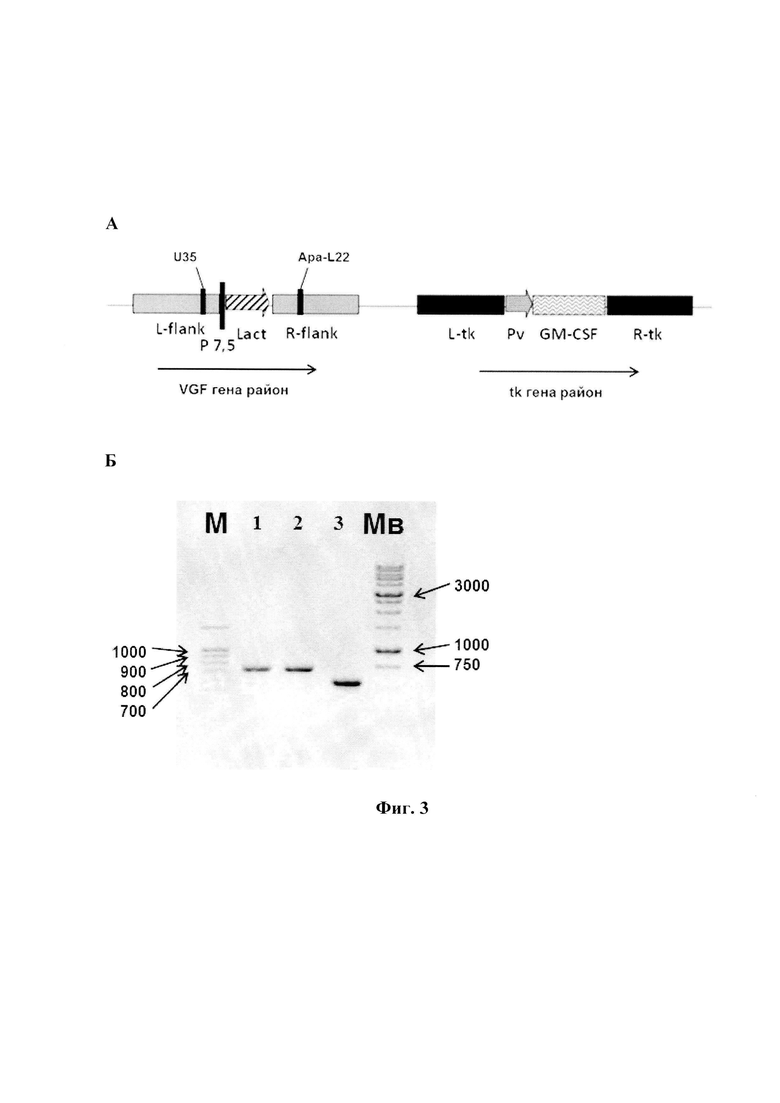
- Фиг. 3. Структура рекомбинантного штамма VV-GMCSF-Lact. А - схема генома с указанием позиций праймеров (подписи как на фиг. 2). Б - результаты ПЦР-анализа рекомбинантов с использованием пары праймеров Up35×Apa-L22. Стабильность встройки гена лактаптина подтверждена в течение 20 пассажей на культуре клеток CV-1. М и Мв - контроли молекулярных весов фрагментов ДНК: М-3000, 1500, 1000, 900, 800, 700…100 п.н.; Мв-10т, 8т, 6т, 5-3т, 2.5т, 2т, 1.5т, 1т, 750, 500, 250 п.н.; 1-2 дорожки - VV-GMCSF-Lact, фрагмент 710 п.н. (3 и 20 пассажи, соответственно); 3 дорожка - исходный штамм VV-GMCSF-S1/3, фрагмент 584 п.н.
- Фиг. 4. Иммуногистохимический анализ клеток ВНК, инфицированных рекомбинантными штаммами вируса осповакцины. В качестве отрицательного контроля использовали инфекцию клеток рекомбинантом VV-GMCSF-S1/3, не содержащим встройки гена лактаптина. Парафиновые срезы, окраска хромогеном АЕС (клетки с лактаптином окрашены в красный цвет) и гематоксилином Эрлиха.
- Фиг. 5. Онколитическая активность рекомбинантного штамма VV-GMCSF-Lact в клетках рака молочной железы человека. Клетки выращивали в 96-ти луночных планшетах, инфицировали 10-кратными разведениями вируса в диапазоне доз 0,001-10 БОЕ на клетку и рассчитывали 50%-ную цитотоксическую дозу для каждого вируса (ЦТД50) в фотометрическом тесте с использованием субстрата для митохондриальных дегидрогеназ 2,3-бис-(2-метокси-4-нитро-5-сульфофенил)-2Н-тетразолий-5-карбоксанилида (реагент ХТТ).
Для лучшего понимания сущности изобретения ниже следуют примеры его осуществления.
Пример 1. Конструирование рекомбинантной плазмидной ДНК pVGF-FR2-PE/L-Pat.
Плазмида pVGF-FR2-PE/L-Pat была получена на основе pXJP5.2 (Заявка на патент РФ №2013132993 [17]). На первом этапе правый и левый ТК-фланки pXJP5.2 были заменены на фрагменты генома ВОВ, расположенные слева (L-фланк) и справа (R-фланк) от гена VGF. Матрицей для амплификации фрагментов служила ДНК ВОВ штамма Л-ИВП (GenBank Acc. KP233807.1), праймеры для амплификации имели следующую структуру:
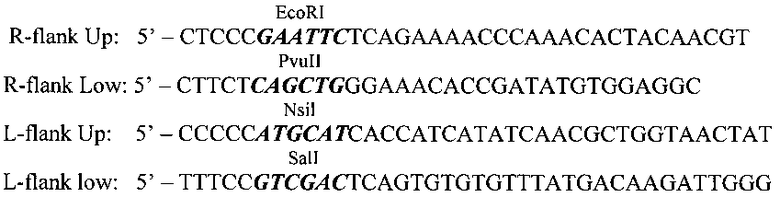
В структуры праймеров были введены сайты узнавания эндонуклеаз рестрикции для встраивания их в вектор pXJP5.2.
На втором этапе природный промотор BOB Р7.5 в плазмиде pXJP5.2 был заменен на синтетический P7.5synth с целью предотвращения внутримолекулярной нестабильности рекомбинантного штамма VV-GMCSF-Lact, в котором природный промотор используется для экспрессии гена ГМ-КСФ. Для проведения замены промотора были синтезированы два олигонуклеотда, которые при отжиге образуют следующую структуру:
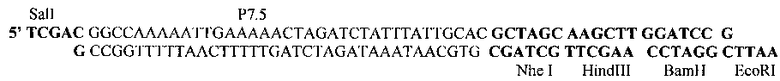
Полученный дуплекс был встроен в pXJP5.2 по SalI - EcoRI сайтам рестрикции. Далее в плазмиду по ClaI-сайту был встроен ген Pat под контролем синтетического промотора PE/L (Merchlinsky, 1997 [20]). Для этой цели сначала были синтезированы два олигонуклеотда, которые содержали нуклеотидную последовательность промотора PE/L и сайты узнавания ряда рестриктаз. При отжиге они образуют дуплекс следующей структуры:
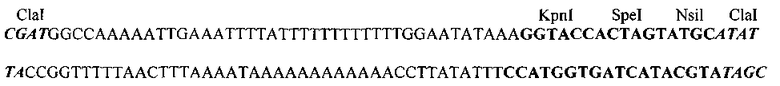
После встройки этого дуплекса по ClaI-сайту в полученную плазмиду по KpnI - Nsil сайтам был встроен ген Pat. Фрагмент ДНК, содержащий ген Pat получали методом ПЦР на матрице pGEM-Puro-DS-Apo (Чумаков, 2013 [22]) с использованием пары праймеров, в состав которых введены сайты узнавания рестриктаз KpnI и Nsil:
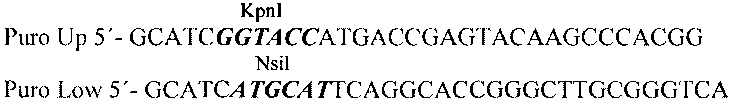
Полученная в результате лигирования плазмидная ДНК, обозначенная как pVGF-PE/L-Pat, содержит ген Pat под контролем синтетического ранне-позднего промотора PE/L (для селекции рекомбинантных клонов ВОВ), левый и правый фланки гена VGF для гомологичной рекомбинации с вирусной ДНК, приводящей к делеции фрагмента гена VGF размером 170 п.н., соответствующего позициям нуклеоти дов 7801-8071 (GenBank Аcc. KP233807.1), синтетический ранне-поздний промотор P7.5synth и следующий за ним полилинкер для встройки трансгенов; селективный маркер - ген устойчивости к ампициллину.
В плазмиду pVGF-PE/L-Pat по HinIII - EcoRI сайтам под контроль промотора P7.5synth был встроен ген лакаптина (Lact), полученный методом ПЦР на матрице плазмидной ДНК pGSDI/RL2 (Semenov, 2010 [21]) с использованием пары праймеров, обеспечивающих наличие в амплификационном фрагменте сайтов рестрикции HindIII и EcoRI:
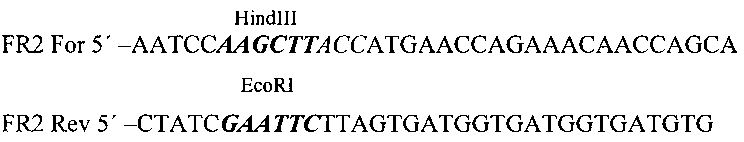
Структура сконструированной плазмидной ДНК, обозначенной как pVGF-FR2-PE/L-Pat (фиг. 1), подтверждена секвенированием района встройки.
Пример 2. Трансфекция клеток CV-1 рекомбинантной плазмидой pVGF-FR2-PE/L-Pat и получение рекомбинантного штамма BOB VV-GMCSF-Lact.
Для проведения трансфекции ДНК плазмиды pVGF-FR2-PE/L-Pat была наработана в препаративных количествах из 1000 мл среды Лурия-Бертани и выделена с использованием набора лабораторных реагентов для выделения плазмидной ДНК, очищенной от эндотоксинов «EndoFree Pksmid Maxi Kit (Qiagen).
Рекомбинантные BOB получали с использованием реагента для трансфекции Lipofectamine™ LTX, 1 мл и реагент Plus (Invitrogen). Трансфекцию проводили на 90%-ном монослое клеток CV-1, выращенном в шестилуночных планшетах (Greiner). Клетки инфицировали вирусом осповакцины с множественностью 0,05 БОЕ/клетка, и через 1 час инкубации при 37°С добавляли смесь плазмидной ДНК (5 мгк) + липофектамин (20 мкл) + Реагент Plus в соответствии с рекомендацией производителя в 1 мл среды Opti-MEM (Invitrogen). Через 1 час инкубации при 37°С в лунки добавляли еще 2 мл среды Opti-MEM и инкубировали при 37°С в атмосфере 5% СО2 еще 24-36 часов до развития цитопатического действия (ЦПД). Материал трижды замораживали-оттаивали и обрабатывали ультразвуком для получения гомогенной вирусной суспензии. Далее проводили селекцию рекомбинантов путем трехкратного пассирования на монослое клеток CV-1 с добавлением пуромицина (Sigma) в концентрации 10 мкг/мл среды DMEM (Invitrogen). Вирус клонировали методом бляшек под твердым агаровым покрытием и анализировали на наличие встройки гена лактаптина методом ПЦР с использованием праймеров 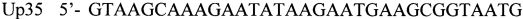
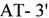 и
и 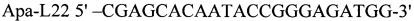 . Вирусную ДНК для проведения ПЦР выделяли с использованием наборов «РИБО-сорб» (ЗАО «Интерлабсервис»). Размер амплифицированного фрагмента ДНК исходного BOB VV-GMCSF-S1/3 составлял 584 п.н. (фиг. 3), а рекомбинантного вируса со встройкой гена лактаптина - 710 п.н. Отобранный рекомбинантный вариант VV-GMCSF-Lact дважды реклонировали, чтобы избежать следовых примесей исходного вируса, нарабатывали на монослое клеток CV-1 и очищали центрифугированием в градиенте плотности сахарозы (25-40%). Титр вируса определяли методом бляшек на монослое клеток CV-1, окрашенном фиксирующим раствором кристаллического фиолетового (2 г/л кристаллический фиолетовый, 50 мл/л формальдегид, 100 мл/л этанол, вода). Очищенный рекомбинантный штамм BOB VV-GMCSF-Lact с титром 109 БОЕ/мл хранится в расфасованном виде при -80°С.
. Вирусную ДНК для проведения ПЦР выделяли с использованием наборов «РИБО-сорб» (ЗАО «Интерлабсервис»). Размер амплифицированного фрагмента ДНК исходного BOB VV-GMCSF-S1/3 составлял 584 п.н. (фиг. 3), а рекомбинантного вируса со встройкой гена лактаптина - 710 п.н. Отобранный рекомбинантный вариант VV-GMCSF-Lact дважды реклонировали, чтобы избежать следовых примесей исходного вируса, нарабатывали на монослое клеток CV-1 и очищали центрифугированием в градиенте плотности сахарозы (25-40%). Титр вируса определяли методом бляшек на монослое клеток CV-1, окрашенном фиксирующим раствором кристаллического фиолетового (2 г/л кристаллический фиолетовый, 50 мл/л формальдегид, 100 мл/л этанол, вода). Очищенный рекомбинантный штамм BOB VV-GMCSF-Lact с титром 109 БОЕ/мл хранится в расфасованном виде при -80°С.
Пример 3. Оценка экспрессии гена лактаптина рекомбинантным штаммом BOB VV-GMCSF-Lact.
Иммуногистохимический анализ проводили в клетках почки китайского хомячка ВНК, которые высокочувствительны к репликации VACV. В качестве первичных антител использовали моноклональные антитела мыши anti-RL2 к рекомбинантному лактаптину (Koval, 2014 [18]).
Подготовку проб для иммуногистохимического анализа проводили следующим образом:
- монослой клеток ВНК выращивали в культуральных матрасах V=550 мл (Greiner) из расчета по 3 матраса на точку;
- клетки инфицировали рекомбинантным вирусом с множественностью 0,5 БОЕ/клетка и инкубировали 1 час при 5°С до полной сорбции вируса и с целью синхронизации инфекции (вирус при температуре 5°С способен сорбироваться на клетке, но не способен проникать в нее, таким образом, прединкубация при пониженной температуре способствует удержанию вируса на поверхности клетки, а последующее перемещение в термостат при 37°С обеспечивает одновременное проникновение сорбированного вируса на всех клетках вируса и синхронное развитие инфекции);
- матрасы переносили в термостат и инкубировали при 37°С в течение 50 часов до появления 70%-ного ЦПД;
- клетки снимали скребком и осаждали цинтрифугированием при 1500 об/мин 10 мин;
- осадки фиксировали в 4% растворе параформальдегида.
Зафиксированные клетки обезвоживали в процессоре Sakura Tissue-TEK II (Sakura), заключали в среду Гистомикс (БиоВитрум), и с блоков готовили срезы на микротоме Leica RM 2255 (Leica). Для иммуногистохимических реакций парафиновые срезы монтировали на стекла, покрытые полилизином (Thermo Scientific). Срезы обрабатывали моноклональными антителами anti-RL2 в концентрации 2,5 мкг/мл. Продукт реакции выявляли с помощью стрептавидинконъюгированной пероксидазы и хромогена АЕС (Novocastra). Срезы докрашивали гематоксилином Эрлиха, заключали в глицерин-желатин. Окрашенные срезы изучали с помощью светового микроскопа Leica DM 2500, оснащенного цифровой камерой Leica DFC420.
На фиг. 4 видно, что клетки, инфицированный рекомбинантом VV-GMCSF-Lact, интенсивно окрашиваются в красный цвет при добавлении хромогена АЕС, что свидетельствует о присутствии в них лактаптина. В клетках, инфицированных исходным штаммом VV-GMCSF-S1/3, специфическое окрашивание не выявлено.
Пример 4. Оценка цитолитической активности рекомбинантного штамма BOB VV-GMCSF-Lact в клетках рака молочной железы человека.
Исследование цитолитической активности рекомбинантного штамма VV-GMCSF-Lact на культурах раковых клеток молочной железы MCF7 и MDA-MB-231 проводили микрометодом на 96-луночных культуральных планшетах (Greiner) с использованием субстрата для митохондриальных дегидрогеназ 2,3-бис-(2-метокси-4-нитро-5-сульфофенил)-2Н-тетразолий-5-карбоксанилида (реагент ХТТ) (Sigma). В качестве отрицательного контроля использовали рекомбинантный штамм VV-GMCSF-dGF, который также был сконструирован на основе VV-GMCSF-S1/3, но содержал только делецию гена ростового фактора и не содержал встройки гена лактаптина.
Цитотоксическую активность вирусов для соответствующих типов клеток выражали как ЦТД50 - эффективная концентрация вируса, выраженная в количестве бляшкообразующих единиц на клетку (БОЕ/кл.), необходимая для гибели 50% клеток. Для определения ЦТД50 в лунки планшета с 50%-ным монослоем клеток вносили десятикратные разведения вирусной суспензии с множественностью инфекции от 10 до 0,001 БОЕ/кл. (multiplicity of infection, MOI) в 100 мкл среды 199 (Биолот) с добавлением 2% фетальной сыворотки коров (HyClone). Планшеты помещали в термостат при температуре 37°С, 5% СО2, влажности 85% и инкубировали 72 часа. После инкубации в каждую тестируемую лунку добавляли по 50 мкл реагента ХТТ и феназинметасульфата (PMS) (Sigma), который получали добавлением к рабочему раствору с содержанием ХТТ 1 мг/мл раствора PMS 1,25 мМ из расчета: на каждый 1 мл ХТТ - 20 мкл PMS. Планшет инкубировали еще 3 часа и определяли оптическую плотность ОП490/620 на планшетном спектрофотометре SpectraCount (Packard). Строили график зависимости ОП от MOI и определяли ЦТД50 - концентрацию вируса, при которой величина ОП490/620, измеренная в зараженных лунках, составляет 50% от величины ОП490/620, измеренной в лунках с незараженной культурой. Сравнивали ЦТД50 для разных культур клеток. Чем больше ЦТД50, тем меньшей цитотоксической активностью обладает исследуемый вирусный препарат для данной культуры клеток. Проведенные эксперименты показали (фиг. 5), что ЦТД50 рекомбинантного штамма VV-GMCSF-Lact составляет 0,019 БОЕ/кл. для клеток MCF-7 и 0,005 БОЕ/кл. для клеток MDA-MB-231, в то время как аналогичные показатели для контрольного вируса без встройки лактаптина VVdGF2/6 в 4-5 раз выше - 0,073 и 0,025 БОЕ/кл. соответственно. Полученные данные свидетельствуют о перспективности использования лактаптина в качестве онкотоксического белка в виротерапии рака молочной железы.
Источники информации
1. Parato K.А. et al. The oncolytic poxvirus JX-594 selectively replicates in and destroys cancer cells driven by genetic pathways commonly activated in cancers. // Molecular Therapy. - 2012. - V. 20. - P. 749-758.
2. Mastrangelo M.J. et al. Met hod of inducing an immune response using vaccinia virus recombinants encoding GM-CSF. // US Patent №6093700, опубл. 2000 г.
3. Mastrangelo M.J. and Lattime E.C. Virotherapy clinical trials for regional disease: in situ immune modulation using recombinant poxvirus vectors. // Cancer Gene Ther. - 2002. - V. 9. - P. 1013-1021.
4. Breitbach C.J. et al. Intravenous delivery of a multi-mechanistic cancer-targeted oncolytic poxvirus in humans. // Nature. - 2011. - Vol. 31; 477 (7362). - P. 99-102.
5. Heo J. et al. Randomized dose-finding clinical trial of oncolytic immunotherapeutic vaccinia JX-594 in liver cancer. // Nat. Med. - 2013. - V. 19. - P. 329-336.
6. Hwang Т.Н. et al. A mechanistic proof-of-concept clinical trial with JX-594, a targeted multi-mechanistic oncolytic poxvirus, in patients with metastatic melanoma. // Mol. Ther. - 2011. - V. 19. - P. 1913-1922.
7. Park B.H. et al. Use of a targeted oncolytic poxvirus, JX-594, in patients with refractory primary or metastatic liver cancer: a phase I trial. // Lancet Oncol. - 2008. - V. 9. - P. 533-542.
8. Liu T.C. et al. The targeted oncolytic poxvirus JX-594 demonstrates antitumoral, antivascular, and anti-HBV activities in patients with hepatocellular carcinoma. // Mol. Ther. - 2008. - V. 16. - P. 1637-1642.
9. Hou W. et al. Oncolytic vaccinia virus demonstrates antiangiogeniceffects mediated by targeting of VEGF. // Int. J. Cancer. - 2014. - V. 135 (5) - P. 1238-1246.
10. Chan W.M. and McFadden G. Oncolytic poxviruses. // Annu. Rev. Virol. - 2014. - Vol. 1 - P. 191-214.
11. McCart A., Bartlett D., Moss B. Combined growth factor-deleted and thymidine kinase-deleted vaccinia virus vector. // US Patent. №7208313, опубл. 2007 г.
12. Thorne S. et al. Rational strain selection and engineering creates a broad-spectrum, systemically effective oncolytic poxvirus, JX-963. // J. Clin. Invest. - 2007. - V. 117. - P. 3350-3358.
13. Russell S.J., Peng K-W., Bell J.C. Oncolytic virotherapy. // Nat. Biotechnol. - 2012. - V. 30 (7). - P. 2-14.
14. Lee J. et al. Oncolytic and immunostimulatory efficacy of a targeted oncolytic poxvirus expressing human GM-CSF following intravenous administration in a rabbit tumor model. // Cancer Gene Therapy. - 2010. - V. 17. - P. 73-79.
15. Lun X. et al. Double-deleted vaccinia virus in virotherapy for refractory and metastatic pediatric solid tumors. // Mol. Oncol. - 2013. - V. 7. - P. 944-954.
16. Маренникова С.С., Щелкунов С.Н. Патогенные для человека ортопоксвирусы. // KMK Scientific Press Ltd. 1998. 386 с.
17. Заявка на патент РФ №2013132993, МПК C12N 15/27, опубл. 27.01.2015 г. (прототип).
18. Koval О.А. et al. Lactaptin induces p53-independent cell death associated with features of apoptosis and autophagy and delays growth of breast cancer cells in mouse xenografts // PLoS one. - 2014. - V. 9 (4). - e93921.
19. Кочнева Г.В. и др. Апоптин усиливает онколитическую активность вируса осповакцины in vitro. //Молекулярная биологияю - 2013. - Т. 47, №5. - С. 842-852.
20. Merchlinsky М. et al. Construction and characterization of vaccinia direct ligation vectors. // Virology. - 1997. - V. 238 - P. 444-451.
21. Semenov D.V. et al. Recombinant analogs of a novel milk pro-apoptotic peptide, lactaptin, and their effect on cultured human cells. // Protein. J. - 2010. - V. 29. - P. 174-180.
22. Чумаков П.М. и др. Рекомбинантная плазмидная ДНК pGEM-Puro-DS-Аро, содержащая синтетический ген апоптина, фланкированный последовательностями генома вируса осповакцины из района C10L-C12L, и рекомбинантный штамм VVdGF-ApoS24/2 вируса осповакцины, продуцирующий апоптин. // Патент РФ №2492238, опубл. Бюл. №25 2013 г.

Изобретение относится к рекомбинантному штамму вируса осповакцины (ВОВ). Представленный рекомбинантный штамм VV-GMCSF-Lact сконструирован на основе штамма Л-ИВП вируса осповакцины, содержащего делеции фрагментов генов вирусной тимидинкиназы и ростового фактора, в районы которых встроены: ген гранулоцитарно-макрофагального колониестимулирующего фактора (ГМ-КСФ) человека, структура которого соответствует к ДНК матричной РНК ГМ-КСФ человека, в центральной части гена вирусной тимидинкиназы; и ген лактаптина, кодирующий фрагмент каппа-казеина человека 23-134 а.о., в левом концевом районе вирусного генома. Ген ГМ-КСФ человека экспрессируется под контролем природного промотора Р7.5k вируса осповакцины и продуцирует секретируемую форму биологически активного ГМ-КСФ человека в клетках млекопитающих. Ген лактаптина экспрессируется под контролем синтетического промотора вируса осповакцины P7.5synth и продуцирует онкотоксический рекомбинантный белок лактаптин. Представленный штамм депонирован в Государственной коллекции возбудителей вирусных инфекций и риккетсиозов ФБУН ГНЦ ВБ «Вектор» под номером V-688. Охарактеризованный штамм обладает высокой онколитической активностью в отношении клеток рака молочной железы человека и может быть использован в биотехнологии. 5 ил., 4 пр.
Рекомбинантный штамм VV-GMCSF-Lact, сконструированный на основе штамма Л-ИВП вируса осповакцины, содержащий делеции фрагментов генов вирусной тимидинкиназы и ростового фактора, в районы которых встроены: ген гранулоцитарно-макрофагального колониестимулирующего фактора (ГМ-КСФ) человека, структура которого соответствует кДНК матричной РНК ГМ-КСФ человека (GenBank Асс. M11220.1), в центральной части гена вирусной тимидинкиназы между позициями 81277 и 81308 п.н. (GenBank Acc. КР233807.1); ген ГМ-КСФ человека экспрессируется под контролем природного промотора Р7.5k вируса осповакцины и продуцирует секретируемую форму биологически активного ГМ-КСФ человека в клетках млекопитающих; ген лактаптина, кодирующий фрагмент каппа-казеина человека 23-134 а.о., в левом концевом районе вирусного генома между позициями 7770 и 8071 п.н. (GenBank Acc. КР233807.1); ген лактаптина экспрессируется под контролем синтетического промотора вируса осповакцины P7.5synth и продуцирует онкотоксический рекомбинантный белок лактаптин; штамм VV-GMCSF-Lact обладает высокой онколитической активностью в отношении клеток рака молочной железы человека и депонирован в Государственной коллекции возбудителей вирусных инфекций и риккетсиозов ФБУН ГНЦ ВБ «Вектор» под номером V-688.
| RU 2013132993 A, 27.01.2015 | |||
| ШТАММ ГИБРИДНЫХ КУЛЬТИВИРУЕМЫХ КЛЕТОК ЖИВОТНЫХ Mus. Musculus, ПРОДУЦИРУЮЩИЙ МОНОКЛОНАЛЬНЫЕ АНТИТЕЛА, СПЕЦИФИЧНЫЕ К ПЕПТИДУ, ОБЛАДАЮЩЕМУ АПОПТОТИЧЕСКОЙ АКТИВНОСТЬЮ ПО ОТНОШЕНИЮ К РАКОВЫМ КЛЕТКАМ ЧЕЛОВЕКА | 2009 |
|
RU2402605C1 |
| US 0006093700 A1, 25.07.2000 | |||
| R | |||
| CHAVAN et al., Expression of CCL20 and Granulocyte-Macrophage Colony-Stimulating Factor, but Not Flt3-L, from Modified Vaccinia Virus Ankara Enhances Antiviral Cellular and Humoral Immune Responses, J Virol., 2006 Aug, Vol.80, No.15, pp.7676-7687. | |||
Авторы
Даты
2016-12-10—Публикация
2015-10-20—Подача