Изобретение относится к области материалов для медицины, в частности к электроформованным волокнистым материалам, используемым для изготовления раневых покрытий.
К настоящему времени опубликовано значительное количество работ, посвященных получению нановолокон хитозана и их применению в медицине. К примеру, известно многослойное раневое покрытие, которое состоит из подложки и нескольких индивидуальных электроформованных нановолокнистых слоев, по меньшей мере один из которых - слой из хитозана (US 2011/0111012 А1, 12.05.2011). Также уже существуют раневые повязки, состоящие полностью из нановолокон хитозана (RU 2522216 С1, 10.07.2014) (прототип) и раневая повязка ХитоПран [РУ на медицинское изделие № ФСР 2012/14071 от 26 августа 2014 года], однако применение этих покрытий в раневой терапии ограничено чистыми ранами на стадии грануляции и не рекомендовано для лечения гнойных, инфицированных ран. Известно, что хитозан обладает биологической активностью по отношению к микроорганизмам, однако часто его позиционируют как бактериостатик, поскольку бактерицидная активность хитозана проявляется в том случае, когда аминогруппы протонированы, что наблюдается в растворе при рН<6. При этом антимикробная активность хитозана увеличивается по отношению к бактериям, имеющим клеточную оболочку с высоким отрицательным зарядом [Ying-chien Chung, Ya-ping Su, Chiing-chang Chen etc. Relationship between antibacterial activity of chitosan and surface characteristics of cell wall. // Acta Pharmacol. Sin., 2004. - V. 25. - N7. - P. 932-936]. Бактериостатический эффект хитозанового нановолокнистого материала был установлен авторами [Фесенко О.А., Матюшин А.Н., Юданова Т.Н., Габриелян Г.А. Получение модифицированного хитозанового нановолокнистого материала с биологической активностью / Пятая всерос. Каргинская конф. «Полимеры - 2010», М., 2010 г. ], а бактерицидный эффект достигался путем обработки нановолокнистого материала раствором левомицетина.
Таким образом, хитозановые нановолокна не вызывают гибель бактерий, более того, являясь биодеградируемыми, они могут являться субстратом для определенных видов бактерий. Очевидно, что для гарантированного предотвращения и подавления развития патогенной микрофлоры необходимо введение в состав волокон антибиотика. На основании проведенного анализа литературных источников установлено, что основными и наиболее устойчивыми возбудителями раневых инфекций являются кишечные палочки, золотистый стафилококк и синегнойная палочка [Фиалкина С.В., 2004, Абрамова Н.В. и др. (2010); Аветисян Л.Р. и др. (2010); Агапова Е.Д. (2010); Исхакова Х.И. (2010) и Материалы 1-го Международного конгресса «Раны и раневые инфекции» (2012)]. Для борьбы с этими возбудителями в гнойной хирургии применяют антибиотики, в том числе ципрофлоксацин [Clin Infect Dis. (2005) 41 (10): 1373-1406.doi: 10.1086/497143].
Многослойный материал, чувствительный к штамму Enterococcus faecalis 49, по настоящему изобретению содержит волокнистый слой из хитозана грибов, или смеси хитозана грибов и хитозана животного происхождения с поверхностной плотностью слоя до 50 г/м2 и диаметром волокон в диапазоне до 1000 нм и/или до 10 мкм и содержит в качестве антибиотика ципрофлоксацин. Материал имеет наружные слои: один - подложка, другой - защитный, который удаляется при наложении на рану. Между ними может находиться по меньшей мере еще один слой из нано- и ультратонких волокон. Количество и состав слоев определяются назначением изделия.
Задачей настоящего изобретения является создание нового антибактериального раневого покрытия, чувствительного к штамму Enterococcus faecalis 49, с хитозановым слоем из нано- и ультратонких волокон, содержащих один или несколько антибиотиков, предназначенного для лечения гнойных и инфицированных ран. Указанная задача решается за счет того, что в формовочный раствор для создания волокнистого материала на основе хитозана (см. RU 2522216) добавляется 0,3% раствор ципрофлоксацина - Ципрофлоксацин АКОС PN001587/02-2003. МНН. Формовочные растворы готовятся растворением хитозана и полиэтиленоксида (ПЭО) в растворе ципрофлоксацина с последующим добавлением уксусной кислоты и этилового спирта. Соотношение ципрофлоксацина к хитозану в полученных образцах варьировалось от 1:30 до 1:3000, массовая доля ципрофлоксацина 0,03 до 3%.
После получения образцы:
- термостатировали при 60°С в течение 3 часов для удаления остаточной уксусной кислоты;
- стерилизовали радиационным методом дозой 20±5 кГр.
Таким образом, тест-объектами служили стерильные, предварительно термообработанные при 60°С в течение 3 часов образцы с разными концентрациями антибиотика ципрофлоксацина размером 1 см × 1 см и плотностью 15 г/м2. Для сравнения использовали 2 объекта:
- образцы нано-/ультратонких волокон хитозана плотностью 15 г/м2 без антибиотика, а именно раневую повязку ХитоПран по РУ ФСР ФСР 2012/14071 от 26 августа 2014 года;
- полиэфирный нетканый волокнистый материал, пропитанный раствором ципрофлоксацина. Пропитку и последующую сушку образцов осуществляли таким образом, чтобы обеспечить соотношение ципрофлоксацина к материалу в полученных образцах от 1:30 до 1:3000.
Изучение антимикробной активности полученных образцов проводили по методике [Методические указания по лабораторной оценке антимикробной активности текстильных материалов, содержащих антимикробные препараты, МЗ РФ. - М.: МЗ РФ, 1984] с использованием в качестве тест-микроорганизмов штаммов музейных бактериальных культур, полученных из коллекции ФГУН ГИСК им. Л.А. Тарасевича и госпитальных штаммов из ГУ НИИ эпидемиологии и микробиологии имени Н.Ф. Гамалеи: Staphylococcus aureus 906, Enterococcus faecalis 49 (VRE) - представителей грамположительной микрофлоры, Escherichia coli 1257 и Pseudomonas aeruginosa 10145 АТСС - представителей грамотрицательной микрофлоры.
При определении чувствительности диско-диффузионным методом на поверхность агара АГВ и MX наносили бактериальную суспензию определенной плотности (обычно эквивалентную стандарту мутности 0,5 по McFarland) и затем помещали испытуемые образцы. Диффузия антибиотика из образца в агар приводила к формированию вокруг них зоны подавления роста микроорганизмов. После инкубации чашек в термостате при температуре 35°-37°С в течение 24 часов учитывали результат путем измерения диаметра зоны лизиса в миллиметрах (так как образцы имеют форму квадрата, измеряли диаметр описанной вокруг квадрата окружности).
При проведении исследований контрольные образцы нановолокон хитозана без антибиотика (ХитоПране) через 14 часов инкубирования чашек с посевами и нанесенными на поверхность посевов образцами ХитоПрана демонстрировали незначительное подавление бактериального роста, однако через 18 ч и 24 ч зон лизиса не выявлено.
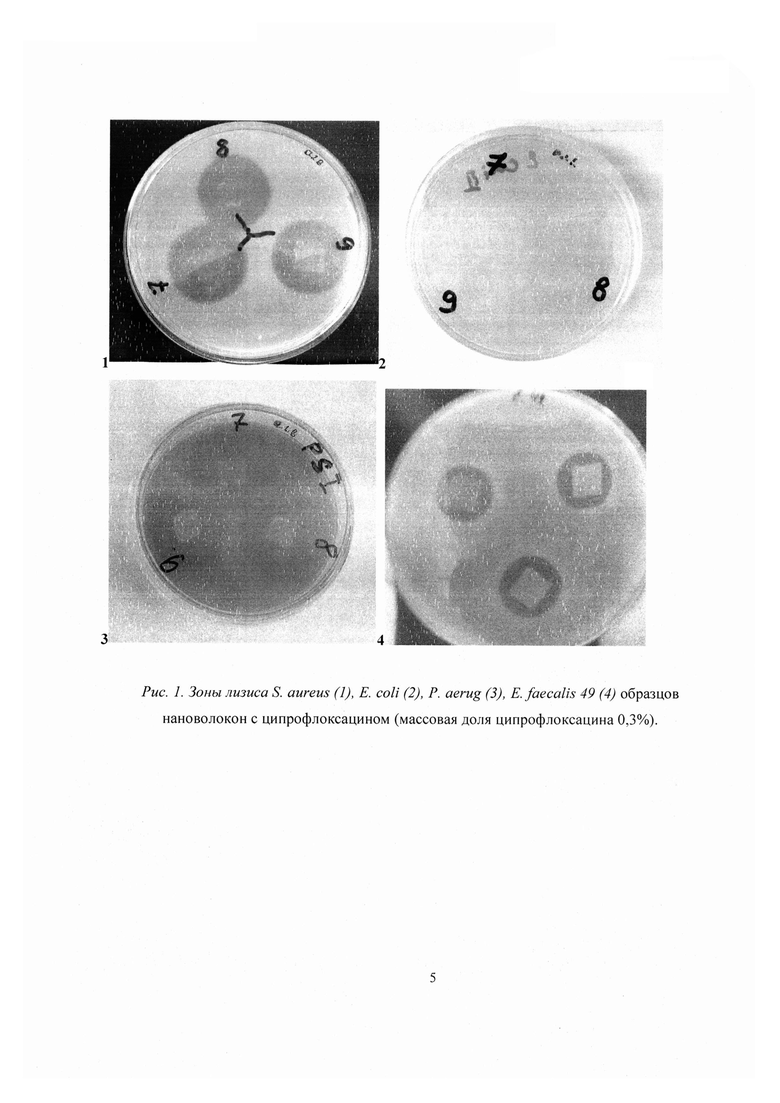
Вокруг образцов, содержащих ципрофлоксацин в различной концентрации, наблюдалась ярко выраженная зона лизиса (Рис. 1.), что свидетельствует о бактерицидном эффекте на всех используемых культурах. Более того, отмечено, что образцы, содержащие ципрофлоксацин в нано- и ультратонких волокнах, обладают повышенной антимикробной активностью по сравнению с образцами сравнения при прочих равных условиях, в частности зона лизиса вокруг хитозановых образцов была в среднем на 7 мм шире при тех же условиях проведения опыта (Табл. 1). Особо следует отметить, что была установлена антимикробная активность хитозановых нано- и ультратонких волокон с ципрофлоксацином в отношении клинического штамма Enterococcus faecalis 49 (VRE), который считается устойчивым к ципрофлоксацину [Salgado С, Sherertz R, Karchmer Т, et al. Public health initiative to control MRSA and VRE in Virginia and North Carolina. In: Program and abstracts of the 11th Annual Scientific Meeting of the Society for Healthcare Epidemiology of America; April 1-3, 2001; Toronto. Abstract 164. // Ostrowsky B, Trick W, Sohn AH, et al. Control of vancomycin-resistant Enterococcus in a region. N EnglJ Med. 2001; 344:1427-1433].

Таким образом, нами зафиксирован технический результат, заключающийся в проявлении синергетического эффекта за счет:
- наноструктурирования волокнистого носителя, в который включен ципрофлоксацин, и благодаря этому повышается биодоступность антибиотика;
- биологической активности хитозановых нановолокон, благодаря чему полученный материал проявляет бактерицидную активность в отношении штамма Enterococcus faecalis 49 (VRE), который считается устойчивым к ципрофлоксацину.
Примечательно также, что снижение содержания ципрофлоксацина в хитозановых нановолокнах в 100 раз с 3% до 0,03% приводит к очень незначительному уменьшению зоны лизиса. Это объясняется полимодальной зависимостью доза - эффект, характерной для биологически активных веществ [Подколзин А.А., Гуревич К.Г. Действие биологически активных веществ в малых дозах. - М.: КМК, 2002. - 170 с.], а также использованием в эксперименте ципрофлоксацина в малой дозе, равномерно распределенного в волокнистой наноструктурированной матрице и вследствие этого имеющего высокую скорость десорбции во внешнюю среду.
| название | год | авторы | номер документа |
|---|---|---|---|
| МНОГОСЛОЙНЫЙ МАТЕРИАЛ С ХИТОЗАНОВЫМ СЛОЕМ ИЗ НАНО- И УЛЬТРАТОНКИХ ВОЛОКОН | 2013 |
|
RU2522216C1 |
| МНОГОСЛОЙНЫЙ НЕТКАНЫЙ МАТЕРИАЛ С ПОЛИАМИДНЫМИ НАНОВОЛОКНАМИ | 2013 |
|
RU2529829C1 |
| МЕСТНОЕ ГЕМОСТАТИЧЕСКОЕ СРЕДСТВО С ПОВЫШЕННОЙ АНТИМИКРОБНОЙ АКТИВНОСТЬЮ | 2018 |
|
RU2675631C1 |
| МЕДИЦИНСКАЯ МНОГОСЛОЙНАЯ ПОВЯЗКА С МНОГОФУНКЦИОНАЛЬНЫМИ НАНОМЕМБРАНАМИ И ИЗДЕЛИЯ НА ЕЕ ОСНОВЕ | 2014 |
|
RU2578458C2 |
| ТЕКСТИЛЬНЫЙ АНТИМИКРОБНЫЙ МАТЕРИАЛ С МНОГОКОМПОНЕНТНЫМИ НАНОМЕМБРАНАМИ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2014 |
|
RU2579263C2 |
| РАСТВОР ДЛЯ ПОЛУЧЕНИЯ МАТЕРИАЛА НА ОСНОВЕ ХИТОЗАНА, СПОСОБ ПОЛУЧЕНИЯ ГЕМОСТАТИЧЕСКОГО МАТЕРИАЛА ИЗ ЭТОГО РАСТВОРА (ВАРИАНТЫ) И МЕДИЦИНСКОЕ ИЗДЕЛИЕ С ИСПОЛЬЗОВАНИЕМ ВОЛОКОН НА ОСНОВЕ ХИТОЗАНА | 2011 |
|
RU2487701C2 |
| СПОСОБ ПРОФИЛАКТИКИ ВОСПАЛИТЕЛЬНЫХ ЗАБОЛЕВАНИЙ ЖЕНСКИХ ПОЛОВЫХ ОРГАНОВ | 2005 |
|
RU2286799C1 |
| ПЕРЕВЯЗОЧНОЕ СРЕДСТВО НА БИОПОЛИМЕРНОЙ ОСНОВЕ ДЛЯ ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ ИНФЕКЦИЙ ПРИ ОЖОГАХ, ТРОФИЧЕСКИХ ЯЗВАХ И НЕКРОЗЕ МЯГКИХ ТКАНЕЙ | 2016 |
|
RU2666012C1 |
| Фармацевтическая комбинированная композиция для лечения гнойных ран на основе фторхинолонов (варианты) | 2016 |
|
RU2682171C2 |
| БИОРЕЗОРБИРУЕМАЯ ГИДРОГЕЛЕВАЯ ПОЛИМЕРНАЯ КОМПОЗИЦИЯ С БИОЛОГИЧЕСКИ АКТИВНЫМИ ВЕЩЕСТВАМИ (ВАРИАНТЫ) | 2012 |
|
RU2519103C2 |
Изобретение относится к медицине, конкретно к электроформованным волокнистым материалам, используемым для изготовления раневых покрытий. Описан многослойный материал, чувствительный к штамму Enterococcus faecalis 49, содержащий слой нано- и ультратонких волокон из хитозана грибов или смеси хитозана грибов и хитозана животного происхождения с поверхностной плотностью слоя до 50 г/м2 и диаметром волокон в диапазоне до 1000 нм и/или до 10 мкм, который содержит ципрофлоксацин. Изобретение приводит к достижению синергетического эффекта от совместного использования ципрофлоксацина и хитозановых нано-/ультратонких волокон. 1 ил., 1 табл.
Многослойный материал, чувствительный к штамму Enterococcus faecalis 49 для изготовления раневых покрытий, содержащий слой нано- и ультратонких волокон из хитозана грибов или смеси хитозана грибов и животного происхождения с поверхностной плотностью слоя до 50 г/м2 и диаметром волокон в диапазоне до 1000 нм и/или до 10 мкм, отличающийся тем, что он содержит ципрофлоксацин.
| МНОГОСЛОЙНЫЙ МАТЕРИАЛ С ХИТОЗАНОВЫМ СЛОЕМ ИЗ НАНО- И УЛЬТРАТОНКИХ ВОЛОКОН | 2013 |
|
RU2522216C1 |
| RU 23312444 С1, 20.08.2008 | |||
| Способ приготовления лака | 1924 |
|
SU2011A1 |
Авторы
Даты
2016-12-10—Публикация
2015-05-06—Подача