Настоящее изобретение относится к различимости медицинских изображений и, в частности, к системам и способам для улучшения различимости устройств на медицинских изображениях.
Визуализация катетера или иглы необходимы во время многих медицинских интервенционных процедур. Существующий стандартный подход к визуализации катетера включает в себя формирование рентгеновского изображения с контрастными красящими веществами (флюороскопия). Данные процедуры являются инвазивными из-за ионизирующего излучения и токсичности самого красящего вещества. Традиционные методы формирования изображения, например получение изображения с помощью ультразвука или магнитно-резонансной томографии (МРВ), не способны обеспечить четкий контраст катетерных материалов. Электромагнитные следящие датчики, устанавливаемые на катетерах для применения при визуализации катетеров, не достаточно точны из-за искажения электромагнитного поля. Кроме того, точная визуализация катетеров является трудной задачей, потому что, в общем, катетеры характеризуются неконтролируемым, зависящим от угла зеркальным отражением.
В соответствии с принципами настоящего изобретения медицинское устройство и способы определения местоположения устройства содержат структуру, имеющую продольный размер и поверхность. Объем ассоциирован с поверхностью и продолжается вдоль, по меньшей мере, участка продольного размера. Наноматериалы включены в объем и сконфигурированы с возможностью реагирования на, по меньшей мере, один сигнал возбуждения, так что сигнал возбуждения генерирует отклик от наноматериалов для создания возможности определения местоположения структуры в объекте.
Система для определения местоположения медицинского устройства содержит медицинское устройство, имеющее включенные в него наноматериалы, при этом наноматериалы сконфигурированы с возможностью реагирования на, по меньшей мере, один сигнал возбуждения. Источник возбуждения сконфигурирован с возможностью генерирования, по меньшей мере, одного сигнала возбуждения для генерирования ответных излучений от наноматериалов. Датчик сконфигурирован с возможностью приема ответных излучений. Модуль обработки изображений сконфигурирован с возможностью отображения медицинского устройства на медицинском изображении с использованием ответных излучений.
Способ определения местоположения медицинского устройства включает в себя этап обеспечения медицинского устройства, имеющего включенные в него наноматериалы, при этом наноматериалы сконфигурированы с возможностью реагирования на, по меньшей мере, один сигнал возбуждения; этап возбуждения наноматериалов с использованием, по меньшей мере, одного сигнала возбуждения для генерирования ответных излучений от наноматериалов; этап измерения ответных излучений; и этап обработки ответных излучений для определения местоположения медицинского устройства относительно медицинского изображения.
Другой способ формирования изображения медицинского устройства содержит этап возбуждения наноматериалов, включенных в медицинское устройство, с использованием первой частоты электромагнитного излучения возбуждения наноматериалов, для получения первого визуализируемого отклика, при этом первый визуализируемый отклик может быть обнаружен по окружающим материалам; этап возбуждения наноматериалов, содержащихся в медицинском устройстве, с использованием второй частоты электромагнитного излучения возбуждения наноматериалов, для получения второго визуализируемого отклика, который содержит доступное для восприятия отличие от первого визуализируемого отклика, причем второй визуализируемый отклик может быть обнаружен по окружающим материалам; и этап вычитания первого визуализируемого отклика из второго визуализируемого отклика для обеспечения изображения медицинского устройства относительно объекта.
Приведенные и другие цели, признаки и преимущества настоящего изобретения будут более очевидны из нижеследующего подробного описания наглядных вариантов осуществления изобретения, которое следует рассматривать в связи с прилагаемыми чертежами.
Настоящее раскрытие изобретения представляет ниже подробное описание предпочтительных вариантов осуществления со ссылкой на следующие фигуры, на которых:
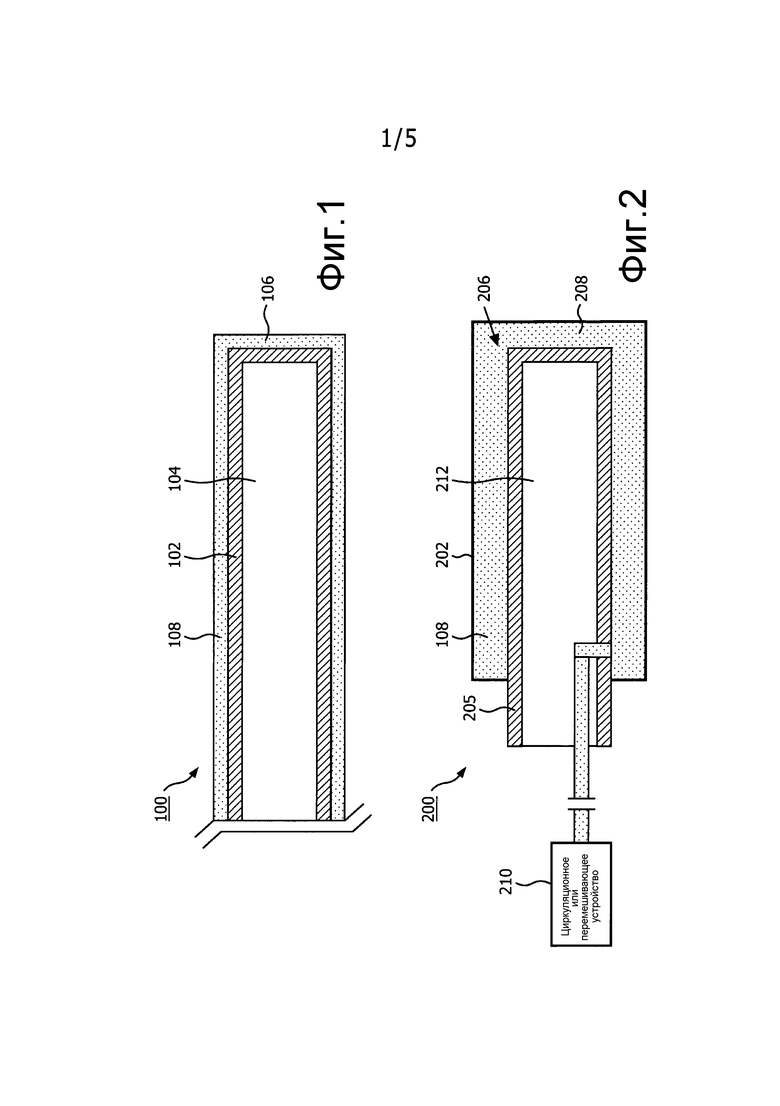
Фиг.1 - частичный разрез медицинского устройства, содержащего твердый слой или покрытие, вмещающий(ее) наноматериалы, в соответствии с одним вариантом осуществления;
Фиг.2 - частичный разрез медицинского устройства, содержащего трубку, формирующую кольцевую полость, вмещающую наноматериалы в суспензии, в соответствии с другим вариантом осуществления;
Фиг.3 - частичный разрез медицинского устройства, содержащего продольную трубку, вмещающую наноматериалы в суспензии, в соответствии с другим вариантом осуществления;
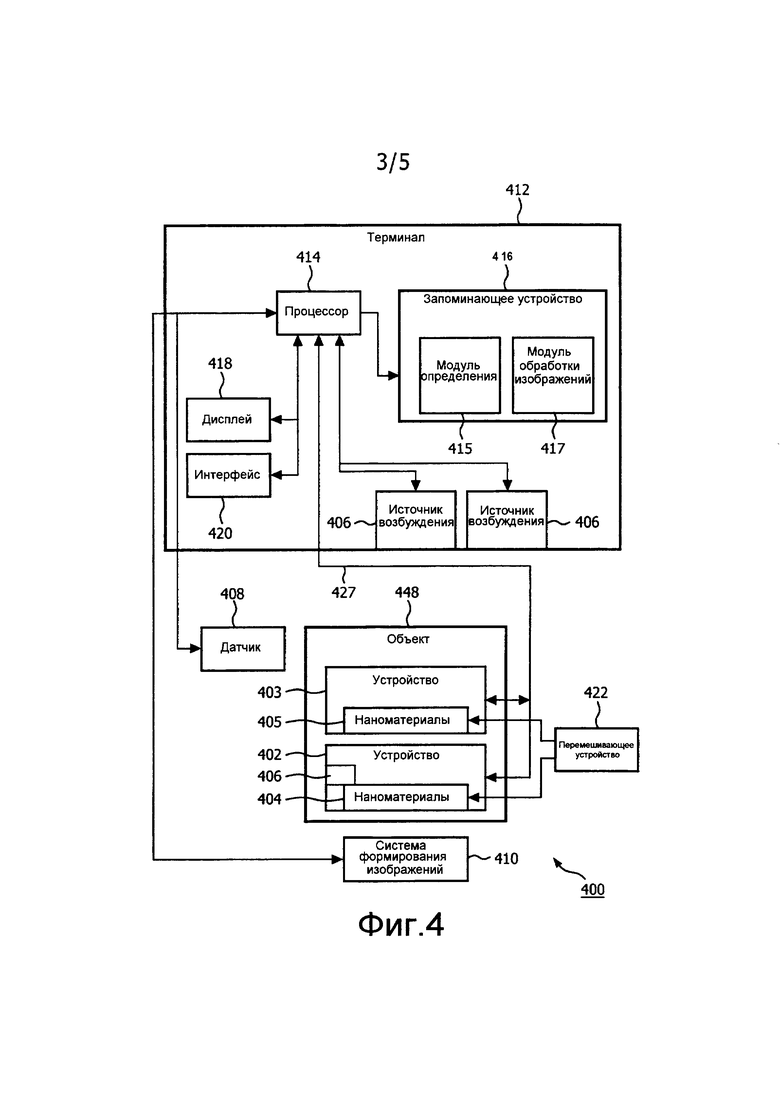
Фиг.4 - блок-схема, показывающая систему для формирования изображения медицинских устройств в соответствии с одним наглядным вариантом осуществления;
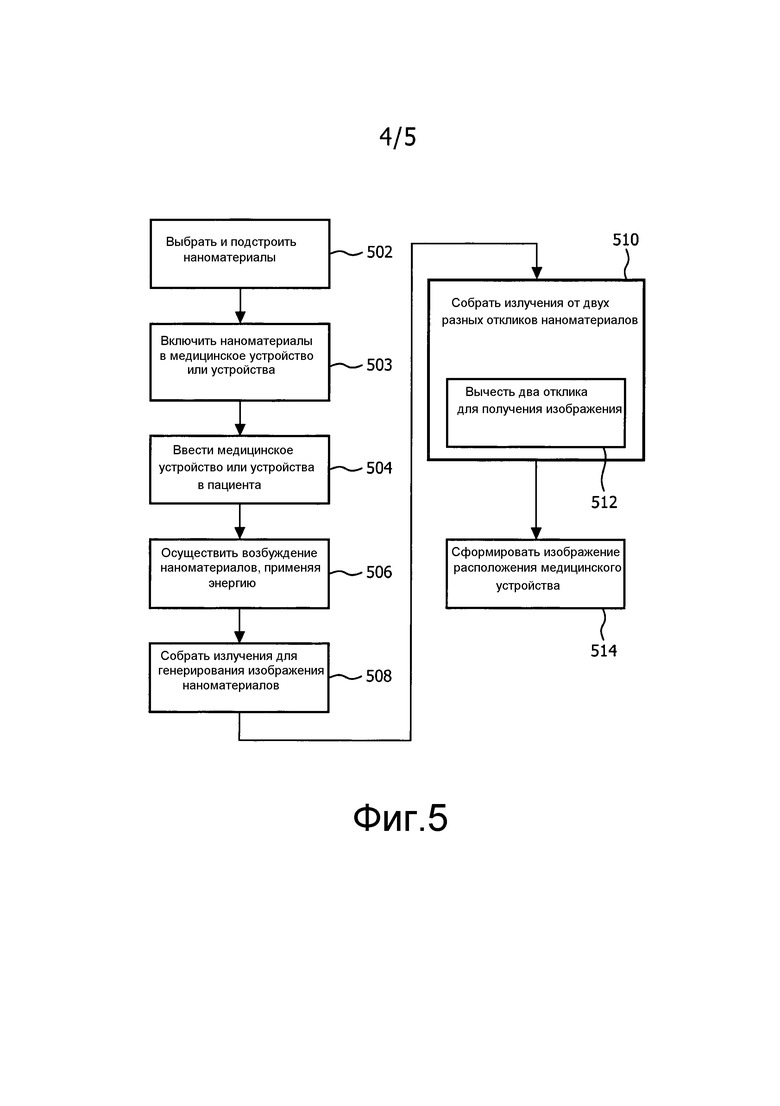
Фиг.5 - блок-схема, показывающая способ определения местоположения и формирования изображения медицинских устройств в соответствии с другим наглядным вариантом осуществления; и
Фиг.6 - блок-схема, показывающая другой способ создания и применения медицинского устройства в соответствии с наглядным вариантом осуществления.
В соответствии с представленными принципами предлагаются системы, устройства и способы, которые модифицируют медицинские устройства включением дополнительного слоя материалов, нанесенного на или внедренного в поверхность устройства. В одном варианте осуществления применяют наноматериалы. Наноматериалы можно выбрать для обеспечения поглощающих свойств на конкретных длинах волн. Во время медицинской процедуры или подобной операции, электромагнитное поле обеспечивают в интересующей области. В ответ на данное поле, наноматериалы генерируют акустическую волновую картину от воздействия падающих электромагнитных волн, которая затем обнаруживается с использованием акустического датчика.
В особенно выгодных вариантах осуществления наноматериалы, которые можно применять, содержат, например, углеродные нанотрубки, наностержни или наносферы. В других вариантах осуществления можно применить способ вычитания изображений, в котором используют электромагнитное излучение двух частот для более точного определения местоположения медицинского устройства внутри пациента.
Следует понимать, что настоящее изобретение описано ниже на примере медицинских инструментов; однако идеи настоящего изобретения намного шире и применимы к любым инструментам, применяемым при отслеживании или анализе комплексных биологических или механических систем. В частности, настоящие принципы применимы к процедурам отслеживания внутри биологических систем, процедурам во всех зонах тела, например легких, желудочно-кишечном тракте, выделительных органах, кровеносных сосудах и т.п. Элементы, описанные на фигурах и, в частности, на фиг.4, могут быть реализованы в различных сочетаниях аппаратных средств и программного обеспечения и обеспечивать функции, которые могут быть объединены в одном элементе или нескольких элементах.
Функции различных элементов, показанных на фигурах, можно обеспечить посредством применения специализированных аппаратных, а также аппаратных средств, способных исполнять программное обеспечение, ассоциированное с соответствующим программным обеспечением. Функции, в случае обеспечения процессором, могут быть обеспечены единственным специализированным процессором, единственным совместно используемым процессором или множеством отдельных процессоров, некоторые из которых могут быть совместно используемыми. Кроме того, явно используемый термин «процессор» или «контроллер» не подлежит интерпретации в смысле применения исключительно к аппаратным средствам, способным исполнять программное обеспечение, и может в неявной форме включать в себя, без ограничения, аппаратные средства цифрового сигнального процессора («DSP»), постоянное запоминающее устройство («ROM») для хранения программного обеспечения, оперативное запоминающее устройство («RAM»), энергонезависимое запоминающее устройство и т.п.
Кроме того, все формулировки в настоящей заявке, излагающие принципы, аспекты и варианты осуществления изобретения, а также конкретные примеры вариантов осуществления изобретения предназначены для охвата как конструктивных, так и функциональных эквивалентов изобретения. Кроме того, предполагается, что упомянутые эквиваленты включают в себя как эквиваленты, известные в настоящее время, так и эквиваленты, созданные в будущем (т.е. любые разработанные элементы, которые выполняют такую же функцию, независимо от исполнения). Следовательно, например, специалистам в данной области техники будет очевидно, что блок-схемы, приведенные в настоящей заявке, дают концептуальные представления о наглядных компонентах и/или схемах систем, осуществляющих принципы настоящего изобретения. Аналогично, следует понимать, что любые структурные схемы, блок-схемы последовательностей операций способов и т.п. представляют различные способы обработки, которые могут быть, по существу, представлены на машиночитаемом носителе информации и, следовательно, исполнены компьютером или процессором, независимо от того, показан ли упомянутый компьютер или процессор в явном виде.
Кроме того, варианты осуществления настоящего изобретения могут быть в форме компьютерного программного продукта, доступного на используемом машиной или машиночитаемом носителе информации, обеспечивающем программный код для применения компьютером или любой системой исполнения команд или на связи с упомянутыми компьютером или системой. В целях настоящего описания, используемый машиной или машиночитаемый носитель информации может быть любым аппаратурным средством, которое может содержать, хранить, передавать, распространять или переносить программу для применения системой, аппаратом или устройством исполнения команд или на связи с ними. Носитель информации может быть электронной, магнитной, оптической, электромагнитной, инфракрасной или полупроводниковой системой (или аппаратом, или устройством) или средой распространения. Примеры машиночитаемого носителя информации включают в себя полупроводниковое или твердотельное запоминающее устройство, магнитную ленту, переносную компьютерную дискету, оперативное запоминающее устройство (RAM), постоянное запоминающее устройство (ROM), жесткий магнитный диск и оптический диск. Текущие примеры оптических дисков включают в себя постоянное запоминающее устройство на компакт-диске (CD-ROM), перезаписываемый компакт-диск (CD-R/W) и (DVD).
На рассматриваемых далее чертежах сходные позиционные обозначения означают одинаковые или похожие элементы, и первоначально на фиг.1 приведен для пояснения разрез участка медицинского устройства 100 в соответствии с одним вариантом осуществления. Устройство 100 может содержать, например, катетер, проволочный направитель, эндоскоп, зонд, робот, электрод, фильтрующее устройство, баллонное устройство, иглу или другой медицинский компонент и т.п. Устройство 100 содержит поверхность или стенку 102 устройства, которая может формировать полость 104. Слой или объем 106 материала сформирован на наружной стороне стенки или поверхности 102 устройства. Слой 106 содержит композицию для поддержки визуализации медицинского устройства 100 на медицинских изображениях.
В одном варианте осуществления слой 106 содержит полимерный материал, содержащий суспендированные наноматериалы 108 в и/или на слое 106. Полимерный материал может содержать пластик, эпоксидный компаунд, адгезив, смолу, краску и т.п. Суспензии наноматериалов могут быть заформованы или иначе включены в твердое вещество и затем встроены в или нанесены на поверхность стенки 102 устройства. Твердое вещество с суспендированными наночастицами может быть изготовлено из ПВА (поливинилацетатного) связующего, агарозного геля, других полимерных гелей или с использованием силикона.
Наноматериалы 108 могут содержать одностенные или мультистенные углеродные нанотрубки, металлические наностержни, наносферы, наноклетки, квантовые точки, которые имеют оптические свойства, зависящие от падающей длины волны, или подобные компоненты. Наноматериалы 108 выбирают для обеспечения селективного поглощения или максимумов рассеяния на заданных длинах волн. Во время медицинской процедуры электромагнитное поле обеспечивают в интересующей зоне. Наноматериалы 108 слоя 106 генерируют электромагнитные или акустические волновые картины в результате взаимодействия падающих электромагнитных волн и наноматериалов 108, которые отличаются от окружающих тканей внутри пациента. Способ обнаружения может использовать фотоакустику, формирование изображений методом обратного рассеяния оптического излучения, термоакустику, либо экстракорпорально, либо с использованием эндоскопического приемника и т.п. Пример электромагнитного излучения, которое можно применить, может включать в себя использование поля инфракрасного излучения с заданной длиной волны. В данном примере можно применить слой золотых наностержней с аспектными отношениями 5,9 и падающее излучение, имеющее длину волны около 1000 нм. При этом наностержни возбуждаются и обеспечивают видимый и/или измеримый отклик, который можно использовать для высокоточного определения местоположения устройства 100 внутри пациента.
Спектры поглощения электромагнитных волн наноматериалами 108, например, металлическими наносферами, наностержнями, углеродными нанотрубками и т.п., зависят от геометрии материалов. Поведение таких квазичастиц, как экситоны, фононы и плазмоны, и их взаимодействие с падающими волнами также существенно влияет на спектры поглощения. Другие модификации, например легирование или сплавление, наноматериалов 108 также могут существенно влиять на их спектры поглощения.
Физической основой поглощения электромагнитных волн металлическими наночастицами являются, например, когерентные колебания электронов зоны проводимости, вызываемые электромагнитным полем. Упомянутые резонансные колебания называют поверхностными плазмонами. Локализованный поверхностный плазмонный резонанс зависит от физических размеров частиц, диэлектрической постоянной окружающей среды и формы наноструктур.
Углеродные нанотрубки (CNT) содержат структуру с атомами углерода, расположенными в виде плоского листа, называемого графеном, свернутым в трубчатую структуру. Трубки CNT можно классифицировать как одностенные или мультистенные. Размеры одностенных трубок CNT могут составлять, приблизительно, 1 нм в диаметре и от нескольких сотен нанометров до нескольких микрометров в длину. Трубки CNT обладают необычными электрическими, тепловыми и механическими свойствами. Поглощение электромагнитного излучения трубками CNT зависит от их геометрии, в частности, их диаметра и хиральности (угла скручивания), а также диэлектрических свойств окружающей среды.
Спектры поглощения трубок CNT достаточно хорошо описываются свойствами их запрещенных зон. Трубки CNT являются материалами с прямыми переходами, и их оптические спектры длительно объясняли переходами между энергетическими состояниями в валентной зоне и зоне проводимости, приводящими к обычным резонансным колебаниям Ван Хова для спектров поглощения. Однако другие явления, в частности поведение экситонов (электронно-дырочных пар), в упомянутых квазиодномерных системах оказывают намного преобладающее влияние на их свойства оптического поглощения.
Трубки CNT имеют четко определенные максимумы поглощения, которые соответствуют переходам экситонных уровней. Кроме того, для существенной настройки резонансных максимумов трубок CNT можно применить легирование. Характеристики поглощения трубок CNT могут быть полезны для формирования изображений. Например, трубки CNT поглощают излучение на длинах волн ближней инфракрасной области, на которых собственное поглощение тканей является минимальным. Таким образом, трубки CNT можно использовать как эффективные фотоакустические контрастные вещества.
Для углеродных нанотрубок (CNT) π-плазмонный резонанс изменяется в зависимости от диаметра нанотрубки в соответствии с эмпирически найденной формулой: 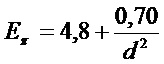
Другая форма наноматериалов 108 содержит наносферы. Наносферы могут содержать, например, золото. Спектры поглощения данных материалов также зависят от геометрии, например, размера и аспектного отношения, и поведения плазмонов (колебаний плотности свободного электронного газа). Золотые наносферы с диаметрами несколько десятков нанометров имеют максимум поглощения на, приблизительно, 550 нм. С увеличением размера максимальное оптическое поглощение сдвигается в красную сторону видимого спектра.
Для одноэлементных металлических наносфер длина волны максимального поглощения металлических наносфер слабо зависит от размера, при общей тенденции к красному сдвигу с увеличением размера. Например, для золотых наносфер с размерами 22 и 99 нм длины волны максимального поглощения равны 520 нм и 575 нм соответственно.
Другой более сильнодействующий фактор, который определяет максимум поглощения сферических наночастиц, представляет собой добавление другого металла для формирования сплава. Максимумы спектров поглощения наночастиц сплава золота с серебром сдвигаются в синюю сторону (сторону меньшей длины волны), при уменьшении молярной доли золота. Например, спектральный максимум наблюдается около 400 нм, когда молярная доля золота приближается к нулю, смещается к 450 нм для молярной доли 0,5 и смещается дальше к 500 нм для молярной доли 0,80. Следовательно, наносферы можно подстраивать по их размеру и легированию для обеспечения конкретных максимумов спектров поглощения.
Для легированных наносфер создание сплава можно использовать, чтобы обеспечить большее разнообразие при выборе данной длины максимума. Чтобы определить длину волны максимума для 18-нм наносфер из сплава золота с серебром, можно воспользоваться следующим уравнением: λmax=130χAu+390, где λmax означает длину волны максимального поглощения в нм и χAu означает молярную долю золота.
Другой формой наноматериалов 108 являются наностержни. В отличие от наносфер, длина волны максимального поглощения, например, золотых наностержней (т.е. цилиндрических золотых наночастиц) зависит от их диаметра очень слабо, но сильно увеличивается с увеличением их аспектного отношения. Например, золотые наностержни со средними аспектными отношениями 5,9 и 3,7 демонстрируют максимальные оптические поглощения на 1000 и 785 нм соответственно.
Например, для одноэлементных металлических наностержней золото может быть выбрано в качестве примерного материала благодаря его биологической совместимости. Длину волны максимального поглощения металлических наностержней можно определить из следующего уравнения:
λmax=33,34εmR-46,31εm+472,31, где λmax означает длину волны максимума в нм, εm означает диэлектрическую постоянную окружающей среды, и R означает аспектное отношение, заданное как длина стержня, деленная на ширину. Следовательно, длина волны максимума поглощения изменяется с линейной зависимостью от аспектного отношения, а также диэлектрической постоянной среды. Предпочтительную длину волны максимума можно выбирать в оптическом окне ткани человека в инфракрасной области, например, от 650 до 1200 нм. Если окружающая среда имеет известную диэлектрическую постоянную (например, εm = 3), то данное значение можно подставить в вышеприведенное уравнение для определения длины волны максимума в зависимости от аспектного отношения R. Диэлектрическая постоянная среды является функцией аспектного отношения и может быть смоделирована в виде монотонно убывающей функции.
Оптические свойства легированных наностержней изменяются в зависимости от композиции сплава и длины. Существует несколько резонансных колебаний, содержащих продольные и поперечные моды. Например, поперечные моды можно использовать для формирования изображений, так как их максимумы изменяются в зависимости от композиции сплава при данной длине. Длина волны (нм) максимальной поперечной моды изменяется в зависимости от молярной доли χAu золота:
λmax=149χAu+360.
Продольные моды также можно использовать для формирования разностных изображений, так как данные длины волн изменяются в зависимости от длины стержня (или, эквивалентно, аспектных отношений для фиксированного размера). При 65% молярной доли золота длина волны максимальной продольной моды сдвигается в красную сторону от 716 нм для длины 123 нм до 1467 нм для длины 328 нм.
Кроме спектральных резонансов наноматериалы 108 имеют, по существу, иные оптические свойства, чем биологические ткани, которые обеспечивают механизмы контрастирования, при использовании таких средств формирования изображений, как оптическая когерентная томография. В подобных обстоятельствах наноматериалы 108 применяют как рассеивающие контрастные вещества.
Наноматериалы 108 обеспечивают множество способов и материалов для настройки их свойств поглощения электромагнитных волн. Упомянутые свойства можно эффективно применить в практике формирования медицинских изображений для обеспечения контраста и непрозрачности изображения. Например, вследствие слабого собственного поглощения большинства биологических тканей на длинах волн в ближней инфракрасной области наноматериалы могут обеспечивать оптические контрастные вещества в, например, крови. Кроме того, поглощающие свойства наноматериалов 108 могут также приводить к фотоакустическим эффектам, которые можно обнаруживать с использованием сканеров для ультразвукового формирования изображений.
На фиг.2 показано другое медицинское устройство 200 в соответствии с другим наглядным вариантом осуществления. Устройство 200 может иметь такую же форму, как устройство 100. Устройство 200 содержит концентрическую трубку 202, которая окружает участок стенки 205 устройства или всю упомянутую стенку. Концентрическая трубка 202 формирует кольцевую полость 206 между стенкой 205 трубки и трубкой 202. Кольцевая полость 206 заполнена наноматериалами 108 в суспензии 208 наноматериалов. Текучая среда суспензии 208 в полости 206 может содержать воду, физиологический раствор или другие биосовместимые материалы. Суспензию наноматериалов можно прокачивать для предотвращения осаждения наноматериалов 108 посредством циркуляционного/перемешивающего устройства 210. Циркуляционное/перемешивающее устройство 210 может содержать, по меньшей мере, одно из внешнего насоса, вибрационного устройства, электромагнитного перемешивающего устройства, которое смешивает посредством смешивания ферромагнитных частиц и т.п. Следует понимать, что циркуляционное/перемешивающее устройство 210 может находиться около или на устройстве 200 или может находиться снаружи пациента во время процедуры.
В другом варианте осуществления суспензией 208 наноматериалов может быть наполнена внутренняя полость 212 устройства 200, вместо или дополнительно к кольцевой полости 206.
На фиг.3 показано другое медицинское устройство 300 в соответствии с другим наглядным вариантом осуществления. Устройство 300 содержит трубку или трубки 302, которая(ые) проходят по длине или участку длины медицинского устройства 300. Трубка или трубки 302 может (могут) также охватывать устройство (например, в виде змеевика, спирали или другой конфигурации). Трубки 302 транспортируют суспензию 208 наноматериалов.
Суспензию 208 наноматериалов можно прокачивать для предотвращения осаждения наноматериалов 108 посредством циркуляционного/перемешивающего устройства 210. Циркуляционное/перемешивающее устройство 210 может содержать, по меньшей мере, одно из внешнего насоса, вибрационного устройства, электромагнитного перемешивающего устройства, которое смешивает посредством смешивания ферромагнитные частицы и т.п. Следует понимать, что циркуляционное/перемешивающее устройство 210 может находиться около или на устройстве 300 или может находиться снаружи пациента во время процедуры.
На фиг.4 представлена, для наглядности, система 400 для выполнения медицинской процедуры. Система 400 может содержать терминал или консоль 412, с которого(ой) осуществляют наблюдение за и управление процедурой. В предпочтительном варианте терминал 412 содержит, по меньшей мере, процессор 414 и запоминающее устройство 416 для хранения программ и приложений. Запоминающее устройство 416 может содержать модуль 415 определения устройства, сконфигурированный с возможностью интерпретации электромагнитных и/или акустических сигналов обратной связи от слоя или суспензии 404 (405) наноматериалов медицинского устройства 402 (403). Модуль 415 определения сконфигурирован с возможностью использования обратной связи по сигналу (и любой другой обратной связи) для обеспечения определения местоположения или для отображения медицинского устройства 402 (или 403) на медицинских изображениях. Медицинское устройство 402 (403) может включать в себя, например, катетер, проволочный направитель, эндоскоп, зонд, робот, электрод, фильтрующее устройство, баллонное устройство, иглу или другой медицинский компонент и т.п. Терминал 412 может содержать дисплей 418 для наблюдения внутренних изображений объекта с использованием системы 410 формирования изображений. Система 410 формирования изображений может включать в себя такие средства формирования изображений, как оптическая когерентная томография, конфокальная микроскопия, фотоакустика и т.п. Система 410 формирования изображений может также содержать, например, систему магнитно-резонансной томографии (МРВ), флюороскопическую систему, систему компьютерной томографии (КТ), ультразвуковую систему или другую систему, в которой можно наблюдать возбужденные наноматериалы. Дисплей 418 может также предоставлять пользователю возможность взаимодействия с терминалом 412 и его компонентами и функциями. Данное взаимодействие дополнительно поддерживается интерфейсом 420, который может содержать клавиатуру, мышь, джойстик или любое другое периферийное устройство или устройство управления для предоставления пользователю возможности взаимодействия с терминалом 412.
Терминал 412 содержит, по меньшей мере, один источник 406 энергии или возбуждения для обеспечения энергии возбуждения на предварительно заданных длинах волн. В альтернативном варианте, по меньшей мере, один источник 406 возбуждения может быть встроен в устройство(а) 403 (или 402), и поэтому падающее излучение не обязательно подавать от источника, внешнего по отношению к телу/объекту 448. Длины волн возбуждения выбирают, и наноматериалы подстраивают для чувствительности к выбранным длинам волн. Приведенные действия могут быть выполнены in-situ или до процедуры. Источники 406 энергии могут обеспечивать электромагнитную энергию в форме инфракрасного излучения, рентгеновского излучения, видимого света и т.п. Спектры поглощения наноматериалов соответственно настраивают для обеспечения измеримого отклика на возбуждение. Блок 408 датчика служит для приема электромагнитной энергии или акустической энергии, возвращаемой от наноматериалов 404 (405). Данный блок позволяет определять излучения энергии, которые будут использованы для интерпретации формы и/или ориентации устройства 402. Сигналы будут применены как сигналы обратной связи для выполнения регулировок или другого выполнения медицинской процедуры. Блок 408 датчика может содержать фотоприемник, ультразвуковой датчик (зонд) или другое сенсорное(ые) устройство или устройства.
Если наноматериалы находятся в суспензии, то можно применить циркуляционное или перемешивающее устройство 422 для перемешивания суспензии, чтобы предотвратить осаждение наноматериалов (404, 405). Для сбора в реальном времени интраоперационных данных формирования изображений может быть обеспечена система 410 формирования изображений. Данные формирования изображений могут показываться на дисплее, и модуль 415 определения устройства может вычислять положения излучения энергии в изображении реального времени. Цифровое визуальное отображение медицинского устройства 402 (с использованием обратной связи с наноматериалами 404) можно отображать для обнаружения положения устройства 402 на изображениях в реальном времени. Цифровое отображение может быть сгенерировано модулем 417 обработки изображений. В одном варианте осуществления система 410 формирования изображений содержит ультразвуковую систему, и излучения от наноматериалов 404 являются акустическими по своему характеру. При этом возможно одновременное отображение как анатомических изображений, так и изображений устройства.
В другом полезном варианте осуществления интервенционное применение содержит использование двух медицинских устройств внутри объекта 448. Например, одно устройство 402 может содержать направляющий катетер, который размещают в одном месте, и другое устройство 403 может содержать иглу для выполнения абляции или биопсии в фиксированных/разных местах по длине катетера. Устройство 402 содержит наноматериалы 404, и устройство 403 содержит наноматериалы 405. В приведенном примере наноматериалы 404 и 405 являются наноматериалами двух разных типов с разными длинами волн максимального поглощения. Наноматериалы 404 применяют для формирования изображения направляющего катетера, и наноматериалы 405 применяют для формирования изображения иглы.
Во время процедуры наноматериалы 404 возбуждают первой длиной волны, и наноматериалы 405 возбуждают отличающейся длиной волны. При этом наноматериалы 404 применяют для определения положения катетера, а наноматериалы 405 на игле применяют для точного позиционирования иглы относительно катетера.
В другом наглядном варианте осуществления применяют способ вычитания изображений для более точного получения положения устройства 402 с использованием включенных в него наноматериалов 404. Поскольку спектры поглощения наноматериалов 404 априорно известны, и спектры поглощения составляющих тканей также известны, то можно выбрать две частоты, на которых коэффициенты поглощения аналогичны коэффициентам поглощения тканей, с обеспечением, при этом, чтобы поглощение наноматериалов 404 на упомянутых двух частотах было разным. Пациент или объект 448 сначала подвергается облучению на первой частоте, что дает, в результате, первый отклик (излучение) наноматериалов 404, и регистрируется на первом изображении. Затем пациент подвергается облучению на второй частоте, что дает, в результате, второй отличающийся отклик (излучение) наноматериалов 404, и регистрируется на втором изображении. Затем модуль 417 обработки изображений вычитает второе изображение из первого изображения для извлечения однозначной информации о наноматериалах 404 и, следовательно, о положении медицинского устройства 402.
Приведенный способ можно применять с любыми из всех вышеописанных вариантов осуществления, чтобы определять местоположения устройств 402, 403 и т.п. (например, катетеров, игл и т.п.). При формировании изображений наноматериалов 404, 405 длины волн падающего электромагнитного излучения зависят от наноматериалов и их геометрии. Например, золотые наностержни со средними аспектными отношениями 5,9 и 3,7 демонстрируют максимальные оптические поглощения на 1000 и 785 нм соответственно. Устройство 410 формирования изображений обеспечивает контраст с наноматериалами 404, 405, которые могут быть отображены.
На фиг.5 представлен способ формирования изображений наноматериалов в соответствии с одним наглядным вариантом осуществления. На этапе 502 выбирают и подстраивают композицию наноматериалов, чтобы реагировать на предварительно заданные длины волн (или частоты) электромагнитного излучения. Подстройка может содержать выбор типа материалов (например, наносфер, нанотрубок, трубок CNT и т.п.), выбор материала (например, золота, графита и т.п.), выбор геометрии (например, размеров и формы), концентрации легирующего вещества и т.п., как изложено в настоящей заявке. На этапе 503 композицию наноматериалов включают в состав, по меньшей мере, одного медицинского устройства или инструмента. Наноматериалы могут содержать материалы с одинаковыми спектрами поглощения или могут содержать материалы с разными спектрами поглощения. В одном варианте осуществления каждый из разных наноматериалов может быть однозначно ассоциирован с разными устройствами, или одно и то же устройство может содержать наноматериалы, реагирующие на разные длины волн/частоты. На этапе 504, по меньшей мере, одно медицинское устройство вводят в пациента (например, млекопитающее) во время медицинской процедуры.
На этапе 506 селективно применяют частоты электромагнитного излучения, соответствующие частотам возбуждения наноматериалов, по меньшей мере, одного типа, чтобы возбуждать наноматериалы. На этапе 508 собирают информацию изображения из ответных излучений от наноматериалов. Излучения зависят от, по меньшей мере, одной частоты электромагнитного излучения возбуждения. Информацию изображения можно использовать для определения местоположения, по меньшей мере, одного из медицинских устройств в анатомических/медицинских изображениях пациента.
На этапе 510, в другом варианте осуществления, информацию изображения для нескольких частот электромагнитного излучения возбуждения можно получать для устройства или устройств. В данном примере устройство содержит наноматериалы, которые характеризуются двумя различающимися частотами возбуждения. В предпочтительном варианте отклик на вторую частоту, обусловленный наноматериалами, можно распознавать как отличающийся от отклика на первую частоту, и упомянутые отклики отличаются от отклика окружающихся тканей. Например, первый, второй и т.п. отклики должны отличаться от отклика окружающих тканей, и отклик тканей является, по существу, одинаковым для возбуждения на всех частотах.
На этапе 512 первое и второе изображения вычитают одно из другого для получения информации изображения, однозначно определяемой для наноматериалов устройства. В результате данного этапа идентифицируют положение медицинского устройства в пациенте. Упомянутая информация служит для определения местоположения, например, катетеров, игл и т.п. Вычитание может содержать простое вычитание значений пикселей, однако возможно применение любых полезных методов обработки изображений.
На этапе 514 положение устройства или устройств может быть наложено на другие медицинские изображения для снабжения специалиста или врача полезным средством для идентификации положений устройства и выполнения процедуры. Упомянутые процедуры могут содержать, например, интервенционные процедуры с использованием катетеров, наблюдательных приборов, игл и т.п., например, катетеризацию сердца, обнаружение катетера, отслеживание и позиционирование во время абляционных процедур, визуализацию иглы для управления процедурами биопсии тканей, визуализацию других инструментов при минимально инвазивном хирургическом вмешательстве (эндоскопов) и т.п.
На фиг.6 наглядно представлен другой способ создания и применения катетера с требуемыми свойствами в соответствии с другим особенно полезным вариантом осуществления. На этапе 602 выбирают длины волн, на которых имеет место минимальное поглощение представляющими интерес тканями (например, свойства тканей человека на падающих длинах волн). Для ткани человека желателен диапазон 650-1200 нм (который содержит окно 700-900 нм в ближней инфракрасной (ИК) области, в котором свет характеризуется максимальной глубиной проникновения в ткань). Если медицинское устройство (например, катетер или игла) находится неглубоко под поверхностью или снаружи тела, то можно выбирать другие длины волн.
На этапе 604 идентифицируют наноматериалы, которые характеризуются оптимальным поглощением на упомянутых длинах волн или частотах. Осуществляют выбор размера, формы и т.п. частиц. Упомянутые наноматериалы дополнительно отсортировывают для оптимизации биосовместимости. Выбор наноматериалов можно осуществлять, как изложено выше.
На этапе 606 создают медицинское устройство (например, катетер) посредством нанесения покрытия, слоя и т.п. наноматериалов на его поверхность или формируют устройство в соответствии с, по меньшей мере, одним из вариантов осуществления, раскрытых в настоящей заявке. Источник электромагнитного излучения для возбуждения частиц можно обеспечить снаружи устройства или можно включить в конструкцию катетера (следовательно, падающее излучение не обязательно обеспечивать источником снаружи тела, внутри которого устройство может быть применено во время процедуры). Для обеспечения возбуждения можно применять мощные светодиоды (СИД), излучающие в инфракрасной области.
Затем, на этапе 608, фотоакустические сигналы или другие сигналы обратной связи, сгенерированные наноматериалами в результате падающего излучения устройства, могут быть отслежены ультразвуковым зондом или другим датчиком на поверхности тела.
При интерпретации прилагаемой формулы изобретения следует понимать, что:
a) слово «содержащий» не исключает присутствия других элементов или операций, кроме тех, которые перечислены в данном пункте формулы изобретения;
b) упоминание элемента в единственном числе не исключает присутствия множества упомянутых элементов;
c) никакие позиционные обозначения в формуле изобретения не ограничивают объема охраны формулы изобретения;
d) несколько «средств» могут быть представлены одним и тем же элементом или аппаратно или программно реализованной структурой или функцией; и
e) никакая конкретная последовательность операций не предполагает ее необходимости, если не указано особо.
В отношении вышеописанных предпочтительных вариантов осуществления систем и способов для визуализации в реальном времени медицинских устройств с использованием наноматериалов (которые необходимо считать наглядными, а не ограничивающими), следует отметить, специалистами в данной области техники, в свете вышеприведенных идей, могут быть созданы модификации и варианты. Поэтому следует понимать, что в конкретные раскрытые варианты осуществления изобретения могут быть внесены изменения, которые не выходят за пределы объема раскрытых вариантов осуществления, определяемого прилагаемой формулой изобретения. После предложенного описания деталей и особенностей в соответствии с требованиями патентного законодательства, предмет изобретения, заявленный и затребованный к охране патентом на изобретение, изложен в прилагаемой формуле изобретения.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ СЕЛЕКТИВНОГО РАЗРУШЕНИЯ РАКОВЫХ КЛЕТОК С ПОМОЩЬЮ МАГНИТНЫХ МИКРОКОНТЕЙНЕРОВ С ФОТОДИНАМИЧЕСКИМИ ИЛИ ФОТОТЕРМИЧЕСКИМИ КРАСИТЕЛЯМИ | 2009 |
|
RU2405600C9 |
| МОДИФИЦИРОВАННАЯ ПОВЕРХНОСТЬ, СПОСОБНАЯ ПРИОБРЕТАТЬ БАКТЕРИОСТАТИЧЕСКУЮ И БАКТЕРИЦИДНУЮ АКТИВНОСТЬ, СПОСОБ ЕЕ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЯ | 2014 |
|
RU2650376C2 |
| СПОСОБ УЛУЧШЕННОЙ ФОТОЭПИЛЯЦИИ НА ОСНОВЕ НАНОКОМПЛЕКСОВ МЕТАЛЛОВ | 2011 |
|
RU2630976C2 |
| СПОСОБ ЛАЗЕРНОГО ФОТОТЕРМОЛИЗА РАКОВЫХ КЛЕТОК | 2009 |
|
RU2424831C1 |
| СПОСОБ СЕЛЕКТИВНОГО РАЗРУШЕНИЯ МЕЛАНОМЫ | 2007 |
|
RU2347563C1 |
| МИКРОКОМПЛЕКС ДЛЯ ПРИМЕНЕНИЯ В ФОТОЭПИЛЯЦИИ, СПОСОБ ЕГО ПОЛУЧЕНИЯ И СОДЕРЖАЩАЯ ЕГО КОМПОЗИЦИЯ | 2015 |
|
RU2681215C2 |
| СПОСОБ ДИАГНОСТИКИ ДЕФЕКТОВ НА МЕТАЛЛИЧЕСКИХ ПОВЕРХНОСТЯХ | 2012 |
|
RU2522709C2 |
| СПОСОБ СЕЛЕКТИВНОГО ЛАЗЕРНОГО ФОТОТЕРМОЛИЗА РАКОВЫХ КЛЕТОК ПЛАЗМОННО-РЕЗОНАНСНЫМИ НАНОЧАСТИЦАМИ | 2015 |
|
RU2653801C1 |
| УСТРОЙСТВО И СПОСОБ МОДУЛЯЦИИ ПОЛЯРИЗАЦИИ СВЕТА С ПОМОЩЬЮ МАГНИТОФОТОННЫХ МЕТАПОВЕРХНОСТЕЙ | 2018 |
|
RU2703487C1 |
| МЕДИЦИНСКОЕ ЗОНДОВОЕ УСТРОЙСТВО ДЛЯ УЛЬТРАЗВУКОВОЙ ВИЗУАЛИЗАЦИИ | 2016 |
|
RU2723941C2 |


Группа изобретений относится к медицинской технике. Медицинское устройство и способы определения местоположения устройства содержат структуру, имеющую продольный размер и поверхность. Слой материала ассоциирован с поверхностью и продолжается вдоль, по меньшей мере, участка продольного размера. Наноматериалы заключены в полости указанного слоя и сконфигурированы с возможностью реагирования на сигнал возбуждения так, что сигнал возбуждения генерирует отклик от наноматериалов для создания возможности определения местоположения структуры в объекте. 4 н. и 11 з.п. ф-лы, 6 ил.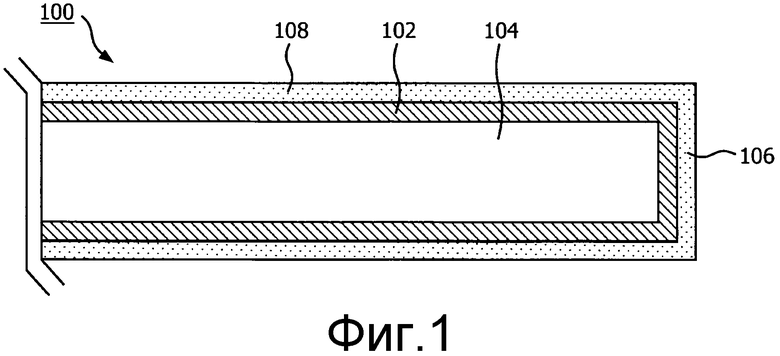
1. Обнаруживаемое медицинское устройство, имеющее продольный размер и поверхность (102) и содержащее:
слой (106) материала, ассоциированный с поверхностью и продолжающийся вдоль, по меньшей мере, участка продольного размера, причем слой материала содержит полость (206); и
наноматериалы (108), заключенные в полости и сконфигурированные с возможностью реагирования на, по меньшей мере, один сигнал возбуждения так, что сигнал возбуждения генерирует отклик от наноматериалов для создания возможности определения местоположения устройства в объекте.
2. Устройство по п. 1, в котором слой (106) материала содержит твердый слой, сформированный на поверхности.
3. Устройство по п. 1, в котором слой (106) материала содержит трубку (202), которая формирует полость, причем полость представляет собой кольцевую полость (206) относительно поверхности, при этом кольцевая полость содержит наноматериалы в суспензии (208).
4. Устройство по п. 3, дополнительно содержащее перемешивающий механизм (210), находящийся в сообщении с суспензией (208), для предотвращения осаждения наноматериалов.
5. Устройство по п. 1, в котором слой (106) материала содержит трубку (302), сформированную продольно вдоль поверхности, при этом трубка содержит полость, и причем в полости находятся наноматериалы в виде суспензии.
6. Система для определения местоположения медицинского устройства, при этом система содержит:
медицинское устройство (402), содержащее включенные в полость медицинского устройства наноматериалы (404), причем наноматериалы сконфигурированы с возможностью реагирования на, по меньшей мере, один сигнал возбуждения;
источник (406) возбуждения, сконфигурированный с возможностью генерирования, по меньшей мере, одного сигнала возбуждения для генерирования ответных излучений от наноматериалов;
датчик (408), сконфигурированный с возможностью приема ответных излучений;
и модуль (417) обработки изображений, сконфигурированный с возможностью отображения медицинского устройства на медицинском изображении с использованием ответных излучений.
7. Система по п. 6, в которой медицинское устройство содержит трубку (302), сформированную продольно вдоль стенки устройства медицинского устройства, при этом трубка формирует полость, и в полости находятся наноматериалы в виде суспензии.
8. Система по п. 6, дополнительно содержащая перемешивающий механизм (422), находящийся в сообщении с суспензией, которая содержит наноматериалы, при этом перемешивающий механизм предназначен для предотвращения осаждения наноматериалов.
9. Способ определения местоположения медицинского устройства, при этом способ содержит следующие этапы:
обеспечивают медицинское устройство (100), содержащее включенные в полость медицинского устройства наноматериалы, причем наноматериалы сконфигурированы с возможностью реагирования на, по меньшей мере, один сигнал возбуждения;
возбуждают (506) наноматериалы с использованием, по меньшей мере, одного сигнала возбуждения для генерирования ответных излучений от наноматериалов;
измеряют (508) ответные излучения; и
обрабатывают (514) ответные излучения для определения местоположения медицинского устройства относительно медицинского изображения.
10. Способ по п. 9, в котором этап обеспечения медицинского устройства, содержащего включенные в полость наноматериалы, содержит включение наноматериалов в виде суспензии в, по меньшей мере, одно из полости, содержащей кольцевую полость (206), сформированную относительно стенки медицинского устройства; или полости, образованной в трубке (302), сформированной продольно вдоль стенки медицинского устройства.
11. Способ по п. 9, дополнительно содержащий этап перемешивания (422) наноматериалов, включенных в медицинское устройство в форме суспензии, содержащей наноматериалы, для предотвращения осаждения наноматериалов.
12. Способ генерирования изображения медицинского устройства, при этом способ содержит следующие этапы:
возбуждают (506) наноматериалы, содержащиеся в медицинском устройстве, с использованием первой частоты электромагнитного излучения возбуждения наноматериалов, для получения первого визуализируемого отклика, причем первый визуализируемый отклик может быть обнаружен по окружающим материалам;
возбуждают (510) наноматериалы, содержащиеся в медицинском устройстве, с использованием второй частоты электромагнитного излучения возбуждения наноматериалов, для получения второго визуализируемого отклика, который содержит реализуемое отличие от первого визуализируемого отклика, причем второй визуализируемый отклик может быть обнаружен по окружающим материалам;
вычитают (512) первый визуализируемый отклик из второго визуализируемого отклика для обеспечения изображения медицинского устройства относительно объекта.
13. Способ по п. 12, в котором медицинское устройство содержит наноматериалы, включенные в него посредством, по меньшей мере, одного из твердого слоя (106), сформированного на медицинском устройстве; суспензии в кольцевой полости (206), сформированной относительно стенки устройства медицинского устройства; или суспензии в трубке (302), сформированной продольно вдоль стенки устройства медицинского устройства.
14. Способ по п. 12, дополнительно содержащий этап перемешивания (422) наноматериалов, включенных в медицинское устройство в форме суспензии, содержащей наноматериалы, для предотвращения осаждения наноматериалов.
15. Способ по п. 12, дополнительно содержащий этап цифрового генерирования (514) изображения медицинского устройства на медицинском изображении.
| WO 2009021064A1, 12.02.2009 | |||
| US 5921933A, 13.07.1999 | |||
| СПОСОБ ФЕРРИМАГНИТО-ТЕРМОХИМИОТЕРАПИИ ЗЛОКАЧЕСТВЕННЫХ ОПУХОЛЕЙ КОМБИНАЦИЯМИ МАГНИТОУПРАВЛЯЕМЫХ НАНОПРЕПАРАТОВ С ВИЗУАЛИЗАЦИЕЙ ОНКОГЕНЕЗА, ОПРЕДЕЛЕНИЕМ ТЕРАПИИ, ПРЕДПОЧТИТЕЛЬНОЙ В РЕЖИМЕ РЕАЛЬНОГО ВРЕМЕНИ, И МОНИТОРИНГОМ РЕЗУЛЬТАТОВ ЛЕЧЕНИЯ В ЭКСПЕРИМЕНТЕ | 2014 |
|
RU2563369C1 |
Авторы
Даты
2017-01-10—Публикация
2012-04-16—Подача