Изобретение относится к новым синтетическим, химическим биологически активным веществам из ряда гетероциклических соединений формулы 1, защищающим проростки подсолнечника от токсического действия гербицида 2,4-дихлорфеноксиуксусной кислоты (2,4-Д).
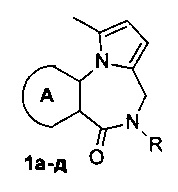
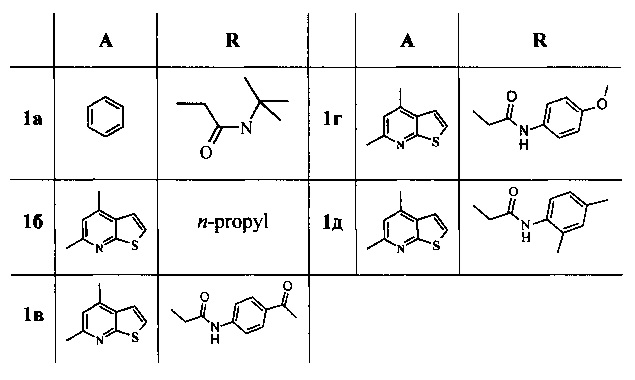
Соединения 1а-д, их химические и биологические свойства, в литературе не описаны.
Известны вещества - антидоты, обладающие способностью ослаблять токсическое действие гербицидов на сельскохозяйственные культуры. Антидоты усиливают метаболическую детоксикацию гербицида в растении, в частности, за счет повышения активности глутатион-S-трансферазной системы. Они вносятся в почву отдельно и совместно с гербицидами, или используются для предпосевной обработки семян [Стрелков В.Д. Поиск новых регуляторов роста растений и гербицидных антидотов. // Актуальные вопросы биологизации растений. Пущино, 2000. - С.152-155; Гилязетдинов Ш.Я., Узянбаев А.Х., Лукьянов С.А., Мухутдинов Ф.Г. Исследование росторегулирующей и протекторной активности иммуностимуляторов в смеси с гербицидами. // Создание высокопродуктивных агроэкосистем на основе новой парадигмы природопользования: Сб. докл. науч.-прак. конф. Уфа, 2001, с. 372-378].
Наиболее близкими аналогами по структуре и свойствам заявляемым соединениям являются N-арил-3-амино-4,6-диметилтиено[2,3-b]пиридин-2-карбоксамиды [Исакова Л.И., Ткач Л.Н., Назаренко Д.Ю.. Надыкта В.Д., Стрелков В.Д., Дядюченко Л.В., Дмитриева И.Г., Голубева Н.В. Антидоты гербицида 2,4-дихлорфеноксиуксусной кислоты, пат. РФ №2421992 от 27.06.2011, заявка №2009149496/04 от 29.12.2009] и N-(4-фторфенил)-3-амино-4,6-диметилтиено[2,3-b]пиридин-2-карбоксамид [Стрелков В.Д., Дядюченко Л.В., Исакова Л.И., Квасенков О.И. Способ защиты вегетирующих растений подсолнечника от повреждающего действия 2,4-Д, пат. РФ №2277333 от 10.06.2006, заявка №2005103585 от 14.02.2005]:
 ,
,
где X = 4-хлор-2,5-диметоксифенил; 3-фторфенил; 2-бромфенил; 4-фторфенил.
Задачей изобретения является синтез новых соединений в ряду конденсированных пирроло[1,2-a][1,4]диазепинов формулы 1а-д с целью расширения арсенала биологически активных веществ, полученных синтетическим путем, для применения их в сельском хозяйстве в качестве антидотов гербицида гормонального действия 2,4-Д.
Техническим результатом является повышение антидотной активности N-алкилзамещенных бензо- и (пиридо[2,3-b]тиено)пирроло[1,2-а][1,4]диазепин-6-онов 1а-д в отношении гербицида гормонального действия 2,4-дихлорфеноксиуксусной кислоты для защиты проростков семян подсолнечника, что позволяет увеличить урожайность культуры подсолнечника.
Соединения 1а-д синтезированы алкилированием пирролодиазепинов 2а, б при обработке йодалканами или N-замещенными хлорацетамидами в абсолютном диоксане в присутствии NaH при комнатной температуре.

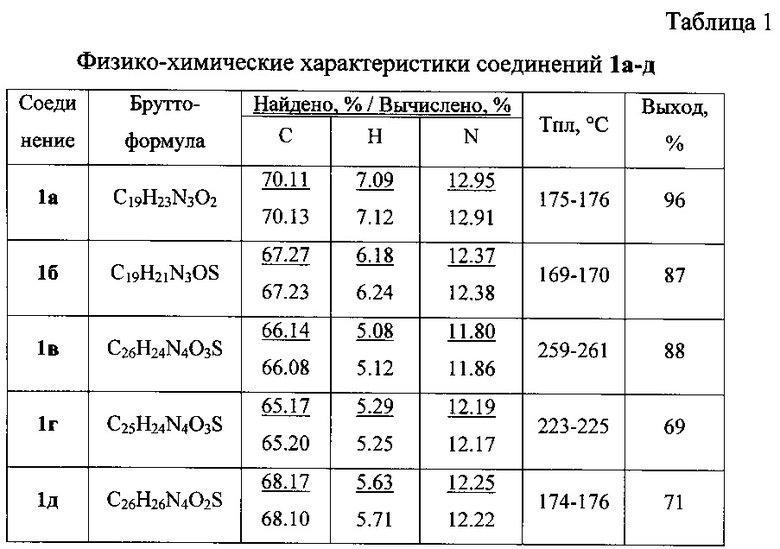
Структуры полученных продуктов N-алкилирования установлены на основании данных ЯМР 1Н и 13С спектроскопии, ИК- и масс-спектрометрии и данных элементного анализа, которые приведены в табл. 1 и 2.
Исходные пирролодиазепины 2а, б, аннелированные с бензольным кольцом или тиено[2,3-b]пиридиновым фрагментом, получены в результате катализируемой кислотами рециклизации N-фурфуриламидов антраниловых и 3-аминотиено[2,3-b]пиридин-2-карбоновых кислот в системе HCl/АсОН по описанной ранее методике [Stroganova, Т.; Vasilin, V.; Butin, A.; Nevolina, Т.; Krapivin, G. Synlett 2007, 1106]:
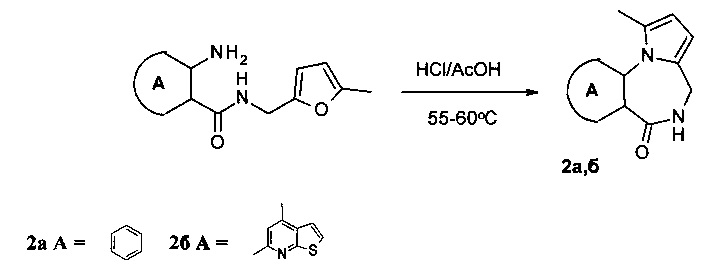
Изучение антидотной активности проведено в лабораторных условиях на проростках подсолнечника сорта «Мастер».
Изобретение иллюстрируется следующими примерами.
Пример 1. Получение N-(трет-бутил)-2-(1-метил-6-оксо-4H-пирроло[1,2-а][1,4]бензодиазепин-5(6H)-ил)ацетамида (1а).
К раствору диазепина 2а (0.414 г, 2 ммоль) в 30 мл безводного диоксана при перемешивании добавляют NaH (60%, 0.12 г, 3 ммоль) и выдерживают реакционную смесь 20 мин. Затем вносят раствор N-трет-бутилхлорацетамида (0.389 г, 2.6 ммоль) в 15 мл диоксана и продолжают перемешивание при КТ в течение 5 ч до полного расходования исходного диазепина (ТСХ). Реакционную смесь выливают в воду (150 мл), перемешивают до формирования осадка, который отделяют фильтрацией, сушат и перекристаллизовывают из смеси СН2Сl2-петролейный эфир, получая соединение 1а в виде порошка белого цвета с выходом 96%.
Пример 2. Получение 1,9,11-триметил-5-пропил-4,5,6а,11b-тетрагидро-6H-пиридо[3',2':4,5]тиено[2,3-ƒ]пирроло[1,2-а][1,4]диазепин-6-она (1б).
К раствору диазепина 2б (0.594 г, 2 ммоль) в 30 мл безводного диоксана при перемешивании добавляют NaH (60%, 0.12 г, 3 ммоль) и выдерживают реакционную смесь 20 мин. Затем вносят раствор 1-йодпропана (0.442 г, 2.6 ммоль) в 15 мл диоксана, и продолжают перемешивание при КТ в течение 4 ч до полного расходования исходного диазепина (ТСХ). Реакционную смесь выливают в воду (150 мл), перемешивают до формирования осадка, который отделяют фильтрацией, сушат и перекристаллизовывают из смеси СН2Сl2-петролейный эфир, получая соединение 1б в виде порошка белого цвета с выходом 87%.
Пример 3. Получение N-(4-ацетилфенил)-2-(1,9,11-триметил-6-оксо-6а,11b-дигидро-4H-пиридо[3',2':4,5]тиено[2,3-ƒ]пирроло[1,2-а][1,4]диазепин-5(6H)-ил)ацетамида (1в).
К раствору диазепина 2б (0.594 г, 2 ммоль) в 30 мл безводного диоксана при перемешивании добавляют NaH (60%, 0.12 г, 3 ммоль) и выдерживают реакционную смесь 20 мин. Затем вносят раствор N-(4-ацетилфенил)-2-хлорацетамида (0.550 г, 2.6 ммоль) в 15 мл диоксана, и продолжают перемешивание при КТ в течение 8 ч до полного расходования исходного диазепина (ТСХ). Реакционную смесь выливают в воду (150 мл), перемешивают до формирования осадка, который отделяют фильтрацией, сушат и перекристаллизовывают из смеси СН2Сl2-петролейный эфир, получая соединение 1в в виде порошка белого цвета с выходом 88%.
Пример 4. Получение N-(4-метоксифенил)-2-(1,9,11-триметил-6-оксо-6а,11b-дигидро-4H-пиридо[3',2':4,5]тиено[2,3-ƒ]пирроло[1,2-а][1,4]диазепин-5(6H)-ил)ацетамида (1г).
К раствору диазепина 2б (0.594 г, 2 ммоль) в 30 мл безводного диоксана при перемешивании добавляют NaH (60%, 0.12 г, 3 ммоль), и выдерживают реакционную смесь 20 мин. Затем вносят раствор N-(4-метоксифенил)-2-хлорацетамида (0.519 г, 2.6 ммоль) в 15 мл диоксана и продолжают перемешивание при КТ в течение 8 ч до полного расходования исходного диазепина (ТСХ). Реакционную смесь выливают в воду (150 мл), перемешивают до формирования осадка, который отделяют фильтрацией, сушат и перекристаллизовывают из смеси CH2Cl2-петролейный эфир, получая соединение 1г в виде порошка белого цвета с выходом 69%.
Пример 5. Получение N-(2,4-диметилфенил)-2-(1,9,11-триметил-6-оксо-6а,11b-дигидро-4H-пиридо[3',2':4,5]тиено[2,3-ƒ]пирроло[1,2-а][1,4]диазепин-5(6H)-ил)ацетамида (1д)
К раствору диазепина 2б (0.594 г, 2 ммоль) в 30 мл безводного диоксана при перемешивании добавляют NaH (60%, 0.12 г, 3 ммоль), и выдерживают реакционную смесь 20 мин. Затем вносят раствор N-(2,4-диметилфенил)-2-хлорацетамида (0.514 г, 2.6 ммоль) в 20 мл диоксана и продолжают перемешивание при КТ в течение 10 ч до полного расходования исходного диазепина (ТСХ). Реакционную смесь выливают в воду (150 мл), перемешивают до формирования осадка, который отделяют фильтрацией, сушат и перекристаллизовывают из смеси CH2Cl2-петролейный эфир, получая соединение 1д в виде порошка белого цвета с выходом 71%.
Физико-химические и спектральные характеристики пирролодиазепинов 1а-д представлены в таблицах 1, 2.

Пример 6. Изучение антидотной активности N-замещенных конденсированных пирроло[1,2-а][1,4]диазепин-6-онов 1а-д (табл. 3)
Эксперименты по изучению антидотной активности новых соединений формулы 1а-д проводили в лабораторных условиях на проростках подсолнечника по ранее разработанной и апробированной методике [Стрелков, В.Д.; Дядюченко, Л.В.; Исакова, Л.И.; Дмитриева, И.Г. Агрохимия, 2010, 28].
Проросшие семена подсолнечника с длиной корешка 2-4 мм помещали на 1 ч в водный раствор 2,4-дихлорфеноксиуксусной кислоты (2,4-Д) в концентрации 10-3 масс. %. Затем проростки промывали водой и помещали в водные растворы испытываемых на антидотную активность веществ в концентрации 10-2, 10-3, 10-4, 10-5 масс. % (вариант «гербицид + антидот») на 1 ч. Спустя 1 ч семена промывали водой и раскладывали на полосы фильтровальной бумаги (размер 10×75 см) по 20 штук, сворачивали в рулоны и помещали в стаканы с водой (50 мл воды).
Семена варианта «гербицид» (эталон сравнения) выдерживали 1 ч в растворе 2,4-Д в концентрации 10-3 масс. % и 1 ч в воде.
Стаканы с рулонами помещали в термостат и выдерживали в течение 3-х суток при постоянной температуре 28°С. Затем измеряли длину гипокотиля и корня проростков.
Защитный (антидотный) эффект изучаемых веществ определяли по увеличению длины гипокотиля и корня в варианте «гербицид + антидот» относительно названных величин в варианте «гербицид» (эталон) и рассчитывали по формуле:
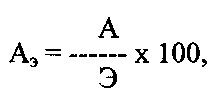
где Аэ - антидотный эффект, %;
А - длина гипокотиля, корня в варианте «гербицид + антидот», мм;
Э - длина гипокотиля, корня в эталоне («гербицид»), мм.
Статистическая обработка экспериментальных данных проведена с использованием t-критерия Стьюдента при Р=0,95.
Результаты испытаний представлены в таблице 3.
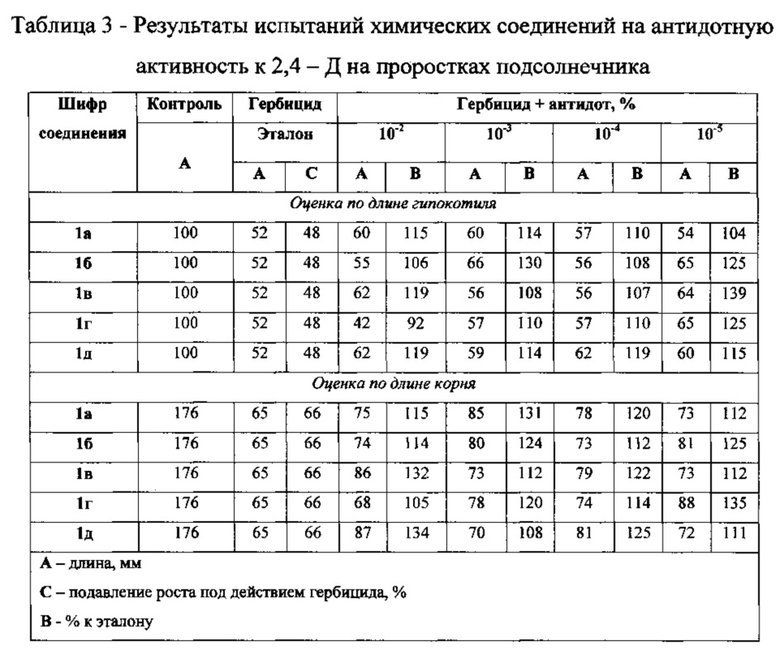
Установлено, что при обработке водными растворами проростков подсолнечника активность по снижению ингибирующего действия 2,4-Д на гипокотиль проявили соединения 1в, 1д, 1а в концентрации 10-2 (от 15 до 19%); 1д, 1б и 1а в концентрации 10-3 (от 14 до 30%); 1д в концентрации 10-4 (19%) и соединения 1б-г в концентрации 10-5 масс. % (от 15 до 39%) (Таблица 3).
Антидотную активность по снижению ингибирующего действия 2,4-Д на корни проростков проявили растворы веществ 1а-д с концентрацией 10-2 (14-34%); 1а-г с концентрацией 10-3 (12-31%); 1а-д с концентрацией 10-4 (12-25%) и 1а-д с концентрацией 10-5 масс. % (11-35%).
Из результатов лабораторных испытаний следует, что в ряду изучаемых веществ наибольший антидотный эффект обнаружен у веществ 1в и 1д в концентрации 10-2, соединения 1а в концентрации 10-3 и 1б, г в концентрации 10-5 масс. %. Указанные соединения достоверно снижают токсическое действие гербицида 2,4-Д на проростки подсолнечника, что может способствовать увеличению урожайности этой культуры.
Таким образом, использование заявляемых N-алкилзамещенных бензо- и (пиридо[2,3-b]тиено)пирроло[1,2-а][1,4]диазепин-6-онов 1а-д в качестве антидота в отношении гербицида гормонального действия 2,4-дихлорфеноксиуксусной кислоты (2,4-Д) на проростках подсолнечника позволяет обеспечить антидотный эффект, а также расширить ассортимент известных антидотов.
| название | год | авторы | номер документа |
|---|---|---|---|
| СРЕДСТВО ДЛЯ СНИЖЕНИЯ ТОКСИЧЕСКОГО ДЕЙСТВИЯ ГЕРБИЦИДА 2,4-ДИХЛОРФЕНОКСИУКСУСНОЙ КИСЛОТЫ НА ПОДСОЛНЕЧНИКЕ | 2003 |
|
RU2242123C1 |
| Применение 1,6-диамино-4-арил-2-оксо-1,2-дигидропиридин-3,5-дикарбонитрилов в качестве антидотов 2,4-Д на подсолнечнике | 2024 |
|
RU2826751C1 |
| 6,6'-[Метиленди(имино)]бис(4-метил-2-оксо-1,2-дигидропиридин-3,5-дикарбонитрил) в качестве антидота 2,4-Д на подсолнечнике | 2023 |
|
RU2812590C1 |
| 3,10-Диметил-1,8-диоксо-5,6,12,13-тетрагидро-1H,8H-дипиридо[1,2-a:1',2'-e][1,3,5,7]тетразоцин-2,4,9,11-тетракарбонитрил в качестве антидота 2,4-Д на подсолнечнике | 2022 |
|
RU2788768C1 |
| ПРИМЕНЕНИЕ 2-(1Н-1-ПИРРОЛИЛ)-4-ДИПРОПИЛАМИНО-6-(4-ЭТОКСИКАРБОНИЛ-5-МЕТИЛ-1,2,3-ТРИАЗОЛ-1-ИЛ)-1,3,5-ТРИАЗИНА В КАЧЕСТВЕ АНТИДОТА ОТ ФИТОТОКСИЧЕСКОГО ДЕЙСТВИЯ ГЕРБИЦИДА 2,4-ДИХЛОРФЕНОКСИУКСУСНОЙ КИСЛОТЫ НА ПРОРАЩЕННЫЕ СЕМЕНА ПОДСОЛНЕЧНИКА | 2008 |
|
RU2378831C1 |
| Замещенные эфиры 6-амино-7-фенил-3-(фенилимино)-4,7-дигидро-3H-[1,2]дитиоло[3,4-b]пиридин-5-карбоновой кислоты в качестве антидотов 2,4-Д на подсолнечнике | 2022 |
|
RU2799422C1 |
| Замещенные 3-(3-амино-4,6-диметилтиено[2,3-b]пиридин-2-ил)-3-оксо-N-фенилпропанамиды в качестве антидотов 2,4-Д на подсолнечнике | 2022 |
|
RU2798590C1 |
| N-арил-3[(цианоацетил)амино]-4,6-диметилтиено[2,3-b]-пиридил-2-карбоксамиды в качестве антидотов 2,4-Д на подсолнечнике | 2021 |
|
RU2776586C1 |
| ЗАМЕЩЕННЫЕ 6а,11-ДИГИДРО-5H-БЕНЗО[4,5][1,3]ОКСАЗИНО[2,3-α]ИЗОИНДОЛ-11-ОНЫ-АНТИДОТЫ ГЕРБИЦИДА ГОРМОНАЛЬНОГО ДЕЙСТВИЯ 2,4-ДИХЛОР-ФЕНОКСИУКСУСНОЙ КИСЛОТЫ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2007 |
|
RU2345083C1 |
| 4,6-ДИМЕТИЛ-2-ХЛОР-3-(5-Х-1,2,4-ОКСАДИАЗОЛИЛ-3)-ПИРИДИНЫ В КАЧЕСТВЕ АНТИДОТОВ 2,4-ДИХЛОРФЕНОКСИУКСУСНОЙ КИСЛОТЫ | 2008 |
|
RU2356900C1 |
Изобретение относится к новым синтетическим, химическим биологически активным веществам из ряда гетероциклических соединений формулы 1
 . Технический результат: синтез новых соединений в ряду конденсированных пирроло[1,2-a][1,4]диазепинов формулы 1а-д с целью расширения арсенала биологически активных веществ, полученных синтетическим путем, для применения их в сельском хозяйстве в качестве антидотов гербицида гормонального действия 2,4-Д. 3 табл., 6 пр.
. Технический результат: синтез новых соединений в ряду конденсированных пирроло[1,2-a][1,4]диазепинов формулы 1а-д с целью расширения арсенала биологически активных веществ, полученных синтетическим путем, для применения их в сельском хозяйстве в качестве антидотов гербицида гормонального действия 2,4-Д. 3 табл., 6 пр.
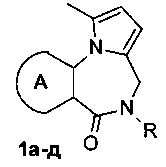
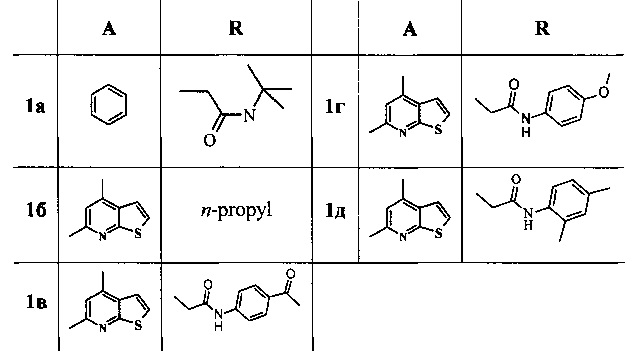
Антидоты гербицида гормонального действия 2,4-дихлорфеноксиуксусной кислоты (2,4-Д) на подсолнечнике, защищающие проростки семян подсолнечника от вышеназванного гербицида и представляющие собой N-алкилзамещенные бензо- и (пиридо[2,3-b]тиено)пирроло[1,2-а][1,4]диазепин-6-оны формулы 1:
| Stroganova, Tat'yana A.; Vasilin, Vladimir K.; Krapivin, Gennady D.; Strelkov, Vladimir D.; Dyadyuchenko, Ludmila V | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Chemistry of Heterocyclic Compounds, 52(1), 45-51, 2016. | |||
Авторы
Даты
2017-01-10—Публикация
2016-02-25—Подача