ПЕРЕКРЕСТНАЯ ССЫЛКА НА РОДСТВЕННЫЕ ЗАЯВКИ
По настоящей заявке испрашивается приоритет предварительных патентных заявок серийные №№ 61/468502, поданная 28 марта 2011 года; 61/530859, поданная 2 сентября 2011 года; и 61/560699, поданная 16 ноября 2011 года; описание каждой из которых включено в настоящее изобретение с помощью ссылки во всей своей полноте.
ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ НАСТОЯЩЕЕ ИЗОБРЕТЕНИЕ
Настоящее изобретение относится к (альфа-замещенным аралкиламино- или гетероарилалкиламино)пиримидинил- и 1,3,5-триазинилбензимидазолам и их фармацевтическим композициям, получению и применению в качестве агентов или лекарственных средств для лечения пролиферативных заболеваний.
УРОВЕНЬ ТЕХНИКИ
Фосфоинозитид-3-киназы (PI3K) представляют собой группу липидных киназ, которые фосфорилируют 3-гидроксил фосфоинозитидов. Их разделяют по меньшей мере на три класса (классы I, II и III), и они играют важную роль в клеточной сигнализации (Stephens et al., Curr. Opin. Pharmacol. 2005, 5, 357). Ферменты I класса дополнительно разделяют на классы Ia и Ib на основании механизма их активации. PI3K класса Ia представляют собой гетеродимерные структуры, состоящие из каталитической субъединицы (p110α, p110β или p110δ) в комплексе с регуляторной субъединицей p85, тогда как PI3K класса Ib (p110γ) являются структурно аналогичными, но не содержат регуляторную субъединицу p85, и вместо этого активируются субъединицами βγ гетеродимерных G-белков (Walker et al., Mol. Cell. 2000, 6, 909).
PI3K выполняют ряд функций в физиологии нормальных тканей (Foukas & Shepherd, Biochem. Soc. Trans. 2004, 32, 330; Shepherd, Acta Physiol. Scand. 2005, 183, 3), причем QUOTE "" ADDIN REFMAN ÿ\11\05‘\19\01\00\00\00\00\01\00\00"X:\5CREFMAN\5CDATABASE\5CAcsrcReferences\03\00\0518399 Foukas & Shepherd 2004 18399 /id\00 \00 QUOTE "" ADDIN REFMAN ÿ\11\05‘\19\01\00\00\00\00\01\00\00"X:\5CREFMAN\5CDATABASE\5CAcsrcReferences\03\00\0518396\17Shepherd 2005 18396 /id\00\17\00 p110α обладает специфической ролью при раковом росте, p110β - в образовании тромбов, опосредованном интегрином αIIβ3 (Jackson et al., Nat. Med. 2005, 11, 507), и p110γ - при воспалении, ревматоидном артрите и других хронических воспалительных заболеваниях (Barber et al., Nat. Med. 2005, 11, 933; Camps et al., Nat. Med. 2005, 11, 936; Rommel et al., Nat. Rev. 2007, 7, 191; и Ito, et al., J. Pharm. Exp. Therap. 2007, 321, 1). Следовательно, существует необходимость в PI3K ингибиторах для лечения рака и/или воспалительных заболеваний.
СУЩНОСТЬ НАСТОЯЩЕГО ИЗОБРЕТЕНИ Я
Настоящее изобретение относится к соединению формулы I:
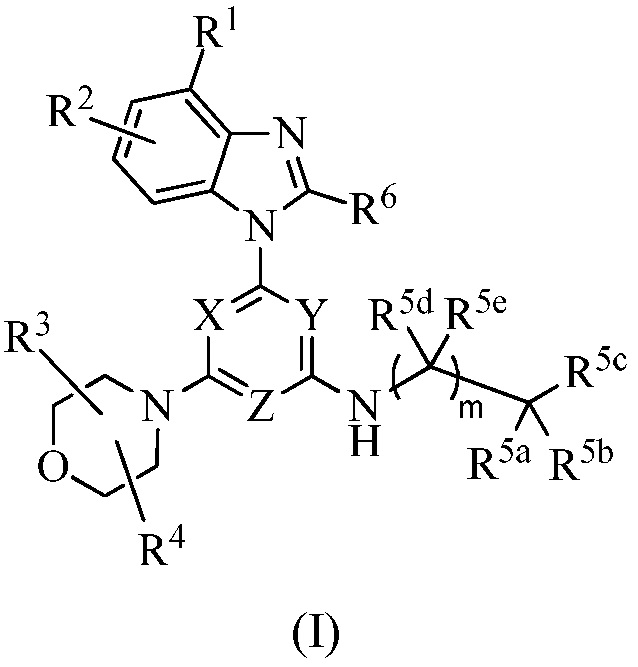
или его энантиомеру, смеси энантиомеров, смеси двух или более диастереомеров или изотопному варианту; или их фармацевтически приемлемой соли, сольвату, гидрату или пролекарству; где:
каждый X, Y и Z независимо представляет собой N или CRX, при условии, что по меньшей мере два из X, Y и Z представляют собой атомы азота; где RX представляет собой водород или C1-6 алкил;
каждый R1 и R2 независимо представляет собой (a) водород, циано, галоген или нитро; (b) C1-6 алкил, C2-6 алкенил, C2-6 алкинил, C3-10 циклоалкил, C6-14 арил, C7-15 аралкил, гетероарил или гетероциклил; или (c) -C(O)R1a, -C(O)OR1a, -C(O)NR1bR1c, -C(NR1a)NR1bR1c, -OR1a, -OC(O)R1a, -OC(O)OR1a, -OC(O)NR1bR1c, -OC(=NR1a)NR1bR1c, -OS(O)R1a, -OS(O)2R1a, -OS(O)NR1bR1c, -OS(O)2NR1bR1c, -NR1bR1c, -NR1aC(O)R1d, -NR1aC(O)OR1d, -NR1aC(O)NR1bR1c, -NR1aC(=NR1d)NR1bR1c, -NR1aS(O)R1d, -NR1aS(O)2R1d, -NR1aS(O)NR1bR1c, -NR1aS(O)2NR1bR1c, -SR1a, -S(O)R1a, -S(O)2R1a, -S(O)NR1bR1c или -S(O)2NR1bR1c; где каждый R1a, R1b, R1c и R1d независимо представляет собой (i) водород; (ii) C1-6 алкил, C2-6 алкенил, C2-6 алкинил, C3-10 циклоалкил, C6-14 арил, C7-15 аралкил, гетероарил или гетероциклил; или (iii) R1b и R1c вместе с атомом N, с которым они соединены, образуют гетероциклил;
каждый R3 и R4 независимо представляет собой водород или C1-6 алкил; или R3 и R4 соединены вместе, образуя связь, C1-6 алкилен, C1-6 гетероалкилен, C2-6 алкенилен или C2-6 гетероалкенилен;
R5a представляет собой (a) водород или галоген; (b) C1-6 алкил, C2-6 алкенил, C2-6 алкинил, C3-10 циклоалкил, C6-14 арил, C7-15 аралкил, гетероарил или гетероциклил; или (c) -C(O)R1a, -C(O)OR1a, -C(O)NR1bR1c, -C(NR1a)NR1bR1c, -OR1a, -OC(O)R1a, -OC(O)OR1a, -OC(O)NR1bR1c, -OC(=NR1a)NR1bR1c, -OS(O)R1a, -OS(O)2R1a, -OS(O)NR1bR1c, -OS(O)2NR1bR1c, -NR1bR1c, -NR1aC(O)R1d, -NR1aC(O)OR1d, -NR1aC(O)NR1bR1c, -NR1aC(=NR1d)NR1bR1c, -NR1aS(O)R1d, -NR1aS(O)2R1d, -NR1aS(O)NR1bR1c, -NR1aS(O)2NR1bR1c, -SR1a, -S(O)R1a, -S(O)2R1a, -S(O)NR1bR1c или -S(O)2NR1bR1c;
R5b представляет собой (a) галоген; (b) C1-6 алкил, C2-6 алкенил, C2-6 алкинил, C3-10 циклоалкил, C6-14 арил, C7-15 аралкил, гетероарил или гетероциклил; или (c) -C(O)R1a, -C(O)OR1a, -C(O)NR1bR1c, -C(NR1a)NR1bR1c, -OR1a, -OC(O)R1a, -OC(O)OR1a, -OC(O)NR1bR1c, -OC(=NR1a)NR1bR1c, -OS(O)R1a, -OS(O)2R1a, -OS(O)NR1bR1c, -OS(O)2NR1bR1c, -NR1bR1c, -NR1aC(O)R1d, -NR1aC(O)OR1d, -NR1aC(O)NR1bR1c, -NR1aC(=NR1d)NR1bR1c, -NR1aS(O)R1d, -NR1aS(O)2R1d, -NR1aS(O)NR1bR1c, -NR1aS(O)2NR1bR1c, -SR1a, -S(O)R1a, -S(O)2R1a, -S(O)NR1bR1c или -S(O)2NR1bR1c;
R5c представляет собой -(CR5fR5g)n-(C6-14 арил) или -(CR5fR5g)n-гетероарил;
каждый R5d и R5e независимо представляет собой (a) водород или галоген; (b) C1-6 алкил, C2-6 алкенил, C2-6 алкинил, C3-10 циклоалкил, C6-14 арил, C7-15 аралкил, гетероарил или гетероциклил; или (c) -C(O)R1a, -C(O)OR1a, -C(O)NR1bR1c, -C(NR1a)NR1bR1c, -OR1a, -OC(O)R1a, -OC(O)OR1a, -OC(O)NR1bR1c, -OC(=NR1a)NR1bR1c, -OS(O)R1a, -OS(O)2R1a, -OS(O)NR1bR1c, -OS(O)2NR1bR1c, -NR1bR1c, -NR1aC(O)R1d, -NR1aC(O)OR1d, -NR1aC(O)NR1bR1c, -NR1aC(=NR1d)NR1bR1c, -NR1aS(O)R1d, -NR1aS(O)2R1d, -NR1aS(O)NR1bR1c, -NR1aS(O)2NR1bR1c, -SR1a, -S(O)R1a, -S(O)2R1a, -S(O)NR1bR1c или -S(O)2NR1bR1c;
каждый R5f и R5g независимо представляет собой (a) водород или галоген; (b) C1-6 алкил, C2-6 алкенил, C2-6 алкинил, C3-10 циклоалкил, C6-14 арил, C7-15 аралкил, гетероарил или гетероциклил; или (c) -C(O)R1a, -C(O)OR1a, -C(O)NR1bR1c, -C(NR1a)NR1bR1c, -OR1a, -OC(O)R1a, -OC(O)OR1a, -OC(O)NR1bR1c, -OC(=NR1a)NR1bR1c, -OS(O)R1a, -OS(O)2R1a, -OS(O)NR1bR1c, -OS(O)2NR1bR1c, -NR1bR1c, -NR1aC(O)R1d, -NR1aC(O)OR1d, -NR1aC(O)NR1bR1c, -NR1aC(=NR1d)NR1bR1c, -NR1aS(O)R1d, -NR1aS(O)2R1d, -NR1aS(O)NR1bR1c, -NR1aS(O)2NR1bR1c, -SR1a, -S(O)R1a, -S(O)2R1a, -S(O)NR1bR1c или -S(O)2NR1bR1c; или (d) когда один экземпляр R5f и один экземпляр R5g соединены с одним и тем же атомом углерода, R5f и R5g вместе с атомом углерода, с которым они соединены, образуют C3-10 циклоалкил или гетероциклил;
R6 представляет собой водород, C1-6 алкил, -S-C1-6 алкил, -S(O)-C1-6 алкил или -SO2-C1-6 алкил;
m равно 0 или 1; и
n равно 0, 1, 2, 3 или 4;
где каждый алкил, алкилен, гетероалкилен, алкенил, алкенилен, гетероалкенилен, алкинил, циклоалкил, арил, аралкил, гетероарил и гетероциклил в R1, R2, R3, R4, R6, RX, R1a, R1b, R1c, R1d, R5a, R5b, R5c, R5d, R5e, R5f и R5g необязательно замещен одним или более, в одном варианте осуществления одним, двумя, тремя или четырьмя, заместителями Q, где каждый заместитель Q независимо выбран из (a) оксо, циано, галогена и нитро; (b) C1-6 алкила, C2-6 алкенила, C2-6 алкинила, C3-10 циклоалкила, C6-14 арила, C7-15 аралкила, гетероарила и гетероциклила, каждый из которых дополнительно необязательно замещен одним или более, в одном варианте осуществления одним, двумя, тремя или четырьмя, заместителями Qa; и (c) -C(O)Ra, -C(O)ORa, -C(O)NRbRc, -C(NRa)NRbRc, -ORa, -OC(O)Ra, -OC(O)ORa, -OC(O)NRbRc, -OC(=NRa)NRbRc, -OS(O)Ra, -OS(O)2Ra, -OS(O)NRbRc, -OS(O)2NRbRc, -NRbRc, -NRaC(O)Rd, -NRaC(O)ORd, -NRaC(O)NRbRc, -NRaC(=NRd)NRbRc, -NRaS(O)Rd, -NRaS(O)2Rd, -NRaS(O)NRbRc, -NRaS(O)2NRbRc, -SRa, -S(O)Ra, -S(O)2Ra, -S(O)NRbRc и -S(O)2NRbRc, где каждый Ra, Rb, Rc и Rd независимо представляет собой (i) водород; (ii) C1-6 алкил, C2-6 алкенил, C2-6 алкинил, C3-10 циклоалкил, C6-14 арил, C7-15 аралкил, гетероарил или гетероциклил, каждый из которых дополнительно необязательно замещен одним или более, в одном варианте осуществления одним, двумя, тремя или четырьмя, заместителями Qa; или (iii) Rb и Rc вместе с атомом N, с которым они соединены, образуют гетероциклил, который дополнительно необязательно замещен одним или более, в одном варианте осуществления одним, двумя, тремя или четырьмя, заместителями Qa;
где каждый Qa независимо выбран из группы, состоящей из (a) оксо, циано, галогена и нитро; (b) C1-6 алкила, C2-6 алкенила, C2-6 алкинила, C3-10 циклоалкила, C6-14 арила, C7-15 аралкила, гетероарила и гетероциклила; и (c) -C(O)Re, -C(O)ORe, -C(O)NRfRg, -C(NRe)NRfRg, -ORe, -OC(O)Re, -OC(O)ORe, -OC(O)NRfRg, -OC(=NRe)NRfRg, -OS(O)Re, -OS(O)2Re, -OS(O)NRfRg, -OS(O)2NRfRg, -NRfRg, -NReC(O)Rh, -NReC(O)ORh, -NReC(O)NRfRg, -NReC(=NRh)NRfRg, -NReS(O)Rh, -NReS(O)2Rh, -NReS(O)NRfRg, -NReS(O)2NRfRg, -SRe, -S(O)Re, -S(O)2Re, -S(O)NRfRg и -S(O)2NRfRg; где каждый Re, Rf, Rg и Rh независимо представляет собой (i) водород; (ii) C1-6 алкил, C2-6 алкенил, C2-6 алкинил, C3-10 циклоалкил, C6-14 арил, C7-15 аралкил, гетероарил или гетероциклил; или (iii) Rf и Rg вместе с атомом N, с которым они соединены, образуют гетероциклил.
В одном варианте осуществления m равно 0; и каждый R5a и R5b независимо представляет собой (a) галоген; (b) C1-6 алкил, C2-6 алкенил, C2-6 алкинил, C3-10 циклоалкил, C6-14 арил, C7-15 аралкил, гетероарил или гетероциклил; или (c) -C(O)R1a, -C(O)OR1a, -C(O)NR1bR1c, -C(NR1a)NR1bR1c, -OR1a, -OC(O)R1a, -OC(O)OR1a, -OC(O)NR1bR1c, -OC(=NR1a)NR1bR1c, -OS(O)R1a, -OS(O)2R1a, -OS(O)NR1bR1c, -OS(O)2NR1bR1c, -NR1bR1c, -NR1aC(O)R1d, -NR1aC(O)OR1d, -NR1aC(O)NR1bR1c, -NR1aC(=NR1d)NR1bR1c, -NR1aS(O)R1d, -NR1aS(O)2R1d, -NR1aS(O)NR1bR1c, -NR1aS(O)2NR1bR1c, -SR1a, -S(O)R1a, -S(O)2R1a, -S(O)NR1bR1c или -S(O)2NR1bR1c.
Настоящее изобретение также относится к фармацевтическим композициям, содержащим соединение, описанное в настоящем изобретении, например, соединение формулы I или его энантиомер, смесь энантиомеров, смесь двух или более диастереомеров или изотопный вариант; или их фармацевтически приемлемую соль, сольват, гидрат или пролекарство; и один или более фармацевтически приемлемых вспомогательных веществ.
Кроме того, настоящее изобретение относится к способу лечения, предотвращения или облегчения одного или более симптомов PI3K-опосредованного расстройства, заболевания или состояния у субъекта, включающему введение субъекту терапевтически эффективного количества соединения, описанного в настоящем изобретении, например, соединения формулы I или его энантиомера, смеси энантиомеров, смеси двух или более диастереомеров или изотопного варианта; или их фармацевтически приемлемой соли, сольвата, гидрата или пролекарства.
Настоящее изобретение относится к способу лечения, предотвращения или облегчения одного или более симптомов PI3Kδ-опосредованного расстройства, заболевания или состояния у субъекта, включающему введение субъекту терапевтически эффективного количества соединения, описанного в настоящем изобретении, например, соединения формулы I или его энантиомера, смеси энантиомеров, смеси двух или более диастереомеров или изотопного варианта; или их фармацевтически приемлемой соли, сольвата, гидрата или пролекарства.
Настоящее изобретение относится к способу лечения, предотвращения или облегчения одного или более симптомов пролиферативного заболевания у субъекта, включающему введение субъекту терапевтически эффективного количества соединения, описанного в настоящем изобретении, например, соединения формулы I или его энантиомера, смеси энантиомеров, смеси двух или более диастереомеров или изотопного варианта; или их фармацевтически приемлемой соли, сольвата, гидрата или пролекарства.
Настоящее изобретение относится к способу регулирования PI3K активности, включающему контакт PI3K с эффективным количеством соединения, описанного в настоящем изобретении, например, соединения формулы I или его энантиомера, смеси энантиомеров, смеси двух или более диастереомеров или изотопного варианта; или их фармацевтически приемлемой соли, сольвата, гидрата или пролекарства.
Настоящее изобретение относится к способу регулирования PI3Kδ активности, включающему контакт PI3Kδ с эффективным количеством соединения, описанного в настоящем изобретении, например, соединения формулы I или его энантиомера, смеси энантиомеров, смеси двух или более диастереомеров или изотопного варианта; или их фармацевтически приемлемой соли, сольвата, гидрата или пролекарства.
Настоящее изобретение относится к способу селективного регулирования PI3Kδ активности, включающему контакт PI3Kδ с эффективным количеством соединения, описанного в настоящем изобретении, например, соединения формулы I или его энантиомера, смеси энантиомеров, смеси двух или более диастереомеров или изотопного варианта; или их фармацевтически приемлемой соли, сольвата, гидрата или пролекарства.
ПОДРОБНОЕ ОПИСАНИЕ
Для того чтобы облегчить понимание описания, излагаемого в настоящем изобретении, ряд терминов определяют ниже.
В общем, номенклатура, применяемая в настоящем изобретении, и лабораторные методики органической химии, медицинской химии и фармакологии, описанные в настоящем изобретении, являются хорошо известными, и их обычно применяют в данной области техники. Если не указано иначе, все технические и научные термины, применяемые в настоящем изобретении, обычно имеют те же значения, которые обычно известны специалисту в области техники, к которой относится настоящее изобретение.
Термин “субъект” относится к животному, включая, но не ограничиваясь, примата (например, человека), корову, свинью, овцу, козу, лошадь, собаку, кошку, кролика, крысу или мышь. Термины “субъект” и “пациент” применяют взаимозаменяемо в настоящем изобретении при ссылке, например, на субъекта, являющегося млекопитающим, такого как субъект, являющийся человеком, в одном варианте осуществления, человека.
Предполагается, что термины “лечить” и “лечение” включают облегчение или прекращение расстройства, заболевания или состояния, или одного или более из симптомов, связанных с расстройством, заболеванием или состоянием; или частичное снятие или устранение причины (причин) самого расстройства, заболевания или состояния.
Предполагается, что термины “предотвращать” и “предотвращение” включают способ задерживания и/или предотвращения возникновения расстройства, заболевания или состояния и/или сопровождающих их симптомов; предотвращения приобретения субъектом расстройства, заболевания или состояния; или снижения риска приобретения субъектом расстройства, заболевания или состояния.
Предполагается, что термин “терапевтически эффективное количество” включает количество соединения, которое при введении является достаточным для предотвращения развития или облегчения до некоторой степени одного или более из симптомов расстройства, заболевания или состояния, которые лечат. Термин “терапевтически эффективное количество” также относится к количеству соединения, которое является достаточным для того, чтобы вызвать биологический или медицинский ответ биологической молекулы (например, белка, фермента, РНК или ДНК), клетки, ткани, системы, животного или человека, которого добивается исследователь, ветеринар, медицинский доктор или клиницист.
Термин “фармацевтически приемлемый носитель”, “фармацевтически приемлемое вспомогательное вещество”, “физиологически приемлемый носитель” или “физиологически приемлемое вспомогательное вещество” относится к фармацевтически приемлемому материалу, композиции или среде, такому как жидкий или твердый наполнитель, разбавитель, растворитель или материал для инкапсулирования. В одном варианте осуществления каждый компонент является “фармацевтически приемлемым” в том смысле, что он совместим с другими ингредиентами фармацевтического состава и является подходящим для применения в контакте с тканью или органом людей и животных без избыточной токсичности, раздражения, аллергической реакции, иммуногенности или других проблем или осложнений, с соразмерным соотношением риск/польза. Смотрите Remington: The Science and Practice of Pharmacy, 21st Edition, Lippincott Williams & Wilkins: Philadelphia, PA, 2005; Handbook of Pharmaceutical Excipients, 5th Edition, Rowe et al., Eds., The Pharmaceutical Press and the American Pharmaceutical Association: 2005; и Handbook of Pharmaceutical Additives, 3rd Edition, Ash and Ash Eds., Gower Publishing Company: 2007; Pharmaceutical Preformulation and Formulation, 2nd Edition, Gibson Ed., CRC Press LLC: Boca Raton, FL, 2009.
Термин “приблизительно” обозначает приемлемую ошибку для конкретной величины, как определено специалистом в данной области техники, которая зависит отчасти от того, как измеряют или определяют данную величину. В определенных вариантах осуществления термин “приблизительно” обозначает в пределах 1, 2, 3 или 4 стандартных отклонений. В определенных вариантах осуществления термин “приблизительно” обозначает в пределах 50%, 20%, 15%, 10%, 9%, 8%, 7%, 6%, 5%, 4%, 3%, 2%, 1%, 0,5% или 0,05% указанной величины или диапазона.
Термины “активный ингредиент” и “активное вещество” относятся к соединению, которое вводят, отдельно или в комбинации с одним или более фармацевтически приемлемыми вспомогательными веществами субъекту для лечения, предотвращения или облегчения одного или более симптомов расстройства, заболевания или состояния. Как применяют в настоящем изобретении, “активный ингредиент” и “активное вещество” может представлять собой оптически чистый изомер соединения, описанного в настоящем изобретении.
Термины “лекарственное средство”, “терапевтический агент” и “химиотерапевтический агент” относятся к соединению или его фармацевтической композиции, которое вводят субъекту для лечения, предотвращения или облегчения одного или более симптомов расстройства, заболевания или состояния.
Термин “встречающийся в природе” или “нативный” при применении в связи с биологическими материалами, такими как молекулы нуклеиновых кислот, полипептиды, клетки-хозяина и подобными, относится к материалам, которые обнаруживают в природе и которые не подвергались модификации человеком. Аналогично, “не встречающийся в природе” или “ненативный” относится к материалу, который не обнаруживают в природе или который модифицирован структурно или получен человеком.
Термин “PI3K” относится к фосфоинозитид 3-киназе или ее варианту, которая способна фосфорилировать инозитольное кольцо PI в положении D-3. Предполагается, что термин “PI3K вариант” включает белки, по существу гомологичные нативной PI3K, т.е. белки, содержащие одну или более делеций, вставок или замещений встречающейся или не встречающейся в природе аминокислотой (например, PI3K производные, гомологи и фрагменты) относительно аминокислотной последовательности нативной PI3K. Аминокислотная последовательность PI3K варианта является по меньшей мере на приблизительно 80% идентичной, по меньшей мере на приблизительно 90% идентичной или по меньшей мере на приблизительно 95% идентичной нативной PI3K. Примеры PI3K включают, но не ограничиваются, p110α, p110β, p110δ, p110γ, PI3K-C2α, PI3K-C2β, PI3K-C2γ, Vps34, mTOR, ATM, ATR и DNA-PK. Смотрите Fry, Biochem. Biophys. Acta 1994, 1226, 237-268; Vanhaesebroeck and Waterfield, Exp. Cell. Res. 1999, 253, 239-254; и Fry, Breast Cancer Res. 2001, 3, 304-312. PI3K разделяют по меньшей мере на четыре класса. Класс I включает p110α, p110β, p110δ и p110γ. Класс II включает PI3K-C2α, PI3K-C2β и PI3K-C2γ. Класс III включает Vps34. Класс IV включает mTOR, ATM, ATR и DNA-PK. В определенных вариантах осуществления PI3K представляет собой киназу I класса. В определенных вариантах осуществления PI3K представляет собой p110α, p110β, p110δ или p110γ. В определенных вариантах осуществления PI3K представляет собой вариант киназы I класса. В определенных вариантах осуществления PI3K представляет собой p110α мутант. Примеры p110α мутантов включают, но не ограничиваются, R38H, G106V, K111N, K227E, N345K, C420R, P539R, E542K, E545A, E545G, E545K, Q546K, Q546P, E453Q, H710P, I800L, T1025S, M1043I, M1043V, H1047L, H1047R и H1047Y (Ikenoue et al., Cancer Res. 2005, 65, 4562-4567; Gymnopoulos et al., Proc. Natl. Acad. Sci., 2007, 104, 5569-5574). В определенных вариантах осуществления PI3K представляет собой киназу II класса. В определенных вариантах осуществления PI3K представляет собой PI3K-C2α, PI3K-C2β или PI3K-C2γ. В определенных вариантах осуществления PI3K представляет собой киназу III класса. В определенных вариантах осуществления PI3K представляет собой Vps34. В определенных вариантах осуществления PI3K представляет собой киназу IV класса. В определенных вариантах осуществления PI3K представляет собой mTOR, ATM, ATR или DNA-PK.
Термины “PI3K-опосредованное расстройство, заболевание или состояние” и “расстройство, заболевание или состояние, опосредованное PI3K” относятся к расстройству, заболеванию или состоянию, характеризующемуся нарушенной или разрегулируемой, например, меньшей или большей, чем нормальная, PI3K активности. Нарушенная PI3K функциональная активность может возникать как результат PI3K сверхэкспрессии в клетках, экспрессии PI3K в клетках, которые обычно не экспрессируют PI3K, или нарушенной регуляции в результате нерегулируемой активации, вызванной, например, мутацией в PI3K. PI3K-опосредованное расстройство, заболевание или состояние может быть полностью или частично опосредованно нарушенной PI3K активностью. В частности, PI3K-опосредованное расстройство, заболевание или состояние представляет собой расстройство, заболевание или состояние, при котором регулирование PI3K активности приводит в результате к некоторому влиянию на лежащее в основе расстройство, заболевание или состояние, например, PI3K ингибитор приводит в результате к некоторому улучшению по меньшей мере для некоторых из пациентов, подвергаемых лечению.
Термины “p110δ-опосредованное расстройство, заболевание или состояние”, “расстройство, заболевание или состояние, опосредованное p110δ”, “PI3Kδ-опосредованное расстройство, заболевание или состояние” и “расстройство, заболевание или состояние, опосредованное PI3Kδ” относятся к расстройству, заболеванию или состоянию, характеризующемуся нарушенной или разрегулируемой, например, меньшей или большей, чем нормальная, p110δ активностью. Нарушенная p110δ функциональная активность может возникать в результате p110δ сверхэкспрессии в клетках, экспрессии p110δ в клетках, которые обычно не экспрессируют p110δ, или нарушенной регуляции в результате нерегулируемой активации, вызванной, например, мутацией в p110δ. p110δ-опосредованное расстройство, заболевание или состояние может быть полностью или частично опосредованно нарушенной p110δ активностью. В частности, p110δ-опосредованное расстройство, заболевание или состояние представляет собой расстройство, заболевание или состояние, при котором регулирование p110δ активности приводит в результате к некоторому влиянию на лежащее в основе расстройство, заболевание или состояние, например, p110δ ингибитор приводит в результате к некоторому улучшению по меньшей мере для некоторых из пациентов, подвергаемых лечению.
Термин “алкил” относится к линейному или разветвленному насыщенному моновалентному углеводородному радикалу, где алкилен может быть необязательно замещен одним или более заместителями Q, как описано в настоящем изобретении. Термин “алкил” также включает и линейный и разветвленный алкил, если не указано иначе. В определенных вариантах осуществления алкил представляет собой линейный насыщенный моновалентный углеводородный радикал, который содержит 1-20 (C1-20), 1-15 (C1-15), 1-10 (C1-10) или 1-6 (C1-6) атомов углерода, или разветвленный насыщенный моновалентный углеводородный радикал, который содержит 3-20 (C3-20), 3-15 (C3-15), 3-10 (C3-10) или 3-6 (C3-6) атомов углерода. Как применяют в настоящем изобретении, линейные C1-6 и разветвленные C3-6 алкильные группы также называют “низшим алкилом”. Примеры алкильных групп включают, но не ограничиваются, метил, этил, пропил (включая все изомерные формы), н-пропил, изопропил, бутил (включая все изомерные формы), н-бутил, изобутил, втор-бутил, трет-бутил, пентил (включая все изомерные формы) и гексил (включая все изомерные формы). Например, C1-6 алкил относится к линейному насыщенному моновалентному углеводородному радикалу, который содержит 1-6 атомов углерода, или разветвленному насыщенному моновалентному углеводородному радикалу, который содержит 3-6 атомов углерода.
Термин “алкилен” относится к линейному или разветвленному насыщенному двухвалентному углеводородному радикалу, где алкилен может быть необязательно замещен одним или более заместителями Q, как описано в настоящем изобретении. Термин “алкилен” включает и линейный и разветвленный алкилен, если не указано иначе. В определенных вариантах осуществления алкилен представляет собой линейный насыщенный двухвалентный углеводородный радикал, который содержит 1-20 (C1-20), 1-15 (C1-15), 1-10 (C1-10) или 1-6 (C1-6) атомов углерода, или разветвленный насыщенный двухвалентный углеводородный радикал, который содержит 3-20 (C3-20), 3-15 (C3-15), 3-10 (C3-10) или 3-6 (C3-6) атомов углерода. Как применяют в настоящем изобретении, линейные C1-6 и разветвленные C3-6 алкиленовые группы также называют “низшим алкиленом”. Примеры алкиленовых групп включают, но не ограничиваются, метилен, этилен, пропилен (включая все изомерные формы), н-пропилен, изопропилен, бутилен (включая все изомерные формы), н-бутилен, изобутилен, трет-бутилен, пентилен (включая все изомерные формы) и гексилен (включая все изомерные формы). Например, C1-6 алкилен относится к линейному насыщенному двухвалентному углеводородному радикалу, который содержит 1-6 атомов углерода, или разветвленному насыщенному двухвалентному углеводородному радикалу, который содержит 3-6 атомов углерода.
Термин “гетероалкилен” относится к линейному или разветвленному насыщенному двухвалентному углеводородному радикалу, который содержит один или более гетероатомов, причем каждый независимо выбран из O, S и N в углеводородной цепи. Например, C1-6 гетероалкилен относится к линейному насыщенному двухвалентному углеводородному радикалу, который содержит 1-6 атомов углерода, или разветвленному насыщенному двухвалентному углеводородному радикалу, который содержит 3-6 атомов углерода. В определенных вариантах осуществления гетероалкилен представляет собой линейный насыщенный двухвалентный углеводородный радикал, который содержит 1-20 (C1-20), 1-15 (C1-15), 1-10 (C1-10) или 1-6 (C1-6) атомов углерода, или разветвленный насыщенный двухвалентный углеводородный радикал, который содержит 3-20 (C3-20), 3-15 (C3-15), 3-10 (C3-10) или 3-6 (C3-6) атомов углерода. Как применяют в настоящем изобретении, линейные C1-6 и разветвленные C3-6 гетероалкиленовые группы также называют “низшим гетероалкиленом”. Примеры гетероалкиленовых групп включают, но не ограничиваются, -CH2O-, -CH2OCH2-, -CH2CH2O-, -CH2NH-, -CH2NHCH2-, -CH2CH2NH-, -CH2S-, -CH2SCH2- и -CH2CH2S-. В определенных вариантах осуществления гетероалкилен может также быть необязательно замещен одним или более заместителями Q, как описано в настоящем изобретении.
Термин “алкенил” относится к линейному или разветвленному моновалентному углеводородному радикалу, который содержит один или более, в одном варианте осуществления одну, две, три, четыре или пять, в другом варианте осуществления одну углерод-углерод двойную связь (связи). Алкенил может быть необязательно замещен одним или более заместителями Q, как описано в настоящем изобретении. Термин “алкенил” также включает радикалы, имеющие “цис” и “транс” конфигурации, или альтернативно, “Z” и “E” конфигурации, как ясно специалисту в данной области техники. Как применяют в настоящем изобретении, термин “алкенил” включает и линейный и разветвленный алкенил, если не указано иначе. Например, C2-6 алкенил относится к линейному ненасыщенному моновалентному углеводородному радикалу, который содержит 2-6 атомов углерода, или разветвленному ненасыщенному моновалентному углеводородному радикалу, который содержит 3-6 атомов углерода. В определенных вариантах осуществления алкенил представляет собой линейный моновалентный углеводородный радикал, который содержит 2-20 (C2-20), 2-15 (C2-15), 2-10 (C2-10) или 2-6 (C2-6) атомов углерода, или разветвленный моновалентный углеводородный радикал, который содержит 3-20 (C3-20), 3-15 (C3-15), 3-10 (C3-10) или 3-6 (C3-6) атомов углерода. Примеры алкенильных групп включают, но не ограничиваются, этенил, пропен-1-ил, пропен-2-ил, аллил, бутенил и 4-метилбутенил.
Термин “алкенилен” относится к линейному или разветвленному двухвалентному углеводородному радикалу, который содержит одну или более, в одном варианте осуществления одну, две, три, четыре или пять, в другом варианте осуществления одну углерод-углерод двойную связь (связи). Алкенилен может быть необязательно замещен одним или более заместителями Q, как описано в настоящем изобретении. Аналогично, термин “алкенилен” также включает радикалы, имеющие “цис” и “транс” конфигурации, или альтернативно, “E” и “Z” конфигурации. Как применяют в настоящем изобретении, термин “алкенилен” включает и линейный и разветвленный алкенилен, если не указано иначе. Например, C2-6 алкенилен относится к линейному ненасыщенному двухвалентному углеводородному радикалу, который содержит 2-6 атомов углерода, или разветвленному ненасыщенному двухвалентному углеводородному радикалу, который содержит 3-6 атомов углерода. В определенных вариантах осуществления алкенилен представляет собой линейный двухвалентный углеводородный радикал, который содержит 2-20 (C2-20), 2-15 (C2-15), 2-10 (C2-10) или 2-6 (C2-6) атомов углерода, или разветвленный двухвалентный углеводородный радикал, который содержит 3-20 (C3-20), 3-15 (C3-15), 3-10 (C3-10) или 3-6 (C3-6) атомов углерода. Примеры алкениленовых групп включают, но не ограничиваются, этенилен, аллилен, пропенилен, бутенилен и 4-метилбутенилен.
Термин “гетероалкенилен” относится к линейному или разветвленному двухвалентному углеводородному радикалу, который содержит одну или более, в одном варианте осуществления одну, две, три, четыре или пять, в другом варианте осуществления одну углерод-углерод двойную связь (связи), и который содержит один или более гетероатомов, причем каждый независимо выбран из O, S и N, в углеводородной цепи. Гетероалкенилен может быть необязательно замещен одним или более заместителями Q, как описано в настоящем изобретении. Термин “гетероалкенилен” включает радикалы, имеющие “цис” или “транс” конфигурацию или их смесь, или альтернативно, “Z” или “E” конфигурацию или их смесь, как ясно специалисту в данной области техники. Например, C2-6 гетероалкенилен относится к линейному ненасыщенному двухвалентному углеводородному радикалу, который содержит 2-6 атомов углерода, или разветвленному ненасыщенному двухвалентному углеводородному радикалу, который содержит 3-6 атомов углерода. В определенных вариантах осуществления гетероалкенилен представляет собой линейный двухвалентный углеводородный радикал, который содержит 2-20 (C2-20), 2-15 (C2-15), 2-10 (C2-10) или 2-6 (C2-6) атомов углерода, или разветвленный двухвалентный углеводородный радикал, который содержит 3-20 (C3-20), 3-15 (C3-15), 3-10 (C3-10) или 3-6 (C3-6) атомов углерода. Примеры гетероалкениленовых групп включают, но не ограничиваются, -CH=CHO-, -CH=CHOCH2-, -CH=CHCH2O-, -CH=CHS-, -CH=CHSCH2-, -CH=CHCH2S- или -CH=CHCH2NH-.
Термин “алкинил” относится к линейному или разветвленному моновалентному углеводородному радикалу, который содержит одну или более, в одном варианте осуществления одну, две, три, четыре или пять, в другом варианте осуществления одну углерод-углерод тройную связь (связи). Алкинил может быть необязательно замещен одним или более заместителями Q, как описано в настоящем изобретении. Термин “алкинил” также включает и линейный и разветвленный алкинил, если не указано иначе. В определенных вариантах осуществления алкинил представляет собой линейный моновалентный углеводородный радикал, который содержит 2-20 (C2-20), 2-15 (C2-15), 2-10 (C2-10) или 2-6 (C2-6) атомов углерода, или разветвленный моновалентный углеводородный радикал, который содержит 3-20 (C3-20), 3-15 (C3-15), 3-10 (C3-10) или 3-6 (C3-6) атомов углерода. Примеры алкинильных групп включают, но не ограничиваются, этинил (-C≡CH) и пропаргил (-CH2C≡CH). Например, C2-6 алкинил относится к линейному ненасыщенному моновалентному углеводородному радикалу, который содержит 2-6 атомов углерода, или разветвленному ненасыщенному моновалентному углеводородному радикалу, который содержит 3-6 атомов углерода.
Термин “циклоалкил” относится к циклическому насыщенному мостиковому и/или немостиковому моновалентному углеводородному радикалу, который может быть необязательно замещен одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления циклоалкил содержит от 3 до 20 (C3-20), от 3 до 15 (C3-15), от 3 до 10 (C3-10) или от 3 до 7 (C3-7) атомов углерода. Примеры циклоалкильных групп включают, но не ограничиваются, циклопропил, циклобутил, циклопентил, циклогексил, циклогептил, бицикло[2,1,1]гексил, бицикло[2,2,1]гептил, декалинил и адамантил.
Термин “циклоалкенил” относится к циклическому ненасыщенному, неароматическому мостиковому и/или немостиковому моновалентному углеводородному радикалу, который может быть необязательно замещен одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления циклоалкенил содержит от 3 до 20 (C3-20), от 3 до 15 (C3-15), от 3 до 10 (C3-10) или от 3 до 7 (C3-7) атомов углерода. Примеры циклоалкильных групп включают, но не ограничиваются, циклобутенил, циклопентенил, циклогексенил или циклогептенил.
Термин “арил” относится к моноциклической ароматической группе и/или мультициклической моновалентной ароматической группе, которая содержит по меньшей мере одно ароматическое углеводородное кольцо. В определенных вариантах осуществления арил содержит от 6 до 20 (C6-20), от 6 до 15 (C6-15) или от 6 до 10 (C6-10) кольцевых атомов. Примеры арильных групп включают, но не ограничиваются, фенил, нафтил, флуоренил, азуленил, антрил, фенантрил, пиренил, бифенил и терфенил. Арил также относится к бициклическим или трициклическим углеродным кольцам, где одно из колец является ароматическим и другие могут быть насыщенными, частично ненасыщенными или ароматическими, например, дигидронафтил, инденил, инданил или тетрагидронафтил (тетралинил). В определенных вариантах осуществления арил может быть необязательно замещен одним или более заместителями Q, как описано в настоящем изобретении.
Термин “аралкил” или “арилалкил” относится к моновалентной алкильной группе, замещенной одной или более арильными группами. В определенных вариантах осуществления аралкил содержит от 7 до 30 (C7-30), от 7 до 20 (C7-20) или от 7 до 16 (C7-16) атомов углерода. Примеры аралкильных групп включают, но не ограничиваются, бензил, 2-фенилэтил и 3-фенилпропил. В определенных вариантах осуществления аралкил необязательно замещен одним или более заместителями Q, как описано в настоящем изобретении.
Термин “гетероарил” относится к моновалентной моноциклической ароматической группе или моновалентной полициклической ароматической группе, которая содержит по меньшей мере одно ароматическое кольцо, где по меньшей мере одно ароматическое кольцо содержит один или более гетероатомов, независимо выбранных из O, S, N и P, в кольце. Гетероарильная группа соединена с остатком молекулы через ее ароматическое кольцо. Каждое кольцо гетероарильной группы может содержать один или два атома O, один или два атома S, 1-4 атома N и/или один или два атома P, при условии, что суммарное количество гетероатомов в каждом кольце равно четырем или меньше, и каждое кольцо содержит по меньшей мере один атом углерода. В определенных вариантах осуществления гетероарил содержит от 5 до 20, от 5 до 15 или от 5 до 10 кольцевых атомов. Примеры моноциклических гетероарильных групп включают, но не ограничиваются, фуранил, имидазолил, изотиазолил, изоксазолил, оксадиазолил, оксадиазолил, оксазолил, пиразинил, пиразолил, пиридазинил, пиридил, пиримидинил, пирролил, тиадиазолил, тиазолил, тиенил, тетразолил, триазинил и триазолил. Примеры бициклических гетероарильных групп включают, но не ограничиваются, бензофуранил, бензимидазолил, бензоизоксазолил, бензопиранил, бензотиадиазолил, бензотиазолил, бензотиенил, бензотриазолил, бензоксазолил, фуропиридил, имидазопиридинил, имидазотиазолил, индолизинил, индолил, индазолил, изобензофуранил, изобензотиенил, изоиндолил, изохинолинил, изотиазолил, нафтиридинил, оксазолопиридинил, фталазинил, птеридинил, пуринил, пиридопиридил, пирролопиридил, хинолинил, хиноксалинил, хиназолинил, тиадиазолопиримидил и тиенопиридил. Примеры трициклических гетероарильных групп включают, но не ограничиваются, акридинил, бензиндолил, карбазолил, дибензофуранил, перимидинил, фенантролинил, фенантридинил, фенарсазинил, феназинил, фенотиазинил, феноксазинил и ксантенил. В определенных вариантах осуществления гетероарил может также быть необязательно замещен одним или более заместителями Q, как описано в настоящем изобретении.
Термин “гетероциклил” или “гетероциклический” относится к моновалентной моноциклической неароматической кольцевой системе или моновалентной полициклической кольцевой системе, которая содержит по меньшей мере одно неароматическое кольцо, где один или более из неароматических кольцевых атомов представляют собой гетероатомы, независимо выбранные из O, S, N и P; и оставшиеся кольцевые атомы представляют собой атомы углерода. В определенных вариантах осуществления гетероциклил или гетероциклическая группа содержит от 3 до 20, от 3 до 15, от 3 до 10, от 3 до 8, от 4 до 7 или от 5 до 6 кольцевых атомов. Гетероциклильная группа соединена с остатком молекулы через ее неароматическое кольцо. В определенных вариантах осуществления гетероциклил представляет собой моноциклическую, бициклическую, трициклическую или тетрациклическую кольцевую систему, которая может быть спиро, конденсированной или мостиковой и в которой атомы азота или серы могут быть необязательно окисленными, атомы азота могут быть необязательно кватернизироваными и некоторые кольца могут быть частично или полностью насыщенными или ароматическими. Гетероциклил может быть соединен с основной структурой по любому гетероатому или атому углерода, который приводит в результате к образованию стабильного соединения. Примеры данных гетероциклических групп включают, но не ограничиваются, азепинил, бензодиоксанил, бензодиоксолил, бензофуранонил, бензопиранонил, бензопиранил, бензотетрагидрофуранил, бензотетрагидротиенил, бензотиопиранил, бензоксазинил, β-карболинил, хроманил, хромонил, циннолинил, кумаринил, декагидроизохинолинил, дигидробензизотиазинил, дигидробензизоксазинил, дигидрофурил, дигидроизоиндолил, дигидропиранил, дигидропиразолил, дигидропиразинил, дигидропиридинил, дигидропиримидинил, дигидропирролил, диоксоланил, 1,4-дитианил, фуранонил, имидазолидинил, имидазолинил, индолинил, изобензотетрагидрофуранил, изобензотетрагидротиенил, изохроманил, изокумаринил, изоиндолинил, изотиазолидинил, изоксазолидинил, морфолинил, октагидроиндолил, октагидроизоиндолил, оксазолидинонил, оксазолидинил, оксиранил, пиперазинил, пиперидинил, 4-пиперидонил, пиразолидинил, пиразолинил, пирролидинил, пирролинил, хинуклидинил, тетрагидрофурил, тетрагидроизохинолинил, тетрагидропиранил, тетрагидротиенил, тиаморфолинил, тиазолидинил, тетрагидрохинолинил и 1,3,5-тритианил. В определенных вариантах осуществления гетероциклил может также быть необязательно замещен одним или более заместителями Q, как описано в настоящем изобретении.
Термин “галоген” или “галогенид” относится к фтору, хлору, брому и/или йоду.
Предполагается, что термин “необязательно замещенный” обозначает то, что группа или заместитель, такой как алкильная, алкиленовая, гетероалкиленовая, алкенильная, алкениленовая, гетероалкениленовая, алкинильная, циклоалкильная, циклоалкенильная, арильная, аралкильная, гетероарильная, гетероарил-C1-6 алкильная и гетероциклильная группа, могут быть замещены одним или более заместителями Q, каждый из которых независимо выбран из, например, (a) оксо (=O), галогена, циано (-CN) и нитро (-NO2); (b) C1-6 алкила, C2-6 алкенила, C2-6 алкинила, C3-10 циклоалкила, C6-14 арила, C7-15 аралкила, гетероарила и гетероциклила, каждый из которых дополнительно необязательно замещен одним или более, в одном варианте осуществления одним, двумя, тремя, четырьмя или пятью, заместителями Qa; и (c) -C(O)Ra, -C(O)ORa, -C(O)NRbRc, -C(NRa)NRbRc, -ORa, -OC(O)Ra, -OC(O)ORa, -OC(O)NRbRc, -OC(=NRa)NRbRc, -OS(O)Ra, -OS(O)2Ra, -OS(O)NRbRc, -OS(O)2NRbRc, -NRbRc, -NRaC(O)Rd, -NRaC(O)ORd, -NRaC(O)NRbRc, -NRaC(=NRd)NRbRc, -NRaS(O)Rd, -NRaS(O)2Rd, -NRaS(O)NRbRc, -NRaS(O)2NRbRc, -P(O)RaRd, -P(O)(ORa)Rd, -P(O)(ORa)(ORd), -SRa, -S(O)Ra, -S(O)2Ra, -S(O)NRbRc и -S(O)2NRbRc, где каждый Ra, Rb, Rc и Rd независимо представляет собой (i) водород; (ii) C1-6 алкил, C2-6 алкенил, C2-6 алкинил, C3-10 циклоалкил, C6-14 арил, C7-15 аралкил, гетероарил или гетероциклил, каждый из которых необязательно замещен одним или более, в одном варианте осуществления одним, двумя, тремя или четырьмя, заместителями Qa; или (iii) Rb и Rc вместе с атомом N, с которым они соединены, образуют гетероарил или гетероциклил, необязательно замещенный одним или более, в одном варианте осуществления одним, двумя, тремя или четырьмя, заместителями Qa. Как применяют в настоящем изобретении, все группы, которые можно заместить, являются “необязательно замещенными”, если не указано иначе.
В одном варианте осуществления каждый заместитель Qa независимо выбран из группы, состоящей из (a) оксо, циано, галогена и нитро; и (b) C1-6 алкила, C2-6 алкенила, C2-6 алкинила, C3-10 циклоалкила, C6-14 арила, C7-15 аралкила, гетероарила и гетероциклила; и (c) -C(O)Re, -C(O)ORe, -C(O)NRfRg, -C(NRe)NRfRg, -ORe, -OC(O)Re, -OC(O)ORe, -OC(O)NRfRg, -OC(=NRe)NRfRg, -OS(O)Re, -OS(O)2Re, -OS(O)NRfRg, -OS(O)2NRfRg, -NRfRg, -NReC(O)Rh, -NReC(O)ORh, -NReC(O)NRfRg, -NReC(=NRh)NRfRg, -NReS(O)Rh, -NReS(O)2Rh, -NReS(O)NRfRg, -NReS(O)2NRfRg, -P(O)ReRh, -P(O)(ORe)Rh, -P(O)(ORe)(ORh), -SRe, -S(O)Re, -S(O)2Re, -S(O)NRfRg и -S(O)2NRfRg; где каждый Re, Rf, Rg и Rh независимо представляет собой (i) водород, C1-6 алкил, C2-6 алкенил, C2-6 алкинил, C3-10 циклоалкил, C6-14 арил, C7-15 аралкил, гетероарил или гетероциклил; или (ii) Rf и Rg вместе с атомом N, с которым они соединены, образуют гетероарил или гетероциклил.
В определенных вариантах осуществления “оптически активный” и “энантиомерно активный” относятся к группе молекул, которые имеют энантиомерный избыток не менее, чем приблизительно 50%, не менее, чем приблизительно 70%, не менее, чем приблизительно 80%, не менее, чем приблизительно 90%, не менее, чем приблизительно 91%, не менее, чем приблизительно 92%, не менее, чем приблизительно 93%, не менее, чем приблизительно 94%, не менее, чем приблизительно 95%, не менее, чем приблизительно 96%, не менее, чем приблизительно 97%, не менее, чем приблизительно 98%, не менее, чем приблизительно 99%, не менее, чем приблизительно 99,5%, или не менее, чем приблизительно 99,8%. В определенных вариантах осуществления соединение содержит приблизительно 95% или более требуемого энантиомера и приблизительно 5% или менее менее предпочтительного энантиомера относительно суммарного веса указанного рацемата.
При описании оптически активного соединения приставки R и S применяют для обозначения абсолютной конфигурации молекулы при ее хиральном центре (центрах). (+) и (-) применяют для обозначения оптического вращения соединения, то есть направления, в котором плоскость поляризованного света вращается оптически активным соединением. Приставка (-) показывает, что соединение является левовращающим, то есть соединение вращает плоскость поляризованного света влево или против часовой стрелки. Приставка (+) показывает, что соединение является правовращающим, то есть соединение вращает плоскость поляризованного света вправо или по часовой стрелке. Однако знак оптического вращения, (+) и (-), не связан с абсолютной конфигурацией молекулы, R и S.
Термин “изотопный вариант” относится к соединению, которое содержит неприродную долю изотопа при одном или более атомов, которые образуют данное соединение. В определенных вариантах осуществления “изотопный вариант” соединения содержит неприродные доли одного или более изотопов, включая, но не ограничиваясь, водород (1H), дейтерий (2H), тритий (3H), углерод-11 (11C), углерод-12 (12C), углерод-13 (13C), углерод-14 (14C), азот-13 (13N), азот-14 (14N), азот-15 (15N), кислород-14 (14O), кислород-15 (15O), кислород-16 (16O), кислород-17 (17O), кислород-18 (18O), фтор-17 (17F), фтор-18 (18F), фосфор-31 (31P), фосфор-32 (32P), фосфор-33 (33P), серу-32 (32S), серу-33 (33S), серу-34 (34S), серу-35 (35S), серу-36 (36S), хлор-35 (35Cl), хлор-36 (36Cl), хлор-37 (37Cl), бром-79 (79Br), бром-81 (81Br), йод-123 (123I), йод-125 (125I), йод-127 (127I), йод-129 (129I) и йод-131 (131I). В определенных вариантах осуществления “изотопный вариант” соединения находится в стабильной форме, то есть является нерадиоактивным. В определенных вариантах осуществления “изотопный вариант” соединения содержит неприродные доли одного или более изотопов, включая, но не ограничиваясь, водород (1H), дейтерий (2H), углерод-12 (12C), углерод-13 (13C), азот-14 (14N), азот-15 (15N), кислород-16 (16O), кислород-17 (17O), кислород-18 (18O), фтор-17 (17F), фосфор-31 (31P), серу-32 (32S), серу-33 (33S), серу-34 (34S), серу-36 (36S), хлор-35 (35Cl), хлор-37 (37Cl), бром-79 (79Br), бром-81 (81Br) и йод-127 (127I). В определенных вариантах осуществления “изотопный вариант” соединения находится в нестабильной форме, то есть является радиоактивным. В определенных вариантах осуществления “изотопный вариант” соединения содержит неприродные доли одного или более изотопов, включая, но не ограничиваясь, тритий (3H), углерод-11 (11C), углерод-14 (14C), азот-13 (13N), кислород-14 (14O), кислород-15 (15O), фтор-18 (18F), фосфор-32 (32P), фосфор-33 (33P), серу-35 (35S), хлор-36 (36Cl), йод-123 (123I), йод-125 (125I), йод-129 (129I) и йод-131 (131I). Ясно, что в соединении, как приведено в настоящем изобретении, любой водород может представлять собой, например, 2H, или любой углерод может представлять собой, например, 13C, или любой азот может представлять собой, например, 15N, или любой кислород может представлять собой, например, 18O, при наличии возможности согласно решению специалиста. В определенных вариантах осуществления “изотопный вариант” соединения содержит неприродные доли дейтерия (D).
Термин “сольват” относится к комплексу или агрегату, образованному одной или более молекулами растворенного компонента, например, соединения, относящегося к настоящему изобретению, и одной или более молекулами растворителя, которые присутствуют в стехиометрическом или нестехиометрическом количестве. Подходящие растворители включают, но не ограничиваются, воду, метанол, этанол, н-пропанол, изопропанол и уксусную кислоту. В определенных вариантах осуществления растворитель является фармацевтически приемлемым. В одном варианте осуществления комплекс или агрегат находится в кристаллической форме. В другом варианте осуществления комплекс или агрегат находится в некристаллической форме. Когда растворителем является вода, сольват представляет собой гидрат. Примеры гидратов включают, но не ограничиваются, гемигидрат, моногидрат, дигидрат, тригидрат, тетрагидрат и пентагидрат.
Фраза “энантиомер, смесь энантиомеров, смесь двух или более диастереомеров или изотопный вариант; или их фармацевтически приемлемая соль, сольват, гидрат или пролекарство” имеет то же значение, что и фраза “энантиомер, смесь энантиомеров, смесь двух или более диастереомеров или изотопный вариант соединения, приводимого в настоящем изобретении; или фармацевтически приемлемая соль, сольват, гидрат или пролекарство соединения, приводимого в настоящем изобретении; или фармацевтически приемлемая соль, сольват, гидрат или пролекарство энантиомера, смесь энантиомеров, смесь двух или более диастереомеров или изотопный вариант соединения, приводимого в настоящем изобретении”.
Соединения
В одном варианте осуществления настоящее изобретение относится к соединению формулы I:

или его энантиомеру, смеси энантиомеров, смеси двух или более диастереомеров или изотопному варианту; или их фармацевтически приемлемой соли, сольвату, гидрату или пролекарству; где:
каждый X, Y и Z независимо представляет собой N или CRX, при условии, что по меньшей мере два из X, Y и Z представляют собой атомы азота; где RX представляет собой водород или C1-6 алкил;
каждый R1 и R2 независимо представляет собой (a) водород, циано, галоген или нитро; (b) C1-6 алкил, C2-6 алкенил, C2-6 алкинил, C3-10 циклоалкил, C6-14 арил, C7-15 аралкил, гетероарил или гетероциклил; или (c) -C(O)R1a, -C(O)OR1a, -C(O)NR1bR1c, -C(NR1a)NR1bR1c, -OR1a, -OC(O)R1a, -OC(O)OR1a, -OC(O)NR1bR1c, -OC(=NR1a)NR1bR1c, -OS(O)R1a, -OS(O)2R1a, -OS(O)NR1bR1c, -OS(O)2NR1bR1c, -NR1bR1c, -NR1aC(O)R1d, -NR1aC(O)OR1d, -NR1aC(O)NR1bR1c, -NR1aC(=NR1d)NR1bR1c, -NR1aS(O)R1d, -NR1aS(O)2R1d, -NR1aS(O)NR1bR1c, -NR1aS(O)2NR1bR1c, -SR1a, -S(O)R1a, -S(O)2R1a, -S(O)NR1bR1c или -S(O)2NR1bR1c; где каждый R1a, R1b, R1c и R1d независимо представляет собой (i) водород; (ii) C1-6 алкил, C2-6 алкенил, C2-6 алкинил, C3-10 циклоалкил, C6-14 арил, C7-15 аралкил, гетероарил или гетероциклил; или (iii) R1b и R1c вместе с атомом N, с которым они соединены, образуют гетероциклил;
каждый R3 и R4 независимо представляет собой водород или C1-6 алкил; или R3 и R4 соединены вместе, образуя связь, C1-6 алкилен, C1-6 гетероалкилен, C2-6 алкенилен или C2-6 гетероалкенилен;
R5a представляет собой (a) водород или галоген; (b) C1-6 алкил, C2-6 алкенил, C2-6 алкинил, C3-10 циклоалкил, C6-14 арил, C7-15 аралкил, гетероарил или гетероциклил; или (c) -C(O)R1a, -C(O)OR1a, -C(O)NR1bR1c, -C(NR1a)NR1bR1c, -OR1a, -OC(O)R1a, -OC(O)OR1a, -C(O)NR1bR1c, -OC(=NR1a)NR1bR1c, -OS(O)R1a, -OS(O)2R1a, -OS(O)NR1bR1c, -OS(O)2NR1bR1c, -NR1bR1c, -NR1aC(O)R1d, -NR1aC(O)OR1d, -NR1aC(O)NR1bR1c, -NR1aC(=NR1d)NR1bR1c, -NR1aS(O)R1d, -NR1aS(O)2R1d, -NR1aS(O)NR1bR1c, -NR1aS(O)2NR1bR1c, -SR1a, -S(O)R1a, -S(O)2R1a, -S(O)NR1bR1c или -S(O)2NR1bR1c;
R5b представляет собой (a) галоген; (b) C1-6 алкил, C2-6 алкенил, C2-6 алкинил, C3-10 циклоалкил, C6-14 арил, C7-15 аралкил, гетероарил или гетероциклил; или (c) -C(O)R1a, -C(O)OR1a, -C(O)NR1bR1c, -C(NR1a)NR1bR1c, -OR1a, -OC(O)R1a, -OC(O)OR1a, -OC(O)NR1bR1c, -OC(=NR1a)NR1bR1c, -OS(O)R1a, -OS(O)2R1a, -OS(O)NR1bR1c, -OS(O)2NR1bR1c, -NR1bR1c, -NR1aC(O)R1d, -NR1aC(O)OR1d, -NR1aC(O)NR1bR1c, -NR1aC(=NR1d)NR1bR1c, -NR1aS(O)R1d, -NR1aS(O)2R1d, -NR1aS(O)NR1bR1c, -NR1aS(O)2NR1bR1c, -SR1a, -S(O)R1a, -S(O)2R1a, -S(O)NR1bR1c или -S(O)2NR1bR1c;
R5c представляет собой -(CR5fR5g)n-(C6-14 арил) или -(CR5fR5g)n-гетероарил;
каждый R5d и R5e независимо представляет собой (a) водород или галоген; (b) C1-6 алкил, C2-6 алкенил, C2-6 алкинил, C3-10 циклоалкил, C6-14 арил, C7-15 аралкил, гетероарил или гетероциклил; или (c) -C(O)R1a, -C(O)OR1a, -C(O)NR1bR1c, -C(NR1a)NR1bR1c, -OR1a, -OC(O)R1a, -OC(O)OR1a, -OC(O)NR1bR1c, -OC(=NR1a)NR1bR1c, -OS(O)R1a, -OS(O)2R1a, -OS(O)NR1bR1c, -OS(O)2NR1bR1c, -NR1bR1c, -NR1aC(O)R1d, -NR1aC(O)OR1d, -NR1aC(O)NR1bR1c, -NR1aC(=NR1d)NR1bR1c, -NR1aS(O)R1d, -NR1aS(O)2R1d, -NR1aS(O)NR1bR1c, -NR1aS(O)2NR1bR1c, -SR1a, -S(O)R1a, -S(O)2R1a, -S(O)NR1bR1c или -S(O)2NR1bR1c;
каждый R5f и R5g независимо представляет собой (a) водород или галоген; (b) C1-6 алкил, C2-6 алкенил, C2-6 алкинил, C3-10 циклоалкил, C6-14 арил, C7-15 аралкил, гетероарил или гетероциклил; или (c) -C(O)R1a, -C(O)OR1a, -C(O)NR1bR1c, -C(NR1a)NR1bR1c, -OR1a, -OC(O)R1a, -OC(O)OR1a, -OC(O)NR1bR1c, -OC(=NR1a)NR1bR1c, -OS(O)R1a, -OS(O)2R1a, -OS(O)NR1bR1c, -OS(O)2NR1bR1c, -NR1bR1c, -NR1aC(O)R1d, -NR1aC(O)OR1d, -NR1aC(O)NR1bR1c, -NR1aC(=NR1d)NR1bR1c, -NR1aS(O)R1d, -NR1aS(O)2R1d, -NR1aS(O)NR1bR1c, -NR1aS(O)2NR1bR1c, -SR1a, -S(O)R1a, -S(O)2R1a, -S(O)NR1bR1c или -S(O)2NR1bR1c; или (d) когда один экземпляр R5f и один экземпляр R5g соединены с одним и тем же атомом углерода, R5f и R5g вместе с атомом углерода, с которым они соединены, образуют C3-10 циклоалкил или гетероциклил;
R6 представляет собой водород, C1-6 алкил, -S-C1-6 алкил, -S(O)-C1-6 алкил или -SO2-C1-6 алкил;
m равно 0 или 1; и
n равно 0, 1, 2, 3 или 4;
где каждый алкил, алкилен, гетероалкилен, алкенил, алкенилен, гетероалкенилен, алкинил, циклоалкил, арил, аралкил, гетероарил и гетероциклил в R1, R2, R3, R4, R6, RX, R1a, R1b, R1c, R1d, R5a, R5b, R5c, R5d, R5e, R5f и R5g необязательно замещен одним или более, в одном варианте осуществления одним, двумя, тремя или четырьмя, заместителями Q, где каждый заместитель Q независимо выбран из (a) оксо, циано, галогена и нитро; (b) C1-6 алкила, C2-6 алкенила, C2-6 алкинила, C3-10 циклоалкила, C6-14 арила, C7-15 аралкила, гетероарила и гетероциклила, каждый из которых дополнительно необязательно замещен одним или более, в одном варианте осуществления одним, двумя, тремя или четырьмя, заместителями Qa; и (c) -C(O)Ra, -C(O)ORa, -C(O)NRbRc, -C(NRa)NRbRc, -ORa, -OC(O)Ra, -OC(O)ORa, -OC(O)NRbRc, -OC(=NRa)NRbRc, -OS(O)Ra, -OS(O)2Ra, -OS(O)NRbRc, -OS(O)2NRbRc, -NRbRc, -NRaC(O)Rd, -NRaC(O)ORd, -NRaC(O)NRbRc, -NRaC(=NRd)NRbRc, -NRaS(O)Rd, -NRaS(O)2Rd, -NRaS(O)NRbRc, -NRaS(O)2NRbRc, -SRa, -S(O)Ra, -S(O)2Ra, -S(O)NRbRc и -S(O)2NRbRc, где каждый Ra, Rb, Rc, и Rd независимо представляет собой (i) водород; (ii) C1-6 алкил, C2-6 алкенил, C2-6 алкинил, C3-10 циклоалкил, C6-14 арил, C7-15 аралкил, гетероарил или гетероциклил, каждый из которых дополнительно необязательно замещен одним или более, в одном варианте осуществления одним, двумя, тремя или четырьмя, заместителями Qa; или (iii) Rb и Rc вместе с атомом N, с которым они соединены, образуют гетероциклил, который дополнительно необязательно замещен одним или более, в одном варианте осуществления одним, двумя, тремя или четырьмя, заместителями Qa;
где каждый Qa независимо выбран из группы, состоящей из (a) оксо, циано, галогена и нитро; (b) C1-6 алкила, C2-6 алкенила, C2-6 алкинила, C3-10 циклоалкила, C6-14 арила, C7-15 аралкила, гетероарила и гетероциклила; и (c) -C(O)Re, -C(O)ORe, -C(O)NRfRg, -C(NRe)NRfRg, -ORe, -OC(O)Re, -OC(O)ORe, -OC(O)NRfRg, -OC(=NRe)NRfRg, -OS(O)Re, -OS(O)2Re, -OS(O)NRfRg, -OS(O)2NRfRg, -NRfRg, -NReC(O)Rh, -NReC(O)ORh, -NReC(O)NRfRg, -NReC(=NRh)NRfRg, -NReS(O)Rh, -NReS(O)2Rh, -NReS(O)NRfRg, -NReS(O)2NRfRg, -SRe, -S(O)Re, -S(O)2Re, -S(O)NRfRg и -S(O)2NRfRg; где каждый Re, Rf, Rg и Rh независимо представляет собой (i) водород; (ii) C1-6 алкил, C2-6 алкенил, C2-6 алкинил, C3-10 циклоалкил, C6-14 арил, C7-15 аралкил, гетероарил или гетероциклил; или (iii) Rf и Rg вместе с атомом N, с которым они соединены, образуют гетероциклил.
В одном варианте осуществления в формуле I
каждый X, Y и Z независимо представляет собой N или CRX, при условии, что по меньшей мере два из X, Y и Z представляют собой атомы азота; где RX представляет собой водород или C1-6 алкил;
каждый R1 и R2 независимо представляет собой (a) водород, циано, галоген или нитро; (b) C1-6 алкил, C2-6 алкенил, C2-6 алкинил, C3-10 циклоалкил, C6-14 арил, C7-15 аралкил, гетероарил или гетероциклил; или (c) -C(O)R1a, -C(O)OR1a, -C(O)NR1bR1c, -C(NR1a)NR1bR1c, -OR1a, -OC(O)R1a, -OC(O)OR1a, -OC(O)NR1bR1c, -OC(=NR1a)NR1bR1c, -OS(O)R1a, -OS(O)2R1a, -OS(O)NR1bR1c, -OS(O)2NR1bR1c, -NR1bR1c, -NR1aC(O)R1d, -NR1aC(O)OR1d, -NR1aC(O)NR1bR1c, -NR1aC(=NR1d)NR1bR1c, -NR1aS(O)R1d, -NR1aS(O)2R1d, -NR1aS(O)NR1bR1c, -NR1aS(O)2NR1bR1c, -SR1a, -S(O)R1a, -S(O)2R1a, -S(O)NR1bR1c или -S(O)2NR1bR1c; где каждый R1a, R1b, R1c и R1d независимо представляет собой (i) водород; (ii) C1-6 алкил, C2-6 алкенил, C2-6 алкинил, C3-10 циклоалкил, C6-14 арил, C7-15 аралкил, гетероарил или гетероциклил; или (iii) R1b и R1c вместе с атомом N, с которым они соединены, образуют гетероциклил;
каждый R3 и R4 независимо представляет собой водород или C1-6 алкил; или R3 и R4 соединены вместе, образуя связь, C1-6 алкилен, C1-6 гетероалкилен, C2-6 алкенилен или C2-6 гетероалкенилен;
R5a представляет собой (a) водород или галоген; (b) C1-6 алкил, C2-6 алкенил, C2-6 алкинил, C3-10 циклоалкил, C6-14 арил, C7-15 аралкил, гетероарил или гетероциклил; или (c) -C(O)R1a, -C(O)OR1a, -C(O)NR1bR1c, -C(NR1a)NR1bR1c, -OR1a, -OC(O)R1a, -OC(O)OR1a, -OC(O)NR1bR1c, -OC(=NR1a)NR1bR1c, -OS(O)R1a, -OS(O)2R1a, -OS(O)NR1bR1c, -OS(O)2NR1bR1c, -NR1bR1c, -NR1aC(O)R1d, -NR1aC(O)OR1d, -NR1aC(O)NR1bR1c, -NR1aC(=NR1d)NR1bR1c, -NR1aS(O)R1d, -NR1aS(O)2R1d, -NR1aS(O)NR1bR1c, -NR1aS(O)2NR1bR1c, -SR1a, -S(O)R1a, -S(O)2R1a, -S(O)NR1bR1c или -S(O)2NR1bR1c;
R5b представляет собой (a) галоген; (b) C1-6 алкил, C2-6 алкенил, C2-6 алкинил, C3-10 циклоалкил, C6-14 арил, C7-15 аралкил, гетероарил или гетероциклил; или (c) -C(O)R1a, -C(O)OR1a, -C(O)NR1bR1c, -C(NR1a)NR1bR1c, -OR1a, -OC(O)R1a, -OC(O)OR1a, -OC(O)NR1bR1c, -OC(=NR1a)NR1bR1c, -OS(O)R1a, -OS(O)2R1a, -OS(O)NR1bR1c, -OS(O)2NR1bR1c, -NR1bR1c, -NR1aC(O)R1d, -NR1aC(O)OR1d, -NR1aC(O)NR1bR1c, -NR1aC(=NR1d)NR1bR1c, -NR1aS(O)R1d, -NR1aS(O)2R1d, -NR1aS(O)NR1bR1c, -NR1aS(O)2NR1bR1c, -SR1a, -S(O)R1a, -S(O)2R1a, -S(O)NR1bR1c или -S(O)2NR1bR1c;
R5c представляет собой -(CR5fR5g)n-(C6-14 арил) или -(CR5fR5g)n-гетероарил;
каждый R5d и R5e независимо представляет собой (a) водород или галоген; (b) C1-6 алкил, C2-6 алкенил, C2-6 алкинил, C3-10 циклоалкил, C6-14 арил, C7-15 аралкил, гетероарил или гетероциклил; или (c) -C(O)R1a, -C(O)OR1a, -C(O)NR1bR1c, -C(NR1a)NR1bR1c, -OR1a, -OC(O)R1a, -OC(O)OR1a, -OC(O)NR1bR1c, -OC(=NR1a)NR1bR1c, -OS(O)R1a, -OS(O)2R1a, -OS(O)NR1bR1c, -OS(O)2NR1bR1c, -NR1bR1c, -NR1aC(O)R1d, -NR1aC(O)OR1d, -NR1aC(O)NR1bR1c, -NR1aC(=NR1d)NR1bR1c, -NR1aS(O)R1d, -NR1aS(O)2R1d, -NR1aS(O)NR1bR1c, -NR1aS(O)2NR1bR1c, -SR1a, -S(O)R1a, -S(O)2R1a, -S(O)NR1bR1c или -S(O)2NR1bR1c;
каждый R5f и R5g независимо представляет собой (a) водород или галоген; (b) C1-6 алкил, C2-6 алкенил, C2-6 алкинил, C3-10 циклоалкил, C6-14 арил, C7-15 аралкил, гетероарил или гетероциклил; или (c) -C(O)R1a, -C(O)OR1a, -C(O)NR1bR1c, -C(NR1a)NR1bR1c, -OR1a, -OC(O)R1a, -OC(O)OR1a, -OC(O)NR1bR1c, -OC(=NR1a)NR1bR1c, -OS(O)R1a, -OS(O)2R1a, -OS(O)NR1bR1c, -OS(O)2NR1bR1c, -NR1bR1c, -NR1aC(O)R1d, -NR1aC(O)OR1d, -NR1aC(O)NR1bR1c, -NR1aC(=NR1d)NR1bR1c, -NR1aS(O)R1d, -NR1aS(O)2R1d, -NR1aS(O)NR1bR1c, -NR1aS(O)2NR1bR1c, -SR1a, -S(O)R1a, -S(O)2R1a, -S(O)NR1bR1c или -S(O)2NR1bR1c; или (d) когда один экземпляр R5f и один экземпляр R5g соединены с одним и тем же атомом углерода, R5f и R5g вместе с атомом углерода, с которым они соединены, образуют C3-10 циклоалкил или гетероциклил;
R6 представляет собой водород, C1-6 алкил, -S-C1-6 алкил, -S(O)-C1-6 алкил или -SO2-C1-6 алкил;
m равно 0 или 1; и
n равно 0, 1, 2, 3 или 4;
при условии, что соединение не является ни 4-(2-(дифторметил)-1H-бензо[d]имидазол-1-ил)-6-морфолино-N-(2-фенил-2-(пирролидин-1-ил)этил)-1,3,5-триазин-2-амином, ни 6-(2-(дифторметил)-1H-бензо[d]имидазол-1-ил)-N-(1-(4-((R)-3-(метоксиметил)морфолино)фенил)этил)-2-морфолинопиримидин-4-амином;
где каждый алкил, алкилен, гетероалкилен, алкенил, алкенилен, гетероалкенилен, алкинил, циклоалкил, арил, аралкил, гетероарил и гетероциклил необязательно замещен одним или более, в одном варианте осуществления одним, двумя, тремя или четырьмя, заместителями Q, как определено в настоящем изобретении.
В другом варианте осуществления, в формуле I
каждый X, Y и Z независимо представляет собой N или CRX, при условии, что по меньшей мере два из X, Y и Z представляют собой атомы азота; где RX представляет собой водород или C1-6 алкил;
каждый R1 и R2 независимо представляет собой (a) водород, циано, галоген или нитро; (b) C1-6 алкил, C2-6 алкенил, C2-6 алкинил, C3-10 циклоалкил, C6-14 арил, C7-15 аралкил, гетероарил или гетероциклил; или (c) -C(O)R1a, -C(O)OR1a, -C(O)NR1bR1c, -C(NR1a)NR1bR1c, -OR1a, -OC(O)R1a, -OC(O)OR1a, -OC(O)NR1bR1c, -OC(=NR1a)NR1bR1c, -OS(O)R1a, -OS(O)2R1a, -OS(O)NR1bR1c, -OS(O)2NR1bR1c, -NR1bR1c, -NR1aC(O)R1d, -NR1aC(O)OR1d, -NR1aC(O)NR1bR1c, -NR1aC(=NR1d)NR1bR1c, -NR1aS(O)R1d, -NR1aS(O)2R1d, -NR1aS(O)NR1bR1c, -NR1aS(O)2NR1bR1c, -SR1a, -S(O)R1a, -S(O)2R1a, -S(O)NR1bR1c или -S(O)2NR1bR1c; где каждый R1a, R1b, R1c и R1d независимо представляет собой (i) водород; (ii) C1-6 алкил, C2-6 алкенил, C2-6 алкинил, C3-10 циклоалкил, C6-14 арил, C7-15 аралкил, гетероарил или гетероциклил; или (iii) R1b и R1c вместе с атомом N, с которым они соединены, образуют гетероциклил;
каждый R3 и R4 независимо представляет собой водород или C1-6 алкил; или R3 и R4 соединены вместе, образуя связь, C1-6 алкилен, C1-6 гетероалкилен, C2-6 алкенилен или C2-6 гетероалкенилен;
R5a представляет собой (a) водород или галоген; (b) C1-6 алкил, C2-6 алкенил, C2-6 алкинил, C3-10 циклоалкил, C6-14 арил, C7-15 аралкил, гетероарил или гетероциклил; или (c) -C(O)R1a, -C(O)OR1a, -C(O)NR1bR1c, -C(NR1a)NR1bR1c, -OR1a, -OC(O)R1a, -OC(O)OR1a, -OC(O)NR1bR1c, -OC(=NR1a)NR1bR1c, -OS(O)R1a, -OS(O)2R1a, -OS(O)NR1bR1c, -OS(O)2NR1bR1c, -NR1bR1c, -NR1aC(O)R1d, -NR1aC(O)OR1d, -NR1aC(O)NR1bR1c, -NR1aC(=NR1d)NR1bR1c, -NR1aS(O)R1d, -NR1aS(O)2R1d, -NR1aS(O)NR1bR1c, -NR1aS(O)2NR1bR1c, -SR1a, -S(O)R1a, -S(O)2R1a, -S(O)NR1bR1c или -S(O)2NR1bR1c;
R5b представляет собой (a) галоген; (b) C1-6 алкил, C2-6 алкенил, C2-6 алкинил, C3-10 циклоалкил, C6-14 арил, C7-15 аралкил, гетероарил или гетероциклил; или (c) -C(O)R1a, -C(O)OR1a, -C(O)NR1bR1c, -C(NR1a)NR1bR1c, -OR1a, -OC(O)R1a, -OC(O)OR1a, -OC(O)NR1bR1c, -OC(=NR1a)NR1bR1c, -OS(O)R1a, -OS(O)2R1a, -OS(O)NR1bR1c, -OS(O)2NR1bR1c, -NR1bR1c, -NR1aC(O)R1d, -NR1aC(O)OR1d, -NR1aC(O)NR1bR1c, -NR1aC(=NR1d)NR1bR1c, -NR1aS(O)R1d, -NR1aS(O)2R1d, -NR1aS(O)NR1bR1c, -NR1aS(O)2NR1bR1c, -SR1a, -S(O)R1a, -S(O)2R1a, -S(O)NR1bR1c или -S(O)2NR1bR1c;
R5c представляет собой -(CR5fR5g)n-(C6-14 арил) или -(CR5fR5g)n-гетероарил;
каждый R5d и R5e независимо представляет собой (a) водород или галоген; (b) C1-6 алкил, C2-6 алкенил, C2-6 алкинил, C3-10 циклоалкил, C6-14 арил, C7-15 аралкил, гетероарил или гетероциклил; или (c) -C(O)R1a, -C(O)OR1a, -C(O)NR1bR1c, -C(NR1a)NR1bR1c, -OR1a, -OC(O)R1a, -OC(O)OR1a, -OC(O)NR1bR1c, -OC(=NR1a)NR1bR1c, -OS(O)R1a, -OS(O)2R1a, -OS(O)NR1bR1c, -OS(O)2NR1bR1c, -NR1bR1c, -NR1aC(O)R1d, -NR1aC(O)OR1d, -NR1aC(O)NR1bR1c, -NR1aC(=NR1d)NR1bR1c, -NR1aS(O)R1d, -NR1aS(O)2R1d, -NR1aS(O)NR1bR1c, -NR1aS(O)2NR1bR1c, -SR1a, -S(O)R1a, -S(O)2R1a, -S(O)NR1bR1c или -S(O)2NR1bR1c;
каждый R5f и R5g независимо представляет собой (a) водород или галоген; (b) C1-6 алкил, C2-6 алкенил, C2-6 алкинил, C3-10 циклоалкил, C6-14 арил, C7-15 аралкил, гетероарил или гетероциклил; или (c) -C(O)R1a, -C(O)OR1a, -C(O)NR1bR1c, -C(NR1a)NR1bR1c, -OR1a, -OC(O)R1a, -OC(O)OR1a, -OC(O)NR1bR1c, -OC(=NR1a)NR1bR1c, -OS(O)R1a, -OS(O)2R1a, -OS(O)NR1bR1c, -OS(O)2NR1bR1c, -NR1bR1c, -NR1aC(O)R1d, -NR1aC(O)OR1d, -NR1aC(O)NR1bR1c, -NR1aC(=NR1d)NR1bR1c, -NR1aS(O)R1d, -NR1aS(O)2R1d, -NR1aS(O)NR1bR1c, -NR1aS(O)2NR1bR1c, -SR1a, -S(O)R1a, -S(O)2R1a, -S(O)NR1bR1c или -S(O)2NR1bR1c; или (d) когда один экземпляр R5f и один экземпляр R5g соединены с одним и тем же атомом углерода, R5f и R5g вместе с атомом углерода, с которым они соединены, образуют C3-10 циклоалкил или гетероциклил;
R6 представляет собой водород, C1-6 алкил, -S-C1-6 алкил, -S(O)-C1-6 алкил или -SO2-C1-6 алкил;
m равно 0 или 1; и
n равно 0, 1, 2, 3 или 4;
при условии, что когда X, Y и Z представляют собой N, и R5a представляет собой водород, R5b не является пирролидинилом; и когда X и Z представляют собой N, Y представляет собой CH, и R5a представляет собой водород, R5b не является 4-((R)-3-(метоксиметил)морфолино)фенилом;
где каждый алкил, алкилен, гетероалкилен, алкенил, алкенилен, гетероалкенилен, алкинил, циклоалкил, арил, аралкил, гетероарил и гетероциклил необязательно замещен одним или более, в одном варианте осуществления одним, двумя, тремя или четырьмя, заместителями Q, как определено в настоящем изобретении.
В еще одном варианте осуществления в формуле I
каждый X, Y и Z независимо представляет собой N или CRX, при условии, что по меньшей мере два из X, Y и Z представляют собой атомы азота; где RX представляет собой водород или C1-6 алкил;
каждый R1 и R2 независимо представляет собой (a) водород, циано, галоген или нитро; (b) C1-6 алкил, C2-6 алкенил, C2-6 алкинил, C3-10 циклоалкил, C6-14 арил, C7-15 аралкил, гетероарил или гетероциклил; или (c) -C(O)R1a, -C(O)OR1a, -C(O)NR1bR1c, -C(NR1a)NR1bR1c, -OR1a, -OC(O)R1a, -OC(O)OR1a, -OC(O)NR1bR1c, -OC(=NR1a)NR1bR1c, -OS(O)R1a, -OS(O)2R1a, -OS(O)NR1bR1c, -OS(O)2NR1bR1c, -NR1bR1c, -NR1aC(O)R1d, -NR1aC(O)OR1d, -NR1aC(O)NR1bR1c, -NR1aC(=NR1d)NR1bR1c, -NR1aS(O)R1d, -NR1aS(O)2R1d, -NR1aS(O)NR1bR1c, -NR1aS(O)2NR1bR1c, -SR1a, -S(O)R1a, -S(O)2R1a, -S(O)NR1bR1c или -S(O)2NR1bR1c; где каждый R1a, R1b, R1c и R1d независимо представляет собой (i) водород; (ii) C1-6 алкил, C2-6 алкенил, C2-6 алкинил, C3-10 циклоалкил, C6-14 арил, C7-15 аралкил, гетероарил или гетероциклил; или (iii) R1b и R1c вместе с атомом N, с которым они соединены, образуют гетероциклил;
каждый R3 и R4 независимо представляет собой водород или C1-6 алкил; или R3 и R4 соединены вместе, образуя связь, C1-6 алкилен, C1-6 гетероалкилен, C2-6 алкенилен или C2-6 гетероалкенилен;
R5a представляет собой (a) галоген; (b) C1-6 алкил, C2-6 алкенил, C2-6 алкинил, C3-10 циклоалкил, C6-14 арил, C7-15 аралкил, гетероарил или гетероциклил; или (c) -C(O)R1a, -C(O)OR1a, -C(O)NR1bR1c, -C(NR1a)NR1bR1c, -OR1a, -OC(O)R1a, -OC(O)OR1a, -OC(O)NR1bR1c, -OC(=NR1a)NR1bR1c, -OS(O)R1a, -OS(O)2R1a, -OS(O)NR1bR1c, -OS(O)2NR1bR1c, -NR1bR1c, -NR1aC(O)R1d, -NR1aC(O)OR1d, -NR1aC(O)NR1bR1c, -NR1aC(=NR1d)NR1bR1c, -NR1aS(O)R1d, -NR1aS(O)2R1d, -NR1aS(O)NR1bR1c, -NR1aS(O)2NR1bR1c, -SR1a, -S(O)R1a, -S(O)2R1a, -S(O)NR1bR1c или -S(O)2NR1bR1c;
R5b представляет собой (a) галоген; (b) C1-6 алкил, C2-6 алкенил, C2-6 алкинил, C3-10 циклоалкил, C6-14 арил, C7-15 аралкил, гетероарил, или гетероциклил; или (c) -C(O)R1a, -C(O)OR1a, -C(O)NR1bR1c, -C(NR1a)NR1bR1c, -OR1a, -OC(O)R1a, -OC(O)OR1a, -OC(O)NR1bR1c, -OC(=NR1a)NR1bR1c, -OS(O)R1a, -OS(O)2R1a, -OS(O)NR1bR1c, -OS(O)2NR1bR1c, -NR1bR1c, -NR1aC(O)R1d, -NR1aC(O)OR1d, -NR1aC(O)NR1bR1c, -NR1aC(=NR1d)NR1bR1c, -NR1aS(O)R1d, -NR1aS(O)2R1d, -NR1aS(O)NR1bR1c, -NR1aS(O)2NR1bR1c, -SR1a, -S(O)R1a, -S(O)2R1a, -S(O)NR1bR1c или -S(O)2NR1bR1c;
R5c представляет собой -(CR5fR5g)n-(C6-14 арил) или -(CR5fR5g)n-гетероарил;
каждый R5d и R5e независимо представляет собой (a) водород или галоген; (b) C1-6 алкил, C2-6 алкенил, C2-6 алкинил, C3-10 циклоалкил, C6-14 арил, C7-15 аралкил, гетероарил или гетероциклил; или (c) -C(O)R1a, -C(O)OR1a, -C(O)NR1bR1c, -C(NR1a)NR1bR1c, -OR1a, -OC(O)R1a, -OC(O)OR1a, -OC(O)NR1bR1c, -OC(=NR1a)NR1bR1c, -OS(O)R1a, -OS(O)2R1a, -OS(O)NR1bR1c, -OS(O)2NR1bR1c, -NR1bR1c, -NR1aC(O)R1d, -NR1aC(O)OR1d, -NR1aC(O)NR1bR1c, -NR1aC(=NR1d)NR1bR1c, -NR1aS(O)R1d, -NR1aS(O)2R1d, -NR1aS(O)NR1bR1c, -NR1aS(O)2NR1bR1c, -SR1a, -S(O)R1a, -S(O)2R1a, -S(O)NR1bR1c или -S(O)2NR1bR1c;
каждый R5f и R5g независимо представляет собой (a) водород или галоген; (b) C1-6 алкил, C2-6 алкенил, C2-6 алкинил, C3-10 циклоалкил, C6-14 арил, C7-15 аралкил, гетероарил или гетероциклил; или (c) -C(O)R1a, -C(O)OR1a, -C(O)NR1bR1c, -C(NR1a)NR1bR1c, -OR1a, -OC(O)R1a, -OC(O)OR1a, -OC(O)NR1bR1c, -OC(=NR1a)NR1bR1c, -OS(O)R1a, -OS(O)2R1a, -OS(O)NR1bR1c, -OS(O)2NR1bR1c, -NR1bR1c, -NR1aC(O)R1d, -NR1aC(O)OR1d, -NR1aC(O)NR1bR1c, -NR1aC(=NR1d)NR1bR1c, -NR1aS(O)R1d, -NR1aS(O)2R1d, -NR1aS(O)NR1bR1c, -NR1aS(O)2NR1bR1c, -SR1a, -S(O)R1a, -S(O)2R1a, -S(O)NR1bR1c или -S(O)2NR1bR1c; или (d) когда один экземпляр R5f и один экземпляр R5g соединены с одним и тем же атомом углерода, R5f и R5g вместе с атомом углерода, с которым они соединены, образуют C3-10 циклоалкил или гетероциклил;
R6 представляет собой водород, C1-6 алкил, -S-C1-6 алкил, -S(O)-C1-6 алкил или -SO2-C1-6 алкил;
m равно 0 или 1; и
n равно 0, 1, 2, 3 или 4;
где каждый алкил, алкилен, гетероалкилен, алкенил, алкенилен, гетероалкенилен, алкинил, циклоалкил, арил, аралкил, гетероарил и гетероциклил необязательно замещен одним или более, в одном варианте осуществления одним, двумя, тремя или четырьмя, заместителями Q, как определено в настоящем изобретении.
В еще одном варианте осуществления в формуле I
X, Y и Z представляют собой N;
каждый R1 и R2 независимо представляет собой (a) водород, циано, галоген или нитро; (b) C1-6 алкил, C2-6 алкенил, C2-6 алкинил, C3-10 циклоалкил, C6-14 арил, C7-15 аралкил, гетероарил или гетероциклил; или (c) -C(O)R1a, -C(O)OR1a, -C(O)NR1bR1c, -C(NR1a)NR1bR1c, -OR1a, -OC(O)R1a, -OC(O)OR1a, -OC(O)NR1bR1c, -OC(=NR1a)NR1bR1c, -OS(O)R1a, -OS(O)2R1a, -OS(O)NR1bR1c, -OS(O)2NR1bR1c, -NR1bR1c, -NR1aC(O)R1d, -NR1aC(O)OR1d, -NR1aC(O)NR1bR1c, -NR1aC(=NR1d)NR1bR1c, -NR1aS(O)R1d, -NR1aS(O)2R1d, -NR1aS(O)NR1bR1c, -NR1aS(O)2NR1bR1c, -SR1a, -S(O)R1a, -S(O)2R1a, -S(O)NR1bR1c или -S(O)2NR1bR1c; где каждый R1a, R1b, R1c и R1d независимо представляет собой (i) водород; (ii) C1-6 алкил, C2-6 алкенил, C2-6 алкинил, C3-10 циклоалкил, C6-14 арил, C7-15 аралкил, гетероарил или гетероциклил; или (iii) R1b и R1c вместе с атомом N, с которым они соединены, образуют гетероциклил;
каждый R3 и R4 независимо представляет собой водород или C1-6 алкил; или R3 и R4 соединены вместе, образуя связь, C1-6 алкилен, C1-6 гетероалкилен, C2-6 алкенилен или C2-6 гетероалкенилен;
R5a представляет собой (a) водород или галоген; (b) C1-6 алкил, C2-6 алкенил, C2-6 алкинил, C3-10 циклоалкил, C6-14 арил, C7-15 аралкил, гетероарил или гетероциклил; или (c) -C(O)R1a, -C(O)OR1a, -C(O)NR1bR1c, -C(NR1a)NR1bR1c, -OR1a, -OC(O)R1a, -OC(O)OR1a, -OC(O)NR1bR1c, -OC(=NR1a)NR1bR1c, -OS(O)R1a, -OS(O)2R1a, -OS(O)NR1bR1c, -OS(O)2NR1bR1c, -NR1bR1c, -NR1aC(O)R1d, -NR1aC(O)OR1d, -NR1aC(O)NR1bR1c, -NR1aC(=NR1d)NR1bR1c, -NR1aS(O)R1d, -NR1aS(O)2R1d, -NR1aS(O)NR1bR1c, -NR1aS(O)2NR1bR1c, -SR1a, -S(O)R1a, -S(O)2R1a, -S(O)NR1bR1c или -S(O)2NR1bR1c;
R5b представляет собой (a) галоген; (b) C1-6 алкил, C2-6 алкенил, C2-6 алкинил, C3-10 циклоалкил, C6-14 арил, C7-15 аралкил или гетероарил; или (c) -C(O)R1a, -C(O)OR1a, -C(O)NR1bR1c, -C(NR1a)NR1bR1c, -OR1a, -OC(O)R1a, -OC(O)OR1a, -OC(O)NR1bR1c, -OC(=NR1a)NR1bR1c, -OS(O)R1a, -OS(O)2R1a, -OS(O)NR1bR1c, -OS(O)2NR1bR1c, -NR1bR1c, -NR1aC(O)R1d, -NR1aC(O)OR1d, -NR1aC(O)NR1bR1c, -NR1aC(=NR1d)NR1bR1c, -NR1aS(O)R1d, -NR1aS(O)2R1d, -NR1aS(O)NR1bR1c, -NR1aS(O)2NR1bR1c, -SR1a, -S(O)R1a, -S(O)2R1a, -S(O)NR1bR1c или -S(O)2NR1bR1c;
R5c представляет собой -(CR5fR5g)n-(C6-14 арил) или -(CR5fR5g)n-гетероарил;
каждый R5d и R5e независимо представляет собой (a) водород или галоген; (b) C1-6 алкил, C2-6 алкенил, C2-6 алкинил, C3-10 циклоалкил, C6-14 арил, C7-15 аралкил, гетероарил или гетероциклил; или (c) -C(O)R1a, -C(O)OR1a, -C(O)NR1bR1c, -C(NR1a)NR1bR1c, -OR1a, -OC(O)R1a, -OC(O)OR1a, -OC(O)NR1bR1c, -OC(=NR1a)NR1bR1c, -OS(O)R1a, -OS(O)2R1a, -OS(O)NR1bR1c, -OS(O)2NR1bR1c, -NR1bR1c, -NR1aC(O)R1d, -NR1aC(O)OR1d, -NR1aC(O)NR1bR1c, -NR1aC(=NR1d)NR1bR1c, -NR1aS(O)R1d, -NR1aS(O)2R1d, -NR1aS(O)NR1bR1c, -NR1aS(O)2NR1bR1c, -SR1a, -S(O)R1a, -S(O)2R1a, -S(O)NR1bR1c или -S(O)2NR1bR1c;
каждый R5f и R5g независимо представляет собой (a) водород или галоген; (b) C1-6 алкил, C2-6 алкенил, C2-6 алкинил, C3-10 циклоалкил, C6-14 арил, C7-15 аралкил, гетероарил или гетероциклил; или (c) -C(O)R1a, -C(O)OR1a, -C(O)NR1bR1c, -C(NR1a)NR1bR1c, -OR1a, -OC(O)R1a, -OC(O)OR1a, -OC(O)NR1bR1c, -OC(=NR1a)NR1bR1c, -OS(O)R1a, -OS(O)2R1a, -OS(O)NR1bR1c, -OS(O)2NR1bR1c, -NR1bR1c, -NR1aC(O)R1d, -NR1aC(O)OR1d, -NR1aC(O)NR1bR1c, -NR1aC(=NR1d)NR1bR1c, -NR1aS(O)R1d, -NR1aS(O)2R1d, -NR1aS(O)NR1bR1c, -NR1aS(O)2NR1bR1c, -SR1a, -S(O)R1a, -S(O)2R1a, -S(O)NR1bR1c или -S(O)2NR1bR1c; или (d) когда один экземпляр R5f и один экземпляр R5g соединены с одним и тем же атомом углерода, R5f и R5g вместе с атомом углерода, с которым они соединены, образуют C3-10 циклоалкил или гетероциклил;
R6 представляет собой водород, C1-6 алкил, -S-C1-6 алкил, -S(O)-C1-6 алкил или -SO2-C1-6 алкил;
m равно 0 или 1; и
n равно 0, 1, 2, 3, или 4;
где каждый алкил, алкилен, гетероалкилен, алкенил, алкенилен, гетероалкенилен, алкинил, циклоалкил, арил, аралкил, гетероарил и гетероциклил необязательно замещен одним или более, в одном варианте осуществления одним, двумя, тремя или четырьмя, заместителями Q, как определено в настоящем изобретении.
В одном варианте осуществления соединение формулы I имеет структуру формулы Ia:
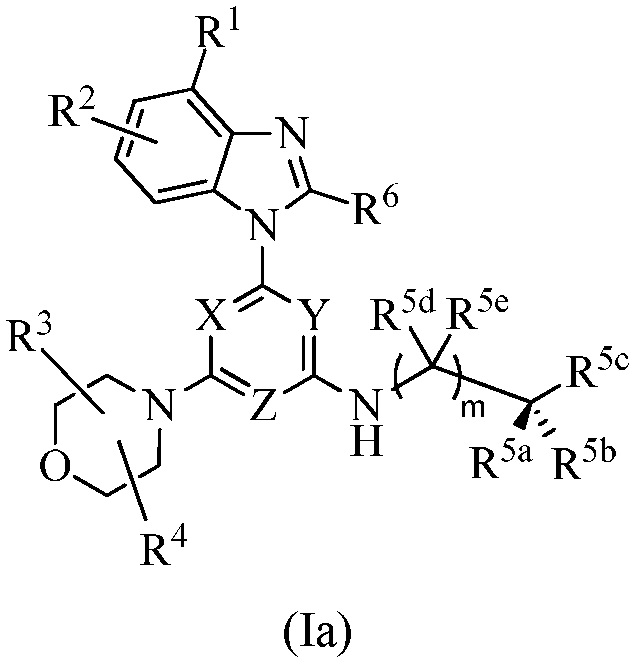
или его изотопный вариант; или их фармацевтически приемлемую соль, сольват, гидрат или пролекарство; где каждый R1, R2, R3, R4, R6, R5a, R5b, R5c, R5d, R5e, m, X, Y и Z представляет собой, как определено в настоящем изобретении. В одном варианте осуществления m равно 0. В другом варианте осуществления m равно 1.
В другом варианте осуществления соединение формулы I имеет структуру формулы Ib:
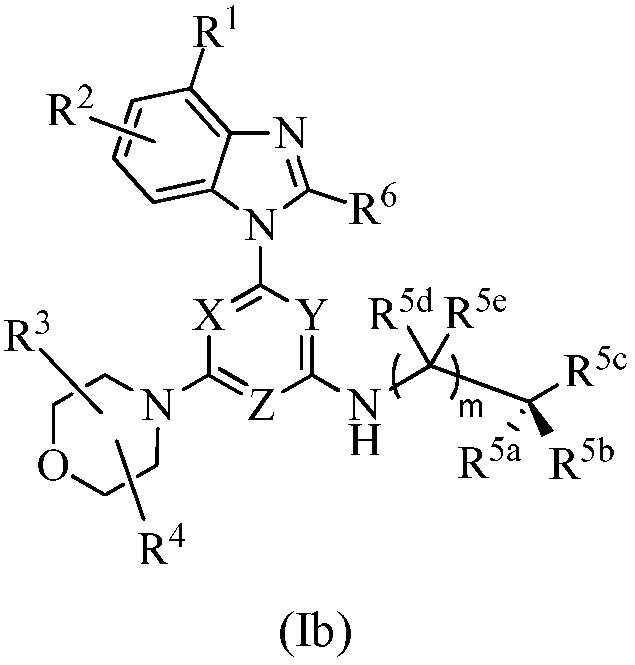
или его изотопный вариант; или их фармацевтически приемлемую соль, сольват, гидрат или пролекарство; где каждый R1, R2, R3, R4, R6, R5a, R5b, R5c, R5d, R5e, m, X, Y и Z представляет собой, как определено в настоящем изобретении. В одном варианте осуществления m равно 0. В другом варианте осуществления m равно 1.
В одном варианте осуществления настоящее изобретение относится к соединению формулы I, Ia или Ib, как описано в настоящем изобретении, или его энантиомеру, смеси энантиомеров, смеси двух или более диастереомеров или изотопному варианту; или их фармацевтически приемлемой соли, сольвату, гидрату или пролекарству; где m равно 0; каждый R5a и R5b независимо представляет собой (a) галоген; (b) C1-6 алкил, C2-6 алкенил, C2-6 алкинил, C3-10 циклоалкил, C6-14 арил, C7-15 аралкил, гетероарил, или гетероциклил; или (c) -C(O)R1a, -C(O)OR1a, -C(O)NR1bR1c, -C(NR1a)NR1bR1c, -OR1a, -OC(O)R1a, -OC(O)OR1a, -OC(O)NR1bR1c, -OC(=NR1a)NR1bR1c, -OS(O)R1a, -OS(O)2R1a, -OS(O)NR1bR1c, -OS(O)2NR1bR1c, -NR1bR1c, -NR1aC(O)R1d, -NR1aC(O)OR1d, -NR1aC(O)NR1bR1c, -NR1aC(=NR1d)NR1bR1c, -NR1aS(O)R1d, -NR1aS(O)2R1d, -NR1aS(O)NR1bR1c, -NR1aS(O)2NR1bR1c, -SR1a, -S(O)R1a, -S(O)2R1a, -S(O)NR1bR1c или -S(O)2NR1bR1c; и R1, R2, R3, R4, R5c, R6, X, Y, Z, R1a, R1b, R1c, и R1d определяют в настоящем изобретении выше.
В еще одном варианте осуществления настоящее изобретение относится к соединению формулы II:
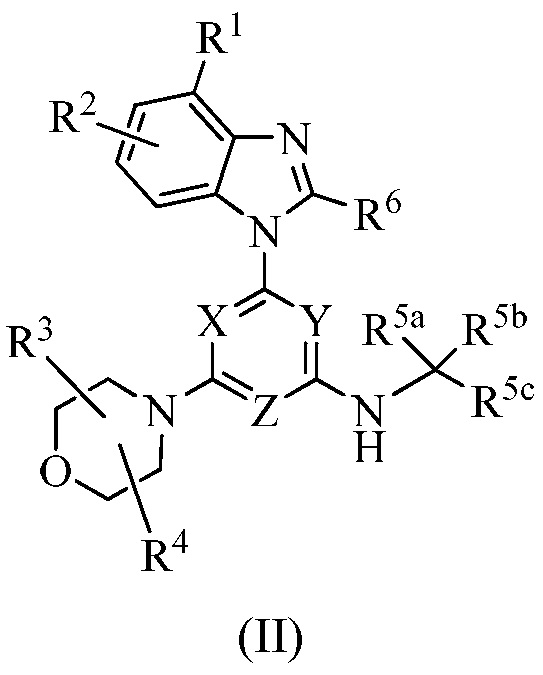
или его энантиомеру, смеси энантиомеров, смеси двух или более диастереомеров или изотопному варианту; или их фармацевтически приемлемой соли, сольвату, гидрату или пролекарству, где:
каждый X, Y и Z независимо представляет собой N или CRX, при условии, что по меньшей мере два из X, Y и Z представляют собой атомы азота; где RX представляет собой водород или C1-6 алкил;
каждый R1 и R2 независимо представляет собой (a) водород, циано, галоген или нитро; (b) C1-6 алкил, C2-6 алкенил, C2-6 алкинил, C3-10 циклоалкил, C6-14 арил, C7-15 аралкил, гетероарил или гетероциклил; или (c) -C(O)R1a, -C(O)OR1a, -C(O)NR1bR1c, -C(NR1a)NR1bR1c, -OR1a, -OC(O)R1a, -OC(O)OR1a, -OC(O)NR1bR1c, -OC(=NR1a)NR1bR1c, -OS(O)R1a, -OS(O)2R1a, -OS(O)NR1bR1c, -OS(O)2NR1bR1c, -NR1bR1c, -NR1aC(O)R1d, -NR1aC(O)OR1d, -NR1aC(O)NR1bR1c, -NR1aC(=NR1d)NR1bR1c, -NR1aS(O)R1d, -NR1aS(O)2R1d, -NR1aS(O)NR1bR1c, -NR1aS(O)2NR1bR1c, -SR1a, -S(O)R1a, -S(O)2R1a, -S(O)NR1bR1c или -S(O)2NR1bR1c; где каждый R1a, R1b, R1c и R1d независимо представляет собой (i) водород; (ii) C1-6 алкил, C2-6 алкенил, C2-6 алкинил, C3-10 циклоалкил, C6-14 арил, C7-15 аралкил, гетероарил или гетероциклил; или (iii) R1b и R1c вместе с атомом N, с которым они соединены, образуют гетероциклил;
каждый R3 и R4 независимо представляет собой водород или C1-6 алкил; или R3 и R4 соединены вместе, образуя связь, C1-6 алкилен, C1-6 гетероалкилен, C2-6 алкенилен или C2-6 гетероалкенилен;
R5a представляет собой (a) водород или галоген; (b) C1-6 алкил, C2-6 алкенил, C2-6 алкинил, C3-10 циклоалкил, C6-14 арил, C7-15 аралкил, гетероарил или гетероциклил; или (c) -C(O)R1a, -C(O)OR1a, -C(O)NR1bR1c, -C(NR1a)NR1bR1c, -OR1a, -OC(O)R1a, -OC(O)OR1a, -OC(O)NR1bR1c, -OC(=NR1a)NR1bR1c, -OS(O)R1a, -OS(O)2R1a, -OS(O)NR1bR1c, -OS(O)2NR1bR1c, -NR1bR1c, -NR1aC(O)R1d, -NR1aC(O)OR1d, -NR1aC(O)NR1bR1c, -NR1aC(=NR1d)NR1bR1c, -NR1aS(O)R1d, -NR1aS(O)2R1d, -NR1aS(O)NR1bR1c, -NR1aS(O)2NR1bR1c, -SR1a, -S(O)R1a, -S(O)2R1a, -S(O)NR1bR1c или -S(O)2NR1bR1c;
R5b представляет собой (a) галоген; (b) C1-6 алкил, C2-6 алкенил, C2-6 алкинил, C3-10 циклоалкил, C6-14 арил, C7-15 аралкил, гетероарил или гетероциклил; или (c) -C(O)R1a, -C(O)OR1a, -C(O)NR1bR1c, -C(NR1a)NR1bR1c, -OR1a, -OC(O)R1a, -OC(O)OR1a, -OC(O)NR1bR1c, -OC(=NR1a)NR1bR1c, -OS(O)R1a, -OS(O)2R1a, -OS(O)NR1bR1c, -OS(O)2NR1bR1c, -NR1bR1c, -NR1aC(O)R1d, -NR1aC(O)OR1d, -NR1aC(O)NR1bR1c, -NR1aC(=NR1d)NR1bR1c, -NR1aS(O)R1d, -NR1aS(O)2R1d, -NR1aS(O)NR1bR1c, -NR1aS(O)2NR1bR1c, -SR1a, -S(O)R1a, -S(O)2R1a, -S(O)NR1bR1c или -S(O)2NR1bR1c;
R5c представляет собой -(CR5fR5g)n-(C6-14 арил) или -(CR5fR5g)n-гетероарил;
каждый R5f и R5g независимо представляет собой (a) водород или галоген; (b) C1-6 алкил, C2-6 алкенил, C2-6 алкинил, C3-10 циклоалкил, C6-14 арил, C7-15 аралкил, гетероарил или гетероциклил; или (c) -C(O)R1a, -C(O)OR1a, -C(O)NR1bR1c, -C(NR1a)NR1bR1c, -OR1a, -OC(O)R1a, -OC(O)OR1a, -OC(O)NR1bR1c, -OC(=NR1a)NR1bR1c, -OS(O)R1a, -OS(O)2R1a, -OS(O)NR1bR1c, -OS(O)2NR1bR1c, -NR1bR1c, -NR1aC(O)R1d, -NR1aC(O)OR1d, -NR1aC(O)NR1bR1c, -NR1aC(=NR1d)NR1bR1c, -NR1aS(O)R1d, -NR1aS(O)2R1d, -NR1aS(O)NR1bR1c, -NR1aS(O)2NR1bR1c, -SR1a, -S(O)R1a, -S(O)2R1a, -S(O)NR1bR1c или -S(O)2NR1bR1c; или (d) когда один экземпляр R5f и один экземпляр R5g соединены с одним и тем же атомом углерода, R5f и R5g вместе с атомом углерода, с которым они соединены, образуют C3-10 циклоалкил или гетероциклил;
R6 представляет собой водород, C1-6 алкил, -S-C1-6 алкил, -S(O)-C1-6 алкил или -SO2-C1-6 алкил; и
n равно 0, 1, 2, 3 или 4;
где каждый алкил, алкилен, гетероалкилен, алкенил, алкенилен, гетероалкенилен, алкинил, циклоалкил, арил, аралкил, гетероарил и гетероциклил в R1, R2, R3, R4, R6, RX, R1a, R1b, R1c, R1d, R5a, R5b, R5c, R5f и R5g необязательно замещен одним или более, в одном варианте осуществления одним, двумя, тремя или четырьмя, заместителями Q, где каждый заместитель Q независимо выбран из (a) оксо, циано, галогена и нитро; (b) C1-6 алкила, C2-6 алкенила, C2-6 алкинила, C3-10 циклоалкила, C6-14 арила, C7-15 аралкила, гетероарила и гетероциклила, каждый из которых дополнительно необязательно замещен одним или более, в одном варианте осуществления одним, двумя, тремя или четырьмя, заместителями Qa; и (c) -C(O)Ra, -C(O)ORa, -C(O)NRbRc, -C(NRa)NRbRc, -ORa, -OC(O)Ra, -OC(O)ORa, -OC(O)NRbRc, -OC(=NRa)NRbRc, -OS(O)Ra, -OS(O)2Ra, -OS(O)NRbRc, -OS(O)2NRbRc, -NRbRc, -NRaC(O)Rd, -NRaC(O)ORd, -NRaC(O)NRbRc, -NRaC(=NRd)NRbRc, -NRaS(O)Rd, -NRaS(O)2Rd, -NRaS(O)NRbRc, -NRaS(O)2NRbRc, -SRa, -S(O)Ra, -S(O)2Ra, -S(O)NRbRc и -S(O)2NRbRc, где каждый Ra, Rb, Rc, и Rd независимо представляет собой (i) водород; (ii) C1-6 алкил, C2-6 алкенил, C2-6 алкинил, C3-10 циклоалкил, C6-14 арил, C7-15 аралкил, гетероарил или гетероциклил, каждый из которых дополнительно необязательно замещен одним или более, в одном варианте осуществления одним, двумя, тремя или четырьмя, заместителями Qa; или (iii) Rb и Rc вместе с атомом N, с которым они соединены, образуют гетероциклил, который дополнительно необязательно замещен одним или более, в одном варианте осуществления одним, двумя, тремя или четырьмя, заместителями Qa;
где каждый Qa независимо выбран из группы, состоящей из (a) оксо, циано, галогена и нитро; (b) C1-6 алкила, C2-6 алкенила, C2-6 алкинила, C3-10 циклоалкила, C6-14 арила, C7-15 аралкила, гетероарила и гетероциклила; и (c) -C(O)Re, -C(O)ORe, -C(O)NRfRg, -C(NRe)NRfRg, -ORe, -OC(O)Re, -OC(O)ORe, -OC(O)NRfRg, -OC(=NRe)NRfRg, -OS(O)Re, -OS(O)2Re, -OS(O)NRfRg, -OS(O)2NRfRg, -NRfRg, -NReC(O)Rh, -NReC(O)ORh, -NReC(O)NRfRg, -NReC(=NRh)NRfRg, -NReS(O)Rh, -NReS(O)2Rh, -NReS(O)NRfRg, -NReS(O)2NRfRg, -SRe, -S(O)Re, -S(O)2Re, -S(O)NRfRg и -S(O)2NRfRg; где каждый Re, Rf, Rg, и Rh независимо представляет собой (i) водород; (ii) C1-6 алкил, C2-6 алкенил, C2-6 алкинил, C3-10 циклоалкил, C6-14 арил, C7-15 аралкил, гетероарил или гетероциклил; или (iii) Rf и Rg вместе с атомом N, с которым они соединены, образуют гетероциклил.
В еще одном варианте осуществления настоящее изобретение относится к соединению формулы II:
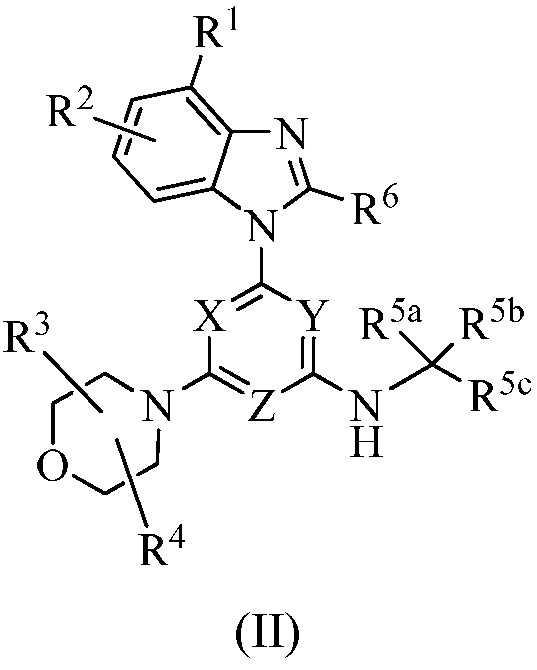
или его энантиомеру, смеси энантиомеров, смеси двух или более диастереомеров или изотопному варианту; или их фармацевтически приемлемой соли, сольвату, гидрату или пролекарству; где:
каждый X, Y и Z независимо представляет собой N или CRX, при условии, что по меньшей мере два из X, Y и Z представляют собой атомы азота; где RX представляет собой водород или C1-6 алкил;
каждый R1 и R2 независимо представляет собой (a) водород, циано, галоген или нитро; (b) C1-6 алкил, C2-6 алкенил, C2-6 алкинил, C3-10 циклоалкил, C6-14 арил, C7-15 аралкил, гетероарил или гетероциклил; или (c) -C(O)R1a, -C(O)OR1a, -C(O)NR1bR1c, -C(NR1a)NR1bR1c, -OR1a, -OC(O)R1a, -OC(O)OR1a, -OC(O)NR1bR1c, -OC(=NR1a)NR1bR1c, -OS(O)R1a, -OS(O)2R1a, -OS(O)NR1bR1c, -OS(O)2NR1bR1c, -NR1bR1c, -NR1aC(O)R1d, -NR1aC(O)OR1d, -NR1aC(O)NR1bR1c, -NR1aC(=NR1d)NR1bR1c, -NR1aS(O)R1d, -NR1aS(O)2R1d, -NR1aS(O)NR1bR1c, -NR1aS(O)2NR1bR1c, -SR1a, -S(O)R1a, -S(O)2R1a, -S(O)NR1bR1c или -S(O)2NR1bR1c; где каждый R1a, R1b, R1c и R1d независимо представляет собой (i) водород; (ii) C1-6 алкил, C2-6 алкенил, C2-6 алкинил, C3-10 циклоалкил, C6-14 арил, C7-15 аралкил, гетероарил или гетероциклил; или (iii) R1b и R1c вместе с атомом N, с которым они соединены, образуют гетероциклил;
каждый R3 и R4 независимо представляет собой водород или C1-6 алкил; или R3 и R4 соединены вместе, образуя связь, C1-6 алкилен, C1-6 гетероалкилен, C2-6 алкенилен или C2-6 гетероалкенилен;
R5a представляет собой (a) водород или галоген; (b) C1-6 алкил, C2-6 алкенил, C2-6 алкинил, C3-10 циклоалкил, C6-14 арил, C7-15 аралкил, гетероарил или гетероциклил; или (c) -C(O)R1a, -C(O)OR1a, -C(O)NR1bR1c, -C(NR1a)NR1bR1c, -OR1a, -OC(O)R1a, -OC(O)OR1a, -OC(O)NR1bR1c, -OC(=NR1a)NR1bR1c, -OS(O)R1a, -OS(O)2R1a, -OS(O)NR1bR1c, -OS(O)2NR1bR1c, -NR1bR1c, -NR1aC(O)R1d, -NR1aC(O)OR1d, -NR1aC(O)NR1bR1c, -NR1aC(=NR1d)NR1bR1c, -NR1aS(O)R1d, -NR1aS(O)2R1d, -NR1aS(O)NR1bR1c, -NR1aS(O)2NR1bR1c, -SR1a, -S(O)R1a, -S(O)2R1a, -S(O)NR1bR1c или -S(O)2NR1bR1c;
R5b представляет собой (a) галоген; (b) C1-6 алкил, C2-6 алкенил, C2-6 алкинил, C3-10 циклоалкил, C6-14 арил, C7-15 аралкил, гетероарил или гетероциклил; или (c) -C(O)R1a, -C(O)OR1a, -C(O)NR1bR1c, -C(NR1a)NR1bR1c, -OR1a, -OC(O)R1a, -OC(O)OR1a, -OC(O)NR1bR1c, -OC(=NR1a)NR1bR1c, -OS(O)R1a, -OS(O)2R1a, -OS(O)NR1bR1c, -OS(O)2NR1bR1c, -NR1bR1c, -NR1aC(O)R1d, -NR1aC(O)OR1d, -NR1aC(O)NR1bR1c, -NR1aC(=NR1d)NR1bR1c, -NR1aS(O)R1d, -NR1aS(O)2R1d, -NR1aS(O)NR1bR1c, -NR1aS(O)2NR1bR1c, -SR1a, -S(O)R1a, -S(O)2R1a, -S(O)NR1bR1c или -S(O)2NR1bR1c;
R5c представляет собой C6-14 арил или гетероарил; и
R6 представляет собой водород, C1-6 алкил, -S-C1-6 алкил, -S(O)-C1-6 алкил или -SO2-C1-6 алкил;
где каждый алкил, алкилен, гетероалкилен, алкенил, алкенилен, гетероалкенилен, алкинил, циклоалкил, арил, аралкил, гетероарил и гетероциклил в R1, R2, R3, R4, R6, RX, R1a, R1b, R1c, R1d, R5a, R5b и R5c необязательно замещен одним или более, в одном варианте осуществления одним, двумя, тремя или четырьмя, заместителями Q, где каждый заместитель Q независимо выбран из (a) оксо, циано, галогена и нитро; (b) C1-6 алкила, C2-6 алкенила, C2-6 алкинила, C3-10 циклоалкила, C6-14 арила, C7-15 аралкила, гетероарила и гетероциклила, каждый из которых дополнительно необязательно замещен одним или более, в одном варианте осуществления одним, двумя, тремя или четырьмя, заместителями Qa; и (c) -C(O)Ra, -C(O)ORa, -C(O)NRbRc, -C(NRa)NRbRc, -ORa, -OC(O)Ra, -OC(O)ORa, -OC(O)NRbRc, -OC(=NRa)NRbRc, -OS(O)Ra, -OS(O)2Ra, -OS(O)NRbRc, -OS(O)2NRbRc, -NRbRc, -NRaC(O)Rd, -NRaC(O)ORd, -NRaC(O)NRbRc, -NRaC(=NRd)NRbRc, -NRaS(O)Rd, -NRaS(O)2Rd, -NRaS(O)NRbRc, -NRaS(O)2NRbRc, -SRa, -S(O)Ra, -S(O)2Ra, -S(O)NRbRc и -S(O)2NRbRc, где каждый Ra, Rb, Rc, и Rd независимо представляет собой (i) водород; (ii) C1-6 алкил, C2-6 алкенил, C2-6 алкинил, C3-10 циклоалкил, C6-14 арил, C7-15 аралкил, гетероарил или гетероциклил, каждый из которых дополнительно необязательно замещен одним или более, в одном варианте осуществления одним, двумя, тремя или четырьмя, заместителями Qa; или (iii) Rb и Rc вместе с атомом N, с которым они соединены, образуют гетероциклил, который дополнительно необязательно замещен одним или более, в одном варианте осуществления одним, двумя, тремя или четырьмя, заместителями Qa;
где каждый Qa независимо выбран из группы, состоящей из (a) оксо, циано, галогена и нитро; (b) C1-6 алкила, C2-6 алкенила, C2-6 алкинила, C3-10 циклоалкила, C6-14 арила, C7-15 аралкила, гетероарила и гетероциклила; и (c) -C(O)Re, -C(O)ORe, -C(O)NRfRg, -C(NRe)NRfRg, -ORe, -OC(O)Re, -OC(O)ORe, -OC(O)NRfRg, -OC(=NRe)NRfRg, -OS(O)Re, -OS(O)2Re, -OS(O)NRfRg, -OS(O)2NRfRg, -NRfRg, -NReC(O)Rh, -NReC(O)ORh, -NReC(O)NRfRg, -NReC(=NRh)NRfRg, -NReS(O)Rh, -NReS(O)2Rh, -NReS(O)NRfRg, -NReS(O)2NRfRg, -SRe, -S(O)Re, -S(O)2Re, -S(O)NRfRg и -S(O)2NRfRg; где каждый Re, Rf, Rg, и Rh независимо представляет собой (i) водород; (ii) C1-6 алкил, C2-6 алкенил, C2-6 алкинил, C3-10 циклоалкил, C6-14 арил, C7-15 аралкил, гетероарил или гетероциклил; или (iii) Rf и Rg вместе с атомом N, с которым они соединены, образуют гетероциклил.
В одном варианте осуществления соединение формулы II имеет структуру формулы IIa:
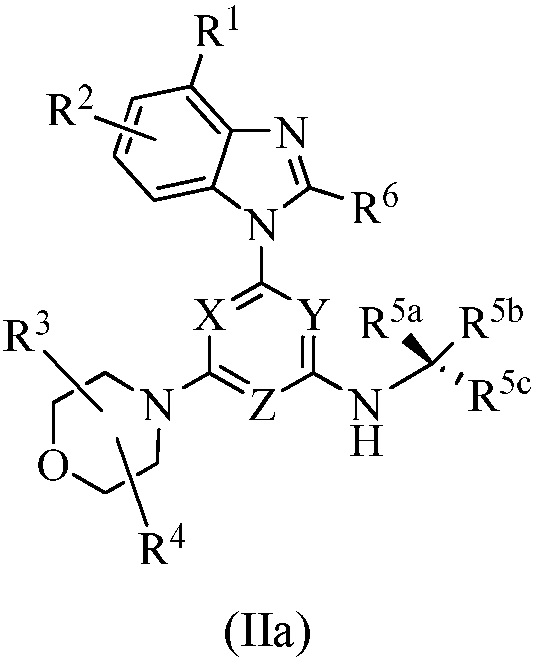
или его изотопный вариант; или их фармацевтически приемлемую соль, сольват, гидрат или пролекарство; где каждый R1, R2, R3, R4, R6, R5a, R5b, R5c, X, Y и Z представляет собой, как определено в настоящем изобретении.
В другом варианте осуществления соединение формулы II имеет структуру формулы IIb:
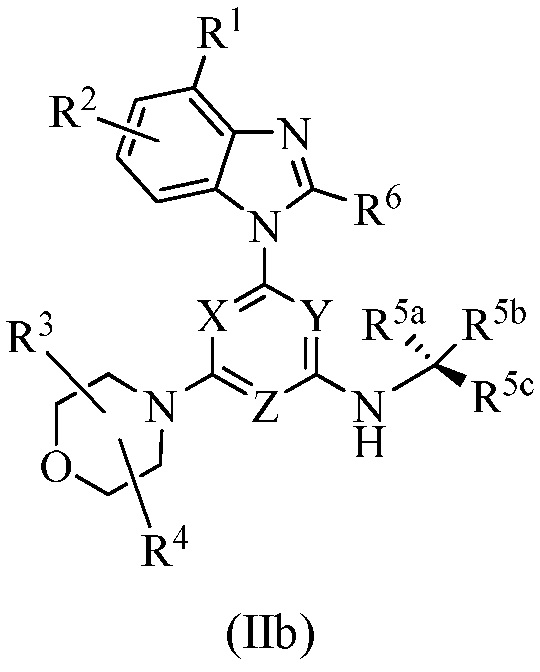
или его изотопный вариант; или их фармацевтически приемлемую соль, сольват, гидрат или пролекарство; где каждый R1, R2, R3, R4, R6, R5a, R5b, R5c, X, Y и Z представляет собой, как определено в настоящем изобретении.
В одном варианте осуществления настоящее изобретение относится к соединению формулы II, IIa или IIb, как описано в настоящем изобретении, или его энантиомеру, смеси энантиомеров, смеси двух или более диастереомеров или изотопному варианту; или их фармацевтически приемлемой соли, сольвату, гидрату или пролекарству; где каждый R5a и R5b независимо представляет собой (a) галоген; (b) C1-6 алкил, C2-6 алкенил, C2-6 алкинил, C3-10 циклоалкил, C6-14 арил, C7-15 аралкил, гетероарил или гетероциклил; или (c) -C(O)R1a, -C(O)OR1a, -C(O)NR1bR1c, -C(NR1a)NR1bR1c, -OR1a, -OC(O)R1a, -OC(O)OR1a, -OC(O)NR1bR1c, -OC(=NR1a)NR1bR1c, -OS(O)R1a, -OS(O)2R1a, -OS(O)NR1bR1c, -OS(O)2NR1bR1c, -NR1bR1c, -NR1aC(O)R1d, -NR1aC(O)OR1d, -NR1aC(O)NR1bR1c, -NR1aC(=NR1d)NR1bR1c, -NR1aS(O)R1d, -NR1aS(O)2R1d, -NR1aS(O)NR1bR1c, -NR1aS(O)2NR1bR1c, -SR1a, -S(O)R1a, -S(O)2R1a, -S(O)NR1bR1c или -S(O)2NR1bR1c; и R1, R2, R3, R4, R5c, R6, X, Y, Z, R1a, R1b, R1c и R1d определяют в настоящем изобретении выше.
В еще одном варианте осуществления настоящее изобретение относится к соединению формулы III:
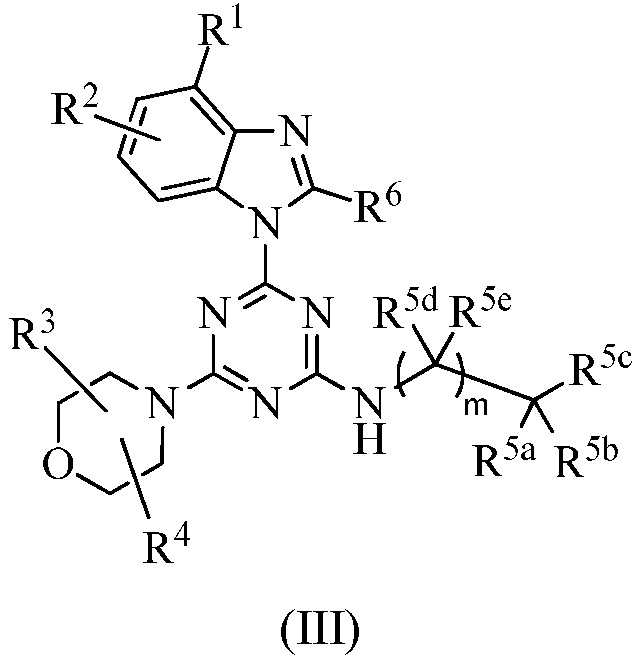
или его энантиомеру, смеси энантиомеров, смеси двух или более диастереомеров или изотопному варианту; или их фармацевтически приемлемой соли, сольвату, гидрату или пролекарству; где каждый R1, R2, R3, R4, R6, R5a, R5b, R5c, R5d, R5e и m представляет собой, как определено в настоящем изобретении. В одном варианте осуществления m равно 0. В другом варианте осуществления m равно 1.
В одном варианте осуществления соединение формулы III имеет структуру формулы IIIa:
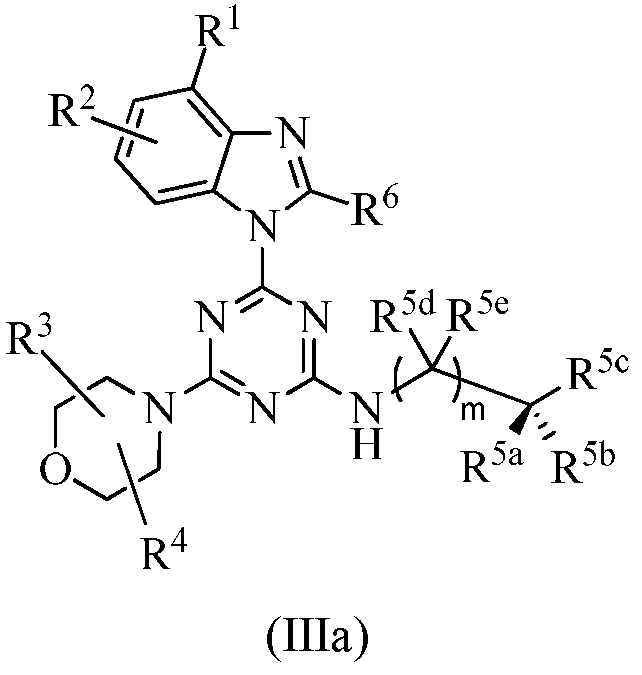
или его изотопный вариант; или их фармацевтически приемлемую соль, сольват, гидрат или его пролекарство; где каждый R1, R2, R3, R4, R6, R5a, R5b, R5c, R5d, R5e и m представляет собой, как определено в настоящем изобретении. В одном варианте осуществления m равно 0. В другом варианте осуществления m равно 1.
В другом варианте осуществления соединение формулы III имеет структуру формулы IIIb:
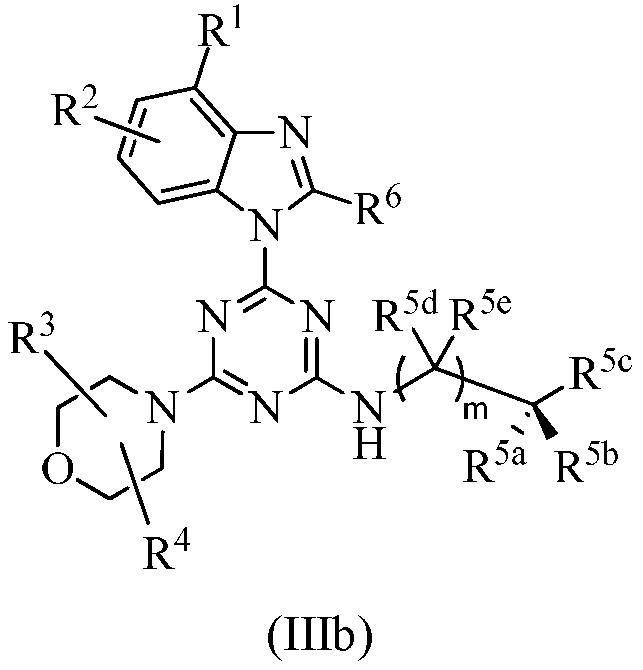
или его изотопный вариант; или их фармацевтически приемлемую соль, сольват, гидрат или его пролекарство; где каждый R1, R2, R3, R4, R6, R5a, R5b, R5c, R5d, R5e и m представляет собой, как определено в настоящем изобретении. В одном варианте осуществления m равно 0. В другом варианте осуществления m равно 1.
В одном варианте осуществления настоящее изобретение относится к соединению формулы III, IIIa или IIIb, как описано в настоящем изобретении, или его энантиомеру, смеси энантиомеров, смеси двух или более диастереомеров или изотопному варианту; или их фармацевтически приемлемой соли, сольвату, гидрату или пролекарству; где m равно 0; каждый R5a и R5b независимо представляет собой (a) галоген; (b) C1-6 алкил, C2-6 алкенил, C2-6 алкинил, C3-10 циклоалкил, C6-14 арил, C7-15 аралкил, гетероарил, или гетероциклил; или (c) -C(O)R1a, -C(O)OR1a, -C(O)NR1bR1c, -C(NR1a)NR1bR1c, -OR1a, -OC(O)R1a, -OC(O)OR1a, -OC(O)NR1bR1c, -OC(=NR1a)NR1bR1c, -OS(O)R1a, -OS(O)2R1a, -OS(O)NR1bR1c, -OS(O)2NR1bR1c, -NR1bR1c, -NR1aC(O)R1d, -NR1aC(O)OR1d, -NR1aC(O)NR1bR1c, -NR1aC(=NR1d)NR1bR1c, -NR1aS(O)R1d, -NR1aS(O)2R1d, -NR1aS(O)NR1bR1c, -NR1aS(O)2NR1bR1c, -SR1a, -S(O)R1a, -S(O)2R1a, -S(O)NR1bR1c или -S(O)2NR1bR1c; и R1, R2, R3, R4, R5c, R6, R1a, R1b, R1c и R1d определяют в настоящем изобретении выше.
В еще одном варианте осуществления настоящее изобретение относится к соединению формулы IV:
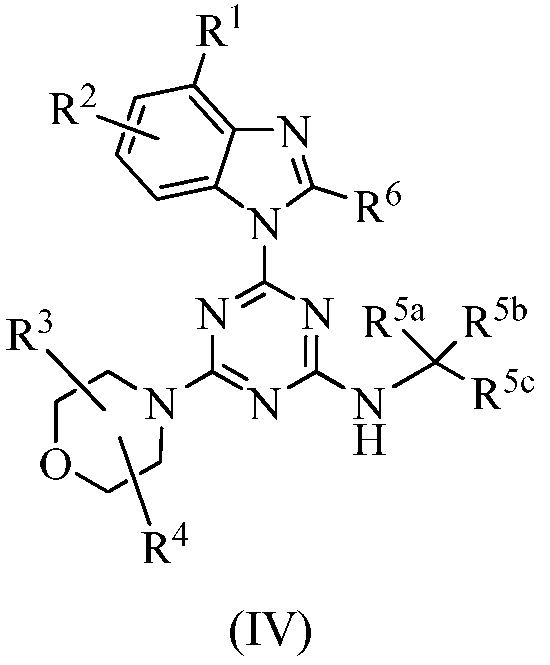
или его энантиомеру, смеси энантиомеров, смеси двух или более диастереомеров или изотопному варианту; или их фармацевтически приемлемой соли, сольвату, гидрату или пролекарству; где каждый R1, R2, R3, R4, R6, R5a, R5b и R5c представляет собой, как определено в настоящем изобретении.
В одном варианте осуществления соединение формулы IV имеет структуру формулы IVa:
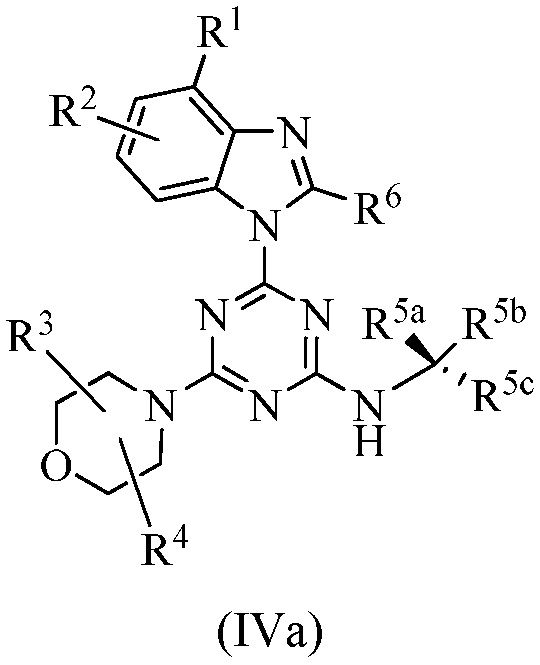
или его изотопный вариант; или их фармацевтически приемлемую соль, сольват, гидрат или пролекарство; где каждый R1, R2, R3, R4, R6, R5a, R5b и R5c представляет собой, как определено в настоящем изобретении.
В другом варианте осуществления соединение формулы IV имеет структуру формулы IVb:
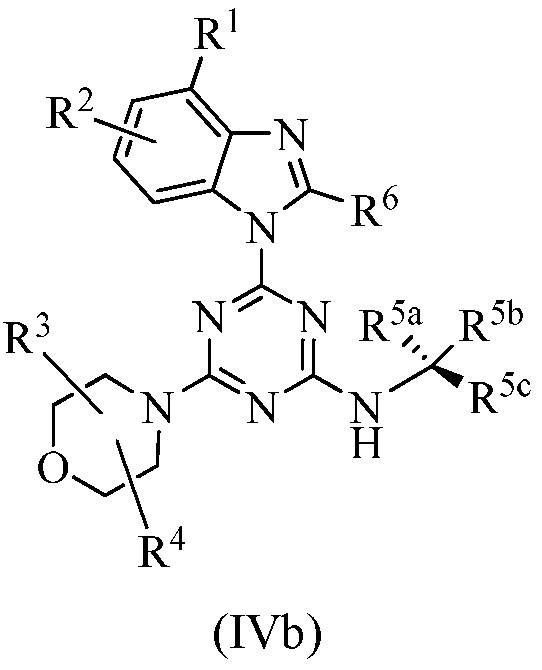
или его изотопный вариант; или их фармацевтически приемлемую соль, сольват, гидрат или пролекарство; где каждый R1, R2, R3, R4, R6, R5a, R5b и R5c представляет собой, как определено в настоящем изобретении.
В одном варианте осуществления настоящее изобретение относится к соединению формулы IV, IVa, или IVb, как описано в настоящем изобретении, или его энантиомеру, смеси энантиомеров, смеси двух или более диастереомеров или изотопному варианту; или их фармацевтически приемлемой соли, сольвату, гидрату или пролекарству; где каждый R5a и R5b независимо представляет собой (a) галоген; (b) C1-6 алкил, C2-6 алкенил, C2-6 алкинил, C3-10 циклоалкил, C6-14 арил, C7-15 аралкил, гетероарил или гетероциклил; или (c) -C(O)R1a, -C(O)OR1a, -C(O)NR1bR1c, -C(NR1a)NR1bR1c, -OR1a, -OC(O)R1a, -OC(O)OR1a, -OC(O)NR1bR1c, -OC(=NR1a)NR1bR1c, -OS(O)R1a, -OS(O)2R1a, -OS(O)NR1bR1c, -OS(O)2NR1bR1c, -NR1bR1c, -NR1aC(O)R1d, -NR1aC(O)OR1d, -NR1aC(O)NR1bR1c, -NR1aC(=NR1d)NR1bR1c, -NR1aS(O)R1d, -NR1aS(O)2R1d, -NR1aS(O)NR1bR1c, -NR1aS(O)2NR1bR1c, -SR1a, -S(O)R1a, -S(O)2R1a, -S(O)NR1bR1c или -S(O)2NR1bR1c; и R1, R2, R3, R4, R5c, R6, R1a, R1b, R1c и R1d определяют в настоящем изобретении выше.
В еще одном варианте осуществления настоящее изобретение относится к соединению формулы V:
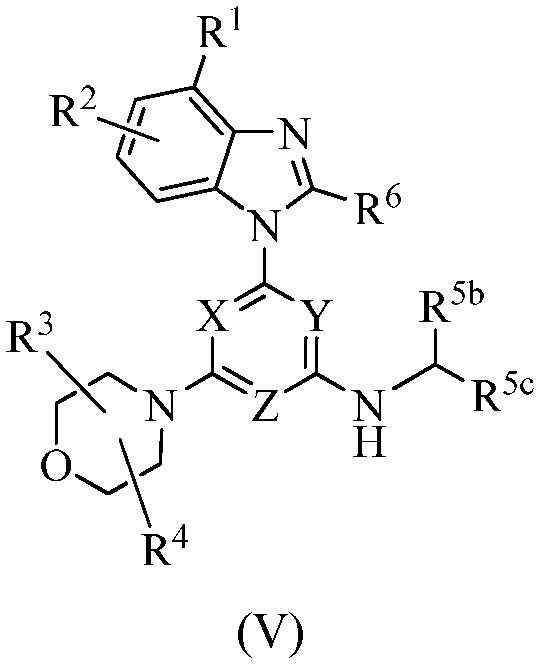
или его энантиомеру, смеси энантиомеров, смеси двух или более диастереомеров или изотопному варианту; или их фармацевтически приемлемой соли, сольвату, гидрату или пролекарству; где каждый R1, R2, R3, R4, R6, R5b, R5c, X, Y и Z представляет собой, как определено в настоящем изобретении.
В одном варианте осуществления соединение формулы V имеет структуру формулы Va:
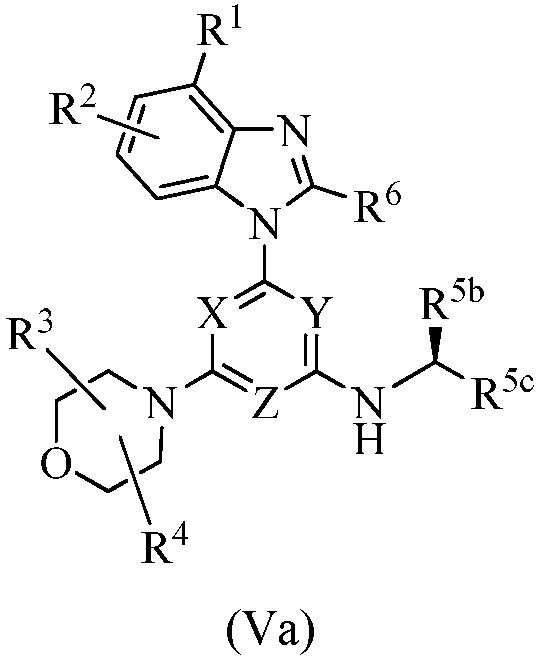
или его изотопный вариант; или их фармацевтически приемлемую соль, сольват, гидрат или пролекарство; где каждый R1, R2, R3, R4, R6, R5b, R5c, X, Y и Z представляет собой, как определено в настоящем изобретении.
В другом варианте осуществления соединение формулы V имеет структуру формулы Vb:
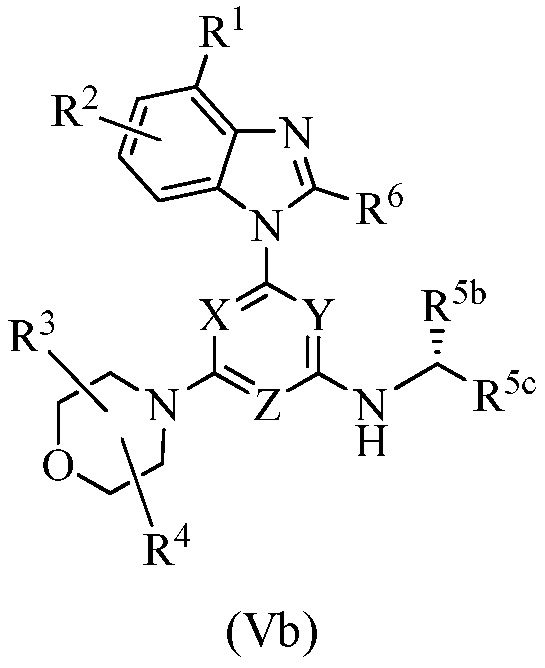
или его изотопный вариант; или их фармацевтически приемлемую соль, сольват, гидрат или пролекарство; где каждый R1, R2, R3, R4, R6, R5b, R5c, X, Y и Z представляет собой, как определено в настоящем изобретении.
В еще одном варианте осуществления настоящее изобретение относится к соединению формулы VI:
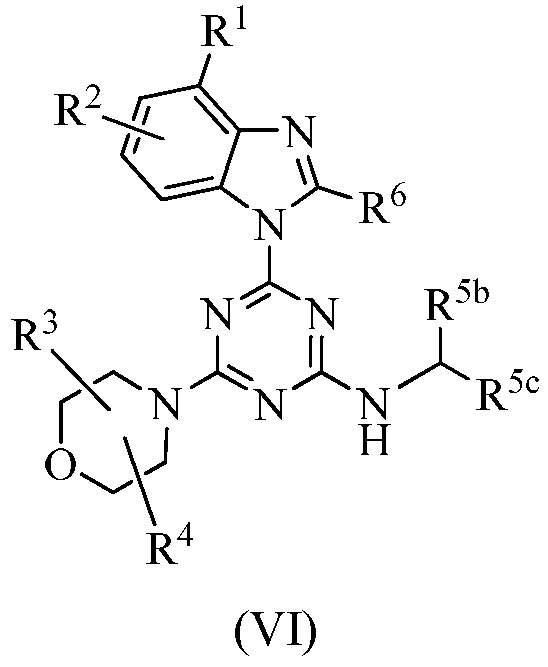
или его энантиомеру, смеси энантиомеров, смеси двух или более диастереомеров или изотопному варианту; или их фармацевтически приемлемой соли, сольвату, гидрату или пролекарству; где каждый R1, R2, R3, R4, R6, R5b и R5c представляет собой, как определено в настоящем изобретении.
В одном варианте осуществления соединение формулы VI имеет структуру формулы VIa:
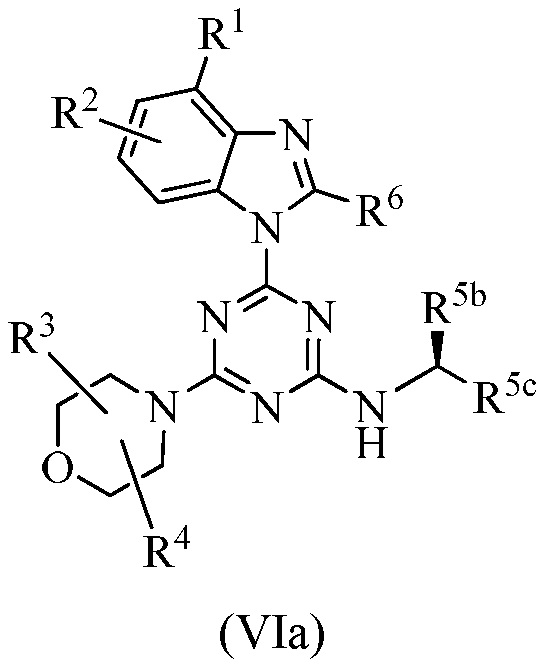
или его изотопный вариант; или их фармацевтически приемлемую соль, сольват, гидрат или пролекарство; где каждый R1, R2, R3, R4, R6, R5b и R5c представляет собой, как определено в настоящем изобретении.
В другом варианте осуществления соединение формулы VI имеет структуру формулы VIb:
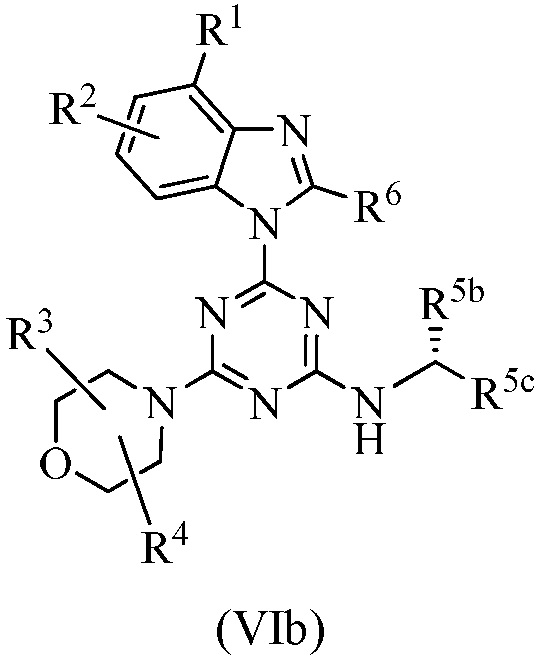
или его изотопный вариант; или их фармацевтически приемлемую соль, сольват, гидрат или пролекарство; где каждый R1, R2, R3, R4, R6, R5b и R5c представляет собой, как определено в настоящем изобретении.
В еще одном варианте осуществления настоящее изобретение относится к соединению формулы VII:
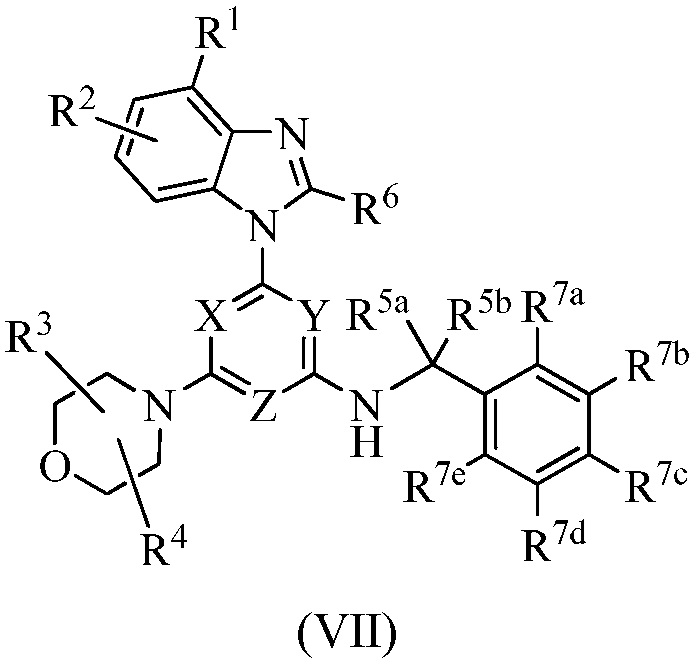
или его энантиомеру, смеси энантиомеров, смеси двух или более диастереомеров или изотопному варианту; или их фармацевтически приемлемой соли, сольвату, гидрату или пролекарству, где:
каждый R7a, R7b, R7c, R7d и R7e независимо представляет собой (a) водород, циано, галоген или нитро; (b) C1-6 алкил, C2-6 алкенил, C2-6 алкинил, C3-10 циклоалкил, C6-14 арил, C7-15 аралкил, гетероарил или гетероциклил, каждый из которых необязательно замещен одним или более заместителями Q; или (c) -C(O)R1a, -C(O)OR1a, -C(O)NR1bR1c, -C(NR1a)NR1bR1c, -OR1a, -OC(O)R1a, -OC(O)OR1a, -OC(O)NR1bR1c, -OC(=NR1a)NR1bR1c, -OS(O)R1a, -OS(O)2R1a, -OS(O)NR1bR1c, -OS(O)2NR1bR1c, -NR1bR1c, -NR1aC(O)R1d, -NR1aC(O)OR1d, -NR1aC(O)NR1bR1c, -NR1aC(=NR1d)NR1bR1c, -NR1aS(O)R1d, -NR1aS(O)2R1d, -NR1aS(O)NR1bR1c, -NR1aS(O)2NR1bR1c, -SR1a, -S(O)R1a, -S(O)2R1a, -S(O)NR1bR1c или -S(O)2NR1bR1c;
два из R7a, R7b, R7c, R7d и R7e, которые находятся рядом друг с другом, образуют C3-10 циклоалкенил, C6-14 арил, гетероарил или гетероциклил, причем каждый необязательно замещен одним или более заместителями Q; и
каждый R1, R2, R3, R4, R6, R1a, R1b, R1c, R1d, R5a, R5b, X, Y и Z представляет собой, как определено в настоящем изобретении.
В одном варианте осуществления соединение формулы VII имеет структуру формулы VIIa:
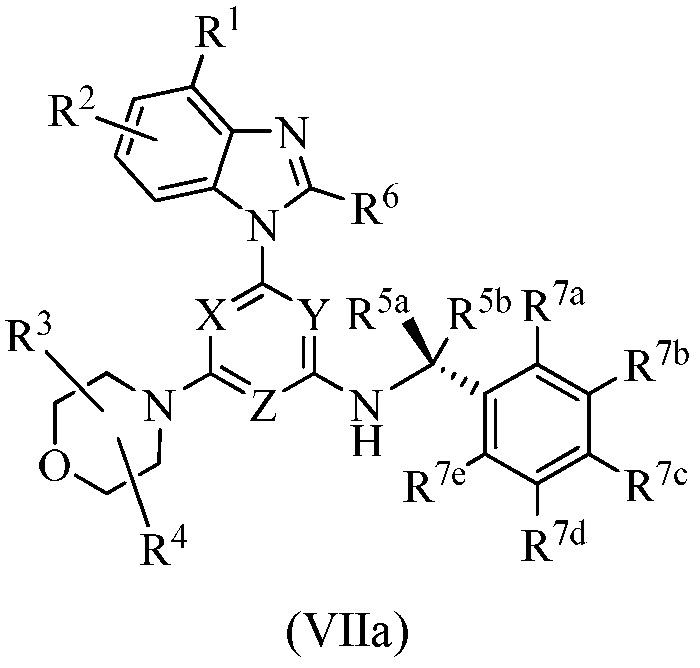
или его изотопный вариант; или его фармацевтически приемлемая соль, сольват, гидрат или пролекарство; где каждый R1, R2, R3, R4, R6, R5a, R5b, R7a, R7b, R7c, R7d, R7e, X, Y и Z представляет собой, как определено в настоящем изобретении.
В другом варианте осуществления соединение формулы VII имеет структуру формулы VIIb:
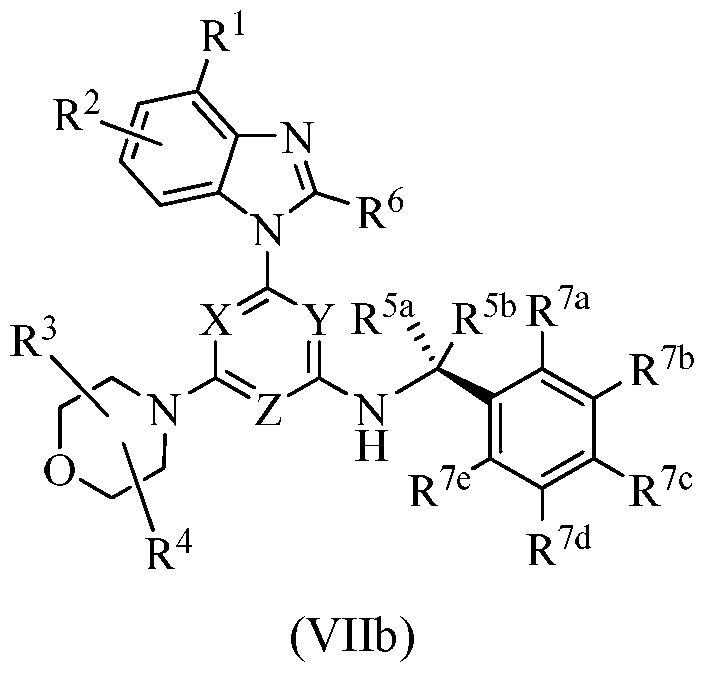
или его изотопный вариант; или его фармацевтически приемлемая соль, сольват, гидрат или пролекарство; где каждый R1, R2, R3, R4, R6, R5a, R5b, R7a, R7b, R7c, R7d, R7e, X, Y и Z представляет собой, как определено в настоящем изобретении.
В еще одном варианте осуществления настоящее изобретение относится к соединению формулы VIII:
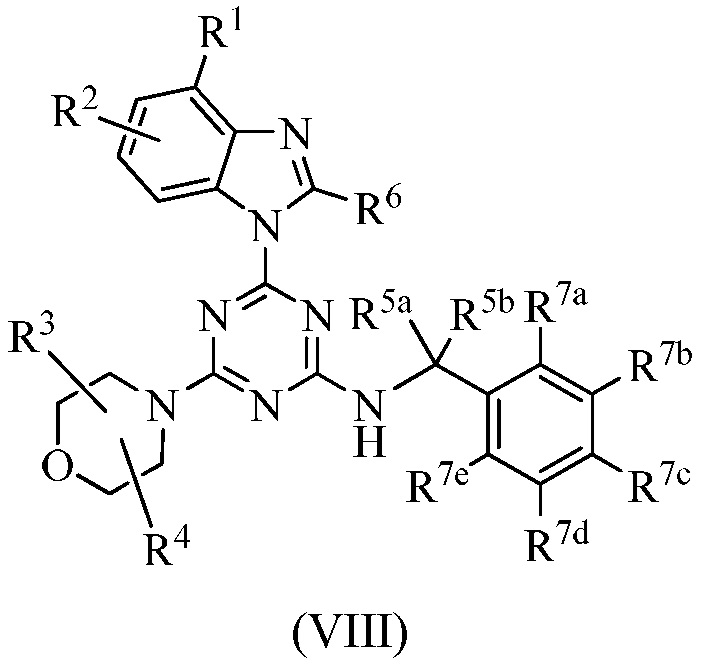
или его энантиомеру, смеси энантиомеров, смеси двух или более диастереомеров или изотопному варианту; или их фармацевтически приемлемой соли, сольвату, гидрату или пролекарству; где каждый R1, R2, R3, R4, R6, R5a, R5b, R7a, R7b, R7c, R7d и R7e представляет собой, как определено в настоящем изобретении.
В одном варианте осуществления соединение формулы VIII имеет структуру формулы VIIIa:
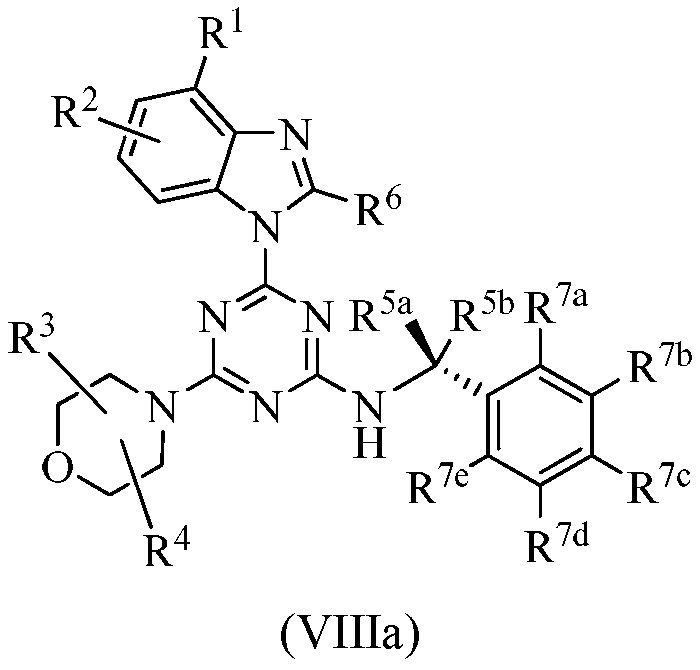
или его изотопный вариант; или его фармацевтически приемлемая соль, сольват, гидрат или пролекарство; где каждый R1, R2, R3, R4, R6, R5a, R5b, R7a, R7b, R7c, R7d и R7e представляет собой, как определено в настоящем изобретении.
В другом варианте осуществления соединение формулы VIII имеет структуру формулы VIIIb:
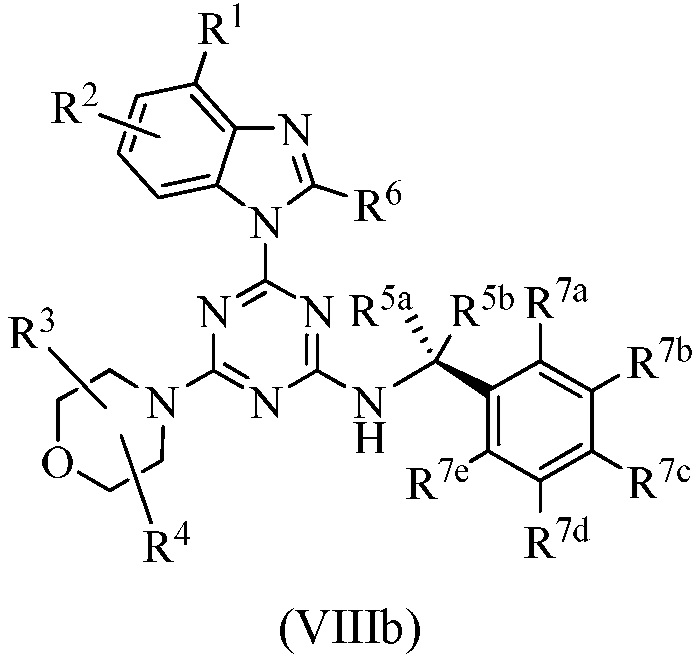
или его изотопный вариант; или его фармацевтически приемлемая соль, сольват, гидрат или пролекарство; где каждый R1, R2, R3, R4, R6, R5a, R5b, R7a, R7b, R7c, R7d и R7e представляет собой, как определено в настоящем изобретении.
В еще одном варианте осуществления настоящее изобретение относится к соединению формулы IX:
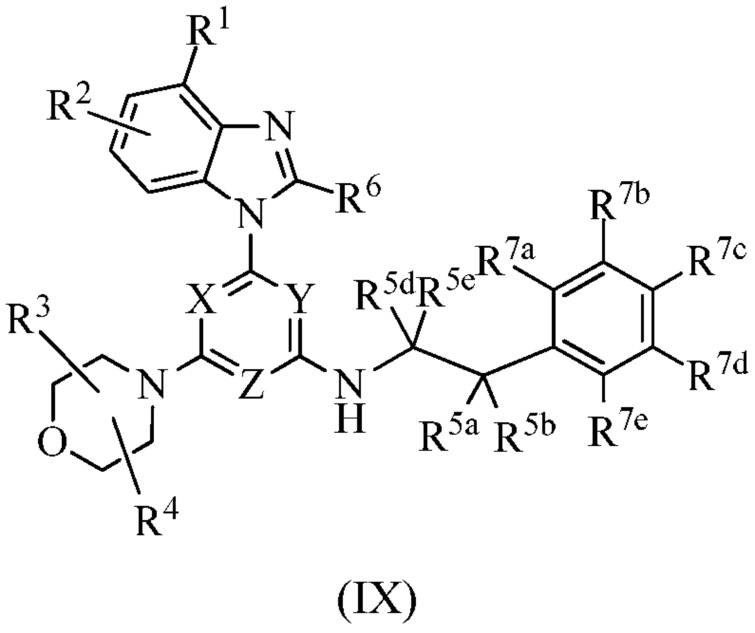
или его энантиомеру, смеси энантиомеров, смеси двух или более диастереомеров или изотопному варианту; или их фармацевтически приемлемой соли, сольвату, гидрату или его пролекарству; где:
каждый R7a, R7b, R7c, R7d и R7e независимо представляет собой (a) водород, циано, галоген или нитро; (b) C1-6 алкил, C2-6 алкенил, C2-6 алкинил, C3-10 циклоалкил, C6-14 арил, C7-15 аралкил, гетероарил или гетероциклил, каждый из которых необязательно замещен одним или более заместителями Q; или (c) -C(O)R1a, -C(O)OR1a, -C(O)NR1bR1c, -C(NR1a)NR1bR1c, -OR1a, -OC(O)R1a, -OC(O)OR1a, -OC(O)NR1bR1c, -OC(=NR1a)NR1bR1c, -OS(O)R1a, -OS(O)2R1a, -OS(O)NR1bR1c, -OS(O)2NR1bR1c, -NR1bR1c, -NR1aC(O)R1d, -NR1aC(O)OR1d, -NR1aC(O)NR1bR1c, -NR1aC(=NR1d)NR1bR1c, -NR1aS(O)R1d, -NR1aS(O)2R1d, -NR1aS(O)NR1bR1c, -NR1aS(O)2NR1bR1c, -SR1a, -S(O)R1a, -S(O)2R1a, -S(O)NR1bR1c или -S(O)2NR1bR1c;
два из R7a, R7b, R7c, R7d и R7e, которые находятся рядом друг с другом, образуют C3-10 циклоалкенил, C6-14 арил, гетероарил или гетероциклил, причем каждый необязательно замещен одним или более заместителями Q; и
каждый R1, R2, R3, R4, R6, R1a, R1b, R1c, R1d, R5a, R5b, R5d, R5e, X, Y и Z представляет собой, как определено в настоящем изобретении.
В одном варианте осуществления соединение формулы IX имеет структуру формулы IXa:
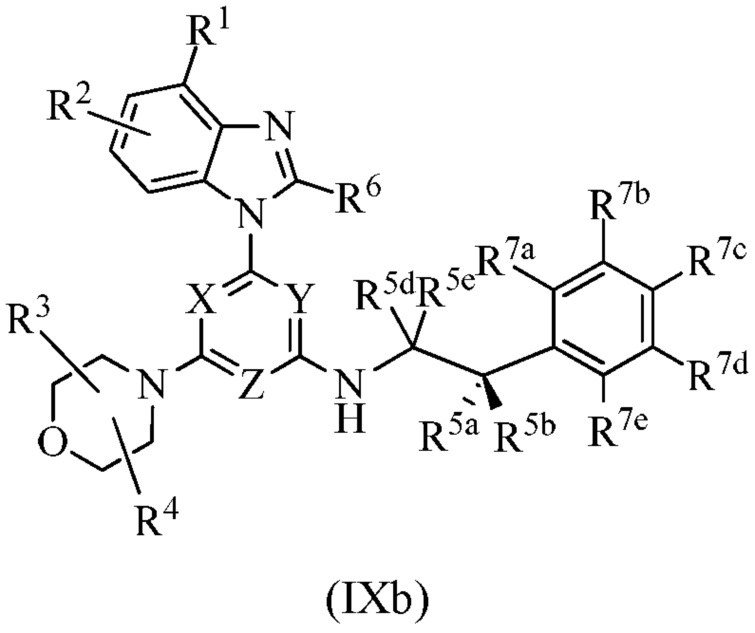
или его изотопный вариант; или их фармацевтически приемлемую соль, сольват, гидрат или пролекарство; где каждый R1, R2, R3, R4, R6, R5a, R5b, R5d, R5e, R7a, R7b, R7c, R7d, R7e, X, Y и Z представляет собой, как определено в настоящем изобретении.
В другом варианте осуществления соединение формулы IX имеет структуру формулы IXb:

или его изотопный вариант; или их фармацевтически приемлемую соль, сольват, гидрат или пролекарство; где каждый R1, R2, R3, R4, R6, R5a, R5b, R5d, R5e, R7a, R7b, R7c, R7d, R7e, X, Y и Z представляет собой, как определено в настоящем изобретении.
В формуле IX, IXa или IXb в определенных вариантах осуществления один из R7a, R7b, R7c, R7d и R7e представляет собой C6-14 арил, гетероарил или гетероциклил, каждый из которых необязательно замещен одним или более заместителями Q; в определенных вариантах осуществления один из R7a, R7b, R7c, R7d и R7e представляет собой C6-14 арил, например, фенил, необязательно замещенный одним или более заместителями Q; в определенных вариантах осуществления один из R7a, R7b, R7c, R7d и R7e представляет собой гетероарил, например, 5-членный или 6-членный гетероарил, необязательно замещенный одним или более заместителями Q; в определенных вариантах осуществления один из R7a, R7b, R7c, R7d и R7e представляет собой гетероциклил, например, 5-членный или 6-членный гетероциклил, необязательно замещенный одним или более заместителями Q; в определенных вариантах осуществления один из R7a, R7b, R7c, R7d, и R7e представляет собой фенил, имидазолил, пиразолил, пиридинил, пиперидинил или пиперазинил, причем каждый необязательно замещен одним или более заместителями Q; в определенных вариантах осуществления один из R7a, R7b, R7c, R7d и R7e представляет собой фенил, имидазолил, пиразолил, пиридинил, пиримидинил, пирролидинил, пиперидинил или пиперазинил, причем каждый необязательно замещен одним или более заместителями Q; в определенных вариантах осуществления один из R7a, R7b, R7c, R7d и R7e представляет собой фенил, 2-фторфенил, 2-хлорфенил, 2-бромфенил, 2-метилфенил, 2-метоксифенил, 3-фторфенил, 3-хлорфенил, 3-метоксифенил, 4-фторфенил, 4-хлорфенил, 4-бромфенил, 4-метоксифенил, имидазол-1-ил, пиразол-4-ил, 1-метилпиразол-4-ил, 2-метилпиразол-3-ил, пиридин-2-ил, пиридин-3-ил, пиридин-4-ил, 2-метилпиридин-4-ил, 2-метоксипиридин-4-ил, 1-метилпиперидин-4-ил или 4-метилпиперазин-1-ил; и в определенных вариантах осуществления один из R7a, R7b, R7c, R7d и R7e представляет собой фенил, 2-фторфенил, 2-хлорфенил, 2-бромфенил, 2-метилфенил, 2-(3-диметиламинопропил)фенил, 2-метоксифенил, 3-фторфенил, 3-хлорфенил, 3-метилфенил, 3-метоксифенил, 4-фторфенил, 4-хлорфенил, 4-бромфенил, 4-метоксифенил, 2,4-дифторфенил, 2,6-дифторфенил, 4-фтор-3-метоксифенил, 3-метоксифенил, 4-метоксифенил, 3-морфолин-4-илметилфенил, имидазол-1-ил, пиразол-4-ил, 1-метилпиразол-4-ил, 2-метилпиразол-3-ил, пиридин-2-ил, пиридин-3-ил, пиридин-4-ил, 2-фторпиридин-3-ил, 2-метилпиридин-4-ил, 2-(4-метилпиперазин-1-ил)пиридин-4-ил, 2-метоксипиридин-4-ил, пиримидин-5-ил, пирролидин-3-ил, 1-метилпирролидин-3-ил, пиперидин-4-ил, 1-метилпиперидин-4-ил, 1-этилпиперидин-4-ил, 1-изопропилпиперидин-4-ил, 1-ацетилпиперидин-4-ил, 1-метилсульфонилпиперидин-4-ил или 4-метилпиперазин-1-ил.
В формуле IX, IXa или IXb в определенных вариантах осуществления R7a представляет собой C6-14 арил, гетероарил или гетероциклил, каждый из которых необязательно замещен одним или более заместителями Q; в определенных вариантах осуществления R7a представляет собой C6-14 арил, например, фенил, необязательно замещенный одним или более заместителями Q; в определенных вариантах осуществления R7a представляет собой гетероарил, например, 5-членный или 6-членный гетероарил, необязательно замещенный одним или более заместителями Q; в определенных вариантах осуществления R7a представляет собой гетероциклил, например, 5-членный или 6-членный гетероциклил, необязательно замещенный одним или более заместителями Q; в определенных вариантах осуществления R7a представляет собой фенил, имидазолил, пиразолил, пиридинил, пиперидинил или пиперазинил, причем каждый необязательно замещен одним или более заместителями Q; в определенных вариантах осуществления R7a представляет собой фенил, имидазолил, пиразолил, пиридинил, пиримидинил, пирролидинил, пиперидинил или пиперазинил, причем каждый необязательно замещен одним или более заместителями Q; в определенных вариантах осуществления R7a представляет собой фенил, 2-фторфенил, 2-хлорфенил, 2-бромфенил, 2-метилфенил, 2-метоксифенил, 3-фторфенил, 3-хлорфенил, 3-метоксифенил, 4-фторфенил, 4-хлорфенил, 4-бромфенил, 4-метоксифенил, имидазол-1-ил, пиразол-4-ил, 1-метилпиразол-4-ил, 2-метилпиразол-3-ил, пиридин-2-ил, пиридин-3-ил, пиридин-4-ил, 2-метилпиридин-4-ил, 2-метоксипиридин-4-ил, 1-метилпиперидин-4-ил или 4-метилпиперазин-1-ил; и в определенных вариантах осуществления R7a представляет собой фенил, 2-фторфенил, 2-хлорфенил, 2-бромфенил, 2-метилфенил, 2-(3-диметиламинопропил)фенил, 2-метоксифенил, 3-фторфенил, 3-хлорфенил, 3-метилфенил, 3-метоксифенил, 4-фторфенил, 4-хлорфенил, 4-бромфенил, 4-метоксифенил, 2,4-дифторфенил, 2,6-дифторфенил, 4-фтор-3-метоксифенил, 3-метоксифенил, 4-метоксифенил, 3-морфолин-4-илметилфенил, имидазол-1-ил, пиразол-4-ил, 1-метилпиразол-4-ил, 2-метилпиразол-3-ил, пиридин-2-ил, пиридин-3-ил, пиридин-4-ил, 2-фторпиридин-3-ил, 2-метилпиридин-4-ил, 2-(4-метилпиперазин-1-ил)пиридин-4-ил, 2-метоксипиридин-4-ил, пиримидин-5-ил, пирролидин-3-ил, 1-метилпирролидин-3-ил, пиперидин-4-ил, 1-метилпиперидин-4-ил, 1-этилпиперидин-4-ил, 1-изопропилпиперидин-4-ил, 1-ацетилпиперидин-4-ил, 1-метилсульфонилпиперидин-4-ил или 4-метилпиперазин-1-ил.
В одном варианте осуществления в формуле IX, IXa или IXb R1 представляет собой водород или -OR1a, где R1a представляет собой C1-6 алкил, необязательно замещенный одним или более заместителями Q;
R2 представляет собой водород;
R3 и R4 представляют собой водород;
R6 представляет собой C6-14 алкил, необязательно замещенный одним или более заместителями Q;
каждый R5a и R5b независимо представляет собой водород, галоген, C1-6 алкил, необязательно замещенный одним или более заместителями Q;
каждый R5d и R5e независимо представляет собой C6-14 алкил, необязательно замещенный одним или более заместителями Q;
R7a представляет собой C6-14 арил, гетероарил или гетероциклил, каждый из которых необязательно замещен одним или более заместителями Q;
R7b, R7c, R7d и R7e представляют собой водород; и
каждый X, Y и Z независимо представляет собой N или CRx, при условии, что по меньшей мере два из X, Y и Z представляют собой N; где Rx представляет собой водород или C1-6 алкил, необязательно замещенный одним или более заместителями Q.
В другом варианте осуществления в формуле IX, IXa или IXb
R1 представляет собой водород или метокси;
R2 представляет собой водород;
R3 и R4 представляют собой водород;
R6 представляет собой C6-14 алкил, необязательно замещенный одним или более галогенами;
R5a и R5b представляют собой водород;
каждый R5d и R5e независимо представляет собой C6-14 алкил;
R7a представляет собой C6-14 арил, гетероарил или гетероциклил, каждый из которых необязательно замещен одним или более заместителями Q;
R7b, R7c, R7d и R7e представляют собой водород; и
каждый X, Y и Z независимо представляет собой N или CH.
В еще одном варианте осуществления в формуле IX, IXa или IXb
R1 представляет собой водород или метокси;
R2 представляет собой водород;
R3 и R4 представляют собой водород;
R6 представляет собой дифторметил;
R5a и R5b представляют собой водород;
R5d и R5e представляют собой метил;
R7a представляет собой C6-14 арил, моноциклический гетероарил или моноциклический гетероциклил, каждый из которых необязательно замещен одним или более заместителями Q;
R7b, R7c, R7d и R7e представляют собой водород; и
каждый X, Y и Z независимо представляет собой N или CH.
В еще одном варианте осуществления в формуле IX, IXa или IXb
R1 представляет собой водород или метокси;
R2 представляет собой водород;
R3 и R4 представляют собой водород;
R6 представляет собой дифторметил;
R5a и R5b представляют собой водород;
R5d и R5e представляют собой метил;
R7a представляет собой фенил, 5- или 6-членный гетероарил или 5- или 6-членный гетероциклил, каждый из которых необязательно замещен одним или более заместителями Q;
R7b, R7c, R7d и R7e представляют собой водород; и
каждый X, Y и Z независимо представляет собой N или CH.
В еще одном варианте осуществления в формуле IX, IXa или IXb
R1 представляет собой водород или метокси;
R2 представляет собой водород;
R3 и R4 представляют собой водород;
R6 представляет собой дифторметил;
R5a и R5b представляют собой водород;
R5d и R5e представляют собой метил;
R7a представляет собой фенил, имидазолил, пиразолил, пиридинил, пиримидинил, пирролидинил, пиперидинил или пиперазинил, каждый из которых необязательно замещен одним или более заместителями Q;
R7b, R7c, R7d и R7e представляют собой водород; и
каждый X, Y и Z независимо представляет собой N или CH.
В еще одном варианте осуществления в формуле IX, IXa или IXb
R1 представляет собой водород или метокси;
R2 представляет собой водород;
R3 и R4 представляют собой водород;
R6 представляет собой дифторметил;
R5a и R5b представляют собой водород;
R5d и R5e представляют собой метил;
R7a представляет собой фенил, имидазолил, пиразолил, пиридинил, пиперидинил или пиперазинил, каждый из которых необязательно замещен одним или более заместителями Q;
R7b, R7c, R7d и R7e представляют собой водород; и
каждый X, Y и Z независимо представляет собой N или CH.
В еще одном варианте осуществления настоящее изобретение относится к соединению формулы X:
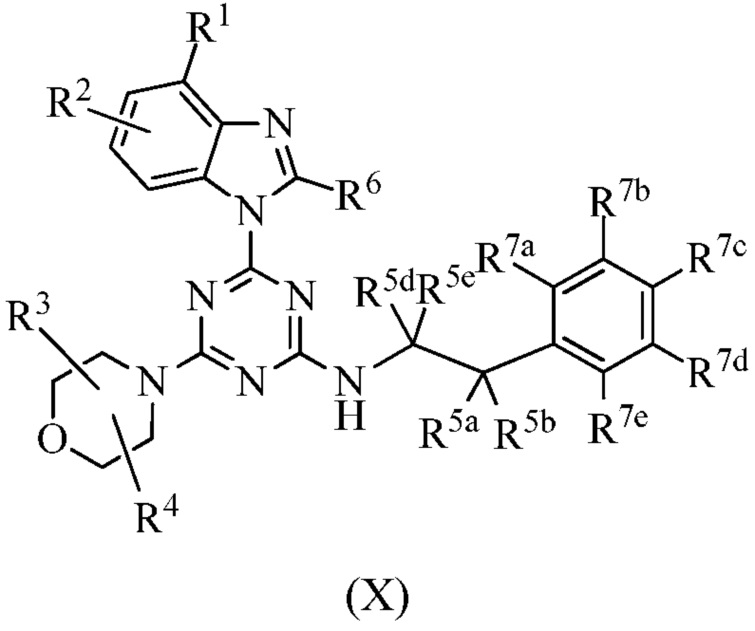
или его энантиомеру, смеси энантиомеров, смеси двух или более диастереомеров или изотопному варианту; или их фармацевтически приемлемой соли, сольвату, гидрату или пролекарству; где каждый R1, R2, R3, R4, R6, R5a, R5b, R5d, R5e, R7a, R7b, R7c, R7d и R7e представляет собой, как определено в настоящем изобретении.
В одном варианте осуществления соединение формулы X имеет структуру формулы Xa:
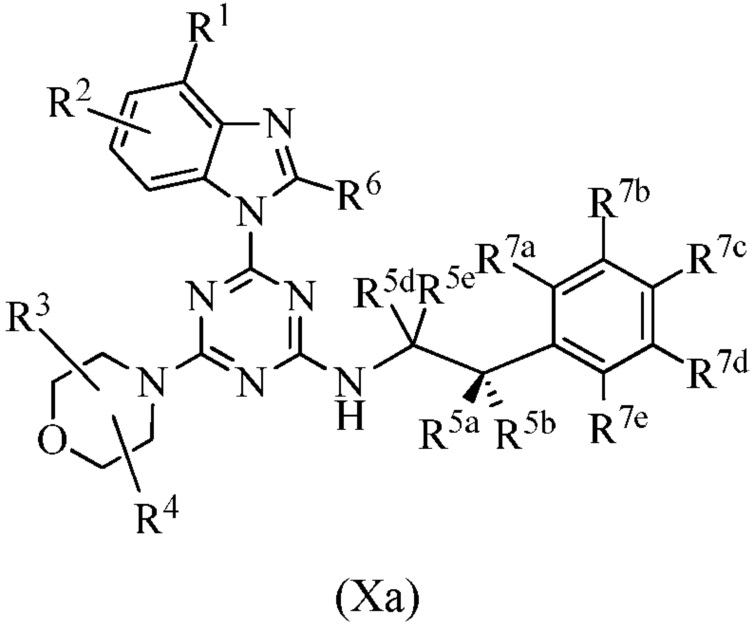
или его изотопный вариант; или их фармацевтически приемлемую соль, сольват, гидрат или пролекарство; где каждый R1, R2, R3, R4, R6, R5a, R5b, R5d, R5e, R7a, R7b, R7c, R7d и R7e представляет собой, как определено в настоящем изобретении.
В другом варианте осуществления соединение формулы X имеет структуру формулы Xb:
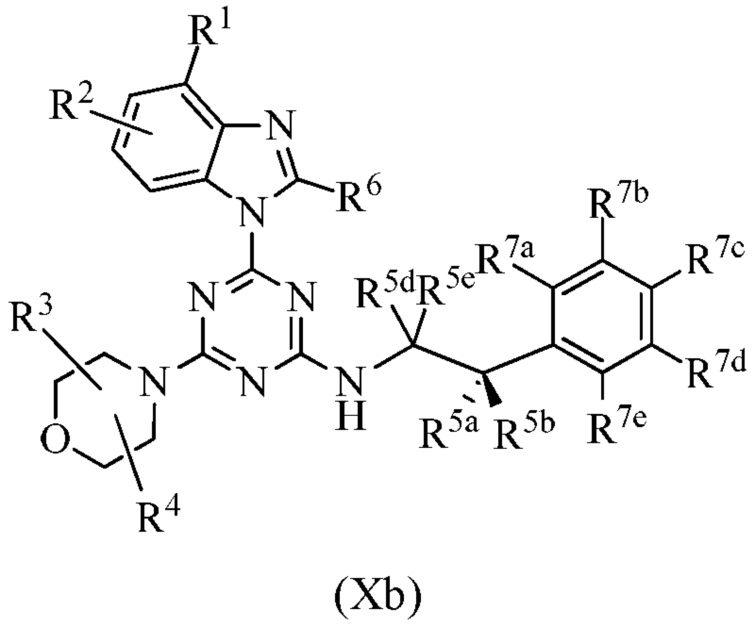
или его изотопный вариант; или их фармацевтически приемлемую соль, сольват, гидрат или пролекарство; где каждый R1, R2, R3, R4, R6, R5a, R5b, R5d, R5e, R7a, R7b, R7c, R7d и R7e представляет собой, как определено в настоящем изобретении.
В формуле X, Xa или Xb в определенных вариантах осуществления один из R7a, R7b, R7c, R7d и R7e представляет собой C6-14 арил, гетероарил или гетероциклил, каждый из которых необязательно замещен одним или более заместителями Q; в определенных вариантах осуществления один из R7a, R7b, R7c, R7d и R7e представляет собой C6-14 арил, например, фенил, необязательно замещенный одним или более заместителями Q; в определенных вариантах осуществления один из R7a, R7b, R7c, R7d и R7e представляет собой гетероарил, например, 5-членный или 6-членный гетероарил, необязательно замещенный одним или более заместителями Q; в определенных вариантах осуществления один из R7a, R7b, R7c, R7d и R7e представляет собой гетероциклил, например, 5-членный или 6-членный гетероциклил, необязательно замещенный одним или более заместителями Q; в определенных вариантах осуществления один из R7a, R7b, R7c, R7d и R7e представляет собой фенил, имидазолил, пиразолил, пиридинил, пиперидинил или пиперазинил, причем каждый необязательно замещен одним или более заместителями Q; в определенных вариантах осуществления один из R7a, R7b, R7c, R7d и R7e представляет собой фенил, имидазолил, пиразолил, пиридинил, пиримидинил, пирролидинил, пиперидинил или пиперазинил, причем каждый необязательно замещен одним или более заместителями Q; в определенных вариантах осуществления один из R7a, R7b, R7c, R7d, и R7e представляет собой фенил, 2-фторфенил, 2-хлорфенил, 2-бромфенил, 2-метилфенил, 2-метоксифенил, 3-фторфенил, 3-хлорфенил, 3-метоксифенил, 4-фторфенил, 4-хлорфенил, 4-бромфенил, 4-метоксифенил, имидазол-1-ил, пиразол-4-ил, 1-метилпиразол-4-ил, 2-метилпиразол-3-ил, пиридин-2-ил, пиридин-3-ил, пиридин-4-ил, 2-метилпиридин-4-ил, 2-метоксипиридин-4-ил, 1-метилпиперидин-4-ил или 4-метилпиперазин-1-ил; и в определенных вариантах осуществления один из R7a, R7b, R7c, R7d и R7e представляет собой фенил, 2-фторфенил, 2-хлорфенил, 2-бромфенил, 2-метилфенил, 2-(3-диметиламинопропил)фенил, 2-метоксифенил, 3-фторфенил, 3-хлорфенил, 3-метилфенил, 3-метоксифенил, 4-фторфенил, 4-хлорфенил, 4-бромфенил, 4-метоксифенил, 2,4-дифторфенил, 2,6-дифторфенил, 4-фтор-3-метоксифенил, 3-метоксифенил, 4-метоксифенил, 3-морфолин-4-илметилфенил, имидазол-1-ил, пиразол-4-ил, 1-метилпиразол-4-ил, 2-метилпиразол-3-ил, пиридин-2-ил, пиридин-3-ил, пиридин-4-ил, 2-фторпиридин-3-ил, 2-метилпиридин-4-ил, 2-(4-метилпиперазин-1-ил)пиридин-4-ил, 2-метоксипиридин-4-ил, пиримидин-5-ил, пирролидин-3-ил, 1-метилпирролидин-3-ил, пиперидин-4-ил, 1-метилпиперидин-4-ил, 1-этилпиперидин-4-ил, 1-изопропилпиперидин-4-ил, 1-ацетилпиперидин-4-ил, 1-метилсульфонилпиперидин-4-ил или 4-метилпиперазин-1-ил.
В формуле X, Xa или Xb в определенных вариантах осуществления R7a представляет собой C6-14 арил, гетероарил или гетероциклил, каждый из которых необязательно замещен одним или более заместителями Q; в определенных вариантах осуществления R7a представляет собой C6-14 арил, например, фенил, необязательно замещенный одним или более заместителями Q; в определенных вариантах осуществления R7a представляет собой гетероарил, например, 5-членный или 6-членный гетероарил, необязательно замещенный одним или более заместителями Q; в определенных вариантах осуществления R7a представляет собой гетероциклил, например, 5-членный или 6-членный гетероциклил, необязательно замещенный одним или более заместителями Q; в определенных вариантах осуществления R7a представляет собой фенил, имидазолил, пиразолил, пиридинил, пиперидинил или пиперазинил, причем каждый необязательно замещен одним или более заместителями Q; в определенных вариантах осуществления R7a представляет собой фенил, имидазолил, пиразолил, пиридинил, пиримидинил, пирролидинил, пиперидинил или пиперазинил, причем каждый необязательно замещен одним или более заместителями Q; в определенных вариантах осуществления R7a представляет собой фенил, 2-фторфенил, 2-хлорфенил, 2-бромфенил, 2-метилфенил, 2-метоксифенил, 3-фторфенил, 3-хлорфенил, 3-метоксифенил, 4-фторфенил, 4-хлорфенил, 4-бромфенил, 4-метоксифенил, имидазол-1-ил, пиразол-4-ил, 1-метилпиразол-4-ил, 2-метилпиразол-3-ил, пиридин-2-ил, пиридин-3-ил, пиридин-4-ил, 2-метилпиридин-4-ил, 2-метоксипиридин-4-ил, 1-метилпиперидин-4-ил или 4-метилпиперазин-1-ил; и в определенных вариантах осуществления R7a представляет собой фенил, 2-фторфенил, 2-хлорфенил, 2-бромфенил, 2-метилфенил, 2-(3-диметиламинопропил)фенил, 2-метоксифенил, 3-фторфенил, 3-хлорфенил, 3-метилфенил, 3-метоксифенил, 4-фторфенил, 4-хлорфенил, 4-бромфенил, 4-метоксифенил, 2,4-дифторфенил, 2,6-дифторфенил, 4-фтор-3-метоксифенил, 3-метоксифенил, 4-метоксифенил, 3-морфолин-4-илметилфенил, имидазол-1-ил, пиразол-4-ил, 1-метилпиразол-4-ил, 2-метилпиразол-3-ил, пиридин-2-ил, пиридин-3-ил, пиридин-4-ил, 2-фторпиридин-3-ил, 2-метилпиридин-4-ил, 2-(4-метилпиперазин-1-ил)пиридин-4-ил, 2-метоксипиридин-4-ил, пиримидин-5-ил, пирролидин-3-ил, 1-метилпирролидин-3-ил, пиперидин-4-ил, 1-метилпиперидин-4-ил, 1-этилпиперидин-4-ил, 1-изопропилпиперидин-4-ил, 1-ацетилпиперидин-4-ил, 1-метилсульфонилпиперидин-4-ил или 4-метилпиперазин-1-ил.
В одном варианте осуществления в формуле X, Xa или Xb
R1 представляет собой водород или -OR1a, где R1a представляет собой C1-6 алкил, необязательно замещенный одним или более заместителями Q;
R2 представляет собой водород;
R3 и R4 представляют собой водород;
R6 представляет собой C6-14 алкил, необязательно замещенный одним или более заместителями Q;
каждый R5a и R5b независимо представляет собой водород, галоген, C1-6 алкил, необязательно замещенный одним или более заместителями Q;
каждый R5d и R5e независимо представляет собой C6-14 алкил, необязательно замещенный одним или более заместителями Q;
R7a представляет собой C6-14 арил, гетероарил или гетероциклил, каждый из которых необязательно замещен одним или более заместителями Q; и
R7b, R7c, R7d и R7e представляют собой водород.
В другом варианте осуществления в формуле X, Xa или Xb
R1 представляет собой водород или метокси;
R2 представляет собой водород;
R3 и R4 представляют собой водород;
R6 представляет собой C6-14 алкил, необязательно замещенный одним или более галогенами;
R5a и R5b представляют собой водород;
каждый R5d и R5e независимо представляет собой C6-14 алкил;
R7a представляет собой C6-14 арил, гетероарил или гетероциклил, каждый из которых необязательно замещен одним или более заместителями Q; и
R7b, R7c, R7d и R7e представляют собой водород.
В еще одном варианте осуществления в формуле X, Xa или Xb
R1 представляет собой водород или метокси;
R2 представляет собой водород;
R3 и R4 представляют собой водород;
R6 представляет собой дифторметил;
R5a и R5b представляют собой водород;
R5d и R5e представляют собой метил;
R7a представляет собой C6-14 арил, моноциклический гетероарил или моноциклический гетероциклил, каждый из которых необязательно замещен одним или более заместителями Q; и
R7b, R7c, R7d и R7e представляют собой водород.
В еще одном варианте осуществления в формуле X, Xa или Xb
R1 представляет собой водород или метокси;
R2 представляет собой водород;
R3 и R4 представляют собой водород;
R6 представляет собой дифторметил;
R5a и R5b представляют собой водород;
R5d и R5e представляют собой метил;
R7a представляет собой фенил, 5- или 6-членный гетероарил или 5- или 6-членный гетероциклил, каждый из которых необязательно замещен одним или более заместителями Q; и
R7b, R7c, R7d и R7e представляют собой водород.
В еще одном варианте осуществления в формуле X, Xa или Xb
R1 представляет собой водород или метокси;
R2 представляет собой водород;
R3 и R4 представляют собой водород;
R6 представляет собой дифторметил;
R5a и R5b представляют собой водород;
R5d и R5e представляют собой метил;
R7a представляет собой фенил, имидазолил, пиразолил, пиридинил, пиримидинил, пирролидинил, пиперидинил или пиперазинил, каждый из которых необязательно замещен одним или более заместителями Q; и
R7b, R7c, R7d и R7e представляют собой водород.
В еще одном варианте осуществления в формуле X, Xa или Xb
R1 представляет собой водород или метокси;
R2 представляет собой водород;
R3 и R4 представляют собой водород;
R6 представляет собой дифторметил;
R5a и R5b представляют собой водород;
R5d и R5e представляют собой метил;
R7a представляет собой фенил, имидазолил, пиразолил, пиридинил, пиперидинил или пиперазинил, каждый из которых необязательно замещен одним или более заместителями Q; и
R7b, R7c, R7d и R7e представляют собой водород.
В еще одном варианте осуществления настоящее изобретение относится к соединению формулы XI:
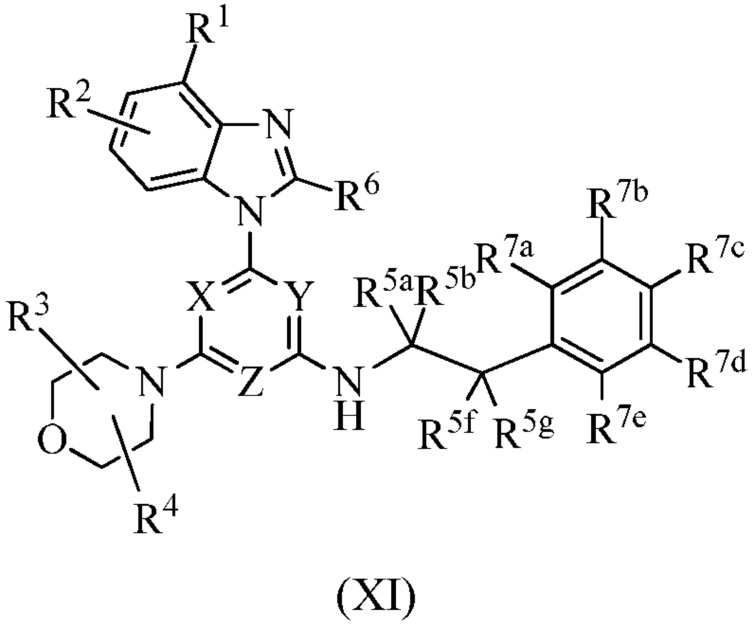
или его энантиомеру, смеси энантиомеров, смеси двух или более диастереомеров или изотопному варианту; или их фармацевтически приемлемой соли, сольвату, гидрату или пролекарству, где:
каждый R7a, R7b, R7c, R7d и R7e независимо представляет собой (a) водород, циано, галоген или нитро; (b) C1-6 алкил, C2-6 алкенил, C2-6 алкинил, C3-10 циклоалкил, C6-14 арил, C7-15 аралкил, гетероарил или гетероциклил, каждый из которых необязательно замещен одним или более заместителями Q; или (c) -C(O)R1a, -C(O)OR1a, -C(O)NR1bR1c, -C(NR1a)NR1bR1c, -OR1a, -OC(O)R1a, -OC(O)OR1a, -OC(O)NR1bR1c, -OC(=NR1a)NR1bR1c, -OS(O)R1a, -OS(O)2R1a, -OS(O)NR1bR1c, -OS(O)2NR1bR1c, -NR1bR1c, -NR1aC(O)R1d, -NR1aC(O)OR1d, -NR1aC(O)NR1bR1c, -NR1aC(=NR1d)NR1bR1c, -NR1aS(O)R1d, -NR1aS(O)2R1d, -NR1aS(O)NR1bR1c, -NR1aS(O)2NR1bR1c, -SR1a, -S(O)R1a, -S(O)2R1a, -S(O)NR1bR1c или -S(O)2NR1bR1c;
два из R7a, R7b, R7c, R7d и R7e, которые находятся рядом друг с другом, образуют C3-10 циклоалкенил, C6-14 арил, гетероарил или гетероциклил, причем каждый необязательно замещен одним или более заместителями Q; и
каждый R1, R2, R3, R4, R6, R1a, R1b, R1c, R1d, R5a, R5b, R5f, R5g, X, Y и Z представляет собой, как определено в настоящем изобретении.
В одном варианте осуществления соединение формулы XI имеет структуру формулы XIa:
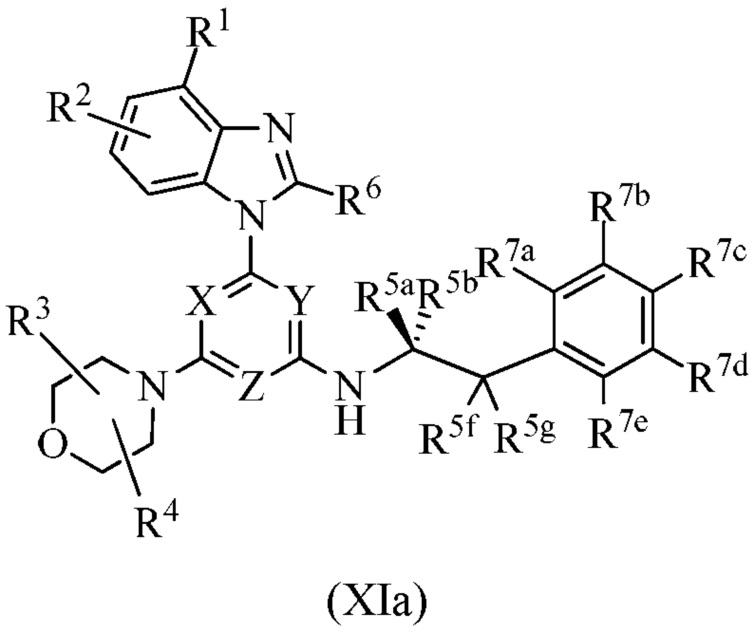
или его изотопный вариант; или их фармацевтически приемлемую соль, сольват, гидрат или пролекарство; где каждый R1, R2, R3, R4, R6, R5a, R5b, R5f, R5g, R7a, R7b, R7c, R7d, R7e, X, Y и Z представляет собой, как определено в настоящем изобретении.
В другом варианте осуществления соединение формулы XI имеет структуру формулы XIb:
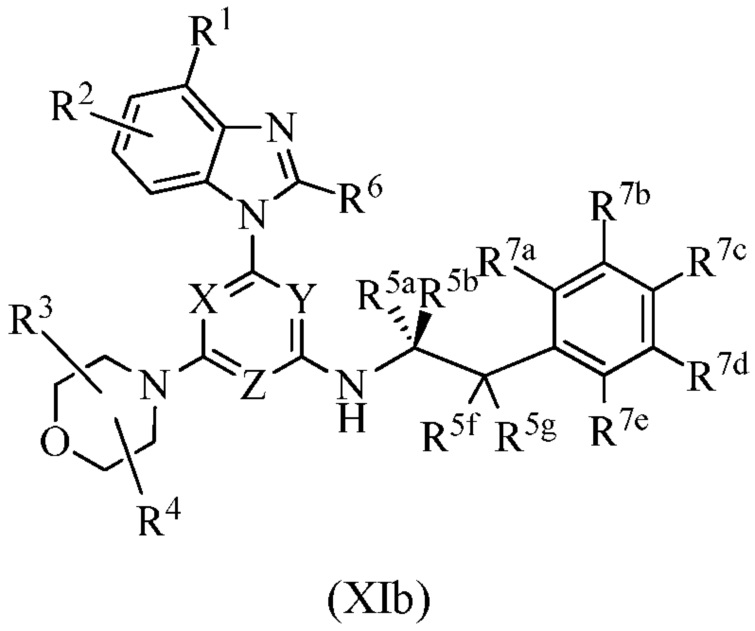
или его изотопный вариант; или их фармацевтически приемлемую соль, сольват, гидрат или пролекарство; где каждый R1, R2, R3, R4, R6, R5a, R5b, R5f, R5g, R7a, R7b, R7c, R7d, R7e, X, Y и Z представляет собой, как определено в настоящем изобретении.
В одном варианте осуществления настоящее изобретение относится к соединению формулы XI, XIa или XIb, как описано в настоящем изобретении, или его энантиомеру, смеси энантиомеров, смеси двух или более диастереомеров или изотопному варианту; или их фармацевтически приемлемой соли, сольвату, гидрату или пролекарству; где каждый R5a и R5b независимо представляет собой (a) галоген; (b) C1-6 алкил, C2-6 алкенил, C2-6 алкинил, C3-10 циклоалкил, C6-14 арил, C7-15 аралкил, гетероарил или гетероциклил; или (c) -C(O)R1a, -C(O)OR1a, -C(O)NR1bR1c, -C(NR1a)NR1bR1c, -OR1a, -OC(O)R1a, -OC(O)OR1a, -OC(O)NR1bR1c, -OC(=NR1a)NR1bR1c, -OS(O)R1a, -OS(O)2R1a, -OS(O)NR1bR1c, -OS(O)2NR1bR1c, -NR1bR1c, -NR1aC(O)R1d, -NR1aC(O)OR1d, -NR1aC(O)NR1bR1c, -NR1aC(=NR1d)NR1bR1c, -NR1aS(O)R1d, -NR1aS(O)2R1d, -NR1aS(O)NR1bR1c, -NR1aS(O)2NR1bR1c, -SR1a, -S(O)R1a, -S(O)2R1a, -S(O)NR1bR1c или -S(O)2NR1bR1c; и R1, R2, R3, R4, R5f, R5g, R6, R7a, R7b, R7c, R7d, R7e, X, Y, Z, R1a, R1b, R1c и R1d определяют в настоящем изобретении выше.
В формуле XI, XIa, или XIb в определенных вариантах осуществления один из R7a, R7b, R7c, R7d и R7e представляет собой C6-14 арил, гетероарил или гетероциклил, каждый из которых необязательно замещен одним или более заместителями Q; в определенных вариантах осуществления один из R7a, R7b, R7c, R7d, и R7e представляет собой C6-14 арил, например, фенил, необязательно замещенный одним или более заместителями Q; в определенных вариантах осуществления один из R7a, R7b, R7c, R7d и R7e представляет собой гетероарил, например, 5-членный или 6-членный гетероарил, необязательно замещенный одним или более заместителями Q; в определенных вариантах осуществления один из R7a, R7b, R7c, R7d и R7e представляет собой гетероциклил, например, 5-членный или 6-членный гетероциклил, необязательно замещенный одним или более заместителями Q; в определенных вариантах осуществления один из R7a, R7b, R7c, R7d и R7e представляет собой фенил, имидазолил, пиразолил, пиридинил, пиперидинил или пиперазинил, причем каждый необязательно замещен одним или более заместителями Q; в определенных вариантах осуществления один из R7a, R7b, R7c, R7d и R7e представляет собой фенил, имидазолил, пиразолил, пиридинил, пиримидинил, пирролидинил, пиперидинил или пиперазинил, причем каждый необязательно замещен одним или более заместителями Q; в определенных вариантах осуществления один из R7a, R7b, R7c, R7d и R7e представляет собой фенил, 2-фторфенил, 2-хлорфенил, 2-бромфенил, 2-метилфенил, 2-метоксифенил, 3-фторфенил, 3-хлорфенил, 3-метоксифенил, 4-фторфенил, 4-хлорфенил, 4-бромфенил, 4-метоксифенил, имидазол-1-ил, пиразол-4-ил, 1-метилпиразол-4-ил, 2-метилпиразол-3-ил, пиридин-2-ил, пиридин-3-ил, пиридин-4-ил, 2-метилпиридин-4-ил, 2-метоксипиридин-4-ил, 1-метилпиперидин-4-ил или 4-метилпиперазин-1-ил; и в определенных вариантах осуществления один из R7a, R7b, R7c, R7d и R7e представляет собой фенил, 2-фторфенил, 2-хлорфенил, 2-бромфенил, 2-метилфенил, 2-(3-диметиламинопропил)фенил, 2-метоксифенил, 3-фторфенил, 3-хлорфенил, 3-метилфенил, 3-метоксифенил, 4-фторфенил, 4-хлорфенил, 4-бромфенил, 4-метоксифенил, 2,4-дифторфенил, 2,6-дифторфенил, 4-фтор-3-метоксифенил, 3-метоксифенил, 4-метоксифенил, 3-морфолин-4-илметилфенил, имидазол-1-ил, пиразол-4-ил, 1-метилпиразол-4-ил, 2-метилпиразол-3-ил, пиридин-2-ил, пиридин-3-ил, пиридин-4-ил, 2-фторпиридин-3-ил, 2-метилпиридин-4-ил, 2-(4-метилпиперазин-1-ил)пиридин-4-ил, 2-метоксипиридин-4-ил, пиримидин-5-ил, пирролидин-3-ил, 1-метилпирролидин-3-ил, пиперидин-4-ил, 1-метилпиперидин-4-ил, 1-этилпиперидин-4-ил, 1-изопропилпиперидин-4-ил, 1-ацетилпиперидин-4-ил, 1-метилсульфонилпиперидин-4-ил или 4-метилпиперазин-1-ил.
В формуле XI, XIa или XIb в определенных вариантах осуществления R7a представляет собой C6-14 арил, гетероарил или гетероциклил, каждый из которых необязательно замещен одним или более заместителями Q; в определенных вариантах осуществления R7a представляет собой C6-14 арил, например, фенил, необязательно замещенный одним или более заместителями Q; в определенных вариантах осуществления R7a представляет собой гетероарил, например, 5-членный или 6-членный гетероарил, необязательно замещенный одним или более заместителями Q; в определенных вариантах осуществления R7a представляет собой гетероциклил, например, 5-членный или 6-членный гетероциклил, необязательно замещенный одним или более заместителями Q; в определенных вариантах осуществления R7a представляет собой фенил, имидазолил, пиразолил, пиридинил, пиперидинил или пиперазинил, причем каждый необязательно замещен одним или более заместителями Q; в определенных вариантах осуществления R7a представляет собой фенил, имидазолил, пиразолил, пиридинил, пиримидинил, пирролидинил, пиперидинил или пиперазинил, причем каждый необязательно замещен одним или более заместителями Q; в определенных вариантах осуществления R7a представляет собой фенил, 2-фторфенил, 2-хлорфенил, 2-бромфенил, 2-метилфенил, 2-метоксифенил, 3-фторфенил, 3-хлорфенил, 3-метоксифенил, 4-фторфенил, 4-хлорфенил, 4-бромфенил, 4-метоксифенил, имидазол-1-ил, пиразол-4-ил, 1-метилпиразол-4-ил, 2-метилпиразол-3-ил, пиридин-2-ил, пиридин-3-ил, пиридин-4-ил, 2-метилпиридин-4-ил, 2-метоксипиридин-4-ил, 1-метилпиперидин-4-ил или 4-метилпиперазин-1-ил; и в определенных вариантах осуществления R7a представляет собой фенил, 2-фторфенил, 2-хлорфенил, 2-бромфенил, 2-метилфенил, 2-(3-диметиламинопропил)фенил, 2-метоксифенил, 3-фторфенил, 3-хлорфенил, 3-метилфенил, 3-метоксифенил, 4-фторфенил, 4-хлорфенил, 4-бромфенил, 4-метоксифенил, 2,4-дифторфенил, 2,6-дифторфенил, 4-фтор-3-метоксифенил, 3-метоксифенил, 4-метоксифенил, 3-морфолин-4-илметилфенил, имидазол-1-ил, пиразол-4-ил, 1-метилпиразол-4-ил, 2-метилпиразол-3-ил, пиридин-2-ил, пиридин-3-ил, пиридин-4-ил, 2-фторпиридин-3-ил, 2-метилпиридин-4-ил, 2-(4-метилпиперазин-1-ил)пиридин-4-ил, 2-метоксипиридин-4-ил, пиримидин-5-ил, пирролидин-3-ил, 1-метилпирролидин-3-ил, пиперидин-4-ил, 1-метилпиперидин-4-ил, 1-этилпиперидин-4-ил, 1-изопропилпиперидин-4-ил, 1-ацетилпиперидин-4-ил, 1-метилсульфонилпиперидин-4-ил или 4-метилпиперазин-1-ил.
В одном варианте осуществления в формуле XI, XIa или XIb
R1 представляет собой водород или -OR1a, когда R1a представляет собой C1-6 алкил, необязательно замещенный одним или более заместителями Q;
R2 представляет собой водород;
R3 и R4 представляют собой водород;
R6 представляет собой C6-14 алкил, необязательно замещенный одним или более заместителями Q;
каждый R5a и R5b независимо представляет собой C6-14 алкил, необязательно замещенный одним или более заместителями Q;
каждый R5f и R5g независимо представляет собой водород, галоген, C1-6 алкил, необязательно замещенный одним или более заместителями Q; или R5f и R5g вместе с атомом углерода, с которым они соединены, образуют C1-10 циклоалкил или гетероциклил, каждый из которых необязательно замещен одним или более заместителями Q;
R7a представляет собой C6-14 арил, гетероарил или гетероциклил, каждый из которых необязательно замещен одним или более заместителями Q;
R7b, R7c, R7d и R7e представляют собой водород; и
каждый X, Y и Z независимо представляет собой N или CRx, при условии, что по меньшей мере два из X, Y и Z представляют собой N; где Rx представляет собой водород или C1-6 алкил, необязательно замещенный одним или более заместителями Q.
В другом варианте осуществления в формуле XI, XIa или XIb
R1 представляет собой водород или метокси;
R2 представляет собой водород;
R3 и R4 представляют собой водород;
R6 представляет собой C6-14 алкил, необязательно замещенный одним или более галогенами;
каждый R5a и R5b независимо представляет собой C6-14 алкил;
каждый R5f и R5g независимо представляет собой водород или C1-6 алкил; или R5f и R5g вместе с атомом углерода, с которым они соединены, образуют C1-10 циклоалкил;
R7a представляет собой C6-14 арил, гетероарил или гетероциклил, каждый из которых необязательно замещен одним или более заместителями Q;
R7b, R7c, R7d и R7e представляют собой водород; и
каждый X, Y и Z независимо представляет собой N или CH.
В еще одном варианте осуществления в формуле XI, XIa или XIb
R1 представляет собой водород или метокси;
R2 представляет собой водород;
R3 и R4 представляют собой водород;
R6 представляет собой дифторметил;
R5a и R5b представляют собой метил;
R5f и R5g представляют собой водород; или R5f и R5g вместе с атомом углерода, с которым они соединены, образуют циклопропил, циклобутил, циклопентил или циклогексил;
R7a представляет собой C6-14 арил, моноциклический гетероарил или моноциклический гетероциклил, каждый из которых необязательно замещен одним или более заместителями Q;
R7b, R7c, R7d и R7e представляют собой водород; и
каждый X, Y и Z независимо представляет собой N или CH.
В еще одном варианте осуществления в формуле XI, XIa или XIb
R1 представляет собой водород или метокси;
R2 представляет собой водород;
R3 и R4 представляют собой водород;
R6 представляет собой дифторметил;
R5a и R5b представляют собой метил;
R5f и R5g представляют собой водород; или R5f и R5g вместе с атомом углерода, с которым они соединены, образуют циклопропил, циклобутил, циклопентил или циклогексил;
R7a представляет собой фенил, 5- или 6-членный гетероарил или 5- или 6-членный гетероциклил, каждый из которых необязательно замещен одним или более заместителями Q;
R7b, R7c, R7d и R7e представляют собой водород; и
каждый X, Y и Z независимо представляет собой N или CH.
В еще одном варианте осуществления в формуле XI, XIa или XIb
R1 представляет собой водород или метокси;
R2 представляет собой водород;
R3 и R4 представляют собой водород;
R6 представляет собой дифторметил;
R5a и R5b представляют собой метил;
R5f и R5g представляют собой водород; или R5f и R5g вместе с атомом углерода, с которым они соединены, образуют циклопропил, циклобутил, циклопентил или циклогексил;
R7a представляет собой фенил, имидазолил, пиразолил, пиридинил, пиримидинил, пирролидинил, пиперидинил или пиперазинил, каждый из которых необязательно замещен одним или более заместителями Q;
R7b, R7c, R7d и R7e представляют собой водород; и
каждый X, Y и Z независимо представляет собой N или CH.
В еще одном варианте осуществления в формуле XI, XIa или XIb
R1 представляет собой водород или метокси;
R2 представляет собой водород;
R3 и R4 представляют собой водород;
R6 представляет собой дифторметил;
R5a и R5b представляют собой метил;
R5f и R5g представляют собой водород; или R5f и R5g вместе с атомом углерода, с которым они соединены, образуют циклопропил, циклобутил, циклопентил или циклогексил;
R7a представляет собой фенил, имидазолил, пиразолил, пиридинил, пиперидинил или пиперазинил, каждый из которых необязательно замещен одним или более заместителями Q;
R7b, R7c, R7d и R7e представляют собой водород; и
каждый X, Y и Z независимо представляет собой N или CH.
В еще одном варианте осуществления настоящее изобретение относится к соединению формулы XII:
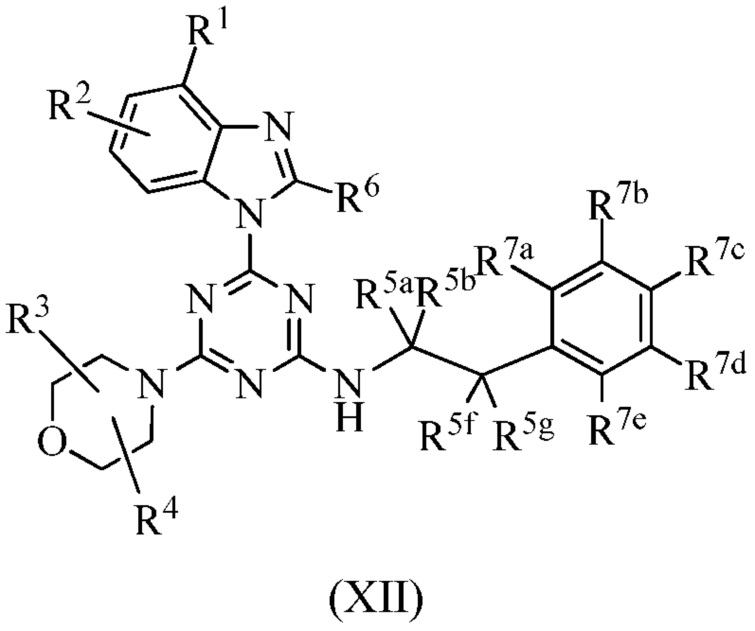
или его энантиомеру, смеси энантиомеров, смеси двух или более диастереомеров или изотопному варианту; или их фармацевтически приемлемой соли, сольвату, гидрату или пролекарству; где каждый R1, R2, R3, R4, R6, R5a, R5b, R5f, R5g, R7a, R7b, R7c, R7d и R7e представляет собой, как определено в настоящем изобретении.
В одном варианте осуществления соединение формулы XII имеет структуру формулы XIIa:
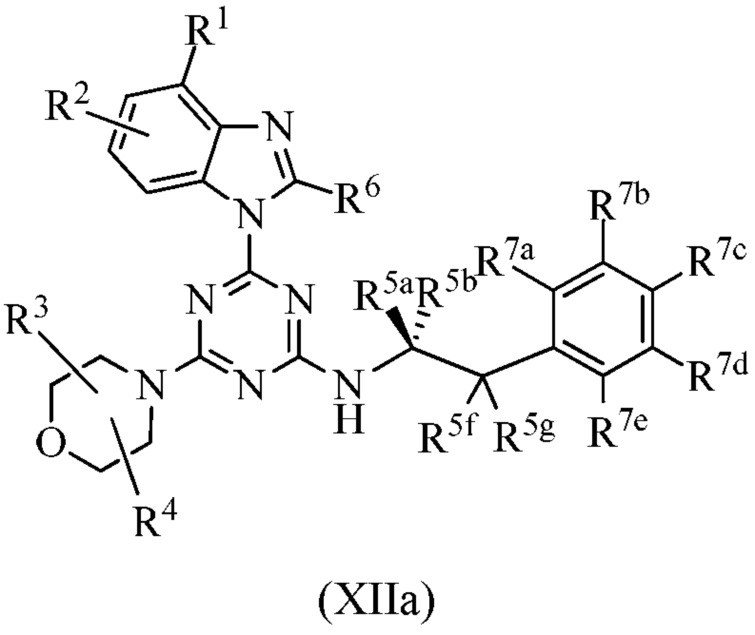
или его изотопный вариант; или их фармацевтически приемлемую соль, сольват, гидрат или пролекарство; где каждый R1, R2, R3, R4, R6, R5a, R5b, R5f, R5g, R7a, R7b, R7c, R7d и R7e представляет собой, как определено в настоящем изобретении.
В другом варианте осуществления соединение формулы XII имеет структуру формулы XIIb:
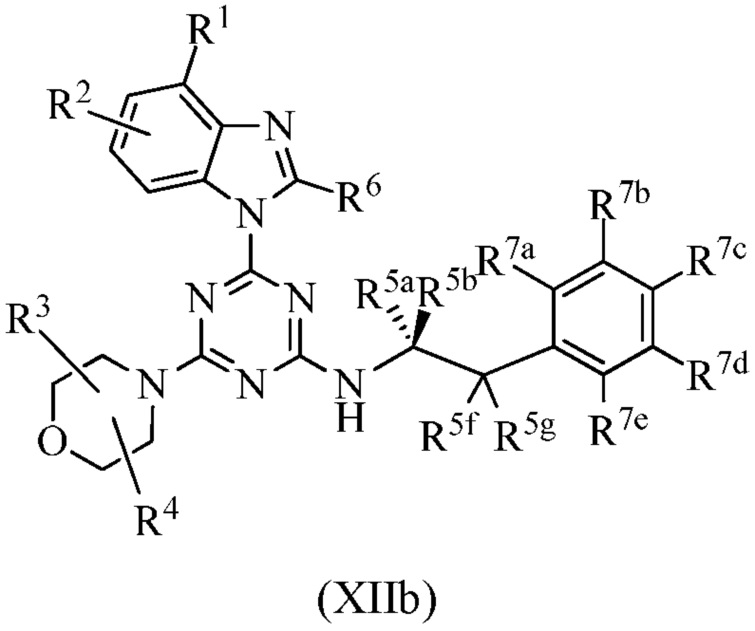
или его изотопный вариант; или их фармацевтически приемлемую соль, сольват, гидрат или пролекарство; где каждый R1, R2, R3, R4, R6, R5a, R5b, R5f, R5g, R7a, R7b, R7c, R7d и R7e представляет собой, как определено в настоящем изобретении.
В одном варианте осуществления настоящее изобретение относится к соединению формулы XII, XIIa или XIIb, как описано в настоящем изобретении, или его энантиомеру, смеси энантиомеров, смеси двух или более диастереомеров или изотопному варианту; или их фармацевтически приемлемой соли, сольвату, гидрату или пролекарству; где каждый R5a и R5b независимо представляет собой (a) галоген; (b) C1-6 алкил, C2-6 алкенил, C2-6 алкинил, C3-10 циклоалкил, C6-14 арил, C7-15 аралкил, гетероарил или гетероциклил; или (c) -C(O)R1a, -C(O)OR1a, -C(O)NR1bR1c, -C(NR1a)NR1bR1c, -OR1a, -OC(O)R1a, -OC(O)OR1a, -OC(O)NR1bR1c, -OC(=NR1a)NR1bR1c, -OS(O)R1a, -OS(O)2R1a, -OS(O)NR1bR1c, -OS(O)2NR1bR1c, -NR1bR1c, -NR1aC(O)R1d, -NR1aC(O)OR1d, -NR1aC(O)NR1bR1c, -NR1aC(=NR1d)NR1bR1c, -NR1aS(O)R1d, -NR1aS(O)2R1d, -NR1aS(O)NR1bR1c, -NR1aS(O)2NR1bR1c, -SR1a, -S(O)R1a, -S(O)2R1a, -S(O)NR1bR1c или -S(O)2NR1bR1c; и R1, R2, R3, R4, R5f, R5g, R6, R7a, R7b, R7c, R7d, R7e, R1a, R1b, R1c и R1d определяют в настоящем изобретении выше.
В формуле XII, XIIa или XIIb в определенных вариантах осуществления один из R7a, R7b, R7c, R7d и R7e представляет собой C6-14 арил, гетероарил или гетероциклил, каждый из которых необязательно замещен одним или более заместителями Q; в определенных вариантах осуществления один из R7a, R7b, R7c, R7d и R7e представляет собой C6-14 арил, например, фенил, необязательно замещенный одним или более заместителями Q; в определенных вариантах осуществления один из R7a, R7b, R7c, R7d и R7e представляет собой гетероарил, например, 5-членный или 6-членный гетероарил, необязательно замещенный одним или более заместителями Q; в определенных вариантах осуществления один из R7a, R7b, R7c, R7d и R7e представляет собой гетероциклил, например, 5-членный или 6-членный гетероциклил, необязательно замещенный одним или более заместителями Q; в определенных вариантах осуществления один из R7a, R7b, R7c, R7d и R7e представляет собой фенил, имидазолил, пиразолил, пиридинил, пиперидинил или пиперазинил, причем каждый необязательно замещен одним или более заместителями Q; в определенных вариантах осуществления один из R7a, R7b, R7c, R7d и R7e представляет собой фенил, имидазолил, пиразолил, пиридинил, пиримидинил, пирролидинил, пиперидинил или пиперазинил, причем каждый необязательно замещен одним или более заместителями Q; в определенных вариантах осуществления один из R7a, R7b, R7c, R7d и R7e представляет собой фенил, 2-фторфенил, 2-хлорфенил, 2-бромфенил, 2-метилфенил, 2-метоксифенил, 3-фторфенил, 3-хлорфенил, 3-метоксифенил, 4-фторфенил, 4-хлорфенил, 4-бромфенил, 4-метоксифенил, имидазол-1-ил, пиразол-4-ил, 1-метилпиразол-4-ил, 2-метилпиразол-3-ил, пиридин-2-ил, пиридин-3-ил, пиридин-4-ил, 2-метилпиридин-4-ил, 2-метоксипиридин-4-ил, 1-метилпиперидин-4-ил или 4-метилпиперазин-1-ил; и в определенных вариантах осуществления один из R7a, R7b, R7c, R7d, и R7e представляет собой фенил, 2-фторфенил, 2-хлорфенил, 2-бромфенил, 2-метилфенил, 2-(3-диметиламинопропил)фенил, 2-метоксифенил, 3-фторфенил, 3-хлорфенил, 3-метилфенил, 3-метоксифенил, 4-фторфенил, 4-хлорфенил, 4-бромфенил, 4-метоксифенил, 2,4-дифторфенил, 2,6-дифторфенил, 4-фтор-3-метоксифенил, 3-метоксифенил, 4-метоксифенил, 3-морфолин-4-илметилфенил, имидазол-1-ил, пиразол-4-ил, 1-метилпиразол-4-ил, 2-метилпиразол-3-ил, пиридин-2-ил, пиридин-3-ил, пиридин-4-ил, 2-фторпиридин-3-ил, 2-метилпиридин-4-ил, 2-(4-метилпиперазин-1-ил)пиридин-4-ил, 2-метоксипиридин-4-ил, пиримидин-5-ил, пирролидин-3-ил, 1-метилпирролидин-3-ил, пиперидин-4-ил, 1-метилпиперидин-4-ил, 1-этилпиперидин-4-ил, 1-изопропилпиперидин-4-ил, 1-ацетилпиперидин-4-ил, 1-метилсульфонилпиперидин-4-ил или 4-метилпиперазин-1-ил.
В формуле XII, XIIa или XIIb в определенных вариантах осуществления R7a представляет собой C6-14 арил, гетероарил или гетероциклил, каждый из которых необязательно замещен одним или более заместителями Q; в определенных вариантах осуществления R7a представляет собой C6-14 арил, например, фенил, необязательно замещенный одним или более заместителями Q; в определенных вариантах осуществления R7a представляет собой гетероарил, например, 5-членный или 6-членный гетероарил, необязательно замещенный одним или более заместителями Q; в определенных вариантах осуществления R7a представляет собой гетероциклил, например, 5-членный или 6-членный гетероциклил, необязательно замещенный одним или более заместителями Q; в определенных вариантах осуществления R7a представляет собой фенил, имидазолил, пиразолил, пиридинил, пиперидинил или пиперазинил, причем каждый необязательно замещен одним или более заместителями Q; в определенных вариантах осуществления R7a представляет собой фенил, имидазолил, пиразолил, пиридинил, пиримидинил, пирролидинил, пиперидинил или пиперазинил, причем каждый необязательно замещен одним или более заместителями Q; в определенных вариантах осуществления R7a представляет собой фенил, 2-фторфенил, 2-хлорфенил, 2-бромфенил, 2-метилфенил, 2-метоксифенил, 3-фторфенил, 3-хлорфенил, 3-метоксифенил, 4-фторфенил, 4-хлорфенил, 4-бромфенил, 4-метоксифенил, имидазол-1-ил, пиразол-4-ил, 1-метилпиразол-4-ил, 2-метилпиразол-3-ил, пиридин-2-ил, пиридин-3-ил, пиридин-4-ил, 2-метилпиридин-4-ил, 2-метоксипиридин-4-ил, 1-метилпиперидин-4-ил или 4-метилпиперазин-1-ил; и в определенных вариантах осуществления один из R7a, R7b, R7c, R7d и R7e представляет собой фенил, 2-фторфенил, 2-хлорфенил, 2-бромфенил, 2-метилфенил, 2-(3-диметиламинопропил)фенил, 2-метоксифенил, 3-фторфенил, 3-хлорфенил, 3-метилфенил, 3-метоксифенил, 4-фторфенил, 4-хлорфенил, 4-бромфенил, 4-метоксифенил, 2,4-дифторфенил, 2,6-дифторфенил, 4-фтор-3-метоксифенил, 3-метоксифенил, 4-метоксифенил, 3-морфолин-4-илметилфенил, имидазол-1-ил, пиразол-4-ил, 1-метилпиразол-4-ил, 2-метилпиразол-3-ил, пиридин-2-ил, пиридин-3-ил, пиридин-4-ил, 2-фторпиридин-3-ил, 2-метилпиридин-4-ил, 2-(4-метилпиперазин-1-ил)пиридин-4-ил, 2-метоксипиридин-4-ил, пиримидин-5-ил, пирролидин-3-ил, 1-метилпирролидин-3-ил, пиперидин-4-ил, 1-метилпиперидин-4-ил, 1-этилпиперидин-4-ил, 1-изопропилпиперидин-4-ил, 1-ацетилпиперидин-4-ил, 1-метилсульфонилпиперидин-4-ил или 4-метилпиперазин-1-ил.
В одном варианте осуществления в формуле XII, XIIa или XIIb
R1 представляет собой водород или -OR1a, где R1a представляет собой C1-6 алкил, необязательно замещенный одним или более заместителями Q;
R2 представляет собой водород;
R3 и R4 представляют собой водород;
R6 представляет собой C6-14 алкил, необязательно замещенный одним или более заместителями Q;
каждый R5a и R5b независимо представляет собой C6-14 алкил, необязательно замещенный одним или более заместителями Q;
каждый R5f и R5g независимо представляет собой водород, галоген, C1-6 алкил, необязательно замещенный одним или более заместителями Q; или R5f и R5g вместе с атомом углерода, с которым они соединены, образуют C1-10 циклоалкил или гетероциклил, каждый из которых необязательно замещен одним или более заместителями Q;
R7a представляет собой C6-14 арил, гетероарил или гетероциклил, каждый из которых необязательно замещен одним или более заместителями Q; и
R7b, R7c, R7d и R7e представляют собой водород.
В другом варианте осуществления в формуле XII, XIIa или XIIb
R1 представляет собой водород или метокси;
R2 представляет собой водород;
R3 и R4 представляют собой водород;
R6 представляет собой C6-14 алкил, необязательно замещенный одним или более галогенами;
каждый R5a и R5b независимо представляет собой C6-14 алкил;
каждый R5f и R5g независимо представляет собой водород или C1-6 алкил; или R5f и R5g вместе с атомом углерода, с которым они соединены, образуют C1-10 циклоалкил;
R7a представляет собой C6-14 арил, гетероарил или гетероциклил, каждый из которых необязательно замещен одним или более заместителями Q; и
R7b, R7c, R7d и R7e представляют собой водород.
В еще одном варианте осуществления в формуле XII, XIIa или XIIb
R1 представляет собой водород или метокси;
R2 представляет собой водород;
R3 и R4 представляют собой водород;
R6 представляет собой дифторметил;
R5a и R5b представляют собой метил;
R5f и R5g представляют собой водород; или R5f и R5g вместе с атомом углерода, с которым они соединены, образуют циклопропил, циклобутил, циклопентил или циклогексил;
R7a представляет собой C6-14 арил, моноциклический гетероарил или моноциклический гетероциклил, каждый из которых необязательно замещен одним или более заместителями Q; и
R7b, R7c, R7d и R7e представляют собой водород.
В еще одном варианте осуществления в формуле XII, XIIa или XIIb
R1 представляет собой водород или метокси;
R2 представляет собой водород;
R3 и R4 представляют собой водород;
R6 представляет собой дифторметил;
R5a и R5b представляют собой метил;
R5f и R5g представляют собой водород; или R5f и R5g вместе с атомом углерода, с которым они соединены, образуют циклопропил, циклобутил, циклопентил или циклогексил;
R7a представляет собой фенил, 5- или 6-членный гетероарил или 5- или 6-членный гетероциклил, каждый из которых необязательно замещен одним или более заместителями Q; и
R7b, R7c, R7d и R7e представляют собой водород.
В еще одном варианте осуществления в формуле XII, XIIa или XIIb
R1 представляет собой водород или метокси;
R2 представляет собой водород;
R3 и R4 представляют собой водород;
R6 представляет собой дифторметил;
R5a и R5b представляют собой метил;
R5f и R5g представляют собой водород; или R5f и R5g вместе с атомом углерода, с которым они соединены, образуют циклопропил, циклобутил, циклопентил или циклогексил;
R7a представляет собой фенил, имидазолил, пиразолил, пиридинил, пиримидинил, пирролидинил, пиперидинил или пиперазинил, каждый из которых необязательно замещен одним или более заместителями Q; и
R7b, R7c, R7d и R7e представляют собой водород.
В еще одном варианте осуществления в формуле XII, XIIa или XIIb
R1 представляет собой водород или метокси;
R2 представляет собой водород;
R3 и R4 представляют собой водород;
R6 представляет собой дифторметил;
R5a и R5b представляют собой метил;
R5f и R5g представляют собой водород; или R5f и R5g вместе с атомом углерода, с которым они соединены, образуют циклопропил, циклобутил, циклопентил или циклогексил;
R7a представляет собой фенил, имидазолил, пиразолил, пиридинил, пиперидинил или пиперазинил, каждый из которых необязательно замещен одним или более заместителями Q; и
R7b, R7c, R7d и R7e представляют собой водород.
В еще одном варианте осуществления настоящее изобретение относится к соединению формулы XIII:
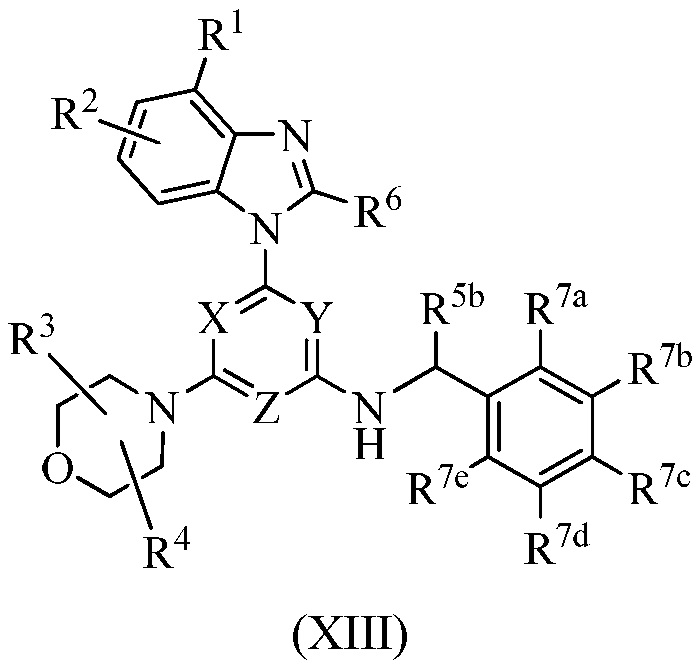
или его энантиомеру, смеси энантиомеров, смеси двух или более диастереомеров или изотопному варианту; или их фармацевтически приемлемой соли, сольвату, гидрату или пролекарству; где каждый R1, R2, R3, R4, R6, R5b, R7a, R7b, R7c, R7d, R7e, X, Y и Z представляет собой, как определено в настоящем изобретении.
В одном варианте осуществления соединение формулы XIII имеет структуру формулы XIIIa:
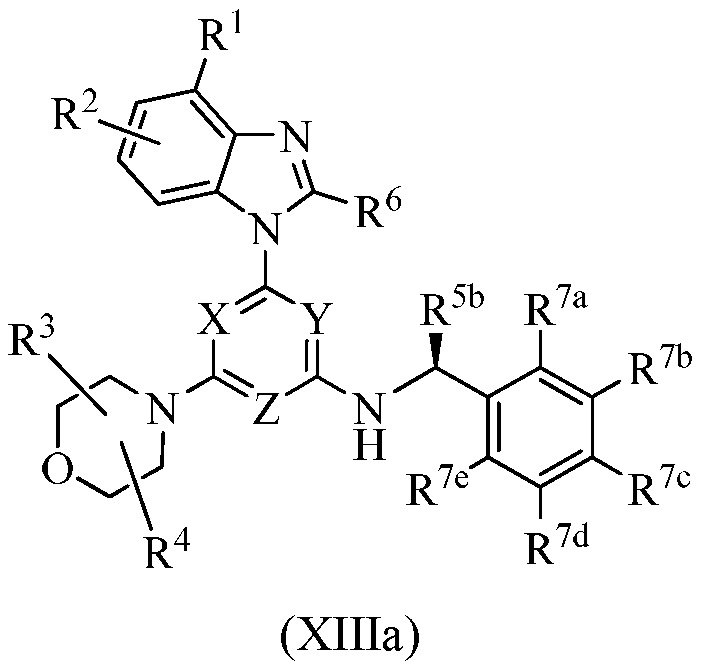
или его изотопный вариант; или их фармацевтически приемлемую соль, сольват, гидрат или пролекарство; где каждый R1, R2, R3, R4, R6, R5b, R7a, R7b, R7c, R7d, R7e, X, Y и Z представляет собой, как определено в настоящем изобретении.
В другом варианте осуществления соединение формулы XIII имеет структуру формулы XIIIb:
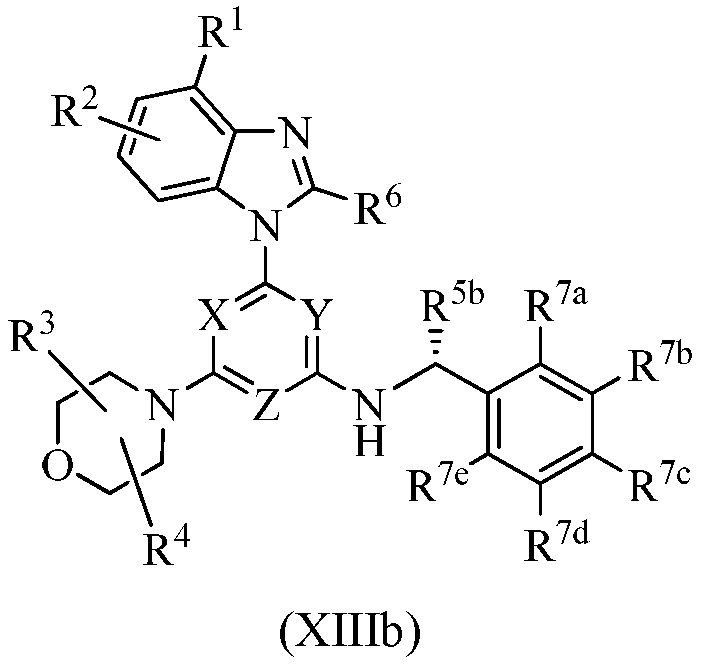
или его изотопный вариант; или их фармацевтически приемлемую соль, сольват, гидрат или пролекарство; где каждый R1, R2, R3, R4, R6, R5b, R7a, R7b, R7c, R7d, R7e, X, Y и Z представляет собой, как определено в настоящем изобретении.
В еще одном варианте осуществления настоящее изобретение относится к соединению формулы XIV:
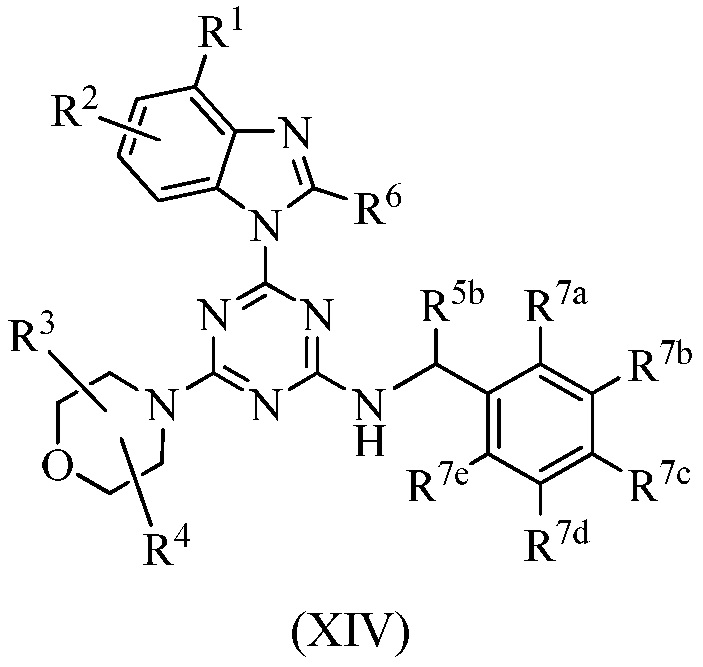
или его энантиомеру, смеси энантиомеров, смеси двух или более диастереомеров или изотопному варианту; или их фармацевтически приемлемой соли, сольвату, гидрату или пролекарству; где каждый R1, R2, R3, R4, R6, R5b, R7a, R7b, R7c, R7d и R7e представляет собой, как определено в настоящем изобретении.
В одном варианте осуществления соединение формулы XIV имеет структуру формулы XIVa:
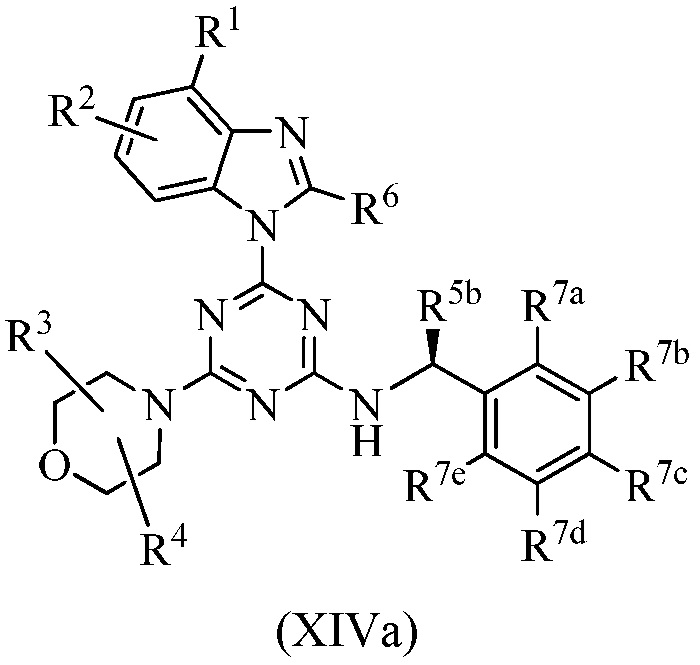
или его изотопный вариант; или их фармацевтически приемлемую соль, сольват, гидрат или пролекарство; где каждый R1, R2, R3, R4, R6, R5b, R7a, R7b, R7c, R7d и R7e представляет собой, как определено в настоящем изобретении.
В другом варианте осуществления соединение формулы XIV имеет структуру формулы XIVb:
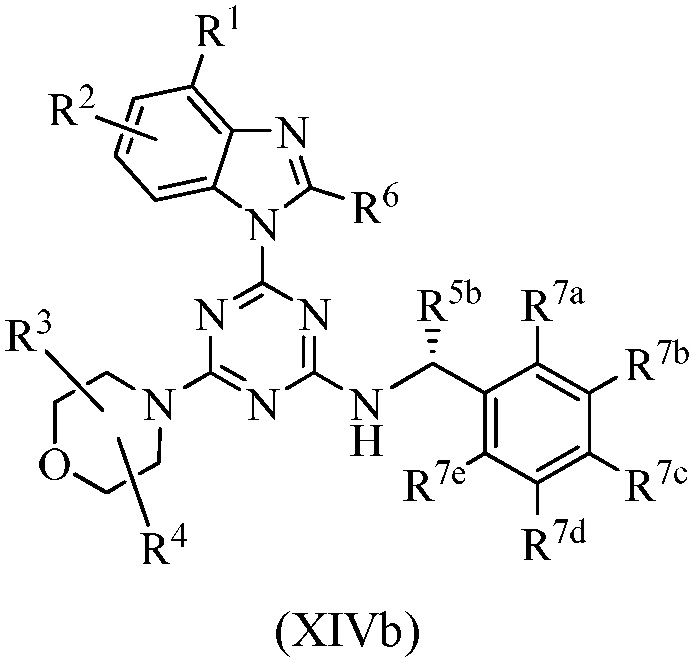
или его изотопный вариант; или их фармацевтически приемлемую соль, сольват, гидрат или пролекарство; где каждый R1, R2, R3, R4, R6, R5b, R7a, R7b, R7c, R7d и R7e представляет собой, как определено в настоящем изобретении.
В еще одном варианте осуществления настоящее изобретение относится к соединению формулы XV:
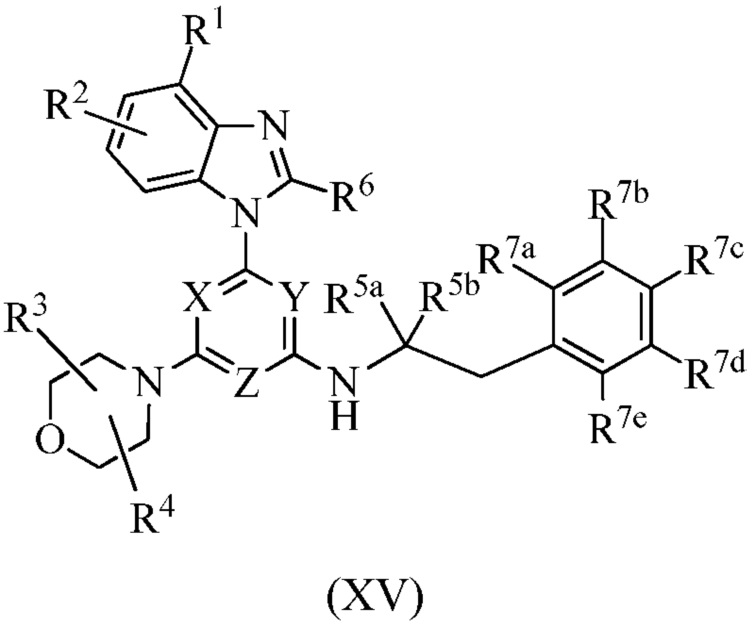
или его энантиомеру, смеси энантиомеров, смеси двух или более диастереомеров или изотопному варианту; или их фармацевтически приемлемой соли, сольвату, гидрату или пролекарству; где каждый R1, R2, R3, R4, R6, R5a, R5b, R7a, R7b, R7c, R7d, R7e, X, Y и Z представляет собой, как определено в настоящем изобретении.
В одном варианте осуществления в формуле XV один из R7a, R7b, R7c, R7d и R7e представляет собой C6-14 арил, гетероарил или гетероциклил, каждый из которых необязательно замещен одним или более заместителями Q; и каждый R1, R2, R3, R4, R6, R5a, R5b, осавшиеся R7a, R7b, R7c, R7d, и R7e, X, Y и Z представляет собой, как определено в настоящем изобретении.
В другом варианте осуществления в формуле XV один из R7a, R7b, R7c, R7d и R7e представляет собой C6-14 арил, который необязательно замещен одним или более заместителями Q; и каждый R1, R2, R3, R4, R6, R5a, R5b, оставшиеся R7a, R7b, R7c, R7d и R7e, X, Y и Z представляет собой, как определено в настоящем изобретении.
В еще одном варианте осуществления в формуле XV один из R7a, R7b, R7c, R7d и R7e представляет собой гетероарил, который необязательно замещен одним или более заместителями Q; и каждый R1, R2, R3, R4, R6, R5a, R5b, оставшиеся R7a, R7b, R7c, R7d и R7e, X, Y и Z представляет собой, как определено в настоящем изобретении.
В еще одном варианте осуществления в формуле XV один из R7a, R7b, R7c, R7d и R7e представляет собой 5-членный или 6-членный гетероарил, который необязательно замещен одним или более заместителями Q; и каждый R1, R2, R3, R4, R6, R5a, R5b, оставшиеся R7a, R7b, R7c, R7d и R7e, X, Y и Z представляет собой, как определено в настоящем изобретении.
В еще одном варианте осуществления в формуле XV один из R7a, R7b, R7c, R7d и R7e представляет собой гетероциклил, который необязательно замещен одним или более заместителями Q; и каждый R1, R2, R3, R4, R6, R5a, R5b, оставшиеся R7a, R7b, R7c, R7d и R7e, X, Y и Z представляет собой, как определено в настоящем изобретении.
В еще одном варианте осуществления в формуле XV один из R7a, R7b, R7c, R7d и R7e представляет собой 5-членный или 6-членный гетероциклил, который необязательно замещен одним или более заместителями Q; и каждый R1, R2, R3, R4, R6, R5a, R5b, оставшиеся R7a, R7b, R7c, R7d и R7e, X, Y и Z представляет собой, как определено в настоящем изобретении.
В еще одном варианте осуществления в формуле XV один из R7a, R7b, R7c, R7d и R7e представляет собой фенил, имидазолил, пиразолил, пиридинил, пиперидинил или пиперазинил, причем каждый необязательно замещен одним или более заместителями Q; и каждый R1, R2, R3, R4, R6, R5a, R5b, оставшиеся R7a, R7b, R7c, R7d и R7e, X, Y и Z представляет собой, как определено в настоящем изобретении.
В еще одном варианте осуществления в формуле XV один из R7a, R7b, R7c, R7d и R7e представляет собой фенил, имидазолил, пиразолил, пиридинил, пиримидинил, пирролидинил, пиперидинил или пиперазинил, причем каждый необязательно замещен одним или более заместителями Q; и каждый R1, R2, R3, R4, R6, R5a, R5b, оставшиеся R7a, R7b, R7c, R7d и R7e, X, Y и Z представляет собой, как определено в настоящем изобретении.
В еще одном варианте осуществления в формуле XV один из R7a, R7b, R7c, R7d и R7e представляет собой фенил, 2-фторфенил, 2-хлорфенил, 2-бромфенил, 2-метилфенил, 2-(3-диметиламинопропил)фенил, 2-метоксифенил, 3-фторфенил, 3-хлорфенил, 3-метилфенил, 3-метоксифенил, 4-фторфенил, 4-хлорфенил, 4-бромфенил, 4-метоксифенил, 2,4-дифторфенил, 2,6-дифторфенил, 4-фтор-3-метоксифенил, 3-метоксифенил, 4-метоксифенил, 3-морфолин-4-илметилфенил, имидазол-1-ил, пиразол-4-ил, 1-метилпиразол-4-ил, 2-метилпиразол-3-ил, пиридин-2-ил, пиридин-3-ил, пиридин-4-ил, 2-фторпиридин-3-ил, 2-метилпиридин-4-ил, 2-(4-метилпиперазин-1-ил)пиридин-4-ил, 2-метоксипиридин-4-ил, пиримидин-5-ил, пирролидин-3-ил, 1-метилпирролидин-3-ил, пиперидин-4-ил, 1-метилпиперидин-4-ил, 1-этилпиперидин-4-ил, 1-изопропилпиперидин-4-ил, 1-ацетилпиперидин-4-ил, 1-метилсульфонилпиперидин-4-ил или 4-метилпиперазин-1-ил.
В еще одном варианте осуществления в формуле XV один из R7a, R7b, R7c, R7d и R7e представляет собой фенил, 2-фторфенил, 2-хлорфенил, 2-бромфенил, 2-метилфенил, 2-метоксифенил, 3-фторфенил, 3-хлорфенил, 3-метоксифенил, 4-фторфенил, 4-хлорфенил, 4-бромфенил, 4-метоксифенил, имидазол-1-ил, пиразол-4-ил, 1-метилпиразол-4-ил, 2-метилпиразол-3-ил, пиридин-2-ил, пиридин-3-ил, пиридин-4-ил, 2-метилпиридин-4-ил, 2-метоксипиридин-4-ил, 1-метилпиперидин-4-ил или 4-метилпиперазин-1-ил; и каждый R1, R2, R3, R4, R6, R5a, R5b, оставшиеся R7a, R7b, R7c, R7d и R7e, X, Y и Z представляет собой, как определено в настоящем изобретении.
В одном варианте осуществления в формуле XV R7a представляет собой C6-14 арил, гетероарил или гетероциклил, каждый из которых необязательно замещен одним или более заместителями Q; и каждый R1, R2, R3, R4, R6, R5a, R5b, R7b, R7c, R7d, R7e, X, Y и Z представляет собой, как определено в настоящем изобретении.
В другом варианте осуществления в формуле XV R7a представляет собой C6-14 арил, который необязательно замещен одним или более заместителями Q; и каждый R1, R2, R3, R4, R6, R5a, R5b, R7b, R7c, R7d, R7e, X, Y и Z представляет собой, как определено в настоящем изобретении.
В еще одном варианте осуществления в формуле XV R7a представляет собой гетероарил, который необязательно замещен одним или более заместителями Q; и каждый R1, R2, R3, R4, R6, R5a, R5b, R7b, R7c, R7d, R7e, X, Y и Z представляет собой, как определено в настоящем изобретении.
В еще одном варианте осуществления в формуле XV R7a представляет собой 5-членный или 6-членный гетероарил, который необязательно замещен одним или более заместителями Q; и каждый R1, R2, R3, R4, R6, R5a, R5b, R7b, R7c, R7d, R7e, X, Y и Z представляет собой, как определено в настоящем изобретении.
В еще одном варианте осуществления в формуле XV R7a представляет собой гетероциклил, который необязательно замещен одним или более заместителями Q; и каждый R1, R2, R3, R4, R6, R5a, R5b, R7b, R7c, R7d, R7e, X, Y и Z представляет собой, как определено в настоящем изобретении.
В еще одном варианте осуществления в формуле XV R7a представляет собой 5-членный или 6-членный гетероциклил, который необязательно замещен одним или более заместителями Q; и каждый R1, R2, R3, R4, R6, R5a, R5b, R7b, R7c, R7d, R7e, X, Y и Z представляет собой, как определено в настоящем изобретении.
В еще одном варианте осуществления в формуле XV R7a представляет собой фенил, имидазолил, пиразолил, пиридинил, пиразолил, пиперидинил или пиперазинил, причем каждый необязательно замещен одним или более заместителями Q; и каждый R1, R2, R3, R4, R6, R5a, R5b, R7b, R7c, R7d, R7e, X, Y и Z представляет собой, как определено в настоящем изобретении.
В еще одном варианте осуществления в формуле XV R7a представляет собой фенил, имидазолил, пиразолил, пиридинил, пиримидинил, пирролидинил, пиперидинил или пиперазинил, причем каждый необязательно замещен одним или более заместителями Q; и каждый R1, R2, R3, R4, R6, R5a, R5b, R7b, R7c, R7d, R7e, X, Y и Z представляет собой, как определено в настоящем изобретении.
В еще одном варианте осуществления в формуле XV R7a представляет собой фенил, 2-фторфенил, 2-хлорфенил, 2-бромфенил, 2-метилфенил, 2-(3-диметиламинопропил)фенил, 2-метоксифенил, 3-фторфенил, 3-хлорфенил, 3-метилфенил, 3-метоксифенил, 4-фторфенил, 4-хлорфенил, 4-бромфенил, 4-метоксифенил, 2,4-дифторфенил, 2,6-дифторфенил, 4-фтор-3-метоксифенил, 3-метоксифенил, 4-метоксифенил, 3-морфолин-4-илметилфенил, имидазол-1-ил, пиразол-4-ил, 1-метилпиразол-4-ил, 2-метилпиразол-3-ил, пиридин-2-ил, пиридин-3-ил, пиридин-4-ил, 2-фторпиридин-3-ил, 2-метилпиридин-4-ил, 2-(4-метилпиперазин-1-ил)пиридин-4-ил, 2-метоксипиридин-4-ил, пиримидин-5-ил, пирролидин-3-ил, 1-метилпирролидин-3-ил, пиперидин-4-ил, 1-метилпиперидин-4-ил, 1-этилпиперидин-4-ил, 1-изопропилпиперидин-4-ил, 1-ацетилпиперидин-4-ил, 1-метилсульфонилпиперидин-4-ил или 4-метилпиперазин-1-ил.
В еще одном варианте осуществления в формуле XV R7a представляет собой фенил, 2-фторфенил, 2-хлорфенил, 2-бромфенил, 2-метилфенил, 2-метоксифенил, 3-фторфенил, 3-хлорфенил, 3-метоксифенил, 4-фторфенил, 4-хлорфенил, 4-бромфенил, 4-метоксифенил, имидазол-1-ил, пиразол-4-ил, 1-метилпиразол-4-ил, 2-метилпиразол-3-ил, пиридин-2-ил, пиридин-3-ил, пиридин-4-ил, 2-метилпиридин-4-ил, 2-метоксипиридин-4-ил, 1-метилпиперидин-4-ил или 4-метилпиперазин-1-ил; и каждый R1, R2, R3, R4, R6, R5a, R5b, R7b, R7c, R7d, R7e, X, Y и Z представляет собой, как определено в настоящем изобретении.
В одном варианте осуществления в формуле XV
R1 представляет собой водород или -OR1a, где R1a представляет собой C1-6 алкил, необязательно замещенный одним или более заместителями Q;
R2 представляет собой водород;
R3 и R4 представляют собой водород;
R6 представляет собой C6-14 алкил, необязательно замещенный одним или более заместителями Q;
каждый R5a и R5b независимо представляет собой C6-14 алкил, необязательно замещенный одним или более заместителями Q;
R7a представляет собой C6-14 арил, гетероарил или гетероциклил, каждый из которых необязательно замещен одним или более заместителями Q;
R7b, R7c, R7d и R7e представляют собой водород; и
каждый X, Y и Z независимо представляет собой N или CRx, при условии, что по меньшей мере два из X, Y и Z представляют собой N; где Rx представляет собой водород или C1-6 алкил, необязательно замещенный одним или более заместителями Q.
В другом варианте осуществления в формуле XV
R1 представляет собой водород или метокси;
R2 представляет собой водород;
R3 и R4 представляют собой водород;
R6 представляет собой C6-14 алкил, необязательно замещенный одним или более галогенами;
каждый R5a и R5b независимо представляет собой C6-14 алкил;
R7a представляет собой C6-14 арил, гетероарил или гетероциклил, каждый из которых необязательно замещен одним или более заместителями Q;
R7b, R7c, R7d и R7e представляют собой водород; и
каждый X, Y и Z независимо представляет собой N или CH.
В еще одном варианте осуществления в формуле XV
R1 представляет собой водород или метокси;
R2 представляет собой водород;
R3 и R4 представляют собой водород;
R6 представляет собой дифторметил;
R5a и R5b представляют собой метил;
R7a представляет собой C6-14 арил, моноциклический гетероарил или моноциклический гетероциклил, каждый из которых необязательно замещен одним или более заместителями Q;
R7b, R7c, R7d и R7e представляют собой водород; и
каждый X, Y и Z независимо представляет собой N или CH.
В еще одном варианте осуществления в формуле XV
R1 представляет собой водород или метокси;
R2 представляет собой водород;
R3 и R4 представляют собой водород;
R6 представляет собой дифторметил;
R5a и R5b представляют собой метил;
R7a представляет собой фенил, 5- или 6-членный гетероарил или 5- или 6-членный гетероциклил, каждый из которых необязательно замещен одним или более заместителями Q;
R7b, R7c, R7d и R7e представляют собой водород; и
каждый X, Y и Z независимо представляет собой N или CH.
В еще одном варианте осуществления в формуле XV
R1 представляет собой водород или метокси;
R2 представляет собой водород;
R3 и R4 представляют собой водород;
R6 представляет собой дифторметил;
R5a и R5b представляют собой метил;
R7a представляет собой фенил, имидазолил, пиразолил, пиридинил, пиримидинил, пирролидинил, пиперидинил или пиперазинил, каждый из которых необязательно замещен одним или более заместителями Q;
R7b, R7c, R7d и R7e представляют собой водород; и
каждый X, Y и Z независимо представляет собой N или CH.
В еще одном варианте осуществления в формуле XV
R1 представляет собой водород или метокси;
R2 представляет собой водород;
R3 и R4 представляют собой водород;
R6 представляет собой дифторметил;
R5a и R5b представляют собой метил;
R7a представляет собой фенил, имидазолил, пиразолил, пиридинил, пиперидинил или пиперазинил, каждый из которых необязательно замещен одним или более заместителями Q;
R7b, R7c, R7d и R7e представляют собой водород; и
каждый X, Y и Z независимо представляет собой N или CH.
В одном варианте осуществления соединение формулы XV имеет структуру формулы XVa:
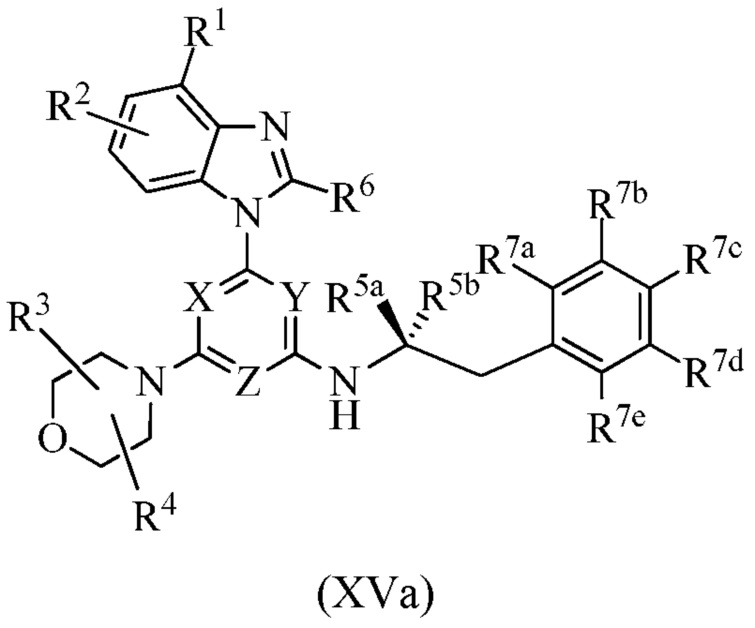
или его изотопный вариант; или их фармацевтически приемлемую соль, сольват, гидрат или пролекарство; где каждый R1, R2, R3, R4, R6, R5a, R5b, R7a, R7b, R7c, R7d, R7e, X, Y и Z представляет собой, как определено в настоящем изобретении.
В одном варианте осуществления в формуле XVa один из R7a, R7b, R7c, R7d и R7e представляет собой C6-14 арил, гетероарил или гетероциклил, каждый из которых необязательно замещен одним или более заместителями Q; и каждый R1, R2, R3, R4, R6, R5a, R5b, оставшиеся R7a, R7b, R7c, R7d, и R7e, X, Y и Z представляет собой, как определено в настоящем изобретении.
В другом варианте осуществления в формуле XVa один из R7a, R7b, R7c, R7d и R7e представляет собой C6-14 арил, который необязательно замещен одним или более заместителями Q; и каждый R1, R2, R3, R4, R6, R5a, R5b, оставшиеся R7a, R7b, R7c, R7d и R7e, X, Y и Z представляет собой, как определено в настоящем изобретении.
В еще одном варианте осуществления в формуле XVa один из R7a, R7b, R7c, R7d и R7e представляет собой гетероарил, который необязательно замещен одним или более заместителями Q; и каждый R1, R2, R3, R4, R6, R5a, R5b, оставшиеся R7a, R7b, R7c, R7d и R7e, X, Y и Z представляет собой, как определено в настоящем изобретении.
В еще одном варианте осуществления в формуле XVa один из R7a, R7b, R7c, R7d и R7e представляет собой 5-членный или 6-членный гетероарил, который необязательно замещен одним или более заместителями Q; и каждый R1, R2, R3, R4, R6, R5a, R5b, оставшиеся R7a, R7b, R7c, R7d и R7e, X, Y и Z представляет собой, как определено в настоящем изобретении.
В еще одном варианте осуществления в формуле XVa один из R7a, R7b, R7c, R7d и R7e представляет собой гетероциклил, который необязательно замещен одним или более заместителями Q; и каждый R1, R2, R3, R4, R6, R5a, R5b, оставшиеся R7a, R7b, R7c, R7d и R7e, X, Y и Z представляет собой, как определено в настоящем изобретении.
В еще одном варианте осуществления в формуле XVa один из R7a, R7b, R7c, R7d и R7e представляет собой 5-членный или 6-членный гетероциклил, который необязательно замещен одним или более заместителями Q; и каждый R1, R2, R3, R4, R6, R5a, R5b, оставшиеся R7a, R7b, R7c, R7d и R7e, X, Y и Z представляет собой, как определено в настоящем изобретении.
В еще одном варианте осуществления в формуле XVa один из R7a, R7b, R7c, R7d и R7e представляет собой фенил, имидазолил, пиразолил, пиридинил, пиперидинил или пиперазинил, причем каждый необязательно замещен одним или более заместителями Q; и каждый R1, R2, R3, R4, R6, R5a, R5b, оставшиеся R7a, R7b, R7c, R7d и R7e, X, Y и Z представляет собой, как определено в настоящем изобретении.
В еще одном варианте осуществления в формуле XVa один из R7a, R7b, R7c, R7d и R7e представляет собой фенил, имидазолил, пиразолил, пиридинил, пиримидинил, пирролидинил, пиперидинил или пиперазинил, причем каждый необязательно замещен одним или более заместителями Q; и каждый R1, R2, R3, R4, R6, R5a, R5b, оставшиеся R7a, R7b, R7c, R7d и R7e, X, Y и Z представляет собой, как определено в настоящем изобретении.
В еще одном варианте осуществления в формуле XVa один из R7a, R7b, R7c, R7d и R7e представляет собой фенил, 2-фторфенил, 2-хлорфенил, 2-бромфенил, 2-метилфенил, 2-(3-диметиламинопропил)фенил, 2-метоксифенил, 3-фторфенил, 3-хлорфенил, 3-метилфенил, 3-метоксифенил, 4-фторфенил, 4-хлорфенил, 4-бромфенил, 4-метоксифенил, 2,4-дифторфенил, 2,6-дифторфенил, 4-фтор-3-метоксифенил, 3-метоксифенил, 4-метоксифенил, 3-морфолин-4-илметилфенил, имидазол-1-ил, пиразол-4-ил, 1-метилпиразол-4-ил, 2-метилпиразол-3-ил, пиридин-2-ил, пиридин-3-ил, пиридин-4-ил, 2-фторпиридин-3-ил, 2-метилпиридин-4-ил, 2-(4-метилпиперазин-1-ил)пиридин-4-ил, 2-метоксипиридин-4-ил, пиримидин-5-ил, пирролидин-3-ил, 1-метилпирролидин-3-ил, пиперидин-4-ил, 1-метилпиперидин-4-ил, 1-этилпиперидин-4-ил, 1-изопропилпиперидин-4-ил, 1-ацетилпиперидин-4-ил, 1-метилсульфонилпиперидин-4-ил или 4-метилпиперазин-1-ил.
В еще одном варианте осуществления в формуле XVa один из R7a, R7b, R7c, R7d и R7e представляет собой фенил, 2-фторфенил, 2-хлорфенил, 2-бромфенил, 2-метилфенил, 2-метоксифенил, 3-фторфенил, 3-хлорфенил, 3-метоксифенил, 4-фторфенил, 4-хлорфенил, 4-бромфенил, 4-метоксифенил, имидазол-1-ил, пиразол-4-ил, 1-метилпиразол-4-ил, 2-метилпиразол-3-ил, пиридин-2-ил, пиридин-3-ил, пиридин-4-ил, 2-метилпиридин-4-ил, 2-метоксипиридин-4-ил, 1-метилпиперидин-4-ил или 4-метилпиперазин-1-ил; и каждый R1, R2, R3, R4, R6, R5a, R5b, оставшиеся R7a, R7b, R7c, R7d и R7e, X, Y и Z представляет собой, как определено в настоящем изобретении.
В одном варианте осуществления в формуле XVa R7a представляет собой C6-14 арил, гетероарил или гетероциклил, каждый из которых необязательно замещен одним или более заместителями Q; и каждый R1, R2, R3, R4, R6, R5a, R5b, R7b, R7c, R7d, R7e, X, Y и Z представляет собой, как определено в настоящем изобретении.
В другом варианте осуществления в формуле XVa R7a представляет собой C6-14 арил, который необязательно замещен одним или более заместителями Q; и каждый R1, R2, R3, R4, R6, R5a, R5b, R7b, R7c, R7d, R7e, X, Y и Z представляет собой, как определено в настоящем изобретении.
В еще одном варианте осуществления в формуле XVa R7a представляет собой гетероарил, который необязательно замещен одним или более заместителями Q; и каждый R1, R2, R3, R4, R6, R5a, R5b, R7b, R7c, R7d, R7e, X, Y и Z представляет собой, как определено в настоящем изобретении.
В еще одном варианте осуществления в формуле XVa R7a представляет собой 5-членный или 6-членный гетероарил, который необязательно замещен одним или более заместителями Q; и каждый R1, R2, R3, R4, R6, R5a, R5b, R7b, R7c, R7d, R7e, X, Y и Z представляет собой, как определено в настоящем изобретении.
В еще одном варианте осуществления в формуле XVa R7a представляет собой гетероциклил, который необязательно замещен одним или более заместителями Q; и каждый R1, R2, R3, R4, R6, R5a, R5b, R7b, R7c, R7d, R7e, X, Y и Z представляет собой, как определено в настоящем изобретении.
В еще одном варианте осуществления в формуле XVa R7a представляет собой 5-членный или 6-членный гетероциклил, который необязательно замещен одним или более заместителями Q; и каждый R1, R2, R3, R4, R6, R5a, R5b, R7b, R7c, R7d, R7e, X, Y и Z представляет собой, как определено в настоящем изобретении.
В еще одном варианте осуществления в формуле XVa R7a представляет собой фенил, имидазолил, пиразолил, пиридинил, пиперидинил или пиперазинил, причем каждый необязательно замещен одним или более заместителями Q; и каждый R1, R2, R3, R4, R6, R5a, R5b, R7b, R7c, R7d, R7e, X, Y и Z представляет собой, как определено в настоящем изобретении.
В еще одном варианте осуществления в формуле XVa R7a представляет собой фенил, имидазолил, пиразолил, пиридинил, пиримидинил, пирролидинил, пиперидинил или пиперазинил, причем каждый необязательно замещен одним или более заместителями Q; и каждый R1, R2, R3, R4, R6, R5a, R5b, R7b, R7c, R7d, R7e, X, Y и Z представляет собой, как определено в настоящем изобретении.
В еще одном варианте осуществления в формуле XVa R7a представляет собой фенил, 2-фторфенил, 2-хлорфенил, 2-бромфенил, 2-метилфенил, 2-(3-диметиламинопропил)фенил, 2-метоксифенил, 3-фторфенил, 3-хлорфенил, 3-метилфенил, 3-метоксифенил, 4-фторфенил, 4-хлорфенил, 4-бромфенил, 4-метоксифенил, 2,4-дифторфенил, 2,6-дифторфенил, 4-фтор-3-метоксифенил, 3-метоксифенил, 4-метоксифенил, 3-морфолин-4-илметилфенил, имидазол-1-ил, пиразол-4-ил, 1-метилпиразол-4-ил, 2-метилпиразол-3-ил, пиридин-2-ил, пиридин-3-ил, пиридин-4-ил, 2-фторпиридин-3-ил, 2-метилпиридин-4-ил, 2-(4-метилпиперазин-1-ил)пиридин-4-ил, 2-метоксипиридин-4-ил, пиримидин-5-ил, пирролидин-3-ил, 1-метилпирролидин-3-ил, пиперидин-4-ил, 1-метилпиперидин-4-ил, 1-этилпиперидин-4-ил, 1-изопропилпиперидин-4-ил, 1-ацетилпиперидин-4-ил, 1-метилсульфонилпиперидин-4-ил или 4-метилпиперазин-1-ил.
В еще одном варианте осуществления в формуле XVa R7a представляет собой фенил, 2-фторфенил, 2-хлорфенил, 2-бромфенил, 2-метилфенил, 2-метоксифенил, 3-фторфенил, 3-хлорфенил, 3-метоксифенил, 4-фторфенил, 4-хлорфенил, 4-бромфенил, 4-метоксифенил, имидазол-1-ил, пиразол-4-ил, 1-метилпиразол-4-ил, 2-метилпиразол-3-ил, пиридин-2-ил, пиридин-3-ил, пиридин-4-ил, 2-метилпиридин-4-ил, 2-метоксипиридин-4-ил, 1-метилпиперидин-4-ил или 4-метилпиперазин-1-ил; и каждый R1, R2, R3, R4, R6, R5a, R5b, R7b, R7c, R7d, R7e, X, Y и Z представляет собой, как определено в настоящем изобретении.
В одном варианте осуществления в формуле XVa
R1 представляет собой водород или -OR1a, где R1a представляет собой C1-6 алкил, необязательно замещенный одним или более заместителями Q;
R2 представляет собой водород;
R3 и R4 представляют собой водород;
R6 представляет собой C6-14 алкил, необязательно замещенный одним или более заместителями Q;
каждый R5a и R5b независимо представляет собой водород или C6-14 алкил, необязательно замещенный одним или более заместителями Q;
R7a представляет собой C6-14 арил, гетероарил или гетероциклил, каждый из которых необязательно замещен одним или более заместителями Q;
R7b, R7c, R7d и R7e представляют собой водород; и
каждый X, Y и Z независимо представляет собой N или CRx, при условии, что по меньшей мере два из X, Y и Z представляют собой N; где Rx представляет собой водород или C1-6 алкил, необязательно замещенный одним или более заместителями Q.
В другом варианте осуществления в формуле XVa
R1 представляет собой водород или метокси;
R2 представляет собой водород;
R3 и R4 представляют собой водород;
R6 представляет собой C6-14 алкил, необязательно замещенный одним или более галогенами;
каждый R5a и R5b независимо представляет собой водород или C6-14 алкил;
R7a представляет собой C6-14 арил, гетероарил или гетероциклил, каждый из которых необязательно замещен одним или более заместителями Q;
R7b, R7c, R7d и R7e представляют собой водород; и
каждый X, Y и Z независимо представляет собой N или CH.
В еще одном варианте осуществления в формуле XVa
R1 представляет собой водород или метокси;
R2 представляет собой водород;
R3 и R4 представляют собой водород;
R6 представляет собой дифторметил;
каждый R5a и R5b независимо представляет собой водород или C6-14 алкил;
R7a представляет собой C6-14 арил, моноциклический гетероарил или моноциклический гетероциклил, каждый из которых необязательно замещен одним или более заместителями Q;
R7b, R7c, R7d и R7e представляют собой водород; и
каждый X, Y и Z независимо представляет собой N или CH.
В еще одном варианте осуществления в формуле XVa
R1 представляет собой водород или метокси;
R2 представляет собой водород;
R3 и R4 представляют собой водород;
R6 представляет собой дифторметил;
каждый R5a и R5b независимо представляет собой водород или C6-14 алкил;
R7a представляет собой фенил, 5- или 6-членный гетероарил или 5- или 6-членный гетероциклил, каждый из которых необязательно замещен одним или более заместителями Q;
R7b, R7c, R7d и R7e представляют собой водород; и
каждый X, Y и Z независимо представляет собой N или CH.
В еще одном варианте осуществления в формуле XVa
R1 представляет собой водород или метокси;
R2 представляет собой водород;
R3 и R4 представляют собой водород;
R6 представляет собой дифторметил;
каждый R5a и R5b независимо представляет собой водород или C6-14 алкил;
R7a представляет собой фенил, имидазолил, пиразолил, пиридинил, пиримидинил, пирролидинил, пиперидинил или пиперазинил, каждый из которых необязательно замещен одним или более заместителями Q;
R7b, R7c, R7d и R7e представляют собой водород; и
каждый X, Y и Z независимо представляет собой N или CH.
В еще одном варианте осуществления в формуле XVa
R1 представляет собой водород или метокси;
R2 представляет собой водород;
R3 и R4 представляют собой водород;
R6 представляет собой дифторметил;
каждый R5a и R5b независимо представляет собой водород или C6-14 алкил;
R7a представляет собой фенил, имидазолил, пиразолил, пиридинил, пиперидинил или пиперазинил, каждый из которых необязательно замещен одним или более заместителями Q;
R7b, R7c, R7d и R7e представляют собой водород; и
каждый X, Y и Z независимо представляет собой N или CH.
В другом варианте осуществления соединение формулы XV имеет структуру формулы XVb:
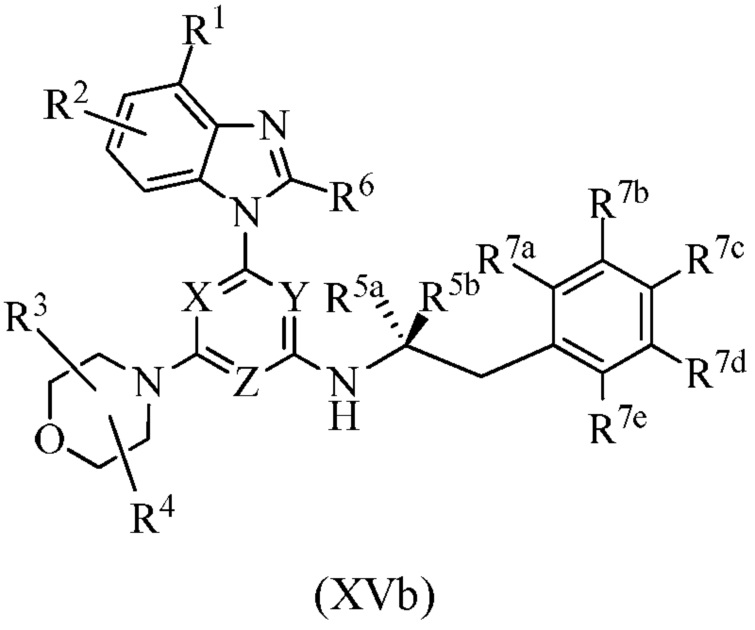
или его изотопный вариант; или их фармацевтически приемлемую соль, сольват, гидрат или пролекарство; где каждый R1, R2, R3, R4, R6, R5a, R5b, R7a, R7b, R7c, R7d, R7e, X, Y и Z представляет собой, как определено в настоящем изобретении.
В одном варианте осуществления в формуле XVb один из R7a, R7b, R7c, R7d и R7e представляет собой C6-14 арил, гетероарил или гетероциклил, каждый из которых необязательно замещен одним или более заместителями Q; и каждый R1, R2, R3, R4, R6, R5a, R5b, оставшиеся R7a, R7b, R7c, R7d и R7e, X, Y и Z представляет собой, как определено в настоящем изобретении.
В другом варианте осуществления в формуле XVb один из R7a, R7b, R7c, R7d и R7e представляет собой C6-14 арил, который необязательно замещен одним или более заместителями Q; и каждый R1, R2, R3, R4, R6, R5a, R5b, оставшиеся R7a, R7b, R7c, R7d и R7e, X, Y и Z представляет собой, как определено в настоящем изобретении.
В еще одном варианте осуществления в формуле XVb один из R7a, R7b, R7c, R7d и R7e представляет собой гетероарил, который необязательно замещен одним или более заместителями Q; и каждый R1, R2, R3, R4, R6, R5a, R5b, оставшиеся R7a, R7b, R7c, R7d и R7e, X, Y и Z представляет собой, как определено в настоящем изобретении.
В еще одном варианте осуществления в формуле XVb один из R7a, R7b, R7c, R7d и R7e представляет собой 5-членный или 6-членный гетероарил, который необязательно замещен одним или более заместителями Q; и каждый R1, R2, R3, R4, R6, R5a, R5b, оставшиеся R7a, R7b, R7c, R7d и R7e, X, Y и Z представляет собой, как определено в настоящем изобретении.
В еще одном варианте осуществления в формуле XVb один из R7a, R7b, R7c, R7d и R7e представляет собой гетероциклил, который необязательно замещен одним или более заместителями Q; и каждый R1, R2, R3, R4, R6, R5a, R5b, оставшиеся R7a, R7b, R7c, R7d и R7e, X, Y и Z представляет собой, как определено в настоящем изобретении.
В еще одном варианте осуществления в формуле XVb один из R7a, R7b, R7c, R7d и R7e представляет собой 5-членный или 6-членный гетероциклил, который необязательно замещен одним или более заместителями Q; и каждый R1, R2, R3, R4, R6, R5a, R5b, оставшиеся R7a, R7b, R7c, R7d и R7e, X, Y и Z представляет собой, как определено в настоящем изобретении.
В еще одном варианте осуществления в формуле XVb один из R7a, R7b, R7c, R7d и R7e представляет собой фенил, имидазолил, пиразолил, пиридинил, пиперидинил или пиперазинил, причем каждый необязательно замещен одним или более заместителями Q; и каждый R1, R2, R3, R4, R6, R5a, R5b, оставшиеся R7a, R7b, R7c, R7d и R7e, X, Y и Z представляет собой, как определено в настоящем изобретении.
В еще одном варианте осуществления в формуле XVb один из R7a, R7b, R7c, R7d и R7e представляет собой фенил, имидазолил, пиразолил, пиридинил, пиримидинил, пирролидинил, пиперидинил или пиперазинил, причем каждый необязательно замещен одним или более заместителями Q; и каждый R1, R2, R3, R4, R6, R5a, R5b, оставшиеся R7a, R7b, R7c, R7d и R7e, X, Y и Z представляет собой, как определено в настоящем изобретении.
В еще одном варианте осуществления в формуле XVb один из R7a, R7b, R7c, R7d и R7e представляет собой фенил, 2-фторфенил, 2-хлорфенил, 2-бромфенил, 2-метилфенил, 2-(3-диметиламинопропил)фенил, 2-метоксифенил, 3-фторфенил, 3-хлорфенил, 3-метилфенил, 3-метоксифенил, 4-фторфенил, 4-хлорфенил, 4-бромфенил, 4-метоксифенил, 2,4-дифторфенил, 2,6-дифторфенил, 4-фтор-3-метоксифенил, 3-метоксифенил, 4-метоксифенил, 3-морфолин-4-илметилфенил, имидазол-1-ил, пиразол-4-ил, 1-метилпиразол-4-ил, 2-метилпиразол-3-ил, пиридин-2-ил, пиридин-3-ил, пиридин-4-ил, 2-фторпиридин-3-ил, 2-метилпиридин-4-ил, 2-(4-метилпиперазин-1-ил)пиридин-4-ил, 2-метоксипиридин-4-ил, пиримидин-5-ил, пирролидин-3-ил, 1-метилпирролидин-3-ил, пиперидин-4-ил, 1-метилпиперидин-4-ил, 1-этилпиперидин-4-ил, 1-изопропилпиперидин-4-ил, 1-ацетилпиперидин-4-ил, 1-метилсульфонилпиперидин-4-ил или 4-метилпиперазин-1-ил.
В еще одном варианте осуществления в формуле XVb один из R7a, R7b, R7c, R7d и R7e представляет собой фенил, 2-фторфенил, 2-хлорфенил, 2-бромфенил, 2-метилфенил, 2-метоксифенил, 3-фторфенил, 3-хлорфенил, 3-метоксифенил, 4-фторфенил, 4-хлорфенил, 4-бромфенил, 4-метоксифенил, имидазол-1-ил, пиразол-4-ил, 1-метилпиразол-4-ил, 2-метилпиразол-3-ил, пиридин-2-ил, пиридин-3-ил, пиридин-4-ил, 2-метилпиридин-4-ил, 2-метоксипиридин-4-ил, 1-метилпиперидин-4-ил или 4-метилпиперазин-1-ил; и каждый R1, R2, R3, R4, R6, R5a, R5b, оставшиеся R7a, R7b, R7c, R7d и R7e, X, Y и Z представляет собой, как определено в настоящем изобретении.
В одном варианте осуществления в формуле XVb R7a представляет собой C6-14 арил, гетероарил или гетероциклил, каждый из которых необязательно замещен одним или более заместителями Q; и каждый R1, R2, R3, R4, R6, R5a, R5b, R7b, R7c, R7d, R7e, X, Y и Z представляет собой, как определено в настоящем изобретении.
В другом варианте осуществления в формуле XVb R7a представляет собой C6-14 арил, который необязательно замещен одним или более заместителями Q; и каждый R1, R2, R3, R4, R6, R5a, R5b, R7b, R7c, R7d, R7e, X, Y и Z представляет собой, как определено в настоящем изобретении.
В еще одном варианте осуществления в формуле XVb R7a представляет собой гетероарил, который необязательно замещен одним или более заместителями Q; и каждый R1, R2, R3, R4, R6, R5a, R5b, R7b, R7c, R7d, R7e, X, Y и Z представляет собой, как определено в настоящем изобретении.
В еще одном варианте осуществления в формуле XVb R7a представляет собой 5-членный или 6-членный гетероарил, который необязательно замещен одним или более заместителями Q; и каждый R1, R2, R3, R4, R6, R5a, R5b, R7b, R7c, R7d, R7e, X, Y и Z представляет собой, как определено в настоящем изобретении.
В еще одном варианте осуществления в формуле XVb R7a представляет собой гетероциклил, который необязательно замещен одним или более заместителями Q; и каждый R1, R2, R3, R4, R6, R5a, R5b, R7b, R7c, R7d, R7e, X, Y и Z представляет собой, как определено в настоящем изобретении.
В еще одном варианте осуществления в формуле XVb R7a представляет собой 5-членный или 6-членный гетероциклил, который необязательно замещен одним или более заместителями Q; и каждый R1, R2, R3, R4, R6, R5a, R5b, R7b, R7c, R7d, R7e, X, Y и Z представляет собой, как определено в настоящем изобретении.
В еще одном варианте осуществления в формуле XVb R7a представляет собой фенил, имидазолил, пиразолил, пиридинил, пиперидинил или пиперазинил, причем каждый необязательно замещен одним или более заместителями Q; и каждый R1, R2, R3, R4, R6, R5a, R5b, R7b, R7c, R7d, R7e, X, Y и Z представляет собой, как определено в настоящем изобретении.
В еще одном варианте осуществления в формуле XVb R7a представляет собой фенил, имидазолил, пиразолил, пиридинил, пиримидинил, пирролидинил, пиперидинил или пиперазинил, причем каждый необязательно замещен одним или более заместителями Q; и каждый R1, R2, R3, R4, R6, R5a, R5b, R7b, R7c, R7d, R7e, X, Y и Z представляет собой, как определено в настоящем изобретении.
В еще одном варианте осуществления в формуле XVb R7a представляет собой фенил, 2-фторфенил, 2-хлорфенил, 2-бромфенил, 2-метилфенил, 2-(3-диметиламинопропил)фенил, 2-метоксифенил, 3-фторфенил, 3-хлорфенил, 3-метилфенил, 3-метоксифенил, 4-фторфенил, 4-хлорфенил, 4-бромфенил, 4-метоксифенил, 2,4-дифторфенил, 2,6-дифторфенил, 4-фтор-3-метоксифенил, 3-метоксифенил, 4-метоксифенил, 3-морфолин-4-илметилфенил, имидазол-1-ил, пиразол-4-ил, 1-метилпиразол-4-ил, 2-метилпиразол-3-ил, пиридин-2-ил, пиридин-3-ил, пиридин-4-ил, 2-фторпиридин-3-ил, 2-метилпиридин-4-ил, 2-(4-метилпиперазин-1-ил)пиридин-4-ил, 2-метоксипиридин-4-ил, пиримидин-5-ил, пирролидин-3-ил, 1-метилпирролидин-3-ил, пиперидин-4-ил, 1-метилпиперидин-4-ил, 1-этилпиперидин-4-ил, 1-изопропилпиперидин-4-ил, 1-ацетилпиперидин-4-ил, 1-метилсульфонилпиперидин-4-ил или 4-метилпиперазин-1-ил.
В еще одном варианте осуществления в формуле XVb R7a представляет собой фенил, 2-фторфенил, 2-хлорфенил, 2-бромфенил, 2-метилфенил, 2-метоксифенил, 3-фторфенил, 3-хлорфенил, 3-метоксифенил, 4-фторфенил, 4-хлорфенил, 4-бромфенил, 4-метоксифенил, имидазол-1-ил, пиразол-4-ил, 1-метилпиразол-4-ил, 2-метилпиразол-3-ил, пиридин-2-ил, пиридин-3-ил, пиридин-4-ил, 2-метилпиридин-4-ил, 2-метоксипиридин-4-ил, 1-метилпиперидин-4-ил или 4-метилпиперазин-1-ил; и каждый R1, R2, R3, R4, R6, R5a, R5b, R7b, R7c, R7d, R7e, X, Y и Z представляет собой, как определено в настоящем изобретении.
В одном варианте осуществления в формуле XVb
R1 представляет собой водород или -OR1a, где R1a представляет собой C1-6 алкил, необязательно замещенный одним или более заместителями Q;
R2 представляет собой водород;
R3 и R4 представляют собой водород;
R6 представляет собой C6-14 алкил, необязательно замещенный одним или более заместителями Q;
каждый R5a и R5b независимо представляет собой водород или C6-14 алкил, необязательно замещенный одним или более заместителями Q;
R7a представляет собой C6-14 арил, гетероарил или гетероциклил, каждый из которых необязательно замещен одним или более заместителями Q;
R7b, R7c, R7d и R7e представляют собой водород; и
каждый X, Y и Z независимо представляет собой N или CRx, при условии, что по меньшей мере два из X, Y и Z представляют собой N; где Rx представляет собой водород или C1-6 алкил, необязательно замещенный одним или более заместителями Q.
В другом варианте осуществления в формуле XVb
R1 представляет собой водород или метокси;
R2 представляет собой водород;
R3 и R4 представляют собой водород;
R6 представляет собой C6-14 алкил, необязательно замещенный одним или более галогенами;
каждый R5a и R5b независимо представляет собой водород или C6-14 алкил;
R7a представляет собой C6-14 арил, гетероарил или гетероциклил, каждый из которых необязательно замещен одним или более заместителями Q;
R7b, R7c, R7d и R7e представляют собой водород; и
каждый X, Y и Z независимо представляет собой N или CH.
В еще одном варианте осуществления в формуле XVb
R1 представляет собой водород или метокси;
R2 представляет собой водород;
R3 и R4 представляют собой водород;
R6 представляет собой дифторметил;
каждый R5a и R5b независимо представляет собой водород или C6-14 алкил;
R7a представляет собой C6-14 арил, моноциклический гетероарил или моноциклический гетероциклил, каждый из которых необязательно замещен одним или более заместителями Q;
R7b, R7c, R7d и R7e представляют собой водород; и
каждый X, Y и Z независимо представляет собой N или CH.
В еще одном варианте осуществления в формуле XVb
R1 представляет собой водород или метокси;
R2 представляет собой водород;
R3 и R4 представляют собой водород;
R6 представляет собой дифторметил;
каждый R5a и R5b независимо представляет собой водород или C6-14 алкил;
R7a представляет собой фенил, 5- или 6-членный гетероарил или 5- или 6-членный гетероциклил, каждый из которых необязательно замещен одним или более заместителями Q;
R7b, R7c, R7d и R7e представляют собой водород; и
каждый X, Y и Z независимо представляет собой N или CH.
В еще одном варианте осуществления в формуле XVb
R1 представляет собой водород или метокси;
R2 представляет собой водород;
R3 и R4 представляют собой водород;
R6 представляет собой дифторметил;
каждый R5a и R5b независимо представляет собой водород или C6-14 алкил;
R7a представляет собой фенил, имидазолил, пиразолил, пиридинил, пиримидинил, пирролидинил, пиперидинил или пиперазинил, каждый из которых необязательно замещен одним или более заместителями Q;
R7b, R7c, R7d и R7e представляют собой водород; и
каждый X, Y и Z независимо представляет собой N или CH.
В еще одном варианте осуществления в формуле XVb
R1 представляет собой водород или метокси;
R2 представляет собой водород;
R3 и R4 представляют собой водород;
R6 представляет собой дифторметил;
каждый R5a и R5b независимо представляет собой водород или C6-14 алкил;
R7a представляет собой фенил, имидазолил, пиразолил, пиридинил, пиперидинил или пиперазинил, каждый из которых необязательно замещен одним или более заместителями Q;
R7b, R7c, R7d и R7e представляют собой водород; и
каждый X, Y и Z независимо представляет собой N или CH.
В одном варианте осуществления настоящее изобретение относится к соединению формулы XV, XVa или XVb, как описано в настоящем изобретении, или его энантиомеру, смеси энантиомеров, смеси двух или более диастереомеров или изотопному варианту; или их фармацевтически приемлемой соли, сольвату, гидрату или пролекарству; где каждый R5a и R5b независимо представляет собой (a) галоген; (b) C1-6 алкил, C2-6 алкенил, C2-6 алкинил, C3-10 циклоалкил, C6-14 арил, C7-15 аралкил, гетероарил или гетероциклил; или (c) -C(O)R1a, -C(O)OR1a, -C(O)NR1bR1c, -C(NR1a)NR1bR1c, -OR1a, -OC(O)R1a, -OC(O)OR1a, -OC(O)NR1bR1c, -OC(=NR1a)NR1bR1c, -OS(O)R1a, -OS(O)2R1a, -OS(O)NR1bR1c, -OS(O)2NR1bR1c, -NR1bR1c, -NR1aC(O)R1d, -NR1aC(O)OR1d, -NR1aC(O)NR1bR1c, -NR1aC(=NR1d)NR1bR1c, -NR1aS(O)R1d, -NR1aS(O)2R1d, -NR1aS(O)NR1bR1c, -NR1aS(O)2NR1bR1c, -SR1a, -S(O)R1a, -S(O)2R1a, -S(O)NR1bR1c или -S(O)2NR1bR1c; и R1, R2, R3, R4, R6, R7a, R7b, R7c, R7d, R7e, X, Y, Z, R1a, R1b, R1c и R1d определяют в настоящем изобретении выше.
В еще одном варианте осуществления настоящее изобретение относится к соединению формулы XVI:
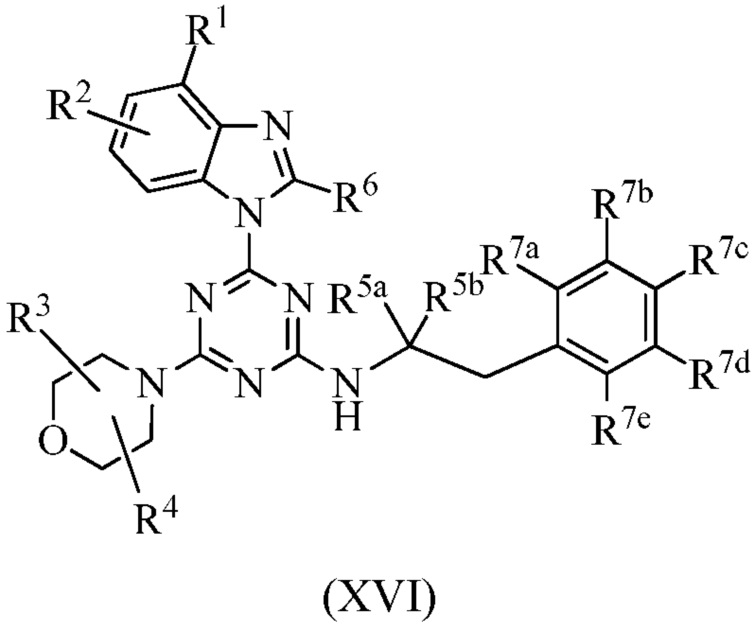
или его энантиомеру, смеси энантиомеров, смеси двух или более диастереомеров или изотопному варианту; или их фармацевтически приемлемой соли, сольвату, гидрату или пролекарству; где каждый R1, R2, R3, R4, R6, R5a, R5b, R7a, R7b, R7c, R7d и R7e представляет собой, как определено в настоящем изобретении.
В одном варианте осуществления в формуле XVI один из R7a, R7b, R7c, R7d и R7e представляет собой C6-14 арил, гетероарил или гетероциклил, каждый из которых необязательно замещен одним или более заместителями Q; и каждый R1, R2, R3, R4, R6, R5a, R5b, оставшиеся R7a, R7b, R7c, R7d и R7e, X, Y и Z представляет собой, как определено в настоящем изобретении.
В другом варианте осуществления в формуле XVI один из R7a, R7b, R7c, R7d и R7e представляет собой C6-14 арил, который необязательно замещен одним или более заместителями Q; и каждый R1, R2, R3, R4, R6, R5a, R5b, оставшиеся R7a, R7b, R7c, R7d и R7e, X, Y и Z представляет собой, как определено в настоящем изобретении.
В еще одном варианте осуществления в формуле XVI один из R7a, R7b, R7c, R7d и R7e представляет собой гетероарил, который необязательно замещен одним или более заместителями Q; и каждый R1, R2, R3, R4, R6, R5a, R5b, оставшиеся R7a, R7b, R7c, R7d и R7e, X, Y и Z представляет собой, как определено в настоящем изобретении.
В еще одном варианте осуществления в формуле XVI один из R7a, R7b, R7c, R7d и R7e представляет собой 5-членный или 6-членный гетероарил, который необязательно замещен одним или более заместителями Q; и каждый R1, R2, R3, R4, R6, R5a, R5b, оставшиеся R7a, R7b, R7c, R7d и R7e, X, Y и Z представляет собой, как определено в настоящем изобретении.
В еще одном варианте осуществления в формуле XVI один из R7a, R7b, R7c, R7d и R7e представляет собой гетероциклил, который необязательно замещен одним или более заместителями Q; и каждый R1, R2, R3, R4, R6, R5a, R5b, оставшиеся R7a, R7b, R7c, R7d и R7e, X, Y и Z представляет собой, как определено в настоящем изобретении.
В еще одном варианте осуществления в формуле XVI один из R7a, R7b, R7c, R7d и R7e представляет собой 5-членный или 6-членный гетероциклил, который необязательно замещен одним или более заместителями Q; и каждый R1, R2, R3, R4, R6, R5a, R5b, оставшиеся R7a, R7b, R7c, R7d и R7e, X, Y и Z представляет собой, как определено в настоящем изобретении.
В еще одном варианте осуществления в формуле XVI один из R7a, R7b, R7c, R7d и R7e представляет собой фенил, имидазолил, пиразолил, пиридинил, пиперидинил или пиперазинил, причем каждый необязательно замещен одним или более заместителями Q; и каждый R1, R2, R3, R4, R6, R5a, R5b, оставшиеся R7a, R7b, R7c, R7d и R7e, X, Y и Z представляет собой, как определено в настоящем изобретении.
В еще одном варианте осуществления в формуле XVI один из R7a, R7b, R7c, R7d и R7e представляет собой фенил, имидазолил, пиразолил, пиридинил, пиримидинил, пирролидинил, пиперидинил или пиперазинил, причем каждый необязательно замещен одним или более заместителями Q; и каждый R1, R2, R3, R4, R6, R5a, R5b, оставшиеся R7a, R7b, R7c, R7d и R7e, X, Y и Z представляет собой, как определено в настоящем изобретении.
В еще одном варианте осуществления в формуле XVI один из R7a, R7b, R7c, R7d и R7e представляет собой фенил, 2-фторфенил, 2-хлорфенил, 2-бромфенил, 2-метилфенил, 2-(3-диметиламинопропил)фенил, 2-метоксифенил, 3-фторфенил, 3-хлорфенил, 3-метилфенил, 3-метоксифенил, 4-фторфенил, 4-хлорфенил, 4-бромфенил, 4-метоксифенил, 2,4-дифторфенил, 2,6-дифторфенил, 4-фтор-3-метоксифенил, 3-метоксифенил, 4-метоксифенил, 3-морфолин-4-илметилфенил, имидазол-1-ил, пиразол-4-ил, 1-метилпиразол-4-ил, 2-метилпиразол-3-ил, пиридин-2-ил, пиридин-3-ил, пиридин-4-ил, 2-фторпиридин-3-ил, 2-метилпиридин-4-ил, 2-(4-метилпиперазин-1-ил)пиридин-4-ил, 2-метоксипиридин-4-ил, пиримидин-5-ил, пирролидин-3-ил, 1-метилпирролидин-3-ил, пиперидин-4-ил, 1-метилпиперидин-4-ил, 1-этилпиперидин-4-ил, 1-изопропилпиперидин-4-ил, 1-ацетилпиперидин-4-ил, 1-метилсульфонилпиперидин-4-ил или 4-метилпиперазин-1-ил.
В еще одном варианте осуществления в формуле XVI один из R7a, R7b, R7c, R7d и R7e представляет собой фенил, 2-фторфенил, 2-хлорфенил, 2-бромфенил, 2-метилфенил, 2-метоксифенил, 3-фторфенил, 3-хлорфенил, 3-метоксифенил, 4-фторфенил, 4-хлорфенил, 4-бромфенил, 4-метоксифенил, имидазол-1-ил, пиразол-4-ил, 1-метилпиразол-4-ил, 2-метилпиразол-3-ил, пиридин-2-ил, пиридин-3-ил, пиридин-4-ил, 2-метилпиридин-4-ил, 2-метоксипиридин-4-ил, 1-метилпиперидин-4-ил или 4-метилпиперазин-1-ил; и каждый R1, R2, R3, R4, R6, R5a, R5b, оставшиеся R7a, R7b, R7c, R7d и R7e, X, Y и Z представляет собой, как определено в настоящем изобретении.
В одном варианте осуществления в формуле XVI R7a представляет собой C6-14 арил, гетероарил или гетероциклил, каждый из которых необязательно замещен одним или более заместителями Q; и каждый R1, R2, R3, R4, R6, R5a, R5b, R7b, R7c, R7d, R7e, X, Y и Z представляет собой, как определено в настоящем изобретении.
В другом варианте осуществления в формуле XVI R7a представляет собой C6-14 арил, который необязательно замещен одним или более заместителями Q; и каждый R1, R2, R3, R4, R6, R5a, R5b, R7b, R7c, R7d, R7e, X, Y и Z представляет собой, как определено в настоящем изобретении.
В еще одном варианте осуществления в формуле XVI R7a представляет собой гетероарил, который необязательно замещен одним или более заместителями Q; и каждый R1, R2, R3, R4, R6, R5a, R5b, R7b, R7c, R7d, R7e, X, Y и Z представляет собой, как определено в настоящем изобретении.
В еще одном варианте осуществления в формуле XVI R7a представляет собой 5-членный или 6-членный гетероарил, который необязательно замещен одним или более заместителями Q; и каждый R1, R2, R3, R4, R6, R5a, R5b, R7b, R7c, R7d, R7e, X, Y и Z представляет собой, как определено в настоящем изобретении.
В еще одном варианте осуществления в формуле XVI R7a представляет собой гетероциклил, который необязательно замещен одним или более заместителями Q; и каждый R1, R2, R3, R4, R6, R5a, R5b, R7b, R7c, R7d, R7e, X, Y и Z представляет собой, как определено в настоящем изобретении.
В еще одном варианте осуществления в формуле XVI R7a представляет собой 5-членный или 6-членный гетероциклил, который необязательно замещен одним или более заместителями Q; и каждый R1, R2, R3, R4, R6, R5a, R5b, R7b, R7c, R7d, R7e, X, Y и Z представляет собой, как определено в настоящем изобретении.
В еще одном варианте осуществления в формуле XVI R7a представляет собой фенил, имидазолил, пиразолил, пиридинил, пиперидинил или пиперазинил, причем каждый необязательно замещен одним или более заместителями Q; и каждый R1, R2, R3, R4, R6, R5a, R5b, R7b, R7c, R7d, R7e, X, Y и Z представляет собой, как определено в настоящем изобретении.
В еще одном варианте осуществления в формуле XVI R7a представляет собой фенил, имидазолил, пиразолил, пиридинил, пиримидинил, пирролидинил, пиперидинил или пиперазинил, причем каждый необязательно замещен одним или более заместителями Q; и каждый R1, R2, R3, R4, R6, R5a, R5b, R7b, R7c, R7d, R7e, X, Y и Z представляет собой, как определено в настоящем изобретении.
В еще одном варианте осуществления в формуле XVI R7a представляет собой фенил, 2-фторфенил, 2-хлорфенил, 2-бромфенил, 2-метилфенил, 2-(3-диметиламинопропил)фенил, 2-метоксифенил, 3-фторфенил, 3-хлорфенил, 3-метилфенил, 3-метоксифенил, 4-фторфенил, 4-хлорфенил, 4-бромфенил, 4-метоксифенил, 2,4-дифторфенил, 2,6-дифторфенил, 4-фтор-3-метоксифенил, 3-метоксифенил, 4-метоксифенил, 3-морфолин-4-илметилфенил, имидазол-1-ил, пиразол-4-ил, 1-метилпиразол-4-ил, 2-метилпиразол-3-ил, пиридин-2-ил, пиридин-3-ил, пиридин-4-ил, 2-фторпиридин-3-ил, 2-метилпиридин-4-ил, 2-(4-метилпиперазин-1-ил)пиридин-4-ил, 2-метоксипиридин-4-ил, пиримидин-5-ил, пирролидин-3-ил, 1-метилпирролидин-3-ил, пиперидин-4-ил, 1-метилпиперидин-4-ил, 1-этилпиперидин-4-ил, 1-изопропилпиперидин-4-ил, 1-ацетилпиперидин-4-ил, 1-метилсульфонилпиперидин-4-ил или 4-метилпиперазин-1-ил.
В еще одном варианте осуществления в формуле XVI R7a представляет собой фенил, 2-фторфенил, 2-хлорфенил, 2-бромфенил, 2-метилфенил, 2-метоксифенил, 3-фторфенил, 3-хлорфенил, 3-метоксифенил, 4-фторфенил, 4-хлорфенил, 4-бромфенил, 4-метоксифенил, имидазол-1-ил, пиразол-4-ил, 1-метилпиразол-4-ил, 2-метилпиразол-3-ил, пиридин-2-ил, пиридин-3-ил, пиридин-4-ил, 2-метилпиридин-4-ил, 2-метоксипиридин-4-ил, 1-метилпиперидин-4-ил или 4-метилпиперазин-1-ил; и каждый R1, R2, R3, R4, R6, R5a, R5b, R7b, R7c, R7d, R7e, X, Y и Z представляет собой, как определено в настоящем изобретении.
В одном варианте осуществления в формуле XVI
R1 представляет собой водород или -OR1a, где R1a представляет собой C1-6 алкил, необязательно замещенный одним или более заместителями Q;
R2 представляет собой водород;
R3 и R4 представляют собой водород;
R6 представляет собой C6-14 алкил, необязательно замещенный одним или более заместителями Q;
каждый R5a и R5b независимо представляет собой C6-14 алкил, необязательно замещенный одним или более заместителями Q;
R7a представляет собой C6-14 арил, гетероарил или гетероциклил, каждый из которых необязательно замещен одним или более заместителями Q; и
R7b, R7c, R7d и R7e представляют собой водород.
В другом варианте осуществления в формуле XVI
R1 представляет собой водород или метокси;
R2 представляет собой водород;
R3 и R4 представляют собой водород;
R6 представляет собой C6-14 алкил, необязательно замещенный одним или более галогенами;
каждый R5a и R5b независимо представляет собой C6-14 алкил;
R7a представляет собой C6-14 арил, гетероарил или гетероциклил, каждый из которых необязательно замещен одним или более заместителями Q; и
R7b, R7c, R7d и R7e представляют собой водород.
В еще одном варианте осуществления в формуле XVI
R1 представляет собой водород или метокси;
R2 представляет собой водород;
R3 и R4 представляют собой водород;
R6 представляет собой дифторметил;
R5a и R5b представляют собой метил;
R7a представляет собой C6-14 арил, моноциклический гетероарил или моноциклический гетероциклил, каждый из которых необязательно замещен одним или более заместителями Q; и
R7b, R7c, R7d и R7e представляют собой водород.
В еще одном варианте осуществления в формуле XVI
R1 представляет собой водород или метокси;
R2 представляет собой водород;
R3 и R4 представляют собой водород;
R6 представляет собой дифторметил;
R5a и R5b представляют собой метил;
R7a представляет собой фенил, 5- или 6-членный гетероарил или 5- или 6-членный гетероциклил, каждый из которых необязательно замещен одним или более заместителями Q; и
R7b, R7c, R7d и R7e представляют собой водород.
В еще одном варианте осуществления в формуле XVI
R1 представляет собой водород или метокси;
R2 представляет собой водород;
R3 и R4 представляют собой водород;
R6 представляет собой дифторметил;
R5a и R5b представляют собой метил;
R7a представляет собой фенил, имидазолил, пиразолил, пиридинил, пиримидинил, пирролидинил, пиперидинил или пиперазинил, каждый из которых необязательно замещен одним или более заместителями Q; и
R7b, R7c, R7d и R7e представляют собой водород.
В еще одном варианте осуществления в формуле XVI
R1 представляет собой водород или метокси;
R2 представляет собой водород;
R3 и R4 представляют собой водород;
R6 представляет собой дифторметил;
R5a и R5b представляют собой метил;
R7a представляет собой фенил, имидазолил, пиразолил, пиридинил, пиперидинил или пиперазинил, каждый из которых необязательно замещен одним или более заместителями Q; и
R7b, R7c, R7d и R7e представляют собой водород.
В одном варианте осуществления, соединение формулы XVI имеет структуру формулы XVIa:
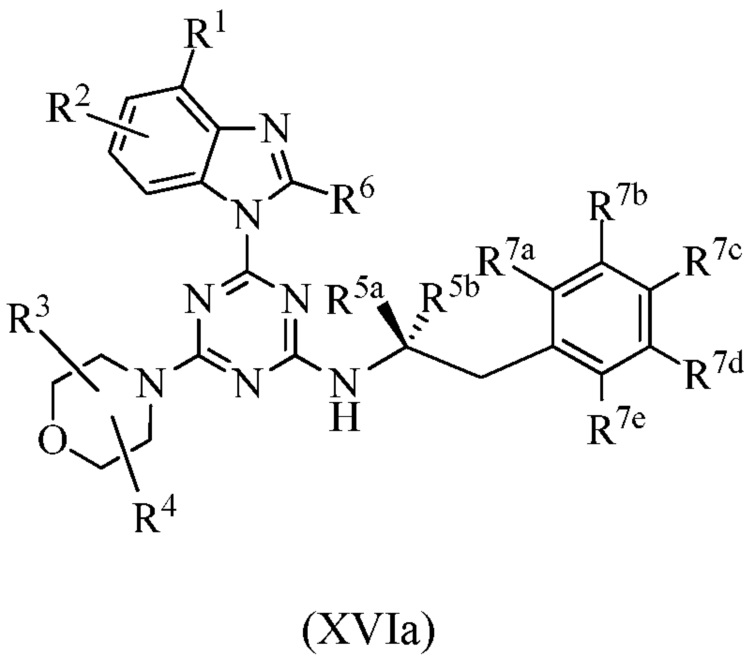
или его изотопный вариант; или их фармацевтически приемлемую соль, сольват, гидрат или пролекарство; где каждый R1, R2, R3, R4, R6, R5a, R5b, R7a, R7b, R7c, R7d и R7e представляет собой, как определено в настоящем изобретении.
В одном варианте осуществления в формуле XVIa один из R7a, R7b, R7c, R7d и R7e представляет собой C6-14 арил, гетероарил или гетероциклил, каждый из которых необязательно замещен одним или более заместителями Q; и каждый R1, R2, R3, R4, R6, R5a, R5b, оставшиеся R7a, R7b, R7c, R7d и R7e, X, Y и Z представляет собой, как определено в настоящем изобретении.
В другом варианте осуществления в формуле XVIa один из R7a, R7b, R7c, R7d и R7e представляет собой C6-14 арил, который необязательно замещен одним или более заместителями Q; и каждый R1, R2, R3, R4, R6, R5a, R5b, оставшиеся R7a, R7b, R7c, R7d и R7e, X, Y и Z представляет собой, как определено в настоящем изобретении.
В еще одном варианте осуществления в формуле XVIa один из R7a, R7b, R7c, R7d и R7e представляет собой гетероарил, который необязательно замещен одним или более заместителями Q; и каждый R1, R2, R3, R4, R6, R5a, R5b, оставшиеся R7a, R7b, R7c, R7d и R7e, X, Y и Z представляет собой, как определено в настоящем изобретении.
В еще одном варианте осуществления в формуле XVIa один из R7a, R7b, R7c, R7d и R7e представляет собой 5-членный или 6-членный гетероарил, который необязательно замещен одним или более заместителями Q; и каждый R1, R2, R3, R4, R6, R5a, R5b, оставшиеся R7a, R7b, R7c, R7d и R7e, X, Y и Z представляет собой, как определено в настоящем изобретении.
В еще одном варианте осуществления в формуле XVIa один из R7a, R7b, R7c, R7d и R7e представляет собой гетероциклил, который необязательно замещен одним или более заместителями Q; и каждый R1, R2, R3, R4, R6, R5a, R5b, оставшиеся R7a, R7b, R7c, R7d и R7e, X, Y и Z представляет собой, как определено в настоящем изобретении.
В еще одном варианте осуществления в формуле XVIa один из R7a, R7b, R7c, R7d и R7e представляет собой 5-членный или 6-членный гетероциклил, который необязательно замещен одним или более заместителями Q; и каждый R1, R2, R3, R4, R6, R5a, R5b, оставшиеся R7a, R7b, R7c, R7d и R7e, X, Y и Z представляет собой, как определено в настоящем изобретении.
В еще одном варианте осуществления в формуле XVIa один из R7a, R7b, R7c, R7d и R7e представляет собой фенил, имидазолил, пиразолил, пиридинил, пиперидинил или пиперазинил, причем каждый необязательно замещен одним или более заместителями Q; и каждый R1, R2, R3, R4, R6, R5a, R5b, оставшиеся R7a, R7b, R7c, R7d и R7e, X, Y и Z представляет собой, как определено в настоящем изобретении.
В еще одном варианте осуществления в формуле XVIa один из R7a, R7b, R7c, R7d и R7e представляет собой фенил, имидазолил, пиразолил, пиридинил, пиримидинил, пирролидинил, пиперидинил или пиперазинил, причем каждый необязательно замещен одним или более заместителями Q; и каждый R1, R2, R3, R4, R6, R5a, R5b, оставшиеся R7a, R7b, R7c, R7d и R7e, X, Y и Z представляет собой, как определено в настоящем изобретении.
В еще одном варианте осуществления в формуле XVIa один из R7a, R7b, R7c, R7d и R7e представляет собой фенил, 2-фторфенил, 2-хлорфенил, 2-бромфенил, 2-метилфенил, 2-(3-диметиламинопропил)фенил, 2-метоксифенил, 3-фторфенил, 3-хлорфенил, 3-метилфенил, 3-метоксифенил, 4-фторфенил, 4-хлорфенил, 4-бромфенил, 4-метоксифенил, 2,4-дифторфенил, 2,6-дифторфенил, 4-фтор-3-метоксифенил, 3-метоксифенил, 4-метоксифенил, 3-морфолин-4-илметилфенил, имидазол-1-ил, пиразол-4-ил, 1-метилпиразол-4-ил, 2-метилпиразол-3-ил, пиридин-2-ил, пиридин-3-ил, пиридин-4-ил, 2-фторпиридин-3-ил, 2-метилпиридин-4-ил, 2-(4-метилпиперазин-1-ил)пиридин-4-ил, 2-метоксипиридин-4-ил, пиримидин-5-ил, пирролидин-3-ил, 1-метилпирролидин-3-ил, пиперидин-4-ил, 1-метилпиперидин-4-ил, 1-этилпиперидин-4-ил, 1-изопропилпиперидин-4-ил, 1-ацетилпиперидин-4-ил, 1-метилсульфонилпиперидин-4-ил или 4-метилпиперазин-1-ил.
В еще одном варианте осуществления в формуле XVIa один из R7a, R7b, R7c, R7d и R7e представляет собой фенил, 2-фторфенил, 2-хлорфенил, 2-бромфенил, 2-метилфенил, 2-метоксифенил, 3-фторфенил, 3-хлорфенил, 3-метоксифенил, 4-фторфенил, 4-хлорфенил, 4-бромфенил, 4-метоксифенил, имидазол-1-ил, пиразол-4-ил, 1-метилпиразол-4-ил, 2-метилпиразол-3-ил, пиридин-2-ил, пиридин-3-ил, пиридин-4-ил, 2-метилпиридин-4-ил, 2-метоксипиридин-4-ил, 1-метилпиперидин-4-ил или 4-метилпиперазин-1-ил; и каждый R1, R2, R3, R4, R6, R5a, R5b, оставшиеся R7a, R7b, R7c, R7d и R7e, X, Y и Z представляет собой, как определено в настоящем изобретении.
В одном варианте осуществления в формуле XVIa R7a представляет собой C6-14 арил, гетероарил или гетероциклил, каждый из которых необязательно замещен одним или более заместителями Q; и каждый R1, R2, R3, R4, R6, R5a, R5b, R7b, R7c, R7d, R7e, X, Y и Z представляет собой, как определено в настоящем изобретении.
В другом варианте осуществления в формуле XVIa R7a представляет собой C6-14 арил, который необязательно замещен одним или более заместителями Q; и каждый R1, R2, R3, R4, R6, R5a, R5b, R7b, R7c, R7d, R7e, X, Y и Z представляет собой, как определено в настоящем изобретении.
В еще одном варианте осуществления в формуле XVIa R7a представляет собой гетероарил, который необязательно замещен одним или более заместителями Q; и каждый R1, R2, R3, R4, R6, R5a, R5b, R7b, R7c, R7d, R7e, X, Y и Z представляет собой, как определено в настоящем изобретении.
В еще одном варианте осуществления в формуле XVIa R7a представляет собой 5-членный или 6-членный гетероарил, который необязательно замещен одним или более заместителями Q; и каждый R1, R2, R3, R4, R6, R5a, R5b, R7b, R7c, R7d, R7e, X, Y и Z представляет собой, как определено в настоящем изобретении.
В еще одном варианте осуществления в формуле XVIa R7a представляет собой гетероциклил, который необязательно замещен одним или более заместителями Q; и каждый R1, R2, R3, R4, R6, R5a, R5b, R7b, R7c, R7d, R7e, X, Y и Z представляет собой, как определено в настоящем изобретении.
В еще одном варианте осуществления в формуле XVIa R7a представляет собой 5-членный или 6-членный гетероциклил, который необязательно замещен одним или более заместителями Q; и каждый R1, R2, R3, R4, R6, R5a, R5b, R7b, R7c, R7d, R7e, X, Y и Z представляет собой, как определено в настоящем изобретении.
В еще одном варианте осуществления в формуле XVIa R7a представляет собой фенил, имидазолил, пиразолил, пиридинил, пиперидинил или пиперазинил, причем каждый необязательно замещен одним или более заместителями Q; и каждый R1, R2, R3, R4, R6, R5a, R5b, R7b, R7c, R7d, R7e, X, Y и Z представляет собой, как определено в настоящем изобретении.
В еще одном варианте осуществления в формуле XVIa R7a представляет собой фенил, имидазолил, пиразолил, пиридинил, пиримидинил, пирролидинил, пиперидинил или пиперазинил, причем каждый необязательно замещен одним или более заместителями Q; и каждый R1, R2, R3, R4, R6, R5a, R5b, R7b, R7c, R7d, R7e, X, Y и Z представляет собой, как определено в настоящем изобретении.
В еще одном варианте осуществления в формуле XVIa R7a представляет собой фенил, 2-фторфенил, 2-хлорфенил, 2-бромфенил, 2-метилфенил, 2-(3-диметиламинопропил)фенил, 2-метоксифенил, 3-фторфенил, 3-хлорфенил, 3-метилфенил, 3-метоксифенил, 4-фторфенил, 4-хлорфенил, 4-бромфенил, 4-метоксифенил, 2,4-дифторфенил, 2,6-дифторфенил, 4-фтор-3-метоксифенил, 3-метоксифенил, 4-метоксифенил, 3-морфолин-4-илметилфенил, имидазол-1-ил, пиразол-4-ил, 1-метилпиразол-4-ил, 2-метилпиразол-3-ил, пиридин-2-ил, пиридин-3-ил, пиридин-4-ил, 2-фторпиридин-3-ил, 2-метилпиридин-4-ил, 2-(4-метилпиперазин-1-ил)пиридин-4-ил, 2-метоксипиридин-4-ил, пиримидин-5-ил, пирролидин-3-ил, 1-метилпирролидин-3-ил, пиперидин-4-ил, 1-метилпиперидин-4-ил, 1-этилпиперидин-4-ил, 1-изопропилпиперидин-4-ил, 1-ацетилпиперидин-4-ил, 1-метилсульфонилпиперидин-4-ил или 4-метилпиперазин-1-ил.
В еще одном варианте осуществления в формуле XVIa R7a представляет собой фенил, 2-фторфенил, 2-хлорфенил, 2-бромфенил, 2-метилфенил, 2-метоксифенил, 3-фторфенил, 3-хлорфенил, 3-метоксифенил, 4-фторфенил, 4-хлорфенил, 4-бромфенил, 4-метоксифенил, имидазол-1-ил, пиразол-4-ил, 1-метилпиразол-4-ил, 2-метилпиразол-3-ил, пиридин-2-ил, пиридин-3-ил, пиридин-4-ил, 2-метилпиридин-4-ил, 2-метоксипиридин-4-ил, 1-метилпиперидин-4-ил или 4-метилпиперазин-1-ил; и каждый R1, R2, R3, R4, R6, R5a, R5b, R7b, R7c, R7d, R7e, X, Y и Z представляет собой, как определено в настоящем изобретении.
В одном варианте осуществления в формуле XVIa
R1 представляет собой водород или -OR1a, где R1a представляет собой C1-6 алкил, необязательно замещенный одним или более заместителями Q;
R2 представляет собой водород;
R3 и R4 представляют собой водород;
R6 представляет собой C6-14 алкил, необязательно замещенный одним или более заместителями Q;
каждый R5a и R5b независимо представляет собой водород или C6-14 алкил, необязательно замещенный одним или более заместителями Q;
R7a представляет собой C6-14 арил, гетероарил или гетероциклил, каждый из которых необязательно замещен одним или более заместителями Q; и
R7b, R7c, R7d и R7e представляют собой водород.
В другом варианте осуществления в формуле XVIa
R1 представляет собой водород или метокси;
R2 представляет собой водород;
R3 и R4 представляют собой водород;
R6 представляет собой C6-14 алкил, необязательно замещенный одним или более галогенами;
каждый R5a и R5b независимо представляет собой водород или C6-14 алкил;
R7a представляет собой C6-14 арил, гетероарил или гетероциклил, каждый из которых необязательно замещен одним или более заместителями Q; и
R7b, R7c, R7d и R7e представляют собой водород.
В еще одном варианте осуществления в формуле XVIa
R1 представляет собой водород или метокси;
R2 представляет собой водород;
R3 и R4 представляют собой водород;
R6 представляет собой дифторметил;
каждый R5a и R5b независимо представляет собой водород или C6-14 алкил;
R7a представляет собой C6-14 арил, моноциклический гетероарил или моноциклический гетероциклил, каждый из которых необязательно замещен одним или более заместителями Q; и
R7b, R7c, R7d и R7e представляют собой водород.
В еще одном варианте осуществления в формуле XVIa
R1 представляет собой водород или метокси;
R2 представляет собой водород;
R3 и R4 представляют собой водород;
R6 представляет собой дифторметил;
каждый R5a и R5b независимо представляет собой водород или C6-14 алкил;
R7a представляет собой фенил, 5- или 6-членный гетероарил или 5- или 6-членный гетероциклил, каждый из которых необязательно замещен одним или более заместителями Q; и
R7b, R7c, R7d и R7e представляют собой водород.
В еще одном варианте осуществления в формуле XVIa
R1 представляет собой водород или метокси;
R2 представляет собой водород;
R3 и R4 представляют собой водород;
R6 представляет собой дифторметил;
каждый R5a и R5b независимо представляет собой водород или C6-14 алкил;
R7a представляет собой фенил, имидазолил, пиразолил, пиридинил, пирролидинил, пиперидинил, пиперидинил или пиперазинил, каждый из которых необязательно замещен одним или более заместителями Q; и
R7b, R7c, R7d и R7e представляют собой водород.
В еще одном варианте осуществления в формуле XVIa
R1 представляет собой водород или метокси;
R2 представляет собой водород;
R3 и R4 представляют собой водород;
R6 представляет собой дифторметил;
каждый R5a и R5b независимо представляет собой водород или C6-14 алкил;
R7a представляет собой фенил, имидазолил, пиразолил, пиридинил, пиперидинил или пиперазинил, каждый из которых необязательно замещен одним или более заместителями Q; и
R7b, R7c, R7d и R7e представляют собой водород.
В другом варианте осуществления соединение формулы XVI имеет структуру формулы XVIb:
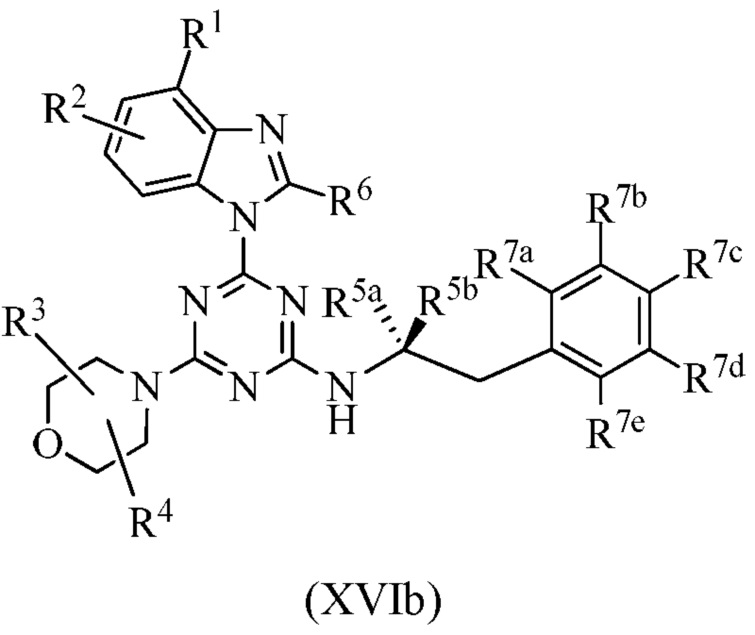
или его изотопный вариант; или их фармацевтически приемлемую соль, сольват, гидрат или пролекарство; где каждый R1, R2, R3, R4, R6, R5a, R5b, R7a, R7b, R7c, R7d и R7e представляет собой, как определено в настоящем изобретении.
В одном варианте осуществления в формуле XVIb один из R7a, R7b, R7c, R7d и R7e представляет собой C6-14 арил, гетероарил или гетероциклил, каждый из которых необязательно замещен одним или более заместителями Q; и каждый R1, R2, R3, R4, R6, R5a, R5b, оставшиеся R7a, R7b, R7c, R7d и R7e, X, Y и Z представляет собой, как определено в настоящем изобретении.
В другом варианте осуществления в формуле XVIb один из R7a, R7b, R7c, R7d и R7e представляет собой C6-14 арил, который необязательно замещен одним или более заместителями Q; и каждый R1, R2, R3, R4, R6, R5a, R5b, оставшиеся R7a, R7b, R7c, R7d и R7e, X, Y и Z представляет собой, как определено в настоящем изобретении.
В еще одном варианте осуществления в формуле XVIb один из R7a, R7b, R7c, R7d и R7e представляет собой гетероарил, который необязательно замещен одним или более заместителями Q; и каждый R1, R2, R3, R4, R6, R5a, R5b, оставшиеся R7a, R7b, R7c, R7d и R7e, X, Y и Z представляет собой, как определено в настоящем изобретении.
В еще одном варианте осуществления в формуле XVIb один из R7a, R7b, R7c, R7d и R7e представляет собой 5-членный или 6-членный гетероарил, который необязательно замещен одним или более заместителями Q; и каждый R1, R2, R3, R4, R6, R5a, R5b, оставшиеся R7a, R7b, R7c, R7d и R7e, X, Y и Z представляет собой, как определено в настоящем изобретении.
В еще одном варианте осуществления в формуле XVIb один из R7a, R7b, R7c, R7d и R7e представляет собой гетероциклил, который необязательно замещен одним или более заместителями Q; и каждый R1, R2, R3, R4, R6, R5a, R5b, оставшиеся R7a, R7b, R7c, R7d и R7e, X, Y и Z представляет собой, как определено в настоящем изобретении.
В еще одном варианте осуществления в формуле XVIb один из R7a, R7b, R7c, R7d и R7e представляет собой 5-членный или 6-членный гетероциклил, который необязательно замещен одним или более заместителями Q; и каждый R1, R2, R3, R4, R6, R5a, R5b, оставшиеся R7a, R7b, R7c, R7d и R7e, X, Y и Z представляет собой, как определено в настоящем изобретении.
В еще одном варианте осуществления в формуле XVIb один из R7a, R7b, R7c, R7d и R7e представляет собой фенил, имидазолил, пиразолил, пиридинил, пиперидинил или пиперазинил, причем каждый необязательно замещен одним или более заместителями Q; и каждый R1, R2, R3, R4, R6, R5a, R5b, оставшиеся R7a, R7b, R7c, R7d и R7e, X, Y и Z представляет собой, как определено в настоящем изобретении.
В еще одном варианте осуществления в формуле XVIb один из R7a, R7b, R7c, R7d и R7e представляет собой фенил, имидазолил, пиразолил, пиридинил, пиримидинил, пирролидинил, пиперидинил или пиперазинил, причем каждый необязательно замещен одним или более заместителями Q; и каждый R1, R2, R3, R4, R6, R5a, R5b, оставшиеся R7a, R7b, R7c, R7d и R7e, X, Y и Z представляет собой, как определено в настоящем изобретении.
В еще одном варианте осуществления в формуле XVIb один из R7a, R7b, R7c, R7d и R7e представляет собой фенил, 2-фторфенил, 2-хлорфенил, 2-бромфенил, 2-метилфенил, 2-(3-диметиламинопропил)фенил, 2-метоксифенил, 3-фторфенил, 3-хлорфенил, 3-метилфенил, 3-метоксифенил, 4-фторфенил, 4-хлорфенил, 4-бромфенил, 4-метоксифенил, 2,4-дифторфенил, 2,6-дифторфенил, 4-фтор-3-метоксифенил, 3-метоксифенил, 4-метоксифенил, 3-морфолин-4-илметилфенил, имидазол-1-ил, пиразол-4-ил, 1-метилпиразол-4-ил, 2-метилпиразол-3-ил, пиридин-2-ил, пиридин-3-ил, пиридин-4-ил, 2-фторпиридин-3-ил, 2-метилпиридин-4-ил, 2-(4-метилпиперазин-1-ил)пиридин-4-ил, 2-метоксипиридин-4-ил, пиримидин-5-ил, пирролидин-3-ил, 1-метилпирролидин-3-ил, пиперидин-4-ил, 1-метилпиперидин-4-ил, 1-этилпиперидин-4-ил, 1-изопропилпиперидин-4-ил, 1-ацетилпиперидин-4-ил, 1-метилсульфонилпиперидин-4-ил или 4-метилпиперазин-1-ил.
В еще одном варианте осуществления в формуле XVIb один из R7a, R7b, R7c, R7d и R7e представляет собой фенил, 2-фторфенил, 2-хлорфенил, 2-бромфенил, 2-метилфенил, 2-метоксифенил, 3-фторфенил, 3-хлорфенил, 3-метоксифенил, 4-фторфенил, 4-хлорфенил, 4-бромфенил, 4-метоксифенил, имидазол-1-ил, пиразол-4-ил, 1-метилпиразол-4-ил, 2-метилпиразол-3-ил, пиридин-2-ил, пиридин-3-ил, пиридин-4-ил, 2-метилпиридин-4-ил, 2-метоксипиридин-4-ил, 1-метилпиперидин-4-ил или 4-метилпиперазин-1-ил; и каждый R1, R2, R3, R4, R6, R5a, R5b, оставшиеся R7a, R7b, R7c, R7d и R7e, X, Y и Z представляет собой, как определено в настоящем изобретении.
В одном варианте осуществления в формуле XVIb R7a представляет собой C6-14 арил, гетероарил или гетероциклил, каждый из которых необязательно замещен одним или более заместителями Q; и каждый R1, R2, R3, R4, R6, R5a, R5b, R7b, R7c, R7d, R7e, X, Y и Z представляет собой, как определено в настоящем изобретении.
В другом варианте осуществления в формуле XVIb R7a представляет собой C6-14 арил, который необязательно замещен одним или более заместителями Q; и каждый R1, R2, R3, R4, R6, R5a, R5b, R7b, R7c, R7d, R7e, X, Y и Z представляет собой, как определено в настоящем изобретении.
В еще одном варианте осуществления в формуле XVIb R7a представляет собой гетероарил, который необязательно замещен одним или более заместителями Q; и каждый R1, R2, R3, R4, R6, R5a, R5b, R7b, R7c, R7d, R7e, X, Y и Z представляет собой, как определено в настоящем изобретении.
В еще одном варианте осуществления в формуле XVIb R7a представляет собой 5-членный или 6-членный гетероарил, который необязательно замещен одним или более заместителями Q; и каждый R1, R2, R3, R4, R6, R5a, R5b, R7b, R7c, R7d, R7e, X, Y и Z представляет собой, как определено в настоящем изобретении.
В еще одном варианте осуществления в формуле XVIb R7a представляет собой гетероциклил, который необязательно замещен одним или более заместителями Q; и каждый R1, R2, R3, R4, R6, R5a, R5b, R7b, R7c, R7d, R7e, X, Y и Z представляет собой, как определено в настоящем изобретении.
В еще одном варианте осуществления в формуле XVIb R7a представляет собой 5-членный или 6-членный гетероциклил, который необязательно замещен одним или более заместителями Q; и каждый R1, R2, R3, R4, R6, R5a, R5b, R7b, R7c, R7d, R7e, X, Y и Z представляет собой, как определено в настоящем изобретении.
В еще одном варианте осуществления в формуле XVIb R7a представляет собой фенил, имидазолил, пиразолил, пиридинил, пиперидинил или пиперазинил, причем каждый необязательно замещен одним или более заместителями Q; и каждый R1, R2, R3, R4, R6, R5a, R5b, R7b, R7c, R7d, R7e, X, Y и Z представляет собой, как определено в настоящем изобретении.
В еще одном варианте осуществления в формуле XVIb R7a представляет собой фенил, имидазолил, пиразолил, пиридинил, пиримидинил, пирролидинил, пиперидинил или пиперазинил, причем каждый необязательно замещен одним или более заместителями Q; и каждый R1, R2, R3, R4, R6, R5a, R5b, R7b, R7c, R7d, R7e, X, Y и Z представляет собой, как определено в настоящем изобретении.
В еще одном варианте осуществления в формуле XVIb R7a представляет собой фенил, 2-фторфенил, 2-хлорфенил, 2-бромфенил, 2-метилфенил, 2-(3-диметиламинопропил)фенил, 2-метоксифенил, 3-фторфенил, 3-хлорфенил, 3-метилфенил, 3-метоксифенил, 4-фторфенил, 4-хлорфенил, 4-бромфенил, 4-метоксифенил, 2,4-дифторфенил, 2,6-дифторфенил, 4-фтор-3-метоксифенил, 3-метоксифенил, 4-метоксифенил, 3-морфолин-4-илметилфенил, имидазол-1-ил, пиразол-4-ил, 1-метилпиразол-4-ил, 2-метилпиразол-3-ил, пиридин-2-ил, пиридин-3-ил, пиридин-4-ил, 2-фторпиридин-3-ил, 2-метилпиридин-4-ил, 2-(4-метилпиперазин-1-ил)пиридин-4-ил, 2-метоксипиридин-4-ил, пиримидин-5-ил, пирролидин-3-ил, 1-метилпирролидин-3-ил, пиперидин-4-ил, 1-метилпиперидин-4-ил, 1-этилпиперидин-4-ил, 1-изопропилпиперидин-4-ил, 1-ацетилпиперидин-4-ил, 1-метилсульфонилпиперидин-4-ил или 4-метилпиперазин-1-ил.
В еще одном варианте осуществления в формуле XVIb R7a представляет собой фенил, 2-фторфенил, 2-хлорфенил, 2-бромфенил, 2-метилфенил, 2-метоксифенил, 3-фторфенил, 3-хлорфенил, 3-метоксифенил, 4-фторфенил, 4-хлорфенил, 4-бромфенил, 4-метоксифенил, имидазол-1-ил, пиразол-4-ил, 1-метилпиразол-4-ил, 2-метилпиразол-3-ил, пиридин-2-ил, пиридин-3-ил, пиридин-4-ил, 2-метилпиридин-4-ил, 2-метоксипиридин-4-ил, 1-метилпиперидин-4-ил или 4-метилпиперазин-1-ил; и каждый R1, R2, R3, R4, R6, R5a, R5b, R7b, R7c, R7d, R7e, X, Y и Z представляет собой, как определено в настоящем изобретении.
В одном варианте осуществления в формуле XVIb
R1 представляет собой водород или -OR1a, где R1a представляет собой C1-6 алкил, необязательно замещенный одним или более заместителями Q;
R2 представляет собой водород;
R3 и R4 представляют собой водород;
R6 представляет собой C6-14 алкил, необязательно замещенный одним или более заместителями Q;
каждый R5a и R5b независимо представляет собой водород или C6-14 алкил, необязательно замещенный одним или более заместителями Q;
R7a представляет собой C6-14 арил, гетероарил или гетероциклил, каждый из которых необязательно замещен одним или более заместителями Q; и
R7b, R7c, R7d и R7e представляют собой водород.
В другом варианте осуществления в формуле XVIb
R1 представляет собой водород или метокси;
R2 представляет собой водород;
R3 и R4 представляют собой водород;
R6 представляет собой C6-14 алкил, необязательно замещенный одним или более галогенами;
каждый R5a и R5b независимо представляет собой водород или C6-14 алкил;
R7a представляет собой C6-14 арил, гетероарил или гетероциклил, каждый из которых необязательно замещен одним или более заместителями Q; и
R7b, R7c, R7d и R7e представляют собой водород.
В еще одном варианте осуществления в формуле XVIb
R1 представляет собой водород или метокси;
R2 представляет собой водород;
R3 и R4 представляют собой водород;
R6 представляет собой дифторметил;
каждый R5a и R5b независимо представляет собой водород или C6-14 алкил;
R7a представляет собой C6-14 арил, моноциклический гетероарил или моноциклический гетероциклил, каждый из которых необязательно замещен одним или более заместителями Q; и
R7b, R7c, R7d и R7e представляют собой водород.
В еще одном варианте осуществления в формуле XVIb
R1 представляет собой водород или метокси;
R2 представляет собой водород;
R3 и R4 представляют собой водород;
R6 представляет собой дифторметил;
каждый R5a и R5b независимо представляет собой водород или C6-14 алкил;
R7a представляет собой фенил, 5- или 6-членный гетероарил или 5- или 6-членный гетероциклил, каждый из которых необязательно замещен одним или более заместителями Q; и
R7b, R7c, R7d и R7e представляют собой водород.
В еще одном варианте осуществления в формуле XVIb
R1 представляет собой водород или метокси;
R2 представляет собой водород;
R3 и R4 представляют собой водород;
R6 представляет собой дифторметил;
каждый R5a и R5b независимо представляет собой водород или C6-14 алкил;
R7a представляет собой фенил, имидазолил, пиразолил, пиридинил, пиримидинил, пирролидинил, пиперидинил или пиперазинил, каждый из которых необязательно замещен одним или более заместителями Q; и
R7b, R7c, R7d и R7e представляют собой водород.
В еще одном варианте осуществления в формуле XVIb
R1 представляет собой водород или метокси;
R2 представляет собой водород;
R3 и R4 представляют собой водород;
R6 представляет собой дифторметил;
каждый R5a и R5b независимо представляет собой водород или C6-14 алкил;
R7a представляет собой фенил, имидазолил, пиразолил, пиридинил, пиперидинил или пиперазинил, каждый из которых необязательно замещен одним или более заместителями Q; и
R7b, R7c, R7d и R7e представляют собой водород.
В одном варианте осуществления настоящее изобретение относится к соединению формулы XVI, XVIa или XVIb, как описано в настоящем изобретении, или его энантиомеру, смеси энантиомеров, смеси двух или более диастереомеров или изотопному варианту; или их фармацевтически приемлемой соли, сольвату, гидрату или пролекарству; где каждый R5a и R5b независимо представляет собой (a) галоген; (b) C1-6 алкил, C2-6 алкенил, C2-6 алкинил, C3-10 циклоалкил, C6-14 арил, C7-15 аралкил, гетероарил или гетероциклил; или (c) -C(O)R1a, -C(O)OR1a, -C(O)NR1bR1c, -C(NR1a)NR1bR1c, -OR1a, -OC(O)R1a, -OC(O)OR1a, -OC(O)NR1bR1c, -OC(=NR1a)NR1bR1c, -OS(O)R1a, -OS(O)2R1a, -OS(O)NR1bR1c, -OS(O)2NR1bR1c, -NR1bR1c, -NR1aC(O)R1d, -NR1aC(O)OR1d, -NR1aC(O)NR1bR1c, -NR1aC(=NR1d)NR1bR1c, -NR1aS(O)R1d, -NR1aS(O)2R1d, -NR1aS(O)NR1bR1c, -NR1aS(O)2NR1bR1c, -SR1a, -S(O)R1a, -S(O)2R1a, -S(O)NR1bR1c или -S(O)2NR1bR1c; и R1, R2, R3, R4, R6, R7a, R7b, R7c, R7d, R7e, R1a, R1b, R1c и R1d определяют в настоящем изобретении выше.
В одном варианте осуществления, в любой из формул, приведенных в настоящем изобретении,
R1 представляет собой водород или -OR1a, где R1a представляет собой C1-6 алкил, необязательно замещенный одним или более заместителями Q;
R2 представляет собой водород;
R3 и R4 представляют собой водород;
R6 представляет собой C6-14 алкил, необязательно замещенный одним или более заместителями Q;
каждый R5a и R5b независимо представляет собой водород или C6-14 алкил, необязательно замещенный одним или более заместителями Q;
R7a представляет собой C6-14 арил, гетероарил или гетероциклил, каждый из которых необязательно замещен одним или более заместителями Q;
R7b, R7c, R7d и R7e представляют собой водород; и
каждый X, Y и Z независимо представляет собой N или CRx, при условии, что по меньшей мере два из X, Y и Z представляют собой N; где Rx представляет собой водород или C1-6 алкил, необязательно замещенный одним или более заместителями Q.
В другом варианте осуществления в любой из формул, приведенных в настоящем изобретении,
R1 представляет собой водород или метокси;
R2 представляет собой водород;
R3 и R4 представляют собой водород;
R6 представляет собой C6-14 алкил, необязательно замещенный одним или более галогенами;
каждый R5a и R5b независимо представляет собой водород или C6-14 алкил;
R7a представляет собой C6-14 арил, гетероарил или гетероциклил, каждый из которых необязательно замещен одним или более заместителями Q;
R7b, R7c, R7d и R7e представляют собой водород; и
каждый X, Y и Z независимо представляет собой N или CH.
В еще одном варианте осуществления в любой из формул, приведенных в настоящем изобретении,
R1 представляет собой водород или метокси;
R2 представляет собой водород;
R3 и R4 представляют собой водород;
R6 представляет собой дифторметил;
каждый R5a и R5b независимо представляет собой водород или C6-14 алкил;
R7a представляет собой C6-14 арил, моноциклический гетероарил или моноциклический гетероциклил, каждый из которых необязательно замещен одним или более заместителями Q;
R7b, R7c, R7d и R7e представляют собой водород; и
каждый X, Y и Z независимо представляет собой N или CH.
В еще одном варианте осуществления в любой из формул, приведенных в настоящем изобретении,
R1 представляет собой водород или метокси;
R2 представляет собой водород;
R3 и R4 представляют собой водород;
R6 представляет собой дифторметил;
каждый R5a и R5b независимо представляет собой водород или C6-14 алкил;
R7a представляет собой фенил, 5- или 6-членный гетероарил или 5- или 6-членный гетероциклил, каждый из которых необязательно замещен одним или более заместителями Q;
R7b, R7c, R7d и R7e представляют собой водород; и
каждый X, Y и Z независимо представляет собой N или CH.
В еще одном варианте осуществления в любой из формул, приведенных в настоящем изобретении,
R1 представляет собой водород или метокси;
R2 представляет собой водород;
R3 и R4 представляют собой водород;
R6 представляет собой дифторметил;
каждый R5a и R5b независимо представляет собой водород или C6-14 алкил;
R7a представляет собой фенил, имидазолил, пиразолил, пиридинил, пиримидинил, пирролидинил, пиперидинил или пиперазинил, каждый из которых необязательно замещен одним или более заместителями Q;
R7b, R7c, R7d и R7e представляют собой водород; и
каждый X, Y и Z независимо представляет собой N или CH.
В еще одном варианте осуществления в любой из формул, приведенных в настоящем изобретении,
R1 представляет собой водород или метокси;
R2 представляет собой водород;
R3 и R4 представляют собой водород;
R6 представляет собой дифторметил;
каждый R5a и R5b независимо представляет собой водород или C6-14 алкил;
R7a представляет собой фенил, имидазолил, пиразолил, пиридинил, пиперидинил или пиперазинил, каждый из которых необязательно замещен одним или более заместителями Q;
R7b, R7c, R7d и R7e представляют собой водород; и
каждый X, Y и Z независимо представляет собой N или CH.
Группы или переменные R1, R2, R3, R4, R6, R5a, R5b, R5c, R5d, R5e, R5f, R5g, R7a, R7b, R7c, R7d, R7e, m, n, X, Y и Z в формулах, приведенных в настоящем изобретении, например, формулах I-XVI, Ia-XVIa и Ib-XVIb, дополнительно определяют в вариантах осуществления, описанных в настоящем изобретении. Все комбинации вариантов осуществления, приведенные в настоящем изобретении для данных групп и/или переменных, включены в объем настоящего описания.
В определенных вариантах осуществления R1 представляет собой водород. В определенных вариантах осуществления R1 представляет собой циано. В определенных вариантах осуществления R1 представляет собой галоген. В определенных вариантах осуществления R1 представляет собой фтор, хлор, бром или йод. В определенных вариантах осуществления R1 представляет собой нитро. В определенных вариантах осуществления R1 представляет собой C1-6 алкил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R1 представляет собой C2-6 алкенил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R1 представляет собой C2-6 алкинил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R1 представляет собой C3-10 циклоалкил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R1 представляет собой C6-14 арил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R1 представляет собой C7-15 аралкил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R1 представляет собой гетероарил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R1 представляет собой гетероциклил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении.
В определенных вариантах осуществления R1 представляет собой -C(O)R1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R1 представляет собой -C(O)OR1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R1 представляет собой -C(O)NR1bR1c, где каждый R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R1 представляет собой -C(NR1a)NR1bR1c, где каждый R1a, R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R1 представляет собой -OR1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R1 представляет собой -O-C1-6 алкил, где алкил необязательно замещен одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R1 представляет собой метокси, этокси, пропокси, изопропокси или 3-диметиламинопропокси. В определенных вариантах осуществления R1 представляет собой -OC(O)R1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R1 представляет собой -OC(O)OR1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R1 представляет собой -OC(O)NR1bR1c, где каждый R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R1 представляет собой -OC(=NR1a)NR1bR1c, где каждый R1a, R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R1 представляет собой -OS(O)R1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R1 представляет собой -OS(O)2R1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R1 представляет собой -OS(O)NR1bR1c, где каждый R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R1 представляет собой -OS(O)2NR1bR1c, где каждый R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R1 представляет собой -NR1bR1c, где каждый R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R1 представляет собой -NR1aC(O)R1d, где каждый R1a и R1d представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R1 представляет собой -NR1aC(O)OR1d, где каждый R1a и R1d представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R1 представляет собой -NR1aC(O)NR1bR1c, где каждый R1a, R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R1 представляет собой -NR1aC(=NR1d)NR1bR1c, где каждый R1a, R1b, R1c и R1d представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R1 представляет собой -NR1aS(O)R1d, где каждый R1a и R1d представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R1 представляет собой -NR1aS(O)2R1d, где каждый R1a и R1d представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R1 представляет собой -NR1aS(O)NR1bR1c, где каждый R1a, R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R1 представляет собой -NR1aS(O)2NR1bR1c, где каждый R1a, R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R1 представляет собой -SR1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R1 представляет собой -S(O)R1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R1 представляет собой -S(O)2R1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R1 представляет собой -S(O)NR1bR1c, где каждый R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R1 представляет собой -S(O)2NR1bR1c; где каждый R1b и R1c представляет собой, как определено в настоящем изобретении.
В определенных вариантах осуществления R2 представляет собой водород. В определенных вариантах осуществления R2 представляет собой циано. В определенных вариантах осуществления R2 представляет собой галоген. В определенных вариантах осуществления R2 представляет собой фтор, хлор, бром или йод. В определенных вариантах осуществления R2 представляет собой нитро. В определенных вариантах осуществления R2 представляет собой C1-6 алкил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R2 представляет собой C2-6 алкенил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R2 представляет собой C2-6 алкинил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R2 представляет собой C3-10 циклоалкил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R2 представляет собой C3-7 циклоалкил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R2 представляет собой C6-14 арил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R2 представляет собой C7-15 аралкил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R2 представляет собой гетероарил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R2 представляет собой гетероциклил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении.
В определенных вариантах осуществления R2 представляет собой -C(O)R1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R2 представляет собой -C(O)OR1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R2 представляет собой -C(O)NR1bR1c, где каждый R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R2 представляет собой -C(NR1a)NR1bR1c, где каждый R1a, R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R2 представляет собой -OR1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R1 представляет собой -O-C1-6 алкил, где алкил необязательно замещен одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R1 представляет собой метокси, этокси, пропокси, изопропокси или 3-диметиламинопропокси. В определенных вариантах осуществления R2 представляет собой -OC(O)R1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R2 представляет собой -OC(O)OR1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R2 представляет собой -OC(O)NR1bR1c, где каждый R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R2 представляет собой -OC(=NR1a)NR1bR1c, где каждый R1a, R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R2 представляет собой -OS(O)R1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R2 представляет собой -OS(O)2R1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R2 представляет собой -OS(O)NR1bR1c, где каждый R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R2 представляет собой -OS(O)2NR1bR1c, где каждый R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R2 представляет собой -NR1bR1c, где каждый R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R2 представляет собой амино (-NH2). В определенных вариантах осуществления R2 представляет собой -NR1aC(O)R1d, где каждый R1a и R1d представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R2 представляет собой -NR1aC(O)OR1d, где каждый R1a и R1d представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R2 представляет собой -NR1aC(O)NR1bR1c, где каждый R1a, R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R2 представляет собой -NR1aC(=NR1d)NR1bR1c, где каждый R1a, R1b, R1c и R1d представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R2 представляет собой -NR1aS(O)R1d, где каждый R1a и R1d представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R2 представляет собой -NR1aS(O)2R1d, где каждый R1a и R1d представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R2 представляет собой -NR1aS(O)NR1bR1c, где каждый R1a, R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R2 представляет собой -NR1aS(O)2NR1bR1c, где каждый R1a, R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R2 представляет собой -SR1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R2 представляет собой -S(O)R1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R2 представляет собой -S(O)2R1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R2 представляет собой -S(O)NR1bR1c, где каждый R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R2 представляет собой -S(O)2NR1bR1c, где каждый R1b и R1c представляет собой, как определено в настоящем изобретении.
В определенных вариантах осуществления R3 представляет собой водород. В определенных вариантах осуществления R3 представляет собой C1-6 алкил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R3 представляет собой водород, метил, этил или пропил (например, н-пропил, изопропил, или 2-изопропил).
В определенных вариантах осуществления R4 представляет собой водород. В определенных вариантах осуществления R4 представляет собой C1-6 алкил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R4 представляет собой водород, метил, этил или пропил (например, н-пропил, изопропил, или 2-изопропил).
В определенных вариантах осуществления R3 и R4 соединены вместе, образуя связь. В определенных вариантах осуществления R3 и R4 соединены вместе, образуя C1-6 алкилен, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R3 и R4 соединены вместе, образуя метилен, этилен или пропилен, причем каждый необязательно замещен одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R3 и R4 соединены вместе, образуя C1-6 гетероалкилен, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R3 и R4 соединены вместе, образуя C2-6 алкенилен, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R3 и R4 соединены вместе, образуя C2-6 гетероалкенилен, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении.
В определенных вариантах осуществления R6 представляет собой водород. В определенных вариантах осуществления R6 представляет собой C1-6 алкил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R6 представляет собой C1-6 алкил, необязательно замещенный одним или более, в одном варианте осуществления одним, двумя или тремя, галогенами. В определенных вариантах осуществления R6 представляет собой C1-6 алкил, необязательно замещенный одним или более, в одном варианте осуществления одним, двумя или тремя, фторами. В определенных вариантах осуществления R6 представляет собой метил, фторметил, дифторметил или трифторметил. В определенных вариантах осуществления R6 представляет собой дифторметил. В определенных вариантах осуществления R6 представляет собой -S-C1-6 алкил, где алкил необязательно замещен одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R6 представляет собой -S(O)-C1-6 алкил, где алкил необязательно замещен одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R6 представляет собой -SO2-C1-6 алкил, где алкил необязательно замещен одним или более заместителями Q, как описано в настоящем изобретении.
В определенных вариантах осуществления R5a представляет собой водород. В определенных вариантах осуществления R5a не является водородом. В определенных вариантах осуществления R5a представляет собой галоген. В определенных вариантах осуществления R5a представляет собой фтор, хлор, бром или йод. В определенных вариантах осуществления R5a представляет собой C1-6 алкил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R5a представляет собой метил, этил, пропил или бутил, причем каждый необязательно замещен одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R5a представляет собой метил, этил, н-пропил, изопропил, н-бутил, изобутил или трет-бутил. В определенных вариантах осуществления R5a представляет собой метил. В определенных вариантах осуществления R5a представляет собой C2-6 алкенил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R5a представляет собой C2-6 алкинил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R5a представляет собой C3-10 циклоалкил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R5a представляет собой C3-7 циклоалкил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R5a представляет собой C6-14 арил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R5a представляет собой C7-15 аралкил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R5a представляет собой гетероарил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R5a представляет собой гетероциклил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении.
В определенных вариантах осуществления R5a представляет собой -C(O)R1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5a представляет собой -C(O)OR1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5a представляет собой -C(O)OR1a, где R1a представляет собой C1-6 алкил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R5a представляет собой -C(O)OCH3. В определенных вариантах осуществления R5a представляет собой -C(O)NR1bR1c, где каждый R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5a представляет собой -C(NR1a)NR1bR1c, где каждый R1a, R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5a представляет собой -OR1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5a представляет собой -OC(O)R1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5a представляет собой -OC(O)OR1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5a представляет собой -OC(O)NR1bR1c, где каждый R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5a представляет собой -OC(=NR1a)NR1bR1c, где каждый R1a, R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5a представляет собой -OS(O)R1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5a представляет собой -OS(O)2R1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5a представляет собой -OS(O)NR1bR1c, где каждый R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5a представляет собой -OS(O)2NR1bR1c, где каждый R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5a представляет собой -NR1bR1c, где каждый R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5a представляет собой амино (-NH2). В определенных вариантах осуществления R5a представляет собой -NR1aC(O)R1d, где каждый R1a и R1d представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5a представляет собой -NR1aC(O)OR1d, где каждый R1a и R1d представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5a представляет собой -NR1aC(O)NR1bR1c, где каждый R1a, R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5a представляет собой -NR1aC(=NR1d)NR1bR1c, где каждый R1a, R1b, R1c и R1d представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5a представляет собой -NR1aS(O)R1d, где каждый R1a и R1d представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5a представляет собой -NR1aS(O)2R1d, где каждый R1a и R1d представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5a представляет собой -NR1aS(O)NR1bR1c, где каждый R1a, R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5a представляет собой -NR1aS(O)2NR1bR1c, где каждый R1a, R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5a представляет собой -SR1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5a представляет собой -S(O)R1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5a представляет собой -S(O)2R1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5a представляет собой -S(O)NR1bR1c, где каждый R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5a представляет собой -S(O)2NR1bR1c, где каждый R1b и R1c представляет собой, как определено в настоящем изобретении.
В определенных вариантах осуществления R5a представляет собой (a) водород или галоген; (b) C1-6 алкил, C2-6 алкенил, C2-6 алкинил, C3-10 циклоалкил, C6-14 арил, C7-15 аралкил или гетероарил, каждый из которых необязательно замещен одним или более заместителями Q; или (c) -C(O)R1a, -C(O)OR1a, -C(O)NR1bR1c, -C(NR1a)NR1bR1c, -OR1a, -OC(O)R1a, -OC(O)OR1a, -OC(O)NR1bR1c, -OC(=NR1a)NR1bR1c, -OS(O)R1a, -OS(O)2R1a, -OS(O)NR1bR1c, -OS(O)2NR1bR1c, -NR1bR1c, -NR1aC(O)R1d, -NR1aC(O)OR1d, -NR1aC(O)NR1bR1c, -NR1aC(=NR1d)NR1bR1c, -NR1aS(O)R1d, -NR1aS(O)2R1d, -NR1aS(O)NR1bR1c, -NR1aS(O)2NR1bR1c, -SR1a, -S(O)R1a, -S(O)2R1a, -S(O)NR1bR1c или -S(O)2NR1bR1c. В определенных вариантах осуществления R5a представляет собой (a) водород или галоген; или (b) C1-6 алкил, C2-6 алкенил, C2-6 алкинил, C3-10 циклоалкил, C6-14 арил, C7-15 аралкил или гетероарил, каждый из которых необязательно замещен одним или более заместителями Q.
В определенных вариантах осуществления R5b представляет собой галоген. В определенных вариантах осуществления R5b представляет собой фтор, хлор, бром или йод. В определенных вариантах осуществления R5b представляет собой C1-6 алкил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R5b представляет собой метил, этил, пропил или бутил, причем каждый необязательно замещен одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R5b представляет собой метил, этил, н-пропил, изопропил, н-бутил, изобутил или трет-бутил. В определенных вариантах осуществления R5b представляет собой метил. В определенных вариантах осуществления R5b представляет собой C2-6 алкенил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R5b представляет собой C2-6 алкинил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R5b представляет собой C3-10 циклоалкил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R5b представляет собой C3-7 циклоалкил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R5b представляет собой C6-14 арил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R5b представляет собой C7-15 аралкил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R5b представляет собой гетероарил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R5b представляет собой гетероциклил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R5b не является гетероциклилом.
В определенных вариантах осуществления R5b представляет собой -C(O)R1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5b представляет собой -C(O)OR1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5b представляет собой -C(O)OR1a, где R1a представляет собой C1-6 алкил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R5b представляет собой -C(O)OCH3. В определенных вариантах осуществления R5b представляет собой -C(O)NR1bR1c, где каждый R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5b представляет собой -C(NR1a)NR1bR1c, где R1a каждый, R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5b представляет собой -OR1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5b представляет собой -OC(O)R1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5b представляет собой -OC(O)OR1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5b представляет собой -OC(O)NR1bR1c, где каждый R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5b представляет собой -OC(=NR1a)NR1bR1c, где каждый R1a, R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5b представляет собой -OS(O)R1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5b представляет собой -OS(O)2R1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5b представляет собой -OS(O)NR1bR1c, где каждый R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5b представляет собой -OS(O)2NR1bR1c, где каждый R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5b представляет собой -NR1bR1c, где каждый R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5b представляет собой амино (-NH2). В определенных вариантах осуществления R5b представляет собой -NR1aC(O)R1d, где каждый R1a и R1d представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5b представляет собой -NR1aC(O)OR1d, где каждый R1a и R1d представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5b представляет собой -NR1aC(O)NR1bR1c, где каждый R1a, R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5b представляет собой -NR1aC(=NR1d)NR1bR1c, где каждый R1a, R1b, R1c и R1d представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5b представляет собой -NR1aS(O)R1d, где каждый R1a и R1d представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5b представляет собой -NR1aS(O)2R1d, где каждый R1a и R1d представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5b представляет собой -NR1aS(O)NR1bR1c, где каждый R1a, R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5b представляет собой -NR1aS(O)2NR1bR1c, где каждый R1a, R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5b представляет собой -SR1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5b представляет собой -S(O)R1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5b представляет собой -S(O)2R1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5b представляет собой -S(O)NR1bR1c, где каждый R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5b представляет собой -S(O)2NR1bR1c, где каждый R1b и R1c представляет собой, как определено в настоящем изобретении.
В определенных вариантах осуществления каждый R5a и R5b независимо представляет собой метил, этил, н-пропил, изопропил, н-бутил, изобутил или трет-бутил, причем каждый необязательно замещен одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления каждый R5a и R5b независимо представляет собой метил, этил, н-пропил, изопропил, н-бутил, изобутил или трет-бутил, причем каждый необязательно замещен одним или более галогенами. В определенных вариантах осуществления каждый R5a и R5b независимо представляет собой метил, этил, н-пропил, изопропил, н-бутил, изобутил или трет-бутил. В определенных вариантах осуществления каждый R5a и R5b представляет собой метил.
В определенных вариантах осуществления R5c представляет собой C6-14 арил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R5b представляет собой C6-14 арил, замещенный по 2 положению одним заместителем Q, как описано в настоящем изобретении. В определенных вариантах осуществления R5c представляет собой фенил или нафтил, причем каждый необязательно замещен одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R5c представляет собой фенил, нафта-1-ил или нафта-2-ил, причем каждый необязательно замещен одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R5c представляет собой фенил, 4-хлорфенил, 4-метоксифенил или нафта-2-ил. В определенных вариантах осуществления R5c представляет собой гетероарил, необязательно замещенный одним или более заместителями, как описано в настоящем изобретении. В определенных вариантах осуществления R5c представляет собой моноциклический гетероарил, необязательно замещенный одним или более заместителями, как описано в настоящем изобретении. В определенных вариантах осуществления R5c представляет собой 5- или 6-членный гетероарил, необязательно замещенный одним или более заместителями, как описано в настоящем изобретении. В определенных вариантах осуществления R5c представляет собой бициклический гетероарил, необязательно замещенный одним или более заместителями, как описано в настоящем изобретении.
В определенных вариантах осуществления R5c представляет собой -(CR5fR5g)n-(C6-14 арил), где C6-14 арил необязательно замещен одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R5c представляет собой бензил, 2-фенэтил, 3-фенилпропил или 4-фенилбутил, где каждая из фенильных групп необязательно замещена одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R5c представляет собой бензил, 2-фенэтил, 3-фенилпропил или 4-фенилбутил. В определенных вариантах осуществления R5c представляет собой бензил, фторбензил, хлорбензил, бромбензил, цианобензил, метилбензил или метоксибензил. В определенных вариантах осуществления R5c представляет собой (нафталин-1-ил)метил, (нафталин-2-ил)метил 2-(нафталин-1-ил)этил, 2-(нафталин-2-ил)этил, 3-(нафталин-1-ил)пропил, 3-(нафталин-2-ил)пропил, 4-(нафталин-1-ил)бутил или 4-(нафталин-2-ил)бутил, где каждая из нафтильных групп необязательно замещена одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления, n равно 0 или 1. В одном варианте осуществления n равно 1. В одном варианте осуществления n равно 1, 2, 3 или 4. В определенных вариантах осуществления R5c представляет собой -CH2-(C6-14 арил), где C6-14 арил необязательно замещен одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R5c представляет собой -C(CH3)2-(C6-14 арил), где C6-14 арил необязательно замещен одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R5c представляет собой -CH2-фенил или -CH2-нафтил, где каждый фенил или нафтил необязательно замещен одним или более заместителями Q, как описано в настоящем изобретении, такими как, например, необязательно замещены одним или более F, Cl, Br, I, -CN, -CH3, -CF3, -OCH3 или -OCF3. В определенных вариантах осуществления R5c представляет собой -CH2-фенил, -CH2-нафта-1-ил или -CH2-нафта-2-ил, где каждый фенил или нафтил необязательно замещен одним или более заместителями Q, как описано в настоящем изобретении, такими как, например, необязательно замещены одним или более F, Cl, Br, I, -CN, -CH3, -CF3, -OCH3 или -OCF3. В определенных вариантах осуществления R5c представляет собой -CH2-фенил, -CH2-нафт-1-ил или -CH2-нафт-2-ил, где каждый фенил или нафтил необязательно замещен одним или более F, Cl, Br, I, -CN, -CH3, -CF3, -OCH3, -OCF3. В других вариантах осуществления R5c представляет собой -CH2-фенил, -CH2-нафта-1-ил или -CH2-нафт-2-ил, где каждый фенил или нафтил необязательно замещен одним или более F, Cl, Br, I, -CN, -CH3, -CF3, -OCH3, -OCF3, -O-(C1-4 алкилен)-N-(C1-4 алкил)2 (например, -O-CH2CH2-N(CH3)2), -O-гетероциклил (например, -O-(N-метилпиперидинил) или -O-пиперидинил), -O-гетероарил (например, -O-пиридил), -NH-гетероциклил (например, -NH-(N-метилпиперидинил), -NH-(N-метилпирролидинил), -NH-пиперидинил, или -NH-пирролидинил), -NH-гетероарил (например, -NH-пиридил), -NCH3-гетероциклил (например, -NCH3-(N-метилпиперидинил), -NCH3-(N-метилпирролидинил), -NCH3-пиперидинил или -NCH3-пирролидинил), -NCH3-гетероарил (например, -NCH3-пиридил), гетероциклил (например, пиперидинил, пиперазинил, N-метилпиперидинил или N-метилпиперазинил) или гетероарил (например, пиридил или имидазолил). В определенных вариантах осуществления R5c представляет собой -CH2-фенил, -C(CH3)2-фенил, -CH2-(2-метилфенил), -CH2-(2-метоксифенил), -CH2-(2-фторфенил), -CH2-(2-хлорфенил), -CH2-(2-бромфенил), -CH2-(3-метилфенил), -CH2-(3-метоксифенил), -CH2-(3-фторфенил), -CH2-(3-хлорфенил), -CH2-(3-бромфенил), -CH2-(4-метилфенил), -CH2-(4-метоксифенил), -CH2-(4-фторфенил), -CH2-(4-хлорфенил), -CH2-(4-бромфенил), -CH2-нафта-1-ил или -CH2-нафта-2-ил.
В определенных вариантах осуществления R5c представляет собой -(CR5fR5g)-(C6-14 арил), где C6-14 арил необязательно замещен одним или более заместителями Q, как описано в настоящем изобретении, и где R5f и R5g вместе с атомом углерода, с которым они соединены, образуют 3-6-членный циклоалкил или гетероциклил. В одном варианте осуществления R5c представляет собой -циклопропилфенил. В одном варианте осуществления R5c представляет собой -циклобутилфенил. В одном варианте осуществления R5c представляет собой -циклопентилфенил. В одном варианте осуществления R5c представляет собой -циклогексилфенил.
В определенных вариантах осуществления R5c представляет собой -(CR5fR5g)n-гетероарил, где гетероарил необязательно замещен одним или более заместителями Q, как описано в настоящем изобретении, где n определяют в настоящем изобретении выше. В определенных вариантах осуществления R5c представляет собой -CH2-(моноциклический гетероарил), где гетероарил необязательно замещен одним или более заместителями, как описано в настоящем изобретении. В определенных вариантах осуществления R5c представляет собой -CH2-(5- или 6-членный гетероарил), где гетероарил необязательно замещен одним или более заместителями, как описано в настоящем изобретении. В определенных вариантах осуществления R5c представляет собой -CH2-(бициклический гетероарил), где гетероарил необязательно замещен одним или более заместителями, как описано в настоящем изобретении.
В определенных вариантах осуществления R5d представляет собой водород. В определенных вариантах осуществления R5d представляет собой галоген. В определенных вариантах осуществления R5d представляет собой фтор, хлор, бром или йод. В определенных вариантах осуществления R5d представляет собой C1-6 алкил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R5d представляет собой метил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R5d представляет собой метил. В определенных вариантах осуществления R5d представляет собой метил, этил, пропил или бутил, причем каждый необязательно замещен одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R5d представляет собой метил, этил, н-пропил, изопропил, н-бутил, изобутил или трет-бутил. В определенных вариантах осуществления R5d представляет собой C2-6 алкенил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R5d представляет собой C2-6 алкинил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R5d представляет собой C3-10 циклоалкил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R5d представляет собой C6-14 арил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R5d представляет собой C7-15 аралкил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R5d представляет собой гетероарил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R5d представляет собой гетероциклил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении.
В определенных вариантах осуществления R5d представляет собой -C(O)R1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5d представляет собой -C(O)OR1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5d представляет собой -C(O)OR1a, где R1a представляет собой C1-6 алкил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R5d представляет собой -C(O)OCH3. В определенных вариантах осуществления R5d представляет собой -C(O)NR1bR1c, где каждый R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5d представляет собой -C(NR1a)NR1bR1c, где каждый R1a, R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5d представляет собой -OR1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5d представляет собой -OC(O)R1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5d представляет собой -OC(O)OR1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5d представляет собой -OC(O)NR1bR1c, где каждый R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5d представляет собой -OC(=NR1a)NR1bR1c, где каждый R1a, R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5d представляет собой -OS(O)R1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5d представляет собой -OS(O)2R1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5d представляет собой -OS(O)NR1bR1c, где каждый R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5d представляет собой -OS(O)2NR1bR1c, где каждый R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5d представляет собой -NR1bR1c, где каждый R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5d представляет собой амино (-NH2). В определенных вариантах осуществления R5d представляет собой -NR1aC(O)R1d, где каждый R1a и R1d представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5d представляет собой -NR1aC(O)OR1d, где каждый R1a и R1d представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5d представляет собой -NR1aC(O)NR1bR1c, где каждый R1a, R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5d представляет собой -NR1aC(=NR1d)NR1bR1c, где каждый R1a, R1b, R1c и R1d представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5d представляет собой -NR1aS(O)R1d, где каждый R1a и R1d представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5d представляет собой -NR1aS(O)2R1d, где каждый R1a и R1d представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5d представляет собой -NR1aS(O)NR1bR1c, где каждый R1a, R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5d представляет собой -NR1aS(O)2NR1bR1c, где каждый R1a, R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5d представляет собой -SR1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5d представляет собой -S(O)R1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5d представляет собой -S(O)2R1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5d представляет собой -S(O)NR1bR1c, где каждый R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5d представляет собой -S(O)2NR1bR1c, где каждый R1b и R1c представляет собой, как определено в настоящем изобретении.
В определенных вариантах осуществления R5e представляет собой водород. В определенных вариантах осуществления R5e представляет собой галоген. В определенных вариантах осуществления R5e представляет собой фтор, хлор, бром или йод. В определенных вариантах осуществления R5e представляет собой C1-6 алкил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R5e представляет собой метил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R5e представляет собой метил. В определенных вариантах осуществления R5e представляет собой метил, этил, пропил или бутил, причем каждый необязательно замещен одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R5e представляет собой метил, этил, н-пропил, изопропил, н-бутил, изобутил или трет-бутил. В определенных вариантах осуществления R5e представляет собой C2-6 алкенил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R5e представляет собой C2-6 алкинил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R5e представляет собой C3-10 циклоалкил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R5e представляет собой C6-14 арил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R5e представляет собой C7-15 аралкил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R5e представляет собой гетероарил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R5e представляет собой гетероциклил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении.
В определенных вариантах осуществления R5e представляет собой -C(O)R1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5e представляет собой -C(O)OR1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5e представляет собой -C(O)OR1a, где R1a представляет собой C1-6 алкил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R5e представляет собой -C(O)OCH3. В определенных вариантах осуществления R5e представляет собой -C(O)NR1bR1c, где каждый R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5e представляет собой -C(NR1a)NR1bR1c, где каждый R1a, R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5e представляет собой -OR1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5e представляет собой -OC(O)R1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5e представляет собой -OC(O)OR1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5e представляет собой -OC(O)NR1bR1c, где каждый R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5e представляет собой -OC(=NR1a)NR1bR1c, где каждый R1a, R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5e представляет собой -OS(O)R1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5e представляет собой -OS(O)2R1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5e представляет собой -OS(O)NR1bR1c, где каждый R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5e представляет собой -OS(O)2NR1bR1c, где каждый R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5e представляет собой -NR1bR1c, где каждый R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5e представляет собой амино (-NH2). В определенных вариантах осуществления R5e представляет собой -NR1aC(O)R1d, где каждый R1a и R1d представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5e представляет собой -NR1aC(O)OR1d, где каждый R1a и R1d представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5e представляет собой -NR1aC(O)NR1bR1c, где каждый R1a, R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5e представляет собой -NR1aC(=NR1d)NR1bR1c, где каждый R1a, R1b, R1c и R1d представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5e представляет собой -NR1aS(O)R1d, где каждый R1a и R1d представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5e представляет собой -NR1aS(O)2R1d, где каждый R1a и R1d представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5e представляет собой -NR1aS(O)NR1bR1c, где каждый R1a, R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5e представляет собой -NR1aS(O)2NR1bR1c, где каждый R1a, R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5e представляет собой -SR1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5e представляет собой -S(O)R1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5e представляет собой -S(O)2R1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5e представляет собой -S(O)NR1bR1c, где каждый R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5e представляет собой -S(O)2NR1bR1c, где каждый R1b и R1c представляет собой, как определено в настоящем изобретении.
В определенных вариантах осуществления R5f представляет собой водород. В определенных вариантах осуществления R5f представляет собой галоген. В определенных вариантах осуществления R5f представляет собой фтор, хлор, бром или йод. В определенных вариантах осуществления R5f представляет собой C1-6 алкил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R5f представляет собой метил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R5f представляет собой метил. В определенных вариантах осуществления R5f представляет собой метил, этил, пропил или бутил, причем каждый необязательно замещен одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R5f представляет собой метил, этил, н-пропил, изопропил, н-бутил, изобутил или трет-бутил. В определенных вариантах осуществления R5f представляет собой C2-6 алкенил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R5f представляет собой C2-6 алкинил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R5f представляет собой C3-10 циклоалкил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R5f представляет собой C6-14 арил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R5f представляет собой C7-15 аралкил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R5f представляет собой гетероарил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R5f представляет собой гетероциклил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении.
В определенных вариантах осуществления R5f представляет собой -C(O)R1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5f представляет собой -C(O)OR1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5f представляет собой -C(O)OR1a, где R1a представляет собой C1-6 алкил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R5f представляет собой -C(O)OCH3. В определенных вариантах осуществления R5f представляет собой -C(O)NR1bR1c, где каждый R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5f представляет собой -C(NR1a)NR1bR1c, где каждый R1a, R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5f представляет собой -OR1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5f представляет собой -OC(O)R1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5f представляет собой -OC(O)OR1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5f представляет собой -OC(O)NR1bR1c, где каждый R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5f представляет собой -OC(=NR1a)NR1bR1c, где каждый R1a, R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5f представляет собой -OS(O)R1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5f представляет собой -OS(O)2R1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5f представляет собой -OS(O)NR1bR1c, где каждый R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5f представляет собой -OS(O)2NR1bR1c, где каждый R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5f представляет собой -NR1bR1c, где каждый R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5f представляет собой амино (-NH2). В определенных вариантах осуществления R5f представляет собой -NR1aC(O)R1d, где каждый R1a и R1d представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5f представляет собой -NR1aC(O)OR1d, где каждый R1a и R1d представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5f представляет собой -NR1aC(O)NR1bR1c, где каждый R1a, R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5f представляет собой -NR1aC(=NR1d)NR1bR1c, где каждый R1a, R1b, R1c и R1d представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5f представляет собой -NR1aS(O)R1d, где каждый R1a и R1d представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5f представляет собой -NR1aS(O)2R1d, где каждый R1a и R1d представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5f представляет собой -NR1aS(O)NR1bR1c, где каждый R1a, R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5f представляет собой -NR1aS(O)2NR1bR1c, где каждый R1a, R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5f представляет собой -SR1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5f представляет собой -S(O)R1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5f представляет собой -S(O)2R1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5f представляет собой -S(O)NR1bR1c, где каждый R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5f представляет собой -S(O)2NR1bR1c, где каждый R1b и R1c представляет собой, как определено в настоящем изобретении.
В определенных вариантах осуществления R5g представляет собой водород. В определенных вариантах осуществления R5g представляет собой галоген. В определенных вариантах осуществления R5g представляет собой фтор, хлор, бром или йод. В определенных вариантах осуществления R5g представляет собой C1-6 алкил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R5g представляет собой метил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R5g представляет собой метил. В определенных вариантах осуществления R5g представляет собой метил, этил, пропил или бутил, причем каждый необязательно замещен одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R5g представляет собой метил, этил, н-пропил, изопропил, н-бутил, изобутил или трет-бутил. В определенных вариантах осуществления R5g представляет собой C2-6 алкенил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R5g представляет собой C2-6 алкинил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R5g представляет собой C3-10 циклоалкил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R5g представляет собой C6-14 арил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R5g представляет собой C7-15 аралкил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R5g представляет собой гетероарил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R5g представляет собой гетероциклил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении.
В определенных вариантах осуществления R5g представляет собой -C(O)R1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5g представляет собой -C(O)OR1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5g представляет собой -C(O)OR1a, где R1a представляет собой C1-6 алкил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R5g представляет собой -C(O)OCH3. В определенных вариантах осуществления R5g представляет собой -C(O)NR1bR1c, где каждый R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5g представляет собой -C(NR1a)NR1bR1c, где каждый R1a, R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5g представляет собой -OR1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5g представляет собой -OC(O)R1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5g представляет собой -OC(O)OR1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5g представляет собой -OC(O)NR1bR1c, где каждый R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5g представляет собой -OC(=NR1a)NR1bR1c, где каждый R1a, R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5g представляет собой -OS(O)R1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5g представляет собой -OS(O)2R1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5g представляет собой -OS(O)NR1bR1c, где каждый R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5g представляет собой -OS(O)2NR1bR1c, где каждый R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5g представляет собой -NR1bR1c, где каждый R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5g представляет собой амино (-NH2). В определенных вариантах осуществления R5g представляет собой -NR1aC(O)R1d, где каждый R1a и R1d представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5g представляет собой -NR1aC(O)OR1d, где каждый R1a и R1d представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5g представляет собой -NR1aC(O)NR1bR1c, где каждый R1a, R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5g представляет собой -NR1aC(=NR1d)NR1bR1c, где каждый R1a, R1b, R1c и R1d представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5g представляет собой -NR1aS(O)R1d, где каждый R1a и R1d представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5g представляет собой -NR1aS(O)2R1d, где каждый R1a и R1d представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5g представляет собой -NR1aS(O)NR1bR1c, где каждый R1a, R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5g представляет собой -NR1aS(O)2NR1bR1c, где каждый R1a, R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5g представляет собой -SR1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5g представляет собой -S(O)R1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5g представляет собой -S(O)2R1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5g представляет собой -S(O)NR1bR1c, где каждый R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R5g представляет собой -S(O)2NR1bR1c, где каждый R1b и R1c представляет собой, как определено в настоящем изобретении.
В определенных вариантах осуществления, когда один экземпляр R5f и один экземпляр R5g соединены с одним и тем же атомом углерода, R5f и R5g вместе с атомом углерода, с которым они соединены, образуют C3-10 циклоалкил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления, когда один экземпляр R5f и один экземпляр R5g соединены с одним и тем же атомом углерода, R5f и R5g вместе с атомом углерода, с которым они соединены, образуют C3-7 циклоалкил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления, когда один экземпляр R5f и один экземпляр R5g соединены с одним и тем же атомом углерода, R5f и R5g вместе с атомом углерода, с которым они соединены, образуют циклопропил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления, когда один экземпляр R5f и один экземпляр R5g соединены с одним и тем же атомом углерода, R5f и R5g вместе с атомом углерода, с которым они соединены, образуют циклобутил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления, когда один экземпляр R5f и один экземпляр R5g соединены с одним и тем же атомом углерода, R5f и R5g вместе с атомом углерода, с которым они соединены, образуют циклопентил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления, когда один экземпляр R5f и один экземпляр R5g соединены с одним и тем же атомом углерода, R5f и R5g вместе с атомом углерода, с которым они соединены, образуют циклогексил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления, когда один экземпляр R5f и один экземпляр R5g соединены с одним и тем же атомом углерода, R5f и R5g вместе с атомом углерода, с которым они соединены, образуют циклогептил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления, когда один экземпляр R5f и один экземпляр R5g соединены с одним и тем же атомом углерода, R5f и R5g вместе с атомом углерода, с которым они соединены, образуют циклопропил.
В определенных вариантах осуществления, когда один экземпляр R5f и один экземпляр R5g соединены с одним и тем же атомом углерода, R5f и R5g вместе с атомом углерода, с которым они соединены, образуют гетероциклил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления, когда один экземпляр R5f и один экземпляр R5g соединены с одним и тем же атомом углерода, R5f и R5g вместе с атомом углерода, с которым они соединены, образуют 3-членный гетероциклил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления, когда один экземпляр R5f и один экземпляр R5g соединены с одним и тем же атомом углерода, R5f и R5g вместе с атомом углерода, с которым они соединены, образуют 4-членный гетероциклил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления, когда один экземпляр R5f и один экземпляр R5g соединены с одним и тем же атомом углерода, R5f и R5g вместе с атомом углерода, с которым они соединены, образуют 5-членный гетероциклил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления, когда один экземпляр R5f и один экземпляр R5g соединены с одним и тем же атомом углерода, R5f и R5g вместе с атомом углерода, с которым они соединены, образуют 6-членный гетероциклил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении.
В определенных вариантах осуществления R7a представляет собой водород. В определенных вариантах осуществления R7a представляет собой циано. В определенных вариантах осуществления R7a представляет собой галоген. В определенных вариантах осуществления R7a представляет собой фтор, хлор, бром или йод. В определенных вариантах осуществления R7a представляет собой нитро. В определенных вариантах осуществления R7a представляет собой C1-6 алкил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R7a представляет собой C2-6 алкенил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R7a представляет собой C2-6 алкинил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R7a представляет собой C3-7 циклоалкил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R7a представляет собой C3-10 циклоалкил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R7a представляет собой C6-14 арил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R7a представляет собой фенил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R7a представляет собой фенил, необязательно замещенный одним или более заместителями, каждый из которых независимо выбран из группы, состоящей из фтора, хлора, брома, метила и метокси. В определенных вариантах осуществления R7a представляет собой фенил, 2-фторфенил, 2-хлорфенил, 2-бромфенил, 2-метилфенил, 2-метоксифенил, 3-фторфенил, 3-хлорфенил, 3-метоксифенил, 4-фторфенил, 4-хлорфенил, 4-бромфенил, 4-метоксифенил. В определенных вариантах осуществления R7a представляет собой C7-15 аралкил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R7a представляет собой гетероарил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R7a представляет собой моноциклический гетероарил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R7a представляет собой 5-членный гетероарил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R7a представляет собой имидазолил или пиразолил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R7a представляет собой имидазол-1-ил, пиразол-4-ил, 1-метилпиразол-4-ил или 2-метилпиразол-3-ил. В определенных вариантах осуществления R7a представляет собой 6-членный гетероарил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R7a представляет собой пиридинил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R7a представляет собой пиридин-2-ил, пиридин-3-ил, пиридин-4-ил, 2-метилпиридин-4-ил или 2-метоксипиридин-4-ил. В определенных вариантах осуществления R7a представляет собой гетероциклил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R7a представляет собой моноциклический гетероциклил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R7a представляет собой 5-членный гетероциклил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R7a представляет собой 6-членный гетероциклил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R7a представляет собой пиперидинил или пиперазинил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R7a представляет собой 1-метилпиперидин-4-ил или 4-метилпиперазин-1-ил. В определенных вариантах осуществления R7a представляет собой -C(O)R1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7a представляет собой -C(O)OR1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7a представляет собой -C(O)NR1bR1c, где каждый R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7a представляет собой -C(NR1a)NR1bR1c, где каждый R1a, R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7a представляет собой -OR1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R1 представляет собой -O-C1-6 алкил, где алкил необязательно замещен одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R1 представляет собой метокси, этокси, пропокси, изопропокси или 3-диметиламинопропокси. В определенных вариантах осуществления R7a представляет собой -OC(O)R1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7a представляет собой -OC(O)OR1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7a представляет собой -OC(O)NR1bR1c, где каждый R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7a представляет собой -OC(=NR1a)NR1bR1c, где каждый R1a, R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7a представляет собой -OS(O)R1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7a представляет собой -OS(O)2R1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7a представляет собой -OS(O)NR1bR1c, где каждый R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7a представляет собой -OS(O)2NR1bR1c, где каждый R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7a представляет собой -NR1bR1c, где каждый R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7a представляет собой амино (-NH2). В определенных вариантах осуществления R7a представляет собой -NR1aC(O)R1d, где каждый R1a и R1d представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7a представляет собой -NR1aC(O)OR1d, где каждый R1a и R1d представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7a представляет собой -NR1aC(O)NR1bR1c, где каждый R1a, R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7a представляет собой -NR1aC(=NR1d)NR1bR1c, где каждый R1a, R1b, R1c и R1d представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7a представляет собой -NR1aS(O)R1d, где каждый R1a и R1d представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7a представляет собой -NR1aS(O)2R1d, где каждый R1a и R1d представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7a представляет собой -NR1aS(O)NR1bR1c, где каждый R1a, R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7a представляет собой -NR1aS(O)2NR1bR1c, где каждый R1a, R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7a представляет собой -SR1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7a представляет собой -S(O)R1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7a представляет собой -S(O)2R1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7a представляет собой -S(O)NR1bR1c, где каждый R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7a представляет собой -S(O)2NR1bR1c; где каждый R1b и R1c представляет собой, как определено в настоящем изобретении.
В определенных вариантах осуществления R7a представляет собой фенил, имидазолил, пиразолил, пиридинил, пиримидинил, пирролидинил, пиперидинил или пиперазинил, причем каждый необязательно замещен одним или более заместителями Q. В определенных вариантах осуществления R7a представляет собой фенил, 2-фторфенил, 2-хлорфенил, 2-бромфенил, 2-метилфенил, 2-(3-диметиламинопропил)фенил, 2-метоксифенил, 3-фторфенил, 3-хлорфенил, 3-метилфенил, 3-метоксифенил, 4-фторфенил, 4-хлорфенил, 4-бромфенил, 4-метоксифенил, 2,4-дифторфенил, 2,6-дифторфенил, 4-фтор-3-метоксифенил, 3-метоксифенил, 4-метоксифенил, 3-морфолин-4-илметилфенил, имидазол-1-ил, пиразол-4-ил, 1-метилпиразол-4-ил, 2-метилпиразол-3-ил, пиридин-2-ил, пиридин-3-ил, пиридин-4-ил, 2-фторпиридин-3-ил, 2-метилпиридин-4-ил, 2-(4-метилпиперазин-1-ил)пиридин-4-ил, 2-метоксипиридин-4-ил, пиримидин-5-ил, пирролидин-3-ил, 1-метилпирролидин-3-ил, пиперидин-4-ил, 1-метилпиперидин-4-ил, 1-этилпиперидин-4-ил, 1-изопропилпиперидин-4-ил, 1-ацетилпиперидин-4-ил, 1-метилсульфонилпиперидин-4-ил или 4-метилпиперазин-1-ил.
В определенных вариантах осуществления R7b представляет собой водород. В определенных вариантах осуществления R7b представляет собой циано. В определенных вариантах осуществления R7b представляет собой галоген. В определенных вариантах осуществления R7b представляет собой фтор, хлор, бром или йод. В определенных вариантах осуществления R7b представляет собой нитро. В определенных вариантах осуществления R7b представляет собой C1-6 алкил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R7b представляет собой C2-6 алкенил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R7b представляет собой C2-6 алкинил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R7b представляет собой C3-10 циклоалкил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R7b представляет собой C3-7 циклоалкил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R7b представляет собой C6-14 арил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R7b представляет собой C7-15 аралкил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R7b представляет собой гетероарил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R7b представляет собой гетероциклил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении.
В определенных вариантах осуществления R7b представляет собой -C(O)R1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7b представляет собой -C(O)OR1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7b представляет собой -C(O)NR1bR1c, где каждый R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7b представляет собой -C(NR1a)NR1bR1c, где каждый R1a, R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7b представляет собой -OR1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R1 представляет собой -O-C1-6 алкил, где алкил необязательно замещен одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R1 представляет собой метокси, этокси, пропокси, изопропокси или 3-диметиламинопропокси. В определенных вариантах осуществления R7b представляет собой -OC(O)R1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7b представляет собой -OC(O)OR1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7b представляет собой -OC(O)NR1bR1c, где каждый R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7b представляет собой -OC(=NR1a)NR1bR1c, где каждый R1a, R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7b представляет собой -OS(O)R1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7b представляет собой -OS(O)2R1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7b представляет собой -OS(O)NR1bR1c, где каждый R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7b представляет собой -OS(O)2NR1bR1c, где каждый R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7b представляет собой -NR1bR1c, где каждый R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7b представляет собой амино (-NH2). В определенных вариантах осуществления R7b представляет собой -NR1aC(O)R1d, где каждый R1a и R1d представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7b представляет собой -NR1aC(O)OR1d, где каждый R1a и R1d представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7b представляет собой -NR1aC(O)NR1bR1c, где каждый R1a, R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7b представляет собой -NR1aC(=NR1d)NR1bR1c, где каждый R1a, R1b, R1c и R1d представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7b представляет собой -NR1aS(O)R1d, где каждый R1a и R1d представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7b представляет собой -NR1aS(O)2R1d, где каждый R1a и R1d представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7b представляет собой -NR1aS(O)NR1bR1c, где каждый R1a, R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7b представляет собой -NR1aS(O)2NR1bR1c, где каждый R1a, R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7b представляет собой -SR1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7b представляет собой -S(O)R1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7b представляет собой -S(O)2R1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7b представляет собой -S(O)NR1bR1c, где каждый R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7b представляет собой -S(O)2NR1bR1c, где каждый R1b и R1c представляет собой, как определено в настоящем изобретении.
В определенных вариантах осуществления R7b представляет собой фенил, имидазолил, пиразолил, пиридинил, пиримидинил, пирролидинил, пиперидинил или пиперазинил, причем каждый необязательно замещен одним или более заместителями Q. В определенных вариантах осуществления R7b представляет собой фенил, 2-фторфенил, 2-хлорфенил, 2-бромфенил, 2-метилфенил, 2-(3-диметиламинопропил)фенил, 2-метоксифенил, 3-фторфенил, 3-хлорфенил, 3-метилфенил, 3-метоксифенил, 4-фторфенил, 4-хлорфенил, 4-бромфенил, 4-метоксифенил, 2,4-дифторфенил, 2,6-дифторфенил, 4-фтор-3-метоксифенил, 3-метоксифенил, 4-метоксифенил, 3-морфолин-4-илметилфенил, имидазол-1-ил, пиразол-4-ил, 1-метилпиразол-4-ил, 2-метилпиразол-3-ил, пиридин-2-ил, пиридин-3-ил, пиридин-4-ил, 2-фторпиридин-3-ил, 2-метилпиридин-4-ил, 2-(4-метилпиперазин-1-ил)пиридин-4-ил, 2-метоксипиридин-4-ил, пиримидин-5-ил, пирролидин-3-ил, 1-метилпирролидин-3-ил, пиперидин-4-ил, 1-метилпиперидин-4-ил, 1-этилпиперидин-4-ил, 1-изопропилпиперидин-4-ил, 1-ацетилпиперидин-4-ил, 1-метилсульфонилпиперидин-4-ил или 4-метилпиперазин-1-ил.
В определенных вариантах осуществления R7c представляет собой водород. В определенных вариантах осуществления R7c представляет собой циано. В определенных вариантах осуществления R7c представляет собой галоген. В определенных вариантах осуществления R7c представляет собой фтор, хлор, бром или йод. В определенных вариантах осуществления R7c представляет собой нитро. В определенных вариантах осуществления R7c представляет собой C1-6 алкил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R7c представляет собой C2-6 алкенил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R7c представляет собой C2-6 алкинил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R7c представляет собой C3-10 циклоалкил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R7c представляет собой C3-7 циклоалкил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R7c представляет собой C6-14 арил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R7c представляет собой C7-15 аралкил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R7c представляет собой гетероарил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R7c представляет собой гетероциклил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении.
В определенных вариантах осуществления R7c представляет собой -C(O)R1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7c представляет собой -C(O)OR1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7c представляет собой -C(O)NR1bR1c, где каждый R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7c представляет собой -C(NR1a)NR1bR1c, где каждый R1a, R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7c представляет собой -OR1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R1 представляет собой -O-C1-6 алкил, где алкил необязательно замещен одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R1 представляет собой метокси, этокси, пропокси, изопропокси или 3-диметиламинопропокси. В определенных вариантах осуществления R7c представляет собой -OC(O)R1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7c представляет собой -OC(O)OR1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7c представляет собой -OC(O)NR1bR1c, где каждый R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7c представляет собой -OC(=NR1a)NR1bR1c, где каждый R1a, R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7c представляет собой -OS(O)R1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7c представляет собой -OS(O)2R1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7c представляет собой -OS(O)NR1bR1c, где каждый R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7c представляет собой -OS(O)2NR1bR1c, где каждый R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7c представляет собой -NR1bR1c, где каждый R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7c представляет собой амино (-NH2). В определенных вариантах осуществления R7c представляет собой -NR1aC(O)R1d, где каждый R1a и R1d представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7c представляет собой -NR1aC(O)OR1d, где каждый R1a и R1d представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7c представляет собой -NR1aC(O)NR1bR1c, где каждый R1a, R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7c представляет собой -NR1aC(=NR1d)NR1bR1c, где каждый R1a, R1b, R1c и R1d представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7c представляет собой -NR1aS(O)R1d, где каждый R1a и R1d представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7c представляет собой -NR1aS(O)2R1d, где каждый R1a и R1d представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7c представляет собой -NR1aS(O)NR1bR1c, где каждый R1a, R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7c представляет собой -NR1aS(O)2NR1bR1c, где каждый R1a, R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7c представляет собой -SR1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7c представляет собой -S(O)R1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7c представляет собой -S(O)2R1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7c представляет собой -S(O)NR1bR1c, где каждый R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7c представляет собой -S(O)2NR1bR1c, где каждый R1b и R1c представляет собой, как определено в настоящем изобретении.
В определенных вариантах осуществления R7c представляет собой фенил, имидазолил, пиразолил, пиридинил, пиримидинил, пирролидинил, пиперидинил или пиперазинил, причем каждый необязательно замещен одним или более заместителями Q. В определенных вариантах осуществления R7c представляет собой фенил, 2-фторфенил, 2-хлорфенил, 2-бромфенил, 2-метилфенил, 2-(3-диметиламинопропил)фенил, 2-метоксифенил, 3-фторфенил, 3-хлорфенил, 3-метилфенил, 3-метоксифенил, 4-фторфенил, 4-хлорфенил, 4-бромфенил, 4-метоксифенил, 2,4-дифторфенил, 2,6-дифторфенил, 4-фтор-3-метоксифенил, 3-метоксифенил, 4-метоксифенил, 3-морфолин-4-илметилфенил, имидазол-1-ил, пиразол-4-ил, 1-метилпиразол-4-ил, 2-метилпиразол-3-ил, пиридин-2-ил, пиридин-3-ил, пиридин-4-ил, 2-фторпиридин-3-ил, 2-метилпиридин-4-ил, 2-(4-метилпиперазин-1-ил)пиридин-4-ил, 2-метоксипиридин-4-ил, пиримидин-5-ил, пирролидин-3-ил, 1-метилпирролидин-3-ил, пиперидин-4-ил, 1-метилпиперидин-4-ил, 1-этилпиперидин-4-ил, 1-изопропилпиперидин-4-ил, 1-ацетилпиперидин-4-ил, 1-метилсульфонилпиперидин-4-ил или 4-метилпиперазин-1-ил.
В определенных вариантах осуществления R7d представляет собой водород. В определенных вариантах осуществления R7d представляет собой циано. В определенных вариантах осуществления R7d представляет собой галоген. В определенных вариантах осуществления R7d представляет собой фтор, хлор, бром или йод. В определенных вариантах осуществления R7d представляет собой нитро. В определенных вариантах осуществления R7d представляет собой C1-6 алкил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R7d представляет собой C2-6 алкенил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R7d представляет собой C2-6 алкинил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R7d представляет собой C3-10 циклоалкил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R7d представляет собой C3-7 циклоалкил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R7d представляет собой C6-14 арил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R7d представляет собой C7-15 аралкил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R7d представляет собой гетероарил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R7d представляет собой гетероциклил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении.
В определенных вариантах осуществления R7d представляет собой -C(O)R1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7d представляет собой -C(O)OR1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7d представляет собой -C(O)NR1bR1c, где каждый R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7d представляет собой -C(NR1a)NR1bR1c, где каждый R1a, R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7d представляет собой -OR1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R1 представляет собой -O-C1-6 алкил, где алкил необязательно замещен одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R1 представляет собой метокси, этокси, пропокси, изопропокси или 3-диметиламинопропокси. В определенных вариантах осуществления R7d представляет собой -OC(O)R1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7d представляет собой -OC(O)OR1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7d представляет собой -OC(O)NR1bR1c, где каждый R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7d представляет собой -OC(=NR1a)NR1bR1c, где каждый R1a, R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7d представляет собой -OS(O)R1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7d представляет собой -OS(O)2R1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7d представляет собой -OS(O)NR1bR1c, где каждый R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7d представляет собой -OS(O)2NR1bR1c, где каждый R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7d представляет собой -NR1bR1c, где каждый R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7d представляет собой амино (-NH2). В определенных вариантах осуществления R7d представляет собой -NR1aC(O)R1d, где каждый R1a и R1d представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7d представляет собой -NR1aC(O)OR1d, где каждый R1a и R1d представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7d представляет собой -NR1aC(O)NR1bR1c, где каждый R1a, R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7d представляет собой -NR1aC(=NR1d)NR1bR1c, где каждый R1a, R1b, R1c и R1d представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7d представляет собой -NR1aS(O)R1d, где каждый R1a и R1d представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7d представляет собой -NR1aS(O)2R1d, где каждый R1a и R1d представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7d представляет собой -NR1aS(O)NR1bR1c, где каждый R1a, R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7d представляет собой -NR1aS(O)2NR1bR1c, где каждый R1a, R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7d представляет собой -SR1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7d представляет собой -S(O)R1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7d представляет собой -S(O)2R1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7d представляет собой -S(O)NR1bR1c, где каждый R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7d представляет собой -S(O)2NR1bR1c, где каждый R1b и R1c представляет собой, как определено в настоящем изобретении.
В определенных вариантах осуществления R7d представляет собой фенил, имидазолил, пиразолил, пиридинил, пиримидинил, пирролидинил, пиперидинил или пиперазинил, причем каждый необязательно замещен одним или более заместителями Q. В определенных вариантах осуществления R7d представляет собой фенил, 2-фторфенил, 2-хлорфенил, 2-бромфенил, 2-метилфенил, 2-(3-диметиламинопропил)фенил, 2-метоксифенил, 3-фторфенил, 3-хлорфенил, 3-метилфенил, 3-метоксифенил, 4-фторфенил, 4-хлорфенил, 4-бромфенил, 4-метоксифенил, 2,4-дифторфенил, 2,6-дифторфенил, 4-фтор-3-метоксифенил, 3-метоксифенил, 4-метоксифенил, 3-морфолин-4-илметилфенил, имидазол-1-ил, пиразол-4-ил, 1-метилпиразол-4-ил, 2-метилпиразол-3-ил, пиридин-2-ил, пиридин-3-ил, пиридин-4-ил, 2-фторпиридин-3-ил, 2-метилпиридин-4-ил, 2-(4-метилпиперазин-1-ил)пиридин-4-ил, 2-метоксипиридин-4-ил, пиримидин-5-ил, пирролидин-3-ил, 1-метилпирролидин-3-ил, пиперидин-4-ил, 1-метилпиперидин-4-ил, 1-этилпиперидин-4-ил, 1-изопропилпиперидин-4-ил, 1-ацетилпиперидин-4-ил, 1-метилсульфонилпиперидин-4-ил или 4-метилпиперазин-1-ил.
В определенных вариантах осуществления R7e представляет собой водород. В определенных вариантах осуществления R7e представляет собой циано. В определенных вариантах осуществления R7e представляет собой галоген. В определенных вариантах осуществления R7e представляет собой фтор, хлор, бром или йод. В определенных вариантах осуществления R7e представляет собой нитро. В определенных вариантах осуществления R7e представляет собой C1-6 алкил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R7e представляет собой C2-6 алкенил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R7e представляет собой C2-6 алкинил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R7e представляет собой C3-10 циклоалкил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R7e представляет собой C3-7 циклоалкил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R7e представляет собой C6-14 арил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R7e представляет собой C7-15 аралкил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R7e представляет собой гетероарил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R7e представляет собой гетероциклил, необязательно замещенный одним или более заместителями Q, как описано в настоящем изобретении.
В определенных вариантах осуществления R7e представляет собой -C(O)R1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7e представляет собой -C(O)OR1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7e представляет собой -C(O)NR1bR1c, где каждый R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7e представляет собой -C(NR1a)NR1bR1c, где каждый R1a, R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7e представляет собой -OR1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R1 представляет собой -O-C1-6 алкил, где алкил необязательно замещен одним или более заместителями Q, как описано в настоящем изобретении. В определенных вариантах осуществления R1 представляет собой метокси, этокси, пропокси, изопропокси или 3-диметиламинопропокси. В определенных вариантах осуществления R7e представляет собой -OC(O)R1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7e представляет собой -OC(O)OR1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7e представляет собой -OC(O)NR1bR1c, где каждый R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7e представляет собой -OC(=NR1a)NR1bR1c, где каждый R1a, R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7e представляет собой -OS(O)R1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7e представляет собой -OS(O)2R1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7e представляет собой -OS(O)NR1bR1c, где каждый R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7e представляет собой -OS(O)2NR1bR1c, где каждый R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7e представляет собой -NR1bR1c, где каждый R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7e представляет собой амино (-NH2). В определенных вариантах осуществления R7e представляет собой -NR1aC(O)R1d, где каждый R1a и R1d представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7e представляет собой -NR1aC(O)OR1d, где каждый R1a и R1d представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7e представляет собой -NR1aC(O)NR1bR1c, где каждый R1a, R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7e представляет собой -NR1aC(=NR1d)NR1bR1c, где каждый R1a, R1b, R1c и R1d представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7e представляет собой -NR1aS(O)R1d, где каждый R1a и R1d представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7e представляет собой -NR1aS(O)2R1d, где каждый R1a и R1d представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7e представляет собой -NR1aS(O)NR1bR1c, где каждый R1a, R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7e представляет собой -NR1aS(O)2NR1bR1c, где каждый R1a, R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7e представляет собой -SR1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7e представляет собой -S(O)R1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7e представляет собой -S(O)2R1a, где R1a представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7e представляет собой -S(O)NR1bR1c, где каждый R1b и R1c представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления R7e представляет собой -S(O)2NR1bR1c, где каждый R1b и R1c представляет собой, как определено в настоящем изобретении.
В определенных вариантах осуществления R7e представляет собой фенил, имидазолил, пиразолил, пиридинил, пиримидинил, пирролидинил, пиперидинил или пиперазинил, причем каждый необязательно замещен одним или более заместителями Q. В определенных вариантах осуществления R7e представляет собой фенил, 2-фторфенил, 2-хлорфенил, 2-бромфенил, 2-метилфенил, 2-(3-диметиламинопропил)фенил, 2-метоксифенил, 3-фторфенил, 3-хлорфенил, 3-метилфенил, 3-метоксифенил, 4-фторфенил, 4-хлорфенил, 4-бромфенил, 4-метоксифенил, 2,4-дифторфенил, 2,6-дифторфенил, 4-фтор-3-метоксифенил, 3-метоксифенил, 4-метоксифенил, 3-морфолин-4-илметилфенил, имидазол-1-ил, пиразол-4-ил, 1-метилпиразол-4-ил, 2-метилпиразол-3-ил, пиридин-2-ил, пиридин-3-ил, пиридин-4-ил, 2-фторпиридин-3-ил, 2-метилпиридин-4-ил, 2-(4-метилпиперазин-1-ил)пиридин-4-ил, 2-метоксипиридин-4-ил, пиримидин-5-ил, пирролидин-3-ил, 1-метилпирролидин-3-ил, пиперидин-4-ил, 1-метилпиперидин-4-ил, 1-этилпиперидин-4-ил, 1-изопропилпиперидин-4-ил, 1-ацетилпиперидин-4-ил, 1-метилсульфонилпиперидин-4-ил или 4-метилпиперазин-1-ил.
В определенных вариантах осуществления R7a и R7b вместе с атомами углерода, с которыми они соединены, образуют C3-10 циклоалкенил, C6-14 арил, гетероарил или гетероциклил, причем каждый необязательно замещен одним или более заместителями Q. В определенных вариантах осуществления R7a и R7b вместе с атомами углерода, с которыми они соединены, образуют C3-10 циклоалкенил, необязательно замещенный одним или более заместителями Q. В определенных вариантах осуществления R7a и R7b вместе с атомами углерода, с которыми они соединены, образуют циклогексенил, необязательно замещенный одним или более заместителями Q. В определенных вариантах осуществления R7a и R7b вместе с атомами углерода, с которыми они соединены, образуют C6-14 арил, необязательно замещенный одним или более заместителями Q. В определенных вариантах осуществления R7a и R7b вместе с атомами углерода, с которыми они соединены, образуют фенил, необязательно замещенный одним или более заместителями Q. В определенных вариантах осуществления R7a и R7b вместе с атомами углерода, с которыми они соединены, образуют гетероарил, необязательно замещенный одним или более заместителями Q. В определенных вариантах осуществления R7a и R7b вместе с атомами углерода, с которыми они соединены, образуют моноциклический гетероарил, необязательно замещенный одним или более заместителями Q. В определенных вариантах осуществления R7a и R7b вместе с атомами углерода, с которыми они соединены, образуют 5- или 6-членный гетероарил, необязательно замещенный одним или более заместителями Q. В определенных вариантах осуществления R7a и R7b вместе с атомами углерода, с которыми они соединены, образуют бициклический гетероарил, необязательно замещенный одним или более заместителями Q. В определенных вариантах осуществления R7a и R7b вместе с атомами углерода, с которыми они соединены, образуют гетероциклил, необязательно замещенный одним или более заместителями Q. В определенных вариантах осуществления R7a и R7b вместе с атомами углерода, с которыми они соединены, образуют моноциклическая гетероциклил, необязательно замещенный одним или более заместителями Q. В определенных вариантах осуществления R7a и R7b вместе с атомами углерода, с которыми они соединены, образуют 5- или 6-членный гетероциклил, необязательно замещенный одним или более заместителями Q. В определенных вариантах осуществления R7a и R7b вместе с атомами углерода, с которыми они соединены, образуют бициклический гетероциклил, необязательно замещенный одним или более заместителями Q.
В определенных вариантах осуществления R7b и R7c вместе с атомами углерода, с которыми они соединены, образуют C3-10 циклоалкенил, C6-14 арил, гетероарил или гетероциклил, причем каждый необязательно замещен одним или более заместителями Q. В определенных вариантах осуществления R7b и R7c вместе с атомами углерода, с которыми они соединены, образуют C3-10 циклоалкенил, необязательно замещенный одним или более заместителями Q. В определенных вариантах осуществления R7b и R7c вместе с атомами углерода, с которыми они соединены, образуют циклогексенил, необязательно замещенный одним или более заместителями Q. В определенных вариантах осуществления R7b и R7c вместе с атомами углерода, с которыми они соединены, образуют C6-14 арил, необязательно замещенный одним или более заместителями Q. В определенных вариантах осуществления R7b и R7c вместе с атомами углерода, с которыми они соединены, образуют фенил, необязательно замещенный одним или более заместителями Q. В определенных вариантах осуществления R7b и R7c вместе с атомами углерода, с которыми они соединены, образуют гетероарил, необязательно замещенный одним или более заместителями Q. В определенных вариантах осуществления R7b и R7c вместе с атомами углерода, с которыми они соединены, образуют моноциклический гетероарил, необязательно замещенный одним или более заместителями Q. В определенных вариантах осуществления R7b и R7c вместе с атомами углерода, с которыми они соединены, образуют 5- или 6-членный гетероарил, необязательно замещенный одним или более заместителями Q. В определенных вариантах осуществления R7b и R7c вместе с атомами углерода, с которыми они соединены, образуют бициклический гетероарил, необязательно замещенный одним или более заместителями Q. В определенных вариантах осуществления R7b и R7c вместе с атомами углерода, с которыми они соединены, образуют гетероциклил, необязательно замещенный одним или более заместителями Q. В определенных вариантах осуществления R7b и R7c вместе с атомами углерода, с которыми они соединены, образуют моноциклический гетероциклил, необязательно замещенный одним или более заместителями Q. В определенных вариантах осуществления R7b и R7c вместе с атомами углерода, с которыми они соединены, образуют 5- или 6-членный гетероциклил, необязательно замещенный одним или более заместителями Q. В определенных вариантах осуществления R7b и R7c вместе с атомами углерода, с которыми они соединены, образуют бициклический гетероциклил, необязательно замещенный одним или более заместителями Q.
В определенных вариантах осуществления R7c и R7d вместе с атомами углерода, с которыми они соединены, образуют C3-10 циклоалкенил, C6-14 арил, гетероарил или гетероциклил, причем каждый необязательно замещен одним или более заместителями Q. В определенных вариантах осуществления R7c и R7d вместе с атомами углерода, с которыми они соединены, образуют C3-10 циклоалкенил, необязательно замещенный одним или более заместителями Q. В определенных вариантах осуществления R7c и R7d вместе с атомами углерода, с которыми они соединены, образуют циклогексенил, необязательно замещенный одним или более заместителями Q. В определенных вариантах осуществления R7c и R7d вместе с атомами углерода, с которыми они соединены, образуют C6-14 арил, необязательно замещенный одним или более заместителями Q. В определенных вариантах осуществления R7c и R7d вместе с атомами углерода, с которыми они соединены, образуют фенил, необязательно замещенный одним или более заместителями Q. В определенных вариантах осуществления R7c и R7d вместе с атомами углерода, с которыми они соединены, образуют гетероарил, необязательно замещенный одним или более заместителями Q. В определенных вариантах осуществления R7c и R7d вместе с атомами углерода, с которыми они соединены, образуют моноциклический гетероарил, необязательно замещенный одним или более заместителями Q. В определенных вариантах осуществления R7c и R7d вместе с атомами углерода, с которыми они соединены, образуют 5- или 6-членный гетероарил, необязательно замещенный одним или более заместителями Q. В определенных вариантах осуществления R7c и R7d вместе с атомами углерода, с которыми они соединены, образуют бициклический гетероарил, необязательно замещенный одним или более заместителями Q. В определенных вариантах осуществления R7c и R7d вместе с атомами углерода, с которыми они соединены, образуют гетероциклил, необязательно замещенный одним или более заместителями Q. В определенных вариантах осуществления R7c и R7d вместе с атомами углерода, с которыми они соединены, образуют моноциклический гетероциклил, необязательно замещенный одним или более заместителями Q. В определенных вариантах осуществления R7c и R7d вместе с атомами углерода, с которыми они соединены, образуют 5- или 6-членный гетероциклил, необязательно замещенный одним или более заместителями Q. В определенных вариантах осуществления R7c и R7d вместе с атомами углерода, с которыми они соединены, образуют бициклический гетероциклил, необязательно замещенный одним или более заместителями Q.
В определенных вариантах осуществления R7d и R7e вместе с атомами углерода, с которыми они соединены, образуют C3-10 циклоалкенил, C6-14 арил, гетероарил или гетероциклил, причем каждый необязательно замещен одним или более заместителями Q. В определенных вариантах осуществления R7d и R7e вместе с атомами углерода, с которыми они соединены, образуют C3-10 циклоалкенил, необязательно замещенный одним или более заместителями Q. В определенных вариантах осуществления R7d и R7e вместе с атомами углерода, с которыми они соединены, образуют циклогексенил, необязательно замещенный одним или более заместителями Q. В определенных вариантах осуществления R7d и R7e вместе с атомами углерода, с которыми они соединены, образуют C6-14 арил, необязательно замещенный одним или более заместителями Q. В определенных вариантах осуществления R7d и R7e вместе с атомами углерода, с которыми они соединены, образуют фенил, необязательно замещенный одним или более заместителями Q. В определенных вариантах осуществления R7d и R7e вместе с атомами углерода, с которыми они соединены, образуют гетероарил, необязательно замещенный одним или более заместителями Q. В определенных вариантах осуществления R7d и R7e вместе с атомами углерода, с которыми они соединены, образуют моноциклическая гетероарил, необязательно замещенный одним или более заместителями Q. В определенных вариантах осуществления R7d и R7e вместе с атомами углерода, с которыми они соединены, образуют 5- или 6-членный гетероарил, необязательно замещенный одним или более заместителями Q. В определенных вариантах осуществления R7d и R7e вместе с атомами углерода, с которыми они соединены, образуют бициклический гетероарил, необязательно замещенный одним или более заместителями Q. В определенных вариантах осуществления R7d и R7e вместе с атомами углерода, с которыми они соединены, образуют гетероциклил, необязательно замещенный одним или более заместителями Q. В определенных вариантах осуществления R7d и R7e вместе с атомами углерода, с которыми они соединены, образуют моноциклический гетероциклил, необязательно замещенный одним или более заместителями Q. В определенных вариантах осуществления R7d и R7e вместе с атомами углерода, с которыми они соединены, образуют 5- или 6-членный гетероциклил, необязательно замещенный одним или более заместителями Q. В определенных вариантах осуществления R7d и R7e вместе с атомами углерода, с которыми они соединены, образуют бициклический гетероциклил, необязательно замещенный одним или более заместителями Q.
В определенных вариантах осуществления m равно 0. В определенных вариантах осуществления m равно 1.
В определенных вариантах осуществления n равно 0. В определенных вариантах осуществления n равно 1. В определенных вариантах осуществления n равно 2. В определенных вариантах осуществления n равно 3. В определенных вариантах осуществления n равно 4. В определенных вариантах осуществления n равно 0, 1 или 2. В определенных вариантах осуществления n равно 0, 1, 2 или 3. В определенных вариантах осуществления, n равно 1, 2 или 3. В определенных вариантах осуществления n равно 1 или 2.
В определенных вариантах осуществления m равно 0, и n равно 0, 1, 2 или 3. В определенных вариантах осуществления m равно 0, n равно 0, 1 или 2. В определенных вариантах осуществления, m равно 0, n равно 0 или 1. В определенных вариантах осуществления, m равно 0, n равно 0. В определенных вариантах осуществления, m равно 0, n равно 1. В определенных вариантах осуществления, m равно 1, n равно 0, 1, 2 или 3. В определенных вариантах осуществления m равно 1, n равно 0, 1 или 2. В определенных вариантах осуществления m равно 1, n равно 0 или 1. В определенных вариантах осуществления m равно 1, n равно 0. В определенных вариантах осуществления, m равно 1, n равно 1.
В конкретных вариантах осуществления, m равно 0, n равно 1, и каждый R5a и R5b представляет собой метил.
В определенных вариантах осуществления X представляет собой N. В определенных вариантах осуществления X представляет собой CRx, где Rx представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления X представляет собой CH.
В определенных вариантах осуществления Y представляет собой N. В определенных вариантах осуществления Y представляет собой CRx, где Rx представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления Y представляет собой CH.
В определенных вариантах осуществления Z представляет собой N. В определенных вариантах осуществления Z представляет собой CRx, где Rx представляет собой, как определено в настоящем изобретении. В определенных вариантах осуществления Z представляет собой CH.
В определенных вариантах осуществления X, Y и Z представляют собой N. В определенных вариантах осуществления X и Y представляют собой N, и Z представляет собой CH. В определенных вариантах осуществления X и Z представляют собой N, и Y представляет собой CH. В определенных вариантах осуществления, Y и Z представляют собой N, и X представляет собой CH.
В определенных вариантах осуществления соединение настоящего изобретения не является 4-(2-(дифторметил)-1H-бензо[d]имидазол-1-ил)-6-морфолино-N-(2-фенил-2-(пирролидин-1-ил)этил)-1,3,5-триазин-2-амином. В определенных вариантах осуществления соединение настоящего изобретения не является 6-(2-(дифторметил)-1H-бензо[d]имидазол-1-ил)-N-(1-(4-((R)-3-(метоксиметил)морфолино)фенил)этил)-2-морфолинопиримидин-4-амином.
В определенных вариантах осуществления, когда X, Y и Z представляют собой N и R5a представляет собой водород, R5b не является гетероциклилом. В определенных вариантах осуществления, когда X, Y и Z представляют собой N и R5a представляет собой водород, R5b не является 5-членным гетероциклилом. В определенных вариантах осуществления, когда X, Y и Z представляют собой N и R5a представляет собой водород, R5b не является пирролидинилом. В определенных вариантах осуществления, когда X, Y и Z представляют собой N и R5a представляет собой водород, R5b не является пирролидин-1-илом.
В определенных вариантах осуществления, когда X и Z представляют собой N, Y представляет собой CH и R5a представляет собой водород, R5b представляет собой замещенный морфолино фенил. В определенных вариантах осуществления, когда X и Z представляют собой N, Y представляет собой CH и R5a представляет собой водород, R5b не является 4-((R)-3-(метоксиметил)морфолино)фенилом.
В одном варианте осуществления настоящее изобретение относится к соединению, выбранному из:
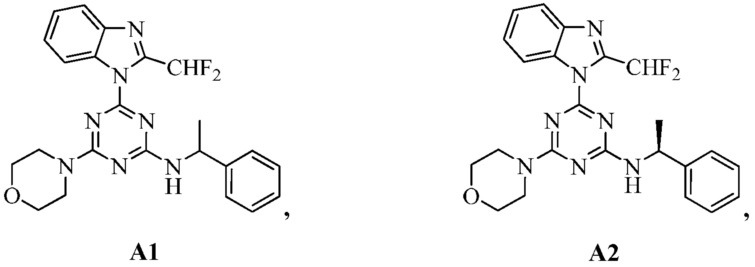
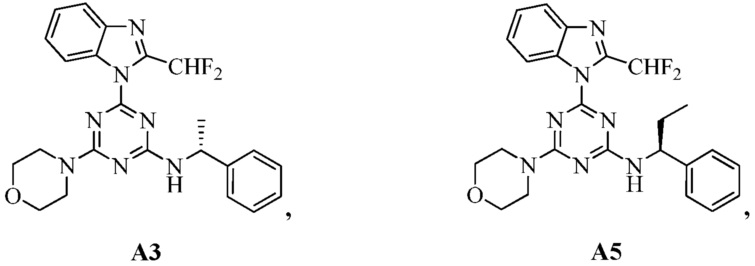
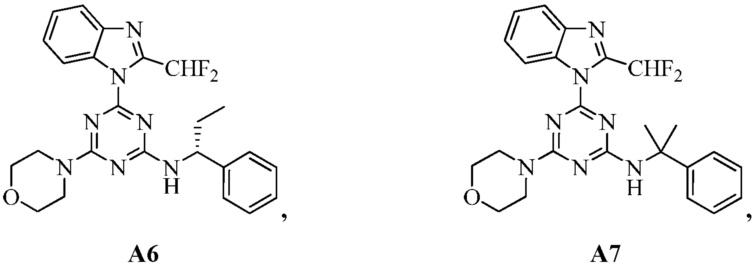
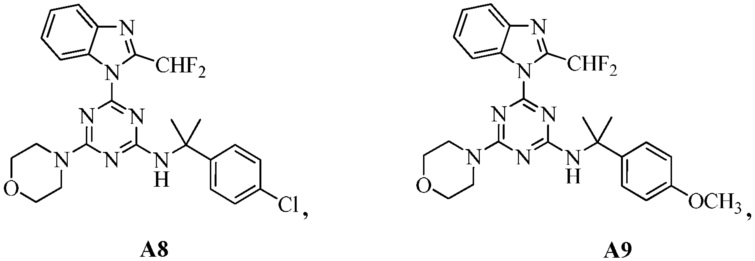
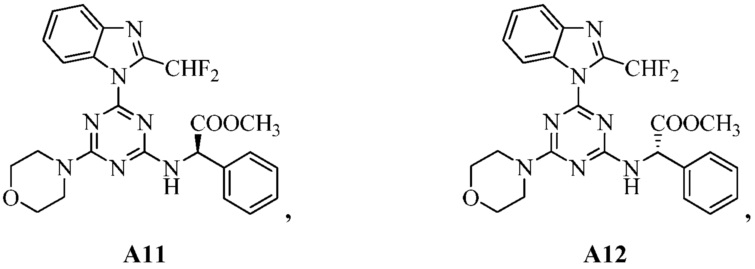
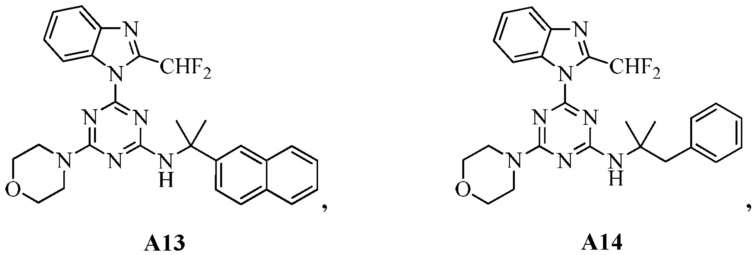
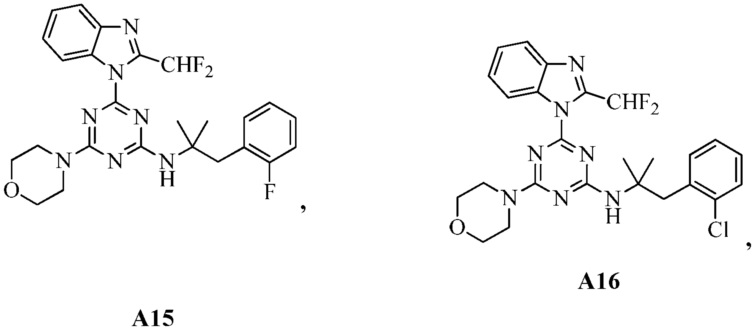
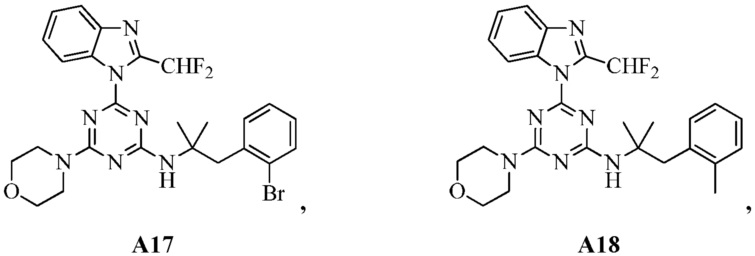
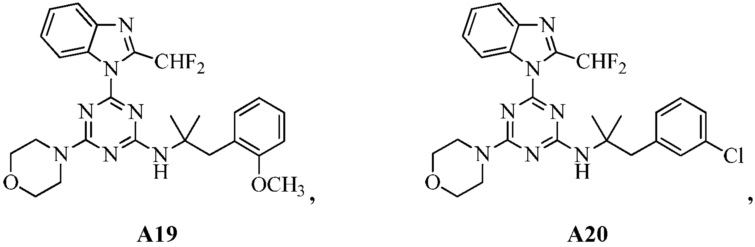
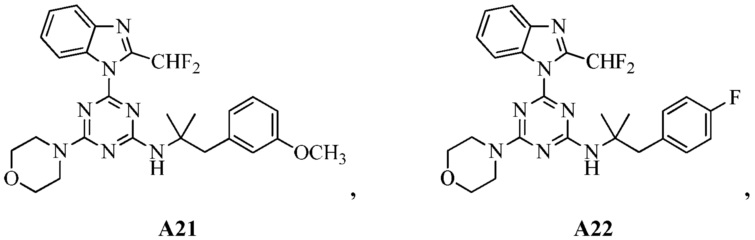
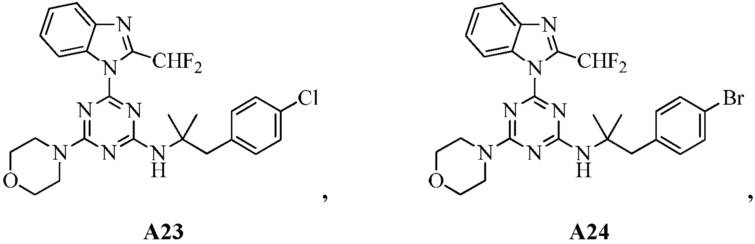
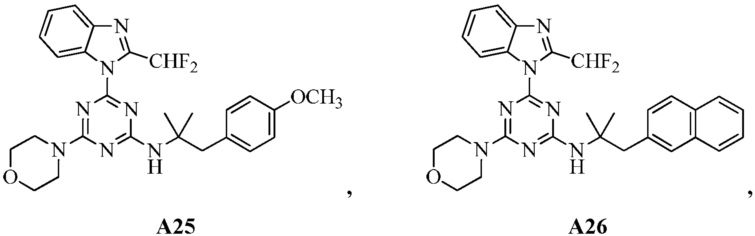
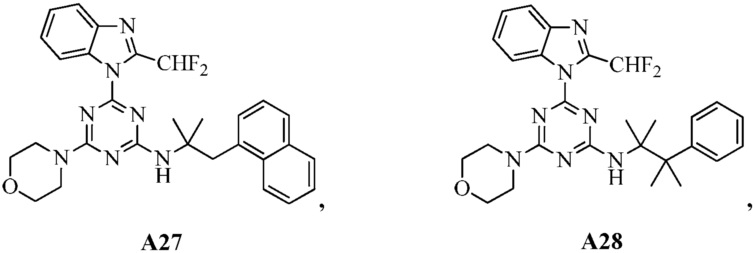
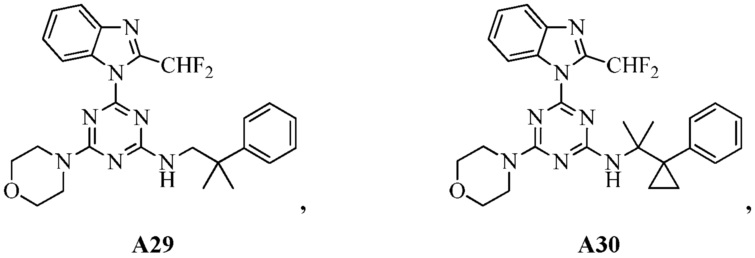

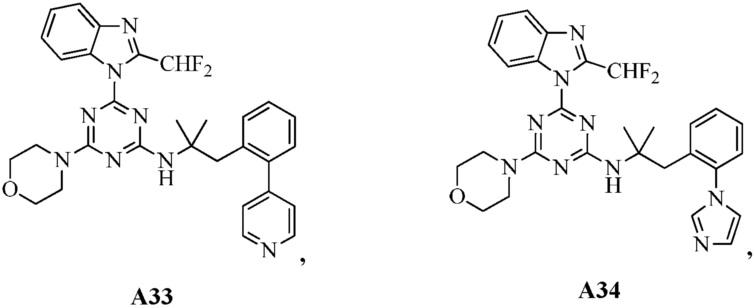
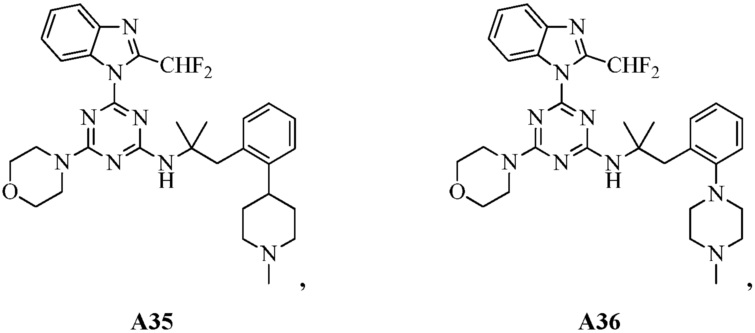
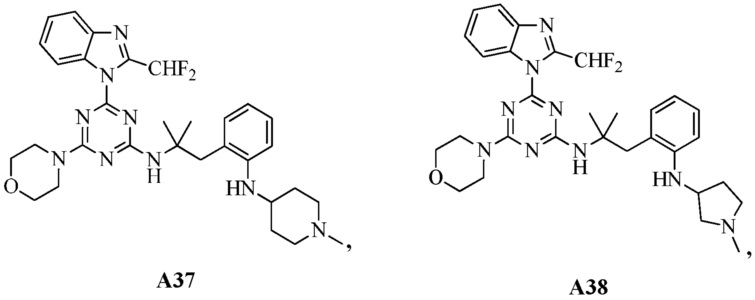
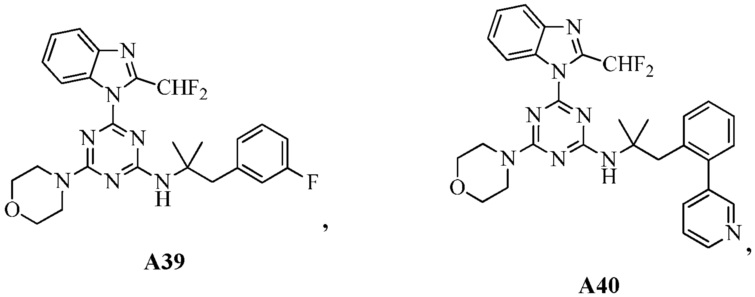
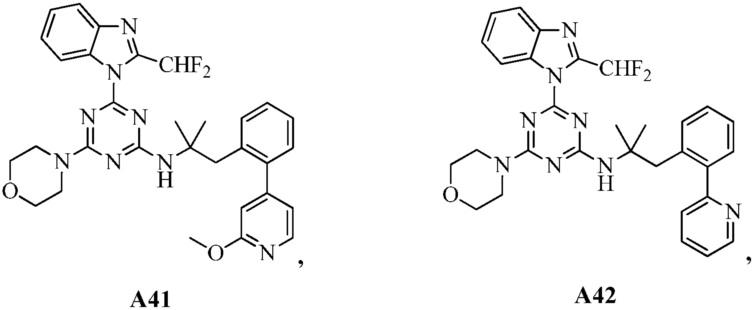
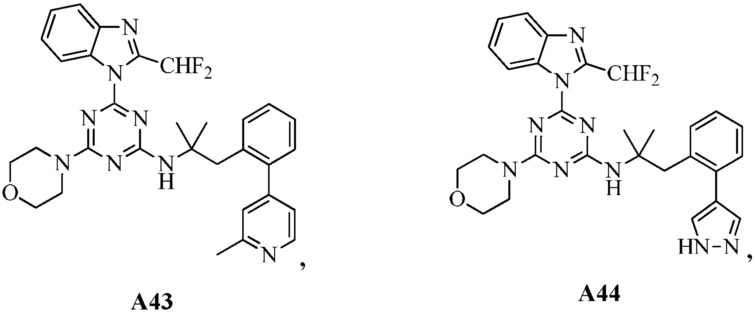
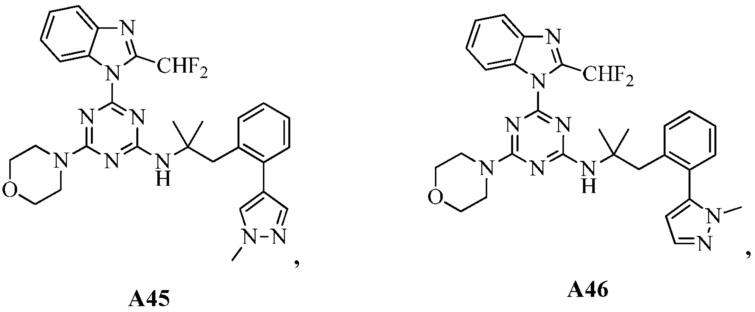
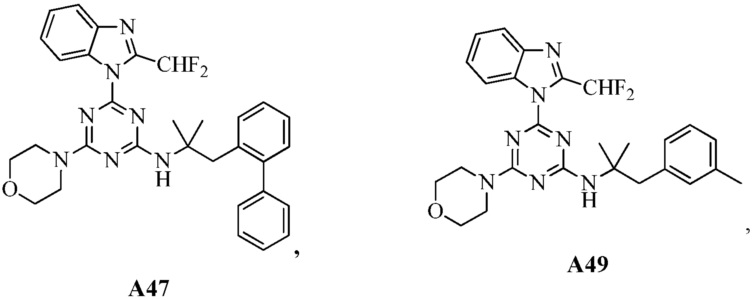
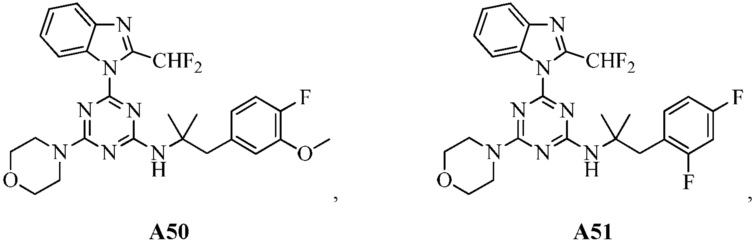
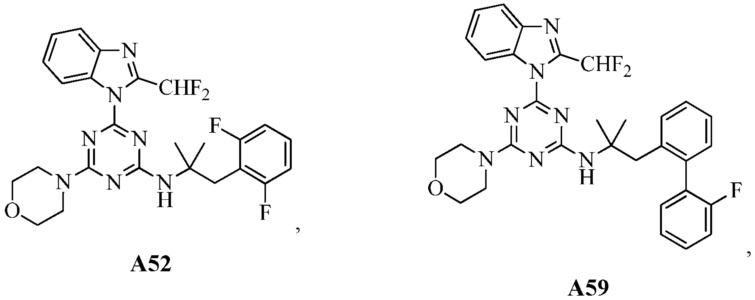
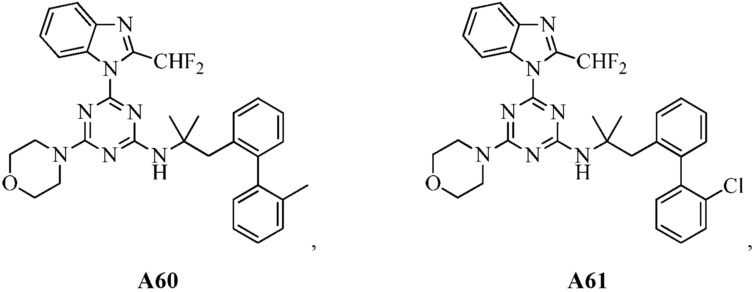
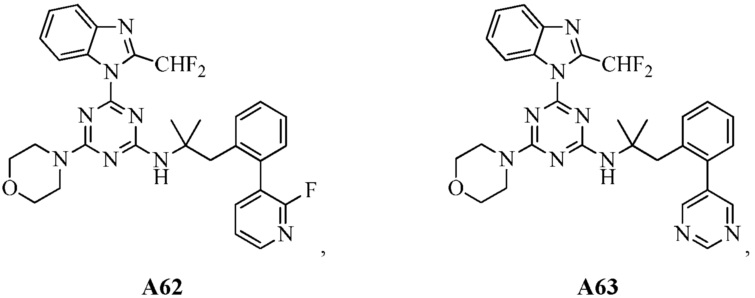
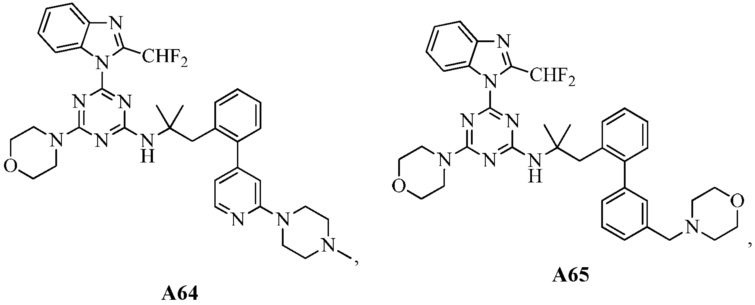
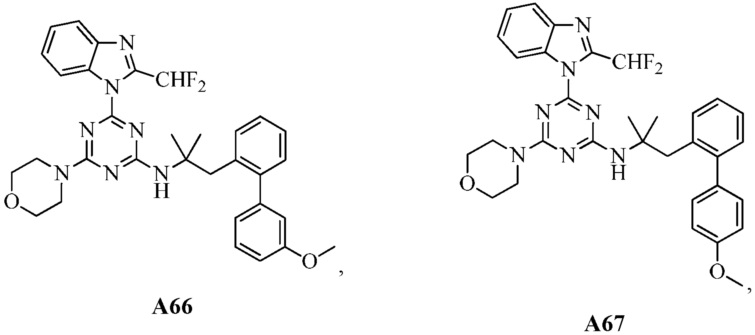
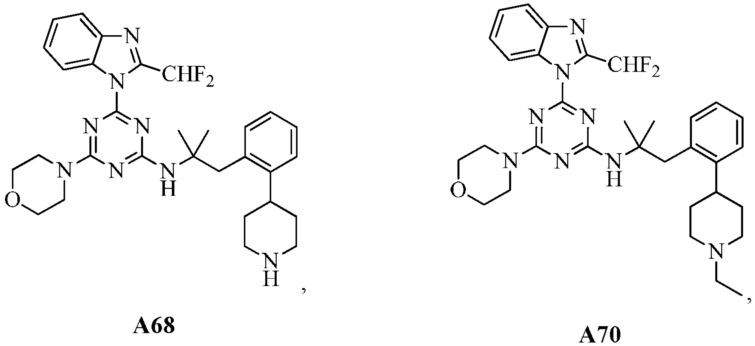
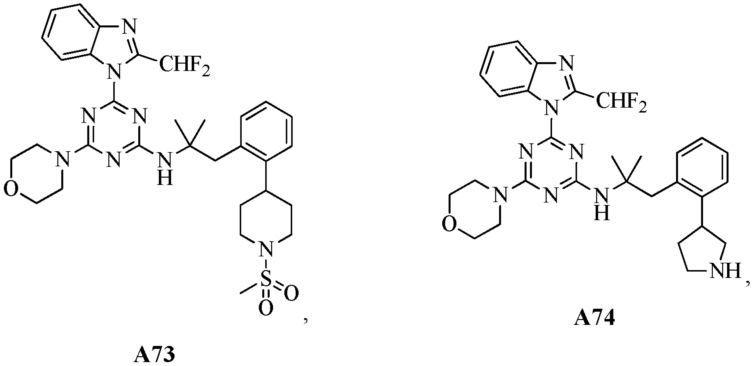
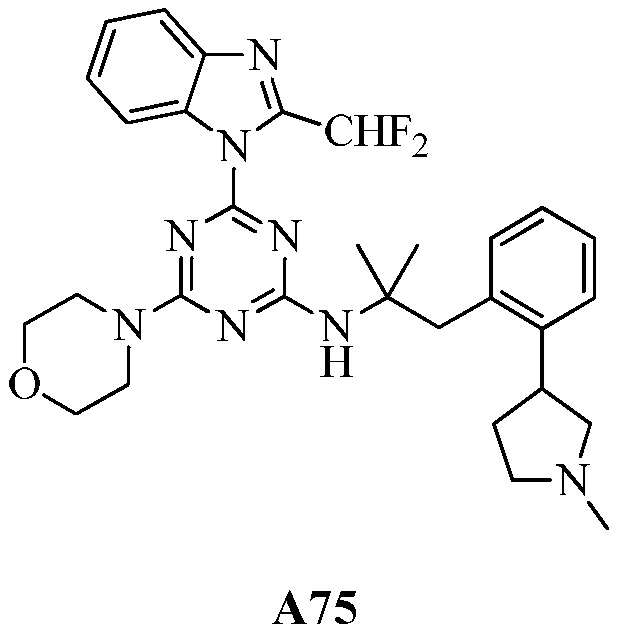 и
и 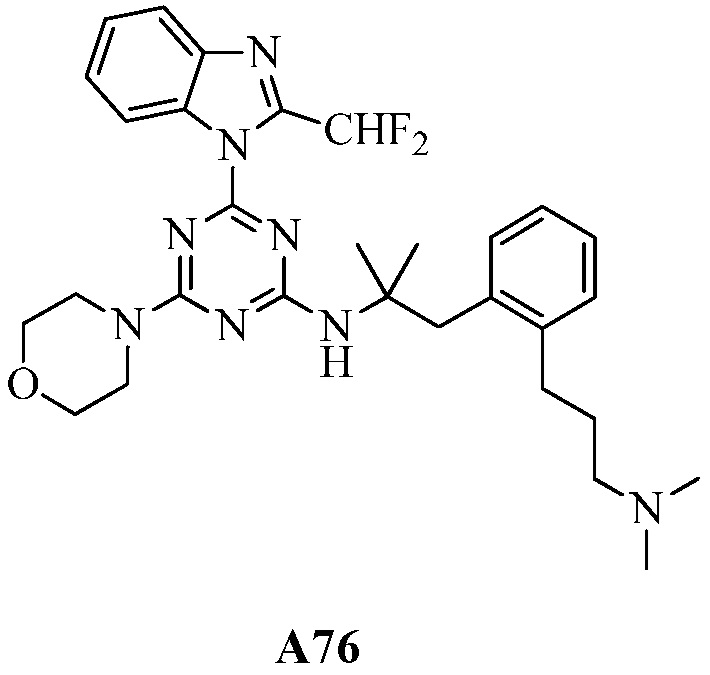 ;
;
и его энантиомерам, смесям энантиомеров, смесям двух или более диастереомеров и изотопным вариантам; и их фармацевтически приемлемым солям, сольватам, гидратам и пролекарствам.
Предполагается, что соединения настоящего изобретения включают все возможные стереоизомеры, если не указана конкретная стереохимия. Когда соединение, относящееся к настоящему изобретению, содержит алкенильную или алкениленовую группу, соединение может существовать в виде одного или смеси геометрических цис/транс (или Z/E) изомеров. Когда структурные изомеры являются взаимопревращающимися, соединение может существовать в виде отдельного таутомера или смеси таутомеров. Это может принимать вид протонной таутомерии в соединении, которое содержит, например, имино-, кето- или оксимную группу; или так называемой валентной таутомерии в соединении, которое содержит ароматическую группу. Отсюда следует, что отдельное соединение может обладать более чем одним видом изомерии.
Соединения, относящиеся к настоящему изобретению, могут быть энантиомерно чистыми, такими как отдельный энантиомер или отдельный диастереомер, или быть стереоизомерными смесями, такими как смеси энантиомеров, например, рацемическая смесь двух энантиомеров; или смесь двух или более диастереомеров. В этой связи, специалисту в данной области техники ясно, что введение соединения в его (R) форме является эквивалентным, для соединений, которые подвергаются эпимеризации in vivo, введению соединения в его (S) форме. Общепринятые способы получения/выделения отдельных энантиомеров включают синтез из подходящих оптически чистых предшественников, асимметрический синтез из ахиральных исходных веществ или разделение энантиомерной смеси, например, хиральную хроматографию, перекристаллизацию, разделение, образование диастереомерной соли или превращение в диастереомерные продукты присоединения с последующим разделением.
Когда соединение, относящееся к настоящему изобретению, содержит кислую или основную группу, его можно также предоставлять в виде фармацевтически приемлемой соли (смотрите, Berge et al., J. Pharm. Sci. 1977, 66, 1-19; и “Handbook of Pharmaceutical Salts, Properties, and Use”, Stahl and Wermuth, Ed.; Wiley-VCH and VHCA, Zurich, 2002).
Подходящие кислоты для применения при получении фармацевтически приемлемых солей включают, но не ограничиваются, уксусную кислоту, 2,2-дихлоруксусную кислоту, ацилированные аминокислоты, адипиновую кислоту, альгиновую кислоту, аскорбиновую кислоту, L-аспарагиновую кислоту, бензолсульфокислоту, бензойную кислоту, 4-ацетамидобензойную кислоту, борную кислоту, (+)-камфорную кислоту, камфорсульфоновую кислоту, (+)-(1S)-камфор-10-сульфоновую кислоту, каприновую кислоту, капроновую кислоту, каприловую кислоту, коричную кислоту, лимонную кислоту, цикламиновую кислоту, циклогексансульфаминовую кислота, додецилсерную кислоту, этан-1,2-дисульфоновую кислоту, этансульфоновую кислоту, 2-гидроксиэтансульфоновую кислоту, муравьиную кислоту, фумаровую кислоту, галактаровую кислоту, гентизиновую кислоту, глюкогептоновую кислоту, D-глюконовую кислоту, D-глюкуроновую кислоту, L-глутаминовую кислоту, α-оксоглутаровую кислоту, гликолевую кислоту, гиппуровую кислоту, бромистоводородную кислоту, хлористоводородную кислоту, йодистоводородную кислоту, (+)-L-молочную кислоту, (±)-DL-молочную кислоту, лактобионовую кислоту, лауриновую кислоту, малеиновую кислоту, (-)-L-яблочную кислоту, малоновую кислоту, (±)-DL-миндальную кислоту, метансульфоновую кислоту, нафталин-2-сульфоновую кислоту, нафталин-1,5-дисульфоновую кислоту, 1-гидрокси-2-нафтойную кислоту, никотиновую кислоту, азотную кислоту, олеиновую кислоту, оротовую кислоту, щавелевую кислоту, пальмитиновую кислоту, памовую кислоту, перхлорную кислоту, фосфорную кислоту, L-пироглютаминовую кислоту, сахарную кислоту, салициловую кислоту, 4-аминосалициловую кислоту, себациновую кислоту, стеариновую кислоту, янтарную кислоту, серную кислоту, дубильную кислоту, (+)-L-винную кислоту, тиоциановую кислоту, п-толуолсульфоновую кислоту, ундециленовую кислоту и валериановую кислоту.
Подходящие основания для применения при получении фармацевтически приемлемых солей включают, но не ограничиваются, неорганические основания, такие как гидроксид магния, гидроксид кальция, гидроксид калия, гидроксид цинка или гидроксид натрия; и органические основания, такие как первичные, вторичные, третичные и четвертичные, алифатические и ароматические амины, включая L-аргинин, бенетамин, бензатин, холин, деанол, диэтаноламин, диэтиламин, диметиламин, дипропиламин, диизопропиламин, 2-(диэтиламино)этанол, этаноламин, этиламин, этилендиамин, изопропиламин, N-метилглюкамин, гидрабамин, 1H-имидазол, L-лизин, морфолин, 4-(2-гидроксиэтил)морфолин, метиламин, пиперидин, пиперазин, пропиламин, пирролидин, 1-(2-гидроксиэтил)пирролидин, пиридин, хинуклидин, хинолин, изохинолин, вторичные амины, триэтаноламин, триметиламин, триэтиламин, N-метил-D-глюкамин, 2-амино-2-(гидроксиметил)-1,3-пропандиол и трометамин.
Соединение, относящееся к настоящему изобретению, можно также предоставлять в виде пролекарства, которое представляет собой функциональное производное соединения, например, формулы I, и легко превращается в исходное соединение in vivo. Пролекарства часто являются полезными, поскольку, в некоторых ситуациях, их можно вводить легче, чем исходное соединение. Они могут быть, например, биодоступными для перорального введения, тогда как исходное соединение не является биодоступным. Пролекарство может также обладать повышенной растворимостью в фармацевтических композициях по сравнению с исходным соединением. Пролекарство может превращаться в исходное лекарственное средство различными механизмами, включая ферментативные способы и метаболический гидролиз. Смотрите Harper, Progress in Drug Research 1962, 4, 221-294; Morozowich et al. in “Design of Biopharmaceutical Properties through Prodrugs and Analogs”, Roche Ed., APHA Acad. Pharm. Sci. 1977; “Bioreversible Carriers in Drug in Drug Design, Theory and Application”, Roche Ed., APHA Acad. Pharm. Sci. 1987; “Design of Prodrugs”, Bundgaard, Elsevier, 1985; Wang et al., Curr. Pharm. Design 1999, 5, 265-287; Pauletti et al., Adv. Drug. Delivery Rev. 1997, 27, 235-256; Mizen et al., Pharm. Biotech. 1998, 11, 345-365; Gaignault et al., Pract. Med. Chem. 1996, 671-696; Asgharnejad in “Transport Processes in Pharmaceutical Systems”, Amidon et al., Ed., Marcell Dekker, 185-218, 2000; Balant et al., Eur. J. Drug Metab. Pharmacokinet. 1990, 15, 143-53; Balimane and Sinko, Adv. Drug Delivery Rev. 1999, 39, 183-209; Browne, Clin. Neuropharmacol. 1997, 20, 1-12; Bundgaard, Arch. Pharm. Chem. 1979, 86, 1-39; Bundgaard, Controlled Drug Delivery 1987, 17, 179-96; Bundgaard, Adv. Drug Delivery Rev. 1992, 8, 1-38; Fleisher et al., Adv. Drug Delivery Rev. 1996, 19, 115-130; Fleisher et al., Methods Enzymol. 1985, 112, 360-381; Farquhar et al., J. Pharm. Sci. 1983, 72, 324-325; Freeman et al., J. Chem. Soc., Chem. Commun. 1991, 875-877; Friis and Bundgaard, Eur. J. Pharm. Sci. 1996, 4, 49-59; Gangwar et al., Des. Biopharm. Prop. Prodrugs Analogs, 1977, 409-421; Nathwani and Wood, Drugs 1993, 45, 866-94; Sinhababu and Thakker, Adv. Drug Delivery Rev. 1996, 19, 241-273; Stella et al., Drugs 1985, 29, 455-73; Tan et al., Adv. Drug Delivery Rev. 1999, 39, 117-151; Taylor, Adv. Drug Delivery Rev. 1996, 19, 131-148; Valentino and Borchardt, Drug Discovery Today 1997, 2, 148-155; Wiebe and Knaus, Adv. Drug Delivery Rev. 1999, 39, 63-80; и Waller et al., Br. J. Clin. Pharmac. 1989, 28, 497-507.
Способы получения
Соединение, относящееся к настоящему изобретению, можно синтезировать, выделить или получить любым способом, известным специалисту в данной области техники, и следующие примеры является только иллюстративными и не исключают другие родственные способы.
Схема I
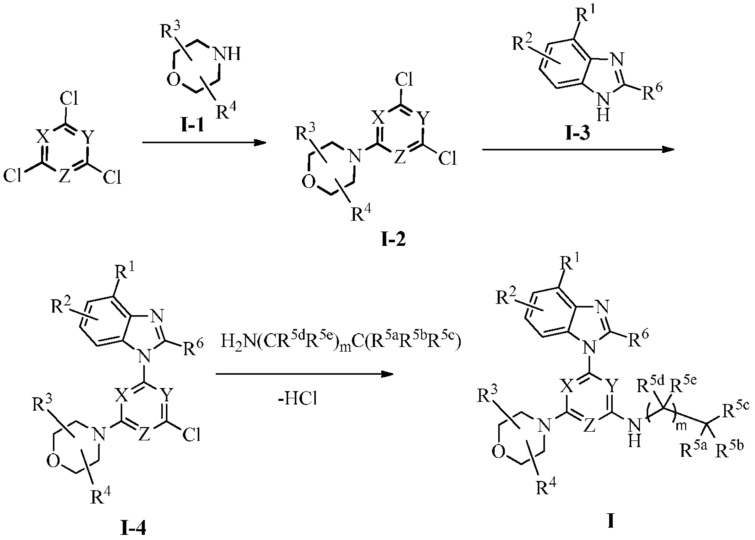
В одном варианте осуществления, например, соединение формулы I можно получить, как показано на схеме I, первой реакцией ароматического замещения тригалоген-замещенного триазина или пиримидина соединением I-1, получая соединение I-2, которое можно затем превратить в соединение I-4 второй реакцией ароматического замещения соединением I-3. Затем соединение I-4 можно превратить в соединение формулы I третьей реакцией ароматического замещения NH2(CR5dR5e)mC(R5aR5bR5c).
В одном варианте осуществления, например, соединение формулы II можно получить, как показано на схеме II, первой реакцией ароматического замещения тригалоген-замещенного триазина или пиримидина соединением I-1, получая соединение I-2, которое можно затем превратить в соединение I-4 второй реакцией ароматического замещения соединением I-3. Соединение I-4 можно затем превратить в соединение формулы II третьей реакцией ароматического замещения NH2C(R5aR5bR5c).
Схема II
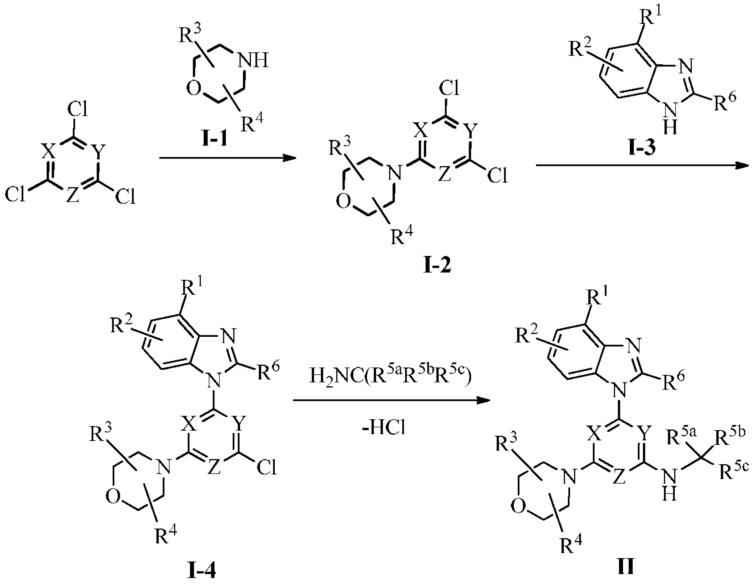
Фармацевтические композиции
В одном варианте осуществления настоящее изобретение относится к фармацевтической композиции, содержащей соединение формулы I или его энантиомер, смесь энантиомеров, смесь двух или более диастереомеров или изотопный вариант; или их фармацевтически приемлемую соль, сольват, гидрат или пролекарство; и фармацевтически приемлемое вспомогательное вещество, адъювант, носитель, буфер или стабилизатор.
В одном варианте осуществления фармацевтические композиции обеспечивают в виде лекарственной формы для пероралного введения, которая содержит соединение, относящееся к настоящему изобретению, и один или более фармацевтически приемлемых вспомогательных веществ или носителей. Фармацевтические композиции, относящиеся к настоящему изобретению, которые формулируют для перорального введения, могут быть в виде таблеток, капсул, порошков или жидкостей. Таблетка может содержать твердый носитель или адъювант. Жидкие фармацевтические композиции обычно содержат жидкий носитель, такой как вода, вазелин, животные или растительные масла, минеральное масло или синтетическое масло. Можно включать физиологический солевой раствор, раствор декстрозы или другого сахарида, или гликоли, такие как этиленгликоль, пропиленгликоль или полиэтиленгликоль. Капсула может содержать твердый носитель, такой как желатин.
В другом варианте осуществления фармацевтические композиции обеспечивают в виде лекарственной формы для парентерального введения, которая содержит соединение, относящееся к настоящему изобретению, и один или более фармацевтически приемлемых вспомогательных веществ или носителей. Когда фармацевтические композиции формулируют для внутривенной, кожной или подкожной инъекции, активный ингредиент будет в виде парентерально приемлемого водного раствора, который является апирогенным и имеет подходящую pH, изотоничность и стабильность. Специалист в данной области техники вполне способен получить подходящие растворы, применяя, например, изотонические среды, такие как раствор хлорида натрия для инъекций, раствор Рингера для инъекций или раствор Рингера с лактатом для инъекций. Консерванты, стабилизаторы, буферы, антиоксиданты и/или другие добавки можно включать, по мере необходимости.
В еще одном варианте осуществления фармацевтические композиции обеспечивают в виде лекарственной формы для местного введения, которая содержит соединение, относящееся к настоящему изобретению, и один или более фармацевтически приемлемых вспомогательных веществ или носителей.
Фармацевтические композиции можно также формулировать в виде лекарственных форм с измененным высвобождением, включая отложенное, растянутое, пролонгированное, замедленное, пульсирующее, контролируемое, ускоренное, быстрое, направленное и программируемое высвобождение, и лекарственных форм с задержкой в кишечнике. Данные лекарственные формы можно получить согласно общепринятым способам и методикам, известным специалиста м в данной области техники (смотрите Remington: The Science and Practice of Pharmacy, выше; Modified-Release Drug Delivery Technology, 2nd Edition, Rathbone et al., Eds., Marcel Dekker, Inc.: New York, NY, 2008).
Фармацевтические композиции, относящиеся к настоящему изобретению, можно предоставлять в виде единичной лекарственной формы или лекарственной формы для многократного применения. Единичная лекарственная форма, как применяют в настоящем изобретении, относится к физиологически дискретной единице, подходящией для введения субъекту, являющемуся человеком и животным, и упакованной отдельно, как это известно в данной области техники. Каждая единичная доза содержит предварительно определенное количество активного ингредиента (ингредиентов), достаточное для продуцирования требуемого терапевтического эффекта, в сочетании с требуемыми фармацевтическими носителями или вспомогательными веществами. Примеры единичной лекарственной формы включают ампулу, шприц и отдельно упакованную таблетку и капсулу. Единичную лекарственную форму можно вводить по частям или многократно. Лекарственная форма для многократного применения представляет собой множество одинаковых единичных лекарственных форм, упакованных в одном контейнере, которые будут вводить в виде отдельных единичных лекарственных форм. Примеры лекарственной формы для многократного применения включают пробирку, банку с таблетками или капсулами, или емкость с пинтами или галлонами.
Фармацевтические композиции, относящиеся к настоящему изобретению, можно вводить за один раз или несколько раз через интервалы времени. Ясно, что точная доза и продолжительность лечения могут изменяться в зависимости от возраста, веса и состояния пациента, которого подвергают лечению, и их можно определить эмпирически, применяя известные протоколы испытаний или экстраполяцией данных in vivo или in vitro испытаний или диагностических данных. Кроме того, ясно, что для любого конкретного индивида конкретные режимы дозирования следует корректировать со временем согласно индивидуальным потребностям и в соответствии с профессиональным решением лица, вводящего или координирующего введение составов.
В некоторых вариантах осуществления фармацевтические композиции, относящиеся к настоящему изобретению, дополнительно содержат один или более химиотерапевтических агентов, как определено в настоящем изобретении.
A. Пероральное введение
Фармацевтические композиции, относящиеся к настоящему изобретению, для перорального введения можно предоставлять в виде твердых, полутвердых или жидких лекарственных форм для перорального введения. Как применяют в настоящем изобретении, пероральное введение также включает буккальное, лингвальное и сублингвальное введение. Подходящие пероральные лекарственные формы включают, но не ограничиваются, таблетки, быстро плавящиеся таблетки, жевательные таблетки, капсулы, пилюли, полоски, пастилки, таблетки для рассасывания, пастилки, крахмальные капсулы, пеллеты, жевательную резинку, содержащую лекарственное средство, сыпучие порошки, шипучие или нешипучие порошки или гранулы, пероральные аэрозоли, растворы, эмульсии, суспензии, пластинки, капсулы, заполненные гранулами, эликсиры и сиропы. В добавление к активному ингредиенту (ингредиентам), фармацевтические композиции могут содержать один или более фармацевтически приемлемых носителей или вспомогательных веществ, включая, но не ограничиваясь, связующие, наполнители, разбавители, разрыхлители, смачивающие агенты, смазывающие агенты, регуляторы сыпучести, красители, ингибиторы подвижности краски, подсластители, ароматизаторы, эмульгаторы, суспендирующие и диспергирующие агенты, консерванты, растворители, неводные жидкости, органические кислоты и источники диоксида углерода.
Связующие или агенты для гранулирования придают связывающую способность таблетки, обеспечивая то, что таблетка остается цельной после прессования. Подходящие связующие или агенты для гранулирования включают, но не ограничиваются, крахмалы, такие как кукурузный крахмал, картофельный крахмал и предварительно желатинизированный крахмал (например КРАХМАЛ 1500); желатин; сахара, такие как сахароза, глюкоза, декстроза, патока и лактоза; натуральные и синтетические камеди, такие как аравийская камедь, альгиновая кислота, альгинаты, экстракт ирландского мха, камедь из кассии тора, гхатти камедь, смесь растворов камедей шелухи исабгола, карбоксиметилцеллюлоза, метилцеллюлоза, поливинилпирролидон (PVP), вигум, лиственничный арабогалактан, порошкообразный трагакант и гуаровая камедь; целлюлозы, такие как этилцеллюлоза, ацетат целлюлозы, карбоксиметилцеллюлоза кальция, карбоксиметилцеллюлоза натрия, метилцеллюлоза, гидроксиэтилцеллюлоза (HEC), гидроксипропилцеллюлоза (HPC), гидроксипропилметилцеллюлоза (HPMC); микрокристаллические целлюлозы, такие как AVICEL-PH-101, AVICEL-PH-103, AVICEL RC-581, AVICEL-PH-105 (FMC Corp., Marcus Hook, PA); и их смеси. Подходящие наполнители включают, но не ограничиваются, тальк, карбонат кальция, микрокристаллическую целлюлозу, порошкообразную целлюлозу, декстраты, каолин, маннитол, кремниевую кислоту, сорбитол, крахмал, прежелатинизированный крахмал и их смеси. Количество связующего или наполнителя в фармацевтических композициях, относящихся к настоящему изобретению, изменяется в зависимости от типа состава, и легко определяется специалистом в данной области техники. Связующее или наполнитель может присутствовать от приблизительно 50 до приблизительно 99% по весу в фармацевтических композициях, относящихся к настоящему изобретению.
Подходящие разбавители включают, но не ограничиваются, фосфат дикальция, сульфат кальция, лактозу, сорбитол, сахарозу, инозитол, целлюлозу, каолин, маннитол, хлорид натрия, сухой крахмал и порошкообразный сахар. Определенные разбавители, такие как маннит, лактоза, сорбит, сахароза и инозитол, при наличие в достаточном количестве, могут придавать свойства некоторым прессованным таблеткам, которые обеспечивают их распад во рту при жевании. Данные прессованные таблетки можно применять в качестве жевательных таблеток. Количество разбавителя в фармацевтических композициях, относящихся к настоящему изобретению, изменяется в зависимости от типа состава и легко определяется специалистом в данной области техники.
Подходящие разрыхлители включают, но не ограничиваются, агар; бентонит; целлюлозы, такие как метилцеллюлоза и карбоксиметилцеллюлоза; продукты из древесины; природные губчатые материалы; катионообменные смолы; альгиновую кислоту; камеди, такие как гуаровая камедь и вигум HV; цитрусовую пульпу; поперечносшитые целлюлозы, такие как кроскармелоза; поперечносшитые полимеры, такие как кросповидон; поперечносшитые крахмалы; карбонат кальция; микрокристаллическую целлюлозу, такую как крахмалгликолят натрия; полакрилин калия; крахмалы, такие как кукурузный крахмал, картофельный крахмал, крахмал тапиока и предварительно желатинизированный крахмал; глины; альгины; и их смеси. Количество разрыхлителя в фармацевтических композициях, относящихся к настоящему изобретению, изменяется в зависимости от типа состава и легко определяется специалистом в данной области техники. Фармацевтические композиции, относящиеся к настоящему изобретению, могут содержать от приблизительно 0,5 до приблизительно 15% или от приблизительно 1 до приблизительно 5% по весу разрыхлителя.
Подходящие смазывающие агенты включают, но не ограничиваются, стеарат кальция; стеарат магния; минеральное масло; легкое минеральное масло; глицерин; сорбитол; маннитол; гликоли, такие как бегенат глицерина и полиэтиленгликоль (PEG); стеариновую кислоту; лаурилсульфат натрия; тальк; гидрогенизированное растительное масло, включая ореховое масло, хлопковое масло, подсолнечное масло, кунжутное масло, оливковое масло, кукурузное масло и соевое масло; стеарат цинка; этилолеат; этиллаурат; агар; крахмал; ликоподий; диоксид кремния или силикагели, такие как AEROSIL® 200 (W.R. Grace Co., Baltimore, MD) и CAB-O-SIL® (Cabot Co. of Boston, MA); и их смеси. Фармацевтические композиции, относящиеся к настоящему изобретению, могут содержать от приблизительно 0,1 до приблизительно 5% по весу смазывающего агента.
Подходящие регуляторы сыпучести включают, но не ограничиваются, коллоидные диоксид кремния, CAB-O-SIL® (Cabot Co. Boston, MA) и безасбестовый тальк. Подходящие красители включают, но не ограничиваются, любой из одобренных, сертифицированных, растворимых в воде красителей для химической и пищевой промышленности, и нерастворимых в воде красителей для химической и пищевой промышленности, помещенных на гидрат оксида алюминия, и окрашивающих лаков и их смесей. Окрашивающий лак представляет собой комбинацию адсорбированием растворимого в воде красителя на гидроксиде тяжелого металла, что приводит в результате к нерастворимой форме красителя. Подходящие ароматизаторы включают, но не ограничиваются, природные ароматизаторы, экстрагированные из растений, таких как фрукты, и синтетические смеси соединений, которые обеспечивают приятные вкусовые ощущения, такие как мята перечная и метилсалицилат. Подходящие подсластители включают, но не ограничиваются, сахарозу, лактозу, маннитол, сиропы, глицерин и искусственные подсластители, такие как сахарин и аспартам. Подходящие эмульгаторы включают, но не ограничиваются, желатин, аравийскую камедь, трагакант, бентонит и поверхностно-активные вещества, такие как полиоксиэтиленсорбитанмоноолеат (TWEEN® 20), полиоксиэтиленсорбитанмоноолеат 80 (TWEEN® 80) и триэтаноламинолеат. Подходящие суспендирующие и диспергирующие агенты включают, но не ограничиваются, карбоксиметилцеллюлозу натрия, пектин, трагакант, вигум, аравийскую камедь, карбоксиметилцеллюлозу натрия, гидроксипропилметилцеллюлозу и поливинилпирролидон. Подходящие консерванты включают, но не ограничиваются, глицерин, метил и пропилпарабен, бензойную кислоту, бензоат натрия и спирт. Подходящие смачивающие агенты включают, но не ограничиваются, моностеарат пропиленгликоля, сорбитанмоноолеат, монолаурат диэтиленгликоля и полиоксиэтиленлауриловый эфир. Подходящие растворители включают, но не ограничиваются, глицерин, сорбитол, этиловый спирт и патоку. Подходящие неводные жидкости, применяемые в эмульсиях, включают, но не ограничиваются, минеральное масло и хлопковое масло. Подходящие органические кислоты включают, но не ограничиваются, лимонную и винную кислоту. Подходящие источники диоксида углерода включают, но не ограничиваются, бикарбонат натрия и карбонат натрия.
Ясно, что многие носители и вспомогательные веществ могут выполнять несколько функций, даже в одном составе.
Фармацевтические композиции, относящиеся к настоящему изобретению, для перорального введения можно обеспечивать в виде прессованных таблеток, измельченных в порошок таблеток, жевательных таблеток для рассасывания, быстро растворяющихся таблеток, таблеток, прошедших несколько стадий прессования, или энтеросолюбильных таблеток, таблеток, покрытых сахаром или покрытых пленкой. Энтеросолюбильные таблетки представляют собой прессованные таблетки, покрытые веществами, устойчивыми к действию желудочной кислоты, но растворяющимися или распадающимися в кишечнике, таким образом, защищая активные ингредиенты от кислотного окружения желудка. Энтеросолюбильные покрытия включают, но не ограничиваются, жирные кислоты, жиры, фенилсалицилат, воски, шеллак, насыщенный аммиаком шеллак и ацетатфаталаты целлюлозы. Покрытие сахаром таблетки представляют собой прессованные таблетки, окруженные сахарным покрытием, которое может быть полезным для маскировки неприятного вкуса или запаха и для защиты таблеток от окисления. Покрытые пленкой таблетки представляют собой прессованные таблетки, которые покрыты тонким слоем или пленкой растворимого в воде материала. Пленочные покрытия включают, но не ограничиваются, гидроксиэтилцеллюлозу, карбоксиметилцеллюлозу натрия, полиэтиленгликоль 4000 и ацетатфталат целлюлозы. Пленочные покрытия придают те же характеристики, что и сахарное покрытие. Таблетки, прошедшие несколько стадий прессования, представляют собой прессованные таблетки, полученные более чем одним циклом прессования, включая слоистые таблетки, и покрытые прессованием таблетки или таблетки, полученные сухим покрытием.
Лекарственные формы в виде таблеток можно получить из активного ингредиента в порошкообразной, кристаллической или гранулированной форме, отдельно или в комбинации с одним или более носителями или вспомогательными веществами, описанными в настоящем изобретении, включая связующие, разрыхлители, полимеры для контролируемого высвобождения, смазывающие агенты, разбавители и/или красители. Ароматизаторы и подсластители является особенно пригодными для получения жевательных таблеток и таблеток для рассасывания.
Фармацевтические композиции, относящиеся к настоящему изобретению, для перорального введения можно обеспечивать в виде мягких или твердых капсул, которые можно получить из желатина, метилцеллюлозы, крахмала или альгината кальция. Твердая желатиновая капсула, также известная как капсула сухого наполнения (DFC), состоит из двух отделений, одно из которых надевается на другое, таким образом полностью окружая активный ингредиент. Мягкая эластичная капсула (SEC) представляет собой мягкую шарообразную оболочку, такую как желатиновая оболочка, которую пластифицируют добавлением глицерина, сорбитола или аналогичного полиола. Мягкие желатиновые оболочки могут содержать консервант, предотвращающий рост микроорганизмов. Подходящие консерванты представляют собой консерванты, как описано в настоящем изобретении, включая метил- и пропилпарабены и сорбиновую кислоту. Жидкие, полутвердые и твердые лекарственные формы, относящиеся к настоящему изобретению, можно инкупсулировать в капсулу. Подходящие жидкие и полутвердые лекарственные формы включают растворы и суспензии в пропиленкарбонате, растительных маслах или триглицеридах. Капсулы, содержащие данные растворы, можно получить, как описано в патентах США №№ 4328245; 4409239 и 4410545. Капсулы можно также покрывать, как известно специалисту в данной области техники, для того чтобы изменять или поддерживать растворение активного ингредиента.
Фармацевтические композиции, относящиеся к настоящему изобретению, для перорального введения можно предоставлять в виде жидких и полутвердых лекарственных форм, включая эмульсии, растворы, суспензии, эликсиры и сиропы. Эмульсия представляет собой двухфазную систему, в которой одна жидкость диспергирована в виде небольших капель в другой жидкости, которая может представлять собой масло в воде или воду в масле. Эмульсии могут содержать фармацевтически приемлемую неводную жидкость или растворитель, эмульгатор и консервант. Суспензии могут содержать фармацевтически приемлемый суспендирующий агент и консервант. Водно-спиртовые растворы могут содержать фармацевтически приемлемый ацеталь, такой как ди(низший алкил)ацеталь низшего алкилальдегида, например, диэтиловый ацеталь ацетальдегида; и смешивающийся с водой растворитель, содержащий одну или более гидроксильных групп, такой как пропиленгликоль и этанол. Эликсиры представляют собой истинные, подслащенные и водно-спиртовые растворы. Сиропы представляют собой концентрированные водные растворы сахара, например, сахарозы, и могут также содержать консервант. Что касается жидкой лекарственной формы, например, раствор в полиэтиленгликоле можно разбавлять достаточным количеством фармацевтически приемлемого жидкого носителя, например, воды, которую удобно измерять для введения.
Другие подходящие жидкие и полутвердые лекарственные формы включают, но не ограничиваются, лекарственные формы, содержащие активный ингредиент (ингредиенты), относящийся к настоящему изобретению, и диалкилированный моно- или полиалкиленгликоль, включая, 1,2-диметоксиметан, диглим, триглим, тетраглим, диметиловый эфир полиэтиленгликоля-350, диметиловый эфир полиэтиленгликоля-550, диметиловый эфир полиэтиленгликоля-750, где 350, 550 и 750 относятся к приблизительному среднему молекулярному весу полиэтиленгликоля. Данные составы могут дополнительно содержать один или более антиоксидантов, таких как бутилированный гидрокситолуол (BHT), бутилированный гидроксианизол (BHA), пропилгаллат, витамин E, гидрохинон, гидроксикумарины, этаноламин, лецитин, кефалин, аскорбиновая кислота, яблочная кислота, сорбитол, фосфорная кислота, бисульфит, метабисульфит натрия, тиодипропиновая кислота и ее эфиры и дитиокарбаматы.
Фармацевтические композиции, относящиеся к настоящему изобретению, для перорального введения можно также предоставлять в виде липосом, мицелл, микросфер или наносистем. Мицеллярные лекарственные формы можно получить, как описано в патенте США № 6350458.
Фармацевтические композиции, относящиеся к настоящему изобретению, для перорального введения можно обеспечить в виде нешипучих или шипучих гранул и порошков, которые будут растворять, получая жидкую лекарственную форму. Фармацевтически приемлемые носители и вспомогательные веществ, применяемые в нешипучих гранулах или порошках, могут включать разбавители, подсластители и смачивающие агенты. Фармацевтически приемлемые носители и вспомогательные веществ, применяемые в шипучих гранулах или порошках, могут содержать органические кислоты и источник диоксида углерода.
Красители и ароматизаторы можно применять во всех приведенных выше лекарственных формах.
Фармацевтические композиции, относящиеся к настоящему изобретению, для перорального введения можно формулировать в виде лекарственных форм с немедленным или измененным высвобождением, включая формы с замедленным, длительным, пульсирующим, контролируемым, направленным и программируемым высвобождением.
B. Парентеральное введение
Фармацевтические композиции, относящиеся к настоящему изобретению, можно вводить парентерально инъекцией, вливанием или имплантацией, для местного или системного введения. Парентеральное введение, как применяют в настоящем изобретении, включает внутривенное, внутриартериальное, внутрибрюшинное, интратекальное, внутрижелудочковое, интрауретральное, внутригрудинное, внутричерепное, внутримышечное, внутрисуставное, внутрипузырное и подкожное введение.
Фармацевтические композиции, относящиеся к настоящему изобретению, для парентерального введения можно формулировать в виде любых лекарственных форм, которые являются пригодными для парентерального введения, включая растворы, суспензии, эмульсии, мицеллы, липосомы, микросферы, наносистемы и твердые формы, пригодные для растворов или суспензий в жидкости перед инъекцией. Данные лекарственные формы можно получить согласно общепринятым способам, известным специалистам в области фармацевтической науки (смотрите Remington: The Science and Practice of Pharmacy, выше).
Фармацевтические композиции, предназначенные для парентерального введения, могут содержать один или более фармацевтически приемлемых носителей и вспомогательных веществ, включая, но не ограничиваясь, водные среды, смешивающиеся с водой среды, неводные среды, антимикробные агенты или консерванты против роста микроорганизмов, стабилизаторы, агенты, улучшающие растворение, изотонические агенты, буферные агенты, антиоксиданты, местные анестетики, суспендирующие и диспергирующие агенты, смачивающие агенты или эмульгаторы, комплексообразующие агенты, секвестранты или хелатирующие агенты, криопротекторы, лиопротекторы, загустители, регуляторы pH и инертные газы.
Подходящие водные среды включают, но не ограничиваются, воду, солевой раствор, физиологический солевой раствор или фосфатно-солевой буферный раствор (PBS), раствор хлорида натрия для инъекции, раствор Рингера для инъекции, изотонический раствор декстрозы для инъекции, стерильный водный раствор для инъекции, раствор Рингера с лактатом и декстрозой. Подходящие неводные среды включают, но не ограничиваются, нелетучие масла растительного происхождения, касторовое масло, кукурузное масло, хлопковое масло, оливковое масло, ореховое масло, масло из перечной мяты, подсолнечное масло, кунжутное масло, соевое масло, гидрогенизированное растительные масла, гидрогенизированное соевое масло и триглицериды со средней длиной цепи кокосового масла, и масло из семян пальмы. Подходящие смешивающиеся с водой среды включают, но не ограничиваются, этанол, 1,3-бутандиол, жидкий полиэтиленгликоль (например, полиэтиленгликоль 300 и полиэтиленгликоль 400), пропиленгликоль, глицерин, N-метил-2-пирролидон, N,N-диметилацетамид и диметилсульфоксид.
Подходящие антимикробные агенты или консерванты включают, но не ограничиваются, фенолы, крезолы, препараты, содержащие ртуть, бензиловый спирт, хлорбутанол, метил и пропил п-гидроксибензоаты, тиомеросал, бензалконийхлорид (например, бензетонийхлорид), метил- и пропилпарабены и сорбиновую кислоту. Подходящие изотонические агенты включают, но не ограничиваются, хлорид натрия, глицерин и декстрозу. Подходящие буферные агенты включают, но не ограничиваются, фосфат и цитрат. Подходящие антиоксиданты представляют собой антиоксиданты, как описано в настоящем изобретении, включая бисульфит и метабисульфит натрия. Подходящие местные анестетики включают, но не ограничиваются, прокаингидрохлорид. Подходящие суспендирующие и диспергирующие агенты представляют собой суспендирующие и диспергирующие агенты, как описано в настоящем изобретении, включая карбоксиметилцеллюлозу натрия, гидроксипропилметилцеллюлозу и поливинилпирролидон. Подходящие эмульгаторы представляют собой эмульгаторы, описанные в настоящем изобретении, включая монолаурат полиоксиэтиленсорбитана, полиоксиэтиленсорбитанмоноолеат 80 и триэтаноламинолеат. Подходящие секвестранты или хелатирующие агенты включают, но не ограничиваются EDTA. Подходящие агенты, регулирующие pH, включают, но не ограничиваются, гидроксид натрия, хлористоводородную кислоту, лимонную кислоту и молочную кислоту. Подходящие комплексообразователи включают, но не ограничиваются, циклодекстрины, включая α-циклодекстрин, β-циклодекстрин, гидроксипропил-β-циклодекстрин, сульфобутиловый эфир β-циклодекстрина и сульфобутиловый эфир 7-β-циклодекстрина (CAPTISOL®, CyDex, Lenexa, KS).
Когда фармацевтические композиции, относящиеся к настоящему изобретению, формулируют для многодозового введения, многодозовые парентеральные составы должны содержать антимикробный агент при бактериостатических или фунгистатических концентрациях. Все парентеральные составы должны быть стерильными, как известно и практикуется в данной области техники.
В одном варианте осуществления фармацевтические композиции для парентерального введения обеспечивают в виде готовых к применению стерильных растворов. В другом варианте осуществления фармацевтические композиции обеспечивают в виде стерильных сухих растворимых продуктов, включая лиофилизированные порошки и таблетки для подкожной инъекции, которые будут растворять в среде перед применением. В еще одном варианте осуществления фармацевтические композиции обеспечивают в виде готовых к применению стерильных суспензий. В еще одном варианте осуществления фармацевтические композиции обеспечивают в виде стерильных сухих нерастворимых продуктов, которые будут растворять в среде перед применением. В еще одном варианте осуществления фармацевтические композиции обеспечивают в виде готовых к применению стерильных эмульсий.
Фармацевтические композиции, относящиеся к настоящему изобретению, для парентерального введения можно формулировать в виде лекарственных форм с немедленным или измененным высвобождением, включая формы с замедленным, длительным, пульсирующим, контролируемым, направленным и программируемым высвобождением.
Фармацевтические композиции, относящиеся к настоящему изобретению, для парентерального введения можно формулировать в виде суспензии, твердой, полутвердой или тиксотропной жидкости, для введения в виде имплантированного депо. В одном варианте осуществления фармацевтические композиции, относящиеся к настоящему изобретению, диспергируют в твердой внутренней матрице, которая окружена наружной полимерной мембраной, которая нерастворима в жидкостях тела, но обеспечивает диффузию активного ингредиента из фармацевтических композиций через мембрану.
Подходящие внутренние матрицы включают, но не ограничиваются, полиметилметакрилат, полибутилметакрилат, пластифицированный или непластифицированный поливинилхлорид, пластифицированный нилон, пластифицированный полиэтилентерефталат, натуральный каучук, полиизопрен, полиизобутилен, полибутадиен, полиэтилен, этиленвинилацетатные сополимеры, силиконовые каучуки, полидиметилсилоксаны, силиконкарбонатные сополимеры, гидрофильные полимеры, такие как гидрогели эфиров акриловой и метакриловой кислот, коллаген, поперечносшитый поливиниловый спирт и поперечносшитый частично гидролизованный поливинилацетат.
Подходящие наружные полимерные мембраны включают, но не ограничиваются, полиэтилен, полипропилен, этилен/пропиленовые сополимеры, этилен/этилакрилатные сополимеры, этилен/винилацетатные сополимеры, силиконовые каучуки, полидиметилсилоксаны, неопреновый каучук, хлорированный полиэтилен, поливинилхлорид, винилхлоридные сополимеры с винилацетатом, винилиденхлорид, этилен и пропилен, иономерный полиэтилентерефталат, бутиловый каучук, эпихлоргидриновый каучук, сополимер этилен/виниловый спирт, терполимер этилен/винилацетат/виниловый спирт и этилен/винилоксиэтанольный сополимер.
C. Местное введение
Фармацевтические композиции, относящиеся к настоящему изобретению, можно вводить местно на кожу, отверстия или слизистые. Местное введение, как применяют в настоящем изобретении, включает (интра)дермальное, конъюнктивальное, внутрироговичное, интраокулярное, офтальмическое, аурикулярное, трансдермальное, назальное, вагинальное, уретральное, респираторное и ректальное введение.
Фармацевтические композиции, относящиеся к настоящему изобретению, можно формулировать в виде любых лекарственных форм, которые являются пригодными для местного введения для местного или системного эффекта, включая эмульсии, растворы, суспензии, крема, гели, гидрогели, мази, присыпки, повязки, эликсиры, лосьоны, суспензии, настойки, пасты, пены, пленки, аэрозоли, промывки, спреи, суппозитории, перевязки и накожные пластыри. Состав для местного введения фармацевтических композиций, относящихся к настоящему изобретению, может также включать липосомы, мицеллы, микросферы, наносистемы и их смеси.
Фармацевтически приемлемые носители и вспомогательные вещества, пригодные для применения в составах для местного применения, относящихся к настоящему изобретению, включают, но не ограничиваются, водные среды, смешиваемые с водой среды, неводные среды, противомикробные агенты или консерванты против роста микроорганизмов, стабилизаторы, агенты, улучшающие растворимость, изотонические агенты, буферные агенты, антиоксиданты, местные анестетики, суспендирующие и диспергирующие агенты, смачивающие агенты или эмульгаторы, комплексообразователи, секвестранты или хелатирующие агенты, агенты, улучшающие проникновение, криопротекторы, лиопротекторы, загустители и инертные газы.
Фармацевтические композиции можно также вводить местно электропорацией, ионтофорезом, фонофорезом, сонофорезом или инъекцией микроиглой или инъекцией без применения иглы, такой как POWDERJECT™ (Chiron Corp., Emeryville, CA) и BIOJECT™ (Bioject Medical Technologies Inc., Tualatin, OR).
Фармацевтические композиции, относящиеся к настоящему изобретению, можно предоставлять в виде мазей, кремов и гелей. Подходящие мазевые среды включают масляные или углеводородные среды, включая свиное сало, бензоилированное свиное сало, оливковое масло, хлопковое масло и другие масла, белый вазелин; эмульгируемые или абсорбционные среды, такие как гидрофильный петролатум, гидроксистеаринсульфат и безводный ланолин; удаляющие воду среды, такие как мазь-эмульсия; растворимые в воде мазевые среды, включая полиэтиленгликоли различного молекулярного веса; эмульсионные среды, или эмульсии вода в масле (W/O) или эмульсии масло в воде (O/W), включая цетиловый спирт, глицерилмоностеарат, ланолин и стеариновую кислоту (смотрите Remington: The Science and Practice of Pharmacy, выше). Данные среды являются смягчающими, но обычно требуют добавления антиоксидантов и консервантов.
Подходящая кремовая основа может представлять собой масло в воде или воду в масле. Подходящие кремовые среды могут быть смываемыми водой и содержать масляную фазу, эмульгатор и водную фазу. Масляную фазу также называют "внутренней" фазой, которая обычно состоит из петролатума и жирного спирта, такого как цетиловый или стеариловый спирт. Водная фаза обычно, хотя это необязательно, превышает масляную фазу по объему и обычно содержит увлажняющий агент. Эмульгатор в кремовом составе может представлять собой неионное, анионное, катионное или амфотерное поверхностно-активное вещество.
Гели представляют собой полутвердые системы типа суспензии. Однофазные гели содержат органические макромолекулы, распределенные по существу однородно по жидкому носителю. Подходящие желатинизирующие агенты включают, но не ограничиваются, поперечносшитые полимеры акриловой кислоты, такие как карбомеры, карбоксиполиалкилены и CARBOPOL®; гидрофильные полимеры, такие как полиэтиленоксиды, полиоксиэтиленполиоксипропиленовые сополимеры и поливиниловый спирт; целлюлозные полимеры, такие как гидроксипропилцеллюлоза, гидроксиэтилцеллюлоза, гидроксипропилметилцеллюлоза, фталат гидроксипропилметилцеллюлозы и метилцеллюлоза; камеди, такие как трагакант и ксантановая камедь; альгинат натрия; и желатин. Для того чтобы получить однородный гель, можно добавлять диспергирующий агент, такой как спирт или глицерин, или желатинизирующий агент можно диспергировать растиранием, механическим смешением и/или перемешиванием.
Фармацевтические композиции, относящиеся к настоящему изобретению, можно вводить ректально, уретрально, вагинально или околовлагалищно в виде суппозиториев, вагинальных суппозиториев, зондов, примочек или припарок, паст, порошков, перевязок, кремов, пластырей, противозачаточных средств, мазей, растворов, эмульсий, суспензий, тампонов, гелей, пен, аэрозолей и клизм. Данные лекарственные формы можно получить, применяя общепринятые способы, как описано в Remington: The Science and Practice of Pharmacy, выше.
Ректальные, уретральные и вагинальные суппозитории представляют собой твердые тела для вставки в отверстия тела, которые являются твердыми при обычной температуре, но плавятся или размягчаются при температуре тела, высвобождая активный ингредиент (активные ингредиенты) внутри отверстий. Фармацевтически приемлемые носители, применяемые в ректальных и вагинальных суппозиториях, содержат основы или среды, такие как загустители, которые дают температуру плавления вблизи температуры тела при формулировании с фармацевтическими композициями, относящимися к настоящему изобретению; и антиоксиданты, как описано в настоящем изобретении, включая бисульфит и метабисульфит натрия. Подходящие среды включают, но не ограничиваются, масло какао (какао-масло), глицерин-желатин, карбовакс (полиоксиэтиленгликоль), спермацет, парафин, белый и желтый воск и подходящие смеси моно-, ди- и триглицеридов жирных кислот, и гидрогели, такие как поливиниловый спирт, гидроксиэтилметакрилат и полиакриловую кислоту. Можно также применять комбинации различных сред. Ректальные и вагинальные суппозитории можно получить прессованием или формованием. Обычно вес ректального и вагинального суппозитория составляет от приблизительно 2 до приблизительно 3 г.
Фармацевтические композиции, относящиеся к настоящему изобретению, можно вводить офтальмически в виде растворов, суспензий, мазей, эмульсий, образующих гель растворов, порошков для растворов, гелей, глазных вставок и имплантатов.
Фармацевтические композиции, относящиеся к настоящему изобретению, можно вводить интраназально или ингаляцией через дыхательные пути. Фармацевтические композиции можно предоставлять в виде аэрозоля или раствора для доставки, применяя емкость под давлением, насос, спрей, ингалятор, такой как ингалятор, применяя электрогидродинамику, получая мелкодисперсный аэрозоль, или распылитель, отдельно или в комбинации с подходящим пропеллентом, таким как 1,1,1,2-тетрафтопентан или 1,1,1,2,3,3,3-гептафторпропан. Фармацевтические композиции можно также обеспечивать в виде сухого порошка для инсуффляции, отдельно или в комбинации с инертным носителем, таким как лактоза или фосфолипиды; и капель для носа. Что касается интраназального применения, порошок может содержать биоадгезивный агент, включая хитозан или циклодекстрин.
Растворы или суспензии для применения в емкости под давлением, насосе, спрее, распылительном устройстве или ингаляторе можно формулировать так, чтобы они содержали этанол, водный этанол или подходящий альтернативный агент для диспергирования, солюбилизирования или продолжительного высвобождения активного ингредиента, относящегося к настоящему изобретению; пропеллент в качестве растворителя; и/или поверхностно-активное вещество, такое как триолеат сорбитана, олеиновая кислота или олигомолочная кислота.
Фармацевтические композиции, относящиеся к настоящему изобретению, можно тонко измельчать до размера, подходящего для доставки ингаляцией, такого как приблизительно 50 микрометром или меньше, или приблизительно 10 микрометров или меньше. Частицы данных размеров можно получить, применяя способ измельчения, известный специалисту в данной области техники, такой как размол на спиральной струйной мельнице, размол на струйной мельнице с кипящим слоем, обработка сверхкритической жидкостью, получая наночастицы, гомогенизация высокого давления или сушка распылением.
Капсулы, блистеры и картриджи для применения в ингаляторе или инсуффляторе можно формулировать так, чтобы они содержали порошковую смесь фармацевтических композиций, относящихся к настоящему изобретению; подходящей порошковой основы, такой как лактоза или крахмал; и агента, изменяющего свойства, такого как l-лейцин, маннитол или стеарат магния. Лактоза может быть безводной или в виде моногидрата. Другие подходящие вспомогательные вещества или носители включают, но не ограничиваются, декстран, глюкозу, мальтозу, сорбитол, ксилит, фруктозу, сахарозу и трегалозу. Фармацевтические композиции, относящиеся к настоящему изобретению, для ингаляционного/интраназального введения могут дополнительно содержать подходящий ароматизатор, такой как ментол и левоментол; и/или подсластители, такие как сахарин и сахарин натрия.
Фармацевтические композиции, относящиеся к настоящему изобретению, для местного введения можно формулировать для немедленного высвобождения или измененного высвобождения, включая замедленное, длительное, пульсирующее, контролируемое, направленное и программируемое высвобождение.
D. Измененное высвобождение
Фармацевтические композиции, относящиеся к настоящему изобретению, можно формулировать в виде лекарственной формы с измененным высвобождением. Как применяют в настоящем изобретении, термин “измененное высвобождение” относится к лекарственной форме, для которой скорость или место высвобождения активного ингредиента (ингредиентов) является отличным от скорости или места высвобождения для лекарственной формы с немедленным высвобождением при введении тем же путем. Лекарственные формы с измененным высвобождением включают, но не ограничиваются, замедленное, длительное, пролонгированное, долговременное, пульсирующее, контролируемое, ускоренное и быстрое, направленное, программируемое высвобождение, и лекарственные формы с задержкой в желудке. Фармацевтические композиции в виде лекарственных форм с измененным высвобождением можно получить, применяя ряд средств для изменения высвобождения и способов, известных специалисту в данной области техники, включая, но не ограничиваясь, матричные средства для контролируемого высвобождения, осмотические средства для контролируемого высвобождения, многочастичные средства для контролируемого высвобождения, ионообменные смолы, энтеросолюбильные покрытия, многослойные покрытия, микросферы, липосомы и их комбинации. Скорость высвобождения активного ингредиента (ингредиентов) можно также изменять изменением размеров частиц и полиморфизмом активного ингредиента (ингредиентов).
Примеры измененного высвобождения включают, но не ограничиваются, примеры, описанные в патентах США №№: 3845770, 3916899, 3536809, 3598123, 4008719, 5674533, 5059595, 5591767, 5120548, 5073543, 5639476, 5354556, 5639480, 5733566, 5739108, 5891474, 5922356, 5972891, 5980945, 5993855, 6045830, 6087324, 6113943, 6197350, 6248363, 6264970, 6267981, 6376461, 6419961, 6589548, 6613358 и 6699500.
1. Матриксные средства для контролируемого высвобождения
Фармацевтические композиции, относящиеся к настоящему изобретению, в лекарственной форме с контролируемым высвобождением можно получать, применяя матриксное средство с контролируемым высвобождением, известное специалисту в данной области техники (смотрите Takada et al. в “Encyclopedia of Controlled Drug Delivery”, Vol. 2, Mathiowitz Ed., Wiley, 1999).
В определенных вариантах осуществления фармацевтические композиции, относящиеся к настоящему изобретению, в лекарственной форме с измененным высвобождением формулируют, применяя размываемое матриксное средство, которое представляет собой набухающие в воде, размываемые или растворимые полимеры, включая, но не ограничиваясь, синтетические полимеры и природные полимеры и производные, такие как полисахариды и белки.
Материалы, пригодные для получения размываемого матрикса, включают, но не ограничиваются, хитин, хитозан, декстран и пуллулан; агар, аравийскую камедь, камедь карайи, камедь бобов рожкового дерева, трагакантовую камедь, каррагенаны, камедь гхатти, гуаровую камедь, ксантановую камедь и склероглюкан; крахмалы, такие как декстрин и мальтодекстрин; гидрофильные коллоиды, такие как пектин; фосфатиды, такие как лецитин; альгинаты; альгинат пропиленгликоля; желатин; коллаген; целлюлозы, такие как этилцеллюлоза (EC), метилэтилцеллюлоза (MEC), карбоксиметилцеллюлоза (CMC), CMEC, гидроксиэтилцеллюлоза (HEC), гидроксипропилцеллюлоза (HPC), ацетат целлюлозы (CA), пропионат целлюлозы (CP), бутират целлюлозы (CB), ацетатбутират целлюлозы (CAB), CAP, CAT, гидроксипропилметилцеллюлоза (HPMC), HPMCP, HPMCAS, ацетаттримеллитат гидроксипропилметилцеллюлозы (HPMCAT) и этилгидроксиэтилцеллюлоза (EHEC); поливинилпирролидон; поливиниловый спирт; поливинилацетат; эфиры глицерина и жирных кислот; полиакриламид; полиакриловая кислота; сополимеры акриловой кислоты или метакриловой кислоты (EUDRAGIT®, Rohm America, Inc., Piscataway, NJ); поли(2-гидроксиэтилметакрилат); полилактиды; сополимеры L-глютаминовой кислоты и этил-L-глютамата; разлагаемые сополимеры молочной кислоты и гликолевой кислоты; поли-D-(-)-3-гидроксимасляная кислота; и другие производные акриловой кислоты, такие как гомополимеры и сополимеры бутилметакрилата, метилметакрилата, этилметакрилата, этилакрилата, (2-диметиламиноэтил)метакрилата и хлорида (триметиламиноэтил)метакрилата.
В определенных вариантах осуществления фармацевтические композиции, относящиеся к настоящему изобретению, формулируют с неразмываемым матриксным средством. Активный ингредиент (ингредиенты) растворяют или диспергируют в инертном матриксе, и он высвобождается в первую очередь диффузией через инертный матрикс после введения. Материалы, пригодные для применения в качестве неразмываемого матриксного средства включают, но не ограничиваются, нерастворимые пластмассы, такие как полиэтилен, полипропилен, полиизопрен, полиизобутилен, полибутадиен, полиметилметакрилат, полибутилметакрилат, хлорированный полиэтилен, поливинилхлорид, сополимеры метилакрилата и метилметакрилата, этиленвинилацетатные сополимеры, этилен/пропиленовые сополимеры, этилен/этилакрилатные сополимеры, винилхлоридные сополимеры с винилацетатом, винилиденхлорид, этилен и пропилен, иономерный полиэтилентерефталат, бутиловые каучуки, эпихлоргидриновые каучуки, сополимер этилен/виниловый спирт, терполимер этилен/винилацетат/виниловый спирт, сополимер этилен/винилоксиэтанол, поливинилхлорид, пластифицированный нилон, пластифицированный полиэтилентерефталат, натуральный каучук, силиконовые каучуки, полидиметилсилоксаны и силиконкарбонатные сополимеры; гидрофильные полимеры, такие как этилцеллюлоза, ацетат целлюлозы, кросповидон и поперечносшитый частично гидролизованный поливинилацетат; и жирные соединения, такие как карнаубский воск, микрокристаллический воск и триглицериды.
В матриксной системе с контролируемым высвобождением требуемую кинетику высвобождения можно контролировать, например, типом применяемого полимера, вязкостью полимера, размером частиц полимера и/или активного ингредиента (ингредиентов), отношением активного ингредиента (ингредиентов) относительно полимера, и других вспомогательных веществ или носителей в композициях.
Фармацевтические композиции, относящиеся к настоящему изобретению, в лекарственной форме с измененным высвобождением можно получить способами, известными специалисту в данной области техники, включая прямое прессование, сухое или мокрое гранулирование с последующим прессованием, и гранулирование из расплава с последующим прессованием.
2. Осмотические средства с контролируемым высвобождением
Фармацевтические композиции, относящиеся к настоящему изобретению, в лекарственной форме с измененным высвобождением можно получить, применяя осмотическое средство с контролируемым высвобождением, включая, но не ограничиваясь, однокамерную систему, двухкамерную систему, технологию с асимметричной мембраной (AMT) и систему с вытеснением из ядра (ECS). В общем, данные системы содержат по меньшей мере два компонента: (a) ядро, которое содержит активный ингредиент; и (b) полупроницаемую мембрану по меньшей мере с одним проницаемым отверстием, которая инкапсулирует ядро. Полупроницаемая мембрана контролирует приток воды в ядро из применяемого водного окружения так, чтобы вызывать высвобождение лекарственного средства вытеснением через проницаемое отверстие (отверстия).
В добавление к активному ингредиенту (ингредиентам), ядро осмотического средства необязательно содержит осмотический агент, который создает движущую силу для транспорта воды из применяемого окружения в ядро устройства. Одним классом осмотических агентов является набухаемые в воде гидрофильные полимеры, которые также называют “осмополимеры” и “гидрогели”. Подходящие набухаемые в воде гидрофильные полимеры в качестве осмотических агентов включают, но не ограничиваются, гидрофильные винильные и акриловые полимеры, полисахариды, такие как альгинат кальция, полиэтиленоксид (PEO), полиэтиленгликоль (PEG), полипропиленгликоль (PPG), поли(2-гидроксиэтилметакрилат), поли(акриловая) кислота, поли(метакриловая) кислота, поливинилпирролидон (PVP), поперечносшитый PVP, поливиниловый спирт (PVA), PVA/PVP сополимеры, PVA/PVP сополимеры с гидрофобными мономерами, такими как метилметакрилат и винилацетат, гидрофильные полиуретаны, содержащие большие PEO блоки, кроскармелоза натрия, каррагенан, гидроксиэтилцеллюлоза (HEC), гидроксипропилцеллюлоза (HPC), гидроксипропилметилцеллюлоза (HPMC), карбоксиметилцеллюлоза (CMC) и карбоксиэтилцеллюлоза (CEC), альгинат натрия, поликарбофил, желатин, ксантановая камедь и крахмалгликолят натрия.
Другой класс осмотических агентов представляет собой осмогены, которые способны впитывать воду, создавая градиент осмотического давления через барьер окружающего покрытия. Подходящие осмогены включают, но не ограничиваются, неорганические соли, такие как сульфат магния, хлорид магния, хлорид кальция, хлорид натрия, хлорид лития, сульфат калия, фосфаты калия, карбонат натрия, сульфит натрия, сульфат лития, хлорид калия и сульфат натрия; сахара, такие как декстроза, фруктоза, глюкоза, инозитол, лактоза, мальтоза, маннитол, раффиноза, сорбитол, сахароза, трегалоза и ксилит; органические кислоты, такие как аскорбиновая кислота, бензойная кислота, фумаровой кислоты, лимонная кислота, малеиновая кислота, себациновая кислота, сорбиновая кислота, адипиновая кислота, этилендиаминтетрауксусная кислота, глутаминовая кислота, п-толуолсульфоновая кислота, янтарная кислота, винная кислота и мочевина; и их смеси.
Осмотические агенты различных скоростей растворения можно применять для влияния на то, как быстро активный ингредиент (ингредиенты) сначала доставляются из лекарственной формы. Например, аморфные сахара, такие как MANNOGEM™ EZ (SPI Pharma, Lewes, DE), можно применять для обеспечения более быстрой доставки в течение первой пары часов, в короткий срок давая требуемый терапевтический эффект, и постепенного и непрерывного высвобождения оставшегося количества, поддерживая требуемую степень терапевтического или профилактического эффекта в течение длительного периода времени. В данном случае активный ингредиент (ингредиенты) высвобождается при такой скорости, чтобы восполнить количество активного ингредиента, который подвергся метаболизму или был выведен из организма.
Ядро может также содержать большое разнообразие других вспомогательных веществ и носителей, как описано в настоящем изобретении, улучшая характеристики лекарственной формы или повышая стабильность или способствуя обработке.
Материалы, пригодные для получения полупроницаемой мембраны, включают различные сорта акриловых полимеров, винилов, эфиров, полиамидов, полиэфиров и целлюлозных производных, которые являются водопроницаемыми и нерастворимыми в воде при физиологически подходящих pH, или способными становиться нерастворимыми в воде при химическом изменении, таком как поперечная сшивка. Примеры подходящих полимеров, пригодных для получения покрытия, включают пластифицированный, непластифицированный и упрочненный ацетат целлюлозы (CA), диацетат целлюлозы, триацетат целлюлозы, CA пропионат, нитрат целлюлозы, ацетатбутират целлюлозы (CAB), CA этилкарбамат, CAP, CA метилкарбамат, CA сукцинат, ацетаттримеллитат целлюлозы (CAT), CA диметиламиноацетат, CA этилкарбонат, CA хлорацетат, CA этилоксалат, CA метилсульфонат, CA бутилсульфонат, CA п-толуолсульфонат, агарацетат, триацетат амилозы, ацетат бета-глюкана, триацетат бета-глюкана, диметилацетат ацетальдегида, триацетат камеди рожкового дерева, гидроксилированный этиленвинилацетат, EC, PEG, PPG, PEG/PPG сополимеры, PVP, HEC, HPC, CMC, CMEC, HPMC, HPMCP, HPMCAS, HPMCAT, поли(акриловые) кислоты и эфиры и поли(метакриловые) кислоты и эфиры и их сополимеры, крахмал, декстран, декстрин, хитозан, коллаген, желатин, полиалкены, полиэфиры, полисульфоны, полиэфирсульфорнаты, полистиролы, поливинилгалогениды, поливиниловые простые и сложные эфиры, природные воски и синтетические воски.
Полупроницаемая мембрана может также представлять собой гидрофобную микропористую мембрану, где поры по существу заполнены газом и не смачиваются водной средой, но являются проницаемыми для водяного пара, как описано в патенте США № 5798119. Данная гидрофобная, но проницаемая для водяного пара мембрана обычно состоит из гидрофобных полимеров, таких как полиалкены, полиэтилен, полипропилен, политетрафторэтилен, производные полиакриловой кислоты, полиэфиры, полисульфоны, полиэфирсульфонаты, полистиролы, поливинилгалогениды, поливинилиденфторид, поливиниловые сложные и простые эфиры, природные воски и синтетические воски.
Пропускающее отверстие (отверстия) в полупроницаемой мембране можно получить после нанесения покрытия механическим или лазерным сверлением. Пропускающее отверстие (отверстия) можно также получить in situ разрушением вставки растворимого в воде материала или разрывом тончайшей части мембраны в углублении в ядре. Кроме того, пропускающие отверстия можно получить в процессе нанесения покрытия, как в случае покрытий с асимметричной мембраной типа, описанного в патентах США №№ 5612059 и 5698220.
Суммарное количество высвобождающегося активного ингредиента (ингредиентов) и скорость высвобождения можно по существу регулировать толщиной и пористостью полупроницаемой мембраны, составом ядра и количеством, размером и положением пропускающих отверстий.
Фармацевтические композиции в виде осмотической лекарственной формы с контролируемым высвобождением содержат дополнительные общепринятые вспомогательные вещества или носители, как описано в настоящем изобретении, улучшающие характеристики или облегчающие обработку состава.
Осмотические лекарственные формы с контролируемым высвобождением можно получить согласно общепринятым способам и методикам, известным специалисту в данной области техники (смотрите Remington: The Science and Practice of Pharmacy, выше; Santus and Baker, J. Controlled Release 1995, 35, 1-21; Verma et al., Drug Development and Industrial Pharmacy 2000, 26, 695-708; Verma et al., J. Controlled Release 2002, 79, 7-27).
В определенных вариантах осуществления фармацевтические композиции, относящиеся к настоящему изобретению, формулируют в виде лекарственной формы с AMT контролируемым высвобождением, которая содержит асимметричную осмотическую мембрану, которая покрывает ядро, содержащее активный ингредиент (ингредиенты) и другие фармацевтически приемлемые вспомогательные вещества или носители. Смотрите патент США № 5612059 и WO 2002/17918. Лекарственные формы с AMT контролируемым высвобождением можно получить согласно общепринятым способам и методикам, известным специалисту в данной области техники, включая прямое прессование, сухое гранулирование, мокрое гранулирование и способ нанесения покровного слоя погружением.
В определенных вариантах осуществления фармацевтические композиции, относящиеся к настоящему изобретению, формулируют в виде лекарственной формы с ESC контролируемым высвобождением, которая содержит осмотическую мембрану, которая покрывает ядро, содержащее активный ингредиент (ингредиенты), гидроксиэтилцеллюлозу и другие фармацевтически приемлемые вспомогательные вещества или носители.
3. Средства, состоящие из большого количества частиц, с контролируемым высвобождением
Фармацевтические композиции, относящиеся к настоящему изобретению, в лекарственной форме с измененным высвобождением можно получить в виде средства, состоящего из большого количества частиц, с контролируемым высвобождением, которое содержит множество частиц, гранул или шариков в диапазоне от приблизительно 10 мкм до приблизительно 3 мм, от приблизительно 50 мкм до приблизительно 2,5 мм или от приблизительно 100 мкм до приблизительно 1 мм в диаметре. Данные средства, состоящие из большого количества частиц, можно получить способами, известными специалисту в данной области техники, включая мокрое и сухое гранулирование, экструзию/сферонизацию, вальцевание, отверждение расплава и нанесение покрытия распылением на ядра зерен. Смотрите, например, Multiparticulate Oral Drug Delivery; Marcel Dekker: 1994; и Pharmaceutical Pelletization Technology; Marcel Dekker: 1989.
Другие вспомогательные вещества или носители, как описано в настоящем изобретении, можно смешивать с фармацевтическими композициями, способствуя обработке и образованию множества частиц. Полученные в результате частицы могут сами образовывать средство, состоящее из множества частиц, или их можно покрывать различными образующими пленку материалами, такими как энтеросолюбильные полимеры, и набухаемые в воде и растворимые в воде полимеры. Множество частиц можно дополнительно обрабатывать как капсулу или таблетку.
4. Направленная доставка
Фармацевтические композиции, относящиеся к настоящему изобретению, можно также формулировать для направленной доставки в конкретную ткань, рецептор или другую область тела субъекта, которого подвергают лечению, включая липосомные системы доставки, системы с применением эритроцитов для доставки лекарственных средств и системы доставки на основе антител. Примеры включают, но не ограничиваются, системы, описанные в патентах США №№ 6316652, 6274552, 6271359, 6253872, 6139865, 6131570, 6120751, 6071495, 6060082, 6048736, 6039975, 6004534, 5985307, 5972366, 5900252, 5840674, 5759542 и 5709874.
Способы применения
В одном варианте осуществления настоящее изобретение относится к способу лечения, предотвращения или облегчения одного или более симптомов PI3K-опосредованного расстройства, заболевания или состояния у субъекта, включающему введение субъекту терапевтически эффективного количества соединения, описанного в настоящем изобретении, например, соединения формулы I или его энантиомера, смеси энантиомеров, смеси двух или более диастереомеров или изотопного варианта; или их фармацевтически приемлемой соли, сольвата, гидрата или пролекарства.
В определенных вариантах осуществления PI3K представляет собой PI3K дикого типа. В определенных вариантах осуществления PI3K представляет собой PI3K вариант.
В определенных вариантах осуществления PI3K представляет собой киназу I класса. В определенных вариантах осуществления PI3K представляет собой PI3Kα, PI3Kβ, PI3Kδ или PI3Kγ. В определенных вариантах осуществления PI3K представляет собой p110α, p110β, p110δ или p110γ. В определенных вариантах осуществления PI3K представляет собой дикий тип киназы I класса. В определенных вариантах осуществления PI3K представляет собой вариант киназы I класса.
В определенных вариантах осуществления PI3K представляет собой p110α. В определенных вариантах осуществления PI3K представляет собой дикий тип p110α. В определенных вариантах осуществления PI3K представляет собой p110α мутант. В определенных вариантах осуществления p110α мутант представляет собой R38H, G106V, K111N, K227E, N345K, C420R, P539R, E542K, E545A, E545G, E545K, Q546K, Q546P, E453Q, H710P, I800L, T1025S, M1043I, M1043V, H1047L, H1047R или H1047Y. В определенных вариантах осуществления p110α мутант представляет собой R38H, K111N, N345K, C420R, P539R, E542K, E545A, E545G, E545K, Q546K, Q546P, I800L, T1025S, M1043I, H1047L, H1047R или H1047Y. В определенных вариантах осуществления p110α мутант представляет собой C420R, E542K, E545A, E545K, Q546K, I800L, M1043I, H1047L или H1047Y.
В определенных вариантах осуществления PI3K представляет собой PI3Kγ. В определенных вариантах осуществления PI3K представляет собой дикий тип PI3Kγ. В определенных вариантах осуществления PI3K представляет собой вариант PI3Kγ.
В определенных вариантах осуществления соединение, относящееся к настоящему изобретению, селективно направлено на PI3Kδ. В определенных вариантах осуществления соединение, относящееся к настоящему изобретению, селективно направлено на дикий тип PI3Kδ. В определенных вариантах осуществления соединение, относящееся к настоящему изобретению, селективно направлено на вариант PI3Kδ.
В определенных вариантах осуществления соединение, относящееся к настоящему изобретению, представляет собой селективный ингибитор PI3Kδ. В определенных вариантах осуществления соединение, относящееся к настоящему изобретению, обладает селективностью относительно PI3Kδ по сравнению с PI3Kα, в диапазоне от приблизительно 2-кратного, приблизительно 4-кратного, приблизительно 8-кратного, приблизительно 20-кратного, приблизительно 50-кратного, приблизительно 100-кратного, приблизительно 200-кратного, приблизительно 500-кратного или приблизительно 1000-кратного. В определенных вариантах осуществления соединение, относящееся к настоящему изобретению, обладает селективностью относительно PI3Kδ по сравнению с PI3Kβ в диапазоне от приблизительно 2-кратного, приблизительно 4-кратного, приблизительно 8-кратного, приблизительно 20-кратного, приблизительно 50-кратного, приблизительно 100-кратного, приблизительно 200-кратного, приблизительно 500-кратного или приблизительно 1000-кратного. В определенных вариантах осуществления соединение, относящееся к настоящему изобретению, обладает селективностью относительно PI3Kδ по сравнению с PI3Kγ в диапазоне от приблизительно 2-кратного, приблизительно 4-кратного, приблизительно 8-кратного, приблизительно 20-кратного, приблизительно 50-кратного, приблизительно 100-кратного, приблизительно 200-кратного, приблизительно 500-кратного или приблизительно 1000-кратного. В определенных вариантах осуществления соединение, относящееся к настоящему изобретению, обладает селективностью относительно PI3Kδ по сравнению с mTOR в диапазоне от приблизительно 2-кратного, приблизительно 4-кратного, приблизительно 8-кратного, приблизительно 20-кратного, приблизительно 50-кратного, приблизительно 100-кратного, приблизительно 200-кратного, приблизительно 500-кратного или приблизительно 1000-кратного.
В определенных вариантах осуществления соединение, относящееся к настоящему изобретению, представляет собой селективный ингибитор PI3Kβ. В определенных вариантах осуществления соединение, относящееся к настоящему изобретению, обладает селективностью относительно PI3Kβ по сравнению с PI3Kα в диапазоне от приблизительно 2-кратного, приблизительно 4-кратного, приблизительно 8-кратного, приблизительно 20-кратного, приблизительно 50-кратного, приблизительно 100-кратного, приблизительно 200-кратного, приблизительно 500-кратного или приблизительно 1000-кратного. В определенных вариантах осуществления, соединение, относящееся к настоящему изобретению, обладает селективностью относительно PI3Kβ по сравнению с PI3Kδ в диапазоне от приблизительно 2-кратного, приблизительно 4-кратного, приблизительно 8-кратного, приблизительно 20-кратного, приблизительно 50-кратного, приблизительно 100-кратного, приблизительно 200-кратного, приблизительно 500-кратного или приблизительно 1000-кратного. В определенных вариантах осуществления соединение, относящееся к настоящему изобретению, обладает селективностью относительно PI3Kβ по сравнению с PI3Kγ в диапазоне от приблизительно 2-кратного, приблизительно 4-кратного, приблизительно 8-кратного, приблизительно 20-кратного, приблизительно 50-кратного, приблизительно 100-кратного, приблизительно 200-кратного, приблизительно 500-кратного или приблизительно 1000-кратного. В определенных вариантах осуществления соединение, относящееся к настоящему изобретению, обладает селективностью относительно PI3Kβ по сравнению с mTOR в диапазоне от приблизительно 2-кратного, приблизительно 4-кратного, приблизительно 8-кратного, приблизительно 20-кратного, приблизительно 50-кратного, приблизительно 100-кратного, приблизительно 200-кратного, приблизительно 500-кратного или приблизительно 1000-кратного.
В определенных вариантах осуществления соединение, относящееся к настоящему изобретению, представляет собой селективный ингибитор PI3Kδ и PI3Kβ. В определенных вариантах осуществления соединение, относящееся к настоящему изобретению, обладает селективностью относительно PI3Kδ и PI3Kβ по сравнению с PI3Kα в диапазоне от приблизительно 2-кратного, приблизительно 4-кратного, приблизительно 8-кратного, приблизительно 20-кратного, приблизительно 50-кратного, приблизительно 100-кратного, приблизительно 200-кратного, приблизительно 500-кратного или приблизительно 1000-кратного. В определенных вариантах осуществления соединение, относящееся к настоящему изобретению, обладает селективностью относительно PI3Kδ и PI3Kβ по сравнению с PI3Kγ в диапазоне от приблизительно 2-кратного, приблизительно 4-кратного, приблизительно 8-кратного, приблизительно 20-кратного, приблизительно 50-кратного, приблизительно 100-кратного, приблизительно 200-кратного, приблизительно 500-кратного или приблизительно 1000-кратного. В определенных вариантах осуществления соединение, относящееся к настоящему изобретению, обладает селективностью относительно PI3Kδ и PI3Kβ по сравнению с mTOR в диапазоне от приблизительно 2-кратного, приблизительно 4-кратного, приблизительно 8-кратного, приблизительно 20-кратного, приблизительно 50-кратного, приблизительно 100-кратного, приблизительно 200-кратного, приблизительно 500-кратного или приблизительно 1000-кратного.
В определенных вариантах осуществления PI3K представляет собой киназу IV класса. В определенных вариантах осуществления PI3K представляет собой дикий тип киназы IV класса. В определенных вариантах осуществления PI3K представляет собой вариант киназы IV класса. В определенных вариантах осуществления PI3K представляет собой mTOR, ATM, ATR или DNA-PK. В определенных вариантах осуществления PI3K представляет собой mTOR.
В других вариантах осуществления настоящее изобретение относится к способу лечения, предотвращения или облегчения одного или более симптомов пролиферативного заболевания у субъекта, включающему введение субъекту терапевтически эффективного количества соединения, описанного в настоящем изобретении, например, соединения формулы I или его энантиомера, смеси энантиомеров, смеси двух или более диастереомеров или изотопного варианта; или их фармацевтически приемлемой соли, сольвата, гидрата или пролекарства.
В определенных вариантах осуществления субъект представляет собой млекопитающее. В определенных вариантах осуществления субъект представляет собой человека. В определенных вариантах осуществления субъект представляет собой примата, отличного от человека, сельскохозяйственное животное, такое как крупный рогатый скот, спортивное животное или домашнее животное, такое как лошадь, собака или кошка.
В определенных вариантах осуществления пролиферативное заболевание представляет собой рак. В определенных вариантах осуществления, пролиферативное заболевание представляет собой гематологический рак. В определенных вариантах осуществления пролиферативное заболевание представляет собой воспалительное заболевание. В определенных вариантах осуществления пролиферативное заболевание представляет собой иммунное заболевание.
Расстройства, заболевания или состояния, которые можно лечить соединением, относящимся к настоящему изобретению, включают, но не ограничиваются, (1) воспалительные или аллергические заболевания, включая системную анафилаксию и аллергические расстройства, атопический дерматит, крапивницу, аллергии на лекарственные средства, аллергии на укусы насекомых, пищевые аллергии (включая целиакию и подобные) и мастоцитоз, (2) воспалительные заболевания кишечника, включая болезнь Крона, язвенный колит, илеит и энтерит, (3) васкулит и синдром Бехчета, (4) псориаз и воспалительные дерматозы, включая дерматит, экзему, атопический дерматит, аллергический контактный дерматит, крапивницу, вирусные кожные патологии, включая патологии из-за вируса папилломы человека, инфицирования ВИЧ или вирусом лейкоза Раушера, бактериальные, грибковые и другие паразитные кожные патологии и кожную красную волчанку, (5) астму и дыхательные аллергические заболевания, включая аллергическую астму, астму, вызванную физической нагрузкой, аллергический ринит, отит, аллергический конъюнктивит, аллергическое заболевание легких и хроническое обструктивное заболевание легких, (6) аутоиммунные заболевания, включая ревматоидный артрит (включая ревматоидный и псориатический артрит), системную красную волчанку, диабет I типа, миастению, рассеянный склероз, болезнь Грейвса и гломерулонефрит, (7) отторжение трансплантата (включая отторжение аллотрансплантата и реакцию "трансплантант против хозяина") например, отторжение кожного трансплантата, отторжение трансплантата твердого органа, отторжение трансплантата костного мозга, (8) лихорадку, (9) сердечнососудистые расстройства, включая острую сердечную недостаточность, гипотонию, гипертонию, стенокардию, инфаркт миокарда, кардиомиопатию, застойную сердечную недостаточность, атеросклероз, заболевание коронарных артерий, рестеноз и сосудистый стеноз, (10) цереброваскулярные заболевания, включая черепно-мозговую травму, инсульт, ишемическое реперфузионное повреждение и аневризм, (11) рак молочной железы, кожи, простаты, шейки матки, матки, яичников, яичек, мочевого пузыря, легкого, печени, гортани, полости рта, толстой кишки и желудочно-кишечного тракта (например, пищевода, желудка, поджелудочной железы), головного мозга, щитовидной железы, крови и лимфатической системы, (12) фиброз, заболевание соединительной ткани и саркоидоз, (13) половые и репродуктивные заболевания, включая эректильные дисфункции, (14) желудочно-кишечные заболевания, включая гастрит, язву, тошноту, панкреатит и рвоту; (15) неврологические расстройства, включая болезнь Альцгеймера, (16) нарушения сна, включая бессонницу, нарколепсию, синдром апноэ во сне и синдром Пиквика (17) боль, (18) заболевания почек, (19) заболевания глаз, включая глаукому и (20) инфекционные заболевания, включая ВИЧ.
В определенных вариантах осуществления рак, который можно лечить способами, относящимися к настоящему изобретению, включает, но не ограничивается, (1) лейкозы, включая, но не ограничиваясь, острый лейкоз, острый лимфоцитарный лейкоз, острые миелоцитарные лейкозы, такие как миелобластный, промиелоцитарный, миеломоноцитарный, моноцитный, эритролейкемии и миелодиспластический синдром или его симптом (например, анемию, тромбоцитопению, нейтропению, бицитопению или панцитопению), рефрактерную анемию (РА), РА с кольцевыми сидеробластами (RARS), РА с избытком бластов (RAEB), RAEB в стадии трансформации (RAEB-T), прелейкоз и хронический миеломоноцитарный лейкоз (CMML), (2) хронические лейкозы, включая, но не ограничиваясь, хронический миелоидный (гранулоцитный) лейкоз, хронический лимфолейкоз и лейкоз волосатых клеток, (3) истинную полицитемию, (4) лимфомы, включая, но не ограничиваясь, болезнь Ходжкина и заболевания неходжкинской лимфомы, (5) множественные миеломы, включая, но не ограничиваясь, вялую множественную миелому, несекреторную миелому, остеосклеротическую миелому, лейкоз плазматических клеток, солитарную плазмоцитому и экстрамедуллярную плазмоцитому; (6) макроглобулинемию Вальденстрема; (7) моноклональную гаммапатию неясного значения, (8) доброкачественную моноклональную гаммапатию; (9) заболевание тяжелых цепей, (10) саркомы костной и соединительной ткани, включая, но не ограничиваясь, костные саркомы, остеосаркому, хондросаркому, саркому Юинга, злокачественную гигантоклеточную опухоль, фибросаркому кости, хордому, периостальную саркому, саркомы мягких тканей, ангиосаркому (гемангиосаркому), фибросаркому, саркому Капоши, лейомиосаркому, липосаркому, лимфангиосаркому, метастатический рак, неврилеммому, рабдомиосаркому и синовиальную саркому, (11) опухоли головного мозга, включая, но не ограничиваясь, глиому, астроцитому, глиому ствола мозга, эпендимому, олигодендроглиому, неглиальную опухоль, неврилеммому слухового нерва, краниофарингиому, медуллобластому, менингиому, пинеоцитому, пинеобластому и первичную лимфому мозга, (12) рак молочной железы, включая, но не ограничиваясь, аденокарциному, дольковую (мелкоклеточную) карциному, внутрипротоковую карциному, медуллярный рак молочной железы, коллоидный рак молочной железы, трубчатый рак молочной железы, папиллярный рак молочной железы, первичный рак, болезнь Педжета и воспалительный рак молочной железы, (13) рак надпочечников, включая, но не ограничиваясь, феохромоцитому и карциному коры надпочечников, (14) рак щитовидной железы, включая, но не ограничиваясь, папиллярный или фолликулярный рак щитовидной железы, медуллярный рак щитовидной железы, анапластический рак щитовидной железы, (15) рак поджелудочной железы, включая, но не ограничиваясь, инсулиному, гастриному, глюкагоному, випому, соматостатин-секретирующую опухоль и карциноидную опухоль или опухоль островковых клеток; (16) гипофизарный рак, включая, но ограничиваясь, болезнь Кушинга, секретирующую пролактин опухоль, акромегалию и несахарный диабет; (17) рак глаз, включая, но не ограничиваясь, глазные меланомы, такие как меланома радужной оболочки, хороидальная меланома и меланома ресничного тела и ретинобластома, (18) рак влагалища, включая, но не ограничиваясь, плоскоклеточный рак, аденокарциному и меланому; (19) рак вульвы, включая, но не ограничиваясь, плоскоклеточный рак, меланому, аденокарциному, базальноклеточную карциному, саркому и болезнь Педжета, (20) рак шейки матки, включая, но не ограничиваясь, плоскоклеточный рак и аденокарциному, (21) рак матки, включая, но не ограничиваясь, эндометриальный рак и саркому матки; (22) рак яичников, включая, но не ограничиваясь, яичниковый эпителиальный рак, пограничную опухоль, опухоль половых клеток и стромальную опухоль, (23) рак пищевода, включая, но не ограничиваясь, плоскоклеточный рак, аденокарциному, аденокистозный рак, слизеобразующий плоскоклеточный рак, железисто-плоскоклеточный рак, саркому, меланому, плазмоцитому, бородавчатый рак и рак овсяновидных клеток (мелкоклеточный), (24) рак желудка, включая, но не ограничиваясь, аденокарциному, образование язв (полиповидных) с неприятным запахом, поверхностное распространение, диффузное распространение, злокачественную лимфому, липосаркому, фибросаркому и карциносаркому, (25) рак толстой кишки, (26) рак прямой кишки, (27) рак печени, включая, но не ограничиваясь, гепатоцеллюлярный рак и гепатобластому, (28) рак желчного пузыря, включая, но не ограничиваясь, аденокарциному, (29) холангиокарциномы, включая, но не ограничиваясь, паппиллярную, узловую и диффузную, (30) рак легких, включая, но не ограничиваясь, немелкоклеточный рак легкого, плоскоклеточный рак (эпидермоидный рак), аденокарциному, крупноклеточный рак и мелкоклеточный рак легкого, (31) рак яичка, включая, но не ограничиваясь, зародышевые опухоли, семиному, анапластическую классический (типичный), сперматоцитный, несеминому, эмбриональный рак, тератомный рак и хориокарциному (опухоль желточного мешка), (32) рак простаты, включая, но не ограничиваясь, аденокарциному, лейомиосаркому и рабдомиосаркому; (33) рак полового члена, (34) рак ротовой полости, включая, но не ограничиваясь, плоскоклеточный рак, (35) базальный рак, (36) рак слюнной железы, включая, но не ограничиваясь, аденокарциному, слизеобразующий плоскоклеточный раки и аденокистозный рак; (37) рак глотки, включая, но не ограничиваясь, бородавчатый и плоскоклеточный рак, (38) рак кожи, включая, но не ограничиваясь, базальноклеточный рак, плоскоклеточный рак и меланому, поверхностно распространяющуюся меланому, узловую меланому, меланому типа злокачественного лентиго и акральную лентигинозную меланому, (39) рак почки, включая, но не ограничиваясь, почечно-клеточный рак, аденокарциному, гипернефрому, фибросаркому и переходно-клеточный рак (почечной лоханки и/или матки), (40) опухоль Вильмса, (41) рак мочевого пузыря, включая, но не ограничиваясь, переходно-клеточный рак, плоскоклеточный рак, аденокарциному и карциносаркому и другой рак, включая, но не ограничиваясь, миксосаркому, остеогенную саркому, эндотелиосаркому, лимфангио-эндотелиосаркому, мезотелиому, синовиому, гемангиобластому, эпителиальную карциному, цистаденокарциному, бронхогенную карциному, рак потовых желез, рак сальных желез, папиллярный рак и папиллярные аденокарциномы (смотрите Fishman et al., 1985, Medicine, 2d Ed., J.B. Lippincott Co., Philadelphia and Murphy et al., 1997, Informed Decisions: The Complete Book of Cancer Diagnosis, Treatment, and Recovery, Viking Penguin, Penguin Books U.S.A., Inc., United States of America).
В зависимости от расстройства, заболевания или состояния, которое лечат, и состояния субъекта, соединения или фармацевтические композиции, относящиеся к настоящему изобретению, можно вводить пероральным, парентеральным (например, внутримышечным, внутрибрюшинным, внутривенным или интрацеребральным введением, интрацестимальной инъекцией или инфузией, подкожной инъекцией или имплантатом), ингаляцией, назальным, вагинальным, ректальным, сублингвальным или местным (например, чрескожным или локальным) путем введения, и их можно формулировать отдельно или вместе в виде подходящей лекарственной формы с фармацевтически приемлемыми вспомогательными веществами, носителями, адъювантами и средами, подходящими для каждого пути введения. Настоящее изобретение также относится к введению соединений или фармацевтических композиций, относящихся к настоящему изобретению, в виде депо состава, в котором активный ингредиент высвобождается в течение предварительно определенного периода времени.
При лечении, предотвращении или облегчении одного или более симптомов расстройств, заболеваний или состояний, описанных в настоящем изобретении, подходящая величина дозы находится в диапазоне от приблизительно 0,001 до 100 мг на кг веса тела субъекта в день (мг/кг в день), от приблизительно 0,01 до приблизительно 75 мг/кг в день, от приблизительно 0,1 до приблизительно 50 мг/кг в день, от приблизительно 0,5 до приблизительно 25 мг/кг в день или от приблизительно 1 до приблизительно 20 мг/кг в день, которые можно вводить в виде одной или нескольких доз. В пределах данных диапазонов доза может находиться в диапазоне от приблизительно 0,005 до приблизительно 0,05, от приблизительно 0,05 до приблизительно 0,5, от приблизительно 0,5 до приблизительно 5,0, от приблизительно 1 до приблизительно 15, от приблизительно 1 до приблизительно 20 или от приблизительно 1 до приблизительно 50 мг/кг в день.
Для перорального введения фармацевтические композиции, относящиеся к настоящему изобретению, можно формулировать в виде таблеток, содержащих от приблизительно 1,0 до приблизительно 1,000 мг активного ингредиента, в одном варианте осуществления приблизительно 1, приблизительно 5, приблизительно 10, приблизительно 15, приблизительно 20, приблизительно 25, приблизительно 50, приблизительно 75, приблизительно 100, приблизительно 150, приблизительно 200, приблизительно 250, приблизительно 300, приблизительно 400, приблизительно 500, приблизительно 600, приблизительно 750, приблизительно 800, приблизительно 900 и приблизительно 1000 мг активного ингредиента для симптоматического регулирования дозы пациенту, подвергаемому лечению. Фармацевтические композиции можно вводить согласно режиму 1-4 раз в день, включая один, два, три раза и четыре раза в день.
Однако ясно, что конкретная величина дозы и частота дозирования для конкретного пациента может изменяться и будет зависить от ряда факторов, включая активность конкретного применяемого соединения, метаболическую стабильность и продолжительность действия конкретного соединения, возраст, вес тела, общее состояние здоровья, пол, рацион, способ и время введения, скорость выведения, комбинацию лекарственных средств, тяжесть конкретного заболевания и терапию, которой подвергается пациент.
Настоящее изобретение также относится к способу регулирования PI3K активности, включающему контакт PIK3 фермента с соединением, относящимся к настоящему изобретению, например, соединением формулы I или его энантиомером, смесью энантиомеров, смесью двух или более диастереомеров или изотопным вариантом; или их фармацевтически приемлемой солью, сольватом, гидратом или пролекарством. В одном варианте осуществления PIK3 фермент находится внутри клетки.
В определенных вариантах осуществления PI3K представляет собой PI3K дикого типа. В определенных вариантах осуществления PI3K представляет собой PI3K вариант.
В определенных вариантах осуществления PI3K представляет собой киназу I класса. В определенных вариантах осуществления PI3K представляет собой PI3Kα, PI3Kβ, PI3Kδ или PI3Kγ. В определенных вариантах осуществления PI3K представляет собой p110α, p110β, p110δ или p110γ. В определенных вариантах осуществления PI3K представляет собой дикий тип киназы I класса. В определенных вариантах осуществления PI3K представляет собой вариант киназы I класса.
В определенных вариантах осуществления PI3K представляет собой p110α. В определенных вариантах осуществления PI3K представляет собой дикий тип p110α. В определенных вариантах осуществления PI3K представляет собой p110α мутант. В определенных вариантах осуществления p110α мутант представляет собой R38H, G106V, K111N, K227E, N345K, C420R, P539R, E542K, E545A, E545G, E545K, Q546K, Q546P, E453Q, H710P, I800L, T1025S, M1043I, M1043V, H1047L, H1047R или H1047Y. В определенных вариантах осуществления p110α мутант представляет собой R38H, K111N, N345K, C420R, P539R, E542K, E545A, E545G, E545K, Q546K, Q546P, I800L, T1025S, M1043I, H1047L, H1047R или H1047Y. В определенных вариантах осуществления p110α мутант представляет собой C420R, E542K, E545A, E545K, Q546K, I800L, M1043I, H1047L или H1047Y.
В определенных вариантах осуществления PI3K представляет собой PI3Kγ. В определенных вариантах осуществления PI3K представляет собой дикий тип PI3Kγ. В определенных вариантах осуществления PI3K представляет собой вариант PI3Kγ.
В определенных вариантах осуществления соединение, относящееся к настоящему изобретению, селективно направлено на PI3Kγ. В определенных вариантах осуществления соединение, относящееся к настоящему изобретению, селективно направлено на дикий тип PI3Kγ. В определенных вариантах осуществления соединение, относящееся к настоящему изобретению, селективно направлено на вариант PI3Kγ.
В определенных вариантах осуществления PI3K представляет собой киназу IV класса. В определенных вариантах осуществления PI3K представляет собой дикий тип киназы IV класса. В определенных вариантах осуществления PI3K представляет собой вариант киназы IV класса. В определенных вариантах осуществления PI3K представляет собой mTOR, ATM, ATR или DNA-PK. В определенных вариантах осуществления PI3K представляет собой mTOR.
В определенных вариантах осуществления соединение, относящееся к настоящему изобретению, например, соединение формулы I или его энантиомер, смесь энантиомеров, смесь двух или более диастереомеров или изотопный вариант; или их фармацевтически приемлемая соль, сольват, гидрат или пролекарство; проявляет ингибирующую активность относительно PI3K и его варианта.
В определенных вариантах осуществления соединение, относящееся к настоящему изобретению, например, соединением формулы I или его энантиомер, смесь энантиомеров, смесь двух или более диастереомеров или изотопный вариант; или их фармацевтически приемлемая соль, сольват, гидрат или пролекарство; проявляет ингибирующую активность относительно дикого типа PI3K. В определенных вариантах осуществления PI3K представляет собой PI3Kγ.
В определенных вариантах осуществления соединение, относящееся к настоящему изобретению, например, соединение формулы I или его энантиомер, смесь энантиомеров, смесь двух или более диастереомеров или изотопный вариант; или их фармацевтически приемлемая соль, сольват, гидрат или пролекарство проявляет ингибирующую активность относительно PI3K варианта. В определенных вариантах осуществления PI3K вариант представляет собой p110α мутант. В определенных вариантах осуществления p110α мутант представляет собой C420R, E542K, E545A, E545K, Q546K, I800L, M1043I, H1047L или H1047Y.
Соединение, относящееся к настоящему изобретению, например, соединение формулы I или его энантиомер, смесь энантиомеров, смесь двух или более диастереомеров или изотопный вариант; или их фармацевтически приемлемую соль, сольват, гидрат или пролекарство; можно также комбинировать или применять в комбинации с другими агентами или терапиями, пригодными для лечения, предотвращения или облегчения одного или более симптомов расстройств, заболеваний или состояний, для которых соединения, относящиеся к настоящему изобретению, являются пригодными, включая астму, аллергический ринит, экзему, псориаз, атопический дерматит, лихорадку, сепсис, системную красную волчанку, сахарный диабет, ревматоидный артрит, рассеянный склероз, атеросклероз, отторжение трансплантата, воспалительную болезнь кишечника, рак, инфекционные заболевания, патологии, которые приведены в настоящем изобретении.
Подходящие другие терапевтические агенты также могут включать, но не ограничиваются, (1) альфа-адренергические агенты; (2) противоаритмические агенты; (3) антиатеросклеротические агенты, такие как ACAT ингибиторы; (4) антибиотики, такие как антрациклины, блеомицины, митомицины, дактиномицин и пликамицин; (5) противораковые агенты и цитотоксические агенты, например, алкилирующие агенты, такие как азотистые иприты, алкилсульфонаты, нитрозомочевины, этиленимины и триазины; (6) антикоагулянты, такие как аценокумарол, аргатробан, бивалирудин, лепирудин, фондапаринукс, гепарин, фениндион, варфарин и ксимелагатран, (7) противодиабетические агенты, таких как бигуаниды (например, метформин), ингибиторы глюкозидазы (например, акарбоза), инсулины, меглитиниды (например, репаглинид), сульфонилмочевины (например, глимепирид, глибенкламид и глипизид), тиозолидиндионы (например, троглитазон, розиглитазон и пиоглитазон) и PPAR-гамма-агонисты, (8) противогрибковые агенты, такие как аморолфин, амфотерицин В, анидулафунгин, бифоназол, бутенафин, бутоконазол, каспофунгин, циклопирокс, клотримазол, эконазол, фентиконазол, филипин, флуконазол, изоконазол, итраконазол, кетоконазол, микафунгин, миконазол, нафтифин, натамицин, нистатин, оксиконазол, равуконазол, позаконазол, римоцидин, сертаконазол, сулконазол, тербинафин, терконазол, тиоконазол и вориконазол, (9) противовоспалительные агенты, например, нестероидные противовоспалительные агенты, такие как ацеклофенак, ацеметацин, амоксиприн, аспирин, азапропазон, бенорилат, бромфенак, карпрофен, целекоксиб, холинсалицилат магния, диклофенак, дифлунизал, этодолак, эторикоксиб, фаизламин, фенбуфен, фенопрофен, флурбипрофен, ибупрофен, индометацин, кетопрофен, кеторолак, лорноксикам, локсопрофен, лумиракоксиб, меклофенамовая кислота, мефенамовая кислота, мелоксикам, метамизол, метилсалицилат, салицилат магния, набуметон, напроксен, нимесулид, оксифенбутазон, парекоксиб фенилбутазон, пироксикам, салициловый эфир салициловой кислоты, сулиндак, сульфинпиразон, супрофен, теноксикам, тиапрофеновая кислота и толметин, (10) антиметаболиты, такие как антагонисты фолата, пуриновые аналоги и пиримидиновые аналоги, (11) антитромбоцитарные агенты, такие как GPIIb/IIIa-блокаторы (например, абциксимаб, эптифибатид и тирофибан), P2Y(AC) антагонисты (например, клопидогрел, тиклопидин и CS-747), цилостазол, дипиридамол и аспирин, (12) антипролиферативные агенты, такие как метотрексат, FK506 (такролимус) и мофетилмикофенолят; (13) анти-TNF антитела или растворимый TNF рецептор, такие как этанерцепт, рапамицин и лефлунимид; (14) аР2 ингибиторы, (15) бета-адренергические агенты, такие как карведилол и метопролол; (16) секвестранты желчных кислот, такие как квестран, (17) блокаторы кальциевых каналов, такие как амлодипинбезилат, (18) химиотерапевтические агенты; (19) ингибитор циклооксигеназы-2 (СОХ-2), такой как целекоксиб и рофекоксиб, (20) циклоспорины; (21) цитостатики, такие как азатиоприн и циклофосфамид; (22) диуретики, такие как хлортиазид, гидрохлортиазид, флюметиазид, гидрофлуметиазид, бендрофлуметиазид, метилхлортиазид, трихлорметиазид, политиазид, бензотиазид, этакриновая кислота, тикринафен, хлорталидон, фуросенид, музолимин, буметанид, триамтерен, амилорид и спиронолактон, (23) ингибиторы конвертирующего эндотелин фермента (ЕСЕ), такие как фосфорамидон; (24) ферменты, такие как L-аспарагиназа, (25) ингибиторы фактора VIIa и ингибиторы фактора Ха, (26) ингибиторы фарнезилпротеинтрансферазы, (27) фибраты, (28) ингибиторы факторов роста, такие как модуляторы активности PDGF, (29) стимуляторы секреции гормона роста; (30) ингибиторы HMG-CoA-редуктазы, такие как правастатин, ловастатин, аторвастатин, симвастатин, NK-104 (также известный как итавастатин, нисвастатин или нисбастатин) и ZD-4522 (также известный как розувастатин, атавастатин или визастатин), ингибиторы нейтральной эндопептидазы (NEP); (31) гормональные препараты, такие как глюкокортикоиды (например, кортизон), эстрогены/антиэстрогены, андрогены/антиандрогены, прогестины и антагонисты гормона, высвобождающего лютеинизирующий гормон, и октреотидацетат, (32) иммунодепрессанты; (33) антагонисты рецепторов минералокортикоидов, такие как спиронолактон и эплеренон; (34) агенты, разрушающие микротрубочки, такие как эктеинасцидин, (35) агенты, стабилизирующие микротрубочки, такие как паклитаксел, доцетаксел и эпотилоны A-F, (36) МТР ингибиторы, (37) никотиновая кислота, (38) ингибиторы фосфодиэстеразы, такие как PDE III ингибиторы (например, цилостазол) и PDE V ингибиторы (например, силденафил, тадалафил и варденафил), (39) растительные продукты, такие как алкалоиды барвинка, эпиподофиллотоксины и таксаны, (40) антагонисты фактора активации тромбоцитов (PAF) (41) координационные комплексы платины, такие как цисплатина, сартаплатина и карбоплатина; (42) агенты, открывающие калиевые каналы, (43) ингибиторы пренилпротеинтрансферазы, (44) ингибиторы протеинтирозинкиназы, (45) ингибиторы ренина, (46) ингибиторы скваленсинтетазы, (47) стероиды, таких как альдостерон, беклометазон, бетаметазон, дезоксикортикостеронацетат, флудрокортизон, гидрокортизон (кортизол), преднизолон, преднизон, метилпреднизолон, дексаметазон и триамцинолон; (48) TNF-альфа ингибиторы, такие как тенидап, (49) ингибиторы тромбина, такие как гирудин, (50) тромболитические агенты, такие как анистреплаз, ретеплаз, тенектеплаз, активатор тканевого плазминогена (tPA), рекомбинантный tPA, стрептокиназа, урокиназа, проурокиназа и анизоилированный активатор комплекса стрептокиназы и плазминогена (APSAC), (51) антагонисты тромбоксанового рецептора, такие как ифетробан, (52) ингибиторы топоизомеразы, (53) ингибиторы вазопептидазы (двойной NEP-ACE ингибиторы), такие как омапатрилат и гемопатрилат и (54) другие различные агенты, такие как гидроксимочевина, прокарбазин, митотан, гексаметилмеламин и соединения золота.
В определенных вариантах осуществления другие терапии, которые можно применять в комбинации с соединениями, относящимися к настоящему изобретению, включают, но не ограничиваются, хирургическую операцию, эндокринную терапию, модификаторы биологического ответа (например, интерфероны, интерлейкины и фактор некроза опухоли (TNF)), гипертермию и криотерапию и агенты, подавляющие любые побочные эффекты (например, противорвотные средства).
В определенных вариантах осуществления другие терапевтические агенты, которые можно применять в комбинации с соединениями, относящимися к настоящему изобретению, включают, но не ограничиваются, алкилирующие лекарственные средства (меклоретамин, хлорамбуцил, циклофосфамид, мелфалан и ифосфамид), антиметаболиты (цитарабин (также известный как цитозинарабинозид или Ara-C), HDAC (высокая доза цитарабина) и метотрексат), пуриновые антагонисты и пиримидиновые антагонисты (6-меркаптопурин, 5-фторурацил, цитабин и гемцитабин), веретенные яды (винблатсин, винкристин и винорелбин), подофиллотоксины (этопозид, иринотекан и топотекан), антибиотики (даунорубицин, доксорубицин, блеомицин и митомицин), нитрозомочевины (кармустин и ломустин), ферменты (аспарагиназа) и гормоны (тамоксифен, лейпролид, флутамид и мегестрол), иматиниб, адриамицин, дексаметазон и циклофосфамид. Что касается более подробного обсуждения современных раковых терапий, смотрите http://www.nci.nih.gov/, список FDA одобренных противоопухолевых лекарственных средств по http://www.fda.gov/cder/cancer/druglistframe.htm и The Merck Manual, Seventeenth Ed. 1999, полное содержание которых включено в настоящее изобретение с помощью ссылки.
В другом варианте осуществления способ, относящийся к настоящему изобретению, включает введение соединения, относящегося к настоящему изобретению, например, соединения формулы I или его энантиомера, смеси энантиомеров, смеси двух или более диастереомеров или изотопного варианта, или их фармацевтически приемлемой соли, сольвата, гидрата или пролекарства, вместе с введением одного или более химиотерапевтических агентов и/или осуществлением терапий, выбранных из: алкилирующих агентов (например, цисплатины, карбоплатины); антиметаболитов (например, метотрексата и 5-FU); противоопухолевых антибиотиков (например, адриамицина и блеомицина); противоопухолевых растительных алкалоидов (например, таксола и этопозида); противоопухолевых гормонов (например, дексаметазона и тамоксифена); противоопухолевых иммунологических агентов (например, интерферона α, β и γ); радиационной терапии и хирургической операции. В определенных вариантах осуществления один или более химиотерапевтических агентов и/или терапий вводят субъекту перед, в течение или после введения соединения, относящегося к настоящему изобретению.
Данные другие агенты или лекарственные средства можно вводить путем и в количестве, обычно применяемых для этой цели, одновременно или последовательно с соединением, относящимся к настоящему изобретению, например, соединением формулы I или его энантиомером, смесью энантиомеров, смесью двух или более диастереомеров или изотопным вариантом; или их фармацевтически приемлемой солью, сольватом, гидратом или пролекарствов. Когда соединение, относящееся к настоящему изобретению, применяют одновременно с одним или более другими лекарственными средствами, можно применять фармацевтическую композицию, содержащую данные другие лекарственные средства в добавление к соединению, относящемуся к настоящему изобретению, но это необязательно. Соответственно, фармацевтические композиции, относящиеся к настоящему изобретению, включают фармацевтические композиции, которые также содержат один или более других активных ингредиентов или терапевтических агентов в добавление к соединению, относящемуся к настоящему изобретению.
Весовое отношение соединения, относящегося к настоящему изобретению, ко второму активному ингредиенту может изменяться и будет зависеть от эффективной дозы каждого ингредиента. Обычно будут применять эффективную дозу каждого ингредиента. Таким образом, например, когда соединение, относящееся к настоящему изобретению, комбинируют с NSAID, весовое отношение соединения к NSAID может быть в диапазоне от приблизительно 1000:1 до приблизительно 1:1000 или от приблизительно 200:1 до приблизительно 1:200. Комбинации соединения, относящегося к настоящему изобретению, и других активных ингредиентов будут обычно в пределах приведенного выше диапазона, но в каждом случае следует применять эффективную дозу каждого активного ингредиента.
Соединения, относящиеся к настоящему изобретению, можно также предоставлять в виде готового изделия, применяя упаковочные материалы, хорошо известные специалисту в данной области техники. Смотрите, например, патенты США №№ 5323907, 5052558 и 5033252. Примеры фармацевтических упаковочных материалов включают, но не ограничиваются, блистерные упаковки, бутылки, тубы, ингаляторы, насосы, пакеты, ампулы, контейнеры, шприцы и любой упаковочный материал, пригодный для выбранного состава и предполагаемого пути введения и способа лечения.
Также к настоящему изобретению относятся наборы, которые, при применении практикующим врачом, могут облегчать введение подходящих количеств активных ингредиентов субъекту. В определенных вариантах осуществления набор, относящийся к настоящему изобретению, включает контейнер и лекарственную форму соединения, относящегося к настоящему изобретению, например, соединения формулы I или его энантиомера, смеси энантиомеров, смеси двух или более диастереомеров или изотопного варианта; или их фармацевтически приемлемой соли, сольвата, гидрата или пролекарства.
В определенных вариантах осуществления набор включает контейнер, содержащий лекарственную форму соединения, относящегося к настоящему изобретению, например, соединения формулы I или его энантиомера, смеси энантиомеров, смеси двух или более диастереомеров или изотопного варианта; или их фармацевтически приемлемой соли, сольвата, гидрата или пролекарства; причем контейнер содержит один или более других терапевтических агентов, описанных в настоящем изобретении.
Наборы, относящиеся к настоящему изобретению, могут дополнительно содержать устройства, которые применяют для введения активных ингредиентов. Примеры данных устройств включают, но не ограничиваются, шприцы, безигольные инъекции, капельницы, пластыри и ингаляторы. Наборы, относящиеся к настоящему изобретению, могут также содержать кондомы для введения активных ингредиентов.
Наборы, относящиеся к настоящему изобретению, могут дополнительно содержать фармацевтически приемлемые среды, которые можно применять для введения одного или более активных ингредиентов. Например, если активный ингредиент предоставляют в твердой форме, то его нужно растворить для парентерального введения, и набор может содержать герметично закрытый контейнер с подходящей средой, в которой можно растворить активный ингредиент, получая стерильный раствор, несодержащий частиц, который является пригодным для парентерального введения. Примеры фармацевтически приемлемых сред включают, но не ограничиваются: водные среды, включая, но не ограничиваясь, USP воду для инъекции, раствор хлорида натрия для инъекции, раствор Рингера для инъекции, раствор декстрозы для инъекции, раствор декстрозы и хлорида натрия для инъекции и лактатный раствор Рингера для инъекции; смешиваемые с водой среды, включая, но не ограничиваясь, этиловый спирт, полиэтиленгликоль и полипропиленгликоль; и неводные среды, включая, но не ограничиваясь, кукурузное масло, хлопковое масло, ореховое масло, кунжутное масло, этилолеат, изопропилмиристат и бензилбензоат.
Описание будет более понятно из следующих неограничивающих примеров.
ПРИМЕРЫ
Как применяют в настоящем изобретении, символы и условные обозначения, применяемые в данных способах, на схемах и в примерах, если конкретное сокращение специально не определено, соответствуют символам и условным обозначениям, применяемым в современной научной литературе, например, the Journal of the American Chemical Society или the Journal of Biological Chemistry. Конкретно, но без ограничения, следующие сокращения можно применять в примерах и во всем описании: г (граммы); мг (миллиграммы); мл (миллилитры); мкл (микролитры); М (молярный); мМ (миллимолярный); мкМ (микромолярный); экв. (эквивалент); ммоль (миллимоли); Гц (герцы); МГц (Мегагерцы); ч (час или часы); мин (минуты); и MS (масс-спектрометрия).
Для всех следующих примеров можно применять стандартные способы обработки и очистки, известные специалисту в данной области техники. Если не указано иначе, все температуры выражены в °C (градусы Цельсия). Все реакции проводили при комнатной температуре, если не указано иначе. Предполагается, что синтетические подходы, показанные в настоящем изобретении, являются только примерами применимой химии посредством применения конкретных примеров, и они не определяют объем настоящего изобретения.
Пример 1
Получение 4-(2-(дифторметил)-1H-бензо[d]имидазол-1-ил)-6-морфолино-N-(1-фенилэтил)-1,3,5-триазин-2-амина A1
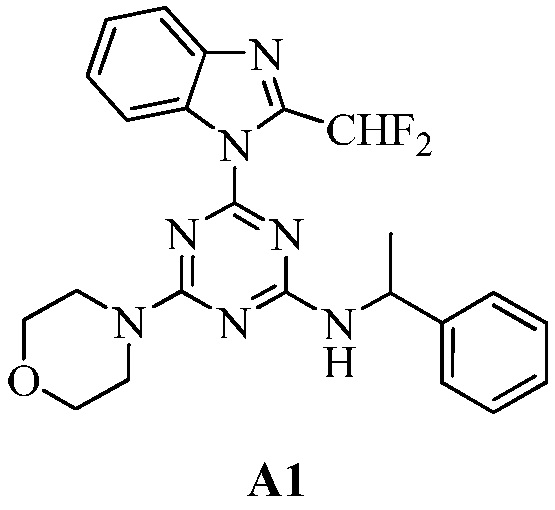
Соединение A1 получали согласно схеме 1, где соединение 1, (1-[4-хлор-6-(4-морфолинил)-1,3,5-триазин-2-ил]-2-(дифторметил)-1H-бензимидазол), получали согласно способу, как описано в опубликованной патентной заявке США № 2007/244110, содержание которой включено в настоящее изобретение с помощью ссылки во всей своей полноте.
Схема 1
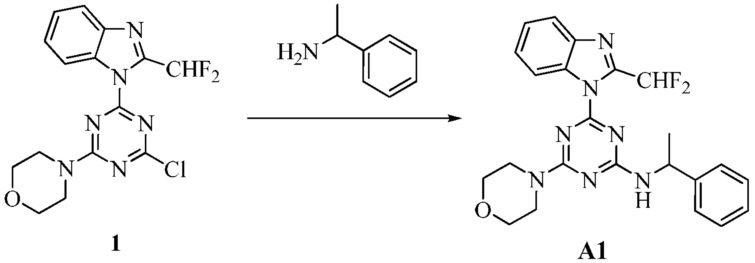
Смесь соединения 1 (184 мг, 0,502 ммоль) и α-метилбензиламина (121 мг, 1,00 ммоль) в диоксане (25 мл) кипятили с обратным холодильником в течение ночи. Смесь выливали в воду, осаждая белый твердый остаток, который перекристаллизовывали из этанола, получая 185 мг (выход 81%) соединения A1 в виде белого твердого остатка: чистота 97,1% (ВЭЖХ); MC m/z: 452,2 (M+1);
1H-ЯМР (CDCl3, 500 МГц) (ротамеры) δ 8,42 (д, J=8,0 Гц, 0,5H), 8,09 (д, J=8,0 Гц, 0,5H), 7,90-7,86 (м, 1H), 7,65 (т, JHF=53,5 Гц, 0,5H), 7,44-7,28 (м, 8H), 5,59 (д, J=6,5 Гц, 0,5H), 5,19-5,06 (м, 1H), 3,76-3,91 (м, 8H), 1,63 (д, J=7,0 Гц, 3H) м.д.
Пример 2
Получение (S)-4-(2-(дифторметил)-1H-бензо[d]имидазол-1-ил)-6-морфолино-N-(1-фенилэтил)-1,3,5-триазин-2-амина A2
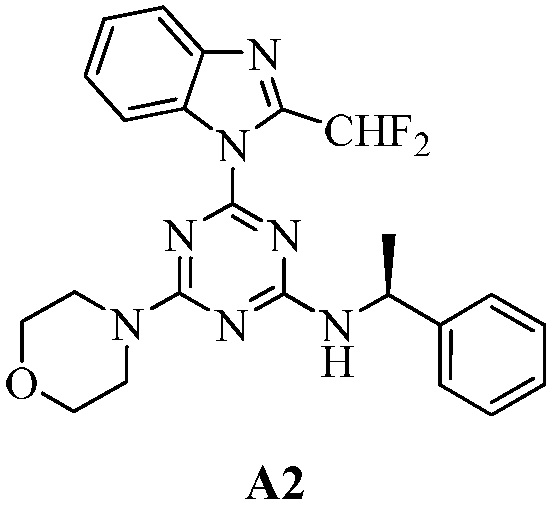
Соединение A2 получали, согласно способу для соединения A1, применяя (S)-α-метилбензиламин вместо α-метилбензиламина, получая продукт с выходом 82%: чистота 90,6% (ВЭЖХ); MC m/z: 452,2 (M+1);
1H-ЯМР (CDCl3, 500 МГц) (ротамеры) δ 8,42 (д, J=8,0 Гц, 0,5H), 8,09 (д, J=7,5 Гц, 0,5H), 7,91-7,85 (м, 1H), 7,65 (т, JHF=54,0 Гц, 0,5H), 7,41-7,22 (м, 8H), 5,61-5,57 (м, 0,5H), 5,25-5,17 (м, 1H), 3,87-3,66 (м, 8H), 1,68-1,61 (м, 3H) м.д.
Пример 3
Получение (R)-4-(2-(дифторметил)-1H-бензо[d]имидазол-1-ил)-6-морфолино-N-(1-фенилэтил)-1,3,5-триазин-2-амина A3
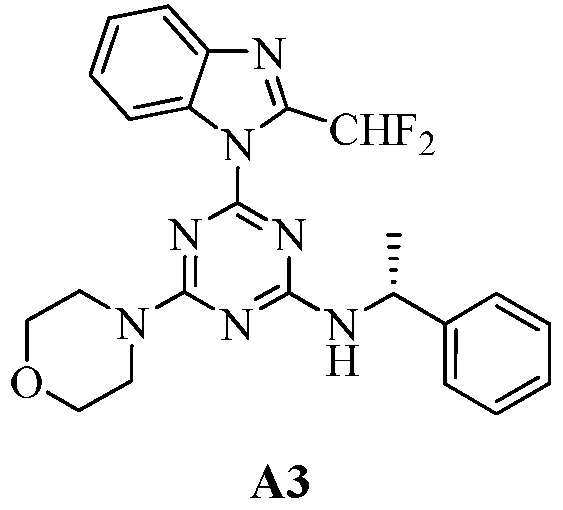
Соединение A3 получали, согласно способу для соединения A1, применяя (R)-α-метилбензиламин вместо α-метилбензиламина, получая выход продукта 68%: чистота 98,7% (ВЭЖХ); MC m/z: 452 (M+1);
1H-ЯМР (CDCl3, 500 МГц) (ротамеры) δ 8,41 (д, J=8,0 Гц, 0,5H), 8,08 (д, J=8,0 Гц, 0,5H), 7,86 (м, 1H), 7,64 (т, JHF=54,0 Гц, 0,5H), 7,44-7,19 (м, 7,5H), 5,58 (д, J=7,5 Гц, 0,5H), 5,20 (м, 1H), 3,88-3,65 (м, 8H), 1,62 (д, J=7,0 Гц, 3H) м.д.
Пример 4
Получение (S)-4-(2-(дифторметил)-1H-бензо[d]имидазол-1-ил)-6-морфолино-N-(1-фенилпропил)-1,3,5-триазин-2-амина A5
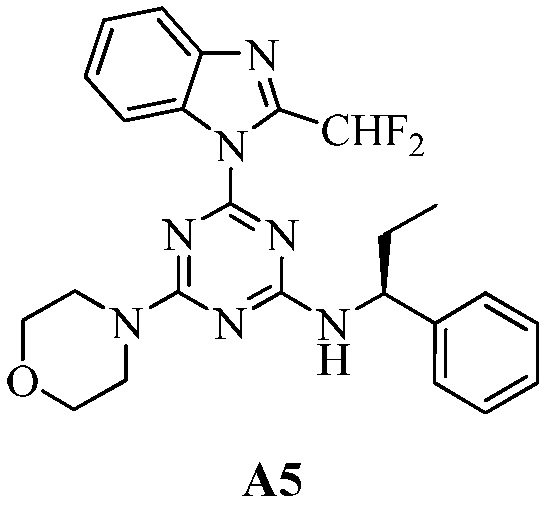
Соединение A5 получали, согласно способу для соединения A1, применяя (S)-α-этилбензиламин вместо α-метилбензиламина, получая продукт с выходом 73%: чистота 96,7% (ВЭЖХ); MC m/z: 466,2 (M+1);
1H-ЯМР (ДМСО-d6, 500 МГц) (ротамеры) δ 8,58 (д, J=8,5 Гц, 0,6H), 8,49 (д, J=8,0 Гц, 0,6H), 8,46 (д, J=8,5 Гц, 0,4H), 8,11 (м, 0,4H), 7,91 (т, JHF=53,0 Гц, 0,6H), 7,85-7,78 (м, 1H), 7,61 (т, JHF=53,0 Гц, 0,4H), 7,49 (т, J=7,5 Гц, 0,5H), 7,45-7,38 (м, 3H), 7,38-7,31 (м, 2H), 7,27-7,20 (м, 1H), 4,90 (м, 1H), 3,88-3,55 (м, 8H), 1,95-1,65 (м, 1H), 0,93 (м, 3H) м.д.
Пример 5
Получение (R)-4-(2-(дифторметил)-1H-бензо[d]имидазол-1-ил)-6-морфолино-N-(1-фенилпропил)-1,3,5-триазин-2-амина A6
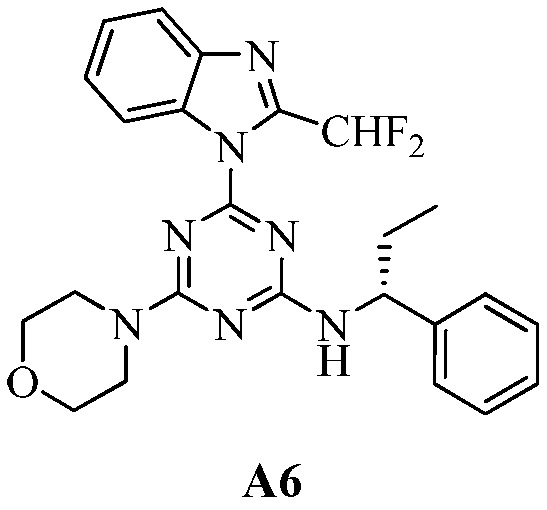
Соединение A6 получали, согласно способу для соединения A1, применяя (R)-α-этилбензиламин вместо α-метилбензиламина, получая выход продукта 62%: чистота 96,2% (ВЭЖХ); MC m/z: 466,2 (M+1);
1H-ЯМР (CDCl3, 500 МГц) (ротамеры) δ 8,41 (д, J=8,0 Гц, 0,4H), 8,11 (д, J=8,0 Гц, 0,6H), 7,89 (д, J=8,0 Гц, 0,4H), 7,86 (д, J=7,5 Гц, 0,6H), 7,65 (т, JHF=53,5 Гц, 0,6H), 7,46-7,25 (м, 7,4H), 5,62 (м, 0,5H), 4,99 (м, 0,5H), 4,92 (м, 0,5H), 3,87-3,65 (м, 8H), 2,02-1,89 (м, 2H), 1,04-0,98 (м, 3H) м.д.
Пример 6
Получение (R)-метил 2-((4-(2-(дифторметил)-1H-бензо[d]имидазол-1-ил)-6-морфолино-1,3,5-триазин-2-ил)амино)-2-фенилацетата A11
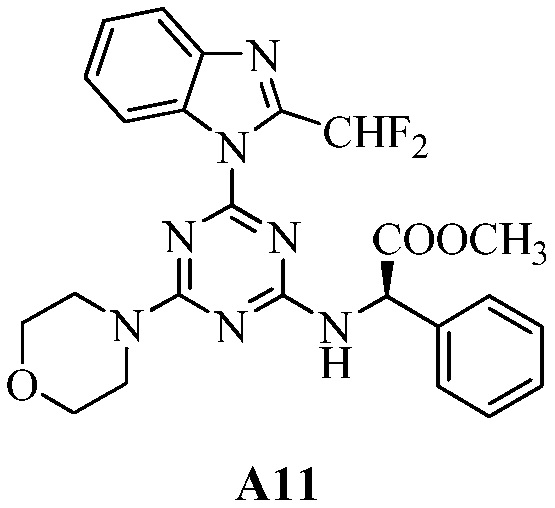
Насыщенный водный бикарбонат натрия добавляли по каплям к раствору гидрохлорида сложного метилового эфира (R)-2-фенилглицина (83 мг, 0,41 ммоль) в воде (4 мл) при 0°C до pH=8. Затем смесь экстрагировали этилацетатом, сушили над безводным сульфатом натрия и концентрировали в вакууме. Остаток добавляли к смеси соединения 1 (50 мг, 0,14 ммоль) в диоксане (5 мл), и полученную в результате смесь кипятили с обратным холодильником в течение 4 часов. После удаления летучих компонентов в вакууме, остаток растворяли в воде и этилацетате. Органические экстракты сушили над безводным сульфатом натрия и концентрировали в вакууме. Сырой продукт очищали колоночной хроматографией на силикагеле (этилацетат/петролейный эфир = 1/5), получая 44 мг (выход 65%) соединения A11 в виде желтого твердого остатка: чистота 98,71% (ЖХМС); MC m/z: 496,1 (M+1);
1H-ЯМР (CDCl3, 500 МГц) (ротамеры) δ 8,43 (д, J=8,0 Гц, 0,5H), 8,11 (д, J=8,0 Гц, 0,5H), 7,88 (м, 1H), 7,64 (т, JHF=53,5 Гц, 0,5H), 7,52-7,35 (м, 7,5H), 6,33 и 6,25 (2д, J=6,5 и 6,0 Гц, 1H), 5,69 и 5,60 (2д, J=6,5 и 6,0 Гц, 1H), 3,89-3,70 (м, 11H) м.д.
Пример 7
Получение (S)-метил 2-((4-(2-(дифторметил)-1H-бензо[d]имидазол-1-ил)-6-морфолино-1,3,5-триазин-2-ил)амино)-2-фенилацетата A12
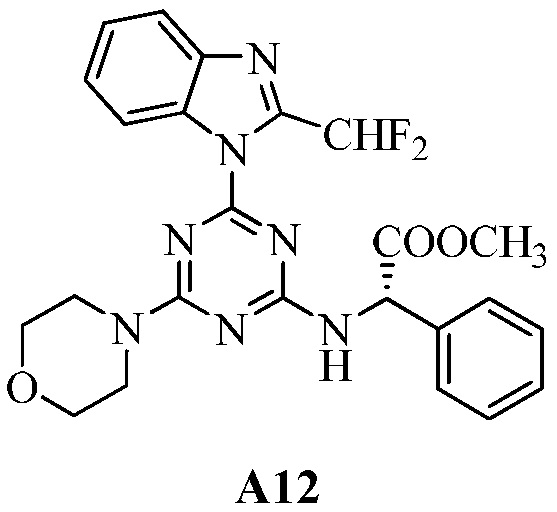
Соединение A12 получали, согласно способу для соединения A11, применяя гидрохлорид сложного метилового эфира (S)-2-фенилглицина вместо гидрохлорида сложного метилового эфира (R)-2-фенилглицина, получая продукт с выходом 67%: чистота 95,5% (ВЭЖХ); MC m/z: 496,1 (M+1);
1H-ЯМР (CDCl3, 500 МГц) (ротамеры) δ 8,45 (д, J=8,5 Гц, 0,5H), 8,13 (д, J=8,0 Гц, 0,5H), 7,89 (м, 1H), 7,64 (т, JHF=53,5 Гц, 0,5H), 7,52-7,36 (м, 7,5H), 6,32 и 6,25 (2д, J=6,0 и 5,5 Гц, 1H), 5,69 и 5,60 (2д, J=6,5 и 6,0 Гц, 1H), 3,89-3,62 (м, 11H) м.д.
Пример 8
Получение 4-(2-(дифторметил)-1H-бензо[d]имидазол-1-ил)-6-морфолино-N-(2-фенилпропан-2-ил)-1,3,5-триазин-2-амина A7
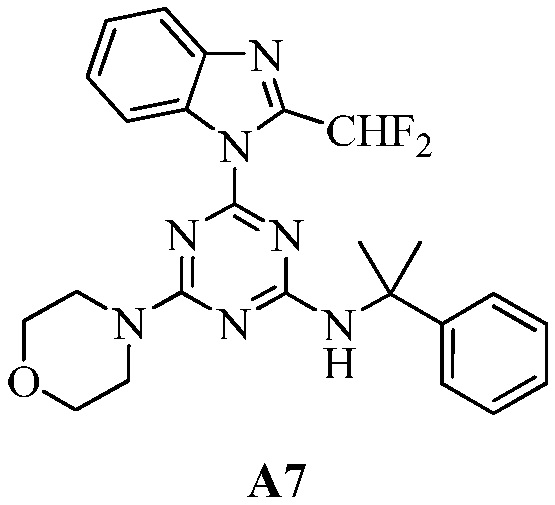
Смесь соединения 1 (184 мг, 0,502 ммоль) и 2-фенилпропан-2-амина (170 мг, 1,26 ммоль) в диоксане (5 мл) кипятили с обратным холодильником в течение ночи. Летучие компоненты удаляли в вакууме, и остаток разделяли между этилацетатом и водой. Органические экстракты промывали последовательно водным гидроксидом натрия (1 н.), водой и соляным раствором, сушили над безводным сульфатом натрия и концентрировали в вакууме. Сырой продукт очищали флэш-хроматографией (10-21% этилацетат в петролейном эфире), получая 148 мг (выход 63%) в виде белого твердого остатка: чистота 99,6% (ВЭЖХ); MC m/z: 466,2 (M+1);
1H-ЯМР (CDCl3, 500 МГц) (ротамеры) δ 8,45 (д, J=8,0 Гц, 0,5H), 7,90 (д, J=7,5 Гц, 0,5H), 7,79 (д, J=8,0 Гц, 0,5H), 7,66 (т, JHF=53,5 Гц, 0,5H), 7,50 (д, J=8,0 Гц, 1H), 7,47-7,38 (м, 3,5H), 7,35-7,26 (м, 2H), 7,22 (т, J=7,5 Гц, 0,5H), 7,13 (т, J=7,5 Гц, 0,5H), 6,82 (т, JHF=53,5 Гц, 0,5H), 5,82 (с, 1H), 3,87 (м, 2H), 3,81 (м, 2H), 3,74 (м, 1H), 3,67 (м, 1H), 3,41 (м, 1H), 3,31 (м, 1H), 1,80 и 1,78 (2с, 6H) м.д.
Пример 9
Получение 4-(2-(дифторметил)-1H-бензо[d]имидазол-1-ил)-6-морфолино-N-(2-(нафталин-2-ил)пропан-2-ил)-1,3,5-триазин-2-амина A13
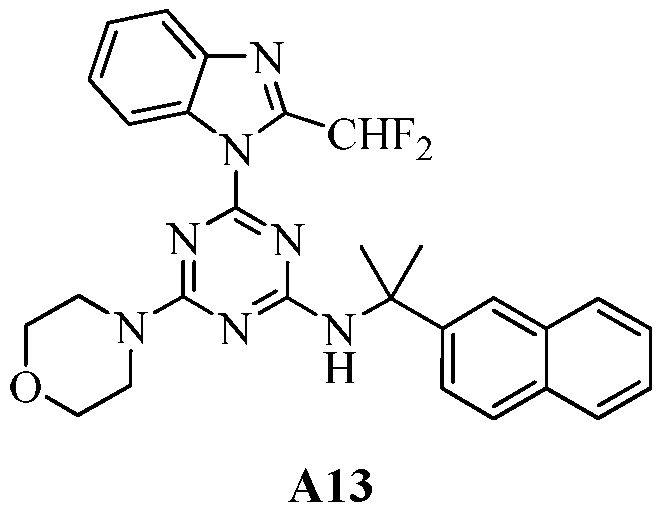
Метилмагнийбромид (3,6 мл, 3,0 M в тетрагидрофуране, 10,5 ммоль) добавляли к раствору нафталин-2-карбонитрила (459 мг, 3,0 ммоль) в безводном тетрагидрофуране (4 мл) при комнатной температуре в атмосфере азота. Реакционную смесь грели в СВЧ-печи при 100°C в течение 10 минут. К полученной в результате смеси добавляли тетраизопропанолят титана (0,9 мл, 3,0 ммоль), и затем облучали микроволновым облучением при 50°C в течение 1 часа. Смесь выливали в воду и экстрагировали дихлорметаном. Объединенные органические экстракты сушили над безводным сульфатом натрия и концентрировали в вакууме, получая неочищенный продукт, который растирали при добавлении по каплям хлористоводородной кислоты в эфире (1 н.), осаждая 2-(нафталин-2-ил)пропан-2-амин в виде его гидрохлоридной соли (600 мг, 90%) в виде желтого твердого остатка: чистота 84,7% (ЖХМС); MC m/z: 171 (M+1).
Неочищенный гидрохлорид 2-(нафталин-2-ил)пропан-2-амина (246 мг, 1,09 ммоль), соединение 1 (200 мг, 0,550 ммоль) и карбонат калия (377 мг, 2,73 ммоль) суспендировали в диоксане (25 мл), и смесь кипятили с обратным холодильником в течение ночи. Смесь разбавляли водой и экстрагировали этилацетатом. Органические экстракты сушили на безводным сульфатом натрия и концентрировали в вакууме. Сырой продукт очищали препаративной-ВЭЖХ, получая 150 мг (выход 53%) соединения A13 в виде белого твердого остатка: чистота 98,5% (ВЭЖХ); MC m/z: 516,2 (M+1);
1H-ЯМР (CDCl3, 500 МГц) (ротамеры) δ 8,43 (д, J=8,0 Гц, 0,6H), 7,98-7,36 (м, 10H), 7,15-6,87 (м, 1H), 6,26 (т, J=8,0 Гц, 0,4H), 5,88 и 5,83 (2с, 1H), 3,87-2,89 (м, 8H), 1,89 и 1,86 (2с, 6H) м.д.
Пример 10
Получение N-(2-(4-хлорфенил)пропан-2-ил)-4-(2-(дифторметил)-1H-бензо[d]имидазол-1-ил)-6-морфолино-1,3,5-триазин-2-амина A8
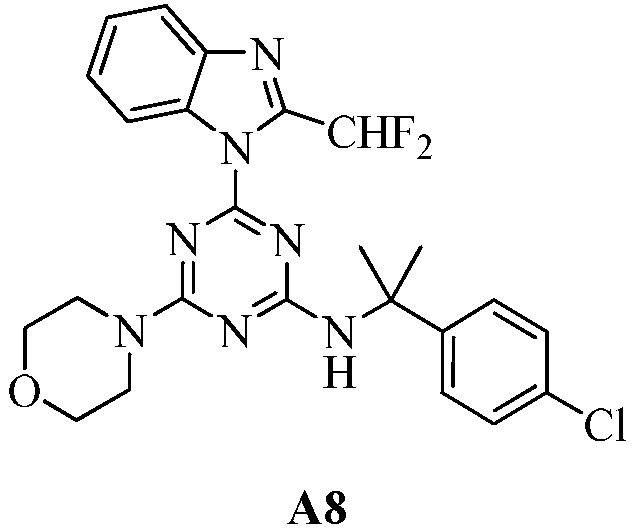
Соединение A8 получали в две стадии, согласно способу для соединения A13, применяя 4-хлорбензонитрил вместо нафталин-2-карбонитрила. Сырой продукт очищали препаративной ВЭЖХ, получая 125 мг (выход для 2 стадий 41%) соединения A8 в виде белого твердого остатка: чистота 99,5% (ВЭЖХ); MC m/z: 500,2 (M+1);
1H-ЯМР (CDCl3, 500 МГц) δ 8,44 (д, J=8,0 Гц, 0,6H), 7,90 (д, J=7,5 Гц, 0,6H), 7,80 (д, J=8,0 Гц, 0,4H), 7,65 (т, JHF=54,0 Гц, 0,6H), 7,49-7,33 (м, 4H), 7,33-7,27 (м, 2H), 7,15-6,87 (м, 0,8H), 5,75 и 5,72 (2с, 1H), 3,86 (м, 2H), 3,81 (м, 2H), 3,76 (м, 1H), 3,69 (м, 1H), 3,46 (м, 1H), 3,30 (м, 1H), 1,79 и 1,76 (2с, 6H) м.д.
Пример 11
Получение 4-(2-(дифторметил)-1H-бензо[d]имидазол-1-ил)-N-(2-(4-метоксифенил)пропан-2-ил)-6-морфолино-1,3,5-триазин-2-амина A9
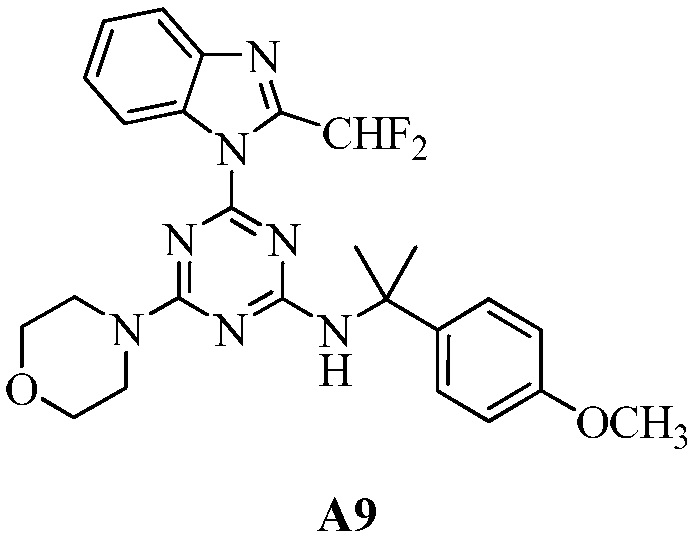
Соединение A9 получали в две стадии, согласно способу для соединения A13, применяя 4-метоксибензонитрил вместо нафталин-2-карбонитрила. Неочищенный соединение A9 очищали препаративной ВЭЖХ, получая 150 мг (выход для 2 стадий 50%) продукта в виде белого твердого остатка: чистота 98,0% (ЖХМС), MC m/z: 496,2 (M+1);
1Н-ЯМР (CDCl3, 500 МГц) δ 8,44 (д, J=8,5 Гц, 0,5H), 7,90 (д, J=8,0 Гц, 0,5H), 7,80 (д, J=8,0 Гц, 0,5H), 7,65 (т, JHF=53,5 Гц, 0,5H), 7,53 (д, J=8,5 Гц, 0,5H), 7,47-7,33 (м, 3H), 7,31 (т, J=7,5 Гц, 0,5H), 7,16 (т, J=7,5 Гц, 0,5H), 6,95 (д, J=9,0 Гц, 1H), 6,85 (д, J=9,0 Гц, 1H), 6,85 (т, JHF=53,0 Гц, 0,5H), 5,77 (д, J=8,5 Гц, 1H), 3,87 (м, 2H), 3,81 (м, 5H), 3,76 (м, 1H), 3,69 (м, 1H), 3,48 (м, 1H), 3,40 (м, 1H), 1,79 и 1,75 (2с, 6H) м.д.
Пример 12
Получение 4-(2-(дифторметил)-1H-бензо[d]имидазол-1-ил)-N-(1-(4-фторфенил)-2-метилпропан-2-ил)-6-морфолино-1,3,5-триазин-2-амина A22
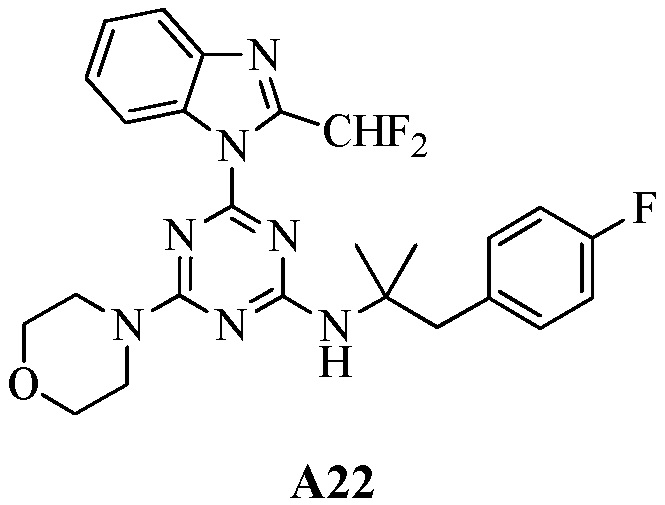
Смесь 1-(4-фторфенил)-2-метилпропан-2-амина (125 мг, 0,748 ммоль) и соединения 1 (183 мг, 0,499 ммоль) в диоксане (15 мл) кипятили с обратным холодильником в течение ночи. Летучие компоненты удаляли в вакууме, и остаток очищали препаративной ВЭЖХ, получая 4-(2-(дифторметил)-1H-бензо[d]имидазол-1-ил)-N-(1-(4-фторфенил)-2-метилпропан-2-ил)-6-морфолино-1,3,5-триазин-2-амин (35 мг, выход 14%) в виде белого твердого остатка: чистота 98,1% (ВЭЖХ); MC m/z: 498,2 (M+1);
1Н-ЯМР (CDCl3, 500 МГц) δ 8,37 (д, J=7,5 Гц, 1H), 7,88 (д, J=7,5 Гц, 1H), 7,63 (т, JHF=54,0 Гц, 1H), 7,41 (м, 2H), 7,04 (т, J=8,0 Гц, 2H), 6,96 (т, J=8,5 Гц, 2H), 5,10 (с, 1H), 4,00-3,72 (м, 8H), 3,18 (с, 2H), 1,45 (с, 6H) м.д.
Пример 13
Получение 4-(2-(дифторметил)-1H-бензо[d]имидазол-1-ил)-N-(2-метил-1-фенилпропан-2-ил)-6-морфолино-1,3,5-триазин-2-амина A14
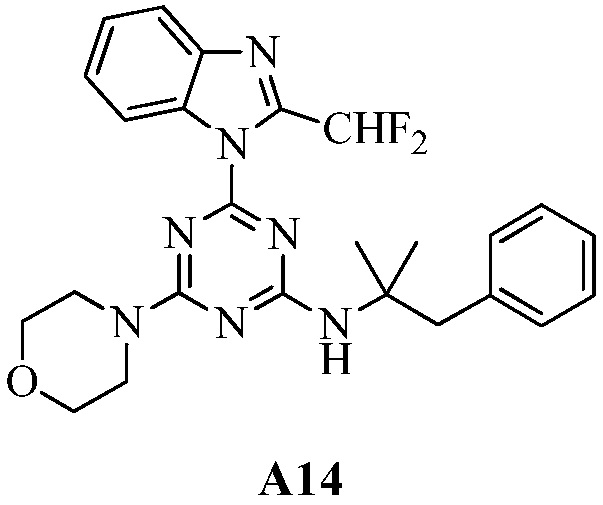
К смеси 2-метил-1-фенил-2-пропанола (1,5 г, 10 ммоль) и ацетонитрила (3 мл) в уксусной кислоте (15 мл) добавляли концентрированную серную кислоту (3 мл) по каплям при комнатной температуре. Смесь перемешивали при 65°C в течение 3 часов и затем выливали в ледяную воду (приблизительно 200 мл). Водный раствор подщелачивали насыщенным водным гидроксидом натрия до pH>11. Суспензию перемешивали в течение следующих 0,5 часа, и затем выпавший осадок фильтровали и промывали водой. Белый твердый остаток сушили на воздухе, получая N-(2-метил-1-фенилпропан-2-ил)ацетамид (1,5 г, выход 78%), который применяли на следующей стадии без дополнительной очистки.
Смесь N-(2-метил-1-фенилпропан-2-ил)ацетамида (191 мг, 1,00 ммоль) и гидроксида калия (1 г) в этиленгликоле (10 мл) кипятили с обратным холодильником в течение 8 часов. Смесь разбавляли ледяной водой и экстрагировали этилацетатом. Объединенные органические фракции промывали водой, сушили над безводным сульфатом натрия и концентрировали в вакууме, получая неочищенный 2-метил-1-фенилпропанамин (200 мг) в виде коричневого масла, которое применяли на следующей стадии без дополнительной очистки.
Соединение A14 получали, согласно способу для соединения A22, применяя неочищенный 2-метил-1-фенилпропанамин вместо 1-(4-фторфенил)-2-метилпропан-2-амина. Продукт очищали препаративной ВЭЖХ, получая соединение A14 (30 мг, выход для 2 стадий 13%) в виде белого твердого остатка: чистота 96,4% (ВЭЖХ); MC m/z: 480,3 (M+1);
1Н-ЯМР (CDCl3, 500 МГц) δ 8,39 (д, J=7,5 Гц, 1H), 7,90 (д, J=7,5 Гц, 1H), 7,65 (т, JHF=54,0 Гц, 1H), 7,42 (м, 2H), 7,28 (м, 3H), 7,16-7,10 (м, 2H), 5,15 (с, 1H), 4,01-3,75 (м, 8H), 3,22 (с, 2H), 1,49 (с, 6H) м.д.
Пример 14
Получение 4-(2-(дифторметил)-1H-бензо[d]имидазол-1-ил)-N-(1-(2-хлорфенил)-2-метилпропан-2-ил)-6-морфолино-1,3,5-триазин-2-амина A16
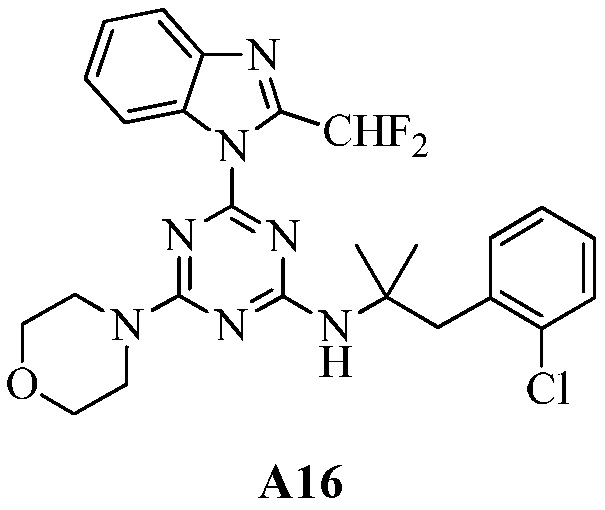
Смесь гидрохлорида 1-(2-хлорфенил)-2-метилпропан-2-амина (165 мг, 0,750 ммоль), соединения 1 (184 мг, 0,502 ммоль) и карбоната калия (138 мг, 1,00 ммоль) в диоксане (15 мл) кипятили с обратным холодильником в течение 12 часов. Летучие компоненты удаляли в вакууме, и остаток очищали обращенно-фазовой флэш-хроматографией (0-80% ацетонитрил в водном 0,5% бикарбонате аммония), получая 4-(2-(дифторметил)-1H-бензо[d]имидазол-1-ил)-N-(1-(2-хлорфенил)-2-метилпропан-2-ил)-6-морфолино-1,3,5-триазин-2-амин (65 мг, выход 25%) в виде белого твердого остатка: чистота 99,2% (ВЭЖХ); MC m/z: 514,2 (M+1);
1Н-ЯМР (CDCl3, 500 МГц) δ 8,41 (д, J=8,0 Гц, 1H), 7,90 (д, J=7,0 Гц, 1H), 7,66 (т, JHF=53,5 Гц, 1H), 7,50-7,36 (м, 3H), 7,24-7,05 (м, 3H), 5,34 (с, 1H), 4,05-3,70 (м, 8H), 3,43 (с, 2H), 1,53 (с, 6H) м.д.
Пример 15
Получение 4-(2-(дифторметил)-1H-бензо[d]имидазол-1-ил)-N-(1-(4-метоксифенил)-2-метилпропан-2-ил)-6-морфолино-1,3,5-триазин-2-амина A25
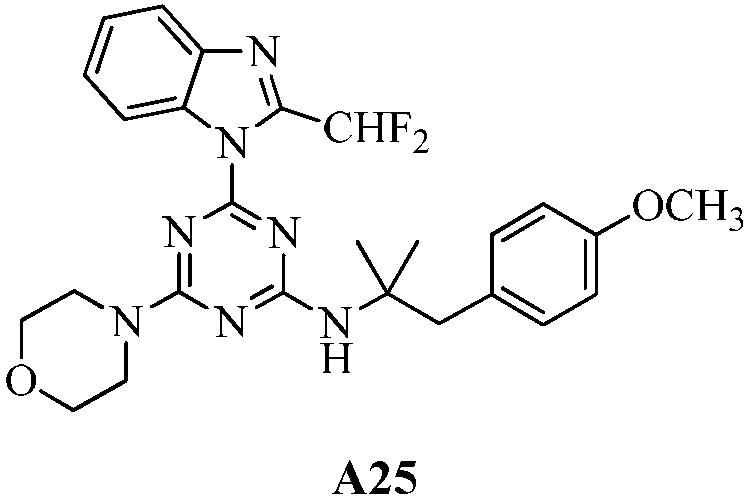
Смесь 4-(гидроксиметил)фенола (1,0 г, 8,1 ммоль) и 2-нитропропана (4,0 г, 45 ммоль) в диглиме (50 мл) охлаждали в бане со льдом. Добавляли порциями трет-бутоксид калия (0,45 г, 4,0 ммоль), затем реакционную смесь кипятили с обратным холодильником в течение ночи. После охлаждения смесь концентрировали, и остаток очищали колоночной хроматографией на силикагеле (петролейный эфир/этилацетат), получая 4-(2-метил-2-нитропропил)фенол (1,3 г, выход 83%) в виде светло-желтого твердого остатка.
Йодметан (0,12 мл, 1,3 ммоль) добавляли к смеси 4-(2-метил-2-нитропропил)фенола (300 мг, 1,5 ммоль) и карбоната калия (425 мг, 3,1 ммоль) в тетрагидрофуране (20 мл) и N,N-диметилформамиде (1 мл). После кипячения с обратным холодильником в течение ночи, смесь охлаждали и концентрировали в вакууме. Остаток растворяли в этилацетате, промывали водой, сушили над безводным сульфатом натрия и концентрировали, получая неочищенный 1-метокси-4-(2-метил-2-нитропропил)бензол (200 мг, выход 62%) в виде желтого масла, которое применяли непосредственно на следующей стадии.
Неочищенный 1-метокси-4-(2-метил-2-нитропропил)бензол (200 мг, 0,96 ммоль) смешивали с палладием на угле (40 мг) в метаноле (30 мл). Суспензию энергично перемешивали при комнатной температуре в атмосфере водорода в течение ночи. Смесь фильтровали через целит, и фильтрат концентрировали, получая 1-(4-метоксифенил)-2-метилпропан-2-амин (150 мг, выход 88%) в виде желтого масла, которое применяли без дополнительной очистки. (MC m/z: 180 (M+1)).
Смесь 1-(4-метоксифенил)-2-метилпропан-2-амина (73 мг, 0,41 ммоль) и соединения 1 (100 мг, 0,27 ммоль) в диоксане (25 мл) кипятили с обратным холодильником в течение ночи. Летучие компоненты удаляли в вакууме, и остаток очищали препаративной ВЭЖХ, получая соединение A25 (40 мг, выход 29%) в виде белого твердого остатка: чистота >99,5% (ВЭЖХ); MC m/z: 510,2 (M+1);
1Н-ЯМР (CDCl3, 500 МГц) δ 8,38 (д, J=8,0 Гц, 1H), 7,89 (д, J=7,5 Гц, 1H), 7,64 (т, JHF=54,0 Гц, 1H), 7,41 (м, 2H), 7,01 (д, J =8,5 Гц, 2H), 6,82 (д, J=8,0 Гц, 2H), 5,10 (с, 1H), 3,93 (м, 3H), 3,83 (м, 5H), 3,77 (с, 3H), 3,13 (с, 2H), 1,45 (s, 6H) м.д.
Пример 16
Получение 4-(2-(дифторметил)-1 H -бензо[ d ]имидазол-1-ил)- N -(1-(2-метоксифенил)-2-метилпропан-2-ил)-6-морфолино-1,3,5-триазин-2-амина A19
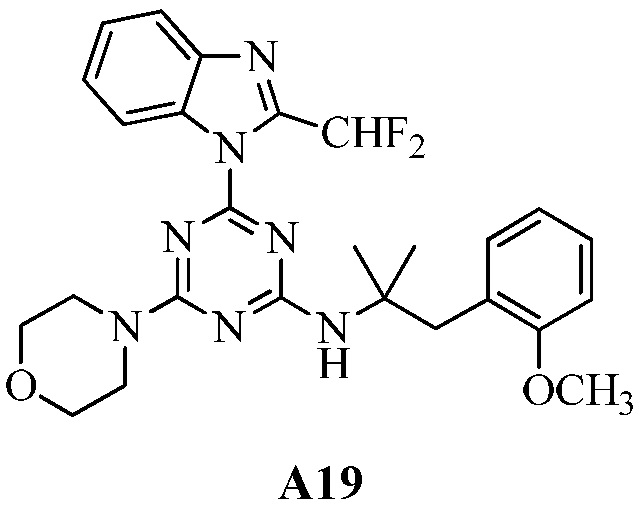
Соединение A19 получали, согласно способу для соединения A16, применяя 1-(2-метоксифенил)-2-метилпропан-2-амин вместо гидрохлорида 1-(2-хлорфенил)-2-метилпропан-2-амина. Продукт очищали обращенно-фазовой флэш-хроматографией (0-80% ацетонитрил в воде), получая соединение A19 (66 мг, выход 81%) в виде белого твердого остатка: чистота >99,5% (ВЭЖХ); MC m/z: 510,2 (M+1);
1Н-ЯМР (CDCl3, 500 МГц) δ 8,42 (дд, J=7,5 Гц и 1,5 Гц, 1H), 7,88 (дд, J=6,5 Гц и 2,5 Гц, 1H), 7,67 (т, JHF=53,5 Гц, 1H), 7,39 (м, 2H), 7,26 (м, 2H), 7,12 (дд, J=7,5 Гц и 1,5 Гц, 1H), 6,95 (м, 2H), 6,68 (с, 1H), 3,97 (с, 3H), 3,93-3,74 (м, 8H), 3,04 (с, 2H), 1,56 (с, 6H) м.д.
Пример 17
Получение N-(1-(4- бром фенил)-2-метилпропан-2-ил)-4-(2-(дифторметил)-1H-бензо[d]имидазол-1-ил)-6-морфолино-1,3,5-триазин-2-амина A24
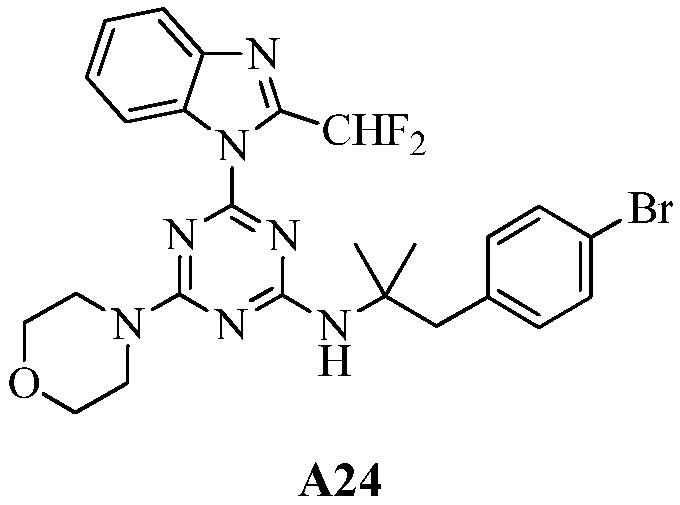
Соединение A24 получали, согласно способу для соединения A16, применяя гидрохлорид 1-(4-бромфенил)-2-метилпропан-2-амина вместо гидрохлорида 1-(2-хлорфенил)-2-метилпропан-2-амина. Продукт очищали обращенно-фазовой флэш-хроматографией (0-80% ацетонитрил в воде), которая давала соединение A24 (110 мг, выход 39%) в виде белого твердого остатка: чистота 98,6% (ВЭЖХ); MC m/z: 558,2 (M+1), 560,2 (M+3);
1Н-ЯМР (CDCl3, 500 МГц) δ 8,38 (д, J=7,5 Гц, 1H), 7,90 (д, J=7,5 Гц, 1H), 7,65 (т, JHF=53,5 Гц, 1H), 7,52-7,38 (м, 4H), 6,97 (д, 2H), 5,07 (с, 1H), 4,00-3,70 (м, 8H), 3,18 (с, 2H), 1,47 (с, 6H) м.д.
Пример 18
Получение 4-(2-(дифторметил)-1H-бензо[d]имидазол-1-ил)-N-(2-метил-1-(o-толил)пропан-2-ил)-6-морфолино-1,3,5-триазин-2-амина A18
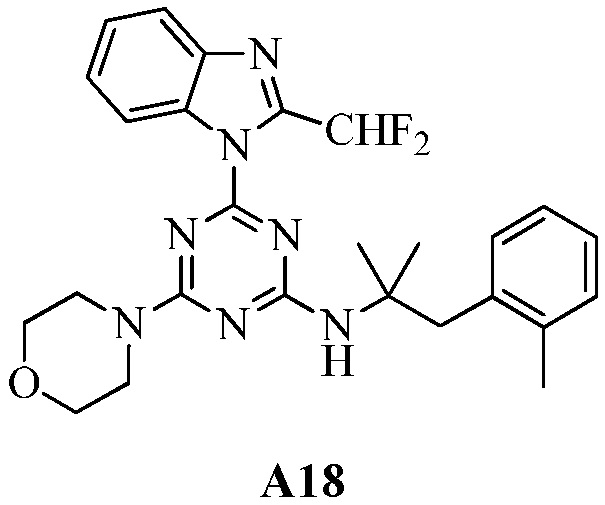
Соединение A18 получали, согласно способу для соединения A16, применяя гидрохлорид 2-метил-1-(o-толил)пропан-2-амина вместо гидрохлорида 1-(2-хлорфенил)-2-метилпропан-2-амина. Продукт очищали колоночной хроматографией на силикагеле (20% этилацетат в петролейном эфире), получая соединение A18 (120 мг, выход 89%) в виде белого твердого остатка: чистота >99,5% (ВЭЖХ); MC m/z: 494,2 (M+1);
1Н-ЯМР (CDCl3, 500 МГц) δ 8,39 (д, J=8,0 Гц, 1H), 7,88 (д, J=7,0 Гц, 1H), 7,64 (т, JHF=53,5, 1H), 7,40 (м, 2H), 7,22-6,98 (м, 4H), 5,24 (с, 1H), 4,00-3,75 (м, 8H), 3,25 (с, 2H), 2,36 (с, 3H), 1,49 (с, 6H) м.д.
Пример 19
Получение N-(1-(4-хлорфенил)-2-метилпропан-2-ил)-4-(2-(дифторметил)-1H-бензо[d]имидазол-1-ил)-6-морфолино-1,3,5-триазин-2-амина A23
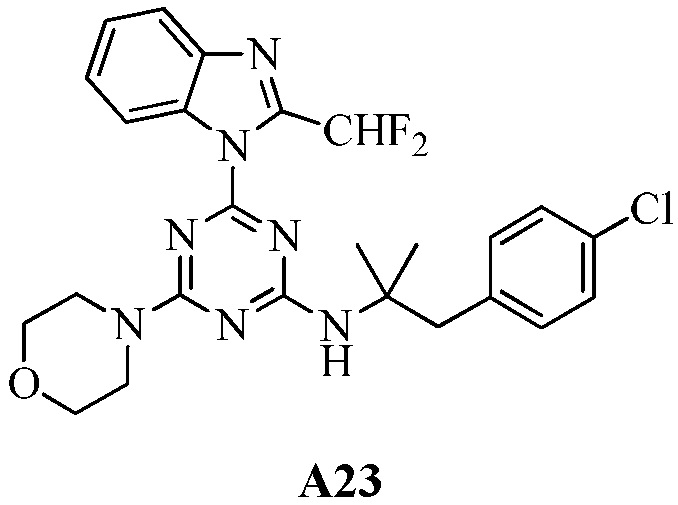
Метилмагнийбромид (3 M в эфире, 5,5 мл, 16,5 ммоль) добавляли по каплям к раствору метил 4-хлорфенилацетата (1,0 г, 5,4 ммоль) в тетрагидрофуране (20 мл) при 0°C в атмосфере азота. Смесь перемешивали при комнатной температуре в течение ночи, и затем гасили добавлением воды (30 мл). Органическую фазу промывали соляным раствором, сушили над сульфатом натрия и концентрировали, получая 1-(4-хлорфенил)-2-метилпропан-2-ол (1,0 г, выход 100%) в виде желтого масла, которое применяли без дополнительной очистки.
Раствор неочищенного спирта (184 мг, 0,996 ммоль) и хлорацетонитрила (150 мг, 1,99 ммоль) в уксусной кислоте (3,0 мл) охлаждали до 0°C. Добавляли к раствору по каплям концентрированную серную кислоту (1,0 мл), поддерживая температуру реакции ниже 10°C. После перемешивания при комнатной температуре в течение 1 часа, полученный в результате раствор выливали на лед и подщелачивали добавлением твердого карбоната калия до pH>8. Смесь экстрагировали этилацетатом, и объединенные органические фракции промывали водой, сушили над сульфатом натрия и концентрировали в вакууме, получая 150 мг 2-хлор-N-(1-(4-хлорфенил)-2-метилпропан-2-ил)ацетамида в виде желтого твердого остатка. Неочищенный материал применяли непосредственно на следующей стадии.
К смеси 2-хлор-N-(1-(4-хлорфенил)-2-метилпропан-2-ил)ацетамида (259 мг, 1,00 ммоль) в диоксане (5,0 мл) добавляли концентрированную хлористоводородную кислоту (20 мл). После перемешивания при 105°C в течение 16 часов, реакционную смесь выливали на лед и подщелачивали добавлением насыщенного водного бикарбоната натрия до pH>8. Смесь экстрагировали этилацетатом, и объединенные органические фракции промывали водой, сушили над сульфатом натрия и концентрировали в вакууме. Затем сырой продукт очищали обращенно-фазовой флэш-хроматографией (0-25% ацетонитрил в водной 0,01% муравьиной кислоте), получая 1-(4-хлорфенил)-2-метилпропан-2-амин (70 мг, выход 38%) в виде белого твердого остатка.
Смесь 1-(4-хлорфенил)-2-метилпропан-2-амина (70 мг, 0,38 ммоль), соединения 1 (93 мг, 0,25 ммоль) и карбоната калия (69 мг, 0,50 ммоль) в диоксане (10 мл) кипятили с обратным холодильником в течение ночи. Летучие компоненты удаляли в вакууме, и остаток очищали обращенно-фазовой флэш-хроматографией (0-70% ацетонитрил в водном 0,01% бикарбонате аммония), получая соединение A23 (57 мг, выход 44%) в виде белого твердого остатка: чистота 93,1% (ВЭЖХ); MC m/z: 514,1 (M+1);
1Н-ЯМР (CDCl3, 500 МГц) δ 8,37 (д, J=8,0 Гц, 1H), 7,89 (д, J=7,5 Гц, 1H), 7,63 (т, JHF=54,0 Гц, 1H), 7,41 (м, 2H), 7,25 (м, 2H), 7,18-6,90 (м, 2H), 5,05 (с, 1H), 4,00-3,72 (м, 8H), 3,19 (с, 2H), 1,45 (с, 6H) м.д.
Пример 20
Получение N-(1-(3-хлорфенил)-2-метилпропан-2-ил)-4-(2-(дифторметил)-1H-бензо[d]имидазол-1-ил)-6-морфолино-1,3,5-триазин-2-амина A20
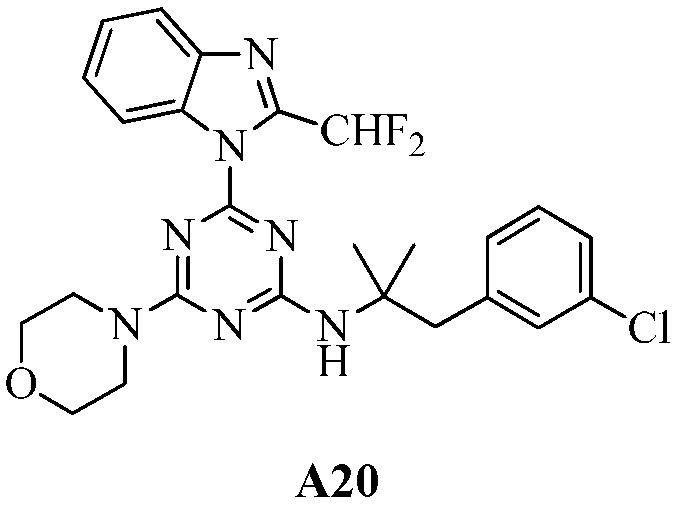
Тионилхлорид (11 г, 100 ммоль) добавляли по каплям к смеси 3-хлорфенилуксусной кислоты (1,7 г, 10 ммоль) в метаноле (20 мл) при 0°C. Полученную в результате смесь кипятили с обратным холодильником при 80°C в течение 12 часов. Летучие компоненты удаляли в вакууме, и остаток разбавляли водой и экстрагировали этилацетатом. Объединенный органический раствор промывали водой, сушили над сульфатом натрия и концентрировали, получая 1,5 г метил 2-(3-хлорфенил)ацетата в виде желтого масла, которое применяли без дополнительной очистки.
Соединение A20 получали в 4 стадии согласно способу для соединения A23, применяя неочищенный метил 2-(3-хлорфенил)ацетат вместо метил 4-хлорфенилацетата. Конечный продукт очищали обращенно-фазовой флэш-хроматографией (0-70% ацетонитрила в водном 0,01% бикарбонате аммония), получая 19 мг соединения A20 в виде белого твердого остатка: чистота >99,5% (ВЭЖХ); MC m/z: 514,1 (M+1);
1Н-ЯМР (CDCl3, 500 МГц) δ 8,37 (д, J=8,0 Гц, 1H), 7,89 (д, J=7,5 Гц, 1H), 7,62 (т, JHF=54,0 Гц, 1H), 7,41 (м, 2H), 7,21 (м, 2H), 7,10 (с, 1H), 6,96 (м, 1H), 5,10 (с, 1H), 4,00-3,69 (м, 8H), 3,19 (с, 2H), 1,47 (с, 6H) м.д.
Пример 21
Получение 4-(2-(дифторметил)-1H-бензо[d]имидазол-1-ил)-N-(1-(3-метоксифенил)-2-метилпропан-2-ил)-6-морфолино-1,3,5-триазин-2-амина A21
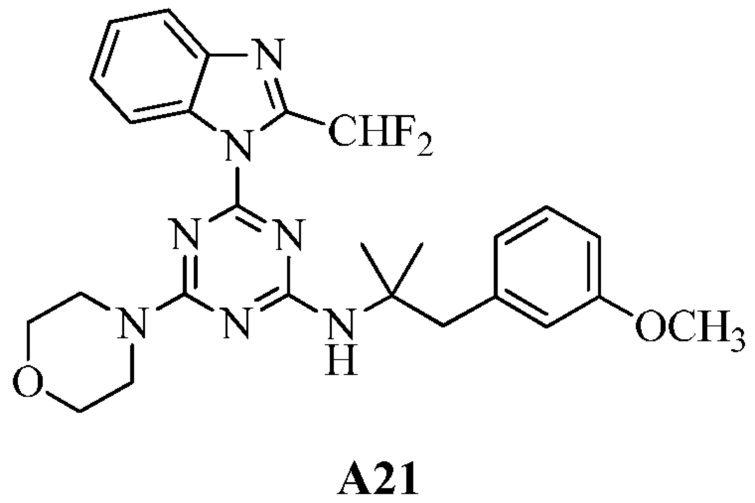
Лития диизопропиламид (2 M в тетрагидрофуране, 2,71 мл, 5,42 ммоль) добавляли к смеси этилизобутирата (600 мг, 5,17 ммоль) в тетрагидрофуране (60 мл) при -78°C и перемешивали при данной температуре в течение 1 часа. Добавляли по каплям 3-метоксибензилхлорид (1,15 г, 7,34 ммоль), и реакционную смесь перемешивали при -78°C в течение следующего 1 часа, и затем при комнатной температуре в течение ночи. Смесь гасили водой и экстрагировали этилацетатом. Объединенные органические фракции промывали водой, сушили над сульфатом натрия и концентрировали в вакууме, получая этил-3-(3-метоксифенил)-2,2-диметилпропаноат (1,3 г) в виде желтого масла, которое применяли на следующей стадии без дополнительной очистки.
Неочищенный этил-3-(3-метоксифенил)-2,2-диметилпропаноат (1,00 г, 4,23 ммоль) растворяли в растворе этанола (50 мл) и гидроксида натрия (2 н., 10 мл). Реакционную смесь кипятили с обратным холодильником в течение ночи, и затем концентрировали в вакууме. Концентрированный водный раствор подкисляли хлористоводородной кислотой (2 н.) до pH 3-4 и экстрагировали этилацетатом. Объединенные органические фракции сушили над сульфатом натрия и упаривали, получая 3-(3-метоксифенил)-2,2-диметилпропионовую кислоту (600 мг) в виде коричневого масла, которое применяли непосредственно на следующей стадии. MC m/z: 207 (M-1).
Смесь 3-(3-метоксифенил)-2,2-диметилпропановой кислоты (200 мг, 0,96 ммоль) в ацетоне (40 мл) и воде (4 мл) охлаждали до 0°C. Добавляли к реакционной смеси триэтиламин (0,18 мл, 1,3 ммоль), с последующим добавлением метилхлорформиата (118 мг, 1,25 ммоль). Смесь перемешивали в течение 1 часа при 0°C, и затем добавляли по каплям раствор азида натрия (94 мг, 1,45 ммоль) в воде (1 мл). Реакционную смесь перемешивали при комнатной температуре в течение следующего 1 часа. Смесь разбавляли водой и экстрагировали этилацетатом. Объединенные органические фракции промывали водой, сушили над сульфатом натрия и концентрировали, получая 3-(3-метоксифенил)-2,2-диметилпропаноилазид (60 мг) в виде неочищенного желтого масла, которое применяли без дополнительной очистки.
Смесь неочищенного 3-(3-метоксифенил)-2,2-диметилпропаноилазида (160 мг, 0,69 ммоль) в толуоле (20 мл) кипятили с обратным холодильником в течение ночи. Растворитель удаляли в вакууме, получая 1,3-бис(1-(3-метоксифенил)-2-метилпропан-2-ил)мочевину (158 мг) в виде коричневого масла, которое применяли без очистки: MC m/z: 383 (M-1).
Смесь неочищенной мочевины (80 мг, 0,21 ммоль) и гидроксида калия (32 мг, 0,57 ммоль) в этиленгликоле (5 мл) кипятили с обратным холодильником в течение 2 часов. Реакционную смесь разбавляли водой и экстрагировали этилацетатом. Объединенные органические фракции промывали водой, сушили над сульфатом натрия и концентрировали, получая 1-(3-метоксифенил)-2-метилпропан-2-амин (75 мг) в виде коричневого масла, которое применяли непосредственно на следующей стадии. MC m/z: 180 (M+1).
Смесь неочищенного амина (63 мг, 0,35 ммоль) и соединения 1 (100 мг, 0,27 ммоль) в диоксане (25 мл) кипятили с обратным холодильником в течение ночи. Летучие компоненты удаляли в вакууме, и остаток очищали препаративной ВЭЖХ, получая соединение A21 (30 мг, выход 22%) в виде белого твердого остатка: чистота >99,5% (ВЭЖХ); MC m/z: 510,2 (M+1);
1Н-ЯМР (CDCl3, 500 МГц) δ 8,37 (д, J=8,0 Гц, 1H), 7,89 (д, J=7,5 Гц, 1H), 7,62 (т, JHF=53,5 Гц, 1H), 7,40 (м, 2H), 7,20 (т, J=7,5 Гц, 1H), 6,79 (дд, J=8,5 Гц и 2,0 Гц, 1H), 6,69 (д, J=7,5 Гц, 1H), 6,65 (с, 1H), 5,14 (с, 1H), 4,00-3,76 (м, 8H), 3,74 (с, 3H), 3,17 (с, 2H), 1,48 (с, 6H) м.д.
Пример 22
Получение 4-(2-(дифторметил)-1H-бензо[d]имидазол-1-ил)-N-(2-метил-1-(нафталин-2-ил)пропан-2-ил)-6-морфолино-1,3,5-триазин-2-амина A26
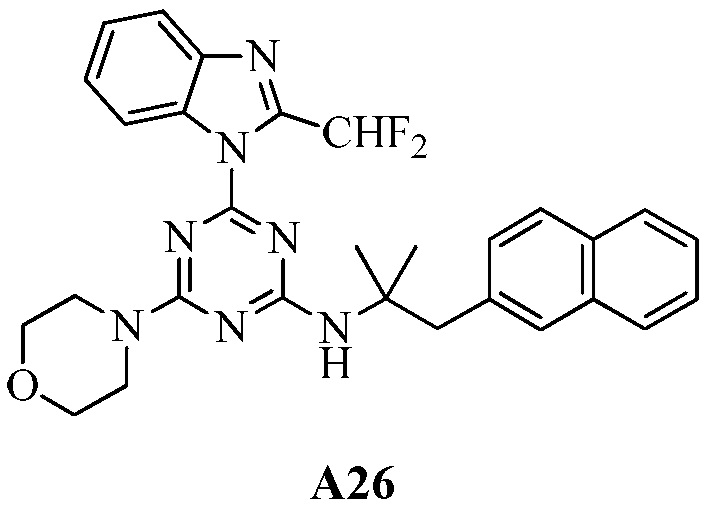
бис(Триметилсилил)амид лития (1 M в тетрагидрофуране, 25,3 мл, 25,3 ммоль) добавляли к смеси этилизобутирата (2,67 г, 23,0 ммоль) в тетрагидрофуране (25 мл) при -78°C. После перемешивания в течение 30 минут, раствор 2-(хлорметил)нафталина (400 мг, 2,30 ммоль) в тетрагидрофуране (10 мл) добавляли по каплям к реакционной смеси. Смесь перемешивали при -78°C в течение следующего часа, и затем при комнатной температуре в течение ночи. Смесь гасили добавлением воды и экстрагировали этилацетатом. Объединенные органические фракции промывали водой, сушили над сульфатом натрия и концентрировали в вакууме, получая этил 2,2-диметил-3-(нафталин-2-ил)пропаноат (1,00 г) в виде желтого масла, которое применяли без дополнительной очистки.
Неочищенный эфир (915 мг) растворяли в диоксане (4 мл) и 20% водном гидроксиде натрия (8 мл). После перемешивания при комнатной температуре в течение 2 часов, реакционную смесь разбавляли этилацетатом. Водную фракцию подкисляли до pH=2 концентрированной хлористоводородной кислотой, и затем экстрагировали этилацетатом. Объединенные органические фракции сушили над сульфатом натрия и концентрировали, получая 2,2-диметил-3-(нафталин-2-ил)пропионовую кислоту (211 мг, выход для двух стадий 40%) в виде белого твердого остатка, который применяли непосредственно на следующей стадии.
Смесь промежуточной кислоты (211 мг, 0,920 ммоль) в ацетоне (3 мл) и воде (0,3 мл) охлаждали до 0°C. Триэтиламин (0,20 мл, 1,40 ммоль) добавляли к реакционной смеси, с последующим добавлением метилхлорформиата (104 мг, 1,10 ммоль). Реакционную смесь перемешивали при комнатной температуре в течение 30 минут и добавляли по каплям раствор азида натрия (120 мг, 1,84 ммоль) в воде (0,5 мл). После перемешивания при комнатной температуре в течение 2 часов, реакционную смесь разбавляли водой и экстрагировали петролейным эфиром. Объединенные органические фракции промывали водой, сушили над сульфатом натрия и упаривали, получая неочищенный 2,2-диметил-3-(нафталин-2-ил)пропаноилазид (117 мг, выход 50%) в виде бесцветного масла, которое применяли без дополнительной очистки.
Неочищенный ацилазид (117 мг, 0,46 ммоль) кипятили с обратным холодильником в толуоле (3 мл) в течение ночи, получая промежуточный изоцианат. Реакционную смесь охлаждали до комнатной температуры и добавляли раствор 10% хлористоводородной кислоты (3 мл). После кипячения с обратным холодильником в течение 4 часов, реакционную смесь концентрировали в вакууме, получая 2-метил-1-(нафталин-2-ил)пропан-2-амин (98 мг, выход 90%) в виде желтого твердого остатка, который применяли непосредственно на следующей стадии.
Смесь неочищенного амина (98 мг, 0,42 ммоль), соединения 1 (103 мг, 0,28 ммоль) и карбоната калия (116 мг, 0,84 ммоль) в диоксане (3 мл) кипятили с обратным холодильником в течение ночи. Реакционную смесь концентрировали, и остаток очищали препаративной ВЭЖХ, получая соединение A26 (12 мг, выход 8%) в виде белого твердого остатка: чистота >99,5% (ВЭЖХ); MC m/z: 530,3 (M+1);
1Н-ЯМР (CDCl3, 500 МГц) δ 8,37 (д, J=8,0 Гц, 1H), 7,85-7,37 (м, 10H), 5,19 (с, 1H), 4,04-3,75 (м, 8H), 3,37 (с, 2H), 1,53 (с, 6H) м.д.
Пример 23
Получение 4-(2-(дифторметил)-1H-бензо[d]имидазол-1-ил)-N-(2-метил-1-(нафталин-1-ил)пропан-2-ил)-6-морфолино-1,3,5-триазин-2-амина A27
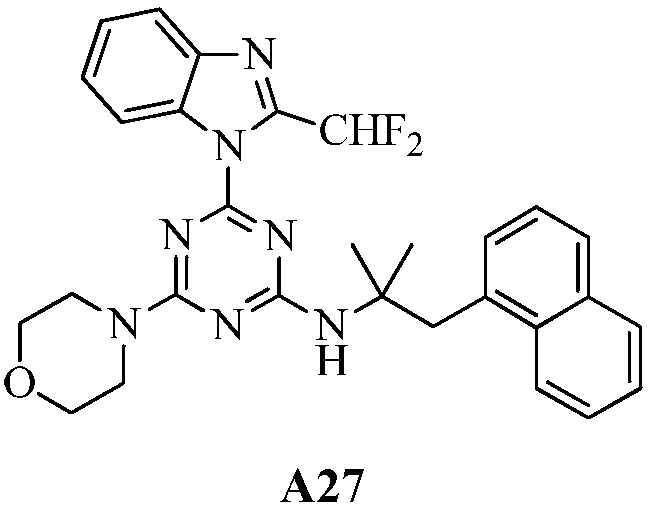
Метилмагнийбромид (3 M в эфире, 10 мл, 30 ммоль) добавляли по каплям к раствору метилнафталин-1-ацетата (2,0 г, 10 ммоль) в тетрагидрофуране (20 мл) при 0°C в атмосфере азота. После перемешивания при комнатной температуре в течение ночи, реакционную смесь гасили добавлением воды. Органическую фракцию промывали соляным раствором, сушили над сульфатом натрия и концентрировали в вакууме, получая неочищенный 2-метил-1-(нафталин-1-ил)пропан-2-ол (2,0 г) в виде желтого масла, которое применяли непосредственно на следующей стадии.
Неочищенный спирт (2,0 г, 10 ммоль) растворяли в ацетонитриле (10 мл) и добавляли по каплям при 0°C концентрированную серную кислоту (4,9 г, 50 ммоль). После перемешивания при комнатной температуре в течение 2 часов, реакционную смесь разбавляли водой и экстрагировали дихлорметаном. Объединенные органические фракции сушили над сульфатом натрия и упаривали. Остаток очищали колоночной хроматографией на силикагеле (петролейный эфир/этилацетат), получая N-(2-метил-1-(нафталин-1-ил)пропан-2-ил)ацетамид (0,90 г, выход 37%) в виде желтого твердого остатка.
Концентрированную хлористоводородную кислоту (10 мл) добавляли к раствору промежуточного ацетамида (0,20 г, 0,83 ммоль) в диоксане (2 мл), и полученную в результате смесь кипятили с обратным холодильником в течение 3 дней. После охлаждения до комнатной температуры реакционную смесь подщелачивали до pH 9 добавлением твердого бикарбоната натрия. Смесь экстрагировали этилацетатом, и объединенные органические фракции сушили над сульфатом натрия и концентрировали, получая неочищенный 2-метил-1-(нафталин-1-ил)пропан-2-амин (0,15 г, выход 23%) в виде желтого масла, которое применяли без дополнительной очистки.
Неочищенный амин (153 мг, 0,25 ммоль), соединение 1 (48 мг, 0,13 ммоль) и карбонат калия (36 мг, 0,25 ммоль) растворяли в диоксане (2 мл) и кипятили с обратным холодильником в течение ночи. Реакционную смесь концентрировали в вакууме, и остаток очищали препаративной ВЭЖХ, получая соединение A27 (16 мг, выход 23%) в виде белого твердого остатка: чистота >99,5% (ВЭЖХ); MC m/z: 530,3 (M+1);
1Н-ЯМР (CDCl3, 500 МГц) δ 8,29 (д, J=8,0 Гц, 1H), 8,15 (д, J=7,0 Гц, 1H), 7,88 (д, J=6,5 Гц, 2H), 7,77 (д, J=8,0 Гц, 1H), 7,56 (т, JHF =54,0 Гц, 1H), 7,48 (м, 2H), 7,39 (м, 3H), 7,27 (д, J=7,0 Гц, 1H), 5,29 (с, 1H), 4,02-3,73 (м, 8H), 3,66 (с, 2H), 1,54 (с, 6H) м.д.
Пример 24
Получение 4-(2-(дифторметил)-1H-бензо[d]имидазол-1-ил)-N-(1-(2-фторфенил)-2-метилпропан-2-ил)-6-морфолино-1,3,5-триазин-2-амина A15
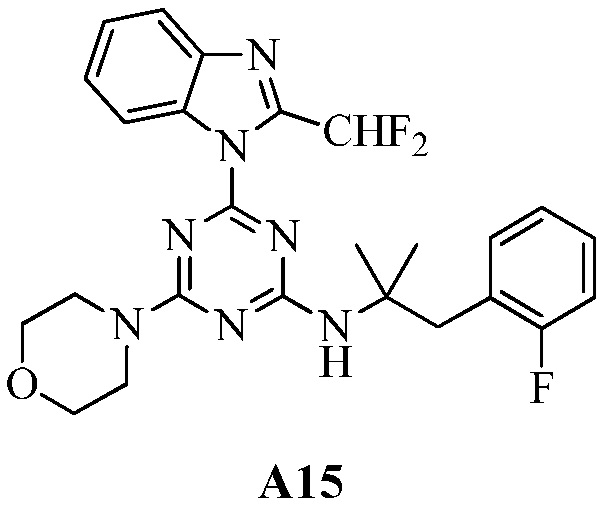
Соединение A15 получали в 6 стадий, согласно способу для соединения A21, применяя 2-фторбензилбромид вместо 3-метоксибензилхлорида. Конечный продукт очищали препаративной ВЭЖХ, получая соединение A15 (30 мг, выход 22%) в виде белого твердого остатка: чистота 99,4% (ВЭЖХ); MC m/z: 498,2 (M+1);
1Н-ЯМР (CDCl3, 500 МГц) δ 8,39 (д, J=8,0 Гц, 1H), 7,89 (д, J=7,5 Гц, 1H), 7,65 (т, JHF=53,5 Гц, 1H), 7,41 (м, 2H), 7,22 (м, 1H), 7,06 (м, 3H), 5,25 (с, 1H), 4,00-3,73 (м, 8H), 3,28 (с, 2H), 1,49 (с, 6H) м.д.
Пример 25
Получение 4-(2-(дифторметил)-1 H -бензо[ d ]имидазол-1-ил)- N -(2-метил-2-фенилпропил)-6-морфолино-1,3,5-триазин-2-амина A29
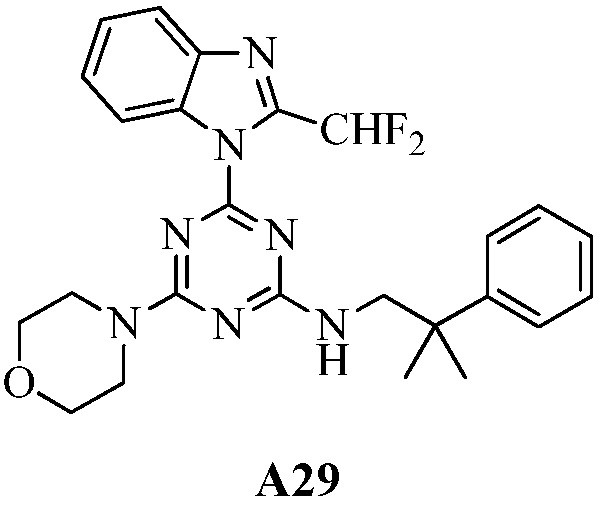
Порошковый литийалюмогидрид (137 мг, 3,61 ммоль) добавляли порциями к раствору 2-метил-2-фенилпропаннитрила (436 мг, 3,00 ммоль) в тетрагидрофуране (20 мл). Полученную в результате смесь перемешивали при 80°C в течение ночи. Затем реакционную смесь охлаждали до 0°C и воду (66 мкл, 3,7 ммоль), 10% гидроксид натрия (1,44 г, 3,6 ммоль) и воду (195 мкл, 10,8 ммоль), соответственно, добавляли по каплям к реакционной смеси. Суспензию фильтровали через безводный сульфат магния, и раствор концентрировали в вакууме, получая 2-метил-2-фенилпропан-1-амин (400 мг) в виде желтого масла, которое применяли на следующей стадии без дополнительной очистки.
Неочищенный амин (400 мг, 2,7 ммоль) и соединение 1 (147 мг, 0,401 ммоль) кипятили с обратным холодильником в диоксане (25 мл) в течение 4 часов. После охлаждения реакционную смесь концентрировали в вакууме. Остаток разбавляли насыщенным бикарбонатом натрия и экстрагировали этилацетатом. Объединенные органические фракции промывали водой и соляным раствором, сушили над сульфатом натрия и концентрировали. Сырой продукт очищали препаративной ВЭЖХ, получая соединение A29 (75 мг, выход для 2 стадий 35%) в виде белого твердого остатка: чистота >99,5% (ВЭЖХ); MC m/z: 480,2 (M+1);
1Н-ЯМР (CDCl3, 500 МГц) (ротамеры) δ 8,45 (д, J=7,5 Гц, 0,5H), 8,33 (д, J=8,0 Гц, 0,5H), 7,92 (д, J=7,5 Гц, 0,5H), 7,88 (д, J=7,5 Гц, 0,5H), 7,64 и 7,60 (2т, JHF=53,5 Гц, 1H), 7,42 (м, 6H), 7,28 (м, 1H), 5,13-5,00 (м, 1H), 4,00-3,70 (м, 10H), 1,45 и 1,44 (2с, 6H) м.д.
Пример 26
Получение 4-(2-(дифторметил)-1H-бензо[d]имидазол-1-ил)-N-(2-(1-фенилциклопропил)пропан-2-ил)-6-морфолино-1,3,5-триазин-2-амина A30
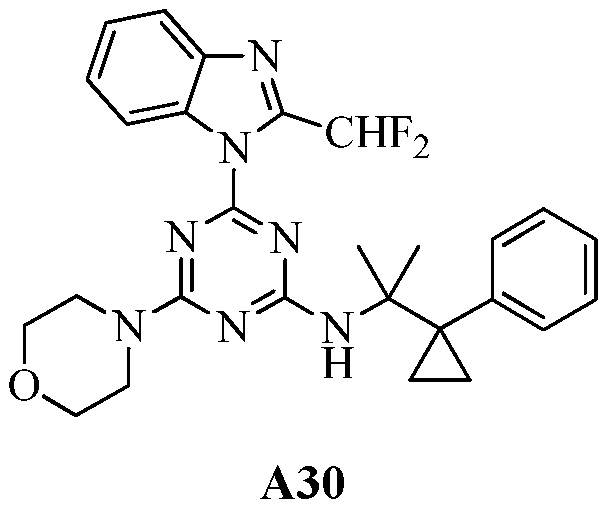
Метилмагнийбромид (3,0 M в тетрагидрофуране, 3,0 мл, 9,0 ммоль) добавляли к раствору 1-фенил-1-циклопропанкарбонитрила (429 мг, 3,0 ммоль) в безводном тетрагидрофуране (4 мл) при комнатной температуре в атмосфере азота. Реакционную смесь грели при 100°C в течение 10 минут в СВЧ-печи. Затем добавляли изопропоксид титана(IV) (0,9 мл, 3,0 ммоль), и реакционную смесь грели при 50°C в течение 1 часа в СВЧ-печи. После охлаждения раствор добавляли по каплям к реакционной смеси 25% водный аммиак (2 мл). Суспензию фильтровали через слой целита, который промывали тетрагидрофураном. Объединенный фильтрат разбавляли водой и экстрагировали этилацетатом. Объединенные органические экстракты сушили над безводным сульфатом натрия и концентрировали в вакууме, получая 2-(1-фенилциклопропил)пропан-2-амин (400 мг) в виде неочищенного желтого масла: MC m/z: 178 (M+1).
Неочищенный амин (200 мг, 1,1 ммоль) смешивали с соединением 1 (100 мг, 0,27 ммоль) и карбонатом калия (150 мг, 1,1 ммоль) в диоксане (20 мл) и кипятили с обратным холодильником в течение ночи. Смесь разбавляли водой и экстрагировали этилацетатом. Органические экстракты сушили безводным сульфатом натрия и концентрировали в вакууме. Сырой продукт очищали обращенно-фазовой флэш-хроматографией (0-85% ацетонитрила в 0,01% бикарбонате аммония), получая соединение A30 (46 мг, выход 34%) в виде белого твердого остатка: чистота 94,4% (ВЭЖХ); MC m/z: 506,2 (M+1);
1Н-ЯМР (CDCl3, 500 МГц) δ 8,34 (д, J=7,5 Гц, 1H), 7,90 (д, J=7,5 Гц, 1H), 7,61 (т, JHF=54,0 Гц, 1H), 7,42 (м, 2H), 7,35 (м, 2H), 7,29 (м, 2H), 7,24 (м, 1H), 5,26 (с, 1H), 4,00-3,65 (м, 8H), 1,48 (с, 6H), 1,17 (м, 2H), 0,84 (м, 2H) м.д.
Пример 27
Получение 4-(2-(дифторметил)-1H-бензо[d]имидазол-1-ил)-N-(1-(2- бром фенил)-2-метилпропан-2-ил) - 6-морфолино-1,3,5-триазин-2-амина A17
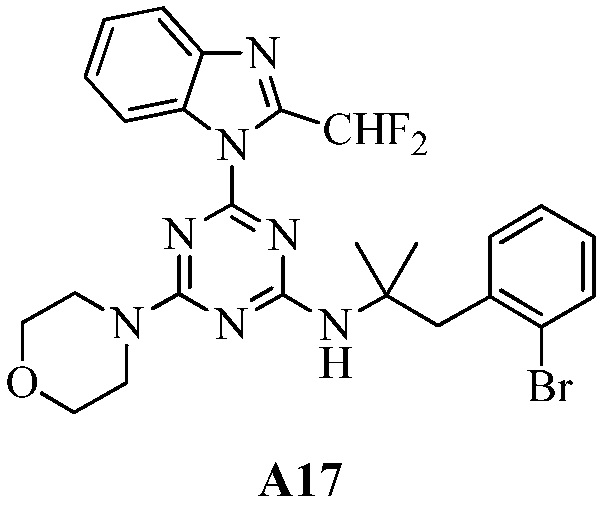
Диизопропиламид лития (2 M в гексане, 1,5 мл, 3,0 ммоль) добавляли к раствору этилизобутирата (233 мг, 2,01 ммоль) в тетрагидрофуране (1 мл) при -78°C, и реакционную смесь перемешивали при данной температуре в течение 30 минут. Затем добавляли по каплям раствор 2-бромбензилбромида (250 мг, 1,00 ммоль) в тетрагидрофуране (1 мл). Реакционную смесь перемешивали при -78°C в течение следующего 1 часа, и затем при комнатной температуре в течение ночи. Смесь разбавляли водой и экстрагировали этилацетатом. Объединенные органические фракции промывали водой, сушили над сульфатом натрия и концентрировали, получая 482 мг этил 3-(2-бромфенил)-2,2-диметилпропаноата в виде желтого масла. Неочищенное промежуточное соединение применяли непосредственно на следующей стадии.
Раствор неочищенного эфира (482 мг) в диоксане (2 мл) смешивали с водным гидроксидом натрия (20%, 4 мл) и перемешивали при комнатной температуре в течение 2 часов. Реакционную смесь разбавляли этилацетатом, и водную фракцию подкисляли до pH 2 концентрированной хлористоводородной кислотой. После экстракции этилацетатом объединенные органические фракции сушили над сульфатом натрия и концентрировали в вакууме, получая 121 мг (выход для двух стадий 47%) 3-(2-бромфенил)-2,2-диметилпропионовой кислоты в виде белого твердого остатка. Неочищенную карбоновую кислоту применяли на следующей стадии без дополнительной очистки: MC m/z: 255,0 (M-1).
Триэтиламин (112 мг, 1,11 ммоль) добавляли к смеси промежуточной карбоновой кислоты (188 мг, 0,731 ммоль) в ацетоне (8 мл) и воде (1 мл). Реакционную смесь охлаждали до 0°C и добавляли метилхлорформиат (84 мг, 0,88 ммоль). Смесь перемешивали при комнатной температуре в течение 30 минут, и затем добавляли по каплям раствор азида натрия (95 мг, 1,46 ммоль) в воде (0,5 мл). После перемешивания при комнатной температуре в течение ночи, полученную в результате смесь разбавляли водой и экстрагировали петролейным эфиром. Объединенные органические фракции промывали водой, сушили над сульфатом натрия и концентрировали, получая 162 мг (выход 79%) 3-(2-бромфенил)-2,2-диметилпропаноилазида в виде белого твердого остатка, который применяли непосредственно на следующей стадии: MC m/z: 252,9 (M-28).
Раствор неочищенного ацилазида (162 мг, 0,574 ммоль) в толуоле (3 мл) кипятили с обратным холодильником в течение ночи, получая 1-бром-2-(2-изоцианато-2-метилпропил)бензол. Затем раствор охлаждали до комнатной температуры и добавляли 10% водную хлористоводородную кислоту (3 мл). Полученную в результате смесь кипятили с обратным холодильником в течение 4 часов. Летучие компоненты удаляли в вакууме, получая 129 мг (выход 85%) гидрохлорида 1-(2-бромфенил)-2-метилпропан-2-амина в виде белого твердого остатка. Неочищенную гидрохлоридную соль амина применяли на следующей стадии без дополнительной очистки: MC m/z: 228,1 (M+1).
Смесь аминовой соли (129 мг, 0,49 ммоль), соединения 1 (121 мг, 0,33 ммоль) и карбоната калия (183 мг, 1,33 ммоль) кипятили с обратным холодильником в диоксане (4 мл) в течение ночи. Летучие компоненты удаляли в вакууме, и остаток очищали колоночной хроматографией на силикагеле (9% этилацетат в петролейном эфире), получая 99 мг (выход 54%) соединения A17, 4-(2-(дифторметил)-1H-бензо[d]имидазол-1-ил)-N-(1-(2-бромфенил)-2-метилпропан-2-ил)-6-морфолино-1,3,5-триазин-2-амина, в виде белого твердого остатка: чистота >99,5% (ВЭЖХ); MC m/z: 558,2 (M+1), 560,2 (M+3);
1Н-ЯМР (CDCl3, 500 МГц) δ 8,42 (д, 1H), 7,91 (д, 1H), 7,67 (т, 1H), 7,60 (д, 1H), 7,48-7,37 (м, 2H), 7,22 (т, 1H), 7,11 (м, 2H), 5,32 (с, 1H), 4,01-3,76 (м, 8H), 3,46 (с, 2H), 1,54 (с, 6H) м.д.
Пример 28
Получение 4-(2-(дифторметил)-1H-бензо[d]имидазол-1-ил)-N-(2-метил-1-(2-(пиридин-4-ил)фенил)пропан-2-ил)-6-морфолино-1,3,5-триазин-2-амина A33
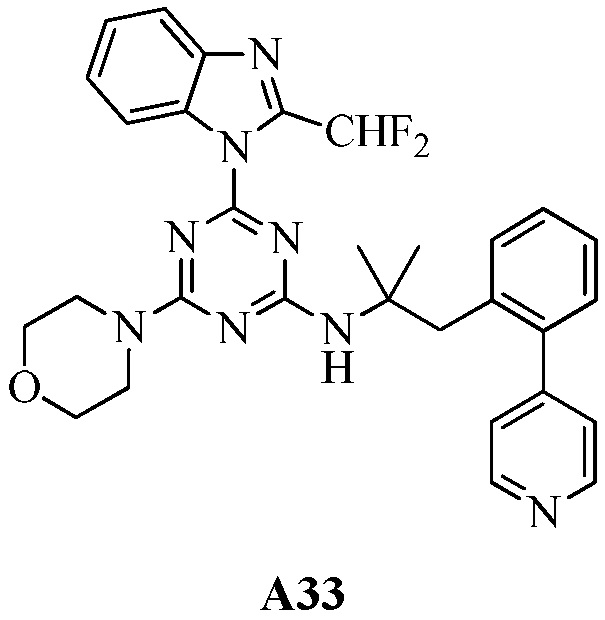
Соединение A17 (200 мг, 0,358 ммоль), пиридинил-4-бороновую кислоту (49 мг, 0,40 ммоль), карбонат натрия (114 мг, 1,08 ммоль) и дихлорметановый комплекс 1,1'-бис(дифенилфосфино)ферроцен-дихлорид палладия(II) (29 мг, 0,036 ммоль) растворяли в N,N'-диметилформамиде (4 мл) и воде (1 мл) и перемешивали в атмосфере азота при 100°C в течение ночи. Реакционную смесь разбавляли этилацетатом и фильтровали через целит. Фильтрат промывали водой и соляным раствором, сушили над сульфатом натрия и концентрировали. Сырой продукт очищали препаративной ВЭЖХ, получая 18 мг (выход 9%) соединения A33, 4-(2-(дифторметил)-1H-бензо[d]имидазол-1-ил)-N-(2-метил-1-(2-(пиридин-4-ил)фенил)-пропан-2-ил)-6-морфолино-1,3,5-триазин-2-амина, в виде белого твердого остатка: чистота >99,5% (ВЭЖХ); MC m/z: 557,3 (M+1);
1Н-ЯМР (CDCl3, 500 МГц) (ротамеры) δ 8,53 (шир.с, 2H), 8,39 (д, 1H), 7,92 (д, 1H), 7,66 (т, 1H), 7,49-7,38 (м, 2H), 7,34 (м, 2H), 7,26 (м, 1H), 7,23-7,15 (м, 3H), 4,88 (с, 1H), 3,95-3,75 (м, 8H), 3,35 (с, 2H), 1,28 (с, 6H) м.д.
Пример 29
Получение 4-(2-(дифторметил)-1H-бензо[d]имидазол-1-ил)-N-(1-(бифенил-2-ил)-2-метилпропан-2-ил)-6-морфолино-1,3,5-триазин-2-амина A47
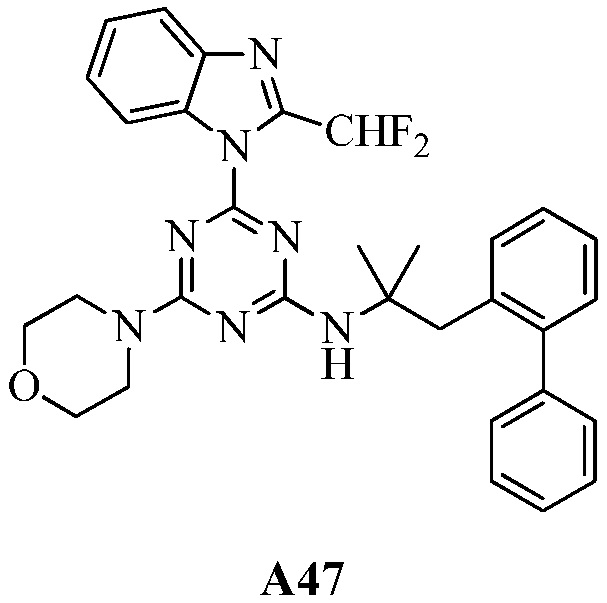
Соединение A17 (140 мг, 0,251 ммоль), фенилбороновую кислоту (61 мг, 0,500 ммоль), карбонат натрия (80 мг, 0,755 ммоль) и дихлорметановый комплекс 1,1'-бис(дифенилфосфино)ферроцен-дихлорид палладия(II) (21 мг, 0,0257 ммоль) растворяли в N,N'-диметилформамиде (8 мл) и воде (2 мл) и перемешивали в атмосфере азота при 100°C в течение ночи. Реакционную смесь разбавляли этилацетатом и фильтровали через целит. Фильтрат промывали водой и соляным раствором, сушили над сульфатом натрия и концентрировали. Сырой продукт очищали хиральной-SFC, получая 60 мг (выход 44%) соединения A47, 4-(2-(дифторметил)-1H-бензо[d]имидазол-1-ил)-N-(1-(бифенил-2-ил)-2-метилпропан-2-ил)-6-морфолино-1,3,5-триазин-2-амина, в виде белого твердого остатка: чистота >99,5% (ВЭЖХ); MC m/z: 556,2 (M+1);
1Н-ЯМР (CDCl3, 500 МГц) (ротамеры) δ 8,39 (д, 1H), 7,92 (д, 1H), 7,66 (т, 1H), 7,44 (м, 2H), 7,28 (м, 7H), 7,22 (м, 2H), 4,94 (с, 1H), 3,92-3,55 (м, 8H), 3,37 (с, 2H), 1,28 (с, 6H) м.д.
Пример 30
Получение 4-(2-(дифторметил)-1 H -бензо[ d ]имидазол-1-ил)- N -(1-(3-фторфенил)-2-метилпропан-2-ил)-6-морфолино-1,3,5-триазин-2-амина A 39
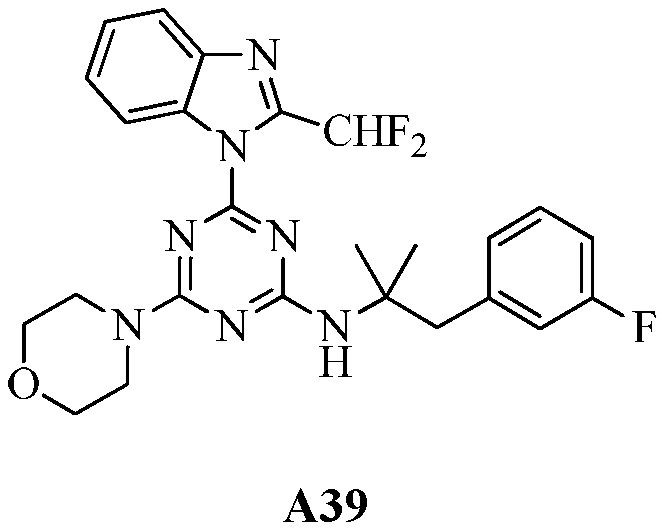
Соединение A39 получали в 6 стадий, согласно способу для A21, применяя 3-фторбензилбромид вместо 3-метоксибензилхлорида. Конечный продукт очищали препаративной ВЭЖХ, получая соединение A39 (35 мг) в виде белого твердого остатка: чистота 99% (ВЭЖХ); MC m/z: 498,2 (M+1);
1Н-ЯМР (ДМСО-d6, 500 МГц) δ 8,60 (д, 1H), 8,01 (т, 1H), 7,84 (д, 1H), 7,54 (с, 1H), 7,45 (м, 2H), 7,30 (м, 1H), 7,03 (м, 1H), 6,94 (м, 2H), 3,85 (м, 4H), 3,75 (м, 4H), 3,25 (с, 2H), 1,40 (с, 6H) м.д.
Пример 31
Получение 4-(2-(дифторметил)-1H-бензо[d]имидазол-1-ил)-N-(2-метил-1-м-толилпропан-2-ил)-6-морфолино-1,3,5-триазин-2-амина A49
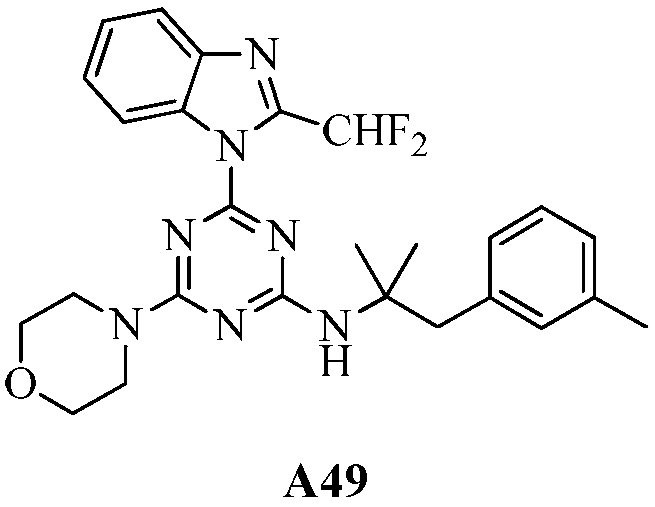
Соединение A49 получали в 6 стадий, согласно способу для A21, применяя 3-метилбензилбромид вместо 3-метоксибензилхлорида. Конечный продукт очищали препаративной ВЭЖХ, получая соединение A49 (15 мг) в виде белого твердого остатка: чистота 98% (ВЭЖХ); MC m/z: 494,2 (M+1);
1Н-ЯМР (CDCl3, 500 МГц) δ 8,38 (д, 1H), 7,90 (д, 1H), 7,64 (т, 1H), 7,48 (с, 1H), 7,42 (м, 1H), 7,19 (т, 1H), 7,10-6,88 (м, 3H), 5,17 (с, 1H), 4,10-3,80 (м, 8H), 3,16 (с, 2H), 2,31 (с, 3H), 1,49 (с, 6H) м.д.
Пример 32
Получение 4-(2-(дифторметил)-1H-бензо[d]имидазол-1-ил)-N-(1-(4-фтор-3-метоксифенил)-2-метилпропан-2-ил)-6-морфолино-1,3,5-триазин-2-амина A50
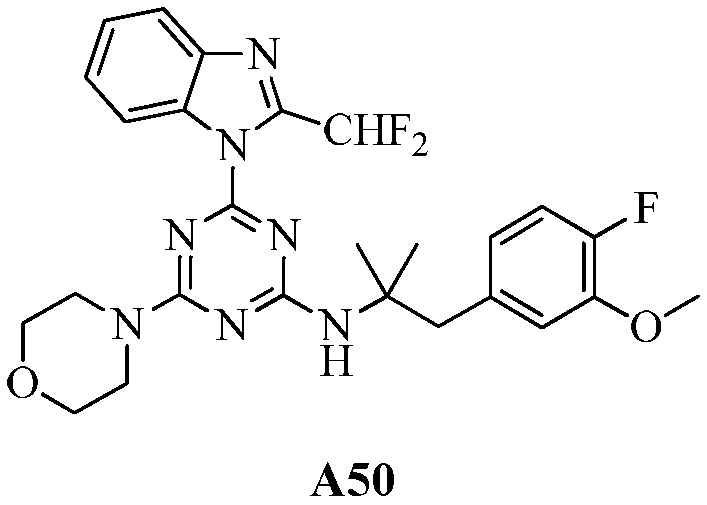
Соединение A50 получали в 6 стадий, согласно способу для A21, применяя 4-фтор-3-метоксибензилбромид вместо 3-метоксибензилхлорида. Конечный продукт очищали препаративной ВЭЖХ, получая соединение A50 (115 мг) в виде белого твердого остатка: чистота 99% (ВЭЖХ); MC m/z: 528,2 (M+1);
1Н-ЯМР (CDCl3, 500 МГц) δ 8,37 (д, 1H), 7,90 (д, 1H), 7,64 (т, 1H), 7,43 (м, 2H), 6,99 (м, 1H), 6,71-6,60 (м, 2H), 5,12 (с, 1H), 4,01-3,78 (м, 8H), 3,77 (с, 3H), 3,17 (с, 2H), 1,49 (с, 6H) м.д.
Пример 33
Получение 4-(2-(дифторметил)-1H-бензо[d]имидазол-1-ил)-N-(1-(2,4-дифторфенил)-2-метилпропан-2-ил)-6-морфолино-1,3,5-триазин-2-амина A51
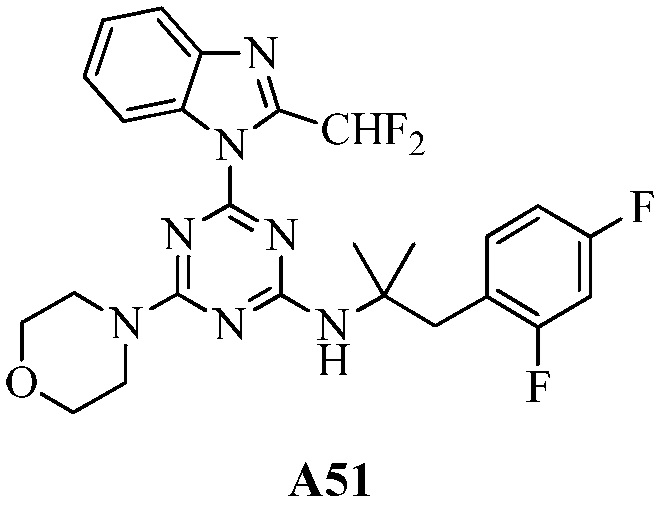
Соединение A51 получали в 5 стадий, согласно способу для A20, применяя 2,4-дифторфенилуксусную кислоту вместо 3-хлорфенилуксусной кислоты. Конечный продукт очищали препаративной ВЭЖХ, получая соединение A51 (60 мг) в виде белого твердого остатка: чистота 99% (ВЭЖХ); MC m/z: 516,2 (M+1);
1Н-ЯМР (CDCl3, 500 МГц) δ 8,40 (д, 1H), 7,90 (д, 1H), 7,65 (т, 1H), 7,43 (м, 2H), 7,04 (м, 1H), 6,84 (м, 2H), 5,19 (с, 1H), 4,00-3,75 (м, 8H), 3,26 (с, 2H), 1,49 (с, 6H) м.д.
Пример 34
Получение 4-(2-(дифторметил)-1H-бензо[d]имидазол-1-ил)-N-(1-(2,6-дифторфенил)-2-метилпропан-2-ил)-6-морфолино-1,3,5-триазин-2-амина A52
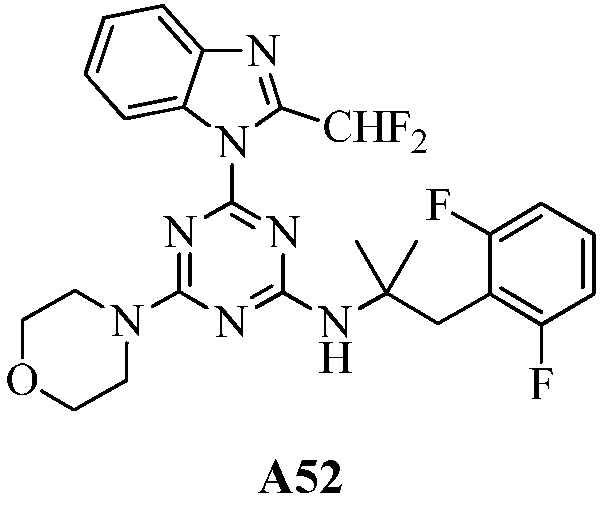
Соединение A52 получали в 5 стадий, согласно способу для A20, применяя 2,6-дифторфенилуксусную кислоту вместо 3-хлорфенилуксусной кислоты. Конечный продукт очищали препаративной ВЭЖХ, получая соединение A52 (38 мг) в виде белого твердого остатка: чистота 98% (ВЭЖХ); MC m/z: 516,3 (M+1);
1Н-ЯМР (CDCl3, 500 МГц) δ 8,41 (д, 1H), 7,90 (д, 1H), 7,66 (т, 1H), 7,43 (м, 2H), 7,23 (м, 1H), 6,91 (т, 2H), 5,43 (с, 1H), 4,05-3,70 (м, 8H), 3,33 (с, 2H), 1,53 (с, 6H) м.д.
Пример 35
Получение 4-(2-(дифторметил)-1H-бензо[d]имидазол-1-ил)-N-(2-метил-1-(2-(пиридин-3-ил)фенил)пропан-2-ил)-6-морфолино-1,3,5-триазин-2-амина A 40
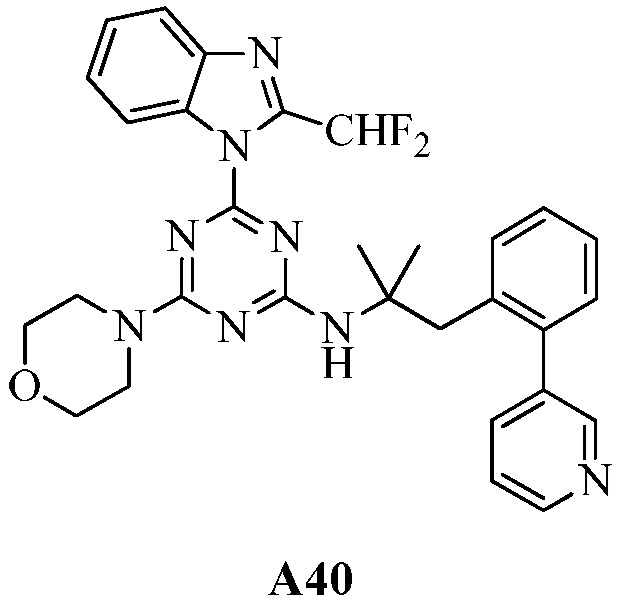
Соединение A40 получали, согласно способу для A33, применяя 3-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиридин вместо пиридинил-4-бороновой кислоты. Сырой продукт очищали препаративной ВЭЖХ, получая соединение A40 (41 мг, выход 41%) в виде белого твердого остатка: чистота 98% (ВЭЖХ); MC m/z: 557,3 (M+1);
1Н-ЯМР (ДМСО-d6, 500 МГц) δ 8,58 (д, 1H), 8,40 (с, 1H), 8,37 (дд, 1H), 8,01 (т, 1H), 7,84 (д, 1H), 7,58 (дд, 1H), 7,48 (т, 1H), 7,43 (т, 1H), 7,40-7,28 (м, 3H), 7,19 (с, 1H), 7,13 (м, 2H), 3,82-3,60 (м, 8H), 3,34 (с, 2H), 1,23 (с, 6H) м.д.
Пример 36
Получение 4-(2-(дифторметил)-1H-бензо[d]имидазол-1-ил)-N-(1-(2-(2-метоксипиридин-4-ил)фенил)-2-метилпропан-2-ил)-6-морфолино-1,3,5-триазин-2-амина A4 1
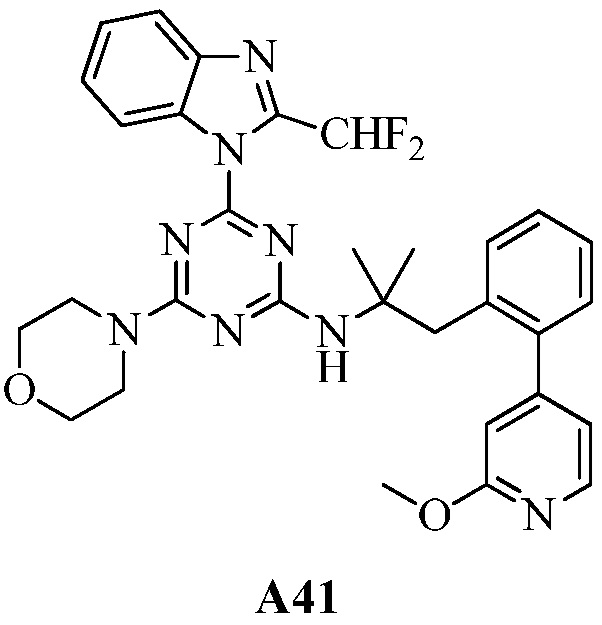
Соединение A41 получали, согласно способу для A33, применяя 2-метоксипиридин-4-бороновую кислоту вместо пиридинил-4-бороновой кислоты. Сырой продукт очищали препаративной ВЭЖХ, получая соединение A41 (250 мг, выход 24%) в виде белого твердого остатка: чистота 95% (ВЭЖХ); MC m/z: 587,3 (M+1);
1Н-ЯМР (CDCl3, 500 МГц) δ 8,40 (д, J=8,0 Гц, 1H), 8,06 (д, 1H), 7,91 (д, 1H), 7,65 (т, 1H), 7,43 (м, 2H), 7,33 (м, 2H), 7,25 (т, 1H), 7,16 (д, 1H), 6,78 (д, 1H), 6,62 (с, 1H), 4,85 (с, 1H), 3,95-3,75 (м, 8H), 3,74 (с, 3H), 3,36 (с, 2H), 1,32 (с, 6H) м.д.
Пример 37
Получение 4-(2-(дифторметил)-1H-бензо[d]имидазол-1-ил)-N-(2-метил-1-(2-(2-метилпиридин-4-ил)фенил)пропан-2-ил)-6-морфолино-1,3,5-триазин-2-амина A 43
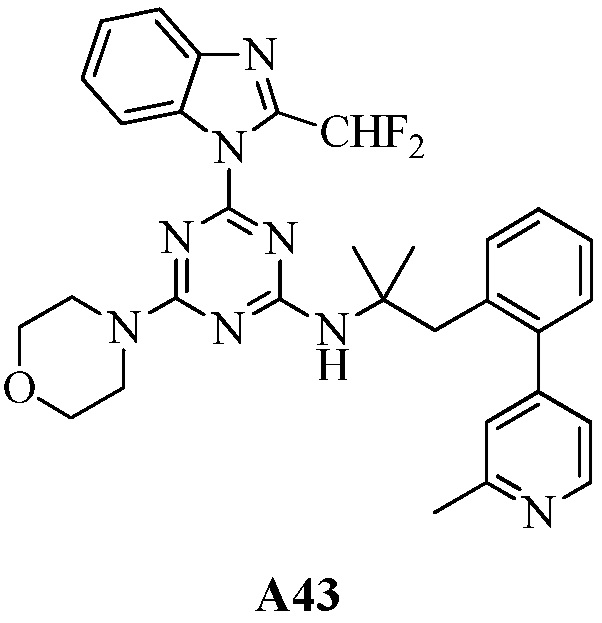
Соединение A43 получали, согласно способу для A33, применяя 2-метилпиридин-4-бороновую кислоту вместо пиридинил-4-бороновой кислоты. Сырой продукт очищали препаративной ВЭЖХ, получая соединение A43 (15 мг, выход 24%) в виде белого твердого остатка: чистота 98% (ВЭЖХ); MC m/z: 571,2 (M+1);
1Н-ЯМР (CDCl3, 500 МГц) δ 8,45 (д, 1H), 8,40 (д, 1H), 7,91 (д, 1H), 7,66 (т, 1H), 7,44 (м, 2H), 7,33 (м, 2H), 7,24 (м, 1H), 7,16 (м, 1H), 7,13-6,95 (м, 2H), 4,88 (с, 1H), 4,00-3,75 (м, 8H), 3,36 (с, 2H), 2,49 (с, 3H), 1,28 (с, 6H) м.д.
Пример 38
Получение 4-(2-(дифторметил)-1H-бензо[d]имидазол-1-ил)-N-(1-(2-(1H-пиразол-4-ил)фенил)-2-метилпропан-2-ил)-6-морфолино-1,3,5-триазин-2-амина A 44
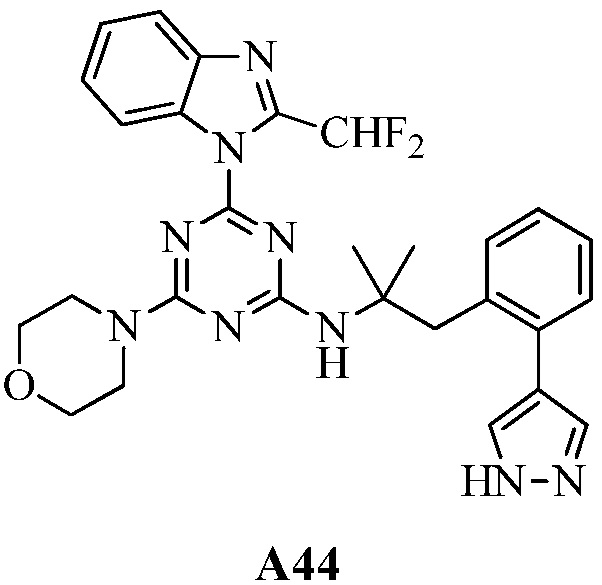
Соединение A44 получали, согласно способу для A33, применяя пинаколовый эфир 1-Boc-пиразол-4-бороновой кислоты вместо пиридинил-4-бороновой кислоты. Сырой продукт очищали препаративной ВЭЖХ, получая соединение A44 (15 мг, выход 31%) в виде белого твердого остатка: чистота 99% (ВЭЖХ); MC m/z: 546,3 (M+1);
1Н-ЯМР (ДМСО-d6, 500 МГц) δ 12,84 (с, 1H), 8,59 (д, 1H), 8,00 (т, 1H), 7,84 (д, 1H), 7,74 (шир.с, 1H), 7,50 (шир.с, 1H), 7,48 (т, 1H), 7,42 (т, 1H), 7,37 (с, 1H), 7,20 (м, 4H), 3,85-3,42 (м, 8H), 3,42 (с, 2H), 1,21 (с, 6H) м.д.
Пример 39
Получение 4-(2-(дифторметил)-1H-бензо[d]имидазол-1-ил)-N-(2-метил-1-(2-(1-метил-1H-пиразол-4-ил)фенил)пропан-2-ил)-6-морфолино-1,3,5-триазин-2-амина A 45
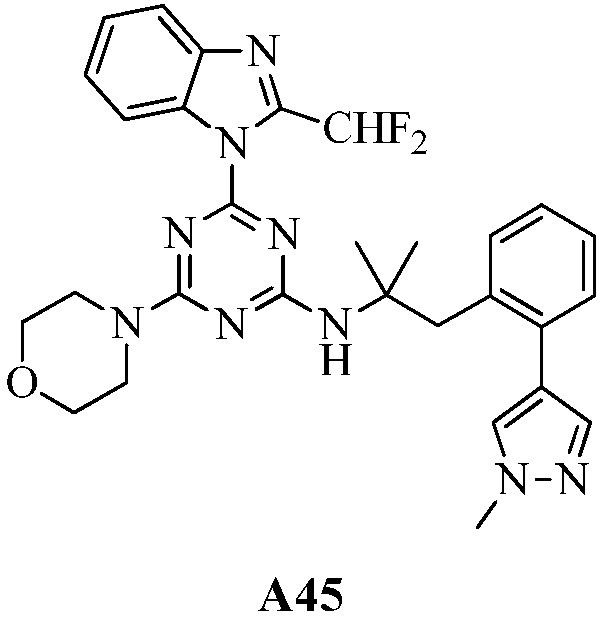
Соединение A45 получали, согласно способу для A33, применяя пинаколовый эфир 1-метил-1H-пиразол-4-бороновой кислоты вместо пиридинил-4-бороновой кислоты. Сырой продукт очищали препаративной ВЭЖХ, получая соединение A45 (35 мг, выход 12%) в виде белого твердого остатка: чистота 98% (ВЭЖХ); MC m/z: 560,3 (M+1);
1Н-ЯМР (CDCl3, 500 МГц) δ 8,38 (д, 1H), 7,91 (д, 1H), 7,65 (т, 1H), 7,51 (с, 1H), 7,48-7,37 (м, 2H), 7,34 (с, 1H), 7,28-7,17 (м, 4H), 5,04 (с, 1H), 3,95-3,78 (м, 11H), 3,40 (с, 2H), 1,35 (с, 6H) м.д.
Пример 40
Получение 4-(2-(дифторметил)-1H-бензо[d]имидазол-1-ил)-N-(2-метил-1-(2-(1-метил-1H-пиразол-5-ил)фенил)пропан-2-ил)-6-морфолино-1,3,5-триазин-2-амина A 46
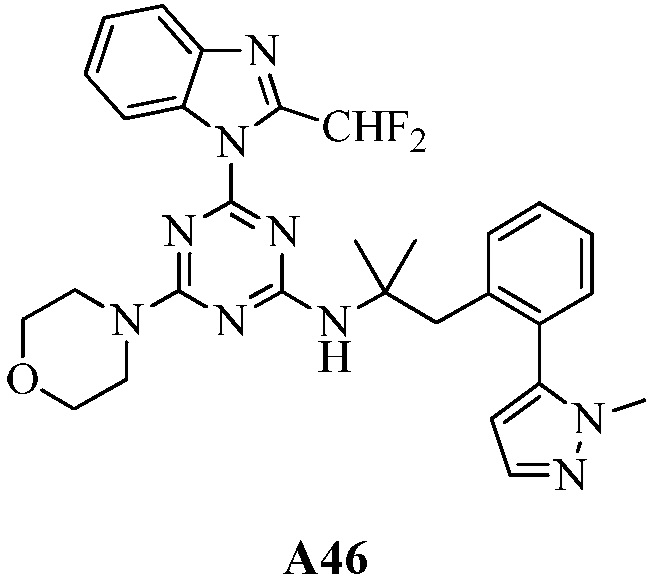
Соединение A46 получали, согласно способу для A33, применяя пинаколовый эфир 1-метил-1H-пиразол-5-бороновой кислоты вместо пиридинил-4-бороновой кислоты. Сырой продукт очищали препаративной ВЭЖХ, получая соединение A46 (7 мг, выход 4%) в виде белого твердого остатка: чистота 98% (ВЭЖХ); MC m/z: 560,3 (M+1);
1Н-ЯМР (CDCl3, 500 МГц) δ 8,40 (д, 1H), 7,91 (д, 1H), 7,67 (т, 1H), 7,50-7,30 (м, 5H), 7,24 (т, 2H), 6,21 (с, 1H), 5,03 (с, 1H), 3,96-3,75 (м, 8H), 3,65 (с, 3H), 3,21 (с, 2H), 1,32 (с, 6H) м.д.
Пример 41
Получение 4-(2-(дифторметил)-1H-бензо[d]имидазол-1-ил)-N-(1-(2 ' -фторбифенил-2-ил)-2-метилпропан-2-ил)-6-морфолино-1,3,5-триазин-2-амина A59
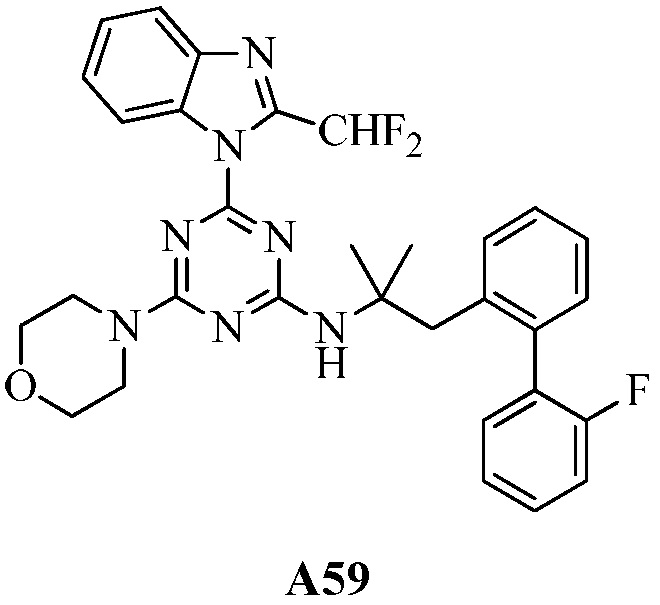
Соединение A59 получали, согласно способу для A33, применяя 2-фторфенилбороновую кислоту вместо пиридинил-4-бороновой кислоты. Сырой продукт очищали препаративной ВЭЖХ, получая соединение A59 (73 мг, выход 71%) в виде белого твердого остатка: чистота 99% (ВЭЖХ); MC m/z: 574,2 (M+1);
1Н-ЯМР (ДМСО-d6, 500 МГц) δ 8,61 (д, 1H), 8,02 (т, 1H), 7,84 (д, 1H), 7,48 (т, 1H), 7,43 (т, 1H), 7,39-7,22 (м, 5H), 7,22 (т, 1H), 7,14 (м, 2H), 6,97 (т, 1H), 3,74 (м, 8H), 3,30 (д, 1H), 3,14 (д, 1H), 1,20 (с, 3H), 1,17 (с, 3H) м.д.
Пример 42
Получение 4-(2-(дифторметил)-1H-бензо[d]имидазол-1-ил)-N-(2-метил-1-(2 ' -метилбифенил-2-ил)пропан-2-ил)-6-морфолино-1,3,5-триазин-2-амина A60
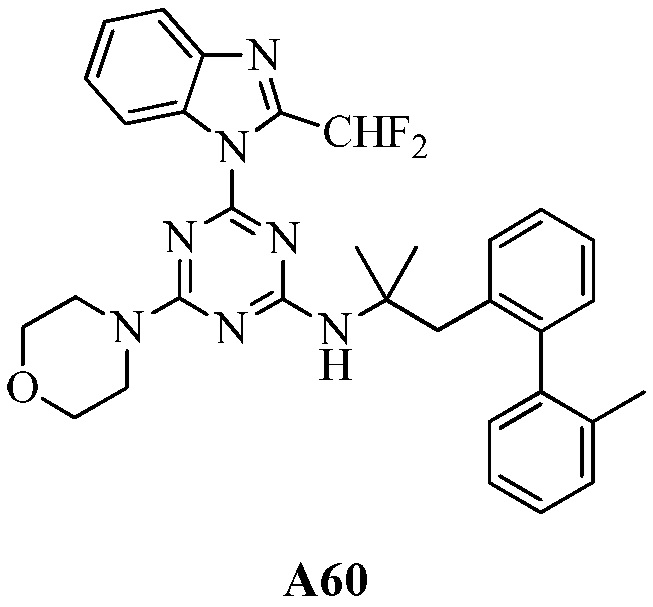
Соединение A60 получали, согласно способу для A33, применяя 2-метилфенилбороновую кислоту вместо пиридинил-4-бороновой кислоты. Сырой продукт очищали препаративной ВЭЖХ, получая соединение A60 (120 мг, выход 47%) в виде белого твердого остатка: чистота 99% (ВЭЖХ); MC m/z: 570,3 (M+1);
1Н-ЯМР (CDCl3, 500 МГц) δ 8,42 (д, 1H), 7,92 (д, 1H), 7,68 (т, 1H), 7,44 (м, 2H), 7,35-6,95 (м, 8H), 5,01 (с, 1H), 4,10-3,70 (м, 8H), 3,30 (д, 1H), 2,99 (д, 1H), 2,06 (с, 3H), 1,36 (с, 3H), 1,30 (с, 3H) м.д.
Пример 43
Получение 4-(2-(дифторметил)-1H-бензо[d]имидазол-1-ил)-N-(1-(6 ' -хлорбифенил-2-ил)-2-метилпропан-2-ил)-6-морфолино-1,3,5-триазин-2-амина A61
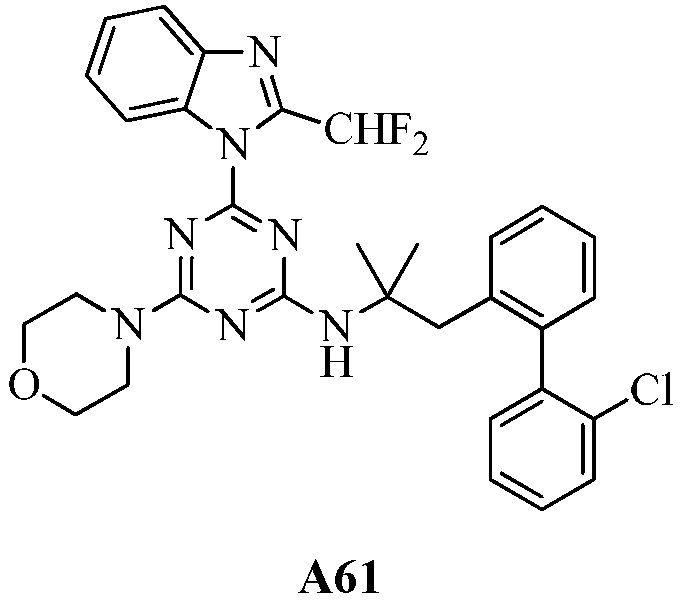
Соединение A61 получали, согласно способу для A33, применяя 2-хлорфенилбороновую кислоту вместо пиридинил-4-бороновой кислоты. Сырой продукт очищали препаративной ВЭЖХ, получая соединение A61 (88 мг, выход 55%) в виде белого твердого остатка: чистота 99% (ВЭЖХ); MC m/z: 590,2 (M+1);
1Н-ЯМР (CDCl3, 500 МГц) δ 7,92 (д, 1H), 7,67 (т, 1H), 7,44 (м, 2H), 7,33 (м, 3H), 7,27-7,00 (м, 5H), 4,96 (с, 1H), 4,00-3,75 (м, 8H), 3,24 (д, 2H), 1,33 (с, 6H) м.д.
Пример 44
Получение 4-(2-(дифторметил)-1H-бензо[d]имидазол-1-ил)-N-(1-(6 ' -хлорбифенил-2-ил)-2-метилпропан-2-ил)-6-морфолино-1,3,5-триазин-2-амина A62
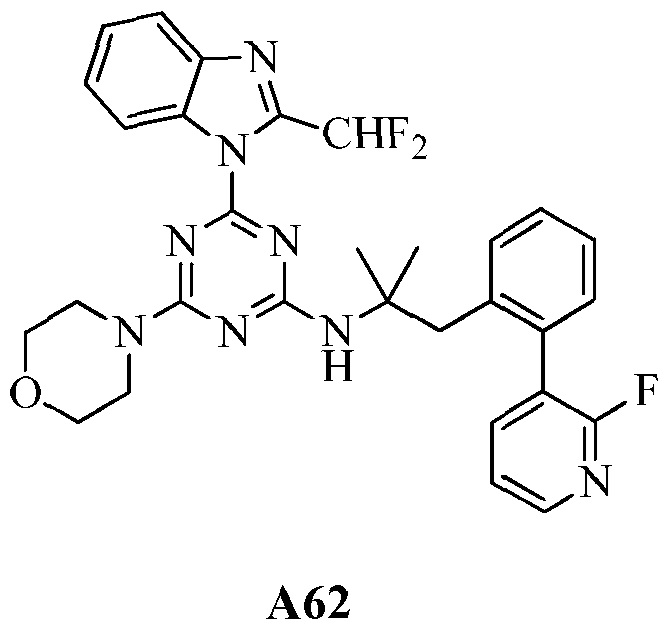
Соединение A62 получали, согласно способу для A33, применяя 2-фтор-3-пиридинилбороновую кислоту вместо пиридинил-4-бороновой кислоты. Сырой продукт очищали препаративной ВЭЖХ, получая соединение A62 (134 мг, выход 65%) в виде белого твердого остатка: чистота 96% (ВЭЖХ); MC m/z: 575,3 (M+1);
1Н-ЯМР (CDCl3, 500 МГц) δ 8,38 (д, 1H), 8,05 (д, 1H), 7,92 (д, 1H), 7,66 (т, 1H), 7,62 (м, 1H), 7,49-7,32 (м, 4H), 7,28 (д, 1H), 7,15 (д, 1H), 6,91 (т, 1H), 4,80 (с, 1H), 4,05-3,70 (м, 8H), 3,60 (д, 1H), 2,99 (д, 1H), 1,42 (с, 3H), 1,27 (с, 3H) м.д.
Пример 45
Получение 4-(2-(дифторметил)-1H-бензо[d]имидазол-1-ил)-N-(2-метил-1-(2-(пиримидин-5-ил)фенил)пропан-2-ил)-6-морфолино-1,3,5-триазин-2-амина A63
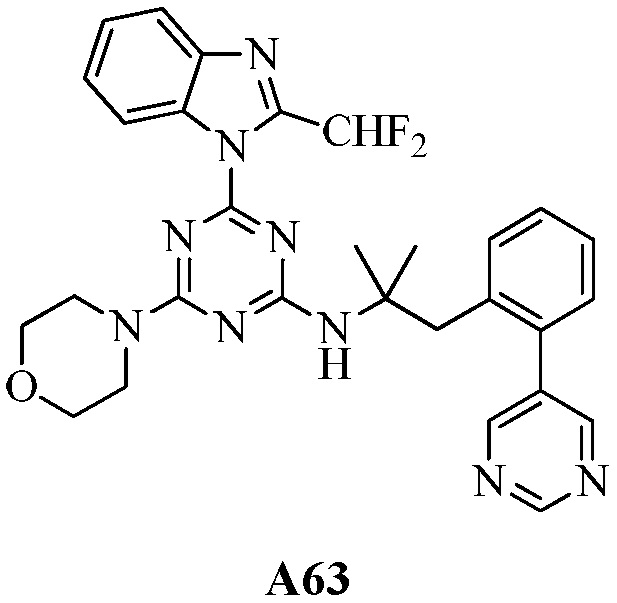
Соединение A63 получали, согласно способу для A33, применяя пинаколовый эфир пиримидин-5-бороновой кислоты вместо пиридинил-4-бороновой кислоты. Сырой продукт очищали препаративной ВЭЖХ, получая соединение A63 (75 мг, выход 50%) в виде белого твердого остатка: чистота 98% (ВЭЖХ); MC m/z: 558,3 (M+1);
1Н-ЯМР (CDCl3, 500 МГц) δ 9,05 (с, 1H), 8,62 (с, 2H), 8,36 (д, 1H), 7,90 (д, 1H), 7,65 (т, 1H), 7,50-7,27 (м, 5H), 7,16 (д, 1H), 4,86 (с, 1H), 3,95-3,80 (м, 8H), 3,34 (с, 2H), 1,32 (с, 6H) м.д.
Пример 46
Получение 4-(2-(дифторметил)-1H-бензо[d]имидазол-1-ил)-N-(2-метил-1-(2-(2-(4-метилпиперазин-1-ил)пиридин-4-ил)фенил)пропан-2-ил)-6-морфолино-1,3,5-триазин-2-амина A64
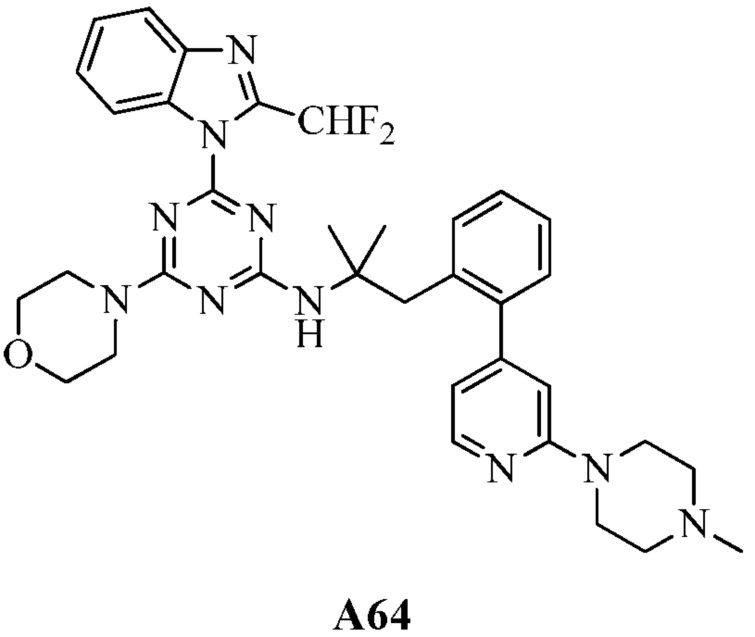
Соединение A64 получали, согласно способу для A33, применяя пинаколовый эфир 2-(4-метилпиперазин-1-ил)пиридин-4-бороновой кислоты вместо пиридинил-4-бороновой кислоты. Сырой продукт очищали препаративной ВЭЖХ, получая соединение A64 (24 мг, выход 20%) в виде белого твердого остатка: чистота 98% (ВЭЖХ); MC m/z: 655,4 (M+1);
1Н-ЯМР (ДМСО-d6, 500 МГц) δ 8,58 (д, 1H), 7,99 (т, 1H), 7,96 (д, 1H), 7,84 (д, 1H), 7,48 (т, 1H), 7,43 (т, 1H), 7,37 (д, 1H), 7,35-7,22 (м, 3H), 7,21 (с, 1H), 7,07 (д, 1H), 6,58 (д, 1H), 3,82-3,62 (м, 8H), 3,37 (с, 2H), 3,26 (шир.с, 4H), 2,25 (шир.с, 4H), 2,16 (с, 3H), 1,23 (с, 6H) м.д.
Пример 47
Получение 4-(2-(дифторметил)-1H-бензо[d]имидазол-1-ил)-N-(2-метил-1-(3 ' -(морфолинометил)бифенил-2-ил)пропан-2-ил)-6-морфолино-1,3,5-триазин-2-амина A65
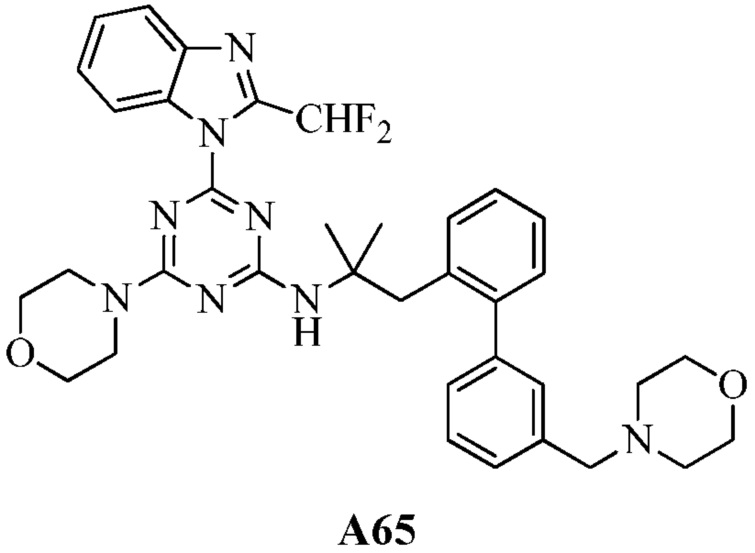
Соединение A65 получали, согласно способу для A33, применяя пинаколовый эфир 3-(морфолинометил)фенилбороновой кислоты вместо пиридинил-4-бороновой кислоты. Сырой продукт очищали препаративной ВЭЖХ, получая соединение A65 (40 мг, выход 17%) в виде белого твердого остатка: чистота 99% (ВЭЖХ); MC m/z: 655,3 (M+1);
1Н-ЯМР (CDCl3, 500 МГц) δ 8,39 (д, 1H), 7,91 (д, 1H), 7,64 (т, 1H), 7,43 (м, 2H), 7,35-7,10 (м, 8H), 4,97 (с, 1H), 3,93-3,74 (м, 8H), 3,68 (м, 4H), 3,50-3,32 (м, 4H), 2,38 (м, 4H), 1,23 (с, 6H) м.д.
Пример 48
Получение 4-(2-(дифторметил)-1H-бензо[d]имидазол-1-ил)-N-(1-(3 ' -метоксибифенил-2-ил)-2-метилпропан-2-ил)-6-морфолино-1,3,5-триазин-2-амина A66
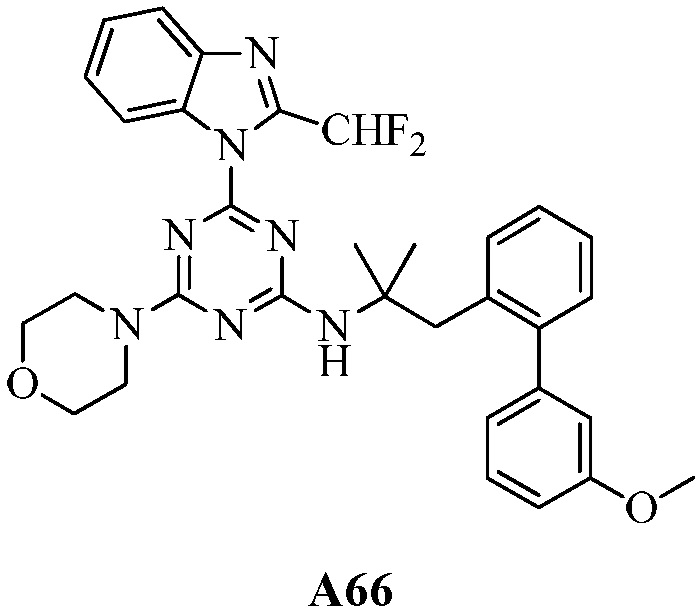
Соединение A66 получали, согласно способу для A33, применяя 3-метоксифенилбороновую кислоту вместо пиридинил-4-бороновой кислоты. Сырой продукт очищали препаративной ВЭЖХ, получая соединение A66 (18 мг, выход 11%) в виде белого твердого остатка: чистота 99% (ВЭЖХ); MC m/z: 586,3 (M+1);
1Н-ЯМР (CDCl3, 500 МГц) δ 8,39 (д, 1H), 7,91 (д, 1H), 7,65 (т, 1H), 7,43 (м, 2H), 7,29 (м, 2H), 7,27-7,17 (м, 3H), 6,88-6,70 (м, 3H), 4,90 (с, 1H), 3,95-3,75 (м, 8H), 3,55 (с, 1H) 3,38 (с, 2H), 1,32 (с, 6H) м.д.
Пример 49
Получение 4-(2-(дифторметил)-1H-бензо[d]имидазол-1-ил)-N-(1-(4 ' -метоксибифенил-2-ил)-2-метилпропан-2-ил)-6-морфолино-1,3,5-триазин-2-амина A67
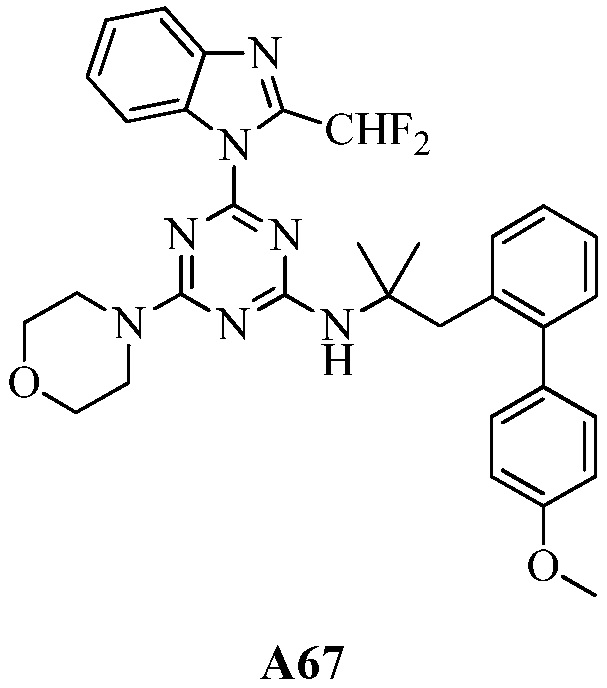
Соединение A67 получали, согласно способу для A33, применяя 4-метоксифенилбороновую кислоту вместо пиридинил-4-бороновой кислоты. Сырой продукт очищали препаративной ВЭЖХ, получая соединение A67 (83 мг, выход 39%) в виде белого твердого остатка: чистота 99% (ВЭЖХ); MC m/z: 586,2 (M+1);
1Н-ЯМР (ДМСО-d6, 500 МГц) δ 8,61 (д, 1H), 7,85 (т, 1H), 7,84 (д, 1H), 7,49 (т, 1H), 7,43 (т, 1H), 7,30-7,19 (м, 4H), 7,08-7,02 (м, 3H), 6,73 (д, 2H), 3,82-3,63 (м, 8H), 3,62 (с, 3H), 3,34 (с, 2H), 1,21 (с, 6H) м.д.
Пример 50
Получение 4-(2-(дифторметил)-1H-бензо[d]имидазол-1-ил)-N-(2-метил-1-(2-(пиперидин-4-ил)фенил)пропан-2-ил)-6-морфолино-1,3,5-триазин-2-амина A68
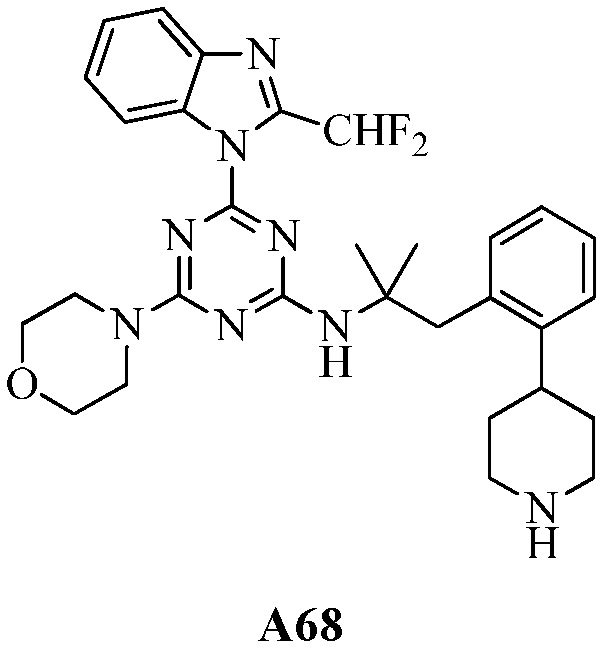
трет-Бутил 4-(2-(2-((4-(2-(дифторметил)-1H-бензо[d]имидазол-1-ил)-6-морфолино-1,3,5-триазин-2-ил)амино)-2-метилпропил)фенил)-5,6-дигидропиридин-1(2H)-карбоксилат получали, согласно способу для A33, применяя пинаколовый эфир N-Boc-1,2,5,6-тетрагидропиридин-4-бороновой кислоты вместо пиридинил-4-бороновой кислоты. Сырой продукт очищали флэш-хроматографией, получая трет-бутил 4-(2-(2-((4-(2-(дифторметил)-1H-бензо[d]имидазол-1-ил)-6-морфолино-1,3,5-триазин-2-ил)амино)-2-метилпропил)фенил)-5,6-дигидропиридин-1(2H)-карбоксилат (270 мг, выход 81%) в виде белого твердого остатка: MC m/z: 586,2 (M+1).
Смесь Boc-защищенного дигидропиридина (215 мг, 0,325 ммоль) и 10% палладия на угле (22 мг) в метаноле перемешивали в атмосфере водорода при 50°C в течение 3 часов. Реакционную смесь фильтровали через целит. Затем фильтрат концентрировали, и остаток очищали флэш-хроматографией, получая 70 мг (выход 33%) трет-бутил 4-(2-(2-((4-(2-(дифторметил)-1H-бензо[d]имидазол-1-ил)-6-морфолино-1,3,5-триазин-2-ил)амино)-2-метилпропил)фенил)пиперидин-1-карбоксилата в виде белого твердого остатка. MC m/z: 663 (M+1).
Смесь Boc-пиперидинового промежуточного соединения (65 мг, 0,098 ммоль) и трифторуксусной кислоты (2 мл) в дихлорметане (2 мл) перемешивали при комнатной температуре в течение 2 часов. Летучие компоненты удаляли при пониженном давлении. Остаток разбавляли водой и подщелачивали при 0°C 1 M гидроксидом натрия до pH~8 и экстрагировали дихлорметаном. Объединенные экстракты сушили над сульфатом натрия и концентрировали. Сырой продукт очищали препаративной ВЭЖХ, получая соединение A68 (12 мг, выход 22%) в виде белого твердого остатка: чистота 98% (ВЭЖХ); MC m/z: 563,3 (M+1);
1Н-ЯМР (CDCl3, 500 МГц) δ 8,37 (д, 1H), 7,89 (д, 1H), 7,66 (т, 1H), 7,41 (м, 2H), 7,33 (д, 1H), 7,28 (т, 1H), 7,16 (т, 1H), 7,07 (д, 1H), 5,16 (с, 1H), 4,00-3,70 (м, 8H), 3,37 (м, 2H), 3,23 (с, 2H), 3,04 (м, 2H), 2,76 (м, 2H), 2,03 (м, 2H), 1,80 (м, 2H), 1,52 (с, 6H) м.д.
Пример 51
Получение 4-(2-(дифторметил)-1H-бензо[d]имидазол-1-ил)-N-(2-метил-1-(2-(1-метилпиперидин-4-ил)фенил)пропан-2-ил)-6-морфолино-1,3,5-триазин-2-амина A 35
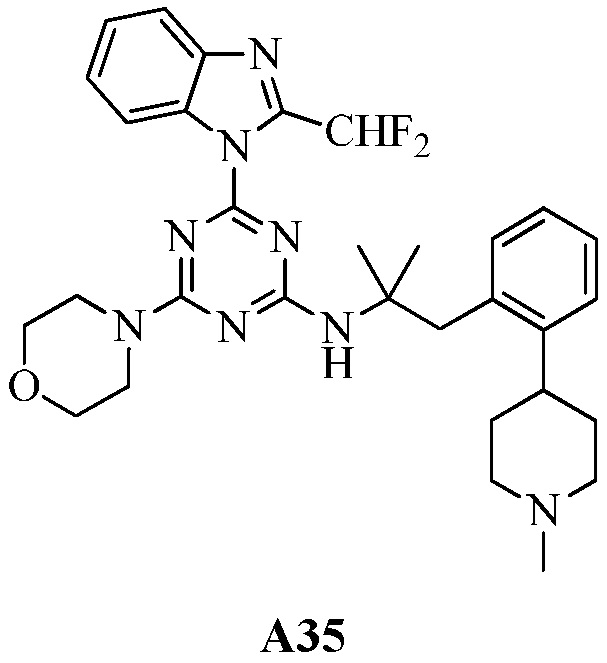
Смесь соединения A35 (80 мг, 0,14 ммоль), водного формальдегида (37%, 23 мг) и цианоборгидрида натрия (11 мг, 0,17 ммоль) в метаноле (2 мл) перемешивали при комнатной температуре в течение 1 часа. Сырой продукт очищали препаративной ВЭЖХ, получая соединение A35 (11 мг, выход 13%) в виде белого твердого остатка: чистота 99% (ВЭЖХ); MC m/z: 577,3 (M+1);
1Н-ЯМР (CDCl3, 500 МГц) δ 8,37 (д, 1H), 7,90 (д, 1H), 7,64 (т, 1H), 7,42 (м, 2H), 7,32 (д, 1H), 7,24 (т, 1H), 7,13 (т, 1H), 7,07 (д, 1H), 5,15 (с, 1H), 4,00-3,70 (м, 8H), 3,28 (с, 2H), 2,94 (м, 2H), 2,78 (м, 2H), 2,28 (с, 3H), 1,89-1,60 (м, 6H), 1,53 (с, 6H) м.д.
Пример 52
Получение 4-(2-(дифторметил)-1H-бензо[d]имидазол-1-ил)-N-(1-(2-(1-этилпиперидин-4-ил)фенил)-2-метилпропан-2-ил)-6-морфолино-1,3,5-триазин-2-амина A70
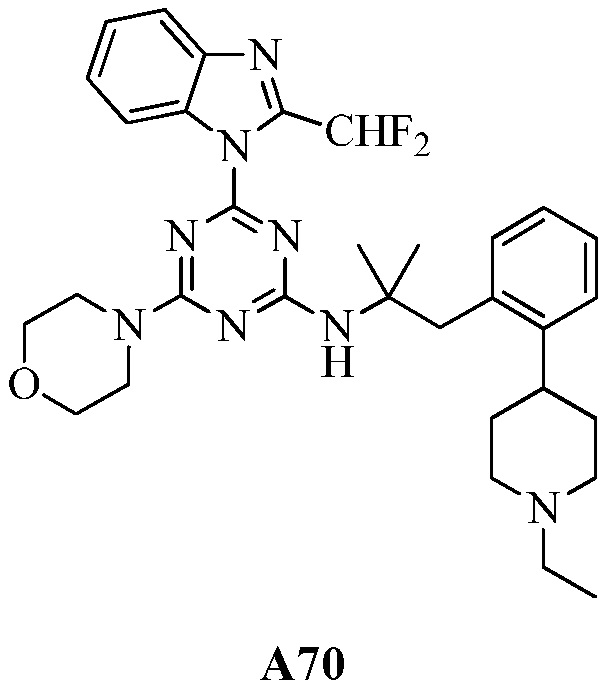
Смесь соединения A68 (0,14 г, 0,25 ммоль), цианоборгидрида натрия (19 мг, 0,30 ммоль), 40% водного ацетальдегида (2 мл) и диизопропилэтиламина (0,16 г, 1,2 ммоль) в ацетонитриле (10 мл) перемешивали при комнатной температуре в течение 1 часа. Реакционную смесь концентрировали в вакууме, и остаток очищали препаративной ВЭЖХ, получая соединение A70 (35 мг, выход 24%) в виде белого твердого остатка: чистота 99% (ВЭЖХ); MC m/z: 591,3 (M+1);
1Н-ЯМР (CDCl3, 500 МГц) δ 8,37 (д, 1H), 7,90 (д, 1H), 7,64 (т, 1H), 7,41 (м, 2H), 7,35 (д, 1H), 7,24 (т, 1H), 7,13 (т, 1H), 7,07 (д, 1H), 5,17 (с, 1H), 4,00-3,71 (м, 8H), 3,28 (с, 2H), 3,08 (м, 2H), 2,85 (м, 1H), 2,46 (м, 2H), 1,91 (м, 4H), 1,70 (м, 2H), 1,53 (с, 6H), 1,11 (т, 3H) м.д.
Пример 53
Получение 4-(2-(дифторметил)-1H-бензо[d]имидазол-1-ил)-N-(1-(2-(1-изопропилпиперидин-4-ил)фенил)-2-метилпропан-2-ил)-6-морфолино-1,3,5-триазин-2-амина A71
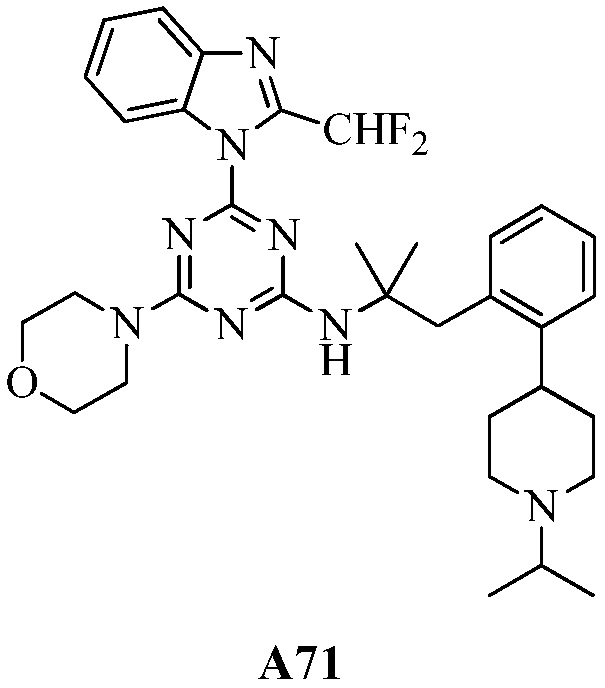
Смесь соединения A68 (70 мг, 0,12 ммоль), ацетона (2 мл), изопропанола (2 мл) и ледяной уксусной кислоты (38 мг, 0,62 ммоль) в герметично закрытой пробирке перемешивали при 120°C в течение 2 часов. После охлаждения смеси до комнатной температуры добавляли боргидрид натрия (24 мг, 0,62 ммоль), и смесь в герметично закрытой пробирке перемешивали при 80°C в течение следующих 3 часов. Реакционную смесь подщелачивали насыщенным водным бикарбонатом натрия до pH 8. Летучие компоненты удаляли при пониженном давлении, и остаток очищали препаративной ВЭЖХ, получая соединение A70 (40 мг, выход 53%) в виде белого твердого остатка: чистота 97% (ВЭЖХ); MC m/z: 605,3 (M+1);
1Н-ЯМР (CDCl3, 500 МГц) δ 8,38 (д, 1H), 7,91 (д, 1H), 7,64 (т, 1H), 7,49-7,35 (м, 3H), 7,24 (т, 1H), 7,13 (т, 1H), 7,07 (д, 1H), 5,15 (с, 1H), 4,01-3,73 (м, 8H), 3,28 (с, 2H), 2,97 (м, 2H), 2,80 (м, 2H), 2,05 (м, 2H), 1,78 (м, 2H), 1,70 (м, 2H), 1,53 (с, 6H), 1,04 (с, 6H) м.д.
Пример 54
Получение 4-(2-(дифторметил)-1H-бензо[d]имидазол-1-ил)-N-(2-метил-1-(2-(1-ацетилпиперидин-4-ил)фенил)пропан-2-ил)-6-морфолино-1,3,5-триазин-2-амина A72
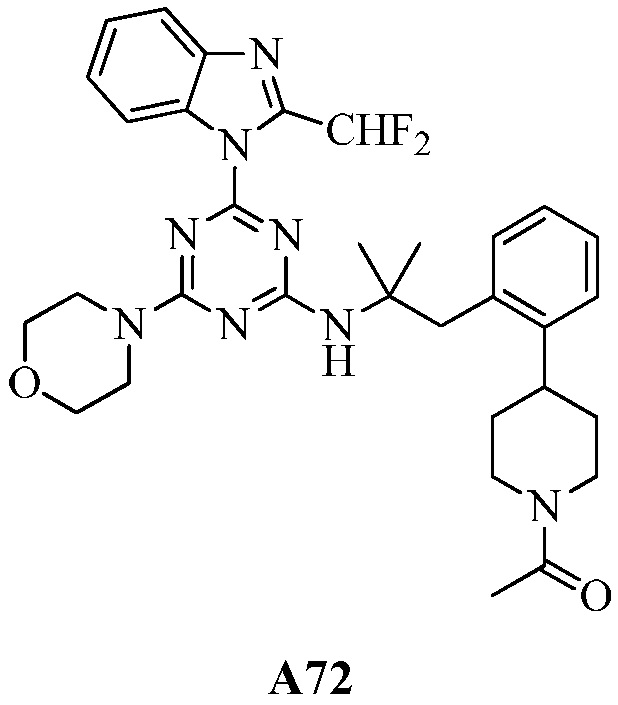
Смесь соединения A68 (50 мг, 0,089 ммоль), ацетилбромида (22 мг, 0,18 ммоль) и триэтиламина (27 мг, 0,27 ммоль) в дихлорметане (2 мл) перемешивали при комнатной температуре в течение 2 часов. Летучие компоненты удаляли в вакууме, и остаток очищали препаративной ВЭЖХ, получая соединение A72 (26 мг, выход 48%) в виде белого твердого остатка: чистота 99% (ВЭЖХ); MC m/z: 605,3 (M+1);
1Н-ЯМР (CDCl3, 500 МГц) δ 8,36 (д, 1H), 7,91 (д, 1H), 7,64 (т, 1H), 7,42 (м, 2H), 7,28-7,20 (м, 2H), 7,15 (т, 1H), 7,08 (д, 1H), 5,15 (с, 1H), 4,78 (м, 1H), 4,00-3,74 (м, 9H), 3,42 (д, 1H), 3,20 (д, 1H), 3,05 (м, 1H), 2,97 (м, 1H), 2,48 (м, 1H), 2,10 (с, 3H), 1,79-1,58 (м, 4H), 1,57 (с, 3H), 1,50 (с, 3H) м.д.
Пример 55
Получение 4-(2-(дифторметил)-1H-бензо[d]имидазол-1-ил)-N-(2-метил-1-(2-(1-(метилсульфонил)пиперидин-4-ил)фенил)пропан-2-ил)-6-морфолино-1,3,5-триазин-2-амина A73
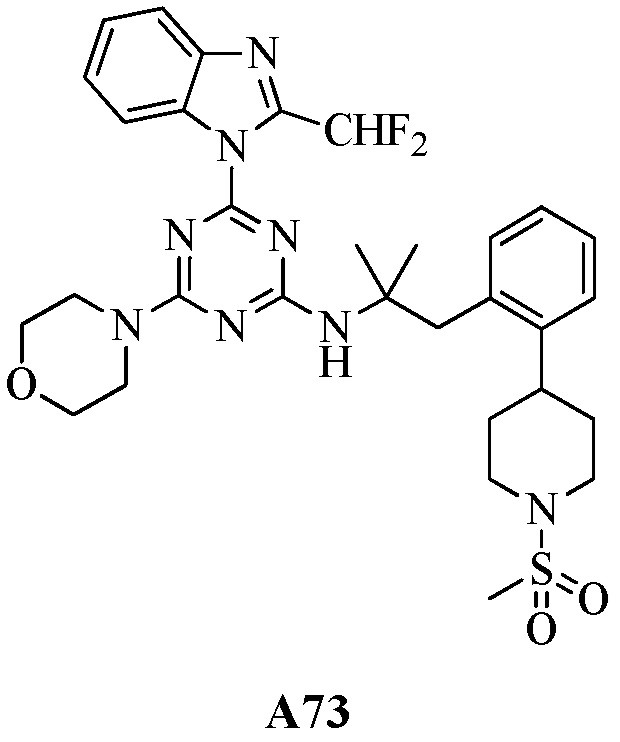
Смесь соединения A68 (50 мг, 0,089 ммоль), метансульфонилхлорида (51 мг, 0,44 ммоль) и триэтиламина (90 мг, 0,89 ммоль) в дихлорметане (4 мл) перемешивали при комнатной температуре в течение 1 часа. Летучие компоненты удаляли в вакууме, и остаток очищали препаративной ВЭЖХ, получая соединение A73 (22 мг, выход 38%) в виде белого твердого остатка: чистота 99% (ВЭЖХ); MC m/z: 641,3 (M+1);
1Н-ЯМР (CDCl3, 500 МГц) δ 8,37 (д, 1H), 7,91 (д, 1H), 7,63 (т, 1H), 7,42 (м, 2H), 7,27 (м, 2H), 7,17 (м, 1H), 7,08 (д, 1H), 5,18 (с, 1H), 3,97-3,71 (м, 10H), 3,29 (с, 2H), 2,92 (м, 1H), 2,76 (с, 3H), 2,59 (м, 2H), 1,90-1,74 (м, 4H), 1,52 (с, 6H) м.д.
Пример 56
Получение 4-(2-(дифторметил)-1H-бензо[d]имидазол-1-ил)-N-(2-метил-1-(2-(пирролидин-3-ил)фенил)пропан-2-ил)-6-морфолино-1,3,5-триазин-2-амина A74
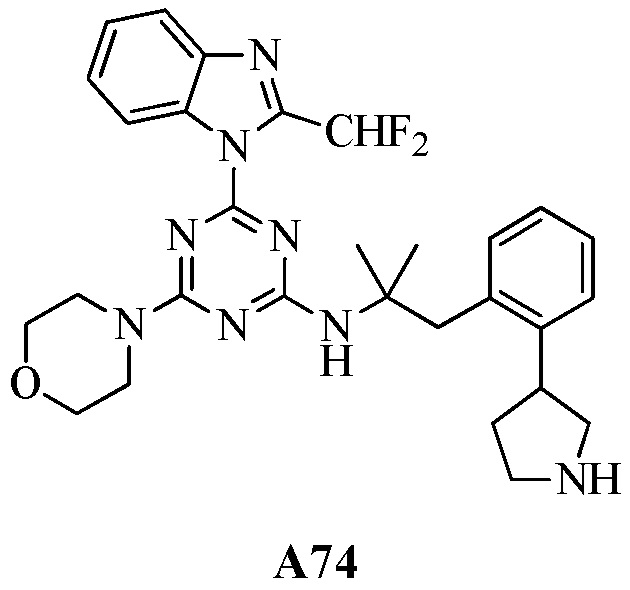
Соединение A74 получали, согласно способу для соединения A68, применяя пинаколовый эфир N-Boc-2,5-дигидропиррол-4-бороновой кислоты вместо пинаколового эфира N-Boc-1,2,5,6-тетрагидропиридин-4-бороновой кислоты. Сырой продукт очищали препаративной ВЭЖХ, получая соединение A74 (13 мг) в виде белого твердого остатка: чистота 92% (ВЭЖХ); MC m/z: 549 (M+1);
1Н-ЯМР (CDCl3, 500 МГц) δ 8,39 (д, 1H), 7,90 (д, 1H), 7,67 (т, 1H), 7,42 (м, 2H), 7,35 (д, 1H), 7,27 (т, 1H), 7,14 (т, 1H), 7,05 (д, 1H), 5,23 (с, 1H), 3,97-3,74 (м, 8H), 3,68 (м, 1H), 3,47-3,25 (м, 4H), 3,17 (м, 1H), 2,93 (м, 1H), 2,25 (м, 1H), 1,92 (м, 1H), 1,51 (с, 6H) м.д.
Пример 57
Получение 4-(2-(дифторметил)-1H-бензо[d]имидазол-1-ил)-N-(2-метил-1-(2-(1-метилпирролидин-3-ил)фенил)пропан-2-ил)-6-морфолино-1,3,5-триазин-2-амина A75
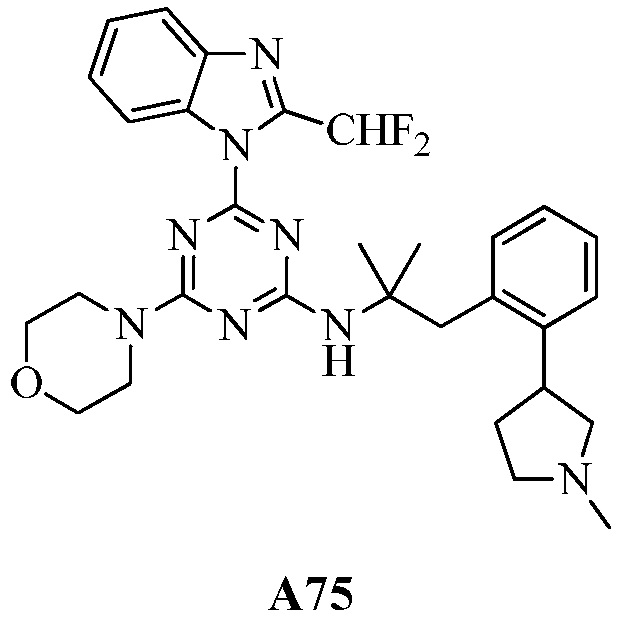
Соединение A75 получали, согласно способу для соединения A69, применяя A74 вместо соединения A68. Сырой продукт очищали препаративной ВЭЖХ, получая соединение A75 (21 мг) в виде белого твердого остатка: чистота 98% (ВЭЖХ); MC m/z: 563,4 (M+1);
1Н-ЯМР (CDCl3, 500 МГц) δ 8,40 (д, J=7,5 Гц, 1H), 7,91 (д, J=7,5 Гц, 1H), 7,65 (т, JHF=53,5 Гц, 1H), 7,50-7,38 (м, 3H), 7,26 (т, J=7,0 Гц, 1H), 7,11 (т, J=7,5 Гц, 1H), 7,01 (д, J=7,5 Гц, 1H), 5,19 (с, 1H), 3,97-3,70 (м, 9H), 3,32 (с, 2H), 2,98 (м, 1H), 2,85 (м, 1H), 2,72 (м, 1H), 2,48 (м, 1H), 2,43 (с, 3H), 2,34 (м, 1H), 1,88 (м, 1H), 1,51 (с, 3H), 1,48 (с, 3H) м.д.
Пример 58
Получение 4-(2-(дифторметил)-1H-бензо[d]имидазол-1-ил)-N-(1-(2-(3-(диметиламино)пропил)фенил)-2-метилпропан-2-ил)-6-морфолино-1,3,5-триазин-2-амина A76
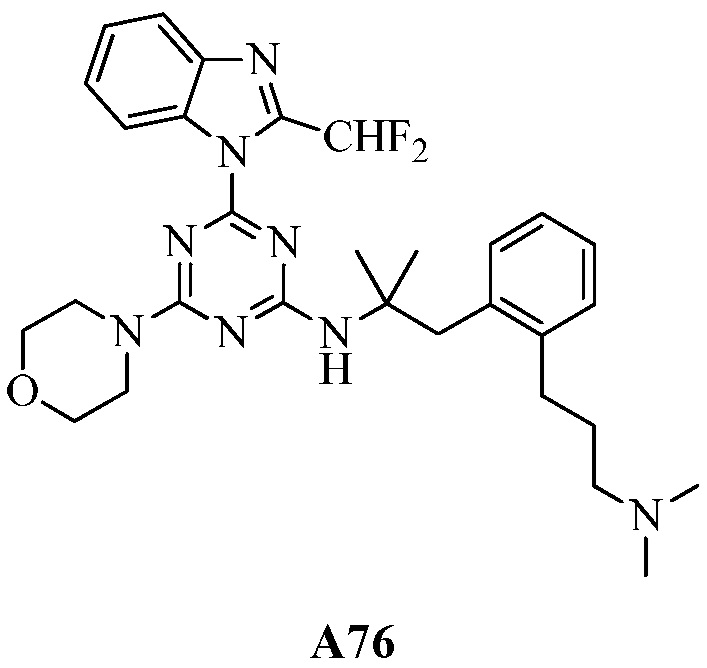
Раствор соединения A17 (0,30 г, 0,54 ммоль), 1-диметиламино-2-пропина (0,13 г, 1,6 ммоль), хлорида бис(трифенилфосфин)палладия(II) (76 мг, 0,11 ммоль) и йодида меди(I) (21 мг, 0,11 ммоль) в N,N'-дициклогексилметиламине (12 мл) перемешивали при 150°C в течение 24 часов. После охлаждения до комнатной температуры смесь разбавляли водой и экстрагировали этилацетатом. Объединенные органические фракции промывали водой, сушили над сульфатом натрия и концентрировали в вакууме, получая неочищенный 4-(2-(дифторметил)-1H-бензо[d]имидазол-1-ил)-N-(1-(2-(3-(диметиламино)проп-1-ин-1-ил)фенил)-2-метилпропан-2-ил)-6-морфолино-1,3,5-триазин-2-амин (200 мг) в виде желтого масла, которое применяли непосредственно на следующей стадии без дополнительной очистки: MC m/z: 561 (M+1).
Смесь неочищенного алкина (120 мг, 0,21 ммоль) и 10% Pd/C (40 мг) в метаноле (30 мл) перемешивали в атмосфере водорода при комнатной температуре в течение ночи. Реакционную смесь фильтровали через целит, и фильтрат концентрировали в вакууме. Остаток очищали препаративной ВЭЖХ, получая соединение A76 (20 мг, выход 17%) в виде белого твердого остатка: чистота 98% (ВЭЖХ); MC m/z: 565,3 (M+1);
1Н-ЯМР (CDCl3, 500 МГц) δ 8,41 (д, 1H), 7,90 (д, 1H), 7,69 (т, 1H), 7,42 (м, 2H), 7,20 (м, 2H), 7,13 (м, 1H), 7,05 (д, 1H), 5,31 (с, 1H), 3,95-3,75 (м, 8H), 3,26 (с, 2H), 2,80-2,24 (м, 10H), 1,88 (м, 2H), 1,51 (с, 6H) м.д.
Пример I
Люминесцентный анализ на основе люциферазы
PI3K катализирует превращение фосфатидилинозитол-4,5-бисфосфата (PIP2) и ATP в фосфатидилинозитол-3,4,5-трисфосфат (PIP3) и ADP. Для всех анализов реакционный буфер состоял из 50 мМ HEPES, pH 7,5, 3 мМ MgCl2, 1 мМ EGTA, 100 мМ NaCl, 0,03% CHAPS и 2 мМ DTT. Соединения для испытания растворяли и последовательно разбавляли в 100% ДМСО (всего 10 концентраций), затем разбавляли 1:25 в реакционном буфере.
Ферментативную активность PI3K-альфа и PI3K-дельта определяли измерением количества ATP, потребленного после киназной реакции, применяя люминесцентный анализ на основе люциферазы (Kinase Glo®, Promega Corp., Madison, WI, USA). Растворы фермента PI3K получали разбавлением PI3K-альфа (Invitrogen Corp., Carlsbad, CA, USA) или PI3K-дельта (Millipore, Billerica, MA, USA) в реакционном буфере до 4× конечной концентрации для анализа (конечные концентрации ферментов составляли 1,65 нМ и 6,86 нМ для PI3K-альфа и PI3K-дельта, соответственно). Раствор субстрата получали смешением PIP2 и ATP в реакционном буфере при 2× конечной концентрации для анализа (конечные концентрации составляли 50 мкм и 25 мкм для PIP2 и ATP, соответственно). 2,5 мкл каждого соединения и киназных смесей добавляли в отдельные лунки белых 384-луночных планшетов с низким объемом для анализа и смешивали встряхиванием. Реакции начинали добавлением 5 мкл субстратной смеси на лунку и встряхиванием. Планшеты для анализа накрывали, и реакции протекали в течение 1 часа (PI3K-альфа) или 2 часов (PI3K-дельта), после чего добавляли 10 мкл реагента Kinase Glo®. Планшеты быстро центрифугировали и выдерживали в течение 10 минут, после чего измеряли люминесценцию, применяя планшет-ридер FlexStation (Molecular Devices, Sunnyvale, CA, USA). Величины IC50 определяли аппроксимацией кривой, применяя программное обеспечение Graphpad Prism (Graphpad Software, La Jolla, CA, USA).
Ферментативную активность PI3K-бета и -гамма определяли измерением количества ADP, полученного после киназной реакции, применяя люминесцентный анализ на основе люциферазы (ADP Glo®, Promega Corp., Madison, WI, USA). Растворы фермента PI3K получали разбавлением PI3K-бета (Millipore, Billerica, MA, USA) или PI3K-гамма (Invitrogen Corp., Carlsbad, CA, USA) в реакционном буфере до 4× конечной концентрации для анализа (конечные концентрации ферментов составляли 4,8 нМ и 7,6 нМ для PI3K-бета и PI3K-гамма, соответственно). Раствор субстрата получали смешением PIP2 и ATP в реакционном буфере при 2× конечной концентрации для анализа (конечные концентрации составляли 50 мкм и 25 мкм для PIP2 и ATP, соответственно). 2,5 мкл каждого соединения и киназных смесей добавляли в отдельные лунки белых 384-луночных планшетов с низким объемом для анализа и смешивали встряхиванием. Реакции начинали добавлением 5 мкл субстратной смеси на лунку и встряхиванием. Планшеты для анализа накрывали, и реакции протекали в течение 1 часа. Затем 5 мкл реакционной смеси переносили в другой белый 384-луночный планшет с небольшим объемом и добавляли 5 мкл реагента ADP-GloTM. Планшеты быстро центрифугировали и выдерживали в течение 40 минут, после чего добавляли 10 мкл буфера для киназной детекции. Затем планшеты быстро центрифугировали, медленно встряхивали и приводили в равновесие при комнатной температуре в течение 30 минут, после чего люминесценцию измеряли, применяя планшет-ридер FlexStation (Molecular Devices, Sunnyvale, CA, USA). Величины IC50 определяли аппроксимацией кривой, применяя программное обеспечение Graphpad Prism (Graphpad Software, La Jolla, CA, USA).
Биологические результаты по ингибированию ферментативной активности PI3K приведены в таблице 1, где A представляет собой величину, не большую чем 100 нМ, B представляет собой величину, большую чем 100 нМ, но меньшую чем 200 нМ, C представляет собой величину, не меньшую чем 200 нМ, но не большую чем 500 нМ, и D представляет собой величину, большую чем 500 нМ; и где A' представляет собой соотношение, большее чем 20, B' представляет собой соотношение, не большее чем 20, но не меньшее чем 10, C' представляет собой соотношение, не большее чем 10, но не меньшее чем 5, и D' представляет собой соотношение, не большее чем 5.
Биологическая активность
В таблице 1 "соотношение α/δ" представляет собой соотношение величины IC50 соединения относительно PK3Kα по сравнению с величиной IC50 того же соединения относительно PK3Kδ; и "стандарт 1" представляет собой N-бензил-4-(2-(дифторметил)-1H-бензо[d]имидазол-1-ил)-6-морфолино-1,3,5-триазин-2-амин.
Пример II
Анализ ELISA для PI3K β
Клеточную активность PI3Kβ определяли измерением фосфорилирования AKT (Ser473), применяя клеточный анализ ELISA. Клетки PC-3 (рак предстательной железы) получали у ATCC (ATCC # CRL-1435). Питательная среда представляла собой DMEM (CellGro # CV-10-013-CV), дополненную 10% фетальной бычьей сывороткой, 100 Ед/мл пенициллина, 100 мкг/мл стрептомицина и 1× MEM заменимых аминокислот. Фосфатно-солевой буферный раствор (PBS) содержал 2,7 M NaCl, 54 мМ KCl, 86 мМ Na3PO4 (двухосновный, безводный), 28 мМ K3PO4 (моноосновный, безводный), pH 7,2. 10× смесь для стимулирования содержала 50 мкм LPA (Cayman # 62215), разбавленного в бессывороточной среде DMEM (CellGro # CV-10-013-CV). Соединения для испытания растворяли и последовательно разбавляли в 100% ДМСО (всего 10 концентраций), затем разбавляли в бессывороточной DMEM до 2× конечной концентрации для анализа. 2× фиксирующий раствор содержал 8% формальдегид (Amresco # M134), разбавленный в PBS. Раствор для пермеабилизации содержал PBS, дополненный 0,1% Triton X-100. Блокирующий буфер получали у LiCor (LiCor # 927-40000). Буфер для промывки содержал PBS, дополненный 0,1% Tween-20. Раствор первичных антител представлял собой кроличье моноклональное антитело анти-pAKTS473 (Cell Signaling # 4060) и мышиный анти-полный S6 (Santa Cruz # 74459), разбавленные 1:500 и 1:2000, соответственно, в блокирующем буфере. Раствор вторичных антител представлял собой IRDye 800CW-конъюгированный козий антикроличий IgG (LiCor # 926-32211) и IRDye 680LT-конъюгированный козий антимышиный IgG (LiCor # 926-68020), разбавленные 1:2000 и 1:1000, соответственно, в блокирующем буфере.
Клетки PC-3 субкультивировали в питательной среде и высевали на плоские 96-луночные планшеты с прозрачным дном (Corning # 3904) при 16000 клеток/лунку, затем выдерживали в течение ночи при 37°C в 5% CO2 инкубаторе. Питательную среду в планшетах заменяли на 100 мкл/лунку бессывороточной DMEM и выдерживали в течение ночи при 37°C в 5% CO2 инкубаторе. Добавляли к планшетам 50 мкл/лунку свежей бессывороточной DMEM. Обработку соединениями осуществляли добавлением к планшетам 50 мкл/лунку 2× смеси соединения и выдерживанием в течение 2 часов при 37°C, 5% CO2, после чего добавляли 11 мкл/лунку 10× смеси для стимулирования, и планшеты выдерживали в течение 10 минут при 37°C, 5% CO2. Фиксацию осуществляли добавлением к планшетам 110 мкл/лунку 2× фиксирующего раствора и выдерживанием в течение 20 минут при комнатной температуре. Пермеабилизацию осуществляли заменой раствора для фиксации 150 мкл/лунку раствором для пермеабилизации и выдерживанием в течение 10 минут при комнатной температуре. Пермеабилизацию повторяли (в сумме 2 раза). Раствор для пермеабилизации заменяли на 100 мкл/лунку блокирующего буфера, и планшеты выдерживали в течение 1 часа при комнатной температуре, после чего добавляли 100 мкл/лунку раствора первичных антител, и планшеты выдерживали в течение ночи при 4°C. Планшеты промывали буфером для промывки, после чего добавляли к планшетам 100 мкл/лунку раствора вторичных антител и выдерживали в темноте в течение 1 часа при комнатной температуре. Планшеты промывали буфером для промывки, с последующей промывкой PBS. После полного удаления PBS, планшеты сканировали на приборе Licor Odyssey для получения изображения. Изображения количественно оценивали, применяя прикладное программное обеспечение Licor Odyssey. Величины IC50 определяли аппроксимацией кривой, применяя базу данных Collaborative Drug Discovery (www.collaborativedrug.com).
Пример III
Анализ ELISA для PI3K δ
Клеточную активность PI3Kδ определяли измерением фосфорилирования AKT (Thr308), применяя сэндвичевый иммуносорбентный ферментный анализ (ELISA). Клетки Раджи (лимфома Беркитта) получали у ATCC (ATCC # CCL-86). Фосфатно-солевой буферный раствор (PBS) содержал 2,7 M NaCl, 54 мМ KCl, 86 мМ Na3PO4 (двухосновный, безводный) и 28 мМ K3PO4 (моноосновный, безводный) при pH 7,2. Буфер для промывки содержал PBS, дополненный 0,05% Tween-20. Блокирующий буфер содержал буфер для промывки, дополненный 1% BSA. 10× смеси для стимулирования содержали 5 мкг/мл античеловеческого антитела IgM (Sigma # I2386), разбавленного в бессывороточной среде RPMI (CellGro # CV-10-040-CV). Соединения для исследования растворяли и последовательно разбавляли в 100% ДМСО (всего 10 концентраций), и затем разбавляли в бессывороточной RPMI до 5× конечной концентрации для анализа.
Клетки Раджи субкультивировали в среде RPMI, дополненной 10% фетальной бычьей сывороткой, 100 Ед/мл пенициллина, 100 мкг/мл стрептомицина и 1× MEM заменимых аминокислот. Планшеты для сэндвичевого ELISA получали нанесением покрытия на 96-луночные планшеты для анализа (Pierce # 15042) 100 мкл/лунку иммобилизованного антитела (Cell Signaling Technology # 7142 или 7144), разбавленного в PBS. Планшеты выдерживали в течение ночи при 4°C, затем промывали буфером для промывки, после чего 200 мкл/лунку блокирующего буфера добавляли к планшетам и выдерживали при комнатной температуре в течение по меньшей мере 2 часов. Клетки Раджи повторно суспендировали в бессывороточной среде RPMI и высевали на 2-мл 96-луночные планшеты с V-образным дном (Corning # 3961) при 106 клеток/лунку, затем выдерживали в течение 2 часов при 37°C в 5% CO2 инкубаторе. Обработку соединениями осуществляли добавлением 5× смеси соединения к клеткам и выдерживанием в течение 2 часов при 37°C, 5% CO2, после чего 10× смесь для стимулирования добавляли к планшетам и выдерживали в течение 30 минут при 37°C, 5% CO2. Клетки осаждали центрифугированием планшетов при 1500 об/мин в течение 5 минут при комнатной температуре. Среду аккуратно удаляли, и клетки лизировали добавлением 100 мкл/лунку буфера для лизиса клеток (Cell Signaling Technology # 9803), дополненного ингибиторами протеаз и фосфатаз (Thermo Fisher # 78443). Планшеты выдерживали на льду в течение 30 минут, затем лизаты (80 мкл для pAKTT308, 10 мкл для всей AKT) переносили в полученные планшеты для анализа и выдерживали при 4°C в течение ночи. После промывки планшетов буфером для промывки, 100 мкл/лунку антитела для детекции (Cell Signaling Technology # 7142 или 7144), разбавленного в блокирующем буфере, добавляли к планшетам и выдерживали в течение 1 часа при 37°C. Планшеты промывали и 100 мкл/лунку HRP-конъюгированного вторичного антитела (Cell Signaling Technology # 7142 или 7144), разбавленного в блокирующем буфере, добавляли к планшетам и выдерживали в течение 1 часа при комнатной температуре. Планшеты промывали буфером для промывки и добавляли к планшетам 100 мкл/лунку люминесцентного субстрата. Через 1 минуту на планшетном шейкере при средней скорости, люминесценцию регистрировали на планшет-ридере Wallac Victor2. Величины IC50 определяли аппроксимацией кривой, применяя базу данных Collaborative Drug Discovery (www.collaborativedrug.com).
Пример IV
Анализ ELISA для PI3K α
Активность PI3K-альфа (PI3Kα) определяли измерением фосфорилирования AKT (Thr308), применяя клеточный анализ ELISA. Клетки MDA-MB-453 (рак молочной железы) получали у ATCC (ATCC # HTB-131). Питательная среда представляла собой DMEM (CellGro # CV-10-013-CV), дополненную 10% фетальной бычьей сывороткой, 100 Ед/мл пенициллина, 100 мкг/мл стрептомицина и 1× MEM заменимых аминокислот. Фосфатно-солевой буферный раствор (PBS) содержал 2,7 M NaCl, 54 мМ KCl, 86 мМ Na3PO4 (двухосновный, безводный) и 28 мМ K3PO4 (моноосновный, безводный) при pH 7,2. Смесь для стимулирования (10×) представляла собой 1000 нг/мл LONG® R3 человеческого IGF-1 (Sigma # I1271), разбавленного в бессывороточной среде DMEM (CellGro # CV-10-013-CV). Соединения для испытания растворяли и последовательно разбавляли в 100% ДМСО (всего 10 концентраций), затем разбавляли в бессывороточной DMEM до 2× конечной концентрации для анализа. Фиксирующий раствор (2×) представлял собой 8% формальдегид (Amresco # M134), разбавленный PBS. Раствор для пермеабилизации представлял собой PBS, дополненный 0,1% Triton X-100. Блокирующий буфер получали у LiCor (LiCor # 927-40000). Буфер для промывки представлял собой PBS, дополненный 0,1% Tween-20. Раствор первичных антител представлял собой кроличье моноклональное антитело анти-pAKTT308 (Cell Signaling # 2965) и мышиный анти-полный S6 (Santa Cruz # 74459), разбавленные 1:500 и 1:2000, соответственно, в блокирующем буфере. Раствор вторичных антител представлял собой IRDye 800CW-конъюгированный козий анти-кроличий IgG (LiCor # 926-32211) и IRDye 680LT-конъюгированный козий анти-мышиный IgG (LiCor # 926-68020), разбавленные 1:1000 и 1:2000, соответственно, в блокирующем буфере.
Клетки MDA-MB-453 субкультивировали в питательной среде и высевали на плоские 96-луночные планшеты с прозрачным дном (Corning # 3904) при 40000 клеток/лунку, затем выдерживали в течение ночи при 37°C в 5% CO2 инкубаторе. Питательную среду в планшетах заменяли 100 мкл/лунку бессыворочной DMEM и выдерживали в течение ночи при 37°C в 5% CO2 инкубаторе. Свежую бессывороточную DMEM (50 мкл/лунку) добавляли к планшетам. Обработку соединениями осуществляли добавлением 50 мкл/лунку 2× смеси соединения к планшетам и выдерживанием в течение 1 часа при 37°C и 5% CO2, после чего добавляли 11 мкл/лунку 10× смеси для стимулирования, и планшеты выдерживали в течение 10 минут при 37°C и 5% CO2. Фиксацию осуществляли добавлением 110 мкл/лунку 2× фиксирующего раствора к планшетам и выдерживанием в течение 20 минут при комнатной температуре. Пермеабилизацию осуществляли заменой раствора для фиксации 150 мкл/лунку раствора для пермеабилизации и выдерживанием в течение 10 минут при комнатной температуре. Пермеабилизацию повторяли (в сумме 2 раза). Раствор для пермеабилизации заменяли на 100 мкл/лунку блокирующего буфера, и планшеты выдерживали в течение 1 часа при комнатной температуре, после чего добавляли 100 мкл/лунку раствора первичных антител, и планшеты выдерживали в течение ночи при 4°C. Планшеты промывали буфером для промывки, после чего 100 мкл/лунку раствора вторичных антител добавляли к планшетам, и выдерживали в темноте в течение 1 часа при комнатной температуре. Планшеты промывали буфером для промывки, с последующей промывкой PBS. После полного удаления PBS, планшеты сканировали на приборе Licor Odyssey для получения изображения. Изображения количественно оценивали, применяя прикладное программное обеспечение Licor Odyssey. Величины IC50 определяли аппроксимацией кривой, применяя базу данных Collaborative Drug Discovery (www.collaborativedrug.com).
Пример V
Анализ ELISA для PI3K γ
Активность PI3K-гамма (PI3Kγ) определяли измерением фосфорилирования AKT (Ser473), применяя клеточный анализ ELISA. Клетки RAW 264.7 (мышиные макрофаги) получали у ATCC (ATCC # TIB-71). Питательная среда представляла собой DMEM (CellGro # CV-10-013-CV), дополненную 10% фетальной бычьей сывороткой, 100 Ед/мл пенициллина, 100 мкг/мл стрептомицина и 1× MEM заменимых аминокислот. Фосфатно-солевой буферный раствор (PBS) содержал 2,7 M NaCl, 54 мМ KCl, 86 мМ Na3PO4 (двухосновный, безводный) и 28 мМ K3PO4 (одноосновный, безводный) при pH 7,2. Смеси для стимулирования (10×) представляли собой 500 нг/мл реакомбинантного человеческого компонента системы комплемента C5a (R&D systems # 2037-C5-025), разбавленного в бессывороточной среде DMEM (CellGro # CV-10-013-CV). Соединения для испытания растворяли и последовательно разбавляли в 100% ДМСО (всего 10 концентраций), затем разбавляли в бессывороточной DMEM до 2× конечной концентрации для анализа. Фиксирующий раствор (2×) представлял собой 8% формальдегид (Amresco # M134), разбавленный в PBS. Раствор для пермеабилизации представлял собой PBS, дополненный 0,1% Triton X-100. Блокирующий буфер получали у LiCor (LiCor # 927-40000). Буфер для промывки представлял собой PBS, дополненный 0,1% Tween-20. Раствор первичных антител представлял собой кроличье моноклональное антитело анти-pAKTS473 (Cell Signaling # 4060) и мышиный анти-полный S6 (Santa Cruz # 74459), разбавленные 1:500 и 1:2000, соответственно, в блокирующем буфере. Раствор вторичных антител представлял собой IRDye 800CW-конъюгированный козий антикроличий IgG (LiCor # 926-32211) и IRDye 680LT-конъюгированный козий антимышиный IgG (LiCor # 926-68020), разбавленные 1:1000 и 1:2000, соответственно, в блокирующем буфере.
Клетки RAW 264.7 субкультивировали в питательной среде и высевали на плоские 96-луночные планшеты с прозрачным дном (Corning # 3904) при 70000 клеток/лунку, затем выдерживали в течение ночи при 37°C в 5% CO2 инкубаторе. Питательную среду в планшетах заменяли на 100 мкл/лунку бессывороточной DMEM и выдерживали в течение ночи при 37°C в 5% CO2 инкубаторе. Свежую бессывороточную DMEM (50 мкл/лунку) добавляли к планшетам. Обработку соединениями осуществляли добавлением 50 мкл/лунку 2× смеси соединения к планшетам и выдерживали в течение 2 часов при 37°C, 5% CO2, после чего добавляли 11 мкл/лунку 10× смеси для стимулирования, и планшеты выдерживали в течение 3 минут при 37°C, 5% CO2. Фиксацию осуществляли добавлением 110 мкл/лунку 2× фиксирующего раствора к планшетам и выдерживанием в течение 20 минут при комнатной температуре. Пермеабилизацию осуществляли заменой раствора для фиксации 150 мкл/лунку раствора для пермеабилизации и выдерживанием в течение 10 минут при комнатной температуре. Пермеабилизацию повторяли (всего 2 раза). Раствор для пермеабилизации заменяли на 100 мкл/лунку блокирующего буфера, и планшеты выдерживали в течение 1 часа при комнатной температуре, после чего добавляли 100 мкл/лунку раствора первичных антител, и планшеты выдерживали в течение ночи при 4°C. Планшеты промывали буфером для промывки, после чего добавляли 100 мкл/лунку раствора вторичных антител к планшетам и выдерживали в темноте в течение 1 часа при комнатной температуре. Планшеты промывали буфером для промывки, с последующей промывкой PBS. После полного удаления PBS, планшеты сканировали на приборе Licor Odyssey для получения изображения. Изображения количественно оценивали, применяя прикладное программное обеспечение Licor Odyssey. Величины IC50 определяли аппроксимацией кривой, применяя базу данных Collaborative Drug Discovery (www.collaborativedrug.com).
Биологические результаты по ингибированию клеточной ферментативной активности PI3K приведены в таблице 2, где каждый A, B, C, D, A', B', C' и D' представляет собой, как определено в таблице 1.
Вышеизложенные примеры приводятся для того, чтобы дать специалисту в данной области техники полное раскрытие и описание того, как получить и применять заявленные варианты осуществления, и не предполагается, что они ограничивают объем того, что описывают в настоящем изобретении. Предполагается, что модификации, которые являются очевидными специалисту в данной области техники, включены в объем следующей формулы изобретения. Все публикации, патенты и патентные заявки, приводимые в настоящем изобретении, включены в настоящее изобретение в качестве ссылки, как если бы указывали, что каждая публикация, патент или патентная заявка специально и отдельно включена в настоящее изобретение в качестве ссылки.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРОИЗВОДНЫЕ БЕНЗИМИДАЗОЛА КАК ИНГИБИТОРЫ ТИРОЗИНКИНАЗ ERBB ДЛЯ ЛЕЧЕНИЯ РАКА | 2015 |
|
RU2741914C2 |
| N1-(4-(5-(ЦИКЛОПРОПИЛМЕТИЛ)-1-МЕТИЛ-1H-ПИРАЗОЛ-4-ИЛ)ПИРИДИН-2-ИЛ)ЦИКЛОГЕКСАН-1,4-ДИАМИНОВЫЕ ПРОИЗВОДНЫЕ И РОДСТВЕННЫЕ СОЕДИНЕНИЯ В КАЧЕСТВЕ ИНГИБИТОРОВ СK1 И/ИЛИ IRAK1 ДЛЯ ЛЕЧЕНИЯ РАКА | 2018 |
|
RU2761457C2 |
| 5,5-КОНДЕНСИРОВАННЫЕ АРИЛЕНОВЫЕ ИЛИ ГЕТЕРОАРИЛЕНОВЫЕ ИНГИБИТОРЫ ВИРУСА ГЕПАТИТА С | 2010 |
|
RU2554087C2 |
| АНТАГОНИСТЫ АРИЛСУЛЬФОНАМИДА CCR3 | 2010 |
|
RU2539591C2 |
| 2,5-ДИЗАМЕЩЕННЫЕ АРИЛСУЛЬФОНАМИДНЫЕ АНТАГОНИСТЫ CCR3 | 2010 |
|
RU2532515C2 |
| КФТР РЕГУЛЯТОРЫ И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2016 |
|
RU2749834C2 |
| КФТР РЕГУЛЯТОРЫ И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2016 |
|
RU2730855C2 |
| КФТР РЕГУЛЯТОРЫ И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2016 |
|
RU2742934C2 |
| ПИРРОЛО[2, 3-В]ПИРИДИНОВЫЕ ПРОИЗВОДНЫЕ В КАЧЕСТВЕ ИНГИБИТОРОВ ПРОТЕИНКИНАЗ | 2006 |
|
RU2418800C2 |
| МОДУЛЯТОРЫ ХЕМОКИНОВОГО РЕЦЕПТОРА И ИХ ПРИМЕНЕНИЕ | 2017 |
|
RU2768827C2 |
Настоящее изобретение относится к новым соединениям формулы I, 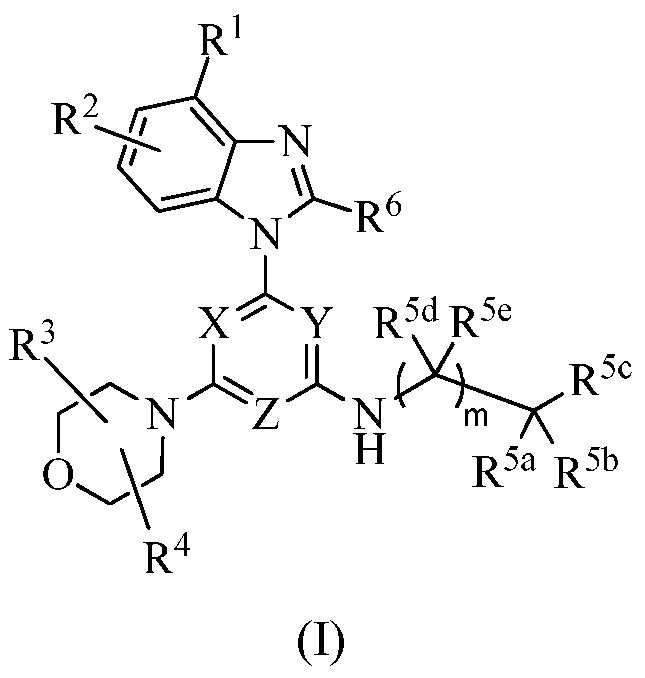 ,
,
обладающим PI3K ферментативной активностью. Технический результат: получены новые соединения формулы I, которые могут быть использованы для регулирования PI3K ферментативной активности, а также фармацевтические композиции на их основе. 3 и 30 з. п. ф-лы, 2 табл., 63 пр., 3 сх.
1. Соединение формулы I:
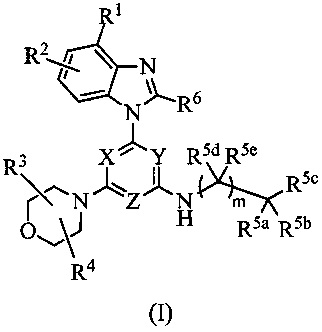
или его энантиомер, смесь энантиомеров, смесь двух или более диастереомеров; или их фармацевтически приемлемая соль; где:
каждый X, Y и Z независимо представляет собой N;
каждый R1 и R2 представляет собой водород;
каждый R3 и R4 представляет собой водород;
R5a представляет собой (а) водород; (b) C1-6 алкил;
R5b представляет собой C1-6 алкил или -C(O)OR1a, где R1a представляет собой C1-6 алкил;
R5c представляет собой -(CR5fR5g)n-(С6-14 арил), где каждая арильная группа в R5c необязательно замещена одним или двумя заместителями Q;
каждый R5f и R5g независимо представляет собой (а) водород; (b) C1-6 алкил; или (с) когда один экземпляр R5f и один экземпляр R5g соединены с одним и тем же атомом углерода, R5f и R5g вместе с атомом углерода, с которым они соединены, образуют С3-10 циклоалкил;
R6 представляет собой C1-6 алкил, замещенный галогеном;
m равно 0; и
n равно 0 или 1;
где каждый алкил необязательно замещен одним или двумя заместителями Q, где каждый заместитель Q независимо выбран из галогена, C1-6 алкила, С6 арила, 6-членного гетероарила, содержащего до 2 атомов азота, и 5-6-членного гетероциклила, содержащего 1 атом азота, каждый из которых дополнительно необязательно замещен одним заместителем Qa;
где каждый Qa независимо выбран из группы, состоящей из галогена, C1-6 алкила, 5-6-членного гетероциклила, содержащего до 2 атомов азота, C1-6 алкиламино, C1-6 алкилсульфонила и -ORe, где Re представляет собой водород или C1-6 алкил.
2. Соединение по п. 1, где каждый R5a и R5b представляет собой метил.
3. Соединение по п. 1, где n равно 1.
4. Соединение по п. 1, где каждый R5f и R5g представляет собой водород.
5. Соединение по п. 1, где n равно 0.
6. Соединение по п. 1, имеющее структуру формулы Ia:
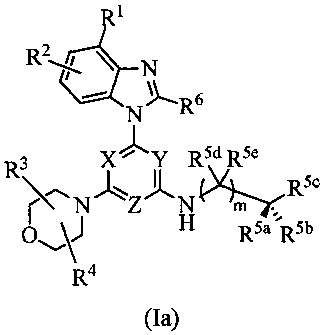 ,
,
или его фармацевтически приемлемая соль.
7. Соединение по п. 1, имеющее структуру формулы Ib:
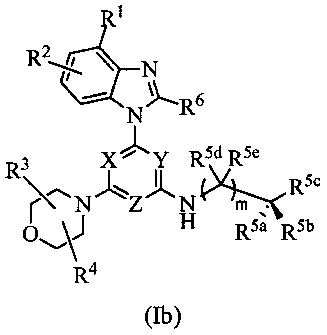 ,
,
или его фармацевтически приемлемая соль.
8. Соединение по п. 1, где R5c представляет собой С6-14 арил, необязательно замещенный одним или двумя заместителями Q.
9. Соединение по п. 8, где R5c представляет собой фенил, необязательно замещенный одним или двумя заместителями Q.
10. Соединение по п. 8, где R5c представляет собой нафтил, необязательно замещенный одним или двумя заместителями Q.
11. Соединение по п. 1, где R5c представляет собой -(CR5fR5g)n-(С6-14 арил), где арил необязательно замещен одним или двумя заместителями Q.
12. Соединение по п. 11, где R5c представляет собой -(СН2)-фенил, где фенил необязательно замещен одним или двумя заместителями Q.
13. Соединение по п. 11, где R5c представляет собой -(СН2)-нафтил, где нафтил необязательно замещен одним или двумя заместителями Q.
14. Соединение по п. 1, где R5a представляет собой водород.
15. Соединение по п. 1, где R5a представляет собой C1-6 алкил.
16. Соединение по п. 1, где R5a представляет собой водород, метил или этил.
17. Соединение по п. 1, где R5b представляет собой C1-6 алкил.
18. Соединение по п. 17, где R5b представляет собой метил или этил.
19. Соединение по п. 1, где R5b представляет собой -C(O)ORla.
20. Соединение по п. 19, где R5b представляет собой -C(O)O-C1-6 алкил.
21. Соединение по п. 20, где R5b представляет собой -С(O)ОСН3.
22. Соединение по п. 1, где R6 представляет собой дифторметил.
23. Соединение по п. 1, выбранное из группы, состоящей из:
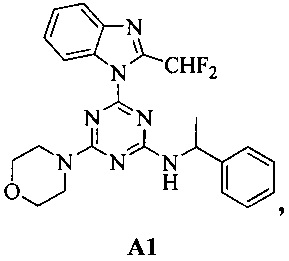
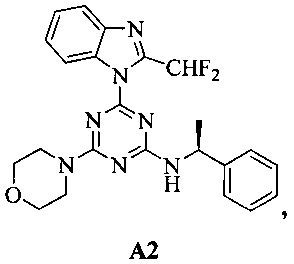
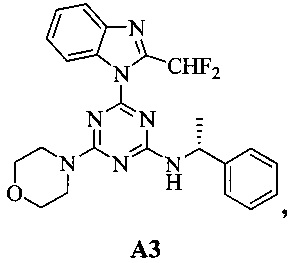
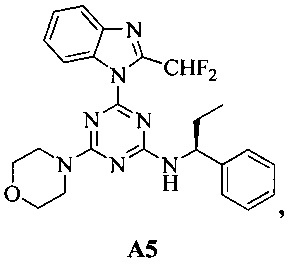
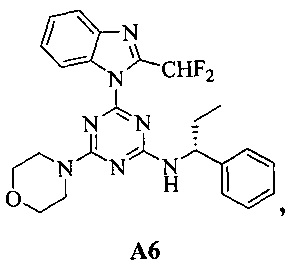
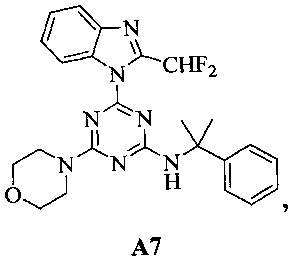
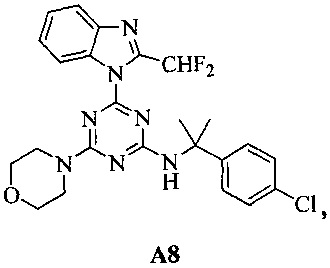
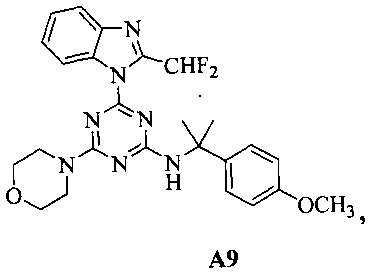
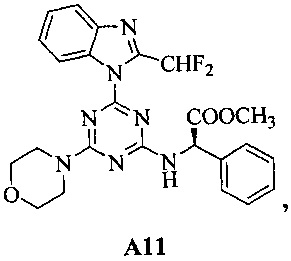
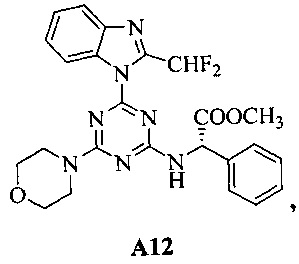
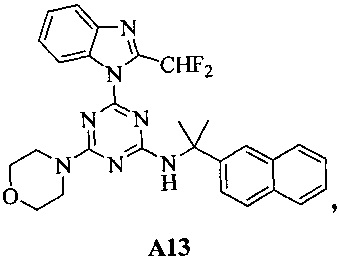
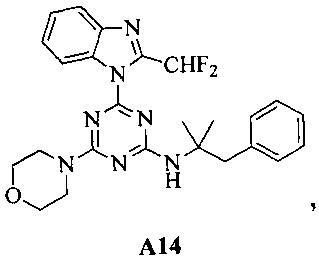
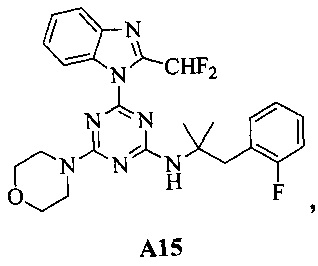
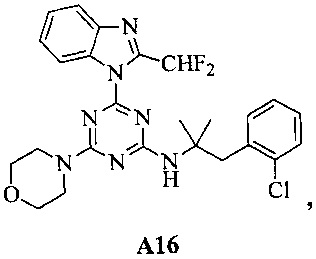
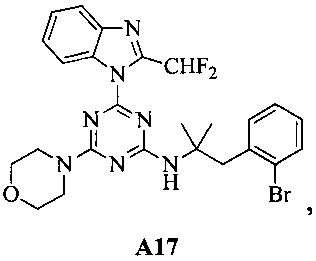
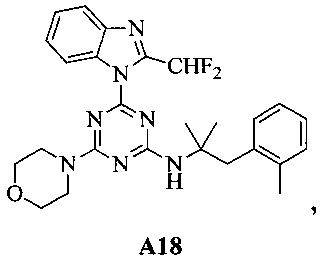
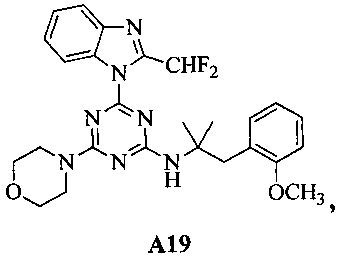
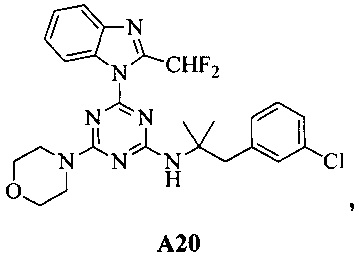
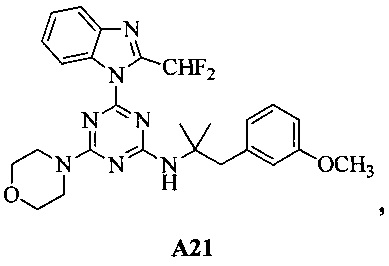
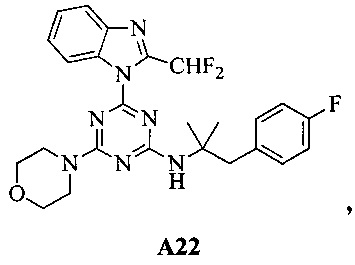
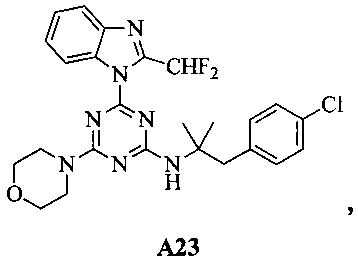
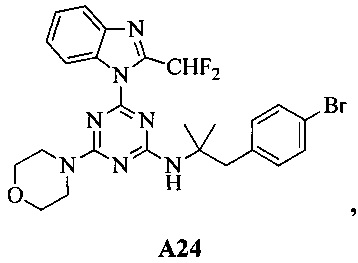
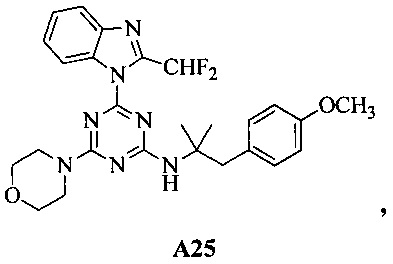
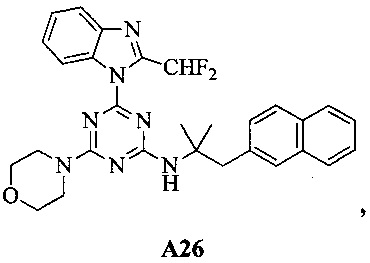
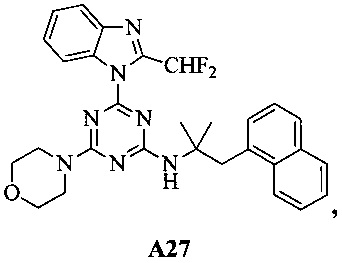
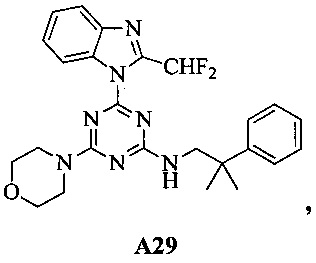
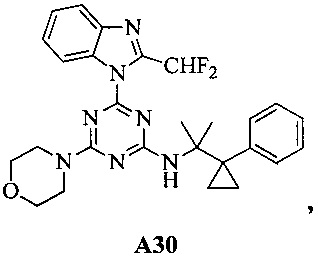
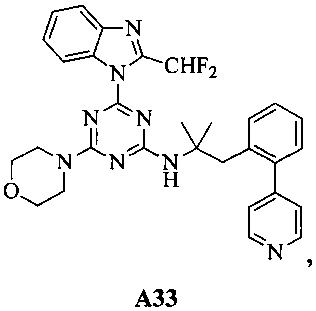
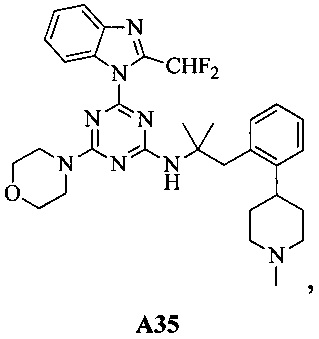
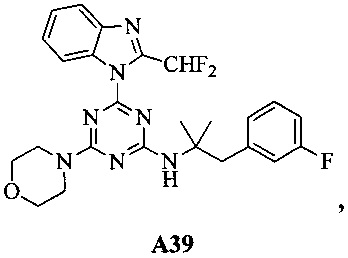
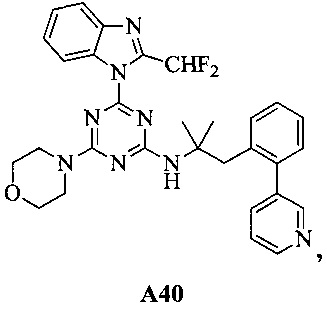
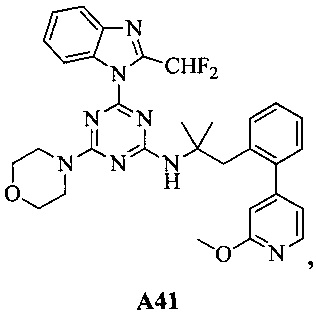
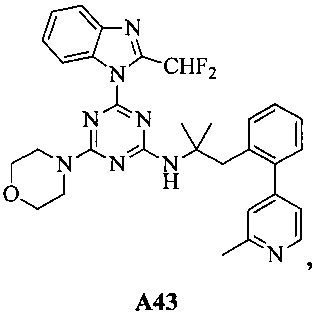
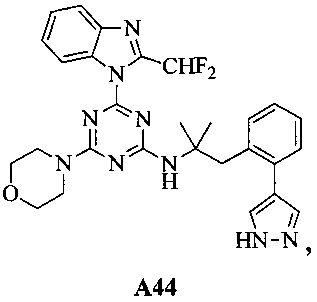
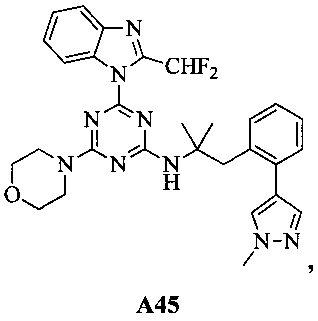
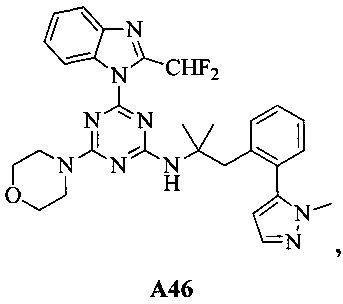
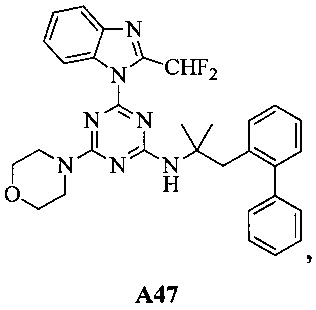
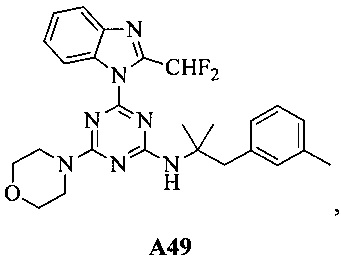
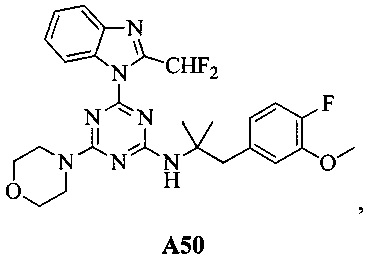
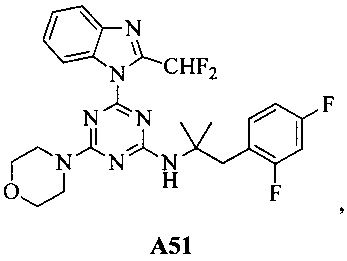
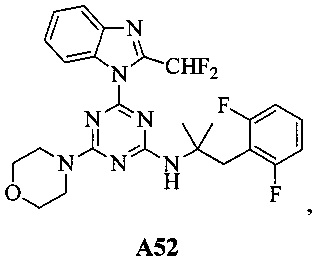
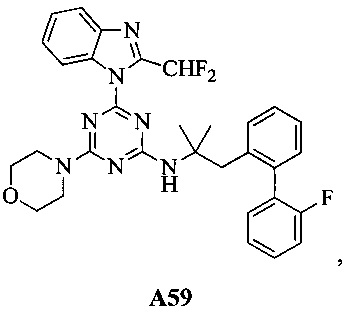
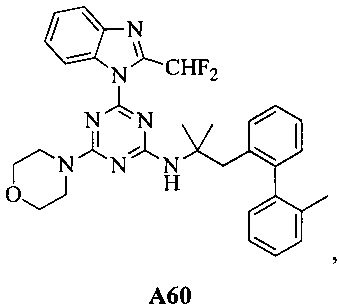
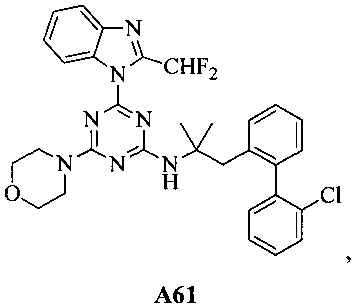
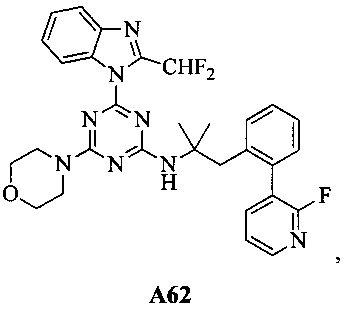
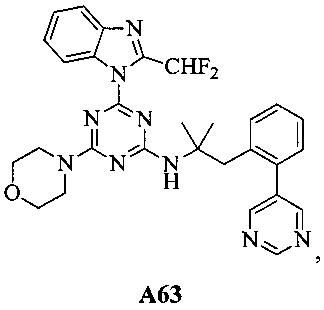
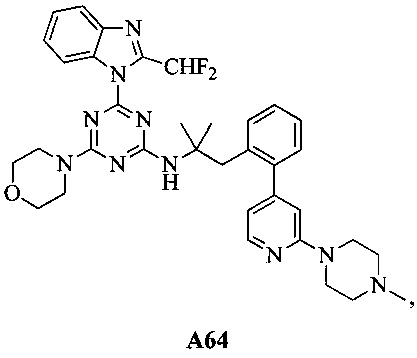
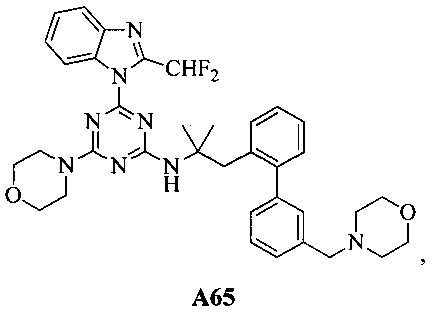
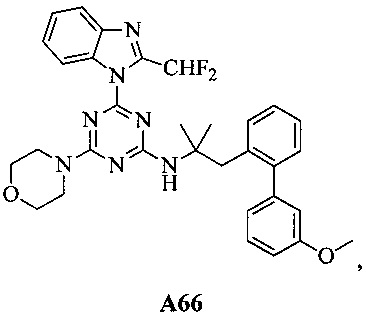
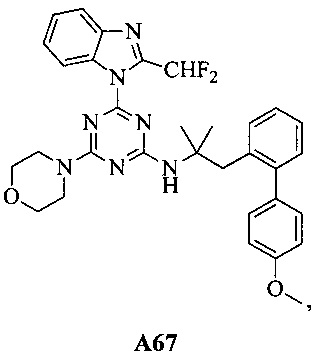
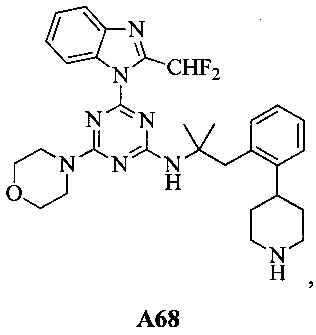
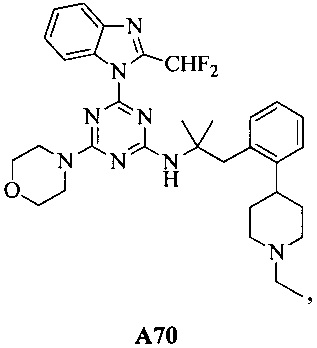
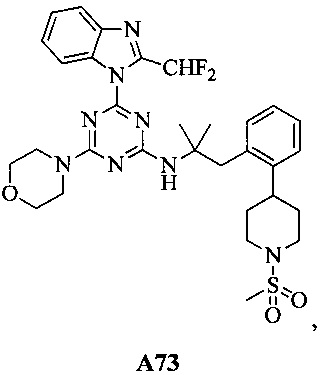
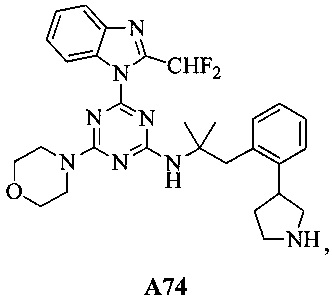
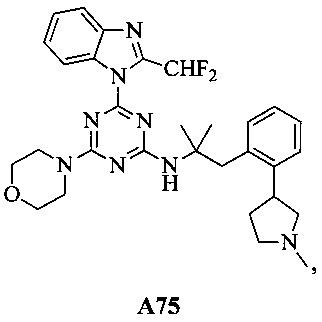 и
и 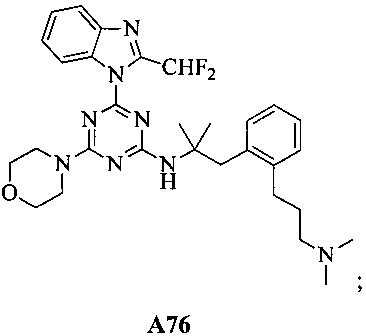
и их энантиомеров, смесей энантиомеров, смесей двух или более диастереомеров; и их фармацевтически приемлемых солей.
24. Фармацевтическая композиция, содержащая соединение по п. 1 или его энантиомер, смесь энантиомеров или смесь двух или более диастереомеров; или их фармацевтически приемлемую соль; и одно или более фармацевтически приемлемых вспомогательных веществ, где композиция предназначена для лечения заболевания, опосредованного PI3K.
25. Фармацевтическая композиция по п. 24, где композицию формулируют для введения в виде одной дозы.
26. Фармацевтическая композиция по п. 25, где композицию формулируют в виде лекарственной формы для перорального, парентерального или внутривенного введения.
27. Фармацевтическая композиция по п. 25, где композицию формулируют в виде пероральной лекарственной формы.
28. Фармацевтическая композиция по п. 27, где пероральная лекарственная форма представляет собой таблетку или капсулу.
29. Способ регулирования PI3K ферментативной активности, включающий контакт PI3K фермента с соединением по п. 1.
30. Способ по п. 29, где PI3K представляет собой дикий тип.
31. Способ по п. 29, где PI3K представляет собой PI3K вариант.
32. Способ по п. 29, где PI3K представляет собой PI3K класса I.
33. Способ по п. 32, где PI3K представляет собой p110γ.
| WO 2011005119 A1, 13.01.2011 | |||
| WO 2010110685 A2, 30.09.2010 | |||
| RU 2008145660, 24.04.2007. |
Авторы
Даты
2017-01-23—Публикация
2012-03-27—Подача