Изобретение относится к производным карбоновых кислот с оксазоло[5,4-d]пиримидиновым циклом, а также к их физиологически приемлемым солям.
На предшествующем уровне техники уже были описаны соединения с подобной структурой (см. WO 2009/154775), являющиеся приемлемыми для лечения множественного склероза. Принцип действия этих соединений состоит в том, чтобы благодаря активации рецептора EDG-1 обуславливать десенсибилизацию сигнального пути EDG-1 (так называемый суперагонизм), которая затем становится равной функциональному антагонизму сигнального пути EDG-1. Системно это означает, что в первую очередь сигнальный путь EDG-1 долговременно угнетается в отношении лимфоцитов, вследствие чего эти клетки больше не могут хемотропически следовать градиенту S1P между кровью и лимфой. Это обуславливает то, что затронутые лимфоциты больше не могут покидать вторичную лимфатическую ткань (усиленный хоминг) и число свободно циркулирующих лимфоцитов в плазме сильно снижается. Этот дефицит лимфоцитов в плазме (лимфопения) способствует иммунодепрессии, которая в обязательном порядке требуется для механизма действия модуляторов рецепторов EDG-1, описанных в WO 2009/154775.
В основе настоящего изобретения лежала задача разработки соединений, проявляющих терапевтически приемлемое действие. В частности, задача состояла в том, чтобы найти новые соединения, которые были бы специфически приемлемыми в отношении заживления ран и, в частности, для терапии нарушений заживления ран пациентов с диабетом.
Далее было желательно разработать соединения, которые были бы приемлемыми для лечения синдрома диабетической стопы (DFS).
Далее было желательно добиться повторяемой активации рецептора EDG-1 сигнального пути, чтобы тем самым сделать возможной фармакологически устойчивую активацию сигнального пути EDG-1.
Таким образом, настоящее изобретение относится к соединениям формулы I:
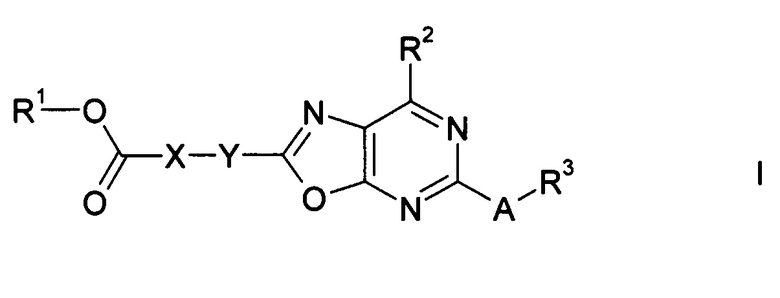
где A, X, Y, R1, R2 и R3 имеют определенные далее значения.
Механизм действия соединений формулы I основан не на десенсибилизации сигнального пути EDG-1 и, таким образом, является диаметрально противоположным по сравнению с механизмом действия, описанным в WO 2009/154775. Настоящее изобретение относится также к способу получения соединений формулы I, к их применению, предпочтительно в качестве активного вещества в лекарственных средствах, и к фармацевтическим композициям, содержащим их.
У пациентов с диабетом по сравнению со здоровыми людьми наблюдается замедленное заживление ран и повышенная частота инфицирования, в первую очередь, в случае более долговременной гипергликемии, например, вызванной плохим регулированием содержания сахара в крови. К причинам относят нарушения кровообращения, в первую очередь, в области мелких сосудов, ведущие к ухудшенному снабжению тканей кислородом и питательными веществами. Кроме того, имеет место пониженная скорость деления клеток и клеточной миграции кератиноцитов, фибробластов и кожных эндотелиальных клеток. Дополнительно ограничивается активность различных защитных клеток (гранулоцитов) с уменьшенным фагоцитозом (поглощение и разрушение бактерий). При высоком содержании сахара в крови ограничивается также функция антител (иммунглобулинов) против бактерий. В соответствии с этим ранам и инфекциям у пациентов с диабетом должно быть обеспечено особое внимание.
Рецептор Edg-1 относится к семейству рецепторов Edg (Edg=Endothelial Differentiation Gene (ген дифференцирования эндотелия)), состоящему в настоящее время из восьми идентифицированных рецепторов GPCR (рецепторы, сопряженные с G-белком) класса A. Это семейство может быть разделено на подсемейство рецепторов, активируемых сфингозин-1-фосфатом (S1P) (пять членов), и рецепторов, активируемых лизофосфатидовой кислотой (LPA) (три члена). Эндогенный лиганд S1P представляет собой плюрипотентный лизофосфолипид, который действует на различные типы клеток благодаря активации рецепторов GPCR из семейства рецепторов Edg, а именно: Edg-1 (=S1P1), Edg-3 (=S1P3), Edg-5 (=S1P2), Edg-6 (=S1P4) и Edg-8 (S1P5). Хотя S1P описан также как внутриклеточный нейромедиатор, многочисленные клеточные ответы S1P опосредуются через активацию рецепторов Edg. S1P продуцируется благодаря ферментам семейства сфингозинкиназ (SPHK) и разлагается различными фосфатазами или лиазами.
Известные показания на агонисты рецептора Edg-1 дают, например, сердечнососудистые заболевания, атеросклероз, сердечная недостаточность, кардиопротекция, периферический облитерирующий эндартериит, заболевания почек и заболевания дыхательных путей.
Объектами настоящего изобретения являются соединения формулы I в любых своих стереоизомерных формах или в виде смеси стереоизомерных форм в любом соотношении или их физиологически приемлемые соли или физиологически приемлемые сольваты соединений такого типа или солей такого типа:
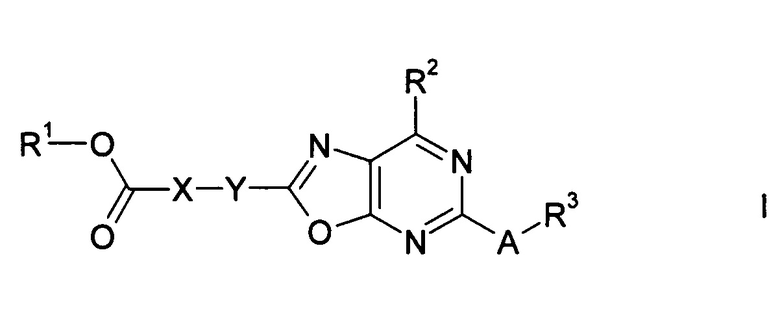
Г-де А выбран из связи, -CH2-, NH, O и S;
X выбран из (C1-C6)-алкандиилов, (C2-C6)-алкендиилов, (C2-C6)-алкиндиилов, (C3-C7)-циклоалкандиилов, (C1-C6)-алкандиилокси- и (C3-C7)-циклоалкандиилоксигрупп, причем все группы при необходимости имеют один или несколько одинаковых или разных заместителей, выбранных из атомов фтора и гидроксигрупп, причем атом кислорода (C1-C6)-алкандиилокси- и (C3-C7)-циклоалкандиилоксигрупп связан с группой Y;
Y выбран из фенилена и двухвалентного радикала ароматического 5-членного или 6-членного моноциклического гетероцикла, содержащего в цикле 1, 2 или 3 одинаковых или разных гетероатома, выбранных из атомов N, O и S, причем один из содержащихся в цикле атомов азота может быть связан с атомом водорода или с заместителем R4, а в фенилене и в двухвалентном радикале ароматического гетероцикла один или несколько содержащихся в цикле атомов углерода при необходимости имеют одинаковые или разные заместители R5;
R1 выбран из атома водорода, (C1-C4)-алкилов и (C3-C7)-циклоалкил-CzH2z-групп, где z выбран из 0, 1 и 2;
R2 выбран из (C1-C6)-алкилов, (C3-C5)-циклоалкил-CxH2x- и Het1-CnH2n-групп, где x и n выбраны из 0, 1 и 2;
R3 выбран из (C1-C6)-алкилов, причем алкил при необходимости имеет один или несколько заместителей в виде атомов фтора, (C2-C6)-алкенилов, (C2-C6)-алкинилов, (C3-C7)-циклоалкил-CuH2u- и Het2-CvH2v-групп, где u и v выбраны из 1 и 2, или R3 представляет собой радикал насыщенного или ненасыщенного включающего от 3 до 10 членов моноцикла или бицикла, который содержит в цикле 0, 1, 2, 3 или 4 одинаковых или разных гетероатома, выбранных из атомов N, O и S, причем один или два содержащихся в цикле атома азота могут быть связаны с атомами водорода или (C1-C4)-алкилами в качестве заместителей и один или два содержащихся в цикле атома серы могут быть связаны с одной или двумя оксогруппами, причем в радикале цикла один или несколько содержащихся в цикле атомов углерода при необходимости имеют одинаковые или разные заместители R31;
R4 выбран из (C1-C4)-алкилов, (C3-C7)-циклоалкил-CwH2W- и оксигрупп, причем w выбран из 0, 1 и 2;
R5 выбран из атомов галогенов, гидроксигруппы, (C1-C4)-алкилов, (C3-C5)-циклоалкил-CzH2z-, (C1-C4)-алкилокси-, (C1-C4)-алкил-S(O)m-, амино-, нитро-, цианогрупп, гидроксикарбонилов, (C1-C4)-алкилоксикарбонилов, аминокарбонилов и аминосульфонилов, причем z выбран из 0, 1 и 2;
R31 выбран из атомов галогенов, гидроксигруппы, (C1-C4)-алкилов, (C1-C4)-алкилоксигрупп, (C3-C7)-циклоалкилов, оксо-, (C1-C4)-алкил-S(O)m-, амино-, (C1-C4)-алкиламино-, ди((C1-C4)-алкил)амино-, (C1-C4)-алкилкарбониламино-, (C1-C4)-алкилсульфониламино-, нитро-, цианогрупп, (C1-C4)-алкилкарбонилов, аминосульфонилов, (C1-C4)-алкиламиносульфонилов и ди((C1-C4)-алкил)аминосульфонилов;
Het1 означает радикал включающего от 4 до 6 членов моноциклического насыщенного гетероцикла, содержащего в цикле 1 или 2 одинаковых или разных гетероатома, выбранных из атомов O и S, и связанного через содержащийся в цикле атом углерода, причем содержащийся в цикле атом серы может быть связан с одной или двумя оксогруппами, причем радикал гетероцикла при необходимости имеет один или несколько одинаковых или разных заместителей, выбранных из атомов фтора и (C1-C4)-алкилов;
Het2 означает радикал включающего от 4 до 7 членов насыщенного моноциклического гетероцикла, содержащего в цикле 1 или 2 одинаковых или разных гетероатома, выбранных из атомов N, O и S, и связанного через содержащийся в цикле атом углерода, причем радикал гетероцикла при необходимости имеет один или несколько одинаковых или разных заместителей, выбранных из атомов фтора и (C1-C4)-алкилов;
m выбран из 0, 1 и 2.
Все структурные элементы, такие, как группы, заместители, члены гетероциклов, индексы или другие отличительные признаки, например алкильные группы, группы, такие, как R5, индексы, такие, как m, которые могут встречаться в соединениях формулы I несколько раз, независимо друг от друга могут иметь любые указанные значения и соответственно случаю быть одинаковыми или отличающимися друг от друга. Например, алкильные группы в диалкиламиногруппе могут быть одинаковыми или разными.
Алкильные, алкенильные и алкинильные группы могут быть линейными, т.е. иметь прямую цепь, или разветвленными. Это положение относится также к случаю, когда они являются частью других групп, например алкилоксигруппы (=алкоксигруппа, алкил-O-группа), алкилоксикарбонильной группы или алкилзамещенной аминогруппы, или к случаю, когда они имеют заместители. В зависимости от соответствующего определения число атомов углерода в алкильной группе может быть равным 1, 2, 3, 4, 5 или 6, или 1, 2, 3 или 4, или 1, 2 или 3. Примеры алкилов представляют собой метил, этил, пропил, включая н-пропил и изопропил, бутил, включая н-бутил, втор-бутил, изобутил и трет-бутил, пентил, включая н-пентил, 1-метилбутил, изопентил, неопентил и трет-пентил, и гексил, включая н-гексил, 3,3-диметилбутил и изогексил. Двойные и тройные связи в алкенильных и алкинильных группах могут находиться в любых положениях. В одном из вариантов осуществления настоящего изобретения алкенильные группы содержат двойную связь, а алкинильные группы содержат тройную связь. В одном из вариантов осуществления настоящего изобретения алкенильная или алкинильная группа содержит по меньшей мере три атома углерода и через атом углерода, который не является элементом двойной или тройной связи, связана с остальной частью молекулы. Примеры алкенилов и алкинилов представляют собой этенил, проп-1-енил, проп-2-енил (= аллил), бут-2-енил, 2-метилпроп-2-енил, 3-метилбут-2-енил, гекс-3-енил, гекс-4-енил, проп-2-инил (= пропаргил), бут-2-инил, бут-3-инил, гекс-4-инил или гекс-5-инил. Замещенные алкильные, алкенильные и алкинильные группы могут иметь заместители в любых положениях при условии, что соответствующее соединение является достаточно стабильным и является приемлемым для поставленной цели, такой, как применение в качестве лекарственного вещества. Условие, заключающееся в том, что специфическая группа и соединение формулы I являются достаточно стабильными и приемлемыми для поставленной цели, такой, как применение в качестве лекарственного вещества, в общем случае относится к определениям любых групп в соединениях формулы I.
В случае возможности применения, приведенные ранее пояснения в отношении алкильных, алкенильных и алкинильных групп соответствующим образом относятся к двухвалентным алкильным группам, таким, как алкандиильные группы CuH2u, CvH2v, CwH2w, CxH2x, CyH2y и CzH2z, и двухвалентным алкенильным и алкинильным группам, таким, как алкендиильные и алкиндиильные группы, которые, таким образом, также могут быть линейными и разветвленными. Двойные и тройные связи в алкендиильных и алкиндиильных группах могут находиться в любых положениях. В одном из вариантов осуществления настоящего изобретения алкендиильные группы содержат двойную связь, а алкиндиильные группы содержат тройную связь. Примеры двухвалентных алкильных групп представляют собой -CH2- (= метилен), -CH2-CH2-, -CH2-CH2-CH2-, -CH2-CH2-CH2-CH2-, -CH(CH3)-, -C(CH3)2-, -CH(CH3)-CH2-, -CH2-CH(CH3)-, -C(CH3)2-CH2-, -CH2-C(CH3)2-, примеры двухвалентных алкенильных групп представляют собой -CH=CH-, -CH2-CH=CH-, -CH=CH-CH2-, -CH2-CH=CH-CH2-, -CH2-CH2-CH=CH-, -C(CH3)=C(CH3)-, а примеры двухвалентных алкинильных групп представляют собой -C≡C-, -CH2-C≡C-, -C≡C-CH2-, -C(CH3)2-C≡C-, -C≡C-C(CH3)2-, -CH2-C≡C-CH2-, -CH2-CH2-C≡C-. Если индекс в двухвалентной группе, такой, как, например, индекс z в группе CzH2z, равен 0 (=отсутствует), то обе группы, которые связаны с упомянутой группой, такой, как CzH2z, непосредственно связаны друг с другом одинарной связью.
Число атомов углерода, содержащихся в цикле циклоалкильной группы, может быть равным 3, 4, 5, 6 или 7. В одном из вариантов осуществления настоящего изобретения число атомов углерода, содержащихся в цикле циклоалкильной группы, независимо от числа атомов углерода, содержащихся в цикле другой циклоалкильной группы, равно 3, 4, 5 или 6, в одном из других вариантов осуществления равно 3, 4 или 5, в одном из других вариантов осуществления равно 3 или 4, в одном из других вариантов осуществления равно 3, в одном из других вариантов осуществления равно 5, 6 или 7, в одном из других вариантов осуществления равно 5 или 6, в одном из других вариантов осуществления равно 6 или 7, в одном из других вариантов осуществления равно 6. Это положение соответствующим образом относится к двухвалентным циклоалкильным группам, т.е. циклоалкандиильным группам, которые через один или два любых атома углерода, содержащихся в цикле, могут быть связаны с соседними группами. Примеры циклоалкильных групп представляют собой циклопропил, циклобутил, циклопентил, циклогексил и циклогептил. Примеры двухвалентных циклоалкильных групп представляют собой циклопропан-1,1-диил, циклопропан-1,2-диил, циклобутан-1,3-диил, циклопентан-1,1-диил, циклопентан-1,2-диил, циклопентан-1,3-диил, циклогексан-1,1-диил, циклогексан-1,2-диил, циклогексан-1,3-диил, циклогексан-1,4-диил, циклогептан-1,4-диил. Независимо друг от друга и от других заместителей циклоалкильные и циклоалкандиильные группы при необходимости могут иметь заместители в виде одного или несколько одинаковых или разных (C1-C4)-алкилов, которые могут находиться в любых положениях, т.е. циклоалкильные группы могут не иметь заместителей в виде алкилов или иметь заместители в виде алкилов, например 1, 2, 3 или 4, или 1 или 2 заместителя в виде (C1-C4)-алкилов, например в виде метильных групп. Примеры алкилзамещенных циклоалкильных и циклоалкандиильных групп представляют собой 4-метилциклогексил, 4-трет-бутилциклогексил или 2,3-диметилциклопентил, 2,2-диметилциклопропан-1,1-диил, 2,2-диметилциклопропан-1,2-диил, 2,2-диметилциклопентан-1,3-диил, 6,6-диметилциклогептан-1,4-диил. Примерами циклоалкилалкильных групп, которые, например, могут представлять собой такие группы, как (C3-C7)-циклоалкил-CzH2z-, являются циклопропилметил, циклобутилметил, циклопентилметил, циклогексилметил, циклогептилметил, 1-циклопропилэтил, 2-циклопропилэтил, 1-циклобутилэтил, 2-циклобутилэтил, 2-циклопентилэтил, 2-циклогексилэтил, 2-циклогептилэтил.
Независимо друг от друга и от других заместителей алкильные группы, двухвалентные алкильные группы, алкенильные группы, двухвалентные алкенильные группы, алкинильные группы, двухвалентные алкинильные группы, циклоалкильные группы и двухвалентные циклоалкильные группы при необходимости могут иметь один или несколько заместителей в виде атомов фтора, которые могут находиться в любых положениях, т.е. эти группы могут не иметь заместителей в виде атомов фтора или иметь заместители в виде атомов фтора, например 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12 или 13 или 1, 2, 3, 4, 5, 6, 7, 8 или 9, или 1, 2, 3, 4, 5, 6 или 7, или 1, 2, 3, 4 или 5, или 1, 2 или 3, или 1 или 2 заместителя в виде атомов фтора. Примеры фторзамещенных групп такого типа представляют собой трифторметил, 2-фторэтил, 2,2,2-трифторэтил, пентафторэтил, 3,3,3-трифторпропил, 2,2,3,3,3-пентафторпропил, 4,4,4-трифторбутил, гептафторизопропил, -CHF-, -CF2-, -CF2-CH2-, -CH2-CF2-, -CF2-CF2-, -CF(CH3)-, -C(CF3)2-, 1-фторциклопропил, 2,2-дифторциклопропил, 3,3-дифторциклобутил, 1-фторциклогексил, 4,4-дифторциклогексил, 3,3,4,4,5,5-гексафторциклогексил, 2,2-дифторциклопропан-1,2-диил. Примеры алкилоксигрупп, в которых алкильная группировка имеет заместители в виде атомов фтора, представляют собой трифторметокси-, 2,2,2-трифторэтокси-, пентафторэтокси- и 3,3,3-трифторпропоксигруппа. В одном из вариантов осуществления настоящего изобретения общее число заместителей в виде атомов фтора и в виде (C1-C4)-алкилов, которые независимо от других заместителей при необходимости содержатся в циклоалкильных и циклоалкандиильных группах соединений формулы I, равно 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или 11, в одном из других вариантов осуществления равно 1, 2, 3, 4, 5, 6, 7, 8 или 9, в одном из других вариантов осуществления равно 1, 2, 3, 4 или 5, в одном из других вариантов осуществления равно 1, 2, 3 или 4.
Группы, такие, как фенил, нафтил (= нафталинил), и радикалы ароматических гетероциклов, которые при необходимости имеют один или несколько заместителей, могут быть незамещенными или замещенными, например иметь одинаковые или разные заместители, число которых равно 1, 2, 3, 4 или 5, или 1, 2, 3 или 4, или 1, 2 или 3, или 1 или 2, или 1 и которые могут находиться в любых положениях. В одном из вариантов осуществления настоящего изобретения общее число заместителей в виде нитрогрупп, содержащихся в соединении формулы I, составляет не более двух. Ароматические азотсодержащие гетероциклы, в которых в циклической системе, лежащей в основе, с атомом водорода связан атом азота, содержащийся в 5-членном цикле, таком, как, например, пиррольный, имидазольный, индольный или бензоимидазольный цикл, могут иметь заместители при атомах углерода и/или при содержащихся в цикле атомах азота такого типа. В одном из вариантов осуществления настоящего изобретения заместители при содержащихся в цикле атомах азота такого типа выбраны из (C1-C4)-алкилов, т.е. атомы азота такого типа, содержащиеся в ароматических гетероциклах, связаны с атомом водорода или с заместителями в виде (C1-C4)-алкилов. Если относительно атомов азота, содержащихся в цикле ароматических гетероциклов и других гетероциклов, указано, что они могут быть связаны с атомом водорода или с заместителем, то содержащиеся в цикле атомы азота такого типа связаны с атомом водорода или необязательно с заместителем. Содержащиеся в цикле атомы азота, связанные с атомом водорода или с заместителем, содержатся в азотсодержащем ароматическом 5-членном цикле, таком, как, например, пиррол, имидазол, индол или бензоимидазол, и в неароматическом цикле, включая насыщенный цикл. Содержащиеся в цикле атомы азота, которые не связаны с атомом водорода или с заместителем, поскольку они не находятся в положительно заряженной форме, включая другие содержащиеся в цикле атомы азота наряду с содержащимися в цикле атомами азота, связанными с атомами водорода или с заместителями, содержатся в ароматическом цикле, таком, как, например, тиазол, имидазол, пиридин или бензоимидазол, и в неароматическом цикле, в котором они представляют собой головные атомы мостиков или связаны двойной связью и представляют собой содержащиеся в цикле атомы азота, через которые связан цикл. Приемлемые атомы азота, содержащиеся в ароматических гетероциклах соединений формулы I, такие, как атом азота, содержащийся в пиридиновом цикле, в специфическом случае атом азота, содержащийся в ароматическом гетероцикле, обозначенном как R2, могут находиться также в виде оксизаместителей -O- и в виде N-оксида, а содержащиеся в цикле атомы азота такого типа могут существовать также в виде четвертичной соли, например в виде N-(C1-C4)-алкильной соли, такой, как N-метиловая соль, причем в одном из вариантов осуществления настоящего изобретения противоанион в четвертичной соли такого типа представляет собой физиологически приемлемый анион, происходящий из кислоты, которая образует физиологически приемлемые соли. В однозамещенных фенильных группах заместитель может находиться в положении 2, 3 или 4. В двузамещенных фенильных группах заместители могут находиться в 2,3-, 2,4-, 2,5-, 2,6-, 3,4- или 3,5-положениях. В тризамещенных фенильных группах заместители могут находиться в 2,3,4-, 2,3,5-, 2,3,6-,и 2,4,5- и 2,4,6- или 3,4,5-положениях. Нафтил может представлять собой 1-нафтил (= нафталин-1-ил) или 2-нафтил (= нафталин-2-ил). В однозамещенной группе 1-нафтил заместитель может находиться в положении 2, 3, 4, 5, 6, 7 или 8. В однозамещенной группе 2-нафтил заместитель может находиться в положении 1, 3, 4, 5, 6, 7 или 8. В двузамещенных нафтильных группах заместители также могут находиться в любых положениях как в цикле, с которым связана нафтильная группа, так и/или в другом цикле. Это положение, относящееся к одновалентным радикалам, соответствующим образом относится к двухвалентным радикалам, таким, как, например, фениленовые группы, которые обозначены как R2 и которые, таким образом, также могут быть незамещенными или замещенными, например иметь одинаковые или разные заместители, число которых равно 1, 2, 3, 4 или 5, или 1, 2, 3 или 4, или 1, 2 или 3, или 1 или 2, или 1 и которые могут находиться в любых положениях.
В ароматических гетероциклах, которые могут быть обозначены как гетероарилы и гетероарилены, а также во всех других гетероциклах и неароматических гетероциклах, содержащиеся в цикле гетероатомы в общем случае выбраны из атомов N, O и S, причем символ N обозначает содержащиеся в цикле атомы азота, связанные с атомом водорода или с заместителем, а также содержащиеся в цикле атомы азота, не связанные с атомом водорода и с заместителем. Содержащиеся в цикле гетероатомы могут находиться в любых положениях в предположении, что гетероциклическая система известна на предшествующем уровне техники, стабильна и является приемлемой в качестве основы для достижения поставленной в отношении соединения формулы I цели, такой, как применение в качестве лекарственного вещества. В одном из вариантов осуществления настоящего изобретения содержащиеся в цикле два атома кислорода могут находиться в гетероцикле не в соседних положениях, в одном из других вариантов осуществления два содержащихся в цикле гетероатома, выбранных из атомов кислорода и серы, могут находиться не в соседних положениях любого гетероцикла. В насыщенных циклах отсутствует двойная связь в цикле. Ненасыщенные циклические системы могут быть ароматическими или частично ненасыщенными, включая частично ароматические, причем в последнем случае цикл в бициклической системе является ароматическим, а циклическая система присоединена через атом в неароматическом цикле. В зависимости от группы ненасыщенные циклы могут содержать в цикле одну, две, три, четыре или пять двойных связей. Ароматические группы содержат циклическую систему с шестью или десятью делокализованными пи-электронами в цикле. В зависимости от соответствующей группы насыщенные и неароматические ненасыщенные гетероциклы, включая гетероциклы и неароматические группы, обозначенные как R3, могут быть 3-членными, 4-членными, 5-членными, 6-членными, 7-членными, 8-членными, 9-членными или 10-членными. В одном из вариантов осуществления настоящего изобретения ароматические гетероциклы представляют собой 5-членные или 6-членные моноциклы или 8-членные, 9-членные или 10-членные бициклы, в одном из других вариантов осуществления они представляют собой 5-членные или 6-членные моноциклы или 9-членные или 10-членные бициклы, в одном из других вариантов осуществления они представляют собой 5-членные или 6-членные моноциклы, причем 8-членные, 9-членные или 10-членные бициклы состоят из двух аннелированных 5-членных циклов, 5-членного цикла и 6-членного цикла, которые сочленены друг с другом, или из двух аннелированных 6-членных циклов. В бициклических ароматических гетероциклических группах один или оба цикла могут содержать в цикле гетерогенные члены, а один или оба цикла могут быть ароматическими. В общем случае бициклические системы с ароматическим циклом и неароматическим циклом считают ароматическими, если они связаны через атом углерода в ароматическом цикле, и неароматическими, если они связаны через атом углерода в неароматическом цикле. Если не указано иное, гетероциклические группы, включая ароматические гетероциклические группы, могут быть связаны через любой приемлемый содержащийся в цикле атом углерода и в случае с азотсодержащими гетероциклами через любой приемлемый содержащийся в цикле атом азота. В одном из вариантов осуществления настоящего изобретения ароматическая гетероциклическая группа в соединении формулы I независимо от любой другой ароматической гетероциклической группы связана через содержащийся в цикле атом углерода, в другом варианте осуществления связана через содержащийся в цикле атом азота. В зависимости от определения соответствующей гетероциклической группы в одном из вариантов осуществления настоящего изобретения число содержащихся в цикле гетероатомов, которые могут содержаться в гетероциклической группе независимо от числа содержащихся в цикле гетероатомов в другой гетероциклической группе, составляет 1, 2, 3 или 4, в одном из других вариантов осуществления составляет 1, 2 или 3, в одном из других вариантов осуществления составляет 1 или 2, в одном из других вариантов осуществления составляет 1, причем содержащиеся в цикле гетероатомы могут быть одинаковыми или разными. Гетероциклические группы, которые при необходимости могут иметь заместители, могут независимо от любой другой гетероциклической группы быть незамещенными или иметь один или несколько одинаковых или разных заместителей, число которых составляет, например, 1, 2, 3, 4 или 5, или 1, 2, 3 или 4, или 1, 2 или 3, или 1 или 2, или 1 и которые указаны при определении соответствующей группы. Заместители в гетероциклических группах могут находиться в любых положениях. Так, заместители в группе пиридин-2-ила могут находиться, например, в положении 3 и/или в положении 4, и/или в положении 5, и/или в положении 6, в группе пиридин-3-ила могут находиться в положении 2 и/или в положении 4, и/или в положении 5, и/или в положении 6, а в группе пиридин-4-ила могут находиться в положении 2 и/или в положении 3, и/или в положении 5, и/или в положении 6.
Примеры основ гетероциклов, из которых могут происходить гетероциклические группы, включая ароматические гетероциклические группы, насыщенные гетероциклические группы и неароматические ненасыщенные гетероциклические группы, представляют собой азет, оксет, пиррол, фуран, тиофен, имидазол, пиразол, [1,3]диоксол, оксазол (=[1,3]оксазол), изоксазол (=[1,2]оксазол), тиазол (=[1,3]тиазол), изотиазол (=[1,2]тиазол), [1,2,3]триазол, [1,2,4]триазол, [1,2,4]оксадиазол, [1,3,4]оксадиазол, [1,2,4]тиадиазол, [1,3,4]тиадиазол, тетразол, пиридин, пиран, тиопиран, пиридазин, пиримидин, пиразин, [1,3]оксазин, [1,4]оксазин, [1,3]тиазин, [1,4]тиазин, [1,2,3]триазин, [1,3]дитиин, [1,4]дитиин, [1,2,4]триазин, [1,3,5]триазин, [1,2,4,5]тетразин, азепин, [1,3]диазепин, [1,4]диазепин, [1,3]оксазепин, [1,4]оксазепин, [1,3]тиазепин, [1,4]тиазепин, азоцин, азецин, циклопента[b]пиррол, 2-азабицикло[3.1.0]гексан, 3-азабицикло[3.1.0]гексан, 2-окса-5-азабицикло[2.2.1]гептан, индол, изоиндол, бензотиофен, бензофуран, [1,3]бензодиоксол (= 1,2-метилендиоксибензол), [1,3]бензоксазол, [1,3]бензотиазол, бензоимидазол, тиено[3,2-c]пиридин, хромен, изохромен, [1,4]бензодиоксин, [1,4]бензоксазин, [1,4]бензотиазин, хинолин, изохинолин, циннолин, хиназолин, хиноксалин, фталазин, тиенотиофен, [1,8]нафтиридин и другие нафтиридины, птеридин и соответствующие насыщенные и частично ненасыщенные гетероциклы, в которых одна или несколько, например, одна, две, три, четыре или все двойные связи в циклической системе, включая двойные связи в ароматическом цикле, замещены одинарными связями, такие, как, например, азетидин, оксетан, пирролидин, тетрагидрофуран, тетрагидротиофен, имидазолидин, оксазолидин, тиазолидин, дигидропиридин, пиперидин, тетрагидропиран, пиперазин, морфолин, тиоморфолин, азепан, хроман, изохроман, [1,4]бензодиоксан (= 1,2-этилендиоксибензол), 2,3-дигидробензофуран, 1,2,3,4-тетрагидрохинолин, 1,2,3,4-тетрагидроизохинолин.
Примеры радикалов ароматических гетероциклов, которые могут содержаться в соединениях формулы I, представляют собой тиофенил (=тиенил), включая тиофен-2-ил и тиофен-3-ил, пиридинил (=пиридил), включая пиридин-2-ил (=2-пиридил), пиридин-3-ил (=3-пиридил) и пиридин-4-ил (=4-пиридил), имидазолил, включая, например, 1H-имидазол-1-ил, 1H-имидазол-2-ил, 1H-имидазол-4-ил и 1H-имидазол-5-ил, [1,2,4]триазолил, включая 1H-[1,2,4]-триазол-1-ил и 4H-[1,2,4]-триазол-3-ил, тетразолил, включая 1H-тетразол-1-ил и 1H-тетразол-5-ил, хинолинил (=хинолил), включая хинолин-2-ил, хинолин-3-ил, хинолин-4-ил, хинолин-5-ил, хинолин-6-ил, хинолин-7-ил и хинолин-8-ил, причем все группы при необходимости, как было указано в определении соответствующей группы, имеют заместители. Примеры радикалов насыщенных и частично ненасыщенных гетероциклов, которые могут содержаться в соединениях формулы I, представляют собой азетидинил, пирролидинил, включая пирролидин-1-ил, пирролидин-2-ил и пирролидин-3-ил, 2,5-дигидро-1H-пирролил, пиперидил, включая пиперидин-1-ил, пиперидин-2-ил, пиперидин-3-ил и пиперидин-4-ил, 1,2,3,4-тетрагидропиридил, 1,2,5,6-тетрагидропиридил, 1,2-дигидропиридил, азепанил, азоканил, азеканил, октагидроциклопента[b]пирролил, 2,3-дигидробензофурил, включая 2,3-дигидробензофуран-7-ил, 2,3-дигидро-1H-индолил, октагидро-1H-индолил, 2,3-дигидро-1H-изоиндолил, октагидро-1H-изоиндолил, 1,2-дигидрохинолинил, 1,2,3,4-тетрагидрохинолинил, декагидрохинолинил, 1,2-дигидроизохинолинил, 1,2,3,4-тетрагидроизохинолил, 1,2,3,4-тетрагидроизохинолил, декагидроизохинолинил, декагидроизохинолинил, 4,5,6,7-тетрагидротиено[3,2-c]пиридил, пиразолидинил, имидазолидинил, гексагидропиримидинил, 1,2-дигидропиримидинил, пиперазинил, [1,3]диазепанил, [1,4]диазепанил, оксазолидинил, [1,3]оксазинанил, [1,3]оксазепанил, морфолинил, включая морфолин-2-ил, морфолин-3-ил и морфолин-4-ил, [1,4]оксазепанил, тиазолидинил, [1,3]тиазинанил, тиоморфолинил, включая тиоморфолин-2-ил, тиоморфолин-3-ил и тиоморфолин-4-ил, 3,4-дигидро-2H-[1,4]тиазинил, [1,3]тиазепанил, [1,4]тиазепанил, [1,4]тиазепанил, оксетанил, тетрагидрофурил, тетрагидротиенил, изоксазолидинил, изотиазолидинил, оксазолидинил, [1,2,4]оксадиазолидинил, [1,2,4]тиадиазолидинил, [1,2,4]триазолидинил, [1,3,4]оксадиазолидинил, [1,3,4]тиадиазолидинил, [1,3,4]триазолидинил, 2,3-дигидрофурил, 2,5-дигидрофурил, 2,3-дигидротиенил, 2,5-дигидротиенил, 2,3-дигидропирролил, 2,3-дигидроизоксазолил, 4,5-дигидроизоксазолил, 2,5-дигидроизоксазолил, 2,3-дигидроизотиазолил, 4,5-дигидроизотиазолил, 2,5-дигидроизотиазолил, 2,3-дигидропиразолил, 4,5-дигидропиразолил, 2,5-дигидропиразолил, 2,3-дигидрооксазолил, 4,5-дигидрооксазолил, 2,5-дигидрооксазолил, 2,3-дигидротиазолил, 4,5-дигидротиазолил, 2,5-дигидротиазолил, 2,3-дигидроимидазолил, 4,5-дигидроимидазолил, 2,5-дигидроимидазолил, тетрагидропиридазинил, тетрагидропиримидинил, тетрагидропиразинил, тетрагидро[1,3,5]триазинил, [1,3]дитианил, тетрагидропиранил, тетрагидротиопиранил, [1,3]диоксоланил, 3,4,5,6-тетрагидропиридил, 4H-[1,3]тиазинил, 1,1-диоксо-2,3,4,5-тетрагидротиенил, 2-азабицикло[3.1.0]гексил, включая 2-азабицикло[3.1.0]гекс-2-ил, 3-азабицикло[3.1.0]гексил, включая 3-азабицикло[3.1.0]гекс-3-ил, 2-окса-5-азабицикло[2.2.1]гептил, включая 2-окса-5-азабицикло[2.2.1]гепт-5-ил, причем все группы связаны через соответствующий содержащийся в цикле атом углерода или атом азота и при необходимости, как было указано в определении соответствующей группы, имеют заместители.
Галоген означает фтор, хлор, бром и/или йод. В одном из вариантов осуществления настоящего изобретения каждый из атомов галогенов в соединении формулы I независимо от любого другого атома галогена выбран из атомов фтора, хлора и брома, в одном из других вариантов осуществления выбран из атомов фтора и хлора.
В случае, когда оксогруппа связана с атомом углерода, она замещает два атома водорода при атоме углерода системы, лежащей в основе. Таким образом, CH2-группа в цепи или в цикле в случае, когда в ней осуществляют замену на оксогруппу, т.е. на связанный двойной связью атом кислорода, превращается в C(O)-группу (= C(=O)-группа). Очевидным образом, оксогруппа не может содержаться в качестве заместителя при атоме углерода в ароматическом цикле, таком, как, например, фенильная группа. Если атом серы, содержащийся в цикле гетероциклической группы, может быть связан с одной или двумя оксогруппами, то в случае, когда он не связан с оксогруппой, речь идет о неокисленном атоме серы S, или если он связан с оксогруппой, то речь идет о S(O)-группе (сульфоксидная группа, S-оксидная группа), или если он связан с двумя оксогруппами, то речь идет о S(O)2-группе (=сульфогруппа, S,S-диоксидная группа).
Настоящее изобретение относится к любым стереоизомерным формам соединений формулы I и их солям и сольватам. Относительно каждого хирального центра независимо от любого другого хирального центра соединения формулы I могут находиться в S-конфигурации или в значительной степени в S-конфигурации или в R-конфигурации или в значительной степени в R-конфигурации или в виде смеси S-изомера и R-изомера в любом отношении. Изобретение относится к любым возможным энантиомерам и диастереомерам и смесям двух или более стереоизомеров, например к смеси энантиомеров и/или диастереоизомеров, в любых соотношениях. Таким образом, соединения по настоящему изобретению могут существовать в виде энантиомеров в энантиомерно чистой форме, как в виде левовращающих, так и в виде правовращающих антиподов, и в форме смесей обоих энантиомеров в любых соотношениях, включая рацематы. В случае E/Z-изомерии или цис/транс-изомерии, например относительно двойных связей или циклов, таких, как циклоалкилы, настоящее изобретение относится как к E-форме, так и к Z-форме, или к цис-форме и к транс-форме, а также к смесям этих форм в любых соотношениях. В одном из вариантов осуществления настоящего изобретения в случае соединения, которое может находиться в двух или более стереоизомерных формах, речь идет о чистом или в значительной степени чистом отдельном стереоизомере. Получение отдельных стереоизомеров может быть осуществлено, например, разделением смеси изомеров традиционными способами, например хроматографией или кристаллизацией, посредством применения стереохимически однородных исходных веществ при синтезе или стереоселективным синтезом. При необходимости перед разделением стереоизомеров может быть осуществлена их дериватизация. Разделение смеси стереоизомеров может быть осуществлено на стадии соединения формулы I или на стадии исходного или промежуточного вещества в ходе синтеза. Настоящее изобретение относится также к любым таутомерным формам соединений формулы I и их солей и сольватов.
В случае, когда соединения формулы I содержат одну или несколько кислотных и/или основных групп, т.е. солеобразующих групп, настоящее изобретение относится также к их соответствующим физиологически или токсикологически приемлемым солям, т.е. к нетоксичным солям, предпочтительно к их фармацевтически приемлемым солям.
Настоящее изобретение относится к любым сольватам соединений формулы I, например к гидратам или аддуктам со спиртами, такими, как (C1-C4)-алканолы, к активным метаболитам соединений формулы I, а также к пролекарствам и производным соединений формулы I, которые in vitro необязательно проявляют фармакологическое действие, но in vivo превращаются в фармакологически эффективные соединения, например к сложным эфирам или амидам карбоновых кислот.
Алкандиильные, алкендиильные и алкиндиильные группы, содержащиеся в группе X, могут быть линейными или разветвленными, как уже было в общем случае указано в отношении групп такого типа, причем эти группы, а также циклоалкандиильные группы, обозначенные как X, могут быть в любых положениях связаны с соседними группами, т.е. с группой R1O-C(O) и группой Y или в случае алкандиилоксигруппы с атомом кислорода алкандиилоксигруппы. Соседние группы могут быть связаны с одинаковыми или разными атомами углерода в группе X. В одном из вариантов осуществления цепь атомов углерода в алкандиильной, алкендиильной и алкиндиильной группе, содержащейся в группе X, которая группу R1O-C(O) связывает непосредственно с группой Y или в случае алкандиилоксигруппы с атомом кислорода алкандиилоксигруппы, состоит из 1, 2, 3 или 4 атомов углерода, в одном из других вариантов осуществления состоит из 1, 2 или 3 атомов углерода, в одном из других вариантов осуществления состоит из 1 или 2 атомов углерода, в одном из других вариантов осуществления состоит из 1 атома углерода. В случае циклоалкандиила, обозначенного как X, в одном из вариантов осуществления группы R1O-C(O) и Y связаны с двумя содержащимися в цикле атомами углерода, находящимися в 1,2-, 1,3- или 1,4-положениях по отношению друг к другу, в одном из других вариантов осуществления находящимися в 1,2- или 1,3-положениях по отношению друг к другу, в одном из других вариантов осуществления находящимися в 1,2-положении по отношению друг к другу, в одном из других вариантов осуществления находящимися в 1,4-положении по отношению друг к другу. В одном из вариантов осуществления X выбран из (C1-C6)-алкандиилов, (C2-C6)-алкендиилов, (C3-C7)-циклоалкандиилов и (C1-C6)-алкандиилоксигрупп, в одном из других вариантов осуществления X выбран из (C1-C6)-алкандиилов, (C2-C6)-алкендиилов и (C1-C6)-алкандиилоксигрупп, в одном из других вариантов осуществления X выбран из (C1-C6)-алкандиилов, (C3-C7)-циклоалкандиилов и (C1-C6)-алкандиилоксигрупп, в одном из вариантов осуществления X выбран из (C1-C6)-алкандиилов и (C1-C6)-алкандиилоксигрупп, в одном из других вариантов осуществления X выбран из (C1-C6)-алкандиилов, (C2-C6)-алкендиилов, (C2-C6)-алкиндиилов и (C3-C7)-циклоалкандиилов, в одном из других вариантов осуществления X выбран из (C1-C6)-алкандиилов, (C2-C6)-алкендиилов и (C3-C7)-циклоалкандиилов, в одном из других вариантов осуществления X выбран из (C1-C6)-алкандиилов и (C2-C6)-алкендиилов, в одном из других вариантов осуществления X означает (C1-C6)-алкандиил, в одном из других вариантов осуществления X означает (C2-C6)-алкендиил, в одном из других вариантов осуществления X означает (C3-C7)-циклоалкандиил и в одном из других вариантов осуществления X означает (C1-C6)-алкандиилоксигруппу, причем все группы при необходимости, как было указано, имеют заместители. В одном из вариантов осуществления (C1-C6)-алкандиил, содержащийся в группе X, представляет собой (C1-C4)-алкандиил, в одном из других вариантов осуществления он представляет собой (C1-C3)-алкандиил, в одном из других вариантов осуществления он представляет собой (C1-C2)-алкандиил. В одном из вариантов осуществления (C2-C6)-алкендиил и (C2-C6)-алкиндиил, обозначенные как X, представляют собой (C2-C4)-алкендиил и (C2-C4)-алкиндиил, в одном из других вариантов осуществления они представляют собой (C2-C3)-алкендиил и (C2-C3)-алкиндиил. В одном из вариантов осуществления (C3-C7)-циклоалкандиил, обозначенный как X, представляет собой (C3-C6)-циклоалкандиил, в одном из других вариантов осуществления он представляет собой (C3-C4)-циклоалкандиил, в одном из других вариантов осуществления он представляет собой циклопропандиил, в одном из других вариантов осуществления он представляет собой циклогександиил. Примеры групп X, из которых в приведенных ранее вариантах осуществления могут быть выбраны соответствующие группы, обозначенные как X, или из которых в одном из других вариантов осуществления изобретения могут быть выбраны группы X, представляют собой метилен, -CH(CH3)- (этан-1,1-диил), -CH2-CH2- (этан-1,2-диил, 1,2-этилен), -C(CH3)2- (1-метилэтан-1,1-диил), -CH2-CH2-CH2- (пропан-1,3-диил, 1,3-пропилен), -CH2-CH(CH3) и -CH(CH3)-CH2- (пропан-1,2-диил, 1,2-пропилен), группы, представляющие собой примеры (C1-C6)-алкандиилов, -CH=CH- (этилен-1,2-диил), -CH=CH-CH2- и -CH2-CH=CH- (проп-1-ен-1,3-диил и проп-2-ен-1,3-диил) и -CH=C(CH3) и -C(CH3)=CH- (проп-1-ен-1,2-диил), группы, представляющие собой примеры (C2-C6)-алкендиилов, -C≡C- (этиндиил) и -CH2-C≡C- и -C≡C-CH2- (проп-1-ин-1,3-диил и проп-2-ин-1,3-диил), группы, представляющие собой примеры (C2-C6)-алкиндиилов, циклопропан-1,1-диил, циклопропан-1,2-диил и циклогексан-1,4-диил, группы, представляющие собой примеры (C3-C7)-циклоалкандиилов, -CH2-O- (метиленоксигруппа), -CH2-CH2-O- (этан-1,2-диилоксигруппа), -CH(CH3)-O- (этан-1,1-диилоксигруппа), -C(CH3)2-O- (1-метилэтан-1,1-диилоксигруппа), -CH2-CH2-CH2-O- (пропан-1,3-диилоксигруппа) и -CH2-CH2-CH2-CH2-O- (бутан-1,4-диилоксигруппа), группы, представляющие собой примеры (C1-C6)-алкандиилоксигрупп, причем все группы при необходимости, как было указано, имеют заместители. Так, в одном из вариантов осуществления группы X выбраны из -CH2-O-, -CH2-CH2-O-, -CH(CH3)-O- и -C(CH3)2-O-групп, в одном из других вариантов осуществления они выбраны из -CH2-O-, -CH2-CH2-O- и -CH(CH3)-O-групп, в одном из других вариантов осуществления они выбраны из -CH2-O- и -CH(CH3)-O-групп, а в одном из других вариантов осуществления X означает -CH2-O-группу, причем все группы при необходимости, как было указано, имеют заместители, а атом кислорода связан с группой Y. В одном из вариантов осуществления число заместителей, содержащихся при необходимости в группе X, равно 1, 2, 3 или 4, в одном из других вариантов осуществления оно равно 1, 2 или 3, в одном из других вариантов осуществления оно равно 1 или 2, в одном из других вариантов осуществления оно равно 1, а в одном из других вариантов осуществления группа X не имеет заместителей, выбранных из атомов фтора и гидроксигрупп. В одном из вариантов осуществления число заместителей в виде гидроксигрупп в группе X составляет не более 2, в одном из других вариантов осуществления оно составляет не более 1. В одном из вариантов осуществления отдельный атом углерода в группе X связан не более чем с одним заместителем в виде гидроксигруппы. В одном из вариантов осуществления атомы углерода, образующие двойную связь в группе (C2-C6)-алкендиил, не имеют заместителей в виде гидроксигрупп. В одном из вариантов осуществления атом углерода в (C1-C6)-алкандиилоксигруппе, связанный с атомом кислорода, не связан с заместителем в виде гидроксигруппы, в одном из других вариантов осуществления атом углерода в (C1-C6)-алкандиилоксигруппе, связанный с атомом кислорода, не имеет заместителей, т.е. в последнем варианте осуществления все атомы углерода, не связанные с атомом кислорода, при необходимости имеют один или несколько одинаковых или разных заместителей, выбранных из атомов фтора и гидроксигрупп. Двойная связь в (C2-C6)-алкендииле может иметь E- или Z-конфигурацию. В одном из вариантов осуществления она имеет E-конфигурацию, в одном из других вариантов осуществления она имеет Z-конфигурацию.
В одном из вариантов осуществления настоящего изобретения R1 выбран из атома водорода и (C1-C4)-алкилов, в одном из других вариантов осуществления R1 выбран из атома водорода, метила, этила, н-пропила, н-бутила и изопропила, в одном из других вариантов осуществления он выбран из атома водорода, метила и этила, в одном из других вариантов осуществления R1 означает атом водорода, в одном из других вариантов осуществления R1 означает (C1-C4)-алкил, в одном из других вариантов осуществления R1 означает метил.
В одном из вариантов осуществления настоящего изобретения число содержащихся в цикле гетероатомов в ароматическом гетероцикле, обозначенном как Y, равно 1 или 2, в одном из других вариантов осуществления оно равно 1. В одном из вариантов осуществления настоящего изобретения Y выбран из фенилена и двухвалентного радикала ароматического 6-членного моноциклического гетероцикла, содержащего в цикле 1, 2 или 3 атома азота, в одном из других вариантов осуществления содержащего в цикле 1 или 2 атома азота, в одном из других вариантов осуществления содержащего в цикле 1 атом азота, причем один из содержащихся в цикле атомов азота может быть связан с заместителем R4, представляющим собой оксигруппу, т.е. один из содержащихся в цикле атомов азота может быть окислен до N-оксида, причем в фенилене и двухвалентном радикале ароматического гетероцикла один или несколько содержащихся в цикле атомов углерода при необходимости имеют одинаковые или разные заместители R5. В одном из других вариантов осуществления Y означает фенилен, причем в фенилене один или несколько содержащихся в кольце атомов при необходимости имеют одинаковые или разные заместители R5, а в одном из других вариантов осуществления Y означает пиридиндиил, причем содержащийся в цикле атом азота может быть связан с заместителем R4, представляющим собой оксигруппу, т.е. содержащийся в цикле атом азота может быть окислен до N-оксида, причем в пиридиндииле при необходимости один или несколько содержащихся в цикле атомов углерода имеют одинаковые или разные заместители R5. В одном из других вариантов осуществления Y означает двухвалентный радикал ароматического 5-членного гетероцикла, содержащего 1, 2 или 3 одинаковых или разных содержащихся в цикле гетероатомов, выбранных из атомов N, O и S, причем один из содержащихся в цикле атомов азота может быть связан с атомом водорода или заместителем R4, причем в двухвалентном радикале ароматического гетероцикла при необходимости один или несколько содержащихся в цикле атомов углерода имеют одинаковые или разные заместители R5. В одном из вариантов осуществления двухвалентный радикал ароматического гетероцикла, обозначенный как Y, выбран из фурандиила, тиофендиила, оксазолдиила, тиазолдиила, пиридиндиила, пиридазиндиила, пиримидиндиила и пиразиндиила, в одном из других вариантов осуществления он выбран из фурандиила, тиофендиила, тиазолдиила, пиридиндиила, пиридазиндиила, пиримидиндиила и пиразиндиила, в одном из других вариантов осуществления он выбран из фурандиила, тиофендиила, пиридиндиила, пиридазиндиила, пиримидиндиила и пиразиндиила, в одном из других вариантов осуществления он выбран из фурандиила, тиофендиила, пиридиндиила и пиримидиндиила, в одном из других вариантов осуществления он выбран из фурандиила, тиофендиила и пиридиндиила, причем все группы при необходимости, как было указано в отношении группы Y, имеют заместители.
Содержащиеся в цикле атомы углерода, через которые фениленовая группа и двухвалентный радикал ароматического гетероцикла, обозначенные как Y, связаны с оксазолопиримидиновым циклом и группой X, могут находиться в любых положениях. Фениленовая группа, обозначенная как Y, может представлять собой 1,2-фенилен, т.е. оксазолопиримидиновый цикл и группа X могут быть связаны в 1,2-положении или в орто-положении по отношению друг к другу, она может представлять собой 1,3-фенилен, т.е. оксазолопиримидиновый цикл и группа X могут быть связаны в 1,3-положении или мета-положении по отношению друг к другу, и она может представлять собой 1,4-фенилен, т.е. оксазолопиримидиновый цикл и группа X могут быть связаны в 1,4-положении или пара-положении по отношению друг к другу. В одном из вариантов осуществления фениленовая группа, обозначенная как Y, выбрана из 1,3-фенилена и 1,4-фенилена, в одном из других вариантов осуществления она представляет собой 1,3-фенилен, в одном из других вариантов осуществления она представляет собой 1,4-фенилен, причем все группы при необходимости, как было указано в отношении группы Y, имеют заместители. В одном из вариантов осуществления группа Y выбрана из одной или нескольких групп фенилена, фуран-2,5-диила, тиофен-2,4-диила, тиофен-2,5-диила, пиридин-2,4-диила, пиридин-2,5-диила, пиридин-3,5-диила, пиридин-2,6-диила и пиримидин-2,5-диила, в одном из других вариантов осуществления она выбрана из фуран-2,5-диила, тиофен-2,4-диила, тиофен-2,5-диила, пиридин-2,4-диила, пиридин-2,5-диила, пиридин-3,5-диила, пиридин-2,6-диила и пиримидин-2,5-диила, в одном из других вариантов осуществления она выбрана из пиридин-2,4-диила, пиридин-2,5-диила, пиридин-3,5-диила и пиридин-2,6-диила, в одном из других вариантов осуществления она выбрана из фенилена, пиридин-2,4-диила, пиридин-2,5-диила, пиридин-3,5-диила и пиридин-2,6-диила, причем все группы при необходимости, как было указано в отношении группы Y, имеют заместители. В одном из вариантов осуществления число заместителей R5, которые при необходимости могут быть связаны с атомами углерода, содержащимися в цикле группы Y, равно 1, 2, 3, 4 или 5, в одном из других вариантов осуществления оно равно 1, 2, 3 или 4, в одном из других вариантов осуществления оно равно 1, 2 или 3, в одном из других вариантов осуществления оно равно 1 или 2, в одном из других вариантов осуществления оно равно 1. Атомы углерода, содержащиеся в цикле группы Y и не связанные с заместителями R5, связаны с атомами водорода.
В одном из вариантов осуществления настоящего изобретения заместители R5, которые при необходимости содержатся в группе Y, выбраны из атомов галогенов, гидроксигрупп, (C1-C4)-алкилов, (C3-C5)-циклоалкил-CzH2z-, (C1-C4)-алкилокси-, (C1-C4)-алкил-S(O)m-, амино-, нитро- и цианогрупп, в одном из других вариантов осуществления они выбраны из атомов галогенов, гидроксигрупп, (C1-C4)-алкилов, (C3-C5)-циклоалкил-CzH2z-, (C1-C4)-алкилокси-, амино- и цианогрупп, в одном из других вариантов осуществления они выбраны из атомов галогенов, гидроксигрупп, (C1-C4)-алкилов и (C1-C4)-алкилоксигрупп, в одном из других вариантов осуществления они выбраны из атомов фтора, хлора, гидроксигрупп, (C1-C4)-алкилов и (C1-C4)-алкилоксигрупп, в одном из других вариантов осуществления они выбраны из атомов фтора, хлора и (C1-C4)-алкилов и в одном из других вариантов осуществления они представляют собой (C1-C4)-алкилы в качестве заместителей, причем z выбран из 0, 1 и 2.
В одном из вариантов осуществления 1, 2 или 3 заместителя R5, в одном из других вариантов осуществления 1 или 2 заместителя R5 и в одном из других вариантов осуществления 1 заместитель R5, которые при необходимости содержатся в группе Y, определены соответственно общему определению группы R5 и, таким образом, выбраны из атомов галогенов, гидроксигрупп, (C1-C4)-алкилов, (C3-C5)-циклоалкил-CzH2z-, (C1-C4)-алкилокси-, (C1-C4)-алкил-S(O)m-, амино-, нитро-, цианогрупп, гидроксикарбонилов, (C1-C4)-алкилоксикарбонилов, аминокарбонилов и аминосульфонилов, и любые другие заместители R5, которые при необходимости содержатся в группе Y, например 1, 2 или 3 других заместителя R5 или 1 или 2 других заместителя R5, или 1 другой заместитель R5, выбраны из атомов галогенов, гидроксигрупп, (C1-C4)-алкилов, (C3-C5)-циклоалкил-CzH2z-, (C1-C4)-алкилокси-, (C1-C4)-алкил-S(O)m-, амино-, нитро- и цианогрупп, причем все эти алкилы независимо друг от друга при необходимости имеют один или несколько заместителей в виде атомов фтора, как это в общем случае определено для алкилов. В одном из вариантов осуществления заместители R5, которые при необходимости содержатся в группе Y и в приведенном ранее варианте осуществления определены соответственно общему определению группы R5, например 1 или 2 заместителя R5 такого типа или 1 заместитель R5 такого типа, выбраны из атомов галогенов, гидроксигрупп, (C1-C4)-алкилов, (C3-C5)-циклоалкил-CzH2z-, (C1-C4)-алкилокси-, (C1-C4)-алкил-S(O)m-, амино- и цианогрупп, причем z выбран из 0, 1 и 2. В одном из вариантов осуществления заместители R5, которые при необходимости содержатся в группе Y и определены в приведенном ранее варианте осуществления соответственно общему определению группы R5, например 1 или 2 заместителя R5 такого типа или 1 заместитель R5 такого типа, не связаны с атомами углерода, содержащимися в цикле, в группе Y, которая находится рядом с атомом, через который группа Y связана с оксазолопиримидиновым циклом, показанным в формуле I. В одном из вариантов осуществления другие заместители R5, которые при необходимости содержатся в группе Y, например 1, 2 или 3 других заместителя R5 или 1 или 2 других заместителя R5, или 1 другой заместитель R5, выбраны из атомов галогенов, гидроксигрупп, (C1-C4)-алкилов, (C1-C4)-алкилокси-, амино- и цианогрупп, в одном из других вариантов осуществления они выбраны из атомов галогенов, гидроксигрупп, (C1-C4)-алкилов и (C1-C4)-алкилоксигрупп, в одном из других вариантов осуществления они выбраны из атомов галогенов, (C1-C4)-алкилов и (C1-C4)-алкилоксигрупп, в одном из других вариантов осуществления они выбраны из атомов галогенов и (C1-C4)-алкилов, причем во всех этих вариантах осуществления все алкилы независимо друг от друга при необходимости имеют один или несколько заместителей в виде атомов фтора.
В одном из вариантов осуществления настоящего изобретения индекс z выбран из 0 и 1, в одном из других вариантов осуществления он равен 0, в одном из других вариантов осуществления он равен 1.
Объектами настоящего изобретения являются любые соединения формулы I, где один или несколько структурных элементов, таких, как группы, заместители и индексы, определены соответственно одному из указанных вариантов осуществления или определений элементов или имеют одно или несколько специфических значений, указанных в данном тексте в качестве примеров для элементов, причем любые комбинации одного или нескольких указанных вариантов осуществления и/или определений, и/или специфических значений элементов являются объектами настоящего изобретения. В отношении любых соединений такого типа формулы I любые их стереоизомерные формы и смеси стереоизомерных форм в любом соотношении и их физиологически приемлемые соли и их физиологически приемлемые сольваты также являются объектами настоящего изобретения.
Другой вариант осуществления относится к соединениям формулы I, где один или несколько радикалов имеют следующие значения:
А выбран из связи, -CH2-, NH, O и S;
X выбран из (C1-C6)-алкандиилов, (C2-C6)-алкендиилов, (C2-C6)-алкиндиилов, (C3-C7)-циклоалкандиилов, (C1-C6)-алкандиилокси- и (C3-C7)-циклоалкандиилоксигрупп, причем все группы при необходимости имеют один или несколько одинаковых или разных заместителей, выбранных из атомов фтора и гидроксигрупп, причем атом кислорода (C1-C6)-алкандиилокси- и (C3-C7)-циклоалкандиилоксигрупп связан с группой Y;
Y выбран из фенилена и двухвалентного радикала ароматического 5-членного или 6-членного моноциклического гетероцикла, содержащего в цикле 1, 2 или 3 одинаковых или разных гетероатома, выбранных из атомов N, O и S, причем один из содержащихся в цикле атомов азота может быть связан с атомом водорода или с заместителем R4, а в фенилене и в двухвалентном радикале ароматического гетероцикла один или несколько содержащихся в цикле атомов углерода при необходимости имеют одинаковые или разные заместители R5;
R1 выбран из атома водорода, (C1-C4)-алкилов и (C3-C7)-циклоалкил-CzH2z-групп, где z выбран из 0, 1 и 2;
R2 выбран из (C1-C6)-алкилов, (C3-C5)-циклоалкил-CxH2x- и Het1-CnH2n-групп, где x и n выбраны из 0, 1 и 2;
R3 выбран из (C1-C6)-алкилов, причем алкил при необходимости имеет один или несколько заместителей в виде атомов фтора, (C2-C6)-алкенилов, (C2-C6)-алкинилов, (C3-C7)-циклоалкил-CuH2u- и Het2-CnH2n-групп, где u и n выбраны из 1 и 2, или R3 представляет собой радикал насыщенного или ненасыщенного включающего от 3 до 10 членов моноцикла или бицикла, который содержит в цикле 0, 1, 2, 3 или 4 одинаковых или разных гетероатома, выбранных из атомов N, O и S, причем один или два содержащихся в цикле атома азота могут быть связаны с атомами водорода или (C1-C4)-алкилами в качестве заместителей и один или два содержащихся в цикле атома серы могут быть связаны с одной или двумя оксогруппами, причем в радикале цикла один или несколько содержащихся в цикле атомов углерода при необходимости имеют одинаковые или разные заместители R31;
R4 выбран из (C1-C4)-алкилов, (C3-C7)-циклоалкил-CwH2W- и оксигрупп, причем w выбран из 0, 1 и 2;
R5 выбран из атомов галогенов, гидроксигруппы, (C1-C4)-алкилов, (C3-C5)-циклоалкил-CzH2z-, (C1-C4)-алкилокси-, (C1-C4)-алкил-S(O)m-, амино-, нитро-, цианогрупп, гидроксикарбонилов, (C1-C4)-алкилоксикарбонилов, аминокарбонилов и аминосульфонилов, причем z выбран из 0, 1 и 2;
R31 выбран из атомов галогенов, гидроксигруппы, (C1-C4)-алкилов, (C1-C4)-алкилоксигрупп, (C3-C7)-циклоалкилов, оксо-, (C1-C4)-алкил-S(O)m-, амино-, (C1-C4)-алкиламино-, ди((C1-C4)-алкил)амино-, (C1-C4)-алкилкарбониламино-, (C1-C4)-алкилсульфониламино-, нитро-, цианогрупп, (C1-C4)-алкилкарбонилов, аминосульфонилов, (C1-C4)-алкиламиносульфонилов и ди((C1-C4)-алкил)аминосульфонилов;
Het1 означает радикал включающего от 4 до 6 членов насыщенного моноциклического гетероцикла, содержащего в цикле 1 или 2 атома кислорода и связанного через содержащийся в цикле атом углерода, причем радикал гетероцикла при необходимости имеет один или несколько одинаковых или разных заместителей, выбранных из атомов фтора и (C1-C4)-алкилов;
Het2 означает радикал включающего от 4 до 7 членов насыщенного моноциклического гетероцикла, содержащего в цикле 1 или 2 одинаковых или разных гетероатома, выбранных из атомов N, O и S, и связанного через содержащийся в цикле атом углерода, причем радикал гетероцикла при необходимости имеет один или несколько одинаковых или разных заместителей, выбранных из атомов фтора и (C1-C4)-алкилов;
m выбран из 0, 1 и 2.
Другой вариант осуществления относится к соединениям формулы I, где один или несколько радикалов имеют следующие значения:
A означает связь, -CH2-, NH, O или S;
X означает (C1-C6)-алкандиилоксигруппу, причем атом кислорода (C1-C6)-алкандиилоксигруппы связан с группой Y;
Y означает фенилен, причем в фенилене один или несколько содержащихся в цикле атомов углерода при необходимости имеют одинаковые или разные заместители R5;
R1 означает атом водорода или (C1-C4)-алкил;
R2 означает (C1-C6)-алкил;
R3 означает (C1-C6)-алкил, причем алкил при необходимости имеет один или несколько заместителей в виде атомов фтора, (C2-C6)-алкенил, (C2-C6)-алкинил, (C3-C7)-циклоалкил-CuH2u- и Het-CvH2v-группу, где u и v выбраны из 1 и 2, или R3 означает радикал насыщенного или ненасыщенного включающего от 3 до 10 членов моноцикла или бицикла, который содержит в цикле 0, 1, 2, 3 или 4 одинаковых или разных гетероатома, выбранных из атомов N, O и S, причем один или два содержащихся в цикле атома азота могут быть связаны с атомами водорода или (C1-C4)-алкилами в качестве заместителей и один или два содержащихся в цикле атома серы могут быть связаны с одной или двумя оксогруппами, причем в радикале цикла один или несколько содержащихся в цикле атомов углерода при необходимости имеют одинаковые или разные заместители R31;
R5 означает атом галогена, гидроксигруппу, (C1-C4)-алкил, (C3-C5)-циклоалкил-CzH2z-, (C1-C4)-алкилокси-, (C1-C4)-алкил-S(O)m-, амино-, нитро-, цианогруппу, гидроксикарбонил, (C1-C4)-алкилоксикарбонил, аминокарбонил или аминосульфонил, причем z выбран из 0, 1 и 2;
R31 означает атом галогена, (C1-C4)-алкил, (C3-C7)-циклоалкил, гидрокси-, (C1-C4)-алкилокси-, оксо-, (C1-C4)-алкил-S(O)m-, амино-, (C1-C4)-алкиламино-, ди((C1-C4)-алкил)амино-, (C1-C4)-алкилкарбониламино-, (C1-C4)-алкилсульфониламино-, нитро-, цианогруппу, (C1-C4)-алкилкарбонил, аминосульфонил, (C1-C4)-алкиламиносульфонил или ди((C1-C4)-алкил)аминосульфонил;
m выбран из 0, 1 и 2, причем все индексы m не зависят друг от друга.
Другой вариант осуществления относится к соединениям формулы I, где один или несколько радикалов имеют следующие значения:
A означает -CH2- или O;
X означает (C1-C6)-алкандиилоксигруппу, причем атом кислорода (C1-C6)-алкандиилоксигруппы связан с группой Y;
Y означает фенилен, причем в фенилене один или несколько содержащихся в цикле атомов углерода при необходимости имеют одинаковые или разные заместители R5;
R1 означает атом водорода или (C1-C4)-алкил;
R2 означает (C1-C6)-алкил;
R3 означает (C1-C6)-алкил, причем алкил при необходимости имеет один или несколько заместителей в виде атомов фтора, или фенил, причем в фениле один или несколько содержащихся в цикле атомов углерода при необходимости имеют одинаковые или разные заместители R31;
R5 означает атом галогена, гидроксигруппу, (C1-C4)-алкил, (C3-C5)-циклоалкил-CzH2z-, (C1-C4)-алкилокси-, (C1-C4)-алкил-S(O)m-, амино-, нитро-, цианогруппу, гидроксикарбонил, (C1-C4)-алкилоксикарбонил, аминокарбонил или аминосульфонил, причем z выбран из 0, 1 и 2;
R31 означает атом галогена, (C1-C4)-алкил, (C3-C7)-циклоалкил, гидроксигруппу, (C1-C4)-алкилокси-, оксо-, (C1-C4)-алкил-S(O)m-, амино-, (C1-C4)-алкиламино-, ди((C1-C4)-алкил)амино-, (C1-C4)-алкилкарбониламино-, (C1-C4)-алкилсульфониламино-, нитро-, цианогруппу, (C1-C4)-алкилкарбонил, аминосульфонил, (C1-C4)-алкиламиносульфонил или ди((C1-C4)-алкил)аминосульфонил;
m выбран из 0, 1 и 2.
Другой вариант осуществления относится к соединениям формулы I, где один или несколько радикалов имеют следующие значения:
A означает -CH2- или O;
X означает (C1-C6)-алкандиилоксигруппу, причем атом кислорода (C1-C6)-алкандиилоксигруппы связан с группой Y;
Y означает фенилен, причем в фенилене один или несколько содержащихся в цикле атомов углерода при необходимости имеют одинаковые или разные заместители R5;
R1 означает атом водорода;
R2 означает (C1-C6)-алкил;
R3 означает (C1-C6)-алкил, причем алкил при необходимости имеет один или несколько заместителей в виде атомов фтора, или фенил, причем в фениле один или несколько содержащихся в цикле атомов углерода при необходимости имеют одинаковые или разные заместители R31;
R5 означает (C1-C4)-алкил;
R31 означает атом галогена.
В отношении любых специфических соединений, описанных в данном тексте, таких, как экспериментальные соединения, представляющие варианты осуществления настоящего изобретения, в которых различные группы и индексы в общем определении соединений формулы I имеют специфические значения, представленные в соответствующем специфическом соединении, также имеет силу положение, что они в любых своих стереоизомерных формах и/или смесях стереоизомерных форм в любом соотношении, в форме их физиологически приемлемых солей и в форме физиологически приемлемых сольватов соединений такого типа или солей такого типа являются объектами настоящего изобретения. Независимо от того, описано ли в данном тексте специфическое соединение в качестве свободного соединения и/или в качестве специфической соли, оно, как в форме свободного соединения, так и в форме любых своих физиологически приемлемых солей, а при описании специфической соли дополнительно в форме этой специфической соли, и в форме физиологически приемлемых сольватов соединения такого типа или солей такого типа является объектом настоящего изобретения. Таким образом, объектом настоящего изобретения является также соединение формулы I, выбранное из одного или нескольких описанных в данном тексте специфических соединений формулы I, включая приведенные далее экспериментальные соединения, и его физиологически приемлемые соли и физиологически приемлемые сольваты соединения такого типа или солей такого типа, причем соединение формулы I в любых своих стереоизомерных формах или в виде смеси стереоизомерных форм в любом соотношении, в случае возможности применения, является объектом настоящего изобретения. В качестве примера можно назвать соединение формулы I или его физиологически приемлемый сольват, выбранные из {4-[7-изобутил-5-(3,3,3-трифторпропокси)оксазоло[5,4-d]пиримидин-2-ил]-2,6-диметилфенокси}уксусной кислоты, {4-[5-(3-хлорфенокси)-7-изобутилоксазоло[5,4-d]пиримидин-2-ил]-2,6-диметилфенокси}уксусной кислоты, {4-[5-(3-хлорфенокси)-7-пропилоксазоло[5,4-d]пиримидин-2-ил]-2,6-диметилфенокси}уксусной кислоты, {4-[5-(4-хлорбензил)-7-изобутилоксазоло[5,4-d]пиримидин-2-ил]-2,6-диметилфенокси}уксусной кислоты, [4-(5-бензил-7-изобутилоксазоло[5,4-d]пиримидин-2-ил)-2,6-диметилфенокси]уксусной кислоты и {4-[5-(4-хлорбензил)-7-изопропилоксазоло[5,4-d]пиримидин-2-ил]-2,6-диметилфенокси}уксусной кислоты.
Другими объектами настоящего изобретения являются способы получения соединений формулы I и их солей и сольватов, по которым эти соединения могут быть получены и которые описаны в дальнейшем тексте. В одном из способов соединение формулы II приводят во взаимодействие с соединением формулы III для получения соединения формулы I:
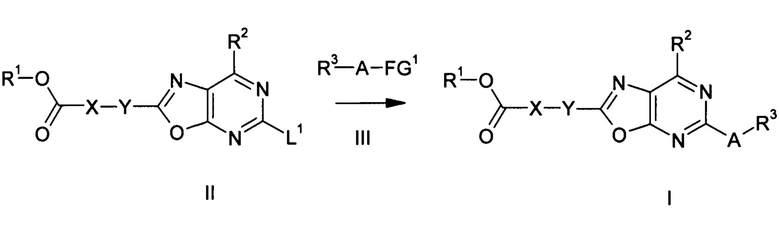
где группы A, X, Y, R1, R2 и R3 в соединениях формул II и III имеют значения, определенные для соединений формулы I, и дополнительно могут содержаться функциональные группы в защищенной форме или в форме групп-предшественниц, которые затем превращают в конечные группы. Группа L1 в соединениях формулы II представляет собой уходящую группу, которая может быть замещена по катализируемой при необходимости реакции ароматического замещения, такую, как атом галогена, например фтора, хлора, брома или йода, или алкилтио- или сульфокси- или сульфогруппу, например группу формулы -S-Alk или -S(O)-Alk, или - S(O)2-Alk, где Alk означает (C1-C4)-алкил, например метил или этил. Группа FG1 в соединениях формулы III представляет собой группу, которая может быть отщеплена в катализируемой при необходимости реакции ароматического замещения из соединения формулы III и не остается в соединении формулы I. Так, например, FG1 может представлять собой протон, в частности, в соединениях формулы III, в которой A означает NH, O или S. Альтернативно FG1 может представлять собой остаток бороновой кислоты или эфира бороновой кислоты, триалкилстаннильный остаток или атом лития, остаток галогенида цинка или магния, в частности, в соединениях формулы III, в которых A означает связь или -CH2-.
Реакция соединений формул II и III представляет собой катализируемую при необходимости реакцию ароматического замещения по атому углерода в положении 6 оксазоло[5,4-d]пиримидинового цикла, т.е. в пиримидиновой группировке, и может быть осуществлена в стандартных для реакций такого типа условиях, хорошо известных специалистам в данной области техники. Реакция может быть осуществлена также в присутствии каталитических систем, например толуолсульфината натрия или солей или комплексов железа, меди или палладия. В общем случае реакцию осуществляют в инертном растворителе, например в углеводородном растворителе, таком, как бензол, толуол, ксилол или хлорбензол, в простом эфире, таком, как тетрагидрофуран (THF), диоксан, дибутиловый эфир, диизопропиловый эфир или 1,2-диметоксиэтан (DME), в амине, таком, как N,N-диметилформамид (DMF), N,N-диметилацетамид (DMA) или N-метилпирролидин-2-он (NMP), или в смеси растворителей при температуре приблизительно от -20 до приблизительно 250°C, например при температуре приблизительно от 40 до приблизительно 200°C, в зависимости от особенностей соответствующего случая. В общем случае для повышения реакционной способности полезно прибавлять основание, например третичный амин, такой, как триэтиламин, этилдиизопропиламин или N-метилморфолин, или неорганическое основание, такое, как гидрид, гидроксид, карбонат или гидрокарбонат щелочно-земельного металла, такой, как гидрид натрия, гидроксид натрия, гидроксид калия, карбонат натрия, карбонат калия, карбонат цезия или гидрокарбонат натрия, или алкоксид, или амид, такой, как метилат натрия, этилат натрия, метилат калия, трет-бутилат калия, амид натрия или диизопропиламид лития. Соединение формулы III, где FG1 представляет собой протон, перед взаимодействием с соединением формулы II также может быть отдельно обработано основанием и превращено в соль. В случае, когда реакцию осуществляют в присутствии каталитической системы, могут применяться катализаторы, которые могут содержать ионы металла или металл в степени окисления 0, при этом предпочтительно применяют железо, медь или палладий. Катализ часто требует присутствия определенных лигандов, образующих с металлами комплексы и только обеспечивающих образование каталитически активных соединений или стабилизирующих их. Комплексы "металл-лиганд" могут прибавляться к реакционной смеси или образовываться in situ. Например, такие каталитические системы могут содержать медь или соли меди (I), предпочтительно галогениды меди (I) или карбоксилаты меди (I), предпочтительно йодид меди (I) или тиофенкарбоксилат меди (I), или также предварительно приготовленные комплексы меди (I), например тетракис-(ацетонитрил)гексафторфосфат меди (I), индивидуально или в присутствии лигандов, например диаминовых лигандов или 1,10-фенантролина. К тому же, такие каталитические системы могут состоять или быть образованы, например, из комплексов палладия или солей палладия в присутствии лигандов, например из комплексов палладия (0), предпочтительно трис-(дибензилиденацетон)дипалладия (0), или ацетата палладия, трифторацетата палладия или галогенидов палладия, предпочтительно хлорида палладия, в присутствии лигандов, предпочтительно дифосфиновых лигандов, таких, как, например, 2,2'-бис-(дифенилфосфино)-1,1'-бинафтил или 4,5-бис-(дифенилфосфино)-9,9-диметилксантен или предварительно приготовленный комплекс, такой, как бис-(три-трет-бутилфосфин)палладий (0). К тому же, такие каталитические системы могут содержать также соли железа (III), такие, как, например, ацетилацетонат железа (III). Кроме того, также могут быть использованы простые катализаторы, например, ароматическое нуклеофильное замещение 2-пиримидингалогенидов, предпочтительно 2-пиримидинхлоридов, может быть катализировано замещенными бензолсульфинатами щелочных и щелочноземельных металлов, предпочтительно толуолсульфинатом натрия.
Исходные соединения формул II и III получают описанными в литературе способами или аналогично им и во многих случаях имеются в продаже. Соединения формулы IIa, т.е. соединения формулы II, в которых L1 представляет собой, например, сульфоксидную группу формулы Alk-S(O) или сульфогруппу формулы Alk-S(O)2-, получают взаимодействием эфира аминомалоновой кислоты формулы IV с активированным производным карбоновой кислоты формулы V для получения соединения формулы VI, взаимодействием последнего соединения с тиомочевиной формулы VII для получения соединения формулы VIII, алкилированием тиола алкилирующим агентом формулы IX для получения простого тиоэфира формулы X, циклизацией последнего соединения с образованием системы оксазоло[5,4-d]пиримидинового цикла для получения соединения формулы XI, превращением последнего соединения в соединение формулы XII, причем радикал R1O-C(O)-X- взаимодействием с соединением формулы XIII превращают в соединение формулы XIV, последующим взаимодействием соединения формулы XIV с соединением формулы XV для получения соединения формулы XVI и окислением группировки простого тиоэфира в полученном соединении формулы XVI до соответствующего сульфоксида или сульфона формулы IIa.
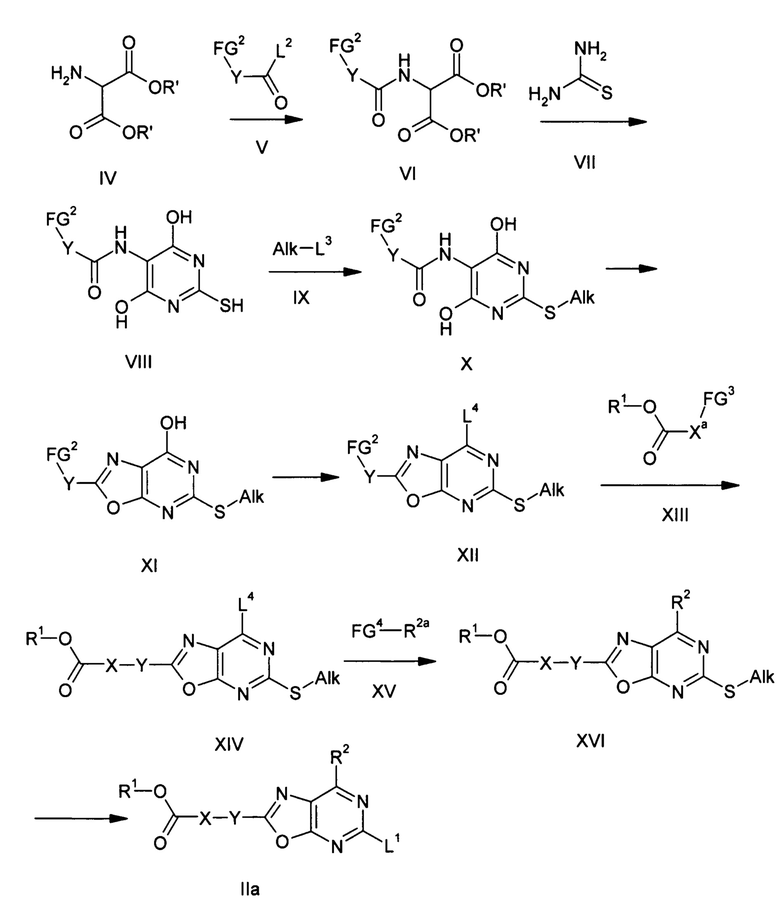
Группы X, Y, R1 и R2 в соединениях формул IIa, V, VI, VIII, X, XI, XII, XIII, XIV и XVI имеют значения, определенные для соединений формулы I, и дополнительно могут содержаться функциональные группы в защищенной форме или в форме групп-предшественниц, которые затем превращают в конечные группы.
Группа R2a в соединении формулы XV имеет значения, определенные для группы R2 в соединении формулы I, но может, кроме того, содержать двойную или тройную связь в соседнем положении со связью с FG4.
Группа Xa в соединениях формулы XIII имеет значения, определенные для группы X в соединениях формулы I, или содержит часть группы X в требуемом соединении формулы II, так что после взаимодействия соединений формул XII и XIII группа Xa и любая из частей групп FG2 и FG3, остающаяся в соединении формулы XIV, совместно образуют требуемую группу X. Так, например, в случае, когда группа X представляет собой алкандиилоксигруппу, группа Xa в соединении формулы XIII может представлять собой требуемую алкандиилоксигруппу, а группа FG3 может представлять собой атом водорода, связанный с атомом кислорода, или группа Xa может быть частью алкандиила, группа FG3 представляет собой уходящую группу, а группа FG2 в соединении формулы XII представляет собой гидроксигруппу, атом кислорода которой затем совместно с частью алкандиила после алкилирования соединения формулы XII соединением формулы XIII образует требуемую алкандиилоксигруппу.
Группы FG2 и FG3 в соединениях формул V, VI, VIII, X, XI, XII и XIII представляют собой функциональные группы, которые являются приемлемыми для применяемого типа сочетания с целью образования требуемой группы X из группы Xa и любой части групп FG2 и FG3, остающейся в соединении формулы XIV. Например, в случае, когда группа Xa по реакции нуклеофильного замещения связана с группой Y2 или с атомом в группе FG2, таким, как атом кислорода в гидроксигруппе, обозначенной как FG2, как было указано ранее, FG3 может представлять собой уходящую группу, такую, как атом галогена, такого, как хлор, бром или йод, или сульфонилоксигруппу, такую, как метансульфонилокси-, трифторметансульфонилокси- или толуолсульфонилоксигруппа. В случае, когда группу Xa связывают с группой Y по реакции, катализируемой переходным металлом, FG3 может представлять собой уходящую группу, такую, как остаток бороновой кислоты, сложного эфира бороновой кислоты, диалкилборана или триалкилстаннила, и в этом случае FG2 может представлять собой атом галогена. FG3 может представлять собой также атом водорода или атом углерода, образующий двойную связь в алкендиильной группе, обозначенной как Xa, когда присоединение группы Xa к группе Y осуществляют по реакции Хека, и в этом случае FG2 может представлять собой атом галогена. Если присоединение группы Xa к группе Y осуществляют по реакции Виттига или реакции Виттига-Горнера, то FG3 может представлять собой фосфониевую группу, такую, как трифенилфосфоний, или фосфонильную группу, такую, как диэтилфосфонил, а соединение формулы XIII может представлять собой соль фосфония или эфир фосфоновой кислоты, и в этом случае FG2 может представлять собой альдегидную группу -C(O)-H или кетогруппу -C(O)-алкил и наоборот. В общем случае группа FG2 связана с атомом углерода в фениленовой или гетероциклической группе, обозначенной как Y, которая в соединениях формул XIV, XVI, IIa и I связана с группой X. Группа FG2 в соединениях формул V, VI, VIII, X, XI и XII также может находиться в защищенной форме или в форме группы-предшественницы, превращаемой затем в группу, которая в соединении формулы XII реагирует с соединением формулы XIII. Так, например, гидроксигруппа, обозначенная в соединении формулы XII как FG2, в соединениях формул V, VI, VIII, X и XI может находиться в защищенной форме, например в виде этерифицированной гидроксигруппы, такой, как группа простого бензилового эфира или простого алкилового эфира, такого, как простой метиловый эфир. Простые эфиры такого типа могут быть расщеплены способами, хорошо известными специалистам в данной области техники. Описание способов отщепления защитных групп представлено в литературе, например, в P.J. Kocienski, Protecting Groups (Thieme Verlag, 1994), или в T.W. Greene and P.G.M. Wuts, Protective Groups in Organic Synthesis (John Wiley & Sons, 1999).
Группа FG4 в соединении формулы XV представляет собой функциональную группу, которая является приемлемой для сочетания соединений XIV и XV для получения соединения формулы XVI. Так, например, FG4 может представлять собой атом лития, остаток галогенида цинка или магния, когда соединение формулы XVI получают катализируемым при необходимости ароматическим нуклеофильным замещением, или FG4 может представлять собой уходящую группу, такую, как остаток бороновой кислоты, сложного эфира бороновой кислоты, диалкилборана или триалкилстаннила, когда соединение формулы XVI получают по реакции сочетания типа реакции Судзуки или реакции Штилле, или FG4 может представлять собой протон, если R2a содержит двойную или тройную связь в соседнем положении со связью с FG4, а соединение XVI получают по реакции сочетания типа реакции Хека или реакции Соногашира с последующим гидрированием.
Группа L1 в соединениях формулы IIa имеет значения, указанные ранее.
Группа L2 в соединениях формулы V представляет собой нуклеофильно замещаемую уходящую группу и может, в частности, представлять собой атом галогена, такого, как хлор или бром, а соединение формулы V может, таким образом, представлять собой галогенангидрид карбоновой кислоты. Группа L2 может представлять собой также группу формулы FG2-Y-C(O)-O, а соединение формулы V может, таким образом, представлять собой, например, ангидрид карбоновой кислоты.
Группа L3 в соединениях формулы IX представляет собой уходящую группу, которая может быть замещена по реакции нуклеофильного замещения, и предпочтительно может представлять собой атом галогена, такого, как хлор, бром или йод, или сульфонилоксигруппу, такую, как метансульфонилокси-, трифторметансульфонилокси- или толуолсульфонилоксигруппа, т.е. соединение формулы IX может представлять собой, например, органический галогенид или сульфат.
Группа L4 в соединениях формул XII и XIV представляет собой уходящую группу, которая может быть замещена по реакции ароматического замещения, и предпочтительно может представлять собой атом галогена, такого, как хлор, бром или йод.
Группа R' в соединениях формул IV и VI может представлять собой алкил, такой, как, например, (C1-C3)-алкил, такой, как метил или этил.
Как было указано, соединения формулы XI могут существовать также в другой таутомерной форме, например, в виде соответствующего 6H-оксазоло[5,4-d]пиримидин-7-она или 4H-оксазоло[5,4-d]пиримидин-7-она. В случае применимости, в отношении любых соединений, используемых при получении соединений формулы I, имеет силу положение, что они могут существовать в другой таутомерной форме, отличающейся от формы, представленной формулой. При осуществлении реакций данного способа для получения соединений формулы II, как и в случае любых других реакций, которые осуществляют для получения соединений формулы I, исходные соединения могут быть применены также в форме солей и/или конечные соединения могут быть получены в форме солей. Так, например, соединения формулы IV могут быть использованы в форме кислотно-аддитивных солей, таких, как гидрохлориды.
Взаимодействие соединений формул IV и V может быть осуществлено в стандартных условиях для ацилирования амина активированным производным карбоновой кислоты, таким, как галогенангидрид или ангидрид кислоты. В общем случае взаимодействие осуществляют в инертном растворителе, например в углеводородном или хлорпроизводном углеводородном растворителе, таком, как бензол, толуол, ксилол, хлорбензол, дихлорметан, хлороформ или дихлорэтан, в простом эфире, таком, как THF, диоксан, дибутиловый эфир, диизопропиловый эфир или DME, в кетоне, таком, как ацетон или бутан-2-он, в сложном эфире, таком, как этиловый или бутиловый эфир уксусной кислоты, или в воде, или в смеси растворителей при температуре приблизительно от -10 до приблизительно 40°C, например при температуре приблизительно от 0 до приблизительно 30°C. В общем случае взаимодействие осуществляют при прибавлении основания, например третичного амина, такого, как триэтиламин, этилдиизопропиламин или N-метилморфолин, или неорганического основания, такого, как гидроксид, карбонат или гидрокарбонат щелочного металла, такой, как гидроксид натрия, гидроксид калия, карбонат натрия, карбонат калия или гидрокарбонат натрия.
Взаимодействие соединений формул VI и VII в общем случае осуществляют в инертном растворителе, например в спирте, таком, как метанол, этанол или изопропанол, или в простом эфире, таком, как THF, диоксан или DME, или в смеси растворителей при температуре приблизительно от 20 до приблизительно 80°C, например при температуре приблизительно от 40 до приблизительно 80°C, в присутствии основания, например алкоксида, такого, как метилат натрия, этилат натрия, метилат калия или трет-бутилат калия.
Взаимодействие соединений формул VIII и IX представляет собой катализируемую при необходимости реакцию нуклеофильного замещения по атому углерода группы Alk, связанной с группой L3, и может быть осуществлено в стандартных для реакций такого типа условиях, хорошо известных специалистам в данной области техники. В общем случае взаимодействие в зависимости от особенностей соответствующего случая осуществляют в инертном растворителе, например в углеводородном или хлорпроизводном углеводородном растворителе, таком, как бензол, толуол, ксилол, хлорбензол, дихлорметан, хлороформ или дихлорэтан, в простом эфире, таком, как THF, диоксан, дибутиловый эфир, диизопропиловый эфир или DME, в спирте, таком, как метанол, этанол или изопропанол, в кетоне, таком, как ацетон или бутан-2-он, в сложном эфире, таком, как этиловый или бутиловый эфир уксусной кислоты, в нитриле, таком, как ацетонитрил, в амиде, таком, как DMF или NMP, или в смеси растворителей, включая двухфазные смеси с водными растворами, при температуре приблизительно от -20 до приблизительно 100°C, например при температуре приблизительно от -10 до приблизительно 30°C. В общем случае для повышения нуклеофильности соединения формулы VIII и/или для связывания кислоты, высвобождаемой при взаимодействии, полезно прибавлять основание, например третичный амин, такой, как триэтиламин, этилдиизопропиламин или N-метилморфолин, или неорганическое основание, такое, как гидрид, гидроксид, карбонат или гидрокарбонат щелочного металла, такой, как гидрид натрия, гидроксид натрия, гидроксид калия, карбонат натрия, карбонат калия, карбонат цезия или гидрокарбонат натрия, или алкоксид, или амид, такой, как метилат натрия, этилат натрия, метилат калия, трет-бутилат калия, амид натрия или диизопропиламид лития. Соединение формулы VIII перед реакцией с соединением формулы IX также может быть отдельно обработано основанием и превращено в соль.
Циклизация соединения формулы X для получения соединения формулы XI в предпочтительном случае может быть осуществлена в присутствии галогенида фосфора, такого, как пентахлорид или оксихлорид фосфора или их смесь, в инертном растворителе, например в углеводородном или хлорпроизводном углеводородном растворителе, таком, как бензол, толуол, ксилол, хлорбензол, дихлорметан, хлороформ или дихлорэтан, при температуре приблизительно от 20 до приблизительно 100°C, например при температуре приблизительно от 50 до приблизительно 80°C.
Превращение соединения формулы XI в соединение формулы XII также может быть осуществлено в присутствии галогенида фосфора, такого, как пентахлорид или оксихлорид фосфора или их смесь, в инертном растворителе, например в углеводородном или хлорпроизводном углеводородном растворителе, таком, как бензол, толуол, ксилол, хлорбензол, дихлорметан, хлороформ или дихлорэтан, при температуре приблизительно от 20 до приблизительно 150°C, например при температуре приблизительно от 50 до приблизительно 100°C. Соединение формулы X также может быть непосредственно превращено в соединение формулы XII без выделения соединения формулы XI.
Сочетание соединений формулы XII с соединениями формулы XIII может быть осуществлено по реакциям разных типов, как уже было указано ранее, например по реакции алкилирования. Так, например, группа Y в случае, когда она связана с гидроксигруппой, обозначенной как FG2, может быть алкилирована при применении соединения формулы XIII, в которой FG3 означает приемлемую для реакции нуклеофильного замещения уходящую группу, такую, как атом галогена, такого, как хлор, бром или йод, или сульфонилоксигруппу, такую, как метансульфонилокси- или толуолсульфонилоксигруппа. Реакция нуклеофильного замещения по атому углерода группы XIII, связанной с группой FG3, может быть осуществлена в стандартных для реакций такого типа условиях, хорошо известных специалистам в данной области техники. В общем случае взаимодействие в зависимости от особенностей соответствующего случая осуществляют в инертном растворителе, например в углеводородном или хлорпроизводном углеводородном растворителе, таком, как бензол, толуол, ксилол, хлорбензол, дихлорметан, хлороформ или дихлорэтан, в простом эфире, таком, как THF, диоксан, дибутиловый эфир, диизопропиловый эфир или DME, в спирте, таком, как метанол, этанол или изопропанол, в кетоне, таком, как ацетон или бутан-2-он, в сложном эфире, таком, как этиловый или бутиловый эфир уксусной кислоты, в нитриле, таком, как ацетонитрил, в амиде, таком, как N,N-диметилформамид или N-метилпирролидин-2-он, или в смеси растворителей при температуре приблизительно от 20 до приблизительно 100°C, например при температуре приблизительно от 40 до приблизительно 80°C. В общем случае для повышения нуклеофильности соединения формулы XIII и/или для связывания кислоты, высвобождаемой при взаимодействии, полезно прибавлять основание, например третичный амин, такой, как триэтиламин, этилдиизопропиламин или N-метилморфолин, или неорганическое основание, такое, как гидрид, гидроксид, карбонат или гидрокарбонат щелочного металла, такой, как гидрид натрия, гидроксид натрия, гидроксид калия, карбонат натрия, карбонат калия, карбонат цезия или гидрокарбонат натрия, или алкоксид, или амид, такой, как метилат натрия, этилат натрия, метилат калия, трет-бутилат калия, амид натрия или диизопропиламид лития. Соединение формулы XII, где FG2 представляет собой гидроксигруппу, перед взаимодействием с соединением формулы XIII также может быть отдельно обработано основанием и превращено в соль. Соединение формулы XII, где FG2 представляет собой гидроксигруппу, может быть превращено в соединение формулы XIV не только взаимодействием с соединением формулы XIII, где FG3 представляет собой, как было указано, уходящую группу, но также и взаимодействием с соответствующим спиртом, т.е. с соединением формулы XIII, где FG3 представляет собой гидроксигруппу, в условиях реакции Мицунобу, известных специалистам в данной области техники. Сочетание соединений формулы XII с соединением формулы XIII по реакции, катализируемой переходным металлом, может быть также осуществлено в условиях катализируемой палладием реакции перекрестного сочетания, такой, как реакция сочетания Хека, Штилле или Судзуки (см. A. de Meijere and F. Diederich (Hrsg.), Metal-Catalyzed Cross-Coupling Reactions (Wiley-VCH, 2004)).
Взаимодействие соединений формулы XIV с соединениями формулы XV для получения соединений формулы XVI может быть осуществлено по реакциям разных типов, как уже было указано ранее, например, по катализируемой при необходимости реакции ароматического замещения, в случае которой FG4 может представлять собой атом лития, остаток галогенида цинка или магния. В общем случае реакцию осуществляют в инертном растворителе, например в углеводородном растворителе, таком, как бензол, толуол, ксилол или хлорбензол, в простом эфире, таком, как тетрагидрофуран (THF), диоксан, дибутиловый эфир, диизопропиловый эфир или 1,2-диметоксиэтан (DME), в амине, таком, как N‚N-диметилформамид (DMF), N,N-диметилацетамид (DMA) или N-метилпирролидин-2-он (NMP), или в смеси растворителей при температуре приблизительно от 20 до приблизительно 250°C, например при температуре приблизительно от 40 до приблизительно 200°C, в зависимости от особенностей соответствующего случая. Реакция может быть осуществлена без катализа или в присутствии каталитической системы, при этом могут быть применены катализаторы, которые могут содержать ион металла или металл в степени окисления 0, при этом предпочтительно применяют железо или палладий. Катализ часто требует присутствия определенных лигандов, образующих с металлами комплексы и только обеспечивающих образование каталитически активных соединений или стабилизирующих их. Комплексы "металл-лиганд" могут прибавляться к реакционной смеси или образовываться in situ. Например, такие каталитические системы могут состоять или быть образованы из комплексов или солей палладия в присутствии лигандов, например из комплексов палладия (0), предпочтительно трис-(дибензилиденацетон)дипалладия (0), или ацетата палладия, трифторацетата палладия или галогенидов палладия, предпочтительно хлорида палладия, в присутствии лигандов, предпочтительно дифосфиновых лигандов, таких, как, например, 2,2'-бис-(дифенилфосфино)-1,1'-бинафтил или 4,5-бис-(дифенилфосфино)-9,9-диметилксантен, или предварительно приготовленного комплекса, такого, как бис-(три-трет-бутилфосфин)палладий (0). К тому же, такие каталитические системы могут содержать также соли железа (III), такие, как, например, ацетилацетонат железа (III). Кроме того, взаимодействие соединений формулы XIV с соединениями формулы XV для получения соединений формулы XVI может быть осуществлено по реакции сочетания типа реакции Судзуки или реакции Штилле, причем FG4 представляет собой уходящую группу, такую, как остаток бороновой кислоты, сложного эфира бороновой кислоты, диалкилборана или триалкилстаннила. Кроме того, взаимодействие соединений формулы XIV с соединениями формулы XV для получения соединений формулы XVI может быть осуществлено по реакции сочетания типа реакции Хека или реакции Соногашира, причем FG4 представляет собой протон, а R2a содержит двойную или тройную связь в соседнем положении со связью с FG4, при этом в отношении двойной или тройной связи, оставшейся после реакции сочетания, сразу или на более поздней стадии осуществляют реакцию гидрирования, которая может быть реализована в стандартных условиях, известных специалистам в данной области техники, в присутствии катализатора, такого, как, например, палладий на активированном угле, в приемлемом инертном растворителе, таком, как, например, этанол или этилацетат, и которая ведет вновь к получению соединений с насыщенным радикалом R2. Эти реакции сочетания типа реакций Судзуки, Штилле, Хека и Соногашира могут быть осуществлены, например, при катализе палладием или в условиях, описанных в литературе (см. A. de Meijere and F. Diederich (Hrsg.), Metal-Catalyzed Cross-Coupling Reactions (Wiley-VCH, 2004)).
Окисление Alk-S-группы в соединениях формулы XVI до сульфокси- или сульфогруппы в соединениях формулы IIa может быть осуществлено пероксидом водорода или пероксикислотой, такой, как 3-хлорпербензойная кислота или монопероксифталевая кислота, в инертном растворителе, например в хлорпроизводном углеводородном растворителе, таком, как дихлорметан или хлороформ, или в сложном эфире, таком, как этиловый или бутиловый эфир уксусной кислоты, при температуре приблизительно от 0 до приблизительно 40°C, например приблизительно при 20°C.
Можно также изменять последовательность стадий при получении соединений формулы I.
Так, например, сначала можно эфир аминомалоновой кислоты формулы IV, такой, как диэтиловый эфир, в присутствии оксида щелочного металла, такого, как этилат натрия, привести во взаимодействие с тиомочевиной, затем алкилировать атом серы, например метилировать метилйодидом, полученное вещество ацилировать соединением формулы V и таким образом получить соединение формулы X.
К тому же, можно, например, соединение формулы XII привести во взаимодействие с соединением формулы XV для получения соединения формулы XVII и последующим взаимодействием последнего соединения с соединением формулы XIII для получения соединения формулы XVI и окислением группировки простого тиоэфира в полученном соединении формулы XVI получить соответствующий сульфоксид или сульфон формулы IIa.
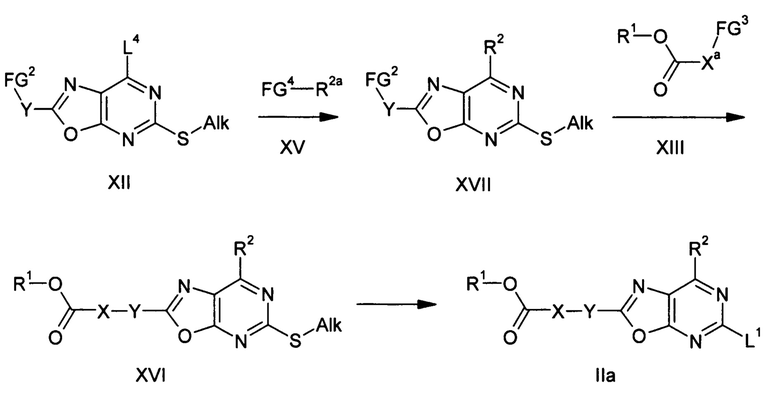
При этом группы X, Y, R1 и R2 в соединениях формул IIa, XII, XIII, XVI и XVII имеют значения, определенные для соединений формулы I, а группы R2a, Xa, L1, L4, FG2, FG3 и FG4 в соединениях формул IIa, XII, XIII, XV и XVII имеют значения, определенные ранее. Превращения могут быть осуществлены в описанных ранее условиях.
По другому способу для синтеза соединений формулы I соединение формулы XVIII приводят во взаимодействие с соединением формулы XV для получения соединения формулы I:
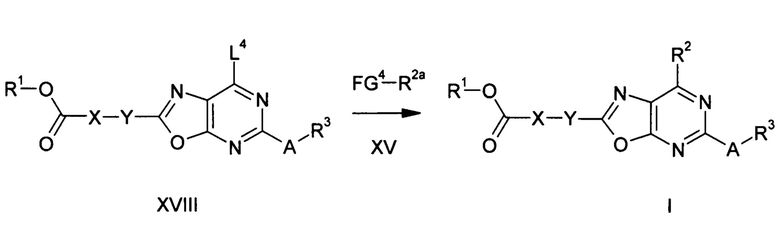
где группы A, X, Y, R1, R2 и R3 в соединениях формулы XVIII имеют значения, определенные для соединений формулы I, и дополнительно могут содержаться функциональные группы в защищенной форме или в форме групп-предшественниц, которые затем превращают в конечные группы. Группы L4, FG4 и R2a в соединениях формул XV и XVII имеют значения, определенные ранее.
Взаимодействие соединений формулы XVIII с соединениями формулы XV для получения соединений формулы I может быть осуществлено по реакциям разных типов, как уже было указано ранее, например, по катализируемой при необходимости реакции ароматического замещения, в случае которой FG4 может представлять собой атом лития, остаток галогенида цинка или магния. В общем случае реакцию осуществляют в инертном растворителе, например в углеводородном растворителе, таком, как бензол, толуол, ксилол или хлорбензол, в простом эфире, таком, как тетрагидрофуран (THF), диоксан, дибутиловый эфир, диизопропиловый эфир или 1,2-диметоксиэтан (DME), в амине, таком, как N‚N-диметилформамид (DMF), N,N-диметилацетамид (DMA) или N-метилпирролидин-2-он (NMP), или в смеси растворителей при температуре приблизительно от -20 до приблизительно 250°C, например при температуре приблизительно от 0 до приблизительно 200°C, в зависимости от особенностей соответствующего случая. Реакция может быть осуществлена без катализа или в присутствии каталитической системы, при этом могут быть применены катализаторы, которые могут содержать ион металла или металл в степени окисления 0, при этом предпочтительно применяют железо или палладий. Катализ часто требует присутствия определенных лигандов, образующих с металлами комплексы и только обеспечивающих образование каталитически активных соединений или стабилизирующих их. Комплексы "металл-лиганд" могут прибавляться к реакционной смеси или образовываться in situ. Например, такие каталитические системы могут состоять или быть образованы из комплексов или солей палладия в присутствии лигандов, например из комплексов палладия (0), предпочтительно трис-(дибензилиденацетон)дипалладия (0), или ацетата палладия, трифторацетата палладия или галогенидов палладия, предпочтительно хлорида палладия, в присутствии лигандов, предпочтительно дифосфиновых лигандов, таких, как, например, 2,2'-бис-(дифенилфосфино)-1,1'-бинафтил или 4,5-бис-(дифенилфосфино)-9,9-диметилксантен, или предварительно приготовленного комплекса, такого, как бис-(три-трет-бутилфосфин)палладий (0). К тому же, такие каталитические системы могут содержать также соли железа (III), такие, как, например, ацетилацетонат железа (III). Кроме того, взаимодействие соединений формулы XVIII с соединениями формулы XV для получения соединений формулы I может быть осуществлено по реакции сочетания типа реакции Судзуки или реакции Штилле, причем FG4 представляет собой уходящую группу, такую, как остаток бороновой кислоты, сложного эфира бороновой кислоты, диалкилборана или триалкилстаннила. Кроме того, взаимодействие соединений формулы XVIII с соединениями формулы XV для получения соединений формулы I может быть осуществлено по реакции сочетания типа реакции Хека или реакции Соногашира, причем FG4 представляет собой протон, а R2a содержит двойную или тройную связь в соседнем положении со связью с FG4, при этом в отношении двойной или тройной связи, оставшейся после реакции сочетания, сразу осуществляют реакцию гидрирования, которая может быть реализована в стандартных условиях, известных специалистам в данной области техники, в присутствии катализатора, такого, как, например, палладий на активированном угле, в приемлемом инертном растворителе, таком, как, например, этанол или этилацетат, и которая ведет вновь к получению соединений с насыщенным радикалом R2. Эти реакции сочетания типа реакций Судзуки, Штилле, Хека и Соногашира могут быть осуществлены, например, при катализе палладием или в условиях, описанных в литературе (см. A. de Meijere and F. Diederich (Hrsg.), Metal-Catalyzed Cross-Coupling Reactions (Wiley-VCH, 2004)).
Исходные соединения формул XV и XVIII получают описанными в литературе способами или аналогично им и во многих случаях имеются в продаже. Соединения формулы XVIII получают превращением соединения формулы XIV, которое может быть получено соответственно описанному ранее, окислением группировки простого тиоэфира в соединении формулы XIV до сульфоксида или сульфона формулы IXX и последующим взаимодействием последнего соединения с соединением формулы III:
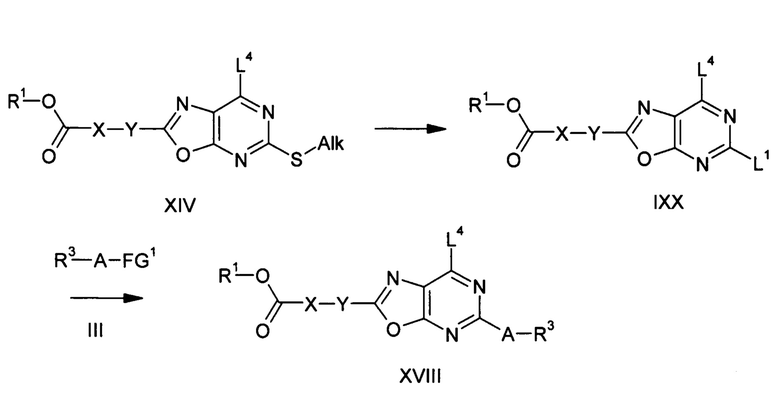
где группы A, X, Y, R1 и R3 в соединениях формул III, XIV, XVIII и IXX имеют значения, определенные для соединений формулы I, и дополнительно могут содержаться функциональные группы в защищенной форме или в форме групп-предшественниц, которые затем превращают в конечные группы. Группа L1 в соединении IXX имеет значения, определенные для соединений IIa, а группы L4 и FG1 в соединениях формул III, XIV, XVIII и IXX имеют значения, определенные ранее.
Окисление Alk-S-группы в соединениях формулы XIV до сульфокси- или сульфогруппы в соединениях формулы IX может быть осуществлено пероксидом водорода или пероксикислотой, такой, как 3-хлорпербензойная кислота или монопероксифталевая кислота, в инертном растворителе, например в хлорпроизводном углеводородном растворителе, таком, как дихлорметан или хлороформ, или в сложном эфире, таком, как этиловый или бутиловый эфир уксусной кислоты, при температуре приблизительно от 0 до приблизительно 40°C, например, приблизительно при 20°C.
Реакция соединений формул IXX и III представляет собой катализируемую при необходимости реакцию ароматического замещения по атому углерода в положении 6 оксазоло[5,4-b]пиримидинового цикла, т.е. в пиримидиновой группировке, и может быть осуществлена в стандартных для реакций такого типа условиях, хорошо известных специалистам в данной области техники. Реакция может быть осуществлена также в присутствии катализаторов, например замещенных бензолсульфинатов щелочных или щелочноземельных металлов, предпочтительно толуолсульфината натрия. В общем случае реакцию осуществляют в инертном растворителе, например в углеводородном растворителе, таком, как бензол, толуол, ксилол или хлорбензол, в простом эфире, таком, как тетрагидрофуран (THF), диоксан, дибутиловый эфир, диизопропиловый эфир или 1,2-диметоксиэтан (DME), в амине, таком, как N‚N-диметилформамид (DMF), N,N-диметилацетамид (DMA) или N-метилпирролидин-2-он (NMP), или в смеси растворителей при температуре приблизительно от -80 до приблизительно 250°C, например при температуре приблизительно от 0 до приблизительно 200°C, в зависимости от особенностей соответствующего случая. В общем случае для повышения реакционной способности полезно прибавлять основание, например третичный амин, такой, как триэтиламин, этилдиизопропиламин или N-метилморфолин, или неорганическое основание, такое, как гидрид, гидроксид, карбонат или гидрокарбонат щелочно-земельного металла, такой, как гидрид натрия, гидроксид натрия, гидроксид калия, карбонат натрия, карбонат калия, карбонат цезия или гидрокарбонат натрия, или алкоксид, или амид, такой, как метилат натрия, этилат натрия, метилат калия, трет-бутилат калия, амид натрия или диизопропиламид лития. Соединение формулы III, где FG1 представляет собой протон, перед взаимодействием с соединением формулы II также может быть отдельно обработано основанием и превращено в соль. Реакция с соединениями формулы III, в которой FG1 представляет собой атом лития, остаток галогенида цинка или магния, а A означает связь или группу -CH2-, может быть катализирована также солями железа (III), такими, как, например, ацетилацетонат железа (III).
Альтернативно может быть осуществлено также прямое взаимодействие соединений формулы XIV с соединениями формулы III для получения соединений формулы XVIII, когда FG1 представляет собой остаток бороновой кислоты или эфира бороновой кислоты, или триалкилстаннила, а A означает связь или группу -CH2-. Это превращение может быть катализировано каталитическими системами, которые содержат медь или соли меди (I), предпочтительно галогениды меди (I) или карбоксилаты меди (I), предпочтительно йодид меди (I) или тиофенкарбоксилат меди (I), или также предварительно приготовленные комплексы меди (I), например тетракис-(ацетонитрил)гексафторфосфат меди (I), индивидуально или в присутствии лигандов, например диаминовых лигандов или 1,10-фенантролина. В общем случае реакцию осуществляют в инертном растворителе, например в углеводородном растворителе, таком, как бензол, толуол, ксилол или хлорбензол, в простом эфире, таком, как тетрагидрофуран (THF), диоксан, дибутиловый эфир, диизопропиловый эфир или 1,2-диметоксиэтан (DME), в амине, таком, как N‚N-диметилформамид (DMF), N,N-диметилацетамид (DMA) или N-метилпирролидин-2-он (NMP), или в смеси растворителей при температуре приблизительно от 20 до приблизительно 250°C, например при температуре приблизительно от 0 до приблизительно 200°C, в зависимости от особенностей соответствующего случая.
Можно также изменять последовательность стадий при получении соединений формулы I.
Так, например, можно сначала соединение формулы XII превратить в соединение формулы XX, затем это соединение привести во взаимодействие с соединением формулы III для получения соединения формулы XXI, далее последнее соединение привести во взаимодействие с соединением формулы XIII для получения соединения формулы XVIII.
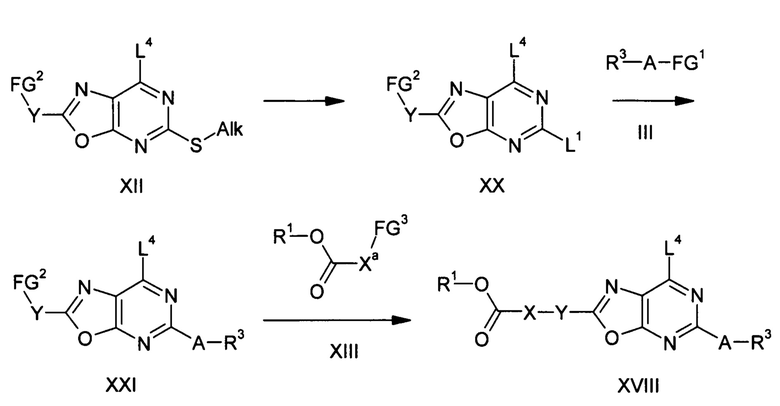
При этом группы A, X, Y, R1 и R3 в соединениях формул III, XII, XIII, XVIII, XX и XXI имеют значения, определенные для соединений формулы I, группа L1 в соединении формулы XX имеет значения, определенные для соединений IIa, а группы Xa, L4, FG1, FG2 и FG3 в соединениях формул III, XII, XIII, XVIII, XX и XXI имеют значения, определенные ранее. Превращения могут быть осуществлены в описанных ранее условиях. Альтернативно может быть осуществлено также прямое взаимодействие соединений формулы XII с соединениями формулы III для получения соединений формулы XXI, когда FG1 представляет собой остаток бороновой кислоты или эфира бороновой кислоты или триалкилстаннила, а A означает связь или группу -CH2-.
Альтернативно соединения формулы XVIIIa, т.е. соединения, в которых A означает связь или группу CH2-, получают взаимодействием эфира аминомалоновой кислоты формулы IV с активированным производным карбоновой кислоты формулы V для получения соединения формулы VI, взаимодействием последнего соединения с амидином формулы XXIIa для получения соединения формулы XXIIIa, циклизацией последнего соединения с образованием системы оксазоло[5,4-d]пиримидинового цикла для получения соединения формулы XXIVa, превращением последнего соединения в соединение формулы XXIa и последующим введением остатка R1O-C(O)-X- взаимодействием с соединением формулы XIII.
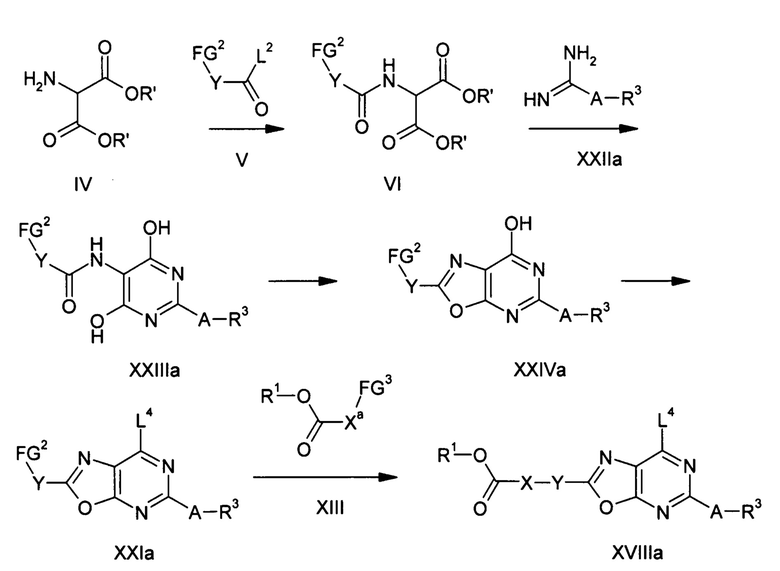
При этом группы X, Y, R1 и R3 в соединениях формул V, VI, XIII, XVIIIa, XXIa, XXIIa, XXIIIa и XXIVa имеют значения, определенные для соединений формулы I, группа A в соединениях формул XVIIIa, XXIa, XXIIa, XXIIIa и XXIVa означает связь или группу CH2-, а значения групп R', Xa, L2, L4, FG2 и FG3 в соединениях формул IV, V, VI, XIII, XVIIIa, XXIa, XXIIa, XXIIIa и XXIVa имеют значения, определенные ранее.
Взаимодействие соединений IV и V для получения соединения VI осуществляют соответственно уже описанному ранее. Взаимодействие соединений формулы VI с соединениями формулы XXIIa в общем случае осуществляют в инертном растворителе, например в спирте, таком, как метанол, этанол или изопропанол, или в простом эфире, таком, как THF, диоксан или DME, или в смеси растворителей при температуре приблизительно от 20 до приблизительно 200°C, например при температуре приблизительно от 20 до приблизительно 100°C, в присутствии основания, например алкоксида, такого, как метилат натрия, этилат натрия, метилат калия или трет-бутилат калия. При этом амидин формулы XXIIa может быть использован также в виде соли, например в виде гидрохлорида. Циклизация соединений формулы XXIIIa для получения соединений формулы XXIVa и превращение в соединения формулы XXIa может быть осуществлена в условиях, описанных ранее для случая превращения соединений формулы X в соединения формулы XI и превращения соединений формулы XI в соединения формулы XII. Взаимодействие соединений формулы XXIa с соединениями формулы XIII для получения соединений формулы XVIIIa может быть осуществлено в условиях, описанных ранее для случая взаимодействия соединений формулы XII с соединениями формулы XIII для получения соединений формулы XIV.
По другому способу для синтеза соединений формулы I соединение формулы XXV приводят во взаимодействие с соединением формулы XIII для получения соединения формулы I:
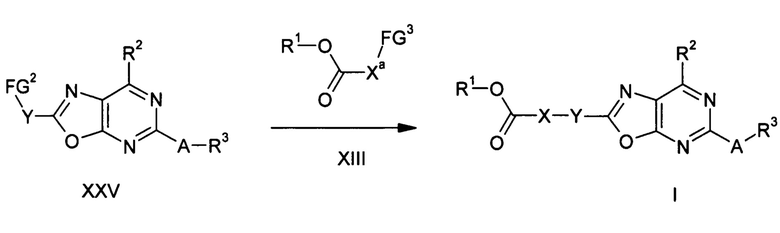
где группы A, X, Y, R1, R2 и R3 в соединениях формул XIII и XXV имеют значения, определенные для соединений формулы I, и дополнительно могут содержаться функциональные группы в защищенной форме или в форме групп-предшественниц, которые затем превращают в конечные группы. Группы Xa, FG2 и FG3 в соединениях формул XIII и XXV имеют значения, определенные ранее.
Превращение соединений формулы XXV в соединения формулы I может быть осуществлено в условиях, уже описанных ранее для случая превращения соединений формулы XII в соединения формулы XIV.
Исходные соединения формул XXV и XIII получают описанными в литературе способами или аналогично им и во многих случаях имеются в продаже. Соединения формулы XXV получают превращением соединения формулы XIV, которое может быть получено соответственно описанному ранее, в соединение формулы XXVI и последующим взаимодействием последнего соединения с соединением формулы III:
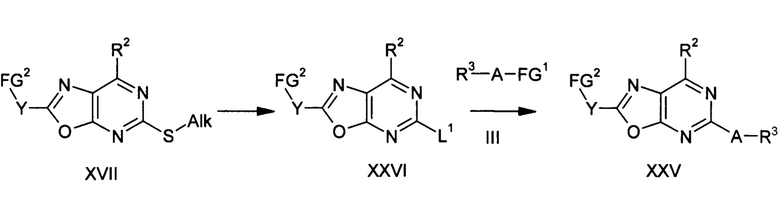
где группы A, Y, R2 и R3 в соединениях формул III, XVII, XXV и XXV имеют значения, определенные для соединений формулы I, и дополнительно могут содержаться функциональные группы в защищенной форме или в форме групп-предшественниц, которые затем превращают в конечные группы. Группа L1 в соединении XXVI имеет значения, определенные для соединений IIa, а группы FG1 и FG2 в соединениях формул III, XVII, XXV и XXVI имеют значения, определенные ранее.
При этом превращение соединения формулы XVII в соединение формулы XXVI может быть осуществлено в условиях, уже описанных ранее для случая превращения соединений формулы XVI в соединения формулы IIa. Взаимодействие соединений формулы XXVI с соединениями формулы III для получения соединений формулы XXV может быть осуществлено в условиях, уже описанных ранее для случая превращения соединений формулы IIa в соединения формулы I.
К тому же, соединения формулы XXV получают взаимодействием соединения формулы XXI, которое может быть получено соответственно описанному ранее, с соединением формулы XV:
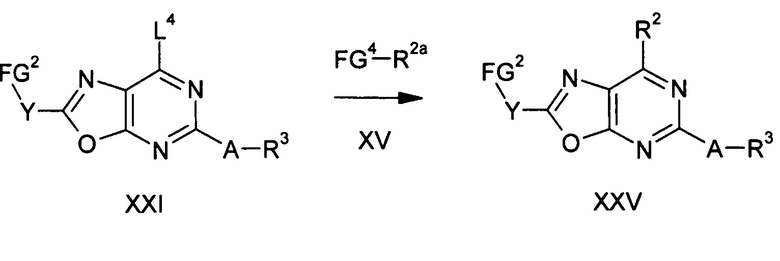
где группы A, Y, R2 и R3 в соединениях формул XXI и XXV имеют значения, определенные для соединений формулы I, и дополнительно могут содержаться функциональные группы в защищенной форме или в форме групп-предшественниц, которые затем превращают в конечные группы. Группы L4, R2a, FG2 и FG4 в соединениях формул XV, XXI и XXV имеют значения, определенные ранее.
Взаимодействие соединений формулы XXI с соединениями формулы XV для получения соединений формулы XXV может быть осуществлено в условиях, уже описанных ранее для случая превращения соединений формулы XIV в соединения формулы XIV.
Другие соединения формулы I получают из приемлемых соединений, получаемых описанными ранее способами путем функционализации или модификации содержащихся функциональных групп стандартными способами, например образованием сложных эфиров, амидированием, гидролизом, образованием простых эфиров, алкилированием, ацилированием, сульфонилированием, восстановлением, окислением, превращением в соли и т.д. Так, например, гидроксигруппа, которая может быть высвобождена из группы простого эфира расщеплением простого эфира, например, посредством бортрибромида или из защищенной гидроксигруппы путем снятия защиты, может быть связана с образованием эфира карбоновой или сульфоновой кислоты. Этерификация гидроксигрупп с образованием простых эфиров может быть осуществлена в предпочтительном случае алкилированием соответствующим галогенпроизводным соединением, например бромидом или йодидом, в присутствии основания, например карбоната щелочного металла, такого, как карбонат калия или карбонат цезия, в инертном растворителе, например в амиде, таком, как DMF или NMP, или в кетоне, таком, как ацетон или бутан-2-он, или в соответствующем спирте в рассмотренных ранее условиях реакции Мицунобу. Гидроксигруппа может быть превращена в галогенид обработкой галогенирующим средством. Атом галогена по реакции замещения, которая может представлять собой также реакцию, катализируемую переходным металлом, может быть замещен различными группами. Нитрогруппа может быть восстановлена до аминогруппы, например, каталитическим гидрированием. Аминогруппа может быть модифицирована в стандартных условиях алкилирования, например взаимодействием с галогенпроизводным соединением или восстановительным аминированием карбонильного соединения, или ацилирования или сульфонилирования, например взаимодействием с реакционноспособным производным карбоновой кислоты, таким, как хлорангидрид или ангидрид кислоты, или сульфохлорид, или с активированной карбоновой кислотой, полученной из карбоновой кислоты, например, обработкой связывающим агентом, таким, как N,N'-карбонилдиимидазол (CDI), карбодиимид, такой, как 1,3-дициклогексилкарбодиимид (DCC) или гидрохлорид 1-(3-диметиламинопропил)-3-этилкарбодиимида (EDC), гексафторфосфат O-(7-азабензотриазол-1-ил)-N,N,N',N'-тетраметилурония (HATU), тетрафторборат O-(циано(этоксикарбонил)метиленамино)-N,N,N',N'-тетраметилурония (TOTU) или тетрафторборат [(бензотриазол-1-илокси)диметиламинометилен]диметиламмония (TBTU). Группа сложного эфира карбоновой кислоты может быть гидролизована в кислых или щелочных условиях с высвобождением карбоновой кислоты. Группа карбоновой кислоты может быть, как было указано ранее, активирована или превращена в реакционноспособное производное и взаимодействием со спиртом или амином или аммиаком превращена в группу сложного эфира или амидную группу. Первичный амид может быть дегидратирован до нитрила. Атом серы, например в алкил-S-группе или в гетероцикле, может быть окислен пероксидом, таким, как пероксид водорода или пероксикислота, до сульфоксидной группировки S(O) или сульфоновой группировки S(O)2. Группа карбоновой кислоты, группа сложного эфира карбоновой кислоты и кетогруппа могут быть восстановлены до спиртовой группы, например, посредством комплексного гидрида, такого, как алюмогидрид лития, борогидрид лития или борогидрид натрия. Соединение формулы I или промежуточное соединение, такое, как соединение формулы II, которое в группе X содержит двойную или тройную связь и которое соответственно описанному ранее может быть легко получено по катализируемой переходным металлом реакции сочетания соединения формулы XIV с двойной или тройной связью в группе Xa и соединения формулы XIII, может быть превращено гидрированием в присутствии катализатора гидрирования, такого, как палладиевый катализатор, в соединение, в котором X представляет собой насыщенную группу.
Все реакции, осуществляемые при описанных ранее синтезах соединений формулы I, по существу хорошо известны специалистам в данной области техники и могут быть осуществлены в стандартных условиях согласно или аналогично способам, описанным в литературе, например, в Houben-Weyl, Methoden der Organischen Chemie (Методы органической химии), Thieme-Verlag, Stuttgart, или в Organic Reactions, John Wiley & Sons, New York. При необходимости полученные соединения формулы I, а также возможные промежуточные соединения могут быть очищены традиционными способами очистки, например перекристаллизацией или хроматографией. Как уже было упомянуто, любые применяемые при описанных ранее синтезах исходные и промежуточные соединения, которые содержат кислотные или основные группы, могут быть использованы также в форме солей, и любые промежуточные и конечные целевые соединения также могут быть получены в форме солей. Так же, как было указано ранее, в зависимости от обстоятельств соответствующего случая для предотвращения нежелательного течения реакции или побочных реакций в ходе синтеза соединений в общем случае может быть необходимо или полезно временно блокировать функциональные группы введением защитных групп и снимать с них защиту на более поздней стадии синтеза или вводить в реакцию функциональные группы в форме групп-предшественниц, которые затем превращают в требуемые функциональные группы. В качестве примеров защитных групп следует упомянуть аминозащитные группы, в случае которых ацильные или алкилоксикарбонильные группы представляют собой, например, трет-бутилоксикарбонильную группу (= Boc), которая может быть отщеплена обработкой трифторуксусной кислотой (= TFA), бензилоксикарбонильную группу, которая может быть отщеплена каталитическим гидрированием, или флуорен-9-илметоксикарбонильную группу, которая может быть отщеплена обработкой пиперидином, и защитные группы карбоксигруппы, которые могут быть защищены в виде сложноэфирных групп, таких, как трет-бутиловый эфир, защитное действие которого может быть устранено обработкой трифторуксусной кислотой, или бензиловый эфир, защитное действие которого может быть устранено каталитическим гидрированием. В качестве примера группы-предшественницы следует упомянуть нитрогруппу, которая восстановлением, например каталитическим гидрированием, может быть превращена в аминогруппу. Такого типа стратегии синтеза, защитные группы и группы-предшественницы, которые являются приемлемыми в соответствующих случаях, известны специалистам в данной области техники.
Другими объектами настоящего изобретения являются новые исходные и промежуточные соединения, которые применяются при синтезе соединений формулы I, включая соединения формул II, III, IV, V, VI, VII, VIII, IX, X, XI, XII, XIII, XIV, XV, XVI, XVII, XVIII, IXX, XX, XXI, XXII, XXIII, XXIV, XXV и XXVI, где Alk, A, X, Xa, R1, R2, R2a, R3, FG1, FG2, FG3, FG4, L1, L2, L3 и L4 имеют значения, определенные ранее, в любых своих стереоизомерных формах или в виде смеси стереоизомерных форм в любом соотношении и их соли и сольваты соединений такого типа или солей такого типа и их применение в качестве промежуточных соединений. Изобретение относится также к любым таутомерным формам промежуточных и исходных соединений. Все пояснения и варианты осуществления, приведенные ранее в отношении соединений формулы I, соответственным образом относятся также и к промежуточным и исходным соединениям. Объектами настоящего изобретения являются, в частности, новые специфические исходные и промежуточные соединения, описанные в данном тексте. Независимо от того, описаны ли они в данном тексте в качестве свободных соединений и/или в качестве специфических солей, они, как в форме свободных соединений, так и в форме своих солей, а в случае описания специфических солей дополнительно в форме этих специфических солей, и в форме сольватов соединений такого типа или солей такого типа являются объектами настоящего изобретения.
Соединения формулы I, применяемые при необходимости в комбинации с другими фармакологически активными соединениями, могут вводиться животным, предпочтительно млекопитающим, включая человека, в виде лекарственных средств в индивидуальной форме, в смеси друг с другом или в форме фармацевтических композиций. Введение может осуществляться орально, например в форме таблеток, таблеток‚ покрытых оболочкой, драже, гранул, жестких и мягких желатиновых капсул, растворов, включая водные, спиртовые и масляные растворы, соки, капли, сиропы, эмульсии или суспензии, ректально, например в форме суппозиториев, или парентерально, например в форме растворов для подкожных, внутримышечных или внутривенных инъекций или инфузий, предпочтительно в форме водных растворов. Соединения формулы I могут, к тому же, применяться в вариантах местного введения лекарственных средств, например, в форме покрытых стентов для предотвращения или уменьшения рестеноза или путем местного применения посредством катетеров. Приемлемая форма введения зависит также от заболевания, подлежащего лечению, и его тяжести.
Введение соединений формулы I может осуществляться также топически. Приемлемые фармацевтические композиции для топического применения на коже предпочтительно представляют собой мазь, крем, лосьон, пасту, гель, гидрогель, спрей, аэрозоль или масло. В качестве носителя могут быть использованы вазелин, ланолин, полиэтиленгликоль, спирты и комбинации двух или нескольких этих веществ. В общем случае активное вещество содержится в композиции с концентрацией от 0,0001 до 15% масс., например от 0,0005 до 2%. В одном из вариантов осуществления композиция для топического применения представляет собой гель. В одном из других вариантов осуществления композиция для топического применения представляет собой гидрогель. Под гидрогелем понимают содержащий воду, но нерастворимый в воде полимер, молекулы которого химически, например посредством ковалентных или ионных связей, или физически, например посредством образования петель полимерных цепей, связаны в трехмерную сетчатую структуру. Благодаря встроенным гидрофильным полимерным компонентам он набухает в воде со значительным увеличением объема, но не теряя своей вещественной связанности. Гидрогель состоит, например, из гидрофильного растворителя (например, воды), регулятора влажности (например, глицерина) и гелеобразователя (например, кроскармеллозы натрия).
В приведенных далее примерах показаны приемлемые гелевые композиции.
Гидрогели представляют собой композиции для применения на коже. Гидрогели могут наноситься на открытые участки ран. Гидрогели содержат лекарственное вещество в растворенной форме, вследствие чего обеспечивается быстрое проникновение в кожу и ткани. Благодаря асептическому процессу изготовления при нанесении лекарственного средства в рану не попадают дополнительные микробиологические загрязнения. В одном из вариантов осуществления в гидрогель дополнительно вводят консервирующее средство (метил- и пропилпарабены) с целью поддержания низкой степени микробной обсемененности.
В одном из вариантов осуществления гидрогель содержит соединения формулы I с концентрацией 0,04-0,0004% (масс./масс.).
Асептический гидрогель хранят в приемлемых стерильных сосудах. В одном из вариантов осуществления гидрогель хранят в стерильных сосудах из полипропилена.
Количество соединения формулы I и/или его физиологически приемлемых солей и/или сольватов в фармацевтических композициях стандартно составляет приблизительно от 0,2 до приблизительно 800 мг, например приблизительно от 0,5 до приблизительно 500 мг, например приблизительно от 1 до приблизительно 200 мг, в одной стандартной дозе, но в зависимости от типа фармацевтической композиции также может быть более высокой. Фармацевтические композиции содержат, как правило, приблизительно от 0,5 до приблизительно 90% масс. соединения формулы I и/или его физиологически приемлемых солей и/или сольватов. Фармацевтические композиции могут быть изготовлены по существу известными способами. С этой целью одно или несколько соединений формулы I и/или его физиологически приемлемые соли и/или сольваты смешивают с одним или несколькими твердыми или жидкими фармацевтическими веществами-носителями или лекарственными основами и/или дополнительными или вспомогательными веществами, а в случае, когда требуется комбинированное лекарственное средство, с другими фармакологически активными соединениями, обладающими терапевтическим или профилактическим действием, в приемлемой для введения и дозировки форме, которая затем может быть использована в медицине или ветеринарии. В качестве веществ-носителей и добавок могут быть использованы приемлемые органические и неорганические вещества, которые с соединениями формулы I или их физиологически приемлемыми солями или сольватами не реагируют нежелательным образом. В качестве примеров типовых добавок, которые могут содержаться в фармацевтических композициях и лекарственных средствах, следует назвать скользящие добавки, консерванты, загустители, стабилизаторы, дезинтеграторы, смачиватели, средства для достижения эффекта депо, эмульгаторы, соли, например для влияния на осмотическое давление, буферирующие вещества, красители, вкусовые добавки и ароматические вещества. Примеры веществ-носителей и добавок представляют собой вода, физиологический раствор хлорида натрия, растительные масла, воски, спирты, такие, как этанол, изопропанол, 1,2-пропандиол, бензиловый спирт или глицерин, полиолы, маннит, полиэтиленгликоль, полипропиленгликоль, глицеринтриацетат, поливинилпирролидон, желатина, целлюлоза, углеводы, такие, как лактоза, глюкоза, сахароза или крахмал, такой, как кукурузный крахмал, стеариновая кислота и соли стеариновой кислоты, такие, как стеарат магния, тальк, ланолин, вазелин или их смеси, например смеси воды с одним или несколькими органическими растворителями, такие, как смеси воды со спиртами. Соединения формулы I и их физиологически приемлемые соли и сольваты можно также лиофилизировать, а полученные лиофилизаты использовать, например, для получения композиций для инъекций.
Дозировка вводимого соединения формулы I и/или его физиологически приемлемой соли и/или сольвата зависит от конкретного случая и, согласно принятой практике, для достижения оптимального действия должна быть адаптирована врачом к индивидуальным условиям соответственно традиционным правилам и способам. Так, например, она зависит от вида и тяжести подлежащего лечению нарушения, от пола, возраста, массы и индивидуальной реакции подвергаемого лечению человека или животного, от эффективности и длительности действия применяемого соединения, от того, направлено ли лечение на терапию острого или хронического заболевания или на профилактику, или от того, применяются ли помимо соединения формулы I другие активные вещества. В общем случае суточная доза составляет, например, приблизительно от 0,01 до приблизительно 100 мг/кг или приблизительно от 0,1 до приблизительно 10 мг/кг, или приблизительно от 0,3 до приблизительно 5 мг/кг (мг на кг массы тела) для введения взрослому пациенту массой 75 кг с целью достижения требуемых результатов. При этом суточная доза может быть введена в виде одной стандартной дозы или, предпочтительно при введении в более значительном количестве, разделена на несколько доз, например на две, три или четыре стандартные дозы. Введение может быть осуществлено также в непрерывном режиме, например в виде непрерывной инфузии или инъекции. В конкретном случае в зависимости от индивидуальных показателей может потребоваться повышение или понижение указанных дозировок.
Настоящее изобретение поясняется примерами, приведенными далее.
Когда экспериментальные соединения, содержавшие основные группы, очищали препаративной высокоэффективной хроматографией (ВЭЖХ) на колонке с обращенной фазой (колонки с RP-материалом), и элюент, согласно принятой практике, представлял собой градиентную смесь воды и ацетонитрила с трифторуксусной кислотой (TFA), их получали в зависимости от особенностей обработки, таких, как упаривание или условия лиофилизации, частично в форме кислотно-аддитивных солей трифторуксусной кислоты. В названиях экспериментальных соединений и в их структурных формулах трифторуксусная кислота, содержащаяся в любом таком виде, не указана.
Полученные соединения в общем случае были охарактеризованы спектроскопическими и хроматографическими данными, в частности масс-спектрами (МС) и значениями времени удерживания при ВЭЖХ (Rt, мин), которые были получены комбинированным анализом ВЭЖХ/МС (ЖХ/МС), и/или спектрами ЯМР (ЯМР=ядерный магнитный резонанс). При исследовании способом ЯМР указаны химический сдвиг δ (м.д.), число атомов водорода и мультиплетность (с=синглет, д=дублет, дд=дублет дублетов, т=триплет, дт=дублет триплетов, к=квартет, м=мультиплет, уш.=уширенный) сигналов. При исследовании способом МС в общем случае указано массовое число (m/z) пика молекулярного иона M, например M+, или родственного иона, такого, как ион M+1, например [M+1]+, т.е. протонированного молекулярного иона [M+H]+, образовавшегося в зависимости от применяемого способа ионизации. Способ ионизации в общем случае представлял собой ионизацию электрораспылением (ESI). ЖХ/МС осуществляли в описанных далее условиях.
Способ LC1
Колонка: Phenomenex, 4 мкМ, 10×2 мм, 1,7 мкм; расход: 1,1 мл/мин; элюент A: вода+0,05% трифторуксусной кислоты; элюент B: ацетонитрил; градиент: от 93% A+7% B до 5% A+95% B в течение 1,2 мин, затем 5% A+95% B в течение 0,2 мин; способ ионизации при МС: ESI+.
Способ LC2
Колонка: UPLC BEH C18, 50×2,1 мм, 1,7 мкм; расход: 0,9 мл/мин; элюент A: вода+0,1% муравьиной кислоты; элюент B: ацетонитрил+0,08% муравьиной кислоты; градиент: от 95% A+5% B до 5% A+95% B в течение 1,1 мин, затем 5% A+95% B в течение 0,6 мин; способ ионизации при МС: ESI+.
Способ LC3
Колонка: UPLC BEH C18, 50×2,1 мм, 1,7 мкм; расход: 0,9 мл/мин; элюент A: вода+0,05% муравьиной кислоты; элюент B: ацетонитрил+0,035% муравьиной кислоты; градиент: от 95% A+5% B до 5% A+95% B в течение 1,1 мин, затем 5% A+95% B в течение 0,6 мин; способ ионизации при МС: ESI+.
Способ LC4
Колонка: Phenomenex, 4 мкМ, 10×2 мм, 1,7 мкм; расход: 1,1 мл/мин; элюент A: вода+0,05% трифторуксусной кислоты; элюент B: ацетонитрил; градиент: от 80% A+20% B до 5% A+95% B в течение 0,8 мин, затем 5% A+95% B в течение 0,6 мин; способ ионизации при МС: ESI+.
Пример 1
{4-[5-(2,5-Дифторфенокси)-7-пропилоксазоло[5,4-d]пиримидин-2-ил]-2,6-диметилфенокси}уксусная кислота
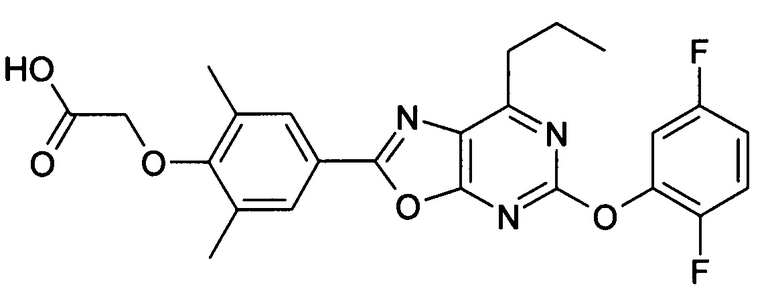
(a) Диэтиловый эфир 2-(4-метокси-3,5-диметилбензоиламино)малоновой кислоты
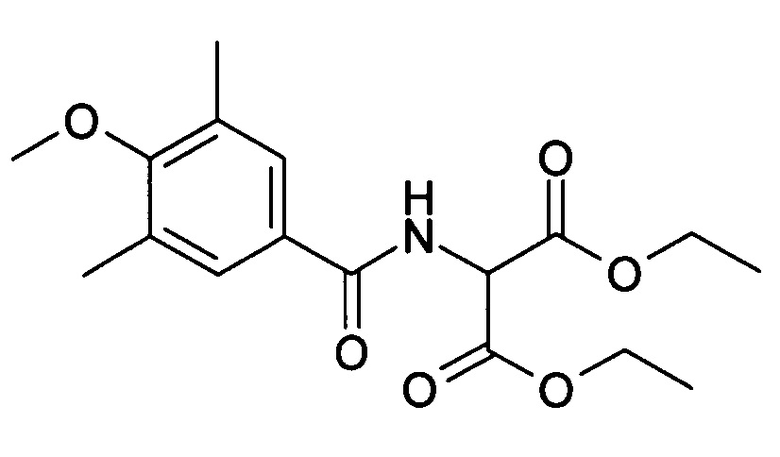
58,4 г гидрохлорида диэтилового эфира аминомалоновой кислоты суспендировали в 300 мл дихлорметана и при охлаждении льдом смешивали с 115 мл триэтиламина. Затем при 0°C по каплям прибавляли 54,8 г 4-метокси-3,5-диметилбензоилхлорида в 250 мл дихлорметана. Через 2 часа при 0°C по каплям прибавляли 100 мл воды, водный слой отделяли и из него осуществляли экстракцию 200 мл дихлорметана. Объединенные органические фракции встряхивали сначала с 2 M водным раствором соляной кислоты и затем с водой, сушили над сульфатом натрия, фильтровали и сгущали. Остаток растирали с метил-трет-бутиловым эфиром, отделяли фильтрованием под вакуумом и сушили в вакууме. Было получено 89,3 г (96%) указанного в заголовке соединения, которое далее использовали без последующей очистки.
ЖХ/МС (способ LC1): Rt=0,94 мин; m/z=338,10 [M+H]+.
(b) 4,6-Дигидрокси-5-(4-метокси-3,5-диметилбензоиламино)пиримидин-2-тиолат натрия
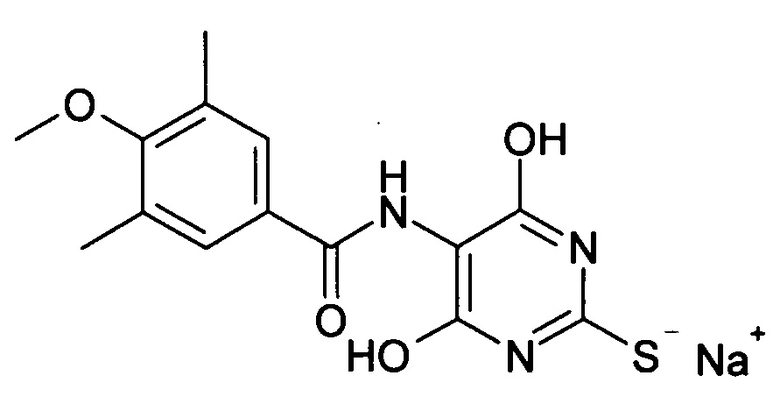
20,6 г тиомочевины суспендировали в 900 мл безводного этанола и прибавляли 75 мл раствора метилата натрия (30%-ный раствор в метаноле). Через 15 мин порциями вносили 91,0 г диэтилового эфира 2-(4-метокси-3,5-диметилбензоиламино)малоновой кислоты. Сначала образовывался прозрачный раствор, из которого вскоре выпадал осадок слегка желтого цвета. Затем реакционную смесь перемешивали в течение 3 часов при 60°C. Твердое вещество, выпавшее в осадок, при комнатной температуре отделяли фильтрованием под вакуумом, промывали приблизительно 100 мл этанола и затем диэтиловым эфиром и сушили в вакууме. Было получено 78,3 г (84%) указанного в заголовке соединения, которое далее использовали без последующей очистки.
ЖХ/МС (способ LC1): Rt=0,41 мин; m/z=322,05 [M-Na+2H]+.
(c) N-(4,6-Дигидрокси-2-метилсульфанилпиримидин-5-ил)-4-метокси-3,5-диметилбензамид
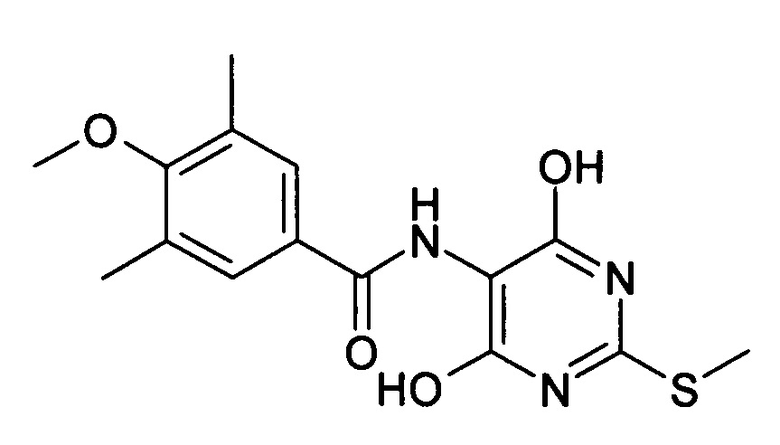
22,78 г гидроксида натрия вносили в 735 мл воды, охлажденной до 0°C, затем прибавляли 78,21 г 4,6-дигидрокси-5-(4-метокси-3,5-диметилбензоиламино)пиримидин-2-тиолата натрия и 365 мл N-метил-2-пирролидона и через 30 мин при 0°C по каплям прибавляли 14,2 мл метилйодида. Через 2 часа при 0°C реакционную смесь осторожно доводили до pH=2 концентрированным водным раствором соляной кислоты. Затем прибавляли приблизительно 200 мл воды, твердое вещество, выпавшее в осадок, отделяли фильтрованием под вакуумом, промывали водой до нейтральной реакции и сушили в вакууме. Было получено 50,89 г (67%) указанного в заголовке соединения, которое далее использовали без последующей очистки.
ЖХ/МС (способ LC1): Rt=0,66 мин; m/z=336,05 [M+H]+.
(d) 7-Хлор-2-(4-метокси-3,5-диметилфенил)-5-метилсульфанилоксазоло[5,4-d]пиримидин
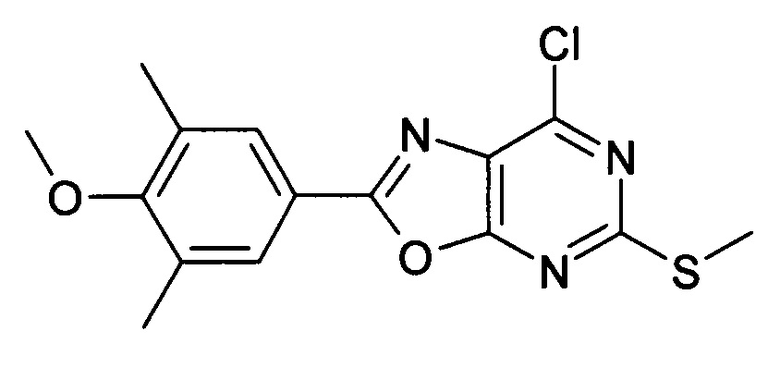
45,95 г N-(4,6-дигидрокси-2-метилсульфанилпиримидин-5-ил)-4-метокси-3,5-диметилбензамида при комнатной температуре при перемешивании суспендировали в 125 мл оксихлорида фосфора и нагревали в течение 36 часов при 70°C. После охлаждения реакционную смесь фильтровали под вакуумом через пористый стеклянный фильтр, полученное твердое вещество желтого цвета при перемешивании вносили в насыщенный водный раствор гидросульфата натрия и перемешивали в течение 10 мин. Затем твердое вещество отделяли фильтрованием под вакуумом, промывали до нейтральной реакции и сушили. Таким образом, было получено 10,47 г (22%) указанного в заголовке соединения, которое далее использовали без последующей очистки.
ЖХ/МС (способ LC4): Rt=0,88 мин; m/z=336,00 [M+H]+.
(e) 4-(7-Хлор-5-метилсульфанилоксазоло[5,4-d]пиримидин-2-ил)-2,6-диметилфенол
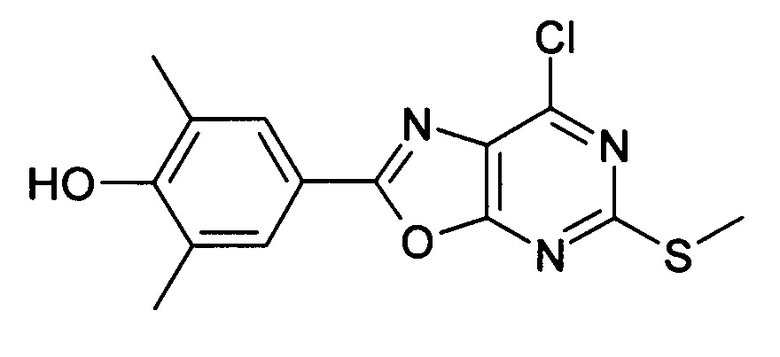
К раствору 6,72 г 7-хлор-2-(4-метокси-3,5-диметилфенил)-5-метилсульфанилоксазоло[5,4-d]пиримидина в 140 мл дихлорметана при -20°C и при перемешивании по каплям прибавляли 5,30 г бортрибромида. Реакционную смесь доводили до комнатной температуры и перемешивали в течение 2 часов. Затем при охлаждении льдом по каплям прибавляли еще 1,33 г бортрибромида. Далее через 2 часа реакционную смесь снова охлаждали до -20°C и по каплям осторожно прибавляли насыщенный водный раствор гидрокарбоната натрия. Слои разделяли при комнатной температуре. Органическую фракцию промывали водой, сушили над сульфатом натрия, фильтровали и сгущали в вакууме. Остаток растирали с диизопропиловым эфиром, отделяли фильтрованием под вакуумом и сушили на воздухе. Было получено 6,20 г (96%) указанного в заголовке соединения, которое далее использовали без последующей очистки.
ЖХ/МС (способ LC1): Rt=1,12 мин; m/z=322,10 [M+H]+.
(f) трет-Бутиловый эфир [4-(7-хлор-5-метилсульфанилоксазоло[5,4-d]пиримидин-2-ил)-2,6-диметилфенокси]уксусной кислоты
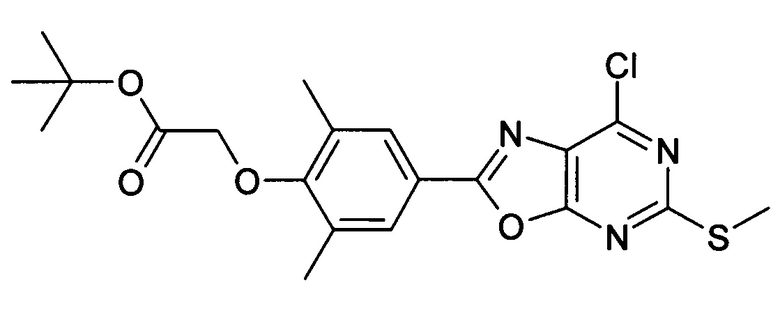
Раствор 4,34 г 4-(7-хлор-5-метилсульфанилоксазоло[5,4-d]пиримидин-2-ил)-2,6-диметилфенола в 45 мл диметилформамида смешивали с 7,46 г карбоната калия и затем прибавляли 2,90 г трет-бутилового эфира бромуксусной кислоты. Смесь перемешивали в течение 1 ч при 60°C. Затем охлажденную реакционную смесь выливали в ледяную воду, твердое вещество, выпавшее в осадок, отделяли фильтрованием под вакуумом и промывали водой. Твердое вещество растворяли в дихлорметане, сушили над сульфатом натрия, смешивали с активированным углем, фильтровали и сгущали в вакууме. Было получено 4,20 г (71%) указанного в заголовке соединения, которое далее использовали без последующей очистки.
ЖХ/МС (способ LC1): Rt=1,28 мин; m/z=436,10 [M+H]+.
(g) трет-Бутиловый эфир [2,6-диметил-4-(5-метилсульфанил-7-пропилоксазоло[5,4-d]пиримидин-2-ил)фенокси]уксусной кислоты
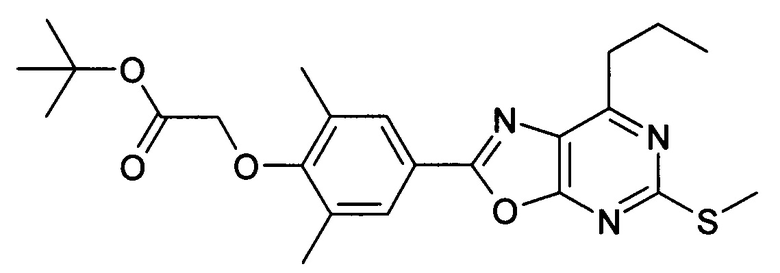
К раствору 1,09 г трет-бутилового эфира [4-(7-хлор-5-метилсульфанилоксазоло[5,4-d]пиримидин-2-ил)-2,6-диметилфенокси]уксусной кислоты и 44 мг ацетилацетоната железа (III) в 100 мл безводного тетрагидрофурана в атмосфере аргона и при -78°C по каплям медленно прибавляли 1,38 мл 2,0 M раствора н-пропилмагнийбромида в тетрагидрофуране. Реакционной смеси давали стоять в течение часа при комнатной температуре и далее перемешивали в течение двух часов. Затем к реакционной смеси прибавляли диэтиловый эфир и при охлаждении льдом смешивали с 10%-ным водным раствором гидросульфата натрия. Далее слои разделяли и из водного слоя два раза осуществляли экстракцию диэтиловым эфиром. Объединенные органические фракции промывали водой, сушили над сульфатом натрия, фильтровали и сгущали в вакууме. Из неочищенного конечного вещества хроматографией на силикагеле (гептан/этилацетат) было выделено 0,11 г (10%) соединения, указанного в заголовке.
ЖХ/МС (способ LC2): Rt=1,55 мин; m/z=444,20 [M+H]+.
(h) трет-Бутиловый эфир [4-(5-метансульфонил-7-пропилоксазоло[5,4-d]пиримидин-2-ил)-2,6-диметилфенокси]уксусной кислоты
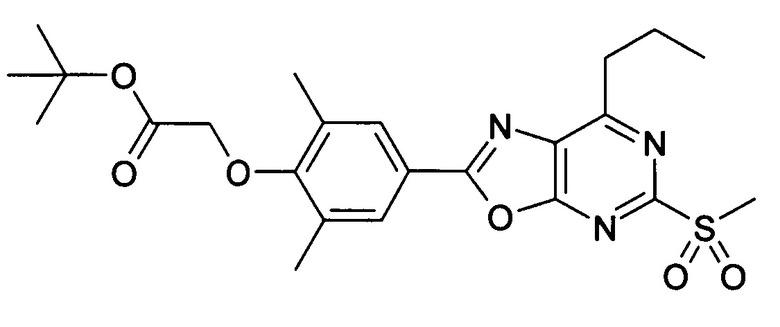
105 мг трет-бутилового эфира [2,6-диметил-4-(5-метилсульфанил-7-пропилоксазоло[5,4-d]пиримидин-2-ил)фенокси]уксусной кислоты вносили в 1,2 мл дихлорметана и при комнатной температуре прибавляли 128 мг 3-хлорпербензойной кислоты. Через 1 ч реакционную смесь разбавляли дихлорметаном и промывали дважды 1 M водным раствором гидроксида натрия, затем насыщенным водным раствором сульфита натрия и в заключение водой. Органические фракции сушили над сульфатом натрия, фильтровали и сгущали, при этом было получено 107 мг (98%) указанного в заголовке соединения, которое далее использовали без последующей очистки.
ЖХ/МС (способ LC2): Rt=1,41 мин; m/z=476,30 [M+H]+.
(i) трет-Бутиловый эфир {4-[5-(2,5-дифторфенокси)-7-пропилоксазоло[5,4-d]пиримидин-2-ил]-2,6-диметилфенокси}уксусной кислоты
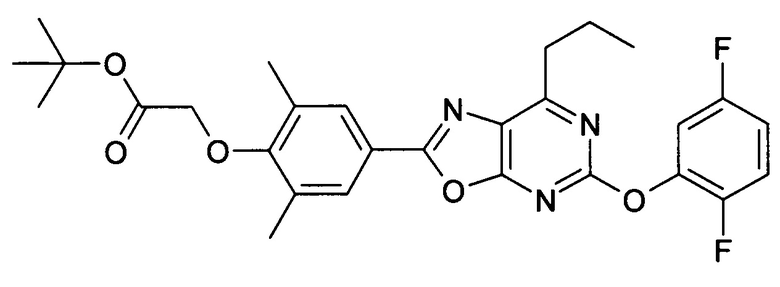
Раствор 107 мг трет-бутилового эфира [4-(5-метансульфонил-7-пропилоксазоло[5,4-d]пиримидин-2-ил)-2,6-диметилфенокси]уксусной кислоты в 1,1 мл NMP смешивали с 68 мг карбоната калия и затем прибавляли 32 мг 2,5-дифторфенола. Реакционную смесь нагревали в реакторе с микроволновым нагревом в течение 5 мин при 110°C, затем смесь охлаждали и выливали на лед. Вещество, выпавшее в осадок, растворяли в этилацетате, промывали водой до нейтральной реакции, сушили над сульфатом натрия, фильтровали и сгущали. Неочищенное вещество очищали хроматографией на силикагеле (гептан/этилацетат), при этом было получено 45 мг (38%) соединения, указанного в заголовке.
ЖХ/МС (способ LC2): Rt=1,53 мин; m/z=526,30 [M+H]+.
(j) {4-[5-(2,5-Дифторфенокси)-7-пропилоксазоло[5,4-d]пиримидин-2-ил]-2,6-диметилфенокси}уксусная кислота
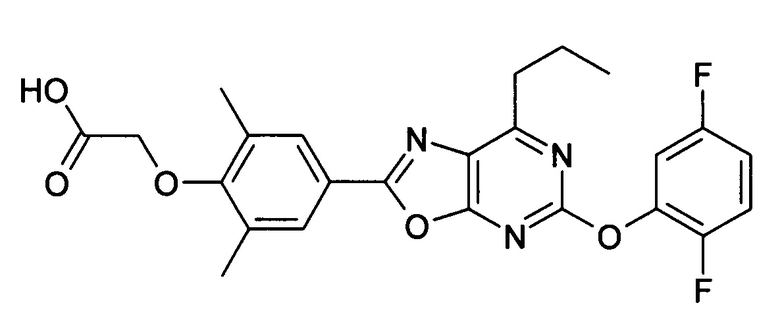
Раствор 39 мг трет-бутилового эфира {4-[5-(2,5-дифторфенокси)-7-пропилоксазоло[5,4-d]пиримидин-2-ил]-2,6-диметилфенокси}уксусной кислоты в 0,4 мл дихлорметана смешивали с 55 мкл трифторуксусной кислоты и перемешивали в течение 16 ч при комнатной температуре. Затем реакционную смесь сгущали в вакууме, остаток растирали с диизопропиловым эфиром, отделяли фильтрованием под вакуумом и сушили. Был получен 21 мг (60%) соединения, указанного в заголовке.
ЖХ/МС (способ LC2): Rt=1,38 мин; m/z=470,20 [M+H]+.
Пример 2
{2,6-Диметил-4-[7-пропил-5-(3,3,3-трифторпропокси)оксазоло[5,4-d]пиримидин-2-ил]фенокси}уксусная кислота
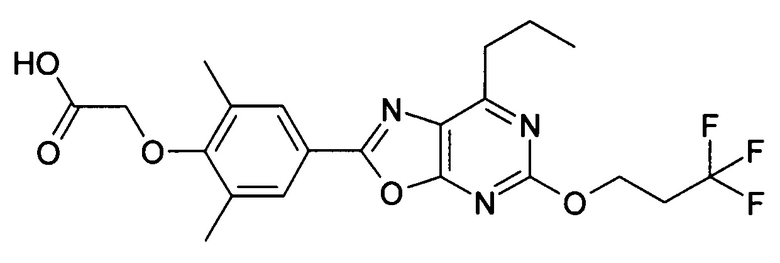
(a) трет-Бутиловый эфир {2,6-диметил-4-[7-пропил-5-(3,3,3-трифторпропокси)оксазоло[5,4-d]пиримидин-2-ил]фенокси}уксусной кислоты
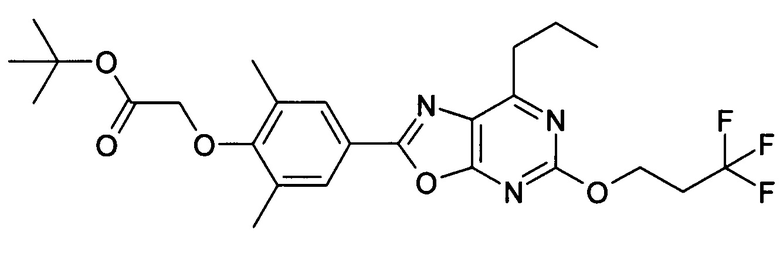
К 46 мг гидрида натрия (60%-ная суспензия в минеральном масле) в 1,5 мл безводного N,N-диметилформамида прибавляли 116 мг 3,3,3-трифторпропан-1-ола. Через 5 мин прибавляли 111 мг трет-бутилового эфира [4-(5-метансульфонил-7-пропилоксазоло[5,4-d]пиримидин-2-ил)-2,6-диметилфенокси]уксусной кислоты и реакционную смесь перемешивали сначала в течение 2 ч при комнатной температуре и затем в течение 15 мин при 80°C. При обработке реакционную смесь смешивали с насыщенным водным раствором лимонной кислоты натрия и три раза осуществляли экстракцию этилацетатом. Объединенные органические фракции промывали водой, сушили над сульфатом натрия, фильтровали и сгущали в вакууме. После очистки препаративной ВЭЖХ было получено 12 мг (10%) соединения, указанного в заголовке.
ЖХ/МС (способ LC4): Rt=0,93 мин; m/z=510,25 [M+H]+.
(b) {2,6-Диметил-4-[7-пропил-5-(3,3,3-трифторпропокси)оксазоло[5,4-d]пиримидин-2-ил]фенокси}уксусная кислота
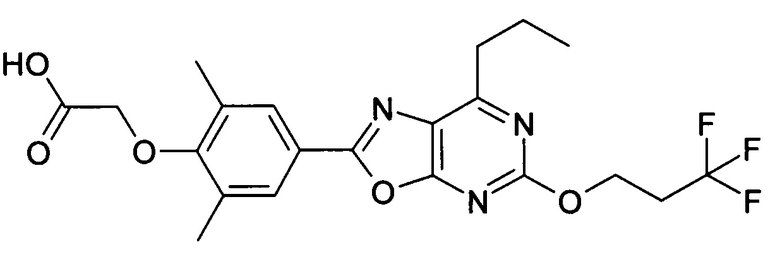
Аналогично примеру 1 (стадия (j)) взаимодействием 12 мг трет-бутилового эфира {2,6-диметил-4-[7-пропил-5-(3,3,3-трифторпропокси)оксазоло[5,4-d]пиримидин-2-ил]фенокси}уксусной кислоты с трифторуксусной кислоты было получено 11 мг (83%) соединения, указанного в заголовке.
ЖХ/МС (способ LC2): Rt=1,36 мин; m/z=454,10 [M+H]+.
Пример 3
{4-[5-(2-Фторфенокси)-7-изобутилоксазоло[5,4-d]пиримидин-2-ил]-2,6-диметилфенокси}уксусная кислота
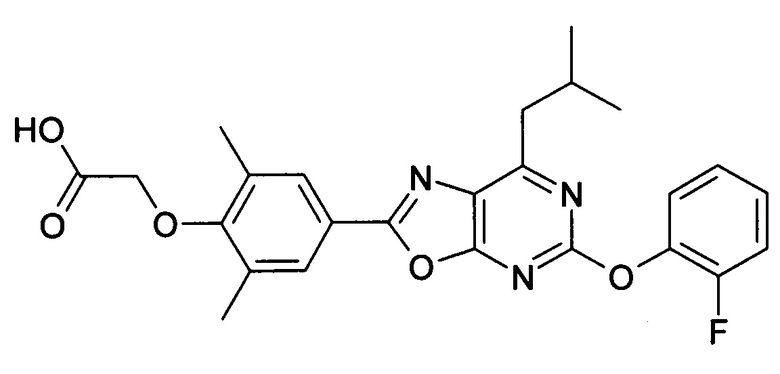
(a) трет-Бутиловый эфир [4-(7-изобутил-5-метилсульфанилоксазоло[5,4-d]пиримидин-2-ил)-2,6-диметилфенокси]уксусной кислоты
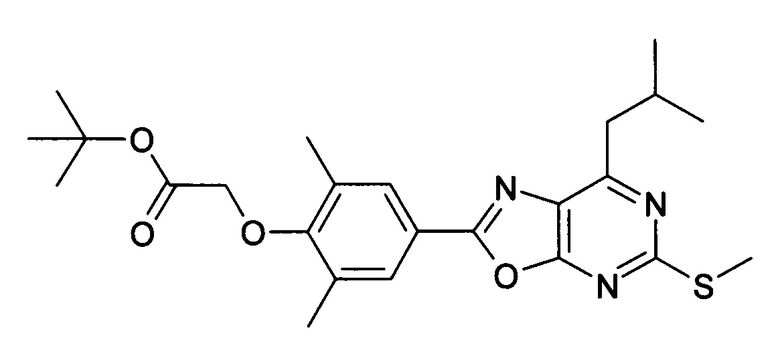
Аналогично примеру 1 (стадия (g)) взаимодействием 1,50 г трет-бутилового эфира [4-(7-хлор-5-метилсульфанилоксазоло[5,4-d]пиримидин-2-ил)-2,6-диметилфенокси]уксусной кислоты с изобутилмагнийбромидом было получено 0,31 г (20%) соединения, указанного в заголовке.
ЖХ/МС (способ LC2): Rt=1,44 мин; m/z=458,30 [M+H]+.
(b) трет-Бутиловый эфир [4-(7-изобутил-5-метансульфонилоксазоло[5,4-d]пиримидин-2-ил)-2,6-диметилфенокси]уксусной кислоты
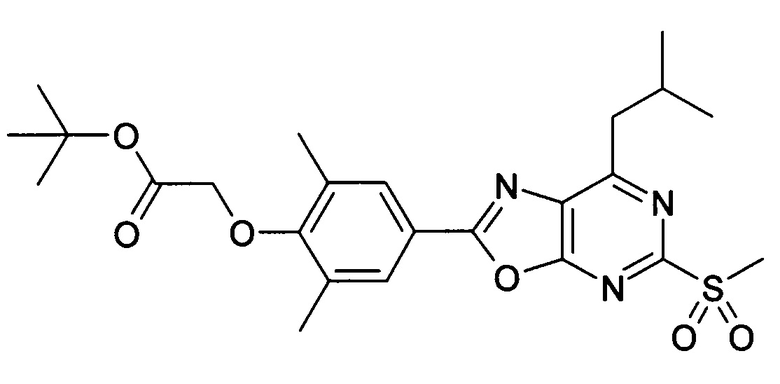
Аналогично примеру 1 (стадия (h)) взаимодействием 0,31 г трет-бутилового эфира [4-(7-изобутил-5-метилсульфанилоксазоло[5,4-d]пиримидин-2-ил)-2,6-диметилфенокси]уксусной кислоты с 3-хлорпербензойной кислотой было получено 0,31 г (93%) соединения, указанного в заголовке.
ЖХ/МС (способ LC2): Rt=1,43 мин; m/z=490,20 [M+H]+.
(c) трет-Бутиловый эфир {4-[5-(2-фторфенокси)-7-изобутилоксазоло[5,4-d]пиримидин-2-ил]-2,6-диметилфенокси}уксусной кислоты
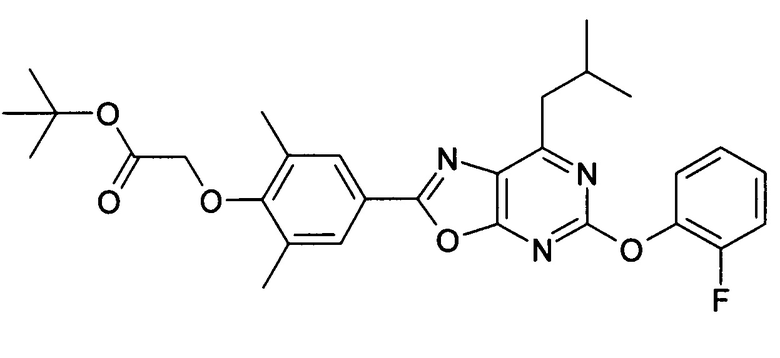
Аналогично примеру 1 (стадия (i)) взаимодействием 60 мг трет-бутилового эфира [4-(7-изобутил-5-метансульфанилоксазоло[5,4-d]пиримидин-2-ил)-2,6-диметилфенокси]уксусной кислоты с 2-фторфенолом было получено 64 мг (100%) соединения, указанного в заголовке.
ЖХ/МС (способ LC4): Rt=1,01 мин; m/z=522,25 [M+H]+.
(d) {4-[5-(2-Фторфенокси)-7-изобутилоксазоло[5,4-d]пиримидин-2-ил]-2,6-диметилфенокси}уксусная кислота
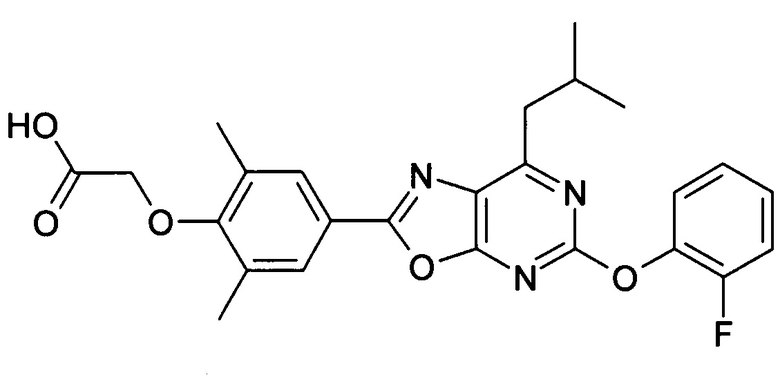
Аналогично примеру 1 (стадия (j)) взаимодействием 64 мг трет-бутилового эфира {4-[5-(2-фторфенокси)-7-изобутилоксазоло[5,4-d]пиримидин-2-ил]-2,6-диметилфенокси}уксусной кислоты с трифторуксусной кислотой было получено 33 мг (56%) соединения, указанного в заголовке.
ЖХ/МС (способ LC2): Rt=1,40 мин; m/z=466,20 [M+H]+.
Пример 4
{4-[7-Изобутил-5-(3,3,3-трифторпропокси)оксазоло[5,4-d]пиримидин-2-ил]-2,6-диметилфенокси}уксусная кислота
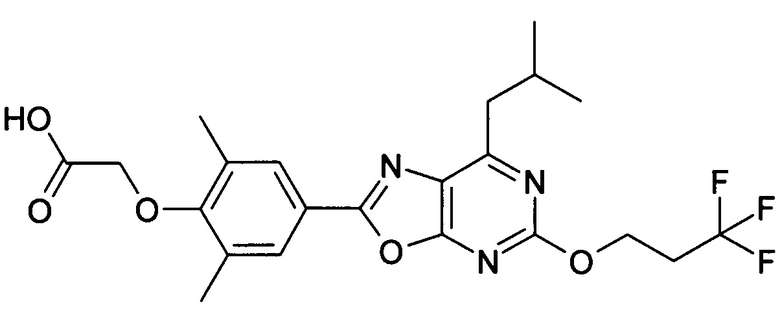
(a) трет-Бутиловый эфир {4-[7-изобутил-5-(3,3,3-трифторпропокси)оксазоло[5,4-d]пиримидин-2-ил]-2,6-диметилфенокси}уксусной кислоты
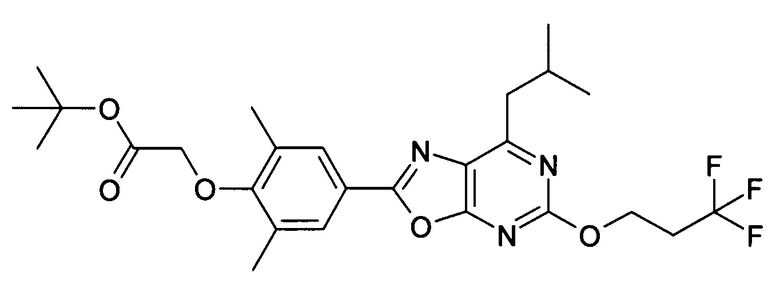
Аналогично примеру 2 (стадия (a) примера 2 взаимодействием 95 мг трет-бутилового эфира [4-(7-изобутил-5-метансульфонилоксазоло[5,4-d]пиримидин-2-ил)-2,6-диметилфенокси]уксусной кислоты с 3,3,3-трифторпропан-1-олом было получено 10 мг (10%) соединения, указанного в заголовке.
ЖХ/МС (способ LC4): Rt=0,96 мин; m/z=524,25 [M+H]+.
(b) {4-[7-Изобутил-5-(3,3,3-трифторпропокси)оксазоло[5,4-d]пиримидин-2-ил]-2,6-диметилфенокси}уксусная кислота
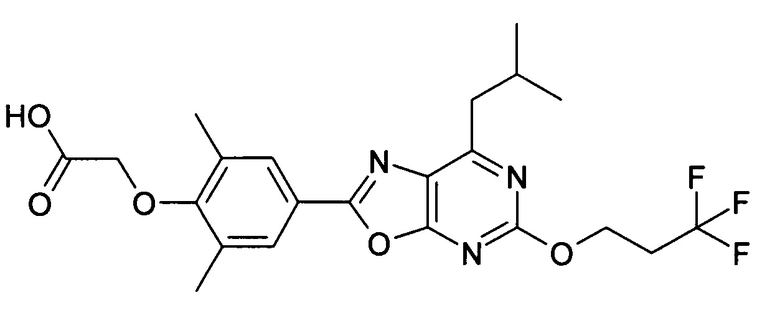
Аналогично примеру 1 (стадия (j)) взаимодействием 8 мг трет-бутилового эфира {4-[7-изобутил-5-(3,3,3-трифторпропокси)оксазоло[5,4-d]пиримидин-2-ил]-2,6-диметилфенокси}уксусной кислоты с трифторуксусной кислотой было получено 4 мг (56%) соединения, указанного в заголовке.
ЖХ/МС (способ LC4): Rt=0,80 мин; m/z=468,15 [M+H]+.
Пример 5
{4-[5-(3-Хлорфенокси)-7-изобутилоксазоло[5,4-d]пиримидин-2-ил]-2,6-диметилфенокси}уксусная кислота
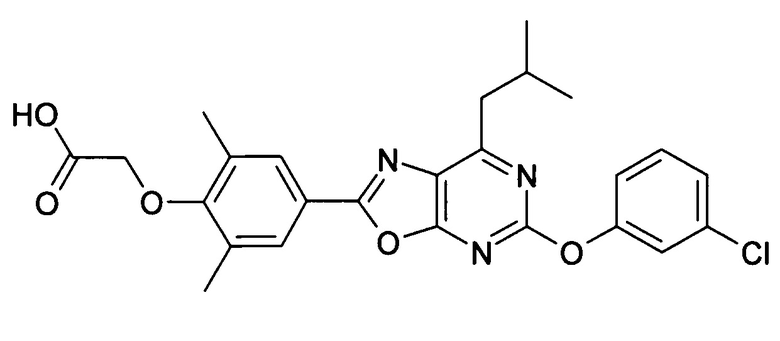
(a) трет-Бутиловый эфир {4-[5-(3-хлорфенокси)-7-изобутилоксазоло[5,4-d]пиримидин-2-ил]-2,6-диметилфенокси}уксусной кислоты
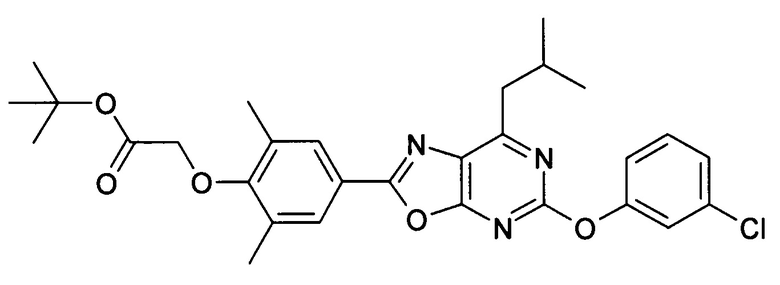
Аналогично примеру 1 (стадия (i)) взаимодействием 60 мг трет-бутилового эфира [4-(7-изобутил-5-метансульфанилоксазоло[5,4-d]пиримидин-2-ил)-2,6-диметилфенокси]уксусной кислоты с 3-хлорфенолом было получено 65 мг (100%) соединения, указанного в заголовке.
ЖХ/МС (способ LC4): Rt=1,04 мин; m/z=538,25 [M+H]+.
(b) {4-[5-(3-Хлорфенокси)-7-изобутилоксазоло[5,4-d]пиримидин-2-ил]-2,6-диметилфенокси}уксусная кислота
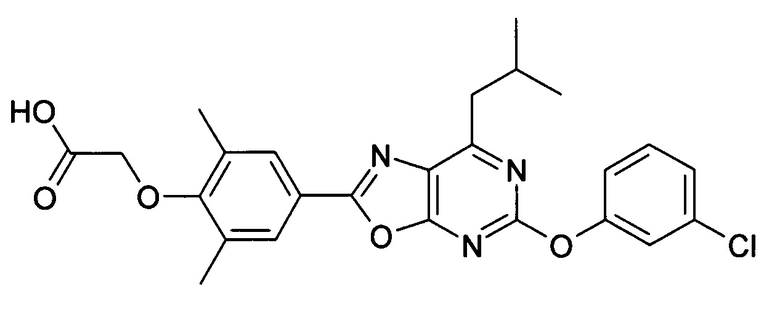
Аналогично примеру 1 (стадия (j)) взаимодействием 62 мг трет-бутилового эфира {4-[5-(3-хлорфенокси)-7-изобутилоксазоло[5,4-d]пиримидин-2-ил]-2,6-диметилфенокси}уксусной кислоты с трифторуксусной кислотой было получено 31 мг (45%) соединения, указанного в заголовке.
ЖХ/МС (способ LC2): Rt=1,44 мин; m/z=482,14 [M+H]+.
Пример 6
{4-[5-(3-Хлорфенокси)-7-пропилоксазоло[5,4-d]пиримидин-2-ил]-2,6-диметилфенокси}уксусная кислота
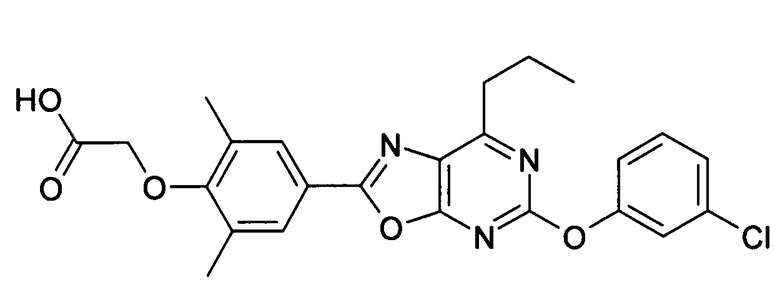
(a) трет-Бутиловый эфир {4-[5-(3-хлорфенокси)-7-пропилоксазоло[5,4-d]пиримидин-2-ил]-2,6-диметилфенокси}уксусной кислоты
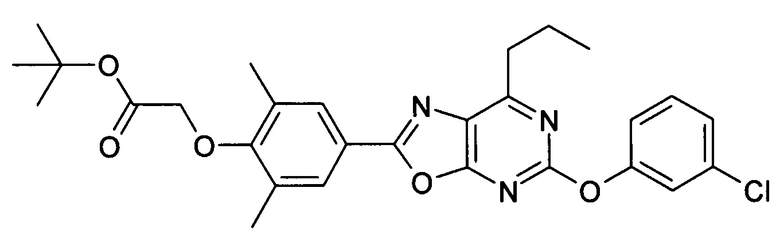
Аналогично примеру 1 (стадия (i)) взаимодействием 104 мг трет-бутилового эфира [4-(5-метансульфонил-7-пропилоксазоло[5,4-d]пиримидин-2-ил)-2,6-диметилфенокси]уксусной кислоты с 3-хлорфенолом было получено 115 мг (100%) соединения, указанного в заголовке.
ЖХ/МС (способ LC2): Rt=1,42 мин; m/z=524,30 [M+H]+.
(b) {4-[5-(3-Хлорфенокси)-7-пропилоксазоло[5,4-d]пиримидин-2-ил]-2,6-диметилфенокси}уксусная кислота
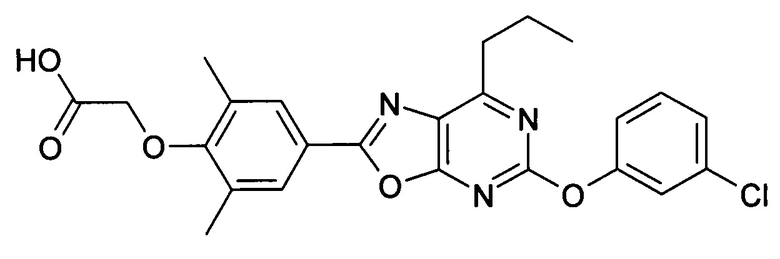
Аналогично примеру 1 (стадия (j)) взаимодействием 115 мг трет-бутилового эфира {4-[5-(3-хлорфенокси)-7-пропилоксазоло[5,4-d]пиримидин-2-ил]-2,6-диметилфенокси}уксусной кислоты с трифторуксусной кислотой было получено 44 мг (43%) соединения, указанного в заголовке.
ЖХ/МС (способ LC2): Rt=1,29 мин; m/z=468,20 [M+H]+.
Пример 7
{4-[5-(4-Хлорбензил)-7-изобутилоксазоло[5,4-d]пиримидин-2-ил]-2,6-диметилфенокси}уксусная кислота
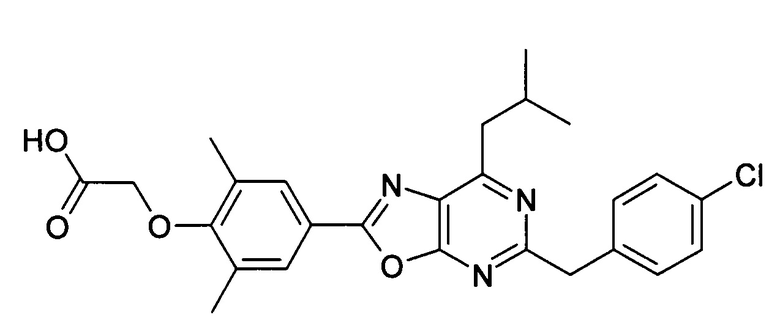
(a) N-[2-(4-Хлорбензил)-4,6-дигидроксипиримидин-5-ил]-4-метокси-3,5-диметилбензамид
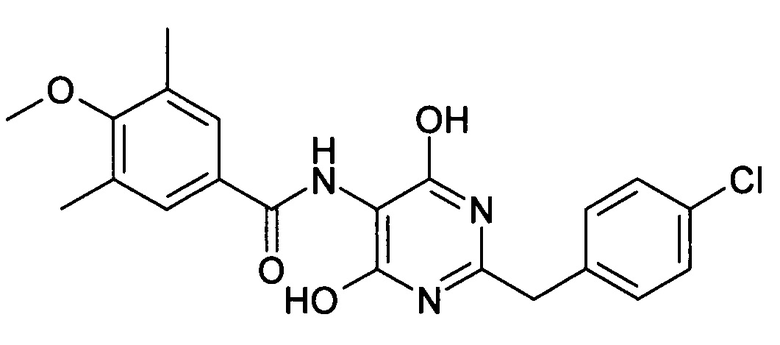
25,6 г гидрохлорида 2-(4-хлорфенил)ацетамидина растворяли в 425 мл безводного этанола и прибавляли 70 мл метилата натрия. Через 15 мин порциями вносили 42,2 г диэтилового эфира 2-(4-метокси-3,5-диметилбензоиламино)малоновой кислоты и затем реакционную смесь перемешивали в течение 2 ч при 80°C. После охлаждения до комнатной температуры твердое вещество, выпавшее в осадок, отделяли фильтрованием под вакуумом, промывали малым количеством этанола и тетрагидрофурана и сушили в вакууме.
Было получено 41,5 г (85%) указанного в заголовке соединения, которое далее использовали без последующей очистки.
ЖХ/МС (способ LC1): Rt=0,81 мин; m/z=414,1 [M+H]+.
(b) 5-(4-Хлорбензил)-2-(4-метокси-3,5-диметилфенил)оксазоло[5,4-d]пиримидин-7-ол
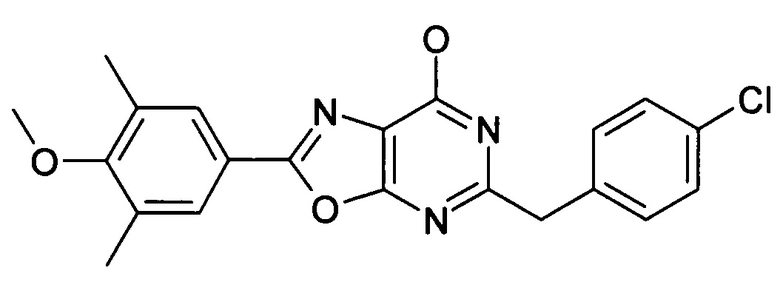
40 г N-[2-(4-хлорбензил)-4,6-дигидроксипиримидин-5-ил]-4-метокси-3,5-диметилбензамида и 150 мл оксихлорида фосфора нагревали в течение 1,5 ч при 70°C. Затем смеси давали охладиться. Образовавшееся твердое вещество отделяли фильтрованием под вакуумом, промывали диэтиловым эфиром и сушили. Было получено 21,1 г (55%) соединения, указанного в заголовке.
ЖХ/МС (способ LC2): Rt=1,24 мин; m/z=396,0 [M+H]+.
(c) 7-Хлор-5-(4-хлорбензил)-2-(4-метокси-3,5-диметилфенил)оксазоло[5,4-d]пиримидин
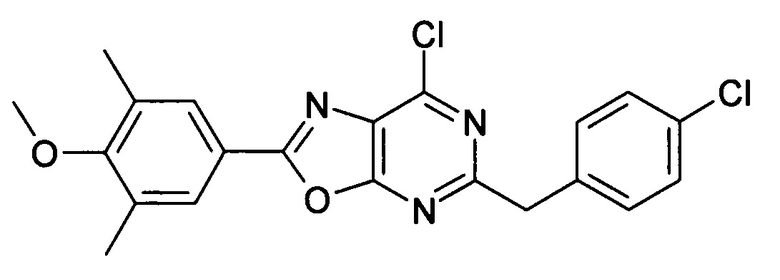
10 г 5-(4-хлорбензил)-2-(4-метокси-3,5-диметилфенил)оксазоло[5,4-d]пиримидин-7-ола и 50 мл оксихлорида фосфора нагревали в течение 5 ч при 90°C. Затем смеси давали охладиться. Образовавшееся твердое вещество отделяли фильтрованием под вакуумом, промывали диэтиловым эфиром и сушили. Было получено 10,4 г (99%) соединения, указанного в заголовке.
ЖХ/МС (способ LC2): Rt=1,09 мин; m/z=414,1 [M+H]+.
(d) 5-(4-Хлорбензил)-7-изобутил-2-(4-метокси-3,5-диметилфенил)оксазоло[5,4-d]пиримидин
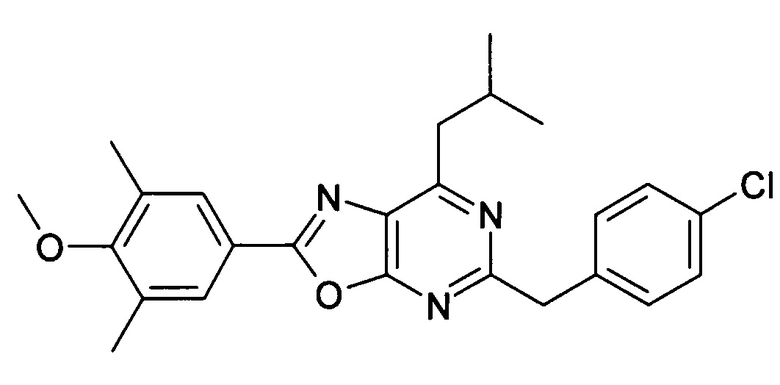
К деаэрированному раствору 1,50 г 7-хлор-5-(4-хлорбензил)-2-(4-метокси-3,5-диметилфенил)оксазоло[5,4-d]пиримидина и 65 мг ацетилацетоната железа (III) в 20 мл безводного тетрагидрофурана и 2 мл N-метилпирролидона в атмосфере аргона и при 0°C по каплям медленно прибавляли 2,0 мл 2,0 M раствора изобутилмагнийбромида в тетрагидрофуране. Через 15 мин при 0°C к реакционной смеси прибавляли диэтиловый эфир и при охлаждении льдом смешивали с 10%-ным водным раствором лимонной кислоты. Далее слои разделяли и из водного слоя два раза осуществляли экстракцию диэтиловым эфиром. Объединенные органические фракции промывали водой, сушили над сульфатом натрия, фильтровали и сгущали в вакууме. Из неочищенного конечного вещества перекристаллизацией из ацетонитрила было выделено 0,80 г (51%) соединения, указанного в заголовке.
ЖХ/МС (способ LC2): Rt=1,60 мин; m/z=436,17 [M+H]+.
(e) 4-[5-4-Хлорбензил)-7-изобутилоксазоло[5,4-d]пиримидин-2-ил]-2,6-диметилфенол
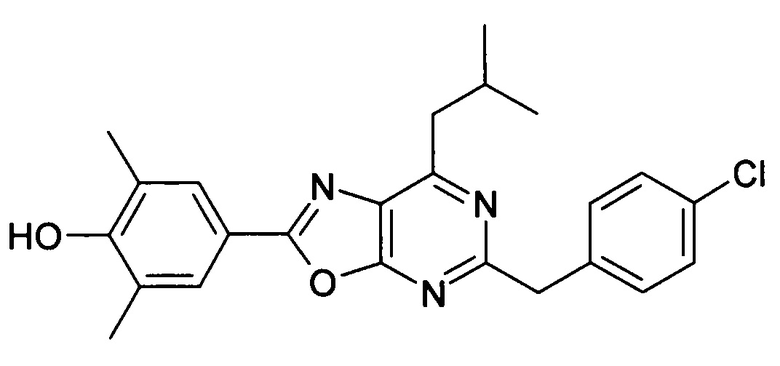
Аналогично примеру 1 (стадия (e)) взаимодействием 850 мг 5-(4-хлорбензил)-7-изобутил-2-(4-метокси-3,5-диметилфенил)оксазоло[5,4-d]пиримидина с бортрибромидом было получено 690 мг (84%) соединения, указанного в заголовке.
ЖХ/МС (способ LC2): Rt=1,51 мин; m/z=422,16 [M+H]+.
(f) трет-Бутиловый эфир {4-[5-(4-хлорбензил)-7-изобутилоксазоло[5,4-d]пиримидин-2-ил]-2,6-диметилфенокси}уксусной кислоты
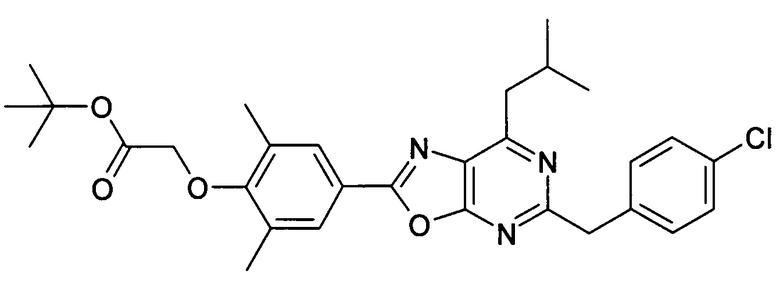
Аналогично примеру 1 (стадия (f)) взаимодействием 684 мг 4-[5-(4-хлорбензил)-7-изобутилоксазоло[5,4-d]пиримидин-2-ил]-2,6-диметилфенола с трет-бутиловым эфиром бромуксусной кислоты было получено 800 мг (92%) соединения, указанного в заголовке.
ЖХ/МС (способ LC2): Rt=1,62 мин; m/z=536,22 [M+H]+.
(g) {4-[5-(4-Хлорбензил)-7-изобутилоксазоло[5,4-d]пиримидин-2-ил]-2,6-диметилфенокси}уксусная кислота
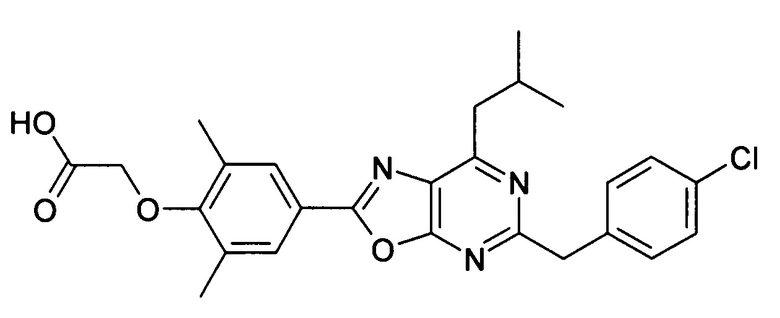
Аналогично примеру 1 (стадия (j)) взаимодействием 784 мг трет-бутилового эфира {4-[5-(4-хлорбензил)-7-изобутилоксазоло[5,4-d]пиримидин-2-ил]-2,6-диметилфенокси}уксусной кислоты с трифторуксусной кислотой было получено 702 мг (100%) соединения, указанного в заголовке.
ЖХ/МС (способ LC2): Rt=1,47 мин; m/z=480,16 [M+H]+.
Пример 8
[4-(5-Бензил-7-изобутилоксазоло[5,4-d]пиримидин-2-ил)-2,6-диметилфенокси]уксусная кислота
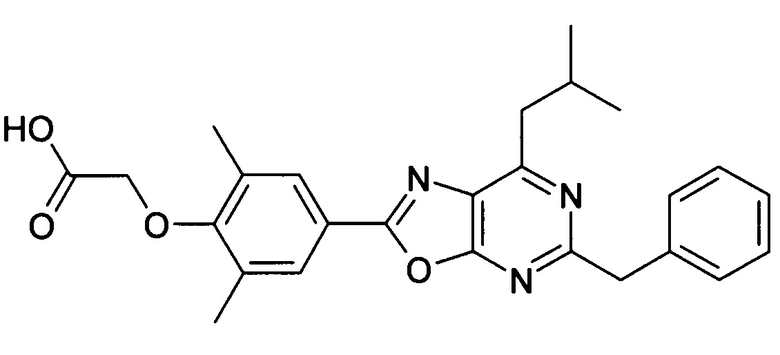
Раствор 50 мг {4-[5-(4-хлорбензил)-7-изобутилоксазоло[5,4-d]пиримидин-2-ил]-2,6-диметилфенокси}уксусной кислоты смешивали с 10 мг палладия на угле (10%) и осуществляли гидрирование в течение суток при 5 бар. Три раза прибавляли по 10 мг палладия на угле (10%) и затем каждый раз осуществляли гидрирование в течение суток. При обработке катализатор отделяли фильтрованием через целит, а полученный раствор сгущали. Остаток очищали способом ВЭЖХ. Было получено 7 мг (18%) соединения, указанного в заголовке.
ЖХ/МС (способ LC2): Rt=1,43 мин; m/z=446,30 [M+H]+.
Пример 9
{4-[5-(4-Хлорбензил)-7-изопропилоксазоло[5,4-d]пиримидин-2-ил]-2,6-диметилфенокси}уксусная кислота
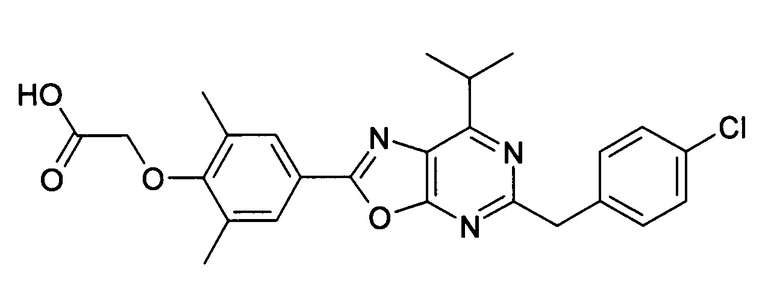
(a) 5-(4-Хлорбензил)-7-изопропил-2-(4-метокси-3,5-диметилфенил)оксазоло[5,4-d]пиримидин
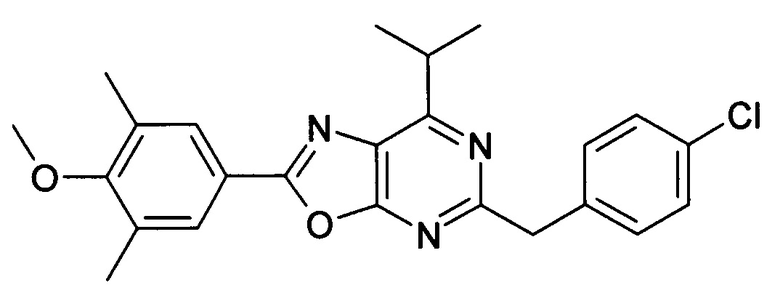
Аналогично примеру 7 (стадия (d)) взаимодействием 1,5 г 7-хлор-5-(4-хлорбензил)-2-(4-метокси-3,5-диметилфенил)оксазоло[5,4-d]пиримидина с изопропилмагнийбромидом было получено 165 мг (11%) соединения, указанного в заголовке.
ЖХ/МС (способ LC2): Rt=1,60 мин; m/z=422,16 [M+H]+.
(b) 4-[5-(4-Хлорбензил)-7-изопропилоксазоло[5,4-d]пиримидин-2-ил]-2,6-диметилфенол
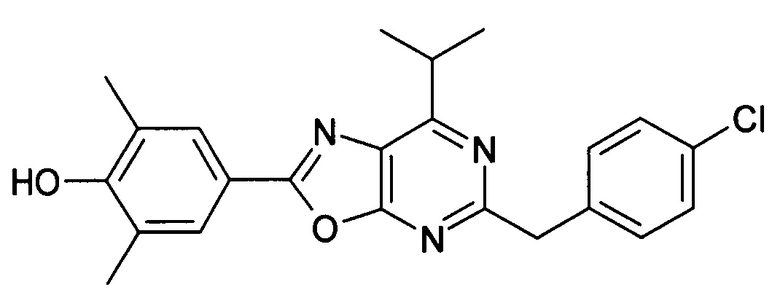
Аналогично примеру 1 (стадия (e)) взаимодействием 170 мг 5-(4-хлорбензил)-7-изопропил-2-(4-метокси-3,5-диметилфенил)оксазоло[5,4-d]пиримидина с бортрибромидом было получено 115 мг (70%) соединения, указанного в заголовке.
ЖХ/МС (способ LC2): Rt=1,50 мин; m/z=408,14 [M+H]+.
(c) трет-Бутиловый эфир {4-[5-(4-хлорбензил)-7-изопропилоксазоло[5,4-d]пиримидин-2-ил]-2,6-диметилфенокси}уксусной кислоты
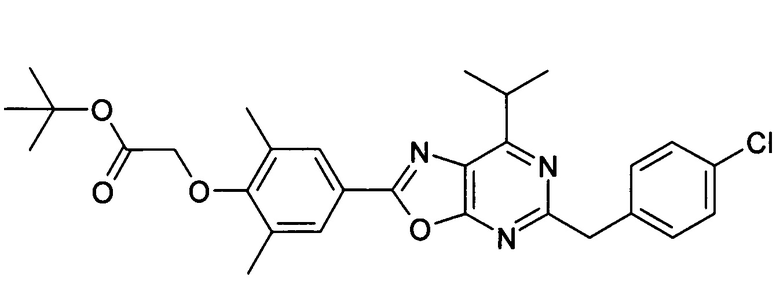
Аналогично примеру 1 (стадия (f)) взаимодействием 80 мг 4-[5-(4-хлорбензил)-7-изопропилоксазоло[5,4-d]пиримидин-2-ил]-2,6-диметилфенола с трет-бутиловым эфиром бромуксусной кислоты было получено 67 мг (65%) соединения, указанного в заголовке.
ЖХ/МС (способ LC4): Rt=1,15 мин; m/z=522,15 [M+H]+.
(d) {4-[5-(4-Хлорбензил)-7-изопропилоксазоло[5,4-d]пиримидин-2-ил]-2,6-диметилфенокси}уксусная кислота
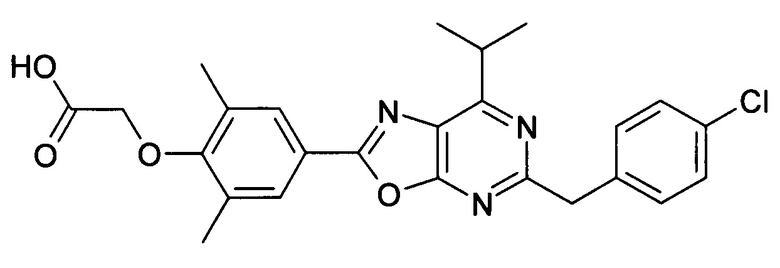
Аналогично примеру 1 (стадия (j)) взаимодействием 67 мг трет-бутилового эфира {4-[5-(4-хлорбензил)-7-изопропилоксазоло[5,4-d]пиримидин-2-ил]-2,6-диметилфенокси}уксусной кислоты с трифторуксусной кислотой было получено 74 мг (100%) соединения, указанного в заголовке.
ЖХ/МС (способ LC2): Rt=1,47 мин; m/z=466,2 [M+H]+.
Определение фармакологического действия
A) Испытание с GTP-γ-S на связывание с рецепторами Edg-1 человека
Для определения активации рецепторов Edg-1 соединениями по настоящему изобретению осуществляли испытание с GTP-γ-S (GTP-γ-S=гуанозин-5'-[тио]трифосфат) на связывание с рецептором, сопряженным с G-белком, на основе принципа сцинтилляционного проксимального анализа, причем был использован препарат клеточных мембран линии клеток CHO-Flp-In, которые конститутивно сверхэкспрессируют рецептор Edg-1 человека.
(a) Получение линии клеток
Экспрессирующая система Flp-In™ (Invitrogen, каталожный номер K6010-01) обеспечивает получение стабильных линий клеток млекопитающих, в которых ген, представляющий интерес, посредством гомологической рекомбинации интегрируется в специфический сайт генома, обозначенный как FRT-сайт (FRT=Flp Recombination Target (мишень Flp-рекомбинации)), посредством Flp-рекомбиназы, кодированной экспрессирующей плазмидой pOG44. Интеграция экспрессирующего конструкта pcDNA5/FRT в геном клеток-хозяев линии Flp-In ведет к транскрипции гена, представляющего интерес. Стабильно трансфицированные клетки становятся гигромицинустойчивыми.
За день до трансфекции 200 000 клеток Flp-In-CHO в среде Ham-F-12 (Invitrogen, каталожный номер 31765) с 10% эмбриональной телячьей сыворотки (FCS; Perbio Science, каталожный номер SH30068.03) высевали в 6-луночный планшет и инкубировали в течение суток при 37°C/5% CO2. С применением трансфицирующего агента FuGENE®-6 (Roche, каталожный номер 11988387001) клетки совместно трансфицировали плазмидой pOG44, экспрессирующей Flp-рекомбиназу, и модифицированной плазмидой, которая дополнительно содержит Edg-1-ген (инвентарный номер NM_001400) и обозначается как pcDNA5-FRT-TO_nFLAG_DEST-EDG-1, в соотношении 9:1. Для получения модифицированной плазмиды pcDNA5-FRT-TO_nFLAG_DEST плазмиду pcDNA5/FRT/TO от компании Invitrogen (Invitrogen, каталожный номер V6520-20) посредством инсерции кластера Gateway с сайтами attR-рекомбинации, фланкирующими ген ccdB и ген хлорамфениколустойчивости, (Gateway Conversion System, Invitrogen, каталожный номер 11828-029) адаптируют к клонирующей системе Gateway® (Invitrogen). Кроме того, перед сайтом 5'-att-рекомбинации добавляли эпитоп метки FLAG для обеспечения возможности рекомбинантной экспрессии белков с N-концевой меткой FLAG.
Для трансфекции в лунке смешивали 1,08 мкг pOG44 и 0,12 мкг pcDNA5-FRT-TO_nFLAG_DEST-EDG-1 с 100 мкл бессывороточной среды Ham-F-12 с 6 мкл трансфицирующего агента FuGENE®-6. После инкубации в течение 20 мин комплекс "трансфицирующий агент/ДНК" по каплям распределяли по клеткам. Клетки инкубировали в течение 24 ч при 37°C. Затем клетки из трех лунок переносили в бутыль T75 (Greiner Cellstar®, каталожный номер 658175) со средой Ham-F-12 с 10% FCS, но без антибиотика, и инкубировали еще в течение 24 ч. Через 48 ч после трансфекции среду заменяли селекционной средой (Ham-F-12 с 10% FCS и 300 мкг/мл гигромицина B (Invitrogen, каталожный номер 10687-010)). Среду меняли каждые 2-3 дня, пока не вырастала резистентная популяция клеток. Клетки несколько раз разделяли и высевали в новые бутыли, так чтобы клетки достигали не более 25%-ной конфлюэнтности. После селекции в течение 2 недель клетки переносили в бутыли T175 (Greiner Cellstar®, каталожный номер 660175) и культивировали для производства партиями. После краткой обработки (от 2 до 5 мин) аккутазой (PAA, каталожный номер L11-007) клетки отбирали из культуральных сосудов, ресуспендировали в селекционной среде (см. выше) и центрифугировали в течение 5 мин при 200 g. Клетки ресуспендировали в смеси 90% FCS и 10% диметилсульфоксида и хранили в жидком азоте в замороженном виде.
(b) Мембранный препарат
Из клеток описанной ранее линии CHO-Flp-In, которые конститутивно сверхэкспрессируют рецептор Edg-1 человека, стандартными способами получали мембранный препарат. С этой целью криоконсервированные клетки переводили в культуру и в бутылях T175 для культивирования клеток (Becton Dickinson, каталожный номер 35 5001) выращивали до конфлюэнтности. Рост культуры клеток останавливали промывкой не содержащим кальция раствором хлорида натрия, забуференным фосфатным раствором, (PBS; Gibco, каталожный номер 14190) и клетки собирали резиновым скребком в охлажденный до 4°C и не содержащий кальция PBS, содержащий смесь ингибиторов протеазы (Complete Protease Inhibitor; Roche, каталожный номер 1697498; 1 таблетка на 50 мл) и затем при 4°C центрифугировали в течение 15 мин при 1100 g (Heraeus Minifuge T). Для лизиса клеток осадок ресуспендировали в охлажденном до 4°C гипотоническом буферном растворе, содержащем 5 мМ HEPES (Sigma-Aldrich, каталожный номер H-0981), 1 мМ ЭДТА (динатриевая соль; Merck, каталожный номер 8418) и смесь ингибиторов протеазы (см. выше), в котором клетки выдерживали еще в течение 15 мин при охлаждении льдом. После лизиса клетки центрифугировали при 4°C в течение 10 мин при 400 g (Heraeus Minifuge T). Осадок разрыхляли в гомогенизаторе Даунса, разбавляли надосадочной жидкостью от предшествующего центрифугирования и затем центрифугировали при 4°C в течение 10 мин при 500 g (Heraeus Minifuge T), чтобы ядра и оставшиеся интактными клетки отделить от мембран, содержащихся в основном в надосадочной жидкости. Затем надосадочную жидкость разбавляли гипотоническим буферным раствором и при 4°C приблизительно при 18600 g центрифугировали в течение 2 ч (Beckmann, Avanti J251). Затем осадок мембран ресуспендировали в буферном растворе для хранения, содержащем 20 мМ HEPES, 150 мМ NaCl (Merck, каталожный номер 6400), 1 мМ ЭДТА (см. выше) и смесь ингибиторов протеазы (см. выше). Отбирали аликвоты мембранного препарата и хранили при -80°C. Концентрацию белка в мембранном препарате определяли в пробе посредством коммерческого набора для определения белков (Bio-Rad, DC Protein Assay, каталожные номера 500-0113, 500-0114, 500-0115).
(c) Испытание с GTP-γ-S
Мембранный препарат Edg-1, полученный по пункту (b), испытывали с коммерческим набором (набор SPA) от компании Amersham Biosciences/GE Healthcare (код RPNQ0210) для сцинтилляционного проксимального анализа на связывание с рецептором, сопряженным с G-белком, основанного на том, что индуцированное лигандами связывание GTP-γ-S, радиоактивно меченного атомами 35S, с содержащей рецепторы мембраной, связанной с сцинтилляционными шариками, вызывает эмиссию света и делает возможным количественное определение действия in vitro Edg-1-агонистических соединений. Испытание осуществляли в 96-луночном планшете по существу в соответствии с указаниями изготовителя. Перед началом эксперимента сцинтилляционные шарики суспендировали в восстановительном буферном растворе, содержащем Tris-HCl (pH 7,4) с 0,1% (масс./об.) азида натрия, и затем при охлаждении льдом разбавляли испытательным буферным раствором (20 мМ HEPES, 100 мМ NaCl, 1 мМ ЭДТА (см. выше), 1 мМ дитиотреитола (DTT), pH 7,4) до конечной концентрации шариков, равной 30 мг/мл.
В лунки вносили по 10 мкл указанного испытательного буферного раствора, 10 мкл 100 мкМ раствора гуанозиндифосфата (раствор GDP) и 10 мкл раствора испытуемого соединения в смеси "испытательный буферный раствор/диметилсульфоксид", что давало конечную концентрацию испытуемого соединения, равную 10 мкМ. В соответствующие лунки для определения верхнего контрольного значения вместо раствора испытуемого соединения вносили по 10 мкл раствора сфингозин-1-фосфата (S1P; Sigma, каталожный номер S-9666), что в итоге давало конечную концентрацию S1P, равную 10 мкМ, а для определения нижнего контрольного значения вносили по 10 мкл испытательного буферного раствора. Во всех лунках содержалось эквивалентное количество диметилсульфоксида. Затем в каждую лунку вносили по 10 мкл раствора [35S]GTP-γ-S (4 нМ) и мембранный препарат Edg-1, полученный по пункту (b) (15 мкг мембранного белка в 100 мкл испытательного буферного раствора). После инкубации планшетов в течение 5 мин при комнатной температуре прибавляли по 50 мкл описанной ранее суспензии сцинтилляционных шариков (30 мг/мл). После дальнейшей инкубации в течение 45 мин при комнатной температуре планшеты центрифугировали в течение 10 мин при 500 g. Количественное определение связывания [35S]GTP-γ-S и, таким образом, активации рецептора осуществляли посредством счетчика бета-излучения (MicroBeta, Wallac) в течение 1 мин. Значения корректировали относительно фона, вычитая соответствующее нижнее контрольное значение. Все определения осуществляли в трех параллельных пробах. Активацию рецептора испытуемым соединением выражали в % от соответствующего верхнего контрольного значения (действие 10 мкМ S1P принято за 100%-ную активацию). Значения степени активации, найденные для экспериментальных соединений при 10 мкМ, представлены в таблице 1.
Степень активации рецептора Edg-1 экспериментальными соединениями при 10 мкМ в процентах от активации 10 мкМ S1P
Из результатов измерений следует, что соединения являются в хорошей степени приемлемыми для заживления ран и, в частности, для терапии нарушений заживления ран пациентов с диабетом.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРОИЗВОДНЫЕ КАРБОНОВОЙ КИСЛОТЫ, СОДЕРЖАЩИЕ 2,5,7-ЗАМЕЩЕННОЕ ОКСАЗОЛОПИРИМИДИНОВОЕ КОЛЬЦО | 2011 |
|
RU2560876C2 |
| ПРОИЗВОДНЫЕ КАРБОНОВЫХ КИСЛОТ С ОКСАЗОЛО[5,4-b] ПИРИДИНОВЫМ КОЛЬЦОМ | 2012 |
|
RU2609002C2 |
| ПРОИЗВОДНЫЕ КАРБОНОВОЙ КИСЛОТЫ, СОДЕРЖАЩИЕ 2,5-ЗАМЕЩЕННОЕ ОКСАЗОЛОПИРИМИДИНОВОЕ КОЛЬЦО | 2011 |
|
RU2564018C2 |
| ПРОИЗВОДНЫЕ ГЕТЕРОЦИКЛИЧЕСКИХ КАРБОНОВЫХ КИСЛОТ, СОДЕРЖАЩИЕ 2,5,7-ЗАМЕЩЕННОЕ ОКСАЗОЛОПИРИМИДИНОВОЕ КОЛЬЦО | 2011 |
|
RU2554869C2 |
| ПРОИЗВОДНЫЕ КАРБОНОВЫХ КИСЛОТ, ИМЕЮЩИЕ ОКСАЗОЛО[4,5-D]ПИРИМИДИНОВОЕ КОЛЬЦО | 2012 |
|
RU2609003C2 |
| ГЕТЕРОЦИКЛИЧЕСКИЕ ПРОИЗВОДНЫЕ КАРБОНОВЫХ КИСЛОТ, ИМЕЮЩИЕ 2,5-ЗАМЕЩЕННОЕ ОКСАЗОЛОПИРИМИДИНОВОЕ КОЛЬЦО | 2011 |
|
RU2559896C2 |
| ПРОИЗВОДНЫЕ КАРБОНОВЫХ КИСЛОТ С ОКСАЗОЛО[4,5-С]ПИРИДИНОВЫМ ЦИКЛОМ | 2012 |
|
RU2609004C2 |
| 2,5-ЗАМЕЩЕННЫЕ ПРОИЗВОДНЫЕ ОКСАЗОЛОПИРИМИДИНА | 2011 |
|
RU2554874C2 |
| ЦИКЛИЧЕСКИЕ АЗАИНДОЛ-3-КАРБОКСАМИДЫ, ИХ ПОЛУЧЕНИЕ И ПРИМЕНЕНИЕ В КАЧЕСТВЕ ЛЕКАРСТВЕННЫХ ПРЕПАРАТОВ | 2009 |
|
RU2487874C2 |
| 2,5,7-ЗАМЕЩЕННЫЕ ПРОИЗВОДНЫЕ ОКСАЗОЛПИРИМИДИНА | 2011 |
|
RU2557246C2 |
Изобретение относится к соединениям формулы I или его физиологически приемлемой соли, где А означает -СН2- или О; X означает (C1-С6)-алкандиилоксигруппу, причем атом кислорода (C1-С6)-алкандиилоксигруппы связан с группой Y; Y означает фенилен, причем в фенилене один или несколько содержащихся в цикле атомов углерода при необходимости замещены одинаковым или разным (C1-С4)-алкилом; R1 означает атом водорода; R2 означает (C1-С6)-алкил; R3 означает (C1-С6)-алкил, причем алкил при необходимости имеет один или несколько заместителей в виде атомов фтора, или R3 представляет собой фенил, причем в фениле один или несколько содержащихся в цикле атомов углерода при необходимости замещены одинаковым или разным галогеном. Изобретение также относится к фармацевтической композиции для активации рецептора EDG-1, содержащей по меньшей мере одно соединение формулы I или его физиологически приемлемую соль и фармацевтически приемлемый носитель. Технический результат – производные карбоновых кислот с оксазоло[5,4-d]пиримидиновым циклом для применения в качестве лекарственного средства для активации рецептора EDG-1. 2 н. и 2 з.п. ф-лы, 1 табл., 9 пр.
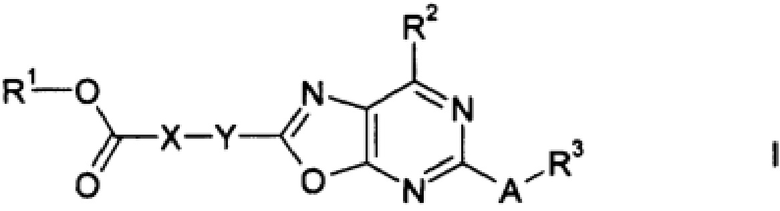
1. Соединение формулы I или его физиологически приемлемая соль
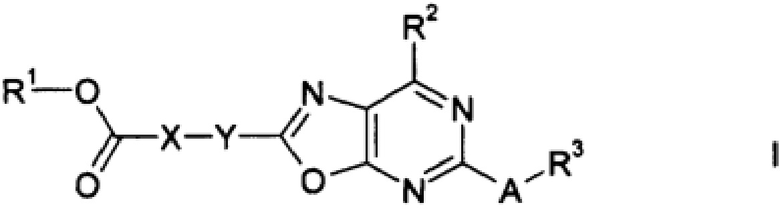
где А означает -СН2- или О;
X означает (C1-С6)-алкандиилоксигруппу, причем атом кислорода (C1-С6)-алкандиилоксигруппы связан с группой Y;
Y означает фенилен, причем в фенилене один или несколько содержащихся в цикле атомов углерода при необходимости замещены одинаковым или разным (C1-С4)-алкилом;
R1 означает атом водорода;
R2 означает (C1-С6)-алкил;
R3 означает (C1-С6)-алкил, причем алкил при необходимости имеет один или несколько заместителей в виде атомов фтора, или R3 представляет собой фенил, причем в фениле один или несколько содержащихся в цикле атомов углерода при необходимости замещены одинаковым или разным галогеном.
2. Фармацевтическая композиция для активации рецептора EDG-1, содержащая по меньшей мере одно соединение формулы I по п. 1 или его физиологически приемлемую соль и фармацевтически приемлемый носитель.
3. Фармацевтическая композиция по п. 2, отличающаяся тем, что она представляет собой гидрогелевую композицию.
4. Соединение формулы I по п. 1 или его физиологически приемлемая соль для применения в качестве лекарственного средства для активации рецептора EDG-1.
| Приспособление для суммирования отрезков прямых линий | 1923 |
|
SU2010A1 |
| Колосоуборка | 1923 |
|
SU2009A1 |
| ГЕРБИЦИД | 0 |
|
SU404193A1 |
| ПРОИЗВОДНЫЕ КАРБОНОВОЙ КИСЛОТЫ, СОДЕРЖАЩИЕ 2,5-ЗАМЕЩЕННОЕ ОКСАЗОЛОПИРИМИДИНОВОЕ КОЛЬЦО | 2011 |
|
RU2564018C2 |
| Колосоуборка | 1923 |
|
SU2009A1 |
Авторы
Даты
2017-01-30—Публикация
2012-07-06—Подача