Настоящее изобретение относится к производным карбоновой кислоты, содержащим 2,5-замещенное оксазолопиримидиновое кольцо, и их физиологически приемлемым солям.
Соединения с подобной структурой, которые являются подходящими для лечения рассеянного склероза, уже были описаны в предшествующем уровне техники (см. WO2009/154775). Механизм действия данных соединений заключается в десенсибилизации EDG-1 сигнального пути путем активации EDG-1 рецептора (так называемый суперагонизм), что в данном случае эквивалентно функциональному антагонизму EDG-1 сигнального пути. В целом это означает, что, особенно в случае лимфоцитов, EDG-1 сигнальный путь непрерывно подавляется, в результате чего данные клетки теряют способность к хемотаксису вдоль градиента S1P между кровью и лимфой. Это означает, что после воздействия лимфоциты больше уже не покидают вторичную лимфоидную ткань (повышенный хоуминг) и количество свободно циркулирующих в плазме лимфоцитов значительно уменьшается. Дефицит лимфоцитов в плазме (лимфопения) вызывает подавление иммунитета, что необходимо для механизма действия модуляторов EDG-1 рецептора, описанных в WO 2009/154775.
Объектом настоящего изобретения является обеспечение соединений, подходящих для заживления ран и, в частности, для лечения нарушений, связанных с заживлением ран у пациентов с сахарным диабетом. Кроме того, желательным является обеспечение соединений, которые являются подходящими для лечения синдрома диабетической стопы (СДС). Кроме того, желательным является достижение воспроизводимой активации рецептора EDG-1 сигнального пути, благодаря чему достигается возможность, в фармакологическом смысле, постоянной активации EDG-1 сигнального пути.
Настоящее изобретение относится к оксазолопиримидинам Формулы I:
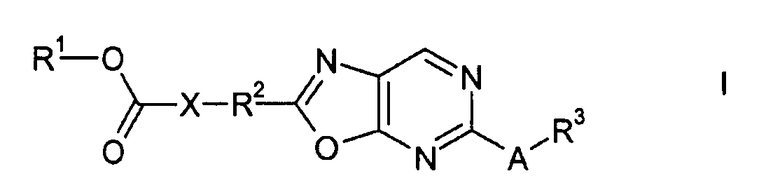 ,
,
где A, R1, R2, R3 и X определены далее. Механизм действия соединений Формулы I, таким образом, основан не на десенсибилизации EDG-1 сигнального пути и поэтому диаметрально противоположен механизму действия, описанному в WO 2009/154775. Следовательно, настоящее изобретение относится к способу получения соединений Формулы I, их применению, в частности, в качестве активных компонентов в лекарственных препаратах, и содержащим их фармацевтическим композициям.
В отличие от здоровых людей, пациенты с диабетом страдают от медленного заживления ран и более высокой частоты инфицирования, особенно в случае длительной гипергликемии, что вызвано, например, плохой регуляцией сахара в крови. Причины включают нарушение кровообращения, в частности в мелких сосудах, что приводит к плохому снабжению тканей кислородом и питательными веществами. Кроме того, понижается деление клеток, а также степень миграции кератиноцитов, фибробластов и эндотелиальных клеток дермы. В дополнение к этому, ограничивается активность различных защитных клеток (гранулоцитов), а также уменьшается фагоцитоз (поглощение и разрушение бактерий). В случае высокого уровня сахара в крови также ограничивается функция антител (иммуноглобулинов) в отношении бактерий. Соответственно, в случае ран и инфекций у пациентов с диабетом требуется особый подход при лечении.
Рецептор EDG-1 является членом семейства рецепторов гена эндотелиальной дифференциации из восьми в настоящее идентифицированных GPCR (рецепторов, сопряженных с G-белком) класса А. Данное семейство может быть разделено на подсемейства сфингозин-1-фосфат(S1P)-активируемых рецепторов (пять членов) и рецепторов, активируемых лизофосфатидной кислотой (LPA; три члена). Эндогенный лиганд S1P является плюрипотентным лизофосфолипидом, действующим на различные типы клеток путем активации GPCR из семейства EDG-рецепторов, а именно EDG-1 (=S1P1), EDG-3 (=S1P3), EDG-5 (=S1P2), EDG-6 (=S1P4) и EDG-8 (S1P5). Хотя S1P также описывается как внутриклеточный мессенджер, многочисленные клеточные ответы на S1P опосредуются активацией EDG-рецепторов. S1P синтезируется семейством ферментов сфингозинкиназ (SPHK) и подвергается деградации под действием фосфатаз и лиаз.
Объектом настоящего изобретения является оксазолопиримидиновое соединение Формулы I в любой его стереоизомерной форме или в виде смеси стереоизомеров в любом соотношении, или его физиологически приемлемая соль или физиологически приемлемый сольват любого из них:
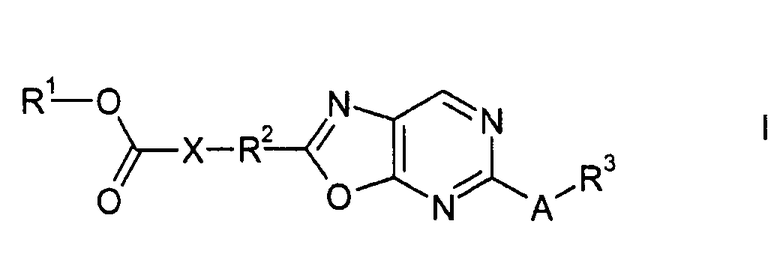 ,
,
где
A выбирают из NH, O и S;
X выбирают из (C1-C6)-алкандиила, (C2-C6)-алкендиила, (C2-C6)-алкиндиила, (C3-C7)-циклоалкандиила и (C1-C6)-алкандиилокси, которые все необязательно замещены одним или несколькими одинаковыми или различными заместителями, выбранными из фтора или гидрокси, где атом кислорода (C1-C6)-алкандиилокси-группы связан с группой R2;
R1 выбирают из водорода, (С1-C4)-алкила и (C3-C7)-циклоалкил-CzH2z-, где z выбирают из 0, 1 и 2;
R2 выбирают из фенилена и двухвалентного остатка ароматического, 5-членного-6-членного моноциклического гетероцикла, который содержит 1, 2 или 3 одинаковых или различных гетероатома в кольце, выбранных из N, O и S, где один из атомов азота в кольце может нести атом водорода или заместитель R21 и где фенилен и двухвалентный остаток ароматического гетероцикла необязательно замещены по одному или нескольким атомам углерода в кольце одинаковыми или различными заместителями R22;
R3 выбирают из (C1-C6)-алкила, (C2-C6)-алкенила, (C2-C6)-алкинила, (C3-C7)-циклоалкил-CuH2u- и Het-CvH2v-, где u и v выбирают из 1 и 2, или R3 является остатком насыщенного или ненасыщенного, 3-членного-10-членного моноциклического или бициклического кольца, которое содержит 0, 1, 2, 3 или 4 одинаковых или различных гетероатома в кольце, выбранных из N, O и S, где один или два атома азота в кольце могут нести атом водорода или (C1-C4)-алкильный заместитель и один или два атома серы в кольце могут нести одну или две оксо-группы, и где остаток кольца необязательно замещен по одному или нескольким атомам углерода в кольце одинаковыми или различными заместителями R31;
R21 выбирают из (С1-C4)-алкила, (C3-C7)-циклоалкил-CwH2w- и окси, где w выбирают из 0, 1 и 2;
R22 выбирают из галогена, гидрокси, (С1-C4)-алкил-, (С1-C4)-алкилокси, (C1-C4)-алкил-S(O)m-, амино, нитро, циано, гидроксикарбонила, (С1-C4)-алкилоксикарбонила, аминокарбонила и аминосульфонила;
R31 выбирают из галогена, (С1-C4)-алкила, (C3-C7)-циклоалкила, гидрокси, (C1-C4)-алкилокси, оксо, (C1-C4)-алкил-S(O)m-, амино, (C1-C4)-алкиламино, ди((С1-C4)-алкил)амино, (C1-C4)-алкилкарбониламино, (C1-C4)-алкилсульфониламино, нитро, циано, (С1-C4)-алкилкарбонила, аминосульфонила (C1-C4)-алкиламиносульфонила и ди((С1-C4)-алкил)аминосульфонила;
Het представляет собой остаток насыщенного, 4-членного-7-членного моноциклического гетероцикла, который содержит 1 или 2 одинаковых или различных гетероатома в кольце, выбранных из N, O и S, и которые соединены через атом углерода в кольце, где остаток гетероцикла необязательно замещен одним или несколькими одинаковыми или различными заместителями, выбранными из фтора и (C1-C4)-алкила;
m выбирают из 0, 1 и 2, где все значения m являются независимыми одно от другого;
где все циклоалкильные и циклоалкандиильные группы, независимо друг от друга и независимо от любых других заместителей, необязательно замещены одним или несколькими одинаковыми или различными заместителями, выбранными из фтора и (C1-C4)-алкила;
где все алкильные, алкандиильные, CuH2u, CvH2v, CwH2w, CzH2z, алкенильные, алкендиильные, алкинильные и алкиндиильные группы, независимо друг от друга и независимо от любых других заместителей, необязательно замещены одним или несколькими фторами.
Структурные элементы, такие как группы, заместители, члены гетероцикла, числовые значения или другие характерные черты, например, алкильные группы, подобные R22 или R31 группы, числовые значения подобно m, u и v, которые могут встречаться несколько раз в соединениях Формулы I, могут все независимо друг от друга иметь любое из указанных значений и в каждом случае могут быть одинаковыми или отличаться друг от друга. Например, алкильные группы в диалкиламино-группе могут быть одинаковыми или различными.
Алкильные, алкенильные и алкинильные группы могут быть линейными, например, с прямой цепью, или разветвленными. Это правило действует также тогда, когда они являются частью других групп, например алкилокси-групп (=алкокси-групп, алкил-O-групп), алкилоксикарбонильных групп или алкил-замещенных аминогрупп, или являются замещенными. В зависимости от определения количество атомов углерода в алкильной группе может быть 1, 2, 3, 4, 5 или 6 или 1, 2, 3 или 4, или 1, 2 или 3. Примерами алкила являются метил, этил, пропил, включая н-пропил и изопропил, бутил, включая н-бутил, втор-бутил, изобутил и трет-бутил, пентил, включая н-пентил, 1-метилбутил, изопентил, неопентил и трет-пентил, и гексил, включая н-гексил, 3,3-диметилбутил и изогексил. Двойные связи и тройные связи в алкенильных группах и алкинильных группах могут присутствовать в любых положениях. В одном варианте осуществления изобретения, алкенильные группы содержат одну двойную связь, и алкинильные группы содержат одну тройную связь. В одном варианте осуществления изобретения, алкенильная группа или алкинильная группа содержит по меньшей мере три атома углерода и соединена с остальной частью молекулы посредством атома углерода, который не является частью двойной связи или тройной связи. Примерами алкенила и алкинила являются этенил, проп-1-енил, проп-2-енил (=аллил), бут-2-енил, 2-метилпроп-2-енил, 3-метилбут-2-енил, гекс-3-енил, гекс-4-енил, проп-2-инил (=пропаргил), бут-2-инил, бут-3-инил, гекс-4-инил или гекс-5-инил. Замещенные алкильные группы, алкенильные группы и алкинильные группы могут быть замещены в любом положении, при условии, что соответствующее соединение является достаточно стабильным и может применяться для желаемой цели, такой как применение в качестве лекарственного вещества. Условие, что конкретная группа и соединение Формулы I являются достаточно стабильными и подходят для применения в качестве лекарственного вещества, является общим условием в отношении определения всех групп в соединениях Формулы I.
Что касается применимости, предшествующие объяснения в отношении алкильных, алкенильных и алкинильных групп касаются, соответственно, двухвалентных алкильных групп, таких как группы алкандиила, CuH2u, CvH2v, CwH2w и CzH2z, и двухвалентных алкенильных групп и алкинильных групп, таких как группы алкендиила и алкиндиила, которые, таким образом, также могут быть линейными или разветвленными. Двойные связи и тройные связи в алкендиильных и алкиндиильных группах могут присутствовать в любых положениях. В одном варианте осуществления изобретения, алкендиильные группы содержат одну двойную связь, и алкиндиильные группы содержат одну тройную связь. Примерами двухвалентных алкильных групп являются -CH2- (=метилен), -CH2-CH2-, -CH2-CH2-CH2-, -CH2-CH2-CH2-CH2-, -CH(CH3)-, -C(CH3)2-, -CH(CH3)-CH2-, -CH2-CH(CH3)-, -C(CH3)2-CH2-, -CH2-C(CH3)2-, примерами двухвалентных алкенильных групп являются -CH=CH-, -CH2-CH=CH-, -CH=CH-CH2-, -CH2-CH=CH-CH2-, -CH2-CH2-CH=CH-, -C(CH3)=C(CH3)-, и примерами двухвалентных алкинильных групп являются -C≡C-, -CH2-C≡C-, -C≡C-CH2-, -C(CH3)2-C≡C-, -C≡C-C(CH3)2-, -CH2-C≡C-CH2-, -CH2-CH2-C≡C-. Если число в двухвалентной группе, такое как z в группе CzH2z, например, равно 0 (=ноль), две группы, которые присоединены к рассматриваемой группе, такой как CzH2z, связаны непосредственно одна с другой посредством одинарной связи.
Число атомов углерода в кольце в циклоалкильной группе может составлять 3, 4, 5, 6 или 7. В одном варианте осуществления изобретения, число атомов углерода в циклоалкильной группе является независимым от числа атомов углерода в любой другой циклоалкильной группе и составляет 3, 4, 5 или 6, в другом варианте осуществления 3, 4 или 5, в другом варианте осуществления 3 или 4, в другом варианте осуществления 3, в другом варианте осуществления 5, 6 или 7, в другом варианте осуществления 5 или 6, в другом варианте осуществления 6 или 7, в другом варианте осуществления 6. Это применимо, соответственно, в случае двухвалентных циклоалкильных групп, например циклоалкандиильных групп, которые могут быть связаны с соседними группами через любой один или два кольцевых атома углерода. Примерами циклоалкильных групп являются циклопропил, циклобутил, циклопентил, циклогексил и циклогептил. Примерами двухвалентных циклоалкильных групп являются циклопропан-1,1-диил, циклопропан-1,2-диил, циклобутан-1,3-диил, циклопентан-1,1-диил, циклопентан-1,2-диил, циклопентан-1,3-диил, циклогексан-1,1-диил, циклогексан-1,2-диил, циклогексан-1,3-диил, циклогексан-1,4-диил, циклогептан-1,4-диил. Независимо друг от друга и независимо от любых других заместителей циклоалкильные группы и циклоалкандиильные группы необязательно замещены одним или несколькими одинаковыми или различными (C1-C4)-алкильными заместителями, которые могут находиться в любом из положений, например, циклоалкильные группы могут быть не замещены алкильными заместителями или замещены алкильными заместителями, например, 1, 2, 3 или 4, или 1 или 2 (C1-C4)-алкильными заместителями, например, метильными группами. Примерами алкилзамещенных циклоалкильных групп и циклоалкандиильных групп являются 4-метилциклогексил, 4-трет-бутилциклогексил или 2,3-диметилциклопентил, 2,2-диметилциклопропан-1,1-диил, 2,2-диметилциклопропан-1,2-диил, 2,2-диметилциклопентан-1,3-диил, 6,6-диметилциклогептан-1,4-диил. Примерами циклоалкилалкильных групп, которые могут представлять собой такие группы, как (C3-C7)-циклоалкил-CzH2z-, например, являются циклопропилметил, циклобутилметил, циклопентилметил, циклогексилметил, циклогептилметил, 1-циклопропилэтил, 2-циклопропилэтил, 1-циклобутилэтил, 2-циклобутилэтил, 2-циклопентилэтил, 2-циклогексилэтил, 2-циклогептилэтил.
Независимо друг от друга и независимо от любых других заместителей алкильные группы, двухвалентные алкильные группы, алкенильные группы, двухвалентные алкенильные группы, алкинильные группы, двухвалентные алкинильные группы, циклоалкильные группы и двухвалентные циклоалкильные группы необязательно замещены одним или несколькими фторами, которые могут находиться в любом из положений, например, указанные группы могут быть не замещены фторами или замещены фторами, например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12 или 13, или 1, 2, 3, 4, 5, 6, 7, 8 или 9, или 1, 2, 3, 4, 5, 6 или 7, или 1, 2, 3, 4 или 5, или 1, 2 или 3, или 1 или 2 фторами. Примерами указанных фторзамещенных групп являются трифторметил, 2-фторэтил, 2,2,2-трифторэтил, пентафторэтил, 3,3,3-трифторпропил, 2,2,3,3,3-пентафторпропил, 4,4,4-трифторбутил, гептафторизопропил, -CHF-, -CF2-, -CF2-CH2-, -CH2-CF2-, -CF2-CF2-, -CF(CH3)-, -C(CF3)2-, 1-фторциклопропил, 2,2-дифторциклопропил, 3,3-дифторциклобутил, 1-фторциклогексил, 4,4-дифторциклогексил, 3,3,4,4,5,5-гексафторциклогексил, 2,2-дифторциклопропан-1,2-диил. Примерами алкилокси-групп, в которых алкильный фрагмент является фторзамещенным, являются трифторметокси, 2,2,2-трифторэтокси, пентафторэтокси и 3,3,3-трифторпропокси. В одном варианте осуществления изобретения, общее число фторов в качестве заместителей и (C1-C4)-алкильных заместителей, которые независимо от любых других заместителей необязательно присутствуют в циклоалкильных группах и циклоалкандиильных группах в соединениях Формулы I, составляет 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или 11, в другом варианте осуществления 1, 2, 3, 4, 5, 6, 7, 8 или 9, в другом варианте осуществления 1, 2, 3, 4 или 5, в другом варианте осуществления 1, 2, 3 или 4.
Такие группы, как фенил, нафтил (=нафталенил) и остатки ароматических гетероциклов, которые необязательно замещены одним или несколькими заместителями, могут быть не замещенными или замещенными, например, 1, 2, 3, 4 или 5, или 1, 2, 3 или 4, или 1, 2 или 3, или 1 или 2, или 1 одинаковыми или различными заместителями, которые могут находиться в любом из положений. В одном варианте осуществления изобретения, общее количество нитро-заместителей в соединении Формулы I составляет не более двух. Ароматические азотсодержащие гетероциклы, которые в родоначальной кольцевой системе несут атом водорода на кольцевом атоме азота в 5-членном кольце, таком как пиррол, имидазол, индол или бензимидазол, например, могут быть замещены по атомам углерода и/или данным кольцевым атомам азота. В одном варианте осуществления изобретения, заместители по данным кольцевым атомам азота выбирают из (C1-C4)-алкильных групп, например, такие кольцевые атомы азота в ароматических гетероциклах несут водород или (C1-C4)-алкильный заместитель. Когда в отношении кольцевых атомов азота в ароматических гетероциклах и в любых других гетероциклах известно, что они могут нести атом водорода или заместитель, такие кольцевые атомы азота либо несут атом водорода или заместитель, либо они не несут атом водорода или заместитель. Кольцевые атомы азота, которые несут атом водорода или заместитель, находятся в азотсодержащем ароматическом 5-членном кольце, таком как присутствующее в пирроле, имидазоле, индоле или бензимидазоле, например, и в неароматическом кольце, включая насыщенное кольцо. Кольцевые атомы азота, которые не несут атом водорода или заместитель, за исключением, когда они присутствуют в положительно заряженной форме, включая любые атомы азота дополнительного кольца помимо кольцевых атомов азота, которые несут атом водорода или заместитель, находятся в ароматическом кольце, таком как присутствующее, например, в тиазоле, имидазоле, пиридине или бензимидазоле, и в неароматическом кольце, в котором они являются мостиковыми атомами или являются частью двойной связи, а также они являются кольцевыми атомами азота, через которые осуществляется присоединение кольца. Подходящие кольцевые атомы азота в ароматических гетероциклах в соединениях Формулы I, такие как кольцевой атом азота в пиридиновом кольце, в частности, кольцевой атом азота в ароматическом гетероцикле, представляющем R2, могут также нести окси-группу -O- и присутствовать в виде N-оксида, и такие кольцевые атомы азота могут также присутствовать в виде четвертичной соли, например в виде соли N-(C1-C4)-алкила, такой как соль N-метила, где в одном варианте осуществления изобретения противоион в указанной четвертичной соли представляет собой физиологически приемлемый анион, который образуется из кислоты для получения физиологически приемлемой соли. В монозамещенных фенильных группах заместитель может находиться в положении 2, положении 3 или положении 4. В дизамещенных фенильных группах заместители могут находиться в 2,3-положении, 2,4-положении, 2,5-положении, 2,6-положении, 3,4-положении или 3,5-положении. В тризамещенных фенильных группах заместители могут находиться в 2,3,4-положении, 2,3,5-положении, 2,3,6-положении, 2,4,5-положении, 2,4,6-положении или 3,4,5-положении. Нафтил может представлять собой 1-нафтил (=нафталин-1-ил) или 2-нафтил (=нафталин-2-ил). В монозамещенных 1-нафтильных группах заместитель может находиться во 2-, 3-, 4-, 5-, 6-, 7- или 8-положении. В монозамещенных 2-нафтильных группах заместитель может находиться в 1-, 3-, 4-, 5-, 6-, 7- или 8-положении. В дизамещенных нафтильных группах заместители также оба могут находиться в любых положениях в кольце, через которое нафтильная группа присоединена, и/или в соседнем кольце. Это утверждение, относящееся к одновалентным остаткам, применяется соответственно для двухвалентных остатков, таких как, например, фениленовые группы, представляющие R2, которые могут также быть незамещенными или замещенными, например, по 1, 2, 3 или 4, или по 1, 2 или 3, или по 1 или 2, или по 1 одинаковыми или различными заместителями, которые могут находиться в любом из положений.
В остатках ароматических гетероциклов, представляющих R2 или R3, которые могут обозначаться как группы гетероарила и гетероарилена, а также во всех других гетероциклах в соединениях Формулы I, включая группу Het и неароматические гетероциклические группы, представляющие R3, гетероатомы в кольце обычно выбирают из N, O и S, где N включает кольцевые атомы азота, которые несут атом водорода или заместитель, а также кольцевые атомы азота, которые не несут атом водорода или заместитель. Кольцевые гетероатомы могут находиться в любом положении, при условии, что гетероциклическая система известна из уровня техники и является стабильной, а также является подходящей в качестве подгруппы для требуемой цели соединения Формулы I, такой как применение в качестве лекарственного вещества. В одном варианте осуществления изобретения, два кольцевых атома кислорода не могут находиться в двух соседних положениях в кольце любого гетероцикла, в другом варианте осуществления два кольцевых гетероатома, выбранных из кислорода и серы, не могут присутствовать в двух соседних положениях в кольце любого гетероцикла. Насыщенные кольца не содержат двойную связь в кольце. Ненасыщенные кольцевые системы могут быть ароматическими или частично ненасыщенными, включая частично ароматические, где в последнем случае одно кольцо в бициклической системе является ароматическим и кольцевая система присоединена через атом в неароматическом кольце. В зависимости от соответствующей группы ненасыщенные кольца могут содержать одну, две, три, четыре или пять двойных связей в кольце. Ароматические группы имеют циклическую систему из шести или десяти делокализованных π-электронов в кольце. В зависимости от соответствующей группы, насыщенные и неароматические ненасыщенные гетероциклические кольца, включая Het и неароматические группы, представляющие R3, могут быть 3-членными, 4-членными, 5-членными, 6-членными, 7-членными, 8-членными, 9-членными или 10-членными. В одном варианте осуществления изобретения, ароматические гетероциклические кольца представляют собой 5-членные или 6-членные моноциклические кольца или 8-членные, 9-членные или 10-членные бициклические кольца, в другом варианте осуществления 5-членные или 6-членные моноциклические кольца или 9-членные или 10-членные бициклические кольца, в другом варианте осуществления 5-членные или 6-членные моноциклические кольца, где 8-членные, 9-членные или 10-членные бициклические кольца состоят из двух конденсированных 5-членных колец, 5-членного кольца и 6-членного кольца, которое конденсировано с другим, и двух конденсированных 6-членных колец, соответственно. В бициклических ароматических гетероциклических группах одно или два кольца могут содержать гетероатомы в кольце, и одно или два кольца могут быть ароматическими. Как правило, бициклические кольцевые системы, содержащие ароматическое кольцо и неароматическое кольцо, рассматриваются как ароматические, когда они присоединены через атом углерода в ароматическом кольце, и как неароматические, когда они присоединены через атом углерода в неароматическом кольце. Если не указано особо, гетероциклические группы, включая ароматические гетероциклические группы, могут быть присоединены через любой подходящий кольцевой атом углерода и, в случае азотсодержащих гетероциклов, через любой подходящий кольцевой атом азота. В одном варианте осуществления изобретения, ароматическая гетероциклическая группа в соединении Формулы I, независимо от любой другой ароматической гетероциклической группы, присоединена через кольцевой атом углерода, в другом варианте осуществления через кольцевой атом азота. В зависимости от определения соответствующей гетероциклической группы, в одном варианте осуществления изобретения количество кольцевых гетероатомов, которое может присутствовать в гетероциклической группе, независимо от количества кольцевых гетероатомов в любой другой гетероциклической группе, составляет 1, 2, 3 или 4, в другом варианте осуществления 1, 2 или 3, в другом варианте осуществления 1 или 2, в другом варианте осуществления 1, где кольцевые гетероатомы могут быть одинаковыми или различными. Гетероциклические группы, которые необязательно являются замещенными, могут независимо от любой другой гетероциклической группы быть незамещенными или замещенными одним или несколькими одинаковыми или различными заместителям, например, 1, 2, 3, 4 или 5, или 1, 2, 3 или 4, или 1, 2 или 3, или 1 или 2, или 1 заместителями, которые указаны при определении соответствующей группы. Заместители гетероциклических групп могут находиться в любом из положений. Например, в случае пиридин-2-ильной группы заместители могут находиться в положении 3 и/или положении 4 и/или положении 5 и/или положении 6, в случае пиридин-3-ильной группы заместители могут находиться в положении 2 и/или положении 4 и/или положении 5 и/или положении 6, и в случае пиридин-4-ильной группы заместители могут находиться в положении 2 и/или положении 3 и/или положении 5 и/или положении 6.
Примерами родоначальных гетероциклов, из которых гетероциклические группы, включая ароматические гетероциклические группы, насыщенные гетероциклические группы и неароматическиие ненасыщенные гетероциклические группы, могут образовываться, являются азет, оксет, пиррол, фуран, тиофен, имидазол, пиразол, [1,3]диоксол, оксазол (=[1,3]оксазол), изоксазол (=[1,2]оксазол), тиазол (=[1,3]тиазол), изотиазол (=[1,2]тиазол), [1,2,3]триазол, [1,2,4]триазол, [1,2,4]оксадиазол, [1,3,4]оксадиазол, [1,2,4]тиадиазол, [1,3,4]тиадиазол, тетразол, пиридин, пиран, тиопиран, пиридазин, пиримидин, пиразин, [1,3]оксазин, [1,4]оксазин, [1,3]тиазин, [1,4]тиазин, [1,2,3]триазин, [1,3]дитиин, [1,4]дитиин, [1,2,4]триазин, [1,3,5]триазин, [1,2,4,5]тетразин, азепин, [1,3]диазепин, [1,4]диазепин, [1,3]оксазепин, [1,4]оксазепин, [1,3]тиазепин, [1,4]тиазепин, азоцин, азецин, циклопента[b]пиррол, 2-азабицикло[3.1.0]гексан, 3-азабицикло[3.1.0]гексан, 2-окса-5-азабицикло[2.2.1]гептан, индол, изоиндол, бензотиофен, бензофуран, [1,3]бензодиоксол (=1,2-метилендиоксибензол), [1,3]бензоксазол, [1,3]бензотиазол, бензимидазол, тиено[3,2-c]пиридин, хромен, изохромен, [1,4]бензодиоксин, [1,4]бензоксазин, [1,4]бензотиазин, хинолин, изохинолин, циннолин, хиназолин, хиноксалин, фталазин, тиенотиофен, [1,8]нафтиридин и другие нафтиридины, птеридин, и соответствующие насыщенные и частично ненасыщенные гетероциклы, в которых одна или несколько, например, одна, две, три, четыре или все двойные связи в кольце, включая двойные связи в ароматическом кольце, заменены на одинарные связи, такие как, например, азетидин, оксетан, пирролидин, тетрагидрофуран, тетрагидротиофен, имидазолидин, оксазолидин, тиазолидин, дигидропиридин, пиперидин, тетрагидропиран, пиперазин, морфолин, тиоморфолин, азепан, хроман, изохроман, [1,4]бензодиоксан (=1,2-этилендиоксибензол), 2,3-дигидробензофуран, 1,2,3,4-тетрагидрохинолин, 1,2,3,4-тетрагидроизохинолин.
Примерами остатков ароматических гетероциклов, которые могут встречаться в соединениях Формулы I, являются тиофенил (=тиенил), включая тиофен-2-ил и тиофен-3-ил, пиридинил (=пиридил) включая пиридин-2-ил (=2-пиридил), пиридин-3-ил (=3-пиридил) и пиридин-4-ил (=4-пиридил), имидазолил, включая, например, 1H-имидазол-1-ил, 1H-имидазол-2-ил, 1H-имидазол-4-ил и 1H-имидазол-5-ил, [1,2,4]триазолил, включая 1H-[1,2,4]-триазол-1-ил и 4H-[1,2,4]-триазол-3-ил, тетразолил, включая 1H-тетразол-1-ил и 1H-тетразол-5-ил, хинолинил (=хинолил), включая хинолин-2-ил, хинолин-3-ил, хинолин-4-ил, хинолин-5-ил, хинолин-6-ил, хинолин-7-ил и хинолин-8-ил, все из которых необязательно замещены, как указано в определении соответствующей группы. Примерами остатков насыщенных и частично ненасыщенных гетероциклов, которые могут встречаться в соединениях Формулы I, являются азетидинил, пирролидинил, включая пирролидин-1-ил, пирролидин-2-ил и пирролидин-3-ил, 2,5-дигидро-1H-пирролил, пиперидинил, включая пиперидин-1-ил, пиперидин-2-ил, пиперидин-3-ил и пиперидин-4-ил, 1,2,3,4-тетрагидропиридинил, 1,2,5,6-тетрагидропиридинил, 1,2-дигидропиридинил, азепанил, азоканил, азеканил, октагидроциклопента[b]пирролил, 2,3-дигидробензофуранил, включая 2,3-дигидробензофуран-7-ил, 2,3-дигидро-1H-индолил, октагидро-1H-индолил, 2,3-дигидро-1H-изоиндолил, октагидро-1H-изоиндолил, 1,2-дигидрохинолинил, 1,2,3,4-тетрагидрохинолинил, декагидрохинолинил, 1,2-дигидроизохинолинил, 1,2,3,4-тетрагидроизохинолинил, 1,2,3,4-тетрагидроизохинолинил, декагидроизохинолинил, декагидроизохинолинил, 4,5,6,7-тетрагидротиено[3,2-c]пиридинил, пиразолидинил, имидазолидинил, гексагидропиримидинил, 1,2-дигидропиримидинил, пиперазинил, [1,3]диазепанил, [1,4]диазепанил, оксазолидинил, [1,3]оксазинанил, [1,3]оксазепанил, морфолинил, включая морфолин-2-ил, морфолин-3-ил и морфолин-4-ил, [1,4]оксазепанил, тиазолидинил, [1,3]тиазинанил, тиоморфолинил, включая тиоморфолин-2-ил, тиоморфолин-3-ил и тиоморфолин-4-ил, 3,4-дигидро-2H-[1,4]тиазинил, [1,3]тиазепанил, [1,4]тиазепанил, [1,4]тиазепанил, оксетанил, тетрагидрофуранил, тетрагидротиенил, изоксазолидинил, изотиазолидинил, оксазолидинил, [1,2,4]-оксадиазолидинил, [1,2,4]-тиадиазолидинил, [1,2,4]триазолидинил, [1,3,4]оксадиазолидинил, [1,3,4]тиадиазолидинил, [1,3,4]триазолидинил, 2,3-дигидрофуранил, 2,5-дигидрофуранил, 2,3-дигидротиенил, 2,5-дигидротиенил, 2,3-дигидропирролил, 2,3-дигидроизоксазолил, 4,5-дигидроизоксазолил, 2,5-дигидроизоксазолил, 2,3-дигидроизотиазолил, 4,5-дигидроизотиазолил, 2,5-дигидроизотиазолил, 2,3-дигидропиразолил, 4,5-дигидропиразолил, 2,5-дигидропиразолил, 2,3-дигидрооксазолил, 4,5-дигидрооксазолил, 2,5-дигидрооксазолил, 2,3-дигидротиазолил, 4,5-дигидротиазолил, 2,5-дигидротиазолил, 2,3-дигидроимидазолил, 4,5-дигидроимидазолил, 2,5-дигидроимидазолил, тетрагидропиридазинил, тетрагидропиримидинил, тетрагидропиразинил, тетрагидро[1,3,5]триазинил, [1,3]дитианил, тетрагидропиранил, тетрагидротиопиранил, [1,3]диоксоланил, 3,4,5,6-тетрагидропиридинил, 4H-[1,3]тиазинил, 1,1-диоксо-2,3,4,5-тетрагидротиенил, 2-азабицикло[3.1.0]гексил, включая 2-азабицикло[3.1.0]гекс-2-ил, 3-азабицикло[3.1.0]гексил, включая 3-азабицикло[3.1.0]гекс-3-ил, 2-окса-5-азабицикло[2.2.1]гептил, включая 2-окса-5-азабицикло[2.2.1]гепт-5-ил, которые все присоединены через подходящий кольцевой атом углерода или кольцевой атом азота и являются необязательно замещенными, как указано в определении соответствующей группы.
Галоген представляет собой фтор, хлор, бром или йод. В одном варианте осуществления изобретения, любой галоген в соединении Формулы I выбирается независимо от любого другого галогена из фтора, хлора и брома, в другом варианте осуществления из фтора и хлора.
В случае если оксо-группа связана с атомом углерода, она заменяет два атома водорода у атома углерода в родоначальной системе. Таким образом, если CH2-группа в цепи или в кольце замещена оксо-группой, то есть присоединенным двойной связью атомом кислорода, она превращается в C(O)-группу (=C(=O)-группу). Очевидно, что оксо-группа не может находиться в качестве заместителя при атоме углерода в ароматическом кольце, таком как, например, фенильная группа. Когда в гетероциклической группе кольцевой атом серы может нести одну или две оксо-группы, атом серы S может быть неокисленным при отсутствии какой-либо оксо-группы, или находиться в виде S(O)-группы (сульфоксидной группы, S-оксидной группы) в случае присутствия одной оксо-группы, или находиться в виде S(O)2-группы (=сульфоновой группы, S,S-диоксидной группы) в случае присутствия двух оксо-групп.
Настоящее изобретение охватывает все стереоизомерные формы соединений Формулы I и их солей и сольватов. Что касается каждого хирального центра, независимо от любого другого хирального центра соединения Формулы I могут находиться в S-конфигурации или главным образом в S-конфигурации, или в R-конфигурации или главным образом в R-конфигурации, или в виде смеси S-изомера и R-изомера в любом соотношении. Изобретение охватывает все возможные энантиомеры и диастереомеры, а также смеси двух или более стереоизомеров, например, смеси энантиомеров и/или диастереомеров во всех соотношениях. Таким образом, соединения по изобретению, которые могут существовать в виде энантиомеров, могут присутствовать в энантиомерно чистой форме, как в виде левовращающих, так и правовращающих антиподов, и в виде смесей двух энантиомеров в любых соотношениях, включая рацематы. В случае E/Z-изомерии или цис/транс-изомерии, например, двойных связей или колец, таких как циклоалкильные кольца, изобретение охватывает как E-форму, так и Z-форму, или цис-форму и транс-форму, а также смеси данных форм во всех соотношениях. В одном варианте осуществления изобретения, соединение, которое может существовать в двух или более стереоизомерных формах, является чистым или по существу чистым индивидуальным стереоизомером. Получение индивидуальных стереоизомеров может осуществляться, например, путем разделения смеси изомеров общепринятыми методами, например, с помощью хроматографии или кристаллизации, путем применения в синтезе стереохимически однородных исходных веществ или путем использования стереоселективных методов синтеза. При необходимости, перед разделением стереоизомеров может быть проведена дериватизация. Разделение смеси стереоизомеров может осуществляться на стадии соединения Формулы I или на стадии исходных веществ или промежуточных соединений в процессе синтеза. Настоящее изобретение также охватывает все таутомерные формы соединений Формулы I и их солей и сольватов.
В случае если соединения Формулы I содержат одну или несколько кислотных и/или основных групп, например, формирующих соли групп, изобретение также охватывает их соответствующие физиологически или токсикологически приемлемые соли, то есть нетоксичные соли, в частности, их фармацевтически приемлемые соли. Таким образом, соединения Формулы I, которые содержат кислотную группу, такую как гидроксикарбонильная группа (=карбоксильная группа=C(O)-OH-группа), могут присутствовать в таких группах и могут применяться в соответствии с изобретением в виде, например, солей с щелочными металлами, солей с щелочноземельными металлами или аммониевых солей. Более конкретные примеры таких солей включают соли натрия, соли калия, соли кальция, соли магния, четвертичные аммониевые соли, такие как тетраалкиламмониевая соль, или соли присоединения кислоты с аммиаком или органическими аминами, такими как, например, этиламин, этаноламин, триэтаноламин или аминокислоты. Соединения Формулы I, содержащие основную группу, то есть группу, которая может протонироваться, такую как амино-группа или азотсодержащий гетероцикл, могут присутствовать в таких группах и могут применяться в соответствии с изобретением в виде их солей присоединения с неорганическими и органическими кислотами. Примеры подходящих кислот включают хлороводород, бромоводород, фосфорную кислоту, серную кислоту, метансульфоновую кислоту, щавелевую кислоту, уксусную кислоту, трифторуксусную кислоту, винную кислоту, молочную кислоту, бензойную кислоту, малоновую кислоту, фумаровую кислоту, малеиновую кислоту, лимонную кислоту и другие кислоты, известные специалисту в данной области техники. Если соединение Формулы I содержит в молекуле кислотную группу и основную группу, соединение также охватывает, в дополнение к упомянутым солевым формам, внутренние соли (=бетаины, цвиттерионы). Соли соединений Формулы I могут быть получены традиционными методами, которые хорошо известны специалисту в данной области техники, например, в результате контактирования соединения Формулы I с органической или неорганической кислотой или основанием в растворителе или разбавителе или при анионном обмене или катионном обмене с другой солью. Изобретение также охватывает все соли соединений Формулы I, которые в результате низкой физиологической совместимости образующей соль кислоты или основания не могут непосредственно применяться в фармацевтических продуктах, но которые могут применяться, например, в качестве промежуточных веществ для химических реакций или для получения физиологически приемлемых солей.
Настоящее изобретение также охватывает все сольваты соединений Формулы I, например гидраты, или аддукты со спиртами, такими как (С1-C4)-спирты, активные метаболиты соединений Формулы I, а также пролекарства и производные соединений Формулы I, которые необязательно могут проявлять физиологическую активность in vitro, но которые in vivo превращаются в фармакологически активные соединения, например, сложные эфиры или амиды карбоксильных групп.
В одном варианте осуществления изобретения, A выбирают из NH и O, в другом варианте осуществления А выбирают из NH и S, в другом варианте осуществления А выбирают из O и S, в другом варианте осуществления A представляет собой NH, в другом варианте осуществления A представляет собой O, в другом варианте осуществления A представляет собой S.
Алкандиильные, алкендиильные и алкиндиильные группы, присутствующие в группе X, могут быть линейными или разветвленными, как уже в общих чертах указывалось в отношении таких групп, и указанные группы, а также циклоалкандиильные группы, представляющие X, могут быть связаны с соседними группами, то есть с группой R4O-C(O) и с группой R2 или, в случае алкандиилокси-группы, с атомом кислорода алкандиилокси-группы, по любому положению. Указанные соседние группы могут быть связаны с одним и тем же атомом углерода или с различными атомами углерода в группе X. В одном варианте осуществления цепь атомов углерода в алкандиильной, алкендиильной и алкиндиильной группах, находящихся в группе X, которая непосредственно связывает группу R4O-C(O) с группой R2 или, в случае алкандиилокси-группы, с атомом кислорода алкандиилокси-группы, состоит из 1, 2, 3 или 4 атомов углерода, в другом варианте осуществления из 1, 2 или 3 атомов углерода, в другом варианте осуществления из 1 или 2 атомов углерода, в другом варианте осуществления из 1 атома углерода. В случае циклоалкандиильной группы, представляющей X, в одном варианте осуществления группы R4O-C(O) и R2 связаны с двумя кольцевыми атомами углерода, которые находятся 1,2-положении, 1,3-положении или 1,4-положении друг относительно друга, в другом варианте осуществления в 1,2-положении или 1,3-положении друг относительно друга, в другом варианте осуществления в 1,2-положении друг относительно друга, в другом варианте осуществления в 1,4-положении друг относительно друга. В одном варианте осуществления X выбирают из (C1-C6)-алкандиила, (C2-C6)-алкендиила, (C3-C7)-циклоалкандиила и (C1-C6)-алкандиилокси, в другом варианте осуществления из (C1-C6)-алкандиила, (C2-C6)-алкендиила и (C1-C6)-алкандиилокси, в другом варианте осуществления из (C1-C6)-алкандиила, (C3-C7)-циклоалкандиила и (C1-C6)-алкандиилокси, в одном варианте осуществления из (C1-C6)-алкандиила и (C1-C6)-алкандиилокси, в другом варианте осуществления из (C1-C6)-алкандиила, (C2-C6)-алкендиила, (C2-C6)-алкиндиила и (C3-C7)-циклоалкандиила, в другом варианте осуществления из (C1-C6)-алкандиила, (C2-C6)-алкендиила и (C3-C7)-циклоалкандиила, в другом варианте осуществления из (C1-C6)-алкандиила и (C2-C6)-алкендиила, в другом варианте осуществления X представляет собой (C1-C6)-алкандиил, в другом варианте осуществления X представляет собой (C2-C6)-алкендиил, в другом варианте осуществления X представляет собой (C3-C7)-циклоалкандиил, и в другом варианте осуществления X представляет собой (C1-C6)-алкандиилокси, которые все необязательно могут быть замещены, как указано. В одном варианте осуществления (C1-C6)- алкандиильная группа, находящаяся в Х, представляет собой (C1-C4)-алкандиильную группу, в другом варианте осуществления (C1-C3)-алкандиильную группу, в другом варианте осуществления (C1-C2)-алкандиильную группу. В одном варианте осуществления (C2-C6)-алкендиильная и (C2-C6)-алкиндиильная группы, представляющие Х, являются (C2-C4)-алкендиильной и (C2-C4)-алкиндиильной группами, в другом варианте осуществления (C2-C3)-алкендиильной и (C2-C3)-алкиндиильной группами. В одном варианте осуществления (C3-C7)-циклоалкандиильная группа, представляющая Х, является (C3-C6)-циклоалкандиильной группой, в другом варианте осуществления (C3-C4)-циклоалкандиильной группой, в другом варианте осуществления циклопропандиильной группой, в другом варианте осуществления циклогександиильной группой. Примерами групп X, из которых любая одна или несколько соответствующих групп, представляющих Х, могут быть выбраны в упомянутых выше вариантах осуществления, или любая одна или несколько из Х выбраны в другом варианте осуществления изобретения, являются метилен, -CH(CH3)- (этан-1,1-диил), -CH2-CH2- (этан-1,2-диил, 1,2-этилен), -C(CH3)2- (1-метилэтан-1,1-диил), -CH2-CH2-CH2- (пропан-1,3-диил, 1,3-пропилен), -CH2-CH(CH3)- и -CH(CH3)-CH2- (пропан-1,2-диил, 1,2-пропилен), которые являются примерами (C1-C6)-алкандиильной группы, -CH=CH- (этен-1,2-диил), -CH=CH-CH2- и -CH2-CH=CH- (проп-1-ен-1,3-диил и проп-2-ен-1,3-диил) и -CH=C(CH3)- и -C(CH3)=CH- (проп-1-ен-1,2-диил), которые являются примерами группы (C2-C6)-алкендиила, -C≡C- (этиндиил) и -CH2-C≡C- и -C≡C-CH2- (проп-1-ин-1,3-диил и проп-2-ин-1,3-диил), которые являются примерами группы (C2-C6)-алкиндиила, циклопропан-1,1-диил, циклопропан-1,2-диил и циклогексан-1,4-диил, которые являются примерами группы (C3-C7)-циклоалкандиила, -CH2-O- (метиленокси), -CH2-CH2-O- (этан-1,2-диилокси), -CH(CH3)-O- (этан-1,1-диилокси), -C(CH3)2-O- (1-метилэтан-1,1-диилокси), -CH2-CH2-CH2-O- (пропан-1,3-диилокси) и -CH2-CH2-CH2-CH2-O- (бутан-1,4-диилокси), которые являются примерами группы (C1-C6)-алкандиилокси, где все группы необязательно замещены, как указано. Таким образом, в одном варианте осуществления X выбирают из -CH2-O-, -CH2-CH2-O-, -CH(CH3)-O- и -C(CH3)2-O-, в другом варианте осуществления из -CH2-O-, -CH2-CH2-O- и -CH(CH3)-O-, в другом варианте осуществления из -CH2-O- и -CH(CH3)-O-, и в другом варианте осуществления X представляет собой -CH2-O-, где все группы необязательно замещены, как указано, и где атом кислорода связан с группой R2. В одном варианте осуществления количество заместителей, которые необязательно присутствуют в X, составляет 1, 2, 3 или 4, в другом варианте осуществления 1, 2 или 3, в другом варианте осуществления 1 или 2, в другом варианте осуществления 1, и в другом варианте осуществления группа X не имеет заместителей, выбранных из фтора и гидрокси. В одном варианте осуществления количество гидрокси-заместителей в X составляет не более 2, в другом варианте осуществления не более 1. В одном варианте осуществления при отдельном атоме углерода присутствует не более одного гидрокси-заместителя. В одном варианте осуществления атомы углерода, которые составляют двойную связь в группе (C2-C6)-алкендиила, не имеют гидрокси-заместителей. В одном варианте осуществления атомы углерода в группе (C1-C6)-алкандиилокси, которые связаны с атомом кислорода, не имеют гидрокси-заместителей, в другом варианте осуществления атомы углерода в группе (C1-C6)-алкандиилокси, которые связаны с атомом кислорода, не имеют заместителей, то есть в последнем варианте осуществления все атомы углерода, которые не связаны с указанным атомом кислорода, являются необязательно замещенными одним или несколькими одинаковыми или различными заместителями, выбранными из фтора или гидрокси. Двойная связь в группе (C2-C6)-алкендиила может иметь E-конфигурацию или Z-конфигурацию. В одном варианте осуществления она имеет E-конфигурацию, в другом варианте осуществления Z-конфигурацию.
В одном варианте осуществления изобретения число z выбирают из 0 и 1, в другом варианте осуществления оно равно 0, в другом варианте осуществления оно равно 1. В одном варианте осуществления изобретения группу R1 выбирают из водорода и (C1-C4)-алкила, в другом варианте осуществления R1 выбирают из водорода, метила, этила, н-пропила, н-бутила и изопропила, в другом варианте осуществления из водорода, метила и этила, в другом варианте осуществления R1 является водородом, в другом варианте осуществления R1 является (C1-C4)-алкилом, в другом варианте осуществления R1 является метилом, и в другом варианте осуществления R4 является этилом. В одном варианте осуществления (C3-C7)-циклоалкильная группа, присутствующая в R1, представляет собой (C3-C6)-циклоалкил, в другом варианте осуществления является циклопропилом.
В одном варианте осуществления изобретения количество кольцевых гетероатомов в ароматическом гетероцикле, представляющем R2, составляет 1 или 2, в другом варианте осуществления составляет 1. В одном варианте осуществления изобретения R2 выбирают из фенилена и двухвалентного остатка ароматического 6-членного моноциклического гетероцикла, который содержит 1, 2 или 3 кольцевых атомов азота, в другом варианте осуществления 1 или 2 кольцевых атома азота, в другом варианте осуществления 1 кольцевой атом азота, где один из кольцевых атомов азота может иметь заместитель R21, который представляет собой окси-группу, то есть где один из кольцевых атомов азота может быть окислен до N-оксида и где фенилен и двухвалентный остаток ароматического гетероцикла являются необязательно замещенными по одному или нескольким кольцевым атомам углерода одинаковыми или различными заместителями R22. В другом варианте осуществления R2 является фениленом, где фенилен является необязательно замещенным по одному или нескольким кольцевым атомам одинаковыми или различными заместителям R22, и в другом варианте осуществления R2 является пиридиндиилом, где кольцевой атом азота может нести заместитель R21, который представляет собой окси-группу, то есть где кольцевой атом азота может быть окислен до N-оксида, и где пиридиндиил необязательно замещен по одному или нескольким атомам углерода в кольце одинаковыми или различными заместителями R22. В другом варианте осуществления R2 представляет собой двухвалентный остаток ароматического 5-членного гетероцикла, который содержит 1, 2 или 3 одинаковых или различных кольцевых гетероатома, выбранных из N, O и S, где один из атомов азота в кольце может нести атом водорода или заместитель R21 и где двухвалентный остаток ароматического гетероцикла необязательно замещен по одному или нескольким кольцевым атомам углерода одинаковыми или различными заместителями R22. В одном варианте осуществления двухвалентный остаток ароматической гетероциклической группы, представляющей R2, выбирают из фурандиила, тиофендиила, оксазолдиила, тиазолдиила, пиридиндиила, пиридазиндиила, пиримидиндиила и пиразиндиила, в другом варианте осуществления из фурандиила, тиофендиила, тиазолдиила, пиридиндиила, пиридазиндиила, пиримидиндиила и пиразиндиила, в другом варианте осуществления из фурандиила, тиофендиила, пиридиндиила, пиридазиндиила, пиримидиндиила и пиразиндиила, в другом варианте осуществления из фурандиила, тиофендиила, пиридиндиила и пиримидиндиила, в другом варианте осуществления из фурандиила, тиофендиила и пиридиндиила, которые являются необязательно замещенными, как указано в отношении R2.
Кольцевые атомы углерода, через которые группа фенилена и двухвалентный остаток ароматического гетероцикла, представляющего R2, присоединены к кольцу оксазолопиримидина и группе X, могут находиться в любом положении. Группа фенилена, представляющая R2, может быть 1,2-фениленом, то есть кольцо оксазолопиримидина и группа X могут быть связаны в 1,2-положении или орто-положении относительно друг друга, она может представлять собой 1,3-фенилен, то есть кольцо оксазолопиримидина и группа X могут быть связаны в 1,3-положении или мета-положении относительно друг друга, а также она может представлять собой 1,4-фенилен, то есть кольцо оксазолопиримидина и группа X могут быть связаны в 1,4-положении или пара-положении относительно друг друга. В одном варианте осуществления группу фенилена, представляющую R2, выбирают из 1,3-фенилена и 1,4-фенилена, в другом варианте осуществления,она представляет собой 1,3-фенилен, и в другом варианте осуществления она представляет собой 1,4-фенилен, которые все являются необязательно замещенными, как указано в отношении R2. В одном варианте осуществления R2 выбирают из одной или нескольких следующих групп: фенилен, фуран-2,5-диил, тиофен-2,4-диил, тиофен-2,5-диил, пиридин-2,4-диил, пиридин-2,5-диил, пиридин-3,5-диил, пиридин-2,6-диил и пиримидин-2,5-диил, в другом варианте осуществления из следующих групп: фуран-2,5-диил, тиофен-2,4-диил, тиофен-2,5-диил, пиридин-2,4-диил, пиридин-2,5-диил, пиридин-3,5-диил, пиридин-2,6-диил и пиримидин-2,5-диил, в другом варианте осуществления из пиридин-2,4-диила, пиридин-2,5-диила, пиридин-3,5-диила и пиридин-2,6-диила, в другом варианте осуществления из фенилена, пиридин-2,4-диила, пиридин-2,5-диила, пиридин-3,5-диила и пиридин-2,6-диила, которые являются необязательно замещенными, как указано в отношении R2. В одном варианте осуществления количество заместителей R22, которые необязательно присутствуют при кольцевых атомах углерода в R2, составляет 1, 2, 3, 4 или 5, в другом варианте осуществления 1, 2, 3 или 4, в другом варианте осуществления 1, 2 или 3, в другом варианте осуществления 1 или 2, в другом варианте осуществления 1. Кольцевые атомы углерода в R2, которые не имеют заместитель R22, несут атом водорода.
В одном варианте осуществления изобретения R3 выбирают из (C1-C6)-алкила, (C2-C6)-алкенила и (C2-C6)-алкинила, в другом варианте осуществления R3 представляет собой (С1-C6)-алкил, в другом варианте осуществления R3 представляет собой (C2-C5)-алкил, и в другом варианте осуществления R3 представляет собой (C1-C4)-алкил. В другом варианте осуществления R3 выбирают из (C1-C6)-алкила, (C3-C7)-циклоалкил-CuH2u- и Het-CvH2v-, в другом варианте осуществления из (C3-C7)-циклоалкил-CuH2u- и Het-CvH2v-, в другом варианте осуществления R3 представляет собой (C3-C7)-циклоалкил-CuH2u-, и в другом варианте осуществления R3 представляет собой Het-CvH2v-, где в данном варианте осуществления u и v независимо друг от друга выбирают из 1 и 2. В одном варианте осуществления u равно 1, в другом варианте осуществления u равно 2. В одном варианте осуществления v равно 1, в другом варианте осуществления v равно 2. В одном варианте осуществления группу (C3-C7)-циклоалкил-CuH2u-, представляющую R3, выбирают из циклопропил-CuH2u-, циклобутил-CuH2u- и циклопентил-CuH2u-, и группа Het-CvH2v-, представляющая R3, является тетрагидрофуранил-CvH2v-. В одном варианте осуществления R3 выбирают из циклопропил-CuH2u-, циклобутил-CuH2u- и циклопентил-CuH2u-.
В одном варианте осуществления R3 выбирают из (C3-C7)-циклоалкил-CuH2u- и Het-CvH2v-, или R3 является остатком насыщенного или ненасыщенного 3-членного-10-членного моноциклического или бициклического кольца, которое содержит 0, 1, 2, 3 или 4 одинаковых или различных кольцевых гетероатома, выбранных из N, O и S, где один или два атома азота в кольце могут нести атом водорода или (C1-C4)-алкильный заместитель и один или два кольцевых атома серы могут нести одну или две оксо-группы, и где остаток кольца необязательно замещен по одному или нескольким кольцевым атомам углерода одинаковыми или различными заместителями R31, и в другом варианте осуществления R3 является остатком насыщенного или ненасыщенного 3-членного-10-членного моноциклического или бициклического кольца, которое содержит 0, 1, 2, 3 или 4 одинаковых или различных кольцевых гетероатома, выбранных из N, O и S, где один или два атома азота в кольце могут нести атом водорода или (C1-C4)-алкильный заместитель и один или два кольцевых атома серы могут нести одну или две оксо-группы, и где остаток кольца необязательно замещен по одному или нескольким кольцевым атомам углерода одинаковыми или различными заместителями R31. В одном варианте осуществления количество кольцевых гетероатомов в кольце, представляющем R3, составляет 0, 1, 2 или 3, в другом варианте осуществления 0, 1 или 2, в другом варианте осуществления 0 или 1, в другом варианте осуществления 0, в другом варианте осуществления количество составляет 1, 2, 3 или 4, в другом варианте осуществления 1, 2 или 3, в другом варианте осуществления 1 или 2, в другом варианте осуществления 1. Остаток кольца, представляющего R3, может, таким образом, являться карбоциклическим или гетероциклическим. В одном варианте осуществления кольцевые гетероатомы в R3 выбирают из N и O, в другом варианте осуществления из N и S, в другом варианте осуществления из O и S, в другом варианте осуществления они представляют собой N, где кольцевые атомы азота могут нести атом водорода или (C1-C4)-алкильный заместитель, который встречается в насыщенных или частично ненасыщенных гетероциклах или в 5-членных ароматических кольцах, таких как, например, пиррол или бензимидазол, или могут не нести атом водорода или (C1-C4)- алкильный заместитель, который встречается в ароматических гетероциклах, таких как, например, имидазол или пиридин. В остатке гетероцикла, представляющего R3, который содержит один или несколько кольцевых атомов серы, в одном варианте осуществления один из кольцевых атомов серы является неокисленным или несет одну или две оксо-группы, а любые другие кольцевые атомы серы являются неокисленными. Остаток моноциклического или бициклического кольца, представляющего R3, может быть связан с группой А через любой подходящий кольцевой атом углерода или кольцевой атом азота. В одном варианте осуществления он может быть связан через кольцевой атом углерода, в другом варианте осуществления он может быть связан через кольцевой атом углерода или, в случае, когда A представляет собой NH, через кольцевой атом азота, и в другом варианте осуществления он может быть связан через кольцевой атом азота. Остаток моноциклического или бициклического кольца, представляющего R3, может быть ненасыщенным и в этом случае содержать 1, 2, 3, 4 или 5, или 1, 2, 3 или 4, или 1, 2 или 3, или 1 или 2, или 1 двойных связей в кольце и может в случае любого одного или двух колец быть ароматическим или неароматическим, или может быть насыщенным и в последнем случае не иметь двойных связей в кольце. В одном варианте осуществления остаток кольца, представляющего R3, является насыщенным или ароматическим, в другом варианте осуществления является насыщенным и в другом варианте осуществления является ароматическим. В одном варианте осуществления остаток 3-членного или 4-членного кольца, представляющего R3, является насыщенным. Если R3 содержит кольцевые атомы азота, которые могут нести атом водорода или (C1-C4)-алкильный заместитель, может присутствовать один из таких кольцевых атомов азота или два из таких кольцевых атомов азота. В одном варианте осуществления количество необязательных заместителей R31 у кольцевых атомов углерода в кольце, представляющем R3, составляет 1, 2, 3, 4, 5 или 6, в другом варианте осуществления 1, 2, 3, 4 или 5, в другом варианте осуществления 1, 2, 3 или 4, в другом варианте осуществления 1, 2 или 3, в другом варианте осуществления 1 или 2, в другом варианте осуществления 1.
Кольцо, которое может представлять R3, может быть 3-членным, 4-членным, 5-членным, 6-членным, 7-членным, 8-членным, 9-членным или 10-членным. В одном варианте осуществления R3 является 4-членным-10-членным, в другом варианте осуществления 4-членным-9-членным, в другом варианте осуществления 4-членным-8-членным, в другом варианте осуществления 4-членным-7-членным, в другом варианте осуществления 5-членным-7-членным, в другом варианте осуществления 5-членным-6-членным, в другом варианте осуществления 6-членным, в другом варианте осуществления 8-членным-10-членным, в другом варианте осуществления 9-членным-10-членным. В одном варианте осуществления 3-членное кольцо, представляющее R3, не содержит какого-либо гетероатома в кольце. В одном варианте осуществления R3 является моноциклическим, в другом варианте осуществления бициклическим. В одном варианте осуществления бициклическая группа, представляющая R3, является по меньшей мере 7-членной. Среди прочего, остаток кольца, представляющего R3, может быть циклоалкильной группой, фенильной группой, нафтильной группой, остатком ненасыщенной, ароматической или неароматической гетероциклической группы или остатком насыщенной гетероциклической группы, которые все необязательно замещены по кольцевым атомам углерода и кольцевым атомам азота, как указано в отношении R3. Насколько это применимо, все представленные выше разъяснения в отношении таких групп относятся соответственно к R3. Другим примером групп, которые могут представлять R3, являются циклоалкенильные группы, такие как (C5-C7)-циклоалкенильные группы, которые могут быть присоединены через любой кольцевой атом углерода и являться необязательно замещенными, как указано в отношении R3. В одном варианте осуществления необязательные заместители R31 у циклоалкенильной группы, представляющей R3, выбирают из фтора и (С1-C4)-алкила. В одном варианте осуществления циклоалкенильные группы содержат одну двойную связь в кольце, которая может находиться в любом положении. Примерами циклоалкенила являются циклопентенил, включая циклопент-1-енил, циклопент-2-енил и циклопент-3-енил, циклогексенил, включая циклогекс-1-енил, циклогекс-2-енил и циклогекс-3-енил, и циклогептенил, включая циклогепт-1-енил, циклогепт-2-енил, циклопент-3-енил и циклогепт-4-енил. Примерами остатков колец из любого одного или нескольких R3, выбранных в одном варианте осуществления изобретения, являются циклопропил, циклобутил, циклопентил, циклогексил, фенил, оксетанил, включая оксетан-3-ил, тетрагидрофуранил, включая тетрагидрофуран-3-ил, тетрагидротиофенил, включая тетрагидротиофен-3-ил, тетрагидропиранил, включая тетрагидропиран-4-ил, азетидинил, включая азетидин-1-ил, пирролидинил, пиперидинил, имидазолидинил, пиперазинил, морфолинил, включая морфолин-1-ил, тиоморфолинил, фуранил, включая фуран-3-ил, тиофенил, включая тиофен-3-ил, пиразолил, включая пиразол-3-ил, имидазолил, тиазолил, включая тиазол-2-ил, пиридинил, включая пиридин-2-ил, пиридин-3-ил и пиридин-4-ил, пиридазинил, включая пиридазин-3-ил, где во всех из них, в соответствующих случаях, один или два кольцевых атома азота могут нести атом водорода или (C1-C4)-алкил, и где все из них необязательно замещены по одному или нескольким кольцевым атомам углерода одинаковыми или различными заместителями R31, и где во всех из них, в соответствующих случаях, кольцевой атом серы может быть неокисленным, то есть присутствовать в виде атома серы, или нести одну или две оксо-группы, то есть присутствовать в виде сульфоксида или сульфона.
В одном варианте осуществления R3 выбирают из фенила и остатка насыщенного или ненасыщенного 3-членного-7-членного моноциклического кольца, в другом варианте осуществления из фенила и остатка насыщенного или ненасыщенного 5-членного-7-членного моноциклического кольца, в другом варианте осуществления из фенила, пиридинила и остатка насыщенного 3-членного-7-членного моноциклического кольца, в другом варианте осуществления из фенила, пиридинила и остатка насыщенного 5-членного-7-членного моноциклического кольца, в другом варианте осуществления из фенила и остатка насыщенного 3-членного-7-членного моноциклического кольца, в другом варианте осуществления из фенила и остатка насыщенного 5-членного-7-членного моноциклического кольца, где во всех данных вариантах осуществления моноциклическое кольцо содержит 1 или 2 одинаковых или различных кольцевых гетероатома, выбранных из N, O и S, где один или два атома азота в кольце могут нести атом водорода или (C1-C4)-алкильный заместитель и один или два кольцевых атома серы могут нести одну или две оксо-группы, и где фенил, пиридинил и остаток кольца необязательно замещен по одному или нескольким кольцевым атомам углерода одинаковыми или различными заместителями R31, и где пиридинил включает пиридин-2-ил, пиридин-3-ил и пиридин-4-ил. В одном варианте осуществления R3 представляет собой фенил, который необязательно замещен одним или несколькими одинаковыми или различными заместителям R31.
В одном варианте осуществления изобретения, число w выбирают из 0 и 1, в другом варианте осуществления оно равно 0, в другом варианте осуществления оно равно 1. В одном варианте осуществления (C3-C7)-циклоалкильной группой, представленной в R21, является (C3-C6)-циклоалкилом, в другом варианте осуществления (C3-C5)-циклоалкилом, в другом варианте осуществления циклопропилом. В одном варианте осуществления R21 выбирают из (C1-C4)-алкила и окси, в другом варианте осуществления R21 является (C1-C4)-алкилом, в другом варианте осуществления (C1-C3)-алкилом, в другом варианте осуществления метилом и в другом варианте осуществления окси.
В одном варианте осуществления изобретения, заместители R22, которые необязательно присутствуют у группы R2, выбирают из галогена, гидрокси, (С1-C4)-алкил-, (С1-C4)-алкилокси-, (C1-C4)-алкил-S(O)m-, амино, нитро и циано, в другом варианте осуществления из галогена, гидрокси, (С1-C4)-алкил-, (С1-C4)- алкилокси-, амино и циано, в другом варианте осуществления из галогена, гидрокси, (С1-C4)-алкил- и (С1-C4)-алкилокси-, в другом варианте осуществления из фтора, хлора, гидрокси, (С1-C4)-алкил- и (С1-C4)-алкилокси-, в другом варианте осуществления из фтора, хлора и (С1-C4)-алкил-, и в другом варианте осуществления они являются (C1-C4)-алкильными заместителями.
В одном варианте осуществления 1, 2 или 3 заместителя R22, в другом варианте осуществления 1 или 2 заместителя R22, и в другом варианте осуществления 1 заместитель R22, которые необязательно присутствуют у группы R2, определяют как в общем определении R22 и, таким образом, выбирают из галогена, гидрокси, (С1-C4)-алкил-, (С1-C4)-алкилокси-, (C1-C4)-алкил-S(O)m-, амино, нитро, циано, гидроксикарбонила, (С1-C4)-алкилоксикарбонила, аминокарбонила и аминосульфонила, и любые дополнительные заместители R22, которые необязательно присутствуют у группы R2, например, 1, 2 или 3 дополнительных заместителя R22 или 1 или 2 дополнительных заместителя R22 или 1 дополнительный заместитель R22, выбирают из галогена, гидрокси, (С1-C4)-алкил-, (С1-C4)-алкилокси-, (С1-C4)-алкил-S(O)m-, амино, нитро и циано, где все алкильные группы независимо друг от друга необязательно замещены одним или несколькими фторами, что обычно используют в отношении алкильных групп. В одном варианте осуществления указанные заместители R22, которые необязательно присутствуют у группы R2 и которые в упомянутом выше варианте осуществления определяют как в общем определении R22, например, 1 или 2 таких заместителя R22 или 1 такой заместитель R22, выбирают из галогена, гидрокси, (С1-C4)-алкил-, (С1-C4)-алкилокси-, (С1-C4)-алкил-S(O)m-, амино и циано. В одном варианте осуществления указанные заместители R22, которые необязательно присутствуют в группе R2 и которые в упомянутом выше варианте осуществления определяют как в общем определении R22, например, 1 или 2 таких заместителя R22 или 1 такой заместитель R22, не располагаются на кольцевых атомах углерода в группе R2, которые находятся рядом с атомом, через который группа R2 связана с оксазолопиримидиновым кольцом, представленным в Формуле I. В одном варианте осуществления указанные дополнительные заместители R22, которые необязательно присутствуют в группе R2, например 1, 2 или 3 дополнительных заместителя R22 или 1 или 2 дополнительных заместителя R22 или 1 дополнительный заместитель R22, выбирают из галогена, гидрокси, (С1-C4)-алкил-, (С1-C4)-алкилокси-, амино, циано, в другом варианте осуществления из галогена, гидрокси, (С1-C4)-алкил-, (С1-C4)-алкилокси-, в другом варианте осуществления из галогена, (С1-C4)-алкил- и (С1-C4)-алкилокси-, в другом варианте осуществления из галогена и (С1-C4)-алкил-, где во всех данных вариантах осуществления все алкильные группы независимо друг от друга необязательно замещены одним или несколькими фторами.
В одном варианте осуществления изобретения, R31 выбирают из галогена, (С1-C4)-алкила, (C3-C7)-циклоалкила, гидрокси, (С1-C4)-алкилокси, оксо, (С1-C4)-алкил-S(O)m-, амино, (С1-C4)-алкиламино, ди((С1-C4)-алкил)амино, (С1-C4)-алкилкарбониламино, (С1-C4)-алкилсульфониламино, циано, (С1-C4)-алкилкарбонила, аминосульфонила, (С1-C4)-алкиламиносульфонила и ди((С1-C4)-алкил)аминосульфонила, в другом варианте осуществления из галогена, (С1-C4)-алкила, (C3-C7)-циклоалкила, гидрокси, (С1-C4)- алкилокси, оксо, (С1-C4)-алкил-S(O)m-, амино, (С1-C4)-алкиламино, ди((С1-C4)-алкил)амино, циано, аминосульфонила, (С1-C4)-алкиламиносульфонила и ди((С1-C4)-алкил)аминосульфонила, в другом варианте осуществления из галогена, (С1-C4)-алкила, (C3-C7)-циклоалкила, гидрокси, (С1-C4)-алкилокси, оксо, (С1-C4)-алкил-S(O)m-, амино, (С1-C4)-алкиламино, ди((С1-C4)-алкил)амино, циано и аминосульфонила, в другом варианте осуществления из галогена, (С1-C4)-алкил, (C3-C7)-циклоалкила, гидрокси, (С1-C4)-алкилокси, оксо, амино, (С1-C4)-алкиламино, ди((С1-C4)-алкил)амино, циано и аминосульфонила, в другом варианте осуществления из галогена, (С1-C4)-алкила, (C3-C7)-циклоалкила, гидрокси, (С1-C4)-алкилокси, оксо, амино, (С1-C4)-алкиламино и ди((С1-C4)-алкил)амино, в другом варианте осуществления из галогена, (С1-C4)-алкила, (C3-C7)-циклоалкила, (С1-C4)-алкилокси и ди((С1-C4)-алкил)амино, в другом варианте осуществления из галогена, (С1-C4)-алкила, (C3-C7)-циклоалкила, гидрокси и (С1-C4)-алкилокси, в другом варианте осуществления из галогена, (С1-C4)-алкила и (С1-C4)-алкилокси, в другом варианте осуществления из фтора, хлора, (С1-C4)-алкила, (C3-C7)-циклоалкила, гидрокси и (С1-C4)-алкилокси, где во всех данных вариантах осуществления все алкильные группы независимо друг от друга необязательно замещены одним или несколькими фторами.
В одном варианте осуществления необязательные заместители R31 остатка ароматического кольца, представляющего R3, например, фенильной группы или пиридильной группы, представляющих R3, выбирают из галогена, (С1-C4)-алкила, (C3-C7)-циклоалкила, гидрокси, (С1-C4)-алкилокси, (С1-C4)-алкил-S(O)m-, амино, (С1-C4)- алкиламино, ди((С1-C4)-алкил)амино, (С1-C4)-алкилкарбониламино, (С1-C4)-алкилсульфониламино, циано, (С1-C4)-алкилкарбонила, аминосульфонила, (С1-C4)-алкиламиносульфонила и ди((С1-C4)-алкил)аминосульфонила, в другом варианте осуществления из галогена, (С1-C4)-алкила, (C3-C7)-циклоалкила, гидрокси, (С1-C4)-алкилокси, (С1-C4)-алкил-S(O)m-, амино, (С1-C4)-алкиламино, ди((С1-C4)-алкил)амино, циано, аминосульфонила, (С1-C4)-алкиламиносульфонила и ди((С1-C4)-алкил)аминосульфонила, в другом варианте осуществления из галогена, (С1-C4)-алкила, (C3-C7)-циклоалкила, гидрокси, (С1-C4)-алкилокси, (С1-C4)-алкил-S(O)m-, амино, (С1-C4)-алкиламино, ди((С1-C4)-алкил)амино, циано и аминосульфонила, в другом варианте осуществления из галогена, (С1-C4)-алкила, (C3-C7)-циклоалкила, гидрокси, (С1-C4)-алкилокси, амино, (С1-C4)-алкиламино, ди((С1-C4)-алкил)амино, циано и аминосульфонила, в другом варианте осуществления из галогена, (С1-C4)-алкила, (C3-C7)-циклоалкила, гидрокси, (С1-C4)-алкилокси, амино, (С1-C4)-алкиламино и ди((С1-C4)-алкил)амино, в другом варианте осуществления из галогена, (С1-C4)-алкила, (C3-C7)-циклоалкила, (С1-C4)-алкилокси и ди((С1-C4)-алкил)амино, в другом варианте осуществления из галогена, (С1-C4)-алкила, (C3-C7)-циклоалкила, гидрокси и (С1-C4)-алкилокси, в другом варианте осуществления из галогена, (С1-C4)-алкила и (С1-C4)-алкилокси, в другом варианте осуществления из фтора, хлора, (С1-C4)-алкила, (C3-C7)-циклоалкила, гидрокси и (С1-C4)-алкилокси, где во всех данных вариантах осуществления все алкильные группы независимо друг от друга необязательно замещены одним или несколькими фторами.
В одном варианте осуществления необязательные заместители R31 у остатка насыщенного или неароматического ненасыщенного кольца, представляющего R3, выбирают из галогена, (С1-C4)-алкила, (C3-C7)-циклоалкила, гидрокси, (С1-C4)-алкилокси, оксо, (С1-C4)-алкил-S(O)m-, амино, (С1-C4)-алкиламино, ди((С1-C4)-алкил)амино, (С1-C4)-алкилкарбониламино, (С1-C4)-алкилсульфониламино и циано, в другом варианте осуществления из галогена, (С1-C4)-алкила, (C3-C7)-циклоалкила, гидрокси, (С1-C4)-алкилокси, оксо, амино, (С1-C4)-алкиламино, ди((С1-C4)-алкил)амино и циано, в другом варианте осуществления из галогена, (С1-C4)-алкила, (C3-C7)-циклоалкила, гидрокси, (С1-C4)-алкилокси и оксо, в другом варианте осуществления из галогена, (С1-C4)-алкила, гидрокси, (С1-C4)-алкилокси и оксо, в другом варианте осуществления из фтора, хлора, (С1-C4)-алкила, гидрокси, (С1-C4)-алкилокси и оксо, в другом варианте осуществления из (С1-C4)-алкила, гидрокси и оксо, в другом варианте осуществления из алкила и гидрокси, и в другом варианте осуществления они представляют собой (С1-C4)-алкил, где во всех данных вариантах осуществления все алкильные группы независимо друг от друга необязательно замещены одним или несколькими фторами. В случае если остаток кольца, представляющего R3, содержит любые оксо-группы в качестве заместителей R31, в одном варианте осуществления присутствует не более двух таких оксо-заместителей, и в другом варианте осуществления присутствует не более одного оксо-заместителя.
В одном варианте осуществления изобретения, кольцевые гетероатомы Het выбирают из N и O, в другом варианте осуществления из O и S, в другом варианте осуществления они являются атомами O. В другом варианте осуществления количество кольцевых гетероатомов в Het составляет 1. В одном варианте осуществления два кольцевых атома кислорода в Het находятся не в соседних положениях в кольце, в другом варианте осуществления два кольцевых гетероатома, выбранных из O и S, находятся не в соседних положениях в кольце, в другом варианте осуществления два кольцевых гетероатома находятся не в соседних положениях в кольце. Кольцевые атомы азота в Het несут атом водорода или указанный заместитель. В одном варианте осуществления необязательными заместителями у кольцевых атомов азота в Het являются (С1-C4)-алкильные заместители. В одном варианте осуществления необязательные заместители у кольцевых атомов азота и кольцевые атомы углерода в Het представляют собой (C1-C4)-алкильный заместитель. В одном варианте осуществления количество необязательных заместителей у Het составляет 1, 2, 3, 4 или 5, в другом варианте осуществления 1, 2, 3 или 4, в другом варианте осуществления 1, 2 или 3, в другом варианте осуществления 1 или 2, в другом варианте осуществления 1. Het может быть присоединен через любой подходящий кольцевой атом углерода. В одном варианте осуществления, Het присоединен через кольцевой атом углерода, который не является соседним с кольцевым гетероатомом. Het может быть 4-членным, 5-членным, 6-членным или 7-членным. В одном варианте осуществления Het может быть 4-членным или 5-членным, в другом варианте осуществления 5-членным-7-членным, в другом варианте осуществления 5-членным или 6-членным, в другом варианте осуществления 4-членным. Примерами Het, из одного или нескольких из которых в одном варианте осуществления выбирают Het, являются оксетанил, включая оксетан-2-ил и оксетан-3-ил, тетрагидрофуранил, включая тетрагидрофуран-2-ил и тетрагидрофуран-3-ил, тетрагидропиранил, включая тетрагидропиран-2-ил, тетрагидропиран-3-ил и тетрагидропиран-4-ил, оксепанил, включая оксепан-2-ил, оксепан-3-ил и оксепан-4-ил, [1,3]диоксоланил, включая [1,3]диоксолан-2-ил и [1,3]диоксолан-4-ил, [1,4]диоксанил, включая [1,4]диоксан-2-ил, тиетанил, включая тиетан-2-ил и тиетан-3-ил, тетрагидротиофенил, включая тетрагидротиофен-2-ил и тетрагидротиофен-3-ил, тетрагидротиопиранил, включая тетрагидротиопиран-2-ил, тетрагидротиопиран-3-ил и тетрагидротиопиран-4-ил, [1,4]дитианил, включая [1,4]дитиан-2-ил, азетидинил, включая азетидин-2-ил и азетидин-3-ил, пирролидинил, включая пирролидинил-2-ил и пирролидинил-3-ил, пиперидинил, включая пиперидинил-2-ил, пиперидинил-3-ил и пиперидинил-4-ил, азепанил, включая азепан-2-ил, азепан-3-ил и азепан-4-ил, оксазолидинил, включая оксазолидин-2-ил, оксазолидин-4-ил и оксазолидин-5-ил, тиазолидинил, включая тиазолидин-2-ил, тиазолидин-4-ил и тиазолидин-5-ил, морфолинил, включая морфолин-2-ил и морфолин-3-ил, тиоморфолинил, включая тиоморфолин-2-ил и тиоморфолин-3-ил, которые являются необязательно замещенными, как указано в отношении Het.
Объектом изобретения являются все соединения Формулы I, где любой один или несколько структурных элементов, таких как группы, заместители и числовые значения, определены в любом из конкретных вариантов осуществления или определениях элементов или имеют одно или несколько конкретных значений, которые упомянуты здесь в качестве примеров элементов, где все комбинации одного или нескольких вариантов осуществления и/или конкретных определений и/или конкретных значений элементов являются объектом настоящего изобретения. Также в отношении всех таких соединений Формулы I, все их стереоизомерные формы и смеси стереоизомеров в любом соотношении и их физиологически приемлемые соли, и физиологически приемлемые сольваты любого из них являются объектом настоящего изобретения.
Примерами соединений по изобретению, которые, что касается любых структурных элементов, определены в конкретных вариантах осуществления изобретения или определениях таких элементов и которые являются объектом изобретения, являются соединения Формулы I, где
R3 выбирают из (C1-C6)-алкила, (C3-C7)-циклоалкил-CuH2u- и Het-CvH2v-, где u и v выбирают из 1 и 2, или R3 является остатком насыщенного или ненасыщенного 3-членного-10-членного моноциклического или бициклического кольца, которое содержит 0, 1 или 2 одинаковых или различных кольцевых гетероатома, выбранных из N, O и S, где один или два кольцевых атома азота могут нести атом водорода или (C1-C4)-алкильный заместитель и один из кольцевых атомов серы может нести одну или две оксо-группы, и где остаток кольца необязательно замещен по одному или нескольким атомам углерода в кольце одинаковыми или различными заместителями R31;
Het представляет собой остаток насыщенного 4-членного-6-членного моноциклического гетероцикла, который содержит 1 кольцевой гетероатом, выбранный из N, O и S, и который присоединен через кольцевой атом углерода, где остаток гетероцикла необязательно замещен одним или несколькими одинаковыми или различными заместителями, выбранными из фтора и (С1-C4)-алкила;
и все другие группы и числовые значения определены в общем определении соединения Формулы I или любых конкретных вариантах осуществления изобретения, или при определении структурных элементов.
Другим таким примером являются соединения Формулы I в любых их стереоизомерных формах или в виде смеси стереоизомерных форм в любом соотношении, и их физиологически приемлемые соли и физиологически приемлемые сольваты любого из них,
где
A выбирают из O и S;
X выбирают из (C1-C6)-алкандиила, (C2-C6)-алкандиила и (C1-C6)-алкандиилокси;
R2 выбирают из фенилена и пиридиндиила, где фенилен и пиридиндиил необязательно замещены по одному или нескольким кольцевым атомам азота одинаковыми или различными заместителями R22;
R3 выбирают из (C1-C6)-алкила, (C3-C7)-циклоалкил-CuH2u- и Het-CvH2v-, где u и v выбирают из 1 и 2, или R3 является остатком насыщенного или ненасыщенного 3-членного-10-членного моноциклического или бициклического кольца, которое содержит 0, 1 или 2 одинаковых или различных кольцевых гетероатома, выбранных из N, O и S, где один или два кольцевых атома азота могут нести атом водорода или (C1-C4)-алкильный заместитель и один из кольцевых атомов серы может нести одну или две оксо-группы, и где остаток кольца необязательно замещен по одному или нескольким атомам углерода в кольце одинаковыми или различными заместителями R31;
Het представляет собой остаток насыщенного 4-членного-6-членного моноциклического гетероцикла, который содержит 1 кольцевой гетероатом, выбранный из N, O и S, и который присоединен через кольцевой атом углерода, где остаток гетероцикла необязательно замещен одним или несколькими одинаковыми или различными заместителями, выбранными из фтора и (С1-C4)-алкила;
и все другие группы и числовые значения определены в общем определении соединения Формулы I или любых конкретных вариантах осуществления изобретения, или при определении структурных элементов.
Другим таким примером являются соединения Формулы I в любых их стереоизомерных формах или в виде смеси стереоизомерных форм в любом соотношении, и их физиологически приемлемые соли и физиологически приемлемые сольваты любого из них,
где
A представляет собой О;
X выбирают из (C1-C6)-алкандиила и (C1-C6)-алкандиилокси;
R1 выбирают из водорода и (С1-C4)-алкила;
R2 представляет собой фенилен, который необязательно замещен по одному или нескольким кольцевым атомам углерода одинаковыми или различными заместителями R22;
R3 выбирают из (C1-C6)-алкила, (C3-C7)-циклоалкил-CuH2u- и Het-CvH2v-, где u и v выбирают из 1 и 2, или R3 является остатком насыщенного или ненасыщенного 3-членного-7-членного моноциклического или бициклического кольца, которое содержит 0, 1 или 2 одинаковых или различных кольцевых гетероатома, выбранных из N, O и S, где один или два кольцевых атома азота могут нести атом водорода или (C1-C4)-алкильный заместитель и один из кольцевых атомов серы может нести одну или две оксо-группы, и где остаток кольца необязательно замещен по одному или нескольким атомам углерода в кольце одинаковыми или различными заместителями R31;
R22 выбирают из галогена, гидрокси, (С1-C4)-алкил- и (С1-C4)-алкилокси;
R31 выбирают из галогена, (С1-C4)-алкила, (C3-C7)-циклоалкила, гидрокси и (С1-C4)-алкилокси;
Het представляет собой остаток насыщенного 4-членного-6-членного моноциклического гетероцикла, который содержит 1 кольцевой гетероатом, выбранный из O и S, и который присоединен через кольцевой атом углерода, где остаток гетероцикла необязательно замещен одним или несколькими одинаковыми или различными заместителями, выбранными из фтора и (С1-C4)-алкила; где все группы алкила и алкандиила, CuH2u и CvH2v независимо друг от друга и независимо от любых других заместителей необязательно замещены одним или несколькими фторами.
Другим таким примером являются соединения Формулы I в любых их стереоизомерных формах или в виде смеси стереоизомерных форм в любом соотношении, и их физиологически приемлемые соли и физиологически приемлемые сольваты любого из них, где
A представляет собой О;
X выбирают из (C1-C6)-алкандиила и (C1-C6)-алкандиилокси;
R1 выбирают из водорода и (С1-C4)-алкила;
R2 представляет собой фенилен, который необязательно замещен по одному или нескольким кольцевым атомам углерода одинаковыми или различными заместителями R22;
R3 является остатком насыщенного или ненасыщенного 3-членного-7-членного моноциклического кольца, которое содержит 0 или 1 кольцевой гетероатом, выбранный из N, O и S, где кольцевой атом азота может нести водород или (C1-C4)-алкильный заместитель и кольцевой атом серы может нести одну или две оксо-группы, и где остаток кольца необязательно замещен по одному или нескольким кольцевым атомам углерода одинаковыми или различными заместителями R31;
R22 выбирают из галогена, гидрокси, (С1-C4)-алкил- и (С1-C4)-алкилокси;
R31 выбирают из галогена, (С1-C4)-алкила, (C3-C7)-циклоалкила, гидрокси и (С1-C4)-алкилокси;
где все циклоалкильные группы независимо друг от друга и независимо от любых других заместителей необязательно замещены одним или несколькими одинаковыми или различными заместителями, выбранными из фтора и (С1-C4)-алкила;
где все алкильные и алкандиильные группы независимо друг от друга и независимо от любых других заместителей необязательно замещены одним или несколькими фторами.
Аналогичным образом, в отношении все описанных здесь конкретных соединений, таких как иллюстративные соединения, которые демонстрируют варианты осуществления изобретения, где различные группы и числовые значения в общем определении соединений Формулы I имеют конкретные значения в соответствующем конкретном соединении, применимо, что они являются объектом настоящего изобретения в любой их стереоизомерной форме и/или в виде смеси стереоизомерных форм в любом соотношении, и в виде их физиологически приемлемых солей, а также в виде физиологически приемлемых сольватов любого из них. Независимо от того, описано ли здесь конкретное соединение как свободное соединение и/или в виде конкретной соли, объектом настоящего изобретения является как форма свободного соединения, так и форма всех его физиологически приемлемых солей, а если описана конкретная соль - кроме того, форма данной конкретной соли, и форма физиологически приемлемых сольватов любого из них. Таким образом, объектом настоящего изобретения также является соединение Формулы I, которое выбирают из одного или нескольких описанных здесь конкретных соединений Формулы I, включая иллюстративные соединения, перечисленные далее, и их физиологически приемлемые соли и физиологически приемлемые сольваты любого из них, где соединение Формулы I является объектом изобретения в любой его стереоизомерной форме или в виде смеси стереоизомерных форм в любом соотношении, в соответствующих случаях. В качестве упомянутого примера выступает соединение Формулы I или его физиологически приемлемый сольват, которое выбирают из следующих:
[2,6-диметил-4-(5-феноксиоксазоло[5,4-d]пиримидин-2-ил)фенокси]уксусная кислота,
(E)-3-{4-[5-(2-фторфенокси)оксазоло[5,4-d]пиримидин-2-ил]фенил}акриловая кислота,
{4-[5-(2,4-дифторфенокси)оксазоло[5,4-d]пиримидин-2-ил]-2,6-диметилфенокси}уксусная кислота,
{4-[5-(2,5-дифторфенокси)оксазоло[5,4-d]пиримидин-2-ил]-2,6-диметилфенокси}уксусная кислота,
{4-[5-(2-фтор-4-метилфенокси)оксазоло[5,4-d]пиримидин-2-ил]-2,6-диметилфенокси}уксусная кислота,
{4-[5-(2-фторфенокси)оксазоло[5,4-d]пиримидин-2-ил]-2,6-диметилфенокси}уксусная кислота,
2-{4-[5-(2-фторфенокси)оксазоло[5,4-d]пиримидин-2-ил]-2,6-диметилфенокси}пропионовая кислота,
{4-[5-(3-хлорфенокси)оксазоло[5,4-d]пиримидин-2-ил]-2,6-диметилфенокси}уксусная кислота,
{4-[5-(3-фтор-4-метилфенокси)оксазоло[5,4-d]пиримидин-2-ил]-2,6-диметилфенокси}уксусная кислота,
{4-[5-(5-фтор-2-метилфенокси)оксазоло[5,4-d]пиримидин-2-ил]-2,6-диметилфенокси}уксусная кислота,
{4-[5-(4-хлорфенокси)оксазоло[5,4-d]пиримидин-2-ил]-2,6-диметилфенокси}уксусная кислота,
[4-(5-циклопентилоксиоксазоло[5,4-d]пиримидин-2-ил)-2,6-диметилфенокси]уксусная кислота,
{4-[5-(2-фторфенокси)оксазоло[5,4-d]пиримидин-2-ил]-2-метилфенокси}уксусная кислота,
{4-[5-(2-фторфенокси)оксазоло[5,4-d]пиримидин-2-ил]фенокси}уксусная кислота,
2-{4-[5-(2-фторфенокси)оксазоло[5,4-d]пиримидин-2-ил]фенокси}-2-метилпропионовая кислота,
2-{4-[5-(2-фторфенокси)оксазоло[5,4-d]пиримидин-2-ил]фенокси}пропионовая кислота,
{4-[5-(2-фторфенокси)оксазоло[5,4-d]пиримидин-2-ил]-2-трифторметилфенокси}уксусная кислота,
3-{4-[5-(2-фторфенокси)оксазоло[5,4-d]пиримидин-2-ил]фенил}пропионовая кислота,
3-{4-[5-(2-фторфенокси)оксазоло[5,4-d]пиримидин-2-ил]фенил}-2-метилпропионовая кислота,
4-{4-[5-(2-фторфенокси)оксазоло[5,4-d]пиримидин-2-ил]фенокси}масляная кислота,
4-{4-[5-(2-фторфенокси)оксазоло[5,4-d]пиримидин-2-ил]-2,6-диметилфенокси}масляная кислота,
{4-[5-(2-циклопропилэтокси)оксазоло[5,4-d]пиримидин-2-ил]-2,6-диметилфенокси}уксусная кислота,
{2,6-диметил-4-[5-(3-метилбутокси)оксазоло[5,4-d]пиримидин-2-ил]фенокси}уксусная кислота
2-[2,6-диметил-4-(5-{2,4-дифторфенокси}оксазоло[5,4-d]пиримидин-2-ил)фенокси]пропионовая кислота,
2-[2,6-диметил-4-(5-{2,3-дифторфенокси}оксазоло[5,4-d]пиримидин-2-ил)фенокси]пропионовая кислота,
2-[2,6-диметил-4-(5-{2,5-дифторфенокси}оксазоло[5,4-d]пиримидин-2-ил)фенокси]пропионовая кислота,
2-[2,6-диметил-4-(5-{2-фтор-5-метилфенокси}оксазоло[5,4-d]пиримидин-2-ил)фенокси]пропионовая кислота,
2-[2,6-диметил-4-(5-{2-фтор-4-метилфенокси}оксазоло[5,4-d]пиримидин-2-ил)фенокси]пропионовая кислота,
2-[2,6-диметил-4-(5-{3-фторфенокси}оксазоло[5,4-d]пиримидин-2-ил)фенокси]пропионовая кислота,
2-[2,6-диметил-4-(5-{3,5-дифторфенокси}оксазоло[5,4-d]пиримидин-2-ил)фенокси]пропионовая кислота,
2-[2,6-диметил-4-(5-{3,4-дифторфенокси}оксазоло[5,4-d]пиримидин-2-ил)фенокси]пропионовая кислота,
2-[2,6-диметил-4-(5-{2-хлор-5-фторфенокси}оксазоло[5,4-d]пиримидин-2-ил)фенокси]пропионовая кислота,
2-[2,6-диметил-4-(5-{4-хлор-3-фторфенокси}оксазоло[5,4-d]пиримидин-2-ил)фенокси]пропионовая кислота,
2-[2,6-диметил-4-(5-{3-фтор-4-метилфенокси}оксазоло[5,4-d]пиримидин-2-ил)фенокси]пропионовая кислота,
2-[2,6-диметил-4-(5-{3-фтор-6-метилфенокси}оксазоло[5,4-d]пиримидин-2-ил)фенокси]пропионовая кислота,
2-[2,6-диметил-4-(5-{3-хлорфенокси}оксазоло[5,4-d]пиримидин-2-ил)фенокси]пропионовая кислота,
2-[2,6-диметил-4-(5-{3-хлор-4-фторфенокси}оксазоло[5,4-d]пиримидин-2-ил)фенокси]пропионовая кислота,
2-[2,6-диметил-4-(5-{4-хлорфенокси}оксазоло[5,4-d]пиримидин-2-ил)фенокси]пропионовая кислота,
2-[2,6-диметил-4-(5-{4-метилфенокси}оксазоло[5,4-d]пиримидин-2-ил)фенокси]пропионовая кислота,
2-[2,6-диметил-4-(5-{3-метилфенокси}оксазоло[5,4-d]пиримидин-2-ил)фенокси]пропионовая кислота,
2-[2,6-диметил-4-(5-{2-метилфенокси}оксазоло[5,4-d]пиримидин-2-ил)фенокси]пропионовая кислота,
2-{2,6-диметил-4-[5-(пиридин-3-илокси)оксазоло[5,4-d]пиримидин-2-ил]фенокси}пропионовая кислота,
2-{2,6-диметил-4-[5-(6-метилпиридин-3-илокси)оксазоло[5,4-d]пиримидин-2-ил]фенокси}пропионовая кислота,
{4-[5-(3-фторфенокси)оксазоло[5,4-d]пиримидин-2-ил]-2,6-диметилфенокси}уксусная кислота,
{2,6-диметил-4-[5-(3-трифторметилфенокси)оксазоло[5,4-d]пиримидин-2-ил]фенокси}уксусная кислота,
[2,6-диметил-4-(5-{3-метилфенокси}оксазоло[5,4-d]пиримидин-2-ил)фенокси]уксусная кислота,
{4-[5-(3-Cycthylфенокси)оксазоло[5,4-d]пиримидин-2-ил]-2,6-диметилфенокси}уксусная кислота,
{4-[5-(3-хлор-4-фторфенокси)оксазоло[5,4-d]пиримидин-2-ил]-2,6-диметилфенокси}уксусная кислота,
{4-[5-(3-хлор-4-метилфенокси)оксазоло[5,4-d]пиримидин-2-ил]-2,6-диметилфенокси}уксусная кислота,
{4-[5-(5-хлор-2-метилфенокси)оксазоло[5,4-d]пиримидин-2-ил]-2,6-диметилфенокси}уксусная кислота,
{4-[5-(3-хлор-2-метилфенокси)оксазоло[5,4-d]пиримидин-2-ил]-2,6-диметилфенокси}уксусная кислота,
{4-[5-(3-хлор-2-фторфенокси)оксазоло[5,4-d]пиримидин-2-ил]-2,6-диметилфенокси}уксусная кислота,
{4-[5-(5-хлор-2-фторфенокси)оксазоло[5,4-d]пиримидин-2-ил]-2,6-диметилфенокси}уксусная кислота,
{4-[5-(3,4-дифторфенокси)оксазоло[5,4-d]пиримидин-2-ил]-2,6-диметилфенокси}уксусная кислота,
{4-[5-(4-фтор-3-метилфенокси)оксазоло[5,4-d]пиримидин-2-ил]-2,6-диметилфенокси}уксусная кислота,
{4-[5-(2,3-дифторфенокси)оксазоло[5,4-d]пиримидин-2-ил]-2,6-диметилфенокси}уксусная кислота,
{4-[5-(3,5-дифторфенокси)оксазоло[5,4-d]пиримидин-2-ил]-2,6-диметилфенокси}уксусная кислота,
{4-[5-(3-хлор-5-фторфенокси)оксазоло[5,4-d]пиримидин-2-ил]-2,6-диметилфенокси}уксусная кислота,
{4-[5-(3-фтор-5-трифторметилфенокси)оксазоло[5,4-d]пиримидин-2-ил]-2,6-диметилфенокси}уксусная кислота,
{4-[5-(3-фтор-5-метилфенокси)оксазоло[5,4-d]пиримидин-2-ил]-2,6-диметилфенокси}уксусная кислота,
{4-[5-(4-фторфенокси)оксазоло[5,4-d]пиримидин-2-ил]-2,6-диметилфенокси}уксусная кислота,
{4-[5-(2-фтор-5-метилфенокси)оксазоло[5,4-d]пиримидин-2-ил]-2,6-диметилфенокси}уксусная кислота,
{4-[5-(2-хлор-5-фторфенокси)оксазоло[5,4-d]пиримидин-2-ил]-2,6-диметилфенокси}уксусная кислота,
{4-[5-(4-хлор-3-фторфенокси)оксазоло[5,4-d]пиримидин-2-ил]-2,6-диметилфенокси}уксусная кислота,
[2,6-диметил-4-(5-{4-метилфенокси}оксазоло[5,4-d]пиримидин-2-ил)фенокси]уксусная кислота,
[2,6-диметил-4-(5-{2-метилфенокси}оксазоло[5,4-d]пиримидин-2-ил)фенокси]уксусная кислота,
{4-[5-(2-хлорфенокси)оксазоло[5,4-d]пиримидин-2-ил]-2,6-диметилфенокси}уксусная кислота,
{4-[5-(2-хлор-3-трифторметилфенокси)оксазоло[5,4-d]пиримидин-2-ил]-2,6-диметилфенокси}уксусная кислота,
{4-[5-(2-хлор-5-трифторметилфенокси)оксазоло[5,4-d]пиримидин-2-ил]-2,6-диметилфенокси}уксусная кислота,
{4-[5-(4-хлор-3-трифторметилфенокси)оксазоло[5,4-d]пиримидин-2-ил]-2,6-диметилфенокси}уксусная кислота,
{4-[5-(4-фтор-3-трифторметилфенокси)оксазоло[5,4-d]пиримидин-2-ил]-2,6-диметилфенокси}уксусная кислота,
{4-[5-(2-фтор-5-трифторметилфенокси)оксазоло[5,4-d]пиримидин-2-ил]-2,6-диметилфенокси}уксусная кислота,
{4-[5-(2-фтор-3-трифторметилфенокси)оксазоло[5,4-d]пиримидин-2-ил]-2,6-диметилфенокси}уксусная кислота,
{2,6-диметил-4-[5-(2-трифторметилфенокси)оксазоло[5,4-d]пиримидин-2-ил]фенокси}уксусная кислота,
{2,6-диметил-4-[5-(4-трифторметилфенокси)оксазоло[5,4-d]пиримидин-2-ил]фенокси}уксусная кислота,
{4-[5-(4-хлор-2-фторфенокси)оксазоло[5,4-d]пиримидин-2-ил]-2,6-диметилфенокси}уксусная кислота,
{4-[5-(2-хлор-4-фторфенокси)оксазоло[5,4-d]пиримидин-2-ил]-2,6-диметилфенокси}уксусная кислота,
{4-[5-(3-метоксифенокси)оксазоло[5,4-d]пиримидин-2-ил]-2,6-диметилфенокси}уксусная кислота,
{2,6-диметил-4-[5-(3-трифторметоксифенокси)оксазоло[5,4-d]пиримидин-2-ил]фенокси}уксусная кислота,
{2,6-диметил-4-[5-(3-трифторметилсульфанилфенокси)оксазоло[5,4-d]пиримидин-2-ил]фенокси}уксусная кислота,
{4-[5-(индан-5-илокси)оксазоло[5,4-d]пиримидин-2-ил]-2,6-диметилфенокси}уксусная кислота,
{4-[5-(индан-4-илокси)оксазоло[5,4-d]пиримидин-2-ил]-2,6-диметилфенокси}уксусная кислота,
{2,6-диметил-4-[5-(нафталин-2-илокси)оксазоло[5,4-d]пиримидин-2-ил]фенокси}уксусная кислота,
{2,6-диметил-4-[5-(2-метилбензотиазол-5-илокси)оксазоло[5,4-d]пиримидин-2-ил]фенокси}уксусная кислота,
{4-[5-(бензотиазол-6-илокси)оксазоло[5,4-d]пиримидин-2-ил]-2,6-диметилфенокси}уксусная кислота,
{2,6-диметил-4-[5-(6-метилпиридин-3-илокси)оксазоло[5,4-d]пиримидин-2-ил]фенокси}уксусная кислота,
{2,6-диметил-4-[5-(2-метилпиридин-3-илокси)оксазоло[5,4-d]пиримидин-2-ил]фенокси}уксусная кислота,
{2,6-диметил-4-[5-(5-метилпиридин-3-илокси)оксазоло[5,4-d]пиримидин-2-ил]фенокси}уксусная кислота,
{4-[5-(5-хлорпиридин-3-илокси)оксазоло[5,4-d]пиримидин-2-ил]-2,6-диметилфенокси}уксусная кислота,
{4-[5-(5-фторпиридин-3-илокси)оксазоло[5,4-d]пиримидин-2-ил]-2,6-диметилфенокси}уксусная кислота,
{2,6-диметил-4-[5-([1,2,5]тиадиазол-3-илокси)оксазоло[5,4-d]пиримидин-2-ил]фенокси}уксусная кислота,
{4-[5-(изотиазол-3-илокси)оксазоло[5,4-d]пиримидин-2-ил]-2,6-диметилфенокси}уксусная кислота,
{2,6-диметил-4-[5-(5-трифторметилтиофен-3-илокси)оксазоло[5,4-d]пиримидин-2-ил]фенокси}уксусная кислота,
{2,6-диметил-4-[5-(тиазол-2-илсульфанил)оксазоло[5,4-d]пиримидин-2-ил]фенокси}уксусная кислота,
{2,6-диметил-4-[5-(4-метилтиазол-2-илсульфанил)оксазоло[5,4-d]пиримидин-2-ил]фенокси}уксусная кислота,
{4-[5-(1,1-диоксотетрагидротиофен-3-илсульфанил)оксазоло[5,4-d]пиримидин-2-ил]-2,6-диметилфенокси}уксусная кислота и
{4-[5-(2,5-диметилфуран-3-илсульфанил)оксазоло[5,4-d]пиримидин-2-ил]-2,6-диметилфенокси}уксусная кислота,
где соединение, такое как, например, 2-{4-[5-(2-фторфенокси)оксазоло[5,4-d]-пиримидин-2-ил]-2,6-диметилфенокси}пропионовая кислота или 2-{4-[5-(2-фторфенокси)оксазоло[5,4-d]пиримидин-2-ил]фенокси}пропионовая кислота, которое может присутствовать в S-конфигурации или R-конфигурации, является объектом изобретения, находясь как в S-конфигурации, так и в R-конфигурации, а также в виде смеси энантиомерных форм в любом соотношении.
Другим объектом настоящего изобретения являются способы получения соединений Формулы I и их солей и сольватов, с помощью которых соединения являются доступными и которые изложены далее. В одном способе соединение Формулы II вводят в реакцию с соединением Формулы III с получением соединения Формулы I:
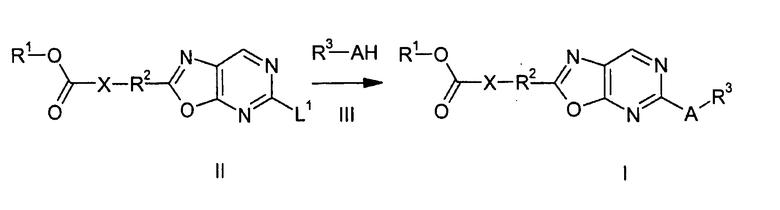 ,
,
где группы A, X, R1, R2 и R3 в соединениях Формул II и III такие, как указано для соединений Формулы I, и могут присутствовать дополнительные функциональные группы в защищенной форме или в форме групп-предшественников, которые потом превращаются в конечную группу. Группа L1 в соединениях Формулы II представляет собой уходящую группу, которая может быть заменена в реакции нуклеофильного ароматического замещения, такую как атом галогена, например, хлор или бром, или группа сульфоксида или сульфоновая группа, например, группа формулы -S(O)-Alk или -S(O)2-Alk, где Alk представляет собой (C1-C4)-алкильную группу, например, метил или этил.
Реакция соединений Формул II и III является реакцией нуклеофильного ароматического замещения при атоме углерода в 5-положении оксазоло[5,4-d]пиримидинового кольца, то есть в пиримидиновом фрагменте, и может проводиться в стандартных для таких реакций условиях, которые хорошо известны специалисту в данной области. Как правило, реакцию проводят в инертном растворителе, например, углеводороде или хлорсодержащем углеводороде, таком как бензол, толуол, ксилол, хлорбензол, дихлорметан, хлороформ или дихлорэтан, простом эфире, таком как тетрагидрофуран (ТГФ), диоксан, дибутиловый эфир, диизопропиловый эфир или 1,2-диметоксиэтан (ДМЭ), кетоне, таком как ацетон или бутан-2-он, сложном эфире, таком как этилацетат или бутилацетат, нитриле, таком как ацетонитрил, амине, таком как Ν,Ν-диметилформамид (ДМФА), N,N-диметилацетамид (ДМА) или N-метилпирролидин-2-он (N-МП), или смеси растворителей, при температуре от приблизительно 20°C до приблизительно 160°C, например, при температуре от приблизительно 40°C до приблизительно 100°C, в зависимости от каждого конкретного случая. Как правило, к повышению нуклеофильности соединения Формулы III приводит добавление основания, например, третичного амина, такого как триэтиламин, этилдиизопропиламин или N-метилморфолин, или неорганического основания, такого как гидрид, гидроксид, карбонат или гидрокарбонат щелочноземельного металла, например, гидрид натрия, гидроксид натрия, гидроксид калия, карбонат натрия, карбонат калия, карбонат цезия или гидрокарбонат натрия, или алкоксид или амид, такой как метоксид натрия, этоксид натрия, метоксид калия, трет-бутоксид калия, амид натрия или диизопропиламид лития. Соединения Формулы III также могут обрабатываться основанием и превращаться в соль отдельно, до реакции с соединением Формулы II.
Исходные соединения Формул II и III могут быть получены способами, описанными в литературе, или аналогично способам, описанным в литературе, а во многих случаях являются коммерчески доступными. Например, соединения Формулы II могут быть получены реакцией 5-амино-пиримидинового производного Формулы IV с производным активированной карбоновой кислоты Формулы V с получением соединения Формулы VI, с циклизацией последнего соединения с образованием оксазоло[5,4-d]пиримидиновой кольцевой системы для получения соединения Формулы VII, и введения фрагмента R1O-C(O)-X- в соединение Формулы VII реакцией с соединением Формулы VIII для получения соединения Формулы IX, которое уже может представлять собой соединение Формулы II в зависимости от значения R' и L1, и необязательно модификации группы R' в соединении Формулы IX для получения соединения II.
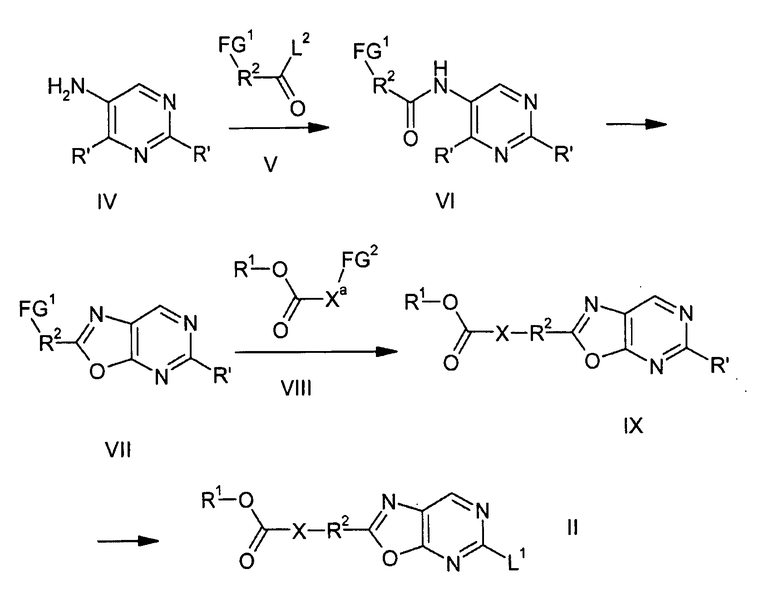
Группы X, R1 и R2 в соединениях Формул V, VI, VIII и IX являются такими, как определено в отношении соединений Формулы I, и дополнительно могут присутствовать функциональные группы в защищенной форме или в форме групп-предшественников, которые затем превращаются в конечную группу. Группа Xa в соединениях Формулы VIII определяется как группа X в соединениях Формулы I или содержит часть группы X в искомом соединении Формулы II, так что после взаимодействия соединений Формул VII и VIII группа Xa и любые части групп FG1 и FG2, оставшиеся в соединении Формулы IX, образуют желаемую группу X. Например, когда группа X представляет собой алкандиилокси-группу, группа Xa в соединении Формулы VIII может быть желаемой алкандиилокси-группой, а группа FG2 может быть атомом водорода, присоединенным к атому кислорода, или группа Xa может быть алкандиильной частью, группа FG2 представляет собой уходящую часть, а группа FG1 в соединении Формулы VII представляет собой гидрокси-группу, атом кислорода которой вместе с алкандиильной частью тогда формирует желаемую алкандиилокси-группу после аклкилирования соединения Формулы VII соединением Формулы VIII.
Группы FG1 и FG2 в соединениях Формул V, VI, VII и VIII являются функциональными группами, которые являются подходящими для типа конденсации, используемого для формирования желаемой группы X из группы Xa и любой части групп FG1 и FG2, оставшейся в соединении Формулы IX. Например, если группа Xa присоединена к группе R2 или к атому группы FG1, такому как атом кислорода в гидрокси-группе, представляющей FG1, как упомянуто выше, посредством реакции нуклеофильного замещения, FG2 может быть уходящей группой, такой как атом галогена, например, хлор, бром или йод, или сульфонилокси-группа, например, метансульфонилокси, трифторметансульфонилокси или толуолсульфонилокси. Если группа Xa присоединена к группе R2 посредством катализируемой переходными металлами реакции, FG2 может быть уходящей группой, такой как борная кислота, сложный эфир борной кислоты, группа диалкил-борана или станнана, и в этом случае FG1 может быть галогеном. FG2 может быть также атомом водорода или атомом углерода, несущим часть двойной связи в алкендиильной группе, представляющей Xa, если для присоединения Xa к R2 используется реакция Хека, и в этом случае FG1 может быть галогеном. Если для присоединения Xa к R2 используется реакция Виттига или реакция Виттига-Хорнера, FG2 может быть группой фосфония, такой как трифенилфосфоний, или фосфонил-группой, такой как диэтилфосфонил, и соединение Формулы XIV может быть фосфониевой солью или сложным эфиром фосфоновой кислоты, и в этом случае FG1 может быть альдегидной группой -C(O)-H или кетоновой группой -C(O)-алкилом, и наоборот. Как правило, группа FG1 находится у атома углерода в группе фенилена или гетероциклической группе, представляющей R2, которая в соединениях Формул IX, II и I несет группу X. Группа FG1 в соединениях Формул V, VI и VII может быть в защищенном виде или в виде группы-предшественника, которую затем превращают в группу, которая в соединении Формулы VII взаимодействует с соединением Формулы VIII. Например, гидрокси-группа, представляющая FG1 в соединении Формулы VII, может присутствовать в соединениях Формул V и VI в защищенной форме, например, в виде превращенной в простой эфир гидрокси-группы, такой как бензиловый эфир или алкиловый эфир, например метиловый эфир. Такие простые эфиры могут быть гидролизованы методами, хорошо известными специалисту в данной области техники. Обзор методов удаления защитных групп может быть найден в литературных источниках, например, у P.J. Kocienski «Protecting Groups» (Thieme Verlag, 1994) или T.W. Greene и P.G.M. Wuts «Protective Groups in Organic Synthesis» (John Wiley & Sons, 1999).
Группа L2 в соединениях Формулы V является уходящей в результате нуклеофильного замещения группой и может, в частности, являться атомом галогена, таким как хлор или бром, а соединение Формулы V, таким образом, может представлять собой галогенангидрид карбоновой кислоты. L2 может также быть группой формулы FG1-R2-C(O)-O, и соединение Формулы V может, таким образом, представлять собой, например, ангидрид карбоновой кислоты. Группы R' в соединениях Формул IV, VI и IX могут представлять собой гидрокси-группу или атом галогена, такой как хлор и бром. Соединения, участвующие в синтезе соединений Формулы I, такие как соединение Формулы IV, могут также находиться в любой таутомерной форме, например, в кето-форме в случае, когда группы R' в соединении Формулы IV являются гидрокси-группами. Соединения, участвующие в синтезе соединений Формулы I, включая исходные соединения, промежуточные соединения и продукты, могут применяться или получаться в виде соли.
Реакция соединений Формул IV и V с активированным производным карбоновой кислоты, таким как галогенангидрид или ангидрид, может проводиться в стандартных для ацилирования амина условиях. Как правило, реакцию проводят в инертном растворителе, например, углеводороде или галогенсодержащем углеводороде, таком как бензол, толуол, ксилол, хлорбензол, дихлорметан, хлороформ или дихлорэтан, простом эфире, таком как ТГФ, диоксан, дибутиловый эфир, диизопропиловый эфир или ДМЭ, кетоне, таком как ацетон или бутан-2-он, сложном эфире, таком как этилацетат или бутилацетат, или воде, или смеси растворителей, при температуре от приблизительно -10°C до приблизительно 40°C, например, при температуре от приблизительно 0°C до приблизительно 30°C. Как правило, реакцию проводят в присутствии основания, например третичного амина, такого как триэтиламин, этилдиизопропиламин или N-метилморфолин, или неорганического основания, такого как гидроксид, карбонат или гидрокарбонат щелочного металла, такой как гидроксид натрия, гидроксид калия, карбонат натрия, карбонат калия или гидрокарбонат натрия. Реакцию соединений Формул VI и VII, как правило, проводят в инертном растворителе, например спирте, таком как метанол, этанол или изопропанол, или простом эфире, таком как ТГФ, диоксан или ДМЭ, или смеси растворителей, при температуре от приблизительно 20°C до приблизительно 80°C, например, температуре от приблизительно 40°C до приблизительно 80°C, в присутствии основания, например алкоксида, такого как метоксид натрия, этоксид натрия, метоксид калия или трет-бутоксид калия.
В случае если группа R' в соединении Формулы VI является гидрокси-группой, циклизация соединения Формулы VI в соединение Формулы VII может быть благополучно проведена в присутствии галогенирующего агента, такого как галогенид фосфора, например пентахлорид фосфора или оксихлорид фосфора или их смеси, в инертном растворителе, например, углеводороде или хлорсодержащем углеводороде, таком как бензол, толуол, ксилол, хлорбензол, дихлорметан, хлороформ или дихлорэтан, при температуре от приблизительно 20°C до приблизительно 100°C, например, температуре от приблизительно 50°C до приблизительно 80°C. В случае если группа R' в соединении Формулы VI является галогеном, таким как хлор, циклизация соединения Формулы VI в соединение Формулы VII может проводиться под действием температуры, например, путем нагревания соединения Формулы VI в инертном растворителе, таком как углеводород или хлорсодержащий углеводород, например, толуол, ксилол или хлорбензол, или амид, например, ДМФА, ДМА или N-МП, или нитрил, например ацетонитрил, до температуры от приблизительно 100°C до приблизительно 200°C, например, до температуры от приблизительно 120°C до приблизительно 180°C, необязательно под давлением и необязательно в присутствии основания, такого как третичный амин, например, триэтиламин, этилдиизопропиламин или N-метилморфолин, или неорганического основания, например, гидроксида, карбоната или гидрокарбоната щелочного металла, такого как гидроксид натрия, гидроксид калия, карбонат натрия, карбонат калия или гидрокарбонат натрия. Циклизация под действием температуры может быть благополучно проведена в микроволновом реакторе.
Конденсация соединений Формулы VIII с соединениями Формулы VII может осуществляться посредством реакций различного типа, как уже указывалось ранее, например, путем реакции алкилирования. Например, группа R2, несущая гидроксильную группу, представляющую FG1, может быть алкилирована с помощью соединения VIII, в котором FG2 является уходящей группой, подходящей для реакций нуклеофильного замещения, такой как атом галогена, например, хлор, бром или йод, или сульфонилокси-группа, например, метансульфонилокси или толуолсульфонилокси. Реакция нуклеофильного замещения при атоме углерода соединения Формулы VIII, несущем группу FG2, может проводиться в стандартных для данных реакций условиях, которые хорошо известны специалисту в данной области. Как правило, реакцию осуществляют в инертном растворителе, например, углеводороде или хлорсодержащем углеводороде, таком как бензол, толуол, ксилол, хлорбензол, дихлорметан, хлороформ или дихлорэтан, простом эфире, таком как ТГФ, диоксан, дибутиловый эфир, диизопропиловый эфир или ДМЭ, спирте, таком как метанол, этанол или изопропанол, кетоне, таком как ацетон или бутан-2-он, сложном эфире, таком как этилацетат или бутилацетат, нитриле, таком как ацетонитрил, амиде, таком как Ν,Ν-диметилформамид или N-метилпирролидин-2-он, или смеси растворителей при температуре от приблизительно 20°C до приблизительно 100°C, например, при температуре от приблизительно 40°C до приблизительно 80°C, в зависимости от каждого конкретного случая. Как правило, подходящим для повышения нуклеофильности соединения Формулы XIII и/или связывания выделяющейся в ходе реакции кислоты является добавление основания, например, третичного амина, такого как триэтиламин, этилдиизопропиламин или N-метилморфолин, или неорганического основания, такого как гидрид, гидроксид, карбонат или гидрокарбонат щелочного металла, такой как гидрид натрия, гидроксид натрия, гидроксид калия, карбонат натрия, карбонат калия, карбонат цезия или гидрокарбонат натрия, или алкоксида или амида, такого как метоксид натрия, этоксид натрия, метоксид калия, трет-бутоксид калия, амид натрия или диизопропиламид лития. Соединение Формулы VII, где FG1 является гидрокси-группой, может быть отдельно предварительно обработано основанием и превращено в соль до введения в реакцию с соединением Формулы VIII. Помимо реакции с соединением Формулы VIII, где FG2 является, как указано, уходящей группой, соединение Формулы VII, где FG1 является гидрокси-группой, может также быть превращено в соединение Формулы IX посредством реакции с соответствующем спиртом, то есть с соединением Формулы VIII, где FG2 является гидрокси-группой, в условиях реакции Мицунобу в присутствии азодикарбоксилатов, таких как диэтилазодикарбоксилат или диизопропилазодикарбоксилат, и фосфинов, таких как трифенилфосфин или трибутилфосфин, в инертном апротонном растворителе, например простом эфире, таком как ТГФ или диоксан (см. O. Mitsunobu, Synthesis (1981), 1-28). Конденсация соединений Формулы VIII с соединениями Формулы VII посредством катализируемой переходными металлами реакции может осуществляться в условиях палладий-катализируемых реакций кросс-сочетания, таких как реакция сочетания Хека, Стилле или Сузуки (см. A. de Meijere and F. Diederich (Eds.) «Metal-Catalyzed Cross-Coupling Reactions» (Wiley-VCH, 2004)).
Соединение Формулы IX уже может быть соединением Формулы II и использоваться в реакции с соединением Формулы III, если оно получено из соединения Формулы VI, где R' является галогеном, таким как хлор, и в продукте циклизации атом галогена не заменен в процессе синтеза, например, на гидрокси-группу в процессе выделения продукта, или если оно получено из соединения Формулы VI, где R' является гидрокси-группой, и параллельно с циклизацией вторая гидрокси-группа в соединении Формулы VI участвует в галогенировании, например, заменяется на атом хлора, что может происходить в течение циклизации посредством галогенида фосфора. В случае если соединение Формулы VII, где R' является гидрокси-группой, получено как продукт циклизации, гидрокси-группа в соединении Формулы IX может быть превращена в уходящую группу в стандартных условиях, например, в атом галогена, такой как атом хлора, путем обработки галогенирующим агентом, таким как галогенид фосфора, или в сульфонилокси-группу, как указано выше, путем обработки сульфонилхлоридом или ангидридом сульфоновой кислоты. В зависимости от каждого конкретного случая, как, например, реакционноспособности конкретного соединения Формулы III, которое должно вводиться в реакцию с соединением Формулы II, может быть выгодно модифицировать группу R' в соединении Формулы IX, даже если она уже является уходящей группой. Например, соединение Формулы IX, где R' является галогеном, таким как хлор, может быть превращено в соединение Формулы II, где L1 представляет собой группу -S(O)2-Alk и которое затем вводят в реакцию с соединением Формулы III, путем обработки алкансульфиновой кислотой формулы Alk-S(O)-OH, где Alk представляет собой (С1-C4)-алкил. Такое превращение обычно осуществляют в присутствии основания, такого как гидрид, гидроксид, карбонат или гидрокарбонат щелочного металла, такие как гидрид натрия, гидроксид натрия, гидроксид калия, карбонат натрия, карбонат калия, карбонат цезия или гидрокарбонат натрия, в инертном растворителе, таком как углеводород или хлорсодержащий углеводород, такой как бензол, толуол, ксилол, хлорбензол, дихлорметан, хлороформ или дихлорэтан, простой эфир, такой как ТГФ, диоксан, дибутиловый эфир, диизопропиловый эфир или ДМЭ, амид, например, ДМФА или N-МП, или смеси растворителей при температуре от приблизительно 20°C до приблизительно 150°C, например, при температуре от приблизительно 50°C до приблизительно 120°C. Алкансульфиновая кислота может также быть обработана основанием и превращена в соль перед реакцией с соединением Формулы IX.
Последовательность стадий получения соединений Формулы I также может изменяться, и, например, группа -A-R3 может быть введена на более ранней стадии путем взаимодействия соединения Формулы VII, где R' является уходящей группой, или путем взаимодействия соединения Формулы VII, которое содержит группу L1, такую как определено выше, которое было получено из соединения Формулы VII путем конверсии группы R' в группу L1, с соединением Формулы III, и полученный продукт взаимодействует с соединением Формулы VIII с получением соединения Формулы I. Представленные выше пояснения для реакции соединений Формул II и III и реакции соединений Формул VII и VIII соответствующим образом применимы для соответствующих реакций стадий в указанном синтезе соединений Формулы I.
Дополнительные соединения Формулы I могут быть получены из подходящих соединений, полученных в соответствии с описанными выше способами, путем функционализации или модификации содержащихся функциональных групп стандартными методами, например, путем получения сложных эфиров, создания амидной связи, гидролиза, получения простых эфиров, алкилирования, ацилирования, сульфонилирования, восстановления, окисления, превращения в соли и другим образом. Например, гидрокси-группа, которая может быть получена в свободном виде из группы простого эфира путем расщепления, например, с помощью трибромида бора, или из защищенной гидрокси-группы путем удаления защиты, может быть этерифицирована с получением эфира карбоновой кислоты или эфира сульфокислоты или превращена в простой эфир. Получение простых эфиров по гидрокси-группам может подходящим образом осуществляться путем алкилирования с помощью соответствующего соединения галогена, например, бромида или йодида, в присутствии основания, например карбоната щелочного металла, такого как карбонат калия или карбонат цезия, в инертном растворителе, например, амиде, таком как ДМФА или N-МП, или кетоне, таком как ацетон или бутан-2-он, или с помощью соответствующего спирта в условиях реакции Мицунобу, о которой шла речь выше. Гидрокси-группа может быть заменена на галоген путем обработки соответствующим галогенирующим агентом. Атом галогена может быть заменен различными группами в реакции замещения, которая может быть реакцией, катализируемой переходными металлами. Нитрогруппа может быть восстановлена до амино-группы, например, путем каталитического гидрирования. Амино-группа может быть модифицирована в стандартных для алкилирования условиях, например, в реакции с галогенсодержащим соединением или в реакции восстановительного аминирования карбонильного соединения, или для ацилирования или сульфонилирования условиях, например, в реакции с реакционноспособным производным карбоновой кислоты, таким как хлорангидрид или ангидрид кислоты или сульфохлорид, или с активированной карбоновой кислотой, которая может быть получена из карбоновой кислоты путем обработки конденсирующим агентом, таким как, например, Ν,Ν'-карбонилдиимидазол (CDI), карбодиимид, например, 1,3-дициклогексилкарбодиимид (DCC) или 1-(3-диметиламинопропил)-3-этилкарбодиимида гидрохлорид (EDC), O-(7-азабензотриазол-1-ил)-N,N,N',N'-тетраметилурония гексафторфосфат (HATU), O-(циано(этоксикарбонил)метиленамино)-N,N,N',N'-тетраметилурония тетрафторборат (TOTU) или [(бензотриазол-1-илокси)диметиламинометилен]диметиламмония тетрафторборат (TBTU). Сложноэфирная группа может быть подвергнута гидролизу в кислых или основных условиях с получением карбоксильной группы. Карбоксильная группа может быть активирована или превращена в реакционноспособное производное, как упомянуто выше, и введена в реакцию со спиртом или амином или аммиаком с получением сложного эфира или амида. Первичный амид может быть дегидратирован с получением нитрила. Атом серы, например, в алкил-S-группе или в гетероциклическом кольце, может быть окислен с помощью пероксида, такого как пероксид водорода, или надкислоты с получением сульфоксидной группы S(O) или сульфоновой группы S(O)2. Карбоксильная группа, сложноэфирная группа или кето-группа может быть восстановлена до спирта, например, посредством комплексного гидрида, такого как алюмогидридрид лития, боргидрид лития или боргидрид натрия. Соединения Формулы I или промежуточные соединения, такие как соединение Формулы II, которые содержат двойную связь или тройную связь в группе X, которые могут быть легко получены по реакции сочетания, катализируемой переходными металлами, из соединения Формулы XIV, содержащего двойную связь или тройную связь в группе Xa, и соединения Формулы XIII, как указано выше, могут быть превращены в соединение, в котором X является насыщенной группой, путем гидрирования в присутствии катализатора гидрирования, такого как палладиевый катализатор.
Все реакции, используемые в описанном выше синтезе соединений Формулы I, хорошо известны специалистам в данной области и могут осуществляться в стандартных условиях в соответствии с или аналогично методикам, описанным в литературе, например, у Houben-Weyl в «Methoden der Organischen Chemie» (Methods of Organic Chemistry), Thieme-Verlag, Stuttgart или в «Organic Reactions», John Wiley & Sons, New York. Если необходимо, полученные соединения Формулы I, а также любые промежуточные соединения, могут быть очищены обычными способами очистки, например, путем перекристаллизации или хроматографии. Как уже упоминалось, все исходные соединения и промежуточные вещества, применяемые в описанных выше синтезах, которые содержат кислотные и основные группы, могут также применяться в виде солей, и все промежуточные вещества и конечные целевые соединения могут также быть получены в форме солей. Как также упоминалось выше, в зависимости от каждого конкретного случая, чтобы избежать нежелательного направления реакции или побочных реакций в течение синтеза соединения, обычно может быть необходимо или предпочтительно временно блокировать функциональные группы путем введения защитных групп и удаления их защиты на последующей стадии синтеза или вводить функциональные группы в виде групп-предшественников, которые позже превращаются в желаемые функциональные группы. В качестве примеров защитных групп могут быть упомянуты группы, защищающие амино-группу, которые могут представлять собой ацильные группы или алкилоксикарбонильные группы, например, трет-бутилоксикарбонильная группа (=Boc), которая может быть удалена путем обработки трифторуксусной кислотой (=ТФУ), бензилоксикарбонильная группа, которая может быть удалена путем каталитического гидрирования, или флуорен-9-илметоксикарбонильная группа, которая может быть удалена с помощью пиперидина, и группы для защиты карбоксильных групп, которые могут быть защищены в виде сложноэфирных групп, таких как трет-бутиловые эфиры, которые могут быть удалены путем обработки трифторуксусной кислотой, или бензиловые эфиры, которые удаляются путем каталитического гидрирования. В качестве примера группы-предшественника может быть упомянута нитрогруппа, которая может быть превращена в амино-группу путем восстановления, например, каталитическим гидрированием. Данные синтетические стратегии и защитные группы и группы-предшественники, которые подходят в каждом конкретном случае, известны специалисту в данной области техники.
Другим объектом настоящего изобретения являются новые исходные соединения и промежуточные вещества, встречающиеся в синтезе соединений Формулы I, включая соединения Формул II, III, IV, V, VI, VII, VIII и XI, где A, X, Xa, R1, R2, R3, R', FG1, FG2, L1 и L2, как определено выше, в любой их стереоизомерной форме или в виде смеси стереоизомерных форм в любом соотношении, и их соли и сольваты любого из них, и их использование в качестве промежуточных веществ. Изобретение также охватывает все таутомерные формы указанных промежуточных и исходных веществ. Все представленные выше пояснения и указанные выше варианты осуществления, касающиеся соединений Формулы I, применимы, соответственно, к указанным промежуточным и исходным соединениям. Объектом изобретения являются, в частности, новые конкретные исходные соединения и промежуточные вещества, описанные здесь. Независимо от того, раскрыты ли они в виде свободного соединения и/или в виде конкретной соли, они являются объектом изобретения как в форме свободных соединений, так и в форме их солей, а если описана конкретная соль - кроме того, в форме данной конкретной соли, и в форме сольватов любого из них.
Соединения Формулы I, необязательно в комбинации с другими фармакологически активными соединениями, могут вводиться животным, в частности млекопитающим, включая людей, в качестве лекарственных средств сами по себе, в виде смесей с другим или в виде фармацевтических композиций. Введение может осуществляться орально, например, в виде таблеток, покрытых оболочкой таблеток, покрытых сахарной оболочкой таблеток, гранул, жестких и мягких желатиновых капсул, растворов, включая водные, спиртовые и масляные растворы, соков, капель, сиропов, эмульсий или суспензий, ректально, например, в виде суппозиториев, или парентерально, например, в виде растворов для подкожных, внутримышечных или внутривенных инъекций или инфузий, в частности, водных растворов. Соединения Формулы I могут дополнительно применяться в устройствах для местной доставки лекарственных средств, например, в покрытых стентах для предотвращения или уменьшения внутристентового рестеноза, или путем их местного применения посредством катетера. Подходящий путь введения зависит, среди прочего, от заболевания, которое подвергается лечению, и его тяжести.
Количество соединения Формулы I и/или его физиологически приемлемых солей и/или сольватов, присутствующее в фармацевтических композициях, обычно варьирует от приблизительно 0,2 до приблизительно 800 мг, например, от приблизительно 0,5 до приблизительно 500 мг, например, от приблизительно 1 до приблизительно 200 мг, на разовую дозу, но в зависимости от типа фармацевтической композиции оно может быть больше. Фармацевтические композиции обычно содержат от приблизительно 0,5 до приблизительно 90 масс.% соединения Формулы I и/или его физиологически приемлемых солей и/или сольватов. Получение фармацевтических композиций может осуществляться известным способом. В связи с этим, одно или несколько соединений Формулы I и/или их физиологически приемлемые соли и/или сольваты вместе с одним или несколькими твердыми или жидкими фармацевтическими носителями или индифферентной основой и/или добавками или вспомогательными веществами и, если необходим комбинированный лекарственный препарат, другими фармакологически активными соединениями, обладающими терапевтическим или профилактическим действием, приводят к подходящей для введения форме и дозировке, которая может применяться у человека или в ветеринарии. В качестве носителей и добавок могут применяться подходящие органические и неорганические вещества, которые не будут вступать в нежелательные взаимодействия с соединениями Формулы I или их физиологически приемлемыми солями или сольватами. В качестве примеров типов добавок, которые могут содержаться в фармацевтических композициях и лекарственных препаратах, могут быть упомянуты лубриканты, консерванты, загустители, стабилизаторы, дезинтегранты, смачивающие агенты, агенты для создания эффекта депо, эмульгаторы, соли, например для влияния на осмотическое давление, буферы, красители, исправляющие вкус агенты и ароматизаторы. Примерами носителей и добавок являются вода, физиологический раствор, растительные масла, воски, спирты, такие как этанол, изопропанол, 1,2-пропандиол, бензиловые спирты или глицерин, полиолы, маннит, полиэтиленгликоли, полипропиленгликоль, триацетат глицерина, поливинилпирролидон, желатин, целлюлоза, углеводы, такие как лактоза, глюкоза, сахароза или крахмал, такой как кукурузный крахмал, стеариновая кислота и ее соли, такие как стеарат магния, тальк, ланолин, вазелин или их смеси, например, смеси воды с одним или несколькими органическими растворителями, такие как смеси воды со спиртами. Соединения Формулы I и их физиологически приемлемые соли и сольваты могут также подвергаться лиофилизации, и полученные лиофилизаты применяться, например, для производства композиций для инъекций.
Доза соединения Формулы I и/или его физиологически приемлемой соли и/или сольвата, которая будет вводиться, зависит от конкретного случая и, как это обычно происходит, должна адаптироваться лечащим врачем в соответствии с общепринятой практикой и способами к конкретным условиям для достижения оптимального действия. Это зависит, например, от природы и тяжести подвергаемого лечению расстройства, пола, возраста, веса и индивидуального отклика пациента человека или животного, эффективности и длительности применяемого соединения, от того осуществляется ли лечение острого или хронического заболевания или профилактика, или от того, вводятся ли другие активные соединения кроме соединения Формулы I. Как правило, дневная доза от, например, приблизительно 0,01 мг/кг до приблизительно 100 мг/кг или от приблизительно 0,1 мг/кг до приблизительно 10 мг/кг, или от приблизительно 0,3 мг/кг до приблизительно 5 мг/кг (в каждом случае мг на кг веса тела) является подходящей для введения взрослому человеку с весом 75 кг для получения желаемых результатов. Ежедневная доза в данном случае может вводиться в виде однократной дозы, в случае, когда вводятся большие количества - в виде поделенной на несколько, например, две, три или четыре, отдельных доз. Введение может также осуществляться непрерывно, например, путем непрерывной инфузии или инъекции. В зависимости от индивидуальных особенностей в каждом случае может быть необходимо изменять в меньшую или большую сторону указанные дозы.
Следующие примеры иллюстрируют изобретение.
Когда соединения примеров, содержащие основную группу, очищали с помощью высокоэффективной препаративной жидкостной хроматографии (ВЭЖХ) на колонке с обращенной фазой (ОФ) и, как обычно, элюент представлял собой смесь градиентного состава воды и ацетонитрила, содержащую трифторуксусную кислоту (ТФУ), они отчасти получались в виде их солей присоединения трифторуксусной кислоты в зависимости от особенностей обработки, таких как условия упаривания или лиофилизации. В названии соединений примеров, а также их структурных формулах, такое содержание трифторуксусной кислоты не указывается.
Полученные соединения, как правило, характеризовали методами спектроскопии и хроматографии, в частности, масс-спектрами (МС) и временем удерживания в ВЭЖХ (Rt; в мин), которые получали с помощью комбинированной аналитической ВЭЖХ/МС (ЖХ/МС), и/или спектрами ядерного магнитного резонанса (ЯМР). В случае характеризации методом ЯМР указываются химический сдвиг δ (в м.д.), количество протонов и мультиплетность (с=синглет, д=дублет, дд=дублет дублетов, т=триплет, дт=дублет триплетов, к=квартет, м=мультиплет; уш.=уширенный). При характеризации МС, как правило, указывается массовое число (m/z) пика молекулярного иона M, например M+, или соответствующего иона, такого как ион M+1, например [M+1]+, то есть протонированного молекулярного иона [M+H]+, который образуется в зависимости от используемого метода ионизации. Как правило, применяемым методом ионизации являлась ионизация электрораспылением (ESI). Условия для проведения ЖХ/МС были следующие.
Метод ЖХ1
Колонка: UPLC BEH C18, 50Ч2,1 мм, 1,7 мкм; скорость потока: 0,9 мл/мин; элюент A: ацетонитрил+0,08% муравьиной кислоты; элюент B: вода+0,1% муравьиной кислоты; градиент: с 5% A+95% B до 95% A+5% B за 1,1 мин, затем 95% A+5% B в течение 0,6 мин; метод ионизации в МС: ESI+.
Метод ЖХ2
Колонка: UPLC BEH C18, 5Ч2,1 мм, 1,7 мкм; скорость потока: 0,9 мл/мин; элюент A: ацетонитрил+0,035% муравьиной кислоты; элюент B: вода+0,05% муравьиной кислоты; градиент: с 5% A+95% B до 95% A+5% B за 1,1 мин, затем 95% A+5% B в течение 0,6 мин; метод ионизации в МС: ESI+.
Метод ЖХ3
Колонка: Waters Xbridge C18, 50Ч4,6 мм, 2,5 мкм; скорость потока: 1,3 мл/мин; элюент A: ацетонитрил+0,1% муравьиной кислоты; элюент B: вода+0,1% муравьиной кислоты; градиент: с 3% A+97% B до 60% A+40% B за 3,5 мин, с 60% A+40% B до 98% A+2% B за 0,5 мин, затем 98% A+2% B в течение 1 мин; метод ионизации в МС: ESI+.
Метод ЖХ4
Колонка: Phenomenex Mercury МС Luna 3 мкм C18(2) 100 Ангстрем, 10Ч2,0 мм; скорость потока 1,1 мл/мин; элюент A: ацетонитрил; элюент B: вода+0,05% ТФУ; градиент: с 20% A+80% B до 95% A+5% B за 0,8 мин; затем 95% A+5% B в течение 0,6 мин; затем 20% A+80% B за 0,05 мин; метод ионизации в МС: ESI+.
Пример 1
[2,6-Диметил-4-(5-феноксиоксазоло[5,4-d]пиримидин-2-ил)фенокси]уксусная кислота
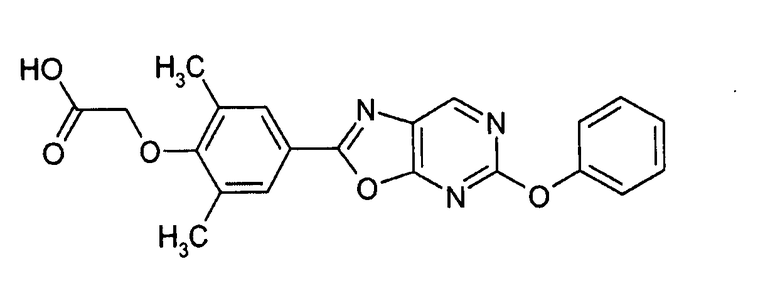
(a) N-(2,4-Дихлорпиримидин-5-ил)-4-метокси-3,5-диметилбензамид
К смеси 25 мл насыщенного водного раствора гидрокарбоната натрия и 25 мл воды добавляли 3,2 г 5-амино-2,4-дихлорпиримидина в 50 мл этилацетата. Добавляли в течение 15 мин при комнатной температуре раствор 4,9 г 3,5-диметил-4-метоксибензоилхлорида. Смесь интенсивно перемешивали в течение 4 ч. Затем слои разделяли, и водный слой дважды экстрагировали этилацетатом. После высушивания над сульфатом натрия и фильтрования растворитель удаляли в вакууме с получением 7,54 г технического продукта. Технический продукт затирали в 25 мл изопропанола. После фильтрования и промывки 10 мл изопропанола получали 2,74 г указанного в заголовке соединения в виде белого твердого вещества.
(b) 5-Хлор-2-(4-метокси-3,5-диметилфенил)оксазоло[5,4-d]пиримидин
Раствор 2,74 г N-(2,4-дихлорпиримидин-5-ил)-4-метокси-3,5-диметилбензамида и 3,2 мл Ν,Ν-диизопропилэтиламина в 17 мл ацетонитрила разделяли на две порции, каждую из которых нагревали в течение 1 ч до 160°C в микроволновом реакторе. Порции затем объединяли, и осадок отделяли фильтрованием с получением 600 мг указанного в заголовке соединения в виде темного, но очень чистого твердого вещества. Маточный раствор удаляли в вакууме, и остаток подвергали колоночной хроматографии на силикагеле (в градиенте гептан/этилацетат) с получением 600 мг указанного в заголовке соединения в виде твердого вещества бледно-желтого цвета.
(c) 4-(5-Хлороксазоло[5,4-d]пиримидин-2-ил)-2,6-диметилфенол
Раствор 1,2 г 5-хлор-2-(4-метокси-3,5-диметилфенил)оксазоло[5,4-d]пиримидина в 42 мл дихлорметана охлаждали до 0°C и добавляли в течение 10 мин 10 мл 1 M раствора трибромида бора в дихлорметане. Смесь перемешивали в течение 1 ч при 0°C и добавляли еще 3 мл 1 M раствора трибромида бора в дихлорметане. После перемешивания в течение еще 1 ч медленно добавляли 20 мл насыщенного водного раствора гидрокарбоната натрия. Осадок отфильтровывали и промывали водой с получением 1 г указанного в заголовке соединения.
(d) Трет-бутиловый эфир [4-(5-хлороксазоло[5,4-d]пиримидин-2-ил)-2,6-диметилфенокси]уксусной кислоты
К суспензии 1,2 мл трет-бутилбромацетата и 1,3 г карбоната калия в 15 мл диметилформамида медленно добавляли раствор 1 г 4-(5-хлороксазоло[5,4-d]пиримидин-2-ил)-2,6-диметилфенола в 5 мл диметилформамида. Смесь перемешивали в течение 30 мин при комнатной температуре и затем в течение 4 ч нагревали до 50°C. После охлаждения твердое вещество удаляли фильтрованием, и растворитель отгоняли в вакууме с получением 1,4 г технического указанного в заголовке соединения в виде бледно-желтого твердого вещества.
(e) Трет-бутиловый эфир [2,6-диметил-4-(5-феноксиоксазоло[5,4-d]пиримидин-2-ил)фенокси]уксусной кислоты
К раствору 38 мг фенола в 5 мл диметилацетамида в атмосфере аргона добавляли 19 мг гидрида натрия. После перемешивания в течение 30 мин при комнатной температуре медленно добавляли раствор 156 мг трет-бутилового эфира [4-(5-хлороксазоло[5,4-d]пиримидин-2-ил)-2,6-диметилфенокси]уксусной кислоты в 3 мл диметилацетамида. Смесь оставляли перемешиваться в течение 1,5 ч при комнатной температуре. После расходования исходного сложного эфира добавляли раствор лимонной кислоты (100 г/л) до достижения нейтрального значения pH. Водный слой экстрагировали дважды 15 мл этилацетата. Объединенные органические слои сушили над сульфатом натрия, фильтровали, и растворитель удаляли в вакууме. Указанное в заголовке соединение элюировали на колонке с силикагелем (в градиенте гептан/этилацетат). Выход: 77 мг белого твердого вещества.
(f) [2,6-Диметил-4-(5-феноксиоксазоло[5,4-d]пиримидин-2-ил)фенокси]уксусная кислота
Раствор 77 мг трет-бутилового эфира [2,6-диметил-4-(5-феноксиоксазоло[5,4-d]пиримидин-2-ил)фенокси]уксусной кислоты в 0,7 мл трифторуксусной кислоты перемешивали в течение 2 ч при комнатной температуре. Затем добавляли 5 мл толуола, и растворитель отгоняли в вакууме. Остаток затирали с 2 мл ацетонитрила, и указанное в заголовке соединение выделяли фильтрованием. Выход: 26 мг белого твердого вещества.
ЖХ/МС (Метод ЖХ1): Rt=1,24 мин; m/z=392,2 [M+H]+.
Пример 2
(E)-3-{4-[5-(2-Фторфенокси)оксазоло[5,4-d]пиримидин-2-ил]фенил}акриловая кислота
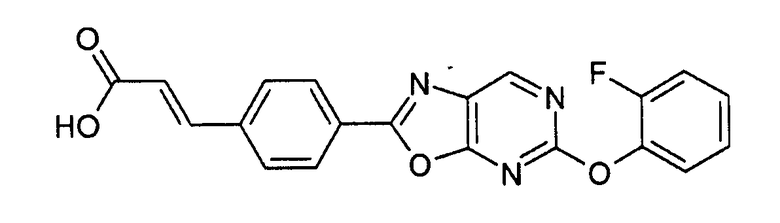
(a) 2-(4-Бромфенил)-5-хлороксазоло[5,4-d]пиримидин
Указанное в заголовке соединение получали, как описано в Примере 1, Стадии (a) и (b), используя 4-бромбензоилхлорид на стадии (a).
(b) 2-(4-Бромфенил)-5-(2-фторфенокси)оксазоло[5,4-d]пиримидин
К раствору 162 мкл 2-фторфенола в 10 мл диметилацетамида добавляли в атмосфере аргона 70 мг гидрида натрия. После перемешивания в течение 30 мин при комнатной температуре медленно добавляли суспензию 450 мг 2-(4-бромфенил)-5-хлороксазоло[5,4-d]пиримидина в 5 мл диметилацетамида. Смесь оставляли перемешиваться в течение 2 ч при комнатной температуре. После расходования исходного оксазоло[5,4-d]пиримидина добавляли водный раствор лимонной кислоты (100 г/л) до достижения нейтрального значения pH. Образующийся при добавлении раствора лимонной кислоты осадок отфильтровывали и промывали водой с получением 472 мг указанного в заголовке соединения.
ЖХ/МС (Метод ЖХ1): Rt=1,38 мин; m/z=386,1 [M+H]+.
(c) Трет-бутиловый эфир (E)-3-{4-[5-(2-фторфенокси)оксазоло[5,4-d]пиримидин-2-ил]фенил}акриловой кислоты
Помещали в реакционный сосуд 300 мг 2-(4-бромфенил)-5-(2-фторфенокси)оксазоло[5,4-d]пиримидина, 36 мг трис(дибензилиденацетон)дипалладия(0) и 23 мг три-трет-бутилфосфония тетрафторбората, который закрывали мембраной и три раза откачивали воздух и заполняли аргоном. Твердое вещество растворяли в 5,5 мл дегазированного 1,4-диоксана, который добавляли с помощью шприца. Затем добавляли с помощью шприца 0,124 мл трет-бутилакрилата и 0,181 мл Ν,Ν-дициклогексилметиламина и смесь в течение 6 ч нагревали до 120°C в микроволновом реакторе. После охлаждения смесь разбавляли 100 мл этилацетата, фильтровали через силикагель и концентрировали в вакууме. Остаток очищали с помощью препаративной ВЭЖХ. Получали 147 мг указанного в заголовке соединения.
ЖХ/МС (Метод ЖХ1): Rt=1,44 мин; m/z=434,14 [M+H]+.
(d) (E)-3-{4-[5-(2-Фторфенокси)оксазоло[5,4-d]пиримидин-2-ил]фенил}уксусная кислота
Раствор 145 мг трет-бутилового эфира (E)-3-{4-[5-(2-фторфенокси)оксазоло[5,4-d]пиримидин-2-ил]фенил}акриловой кислоты в 2 мл дихлорметана и 1 мл трифторуксусной кислоты перемешивали в течение 1,5 ч при комнатной температуре. Затем смесь концентрировали в вакууме и лиофилизовали. Получали 154 мг указанного в заголовке соединения.
ЖХ/МС (Метод ЖХ1): Rt=1,25 мин; m/z=378,08 [M+H]+.
По аналогии с получением описанных выше в примерах соединений были синтезированы соединения примеров Формулы I, перечисленные в Таблице 1. Частично, они были получены в виде соли трифторуксусной кислоты.
По аналогии с получением описанных выше в примерах соединений были синтезированы соединения примеров Формулы I, перечисленные в Таблице 1.
Соединения примеров формулы I
Определение фармакологической активности
A) ГТФ-γ-S-анализ на рецепторах EDG-1 человека
Для того чтобы определить активацию рецептора EDG-1 соединениями по изобретению, применяли ГТФ-γ-S-анализ (ГТФ-γ-S=гуанозин-5'-[тио]трифосфат) связывания рецептора, сопряженного с G-белком, основанный на принципе сцинтилляционного анализа сближения, применяя препарат мембран клеток из линии клеток CHO-Flp-In, постоянно сверхэкспрессирующих рецептор EDG-1 человека.
(a) Генерация линии клеток
Система экспрессии Flp-In™ (Invitrogen, номер по каталогу K6010-01) позволяет генерировать стабильные линии клеток млекопитающих, в которые интегрирован интересующий ген посредством гомологичной рекомбинации по особым геномным участкам, называемым сайтами узнавания флипазы (Flp) (Flipase Recognition Target (FRT)) с помощью Flp рекомбиназы, кодируемой экспрессирующей плазмидой pOG44. Интеграция экспрессирующей конструкции pcDNA5/FRT в геном линии клеток-мишеней Flp-In приводила к транскрипции интересующего гена. Стабильно трансфицированные клетки становились устойчивыми к гигромицину.
За день до трансфекции высевали 200000 клеток Flp-In-CHO в среде Ham F-12 (Invitrogen, номер по каталогу 31765), поддержанной 10% фетальной телячьей сыворотки (ФТС; Perbio Science, номер по каталогу SH30068.03) в 6-луночный планшет и инкубировали при 37°C/5% CO2 в течение ночи. Используя реагент для трансфекции FuGENE® 6 (Roche, номер по каталогу 11988387001) клетки контрансфицировали плазмидой pOG44, вызывающей экспрессию Flp-рекомбиназы, и модифицированной плазмидой, дополнительно содержащей edg-1-ген (номер доступа NM_001400), именуемой pcDNA5-FRT-TO_nFLAG_DEST-EDG-1, в соотношении 9:1. Для получения модифицированной плазмиды pcDNA5-FRT-TO_nFLAG_DEST плазмиду от Invitrogen pcDNA5/FRT/TO (Invitrogen, номер по каталогу V6520-20) адаптировали для системы клонирования Gateway® (Invitrogen) путем вставки кассеты Gateway, содержащей сайты рекомбинации attR, фланкирующие ген ccdB и ген устойчивости к хлорамфениколу (Gateway Conversion System, Invitrogen, номер по каталогу 11828-029). Дополнительно был добавлен эпитоп FLAG-метки перед 5'att-сайтом рекомбинации, что дает экспрессию рекомбинантных белков с FLAG-меткой на N-конце.
Для трансфекции в одной лунке смешивали 1,08 мкг pOG44 и 0,12 мкг pcDNA5-FRT-TO_nFLAG_DEST-EDG-1 в 100 мкл бессывороточной среды Ham F-12, содержащей 6 мкл агента трансфекции FuGENE® 6. Через 20 мин инкубации агент трансфекции/ДНК-комплекс распределяли по каплям на клетки. Клетки инкубировали в течение 24 ч при 37°C. Затем из трех лунок клетки переносили в колбу T75 (Greiner Cellstar®, номер по каталогу 658175), содержащую среду Ham F-12 с 10% ФТС, но без антибиотика, и инкубировали еще 24 ч. Через 48 ч после трансфекции среду заменяли на среду для селекции (Ham F-12 с 10% ФТС и 300 мкг/мл гигромицина В (Invitrogen, номер по каталогу 10687-010)). Среду меняли каждые 2-3 дня до тех пор, пока не выросла популяция резистентных клеток. Клетки несколько раз разделяли и высевали в новую колбу, так что клетки достигали не более 25% конфлюентности. После 2-недельной селекции клетки переносили в колбы T175 (Greiner Cellstar®, номер по каталогу 660175) и культивировали для получения партии. Клетки собирали из культуральных колб после краткой обработки (2-5 мин) аккутазой (PAA, номер по каталогу L11-007), ресуспендировали в среде для селекции (см. выше) и центрифугировали при 200×g в течение 5 мин. Клетки ресуспендировали в смеси 90% ФТС и 10% диметилсульфоксида и хранили заморожеными в жидком азоте.
(b) Мембранный препарат
Мембранный препарат получали стантартными методами из описанной выше линии клеток CHO Flp-In, постоянно экспрессирующих рецептор EDG-1. Вкратце, замороженные клетки помещали в культуру и выращивали до слияния в колбах для культивирования клеток T175 (Becton Dickinson, номер по каталогу 35 5001). Культивирование клеток останавливали промыванием натрий-фосфатным буфером, не содержащим кальций (НФБ; Gibco, номер по каталогу 14190), и клетки собирали с помощью резинового скребка и не содержащего кальций НФБ, содержащего смесь ингибиторов протеаз (полный ингибитор протеаз; Roche, номер по каталогу 1697498; 1 таблетка на 50 мл), на холоде при 4°C и затем центрифугировали при 4°C в течение 15 мин при 1100×g (Heraeus Minifuge T). Для проведения лизиса клеток осадок после центрифугирования ресуспендировали в холодном (4°C) гипотоничном буфере, состоящем из 5 мМ HEPES (Sigma-Aldrich, номер по каталогу H-0981), 1 мМ EDTA (динатриевая соль; Merck, номер по каталогу 8418), поддержанном смесью ингибиторов протеаз (как указано выше), в котором клетки выдерживали еще 15 мин на льду. После лизиса клетки центрифугировали при 4°C в течение 10 мин при 400×g (Heraeus Minifuge T). Осадок после центрифугирования разрушали в гомогенизаторе Даунса, разбавляли супернатантом из предшествующего центрифугирования и затем центрифугировали при 4°C в течение 10 мин при 500×g (Heraeus Minifuge T), чтобы отделить ядра и еще интактные клетки от мембран, главным образом, присутствующих в супернатанте. Затем супернатант разбавляли гипотоничным буфером и центрифугировали (Beckmann, Avanti J251) при приблизительно 18600×g в течение 2 ч при 4°C. После центрифугирования осадок ресуспендировали в буфере для хранения, состоящем из 20 мМ HEPES, 150 мМ NaCl (Merck, номер по каталогу 6400), 1 мМ EDTA (как указано выше), поддержанном смесью ингибиторов протеаз (как указано выше). Мембранный препарат делили на аликвоты и хранили при -80°C. Концентрацию белка в мембранном препарате определяли в образце посредством коммерчески доступной системы для количественного определения белка (Bio-Rad, DC Protein Assay, номер по каталогу 500-0113, 500-0114, 500-0115).
(c) ГТФ-γ-S-анализ
Мембранный препарат EDG-1, полученный на стадии (b), применяли в коммерчески доступном наборе от Amersham Biosciences/GE Healthcare (код RPNQ0210) для сцинтилляционного анализа сближения (Scintillation proximity assay, SPA) на связывание рецептора, сопряженного с G-белком, в котором лиганд-индуцируемое связывание 35S-меченного ГТФ-γ-S с содержащей рецептор мембраной, которая связана с содержащими сцинтиллятор микросферами, стимулирует испускание света и позволяет количественно определить активность in vitro соединения агониста EDG-1. Анализ осуществляли в 96-луночных планшетах в соответствии с инструкциями производителя. Перед началом эксперимента содержащие сцинтиллятор микросферы суспендировали в восстанавливающем буфере, состоящем из Трис-HCl (pH 7,4) с 0,1% (масс./об.) азида натрия, затем разбавляли на льду буфером для анализа (состоящим из 20 мМ HEPES, 100 мМ NaCl, 1 мМ EDTA (как указано выше), 1 мМ дитиотреитола (DTT), доведенным до pH 7,4) до конечной концентрации сфер 30 мг/мл.
В лунки вносили по 10 мкл упомянутого буфера для анализа, 10 мкл 100 мкМ раствора гуанозиндифосфата (ГДФ) и 10 мкл раствора тестируемого соединения в буфере для анализа/диметилсульфоксиде, получая конечную концентрацию тестируемого соединения 10 мкМ. В соответствующие лунки вместо раствора тестируемого соединения добавляли, в случае контроля верхнего предела, 10 мкл раствора сфингозин-1-фосфата (С1Ф; Sigma, номер по каталогу S-9666), приводя к конечной концентрации С1Ф 10 мкМ, и в случае контроля нижнего предела, 10 мкл буфера для анализа. Все лунки содержали равное количество диметилсульфоксида. Затем в каждую лунку добавляли 10 мкл раствора [35S]ГТФ-γ-S (4 нМ) и полученный в (b) мембранный препарат EDG-1 (15 мкг мембранных белков в 100 мкл буфера для анализа). После инкубации планшетов при комнатной температуре в течение 5 мин, добавляли 50 мкл указанной суспензии содержащих сцинтиллятор микросфер (30 мг/мл). После дополнительной инкубации в течение 45 мин при комнатной температуре, планшеты центрифугировали в течение 10 мин при 500×g. Количественное определение связывания [35S]ГТФ-γ-S и, таким образом, активацию рецептора измеряли с помощью счетчика бета-излучения (MicroBeta, Wallac) в течение 1 мин. Величины корректировали по фоновому значению путем вычитания соответствующего контроля нижнего предела. Все измерения повторяли три раза. Активацию рецептора тестируемым соединением выражали как процент от соответствующего значения, полученного для контроля верхнего предела (10 мкМ С1Ф; принимали за 100%активации). В Таблице 2 представлены значения активации, наблюдаемые для соединений примеров при 10 мкМ.
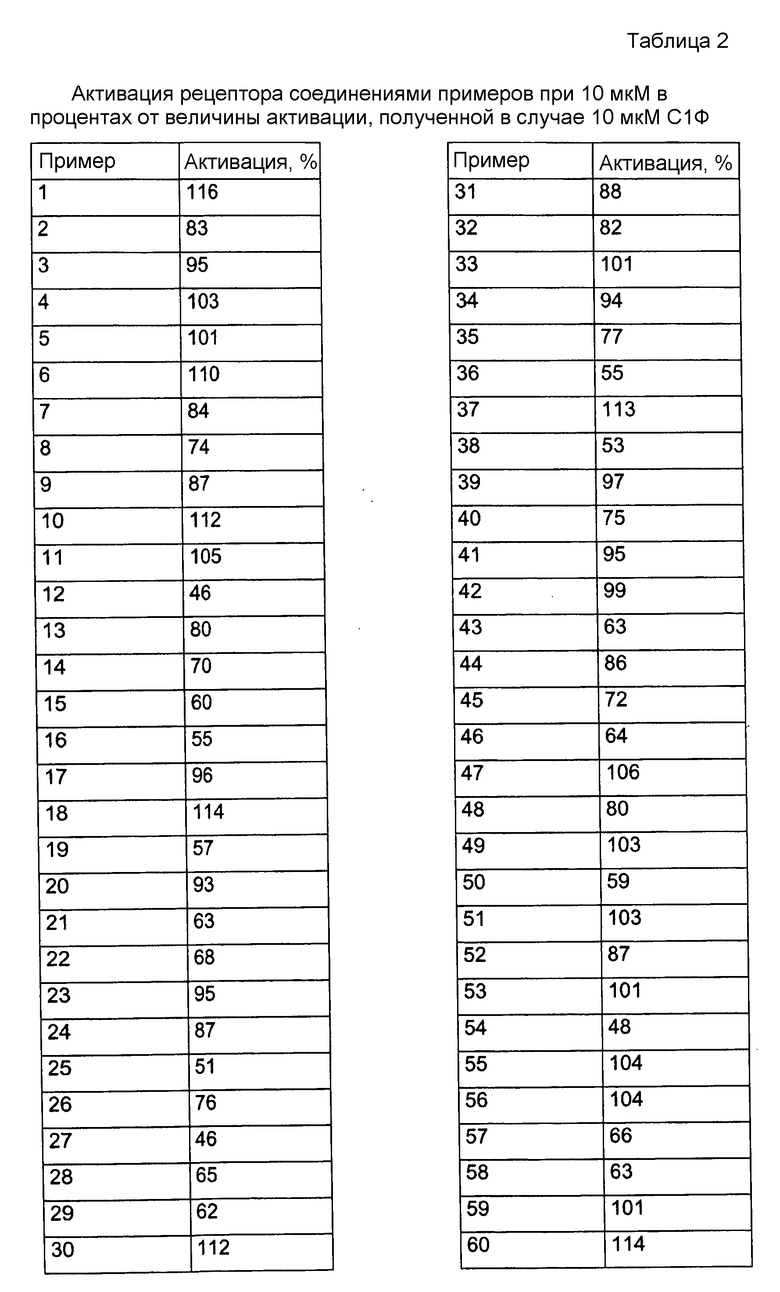

Как видно из данных исследования, соединения очень подходят для заживления ран и, в частности, для лечения нарушений, связанных с заживлением ран у пациентов с сахарным диабетом.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРОИЗВОДНЫЕ КАРБОНОВОЙ КИСЛОТЫ, СОДЕРЖАЩИЕ 2,5,7-ЗАМЕЩЕННОЕ ОКСАЗОЛОПИРИМИДИНОВОЕ КОЛЬЦО | 2011 |
|
RU2560876C2 |
| ПРОИЗВОДНЫЕ ГЕТЕРОЦИКЛИЧЕСКИХ КАРБОНОВЫХ КИСЛОТ, СОДЕРЖАЩИЕ 2,5,7-ЗАМЕЩЕННОЕ ОКСАЗОЛОПИРИМИДИНОВОЕ КОЛЬЦО | 2011 |
|
RU2554869C2 |
| ГЕТЕРОЦИКЛИЧЕСКИЕ ПРОИЗВОДНЫЕ КАРБОНОВЫХ КИСЛОТ, ИМЕЮЩИЕ 2,5-ЗАМЕЩЕННОЕ ОКСАЗОЛОПИРИМИДИНОВОЕ КОЛЬЦО | 2011 |
|
RU2559896C2 |
| 2,5-ЗАМЕЩЕННЫЕ ПРОИЗВОДНЫЕ ОКСАЗОЛОПИРИМИДИНА | 2011 |
|
RU2554874C2 |
| ПРОИЗВОДНЫЕ КАРБОНОВЫХ КИСЛОТ С ОКСАЗОЛО[5, 4-d]ПИРИМИДИНОВЫМ ЦИКЛОМ | 2012 |
|
RU2609008C2 |
| ПРОИЗВОДНЫЕ КАРБОНОВЫХ КИСЛОТ С ОКСАЗОЛО[5,4-b] ПИРИДИНОВЫМ КОЛЬЦОМ | 2012 |
|
RU2609002C2 |
| ПРОИЗВОДНЫЕ КАРБОНОВЫХ КИСЛОТ, ИМЕЮЩИЕ ОКСАЗОЛО[4,5-D]ПИРИМИДИНОВОЕ КОЛЬЦО | 2012 |
|
RU2609003C2 |
| 2,5,7-ЗАМЕЩЕННЫЕ ПРОИЗВОДНЫЕ ОКСАЗОЛПИРИМИДИНА | 2011 |
|
RU2557246C2 |
| ПРОИЗВОДНЫЕ КАРБОНОВЫХ КИСЛОТ С ОКСАЗОЛО[4,5-С]ПИРИДИНОВЫМ ЦИКЛОМ | 2012 |
|
RU2609004C2 |
| ЦИАНОИЗОХИНОЛИНОВЫЕ СОЕДИНЕНИЯ (ВАРИАНТЫ), ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ, СПОСОБ ИНГИБИРОВАНИЯ АКТИВНОСТИ ГИДРОКСИЛАЗЫ ГИПОКСИЯ-ИНДУЦИБЕЛЬНОГО ФАКТОРА (HIF) И СПОСОБ ЛЕЧЕНИЯ И/ИЛИ ПРОФИЛАКТИКИ СОСТОЯНИЯ, СВЯЗАННОГО С HIF, И/ИЛИ СОСТОЯНИЯ, СВЯЗАННОГО С ЭРИТРОПОЭТИНОМ, И/ИЛИ АНЕМИИ | 2007 |
|
RU2457204C2 |
Изобретение относится к оксазолопиримидиновым соединениям формулы I в любой из его стереоизомерных форм или его физиологически приемлемой соли, где А выбирают из NH, О и S; X выбирают из (C1-С6)-алкандиила, (С2-С6)-алкендиила, и (С1-С6)-алкандиилокси, где атом кислорода (C1-C6)-алкандиилокси-группы связан с группой R2; R1 выбирают из водорода и (C1-C4)-алкила; R2 выбирают из фенилена, который необязательно замещен по одному или двум атомам углерода в кольце одинаковыми или различными заместителями R22; R3 выбирают из (C1-C6)-алкила, необязательно замещенного 1-3 атомами фтора, или R3 является остатком насыщенного или ненасыщенного 5-членного - 10-членного моноциклического или бициклического кольца, которое содержит 0, 1 или 2 гетероатома в кольце, выбранных из N, О и S, и представляет собой циклопентил, инданил, фенил, нафтил, тиазолил, изотиазолил, пиридил, бензотиазолил или хинолин, и где остаток кольца необязательно замещен по одному или двум атомам углерода в кольце одинаковыми или различными заместителями R31; R22 выбирают из (C1-C4)-алкила, необязательно замещенного 1-3 атомами фтора; R31 выбирают из галогена, (С1-С4)-алкила, необязательно замещенного 1-3 атомами фтора, (C1-C4)-алкилокси, необязательно замещенного 1-3 атомами фтора, и (C1-C4)-алкил-S(О)m-, необязательно замещенного 1-3 атомами фтора; m равен 0. Также изобретение относится к фармацевтической композиции, содержащей соединения формулы I, и к способу получения соединений формулы I. Технический результат - соединения формулы I, предназначенные для активации рецептора EDG-1. 3 н. и 11 з.п. ф-лы, 2 табл., 2 пр.
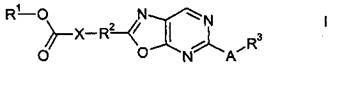
1. Соединение Формулы I в любой его стереоизомерной форме или его физиологически приемлемая соль:
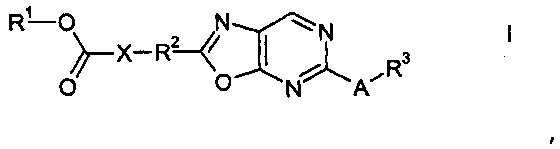
где А выбирают из NH, О и S;
X выбирают из (C1-С6)-алкандиила, (С2-С6)-алкендиила и (С1-С6)-алкандиилокси, где атом кислорода (C1-C6)-алкандиилокси-группы связан с группой R2;
R1 выбирают из водорода и (C1-C4)-алкила;
R2 выбирают из фенилена, который необязательно замещен по одному или двум атомам углерода в кольце одинаковыми или различными заместителями R22;
R3 выбирают из (C1-C6)-алкила, необязательно замещенного 1-3 атомами фтора, или R3 является остатком насыщенного или ненасыщенного 5-членного - 10-членного моноциклического или бициклического кольца, которое содержит 0, 1 или 2 гетероатома в кольце, выбранных из N, О и S, и представляет собой циклопентил, инданил, фенил, нафтил, тиазолил, изотиазолил, пиридил, бензотиазолил или хинолин, и где остаток кольца необязательно замещен по одному или двум атомам углерода в кольце одинаковыми или различными заместителями R31;
R22 выбирают из (C1-C4)-алкила, необязательно замещенного 1-3 атомами фтора;
R31 выбирают из галогена, (С1-С4)-алкила, необязательно замещенного 1-3 атомами фтора, (C1-C4)-алкилокси, необязательно замещенного 1-3 атомами фтора, и (C1-C4)-алкил-S(О)m-, необязательно замещенного 1-3 атомами фтора;
m равно 0.
2. Соединение Формулы I в любой его стереоизомерной форме или его физиологически приемлемая соль по п.1, где А выбирают из O и S.
3. Соединение Формулы I в любой его стереоизомерной форме или его физиологически приемлемая соль по п.1,
где А выбирают из О и S;
R3 выбирают из (C1-C6)-алкила, или R3 является остатком насыщенного или ненасыщенного 5-членного - 10-членного моноциклического или бициклического кольца, которое содержит 0, 1 или 2 одинаковых или различных кольцевых гетероатома, выбранных из N, О и S, и представляет собой циклопентил, инданил, фенил, нафтил, тиазолил, изотиазолил, пиридил, бензотиазолил или хинолин, и где остаток кольца необязательно замещен по одному или двум атомам углерода в кольце одинаковыми или различными заместителями R31.
4. Соединение Формулы I в любой его стереоизомерной форме или его физиологически приемлемая соль по п.1, где А представляет собой О.
5. Соединение Формулы I в любой его стереоизомерной форме или его физиологически приемлемая соль по одному или нескольким из пп.1-4,
где А представляет собой О;
X выбирают из (C1-С6)-алкандиила и (C1-C6)-алкандиилокси;
R1 выбирают из водорода и (С1-С4)-алкила;
R2 представляет собой фенилен, который необязательно замещен по одному или двум кольцевым атомам углерода одинаковыми или различными заместителями R22;
R3 выбирают из (C1-C6)-алкила, или R3 является остатком насыщенного или ненасыщенного 5-членного - 7-членного моноциклического кольца, которое содержит 0, 1 или 2 одинаковых или различных кольцевых гетероатома, выбранных из N, О и S, и где остаток кольца необязательно замещен по одному или нескольким атомам углерода в кольце одинаковыми или различными заместителями R31;
R22 выбирают из (C1-C4)-алкила;
R31 выбирают из галогена, (С1-С4)-алкила.
6. Соединение Формулы I в любой его стереоизомерной форме или его физиологически приемлемая соль по п.1, где
А представляет собой О;
X выбирают из (C1-C6)-алкандиила и (C1-C6)-алкандиилокси;
R1 выбирают из водорода и (C1-C4) -алкила;
R3 выбирают из (C1-C6)-алкила, или R3 является остатком насыщенного или ненасыщенного 5-членного - 7-членного моноциклического кольца, которое содержит 0, 1 или 2 одинаковых или различных кольцевых гетероатома, выбранных из N, О и S, и представляет собой циклопентил, фенил, тиазолил, изотиазолил, пиридил, и где остаток кольца необязательно замещен по одному или нескольким атомам углерода в кольце одинаковыми или различными заместителями R31;
R22 выбирают из (C1-C4)-алкила;
R31 выбирают из галогена и (С1-С4)-алкила.
7. Соединение Формулы I в любой его стереоизомерной форме или его физиологически приемлемая соль по одному или нескольким из пп.1-4 и 6,
где А представляет собой О;
X выбирают из (C1-C6) -алкандиила и (C1-C6)-алкандиилокси;
R1 выбирают из водорода и (С1-С4)-алкила;
R3 является остатком насыщенного или ненасыщенного 5-членного - 7-членного моноциклического кольца, которое содержит 0 или 1 кольцевой гетероатом, выбранный из N, О и S, и представляет собой циклопентил, фенил, тиазолил, изотиазолил, пиридил, и где остаток кольца необязательно замещен по одному или нескольким кольцевым атомам углерода одинаковыми или различными заместителями R31;
R22 выбирают из (С1-С4)-алкила;
R31 выбирают из галогена и (С1-С4)-алкила.
8. Соединение Формулы I или его физиологически приемлемая соль по одному или нескольким из пп.1-4 и 6, выбранное из
[2,6-диметил-4-(5-феноксиоксазоло[5,4-d]пиримидин-2-ил)фенокси}уксусной кислоты,
(Е)-3-{4-[5-(2-фторфенокси)оксазоло[5,4-d]пиримидин-2-ил]фенил}акриловой кислоты,
{4-[5-(2,4-дифторфенокси)оксазоло[5,4-d]пиримидин-2-ил]-2,6-диметилфенокси}уксусной кислоты,
{4-[5-(2,5-дифторфенокси)оксазоло[5,4-d]пиримидин-2-ил]-2,6-диметилфенокси}уксусной кислоты,
{4-[5-(2-фтор-4-метилфенокси)оксазоло[5,4-d]пиримидин-2-ил]-2,6-диметилфенокси}уксусной кислоты,
{4-[5-(2-фторфенокси)оксазоло[5,4-d]пиримидин-2-ил]-2,6-диметилфенокси}уксусной кислоты,
2-{4-[5-(2-фторфенокси)оксазоло[5,4-d]пиримидин-2-ил]-2,6-диметилфенокси}пропионовой кислоты,
{4-[5-(3-хлорфенокси)оксазоло[5,4-d]пиримидин-2-ил]-2,6-диметилфенокси}уксусной кислоты,
{4-[5-(3-фтор-4-метилфенокси)оксазоло[5,4-d]пиримидин-2-ил]-2,6-диметилфенокси}уксусной кислоты,
{4-[5-(5-фтор-2-метилфенокси)оксазоло[5,4-d]пиримидин-2-ил]-2,6-диметилфенокси}уксусной кислоты и
{4-[5-(4-хлорфенокси)оксазоло[5,4-d]пиримидин-2-ил]-2,6-диметилфенокси}уксусной кислоты.
9. Соединение Формулы I или его физиологически приемлемая соль по п. 1, выбранное из
[2,6-диметил-4-(5-феноксиоксазоло[5,4-d]пиримидин-2-ил)фенокси}уксусной кислоты,
(Е)-3-{4-[5-(2-фторфенокси)оксазоло[5,4-d]пиримидин-2-ил]фенил}акриловой кислоты,
{4-[5-(2,4-дифторфенокси)оксазоло[5,4-d]пиримидин-2-ил]-2,6-диметилфенокси}уксусной кислоты,
{4-[5-(2,5-дифторфенокси)оксазоло[5,4-d]пиримидин-2-ил]-2,6-диметилфенокси}уксусной кислоты,
{4-[5-(2-фтор-4-метилфенокси)оксазоло[5,4-d]пиримидин-2-ил]-2,6-диметилфенокси}уксусной кислоты,
{4-[5-(2-фторфенокси)оксазоло[5,4-d]пиримидин-2-ил]-2,6-диметилфенокси}уксусной кислоты,
2-{4-[5-(2-фторфенокси)оксазоло[5,4-d]пиримидин-2-ил]-2,6-диметилфенокси}пропионовой кислоты,
{4-[5-(3-хлорфенокси)оксазоло[5,4-d]пиримидин-2-ил]-2,6-диметилфенокси}уксусной кислоты,
{4-[5-(3-фтор-4-метилфенокси)оксазоло[5,4-d]пиримидин-2-ил]-2,6-диметилфенокси}уксусной кислоты,
{4-[5-(5-фтор-2-метилфенокси)оксазоло[5,4-d]пиримидин-2-ил]-2,6-диметилфенокси}уксусной кислоты и
{4-[5-(4-хлорфенокси)оксазоло[5,4-d]пиримидин-2-ил]-2,б-диметилфенокси}уксусной кислоты.
10. Соединение Формулы I или его физиологически приемлемая соль по п. 1, выбранное из
{4-[5-(2-фтор-4-метилфенокси)оксазоло[5,4-d]пиримидин-2-ил]-2,6-диметилфенокси}уксусной кислоты,
{4-[5-(2-фторфенокси)оксазоло[5,4-d]пиримидин-2-ил]-2,6-диметилфенокси}уксусной кислоты,
{4-[5-(3-хлорфенокси)оксазоло[5,4-d]пиримидин-2-ил]-2,6-диметилфенокси}уксусной кислоты,
{4-[5-(3-фтор-4-метил-фенокси)оксазоло[5,4-d]пиримидин-2-ил]-2,6-диметилфенокси}уксусной кислоты,
{4-[5-(5-фтор-2-метил-фенокси)оксазоло[5,4-d]пиримидин-2-ил]-2,6-диметилфенокси}уксусной кислоты и
{4-[5-(4-хлорфенокси)оксазоло[5,4-d]пиримидин-2-ил]-2,6-диметилфенокси}уксусной кислоты.
11. Соединение Формулы I или его физиологически приемлемая соль по п. 1, выбранное из
{4-[5-(2-фтор-4-метилфенокси)оксазоло[5,4-d]пиримидин-2-ил]-2,6-диметилфенокси}уксусной кислоты,
{4-[5-(2-фторфенокси)оксазоло[5,4-d]пиримидин-2-ил]-2,6-диметилфенокси}уксусной кислоты,
{4-[5-(3-хлорфенокси)оксазоло[5,4-d]пиримидин-2-ил]-2,6-диметилфенокси}уксусной кислоты,
{4-[5-(3-фтор-4-метил-фенокси)оксазоло[5,4-d]пиримидин-2-ил]-2,6-диметилфенокси}уксусной кислоты,
{4-[5-(5-фтор-2-метил-фенокси)оксазоло[5,4-d]пиримидин-2-ил]-2,6-диметилфенокси}уксусной кислоты и
{4-[5-(4-хлорфенокси)оксазоло[5,4-d]пиримидин-2-ил]-2,6-диметилфенокси}уксусной кислоты.
12. Способ получения соединения Формулы I по любому из пп.1-11, включающий взаимодействие соединения Формулы II с соединением Формулы III:
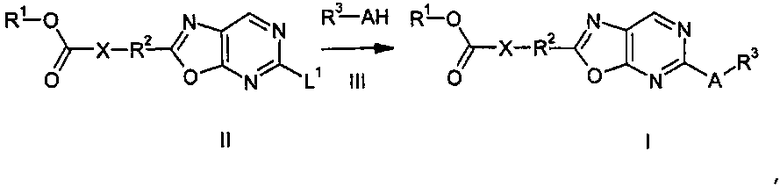
где группы А, X, R1, R2 и R3 в соединениях Формул II и III такие, как указано для соединений Формулы I, и могут присутствовать дополнительные функциональные группы в защищенной форме или в форме групп-предшественников, и группа L1 является атомом галогена или группой формулы -S(O)-Alk или -S(O)2-Alk, где Alk представляет собой (C1-C4)-алкильную группу.
13. Фармацевтическая композиция для активации рецептора EDG-1, содержащая по меньшей мере одно соединение Формулы I по любому из пп.1-11 или его физиологически приемлемую соль и фармацевтически приемлемый носитель.
14. Соединение Формулы I по п.1 или его физиологически приемлемая соль для применения в качестве фармацевтического препарата для активации рецептора EDG-1.
| Колосоуборка | 1923 |
|
SU2009A1 |
| Способ обработки целлюлозных материалов, с целью тонкого измельчения или переведения в коллоидальный раствор | 1923 |
|
SU2005A1 |
| Способ приготовления мыла | 1923 |
|
SU2004A1 |
| Пресс для выдавливания из деревянных дисков заготовок для ниточных катушек | 1923 |
|
SU2007A1 |
| Пресс для выдавливания из деревянных дисков заготовок для ниточных катушек | 1923 |
|
SU2007A1 |
| Станок для изготовления деревянных ниточных катушек из цилиндрических, снабженных осевым отверстием, заготовок | 1923 |
|
SU2008A1 |
| ГЕРБИЦИД | 0 |
|
SU404193A1 |
Авторы
Даты
2015-09-27—Публикация
2011-01-12—Подача