Изобретение относится к способу получения нерацемического 1-(адамант-1-ил)-2-(2-нитро-1-фенилэтил)бутан-1,3-диона формулы I
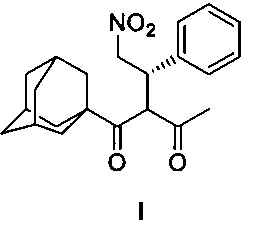
путем энантиоселективного присоединения 1-(адамант-1-ил)бутан-1,3-диона к ω-нитростиролу в присутствии комплекса никеля формулы II в соответствии со схемой 1,

где R = H, отличающийся тем, что в качестве донора Михаэля используется 1,3-дикетон, содержащий адамантильный заместитель.
2-(1-Арил-2-нитроэтил)бутан-1,3-дионы являются исходными соединениями для синтеза гетероциклических производных - ингибиторов калиевых каналов, проявляющих антиаритмическую активность и перспективных в терапии аутоимунных и хронических воспалительных заболеваний (Pat. WO WO 2007030582 (A2), дата публикации 15.03.2007). Введение в такие производные липофильного адамантильного заместителя может способствовать их более высокой биодоступности и эффективности действия (Wanka, L., Iqbal, K., Schreiner, P.R. // Chem. Rev. 2013. Vol. 113. № 5. P. 3516). Известно также, что ряд адамантилсодержащих гетероциклических соединений на основе 1,3-дикетонов проявляет антивирусную активность (Макарова Н.В., Бореко Е.И., Моисеев И.К., Павлова Н.И., Николаева С.Н., Земцова М.Н., Владыко Г.В. Антивирусная активность адамантансодержащих гетероциклов// Хим.-фарм. журнал. 2002. Т. 36. №1. С. 5-7; Моисеев И.К., Коньков С.А., Овчинников К.А., Киляева Н.М., Бормашева К.М., Нечаева О.Н., Леонова М.В., Климочкин Ю.Н., Балахнин С.М., Бормотов Н.И., Серова О.А., Беланов Е.Ф. Хим.-фарм. журнал. 2011. Т. 45. Вып. 10. С. 9).
Данным изобретением решена задача энантиоселективного синтеза 1-(адамант-1-ил)-2-(2-нитро-1-фенилэтил)бутан-1,3-диона формулы I с использованием легкодоступного и дешевого комплекса Ni(II) формулы II в качестве катализатора. Формирование асимметрического центра требуемой конфигурации на стадии синтеза соединения формулы I исключает необходимость дополнительных стадий разделения рацемических смесей в производстве фармацевтических препаратов.
Один из первых способов получения рацемических 2-(2-нитроэтил)бутан-1,3-дионов из натриевой соли ацетилацетона и нитроалкенов предложен в Pat. US 2447626 (24.08.1948).
Известен ряд способов получения нерацемических 2-(1-арил-2-нитроэтил)бутан-1,3-дионов, основанных на энантиоселективном присоединении 1,3-дикетонов к транс-β-нитростиролу в присутствии катализаторов - хиральных органических соединений и комплексов переходных металлов.
Асимметрическое присоединение 1,3-дикетонов к нитроалкенам осуществлено в присутствии органокатализаторов. В качестве органокатализаторов были использованы производных алкалоидов ряда хинина (Pat. US 2005/018973, дата публикации 22.12.2005; Pat. US 2012/0004424 A1, дата публикации 05.01.2012 г; Min С., Han X., Liao Z., Wu X., Zhou H.-B.; Dong C. Adv. Synth. Cat. 2011, V. 353, N 14-15, P. 2715; Malerich J.P., Hagihara K., Rawal V.H. J. Am. Chem. Soc. 2008, V. 130, N 44, P. 14416), хиральные полифункциональные тиомочевины на основе L-пролина (Vinayagam P., Vishwanath M., Kesavan V. Tetrahedron Asym. 2014, V. 25, N 6-7, P. 568), углеводов (Gao P., Wang C., Wu Y., Zhou Z., Tang C. Eur. J. Org. Chem. 2008, N 27, P. 4563), (S)-1-(3,5-бис(трифторметил)фенил)-3-(1-(диметиламино)-3-метилбутан-2-ил)тиомочевины (Andres J.M., Manzano R., Pedrosa R. Chemistry - A European Journal 2008, V. 14, N 17, P. 5116; Flock A.M., Krebs A., Bolm C. Synlett 2010, N 8, P. 1219), бифункциональные сульфонамиды (McGarraugh P.G., Brenner S.E. Tetrahedron 2009, V. 65, N 2, P. 449), хиральные 2-аминобензимидазолы (Almasi D., Alonso D.A., Gomez-Bengoa E., Najera C. J. Org. Chem. 2009, V. 74, N 16, P. 6163), производные ферроцена (Rao K.S., Trivedi R., Kantam M.L. Synlett, 2015, V. 26, N 2, P. 221), иммобилизованные органокатализаторы (Kardos G., Soos T. Eur. J. Org. Chem. 2013, N 21, P. 4490).
Однако для проведения реакции требуется высокая концентрация катализаторов (5-20 мол.%) и, в ряде случае, низкая температура (-20°C), требующая использования специального криогенного оборудования.
Более перспективным с точки зрения промышленной реализации процесса является использование катализаторов на основе комплексов металлов, поскольку в этом случае исключается необходимость использования синтетически малодоступных хиральных органических соединений, а концентрация катализатора для достижения приемлемой скорости реакции может быть снижена.
Каталитическая система (p-MeOC6H4O)2Ca/Pybox была использована в реакции асимметрического присоединения 1,3-дикетонов к серии нитроалкенов (Т. Tsubogo, Y. Yamashita, S. Kobayashi // Angew. Chem., Int. Ed. - 2009. - V. 48. - N 48. - P. 9117-9120).
Комплексы Ni(II) с хиральными диаминами были использованы в реакции асимметрического присоединения ацетилацетона к нитростиролу (J. Am. Chem. Soc. 2007. V. 129, N 37, P. 11583).
Во всех случаях в качестве доноров Михаэля были использованы 1,3-дикетоны с нормальными алкильными или ароматическими заместителями. 1,3-Дикетоны с адамантильным заместителем ранее не использовались в качестве реагентов в асимметрическом присоединении по Михаэлю.
Наиболее близким по технической сущности является способ асимметрического присоединения ацетилацетона к ω-нитростиролу в присутствии комплексов рутения (Watanabe М., Murata K., Ikariya Т. Pat. Ep 1512678 A1. Process for preparing optically active nitro compounds and cyano compounds, дата публикации 09.03.2005).
Описанный в Pat. EP 1512678 A1 способ заключается в том, что [(S,S)-N-(пентаметилбензолсульфонил)-1,2-дифенилэтиленди-амин](гексаметилбензол)рутений (0.02 ммоль), ω-нитростирол (1.0 ммоль), ацетилацетон (1.2 ммоль) и 1 мл толуола помещали в сосуд Шленка емкостью 20 мл, заполненный аргоном, и реакционную смесь перемешивали при -20°C в течение 48 ч. Продукт реакции выделяли флэш-хроматографией на силикагеле с использованием элюента гексан/ацетон 90:10. Выход соединения составил 90%, а энантиомерный избыток (R)-изомера 93%.
Указанный способ обладает целым рядом существенных недостатков:
1) использование дорогостоящих комплексов рутения в концентрациях 2 мол.%.
2) использование труднодоступного хирального лиганда - (S,S)-N-(пентаметил-бензолсульфонил)-1,2-дифенилэтилендиамина.
3) длительность процесса (48 ч) и необходимость его проведения в инертной атмосфере с использованием специального оборудования, что обусловлено чувствительностью катализатора к кислороду воздуха.
Технический результат - получение соединений формулы I с энантиомерным избытком 93% с использованием дешевого и легкодоступного комплекса никеля(II) с хиральным диамином, устойчивым к кислороду и влаге воздуха, упрощение и удешевление технологического процесса.
Технический результат достигается тем, что в энантиоселективном присоединении 1-(адамант-1-ил)бутан-1,3-диона к ω-нитростиролу катализатор - дибромобис[(R,R)-N,N'-дибензилциклогексан-1,2-диамин]никель(II) - добавляется к реакционной смеси в количестве 2 мол.% и реакционная смесь выдерживается при температуре 25°C в течение 12 ч до полного прохождения реакции.
Отличительные признаки:
1) Использование в качестве донора Михаэля адамантилсодержащего 1,3-дикетона.
2) Использование в качестве катализатора хирального комплекса никеля - дибромобис[(R,R)-N,N'-дибензилциклогексан-1,2-диамин]никеля(II).
3) Возможность проведения реакции на воздухе при температуре 25°C.
Заявляемое изобретение имеет следующие преимущества:
Удешевление производства за счет применения в качестве катализатора энантиоселективного присоединения 1-(адамант-1-ил)бутан-1,3-диона к ω-нитростиролу комплекса никеля и отказа от использования дорогостоящих и труднодоступных комплексов рутения.
Упрощения технологического процесса за счет применения в качестве хирального лиганда для приготовления катализатора легкодоступного (R,R)-N,N'-дибензилциклогексан-1,2-диамина, возможности проведения реакции без использования инертной атмосферы и при комнатной температуре.
Примеры выполнения способа
Спектры ЯМР регистрировали на приборе Jeol JNM-ECX400 с использованием растворителя CDCl3 [399.78 (1Н) и 100.53 МГц (13С)]. Измерения проводили без использования дополнительных эталонов с привязкой частоты к сигналу дейтерированного растворителя.
Энантиомерный избыток 1-(адамант-1-ил)-2-(2-нитро-1(S)-фенилэтил)бутан-1,3-диона формулы I определен по основному диастереомеру методом ВЭЖХ с использованием колонки с неподвижной хиральной фазой Chiralcel AD. Условия анализа для соединения формулы I: элюент гексан:изопропанол (95:5), расход 1.0 мл/мин. Время выхода (R)-изомера tr=12.3 мин, (S)-изомера tr=25.6 мин.
Определение удельных углов вращения проводилось на поляриметре RudolphResearchAnalitical.
Пример 1
К раствору 1.25 г (5.67 ммоль) 1-(адамант-1-ил)бутан-1,3-диона и 0.846 г (5.67 ммоль) ω-нитростирола в 10 мл толуола добавляют 91.6 мг (0.113 ммоль, 2 мол.%) дибромобис[(R,R)-N,N'-дибензилциклогексан-1,2-диамин]никеля(II) формулы II и реакционную смесь выдерживают в течение 12 ч при 25°C. Растворитель упаривают в вакууме. Твердый остаток перекристаллизовывают из метанола. Получают продукт в виде смеси диастереомеров (dr 1.57:1). Выход: 1.34 г (64%). Энантиомерный избыток 1-(адамант-1-ил)-2-(2-нитро-1(S)-фенилэтил)бутан-1,3-диона 92%. [α]D20+2.65° (с 1.0, МеОН). Найдено, %: С 71.47; Н 7.42; N 3.81. C22H27NO4. Вычислено, %: C 71.52; H 7.37; N 3.79. Спектр ЯМР 1Н, δ, м.д.: 1.39-1.48 м (6Н, Ad, первый диастереомер), 1.51-1.57 м (6Н, Ad, второй диастереомер), 1.60-1.67 м (6Н, Ad, второй диастереомер), 1.70-1.77 (6Н, Ad, первый диастереомер), 1.90-1.95 м (3Н, Ad, первый диастереомер), 2.03-2.09 (3Н, Ad, второй диастереомер), 2.16 с (3Н, CH3, второй диастереомер), 2.21 с (3Н, CH3, первый диастереомер), 4.57-4.65 м (1H, СН), 4.98-5.05 м (1Н, СН, 1Н, CH2NO2), 5.20-5.25 м (1Н, CH2NO2), 7.15-7.44 м (5H, Ph). Спектр ЯМР13С, δ, м.д.: 27.59 (СН, Ad, первый диастереомер), 27.73 (СН, Ad, второй диастереомер), 28.17 (CH3, первый диастереомер), 28.40 (CH3, второй диастереомер), 36.17 (CH2, Ad, первый диастереомер), 36.27 (CH2, Ad, второй диастереомер), 37.41 (CH2, Ad, первый диастереомер), 37.81 (CH2, Ad, второй диастереомер), 44.29 (CH, первый диастереомер), 44.49 (CH, второй диастереомер), 48.29 (С, Ad), 64.74 (СН, второй диастереомер), 65.84 (СН, первый диастереомер), 77.33 (CH2NO2, первый диастереомер), 78.16 (CH2NO2, второй диастереомер), 128.32 (3-С, Ph, второй диастереомер), 128.40 (первый диастереомер), 128.69 (4-С, Ph), 129.03 (2-С, Ph, первый диастереомер), 129.34 (2-С, Ph, второй диастереомер), 135.59 (1-С, Ph, второй диастереомер), 136.75 (1-С, Ph, первый диастереомер), 201.31 (С=O, второй диастереомер), 202.88 (C=O, первый диастереомер), 208.03 (С=O, первый диастереомер), 208.66 (С=O, второй диастереомер). ИК (KBr), ν, см-1: 2928, 2909, 2855, 1716, 1686, 1551, 1454, 1362, 1273, 1003, 771,702,529.
Пример 2
К раствору 1.00 г (4.55 ммоль) 1-(адамант-1-ил)бутан-1,3-диона и 0.68 г (4.55 ммоль) ω-нитростирола в 10 мл толуола добавляют 73.5 мг (0.091 ммоль, 2 мол.%) дибромобис[(R,R)-N,N'-дибензилциклогексан-1,2-диамин]никеля(II) формулы II и реакционную смесь выдерживают в течение 12 ч при 25°C. Растворитель упаривают в вакууме. Твердый остаток перекристаллизовывают из метанола. Выход: 0.82 г (50%). Физико-химические и спектральные характеристики полученного соединения идентичны приведенным в примере 1.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ЭНАНТИОСЕЛЕКТИВНОГО СИНТЕЗА (R)-ДИЭТИЛ(2-НИТРО-1-ФЕНИЛЭТИЛ) МАЛОНАТА В ПРИСУТСТВИИ КОМПЛЕКСА НИКЕЛЯ | 2011 |
|
RU2488576C2 |
| СПОСОБ ЭНАНТИОСЕЛЕКТИВНОГО СИНТЕЗА ДИЭТИЛ[3-МЕТИЛ-(1S)-(НИТРОМЕТИЛ)БУТИЛ]МАЛОНАТА ФОРМУЛЫ I | 2014 |
|
RU2555370C1 |
| СПОСОБ ПОЛУЧЕНИЯ (S)-3-(АМИНОМЕТИЛ)-5-МЕТИЛГЕКСАНОВОЙ КИСЛОТЫ | 2015 |
|
RU2643373C2 |
| СПОСОБ ЭНАНТИОСЕЛЕКТИВНОГО СИНТЕЗА (S)-ПРЕГАБАЛИНА | 2012 |
|
RU2529996C2 |
| СПОСОБ ПОЛУЧЕНИЯ 1-(1-АДАМАНТИЛ)-3,4-ДИНИТРО-5-(ТИО-R)-1Н-ПИРАЗОЛОВ | 2013 |
|
RU2533711C1 |
| СПОСОБ ПОЛУЧЕНИЯ 1-(1-АДАМАНТИЛ)-3,4,5-ТРИНИТРО-1Н-ПИРАЗОЛА | 2012 |
|
RU2528404C2 |
| СПОСОБ ПОЛУЧЕНИЯ 1-(1-АДАМАНТИЛ)-3,4-ДИНИТРО-5-(O-R)-1H-ПИРАЗОЛОВ | 2013 |
|
RU2533558C1 |
| СПОСОБ ПОЛУЧЕНИЯ 5-АМИНОЗАМЕЩЕННЫХ 1-(1-АДАМАНТИЛ)-3,4-ДИНИТРО-1Н-ПИРАЗОЛОВ | 2013 |
|
RU2533557C1 |
| СПОСОБ ПОЛУЧЕНИЯ 1-(1-АДАМАНТИЛ)-3,4-ДИНИТРО-5(N-НИТРОПИРАЗОЛИЛ)-1H-ПИРАЗОЛОВ | 2013 |
|
RU2532268C1 |
| СПОСОБ ПОЛУЧЕНИЯ АДАМАНТИЛСОДЕРЖАЩИХ ПРОИЗВОДНЫХ СИММЕТРИЧНЫХ 1,4-ДИКЕТОНОВ | 2006 |
|
RU2330013C1 |
Изобретение относится к способу получения нерацемического 1-(адамант-1-ил)-2-(2-нитро-1-фенилэтил)бутан-1,3-диона формулы I. Способ осуществляют путем энантиоселективного присоединения 1-(адамант-1-ил)бутан-1,3-диона к ω-нитростиролу в присутствии комплекса никеля формулы II в соответствии с приведенной схемой (R=H). Способ характеризуется тем, что в качестве донора Михаэля используют 1,3-дикетон, содержащий адамантильный заместитель. Предлагаемый способ позволяет упростить и удешевить процесс и получить продукт с хорошим выходом. 2 пр.
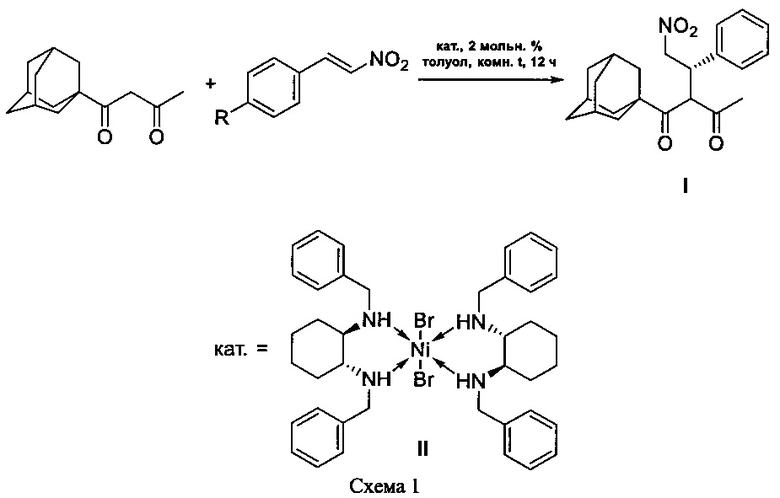
Способ получения нерацемического 1-(адамант-1-ил)-2-(2-нитро-1-фенилэтил)бутан-1,3-диона формулы I

путем энантиоселективного присоединения 1-(адамант-1-ил)бутан-1,3-диона к ω-нитростиролу в присутствии комплекса никеля формулы II в соответствии со схемой
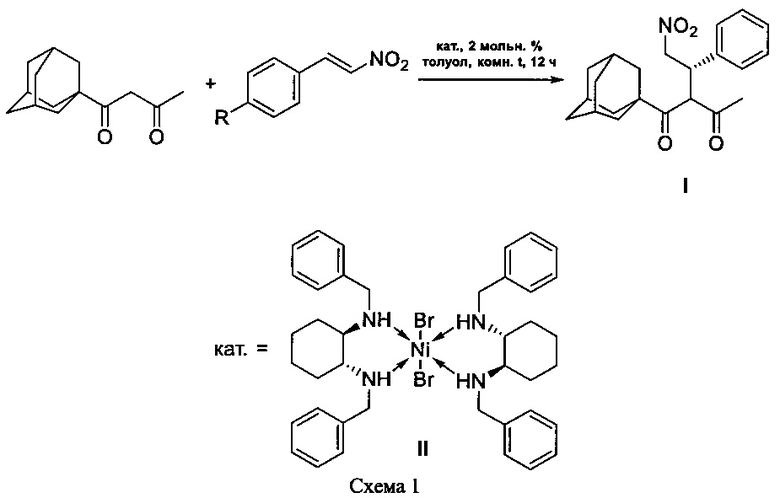 ,
,
где R=H, отличающийся тем, что в качестве донора Михаэля используют 1,3-дикетон, содержащий адамантильный заместитель.
| Устройство для разбрызгивания жидкости | 1987 |
|
SU1512678A1 |
| D.A | |||
| EVANS et al., Scope and Mechanism of Enantioselective Michael Additions of 1,3-Dicarbonyl Compounds to Nitroalkenes Catalyzed by Nickel(II)-Diamine Complexes, J | |||
| AM | |||
| CHEM | |||
| SOC., 2007, 129(37), pp.11583-11592 | |||
| А.Н.РЕЗНИКОВ и др | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| ОРГАН | |||
| ХИМИИ, 2013, Т.49, Вып.11, стр.1623-1626 | |||
| СПОСОБ ЭНАНТИОСЕЛЕКТИВНОГО СИНТЕЗА (R)-ДИЭТИЛ(2-НИТРО-1-ФЕНИЛЭТИЛ) МАЛОНАТА В ПРИСУТСТВИИ КОМПЛЕКСА НИКЕЛЯ | 2011 |
|
RU2488576C2 |
Авторы
Даты
2017-03-14—Публикация
2015-12-04—Подача