Изобретение относится к химии производных адамантана, а именно к новому способу получения адамантилсодержащих производных симметричных 1,4-дикетонов общей формулы:
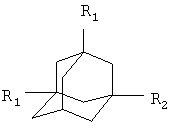
где R1=Н или СН3, 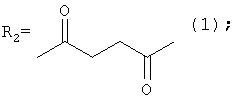
R1=Н или СН3, 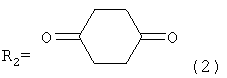
которые являются потенциально биологически активными веществами.
Известен способ получения адамантилсодержащих β-дикетонов [Патент РФ №2187493 С07С 49/15, 49/792, 45/45, 45/61, С07D 307/46, 333/16. Опубл. БИ №23, 2002 г.], состоящий во взаимодействии 1,3-дегидроадамантана с некоторыми β-дикетонами.
Однако данный способ не приводит к получению веществ заявляемой структурной формулы. Кроме этого, γ-дикетоны в отличие от β-дикетонов не являются сильными СН-кислотами, имеют несколько реакционных центров и образование веществ заявляемой структурной формулы при взаимодействии γ-дикетонов с 1,3-дегидроадамантаном и 5,7-диметил-1,3-дегидроадамантаном не является очевидным.
Известен способ получения адамантилсодержащих γ-дикетонов, например 1,4-ди-(1-адамантил)бутан-1,4-диона взаимодействием (1-адамантилацетил)малоната с натрием [Stetter H., Rauscer E. // Chem. Ber. 1960. Bd. 93. №9. S.2054-2057].
Существенным недостатком данного способа является, прежде всего, многостадийность, невысокий выход целевых продуктов и получение диадамантилсодержащего соединения.
Задачей предлагаемого изобретения является разработка технологичного одностадийного метода синтеза адамантилсодержащих производных симметричных 1,4-дикетонов, протекающего с высоким выходом.
Техническим результатом является расширение арсенала химических соединений, получаемых с высоким выходом новым способом.
Поставленный технический результат достигается в новом способе получения адамантилсодержащих производных симметричных 1,4-дикетонов общей формулы:

где R1=Н или СН3, 
R1=Н или СН3, 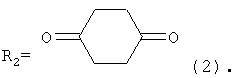
заключающийся в присоединении к производному адамантана соответствующего симметричного 1,4-дикетона, причем в качестве производного адамантана используются 1,3-дегидроадамантан или 5,7-диметил-1,3-дегидроадамантан, а в качестве исходных симметричных 1,4-дикетонов используются 2,5-гександион или 1,4-циклогескандион, и процесс проводят при их мольном соотношении, равном 1:1, при температуре 80°С в течение 5 часов.
Сущностью метода является реакция присоединения к 1,3-дегидроадамантану (1,3-ДГА) и его 5,7-диметильному производному (5,7-ДМ-1,3-ДГА) симметричных 1,4-дикетонов:
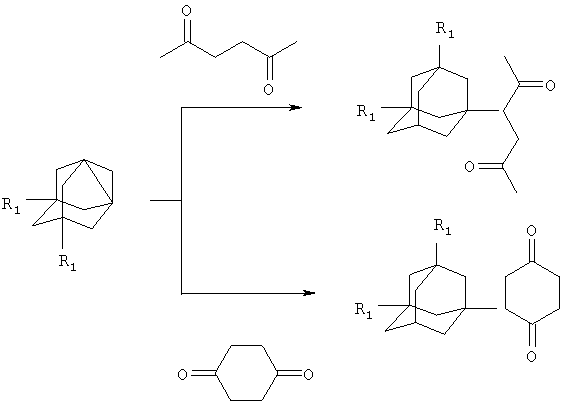
где R1=H или СН3.
Высокая нуклеофильность 1,3-дегидроадамантана и его 5,7-диметильного производного позволяет получать продукты присоединения данных симметричных 1,4-дикетонов с высокими выходами в достаточно мягких условиях в одну стадию.
Преимуществом данного метода является высокий выход (≈80%), а также возможность получения практически любых гомологов данного ряда, которые также являются потенциально биологически активными веществами.
При взаимодействии 1,3-ДГА или 5,7-ДМ-1,3-ДГА с 2,5-гександионом или 1,4-циклогесандионом единственным направлением реакции является С-адамантилирование по α-углеродному атому исходного γ-дикетона. Причем при взаимодействии 1,3-ДГА или 5,7-ДМ-1,3-ДГА с 1,4-циклогександином вследствие его полной симметричности образуется по одному целевому продукту. При взаимодействии 1,3-ДГА или 5,7-ДМ-1,3-ДГА с 2,5-гександионом образуется по одному целевому продукта - по СН2-группе, количество продуктов присоединения по СН3-группе мало, что объясняется термодинамической устойчивостью образующихся вторичных радикалов. Продукты O-адамантилирования отсутствую полностью, что связано низкой степенью енолизации исходных γ-дикетонов.
Как показали проведенные исследования, реакция чувствительна к температуре. Обнаружено, что при уменьшении температуры реакции с 80 до 35-40°С выход уменьшается, так как проведение взаимодействия в среде кипящего диэтилового эфира не приводило к получению целевых продуктов реакции. Дальнейшее повышение температуры (более 80°С) ведет к снижению выхода целевых продуктов, что по-видимому связано с протеканием побочной реакции рекомбинации адамантильных радикалов.
Целесообразным молярным соотношением реагентов 1,3-ДГА (или 5,7-диметил-1,3-ДГА): симметричный 1,4-дикетон является 1:1, так как при нем достигается высокий выход целевых соединений.
Уменьшение продолжительности реакции менее 5 часов при прочих равных условиях ведет к некоторому уменьшению выхода целевых продуктов. Увеличение продолжительности реакции свыше 5 часов не приводит к существенному изменению выхода целевых продуктов.
Способ осуществляется следующим образом.
К эквимолярному количеству симметричного 1,4-дикетона приливают раствор 1,3-дегидроадамантана (или 5,7-диметил-1,3-дегидроадамантана) в абсолютном диэтиловом эфире. Эфир отгоняют и смесь 1,3-дегидроадамантана (или 5,7-диметил-1,3-дегидроадамантана) и симметричного 1,4-дикетона нагревают в течение 5 часов при температуре 80°С. Синтезированные адамантилсодержащие производные симметричных 1,4-дикетонов направляются на стадию очистки. Выход целевых продуктов составляет 80%.
Изобретение иллюстрируется следующими примерами.
Пример 1
Синтез 3-(1-адамантил)гексан-2,5-диона.
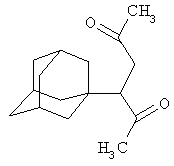
К 1,1414 г (0,01 моль) 2,5-гександиона в атмосфере сухого азота при комнатной температуре прикалывают раствор 1,34 г (0,01 моль) свежевозогнанного 1,3-ДГА в 20 мл абсолютного диэтилового эфира.
Растворитель отгоняют, после чего доводят температуру реакционной массы до 80°С, выдерживают без перемешивании 5 часов. По окончании реакции массу вакуумируют и получают 1,99 г (0,008 моль, 80%) 3-(1-адамантил)гексан-2,5-диона, представляющего собой бесцветные кристаллы с Тпл=70-73°С.
Масс-спектр, м/е: 248(5%)M+, 205 (5%) [М-СН3СО]+, 135(100%) Ad+.
Пример 2
Синтез 3-(3,5-диметил-1-адамантил)гексан-2,5-диона.
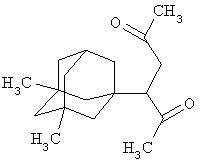
Аналогично, из 1,1414 г (0,01 моль) 2,5-гександиона и 1,62 г (0,01 моль) свежевозогнанного 5,7-ДМ-1,3-ДГА получают 2,2 г (0,008 моль, 80%) 3-(3,5-диметил-1-адамантил)гексан-2,5-диона, представляющего собой вязкую жидкость с Ткип=210°С/20 мм рт.ст.
Масс-спектр, м/е: 276(3%)M+, 233 (3%) [М-СН3СО]+, 163 (100%) (СН3)2Ad+.
Пример 3
Синтез 2-(1-адамантил)циклогексан-1,4-диона
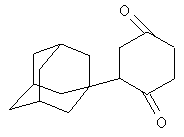
Аналогично, из 1,1213 г (0,01 моль) 1,4-циклогександиона и 1,34 г (0,01 моль) свежевозогнанного 1,3-ДГА получают 1,97 г (0,008 моль, 80%) 2-(1-адамантил)циклогексан-1,4-диона, представляющего собой бесцветные кристаллы с Тпл=125-128°С.
Масс-спектр, м/е: 246 (1%) М+, 135 (100%) Ad+.
Пример 4
Синтез 2-(3,5-диметил-1-адамантил)циклогексан-1,4-диона
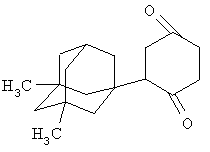
Аналогично, из 1,1213 г (0,01 моль) 1,4-циклогександиона и 1,62 г (0,01 моль) свежевозогнанного 5,7-ДМ-1,3-ДГА получают 2,19 г (0,008 моль, 80%) 2-(3,5-диметил-1-адамантил)циклогексан-1,4-диона, представляющего собой бесцветные кристаллы с Тпл=68-70°С.
Масс-спектр, м/е: 274 (1%) M+, 163 (100%) (CH3)2Ad+.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ α-АДАМАНТИЛСОДЕРЖАЩИХ АЛИФАТИЧЕСКИХ И ЖИРНОАРОМАТИЧЕСКИХ КЕТОНОВ | 2000 |
|
RU2186760C2 |
| СПОСОБ ПОЛУЧЕНИЯ 1,3-ДИ (4-R-ФЕНИЛСЕЛЕНО)АДАМАНТАНОВ | 2007 |
|
RU2333214C1 |
| СПОСОБ ПОЛУЧЕНИЯ АДАМАНТИЛСОДЕРЖАЩИХ β-ДИКЕТОНОВ И КЕТОЭФИРОВ | 2000 |
|
RU2187493C1 |
| СПОСОБ ПОЛУЧЕНИЯ АДАМАНТИЛСОДЕРЖАЩИХ НИТРИЛОВ | 2003 |
|
RU2240310C1 |
| СПОСОБ ПОЛУЧЕНИЯ АЛЬФА-АДАМАНТИЛСОДЕРЖАЩИХ АЛЬДЕГИДОВ | 2003 |
|
RU2240303C1 |
| СПОСОБ ПОЛУЧЕНИЯ АЛЬФА-АДАМАНТИЛСОДЕРЖАЩИХ ПРОИЗВОДНЫХ ТРИМЕТИЛБИЦИКЛО[2.2.1]ГЕПТАН-2-ОНА | 2006 |
|
RU2311401C1 |
| СПОСОБ ПОЛУЧЕНИЯ АДАМАНТИЛСОДЕРЖАЩИХ АРОМАТИЧЕСКИХ СОЕДИНЕНИЙ | 2006 |
|
RU2309932C1 |
| СПОСОБ ПОЛУЧЕНИЯ 1-(4-R-АРИЛ)АДАМАНТАНОВ ИЛИ ИХ ПРОИЗВОДНЫХ | 2006 |
|
RU2307116C1 |
| СПОСОБ ПОЛУЧЕНИЯ АДАМАНТИЛСОДЕРЖАЩИХ ПРОИЗВОДНЫХ ФЕНОЛА | 2006 |
|
RU2326104C1 |
| СПОСОБ ПОЛУЧЕНИЯ N-ФТАЛИМИДОАЛКИЛАДАМАНТАНА ИЛИ ЕГО ПРОИЗВОДНЫХ | 2003 |
|
RU2247114C1 |
Изобретение относится к способу получения новых адамантилсодержащих производных симметричных 1,4-дикетонов общей формулы:
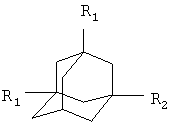 ,
,
где R1=Н или СН3, 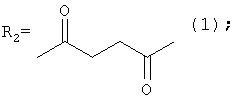
R1=Н или СН3, 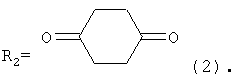
которые являются потенциально биологически активными веществами. Способ заключается в присоединении к 1,3-дегидроадамантану или 5,7-диметил-1,3-дегидроадамантану симметричного 1,4-дикетона: 2,5-гександиона или 1,4-циклогескандиона при их мольном соотношении, равном 1:1, при температуре 80°С в течение 5 часов. Способ позволяет получать новые соединения с высоким выходом.
Способ получения адамантилсодержащих производных симметричных 1,4-дикетонов общей формулы
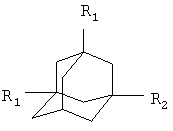 ,
,
где R1 - Н или СН3, R2- 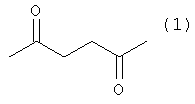
R1 - Н или СН3, R2- 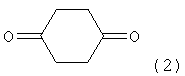
заключающийся в присоединении к производному адамантана соответствующего симметричного 1,4-дикетона, причем в качестве производного адамантана используются 1,3-дегидроадамантан или 5,7-диметил-1,3-дегидроадамантан, а в качестве исходных симметричных 1,4-дикетонов используются 2,5-гександион или 1,4-циклогескандион, и процесс проводят при их мольном соотношении 1:1 при температуре 80°С в течение 5 ч.
| СПОСОБ ПОЛУЧЕНИЯ АДАМАНТИЛСОДЕРЖАЩИХ β-ДИКЕТОНОВ И КЕТОЭФИРОВ | 2000 |
|
RU2187493C1 |
| СПОСОБ ПОЛУЧЕНИЯ α-АДАМАНТИЛСОДЕРЖАЩИХ АЛИФАТИЧЕСКИХ И ЖИРНОАРОМАТИЧЕСКИХ КЕТОНОВ | 2000 |
|
RU2186760C2 |
| US 3591642 A, 06.07.1971 | |||
| М.- Швехгеймер Г.А., Производные адамантана, содержащие в узловых положениях гетероциклические заместители | |||
| Синтез и свойства | |||
| Успехи химии, 1996, 65(7), стр.603. | |||
Авторы
Даты
2008-07-27—Публикация
2006-12-20—Подача