Отсылки к родственным заявкам
Данная заявка испрашивает приоритет по отношению к предварительной заявке на патент США номер 61/673500, представленной 19 июля 2012 г., содержание которой явным образом включается в настоящий документ путем отсылки.
Уровень техники
Природный витамин Ε представляет собой жирорастворимое вещество, существующее в восьми различных формах. Каждая из этих форм обладает своей биологической активностью, определяющей ее эффективность и пользу в организме. Витамин Ε - пищевой антиоксидант, участвующий в поддержании целостности клетки. В организм человека он поступает из таких продуктов, как растительные масла (подсолнечное, сафлоровое, рапсовое, оливковое), крупы, орехи, фрукты, а также из жирных частей мясных продуктов.
В природном витамине Ε два основных типа соединений: токоферолы (80%) и токотриенолы (20%). В структуру как тех, так и других входит хроманоловое кольцо. Токоферолы отличаются насыщенной боковой цепью, а в токотриенолах имеется изопреноидная боковая цепь с двойными связями при С-3, -7 и -11.
Клинические испытания, в которых изучалось действие природного витамина Ε при различных серьезных расстройствах здоровья, привели к выводу, что природный витамин Ε либо бесполезен, либо при некоторых состояниях может быть вредным.
Богатым источником природных токотриенолов служит пальмовое масло. Токотриенолы являются мощными нейропротекторами и антиоксидантами, обладают противораковым действием и понижают уровень холестерина в крови; эти их свойства биологически отличны от свойств токоферолов и независимы от антиоксидантной функции. Токотриенолы в микромолярных количествах подавляют активность печеночного фермента 3-гидрокси-3-метилглютарил-кофермент А-редуктазы, ответственной за синтез холестерина. Токотриенолы считаются более сильными антиоксидантами, чем токоферолы. Благодаря ненасыщенной боковой цепи токотриенолы лучше проникают в ткани, в которых есть слои насыщенных жиров, как в мозге и печени. Сравнительное изучение антиоксидантных свойств токоферолов и токотриенолов показало, что токотриенолы предпочтительны, потому что лучше распределяются в жировых слоях клеточной мембраны. Недавно сообщалось о том, что токотриенолы противодействуют ангиогенезу.
Как и в случае токоферолов, в отношении токотриенолов установлено наличие определенных функций, которые могут быть полезны для здоровья человека. Однако на долю токотриенолов приходится лишь небольшая доля исследований, посвященных витамину Е.
В США каждый год регистрируется приблизительно 795 тыс. случаев инсульта и более 200 тыс. случаев транзиторной ишемической атаки; эти нарушения имели место у 7 млн. человек. Для тех кто перенес инсульт, риск рецидива в первый год после инцидента составляет 11%, в первые пять лет - 26%. В течение 90 суток после транзиторной ишемической атаки риск инсульта составляет 9-11%.
В некоторых случаях рецидивных сердечно-сосудистых нарушений, в том числе инсульта, у лиц, страдающих сердечно-сосудистыми заболеваниями и принимающих аспирин и клопидогрел, могут быть связаны с неспособностью этих средств лечения поддавить агрегацию тромбоцитов in vitro. Частота случаев устойчивости к действию аспирина и клопидогрела оценивается в 20%.
По некоторым оценкам, в США около 30 млн. человек (9,5% населения) принимают аспирин и около 48 млн. человек (15,3% населения) принимают клопидогрел для защиты сердечно-сосудистой системы. При том что 20% населения устойчивы к этим средствам, миллионам людей нужно иное лечение.
После транзиторной ишемической атаки или инсульта аспирин снижает риск рецидивного инсульта, инфаркта миокарда и смерти от поражения сосудов на 13%, не летального ишемического инсульта - на 19%. Для предотвращения инсульта или комбинированного поражения сердечно-сосудистой системы препараты, противодействующие агрегации тромбоцитов, как клопидогрел и комбинированный препарат дипиридамола и аспирина замедленного высвобождения, несколько более эффективны, чем аспирин сам по себе; однако у больных с инсультом, обусловленным фибрилляцией предсердий, эти препараты не столь действенны, как варфарин в индивидуально подобранной дозировке, который снижает риск инсульта на 62%. У больных с инсультом аторвастатин снижает уровень холестерина в крови и риск рецидивного инсульта, но лишь на примерно 2% за период в пять лет. Также хронический прием клопидогрела (как альтернативы аспирину) и статинов не лишен вредных побочных эффектов, включая язвы желудка и кишечника, нейтропению, миалгию и повышенные показатели функции печени.
Раскрытие изобретения
Настоящим изобретением предлагаются способы ослабления свертывания крови у нуждающихся в том пациентов, включающие введение пациенту фармацевтически эффективной композиции, в которой содержится по меньшей мере одна изоформа токотриенола и которая ослабляет свертывание крови у этого пациента.
Также предлагаются такие способы, в которых указанная композиция содержит токотриенол в дозе, выбираемой из группы, состоящей из: от приблизительно 10 мг/сут до приблизительно 1000 мг/сут; от приблизительно 50 мг/сут до приблизительно 500 мг/сут; от приблизительно 100 мг/сут до приблизительно 500 мг/сут; от приблизительно 200 мг/сут до приблизительно 500 мг/сут; от приблизительно 300 мг/сут до приблизительно 500 мг/сут; до приблизительно 400 мг/сут.
Также предлагаются такие способы, в которых указанная композиция содержит токотриенол в дозе, выбираемой из группы, состоящей из: от приблизительно 200 мг 1 раз в неделю до приблизительно 1000 мг 1 раз в неделю; от приблизительно 300 мг 1 раз в неделю до приблизительно 1000 мг 1 раз в неделю; от приблизительно 400 мг 1 раз в неделю до приблизительно 500 мг 1 раз в неделю.
Также предлагаются такие способы, в которых указанная композиция вводится пациенту по схеме приема, выбираемой из группы, состоящей из: приблизительно через день; приблизительно 1 раз в 3 дня; приблизительно 1 раз в 4 дня; приблизительно 1 раз в 5 дней; приблизительно 1 раз в 6 дней; приблизительно 1 раз в 7 дней; приблизительно 1 раз в 2 недели; приблизительно 1 раз в месяц; приблизительно 2 раза в месяц; приблизительно 3 раза в месяц; приблизительно 4 раза в месяц; приблизительно 5 раз в месяц; приблизительно 6 раз в месяц; приблизительно 7 раз в месяц и приблизительно 8 раз в месяц.
Также предлагаются такие способы, в которых указанная композиция представляет собой добавку к пище, принимаемую перорально.
Также предлагаются такие способы, в которых указанную пероральную добавку к пище принимают в одной или более из следующих форм: капсулы, таблетки, коллоидный препарат, жевательная резинка, гель, напиток, компонент пищевого продукта, полоска тонкой растворимой пленки, эмульгированная съедобная паста, эмульсия, сироп, мясной пищевой продукт, молочный пищевой продукт, яйцо.
Также предлагаются такие способы, в которых указанного пациента выбирают из группы повышенного риска в отношении патологических состояний, связанных с нарушениями свертывания крови, выбираемых из группы, состоящей из транзиторной ишемической атаки, инсульта, эмболии и дисфункции сердца.
Также предлагаются такие способы, в которых указанного пациента выбирают из группы, состоящей из: лиц, у которых ранее было нарушение свертывания крови; лиц, перенесших инсульт; лиц, у которых было какое-либо острое или тяжелое состояние сердечно-сосудистой системы; лиц, перенесших транзиторную ишемическую атаку; лиц, у которых имела место эмболия; лиц, у которых имел место тромбоз; лиц с наследственным предрасположением к нарушениям свертывания крови; лиц, у которых имеются биологические маркеры, указывающие на нарушение свертывания крови, и лиц, принимающих противосвертывающие средства.
Также предлагаются такие способы, в которых указанного пациента выбирают из группы, состоящей из: космонавтов, летчиков, профессиональных автогонщиков, водолазов, альпинистов, пациентов перед хирургическим вмешательством, больных серповидно-клеточной анемией, пациентов с сонным апноэ, пациентов, проходящих лечение в связи со злоупотреблением наркотическими веществами, пожилых людей, старых животных и животных-компаньонов (домашних питомцев).
Настоящим изобретением также предлагается фармацевтическая композиция для лечения нарушений свертывания крови, включающая один или более агентов, противодействующих агрегации тромбоцитов, и одно или более токотриенольных соединений.
Также предлагаются такие композиции, в которых тромболитический агент выбирают из группы, состоящей из аспирина, клопидогрела и дипиридамола.
Настоящим изобретением также предлагаются способы снижения риска второго инсульта у нуждающихся в том больных, перенесших инсульт; эти способы включают введение нуждающемуся в том пациенту фармацевтически эффективной композиции, содержащей по меньшей мере одну изоформу токотриенола и снижающей риск повторения инсульта.
Также предлагаются такие способы, которые применяются к пациентам, устойчивым к действию аспирина или клопидогрела.
Также предлагаются такие способы, которые включают введение пациенту до 400 мг по меньшей мере одного токотриенола в течение по меньшей мере 30 дней и последующего введения фармацевтически эффективной дозы по меньшей мере одного токотриенола раз в неделю.
Настоящим изобретением также предлагаются способы снижения риска второго инсульта у нуждающихся в том больных, перенесших инсульт; эти способы включают введение нуждающемуся в том пациенту фармацевтически эффективной композиции, содержащей по меньшей мере одну изоформу токотриенола и снижающей риск повторения инсульта.
Также предлагаются такие способы, которые включают введение пациенту также фармацевтически эффективного количества аспирина или клопидогрела.
Также предлагаются такие способы, которые включают введение пациенту до 400 мг по меньшей мере одного токотриенола в течение по меньшей мере 30 дней и последующего введения фармацевтически эффективной дозы по меньшей мере одного токотриенола раз в неделю.
Настоящим изобретением также предлагается способ подавления агрегации тромбоцитов, опосредованной арахидоновой кислотой и связанной с 12-липоксигеназой (12-LOX), у нуждающихся в том пациентов, который включает введение указанному пациенту фармацевтически эффективного количества смеси токотриенолов раз в неделю.
Настоящим изобретением также предлагаются способы снижения риска или ослабления симптомов патологической агрегации тромбоцитов у нуждающихся в том пациентов, которым противопоказан аспирин; эти способы включают введение указанному пациенту фармацевтически эффективной смеси токотриенолов.
Также предлагаются такие способы, которые применяются в случаях, когда аспирин противопоказан по причинам, выбираемым из группы, состоящей из алкоголизма, патологических изменений печени, нарушений свертывания крови, аллергии, непереносимости салицилатов, астмы, бронхоспазма, пептических язв или язв кишечника, диабета, гастрита, гемофилии, недостаточности глюкозо-6-фосфат-дегидрогеназы, лихорадки денге, детского или подросткового возраста, заболеваний почек, гиперурикемии и подагры.
Настоящим изобретением также предлагаются способы снижения риска или ослабления симптомов патологической агрегации тромбоцитов у нуждающихся в том пациентов, которым противопоказан клопидогрел; эти способы включают введение указанному пациенту фармацевтически эффективной смеси токотриенолов.
Также предлагаются такие способы, которые применяются в случаях, когда аспирин противопоказан по причинам, выбираемым из группы, состоящей из алкоголизма, патологических изменений печени, аллергии, низкой скорости метаболизма субстратов цитохрома р450 из-за наличия его аллельного варианта CYP2C19, язв желудка или кишечника и поражений почек.
Настоящим изобретением также предлагаются способы снижения риска сердечного приступа у нуждающихся в том пациентов, включающие введение указанному пациенту фармацевтически эффективного количества смеси токотриенолов раз в неделю.
Настоящим изобретением также предлагаются способы снижения риска сердечного приступа у нуждающихся в том пациентов, включающие введение указанному пациенту фармацевтически эффективного количества смеси токотриенолов раз в неделю.
Краткое описании фигур
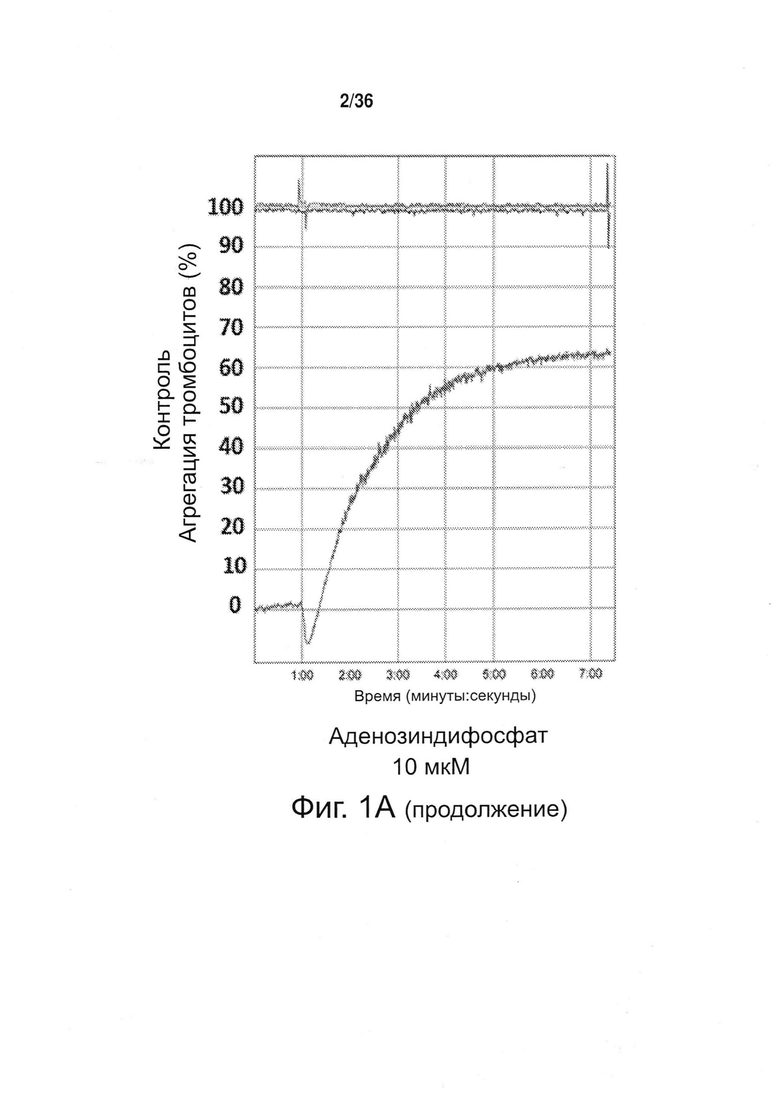
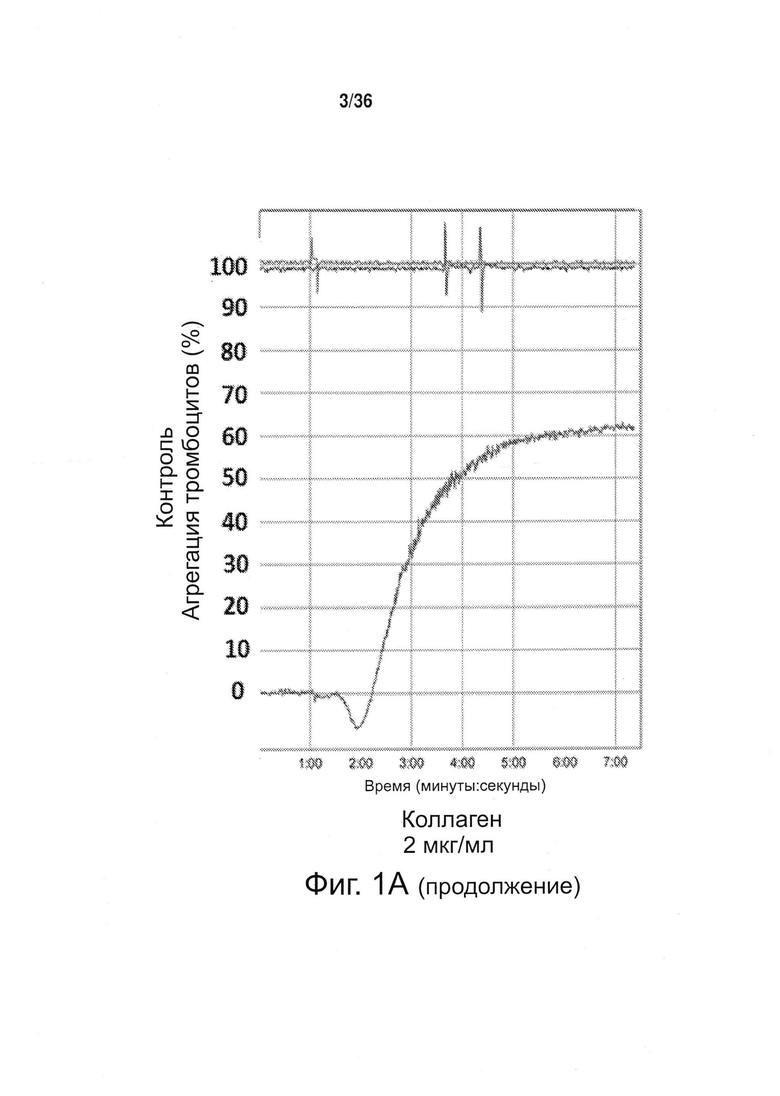
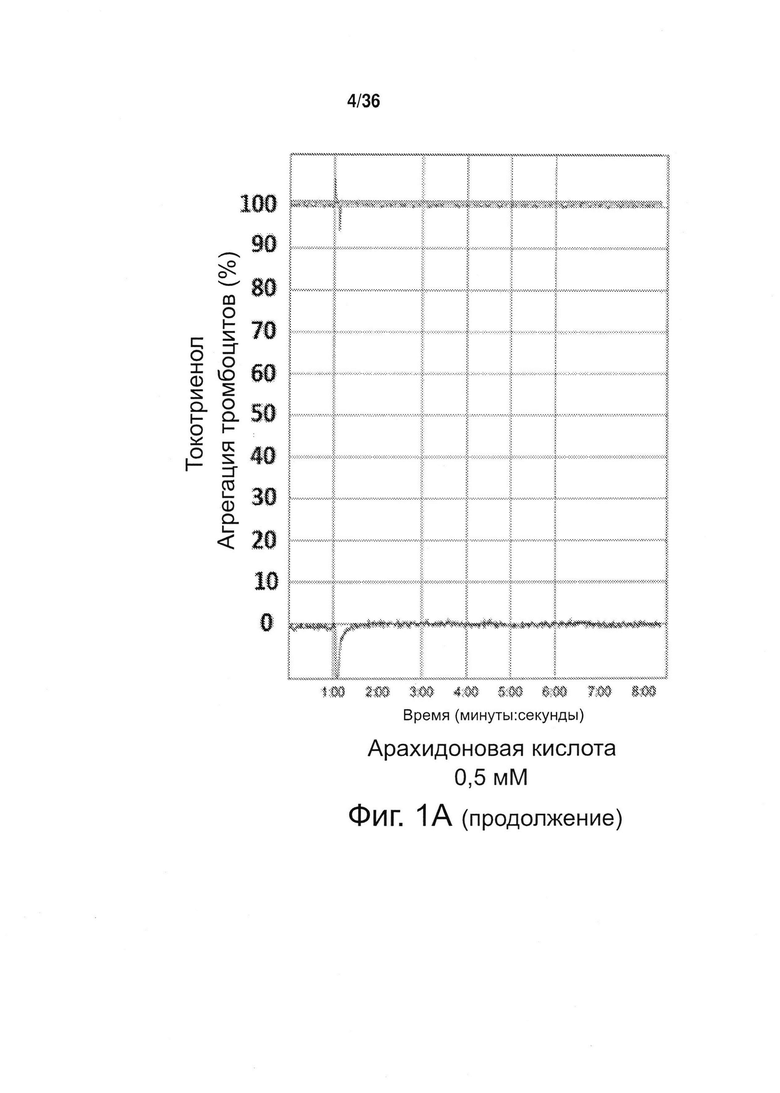
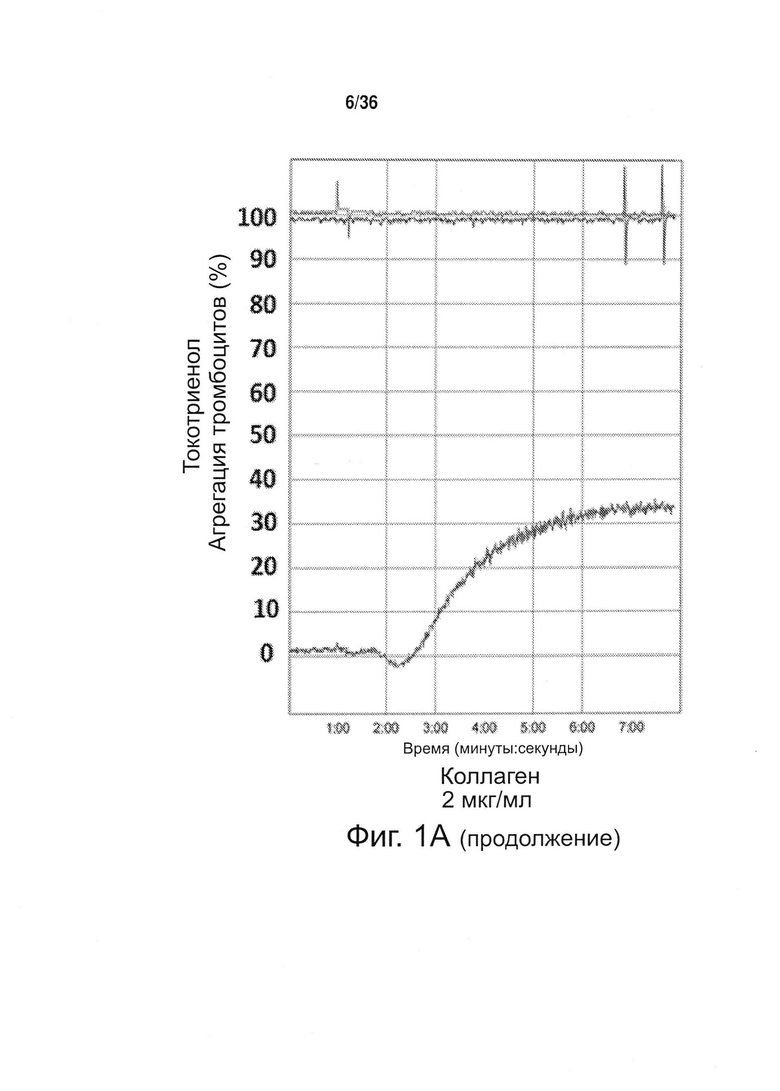
Фиг. 1. Противодействие токотриенола витамина Ε агрегации тромбоцитов в человеческой крови. Здоровые пациенты на протяжении 4 недель получали токотриенол витамина Ε (400 мг/сут) либо носитель в качестве плацебо (контроль). Функцию тромбоцитов определяли путем оптической агрегометрии, используя следующие агонисты: арахидоновую кислоту (АА; 0,5 мМ), аденозиндифосфат (ADP; 10 мкМ) и коллаген (2 мкг/мл). А. Примерные кривые изменения функции тромбоцитов у пациентов, получавших плацебо (контроль) и токотриенолы (ТСТ). В. Токотриенол (ТСТ) полностью подавлял опосредуемую арахидоновой кислотой (АА) агрегацию тромбоцитов по сравнению с контролем. Токотриенол (ТСТ) значительно ослаблял агрегацию тромбоцитов при использовании аденозиндифосфата (ADP) и коллагена по сравнению с контролем (42 и 37% соответственно).
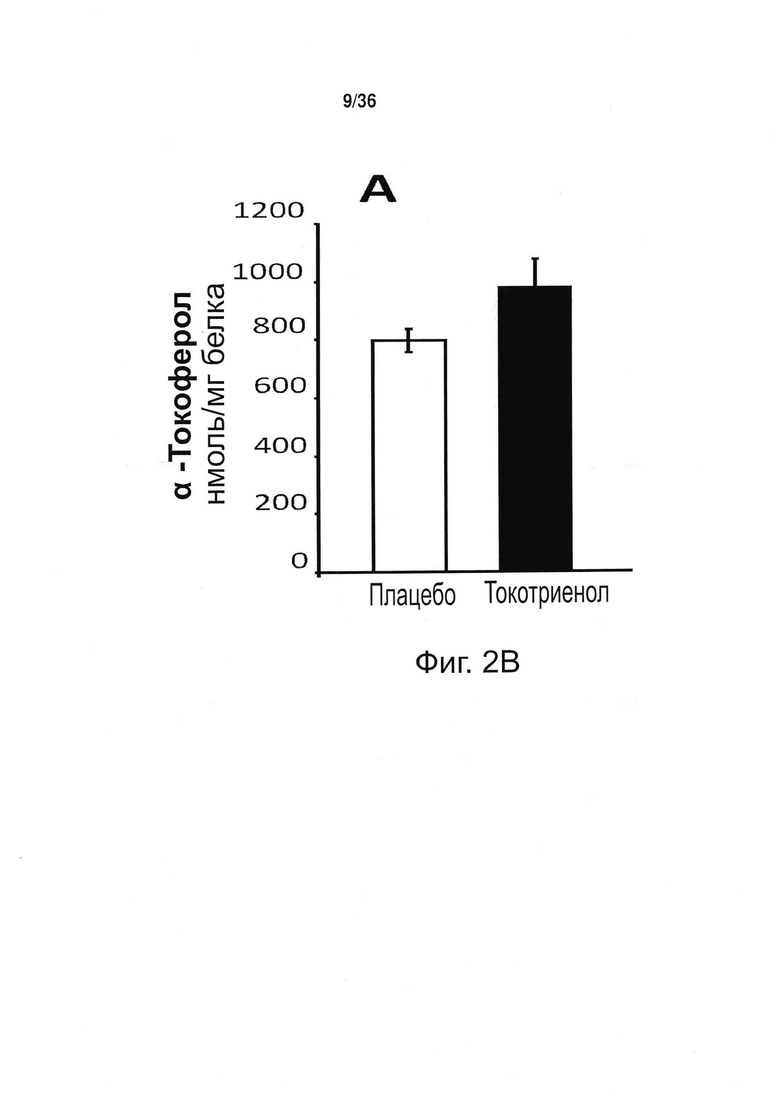
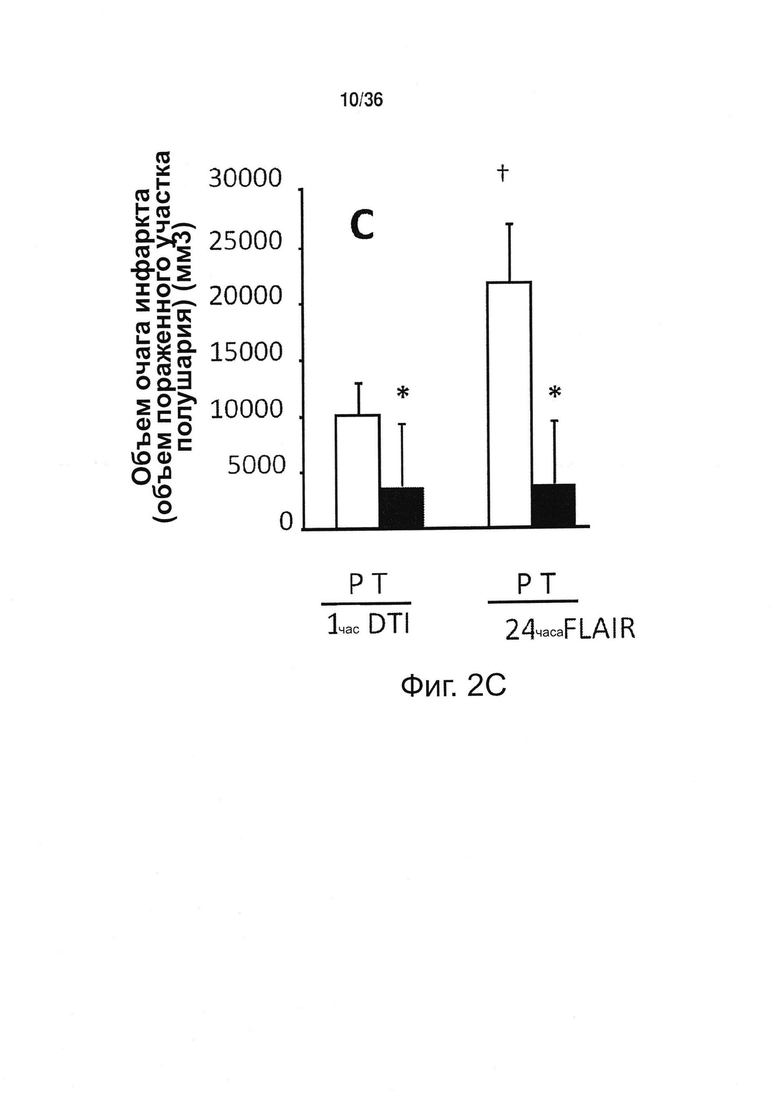
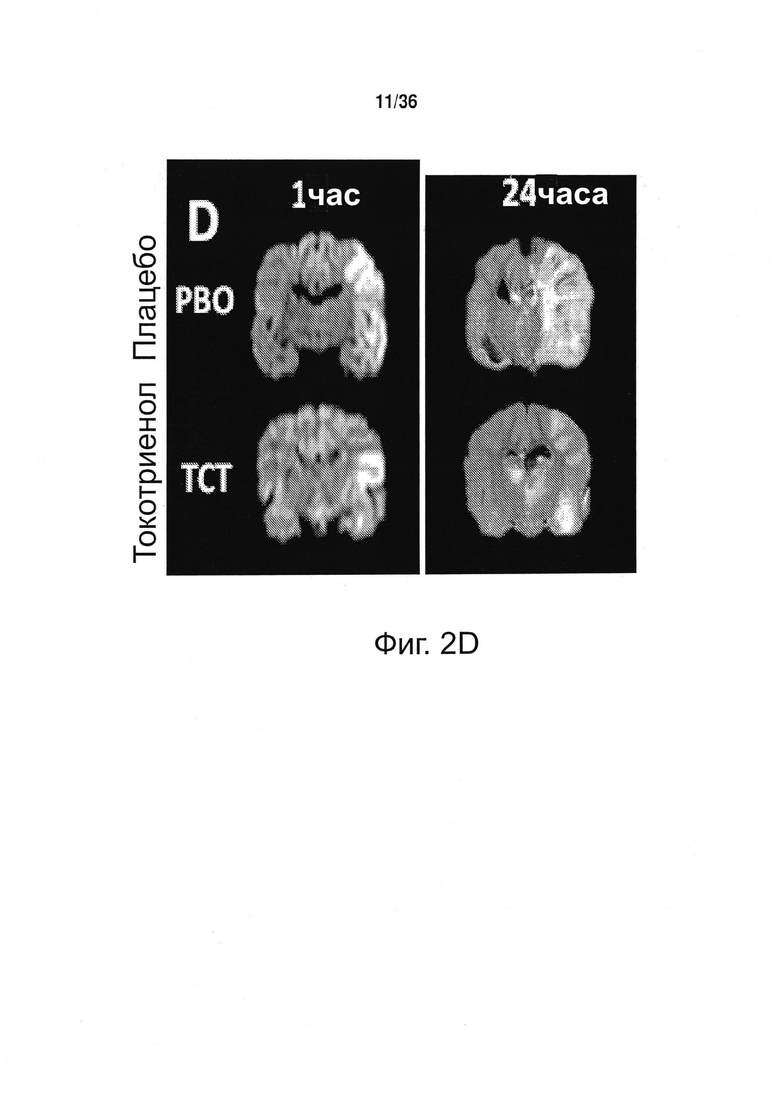
Фиг. 2. Токотриенол природного витамина Ε защищает от связанного с инсультом повреждения мозга. (А и В) Влияние перорального приема токотриенола (ТСТ) либо плацебо (РВО) на концентрацию α-токоферола и α-токотриенола в коре головного мозга у собак. У животных, получавших плацебо, токотриенол в мозге не обнаруживался. Прием токотриенола существенно увеличивал концентрацию α-токотриенола в коре головного мозга. (С) Обусловленный инсультом объем очага инфаркта головного мозга. DTI = диффузионная тензорная визуализация, проведенная через 1 ч FLAIR = инверсия - восстановление с подавлением сигнала от воды, проводили через 24 ч. (D) Примеры изображения головного мозга, полученные путем магнитно-резонансной томографии во фронтальной проекции через 1 ч и через 24 ч после инсульта. *p<0,05.
Фиг. 3. Концентрация токотриенола в цельной крови у людей после ежедневного перорального приема токотриенола в дозе 400 мг. Уровни токотриенола (ТСТ) в крови определяли путем высокоэффективной жидкостной хроматографии, как сообщалось10. Представлены идивидуальные значения (мужчины n=6, женщины n=10) и средние значения ± стандартное отклонение (SD) на исходном уровне (0 недель), через 6 недель и через 12 недель. В каждый из указанных моментов времени уровни, обозначенные разными символами, различаются (p<0,05).
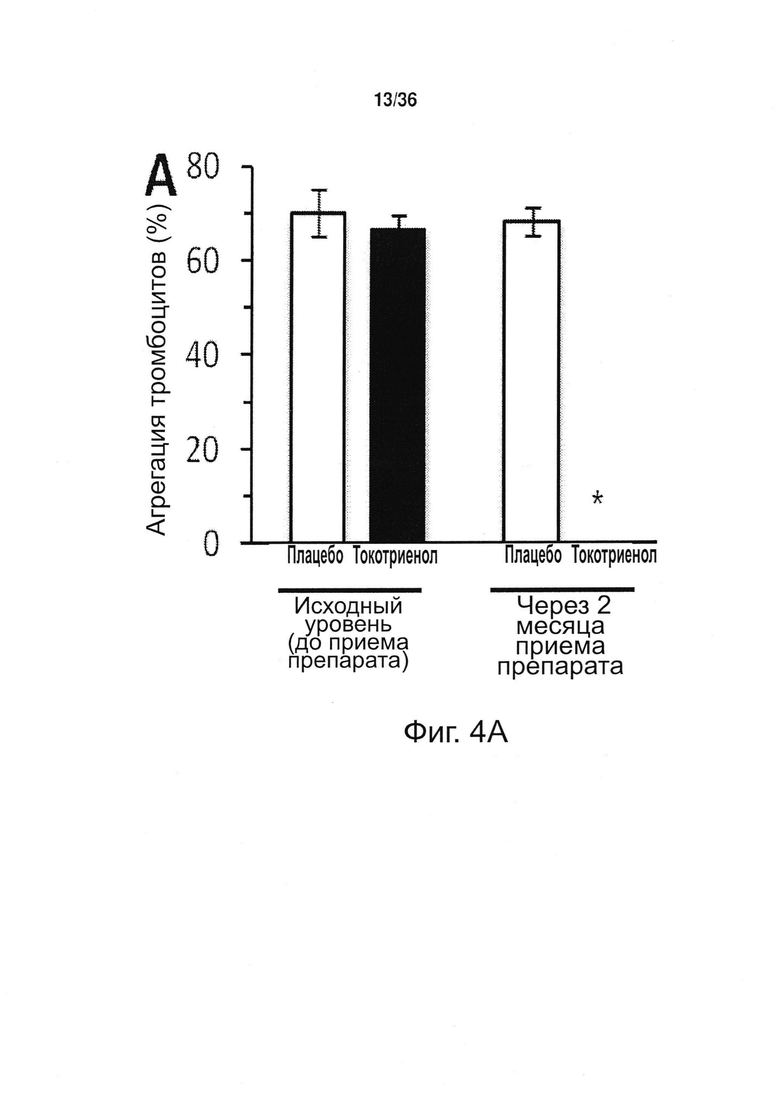
Фиг. 4. Имитирующее эффект аспирина противосвертывающее действие токотриенола природного витамина Е. Определяли функцию тромбоцитов у здоровых пациентов (n=3) в исходном состоянии и после перорального приема токотриенола (ТСТ) в дозировке 400 мг/сут либо плацебо (РВО) на протяжении 2 месяцев. (А) Определение агрегации (%) тромбоцитов путем оптической агрегометрии с арахидоновой кислотой в качестве агониста агрегации (АА, 0,5 мМ). Этот же агонист использовали для определения изменения функции тромбоцитов в ответ на аспирин. *p<0,05 для РВО по сравнению с ТСТ в данный момент времени. (В и С) Примеры регистрации светопропускания для пациентов, принимавших на протяжении 2 месяцев токотриенол либо плацебо.
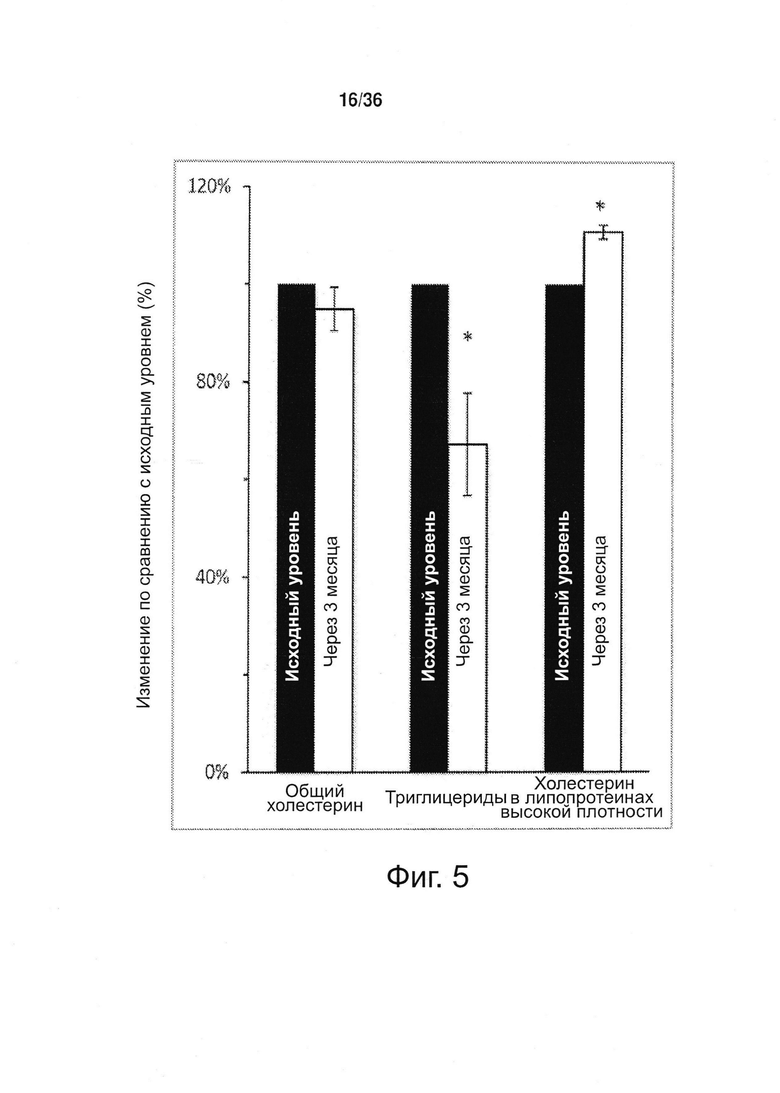
Фиг. 5. Пероральный прием токотриенола вызывает снижение уровня триглицеридов и повышение уровня холестерина в составе липопротеинов высокой плотности (HDL) в крови у здоровых пациентов. Определяли уровень холестерина в крови у здоровых пациентов (n=3) - исходный и спустя 3 месяца, в течение которых испытуемые принимали ежедневно токотриенол в дозе 400 мг. Исходный средний уровень общего холестерина составлял 204,0±11,5. Через 3 месяца приема токотриенола было отмечено умеренное (-5,1%±4,5%), но не существенное снижение уровня общего холестерина; уровень триглицеридов уменьшился значительно - на 32,8%±10,5%, а уровень холестеринам в составе HDL значительно возрос - на 10,8%±1,4% по сравнению с исходными уровнями. *p<0,05 (парный t-критерий Стьюдента).
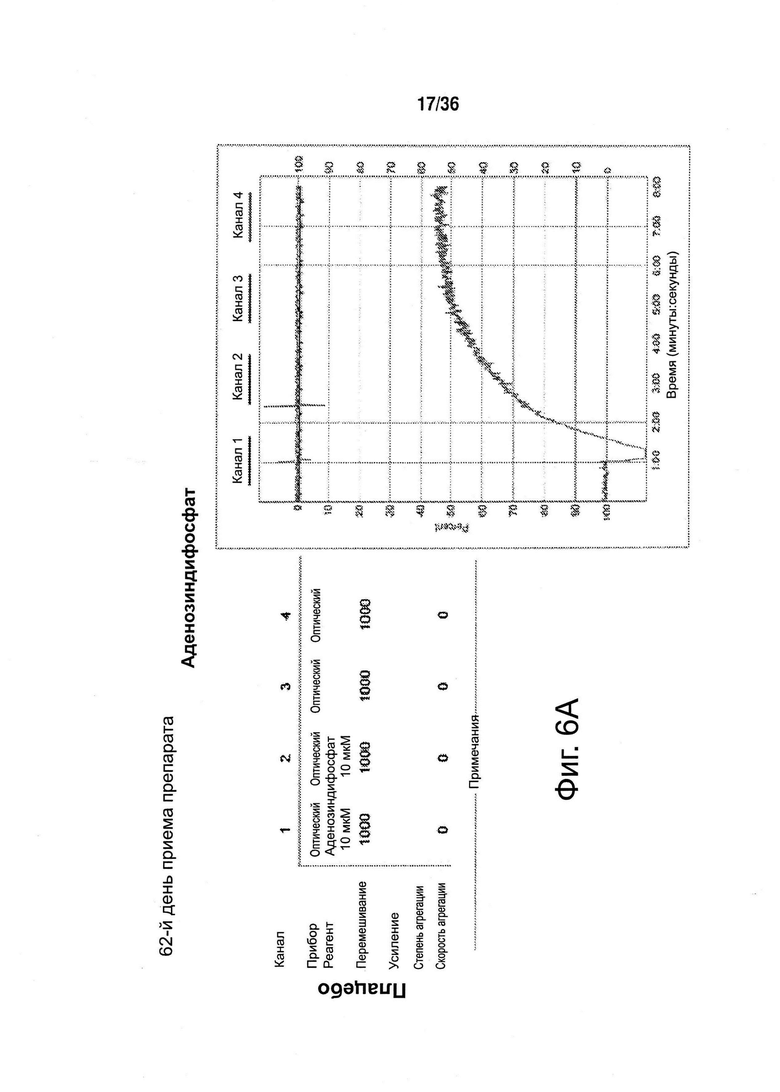
Фиг. 6. Агрегация тромбоцитов, 62-й день приема препарата (токотриенола либо плацебо).
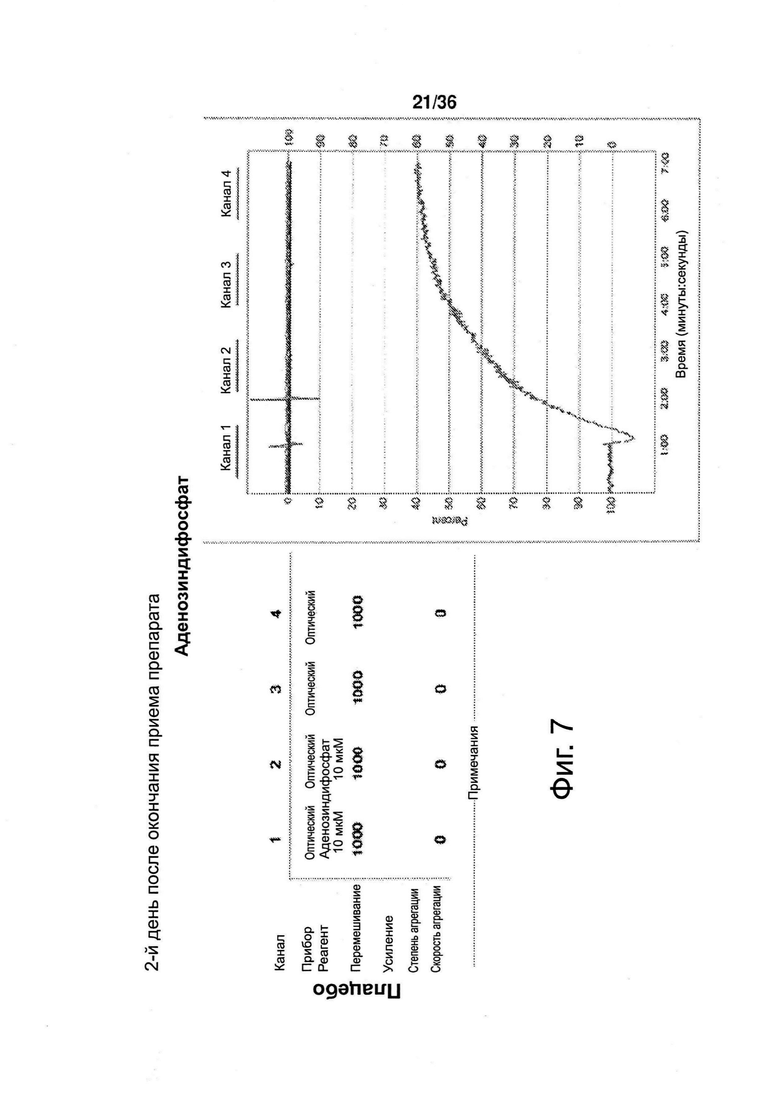
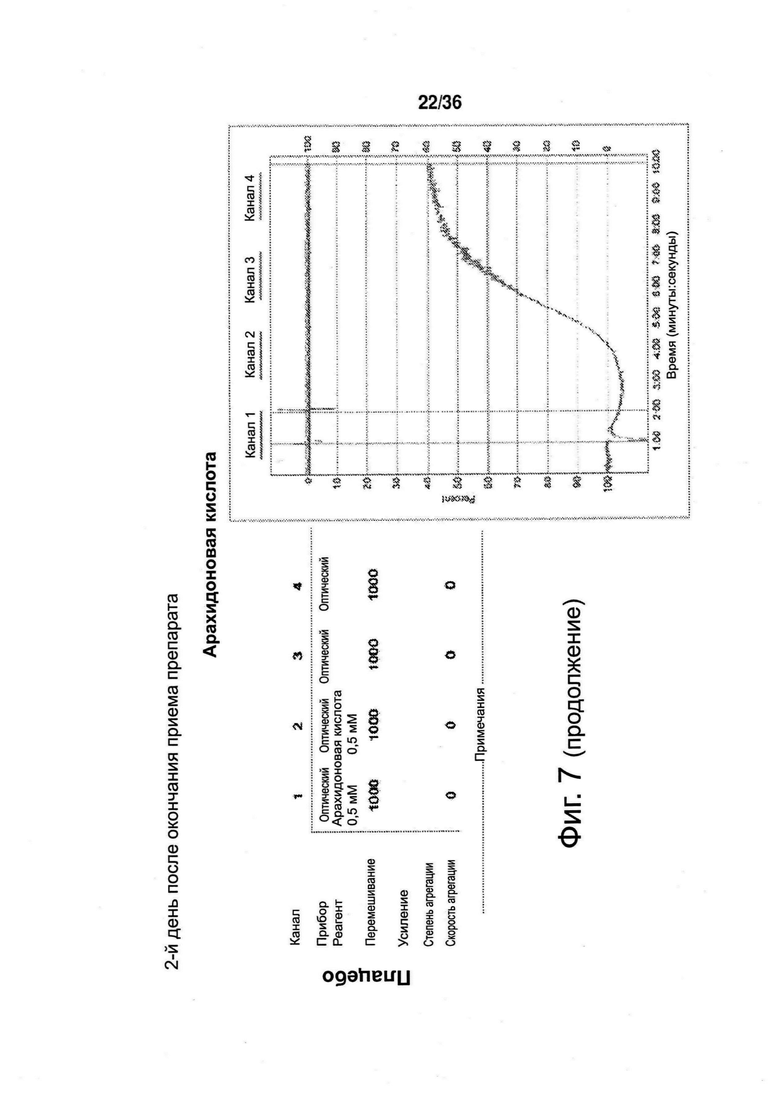
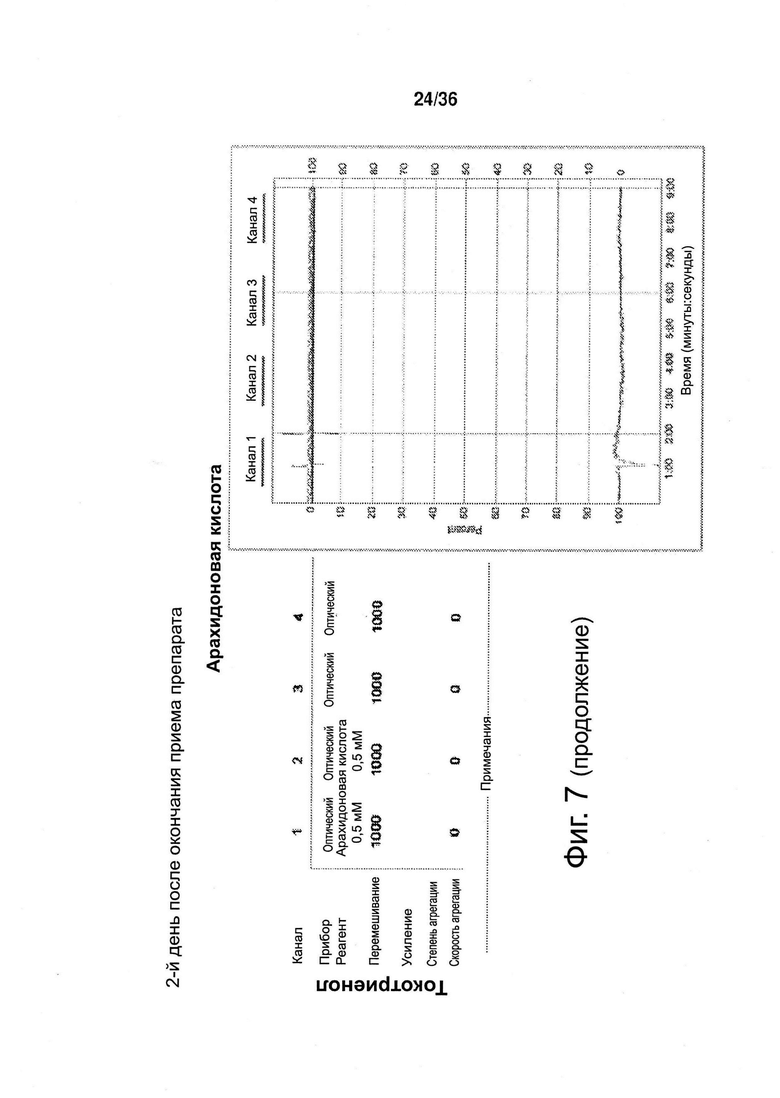
Фиг. 7. Агрегация тромбоцитов, 2-й день после окончания приема препарата (токотриенола либо плацебо).
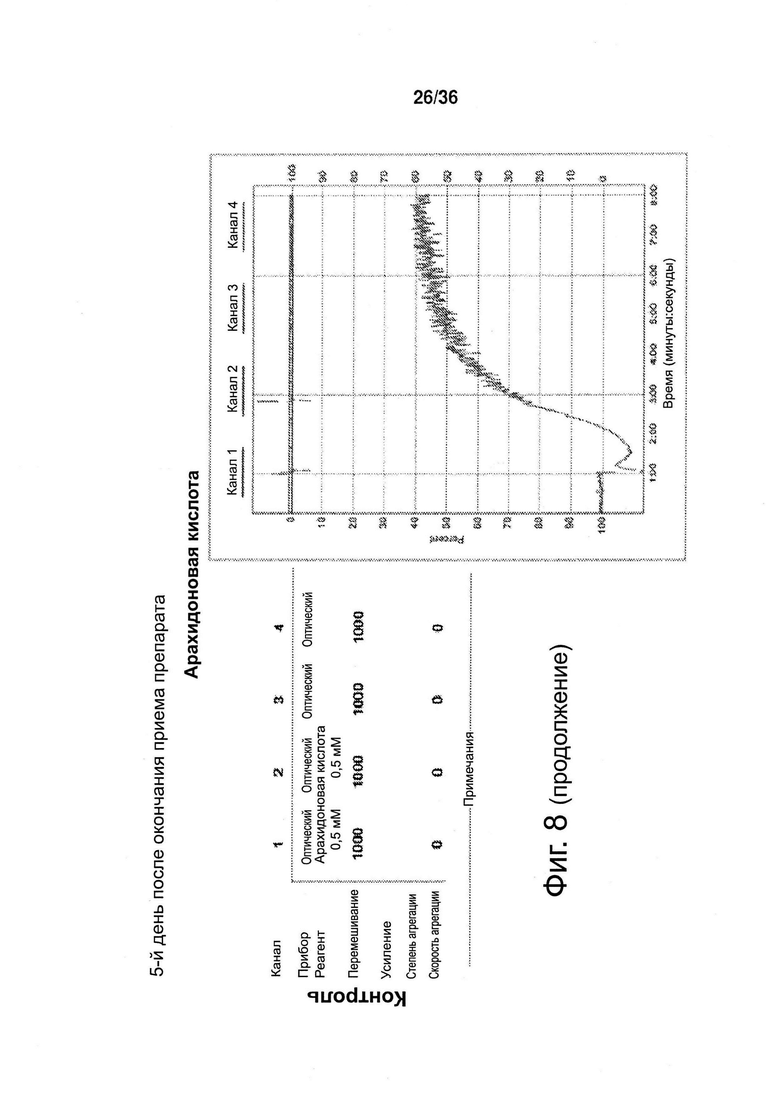
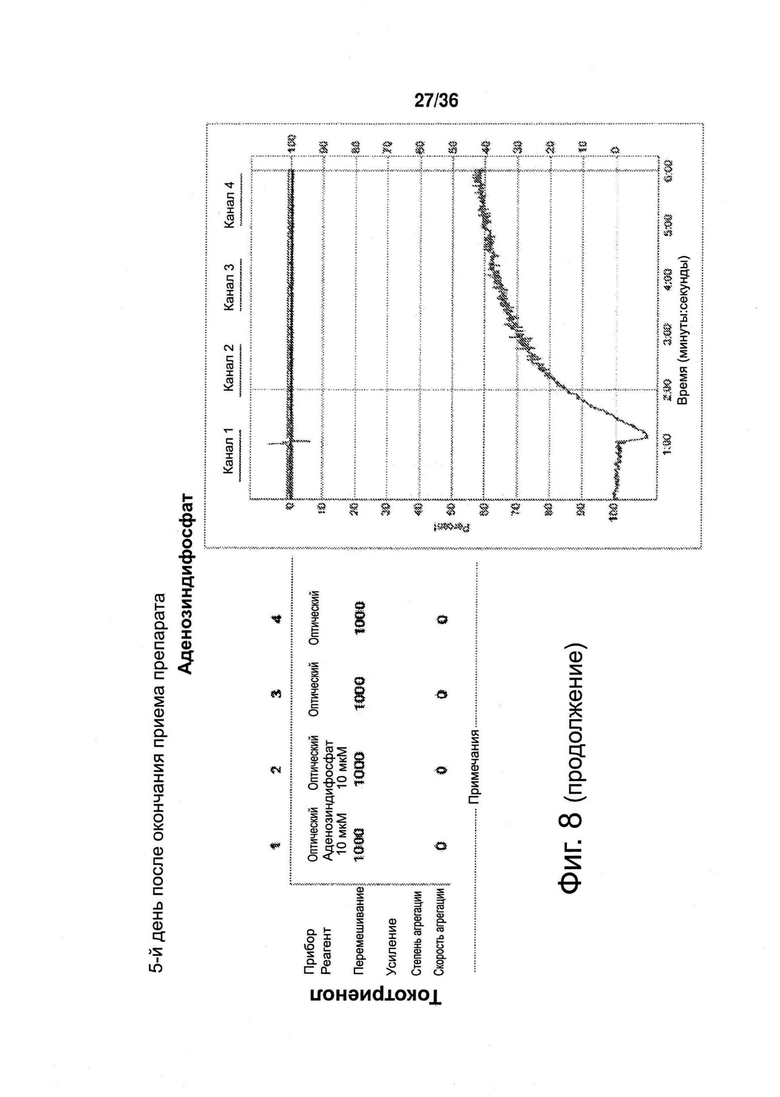
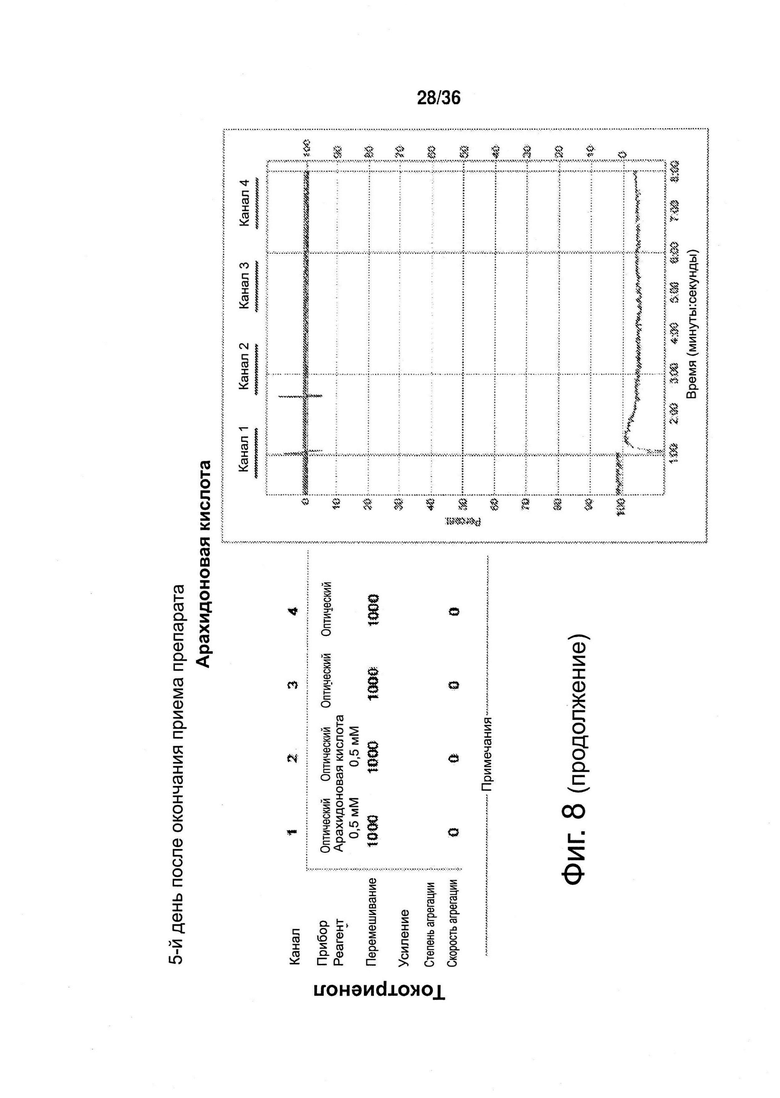
Фиг. 8. Агрегация тромбоцитов, 5-й день после окончания приема препарата (токотриенола либо плацебо).
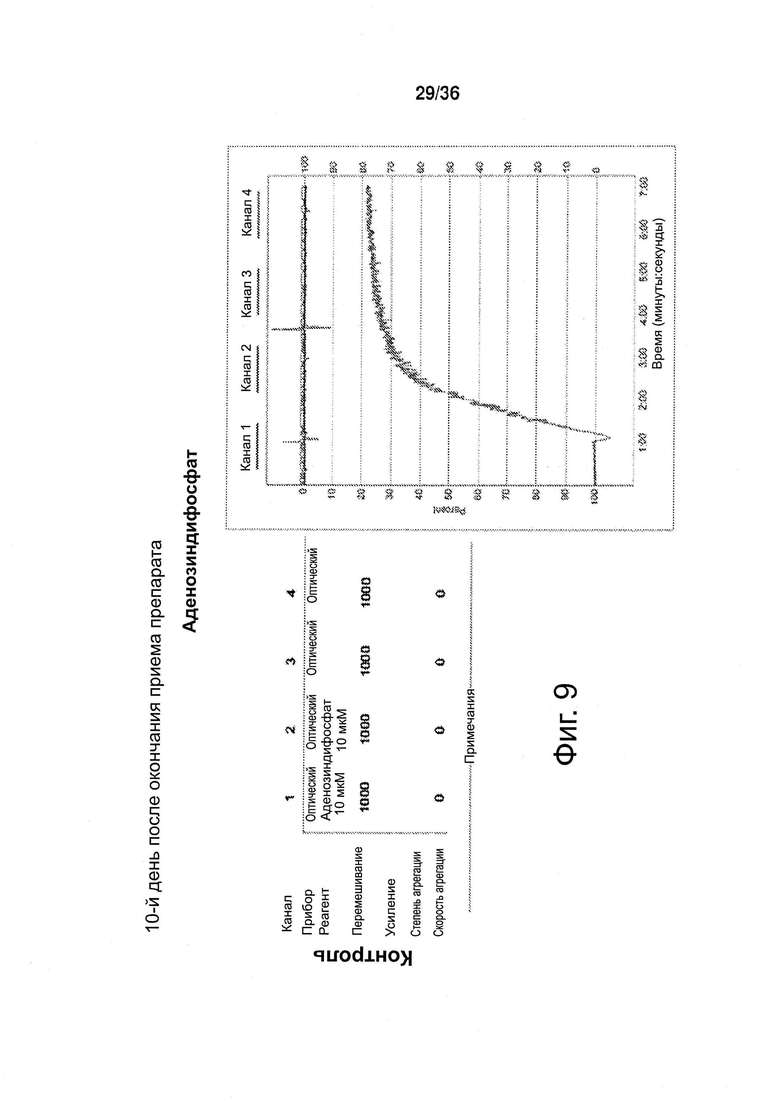
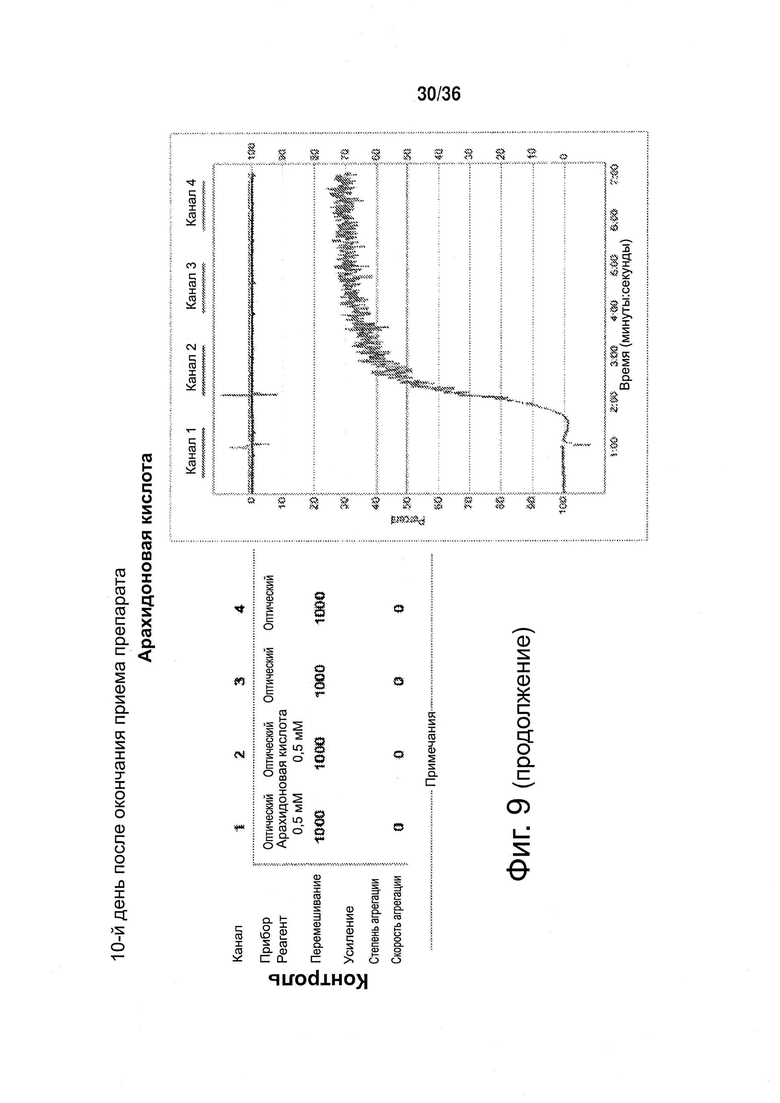
Фиг. 9. Агрегация тромбоцитов, 10-й день после окончания приема препарата (токотриенола либо плацебо).
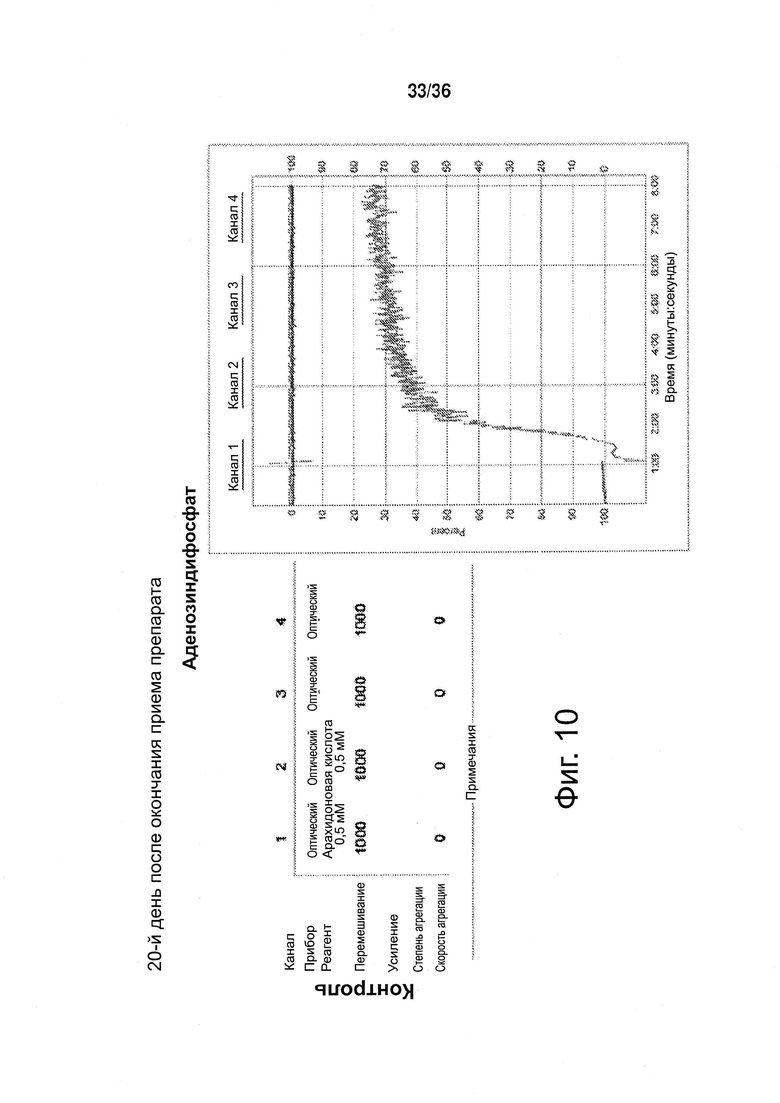
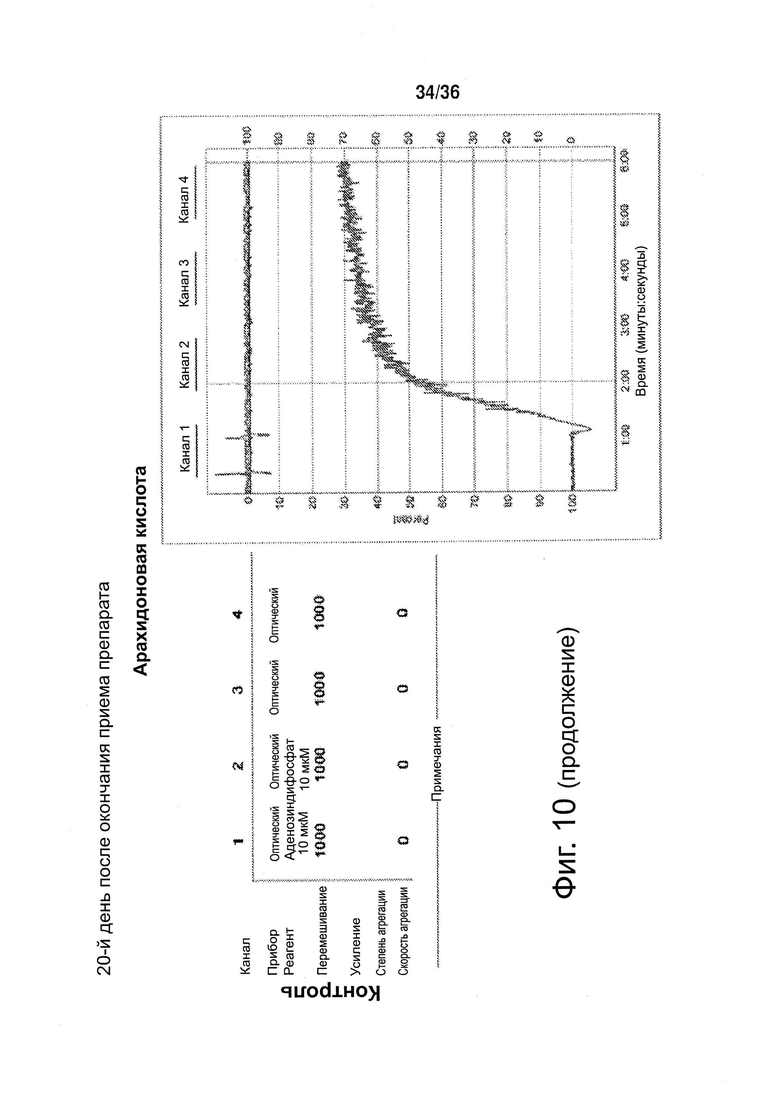
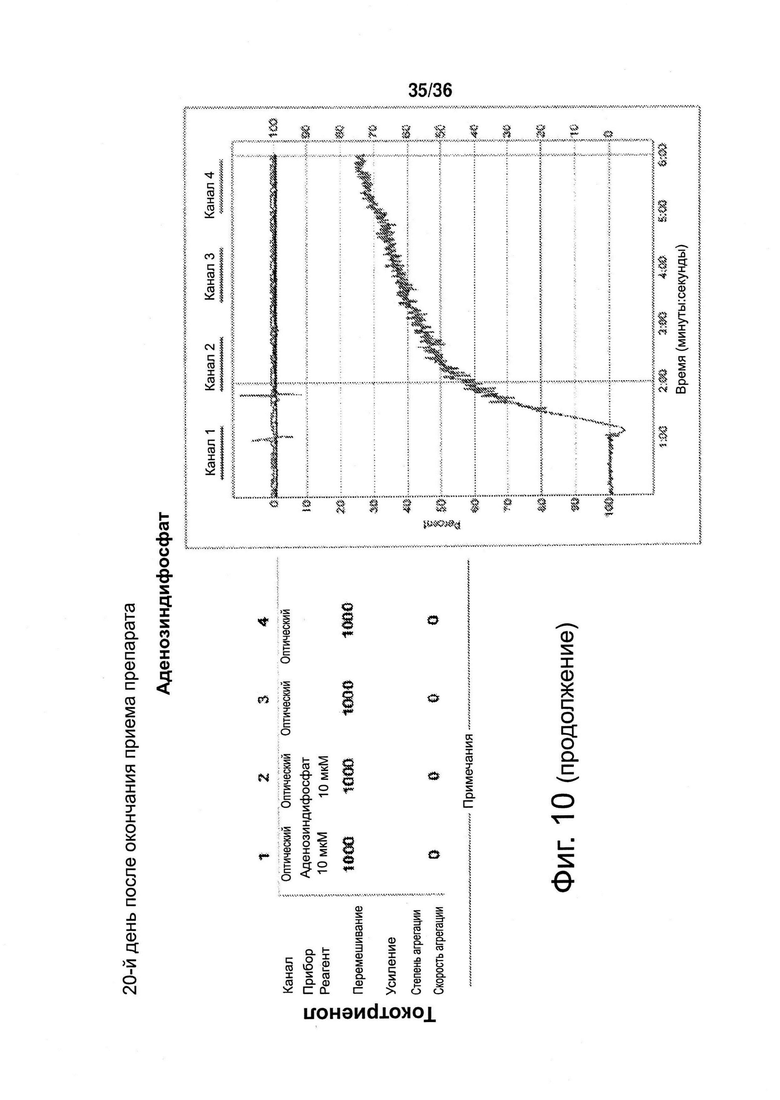
Фиг. 10. Агрегация тромбоцитов, 20-й день после окончания приема препарата (токотриенола либо плацебо).
Осуществление изобретения
Настоящее изобретение позволило идентифицировать конкретные механизмы, определяющие подобные эффекту аспирина свойства изоформы токотриенола природного витамина Е, называемой альфа-токотриенолом (ТСТ), а именно противодействие агрегации тромбоцитов. У человека ТСТ, принимаемый перорально, полностью подавляет опосредованную арахидоновой кислотой агрегацию тромбоцитов. ТСТ также подавляет агрегацию тромбоцитов, индуцированную другими агонистами, в том числе аденозиндифосфатом (ADP) и коллагеном (фиг. 1).
Аспирин обладает рядом побочных эффектов, включая гепатотоксичность и язвенный колит. Кроме того, этот препарат противопоказан при ряде состояний, в том числе при алкоголизме и аллергии на ибупрофен или напроксен. А альфа-токотриенол, будучи изоформой природного токотриенола, содержащейся в пищевых продуктах, в частности в кулинарных маслах (например, в пальмовом масле), одобрен Управлением по контролю качества пищевых продуктов, медикаментов и косметических средств США (FDA) для потребления людьми в качестве добавки к пище по категории GRAS (признан безопасным).
У 25% людей аспирин не оказывает антиагрегантного действия. Механизм действия аспирина состоит в ацетилировании активного центра циклооксигеназ СОХ-1 и СОХ-2, в результате чего подавляется метаболизм арахидоновой кислоты с участием этих ферментов. Мишенью альфа-токотриенола является другой фермент, участвующий в метаболизме арахидоновой кислоты, а именно 12-липоксигеназа (12-LOX). В данном изобретении впервые описывается эффект альфа-токотриенола, состоящий в противодействии агрегации тромбоцитов, с участием липоксигеназного пути. Поскольку механизм противодействия ТСТ агрегации тромбоцитов, опосредованной арахидоновой кислотой, иной, чем аспирина, токотриенол эффективен у тех пациентов, которые устойчивы к аспирину.
Применения данного изобретения в клинической практике и в коммерческих предприятиях включают использование альфа-токотриенола в качестве природного антиагрегантного агента, составляющего альтернативу аспирину и не обладающего замеченными побочными эффектами.
Альфа-токотриенол можно использовать вместо аспирина для противодействия агрегации тромбоцитов у пациентов, для которых аспирин не эффективен, и у тех, кому он противопоказан (например, при алкоголизме или аллергии).
Термины
Следует заметить, что изложенное выше общее описание и нижеследующее подробное описание носят лишь примерный и пояснительный характер, не ограничивая объем приведенных в настоящем документе утверждений. В данной заявке употребление единственного числа включает значение множественного числа, если не оговорено иного.
В настоящем документе при употреблении неопределенного артикля (а/ап) в сочетании с выражениями «содержащий/включающий» в формуле изобретения и/или в описании может подразумеваться значение «один», но также и значения «один или более», «по меньшей мере один» и «один или более чем один».
В настоящем документе слова «содержать», «включать» и их производные («содержащий», «включающий» и др.) не следует понимать как имеющие ограничительный характер. Оборот «и/или» означает, что указанное перед ним и после него можно объединить или рассматривать раздельно. Например, "X и/или Y" может означать "X либо Y" или же "X и Y" (данный пример не имеет ограничительного характера).
Выражение «их сочетания/комбинации» в настоящем документе относится ко всем перестановкам и сочетаниям объектов, перечисленных перед этим выражением. Например, фраза «А, В, С или их сочетания/комбинации» подразумевает, что в рассмотрение включен по меньшей мере один вариант из следующих: А, В, С, АВ, АС, ВС или ABC, а если в данном контексте имеет значение порядок объектов, то также ВА, СА, СВ, АСВ, СВА, ВСА, ВАС или CAB.
Пациент/индивид. В настоящем документе термин «пациент» включает человека и животных. Предпочтительно лечение применялось к пациентам-людям. Термины «пациент» и «индивид» употребляются в настоящем документе взаимозаменяемо.
Фармацевтически приемлемые носители/средства доставки. В настоящем изобретении используются обычные в данной области техники носители (средства доставки). В работе Remington's Pharmaceutical Sciences, by Ε.W. Martin, Mack Publishing Co., Easton, PA, 15th Edition (1975), описываются композиции и составы, пригодные для фармацевтической доставки одного или более лечебных субстанций, веществ или агентов.
Вообще говоря, природа взятого для композиции носителя зависит от того, какой конкретно используется путь введения препарата. Например, в составы для парентерального введения обычно в качестве носителя (средства доставки) входят жидкости, пригодные для инъекций, что включает фармацевтическим и физиологически приемлемые жидкости, например воду, физиологический солевой раствор, сбалансированные солевые растворы, водный раствор декстрозы, глицерин или другие подобные компоненты. Твердые композиции (например, порошки, пилюли, таблетки или капсулы) могут включать обычно применяемые нетоксичные твердые носители, например фармацевтически чистые маннит, лактозу, крахмал или стеарат магния. Помимо биологически нейтральных носителей фармацевтические композиции для введения в организм могут содержать небольшие количества нетоксичных вспомогательных веществ, например увлажняющие или эмульгирующие агенты, консерванты, забуферивающие агенты и проч., например ацетат натрия или сорбитан-монолаурат.
Предотвращение, лечение или ослабление заболевания. Термин «предотвращение/профилактика» заболевания относится к подавлению всего развития заболевания. Термин «лечение» относится к лечебному/терапевтическому вмешательству, ослабляющему симптомы/признаки/проявления заболевания или патологическое состояние, возникающее после начала развития заболевания. Термин «ослабление/облегчение» относится к снижению количества или тяжести симптомов/признаков/проявлений заболевания.
Терапевтический. Это обобщающий термин, который включает как диагностику, так и лечение.
Терапевтический агент. Под терапевтическим агентом понимается композиция, способная вызвать желаемый лечебный или профилактический эффект при адекватном введении пациенту. «Инкубация» подразумевает промежуток времени, достаточный для взаимодействия агента с клеткой или тканью. «Контактирование» подразумевает инкубацию агента в твердой или жидкой форме с клетками или тканями. «Обработка» клетки или ткани агентом подразумевает контактирование или инкубацию агента с клеткой или тканью.
Терапевтически эффективное количество. Количество конкретного фармацевтического или терапевтического агента, достаточное для достижения желаемого эффекта у пациента или в клетке при обработке данным агентом. Эффективное количество агента зависит от ряда факторов, включая (но не ограничиваясь перечисленным здесь) природу обрабатываемого объекта (пациент, клетка и проч.) и способ введения терапевтической композиции.
Фармацевтические препараты
Фармацевтические композиции по данному изобретению содержат эффективное количество соединения (соединений) или композиции (композиций), описанных в настоящем документе, и/или дополнительные агенты, растворенные или диспергированные в фармацевтически приемлемом носителе. Определения «фармацевтический» или «фармакологически приемлемый» относятся к веществам и композициям, которые будучи введены в организм человека или животного, не вызывают у него негативных, аллергических или иных нежелательных реакций. В свете настоящего описания и на примерах, приведенных в работе Remington's Pharmaceutical Sciences, 2003, включаемой в настоящий документ путем отсылки, получение фармацевтических композиций, содержащих по меньшей мере одно вещество или дополнительный активный ингредиент, должно быть ясно специалистам в данной области техники. Кроме того, препараты для введения человеку или животным должны отвечать требованиям стерильности, пирогенности и общей безопасности, а также стандартам чистоты, согласно установлениям Отдела стандартов и качества биологических препаратов FDA.
В настоящем документе понятие «фармацевтически приемлемый носитель» включает любые и все растворители, дисперсионные среды, оболочки, поверхностно-активные вещества, антиоксиданты, консерванты (например, антибактериальные агенты, противогрибковые агенты), агенты, обеспечивающие нужное осмотическое давление (изотонические), агенты, замедляющие абсорбцию, соли, консерванты, лекарственные вещества, агенты, стабилизирующие лекарственные вещества, гели, связующие агенты, дезинтегрирующие агенты, агенты, улучшающие скольжение, подсластители, ароматизаторы, красители и другие эксципиенты, а также подобные материалы и их комбинации, которые должны быть известны рядовым специалистам в данной области техники (см., например, работу Remington's Pharmaceutical Sciences, 995, pp. 1289-1329, включаемую в настоящий документ путем отсылки). За исключением тех случаев, когда обычно используемый носитель не совместим с активным ингредиентом, его применение в фармацевтических композициях подразумевается.
Композиция по данному изобретению может содержать носители различного типа в зависимости от того, в какой форме она должна быть введена пациенту - твердой, жидкой или аэрозольной, и есть ли необходимость в ее стерильности, как, например, при введении путем инъекций. Композиция по данному изобретению может быть введена внутривенно, внутрикожно, подкожно, интратекально, интраартериально, внутрибрюшинно, интраназально, интравагинально, интраректально, местно, внутримышечно, подкожно, в слизистую оболочку, перорально, местно, локально, путем вдыхания (например, путем вдыхания аэрозоля), путем инъекции, инфузии, непрерывной инфузии, локальной непосредственной перфузии клеток-мишеней, через катетер, путем лаважа, в составе крема, в составе липидной конструкции/композиции (например, в липосомах) или другим способом, или путем сочетания перечисленных выше способов, которые должны быть известны рядовому специалисту в данной области техники (см., например, работу Remington's Pharmaceutical Sciences, 2003, включаемую в настоящий документ путем отсылки).
Также по данному изобретению предлагаются композиции, пригодные для введения в фармацевтически приемлемом носителе с инертным разбавителем (или без него). Указанный носитель, включая жидкие, твердые и полужидкие (например, пасты) носители, должен быть усвояемым. За исключением тех случаев, когда какой-либо обычно используемый агент, разбавитель, среда или носитель вреден для данного пациента или снижает терапевтическую эффективность содержащей его композиции, допустимо применение указанных ингредиентов в композиции, подлежащей введению пациентам, при практическом осуществлении способа по данному изобретению. Примеры носителей или разбавителей включают жиры, масла, воду, солевые растворы, липиды, липосомы, смолы, связующие агенты, наполнители и проч. или их комбинации. Композиция по данному изобретению может также содержать различные антиоксиданты для замедления окисления одного или более ее компонентов. Кроме того, можно предотвратить воздействие микроорганизмов при помощи таких консервантов, как различные антибактериальные и противогрибковые агенты, включая (но не ограничиваясь перечисленным здесь) парабены (например, метилпарабены, пропилпарабены), хлорбутанол, фенол, сорбиновую кислоту, тимеросал или их комбинации.
Композицию по данному изобретению объединяют с носителем любым удобным и практичным способом, например, путем растворения, суспендирования, эмульгирования, подмешивания, заключения в капсулы, абсорбции и проч. Такие способы обычны для специалистов в данной области техники.
В одном из конкретных воплощений данного изобретения композицию объединяют или тщательно смешивают с твердым или полужидким носителем. Их смешивание может осуществляться любым удобным способом, например путем растирания. В процессе смешивания можно также добавлять стабилизирующие агенты, чтобы защитить композицию от потери терапевтической активности, например в результате денатурации в желудке. Примеры стабилизирующих агентов для использования в композициях по данному изобретению включают забуферивающие вещества, аминокислоты (например, глицин и лизин), углеводы (например, декстрозу, маннозу, галактозу, фруктозу, лактозу, сахарозу, мальтозу, сорбит, маннит и др.).
В других воплощениях данного изобретения фармацевтическая композиция может включать в небольших количествах фармакологически приемлемые хелатирующие агенты или коантиоксиданты. Примеры хелатирующих агентов включают этилендиаминтетрауксусную кислоту (EDTA) и этиленгликоль-бис(бета-аминоэтиловый эфир)-N,N,N',N'-тетрауксусную кислоту (EGTA). Примеры антиоксидантов включают эфиры галловой кислоты, аскорбиновую кислоту, витамин Ε (или другие токоферолы), бутилгидрокситолуол и/или бензойную кислоту. Эти хелатирующие агенты и/или коантиоксиданты можно использовать для стабилизации композиций по данному изобретению. В некоторых воплощениях данного изобретения эти хелатирующие агенты и/или антиоксиданты могут стабилизировать композиции по данному изобретению от разложения в результате самоокисления.
В других своих воплощениях данное изобретение касается применения фармацевтических липидных средств доставки, заключающих в себе композицию по данному изобретению, один или более липидов и водный растворитель. В настоящем документе термин «липид» включает любое из широкого спектра веществ, отличающихся тем, что они нерастворимы в воде и экстрагируются органическими растворителями. Специалистам в данной области техники должно быть ясно, о каких веществах идет речь, и в настоящем документе употребление термина «липид» не ограничено какой-либо конкретной структурой. Примеры липидов включают соединения, содержащие длинноцепочечные алифатические углеводороды, и их производные. Липиды могут быть природными или синтетическими (например, созданными или полученными человеком). Впрочем, под липидом обычно подразумевается биологическое вещество. Липиды биологического происхождения хорошо известны в данной области техники; они включают, например, нейтральные жиры, фосфолипиды, фосфоглицериды, стероиды, терпены, лизолипиды, гликосфинголипиды, гликолипиды, сульфатиды, эфиры жирных кислот, полимеризующиеся липиды и их комбинации. Как должно быть ясно специалистам в данной области техники, в композиции и способы по данному изобретению могут входить также другие соединения такого рода, не упомянутые конкретно в настоящем документе.
Рядовому специалисту в данной области техники знакомы различные методы, применяемые для включения композиции в липидное средство доставки. Например, композиция по данному изобретению может быть диспергирована в растворе, содержащем липиды, растворена в липиде, эмульгирована с липидом, смешана с липидом, объединена с липидом, ковалентно связана с липидом, взвешена в липиде, содержатся в липидной мицелле или липосоме, образовывать с ней комплекс или иным образом ассоциирована с липидом или липидной структурой любыми средствами, известными рядовому специалисту в данной области техники. Диспергирование может приводить (или не приводить) к образованию липосом.
На практике доза (вводимое количество) композиции по данному изобретению для конкретного пациента (животного) может определяться такими физическими и физиологическими факторами, как масса тела, степень тяжести патологического состояния, характер подлежащего лечению заболевания, предыдущие или текущие терапевтические вмешательства, идиопатичность заболевания/состояния у данного пациента и путь введения композиции. В зависимости от дозировки и пути введения число приемов предпочтительной дозы и/или эффективного количества может варьировать соответственно реакции пациента. На практике медицинский работник, осуществляющий введение препарата, в любом случае определяет концентрацию активного ингредиента (ингредиентов) в композиции и подходящую для данного пациента дозу (дозы).
Разумеется, количество активного ингредиента (ингредиентов) в каждой терапевтически полезной композиции может быть подобрано таким образом, чтобы с любой единичной дозой достигалась подходящая дозировка нужного вещества. При составлении таких фармацевтических композиций специалисту в данной области техники следует учитывать такие факторы, как растворимость, биологическая доступность, время полужизни, путь введения, срок хранения препарата, а также другие фармакологически значимые показатели; при этом могут быть желательны различные дозировки и схемы лечения.
Композиции для алиментарного применения и их состав
В некоторых воплощениях данного изобретения описываемые в настоящем документе композиции и/или дополнительные агенты составляют и получают таким образом, чтобы их введение в организм происходило алиментарным путем. Алиментарный путь введения включает всевозможные способы введения, при которых фармацевтическая композиция оказывается в непосредственном контакте с пищеварительным трактом. А именно, описываемые в настоящем документе фармацевтические композиции могут вводиться перорально, буккально, ректально или подъязычно. При этом в состав указанных композиций входит инертный разбавитель или усваиваемый съедобный носитель, или же композиция может быть заключена в жесткие или полужесткие желатиновые капсулы, или она может быть в виде прессованных таблеток, или же она может входить в состав пищевого продукта.
В некоторых воплощениях данного изобретения активные вещества могут быть включены вместе с теми или иными эксципиентами в состав таблеток, подлежащих проглатыванию или же рассасыванию в полости рта, пастилок, капсул, эликсиров, суспензий, сиропов, облаток и проч. (Mathiowitz et al., 1997; Hwang et al., 1998; патенты США №5641515, №5580579 и №5792451; каждая из этих работ полностью включается в настоящий документ путем отсылки). Таблетки, пастилки, пилюли, капсулы и подобные лекарственные формы могут также содержать следующие компоненты: связующие агенты, например трагакантовую камедь, аравийскую камедь, кукурузный крахмал, желатин или их комбинации; другие эксципиенты, например двузамещенный фосфорнокислый кальций, маннит, лактозу, крахмал, стеарат магния, сахарин (сахаринат натрия), целлюлозу, карбонат магния или их комбинации; дезинтегрирующие агенты, например кукурузный крахмал, картофельный крахмал, альгиновую кислоту или их комбинации; агенты, улучшающие скольжение, например стеарат магния; подсластители, например сахарозу, лактозу, сахарин или их комбинации; ароматизирующие агенты, например перечную мяту, масло грушанки (винтергриновое), вишневый ароматизатор, апельсиновый ароматизатор и проч. Если лекарственной формой являются капсулы, то они могут содержать в дополнение к указанным выше веществам жидкий носитель. Могут использоваться также различные другие материалы для создания оболочки или иной физической модификации лекарственной формы. Например, таблетки, пилюли или капсулы могут быть покрыты шеллаком, сахаром или тем и другим вместе. Если лекарственной формой являются капсулы, то они могут содержать в дополнение к указанным выше веществам жидкий носитель. Желатиновые капсулы, таблетки или пилюли могут быть покрыты кишечнорастворимой оболочкой. Кишечнорастворимая оболочка предотвращает разложение композиции в желудке и в верхней части кишечника, где рН кислый (см., например, патент США №5629001). Когда препарат доходит до тонкого кишечника, где рН щелочной, оболочка растворяется, так что композиция высвобождается и поглощается специализированными клетками, например клетками эпителия кишечника и М-клетками пейеровых бляшек. Сироп или эликсир может содержать активное вещество, сахарозу в качестве подсластителя, метил- и пропилпарабены в качестве консервантов, краситель и ароматизирующий агент, например вишневый или апельсиновый ароматизатор. Разумеется, любые вещества и материалы, используемые для получения любых лекарственных форм, должны быть пригодными для фармацевтического применения степени чистоты и в используемых количествах практически не токсичными. Кроме того, активные вещества могут включаться в препараты и композиции с замедленным высвобождением.
Для перорального введения композиции по данному изобретению могут вместе с одним или более эксципиентами входить в состав полоскания для полости рта, зубного эликсира, таблеток для рассасывания, спрея для полости рта или пероральных препаратов, принимаемых подъязычно. Например, полоскание для полости рта может включать активный ингредиент в необходимом количестве подходящего растворителя, например раствора буры (раствора Добелла). Или же активный ингредиент может входить в состав раствора для применения в полости рта, например раствора, содержащего буру, глицерин и бикарбонат калия, или зубного эликсира, или может быть добавлен в терапевтически эффективном количестве в композицию, включающую воду, связующие агенты, абразивный материал, ароматизирующие агенты, пенообразующие агенты и увлажняющие агенты. Или же указанные композиции могут быть включены в состав таблеток или растворов для рассасывания под языком или растворения в полости рта иным способом.
Кроме того, композиции, пригодные для других способов алиментарного введения, включают суппозитории. Суппозитории - это твердая лекарственная форма для введения в прямую кишку; они могут быть различными по массе и форме и обычно содержат лекарственный компонент. Будучи введен в прямую кишку, суппозиторий размягчается, тает или растворяется в содержимом кишки. Как правило, обычно используемые в суппозиториях носители включают, например, полиалкиленгликоли, триглицериды или их сочетания.
Композиции для парентерального применения и их состав
В других воплощениях данного изобретения предлагаемые композиции вводят пациентам парентеральным путем. В настоящем документе термин «парентеральный путь введения» включает способы введения препарата помимо пищеварительного тракта. А именно, описываемые в настоящем документе фармацевтические композиции могут быть введены пациенту следующими способами (не ограничиваясь перечисленным здесь): внутривенно, внутрикожно. внутримышечно, интраартериально, интратекально, подкожно или внутрибрюшинно.
Для парентерального введения готовят пригодные для инъекций стерильные растворы, содержащие активные соединения в требующемся количестве подходящего растворителя и различные другие ингредиенты, перечисленные выше, в нужных количествах; стерилизацию проводят путем фильтрования. Как правило, дисперсии готовят, включая различные стерилизованные активные ингредиенты в стерильное средство доставки, содержащее основную дисперсионную среду и другие ингредиенты, перечисленные выше. В случае стерильных порошков для приготовления стерильных растворов, пригодных для инъекций, предпочтительными методами получения являются высушивание под вакуумом и лиофилизация; в результате из предварительно полученного раствора, стерилизованного путем фильтрования, получают порошок активного ингредиента и любой дополнительный желаемый ингредиент. Композицию в форме порошка объединяют с жидким носителем, например водой или солевым раствором, содержащим (или не содержащим) стабилизирующий агент.
Фармацевтические композиции различного назначения
В других предпочтительных воплощениях данного изобретения активное соединение входит в состав препаратов для введения различными путями, например для местного (например, трансдермального) применения, для введения через слизистые оболочки (интраназально, интравагинально и проч.) и/или для вдыхания.
В фармацевтических композициях, предназначенных для местного применения, активное вещество может входить в состав препаратов, наносимых на поверхности тела, например мазей, паст, кремов или порошков. Мази включают все композиции на масляной, абсорбционной, эмульсионной или водорастворимой основе для местного применения, а кремы и лосьоны - композиции только на эмульсионной основе.
Медикаменты для местного применения могут содержать усилитель проникновения для облегчения впитывания активных ингредиентов через кожу. Пригодные по данному изобретению усилители проникновения включают глицерин, спирты, алкилметилсульфоксиды, пирролидоны и лаурокапрам. В качестве основы в композициях для местного применения могут служить полиэтиленгликоль, ланолин, кольдкрем и вазелин, а также любые другие подходящие эмульсионные, абсорбционные или водорастворимые мазевые основы. В состав препаратов для местного применения могут также входить эмульгирующие агенты, желирующие агенты и противомикробные консерванты для сохранения активного ингредиента и обеспечения гомогенности смеси. Трансдермальное введение по данному изобретению может также включать использование пластырей/наклеек/накладок. Например, пластырь/наклейка/накладка может обеспечить непрерывное, на протяжении нужного периода времени, поступление в организм одного или более активных веществ с заранее определенной скоростью.
В некоторых воплощениях данного изобретения средства доставки фармацевтических композиций в организм могут быть в аэрозольной форме (интраназальные спреи, вдыхаемые препараты) и/или в виде капель, например глазных. Способы доставки композиций непосредственно в легкие путем впрыскивания аэрозольного препарата в носовые ходы описаны, например, в патентах США №№5756353 и 5804212 (которые полностью включается в настоящий документ путем отсылки). В области фармацевтики известна также доставка лекарственных препаратов интраназальным путем с помощью полимерных микрочастиц (Takenaga et al., 1998) и с использованием лизофосфатидилглицерина (патент США №5725 871, который полностью включается в настоящий документ путем отсылки). В патенте США №5780045 описана система доставки лекарственного препарата через слизистую оболочку на основе политетрафторэтиленового опорного матрикса.
Термин «аэрозоль» в настоящем документе относится к коллоидным системам тонкодисперсных твердых или жидких частиц, взвешенных в ожиженном или находящемся под давлением газе-пропелленте. Типичный аэрозоль по данному изобретению, предназначенный для вдыхания, состоит из суспензии активных ингредиентов в жидком пропелленте или в смеси жидкого пропеллента и подходящего растворителя. В качестве пропеллентов по данному изобретению подходят углеводороды и простые эфиры. Емкости для аэрозольного препарата могут быть разными в зависимости от давления пропеллента. Введение препарата в аэрозольной форме зависит от возраста пациента, его массы тела, степени тяжести симптомов и индивидуальной реакции.
Примеры
Пример 1. Клинические испытания
Здоровым пациентам в течение 2 месяцев ежедневно давали плацебо (носитель) либо токотриенол природного витамина Ε (800 мг/сут). Функцию тромбоцитов определяли путем оптической агрегометрии. На протяжении 30 дней приема указанных препаратов токотриенолы полностью подавляли функцию тромбоцитов при использовании арахидоновой кислоты в качестве их агониста.
У пациентов, принимавших токотриенолы, после прекращения приема функциональная агрегация тромбоцитов не наблюдалась в течение 20 дней. А у здоровых добровольцев, принимавших аспирин в низкой дозе (81 мг), функция тромбоцитов восстанавливалась через 48-72 ч после прекращения приема (см. фиг. 1).
Пример 2. Определение безопасности приема токтриенола в дозировке 400 мг/сут у больных с инсультом или транзиторной ишемической атакой
Изучалась безопасность перорального приема токотриенола (ТСТ) у лиц с инсультом/транзиторной ишемической атакой. Этот важный начальный этап нужен для того, чтобы ограничить риск и продемонстрировать безопасность токотриенола в небольшой (N=100) когорте лиц с инсультом/транзиторной ишемической атакой, получающих препараты, противодействующие агрегации тромбоцитов, и статины (стандартное на сегодняшний день лечение).
Как показано на фиг. 11, у больных с инсультом/транзиторной ишемической атакой получали согласие и случайным образом распределяли их на две группы: в одной группе пациенты получали токотриенол (ТСТ), в другой - плацебо (РВО); это делалось специалистом по медико-санитарной статистике в течение 6 месяцев после критического события (инсульта/транзиторной ишемической атаки).
Первое посещение. На первой назначенной сотрудником исследования встрече пациент официально выражал/подписывал согласие на участие в исследовании и документы, касающиеся медицинского страхования и конфиденциальности (HIPАА). Медицинская сестра клинического исследования измеряла у пациента кровяное давление и брала пробу крови (20 мл) для общего клинического анализа и определения уровней глюкозы и гликированного гемоглобина (HbA1C) в крови, показателей функции печени, показателей функции тромбоцитов, липидного состава и содержания витамина Е. Участников исследования снабжали месячным запасом препарата (400 мг токотриенола или плацебо). Желатиновые капсулы, содержащие токотриенол (ТСТ) или только носитель (РВО), были предоставлены компанией Carotech Inc. (Нью-Джерси). Пациентам сообщали необходимую информацию о симптомах, связанных с возможным инсультом/транзиторной ишемической атакой, и просили в случае возникновения таких симптомов обращаться за медицинской помощью. Их просили в случае повторения инсульта/транзиторной ишемической атаки связываться как можно скорее с сотрудниками исследования. Пациентам также давали опросник по состоянию здоровья, который включал пункты, касающиеся симптомов инсульта/транзиторной ишемической атаки.
Соскоб липкой лентой. Соскоб липкой лентой является минимально инвазивной процедурой для определения доставки изучаемого агента и его биологической доступности. Процедуру проводили согласно инструкциям, одобренным Управлением по контролю качества пищевых продуктов, медикаментов и косметических средств США (FDA). Медицинская сестра клинического исследования очищала место соскоба (на левом предплечье пациента) пропитанной спиртом салфеткой, после чего накладывала липкую ленту (Cuderm, ТХ). Два первых последовательных соскоба с очищенного участка отбрасывали, после чего с этого же места брали десять последовательных соскобов, которые использовались для анализа. Эти последовательные соскобы (за один раз с рогового слоя кожи снимается слой толщиной 0,5-1 мкм) не ухудшают барьерную функцию кожи. Для проверки соблюдения пациентом предписанного режима приема препарата определяли содержание витамина Ε в соскобах, взятых липкой лентой, методом высокоэффективной жидкостной хроматографии (по сообщению заявителя30).
Посещение через 1 месяц. Медицинская сестра клинического исследования измеряла у пациента кровяное давление и брала соскобы липкой лентой, после чего пациента снабжали запасом препарата еще на 2 месяца. Проводили краткий опрос по поводу конкретных изменений в состоянии здоровья (кровотечения, синяки и проч.), потенциально связанных с приемом токотриенола.
Посещения через 2, 4, 5, 7, 8, 10 и 11 месяцев. С пациентами связывались по телефону и проводили опрос об изменениях в состоянии здоровья. Если ответы на поставленные вопросы свидетельствовали о потенциально негативных явлениях, то пациент подлежал дополнительному клиническому наблюдению, и его лечащего врача соответственно информировали.
Посещения через 3, 6, 9 и 12 месяцев. Медицинская сестра клинического исследования измеряла у пациента кровяное давление и брала пробу крови (20 мл) для общего клинического анализа, определения уровней глюкозы и гликированного гемоглобина (HbA1C) в крови, показателей функции печени, показателей функции тромбоцитов, липидного состава и содержания витамина Е. Медицинская сестра клинического исследования брала соскобы липкой лентой для проверки соблюдения пациентом предписанного режима приема препарата, после чего пациента снабжали запасом препарата еще на 3 месяца (за исключением последнего посещения через 12 месяцев). С целью дополнительной проверки соблюдения режима приема препарата, пациентов просили возвращать упаковки от препарата, выданного в предыдущее посещение, для подсчета истраченного количества.
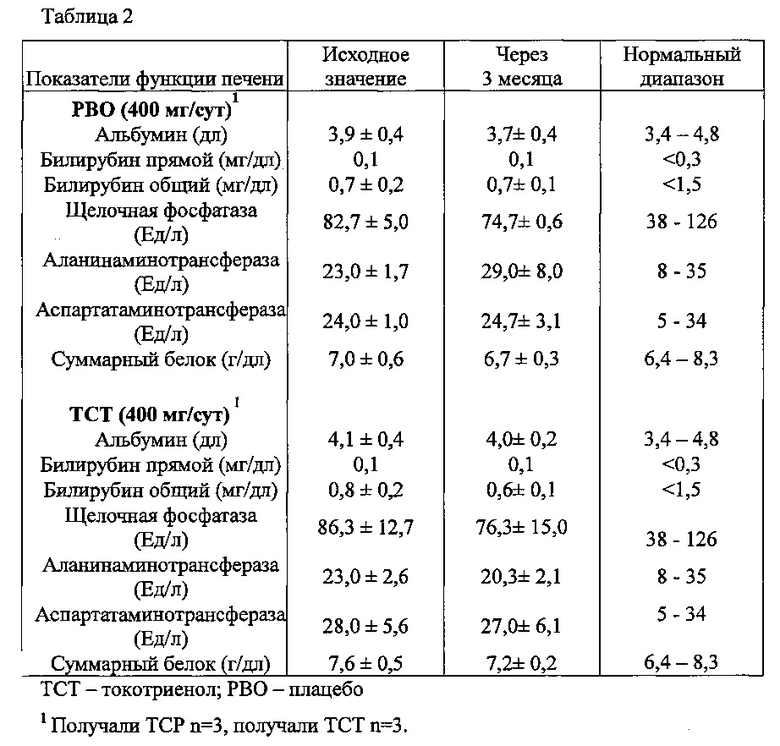
Результаты. Пациенты, испытавшие инсульт, переносили прием токотриенола в дозе 400 мг без вреда для здоровья. Не отмечалось существенной разницы в показателях функции печени между здоровыми пациентами, принимавшими токотриенол в дозировке 400 мг/сут на протяжении 3 месяцев, и теми, кто принимал плацебо (см. таблицу 2).
Пример 3. Характеристика влияния перорального приема токотриенола на агрегацию тромбоцитов у пациентов, перенесших инсульт или транзиторную ишемическую атаку и получавших аспирин или клопидогрел
Авторы изобретения исследовали, усиливает ли токотриенол противосвертывающий эффект аспирина и клопидогрела (эти два препарата чаще прочих используются в качестве противосвертывающих агентов для предотвращения повторения инсульта) и безопасно ли такое его действие.
Схема исследования, рандомизация участников и сбор образцов подробно изображены на фиг. 11. Вкратце, проделывали следующее. У пациентов, перенесших инсульт, брали образцы цельной крови и проводили агрегометрический анализ (фиг. 4) для определения уровня агрегации тромбоцитов - вначале исходного (на фоне стандартной противосвертывающей терапии) и затем после рандомизированного распределения по группам (в одной группе пациенты принимали токотриенол, в другой -плацебо) через 1, 3, 6, 9 и 12 месяцев. Для оценки функции тромбоцитов применяли как метод оптической агрегометрии, так и метод электрического импеданса. Оптическая агрегометрия остается наилучшим стандартным методом определения функции тромбоцитов в богатой тромбоцитами плазме крови, но все больше данных свидетельствует о том, что импедансная агрегометрия, при которой измерения происходят в присутствии всех нативных элементов цельной крови, включая гигантские тромбоциты, эритроциты и лейкоциты, более точно представляет реакцию тромбоцитов in vivo. Агрегометрия (оптическая и импедансная) для определения функции тромбоцитов проводилась с использованием следующих агонистов: арахидоновой кислоты (0,5 мМ), аденозиндифосфата (10 мкМ) и коллагена (2 мкг/мл).
Чтобы ограничить преждевременную активацию тромбоцитов, забор цельной крови производили путем венепункции промежуточной локтевой вены, используя иглы калибра 20 G, вакуумные пробирки (BD Medical, Нью-Джерси) с цитратом натрия (0,105 М). Образцы крови держали при комнатной температуре в течение 30 минут, после чего подготовляли их к агрегометрии. Чтобы ограничить вариабельность рН, использовали пластиковые пробирки и другую лабораторную посуду, которые закрывались так, что в них оставалось очень мало воздушного пространства по сравнению с объемом крови или изолированных тромбоцитов. Для оптической агрегометрии цельной крови и изолированных тромбоцитов использовали агрегометр 700-й модели производства компании Chrono-Log Corp.(Нью-Джерси).
Импедансная агрегометрия. Цельную кровь разбавляли 1:1 стерильным физиологическим раствором и инкубировали 5 минут при температуре 37°С, после чего проводили агрегометрию методом электрического импеданса при следующих параметрах: температура инкубирования 37°С, скорость перемешивания 1000 об/мин, усиление 0,1х. Сигнал регистрировали в течение 10 минут после добавления агонистов: арахидоновой кислоты (0,5 мМ), аденозиндифосфата (10 мкМ) и коллагена (2 мкг/мл, Chrono-log Corp., Пенсильвания).
Оптическая агрегометрия. Через 30 минут после венепункции из цельной крови отделяли богатую тромбоцитами плазму (PRP) и бедную тромбоцитами плазму (РРР). Для получения богатой тромбоцитами плазмы цельную кровь центрифугировали при комнатной температуре в течение 15 минут при ускорении 135 g, после чего медленно отсасывали плазму, обогащенную тромбоцитами, при помощи пипетки объемом 1 мл. Оставшийся образец центрифугировали еще 15 минут при 1500 g. Собирали бедную тромбоцитами плазму (при помощи пипетки на 1 мл) и хранили отдельно. При оптической агрегометрии измеряется увеличение прохождения света через перемешиваемую суспензию изолированных тромбоцитов после добавления к ним агонистов агрегации. Прохождение света через бедную тромбоцитами плазму брали за 100% (для данного агрегометра). За 0% брали исходный уровень соответствующего показателя для богатой тромбоцитами плазмы. После добавления агонистов (арахидоновой кислоты, аденозиндифосфата и коллагена) сигнал регистрировали через 10 минут.
Результаты. У здоровых пациентов ежедневный пероральный прием токотриенола (ТСТ) в дозе 400 мг значительно ослаблял агрегацию тромбоцитов, индуцированную арахидоновой кислотой (фиг. 4). Принимаемый через рот токотриенол по сравнению с плацебо усиливал противосвертывающее действие аспирина и клопидогрела и снижал частоту устойчивости к этим препаратам, не вызывая возрастания риска кровотечения. Для пациентов с устойчивостью к аспирину и/или клопидогрелу токотриенол представляет естественный и безопасный компонент для комбинированной противосвертывающей терапии
Пример 4. Снижает ли токотриенол частоту повторного инсульта
Авторы изобретения исследовали, снижает ли добавление токотриенола к стандартной противосвертывающей терапии частоту повторного инсульта/транзиторной ишемической атаки у перенесших эти состояния пациентов.
Схема исследования, рандомизация участников и сбор образцов изображены на фиг. 11. На основании опубликованных данных ожидаемая частота повторения инсульта через 1 год составляет 11%.
Пациентов просили в случае повторения инсульта/транзиторной ишемической атаки как можно скорее связаться с сотрудниками, проводящими клиническое исследование. В этих случаях анализировали историю болезни и копии результатов исследований мозга лучевыми методами, а также срочно организовывали дополнительное посещение пациента для контрольного наблюдения. Пациентов осматривал и обследовал невролог Эндрью Сливка (специалист по инсульту, сотрудник клинического исследования), которому не было известно, кто из пациентов, какой препарат получал. Оценив состояние пациента, изучив его историю болезни и результаты лучевых исследований, он определял, имел ли место у данного пациента инсульт/транзиторная ишемическая атака. Лицам, испытывавшим не тяжелые симптомы инсульта и потому не обращавшимся за лечением, предлагался опросник (при посещении медицинского учреждения или по телефону) по поводу состояния здоровья, содержащий вопросы, связанные с выявлением инсульта/транзиторной ишемической атаки. Все случаи положительных ответов на такие вопросы служили поводом к клинической оценке, проводимой Э. Сливкой, и обследованию, включавшему применение лучевых методов исследования мозга для установления факта инсульта/транзиторной ишемической атаки.
Анализ данных. Статистический анализ осуществляли с помощью пакета программ SAS 9.3 (SAS Institute, Inc., Кэри, шт. Северная Каролина, США). Для собранных значений переменных определяли описательные статистические показатели (среднее значение, медиану, стандартное отклонение, частоту и проч.). Частоту угрожающих жизни и крупных кровотечений, а также частоту побочных эффектов, связанных с применением статинов (включая повышение показателей функции печени в 2 раза по сравнению с нормой, развитие диабета, миалгии, требующие прекращения приема лекарства), в двух группах пациентов сравнивали, используя критерий хи-квадрат. При анализе функции тромбоцитов брали четыре результата, полученных на протяжении исследования, и сравнивали их с исходными показателями. Среди пациентов с изначальной устойчивостью к противосвертывающей терапии для каждой из лечебных групп долю (в процентах) пациентов, у которых по меньшей мере четыре результата, полученных в период наблюдения после окончания приема препарата, демонстрировали подавление агрегации тромбоцитов, сравнивали с контрольной группой, используя критерий хи-квадрат. Также долю (в процентах) пациентов, у которых по меньшей мере два из четырех результатов анализа на агрегацию демонстрировали более чем 10%-ное превышение подавления агрегации по сравнению с исходным значением, для каждой из лечебных групп сравнивали с контрольной группой, используя критерий хи-квадрат. Группы сравнивали по средним значениям уровня липопротеинов низкой плотности (LDL) до начала приема препаратов и на протяжении исследования, используя дисперсионный анализ. Три группы сравнивали по частоте инсульта/транзиторной ишемической атаки на протяжении исследования, используя критерий хи-квадрат.
Результаты. Полученные данные - первое свидетельство способности природного витамина с противосвертывающим действием и статиновым эффектом снижать частоту инсульта. Токотриенол, дополняющий современную противосвертывающую терапию, снижает частоту повторного инсульта. При всех известных преимуществах фармакологической противосвертывающей и статиновой терапии для снижения частоты рецидивных инсультов токотриенол представляет дополнительный противосвертывающий агент со статиновым эффектом природного происхождения.
В настоящем документе обсуждается ряд примерных аспектов и воплощений данного изобретения, но специалистам в данной области техники должны быть ясны их модификации, перестановки, добавления и сочетания. Поэтому подразумевается, что приведенная ниже формула изобретения включает все такие модификации, перестановки, добавления и сочетания в пределах сущности и объема данного изобретения.
Термины и обороты речи, употребляемые в настоящем документе, используются как описательные и не имеют ограничительного характера, и использование таких терминов и выражений не следует понимать как исключающее полностью или частично признаки, эквивалентные описанным здесь; подразумевается, что в пределах объема данного изобретения согласно прилагаемой его формуле возможны различные модификации. Таким образом, следует учесть, что хотя данное изобретение конкретно описано на примере предпочтительных воплощений и факультативных признаков, специалисты в данной области техники могут прибегнуть к модификациям и вариантам описанных в настоящем документе понятий изобретения, и что такие модификации и варианты считаются входящими в объем данного изобретения, определяемый прилагаемой его формулой. В тех случаях, когда в настоящем описании приводится диапазон значений, подразумевается, что данным описанием охватываются все промежуточные диапазоны и субдиапазоны, а также отдельные значения из приведенного диапазона. В тех случаях, когда в настоящем документе используются группы Маркуша или группы, организованные по иным принципам, подразумевается, что данным описанием охватываются также все отдельные члены группы и все возможные их комбинации и субкомбинации по отдельности.
В целом, термины и обороты речи, употребляемые в настоящем документе, имеют те значения, которые общеприняты в данной области техники и которые можно найти по ссылке на стандартные тексты, публикации в журналах и по контексту, ясному для специалиста в данной области техники. Определения терминов, приведенные выше в настоящем документе, предлагаются для пояснения их конкретного употребления в контексте данного изобретения.
Все патенты и публикации, упоминаемые в настоящем описании, ориентируют на профессиональный уровень специалистов в области техники, к которой относится данное изобретение. Дополнительная информация дается на интернет-сайте the Journal of Cerebral Blood Flow and Metabolism, а указанный источник включается в настоящий документ путем отсылки.















Настоящая группа изобретений относится к медицине, а именно к терапии и коагулологии, и касается ослабления нарушений свертывания крови. Для этого вводят фармацевтическую композицию, включающую эффективное количество альфа-токотриеноловой изоформы природного витамина Е в количестве, достаточном для снижения агрегации тромбоцитов, опосредуемой арахидоновой кислотой. Это обеспечивает уменьшение риска развития тромбозов у больных с патологически повышенной агрегационной активностью тромбоцитов, в том числе у тех, кому противопоказана терапия другими антиагрегантами, в частности аспирином. 6 н. и 3 з.п. ф-лы, 36 ил., 2 табл., 4 пр.
1. Фармацевтическая композиция для лечения нарушений свертывания крови, включающая:
i) один или более тромболитических агентов и
ii) фармацевтически эффективное количество перорально вводимой альфа-токотриеноловой изоформы природного витамина Е в количестве, достаточном для подавления агрегации тромбоцитов, опосредуемой арахидоновой кислотой.
2. Фармацевтическая композиция по п. 1, в которой тромболитический агент выбирают из группы, состоящей из аспирина, клопидогрела и дипиридамола.
3. Способ подавления агрегации тромбоцитов, опосредуемой арахидоновой кислотой, у нуждающегося в этом пациента, включающий введение пациенту фармацевтически эффективного количества перорально вводимой альфа-токотриеноловой изоформы природного витамина Е в количестве, достаточном для подавления агрегации тромбоцитов, опосредуемой арахидоновой кислотой, где указанная доза составляет от 400 до 500 мг и где указанное введение осуществляется ежедневно в течение 30 дней, а затем еженедельно.
4. Способ снижения риска или ослабления симптомов патологической агрегации тромбоцитов у нуждающегося в этом пациента, которому противопоказан аспирин, включающий введение пациенту фармацевтически эффективного количества перорально вводимой альфа-токотриеноловой изоформы природного витамина Е в количестве, достаточном для подавления агрегации тромбоцитов, опосредуемой арахидоновой кислотой, где указанная доза составляет от 400 до 500 мг и где указанное введение осуществляется ежедневно в течение 30 дней, а затем еженедельно.
5. Способ по п. 4, в котором аспирин противопоказан пациенту по причине, выбираемой из группы, состоящей из: алкоголизма, патологических изменений печени, нарушений свертывания крови, аллергии, непереносимости салицилатов, астмы, бронхоспазма, пептических язв или язв кишечника, диабета, гастрита, гемофилии, недостаточности глюкозо-6-фосфат-дегидрогеназы, лихорадки денге, детского или подросткового возраста, заболеваний почек, гиперурикемии и подагры.
6. Способ снижения риска или ослабления симптомов патологической агрегации тромбоцитов у нуждающегося в этом пациента, которому противопоказан клопидогрел, включающий введение пациенту фармацевтически эффективного количества перорально вводимой альфа-токотриеноловой изоформы природного витамина Е в количестве, достаточном для подавления агрегации тромбоцитов, опосредуемой арахидоновой кислотой, где указанная доза составляет от 400 до 500 мг и где указанное введение осуществляется ежедневно в течение 30 дней, а затем еженедельно.
7. Способ по п. 6, в котором клопидогрел противопоказан пациенту по причине, выбираемой из группы, состоящей из алкоголизма, патологических изменений печени, аллергии, низкой скорости метаболизма субстратов цитохрома р450 из-за наличия его аллельного варианта CYP2C19, язв желудка или кишечника и поражений почек.
8. Способ снижения риска сердечного приступа у нуждающегося в этом пациента, включающий введение пациенту фармацевтически эффективного количества перорально вводимой альфа-токотриеноловой изоформы природного витамина Е в количестве, достаточном для подавления агрегации тромбоцитов, опосредуемой арахидоновой кислотой, где указанная доза составляет от 400 до 500 мг и где указанное введение осуществляется ежедневно в течение 30 дней, а затем еженедельно.
9. Фармацевтическая композиция для лечения нарушений свертывания крови, включающая:
i) фармацевтически эффективное количество одного или более тромболитических агентов в количестве, достаточном для лечения нарушений свертывания крови у пациента, где тромболитический агент выбирают из группы, состоящей из аспирина, клопидогрела и дипиридамола, и
ii) фармацевтически эффективное количество перорально вводимой альфа-токотриеноловой изоформы природного витамина Е в количестве, достаточном для подавления агрегации тромбоцитов, опосредуемой арахидоновой кислотой, где указанная доза составляет от 400 до 500 мг ежедневно.
| US 6239171 B1 29.05.2001 | |||
| US2002172721 A1 21.11.2002 | |||
| QURESHI AA et al | |||
| "Tocotrienols-induced inhibition of platelet thrombus formation and platelet aggregation in stenosed canone coronary arteries" | |||
| Lipids Health Dis | |||
| Перекатываемый затвор для водоемов | 1922 |
|
SU2001A1 |
| ПАНЧЕНКО Е.П | |||
| и др | |||
| "Рекомендации по антитромботической терапии у больных со стабильными проявлениями атеротромбоза" | |||
| Кипятильник для воды | 1921 |
|
SU5A1 |
| HAN-A PARK et al | |||
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| YEUNG J | |||
| et al | |||
| Способ гальванического снятия позолоты с серебряных изделий без заметного изменения их формы | 1923 |
|
SU12A1 |
| Изложница с суживающимся книзу сечением и с вертикально перемещающимся днищем | 1924 |
|
SU2012A1 |
Авторы
Даты
2017-03-15—Публикация
2013-03-15—Подача