РОДСТВЕННЫЕ ЗАЯВКИ
[0001] Настоящая заявка испрашивает приоритет на основании предварительной заявки на патент США 61/604504, поданной 28 февраля 2012 г, содержание которой во всей полноте, в том числе любые чертежи, включено в настоящее описание посредством ссылки.
УРОВЕНЬ ТЕХНИКИ
Область техники
[0002] Настоящее изобретение относится к композициям, содержащим композиции алкилированного циклодекстрина с низким содержанием хлоридов, и способам их получения и применения.
Уровень техники
[0003] Разработаны гидрофобные, гидрофильные, полимеризованные, ионизированные, неионизированные и множество других производных циклодекстринов, которые находят применение в различных отраслях промышленности. В целом, дериватизацию циклодекстрина осуществляют посредством реакций, в которых группы -ОН в положениях 2-, 3- и/или 6-амилозных колец циклодекстрина заменяют замещающими группами. Заместители включают нейтральные, анионные и/или катонные функциональные группы.
[0004] Известные производные циклодекстринов, такие как алкилированные циклодекстрины, включают, но не ограничиваются ими, сульфоалкильные эфиры циклодекстринов, алкильные эфиры циклодекстринов (например, метиловые, этиловые и пропиловые эфиры циклодекстринов), гидроксиалкильные циклодекстрины, тиоалкильные эфиры циклодекстринов, карбоксилированные циклодекстрины (например, сукцинил-β-циклодекстрин, и тому подобные), сульфатированные циклодекстрины, и тому подобные. Также известны алкилированные циклодекстрины, содержащие более одного вида функциональных групп, например, сульфоалкильные эфиры- алкильные эфиры - циклодекстринов (см., например, WO 2005/042584 и US 2009/0012042, каждая из которых во всей полноте включена в настоящее описание посредством ссылки). В частности, алкилированные циклодекстрины, содержащие 2-гидроксипропильные группы и/или сульфоалкильные эфирные группы используют в фармацевтических составах.
[0005] Сульфобутилэфирное производное β-циклодекстрина ("SBE-β-CD") было запущено в производство компанией CyDex Pharmaceuticals, Inc. в виде CAPTISOL® и ADVASEP®. Анионный сульфобутилэфирный заместитель повышает растворимость в воде и безопасность исходного β-циклодекстрина, который может обратимо образовывать комплексы с активными фармацевтическими агентами, повышая растворимость активных фармацевтических агентов и, в некоторых случаях, повышать стабильность активных фармацевтических агентов в водном растворе. CAPTISOL® имеет химическую структуру согласно формуле X:
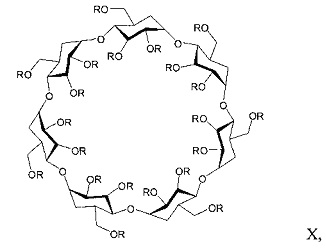
где R представляет собой (-Н)21-n или 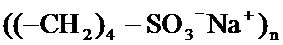
[0006] Сульфоалкилэфирные производные циклодекстринов (такие как, CAPTISOL®) получают с использованием периодических способов, описанных, например, в патентах США №№5,134,127, 5,376,645 и 6,153,746, описание каждого из которых во всей полноте включено в настоящее описание посредством ссылки.
[0007] Сульфоалкильные эфиры циклодекстринов и другие дериватизированные циклодекстрины можно также получать согласно способам, описанным в следующих патентах и опубликованных заявках на патенты: US 3,426,011, US 3,453,257, US 3,453,259, US 3,459,731, US 4,638,058, US 4,727,06, US 5,019,562, US 5,173,481, US 5,183,809, US 5,241,059, US 5,536,826, US 5,594,125, US 5,658,894, US 5,710,268, US 5,756,484, US 5,760,015, US 5,846,954, US 6,407,079, US 7,625,878, US 7,629,331, US 7,635,773, US2009/0012042, JP 05001102 и WO 01/40316, а также в следующих непатентных публикациях: Lammers et al., Recl. Trav. Chim. Pays-Bas 91:133 (1972); Staerke 23:161 (1971), Adam et al., J. Med. Chem. 45:1806 (2002), Qu et al., J. Inclusion Phenom. Macrocyclic Chem. 43:213 (2002), Tarver et al., Bioorg. Med. Chem. 10:1819 (2002), Fromming et al., Cyclodextrins in Pharmacy (Kluwer Academic Publishing, Dordrecht, 1994), Modified Cyclodextrins: Scaffolds и Templates for Supramolecular Chemistry (C.J. Easton et al. eds., Imperial College Press, London, UK, 1999), New Trends in Cyclodextrins и Derivatives (Dominique Duchene ed., Editions de Santé, Paris, FR, 1991), Comprehensive Supramolecular Chemistry 3 (Elsevier Science Inc., Tarrytown, NY), полные описания которых включены в настоящее описание посредством ссылки.
[0008] Примеси, содержащиеся в композиции алкилированного циклодекстрина, могут сократить срок годности и активность композиции активного агента. Примеси могут быть удалены из композиции алкилированного циклодекстрина под действием активированного угля (например, путем смешивания с ним). Обработка активированным углем водных растворов и суспензий, содержащих циклодекстрин, известна. См., например, патенты США №№4738923, 5393880 и 5569756. Тем не менее, существует постоянная потребность в композициях алкилированного циклодекстрина более высокой чистоты.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
[0009] В настоящем изобретении предложен способ получения композиции алкилированного циклодекстрина, содержащей алкилированный циклодекстрин, включающий: (а) смешивание циклодекстрина с алкилирующим агентом с получением реакционной среды, содержащей алкилированный циклодекстрин, один или более нежелательных компонентов и одну или более примесей, разлагающих лекарственное средство; (b) проведение одного или более разделений с удалением одного или более нежелательных компонентов из реакционной среды с получением частично очищенного раствора, содержащего алкилированный циклодекстрин и одну или более примесей, разлагающих лекарственное средство, где одно или более разделений представляют собой ультрафильтрацию, диафильтрацию, центрифугирование, экстракцию, осаждение с растворителем или диализ; и (с) обработку указанного частично очищенного раствора бесфосфатным активированным углем, имеющим остаточную проводимость 10 мкСм или менее и получение алкилированного циклодекстрина.
[0010] Согласно некоторым вариантам реализации композиция алкилированного циклодекстрина дополнительно содержит менее 500 ppm фосфата. Согласно некоторым вариантам реализации композиция алкилированного циклодекстрина дополнительно содержит менее 125 ppm фосфата.
[0011] Согласно некоторым вариантам реализации остаточная проводимость бесфосфатного активированного угля составляет 9 мкСм или менее. Согласно некоторым вариантам реализации остаточная проводимость бесфосфатного активированного угля составляет 8 мкСм или менее.
[0012] Согласно некоторым вариантам реализации композиция алкилированного циклодекстрина дополнительно содержит менее 0,5% (масс./масс.) хлорида. Согласно некоторым вариантам реализации указанная композиция алкилированного циклодекстрина дополнительно содержит менее 0,1% (масс./масс.) хлорида. Согласно некоторым вариантам реализации указанная композиция алкилированного циклодекстрина дополнительно содержит менее 0,05%) (масс./масс.) хлорида.
[0013] Согласно некоторым вариантам реализации указанная композиция алкилированного циклодекстрина имеет среднюю степень замещения от 2 до 9. Согласно некоторым вариантам реализации указанная композиция алкилированного циклодекстрина имеет среднюю степень замещения от 4,5 до 7,5. Согласно некоторым вариантам реализации указанная композиция алкилированного циклодекстрина имеет среднюю степень замещения от 6 до 7,5.
[0014] Согласно некоторым вариантам реализации указанная композиция алкилированного циклодекстрина имеет оптическую плотность менее 1 Е.П. (единицы оптической плотности, англ. A.U.), измеренную с помощью спектрофотометрии в УФ/видимой области в диапазоне длин волн от 245 нм до 270 нм для водного раствора, содержащего 300 мг композиции алкилированного циклодекстрина на мл раствора, в кювете с толщиной поглощающего слоя 1 см. Согласно некоторым вариантам реализации указанная оптическая плотность менее 1 Е.П. связана с агентом, разлагающим лекарственное средство.
[0015] Согласно некоторым вариантам реализации композиция алкилированного циклодекстрина имеет оптическую плотность менее 0,5 Е.П., измеренную с помощью спектрофотометрии в УФ/видимой области в диапазоне длин волн от 245 нм до 270 нм для водного раствора, содержащего 300 мг указанной композиции алкилированного циклодекстрина на мл раствора, в кювете с толщиной поглощающего слоя 1 см. Согласно некоторым вариантам реализации указанная оптическая плотность менее 0,5 Е.П. связана с агентом, разлагающим лекарственное средство.
[0016] Согласно некоторым вариантам реализации оптическую плотность определяют с помощью спектрофотометрии в УФ/видимой области в диапазоне длин волн от 245 нм до 270 нм для водного раствора, содержащего 500 мг композиции SAE-CD на мл раствора, в кювете с толщиной поглощающего слоя 1 см.
[0017] Согласно некоторым вариантам реализации композиция алкилированного циклодекстрина имеет оптическую плотность менее 1 Е.П., измеренную с помощью спектрофотометрии в УФ/видимой области в диапазоне длин волн от 320 нм до 350 нм для водного раствора, содержащего 300 мг композиции алкилированного циклодекстрина на мл раствора, в кювете с толщиной поглощающего слоя 1 см. Согласно некоторым вариантам реализации указанная оптическая плотность менее 1 Е.П. связана с окрашивающим агентом.
[0018] Согласно некоторым вариантам реализации композиция алкилированного циклодекстрина имеет оптическую плотность менее 0,5 Е.П., измеренную с помощью спектрофотометрии в УФ/видимой области в диапазоне длин волн от 320 нм до 350 нм для водного раствора, содержащего 300 мг композиции алкилированного циклодекстрина на мл раствора, в кювете с толщиной поглощающего слоя 1 см. Согласно некоторым вариантам реализации указанная оптическая плотность менее 0,5 Е.П. связана с окрашивающим агентом.
[0019] Согласно некоторым вариантам реализации оптическую плотность определяют с помощью спектрофотометрии в УФ/видимой области в диапазоне длин волн от 320 нм до 350 нм для водного раствора, содержащего 500 мг композиции алкилированного циклодекстрина на мл раствора, в кювете с толщиной поглощающего слоя 1 см.
[0020] Согласно некоторым вариантам реализации бесфосфатный активированный уголь промывают растворителем до достижения элюированным растворителем остаточной проводимости, указанной для стадии (с). Согласно некоторым вариантам реализации указанный бесфосфатный активированный уголь промывают водой до достижения элюированной водой остаточной проводимости, указанной для стадии (с).
[0021] Согласно некоторым вариантам реализации, алкилированный циклодекстрин представляет собой сульфоалкильный эфир циклодекстрина формулы (II):
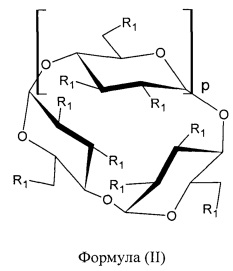
где p представляет собой 4, 5 или 6, и R1 независимо в каждом случае выбран из -ОН или 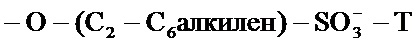
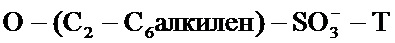
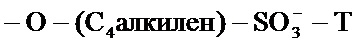
[0022] Согласно некоторым вариантам реализации, композицию алкилированного циклодекстрина комбинируют с одним или более вспомогательными веществами.
[0023] Согласно некоторым вариантам реализации композицию алкилированного циклодекстрина комбинируют с активным агентом.
[0024] Настоящее изобретение также относится к продуктам, полученным согласно способам, описанным в настоящем документе.
[0025] Дополнительные варианты реализации, признаки и преимущества настоящих изобретений, а также композиции, структуры и принцип действия различных вариантов реализации настоящего изобретения, подробно описаны ниже со ссылкой на прилагаемые чертежи.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
[0026] Прилагаемые чертежи, включенные в настоящий документ и являющиеся частью описания, иллюстрируют один или несколько вариантов реализаций настоящего изобретения и, совместно с описанием, служат для дальнейшего описания принципов изобретения и для того, чтобы помочь специалисту в соответствующей области реализовать и применять настоящее изобретение. Следующие чертежи приводятся только для иллюстрации и, таким образом, не предназначены для ограничения объема настоящего изобретения.
[0027] На Фиг. 1 приведено графическое представление результатов сканирования в УФ/видимых спектрах (190--400 нм) растворов, содержащих композицию SAE-CD, после однократной обработки активированным углем при варьировании концентрации сульфоалкильного эфира циклодекстрина от 1% до 60% по массе.
[0028] На Фиг. 2 приведено графическое представление результатов сканирования в УФ/видимых спектрах (190-400 нм) растворов, содержащих композицию SAE-CD, после второй обработки активированным углем при варьировании концентрации сульфоалкильного эфира циклодекстрина от 1% до 60% по массе.
[0029] На Фиг. 3 приведено графическое представление результатов сканирования в УФ/видимых спектрах (190-400 нм) раствора SBE6.6-β-CD после тепловой и щелочной обработки при температуре 60°C в течение 0, 24, 72, 96 и 168 часов для демонстрации разложения β-циклодекстрина и образования примесей, разлагающих лекарственное средство, с оптической плотностью при длинах волн от 245 нм до 270 нм, и/или окрашивающих компонентов с оптической плотностью при длинах волн от 320 нм до 350 нм.
[0030] На Фиг. 4 приведено графическое представление результатов сканирования в УФ/видимых спектрах (190-400 нм) раствора, содержащего SAE-β-CD, после обработки при температуре 70°C в течение 48 часов с последующей обработкой разными количествами активированного угля.
[0031] На Фиг. 5 приведено графическое представление воздействия начальной оптической плотности раствора SBE6.6-β-CD в УФ/видимой области на стабильность активного лекарственного компонента.
[0032] На Фиг. 6 приведено графическое представление содержания примесей в результате способа получения SBE6.6-β-CD, где примеси измеряют с использованием детектора заряженного аэрозоля.
[0033] На Фиг. 7 приведено графическое представление уровня концентрации хлоридов в результате способа получения SBE6.6-β-CD, где концентрацию хлоридов измеряют с использованием детектора заряженного аэрозоля.
[0034] На Фиг. 8 приведено графическое представление уровня концентрации хлоридов для двух партий SBE6.6-β-CD в ходе ультрафильтрации, в конце обработки ультрафильтрацией, 5, 10 и 20 минут после добавления в первую колонку с активированным углем, и 5, 10 и 20 минут после добавления во вторую колонку с активированным углем, измеренных с использованием детектора заряженного аэрозоля.
[0035] На Фиг. 9 приведено графическое представление уровня остаточных хлоридов после (а) первой колонки с активированным углем (помеченная маленькая) и после (b) первой колонки с активированным углем (помеченная большой), измеренного с использованием ионообменной хроматографии от уровня остаточной проводимости (помечен ZIC pHILIC % Cl-) конечного продукта SBE6.6-β-CD, измеренного с использованием колонки ZIC pHILIC с применением детектора заряженного аэрозоля (партии №17CX01.HQ00056-17CX01.HQ00064).
[0036] На Фиг. 10 приведено графическое представление концентрации хлорида натрия (масс./масс.) у образцов SBE6.6-β-CD после (а) одного цикла обработки активированным углем (партии №17CX01.HQ00001-17CX001.HQ00003, 17CX01.HQ00004.02, и 17CX01.HQ00005-17CX01.HQ00034) и (b) двух циклов обработки активированным углем (партии №17CX01.HQ00035-17CX01.HQ00079), измеренных с использованием ионообменной хроматографии. Предел обнаружения для ионообменной хроматографии составляет 0,05% по массе хлоридов.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
[0037] Изобретение охватывает комбинации и подкомбинации различных аспектов и вариантов реализации, описанных в настоящем документе. Кроме того, когда конкретный признак, структура или характеристика описана в контексте варианта реализации, следует понимать, что влияние такого признака, структуры или характеристики на другие варианты реализации будет понятно специалисту в данной области техники, независимо от того, описано ли это в явном виде или нет. Эти и другие аспекты настоящего изобретения будут понятны со ссылкой на нижеследующее подробное описание, примеры, формулу изобретения и приложенные чертежи.
[0038] Используемые в настоящем документе проценты относятся к «% по массе» и/или «масс./масс.» (массовая концентрация), если не указано иное.
[0039] Используемые в настоящем документе пространственные описания (например, «выше», «ниже», «вверх», «вниз», «верх», «низ» и т.д.) служат только для описания и иллюстрации и не должны трактоваться как ограничивающие по отношению к способам, оборудованию, композициям и продуктам какого-либо способа настоящего изобретения, которые могут быть пространственно расположены любым образом и в любой ориентации.
Алкилированный циклодекстрин
[0040] «Композиция алкилированного циклодекстрина» представляет собой композицию, содержащую алкилированные циклодекстрины, имеющие степень замещения или среднюю степень замещения (ADS) для конкретного заместителя. Композиция алкилированного циклодекстрина имеет распределение звеньев алкилированного циклодекстрина, отличающихся по индивидуальной степени замещения конкретными заместителями, где конкретные заместители для каждого звена одинаковые. В настоящем документе «композиция алкилированного циклодекстрина» представляет собой по существу фармацевтически неактивную композицию (т.е., композицию, которая не содержит фармацевтически активного агента). Например, композиция циклодекстрина может содержать по меньшей мере 90% (масс./масс.) циклодекстрина, по меньшей мере 95% (масс./масс.) циклодекстрина, по меньшей мере 97% (масс./масс.) циклодекстрина, по меньшей мере 99% (масс./масс.) циклодекстрина, по меньшей мере 99,9% (масс./масс.) циклодекстрина или по меньшей мере 99,99%) (масс./масс.) циклодекстрина.
[0041] Алкилированный циклодекстрин может представлять собой водорастворимый алкилированный циклодекстрин, который представляет собой любой алкилированный циклодекстрин, демонстрирующий повышенную растворимость в воде по сравнению с недериватизированным исходным циклодекстрином и имеющий молекулярную структуру, основанную на α-, β- или γ-циклодекстрине. Согласно некоторым вариантам реализации дериватизированный циклодекстрин, полученный по способу согласно настоящему изобретению, имеет растворимость в воде 100 мг/мл или выше или растворимость в воде менее 100 мг/мл.
[0042] Циклодекстрин может быть дериватизирован нейтральными, анионными или катионными заместителями по положениям С2, С3 или С6 отдельных сахаридов, образуя циклодекстриновое кольцо. Подходящие водорастворимые алкилированные циклодекстрины описаны в настоящем документе. Алкилированный циклодекстрин может также представлять собой водонерастворимый алкилированный циклодекстрин или алкилированный циклодекстрин, имеющий растворимость в воде ниже, чем у соответствующего недериватизированного исходного циклодекстрина.
[0043] В настоящем документе «предшественник заместителя» или «алкилирующий агент» относятся к соединению, реагенту, фрагменту или веществу, способному взаимодействовать с группой -ОН, присутствующей на циклодекстрине. Согласно некоторым вариантам реализации дериватизированный циклодекстрин включает заместитель, такой как сульфоалкилэфирная группа, эфирная группа, алкилэфирная группа, алкенилэфирная группа, гидроксиалкилэфирная группа, гидроксиалкенилэфирная группа, тиоалкилэфирная группа, аминоалкилэфирная группа, меркаптограппа, аминогруппа, алкиламиногруппа, карбоксильная группа, сложноэфирная группа, нитрогруппа, группа галогена, группа альдегида, группа 2,3-эпоксипропила и их комбинации. Согласно некоторым вариантам реализации алкилирующие агенты включают алкилсультон (например, 1,4-бутансультон, 1,5-пентансультон, 1,3-пропансультон, и тому подобные). Алкилированный циклодекстрин представляет собой циклодекстрин, в котором одна или более групп-ОН замещена группой -O-R, где R содержит алкильный фрагмент. Например, группа -O-R может представлять собой алкиловый эфир или сульфоалкиловый эфир.
[0044] Согласно некоторым вариантам реализации алкилированные циклодекстрины, такие как алкилированные циклодекстрины со смешанными эфирными группами включают, например, приведенные в Таблице 1 ниже.
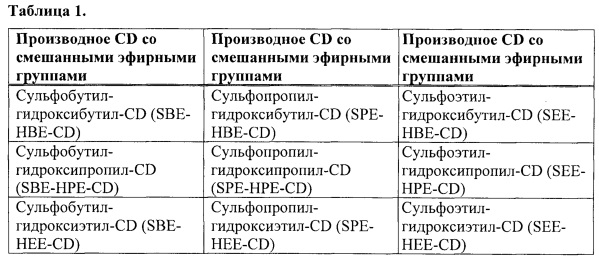
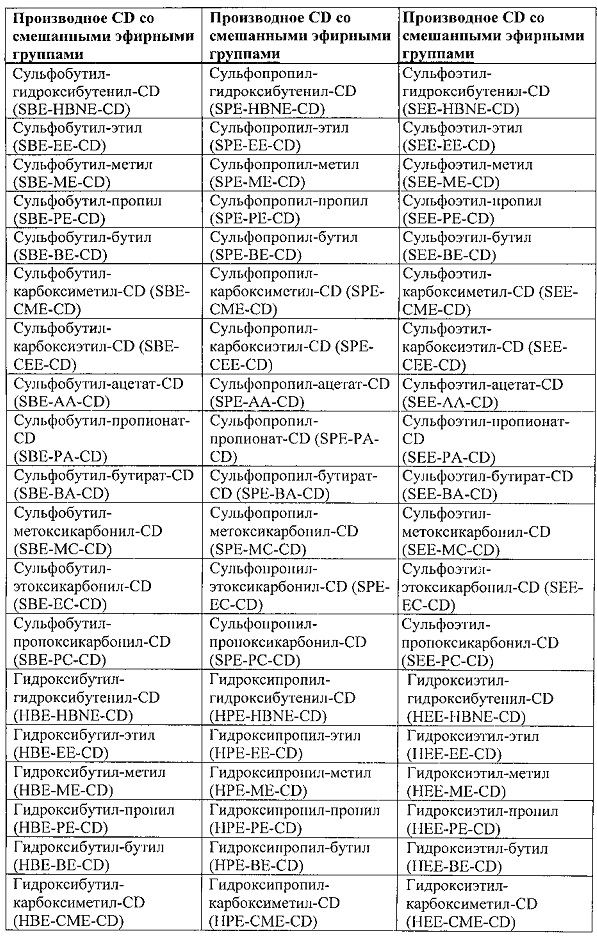
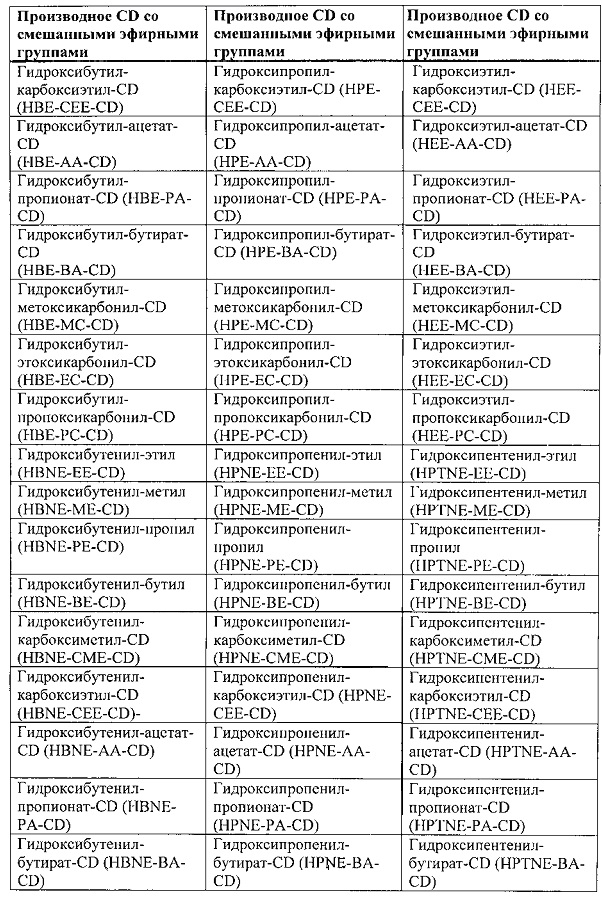
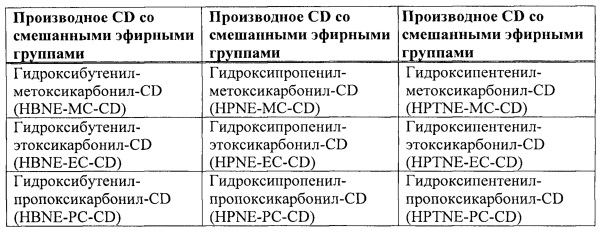
[0045] После реакции, очистки и/или выделения, композиция алкилированного циклодекстрина согласно настоящему изобретению может содержать небольшие количества (например, 1% или менее, 0,5% или менее, 0,1% или менее, 0,05% или менее, 0,001% или менее, 0,0005% или менее, или 0,0001% или менее, по массе) исходного вещества циклодекстрина (например, недериватизированного исходного циклодекстрина).
[0046] Алкилированный циклодекстрин может присутствовать в форме с высокой степенью чистоты. См. патент США №7635773. Согласно некоторым вариантам реализации алкилированный циклодекстрин представляет собой композицию SAE-CD высокой чистоты, имеющую сниженное количество агента, разлагающего лекарственное средство, по сравнению с известными коммерческими лотами CAPTISOL®. Композиция необязательно содержит сниженное количество фосфата или совсем не содержит фосфат по сравнению с известными коммерческими лотами CAPTISOL®. Композиция необязательно содержит сниженное количество окрашивающего агента по сравнению с известными коммерческими лотами CAPTISOL®. Композиция SAE-CD может также содержать сниженное количество 1,4-бутансультона и 4-гидроксибутан-1-сульфоновой кислоты по сравнению с известными коммерческими лотами CAPTISOL®.
[0047] Композиция алкилированного циклодекстрина согласно настоящему изобретению имеет неожиданные преимущества по сравнению с другими структурно сходными композициями алкилированного циклодекстрина. Под «структурным сходством» понимают, например, что заместитель алкилированного циклодекстрина в композиции по существу аналогичен заместителю другого алкилированного циклодекстрина, с которым его сравнивают. Примеры преимуществ могут включать повышенную чистоту, пониженное содержание пирогенов, пониженное содержание компонентов, разлагающих лекарственное средство, пониженное содержание окрашивающих агентов, пониженное содержание непрореагировавшего предшественника заместителя и/или пониженное содержание непрореагировавшего исходного вещества циклодекстрина. Пример преимущества также может включать сниженное содержание хлоридов.
[0048] Композиция водорастворимого алкилированного циклодекстрина может содержать соединение сульфоалкильного эфира циклодекстрина (SAE-CD) или смесь соединений Формулы I:

где: n представляет собой 4, 5 или 6; где R1, R2, R3, R4, R5, R6, R7, R8 и R9 независимо представляют собой -Н, группу 

[0049] Согласно некоторым вариантам реализации композиция SAE-CD содержит водорастворимый алкилированный циклодекстрин формулы II:
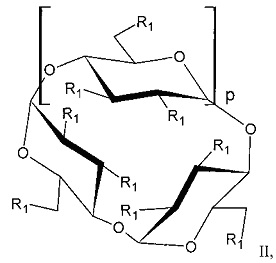
где: p представляет собой 4, 5 или 6;
R1 независимо в каждом случае выбран из -ОН или -SAE-T;
-SAE- представляет собой группу 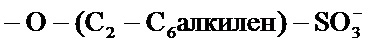
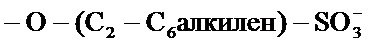
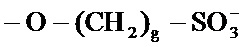
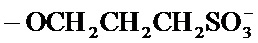
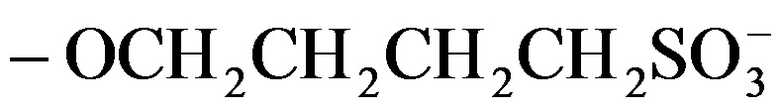 ); и -Т независимо в каждом случае выбран из группы, состоящей из фармацевтически приемлемых катионов, включающей, среди прочего, например, Н+, щелочные металлы (например, Li+, Na+, K+), щелочноземельные металлы (например, Са+2, Mg+2), ионы аммония и катионы амина, такие как катионы (С1-С6)-алкиламинов, пиперидин, пиразин, (C1-С6)-алканоламин, этилендиамин и (С4-С8)-циклоалканоламин; при условии, что по меньшей мере один R1 представляет собой гидроксильный фрагмент и по меньшей мере один R1 представляет собой -SAE-T.
); и -Т независимо в каждом случае выбран из группы, состоящей из фармацевтически приемлемых катионов, включающей, среди прочего, например, Н+, щелочные металлы (например, Li+, Na+, K+), щелочноземельные металлы (например, Са+2, Mg+2), ионы аммония и катионы амина, такие как катионы (С1-С6)-алкиламинов, пиперидин, пиразин, (C1-С6)-алканоламин, этилендиамин и (С4-С8)-циклоалканоламин; при условии, что по меньшей мере один R1 представляет собой гидроксильный фрагмент и по меньшей мере один R1 представляет собой -SAE-T.
[0050] Когда по меньшей мере один R1 молекулы дериватизированного циклодекстрина представляет собой -SAE-T, полагают, что степень замещения, в расчете на фрагмент -SAE-T, составляет по меньшей мере один (1). Когда термин -SAE- используют для обозначения сульфоалкил-(алкилсульфоновая кислота)-эфирного фрагмента, следует понимать, что фрагмент -SAE- содержит катион (-Т), если не указано иное. Соответственно, термины «SAE» и «-SAE-T» можно, по необходимости, использовать взаимозаменяемо.
[0051] Поскольку SAE-CD представляет собой полианионный циклодекстрин, он может находиться в различных солевых формах. Подходящие противоионы включают катионные органические атомы или молекулы и катионные неорганические атомы или молекулы. SAE-CD может включать противоионы одного вида или собой смесь различных противоионов. Свойства SAE-CD можно модифицировать путем изменения вида присутствующего противоиона. Например, композиция первой солевой формы SAE-CD может иметь больший осмотический потенциал или большую способность по снижению активности воды, чем другая вторая солевая форма того же SAE-CD.
[0052] Согласно некоторым вариантам реализации сульфоалкильный эфир циклодекстрина образует комплекс с одним или более фармацевтически приемлемыми катионами, выбранными из, например, Н+, щелочных металлов (например, Li+, Na+, K+), щелочноземельных металлов (например, Са+2, Mg+2), ионов аммония и катионов амина, таких как катионы (С1-С6)-алкиламинов, пиперидин, пиразин, (С1-С6)-алканоламин, этилендиамин и (С4-С8)-циклоалканоламин и т.п., и их комбинаций.
[0053] Дополнительные примеры производных сульфоалкиловых эфиров (SAE)-CD включают:
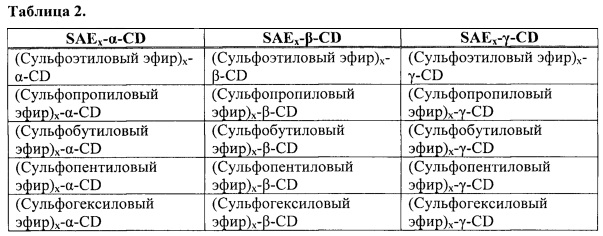
где x обозначает среднюю степень замещения. Согласно некоторым вариантам реализации алкилированные циклодекстрины образованы в виде солей.
[0054] Различные варианты реализации сульфоалкильных эфиров циклодекстрина включают эйкоза-O-(метил)-6G-O-(4-сульфобутил)-β-циклодекстрин, гептакис-O-(сульфометил)-тетрадекакис-O-(3-сульфопропил)-β-циклодекстрин, гептакис-O-[(1,1-диметилэтил)диметилсилил]-тетрадекакис-O-(3-сульфопропил)-β-циклодекстрин, гептакис-O-(сульфометил)-тетрадекакис-O-(3-сульфопропил)-β-циклодекстрин, и гептакис-O-[(1,1-диметилэтил)диметилсилил]-тетрадекакис-О-(сульфометил)-β-циклодекстрин. Другие известные алкилированные циклодекстрины, содержащие сульфоалкильный фрагмент включают сульфоалкилтио и сульфоалкилтиоалкильные эфирные производные, такие как октакис-(S-сульфопропил)-октатио-γ-циклодекстрин, октакис-O-[3-[(2-сульфоэтил)тио]пропил]-β-циклодекстрин] и октакис-S-(2-сульфоэтил)-октатио-γ-циклодекстрин.
[0055] Согласно некоторым вариантам реализации композиция алкилированного циклодекстрина согласно настоящему изобретению представляет собой композицию сульфоалкильного эфира-β-циклодекстрина, имеющего ADS от 2 до 9, от 4 до 8, от 4 до 7,5, от 4 до 7, от 4 до 6,5, от 4,5 до 8, от 4,5 до 7,5, от 4,5 до 7, от 5 до 8, от 5 до 7,5, от 5 до 7, от 5,5 до 8, от 5,5 до 7,5, от 5,5 до 7, от 5,5 до 6,5, от 6 до 8, от 6 до 7,5, от 6 до 7,1, от 6,5 до 7,1, от 6,2 до 6,9 или 6,5 на алкилированный циклодекстрин, и остальные заместители представляют собой -H.
[0056] Согласно некоторым вариантам реализации алкилированный циклодекстрин представляет собой соединение формулы III:
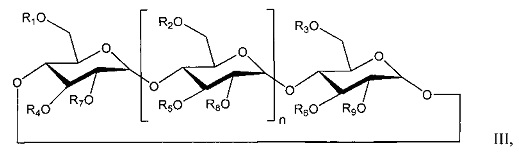
где n представляет собой 4, 5 или 6, где R1, R2, R3, R4, R5, R6, R7, R8 и R9 независимо выбраны из: -Н, группы 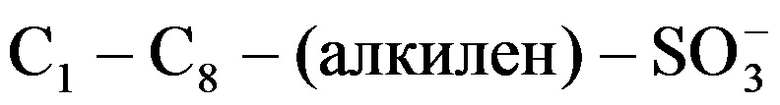 с прямой или разветвленной цепью, и необязательно замещенной группы C1-С6 с прямой или разветвленной цепью.
с прямой или разветвленной цепью, и необязательно замещенной группы C1-С6 с прямой или разветвленной цепью.
[0057] Композиция водорастворимого алкилированного циклодекстрина может содержать соединение алкильного эфира (АЕ)-циклодекстрина или смесь соединений Формулы IV:
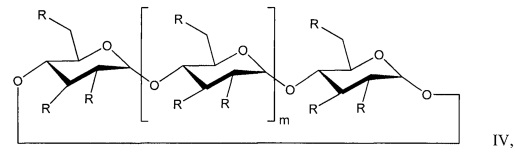
где: m представляет собой 4, 5 или 6; R независимо в каждом случае выбран из группы, состоящей из -ОН и АЕ; и АЕ представляет собой -O-(С1-С6алкил); при условии, что по меньшей мере один R представляет собой -ОН; и присутствует по меньшей мере один АЕ.
[0058] Дополнительные примеры производных AE-CD включают:
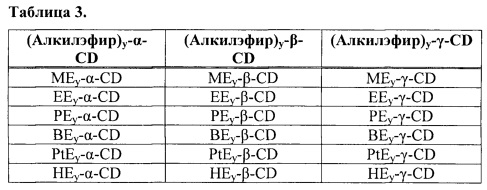
где ME обозначает метиловый эфир, ЕЕ обозначает этиловый эфир, РЕ обозначает пропиловый эфир, BE обозначает бутиловый эфир, PtE обозначает пентиловый этил, НЕ обозначает гексиловый эфир, и y обозначает среднюю степень замещения.
[0059] Композиция водорастворимого алкилированного циклодекстрина может содержать соединение НАЕ-циклодекстрина или смесь соединений Формулы V:
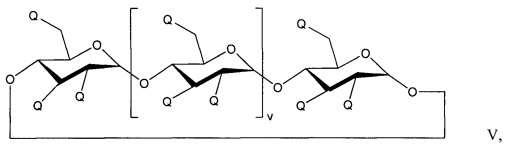
где: "v" представляет собой 4, 5 или 6; «Q» независимо в каждом случае выбран из группы, состоящей из -ОН, и -НАЕ; и НАЕ представляет собой НО(С1-С6алкил)-O-, при условии, что присутствует по меньшей мере один фрагмент -НАЕ.
[0060] Дополнительные примеры производных гидроксиалкильного эфира (HAE)-CD включают:
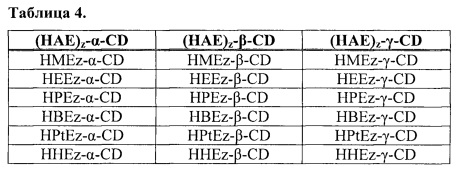
где НМЕ обозначает гидроксиметиловый эфир, НЕЕ обозначает гидроксиэтиловый эфир, НРЕ обозначает гидроксипропиловый эфир, НВЕ обозначает гидроксибутиловый эфир, HPtE обозначает гидроксипентиловый эфир, ННЕ обозначает гидроксигексиловый эфир и z обозначает среднюю степень замещения.
[0061] Композиция водорастворимого алкилированного циклодекстрина может содержать соединение SAE-AE-CD или смесь соединений Формулы VI:
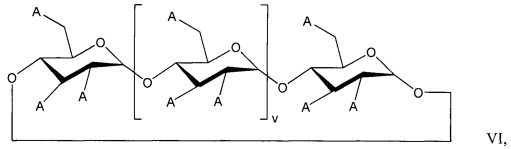
где: «v» представляет собой 4, 5 или 6; «А» независимо в каждом случае выбран из группы, состоящей из -ОН, -SAET и -АЕ; x представляет собой степень замещения для фрагмента SAET и составляет от 1 до 3v+5; y представляет собой степень замещения для фрагмента АЕ и составляет от 1 до 3v+5; -SAE представляет собой 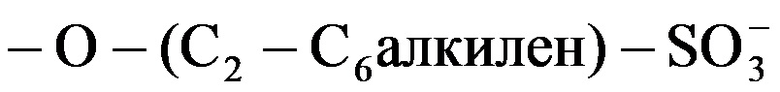 ; Т независимо в каждом случае представляет собой катион; и АЕ представляет собой -O(С1-С3алкил); при условии, что по меньшей мере один фрагмент -SAET и присутствуют по меньшей мере один фрагмент -АЕ; и сумма x, y и общее количество групп -ОН в алкилированном циклодекстрине составляет 3v+6.
; Т независимо в каждом случае представляет собой катион; и АЕ представляет собой -O(С1-С3алкил); при условии, что по меньшей мере один фрагмент -SAET и присутствуют по меньшей мере один фрагмент -АЕ; и сумма x, y и общее количество групп -ОН в алкилированном циклодекстрине составляет 3v+6.
[0062] Конкретные варианты реализации производных согласно настоящему изобретению включают производные, где: 1) алкиленовый фрагмент SAE имеет то же количество атомов углерода, что и алкильный фрагмент АЕ; 2) алкиленовый фрагмент SAE имеет другое количество атомов углерода, по сравнению с алкильным фрагментом АЕ; 3) алкильные и алкиленовые фрагменты независимо выбраны из группы, состоящей из фрагмента с прямой или разветвленной цепью; 4) алкильные и алкиленовые фрагменты независимо выбраны из группы, состоящей из насыщенного или ненасыщенного фрагмента; 5) ADS для группы SAE выше чем или приблизительно равняется ADS для группы АЕ; или 6) ADS для группы SAE меньше, чем ADS для группы АЕ.
[0063] Композиция водорастворимого алкилированного циклодекстрина может содержать соединение SAE-HAE-CD или смесь соединений Формулы VII:
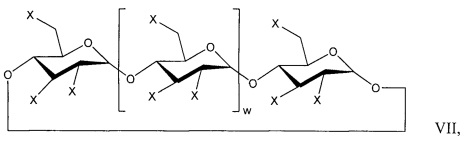
где: «v» представляет собой 4, 5 или 6; «X» независимо в каждом случае выбран из группы, состоящей из -ОН, SAET и НАЕ; x представляет собой степень замещения для фрагмента SAET и составляет от 1 до 3w+5; y представляет собой степень замещения для фрагмента НАЕ и составляет от 1 до 3w+5; -SAE представляет собой 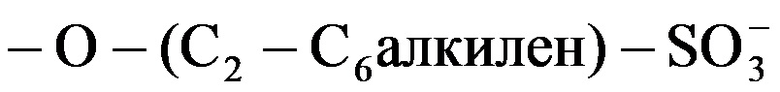 ; Т независимо в каждом случае представляет собой катион; и НАЕ представляет собой HO-(C)-С6алкил)-O-; при условии, что по меньшей мере один фрагмент -SAET и по меньшей мере один фрагмент -НАЕ присутствуют; и сумма x, y и общего количества групп -ОН в алкилированном циклодекстрине составляет 3v+6.
; Т независимо в каждом случае представляет собой катион; и НАЕ представляет собой HO-(C)-С6алкил)-O-; при условии, что по меньшей мере один фрагмент -SAET и по меньшей мере один фрагмент -НАЕ присутствуют; и сумма x, y и общего количества групп -ОН в алкилированном циклодекстрине составляет 3v+6.
[0064] Алкилированный циклодекстрин может включать SAE-CD, HAE-CD, SAE-HAE-CD, HANE-CD, HAE-AE-CD, HAE-SAE-CD, AE-CD, SAE-AE-CD, нейтральный циклодекстрин, анионный циклодекстрин, катионный циклодекстрин, галоген-дериватизированный циклодекстрин, амино-дериватизированный циклодекстрин, нитрил-дериватизированный циклодекстрин, альдегид-дериватизированный циклодекстрин, карбоксилат-дериватизированный циклодекстрин, сульфат-дериватизированный циклодекстрин, сульфонат-дериватизированный циклодекстрин, меркапто-дериватизированный циклодекстрин, алкиламино-дериватизированный циклодекстрин или сукцинил-дериватизированный циклодекстрин.
[0065] Внутри заданной композиции алкилированного циклодекстрина заместители алкилированного циклодекстрина(-ов) могут быть одинаковыми или различными. Например, в каждом случае в композиции алкилированного циклодекстрина фрагменты SAE или НАЕ могут содержать алкиленовый (алкильный) радикал одного типа или различных типов. В таких вариантах реализации в каждом случае в композиции алкилированного циклодекстрина алкиленовый радикал во фрагменте SAE или НАЕ может представлять собой этил, пропил, бутил, пентил или гексил.
[0066] Алкилированные циклодекстрины могут различаться степенью замещения функциональными группами, количеством атомов углерода в функциональных группах, их молекулярной массой, количеством глюкопиранозных единиц в исходном циклодекстрине, используемых для образования дериватизированного циклодекстрина и/или расположением их заместителей. Кроме того, дериватизация циклодекстрина функциональными группами происходит контролируемым образом, хотя и не с полной точностью. По этой причине, степень замещения на самом деле представляет собой число, отражающее среднее количество функциональных групп на молекулу циклодекстрина (например, SBE7-β-CD имеет в среднем 7 заместителей на молекулу циклодекстрина). Таким образом, средняя степень замещения («ADS») для него составляет 7. Кроме того, региохимия замещения гидроксильных групп циклодекстрина является переменной с учетом замещения конкретных гидроксильных групп в гексозном кольце. По этой причине, при производстве дериватизированного циклодекстрина возможно замещение разных гидроксильных групп, и конкретный дериватизированный циклодекстрин будет иметь преимущественную, хотя и не исключительную и не специфичную, схему замещения. Исходя из вышесказанного, молекулярная масса композиции конкретного дериватизированного циклодекстрина может варьироваться от партии к партии.
[0067] В одной молекуле исходного циклодекстрина присутствуют 3v+6 гидроксильных фрагмента, доступных для дериватизации. Когда v=4 (α-циклодекстрин), «y» степень замещения для указанного фрагмента может варьироваться со значением от 1 до 18. Когда v=5 (β-циклодекстрин), «y» для указанного фрагмента может варьироваться со значением от 1 до 21. Когда v=6 (γ-циклодекстрин), «y» степень замещения для указанного фрагмента может варьироваться со значением от 1 до 24. В целом, «y» также варьируется со значением от 1 до 3v+g, где g имеет значение от 0 до 5. Согласно некоторым вариантам реализации «y» составляет от 1 до 2v+g или от 1 до 1v+g.
[0068] Степень замещения («DS») для конкретного фрагмента (SAE, НАЕ или АЕ, например) является мерой количества заместителей SAE (НАЕ или АЕ), присоединенных к отдельной молекуле циклодекстрина, другими словами, количества молей заместителя на моль циклодекстрина. Следовательно, каждый заместитель имеет свою DS для отдельной молекулы алкилированного циклодекстрина. Средняя степень замещения («ADS») для заместителя является мерой общего количества присутствующих заместителей на молекулу циклодекстрина при распределении алкилированных циклодекстринов в композиции алкилированных циклодекстринов согласно настоящему изобретению. Следовательно, SAE4-CD имеет ADS (на молекулу CD), равную 4.
[0069] Некоторые варианты реализации настоящего изобретения включают варианты, где: 1) больше половины гидроксильных фрагментов алкилированного циклодекстрина являются дериватизированными; 2) половина или менее половины гидроксильных фрагментов алкилированного циклодекстрина являются дериватизированными; 3) заместители алкилированного циклодекстрина одинаковые в каждом случае; 4) заместители алкилированного циклодекстрина содержат по меньшей мере два различных заместителя; или 5) заместители алкилированного циклодекстрина содержат один или более заместителей, выбранных из группы, состоящей из незамещенного алкила, замещенного алкила, галогена (гало), галогеналкила, амина (амино), аминоалкила, альдегида, карбонилалкила, нитрила, цианоалкила, сульфоалкила, гидроксиалкила, карбоксиалкила, тиоалкила, незамещенного алкилена, замещенного алкилена, арила, арилалкила, гетероарила и гетероарилалкила.
[0070] Композиции алкилированного циклодекстрина могут содержать множество отдельных молекул алкилированного циклодекстрина, отличающихся индивидуальной степенью замещения, таким образом, что среднюю степень замещения вычисляют, как описано в настоящем документе, исходя из индивидуальных степеней замещения молекул. В частности, композиция производного SAE-CD может содержать множество молекул SAE-CD, каждая из которых имеет определенную индивидуальную степень замещения по отношению к заместителю SAE. Как следствие, ADS для SAE в композиции производного SAE-CD обозначает среднее значений IDS количества отдельных молекул в композиции. Например, композиция SAE5.2-CD содержит набор множества молекул SAEx-CD, где «x» (DS для групп SAE) может составлять от 1 до 10-11 для отдельных молекул циклодекстрина; однако, совокупность молекул SAE-циклодекстрина такова, что среднее значение «x» (ADS для групп SAE) составляет 5.2.
[0071] Композиции алкилированного циклодекстрина могут иметь ADS от высокой до средней и низкой. Композиции алкилированного циклодекстрина могут также иметь широкий или узкий «диапазон», что соответствует количеству разновидностей молекул с индивидуальной DS в композиции алкилированного циклодекстрина. Например, композиция алкилированного циклодекстрина, содержащая одну разновидность молекул алкилированного циклодекстрина с единственной заданной индивидуальной DS имеет диапазон, равный единице и в этом случае индивидуальная DS производного алкилированного циклодекстрина равна ADS композиции алкилированного циклодекстрина. Электроферограмма, например, алкилированного циклодекстрина с диапазоном равным единице должна показывать только одну разновидность молекул алкилированного циклодекстрина в отношении DS. Композиция алкилированного циклодекстрина, имеющая диапазон, равный двум, содержит два вида разновидностей алкилированного циклодекстрина, отличающихся индивидуальной DS, и его электроферограмма, например, покажет наличие двух разных разновидностей алкилированного циклодекстрина, различающихся DS. Аналогично, композиция алкилированного циклодекстрина с диапазоном, равным трем, содержит три вида разновидностей алкилированного циклодекстрина, отличающихся их индивидуальной DS. Диапазон композиции алкилированного циклодекстрина как правило составляет от 5 до 15 или от 7 до 12 или от 8 до 11.
[0072] Исходный циклодекстрин имеет вторичную гидроксильную группу в положениях глюкопиранозных остатков С-2 и С-3, что приводит к образованию циклодекстрина с первичным гидроксилом в положении С-6. Под действием предшественника заместителя возможно образование производных по каждому из этих гидроксильных фрагментов. В зависимости от используемой методологии синтеза, фрагменты заместителей могут быть распределены случайным образом или в некоторой степени упорядочены по доступным положениям, содержащим гидроксилы. Региостереомерию дериватизации с помощью заместителя можно также изменять при необходимости. Региостереомерию каждой композиции выбирают независимо. Например, большая часть присутствующих заместителей может быть расположена на первичной гидроксильной группе или на одной или обоих вторых гидроксильных группах исходного циклодекстрина. Согласно некоторым вариантам реализации первичное распределение заместителей представляет собой С-3>С-2>С-6, в то время как согласно другим вариантам реализации первичное распределение заместителей представляет собой С-2>С-3>С-6. Некоторые варианты реализации настоящего изобретения включают молекулу алкилированного циклодекстрина, в которой меньшая часть фрагментов заместителей расположена в положении С-6, и большая часть фрагментов заместителей расположена в положениях С-2 и/или С-3. Согласно другим вариантам реализации настоящего изобретения включают молекулу алкилированного циклодекстрина, в которой фрагменты заместителей по существу равномерно распределены по позициям С-2, С-3 и С-6.
[0073] Композиция алкилированного циклодекстрина содержит распределение множества разновидностей отдельных молекул алкилированного циклодекстрина, где каждая разновидность имеет индивидуальную степень замещения («IDS»). Содержание каждой разновидности молекул циклодекстрина в конкретной композиций может быть подсчитано с помощью капиллярного электрофореза. Указанный способ анализа (например, капиллярный электрофорез для заряженных алкилированных циклодекстринов) достаточно чувствителен, чтобы отличить композиции, содержащие только 5% одного алкилированного циклодекстрина и 95% другого алкилированного циклодекстрина от исходной композиции, содержащей алкилированный циклодекстрин.
[0074] Указанные выше вариации отдельных разновидностей алкилированных циклодекстринов в распределении могут приводить к изменению константы равновесия комплексообразования K1:1, которая в свою очередь влияет на требуемые молярные соотношения дериватизированного циклодекстрина к активному агенту. Константа равновесия также в некоторой степени зависит от температуры и требуются такие допуски соотношений, чтобы указанный агент оставался солюбилизированным при колебаниях температуры, происходящих в ходе производства, хранения, транспортировки и применения. Константа равновесия может также изменяться в зависимости от pH и требуются такие допуски соотношений, чтобы указанный агент оставался солюбилизированным при колебаниях pH, происходящих в ходе производства, хранения, транспортировки и применения. Константа равновесия может также изменяться в зависимости от присутствия других вспомогательных веществ (например, буферных агентов, консервантов, антиоксидантов). Соответственно, отношение дериватизированного циклодекстрина к активному агенту можно изменять относительно соотношений, приведенных в настоящем описании, с целью компенсировать упомянутые выше переменные.
[0075] Алкилированные циклодекстрины, полученные по способу согласно настоящему изобретению, можно использовать в композициях, составах, способах и системах, описанных, например, в патентах США №№5134127, 5376645, 5914122, 5874418, 6046177, 6133248, 6153746, 6407079, 6869939, 7034013, 7625878, 7629331, и 7635773; публикациях заявок на патент США №№2005/0164986, 2005/0186267, 2005/0250738, 2006/0258537, 2007/0020196, 2007/0020298, 2007/0020299, 2007/0175472, 2007/0202054, 2008/0194519, 2009/0011037, 2009/0012042, 2009/0123540; заявках на патент США №№12/404174, 12/407734, 61/050918, 61/177718, и 61/182560; и международных заявках РСТ №№ PCT/US 06/62346, PCT/US 07/71758, PCT/US 07/71748, PCT/US 07/72387, PCT/US 07/72442, PCT/US 07/78465, PCT/US 08/61697, PCT/US 08/61698, PCT/US 08/70969, и PCT/US 08/82730, полное описание которых включено в настоящую заявку посредством ссылки. Алкилированные циклодекстрины, полученные по способам, приведенным в настоящем документе, можно также использовать в качестве подходящих заменителей для других известных сортов алкилированных циклодекстринов, имеющих те же функциональные группы.
[0076] Согласно некоторым вариантам реализации алкилированный циклодекстрин проявляет большую растворимость в воде, чем соответствующий циклодекстрин, из которого получают композицию алкилированного циклодекстрина согласно настоящему изобретению. Например, согласно некоторым вариантам реализации недериватизированный циклодекстрин используют в качестве исходного материала, например, α-, β- или γ-циклодекстрин, коммерчески доступные от, например, WACKER BIOCHEM CORP. (Adrian, MI), и других источников. Недериватизированные циклодекстрины имеют ограниченную растворимость по сравнению с композициями алкилированного циклодекстрина согласно настоящему изобретению. Например, недериватизированные α-CD, β-CD, γ-CD имеют растворимость в воде при насыщении примерно 145 г/л, 18,5 г/л, и 232 г/л, соответственно.
[0077] Композицию водорастворимого алкилированного циклодекстрина необязательно обрабатывают для удаления большей части (например, >50%) недериватизированного циклодекстрин или других загрязняющих веществ.
[0078] В настоящем документе термины «алкилен» и «алкил» (например, в группе 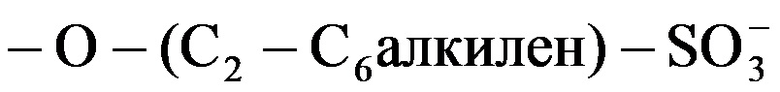 или в алкиламинных катионах), включают линейные, циклические и разветвленные, насыщенные и ненасыщенные (т.е., содержащие одну или более двойных связей) двухвалентные алкиленовые группы и одновалентные алкильные группы, соответственно. Например, фрагменты SAE или НАЕ в каждом случае в композиции алкилированного циклодекстрина могут содержать алкиленовый (алкильный) радикал одного типа или различных типов. Согласно таким вариантам реализации алкиленовый радикал во фрагменте SAE или НАЕ может представлять собой этил, пропил, бутил, пентил или гексил в каждом случае в композиции алкилированного циклодекстрина.
или в алкиламинных катионах), включают линейные, циклические и разветвленные, насыщенные и ненасыщенные (т.е., содержащие одну или более двойных связей) двухвалентные алкиленовые группы и одновалентные алкильные группы, соответственно. Например, фрагменты SAE или НАЕ в каждом случае в композиции алкилированного циклодекстрина могут содержать алкиленовый (алкильный) радикал одного типа или различных типов. Согласно таким вариантам реализации алкиленовый радикал во фрагменте SAE или НАЕ может представлять собой этил, пропил, бутил, пентил или гексил в каждом случае в композиции алкилированного циклодекстрина.
[0079] Аналогично в данном тексте термин «алканол» включает как линейные, циклические и разветвленные, так и насыщенные и ненасыщенные алкильные компоненты алканольных групп, в которых гидроксильные группы могут быть расположены в любом положении алкильного фрагмента. Термин «циклоалканол» включает незамещенные или замещенные (например, метилом или этилом) циклические спирты.
[0080] Согласно некоторым вариантам реализации в настоящем изобретении предложена композиция алкильного эфира циклодекстрина (AE-CD), содержащая алкильный эфир циклодекстрина, имеющий среднюю степень замещения от 2 до 9, менее 500 ppm фосфата и менее 0,5% (масс./масс.) хлорида, где указанная композиция АЕ-CD имеет оптическую плотность менее 1 Е.П., измеренную с помощью спектрофотометрии в УФ/видимой области в диапазоне длин волн от 245 нм до 270 нм для водного раствора, содержащего 300 мг композиции AE-CD на мл раствора, в кювете с толщиной поглощающего слоя 1 см. Согласно некоторым вариантам реализации указанная оптическая плотность менее 1 Е.П. связана с агентом, разлагающим лекарственное средство. Согласно некоторым вариантам реализации композиция алкильного эфира циклодекстрина не представляет собой композицию сульфобутилового эфира циклодекстрина. Согласно некоторым вариантам реализации алкильный эфир циклодекстрина не представляет собой сульфобутиловый эфир β-циклодекстрина. Согласно некоторым вариантам реализации композиция AE-CD имеет оптическую плотность 0,5 Е.П. или менее, измеренную с помощью спектрофотометрии в УФ/видимой области в диапазоне длин волн от 245 нм до 270 нм для водного раствора, содержащего 300 мг композиции AE-CD на мл раствора, в кювете с толщиной поглощающего слоя 1 см. Согласно некоторым вариантам реализации указанная оптическая плотность 0,5 Е.П. или менее связана с агентом, разлагающим лекарственное средство. Согласно некоторым вариантам реализации композиция AE-CD имеет оптическую плотность 0,2 Е.П. или менее, измеренную с помощью спектрофотометрии в УФ/видимой области в диапазоне длин волн от 245 нм до 270 нм для водного раствора, содержащего 300 мг композиции AE-CD на мл раствора, в кювете с толщиной поглощающего слоя 1 см. Согласно некоторым вариантам реализации указанная оптическая плотность 0,2 Е.П. или менее связана с агентом, разлагающим лекарственное средство. Согласно некоторым вариантам реализации указанную оптическую плотность композиции AE-CD определяют с помощью спектрофотометрии в УФ/видимой области в диапазоне длин волн от 245 нм до 270 нм для водного раствора, содержащего 500 мг композиции AE-CD на мл раствора, в кювете с толщиной поглощающего слоя 1 см.
[0081] Согласно некоторым вариантам реализации в настоящем изобретении предложена композиция алкильного эфира циклодекстрина (AE-CD), содержащая алкильный эфир циклодекстрина, имеющий среднюю степень замещения от 2 до 9, менее 500 ppm фосфата и менее 0,5% (масс./масс.) хлорида, где композиция AE-CD имеет оптическую плотность менее 1 Е.П., измеренную с помощью спектрофотометрии в УФ/видимой области в диапазоне длин волн от 320 нм до 350 нм для водного раствора, содержащего 300 мг композиции AE-CD на мл раствора, в кювете с толщиной поглощающего слоя 1 см. Согласно некоторым вариантам реализации указанная оптическая плотность менее 1 Е.П. связана с окрашивающим агентом. Согласно некоторым вариантам реализации композиция алкильного эфира циклодекстрина не представляет собой композицию сульфобутилового эфира циклодекстрина. Согласно некоторым вариантам реализации алкильный эфир циклодекстрина не представляет собой сульфобутиловый эфир β-циклодекстрина. Согласно некоторым вариантам реализации композиция AE-CD имеет оптическую плотность 0,5 Е.П. или менее, измеренную с помощью спектрофотометрии в УФ/видимой области в диапазоне длин волн от 320 нм до 350 нм для водного раствора, содержащего 300 мг композицию SAE-CD на мл раствора, в кювете с толщиной поглощающего слоя 1 см. Согласно некоторым вариантам реализации указанная оптическая плотность 0,5 Е.П. или менее связана с окрашивающим агентом. Согласно некоторым вариантам реализации композиция AE-CD имеет оптическую плотность 0,2 Е.П. или менее, измеренную с помощью спектрофотометрии в УФ/видимой области в диапазоне длин волн от 245 нм до 270 нм для водного раствора, содержащего 300 мг композиции AE-CD на мл раствора, в кювете с толщиной поглощающего слоя 1 см. Согласно некоторым вариантам реализации указанная оптическая плотность 0,2 Е.П. или менее связана с окрашивающим агентом. Согласно некоторым вариантам реализации оптическую плотность композиции AE-CD определяют с помощью спектрофотометрии в УФ/видимой области в диапазоне длин волн от 320 нм до 350 нм для водного раствора, содержащего 500 мг композиции SAE-CD на мл раствора, в кювете с толщиной поглощающего слоя 1 см.
[0082] Согласно некоторым вариантам реализации средняя степень замещения в AE-CD составляет от 4,5 до 7,5. Согласно некоторым вариантам реализации средняя степень замещения в AE-CD составляет от 6 до 7,5. Согласно некоторым вариантам реализации средняя степень замещения в AE-CD составляет от 6,2 до 6,9.
[0083] Согласно некоторым вариантам реализации в настоящем изобретении предложена композиция, содержащая композицию AE-CD и активный агент.
[0084] Согласно некоторым вариантам реализации в настоящем изобретении предложена композиция сульфоалкильного эфира циклодекстрина (SAE-CD), содержащая сульфоалкильный эфир циклодекстрина, имеющий среднюю степень замещения ль 2 до 9, менее 500 ppm фосфата и менее 0,5% (масс./масс.) хлорида, где композиция SAE-CD имеет оптическую плотность менее 1 Е.П., измеренную с помощью спектрофотометрии в УФ/видимой области в диапазоне длин волн от 245 нм до 270 нм для водного раствора, содержащего 300 мг композиции SAE-CD на мл раствора, в кювете с толщиной поглощающего слоя 1 см. Согласно некоторым вариантам реализации указанная оптическая плотность менее 1 Е.П. обусловлена присутствием агента, разлагающего лекарственное средство. Согласно некоторым вариантам реализации композиция сульфоалкильного эфира циклодекстрина не представляет собой композицию сульфобутилового эфира циклодекстрина. Согласно некоторым вариантам реализации сульфоалкильный эфир циклодекстрина не представляет собой сульфобутиловый эфир β-циклодекстрина. Согласно некоторым вариантам реализации композиция SAE-CD имеет оптическую плотность 0,5 Е.П. или менее, измеренную с помощью спектрофотометрии в УФ/видимой области в диапазоне длин волн от 245 нм до 270 нм для водного раствора, содержащего 300 мг композиции SAE-CD на мл раствора, в кювете с толщиной поглощающего слоя 1 см. Согласно некоторым вариантам реализации указанная оптическая плотность 0,5 Е.П. или менее обусловлена присутствием агента, разлагающего лекарственное средство. Согласно некоторым вариантам реализации композиция SAE-CD имеет оптическую плотность 0,2 Е.П. или менее, измеренную с помощью спектрофотометрии в УФ/видимой области в диапазоне длин волн от 245 нм до 270 нм для водного раствора, содержащего 300 мг композиции SAE-CD на мл раствора, в кювете с толщиной поглощающего слоя 1 см. Согласно некоторым вариантам реализации указанная оптическая плотность 0,2 Е.П. или менее обусловлена наличием агента, разлагающего лекарственное средство. Согласно некоторым вариантам реализации оптическую плотность композиции SAE-CD определяют с помощью спектрофотометрии в УФ/видимой области в диапазоне длин волн от 245 нм до 270 нм для водного раствора, содержащего 500 мг композиции SAE-CD на мл раствора, в кювете с толщиной поглощающего слоя 1 см.
[0085] Согласно некоторым вариантам реализации указанный сульфоалкильный эфир циклодекстрина представляет собой соединение формулы (II):
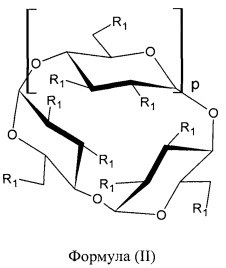
где p представляет собой 4, 5 или 6, и R1 независимо в каждом случае выбран из -OH или 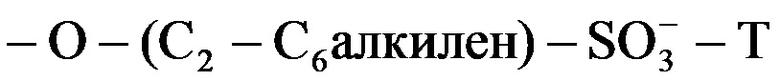 , где T независимо в каждом случае выбран из фармацевтически приемлемых катионов, при условии, что по меньшей мере один R1 представляет собой -OH и по меньшей мере один R1 представляет собой
, где T независимо в каждом случае выбран из фармацевтически приемлемых катионов, при условии, что по меньшей мере один R1 представляет собой -OH и по меньшей мере один R1 представляет собой 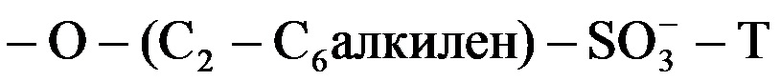 . Согласно некоторым вариантам реализации R1 независимо в каждом случае выбран из
. Согласно некоторым вариантам реализации R1 независимо в каждом случае выбран из 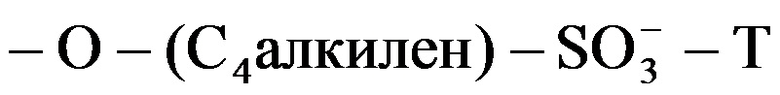 , и -T в каждом случае представляет собой Na+.
, и -T в каждом случае представляет собой Na+.
[0086] Согласно некоторым вариантам реализации в настоящем изобретении предложена композиция сульфоалкильного эфира циклодекстрина (SAE-CD), содержащая сульфоалкильный эфир циклодекстрина, имеющий среднюю степень замещения от 2 до 9, менее 500 ppm фосфата и менее 0,5% (масс./масс.) хлорида, где композиция SAE-CD имеет оптическую плотность 1 Е.П. или менее, измеренную с помощью спектрофотометрии в УФ/видимой области в диапазоне длин волн от 320 нм до 350 нм для водного раствора, содержащего 300 мг композиции SAE-CD на мл раствора, в кювете с толщиной поглощающего слоя 1 см. Согласно некоторым вариантам реализации указанная оптическая плотность 1 Е.П. или менее обусловлена наличием окрашивающего агента. Согласно некоторым вариантам реализации композиция сульфоалкильного эфира циклодекстрина не представляет собой композицию сульфобутилового эфира циклодекстрина. Согласно некоторым вариантам реализации сульфоалкильный эфир циклодекстрина не представляет собой сульфобутиловый эфир β-циклодекстрина. Согласно некоторым вариантам реализации композиция SAE-CD имеет оптическую плотность 0,5 Е.П. или менее, измеренную с помощью спектрофотометрии в УФ/видимой области в диапазоне длин волн от 320 нм до 350 нм для водного раствора, содержащего 300 мг композиции SAE-CD на мл раствора, в кювете с толщиной поглощающего слоя 1 см. Согласно некоторым вариантам реализации указанная оптическая плотность 0,5 Е.П. или менее обусловлена наличием окрашивающего агента. Согласно некоторым вариантам реализации композиция SAE-CD имеет оптическую плотность 0,2 Е.П. или менее, измеренную с помощью спектрофотометрии в УФ/видимой области в диапазоне длин волн от 245 нм до 270 нм для водного раствора, содержащего 300 мг композиции SAE-CD на мл раствора, в кювете с толщиной поглощающего слоя 1 см. Согласно некоторым вариантам реализации указанная оптическая плотность 0,2 Е.П. или менее обусловлена наличием окрашивающего агента. Согласно некоторым вариантам реализации оптическую плотность композиции SAE-CD определяют с помощью спектрофотометрии в УФ/видимой области в диапазоне длин волн от 320 нм до 350 нм для водного раствора, содержащего 500 мг композиции SAE-CD на мл раствора, в кювете с толщиной поглощающего слоя 1 см.
[0087] Согласно некоторым вариантам реализации средняя степень замещения в SAE-CD составляет от 4,5 до 7,5. Согласно некоторым вариантам реализации средняя степень замещения в SAE-CD составляет от 6 до 7,5. Согласно некоторым вариантам реализации средняя степень замещения в SAE-CD составляет от 6,2 до 6,9.
[0088] Согласно некоторым вариантам реализации в настоящем изобретении предложена композиция, содержащая композицию SAE-CD и активный агент.
[0089] Настоящее изобретение также относится к способу стабилизации активного агента, включающему обеспечение композиции алкилированного циклодекстрина, содержащей алкилированный циклодекстрин, менее 500 ppm фосфата и менее 0,5% хлорида, где указанная композиция алкилированного циклодекстрина имеет оптическую плотность менее 1 Е.П., измеренную с помощью спектрофотометрии в УФ/видимой области в диапазоне длин волн от 245 нм до 270 нм для водного раствора, содержащего 300 мг указанной композиции алкилированного циклодекстрина на мл раствора, в кювете с толщиной поглощающего слоя 1 см; и комбинирование указанной композиции алкилированного циклодекстрина с активным агентом. Согласно некоторым вариантам реализации указанная оптическая плотность менее 1 Е.П. связана с агентом, разлагающим лекарственное средство.
[0090] Настоящее изобретение также относится к способу стабилизации активного агента, включающему обеспечение композиции алкилированного циклодекстрина, содержащей алкилированный циклодекстрин, менее 500 ppm фосфата и менее 0,5% хлорида, где указанная композиция алкилированного циклодекстрина имеет оптическую плотность менее 1 Е.П., измеренную с помощью спектрофотометрии в УФ/видимой области в диапазоне длин волн от 245 нм до 270 нм для водного раствора, содержащего 300 мг указанной композиции алкилированного циклодекстрина на мл раствора, в кювете с толщиной поглощающего слоя 1 см; и комбинирование указанной композиции алкилированного циклодекстрина с активным агентом. Согласно некоторым вариантам реализации указанная оптическая плотность менее 1 Е.П. связана с окрашивающим агентом.
[0091] В настоящем изобретении предложен способ получения композиции алкилированного циклодекстрина, включающий:
(a) смешивание циклодекстрина с алкилирующим агентом в присутствии подщелачивающего агента с получением реакционной среды, содержащей алкилированный циклодекстрин, один или более нежелательных компонентов и одной или более примесей, разлагающих лекарственное средство;
(b) проведение одного или более разделений с удалением одного или более нежелательных компонентов из реакционной среды с получением частично очищенного раствора, содержащего алкилированный циклодекстрин и одну или более примесей, разлагающих лекарственное средство, где одно или более разделений представляют собой ультрафильтрацию, диафильтрацию, центрифугирование, экстракцию, осаждение с растворителем или диализ;
(c) обработку частично очищенного раствора бесфосфатным активированным углем, имеющим проводимость 10 мкСм или менее и получение алкилированного циклодекстрина.
[0092] В настоящем документе термины «партия» или «лот» относятся к дискретному производственному циклу или циклу обработки от начала цикла обработки до конца цикла обработки. Согласно некоторым вариантам реализации в настоящем изобретении предложен способ получения более одного лота композиции алкилированного циклодекстрина, содержащей алкилированный циклодекстрин, включающий: (а) смешивание циклодекстрина с алкилирующим агентом с получением реакционной среды, содержащей алкилированный циклодекстрин, один или более нежелательных компонентов и одну или более примесей, разлагающих лекарственное средство; (b) проведение одного или более разделений с удалением одного или более нежелательных компонентов из реакционной среды с получением частично очищенного раствора, содержащего алкилированный циклодекстрин и одну или более примесей, разлагающих лекарственное средство, где одно или более разделений представляют собой ультрафильтрацию, диафильтрацию, центрифугирование, экстракцию, осаждение с растворителем или диализ; (с) обработку указанного частично очищенного раствора бесфосфатным активированным углем, имеющим остаточную проводимость 10 мкСм или менее и получение лота алкилированного циклодекстрина; и (d) повторение (а)-(с) с получением другого лота композиции алкилированного циклодекстрина.
[0093] Согласно некоторым вариантам реализации указанные более одного лота композиции алкилированного циклодекстрина представляют собой по меньшей мере 4 лота, по меньшей мере 5 лотов, по меньшей мере 6 лотов, по меньшей мере 7 лотов, по меньшей мере 8 лотов, по меньшей мере 9 лотов, по меньшей мере 10 лотов, по меньшей мере 11 лотов, по меньшей мере 12 лотов, по меньшей мере 13 лотов, по меньшей мере 14 лотов, по меньшей мере 15 лотов, по меньшей мере 16 лотов, по меньшей мере 17 лотов, по меньшей мере 18 лотов, по меньшей мере 19 лотов, по меньшей мере 20 лотов, по меньшей мере 30 лотов, по меньшей мере 40 лотов, по меньшей мере 50 лотов, по меньшей мере 60 лотов, по меньшей мере 70 лотов, по меньшей мере 80 лотов, по меньшей мере 90 лотов или по меньшей мере 100 лотов. Согласно некоторым вариантам реализации указанные более одного лота композиции алкилированного циклодекстрина представляют собой от 4 до 100 лотов, от 10 до 100 лотов, от 20 до 100 лотов, от 30 до 100 лотов, от 40 до 100 лотов, от 50 до 100 лотов, от 10 до 20 лотов, от 10 до 30 лотов, от 10 до 40 лотов или от 10 до 50 лотов.
[0094] Согласно некоторым вариантам реализации 50% или более лотов указанной композиции алкилированного циклодекстрина имеют содержание хлоридов менее 0,1% (масс./масс.), 65% или более лотов указанной композиции алкилированного циклодекстрина имеют содержание хлоридов менее 0,1% (масс./масс.), 75% или более лотов указанной композиции алкилированного циклодекстрина имеют содержание хлоридов менее 0,1% (масс./масс.), 80% или более лотов указанной композиции алкилированного циклодекстрина имеют содержание хлоридов менее 0,1% (масс./масс.), 85% или более лотов указанной композиции алкилированного циклодекстрина имеют содержание хлоридов менее 0,1% (масс./масс.), 90% или более лотов указанной композиции алкилированного циклодекстрина имеют содержание хлоридов менее 0,1% (масс./масс.), 95% или более лотов указанной композиции алкилированного циклодекстрина имеют содержание хлоридов менее 0,1% (масс./масс.), 98% или более лотов указанной композиции алкилированного циклодекстрина имеют содержание хлоридов менее 0,1% (масс./масс.), 50% или более лотов указанной композиции алкилированного циклодекстрина имеют содержание хлоридов менее 0,08% (масс./масс.), 65% или более лотов указанной композиции алкилированного циклодекстрина имеют содержание хлоридов менее 0,08% (масс./масс.), 75% или более лотов указанной композиции алкилированного циклодекстрина имеют содержание хлоридов менее 0,08% (масс./масс.), 80% или более лотов указанной композиции алкилированного циклодекстрина имеют содержание хлоридов менее 0,08% (масс./масс.), 85% или более лотов указанной композиции алкилированного циклодекстрина имеют содержание хлоридов менее 0,08% (масс./масс.), 90% или более лотов указанной композиции алкилированного циклодекстрина имеют содержание хлоридов менее 0,08% (масс./масс.), 95% или более лотов указанной композиции алкилированного циклодекстрина имеют содержание хлоридов менее 0,08% (масс./масс.), 98% или более лотов указанной композиции алкилированного циклодекстрина имеют содержание хлоридов менее 0,08% (масс./масс.), 50% или более лотов указанной композиции алкилированного циклодекстрина имеют содержание хлоридов менее 0,05% (масс./масс.), 65% или более лотов указанной композиции алкилированного циклодекстрина имеют содержание хлоридов менее 0,05% (масс./масс.), 75% или более лотов указанной композиции алкилированного циклодекстрина имеют содержание хлоридов менее 0,05% (масс./масс.), 80% или более лотов указанной композиции алкилированного циклодекстрина имеют содержание хлоридов менее 0,05% (масс./масс.), 85% или более лотов указанной композиции алкилированного циклодекстрина имеют содержание хлоридов менее 0,05% (масс./масс.), 90% или более лотов указанной композиции алкилированного циклодекстрина имеют содержание хлоридов менее 0,05% (масс./масс.), 95% или более лотов указанной композиции алкилированного циклодекстрина имеют содержание хлоридов менее 0,05% (масс./масс.) или 98% или более лотов указанной композиции алкилированного циклодекстрина имеют содержание хлоридов менее 0,05% (масс./масс.).
[0095] Согласно некоторым вариантам реализации лоты указанной композиции алкилированного циклодекстрина получают последовательно.
Получение композиции алкилированного циклодекстрина
[0096] В настоящем изобретении описаны несколько способов получения композиции алкилированного циклодекстрина. В целом, исходный материл недериватизированного циклодекстрина подвергается действию предшественника заместителя в средах от нейтральных до щелочных. Предшественник заместителя можно добавлять постепенно или за один раз; кроме того, предшественник заместителя можно добавлять до, во время или после воздействия на исходный циклодекстрин необязательно щелочной водной среды. Для поддержания pH в требуемом диапазоне возможно добавление дополнительного количества щелочного или буферирующего вещества. Реакцию получения производных можно проводить при температуре от температуры окружающей среды до повышенных температур. После того, как дериватизация прошла в требуемой степени, ее можно гасить путем добавления кислоты. Реакционную среду подвергают дополнительной обработке (например, осаждению растворителями, фильтрованию, центрифугированию, упариванию, концентрированию, высушиванию, хроматографии, диализу и/или ультрафильтрации) для удаления нежелательных веществ и получения целевой композиции. После завершения обработки композиция может быть в форме твердого вещества, жидкости, полутвердого вещества, геля, сиропа, пасты, порошка, агрегата, гранул, пеллет, прессованного материала, восстанавливаемого разведением твердого вещества, суспензии, стекла, кристаллической массы, аморфной массы, дисперсных частиц, дробинок, эмульсии или влажной массы.
[0097] В настоящем изобретении предложен способ получения композиции алкилированного циклодекстрина, содержащей алкилированный циклодекстрин, который необязательно может иметь заданную степень замещения, включающий: комбинирование исходного незамещенного циклодекстрина с алкилирующим агентом в количестве, достаточном для достижения заданной степени замещения, в присутствии гидроксида щелочного металла; проведение алкилирования указанного циклодекстрина при pH от 9 до 11 до тех пор, пока не останется менее 0,5% по массе или менее 0,1%, непрореагировавшего циклодекстрина; добавление дополнительного количества гидроксида в количестве, достаточном для достижения требуемой степени замещения и позволяющем реакции алкилирования пройти до конца; добавление дополнительного количества гидроксида для полного разрушения остатков алкилирующего агента.
[0098] Добавление дополнительного количества гидроксида может быть проведено с использованием такого количества гидроксида и при таких условиях (т.е. дополнительного количества добавляемого гидроксида, температуры, времени проведения гидролиза алкилирующего агента), которые обеспечивают снижение количества остаточного алкилирующего агента в неочищенном водном продукте до уровня менее 20 ppm или менее 2 ppm.
[0099] Существует возможность, что реакционная среда или частично очищенный водный раствор будет содержать непрореагировавший алкилирующий агент. Алкилирующий агент может быть разложен in situ путем добавления дополнительного количества подщелачивающего агента или путем нагревания раствора, содержащего указанный агент. Разложение избытка алкилирующего агента потребуется в случае, если после прекращения перемешивания в реакционной среде присутствует недопустимое количество указанного алкилирующего агента. Алкилирующий агент может быть разложен in situ путем добавления дополнительного количества подщелачивающего агента или путем нагревания раствора, содержащего указанный агент.
[00100] Разложение можно проводить путем: действия высокой температуры - по меньшей мере 60°C, по меньшей мере 65°C или от 60°C до 85°C, от 60°C до 80°C или от 60°C до 95°C, на реакционную среду в течение по меньшей мере 6 ч, по меньшей мере 8 ч, от 8 ч до 12 ч, от 6 ч до 72 ч или от 48 ч до 72 ч, что вызывает разложение алкилирующего агента in situ и снижение количества или удаление алкилирующего агента из водной среды.
[0100] После проведения реакции как описано в настоящем документе, водную вреду, содержащую алкилированный циклодекстрин, можно нейтрализовать до pH 7 с целью гашения реакции. Затем раствор может быть разбавлен водой для снижения вязкости, особенно если требуется провести дальнейшую очистку. Дальнейшую очистку можно проводить различными методами, включая следующие методы, но не ограничиваясь ими: диафильтрация на установке для ультрафильтрации для освобождения раствора от побочных продуктов реакции, таких как соли (например, NaCl, если в качестве основания использовали гидроксид натрия) и другие низкомолекулярные побочные продукты. Продукт может быть дополнительно концентрирован путем ультрафильтрации. Затем раствор продукта может быть обработан активированным углем для улучшения цвета, снижения содержания биологических компонентов и удаления существенной доли одной или более примесей, разлагающих лекарственное средство. Продукт может быть выделен подходящим методом сушки, таким как лиофилизации, распылительная сушка или сушка с помощью вакуумного барабана.
[0101] Реакционную смесь можно получать путем растворения исходного незамещенного α -, β- или γ-циклодекстрина в водном растворе основания, обычно гидроксида, в частности, гидроксида лития, натрия или калия. Основание используют в каталитическом количестве (т.е. при мольном отношении к циклодекстрину менее 1:1), которое выбирают так, чтобы получить заданную или требуемую степень замещения. То есть, основание присутствует в количестве менее одного мольного экв. на каждый гидроксил, подлежащий дериватизации в молекуле циклодекстрина. Поскольку растворимость циклодекстринов в водных растворах увеличивается при повышении температуры, для обеспечения полноты растворения водную реакционную смесь, содержащую основание и циклодекстрин, необходимо нагреть до температуры -50°C. Как правило, в ходе реакции алкилирования используют перемешивание.
[0102] После завершения растворения вводят алкилирующий агент, чтобы начать реакцию алкилирования. Общее количество алкилирующего агента, вводимого в ходе реакции, как правило, превышает стехиометрическое количество, требуемое для завершения реакции, относительно количества циклодекстрина, поскольку некоторая часть алкилирующего агента гидролизуется и/или разрушается/разлагается другим образом в ходе реакции и за счет этого становится недоступна для использования в реакции алкилирования. Точное количество алкилирующего агента, которое необходимо использовать для достижения требуемой степени замещения, можно определить в пробных экспериментах. Полное количество алкилирующего агента, требуемое для полного завершения реакции, может быть введено до начала реакции. Поскольку используют водную систему, реакцию, как правило, проводят при температуре между 50°C и 100°C. Реакцию можно проводить при температуре менее 100°C, чтобы не возникала необходимость использовать специальное оборудование для работы под давлением. В целом, подходят температуры от 65°C до 95°С.
[0103] На начальной фазе реакции (называемой далее фазой с контролем pH) следует тщательно следить за величиной pH и поддерживать ее по меньшей мере в области основных значений, либо в диапазоне pH от 8 до 11. Следить за величиной pH можно традиционными методами с использованием стандартного pH-метра. Корректировку pH можно осуществлять путем добавления водного раствора гидроксида, например, 10-15% раствора. В ходе начальной фазы с контролем pH непрореагировавший циклодекстрин взаимодействует в такой степени, что в растворе остается менее 0,5% по массе или менее 0,1% по массе, непрореагировавшего циклодекстрина. Таким образом, по существу все исходное количество циклодекстрина вступает в реакцию частичного замещения, но степень замещения при этом меньше, чем требуемая заданная степень замещения. Количество остаточного циклодекстрина можно отслеживать на протяжении этой начальной фазы, например, с помощью ВЭЖХ, как описано ниже, до достижения требуемой конечной точки, составляющей менее 0,5% или менее 0,1%, остаточного исходного циклодекстрина. Значение pH можно поддерживать и/или повышать путем добавления концентрированного раствора гидроксида к реакционной среде; указанное добавление можно осуществлять непрерывно или отдельными небольшими порциями. Особо рекомендуется проводить добавление отдельными небольшими порциями.
[0104] После стандартизации или оптимизации процедуры алкилирования, когда уже известно, какие конкретно количества реагентов можно использовать в процедуре для получения требуемой степени замещения наряду с низким содержанием остаточного циклодекстрина, процедуру достаточно контролировать после его завершения, а не на начальной стадии с контролем pH, чтобы гарантировать достижение низкого уровня остаточного (непрореагировавшего) исходного циклодекстрина. В следующей таблице описана связь между количеством бутансультона, загружаемого в реактор, и получаемой в результате средней степенью замещения SAE-CD.
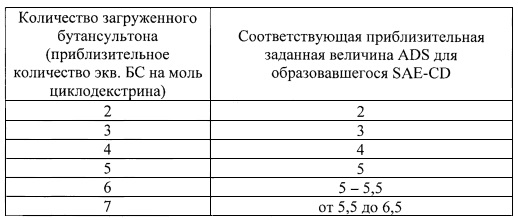

[0105] Следует отметить, что исходное значение pH реакционной среды может превышать 11, например, после комбинирования исходного загруженного количества исходного циклодекстрина и основания, но до добавления алкилирующего агента. Однако после добавления алкилирующего агента и начала реакции pH быстро снижается, что приводит к необходимости добавления основания для поддержания основного значения pH от 8 до 11.
[0106] После достижения требуемого уровня остаточного непрореагировавшего циклодекстрина, например, ниже 0,5 масс. %, в ходе фазы с контролем pH, значение pH можно увеличить выше 11, например до уровня выше 12, путем добавления дополнительного количества основания, чтобы заставить реакцию пройти до конца. Значение pH может быть по меньшей мере 12, чтобы реакция протекала с приемлемой скоростью, но не таким высоким, чтобы непрореагировавший алкилирующий агент быстро гидролизовался, вместо того чтобы реагировать с цикл о декстрином. В ходе этой последней фазы реакции происходит дополнительное замещение молекулы циклодекстрина, пока не будет достигнута заданная степень замещения. Суммарное количество гидроксида, добавляемого в ходе реакции, как правило, составляет порядка требуемого по стехиометрии плюс 10-20%-ный мольный избыток относительно количества используемого алкилирующего агента. Возможно также добавление более чем 10-20%-ного избытка. Как упоминалось выше, конечную точку реакции можно определять с помощью ВЭЖХ. Подходящая температура составляет от 65°C до 95°C. В системе ВЭЖХ обычно используется анионообменная аналитическая колонка с регистрацией методом импульсной амперометрии (PAD). Элюирование можно производить с использованием градиента в системе из двух растворителей, например, растворитель А - 25 мМ (миллимолярный) водный раствор гидроксида натрия, растворитель Б - 1 М раствор нитрата натрия в 250 мМ растворе гидроксида натрия.
[0107] После завершения реакции алкилирования и достижения конечной точки с низким остаточным содержанием циклодекстрина можно добавлять дополнительное количество гидроксида для разрушения и/или разложения всего алкилирующего агента, оставшегося в растворе. Дополнительный гидроксид обычно добавляют в количестве от 0,5 до 3 мольных экв. относительно циклодекстрина; нагрев реакционной смеси продолжают при 65°C - 95°C, как правило, в течение 6-72 часов.
[0108] После разложения остаточного алкилирующего агента полученный неочищенный продукт можно дополнительно обработать с получением конечного продукта путем разбавления, диафильтрации для уменьшения количества или полной очистки продукта от низкомолекулярных компонентов, таких как соли, концентрирования, обработки углем и высушивания.
[0109] В начале процесса pH контролируется, чтобы в процессе протекания реакции алкильной дериватизации значение pH оставалось в диапазоне от 8 до 11. На этой начальной стадии гидроксид, предназначенный для облегчения реакции алкилирования, можно добавлять поэтапно или порциями. Контролирование pH реакции позволяет обеспечить возможность контроля данной реакции таким образом, что практически весь исходный циклодекстрин прореагирует, давая, в среднем, степень замещения по меньшей мере одну алкильную группу на молекулу циклодекстрина. Таким образом, реагент циклодекстрина полностью расходуется в начале процесса, так что уровень остаточного (непрореагировавшего) циклодекстрина в неочищенном продукте оказывается мал по сравнению с его содержанием в неочищенным продукте, получаемом с помощью процесса, характеризующегося первоначальным смешиванием стехиометрического или превышающего стехиометрическое количества основания с циклодекстрином и алкилирующим агентом, а также неконтролируемым протеканием реакции. После того, как весь исходный загруженный циклодекстрин частично прореагировал, можно добавить оставшийся гидроксид для доведения реакции до конца, с тем чтобы получить заданную требуемую степень замещения алкилом. После того, как исходное загруженное количество циклодекстрина израсходовано на первой фазе с контролем pH, скорость дальнейшего добавления гидроксида уже не существенна. Таким образом, гидроксид можно вводить (например, в виде раствора) непрерывно или отдельными порциями. Кроме того, pH реакционной среды необходимо поддерживать на уровне около 12, чтобы скорость реакции была приемлемой с коммерческой точки зрения.
Снижение количества и удаление примесей в композиции циклодекстрина
[0110] Контроль pH на начальной фазе позволяет уменьшить количество некоторых побочных продуктов в реакционной смеси. Например, в результате алкилирования выделяется кислота, и pH реакционной смеси снижается (т.е. среда становится кислой) по мере протекания реакции. С одной стороны, реакционную смесь поддерживают в области основных значений, поскольку если реакционная смесь становится кислой, реакция существенно замедляется или прекращается. Соответственно, pH реакционной смеси следует поддерживать на уровне по меньшей мере 8 путем добавления по мере необходимости водного раствора гидроксида. С другой стороны, если допустить возрастание pH выше некоторого уровня, например, выше 12, реакция может приводить к образованию большого количество побочных продуктов, например, 4-гидроксиалкилсульфоната и бис-сульфоалкильного эфира, что приводит к расходованию исходного алкилирующего агента. Путем контроля pH реакционного раствора и поддержания pH в пределах 8-12, либо 8-11, реакция протекает с образованием относительно небольшого количества побочных продуктов, приводя к получению относительно чистой реакционной смеси, содержащей относительно небольшое количество указанных выше побочных продуктов.
[0111] Сделанное выше упоминание о том, что реагент используется в количестве, «требуемом по стехиометрии» и т.п., относится к количеству реагента, требуемому для полной дериватизации рассматриваемого циклодекстрина до требуемой степенью замещения. В настоящем документе «гидроксид щелочного металла» относится к LiOH, NaOH, KOH и т.п. Если требуется получить продукт, подходящий для парентерального введения, можно использовать NaOH.
[0112] Степень замещения можно контролировать путем использования соответственно меньшего или большего количества алкилирующего агента в зависимости от того, требуется ли более низкая или более высокая степень замещения, соответственно. В целом, в среднем можно достичь степени замещения от 4,5 до 7,5, от 5,5 до 7,5 или от 6 до 7,1.
[0113] Неочищенный продукт процесса, описываемого в настоящем документе, т.е. продукт, получаемый после разрушения остаточного алкилирующего агента, содержит более низкое количество остаточного циклодекстрина по сравнению с продуктом, полученным в процессе, при котором основание добавляют в начале одной порцией, что является еще одним отличительным признаком настоящего изобретения. Неочищенный продукт, получаемый с помощью способа согласно настоящему изобретению, как правило, содержит менее 0,5 масс. % или менее 0,1%, остаточного циклодекстрина. Как объясняется ниже, неочищенный продукт также обладает тем преимуществом, что содержит очень низкое количество остаточного алкилирующего агента.
[0114] Как правило, водный раствор неочищенного продукта циклодекстрина, полученный после разложения остаточного алкилирующего агента, очищают посредством ультрафильтрации, процесса, при котором неочищенный продукт приводят в контакт с полупроницаемой мембраной, способной пропускать низкомолекулярные примеси. Молекулярная масса примесей, пропускаемых через мембрану, зависит от границы пропускания мембраны. Для данного изобретения обычно используют мембрану с границей пропускания 1000 Дальтонов («Да»). Диафильтрацию и/или ультрафильтрацию можно проводить при помощи фильтрующих мембран с границей пропускания 500-2000 Да, 500-1500 Да, 750-1250 Да или 900-1100 Да или около 1000 Да. Требуемый продукт, содержащийся в ретентате, затем подвергают дальнейшей обработке активированным углем для по существу полного удаления примесей, разлагающих лекарственные средства. Неочищенный водный раствор продукта циклодекстрина (т.е. раствор, получаемый после разрушения остаточного алкилирующего агента, но до очистки) обладает тем преимуществом, что он содержит менее 2 ррт остаточного алкилирующего агента в расчете на массу раствора или менее 1 ppm, или менее 250 ppb. Неочищенный раствор может также практически не содержать остаточного алкилирующего агента.
[0115] Конечный товарный продукт может быть выделен на любом этапе, например, путем фильтрования для удаления активированного угля с последующим упариванием воды (например, посредством отгонки, распылительной сушки, лиофилизации и т.п.). Преимуществом конечного продукта, получаемого согласно настоящему изобретению, является очень низкое остаточное содержание алкилирующего агента, например, менее 2 ppm в расчете на массу сухого (т.е. содержащего менее 10% воды по массе) конечного продукта или менее 1 ppm, или менее 250 ppb, или по существу полное отсутствие остаточного алкилирующего агента. Конечный продукт, содержащий менее 250 ppb алкилирующего агента, соответственно является дополнительным отличительным признаком настоящего изобретения. После завершения алкилирования до достижения требуемой степени замещения алкилирующий агент восстанавливают путем гидролизующей щелочной обработки, как описано выше, т.е. путем дополнительного добавления гидроксида в количестве и при условиях, достаточных для снижения количества непрореагировавшего алкилирующего агента в сухом продукте до требуемого уровня ниже 2 ppm, ниже 1 ppm или ниже 250 ppb.
[0116] Активированный уголь, подходящий для использования в способе согласно настоящему изобретению, может не содержать фосфатов, а также может быть порошкообразным или гранулированным, или представлять собой суспензию или пастообразную смесь, приготовленную из такого угля. В целом, не содержащий фосфатов активированный уголь представляет собой уголь, не подвергавшийся активированию фосфорной кислотой, либо другому ее воздействию.
[0117] Существует широкий ассортимент активированных углей. Например, компания Norit-Americas промышленно выпускает более 150 различных сортов и разновидностей активированного угля под товарными знаками Darco®, Hydrodarco®, Norit®, Bentonorit®, Petrodarco® и Sorbonorit®. Указанные угли различаются по размеру частиц, области применения, методу активации и эффективности. Например, некоторые активированные угли оптимизированы для удаления окраски и/или запаха. Другие активированные угли оптимизированы для удаления белков, фрагментов минеральных кислот и/или аминокислот, либо для осветления растворов.
[0118] Для использования в настоящем изобретении подходят, но не ограничиваются ими, следующие активированные угли: гранулированный уголь Darco® 4×12, 12×20 или 20×40 из лигнита, активированный паром (Norit Americas, Inc., Amersfoort, NE); Darco® S 51 HF (из лигнита, активированный паром, порошок), а также Shirasagi® DC-32, порошкообразный или гранулированный уголь из дерева, активированный хлоридом цинка (Takeda Chemical Industries, Ltd., Osaka, JP).
[0119] Угли, активированные фосфорной кислотой и использовавшиеся в уровне технике для очистки алкильных эфиров циклодекстрина, как правило, не подходят для использования в настоящем изобретении; к ним относятся: Darco® KB-G, Darco® KB-B и Darco® KB-WJ, а также Norit® CASP и Norit® CN1.
[0120] Согласно некоторым вариантам реализации содержание фосфатов в указанной композиции алкилированного циклодекстрина составляет менее 200 ppm, менее 150 ppm, менее 125 ppm, менее 100 ppm, менее 95 ppm, менее 90 ppm, менее 85 ppm, менее 80 ppm, менее 75 ppm, менее 70 ppm, менее 65 ppm, менее 60 ppm, менее 55 ppm, менее 50 ppm, менее 45 ppm, менее 40 ppm, менее 35 ppm, менее 30 ppm, менее 25 ppm, менее 20 ppm, менее 15 ppm, менее 10 ppm или менее 5 ppm. Согласно некоторым вариантам реализации содержание фосфатов в указанной композиции алкилированного циклодекстрина составляет от 200 ppm до 5 ppm, от 150 ppm до 5 ppm, от 125 ppm до 5 ppm, от 100 ppm до 5 ppm, от 75 ppm до 5 ppm, о 50 ppm до 5 ppm, от 150 ppm до 10 ppm, от 125 ppm до 10 ppm, от 100 ppm до 10 ppm или от 75 ppm до 10 ppm.
[0121] Относительное количество загружаемого активированного угля, в конечном счете, зависит от количества или концентрации алкилированного циклодекстрина, окрашивающих агентов и примесей, разлагающих лекарственные средства, а также от физических свойств используемого активированного угля. В целом, массовое соотношение циклодекстрина к активированному углю на каждом цикле обработки составляет от 5:1 до 10:1, от 6:1 до 9:1, от 7:1 до 9:1, от 8:1 до 9:1, от 8,3:1 до 8,5:1, от 8,4:1 до 8,5:1 или 8,44:1 по массе.
[0122] Используемый в настоящем документе термин «цикл обработки» относится к приведению в контакт заданного количества композиции циклодекстрина с заранее количеством активированного угля. Цикл обработки можно осуществлять в виде одной обработки или многократной (с возвратом) проточной обработки.
[0123] В примерах, приводимых в настоящем документе, подробно описаны процедуры, используемые для оценки и сравнения эффективности различных сортов, лотов, источников и типов активированного угля при удалении одной или более примесей, разлагающих лекарственные средства, и одного или более окрашивающих компонентов, присутствующих в реакционной среде или в растворе SAE-CD. В целом, реакционная среда или раствор обрабатывают активированным углем при перемешивании в течение 120 мин. Если используется сыпучий, мелкодисперсный или порошкообразный активированный уголь, он может быть удален путем фильтрования жидкости, содержащей уголь, через фильтрующий материал с получением осветленного раствора.
[0124] Фильтрующие мембраны могут быть изготовлены из нейлона, тефлона (Teflon®), поливинилиденфторида (PVDF) или другого совместимого материала. Размер пор в фильтрующей мембране при необходимости можно варьировать в зависимости от размера или молекулярной массы частиц, отделяемых от раствора, содержащего SAE-CD.
[0125] В приводимых в настоящем документе примерах подробно описаны методики одного или более процессов разделения и/или очистки водной реакционной среды согласно настоящему изобретению. Реакционную среду разбавляют водным раствором и подвергают диафильтрации, во время которой объем ретентата поддерживают по существу постоянным. Диафильтрацию можно проводить через фильтр на 1000 Да, так чтобы один или более нежелательных компонентов проходили через фильтр, но основная часть алкильного эфира, присутствующего в композиции алкилированного циклодекстрина, оставалась в ретентате, а не проходила через фильтр вместе с фильтратом. Затем проводят ультрафильтрацию, при которой объем ретентата уменьшается, а концентрация в ретентате тем самым увеличивается. Фильтр с границей пропускания по молекулярной массе около 1000 Да можно также использовать для ультрафильтрации. Ретентат содержит алкилированный циклодекстрин, который затем может быть подвергнут обработке активированным углем, как описано в настоящем документе.
[0126] Один или более нежелательных компонентов могут включать, не ограничиваться ими, низкомолекулярные примеси (т.е. примеси с молекулярной массой 500 Да или менее), водорастворимые и/или нерастворимые ионы (т.е. соли), гидролизованный сульфоалкилирующий агент, 5-(гидроксиметил)-2-фуральдегид, непрореагировавший исходный циклодекстрин, продукты разложения циклодекстрина (например, продукты разложения и/или разрыва колец, образующиеся из непрореагировавшего циклодекстрина, частично прореагировавшего циклодекстрина и/или SAE-CD), непрореагировавший алкилирующий агент (например, 1,4-бутансультон) и их комбинации.
[0127] Согласно некоторым вариантам реализации композиции согласно настоящему изобретению по существу не содержат один или более агентов, разлагающих лекарственное средство. Присутствие одного или более агентов, разлагающих лекарственное средство, можно определить, inter alia, с помощью спектрофотометрии в УФ/видимой области («УФ/вид.обл.»). В настоящем документе «агент, разлагающий лекарственное средство» или «примесь, разлагающая лекарственное средство» относится к молекуле, фрагменту, и тому подобному, которая разлагает некоторые активные компоненты в водном растворе. Следует понимать, что агент, разлагающий лекарственное средство, может разлагать не все лекарственные средства, с которыми можно комбинировать композицию алкилированного циклодекстрина, в зависимости от химической структуры лекарственного средства и механизма разложения. Согласно некоторым вариантам реализации молекула, разлагающая лекарственное средство, имеет оптическую плотность в УФ/видимой области спектра, например, максимум оптической плотности при длине волны от 245 нм до 270 нм.
[0128] Присутствие агентов, разлагающих лекарственное средство, в композиции алкилированного циклодекстрина можно измерить в единицах поглощения (Е.П.) в УФ/видимой области спектра. Согласно некоторым вариантам реализации указанная композиция алкилированного циклодекстрина имеет оптическую плотность менее 1 Е.П., менее 0,9 Е.П., менее 0,8 Е.П., менее 0,7 Е.П., менее 0,6 Е.П., 0,5 Е.П., менее 0,4 Е.П., менее 0,3 Е.П., менее 0,2 Е.П. или менее 0,1 Е.П.
[0129] Оптическая плотность раствора становится линейной от концентрации согласно формуле:
А=εlc
где
А = оптическая плотность
ε = коэффициент поглощения
l = толщина поглощающего слоя (длина оптического пути)
c = мольная концентрация.
[0130] Присутствие агента, разлагающего лекарственное средство, в композиции алкилированного циклодекстрина можно измерять с помощью спектрофотометрии в УФ/видимой области в диапазоне длин волн 245 до 270 нм с использованием кюветы, имеющей толщину поглощающего слоя 1 см. Согласно некоторым вариантам реализации композиция алкилированного циклодекстрина имеет оптическую плотность менее 1 Е.П. при длине волны от 245 нм до 270 нм для водного раствора, содержащего 200 мг композиции алкилированного циклодекстрина на мл раствора, менее 1 Е.П. при длине волны от 245 нм до 270 нм для водного раствора, содержащего 300 мг композиции алкилированного циклодекстрина на мл раствора, менее 1 Е.П. при длине волны от 245 нм до 270 нм для водного раствора, содержащего 400 мг композиции алкилированного циклодекстрина на мл раствора, менее 1 Е.П. при длине волны от 245 нм до 270 нм для водного раствора, содержащего 500 мг композиции алкилированного циклодекстрина на мл раствора, 0,9 Е.П. или менее при длине волны от 245 нм до 270 нм для водного раствора, содержащего 200 мг композиции алкилированного циклодекстрина на мл раствора, 0,9 Е.П. или менее при длине волны от 245 нм до 270 нм для водного раствора, содержащего 300 мг композиции алкилированного циклодекстрина на мл раствора, 0,9 Е.П. или менее при длине волны от 245 нм до 270 нм для водного раствора, содержащего 400 мг композиции алкилированного циклодекстрина на мл раствора, 0,9 Е.П. или менее при длине волны от 245 нм до 270 нм для водного раствора, содержащего 500 мг композиции алкилированного циклодекстрина на мл раствора, 0,8 Е.П. или менее при длине волны от 245 нм до 270 нм для водного раствора, содержащего 200 мг композиции алкилированного циклодекстрина на мл раствора, 0,8 Е.П. или менее при длине волны от 245 нм до 270 нм для водного раствора, содержащего 300 мг композиции алкилированного циклодекстрина на мл раствора, 0,8 Е.П. или менее при длине волны от 245 нм до 270 нм для водного раствора, содержащего 400 мг композиции алкилированного циклодекстрина на мл раствора, 0,8 Е.П. или менее при длине волны от 245 нм до 270 нм для водного раствора, содержащего 500 мг композиции алкилированного циклодекстрина на мл раствора, 0,7 Е.П. или менее при длине волны от 245 нм до 270 нм для водного раствора, содержащего 200 мг композиции алкилированного циклодекстрина на мл раствора, 0,7 Е.П. или менее при длине волны от 245 нм до 270 нм для водного раствора, содержащего 300 мг композиции алкилированного циклодекстрина на мл раствора, 0,7 Е.П. или менее при длине волны от 245 нм до 270 нм для водного раствора, содержащего 400 мг композиции алкилированного циклодекстрина на мл раствора, 0,7 Е.П. или менее при длине волны от 245 нм до 270 нм для водного раствора, содержащего 500 мг композиции алкилированного циклодекстрина на мл раствора, 0,6 Е.П. или менее при длине волны от 245 нм до 270 нм для водного раствора, содержащего 200 мг композиции алкилированного циклодекстрина на мл раствора, 0,6 Е.П. или менее при длине волны от 245 нм до 270 нм для водного раствора, содержащего 300 мг композиции алкилированного циклодекстрина на мл раствора, 0,6 Е.П. или менее при длине волны от 245 нм до 270 нм для водного раствора, содержащего 400 мг композиции алкилированного циклодекстрина на мл раствора, 0,6 Е.П. или менее при длине волны от 245 нм до 270 нм для водного раствора, содержащего 500 мг композиции алкилированного циклодекстрина на мл раствора, 0,5 Е.П. или менее при длине волны от 245 нм до 270 нм для водного раствора, содержащего 200 мг композиции алкилированного циклодекстрина на мл раствора, 0,5 Е.П. или менее при длине волны от 245 нм до 270 нм для водного раствора, содержащего 300 мг композиции алкилированного циклодекстрина на мл раствора, 0,5 Е.П. или менее при длине волны от 245 нм до 270 нм для водного раствора, содержащего 400 мг композиции алкилированного циклодекстрина на мл раствора, 0,5 Е.П. или менее при длине волны от 245 нм до 270 нм для водного раствора, содержащего 500 мг композиции алкилированного циклодекстрина на мл раствора, 0,4 Е.П. или менее при длине волны от 245 нм до 270 нм для водного раствора, содержащего 200 мг композиции алкилированного циклодекстрина на мл раствора, 0,4 Е.П. или менее при длине волны от 245 нм до 270 нм для водного раствора, содержащего 300 мг композиции алкилированного циклодекстрина на мл раствора, 0,4 Е.П. или менее при длине волны от 245 нм до 270 нм для водного раствора, содержащего 400 мг композиции алкилированного циклодекстрина на мл раствора, 0,4 или менее Е.П. при длине волны от 245 нм до 270 нм для водного раствора, содержащего 500 мг композиции алкилированного циклодекстрина на мл раствора, 0,3 Е.П. или менее при длине волны от 245 нм до 270 нм для водного раствора, содержащего 200 мг композиции алкилированного циклодекстрина, 0,3 Е.П. или менее при длине волны от 245 нм до 270 нм для водного раствора, содержащего 300 мг композиции алкилированного циклодекстрина на мл раствора, 0,3 Е.П. или менее при длине волны от 245 нм до 270 нм для водного раствора, содержащего 400 мг композиции алкилированного циклодекстрина на мл раствора, 0,3 Е.П. или менее при длине волны от 245 нм до 270 нм для водного раствора, содержащего 500 мг композиции алкилированного циклодекстрина на мл раствора, 0,2 Е.П. или менее при длине волны от 245 нм до 270 нм для водного раствора, содержащего 200 мг композиции алкилированного циклодекстрина на мл раствора, 0,2 Е.П. или менее при длине волны от 245 нм до 270 нм для водного раствора, содержащего 300 мг композиции алкилированного циклодекстрина на мл раствора, 0,2 Е.П. или менее при длине волны от 245 нм до 270 нм для водного раствора, содержащего 400 мг композиции алкилированного циклодекстрина на мл раствора или 0,2 Е.П. или менее при длине волны от 245 нм до 270 нм для водного раствора, содержащего 500 мг композиции алкилированного циклодекстрина на мл раствора.
[0131] Присутствие окрашивающего агента в композиции алкилированного циклодекстрина можно измерять с использованием спектрофотометрии в УФ/видимой области в диапазоне длин волн от 320 нм до 350 нм с использованием кюветы, имеющей толщину поглощающего слоя 1 см. Согласно некоторым вариантам реализации композиция алкилированного циклодекстрина имеет оптическую плотность менее 1 Е.П. при длине волны от 320 нм до 350 нм для водного раствора, содержащего 200 мг композиции алкилированного циклодекстрина на мл раствора, менее 1 Е.П. при длине волны от 320 нм до 350 нм для водного раствора, содержащего 300 мг композиции алкилированного циклодекстрина на мл раствора, менее 1 Е.П. при длине волны от 320 нм до 350 нм для водного раствора, содержащего 400 мг композиции алкилированного циклодекстрина на мл раствора, менее 1 Е.П.при длине волны от 320 нм до 350 нм для водного раствора, содержащего 500 мг композиции алкилированного циклодекстрина на мл раствора, 0,9 Е.П. или менее при длине волны от 320 нм до 350 нм для водного раствора, содержащего 200 мг композиции алкилированного циклодекстрина на мл раствора, 0,9 Е.П. или менее при длине волны от 320 нм до 350 нм для водного раствора, содержащего 300 мг композиции алкилированного циклодекстрина на мл раствора, 0,9 Е.П. или менее при длине волны от 320 нм до 350 нм для водного раствора, содержащего 400 мг композиции алкилированного циклодекстрина на мл раствора, 0,9 Е.П. или менее при длине волны от 320 нм до 350 нм для водного раствора, содержащего 500 мг композиции алкилированного циклодекстрина на мл раствора, 0,8 Е.П. или менее при длине волны от 320 нм до 350 нм для водного раствора, содержащего 200 мг композиции алкилированного циклодекстрина на мл раствора, 0,8 Е.П. или менее при длине волны от 320 нм до 350 нм для водного раствора, содержащего 300 мг композиции алкилированного циклодекстрина на мл раствора, 0,8 Е.П. или менее при длине волны от 320 нм до 350 нм для водного раствора, содержащего 400 мг композиции алкилированного циклодекстрина на мл раствора, 0,8 Е.П. или менее при длине волны от 320 нм до 350 нм для водного раствора, содержащего 500 мг композиции алкилированного циклодекстрина на мл раствора, 0,7 Е.П. или менее при длине волны от 320 нм до 350 нм для водного раствора, содержащего 200 мг композиции алкилированного циклодекстрина на мл раствора, 0,7 Е.П. или менее при длине волны от 320 нм до 350 нм для водного раствора, содержащего 300 мг композиции алкилированного циклодекстрина на мл раствора, 0,7 Е.П. или менее при длине волны от 320 нм до 350 нм для водного раствора, содержащего 400 мг композиции алкилированного циклодекстрина на мл раствора, 0,7 Е.П. или менее при длине волны от 320 нм до 350 нм для водного раствора, содержащего 500 мг композиции алкилированного циклодекстрина на мл раствора, 0,6 Е.П. или менее при длине волны от 320 нм до 350 нм для водного раствора, содержащего 200 мг композиции алкилированного циклодекстрина на мл раствора, 0,6 Е.П. или менее при длине волны от 320 нм до 350 нм для водного раствора, содержащего 300 мг композиции алкилированного циклодекстрина на мл раствора, 0,6 Е.П. или менее при длине волны от 320 нм до 350 нм для водного раствора, содержащего 400 мг композиции алкилированного циклодекстрина на мл раствора, 0,6 Е.П. или менее при длине волны от 320 нм до 350 нм для водного раствора, содержащего 500 мг композиции алкилированного циклодекстрина на мл раствора, 0,5 Е.П. или менее при длине волны от 320 нм до 350 нм для водного раствора, содержащего 200 мг композиции алкилированного циклодекстрина на мл раствора, 0,5 Е.П. или менее при длине волны от 320 нм до 350 нм для водного раствора, содержащего 300 мг композиции алкилированного циклодекстрина на мл раствора, 0,5 Е.П. или менее при длине волны от 320 нм до 350 нм для водного раствора, содержащего 400 мг композиции алкилированного циклодекстрина на мл раствора, 0,5 Е.П. или менее при длине волны от 320 нм до 350 нм для водного раствора, содержащего 500 мг композиции алкилированного циклодекстрина на мл раствора, 0,4 Е.П. или менее при длине волны от 320 нм до 350 нм для водного раствора, содержащего 200 мг композиции алкилированного циклодекстрина на мл раствора, 0,4 Е.П. или менее при длине волны от 320 нм до 350 нм для водного раствора, содержащего 300 мг композиции алкилированного циклодекстрина на мл раствора, 0,4 Е.П. или менее при длине волны от 320 нм до 350 нм для водного раствора, содержащего 400 мг композиции алкилированного циклодекстрина на мл раствора, 0,4 Е.П. или менее при длине волны от 320 нм до 350 нм для водного раствора, содержащего 500 мг композиции алкилированного циклодекстрина на мл раствора, 0,3 Е.П. или менее при длине волны от 320 нм до 350 нм для водного раствора, содержащего 200 мг композиции алкилированного циклодекстрина, 0,3 Е.П. или менее при длине волны от 320 нм до 350 нм для водного раствора, содержащего 300 мг композиции алкилированного циклодекстрина на мл раствора, 0,3 Е.П. или менее при длине волны от 320 нм до 350 нм для водного раствора, содержащего 400 мг композиции алкилированного циклодекстрина на мл раствора, 0,3 Е.П. или менее при длине волны от 320 нм до 350 нм для водного раствора, содержащего 500 мг композиции алкилированного циклодекстрина на мл раствора, 0,2 Е.П. или менее при длине волны от 320 нм до 350 нм для водного раствора, содержащего 200 мг композиции алкилированного циклодекстрина на мл раствора, 0,2 Е.П. или менее при длине волны от 320 нм до 350 нм для водного раствора, содержащего 300 мг композиции алкилированного циклодекстрина на мл раствора, 0,2 Е.П. или менее при длине волны от 320 нм до 350 нм для водного раствора, содержащего 400 мг композиции алкилированного циклодекстрина на мл раствора или 0,2 Е.П. или менее при длине волны от 320 нм до 350 нм для водного раствора, содержащего 500 мг композиции алкилированного циклодекстрина на мл раствора.
[0132] Не будучи связанными конкретной теорией, полагают, что агент, вещество или фрагмент, разлагающие лекарственные средства, может включать одно или более низкомолекулярных веществ (например, вещество с молекулярной массой менее 1000 Да), в том числе, не ограничиваясь ими, вещества, образующиеся как побочный продукт и/или продукт разложения в реакционной смеси. В частности, к веществам, разлагающим лекарственные средства, относятся, не ограничиваясь ими, гликозидный фрагмент, молекула циклодекстрина с раскрытым кольцом, восстанавливающий сахар, продукт разложения глюкозы (например, 3,4-дидеоксиглюкозон-3-ен, карбонилсодержащие разлагающие вещества, такие как 2-фуральдегид, 5-гидроксиметил-2-фуральдегид и т.п.), а также их комбинации.
[0133] Согласно некоторым вариантам реализации композиция алкилированного циклодекстрина содержит менее 1 масс. %, менее 0,5 масс. %, менее 0,2 масс. %, менее 0,1 масс. %, менее 0,08 масс. % или менее 0,05 масс. % галогенидной соли щелочного металла.
[0134] Согласно некоторым вариантам реализации указанная композиция алкилированного циклодекстрина содержит менее 1 масс. %, менее 0,5 масс. %, менее 0,25 масс. %, менее 0,1 масс. %, менее 0,08 масс. % или менее 0,05 масс. % гидролизованного алкилирующего агента.
[0135] Согласно некоторым вариантам реализации композиция алкилированного циклодекстрина содержит менее 500 ppm, менее 100 ppm, менее 50 ppm, менее 20 ppm, менее 10 ppm, менее 5 ppm, менее 2 ppm, менее 1 ppm, менее 500 ppb или менее 250 ppb алкилирующего агента.
[0136J Согласно некоторым вариантам реализации композиция алкилированного циклодекстрина содержит менее 0,5 масс. %, менее 0,2 масс. %, менее 0,1 масс. % или менее 0,08 масс. % недериватизированного циклодекстрина.
[0137] Под «входящий в комплекс» понимают «являющийся частью клатрата или комплекса включения с», т.е. «входящее в комплекс» лекарственное средство является частью клатрата или комплекса включения с алкилированным циклодекстрином. Термин «большая часть» означает 50% или больше по массе или по молям. Таким образом, композиция согласно настоящему изобретению может содержать активный агент, более 50 масс. % которого входит в комплекс с алкилированным циклодекстрином, Фактическая процентная доля входящего в комплекс активного агента варьируется в зависимости от константы равновесия комплексообразования, характеризующей комплексообразование конкретного циклодекстрина с конкретным активным агентом. Настоящее изобретение также включает варианты реализации, в которых активный агент не образует в комплекс с циклодекстрином или в которых лишь незначительная доля активного агента образует комплекс с алкилированным циклодекстрином. Следует отметить, что алкилированный циклодекстрин может образовывать одну или несколько ионных связей с положительно заряженным соединением. Такая ионная ассоциация может иметь место независимо от того, связано ли положительно заряженное вещество в комплекс включения с циклодекстрином.
[0138] Как показано на ФИГ. 6, после ультрафильтрации неочищенного продукта SBE-CD, в нем присутствуют примеси, такие как β-циклодекстрин и 4-гидроксибутан-1-сульфоновая кислота (4-HBSA). После второй колонки с активированным углем, количество примесей β-циклодекстрина и 4-гидроксибутан-1-сульфоновой кислоты было снижено. Однако как показано на ФИГ. 6, после двух колонок в продукте присутствуют большие количества хлоридов.
[0139] В процессе очистки с использованием активированного угля, несмотря на то, что количество агентов, разлагающих лекарственное средство, снижается, в продукте алкилированного циклодекстрина присутствуют большие количества хлоридов. Это большое количество хлоридов в продукте алкилированного циклодекстрина может взаимодействовать с активным агентом и приводить к разложению активного агента. Следовательно, необходимо снижать содержание хлоридов в продукте алкилированного циклодекстрина, особенно если активный агент чувствителен к хлоридам.
[0140] Определение того, чувствительно ли активное вещество к хлоридам, может быть осуществлено специалистом в данной области техники с использованием известных методов.
[0141] Как показано на ФИГ. 7, после ультрафильтрации уровень остаточных хлоридов падает приблизительно до нуля. После дальнейшей очистки с использованием двух колонок активированного угля, содержание хлоридов восстанавливается в растворе SBE-CD.
[0142] В ходе очистки активированным углем, вода проходит через колонку активированного угля до установления проводимости га постоянном уровне до добавления раствора SBE-CD. В следующей Таблице приведены подробные данные по количеству воды и полученных уровнях проводимости, измеренных для колонок с активированным углем. Как видно в Таблице, даже в партиях, в которых использовали 70000 литров воды для промывки активированного угля перед добавлением раствора SBE-CD, примеси хлоридов были обнаружены в конечном растворе SBE-CD.
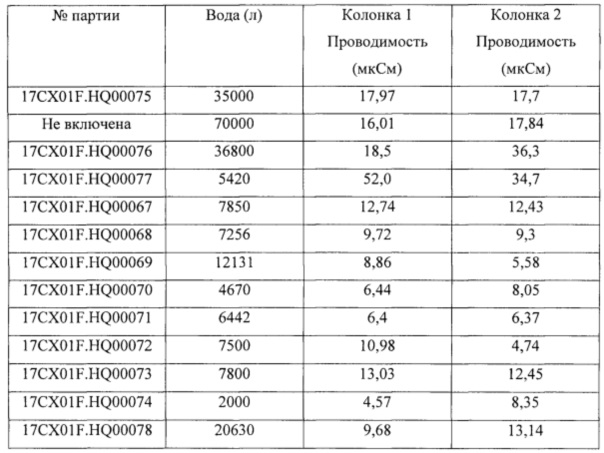
[0143] Более обширное исследование обработки до и в ходе циркуляции с активированным углем показало, что самое большое добавление хлоридов происходит в первые несколько минут циркуляции раствора SBE-CD через слой активированного угля. Как показано на ФИГ. 8, содержание примесей хлоридов у двух коммерческих партий SBE-CD равно приблизительно нулю после ультрафильтрации и значительно возрастает после обработки активированным углем в течение первых 5 минут с падением содержания через 10 и 20 минут.
[0144] Как показано на ФИГ. 9, существует прямая корреляция между уровнем хлоридов, перенесенных в раствор SBE-CD, и уровнем проводимости воды для промывки. На ФИГ. 9 измеряли уровень проводимости в первой колонке с активированным углем и во второй колонке с активированным углем. Было обнаружено, что уровни проводимости соотносятся с уровнем остаточного хлорида в конечном твердом веществе SBE-CD, как измерено с помощью метода ZIC pHILIC для измерения содержания остаточного хлорида. Следовательно, данные измерения проводимости, полученные в конце процесса промывки, соотносятся с уровнем остаточного хлорида в конечном продукте SBE-CD.
[0145] Уровень хлоридов в композиции алкилированного циклодекстрина может быть определен с использованием любого способа, обычно используемого специалистами в данной области техники. Согласно некоторым вариантам реализации уровень хлоридов измеряют с использованием детектора заряженного аэрозоля (CAD).
[0146] Согласно некоторым вариантам реализации уровень хлоридов, измеренный в пересчете на массовое соотношение (масс./масс.), в композиции алкилированного циклодекстрина составляет 1% или менее, 0,9% или менее, 0,8% или менее, 0,7% или менее, 0,6% или менее, 0,5% или менее, 0,4% или менее, 0,3% или менее, 0,2% или менее, 0,1% или менее, 0,09% или менее, 0,08% или менее, 0,07% или менее, 0,06% или менее, 0,05% или менее, 0,04% или менее, 0,03% или менее, 0,02% или менее или 0,01% или менее. Согласно некоторым вариантам реализации уровень хлоридов в композиции алкилированного циклодекстрина составляет от 1% до 0,01%, от 0,9% до 0,01%, от 0,8% до 0,01%, от 0,7% до 0,01%, от 0,6% до 0,01%, от 0,5% до 0,01%, от 0,4% до 0,01%, от 0,3% до 0,01%, от 0,2% до 0,01%, от 0,1% до 0,01%, от 0,09% до 0,01%, от 0,08% до 0,01%, от 0,07% до 0,01%, от 0,06% до от 0,01%, от 0,05% до 0,01%, от 0,04% до 0,01% или от 0,03% до 0,01%.
[0147] Проводимость элюента промывочной воды активированного угля может быть определена с использованием любого способа, обычно используемого специалистами в данной области техники. Согласно некоторым вариантам реализации проводимость измеряют с использованием измерителя проводимости. Согласно некоторым вариантам реализации проводимость измеряют с использованием ионообменной хроматографии.
[0148] Согласно некоторым вариантам реализации проводимость элюента промывочной воды бесфосфатного активированного угля измеряют до добавления частично очищенного раствора алкилированного циклодекстрина. Согласно некоторым вариантам реализации проводимость элюента промывочной воды активированного угля до добавления частично очищенного раствора алкилированного циклодекстрина составляет менее 35 мкСм, менее 34 мкСм, менее 33 мкСм, менее 32 мкСм, менее 31 мкСм, менее 30 мкСм, менее 29 мкСм, менее 28 мкСм, менее 27 мкСм, менее 26 мкСм, менее 25 мкСм, менее 24 мкСм, менее 23 мкСм, менее 22 мкСм, менее 21 мкСм, менее 20 мкСм, менее 19 мкСм, менее 18 мкСм, менее 17 мкСм, менее 16 мкСм, менее 15 мкСм, менее 14 мкСм, менее 13 мкСм, менее 12 мкСм, менее 11 мкСм, менее 10 мкСм, менее 9 мкСм, менее 8 мкСм, менее 7 мкСм, менее 6 мкСм, менее 5 мкСм, менее 4 мкСм, менее 3 мкСм, менее 2 мкСм или менее 1 мкСм. Согласно некоторым вариантам реализации проводимость элюента промывочной воды активированного угля до добавления частично очищенного раствора алкилированного циклодекстрина составляет от 10 мкСм до 15 мкСм, от 5 мкСм до 15 мкСм, от 5 мкСм до 10 мкСм, от 4 мкСм до 10 мкСм, от 3 мкСм до 10 мкСм или от 4 мкСм до 8 мкСм.
[0149] Согласно некоторым вариантам реализации активированный уголь промывают 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14 или 15 раза до добавления частично очищенного раствора алкилированного циклодекстрина. Согласно некоторым вариантам реализации активированный уголь промывают 1 или более, 2 или более, 3 или более, 4 или более, 5 или более, 6 или более, 7 или более, 8 или более, 9 или более или 10 или более раза до добавления частично очищенного раствора алкилированного циклодекстрина.
[0150] Даже когда активированный уголь в колонке промывают водой, может иметь место неполное смачивание активированного угля. При осуществлении процедуры промывки невозможно контролировать канализацию через слой угля. Полагают, что более тщательная промывка угля до начала циркуляции раствора алкилированного циклодекстрина, приведет к снижению или предотвращению всех дальнейших добавлений остаточных хлоридов из продукта композиции алкилированного циклодекстрина.
[0151] Согласно некоторым вариантам реализации активированный уголь добавляют в специальную систему емкостей с перемешивающим устройством и системой сит. Активированный уголь загружают с последующим промыванием несколькими порциями воды при заданной скорости перемешивания в течение заданного периода времени. После промывки водой слой воды удаляют из указной специальной емкости и проводят дополнительное промывание водой. После дополнительных промывок водой определяют проводимость активированного угля и когда значение проводимости становится ниже заданного уровня, уголь суспендируют в воде и закачивают в камеру для угля. После этого активированный уголь будет готов для добавления раствора алкилированного циклодекстрина. Заданный уровень проводимости может составлять, например, менее 35 мкСм, менее 34 мкСм, менее 33 мкСм, менее 32 мкСм, менее 31 мкСм, менее 30 мкСм, менее 29 мкСм, менее 28 мкСм, менее 27 мкСм, менее 26 мкСм, менее 25 мкСм, менее 24 мкСм, менее 23 мкСм, менее 22 мкСм, менее 21 мкСм, менее 20 мкСм, менее 19 мкСм, менее 18 мкСм, менее 17 мкСм, менее 16 мкСм, менее 15 мкСм, менее 14 мкСм, менее 13 мкСм, менее 12 мкСм, менее 11 мкСм, менее 10 мкСм, менее 9 мкСм, менее 8 мкСм, менее 7 мкСм, менее 6 мкСм, менее 5 мкСм, менее 4 мкСм, менее 3 мкСм, менее 2 мкСм или менее 1 мкСм.
[0152] Перемешивание может быть измерено в оборотах в минуту (об/мин). Согласно некоторым вариантам реализации скорость перемешивания может составлять, например, от 5 об/мин до 300 об/мин. Например, скорость перемешивания может составлять 5 об/мин, 10 об/мин, 20 об/мин, 30 об/мин, 40 об/мин, 50 об/мин, 60 об/мин, 70 об/мин, 80 об/мин, 90 об/мин или 100 об/мин. Время перемешивания может составлять от 1 минуты до 5 суток. Время перемешивания может составлять, например, 5 минут, 10 минут, 20 минут, 30 минут, 40 минут, 50 минут, 60 минут, 2 часа, 3 часа, 4 часа, 5 часов, 6 часов, 7 часов, 8 часов, 9 часов, 10 часов, И часов, 12 часов, 24 часов, 2 суток, 3 суток или 4 суток. Согласно некоторым вариантам реализации время перемешивания составляет от 5 минут до 1 часа, от 5 минут до 2 часов, от 5 минут до 3 часов, от 5 минут до 4 часов, от 5 минут до 5 часов, от 10 минут до 1 часа, от 10 минут до 2 часов, от 10 минут до 3 часов, от 10 минут до 4 часов, от 20 минут до 1 часа, от 20 минут до 2 часов, от 20 минут до 3 часов, от 20 минут до 4 часов, о 30 минут до 1 часа, от 30 минут до 2 часов, от 30 минут до 3 часов или от 30 минут до 4 часов.
[0153] Согласно некоторым вариантам реализации в системе емкостей поддерживают комнатную температуру (25°C) в ходе промывки водой. Согласно некоторым вариантам реализации систему емкостей можно нагревать в ходе процесса промывки водой. Согласно некоторым вариантам реализации температура может составлять, например, от 30°C до 100°C. Например, температура охлаждения может составлять 30°C, 40°C, 50°C, 60°C, 70°C, 80°C, 90°C или 100°C. Время нагревания может составлять от 1 минуты до 5 суток. Время нагревания может составлять, например, от 5 минут до 4 суток, от 5 минут до 60 минут, от 10 минут до 50 минут, от 20 минут до 40 минут, от 30 минут до 60 минут, от 2 часов до 24 часов, от 3 часов до 12 часов, от 4 часов до 10 часов, от 5 часов до 9 часов, от 6 часов до 8 часов, от 2 суток до 4 суток или от 3 суток до 4 суток. Согласно некоторым вариантам реализации время нагревания составляет от 5 минут до 1 часа, от 5 минут до 2 часов, от 5 минут до 3 часов, от 5 минут до 4 часов, от 5 минут до 5 часов, от 10 минут до 1 часа, от 10 минут до 2 часов, от 10 минут до 3 часов, от 10 минут до 4 часов, от 20 минут до 1 часа, от 20 минут до 2 часов, от 20 минут до 3 часов, от 20 минут до 4 часов, от 30 минут до 1 часа, от 30 минут до 2 часов, от 30 минут до 3 часов или от 30 минут до 4 часов.
[0154] Согласно некоторым вариантам реализации активированный уголь промывают в камере для угля до достижения определенного уровня проводимости. После этого активированный уголь будет готов для добавления раствора алкилированного циклодекстрина.
[0155] Согласно некоторым вариантам реализации активированный уголь промывают до достижения постоянного уровня проводимости с последующим добавлением известного количества раствора алкилированного циклодекстрина через активированный уголь, который отбрасывают перед добавлением дополнительного раствора алкилированного циклодекстрина.
[0156] Конечный выход алкилированного циклодекстрина (в выделенной и/или очищенной или частично очищенной форме), полученного после завершения процесса будет варьироваться. Конечный выход алкилированного циклодекстрина в пересчете на исходный циклодекстрин может составлять от 10% до 95%, от 15% до 90%, от 20% до 85%, от 30% до 85%, от 35% до 85%, от 40% до 85%, от 45% до 80%, от 50% до 80%, от 55% до 80%, от 60% до 80%, от 50% до 90%, от 55% до 90%, от 60% до 90%, от 70% до 90%, от 80% до 90%, от 60% до 98%, от 70% до 98%, от 80%о до 98%) или от 90% до 98%. Согласно некоторым вариантам реализации конечный выход алкилированного циклодекстрина в пересчете на исходный циклодекстрин составляет 80% или больше, 85% или больше, 90% или больше или 95% или больше.
Применения композиций алкилированного циклодекстрина
[0157] Помимо других способов применения, композицию алкилированного циклодекстрина согласно настоящему изобретению можно использовать для солюбилизации и/или стабилизации широкого спектра различных материалов и для получения составов для различных способов применения. Настоящая композиция алкилированного циклодекстрина может обеспечивать повышенную растворимость и/или повышенную химическую, термохимическую, гидролитическую и/или фотохимическую стабильность других компонентов в композиции. Например, композицию алкилированного циклодекстрина можно = использовать для стабилизации активного компонента в водной среде. Композицию алкилированного циклодекстрина можно также использовать для повышения растворимости активного компонента в водной среде.
[0158] Указанная композиция алкилированного циклодекстрина согласно настоящему изобретению включает один или более активных агентов. Указанные один или более активных агентов, содержащиеся в композиции согласно настоящему изобретению, могут сильно различаться по растворимости в воде, биодоступности и гидрофильности. К активным агентам, для которых особенно целесообразно использовать настоящее изобретение, относятся следующие: нерастворимые в воде, плохо растворимые в воде, малорастворимые в воде, умеренно растворимые в воде, растворимые в воде, очень хорошо растворимые в воде, гидрофобные и/или гидрофильные терапевтические агенты. Как будет понятно специалисту в данной области техники, один или более активных агентов, содержащихся в композиции согласно настоящему изобретению, в каждом случае независимо выбирают среди любых известных активных агентов, а также среди компонентов, раскрываемых в настоящем документе. Необязательно, чтобы указанные один или более активных агентов образовывали комплекс с алкилированным циклодекстрином или образовывали ионный ассоциат с алкилированным циклодекстрином.
[0159] К активным агентам, в целом, относятся физиологически или фармакологически активные вещества, оказывающие системное или местное воздействие, либо воздействие нескольких видов, на животных и человека. Активные агенты также включают пестициды, гербициды, инсектициды, антиоксиданты, инициаторы роста растений, средства стерилизации, катализаторы, химические реагенты, пищевые продукты, питательные вещества, косметические препараты, витамины, ингибиторы стерильности, инициаторы плодородия, микроорганизмы, вкусовые добавки, подсластители, очищающие средства, фармацевтически эффективные активные агенты и другие подобные соединения для применения в фармацевтике, ветеринарии, садоводстве, домашнем хозяйстве, пищевой отрасли, кулинарии, сельском хозяйстве, косметике, промышленности, при чистке, в кондитерских изделиях и в качестве ароматизаторов. Активный агент может присутствовать в нейтральной, ионной, солевой, основной, кислотной, природной, синтетической, диастереомерной, изомерной, энантиомерно чистой, рацемической, гидратной, хелатной форме, а также в виде производного, аналога или другой распространенной формы.
[0160] Типичные фармацевтически эффективные активные агенты включают питательные вещества и агенты, гематологические агенты, эндокринные и метаболические агенты, сердечно-сосудистые агенты, почечные и мочеполовые агенты, респираторные агенты, агенты центральной нервной системы, желудочно-кишечные агенты, фунгицидные агенты, противоинфекционные агенты, биологические и иммунологические агенты, дерматологические агенты, офтальмические агенты, антинеопластичные агенты, диагностические средства. К примерам питательных веществ и агентов относятся минеральные вещества, микроэлементы, аминокислоты, липотропные вещества, ферменты и хелатообразующие агенты. Примерами гематологических агентов являются кровообразующие агенты, антитромбоцитарные агенты, антикоагулянты, производные кумарина и индандиона, коагулянты, тромболитические средства, агенты против серповидно-клеточной анемии, гемореологические агенты, антигемофилические агенты, кровоостанавливающие агенты, плазмозаменители и гемины. Примерами эндокринных и метаболических агентов являются половые гормоны, агенты маточного сокращения, бисфосфонаты, противодиабетические агенты, агенты для повышения содержания глюкозы, кортикостероиды, адренокортикальные стероиды, паратиреоидный гормон, лекарства для лечения щитовидной железы, гормоны роста, гормоны задней доли гипофиза, октреоида ацетат, имиглуцераза, кальцитонин лосося, натрия фенилбутират, бетаин безводный, цистеамина битартрат, натрия бензоат и натрия фенилацетат, бромокриптина мезилат, каберголин, агенты от подагры, антидоты. К фунгицидным агентам, подходящим для использования в сочетании с композицией алкилированного циклодекстрина согласно настоящему изобретению, относятся, но не ограничиваются ими, посаконазол, вориконазол, клотримазол, кетоконазол, оксиконазол, сертаконазол, тетконазол, флуконазол, итраконазол и миконазол. К нейролептическим средствам, подходящим для использования в сочетании с композицией алкилированного циклодекстрина согласно настоящему изобретению, относятся, но не ограничиваются ими, клозапин, прохлорперазин, гатоперидол, тиоридазин, тиотиксен, рисперидон, трифлуоперазина гидрохлорид, хлорпромазин, арипипразол, локсапин, локситан, оланзапин, кветиапина фумарат, рисперидон и зипрасидон.
[0161] Примеры сердечно-сосудистых агентов включают ноотропные агенты, противоаритмические агенты, блокаторы кальциевых каналов, сосудорасширяющие средства, антиадренергические/симпатолитические средства, антагонисты системы ренин-ангиотензин, комбинации антигипертензивных агентов, агенты против феохромоцитомы, агенты для гипертонических кризов, агенты против гиперлипидемии, комбинации агентов против гиперлипидемии, сосудосуживающие агенты для использования при шоке, смолы для удаления калия, динатриевая соль этилендиаминтетрауксусной кислоты, кардиоплегические растворы, агенты для использования при незаращении Боталлова протока, склерозирующий агенты. Примеры почечных средств и средств для мочеполовой системы включают: внутритканевые агенты против цистита, фосфат целлюлозы натрия, агенты против импотенции, ацетогидроксамовую кислоту (aha), агенты для ирригации мочеполовой системы, агенты для снижения содержания цистина, подщелачиватели мочи, подкислители мочи, антихолинергические средства, мочевые холинергические средства, полимерные реагенты для связывания фосфатов, вагинальные препараты и диуретики. Примерами респираторных агентов являются бронхолитические средства, антагонисты лейкотриеновых рецепторов, ингибиторы образования лейкотриенов, средства для ингаляции, агенты против заложенности носа, дыхательные ферменты, легочные ПАВ, антигистаминные препараты, ненаркотические противокашлевые средства и отхаркивающие средства. Примерами агентов для центральной нервной системы являются стимуляторы ЦНС, наркотические анальгетики-агонисты, наркотические анальгетики-агонисты-антагонисты, анальгетики центрального действия, ацетаминофен, салицилаты, ненаркотические анальгетики, нестероидные противовоспалительные агенты, агенты от мигрени, противорвотные средства/агенты от укачивания, седативные агенты, антидепрессанты, нейролептические агенты, ингибиторы холинэстеразы, небарбитуратные успокаивающие и снотворные агенты, продаваемые без рецепта снотворные, барбитуратные успокаивающие и снотворные агенты, анестезирующие средства общего действия, инъецируемые местные обезболивающие, противосудорожные средства, мышечные релаксанты, антипаркинсонические агенты, аденозинфосфат, холинергические стимуляторы мышц, дисульфурам, агенты для сдерживания тяги к курению, рилузол, производные гиалуроновой кислоты, токсины ботулинуса. Примерами желудочно-кишечных агентов являются средства для агенты Н pylori желудка, антагонисты Н2-гистаминовых рецепторов, ингибиторы протонного насоса, сукралфат, простагландины, антациды, желудочно-кишечные антихолинергические/противосудорожные агенты, месаламин, натрий олсалазин, динатрий балсалазид, сульфасалазин, целекоксиб, инфликсимаб, тегасерод малеат, слабительные, противодиарейные средства, антифлатуленты, ингибиторы липазы, желудочно-кишечные стимуляторы, пищеварительные ферменты, желудочные подкислители, гидрохолеретики, агенты для растворения желчного камня, продукты для обработки рта и горла, общие дезодоранты, аноректальные препараты. Примерами противоинфекционных агентов являются пенициллины, цефалоспорины и родственные им антибиотики, карбапенемы, монобаюгамы, хлорамфеникол, хинолоны, фторхинолоны, тетрациклины, макролиды, спектиномицин, стрептограмины, ванкомицин, оксалодиноны, линкозамиды, оральные и парэнтеральные аминогликозиды, колистиметат натрия, полимиксина b сульфат, бацитрацин, метронидазол, сульфонамиды, нитрофураны, уротроиины, антагонисты фолатов, противогрибковые препараты, противомалярийные препараты, противотуберкулезные средства, амебоциды, противовирусные средства, средства против ретровирусов, лепростатические средства, противопротозойные средства, глистогонные средства, а также противоинфекционные вещества, рекомендованные cdc (Центрами по контролю и профилактике заболеваний). Примеры биологических и иммунологических агентов включают иммуноглобулины, агенты на основе моноклональных антител, антивенины, агенты активной иммунизации, аллергенные экстракты, иммунологические агенты, противоревматические агенты. Примеры дерматологических агентов включают местные антигистаминные препараты, местные противоинфекционные агенты, противовоспалительные агенты, противопсориазные агенты, противосеборейные агенты, арнику, вяжущие средства, очищающие средства, капсайцин, разрушающие средства, осушающие агенты, ферментные препараты, местные иммуномодуляторы, кератолитические агенты, экстракт свиной печени, местные обезболивающие средства, миноксидил, элфлорнитина гидрохлорид, агенты для фотохимиотерапии, пигментирующие агенты, продукты из сумаха ядоносного для местного применения, антагонист пиримидина для местного применения, пиритион цинк, ретиноиды, рексиноиды, скабициды/педикулициды, агенты для заживления ран, смягчающие агенты, защитные вещества, солнцезащитные вещества, основы мазей и лосьонов, абразивы и линименты, перевязочные материалы и гранулы, физиологические промывочные растворы. Примерами офтальмологических агентов служат препараты для лечения глаукомы, стабилизаторы мастоцитов, офтальмологические антисептики, агенты для глазной фототерапии, глазные смазки, искусственные слезы, офтальмологические гиперосмолярные препараты, продукты для контактных линз. Примерами антинеопластичных агентов являются алкилирующие агенты, антиметаболиты, антимитотические агенты, эпиподофиллотоксины, антибиотики, гормоны, ферменты, радиофармацевтические препараты, координационные комплексы платины, антрацендион, замещенные мочевины, производные метилгидразина, производные имидазотетразина, цитопротекторные средства, ингибиторы топоизомеразы ДНК, модификаторы биологического ответа, ретиноиды, рексиноиды, моноклональные антитела, ингибиторы протеинтирозинкиназы, порфимер натрия, митотан (о, p’-ddd), триоксид мышьяка. Примеры диагностических агентов включат средства диагностики in vivo, биологические препараты для диагностики in vivo, рентгеноконтрастные агенты.
[0162] Примеры активных агентов также включают соединения, чувствительные к содержанию хлоридов. Примерами активных агентов, чувствительных к содержанию хлоридов, являются ингибиторы протеосом, такие как бортезомиб, дисульфирам, эпигаллокатехин-3-галлат, салиноспорамид А и карфилзомиб.
[0163] Приведенный выше список активных агентов не следует рассматривать как исчерпывающий; это лишь примеры множества вариантов реализаций, рассматриваемых в рамках настоящего изобретения. В составы по настоящему изобретению можно также вводить многие другие активные агенты.
[0164] Состав согласно настоящему изобретению можно использовать для доставки двух или более активных агентов. В составе согласно настоящему изобретению могут быть представлены те или иные конкретные комбинации активных агентов. Некоторые комбинации активных агентов включают: 1) первое лекарственное средство из первого класса лекарственных препаратов и второе лекарство из того же класса лекарственных препаратов; 2) первое лекарственное средство из первого класса лекарственных препаратов и второе лекарство из другого класса лекарственных препаратов; 3) первое лекарственное средство с первым типом биологического действия и второе лекарство с тем же типом биологического действия; 4) первое лекарственное средство с первым типом биологического действия и второе лекарство с другим типом биологического действия. Примеры комбинаций активных агентов приведены в настоящем документе.
[0165] Активный агент, содержащийся в составе согласно настоящему изобретению, может присутствовать в виде своей фармацевтически приемлемой соли. Используемый в настоящем документе термин «фармацевтически приемлемая соль» относится к производным раскрываемых соединений, получаемых модификацией активного агента посредством взаимодействия с кислотой и/или основанием, требуемой для образования пары, связанной посредством. Примерами фармацевтически приемлемых солей являются традиционные нетоксичные соли или соли четвертичного аммония соединения, образованного, например, с нетоксичными неорганическими или органическими кислотами. Подходящие нетоксичные соли включают соли, полученные из неорганических кислот, таких как соляная, бромистоводородная, серная, сульфоновая, сульфаминовая, фосфорная, азотная и другие кислоты, известные специалистам в данной области техники. Соли, полученные из органических кислот, включают соли аминокислот, уксусной, пропионовой, янтарной, гликолевой, стеариновой, молочной, яблочной, винной, лимонной, аскорбиновой, памовой, малеиновой, оксималеиновой, фенилуксусной, глутаминовой, бензойной, салициловой, сульфаниловой, 2-ацетоксибензойной, фумаровой, толуолсульфоновой, метансульфоновой, этандисульфоновой, щавелевой, изэтиновой и других кислот, известных специалистам в данной области техники. Фармацевтически приемлемые соли, подходящие для использования в настоящем изобретении, могут быть получены из активного агента, содержащего основную или кислотную группу, традиционными химическими методами. Другие подходящие соли можно найти в справочнике по фармацевтике «Remington’s Pharmaceutical Sciences» (17th ed., Mack Publishing Co., Easton, PA, 1985); раскрываемая в этом источнике информация, относящаяся к настоящему изобретению, включена в настоящее описание посредством ссылки во всей полноте.
[0166] Настоящее изобретение также относится к способу стабилизации активного агента, включающему обеспечение композиции алкилированного циклодекстрина, содержащей алкилированный циклодекстрин, менее 500 ppm фосфата и менее 0,5% хлорида, где указанная композиция алкилированного циклодекстрина имеет оптическую плотность менее 1 Е.П., измеренную с помощью спектрофотометрии в УФ/видимой области в диапазоне длин волн от 245 нм до 270 нм для водного раствора, содержащего 300 мг композиции алкилированного циклодекстрина на мл раствора, в кювете с толщиной поглощающего слоя 1 см; и комбинирование указанной композиции алкилированного циклодекстрина с активным агентом. Согласно некоторым вариантам реализации указанная оптическая плотность менее 1 Е.П. связана с агентом, разлагающим лекарственное средство.
[0167] Настоящее изобретение также относится к способу стабилизации активного агента, включающему обеспечение композиции алкилированного циклодекстрина, содержащей алкилированный циклодекстрин, менее 500 ppm фосфата и менее 0,5% хлорида, где указанная композиция алкилированного циклодекстрина имеет оптическую плотность менее 1 Е.П., измеренную с помощью спектрофотометрии в УФ/видимой области в диапазоне длин волн от 245 нм до 270 нм для водного раствора, содержащего 300 мг композиции алкилированного циклодекстрина на мл раствора, в кювете с толщиной поглощающего слоя 1 см; и комбинирование указанная композиция алкилированного циклодекстрина с активным агентом. Согласно некоторым вариантам реализации указанная оптическая плотность менее 1 Е.П. связана с окрашивающим агентом.
[0168] Способ стабилизации активного агента может быть реализован для композиции, содержащей один или более активных агентов и композицию алкилированного циклодекстрина, содержащую алкилированный циклодекстрин и менее 100 ppm фосфата, в виде «сухого» раствора, жидкого раствора, состава для ингаляции, композиции для парентерального применения, твердого раствора, твердой смеси, гранулята, геля, а также в виде других вариантов композиций с активными агентами, известными специалистам в данной области техники.
[0169] Согласно некоторым вариантам реализации способ стабилизации активного агента обеспечивает присутствие 2% или менее, 1,5% или менее, 1% или менее или 0,5% или менее агента, разлагающего лекарственное средство, или окрашивающего агента после выдерживания композиции, содержащей один или более активных агентов и композицию алкилированного циклодекстрина, содержащую алкилированный циклодекстрин и менее 500 ppm фосфата, при температуре 80°C в течение 120 минут.
[0170] Согласно некоторым вариантам реализации способ стабилизации активного агента обеспечивает присутствие 2% или менее, 1,9% или менее, 1,8% или менее, 1,7% или менее, 1,6% или менее, 1,5% или менее, 1,4% или менее, 1,3% или менее, 1,2% или менее, 1,1% или менее, 1% или менее, 0,9% или менее, 0,8% или менее, 0,7% или менее, 0,6% или менее, 0,5% или менее, 0,4% или менее, 0,3% или менее, 0,2% или менее или 0,1% или менее хлорида после выдерживания композиции, содержащей один или более активных агентов и композицию алкилированного циклодекстрина, содержащую алкилированный циклодекстрин и менее 500 ppm фосфата, при температуре 80°C в течение 120 минут.
[0171] Аналогично, согласно некоторым вариантам реализации способ стабилизации активного агента обеспечивает присутствие активного агента по результатом анализа 98% или более, 98,5% или более, 99% или более или 99,5% или более активного агента после выдерживания композиции, содержащей один или более активных агентов и композицию алкилированного циклодекстрина, содержащую алкилированный циклодекстрин и менее 500 ppm фосфата, при температуре 80°C в течение 120 минут.
[0172] Согласно некоторым вариантам реализации способ стабилизации активного агента обеспечивает композицию алкилированного циклодекстрина, содержащую алкилированный циклодекстрин, с содержанием фосфатов менее 400 ppm, менее 300 ppm, менее 200 ppm, менее 125 ppm, менее 100 ppm, менее 75 ppm или менее 50 ppm.
[0173] Согласно некоторым вариантам реализации способ стабилизации активного агента обеспечивает композицию алкилированного циклодекстрина, содержащую алкилированный циклодекстрин, где указанная композиция алкилированного циклодекстрина имеет оптическую плотность 0,5 Е.П. или менее, измеренную с помощью спектрофотометрии в УФ/видимой области в диапазоне длин волн от 245 нм до 270 нм для водного раствора, содержащего 300 мг композиции алкилированного циклодекстрина на мл раствора, в кювете с толщиной поглощающего слоя 1 см. Согласно некоторым вариантам реализации указанная оптическая плотность 0,5 Е.П. или менее связана с агентом, разлагающим лекарственное средство.
[0174] В целом, алкилированный циклодекстрин присутствует в количестве, достаточном для стабилизации активного агента. Достаточным количеством может быть мольное соотношение от 0,1:1 до 10:1, от 0,5:1 до 10:1, от 0,8:1 до 10:1 или от 1:1 до 5:1 (алкилированный циклодекстрин:активный агент).
[0175] Циклодекстрин в такой комбинированной композиции не обязательно должен образовать связь с другими содержащимися в ней веществами, например, с активным агентом. Однако, если циклодекстрин образует связь с другим веществом, это может произойти в результате формирования комплекса включения, ионной пары, водородной связи и/или ван-дер-ваальсового взаимодействия.
[0176] Анионный дериватизированный циклодекстрин может образовывать комплекс или образовывать связь иного типа с агентом, ионизуемым под действием кислоты. Используемый в настоящем документе термин «агент, ионизуемый под действием кислоты» понимают как любое соединение, которое ионизуется в присутствии кислоты. Агент, ионизуемый под действием кислоты, содержит по меньшей мере одну функциональную группу, ионизирующуюся под действием кислоты или при попадании в кислую среду. Примерами функциональных групп, ионизирующихся под действием кислоты, являются первичные амины, вторичные амины, третичные амины, четвертичные амины, ароматические амины, ненасыщенные амины, первичные тиолы, вторичные тиолы, сульфониевые соединения, гидроксильные соединения, енолы и другие вещества, известные специалистам в области химии.
[0177] Степень, в которой ионизуемый кислотой агент связывается за счет нековалентного ионного связывания по сравнению с образованием комплексов включения, может быть определена спектрометрическими методами, например, методами 1Н-ЯМР, 13С-ЯМР или кругового дихроизма, а также путем анализа данных фазовой растворимости для ионизуемого кислотой компонента и анионного дериватизированного циклодекстрина. Специалист в данной области техники сможет использовать указанные традиционные методы для приблизительного определения степени связывания каждого типа, имеющего места в растворе, для определения того, происходит ли образование связей между частицами преимущественно за счет нековалентного ионного связывания или за счет образования комплексов включения. В условиях преобладания нековалентного ионного связывания над образованием комплексов включения, степень образования комплексов включения, по данным измерения методом ЯМР или кругового дихроизма, будет понижена, несмотря на то, что данные по фазовой растворимости указывают на значительное связывание между частицами при указанных условиях; кроме того, истинная растворимость ионизуемого кислотой агента, определенная исходя из данных по фазовой растворимости, как правило, будет выше ожидаемой при этих условиях.
[0178] Используемый в настоящем документе термин «нековалентная ионная связь» относится к связи, образуемой между анионной частицей и катионной частицей. Связь является нековалентной, так что указанные частицы совместно образуют соль или ионную пару. Анионный дериватизированный циклодекстрин предоставляет анионную частицу ионной пары, а ионизуемый кислотой агент предоставляет катионную частицу ионной пары. Поскольку анионный дериватизированный циклодекстрин является многовалентным, алкилированный циклодекстрин может образовывать ионную пару с одной или несколькими молекулами ионизуемых кислотами или иных катионных агентов.
[0179] Жидкий состав согласно настоящему изобретению может быть преобразован в твердый состав для последующего восстановления. Восстанавливаемая твердая композиция согласно настоящему изобретению содержит активный агент, дериватизированный циклодекстрин и, необязательно, по меньшей мере одно фармацевтическое вспомогательное вещество. Восстанавливаемая композиция может быть восстановлена путем добавления водной жидкости с образованием жидкого состава, допускающего хранение. Композиция может содержать примесь (от минимального содержания комплекса включения до его отсутствия) твердого дериватизированного циклодекстрина и твердое вещество, содержащее активный агент, и, необязательно, по меньшей мере одно твердое фармацевтическое вспомогательное вещество, причем до восстановления состава большая часть активного агента не связана в комплекс с дериватизированным циклодекстрином. Альтернативно, композиция может содержать твердую смесь дериватизированного циклодекстрина и активного агента, в которой большая часть активного агента связана в комплекс с дериватизированным циклодекстрином до восстановления. Восстанавливаемая твердая композиция может также содержать дериватизированный циклодекстрин и активный агент, причем по существу весь или по меньшей мере большая часть активного агента связана в комплекс с дериватизированным циклодекстрином.
[0180] Восстанавливаемая твердая композиция может быть получена по любому из следующих способов. Вначале получают жидкий состав согласно настоящему изобретению, затем получают твердый состав путем лиофилизации (сублимационной сушки), сушки распылением, сублимационной сушки с распылением, осаждением анти-растворителем, стерильной сушки распылением, различными процессами с использованием сверхкритических или около-сверхкритических жидкостей, или другими методами получения твердых составов для восстановления, известными специалистам в данной области техники.
[0181] Жидкая носитель, входящий в состав согласно настоящему изобретению, может включать жидкий водный носитель (например, воду), водный раствор спирта, водный раствор органического растворителя, неводный жидкий носитель и их комбинации.
[0182] Состав согласно настоящему изобретению может включать одно или более дополнительных фармацевтических вспомогательных веществ, таких как традиционный консервант, противопенный агент, антиоксидант, буферный агент, подкисляющий агент, подщелачивающий агент, объемообразующий агент, краситель, усилитель комплексообразования, криозащитное средство, электролит, глюкоза, эмульсификатор, масло, пластификатор, усилитель растворимости, стабилизатор, модификатор тоничности, ароматизатор, подсластители, адсорбенты, антиадгезив, связующее, разбавитель, наполнитель для прямого прессования, разрыхлитель, скользящее вещество, смазывающий агент, агент для придания непрозрачности, полирующий агент, комплексообразователь, душистые вещества, другие вспомогательные вещества, известные специалистам в данной области техники, или комбинации указанных веществ.
[0183] Используемый в настоящем документе термин «адсорбент» подразумевает агент, способный удерживать другие молекулы на своей поверхности за счет физических или химических (хемосорбция) факторов. Такие соединения, в качестве примеров и без ограничения, включают порошкообразный и активированный древесный уголь и другие материалы, известные специалистам в данной области техники.
[0184] Используемый в настоящем документе термин «подщелачивающий агент» означает соединение, используемое для обеспечения щелочной среды с целью придания стабильности продукту. Такие соединения, в качестве примеров и без ограничения, включают раствор аммиака, карбонат аммония, диэтаноламин, моноэтаноламин, гидроксид калия, борат натрия, карбонат натрия, бикарбонат натрия, гидроксид натрия, триэтаноламин, диэтаноламин, органические основания аминного типа, щелочные аминокислоты, троламин и другие вещества, известные специалистам в данной области техники.
[0185] Используемый в настоящем документе термин «подкисляющий агент» означает соединение, используемое для обеспечения кислой среды с целью придания стабильности продукту, Такие соединения, в качестве примеров и без ограничения, включают уксусную кислоту, кислые аминокислоты, лимонную кислоту, фумаровую кислоту и другие α-гидроксикислоты, соляную кислоту, аскорбиновую кислоту, фосфорную кислоту, серную кислоту, винную кислоту, азотную кислоту и другие вещества, известные специалистам в данной области техники.
[0186] Используемый в настоящем документе термин «антиадгезив» означает компонент, предотвращающий прилипание ингредиентов твердого дозируемого состава к прессам и пресс-формам таблетирующих машин в процессе производства таблеток. Такие соединения, в качестве примеров и без ограничения, включают стеарат магния, тальк, стеарат кальция, глицерилбегенат, полиэтиленгликоль, гидрированное растительное масло, минеральное масло, стеариновую кислоту и другие вещества, известные специалистам в данной области техники.
[0187] Используемый в настоящем документе термин «связующее» означает соединение, используемое, чтобы вызвать адгезию частиц порошка в твердых дозируемых составах. Такие соединения, в качестве примеров и без ограничения, включают гуммиарабик, альгиновую кислоту, натриевую соль карбоксиметилцеллюлозы, поли(винилпирролидон), прессуемый сахар, этилцеллюлозу, желатин, жидкую глюкозу, метилцеллюлозу, повидон, желатинированный крахмал и другие вещества, известные специалистам в данной области техники.
[0188] При необходимости связующие можно также вводить в лекарственные формы. Примеры связующих включают гуммиарабик, трагакантовую камедь, желатин, крахмал, материалы на основе целлюлозы, такие как метилцеллюлоза и натриевая соль карбоксиметилцеллюлозы, альгиновые кислоты и их соли, полиэтиленгликоль, гуаровую камедь, полисахариды, бентониты, сахара, инвертированные сахара, полоксамеры (Pluronic™ F68, Pluronic™ FI27), коллагены, альбумин, желатин, целлюлозные полимеры в неводных растворителях, комбинации указанных веществ и другие вещества, известные специалистам в данной области техники. К другим связующим относятся, например, полипропиленгликоль, сополимер полиоксиэтилен-полипропилен, эфиры на основе полиэтилена, полиэтиленсорбитановый эфир, полиэтиленоксид, комбинации упомянутых веществ и другие вещества, известные специалистам в данной области техники.
[0189] Используемый в настоящем документе термин традиционный консервант означает соединение, используемое по меньшей мере для уменьшения скорости, с которой возрастает биологическая нагрузка, а также может поддерживать биологическую нагрузку на постоянном уровне или снижать ее после загрязнения. Такие соединения, в качестве примеров и без ограничения, включают бензалкония хлорид, бензетония хлорид, бензойную кислоту, бензиловый спирт, цетилпиридиния хлорид, хлоробутанол, фенол, фенилэтиловый спирт, нитрат фенилртути, ацетат фенилртути, тимерозал, мета-крезол, миристил-гамма пиколиния хлорид, бензоат калия, сорбат калия, бензоат натрия, пропионат натрия, сорбиновую кислоту, тимол, метил-, этил-, пропил- и бутилпарабены, а также другие вещества, известные специалистам в данной области техники. Следует понимать, что некоторые консерванты могут взаимодействовать с алкилированным циклодекстрином, что снижет эффективность консерванта. Тем не менее, за счет подбора консервантов и концентраций консерванта и алкилированного циклодекстрина можно получить составы с достаточно высокой степенью защиты.
[0190] Используемые в настоящем документе термины «разбавитель» или «наполнитель» означают инертное вещество, используемое в качестве наполнителя для придания объемных, текучих свойств и характеристик сжимаемости, требуемых при получении жидкой или твердой лекарственной формы. Такие соединения, в качестве примеров и без ограничения, включают жидкий носитель (например, воду, спирт, растворители и т.п.), гидроортофосфат кальция, каолин, лактозу, декстрозу, карбонат магния, сахарозу, маннит, микрокристаллическую целлюлозу, порошкообразную целлюлозу, осажденный карбонат кальция, сорбит и крахмал, и другие вещества, известные специалистам в данной области техники.
[0191] Используемый в настоящем документе термин «наполнитель для прямого прессования» означает соединение, используемое в прессованных твердых лекарственных формах. Такие соединения, в качестве примеров и без ограничения, включают гидроортофосфат кальция, а также другие вещества, известные специалистам в данной области техники.
[0192] Используемый в настоящем документе термин «антиоксидант» означает агент, ингибирующий окисление и таким образом используемый для предотвращения разрушения препаратов в результате окислительного процесса. Такие соединения, в качестве примеров и без ограничения, включают ацетон, метабисульфит калия, сульфит калия, аскорбиновую кислоту, аскорбилпальмитат, лимонную кислоту, бутилированный гидроксианизол, бутилированный гидрокситолуол, гипофосфористую кислоту, монотиоглицерин, пропилгаллат, аскорбат натрия, цитрат натрия, сульфид натрия, сульфит натрия, бисульфит натрия, формальдегид-сульфоксилат натрия, тиогликолевую кислоту, ЭДТА, пентетат, метабисульфит натрия и другие вещества, известные специалистам в данной области техники.
[0193] Используемый в настоящем документе термин «буферный агент» означает соединение, используемое для предотвращения изменения pH при разбавлении либо добавлении кислоты или щелочи. Такие соединения, в качестве примеров и без ограничения, включают уксусную кислоту, ацетат натрия, адипиновую кислоту, бензойную кислоту, бензоат натрия, борную кислоту, борат натрия, лимонную кислоту, глицин, малеиновую кислоту, однозамещенный фосфат натрия, двузамещенный фосфат натрия, 4-(2-гидроксиэтил)-1-пиперазинэтан сульфоновую кислоту, молочную кислоту, винную кислоту, метафосфат калия, фосфат калия, одноосновной ацетат натрия, бикарбонат натрия, трис, тартрат натрия, безводный цитрат натрия и дигидрат, а также другие вещества, известные специалистам в данной области техники.
[0194] К составу согласно настоящему изобретению может быть добавлен усилитель комплексообразования. Присутствие такого агента позволяет изменить соотношение циклодекстрин/активный компонент. Усилитель комплексообразования представляет собой соединение или соединения, усиливающее(ие) комплексообразование активного компонента с циклодекстрином. Подходящие усилители комплексообразования включают один или более фармакологически инертных водорастворимых полимеров, гидроксикислоты и другие органические соединения, обычно используемые в консервированных составах для усиления комплексообразования конкретного компонента с циклодекстринами.
[0195] Гидрофильные полимеры могут быть использованы в качестве агентов, усиливающих комплексообразование и растворимость и/или снижающих активность воды с целью повышения характеристик составов, содержащих консервант на основе циклодекстрина. Лофтссон (Loftsson) раскрыл ряд полимеров, подходящих для использования в комбинации с циклодекстрином (недериватизированным или дериватизированным) для усиления эффективности и/или свойств циклодекстрина. Подходящие полимеры раскрыты в следующих источниках: Pharmazie 56:746 (2001); Int. J. Pharm. 212:29 (2001); Cyclodextrin: From Basic Research to Market, 10th Int’l Cyclodextrin Symposium, Ann Arbor, MI, US, May 21-24, p. 10-15 (2000); PCT Int’l Pub. No. WO 99/42111; Pharmazie 53:733 (1998); Pharm. Technol. Eur. 9:26 (1997); J. Pharm. Sci. 55:1017 (1996); European Patent Appl. No. 0579435; Proc. of the 9th Int’l Symposium on Cyclodextrins, Santiago de Comostela, ES, May 31-June 3, 1998, pp. 261-264 (1999); S.T.P. Pharma Sciences 9:237 (1999); Amer. Chem. Soc. Symposium Series 737 (Polysaccharide Applications):24-45 (1999); Pharma. Res. 15:1696 (1998); Drug Dev. Ind. Pharm. 24:365 (1998); Int. J. Pharm. 163:115 (1998); Book of Abstracts, 216th Amer. Chem. Soc. Nat’l Meeting, Boston, Aug. 23-27 CELL-016 (1998); J. Controlled Release 44:95 (1997); Pharm. Res. (1997) 14(11), S203; Invest. Ophthalmol. Vis. Sci. 37:1199 (1996); Proc. of the 23rd Int’l Symposium on Controlled Release of Bioactive Materials 453-454 (1996); Drug Dev. Ind. Pharm. 22:401 (1996); Proc. of the 8th Int’l Symposium on Cyclodextrins, Budapest, HU, Mar. 31-Apr. 2, 1996, pp. 373-376 (1996); Pharma. Sci. 2:277 (1996); Eur. J. Pharm. Sci. 4S:S144 (1996); 3rd Eur. Congress of Pharma. Sci. Edinburgh, Scotland, UK September 15-17, 1996; Pharmazie 57:39 (1996); Eur. J. Pharm. Sci. 4S:S143 (1996); U.S. Patents Nos. 5,472,954 and 5,324,718; Int. J. Pharm. 126:13 (1995); Abstracts of Papers of the Amer. Chem. Soc. 209:33-CELL (1995); Eur. J. Pharm. Sci. 2:297 (1994); Pharm. Res. 11:S225 (1994); Int. J. Pharm. 104:181 (1994); and Int. J. Pharm. 110:169 (1994); описание которых включено в настоящую заявку посредством ссылок во всей полноте.
[0196] Другими подходящими полимерами являются хорошо известные вспомогательные вещества, широко используемые в фармацевтических составах и описываемые, например, в следующих источниках: Remington's Pharmaceutical Sciences, 18th ed., pp. 291-294, A.R. Gennaro (editor), Mack Publishing Co., Easton, PA (1990); A. Martin et al., Physical Pharmacy. Physical Chemical Principles in Pharmaceutical Sciences, 3d ed, pp. 592-638 (Lea & Febinger, Philadelphia, PA (1983); A.T. Florence et al, Physicochemical Principles of Pharmacy, 2d ed., pp. 281-334, MacMillan Press, London, UK (1988), описание которых включено в настоящую заявку посредством ссылок во всей полноте. Кроме того, подходящими являются водорастворимые природные полимеры, водорастворимые полусинтетические полимеры (например, водорастворимые производные целлюлозы) и водорастворимые синтетические полимеры. К природным полимерам относятся полисахариды, в частности, инулин, пектин, производные альгина (например, альгинат натрия) и агар-агар, а также полипептиды, такие как казеин и желатин. К полусинтетическим полимерам относятся производные целлюлозы, такие как метилцеллюлоза, гидроксиэтилцеллюлоза, гидроксипропилцеллюлоза, их смешанные эфиры, такие как гидроксипропилметилцеллюлоза и другие смешанные эфиры, например гидроксиэтил-этилцеллюлоза и гидроксипропилэтилцеллюлоза, фталат гидроксипропилметилцеллюлозы, карбоксиметилцеллюлоза и ее соли, особенно натриевая соль карбоксиметилцеллюлозы. К синтетическим полимерам относятся производные полиоксиэтилена (полиэтиленгликоли), поливинильные производные (поливиниловый спирт, поливинилпирролидон и полистиролсульфонат) и различные сополимеры акриловой кислоты (например, карбомер). Другие природные, полусинтетические и синтетические полимеры, не упомянутые в настоящем описании, но удовлетворяющие критериям растворимости в воде, фармацевтической приемлемости и фармакологической пассивности, также считаются относящимися к сфере настоящего изобретения.
[0197] Используемый в настоящем документе термин «душистое вещество» означает сравнительно летучее вещество или комбинацию веществ, придающих выраженный аромат, запах или благоухание. Примерами душистых веществ являются те душистые вещества, безопасность которых, в целом, утверждена Управлением по контролю за продуктами и лекарствами США.
[0198] Используемый в настоящем документе термин «скользящее вещество» означает агент, используемый в твердых лекарственных формах для облегчения текучести твердой массы. Такие соединения, в качестве примеров и без ограничения, включают коллоидный оксид кремния, кукурузный крахмал, тальк, силикат кальция, силикат магния, коллоидный кремний, трехосновной фосфат кальция, гидрогель кремнезема и другие вещества, известные специалистам в данной области техники.
[0199] Используемый в настоящем документе термин «смазывающее вещество» означает вещество, используемое в твердых лекарственных формах для уменьшения трения при прессовании. Такие соединения, в качестве примеров и без ограничения, включают стеарат кальция, стеарат магния, полиэтиленгликоль, тальк, минеральное масло, стеариновую кислоту, стеарат цинка и другие вещества, известные специалистам в данной области техники.
[0200] Используемый в настоящем документе термин «агент для придания непрозрачности» означает соединение, используемое для придания покрытию непрозрачности. Агент для придания непрозрачности можно использовать по отдельности или в сочетании с красителем. Такие соединения, в качестве примеров и без ограничения, включают диоксид титана, тальк, а также другие вещества, известные специалистам в данной области техники.
[0201] Используемый в настоящем документе термин «полирующий агент» означает соединение, используемое для придания твердым лекарственным формам приятного блеска. Такие соединения, в качестве примеров и без ограничения, включают карнаубский воск, белый воск, а также другие вещества, известные специалистам в данной области техники.
[0202] Используемый в настоящем документе термин «разрыхлитель» означает соединение, используемое в твердых лекарственных формах для облегчения разрушения твердой массы на более мелкие частицы, которые легче диспергируются или растворяются. Примеры разрыхлителей, в качестве примеров и без ограничения, включают крахмалы, такие как кукурузный крахмал, картофельный крахмал, предварительно желатинированные и модифицированные крахмалы на их основе, подсластители, глины, бентонит, микрокристаллическую целлюлозу (например, Avicel®), кальциевую соль карбоксиметилцеллюлозы, натриевую соль кроскармеллозы, альгиновую кислота, альгинат натрия, целлюлозу-полакрилин калия (например, Amberlite®), альгинаты, крахмалгликолят натрия, камедь, агар, гуар, плоды рожкового дерева, карайю, пектин, трагакантовую камедь, кросповидон и другие вещества, известные специалистам в данной области техники.
[0203] Используемый в настоящем документе термин «стабилизатор» означает соединение, используемое для стабилизации лекарственного средства от воздействия физических, химических или биохимических процессов, которые могли бы снизить терапевтическую активность агента. Примеры стабилизаторов, в качестве примеров и без ограничения, включают альбумин, сиаловую кислоту, креатинин, глицин и другие аминокислоты, ниацинамид, ацетилтриптофанат натрия, оксид цинка, сахарозу, глюкоза, лактозу, сорбит, маннит, глицерин, полиэтиленгликоли, каприлат натрия, сахаринат натрия и другие вещества, известные специалистам в данной области техники.
[0204] Используемый в настоящем документе термин «модификатор тоничности» означает соединение, используемое для регулирования тоничности жидкого состава. Подходящие модификаторам тоничности включают глицерин, лактозу, маннит, декстрозу, хлорид натрия, сульфат натрия, сорбит, трегалозу и другие вещества, известные специалистам в данной области техники. В одном из вариантов реализации изобретения тоничность жидкого состава приближенно равна тоничности крови или кровяной плазмы.
[0205] Используемый в настоящем документе термин «противопенный агент» означает соединение или соединения, предотвращающие или снижающие количество пены, образующейся на поверхности жидкого состава. Подходящие противопенные агенты включают диметикон, симетикон, октоксинол и другие вещества, известные специалистам в данной области техники.
[0206] Используемый в настоящем документе термин «объемообразующий агент» означает соединение, используемое для увеличения объема твердого продукта и/или помогающее контролировать свойства состава в процессе лиофилизации. Такие соединения, в качестве примеров и без ограничения, включают декстран, трегалозу, сахарозу, поливинилпирролидон, лактозу, инозит, сорбит, диметилсульфоксид, глицерин, альбумин, лактобионат кальция, а также другие вещества, известные специалистам в данной области техники.
[0207] Используемый в настоящем документе термин «криозащитное средство» означает соединение, используемое для защиты активного лекарственного компонента от физического или химического разложения в процессе лиофилизации. Такие соединения, в качестве примеров и без ограничения, включают: диметилсульфоксид, глицерин, трегалоза, пропиленгликоль, полиэтиленгликоль, а также другие вещества, известные специалистам в данной области техники.
[0208] Используемый в настоящем документе термин «эмульгатор» или «эмульгирующий агент» означает соединение, добавляемое к одному или нескольким фазовым компонентам эмульсии с целью стабилизации капель дисперсной фазы в сплошной фазе. Такие соединения, в качестве примеров и без ограничения, включают лецитин, полиоксиэтилен-полиоксипропиленовые простые эфиры, полиоксиэтилен-сорбитан монолаурат, полисорбаты, сложные эфиры сорбитана, стеариловый спирт, тилоксапол, трагакантовую камедь, ксантановую камедь, гуммиарабик, агар, альгиновую кислоту, альгинат натрия, бентонит, карбомер, натриевую соль карбоксиметилцеллюлозы, холестерин, желатин, гидроксиэтилцеллюлозу, гидроксипропилцеллюлозу, октоксинол, олеиловый спирт, поливиниловый спирт, повидон, пропиленгликоль моностеарат, лаурилсульфат натрия, а также другие вещества, известные специалистам в данной области техники.
[0209] К составу согласно настоящему изобретению может быть добавлен усилитель растворимости. Усилитель растворимости представляет собой соединение или соединения, усиливающее(ие) растворимость активного агента в жидком составе. Присутствие такого агента позволяет изменить соотношение циклодекстрин/активный агент. Подходящие усилители растворимости включают один или более органических растворителей, детергентов, мыл, поверхностно-активных веществ и других органических веществ, обычно используемых в формах для парентерального введения с целью повышения растворимости определенного агента.
[0210] Подходящие органические растворители включают, например, этанол, глицерин, полиэтиленгликоли, пропиленгликоль, полоксомеры и другие растворители, известные специалистам в данной области техники.
[0211] Составы, включающие композиции алкилированного циклодекстрина согласно настоящему изобретению, могут содержать масла (например, нелетучие масла, арахисовое масло, кунжутное масло, хлопковое масло, кукурузное масло, оливковое масло и т.п.), жирные кислоты (например, олеиновую кислоту, стеариновую кислоту, изостеариновую кислоту и т.п.), эфиры жирных кислот (например, этилолеат, изопропилмиристат и т.п.), глицериды жирных кислот, ацетилированные глицериды жирных кислот и их комбинации. Составы, включающие композиции алкилированного циклодекстрина согласно настоящему изобретению, могут также содержать спирты (например, этанол, изопропанол, гексадециловый спирт, глицерин, пропиленгликоль и т.п.), кетали глицерина (например, 2,2-диметил-1,3-диоксолан-4-метанол и т.п.), простые эфиры (например, поли(этиленгликоль) 450 и т.п.), нефтяные углеводороды (например, минеральное масло, петролатум и т.п.), воду, поверхностно-активные вещества, суспендирующие агенты, эмульгирующие агенты, а также их комбинации.
[0212] Следует понимать, что соединения, используемые в области фармацевтических составов, обычно имеют несколько функций или служат нескольким целям. Таким образом, если названное в настоящем описании соединение упоминается лишь один раз или используется при определении нескольких терминов, его задача или функция не должны рассматриваться как ограничивающиеся исключительно этими названными задачами или функциями.
[0213] Составы, включающие композицию алкилированного циклодекстрина согласно настоящему изобретению, могут также содержать биологическую соль (соли), хлорид натрия, хлорид калия и другие электролиты.
[0214] Поскольку некоторые активные агенты могут подвергаться окислительному разложению, жидкий состав согласно настоящему изобретению может по существу не содержать кислорода. Например, свободное пространство над продуктом в контейнере, содержащем жидкий состав, может быть освобождено от кислорода или по существу освобождено от кислорода, или количество кислорода может быть уменьшено путем продувки свободного пространства над продуктом инертным газом (например, азотом, аргоном, диоксидом углерода и т.п.), либо барботированием инертного газа через жидкий состав. В случае продолжительного хранения, жидкий состав, содержащий активный агент, подверженный окислительному разложению, можно хранить в обескислороженной среде или в среде с пониженным содержанием кислорода. Удаление кислорода из состава улучшит его сохранность относительно воздействия аэробных микроорганизмов; вместе с тем, добавление кислорода в состав улучшит его сохранность относительно воздействия анаэробных микроорганизмов.
[0215] Выражение «фармацевтически приемлемый» используется для обозначения таких веществ, материалов, композиций и/или лекарственных форм, которые, согласно тщательному медицинскому исследованию, подходят для применения в контакте с тканями человека и животных без проявления излишней токсичности, раздражения, аллергической реакции и других проблем или осложнений, соизмеримых с разумным соотношением преимуществ и рисков.
[0216] Используемые в настоящем документе термины «пациент» или «субъект» понимаются как теплокровные животные, в частности, млекопитающие, например, кошки, собаки, мыши, морские свинки, лошади, коровы, овцы, животные, не являющиеся людьми, а также люди.
[0217] Состав согласно настоящему изобретению включает активный агент в эффективном количестве. Под термином «эффективное количество» понимают количество активного агента, достаточное количество для того, чтобы добиться требуемого или желаемого ответа, или другими словами, количество, достаточное для того, чтобы добиться существенного биологического ответа при введении субъекту.
[0218] Композиции согласно настоящему изобретению могут входить в составы для лекарственных форм, такие как восстанавливаемая твердая форма, таблетка, капсула, пилюля, пастилка, пластырь, осмотическое устройство, карандаш, свеча, имплантат, камедь, шипучая композиция, жидкость для инъекций, растворы для глаз или носовой полости, а также порошки или растворы для ингаляций.
[0219] В настоящем изобретении также предложены способы получения жидкого состава, содержащего один или более активных агентов и композицию алкилированного циклодекстрина, содержащую алкилированный циклодекстрин и менее 500 ppm фосфата. Первый способ включает: приготовление первого водного раствора, содержащего композицию алкилированного циклодекстрина; приготовление второго раствора или суспензии, содержащих один или более активных агентов; перемешивание первого и второго раствора с получением жидкого состава. Аналогичный второй способ включает добавление одного или более активных агентов непосредственно к первому раствору без приготовления второго раствора. Третий способ включает добавление композиции алкилированного циклодекстрина непосредственно к раствору/суспензии, содержащим один или более активных агентов. Четвертый способ включает добавление раствора, содержащего один или более активных агентов, к порошкообразной или мелкодисперсной композиции алкилированного циклодекстрина. Пятый способ включает добавление одного или более активных агентов непосредственно к порошкообразной или мелкодисперсной композиции алкилированного циклодекстрина с последующем добавлением полученной смеси ко второму раствору. Шестой способ включает приготовление жидкого состава по любому из указанных выше способов, затем отделение твердого материала путем лиофилизации, сушки распылением, стерильной сушки распылением, сублимационной сушки с распылением, осаждением анти-растворителем, процессом с использованием сверхкритической или около-сверхкритической жидкости либо другими методами приготовления порошка для восстановления, известными средним специалистам в данной области техники.
[0220] Конкретные варианты реализации способов получения жидкого состава включают следующие варианты: 1) способ, дополнительно включающий фильтрование состава в стерильных условиях через фильтрующий материал с размерами пор 0,1 мкм или более; 2) жидкий состав стерилизуют путем облучения или обработки в автоклаве; 3) способ дополнительно включает отделение твердого продукта из раствора; 4) раствор продувают азотом, аргоном или другим инертным фармацевтически приемлемым газом, так что удаляется значительная доля кислорода, растворенного в растворе и/или находящегося в контакте с его поверхностью.
[0221] В настоящем изобретении также предложен восстанавливаемая твердая фармацевтическая композиция, содержащая один или более активных агентов, композицию алкилированного циклодекстрина и, необязательно, по меньшей мере еще одно фармацевтическое вспомогательное вещество. Если такую композицию восстанавливают жидкостью на водной основе с получением консервированного жидкого состава, ее можно вводить субъекту путем инъекций, инфузией, местным нанесением, ингаляцией или перорально.
[0222] Некоторые варианты реализации восстанавливаемой твердой фармацевтической композиции характеризуются тем, что: 1) фармацевтическая композиция содержит смесь композиции алкилированного циклодекстрина и твердого вещества, содержащего один или более активных агентов и, необязательно, по меньшей мере еще одно фармацевтическое вспомогательное вещество, причем до восстановления большая часть активного агента не связана в комплекс с алкилированным циклодекстрином; и/или 2) композиция содержит твердую смесь композиции алкилированного циклодекстрина и одного или более активных агентов, причем до восстановления большая часть указанных одного или более активных агентов связана в комплекс алкилированным циклодекстрином.
[0223] Композиция согласно настоящему изобретению может быть использована в фармацевтической лекарственной форме, фармацевтической композиции или в другой подобной комбинации материалов. Композиции алкилированного циклодекстрина также применимы, не ограничиваясь указанным, в качестве аналитических реагентов, вспомогательных веществ и/или добавок к пищевым и косметическим продуктам, а также в качестве агентов для очистки окружающей среды.
[0224] На основе приведенного выше описания и приведенных ниже примеров обычный специалист в данной области техники сможет применять настоящее изобретение в соответствии с формулой изобретения без необходимости проведения слишком обширных экспериментов. Упомянутое выше описание будет лучше понятно с учетом следующих примеров, подробно описывающих некоторые процедуры для получения молекул, композиций и составов в соответствии с настоящим изобретением. Все ссылки на эти примеры делаются с иллюстративными целями. Нижеприведенные примеры должны рассматриваться не как исчерпывающие, а лишь как иллюстрации нескольких из большого числа вариантов реализаций, предполагаемых данным изобретением.
ПРИМЕРЫ
ПРИМЕР 1
Определение растворимости активного агента
[0225] Сравнительная оценка эффекта солюбилизации различных композиций сульфоалкильных эфиров циклодекстрина на фармацевтические активные агенты проводили следующим образом. Базовые растворы каждого из выбранных циклодекстринов с концентрацией 0,04 М готовили с использованием очищенной воды. Прозрачность растворов определяли визуальным обследованием или с помощью инструментальных средств. Раствор считается прозрачным, если он прозрачен по меньшей мере при оценке невооруженным взглядом. Каждый из фармацевтических активных агентов, которые исследовали в двух опытах, смешивали с 2 мл или 4 мл водного раствора SAE-CD.
[0226] Взвешивали количества фармацевтических активных агентов, превышающие их предполагаемую растворимость, и помещали их в виалы с тефлоновым покрытием и завинчивающейся крышкой. Количество каждого из активных агентов составляло по меньшей мере 3 мг/мл. Затем в каждую виалу вводили соответствующее количество раствора циклодекстрина (либо 2 мл, либо 4 мл). Виалы встряхивали и подвергали ультразвуковой обработке, чтобы облегчить смачивание твердых веществ жидкостью. Затем виалы помещали на шейкер lab quake или барабанный смеситель для установления равновесия. Виалы периодически подвергали визуальному обследованию, чтобы убедиться, что твердые компоненты смачиваются должным образом и находятся в контакте с жидкостью. Затем из жидкости в виалах периодически отбирали пробы для определения концентрации фармацевтического активного агента в растворе. Как правило, измерения на образцах проводили с периодичностью в 24 часа.
[0227] Отбор проб из виал для определения растворимости активного агента осуществляли декантированием по 1 мл раствора из виалы с возможным последующим центрифугированием. Затем отделенный супернатант отфильтровывали с помощью шприцевого фильтра 0,22 мкм и разбавляли подвижной фазой до требуемой концентрации в диапазоне стандартной кривой. После этого образцы анализировали методом ВЭЖХ для определения концентрации солюбилизированных лекарственных производных.
ПРИМЕР 2
Определение содержания влаги
[0228] Для определения содержания влаги в алкилированных циклодекстринах использовали следующую процедуру. Определение осуществляли в двух опытах с использованием образцов по 250 мг на кулонометре по методу Карла Фишера компании Brinkman (Brinkman Instruments Co., IL). Известную навеску твердого циклодекстрина вводили в кулонометре Карла Фишера и измеряли общее количество воды в образце. Далее общее количество присутствующей в образце воды пересчитывали на массу твердого вещества, получая процентное содержание влаги в образце.
ПРИМЕР 3
Анализ методом капиллярного электрофореза
[0229] Анализ композиций производных SAE-CD методом капиллярного электрофореза проводили согласно следующей процедуре. Для анализа растворов производных SBE-β-CD и SBE-γ-CD использовали систему для капиллярного электрофореза Beckman Р/АСЕ 2210, оборудованную детектором УФ поглощения (Beckman instruments, Inc., Fullereton, CA). Разделение производили при 25°C с помощью капилляра из плавленого кварца (внутренний диаметр 50 мкм, общая длина 57 см, эффективная длина 50 см) с использованием проточного буфера со скорректированным pH, содержащего 30 мМ бензойной кислоты и 100 мМ ТРИС (трис-гидроксиметил-аминометанол).
[0230] Перед каждым введением образца капилляр промывали водой, 0,01 н. раствором NaOH и проточным буфером. Детектор был установлен на 214 нм. Величина подаваемого напряжения - 30 кВ. Образцы вводили методом впрыскивания под давлением: 20 секунд при давлении 0,5 psi.
ПРИМЕР 4
[0231] Композиция производного α-CD, имеющая одномодальный профиль распределения, может быть получена по примеру 5 или по любому методу из цитируемых в настоящем документе литературных источников, за исключением того, что вместо β-CD или γ-CD используют α-CD. Типовой SBE-α-CD получают по следующей процедуре, при которой α-циклодекстрин в водной щелочной среде дериватизируют с помощью предшественника SBE с получением SBE-α-CD. α-CD растворяют в водном растворе NaOH, нагревают до 70°C и перемешивают до полного растворения. По завершении растворения температуру реакционной смеси повышают до 70-75°C. Затем в течение по меньшей мере 30 минут добавляют 1,4-бутансультон. Величину pH контролируют в течение первых 4 часов; и реакции позволяют протекать при 70°C по меньшей мере дополнительные 16 часов. Реакционную смесь охлаждают и разбавляют водой (приблизительно одна треть суммарного объема реакционной смеси). Далее раствор обрабатывают углем (0,07 г угля на 1 г циклодекстрина), нейтрализуют раствором HCl до pH 6-6,5 и фильтруют через фильтр 0,45 мкм. Раствор очищают посредством ультрафильтрации на мембране 650 MWCO. Конечную точку ультрафильтрации определяют путем капиллярного электрофореза, причем фильтрат показывал полное или практически полное отсутствие 4-гидроксибутан-1-сульфоновой кислоты и/или динатриевой соли бис(4-сульфобутилового) эфира, а также по осмолярности, причем образцы фильтрата содержали мало или совсем не содержали ионов. Раствор фильтровали через фильтр 0,22 мкм и нейтрализовали до pH 6-6,5. Полученный раствор концентрировали до примерно 50% на роторном испарителе при температуре 50-60°C под вакуумом с давлением ниже 30 мм рт.ст. Раствор подвергали сублимационной сушке с получением SBE-α-CD в виде белого твердого вещества.
ПРИМЕР 5
Синтез SBE6.6-β-CD
[0232] Композицию SBE6.6-β-CD синтезировали по следующей процедуре, в которой β-циклодекстрин дериватизировали с помощью предшественника SBE в щелочной водной среде с образованием SBE6.6-β-CD. Водный раствор гидроксида натрия готовили путем добавления 61,8 кг гидроксида натрия к 433 кг воды с образованием 12,5%-го раствора (масс./масс.). Содержимое реактора нагревали до 40-50°C, после чего за 30-60 минут вводили 270 кг β-CD. Температуру реакционной смеси доводили до 65-95°C до введения в течение 30-60 минут 259 кг 1,4-бутансультона. В течение следующих 6 часов pH раствора поддерживали выше 9, добавляя водный раствор гидроксида натрия. По окончании реакции в реакционную смесь добавляли еще 13,5 кг гидроксида натрия в виде 20%-ного раствора. Температуру реакционной смеси поддерживали в пределах 70-80°C до достижения достаточно низкого содержания 1,4-бутансультона. Содержимое охлаждали до температуры ниже 30°C, затем pH реакционной смеси доводили до 6,5-7,5 с помощью водного раствора соляной кислоты. В результате данного процесса получали 350-450 кг SAE-CD.
ПРИМЕР 6
Диафильтрация и ультрафильтрация SBE6.6-β-CD
[0233] SBE6.6-β-CD из примера 5 очищали по следующей методике. Реакционный раствор разбавляли путем добавления 800 кг воды. Раствор переносили и разбавляли, добавляя еще 500 кг воды. Начинали диафильтрацию с помощью автоматической системы ультрафильтрации Helicon компании Millipore с использованием регенерируемых целлюлозных мембран 1000 MWCO, намотанных в виде спирали, имеющих площадь мембран по меньшей мере 750 кв. футов и поддерживающих постоянство объема раствора (±1%) до тех пор, пока образец ультрафильтрата не будет содержать 25 ppm или менее хлорида натрия. Раствор концентрировали методом ультрафильтрации до получения нужной массы раствора.
ПРИМЕР 7
Обработка SBE6.6-β-CD углем согласно настоящему изобретению
[0234] После диафильтрации и ультрафильтрации в примере 6, SBE6.6-β-CD очищали углем по следующей процедуре. В колонку загрузили 32 кг (приблизительно 11-12 масс. % (11,8-12 масс. %) от исходного количества β-циклодекстрина) гранулированного активированного угля Shirasagi® DC32 и тщательно промыли водой до достижения постоянной проводимости образцов промывочной воды. Отношение SBE6.6-β-CD к активированному углю составляло около 8,4:1-8,5:1 (примерно 8,44:1). По окончании промывки завершали первый цикл обработки путем пропускания (с рециркуляцией) реакционного раствора через уголь в течение по меньшей мере 2 часов.
[0235] Во вторую колонку загрузили 32 кг (приблизительно 11-12 масс. % от исходного количества β-циклодекстрина) гранулированного активированного угля Shirasagi® DC32 и тщательно промыли водой до достижения постоянной проводимости образцов промывочной воды. По окончании промывки завершали второй цикл обработки путем пропускания реакционного раствора через уголь в течение по меньшей мере 2 часов.
ПРИМЕР 8
Концентрирование и выделение SBE6.6-β-CD
[0236] Обработанные углем растворы SBE6.6-β-CD, полученные в примере 7, концентрировали и выделяли по следующей процедуре: раствор SBE6.6-β-CD фильтровали через фильтры 0,65 нм и 0,22 нм и затем концентрировали при пониженном давлении от -0,6 бар до -0,7 бар при температуре от 65°C до 72°C и перемешивании со скоростью 70-100 об./мин до получения раствора SBE6.6-β-CD с концентрацией 50 масс. %. Концентрированный раствор охлаждали до температуры ниже 60°C и фильтровали через фильтры 0,65 мкм и 0,22 мкм. Фильтрованный раствор подвергали распылительной сушке с помощью системы для сушки в кипящем слое («FSD») при температуре на входе 170°C, начальном давлении 20 бар и установках на камерах 1-3, равных 125°C, 105°C и 100°C, соответственно.
ПРИМЕР 9
Определение характера замещения циклодекстрина методами 1Н-ЯМР, 13С-ЯМР, COSY-ЯМР и HMQC на приборе Bruker Avance® 400 или 500 в растворах D2O
[0237] Определение характера замещения проводили согласно методу, описываемому в Примере 6 публикации WO 2005/042584; релевантные части описания которой включены в настоящую заявку посредством ссылки.
ПРИМЕР 10
Сравнительная обработка углем SBE6.6-β-CD
[0238] Типовой продукт SBE6.6-β-CD очищали углем по следующей процедуре: В колонку загрузили 32 кг (приблизительно 11-12 масс. % (11,8-12 масс. %) от исходного количества β-циклодекстрина в примере 5) гранулированного активированного угля Shirasagi® DC32 и тщательно промыли водой до достижения постоянной проводимости образцов промывочной воды. По окончании промывки реакционный раствор пропускали через уголь в течение по меньшей мере 2 часов.
ПРИМЕР 11
Анализ примесей I в SBE6.6-β-CD
[0239] Образцы SBE6.6-β-CD обрабатывали активированным углем один или два раза согласно примерам 10 и 7, соответственно, концентрировали и выделяли по методике, описанной в примере 8, и затем анализировали с помощью спектрофотометрии в УФ/видимой области. Анализ проводили путем растворения подходящего количества SBE6.6-β-CD в воде (например, от 0,1 г до 6 г SBE6.6-β-CD с корректировкой на содержание воды растворяли в 10 мл воды) с получением растворов, содержащих от 1 масс. % до 60 масс. % дериватизированного циклодекстрина.
[0240] Обработанные углем растворы циклодекстрина анализировали с помощью спектрофотометра УФ/видимой области Perkin Elmer Lambda 35 при сканировании от 190 нм до 400 нм со скоростью 240 нм/мин и ширине щели 1,0 нм. Перед анализом данные для образцов корректировали на поглощение воды. УФ/видимые спектры поглощения растворов SBE6.6-β-CD с различными концентрациями после одной или двух обработок активированным углем представлены в графической форме на Фиг. 1 и 2, соответственно, на которых приведено графическое представление для лотов SBE6.6-β-CD после одной или двух обработок активированным углем, проанализированных с помощью УФ метода. Данные Фиг. 1 демонстрируют, что при однократной обработке раствора SBE6.6-β-CD активированным углем этот раствор содержит более высокую концентрацию примесей, имеющих поглощение в УФ/видимом спектре. Данные Фиг. 2 демонстрируют, что вторая обработка углем снижает содержанием примесей, имеющих поглощение в УФ/видимом диапазоне, в пять раз или более.
ПРИМЕР 12
Анализ примесей II в SBE6.6-β-CD
[0241] Типовой образец SBE6.6-β-CD анализировали методом спектрофотометрии в УФ/видимой области по следующей процедуре: 50 масс. % раствор SBE6.6-β-CD готовили путем растворения 54,1 г SBE6.6-β-CD, с корректировкой на содержание воды в щелочном растворе, содержащем 12,5 г гидроксида натрия в 100 мл воды. Исходный раствор анализировали с помощью спектрофотометра УФ/видимой области Perkin Elmer Lambda 35; сканирование проводили в диапазоне от 190 нм до 400 нм со скоростью 240 нм/мин и ширине щели 1,0 нм. Перед анализом данные образца корректировали на поглощение воды. Раствор помещали печь при 60°C до 168 ч. Образцы раствора анализировали через 24 ч, 72 ч, 96 ч и 168 ч.
[0242] На Фиг. 3 приведено графическое представление результатов воздействия жестких условий нагрева и щелочной среды на композиции SBE6.6-β-CD. Данные Фиг. 3 демонстрируют, что за 24 ч возникло сильное поглощение при длине волны 245-270 нм, причем это поглощение возрастает по мере воздействия нагрева и щелочи на образец. Через 168 ч (7 суток) максимум поглощения при длине волны 245-270 нм возрос до такой же величины, как для поглощения с максимумом примерно 230 нм. Следует также отметить, что поглощение при длине волны 320-350 нм также возрастает по мере воздействия на образец. Эти данные показывают, что концентрации примеси, разлагающей лекарственное средства, имеющей поглощение при длине волны 245-270 нм, и окрашивающего компонента с поглощением при длине волны 320-350 нм возрастают по мере воздействия нагрева и/или щелочи на образец.
ПРИМЕР 13
Измерения окрашивающих агентов
[0243] Композиции SBE6.6-β-CD, подвергнутые одно- или двукратной обработке активированным углем (согласно примерам 10 и 7, соответственно) объединяли с фунгицидным активным лекарственным ингредиентом (API) триазольного типа (посаконазол, приобретенный у компании Schering-Plough в виде водной суспензии для орального введения, Noxafil®). Процедура приготовления состава описана ниже.
[0244] Образцы водного раствора фунгицидного триазольного API (5 мг/мл) и композицию SBE6.6-β-CD (100 мМ, рН 3) получали с использованием SBE6.6-β-CD лота №№17CX01.HQ00044, 17CX01.HQ00037, 17CX01.HQ00035, 17CX01.HQ00033 и 17CX01.HQ00029. Все образцы растворов фильтровали через 0,22 мкм ПВДФ фильтр и разливали по виалам. Для проб исходных растворов измеряли поглощение в УФ/видимой области в кювете толщиной 1 см фирмы Hunter на спектрофотометра УФ/видимой области Perkin Elmer Lambda 35, сканирование от 190 нм до 400 нм со скоростью 240 нм/мин и шириной щели 1,0 нм, и анализировали пробы на колориметре Hunter Labs Ultrascan® с использованием универсального программного обеспечения Hunter Labs, версия 4,10. Перед измерениями данные для образцов корректировали на поглощение воды. Затем оставшиеся порции образцов помещали в печь с температурой 60°C в течение 7 дней и затем заново анализировали изменения цвета с помощью той же процедуры. Полученные данные приведены в следующих таблицах.
Исходные растворы SBE6.6-β-CD: анализ УФ/видимых спектров
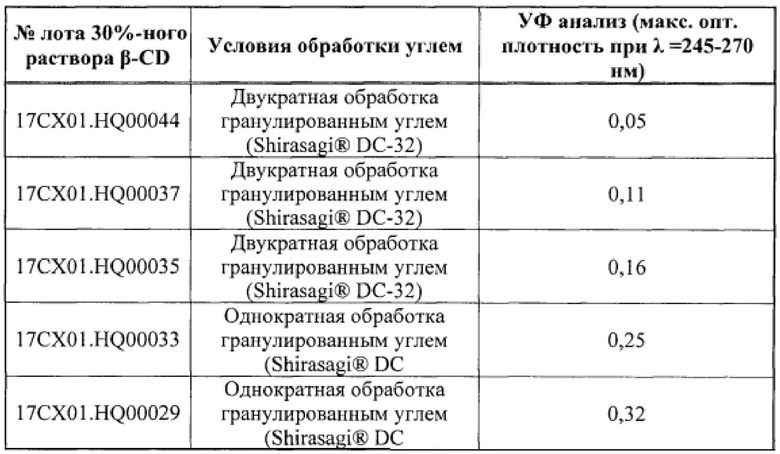
Колориметрический анализ раствора SBE6.6-β-CD

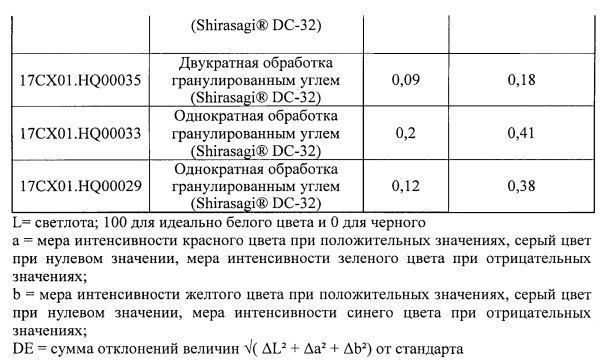
Колориметрический анализ раствора триазольного API/SBE6.6-β-CD
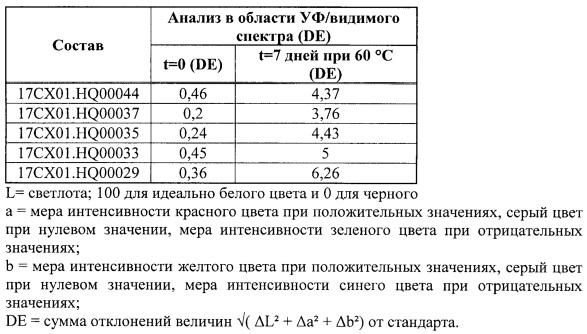
[0245] УФ анализ продемонстрировал, что содержание УФ-активных примесей, присутствующих в исходной композиции SBE6.6-β-CD, значительно ниже после двукратной обработки композиций циклодекстрина активированным углем. Анализ на колориметре Hunter композиции SBE6.6-β-CD показал более низкие значения DE для тех лотов SBE6.6-β-CD, которые были двукратно обработаны активированных углем. Таким образом, более низкие уровни примесей в композиции SBE6.6-β-CD, подвергнутой двукратной обработке активированным углем, приводят к снижению образования окрашивающих агентов.
ПРИМЕР 14
Раздельные растворы SBE6.6-β-CD, подвергнутые тепловой обработке, а затем обработке углем
[0246] Эффект от нагрева композиции дериватизированного циклодекстрина согласно настоящему изобретению изучали следующим образом. Композицию SBE6.6-β-CD, полученную в соответствии с примером 5, растворяли в водном растворе и анализировали методом спектрофотометрии в УФ/видимой области. В частности, получали 30 масс. % раствор β-циклодекстрина путем растворения 70 г SBE6.6-β-CD, лот №17CX01.HQ00044 (масса корректировалась на содержание воды), в 230 мл воды. Данный исходный раствор анализировали с помощью спектрофотометра УФ/видимой области Perkin Elmer Lambda 35 при сканировании от 190 нм до 400 нм со скоростью 240 нм/мин и ширине щели 1,0 нм. Перед анализом данные образца корректировали на поглощение воды. Раствор нагревали при перемешивании до 70°C в течение 48 часов. Раствор охлаждали до комнатной температуры и разделяли. К каждой из порций раствора добавляли предварительно промытый гранулированный активированный уголь Shirasagi® DC32. Растворы SBE6.6-β-CD перемешивали в течение 3 часов, затем активированный уголь отфильтровывали на 0,22 мкм ПВДФ фильтре. Растворы анализировали с помощью спектрофотометра УФ/видимой области Perkin Elmer Lambda 35 при сканировании от 190 нм до 400 нм со скоростью 240 нм/мин и ширине щели 1,0 нм. Перед анализом данные для образцов корректировали на поглощение воды.
[0247] Полученные данные приведены в графической форме на Фиг. 4. На Фиг, 4 показаны данные по поглощению раствора в УФ/видимой области до тепловой обработки (++++), сразу после тепловой обработки в течение 48 часов (▪▪▪▪) и после воздействия активированного угля при загрузке 0,24 масс. % (……), 10 масс. %) (-), 25 масс. % (♦♦♦♦) и 50 масс. % (оооо) (в расчете на концентрацию SBE6.6-β-CD). Эти данные показывают, что воздействие тепловой обработки раствора SBE6.6-β-CD в течение 48 часов приводит к существенному (примерно на 95%) возрастанию максимума поглощения при длине волны 245-270 нм. Тем не менее, обработка активированным углем снижает поглощение в этом диапазоне длин волн. Таким образом, количество примеси, разлагающей лекарственные средства, имеющая поглощение при длине волны 245-270 нм, возрастает при нагреве, но может быть уменьшено посредством обработки углем.
ПРИМЕР 15
Стабильность SBE6.6-β-CD DS и API
[0248] Сравнительная оценка различных партий SBE6.6-β-CD, подвергнутых однократной или двукратной обработке активированным углем, в комбинации с антипсихотическим API (арипиразолом), проводили с помощью спектрофотометрии в УФ/видимой области и анализа ВЭЖХ. Общая процедура, используемая для оценки стабильности составов SBE6.6-β-CD/API, приводится ниже.
[0249] Были получены водные растворы, содержащие образцы API (арипиразола) с концентрацией 7,5 мг/мл API и 150 мг/мл SBE6.6-β-CD. В воду добавляли винную кислоту до прекращения растворения, затем в раствор винной кислоты вводили SBE6.6-β-CD. После этого в растворы вводили API, который растворялся приблизительно через 10 минут после введения. Смесь перемешивали примерно 1 час, обрабатывали нагреванием и фильтровали через стерильный фильтр. Данный процесс выполняли со следующими лотами SBE6.6-β-CD, некоторые из которых подвергались однократной обработке активированным углем, а другие двукратной обработке активированным углем (SBE6.6-β-CD, лоты №№17CX01.HQ00021, 17CX01.HQ00025, 17CX01.HQ00029, 17CX01.HQ00035, 17CX01.HQ00036, 17CX01.HQ00037, 17CX01.HQ00038, 17CX01.HQ00039, 17CX01.HQ00040, 17CX01.HQ00041, 17CX01.HQ00042, 17CX01.HQ00043 и 17CX01.HQ00044). Образцы растворов помещали в камеру со стабилизированными условиями при 50°C на срок до 9 недель. Образцы отбирали через 4 недели и через 9 недель и анализировали методом ВЭЖХ для определения степени разложения API.
[0250] Образцы водных растворов анализировали методом спектрофотометрии в УФ/видимой области посредством следующей процедуры. Были получены 30 масс. % растворы β-циклодекстрина путем растворения образцов указанных выше лотов SBE6.6-β-CD (масса корректировалась на содержание воды) в воде. Растворы анализировали с помощью спектрофотометра УФ/видимой области Perkin Elmer Lambda 35 при сканировании от 190 нм до 400 нм со скоростью 240 нм/мин и ширине щели 1,0 нм, кювета 1 см. Перед анализом данные для образцов корректировали на поглощение воды. Ниже приведены таблицы с данными, полученными в указанных исследованиях.
Данные о лотах SBE6.6-β-CD и содержание ингредиентов, поглощающих УФ
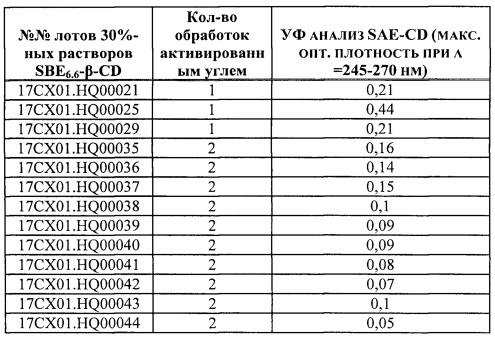
Анализ примесей в SAE-CD и API
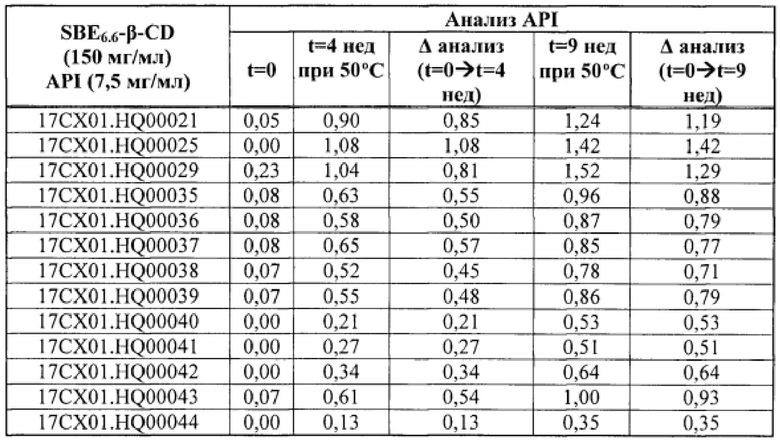
[0251] Эти данные показывают, что API претерпевает значительно более сильное разложение, когда оно находится в объединено с лотами SBE6.6-β-CD, подвергнутыми только однократной обработке активированным углем. Состав API, содержащий SBE6.6-β-CD, лот 17CX01.HQ00025, имел наибольшее содержание примесей, обладающих поглощением в УФ области (макс. опт. плотность = 0,44 ед. погл.), причем суммарное разложение API через 9 недель составило 1,42%. Лоты SBE6.6-β-CD, подвергнутые двукратной обработке активированным углем, отличались заметно более низким содержанием примесей, обладающих поглощением в УФ области, и степенью разложения API. Степень разложения API при хранении в течение 9 недель при 50°C коррелировала с концентрацией присутствующих в композициях примесей, обладающих поглощением в УФ области. Например, в составе API, содержавшем SBE6.6-β-CD лота 17CX01.HQ00044 (содержащем примеси, поглощающие в УФ области с максимальным поглощением = 44 ед. погл.) суммарное разложение API через 9 недель при 50°C составило только 0,35 при 50°C.
[0252] На ФИГ. 5 графически представлена корреляция между начальным поглощением в УФ/видимой области различных лотов SBE6.6-β-CD) при длинах волн 245-270 нм и степенью разложения активного лекарственного компонента, измеренной через 4 и 9 недель. Исходя из данных на Фиг. 5, можно сделать вывод, что как через 4 недели 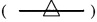 , так и через 9 недель
, так и через 9 недель  степень разложения API возрастает с концентрацией примесей, разлагающих лекарственные средства, поглощающих в УФ/видимой области, присутствующих композиции SBE6.6-β-CD.
степень разложения API возрастает с концентрацией примесей, разлагающих лекарственные средства, поглощающих в УФ/видимой области, присутствующих композиции SBE6.6-β-CD.
ПРИМЕР 16
Измерение примесей путем обработки
[0253] Образцы SBE6.6-β-CD после реакционной обработки (Пример 5), после ультрафильтрации (Пример 6), после второй колонки с углем (Пример 7), после концентрирования (Пример 8) и в виде конечного продукта отделяли, идентифицировали и количественно оценивали с помощью аппарата Shimadzu Prominence 20А HPLC и колонки ZIC® pHILIC (150×4,6 мм, 5 мкм, 200 А, PEEK Merck SeQuant™ SN 1479) с использованием детектора заряженного аэрозоля Corona (ESA Bioscience). Метод градиента подвижной фазы осуществляли с использованием смеси 100 мМ формиата аммония (рН доводили до 4,6), метанола, 2-пропанола, и ацетонитрила 15/5/20/65 (А) и смеси раствора 30 мМ формиата аммония (pH доводили до 4,6), метанола, 2-пропанола, и ацетонитрил 65/5/20/10 (В). Раствор образца Captisol® получали при концентрации приблизительно 40 мг/мл в смеси ацетонитрил для ВЭЖХ/вода и анализировали в сравнении с полученным раствором сравнения с известной концентрацией 4-гидроксибутан-1-сульфоновой кислоты, бис-(4-сульфобутилового) эфира динатрия, хлорида, натрия, фосфата, диоксида кремния и β-циклодекстрина в смеси ацетонитрил/вода в пределах допустимого содержания примесей. Валидационное исследование показало, что способ является специфичным, линейным в пределах допустимого содержания примесей, точным и стабильным. Использованный градиент приведен в следующей таблице.
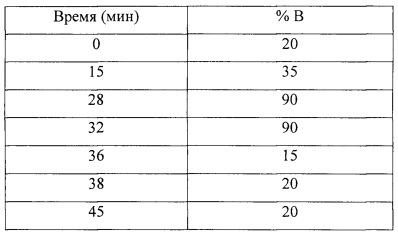
[0254] Как показано на ФИГ. 6, после ультрафильтрации неочищенного SBE6.6-β-CD продукта, присутствуют примеси, такие как β-циклодекстрин и 4-гидроксибутан-1-сульфоновая кислота (4-HBSA). После второй колонки с активированным углем количество примесей β-циклодекстрина и 4-гидроксибутан-1-сульфоновой кислоты было снижено. Однако, как показано на ФИГ. 6 в продукте после двух колонок присутствуют большие количества хлорида.
ПРИМЕР 17
Измерение концентрации хлоридов
[0255] Образцы SBE6.6-β-CD после реакционной обработки (Пример 5), после ультрафильтрации (Пример 6), после второй колонки с углем (Пример 7), после концентрирования (Пример 8) и в виде конечного продукта анализировали с использованием детектора заряженного аэрозоля Corona (ESA Bioscience).
[0256] Как показано на ФИГ. 7, после ультрафильтрации остаточный уровень хлоридов упал приблизительно до нуля. После дополнительной очистки с использованием двух колонок с активированным углем содержание хлоридов восстановилось в растворе SBE6.6-β-CD.
ПРИМЕР 18
Измерение концентрации хлоридов
[0257] Образцы SBE6.6-β-CD после реакционной обработки (Пример 5), после ультрафильтрации (Пример 6) через 5, 10 и 20 минут после добавления в первую колонку с активированным углем и через 5, 10, и 20 минут после добавления во вторую колонку с активированным углем анализировали с использованием детектора заряженного аэрозоля Corona (ESA Bioscience).
[0258] Как показано на ФИГ. 8 содержание примесей хлоридов у двух коммерческих партий SBE6.6-β-CD составляет приблизительно ноль после ультрафильтрации и существенно возрастает после обработки активированным углем в течение первых 5 минут и падает через 10 и 20 минут.
ПРИМЕР 19
Очистка активированного угля с использованием специальной системы емкостей
[0259] Активированный уголь можно добавить в специальную систему емкостей с мешалкой и системой сит. Активированный уголь можно загрузить с последующей промывкой несколькими порциями воды при заданной скорости перемешивания в течение заданного периода. После промывки водой слой воды можно удалить из специальной системы емкостей и промыть дополнительным количеством воды. После дополнительных промывок водой проводимость элюированной воды можно определить с использованием ионообменной хроматографии (колонка 4,0×250 мм USP L50 или аналогичная с подвижной фазой 4 мМ бикарбоната натрия в смеси метанол/вода (1:9), скорость потока 1 мл/мин, объем образца 20 мкл и время хроматографирования 10 мин), и когда проводимость составляет ниже заданного уровня, уголь можно суспендировать в воде и закачать обратно в камеру для угля. После этого активированный уголь будет готов для добавления к раствору алкилированного циклодекстрина.
ПРИМЕР 20
Очистка SBE6.6-β-CD с использованием активированного угля с заданным уровнем проводимости
[0260] В колонку загрузили 32 кг (приблизительно 11-12 масс. % (11,8-12 масс. %) от исходного количества β-циклодекстрина) гранулированного активированного угля Shirasagi® DC32 и тщательно промыли водой до достижения проводимости образцов промывочной воды менее 10 мкСм, как показано в следующей Таблице. Проводимость определяли с использованием ионообменной хроматографии (колонка 4,0×250 мм USP L50 или аналогичная с подвижной фазой 4 мМ бикарбоната натрия в смеси метанол/вода (1:9), скорость потока 1 мл/мин, объем образца 20 мкл и время хроматографирования 10 мин).
[0261] Отношение SBE6.6-β-CD и активированному углю составляло примерно от 8,4:1 до 8,5:1 (примерно 8,44:1). После промывки реакционный раствор пропускали (циклично) через уголь в течение по меньшей мере 2 часов для завершения первого цикла обработки.
[0262] Во вторую колонку загрузили 32 кг (приблизительно 11-12 масс. % (11,8-12 масс. %) от исходного количества β-циклодекстрина) гранулированного активированного угля Shirasagi® DC32 и тщательно промыли водой до достижения проводимости образцов промывочной воды менее 10 мкСм, измеренной с использованием ионообменной хроматографии (колонка 4,0×250 мм USP L50 или аналогичная с подвижной фазой 4 мМ бикарбоната натрия в смеси метанол/вода (1:9), скорость потока 1 мл/мин, объем образца 20 мкл и время хроматографирования 10 ми), как показано в следующей Таблице. После промывки реакционный раствор пропускали через уголь в течение по меньшей мере 2 часов для завершения второго цикла обработки.
[0263] После второго цикла обработки SBE6.6-β-CD анализировали с использованием детектора заряженного аэрозоля Corona (ESA Bioscience) для определения концентрации хлоридов.
[0264] Как показано в указанной Таблице, все образцы имели содержание хлорида 0,07% или менее, где 6 из 9 образцов имели содержание менее 0,05% (предел обнаружения для ионного хроматографа). Это является улучшением относительно измерений с использованием предыдущего метода, показанного на ФИГ. 10, в котором показатель эффективности при достижении уровня хлорида менее 0,10%. составлял только 65% (44 из 68 образцов). Это также является значительным улучшением относительно предыдущего метода для образцов, которые for пропускали через два цикла обработки активированным углем, как показано на ФИГ. 10, в котором показатель эффективности при достижении уровня хлорида менее 0,10% составлял только 48% (20 из 42 образцов).
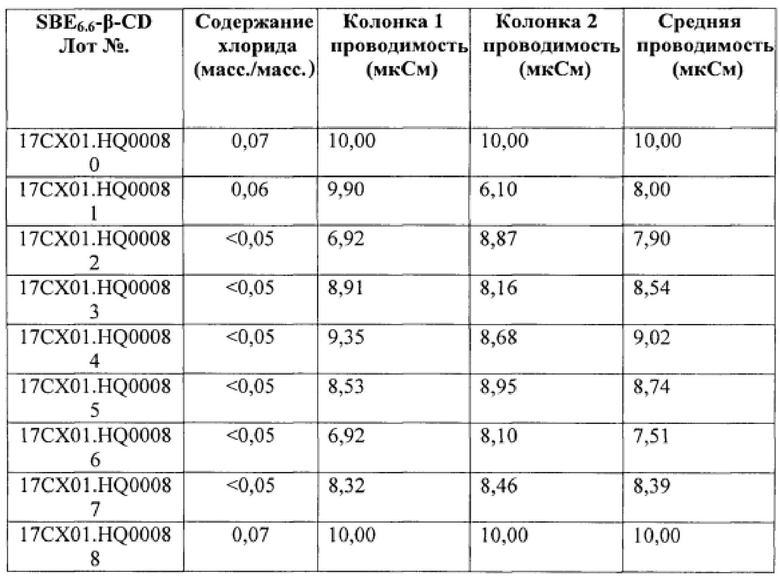
ПРИМЕР 21
Очистка активированного угля до постоянного уровня проводимости
[0265] В колонку загрузили 32 кг (приблизительно 11-12 масс. % (11,8-12 масс. %) от исходного количества β-циклодекстрина) гранулированного активированного угля Shirasagi® DC32 и тщательно промыли водой до достижения постоянной проводимости образцов промывочной воды. После промывки водой часть раствора алкилированного циклодекстрина можно добавить в емкость и пропустить через уголь в течение заданного периода времени до выгрузки. Дополнительное количество раствора алкилированного циклодекстрина можно добавить в емкость и пропустить через уголь в течение по меньшей мере 2 часов для завершения первого цикла обработки.
[0266] Во вторую колонку загрузили 32 кг (приблизительно 11-12 масс. % (11,8-12 масс. %) от исходного количества β-циклодекстрина) гранулированного активированного угля Shirasagi® DC32 и тщательно промыли водой до достижения постоянной проводимости образцов промывочной воды. После промывки водой часть раствора алкилированного циклодекстрина можно добавить в емкость и пропустить через уголь в течение заданного периода времени до выгрузки. Дополнительное количество раствора алкилированного циклодекстрина можно добавить в емкость и пропустить через уголь в течение по меньшей мере 2 часов для завершения первого цикла обработки.
ВЫВОДЫ
[0267] Эти примеры иллюстрируют возможные варианты реализации настоящего изобретения. Хотя выше описаны различные варианты реализации настоящего изобретения, следует понимать, что они представлены лишь в качестве примеров и не ограничивают рамки настоящего изобретения. Для специалиста в соответствующей области техники будет очевидно, что можно внести различные изменения в форму и детали реализации не отклоняясь от сущности и объема изобретения. Таким образом, широту и объем настоящего изобретения не следует ограничивать каким-либо из описанных выше вариантов реализаций; но следует определять только на основании формулы изобретения, представленной ниже, и эквивалентов ее пунктов.
[0268] Следует принимать во внимание, что для интерпретации формулы изобретения следует использовать раздел «Подробное описание изобретения», а не разделы «Краткое описание изобретение» и «Реферат». В разделах «Краткое описание изобретение» и «Реферат» могут излагаться один или более, но не все примеры вариантов реализаций настоящего изобретения в том виде, как оно предполагалось изобретателем (изобретателями); следовательно, они не предназначены для ограничения объема настоящего изобретения и прилагаемой формулы изобретения.
[0269] Все различные аспекты, варианты реализаций и модификации, описанные в настоящей заявке, можно объединять в любой комбинации.
[0270] Все документы, приведенные в настоящем документе, включая журнальные статьи или рефераты, опубликованные или соответствующие заявки на патент США или иностранные заявки, выданные или иностранные патенты, или любые другие документы, во все полноту включены в настоящий документ посредством ссылки, включая все данные, таблицы, фигуры и текст, содержащиеся в приведенных документах.
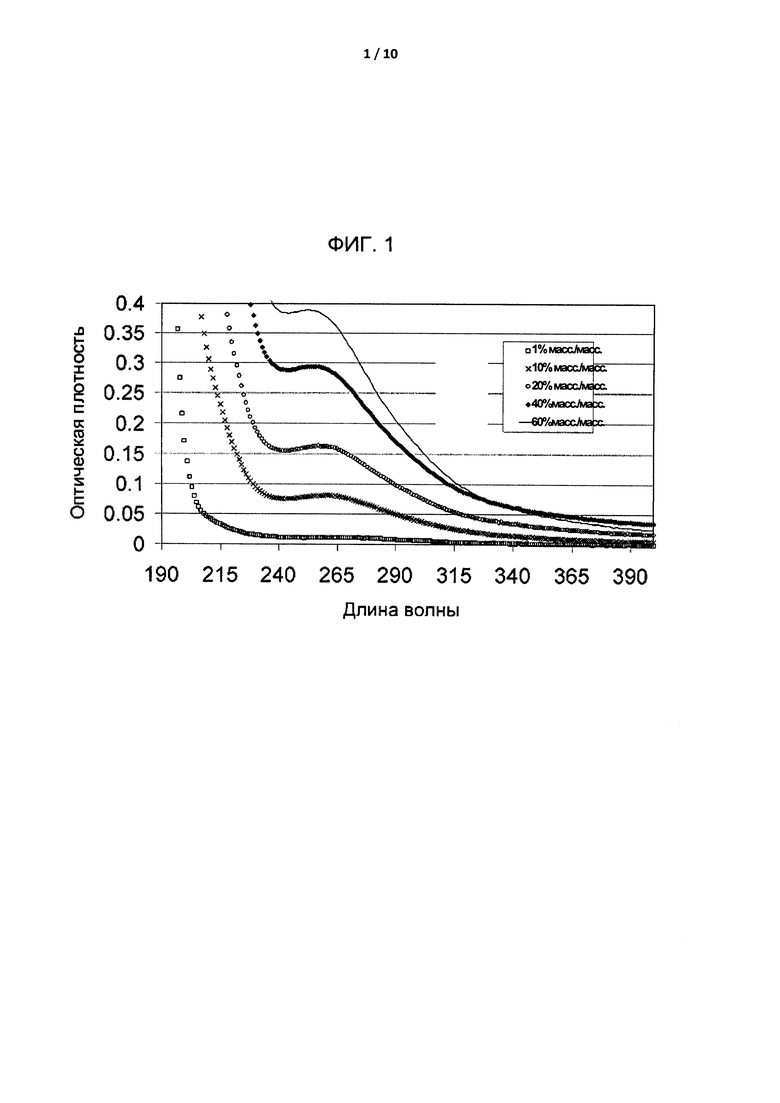
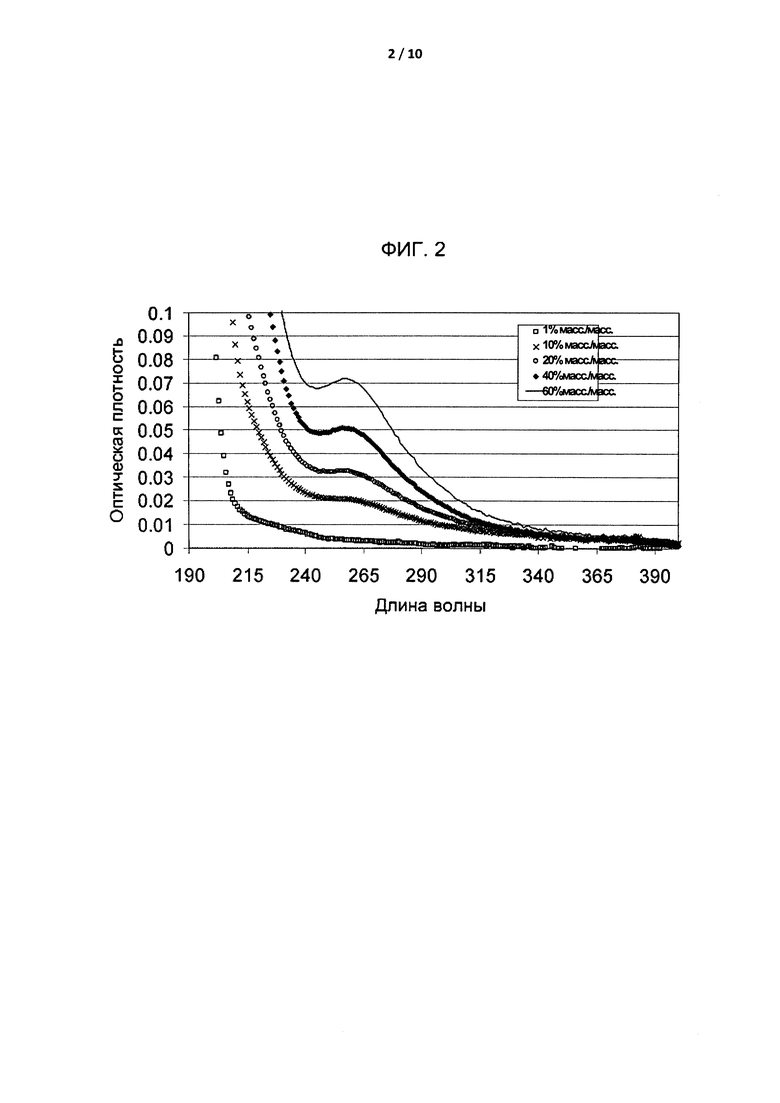
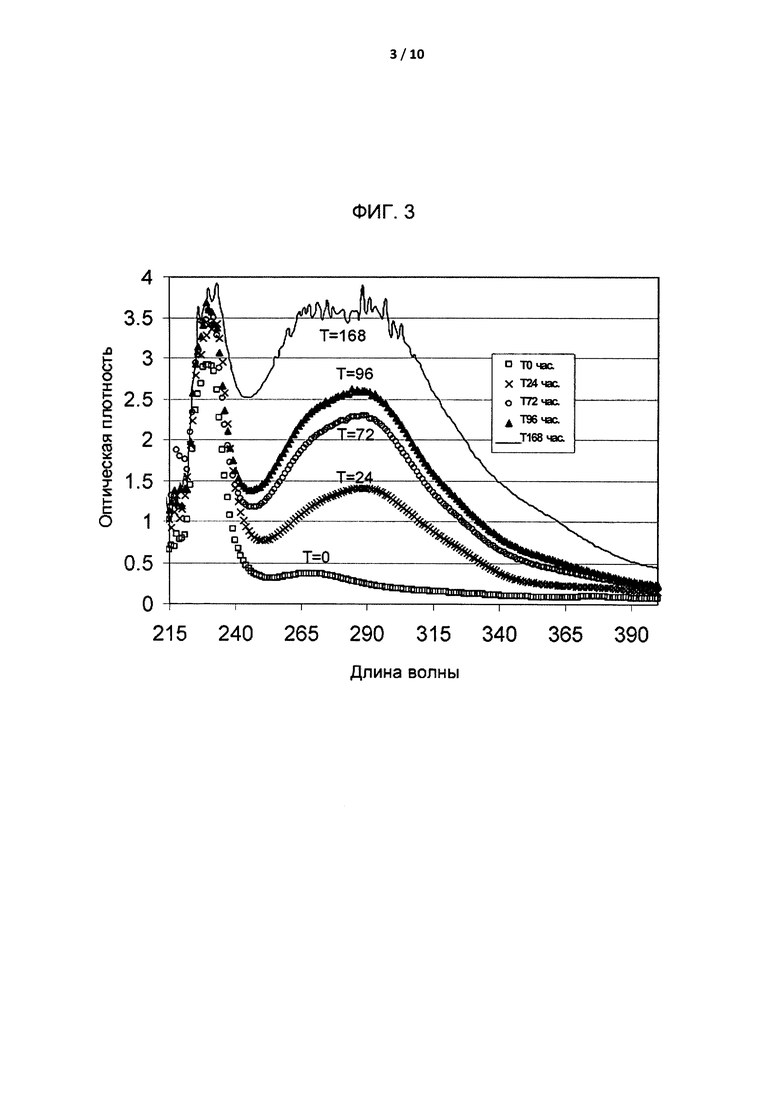
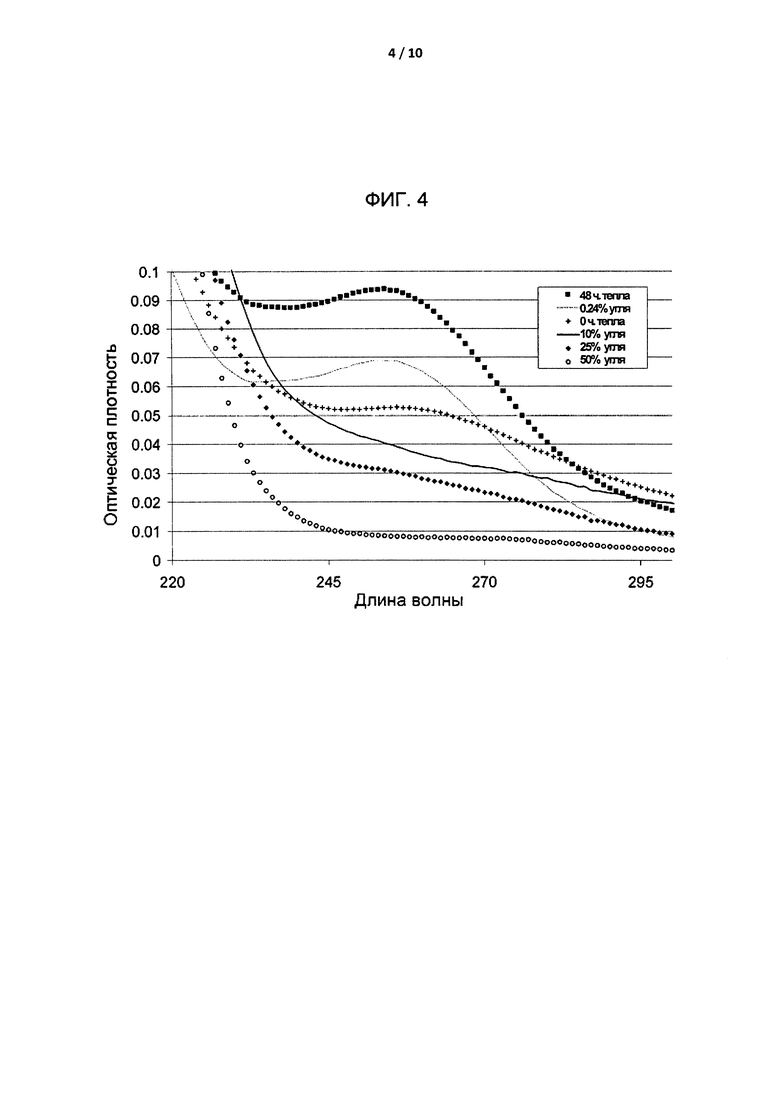
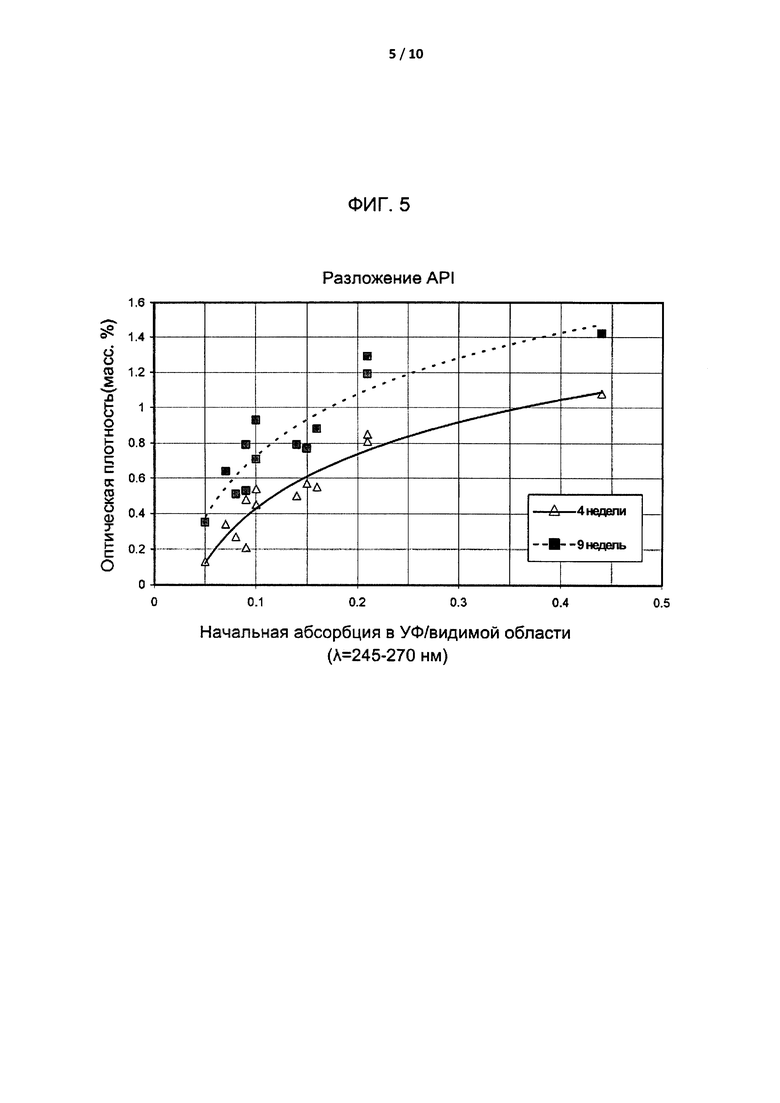
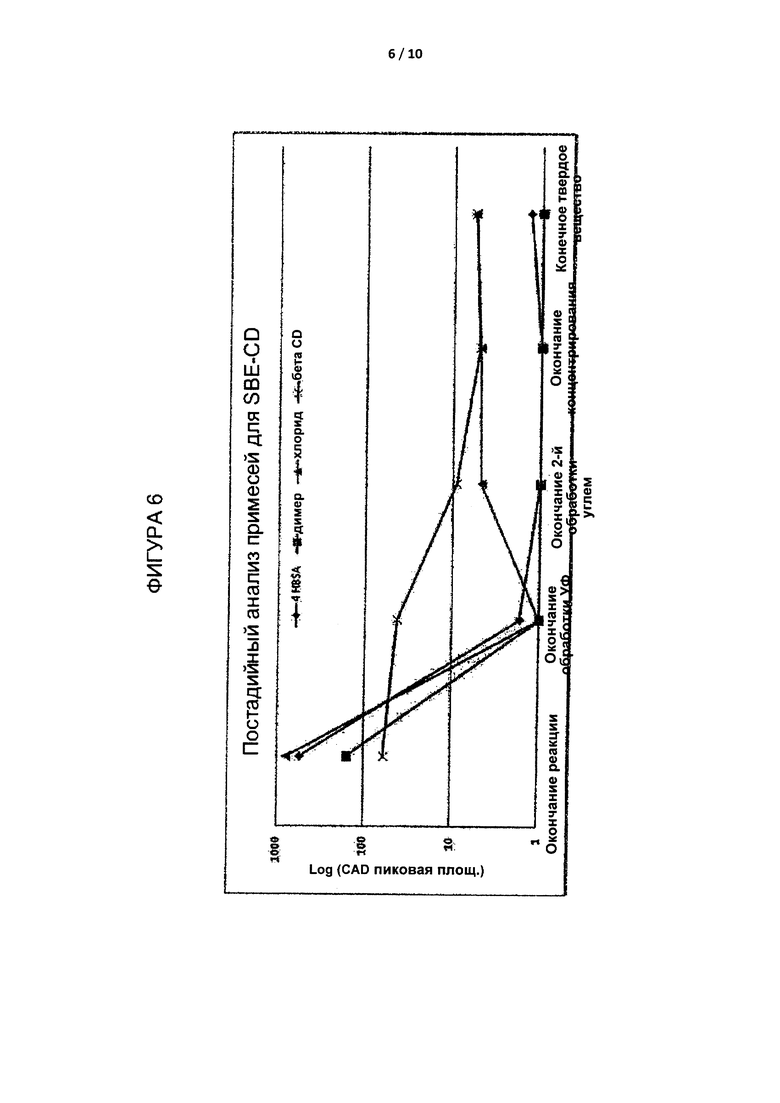
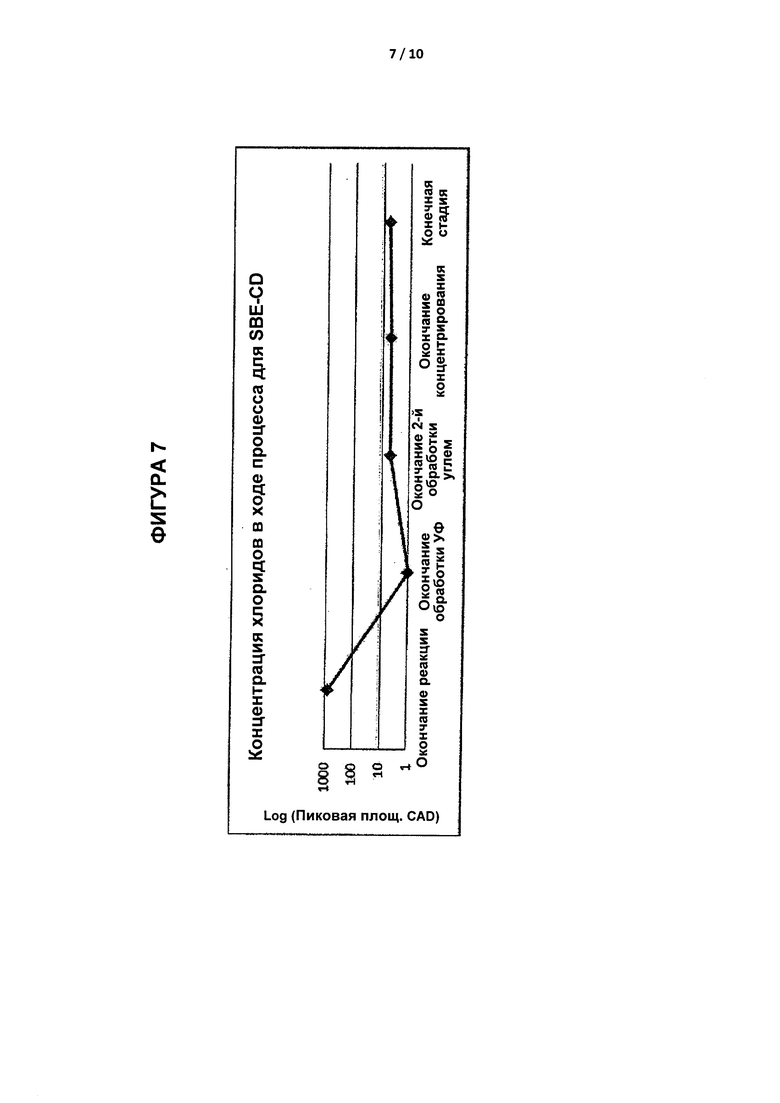
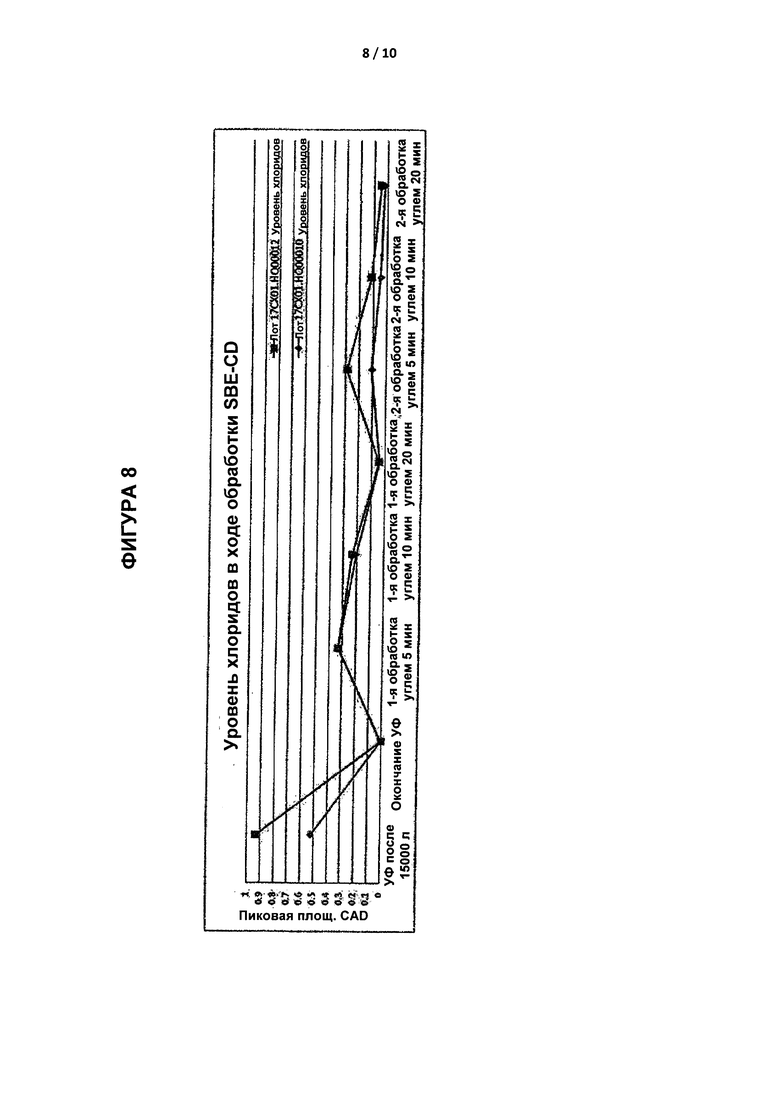
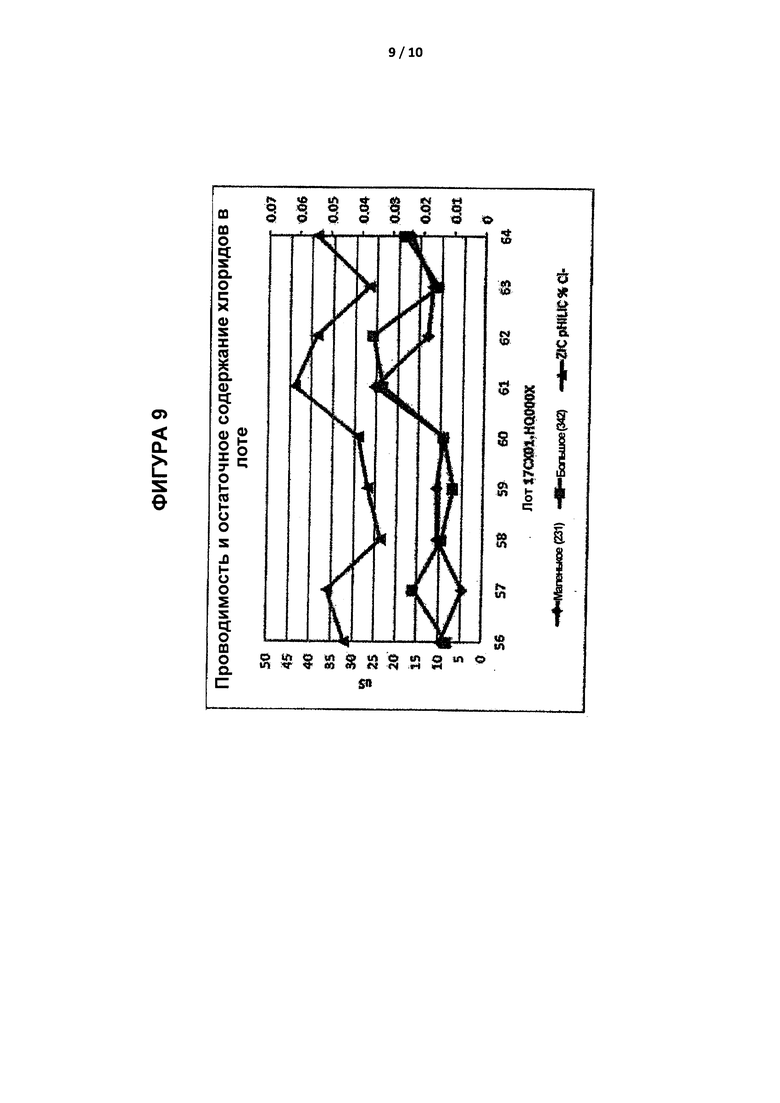
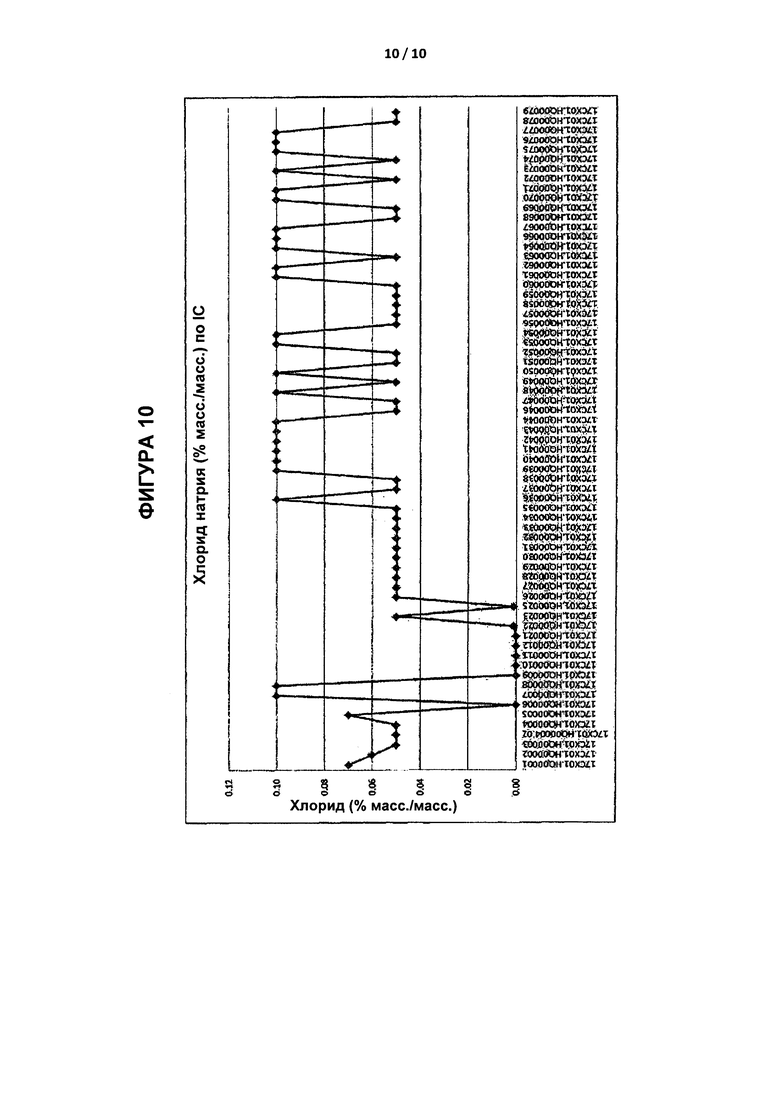
Группа изобретений относится к области фармацевтики и представляет собой способ получения сульфоалкильных эфиров циклодекстрина, обеспечивающий низкое содержание компонентов, разлагающих лекарственное средство, в частности хлоридов, за счет стадии обработки активированным углем с проводимостью 10 мкСм или менее, а также к продукту, полученному указанным способом, и композиции для доставки активных агентов, чувствительных к содержанию хлоридов. Группа изобретений позволяет воспроизводимо получать сульфоалкильные эфиры циклодекстрина с пониженным содержанием хлоридов и обеспечивает повышенную стабильность композиций с активными агентами, чувствительными к содержанию хлоридов. 3 н. и 30 з.п. ф-лы, 10 ил., 13 табл., 21 пр.
1. Способ получения алкилированного циклодекстрина, содержащего сульфоалкильный эфир циклодекстрина формулы (II):
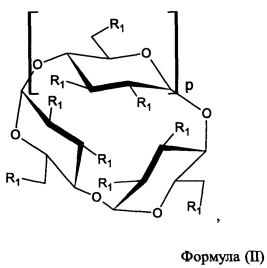
где р представляет собой 4, 5 или 6, и R1 независимо в каждом случае выбран из -ОН или -О-(С2-С6 алкилен)-SO3--Т, где Т независимо в каждом случае выбран из фармацевтически приемлемых катионов, при условии, что по меньшей мере один R1 представляет собой -ОН и по меньшей мере один R1 представляет собой О-(С2-С6 алкилен)-SO3--Т;
включающий:
(a) смешивание циклодекстрина с алкилирующим агентом с получением реакционной среды, содержащей алкилированный циклодекстрин, один или более нежелательных компонентов и одну или более примесей, разлагающих лекарственное средство;
(b) проведение одного или более разделений с удалением одного или более нежелательных компонентов из реакционной среды с получением частично очищенного раствора, содержащего указанный алкилированный циклодекстрин и указанную одну или более примесей, разлагающих лекарственное средство, где указанное одно или более разделений представляют собой ультрафильтрацию, диафильтрацию, центрифугирование, экстракцию, осаждение с растворителем или диализ; и
(с) обработку указанного частично очищенного раствора бесфосфатным активированным углем, имеющим остаточную проводимость 10 мкСм или менее, и получение алкилированного циклодекстрина.
2. Способ по п. 1, отличающийся тем, что указанный алкилированный циклодекстрин дополнительно содержит менее 500 ppm фосфата.
3. Способ по п. 1, отличающийся тем, что указанный алкилированный циклодекстрин также содержит менее 200 ppm фосфата.
4. Способ по п. 1, отличающийся тем, что указанный алкилированный циклодекстрин дополнительно содержит менее 125 ppm фосфата.
5. Способ по п. 1, отличающийся тем, что указанная остаточная проводимость на этапе (с) составляет 9 мкСм или менее.
6. Способ по п. 1, отличающийся тем, что указанная остаточная проводимость на этапе (с) составляет 8 мкСм или менее.
7. Способ по п. 1, отличающийся тем, что указанный алкилированный циклодекстрин дополнительно содержит менее 0,5% (масс./масс.) хлорида.
8. Способ по п. 1, отличающийся тем, что указанный алкилированный циклодекстрин дополнительно содержит менее 0,1% (масс./масс.) хлорида.
9. Способ по п. 1, отличающийся тем, что указанный алкилированный циклодекстрин также содержит менее 0,07% (масс./масс.) хлорида.
10. Способ по п. 1, отличающийся тем, что указанный алкилированный циклодекстрин дополнительно содержит менее 0,05% (масс./масс.) хлорида.
11. Способ по п. 1, отличающийся тем, что указанный алкилированный циклодекстрин не содержит поддающихся определению методом ионной хроматографии уровней хлоридов при измерении с использованием детектора заряженного аэрозоля.
12. Способ по п. 1, отличающийся тем, что указанный алкилированный циклодекстрин имеет среднюю степень замещения от 2 до 9.
13. Способ по п. 1, отличающийся тем, что указанный алкилированный циклодекстрин имеет среднюю степень замещения от 4,5 до 7,5.
14. Способ по п. 1, отличающийся тем, что указанный алкилированный циклодекстрин имеет среднюю степень замещения от 6 до 7,5.
15. Способ по п. 1, отличающийся тем, что указанный алкилированный циклодекстрин имеет оптическую плотность менее 1 Е.П., измеренную с помощью спектрофотометрии в УФ/видимой области в диапазоне длин волн от 245 нм до 270 нм для водного раствора, содержащего 300 мг указанного алкилированного циклодекстрина на мл раствора, в кювете с толщиной поглощающего слоя 1 см.
16. Способ по п. 1, отличающийся тем, что указанный алкилированный циклодекстрин имеет оптическую плотность менее 0,5 Е.П., измеренную с помощью спектрофотометрии в УФ/видимой области в диапазоне длин волн от 245 нм до 270 нм для водного раствора, содержащего 300 мг указанного алкилированного циклодекстрина на мл раствора, в кювете с толщиной поглощающего слоя 1 см.
17. Способ по п. 15, отличающийся тем, что указанная оптическая плотность связана с агентом, разлагающим лекарственное средство.
18. Способ по п. 15, отличающийся тем, что указанную оптическую плотность определяют с помощью спектрофотометрии в УФ/видимой области в диапазоне длин волн от 245 нм до 270 нм для водного раствора, содержащего 500 мг указанного алкилированного циклодекстрина на мл раствора, в кювете с толщиной поглощающего слоя 1 см.
19. Способ по п. 1, отличающийся тем, что указанный алкилированный циклодекстрин имеет оптическую плотность менее 1 Е.П., измеренную с помощью спектрофотометрии в УФ/видимой области в диапазоне длин волн от 320 нм до 350 нм для водного раствора, содержащего 300 мг указанного алкилированного циклодекстрина на мл раствора, в кювете с толщиной поглощающего слоя 1 см.
20. Способ по п. 1, отличающийся тем, что указанный алкилированный циклодекстрин имеет оптическую плотность менее 0,5 Е.П., измеренную с помощью спектрофотометрии в УФ/видимой области в диапазоне длин волн от 320 нм до 350 нм для водного раствора, содержащего 300 мг указанного алкилированного циклодекстрина на мл раствора, в кювете с толщиной поглощающего слоя 1 см.
21. Способ по п. 19, отличающийся тем, что указанная оптическая плотность связана с окрашивающим агентом.
22. Способ по п. 19, отличающийся тем, что указанную оптическую плотность определяют с помощью спектрофотометрии в УФ/видимой области в диапазоне длин волн от 320 нм до 350 нм для водного раствора, содержащего 500 мг указанного алкилированного циклодекстрина на мл раствора, в кювете с толщиной поглощающего слоя 1 см.
23. Способ по п. 1, отличающийся тем, что указанный бесфосфатный активированный уголь промывают растворителем до достижения элюированным растворителем остаточной проводимости на этапе (с).
24. Способ по п. 1, отличающийся тем, что указанный бесфосфатный активированный уголь промывают водой до достижения элюированной водой остаточной проводимости на этапе (с).
25. Способ по п. 1, отличающийся тем, что R1 независимо в каждом случае выбран из -ОН или -О-(С4 алкилен)-SO3--Т, и -Т в каждом случае представляет собой Na+.
26. Способ по п. 1, дополнительно включающий комбинирование указанного алкилированного циклодекстрина с одним или более вспомогательными веществами.
27. Способ по п. 1, дополнительно включающий комбинирование указанного алкилированного циклодекстрина с активным агентом.
28. Способ по п. 27, отличающийся тем, что активный агент представляет собой активный агент, чувствительный к содержанию хлоридов, выбранный из группы, состоящей из бортезомиба, дисульфирама, эпигаллокатехин-3-галлата, салиноспорамида А и карфилзомиба.
29. Способ по п. 28, отличающийся тем, что активный агент, чувствительный к содержанию хлоридов, представляет собой карфилзомиб.
30. Продукт для доставки активного агента, чувствительного к содержанию хлоридов, представляющий собой циклодекстрин, полученный по способу по любому из пп. 1-29.
31. Фармацевтическая композиция, содержащая продукт по п. 30 и активный фармацевтический агент, чувствительный к содержанию хлоридов.
32. Фармацевтическая композиция по п. 31, отличающаяся тем, что указанный активный агент, чувствительный к содержанию хлоридов, выбран из группы, состоящей из бортезомиба, дисульфирама, эпигаллокатехин-3-галлата, салиноспорамида А и карфилзомиба.
33. Фармацевтическая композиция по п. 32, отличающаяся тем, что указанный активный агент, чувствительный к содержанию хлоридов, представляет собой карфилзомиб.
| WO 2009134347 A2, 05.11.2009 | |||
| WO 2009045497 A1, 09.04.2009 | |||
| WO 2009018069 A2, 05.02.2009 | |||
| US 6153746 A, 28.11.2000 | |||
| US 5134127 A, 28.07.1992 | |||
| YANG J | |||
| et al | |||
| Pharmacokinetics, Pharmacodynamics, Metabolism, Distribution, and Excretion of Carfilzomib in Rats // Drug metabolism and disposition | |||
| Перекатываемый затвор для водоемов | 1922 |
|
SU2001A1 |
Авторы
Даты
2017-04-04—Публикация
2013-02-27—Подача